Родственные заявки
Приоритет настоящей заявки заявлен на основании предварительной заявки на патент №60/755839, поданной 3 января 2006 г.
Известный уровень техники
Настоящее изобретение относится, в общем, к диссоциации и удалению сильно гидратированных макроскопических объемов белковой ткани и более конкретно к диссоциации и удалению сильно гидратированных макроскопических объемов белковой ткани с использованием фракционирования потоком быстро изменяющего направление энергетического поля.
Настоящее изобретение описано в контексте витреоретинальной хирургии, однако специалистам будет понятно, что изобретение можно также применять в медицинских процедурах, проводимых на других областях организма человека или животных.
В течение десятилетий традиционные процедуры витреоретинальной хирургии на заднем сегменте глаза были основаны на механических или тракционных методах: 1) удаление ткани с помощью режущих зондов (с ножовочным или дисковым ножом), 2) рассечение оболочек с помощью ножниц, лезвий или скальпелей для стекловидного тела; 3) отведение оболочки с помощью пинцетов и захватов, и (4) отделение оболочки с помощью пинцета и вязких жидкостей. Несмотря на достигнутые усовершенствования механизмов и материалов, повышение качества, технологичности, системной поддержки и эффективности, улучшение результатов интраокулярной хирургии на заднем сегменте глаза в основном обеспечивается благодаря знаниям, устремленности, квалификации и опыту хирургов-офтальмологов.
Бестракционное удаление внутриглазной ткани в ходе витреоретинальной операции практически невозможно с помощью существующего арсенала механических медицинских инструментов. Хотя высокая квалификация, точность движений, опыт и знания практикующих хирургов позволяют свести к минимуму тракцию, обусловленную применением механических медицинских инструментов во время удаления ткани, ее невозможно исключить полностью. В механических или тракционных хирургических методах используется режущее действие для рассечения связей между тканями. Характерной чертой этого режущего действия является натяжение подлежащей удалению ткани, которое, в свою очередь, передается сетчатой оболочке глаза. При применении механических или тракционных хирургических методов силы, движущие режущим элементом механических медицинских устройств, которые используются для рассечения связей тканей, накладываются на сетчатую оболочку. Несмотря на опыт и осторожность хирурга-офтальмолога, это наложение сил на сетчатую оболочку, связанное с тракционными хирургическими методами, создает возможность ее повреждения.
В потенциальном бестракционном хирургическом методе, который используется для осуществления конформационных изменений в компонентах белка, применяются высокоинтенсивные импульсные электрические поля; однако высокоинтенсивное импульсное электрическое поле не нашло своего применения в таких тонких хирургических процедурах, как витреоретинальная хирургия.
Высокоинтенсивные импульсные электрические поля широко применяются в медицине, пищевой промышленности и в обработке микромеханических устройств. Примеры применения в области медицины включают в себя доставку химиотерапевтических препаратов в опухолевые клетки, генную терапию, трансдермальную доставку лекарств, а также бактериальную очистку воды и жидких пищевых продуктов. В пищевой промышленности высокоинтенсивные электрические поля с ультракороткими импульсами применяются при стерилизации и очистке. И наконец, высокоинтенсивные электрические поля с ультракороткими импульсами применяются в методах механической обработки и изменения поверхности, используемых для микросхем на основе микроэлектрических механических систем (МЭМС).
В последнее время исследования ученых-биофизиков и биохимиков сконцентрированы на манипулировании биологическими структурами, такими как макромолекулы, клеточные мембраны, внутриклеточные органеллы и внеклеточные объекты. Реакция биологических тканей на электрические поля, в общем известная как "электрокинетика", используется в исследованиях, диагностике и терапии.
Электрокинетические исследования и разработки нехирургического характера
Основную идею предлагаемого изобретения легче представить в контексте некоторых известных нехирургических методов, применяемых в настоящее время в биохимических молекулярных исследованиях, терапевтических фармацевтических разработках, методах стерилизации, промышленной полимеризации, исследованиях плазмы и разработках МЭМС ("лаборатория на чипе"). Далее будут описаны основные аспекты этих известных методов, чтобы проиллюстрировать другие системы, в которых осуществляются манипуляции и воздействия на белковый материал посредством подведения высокоинтенсивного импульсного электрического поля.
Электрореология
Электрореология (ЭР) - это явление, при котором реология жидкостей, включая биологические жидкости, изменяется посредством приложения электрических полей (обычных слабых полей постоянного тока). Электрическое поле, приложенное к жидкости, вызывает в ней объемно-фазовый переход, наиболее важным параметром которого является напряженность электрического поля, а наименее важным параметром является частота электрического поля. Большинство коллоидных ЭР жидкостей проявляет увеличение эффектов вязкоэластичности при увеличении амплитуды поля. Интересно, что уменьшение вязкоэластичности жидкости возникает при самых высоких напряженностях поля, однако определенных исследований влияния напряженности поля на вязкоэластичность не проводилось, и механизм ЭР остается неизвестным.
Электрофорез
Электрофорез (или диэлектрофорез) вызывает движение частиц в электрическом поле по направлению к одному или другому электрическому полюсу, аноду или катоду. Процесс электрофореза используется для разделения и очистки биомолекул (например, для разделения ДНК и РНК). Для материалов размером в интервале от нанометров до микрометров процесс электрофореза эффективен как для высоко специфического разделения материалов, так и для определения свойств материала. Во время электрофореза вызванный электрическим полем фазовый переход в изолированной суспензии подвергается действию пространственно-однородного электрического поля переменного тока. Этот вызванный электрическим полем фазовый переход следует за хорошо известным, индуцированным полем образованием столбчатой структуры в суспензии. Под действием внешнего электрического поля частицы, находящиеся в электрическом поле, ориентируются вдоль направления поля, образуя цепочки и столбики. Эти цепочки и столбики частиц затем вытягиваются под действием электрического поля и потока жидкости. Время, необходимое для разделения и изоляции частиц, находится в интервале от минут до часов, и при этом часто применяется множество вторичных процессов. Для усиления макромолекулярного разделения часто используют ионное поверхностно-активное вещество (например, додецилсульфат натрия) и разбавление образца. Ионные поверхностно-активные вещества способны образовывать химический мостик между гидрофобной и гидрофильной средами, тем самым разрушая или уменьшая гидрофобные соединительные силы, необходимые для сохранения структуры нативного белка.
Фракционирование в потоке при наличии поля
Фракционирование в потоке при наличии поля (FFF) представляет собой лабораторный метод разделения раствора, который по многим параметрам сопоставим с жидкостной хроматографией. Обычно материалы и градация размеров материалов, разделяемых в системах FFF, являются дополнительными к тем, которые анализируются с помощью электрофореза и жидкостной хроматографии. В системах FFF протагонист разделения (электрическое поле) прикладывается в направлении, перпендикулярном направлению разделения, и создает пространственное и временное разделение компонентов образца на выходе канала FFF. Разделение в канале FFF основано на различиях удержания (времени) компонентов образца. В свою очередь удержание в системах FFF является функцией различий физиохимических свойств образца, силы и режима применяемого воздействия, а также профиля скорости жидкости в разделительном канале. Благодаря применению FFF время электрофореза уменьшается от часов до минут.
Фракционирование в потоке при наличии электрического поля
В работе по обработке микроэлектрических механических систем (МЭМС) был разработан метод фракционирования в потоке при наличии электрического поля (EFFF). EFFF представляет собой процесс для разделения ex-vivo наночастиц, белков и макромолекул, захваченных в микроканалы, путем приложения электрических полей в осевом или поперечном направлении. Этот метод в настоящее время исследуется в связи с устройствами МЭМС для микрофореза. Метод основан на осевом потоке аналита под действием электрического потенциала (однонаправленного поперечного электрического поля). Эффективность разделения и время удержания частиц образцов в протоке зависит от взаимодействия образца с электрическим полем, которое прикладывается поперечно полю потока в канале. С помощью EFFF были достигнуты диссоциация белковых комплексов, разрушение белковых связей и последующее фракционирование. Также при применении периодических (пульсирующих) электрических полей в EFFF было отмечено увеличение удержания, которое привело к гораздо лучшему разделению.
Кроме того, было замечено, что применение импульсных потенциалов с переменной полярностью повышает эффективность электрического поля. Предполагается, что в рассечении цепочки значительную роль играет сдвиг, поскольку локальная деформация белковой ткани в любом градиенте электрического поля представляет собой просто удлинение. При количественном определении скорости деформации и осей растяжения и сжатия осторожная манипуляция геометрией матрицы и силой поля потока может обеспечить существенное вытяжение большинства макромолекул. Были разработаны микросхемы, которые могут генерировать электрические поля вращательного, растягивающего и сдвигового типов посредством изменения входных напряжений. Время разделения на микросхеме 1,25 см было уменьшено до приблизительно 5 секунд.
Электропорация
Электропорация представляет собой еще один известный нехирургический метод, который используется для обратимого кратковременного повышения проницаемости клеточной мембраны. Разработанная приблизительно в 1994 г. электропорация (ЭП) для улучшения доставки лекарств и генов через клеточные мембраны in-vitro за последнее десятилетие стала стандартной процедурой в лабораториях молекулярной биологии. Электропорация - это метод, в котором импульсы электрической энергии, измеряемые в киловольтах на см, длительностью в интервале от микросекунд до миллисекунд, вызывают временную потерю полупроницаемости клеточных мембран. Эта временная потеря полупроницаемости клеточных мембран вызывает утечку ионов, выход метаболитов и повышение клеточного поглощения лекарств, молекулярных зондов и ДНК. Некоторые известные применения электропорации включают в себя введение плазмидов или чужеродных ДНК в живые клетки для трансфекции, слияния клеток для приготовления гибридом и для введения белков в клеточные мембраны. Обычно используется длительность импульса порядка 0,1-10 миллисекунд и напряженность электрического поля порядка кВ/см в зависимости от типа клеток и суспензии. Механизм электропорации (т.е. открытия и закрытия клеточных каналов) еще не изучен окончательно.
Адаптации метода электропорации использовались для доставки лекарств. В патенте США №5869326 и опубликованной заявке на патент США 2004/0176716 описаны аппараты для чрескожной доставки лекарств. В опубликованной заявке на патент США 2004/021966 описан катетер для внутрисосудистой доставки лечебных препаратов и доставки лекарств in-vitro с помощью систем матриц электродов. В патенте США №6653114 описано средство для переключения электродов. В патентах США №№6773736 и 6746613 метод электропорации адаптирован для очистки продуктов и жидкостей посредством дезактивации и гибели клеток. В патенте США №6795728 гибель клеток, вызванная электропорацией, лежит в основе устройства и способа для уменьшения подкожных отложений жира in-vitro.
Электрическое поле c наносекундными импульсами
Метод электрического поля с наносекундными импульсами (nsPEF) является расширением применения описанного выше метода электропорации для применения in-vitro, в котором используется прямоугольный или трапецеидальный импульс значительно более короткой длительности (1-300 нс) вместе со значительно более сильными электрическими полями (до 300 кВ/см). Технология nsPEF возникла благодаря достижениям в технологии мощности импульса. Использование технологии мощности импульсов позволило подводить электронные поля с наносекундными импульсами (nsPEF), имеющие напряженность поля в несколько сот раз выше, чем импульсы электрической энергии, используемой в электропорации, к клеткам и тканям, не вызывая при этом биологически значимых повышений температуры в исследуемых образцах. При использовании очень небольшого количества импульсов электрической энергии эффекты nsPEF по существу не имеют термического характера. В отличие от классического метода электропорации влияние nsPEF на клетки млекопитающих было обнаружено совсем недавно. Применение nsPEF соответствующей амплитуды и длительности вызывает кратковременное повышение клеточной проницаемости, клеточные или субклеточные повреждения или даже апоптоз. Целью наносекундной электропорации in-vivo является получение равномерного распределения эффективного электрического поля в узком временном окне.
Недавние исследования показали, что приложение наносекундных импульсов (кВ/см) к тканям может возбуждать электроны без нагрева ионов или нейтральных частиц. Было обнаружено, что можно использовать энергетическое поле с ультракороткими импульсами (электромагнитная ЭМ, лазер или интенсивный сфокусированный ультразвук, HIFU) для временного и обратимого повышения проницаемости клеточных мембран или даже воздействия на внутриклеточные компоненты без повреждения клеточной мембраны. Было также обнаружено, что более высокие энергии возбуждают ионы и могут вызывать образование короткоживущих радикалов (ОН и О2 +). Это заключение привело к созданию процессов стерилизации и очистки, позволяющих убивать клетки. Использование еще более высоких энергий может вызвать образование сверхзаряженных плазменных дуг, которые действуют на клеточные связи на молекулярном уровне.
Электроосмос
Электроосмос (ЭО) - это метод, используемый для переноса или смешивания жидкостей для применения в микроустройствах. Основная концепция заключается в использовании различных механизмов зарядки и интенсивности поляризации двойного слоя на границе электрод/электролит для создания однонаправленной силы Максвелла на жидкости, которая генерирует сквозную накачку. В электроосмосе с индуцированным зарядом (ICEO) создается эффект, который вызывает микрозавихрения в жидкости, усиливающий перемешивание в микрофлюидальных устройствах. Перемешивание можно существенно усилить в режиме ламинарного потока, подвергнув жидкость воздействию кинематики хаотического потока. Путем изменения полярности и прикладываемого напряжения можно регулировать силу и направление радиального электроосмотического потока.
Прочие электрокинетические явления
Электрокинетические явления не ограничены теми, которые были описаны выше. Недавно разработанные варианты, связанные с очень большими напряжениями и уникальными электрическими полями в исследованиях МЭМС, продемонстрировали интересные и неожиданные эффекты, возникающие при прикладываемых переменных электрических полях, включая установление того факта, что электрофоретическая мобильность коллоидов чувствительна не просто к общему результирующему заряду, а к распределению зарядов.
Удаление ткани
Все описанные выше процессы могут применяться для манипулирования макромолекулами, однако не для экстракции или удаления макроскопических объемов белковой ткани путем диссоциации ткани. Так как в других системах с использованием импульсной энергии на тканях применяется энергия высокого уровня, было обнаружено, что более высокие энергии, создаваемые за счет увеличения длительности импульсов, серий импульсов, частоты следования и времени воздействия, вызывают термические эффекты или образование сверхзаряженной плазмы. Эти термические эффекты или образование сверхзаряженной плазмы эффективно используются в некоторых устройствах для создания хирургических инструментов для разрезания тканей. В этих инструментах вокруг инструмента создается область плазмы, имеющая микроразмеры (по толщине или высоте). Внутри сверхзаряженной плазмы находятся заряженные электроды, ионы и молекулы с беспорядочным движением, которые при контакте с тканями или клетками действуют на связи на молекулярном уровне, вызывая тем самым абляцию или облитерацию в результате сублимации целевой ткани или поверхности ткани. В основе образования сверхзаряженной плазмы лежат процессы электронных лавин, высокой степени туннелирования электронами из валентной зоны в сплошную среду с образованием лавинной ионизации электронной плазмы. Плотность этой сверхзаряженной плазмы быстро нарастает за счет дополнительного туннелирования, а также вызванных полем столкновений между свободными электронами и молекулами. Основной целью воздействия на ткань сверхзаряженной плазмой является неразрушающая хирургия, то есть управляемое, высокоточное удаление пораженных частей с минимальным вредом для здоровой ткани. Размер и форма активной плазмы регулируются конструктивным выполнением зонда, размерами и средой. Используются как газовые, так и жидкие среды. В жидкости может образоваться взрывчатый пар.
Импульсный электронно-лавинный нож
Импульсный электронно-лавинный нож ("PEAK"), предложенный в заявке на патент США 2004/0236321, описан как бестракционное устройство для холодной резки. Сильное электрическое поле (nsPEF 1-8 кВ; 150-670 мкДж) прикладывается между открытым микроэлектродом и частично изолированным электродом. Приложение этого сильного электрического поля вызывает образование плазмы, выражающееся в форме стримеров плазмы длиной порядка микрометра. Размеры стримеров плазмы регулируются размером открытого электрода. Стримеры плазмы, в свою очередь, создают взрывчатое испарение воды на микронном уровне. Импульсная энергия имеет критическое значение. Был продемонстрирован точный, безопасный и экономичный разрез ткани. При уменьшении размера электрода до микронного уровня разряды плазмы должны быть заключены в наконечнике зонда, потому что ионизация и взрывчатое испарение жидкой среды могут разрушить соседнюю ткань и привести к образованию кавитационных пузырьков. Высокое давление, достигаемое во время образования плазмы, быстрое расширение пузырька пара (более 100 м/сек) и последующее сплющивание полости, которые могут распространиться на зону взаимодействия, имеют в основном механический характер из-за быстрого охлаждения пара в пузырьках. В офтальмологической хирургии испаряемость и агрессивность эффекта, вызванного использованием "PEAK", могут оказаться пагубными для целостности сетки.
Кобляция
В кобляции, или "холодной абляции", используется радиочастота (РЧ) в биполярном режиме с проводящим раствором, таким как солевой раствор, для генерации плазмы, которая при контакте с целевой тканью сублимирует поверхностный слой целевой ткани. Дальность ускоренных заряженных частиц небольшая и ограничена граничным слоем плазмы около зонда и поверхностью контакта с тканью. Кобляция возбуждает ионы в солевом (проводящем) растворе, образуя небольшое поле плазмы. Эта плазма имеет достаточную энергию для разрыва молекулярных связей ткани и создания абляционного пути. Сообщается, что термический эффект этого процесса составляет приблизительно 45-85°С. Обычно электрохирургические РЧ устройства используют тепло для изменения структуры ткани. Однако генерация РЧ-индуцированного поля плазмы рассматривается как "холодный" процесс, так как влияние плазмы ограничено собственно плазмой, и слой плазмы удерживается микроскопически тонким. Плазма состоит из высокоионизированных частиц, имеющих достаточную энергию для достижения молекулярной диссоциации молекулярных связей. Энергия, необходимая для разрыва связей углерод-углерод и углерод-азот, составляет порядка 3-4 эВ. Метод кобляции предположительно создает около 8 эВ. Благодаря биполярной конфигурации электродов и разности импеданса между тканью и солевым раствором большая часть тока проходит через проводящую среду, находящуюся между электродами, что приводит к минимальному проникновению тока в ткань и минимальному термическому повреждению ткани. Если порог энергии, необходимый для создания плазмы, не достигнут, ток проходит через проводящую среду и ткань. Энергия, поглощенная тканью и проводящей средой, рассеивается в виде тепла. После достижения порога энергии, необходимого для создания плазмы, импеданс к потоку РЧ тока изменяется от почти чисто резистивного типа к более емкостному типу импеданса. Как и в случае использования PEAK в офтальмологической хирургии, использование методов кобляции может быть слишком рискованным для хирургического применения вблизи сетчатки.
Плазменная игла
Плазменная игла представляет собой еще одно устройство, которое позволяет удалять или трансформировать конкретные клетки, не влияя на окружающую ткань. Применение плазменной иглы является очень точным методом, в котором используется миниатюрная игла, прикрепленная к ручному инструменту, для создания небольшого плазменного разряда. Электрическое поле создается между кончиком иглы и проксимальным электродом при прохождении инертного газа (гелия) между ними. Небольшой плазменный разряд содержит электроны, ионы и радикалы, причем ионы и радикалы регулируются путем введения в инертный газ загрязнителя, такого как воздух. Предполагается, что малый размер источника плазмы (плазменная игла) создает активные формы кислорода (ROS) и УФ-излучение такого мизерного уровня, который позволяет изменять функцию или адгезию клеток без повреждения самих клеток. Однако увеличение ROS (например, воздуха) в инертном газе вместе с увеличением времени облучения может приводить к гибели клеток. Хотя плазменная игла и оказывает влияние на тонкие слои жидкости, ее использование не является оптимальным в сплошной жидкой среде, которая часто используется в офтальмологической хирургии.
Электроэрозия
Метод электроэрозии является родственным обсуждавшимся выше пламенным методам. В устройстве для электроэрозии используется импульсное энергетическое поле 250 кГц, длительностью 10 мс и до 1,2 кВ для создания пара. При возникновении электрического пробоя пара образуется небольшая искра (менее 1 мм). При эффекте дальней зоны до 1,7 мм разрез с помощью электроэрозии выполняется как в электрохирургии, но как при использовании плазмы с тканью контактирует только плазма.
Лазеры
Лазеры представляют собой еще одну бестракционную технологию, которая используется для разрушения макромолекул ткани. Лазеры применяются в офтальмологической хирургии с 1960 г. Наиболее успешно лазеры применяются в области неинвазивной коагуляции сетчатки глаза при таких заболеваниях, как диабетическая ретинопатия, окклюзия центральной вены и хороидальная неоваскуляризация при возрастной дегенерации желтого пятна или ишемическом ретинальном васкулите. Лазеры также широко используются применительно к переднему сектору глаза при пластике роговицы и глаукоме. Попытки использования лазеров в офтальмологической хирургии заднего сектора глаза дали смешанные результаты. Неинвазивные методы (транскорнеальный подход, через хрусталик или склеру) не практичны из-за поглощающих свойств этих промежуточных тканей. Чрезвычайная точность, необходимая при интраокулярной хирургии сетчатки и стекловидного тела глаза, требует использования все более совершенных инвазивных методов для манипуляции тканью и ее удаления. Режимы взаимодействия ткань/лазер включают в себя: (1) термический - преобразование электромагнитной энергии в тепловую; (2) фотохимический - внутренние (эндогенные) или введенные (экзогенные) светочувствительные химические вещества (хромофоры), активизируемые поглощением лазерных фотонов; (3) фотоабляционный - прямая фотодиссоциация внутримолекулярных связей поглощения лазерных фотонов; (4) электромеханический - термоэлектронная эмиссия или мультифотонное образование свободных электронов, вызывающее пробой диэлектрика и образование плазмы. Было обнаружено, что применение лазеров экономически невыгодно и требует использования экранов и заслонов на лазерных зондах уникальной конструкции, чтобы защитить тонкие внутриглазные ткани от лазерной энергии и тепловых эффектов дальней зоны. Однако недавние разработки в области фемтосекундных импульсных лазеров открыли новые возможности для точных хирургических применений.
Прочие методы удаления ткани
Используемые в настоящее время методы разрушения внутриглазных тканей включают в себя удаление по частям (фрагментацию), для которого предназначены механические режущие инструменты для витрэктомии; разжижение, обусловленное термическими (денатурирование белка) или ферментативными реакциями, и сублимацию посредством воздействия лазером или плазмой. Сублимация посредством воздействия лазером или плазмой действительно действует на связи на молекулярном уровне, тогда как удаление по частям и разжижение влияют на механизм связи меньшей силы (т.е. нековалентные связи).
Поэтому, несмотря на множество достижений в витреоретинальной хирургии, все еще существует потребность в эффективном устройстве и способе для диссоциации и удаления сильно гидратированных макроскопических объемов белковых тканей, таких как стекловидное тело и внутриглазные ткани, в ходе витреоретинальных операций.
Сущность изобретения
Предложены устройство и способ для диссоциации и удаления сильно гидратированных макроскопических объемов белковых тканей, таких как стекловидное тело и внутриглазная ткань, в ходе витреоретинальных операций.
Несмотря на то что изобретение описано в контексте устройства и способа для бестракционного удаления стекловидного тела и внутриглазных мембран из заднего сегмента глаза без повреждения ультратонкой структуры и функции соседней или прилегающей сетчатки, специалистам будет понятно, что описанное изобретение также применимо и в других медицинских процедурах, выполняемых как на людях, так и на животных.
Изобретение описано в контексте нового средства для выполнения витреоретинальной операции с использованием высокоинтенсивного, короткого, изменяющего направление электрического поля в отличие от классических механических средств для захвата, разложения и удаления стекловидного тела и внутриглазных тканей. В частности, было обнаружено, что кратковременное изменение состояния ткани, вызванное приложением высокоинтенсивного, короткого, изменяющего направление электрического поля, достаточно для удаления макроскопических объемов белковой ткани. Технический успех механических и разжижающих средств подтверждает тот факт, что нет необходимости в облитерации или разрушении материала стекловидного тела на молекулярном уровне для его удаления, напротив, для удаления ткани требуется всего лишь безопасное макроскопическое изменение состояния. Соответственно, удаление внутриглазной ткани с помощью настоящего изобретения может осуществляться совершенно бестракционно.
Предложенные устройство и способ вызывают локальную временную диссоциацию адгезионных и структурных связей компонентов внутриглазной белковой ткани с помощью быстро изменяющегося электрического поля. Эта локализованная временная диссоциация адгезионных и структурных связей внутриглазной белковой ткани позволяет осуществлять бестракционное разделение компонентов внутриглазной ткани и сетчатой оболочки. Во время процесса диссоциации ткани применяются струйные методы (ирригация и аспирация), способствующие образованию высокоинтенсивного электрического поля с ультракороткими импульсами и удалению разрушенной ткани в момент диссоциации. При этом разрушается и удаляется только материал в пределах прикладываемого высокоинтенсивного электрического поля с ультракороткими импульсами. Следовательно, поскольку только материал, подвергающийся воздействию подводимых ультракоротких импульсов, принимает высокоинтенсивное электрическое поле с ультракороткими импульсами, во время процесса экстракции ткани отсутствует эффект дальней зоны.
Конструкция зонда, применяемого для создания импульсного электрического поля вместе с использованием струйных методов, захватывает целевой макроскопический объем ткани, подлежащей диссоциации. Этот захваченный целевой макроскопический объем внутриглазной ткани одновременно подвергается воздействию высокоинтенсивного электрического поля с ультракороткими импульсами. Поражение высокоинтенсивным электрическим полем с ультракороткими импульсами вызывает диссоциацию захваченного макроскопического объема внутриглазной белковой ткани, после чего диссоциированный захваченный макроскопический объем ткани удаляется посредством аспирации.
В соответствии с настоящим изобретением зонд с двумя или более электродами вводится в целевую гидратированную ткань, стекловидное тело или внутриглазную ткань. Концы электродов открыты на дистальном конце зонда. Электрический импульс передается по меньшей мере на один электрод, в то время как другой один или более электродов действуют в качестве обратного проводника. Неплазменное электрическое поле создается между подводящим электродом(ами), действующим как анод, и обратным электродом(ами), действующим как катод. В каждом электрическом импульсе направление создаваемого электрического поля изменяется посредством обращения полярности, переключения электродов или комбинации этих мер. Импульсы могут группироваться в пачку, которая повторяется с различной частотой и различными амплитудами. Такие группы импульсов можно направить на неоднородную ткань. Амплитуда, длительность, рабочий цикл и частота следования электрических импульсов вместе с постоянно изменяющимся направлением поля создают разрушающее электрическое поле на отверстии аспирационного просвета. Ткань всасывается в отверстие аспирационного просвета струйным методом (аспирацией). Затем эта ткань смешивается или разбавляется с ирригационной жидкостью и диссоциирует при ее пересечении высокоинтенсивного, изменяющего направление электрического поля с ультракороткими импульсами. В любой данный момент времени в электрическом поле создается беспорядок посредством изменения направления электрического поля между одним или более электродами в наконечнике зонда. Пораженная среда между концами электродов на конце зонда состоит из смеси целевой ткани (например, стекловидного тела) и вспомогательной жидкости (ирригационной жидкости). Импеданс целевой среды, в которой создается электрическое поле, поддерживается посредством контролируемого подвода вспомогательной жидкости (ирригационной жидкости). В предпочтительном варианте в качестве вспомогательной жидкости, обеспечивающей импеданс, используется проводящий солевой раствор. Вспомогательную жидкость можно доставлять из ирригационного источника, находящегося вне зонда, через один или более просветов внутри зонда, или их комбинации. Когда вспомогательная жидкость подается внутрь ограниченного зондом пространства, она может иметь свойства (например, рН) и ингредиенты (например, поверхностно-активные вещества), способствующие диссоциации белков.
Для работы изобретения большое значение имеют свойства поля электрической энергии, создаваемого в целевой среде. При этом применяются высокоинтенсивные ультракороткие (субмикросекундные) импульсы электрической энергии. Импеданс, проводимость и разбавление ткани поддерживаются в целевой среде посредством ирригации вспомогательной жидкостью. Форма импульса, частота следования и длина серии импульсов регулируются в соответствии со свойствами внутриглазных тканей. Можно применять многофазные модели для решения проблемы неоднородности внутриглазной ткани. Кроме того, важную роль в диссоциации ткани играют пространственный конец электродов и последовательность активизации электродов в наконечнике зонда вместе с профилем генерированного поля. Скорость аспирации ткани согласуется со скоростью диссоциации ткани. Эффект импульсного быстроразрушающего электрического поля в целевой среде имеет такую высокую интенсивность и при этом такую короткую продолжительность (т.е. низкую энергию), что реальная диссоциация целевой ткани от окружающей ткани представляет собой кратковременный эффект (от микросекунд до миллисекунд), который не имеет термического характера и лишен взрывчатой кавитации.
Энергия, передаваемая высокоинтенсивными электрическими импульсами ультракороткой длительности, не вызывает образования плазмы, поэтому отсутствует агрессивный эффект дальней зоны. Высокоинтенсивные электрические импульсы ультракороткой длительности используются для создания неконтактной разрушающей электрической силы внутри ткани не электронной лавиной, а посредством непрерывного изменения направления поля. В частности, в белковой ткани, подлежащей диссоциации, создается неплазменная неконтактная возбужденная область беспорядка. Любой заряженный материал, попадающий в электрическое поле, подвергается воздействию этого поля, и внутриглазные ткани (например, белки) изменяются. При создании разрушающего электрического поля вокруг белковых тканей без электронной лавины механизмы соединения между компонентами ткани испытывают кратковременное нарушение. Это кратковременное нарушение приводит к диссоциации компонентов ткани, свободной от возмущающего влияния дальней зоны. Кратковременное нарушение механизмов соединения между комплексами ткани приводит к разворачиванию белковых комплексов и раскручиванию спиралей, что позволяет разрушать коллагеновые сегменты и адгезионные связи (фрагментация смещенных фибрилл).
Целью настоящего изобретения является обеспечение бестракционной экстракции стекловидного тела и внутриглазных тканей из задней внутриглазной области. Предложенные устройство и способ захватывают и разрушают гидратированную белковую гелевую матрицу, вызывая кратковременное нарушение или диссоциацию адгезионных механизмов между компонентами ткани. Во время этого кратковременного нарушения или диссоциации адгезионных механизмов между компонентами ткани применяются струйные методы для разбавления и аспирации комплекса диссоциированной ткани из окружающей ткани.
Целью описанной системы является также изменение состояния белковой ткани стекловидного тела для ее безопасного удаления. Это изменение состояния белковой ткани стекловидного тела вызывает нарушение взаимодействия между компонентами белковой ткани, способствует разделению и отсоединению компонентов белковой ткани от соседних структур и удалению компонентов белковой ткани в процессе их разделения и отсоединения.
Соответственно, в основу настоящего изобретения положена задача создания нового хирургического способа и устройства, которые позволяют удовлетворить потребности современной витреоретинальной хирургии, а именно устройства для усовершенствованной и более точной экстракции стекловидного тела и внутриглазных мембран при сохранении целостности сетчатки глаза. Хотя предложенная система сфокусирована на новом устройстве для изменения состояния и удаления стекловидного тела и связанных с ним внутриглазных мембран, специалистам будет понятно, что кроме офтальмологии представленную информацию можно применить также и в других областях хирургии.
Краткое описание чертежей
Более полное представление о предложенной системе для диссоциации и удаления белковой ткани можно получить из прилагаемых чертежей, на которых
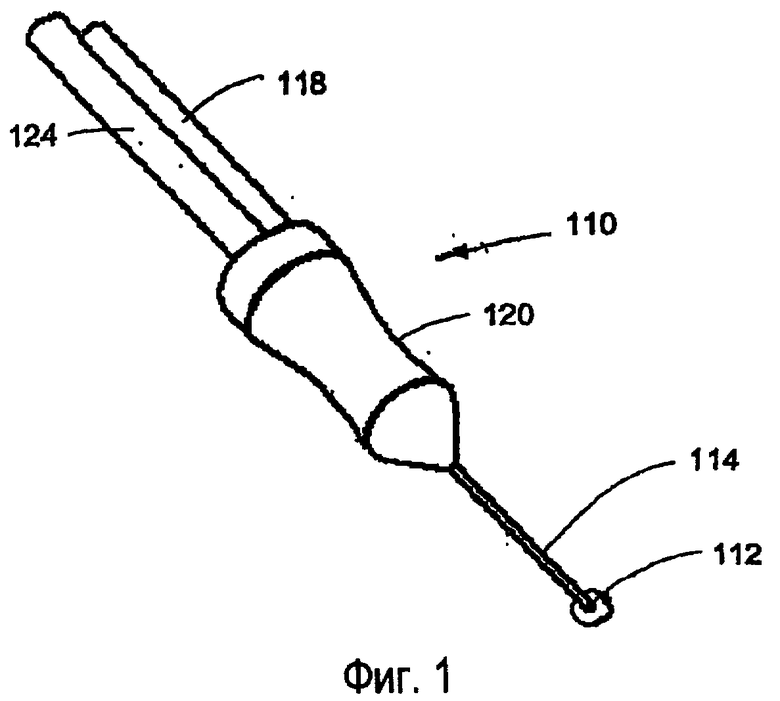
фиг.1 изображает перспективный вид зонда, применяемого для интраокулярной хирургии на заднем сегменте глаза, с использованием предложенной системы;
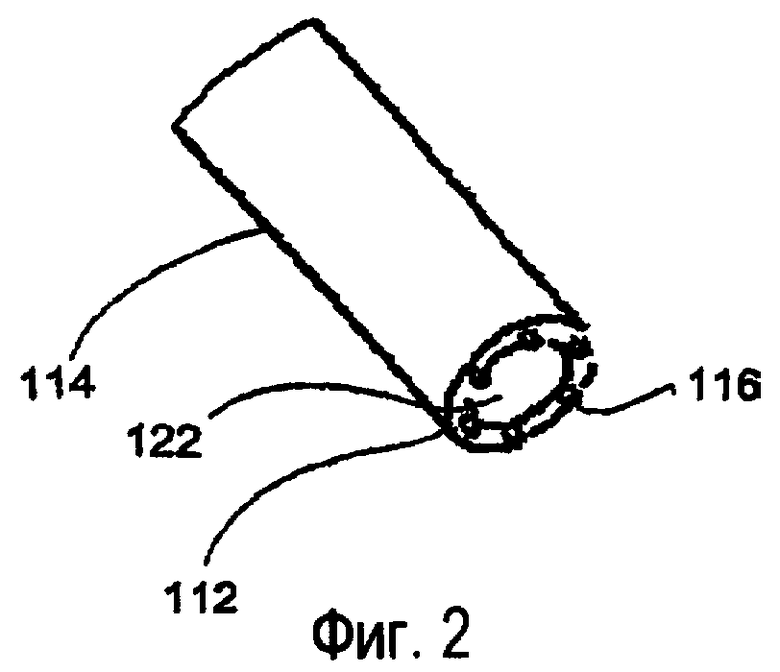
фиг.2 изображает увеличенный перспективный вид наконечника зонда, показанного на фиг.1;
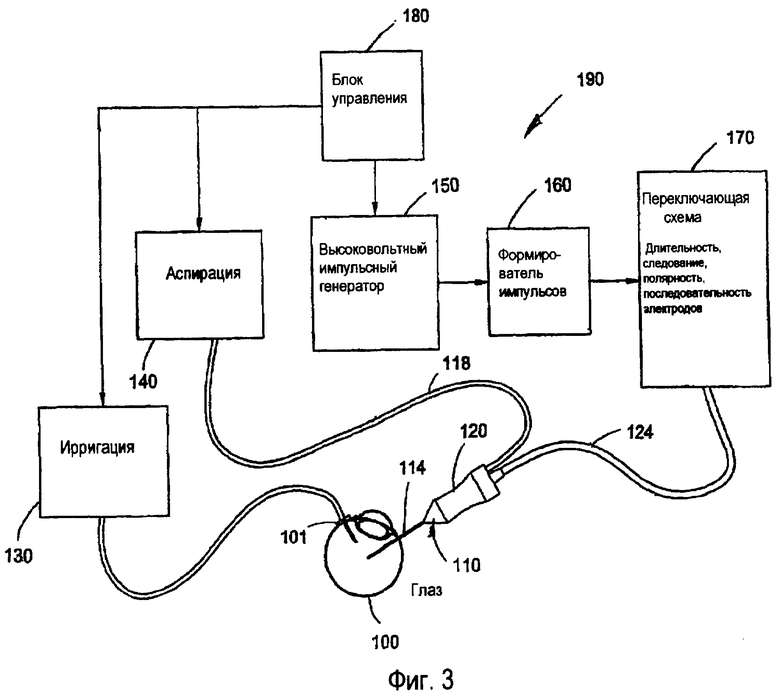
фиг.3 изображает структурную схему предпочтительного варианта предложенной системы;
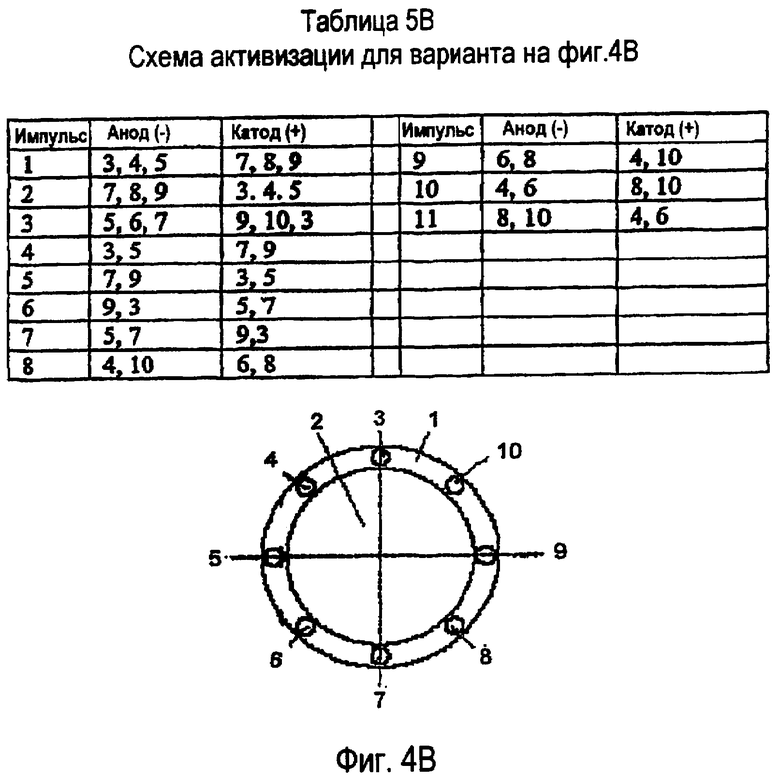
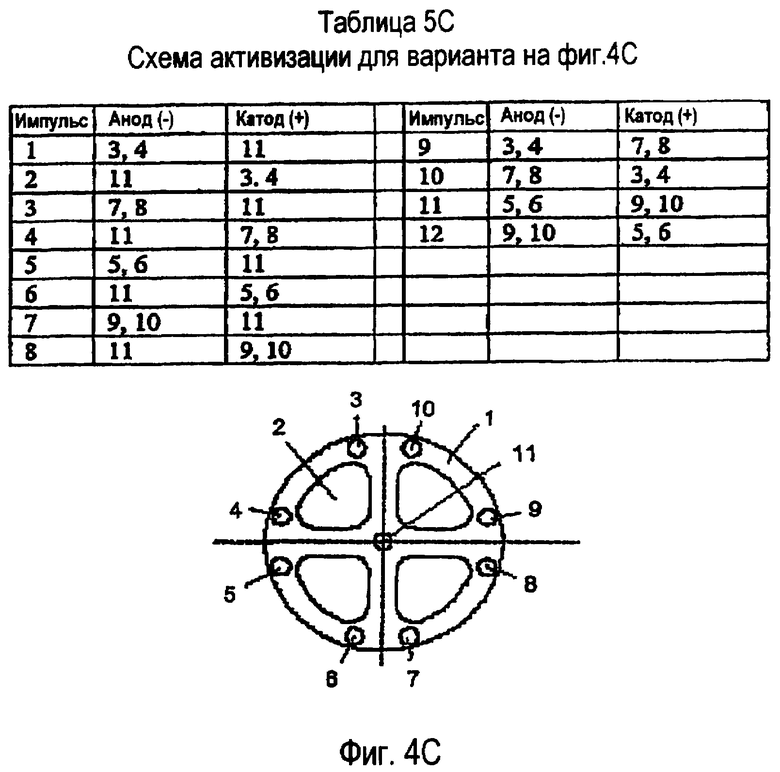
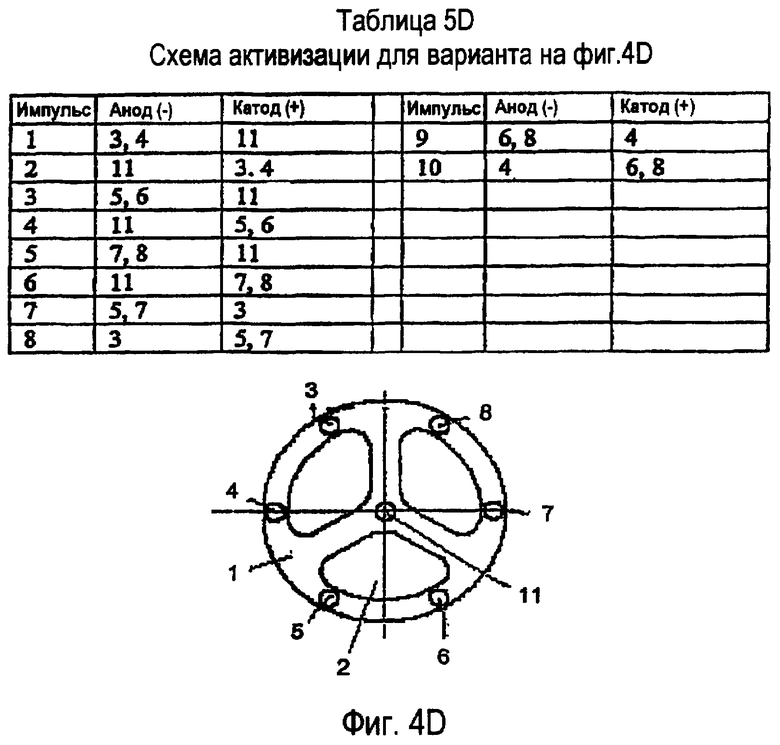
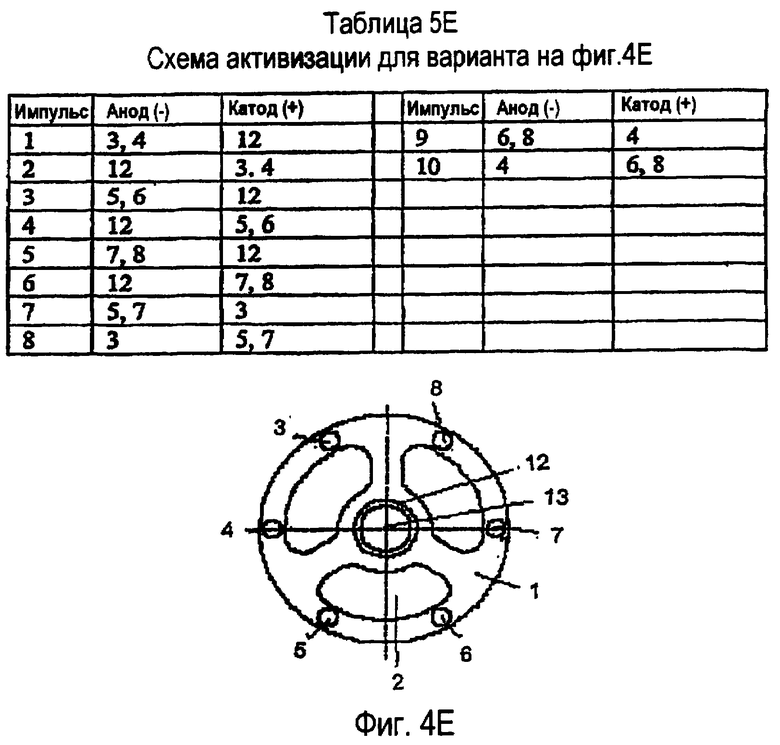
фиг.4А, 4В, 4С, 4D и 4E изображают виды спереди альтернативных расположений электродов в наконечнике зонда;
Таблицы 5А, 5В, 5С, 5D и 5Е представляют схемы активизации, связанные с матрицами зондов, показанными на фиг.4А, 4В, 4С, 4D и 4Е, соответственно;
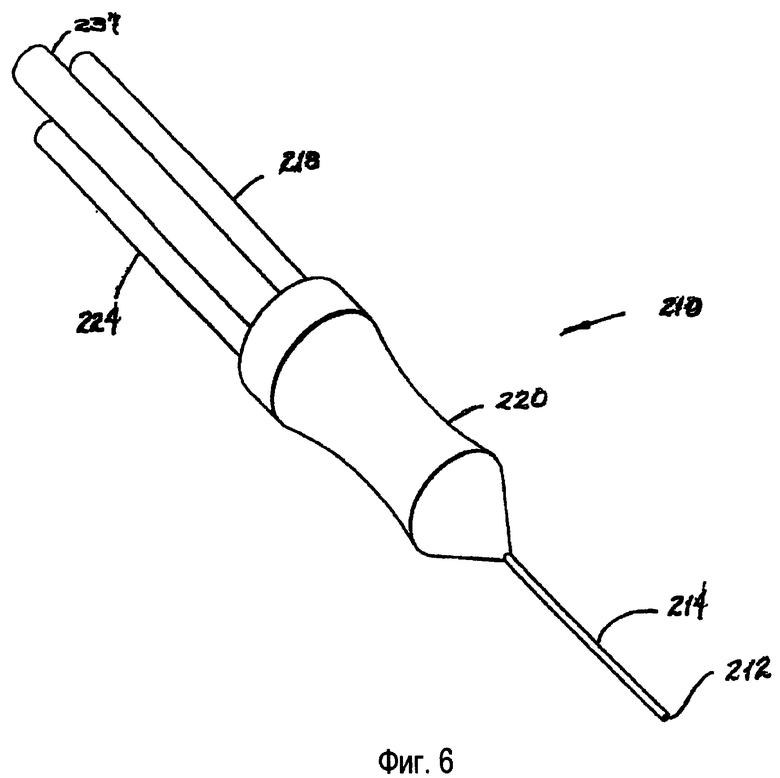
фиг.6 изображает перспективный вид трехэлектродного варианта зонда, используемого для интраокулярной хирургии на заднем сегменте глаза, с применением системы в соответствии с настоящим изобретением;
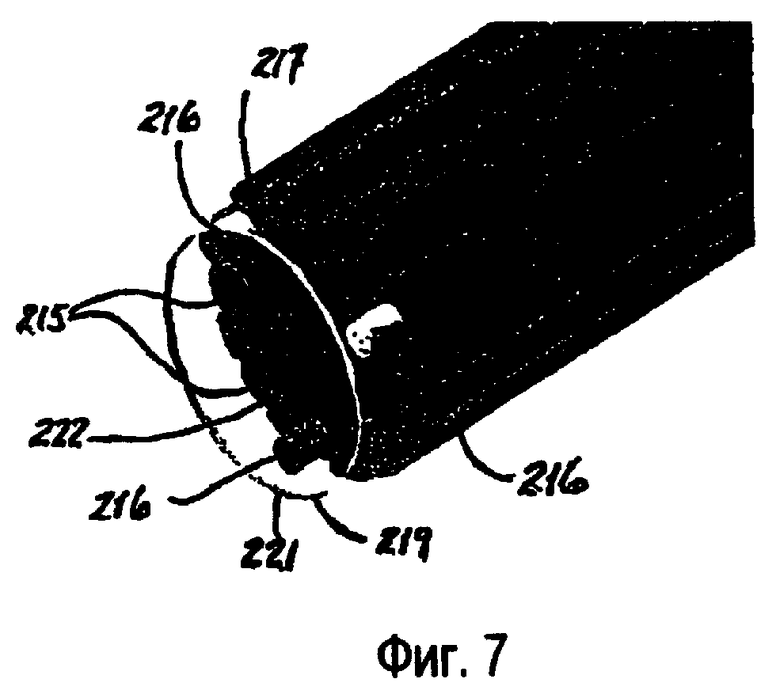
фиг.7 изображает увеличенный перспективный вид наконечника зонда, показанного на фиг.6, с прозрачным покрытием, чтобы показать внутренние элементы;
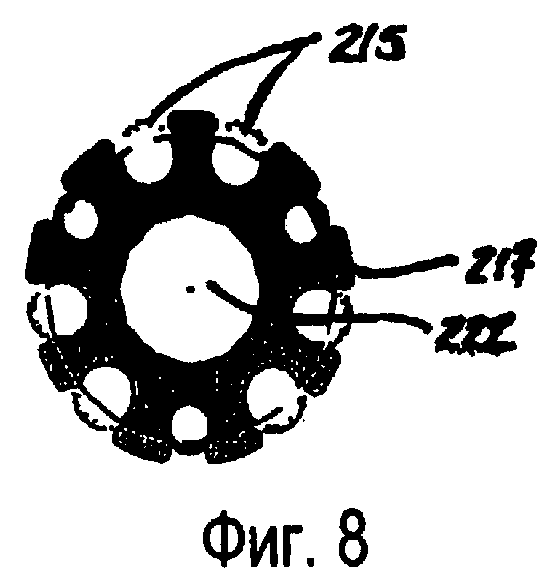
фиг.8 изображает вид с торца зонда, показанного на фиг.7;
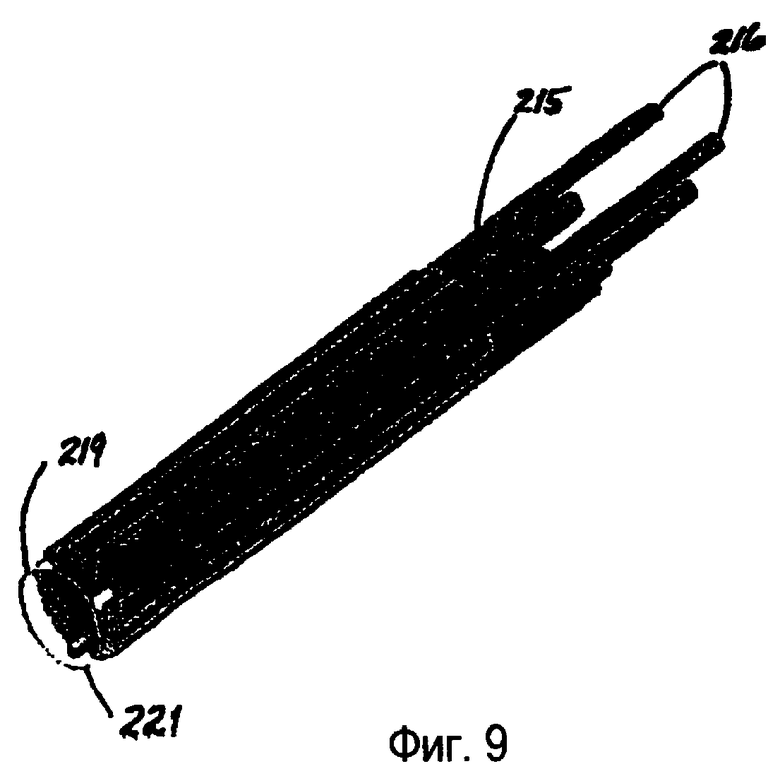
фиг.9 изображает увеличенный перспективный вид зонда, аналогичного показанному на фиг.7;
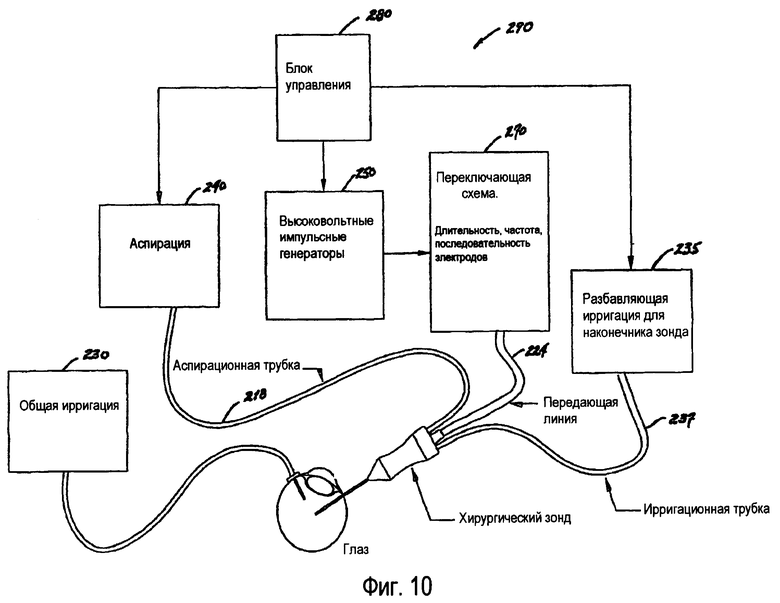
фиг.10 изображает схематически альтернативный вариант предложенной системы с вспомогательным ирригационным средством в составе зонда;
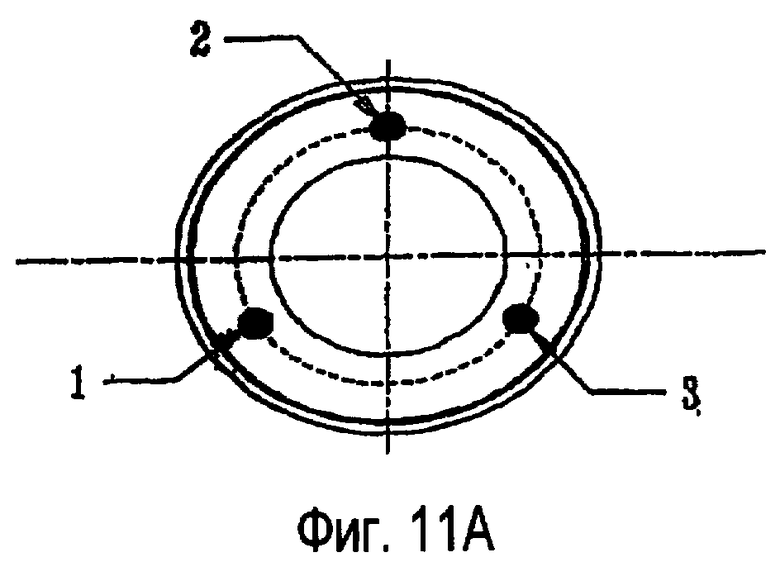
фиг.11А изображает вид с торца наконечника зонда, показывающий размещение трех электродов, как в варианте, показанном на фиг.7, 8 и 9;
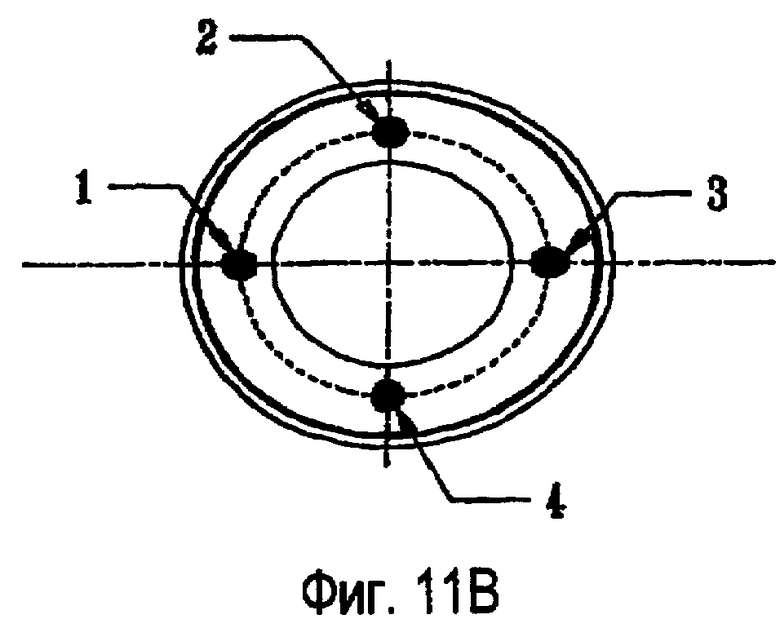
фиг.11В изображает вид с торца наконечника зонда, имеющего четыре электрода;
фиг.12А изображает схему активизации, связанную с матрицей электродов, показанной на фиг.11А;
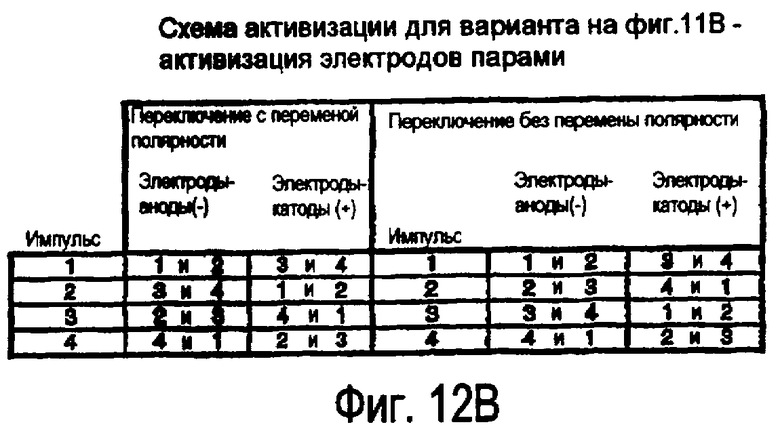
фиг.12В изображает схему активизации, связанную с матрицей электродов, показанной на фиг.11В;
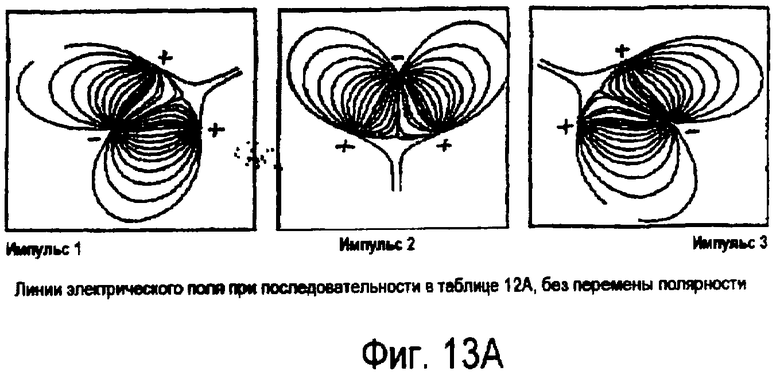
фиг.13А иллюстрирует примерные линии поля, обусловленные положением заряда на одном или более электродах, изображенных на фиг.11А;
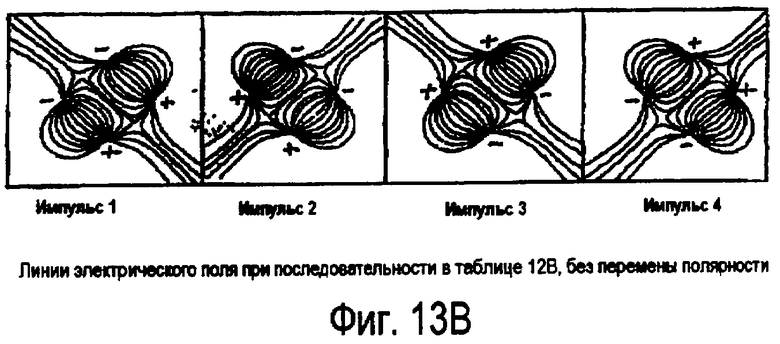
фиг.13В иллюстрирует примерные линии поля, обусловленные положением заряда на одном или более электродах, показанных на фиг.11В;
фиг.14 изображает схематически пример трехканального генератора импульсов, используемого с трехэлектродным зондом;
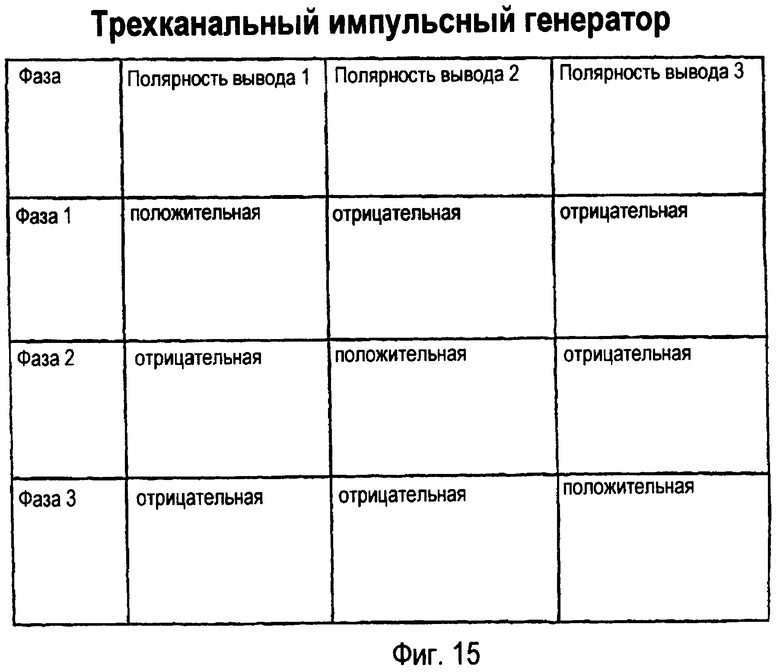
фиг.15 изображает схематически состояние каналов во время одного цикла выработки импульсов генераторами, показанными на фиг.14;
фиг.16 изображает увеличенный перспективный вид другого варианта наконечника зонда, показанного на фиг.6, с прозрачным покрытием, чтобы показать внутренние элементы;
фиг.17 изображает увеличенный перспективный вид зонда, показанного на фиг.16, содержащего кожух, покрывающий внутренние элементы;
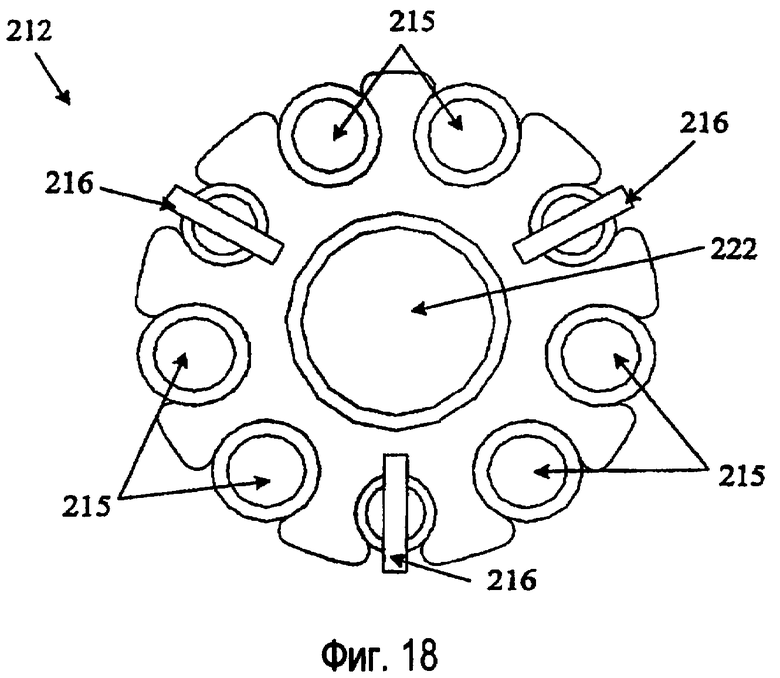
фиг.18 изображает вид с торца зонда, показанного на фиг.16;
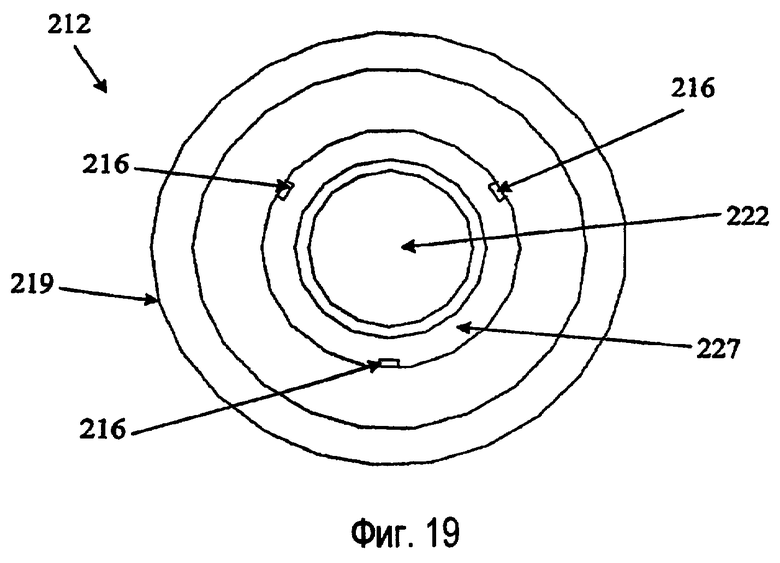
фиг.19 изображает вид с торца зонда, показанного на фиг.17;
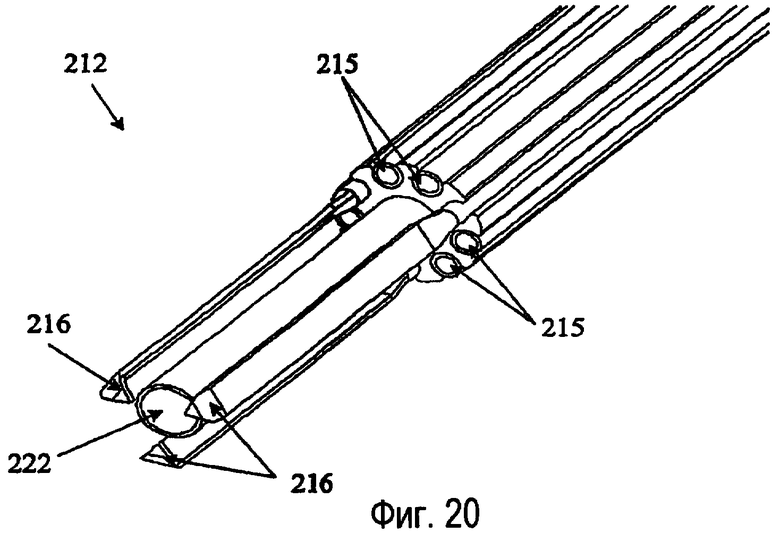
фиг.20 изображает увеличенный перспективный вид другого варианта наконечника зонда, показанного на фиг.6, с прозрачным покрытием, чтобы показать внутренние элементы;
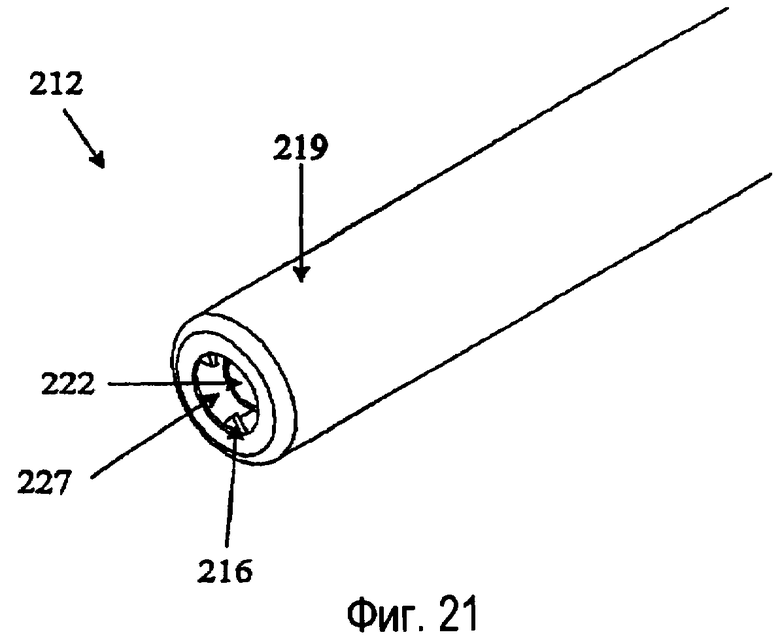
фиг.21 изображает увеличенный перспективный вид зонда, показанного на фиг.20, содержащего кожух, покрывающий внутренние элементы;
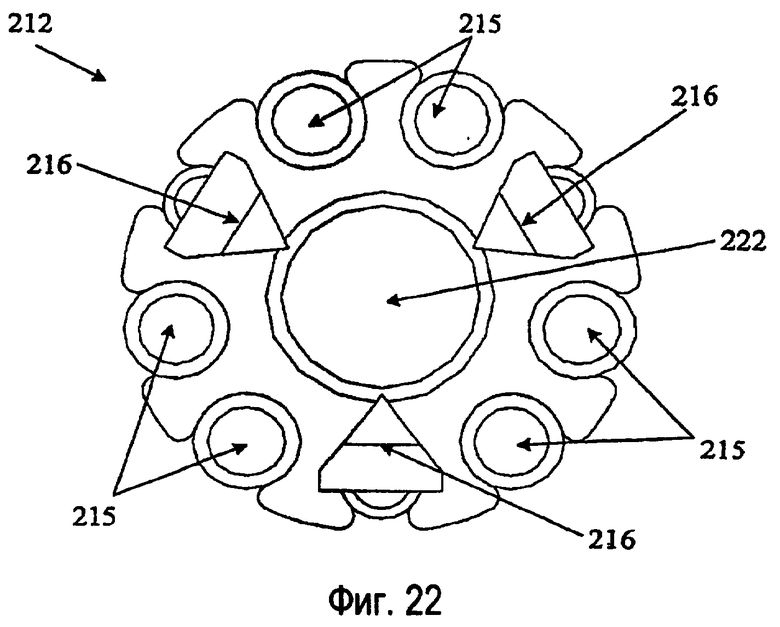
фиг.22 изображает вид с торца зонда, показанного на фиг.20, и
фиг.23 изображает вид с торца зонда, показанного на фиг.21.
Подробное описание вариантов осуществления изобретения
Разжижение (synchysis - лат.) возникает в стекловидной части глаза как естественный результат старения. Когда человек достигает возраста 70-90 лет, приблизительно 50% гелевой стриктуры стекловидного тела изменяет свое состояние или становится разжиженным. Результаты разжижения проявляются в стекловидном теле заднего сегмента глаза в виде дестабилизации стекловидной матрицы, растворения НА-коллагеновой связи, раскручивании коллагеновых спиралей, молекулярных перестановок, увеличения объема разжиженного пространства, освобождения сплетенных связей, увеличения отделения стекловидного тела от сетчатки, фрагментации и агрегации коллагеновых волокон, потери протеогликанов, нековалентно связанных макромолекул и адгезионного коллагена (типа IX). Настоящее изобретение позволяет имитировать многие активности, ведущие к разжижению в стекловидном теле глаза, на клеточном уровне.
В предложенных устройстве и способе применяется высокоинтенсивное, разрушающее, изменяющее направление электрическое поле с импульсами ультракороткой длительности (низкоэнергетическое), в котором продолжительность импульсов, частота их следования, импульсная последовательность и длина серии импульсов регулируются в соответствии со свойствами компонентов внутриглазного внеклеточного матрикса (ЕСМ), чтобы создать короткий период диссоциации ткани. Рекомендованный способ применения разрушающего электрического поля с ультракороткими импульсами основан на подводе высоких мощностей низкой энергии.
Как показано на фиг.1, предложенное устройство для реализации настоящего изобретения содержит зондовую систему 110, которая подводит, канализирует и распределяет энергию, прикладываемую к мягкой ткани, таким образом, чтобы создать ограниченную, локализованную, нетермическую динамическую область электрических сил внутри макроскопического объема внеклеточного матрикса, ЕСМ (например, стекловидного тела и внутриглазных мембран), вызывающую мгновенную диссоциацию белковых комплексов и локальное разжижение захваченного макроскопического объема ткани. Наконечник 112 полого зонда 114 располагают так, чтобы окружить захваченный макроскопический объем белковой ткани. Струйные методы (ирригация) используются, чтобы сначала создать область стабильного импеданса и разбавления между электродами 116 в наконечнике 112 полого зонда 114 и затем всасывать и удалять (аспирация) пораженный макроскопический объем белковой ткани до воссоединения нековалентных белковых связей. Струйный метод, используемый с зондовой системой 110, может включать в себя как ирригацию солевым раствором, так и аспирацию вытекающей жидкости.
Изменяющее направление электрическое поле, создаваемое на наконечнике 112 полого зонда 114, располагается по существу перпендикулярно или ортогонально к направлению движения жидкости-носителя (т.е. белкового материала в водном растворе). Направление электрического поля изменяется с каждым или почти каждым импульсом. Длительность импульса (наносекунды) короткая по сравнению со временем диэлектрической релаксации белковых комплексов (около 1 мс). Множество изменений направления импульсов можно осуществить за интервал времени диэлектрической релаксации. Длительность импульсов, частота следования, импульсная последовательность и длина серии импульсов выбираются так, чтобы исключить развитие термических эффектов ("холодный" процесс). Описанная система генерирует и передает прямоугольные импульсы переменного направления с быстрым (менее 5 наносекунд) временем подъема и спада. Чем короче время подъема и спада импульса, тем выше частотные составляющие в Фурье-спектре импульса и тем меньше структуры, которые могут подвергаться воздействию этого импульса. В предложенной системе диссоциации и удаления белковой ткани длительность импульсов находится в наносекундном интервале, а напряженность электрического поля составляет более 1 кВ/см, предпочтительно в интервале сотен кВ/см.
Устройство и способ, реализуемые в предложенной системе, используют фракционирование потоком высокоинтенсивного электрического поля с ультракороткими хаотическими импульсами (CHIP EFFF) для захвата, диссоциации и удаления материала стекловидного тела и внутриглазных мембран. Ступенчатое непрерывное изменение направления поля (с помощью матрицы электродов 116), обеспечиваемое посредством перемены полярности, переключения активных электродов или комбинации этих мер, реализуется в наконечнике 112 полого зонда 114 для оказания разрушающего действия на заряды, участвующие в нековалентных связях, удерживающих вместе комплексы стекловидного тела (группы белков). За счет создания макроскопического объема внутриглазной, электрически нестабильной ткани можно дополнительно ослабить гидрофобные и гидростатические связи с захваченной белковой тканью, мембранами и многокомпонентными ферментами, повысив тем самым текучесть или разжижение ткани. Достигаемое поражение гидрофобных и гидростатических связей белковой ткани достаточно для кратковременного разрыва связующих механизмов адгезионных макромолекул стекловидного тела и связанной с ним внутриглазной ткани, и тем самым малая доля объемного материала стекловидного тела временно уменьшается до управляемого свободного жидкого белкового комплекса.
Для обеспечения эффективности настоящего изобретения большое значение имеет выбор энергии. Целью поражения связей, которые удерживают белковую ткань вместе, является создание беспорядка среди электронов во внешней оболочке макромолекул, связанных нековалентными связями. Предпочтительной формой энергии является электричество, возбуждение электронов прямым созданием электрического поля. Для создания разрушающего поля можно также использовать и другие источники энергии, такие как микроволны и ультразвук, в которых используются фотоны и фононы для возбуждения электронов. Понятно, что в качестве альтернативного источника энергии можно также использовать лазеры, особенно те, которые работают с импульсами длительностью в фемтосекундном диапазоне и на частотах, по существу равных пику поглощения энергии молекулами воды.
В предпочтительном варианте описанных устройства и способа используется фракционирование потоком быстро изменяющего направление электрического поля для захвата, диссоциации и удаления материала стекловидного тела и внутриглазных мембран. В частности, в описанной системе используется высокоинтенсивное разрушающее электрическое поле с ультракороткими импульсами, характеризующееся непрерывными изменениями направления поля, вместе со струйными методами, облегчающими создание электрического поля и последующее удаление белковой диссоциированной ткани. Высокоинтенсивное разрушающее электрическое поле с ультракороткими импульсами создается при использовании напряженности поля порядка кВ/см и ширины импульсов порядка наносекунд. Это высокоинтенсивное разрушающее электрическое поле с ультракороткими импульсами удерживается по существу ортогонально по отношению к направлению потока аспирационной жидкости-носителя. Ступенчатое непрерывное изменение направления электрического поля (создаваемое путем перемены полярности или переключения между матрицей электродов) используется для создания беспорядка среди электронов, участвующих в нековалентных связях, удерживающих вместе комплексы ткани (группы белков). При использовании длительности и серий импульсов, коротких по сравнению со временем, необходимым для термических эффектов, поражение связующих ткань механизмов по существу является "холодным" процессом и достаточным для мгновенной диссоциации матрицы ткани. Поражение связующих ткань механизмов разрушает связующие механизмы адгезионных макромолекул стекловидного тела и связанной с ним внутриглазной ткани, тем самым временно уменьшая малую долю материала объемного стекловидного тела до управляемого жидкого белкового комплекса. Напряженность электрического поля, вызывающая эту диссоциацию, подчиняется закону обратных квадратов. Напряженность поля, как таковая, имеет максимальное значение в области между электродами. В предпочтительном варианте это расстояние составляет менее 0,5 миллиметров. Пораженный жидкий белковый комплекс локализован в области подведения импульсного, быстро изменяющего направление электрического поля между электродами зонда и удаляется с помощью струйного метода (аспирации) до прекращения действия кратковременных эффектов поражения на связующий ткань механизма (релаксации). Когда объем белковой ткани попадает в экстракционный канал (т.е. жидкий аспирационный поток), измененный белковый комплекс может возвратиться в состояние, как перед поражением.
Описанное примерное применение предложенной системы предназначено для лечения патологических состояний сетчатки глаза; при этом, как показано на фиг.1, описанный полый зонд 114 с помощью рукоятки 120 вводится хирургом в задний сегмент глаза 100 через область pars plana 101, как показано на фиг.1. С помощью стандартного процесса визуализации стекловидное тело и/или внутриглазные мембраны и ткани захватываются наконечником 112 полого зонда 114, активизируются механизмы ирригации 130 и аспирации 140, и высокоинтенсивная электрическая энергия с ультракороткими импульсами передается из высоковольтного импульсного генератора 150 через формирователь 160 импульсов, переключающую схему 170 и кабель 124, создавая разрушающее высокоинтенсивное электрическое поле с ультракороткими импульсами в захваченном объеме ткани. Адгезионные механизмы захваченных компонентов ткани, которые притягиваются к наконечнику 112 зонда за счет аспирации через аспирационную линию 118, присоединенную к аспирационному просвету 122 в полом зонде 114, диссоциируются, и применяемые струйные методы удаляют разрушенную ткань. Захват может осуществляться аксиально или поперечно наконечнику 112 полого зонда 114. Извлеченная ткань удаляется через аспирационный просвет 122 вместе с аспирационным носителем, солевым раствором, в удаленный модуль сбора.
Можно удалить всю стекловидную ткань заднего сегмента глаза или выполнить только конкретные отделения стекловидного тела от сетчатки или других внутриглазных тканей или мембран.
Захват, разрушение и удаление ткани стекловидного тела, витреоретинальных мембран и сосудисто-волокнистых оболочек из задней полости глаза и поверхностей сетчатки являются наиболее важными процессами, которые выполняются витреоретинальными хирургами для хирургического лечения таких угрожающих зрению заболеваний, как диабетическая ретинопатия, отслойка сетчатки, прогрессирующая витреоретинопатия, витреоретинальная тракция, проникающие ранения, эпимакулярные мембраны и другие патологии сетчатки.
Хотя предложенные устройство и способ предназначены для постериорной интраокулярной хирургии на стекловидном теле и сетчатке, понятно, что они также могут найти применение в антериорной офтальмологии, включая устранение тракции (частичную витрэктомию), уменьшение адгезии мицелл, разрушение, манипулирование, реорганизацию и/или стимуляцию трабекулярной сетчатой структуры, трабекулопластику для лечения хронической глаукомы, манипуляции венозным синусом склеры, удаление остаточного эпителия хрусталика и удаление остатков ткани. Возможность применения предложенных устройства и способа для других медицинских целей будет очевидна для специалистов.
Части системы:
блок управления (180);
импульсный генератор мощности (150);
формирователь импульсов (160);
переключающая схема (170);
передающая линия (124);
система многоэлектродного хирургического зонда (110);
струйная система (130, 140).
Предложенные устройство и способ подводят высокоинтенсивное электрическое поле с импульсами ультракороткой длительностью (с низкой энергией), в котором длительность, частота следования, импульсная последовательность и длина серий импульсов устанавливаются в соответствии со свойствами компонентов внутриглазного внеклеточного матрикса (ЕСМ). Импульсный генератор мощности 150 для системы 190 вырабатывает импульсный постоянный ток или стробированный переменный ток против низкого импеданса стекловидного тела и ирригационного раствора. Система 190 включает в себя компоненты для накопления энергии, формирования импульсов, передачи и согласования нагрузки. Пиковое выходное напряжение высоковольтного генератора 150 достаточно для создания поля с напряженностью до 300 кВ/см с помощью электродов 116 на дистальном конце 112 полого хирургического зонда 114. Длительность импульсов должна быть короткой относительно времени диэлектрической релаксации белковых комплексов. Кроме того, длительность импульсов, частота следования и длина серии импульсов (т.е. рабочий цикл) выбираются так, чтобы исключить развитие термических эффектов ("холодный" процесс). Система 190 генерирует и выдает прямоугольные импульсы с быстрым временем подъема и спада (менее 5 наносекунд). В предложенных устройстве и способе длительность импульсов находится в наносекундном диапазоне, а напряжение составляет более одного кВ, предпочтительно десятки кВ.
Переключающая схема 170 предназначена для управления длительностью импульсов, частотой следования и для обеспечения ступенчатого непрерывного изменения направления электрического поля посредством переключения между электродами, перемены полярности между электродами или комбинации этих мер в матрице электродов в наконечнике 112 полого зонда 114, чтобы тем самым создать беспорядок в электрическом поле, не вызывая пробоя диэлектрика несущей жидкости между электродами или термических эффектов.
Особенную важность для эффективности настоящего изобретения представляет выбор энергии. Его целью является создание беспорядка среди электродов во внешней оболочке макромолекул, связанных с нековалентными связями, связывающими между собой белковые комплексы. Предпочтительной формой энергии является электричество, возбуждение электронов путем прямого создания электрического поля. Для создания беспорядка среди электронов во внешней оболочке макромолекул можно использовать такие источники энергии, как микроволны, лазер и ультразвук, в которых используются фотоны и фононы для возбуждения электронов.
Предложенное устройство содержит передающую линию 124 и полый хирургический зонд 114, который подводит, канализирует и распределяет прикладываемую энергию таким образом, чтобы создать ограниченную локализованную область электрической силы в макроскопическом объеме внеклеточного матрикса, ЕСМ (например, стекловидном теле и внутриглазных мембранах). Электрическое поле расположено по существу перпендикулярно или ортогонально к направлению движения жидкости-носителя (т.е. белкового материала в водном растворе). На фиг.4А, 4В, 4С, 4D и 4Е показано несколько возможных вариантов матрицы электродов на дистальном конце 112 хирургического зонда 114.
Например, ссылочный номер 1 на фиг.4А, 4В, 4С, 4 и 4Е обозначает полимерный экструдированный профиль с одним или более просветами. Ссылочный номер 2 обозначает просвет для аспирируемого потока жидкости. Ссылочные номера 3, 4, 5, 6, 7, 8, 9 и 10 относятся к электродным проволокам, вложенным в экструдированный профиль 1. На фиг.4А, 4С и 4D используется центральная проволока 11. На фиг.4Е используется центральный трубчатый электрод 12. Также на фиг.4Е используется центральный просвет 13 для оптоволоконной оснастки или инструмента какой-либо другой формы. Специалистам будет понятно, что возможны многочисленные другие конфигурации для создания требуемой формы импульсного, быстрого, сильного электрического поля. Несмотря на то что на чертеже показана по существу плоская дистальная поверхность каждого электрода 116, она может быть смещенной или выровненной по оси, утопленной или выступающей, или сочетать в себе комбинацию этих конфигураций, относительно дистального конца 112 полого зонда 114. Хотя на чертежах электроды 116 заканчиваются в плоскости, перпендикулярной осевому направлению стержня зонда, они могут заканчиваться аксиально относительно поперечного окна (не показано).
В предпочтительном варианте внешний диаметр экструдированного профиля 1 меньше, чем 0,040 дюйма. Предполагается, что материал стекловидного тела или внутриглазной ткани притягивается к аспирационному каналу(ам) и всасывается в него, а когда материал достигает области, ортогональной к электродам 116, электроды активизируются, создавая высокоинтенсивное разрушающее электрическое поле с ультракороткими импульсами между электродами 116.
За счет расположения и последовательной активизации матриц электродов создаются переменные проекции поля с постоянно изменяющимся направлением. В таблицах 5А, 5В, 5С, 5D и 5Е показан план активизации электродов для вариантов, показанных на фиг.4А, 4В, 4С, 4D и 4Е, соответственно. В таблице 5А содержится 12 импульсов, которые иллюстрируют последовательность импульсов, применяемую в варианте конца зонда 114, показанного на фиг.4А. Первый импульс используется электродом 116 под номером 11 в качестве анода, а катодами являются 3, 4, 5. Для второго импульса все наоборот. Остальные импульсы иллюстрируют порядок импульсов для создания электрического поля с переменным направлением.
В таблице 5В показано 11 импульсов, которые иллюстрируют последовательность импульсов, применяемую в варианте зонда 114 на фиг.4В.
В таблице 5С показана последовательность 12 импульсов, как на фиг.5А, для применения в зонде, показанном на фиг.4С.
В таблицах 5D и 5Е показана последовательность 10 импульсов для зондов, изображенных на фиг.4D и 4Е, соответственно. Возможны и многие другие формы поля в зависимости от варианта и последовательности активизации электродов. Целью активизации электродов является использование полярных свойств воды и белка, создание беспорядка с помощью быстрого изменения направления высокоинтенсивного электрического поля, вызывающего конформные изменения воды и белка, ведущие к мгновенной диссоциации ткани. Затем комплекс диссоциированной ткани, локализованный в области прикладываемого электрического поля, удаляется с помощью согласованных струйных методов до того, как произойдет завершение (релаксация) кратковременных эффектов поражения.
В варианте 4Е центральный электрод 12 может быть трубчатым проводящим электродом с центральной областью 13. Центральная область 13 может представлять собой сквозной просвет для ирригационного или инструментального канала, или же центральная область может содержать оптоволоконное устройство для подведения света.
Как отмечалось выше, положение электродов в матрицах и количество электродов можно подобрать так, чтобы обеспечить максимально эффективные разрушающие электрические поля. Электроды можно также расположить по оси таким образом, чтобы ни один или несколько электродов не заканчивались на одинаковом расстоянии или в одинаковом осевом положении. Крайний конец электродов может иметь форму, позволяющую оптимизировать пространственную напряженность поля между электродами. Окончания электродов могут иметь форму прямых кромок, углов, острых кромок, кривизны (постоянной и переменной) или их комбинаций, выбираемых из расчета оптимальной проекции и распределения напряженности электрического поля между электродами.
Струйные методы (аспирация) используются для всасывания и удаления объема диссоциированной ткани до того, как может произойти воссоединение нековалентных белковых связей. Струйные методы, используемые в предпочтительном варианте, включают в себя ирригацию солевым раствором и аспирацию вытекающей жидкости. В предпочтительном варианте струйная система включает в себя элементы ирригации и аспирации, индивидуально согласованные так, чтобы поддерживать объем и давление внутри глаза в физиологических пределах. Задняя часть стекловидного тела содержит более 97% воды, и важной функцией струйной системы является обеспечение разбавления, гидратации и стабильного импеданса захваченного материала. В предпочтительном варианте предусмотрен аспирационный канал в полом хирургическом зонде 114, чтобы внутриглазные ткани всасывались в аспирационный просвет 122 или каналы, когда они подвергаются воздействию описанного выше разрушающего электрического поля. Объемный расход аспирированного истока согласован со скоростью диссоциации гидратированного белкового материала под действием разрушающего электрического поля. Предполагается, что будет использоваться ирригация раствором BSS® или BSS PLUS® компании Alcon Laboratories, Inc. Для усиления диссоциации можно предусмотреть безвредные свойства и ингредиенты в ирригационной жидкости. Ирригационный путь/канал можно выполнить в хирургическом зонде, как показано на фиг.4Е, или же реализовать его в независимой канюле, или в комбинации этих средств.
На фиг.6 показан перспективный вид альтернативного варианта зондовой системы 210, содержащей три электрода. Как и в предпочтительном варианте 110, зондовая система 210 содержит полый зонд 214 и рукоятку 220. Ткань захватывается наконечником 212 полого зонда 214. Более полное представление о зондовой системе 210 можно получить на фиг.6, 7 и 8. Три электрода 216 разнесены по существу через равные угловые интервалы вокруг центрального каркаса 217 в зонде 214. Между электродами 216 находятся ирригационные каналы 215. В центре каркаса 217 расположен аспирационный просвет 222. Сверху центрального каркаса 217, ирригационных каналов 215 и электродов расположен внешний кожух 219, который заканчивается в атравматическом наконечнике 221. Зондовая система 210 располагается так, чтобы удаляемая ткань находилась внутри наконечника 221.
Опорная система 290 для зондовой системы 210, показанной на фиг.10, аналогична предпочтительному варианту, показанному на фиг.3, но дополнительно содержит ирригационную систему 235 наконечника. Также имеется общая ирригационная система 230, аспирационная система 240, присоединенная к аспирационной линии 218, блок 280 управления, один или более высоковольтных импульсных генераторов 250, переключающая схема 270, присоединенная к передающей линии 224, и разбавляющая ирригационная система 235 для наконечника зонда, присоединенная к ирригационной трубке 237 наконечника зонда.
Как и фиг.4А, 4В, 4С, 4D и 4Е, изображающие электроды в наконечнике зонда, фиг.11А и 11В иллюстрируют альтернативные компоновки электродов 1, 2, 3 и 4 в зондовой системе 210. Фиг.12А и 12В соответствуют фиг.11А и 11В, показывающим примерные последовательности активизации электродов для создания неплазменной, бесконтактной, возбужденной разрушающей области вокруг белковой ткани. Для лучшего понимания, как создается эта неплазменная, бесконтактная возбужденная разрушающая область, на фиг.13А и 13В показаны линии поля для последовательности импульсов, проиллюстрированной на фиг.12А и 12В, соответственно, где полярность электродов не меняется.
На фиг.14 показана схема трехканального импульсного генератора 250 с регулируемыми длительностью отдельных импульсов, частотой следования отдельных импульсов и длиной серии импульсов.
На фиг.15 представлена таблица, иллюстрирующая состояние каналов одного примерного цикла генерации импульсов трехканального импульсного генератора 250, показанного на фиг.14.
Система 290, показанная на фиг.10, будет более понятной, если учесть, что зондовая система 210 содержит множество сквозных просветов 215 для вспомогательной ирригации, как показано на фиг.6, 7, 8 и 9, соответственно. Ирригационный расход меньше, чем аспирационный расход через центральный просвет 222, поэтому скорость выпуска вспомогательной ирригационной жидкости меньше, чем скорость поступления разбавленной гидратированной внутриглазной ткани. Дополнительную ирригационную жидкость подводит разбавляющий ирригационный механизм 235 наконечника зонда, расположенный снаружи зонда (фиг.10). Ирригационная жидкость используется для разбавления внутриглазной ткани и сохранения стабильного или почти постоянного импеданса между электродами 216, чтобы исключить существенные сдвиги в реализуемом подводе энергии и напряженности поля. Можно подобрать свойства ирригационной жидкости, такие как рН и ингредиенты, позволяющие усилить диссоциацию стекловидного тела.
Третья трубка для ирригации 237 соединяет систему 210 с вспомогательным ирригационным источником 235. Следует отметить, что на фиг.10 формирователь импульсов входит в состав высоковольтного импульсного генератора 250.
На фиг.11А и 12А видно, что вместо перемены полярности электродов 216 между импульсами происходит переключение активных анодов и катодов между электродами. На фиг.13А показаны линии создаваемого поля для иллюстрации примера электрического поля для каждого импульса. Для конфигурации с тремя электродами 1,2 и 3, показанной на фиг.11А, один цикл включает в себя три импульса, исходящих из различных направлений. В таблице на фиг.12А показаны последовательные примеры для случаев, в которых осуществляется переключение электродов, а не перемена (обращение) действительной полярности. Таблица на фиг.12В и линии поля, показанные на фиг.13В, иллюстрируют возможный вариант с четырьмя электродами 1, 2, 3 и 4, показанный на фиг.11В, где электроды работают в парах как аноды и катоды.
Трехканальный импульсный генератор, схематически показанный на фиг.14, демонстрирует, что запуск одного канала посылает импульс электроду, затем запускается второй канал, который, в свою очередь, посылает импульс другому электроду, затем запускается третий канал, который, в свою очередь, посылает импульс другому электроду и запускает первый канал для того, чтобы снова начать эту последовательность. Когда один канал выдает импульс, другие два канала обеспечивают нулевое сопротивление и действуют как обратные схемы для выданного импульса. Последовательность каналов может быть упорядоченной или иметь случайный характер.
На фиг.15 проиллюстрировано условие полярности каждого канала во время выпуска импульса. Условие полярности каждого канала обусловлено переключением электродов, а не действительной переменой полярности на одном канале.
Следующий вариант зондовой системы 210 показан на фиг.16-23. На фиг.16-19 показан вариант с электродами 216, имеющими плоскую и вытянутую по оси форму. В электродах 216 большая плоская часть ориентирована в радиальном направлении относительно аспирационного канала 222. Острые углы электродов 216 позволяют создавать более интенсивно сфокусированное электрическое поле в аспирационном канале 222. Эти электроды 216 заканчиваются в отверстии кожуха 219.
На фиг.20-23 показан вариант с электродами 216, имеющими заостренные концы. Эти электроды 216 уплощены и имеют большую плоскую часть, ориентированную в радиальном направлении относительно аспирационного канала 222. Электроды 216 заканчиваются в загнутом заостренном наконечнике так, что их острия направлены радиально внутрь к аспирационному каналу 222. Острые углы электродов 216 позволяют создавать более интенсивно сфокусированное электрическое поле в аспирационном канале 222.
В двух вариантах, показанных на фиг.16-23, три электрода 216 расположены по существу с одинаковыми угловыми интервалами вокруг центрального каркаса 217 внутри зонда 214. Между электродами 216 находятся ирригационные каналы 215. В центре центрального каркаса 217 расположен аспирационный просвет 222. Центральный каркас 217, ирригационные каналы 215 и электроды покрыты внешним кожухом 219, который заканчивается в атравматическом наконечнике 221. Зондовую систему 210 располагают так, чтобы подлежащая удалению ткань находилась как раз внутри атравматического наконечника 221. На фиг.17, 19, 21 и 23 отверстие 227 между кожухом 219 и аспирационным каналом 222 позволяет ирригационной жидкости проходить в форме каскада вблизи электродов 216.
Работа зондовой системы по фиг.16-23 аналогична работе, описанной со ссылками на фиг.11А, 12А и 13А. Другие режимы работы, описанные ранее, также возможны в зондовой системе на фиг.16-23.
Преимущества, обеспечиваемые предложенной системой:
(а) Бестракционное удаление внутриглазных тканей из заднего сегмента глаза.
(b) Управляемая диссоциация небольших объемов ткани без эффекта дальней зоны.
В частности, отсутствует миграция дальней зоны, утечка или рассеивание электрического поля. В отличие от ферментативных процессов, которые влияют на весь задний сегмент глаза, включая сетчатку, эффект описанного CHIP EFFF локализован.
(с) Частичная витрэктомия или устранение тракции без общей витрэктомии.
В большинстве витреоретинальных операций требуется экстракция всего стекловидного тела в заднем сегменте глаза. Предложенная система позволяет избирательно отделять белковую ткань и коллаген от сетчатки без удаления всего стекловидного тела. Соответственно, исключается необходимость в послеоперационном искусственном стекловидном теле.
(d) Не образуются активные формы кислорода.
В отличие от абляционных методов, таких как лазеры, плазма и вырабатывающие тепло методы, предложенная система воздействует только на нековалентные адгезионные аспекты стекловидного тела и внутриглазных мембран, поэтому не порождается и не выделяется никаких токсических химических веществ или ROS. Вырабатываемой энергии недостаточно, чтобы вызвать термические эффекты.
(е) Безопасность.
Прерывистость подведения энергии позволяет белковой ткани соединяться снова. Поэтому предложенный способ можно прервать практически мгновенно в любой момент, не вызывая необратимого повреждения целевой ткани.
(f) Многомодальность (экстракция, коагуляция, разрез, стимуляция).
Так как зонд содержит множество электродов, это позволяет изменять установки мощности для достижения различных функциональных результатов. В режиме CHIP EFFF зонд используется для экстракции стекловидного тела и внутриглазных мембран. В режиме коагулятора можно подводить РЧ энергию, чтобы остановить сосудистое кровотечение. В режиме разреза можно подводить РЧ энергию соответствующей мощности и частоты для действительного создания плазменной или искровой эрозии для осуществления разреза ткани. В режиме стимуляции можно подводить электрический импульс более низкой мощности в терапевтических целях.
(g) Уменьшение необходимости смены инструментов.
В ходе операции на задней глазничной области требуется большое количество обычных и специальных инструментов для захвата, препарирования, отделения и удаления материала стекловидного тела и внутриглазных мембран. Смена инструментов во время операции является основной причиной послеоперационных осложнений. При использовании изобретения многие известные инструменты становятся ненужными, и смена инструментов сводится к минимуму.
(h) Отсутствие движущихся частей.
Обеспечивается снижение стоимости и трудовых затрат на изготовление зондов. Изготовление механических зондов для витрэктомии очень трудоемкое. Предложенный одноразовый полый зонд состоит из небольшой рукоятки с присоединенным многопросветным, совместно экструдированным профилем или узлами с проводами в просветах или каналах. По сравнению с известными механическими узлами требуются меньшие навыки для его сборки.
(i) Применения на переднем и заднем сегментах глаза.
Хотя предложенное устройство предназначено для бестракционного удаления стекловидного тела и внутриглазных тканей, его можно использовать, помимо прочего, для некоторых операций на переднем сегменте глаза, таких как стимуляция трабекулярной сетчатой структуры, удаление остаточного эпителия хрусталика, а также для удаления остатков ткани и передней витрэктомии.
(j) Возможность комбинированного применения.
Простота конструкции предложенной системы позволяет применять ее как самостоятельно, так и как дополнительное средство вместе с другими средствами для разрушения и экстракции тканей, такими как хирургические инструменты для механической витрэктомии, производимые компанией AquaLase®, и для химической витрэктомии (ферментативного действия).
Несмотря на то что изобретение было описано в контексте его предпочтительных и альтернативных вариантов, специалистам будет понятно, что представленное выше описание позволяет реализовать и другие варианты.
| название | год | авторы | номер документа |
|---|---|---|---|
| РЕГУЛИРОВАНИЕ ВНУТРИГЛАЗНОГО ДАВЛЕНИЯ | 2006 |
|
RU2555125C2 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПОМУТНЕНИЯ СТЕКЛОВИДНОГО ТЕЛА, СОЧЕТАННОГО С КАТАРАКТОЙ | 2005 |
|
RU2293546C1 |
| Способ профилактики геморрагических осложнений витреоретинальной хирургии | 2021 |
|
RU2773104C1 |
| Ультразвуковая игла для офтальмохирургии | 2017 |
|
RU2685918C1 |
| ЧУВСТВИТЕЛЬНЫЕ К ДАВЛЕНИЮ ХИРУРГИЧЕСКИЕ СИСТЕМЫ И СПОСОБЫ ДЛЯ ВИТРЭКТОМИИ | 2014 |
|
RU2651086C2 |
| Ультразвуковая игла для офтальмохирургии | 2017 |
|
RU2685902C1 |
| Способ устранения витреомакулярной адгезии | 2020 |
|
RU2745303C1 |
| Способ хирургического лечения макулярного разрыва с применением аутологичной кондиционированной плазмы | 2023 |
|
RU2816630C1 |
| СПОСОБ ЛЕЧЕНИЯ ТРОМБОЗА ЦЕНТРАЛЬНОЙ ВЕНЫ СЕТЧАТОЙ ОБОЛОЧКИ ГЛАЗА | 2007 |
|
RU2346678C1 |
| Способ удаления силиконового масла с помощью ультразвукового витреотома | 2020 |
|
RU2744151C1 |






Изобретение относится к медицинской технике, а именно к устройствам для диссоциации и удаления гидратированных объемов белковой ткани потоком энергетического поля. Система содержит зонд для окружения мягкой ткани, включающий множество электродов, систему для создания импульсного разрушающего ткани электрического поля между множеством пар множества электродов и аспирационную систему, связанную с зондом. Система для создания импульсного разрушающего ткани электрического поля выполнена с возможностью частично разжижать белковый комплекс и вызывать мгновенную диссоциацию адгезионного механизма между составными частями мягкой ткани, а аспирационная система выполнена с возможностью удалять упомянутую диссоциированную ткань. Использование изобретения позволяет более точно проводить экстракцию стекловидного тела и внутриглазных мембран при сохранении целостности сетчатки глаза. 9 з.п. ф-лы, 34 ил.
1. Система для разрыва связей, удерживающих вместе части мягкой ткани, содержащая
зонд для окружения мягкой ткани,
причем зонд содержит множество электродов,
систему для создания импульсного разрушающего ткани электрического поля между множеством пар упомянутого множества электродов,
аспирационную систему, связанную с упомянутым зондом,
причем система для создания импульсного разрушающего ткани электрического поля выполнена с возможностью частично разжижать белковый комплекс и вызывать мгновенную диссоциацию адгезионного механизма между составными частями мягкой ткани, и
аспирационная система выполнена с возможностью удалять упомянутую диссоциированную ткань.
2. Система по п.1, в которой упомянутое импульсное разрушающее электрическое поле:
является, по существу, ортогональным по отношению к мягкой ткани, подлежащей диссоциации, или
создается между множеством пар электродов посредством непрерывной перемены полярности электродов и последовательного переключения активных электродов, или
создается между множеством пар электродов посредством перемены полярности, переключения активных электродов или комбинации этих мер.
3. Система по п.1, в которой упомянутая аспирационная система удаляет диссоциированную мягкую ткань в момент диссоциации.
4. Система по п.1, в которой упомянутое множество электродов погружено в проводящую среду.
5. Система по п.1, в которой предусмотрена подача ирригационной жидкости для поддержания стабильного импеданса между электродами.
6. Система по п.1, в которой форма импульсов, частота следования импульсов и длина серии импульсов регулируются в соответствии с тканью, подлежащей диссоциации.
7. Система по п.1, в которой зонд выполнен с возможностью создания электрического поля с ультракороткими импульсами между электродами наконечника полого хирургического зонда, окружающего объем ткани, при этом указанное электрическое поле является достаточным для создания жидкого белкового комплекса, позволяющего осуществить мгновенную диссоциацию объема ткани, и система дополнительно содержит:
импульсный генератор мощности,
формирователь импульсов, присоединенный к импульсному генератору мощности,
переключающую схему, присоединенную к формирователю импульсов, для регулирования длительности и частоты электрических импульсов между электродами.
8. Система по п.1, в которой переключающая схема выполнена с возможностью изменения последовательности активизации электродов,
или
изменения полярности электродов, или
изменения направления поля между электродами, или
изменения амплитуды напряжения в каждом цикле серии импульсов, или
изменения частоты в каждом цикле пачки импульсов, или
изменения рабочего цикла в каждом цикле пачки импульсов, или
изменения импульсной последовательности в каждом цикле пачки импульсов.
9. Система по п.7, дополнительно содержащая проводящую среду между электродами или дополнительно содержащая жидкость между электродами, которая сохраняет стабильную электрическую среду, и аспирационная система выполнена с возможностью удаления диссоциированной ткани в момент диссоциации.
10. Система по п.7, дополнительно содержащая ирригационную жидкость со свойствами рН или с ингредиентами, способствующими вызванной электрическим полем диссоциации белковой ткани.
| DE 19740530 A1, 18.03.1999 | |||
| WO 200110319 A1, 15.02.2001 | |||
| US 6135998 A, 24.10.2000 | |||
| Приспособление для выбирания невода на рыбацкое судно | 1934 |
|
SU42752A1 |
| Устройство для офтальмологической хирургии | 1981 |
|
SU1052232A1 |
| Б.М.АЗНАБАЕВ Ультразвуковая хирургия катаракты - факоэмульсификация | |||
| - М., 2005, с.5-13. | |||
Авторы
Даты
2011-05-27—Публикация
2006-12-11—Подача