Эта заявка притязает на преимущество приоритета Предварительной заявки No. 60/750733, зарегистрированной 15 декабря 2005 г., которая включена в этот документ полностью в качестве ссылки.
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым фосфорным лигандам и к их применению в гидроформилировании и родственных реакциях. Более конкретно, настоящее изобретение относится к комплексам переходных металлов, имеющих хелатирующие тетрафосфорные лиганды с несколькими способами хелатирования. Тетрафосфорные лиганды с несколькими способами хелатирования могут усиливать координирующие способности для переходных металлов, таких как Rh и Ni, и таким образом улучшать селективности каталитических реакций. Комплексы переходных металлов и тетрафосфорных лигандов в соответствии с настоящим изобретением являются полезными в качестве катализаторов в гидроформилировании, изомеризации-гидроформилировании, гидрокарбоксилировании, гидроцианировании, тандемных реакциях, таких как изомеризация-формилирование, и в гидроаминометилировании.
Гидроформилирование, открытое Роеленом в 1938, г., представляло собой самый большой сектор из гомогенных каталитических процессов в промышленности. Более 15 биллионов фунтов альдегидов и спиртов в год производили посредством катализаторов на основе Fe, Zn, Mn, Co, Cu, Ag, Ni, Pt, Pd, Rh, Ru и Ir. В этих процессах достижение высокой селективности по отношению к линейным продуктам является чрезвычайно важным для промышленного применения. Несмотря на широкие исследования, проводимые как академическими, так и промышленными/отраслевыми группами, такими как BASF, Dow, Shell и Eastman, и прочими другими, по-прежнему остаются проблемы фундаментального и практического плана, касающиеся селективности. Новые концепции для регулирования селективностей являются очень важными в каталитических реакциях. Высокоэффективные селективные катализаторы позволят производить некоторые химические реагенты в большом объеме, допустимым с экологической точки зрения образом и в более мягких условиях.
Кобальтовые катализаторы (например, HCo(CO)4) преобладали в промышленном гидроформилировании до тех пор, пока не ввели в начале 1970-х годов родиевые катализаторы (например, HRh(CO)2(PPh3)3). В 2004 г., как оценивают, приблизительно 75% всех процессов гидроформилирования было основано на родий-триарилфосфиновых катализаторах. Достижение высокого значения региоселективности по отношению к линейным альдегидам является определяющим для гидроформилирования и родственных реакций. Получающиеся в результате альдегиды превращаются в спирты, карбоновые кислоты или другие производные, которые используют в качестве пластификаторов, моющих средств, поверхностно-активных веществ, растворителей, смазочных веществ и промежуточных химических соединений (полупродуктов).
Схема 1 ниже показывает диссоциацию катализатора гидроформилирования, катализированного посредством Rh.
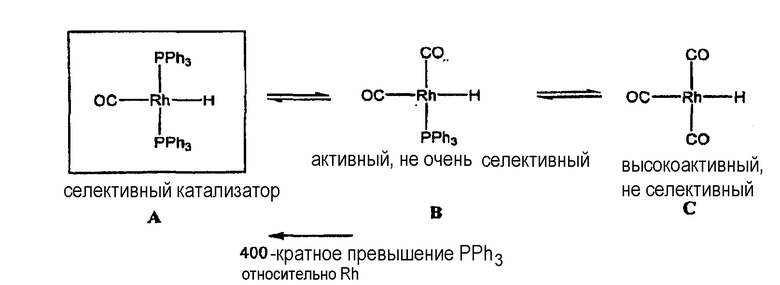
Успешное промышленное внедрение технологии производства HRh(CO)(PPh3)2 было основано на ключевом открытии Pruett в компании Union Carbide и Booth в компании Union oil того факта, что использование родия с избытком фосфинового лиганда может приводить к образованию активных, селективных катализаторов гидроформилирования. Необходимость избытка фосфинов является следствием легкой диссоциации Rh-PPh3 в каталитичесой системе, которая проиллюстрирована схемой 1. Потеря группы PPh3 соединением HRh(CO)(PPh3)2 приводит к более активным, но менее региоселективным катализаторам гидроформилирования В и С. В промышленном процессе используют вплоть до 820-кратного избытка PPh3 относительно Rh для гарантированного обеспечения высокого коэффициента селективности относительно линейных и разветвленных продуктов, то есть вплоть до 17:1, для гидроформилирования 1-гексена. Промышленное гидроформилирование пропилена осуществляют с 440-кратным избытком PPh3 относительно Rh, где достигают коэффициента селективности относительно линейных и разветвленных продуктов 8-9:1.
Rh/PPh3-катализированное гидроформилирование представляет собой ключ для изготовления всех оксоспиртов. Пропилен представляет собой наиболее применяемый моноалкен, подвергаемый гидроформилированию для получения бутилальдегида, который может быть гидрогенизирован с получением бутанола или димеризован посредством альдольной конденсации и затем гидрогенизирован с образованием 2-этил-1-гексанола, наиболее распространенного монопродукта, получаемого гидроформилированием (свыше 5 биллионов фунтов в год). 2-Этил-1-гексанол обычно подвергают реакции с фталевым ангидридом с получением диалкилфталевых сложных эфиров, которые используют в качестве пластификаторов для поддержания поливинилхлоридных пластиков мягкими и гибкими.
В процессе гидроформилирования решающим является получить более дешевое сырье для промышленности. Например, внутренние более высокомолекулярные высшие алкены (производственные сжатые алкены), такие как 3-октены, желательны для превращения алкенов в линейные альдегиды. Непосредственное использование рафината II (смесь н-бутенов/бутанов) и смесей 1-бутена и 2-бутена является полезным для гидроформилирования. Для гидроформилирования н-алкенов важно получить высокую селективность по линейным продуктам. Гидроформилирование аллильного спирта и последующее восстановление может приводить к 1,4-бутенолу. Функционализированные внутренние алкены могут быть использованы в качестве альтернативных путей к бифункциональным билдинг-блокам для полимеров. Гидроформилирование метил-3-пентеноата приводит к получению исходных веществ для полиамидов и полиэфиров. В процессах тандемной изомеризации и гидроформилирования высокие скорости изомеризации в сочетании с высокой селективностью по отношению к конечным альдегидам желательны при минимизированных нежелательных реакциях гидрогенизации и минимальной изомеризации в отношении сопряженных соединений.
Для преодоления необходимости использования большого избытка фосфинов в процессах гидроформилирования и для достижения высокой региоселективности было разработано новое поколение катализаторов на основе переходных металлов при использовании бисфосфиновых лигандов, например, Bisbi от компании Eastman Chemical; Xantphos от Prof. Leeuwen (University of Amsterdam), (Bernhard Breit, Acc. Chem. Res. 2003, 36, 264-275, Bernhard Breit, Wolfgang Seiche, Synthesis, 2001, 1, 1-36) и UC-44 от компании Union Carbide. Эти лиганды проиллюстрированы ниже.
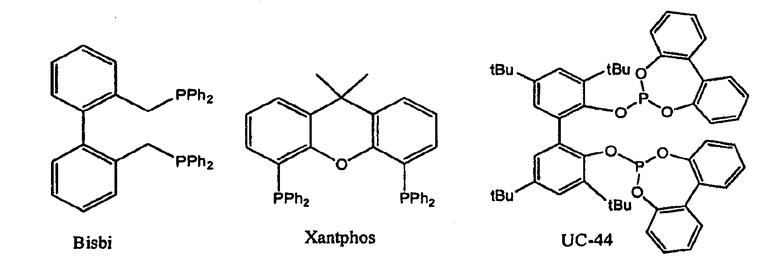
Посредством использования этих лигандов типичный 400-кратный избыток PPh3 был снижен до 5-кратного избытка хелатирующих фосфинов. Это новое поколение хелатирующих фосфинов привело к высоким соотношениям линейных продуктов к разветвленным продуктам, а также к более высоким каталитическим активностям. Например, для гидроформилирования 1-гексена наблюдали соотношение линейных продуктов к разветвленным продуктам 70-120:1. Casey и van Leeuwen предположили, что часть региоселективности в Rh-катализированном гидроформилировании происходит вследствие того, что образуется угол захвата металла бисфосфином приблизительно 120 градусов, то есть предложили «гипотезу угла захвата», которая проиллюстрирована ниже.
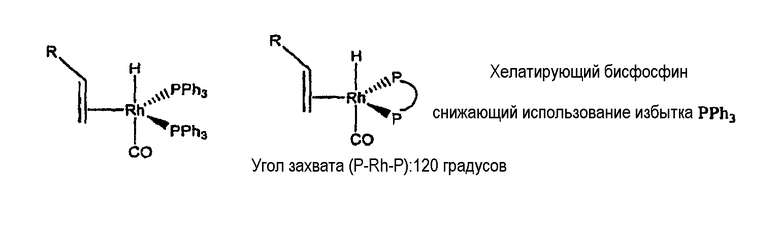
Несмотря на то, что целый ряд хиральных бисфосфорных лигандов используют в качестве катализаторов для гидроформилирования и родственных реакций, высокоселективные, активные фосфорные лиганды для гидроформилирования по-прежнему остаются областью пристального исследовательского интереса. Однако вследствие отделения фосфинов от фрагмента-координации Rh-CO имеет место проблема достижения высокой региоселективности, то есть высоких соотношений линейных продуктов к разветвленным продуктам в получаемых продуктах. Разработка семейства фосфорных лигандов с несколькими способами координации при хелатировании является привлекательной. Тетрафосфорные лиганды по настоящему изобретению, вследствие их координирующих способностей благодаря нескольким способам координации при хелатировании, приводят к высокорегиоселективному переходу при гидроформилировании катализированным комплексом металл-лиганд, и в родственных реакциях, с обеспечением высоких соотношений линейных продуктов к разветвленным продуктам по сравнению с соответствующими соотношениями, получаемыми ранее. Также симметричная природа этих лигандов позволяет легко получать эти лиганды.
Краткое изложение сущности изобретения
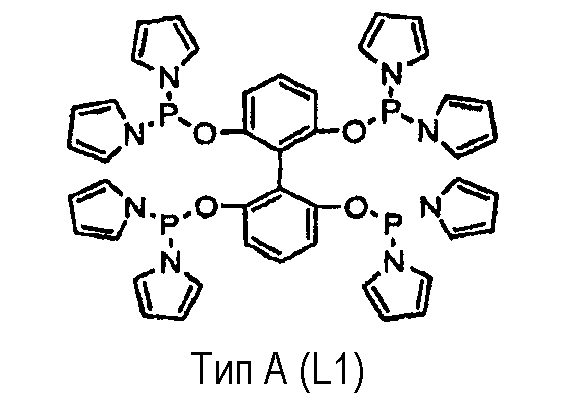
В настоящем изобретении мы вводим ряд тетрафосфорных лигандов (Тип А) с несколькими способами координации при хелатировании, которые проиллюстрированы ниже, для усиления координационных способностей:
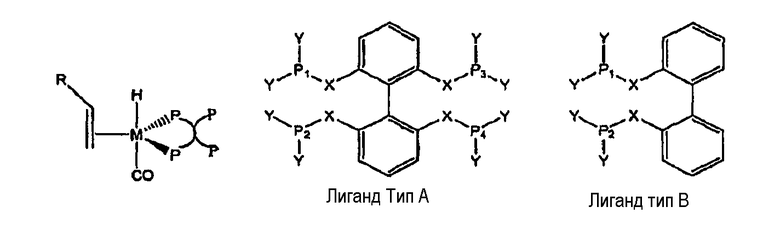
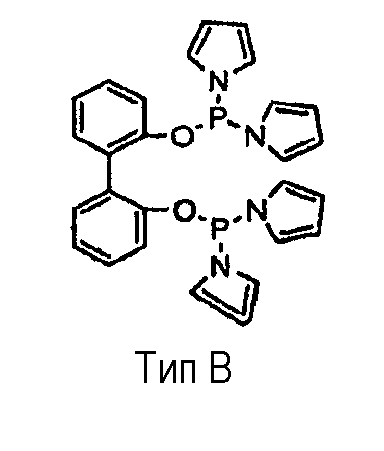
где М представляет собой металл, выбранный из группы, состоящей из Fe, Zn, Mn, Co, Cu, Ag, Ni, Pt, Pd, Rh, Ru и Ir; Х выбирают из группы, состоящей из О, NH, NR и CH2; Y выбирают из группы, состоящей из Ar, OАr и пиррола; R представляет собой органическую группу и Ar представляет собой арильную группу. Лиганд (Тип А) представляет собой тетрафосфорный лиганд по настоящему изобретению. Лиганд (Тип В) представляет собой бисфосфорный лиганд. Как проиллюстрировано ниже, тетрафосфорный лиганд (Тип А) имеет, по меньшей мере, четыре способа координации при хелатировании, что усиливает координационные способности, тогда как бисфосфорный лиганд (Тип В) имеет единственный способ, а именно P1-M-P2.
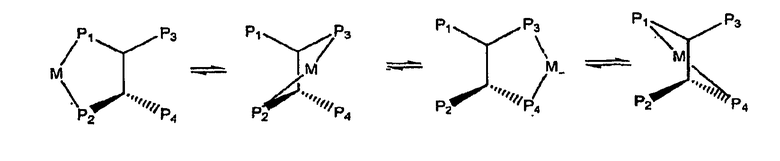
По сравнению с обычными бисфосфорными лигандами (Тип В) тетрафосфорные лиганды с несколькими способами хелатирования (Тип А) по настоящему изобретению усиливают координирующие способности лигандов без существенного изменения электронных свойств лигандов.
Настоящее изобретение относится к тетрафосфорным лигандам, имеющим много вариантов координации при хелатировании, которые используют в качестве катализаторов для гидроформилирования и родственных реакций. Катализаторы на основе переходных металлов, изготовленные при использовании тетрафосфорных лигандов по настоящему изобретению, являются высокоактивными и региоселективными. Тетрафосфорные лиганды по настоящему изобретению имеют следующую общую структуру:
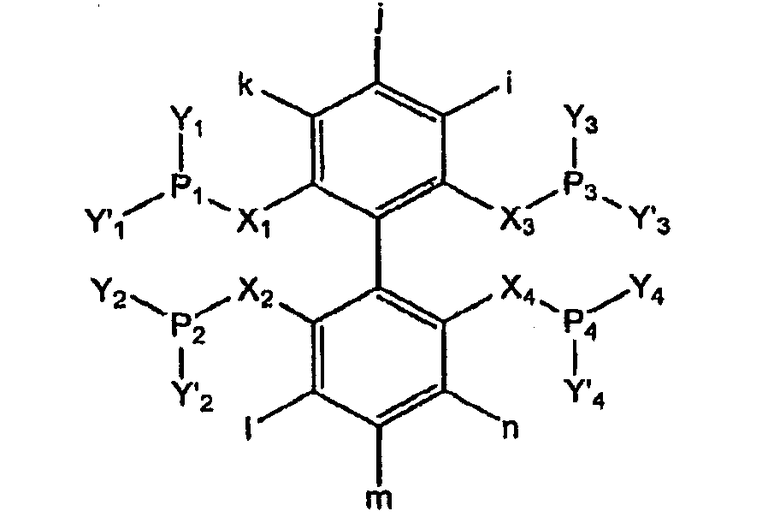
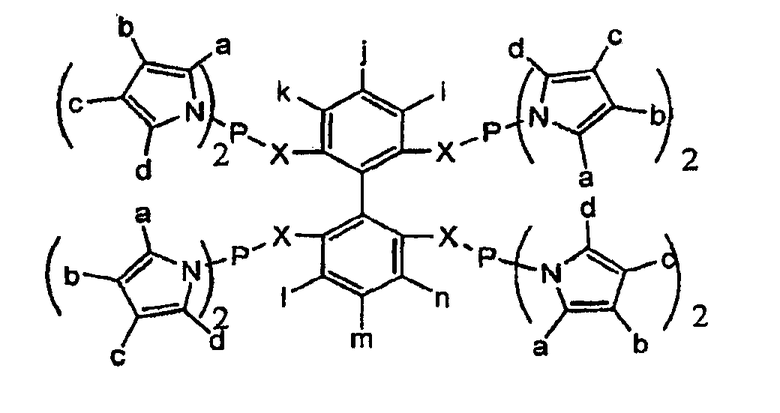
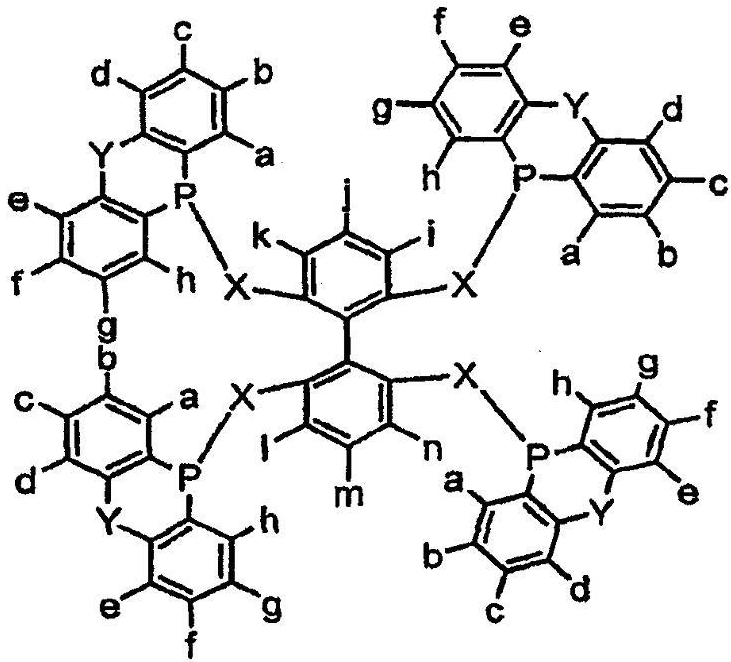
где i, j, k, l, m и n являются, независимо, H, R, Ar, замещенным Ar, OR, OAr, COOEt, галогенидом, SO2R, SO3H, SO2NHR, POR2, POAr2 или NR2, где R представляет собой алкил, замещенный алкил, арил или замещенный арил, и Ar представляет собой арил; Х1-Х4 являются, независимо, O, CH2, NH, NR, NSO2R или NSO2Ar, где R представляет собой алкил, замещенный алкил, арил или замещенный арил, Ar представляет собой арил и Y1, Y'1, Y2, Y'2, Y3, Y'3 Y4, Y'4 являются, независимо, R, Ar, OR, OAr, пирролом или замещенным пирролом, где R представляет собой алкил, замещенный алкил, арил или замещенный арил и Ar представляет собой арил или где R, Ar, OR, OAr, пиррол и замещенный пиррол являются связанными посредством углерод-углеродной связи, CH2, NH, NR и O. Замещенные группы будут включать, например, метил, этил, трет-бутил и фенил.
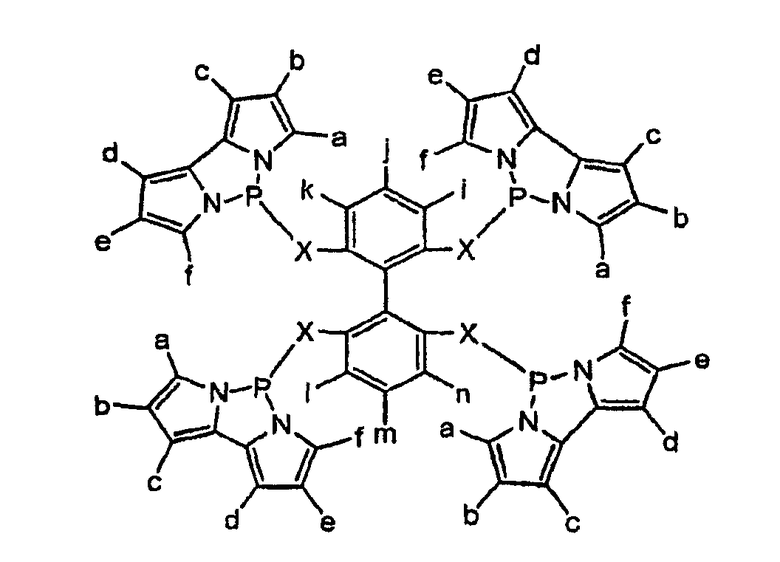
Следующее иллюстрирует первый вариант осуществления изобретения:
где Х является O, CH2, NH, NR, NSO2R или NSO2Ar, где R представляет собой алкил, замещенный алкил, арил или замещенный арил Ar представляет собой арил; и a, b, c, d, i, j, k, l, m и n являются, независимо, Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, CF3, COOR, SO3R, SO3H, POR2, галогенидом, или две группы из следующих групп: a, b, c, d, i, j, k, l, m и n могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо, где R представляет собой алкил, замещенный алкил, арил или замещенный арил и Ar представляет собой арил.
Второй вариант осуществления изобретения проиллюстрирован ниже:
где Х является O, CH2, NH, NR, NSO2R или NSO2Ar, где R представляет собой алкил, замещенный алкил, арил или замещенный арил; Ar представляет собой арил и a, b, c, d, е, f, i, j, k, l, m и n являются, независимо, Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, COOR, SO3R, SO3H, POR2, галогенидом, или две группы из следующих групп: a, b, c, d, е, f, i, j, k, l, m и n, могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо, где R представляет собой алкил, замещенный алкил, арил или замещенный арил и Ar представляет собой арил.
Третий вариант осуществления изобретения проиллюстрирован ниже:
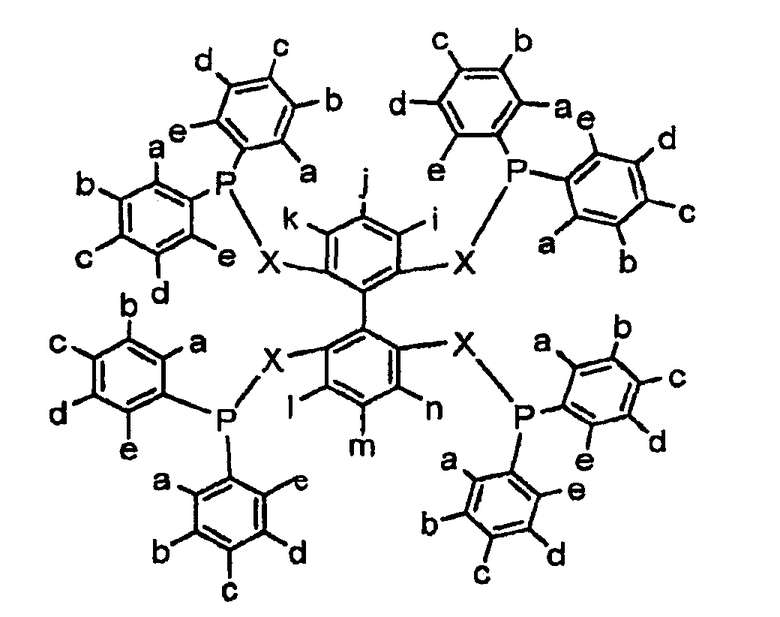
где Х является O, CH2, NH, NR, NSO2R или NSO2Ar, где R представляет собой алкил, замещенный алкил, арил или замещенный арил; Ar представляет собой арил и a, b, c, d, е, i, j, k, l, m и n являются, независимо, Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, CF3, COOR, SO3R, SO3H, POR2, галогенидом, NR2, или две группы из следующих групп: a, b, c, d, е, i, j, k, l, m и n, могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо, где R представляет собой алкил, замещенный алкил, арил или замещенный арил и Ar представляет собой арил.
Четвертый вариант осуществления изобретения проиллюстрирован ниже:
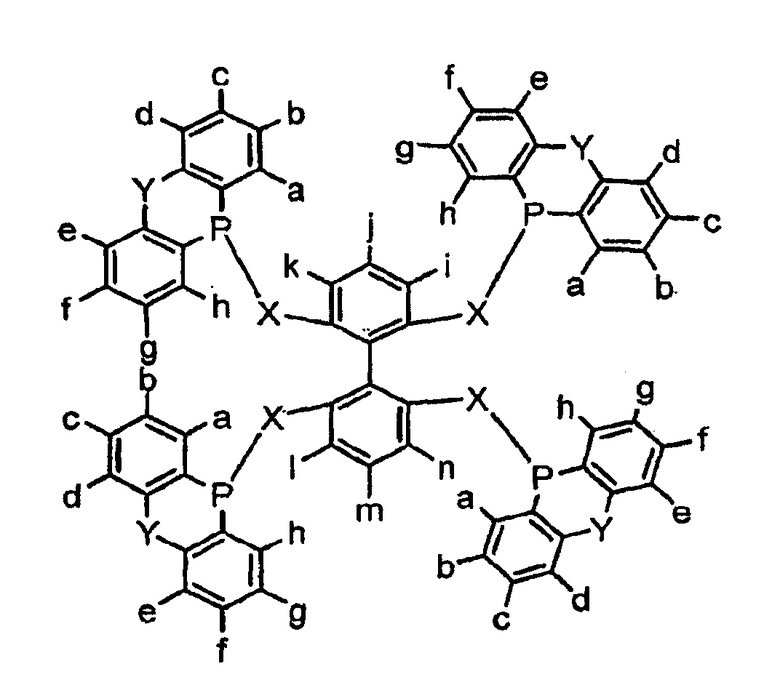
где Х является O, CH2, NH, NR, NSO2R или NSO2Ar, где R представляет собой алкил, замещенный алкил, арил или замещенный арил; Ar представляет собой арил; Y представляет собой углерод-углеродную связь, O, CH2, NH или NR, где R представляет собой алкил, замещенный алкил, арил или замещенный арил, и a-n являются, независимо, Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, CF3, COOR, SO3R, SO3H, POR2, галогенидом, NR2, или две группы из групп a-n могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо, где R представляет собой алкил, замещенный алкил, арил или замещенный арил и Ar представляет собой арил.
Пятый вариант осуществления изобретения проиллюстрирован ниже:
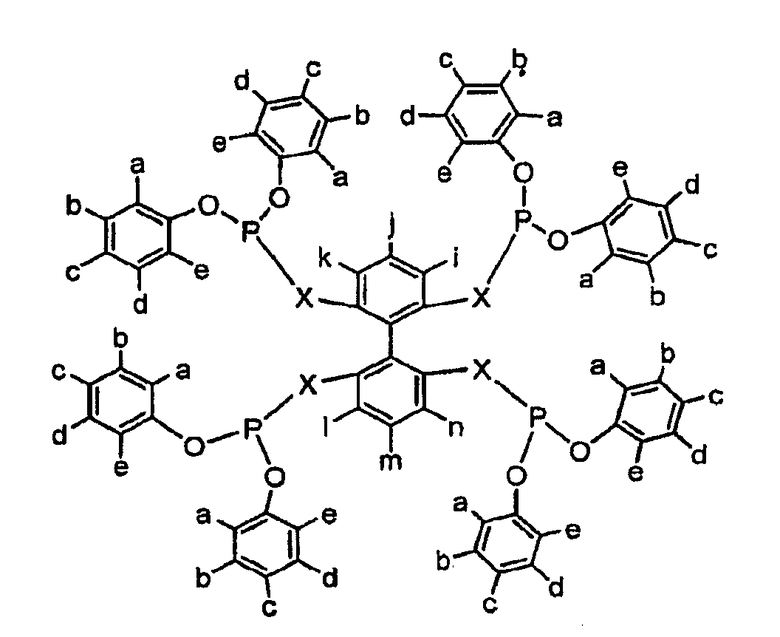
где Х является O, CH2, NH, NR, NSO2R или NSO2Ar, где R представляет собой алкил, замещенный алкил, арил или замещенный арил; Ar представляет собой арил и a, b, c, d, е, i, j, k, l, m и n являются, независимо, Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, CF3, COOR, SO3R, SO3H, POR2, галогенидом, NR2, или две группы из следующих групп: a, b, c, d, е, i, j, k, l, m и n, могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо, где R представляет собой алкил, замещенный алкил, арил или замещенный арил и Ar представляет собой арил.
Шестой вариант осуществления изобретения проиллюстрирован ниже:
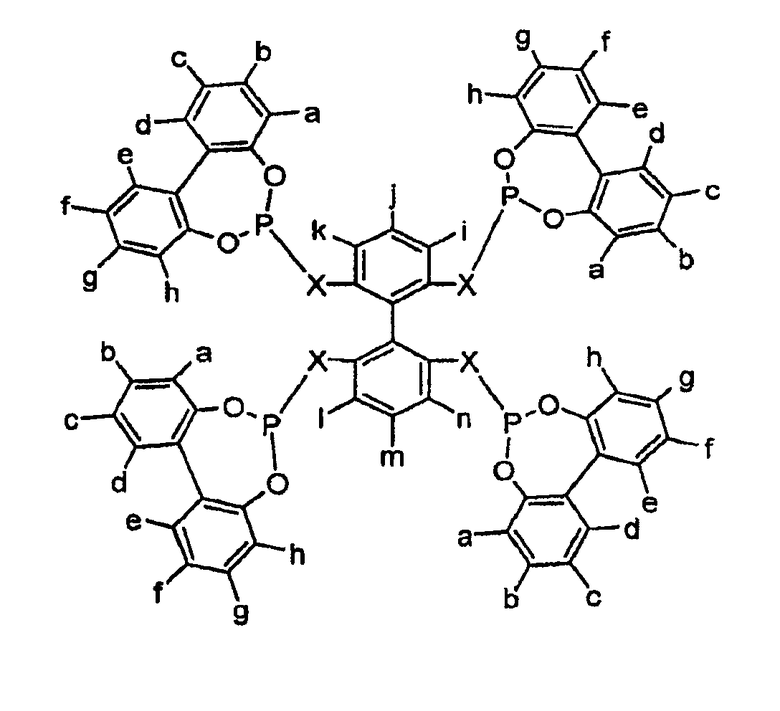
где Х является O, CH2, NH, NR, NSO2R или NSO2Ar, где R представляет собой алкил, замещенный алкил, арил или замещенный арил; Ar представляет собой арил и a-n являются, независимо, Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, CF3, COOR, SO3R, SO3H, POR2, галогенидом, NR2, или две группы из групп a-n могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо, где R представляет собой алкил, замещенный алкил, арил или замещенный арил, и Ar представляет собой арил. В том случае, когда d и e не являются водородом, то могут быть получены энантиомеры этих лигандов для асимметрических каталитических реакций.
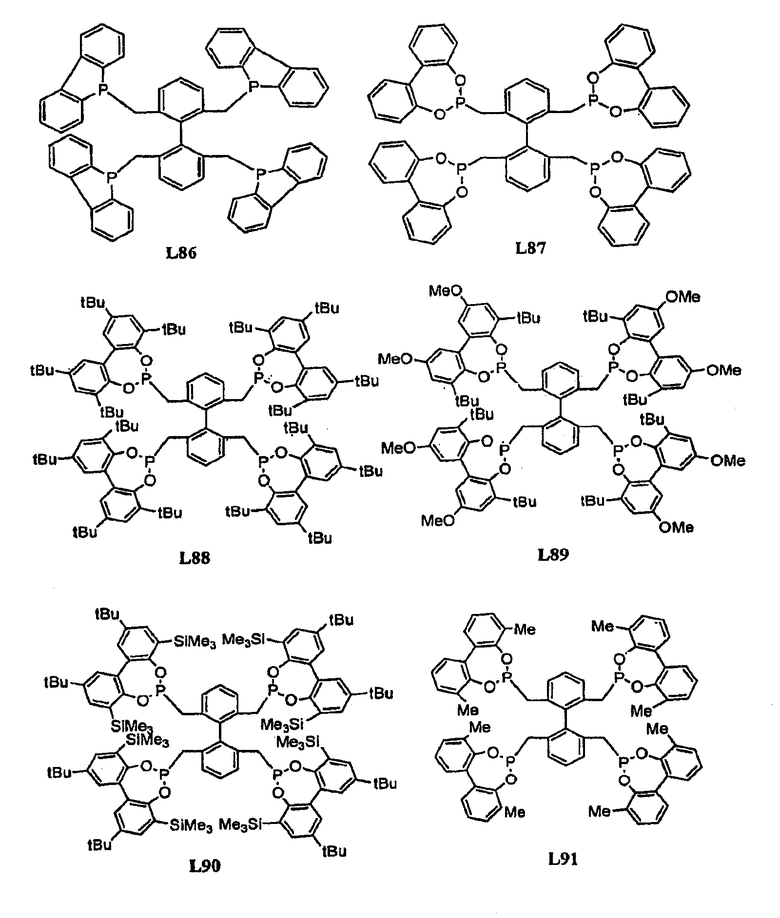
Примеры тетрафосфорных лигандов по настоящему изобретению (L1 - L91) показаны ниже:
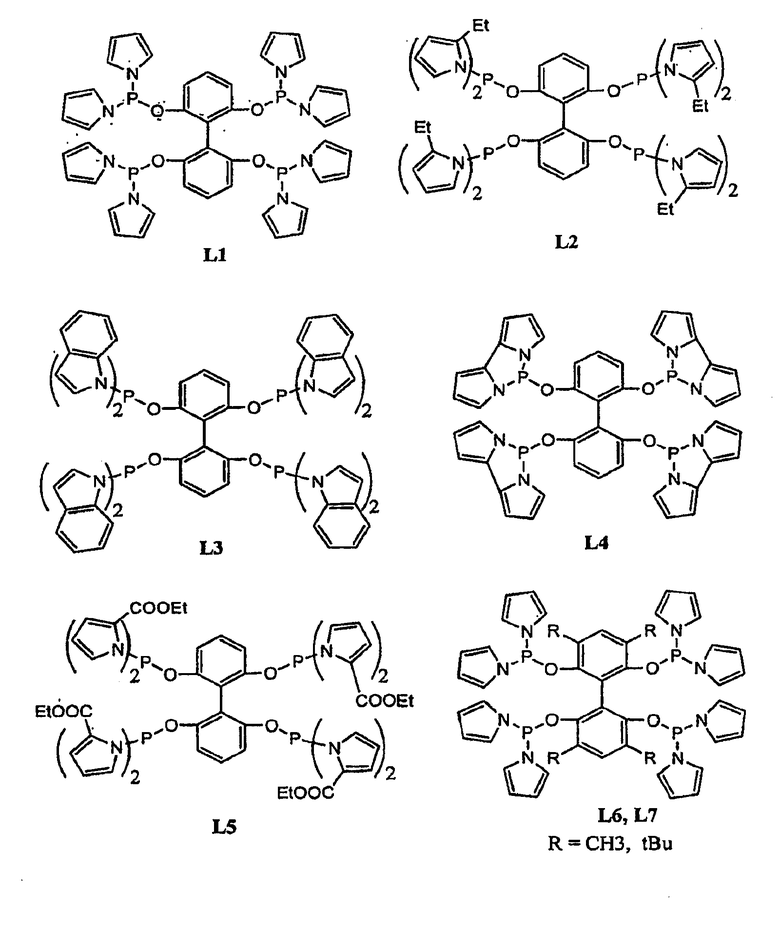
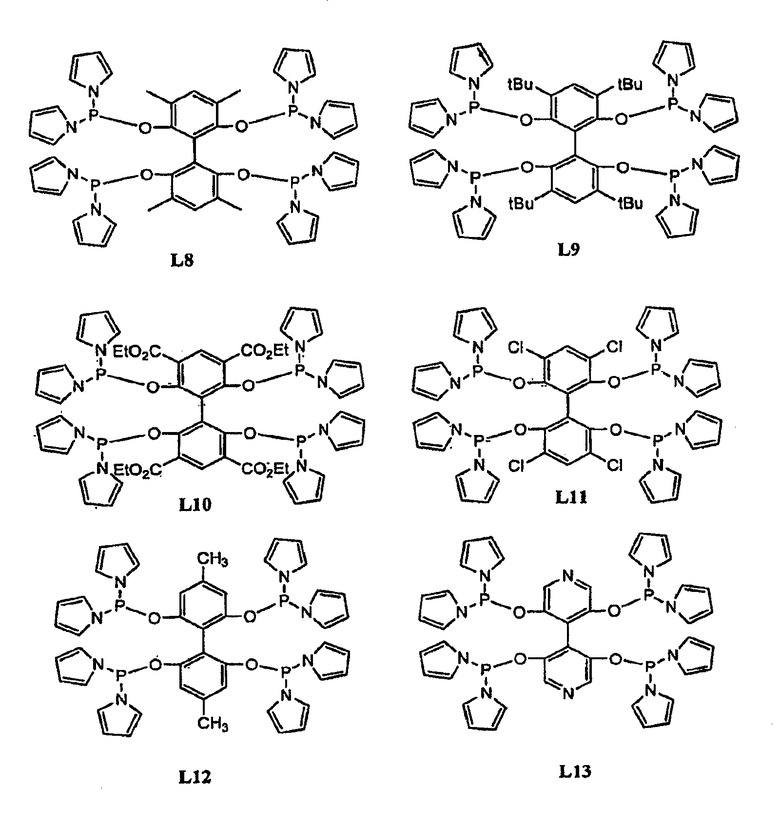
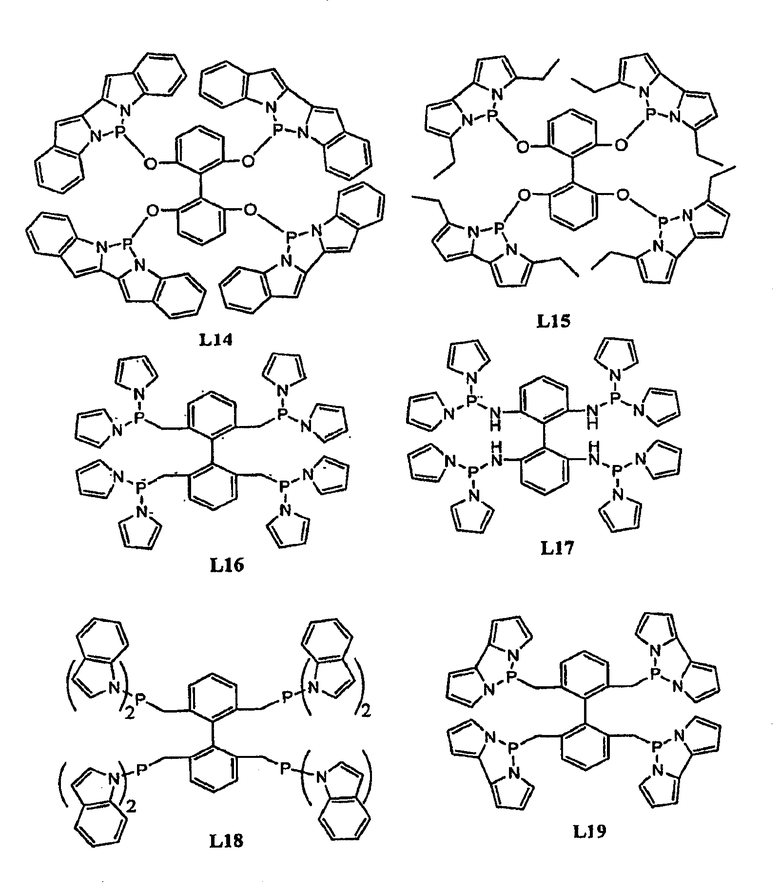
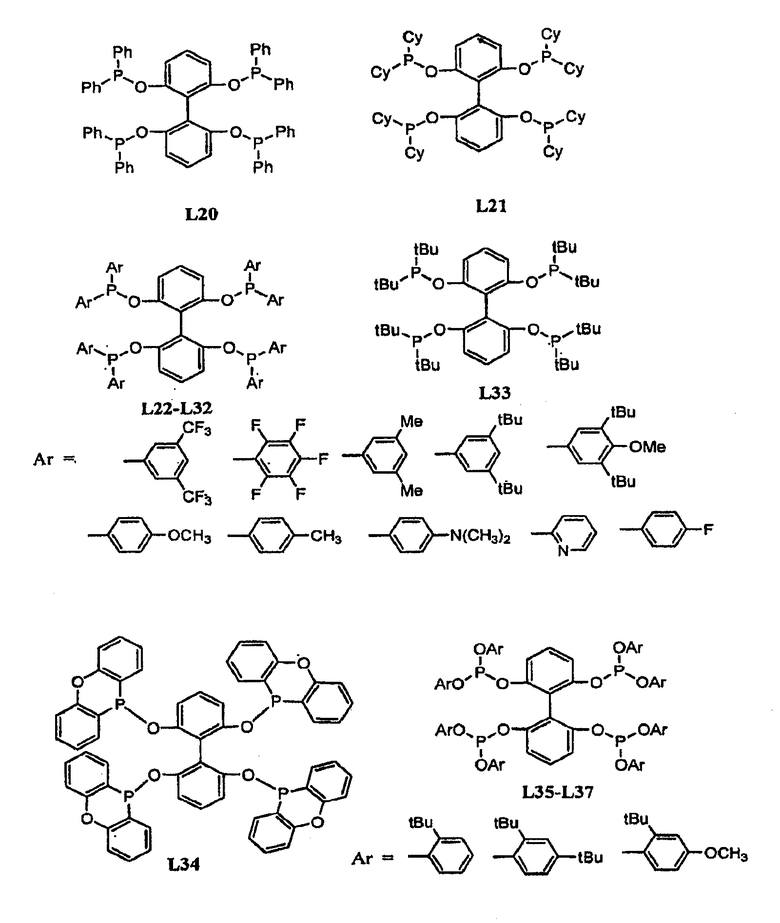
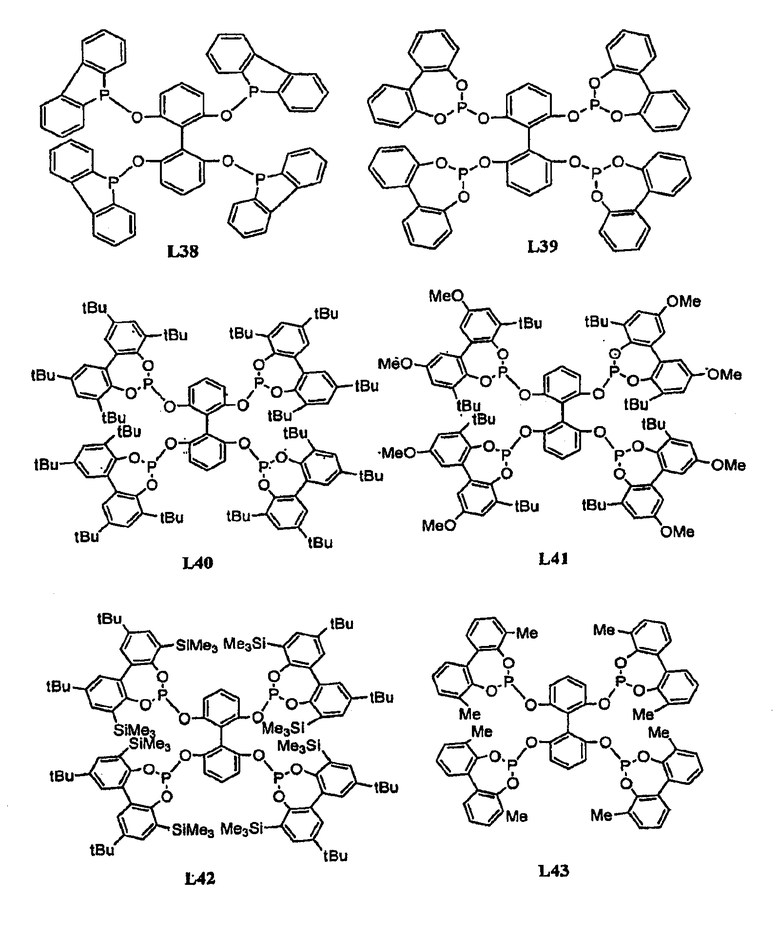
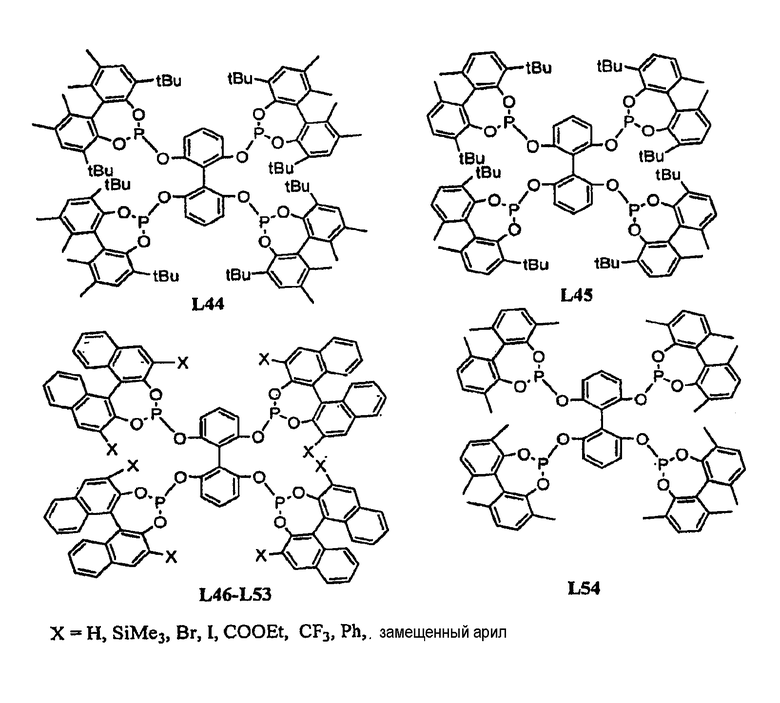
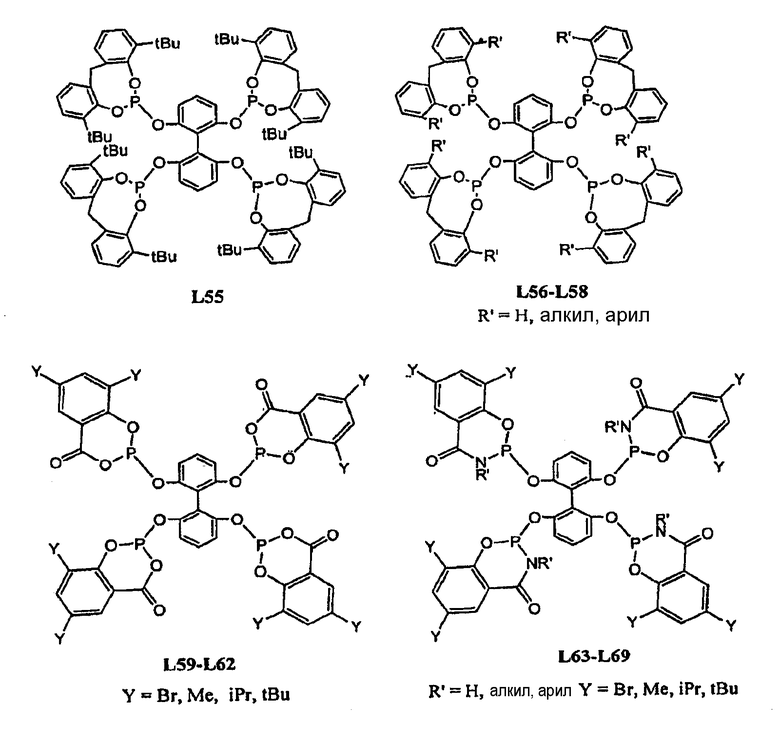
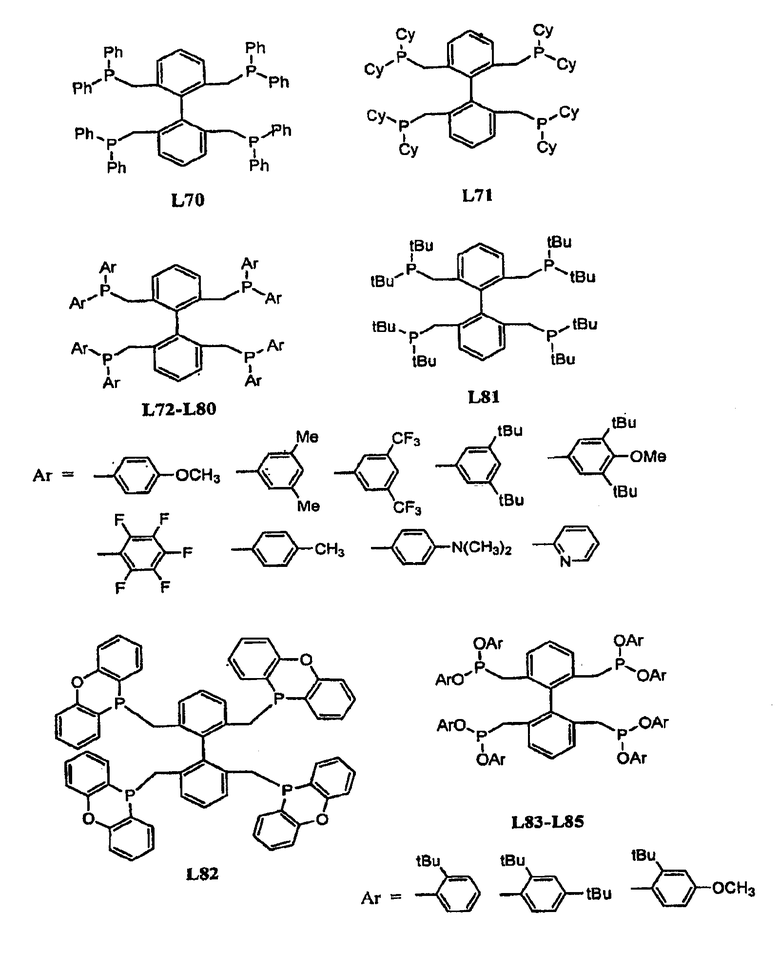
В гидроформилировании или родственных реакциях комплекс переходный металлтетрафосфорный лиганд получают путем смешения соли переходного металла с лигандом. Соль переходного металла представляет собой соль переходного металла, выбранного из группы, состоящей из Fe, Zn, Mn, Co, Cu, Ag, Ni, Pt, Pd, Rh, Ru и Ir. Примерами солей переходных металлов являются FeX3, Fe(OTf)3, Fe(OAc)3, Mn(OAc)3, Mn(OTf)3, MnX3, Zn(OTf)2, Co(OAc)2, AgX, Ag(OTf), Ag(OTf)2, AgOAc, PtCl2, H2PtCl4, Pd2(DBA)3, Pd(OAc)2, PdCl2(RCN)2, (Pd(аллил)Cl)2, Pd(PR3)4, (Rh(NBD)2)X, (Rh(NBD)Cl)2, (Rh(COD)Cl)2, (Rh(COD)2)X, Rh(acac)(CO)2, Rh(этилен)2(acac), (Rh(этилен)2Сl)2, RhCl(PPh3)3, Rh(CO)2Cl2, RuH(CO)2(PPh3)2, Ru(Ar)X2, Ru(Ar)X2(PPh3)3, Ru(COD)(COT), Ru(COD)(COT)X, RuX2(cymen), Ru(COD)n, RuCl2(COD), (Ru(COD)2)X, RuX2(PN), RuCl2(=CHR)(PR'3)2, Ru(ArH)Cl2, Ru(COD)(металлил)2, (Ir(NBD)2Cl)2, (Ir(NBD)2)X, (Ir(COD)2Cl)2, (Ir(COD)2)X, CuX(NCCH3)4, Cu(OTf)2, Cu(OTf)2, Cu(Ar)X, CuX, Ni(acac)2, NiX2, (Ni(аллил)X)2, Ni(COD)2, MoO2(acac)2, Ti(OiPr)4, VO(acac)2 и MeReO3, где каждый R и R', независимо, выбирают из группы, состоящей из алкила или арила; Ar представляет собой арильную группу; Х представляет собой противоанион, такой как BF4, ClO4, OTf, SbF6, CF3SO3, B(C6H3(CF3)2)4, Cl, Br или I; OТf представляет собой OSO2CF3; DBA представляет собой PhCH=CHCOCH=CHPh, NDB представляет собой норборнадиен; COD представляет собой циклооктадиен и COT представляет собой циклооктатриен. Смесь помещают в автоклав, который продувают азотом и впоследствии подают СО и Н2.
Синтез тетрафосфатного лиганда
Все реакции и манипуляции в примере, изложенном ниже, выполняют в заполненном азотом герметичном перчаточном боксе, или используя стандартную технику Шленка (Schlenk). ТГФ и толуол сушат и перегоняют над натрий-бензофенон-кетилом в токе азота. Метиленхлорид перегоняют над CaH2. Метанол перегоняют над Mg в токе азота. Колоночную хроматографию выполняют, используя силикагель ЕМ 60 (230~400 меш). Данные 1Н-, 13С- и 31Р-ЯМР регистрируют на спектрометрах Bruker WP-200, AM-300 и AMX-360. Химические сдвиги приводят в миллионных долях (ppm) в слабом поле относительно тетраметилсилана с резонансным сигналом растворителя в качестве внутреннего стандарта. Масс-спектры записывают на масс-спектрометре KRATOS MS 9/50 для LR-E1 и HR-E1. Анализ методом газовой хроматографии осуществляют на газовом хроматографе Helwett-Packard 6890, используя хиральные капиллярные колонки. Анализ методом высокоэффективной жидкостной хроматографии осуществляют на хроматографе WatersTM 600.
Следующую методику обычно используют для синтезирования лиганда, имеющего структуру L1. К раствору дипирролилхлорфосфина (4,4 ммоль, 0,87 г) в ТГФ (10 мл) добавляют по каплям триэтиламин (1 мл) и раствор тетраола (1 ммоль, 0,218 г) в ТГФ (5 мл) при комнатной температуре. Тетраол синтезируют в соответствии с публикацией: Lindsten, G.; Wennerstroem, O.; Isaksson, R., J. Org. Chem. 1987, 52, 547-54, а дипирролилхлорфосфин получают в соответствии с публикацией: van der Slot, S.C.; Duran, J.; Luten, J.; Kamer, P.C.J.; van Leeuwen, P.W.N.M. Organometallics 2002, 21, 3873-3883. Триэтиламингидрохлоридные соли образуются немедленно после добавления. Реакционную смесь перемешивают в течение 6 часов при комнатной температуре. Триэтиламингидрохлоридные соли затем отфильтровывают и растворитель удаляют под вакуумом. Сырой продукт очищают флэш-хроматографией на основном оксиде алюминия при элюировании смесью гексан/EtOAc/Net3 (6:1:0,01) с получением лиганда L1 (0,31 г, 36%) в виде стабильного на воздухе бесцветного твердого вещества. 1Н ЯМР (300 Гц, CDCl2): δ 7,23 (т, 2Н, J=8,3 Гц), 6,68 (м, 20Н), 6,21 (м, 16Н) 13С ЯМР (90 Гц, CDCl2): δ 152,86 (д, J=12,2 Гц), 131,0, 121,4 (д, J=16,8 Гц), 118,1, 115,3 (д, J=13,7 Гц), 112,7 31Р ЯМР (146 Гц, CDCl2): δ 107,3. Масс-спектрометрия высокого разрешения с ионизацией электрораспылением (HRMS (ES+)) рассчитанный для C44H39N8O4P4 [MH+] №8672045, раскрытый в №8672021.
Типичный процесс гидроформилирования
В ампулу объемом 2 мл с магнитной мешалкой загружают тетрафосфорный лиганд L1, полученный в предыдущем примере (3 мкмоль, 2,6 мг) и Rh(acac)(CO)2 (1 мкмоль, 0,1 мл 10 мМ раствора в толуоле). Смесь перемешивают в течение 5 минут. Затем добавляют 2-октен (10 ммоль, 1,56 мл), после этого - декан (0,01 мл) в качестве внутреннего стандарта. Реакционную смесь перемещают в автоклав. Автоклав продувают азотом три раза и потом подают СО (5 бар) и Н2 (5 бар). Затем автоклав нагревают до 100°С (масляная баня). По истечении 12 часов автоклав охлаждают в ледяной воде, и давление осторожно сбрасывают в хорошо вентилируемом вытяжном шкафу. Реакционную смесь немедленно подвергают анализу методом газовой хроматографии (GC).
Высокие значения региоселективности, получаемые при использовании тетрафосфорного лиганда L1, имеющего много способов хелатирования, для гидроформилирования стирола, 1-октена и 1-гексена, продемонстрированы в Таблице 1. Обычно стирол представляет собой трудный в реакционном отношении субстрат для достижения соотношения линейных продуктов к разветвленным продуктам более чем 2:1 при сравнении с бисфосфорными лигандами известного уровня техники, такими как ксантфос и UC-44. Как показано в Таблице 1, новые тетрафосфорные лиганды (Тип А), такие как L1, являются более селективными лигандами гидроформилирования, чем бисфосфорный лиганд (Тип В) известного уровня техники. Реакционные условия включают 0,1 мол.% Rh(CO)2(acac) и лиганда, температуру реакции 80°С в течение 1 часа при 20 атм СО и Н2. Эти результаты указывают, что тетрафосфорные лиганды с несколькими способами координации при хелатировании могут быть использованы для увеличения координирующих способностей бисфосфорных лигандов. Региоселективность с Типом А является самой высокой из представленных на настоящий момент.
Результаты гидроформилирования 2-гексена и 2-октена при использовании тетрафосфорного лиганда (Тип А) относительно бисфосфорного лиганда (Тип В) с получением альдегида суммированы ниже в Таблице 2. В Таблицах 2-11, которые следуют далее, n:i означает соотношение линейного альдегида к разветвленному альдегиду и TOF означает частоту оборота в катализе (оборот на катализатор в час). Тетрафосфорные лиганды по настоящему изобретению дают более высокие соотношения «n:i», чем бисфосфорные лиганды.
Условия гидроформилирования включают S/C=10000, [Rh] составляет 0,69 мМ (для 2-гексена) и 0,57 мМ (для 2-октена), соотношение Лиганд/Rh cоставляет 3:1, температура реакции составляет 100°С, СO/H2 составляет 5/5 атм, толуол является растворителем, и декан представляет собой внутренний стандарт.
Таблица 3 ниже показывает результаты гидроформилирования 1-гексена и 1-октена при использовании тетрафосфорного лиганда (Тип А) относительно бисфосфорного лиганда (Тип В) с получением альдегида посредством реакции гидроформилирования:
Реакционные условия: S/C=10000, концентрация Rh составляет 0,2 мМ, соотношение Лиганд/Rh cоставляет 3:1, температура реакции составляет 80°С, СO/H2 составляет 10/10 атм, толуол является растворителем, и декан представляет собой внутренний стандарт.
Реакция гидроформилирования сильно зависит от реакционных условий. Типичные реакционные условия включают S/C = 10000, соотношение лиганд/металл приблизительно 3, концентрацию переходного металла приблизительно 0,2-0,7 мМ, температуру реакции 100°С и время реакции 12 часов. Для оптимизации реакционных условий проводят следующие эксперименты с тетрафосфорным лигандом (L1). Как видно из соотношений n:i в Таблицах 2 и 3, имеет место существенное и значительное увеличение количества линейного альдегида, получаемого при использовании тетрафосфорного лиганда по настоящему изобретению в противоположность использованию бисфосфорного лиганда.
Соотношение лиганда к металлу
Гидроформилирование сначала проводят с различными соотношениями лиганда к металлу. Как показано в Таблице 4, увеличение соотношения лиганда к металлу слегка снижает скорость реакции. С другой стороны, соотношение лиганда к металлу значительно влияет на региоселективность. При более низких соотношениях наблюдают низкую региоселективность. Для достижения высокой региоселективности существенным является минимальное соотношение лиганда к металлу 2, которое позволяет тетрафосфорному лиганду быть координированным способом при участии нескольких центров координации. Дальнейшее увеличение соотношения лиганда к металлу значительно не улучшает региоселективность.
L/Rh
Реакционные условия: субстрат представляет собой 2-октен, S/C=10000, концентрация Rh составляет 0,57 мМ, температура реакции составляет 100°С, СO/H2 составляет 10/10 атм, реакционное время составляет 1 час, толуол является растворителем, и декан представляет собой внутренний стандарт. Результаты в Таблице 4 показывают, что присутствие двух свободных фосфорных лигандов с тетрафосфорным лигандом является важным для достижения высокой региоселективности (n:i увеличивается от 2,92 до 17,7). Таблица 5 ниже показывает подобные результаты с 2-гексеном в качестве субстрата.
L/Rh
Реакционные условия: субстрат представляет собой 2-гексен, S/C=10000, концентрация Rh составляет 0,69 мМ, температура реакции составляет 100°С, СO/H2 составляет 10/10 атм, реакционное время составляет 1 час, толуол является растворителем, и внутренний стандарт представляет собой декан. Результаты в Таблице 5 показывают, что присутствие двух свободных фосфорных лигандов, с тетрафосфорным лигандом, является важным для достижения высокой региоселективности (n:i увеличивается от 12,7 до 42).
Температура
Температура реакции также играет ключевую роль в гидроформилировании. Как показано в Таблицах 6 и 7 ниже, при низкой температуре, хотя и наблюдают высокую региоселективность, скорость реакции остается низкой. Для способствования изомеризации и гидроформилирования олефинов высокая температура (100°С) является предпочтительной для достижения высокой скорости реакции, а также приемлемой региоселективности.
Реакционные условия: субстрат представляет собой 2-октен, S/C = 10000, концентрация Rh составляет 0,57 мМ, соотношение лиганд/Rh составляет 3:1, СO/H2 составляет 10/10 атм, реакционное время составляет 1 час, толуол является растворителем, и декан представляет собой внутренний стандарт.
Реакционные условия: субстрат представляет собой 2-гексен, S/C=10000, концентрация Rh составляет 0,69 мМ, соотношение лиганд/Rh составляет 3:1, СO/H2 составляет 10/10 атм, реакционное время составляет 1 час, толуол является растворителем, и декан представляет собой внутренний стандарт.
Давление
Общее давление CO/H2 также оказывает влияние на реакцию. При высоком давлении как скорость реакции, так и региоселективность являются низкими. Понижение давления, как правило, приводит к более высоким скорости реакции и региоселективности. Снижение давления CO/H2 от 10/10 атм до 5/5 атм не изменяет скорость реакции намного, но региоселективность улучшается дополнительно. Результаты по гидроформилированию 2-октена и 2-гексена показаны в Таблицах 8 и 9.
Реакционные условия: субстрат представляет собой 2-октен, S/C=10000, концентрация Rh составляет 0,57 мМ, соотношение лиганд/Rh составляет 3:1, температура реакции составляет 100°С, реакционное время составляет 1 час, толуол является растворителем, и декан представляет собой внутренний стандарт.
Реакционные условия: субстрат представляет собой 2-гексен, S/C=10000, концентрация Rh составляет 0,69 мМ, соотношение лиганд/Rh составляет 3:1, температура реакции составляет 100°С, реакционное время составляет 1 час, толуол является растворителем, и декан представляет собой внутренний стандарт.
Реакционное время
Реакционное время также оказывает влияние на селективность гидроформилирования. Как показано в Таблицах 10 и 11 ниже, чем больше реакционное время, тем ниже региоселективность. Дополнительное увеличение реакционного времени от 12 часов до 18 часов лишь слегка улучшает число оборотов (TON), то есть оборот субстрата на катализатор, за счет сниженной региоселективности.
Реакционные условия: субстрат представляет собой 2-октен, S/C=10000, концентрация Rh составляет 0,57 мМ, соотношение лиганд/Rh составляет 3:1, температура реакции составляет 100°С, СO/H2 составляет 5/5 атм, толуол является растворителем, и декан представляет собой внутренний стандарт.
Реакционные условия: субстрат представляет собой 2-гексен, S/C=10000, концентрация Rh составляет 0,69 мМ, соотношение лиганд/Rh составляет 3:1, температура реакции составляет 100°С, СO/H2 составляет 5/5 атм, толуол является растворителем, и декан представляет собой внутренний стандарт.
Хотя это изобретение было описано со ссылкой на несколько предпочтительных вариантов осуществления, предполагается, что его различные изменения и модификации будут очевидны специалистам в данной области при прочтении предшествующего подробного описания. Таким образом, подразумевается, что следующие прилагаемые пункты формулы следует истолковывать как включающие все такие изменения и модификации, которые являются частью сущности и объема этого изобретения.
Настоящее изобретение относится к лигандам, используемым в катализаторах на основе переходных металлов для гидроформилирования, изомеризации-гидроформилирования, гидрокарбоксилирования, гидроцианирования, изомеризации-формилирования, гидроаминометилирования и родственных реакций, формулы

где i, j, k, l, m и n являются Н, R, Аr, замещенным Ar, OR, OAr, COOEt, галогенидом, SO2R, SO2H, SO2NHR, POR2, РОАr2 или NR2, где R - необязательно замещенный алкил или арил, Ar - арил; X1-X4 являются О или CH2; Y1, Y'1, Y2, Y'2, Y3, Y'3, Y4, Y'4 являются R, Ar, OR, OAr, необязательно замещенным пирролом, или где R, Ar, OR, OAr, пиррол и замещенный пиррол являются связанными посредством углерод-углеродной связи, СН2, NH, NR или О. Технический результат - получение новых эффективных катализаторов. 4 н. и 10 з.п. ф-лы, 11 табл.
1. Фосфорный лиганд, имеющий следующую формулу:

в которой i, j, k, l, m и n являются независимо Н, R, Аr, замещенным Ar, OR, OAr, COOEt, галогенидом, SO2R, SO3Н, SO2NHR, POR2, РОАr2 или NR2, где R представляет собой алкил, замещенный алкил, арил или замещенный арил, и Ar представляет собой арил; X1-X4 являются независимо О или СН2;
и Y1, Y'1, Y2, Y'2, Y3, Y'3, Y4, Y'4 являются независимо R, Ar, OR, OAr, пирролом или замещенным пирролом, или где R, Ar, OR, OAr, пиррол и замещенный пиррол являются связанными посредством углерод-углеродной связи, СН2, NH, NR или О.
2. Фосфорный лиганд по п.1, где лиганд имеет следующую структуру:

где X является О или СН2; и а, b, с и d являются независимо Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, СF3, COOR, SO3R, SO3Н, POR2, галогенидом, или две группы из следующих групп: а, b, с и d могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо.
3. Фосфорный лиганд по п.1, где лиганд имеет следующую структуру:

где Х является О или СН2; и а, b, с, d, e, f являются независимо Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, СFз, COOR, SO3R, SO3Н, POR2, галогенидом, или две группы из следующих групп: а, b, с, d, e, f могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо.
4. Фосфорный лиганд по п.1, где лиганд имеет следующую структуру:

где Х является О или СН2 и а, b, с, d, e являются независимо Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, СFз, COOR,
SO3R, SO3Н, POR2, галогенидом, NR2, или две группы из следующих групп: а, b, с, d, e могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо.
5. Фосфорный лиганд по п.1, где лиганд имеет следующую структуру:
где Х является О или СН2; Y представляет собой углерод-углеродную связь, О, СН2, NH или NR, где R представляет собой алкил, замещенный алкил, арил или замещенный арил; и a-h являются независимо Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, СF3, COOR, SO3R, SO3Н, POR2, галогенидом, NR2, или две группы из групп a-h могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо.
6. Фосфорный лиганд по п.1, где лиганд имеет следующую структуру:
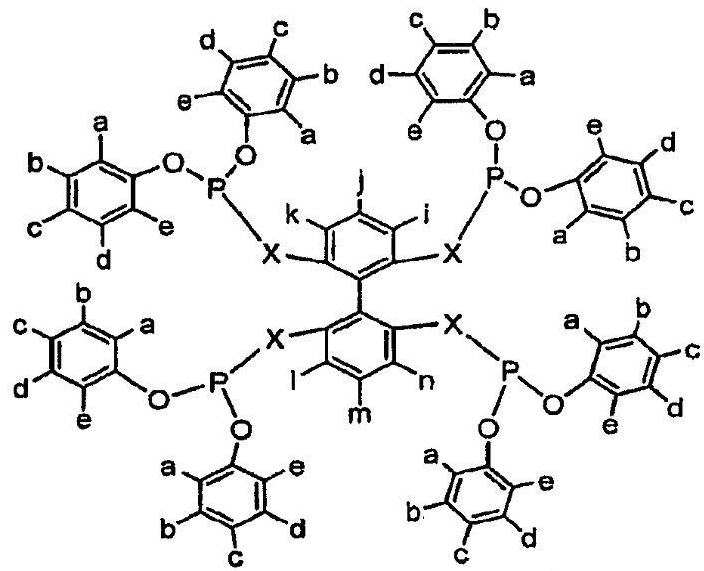
где X является О или СН2; и а, b, с, d, е являются независимо Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, СF3, COOR, SO3R, SO3H, POR2, галогенидом, NR2, или две группы из следующих групп: а, b, с, d, е могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо.
7. Фосфорный лиганд по п.1, где лиганд имеет следующую структуру:

где Х является О или СН2; и а-n являются независимо Н, алкилом, арилом, замещенным алкилом, замещенным арилом, OR, OAr, SiR3, СF3, COOR, SO3R, SO3Н, POR2, галогенидом, NR2, или две группы из групп а-n могут представлять собой циклическое конденсированное кольцо или расширенное ароматическое кольцо.
8. Фосфорный лиганд по п.1, где лиганд имеет следующую структуру:
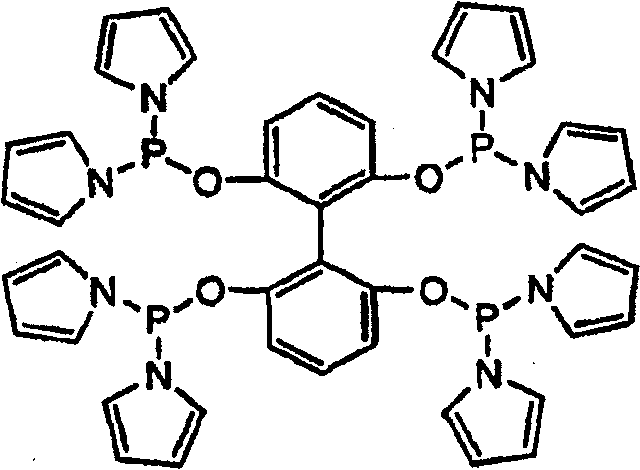
9. Катализатор, содержащий лиганд по пп.1-8 и соль переходного металла, где металл упомянутой соли металла выбирают из группы, состоящей из: Fe, Zn, Mn, Со, Сu, Ag, Ni, Pt, Pd, Rh, Ru и Ir.
10. Катализатор по п.9, где упомянутую соль переходного металла выбирают из группы, состоящей из FеХ3, Fе(ОТf)3, Ре(ОАс)3, Мn(ОАс)3, Мn(ОТf)3, МnХ3, Zn(OTf)2, Co(OAc)2, AgX, Ag(OTf), Ag(OTf)2, AgOAc, PtCl2, H2PtCl4, Pd2(DBA)3, Pd(OAc)2, PdCl2(RCN)2, (Pd(аллил)Cl)2, Pd(PR3)4, (Rh(NBD)2)X, (Rh(NBD)Cl)2, (Rh(COD)Cl)2, (Rh(COD)2)X, Rh(acac)(CO)2, Ph(этилен)2(асас), (Rh(этилен)2Сl)2, RhСl(РРh3)3, Rh(CO)2Cl2, RuН(СО)2(РРh3)2, Ru(Ar)X2, Ru(Аr)Х2(РРh3)3, Ru(COD)(COT), Ru(COD)(COT)X, RuX2(cymen), Ru(COD)n, RuCl2(COD), (Ru(COD)2)X, RuX2(PN), RuCl2(=CHR)(PR'3)2, Ru(ArH)Cl2, Ru(СОD)(металлил)2, (Ir(NBD)2Cl)2, (Ir(NBD)2)X, (Ir(COD)2Cl)2, (Ir(COD)2)X, CuX(NCCH3)4, Cu(OTf), Cu(OTf)2, Cu(Ar)X, CuX, Ni(acac)2, NiХ2, (Ni(аллил)Х)2, Ni(COD)2, MoO2(acac)2, Ti(OiPr)4, VO(acac)2 и МеRеО3, где каждый R и R' независимо выбирают из группы, состоящей из алкила или арила; Аr представляет собой арильную группу; Х представляет собой противоанион, такой как BF4, СlO4, OTf, SbF6, СF3SO3, В(С6Н3(СF3)2)4, Сl, Вr или I; OTf представляет собой ОSO2CF3, DBA представляет собой PhCH=CHCOCH=CHPh, NDB представляет собой норборнадиен; COD представляет собой циклооктадиен и СОТ представляет собой циклооктатриен.
11. Катализатор по п.10, где соль переходного металла выбирают из группы, состоящей из (Rh(COD)Cl)2, (Rh(COD)2)X, Rh(acac)(CO)2 и RuH(CO)2(PPh3)2.
12. Способ применения катализатора по п.10, где катализатор представляет собой катализатор в реакции, выбираемой из группы, состоящей из реакций гидроформилирования, изомеризации-гидроформилирования, гидрокарбоксилирования, гидроцианирования, изомеризации-формилирования и гидроаминометилирования алкенов.
13. Способ по п.12, где реакция представляет собой реакцию гидроформилирования.
14. Способ применения катализатора в реакции гидроформилирования, где катализатор содержит лиганд по п.8 и соль переходного металла, выбранную из группы, состоящей из (Rh(COD)Cl)2, (Rh(COD)2)X, Rh(acac)(CO)2, и RuН(СО)2(РРh3)2.
| Способ получения дифосфор (у) замещенных фосфинов или их бис-аналогов | 1980 |
|
SU910645A1 |
| US 3420864 A, 07.01.1969 | |||
| US 6437192 B, 20.08.2002 | |||
| US 6846945 B2, 25.01.2005. | |||
Авторы
Даты
2011-06-27—Публикация
2006-12-15—Подача