Изобретение относится к медицинской вирусологии и может быть использовано в здравоохранении для профилактики эпидемического гриппа среди взрослых и детей живой интраназальной гриппозной вакциной из штамма вируса гриппа В/60/Брисбен/08/83, семейства Orthomyxoviridae, рода Influenzavirus В.
Известный вакцинный штамм вируса гриппа - В/60/Джилин/03/1-прототип [Патент №2307161, гос. рег. 09.11.2005. БИ. №27, 27.09.2007 г.Руденко Л.Г., Александрова Г.И., Ларионова Н.В., Климов А.И. Штамм вируса гриппа В/60/Джилин/03/1 для производства живой гриппозной интраназальной вакцины для взрослых и для детей] - утратил антигенную актуальность и вследствие этого не сможет вызвать защитную реакцию во время эпидемии гриппа, вызванной штаммом вируса гриппа, аналогичным вирусу В/Брисбен/60/2008.
Задачей, на решение которой направлено заявляемое изобретение, является получение вакцинного штамма актуальной антигенной разновидности на основе эпидемического вируса В/Брисбен/60/2008.
Вакцинный штамм В/60/Брисбен/08/83 получен методом генетической реассортации эпидемического вируса В/Брисбен/60/2008 со штаммом В/СССР/60/69 - донором аттенуирующих свойств, с последующей селекцией в присутствии антисыворотки к вирусу В/СССР/60/69. Донор аттенуации - холодоадаптированный температурочувствительный штамм вируса гриппа В/СССР/60/69, разрешенный для получения безвредных живых интраназальных вакцин [Александрова Г.И., Климов А.И. Живая вакцина против гриппа. - СПб.: Наука. - 1994. - 151 с.].
В реакции торможения гемагглютинации (РТГА) установлена принадлежность гена, кодирующего поверхностный белок гемагглютинин (НА), вирусу В/Брисбен/60/2008, антисывороткой к которому полностью нейтрализуется.
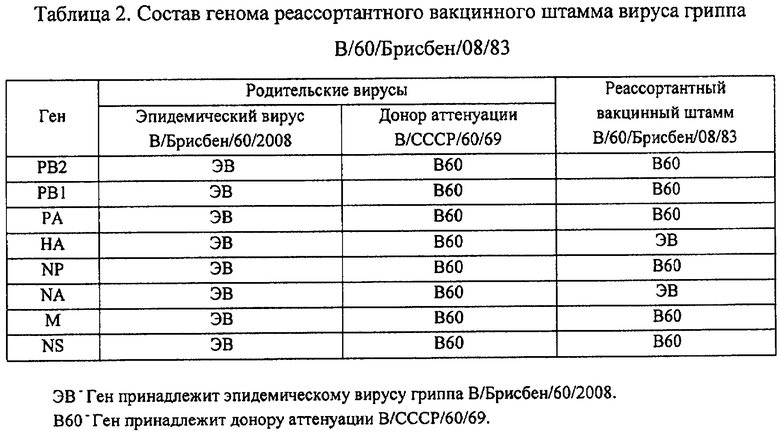
Состав внутренних генов и гена, кодирующего нейраминидазу (NA), вакцинного штамма В/60/Брисбен/08/83 установлен методом рестрикционного анализа амплифицированных ДНК-копий генов. Рестрикционный метод [Klimov A.I., Сох N.J. PCR restriction analysis of genome composition and stability of cold-adapted reassortant live influenza vaccines // J.Virol. Methods. - 1995. - Vol.52. - №1-2. - P.41-49] основан на амплификации участков РНК длиной около 150-400 нуклеотидов, включающих уникальные нуклеотидные последовательности, характерные только для донора аттенуации, но не для современных эпидемических вирусов гриппа, или наоборот. Обработка амплифицированных фрагментов ДНК специфическими эндонуклеазами (рестриктазами) с последующим электрофорезом обработанных рестриктазами фрагментов ДНК в 1.7%-ном агарозном геле, в присутствии 0.5 мкг/мл этидиума бромида, позволяет четко дифференцировать принадлежность генов исследуемых реассортантных штаммов к эпидемическому вирусу или донору аттенуации. Нами были подобраны праймеры, позволяющие амплифицировать фрагменты ДНК-копий генов вируса, которые имеют специфичные для донора аттенуации В/СССР/60/69 и для современных эпидемических вирусов гриппа В последовательности. Подобран набор рестриктаз для специфичных последовательностей донора или эпидемического вируса гриппа В «викторианской» ветви, к которой относится эпидемический вирус В/Брисбен/60/2008 (таблица 1). Установлено, что вакцинный штамм В/60/Брисбен/08/83 унаследовал шесть генов, кодирующих внутренние негликозилированные белки (РВ1, РВ2, PA, NP, М, NS) от донора аттенуации В/СССР/60/69, и два гена, кодирующих поверхностные белки - НА и NA - от эпидемического вируса В/Брисбен/60/2008 (таблица 2).

ОЦЕНКУ ФЕНОТИПИЧЕСКИХ СВОЙСТВ вакцинного штамма В/60/Брисбен/08/83 проводили путем его параллельного титрования в РКЭ при разных температурах. Показано, что вакцинный штамм является температурочувствительным (разность в показателях инфекционной активности при температуре инкубации 32°C и 37°C составляет 7.0 lg ЭИД50/0,2 мл) и холодоадаптированным (разность в показателях инфекционной активности при температуре инкубации 32°C и 25°C равна 2.5 lg ЭИД50/0,2 мл), что свидетельствует о его безвредности для человека, поскольку по этим показателям он идентичен донору аттенуации В/СССР/60/69.
ОЦЕНКУ ТОКСИЧНОСТИ вакцинного штамма В/60/Брисбен/08/83 осуществляли путем подкожного и внутрибрюшинного введения вирусного материала мышам. Для этого группе из 10 мышей (самцов линии СВА весом 18-20 г) вводили соответствующим способом 0,5 мл вируссодержащей аллантоисной жидкости с титром 8.0 lg ЭИД50/0,2 мл и оценивали патогенность вируса по проценту выживших мышей в течение 7 дней после введения вируса. Вакцинный штамм В/60/Брисбен/08/83 в эксперименте на мышах оказался полностью безвредным - 100% мышей выжили в течение всего периода наблюдения.
ОЦЕНКУ РЕАКТОГЕННОСТИ ДЛЯ ЛЮДЕЙ вакцинного штамма В/60/Брисбен/08/83 изучали при его интраназальном введении взрослым и детям.
Пример 1. Штамм В/60/Брисбен/08/83 ареактогенен для взрослых лиц.
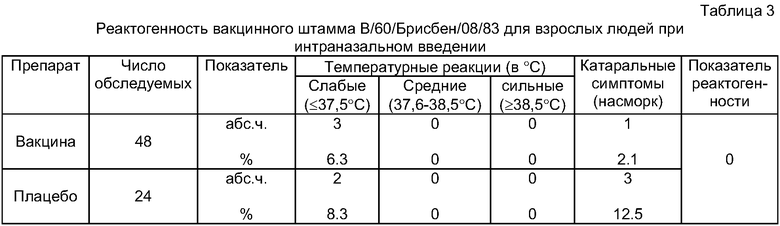
При интраназальной вакцинации 48 взрослых лиц реассортантным вакцинным штаммом В/60/Брисбен/08/83 с инфекционной активностью 7.5 lg ЭИД50/0,2 мл в разведении 1:2 в объеме 0.5 мл сильных, температурных реакций с повышением температуры тела свыше 38,5°C не наблюдалось. Средних реакций с кратковременным повышением температуры в диапазоне 37,6-38,5°C также не наблюдалось. Слабые температурные реакции (до 37,5°C) наблюдались в 6.3% случаев в группе привитых, тогда как в группе лиц, получивших плацебо (24 человека), такие реакции зарегистрированы в 8.3% случаев. Легкие катаральные явления, в виде насморка, отмечены у 1 человека (2.1%) среди вакцинированных и у троих лиц (12.5%) среди получивших плацебо. Прочих катаральных симптомов и интоксикации не наблюдалось. Показатель реактогенности (разница в проценте средних реакций у привитых вакциной и получивших плацебо) составил 0%. Результаты обследования приведены в таблице 3.
Пример 2. Штамм В/60/Брисбен/08/83 ареактогенен для детей 7-14 лет.
Группу из 20 детей в возрасте 7-14 лет вакцинировали интраназально в объеме 0.5 мл реассортантным вакцинным штаммом В/60/Брисбен/08/83 с инфекционной активностью 7.5 lg ЭИД50/МЛ в разведении 1:2. Группа детей того же возраста из 21 человека получила плацебо. В группе вакцинированных детей сильных, средних и слабых температурных реакций не наблюдалось. Легкие катаральные явления, в виде насморка, отмечены у троих детей (15%). Интоксикации и прочих симптомов отмечено не было. В группе детей, получивших плацебо, сильных, средних и слабых температурных реакций также не наблюдалось. Катаральные симптомы отмечены у одного ребенка (4.8%). Показатель реактогенности составил 0%. Результаты исследований приведены в таблице 4.

Испытания на волонтерах подтвердили, что вакцинный штамм В/60/Брисбен/08/83 по показателям реактогенности соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей ФСП 42-0504-4097-04 на живую сухую гриппозную аллантоисную вакцину для интраназального применения.
Представленный вакцинный штамм В/60/Брисбен/08/83 характеризуется сочетанием полезных признаков, необходимых вакцинному штамму: антигенной специфичностью поверхностных белков эпидемического вируса В/Брисбен/60/2008, структурой генома, оптимальной для реассортантных вакцинных штаммов, температурочувствительностью и холодоадаптированностью, что коррелирует с аттенуацией для человека, характерной для донора аттенуации. Вакцинный штамм В/60/Брисбен/08/83 ареактогенен для взрослых и для детей при интраназальном введении. Штамм задепонирован в ФГУН «Государственный НИИ стандартизации и контроля медицинских биологических препаратов имени Л.А.Тарасевича» Роспотребнадзора (ФГУН ГИСК им. Л.А.Тарасевича Роспотребнадзора) под №796.
Морфология штамма - полиморфная, типичная для вируса гриппа.
На основании вышесказанного предлагаемый вакцинный штамм вируса гриппа может быть использован для профилактики гриппа как у взрослых, так и у детей.
ХАРАКТЕРИСТИКА ВАКЦИННОГО ШТАММА ВИРУСА ГРИППА В/60/БРИСБЕН/08/83 СЕМЕЙСТВА ORTHOMYXOVIRIDAE, РОДА INFLUENZAVIRUS В
Инфекционная активность при репродукции в развивающихся куриных эмбрионах при 32-33°C в течение 72 часов - 8.0 lg ЭИД50/0.2 мл.
Гемагглютинирующая активность - 1:1024.
Штамм проявляет генетическую стабильность биологических признаков после 5 пассажей на куриных эмбрионах (при использовании больших заражающих доз).
Характеристики вакцинного штамма В/60/Брисбен/08/83 представлены в прилагаемом паспорте. На основании этих характеристик штамм использовали в приготовлении вакцины и проверили вакцину на волонтерах.
ПАСПОРТ ШТАММА
1. Название штамма - В/60/Брисбен/08/83.
2. Серия - серия 1 (первая).
3. Метод получения - реассортация; характеристика родительских вирусов:
а) эпидемический вирус - В/Брисбен/60/2008;
б) донор аттенуации - В/СССР/60/69.
4. Количество пассажей - 5 в процессе реассортации.
5. Характеристика штамма до лиофилизации:
а) оптимальные условия репродукции - 32°C, 72 часа;
б) гемагглютинирующая активность - 1:512;
в) инфекционная активность - 8.0 lg ЭИД50/0,2 мл;
г) чувствительность к ингибиторам - ингибитороустойчивый в РТГА с нормальной лошадиной сывороткой;
д) разность в показателях инфекционной активности при 32°C/37°C: 8.0 lg ЭИД50/0,2 мл;
е) разность в показателях инфекционной активности при 32°C/25°C: 2.5 lg ЭИД50/0,2 мл;
ж) структура генома реассортанта по данным рестрикционного анализа амплифицированных в RT-PCR фрагментов вирусных РНК:
гены от эпидемического вируса - HA, NA;
гены от донора аттенуации - РВ2, РВ1, PA, NP, M, NS.
6. Характеристика штамма после лиофилизации:
а) дата лиофилизации -10 апреля 2009 г.;
б) объем материала в ампуле - 1.0 мл;
в) количество доз в ампуле - 4;
г) инфекционная активность - 7,5 lg ЭИД50/0.2 мл;
д) гемагглютинирующая активность - 1:256.
7. Рекомендуемое разведение при вакцинации - 1:2.
8. Антигенная специфичность гемагглютинина:
гемагглютинин в РТГА - идентичен вирусу В/Брисбен/60/2008, крысиной антисывороткой к которому полностью нейтрализуется.
9. Безвредность для мышей при подкожном и внутрибрюшинном введении - безвреден.
10. Бактериологический контроль: дата проведения - с 10 по 24 апреля 2006 г., результат - стерилен.
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А/17/БРИСБЕН/07/1 (H3N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2010 |
|
RU2416640C1 |
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А/17/БРИСБЕН/07/28 (H1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2010 |
|
RU2416641C1 |
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА В/60/ФЛОРИДА/04/181 ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2010 |
|
RU2422519C1 |
| ШТАММ ВИРУСА ГРИППА В/60/Джилин/03/1 ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2005 |
|
RU2307161C2 |
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА В/60/МАЛАЙЗИЯ/04/898 ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2009 |
|
RU2416639C1 |
| ВАКЦИННЫЙ ШТАММ ВИРУСА ГРИППА А/17/СОЛОМОНОВЫ ОСТРОВА/06/9 (H1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2010 |
|
RU2422518C1 |
| ШТАММ ВИРУСА ГРИППА В/60/ ИОХАННЕСБУРГ/99/50 ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2002 |
|
RU2215786C1 |
| ШТАММ ВИРУСА ГРИППА А/17/ ВАЙОМИНГ/03/8(H3N2) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2004 |
|
RU2285723C2 |
| ШТАММ ВИРУСА ГРИППА В/60/МАССАЧУСЕТС/2012/10 ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2013 |
|
RU2546190C1 |
| ШТАММ ВИРУСА ГРИППА ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЕТЕЙ | 2011 |
|
RU2464311C1 |
Вакцинный штамм вируса гриппа В/60/Брисбен/08/83 - реассортант, полученный путем скрещивания эпидемического вируса В/Брисбен/60/2008 с холодоадаптированным температурочувствительным вирусом В/СССР/60/69 - донором аттенуации, безвредным для людей. Штамм В/60/Брисбен/08/83 активно размножается в развивающихся куриных эмбрионах при оптимальной температуре 32°С. Штамм характеризуется температурочувствительностью и холодоадаптированностью. Реассортант унаследовал гены, кодирующие поверхностные антигены вируса гемагглютинин (НА) и нейраминидазу (NA), от эпидемического родительского вируса и шесть генов, кодирующих внутренние негликозилированные белки, от донора аттенуации. Штамм В/60/Брисбен/08/83 ареактогенен для взрослых и для детей при интраназальном введении. Вакцинный штамм вируса гриппа В/60/Брисбен/08/83 по показателям реактогенности соответствует требованиям, предъявляемым Фармакопейной статьей ФСП 42-0504-4097-04 к вакцинным штаммам для живой сухой гриппозной аллантоисной вакцины для интраназального применения. 4 табл.
Штамм вируса гриппа В/60/Брисбен/08/83, депонированный в ФГУН «Государственный НИИ стандартизации и контроля медицинских биологических препаратов имени Л.А.Тарасевича» Роспотребнадзора (ФГУН ГИСК им. Л.А.Тарасевича Роспотребнадзора) под №796, используемый для получения живой гриппозной интраназальной эпидемической вакцины для взрослых и для детей.
| ШТАММ ВИРУСА ГРИППА В/60/Джилин/03/1 ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЛЯ ДЕТЕЙ | 2005 |
|
RU2307161C2 |
| ШТАММ В/60/ПЕТЕРБУРГ/95/20 ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ И ДЕТЕЙ | 1997 |
|
RU2128224C1 |
| ШТАММ ВИРУСА INFLUENZA В (ЛЕНИНГРАД) 14/76/50, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ПОЛУЧЕНИЯ БЕЗВРЕДНЫХ И ВЫСОКОРЕПРОДУКТИВНЫХ ВИРУСОВ ГРИППА В ДЛЯ ПРОИЗВОДСТВА ИНАКТИВИРОВАННЫХ И ЖИВЫХ ГРИППОЗНЫХ ВАКЦИН | 1995 |
|
RU2105063C1 |
| ШТАММ ВИРУСА ГРИППА B (СЕМИПАЛАТИНСК) 151/91 ДЛЯ ПРИГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ ПРЕПАРАТОВ | 1992 |
|
RU2031118C1 |
Авторы
Даты
2011-06-27—Публикация
2010-01-28—Подача