Изобретение относится к медицинской вирусологии и может быть использовано в практическом здравоохранении для профилактики заболеваемости гриппом среди взрослых и детей с помощью живой гриппозной интраназальной вакцины из штамма вируса гриппа типа А, семейства Orthomyxoviridae, рода Influenzavirus А, А/17/Соломоновы острова/06/9 (H1N1).
В результате появления в циркуляции нового дрейфового варианта - вируса гриппа А/Соломоновы острова/03/2006 (H1N1), известный вакцинный штамм А/17/Новая Каледония/99/145 (H1N1)-прототип [Патент РФ №2183672 от 20.06.2002. - Опубл. БИ 2002. - №17] - утратил антигенную актуальность. Вследствие этого он не может вызвать защитную реакцию во время эпидемии, вызванной штаммами вируса гриппа, подобными А/Соломоновы острова/03/2006 (H1N1).
Задачей, на решение которой направлено заявляемое изобретение, является получение вакцинного штамма актуальной антигенной разновидности на основе современного эпидемического вируса А/Соломоновы острова/03/2006 (H1N1) для производства живой гриппозной вакцины. Вакцина должна быть пригодна для взрослых и для детей, то есть соответствовать нормативным требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей ФСП 42-0417-4097-03 на живую гриппозную вакцину для интраназального применения.
Целью изобретения было получение промышленно значимого и антигенно актуального реассортантного вакцинного штамма. Для его получения выбраны два родительских штамма вируса гриппа: эпидемический штамм вируса гриппа А/Соломоновы острова/03/2006 (H1N1) и безвредный для человека холодоадаптированный донор аттенуации А/Ленинград/134/17/57 (H2N2).
Применяемые в настоящее время штаммы для живых гриппозных вакцин получают методом генетической реассортации эпидемически актуальных вирусов с холодоадаптированными штаммами - донорами аттенуации [Александрова Г.И. Применение метода генетической рекомбинации для получения вакцинных штаммов вируса гриппа // Вопр. Вирусол - 1977 - №4 - С.387-395].
Донор аттенуации А/Ленинград/134/17/57 (H2N2) - холодоадаптированный (са) и температурочувствительный (ts) штамм вируса гриппа, разрешенный для получения безвредных живых интраназальных вакцин для взрослых и детей [Александрова Г.И. Новое в эпидемиологии и профилактике вирусных инфекций. Л., 1968 - С.66-83].
Донор аттенуации А/Ленинград/134/17/57 (H2N2), характеризующийся устаревшей антигенной структурой, был ранее получен из эпидемического вируса А/Ленинград/134/57 (H2N2) методом холодовой адаптации [Александрова Г.И., Климов А.И. Живая вакцина против гриппа. - СПб.: Наука - 1994 - 151 с.], в результате чего он стал безвредным для человека, т.е. приобрел способность бессимптомно размножаться в верхних дыхательных путях привитых лиц, вызывая выработку противовирусного иммунитета.
Целью реассортации является получение штамма с вакцинной формулой генома 6:2. Гены, кодирующие поверхностные белки вируса гриппа гемагглютинин (НА) и нейраминидазу (NA), наследуются от антигенно актуального циркулирующего эпидемического (пандемического) штамма, а шесть генов, кодирующих внутренние и неструктурные белки (PB2, PB1, PA, NP, M, NS) - от безвредного донора аттенуации.
На основе донора аттенуации А/Ленинград/134/17/57 (H2N2) и эпидемического штамма А/Новая Каледония/20/99 (H1N1) был создан вакцинный штамм А/17/Новая Каледония/99/145 (H1N1)-прототип. Работа с иным эпидемическим штаммом требует подбора оптимальных условий реассортации, иного числа пассажей при отборе клонов, оптимизации методики их отбора и оценки их фенотипических свойств.
Получение вакцинного штамма. Вакцинный штамм А/17/Соломоновы острова/06/9 (H1N1) получен методом генетической реассортации эпидемического вируса А/Соломоновы острова/03/2006 (H1N1) с донором аттенуации А/Ленинград/134/17/57 (H2N2) посредством одновременного инфицирования развивающихся куриных эмбрионов (РКЭ) смесью родительских вирусов в эквивалентных инфекционных дозах, с последующей селекцией клонов с заданными свойствами при пониженной до 25°C температуре инкубации в присутствии антисыворотки к донору аттенуации. Клоны дополнительно очищены трехкратным клонированием методом предельных разведений в присутствии антисыворотки к донору при пониженной (25°C) и оптимальной (32°C) температурах инкубации. Чистые клоны проверены по фенотипическим характеристикам (ts-, са-фенотип) и по формуле генома на соответствие вакцинному штамму.
Для анализа состава генома реассортантных клонов использовали следующие методы:
а) Реакцию торможения гемагглютинации (РТГА), позволяющую определить принадлежность поверхностного антигена - гемагглютинина (НА) одному из родительских вирусов [Методы определения показателей качества иммунобиологических препаратов для профилактики и диагностики гриппа. МУК 3.3.2.1758-03].
б) Метод рестрикционного анализа ДНК копий генов [Klimov A.I., Сох N.J. PCR restriction analysis of genome composition and stability of cold-adapted reassortant live influenza vaccines // J.Virol. Methods. - 1995 - Vol.52. - №1-2 - P.41-49], основанный на амплификации относительно коротких участков РНК длиной около 150-300 нуклеотидов, включающих уникальные нуклеотидные последовательности, характерные только для донора аттенуации А/Ленинград/134/17/57 (H2N2), но не для современных эпидемических вирусов гриппа. Обработку амплифицированных фрагментов ДНК производят специфическими рестриктазами с их последующим электрофорезом в 1,7%-ном агарозном геле, содержащем 0,5 мкг/мл этидиума бромида. Это позволяет четко дифференцировать принадлежность генов исследуемых реассортантных штаммов к эпидемическому вирусу или донору аттенуации.
Антигенная характеристика вакцинного штамма. Полученный нами вакцинный штамм А/17/Соломоновы острова/06/9 (H1N1) в РТГА идентичен эпидемическому вирусу А/Соломоновы острова/03/2006 (H1N1), антисывороткой к которому полностью нейтрализуется.
Рестрикционным методом установлено, что в вакцинном штамме А/17/Соломоновы острова/06/9 (H1N1) присутствуют оба гена, кодирующие поверхностные белки - гемагглютинин (НА) и нейраминидазу (NA) - от эпидемического вируса А/Соломоновы острова/03/2006 (H1N1).
Формула генома. Формула генома 6:2 вакцинного штамма А/17/Соломоновы острова/06/9(H1N1) подтверждена методом RT-PCR с помощью специфических праймеров. Вакцинный штамм А/17/Соломоновы острова/06/9 (H1N1) унаследовал все шесть генов, кодирующих внутренние белки (PB1, PB2, PA, NP, M, NS), от донора аттенуации А/Ленинград/134/17/57 (H2N2).
На чертеже в качестве примера представлена рестрикция ДНК-копии фрагмента гена NS эндонуклеазой Сас I. 1-я дорожка - ДНК маркер молекулярного веса IX; 2-я дорожка - эпидемический вирус А/Соломоновы острова/03/2006 (H1N1); 3-я дорожка - донор аттенуации А/Ленинград/134/17/57 (H2N2); 4-я дорожка - кандидат в вакцинные штаммы А/17/Соломоновы острова/06/9 (H1N1). В NS гене донора аттенуации А/Ленинград/134/17/57 (H2N2) в позиции нуклеотида 798 имеется замена G→A по сравнению с современными эпидемическими штаммами, приведшая к аминокислотной замене метионина эпидемических вирусов на изолейцин у донора аттенуации. Эпидемические вирусы имеют на этом участке сайт рестрикции для экзогенной рестриктазы Сас I. У донора аттенуации А/Ленинград/134/17/57 (H2N2) этот рестрикционный сайт отсутствует. Таким образом, обработка всех исследуемых фрагментов ДНК данным ферментом приводит к разрезанию участка гена NS на два более мелких фрагмента, если он происходит от эпидемического вируса. В случае NS гена донора аттенуации А/Ленинград/134/17/57 (H2N2) расщепления не происходит.
Результаты рестрикционного анализа всех генов вакцинного штамма А/17/Соломоновы острова/06/9 (H1N1) представлены в таблице 1.
Оценку фенотипических свойств вакцинного штамма А/17/Соломоновы острова/06/9 (H1N1) проводили путем его параллельного титрования в РКЭ при разных температурах. Было показано, что вакцинный вирус является температурочувствительным (разность в показателях инфекционной активности при температуре инкубации 32°C и 39°C составляет 7,5 lg ЭИД50/0,2 мл) и холодоадаптированным (разность в показателях инфекционной активности при температуре инкубации 32°C и 25°C равна 2,0 lg ЭИД50/0,2 мл), что свидетельствует о его безвредности для человека, поскольку по этим показателям он идентичен донору аттенуации А/Ленинград/134/17/57 (H2N2).
Оценку токсичности вакцинного штамма А/17/Соломоновы острова/06/9 (H1N1) определяли путем подкожного и внутрибрюшинного введения вирусного материала мышам. Для этого группе из 10 мышей (самцов линии СВА весом 18-20 граммов) вводили соответствующим способом 0,5 мл вируссодержащей аллантоисной жидкости с титром 8.0 lg ЭИД50/0.2 мл и оценивали патогенность вируса по проценту выживших мышей в течение 7 дней после введения вируса. Вакцинный штамм А/17/Соломоновы острова/06/9 (H1N1) в эксперименте на мышах оказался полностью безвредным - 100% мышей выжили в течение всего периода наблюдения.
В результате проведенных доклинических исследований установлено, что заявляемый вакцинный штамм живой гриппозной вакцины А/17/Соломоновы острова/06/9 (H1N1) характеризуется сочетанием полезных признаков, необходимых вакцинному штамму: антигенной специфичностью эпидемического вируса А/Соломоновы острова/03/2006 (H1N1), структурой генома 6:2, оптимальной для реассортантных вакцинных штаммов, а также характерной для донора аттенуации температурочувствительностью и холодоадаптированностью, что коррелирует с аттенуацией для человека. Штамм аттенуирован и безвреден для мышей.
Морфология штамма полиморфная, типичная для вируса гриппа.
Штамм А/17/Соломоновы острова/06/9 (H1N1) ареактогенен для взрослых и для детей при интраназальном введении.
Таким образом, вакцинный штамм А/17/Соломоновы острова/06/9 (H1N1) по биологическим свойствам и показателям реактогенности соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей ФСП 42-0417-4097-03 на живую гриппозную вакцину для интраназального применения.
Полученный штамм А/17/Соломоновы острова/06/9 (H1N1) депонирован в коллекции вирусов ФГУН «Государственный НИИ стандартизации и контроля медицинских биологических препаратов имени Л.А.Тарасевича» Роспотребнадзора (ФГУН ГИСК им. Л.А.Тарасевича Роспотребнадзора, Россия RU, 119002, город Москва, Сивцев-Вражек, дом 41) под №751 и имеет характеристики, представленные в паспорте штамма.
ПАСПОРТ ШТАММА
1. Название штамма А/17/Соломоновы острова/06/9 (H1N1).
2. Серия: серия 1 (первая).
3. Метод получения - реассортация; характеристика родительских вирусов:
а) эпидемический вирус: А/Соломоновы острова/03/2006 (H1N1).;
б) донор аттенуации:А/Ленинград/134/17/57 (H2N2).
4. Количество пассажей: 5 в процессе реассортации.
5. Характеристика штамма до лиофилизации:
а) оптимальные условия репродукции: 32°C, 48 часов;
б) гемагглютинирующая активность: 1:256;
в) инфекционная активность: 8.5 lg ЭИД50/0,2 мл;
г) чувствительность к ингибиторам: ингибитороустойчивый в РТГА с нормальной лошадиной сывороткой;
д) разность в показателях инфекционной активности при 32°C/39°C: 7.5 lg ЭИД50/0,2 мл;
е) разность в показателях инфекционной активности при 32°C/25°C: 2,0 lg ЭИД50/0,2 мл;
ж) структура генома реассортанта по данным рестрикционного анализа амплифицированных в RT-PCR фрагментов вирусных РНК:
гены от эпидемического вируса: HA, NA;
гены от донора аттенуации: PB2, PB1, PA, NP, M, NS.
6. Характеристика штамма после лиофилизации:
а) дата лиофилизации: 2 апреля 2007 г.;
б) объем материала в ампуле: 1,0 мл;
в) количество доз в ампуле: 4;
г) инфекционная активность: 8,0 lg ЭИД50/0.2 мл;
д) гемагглютинирующая активность: 1:128.
7. Рекомендуемое разведение при вакцинации: 1:2.
8. Антигенная специфичность гемагглютинина:
гемагглютинин в РТГА идентичен вирусу А/Соломоновы острова/03/2006 (H1N1), крысиной антисывороткой к которому полностью нейтрализуется.
9. Безвредность для мышей при подкожном и внутрибрюшинном введении: безвреден.
10. Бактериологический контроль: - стерилен.
11. Контроль на посторонние вирусы: посторонние вирусы отсутствуют.
ХАРАКТЕРИСТИКА ШТАММА
Инфекционная активность штамма А/17/Соломоновы острова/06/9 (H1N1) при репродукции в развивающихся куриных эмбрионах при 32°C в течение 48 часов - 8,5 lg ЭИД50/0,2 мл.
Гемагглютинирующая активность - 1:256.
Штамм проявляет генетическую стабильность аттенуирующих мутаций и биологических признаков после 5 пассажей на куриных эмбрионах (при использовании больших заражающих доз).
ОЦЕНКА РЕАКТОГЕННОСТИ ШТАММА А/17/СОЛОМОНОВЫ ОСТРОВА/06/9 (H1N1)
До 2004 года реассортантные вакцинные штаммы живой гриппозной вакцины для детей и для взрослых готовили на двух разных донорах аттенуации. Вакцинные штаммы живой гриппозной вакцины для взрослых готовили на доноре аттенуации А/Ленинград/134/17/57 (H2N2) [Александрова Г.И., Климов А.И. Живая вакцина против гриппа. - СПб.: Наука - 1994 - 151 с.], а вакцинные штаммы живой гриппозной вакцины для детей - на более аттенуированном доноре А/Ленинград/134/47/57 (H2N2) [Александрова Г.И., Климов А.И. Живая вакцина против гриппа. - СПб.: Наука - 1994-151 с.]. В 2003 году Комитет медицинских иммунобиологических препаратов счел целесообразным рекомендовать «Вакцину гриппозную аллантоисную интраназальную живую сухую для взрослых» для иммунизации детей в возрасте 3-6 лет с внесением соответствующих изменений в «Инструкцию по применению» препарата [Инструкция по применению вакцины гриппозной аллантоисной интраназальной живой сухой. Утверждена Главным санитарным врачом РФ Г.Г.Онищенко 16.06.2004]. В связи с этим нами проведена оценка реактогенности вакцинного штамма А/17/Соломоновы острова/06/9 (H1N1) на взрослых и детях.
ШТАММ А/17/СОЛОМОНОВЫ ОСТРОВА/06/9 (H1N1)
АРЕАКТОГЕНЕН ДЛЯ ВЗРОСЛЫХ ЛИЦ
Пример 1. При вакцинации 53 взрослых лиц интраназально реассортантным вакцинным штаммом А/17/Соломоновы острова/06/9 (H1N1) с инфекционной активностью 8,0 lg ЭИД50/0,2 мл в разведении 1:2 в объеме 0,5 мл сильных температурных реакций с повышением температуры свыше 38,6°C, средних температурных реакций с повышением температуры в диапазоне 37,6-38,5°C не наблюдалось. Были отмечены одна (1,89% случаев) температурная реакция слабой степени выраженности (до 37,1-37,2°C) и легкие катаральные явления продолжительностью менее 2-х дней у двух привитых (3,77% случаев).
В группе из 44 лиц, получившей плацебо, сильных и средних температурных реакций не наблюдалось. Как и в группе вакцинированных, была зарегистрирована одна слабая температурная реакция (2,27% случаев). Катаральные явления (насморк) отмечены у одного пациента (2,27% случаев). Результаты обследования приведены в таблице 2.
Показатель реактогенности (разница в проценте средних реакций у привитых вакциной и получивших плацебо) составил 0%.
ШТАММ А/17/СОЛОМОНОВЫ ОСТРОВА/06/9 (H1N1)
АРЕАКТОГЕНЕН ДЛЯ ДЕТЕЙ 3-14 ЛЕТ
Пример 2. Группу из 40 детей в возрасте 3-14 лет вакцинировали интраназально в объеме 0,5 мл реассортантным вакцинным штаммом А/17/Соломоновы острова/06/9 (H1N1) с инфекционной активностью 8,0 lg ЭИД50/мл в разведении 1:2. Результаты исследований приведены в таблице 3. Сильных температурных реакций с повышением температуры свыше 38,5°C, средних температурных реакций с повышением температуры в диапазоне 37,6-38,5°C и слабых температурных реакций (до 37,5°C) не отмечено. Легкие катаральные симптомы наблюдались у 3 детей (7,5% случаев). Показатель реактогенности составил 0%.
Испытания на волонтерах подтвердили, что вакцинный штамм А/17/Соломоновы острова/06/9 (H1N1) по показателям реактогенности соответствует требованиям, предъявляемым к вакцинным штаммам Фармакопейной статьей ФСП 42-0417-4097-03 на живую сухую гриппозную аллантоисную вакцину для интраназального применения.
Полезным свойством вакцинного штамма вируса гриппа А/17/Соломоновы острова/06/9 (H1N1) является его пригодность для наработки живой гриппозной вакцины. Предлагаемый по изобретению вакцинный штамм вируса гриппа А/17/Соломоновы острова/06/9 (H1N1) может быть использован для профилактики гриппа как у взрослых, так и у детей с трехлетнего возраста, что подтверждают результаты изучения его реактогенности для разных возрастных групп.
Изобретение относится к биотехнологии. Может быть использовано в практическом здравоохранении для профилактики заболеваемости сезонным гриппом среди взрослых и детей с помощью живой гриппозной интраназальной вакцины из штамма вируса гриппа А/Соломоновы острова/03/2006 (H1N1). Вакцинный штамм А/17/Соломоновы острова/06/9 (H1N1) - реассортант, полученный путем скрещивания эпидемического вируса А/Соломоновы острова/03/2006 (H1N1) с холодоадаптированным температурочувствительным вирусом А/Ленинград/134/17/57 (H2N2) - донором аттенуации, безвредным для людей. Вакцинный штамм А/17/Соломоновы острова/06/9 (H1N1) активно размножается в развивающихся куриных эмбрионах при оптимальной температуре 32°С, характеризуется температурочувствительностью и холодоадаптированностью. Реассортант унаследовал гены, кодирующие поверхностные антигены вируса гемагглютинин (НА) и нейраминидазу (NA) от эпидемического родительского вируса и остальные шесть генов, кодирующих внутренние негликозилированные белки, от донора аттенуации. Штамм А/17/Соломоновы острова/06/9 (H1N1) ареактогенен для взрослых и для детей при интраназальном введении. 1 ил., 3 табл.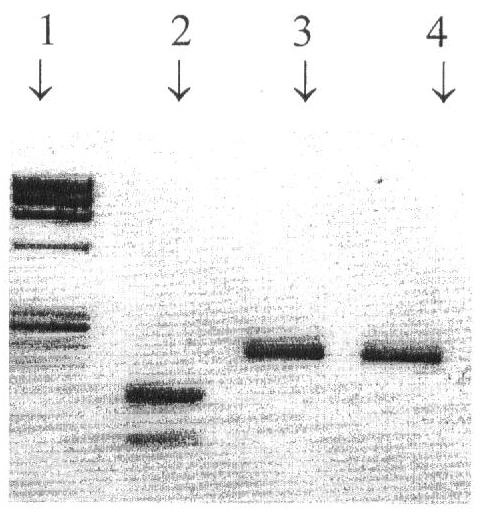
Штамм вируса гриппа А/17/Соломоновы острова/06/9 (H1N1), депонированный в ФГУН «Государственный НИИ стандартизации и контроля медицинских и биологических препаратов имени Л.А.Тарасевича» Роспотребнадзора (ФГУН ГИСК им. Л.А.Тарасевича Роспотребнадзора) под №751, используемый для получения живой гриппозной интраназальной вакцины для взрослых и для детей.
| ШТАММ ВИРУСА ГРИППА A/17/НОВАЯ КАЛЕДОНИЯ/99/145(H1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ | 2000 |
|
RU2183672C1 |
| ШТАММ ВИРУСА ГРИППА А/17/ПЕРТ/95/29 (Н1N1) ДЛЯ ПРОИЗВОДСТВА ЖИВОЙ ГРИППОЗНОЙ ИНТРАНАЗАЛЬНОЙ ВАКЦИНЫ ДЛЯ ВЗРОСЛЫХ | 1998 |
|
RU2144955C1 |
Авторы
Даты
2011-06-27—Публикация
2010-01-11—Подача