Предлагаемое изобретение относится к биотехнологии, иммунологии и генетической инженерии и может быть использовано при экспресс-идентификации всех штаммов, принадлежащих к видам Yersinia pestis и Yersinia pseudotuberculosis, их дифференциации друг от друга.
В настоящее время отсутствуют диагностические тест-системы, имеющие высокую степень достоверности для проведения идентификации штаммов возбудителей чумы и псевдотуберкулеза вообще, и в том числе антигенизмененных штаммов, выделенных от больных людей, животных и из объектов окружающей среды.
Известен способ идентификации возбудителя чумы (Н.В.Божко, С.А.Лебедева и др. «Изучение возможности конструирования чумного диагностикума для реакции коагглютинации на основе иммуноглобулинов к антигену «фракция V» и выяснение его диагностической ценности». Клиническая лабораторная диагностика, №7, 2006, стр.49) путем использования жидкого диагностикума на основе кроличьих иммуноглобулинов к фракции V, дающий возможность выявлять все штаммы чумного микроба, независимо от наличия или отсутствия капсульного антигена F1.
Однако недостаточно высокая чувствительность способа (108 м.к.) и наличие случаев перекрестной реакции у части штаммов Y.pestis и Y.pseudotuberculosis требуют его совершенствования, так как имеют недостаточную степень достоверности результата при идентификации штаммов. Известен способ экспресс-диагностики чумы в полимеразной цепной реакции (ПЦР) (см. «Ген Пест» ТУ 8895-005-0189), включающей праймеры, выявляющие фрагменты генов cafl и pla, расположенные на плазмидах чумного микроба, отвечающих за синтез фракции 1 и пестицина.
Применяемая тест-система предназначена исключительно для детекции типичных штаммов со специфическими плазмидами и не способна выявлять штаммы возбудителя чумы с атипичной структурой генома (в т.ч. с дефицитом плазмид или с дефектами отдельных плазмидных генов), что сужает ее диагностические возможности.
Наиболее близким к предлагаемому изобретению является способ идентификации бактерий рода Yersinia и дифференциация патогенных видов Yersinia pestis, Y.pseudotuberculosis и Y.enterocolitica (см. A.M.Стенкова, М.П.Исаев, В.А.Рассказов «Разработка многопраймеровой ПЦР для идентификации бактерий рода Yersinia и дифференциации патогенных видов Y.pestis, Y.pseudotuberculosis, Y.enterocolitica», журнал «Молекулярная генетика, микробиология и вирусология», М.: Медицина, №3, 2008, стр.18), заключающийся в том, что используют шесть различных праймеров, два из которых - родоспецифические, а четыре - видоспецифические.
Однако известный способ требует много времени и затрат, что повышает его стоимость и срок выполнения, а кроме того, диагностическая достоверность требует доработки на большом числе образцов, что в итоге позволяет сделать вывод о низкой эффективности способа.
Технической задачей предлагаемого изобретения является разработка нового эффективного способа, позволяющего с высокой степенью достоверности проводить идентификацию всех штаммов видов Y.pestis и Y.pseudotuberculosis.
Поставленная задача достигается тем, что в известном способе идентификации видов Yersinia pestis и Yersinia pseudotuberculosis путем обнаружения капсульного диагностического антигена F1 и поверхностного белка PFV в серологической реакции с исследуемой пробой и выделения ДНК из бактерий с последующим тестированием в ПЦР, исследуемую пробу изучают параллельно двумя методами, путем постановки реакции непрямой иммунофлуоресценции (НИМФ) и (ПЦР), причем НИМФ проводят с моноклональными антителами ВСКК (П-384Д и 434Д), последние взаимодействуют со специфическим для вида Y.pestis капсульным антигеном F1 или плазмидо-температуро-независимым поверхностным белком PFV, который имеется у всех штаммов Y.pestis и редких штаммов в R-форме Y. pseudotuberculosis, при этом по свечению бактерий определяют присутствие в пробе полноценных или бесфракционных бактерий Y. pestis или типичных и PFV-атипичных штаммов Y.pseudotuberculosis, а ПЦР выполняют с помощью двух пар праймеров: vlm33rev/ISfor1754 - специфических для вида Y. pestis и JS - специфических для вида Y.pseudotuberculosis, причем синтез специфических фрагментов ДНК, направленный парой праймеров vlm33rev/ISfor1754, подтверждает наличие в пробе штаммов возбудителя чумы, а синтез специфических фрагментов ДНК, направленный парой праймеров JS, подтверждает наличие в пробе ДНК штаммов возбудителя псевдотуберкулеза, причем полученные с первой парой праймеров результаты оценивают как положительные при наличии ампликонов в 400 п.н., а второй пары при наличии ампликонов в 223 п.н., идентификацию исследуемой пробы проводят путем совмещения результатов НИМФ и ПЦР с контрольными штаммами.
Способ осуществляется следующим образом.
Идентификацию штаммов видов Y.pestis и Y.pseudotuberculosis в исследуемой пробе проводят параллельно двумя приемами экспрессной диагностики, а именно:
- один представляет собой реакцию непрямой иммунофлуоресценции (НИМФ), (I метод);
- второй полимеразную реакции (ПЦР), (II метод).
Для осуществления НИМФ необходимы моноклональные антитела (МКА), продуцируемые гибридомами Г4-В8/Е5 (NN ВСКК(П) 384Д) и Г4-Е6/Н8(ВСКК (П)-434Д), последние получены в Ростовском научно-исследовательском противочумном институте и депонированы в Российской коллекции перевиваемых культур.
МКА, (продуцируемые гибридомой Г4-В8/Е5), видоспецифичны к капсульному антигену F1 возбудителя чумы, который продуцируется большинством, но не всеми штаммами чумного микроба, под контролем одной из его плазмид при 28-37°С.
МКА, (продуцируемые гибридомой Г4-Е6/Н8), специфичны к поверхностному белку чумного микроба (PFV), который синтезируется у всех штаммов Y.pestis независимо от температуры выращивания и плазмидного состава бактерий (входит в состав ранее описанного антигенного комплекса фракция V) и может включать бесфракционные штаммы, у которых при диагностике не обнаруживают F1, с помощью МКА (продуцируемые гибридомой Г4-В8/Н5). Кроме того, упомянутые МКА максимально сокращают перекрестную реактивность с Y.pseudotuberculosis до уровня редких единичных атипичных штаммов.
МЕТОД 1.
По инструкции для осуществления НИМФ на предметном стекле готовят парные мазки из взвеси исследуемых бактерий из имеющейся музейной культуры, или культуры из первичных посевов пробы, или из культуры, выделенной после экспериментального заражения животных взвесями исследуемых бактерий. Для обнаружения искомых бактерий в поле зрения при визуальном обследовании мазков необходимо содержание бактерий в исследуемой пробе не менее 106 м.к. Мазки высушивают на воздухе, фиксируют в течение 2 часов в 70% этиловом спирте, просушивают на воздухе и наносят на один мазок мышиные МКА к F1, на другой мазок мышиные МКА к PEV с титром 1:10, затем мазки выдерживают 1 час во влажной камере при 37°С, промывают ПБС буфером, затем наносят на мазки ФИТЦ против мышиных иммуноглобулинов в титре 1:16, снова выдерживают их во влажной камере 1 час при 37°С и промывают тем же буфером. Опять высушивают на воздухе, наносят минеральное масло и просматривают в люминесцентном микроскопе в поиске ярко светящихся бактерий (++++, +++) для большинства клеток или (+++) - для единичных, подтверждая наличие специфической реакции МКА с F1 и PFV. Свечение бактерий в мазках, обработанных МКА к F1 и МКА к PEV, свидетельствует о наличии бактерий Y.pestis, наличие свечения только в мазке, обработанном МКА к PEV при отсутствии свечения в мазке, обработанном МКА к F1, свидетельствует о наличии в мазке бактерий Y.pestis, не продуцирующих F1 или бактерий редких R-штаммов Y.pseudotuberculosis, отсутствие свечения в обоих мазках свидетельствует о наличии в них типичных бактерий Y.pseudotuberculosis или других бактерий. Для подтверждения этих результатов проводят метод II.
МЕТОД 2 (ПЦР)
Перед постановкой ПЦР проводят предварительную подготовку материала. Массу бактерий, сформировавших колонию или газон, в каждой из проб стерильной стеклянной палочкой перемещают в бактериологическую стеклянную пробирку, содержащую 200 мкл физиологического раствора, после чего выделяют ДНК как принято (Методические указания МУ 1.3.1794-03 «Организация работы при исследовании методом ПЦР материала, инфицированного микроорганизмами I и II группы патогенности» - М., 2003, - 38 с.).
Полученную тотальную ДНК исследуют в ПЦР парой праймеров, которые характеризуются как:
- vlm33for/ISrev1754 - праймеры, специфические для вида Y.pestis, направляющие синтез специфической последовательности (ампликона) длиной 400 пар нуклеотидов (п.н.);
- JS - праймеры, специфически реагирующие с ДНК Y.pseudotuberculosis, направляющие синтез специфической последовательности (ампликона) длиной 223 п.н.
Учет результатов проводят по каждой паре праймеров. Все результаты с использованными праймерами оцениваются как положительные при наличии в ПЦР ампликонов известной длины, а именно: JS - 223 п.н., vlm33for/ISrev 1754 - 400 п.н. Отрицательными считают результаты при отсутствии ампликонов или при их наличии, но с нехарактерным числом пар нуклеотидов.
Во время проведения этапов специфической индикации с целью определения штаммов возбудителя чумы можно применять праймеры в различных вариантах:
а) при идентификации по виду бактерий из отдельных колоний в посевах проб при положительных результатах НИМФ при проведении ПЦР используют две пары праймеров - vlm33for/ISrev1754 и JS отдельно;
б) при идентификации Y.pseudotuberculosis из отдельных колоний в посевах проб при отрицательных результатах НИМФ при проведении ПЦР используют только пару праймеров JS.
Анализ суммарных результатов НИМФ и ПЦР-тестирования проводят, руководствуясь таблицей 1.
Предлагаемое изобретение иллюстрируется примерами проведения идентификации и межвидовой дифференциации штаммов видов Yersinia pestis и Yersinia pseudotuberculosis.
Пример 1.
На исследование поступила культура, полученная после высева из органов белой мышки, зараженной материалом, подозрительным на наличие возбудителя чумы, из ее взвеси делают мазки на обезжиренном предметном стекле для НИМФ, часть оставшейся культуры обеззараживают и выделяют ДНК, как описано ранее для проведения ПЦР.
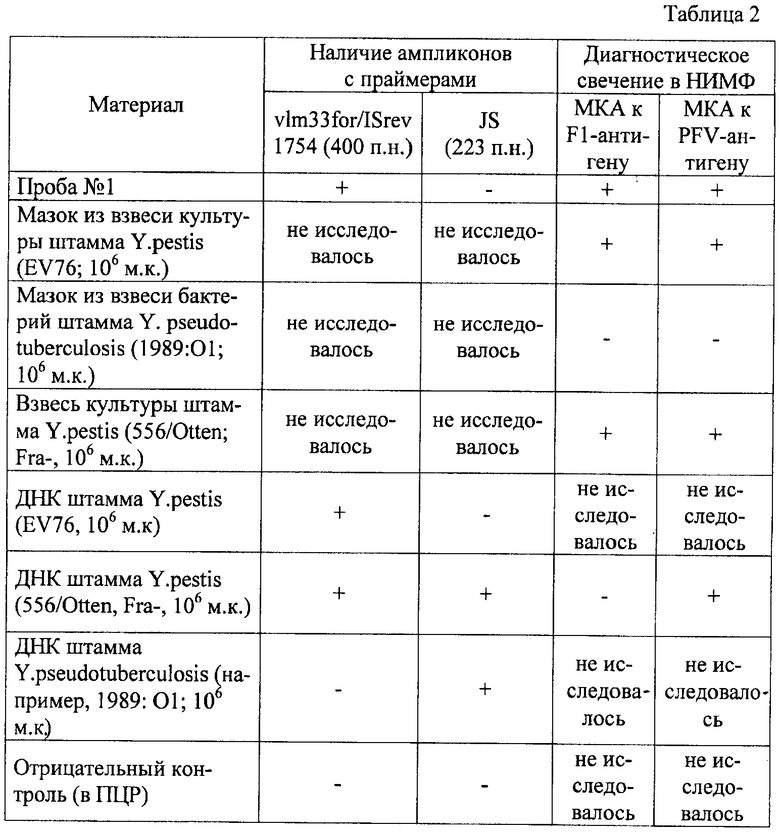
Затем первоначально мазки обеззараживают и исследуют в НИМФ, как описано выше, а с ДНК производят постановку ПЦР с праймерами: vlm33for/ISrev l754 и JS. Для каждой пары праймеров применяют отдельную пробирку. Реакция проходит в объеме 25 мкл реакционной смеси, содержащей 60 mM Трис HCl, рН 8,5, 25 mM KCl, 1,5 mM MgCl2, по 200 mkM каждого дНТФ, 0,1% ТритонХ-100, 10mM 2-меркаптоэтанол, 1 ед Taq-полимеразы и по 5 рмоль каждого праймера. Реакцию амплификации проводят в программируемом термостате «Терцик». Условия амплификации включали стадии денатурации, отжига и элонгации, как описано выше. Продукты амплификации анализируют в 2% агарозном геле. В качестве контролей используют: а) отрицательный контроль - в пробирки с реакционной смесью вносят по 5 мкл дистиллированой воды; б) положительный контроль в виде ДНК штамма возбудителя чумы Yersinia pestis EV76 - в пробирки с реакционной смесью вносят по 5 мкл выделенной ДНК; в) положительный контроль для праймеров, «узнающих» только последовательности возбудителя псевдотуберкулеза, - JS. В пробирки с реакционной смесью вносят по 5 мкл выделенной ДНК любого ранее идентифицированного штамма Yersinia pseudotuberculosis. Результаты идентификации представлены в таблице 2.
Таким образом, ПЦР и НИМФ показали, проба №1 содержит ДНК, взаимодействующую с vlm33for/ISrev1754, итогом чего стала амплификация специфических фрагментов (400 п.н.), характерных для возбудителя чумы, и содержит бактерии, на поверхности которых имеется специфический капсульный антиген F1, синтезируемый популяцией бактерий при 28°С и связанный с Fra-плазмидой, а также обязательный и специфический для чумного микроба белок (PFV), синтез которого не требует повышения температуры культивирования и характерных для возбудителя чумы плазмид. Это свидетельствовало о том (см. таблицу 1), что обнаруженные бактерии представляют штамм вида Y.pestis.
Пример 2.
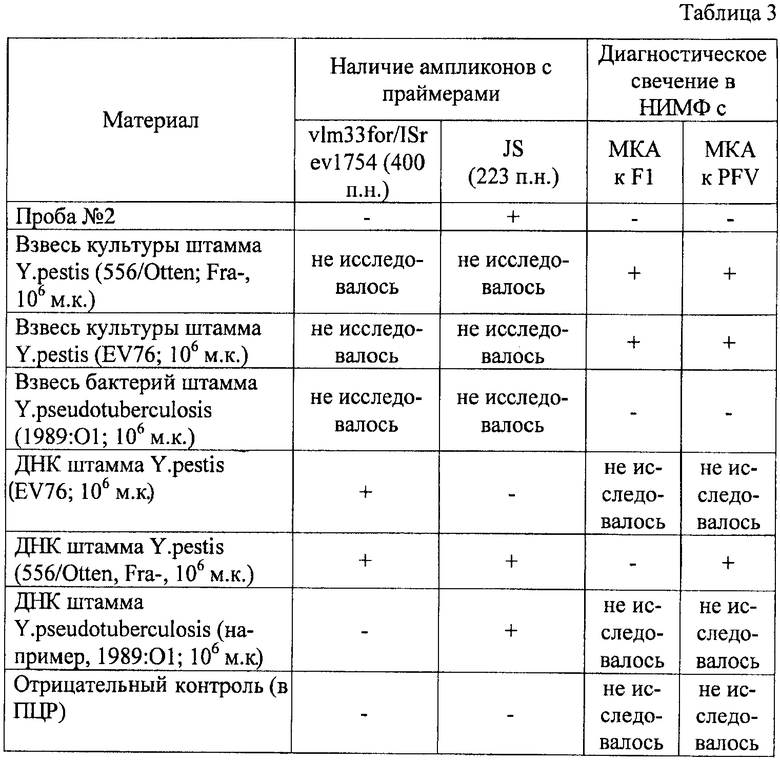
На исследование поступили колонии из посева на агаровую чашку крови больной крысы, подозрительной на заболевание чумой или псевдотуберкулезом. Из них сделана взвесь для приготовления мазков на обезжиренном предметном стекле для НИМФ, часть оставшейся культуры обеззаражена и выделена ДНК, как описано ранее для проведения ПЦР. Этапы постановки проб описаны в примере 1. Учет результатов приведен в таблице 3.
Таким образом, ПЦР и НИМФ показали, что проба №2 содержит ДНК, взаимодействующую с JS парой праймеров, итогом чего стала амплификация специфических фрагментов 223 п.н., характерных для возбудителя псевдотуберкулеза, и содержит бактерии, на поверхности которых нет специфического F1-антигена и обязательного для чумного микроба белка PFV, синтез которого не требует повышения температуры культивирования и характерных для возбудителя чумы плазмид. Это свидетельствует о том (см. таблицу 1), что выявленная ДНК и обнаруженные бактерии принадлежат виду Y.pseudotuberculosis.
Пример 3.
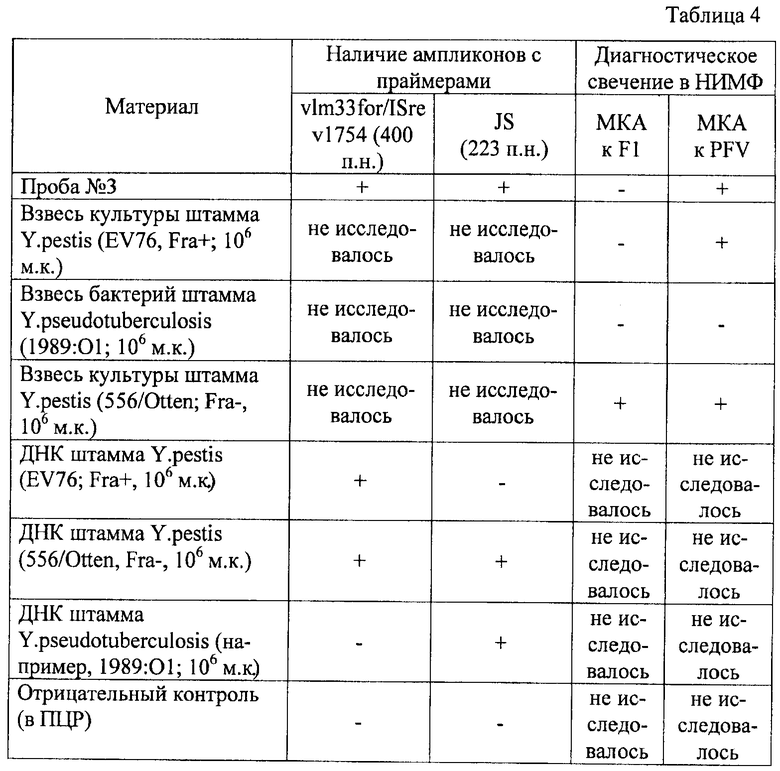
На исследование поступила культура неизвестного возбудителя (проба №3), выделенная из органов лесной мыши, труп которой обнаружен в одном из сельских районов. После приготовления взвеси и выделения ДНК, как это описано выше, выполнены НИМФ и ПЦР. Результаты приведены в таблице 4.
Таким образом, ПЦР и НИМФ показали, что проба №3 содержит ДНК, взаимодействующую с двумя парами праймеров vlm33for/ISrev1754 и JS, итогом чего стала амплификация специфических фрагментов 400 п.н. и 223 п.н., характерных соответственно для возбудителей чумы и псевдотуберкулеза, и содержит бактерии, на поверхности которых нет специфического F1-антигена, но есть обязательный для чумного микроба белок PFV, синтез которого не требует повышения температуры культивирования и плазмид, характерных для возбудителя чумы. Это свидетельствует о том (см. таблицу 1), что в пробе обнаружены бактерии, принадлежащие к двум видам - Y.pestis и Y.pseudotuberculosis, что имеет место при микс-инфекции. Проба нуждается в дополнительном исследовании по разделению бактерий двух видов специальными методами с последующим их исследованием предлагаемым способом.
Пример 4.
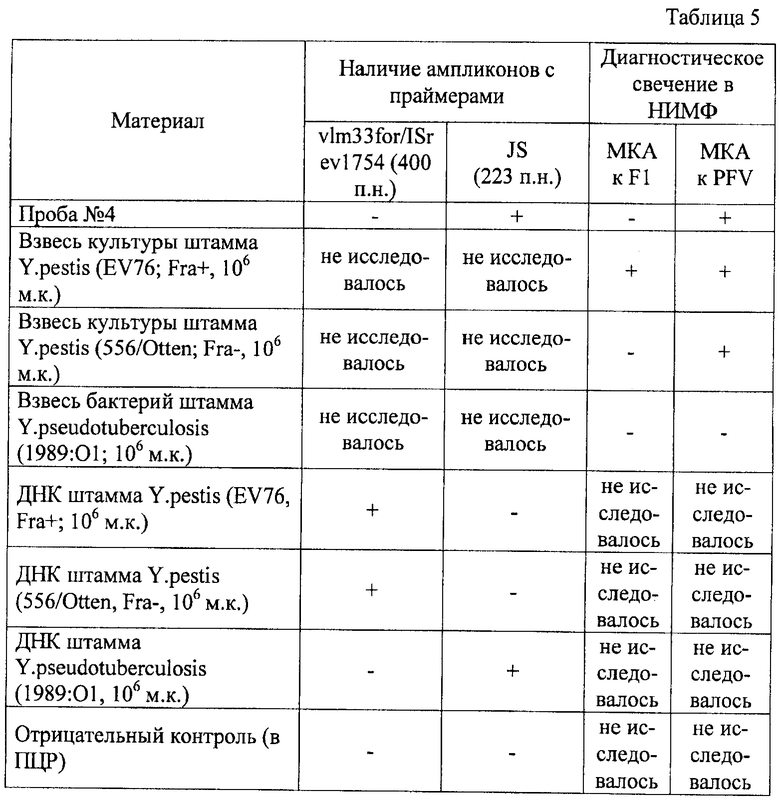
Из порта, принимающего корабли из длительных зарубежных рейсов, на исследование поступили крысы, выловленные с признаками инфекционного заражения. Из крыс высеяны однотипные чистые культуры возбудителя, которые не идентифицированы и обозначены как проба №4. После приготовления взвеси бактерий, а из нее мазков и ДНК были выполнены НИМФ и ПЦР. Результаты исследований представлены в таблице 5.
Таким образом, ПЦР и НИМФ показали, что проба №4 содержит ДНК, взаимодействующую с парой праймеров JS, итогом чего стала амплификация специфических фрагментов 223 п.н., характерных для возбудителя псевдотуберкулеза, и содержит бактерии, на поверхности которых нет специфического F1-антигена, но присутствует обязательный для чумного микроба белок PFV, синтез которого не требует повышения температуры культивирования и характерных для возбудителя чумы плазмид. Это свидетельствует о том (см. таблицу 1), что обнаруженные бактерии принадлежат виду Y.pseudotuberculosis и являются атипичными для этого вида по PFV-белку, имея определенное сходство с бактериями Y.pestis.
Пример 5.
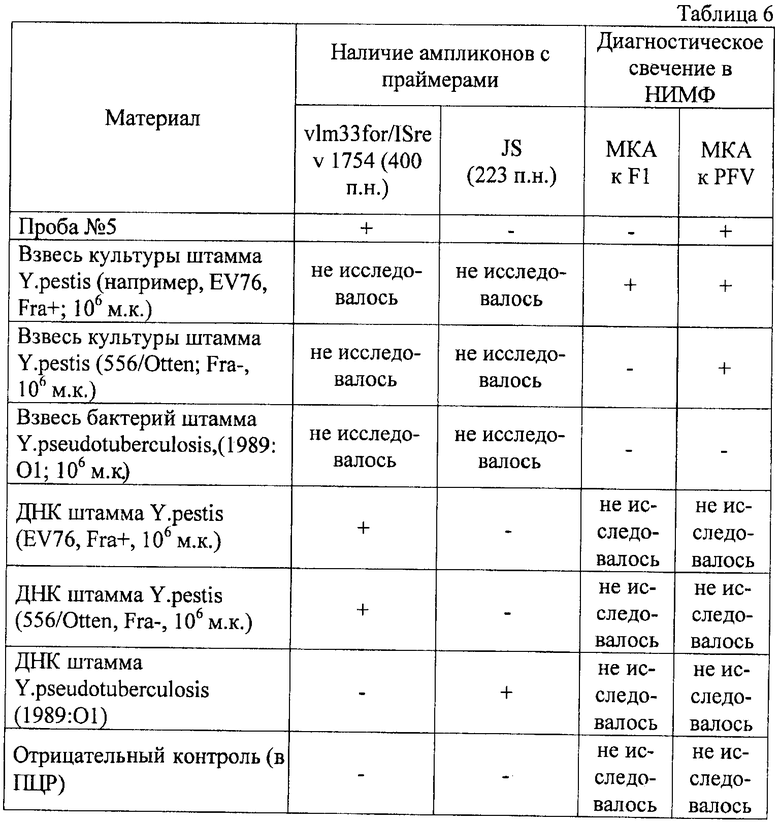
На исследование поступила культура возбудителя (проба 5), полученная из музея живых культур противочумного института, идентифицированная ранее как возбудитель псевдотуберкулеза, но имеющая некоторые свойства, похожие на Y.pestis. После приготовления из этой культуры взвеси, а из нее мазков и ДНК были выполнены НИМФ и ПЦР. Результаты исследования представлены в таблице 6.
Таким образом, ПЦР и НИМФ показали, что проба №5 содержит ДНК, взаимодействующую с парой праймеров, vlm33for/ISrev1754, итогом чего стала амплификация специфических фрагментов 400 п.н., характерных для возбудителя чумы, и содержит бактерии, на поверхности которых нет специфического F1-антигена, однако присутствует обязательный для чумного микроба белок PFV, синтез которого не требует повышения температуры культивирования и характерных для возбудителя чумы плазмид. Это свидетельствует о том (см. таблицу 1), что обнаруженные в пробе №5 бактерии принадлежат виду Y.pestis, но не способны продуцировать F1 антиген.
Пример 6.
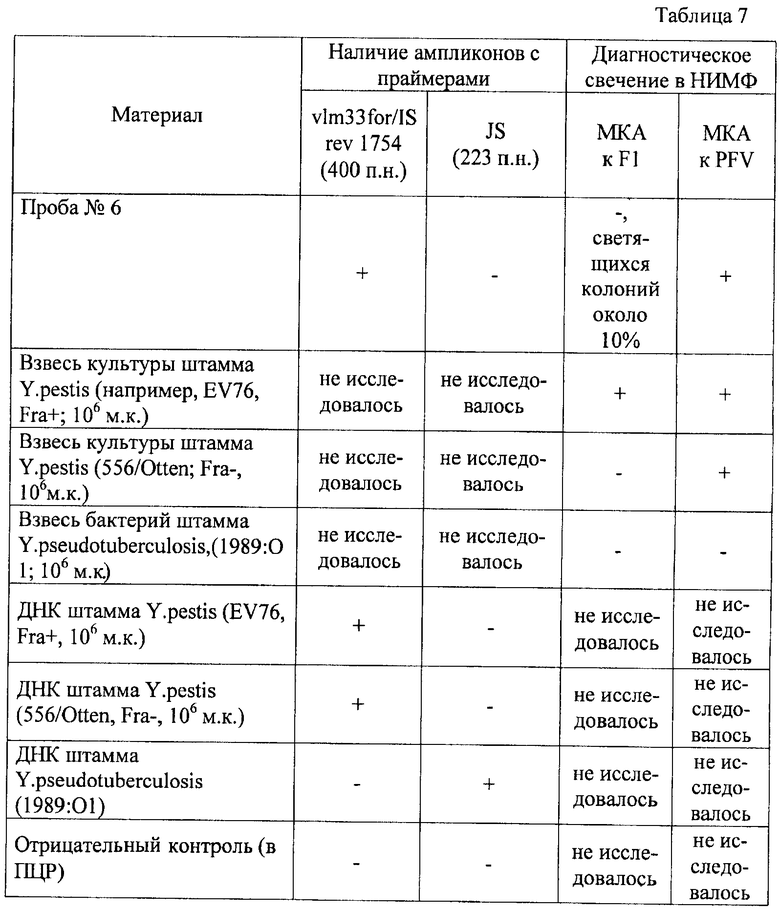
На исследование поступила культура возбудителя, полученная при 28°С после высева из органов белой мышки, зараженной материалом, подозрительным на наличие возбудителя чумы (проба №6). После приготовления взвеси и выделения ДНК были выполнены НИМФ и ПЦР. Результаты тестов представлены в таблице 7.
Таким образом, ПЦР и НИМФ показали, что проба №6 содержит ДНК, взаимодействующую с парой праймеров vlm33for/ISrev1754, итогом чего стала амплификация специфических фрагментов 400 п.н., характерных для возбудителя чумы, и содержит бактерии, на поверхности большинства из них нет специфического F1-антигена, который у этого штамма при 28°С или очень слабо продуцируется, или вообще не синтезируется, и только отдельные клетки продуцируют его, однако присутствует обязательный для чумного микроба белок PFV, синтез которого не требует повышения температуры культивирования и характерных для возбудителя чумы плазмид. Это свидетельствует о том (см. таблицу 1), что обнаруженные в пробе №6 бактерии принадлежат виду Y.pestis и являются атипичными, для этого вида по регуляции синтеза F1 антигена и с неоднородным составом по данному признаку.
Использование предложенного способа позволяет эффективно с высокой степенью достоверности проводить идентификацию двух иерсиний: Y.pestis и Y.pseudotuberculosis благодаря применению комплекса более специфических праймеров (JS, vlm33for/ISrev1754) в сочетании с НИМФ на специфический для чумного микроба F1-антиген и обязательный поверхностный антигенный белок PFV, синтез которого не зависит от температуры культивирования микроба, наличия в бактериях чумы характерных для вида Y.pestis плазмид, и который продуцируется всеми штаммами чумного микроба даже в отсутствие других диагностических антигенов, позволяет:
- с высокой степенью достоверности ускоренно проводить идентификацию бактерий штаммов видов Y.pestis и Y.pseudotuberculosis независимо от их сходства и формы изменчивости;
- ускоренно выявлять случаи смешанной инфекции двумя иерсиниями и факты циркуляции их в одном очаге;
- проводить экспресс-детекцию микс-культур Y.pestis и Y.pseudotuberculosis;
- обнаруживать штаммы Y.pestis с популяциями, которые отличаются по характеру терморегуляции F1-антигена и клеточному составу, необходимые для выяснения механизма температурозависимости синтеза этого антигена.
- выявлять редкие штаммы Y. pseudotuberculosis, способные продуцировать обязательный для Y.pestis PFV-антиген, и перспективные в качестве модели для изучения биологии и эволюции иерсиний.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ВИДОВОЙ ИДЕНТИФИКАЦИИ И ДИФФЕРЕНЦИАЦИИ ШТАММОВ Yersinia pseudotuberculosis ОТ Yersinia pestis И Yersinia enterocolitica | 2012 |
|
RU2486252C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ И ВНУТРИВИДОВОЙ ДИФФЕРЕНЦИАЦИИ ШТАММОВ ВИДА YERSINIA PESTIS | 2009 |
|
RU2404251C1 |
| СПОСОБ ДИФФЕРЕНЦИАЦИИ ШТАММОВ ВОЗБУДИТЕЛЯ ЧУМЫ ОСНОВНОГО И НЕОСНОВНЫХ ПОДВИДОВ И ВОЗБУДИТЕЛЯ ПСЕВДОТУБЕРКУЛЕЗА МЕТОДОМ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2010 |
|
RU2425891C1 |
| НАБОР И СПОСОБ ДЛЯ УСКОРЕННОЙ ИДЕНТИФИКАЦИИ ЧУМНОГО МИКРОБА С ОДНОВРЕМЕННОЙ ДИФФЕРЕНЦИАЦИЕЙ ВИРУЛЕНТНЫХ И АВИРУЛЕНТНЫХ ШТАММОВ Y.PESTIS, ОПРЕДЕЛЕНИЕМ ИХ ПЛАЗМИДНОГО ПРОФИЛЯ | 2011 |
|
RU2473701C1 |
| НАБОР РОДО- И ВИДОСПЕЦИФИЧНЫХ ОЛИГОНУКЛЕОТИДНЫХ ПРАЙМЕРОВ ДЛЯ ДЕТЕКЦИИ И ВИДОВОЙ ИДЕНТИФИКАЦИИ ИЕРСИНИЙ МЕТОДОМ МУЛЬТИПЛЕКСНОЙ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2006 |
|
RU2354700C2 |
| СПОСОБ ДИФФЕРЕНЦИАЦИИ БИОВАРОВ И ГЕНОВАРИАНТОВ ШТАММОВ Yersinia pestis ОСНОВНОГО ПОДВИДА С ПОМОЩЬЮ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2014 |
|
RU2565554C2 |
| ТЕСТ-ШТАММ YERSINIA PSEUDOTUBERCULOSIS ДЛЯ ДИФФЕРЕНЦИАЦИИ БАКТЕРИЙ YERSINIA PSEUDOTUBERCULOSIS ГЕНЕТИЧЕСКОЙ ГРУППЫ I | 2011 |
|
RU2465319C1 |
| ТЕСТ-ШТАММ YERSINIA PSEUDOTUBERCULOSIS ДЛЯ ДИФФЕРЕНЦИАЦИИ БАКТЕРИЙ YERSINIA PSEUDOTUBERCULOSIS ГЕНЕТИЧЕСКОЙ ГРУППЫ II | 2011 |
|
RU2465317C1 |
| СПОСОБ ПОДВИДОВОЙ ДИФФЕРЕНЦИАЦИИ ШТАММОВ ВОЗБУДИТЕЛЯ ЧУМЫ МЕТОДОМ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 2014 |
|
RU2552611C2 |
| ТЕСТ-ШТАММ YERSINIA PSEUDOTUBERCULOSIS ДЛЯ ДИФФЕРЕНЦИАЦИИ БАКТЕРИЙ YERSINIA PSEUDOTUBERCULOSIS ГЕНЕТИЧЕСКОЙ ГРУППЫ I | 2011 |
|
RU2465321C1 |
Сущность изобретения заключается в том, что исследуемую пробу изучают параллельно двумя способами: первый - в реакции непрямой иммунофлюоресценции (НИМФ), а второй - в полимеразной цепной реакции (ПЦР), причем НИМФ проводят с моноклональными антителами ВСКК (П-384Д и 434Д). Антитела взаимодействуют со специфическим для вида Y.pestis капсульным антигеном F1 или плазмидо-температуро-независимым поверхостным белком PFV, который имеется у всех штаммов Y.pestis и редких штаммов в R-форме Y. pseudotuberculosis. По свечению бактерий определяют присутствие в пробе полноценных или «бесфракционных» бактерий Y.pestis или типичных и PFV-атипичных штаммов Y.pseudotuberculosis. ПЦР выполняют с помощью двух пар праймеров «vlm33for/ISrevl754» - специфичных для вида Y.pestis и «JS» - специфичных для вида Y.pseudotuberculosis. Полученные с первой парой праймеров результаты оценивают как положительные при наличии ампликонов в 400 п.н., а второй пары - при наличии ампликонов в 223 п.н., идентификацию исследуемой пробы проводят путем совмещения результатов НИМФ и ПЦР с контрольными штаммами. Способ обеспечивает экспресс-идентификацию всех штаммов, принадлежащих к видам Y.pestis и Y.pseudotuberculosis, и их дифференциацию с высокой степенью достоверности. 8 табл.
Способ идентификации штаммов видов Y.pestis и Y.pseudotuberculosis путем обнаружения капсульного диагностического антигена FI и поверхностного антигенного белка PFV в серологической реакции с исследуемой пробой и выделения ДНК из бактерий с последующим тестированием в ПЦР, отличающийся тем, что исследуемую пробу изучают параллельно двумя методами путем постановки реакции непрямой иммунофлюоресценции (НИМФ) и ПЦР, причем НИМФ проводят с моноклональными антителами ВСКК (П-384Д и 434Д), последние взаимодействуют со специфическим для вида Y.pestis капсульным антигеном FI или плазмидо-температуро-независимым поверхностным белком PFV, который имеется у всех штаммов Y.pestis и редких штаммов в R-форме Y.pseudotuberculosis, при этом по свечению бактерий определяют присутствие в пробе полноценных или бесфракционных бактерий Y.pestis или типичных и PFV-атипичных штаммов Y.pseudotuberculosis, а ПЦР выполняют с помощью 2 пар праймеров: vlm33for/ISrevl754 - специфичных для вида Y.pestis и JS - специфичных для вида Y.pseudotuberculosis, причем синтез специфических фрагментов ДНК, направленный парой праймеров vlm33for/ISrevl754, подтверждает наличие в пробе штаммов возбудителя чумы, а синтез специфических фрагментов ДНК, направленный парой праймеров JS, подтверждает наличие в пробе штаммов возбудителя псевдотуберкулеза, причем полученные с первой парой праймеров результаты оценивают как положительные при наличии ампликонов в 400 п.н., а второй пары при наличии ампликонов в 223 п.н., идентификацию исследуемой пробы проводят путем совмещения результатов НИМФ и ПЦР с контрольными штаммами.
| СТЕНКОВА А.Н | |||
| с соавт | |||
| Разработка многопраймеровой ПЦР для идентификации бактерий рода Yersinia и дифференциации патогенных видов Y.pestis, Y.pseudotuberculosis, Y.enterocolitica | |||
| Молекулярная генетика, микробиология и вирусология | |||
| - М.: Мед., №3, 2008, с.18 | |||
| WO 2004106553 А2, 09.12.2004 | |||
| US 5654144 В, 05.08.1997 | |||
| СПОСОБ ПОДГОТОВКИ ПРОБ ДЛЯ ДИАГНОСТИКИ ПСЕВДОТУБЕРКУЛЕЗА МЕТОДОМ ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ | 1999 |
|
RU2153671C1 |
| СПОСОБ ДИАГНОСТИКИ ПСЕВДОТУБЕРКУЛЕЗА | 1998 |
|
RU2153172C1 |
| СПОСОБ ДИАГНОСТИКИ ИЕРСИНИОЗА | 1990 |
|
RU2008684C1 |
Авторы
Даты
2011-06-27—Публикация
2010-01-11—Подача