Область техники
Настоящее изобретение касается структуры ядро-оболочка, способа ее получения и катализатора очистки выхлопных газов, содержащего структуру ядро-оболочка.
Уровень техники
Трехмаршрутные катализаторы, которые одновременно осуществляют окисление моноксида углерода (СО) и углеводородов (УВ) и восстановление оксидов азота (NОх), используются в предшествующем уровне техники в качестве катализаторов очистки выхлопных газов для автомобилей. Такие катализаторы, которые широко известны, включают в себя катализаторы, содержащие благородные металлы, такие как платина (Pt), родий (Rh) или палладий (Pd), нанесенные на пористые оксидные носители, такие как оксид алюминия (Al2O3). Чтобы трехмаршрутный катализатор одновременно и эффективно выполнял очистку от трех компонентов СО, УВ и NОх, важно, чтобы отношение воздух/топливо (В/Т отношение), подаваемое в двигатель автомобиля, поддерживалось вблизи теоретического отношения воздух/топливо (стехиометрическое отношение).
Однако так как действительное отношение воздух/топливо колеблется вокруг стехиометрического значения от богатого (богатая топливом атмосфера) состояния до бедного (бедная топливом атмосфера) состояния в зависимости от условий езды автомобиля, а также других факторов, атмосфера выхлопных газов также колеблется от богатого состояния до бедного состояния. Следовательно, не всегда возможно обеспечить высокую производительность очистки только с трехмаршрутным катализатором. Чтобы поглощать колебания концентрации кислорода в выхлопном газе, чтобы увеличить мощность очистки выхлопного газа трехмаршрутными катализаторами, в катализаторах очистки выхлопных газов стали применять такие материалы, как оксид церия (СеО2), которые имеют определенную емкость сохраняемого кислорода (ЕСК), которая позволяет им сохранять кислород, когда выхлопной газ имеет высокую концентрацию кислорода, и высвобождать кислород, когда выхлопной газ имеет низкую концентрацию кислорода.
Чтобы предотвратить спекание благородных металлов, действующих в качестве активных частиц в таких катализаторах очистки выхлопных газов, даже когда они используются при высоких температурах (например, около 1000°С), важно сохранять благородные металлы в высокодисперсном состоянии в виде тонких частиц на носителе. В целом, известно, что редкоземельные оксиды имеют сильное сродство к нанесенным на них благородным металлам, и поэтому предотвращают спекание благородных металлов. Однако редкоземельные оксиды, такие как оксид церия, имеют низкую термостойкость и сами подвергаются спеканию при высоких температурах 1000°С и выше, и в результате благородные металлы, нанесенные на такие редкоземельные оксиды, также подвергаются спеканию. Для таких катализаторов очистки выхлопных газов, следовательно, нужно улучшать термостойкость самих редкоземельных оксидов, таких как оксид церия.
Японская нерассмотренная патентная публикация № 2005-313024 (патентный документ 1) описывает катализатор очистки выхлопных газов, отличающийся тем, что он представляет собой катализатор с благородным металлом, нанесенным на мелкозернистый носитель, причем данный мелкозернистый носитель содержит центральную секцию, образованную, главным образом, из оксида циркония (ZrO2), и оболочечную секцию, образованную, главным образом, из оксида церия (СеО2), и содержание СеО2 в мелкозернистом носителе составляет от 40 до 65 мол.%, и констатирует, что данный катализатор одновременно имеет улучшенную термостойкость благодаря ZrO2 и пониженное спекание благородных металлов благодаря СеО2.
Также японская нерассмотренная патентная публикация № 2005-254047 (патентный документ 2) описывает катализатор очистки выхлопных газов, который содержит металлоксидные частицы, содержащие оксид церия, и оксид алюминия и/или оксид кремния, и благородный металл, нанесенный на данные металлоксидные частицы, где металлоксидные частицы имеют центральную секцию с большим суммарным мольным содержанием оксида алюминия и оксида кремния, чем мольное содержание оксида церия, и поверхностный слой с большим числом молей оксида церия, чем общее число молей оксида алюминия и оксида кремния, и данная публикация констатирует, что этот катализатор имеет улучшенную термостойкость для катализатора очистки выхлопных газов с ЕСК от оксида церия благодаря центральной секции, которая обогащена оксидом алюминия и/или оксидом кремния.
Японская нерассмотренная патентная публикация № 2005-314134 (патентный документ 3) описывает металлоксидные частицы, имеющие центральную секцию, содержащую относительно большое количество твердого раствора оксидов церия-циркония, и оболочечную секцию, содержащую относительно большое количество второго оксида металла, содержащего оксид церия или оксид циркония, и констатирует, что использование оксида церия в качестве второго оксида металла может обеспечить ЕСК благодаря твердому раствору оксидов церия-циркония в центральной секции, в то же время предотвращая спекание благородного металла с помощью оксида церия в оболочечной секции.
Японская нерассмотренная патентная публикация № 2005-313028 (патентный документ 4) описывает катализатор очистки выхлопных газов, содержащий родий, нанесенный на металлоксидные частицы, где металлоксидные частицы содержат центральную секцию, содержащую относительно большое количество оксида церия, и оболочечную секцию, содержащую относительно большое количество оксида циркония, и констатирует, что данный катализатор демонстрирует ЕСК с помощью оксида церия в центральной секции и высокую термостойкость с помощью оксида циркония в оболочечной секции.
Наконец, японская нерассмотренная патентная публикация НЕI № 2005-313028 (патентный документ 5) описывает способ получения наноразмерных монодисперсных частиц редкоземельного оксида и ультратонких частиц смешанного оксида, где водные растворы, содержащие различные растворенные редкоземельные ионы и осаждающий агент, растворенный аналогичным образом, смешиваются и реагируют, причем центром реакции являются внутренности обратных мицелл, образованных с поверхностно-активным веществом, в неполярном органическом растворителе, и констатирует, что данный способ позволяет получать монодисперсные ультратонкие частицы оксидов редких земель и ультратонкие частицы смешанных оксидов с очень маленькими средними размерами частиц без применения высокотемпературного процесса с высоким давлением.
В патентных документах 1-4 золи оксидов металлов, которые должны формировать центральную секцию и оболочечную секцию, последовательно агрегируют, используя различие их изоэлектрических точек, получая структуру ядро-оболочка, содержащую центральную секцию, образованную, главным образом, из первого оксида металла, и оболочечную секцию, образованную, главным образом, из второго оксида металла. Однако структуры ядро-оболочка, получаемые с помощью таких способов, не позволяют легко регулировать толщину оболочечной секции на наноуровне, и, таким образом, существует необходимость в улучшении, чтобы достичь эффекта увеличения термостойкости структуры ядро-оболочка, приходящей от оксидов металлов, образующих центральные секции.
Хотя патентный документ 5 описывает получение наноразмерных монодисперсных частиц редкоземельного оксида и ультратонких частиц смешанного оксида с помощью способа с обратными мицеллами, он не упоминает и не предполагает получения частиц смешанного оксида со структурой ядро-оболочка.
Следовательно, задачей настоящего изобретения является обеспечить структуру ядро-оболочка, имеющую регулируемую толщину оболочечной секции на наноуровне, и, следовательно, улучшенные свойства и особенно термостойкость, происходящую от материала центральной секции, а также способ ее получения.
Другой задачей данного изобретения является обеспечить катализатор очистки выхлопных газов, который содержит данную структуру ядро-оболочка.
Описание изобретения
Изобретение, которое решает вышеуказанные задачи, представляет собой следующее.
(1) Структура ядро-оболочка, отличающаяся наличием центральной секции, образованной, главным образом, из первого оксида металла, и оболочечной секции, образованной, главным образом, из второго оксида металла, отличного от первого оксида металла, где толщина оболочечной секции не превышает 20 нм.
(2) Структура ядро-оболочка согласно пункту (1) выше, отличающаяся тем, что первый оксид металла выбирают из группы, состоящей из оксида циркония, оксида алюминия, оксида кремния, оксида титана и их комбинаций.
(3) Структура ядро-оболочка согласно пункту (1) или (2) выше, отличающаяся тем, что второй оксид металла выбирают из группы, состоящей из редкоземельных оксидов или комбинаций двух или более редкоземельных оксидов.
(4) Способ получения структуры ядро-оболочка, отличающийся наличием (а) этапа смешивания органического растворителя, содержащего поверхностно-активное вещество, с водным раствором, содержащим предшественник первого оксида металла, с образованием обратных мицелл, которые содержат внутри себя водный раствор, содержащий предшественник первого оксида металла, (b) этапа введения основного водного раствора внутрь обратных мицелл с образованием гидроксида предшественника первого оксида металла, (с) этапа обработки полученного гидроксида водным раствором, содержащим соединение с, по меньшей мере, двумя карбоксильными группами, чтобы связать данный гидроксид с, по меньшей мере, одной карбоксильной группой, (d) этапа добавления водного раствора, содержащего предшественник второго оксида металла, отличного от предшественника первого оксида металла, к обработанному гидроксиду, чтобы связать предшественник второго оксида металла с, по меньшей мере, одной из оставшихся карбоксильных групп данного соединения с, по меньшей мере, двумя карбоксильными группами, (е) этапа введения основного водного раствора в обратные мицеллы этапа (d) с образованием осадка и (f) этапа сушки и прокаливания данного осадка.
(5) Способ согласно пункту (4) выше, отличающийся тем, что мольное отношение элементов металлов М1 и М2 (М2/М1), образующих предшественник первого оксида металла и предшественник второго оксида металла, больше чем 0,2 и меньше чем 2,0.
(6) Способ согласно пункту (4) или (5) выше, отличающийся тем, что данное соединение с, по меньшей мере, двумя карбоксильными группами выбирают из группы, состоящей из щавелевой кислоты, малоновой кислоты, янтарной кислоты, глутаровой кислоты, адипиновой кислоты, пимелиновой кислоты, гемимеллитовой кислоты, тримезиновой кислоты и меллофановой кислоты.
(7) Катализатор очистки выхлопных газов, содержащий структуру ядро-оболочка согласно любому из пунктов (1)-(3) выше или структуру ядро-оболочка, полученную с помощью способа согласно любому из пунктов (4)-(6) выше.
Согласно структуре ядро-оболочка данного изобретения можно регулировать толщину оболочечной секции на наноуровне и, следовательно, заметно улучшать свойства, особенно термостойкость, приносимые материалом центральной секции. Кроме того, так как оксид циркония используется в качестве материала центральной секции и оксид церия используется в качестве материала оболочечной секции, катализатор очистки выхлопных газов с нанесенным благородным металлом в качестве каталитически активных частиц не только имеет улучшенную термостойкость структуры ядро-оболочка благодаря сильному сродству оксида церия к благородным металлам, но может также ограничивать спекание благородного металла в условиях применения высокой температуры и, следовательно, имеет заметно улучшенную каталитическую активность.
Краткое описание чертежей
Фиг.1 представляет собой схематичное изображение разреза структуры ядро-оболочка согласно данному изобретению.
Фиг.2(а) представляет собой ПЭМ фотографию, показывающую агрегат, полученный путем агрегирования множества структур ядро-оболочка, приготовленных в примере 1.
Фиг.2(b) представляет собой увеличенную ПЭМ фотографию, показывающую края агрегата, показанного на фиг.2(а).
Фиг.3 представляет собой ПЭМ фотографию, показывающую агрегат, полученный путем агрегирования множества структур ядро-оболочка, приготовленных согласно предшествующему уровню техники.
Лучший вариант осуществления данного изобретения
Настоящее изобретение будет теперь объяснено более подробно в отношении структуры ядро-оболочка, образованной из двух или более разных оксидов металлов, используемой для катализаторов очистки выхлопных газов, и способа ее получения, но данное изобретение не ограничивается данным конкретным применением и, не нуждаясь в упоминании, может использоваться для любого из широкого диапазона применений, которые содержат структуру ядро-оболочка, образованную из двух или более разных оксидов металлов.
Структура ядро-оболочка данного изобретения отличается наличием центральной секции, образованной, главным образом, из первого оксида металла, и оболочечной секции, образованной, главным образом, из второго оксида металла, отличного от первого оксида металла, где толщина оболочечной секции не превышает 20 нм.
Фиг.1 представляет собой схематичное изображение разреза структуры ядро-оболочка согласно данному изобретению. Структура ядро-оболочка 1 данного изобретения содержит центральную секцию 2, образованную, главным образом, из первого оксида металла, и оболочечную секцию 3, образованную, главным образом, из второго оксида металла, отличного от первого оксида металла.
Согласно данному изобретению нет особых ограничений на первый оксид металла, образующий центральную секцию структуры ядро-оболочка, и любой оксид металла, обычно применяемый в каталитических носителях или материалах поглощения/выделения кислорода, может быть использован. В качестве предпочтительных примеров первого оксида металла можно упомянуть оксид циркония, оксид алюминия, оксид кремния, оксид титана и их смеси. Эти оксиды металлов имеют высокую термостойкость и, следовательно, при использовании в качестве материалов, образующих центральные секции согласно данному изобретению, они заметно улучшают термостойкость структуры ядро-оболочка. Содержание первого оксида металла в центральной секции предпочтительно составляет 50 мол.% или больше.
Согласно данному изобретению оксид циркония наиболее предпочтительно использовать в качестве первого оксида металла.
Центральная секция структуры ядро-оболочка данного изобретения может дополнительно содержать оксид металла, который отличается от первого оксида металла, в добавление к первому оксиду металла. Например, центральная секция может дополнительно содержать оксид одного или нескольких металлов, выбранных из группы, состоящей из щелочноземельных металлов и редкоземельных элементов. Путем добавления таких дополнительных оксидов металлов можно дополнительно увеличить термостойкость структуры ядро-оболочка данного изобретения. В качестве конкретных примеров дополнительных оксидов металлов можно упомянуть оксид лантана (La2O3), оксид церия (СеО2), оксид празеодима (Pr6O11), оксид иттрия (Y2О3), оксид неодима (Nd2O3) и их комбинации, причем оксид лантана является особенно предпочтительным согласно данному изобретению.
Согласно данному изобретению нет особых ограничений для второго оксида металла, образующего оболочечную секцию структуры ядро-оболочка, и любой оксид металла, обычно применяемый в каталитических носителях или материалах поглощения/выделения кислорода, может быть использован. В качестве предпочтительных примеров второго оксида металла можно упомянуть редкоземельные оксиды и комбинации двух или более редкоземельных оксидов. Эти оксиды металлов имеют сильное сродство к благородным металлам, и, следовательно, при использовании в качестве материалов для оболочечной секции согласно данному изобретению они могут предохранять нанесенные на них благородные металлы от спекания при высокой температуре. Содержание второго оксида металла в оболочечной секции предпочтительно составляет 20 мол.% или больше.
Согласно данному изобретению оксид церия наиболее предпочтительно использовать в качестве второго оксида металла.
Также согласно данному изобретению толщина оболочечной секции предпочтительно не превышает 20 нм.
Путем ограничения толщины оболочечной секции до не больше чем 20 нм можно заметно улучшать термостойкость структуры ядро-оболочка и, следовательно, предотвращать термическое спекание второго оксида металла в оболочечной секции и, таким образом, сохранять высокую площадь поверхности структуры ядро-оболочка. Кроме того, так как редкоземельный оксид, такой как оксид церия, используется в качестве второго оксида металла, и такие редкоземельные оксиды имеют высокое сродство к благородным металлам в катализаторах с нанесенными благородными металлами в качестве каталитически активных частиц, можно минимизировать спекание благородного металла при применении условий высокой температуры и, следовательно, заметно улучшать активность катализатора. Если толщина оболочечной секции превышает 20 нм, термостойкость структуры ядро-оболочка будет снижаться, и второй оксид металла, образующий оболочечную секцию, будет агрегироваться, приводя к меньшей площади поверхности структуры ядро-оболочка, и, следовательно, толщина оболочечной секции предпочтительно составляет не больше чем 20 нм и еще более предпочтительно не больше чем 10 нм. С другой стороны, толщина оболочечной секции предпочтительно составляет, по меньшей мере, 3 нм, чтобы предотвратить спекание благородного металла.
Размер частиц структуры ядро-оболочка данного изобретения предпочтительно составляет 10-100 нм.
Структура ядро-оболочка данного изобретения, которая содержит центральную секцию, образованную, главным образом, из первого оксида металла, и оболочечную секцию, образованную, главным образом, из второго оксида металла, отличного от первого оксида металла, может быть приготовлена, используя способ с обратными мицеллами.
В структурах ядро-оболочка, полученных с помощью обычных способов, а именно структурах ядро-оболочка, полученных путем изменения рН смешанного золя, содержащего золь первого оксида металла и золь второго оксида металла, которые имеют разные изоэлектрические точки, чтобы последовательно агрегировать оксиды металлов, можно формировать оболочечные секции с толщиной на микроуровне, но трудно формировать оболочечные секции с толщиной на наноуровне. Следовательно, эффекты, получаемые от первого оксида металла, образующего центральную секцию, такие как эффекты улучшенной термостойкости, часто не демонстрируются в достаточной степени в структурах ядро-оболочка. Такие способы требуют, чтобы первый оксид металла и второй оксид металла имели разные изоэлектрические точки, и, следовательно, не могут легко применяться, когда изоэлектрические точки оксидов металлов одинаковы или очень близки.
Согласно способу данного изобретения можно снижать толщину оболочечной секции до наноуровня путем приготовления с использованием способа обратных мицелл и, таким образом, заметно улучшать свойства и особенно термостойкость полученной структуры ядро-оболочка. Также согласно данному изобретению, в отличие от обычного способа, структура ядро-оболочка, образованная из первого оксида металла и второго оксида металла, может быть приготовлена безотносительно к изоэлектрическим точкам оксидов металлов, образующих центральную секцию и оболочечную секцию, так что могут быть получены структуры ядро-оболочка с различными комбинациями.
Более конкретно, структура ядро-оболочка данного изобретения может быть получена с помощью способа, отличающегося наличием (а) этапа смешивания органического растворителя, содержащего поверхностно-активное вещество, с водным раствором, содержащим предшественник первого оксида металла, с образованием обратных мицелл, которые содержат внутри себя водный раствор, содержащий предшественник первого оксида металла, (b) этапа введения основного водного раствора внутрь обратных мицелл с образованием гидроксида предшественника первого оксида металла, (с) этапа обработки полученного гидроксида водным раствором, содержащим соединение с, по меньшей мере, двумя карбоксильными группами, чтобы связать данный гидроксид с, по меньшей мере, одной карбоксильной группой, (d) этапа добавления водного раствора, содержащего предшественник второго оксида металла, отличного от предшественника первого оксида металла, к обработанному гидроксиду, чтобы связать предшественник второго оксида металла с, по меньшей мере, одной из оставшихся карбоксильных групп данного соединения с, по меньшей мере, двумя карбоксильными группами, (е) этапа введения основного водного раствора в обратные мицеллы этапа (d) с образованием осадка и (f) этапа сушки и прокаливания данного осадка, отличающегося тем, что мольное отношение элементов металлов М1 и М2 (М2/М1), образующих предшественник первого оксида металла и предшественник второго оксида металла, больше чем 0,2 и меньше чем 2,0.
Органический растворитель, используемый в способе данного изобретения, не ограничивается особо, и могут быть упомянуты углеводороды, такие как циклогексан и бензол, линейные спирты, такие как гексанол, и кетоны, такие как ацетон. Критериями выбора органического растворителя могут быть растворимость поверхностно-активного вещества или диапазон, в котором образуется микроэмульсия (большое мольное отношение вода/поверхностно-активное вещество).
Нет особых ограничений на поверхностно-активное вещество, используемое для образования обратных мицелл в способе данного изобретения, и можно упомянуть неионогенные поверхностно-активные вещества, анионные поверхностно-активные вещества и катионные поверхностно-активные вещества, соответствующе выбираемые в комбинации с органическим растворителем. Эти поверхностно-активные вещества могут добавляться к органическому растворителю в количествах и концентрациях, достаточных для образования обратных мицелл, содержащих предшественник первого оксида металла - содержащих водный раствор внутри.
В качестве неионогенных поверхностно-активных веществ могут быть использованы поверхностно-активные вещества на основе полиоксиэтиленнонилфенилового простого эфира, такие как полиоксиэтилен (n=5) нонилфениловый простой эфир, поверхностно-активные вещества на основе полиоксиэтиленоктилфенилового простого эфира, такие как полиоксиэтилен (n=10) октилфениловый простой эфир, поверхностно-активные вещества на основе полиоксиэтиленалкилового простого эфира, такие как полиоксиэтилен (n=7) цетиловый простой эфир, и поверхностно-активные вещества на основе полиоксиэтиленсорбита, такие как триолеат полиоксиэтиленсорбита.
В качестве анионных поверхностно-активных веществ могут быть использованы ди-2-этиленгексилсульфосукцинат натрия и подобные, и в качестве катионных поверхностно-активных веществ могут быть использованы хлорид цетилтриметиламмония и бромид цетилтриметиламмония.
Согласно способу данного изобретения небольшое количество С4-С8 спирта, такого как гексанол, может добавляться в качестве вспомогательного агента для поверхностно-активного вещества, чтобы стабилизировать образованные обратные мицеллы.
Путем смешения водного раствора, содержащего предшественник первого оксида металла, с раствором, содержащим органический растворитель, поверхностно-активное вещество и необязательно вспомогательный агент для поверхностно-активного вещества, можно сформировать обратные мицеллы, внутренняя область которых содержит раствор, содержащий предшественник первого оксида металла.
Согласно способу данного изобретения гидроксид предшественника первого оксида металла образуется путем введения основного водного раствора, такого как аммиачная вода, в водную фазу обратных мицелл, которые были сформированы для гидролиза предшественника первого оксида металла.
Предшественник первого оксида металла представляет собой соединение металла, соответствующего первому оксиду металла, который должен формироваться в центральной секции, и любое желаемое соединение металла, которое образует гидроксид с основным водным раствором/гидролиз, может быть использовано. В качестве примеров таких соединений металла могут быть упомянуты соли азотной кислоты, оксисоли азотной кислоты, хлориды, соли угольной кислоты и соли уксусной кислоты металлов, выбранных из группы, состоящей из циркония, алюминия, кремния и титана.
Согласно способу данного изобретения одно или несколько соединений металлов, выбранных из группы, состоящей из щелочноземельных металлов и редкоземельных элементов, могут быть добавлены в дополнение к предшественнику первого оксида металла во время формирования обратных мицелл. Такие добавочные соединения металлов будут образовывать твердый раствор с предшественником первого оксида металла в центральной секции окончательной структуры ядро-оболочка в форме их соответствующих оксидов. Путем добавления таких добавочных соединений металлов можно дополнительно увеличить термостойкость структуры ядро-оболочка данного изобретения. В качестве конкретных примеров таких добавочных соединений металлов можно упомянуть соли азотной кислоты, оксисоли азотной кислоты, хлориды, соли угольной кислоты и соли уксусной кислоты металлов, выбранных из группы, состоящей из лантана (La), церия (Се), празеодима (Pr), иттрия (Y), неодима (Nd) и их комбинаций.
Согласно способу данного изобретения гидроксид металла, полученный гидролизом предшественника первого оксида металла основным водным раствором, может быть обработан водным раствором, содержащим соединение с, по меньшей мере, двумя карбоксильными группами, чтобы связать гидроксид металла с, по меньшей мере, одной из карбоксильных групп. Более конкретно, происходит реакция замещения между гидроксильной группой гидроксида металла и соединением с, по меньшей мере, двумя карбоксильными группами или, другими словами, гидроксильная группа гидроксида металла подвергается дегидратирующей конденсации с, по меньшей мере, одной из карбоксильных групп данного соединения, образуя связь между гидроксидом металла и данным соединением. Последующее добавление водного раствора, содержащего предшественник второго оксида металла, к обработанному гидроксиду металла приводит к связыванию предшественника второго оксида металла с, по меньшей мере, одной из оставшихся карбоксильных групп соединения с двумя или более карбоксильными группами. В результате предшественник второго оксида металла и гидроксид металла, полученный из предшественника первого оксида металла, становятся связанными через соединение с двумя или более карбоксильными группами.
Связь между предшественником второго оксида металла и, по меньшей мере, одной из оставшихся карбоксильных групп соединения с двумя или более карбоксильными группами может быть любого типа связи, такого как координационная связь или ионная связь.
Предшественник второго оксида металла, используемый в способе данного изобретения, представляет собой соединение металла, соответствующего второму оксиду металла, который должен формировать оболочечную секцию, и может быть любым соединением металла, которое образует связь путем реакции с карбоксильными группами. В качестве примеров таких соединений металлов можно упомянуть соли азотной кислоты, оксисоли азотной кислоты, хлориды, соли угольной кислоты и соли уксусной кислоты, по меньшей мере, одного типа металла, выбранного из редкоземельных элементов.
Согласно способу данного изобретения соединение с, по меньшей мере, двумя карбоксильными группами может быть любой желаемой карбоновой кислотой, которая растворима в воде и имеет две или больше карбоксильных групп, способных к связыванию с гидроксидом металла, полученным из предшественника первого оксида металла, и предшественником второго оксида металла, и, например, могут использоваться С2-С30 и особенно С2-С10 дикарбоновые кислоты, трикарбоновые кислоты, тетракарбоновые кислоты, бензодикарбоновые кислоты, бензотрикарбоновые кислоты и бензотетракарбоновые кислоты. Эти соединения могут быть введены в водную фазу обратных мицелл в достаточных количествах и концентрациях, чтобы сделать возможным связывание между предшественником второго оксида металла и гидроксидом металла, полученным из предшественника первого оксида металла.
В качестве более конкретных дикарбоновых кислот могут быть упомянуты щавелевая кислота, малоновая кислота, янтарная кислота, глутаровая кислота, адипиновая кислота и пимелиновая кислоты. В качестве более конкретных трикарбоновых кислот могут быть упомянуты гемимеллитовая кислота (1,2,3-бензолтрикарбоновая кислота) и тримезиновая кислота (1,3,5-бензолтрикарбоновая кислота). В качестве более конкретных тетракарбоновых кислот может быть упомянута меллофановая кислота (1,2,3,4-бензолтетракарбоновая кислота). Щавелевая кислота наиболее предпочтительно используется в способе данного изобретения.
Основный водный раствор, такой как аммиачная вода, затем вводят в водную фазу внутри обратных мицелл, содержащую предшественник второго оксида металла и гидроксид металла, полученный из предшественника первого оксида металла, которые связаны через карбоновую кислоту, до достижения рН раствора величины 9 или выше, например, чтобы образовать осадок, который затем сушат и прокаливают, получая структуру ядро-оболочка, содержащую центральную секцию, образованную, главным образом, из первого оксида металла, и оболочечную секцию, образованную, главным образом, из второго оксида металла, который отличается от первого оксида металла. Это обеспечивает надежное и высокодисперсное связывание предшественника второго оксида металла на гидроксиде металла, полученном из предшественника первого оксида металла, через карбоновую кислоту, так что сушка и прокаливание полученного осадка могут давать структуру ядро-оболочка с центральной секцией, образованной, главным образом, из первого оксида металла, равномерно покрытую оболочечной секцией, образованной, главным образом, из второго оксида металла.
Сушку и прокаливание осадка выполняют при достаточной температуре и в течение достаточного времени для удаления соединения с, по меньшей мере, двумя карбоксильными группами и получения структуры ядро-оболочка, содержащей центральную секцию, образованную, главным образом, из первого оксида металла и содержащую необязательно выбранный добавочный оксид металла, и оболочечную секцию, образованную, главным образом, из второго оксида металла. Например, сушку можно выполнять при пониженном давлении или при обычном давлении в течение 3-24 часов при температуре 80-250°С, и прокаливание выполняется при 500-800°С в течение 1-5 часов.
В способе данного изобретения предшественник первого оксида металла и предшественник второго оксида металла предпочтительно добавляют в таких диапазонах, что мольное отношение элементов металлов М1 и М2, образующих их (М2/М1), составляет больше чем 0,2 и меньше чем 2,0.
Путем добавления предшественника первого оксида металла и предшественника второго оксида металла в таких диапазонах можно регулировать толщину оболочечной секции полученной структуры ядро-оболочка на наноуровне, например, ниже 20 нм и особенно ниже 10 нм. Так как термостойкость структуры ядро-оболочка увеличивается с помощью первого оксида металла, такого как оксид циркония, в центральной секции структуры ядро-оболочка, можно минимизировать вызываемое теплом спекание второго оксида металла, такого как оксид церия, в оболочечной секции и, таким образом, сохранять высокую площадь поверхности структуры ядро-оболочка.
Если отношение М2/М1 меньше чем 0,2, низкое количество добавленного предшественника второго оксида металла может давать секции структуры ядро-оболочка, которые не полностью покрыты вторым оксидом металла, тогда как, если отношение М2/М1 больше чем 2,0, большое количество добавленного предшественника второго оксида металла может давать толщину оболочечной секции (второго оксида металла) больше чем 20 нм в полученной структуре ядро-оболочка. Таким образом, предшественник первого оксида металла и предшественник второго оксида металла предпочтительно добавляют в таких количествах, что мольное отношение элементов металлов М1 и М2, составляющих их (М2/М1), находится в диапазоне 0,2<М2/М1<2,0 и более предпочтительно в диапазоне 0,4<М2/М1<1,6.
Согласно другому варианту данного изобретения структура ядро-оболочка используется в качестве носителя катализатора, и благородный металл, выбранный из группы, состоящей из платины (Pt), родия (Rh), палладия (Pd), иридия (Ir), рутения (Ru) и их комбинаций, наносят в качестве активного компонента на носитель катализатора. Когда редкоземельный оксид, такой как оксид церия, используется в оболочечной секции структуры ядро-оболочка, высокое сродство редкоземельного оксида к благородному металлу предотвращает спекание нанесенного благородного металла при высокой температуре, позволяя получить катализатор очистки выхлопных газов с заметно улучшенной каталитической активностью.
Нанесение благородного металла на структуру ядро-оболочка может выполняться с помощью любого способа, известного специалистам в данной области техники.
Например, такой благородный металл может наноситься путем использования соединения, содержащего благородный металл в катионной форме, в качестве источника благородного металла, погружая структуру ядро-оболочка в раствор данного соединения заданной концентрации и затем высушивая и прокаливая ее, или путем использования комплекса благородного металла в качестве источника благородного металла, погружая структуру ядро-оболочка в раствор данного комплекса заданной концентрации и затем высушивая и прокаливая ее. Такие благородные металлы обычно будут наноситься на структуру ядро-оболочка при массовом нанесении 0,1-10 мас.%.
Прокаливание и сушку структуры ядро-оболочка, которая была погружена в раствор, содержащий соединение или комплекс благородного металла, можно выполнять при достаточной температуре и в течение достаточного времени, чтобы нанести благородный металл на структуру. Например, сушку можно выполнять при 80-250°С в течение 6-24 часов, а прокаливание выполняется при температуре 500-800°С в течение 1-5 часов.
Примеры
Настоящее изобретение будет объясняться теперь более подробно с помощью следующих примеров с пониманием того, что эти примеры никоим образом не ограничивают данное изобретение.
В этих примерах смешанные оксиды, имеющие структуру ядро-оболочка с центральной секцией, образованной, главным образом, из оксида циркония, и оболочечной секцией, образованной, главным образом, из оксида церия, готовили с помощью способа данного изобретения, и их структуры и термостойкость испытывали.
Пример 1
Сначала циклогексан в качестве органического растворителя, поли(оксиэтилен)октилфениловый эфир (Triton X-100) в качестве поверхностно-активного вещества и n-гексанол в качестве вспомогательного агента поверхностно-активного вещества объединяли в объемном отношении 2,3:1:1,6, и их раствор доводили до 1710 см3, после чего туда добавляли раствор 21 г дигидрата оксинитрата циркония (ZrO(NO3)2·2H2O) и 0,7 г гексагидрата нитрата лантана (La(NO3)3·6H2O) в 81 г очищенной воды. Затем добавляли 9 см3 28% аммиачной воды, и смесь перемешивали в течение 1 часа. После этого добавляя туда 10 мл 1 М водного раствора щавелевой кислоты и перемешивая в течение 3 часов, раствор нитрата церия аммония (Се(NН4)2(NО3)6), растворенного в 40 см3 очищенной воды, добавляли до мольного отношение Се/Zr 1,2 и перемешивание продолжали в течение 15 часов. Затем 28% аммиачную воду добавляли до достижения рН 9 смеси, получая осадок, который отделяли центрифугированием и затем сушили в вакууме при 120°С в течение 3 часов, и прокаливали при 700°С в течение 5 часов, получая смешанный оксид со структурой ядро-оболочка, содержащей центральную секцию, образованную, главным образом, из оксида циркония, и оболочечную секцию, образованную, главным образом, из оксида церия.
Примеры 2-6
Смешанные оксиды со структурой ядро-оболочка, содержащей центральную секцию, образованную, главным образом, из оксида циркония, и оболочечную секцию, образованную, главным образом, из оксида церия, получали таким же образом, как в примере 1, за исключением того, что количество нитрата церия аммония изменяли до мольного отношения Се/Zr 0,2 (пример 2), 0,4 (пример 3), 0,8 (пример 4), 1,6 (пример 5) или 2,0 (пример 6).
Сравнительный пример 1
Смешанный оксид, содержащий оксид циркония и оксид церия, получали таким же образом, как в примере 1, за исключением того, что не добавляли щавелевую кислоту.
Сравнительный пример 2
Смешанный оксид, образованный из твердого раствора оксида циркония и оксида церия без структуры ядро-оболочка, готовили для этого примера.
Сначала 21 г оксинитрата циркония, 0,7 г гексагидрата нитрата лантана и 51 г нитрата церия аммония растворяли в 582 см3 очищенной воды. Затем 9 см3 28% аммиачной воды добавляли к данной смеси, получая осадок, который отделяли центрифугированием и затем сушили в вакууме при 120°С в течение 3 часов, и прокаливали при 700°С в течение 5 часов, получая смешанный оксид, образованный из твердого раствора оксида циркония и оксида церия.
Сравнительный пример 3
Для этого примера смешанный оксид, имеющий структуру ядро-оболочка с центральной секцией, образованной, главным образом, из оксида циркония, и оболочечной секцией, образованной, главным образом, из оксида церия, получали обычным способом.
Сначала водный раствор золя оксида церия, водный раствор золя оксида циркония и водный раствор золя оксида иттрия (Y2О3) объединяли в таких количествах, что CeO2:ZrO2:Y2O3=60:36:4 (массовое отношение). К смешанному раствору золей добавляли по каплям водный раствор азотной кислоты до рН 3, а затем аммиачную воду до рН 10. Смесь затем сушили при 120°С в течение 24 часов и прокаливали при 700°С в течение 5 часов, получая смешанный оксид со структурой ядро-оболочка, содержащей центральную секцию, образованную, главным образом, из оксида циркония, и оболочечную секцию, образованную, главным образом, из оксида церия.
[Определение структуры и производительности смешанного оксида]
Смешанные оксиды, полученные в данных примерах и сравнительных примерах, изучали, используя просвечивающий электронный микроскоп с энергорассеивающим рентгеновским спектрометром (ПЭМ-ЭРР) (НF-2000 от Hitachi), чтобы определить толщину и концентрацию церия слоя оксида церия оболочечной секции.
Фиг.2(а) представляет собой ПЭМ фотографию, показывающую агрегат, полученный путем агрегации многочисленных структур ядро-оболочка, приготовленных в примере 1, и фиг.2(b) представляет собой увеличенную ПЭМ фотографию, показывающую края агрегата, показанного на фиг.2(а). Числа на фиг.2(b) отражают концентрации церия (Се) в окруженных секциях. Концентрация Се явно снижается от края к центру агрегата. Так как фотография на фиг.2 представляет собой просвечивающее изображение, измеренная концентрация Се в центре агрегата является не только концентрацией Се поверхности агрегата, но также включает в себя объем агрегата. Концентрацию Се на краях агрегата, следовательно, измеряли, чтобы проанализировать состав поверхности полученной структуры ядро-оболочка.
Как ясно видно из ПЭМ фотографии, показанной на фиг.2(b), концентрация Се на краях агрегата, т.е. в оболочечных секциях структур ядро-оболочка, образующих агрегат, была 80 или много выше чем концентрация Zr. Таким образом, было доказано, что способ данного изобретения формирует смешанный оксид, имеющий структуру ядро-оболочка, содержащую центральную секцию, образованную, главным образом, из оксида циркония, и оболочечную секцию, образованную, главным образом, из оксида церия.
Фиг.3 представляет собой ПЭМ фотографию, показывающую агрегат, полученный путем агрегации многочисленных структур ядро-оболочка, приготовленных в сравнительном примере 3. Фиг.3, в противоположность фиг.2(b), показывает края агрегата с низкой концентрацией Се 34%, тогда как некраевые области включали в себя области с концентрацией Се 78%, что выше, чем концентрация Zr. Он также показывает, что использование способа данного изобретения делает возможным более надежный синтез структуры ядро-оболочка с центральной секцией, образованной, главным образом, из оксида циркония, и оболочечной секцией, образованной, главным образом, из оксида церия, по сравнению со способом предшествующего уровня техники.
Смешанные оксиды, приготовленные в примере 1, сравнительном примере 1 и сравнительном примере 2, затем подвергали тестированию, выдерживая при 1000°С в течение 3 часов при переключении между богатым модельным газом и бедным модельным газом каждую минуту, используя модельные газы для тестирования долговечности, показанные в таблице 1 ниже.
Составы модельных газов для тестирования
долговечности
Таблица 2 показывает величины изоэлектрических точек и удельных площадей поверхности (УПП) по БЭТ после тестирования долговечности для каждого из смешанных оксидов, приготовленных в примере 1, сравнительном примере 1 и сравнительном примере 2. Для сравнения также показаны значения изоэлектрических точек и удельных площадей поверхности (УПП) по БЭТ после тестирования долговечности одиночного оксида церия (СеО2) и оксида циркония (ZrO2). Измерения изоэлектрической точки проводили, используя аппарат измерения дзета-потенциала (МАRК2, продукт Rank Brothers).
Влияние способа приготовления
Результаты в таблице 2 демонстрируют явное различие в изоэлектрических точках смешанных оксидов из примера 1 и сравнительных примеров 1 и 2, причем смешанный оксид из примера 1 демонстрирует изоэлектрическую точку, близкую к изоэлектрической точке одного СеО2, а смешанный оксид из сравнительного примера 1, в котором не добавляли щавелевой кислоты, демонстрирует изоэлектрическую точку, близкую к изоэлектрической точке твердого раствора оксида церия-оксида циркония из сравнительного примера 2. Смешанные оксиды примера 1 и сравнительных примеров 1 и 2 имели одинаковый состав церия и циркония (мольное отношение Се/Zr 1,2), и, следовательно, различие между ними было приписано различию в формах оксида церия (СеО2) и оксида циркония (ZrO2) в смешанных оксидах. Более конкретно, считается, что смешанный оксид примера 1 показал величину изоэлектрической точки, близкую к величине для одного СеО2 потому, что присутствовал СеО2, окружающий ядро из ZrO2, как показано на фиг.1, тогда как смешанные оксиды сравнительных примеров 1 и 2 показали изоэлектрические точки, средние между отдельными СеО2 и ZrO2, потому что СеО2 и ZrO2 присутствовали в виде твердого раствора. Эти результаты указывают на то, что соединение с, по меньшей мере, двумя карбоксильными группами и особенно щавелевая кислота, исключительно важно для формирования структуры ядро-оболочка согласно данному изобретению.
Как показывает таблица 2, удельные площади поверхности после тестирования долговечности смешанных оксидов и в отдельности СеО2 и ZrO2 были самыми высокими для смешанного оксида примера 1, причем данная величина была даже выше, чем для отдельного ZrO2.
Смешанные оксиды, приготовленные в примерах 1-6, затем испытывали, чтобы определить изоэлектрические точки и удельные площади поверхности (УПП) по БЭТ после тестирования долговечности, таким же образом, как описано выше, а также толщины их оболочечных секций (нм). Результаты показаны в таблице 3 ниже.
Влияние отношения Се/Zr
(нм)
Как показано в таблице 3, смешанные оксиды с мольными отношениями Се/Zr в диапазоне 0,2<Се/Zr<2,0 (примеры 1, 3, 4 и 5) имели величины изоэлектрических точек, которые были почти такие же, как для одного СеО2, и толщины оболочечных секций также были не больше чем приблизительно 10 нм, и поэтому высокие удельные площади поверхности могли сохраняться после тестирования долговечности. Однако смешанный оксид, который имел мольное отношение Се/Zr 0,2 (пример 2) имел величину изоэлектрической точки, смещенную в направлении одного ZrO2, и ПЭМ-ЭРР анализ также показывал структуру ядро-оболочка с несколькими областями, не покрытыми СеО2. Смешанный оксид, который имел мольное отношение Се/Zr 2,0 (пример 6), имел большую толщину оболочечной секции 23,0 нм, и поэтому удельная площадь поверхности после тестирования долговечности была заметно ниже по сравнению с другими примерами. Эти результаты показывают, что, если мольное отношение Се/Zr регулируют в диапазоне 0,2<Се/Zr<2,0 и особенно в диапазоне 0,4<Се/Zr<1,6, можно получить структуру ядро-оболочка, имеющую оболочечную секцию, образованную, главным образом, из оксида церия, с толщиной на наноуровне, и, таким образом, демонстрирующую заметно улучшенную термостойкость.


Настоящее изобретение относится к структуре ядро-оболочка, способу ее получения и катализатору очистки выхлопных газов, содержащему структуру ядро-оболочка. Описана структура ядро-оболочка для применения в качестве носителя катализатора, характеризующаяся наличием центральной секции, образованной, главным образом, из первого оксида металла, и оболочечной секции, образованной, главным образом, из второго оксида металла, отличного от первого оксида металла, где мольное отношение церия к цирконию находится в диапазоне 0,2<Ce/Zr<2,0, а толщина оболочечной секции не превышает 20 нм. Описан способ получения структуры ядро-оболочка, который включает этапы, на которых(а) смешивают органический растворитель, содержащий поверхностно-активное вещество, с водным раствором, содержащим предшественник первого оксида металла, с образованием обратных мицелл, которые содержат внутри себя водный раствор, содержащий предшественник первого оксида металла, (b) вводят основной водный раствор внутрь обратных мицелл с образованием гидроксида предшественника первого оксида металла, (с) обрабатывают полученный гидроксид водным раствором, содержащим соединение с, по меньшей мере, двумя карбоксильными группами, чтобы связать данный гидроксид с, по меньшей мере, одной карбоксильной группой, (d) добавляют водный раствор, содержащий предшественник второго оксида металла, отличный от предшественника первого оксида металла, к обработанному гидроксиду, чтобы связать предшественник второго оксида металла с, по меньшей мере, одной из оставшихся карбоксильных групп данного соединения с, по меньшей мере, двумя карбоксильными группами, (е) вводят основный водный раствор в обратные мицеллы этапа (d) с образованием осадка и (f) сушат и прокаливают данный осадок, причем мольное отношение элементов металлов M1 и М2 (М2/М1), образующих предшественник первого оксида металла и предшественник второго оксида металла, больше, чем 0,2 и меньше, чем 2,0, первый оксид металла выбирают из группы, состоящей из оксида циркония, оксида алюминия, оксида кремния, оксида титана и их комбинаций и второй оксид металла выбирают из группы, состоящей из редкоземельных оксидов или комбинаций двух или более редкоземельных оксидов. Описан также катализатор очистки выхлопных газов, содержащий описанную выше структуру ядро-оболочка или структуру ядро-оболочка, полученную с помощью способа ее получения, в качестве носителя катализатора. Технический эффект - получение структуры ядро-оболочка, имеющей регулируемую толщину оболоченной секции и улучшенной термостойкости. 3 н. и 1 з.п., 3 ил., 3 табл.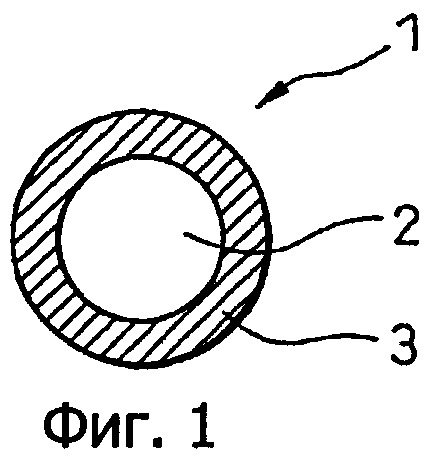
1. Структура ядро-оболочка для применения в качестве носителя катализатора, отличающаяся наличием центральной секции, образованной, главным образом, из оксида циркония в качестве первого оксида металла, и оболочечной секции, образованной, главным образом, из оксида церия в качестве второго оксида металла, отличного от первого оксида металла, где мольное отношение церия к цирконию находится в диапазоне 0,2<Ce/Zr<2,0, а толщина оболочечной секции не превышает 20 нм.
2. Способ получения структуры ядро-оболочка, отличающийся тем, что включает этапы, на которых
(a) смешивают органический растворитель, содержащий поверхностно-активное вещество, с водным раствором, содержащим предшественник первого оксида металла, с образованием обратных мицелл, которые содержат внутри себя водный раствор, содержащий предшественник первого оксида металла,
(b) вводят основный водный раствор внутрь обратных мицелл с образованием гидроксида предшественника первого оксида металла,
(c) обрабатывают полученный гидроксид водным раствором, содержащим соединение с, по меньшей мере, двумя карбоксильными группами, чтобы связать данный гидроксид с, по меньшей мере, одной карбоксильной группой,
(d) добавляют водный раствор, содержащий предшественник второго оксида металла, отличный от предшественника первого оксида металла, к обработанному гидроксиду, чтобы связать предшественник второго оксида металла с, по меньшей мере, одной из оставшихся карбоксильных групп данного соединения с, по меньшей мере, двумя карбоксильными группами,
(e) вводят основный водный раствор в обратные мицеллы этапа (d) с образованием осадка, и
(f) сушат и прокаливают данный осадок,
причем мольное отношение элементов металлов M1 и М2 (М2/М1), образующих предшественник первого оксида металла и предшественник второго оксида металла, больше чем 0,2 и меньше чем 2,0, первый оксид металла выбирают из группы, состоящей из оксида циркония, оксида алюминия, оксида кремния, оксида титана и их комбинаций и второй оксид металла выбирают из группы, состоящей из редкоземельных оксидов или комбинаций двух или более редкоземельных оксидов.
3. Способ по п.2, отличающийся тем, что данное соединение с, по меньшей мере, двумя карбоксильными группами выбирают из группы, состоящей из щавелевой кислоты, малоновой кислоты, янтарной кислоты, глутаровой кислоты, адипиновой кислоты, пимелиновой кислоты, гемимеллитовой кислоты, тримезиновой кислоты и меллофановой кислоты.
4. Катализатор очистки выхлопных газов, содержащий структуру ядро-оболочка по п.1 или структуру ядро-оболочка, полученную с помощью способа по любому из пп.2-4, в качестве носителя катализатора.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| Композиция для изготовления строительных изделий | 1988 |
|
SU1579912A1 |
| DE 9403581 U1, 28.04.1994 | |||
| EP 1284217 A, 19.02.2003 | |||
| СПОСОБ ПРИГОТОВЛЕНИЯ КАТАЛИЗАТОРА И КАТАЛИЗАТОР ДЛЯ ОЧИСТКИ ВЫХЛОПНЫХ ГАЗОВ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ | 2000 |
|
RU2169614C1 |
| RU 200109780 C1, 27.03.2002. | |||
Авторы
Даты
2011-07-10—Публикация
2008-05-21—Подача