Уровень техники изобретения
Процесс кариеса является объектом пристального изучения. Кариес обычно возникает в результате процесса, который начинается с образования налета, содержащего выделяющие кислоту бактерии, которые разъедают и разрушают поверхность зубов и иным способом раздражают или разъедают поверхность десен и мягких тканей зубов. Образование налета начинается в течение минут после рутинной чистки или профессиональной очистки зубов, и в течение последующих нескольких часов происходит адгезия бактерий.
Обычно регулярное удаление налета представляет собой основной способ, с помощью которого удается сдерживать кариес, хотя профессионально применяемые твердые полимерные профилактические покрытия используют в качестве сменных защитных покрытий для предотвращения прямого контакта бактерий из налета и выделяемых ими кислот с поверхности зубов. В композиции для обработки зубов также включают антибактериальные средства как для того, чтобы уничтожать бактерии в ротовой полости, так и, в некоторых случаях, чтобы обеспечивать временный остаточный эффект, препятствующий размножению бактерий в слое налета, который образуется после чистки зубов при помощи композиции.
Однако было бы желательно создать эффективную стратегию для предотвращения или ингибирования прикрепления бактерий к зубам и поверхностям мягких тканей ротовой полости без необходимости герметизировать зубы сплошным полимерным слоем и без необходимости прибегать к вмешательству профессионалов в области стоматологии.
Краткая сущность изобретения
Изобретение относится к частицам, которые нарушают и/или препятствуют прикреплению бактерий к поверхности ротовой полости, и композициям, содержащим данные частицы. Частица включает (i) ядро, которое содержит оксидное соединение или соль, а также (ii) биоадгезивный полимер. Биоадгезивный полимер соединяют с оксидным соединением или солью. Также предлагают способы получения частицы, способы ингибирования или уменьшения образования налета на поверхности ротовой полости с применением частицы, а также другие относящиеся к делу способы.
Подробное описание чертежей
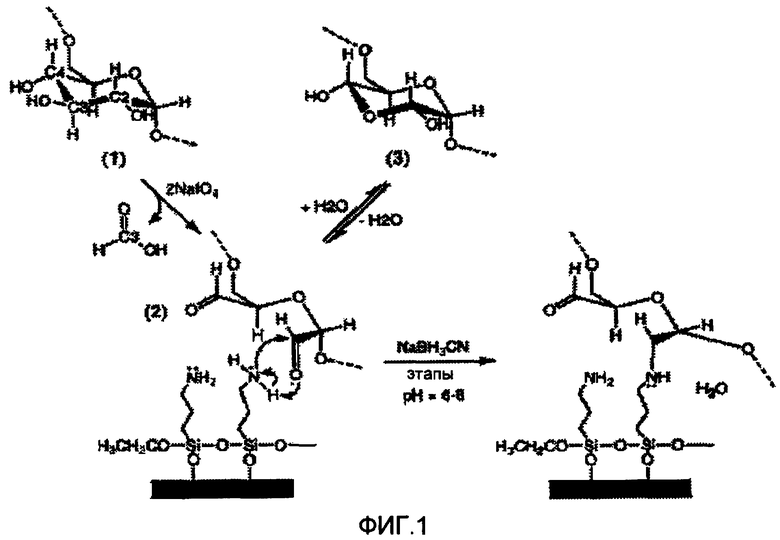
На фиг.1 представлена схема реакции окисления полисахарида для получения карбонильных групп, с последующим проведением реакции с полученным полимером для прикрепления его к поверхности твердого ядра частицы посредством взаимодействия карбонильных групп с аминогруппами.
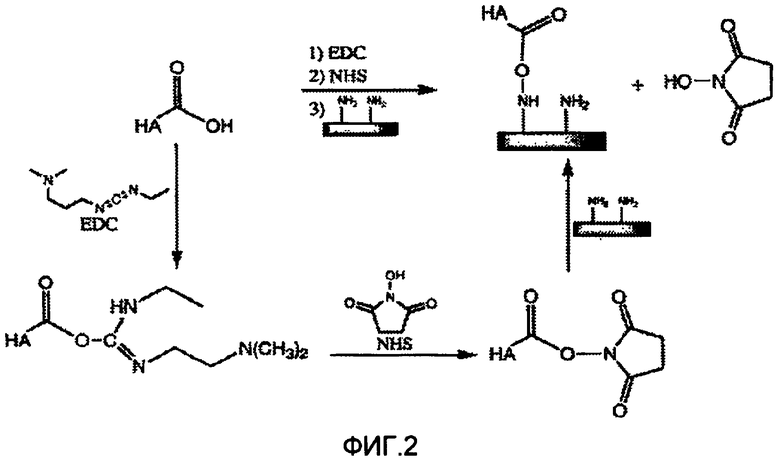
На фиг.2 представлена схема реакции прикрепления содержащего карбоновую кислоту полимера к поверхности твердого ядра частицы посредством реакции карбоксильной гидроксигруппы, с применением карбодиимидной химической реакции и N-гидроксисукцинимида для получения сложного эфира сукцинимида, который затем вступает в реакцию с аминогруппами, связанными с поверхностью ядра частицы для получения аминоалканоатной (то есть, алканоилокси-амино) связи.
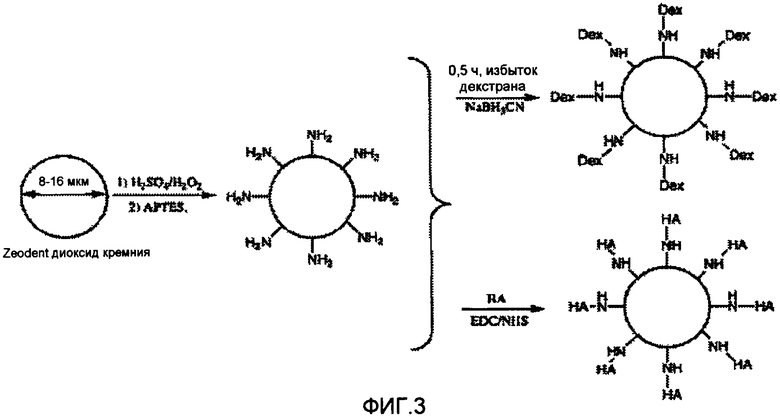
На фиг.3 представлено графическое изображение способа в целом для получения частицы по варианту осуществления настоящего изобретения посредством предварительной обработки ядра частицы (например, диоксида кремния) соединением, которое создает связанные аминогруппы, прикрепленные к его поверхности, с последующей химической реакцией для связывания полимера, содержащего карбонильные или кислые группы, с прикрепленными аминогруппами.
Подробное описание изобретения
Настоящее изобретение относится к композициям и способам ингибирования образования биопленки и бактериальной адгезии к поверхностям, включая промышленные, бытовые, медицинские, поверхности тела человека и животных, особенно отложения налета в ротовой полости и бактериальной адгезии к поверхности зубов.
Композиции, описанные здесь, предотвращают и/или нарушают прикрепление бактерий к зубам, деснам и другим поверхностям ротовой полости без необходимости применения сплошного полимерного слоя.
Настоящее изобретение также относится к подходу в целом для создания эффекта для предотвращения адгезии/прикрепления бактерий к биологическим и другим поверхностям (например, поверхности зубов, слизистым поверхностям и/или кожным поверхностям). Данный подход основан на свойствах, препятствующих отложениям, которые присущи биоадгезивным полимерам, предпочтительно полисахаридам и родственным полимерам, таким как полисахариды, декстран и гиалуронат (HA). Настоящее изобретение относится к частицам, которые содержат подобные полимеры, прочно связанные с твердыми ядрами частиц, такими как ядра частиц из диоксида кремния (SiO2) или оксида цинка (ZnO). Данные частицы применяют к поверхностям, которые могут представлять собой биологические поверхности, такие как поверхности ротовой полости, с целью создания барьера, препятствующего прикреплению к ним микробов (например, бактерий), а также препятствующего прикреплению к обработанной поверхности органических молекул (например, органических компонентов пены). Настоящее изобретение относится к способам ингибирования прикрепления бактерий к таким поверхностям, как, например, поверхности мягких тканей зубов и ротовой полости, тем самым ингибирования начала и/или скорости образования биопленок и налета и/или уменьшения силы адгезии биопленок, что в случае орального применения может ингибировать возникновение кариеса зубов и периодонтальных болезней, таких как гингивит и периодонтит. Частицы, например, из SiO2 или ZnO могут являться, и предпочтительно являются, включенными в препараты для применения к поверхности, например средства для чистки зубов и другие потребительские товары для ухода за полостью рта, и могут также входить в состав продуктов для ухода за полостью рта, применяемых профессионалами в области стоматологии.
Частицы по настоящему изобретению содержат ядро. Ядро (ядра) частиц может представлять собой твердое ядро (ядра), которое является, по меньшей мере, в основном нерастворимым в воде. В одном варианте осуществления ядра частиц представляют собой отдельные элементы частиц, содержащие один или более, по меньшей мере, в основном нерастворимых в воде металлов, полуметаллов и неметаллов; металлических, полуметаллических, неметаллических и смешанно-металлических галогенидов, карбидов, нитридов, сульфидов, оксидов (включая, например, карбонаты, фосфаты, сульфаты) и тому подобное, а также керамику, минералы (включая биоминералы) и их сплавы. Примеры подобных веществ включают AgBr, AlN, Al2O3, BaLiF3, BaY2F8, Bi2O3, CdS, CdSe, CdTe, CuCl, FeC, Fe4N, Fe2O3, GaAs, GaP, HgS, HgSe, HgTe, InAs, InP, InSn, KI, LiCaAlF6, LiNb, NaCl, NiO, SiC, Si3N4, SiO2, SnO2, TiN, TiO2, WO3, YLiF4, ZnC, ZnS, ZnSe, ZnTe, ZrN, ZnO, Sn, Ag, Au, Cu, Ni, Pt, углерод, кремний, германий; соединения, соли и содержащие их комплексы; и смеси любого из вышеуказанных друг с другом или дополнительным компонентом.
В одном варианте осуществления металл(ы) для использования в подобных металлических соединениях, солях и смесях выбирают из щелочных металлов, щелочноземельных металлов, Zn, Sn, Fe, Se, Cu, Mn, Mo, Co, Ni, Cr, V, W, Ti и Al, предпочтительно из щелочных металлов, щелочноземельных металлов, Zn, Sn, Fe, Cu, Mn, Mo и Ti, более предпочтительно из щелочных металлов, щелочноземельных металлов и Zn. В одном предпочтительном варианте осуществления металл(ы) представляют собой любой из щелочноземельных металлов, Zn, или их сочетание друг с другом или со щелочным металлом(ами) или с обоими.
В одном варианте осуществления твердые ядра частиц содержат оксидное соединение или его соль. Предпочтительные оксиды включают в основном нерастворимые в воде: простые оксиды, оксиды углерода (например, карбонаты металлов), оксиды фосфора (например, фосфаты металлов, полифосфаты металлов), оксиды серы (например, сульфаты металлов), силикаты и их сочетания. В одном варианте осуществления ядро частицы содержит простое оксидное соединение. Примеры простых оксидных соединений включают Al2O3, Fe2O3, MgAl2O4, SiO2, SnO2, TiO2 и ZnO, а также их сочетания, например системы xMOy-zAl2O3-SiO2 (M представляет собой катион(ы) металла). В предпочтительном варианте осуществления простое оксидное соединение может представлять собой SiO2 или ZnO.
В одном варианте осуществления ядро частицы содержит, по меньшей мере, одно оксидное соединение или соль, которое представляет собой оксид углерода, оксид фосфора, оксид серы или силикат. Предпочтительные примеры каждого из них, соответственно, включают гомо- и гетерометаллы: 1) карбонаты, например, CaCO3, CaMg(CO3)2; 2a) полифосфаты, такие как пирофосфаты, например, Ca2P2O7, CaMgP2O7 и 2b) фосфаты, например, Ca3(PO4)2, гидроксиапатиты, такие как Ca10(PO4)6(OH)2), оксиапатиты, такие как Ca10(PO4)6O, галоапатиты, галогидроксиапатиты и галооксиапатиты, такие как Ca15(PO4)9(F)O; 3) сульфаты, например, CaSO4 и сульфатапатиты, такие как Na6Ca4(SO4)6(F,Cl)2; и 4) силикаты, например, Al2SiO5, силикаты натрия, силикаты кальция и слюды. В одном варианте осуществления карбонаты, фосфаты и сульфаты металлов являются предпочтительными. Можно использовать сочетание оксидов, принадлежащих более чем к одному подобному классу, например, карбонатапатиты, такие как Ca10(PO4)6CO3, силикатсульфатапатиты, такие как Ca10(SiO4)3(SO4)3(OH,F,Cl)2, карбонатсульфаты, такие как Ca2(SO4)(СО3), фосфатсульфаты, такие как Са2НРO4SO4, а также силикатфосфаты и сульфатфосфаты, такие как силикатфосфаты кальция или сульфатфосфаты, например, Cas(SiO4, РO4, SO4)3(F, Сl, O, ОН).
Твердые ядра частиц могут альтернативно или дополнительно содержать полимер(ы), которые являются, по меньшей мере, в основном нерастворимыми в воде, и предпочтительно незначительно набухающими в воде, такие как полиолефины, полистиролы, поликарбонаты, сложные полиэфиры (включая полигидроксиалканоаты), и тому подобное. В тех случаях, когда ядро частицы выбирают для использования в композиции для ухода за полостью рта, оно должно быть приемлемо для орального применения, например не обладать значительной токсичностью в применяемых условиях и концентрациях, и так далее.
Ядра частиц являются предпочтительно в основном нерастворимыми в воде. Как используют здесь, это означает, что ядра частиц сохраняют свои размеры в водных условиях при рН между рН 6 и рН 8 в течение, по меньшей мере, 3 часов, предпочтительно, по меньшей мере, 4, по меньшей мере, 5 или, по меньшей мере, 6 часов. В некоторых случаях частицы, осевшие на поверхности ротовой полости, могут вступать в контакт с кислотами бактериального или пищевого происхождения. В тех случаях, когда имеются в наличии подобные кислые условия, материал для ядер частиц предпочтительно должен быть таким, который либо является устойчивым к такому кислотному разъеданию, либо разрушается или разлагается с образованием нетоксичных продуктов. Примеры материалов для ядер частиц, которые могут разлагаться в кислых условиях с образованием нетоксичных продуктов, включают нетоксичные карбонаты, сульфаты и фосфаты металлов, предпочтительно, когда металл представляет собой нетоксичный щелочноземельный металл, предпочтительно кальций (то есть, катион Са(II)).
Использование подобных разрушаемых кислотой материалов для ядер частиц в композиции для орального применения может способствовать созданию слоя частиц, покрывающего поверхности ротовой полости, такие частицы остаются нерастворимыми до тех пор, пока скопление бактерий не достигает такого уровня, что продукция кислоты микробами становится значительной. С этого момента такой слой частиц действует как принимающий удар на себя, нейтрализующий кислоту слой, который обеспечивает дальнейшую защиту зубов от агрессивного действия кислоты. Такие частицы могут также приносить пользу, помогая нейтрализовать кислоты другого происхождения, такие как пищевые кислоты (например, насыщенные и ненасыщенные карбоновые кислоты, включая уксусную, щавелевую, лимонную, яблочную и винную кислоты; а также фосфорную кислоту) и кислоты желудочного сока, которые способны аналогичным образом разрушать зубную эмаль.
Ядра частиц могут обладать различной морфологией. Предпочтительные морфологические формы включают такие, которые являются, по меньшей мере, в основном сферическими, эллипсоидными или плоскими. Ядра частиц могут иметь любой размер, предпочтительно меньше чем 1 мм. В одном варианте осуществления средний максимальный размер ядер частиц, то есть их средний максимальный диаметр или другой осевой размер составляет, предпочтительно, от примерно 1 нм до примерно 100 мкм, более предпочтительно от примерно 10 нм до примерно 100 мкм. Таким образом, в одном варианте осуществления размеры ядер являются наноскопическими или микроскопическими по своим масштабам. В одном варианте осуществления ядра частиц обладают средним размером от примерно 1 до примерно 100 мкм, предпочтительно от примерно 5 до примерно 50 мкм, более предпочтительно от примерно 5 до примерно 25 мкм. В одном варианте осуществления размеры ядер частиц составляют от примерно 1 нм до примерно 1 мкм; таким образом, ядро частицы может обладать размерами коллоида. В одном варианте осуществления ядро частицы может обладать размерами единичной молекулы. Таким образом, в целом частица может иметь форму правильной или неправильной сверхразветвленной структуры, например конфигурацию дендримера или щетки. Такие ядра молекулярного уровня отличаются от большего размера «супермолекулярного» уровня частиц, используемых в качестве ядер, например, тех, размер которых составляет от 1 нм до 1 мм.
Ядра частиц супермолекулярного уровня могут быть пористыми или непористыми; в одном варианте осуществления они являются, по меньшей мере, в основном непористыми. Если в ядре частицы, или в качестве такового, используют пористый материал, его поры могут по выбору содержать приемлемое орально, например, лекарственное средство, такое как антибактериальное средство (например, триклозан), антиоксидант или обезболивающее средство; нутрицевтик, такой как растительный экстракт (например, экстракт магнолии, экстракт чая); витамин; освежающее дыхание средство или другое средство или их сочетание, которые высвобождаются в ротовой полости.
Добавки могут являться и средствами, известными в данной области, и могут включать любой тип связывания и/или одну или больше промежуточную или линкерную молекулу(ы). Частица содержит ядро частицы, соединенное с, по меньшей мере, одним биоадгезивным полимером, который соединяют с частицей ковалентным или нековалентным связыванием. В случае ковалентного связывания с ядром это происходит в результате реакции с вовлечением пар реакционно-способных групп: один член пары принадлежит ядру частицы или линкеру, или другой реакционно-способной группе, предварительно присоединенной к нему, и один член принадлежит полимеру или линкеру, или другой реакционно-способной группе, предварительно присоединенной к нему. В одном варианте осуществления реакционноспособная группа, принадлежащая полимеру, представляет собой первичную или вторичную карбонильную группу(ы) или кислую группу(ы).
Биоадгезивные полимеры включают любой природный или синтетический гомо- или гетерополимер, который способен прикрепляться посредством либо физического притяжения, либо химической реакции, к желаемой целевой поверхности, например твердой или мягкой поверхности ротовой полости, на протяжении минимального времени, считающегося эффективным для выбранного применения. Предпочтительные примеры классов биоадгезивных полимеров включают
(1) полисахариды и родственные полимеры;
(2) полипептиды (включая дипептиды, олигопептиды), такие как альбумины, казеины, коллагены, фибрины, желатины, глобулины (например, иммуноглобулины), лектины, проламины (такие как авенины, глиадины, глютелины, глютены, глютенины, хордеины, кафирины, оризины, пеннисетины, секалины, зеины), синтетические полиамиды и направленные полипептиды (например, полипептидные аптамеры);
(3) акриловые полимеры, такие как гомо- и гетерополимеры из акрилатных и/или акриламидных мономеров, включая акрилатные и (например, C1-C4) алкилакрилатные соли и сложные эфиры, и (например, C1-C4) алкилакриламиды, друг с другом (например, полиметилметакрилаты) и/или с альгиновой кислотой или другими сомономерами, цианоакрилаты;
(4) другие поликислотные полимеры, такие как гомо- и гетерополимеры из
неакриловых, ненасыщенных карбоновых кислот, например другие полимеры поли(ненасыщенной карбоновой, то есть моно-, ди- и поликарбоновой кислоты), такие как полимеры поли(кротоновой, итаконовой и/или малеиновой кислоты), полифосфаты, полимеры поли(органического фосфата или фосфоната), полимеры поли(органического сульфата или сульфоната), полимеры поли(ненасыщенной гидроксикарбоновой кислоты) и тому подобное;
(5) сложные полиэфиры, включая гомо- и гетерополигидроксиалканоаты (например, полимеры полимолочной кислоты, полигликолиды, и тому подобное), функционализированные сложные полиэфиры (например, карбоксилированные сложные полиэфиры, сложные гидроксиполиэфиры) и сложные полиортоэфиры;
(6) полиангидриды, такие как полимеры поли(фумаровой-со-себациновой) кислоты;
(7) полиалкиленовые полимеры, такие как синтетические полиалкилены, полиалкиленгликоли (например, полиэтиленгликоли), полиалкиленоксиды, полиалкилентерефталаты, и тому подобное;
(8) полисилоксаны;
(9) полиуретаны и
(10) поливиниловые полимеры, такие как поли(виниловые спирты), поливиниловые сложные эфиры, поливиниловые эфиры, поливиниловые галогениды, поливинилфенолы и поливинилпирролидоны.
Подобные биоадгезивные полимеры можно применять в форме линейных или разветвленных полимеров, или можно применять в форме более крупных структур, содержащих такие полимеры, например, коллоидов или латексов. В некоторых случаях мономер такого биоадгезивного полимера может сам обеспечивать биоадгезию. Таким образом, в некоторых вариантах осуществления биоадгезивное вещество может представлять собой биоадгезивный мономер, такой как аминокислота или моносахарид.
Биоадгезивные полимеры можно легко получать из коммерческих источников, включая, например, Fluka (Ronkonkoma, NY, USA), Polysciences (Warrenton, PA, USA) и Sigma-Aldrich (Milwaukee, WI, USA; и St. Louis, MO, USA); или можно синтезировать из мономеров, полученных от данных поставщиков, используя хорошо известные методы.
В одном варианте осуществления биоадгезивный полимер представляет собой биосовместимый полимер. В одном варианте осуществления полимер представляет собой полисахарид или родственный полимер. Примеры применимых полисахаридов и родственных полимеров включают поли(сахариды); поли(моно- и дидезоксисахариды); поли(сахарные кислоты), например поли(глюк-уроновые, -оновые, -аровые и -улозоновые кислоты); поли(сахарные спирты) и поли(аминосахара).
Подобные полисахариды и родственные полимеры могут иметь в основе любые альдозные или кетозные мономеры, такие как альдо- или кетотриоза, тетрозы, пентозы, гексозы, гептозы; их дезокси, кислые, спиртовые и аминовые родственные соединения; их замещенные производные и тому подобное. Таким образом, полисахариды и родственные полимеры, применяемые здесь, могут содержать замещенную или незамещенную мономерную единицу(ы) или и то и другое. В случае, когда в полисахариде или родственном полимере присутствует замещенная мономерная единица(ы), замещения предпочтительно выбирают из C1-C4: замещений алкиловым эфиром (например, метиловым, этиловым или пропиловым эфиром), гидроксиалкиловым эфиром и карбоксиалкиловым эфиром; замещений алкиламином и алканоиламином (например, N-ацетилом) или сульфамидом, сульфонамидом и сульфамином (например, N-сульфо); замещений алканоиловым сложным эфиром, например пировиноградным, уксусным и муравьиным сложным эфиром, или замещений сложным эфиром сульфокси- или фосфоксикислоты (на гидроксильных группах полимера); а также замещений алканоловым, диоловым и полиоловым сложным эфиром (на кислых группах полимера).
В одном варианте осуществления мономерные единицы полисахарида или родственного полимера предпочтительно выбирают из остатков замещенной или незамещенной гексозы, гексулозы, гексоновой кислоты, гексуроновой кислоты, гексаровой кислоты, гексулозоновой кислоты, пентозы, пентулозы, пентоновой кислоты, пентуроновой кислоты, пентоновой кислоты и пентулозоновой кислоты. В одном варианте осуществления полимер представляет собой полимер или сополимер глюкозы, глюкозной кислоты и/или глюкозного спирта.
Репрезентативные примеры предпочтительных полисахаридов и родственных полимеров включают целлюлозы; хитозаны; крахмалы; гликогены; камеди, например камеди из растений, микробов и водорослей, такие как агарозы, гуары, декстраны и каррагенаны, и синтетические камеди на основе полисахаридов; а также гликозаминогликаны, например дерматаны, хондроитины, гепараны, гиалуронаты и кератины, включая сульфат дерматана, сульфат хондроитина, сульфат гепарана, сульфат гепарина и кератана; замещенные сахаридные полимеры, например алкилцеллюлозы, гидроксиалкилцеллюлозы, карбоксиалкилцеллюлозы, сложные эфиры целлюлозы (включая, например, нитроцеллюлозы) и тому подобное; микробные экзополимеры; а также структуры, содержащие подобные полимеры, например морские коллоиды и синтетические гидроколлоиды из полисахаридов. В одном предпочтительном варианте осуществления полисахарид или родственный полимер представляет собой поли- или сополи(сахарид), камедь или гликозаминогликан; предпочтительные камеди включают декстран; предпочтительные гликозаминогликаны включают гиалуроновую кислоту.
В одном варианте осуществления биоадгезивный полимер представляет собой поликарбоксилатный полимер, например, любой из следующих: поли(акрилатные и/или метакрилатные) полимеры; другие поли(кислотные) полимеры и карбоксилированные производные любого класса полимеров, такие как карбоксилированный полисахарид или родственный полимер, карбоксилированный полипептид (например, поли(кислая боковая цепь)пептид) или карбоксилированный сложный полиэфир. Примеры карбоксилированных полисахаридов и родственных полимеров включают альгинаты, карбоксиметилированные полисахариды (например, карбоксиметилкрахмал, карбоксиметилцеллюлоза), гиалуронаты, окисленные полисахариды (например, окисленный крахмал, окисленная гуаровая камедь), пектаты, полиаспартат, полиглютаматы, ксантаны и тому подобное.
Полимеры, которые прикрепляют к ядру, можно химически модифицировать для усиления биоадгезивности. Например, полимеры можно модифицировать, изменяя количество отрицательно заряженных (например, карбоксилатных) групп и/или положительно заряженных (например, амино) групп, находящихся на поверхности полимера. Такие модификации можно осуществлять для того, чтобы усиливать способность полимера прикрепляться к заряженным поверхностным областям зубных тканей. Например, незащищенные участки зубной эмали могут иметь целый ряд положительно заряженных поверхностных доменов, тогда как покрытые гликопротеинами слюны зоны на эмали часто имеют отрицательно заряженные домены. Полимеры, обладающие, соответственно, отрицательными или положительными зарядами, то есть в условиях применения, можно выбирать, готовить или модифицировать, получая, таким образом, преимущественную степень прикрепления полимера к таким поверхностным зарядам. Химические модификации полимеров можно осуществлять, используя любой из подходящих способов химического связывания, известных в данной области, таких как те, что описаны в патентной заявке США номер публикации 2005/064027 A1 авторов Jacob et al., содержание которой включено сюда в качестве ссылки.
В одном варианте осуществления биоадгезивный полимер представляет собой гидрофильный биоадгезивный полимер. В одном варианте осуществления гидрофильный биоадгезивный полимер представляет собой любой, который обеспечивает адгезивный эффект, когда откладывается на поверхности или прикрепляется к ней в водной среде; предпочтительно он представляет собой гидрофильный полимер, который способен образовывать гидрогели (включая, например, истинные гели, микрогели, квазигели, псевдогели и тому подобное) или гидроколлоиды.
Подходящими биоадгезивными полимерами для присоединения к ядру частицы являются такие, которые способны физически или химически прикрепляться к ядру частицы таким образом, что в условиях применения полимер не отделяется от ядра в течение примерно 3 часов или больше, и предпочтительно до тех пор, пока, например, ядро не разрушится или полимер химически или биологически не гидролизуется компонентами окружающей среды.
В одном варианте осуществления биоадгезивный полимер является ковалентно связанным с ядром. В одном варианте осуществления биоадгезивный полимер является ковалентно связанным с фрагментом, который представляет собой линкер, который сам ковалентно или нековалентно связан с ядром. Такой линкер можно сначала присоединять к ядру, а затем приводить в контакт с биоадгезивным полимером, или можно сначала присоединять к биоадгезивному полимеру, а затем приводить в контакт с ядром. Все три компонента можно последовательно присоединять друг к другу. Альтернативно, первый линкер можно присоединять к ядру, а второй линкер можно независимо присоединять к полимеру, первый и второй линкеры совместно обладают парой реакционно-способных групп, которые можно связывать ковалентно, или совместно образуют нековалентно взаимодействующие поверхности, которые образуют стабильное нековалентное связывание; вслед за этим приводят в контакт модифицированные ядра и модифицированные полимеры. Альтернативно, ядро частицы можно ковалентно связывать с линкером, который способен образовывать стабильную нековалентную связь с биоадгезивным полимером.
В вариантах осуществления, в которых биоадгезивный полимер является ковалентно связанным либо с линкером, либо непосредственно с поверхностью ядра, полимер обладает, по меньшей мере, одной реакционно-способной группой, которая используется в реакции для создания ковалентной связи, например, любой из следующих: карбонильная группа, такая как альдегидная группа; аминогруппа, такая как первичная аминогруппа, кислая группа или производное, такое как амид или сложный эфир, например карбоновая кислота, амид или сложный эфир; гидроксидная группа и тому подобное. В одном варианте осуществления предпочтительный биоадгезивный полимер представляет собой такой, который содержит или который был модифицирован, чтобы содержать группу(ы) альдегида или карбоновой кислоты.
В ситуации с любым из биополимеров, у которых отсутствует желательная реакционно-способная группа, когда выбирают биоадгезивный полимер, который не обладает карбонильной или кислой группами, или любыми группами альдегида или карбоновой кислоты в частности (при желании), или не обладает числом карбонильных или кислых групп, достаточным для целей специалиста, тогда полимер предварительно обрабатывают для создания подобной группы(групп), прежде чем проводить реакцию для связывания полимера с ядром частицы или с линкером. Таким же образом, если выбирают другой химический способ связывания, реакционно-способные группы могут уже присутствовать в полимере и ядре частицы, или их можно туда добавлять посредством предварительной обработки.
Таким образом, можно альтернативно использовать другие способы химического связывания, при которых полимер и ядро частицы или линкер вместе образуют пару реакционно-способных групп, при этом одна из двух представляет собой нуклеофильную группу, а другая представляет собой электрофильную группу. Нуклеофильные и электрофильные группы могут уже присутствовать на ядре частицы или линкере, или полимере, либо ядро частицы или линкер и/или полимер можно обрабатывать для их создания, применяя любой из множества химических способов, применимых для этих целей в данной области. Репрезентативные примеры подобных химических способов включают те, что используют пары нуклеофильных и электрофильных групп, такие как те, что перечислены в таблице.
В одном предпочтительном варианте осуществления пара реакционно-способных групп представляет собой аминогруппу, относящуюся к ядру частицы, и полимерную альдегидную группу, с которой она образует шиффово основание, которое затем восстанавливают (например, используя цианоборгидратную соль) для получения вторичной аминосвязи. В одном предпочтительном варианте осуществления пара реакционно-способных групп представляет собой аминогруппу, относящуюся к ядру частицы, и полимерную кислую группу, которую модифицировали способом с использованием химической реакции с карбодиимидом для получения сукцинимидного сложного эфира.
Группа молекул биоадгезивного полимера, сопряженных с ядром(ами) частиц, может включать больше чем один тип полимера, и/или больше чем один тип связывания с ядром частицы. Например, ядро частицы может иметь участки связывания различной длины, к которым присоединяется полимер(ы), или различные электрофильные или нуклеофильные группы могут присутствовать на поверхности ядра частицы или на дальнем конце линкера таким образом, что применяют множество различных химических реакций для прикрепления туда полимера(ов).
В варианте осуществления, в котором на ядре частицы присутствует аминогруппа для реакции связывания, она предпочтительно представляет собой связанную первичную или вторичную аминогруппу, предпочтительно связанную первичную аминогруппу, которую добавили на поверхность ядра частицы посредством предварительной обработки с помощью содержащего аминогруппу средства. Предпочтительные содержащие аминогруппы средства для данных целей включают, например, аминосиликоновые соединения.
В одном предпочтительном варианте осуществления аминосиликоновое соединение представляет собой (омега-аминоалифатил)-три(алифатокси)силоксан формулы
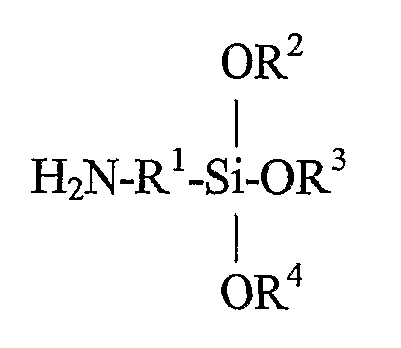
где R1 представляет собой C1-C8 гомо- или гетероуглеводородную группу, а R2, R3 и R4 независимо выбирают из C1-C8 гомо- или гетероуглеводородных групп, и в том и в другом случае углеводород обозначает циклические, алициклические, разветвленные и линейные углеводороды. Как используют здесь, термин «C1 гомо- или гетероуглеводородная группа» обозначает органические группы, содержащие один атом углерода, примеры которых включают -CH3-, -CH2-, -CH2SiH2-.
В одном варианте осуществления с его использованием R1 выбирают из C1-C8 алифатических (включая циклоалифатические) групп. В одном варианте осуществления R2, R3, и R4 независимо выбирают из C1-C8 алифатических групп.
В одном варианте осуществления с его использованием R1 выбирают из C1-C5 алкильных групп. В одном варианте осуществления R2, R3 и R4 независимо выбирают из C1-C5 алкильных групп. В одном варианте осуществления выбранная R1 группа является большей, чем любая из выбранных групп для R2, R3 и R4. В одном варианте осуществления R2 и R4 представляют собой идентичные группы. В одном варианте осуществления R2, R3 и R4 представляют собой идентичные группы. В одном варианте осуществления R1 представляет собой C1-, C2-, C3- или C4-группу; предпочтительно н-пропа-1,3-диил группу. В одном варианте осуществления R2, R3 и R4 независимо представляют собой этил или метил; предпочтительно R2, R3 и R4, все, представляют собой этил или все представляют собой метил.
Предпочтительные примеры применимых (омега-аминоалкил)триалкоксисилоксанов включают 3-аминопропилтриэтоксисилан, H2N(CH2)3Si(OCH2CH3)3; 3-аминопропилтриметоксисилан, H2N(CH2)3Si(OCH3)3; 2-аминоэтилтриметоксисилан, H2N(CH2)2Si(OCH3)3 и 2-аминоэтилтриэтоксисилан, H2N(CH2)2Si(OCH2CH3)3.
Условия реакций, используемых для предварительной обработки частиц и для реакций связывания, хорошо известны в данной области. Можно использовать любые подобные условия, такие как те, что описаны в приведенных ниже примерах.
Описанные здесь частицы можно предлагать для использования в форме содержащей их композиции. Композиция по настоящему изобретению может содержать смесь различных частиц, которые различаются между собой по особенностям материала ядра, пористости, размеру, морфологии, природе полимера или связыванию полимера с частицей.
Приведенная здесь композиция может представлять собой средство для ухода за зубами (например, пасту, гель, порошок или жидкое средство для ухода за зубами), профилактическую пасту, зубной краситель, пастилку, жевательную резинку или другой абразив, детергент, либо чистящую композицию, способную или самостоятельно, или в сочетании с действием аппликатора удалять отложения, такие как налет, с зубов и/или с мягких тканей ротовой полости. Аналогичные твердые, полутвердые и жидкие формы можно использовать для других местных и системных применений, например, в виде таблеток, капсул, мазей, кремов, гелеобразователей, лаважей, жидкостей для промывания хирургических поверхностей, парентеральных растворов и суспензий и суппозиториев. Композиции можно также составлять в виде красителей, аэрозолей, очищающих средств, дезинфицирующих растворов, средства для ополаскивания, и тому подобного, для промышленных или потребительских товаров.
Альтернативно, местную или оральную композицию можно разработать как композицию для обработки зубов после чистки, такую как полоскание для рта или зубной эликсир в виде жидкого геля, взвеси или суспензии. При оральном, местном и системном соматическом применениях композиция будет, соответственно, содержать орально, местно или системно приемлемые вещества. Такие вещества включают твердый, полутвердый или жидкий носитель и могут необязательно включать один или больше других активных ингредиентов, например, антибактериальных средств (например, нерастворимое в воде некатионное антибактериальное средство, такое как триклозан), антиоксидантов, фармацевтических препаратов, витаминов, источников фтористых соединений, нутрицевтиков и тому подобного; вспомогательных веществ и инертных ингредиентов, например смачивающих средств, желирующих компонентов, загустителей, растворителей, разбавителей, связующих, наполнителей, пластификаторов, средств, предотвращающих слеживание, дезинтегрирующих средств, камедей, мягчителей, продуктов переработки масел, красителей, ароматизаторов, отдушек, регулирующих рН средств (кислот, оснований), буферных растворов, поверхностно-активных веществ, эмульгаторов, суспендирующих средств, ферментов, покрытий (например, энтеросолюбильное, акриловое или углеводородное или целлюлозное покрытия), хелатирующих агентов, консервантов и тому подобного. Репрезентативные примеры подобных хорошо известных дополнительных средств описаны, например, в находящихся в процессе одновременного рассмотрения патентной заявке США серийный номер 60/639080 авторов Worrell et al. на средство для ухода за зубами, содержащее экстракт зеленого чая (внесенной в реестр 23 декабря 2004 г.); 60/639331 авторов Хu et al. на композиции для ухода за полостью рта, содержащие флавоноиды и флаваны (внесенной в реестр 22 декабря 2004 г.), и 60/639169 авторов Boyd et al. на оральные композиции, содержащие экстракт чая улунг (внесенной в реестр 23 декабря 2004 г.); а также в L.V.Alien Jr., The Art, Science, and Technology of Pharmaceutical Compounding (2е издание, 2003); J.G.Hardman et al., Goodman & Gilman's The Pharmacological Basis of Therapeutics (10е издание, 2001); и R.C. Rowe et al., Handbook of Pharmaceutical Excipients (4е издание, 2003); полное содержание каждой из которых включено сюда в качестве ссылки.
Композиция по настоящему изобретению содержит носитель. Носители обычно представляют собой воду, водное смачивающее средство и/или водно-спиртовые смеси консистенции, подходящей для выбранного способа введения композиции, например, в виде пасты, геля, таблетки, пастилки, сиропа, полоскания и так далее. Носители для оральных композиций по настоящему изобретению включают все известные в данной области.
Такие орально приемлемые носители включают обычные компоненты зубных паст, зубных порошков, профилактических паст, полосканий для рта, пастилок, жевательных резинок и тому подобного, и более полно описаны далее в данном документе. Выбор конкретных компонентов-носителей зависит от желаемой формы продукта, включая средства для ухода за зубами, полоскания, гели и кондитерские изделия.
В различных вариантах осуществления орально приемлемый носитель для средств ухода за зубами, используемый для получения оральной композиции, содержит водную фазу. Как очевидно для специалиста в данной области, оральные композиции по настоящему изобретению могут содержать другие материалы, такие как, например, модификаторы вязкости, разбавители, поверхностно-активные вещества, такие как поверхностно-активные вещества, эмульгаторы и регуляторы пенообразования, рН-модифицирующие средства, абразивы, смачивающие средства, мягчители и увлажнители, средства для разжевывания, подсластители, отдушки, красители, консерванты и их сочетания. Является очевидным, что в то время как основные характеристики каждой из вышеперечисленных категорий материалов могут различаться, могут существовать некоторые общие характерные признаки, и любой из материалов может служить многим целям в рамках двух или более подобных категорий материалов. Предпочтительно такие материалы-носители выбирают с точки зрения сочетаемости с частицами, а также с другими ингредиентами композиции.
В случае полосканий для рта, аэрозолей или эликсиров орально приемлемые носители обычно содержат водную фазу, представляющую собой воду или смесь воды и спирта. Кроме того, в различных вариантах осуществления оральный носитель содержит смачивающее средство и/или ПАВ. Обычно весовое соотношение воды и спирта находится в пределах от примерно 1:1 до примерно 20:1, предпочтительно от примерно 3:1 до 10:1 и более предпочтительно от примерно 4:1 до примерно 6:1. Общее количество водно-спиртовой смеси в данном типе препарата обычно находится в пределах от примерно 70 до примерно 99,9% препарата. В различных вариантах осуществления спирт обычно представляет собой этанол или изопропанол. Значение рН такой жидкости и других препаратов по изобретению обычно находится в пределах от примерно 4,5 до примерно 10, какое можно получить и/или поддерживать с помощью регулирующего рН средства (кислоты или основания) и/или буферного раствора, такого как цитрат, бензоат, карбонат или бикарбонат натрия, двузамещенного фосфата натрия или однозамещенного фосфата натрия.
В случае, например, пастилок, таблеток и гранул орально приемлемый носитель может представлять собой некариесогенный твердый водорастворимый многоатомный спирт (полиол), такой как маннитол, ксилитол, сорбитол, малитол, гидрогенизированный гидролизат крахмала, гидрогенизированная глюкоза, гидрогенизированные дисахариды или гидрогенизированные полисахариды, в количестве от примерно 85 до примерно 95% от всей композиции. Эмульгаторы, такие как глицерин и смазывающие вещества для изготовления таблеток, в незначительных количествах от примерно 0,1 до 5% можно вводить в состав препарата для таблетки, гранулы или пастилки для облегчения изготовления таблеток, гранул или пастилок. В случае средств для ухода за зубами, включая зубные порошки, зубные пасты (зубные кремы) и гели, орально приемлемый носитель может содержать воду и смачивающее средство обычно в количествах, находящихся в пределах от примерно 10% до примерно 80% от оральной композиции.
В одном варианте осуществления композиция по настоящему изобретению составленная для использования в соответствии с выбранным конечным применением содержит количество частиц, которое составляет примерно 50% или меньше по весу от композиции, либо примерно или меньше, чем 40%, 30%, 20% или 10% от композиции. В одном варианте осуществления композиция содержит от примерно 1% до примерно 10% по весу от композиции, более предпочтительно примерно 5%. Композиции, описанные здесь, можно также предоставлять в виде концентрированных заранее составленных смесей или частицы можно предоставлять отдельно в замороженной, сухой или лиофилизированной форме с инструкциями по способу их использования для получения конечного препарата для применения. В подобных композициях композиция может содержать более чем 50%, и вплоть до 100% от ее веса.
Частицы по настоящему изобретению являются применимыми для эффективной доставки биоадгезивных полимеров к поверхностям ротовой полости, где они прикрепляются, чтобы препятствовать прикреплению или адгезии бактерий. Предпочтительно орально приемлемую композицию, содержащую частицы, применяют к ротовой полости посредством создания контакта поверхности(ей) ротовой полости с композицией. В варианте осуществления частицы, введенные в ротовую полость либо в процессе, либо после чистки поверхностей ротовой полости, могут задерживаться, оседая на очищенных поверхностях ротовой полости, чтобы ингибировать или уменьшать прикрепление бактерий, образование налета и тому подобное. Описанные здесь композиции можно также применять для предотвращения или уменьшения прикрепления бактерий к волосам кожи, медицинским имплантатам, стентам, системам для внутривенного введения, инструментам и тому подобному.
Описанные здесь композиции можно также применять для предотвращения или уменьшения образования биопленок или адгезии микробов в контекстах, отличных от орального, местного, системного или даже соматического применения. Например, можно уменьшать образование биопленок, адгезию микробов и биообрастание в морских и пресноводных условиях, или в водных системах эксплуатации (хранения или транспортировки) или обработки, посредством применения подобной композиции к тем поверхностям, которые находятся или будут приведены в контакт с водной средой. Подобные композиции можно также применять в качестве средств для облегчения удаления биопленок, таких как для использования на многоразовых компонентах морских, пресноводных и водных систем эксплуатации или обработки, например ячеистых экранах, фильтровальных пластинах, фильтрующих элементах и тому подобном.
Такие композиции можно применять к компонентам промышленных и бытовых систем для ингибирования образования биопленок и/или создания средства для удаления биопленок, чтобы облегчить удаление, например, плесени, водорослей, грибков, бактерий и органических нечистот в процессе очистки. Например, композиции можно успешно использовать, например, для лодок, кораблей, паромов, плавучих платформ, понтонных мостов, доков, поверхностей для обработки пищевых продуктов, цементного раствора, раковин, водопроводных кранов, водных фонтанов и резервуаров, купален для птиц, плавательных бассейнов и вспомогательных принадлежностей (например, трапов, горок), увлажнителей воздуха, сливных отверстий и труб, резервуаров для хранения, водяных насосов и перемешивающих лопастей, пробок сливных отверстий и сетчатых фильтров, поддонов для конденсата, унитазов, санузлов, настилов для ванной и других принадлежностей для ванной (полок, ковриков для ног, занавесок для душа), покрытий для ванн и бассейнов, полозков задвижных дверей, кабинок для ванны и душа, поверхностей в аквариумах, бутылок и мисок для поения животных, и тому подобное.
Таким образом, в одном способе по настоящему изобретению композицию, содержащую заявленные частицы, применяют к поверхности, на которой отложение частиц является желательным. Неотложившиеся ингредиенты композиции могут в дальнейшем оставаться в контакте с поверхностью, но чаще всего они смываются или биоабсорбируются. В одном предпочтительном варианте осуществления композиция представляет собой чистящую композицию (например, абразивную и/или детергентную композицию), предназначенную для очистки поверхности, например, мытья. В одном варианте осуществления композиция позволяет частицам откладываться на новой или уже очищенной поверхности, например, при споласкивании.
В способе по настоящему изобретению заявленные частицы получают при помощи метода, включающего получение ядра, биоадгезивного полимера и, при желании, линкера, и присоединение биоадгезивного полимера к ядру.
ПРИМЕРЫ
Пример 1 - Предварительная обработка частиц для добавления связанных аминогрупп
SiO2 (ZEODENT® диоксид кремния, средний диаметр частиц 8-16 мкм, поставщик J.M Huber Corp., Edison, NJ, USA) чисто протравливали сильным разъедающим раствором H2SO4/H2O2 (75%/25% об./об.). Затем SiO2 модифицировали наслаиванием 3-аминопропилтриэтоксисилана (APTES). Хотя наслаивание при помощи раствора является предпочтительным, вместо этого можно использовать наслаивание при помощи пара. Наслаивание при помощи пара проводят в строгих безводных условиях, которые можно создавать, например, используя сухую защитную камеру с перчатками, чтобы избежать нежелательных реакций гидролиза. Наслаивание при помощи раствора в кислых условиях представляет собой более широко применимый способ. При данном подходе SiO2 диспергируют в дистиллированной H2O и значение pH полученного раствора доводят до примерно 6,5 с помощью HNO3. Затем суспензию перемешивают в течение 1 часа, после чего добавляют 1 мл APTES и суспензию вновь перемешивают. После перемешивания в течение 24 часов избыток APTES удаляют фильтрованием и промывают этанолом и ацетоном. Перекрестная сшивка наслоенных молекул APTES является желательной. Чтобы способствовать перекрестной сшивке (то есть, конденсации) отдельных молекул APTES на поверхности SiO2, модифицированный диоксид кремния высушивают при 800°C предпочтительно в течение примерно 8 часов. Частицы ZnO можно обрабатывать аналогичным образом для получения подвешенных аминогрупп.
Пример 2 - Получение частиц, конъюгированных с полисахаридной камедью
Камедь микробного происхождения, декстран, ковалентно связывают с модифицированными аминогруппами ядрами частиц, полученными по примеру 1, то есть модифицированными APTES частицами SiO2 (далее SiO2+APTES). Полисахарид сначала предварительно обрабатывают для создания на нем карбонильных групп. Как показано на фиг.1, декстран обрабатывают периодатом натрия (NaIO4) для окисления сахаридного кольца(колец), с образованием альдегидных карбонильных групп и высвобождением муравьиной кислоты. Продукт реакции окисления представляет собой диальдегид, соответствующий (2). Связанный с поверхностью APTES способен к восстановительному аминированию (2) с образованием шиффова основания (структура не представлена), которое восстанавливают при помощи цианоборгидрата натрия (NaBH3CN) с образованием стабильной вторичной аминосвязи. Поскольку степень окисления декстрана обуславливает количество полученного (2), она также обуславливает плотность прививки (то есть, число связей) между декстраном и SiO2+APTES. Для того чтобы оптимизировать плотность прививки декстрана, использовали различные временные интервалы для окисления декстрана, например: 0,5, 1, 2, 4 и 24 часа. Другими экспериментальными параметрами, которые принимают во внимание, являются размер (то есть, молекулярный вес) и полидисперсность (то есть, величина разброса молекулярных весов) декстрана. Эти два структурных свойства также влияют на степень взаимодействия между отдельными частицами SiO2. Результатом являются связанные с декстраном частицы SiO2.
Пример 3 - Получение частиц, конъюгированных с гликозаминогликаном
Гиалуронат (HA) ковалентно прививают к частицам, далее называемым SiO2+APTES, полученным по способу примера 1. Поскольку НА обладает карбоксилатными функциональными группами, для прививания нет необходимости в предварительной модификации. Ковалентное связывание гиалуроната с SiO2+APTES осуществляют в результате химической реакции сочетания с N-этил-N'-(3-диметиламинопропил)карбодиимид(EDC)/N-гидроксисукцинимидом (NHS) (см. фиг.2). Плотность прививки гиалуроната на SiO2+APTES регулируют, изменяя соотношение EDC/NHS.
Следует заметить, что для НА периодатную химическую реакцию, такую как описано в примере 2, можно альтернативно использовать для создания альдегидных карбонильных групп, чтобы получить производное НА, которое можно ковалентно связывать с ядром частицы посредством реакции, в которой задействованы такие карбонильные группы. Аналогично, полимеры, обладающие первичными аминогруппами, гидроксильными группами или кислыми (или сложноэфирными или амидными) группами, можно ковалентно связывать с необработанным или модифицированным ядром частицы по реакции, в которой принимает участие любая одна или большее количество этих химических групп, присутствующих в полимере, с соответствующей реакционно-способной парной группой, присутствующей на ядре частицы.
Полностью способ модификации представлен схематически на фиг.3, которая иллюстрирует получение частиц SiO2+APTES, конъюгированных с производным декстрана, как описано в примере 2, или с остатками НА, как описано в примере 3.
Предпочтительные концентрации частиц в орально приемлемой композиции можно определять посредством рутинного анализа серий тестовых композиций, содержащих, например, различные концентрации частиц любого заданного размера(ов) или диапазона(ов) размеров, с которыми конъюгировали полимер(ы), например, при ряде условий, таких как степень предварительной обработки полимера или ядра частицы, или время, отведенное для реакции конъюгации. Величину или степень ингибирования прикрепления бактерий во рту или в модели ротовой полости (такой как «искусственный рот»), обработанных композициями, можно оценивать количественным или полуколичественным анализом, таким как при помощи колориметрического метода для оценки скопления бактерий или образования налета на гидроксиапатитных дисках.
Группа изобретений относится к области средств для ухода за зубами и полостью рта. Предложена оральная композиция, включающая частицы, обладающие ядрами, содержащими оксид цинка или диоксид кремния, где внешняя поверхность ядра связана с биоадгезивным полимером с помощью линкера, который содержит аминосиликоновую группу. Композиция включает орально приемлемый носитель и может быть выполнена в форме средства для ухода за зубами, зубного красителя, пастилки или кондитерского изделия. Предложены также способы обработки поверхностей ротовой полости с применением указанной композиции. Использование средств, включающих вышеуказанные частицы, обеспечивает ингибирование или уменьшение образования налета на поверхности ротовой полости, а также ингибирование или уменьшение отложения биопленки или прикрепления микробов к поверхности ротовой полости. 5 н. и 8 з.п. ф-лы, 3 ил., 1 табл.
1. Оральная композиция, содержащая
частицы, содержащие
ядро, содержащее оксидное соединение, выбранное из SiO2 и ZnO, и биоадгезивный полимер, где биоадгезивный полимер связан с внешней поверхностью ядра при помощи линкера, где линкер содержит аминосиликоновую группу; и орально приемлемый носитель,
где указанная композиция находится в форме средства для ухода за зубами, зубного красителя, пастилки или кондитерского изделия.
2. Оральная композиция по п.1, где биоадгезивный полимер выбирают из полисахарида, полипептида, полиангидридного полимера или поликарбоксилатного полимера.
3. Оральная композиция по п.1, где биоадгезивный полимер выбирают из полисахарида и поликарбоксилатного полимера.
4. Оральная композиция по п.1, где биоадгезивный полимер выбирают из замещенного или незамещенного поли(сахаридного) полимера, поли(дезоксисахаридного) полимера, полимера поли(сахарной кислоты), полимера поли(сахарного спирта), полимера акриловой или другой поликислоты и карбоксиалкилполисахарида.
5. Оральная композиция по п.1, где биоадгезивный полимер выбирают из целлюлозы, хитозана, крахмала, гликогена, замещенного сахаридного полимера и микробного экссудата.
6. Оральная композиция по п.1, где биоадгезивный полимер выбирают из полисахаридной камеди и гликозаминогликана.
7. Оральная композиция по п.1, где биоадгезивный полимер выбирают из декстрана и гиалуроната.
8. Способ ингибирования или уменьшения образования налета на поверхности ротовой полости, включающий контактирование поверхности ротовой полости с оральной композицией по п.1.
9. Способ ингибирования или уменьшения прикрепления бактерий к поверхности ротовой полости, включающий контактирование поверхности ротовой полости с оральной композицией по п.1.
10. Способ поддержания или стимуляции общего здорового состояния млекопитающего, включающий нанесение оральной композиции по п.1 на поверхность ротовой полости.
11. Способ ингибирования или уменьшения отложения биопленки или прикрепления микробов к поверхности ротовой полости, включающий контактирование поверхности с оральной композицией по п.1.
12. Оральная композиция по п.1, где линкер, содержащий аминосиликоновую группу, выбирают из группы, включающей 3-аминопропилтриметоксисилан, 3-аминопропилтриэтоксисилан, 2-аминоэтилтриметоксисилан, и 2-аминоэтилтриэтоксисилан.
13. Оральная композиция по п.12, где линкер, содержащий аминосиликоновую группу, представляет собой 3-аминопропилтриэтоксисилан.
| Механизм наклона печи | 1978 |
|
SU737470A1 |
| US 5547682 А, 20.08.1996 | |||
| ЕР 0625353 A1, 23.11.1994 | |||
| US 2002028455 A1, 07.03.2002 | |||
| БИОАДГЕЗИВНАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), СПОСОБ ЕЕ ПОЛУЧЕНИЯ (ВАРИАНТЫ), УСТРОЙСТВО ДЛЯ ДОСТАВКИ ЧЕРЕЗ СЛИЗИСТУЮ ОБОЛОЧКУ АКТИВНОГО АГЕНТА, СПОСОБ ПРОЛОНГИРОВАННОГО МЕСТНОГО ВВЕДЕНИЯ ОДНОГО ИЛИ БОЛЕЕ АКТИВНЫХ АГЕНТОВ СУБЪЕКТУ (ВАРИАНТЫ) И СПОСОБ СОКРАЩЕНИЯ ВРЕМЕНИ, ТРЕБУЕМОГО ДЛЯ ПРИКЛЕИВАНИЯ КОМПОЗИЦИИ К СЛИЗИСТОЙ ТКАНИ | 1998 |
|
RU2234337C2 |
| US 2005064027 A1, 24.03.2005 | |||
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| СОСТАВ ДЛЯ ОБРАБОТКИ ПОРИСТОЙ ПОВЕРХНОСТИ | 1995 |
|
RU2074275C1 |
| WO 2005030141 A2, 07.04.2005 | |||
| ХИМИЧЕСКАЯ ЭНЦИКЛОПЕДИЯ, т.3 | |||
| Большая Российская энциклопедия | |||
| - М., 1992, с.353. | |||
Авторы
Даты
2011-09-10—Публикация
2006-11-10—Подача