Область техники
Настоящее изобретение в общем имеет отношение к электрохимической энергетике, а в частности имеет отношение к химическим источникам электрической энергии (к гальваническим элементам или батареям), которые имеют отрицательные электроды, изготовленные из щелочных металлов, и положительные электроды, содержащие серу и/или неорганические соединения на базе серы или органические (в том числе полимерные) соединения на базе серы в качестве материала деполяризатора электрода.
Предпосылки к созданию изобретения
Литий-серная электрохимическая система имеет высокую теоретическую удельную энергию, составляющую 2600 Wh/kg (ватт-часов на кг) (D.Linden, T.B.Reddy, Handbook of batteries, third ed., McGraw-Hill, New-York, 2001), и поэтому в настоящее время представляет большой интерес. Удельную энергию определяют как отношение энергии, вырабатываемой гальваническим элементом или батареей, к весу и выражают ее в ватт-часах на кг (Wh/kg). Термин удельная энергия эквивалентен термину гравиметрическая плотность энергии.
Уже было предложено использовать различные материалы в качестве материала деполяризатора положительного электрода в литий-серных батареях, в том числе: элементарную серу (US 5,789,108; US 5,814,420), сераорганические соединения (US 6,090,504), содержащие серу полимеры (US 6,201,100; US 6.174,621; US 6.117,590) и растворы полисульфидов серы или лития в апротонных системах электролита (Rauh R.D., Abraham K.M., Pearson G.F., Surprenant J.K., Brummer S.B.: "A lithium/dissolved sulfur battery with organic electrolyte", J.Electrochem. Soc. 1979, vol.126, no.4, pp.523-527; Yamin H., Peled E.: "Electrochemistry of nonaqueous lithium/sulfur cell", J. of Power Sources, 1983, vol.9, pp.281-287).
Растворы солей лития в апротонных биполярных растворителях (а типично в линейных или циклических эфирах) или их смеси уже используют в качестве электролитов в литий-серных батареях (Yamin H., Penciner J., Gorenshtain., Elam M., Peled E.: "The electrochemical behavior of polysulphides in tetrahydrofuran", J. of Power Sources, 1985, vol.14, pp.129-134; Yamin H., Gorenshtein., Penciner J., Stemberg Y., Peled E.: "Lithium sulfur battery. Oxidation/reduction mechanisms of polysulphides in THF solution", J Electrochem Soc., 1988, vol. 135, no.5, pp.1045-1048; Duck-Rye Chang, Suck-Hyun Lee, Sun-Wook Kim, Hee-Tak Kim: "Binary electrolyte based on tetra(ethylene glycol) dimethyl etner and 1,3-dioxolane for lithium-sulfur battery", J. of Power Sources, 2002, vol.112, pp.452-460).
Практическая удельная энергия типичного химического источника электрической энергии обычно достигает 20-30% теоретического максимального значения удельной энергии используемой электрохимической системы. Это происходит потому, что различные вспомогательные элементы (сепаратор, коллекторы тока электродов, электролит и другие компоненты) батареи увеличивают ее вес в дополнение к электродным деполяризаторам. Вспомогательные элементы батареи сами участия в электрохимической реакции не принимают, однако они необходимы для облегчения протекания реакции и для содействия нормальному функционированию батареи.
Значение практической удельной энергии для лабораторных литий-серных гальванических элементов обычно достигает только 10-15% теоретического значения удельной энергии и типично составляет около 250-350 Wh/kg (J.Broadhead, T.Skotheim: "A safe, fast-charge, two-volt lithium/polymer cathode 'AA'-size cell with greater than 250 Wh kg-1 energy density". Journal of Power Sources, 65 (1997), 1-2, 213-218; Peled E., Gorenshtein., Segal M., Stemberg Y.: "Rechargeable lithium-sulfur battery (extended abstract)", J. of Power Sources, 1989, vol.26, pp.269-271).
Сущность изобретения
Если не учитывать вес вспомогательных элементов батареи, то можно сказать, что различие между теоретическим и практическим значениями удельной энергии лабораторных литий-серных гальванических элементов вызвано недостаточным использованием деполяризатора положительного электрода (серы или соединений на базе серы) и чрезмерным количеством обычно вводимого электролита.
Варианты настоящего изобретения направлены по меньшей мере в значительной степени на оптимизацию количества электролита в литий-серных гальванических элементах, чтобы за счет этого повысить их практическую удельную энергию.
Подробное описание изобретения
Удельная энергия химического источника электрической энергии определяется как теоретической удельной энергией выбранной электрохимической системы, так и весом вспомогательных компонентов, которые требуются для обеспечения надлежащей работы химического источника электрической энергии (например, таких как сепаратор, коллекторы тока электродов, связующий материал, токопроводящие добавки, электролит и другие компоненты), а также степенью (эффективностью) использования деполяризатора. Вес вспомогательных компонентов обычно составляет до 70-80% полного веса гальванического элемента. Для повышения значений удельной энергии необходимо снижать вес вспомогательных компонентов.
Вес электролита образует значительную часть полного веса химического источника электрической энергии. Электролит выполняет дополнительные функции в химических источниках электрической энергии с твердыми деполяризаторами, например поддерживает процесс электрохимической реакции и обеспечивает перенос ионов между электродами. Поэтому в таких системах желательно снижать до минимума количество электролита.
Однако в химических источниках электрической энергии, содержащих жидкие катоды, электролит может содержать раствор соли в жидком деполяризаторе (например, раствор тетрахлоралюмината лития в тионил хлориде), или раствор соли в смеси жидкого деполяризатора и апротонного растворителя (например, раствор бромида лития в смеси серного ангидрида и ацетонитрила), или раствор соли в растворе жидкого деполяризатора в апротонном растворителе (например раствор перхлората лития в растворе полисульфида лития в тетрагидрофуране) (D.Linden, T.B.Reddy: "Handbook of batteries", third ed., McGraw-Hill, New York, 2001).
Электролит в химических источниках электрической энергии, содержащих жидкие катоды, выполняет более широкий диапазон функций, чем электролит, используемый в системах, имеющих твердые катоды. Электролит не только поддерживает электрохимическую реакцию и обеспечивает перенос ионов между электродами, но служит в качестве растворителя для деполяризатора положительного электрода. Таким образом, когда апротонные растворители используют как компонент жидкого катода, характеристики удельной мощности химических источников электрической энергии с жидкими катодами зависят от содержания апротонных растворителей и, следовательно, от содержания жидкого катода.
Несмотря на то, что сера и сульфид лития плохо растворяются в апротонных растворителях, литий-серные батареи классифицируют как батареи с жидкими катодами. Это связано с тем, что в ходе зарядки и разрядки таких батарей образуются хорошо растворимые продукты.
Жидкий катод образуют в литий-серных батареях в ходе разрядки серного электрода. Электрохимическое окисление серы протекает в два этапа. На первой стадии полисульфиды лития с длинной цепью (которые хорошо растворимы в апротонных электролитах) образуются в ходе электрохимического окисления элементарной серы, которая нерастворима или плохо растворима в большинстве электролитных систем (Уравнение 1).
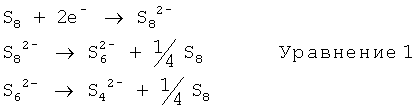
Раствор полисульфидов лития в электролите, который образуется на начальной фазе разрядки, является жидким катодом.
На второй стадии протекает электрохимическая реакция растворимых полисульфидов лития (Уравнение 2). Во время этой фазы образуются анионы сульфидов или дисульфидов, которые за счет реакции с катионами лития образуют нерастворимые продукты: сульфид лития и дисульфид лития.
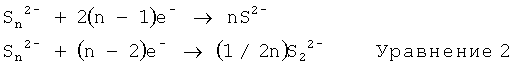
Восстановление растворимых полисульфидов лития сопровождается реакциями диспропорционирования (Уравнение 3).
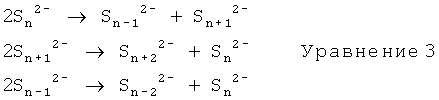
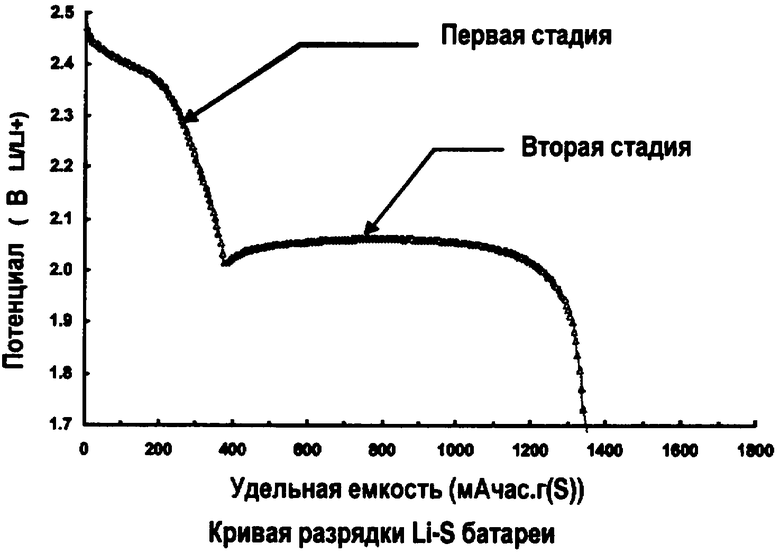
Двухэтапный механизм восстановления серы четко виден на кривых разрядки литий-серных батарей, показанных на чертеже. Эти кривые имеют две области разрядки: первую область при напряжении в диапазоне от 2.5-2.4 В до 2.1-1.9 В, которая соответствует первой фазе разрядки (Уравнение 1); и вторую область при напряжении в диапазоне от 2.1-1.9 В до 1.8-1.5 В, которая соответствует второй фазе разрядки (Уравнение 2).
Эффективность использования серы в литий-серных батареях определяется количественным отношением серы к электролиту.
Когда количество электролита является относительно низким, не вся сера и полисульфиды лития с длинной цепью претерпевают последующее электрохимическое восстановление по причине образования имеющих высокую вязкость насыщенных растворов полисульфидов. Это приводит к снижению практической удельной энергии литий-серных батарей.
Когда имеется избыток электролита, удельная энергия литий-серных батарей будет еще более низкой в сравнении с максимально возможной за счет количественного избытка электролита, который повышает полный вес гальванического элемента. Особое отношение серы к электролиту следует поддерживать для каждого типа электролита, чтобы достичь или по меньшей мере приблизиться к максимально возможной практической удельной энергии.
Это отношение зависит от свойств системы электролита. В частности, это отношение зависит от растворимости исходного, промежуточного и конечного компонентов.
Для достижения наилучших характеристик практической удельной энергии литий-серных батарей содержание электролита в батареях следует выбирать так, чтобы обеспечивать полное растворение полисульфидов лития (образованных на первой стадии) с образованием жидких катодов с умеренной вязкостью. Заявитель настоящего изобретения обнаружил, что такое условие выполняется в том случае, когда в ходе разрядки серного электрода концентрация растворимых полисульфидов лития в электролите составляет по меньшей мере 70%, а преимущественно от 70 до 90% концентрации насыщения.
В соответствии с настоящим изобретением предлагается химический источник электрической энергии, который содержит положительный электрод (катод), содержащий серу или органические соединения на базе серы, полимерные соединения на базе серы или неорганические соединения на базе серы в качестве деполяризатора, отрицательный электрод (анод), изготовленный из металлического лития или из содержащих литий сплавов, и электролит, содержащий раствор по меньшей мере одной соли по меньшей мере в одном апротонном растворителе, причем химический источник электрической энергии конфигурирован так, чтобы вырабатывать растворимые полисульфиды в электролите во время первой стадии двухстадийного процесса разрядки, отличающийся тем, что количество серы в деполяризаторе и объем электролита выбраны так, что после первой стадии разрядки катода концентрация растворимых полисульфидов лития в электролите составляет по меньшей мере 70% концентрации насыщения полисульфидов лития в электролите.
Преимущественно количество серы в положительном электроде и объем электролита выбраны так, что после первой стадии разрядки катода концентрация растворимых полисульфидов лития в электролите составляет от 70% до 90% концентрации насыщения полисульфидов лития в электролите.
В соответствии со специфическим вариантом деполяризатор содержит серу, углеродную сажу и полиэтилен оксид.
Электролит может содержать раствор одной или нескольких солей лития, выбранных из группы, в которую входят трифторметансульфонат лития, перхлорат лития, трифторметансульфонимид лития, гексафторфосфат лития, гексафторарсенат лития, тетрахлоралюминат лития, тетраалкиламмоний лития, хлорид лития, бромид лития и иодид лития; в одном или нескольких растворителях, выбранных из группы, в которую входят диоксолан, тетрагидрофуран, диметоксиэтан, диглим, триглим, тетраглим, диалкил карбонаты, сульфолан и бутиролактон.
В тексте описания настоящего изобретения и в формуле изобретения слова "содержит" и "включает в себя" и их производные, такие как, например, "содержащий", означают " включает в себя, но без ограничения " и не предназначены для того, чтобы исключать (и не исключают) использование других долей, добавок, компонентов, целых чисел или операций способа.
В тексте описания настоящего изобретения и в формуле изобретения использование единственного числа не исключает использование множественного числа, если только обратное не следует из контекста.
Характеристики, признаки, целые числа, соединения, химические доли или группы, описанные в сочетании с конкретным аспектом, вариантом или примером изобретения, применимы к любому другому его аспекту, варианту или примеру, если только нет несовместимости с ними.
Указанные ранее и другие характеристики изобретения будут более ясны из последующего детального описания, данного в качестве примера, не имеющего ограничительного характера и приведенного со ссылкой на сопроводительный чертеж.
Краткое описание чертежей
На чертеже показан график двухстадийного процесса разрядки литий-серной батареи в соответствии с вариантом настоящего изобретения.
ПРИМЕРЫ
Пример 1
Положительный электрод, содержащий 70% элементарной сублимированной серы (закупленной на фирме Fisher Scientific, Loughborough, Великобритания), 10% электропроводящей углеродной сажи (марки Ketjenblack® EC-600JD, закупленной на фирме Akzo Nobel Polymer Chemicals BV, Нидерланды) и 20% полиэтилен оксида (РЕО, молекулярная масса 4.000,000, закупленного на фирме Sigma-Aldrich Company Ltd., Gillingham, Великобритания), был получен при помощи следующего процесса.
Сухую смесь указанных компонентов размалывали в имеющей высокую скорость мельнице типа Microtron® MB550 в течение 10-15 минут. Затем к сухой смеси добавили ацетонитрил в качестве растворителя и суспензию перемешивали в течение 15-20 часов в лабораторной мешалке типа DLH. Содержание твердых веществ в суспензии составляет 10-15%. Полученную указанным образом суспензию наносили при помощи автоматического аппликатора пленки типа Elcometer® SPRL на одну сторону алюминиевой фольги толщиной 12 мкм, имеющей электропроводное углеродное покрытие (Продукт No. 60303, закупленный на фирме Rexam Graphics, South Hadley, Mass., США) в качестве коллектора тока.
Покрытие сушили в условиях окружающей среды в течение 20 часов и затем в вакууме при 50°С в течение 5 часов. Полученный сухой активный слой катода имеет толщину 19 мкм и содержит 2.01 мг/см2 катодной смеси. Удельная поверхностная емкость электрода составляет 2.35 мА* ч/см2.
Пример 2
Положительный электрод из Примера 1 был использован в небольшой сборке гальванических элементов, изготовленной из нержавеющей стали. Площадь поверхности катода составила 5.1 см2. Давление 400 кг/см2 было приложено к электроду до того, как он был использован в гальваническом элементе. Толщина катода после сжатия составила 16 мкм. 1.0М раствор трифторметансульфоната лития (закупленного на фирме 3М Corporation, St. Paul, Minn., США) в сульфолане был использован в качестве электролита. Материал Celgard® 2500 (торговая марка материала фирмы Tonen Chemical Corporation, Tokyo, Япония, который также может быть закуплен на фирме Mobil Chemical Company, Films Division, Pittsford, N.Y., США) был использован в качестве сепаратора. Эти компоненты были собраны для создания слоистой конструкции, содержащей положительный электрод/ сепаратор/ анод, вместе с жидким электролитом, заполняющим свободный объем сепаратора и положительного электрода. Сборку гальванических элементов производили следующим образом. Сначала был введен положительный электрод. Затем 4 микролитра электролита были нанесены на электрод с использованием шприца с постоянным расходом типа CR-700 (Hamilton Co). Сепаратор был помещен сверху на смоченный электрод и 3 микролитра электролита были нанесены на сепаратор. Затем литиевый электрод, изготовленный из литиевой фольги толщиной 38 мкм, был помещен сверху на сепаратор. После сборки электродного пакета гальванический элемент был герметично уплотнен при помощи крышки, имеющей уплотнение из тефлона. Отношение серы к электролиту составляет 1 мл электролита на 1 г серы. После полного растворения серы в виде полисульфида лития в ходе разрядки гальванического элемента измеренная максимальная концентрация серы в электролите составляет 31.25 моль на литр.
Циклы зарядки-разрядки гальванического элемента проводили при токе 1.5 мА, что было эквивалентно плотности тока 0.3 мА/см2, с напряжением отсечки разрядки 1.5 В и окончанием зарядки при 2.8 В. Полный вес гальванического элемента и распределение веса между компонентами гальванического элемента приведены в Таблице 1, а характеристики гальванического элемента показаны в Таблице 2.
Удельная энергия гальванического элемента была рассчитана из емкости на втором цикле путем деления емкости на вес электродного пакета, включая электролит.
Пример 3
Был собран литий-серный гальванический элемент аналогично тому, что описано в Примере 2, за исключением того, что 11 микролитров электролита были нанесены на положительный электрод и 3 микролитра электролита были нанесены на сепаратор. Полное содержание электролита в гальваническом элементе составляет 14 микролитров, что дает 2 мл электролита на 1 г серы. Циклические испытания гальванического элемента проводили аналогично описанному в Примере 2. Параметры гальванического элемента приведены в Таблицах 3 и 4.
Пример 4
Был собран литий-серный гальванический элемент аналогично тому, что описано в Примере 2, за исключением того, что 22 микролитра электролита были нанесены на положительный электрод и 3 микролитра электролита были нанесены на сепаратор. Полное содержание электролита в гальваническом элементе составляет 25 микролитров, что дает 3.5 мл электролита на 1 г серы. Циклические испытания гальванического элемента проводили аналогично описанному в Примере 2. Параметры гальванического элемента приведены в Таблицах 5 и 6.
Пример 5
Был собран литий-серный гальванический элемент аналогично тому, что описано в Примере 2, за исключением того, что 49 микролитров электролита были нанесены на положительный электрод и 3 микролитра электролита были нанесены на сепаратор. Полное содержание электролита в гальваническом элементе составляет 52 микролитра, что дает 5.2 мл электролита на 1 г серы. Циклические испытания гальванического элемента проводили аналогично описанному в Примере 2. Параметры гальванического элемента приведены в Таблицах 7 и 8.
Пример 6
Был собран литий-серный гальванический элемент аналогично тому, что описано в Примере 2, за исключением того, что 69 микролитров электролита были нанесены на положительный электрод и 3 микролитра электролита были нанесены на сепаратор. Полное содержание электролита в гальваническом элементе составляет 72 микролитра, что дает 7.2 мл электролита на 1 г серы. Циклические испытания гальванического элемента проводили аналогично описанному в Примере 2. Параметры гальванического элемента приведены в Таблицах 9 и 10.
Пример 7
Была проведена оценка конечной растворимости или растворимости насыщения серы в виде октасульфата лития в 1.0 М растворе трифторметансульфоната лития в сульфолане. Оценку растворимости проводили следующим образом: 1.0 г смеси сульфида лития и серы (при содержании серы в смеси 0.86 г) при молярном отношении 1:7 поместили в герметичный стеклянный реактор в воздушном термостате, причем указанный реактор был снабжен механическим смесителем и измерительным устройством. Температуру термостата повышали до 30°С. 1.0 М раствор трифторметансульфоната лития в сульфолане добавляли небольшими порциями в реактор при постоянном перемешивании. После добавления каждой новой порции реакционную смесь тщательно перемешивали в течение 5-6 часов, так чтобы установить термодинамическое равновесие. Растворимость твердой фазы оценивали визуально. Если реакционная смесь содержит некоторые остатки твердой фазы, то тогда добавляли дополнительную порцию электролита. Эксперимент проводили до полного растворения твердой фазы. Результаты показывают, что 1.0 г смеси сульфида лития и серы при молярном отношении 1:7 полностью растворяется в 3.3 мл раствора электролита; другими словами, было установлено, что растворимость серы в виде октосульфида лития составляет около 0.96М/ литр электролита.
Пример 8
Результаты Примеров 2-7 суммированы на чертеже, где показана зависимость удельной энергии голого литий-серного гальванического элемента от отношения электролита к сере. Можно видеть, что эта зависимость имеет максимум, который достигается при отношении электролита к сере около 3. Другими словами, максимальная емкость литий-серного гальванического элемента достигается при объемно-весовом отношении электролита к сере, которое близко к конечной растворимости или растворимости насыщения октосульфида лития в электролите.
Наличие максимума объясняется тем фактом, что при низких значениях отношения электролита к сере эффективность использования серы является низкой, в то время как при более высоких отношениях избыток электролита создает дополнительную массу гальванического элемента, в результате чего снижается удельная энергия.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭЛЕКТРОЛИТ И ХИМИЧЕСКИЙ ИСТОЧНИК ЭЛЕКТРИЧЕСКОЙ ЭНЕРГИИ | 2006 |
|
RU2402840C2 |
| ХИМИЧЕСКИЙ ИСТОЧНИК ЭЛЕКТРОЭНЕРГИИ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2006 |
|
RU2402842C2 |
| Способ получения литий-серного катода | 2022 |
|
RU2796628C2 |
| АККУМУЛЯТОРНАЯ БАТАРЕЯ НА ОСНОВЕ СЕРООРГАНИЧЕСКОГО СОЕДИНЕНИЯ | 2017 |
|
RU2755479C2 |
| ЭЛЕКТРОЛИТ ДЛЯ ЛИТИЙ-СЕРНЫХ АККУМУЛЯТОРОВ И ЛИТИЙ-СЕРНЫЕ АККУМУЛЯТОРЫ, В КОТОРЫХ ИСПОЛЬЗУЕТСЯ ЭТОТ ЭЛЕКТРОЛИТ | 2004 |
|
RU2321104C2 |
| Металл-серный проточный аккумулятор | 2023 |
|
RU2820527C2 |
| БАТАРЕЯ НА ОСНОВЕ СЕРАОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 2013 |
|
RU2702337C2 |
| БАТАРЕЯ НА ОСНОВЕ СЕРАОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 2013 |
|
RU2702115C2 |
| БАТАРЕЯ НА ОСНОВЕ СЕРАОРГАНИЧЕСКИХ СОЕДИНЕНИЙ | 2013 |
|
RU2669362C2 |
| ЭЛЕКТРОД, СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ И СОДЕРЖАЩАЯ ЕГО АККУМУЛЯТОРНАЯ БАТАРЕЯ | 2005 |
|
RU2352029C2 |
Изобретение относится к перезаряжаемому литий-серному химическому источнику электрической энергии. Техническим результатом изобретения является повышение удельной энергии. Согласно изобретению перезаряжаемый химический источник электрической энергии содержит положительный электрод (катод), содержащий серу или органические соединения на базе серы, полимерные соединения на базе серы или неорганические соединения на базе серы в качестве деполяризатора, отрицательный электрод (анод), изготовленный из металлического лития или из содержащих литий сплавов, и электролит, содержащий раствор по меньшей мере одной соли по меньшей мере в одном апротонном растворителе. Химический источник электрической энергии вырабатывает растворимые полисульфиды в электролите во время первой стадии двухстадийного процесса разрядки, причем количество серы в деполяризаторе и объем электролита выбраны так, что после первой стадии разрядки катода (до потенциала 2.1-1.9 В) концентрация растворимых полисульфидов лития в электролите составляет по меньшей мере 70% концентрации насыщения полисульфидов лития в электролите. 3 з.п. ф-лы, 10 табл., 1 ил.
1. Перезаряжаемый химический источник электрической энергии, который содержит положительный электрод (катод), содержащий серу или органические соединения на базе серы, полимерные соединения на базе серы или неорганические соединения на базе серы в качестве деполяризатора, отрицательный электрод (анод), изготовленный из металлического лития или из содержащих литий сплавов, и электролит, содержащий раствор по меньшей мере одной соли по меньшей мере в одном апротонном растворителе, причем химический источник электрической энергии вырабатывает растворимые полисульфиды в электролите во время первой стадии двухстадийного процесса разрядки, отличающийся тем, что количество серы в деполяризаторе и объем электролита выбраны так, что после первой стадии разрядки катода концентрация растворимых полисульфидов лития в электролите составляет по меньшей мере 70% концентрации насыщения полисульфидов лития в электролите.
2. Источник электрической энергии по п.1, в котором количество серы в деполяризаторе и объем электролита выбраны так, что после полной разрядки катода концентрация растворимых полисульфидов лития в электролите составляет от 70 до 90% концентрации насыщения полисульфидов лития в электролите.
3. Источник электрической энергии по п.1, в котором деполяризатор содержит серу, углеродную сажу и полиэтилен оксид.
4. Источник электрической энергии по одному из пп.1-3, в котором электролит содержит раствор одной или нескольких солей лития, выбранных из группы, в которую входят трифторметансульфонат лития, перхлорат лития, трифторметансульфонимид лития, гексафторфосфат лития, гексафторарсенат лития, тетрахлоралюминат лития, тетраалкиламмоний лития, хлорид лития, бромид лития и иодид лития; в одном или нескольких растворителях, выбранных из группы, в которую входят диоксолан, тетрагидрофуран, диметоксиэтан, диглим, триглим, тетраглим, диалкил карбонаты, сульфолан и бутиролактон.
| СИСТЕМА ПРИВОДА ДВЕРИ КАБИНЫ ЛИФТА | 1995 |
|
RU2084391C1 |
| Топчак-трактор для канатной вспашки | 1923 |
|
SU2002A1 |
| Устройство для разделения заготовок | 1982 |
|
SU1178555A1 |
| RU 99114422 А, 20.05.2001. | |||
Авторы
Даты
2011-10-20—Публикация
2006-09-21—Подача