Настоящее изобретение относится к новым соединениям, способам их получения, промежуточным соединениям, используемым при их получении, фармацевтическим композициям, содержащим их, и их применению при лечении в качестве модуляторов допаминовых рецепторов D3.
В WO 2002/40471 (SmithKline Beecham) раскрываются некоторые бензазепины, обладающие активностью в отношении допаминового рецептора D3.
Найден новый класс соединений, обладающих аффинностью в отношении допаминовых рецепторов, в частности рецептора D3. Указанные соединения потенциально применимы при лечении состояний, при которых благоприятна модуляция, в частности антигонизм/ингибирование, рецептора D3, например, для лечения лекарственной зависимости или в качестве антипсихотических средств.
Настоящее изобретение относится к соединению формулы (I)

или его соли,
где в указанной формуле
- G выбирают из группы, состоящей из фенила, пиридила, бензотиазолила, индазолила;
- р равен целому числу от 0 до 5;
- R1 выбирают независимо из группы, состоящей из галогена, гидрокси, циано, С1-4-алкила, галоген-С1-4-алкила, С1-4-алкокси, галонен-С1-4-алкокси, С1-4-алканоила; или R1 соответствует группе R5;
- R2 представляет собой водород или С1-4-алкил;
- R3 представляет собой С1-4-алкил;
- R4 представляет собой водород или фенильную группу, гетероциклильную группу, 5- или 6-членную гетероароматическую группу или 8-11-членную бициклическую группу, любая из которых необязательно замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, циано, С1-4-алкила, галоген-С1-4-алкила, С1-4-алкокси, С1-4-алканоила;
- R5 представляет собой фрагмент, выбранный из группы, состоящей из изоксазолила, -CH2-N-пирролила, 1,1-диоксидо-2-изотиазолидинила, тиенила, тиазолила, пиридила, 2-пирролидинонила, и такая группа необязательно замещена одним или двумя заместителями, выбранными из числа галогена, циано, С1-4-алкила, галоген-С1-4-алкила, С1-4-алкокси, С1-4-алканоила;
и когда R1 представляет собой хлор, и р равен 1, тогда R1 не находится в положении относительно связи с остальной частью молекулы; и когда R1 соответствует R5, р равен 1.
Предполагается, что в силу присутствия конденсированного циклопропана соединения формулы (I) имеют расположение заместителей "цис" (обе группы, связанные с бициклической системой, находятся в одной и той же плоскости такой бициклической системы).
В другом воплощении настоящее изобретение относится к соединениям формулы (I)', соответствующим соединениям формулы (I) с расположением "цис", характеризующимся отчетливым просветом между связями

где G, p, R1, R2, R3, R4 и R5 имеют значения, указанные выше для соединений формулы (I).
Следует иметь в виду, что соединения формулы (I)' обладают, по меньшей мере, двумя хиральными центрами, а именно в положениях 1 и 5 в 3-азабицикло[3.1.0]гексановой части молекулы. В силу фиксированного цисположения соединения могут существовать в виде двух стереоизомеров, которые являются энантиомерами относительно хиральных центров в циклопропане. Также следует иметь в виду, что подобно большинству биологически активных молекул, уровень биологической активности отдельных стереоизомеров данной молекулы может изменяться. Кроме того, объем изобретения включает отдельные стереоизомеры (диастереоизомеры и энантиомеры) и все их смеси, в том числе рацемические смеси и другие, которые демонстрируют подходящую биологическую активность в связи с процедурами, описанными в данном описании.
В соединениях формулы (I)' имеются, по меньшей мере, два хиральных центра, расположенных в циклопропановой части, как отображено ниже (отчетливый просвет между связями означает "цис"-конфигурацию).

Когда G представляет собой 2-пиридильное производное,
конфигурация становится (1R,5R) в силу приоритетов
номенклатуры Кана-Ингольда-Прелога.
В другом воплощении настоящее изобретение относится к соединениям формулы (IA), которые соответствуют стереохимическим изомерам соединений формулы (I)', обогащенным конфигурацией (1S,5R) или (1R,5R)
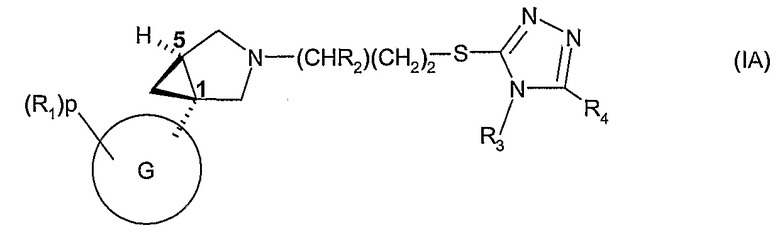
где G, p, R1, R2, R3, R4 и R5 имеют значения, указанные выше для соединений формулы (I), или их фармацевтически приемлемым солям.
В контексте настоящего изобретения подразумевается, что стереохимические изомеры, обогащенные конфигурацией (1S,5R) или (1R,5R) формулы (IA), соответствуют, в одном воплощении, по меньшей мере 90% э.и. (е.е.). В другом воплощении изомеры соответствуют по меньшей мере 95% э.и. В другом воплощении изомеры соответствуют по меньшей мере 99% э.и.
В другом воплощении настоящее изобретение относится к стереохимическим изомерам, обогащенным конфигурацией (1S,5R), к которым относятся
- 5-[5-({3-[(1R,5S)-1-(4-метоксифенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин - энантиомер 2;
- 5-[5-({3-[(1R,5S)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин - энантиомер 1;
- 5-[5-({3-[(1R,5S)-1-(4-трет-бутилфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин - энантиомер 1;
- (1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан - энантиомер 2;
- (1R,5S)-1-(3-хлорфенил)-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан - энантиомер 2;
- 1-[5-[(1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон - энантиомер 2;
- 2-метил-5-[(1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол - энантиомер 2; или их фармацевтически приемлемым солям.
Термин "5- или 6-членная гетероароматическая группа" относится к моноциклической 5- или 6-членной гетероциклической группе, содержащей 1, 2, 3 или 4 гетероатома, например, 1-3 гетероатома, выбранных из числа атомов O, N и S. Когда группа содержит 2-4 гетероатома, их можно выбрать из числа атомов O, N и S, а остальные гетероатомы могут являться атомами N. Примерами 5- или 6-членной гетероароматической группы являются пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, оксадиазолил, изотиазолил, тиазолил, фурил, тиенил, тиадиазолил, пиридил, триазолил, триазинил, пиридазинил, пиримидинил и пиразинил.
Термин "С1-4-алкил" относится к алкильной группе с одним-четырьмя атомами углерода во всех изомерных формах, такой как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил и трет-бутил. Термин "н-С1-4-алкил" относится к линейным алкилам, имеющим указанные выше значения.
Термин "С1-4-алкокси" относится к линейной или разветвленной алкокси(или "алкилокси")группе с одним-четырьмя атомами углерода, такой как метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси и трет-бутокси.
Термин "галоген" и его сокращение "гало" относятся к фтору (F), хлору (Cl), брому (Br) или йоду (I). Когда термин "галоген" используют перед другой группой, это указывает, что группа замещена одним, двумя, тремя или четырьмя атомами галогена. Например, термин "галоген-С1-4-алкил" относится к группам, таким как трифторметил, бромэтил, трифторпропил и другим группам, образованным от С1-4-алкильных групп, имеющих значения, указанные выше; и термин "галоген-С1-4-алкокси" относится к группам, таким как трифторметокси, бромэтокси, трифторпропокси и другим группам, образованным от С1-4-алкоксигрупп, имеющих значения, указанные выше.
Термин "8-11-членная бициклическая группа" относится к двухатомной циклической системе, содержащей в целом 8, 9, 10 или 11 атомов углерода, где 1, 2, 3, 4 или 5 атомов углерода, необязательно, заменены на гетероатомы, выбранные независимо из числа атомов О, S и N. Термин включает бициклические системы, где оба цикла являются ароматическими, а также бициклические системы, где один из циклов является частично или полностью насыщенным. Примеры 8-11-членных бициклических групп, где оба цикла являются ароматическими, включают инденил, нафтил и азуленил. Примеры 8-11-членных бициклических групп, содержащих 1, 2, 3, 4 или 5 гетероатомов, в которых оба цикла являются ароматическими, включают 6Н-тиено[2,3-b]пирролил, имидазо[2,1-b][1,3]тиазолил, имидазо[5,1-b][1,3]тиазолил, [1,3]тиазоло[3,2-b][1,2,3]тиазолил, индолил, изоиндолил, индазолил, бензимидазолил, например, бензимиазол-2-ил, бензоксазолил, например, бензоксазол-2-ил, бензизоксазолил, бензотиазолил, бензизотиазолил, бензотиенил, бензофуранил, нафтиридинил, хинолил, хиноксалинил, хиназолинил, циннолинил и изохинолил. Примеры 8-11-членных бициклических групп, содержащих 1, 2, 3, 4 или 5 гетероатомов, в которых один из циклов является частично или полностью насыщенным, включают дигидробензофуранил, инданил, тетрагидронафтил, индолинил, изоиндолинил, тетрагидроизохинолинил, тетрагидрохинолил, бензоксазинил и бензоазепинил.
Термин "гетероциклил" относится к 5- или 6-членной моноциклической или 8-11-членной бициклической группе, где 1, 2, 3, 4 или 5 атомов углерода заменены на гетероатомы, выбранные, независимо, из числа атомов О, S и N и которая является частично или полностью насыщенной. Примеры "гетероциклила", который представляет собой полностью насыщенный 5- или 6-членный одноатомный цикл, включают пирролидинил, имидазолидинил, пиразолидинил, изотиазолил, тиазолил, тетрагидрофуранил, диоксоланил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, тетрагидротиенил, диоксанил, тетерагидро-2Н-пиранил и дитианил. Примеры "гетероциклильных" групп, которые представляют собой частично насыщенные 5- или 6-членные одноатомные циклы, включают оксазолинил, изоксазолинил, имидазолинил, пиразолинил, 1,2,3,6-тетрагидропиридил и 3,6-дигидро-2Н-пиранил. Примеры "гетероциклильных" групп, которые представляют собой полностью насыщенные 8-11-членные двухатомные циклы, включают декагидрохинолинил, октагидро-2Н-1,4-бензоксазинил и октагидро-1Н-циклопента[b]пиридинил. Примеры "гетероциклильных" групп, которые представляют собой частично насыщенные 8-11-членные двухатомные циклы, включают 2,3-дигидро-1Н-индолил, 1,2,3,4-тетрагидрохинолинил, 1,2,3,4-тетрагидроизохинолинил и 2,3,4,5-тетрагидро-1Н-3-бензазепинил.
Любые из указанных групп могут присоединяться к остальной части молекулы в любом подходящем положении.
Используемый в данном описании термин "соль" относится к любой соли соединения по настоящему изобретению, полученной с неорганическими или органическими кислотой или основанием, соли четвертичных аммониевых оснований и внутренние соли. Физиологически приемлемые соли, в частности, подходят для применения в медицинских целях из-за их большей водорастворимости относительно исходных соединений. Такие соли должны непременно содержать физиологически приемлемый анион или катион. Подходящие физиологически приемлемые соли соединений настоящего изобретения включают кислотно-аддитивные соли, образованные с неорганическими кислотами, такими как хлороводородная, бромоводородная, йодоводородная, фосфорная, метафосфорная, азотная и серная кислоты, и с органическими кислотами, такими как винная, уксусная, трифторуксусная, лимонная, яблочная, молочная, фумаровая, бензойная, муравьиная, пропионовая, гликолевая, глюконовая, малеиновая, янтарная, камфорсульфоновая, изотионовая, слизевая, гентизиновая, изоникотиновая, сахарная, глюкуроновая, фуроиновая, глутаминовая, аскорбиновая, антраниловая, салициловая, фенилуксусная, миндальная, эмбоновая (памовая), метансульфоновая, этансульфоновая, пантотеновая, стеариновая, сульфиниловая, альгиновая, галактуроновая и арилсульфновая, например, бензолсульфоновая и п-толуолсульфновая, кислоты; основно-аддитивные соли, образованные с щелочными металлами и щелочноземельными металлами и органическими основаниями, такими как N,N-дибензилэтилендиамин, хлорпрокаин, холин, диэтаноламин, этилендиамин, меглумаин (N-метилглюкамин), лизин и прокаин; и внутренние соли. Соли с физиологически неприемлемым анионом или катионом входят в объем изобретения как промежуточные соединения, применимые для получения физиологически приемлемых солей и/или для применения не для лечебных целей, например, ситуациях in vitro.
В одном воплощении R1 представляет собой галоген, циано, ацетил, трифторметил, трифторметокси.
В одном воплощении R2 представляет собой водород. В другом воплощении R2 представляет собой С1-4-алкил (например, метил).
В одном воплощении R5 представляет собой группу, выбранную из изоксазолила, 2-пирролидинонила, 1,1-диоксидо-2-изотиазолидинила, которая необязательно замещена одним или двумя заместителями, выбранными из галогена, циано, С1-2-алкила (например, метила), галоген-С1-2-алкила (например, трифторметила), С1-2-алкокси (например, метокси), С1-2-алканоила (например, ацетила).
Соответственно R1 представляет собой бром, фтор, трифторметокси, циано, гидрокси, хлор, метокси, трет-бутил, трифторметил.
Соответственно R2 представляет собой изоксазолил, 2-пирролидинонил, -CH2-N-пирролил, 1,1-диоксидо-2-изотиазолидинил, 2-тиенил, 2-пиридил, 2-тиазолил.
В одном воплощении р равен 1 или 2.
В другом воплощении р равен 0.
В одном воплощении R4 может представлять собой необязательно замещенный фенил (например, фенил, 4-трифторметилфенил, 3,4-дифторфенил), необязательно замещенную бициклическую группу, такую как хинолинил (например, 2-метилхинолин, 8-фтор-2-метилхинолин), необязательно замещенный пиранил (например, 4-тетрагидро-2Н-пиранил), необязательно замещенный пиридинил (например, 3-метил-2-пиридинил, 2-метил-3-пиридинил, 3-пиридинил, 2-метил-6-трифторметил-3-пиридинил), необязательно замещенный пиразолил (например, 5-хлор-1-метил-1Н-пиразол-4-ил, 1-метил-3-трифторметил-1Н-пиразол-4-ил, 1,5-диметил-1Н-пиразол-4-ил), необязательно замещенный пиримидил (например, 5-пиримидинил), необязательно замещенный пиридазинил (например, 4-пиридазинил), необязательно замещенный пиразинил (например, 5-метил-2-пиразинил), необязательно замещенный фуранил (например, 3-метил-2-фуранил, 2,5-диметил-3-фуранил), необязательно замещенный тиенил (например, 5-хлор-2-тиенил), необязательно замещенный оксазолил (например, 4-метил-1,3-оксазол-5-ил, 2-метил-5-трифторметил-1,3-оксазол-4-ил), необязательно замещенный изоксазолил (например, 3-метил-5-изоксазолил), необязательно замещенный тиазолил (например, 2,4-диметил-1,3-тиазол-5-ил), необязательно замещенный триазолил (например, 1-метил-1Н-1,2,3-триазол-4-ил).
В одном воплощении R3 представляет собой метил.
Одно воплощение относится к соединению формулы (IB) или его соли, где R1, p, R3 и R4 имеют значения, указанные для формулы (I)

В формуле (IB) в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых, необязательно, замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы.
Примеры R4 включают необязательно замещенный фенил (например, фенил, 4-трифторметилфенил, 3,4-дифторфенил), необязательно замещенную бициклическую группу, такую как хинолинил (например, 2-метилхинолинил, 8-фтор-2-метилхинолинил), необязательно замещенный пиранил (например, 4-тетрагидро-2Н-пиранил), необязательно замещенный пиридинил (например, 3-метил-2-пиридинил, 2-метил-3-пиридинил, 3-пиридинил, 2-метил-6-трифторметил-3-пиридинил), необязательно замещенный пиразолил (например, 5-хлор-1-метил-1Н-пиразол-4-ил, 1-метил-3-тритформетил-1Н-пиразол-4-ил, 1,5-диметил-1Н-пиразол-4-ил), необязательно замещенный пиримидил (например, 5-пиримидинил), необязательно замещенный пиридазинил (например, 4-пиридазинил), необязательно замещенный пиразинил (например, 5-метил-2-пиразинил), необязательно замещенный фуранил (например, 3-метил-2-фуранил, 2,5-диметил-3-фуранил), необязательно замещенный тиенил (например, 5-хлор-2-тиенил), необязательно замещенный оксазолил (например, 4-метил-1,3-оксазол-5-ил, 2-метил-5-трифторметил-1,3-оксазол-4-ил), необязательно замещенный изоксазолил (например, 3-метил-5-изоксазолил), необязательно замещенный тиазолил (например, 2,4-диметил-1,3-тиазол-5-ил), необязательно замещенный триазолил (например, 1-метил-1Н-1,2,3-триазол-4-ил).
Другое воплощение относится к соединению формулы (IC) или его соли, где R1, p, R3 и R4 имеют значения, указанные для формулы (I)

В формуле (IC) в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых, необязательно, замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы. Примерами R4 являются группы, указанные ранее для соединений (IB).
Другое воплощение относится к соединению формулы (ID) или его соли, где R1, p, R3 и R4 имеют значения, указанные для формулы (I)
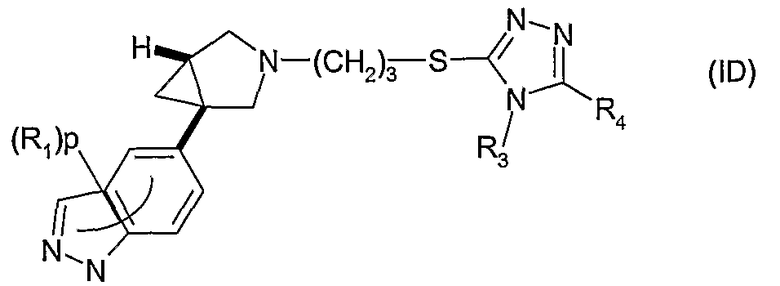
В формуле (ID) в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых, необязательно, замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы.
Примерами R4 являются группы, указанные ранее для соединений (IB).
Другое воплощение относится к соединению формулы (IE) или его соли, где G представляет собой 2-пиридил или 3-пиридил, и R1, p, R3 и R4 имеют значения, указанные для формулы (I)

В формуле (IE) в одном воплощении G соответствует 2-пиридилу (соединения (IE1)), а в другом воплощении 3-пиридилу (соединения (IE2)), что иллюстрируется ниже
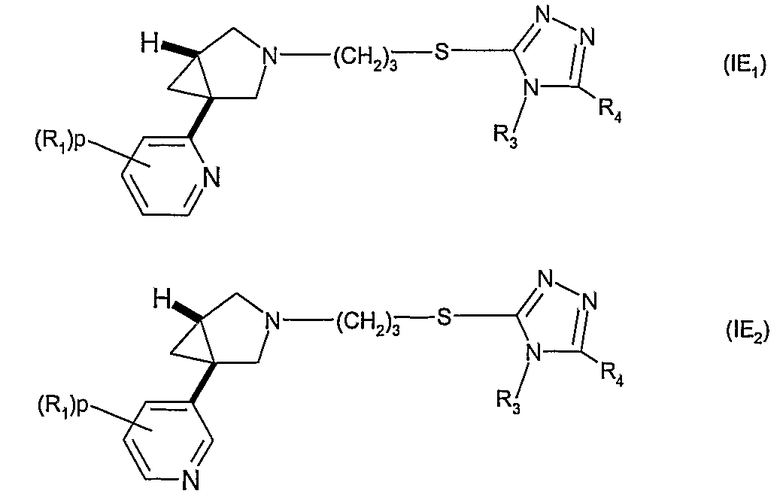
В формулах (IE), (IE1) и (IE2) в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых, необязательно, замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы.
Примерами R4 являются группы, указанные ранее для соединений (IB).
Другое воплощение относится к соединению формулы (IF) или его соли, где R1, p, R3 и R4 имеют значения, указанные для формулы (I)
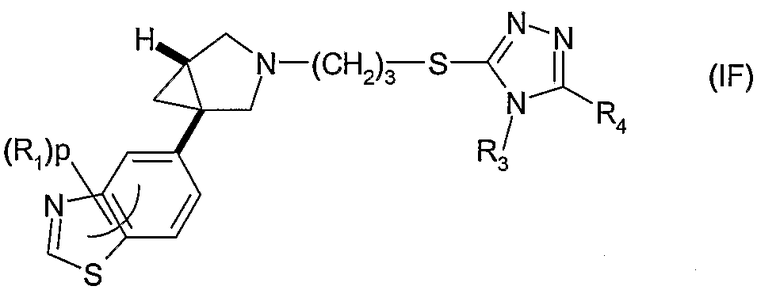
В формуле (IF) в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых, необязательно, замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы.
Примерами R4 являются группы, указанные ранее для соединений (IB).
Стратегия определения абсолютной конфигурации соединений настоящего изобретения включает в качестве первой стадии получение хирального промежуточного соединения (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана

(препаративный пример 18) с использованием в качестве расщепляющего агента (S)-(+)-ацетилминдальной кислоты.
Абсолютная конфигурация ряда соединений, подобных такому хиральному промежуточному соединению, известна из литературы, см. J. Med. Chem., 1981, 24(5), 481-90. Для некоторых соединений, раскрытых в указанной ссылке, абсолютная конфигурация установлена обычным рентгеноструктурным анализом монокристалла.
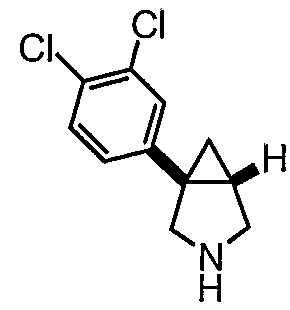
В числе таких соединений раскрыт 1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексан.
Абсолютную конфигурацию оптических изомеров соединений настоящего изобретения устанавливают с использованием сравнительных анализов методом VCD (колебательного кругового дихроизма) и OR (оптического вращения).
Конфигурацию (1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексана установили, сравнивая его экспериментальный спектр VCD и наблюдаемое удельное вращение с ab initio полученными вычисленными данными для (1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексана (см. препаративный пример 48) как ссылочного образца.
Определение абсолютной конфигурации названного в заголовке соединения подтверждают рентгеновской структурой монокристалла, полученной для кристалла соли (S)-(+)-ацетилминдальной кислоты (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана. Как анализ, основанный на известной конфигурации (S)-(+)-ацетилминдальной кислоты, так и анализ на основе эффектов аномальной дисперсии подтверждает определение названного в заголовке соединения как (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана.
Для тех соединений, которые подвергали детальному анализу (VCD; OR, включены в экспериментальные данные), выявлена общая взаимосвязь между абсолютной конфигурацией 3-азабицикло[3.1.0]гексановой группы и измеренной активностью связывания с допаминовым рецептором D3 для каждой пары энантиомеров. Для остальных соединений настоящего изобретения, где стереоизомеры оценивали по отдельности, абсолютную конфигурацию устанавливали на основе разумного предположения специалиста в данной области техники, т.е. абсолютную конфигурацию оценивали, основываясь на измеренной активности связывания с допаминовым рецептором D3 для обоих энантиомеров и сравнении с данными для тех соединений, которые подвергали детальному анализу.
Хиральные молекулы показывают колебательный круговой дихроизм (VCD). Колебательный круговой дихроизм (VCD) представляет собой различное взаимодействие хиральной молекулы с инфракрасным излучением с левой и правой круговой поляризацией во время колебательного возмущения.
Спектр VCD хиральной молекулы зависит от ее трехмерной структуры. Наиболее важно, что спектр VCD хиральной молекулы является чувствительной функцией ее абсолютной конфигурации и, в случае гибких молекул, ее конформации. Поэтому в принципе VCD дает возможность определить структуру хиральной молекулы. Спектры VCD впервые измерили в 1970-е годы. В дальнейшем приборы для измерения VCD разрабатывались строго с учетом области спектра и чувствительности. В настоящее время спектры VCD жидкостей и растворов можно измерить в большей части фундаментальной инфракрасной (ИК) области спектра (v ≥ 650 см-1) с высокой чувствительностью при приемлемом разрешении (1-5 см-1) с использованием приборов VCD как c рассеиванием, так и с преобразованием Фурье (FT). Совсем недавно стали доступны коммерческие приборы FT VCD, что значительно расширило доступность спектров VCD.
Использование VCD как надежного метода определения абсолютной конфигурации хиральных молекул теперь вполне признано (см., например, Shan R.D. et al., Curr. Opin. Drug Disc. Dev., 2001, 4:764-774; Freedman T.B. et al., Helv. Chim. Acta, 2002, 85:1160-1165; Dyatkin A.B. et al., Chirality, 2002, 14:215-219; Solladie'-Cavallo A., Balaz. M. et al., Tetrahedron Assym., 2001, 12:2605-2611; Nafie L.A. et al., Circular dichroism, principles and applications, 2nd ed., New York, John Wiley & Sons, 2000, p.97-131; Nafie L.A. et al., в Yan B., Gremlish H-U., editors, Infrared and Raman spectroscopy of biological materials, New York, Marcel Dekker, 2001, p.15-54; Polavarapu P.L. et al., J. Anal. Chem., 2000, 366:727-734; Stephens P.J. et al., Chirality, 2000, 12:172-179; Solladie'-Cavallo A. et al., Eur. J. Org. chem., 2002:1788-1796).
Способ включает сравнение наблюдаемых ИК- и VCD-спектров с расчетами спектров для определенной конфигурации и дает информацию как об абсолютной конфигурации, так и о конформации в растворе.
С учетом экспериментального спектра хиральной молекулы, абсолютная конфигурация и/или конформация которой неизвестна и должна быть определена, общая процедура выглядит следующим образом: 1) определяют все возможные структуры; 2) прогнозируют спектры таких структур и 3) предсказанные спектры сравнивают с экспериментальным спектром. Правильная структура будет давать спектр, согласующийся с экспериментом; неправильные структуры будут давать спектры, расходящиеся с экспериментом.
Спектры VCD всегда измеряют одновременно с колебательными неполяризованными спектрами поглощения ("инфракрасные (ИК) спектры"), и два колебательных спектра вместе дают больше информации, чем один спектр VCD. Кроме того, колебательные неполяризованные спектры поглощения автоматически прогнозируют одновременно со спектрами VCD.
Для определений ab initio спектры VCD и неполяризованные ИК рассчитывают с использованием пакета программ Gaussian 98.
Когда синтезируют хиральные молекулы (или, если это природные продукты, выделяют), их оптическое вращение обычно измеряют при одной частоте или при небольшом числе дискретных частот в видимой области спектра или вблизи ультрафиолетовой области. Чаще всего удельное вращение измеряют при одной частоте - частоте линии D натрия ([α]D). Используемые частоты лежат ниже порога поглощения электронов, т.е. они находятся в области "пропускания" спектра. Оптическое вращение является отражением энантиомерного избытка (эи) образца и абсолютной конфигурации (АС) преобладающего энантиомера.
Когда имеется оптическое вращение при данной частоте для 100% эи, измеренное оптическое вращение при той же частоте дает возможность определить эи образца. Определение эи является основным применением дискретной частоты, оптического вращения в области пропускания спектра. В принципе также можно определить АС преобладающего энантиомера, если она неизвестна. Однако определение АС из оптического вращения требует алгоритма, который легко предскажет оптическое вращение молекул неизвестной АС, и предложено несколько методологий для прогнозирования дискретной частоты, оптического вращения в области пропускания спектра (Eliel E.L., Wilen S.H., Stereochemistry of organic compounds, New York, John Wiley & Sons, 1994, Chapter 13).
Совсем недавно разработки в области функциональной теории плотности ab initio (DFT) радикально улучшили точность вычисления оптического вращения. В результате впервые стало возможным простое получение АС из оптического вращения.
Для установления ab initio OR используют программу Dalton Quantum Chemistry.
Другими воплощениями настоящего изобретения являются соединения формулы (IB)', (IC)', (ID)' и (IF)', которые соответственно соответствуют стереохимическим изомерам соединений формул (IB), (IC), (ID) и (IF), определение которых дано выше, обогащенных конфигурацией (1S,5R).
Соединения формулы (IE)' соответствуют стереохимическим изомерам соединений формулы (IE), определение которых дано выше, обогащенным конфигурацией (1R,5R) или (1S,5R) в зависимости от наличия 2-пиридинового цикла.
Одно воплощение относится к обогащенному конфигурацией (1S,5R) стереохимическому изомеру формулы (IB)' или его соли, где R1, p, R3 и R4 имеют значения, указанные для формулы (I)

В формуле (IB)' в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых необязательно замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы.
Примеры R4 включают необязательно замещенный фенил (например, фенил, 4-трифторметилфенил, 3,4-дифторфенил), необязательно замещенную бициклическую группу, такую как хинолинил (например, 2-метилхинолинил, 8-фтор-2-метилхинолинил), необязательно замещенный пиранил (например, 4-тетрагидро-2Н-пиранил), необязательно замещенный пиридинил (например, 3-метил-2-пиридинил, 2-метил-3-пиридинил, 3-пиридинил, 2-метил-6-трифторметил-3-пиридинил), необязательно замещенный пиразолил (например, 5-хлор-1-метил-1Н-пиразол-4-ил, 1-метил-3-тритформетил-1Н-пиразол-4-ил, 1,5-диметил-1Н-пиразол-4-ил), необязательно замещенный пиримидил (например, 5-пиримидинил), необязательно замещенный пиридазинил (например, 4-пиридазинил), необязательно замещенный пиразинил (например, 5-метил-2-пиразинил), необязательно замещенный фуранил (например, 3-метил-2-фуранил, 2,5-диметил-3-фуранил), необязательно замещенный тиенил (например, 5-хлор-2-тиенил), необязательно замещенный оксазолил (например, 4-метил-1,3-оксазол-5-ил, 2-метил-5-трифторметил-1,3-оксазол-4-ил), необязательно замещенный изоксазолил (например, 3-метил-5-изоксазолил), необязательно замещенный тиазолил (например, 2,4-диметил-1,3-тиазол-5-ил), необязательно замещенный триазолил (например, 1-метил-1Н-1,2,3-триазол-4-ил).
Другое воплощение относится к обогащенному конфигурацией (1S,5R) стереохимическому изомеру формулы (IC)' или его соли, где R1, p, R3 и R4 имеют значения, указанные для формулы (I)
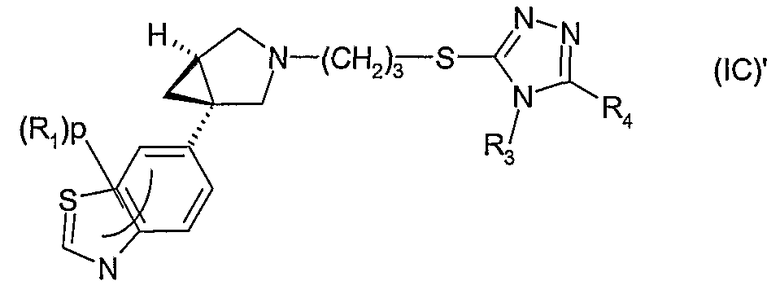
В формуле (IC)' в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых, необязательно, замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы. Примерами R4 являются группы, указанные ранее для соединений (IB)'.
Другое воплощение относится к обогащенному конфигурацией (1S,5R) стереохимическому изомеру формулы (ID)' или его соли, где R1, p, R3 и R4 имеют значения, указанные для формулы (I)
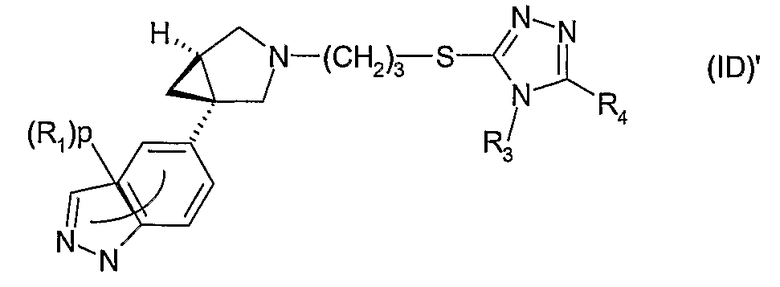
В формуле (ID)' в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых необязательно замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы. Примерами R4 являются группы, указанные ранее для соединений (IB)'.
Другое воплощение относится к обогащенному конфигурацией (1S,5R) или конфигурацией (1R,5R) стереохимическому изомеру формулы (IE)' или его соли, где G представляет собой 2-пиридил или 3-пиридил, и R1, p, R3 и R4 имеют значения, указанные для формулы (I)
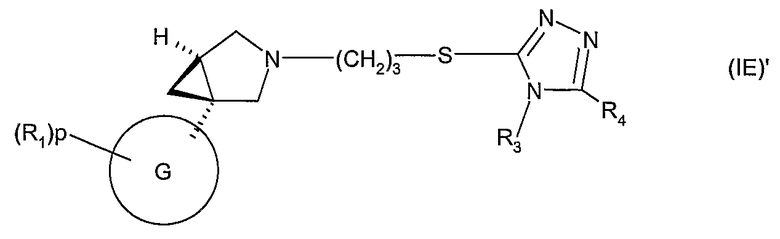
В формуле (IE)' в одном воплощении G соответствует 2-пиридилу (соединения (IE)1'), и в другом воплощении G соответствует 3-пиридилу (соединения (IE)2'), как показано ниже

Итак, конфигурация изменяется в зависимости от типа пиридинового цикла, как указано выше.
В формулах (IE)', (IE)1') и (IE)2' в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых необязательно замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы. Примерами R4 являются группы, указанные ранее для соединений (IB)'.
Другое воплощение относится к обогащенному конфигурацией (1S,5R) стереохимическому изомеру формулы (IF)' или его соли, где R1, p, R3 и R4 имеют значения, указанные для формулы (I)

В формуле (IF)' в одном воплощении R3 представляет собой метил. R4 может представлять собой фенил, гетероциклил, 5- или 6-членную гетероароматическую группу или 9-11-членную бициклическую группу, любая из которых необязательно замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, гидрокси, оксо, циано, нитро, С1-4-алкила, фтор-С1-4-алкила, С1-4-алкокси, фтор-С1-4-алкокси, С1-4-алканоила; и когда R1 представляет собой хлор и р равен 1, тогда R1 не присутствует в положении относительно связи с остальной частью молекулы. Примерами R4 являются группы, указанные ранее для соединений (IB)'.
Некоторые соединения изобретения могут образовывать кислотно-аддитивные соли с одним или несколькими эквивалентами кислоты. Настоящее изобретение включает в свой объем все возможные стехиометрические и нестехиометрические формы.
Фармацевтически приемлемые соли можно получить из других солей, в том числе других фармацевтически приемлемых солей, соединений формулы (I) с использованием обычных способов.
Специалистам в области органической химии будет понятно, что многие органические соединения могут образовывать комплексы с растворителями, в которых они вступают в реакции или из которых они выпадают в осадок или кристаллизуются. Такие комплексы известны как "сольваты". Например, комплекс с водой известен как "гидрат". Сольваты соединений изобретения входят в объем изобретения. Соединения формулы (I) можно легко извлечь в сочетании с молекулами растворителя кристаллизацией или выпариванием соответствующего растворителя и получить соответствующие сольваты.
Кроме того, в контекст данного изобретения также входят пролекарства. Используемый в данном описании термин "пролекарство" обозначает соединение, которое превращается в организме, например, гидролизом в крови, в его активную форму, которая обладает лечебным действием. Фармацевтически приемлемые пролекарства описаны в работе T. Higuchi and V. Stella, Prodrugs as Novel Delivery Systems, Vol.14 of the A.C.S. Symposium Series, Edward B. Roche, ed., Bioreversible Carriers in Drug Design, American Pharmaceutical Association and Pergamon Press, 1987; и в работе D. Fleisher, S. Ramon and H. Barba, "Improved oral drug delivary: solubility limitations overcome by the use of prodrugs", Advanced Drug Delivery Reviews (1996), 19(2), 115-130, включенных в данное описание в качестве ссылок.
Пролекарства являются ковалентно-связанными носителями, которые высвобождают соединение структуры (I) in vivo, когда такое пролекарство вводят пациенту. Пролекарства, как правило, получают модификацией функциональных групп таким образом, что модификация расщепляется, или обычными манипуляциями или in vivo с образованием исходного соединения. Пролекарства включают, например, соединения данного изобретения, в которых гидрокси-, аминные или сульфгидрильные группы связаны с любой группой таким образом, что при введении пациенту происходит расщепление с образованием гидрокси-, аминных или сульфгидрильных групп. Так, характерными примерами пролекарств являются (но не ограничиваются перечисленным) ацетаты, формиаты и бензоаты, образованные по спиртовым, сульфгидрильным и аминным фунциональным группам соединений структуры (I). Кроме того, в случае карбоновой кислоты (-СООН) можно использовать эфиры, такие как метиловые эфиры, этиловые эфиры и т.п. Эфиры могут быть активны сами по себе и/или способны к гидролизу в условиях in vivo в организме человека. Подходящие фармацевтически приемлемые способные к гидролизу in vivo сложноэфирные группы включают группы, которые легко разрушаются в организме человека с образованием исходной кислоты или ее соли.
Кроме того, некоторые кристаллические формы соединений структуры (I) могут существовать как полиморфы, которые входят в объем настоящего изобретения.
Специалистам в данной области техники будет понятно, что при получении соединения изобретения или его сольвата может быть необходимой и/или желательной защита одной или нескольких чувствительных групп в молекуле для предотвращения нежелательных побочных реакций. Подходящие защитные группы для применения согласно настоящему изобретению хорошо известны специалистам в области органического синтеза и могут быть использованы обычным образом. См., например, "Protective groups in organic synthesis", T.W. Greene and P.G.M. Wuts (John Wiley & Sons, 1991), или "Protecting Groups", P.J. Kocienski (Georg Thieme Verlag, 1994). Примеры подходящих аминозащитных групп включают защитные группы ацильного типа (например, формил, трифторацетил, ацетил), ароматические защитные группы уретанового типа (например, бензилоксикарбонил (Cbz) и замещенный Cbz), алифатические защитные группы уретанового типа (например, 9-флуоренилметоксикарбонил (Fmoc), трет-бутилоксикарбонил (Вос), изопропилоксикарбонил, циклогексилоксикарбонил) и защитные группы алкильного типа (например, бензил, тритил, хлортритил). Примеры подходящих кислородзащитных групп могут включать, например, алкилсилильные группы, такие как триметилсилил или трет-бутилдиметилсил; простые алкилэфирные группы, такие как тетрагидропиранил или трет-бутил; или сложноэфирные группы, такие как ацетатная группа.
Когда требуется определенный энантиомер соединения общей формулы (I), его можно получить, например, расщеплением соответствующей энантиомерной смеси соединения формулы (I) с использованием обычных способов. Так, необходимый энантиомер можно получить из рацемического соединения формулы (I) с использованием процедуры хиральной ВЭЖХ.
Данное изобретение также включает соединения, меченные радиоизотопами, идентичные соединениям, обозначенным формулой (I) и другими формулами, но в которых фактически один или несколько атомов заменены на атом с атомной массой или массовым числом, отличающимися от атомной массы или атомного числа, как правило, встречающихся в природе. Примерами изотопов, которые можно вводить в соединения изобретения и их фармацевтически приемлемые соли, являются изотопы водорода, углерода, азота, кислорода, фосфора, серы, фтора, йода и хлора, такие как 2H, 3H, 11C, 13C, 14C, 15N, 17O, 18O, 31P, 32P, 35S, 18F, 35Cl, 123I и 125I.
Соединения настоящего изобретения и фармацевтически приемлемые соли таких соединений, содержащие вышеуказанные изотопы и/или другие изотопы других атомов, входят в объем настоящего изобретения. Меченные радиоизотопами соединения настоящего изобретения, например, соединения, в которые введены такие радиоизотопы, как 3H, 14C, применимы в анализах распределения лекарственного средства и/или субстрата в тканях. Тритированный изотоп, т.е. 3H, и изотоп углерода-14, т.е. 14C, особенно предпочтительны за легкость их получения и обнаружения. Изотопы 11C и 18F особенно применимы при РЕТ (позитронная эмиссионная томография), и изотопы 125I особенно применимы при SPECT (эмиссионная компьютерная томография одиночных фотонов), применимых при получении изображения головного мозга. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий, т.е. 2Н, может предоставить определенные лечебные преимущества, являющиеся результатом большей устойчивости к метаболизму, например, увеличенный период полувыведения in vivo или потребность в пониженной дозировке, и вследствие этого может стать предпочтительным в некоторых обстоятельствах. Меченные радиоизотопами соединения формулы I и других формул данного изобретения можно получить, как правило, осуществляя процедуру, раскрытую на схемах и/или в примерах, приведенных ниже, путем замены реагента, немеченного радиоизотопами, на легко доступный реагент, меченный радиоизотопами.
Некоторые группы/заместители, включенные в настоящее изобретение, могут присутствовать в виде изомеров. Настоящее изобретение включает в свой объем все такие изомеры, в том числе рацематы, энантиомеры, таутомеры и их смеси. Некоторые замещенные гетероароматические группы, входящие в соединения формулы (I), могут существовать в одной или нескольких таутомерных формах. Настоящее изобретение включает в свой объем все такие таутомерные формы, включая смеси.
Одно воплощение настоящего изобретения относится к соединениям с молекулярной массой 800 или менее. Другое воплощение относится к соединениям с молекулярной массой 600 или менее. Как правило, и без ограничения, такие соединения могут обладать более высокой пероральной доступностью и иногда более высокими растворимостью и/или прониканием в головной мозг. Молекулярная масса в данном случае обозначают массу несольватированного соединения в форме свободного основания, причем исключается молекулярная масса, в которую вносят вклад соли присоединения, молекулы растворителя (например, воды), молекулярные части пролекарства, отщепляемые in vivo, и т.д.
Как правило, соединения или соли по изобретению следует расценивать таким образом, что из их числа исключаются такие соединения (если они есть), которые химически неустойчивы или сами по себе или в воде, и которые явно не подходят для фармацевтического применения при всех способах введения - пероральном, парентеральном или любом другом. Такие соединения известны специалистам в области химии. Однако включаются пролекарства или соединения, устойчивые ex vivo, которые могут превращаться в организме млекопитающего (например, человека) в соединения изобретения.
Примерами соединений настоящего изобретения являются
- 5-[5-({3-[(1R,5S/1S,5R)-1-(4-метоксифенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
- 5-[5-({3-[(1S,5R)-1-(4-метоксифенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 1;
- 5-[5-({3-[(1R,5S/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
- 5-[5-({3-[(1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 2;
- 2-метил-5-[4-метил-5-({3-[(1R,5S/1S,5R)-1-фенил-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4Н-1,2,4-триазол-3-ил]хинолин;
- 2-метил-5-[4-метил-5-({3-[(1S,5R)-1-фенил-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4Н-1,2,4-триазол-3-ил]хинолин, энантиомер 2;
- 5-[5-({3-[(1R,5S/1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
- 5-[5-({3-[(1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 1;
- 5-[5-({3-[(1R,5S/1S,5R)-1-(4-трет-бутилфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
- 5-[5-({3-[(1S,5R)-1-(4-трет-бутилфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 2;
- 4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]бензонитрил;
- 4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенол;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-фенил-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1R,5S/1S,5R)-1-(4-трет-бутилфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(3,4-дихлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(3,4-дихлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 2;
- (1R,5S/1S,5R)-1-(4-метоксифенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-метоксифенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 2;
- (1R,5S/1S,5R)-1-[4-(5-метил-3-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[4-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- 1-[5-[(1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-[5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон, энантиомер 1;
- (1S,5R/1R,5S)-1-(4-хлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-хлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-1-(4-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-1-(3-хлорфенил)-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(3-хлорфенил)-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-1-(3-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(3-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(метилокси)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(метилокси)фенил]-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-[3-{[4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- 5-[5-({3-[(1S,5R/1R,5S)-1-(4-хлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
- 5-[5-({3-[(1S,5R/1R,5S)-1-(4-хлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 1;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-метил-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан, энантиомер 2;
- (1R,5S/1S,5R)-1-(3-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(1-метил-3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(1-метил-3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан, диастереоизомер 1;
- (1S,5R)-3-(1-метил-3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан, диастереоизомер 2;
- (1R,5S/1S,5R)-1-[2-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 2;
- 1-[4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-[4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-пиридазинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(1,5-диметил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(5-пиримидинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(3-метил-2-фуранил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- 2-метил-6-{4-метил-5-[(3-{(1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4Н-1,2,4-триазол-3-ил}хинолин;
- 8-фтор-2-метил-5-{4-метил-5-[(3-{(1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4Н-1,2,4-триазол-3-ил}хинолин;
- 2-метил-5-{4-метил-5-[(3-{(1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4Н-1,2,4-триазол-3-ил}хинолин;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-пиридазинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(5-пиримидинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- 1-{4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}-2-пирролидинон;
- 5-{5-[(3-{(1R,5S/1S,5R)-1-[4-(1,1-диоксидо-2-изотиазолидинил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил}-2-метилхинолин;
- (1R,5S/1S,5R)-1-[3-фтор-4-(трифторметил)фенил]-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- 1-(2-(метилокси)-5-{(1R,5S/1S,5R)-3-(3-{[4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанон;
- 1-[5-[(1R,5S/1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-{2-(метилокси)-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-[5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-{2-(метилокси)-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-(2-гидрокси-5-{(1R,5S/1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанон;
- 1-{5-[(1R,5S/1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанон;
- 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-[5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон;
- 1-[5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон, энантиомер 1;
- 2-метил-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- 2-метил-5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол, энантиомер 1;
- 2-метил-6-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- 1-метил-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1Н-индазол;
- 1-метил-5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1Н-индазол, энантиомер 1;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-пиридазинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(5-хлор-1-метил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(1-метил-1Н-1,2,3-триазол-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(1,5-диметил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(5-пиримидинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[1-метил-3-(трифторметил)-1Н-пиразол-4-ил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-2-фуранил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-5-изоксазолил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(1-метил-1Н-пиразол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(5-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[2-метил-3-(трифторметил)-1,3-оксазол-4-ил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-2-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(2,5-диметил-3-фуранил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(5-хлор-2-тиенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-этил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[2-метил-6-(трифторметил)-3-пиридинил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- 5-[5-({3-[(1R,5S/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-1-метил-3-(трифторметил)-1Н-тиено[2,3-c]пиразол;
- 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R/1S,5S)-1-[5-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан;
- 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R)-1-[5-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан, энантиомер 2;
- 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R/1S,5S)-1-[6-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[3-фтор-4-(1Н-пиррол-1-илметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-{3-{[4-метил-5-фенил-4Н-1,2,4-триазол-3-ил)тио]пропил}-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-2-метил-5-[3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R/1R,5S)-2-метил-5-[3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R/1R,5S)-2-метил-5-[3-{3-[(4-метил-5-фенил-4Н-1,2,4-триазол-3-ил)тио]пропил}-3-азабицикло[3.1.0]гекс-1-ил)-1,3-бензотиазол;
- (1S,5R/1R,5S)-5-[3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-метил-1,3-бензотиазол;
- (1S,5R/1R,5S)-2-метил-5-{3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}-1,3-бензотиазол;
- (1R,5S/1S,5R)-1-[3-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан, энантиомер 1;
- (1R,5S/1S,5R)-1-[2-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан, энантиомер 2;
- (1R,5S/1S,5R)-1-[4-(метилокси)-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[4-(4-хлор-2-фторфенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-(3-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(2-хлор-4-метилфенил)-3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[3-хлор-4-(метилокси)фенил]-3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[4-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[6-(трифторметил)-2-пиридинил]фенил}-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[3-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(5-метил-2-тиенил)фенил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[4-(3,5-диметил-4-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-оксазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан
и их фармацевтически приемлемые соли.
Примерами соединений настоящего изобретения являются следующие соединения, которые можно получить способами настоящего изобретения:
- 4-[(1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]бензонитрил;
- 4-[(1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенол;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-фенил-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-трет-бутилфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[4-(5-метил-3-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[4-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-метил-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(3-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- 1-[4-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-[4-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- 1-{4-[(1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}-2-пирролидинон;
- 5-{5-[(3-{(1S,5R)-1-[4-(1,1-диоксидо-2-изотиазолидинил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил}-2-метилхинолин;
- 1-(2-(метилокси)-5-{(1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанон;
- 1-[5-[(1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-{2-(метилокси)-5-[(1S,5R)-3-(3-{[4-метил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-[5-[(1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-{2-(метилокси)-5-[(1S,5R)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-(2-гидрокси-5-{(1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанон;
- 1-{5-[(1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанон;
- 1-{2-гидрокси-5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-{2-гидрокси-5-[(1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 2-метил-6-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-пиридазинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(5-хлор-1-метил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(1-метил-1Н-1,2,3-триазол-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(1,5-диметил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(5-пиримидинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[1-метил-3-(трифторметил)-1Н-пиразол-4-ил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-2-фуранил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-5-изоксазолил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(1-метил-1Н-пиразол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(5-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[2-метил-5-(трифторметил)-1,3-оксазол-4-ил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-2-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(2,5-диметил-3-фуранил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(5-хлор-2-тиенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-этил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[2-метил-6-(трифторметил)-3-пиридинил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- 5-[5-({3-[(1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-1-метил-3-(трифторметил)-1Н-тиено[2,3-c]пиразол;
- 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R)-1-[6-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-фтор-4-(1Н-пиррол-1-илметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-{3-[(4-метил-5-фенил-4Н-1,2,4-триазол-3-ил)тио]пропил}-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-2-метил-5-[3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R)-2-метил-5-[3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R)-2-метил-5-(3-{3-[(4-метил-5-фенил-4Н-1,2,4-триазол-3-ил)тио]пропил}-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R)-5-[3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-метил-1,3-бензотиазол;
- (1S,5R/1R,5S)-2-метил-5-{3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}-1,3-бензотиазол;
- (1S,5R)-1-[4-(4-хлор-2-фторфенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{3-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(2-хлор-4-метилфенил)-3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-хлор-4-(метилокси)фенил]-3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[4-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[6-(трифторметил)-2-пиридинил]фенил}-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(5-метил-2-тиенил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[4-(3,5-диметил-4-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-оксазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан и
их фармацевтически приемлемые соли.
Настоящее изобретение также относится к способу получения соединения формулы (I) или его соли, определение которым дано выше.
Способ настоящего изобретения получения соединений формулы (I), в которых G представляет собой фенильное производное, включает стадии
(а) взаимодействия соединения формулы (II)

где R1 и р имеют значения, указанные для формулы (I), с соединением формулы (III)

где R2, R3 и R4 имеют значения, указанные для формулы (I), и Х представляет собой уходящую группу,
или
(b) в случае соединения формулы (I), где р равен 1 или 2, взаимодействие соединения формулы (IV)
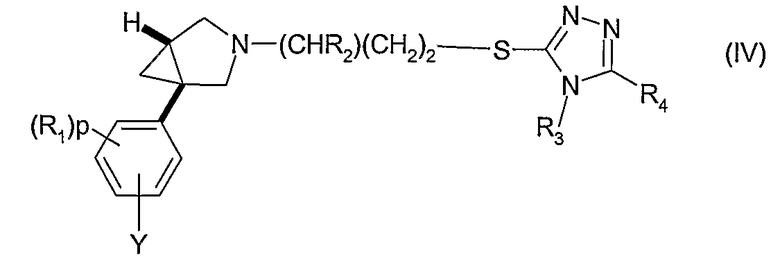
где R1, R2, R3 и R4 имеют значения, указанные для формулы (I), р равен 0 или 1, и Y представляет собой галоген, перфторалкилсульфонилоксигруппу (например, трифторметилсульфонилокси), или Y представляет собой группу М, выбранную из числа производного бора (например, с функцией бороновой кислоты В(ОН)2) или металлосодержащего соединения, такого как триалкилолово (например, SnBu3), галогенид цинка или галогенид магния, с соединением R1-Y1, где Y1 представляет собой галоген, когда Y представляет собой группу М; или когда Y представляет собой галоген или перфторалкилсульфонилоксигруппу, Y1 представляет собой группу М, имеющую значения, указанные выше, или водород, который можно активировать подходящим основанием (например, Cs2CO3) в присутствии подходящего переходного металла (например, Pd); "уходящая группа" является такой группой, которую имеют в виду специалисты в области химии, т.е. группой, которую можно заменить нуклеофильной группой в, например, реакции типа SN2, SN1 или SNAr;
и последующие, в случае способа (а) и способа (b), необязательно
(i) удаление любой(ых) защитной(ых) группы; и/или
(ii) получение соли; и/или
(iii) превращение соединения формулы (I) или его соли в другое соединение формулы (I) или его соль.
Способ (а) можно осуществить с использованием обычных способов получения третичного амина. Уходящая группа Х может представлять собой галоген, такой как хлор. С другой стороны, Х может представлять собой сульфонилоксигруппу, такую как С1-4-алкилсульфонилокси (например, метансульфонилокси) или галоген-С1-4-алкилсульфонилокси (например, трифторметансульфонилокси); или арилсульфонилокси, где арил представляет собой необязательно замещенный фенил, необязательно замещенную 5- или 6-членную гетероароматическую группу или необязательно замещенную бициклическую группу, например, необязательно замещенный фенил, где в каждом случае необязательными заместителями являются одна или несколько С1-2-алкильных групп, например, пара-толуолсульфонилокси. Когда Х представляет собой галоген, взаимодействие можно осуществить с использованием основания, такого как карбонат калия, в присутствии источника йодид-иона, такого как иодид натрия, в растворителе, таком как N,N-диметилформамид, при подходящей температуре, например при 60°С.
Соединения формулы (II) можно получить способами, хорошо известными в технике (см., например, J. Med. Chem., 1981, 24, 481-490). Типичные условия см. далее в настоящем описании в препаративных примерах 1-6 и 15-18. Взаимопревращение групп R1 можно осуществить по методологиям, хорошо известным в технике (например, деметилированием метоксигруппы с образованием гидроксигруппы с использованием в качестве реагента подходящей кислоты Льюиса, такой как трибромид бора, в инертном растворителе, таком как дихлорметан). Приведенные далее препаративные примеры 7-11 являются дополнительными примерами таких взаимопревращений при наличии подходящей защитной группы для вторичного амина, такой как N-трифторацетил.
Взаимодействие соединения формулы (IV) с R1-Y1 согласно способу (b) можно осуществить в присутствии переходного металла, например, палладиевого катализатора, такого как дихлорид бис-трифенилфосфинпалладия, тетракистрифенилфосфинпалладий(0) или комплекс, образованный in situ из трис(дибензилиденацетон)дипалладия(0) и 4,5-бис(дифенилфосфино)-9,9-диметилксантена. Когда М представляет собой группу с функцией бороновой кислоты, такой как В(ОН)2, взаимодействие можно осуществить в щелочной среде, например, с использованием водного раствора карбоната натрия, в подходящем растворителе, таком как диоксан. Когда М представляет собой триалкилстаннил, взаимодействие можно осуществить в инертном растворителе, таком как ксилол или диоксан, необязательно, в присутствии LiCl. Когда М представляет собой галогенид цинка или магния, взаимодействие можно осуществить в апротонном растворителе, таком как тетрагидрофуран. Когда М представляет собой водород, который можно активировать подходящим основанием (например, Cs2CO3) в присутствии подходящего переходного металла (например, Pd), взаимодействие можно осуществить в инертном растворителе, таком как диоксан, в присутствии подходящего основания, такого как Cs2CO3. Заместитель Y может представлять собой галоген, такой как бром, или сульфонилоксигруппу, такую как трифторметилсульфонилокси; и Y1 может представлять собой группу М, такую как водород, который можно активировать подходящим основанием (например, Cs2CO3) в присутствии подходящего переходного металла (например, Pd).
В одном аспекте настоящее изобретение относится к способу синтеза для получения соединений формулы (II). Способ также можно обычно осуществлять для получения соединений формулы (IIa), в которых фенильная группа заменена на пиридин, применимый для получения соединений формулы (IE). Данный способ включает стадии

где
стадия (a') является стадией диазотирования анилина (VII) с последующим взаимодействием с малеимидом с образованием 3-арилмалеимида (VIII);
стадия (b') является стадией циклопропанирования (VIII) с образованием бициклического имида (IX);
стадия (с') является стадией восстановления имида (IX) с образованием соединений формулы (II).
Стадию (a') можно осуществить с использованием способов осуществления реакции Меервейна (например, в J. Am. Chem. Soc., 1955, 77, 2313, описывается получение арилмалеимидов с использованием такого подхода). С другой стороны, во многих случаях данную стадию удобно осуществлять с применением процедуры, где к смеси малеимида, соответствующей соли меди(II), такой как безводный CuCl2, и подходящего органического нитрила, такого как трет-бутилнитрил, в совместимом растворителе, таком как ацетонитрил, постепенно добавляют раствор соединения формулы (VII). Далее предоставляется соответствующее время для взаимодействия и соответствующая обработка. Примером такого способа является препаративный пример 37.
Стадия (b') заключается в постепенном добавлении раствора очищенного соединения формулы (VIII) или смесей, содержащих соединение формулы (VIII), растворенных в подходящем растворителе, таком как диметилсульфоксид, к раствору иодида триметилсульфоксония в подходящем растворителе, таком как диметилсульфоксид, и основания, такого как гидрид натрия. За добавлением следует предоставление соответствующего времени для взаимодействия и соответствующая обработка. Примером такого способа является препаративный пример 37.
Стадию (с') можно осуществить с использованием подходящего восстановителя в совместимом растворителе, как например, боран в тетрагидрофуране или Red-Al® в толуоле, при соответствующей температуре, например, при 65°С в случае борана как восстановителя. За этим следует соответствующая обработка. Примером такого способа является препаративный пример 38.
В другом аспекте настоящее изобретение относится к другому способу синтеза для получения соединений формулы (II) или, как правило, формулы (XIII). Данный способ включает стадии

где
R1, р и G имеют значения, указанные для формулы (I), R14Q представляет собой подходящую алкоксигруппу, PG представляет собой соответствующую защитную группу, и Y может представлять собой галоген, такой как бром, или сульфонилоксигруппу, такую как трифторметилсульфонилокси, и включает следующие стадии:
стадию (a"), являющуюся реакцией сочетания (2,5-дигидро-1Н-пиррол-3-ил)бороната (Х) с ароматическим галоген- или сульфонилоксисодержащим производным (XI);
стадию (b"), являющуюся реакцией циклопропанирования (XII) с последующим, если требуется, удалением защитной группы с образованием бициклического амина (XIII).
Стадию (a") можно осуществить с использованием обычных способов сочетания по Судзуки, например, с использованием тетракис(трифенилфосфин)палладия(0) в качестве источника каталитического палладия(0), в присутствии фторида цезия в подходящем растворителе, таком как тетрагидрофуран, при подходящей температуре. Подходящий (R14Q)2В может представлять собой 4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил, и PG может представлять собой бензил, представляя соединение формулы (Х), описанное в Synlett., 2002, 5, 829-831. Примером такого способа является препаративный пример 50.
Стадия (b") заключается в реакции циклопропанирования, осуществляемой, например, с использованием реагента, полученного из иодида триметилсульфоксония и подходящего основания, такого как гидрид натрия, в совместимом растворителе, например, диметилсульфоксиде. Примером такого способа является препаративный пример 52. Затем следует реакция удаления защитной группы, как например, в препаративном примере 54.
Само соединение формулы (III) можно получить взаимодействием соединения формулы (V)

где R3 и R4 имеют значения, указанные в данном описании ранее, с соединением формулы (VI)
L(CHR2)(CH2)2X (VI),
где Х имеет значения, указанные для формулы (I), и L представляет собой уходящую группу, например, атом брома. Типичные условия взаимодействия см. в приведенном в данном описании препаративном примере 13.
Соединения формулы (I), где R1, R2, R3, R4, G и р имеют указанные выше значения, можно получить взаимодействием соединения формулы (XIV)
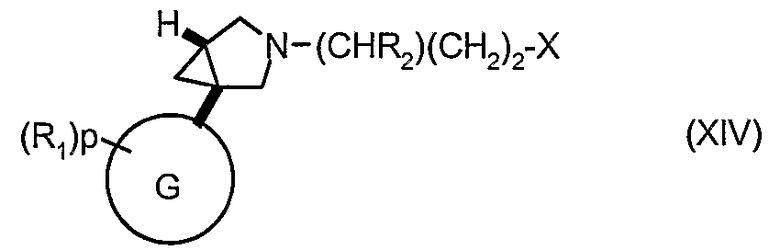
где R1, R2, G и р имеют значения, указанные выше для формулы (I), и Х представляет собой уходящую группу, с соединением формулы (V)

где R3 и R4 имеют значения, указанные в данном описании выше. Типичные условия взаимодействия, когда Х представляет собой хлор, см. в примере 35 или, с другой стороны, в примерах 41-52.
Соединение формулы (XIV), где R1, G и р имеют значения, указанные для формулы (I), Х представляет собой уходящую группу, и R2 представляет собой Н (водород), можно получить алкилированием соединения формулы (XIII) в присутствии подходящего основания, такого как третичный амин, например, диизопропилэтиламин, с пропилсодержащим производным с двумя уходящими группами, предпочтительно, различной реакционноспособности, в положениях 1 и 3, например, 1-бром-3-хлорпропаном. Типичные условия взаимодействия для такого превращения приводятся в препаративном примере 40.
Соединение формулы (XIV), где R1, G и р имеют значения, указанные для формулы (I), Х представляет собой уходящую группу, и R2 представляет собой С1-4-алкил, можно получить взаимодействием между бета-гидроксикетоном, например, 4-гидрокси-2-бутаноном, если R2 представляет собой метил, и соединением формулы (XIII) в присутствии подходящего источника борогидрида, такого как NaBH(OAc)3, с последующим превращением гидроксильной группы в уходящую группу способами, известными специалистам в данной области техники, например, воздействием тионилхлорида. Типичные условия взаимодействия для таких превращений приводятся в препаративных примерах 19 и 20.
Реакции взаимопревращения между соединениями формулы (I) и их солями можно осуществить с использованием способов, хорошо известных специалистам в данной области техники. Примерами являются
(i) превращение одного или нескольких R1 из алкокси (например, метокси) в гидрокси,
(ii) превращение одного или нескольких R1 из гидрокси в сульфонилокси, такой как алкилсульфонилокси или галогеналкилсульфонилокси, например, метансульфонилокси или трифторметансульфонилокси,
(iii) превращение одного или нескольких R1 из галогена или перфторалкилсульфонилокси в циано;
и последующее необязательное получение соли соединения формулы (I).
Обнаружено, что соединения формулы (I) проявляют аффинность в отношении допаминовых рецепторов, в частности рецептора D3, и ожидается их применимость при лечении болезненных состояний, при которых требуется модуляция таких рецепторов, таких как психотические состояния.
Такую аффинность типично рассчитывают из IC50 как концентрации соединения, необходимой для вытеснения 50% радиоактивного лиганда из рецептора, и приводят в виде величины Ki, вычисленной с помощью следующего уравнения:

где L = радиолиганд и KD = аффинность радиолиганда в отношении рецептора (Cheng and Prusoff, Biochem. Pharmacol., 22:3099, 1973).
В контексте настоящего изобретения вместо Ki используют pKi (соответствующий антилогарифму Ki), и соединения настоящего изобретения типично показывают pKi свыше 7. В одном аспекте настоящее изобретение относится к соединениям формулы (I) с pKi от 7 до 8. В другом аспекте настоящее изобретение относится к соединениям формулы (I) с pKi от 8 до 9. В еще одном аспекте настоящее изобретение относится к соединениям формулы (I) с pKi свыше 9.
Также обнаружено, что многие соединения формулы (I) имеют аффинность к допаминовым рецепторам D3 большую, чем к D2. Полагают, что лечебное действие доступных в настоящее время антипсихотических средств (нейролептиков) проявляется через блокаду рецепторов D2; однако также считается, что такой механизм ответственен за нежелательное экстрапирамидное побочное действие (eps), связанное с многими нейролептическими средствами. Предполагается, что блокада недавно охарактеризованного допаминового рецептора D3 может вызвать благоприятную антипсихотическую активность без существенного eps (см., например, Sokoloff et al., Nature, 1990, 347:146-151; и Schwartz et al., Clinical Neuropharmacology, Vol.16, No.4, 295-314, 1993). Одно воплощение относится к соединениям настоящего изобретения с более высокой (например, в ≥10х или ≥100х более высокой) аффинностью к допаминовым рецепторам D3, чем к D2 (такую аффинность можно измерить с использованием стандартной методологии, например, с использованием клонированных допаминовых рецепторов - см. в данном описании). Указанные соединения можно соответственно использовать в качестве селективных модуляторов допаминовых рецепторов D3.
Из локализации рецепторов D3 также можно представить, что соединения также можно применять для лечения токсикомании, в которой, как предполагается, участвуют рецепторы D3 (см., например, Levant, 1997, Pharmacol. Rev., 49, 231-252). Примерами такой токсикомании являются злоупотребление алкоголем, кокаином, героином и никотином. К другим состояниям, которые можно лечить указанными соединениями, относятся дискинетические расстройства, такие как болезнь Паркинсона, вызванный нейролептиками паркинсонизм, и поздняя дискинезия; депрессия; тревога, ухудшение познавательной способности, в том числе расстройства памяти, такие как болезнь Альцгеймера, пищевые расстройства, половая дисфункция, расстройства сна, рвота, нарушения движений, обсессивно-компульсивные расстройства, амнезия, агрессия, аутизм, головокружение, деменция, нарушения циркадного ритма и расстройства двигательной функции желудка, например, IBS.
Соединения формулы (I) можно использовать для лечения всех аспектов лекарственной зависимости, включая абстинентный синдром от злоупотребления лекарственными средствами, такими как алкоголь, кокаин, опиаты, никотин, бензодиазепины, и ингибирование толерантности, вызванное опиоидами. Кроме того, соединения формулы (I) и их фармацевтически приемлемые соли и сольваты можно использовать для ослабления пристрастия, и поэтому они будут применимы при лечении пристрастия к лекарственным средствам. Пристрастие к лекарственным средствам можно определить как побудительную мотивацию к самоназначению психотически активного вещества, которое потреблялось ранее. Три основных фактора участвуют в развитии и поддержании пристрастия к лекарственным средствам: (1) состояния подавленности из-за отмены лекарственного средства могут действовать как негативный усилитель, приводящий к пристрастию; (2) раздражители окружающей среды, связанные с действием лекарственных средств, могут стать постепенно более сильными (сенсибилизация) при борьбе со стремлением и пристрастием и (3) знание (память) о способности лекарственных средств усиливать приятное действие и облегчать подавленное состояние во время отмены. Пристрастие может отвечать за трудности, с которыми сталкиваются индивидуумы при отказе от злоупотребления лекарственными средствами, и поэтому вносит существенный вклад в развитие и сохранение лекарственной зависимости.
Соединения формулы (I) имеют потенциальное применение в качестве антипсихотических средств, например, при лечении шизофрении, шизоаффективных расстройств, психотической депрессии, мании, параноидных и бредовых расстройств. Кроме того, они могут применяться в качестве дополнительных лечебных мероприятий при болезни Паркинсона, в частности, с такими соединениями, как L-DOPA, и, возможно, допаминергическими агонистами, для ослабления побочного действия, испытываемого при применении такого рода лечения в течение длительного времени (например, см. Schwartz et al., Brain Res. Reviews, 1998, 26, 236-242).
В контексте настоящего изобретения термины, описывающие показания, используемые в данном описании, классифицируются по the Diagnostic and Statistical Manual of Mental Disorders, 4th Edition, опубликован American Psychiatric Association (DSM-IV), и/или по International Classification of Diseases, 10th Edition (ICD-10). Различные подтипы расстройств, указанные в данном описании, рассматриваются как часть настоящего изобретения. Числа в скобках после перечисленных ниже заболеваний относятся к классификационным индексам в DSM-IV.
В контексте настоящего изобретения термин "психотическое расстройство" включает
шизофрению, в том числе подтипы параноидный тип (295.30), дезорганизационный тип (295.10), кататонический тип (295.20), неустановленный тип (295.90) и остаточный тип (195.60); расстройство шизофренической формы (295.40); шизоаффективное расстройство (295.70), в том числе подтипы биполярный тип и депрессивный тип; бредовое расстройство (297.1), в том числе подтипы тип эротомании, тип величия, тип ревности, тип преследования, соматический тип, смешанный тип и неустановленный тип; кратковременное психотическое расстройство (298.8); разделенное (shared) психотическое расстройство (297.3); психотическое расстройство из-за общего состояния здоровья, в том числе подтипы с бредами и с галлюцинациями; вызванное веществами психотическое расстройство, в том числе подтипы с бредами (293.81) и с галлюцинациями (293.82); и психотическое расстройство, не имеющее другого определения (298.9).
В контексте настоящего изобретения термин "расстройство, связанное с веществом" включает
связанные с веществами расстройства, в том числе расстройства из-за применения веществ, такие как зависимость от вещества, пристрастие к веществу и злоупотребление веществом; вызванные веществами расстройства, такие как интоксикация, отмена вещества, вызванный веществом делирий, вызванная веществом стойкая деменция, вызванное веществом стойкое амнестическое расстройство, вызванное веществом психотическое расстройство, вызванное веществом расстройство настроения, вызванное веществом тревожное расстройство, вызванная веществом половая дисфункция, вызванное веществом расстройство сна и галюцинногенное стойкое расстройство восприятия ("стоп-кадры"); связанные с алкоголем расстройства, такие как алкогольная зависимость (303.90), злоупотребление алкоголем (305.00), алкогольная интоксикация (303.00), отмена алкоголя (291.81), делирий алкогольной интоксикации, делирий отмены алкоголя, вызванная алкоголем стойкая деменция, вызванное алкоголем стойкое амнестическое расстройство, вызванное алкоголем психотическое расстройство, вызванное алкоголем расстройство настроения, вызванное алкоголем тревожное расстройство, вызванная алкоголем половая дисфункция, вызванное алкоголем расстройство сна и связанное с алкоголем расстройство, не имеющее другого определения (291.9); расстройства, связанные с амфетамином (или подобными амфетамину веществами), такие как амфетаминная зависимость (304.40), злоупотребление амфетамином (305.70), амфетаминная интоксикация (292.89), отмена амфетамина (292.0), делирий амфетаминной интоксикации, вызванное амфетамином психотическое расстройство, вызванное амфетамином расстройство настроения, вызванное амфетамином тревожное расстройство, вызванная амфетамином половая дисфункция, вызванное амфетамином расстройство сна и связанное с амфетамином расстройство, не имеющее другого определения (292.9); расстройства, связанные с кофеином, такие как кофеиновая интоксикация (305.90), вызванное кофеином тревожное расстройство, вызванное кофеином расстройство сна и связанное с кофеином расстройство, не имеющее другого определения (292.9); расстройства, связанные с коноплей, такие как зависимость от конопли (304.30), злоупотребление коноплей (305.20), делирий конопляной интоксикации, вызванное коноплей психотическое расстройство, вызванное коноплей тревожное расстройство и связанное с коноплей расстройство, не имеющее другого определения (292.9); расстройства, связанные с кокаином, такие как кокаиновая зависимость (304.20), злоупотребление кокаином (305.60), кокаиновая интоксикация (292.89), синдром отмены кокаина (292.0), делирий из-за кокаиновой интоксикации, вызванное кокаином психотическое расстройство, вызванное кокаином нарушение настроения, вызванное кокаином тревожное расстройство, вызванная кокаином половая дисфункция, вызванное кокаином расстройство сна и связанное с кокаином расстройство, не имеющее другого определения (292.9); расстройства, связанные с галлюциногеном, такие как галлюциногеновая зависимость (304.50), злоупотребление галлюциногеном (305.30), галлюциногеновая интоксикация (292.89), стойкое расстройство восприятия из-за галлюциногена ("стоп-кадры") (292.89), делирий из-за галлюциногенной интоксикации, вызванное галлюциногеном психотическое расстройство, вызванное галлюциногеном нарушение настроения, вызванное галлюциногеном тревожное расстройство и связанное с галлюциногеном расстройство, не имеющее другого определения (292.9); расстройства, связанные с аспиратом, такие как зависимость от аспирата (304.60), злоупотребление аспиратом (305.90), аспиратная интоксикация (292.89), делирий из-за аспиратной интоксикации, вызванная аспиратом стойкая деменция, вызванное аспиратом психотическое расстройство, вызванное аспиратом нарушение настроения, вызванное аспиратом тревожное расстройство и связанное с аспиратом расстройство, не имеющее другого определения (292.9); расстройства, связанные с никотином, такие как никотиновая зависимость (305.1), синдром отмены никотина (292.0) и связанное с никотином расстройство, не имеющее другого определения (292.9); расстройства, связанные с опиоидами, такие как опиоидная зависимость (304.00), злоупотребление опиоидами (305.50), опиоидная интоксикация (292.89), синдром отмены опиоида (292.0), делирий из-за опиоидной интоксикации, вызванное опиоидом психотическое расстройство, вызванное опиоидом нарушение настроения, вызванная опиоидом половая дисфункция, вызванное опиоидом расстройство сна и связанное с опиоидом расстройство, не имеющее другого определения (292.9); расстройства, связанные с фенциклидином (или феклицидиноподобные), такие как фенклицидиновая зависимость (304.60), злоупотребление фенклицидином (305.90), фенклицидиновая интоксикация (292.89), делирий из-за фенклицидиновой интоксикации, вызванное фенклицидином психотическое расстройство, вызванное фенклицидином нарушение настроения, вызванное фенклицидином тревожное расстройство и связанное с фенклицидином расстройство, не имеющее другого определения (292.9); расстройства, связанные с седативными, снотворными или успокаивающими средствами, такие как зависимость от седативного, снотворного или успокаивающего средства (304.10), злоупотребление седативным, снотворным или успокаивающим средством (305.40), интоксикация седативным, снотворным или успокаивающим средством (292.89), синдром отмены седативного, снотворного или успокаивающего средства (292.0), делирий из-за снотворного или успокаивающего средства, вызванная седативным, снотворным или успокаивающим средством стойкая деменция, вызванное седативным, снотворным или успокаивающим средством стойкое амнестическое расстройство, вызванное седативным, снотворным или успокаивающим средством психотическое расстройство, вызванное седативным, снотворным или успокаивающим средством нарушение настроения, вызванное седативным, снотворным или успокаивающим средством тревожное расстройство, вызванная седативным, снотворным или успокаивающим средством половая дисфункция, вызванное седативным, снотворным или успокаивающим средством расстройство сна и связанное с седативным, снотворным или успокаивающим средством расстройство, не имеющее другого определения (292.9); расстройства, связанные с несколькими веществами, такие как зависимость от нескольких веществ (304.80); и другие (или неизвестные) расстройства, связанные с веществами, такими как анаболические стероиды, нитратные аспираты и оксид диазота.
Поэтому в другом аспекте настоящее изобретение относится к способу лечения состояния, для которого благоприятна модуляция (в частности, антагонизм/ингибирование) допаминовых рецепторов (в особенности рецепторов D3), включающему введение млекопитающему (например, человеку), нуждающемуся в этом, эффективного количества соединения формулы (I) или его фармацевтически (т.е. физиологически) приемлемой соли. К таким состояниям относятся, в частности, психозы/психотические состояния, такие как шизофрения, и токсикомания.
Изобретение также относится к применению соединения формулы (I) или его фармацевтически приемлемой соли для получения лекарственного средства для лечения состояния у млекопитающего, для которого благоприятна модуляция (в частности, антагонизм/ингибирование) допаминовых рецепторов (в особенности рецепторов D3).
Изобретение также относится к соединению формулы (I) или его фармацевтически приемлемой соли для применения для лечения состояния у млекопитающего, для которого благоприятна модуляция (в частности, антагонизм/ингибирование) допаминовых рецепторов (в особенности рецепторов D3).
Изобретение также относится к соединению формулы (I) или его фармацевтически приемлемой соли, используемому для лечения состояний у млекопитающиего, в котором модуляция ( в частности, антагонизм/ингибирование) допаминовых рецепторов является благоприятным.
В одном воплощении антагонистов D3 по изобретению используют для лечения психозов, таких как шизофрения, или при лечении токсикомании.
Таким образом, в еще одном аспекте настоящее изобретение относится к способу лечения психотического состояния (например, шизофрении) или токсикомании, включающему введение млекопитающему (например, человеку), нуждающемуся в этом, эффективного количества соединения формулы (I), определение которому дано в настоящем описании, или его фармацевтически приемлемой соли.
Изобретение также относится к применению соединения формулы (I) или его фармацевтически приемлемой соли для получения лекарственного средства для лечения психотического состояния (например, шизофрении) или токсикомании у млекопитающего.
Изобретение также относится к соединению формулы (I) или его фармацевтически приемлемой соли для применения для лечения психотического состояния (например, шизофрении) или токсикомании у млекопитающего.
Изобретение также относится к соединению формулы (I) или его фармацевтически приемлемой соли для применения в качестве активного лечебного средства для лечения млекопитающего, например, для применения для лечения любого из состояний, описанных в данном описании.
"Лечение" включает профилактику, когда это соответствует релевантному(ым) состоянию(ям).
В случае применения в медицине соединения настоящего изобретения, как правило, вводят в виде стандартной фармацевтической композиции. Следовательно, настоящее изобретение относится в другом аспекте к фармацевтической композиции, содержащей соединение формулы (I) или его фармацевтически (т.е. физиологически) приемлемую соль и фармацевтически (т.е. физиологически) приемлемый носитель. Фармацевтическая композиция может являться композицией для применения при лечении любого из состояний, описанных в данном описании.
Соединения формулы (I) можно вводить любым подходящим способом, например, методом перорального, парентерального (например, внутривенного), трансбуккального, подъязычного, назального, ректального или трансдермального введения, и фармацевтические композиции адаптируют соответственно.
Соединения формулы (I) и их фармацевтически приемлемые соли, которые активны при пероральном приеме, можно ввести в состав жидких или твердых композиций, например, сиропов, суспензий или эмульсий, таблеток, капсул и лепешек.
Жидкий препарат, как правило, будет представлять собой суспензию или раствор соединения или его фармацевтически приемлемой соли в подходящем(их) жидком(их) носителе(ях), например, в водном растворителе, таком как вода, этанол или глицерин, или в неводном растворителе, таком как полиэтиленгликоль или масло. Препарат также может содержать суспендирующее вещество, консервант, корригент или краситель.
Композицию в форме таблетки можно получить с использованием любого(ых) фармацевтического(их) носителя(ей), обычно используемого(ых) для получения твердых препаратов. Примерами таких носителей являются стеарат магния, крахмал, лактоза, сахароза и целлюлоза.
Композицию в форме капсулы можно получить с использованием обычных процедур инкапсулирования. Например, с использованием стандартных носителей можно получить гранулы, содержащие активный ингредиент, и затем заполнить ими твердую желатиновую капсулу; с другой стороны, можно получить дисперсию или суспензию с использованием любого(ых) обычного(ых) фармацевтического(их) носителя(ей), например, водорастворимых камедей, целлюлоз, силикатов или масел, и затем заполнить дисперсией или суспензией мягкую желатиновую капсулу.
Типичная парентеральная композиция представляет собой раствор или суспензию соединения или его фармацевтически приемлемой соли в стерильном водном носителе или парентерально приемлемом масле, например, полиэтиленгликоле, поливинилпирролидоне, лецитине, арахисовом масле или сезамовом масле. С другой стороны, раствор можно лиофилизовать и затем восстановить подходящим растворителем непосредственно перед введением.
Композиции для назального введения можно удобно получить в виде аэрозолей, капель, гелей и порошков. Аэрозольные препараты типично содержат раствор или тонкую суспензию активного вещества в фармацевтически приемлемом водном или неводном растворителе и, как правило, представлены в количестве одной или нескольких доз в стерильной форме в плотно закрытой емкости, которая может принимать форму картриджа или сменного баллончика для применения с распыляющим устройством. С другой стороны, герметично закрытая емкость может представлять собой унитарный дозатор, такой как однодозовый назальный ингалятор, или аэрозольный дозатор, снабженный дозирующим клапаном, предназначенный для удаления содержимого емкости при однократном использовании. Когда лекарственная форма содержит дозатор аэрозоля, она будет содержать пропеллент, который может представлять собой сжатый газ, такой как сжатый воздух, или органический пропеллент, такой как фторхлорсодержащий углеводород. Аэрозольные лекарственные формы также могут принимать форму насоса-распылителя.
Композиции, подходящие для трансбуккального и подъязычного введения, включают таблетки, лепешки и пастилки, где активный ингредиент образует композицию с носителем, таким как сахар и аравийская камедь, трагакант или желатин и глицерин.
Композиции для ректального введения обычно имеют форму суппозиториев, содержащих обычную основу для суппозиториев, такую как масло какао.
Композиции, подходящие для трансдермального введения, включают мази, гели и пэтчи.
В одном воплощении композиция представляет собой стандартную лекарственную форму, такую как таблетка, капсула или ампула.
Каждая стандартная лекарственная форма для перорального введения содержит, например, от 1 до 250 мг (а для парентерального введения содержит, например, от 0,1 до 25 мг) соединения формулы (I) или его фармацевтически приемлемой соли в рассчете на свободное основание.
Фармацевтически приемлемые соединения изобретения, как правило, будут вводиться по схеме ежесуточного приема лекарственного средства (для взрослого пациента), например, в пероральной дозе от 1 мг до 500 мг, например, от 10 мг до 400 мг, например, от 10 мг до 250 мг, или внутривенно, подкожно или внутримышечно в дозе от 0,1 мг до 100 мг, например, от 0,1 мг до 50 мг, например, от 1 до 25 мг, соединения формулы (I) или его фармацевтически приемлемой соли в рассчете на свободное основание, причем соединение вводят 1-4 раза в сутки. Подходящим будет введение соединений в период длительной терапии, например, в течение недели или долее.
Методы биологических испытаний
Функциональную возможность и свойственную активность соединений данного изобретения можно измерить описаным далее сцинтилляционным приближенным анализом GTPγS (GTPγS-SPA). Клетки, используемые в исследовании, являются клетками яичника китайского хомячка (СНО).
Клеточная линия
CHO_D2
CHO_D3
Клеточные мембраны получают следующим образом. Клеточные осадки ресуспендируют в 10 объемах 50 мМ HEPES, 1 мМ ЭДТК, рН 7,4, с использованием КОН. На следующий день в буфер непосредственно перед получением буфера для гомогенизации добавляют следующие протеазы:
10-6 М лейпептина (Sigma L2884) - 5000 х исходный = 5 мг/мл в буфере;
25 мкг/мл бактирацина (Sigma В0125) - 1000 х исходный = 25 мг/мл в буфере;
1 мМ PMSF - 1000 х исходный = 17 мг/мл в 100% этаноле;
2 × 10-6 М пепстаина А - 1000 х исходный = 2 мМ в 100% ДМСО.
Клетки гомогенизируют включениями 2 × 15 секунд в 1-л стакане Glass Warning в камере класса биологической опасности. Полученную суспензию центрифугируют при 500 g в течение 20 мин (центрифуга Beckman T21, 1550 об/мин). Супернатант извлекают 25-мл пипеткой, распределяют аликвоты в предварительно охлажденные центрифужные пробирки и центрифугируют при 48000 g для высаживания в осадок клеточных мембран (Beckman T1270: 23000rpm за 30 мин). Полученный при 48000 g осадок ресуспендируют в буфере для гомогенизации (4х объема начального клеточного осадка). Полученный при 48000 g осадок ресуспендируют круговыми вращениями в течение 5 секунд и гомогенизируют в гомогенизаторе Даунса 10-15 раз. Препарат распределяют на аликвоты соответствующего размера (200-1000 мкл) в полипропиленовые пробирки и хранят при -80°С. Содержание белка в мембранных препаратах оценивают анализом на белки по Брэдфорду.
Конечная высшая концентрация лекарственного средства в анализе 3 мкМ, и для построения кривой по 11 точкам осуществляют серийные разведения 1:4 в 100% ДМСО с использованием Biomek FX. Испытываемое лекарственное средство в количестве 1% от общего объема аналитической смеси (TAV) добавляют в полностью белые 384-луночные аналитические планшеты. Добавляют 50% TAV предварительно связанных (в течение 90 мин при 4°С) мембран, 5 мкг/мл, и агглютинин-полистирольные гранулы c зародышами пшеницы для сцинтилляционного приближенного анализа (RPNQ0260, Amersham), 0,25 мг/лунку, в 20 мМ HEPES, рН 7,4, 100 мМ NaCl, 10 мМ MgCl2, 60 мкг/мл сапонина и 30 мкМ GDP. Третья добавка представляет собой 20% TAV или буфера (формат агониста) или конечной концентрации в анализе ЕС80 агониста квинелорана в буфере для анализа (формат антагониста). Анализ начинают, добавляя 29% TAV GTPγ[35S] до конечной концентрации 0,38 нМ (37 МБк/мл, 1160 Ки/ммоль, Amersham). После всех добавлений аналитические планшеты центрифугируют в течение 1 мин при 1000 об/мин. Осуществляют подсчет на Viewlux, фильтр 613/55, в течение 5 мин в промежутке 2-6 часов после последнего добавления.
Действие испытываемого лекарственного средства на основу дает величину ЕС50 с помощью программы интерактивного подбора кривой методом наименьших квадратов, представленное в таблице в виде рЕС50 (т.е. -logEC50). Соотношение между максимальным воздействием испытываемого лекарственного средства и максимальным действием полного агониста квинелорана дает величину действительной активности (IA) (т.е. IA = 1 для полного агониста, IA < 1 для неполного агониста). Величины fpKi испытываемого лекарственного средства вычисляют из IC50, полученной в эксперименте "формат антагониста", с использованием уравнения Чанга и Прусоффа (Prusoff) fKi = IC50/1+([A]/EC50), где [A] представляет собой концентрацию агониста 5-НТ в анализе, и ЕС50 представляет собой величину ЕС50 5-НТ, полученную в том же эксперименте. fpKi определяется как -logfKi.
Соединения изобретения, перечисленные выше, имеют величины pKi в интервале 7,0-10,5 при допаминовом рецепторе D3. Результаты по pKi оцениваются только с точностью примерно ±0,3-0,5.
Соединения изобретения, перечисленные выше, имеют селективность относительно D2, превышающую 30.
Примеры
Далее изобретение поясняется примерами, не являющимися ограничительными. Препаративные примеры 1-5 осуществляют по аналогии со способом синтеза, описанным в J. Med. Chem., 1981, 24, 481-490.
Все температуры приводятся в °С. Инфракрасные спектры получают на приборе FT-IR. Соединения анализируют путем непосредственного введения образца, растворенного в ацетонитриле, в масс-спектрометр, работающий в режиме ионизации положительным распылением электронов (ES+). Спектры протонного магнитного резонанса (1Н-ЯМР) регистрируют при 400 МГц, химические сдвиги приводятся в м.д. нисходящего поля (d) от Me4Si, используемого в качестве внутреннего стандарта, и приводят как синглеты (с), уширенные синглеты (ушс), дублеты (д), дублеты дублетов (дд), триплеты (т), квартеты (к) или мультиплеты (м).
Экспериментальные спектры колебательного кругового дихроизма (VCD) получают с использованием спектрометра ChiralIRTM VCD, работающего в интервале частот 2000-800 см-1. Спектры получают при комнатной температуре (23°С) с использованием герметично закрытой прозрачной кюветы с окнами из фторида бария и длиной пробега 100 микрон (время сканирования изменяется от 60 до 120 минут на изомер). Растворы образцов типично получают, растворяя 10 мг каждого энантиомера в 100 мкл дейтерохлороформа (CDCl3). Для установлений ab initio рассчитывают спектры VCD и неполяризованного ИК с использованием пакета программ 1 Gaussian 98.
Оптическое вращение измеряют с использованием поляриметра (Perkin Elmer, модель 241), работающего при 589 нм (натриевый источник). Измерения проводят с использованием 1-дециметровой микроячейки, термостатированной при 23°С. Концентрации типично составляют 10 мг/мл (с=0,01). Для установлений OR ab initio используют программу Dalton Quantum Chemistry.
Колоночную хроматографию осуществляют на силикагеле (Merck AG, Darmstaadt, Германия). В тексте используются следующие аббревиатуры: NBS = N-бромсукцинимид, витрид = "Red-Al®", HOBt = 1-гидроксибензотриазол, EtOAc = этилацетат, Et2O = диэтиловый эфир, ДМФА = N,N'-диметилформамид, МеОН = метанол, ТФК = трифторуксусная кислота, ТГФ = тетрагидрофуран, IPA = изопропанол, ТЕА = триэтиламин, DCC = 1,3-дициклогексилкарбодиимид, SCX = сильный катионообменник, ТСХ обозначает тонкослойную хроматографию на пластинах из диоксида кремния, и "осушенный" относится к раствору, осушенному над безводным сульфатом натрия, r.t. (RT) обозначает комнатную температуру, Rt = время удерживания, ДМСО = диметилсульфоксид.
Препаративный пример 1. Метилбром(4-метоксифенил)ацетат

К смеси метил-4-метоксифенилацетата (20 г, 0,11 моль) и NBS (0,11 моль) в CCl4 (0,2 л) добавляют 3 капли 48% HBr и полученную смесь кипятят с обратным холодильником в течение 8 час. Охлажденный раствор фильтруют через слой силикагеля, фильтрат упаривают в вакууме и получают 29 г названного в заголовке соединения в виде бледно-желтого масла, которое используют на последующей стадии без дополнительной очистки.
ЯМР (1H, CDCl3): δ 7,3 (д, 2Н), 6,8 (д, 2Н), 5,1 (с, 1Н), 3,8 (с, 3Н), 3,5 (с, 3Н).
Препаративный пример 2. Диметил-1-(4-метоксифенил)-1,2-циклопропандикарбоксилат
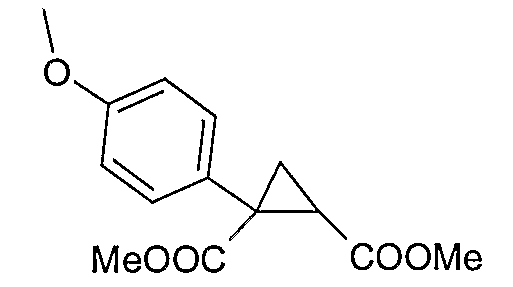
К взвеси NaH (4,4 г, 60% в минеральном масле) в безводном Et2O (0,3 л) при перемешивании при 0°С в течение 30 мин добавляют метанол (10,3 мл), а затем раствор полученного в препаративном примере 1 бромсодержащего эфира метилбром(4-метоксифенил)ацетата (29 г) в метилакрилате (19,8 мл) (в примерах, где исходят из этилфенилацетатного производного, используют этанол и этилацетат соответственно) и метаноле (3 мл). Смесь перемешивают при 25°С в течение 24 час и затем непрореагировавший NaH разлагают 3 мл метанола. Добавляют воду (75 мл), органическую фазу отделяют, сушат над Na2SO4 и фильтруют. Летучие вещества выпаривают в вакууме и получают 31,5 г названного в заголовке соединения в виде масла, которое используют на последующей стадии без дополнительной очистки.
ЯМР (1H, CDCl3): δ 7,3 (д, 2Н), 6,8 (д, 2Н), 3,77 (с, 3Н), 3,73 (с, 3Н), 3,64 (с, 3Н), 2,18 (дд, 1Н), 2,05 (дд, 1Н), 1,46 (дд, 1Н). МС (m/z): 265,4 [MH]+.
Препаративный пример 3. 1-(4-Метоксифенил)-1,2-циклопропандикарбоновая кислота
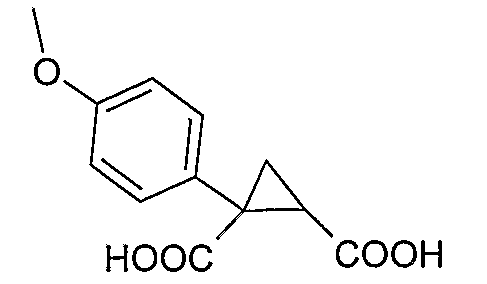
Смесь диэфира, полученного в препаративном примере 2 (31,5 г) и КОН (13,5 г) в смеси EtOH:H2O, 1:1 (240 мл), кипятят с обратным холодильником в течение 6 час и затем концентрируют до половины исходного объема. Водный раствор экстрагируют Et2O, охлаждают на льду и затем подкисляют 25 мл 12 н HCl. Белый кристаллический продукт реакции собирают фильтрацией и сушат в вакууме и получают 12,8 г названного в заголовке соединения (общий выход из рассчета на метилбром(4-метоксифенил)ацетат 50%).
ЯМР (1H, ДМСО): δ 12,5 (ушс, 2H), 7,25 (д, 2H), 6,85 (д, 2H), 3,7 (с, 3H), 2,0 (дд, 1H), 1,85 (дд, 1H), 1,38 (дд, 1H). МС (m/z): 235,0 [M-H]-.
Препаративный пример 4. (1R,5S/1S,5R)-1-[4-(Метокси)фенил]-3-азабицикло[3.1.0]гексан-2,4-дион

Смесь 12,8 г дикислоты, полученной в препаративном примере 3, и 6,5 г мочевины в 300 мл м-ксилола кипятят с обратным холодильником в течение 8 час и затем концентрируют досуха в вакууме. Сырое вещество очищают колоночной хроматографией (AcOEt:циклогексан = 1(?):10 - 4:6) и получают 5,5 г названного в заголовке соединения (выход = 46%).
МС (m/z): 218,1 [MH]+.
Препаративный пример 5. (1R,5S/1S,5R)-1-[4-(Метокси)фенил]-3-азабицикло[3.1.0]гексан

К взвеси 5,5 г имида, полученного в препаративном примере 4, в 170 мл толуола при перемешивании в атмосфере азота постепенно добавляют 45 мл раствора витрида (3,4 М в толуоле). Полученный раствор перемешивают при кипячении с обратным холодильником в течение 2 час. К охлажденному раствору осторожно добавляют водный раствор NaOH (10 М, 40 мл) и органический слой промывают двумя порциями воды и сушат над Na2SO4. Полученный раствор фильтруют, фильтрат упаривают в вакууме и получают 4,8 г названного в заголовке соединения (выход = 100%).
ЯМР (1H, CDCl3): δ 7,10 (д, 2H), 6,82 (д, 2H), 3,77 (с, 3H), 3,35-2,98 (м, 4H), 2,58 (дд, 1H), 0,87 (дд, 1H), 0,78 (дд, 1H), NH не наблюдают. МС (m/z): 190,1 [MH]+.
Препаративный пример 6. (1R,5S/1S,5R)-1-(4-Бромфенил)-3-азабицикло[3.1.0]гексан

К 20 мл 1 М раствора ВН3-тетрагидрофуран при перемешивании при 0°С в атмосфере азота постепенно добавляют раствор 1,32 г (5 ммоль) (1R,5S/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексан-2,4-диона, полученного по аналогии с препаративным примером 4, в 20 мл сухого тетрагидрофурана. Полученный раствор перемешивают при комнатной температуре в течение 15 мин и затем греют на паровой бане в течение 1 часа. Затем раствор охлаждают на ледяной бане, осторожно добавляют 2,5 мл 6 М HCl, и растворитель удаляют в вакууме. Оставшееся вещество объединяют с 12,5 мл 5 М раствора NaOH и смесь экстрагируют эфиром. Эфирный экстракт дважды промывают водой, сушат над Na2SO4 и фильтруют и получают 1,19 г названного в заголовке соединения (выход = 100%).
ЯМР (1H, CDCl3): δ 7,35 (д, 2H), 7,02 (д, 2H), 3,25-2,96 (м, 4H), 1,63 (дд, 1H), 1,55 (дд, 1H), 1,30 (дд, 1H), NH не наблюдают. МС (m/z): 238,1 [MH]+, 1Br.
Препаративный пример 7. (1R,5S/1S,5R)-4-[3-(Трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]бензонитрил
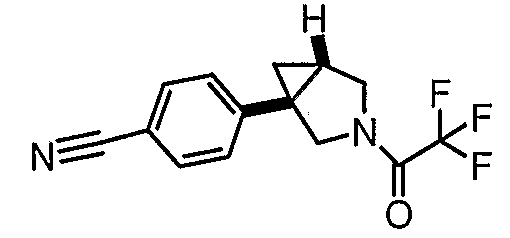
К раствору 4-[3-азабицикло[3.1.0]гекс-1-ил]бензонитрила (280 мг, получен способом, аналогичным описанному в препаративном примере 5) и триэтиламина (0,25 мл) в дихлорметане (15 мл) при 0°С добавляют ангидрид трифторуксусной кислоты (0,21 мл). Реакционную смесь оставляют нагреваться до комнатной температуры на 2 часа, затем промывают насыщенным раствором NaHCO3, органический слой сушат и упаривают и получают 269 мг названного в заголовке соединения.
МС (m/z): 281,2 [MH]+.
Препаративный пример 8. (1R,5S/1S,5R)-4-[3-(Трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]бензальдегид

Смесь 4-[3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]бензонитрила (283 мг), сплава Ni-Al (450 мг), муравьиной кислоты (3,9 мл) и воды (1,1 мл) перемешивают при 80°С в течение 3 час. Реакционную смесь охлаждают до комнатной температуры и фильтруют. Фильтрат экстрагируют этилацетатом, органическую фазу промывают раствором NaHCO3, сушат над Na2SO4 и упаривают в вакууме и получают 195 мг названного в заголовке соединения в виде желтого масла.
МС (m/z): 284,2 [MH]+.
Препаративный пример 9. Оксим (1R,5S/1S,5R)-4-[3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]бензальдегида
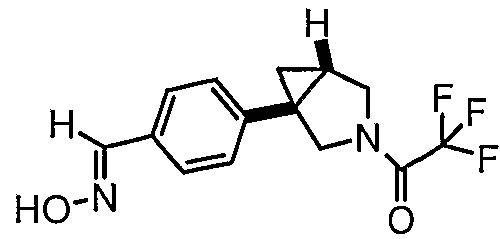
К раствору 4-[3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]бензальдегида (195 мг) в 5 мл пиридина добавляют гидрохлорид гидроксиламина (57,5 мг) и смесь перемешивают в течение 3 час при комнатной температуре. Растворитель выпаривают, сырое вещество растворяют в этилацетате, органическую фазу промывают 10% раствором Na2CO3 и рассолом, сушат над Na2SO4 и упаривают в вакууме и получают 225 мг названного в заголовке соединения в виде желтого масла.
МС (m/z): 299,2 [MH]+.
Препаративный пример 10. (1R,5S/1S,5R)-4-[3-(Трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]-N-гидроксибензолкарбоксимидоилхлорид

К раствору оксима 4-[3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]бензальдегида (0,69 ммоль) в 3,5 мл диметилформамида при 0°С добавляют по частям N-хлорсукцинимид (97 мг). После перемешивания в течение 1,5 час при 40°С растворитель выпаривают. Сырой продукт реакции растворяют в смеси диэтиловый эфир/дихлорметан (4/1), органическую фазу промывают водой, сушат над Na2SO4 и концентрируют в вакууме и получают 243 мг названного в заголовке соединения в виде коричневого масла.
Препаративный пример 11. (1R,5S/1S,5R)-1-[4-(5-Метил-3-изоксазолил)фенил]-3-(трифторацетил)-3-азабицикло[3.1.0]гексан

К раствору 4-[3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]-N-гидроксибензолкарбоксимидоилхлорида (0,69 ммоль) в 6 мл хлороформа добавляют триэтиламин (0,24 мл) и 2-хлорпропен (0,29 мл) и реакционную смесь перемешивают в течение 18 час при комнатной температуре. Раствор промывают водой, сушат над Na2SO4 и летучие вещества выпаривают в вакууме. Сырое вещество очищают колоночной хроматографией (AcOEt:циклогексан = 1:10 - 4:6) и получают 180 мг названного в заголовке соединения.
МС (m/z): 337,2 [MH]+.
Препаративный пример 12. (1R,5S/1S,5R)-1-[4-(5-Метил-3-изоксазолил)фенил]-3-азабицикло[3.1.0]гексан

Смесь 1-[4-(5-метил-3-изоксазолил)фенил]-3-(трифторацетил)-3-азабицикло[3.1.0]гексана (0,54 ммоль) и К2СО3 (296 мг) в метаноле (5 мл) и воде (5 мл) перемешивают в течение 4 час при 50°С. Растворитель выпаривают в вакууме и продукт реакции обрабатывают смесью дихлорметан/изопропанол, 1/1 и фильтруют. Фильтрат сушат над Na2SO4, летучие вещества выпаривают в вакууме и получают 105 мг названного в заголовке соединения (выход = 81%).
МС (m/z): 241,2 [MH]+.
Препаративный пример 13. 5-{5-[(3-Хлорпропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил}-2-метилхинолин
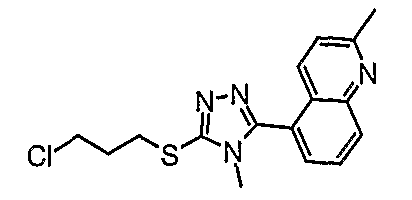
К 4-метил-5-(2-метил-5-хинолинил)-2,4-дигидро-3Н-1,2,4-триазол-3-тиону (3,6 г, получен способом, аналогичным описанному в WO 200240471) в этаноле (60 мл), содержащем 1-бром-3-хлорпропан (2,0 мл), осторожно добавляют при перемешивании гидрид натрия (0,60 г, 60% в вазелине). Смесь кипятят с обратным холодильником в течение 45 мин. Летучие вещества выпаривают в вакууме и остаток подвергают колоночной хроматографии (градиент EtOAc-ацетон). Полученное таким образом вещество высаживают из горячего EtOAc (20 мл), добавляя петролейный эфир (40-60, 50 мл), охлаждают и собирают фильтрацией и получают названное в заголовке соединение в виде бесцветного кристаллического вещества (2,1 г).
ЯМР (1H, CDCl3): δ 8,18 (д, 1H), 8,12 (д, 1H), 7,76 (т, 1H), 7,55 (д, 1H), 7,30 (д, 1H), 3,75 (т, 2H), 3,50 (т, 2H), 3,40 (с, 3H), 2,76 (с, 3H), 2,37 (м, 2H).
Препаративный пример 14. 3-[(3-Хлорпропил)тио]-4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол

Этил-2-хлорацетоацетат (1 мас.ч.; 1 экв., 1000 г) обрабатывают формамидом (0,68 об.ч.; прибл. 2,8 экв.) и полученный раствор греют при 120°С. Через 5 часов смесь охлаждают до комнатной температуры и выдерживают в атмосфере азота в течение ночи. Смесь обрабатывают NaOH (3 М, 6 об.ч., реакция умеренно экзотермическая) и перемешивают при комнатной температуре в течение 4 часов. Добавляют этилацетат 6 об.ч.) и фазы разделяют. Органический слой отбрасывают, в то время как водный слой подкисляют конц. (32%) соляной кислотой до рН 2 (прибл. 2,0 об.ч.). Начинает выпадать осадок. Суспензию обрабатывают AcOEt (8 об.ч.) и энергично перемешивают до тех пор, пока весь осадок не растворится. Водную фазу еще дважды экстрагируют AcOEt (каждый раз по 6 об.) и объединенные органические слои подвергают перегонке до небольшого объема (в маленьком объеме снова видят суспензию). Добавляют свежую порцию AcOEt (8 об.ч.) и смесь упаривают досуха. Собранное твердое вещество помещают в печь при 40°С на ночь при уменьшенном давлении и получают 4-метил-1,3-оксазол-5-карбоновую кислоту (498 г, 64,5%).
Полученное вещество (498 г, 1 мас.ч.) растворяют в сухом тетрагидрофуране (5 об.ч.) в атмосфере азота при охлаждении до 0°С. Добавляют порциями DCC (1,62 мас.ч., 1 экв.), а затем HOBt (1,07 мас.ч., 1 экв.). Смесь нагревают до 25±2°С и перемешивают в течение 30 мин. Затем добавляют 4-метил-3-тиосемикарбазид (0,83 мас.ч., 1 экв.) и смесь перемешивают еще в течение 2 час при 25±2°С. Смесь фильтруют и остаток на фильтре промывают свежей порцией тетрагидрофурана (1 об.ч.) и сушат на фильтре в течение нескольких часов. Остаток на фильтре суспендируют в 1 М водном растворе NaOH (13 об.ч.) и греют при 70°С в течение 30 мин. По окончании указанного времени смесь охлаждают до 25±2°С и твердое вещество удаляют фильтрацией. Остаток на фильтре промывают 1 М водным раствором NaOH (10 об.ч.). Объединенные маточные растворы охлаждают до 0°С и подкисляют до прибл. рН 5 HCl (водный раствор; 16%; примечание: во время добавления HCl поддерживают температуру ниже +10°С). Суспендировнный продукт реакции извлекают фильтрацией и промывают водой (2×3 об.ч.). Остаток на фильтре сушат при 40°С в течение 18 час в высоком вакууме и получают 4-метил-5-(4-метил-1,3-оксазол-5-ил)-2,4-дигидро-3Н-1,2,4-триазол-3-тион (в его соответствующей таутомерной форме; 290 г, 37%).
В атмосфере азота NaOEt (21% раствор в EtOH, 2,08 об.ч., 1,1 экв.) добавляют к EtOH (20 об.ч.). Добавляют в один прием 4-метил-5-(4-метил-1,3-оксазол-5-ил)-2,4-дигидро-3Н-1,2,4-триазол-3-тион (в его соответствующей таутомерной форме; 290 г, 1 мас.ч.) и полученную смесь перемешивают при 25±2°С до тех пор, пока не получат прозрачный раствор. Затем добавляют 1-бром-3-хлорпропан (0,54 об.ч., 1,1 экв.) и раствор перемешивают при 40°С в течение 24 час и затем охлаждают до 25°С. После фильтрации добавляют воду (20 об.ч.) и этанольную фазу удаляют перегонкой в вакууме (внутренняя температура ~40°C). Смесь экстрагируют EtOAc (41 об.ч.). Водный слой удаляют, а органическую фазу упаривают досуха. Добавляют дихлорметан (4 об.ч.). Органический раствор очищают на короткой колонке с силикагелем (18 мас.ч. диоксида кремния) с элюированием EtOAc (200 об.ч.) и получают названное в заголовке соединение в виде твердого пенообразного вещества (267,64 г, 66%).
ЯМР (1H, CDCl3): δ 7,90 (с, 1H), 3,70 (с, 5H), 3,40 (т, 2H), 2,52 (с, 3H), 2,30 (м, 2H).
Препаративный пример 15. 3-[4-(Трифторметил)фенил]-1Н-пиррол-2,5-дион

При комнатной температуре при энергичном перемешивании смесь соляной кислоты (37%, 285 мл) и воды (190 мл) добавляют к 4-(трифторметил)анилину (150 г, 116 мл) и образовавшийся осадок перемешивают еще в течение 30 минут. Температуру понижают до 0°С и к суспензии при перемешивании добавляют по каплям раствор нитрита натрия (70,6 г) в 180 мл воды. По окончании диазотирования получают прозрачный желтый раствор. При 0°С добавляют по каплям раствор малеимида (180 г) в ацетоне (1,1 л) и затем рН раствора доводят до 3-3,5, добавляя ацетат натрия. К смеси при энергичном перемешивании добавляют хлорид меди(II) (18,8 г). Через несколько минут начинает выделяться газ (видимое пенообразование). Реакционную смесь перемешивают при 0°С в течение 1 часа и в течение ночи при комнатной температуре.
Ацетон удаляют в вакууме, остаток отфильтровывают и сушат в течение ночи в вакууме и получают названное в заголовке соединение (155 г) в виде светло-коричневого твердого вещества (выход = 63%).
МС (m/z): 242,2 [MH]+.
Препаративный пример 16. (1R,5S/1S,5R)-1-[4-(Трифторметил)фенил]-3-азабицикло[3.1.0]гексан-2,4-дион

К раствору иодида триметилсульфоксония (219 г) в ДМСО (безводный, 2 л) при перемешивании небольшими порциями добавляют измельченный гидроксид натрия (40 г). Полученную смесь перемешивают при комнатной температуре в течение 1,5 час.
Затем добавляют по каплям раствор 3-[4-(трифторметил)фенил]-1Н-пиррол-2,5-диона (препаративный пример 15, 120 г) в ДМСО (безводный, 0,5 л) и полученную смесь перемешивают при комнатной температуре в течение 20 минут. Затем понижают температуру до 0°С и постепенно добавляют NH4Cl (насыщенный водный раствор, 2 л), а затем Et2O (1 л). После разделения двух фаз водный слой повторно экстрагируют Et2O (3×1 л). Объединенные органические слои промывают рассолом (2×1 л) и затем сушат над Na2SO4. Выпаривание растворителя дает светло-коричневое твердое вещество, которое суспендируют в 1 л дихлорметана и 1 л циклогексана. Смесь перемешивают при комнатной температуре в течение 45 минут и затем фильтруют и получают названное в заголовке соединение (116 г) в виде белого твердого вещества (выход = 71%).
МС (m/z): 256,1 [MH]+.
Препаративный пример 17. (1R,5S/1S,5R)-1-[4-(Трифторметил)фенил]-3-азабицикло[3.1.0]гексан

Боран (1 М раствор в тетрагидрофуране, 1,4 л) загружают в 5-л реактор в атмосфере азота и охлаждают до 0°С. Затем при энергичном перемешивании добавляют по каплям раствор (1R,5S/1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан-2,4-диона (препаративный пример 16, 101 г) в тетрагидрофуране (безводный, 1 л), при этом постоянно поддерживая температуру ниже 5°С, и контролируют выделение газа. По окончании добавления полученную смесь перемешивают при 0°С в течение 1 часа и затем при комнатной температуре в течение ночи.
Затем смесь охлаждают до 0°С и добавляют метанол (200 мл), а затем осторожно соляную кислоту (6 М раствор, 0,8 л), контролируя выделение газа. Затем тетрагидрофуран удаляют в вакууме, остаток охлаждают до 0°С и добавляют гидроксид натрия (5 М раствор) до достижения рН 9-10. Водный слой экстрагируют Et2O (3×1 л). Удаление растворителя в вакууме дает названное в заголовке соединение (140 г) в виде белого бесцветного масла.
МС (m/z): 228,1 [MH]+.
Препаративный пример 18. (1S,5R)-1-[4-(Трифторметил)фенил]-3-азабицикло[3.1.0]гексан

К раствору (1R,5S/1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (препаративный пример 17, 140 г) в 1,4 л тетрагидрофурана при перемешивании добавляют по частям (S)-(+)-миндальную кислоту (94 г). Полученную смесь перемешивают при комнатной температуре в течение 2 час до образования белого осадка. Затем смесь нагревают до температуры образования флегмы, перемешивают в течение 45 минут и затем медленно охлаждают до комнатной температуры. Белое твердое вещество собирают фильтрацией и сушат в вакууме. Вещество перекристаллизовывают 4 раза из тетрагидрофурана (10 объемов) и получают 32,5 г белого твердого вещества. Затем полученное вещество суспендируют в растворе гидроксида натрия (1 М, 400 мл) и Et2O (400 мл) и все перемешивают при комнатной температуре до полного растворения. После разделения двух фаз водный слой снова экстрагируют Et2O (3 × 250 мл). Объединенные органические слои промывают раствором гидроксида натрия (1 М, 3 × 200 мл) и затем сушат над Na2SO4. Выпаривание растворителя в вакууме дает названное в заголовке соединение (19 г) в виде белого твердого вещества (выход = 37%).
Абсолютную конфигурацию оптических изомеров устанавливают с использованием сравнительных анализов VCD (колебательный круговой дихроизм) и OR (оптическое вращение).
Конфигурацию названного в заголовке соединения устанавливают, сравнивая экспериментальный спектр VCD и наблюдаемое удельное вращение с данными, полученными для (1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексана (см. препаративный пример 48) как ссылочного образца. Установление абсолютной конфигурации названного в заголовке соединения подтверждают рентгеновской структурой монокристалла, полученной для кристалла соли (S)-(+)-миндальной кислоты (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана. Оба анализа на основе известной конфигурации (S)-(+)-миндальной кислоты и на основе явления аномальной дисперсии подтверждают определение названного в заголовке соединения как представляющего собой (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан.
ЯМР (1H, CDCl3): δ 7,51 (д, 2H), 7,25 (д, 2H), 3,20 (д, 1H), 3,0-3,1 (м, 3H), 1,69 (м, 1H), 0,8-1,0 (м, 2H), NH не наблюдают. МС (m/z): 228,1 [MH]+.
Аналитическая хроматография
Колонка: chiralcel OD 10 мкм, 250 × 4,6 мм;
подвижная фаза: А - н-гексан; В - изопропанол + 0,1% изопропиламина;
градиент: изократный 2% В;
скорость потока 1 мл/мин;
интервал длин волн УФ 200-400 нм;
время анализа 25 мин;
Удельное оптическое вращение [α]D = -10° (CDCI3, T=20°C, C = 0,004 г/0,8 мл).
Препаративный пример 19. 3-{(1S,5R)-1-[4-(Трифторметил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}-1-бутанол
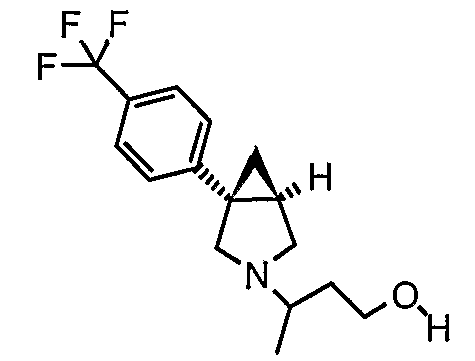
К суспензии (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (препаративный пример 18, 100 мг) в тетрагидрофуране (1,1 мл) добавляют 4-гидрокси-2-бутанон (0,66 ммоль), уксусную кислоту (0,66 ммоль) и NaBH(OAc)3 (0,88 ммоль). Смесь перемешивают при комнатной температуре в течение 2 час. После добавления NaOH (1 М) растворитель удаляют в вакууме, остаток растворяют в этилацетате и органический слой промывают Н2О и сушат над Na2SO4. Раствор концентрируют в вакууме и получают 130 мг названного в заголовке соединения, которое используют без дополнительной очистки.
МС (m/z): 300 [MH]+.
Препаративный пример 20. (1S,5R)-3-(3-Хлор-1-метилпропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан

К раствору 3-{(1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}-1-бутанола (препаративный пример 19, 130 мг) в хлороформе (4 мл) добавляют тионилхлорид (0,87 ммоль) и смесь перемешивают при комнатной температуре в течение 6 час. После добавления NaOH (1 М) добавляют дихлорметан и органический слой промывают рассолом и сушат над Na2SO4. Раствор концентрируют в вакууме, сырой продукт реакции очищают флэш-хроматографией (этилацетат:циклогексан = 5:95) и получают 106 мг названного в заголовке соединения.
МС (m/z): 318 [MH]+.
Препаративный пример 21. 1-{5-[(1S,5R/1R,5S)-3-Азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил}этанон

Названное в заголовке соединение получают с выходом 32 мг из 1-[4-(метилокси)фенил]-3-(трифторацетил)-3-азабицикло[3.1.0]гексана (94 мг) так, как описано в препаративном примере 34.
МС (m/z): 232 [MH]+. ВЭЖХ: условие 1, Rt = 3,393 мин.
Препаративный пример 22. (1S,5R/1R,5S)-1-(4-Хлорфенил)-3-азабицикло[3.1.0]гексан
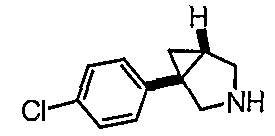
Названное в заголовке соединение получают с выходом 230 мг из коммерчески доступного метил-4-хлорфенилацетата (1 г, 5,5 ммоль), следуя способам, описанным в препаративных примерах 1, 2, 3, 4, 6.
МС (m/z): 194 [MH]+.
Препаративный пример 23. (1S,5R/1R,5S)-1-(4-Фторфенил)-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 160 мг из коммерчески доступного метил-4-фторфенилацетата (1 г, 6 ммоль), следуя способам, описанным в препаративных примерах 1, 2, 3, 4, 6.
МС (m/z): 178 [MH]+.
Препаративный пример 24. (1S,5R/1R,5S)-1-(3-Хлорфенил)-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 1,25 г из коммерчески доступного метил-3-хлорфенилацетата (5 г, 27 ммоль), следуя способам, описанным в препаративных примерах 1, 2, 3, 4, 5.
МС (m/z): 194 [MH]+. ВЭЖХ: условие 1, Rt = 3,469 мин.
Препаративный пример 25. (1S,5R/1R,5S)-1-(3-Фторфенил)-3-азабицикло[3.1.0]гексан
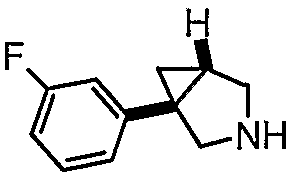
Названное в заголовке соединение получают с выходом 1,97 г из коммерчески доступного метил-3-фторфенилацетата (5 г, 29,7 ммоль), следуя способам, описанным в препаративных примерах 1, 2, 3, 4, 5.
МС (m/z): 178 [MH]+.
Препаративный пример 26. (1S,5R/1R,5S)-1-[3-(Метилокси)фенил]-3-азабицикло[3.1.0]гексан
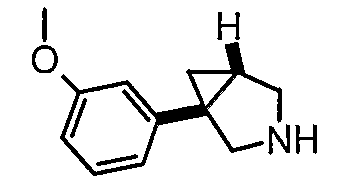
Названное в заголовке соединение получают с выходом 1,2 г из коммерчески доступного метил-3-метоксифенилацетата (5 г, 27,7 ммоль), следуя способам, описанным в препаративных примерах 1, 2, 3, 4, 5.
МС (m/z): 190 [MH]+. ВЭЖХ: условие 1, Rt = 3,219 мин.
Препаративный пример 27. (1S,5R/1R,5S)-1-[2-Метил-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 71 мг из коммерчески доступного 2-метил-4-(трифторметил)анилина (1 г, 5,7 ммоль), следуя способам, описанным в препаративных примерах 15, 16, 17.
МС (m/z): 242 [MH]+.
Препаративный пример 28. Метилбром{4-[(трифторметил)окси]фенил}ацетат
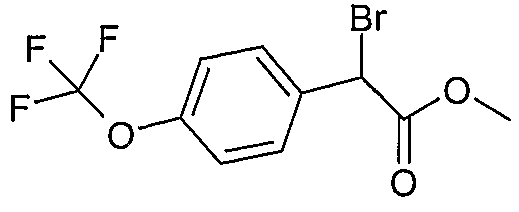
К раствору 4-трифторметоксифенилуксусной кислоты (5 г, 23 ммоль) в четыреххлористом углероде при 0°С добавляют оксалилхлорид (25 ммоль) и две капли ДМФА. После перемешивания раствора при комнатной температуре в течение 1 часа добавляют NBS (25 ммоль) и несколько капель 48% HBr и смесь кипятят с обратным холодильником в течение 4 час. Раствор охлаждают, добавляют МеОН (5 мл) и смесь перемешивают при комнатной температуре в течение 1 часа. После фильтрации через слой силикагеля фильтрат упаривают в вакууме и получают 7,2 г названного в заголовке соединения в виде желтой пены, которое используют на следующей стадии без дополнительной очистки.
МС (m/z): 314 [MH]+.
Препаративный пример 29. (1S,5R/1R,5S)-1-{4-[(Трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 1,2 г из метил-3-трифторметоксифенилацетата (препаративный пример М, 23 ммоль), следуя способам, описанным в препаративных примерах 2, 3, 4, 5.
МС (m/z): 244 [MH]+. ВЭЖХ: условие 1, Rt = 3,942 мин.
Препаративный пример 30. (1S,5R/1R,5S)-1-[3-(Трифторметил)фенил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 1,5 г из коммерчески доступной 3-трифторметилфенилуксусной кислоты (5 г, 24,5 ммоль), следуя способам, описанным в препаративных примерах 28, 2, 3, 4, 5.
МС (m/z): 228 [MH]+. ВЭЖХ: условие 1, Rt = 3,665 мин.
Препаративный пример 31. (1S,5R/1R,5S)-1-(3-Бромфенил)-3-азабицикло[3.1.0]гексан
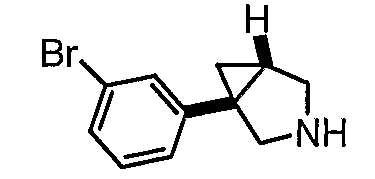
Названное в заголовке соединение получают с выходом 1,6 г из коммерчески доступной 3-бромфенилуксусной кислоты (5 г, 23,2 ммоль), следуя способам, описанным в препаративных примерах 28, 2, 3, 4, 6.
МС (m/z): 239 [MH]+. ВЭЖХ: условие 1, Rt = 3,528 мин.
Препаративный пример 32. (1S,5R)1-(4-Бромфенил)-3-азабицикло[3.1.0]гексан

К раствору (1R,5S/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексана (препаративный пример 6, 3,96 г) в 80 мл IPA добавляют по частям (S)-(+)-ацетилминдальную кислоту (3,22 г). Полученную смесь перемешивают при комнатной температуре в течение 2 час, пока не образуется белый осадок. Затем смесь нагревают до температуры образования флегмы, перемешивают в течение 45 минут и затем медленно охлаждают до комнатной температуры. Белое твердое вещество собирают фильтрацией и сушат в вакууме. Полученное вещество перекристаллизовывают 4 раза из IPA (10 объемов), и получают 2,3 г белого твердого вещества.
Затем полученное вещество суспендируют в растворе гидроксида натрия (1 М, 400 мл) и Et2O (400 мл), и все перемешивают при комнатной температуре до полного растворения. После разделения двух фаз водный слой снова экстрагируют Et2O (3 × 250 мл). Объединенные органические слои промывают раствором гидроксида натрия (1 М, 3 × 200 мл) и затем сушат над Na2SO4. Выпаривание растворителя в вакууме дает названное в заголовке соединение (1,24 г) в виде белого твердого вещества.
Абсолютную конфигурацию оптических изомеров устанавливают так, как описано в препаративном примере 18.
Установление абсолютной конфигурации названного в заголовке соединения подтверждают рентгеновской структурой монокристалла, полученной для кристалла соли (S)-(+)-О-ацетилминдальной кислоты (1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексана. Оба анализа на основе известной конфигурации (S)-(+)-ацетилминдальной кислоты и на основе явления аномальной дисперсии подтверждают определение названного в заголовке соединения как представляющего собой (1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексан.
ЯМР (1H, CDCl3): δ 7,43 (д, 2H), 7,09 (д, 2H), 3,25 (д, 1H), 3,15 (м, 2H), 3,06 (д, 1H), 1,71 (м, 1H), 0,95 (дд, 1H), 0,89 (т, 1H), NH не наблюдают.
МС (m/z): 239 [MH]+.
Аналитическая хроматография
Колонка: chiralcel OD 5 мкм, 250 × 4,6 мм;
подвижная фаза: А - н-гексан; В - изопропанол + 0,1% изопропиламина;
градиент: изократный 2% В;
скорость потока 1 мл/мин;
интервал длин волн УФ 200-400 нм;
время анализа 25 мин;
время удерж. 22,3 мин, чистота >99% а/а;
удельное оптическое вращение [α]D = -86° (CDCl3, T = 20°C, c = 0,0053 г/0,8 мл).
Препаративный пример 33. (1R,5S/1S,5R)-1-[2-(Трифторметил)фенил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 53 мг из коммерчески доступного метил[2-(трифторметил)фенил]ацетата (944 мг), следуя способам, описанным в препаративных примерах 1, 2, 3, 4 и 5.
МС (m/z): 228 [MH]+.
Препаративный пример 34. 1-[4-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон

К смеси AlCl3 (2 экв.) и 1,2-дихлорэтана (безводный, 9 мл) при 0°С добавляют ацетилхлорид (1,05 экв.). Реакционную смесь перемешивают при 0°С в течение 15 мин, и добавляют раствор 1-[3-(метилокси)фенил]-3-(трифторацетил)-3-азабицикло[3.1.0]гексана (1,1 г, получен способом, аналогичным описанному в препаративном примере 7, из 1-[3-(метилокси)фенил]-3-азабицикло[3.1.0]гексана) в 1,2-дихлорэтане (безводный, 9 мл). Реакционную смесь перемешивают при RT в течение 1,5 час. Добавляют HCl (1 М, 4 мл), а затем воду (20 мл) и смесь экстрагируют дихлорметаном. Органический слой промывают насыщенным водным раствором NaHCO3 и сушат над Na2SO4. Раствор фильтруют и фильтрат концентрируют в вакууме. Сырой продукт реакции очищают флэш-хроматографией (циклогексан:EtOAc, 6:4) и получают 593 мг содержащего защитную группу амина в виде бесцветной жидкости. Растворяют 143 мг содержащего защитную группу амина в смеси МеОН:Н2О (3 мл : 3 мл) и добавляют К2СО3 (4 экв.), перемешивая смесь при 50°С в течение 2,5 час. Реакционную смесь экстрагируют дихлорметаном и органический слой промывают насыщенным водным раствором NaHCO3 и сушат над Na2SO4. Раствор фильтруют, фильтрат концентрируют в вакууме и получают названное в заголовке соединение в виде белого твердого вещества (88 мг).
МС (m/z): 232 [MH]+.
ВЭЖХ: условия 1
Аналитическая ВЭЖХ
Колонка: Supelcosil ABZ+Plus, 33 × 4,6 мм, 3 мкм;
подвижная фаза: А - Н2О + 0,1% НСООН, В - CH3CN;
градиент: 0% (В) в течение 1 мин, от 0% (В) до 95% (В) за 5 мин, 95% (В) в течение 2 мин;
скорость потока 1 мл/мин;
длина волны УФ 285 нм, ширина полосы 130 нм;
массовый интервал 100-1000 amu;
ионизация ES+;
Rt 2,971 мин.
Препаративный пример 35. 1-[4-[(1R,5S/1S,5R)-3-Азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон
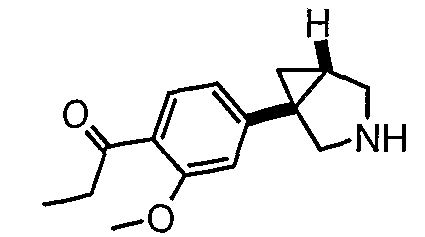
Названное в заголовке соединение получают с использованием пропионилхлорида вместо ацетилхлорида с выходом 106 мг из 147 мг амина с защитной группой, полученного (в 705 мг) из 1-[3-(метилокси)фенил]-3-(трифторацетил)-3-азабицикло[3.1.0]гексана (1,07 г), как описано в препаративном примере 34.
МС (m/z): 246 [MH]+.
ВЭЖХ, условия 1.
Rt 3,249 мин.
Препаративный пример 36. 1(1R,5S/1S,5R)-[2-Фтор-5-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 112 мг из 2-фтор-5-(трифторметил)анилина (1,09 г), следуя процедурам, описанным в препаративных примерах 37 и 6.
ЯМР (1H, CDCl3): δ 7,45 (м, 2H), 7,1 (м, 1H), 3,2 (м, 2H), 3,05 (м, 2H), 1,7 (м, 1H), 0,95 (м, 1H), 0,9 (м, 1H), NH не наблюдают. МС (м/z): 246[MH]+.
Препаративный пример 37. 1(1R,5S/1S,5R)-[2-Фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан-2,4-дион

К взвеси малеимида (1,7 экв.), безводного CuCl2 (1,2 экв.) и трет-бутилнитрита (1,5 экв.) в CH3CN (35 мл) при 0°С добавляют по каплям раствор 2-фтор-4-(трифторметил)анилина (16,3 г) в CH3CN (6,5 мл). Реакционную смесь перемешивают при комнатной температуре в течение 1 часа и добавляют HCl (10% водная, 196 мл). Смесь экстрагируют EtOAc, органический слой промывают насыщенным водным раствором NaCl и сушат над Na2SO4. Раствор фильтруют и фильтрат концентрируют в вакууме. Анализ методом ЯМР сырой смеси показывает смесь 1:4 аддукта гидрохлорида арилированного малеимида (компонент А) и непрореагировавшего малеимида (компонент В).
Раствор этого сырого продукта реакции в ДМСО (140 мл) добавляют по каплям к предварительно полученному раствору иодида триметилсульфоксония (2 экв. относительно компонента А с добавлением 2 экв. относительно компонента В) в безводном ДМСО (412 мл), к которому добавлен по частям NaH (3 экв. относительно компонента А с добавлением 2 экв. относительно компонента В). Реакционную смесь перемешивают в течение 30 мин и добавляют АсОН (2 экв.), а затем воду. Реакционную смесь экстрагируют Et2O и затем EtOAc, объединенные органические слои промывают насыщенным водным раствором NaCl и сушат над Na2SO4. Раствор фильтруют и фильтрат концентрируют в вакууме. Полученный сырой продукт реакции обрабатывают водой и затем циклогексаном и получают названное в заголовке соединение в виде светло-коричневого твердого вещества (5,98 г).
ЯМР (1H, CDCl3): δ 7,55-7,3 (м, 3H), 2,8-2,7 (м, 1H), 2,1 (м, 1H), 2,0 (м, 1H), NH не наблюдают. МС (m/z): 274[MH]+.
Препаративный пример 38. (1R,5S/1S,5R)-1-[2-Фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан

К раствору (1R,5S/1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан-2,4-она (2,6 г) в безводном тетрагидрофуране (56 мл) при 0°С добавляют ВН3 в тетрагидрофуране (1 М, 4 экв.). Реакционную смесь перемешивают при 65°С в течение 24 час, охлаждают до RT и добавляют МеОН до тех пор, пока не прекратится выделение газа. Растворитель удаляют в вакууме, добавляют МеОН (200 мл), добавляют п-толуолсульфоновую кислоту (3 экв.), реакционную смесь перемешивают при 65°С в течение 6 час, охлаждают до комнатной температуры и добавляют насыщенный раствор К2СО3 (1,7 экв.). Смесь экстрагируют дихлорметаном, органический слой промывают насыщенным водным раствором NaCl и сушат над Na2SO4. Раствор фильтруют, фильтрат концентрируют в вакууме и получают названное в заголовке соединение в виде бесцветного масла (2,1 г).
ЯМР (1H, CDCl3): δ 7,2-7,4 (м, 3H), 3,2 (м, 2H), 3,1 (м, 2H), 1,8 (м, 1H), 0,8 (м, 2H), NH не наблюдают. МС (m/z): 246[MH]+.
Препаративный пример 39. (1S,5R)-1-[2-Фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан
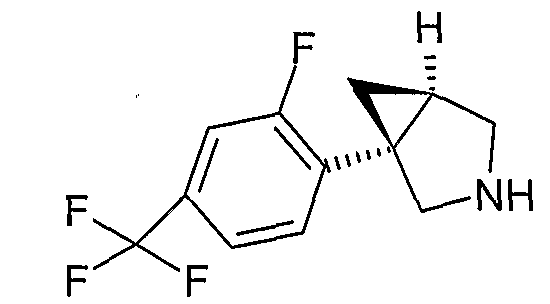
К раствору (1R,5S/1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (4,4 г) в CH3CN (44 мл) при перемешивании добавляют по частям (1R)-(-)-10-камфорсульфоновую кислоту (4,19 г). Полученную смесь перемешивают при комнатной температуре в течение 20 мин до образования белого осадка. Затем смесь нагревают до температуры образования флегмы, перемешивают в течение 45 минут и затем медленно охлаждают до комнатной температуры. Белое твердое вещество собирают фильтрацией и сушат в вакууме. Полученное вещество 2 раза перекристаллизовывают из CH3CN (25 мл на г твердого вещества) и получают 1,57 г белого твердого вещества.
Затем это вещество суспендируют в растворе гидроксида натрия (1 М, 1,1 экв.) и дихлорметане (100 мл) и перемешивают при комнатной температуре до полного растворения. После разделения двух фаз водный слой снова экстрагируют дихлорметаном. Объединенные органические слои промывают раствором гидроксида натрия и затем сушат над Na2SO4. Выпаривание растворителя в вакууме дает названное в заголовке соединение (874 мг) в виде бесцветной жидкости.
Аналитическая хроматография
Колонка: chiralcel OD 10 мкм, 250 × 4,6 мм;
подвижная фаза: А - н-гексан; В - изопропанол + 0,1% изопропиламина;
градиент: изократный 2% В;
скорость потока 0,8 мл/мин;
интервал длин волн УФ 200-400 нм.
Анализ
Препаративный пример 40. (1S,5R)-3-(3-Хлорпропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан
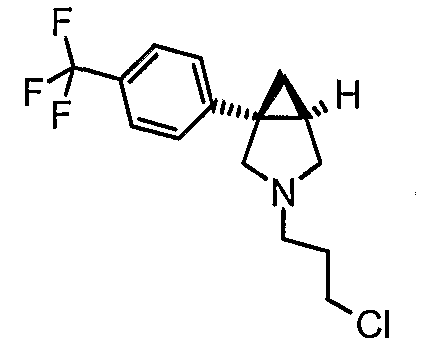
К раствору (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (1,00 г) в сухом тетрагидрофуране (5 мл) добавляют диизопропилэтиламин (2,4 мл) и 1-бром-3-хлорпропан (3,7 мл) и полученную смесь кипятят с обратным холодильником в течение 3 часов. После охлаждения до комнатной температуры смесь разбавляют этилацетатом (30 мл), дважды промывают насыщенным водным раствором NH4Cl (20 мл) и один раз насыщенным водным раствором NaHCO3 (20 мл), сушат над безводным Na2SO4 и концентрируют при пониженном давлении. Сырой продукт реакции очищают хроматографией на силикагеле с элюированием смесью циклогексан/EtOAc, 7:3 и получают названное в заголовке соединение в виде бесцветного масла (1,26 г).
ЯМР (1H, CDCl3): δ 7,50 (д, 2H), 7,19 (д, 2H), 3,59 (т, 2H), 3,33 (д, 1H), 3,09 (д, 1H), 2,58 (м, 2H), 2,66 (дд, 1H), 2,46 (дд, 1H), 1,92 (м, 2H), 1,74 (м, 1H), 1,67 (т, 1H), 0,81 (дд, 1H). МС (m/z): 304 [MH]+.
Препаративный пример 41. (1S,5R)-3-(3-Хлорпропил)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан
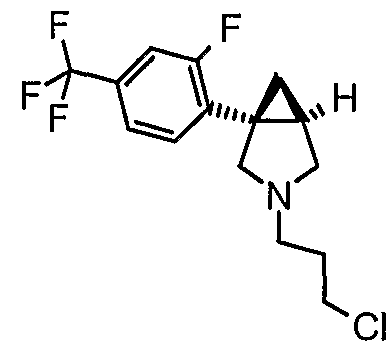
К раствору (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (300 мг) в сухом тетрагидрофуране (3 мл) добавляют диизопропилэтиламин (0,65 мл) и 1-бром-3-хлорпропан (1,01 мл) и полученную смесь кипятят с обратным холодильником в течение 3 часов. После охлаждения до комнатной температуры смесь разбавляют этилацетатом (15 мл), дважды промывают насыщенным водным раствором NH4Cl (10 мл) и один раз насыщенным водным раствором NaHCO3 (10 мл), сушат над безводным Na2SO4 и концентрируют при пониженном давлении. Сырой продукт реакции очищают хроматографией (силикагель) с элюированием смесью циклогексан/EtOAc, 6:4 и получают названное в заголовке соединение в виде желтого масла (345 мг).
ЯМР (1H, CDCl3): δ 7,24 (д, 2H), 7,16 (т, 1H), 3,51 (т, 2H), 3,18 (дд, 1H), 3,03 (д, 1H), 2,54 (т, 2H), 2,48 (дд, 1H), 2,37 (д, 1H), 1,83 (м, 2H), 1,69 (м, 1H), 1,34 (т, 1H), 0,70 (дд, 1H). МС (m/z): 322 [MH]+.
Препаративный пример 42. (1R,5S/1S,5R)-1-[3-Фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 338 мг из 3-фтор-4-(тритформетил)анилина (2 г), следуя процедурам, описанным для препаративных примеров 37 и 6.
ЯМР (1H, CDCl3): δ 7,5 (м, 1H), 6,9 (м, 2H), 3,3-3,0 (м, 4H), 1,7 (м, 1H), 0,95 (м, 2H), NH не наблюдают. МС (m/z): 246 [MH]+.
Препаративный пример 43. (1R,5S/1S,5R)-1-[4-(Метилокси)фенил]-3-(трифторацетил)-3-азабицикло[3.1.0]гексан
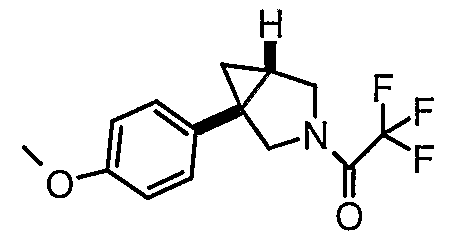
Названное в заголовке соединение получают в виде бесцветного масла с выходом 1,80 г (95%) из (1R,5S/1S,5R)-1-[4-(метокси)фенил]-3-азабицикло[3.1.0]гексана (1,25 г) способом, аналогичным описанному в препаративном примере 7.
МС (m/z): 286 [MH]+.
Препаративный пример 44. 1-{2-(Метилокси)-5-[(1R,5S/1S,5R)-3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон и 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон
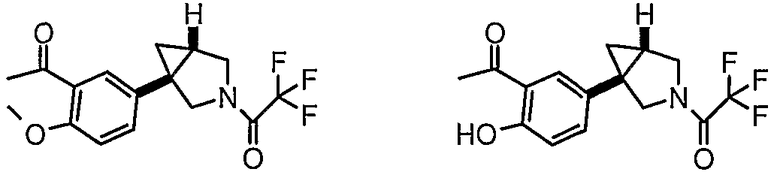
К суспензии AlCl3 (12,6 ммоль) в сухом 1,2-дихлорэтане (16 мл) при 0°С добавляют ацетилхлорид (6,6 ммоль) и смесь перемешивают при указанной температуре в течение 15 мин. Затем добавляют раствор (1R,5S/1S,5R)-1-[4-(метилокси)фенил]-3-(трифторацетил)-3-азабицикло[3.1.0]гексана (1,81 г, 6,3 ммоль) в 1,2-дихлорэтане (16 мл). Реакционную смесь перемешивают при 0°С в течение 15 мин и в течение ночи при комнатной температуре. Затем добавляют 1 М соляную кислоту и смесь экстрагируют дихлорметаном. Органическую фазу промывают 5% раствором NaHCO3 и водой, сушат над Na2SO4 и концентрируют в вакууме. Два продукта реакции разделяют флэш-хроматографией (циклогексан/этилацетат от 95/5 до 80/29) и получают 965 мг 1-{2-(метилокси)-5-[(1R,5S/1S,5R)-3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанона (48%) и 266 мг 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанона (18%) в виде желтых масел.
МС (m/z): 328 [MH]+, 1-{2-(метилокси)-5-[(1R,5S/1S,5R)-3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон; 312 [M-H]-, 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон.
Препаративный пример 45. 1-[5-[(1R,5S/1S,5R)-3-Азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон

Названное в заголовке соединение получают в виде бесцветного масла с выходом 624 мг (91%) из 1-{2-(метилокси)-5-[(1R,5S/1S,5R)-3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанона (965 мг) способом, аналогичным описанному в препаративном примере 12.
МС (m/z): 232 [MH]+.
Препаративный пример 46. 1-{5-[(1R,5S/1S,5R)-3-Азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанон
 .
.
Названное в заголовке соединение получают в виде бесцветного масла с выходом 151 мг (82%) из 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(трифторацетил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанона (266 мг) способом, аналогичным описанному в препаративном примере 12.
МС (m/z): 216 [MH]+.
Препаративный пример 47. (1S,5R/1R,5S)-1-(4-Бромфенил)-3-(3-хлорпропил)-3-азабицикло[3.1.0]гексан
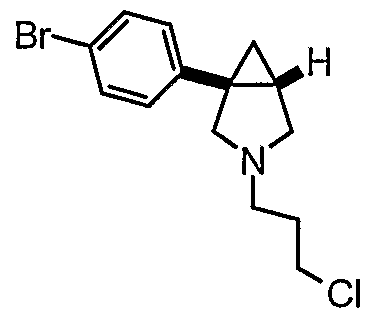
К раствору рацемического (1S,5R/1R,5S)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексана (0,12 г) в сухом тетрагидрофуране (2 мл) добавляют диизопропилэтиламин (0,22 мл) и 1-бром-3-хлорпропан (0,062 мл) и полученную смесь кипятят с обратным холодильником в течение 3 часов. После охлаждения до комнатной температуры растворитель удаляют в вакууме и полученное сырое масло растворяют в дихлорметане (10 мл). Затем полученный раствор дважды промывают насыщенным водным раствором NH4Cl (5 мл), сушат над безводным Na2SO4 и концентрируют при пониженном давлении. Сырой продукт реакции очищают, пропуская образец через картридж с 2 г диоксида кремния (Varian) с элюированием с градиентом от циклогексана к смеси циклогексан/EtOAc, 7:3, и получают названное в заголовке соединение в виде бесцветного масла (0,10 г).
ЯМР (1H, ДМСО): δ 7,45 (д, 2H), 7,10 (д, 2H), 3,65 (т, 2H), 3,30 (д, 1H), 3,00 (д, 1H), 2,55 (т, 2H), 2,45 (м, 1H), 2,40 (дд, 1H), 1,85 (м, 2H), 1,80 (м, 1H), 1,30 (т, 1H), 0,70 (м, 1H). МС (m/z): 314, 316, 318 [MH]+.
Препаративный пример 48. (1R,5S/1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексан

Сырое названное в заголовке соединение получают с выходом 0,36 г из коммерчески доступного 3,4-дихлорфенилацетата (1 г, 4,57 ммоль), следуя способам, описанным в препаративных примерах 1, 2, 3, 4, 6.
Названное в заголовке соединение разделяют и получают отдельные энантиомеры препаративной хроматографией с использованием хиральной колонки с chiralcel AD, 10 мкм, 250 × 21 мм, элюент А - н-гексан; В - изопропанол + 0,1% изопропиламина; градиент изократный 2% В, скорость потока 7 мл/мин; УФ-детекция при 200-400 нм. Приведенные времена удерживания получают с использованием аналитической ВЭЖХ с использованием хиральной колонки с chiralcel AD, 5 мкм, 250 × 4,6 мм, элюент А - н-гексан; В - изопропанол + 0,1% изопропиламина; градиент изократный 2% В, скорость потока 1,2 мл/мин, УФ-детекция при 200-400 нм.
Энантиомер 1 - (1R,5S)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексан извлекают из рацемата (60 мг) с выходом 20 мг в виде белого твердого вещества. Rt = 41 мин.
Энантиомер 2 - (1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексан извлекают из рацемата (60 мг) с выходом 28 мг в виде белого твердого вещества. Rt = 43,4 мин.
Абсолютную конфигурацию (1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексана устанавливают с использованием анализов ab initio VCD и ab initio OR.
Удельное оптическое вращение (1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексана [α]D = -67,9° (CDCl3, T = 20°C, c ≈ 0,01 г/мл).
ЯМР (1H, CDCl3): δ 7,35 (д, 1H), 7,27 (с, 1H), 7,02 (дд, 1H), 3,25 (д, 1H), 3,13 (ушм, 2H), 3,06 (д, 1H), 1,71 (м, 1H), 0,93 (м, 2H), NH не наблюдают. МС (m/z): 228 [MH]+.
Препаративный пример 49. 1-(Фенилметил)-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2,5-дигидро-1Н-пиррол

Получают диизопинокамфеилборан, следуя процедуре, описанной в J. Org. Chem., 1984, 49, 945-947. 2-[(1Z)-3-Хлор-1-(хлорметил)-1-пропен-1-ил]-4,4,5,5-тетраметил-1,3,2-диоксаборолан (описанный ранее в Tetrahedron Lett., 1993, 34, 4827-4828) получают, следуя общей процедуре, описанной в Tetrahedron Lett., 1989, 30, 2929, с использованием 1,4-дихлор-2-бутина. Затем осуществляют дальнейшее превращение полученного таким образом вещества, следуя процедуре, описанной в Synlett, 2002, 5, 829-831. Последнюю указанную процедуру модифицируют в том отношении, что выделение названного в заголовке продукта реакции достигают экстрагированием (не перегонкой) раствора сырых продуктов реакции ацетонитрилом с циклогексаном и получают названное в заголовке соединение (содержащее ~10 мол.% бензиламина) после выпаривания летучих веществ из циклогексановой фазы.
Препаративный пример 50. 2-[1-(Фенилметил)-2,5-дигидро-1Н-пиррол-3-ил]-5-(трифторметил)пиридин

К раствору 2-бром-5-(трифторметил)пиридина (4,42 ммоль) в сухом тетрагидрофуране (45 мл) при комнатной температуре добавляют 1-(фенилметил)-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2,5-дигидро-1Н-пиррол (3,4 ммоль), тетракис(трифенилфосфин)палладий(0) (0,196 ммоль) и фторид цезия (13,2 ммоль). Полученную смесь перемешивают при 80°С в течение 1,5 часов. После охлаждения растворитель выпаривают при пониженном давлении и остаток обрабатывают дихлорметаном (25 мл) и раствором гидроксида натрия (15 мл, 1 М). Органическую фазу упаривают при пониженном давлении. Сырой продукт реакции очищают колоночной хроматографией на силикагеле (AcOEt:циклогексан = 1:10 - 4:6) и получают 0,33 г названного в заголовке соединения (выход = 24%).
ЯМР (1H, CDCl3): δ 9,8 (с, 1H), 7,85 (дд, 1H), 7,5-7,2 (м, 6H), 6,7 (с, 1H), 3,95 (м, 2H), 3,9 (с, 2H), 3,75 (м, 2H). МС (m/z): 305 [MH]+.
Препаративный пример 51. 2-[1-(Фенилметил)-2,5-дигидро-1Н-пиррол-3-ил]-6-(трифторметил)пиридин

2-[1-(Фенилметил)-2,5-дигидро-1Н-пиррол-3-ил]-6-(трифторметил)пиридин получают способом, аналогичным описанному в препаративном примере 50, в количестве 0,56 г (выход = 42%) в виде масла.
ЯМР (1H, CDCl3): δ 7,7 (т, 1H), 7,85 (дд, 1H), 7,4-7,1 (м, 6H), 6,5 (с, 1H), 3,90 (суш, 2H), 3,8 (с, 2H), 3,6 (м, 2H). МС (m/z): 305 [MH]+.
Препаративный пример 52. 3-(Фенилметил)-1-[5-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан

К взвеси гидрида натрия (83 г) и иодида триметилсульфоксония (0,46 г) добавляют по каплям ДМСО (безводный, 3 мл) (выделение газа). Полученную смесь перемешивают при комнатной температуре в течение 0,5 часа. При комнатной температуре добавляют раствор 2-[1-(фенилметил)-2,5-дигидро-1Н-пиррол-3-ил]-5-(трифторметил)-2-пиридина (330 мг) в ДМСО (безводный, 6 мл). Через 1 час добавляют насыщенный раствор хлорида аммония (4 мл) и смесь экстрагируют дихлорметаном (2 × 10 мл). Из органической фазы при пониженном давлении выпаривают летучие вещества, остаток загружают в колонку с SCX и элюируют МеОН, а затем МеОН/NH3, 0,25 М. Фракции, элюированные раствором метанол/аммиак, концентрируют при пониженном давлении и получают 0,31 г названного в заголовке соединения (выход = 89%).
ЯМР (1H, CDCl3): δ 8,78 (с, 1H), 8,03 (дд, 1H), 7,32 (м, 5H), 7,25 (м, 1H), 3,66 (дд, 2H), 3,25 (д, 1H), 2,96 (д, 1H), 2,80 (д, 1H), 2,46 (суш, 1H), 2,05 (кв, 1 H), 1,58 (м, 1H), 1,22 (м, 1H). МС (m/z):317 [MH]+.
Препаративный пример 53. 3-(Фенилметил)-1-[6-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан

3-(Фенилметил)-1-[6-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан получают в виде масла способом, аналогичным описанному в препаративном примере 52 (0,46 г, 79%).
ЯМР (1H, CDCl3): δ 7,7 (т, 1H), 7,4 (д, 1H), 7,35 (м, 5H), 7,2 (д, 1H), 3,7 (с, 2H), 3,4 (д, 1H), 3,1 (д, 1H), 2,85 (д, 1H), 2,55 (м, 1H), 2,1 (м, 1H), 1,7 (м, 1H), 1,3 (м, 1H). МС (m/z): 317 [MH]+.
Препаративный пример 54. 1-[5-(Трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан

3-(Фенилметил)-1-[5-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан растворяют в этаноле (15 мл), добавляют соляную кислоту (3 М, 0,76 мл), а затем в инертной атмосфере 10%, мас./мас., Pd/C (120 мг). После 20 час пребывания в атмосфере водорода (1 атм) смесь фильтруют. Растворитель удаляют при пониженном давлении. Добавляют насыщенный раствор бикарбоната натрия (10 мл), смесь экстрагируют диэтиловым эфиром (2 × 10 мл) и после выпаривания летучих веществ получают названное в заголовке соединение (0,14 г, 81%).
ЯМР (1H, ДМСО-d6): δ 8,7 (с, 1H), 7,8 (д, 1H), 7,15 (д, 1H), 3,4-3,2 (дд, 2H), 3,1 (м, 2H), 2,05 (м, 1H), 1,4 (м, 1H), 1,05 (т, 1H).
Препаративный пример 55. 2-Фтор-4-[1-(фенилметил)-2,5-дигидро-1Н-пиррол-3-ил]бензонитрил

Названное в заголовке соединение получают способом, аналогичным описанному в препаративном примере 50, в количестве 0,44 г (выход = 31%) в виде масла.
ЯМР (1H, CDCl3): δ 7,55 (т, 1H), 7,4-7,2 (м, 5H), 7,2 (д, 1H), 7,1 (д, 1H), 6,4 (ушс, 1H), 3,9 (с, 2H), 3,8 (м, 2H), 3,75 (м, 2H), МС (m/z): 279 [MH]+.
Препаративный пример 56. 2-Фтор-4-[3-(фенилметил)-3-азабицикло[3.1.0]гекс-1-ил]бензонитрил

Названное в заголовке соединение получают способом, аналогичным описанному в препаративном примере 52, в количестве 0,39 г (выход = 84%) в виде масла.
ЯМР (1H, CDCl3): δ 7,41 (т,1H), 7,25-7,15 (м, 5H), 6,85-6,8 (дд, 2H), 3,64-3,56 (дд, 2H), 3,19 (дд, 1H), 3,01 (дд, 1H), 2,53 (дд, 1H), 2,47 (дд, 1H), 1,73 (кв, 1H), 1,67 (м, 1H), 0,81 (м, 1H). МС (m/z): 293 [MH]+.
Препаративный пример 57. 1-[3-Фтор-4-(1Н-пиррол-1-илметил)фенил]-3-азабицикло[3.1.0]гексан

К раствору дигидрохлорида {[4-(3-азабицикло[3.1.0]гекс-1-ил)-2-фторфенил]метил}амина, который получают способом, аналогичным описанному в препаративном примере 54, исходя из 1,1 моль 2-фтор-4-[3-(фенилметил)-3-азабицикло[3.1.0]гекс-1-ил]бензонитрила, и используют без дополнительной очистки, при комнатной температуре в течение 5 мин добавляют по каплям раствор 2,5-бис(метилокси)тетрагидрофурана (2,53 ммоль) и H2SO4 (4,4 моль) в смеси метанол/тетрагидрофуран (безводная, 1/1, 5 мл). После выстаивания в течение ночи при комнатной температуре добавляют постепенно насыщенный раствор NaHCO3, и экстракция 2 × 15 мл дихлорметана с последующей очисткой перпаративной ВЭЖХ дают 14 мг названного в заголовке соединения в виде масла (выход = 5%).
ЯМР (1H, CDCl3): δ 6,88-6,82 (м, 3H), 6,67 (т, 2H), 6,14 (т, 2H), 5,04 (с, 2H), 3,21 (д, 1H), 3,1 (д, 1H), 3,09 (д, 1H), 3,01 (д, 1H), 1,67 (м, 1H), 0,88 (м, 2H). МС (m/z): 257 [MH]+.
Препаративный пример 58. (1R,5S)/1S,5R)-3-(3-Хлорпропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают в виде бесцветного масла с выходом 522 мг (84%) из (1R,5S)/1S,5R)-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексана (584 мг) способом, аналогичным описанному в препаративном примере 40.
ЯМР (1H, CDCl3): δ 8,47 (с, 1H), 7,55 (м, 2H), 3,59 (т, 2H), 3,33 (д, 1H), 3,09 (д, 1H), 2,6 (м, 3Н), 2,52 (дд, 1H), 1,92 (м, 2H), 1,78 (м, 1H), 0,85 (м, 1H), 0,81 (дд, 1H). МС (m/z): 305 [MH]+.
Препаративный пример 59. 5-[(1R,5S)/1S,5R)-3-(3-Хлорпропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-метил-1,3-бензотиазол
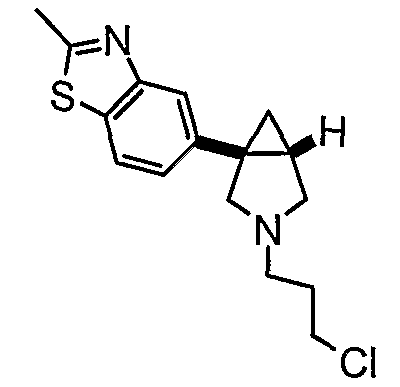
Названное в заголовке соединение получают в виде бесцветного масла с выходом 480 мг (84%) из 5-[(1R,5S)/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-метил-1,3-бензотиазола (374 мг) способом, аналогичным описанному в препаративном примере 40.
ЯМР (1H, CDCl3): δ 7,70 (м, 2H), 7,11 (д, 1H), 3,59 (т, 2H), 3,38 (д, 1H), 3,09 (д, 1H), 2,8 (с, 3H), 2,66 (м, 3H), 2,53 (дд, 1H), 1,95 (м, 2H), 1,74 (м, 1H), 1,44 (т, 1H), 0,83 (дд, 1H). МС (m/z): 307 [MH]+.
Препаративный пример 60. 1-(1R,5S)/1S,5R)-[3-Фтор-5-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан-2,4-дион

К взвеси малеимида (1,8 экв.), безводного CuCl2 (1,2 экв.) и трет-бутилнитрита (1,5 экв.) в CH3CN (5 мл) при 0°С добавляют по каплям раствор 3-фтор-5-(трифторметил)анилина (2,2 г) в CH3CN (4 мл). Реакционную смесь перемешивают при комнатной температуре в течение 2 час и добавляют HCl (6 М водный раствор, 30 мл). Смесь экстрагируют EtOAc и органический слой сушат над Na2SO4. Раствор фильтруют и фильтрат концентрируют в вакууме. Остаток обрабатывают водой, отфильтровывают и сушат в вакууме. Раствор полученного сырого продукта реакции в ДМСО (10 мл) добавляют по каплям к предварительно полученному раствору иодида триметилсульфоксония (2 экв.) в безводном ДМСО (20 мл), к которому добавлен по частям NaH (15 экв.). Реакционную смесь перемешивают в течение 30 мин и добавляют воду, а затем насыщенный раствор NH4Cl (до рН 6,5). Реакционную смесь экстрагируют Et2O, объединенные органические слои промывают насыщенным водным раствором NaCl и сушат над Na2SO4. Раствор фильтруют и фильтрат концентрируют в вакууме. Полученный сырой продукт реакции обрабатывают циклогексаном и получают названное в заголовке соединение в виде светло-зеленого твердого вещества (1,02 г).
ЯМР (1H, CDCl3): δ 7,4-7,20 (м, 3H), 2,85-2,75 (м, 1H), 2,0 (м, 1H), 1,85 (м, 1H), NH не наблюдают. МС (m/z): 274[MH]+.
Препаративный пример 61. (1R,5S)/1S,5R)-1-[3-Фтор-5-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 650 мг из (1R,5S)/1S,5R)-1-[3-фтор-5-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан-2,4-диона, следуя процедуре, описанной в препаративном примере 38.
ЯМР (1H, CDCl3): δ 7,05-7,40 (м, 3H)r 3,1-3,3 (м, 4H), 1,7 (м, 1H), 0,9 (м, 2H), NH не наблюдают. МС (m/z): 246 [MH]+.
Препаративный пример 62. (1R,5S)/1S,5R)-1-[2-Фтор-3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан
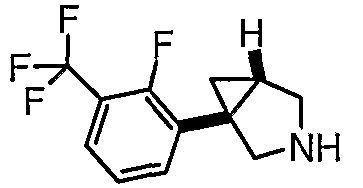
Названное в заголовке соединение получают с выходом 947 мг из 2-фтор-3-(трифторметил)анилина (3 г), следуя процедурам, описанным в препаративных примерах 60 и 38.
ЯМР (1H, CDCl3): δ 7,2 (м, 2H), 6,9 (м, 1H), 3,0-2,7 (м, 4H), 1,6 (м, 1H), 0,7 (м, 2H). МС (m/z): 246 [MH]+.
Препаративный пример 63. (1R,5S)/1S,5R)-1-[4-(Метилокси)-5-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 430 мг из 4-(метилокси)-5-(трифторметил)анилина (2,2 г), следуя процедурам, описанным в препаративных примерах 60 и 38.
ЯМР (1H, CDCl3): δ 7,4-7,3 (м, 2H), 6,9 (м, 1H), 3,9 (с, 3H), 3,2-3,0 (м, 4H), 1,9 (с, 1H), 1,65 (м, 1H), 0,8 (м, 2H). МС (m/z): 258 [MH]+.
Препаративный пример 64. (1R,5S)/1S,5R)-1-(4-Хлор-2-фторфенил)-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 360 мг из 4-хлор-2-фторанилина (1,87 г), следуя процедурам, описанным в препаративных примерах 60 и 38.
ЯМР (1H, CDCl3): δ 7,2-7,0 (м, 3H), 3,2-3,0 (м, 4H), 2,0 (с, 1H), 1,75 (м, 1H), 0,8 (м, 2H). МС (m/z): 212 [MH]+.
Препаративный пример 65. (1R,5S)/1S,5R)-1-{3-[(Трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан
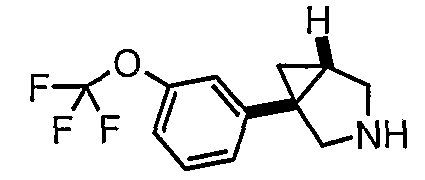 .
.
Названное в заголовке соединение получают с выходом 600 мг из 3-трифторметилоксианилина (2,65 г), следуя процедурам, описанным в препаративных примерах 60 и 38.
ЯМР (1H, CDCl3): δ 7,3-7 (м, 4H), 3,3-3,0 (м, 4H), 1,8 (с, 1H), 1,75 (м, 1H), 0,95 (м, 2H). МС (m/z): 212 [MH]+.
Препаративный пример 66. (1R,5S)/1S,5R)-1-(2-Фтор-4-метилфенил)-3-азабицикло[3.1.0]гексан
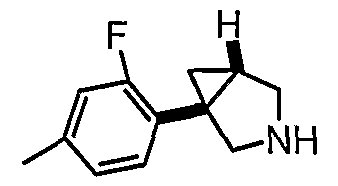
Названное в заголовке соединение получают с выходом 148 мг из 2-фтор-4-метиланилина (2,18 г), следуя процедурам, описанным в препаративных примерах 60 и 38.
ЯМР (1H, CDCl3): δ 7,2 (м, 1H), 6,85 (м, 2H), 3,2-2,9 (м, 4H), 2,25 (с, 3H), 1,75 (с, 1H), 1,65 (м, 1H), 0,9 (м, 2H). МС (m/z): 192 [MH]+.
Препаративный пример 67. (1R,5S)/1S,5R)-1-[3-Хлор-4-(метилокси)фенил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 60 мг из 2-хлор-4-метиланилина (2,36 г), следуя процедурам, описанным в препаративных примерах 60 и 38.
ЯМР (1H, CDCl3): δ 7,15-7 (м, 2H), 6,85 (м, 1H), 3,85 (с, 3H), 3,2-2,9 (м, 4H), 1,8-1,6 (м, 2H), 0,75 (м, 2H). МС (m/z): 224 [MH]+.
Препаративный пример 68. (1R,5S)/1S,5R)-1,1-Диметилэтил-1-(4-бромфенил)-3-азабицикло[3.1.0]гексан-3-карбоксилат
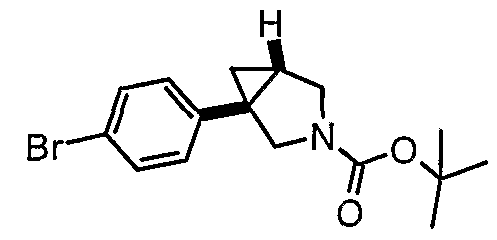
К раствору (1R,5S)/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексана (препаративный пример 6, 1,3 г) в дихлорметане (20 мл) при перемешивании при комнатной температуре добавляют триэтиламин (0,99 мл) и бис(1,1-диметилэтил)дикарбонат. Перемешивание продолжают в течение 6 час, затем реакционную смесь концентрируют в вакууме и сырой продукт реакции обрабатывают диэтиловым эфиром и водой. Органическую фазу промывают насыщенным раствором хлорида аммония, сушат над сульфатом натрия, выпаривают растворитель в вакууме и получают сырой продукт реакции, который очищают хроматографией на силикагеле (циклогексан/EtOAc, 9/1) и получают названное в заголовке соединение (1,68 г, 91%).
МС (m/z): 282,1 [MH-C4H8]+, 1Br.
Препаративный пример 69. (1R,5S)/1S,5R)-1,1-Диметилэтил-1-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]-3-азабицикло[3.1.0]гексан-3-карбоксилат

К раствору (1R,5S)/1S,5R)-1,1-диметилэтил-1-(4-бромфенил)-3-азабицикло[3.1.0]гексан-3-карбоксилата (2 г) в ДМФА (30 мл) при перемешивании при RT последовательно добавляют биспинаколят дибора (2,25 г), ацетат калия (1,75 г) и PdCl2(dppf) (0,15 г). Реакционную смесь греют при 85°С в течение 1,5 час, выливают в воду и дважды экстрагируют диэтиловым эфиром и органическую фазу промывают рассолом и сушат над сульфатом натрия. Растворитель выпаривают в вакууме, сырой продукт реакции очищают хроматографией на силикагеле (циклогексан/EtOAc, 9/1) и получают названное в заголовке соединение в виде белого твердого вещества (2,1 г, 92%).
МС (m/z): 330,3 [MH-C4H8]+, 1Br.
Препаративный пример 70. (1R,5S)/1S,5R)-1,1-Диметилэтил-1-(3-бромфенил)-3-азабицикло[3.1.0]гексан-3-карбоксилат
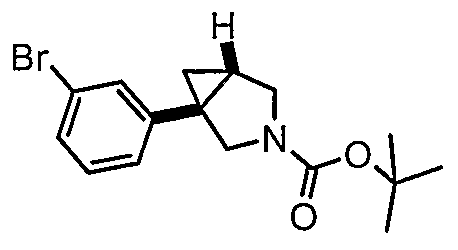
Названное в заголовке соединение получают в виде белого твердого вещества с выходом 94% из (1R,5S)/1S,5R)-1-(3-бромфенил)-3-азабицикло[3.1.0]гексана (7,4 г) способом, аналогичным описанному в препаративном примере 68.
МС (m/z): 282,1 [MH-C4H8]+, 1Br.
Препаративный пример 71. (1R,5S)/1S,5R)-1,1-Диметилэтил-1-[3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]-3-азабицикло[3.1.0]гексан-3-карбоксилат

Названное в заголовке соединение получают в виде белого твердого вещества с выходом 84% из (1R,5S)/1S,5R)-1,1-диметилэтил-1-(3-бромфенил)-3-азабицикло[3.1.0]гексан-3-карбоксилата (2,5 г) способом, аналогичным описанному в препаративном примере 69.
МС (m/z): 330,3 [MH-C4H8]+, 1Br.
Препаративный пример 72. (1R,5S)/1S,5R)-1-[4-(2,4-Диметил-1,3-тиазол-5-ил)фенил]-3-азабицикло[3.1.0]гексан
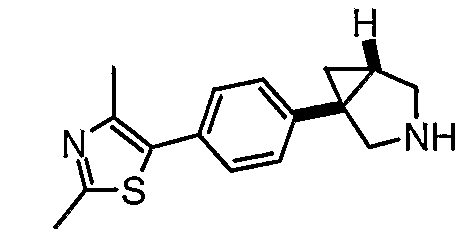
К раствору (1R,5S)/1S,5R)-1,1-диметилэтил-1-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]-3-азабицикло[3.1.0]гексан-3-карбоксилата (0,3 г) в тетрагидрофуране (12 мл) при перемешивании при RT и в атмосфере азота последовательно добавляют 5-бром-2,4-диметил-1,3-тиазол (0,22 г), фторид цезия (0,47 г) и тетракис(трифенилфосфин)палладий(0) (0,06 г). Реакционную смесь греют при 80°С в течение 4 часов и растворитель выпаривают в вакууме. Сырой продукт реакции обрабатывают диэтиловым эфиром и насыщенным водным раствором хлорида аммония, органическую фазу промывают рассолом, сушат над сульфатом натрия и концентрируют в вакууме. Сырой продукт реакции очищают хроматографией на силикагеле (циклогексан/EtOAc, 8/1). Затем очищенный продукт растворяют в CH2Cl2 (10 мл) и добавляют трифторуксусную кислоту (4 мл). Через 2 часа реакционную смесь обрабатывают твердым карбонатом натрия и выпаривают растворитель. Остаток обрабатывают твердым карбонатом натрия и выпаривают растворитель. Остаток обрабатывают водой и экстрагируют CH2Cl2, органическую фазу промывают рассолом, сушат над сульфатом натрия и упаривают и получают названное в заголовке соединение (0,1 г, 34%).
МС (m/z): 271,2 [MH]+.
Препаративный пример 73. (1R,5S)/1S,5R)-1-{4-[6-(Трифторметил)-2-пиридинил]фенил}-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 60% способом, аналогичным описанному в препаративном примере 72 (с использованием 2-бром-6-(трифторметил)пиридина).
МС (m/z): 305,3 [MH]+.
Препаративный пример 74. (1R,5S)/1S,5R)-1-[4-(3,5-Диметил-4-изоксазолил)фенил]-3-азабицикло[3.1.0]гексан
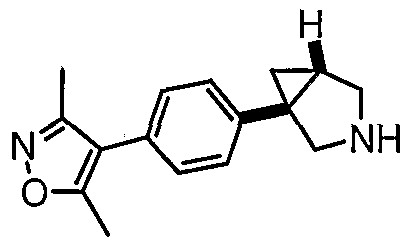
К раствору (1R,5S)/1S,5R)-1,1-диметилэтил-1-(4-бромфенил)-3-азабицикло[3.1.0]гексан-3-карбоксилата (0,37 г) в толуоле (5 мл) и этиловом спирте (2 мл) при перемешивании при RT в атмосфере азота последовательно добавляют (3,5-диметил-4-изоксазолил)бороновую кислоту (0,25 г), тетракис(трифенилфосфин)палладий(0) (0,03 г) и насыщенный раствор карбоната калия (2 мл). Реакционную смесь греют при 88°С в течение 2 час и растворители выпаривают в вакууме. Сырой продукт реакции обрабатывают диэтиловым эфиром и водой, органическую фазу промывают рассолом, сушат над сульфатом натрия, концентрируют в вакууме и дважды экстрагируют эфиром. Растворитель выпаривают и сырой продукт реакции очищают хроматографией на силикагеле (циклогексан/EtOAc, 8/1). Затем очищенный продукт растворяют в CH2Cl2 (10 мл) и добавляют трифторуксусную кислоту (4 мл). Через 3 часа реакционную смесь обрабатывают твердым карбонатом натрия и выпаривают растворитель. Остаток обрабатывают водой и экстрагируют CH2Cl2, органическую фазу промывают рассолом, сушат над сульфатом натрия и упаривают и получают названное в заголовке соединение (0,12 г, 45%).
МС (m/z): 255,2 [MH]+.
Препаративный пример 75. (1R,5S)/1S,5R)-1-[3-(2,4-Диметил-1,3-тиазол-5-ил)фенил]-3-азабицикло[3.1.0]гексан

Названное в заголовке соединение получают с выходом 50% способом, аналогичным описанному в препаративном примере 72, с использованием (1R,5S)/1S,5R)-1,1-диметилэтил-1-[3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]-3-азабицикло[3.1.0]гексан-3-карбоксилата (промежуточное соединение 4).
МС (m/z): 271,3 [MH]+.
Препаративный пример 76. (1R,5S)/1S,5R)-1-[3-(5-Метил-2-тиенил)фенил]-3-азабицикло[3.1.0]гексан
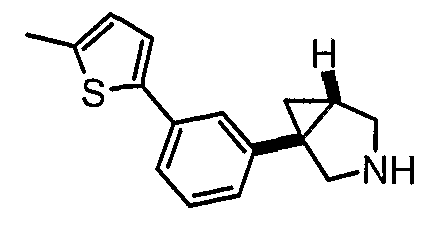
Названное в заголовке соединение получают с выходом 55% способом, аналогичным описанному в препаративном примере 72, с использованием (1R,5S)/1S,5R)-1,1-диметилэтил-1-[3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]-3-азабицикло[3.1.0]гексан-3-карбоксилата (промежуточное соединение 4).
МС (m/z): 256,2 [MH]+.
Препаративный пример 77. 5-(2,4-Диметил-1,3-оксазол-5-ил)-4-метил-2,4-дигидро-3Н-1,2,4-триазол-3-тион
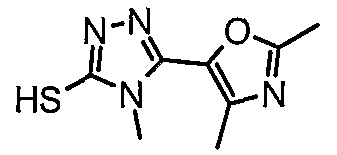
В атмосфере азота при комнатной температуре растворяют 2,4-диметил-1,3-оксазол-5-карбоновую кислоту (0,8 г), N-метилгидразинкарбоксамид (0,6 г), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (1,09 г), HOBt (0,038 г) и триэтиламин (0,86 мл) в сухом ДМФА (15 мл). Смесь перемешивают в течение ночи и затем ДМФА удаляют в вакууме. Добавляют раствор NaOH (0,75 М, 10 мл) и смесь греют при 80°С в течение 3 час. Реакционную смесь охлаждают до 0°С и подкисляют до прибл. рН 5 HCl (водный раствор, 37%). Суспендированный продукт извлекают фильтрацией, промывая водой (2 × 3 мл). Остаток на фильтре сушат при комнатной температуре в течение ночи в вакууме и получают названное в заголовке соединение в смеси 3:2 с 2,4-диметил-1,3-оксазол-5-карбоновой кислотой в виде твердого вспененного вещества (0,68 г, выход 57%).
ЯМР (1H, CDCl3): δ 3,80 (с, 3H), 2,60 (с, 3H), 2,40 (с, 3H), NH/CH не наблюдают.
Препаративный пример 78. 3-[(3-Хлорпропил)тио]-5-(2,4-диметил-1,3-оксазол-5-ил)-4-метил-4Н-1,2,4-триазол

Смесь продуктов реакции из препаративного примера 77 суспендируют в EtOH (10 мл). Добавляют NaOEt (21% раствор в EtOH, 1,14 мл), а затем 1-бром-3-хлорпропан (0,41 мл), раствор перемешивают при 90°С в течение 45 мин и затем охлаждают до 25°С. Добавляют уксусную кислоту (0,1 экв.) и затем растворитель удаляют в вакууме. Твердое вещество очищают колоночной хроматографией на силикагеле с элюированием смесью циклогексан/EtOAc и получают названное в заголовке соединение в виде твердого вспененного вещества (0,44 г, выход 54%).
ЯМР (1H, CDCl3): δ 3,70 (т+с, 5H), 3,35 (т, 2H), 2,50 (с, 3H), 2,4 (с, 3H), 2,30 (м, 2H). МС (m/z): 287 [MH]+.
Пример 1. Гидрохлорид 5-[5-({3-[(1R,5S)/1S,5R)-1-(4-метоксифенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолина
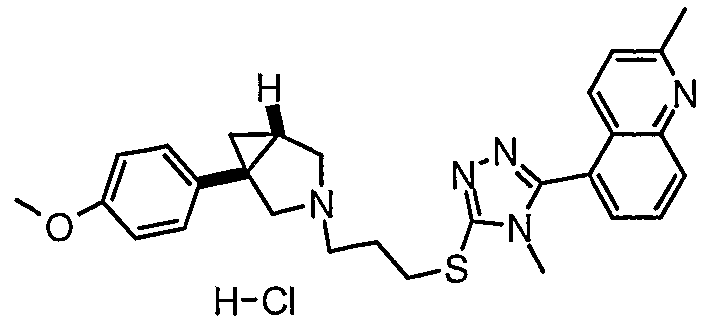
Смесь (1R,5S)/1S,5R)-1-[4-(метокси)фенил]-3-азабицикло[3.1.0]гексана (препаративный пример 5, 42 мг), 5-{5-[(3-хлорпропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил}-2-метилхинолина (0,26 ммоль), Na2CO3 (0,44 ммоль) и NaI (0,22 ммоль) в ДМФА (безводный, 0,4 мл) греют при 60°С в течение 24 час. После удаления растворителя в вакууме остаток растворяют в этилацетате и органический слой промывают насыщенным водным раствором NaHCO3 и сушат над Na2SO4. Полученный раствор фильтруют и фильтрат концентрируют в вакууме. Сырой продукт реакции очищают флэш-хроматографией (дихлорметан - 10% МеОН в дихлорметане) и получают 65 мг свободного основания названного в заголовке соединения. К раствору полученного вещества в дихлорметане (0,2 мл) добавляют 0,14 ммоль HCl (1 M раствор в Et2O), растворитель выпаривают в вакууме, полученное таким образом вещество обрабатывают Et2O, и получают 69 мг названного в заголовке соединения в виде белого слабогигроскопичного твердого вещества (выход 59%).
[Процедуру можно аналогично адаптировать для других сочетаний 1-замещенных 3-азабицикло[3.0.1]гексанов и 3-замещенных 5-[(3-хлорпропил)тио]-4-метил-4Н-1,2,4-триазолов. Можно использовать эквивалентное молярное количество К2СО3 вместо Na2CO3.]
ЯМР (1H, ДМСО): δ 10,57 (ушс, 1H), 8,28 (ушс, 1H), 8,2 (д, 1H), 7,94 (т, 1H), 7,82 (д, 1H), 7,56 (д, 1H), 7,25 (д, 2H), 6,91 (д, 2H), 4,01 (дд, 1H), 3,7 (м, 1H), 3,74 (с, 3H), 3,6-3,2 (м, 6H), 3,42 (с, 3H), 2,75 (с, 3H), 2,24 (квинт, 2H), 2,08 (квинт, 1H), 1,62/1,05 (т/т, 2H). МС (m/z): 486,3 [MH]+.
Соединение, полученное в примере 1, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpack AD-H, 25 × 2,1 см, элюент СО2, содержащий 20% смеси (этанол + 0,1% изопропанола), скорость потока 25 мл/мин, Р 194 бар, Т 35°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpack AD-H, 25 × 0,46 см, элюент СО2, содержащий 20% смеси (этанол + 0,1% изопропанола), скорость потока 2,5 мл/мин, Р 194 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (60 мг) в виде белого твердого вещества с выходом 15 мг (выход = 27%). Rt = 39,2 мин.
Энантиомер 2 извлекают из рацемата (60 мг) в виде белого твердого вещества с выходом 17 мг (выход = 30%). Rt = 43,4 мин.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 2. Гидрохлорид 5-[5-({3-[(1R,5S/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолина

Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-(4-бромфенил)-3-азабицкило[3.1.0]гексана (40 мг) способом, аналогичным описанному в примере 1, с выходом 39 мг в виде белого слабогигроскопичного твердого вещества (выход = 40%).
ЯМР (1H, ДМСО): δ 10,28 (ушс,1H), 8,16 (дд, 2H), 7,89 (дд, 1H), 7,76 (д, 1H), 7,55 (д, 2H), 7,49 (д, 1H), 7,28 (д, 2H), 4,06 (ушм, 1H), 3,77 (ушм, 1H), 3,6 (ушм, 2H), 3,44 (с, 3H), 3,5-3,2 (ушм, 4H), 2,71 (с, 3H), 2,23 (м, 3H), 1,58/1,14 (т/м, 2H). МС (m/z): 534,1 [MH]+, 1Br.
Соединение, полученное в примере 2, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralcel OJ-H, 25 × 2,1 см, элюент СО2, содержащий 12% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 196 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralcel OJ-H, 25 × 0,46 см, элюент СО2, содержащий 10% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 196 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (39 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 7 мг. Rt = 56,8 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (39 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 7 мг. Rt = 62,5 мин. Чистота >99% a/a по УФ.
Абсолютную конфигурацию энантиомера 1 устанавливают с использованием сравнительных анализов VCD и сравнительных анализов OR соответствующего свободного основания, представляющего собой 5-[5-({3-[(1R,5S)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин. В качестве эталона используют (1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексан (см. препаративный пример 48).
Абсолютную конфигурацию энантиомера 2 устанавливают так, как описано для энантиомера 1, как представляющего собой 5-[5-({3-[(1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин.
Энантиомер 1: удельное оптическое вращение соответствующего свободного основания [α]D = +47° (CHCl3, T = 20°C, c = 0,066 г/мл).
Энантиомер 2: удельное оптическое вращение соответствующего свободного основания [α]D = -42o (CHCl3, T = 20°C, c = 0,065 г/мл).
Энантиомер 2 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 1.
Пример 3. Гидрохлорид 2-метил-5-[4-метил-5-({3-[(1R,5S/1S,5R)-1-фенил-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4Н-1,2,4-триазол-3-ил]хинолина

Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-фенил-3-азабицкило[3.1.0]гексана (40 мг) способом, аналогичным описанному в примере 1, с выходом 74 мг в виде белого слабогигроскопичного твердого вещества (выход = 40%).
ЯМР (1H, ДМСО): δ 10,4 (ушс,1H), 8,3 (ушс, 1H), 8,2 (д, 1H), 7,9 (т, 1H), 7,8 (д, 1H), 7,6 (ушд, 1H), 7,4-7,3 (м, 5H), 4,0-3,5 (м/м, 2H), 3,7-3,45 (м/м, 2H), 3,5-3,3 (м, 7H), 2,73 (с, 3H), 2,3 (м, 3H), 1,60, 1,1 (т,т 2H). МС (m/z): 456,3 [MH]+.
Соединение, полученное в примере 3, разделяют для получения отдельных энантиомеров методом полупрепаративной ВЭЖХ с использованием хиральной колонки с Chiralcel OD, 10 мкм, 250 × 20 мм, элюент А - н-гексан; В - изопропанол, градиент изократный 35% В, скорость потока 7 мл/мин, УФ-детекция при 200-400 нм, CD 230 нм. Приведенные времена удерживания получают с использованием аналитической ВЭЖХ с использованием хиральной колонки с Chiralcel OD, 5 мкм, 250 × 4,6 мм, элюент А - н-гексан; В - изопропанол, градиент изократный 25% В, скорость потока 1 мл/мин, УФ-детекция при 200-400 нм.
Энантиомер 1 извлекают из рацемата (60 мг) в виде белого твердого вещества с выходом 15 мг (выход = 27%). Rt = 39,2 мин.
Энантиомер 2 извлекают из рацемата (60 мг) в виде белого твердого вещества с выходом 17 мг (выход = 30%). Rt = 43,4 мин.
Энантиомер 2 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 1.
Пример 4. Гидрохлорид 5-[5-({3-[(1R,5S/1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолина

Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексана (50 мг) способом, аналогичным описанному в примере 1, с выходом 65 мг в виде белого слабогигроскопичного твердого вещества (выход = 52%).
ЯМР (1H, ДМСО): δ 10,6 (с, 1H), 8,32 (ушс, 1H), 8,21 (д, 1H), 7,96 (д, 1H), 7,84 (д, 1H), 7,66 (д, 1H), 7,61 (д, 1H), 7,6 (д, 1H), 7,31 (дд, 1H), 4,06 (м, 2H), 3,74 (м, 2H), 3,7-3,2 (м, 4H), 3,36 (с, 3H), 2,76 (с, 3H), 2,25 (м, 4H), 1,69 (м, 1H), 1,2 (м, 1H). МС (m/z): 524,3 [MH]+, 2Cl.
Соединение, полученное в примере 4, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson), как описано в примере 1.
Энантиомер 1 извлекают из рацемата (56 мг) в виде белого твердого вещества с выходом 19 мг (выход = 36%). Rt = 26,9 мин.
Абсолютную конфигурацию энантиомера 1 устанавливают с использованием сравнительных анализов VCD и сравнительных анализов OR соответствующего свободного основания, представляющего собой 5-[5-({3-[(1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин. В качестве эталона используют (1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексан (см. препаративный пример 48).
Абсолютную конфигурацию энантиомера 2 устанавливают так, как описано для энантиомера 1, как представляющего собой 5-[5-({3-[(1R,5S)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин.
Энантиомер 1: удельное оптическое вращение соответствующего свободного основания [α]D =-38,4° (CDCl3, T = 20°C, c = 0,010 г/мл).
Энантиомер 2 извлекают из рацемата (56 мг) в виде белого твердого вещества с выходом 14 мг (выход = 26%). Rt = 31,4 мин.
Энантиомер 2: удельное оптическое вращение соответствующего свободного основания [α]D = +34,4° (CDCl3, T = 20°C, c = 0,010 г/мл).
Энантиомер 1 показывает fpKi (D3) > 0,61 log-единицы выше, чем энантиомер 2.
Пример 5. Гидрохлорид 5-[5-({3-[(1R,5S/1S,5R)-1-(4-трет-бутилфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолина
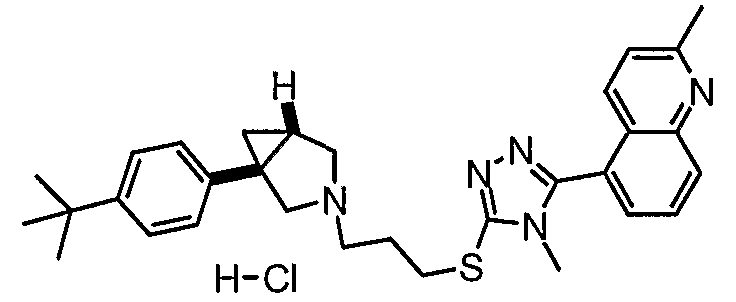
Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-(4-трет-бутилфенил)-3-азабицикло[3.1.0]гексана (29 мг) способом, аналогичным описанному в примере 1, с выходом 38 мг в виде белого слабогигроскопичного твердого вещества (выход = 51%).
ЯМР (1H, ДМСО): δ 10,16 (ушс,1H), 8,15 (дд, 2H), 7,89 (т, 1H), 7,76 (д, 1H), 7,49 (д, 1H), 7,36 (д, 2H), 7,23 (д, 2H), 4,05 (дд, 1H), 3,77 (дд, 1H), 3,58 (м, 2H), 3,44 (с, 3H), 2,7 (ушм, 4H), 2,34 (с, 3H), 2,23 (т, 2H), 2,15 (т, 1H), 1,51 (т, 1H), 1,27 (с, 9H), 1,14 (м, 1H). МС (m/z): 512,4 [MH]+.
Соединение, полученное в примере 5, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson), как описано в примере 1, но применяя давление 200 бар вместо 194 бар.
Энантиомер 1 извлекают из рацемата (23 мг) в виде белого твердого вещества с выходом 6,5 мг (выход = 30%). Rt = 7,0 мин.
Энантиомер 2 извлекают из рацемата (23 мг) в виде белого твердого вещества с выходом 5 мг (выход = 23%). Rt = 7,8 мин.
Энантиомер 2 показывает fpKi (D3) > 0,9 log-единицы выше, чем энантиомер 1.
Пример 6. Гидрохлорид 4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]бензонитрила
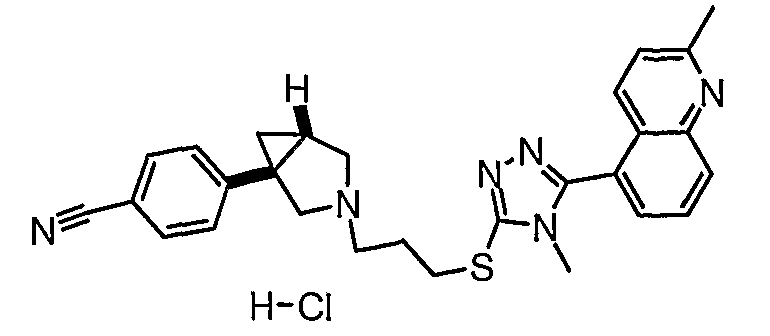
Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-(4-цианофенил)-3-азабицикло[3.1.0]гексана (25 мг) способом, аналогичным описанному в примере 1, с выходом 19 мг в виде белого слабогигроскопичного твердого вещества (выход = 27%).
ЯМР (1H, ДМСО): δ 10,45 (ушс, 1H), 8,26 (ушд, 1H), 8,17 (д, 1H), 7,93 (т, 1H), 7,8 (д/д, 3H), 7,5 (д, 1H), 7,46 (д, 2H), 4,09 (д, 1H), 3,76 (д, 1H), 3,67 (т, 1H), 3,6-3,2 (ушм, 5H), 3,43 (с, 3H), 2,73 (с, 3H), 2,34 (м, 1H), 2,25 (квинт, 2H), 1,71/1,22 (дт, 2H).
Пример 7. Гидрохлорид 4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенола

Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-(4-гидроксифенил)-3-азабицикло[3.1.0]гексана (38 мг) способом, аналогичным описанному в примере 1, с выходом 10 мг в виде белого слабогигроскопичного твердого вещества (выход = 11%).
ЯМР (1H, ДМСО): δ 10,17 (ушс, 1H), 9,4 (с,1H), 8,15 (ушд, 2H), 7,89 (д, 1H), 7,75 (д, 1H), 7,48 (д, 1H), 7,12 (д, 2H), 6,73 (д, 2H), 3,98 (дд, 1H), 3,74 (м, 1H), 3,5 (ушм, 2H), 3,44 (с, 3H), 3,5-3,2 (ушм, 4H), 2,7 (с, 3H), 2,22 (ушквинт, 2H), 2,03 (м, 1H), 1,46/1,03 (дм, 2H). МС (m/z): 486,2 [MH]+.
Пример 8. Гидрохлорид (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-фенил-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-фенил-3-азабицикло[3.1.0]гексана (40 мг) способом, аналогичным описанному в примере 1, с выходом 75 мг в виде белого слабогигроскопичного твердого вещества (выход = 70%).
ЯМР (1H, ДМСО): δ 10,46 (ушс, 1H), 8,58 (с, 1H), 7,4-7,2 (м, 5H), 4,04 (дд, 1H), 3,73 (м, 1H), 3,7 (с, -3H), 3,7-3,4 (м, 2H), 3,4-3,2 (м+т, 4H), 2,39 (с, 3H), 2,17 (м, 3H), 1,64, 1,1 (2т, 2H).
Пример 9. Гидрохлорид (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана
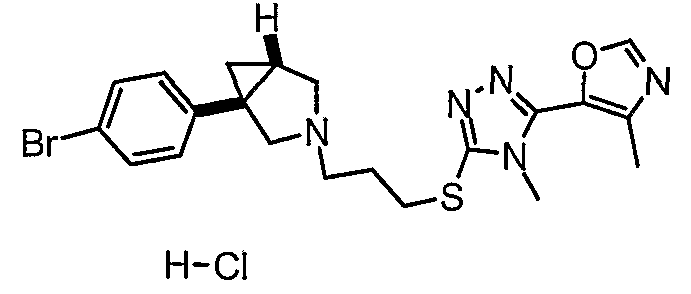
Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексана (40 мг) способом, аналогичным описанному в примере 1, с выходом 24 мг в виде белого слабогигроскопичного твердого вещества (выход = 28%).
ЯМР (1H, ДМСО): δ 10,29 (ушс, 1H), 8,58 (с, 1H), 7,55 (дд, 2H), 7,27 (дд, 2H), 4,03 (дд, 1H), 3,73 (дд, 1H), 3,7(с, 3H), 3,55 (м, 2H), 3,5-3,2/3,28 (м+т, 4H), 2,39 (с, 3H), 2,19 (м, 3H), 1,59/1,12 (2т, 2H). МС (m/z): 474,1 [MH]+.
Соединение, полученное в примере 9, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralcel AS-H, 25 × 2,1 см, элюент СО2, содержащий 11% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 192 бар, Т 36°С, УФ-детекция при 220 нм, петля 2 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 0,46 см, элюент СО2, содержащий 10% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 199 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (138 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 59 мг. Rt = 22,2 мин. Чистота >99%, a/a по УФ.
Энантиомер 2 извлекают из рацемата (138 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 50 мг. Rt = 30,8 мин. Чистота >99%, a/a по УФ.
Абсолютную конфигурацию энантиомера 1 устанавливают с использованием сравнительных анализов VCD и сравнительных анализов OR соответствующего свободного основания, представляющего собой (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан. В качестве эталона используют (1R,5S)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексан (сравните препаративный пример 32).
Абсолютную конфигурацию энантиомера 2 устанавливают так, как описано для энантиомера 1, как представляющего собой (1R,5S)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан.
Энантиомер 1: удельное оптическое вращение соответствующего свободного основания [α]D = -51° (CHCl3, T = 20°C, c = 0,00913 г/мл).
Энантиомер 2: удельное оптическое вращение соответствующего свободного основания [α]D = +27° (CHCl3, T = 20°C, c = 0,0113 г/мл).
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 10. Гидрохлорид (1R,5S/1S,5R)-1-(4-трет-бутилфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-(4-трет-бутилфенил)-3-азабицикло[3.1.0]гексана (40 мг) способом, аналогичным описанному в примере 1, с выходом 52 мг в виде белого слабогигроскопичного твердого вещества (выход = 57%).
ЯМР (1H, CD3OD): δ 8,4 (с, 1H), 7,42 (д, 2H), 7,28 (д, 2H), 4,11 (д, 1H), 3,88 (д, 1H), 3,8 (с, 3H), 3,65 (м, 2H), 3,43 (т, 2H), 3,39 (т, 2H), 2,47 (с, 3H), 2,29 (м, 2H), 2,21 (м, 1H), 1,44 (м, 1H), 1,33 (с, 9H), 1,3 (м, 1H). МС (m/z): 452,3 [MH]+.
Пример 11. Гидрохлорид (1R,5S/1S,5R)-1-(3,4-дихлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гексана (50 мг) способом, аналогичным описанному в примере 1, с выходом 35 мг в виде белого слабогигроскопичного твердого вещества (выход = 32%).
ЯМР (1H, ДМСО): δ 10,11 (сушс, 1H), 8,58 (с, 1H), 7,6 (д+д, 2H), 6,29 (дд, 1H), 4,04/3,74 (2дд, 2H), 3,7 (с, 3H), 3,6-3,2 (м, 4H), 3,28 (т, 2H), 2,39 (с, 3H), 2,26 (квинт, 1H), 2,15 (квинт, 2H), 1,53/1,2 (2т, 2H). МС (m/z): 464,1 [MH]+, 2Cl.
Соединение, полученное в примере 11, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 2,1 см, элюент СО2, содержащий 8% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 194 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 0,46 см, элюент СО2, содержащий 8% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 190 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (29 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 12,5 мг. Rt = 38,0 мин. Чистота 98,6% a/a по УФ.
Энантиомер 2 извлекают из рацемата (29 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 12,5 мг. Rt = 40,8 мин. Чистота 98,6% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 0,5 log-единицы, выше, чем энантиомер 2.
Пример 12. Гидрохлорид (1R,5S/1S,5R)-1-(4-метоксифенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-(4-метоксифенил)-3-азабицикло[3.1.0]гексана (40 мг) способом, аналогичным описанному в примере 1, с выходом 38 мг в виде белого слабогигроскопичного твердого вещества (выход = 39%).
ЯМР (1H, ДМСО): δ 10,18 (ушс, 1H), 8,58 (с, 1H), 7,24 (д, 2H), 6,91 (д, 2H), 3,97 (дд, 1H), 3,74 (с, 3H), 3,7 (с, 3H), 3,7 (м, 1H), 3,6-3,2 (м, 4H), 3,27 (т, 2H), 2,39 (с, 3H), 2,15 (квинт, 2H), 2,07 (квинт, 1H), 1,49/1,05 (2т, 2H). МС (m/z): 426,2 [MH]+.
Соединение, полученное в примере 12, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 2,1 см, элюент СО2, содержащий 9% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 192 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 0,46 см, элюент СО2, содержащий 8% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 190 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (30 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 5 мг. Rt = 28,7 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (30 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 12,5 мг. Rt = 36,4 мин. Чистота >99% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы, выше, чем энантиомер 2.
Пример 13. Гидрохлорид (1R,5S/1S,5R)-1-[4-(5-метил-3-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S)/1S,5R)-1-[4-(5-метил-3-изоксазолил)фенил]-3-азабицикло[3.1.0]гексана (55 мг) способом, аналогичным описанному в примере 1, с выходом 30 мг в виде белого слабогигроскопичного твердого вещества (выход = 25%).
ЯМР (1H, CD3OD): δ 8,37 (с, 1H), 7,8 (д, 2H), 7,43 (д, 2H), 6,55 (с, 1H), 4,16/3,88 (2д, 2H), 3,78 (с, 3H), 3,7 (м, 2H), 3,48-3,4 (2т, 4H), 2,48 (с, 3H), 2,45 (с, 3H), 2,29 (м, 3H), 1,51/1,37 (2т, 2H). МС (m/z): 477,2 [MH]+.
Пример 14. (1S,5R)-3-(3-{[4-Метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан

Смесь (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (препаративный пример 18, 10,4 г), 3-[(3-хлорпропил)тио]-4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазола (препаративный пример 14, 15,0 г), K2CO3 (7,5 г) и NaI (8,23 г) в ДМФА (безводный, 100 мл) греют при 60°С в течение 15 час. Затем смесь охлаждают до комнатной температуры и разбавляют Et2O (250 мл) и водой (200 мл). После разделения двух фаз водный слой снова экстрагируют Et2O (2 × 200 мл). Объединенные органические слои промывают водой (2 × 150 мл) и затем сушат над Na2SO4. После выпаривания растворителя в вакууме сырой продукт реакции очищают флэш-хроматографией (дихлорметан - 10% МеОН в дихлорметане), и получают 16,5 г свободного желтого твердого вещества. Полученное таким образом вещество обрабатывают Et2O и получают названное в заголовке соединение (13 г) в виде белого твердого вещества (выход 61%).
Установление конфигурации названного в заголовке соединения основывается на фактах двух видов: том факте, что его получают из (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (известной конфигурации, см. препаративный пример 14), и сравнении с данными спектроскопии, полученными для (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана. Полосы в спектре VCD названного в заголовке соединения совпадают с соответствующими полосами в спектре (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.0.1]гексана, кроме того, направление удельного вращения одно и то же для обоих соединений.
ЯМР (1H, CDCl3): δ 7,89 (м, 1H), 7,49 (д, 2H), 7,18 (д, 2H), 3,67 (с, 3H), 3,31 (м, 2H), 3,30 (д, 1H), 3,09 (д, 1H), 2,61 (м, 2H), 2,56 (д, 1H), 2,5 (с, 3H), 2,45 (д, 1H), 1,97 (м, 2H), 1,73 (м, 1H), 1,47 (т, 1H), 0,8 (дд, 1H). МС (m/z): 464 [MH]+.
Пример 15. Гидрохлорид (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана
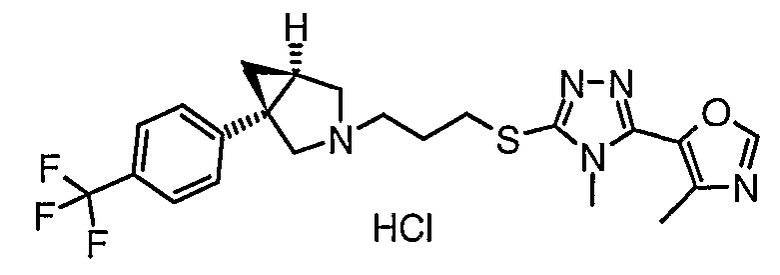
К раствору (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (пример 14, 9 г) в Et2O (безводный, 135 мл) в атмосфере азота добавляют по каплям хлороводородную кислоту (1 М раствор в Et2O, 19,4 мл). Полученную суспензию перемешивают при комнатной температуре в течение 2 час. Затем твердое вещество отфильтровывают, промывают Et2O и сушат в вакууме в течение ночи и получают названное в заголовке соединение (8,9 г) в виде не совсем белого твердого вещества (выход = 92%).
ЯМР (1H, ДМСО): δ 10,16 (ушс, 1H), 8,58 (с, 1H), 7,72 (д, 2H), 7,51 (д, 2H), 4,1 (дд, 1H), 3,78 (дд, 1H), 3,70 (с, 3H), 3,66 (м, 2H), 3,29 (т, 2H), 2,5 (ушм, 2H), 2,39 (с, 3H), 2,33 (квинт, 2H), 2,19 (м, 1H), 1,62/1,23 (т/т, 2H). МС (m/z): 464 [MH]+.
Пример 16. Гидрохлорид (1R,5S/1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана
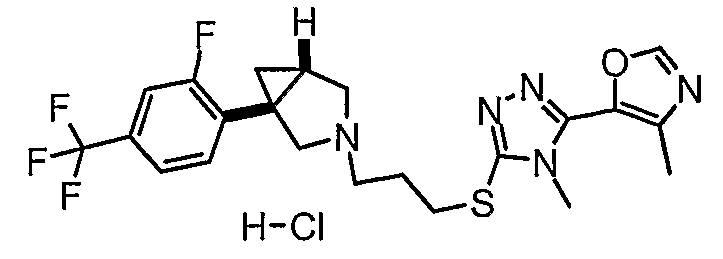
Смесь (1R,5S/1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (препаративный пример 38, 700 мг, 2,8 ммоль), 3-[(3-хлорпропил)тио]-4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазола (препаративный пример 14, 3,4 ммоль), Na2CO3 (3,4 ммоль) и NaI (3,4 ммоль) в ДМФА (безводный, 6 мл) греют при 60°С в течение 24 час. После удаления растворителя в вакууме остаток растворяют в этилацетате и органический слой промывают насыщенным водным раствором NaHCO3 и сушат над Na2SO4. Полученный раствор фильтруют и фильтрат концентрируют в вакууме. Сырой продукт реакции очищают флэш-хроматографией (дихлорметан - 10% МеОН в дихлорметане) и получают 503 мг свободного основания названного в заголовке соединения.
ЯМР (1H, CDCl3): δ 7,89 (с, 1H), 7,32-7,2 (м, 3H), 3,70 (с, 3H), 3,30 (т, 2H), 3,26 (дд, 1H), 3,10 (дд, 1H), 2,60 (т, 2H), 2,52 (дд, 1H), 2,51 (с, 3H), 2,43 (дд, 1H), 1,94 (м, 2H), 1,74 (м, 1H), 1,40 (т, 1H), 0,76 (дд, 1H). МС (m/z): 482,2 [MH]+.
Названное в заголовке соединение получают в виде белого твердого вещества, следуя способу, описанному в примере 15.
ЯМР (1H, ДМСО): δ 10,28 (ушс, 1H), 8,58 (с, 1H), 7,73 (д, 1H), 7,6 (м, 2H), 4/3,57 (д/м, 2H), 3,79 (д, 1H), 3,69 (с, 3H), 3,5-3,2 (сушм, 1H), 3,27 (т, 2H), 2,5 (м, 2H), 2,4 (м, 1H), 2,38 (с, 3H), 2,14 (квинт, 2H), 1,62/1,16 (2т, 2H). МС (m/z): 481[MH]+.
Соединение, полученное в примере 16, разделяют для получения отдельных энантиомеров методом полупрепаративной ВЭЖХ с использованием хиральной колонки с Chiralpak AD, 10 мкм, 250 х 21 мм, элюент А - н-гексан; В - изопропанол + 0,1% изопропиламина, градиент изократный 9% В, скорость потока 7 мл/мин, УФ-детекция при 200-400 нм. Приведенные времена удерживания получают с использованием аналитической ВЭЖХ с использованием хиральной колонки с Chiralpak AD-H, 5 мкм, 250 × 4,6 мм, элюент А - н-гексан; В - изопропанол, градиент изократный 15% В, скорость потока 0,8 мл/мин, УФ-детекция при 200-400 нм.
Энантиомер 1 извлекают в виде белого твердого вещества, Rt = 15,4 мин.
Энантиомер 2 извлекают в виде белого твердого вещества, Rt = 16,3 мин.
Энантиомер 2 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 1.
Пример 17. Гидрохлорид (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана
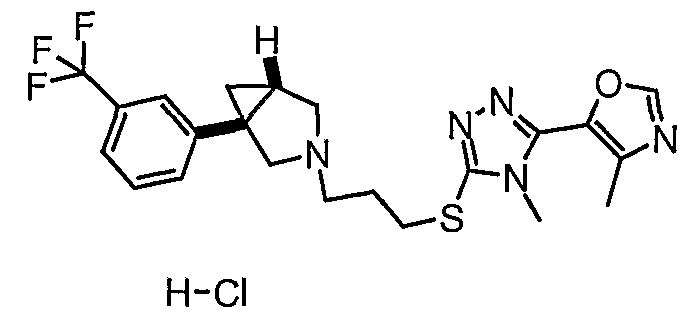
Получают (1R,5S/1S,5R)-[3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан способами, аналогичными описанным в препаративных примерах 15, 16 и 17. Из полученного вещества получают названное в заголовке соединение в виде белого слабогигроскопичного твердого вещества, следуя способам, описанным в примерах 14 и 15.
ЯМР (1H, ДМСО) δ 10,5 (ушс, 1H), 8,58 (с, 1H), 7,7-7,5 (м, 4H), 4,09 (м, 1H), 3,8-3,2 (м, 8H), 3,29 (т, 2H), 2,39 (с, 3H), 2,3 (м, 1H), 2,18 (м, 2H), 1,68 (т, 1H), 1,21 (т, 1H). МС (m/z): 464 [MH]+.
Соединение, полученное в примере 17, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 25 × 0,46 см, элюент СО2, содержащий 10% смеси (этанол + 0,1% изопропанола), скорость потока 2,5 мл/мин, Р 180 бар, Т 35°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 25 × 0,46 см, элюент СО2, содержащий 10% смеси (этанол + 0,1% изопропанола), скорость потока 22 мл/мин, Р 190 бар, Т 36°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают в виде белого твердого вещества, Rt = 17,6 мин.
Энантиомер 2 извлекают в виде белого твердого вещества, Rt = 18,4 мин.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 18. Гидрохлорид (1R,5S/1S,5R)-1-[4-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Получают (1R,5S/1S,5R)-[4-фтор-3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан способами, аналогичными описанным в препаративных примерах 15, 16 и 17. Из полученного вещества получают названное в заголовке соединение в виде белого слабогигроскопичного твердого вещества, следуя способам, описанным в примерах 14 и 15.
ЯМР (1H, ДМСО): δ 10,2 (ушс, 1H), 8,58 (с, 1H), 7,75 (дм, 1H), 7,72 (м, 1H), 7,53 (т, 1H), 4,06 (дд, 1H), 3,74 (дд, 1H), 3,7 (с, 3H), 3,6 (м, 2H), 3,4 (м, 2H), 3,28 (т, 2H), 2,39 (с, 3H), 2,26 (м, 1H), 2,18 (м, 2H), 1,54 (т, 1H), 1,22 (дд, 1H). МС (m/z): 481 [MH]+.
Пример 19. Гидрохлорид 1-[5-[(1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона

Названное в заголовке соединение получают из (1R,5S/1S,5R)-[5-(3-азабицикло[3.1.0]гекс-1-ил)-2-(метилокси)фенил]этанона (32 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 25 мг.
ЯМР (1H, ДМСО): δ 10,31 (ушс, 1H), 8,58 (с, 1H), 7,52 (д, 1H), 7,49 (дд, 1H), 7,16 (д, 1H), 3,98 (дд, 1H), 3,89 (с, 3H), 3,7 (м, 4H), 3,6-3,2 (ушм, 4H), 3,27 (т, 2H), 2,5 (м, 3H), 2,39 10 (с, 3H), 2,15 (квинт, 2H), 2,09 (квинт, 1H), 1,54-1,08 (2т, 2H). МС (m/z): 468 [MH]+.
Соединение, полученное в примере 19, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 2,1 см, элюент СО2, содержащий 15% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 196 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 0,46 см, элюент СО2, содержащий 15% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 190 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 14 мг. Rt = 12,5 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 16 мг, Rt = 16,8 мин. Чистота >99% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 20. Гидрохлорид (1S,5R/1R,5S)-1-(4-хлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-(4-хлорфенил)-3-азабицикло[3.1.0]гексана (58 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 99 мг.
ЯМР (1H, ДМСО): δ 9,93 (ушс, 1H), 8,58 (с, 1H), 7,42 (д, 2H), 7,33 (д, 2H), 4,04 (дд, 1H), 3,75 (дд, 1H), 3,7 (с, 3H), 3,5 (м, 2H), 3,3 (ушм, 4H), 2,39 (с, 3H), 2,2 (м, 1H), 2,15 (м, 2H), 1,47-1,14 (2т, 2H). МС (m/z): 431 [MH]+.
Соединение, полученное в примере 20, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 2,1 см, элюент СО2, содержащий 15% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 192 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 0,46 см, элюент СО2, содержащий 15% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 190 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 17 мг. Rt = 7,8 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 17 мг, Rt = 9,7 мин. Чистота >99% a/a по УФ.
Абсолютную конфигурацию энантиомера 1 устанавливают с использованием сравнительных анализов VCD и сравнительных анализов OR соответствующего свободного основания, представляющего собой (1S,5R)-1-(4-хлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан. В качестве эталона используют 5-[5-({3-[(1R,5S)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин (сравните с примером 2).
Абсолютную конфигурацию энантиомера 2 устанавливают так, как описано для энантиомера 1, как представляющего собой (1R,5S)-1-(4-хлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан.
Энантиомер 1: удельное оптическое вращение соответствующего свободного основания [α]D = -25° (CHCl3, T = 20°C, c = 0,0066 г/мл).
Энантиомер 2: удельное оптическое вращение соответствующего свободного основания [α]D = +29° (CHCl3, T = 20°C, c = 0,0068 г/мл).
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 21. Гидрохлорид (1S,5R/1R,5S)-1-(4-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана
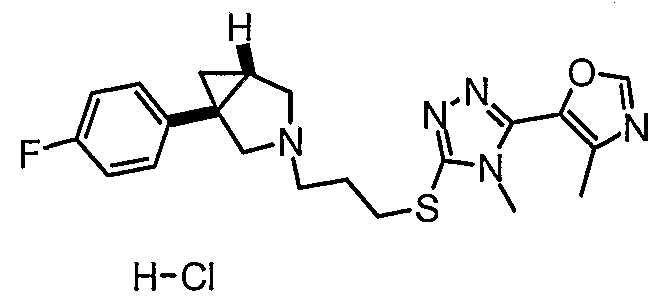
Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-(4-фторфенил)-3-азабицикло[3.1.0]гексана (49 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 78 мг.
ЯМР (1H, ДМСО): δ 10,06 (ушс, 1H), 8,58 (с, 1H), 7,36 (дд, 2H), 7,19 (т, 2H), 4,02 (дд, 1H), 3,74 (дд, 1H), 3,7 (с, 3H), 3,55 (м, 2H), 3,5-3,2 (ушм, 4H), 2,39 (с, 3H), 2,15 (м, 3H), 1,49-1,1 (2т, 2H). МС (m/z): 414 [MH]+.
Соединение, полученное в примере 21, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 2,1 см, элюент СО2, содержащий 7% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 196 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 0,46 см, элюент СО2, содержащий 6% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 190 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 14 мг. Rt = 26,2 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 16 мг, Rt = 32,4 мин. Чистота >99% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 22. Гидрохлорид (1S,5R/1R,5S)-1-(3-хлорфенил)-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-(3-хлорфенил)-3-азабицикло[3.1.0]гексана (116 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 184 мг.
ЯМР (1H, ДМСО): δ 9,88 (ушс, 1H), 8,58 (с, 1H), 7,43 (д, 1H), 7,4-7,2 (м, 3H), 4,06 (дд, 1H), 3,75 (дд, 1H), 3,7 (с, 3H), 3,62-3,54 (т/м, 2H), 3,5-3,3 (ушм, 4H), 2,39 (с, 3H), 2,25 (м, 1H), 2,15 (м, 2H), 1,46-1,19 (2м, 2H). МС (m/z): 431 [MH]+.
Соединение, полученное в примере 22, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 25 × 0,46 см, элюент СО2, содержащий 15% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 192 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Berger) с использованием хиральной колонки с Chiralpak AD-H, 25 × 0,46 см, элюент СО2, содержащий 15% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 180 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 14 мг. Rt = 26,2 мин. Чистота 100% a/a по УФ.
Энантиомер 2 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 16 мг, Rt = 32,0 мин. Чистота 100% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 23. Гидрохлорид (1S,5R/1R,5S)-1-(3-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-(3-фторфенил)-3-азабицикло[3.1.0]гексана (116 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 150 мг.
ЯМР (1H, ДМСО): δ 10,21 (ушс, 1H), 8,58 (д, 1H), 7,4 (м, 1H), 7,2-7,0 (м, 3H), 4,03 (дд, 1H), 3,75 (дд, 1H), 3,7 (с, 3H), 3,61 (т/м, 1H), 3,52 (м, 1H), 3,3 (м, 2H), 3,28 (т, 2H), 2,38 (с, 3H), 2,25 (м, 1H), 2,16 (м, 2H), 1,57-1,17 (т/м, 2H). МС (m/z): 414 [MH]+.
Соединение, полученное в примере 23, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 2,1 см, элюент СО2, содержащий 7% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 192 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 0,46 см, элюент СО2, содержащий 6% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 190 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 12 мг. Rt = 24,6 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 14,5 мг, Rt = 26,0 мин. Чистота >99% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 24. Гидрохлорид (1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(метилокси)фенил]-3-азабицикло[3.1.0]гексана
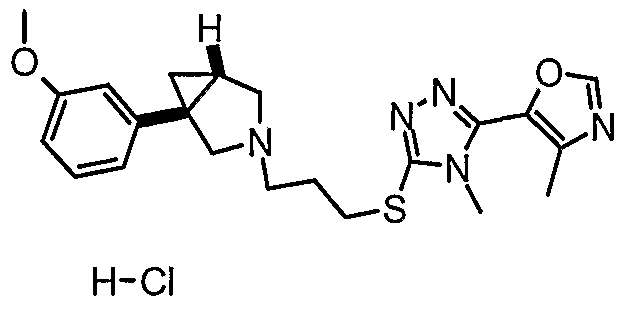
Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-(3-метилоксифенил)-3-азабицикло[3.1.0]гексана (116 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 140 мг.
ЯМР (1H, ДМСО): δ 10,16 (ушс, 1H), 8,58 (д, 1H), 7,26 (дд, 1H), 6,85 (м, 3H), 4,03 (дд, 1H), 3,77 (с, 3H), 3,72 (дд, 1H), 3,7 (с, 3H), 3,6-3,3 (ушм, 4H), 3,28 (т/м, 2H), 2,39 (с, 3H), 2,18 (м, 3H), 1,53-1,1 (т/м, 2H). МС (m/z): 426 [MH]+.
Соединение, полученное в примере 24, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralcel OJ-H, 25 × 2,1 см, элюент СО2, содержащий 13% смеси (2-пропанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 200 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Berger) с использованием хиральной колонки с Chiralcel OJ-H, 25 × 0,46 см, элюент СО2, содержащий 13% смеси (2-пропанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 180 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 13,5 мг. Rt = 24,2 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 13,5 мг, Rt = 26,8 мин. Чистота >99% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 25. Гидрохлорид (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексана (препаративный пример 32, 30 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 33 мг.
ЯМР (1H, CD3OD): δ 7,54 (д, 2H), 7,28 (д, 2H), 4,08 (м, 3H), 3,8-3,6 (м, 2H), 3,72 (с, 3H), 3,65 (м, 3H), 3,47 (т, 2H), 3,3 (м, 3H), 2,25 (м, 3H), 1,93 (м, 4H), 1,48-1,34 (2м, 2H). МС (m/z): 478 [MH]+.
Пример 26. Гидрохлорид (1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексана
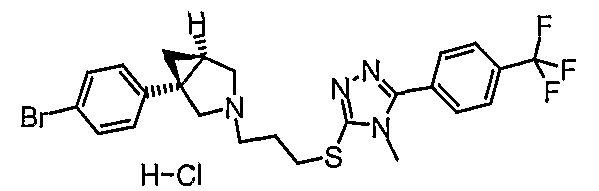
Названное в заголовке соединение получают из (1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексана (препаративный пример 32, 30 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 36 мг.
ЯМР (1H, CD3OD): δ 7,96 (м, 4H), 7,54 (д, 2H), 7,29 (т, 2H), 4,14 (д, 1H), 3,90 (м, 1H), 3,75 (с, 3H), 3,66 (м, 2H), 3,50 (м, 2H), 3,43 (т, 2H), 2,30 (м, 3H), 1,50 (м, 1H), 1,34 (т, 1H). МС (m/z): 578 [MH]+.
Пример 27. Гидрохлорид (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гексана (препаративный пример 32, 30 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 49 мг.
ЯМР (1H, CD3OD): δ 8,97 (м, 1H), 8,82 (м, 1H), 8,31 (м, 1H), 7,75 (м, 1H), 7,53 (д, 2H), 7,29 (т, 2H), 4,15 (д, 1H), 3,90 (д, 1H), 3,75 (с, 3H), 3,67 (м, 2H), 3,50 (м, 2H), 3,42 (т, 2H), 2,29 (м, 3H), 1,51 (м, 1H), 1,34 (т, 1H). МС (m/z): 471 [MH]+.
Пример 28. Гидрохлорид (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1S,5R)-1-(4-бромфенил)-3-азабицикло[3.0.1]гексана (препаративный пример 32, 30 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 26 мг.
ЯМР (1H, CD3OD): δ 7,72 (м, 1H), 7,55 (м, 4H), 7,28 (д, 2H), 4,13 (д, 1H), 3,89 (д, 1H), 3,7 (с, 3H), 3,64 (м, 2H), 3,43 (т, 2H), 3,38 (м, 2H), 2,29 (м, 3H), 1,48 (м, 1H), 1,34 (т, 1H). МС (m/z): 506 [MH]+.
Пример 29. Гидрохлорид 6-[5-({3-[(1S,5R/1R,5S)-1-(4-хлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолина

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-(4-хлорфенил)-3-азабицикло[3.1.0]гексана (87 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 110 мг.
ЯМР (1H, CD3OD): δ 8,95 (д,1H), 8,39 (д, 1H), 8,28 (т, 1H), 8,13 (д, 1H), 7,96 (д, 1H), 7,37 (м, 4H), 4,17 (д, 1H), 3,93 (д, 1H), 3,71 (м, 2H), 3,62 (с, 3H), 3,5 (2м, 4H), 3,04 (с, 3H), 2,37 (м, 2H), 2,27 (м, 1H), 1,55 (м, 1H), 1,31 (м, 1H). МС (m/z): 490 [MH]+.
Соединение, полученное в примере 29, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 25 × 0,46 см, элюент СО2, содержащий 25% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 199 бар, Т 36°С, УФ-детекция при 220 нм, петля 1 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Berger) с использованием хиральной колонки с Chiralpak AD-H, 25 × 0,46 см, элюент СО2, содержащий 25% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 180 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 13,5 мг. Rt = 24,3 мин. Чистота 87,6% a/a по УФ.
Энантиомер 2 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 5 мг, Rt = 26,5 мин. Чистота 100% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 30. Гидрохлорид (1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексана (205 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 246 мг.
ЯМР (1H, ДМСО): δ 10,33 (ушс, 1H), 8,58 (с, 1H), 7,43 (д, 2H), 7,36 (д, 2H), 4,04 (дд, 1H), 3,73 (дд, 1H), 3,7 (с, 3H), 3,6-3,2 (ушм, 6H), 2,39 (с, 3H), 2,2 (м, 3H), 1,61-1,16 (2т, 2H). МС (m/z): 480 [MH]+.
Соединение, полученное в примере 30, разделяют для получения отдельных энантиомеров методом полупрепаративной ВЭЖХ с использованием хиральной колонки с Chirapak AS-H, 25 × 2 см, элюент А - н-гексан; В - изопропанол, градиент изократный 15% В, об./об., скорость потока 7 мл/мин, УФ-детекция при 220 нм. Приведенные времена удерживания получают с использованием хиральной колонки с Chiralcel OD, 25 × 0,46 см, элюент А - н-гексан; В - изопропанол, градиент изократный 10% В, об./об., скорость потока 1 мл/мин, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 15 мг. Rt = 28,3 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (40 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 16 мг. Rt = 50,6 мин. Чистота >99% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 31. Гидрохлорид (1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-метил-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-[2-метил-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (71,5 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 46 мг.
ЯМР (1H, ДМСО): δ 10,25 (ушс, 1H), 8,58 (с, 1H), 7,6 (м, 3H), 3,97-3,7 (дд/м, 2H), 3,79/3,4 (дд/м, 2H), 3,69 (с, 3H), 3,27 (т, 2H), 2,5 (м, 2H), 2,48 (с, 3H), 2,38 (с, 3H), 2,2 (м, 1H), 2,13 (квинт, 2H), 1,61-1,01 (2т, 2H). МС (m/z): 478 [MH]+.
Пример 32. Не использован
Пример 33. Гидрохлорид (1S,5R/1R,5S)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексана (100 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 72 мг.
ЯМР (1н, ДМСО): δ 10,15 (ушс, 1H), 7,44 (д, 2H), 7,36 (д, 2Н), 4,04 (ушм, 1Н), 3,94 (дм, 2H), 3,73 (ушм, 1H), 3,55 (с, 3Н), 3,6-3,3 (ушм, 6H), 3,22 (т, 2H), 3,13 (т, 1Н), 2,23 (т, 1H), 2,,21 (м, 2H), 1,9-1,7 (м, 4H), 1,63-1,16 (2т, 2H). МС (m/z): 483 [МН]+.
Соединение, полученное в примере 33, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 25 × 2,1 см, элюент СО2, содержащий 8% смеси (2-пропанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 200 бар, Т 36°С, УФ-детекция при 220 нм. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Berger) с использованием хиральной колонки с Chiralpak AS-H, 25 × 0,46 см, элюент СО2, содержащий 8% смеси (2-пропанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 180 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (65 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 15 мг. Rt = 23,2 мин. Чистота 100% a/a по УФ.
Энантиомер 2 извлекают из рацемата (65 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 12 мг, Rt = 24,6 мин. Чистота 100% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 34. Гидрохлорид (1R,5S/1S,5R)-1-(3-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-(3-бромфенил)-3-азабицикло[3.1.0]гексана (140 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 23 мг, и очищая свободное основание названного в заголовке соединения препаративной ВЭЖХ с использованием колонки Х Terra MS C18, 5 мкм, 100 × 19 мм, элюент А - Н2О + 0,1% ТФК; В - CH3CN + 0,1% ТФК, градиент 10% (В) в течение 1 мин, от 10% (В) до 35% (В) за 12 мин, скорость потока 17 мл/мин, УФ-детекция при 200-400 нм. Приведенные времена удерживания получают с использованием колонки Х Terra MS C18, 5 мкм, 50 × 4,6 мм, элюент А - Н2О + 0,1% ТФК; В - CH3CN + 0,1% ТФК, градиент изократный 25% В, об./об., скорость потока 1 мл/мин, УФ-детекция при 200-400 нм. Rt = 6,26 мин. Чистота 96,4%, а/а по УФ.
ЯМР (1H, ДМСО): δ 9,9 (ушс, 1H), 8,58 (с, 1H), 7,57 (с, 1H), 7,47 (м, 1H), 7,3 (м, 2H), 4,04 (м, 1H), 3,75 (дд, 1H), 3,7-3,2 (м, 6H), 3,7 (с, 3H), 2,39 (с, 3H), 2,23 (м, 1H), 2,15 (м, 2H), 1,47 (т, 1H), 1,2 (т, 1H). МС (m/z): 512 [MH]+.
Пример 35. Гидрохлорид (1S,5R)-3-(1-метил-3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана

Смесь (1S,5R)-(3-хлор-1-метилпропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.0.1]гексана (препаративный пример 20, 105 мг), 4-метил-5-(4-метил-1,3-оксазол-5-ил)-2,4-дигидро-3Н-1,2,4-триазол-3-тиона (0,43 ммоль), ТЕА (0,46 ммоль) и NaI (0,43 ммоль) в ДМФА (безводный, 1,6 мл) греют при 60°С в течение 12 час. После удаления растворителя в вакууме остаток растворяют в этилацетате и органический слой промывают Н2О и сушат над Na2SO4. Полученный раствор концентрируют в вакууме, обрабатывают циклогексаном и фильтруют и получают 125 мг свободного основания названного в заголовке соединения. К раствору полученного вещества в дихлорметане (0,2 мл) добавляют 0,34 ммоль HCl (1 М раствор в Et2O), растворитель выпаривают в вакууме, вещество, полученное таким образом, обрабатывают Et2O и получают 105 мг названного в заголовке соединения в виде белого слабогигроскопичного твердого вещества.
МС (m/z): 478 [MH]+.
Соединение, полученное в примере 35, разделяют для получения отдельных диастереоизомеров методом полупрепаративной ВЭЖХ с использованием хиральной колонки с Chirapak AD, 25 × 2 см, элюент А - н-гексан; В - этанол + 0,1% изопропиламина, градиент изократный 15% В, об./об., скорость потока 7 мл/мин, УФ-детекция в интервале 220-400 нм. Приведенные времена удерживания получают с использованием хиральной колонки с Chirapak AD-Н, 25 × 0,46 см, элюент А - н-гексан; В - этанол + 0,1% изопропиламина, градиент изократный 17% В, об./об., скорость потока 1 мл/мин, УФ-детекция в интервале 220-400 нм.
Диастереоизомер 1 извлекают из смеси диастереомеров (105 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 30 мг. Rt = 17,9 мин. Чистота 99,4% a/a по УФ.
ЯМР (1H, ДМСО): δ 10,33 (ушс, 1H), 8,58 (с, 1H), 7,71 (д, 2H), 7,53 (д, 2H), 4,07 (дд, 1H), 3,78 (дд, 1H), 3,7 (с, 3H), 3,7 (м, 1H), 3,56 (ушс, 2H), 3,4 (м, 1H), 3,18 (м, 1H), 2,4 (с, 3Н), 2,4-2,3 (м, 1H), 2,26-2,09 (м, 2H), 1,72 (м, 1H), 1,42 (д, 3Н), 1,2 (м, 1H). МС (m/z): 478 [MH]+.
Диастереоизомер 2 извлекают из смеси диастереомеров (105 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 46 мг. Rt = 21,2 мин. Чистота >99% a/a по УФ.
ЯМР (1H, ДМСО): δ 10,26 (ушс, 1H), 8,58 (с, 1H), 7,7 (д, 2H), 7,51 (д, 2H), 4,14 (дд, 1H), 3,8-3,6 (м, 3H), 3,7 (с, 3H), 3,53 (ушс, 1H), 3,4 (м, 1H), 3,18 (м, 1H), 2,38 (с, 3H), 2,4-2,25 (м, 2H), 2,1 (м, 1H), 1,69 (м, 1H), 1,39 (д, 3H), 1,2 (м, 1H). МС (m/z): 478 [MH]+.
Пример 36. Гидрохлорид (1R,5S/1S,5R)-1-[2-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана
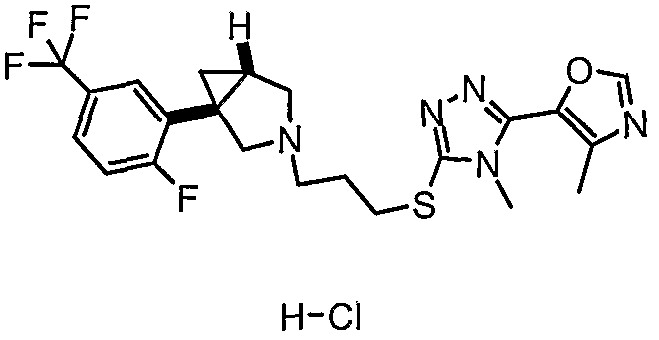
Названное в заголовке соединение получают из 1(1R,5S/1S,5R)-[2-фтор-5-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (109 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 144 мг.
ЯМР (1H, CD3OD): δ 8,41 (с,1H), 7,8 (м, 1H), 7,74 (м, 1H), 7,39 (т, 1H), 4,13 (д, 1H), 3,95 (д, 1H), 3,81 (с, 3H), 3,73 (ушд, 1H), 3,54 (д, 1H), 3,48 (м, 2H), 3,41 (м, 2H), 2,48 (с, 3H), 2,39 (м, 1H), 2,28 (кв, 2H), 1,58 (м, 1H), 1,35 (м, 1H). МС (m/z): 482 [MH]+.
Соединение, полученное в примере 36, разделяют для получения отдельных энантиомеров методом полупрепаративной ВЭЖХ с использованием хиральной колонки с Chirapak AS-H, 25 × 2 см, элюент А - н-гексан; В - изопропанол + 0,1% изопропиламина, градиент изократный 10% В, об./об., скорость потока 7 мл/мин, УФ-детекция при 220 нм. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Berger) с использованием хиральной колонки с Chiralpak AD-H, 25 × 0,46 см, элюент СО2, содержащий 7% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 180 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (138 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 48 мг. Rt = 21,2 мин. Чистота 100% a/a по УФ.
Энантиомер 2 извлекают из рацемата (138 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 46 мг. Rt = 22,7 мин. Чистота 99% a/a по УФ.
Энантиомер 2 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 1.
Пример 37. Гидрохлорид 1-[4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона
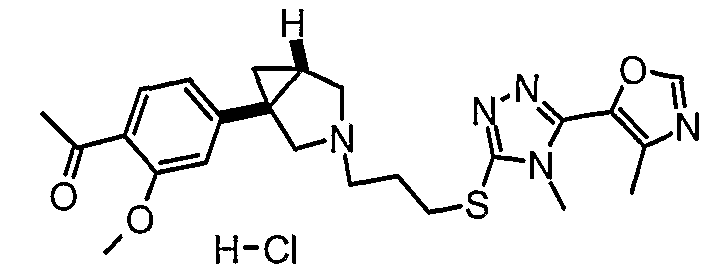
Названное в заголовке соединение получают из 1-[4-[(1S,5R/1R,5S)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона (87 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 70 мг.
ЯМР (1Н, CDCl3) соответствующего свободного основания: δ 8,0 (с, 1H), 7,7 (д, 1H), 6,7-6,8 (м, 2H), 3,9 (с, 3H), 3,7 (с, 3H), 3,35 (м, 4H), 3,1 (д, 1H), 2,6 (м, 3H), 2,55 (с, 3H), 2,5 (с, 3H), 2,45 (м, 1H), 2,0 (м, 2H), 1,75 (м, 1H), 0,8 (м, 1H). МС (m/z): 468 [MH]+.
Пример 38. Гидрохлорид 1-[4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанона

Названное в заголовке соединение получают из 1-[(1S,5R/1R,5S)-3-азабицикло[3.1.0]гекс-1-ил)-2-(метилокси)фенил]-1-пропанона (106 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 75 мг.
ЯМР (1Н, CDCl3) свободного основания: δ 7,9 (с, 1H), 6,65 (д, 1H), 6,7 (м, 2H), 3,9 (с, 3H), 3,7 (с, 3H), 3,35 (м, 3H), 3,1 (д, 1H), 2,9 (м, 2H), 2,6 (м, 3H), 2,5 (с, 3H), 2,45 (м, 1H), 2,0 (м, 2H), 1,8 (м, 1H), 1,1 (м, 3H), 0,8 (м, 1H). МС (m/z): 482 [MH]+.
Пример 39. Гидрохлорид (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-[2-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (53 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 7 мг.
ЯМР (1H, ДМСО): δ 10,48 (ушс, 1H), 8,55 (с, 1H), 7,9-7,6 (м, 4H), 3,9-3,1 (ушм, 8H), 3,68 (с, 3H), 2,36 (с, 3H), 2,13 (м, 2H), 1,66 (м, 1H), 1,2 (м, 1H), 1,1 (м, 1H). МС (m/z): 464[MH]+.
Пример 40. Гидрохлорид (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана
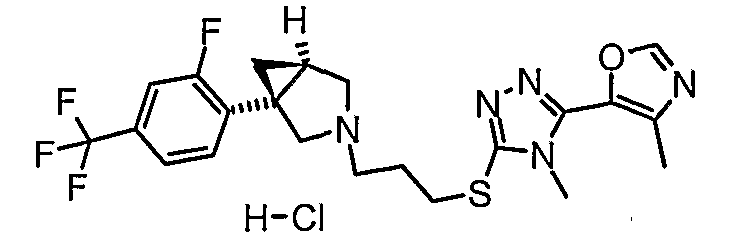
Свободное основание названного в заголовке соединения получают из (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана. Смесь (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (препаративный пример 39, 727 мг, 2,97 ммоль), 3-[(3-хлорпропил)тио]-4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазола (препаративный пример 14, 3,6 ммоль), K2CO3 (3,6 ммоль) и NaI (2,97 ммоль) в безводном ДМФА греют при 60°С в течение 24 час. После удаления растворителя в вакууме остаток растворяют в этилацетате и органический слой промывают насыщенным водным раствором NaHCO3 и сушат над Na2SO4. Полученный раствор фильтруют и фильтрат концентрируют в вакууме. Сырой продукт реакции очищают флэш-хроматографией (дихлорметан - 10% МеОН в дихлорметане) и получают 940 мг свободного основания названного в заголовке соединения.
Свободное основание (886 мг) превращают в соль гидрохлорид (847 мг) согласно способу, описанному в примере 1. Названное в заголовке соединение получают в виде белого твердого вещества. Аналитическая хиральная ВЭЖХ подтверждает, что продукт идентичен энантиомеру 2, полученному в примере 16.
Данные ЯМР и МС соответствуют данным, приведенным в примере 16.
Абсолютную конфигурацию названного в заголовке соединения подтверждают с использованием сравнительных анализов VCD и сравнительных анализов OR соответствующего свободного основания, представляющего собой (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан. В качестве эталона используют (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан (см. пример 14).
Удельное оптическое вращение соответствующего свободного основания [α]D = -42° (CDCl3, T = 25°C, c = 0,005 г/0,8 мл).
Примеры 41-52
К раствору соответствующего 3-тио-5-арил-1,2,4-триазола (полученного способом, аналогичным описанному в препаративном примере 13, 0,131 ммоль) в сухом ацетонитриле (2 мл) добавляют 2-трет-бутилимино-2-диэтиламино-1,3-диметилпергидро-1,3,2-диазафосфорин на полистироле (90 мг, 2,2 ммоль/г) и полученную смесь встряхивают в течение 30 минут при комнатной температуре. Добавляют (1S,5R)-3-(3-хлорпропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан (40 мг) и полученную смесь встряхивают при 70°С в течение трех часов. После охлаждения смеси смолу удаляют фильтрацией, промывают метанолом (2 мл) и затем удаляют растворитель при пониженном давлении. Осуществляют очистку с использованием масснаправленной ВЭЖХ с использованием колонки Waters XTerra Prep MS C18, 10 мкм, 30 × 150 мм, с использованием условий, указанных в таблице.
В = ACN + 0,1% муравьиной кислоты
Затем растворитель удаляют при пониженном давлении, и получают соответствующие соединения в виде солей формиатов. Остатки растворяют в метаноле (1 мл) и загружают в картриджи SCX SPE (1 г), промывают метанолом (3 мл) и элюируют 2 М раствором аммиака в метаноле (3 мл), и затем растворитель удаляют при пониженном давлении. Остатки растворяют в дихлорметане (1 мл), добавляют 1,0 М раствор HCl в диэтиловом эфире (0,131 ммоль), затем растворитель удаляют при пониженном давлении и получают продукты реакций - соединения в виде гидрохлоридов, сведенные в табл.1.
Условия аналитической хроматографии
Колонка X Terra MS C18, 5 мм, 50 х 4,6 мм;
подвижная фаза: А - раств. NH4HCO3, 10 мМ, рН 10; В - CH3CN;
градиент: 10% (В) в течение 1 мин, от 10% (В) до 95% (В) за 12 мин, 95% (В) в течение 3 мин;
скорость потока 1 мл/мин;
интервал длин волн УФ 210-350 нм;
интервал масс 100-900 amu;
ионизация ES+.

ЯМР (19F, ДМСО): δ -60,8.
МС (m/z): 474 [MH]+.
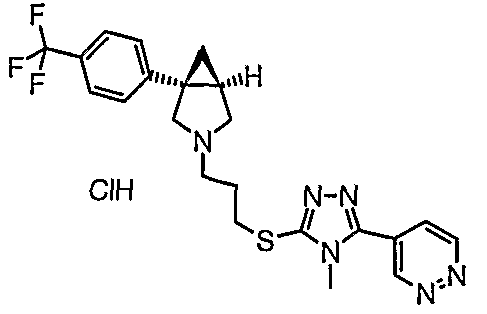
МС (m/z): 461 [MH]+.


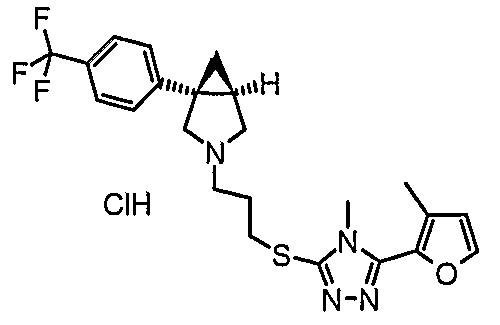
МС (m/z): 463 [MH]+.



МС (m/z): 475 [MH]+.


МС (m/z): 524 [MH]+.
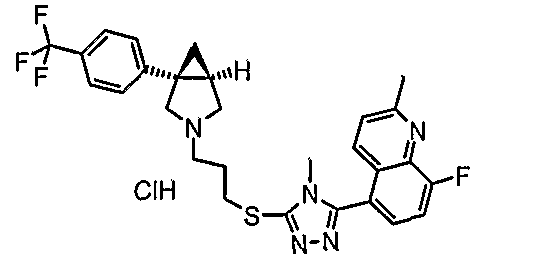

Примеры 53-58
К раствору соответствующего 3-тио-5-арил-1,2,4-триазола (0,124 ммоль) в сухом ацетонитриле (2 мл) добавляют 2-трет-бутилимино-2-диэтиламино-1,3-диметилпергидро-1,3,2-диазафосфорин на полистироле (85 мг, 2,2 ммоль/г) и полученную смесь встряхивают в течение 30 минут при комнатной температуре, затем добавляют (1S,5R)-3-(3-хлорпропил)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан (40 мг) и полученную смесь встряхивают при 50°С в течение ночи. После охлаждения смеси смолу удаляют фильтрацией, промывают метанолом (2 мл) и затем удаляют растворитель при пониженном давлении. Осуществляют очистку с использованием масснаправленной ВЭЖХ.
Условия препаративной хроматографии (преп. ВЭЖХ 6 из 6 соединений)
Колонка X Terra MS C18, 5 мм, 100 × 19 мм;
подвижная фаза: А - раств. NH4HCO3, 10 мМ, рН 10; В - CH3CN;
градиент: 30% (В) в течение 1 мин, от 30% (В) до 95% (В) за 9 мин, 95% (В) в течение 3 мин;
скорость потока 17 мл/мин;
интервал длин волн УФ 210-350 нм;
интервал масс 100-900 amu;
ионизация ES+.
Затем растворитель удаляют при пониженном давлении и получают соединения в виде свободных оснований. Остатки растворяют в дихлорметане (2 мл), добавляют 1,0 М раствор HCl в диэтиловом эфире (0,124 ммоль), затем растворитель удаляют при пониженном давлении и получают продукты реакций - соединения в виде гидрохлоридов, сведенные в табл.2.
Условия аналитической хроматографии
Колонка X Terra MS C18, 5 мм, 50 × 4,6 мм;
подвижная фаза: А - раств. NH4HCO3, 10 мМ, рН 10; В - CH3CN;
градиент: 30% (В) в течение 1 мин, от 30% (В) до 95% (В) за 9 мин, 95% (В) в течение 3 мин;
скорость потока 1 мл/мин;
интервал длин волн УФ 210-350 нм;
интервал масс 100-900 amu;
ионизация ES+.

МС (m/z): 492 [MH


МС (м/z): 479 [MH]+.

МС (m/z):512 [MH]+

МС (m/z): 493 [MH

МС (м/z): 545 [MH
Пример 59. Гидрохлорид 1-{4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}-2-пирролидинона
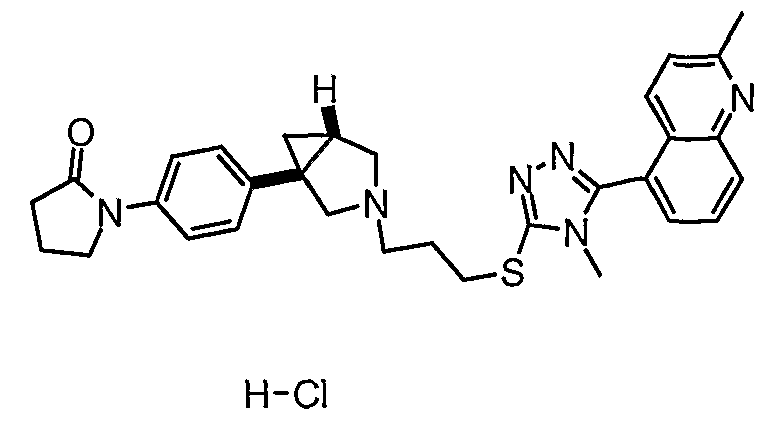
В пробирку Шленка загружают 5-[5-({3-[(1R,5S/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин (сравн. пример 2; 0,15 г), 2-пирролидинон (32 мг), трис(дибензилиденацетон)дипалладий(0) (6 мг), 4,5-бис(дифенилфосфино)-9,9-диметилксантен (10 мг), карбонат цезия (130 мг) и 1,4-диоксан (2 мл). Пробирку Шленка герметично закрывают тефлоновой завинчивающейся крышкой и реакционную смесь перемешивают при 100°С в течение 12 час. Реакционную смесь охлаждают до комнатной температуры, разбавляют дихлорметаном (10 мл), фильтруют и концентрируют в вакууме. Сырой продукт реакции очищают флэш-хроматографией (от дихлорметана до 10% МеОН в дихлорметане) и получают 60 мг свободного основания названного в заголовке соединения. К раствору полученного вещества в дихлорметане (0,4 мл) добавляют HCl (0,11 мл, 1 М раствор в Et2O), растворитель выпаривают в вакууме, вещество, полученное таким образом, обрабатывают Et2O и получают 64 мг названного в заголовке соединения в виде белого твердого вещества.
ЯМР (1H, ДМСО): δ 10,48 (ушс, 1H), 8,24 (ушд, 1H), 8,18 (д, 1H), 7,93 (т, 1H), 7,81 (д, 1H), 7,62 (д, 2H), 7,54 (д, 1H), 7,31 (д, 2H), 4,04 (дд, 1H), 3,82 (т, 2H), 3,76 (дд, 1H), 3,70/3,10 (ушм, 8H), 3,45 (с, 3H), 2,74 (с, 3H), 2,25 (м, 2H), 2,16 (м, 1H), 2,07 (м, 2H), 1,63/1,10 (т/т, 2H). МС (m/z): 539 [MH]+.
Пример 60. Гидрохлорид 5-{5-[(3-{(1R,5S/1S,5R)-1-[4-(1,1-диоксидо-2-изотиазолидинил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолина
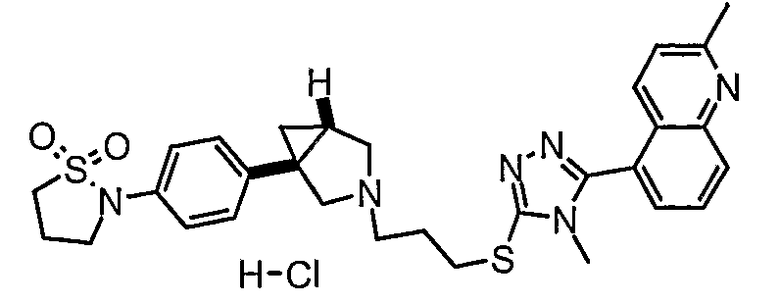
В пробирку Шленка загружают 5-[5-({3-[(1R,5S/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин (сравн. пример 2; 0,15 г), 1,1-диоксид изотиазолидина (46 мг), трис(дибензилиденацетон)дипалладий(0) (6 мг), 4,5-бис(дифенилфосфино)-9,9-диметилксантен (10 мг), карбонат цезия (130 мг) и 1,4-диоксан (2 мл). Пробирку Шленка герметично закрывают тефлоновой завинчивающейся крышкой и реакционную смесь перемешивают при 100°С в течение 12 час. Реакционную смесь охлаждают до комнатной температуры, разбавляют дихлорметаном (10 мл), фильтруют и концентрируют в вакууме. Сырой продукт реакции очищают флэш-хроматографией (от дихлорметана до 10% МеОН в дихлорметане) и получают 50 мг свободного основания названного в заголовке соединения. К раствору полученного вещества в дихлорметане (0,3 мл) добавляют HCl (0,087 мл, 1 М раствор в Et2O), растворитель выпаривают в вакууме, вещество, полученное таким образом, обрабатывают Et2O и получают 52 мг названного в заголовке соединения в виде белого твердого вещества.
ЯМР (1H, ДМСО): δ 10,57 (ушс, 1H), 8,27 (ушд, 1H), 8,19 (д, 1H), 7,94 (т, 1H), 7,82 (д, 1H), 7,55 (д, 1H), 7,32 (д, 2H), 7,18 (д, 2H), 4,03 (дд, 1H), 3,72 (м, 3H), 3,60/3,20 (ушм, 8H), 3,45 (с, 3H), 2,75 (с, 3H), 2,41 (м, 2H), 2,25 (м, 2H), 2,14 (м, 1H), 1,66/1,10 (т/м, 2H). МС (m/z): 575 [MH]+.
Пример 61. Гидрохлорид (1R,5S/1S,5R)-1-[3-фтор-4-(трифторметил)фенил]-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-[3-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (338 мг) способом, аналогичным описанному в примере 1, с выходом 247 мг.
ЯМР (1H, CD3OD): δ 8,4 (с, 1H), 7,55 (т, 1H), 7,37 (д, 1H), 7,32 (д, 1H), 4,2 (д, 1H), 3,91 (д, 1H), 3,81 (с, 3H), 3,76 (д, 1H), 3,67 (д, 1H), 3,51 (т, 2H), 3,43 (т, 2H), 2,47 (с, 3H), 2,41 (м, 1H), 2,31 (м, 2H), 1,61 (т, 1H), 1,45 (т, 1H). МС (m/z): 496 [MH]+.
Соединение, полученное в примере 61, разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 25 × 2,1 см, элюент СО2, содержащий 12% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 194 бар, Т 36°С, УФ-детекция при 220 нм. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Berger) с использованием хиральной колонки с Chiralpak AD-H, 25 х 0,46 см, элюент СО2, содержащий 10% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 180 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (100 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 42 мг. Rt = 27,1 мин. Чистота 100% a/a по УФ.
Энантиомер 2 извлекают из рацемата (100 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 34 мг, Rt = 31,0 мин. Чистота 100% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 2 log-единицы выше, чем энантиомер 2.
Пример 62. Гидрохлорид 1-(2-(метилокси)-5-{(1R,5S/1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанона
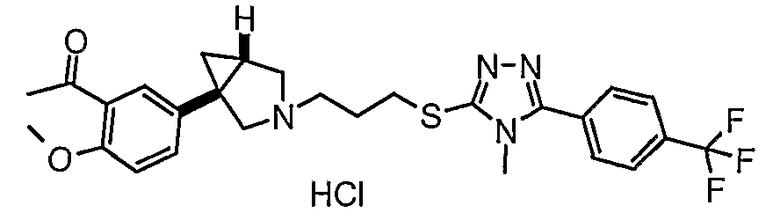
Названное в заголовке соединение получают в виде белого твердого вещества с выходом 51 мг (выход = 60%) способом, аналогичным описанному в примере 1, из 1-[5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона (35 мг) и 3-[(3-хлорпропил)тио]-4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазола (60 мг, получен способом, аналогичным описанному в препаративном примере 13).
ЯМР (1H, CDCl3, свободное основание): δ 7,80-7,70 (м, 4H), 7,50 (с, 1H), 7,27-7,20 (м, 1H), 6,85 (д, 1H), 3,86 (с, 3H), 3,62 (с, 3H), 3,40-3,24 (м, 3H), 3,15 (д, 1H), 2,58 (с, 3H), 2,65-2,55 (м, 2H), 2,54-2,45 (м, 2H), 2,10-1,90 (квинт, 2H), 1,65-1,57(м, 1H), 1,35 (м, 1H), 0,75 (м, 1H). МС (m/z):531 [MH]+.
Пример 63. Гидрохлорид 1-[5-[(1R,5S/1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона
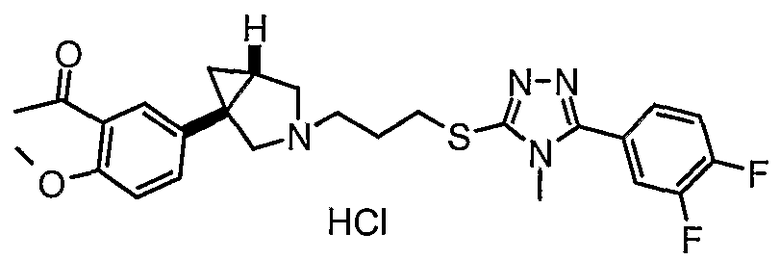
Названное в заголовке соединение получают в виде белого твердого вещества с выходом 40 мг (выход = 50%) способом, аналогичным описанному в примере 1, из 1-[5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона (35 мг) и 3-[(3-хлорпропил)тио]-5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазола (54 мг, получен способом, аналогичным описанному в препаративном примере 13).
ЯМР (1H, CDCl3, свободное основание): δ 7,56-7,19 (м, 5H), 6,84 (д, 1H), 3,86 (с, 3H), 3,62 (с, 3H), 3,38-3,24 (м, 3H), 3,10 (д, 1H), 2,58 (с, 3H), 2,65-2,42 (м, 4H), 2,10-1,90 (квинт, 2H), 1,65-1,57(м, 1H), 1,35 (м, 1H), 0,75 (м, 1H). МС (m/z): 499 [MH]+.
Пример 64. Гидрохлорид 1-{2-(метилокси)-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанона
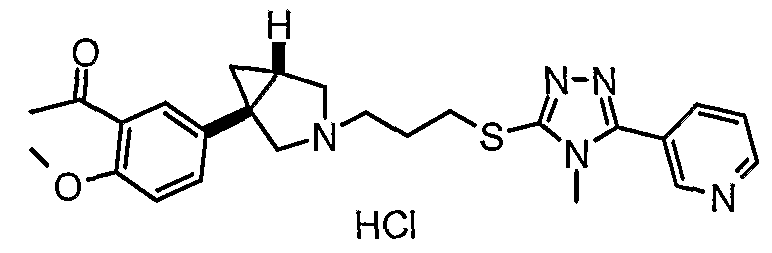
Названное в заголовке соединение получают в виде желтого твердого вещества с выходом 32 мг (выход = 42%) способом, аналогичным описанному в примере 1, из 1-[5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона (35 мг) и 3-{5-[(3-хлорпропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил}пиридина (48 мг, получен способом, аналогичным описанному в препаративном примере 13).
ЯМР (1H, CDCl3, свободное основание): δ 8,87 (с, 1H), 8,70 (д, 1H), 8,0 (д, 1H), 7,48 (с, 1H), 7,43 (м, 1H), 7,23 (м, 1H), 6,84 (д, 1H), 3,86 (с, 3H), 3,62 (с, 3H), 3,40-3,25 (м, 3H), 3,10 (д, 1H), 2,58 (с, 3H), 2,67-2,42 (м, 4H), 2,10-1,90 (квинт, 2H), 1,65-1,57(м, 1H), 1,35 (м, 1H), 0,75 (м, 1H). МС (m/z): 464 [MH]+.
Пример 65. Гидрохлорид 1-[5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицило[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона

Названное в заголовке соединение получают в виде желтого твердого вещества с выходом 50 мг (выход = 60%) способом, аналогичным описанному в примере 1, из 1-[5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона (35 мг) и 5-{5-[(3-хлорпропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил}-2-метилхинолина (60 мг).
ЯМР (1H, CDCl3, свободное основание): δ 10,38 (ушс,1H), 8,2 (м, 2H), 7,91 (т, 1H), 7,78 (д, 1H), 7,5 (м, 3H), 7,17 (д, 1H), 4,02 (д, 1H), 3,89 (с, 3H), 3,74 (дд, 1H), 3,6-3,2 (м, 6H), 3,45 (с, 3H), 2,72 (с, 3H), 2,5 (с, 3H), 2,23 (квинт, 2H), 2,11 (квинт, 1H), 1,57 (т, 1H), 1,1 (т, 1H). МС (m/z): 528 [MH]+.
Пример 66. Гидрохлорид 1-{2-(метилокси)-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанона

Названное в заголовке соединение получают в виде белого твердого вещества с выходом 24 мг (выход = 32%) способом, аналогичным описанному в примере 1, из 1-[5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанона (35 мг) и 3-[(3-хлорпропил)тио]-4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазола (50 мг, получен способом, аналогичным описанному в препаративном примере 13).
ЯМР (1H, CDCl3, свободное основание): δ 7,49 (с, 1H), 7,24 (м, 1H), 6,85 (д, 1H), 4,14-4,05 (м, 2H), 3,86 (с, 3H), 3,62 (с, 3H), 3,57-3,40 (м, 2H), 3,29-3,15 (м, 3H), 3,05 (д, 1H), 2,82-2,95 (м, 1H), 2,63-2,40 (м, 4H), 2,58 (с, 3H), 2,15-1,77 (м, 6H), 1,62 (м, 1H), 1,32 (м, 1H), 0,70 (м, 1H). МС (m/z); 471 [MH]+.
Пример 67. Гидрохлорид 1-(2-гидрокси-5-{(1R,5S/1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанона

Названное в заголовке соединение получают в виде белого твердого вещества с выходом 35 мг (выход = 33%) способом, аналогичным описанному в примере 1, из 1-{5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанона (43 мг) и 3-[(3-хлорпропил)тио]-4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазола (80 мг, получен способом, аналогичным описанному в препаративном примере 13).
ЯМР (1H, CDCl3, свободное основание): δ 12,2 (с, 1H), 7,80-7,70 (м, 4H), 7,50 (с, 1H), 7,30 (м, 5 1H), 6,88 (д, 1H), 3,86 (с, 3H), 3,40-3,25 (м, 3H), 3,10 (д, 1H), 2,58 (с, 3H), 2,65-2,35 (м, 4H), 2,0 (квинт, 2H), 1,58 (м, 1H), 1,35 (м, 1H), 0,70 (м, 1H). МС (m/z): 517 [MH]+.
Пример 68. Гидрохлорид 1-{5-[(1R,5S/1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанона

Названное в заголовке соединение получают в виде белого твердого вещества с выходом 27 мг (выход = 29%) способом, аналогичным описанному в примере 1, из 1-{5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанона (40 мг) и 3-[(3-хлорпропил)тио]-5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазола (67 мг, получен способом, аналогичным описанному в препаративном примере 13).
ЯМР (1H, ДМСО): δ 11,82 (с,1H), 10,26 (ушс, 1H), 7,85 (м, 1H), 7,76 (д, 1H), 7,67 (м, 1H), 7,61 (м, 1H), 7,51 (дд, 1H), 6,97 (д, 1H), 4,02 (дд, 1H), 3,74 (дд, 1H), 3,64 (с, 3H), 3,55 (м, 2H), 3,3 (м, 4H), 2,67 (с, 3H), 2,15 (м, 3H), 1,52 (т, 1H), 1,13 (т, 1H). МС (m/z): 485 [MH]+.
Пример 69. Гидрохлорид 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанона

Названное в заголовке соединение получают в виде белого твердого вещества с выходом 36 мг (выход = 43%) способом, аналогичным описанному в примере 1, из 1-{5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанона (38 мг) и 3-[(3-хлорпропил)тио]-4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазола (57 мг).
ЯМР (1H, CDCl3, свободное основание): δ 12,2 (с, 1H), 7,88 (с, 1H), 7,50 (с, 1H), 7,24 (м, 1H), 6,58 (д, 1H), 3,68 (с, 3H), 3,32 (м, 3H), 3,10 (д, 1H), 2,58-2,47 (м, 4H), 2,58 (с, 3H), 2,47 (с, 3H), 2,0 (м, 2H), 1,62 (м, 1H), 1,35 (м, 1H), 0,68 (м, 1H). МС (m/z): 454 [MH]+.
Пример 70. Гидрохлорид 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанона

Названное в заголовке соединение получают в виде желтого твердого вещества с выходом 24 мг (выход = 32%) способом, аналогичным описанному в примере 1, из 1-{5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанона (30 мг) и 5-{5-[(3-хлорпропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил}-2-метилхинолина (55 мг).
ЯМР (1H, CDCl3, свободное основание): δ 12,1 (с, 1H), 8,10 (дд, 2H), 7,67 (т, 1H), 7,50 (м, 2H), 7,23 (м, 2H), 6,85 (д, 1H), 3,45-3,23 (м, 3H), 3,40 (с, 3H), 3,08 (д, 1H), 2,67 (с, 3H), 2,65-2,41 (м, 4H), 2,55 (с, 3H), 2,02 (м, 2H), 1,58 (м, 1H), 1,32 (м, 1H), 0,64 (м, 1H). МС (m/z): 514 [MH]+.
Пример 71. Гидрохлорид 1-[5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанона

Названное в заголовке соединение получают в виде белого твердого вещества с выходом 51 мг (выход = 47%) способом, аналогичным описанному в примере 1, из 1-[5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанона (52 мг, получен способом, аналогичным способам, описанным в препаративных примерах 43-45) и 3-[(3-хлорпропил)тио]-4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазола (69 мг).
ЯМР (1H, ДМСО): δ 10,24 (ушс, 1H), 8,52 (м, 1H), 7,42 (д, 1H), 7,40 (дд, 1H), 7,08 (д, 1H), 3,93 (дд, 1H), 3,81 (с, 3H), 3,67 (дд, 1H), 3,64 (с, 3H), 3,48 (м, 2H), 3,28 (м, 2H), 3,22 (т, 2H), 2,86 (q, 2H), 2,33 (с, 3H), 2,1 (м, 2H), 2,03 (м, 1H), 1,48 (т, 1H), 1,0 (т, 1H), 1,04 (т, 3H). МС (m/z): 482 [MH]+.
Названное в заголовке соединение разделяют для получения отдельных энантиомеров методом полупрепаративной ВЭЖХ с использованием хиральной колонки с Chiralpak AS-H, 5 мкм, 250 х 21 мм, элюент А - н-гексан; В - этанол + 0,1% изопропиламина, градиент изократный 40% В, скорость потока 7 мл/мин, УФ-детекция при 200-400 нм. Приведенные времена удерживания получают с использованием аналитической ВЭЖХ с использованием хиральной колонки с Chiralpak AS-Н, 5 мкм, 250 х 4,6 мм, элюент А - н-гексан; В - этанол + 0,1% изопропиламина, градиент изократный 40% В, скорость потока 0,8 мл/мин, УФ-детекция при 200-400 нм.
Энантиомер 1 извлекают из рацемата (66 мг) в виде белого твердого вещества с выходом 10 мг (выход = 30%). Rt = 17,2 мин.
Энантиомер 2 извлекают из рацемата (66 мг) в виде белого твердого вещества с выходом 10 мг (выход = 30%). Rt = 19,1 мин.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 72. Гидрохлорид 2-метил-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазола

Получают 5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-метил-1,3-бензотиазол из дигидрохлорида 2-метил-1,3-бензотиазол-5-амина способом, аналогичным способам, описанным в препаративных примерах 15, 16 и 17. Из полученного вещества получают названное в заголовке соединение в виде желтого твердого вещества, следуя способам, описанным в примерах 14 и 15.
ЯМР (1H, ДМСО): δ 10,54 (ушс, 1H), 8,58 (м, 1H), 8,0 (д, 1H), 7,9 (д, 1H), 7,34 (дд, 1H), 10 4,0 (дд, 1H), 3,75 (дд, 1H), 3,70 (с, 3H), 3,65 (м, 1H), 3,57 (м, 1H), 3,35 (м, 2H), 3,30 (т, 2H), 2,8 (с, 3H), 2,39 (с, 3H), 2,27 (м, 1H), 2,19 (м, 2H), 1,7 (т, 1H), 1,19 (т, 1H). МС (m/z): 467 [MH]+.
Названное в заголовке соединение разделяют для получения отдельных энантиомеров методом полупрепаративной ВЭЖХ с использованием хиральной колонки с Chiralpak AS-H, 5 мкм, 250 × 21 мм, элюент А - н-гексан; В - этанол + 0,1% изопропиламина, градиент изократный 13% В, скорость потока 7 мл/мин, УФ-детекция при 200-400 нм. Приведенные времена удерживания получают с использованием аналитической ВЭЖХ с использованием хиральной колонки с Chiralpak AS-Н, 5 мкм, 250 х 4,6 мм, элюент А - н-гексан; В - этанол + 0,1% изопропиламина, градиент изократный 13% В, скорость потока 1 мл/мин, УФ-детекция при 200-400 нм.
Энантиомер 1 извлекают из рацемата (55 мг) в виде белого твердого вещества с выходом 17 мг (выход = 62%). Rt = 17,1 мин.
Энантиомер 2 извлекают из рацемата (55 мг) в виде белого твердого вещества с выходом 18 мг (выход = 65%). Rt = 19,3 мин.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 73. Гидрохлорид 2-метил-6-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазола

Получают 6-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-2-метил-1,3-бензотиазол из 2-метил-1,3-бензотиазол-6-амина способом, аналогичным способам, описанным в препаративных примерах 15, 16 и 5. Из полученного вещества получают названное в заголовке соединение в виде желтого твердого вещества, следуя способам, описанным в примерах 14 и 15.
ЯМР (1H, CD3OD): δ 8,39 (с,1H), 7,98 (д, 1H), 7,89 (д, 1H), 7,5 (дд, 1H), 4,19 (д, 1H), 3,92 (д, 1H), 3,8 (с, 3H), 3,72 (д, 2H), 3,52 (т, 2H), 3,42 (т, 2H), 2,85 (с, 3H), 2,47 (с, 3H), 2,31 (м, 3H), 1,54 (т, 1H), 1,41 (т, 1H). МС (m/z): 467 [МН]+.
Пример 74. Гидрохлорид 1-метил-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1Н-индазола

Получают 5-[(1R,5S/1S,5R)-3-азабицикло[3.1.0]гекс-1-ил]-1-метил-1Н-индазол из 1-метил-1Н-индазол-5-амина способом, аналогичным способам, описанным в препаративных примерах 15, 16 и 5. Из полученного вещества получают названное в заголовке соединение в виде желтого твердого вещества, следуя способам, описанным в примерах 14 и 15.
ЯМР (1H, ДМСО): δ 10,4 (ушс,1H), 8,58 (м, 1H), 8,01 (с, 1H), 7,70 (д, 1H), 7,63 (д, 1H), 7,39 (дд, 1H), 4,05 (м, 1H), 4,04 (с, 3H), 3,75 (д, 1H), 3,70 (с, 3H), 3,59 (м, 2H), 3,39 (т, 2H), 3,26 (т, 2H), 2,39 (с, 3H), 2,18 (м, 3H), 1,61 (т, 1H), 1,14 (т, 1H). МС (m/z): 450 [MH]+.
Названное в заголовке соединение разделяют для получения отдельных энантиомеров методом полупрепаративной SFC (Gilson) с использованием хиральной колонки с Chiralpak AS-H, 250 × 21 мм, модификатор: этанол + 0,1% изопропиламина 12%, скорость потока 22 мл/мин, Р 200 бар, Т 36°С, УФ-детекция при 220 нм. Приведенные времена удерживания получают с использованием аналитической SFC (Berger) с использованием хиральной колонки с Chiralpak AS-Н, 5 мкм, 250 × 4,6 мм, модификатор: этанол + 0,1% изопропиламина 12%, скорость потока 2,5 мл/мин, Р 180 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (80 мг) в виде белого твердого вещества с выходом 25 мг (выход = 62%). Rt = 19,5 мин.
Энантиомер 2 извлекают из рацемата (80 мг) в виде белого твердого вещества с выходом 28 мг (выход = 70%). Rt = 22,8 мин.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 75. Гидрохлорид (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексана

Получают (1R,5S/1S,5R)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан из 6-(трифторметил)-3-пиридинамина способом, аналогичным способам, описанным в препаративных примерах 37 и 5. Из полученного вещества получают названное в заголовке соединение в виде желтого твердого вещества, следуя способам, описанным в примерах 14 и 15.
ЯМР (1H, ДМСО): δ 10,46 (ушс, 1H), 8,73 (ушс, 1H), 8,58 (м, 1H), 8,0 (дд, 1H), 7,90 (д, 1H), 4,12 (м, 1H), 3,78 (д, 1H), 3,70 (с, 3H), 3,7 (м, 1H), 3,54 (м, 1H), 3,39 (т, 2H), 3,29 (с, 2H), 2,39 (м, 3H), 2,47 (м, 1H), 2,18 (м, 2H), 1,71 (м, 1H), 1,33 (м, 1H). ЯМР (19F, ДМСО): δ -66,2 (с). МС (m/z): 465 [MH]+.
Примеры 76-94
К раствору соответствующего 3-тио-5-арил-1,2,4-триазола (полученного способом, аналогичным описанному в препаративном примере 13, 0,063 ммоль) в сухом ацетонитриле (2 мл) добавляют 2-трет-бутилимино-2-диэтиламино-1,3-диметилпергидро-1,3,2-диазафосфорин на полистироле (43 мг, 2,2 ммоль/г), и полученную смесь встряхивают в течение 1 часа при комнатной температуре, затем добавляют (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-хлорпропил)-3-азабицикло[3.1.0]гексан (20 мг) и полученную смесь встряхивают при 70°С в течение 3,5 часов. После охлаждения смеси смолу удаляют фильтрацией, промывают дихлорметаном (2 мл) и метанолом (2 мл) и собранную жидкую фазу упаривают при пониженном давлении. Образуются два изомера за счет S- и N-алкилирования, причем главным изомером является нужный S-алкилированный изомер. Полученные изомеры разделяют с использованием масснаправленной ВЭЖХ с использованием колонки Waters XTerra Prep MS C18, 10 мкм, 30 × 150 мм, с использованием условий, указанных в таблице.
А = Н2О + 0,1% муравьиной кислоты
В = ацетонитрил + 0,1% муравьиной кислоты
Затем растворитель удаляют при пониженном давлении и получают названные в заголовках соединения в виде солей формиатов.
В случае примеров 93 и 94 изомеры разделяют флэш-хроматографией на силикагеле. S-Алкилированные изомеры растворяют в сухом диэтиловом эфире и охлаждают при 0°С. Постепенно добавляют 1,2 экв. HCl (в виде 1,0 М раствора в диэтиловом эфире). Полученное выпавшее в осадок вещество декантируют, промывают пентаном и отфильтровываю, и получают продукты реакций в виде солей гидрохлоридов.
Условия аналитической хроматографии
Примеры 76-90
Пример 91
Пример 93
Пример 94
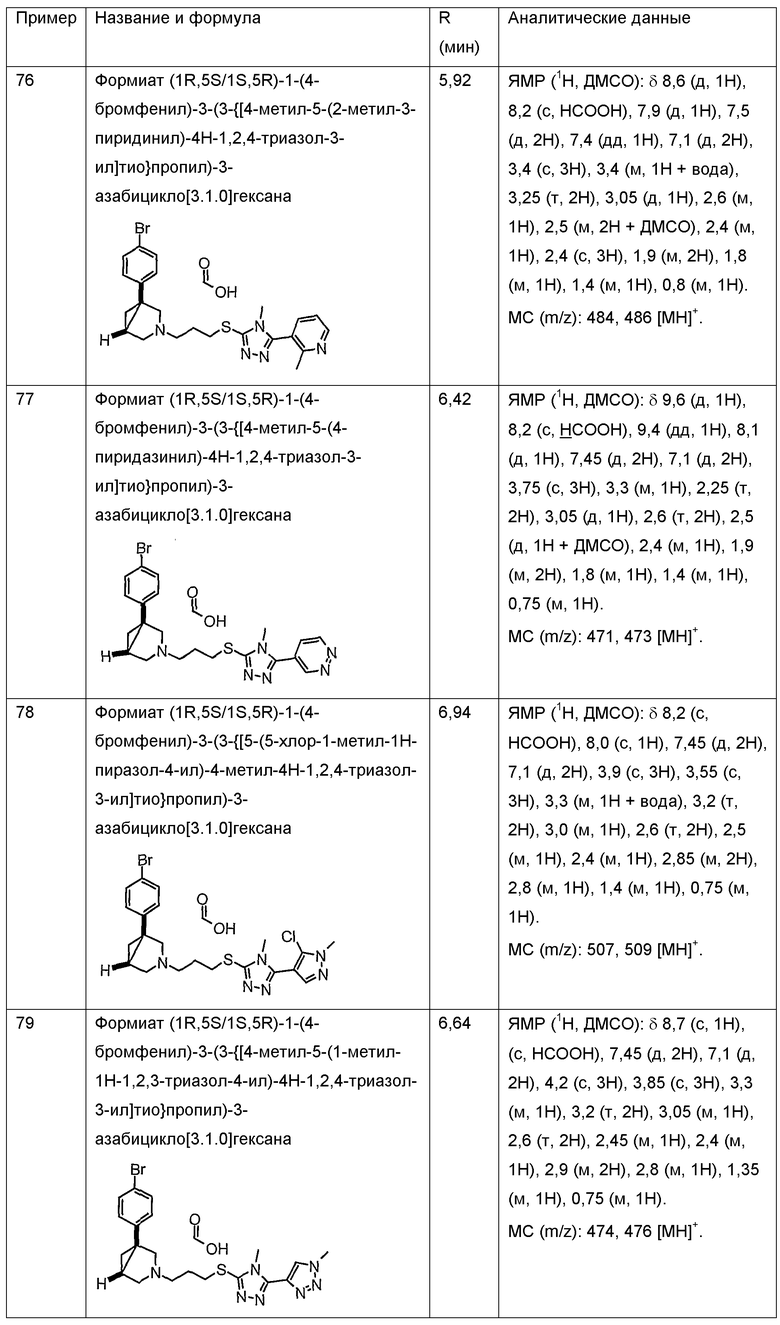

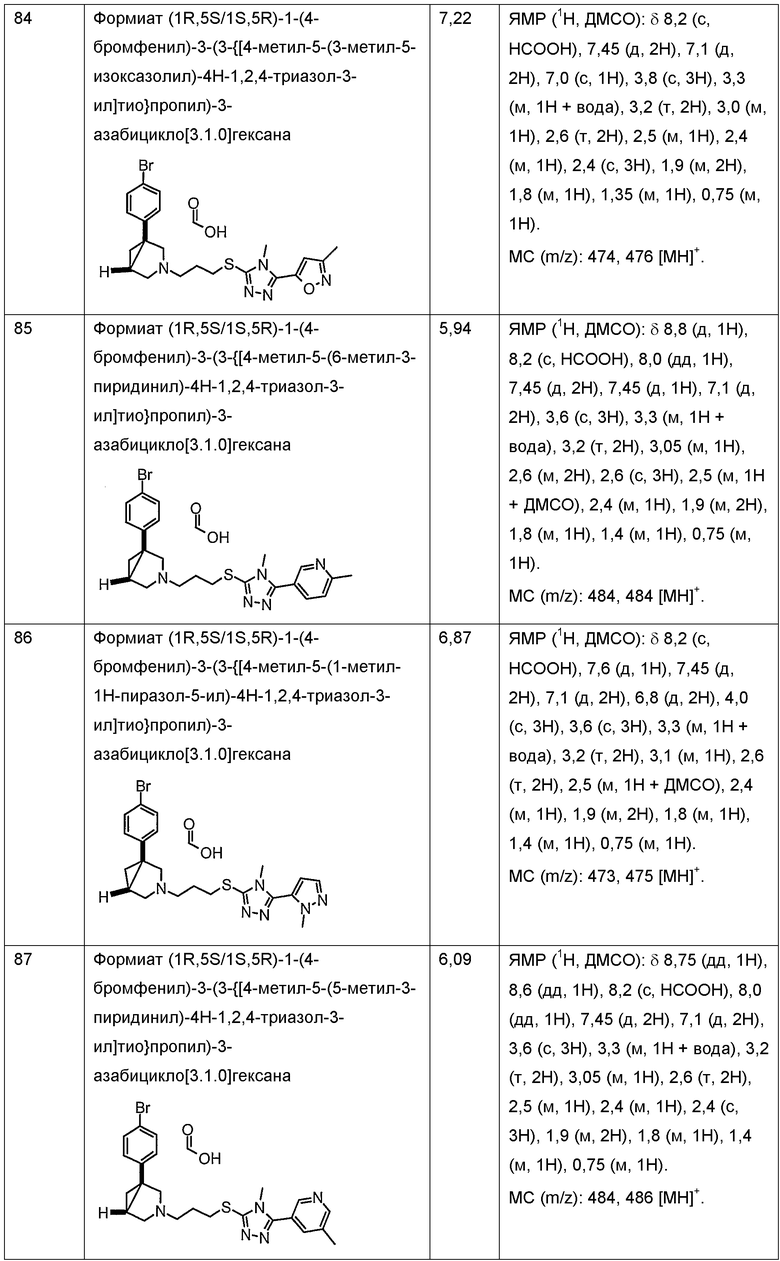

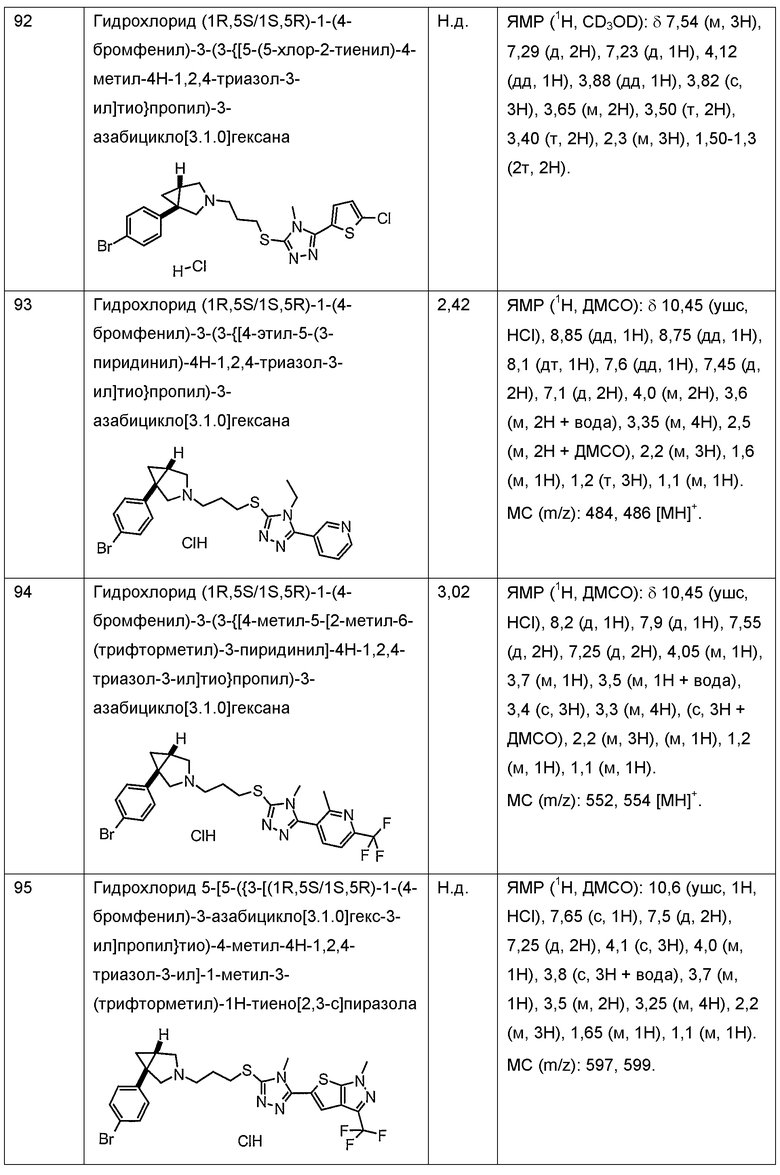
Пример 96. Гидрохлорид 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R/1S,5S)-1-[5-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексана
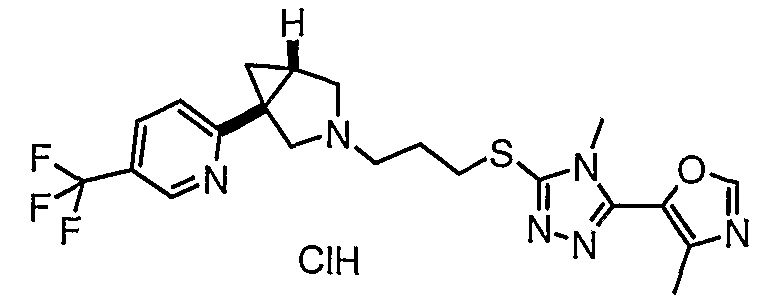
Названное в заголовке соединение получают из 1-[5-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексана способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества (70 мг, 45%).
ЯМР (соответствующий свободному основанию, 1Н, CD3OD): δ 8,71 (с, 1H), 7,93 (с, 1H), 7,78 (дд, 1H), 7,15 (д, 1H), 3,72 (с, 3H), 3,41 (д, 1H), 3,36 (т, 2H), 3,13 (д, 1H), 2,8 (д, 1H), 2,68 (м, 2H), 2,54 (с, 3H), 2,48 (дд, 1H), 2,04 (м, 3H), 1,6 (м, 1H), 1,26 (дд, 1H). МС (m/z): 465 [MH]+.
Соединение, полученное в примере 96, разделяют для получения отдельных энантиомеров методом полупрепаративной ВЭЖХ с использованием хиральной колонки с Chirapak AD-H, 5 мкм, 250 × 4,6 мм, элюент А - н-гексан; В - этанол + 0,1% изопропиламина, градиент изократный 30% В, об./об., скорость потока 6 мл/мин, УФ-детекция при 270 нм. Приведенные времена удерживания получают с использованием хиральной колонки с Chirapak AD-Н, 5 мкм, 250 × 4,6 мм, элюент А - н-гексан; В - этанол, градиент изократный 30% В, об./об., скорость потока 0,8 мл/мин, УФ-детекция при 200-400 нм.
Энантиомер 1 извлекают из рацемата (70 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 18 мг. Rt = 19,09 мин. Чистота 100% а/а по УФ.
Энантиомер 2 извлекают из рацемата (70 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 18 мг. Rt = 21,6 мин. Чистота 99% а/а по УФ.
Энантиомер 2 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 1.
Пример 97. Дигидрохлорид 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R/1S,5S)-1-[6-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексана

3-(Фенилметил)-1-[5-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан (0,19 ммоль) растворяют в 1,2-дихлорэтане (1 мл) и добавляют 1-хлорэтилхлордикарбонат (0,21 ммоль). После двух циклов воздействия частот микроволнового диапазона (5 мин при 120°С и 10 мин при 140°С) растворитель удаляют при пониженном далении. Добавляют метанол (2 мл) и раствор подвергают воздействию дополнительного микроволнового цикла (10 мин, 120°С). Растворитель удаляют при пониженном давлении и получают 47 мг промежуточного соединения, которое используют без дополнительной очистки и обрабатывают способом, аналогичным описанному в примере 1, и получают названное в заголовке соединение (5 мг, 5%) в виде белого слабогигроскопичного вещества.
ЯМР (1H, CD3OD): δ 8,38 (с, 1H), 7,99 (дд, 1H), 7,67 (дд, 1H), 7,48 (дд, 1H), 4,18 (д, 1H), 4,06 (д, 1H), 3,88 (д, 1H), 3,79 (с, 3H), 3,63 (дд, 1H), 3,50 (м, 2H), 3,41 (т, 2H), 2,49 (м, 1H), 2,44 (с, 3H), 2,31 (м, 2H), 1,69 (м, 1H), 1,65 (дд, 1H). МС (m/z): 465 [MH]+.
Пример 98. Гидрохлорид (1R,5S/1S,5R)-1-[3-фтор-4-(1Н-пиррол-1-илметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из 1-[3-фтор-4-(1Н-пиррол-1-илметил)фенил]-3-азабицикло[3.1.0]гексана (препаративный пример 57) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества (5,4 мг, выход = 19%).
ЯМР (соли формиата) (1Н, CDCl3): δ 7,9 (с, 1H), 6,8 (м, 4H), 6,65 (с, 2H), 6,15 (с, 2H), 5,05 (с, 2H), 3,66 (с, 3H), 3,4 (д, 1H), 3,25 (т, 2H), 3,2 (д, 1H), 2,75 (т, 2H), 2,6 (д, 1H), 2,55 (м, 1H), 2,5 (с, 3H), 2,0 (м, 2H), 1,7 (м, 1H), 1,45 (т, 1H), 0,8 (м, 1H); кислотный протон не наблюдают. МС (соль гидрохлорид) (m/z): 475 [MH]+.
Примеры 99-104
Соединения примеров 99-104 получают из (1R,5S/1S,5R)-3-(3-хлорпропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексана (40 мг) способом, аналогичным способам, описанным в примерах 53-58, в виде белых слабогигроскопичных твердых веществ.
(мин)

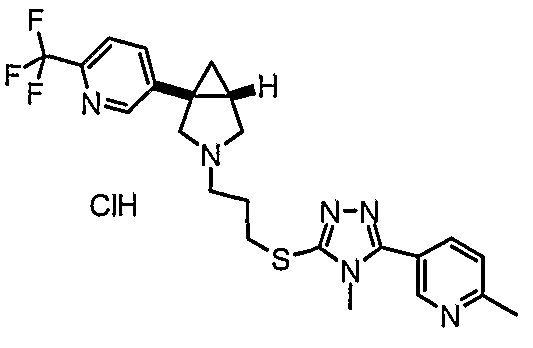




Примеры 105-109
Соединения примеров 105-109 получают из 5-[(1R,5S/1S,5R)-3-(3-хлорпропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-метил-1,3-бензотиазола (40 мг) способом, аналогичным способам, описанным в примерах 53-58, в виде белых слабогигроскопичных твердых веществ.




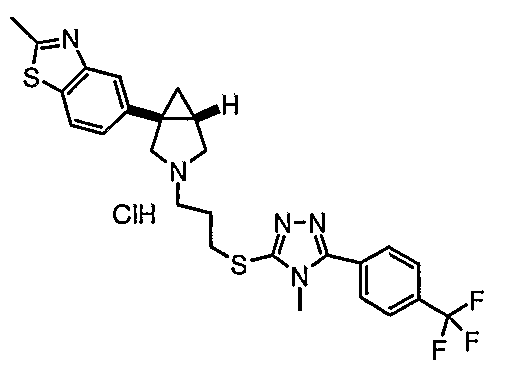
Пример 110. Гидрохлорид (1R,5S/1S,5R)-1-[3-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-[3-фтор-5-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (400 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 383 мг (выход = 46%).
ЯМР (1H, CD3OD): δ 8,46 (с, 1H), 7,54 (ушс, 1H), 7,47 (ушд, 1H), 7,41 (ушд, 1H), 4,19 (д, 1H), 3,09 (д, 1H), 3,87 (с, 3H), 3,71 (м, 2H), 3,51 (т, 2H), 3,46 (т, 2H), 2,49 (с, 3H), 2,33 (м, 3H), 1,67 (м, 1H), 1,39 (м, 1H). МС (m/z): 482 [MH]+.
Гидрохлорид (1R,5S/1S,5R)-1-[3-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексана разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralcel AD-H, 25 × 2,1 см, элюент СО2, содержащий 9% смеси (этанол + 0,1% изопропиламина), скорость потока 22 мл/мин, Р 192 бар, Т 36°С, УФ-детекция при 220 нм, петля 2 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 25 × 0,46 см, элюент СО2, содержащий 10% смеси (этанол + 0,1% изопропиламина), скорость потока 2,5 мл/мин, Р 180 бар, Т 35°С, УФ-детекция при 220 нм.
Энантиомер 1 извлекают из рацемата (100 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 19,4 мг. Rt = 12,6 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (100 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 18,3 мг, Rt = 14,7 мин. Чистота >99% a/a по УФ.
Энантиомер 1 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 2.
Пример 111. Гидрохлорид (1R,5S/1S,5R)-1-[2-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-[2-фтор-3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (400 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 349 мг (выход = 45%).
ЯМР (1H, CD3OD): δ 8,46 (с, 1H), 7,75-7,65 (м, 2H), 7,38 (т, 1H), 4,1 (д, 1H), 3,93 (д, 1H), 3,78 (с, 3H), 3,71 (д, 1H), 3,54 (д, 1H), 3,48 (т, 2H), 3,38 (т, 2H), 2,45 (с, 3H), 2,36 10 (м, 1H), 2,25 (м, 2H), 1,54 (м, 1H), 1,34 (м, 1H). МС (m/z): 481 [MH]+.
Гидрохлорид (1R,5S/1S,5R)-1-[2-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексана разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 250 × 4,6 мм, элюент н-гексан/этанол, 88/12 (изократный), скорость потока 1 мл/мин, Р 200-400 бар, Т 36°С, УФ-детекция при 200-400 нм, петля 2 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 250 × 4,6 мм, элюент н-гексан/этанол, 88/12 (изократный), скорость потока 1 мл/мин, Р 200-400 бар, Т 36°С, УФ-детекция при 200-400 нм.
Энантиомер 1 извлекают из рацемата (98 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 37 мг. Rt = 20,4 мин. Чистота 98,5% a/a по УФ.
Энантиомер 2 извлекают из рацемата (98 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 35 мг, Rt = 23,0 мин. Чистота 99,5% a/a по УФ.
Энантиомер 2 показывает fpKi (D3) > 1 log-единицы выше, чем энантиомер 1.
Пример 112. Гидрохлорид (1R,5S/1S,5R)-1-[4-(метилокси)-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-[4-(метилокси)-5-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (430 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 658 мг (выход = 76%).
Гидрохлорид (1R,5S/1S,5R)-1-[4-(метилокси)-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексана разделяют для получения отдельных энантиомеров методом полупрепаративной сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 250 × 4,6 мм, элюент н-гексан/этанол + 0,1% изопропиламина, 70/30 (изократный), скорость потока 6 мл/мин, УФ-детекция при 270 нм, петля 2 мл. Приведенные времена удерживания получают с использованием аналитической сверхкритической флюидной хроматографии (Gilson) с использованием хиральной колонки с Chiralpak AD-H, 250 × 4,6 мм, элюент н-гексан/этанол, 70/30 (изократный), скорость потока 0,8 мл/мин, УФ-детекция при 200-400 нм.
Энантиомер 1 извлекают из рацемата (100 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 18,3 мг. Rt = 15,5 мин. Чистота >99% a/a по УФ.
Энантиомер 2 извлекают из рацемата (100 мг) как соль гидрохлорид в виде белого твердого вещества с выходом 22,2 мг, Rt = 17,5 мин. Чистота >99% a/a по УФ.
Энантиомер 2 показывает fpKi (D3) > 2 log-единицы выше, чем энантиомер 1.
Пример 113. Гидрохлорид (1R,5S/1S,5R)-1-[4-(4-хлор-2-фторфенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из (1R,5S/1S,5R)-1-[4-хлор-2-фторфенил]-3-азабицикло[3.1.0]гексана (130 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 112 мг.
ЯМР (1H, CD3OD): δ 8,27 (с, 1H), 7,3 (т, 1H), 7,1 (м, 2H), 3,95 (д, 1H), 3,8 (д, 1H), 3,67 (с, 3H), 3,56 (дд, 1H), 3,4-3,2 (м, 5H), 2,34 (с, 3H), 2,15 (м, 3H), 1,4 (т, 1H), 1,18 (т, 1H). МС (m/z): 448 [MH]+.
Пример 114. Гидрохлорид (1R,5S/1S,5R)-1-[3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{3-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из 1-{3-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексана (150 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 160 мг.
ЯМР (1H,CD3OD): δ 8,41 (с, 1H), 7,49 (т, 1H), 7,3 (с, 1H), 7,37 (д, 1H), 7,24 (м, 1H), 4,17 (д, 1H), 3,9 (д, 1H), 3,8 (с, 3H), 3,69 (д, 2H), 3,51 (т, 2H), 3,42 (т, 2H), 2,47 (с, 3H), 2,3 (м, 3H), 1,57 (дд, 1H), 1,36 (т, 1H). МС (m/z): 480 [MH]+.
Пример 115. Гидрохлорид (1R,5S/1S,5R)-1-(2-фтор-4-метилфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана
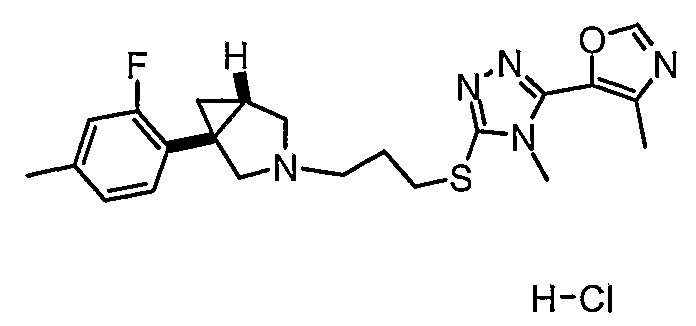
Названное в заголовке соединение получают из 1-(2-фтор-4-метилфенил)-3-азабицикло[3.1.0]гексана (148 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 60 мг.
ЯМР (1H, CD3OD): δ 8, 39 (с, 1H), 7,26 (т, 1H), 7,01 (м, 2H), 3,93 (м, 1H), 3,77 (м, 4H), 3,61 (м, 1H), 3,41-3,38 (м, 5H), 2,47 (с, 3H), 2,36 (с, 3H), 2,23 (м, 2H), 2, 19 (м, 1H), 1,45 (т, 1H), 1,21 (т, 1H). МС (m/z): 428 [MH]+.
Пример 116. Гидрохлорид (1R,5S/1S,5R)-1-[3-хлор-4-(метилокси)фенил]-3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают из 1-[3-хлор-4-(метилокси)фенил]-3-азабицикло[3.1.0]гексана (60 мг) способом, аналогичным описанному в примере 1, в виде белого слабогигроскопичного твердого вещества с выходом 56 мг.
ЯМР (1H, CD3OD): δ 8,4 (с, 1H), 7,35 (м, 1H ), 7,1 (м, 2H), 4,01 (м, 1H), 3,89 (м, 4H), 3,8 (с, 3H), 3,6-3,3 (м, 6H), 2,47 (с, 3H), 2,23 (м, 2H), 2,19 (м, 1H), 1,4 (м, 1H), 1,2 (м, 1H). МС (m/z): 460 [MH]+.
Пример 117. Гидрохлорид (1R,5S/1S,5R)-1-[4-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Смесь (1R,5S/1S,5R)-1-[4-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-азабицило[3.1.0]гексана (70 мг), 3-[(3-хлорпропил)тио]-4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазола (85 мг), карбоната калия (43 мг), Na2CO3 и иодида натрия (45 мг) в безводном ДМФА (0,6 мл) греют при 60°С в течение 24 час. После удаления растворителя в вакууме остаток растворяют в этилацетате и органическую фазу промывают насыщенным водным раствором бикарбоната натрия, сушат над сульфатом натрия и концентрируют в вакууме. Сырой продукт реакции очищают флэш-хроматографией (дихлорметан - 10% МеОН в дихлорметане) и получают 65 мг свободного основания названного в заголовке соединения. К раствору полученного вещества в дихлорметане (1 мл) добавляют HCl (1 М раствор в Et2O, 0,13 мл), растворитель выпаривают в вакууме, полученное таким образом вещество обрабатывают Et2O и получают 69 мг названного в заголовке соединения в виде белого твердого вещества (выход 50%).
ЯМР (1H, ДМСО): δ 10,39 (ушс, 1H), 8,56 (с, 1H), 7,39 (д, 2H), 7,35 (д, 2H), 4,02 (м, 1H), 3,72 (м, 1H), 3,68 (с, 3H), 3,60 (т, 1H), 3,51 (ушм, 1H), 3,27 (м, 4H), 2,60 (с, 3H), 2,37 (с, 3H), 2,35 (с, 3H), 2,19 (м, 1H), 2,16 (м, 2H), 1,62 (м, 1H), 1,15 (м, 1H). МС (m/z): 507,2 [MH]+.
Пример 118. Гидрохлорид (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[6-(трифторметил)-2-пиридинил]фенил}-3-азабицикло[3.1.0]гексана
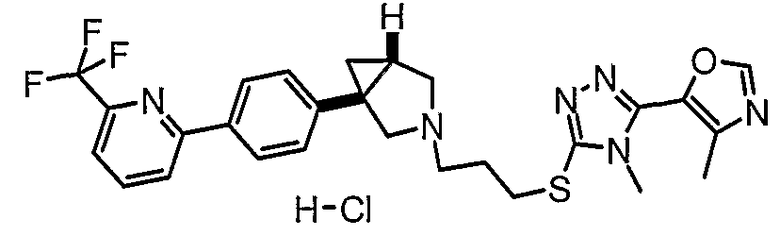
Названное в заголовке соединение получают способом, аналогичным описанному в примере 117 (с использованием (1R,5S/1S,5R)-1-{4-[6-(трифторметил)-2-пиридинил]фенил}-3-азабицикло[3.1.0]гексана), в виде белого твердого вещества с выходом 55%.
ЯМР (1H, CDCl3): δ 10,44 (ушс, 1H), 8,56 (с, 1H), 8,29 (д, 1H), 8,17 (т, 1H), 8,09 (д, 2H), 25 7,84 (д, 1H), 7,43 (д, 2H), 4,08 (м, 1H), 3,75 (м, 1H), 3,68 (с, 3H), 3,64 (т, 1H), 3,53 (ушм, 1H), 3,28 (м, 4H), 2,37 (с, 3H), 2,27 (м, 1H), 2,17 (м, 2H), 1,68 (м, 1H), 1,17 (м, 1H). МС (m/z): 541,2 [MH]+.
Пример 119. Гидрохлорид (1R,5S/1S,5R)-1-[3-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают способом, аналогичным описанному в примере 117 (с использованием (1R,5S/1S,5R)-1-[3-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-азабицикло[3.1.0]гексана), в виде белого твердого вещества с выходом 53%.
ЯМР (1H, CDCl3): δ 10,53 (уш, 1H), 8,58 (с, 1H), 7,43 (д, 1H), 7,28-7,38 (м, 3H), 4,07 (дд, 1H), 3,73 (дд, 1H), 3,70 (с, 3H), 3,61 (т, 1H), 3,53 (м, 1H), 3,34 (м, 2H), 3,29 (т, 2H), 2,64 (с, 3H), 2,39 (с, 3H), 2,73 (с, 3H), 2,23 (м, 1H), 2,20 (м, 2H), 1,68 (т, 1H), 1,16 (т, 1H). МС (m/z): 507,1 [MH]+.
Пример 120. Гидрохлорид (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(5-метил-2-тиенил)фенил]-3-азабицикло[3.1.0]гексана
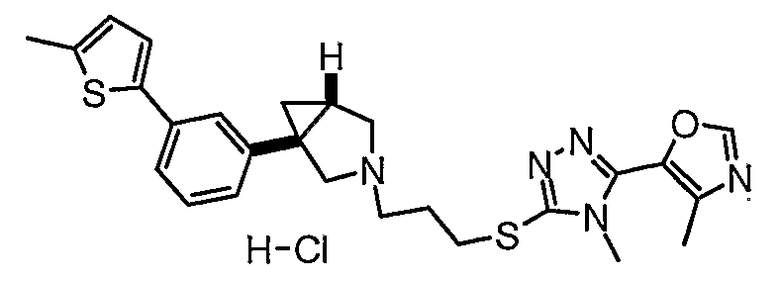
Названное в заголовке соединение получают способом, аналогичным описанному в примере 117 (с использованием (1R,5S/1S,5R)-1-[3-(5-метил-2-тиенил)фенил]-3-азабицикло[3.1.0]гексана), в виде белого твердого вещества с выходом 51%.
ЯМР (1H, CDCl3): δ 10,44 (уш, 1H), 8,58 (с, 1H), 7,49 (д, 1H), 7,45 (дт, 1H), 7,37 (т, 2H), 7,18 (дт, 1H), 6,84 (т, 1H), 4,08 (дд, 1H), 3,76 (дд, 1H), 3,70 (с, 3H), 3,62 (т, 1H), 3,54 (тм, 1H), 3,28 (т, 4H), 2,48 (с, 3H), 2,39 (с, 3H), 2,24 (м, 1H), 2,19 (т, 2H), 1,65 (т, 1H), 1,16 (т, 1H). МС (m/z): 472,0 [MH]+.
Пример 121. Гидрохлорид (1R,5S/1S,5R)-1-[4-(3,5-диметил-4-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексана

Названное в заголовке соединение получают способом, аналогичным описанному в примере 117 (с использованием (1R,5S/1S,5R)-1-[4-(3,5-диметил-4-изоксазолил)фенил]-3-азабицикло[3.1.0]гексана), в виде белого твердого вещества с выходом 55%.
МС (m/z): 491,2 [MH]+.
Пример 122. Гидрохлорид (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-оксазол-5-ил)]-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана

Смесь (1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексана (препаративный пример 18, 60 мг), 3-[(3-хлорпропил)тио]-5-(2,4-диметил-1,3-оксазол-5-ил)-4-метил-4Н-1,2,4-триазола (препаративный пример 78, 78 мг), 2-трет-бутилимино-2-диэтиламино-1,3-диметилпергидро-1,3,2-диазафосфорина на полистироле (2,2 ммоль/г, 140 мг) и каталитического количества NaI в сухом ацетонитриле (3 мл) греют при 70°С в течение 4 час и затем в течение ночи при 55°С. Смолу удаляют фильтрацией и промывают ацетонитрилом (2 × 3 мл). Удаляют растворитель в вакууме, оставшееся твердое вещество растворяют в сухом ДМФА (0,5 мл) и добавляют 3-[(3-хлорпропил)тио]-5-(2,4-диметил-1,3-оксазол-5-ил)-4-метил-4Н-1,2,4-триазол (препаративный пример 78, 60 мг), а затем карбонат калия (118 мг). Полученную суспензию греют при 60°С в течение ночи. При комнатной температуре добавляют насыщенный раствор бикарбоната натрия (4 мл) и суспензию экстрагируют DCM (2 × 6 мл). Полученный раствор загружают в колонку SCX и элюируют МеОН, а затем 0,25 М раствором МеОН/NH3. Полученное вещество очищают препаративной ВЭЖХ и затем превращают в гидрохлорид, следуя способу, описанному в примере 15, и получают названное в заголовке соединение в виде белого слабогигроскопичного твердого вещества (37 мг, выход 27%).
ЯМР (1H, ДМСО): δ 10,38 (уш, 1H), 7,71 (д, 1H), 7,64 (т, 1H), 7,59 (д, 1H), 3,98 (ушд, 1H), 3,76 (ушд, 1H), 3,65 (с, 3H), 3,54 (уш, 1H), 3,44 (ушт, 1H), 3,31 (уш, 2H), 3,24 (т, 2H), 2,47 (с, 3H), 2,35 (м, 1H), 2,29 (с, 3H), 2,11 (м, 2H), 1,63 (т, 1H), 1,13 (т, 1H). МС (m/z): 496 [MH]+.
Все публикации, в том числе патенты и заявки на патенты, без ограничения, цитированные в данном описании, включены в него в качестве ссылок, как если бы каждая отдельная публикация была специально отдельно указана как включенная посредством ссылки в настоящую заявку во всей ее полноте.
Следует иметь в виду, что настоящее изобретение охватывает все сочетания отдельных групп, описанных в данном описании выше.
Заявка, частью которой являются данное описание и формула изобретения, может быть использована как основание для приоритета в отношении любой последующей заявки. Формула изобретения такой последующей заявки может быть направлена на любой признак или сочетание признаков, описанных в данной заявке. Она может относиться к продукту, композиции, способу или применению и может включать, как пример и без ограничения, формулу изобретения, приведенную далее.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ, ОБЛАДАЮЩЕЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ KDM5, И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2021 |
|
RU2840256C1 |
| ПРОИЗВОДНЫЕ АМИНОПИРИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ ИНГИБИТОРОВ ALK-2 | 2017 |
|
RU2777979C2 |
| ПРОИЗВОДНЫЕ АМИНОПИРИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ ИНГИБИТОРОВ ALK-2 | 2017 |
|
RU2747318C2 |
| ПРОИЗВОДНЫЕ АМИНОПИРИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ ИНГИБИТОРОВ ALK-2 | 2022 |
|
RU2803084C1 |
| ПРОИЗВОДНЫЕ АМИНОПИРИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ СЕЛЕКТИВНЫХ ИНГИБИТОРОВ ALK-2 | 2023 |
|
RU2826177C1 |
| БИЦИКЛИЧЕСКИЕ КЕТОНЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2797922C2 |
| НИТРИЛСОДЕРЖАЩИЕ ПРОТИВОВИРУСНЫЕ СОЕДИНЕНИЯ | 2021 |
|
RU2786722C1 |
| ИНГИБИТОРЫ МУТАЦИИ HER2 | 2022 |
|
RU2834124C2 |
| НИТРИЛСОДЕРЖАЩИЕ ПРОТИВОВИРУСНЫЕ СОЕДИНЕНИЯ | 2021 |
|
RU2820150C2 |
| ПРОЛЕКАРСТВО ПРОИЗВОДНОГО АМИНОКИСЛОТЫ | 2017 |
|
RU2739318C2 |
Описываются новые производные азабицикло{3.1.0}гексана общей формулы (I)

или их фармацевтически приемлемые соли (значения радикалов приведены в формуле изобретения) способ их получения, промежуточные соединения, фармацевтическая композиция и применение новых соединений в терапии в качестве модуляторов допаминовых рецепторов D3, например, для лечения лекарственной зависимости или в качестве антипсихотических средств. 17 н.з. и 17 з.п. ф-лы, 4 табл.
1. Производное азабицикло[3.1.0]гексана общей формулы (I)

или его фармацевтически приемлемая соль, где
G означает фенил, необязательно замещенный R1;
R1 выбирают независимо, из группы, состоящей из галогена, гидрокси, циано, С1-4-алкила, галоген-С1-4-алкила, С1-4-алкокси, галонен-С1-4-алкокси, С1-4-алканоила; или R1 соответствует группе R5;
R5 представляет собой фрагмент, выбранный из группы, состоящей из изоксазолила, одно или дважды замещенного С1-4-алкилом, -CH2-N-пирролила, 1,1-диоксидо-2-изотиазолидинила, тиенила, замещенного C1-4-алкилом, тиазолила, дважды замещенного С1-4-алкилом, пиридила, замещенного одно или дважды галоген-С1-4-алкилом, или 2-пирролидинонила;
или G означает пиридил, бензотиазолил или индазолил, а R1 означает С1-4-алкил или галоген-С1-4-алкил, и p равен 1;
R1 представляет собой водород или С1-4-алкил;
R3 представляет собой С1-4-алкил;
R4 представляет собой водород или фенильную группу, необязательно одно или дважды замещенную галоген-С1-4-алкилом или галогеном; хинолинил, замещенный галогеном или С1-4-алкилом; оксазолил, замещенный галоген-С1-4-алкилом или C1-4-алкилом; тиено[2,3-с]пиразолил, замещенный галоген-С1-4-алкилом или C1-4-алкилом; тетрагидропиранил; пиридинил, необязательно одно или дважды замещенный галоген-С1-4-алкилом или С1-4-алкилом; пиридазинил; пиразолил, одно или дважды замещенный галогеном, C1-4-алкилом, галоген-С1-4-алкилом; пиримидинил; фуранил, одно или дважды замещенный C1-4-алкилом; тиазолил, замещенный дважды C1-4-алкилом; пиразинил, замещенный C1-4-алкилом; триазолил, замещенный С1-4-алкилом; изоксазолил, замещенный C1-4-алкилом; тиенил, замещенный галогеном;
р означает целое число от 0 до 2;
и когда R1 представляет собой хлор, и p равен 1, тогда R1 не находится в орто-положении относительно связи с остальной частью молекулы; и когда R1 соответствует R5, p равен 1.
2. Соединение формулы (I)' по п.1

или его фармацевтически приемлемая соль,
где G, p, R1, R2, R3, R4 и R5 имеют значения, указанные в п.1.
3. Соединение по п.1, где R1 представляет собой бром, фтор, трифторметокси, циано, гидрокси, хлор, метокси, трет-бутил, трифторметил; и R5 представляет собой изоксазолил, одно или дважды замещенный C1-4-алкилом, 2-пирролидинонил, -СН2-N-пирролил, 1,1-диоксидо-2-изотиазолидинил, 2-тиенил, замещенный C1-4-алкилом, 2-пиридил, замещенный одно или дважды галоген-С1-4-алкилом, 2-тиазолил, дважды замещенный C1-4-алкилом.
4. Соединение по п.1, где p равен 1 или 2.
5. Соединение по п.1, где R2 представляет собой водород.
6. Соединение по п.1, где R4 представляет собой необязательно замещенный фенил, замещенный хинолинил, необязательно замещенный пиридинил, замещенный пиразолил, пиримидил, пиридазинил, пиразинил, замещенный фуранил, замещенный тиенил, замещенный оксазолил, замещенный изоксазолил, замещенный тиазолил, замещенный триазолил.
7. Соединение формулы (IB)

или его фармацевтически приемлемая соль,
где R1, p, R3 и R4 имеют значения, указанные в любом из пп.1-6.
8. Соединение формулы (IC)
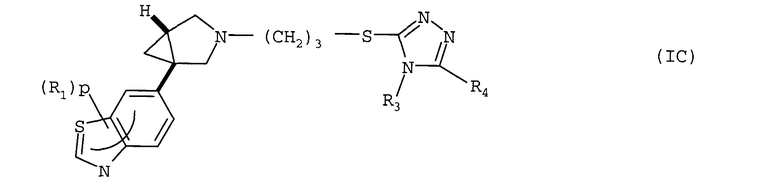
или его фармацевтически приемлемая соль,
где R1 означает С1-4-алкил;
p означает 1;
R3 означает С1-4-алкил;
R4 означает оксазолил, замещенный С1-4-алкилом.
9. Соединение формулы (ID)
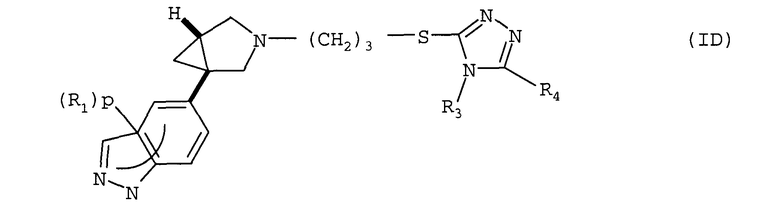
или его фармацевтически приемлемая соль,
где R1 означает C1-4-алкил;
p означает 1;
R3 означает С1-4-алкил;
R4 означает оксазолил, замещенный С1-4-алкилом.
10. Соединение формулы (IE)
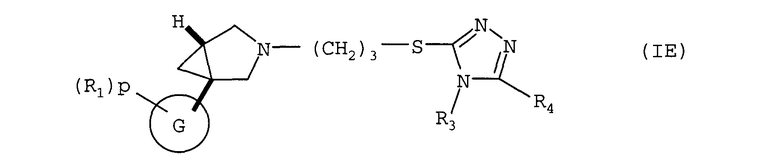
или его фармацевтически приемлемая соль, где
G представляет собой 2-пиридил или 3-пиридил,
R1 означает галоген-С1-4-алкил;
p означает 1;
R3 означает С1-4-алкил;
R4 означает фенил, необязательно замещенный галоген-С1-4-алкилом, оксазолил, одно или дважды замещенный C1-4-алкилом, пиразинил, пиридинил или тиазолил, замещенные С1-4-алкилом.
11. Соединение формулы (IF)
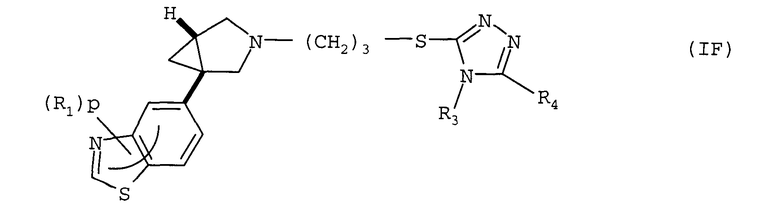
или его фармацевтически приемлемая соль, где
R1 означает С1-4-алкил;
p означает 1;
R3 означает С1-4-алкил;
R4 означает фенил, оксазолил, пиразинил, пиридинил или тиазолил, необязательно замещенные С1-4-алкилом или галоген-С1-4-алкилом.
12. Стереохимический изомер, обогащенный конфигурацией (1S,5R) формулы (IA)

или его фармацевтически приемлемая соль, где
G выбирают из группы, состоящей из фенила, пиридила, бензотиазолила, индазолила;
p равен целому числу от 0 до 5;
R1 выбирают независимо из группы, состоящей из галогена, гидрокси, циано, С1-4-алкила, галоген-С1-4-алкила, C1-4-алкокси, галоген-С1-4-алкокси, С1-4-алканоила; или R1 соответствует группе R5;
R2 представляет собой водород или C1-4-алкил;
R3 представляет собой С1-4-алкил;
R4 представляет собой водород или фенильную группу, гетероциклильную группу, 5- или 6-членную гетероароматическую группу или 8-11-членную бициклическую группу, любая из которых необязательно замещена 1, 2, 3 или 4 заместителями, выбранными из группы, состоящей из галогена, циано, С1-4-алкила, галоген-С1-4-алкила, С1-4-алкокси, С1-4-алканоила;
R5 представляет собой фрагмент, выбранный из группы, состоящей из изоксазолила, -СН2-N-пирролила, 1,1-диоксидо-2-изотиазолидинила, тиенила, тиазолила, пиридила, 2-пирролидинонила, и такая группа необязательно замещена одним или двумя заместителями, выбранными из галогена, циано, С1-4-алкила, галоген-С1-4-алкила, С1-4-алкокси, С1-4-алканоила;
и когда R1 представляет собой хлор, и p равен 1, тогда R1 не находится в орто-положении относительно связи с остальной частью молекулы; и когда R1 соответствует R5, p равен 1.
13. Стереохимический изомер, обогащенный конфигурацией (1S,5R) формулы (IB)'

или его фармацевтически приемлемая соль, где
R1, p, R3 и R4 имеют значения, указанные в любом из пп.1-6.
14. Стереохимический изомер, обогащенный конфигурацией (1S,5R) формулы (IC)'

или его фармацевтически приемлемая соль, где R1, p, R3 и R4 имеют значения, указанные в любом из пп.1-6.
15. Стереохимический изомер, обогащенный конфигурацией (1S,5R) формулы (ID)'
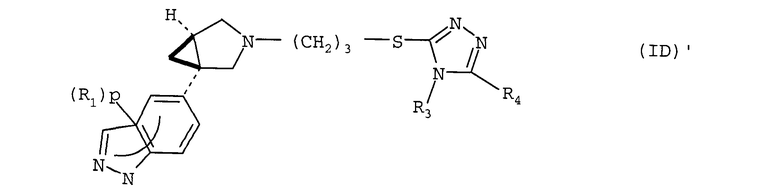
или его фармацевтически приемлемая соль, где
R1, p, R3 и R4 имеют значения, указанные в любом из пп.1-6.
16. Стереохимический изомер, обогащенный конфигурацией (1S,5R) или (1R,5R) формулы (IE)'

или его фармацевтически приемлемая соль, где
G представляет собой 2-пиридил или 3-пиридил, и R1, p, R3 и R4 имеют значения, указанные в любом из пп.1-6.
17. Стереохимический изомер, обогащенный конфигурацией (1S,5R) формулы (IF)'
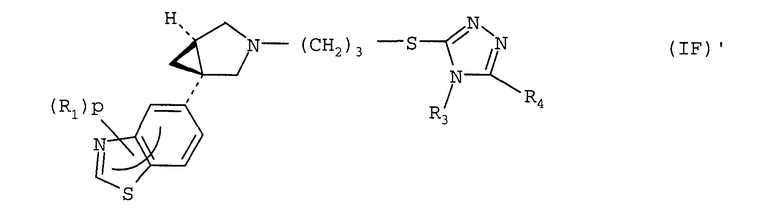
или его фармацевтически приемлемая соль, где
R1, p, R3 и R4 имеют значения, указанные в любом из пп.1-6.
18. Стереохимический изомер, обогащенный конфигурацией (1R,5S), выбранный из группы, в которую входят
- 5-[5-({3-[(1R,5S)-1-(4-метоксифенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 2;
- 5-[5-({3-[(1R,5S)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 1;
- 5-[5-({3-[(1R,5S)-1-(4-трет-бутилфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 1;
- (1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан, энантиомер 2;
- (1R,5S)-1-(3-хлорфенил)-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 2;
1-[5-[(1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон, энантиомер 2;
- 2-метил-5-[(1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол, энантиомер 2; или его фармацевтически приемлемая соль.
19. Соединение по любому из пп.1-17 или его фармацевтически приемлемая соль, выбранное из группы, в которую входят
- 5-[5-({3-[(1R,5S/1S,5R)-1-(4-метоксифенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
- 5-[5-({3-[(1S,5R)-1-(4-метоксифенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 1;
- 5-[5-({3-[(1R,5S/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
- 5-[5-({3-[(1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 2;
- 2-метил-5-[4-метил-5-({3-[(1R,5S/1S,5R)-1-фенил-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4Н-1,2,4-триазол-3-ил]хинолин;
- 2-метил-5-[4-метил-5-({3-[(1S,5R)-1-фенил-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4Н-1,2,4-триазол-3-ил]хинолин, энантиомер 2;
- 5-[5-({3-[(1R,5S/1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
5-[5-({3-[(1S,5R)-1-(3,4-дихлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 1;
- 5-[5-({3-[(1R,5S/1S,5R)-1-(4-трет-бутилфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
- 5-[5-({3-[(1S,5R)-1-(4-трет-бутилфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 2;
- 4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]бензонитрил;
- 4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенол;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-фенил-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1R,5S/1S,5R)-1-(4-трет-бутилфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(3,4-дихлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(3,4-дихлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 2;
- (1R,5S/1S,5R)-1-(4-метоксифенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-метоксифенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 2;
- (1R,5S/1S,5R)-1-[4-(5-метил-3-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1,0]гексан;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[4-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- 1-[5-[(1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-[5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон, энантиомер 1;
- (1S,5R/1R,5S)-1-(4-хлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-хлорфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-1-(4-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-1-(3-хлорфенил)-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло [3,1.0]гексан;
- (1S,5R)-1-(3-хлорфенил)-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-1-(3-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(3-фторфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(метилокси)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(метилокси)фенил]-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-[3-{[4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- 5-[5-({3-[(1S,5R/1R,5S)-1-(4-хлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин;
- 5-[5-({3-[(1S,5R/1R,5S)-1-(4-хлорфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-2-метилхинолин, энантиомер 1;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан, энантиомер 1;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-метил-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан, энантиомер 2;
- (1R,5S/1S,5R)-1-(3-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(1-метил-3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(1-метил-3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан, диастереоизомер 1;
- (1S,5R)-3-(1-метил-3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан, диастереоизомер 2;
- (1R,5S/1S,5R)-1-[2-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан, энантиомер 2;
- 1-[4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-[4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-пиридазинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(1,5-диметил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(5-пиримидинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(3-метил-2-фуранил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- 2-метил-6-{4-метил-5-[(3-{(1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4Н-1,2,4-триазол-3-ил}хинолин;
- 8-фтор-2-метил-5-{4-метил-5-[(3-{(1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4Н-1,2,4-триазол-3-ил}хинолин;
- 2-метил-5-{4-метил-5-[(3-{(1S,5R)-1-[4-(трифторметил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4Н-1,2,4-триазол-3-ил}хинолин;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-пиридазинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(5-пиримидинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[2-фтор-4-(трифторметил)фенил]-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- 1-{4-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}-2-пирролидинон;
- 5-{5-[(3-{(1R,5S/1S,5R)-1-[4-(1,1-диоксидо-2-изотиазолидинил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил}-2-метилхинолин;
- (1R,5S/1S,5R)-1-[3-фтор-4-(трифторметил)фенил]-5-метил-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- 1-(2-(метилокси)-5-{(1R,5S/1S,5R)-3-(3-{[4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанон;
- 1-[5-[(1R,5S/1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-{2-(метилокси)-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-[5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-{2-(метилокси)-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-(2-гидрокси-5-{(1R,5S/1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанон;
- 1-{5-[(1R,5S/1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанон;
- 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-{2-гидрокси-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4H-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-[5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон;
- 1-[5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон, энантиомер 1;
- 2-метил-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- 2-метил-5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол, энантиомер 1;
- 2-метил-6-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,1,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- 1-метил-5-[(1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1Н-индазол;
- 1-метил-5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-lH-индазол, энантиомер 1;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-пиридазинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(5-хлор-1-метил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(1-метил-1Н-1,2,3-триазол-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(1,5-диметил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(5-пиримидинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[1-метил-3-(трифторметил)-1Н-пиразол-4-ил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-2-фуранил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-5-изоксазолил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло [3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(1-метил-1Н-пиразол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(5-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[2-метил-3-(трифторметил)-1,3-оксазол-4-ил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-2-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(2,5-диметил-3-фуранил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[5-(5-хлор-2-тиенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-(3-{[4-этил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло [3.1.0]гексан;
- (1R,5S/1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[2-метил-6-(трифторметил)-3-пиридинил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- 5-[5-({3-[(1R,5S/1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-1-метил-3-(трифторметил)-1Н-тиено[2,3-с]пиразол;
- 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R/1S,5S)-1-[5-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан;
- 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R)-1-[5-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан, энантиомер 2;
- 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R/1S,5S)-1-[6-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[3-фтор-4-(1Н-пиррол-1-илметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-{3-{[4-метил-5-фенил-4Н-1,2,4-триазол-3-ил)тио]пропил}-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R/1R,5S)-2-метил-5-[3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R/1R,5S)-2-метил-5-[3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R/1R,5S)-2-метил-5-[3-{3-[(4-метил-5-фенил-4Н-1,2,4-триазол-3-ил)тио]пропил}-3-азабицикло[3.1.0]гекс-1-ил)-1,3-бензотиазол;
- (1S,5R/1R,5S)-5-[3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-метил-1,3-бензотиазол;
- (1S,5R/1R,5S)-2-метил-5-{3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}-1,3-бензотиазол;
- (1R,5S/1S,5R)-1-[3-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-фтор-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан, энантиомер 1;
- (1R,5S/1S,5R)-1-[2-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1,0]гексан;
- (1S,5R)-1-[2-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан, энантиомер 2;
- (1R,5S/1S,5R)-1-[4-(метилокси)-5-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[4-(4-хлор-2-фторфенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-(3-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-(2-хлор-4-метилфенил)-3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[3-хлор-4-(метилокси)фенил]-3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[4-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[6-(трифторметил)-2-пиридинил]фенил}-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[3-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(5-метил-2-тиенил)фенил]-3-азабицикло[3.1.0]гексан;
- (1R,5S/1S,5R)-1-[4-(3,5-диметил-4-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-оксазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-фтор-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан.
20. Соединение по любому из пп.1-17 или его фармацевтически приемлемая соль, выбранное из группы, в которую входят
- 4-[(1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]бензонитрил;
- 4-[(1S,5R)-3-(3-{[4-метил-5-(2-метилхинолин-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенол;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-фенил-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-трет-бутилфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[4-(5-метил-3-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[4-фтор-3-(трифторметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-метил-4-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(3-бромфенил)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- 1-[4-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-[4-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]-1-пропанон;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-(трифторметил)фенил]-3-азабицикло[3.1.0]гексан;
- 1-{4-[(1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}-2-пирролидинон;
- 5-{5-[(3-{(1S,5R)-1-[4-(1,1-диоксидо-2-изотиазолидинил)фенил]-3-азабицикло[3.1.0]гекс-3-ил}пропил)тио]-4-метил-4Н-1,2,4-триазол-3-ил}-2-метилхинолин;
- 1-(2-(метилокси)-5-{(1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанон;
- 1-[5-[(1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-{2-(метилокси)-5-[(1S,5R)-3-(3-{[4-метил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-[5-[(1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-(метилокси)фенил]этанон;
- 1-{2-(метилокси)-5-[(1S,5R)-3-(3-{[4-метил-5-(тетрагидро-2Н-пиран-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-(2-гидрокси-5-{(1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}фенил)этанон;
- 1-{5-[(1S,5R)-3-(3-{[5-(3,4-дифторфенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-гидроксифенил}этанон;
- 1-{2-гидрокси-5-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 1-{2-гидрокси-5-[(1S,5R)-3-(3-{[4-метил-5-(2-метил-5-хинолинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]фенил}этанон;
- 2-метил-6-[(1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4H-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(4-пиридазинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(5-хлор-1-метил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(1-метил-1Н-1,2,3-триазол-4-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(1,5-диметил-1Н-пиразол-4-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(5-пиримидинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[1-метил-3-(трифторметил)-1Н-пиразол-4-ил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-2-фуранил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-5-изоксазолил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(1-метил-1Н-пиразол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(5-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[2-метил-5-(трифторметил)-1,3-оксазол-4-ил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-метил-5-(3-метил-2-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(2,5-диметил-3-фуранил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[5-(5-хлор-2-тиенил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-(3-{[4-этил-5-(3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(4-бромфенил)-3-[3-({4-метил-5-[2-метил-6-(трифторметил)-3-пиридинил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гексан;
- 5-[5-({3-[(1S,5R)-1-(4-бромфенил)-3-азабицикло[3.1.0]гекс-3-ил]пропил}тио)-4-метил-4Н-1,2,4-триазол-3-ил]-1-метил-3-(трифторметил)-1Н-тиено[2,3-с]пиразол;
- 3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-(1R,5R)-1-[6-(трифторметил)-2-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-фтор-4-(1Н-пиррол-1-илметил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(2-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-{3-[(4-метил-5-фенил-4Н-1,2,4-триазол-3-ил)тио]пропил}-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-1-[6-(трифторметил)-3-пиридинил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-2-метил-5-[3-(3-{[4-метил-5-(5-метил-2-пиразинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R)-2-метил-5-[3-(3-{[4-метил-5-(6-метил-3-пиридинил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R)-2-метил-5-(3-{3-[(4-метил-5-фенил-4Н-1,2,4-триазол-3-ил)тио]пропил}-3-азабицикло[3.1.0]гекс-1-ил]-1,3-бензотиазол;
- (1S,5R)-5-[3-(3-{[5-(2,4-диметил-1,3-тиазол-5-ил)-4-метил-4Н-1.2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гекс-1-ил]-2-метил-1,3-бензотиазол;
- (1S,5R/1R,5S)-2-метил-5-{3-[3-({4-метил-5-[4-(трифторметил)фенил]-4Н-1,2,4-триазол-3-ил}тио)пропил]-3-азабицикло[3.1.0]гекс-1-ил}-1,3-бензотиазол;
- (1S,5R)-1-[4-(4-хлор-2-фторфенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{3-[(трифторметил)окси]фенил}-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-(2-хлор-4-метилфенил)-3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-хлор-4-(метилокси)фенил]-3-(2-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[4-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-{4-[6-(трифторметил)-2-пиридинил]фенил}-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[3-(2,4-диметил-1,3-тиазол-5-ил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[3-(5-метил-2-тиенил)фенил]-3-азабицикло[3.1.0]гексан;
- (1S,5R)-1-[4-(3,5-диметил-4-изоксазолил)фенил]-3-(3-{[4-метил-5-(4-метил-1,3-оксазол-5-ил)-4Н-1,2,4-триазол-3-ил]тио}пропил)-3-азабицикло[3.1.0]гексан;
- (1S,5R)-3-(3-{[5-(2,4-диметил-1,3-оксазол-5-ил)-4-метил-4Н-1,2,4-триазол-3-ил]тио}пропил)-1-[2-фтор-4-(трифториметил)фенил]-3-азабицикло[3.1.0]гексан.
21. Способ получения соединения по п.1, включающий стадии взаимодействия соединения формулы (XIV)

где R1, R2, G и р имеют значения, указанные в п.1, и Х представляет собой уходящую группу, с соединением формулы (V)

где R3 и R4 имеют значения, указанные в п.1.
22. Способ лечения состояния, для которого благоприятна модуляция допаминовых рецепторов D3, включающий введение млекопитающему (например человеку), нуждающемуся в этом, эффективного количества соединения по любому из пп.1-20.
23. Способ по п.22, где состоянием является психоз, или психотическое состояние, или токсикомания.
24. Способ по п.23, где состоянием является токсикомания.
25. Способ по п.23, где психотическим состоянием является шизофрения.
26. Применение соединения по любому из пп.1-20 для получения лекарственного средства для лечения состояния у млекопитающего, для которого благоприятна модуляция допаминовых рецепторов D3.
27. Применение по п.26, где состоянием является психоз, или психотическое состояние, или токсикомания.
28. Применение по п.27, где состоянием является токсикомания.
29. Применение по п.27, где психотическим состоянием является шизофрения.
30. Соединение по п.1 для применения в терапии.
31. Соединение по п.1 для применения для лечения состояния у млекопитающего, для которого благоприятна модуляция допаминовых рецепторов D3.
32. Соединение по п.1 для применения для лечения психоза, или психотического состояния, или для лечения токсикомании.
33. Соединение по п.1 для применения для лечения шизофрении.
34. Фармацевтическая композиция, обладающая модулирующим действием в отношении допаминовых рецепторов D3, содержащая соединение по любому из пп.1-20 и фармацевтически приемлемый носитель.
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| WO 00/42037 A, 20.07.2000 | |||
| СПОСОБ ПРОИЗВОДСТВА ХЛЕБОБУЛОЧНОГО ИЗДЕЛИЯ | 2010 |
|
RU2428844C1 |
Авторы
Даты
2011-11-20—Публикация
2005-02-21—Подача