Область техники
Настоящее изобретение относится к способу промышленного производства чистого карбоната магния (магнезита) из горной породы, содержащей оливин, путем связывания CO2. Способ позволяет одновременно получать и другие ценные вещества, в частности аморфный диоксид кремния.
Уровень техники
В настоящее время многие считают антропогенные выбросы CO2 одной из самых больших проблем охраны окружающей среды. Обязательства Киотского Протокола предполагают различные виды пошлин в случаях выбросов СO2. Таким образом, существует требование внедрения экономичных способов технологической обработки CO2. Одним из способов сбора/утилизации CO2, при котором CO2 используют для вытеснения большего количества углеводородов из пласта, является введение CO2 в истощенные или заполненные водой нефтяные пласты. Добыча нефти вторичными методами может иметь преимущества с экономической точки зрения.
Другая возможность заключается в связывании СО2 в виде карбонатов при его взаимодействии с горными породами/минералами, содержащими элементы, образующие при реакции с СО2 твердые вещества/минералы (карбонаты), наиболее важными из которых для производства являются Са, Mg и Fe.
Так, например, CO2 может связываться с MgО, образуя осадок MgCO3. Эта реакция предполагает возможность связывать CO2, образующийся на промышленных производствах, таких как газовые энергетические установки, производство водорода из природного газа или при получении метана.
Однако производство MgО из магнезита (MgCO3) или доломита (СаMg(CO3)2) не представляет интереса, поскольку получение MgО в этих случаях подразумевает образование такого же количества CO2, какое можно связать, а следовательно, суммарный эффект по CO2 равен нулю.
В отношении производства MgО из другого сырья, такого как магнийсодержащие силикаты (сульфаты и фосфаты), ситуация иная. Такое производство MgО только для связывания CO2 очень дорогое. С другой стороны, экономический потенциал такого способа связывания CO2 можно значительно повысить и, возможно, сделать производство рентабельным, если СО2 и воду в разных количествах привести во взаимодействие с горной породой или минералом в условиях промышленного способа производства, когда при связывании СO2 образуются ценные продукты реакции. Примером подходящей горной породы является дунит, состоящий преимущественно из минерала оливина (+90%), большие залежи которого найдены в Норвегии в Санмоэре и в Нордфьорде. (В 2006 году одно только месторождение Аахейм поставило на мировой рынок 65% этого сырья). В различных кислотных способах эту горную породу рассматривают в качестве сырья для производства магния и аморфного диоксида кремния.
CO2 с разным количеством воды или без нее в качестве промышленного химического реагента в промышленном производстве для получения комбинированных пригодных для продажи продуктов, MgCO3, аморфного диоксида кремния, Fе2О3, (Fе, Mg)Сr2O4 и Pt при одновременном связывании СO2 ранее никогда не использовали.
Горная порода дунит обычно более чем на 90% состоит из минерала оливина. Оливин залегает смешанной (изоморфной) полосой, в которой чаще всего присутствует смесь минералов (конечных образований) форстерита Mg2SiO4 и фаялита Fe2SiO4. В месторождении дунита Аахейм количество форстерита и фаялита составляет 93% и 7% соответственно. В условиях температуры и давления поверхности земли оливин нестабилен. Например, он вступает в реакцию с растворенным в воде СO2 с образованием карбонатов. Однако в природных условиях эта основная реакция протекает относительно медленно:
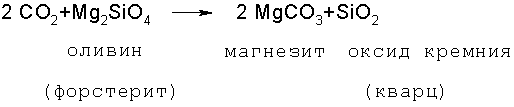
Скорость реакции можно увеличить до подходящей величины в условиях лаборатории или промышленного производства и оптимизировать, вариируя давление и температуру, а также количественное соотношение СО2 к Н2O.
Кроме основного компонента оливина горная порода дунит содержит также такие минералы, как хромит/хромит магния (Fe,Mg)Cr2O4 (0,2-0,5%) и хромсодержащий хлорит. Хромит, который образуется в глубоких слоях земной коры при отвердевании мафических выплавов или верхних слоев мантии (дунит, периодит и другие ультрамафические горные породы), содержит также благородный металл платину и металлы платиновой группы, такие как палладий, осмий, иридий и рутений. Богатая хромитом горная порода может содержать от 0,1 до 6-7 м.д. (ррт) металлов платиновой группы. В отдельных случаях это содержание достигает 50 м.д.
До недавнего времени прямую карбонизацию описывали как одностадийный способ производства (Фот и др. 2000; О'Коннор и др. 2002, 2005). В процессе использовали смесь воды, CO2 и оливина; растворение оливина и выпадение в осадок карбоната и диоксида кремния проходили в одну стадию. В закрытых автоклавах проводили эксперименты в диапазонах температур и давлений для CO2 от 25 до 250°С и от 22,5 до 25 МПа (25 до 250 бар). Продуктами реакции считают карбонат магния и диоксид кремния. Скорость реакции и степень превращения невысоки, особенно при низких температурах и давлениях. Влияние размера зерна, температуры и давления CO2 систематически исследовали. Однако этим способом практически невозможно провести различие между продуктами реакции.
Многостадийные способы карбонизации оливина, серпентина и других силикатов также исследовали. Однако в этих способах CO2 не включали в качестве реагента на первой стадии. Бланко и др. (2004) описывают способ, в котором силикаты растворяют в крепком щелочном растворе в первой реакционной камере. Затем растворенный гидроксид металла вступает в реакцию с газом в отдельной реакционной камере с образованием карбонатов. В некоторых способах для растворения силикатов используют кислоту (Марото-Валер и др., 2005; Парк и др., 2005). СО2 добавляют в раствор потом, после растворения силикатных минералов в кислотном растворе. Джидик и др. (2004) описывают способ растворения CO2 в воде, в которую добавляют ионы металлов (Na, Mg, Ca) для осаждения солей из угольной кислоты. Однако в этом способе не рассматривается вопрос о введении ионов металлов.
Цели
На основании известного уровня техники цель настоящего изобретения - обеспечение способа экономичного производства карбоната магния из природной горной породы, такой как дунит.
Одна из особенностей настоящего изобретения - сочетание вышеуказанного способа с эффективным связыванием CO2.
Другая особенность - осуществление вышеуказанного способа как экологичного и не требующего сильных химических реагентов, таких как сильные кислоты.
Кроме того, данный способ позволяет одновременно получать другие ценные продукты из той же горной породы.
Раскрытие изобретения
Вышеперечисленные цели достигают способом по п.1 формулы настоящего изобретения.
Настоящее изобретение обеспечивает простой, рациональный, экономичный и экологичный способ производства химически чистого карбоната магния из природных запасов дунита (оливина).
В соответствии с настоящим изобретением способ включает по меньшей мере две стадии, первую из которых можно назвать процессом растворения. На первой стадии магний из форстерита, который является основным компонентом оливина, переводят в раствор. Однако уже на этой первой стадии выпадает осадок гидроксидов железа, поскольку железо всегда присутствует в природных месторождениях дунита/оливина.
На второй стадии осаждают химически чистый карбонат магния, как показано в следующих примерах. Условия проведения процесса на стадии 2, как и на стадии 1, возможны в широком диапазоне, но характерной особенностью стадии 2 является то, что величина рН на этой стадии больше, чем на стадии 1. Как детально показано ниже, необходимую величину рН можно обеспечить без добавления дополнительных химических реагентов.
В соответствии с изобретением способ не требует использования сильных химических реагентов и основан, главным образом, на реакции между CO2, водой и горной породой, вопрос только в соответствующем количественном сочетании.
Предпочтительно, чтобы в соответствии с настоящим изобретением способ включал стадию отделения аморфного диоксида кремния от осадка, что наиболее удобно осуществлять на стадии, последующей стадии осаждения магнезита. Если осаждение магнезита в значительной степени определяется величиной рН, то осаждение диоксида кремния в значительной степени определяется температурой. Тщательный контроль этих параметров дает возможность количественного разделения названных компонентов на отдельных стадиях.
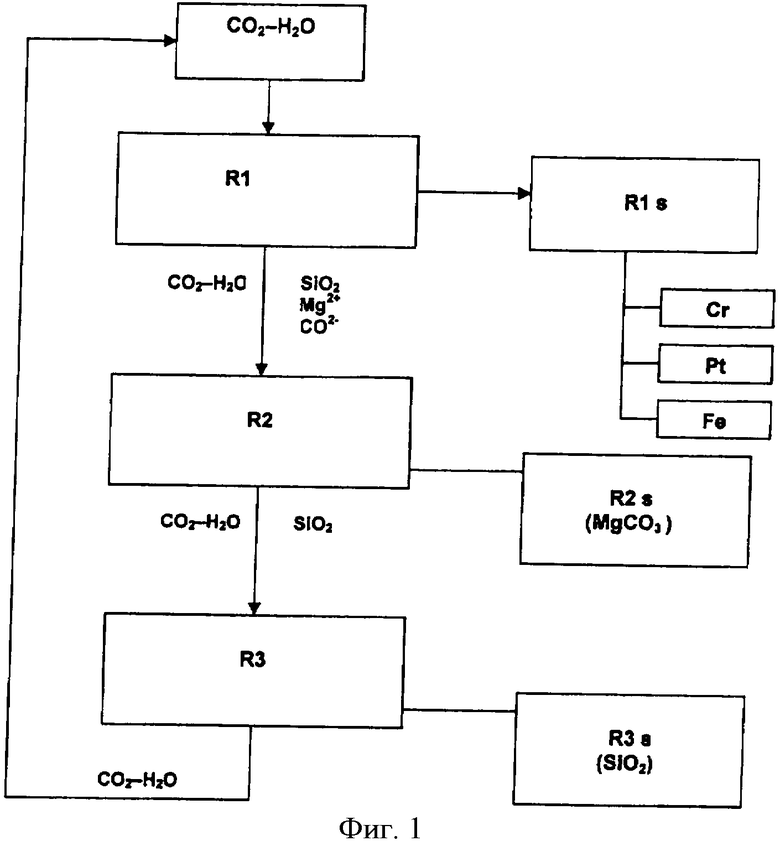
Фиг.1 - это блок-схема, которая схематично отражает основные стадии технологического процесса в соответствии с настоящим изобретением.
Фиг.2 - это схематичное изображение размещения оборудования для проведения эксперимента, описанного в примере 1.
Фиг.3 - это схематичное изображение размещения оборудования для проведения эксперимента, описанного в примере 2.
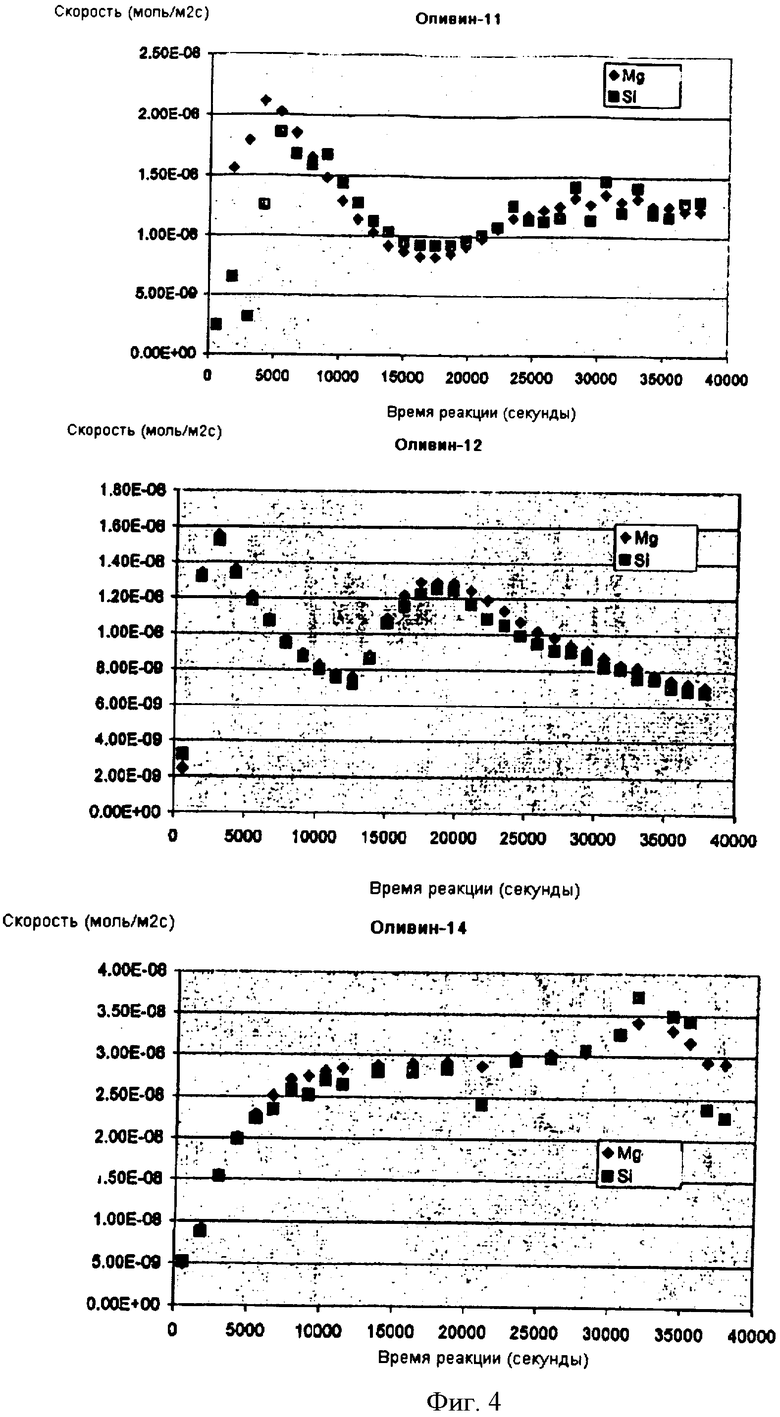
Фиг.4 - это диаграммы, показывающие вычисленные в примерах скорости реакций растворения оливина.
На фиг.1 показано, как CO2 из источника, которым может быть мусоросжигательный завод или любой другой источник СО2, смешивают с водой в верхнем блоке фиг.1. Затем в реакционную камеру, обозначенную R1, к смеси добавляют или смешивают с ней дунит. Перед этим или непосредственно в реакторе R1 дунит тонко измельчают для получения большего соотношения поверхности к объему. В воде СО2 образует угольную кислоту. Однако СO2 обладает ограниченной растворимостью в воде и большей растворимостью при высоком давлении, чем при низком. Если добавлять достаточное количество CO2 так, чтобы вода все время была насыщена СО2, рН раствора напрямую будет зависеть от давления.
На первой стадии, R1, этого способа растворение форстерита можно описать уравнением
Mg2SiO4(s)+4H+=2Mg2++SiO2(aq)+2Н2О
Для промышленных целей эта реакция протекает достаточно быстро в широком диапазоне давлений и температур, но требует кислого диапазона рН и, следовательно, определенного избыточного давления (чтобы растворить необходимое количество CO2) для достижения оптимального результата. Присутствующее железо из фаялита и другие вещества, которые в данном случае рассматривают как примеси, уже на этой стадии растворяют и осаждают в виде гидроксидов и, возможно, оксидов.
Перед тем, как жидкую реакционную смесь направляют на следующую стадию R2, твердый материал из первой стадии в виде непрореагировавших твердых компонентов и осадка из железа и возможных других осевших веществ выгружают в R1s. Твердую массу в R1s можно по желанию дополнительно переработать до конечных продуктов, таких как хром, железо и небольшие количества платины. Богатую ионами магния жидкую реакционную смесь направляют на следующую стадию, R2, на которой величина рН выше, чем на первой, для облегчения осаждения магния в виде магнезита. В соответствии с настоящим изобретением вторую стадию R2 проводят при величине рН выше, чем на первой стадии R1, а регулирование требуемого уровня рН возможно исключительно за счет понижения давления реакционной смеси, так что количество растворенного в воде СO2 автоматически снижается, что влечет снижение концентрации угольной кислоты в воде. В рамках настоящего изобретения возможно также регулировать величину рН химическим путем, но тогда способ становится менее экологичным. Более того, осаждению магнезита способствует высокая температура, поэтому температуру на стадии 2 предпочитают более высокую, чем на стадии 1. Осаждение можно также проводить без регулирования давления между стадиями 1 и 2. Обычно более высокая температура дает и более высокую величину рН. Реакцию на второй стадии R2 можно описать уравнением
Mg2++НCO3 -=MgCO3(s)+Н+, оg
Mg2++CO3 2-=MgCO3(s)
Твердую массу магнезита, MgCO3(s), направляют в R2s для дальнейшей переработки, хранения или транспортировки. Для определенных целей можно из этого продукта производить чистый (элементарный) магний.
Между первой и второй стадиями способа можно, но необязательно, возвращать часть реакционной смеси на первую стадию.
Кремний, участвующий в процессе, желательно получать в таком виде, чтобы его можно было использовать как ценный компонент в различных продуктах производства. Удобнее всего это делать на третьей стадии R3, как показано на Фиг.1, которая следует сразу за стадией 2. Осаждение кремния в виде аморфного диоксида кремния практически не зависит от рН, но проходит лучше при низкой температуре. Поэтому при переходе от стадии R2 к возможной стадии R3 температуру необходимо понизить. Перед осаждением диоксида кремния может оказаться целесообразным выпаривание раствора до более высокой концентрации. Осажденный аморфный диоксид кремния направляют в R3s. Оставшуюся жидкую фракцию возвращают на предыдущую стадию, предпочтительно на стадию 1. Между стадиями R2 и R3 можно также отбирать определенное количество жидкости для рециркуляции (не показано).
Ниже кратко перечислены наиболее типичные области применения различных компонентов продукта, но следует отметить, что настоящее изобретение не ограничено только таким применением или такими продуктами.
Твердые компоненты после стадии 1 содержат преимущественно железо, но зачастую также небольшие количества хрома и металлов платиновой группы, как отмечено выше. Из этих компонентов можно выделить соответствующие чистые металлы, которые можно использовать для производства каких-то продуктов на основе этих металлов.
Магнезит или карбонат магния после стадии 2 используют как наполнитель в бумажных и пластмассовых изделиях.
Диоксид кремния также можно использовать в качестве наполнителя в некоторых изделиях, таких как автомобильные шины, а также для производства металлического кремния, который очень ценен при высокой степени чистоты.
Как отмечено выше, настоящее изобретение требует регулирования величины рН путем добавления СO2 к воде и регулирования давления. Для облегчения процесса растворения минералов горной породы возможно, но крайне нежелательно, добавлять сильные минеральные кислоты или сильные органические кислоты. Для обеспечения промышленного способа протекания процесса горную породу необходимо дробить. Горную породу предпочтительно измельчать тонко до размера частиц (наибольшего размера) менее 3 мм, еще предпочтительнее менее 0,5 мм и для некоторых областей применения менее 0,1 мм. При традиционном способе дробления измельчение, просеивание, рециркуляция, повторное измельчение и повторное просеивание дают гарантию получения желаемого размера частиц в заданных пределах. Хотя следует подчеркнуть, что настоящее изобретение не выдвигает абсолютных требований к размеру частиц. Изобретение будет хорошо работать, если в пределах указанного размера окажется, например, только 80% объема всех частиц.
На первой стадии способа величина рН должна находиться в кислом диапазоне, то есть быть меньше приблизительно 7. Предпочтительно, чтобы величина рН на первой стадии находилась в диапазоне 3-5, хотя допустимы и более низкие значения. Величина давления в первом реакторе или реакционной камере, как правило, в интервале от 0,1 до 20 МПа (1 до 200 бар), более предпочтительно от 2 до 17 МПа (от 20 до 170 бар) и лучше всего от 5 до 15 МПа (от 50 до 150 бар). Температура на этой стадии желательна в диапазоне от 50 до 220°С и более предпочтительно в диапазоне от 100 до 170°С.
На второй стадии способа величина рН всегда выше, чем на первой, и находится предпочтительно в диапазоне 5-13. Величина давления обычно находится в диапазоне от 0,1 до 15 МПа (от 1 до 150 бар), предпочтительно от 2 до 13 МПа (от 20 до 130 бар) и более предпочтительно от 5 до 8 МПа (50 до 80 бар). Температуру на этой стадии задают в диапазоне от 100 до 300°С, лучше всего от 140 до 250°С.
Существуют различные пути разделения стадий этого способа. При непрерывном способе необходимо использование отдельных реакторов или отдельных реакционных камер для каждой стадии для поддержания постоянных условий проведения процесса в каждом реакторе или в каждой реакционной камере. Таким образом, первую стадию проводят в первой реакционной камере, а осаждение карбоната магния проводят в другой реакционной камере, в которую направляют только жидкую фракцию из первой реакционной камеры, а непрореагировавший реагент и осажденные побочные продукты из первой реакционной камеры предварительно отделяют.
Как отмечено выше, при переходе от первой реакционной камеры ко второй давление снижают, чтобы некоторое количество CO2 освободилось из раствора и величина рН соответственно возросла. Более того, при переходе от первой реакционной камеры ко второй повышают температуру, способствуя тем самым осаждению МgСО3.
Когда настоящий способ включает третью стадию, состоящую в осаждении аморфного диоксида кремния, процесс на этой стадии протекает обычно при более низкой температуре, чем на стадии 2.
В качестве оливинсодержащей горной породы предпочтительно использовать дунит.
В этом способе производства, как правило, непрерывен поток жидкости и желательно, чтобы весь процесс в целом был непрерывен.
Оксиды/гидоксиды железа вместе с нерастворимым хромитом, как правило, содержащим элементы платиновой группы (ЭПГ), выгружают из реактора растворения (стадия 1) для дополнительной промышленной переработки с целью производства железа, хрома и металлов платиновой группы.
Следует подчеркнуть, что способ производства в соответствии с настоящим изобретением ценен также тем, что он включает стадию связывания СO2, который в больших количествах является нежелательным парниковым газом и представляет большую проблему, поскольку традиционные способы производства энергии и автомобильный транспорт продолжают выбрасывать огромное количество CO2 в атмосферу во всем мире.
Примеры
Приведены два примера. Эти примеры наглядно иллюстрируют первую стадию и связь первой стадии со второй. В обоих примерах использовали оливин GL50 из месторождения Норт Кейп Минералз. Характеристика оливина ХMg=Mg/(Mg+Fе)=0,93.
Использована схема полунепрерывного способа производства с непрерывным прогоном жидкости, при котором твердую массу удерживают в реакторе. Под высоким давлением, при высокой температуре и постоянной скорости потока СO2 и Н2O закачивают в автоклав для смешивания. Затем смесь воды и растворенного CO2 направляют в реактор растворения, где она вступает в реакцию с оливином. Для предотвращения выброса твердых частиц в реакторе устанавливают фильтры.
В примере 1 водный раствор подавали в реактор растворения через клапан обратного давления для отбора проб текучей среды при комнатной температуре и атмосферном давлении. Экспериментальная схема примера 1 приведена на фиг.2.
В примере 2 водный раствор подавали из реактора растворения в реактор осаждения для кристаллизации магнезита. Для предотвращения выброса твердых частиц в этом реакторе также установлены фильтры. Ниже по потоку в реакторе осаждения раствор направляли для отбора проб при комнатной температуре и атмосферном давлении. Экспериментальная схема примера 2 приведена на фиг.3.
Пример 1. Растворение оливина на стадии 1.
Проводили серию из трех экспериментов (табл.1). Два образца измельчали и сушили в планетарной мельнице в течение различных отрезков времени. Третий образец был тщательно истолчен в ступке и просеян, при этом получена фракция с размером частиц от 75 до 150 мкм.
Все три эксперимента проводили при температуре 130°С и давлении 15 МПа (150 бар). Суммарная скорость потока 0,75 мл/мин, из которых 0,71 мл/мин - скорость H2O и 0,04 мл/мин - скорость СO2. Все звенья экспериментальной схемы были сбалансированы по высокой температуре и высокому давлению перед введением образца в реактор растворения
Скорость реакции вычисляли по следующему уравнению:
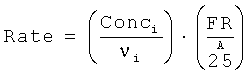
где Rate - это скорость реакции; Conci - это концентрация Mg или Si в пробах воды, vi - стехиометрические коэффициенты в оливине, 1,85 для Mg и 100 для Si соответственно; FR - скорость потока и А - площадь поверхности, анализируемая с помощью БЭТ.
Краткое изложение экспериментов приведено в табл.1. Оставшаяся после экспериментов в реакторе твердая масса включает хромит, остатки оливина, силикаты и гидроксиды железа. Скорость реакции показана на фиг.4. В вычислениях скоростей реакций не сделаны поправки на изменения площади поверхности во время эксперимента. Корреляция между скоростями реакций, вычисленных по Mg и Si на фиг.4, показывает, что реакция растворения сходная, что означает, что растворение оливина стехиометрическое (полное). Снижение массы твердого материала колеблется от 67% до 98%.
до
Пример 2. Связь между стадией 1 и осаждением магнезита на стадии 2.
В этом тесте в качестве реактора растворения использовали насадочную колонну. Условия проведения эксперимента те же, что и в предыдущем примере: температура 130°С, давление 15 МПА (150 бар), суммарная скорость потока 0,75 мл/мин, из них 0,71 мл/мин - скорость Н2O и 0,04 мл/мин - скорость СO2.
Водный раствор вводили прямо в реактор осаждения, в котором поддерживали температуру 250°С и давление 15 МПа (150 бар). На этой стадии осаждали только магнезит и получали кристаллы размером до 500 мк. При этом в реакторе осаждения не было перемешивания. Результаты анализа магнезита приведены в табл.2. Анализ проводили на микропробе. Способ предоставляет несколько возможностей определения содержания тяжелых элементов (Са, Fe, Mg, Мn) и содержания СO2, поэтому их вычисляют из стехиометрии.
Табл.2 демонстрирует высокую степень чистоты полученного магнезита, от 99,275 до 99,440%. В целом примеры показывают, что настоящее изобретение обеспечивает описанные результаты и что производить ценные продукты из горной породы с одновременным связыванием СO2 возможно.
Другие аспекты настоящего изобретения
Используя дунит как источник магния, получают очень удобное сочетание промышленных гидрометаллургических способов производства, в которых смесь СO2-H2O выступает как химический реагент.CO2 связывают с получением твердого вещества (MgCO3), которое можно оставлять на хранение или использовать. Кратко, этот другой аспект настоящего изобретения включает:
- CO2 в виде карбоната используют как анион для кристаллизации экстрагированного магния (связывание CO2);
- экстрагированный, аморфный SiO2 производят как сырье для производства металлического кремния и используют как наполнитель, например, в автомобильных шинах;
- экстрагированные Fe2O3, (Mg,Fe)Cr2O4, содержащий Pt, производят как сырье для производства Fe, Сr и Pt.
Это способ для одновременного связывания CO2 с мусоросжигательного завода или иного источника CO2, например энергетической установки, работающей на природном топливе, при котором содержащая магний, но не содержащая карбонатов горная порода, например силикатная, такая как дунит или другие оливинсодержащие горные породы, такие как периодит или подобные горные породы, вступает в реакцию со смесью CO2-Н2О с получением раствора, содержащего ионы магния и карбоната, и аморфного диоксида кремния в условиях непрерывной динамичной реакции в диапазоне температур от 50 до 300°С и диапазоне давления от 0,1 до 20 МПа (1 до 200 бар). Этот способ организован так, что преобладающий в дуните или другой оливинсодержащей породе оливин растворяют в реакторе растворения таким образом, что основная часть железа из оливина остается в реакторе растворения в виде оксида/гидроксида железа вместе с нерастворимым хромитом (Mg,Fe)Cr2O4, содержащим ЭПГ. Раствор, содержащий магний и кремний, направляют в реакторы осаждения для осаждения соответственно карбоната магния и аморфного диоксида кремния, практически не содержащих железа. Карбонат магния осаждают в первом реакторе осаждения при температуре от 100 до 300°С, давлении от 0,1 до 20 МПа (1 до 200 бар) и рН от 5 до 13, а аморфный диоксид кремния (SiO2) осаждают во втором реакторе осаждения при температуре от 20 до 300°С и давлении от 0,1 до 20 МПа (1 до 200 бар).
В способе по предыдущему абзацу оксиды/гидроксиды железа вместе с нерастворимым хромитом (Mg,Fе)Сr2O4, содержащим ЭПГ, выгружают из реактора растворения с целью дополнительной промышленной переработки для производства железа, хрома и металлов платиновой группы.
В способе по двум предыдущим соседним абзацам СO2 связывают в карбонат магния (MgCO3), который выгружают из реактора осаждения для хранения или дополнительной переработки с целью использования в качестве наполнителя, например, в бумажной или полимерной промышленности или как сырье для производства магния.
В способе по трем предыдущим соседним абзацам аморфный SiO2 выгружают из реактора осаждения и дополнительно обрабатывают, например, кислотой для получения различных свойств аморфного SiO2 с целью использования его как наполнителя в автомобильных шинах или в качестве сырья для производства кремния.
Источники информации
Фот Д.Дж., Джонс Дж.р., Ноер Дж.П., Сонг И. (2000). Связывание диоксида углерода в виде карбонатов. Проц. ежегодная междунар. конференция угля в Питтсбурге 17:1154-1160.
Бланке Дж.Ж. (2004). Карбонизация металлических силикатов для продолжительного связывания СO2. Заявка на патент США 20050180910.
Джидик Д., Гросс К.Б., Горский Р.А., Джонсон Дж.Т. (2004). Связывание диоксида углерода. Заявка на патент США 20040219090.
Марото-Валер М.М., Жанг И., Кутча М.Е., Андресен Дж.М., Фот Д.Дж. (2005). Способ связывания диоксида углерода и диоксида серы. Заявка на патент США 20050002847.
О'Коннор В.К., Далин Д.К., Раш Ж.Е., Далин К.Л., Коллинз В.К. (2002). Связывание диоксида углерода путем прямой карбонизации минералов: обработанный минералогический состав первоначального материала и продуктов. Минералы и металлургическое производство 19:95-101.
О'Коннор В.К., Далин Д.К., Раш Ж.Е., Гердеманн С.Дж., Пеннер Л.Р., Нильсен Д.Н. (2005). Итоговый доклад - карбонизация минералов в воде. Добыча минералов, предварительная обработка, параметрика реакции и исследование процесса. DOE/ARC-TR-04-002.
Парк А.Х., Фэн Л.С.(2005). Связывание диоксида углерода с использованием минералов, содержащих щелочно-земельные металлы. Заявка на патент США 20050180910.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОБРАБОТКИ СИЛИКАТНОГО МИНЕРАЛА | 2013 |
|
RU2654983C2 |
| СПОСОБ ПОЛУЧЕНИЯ CaCO ИЛИ MgCO | 2005 |
|
RU2389687C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРИДА МАГНИЯ ШЕСТИВОДНОГО | 2020 |
|
RU2737659C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА МАГНИЯ ИЗ ТАЛЬКОМАГНЕЗИТОВЫХ РУД И ОТХОДОВ ОБОГАЩЕНИЯ ТАЛЬКА ИЗ ТАЛЬКОМАГНЕЗИТОВЫХ РУД | 2008 |
|
RU2372289C1 |
| СОВМЕСТНО ПРОВОДИМЫЙ ХИМИЧЕСКИЙ ПРОЦЕСС | 2007 |
|
RU2446871C2 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ МАГНИЙ-СИЛИКАТСОДЕРЖАЩЕГО СЫРЬЯ | 2005 |
|
RU2285666C1 |
| ОСАЖДЕННЫЙ КАРБОНАТ МАГНИЯ | 2010 |
|
RU2518895C2 |
| Способ получения оксида алюминия и карбоната из богатых Al материалов с интегрированной утилизацией CO | 2015 |
|
RU2683754C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛИЧЕСКОГО МАГНИЯ, СПОСОБ ПОЛУЧЕНИЯ ЧИСТОГО ОКСИДА МАГНИЯ (ВАРИАНТЫ) И СПОСОБ ПЕРЕРАБОТКИ ИСХОДНОГО МАТЕРИАЛА | 1992 |
|
RU2109078C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДА МАГНИЯ ИЗ ПРИРОДНЫХ РАССОЛОВ | 2001 |
|
RU2211803C2 |


Изобретение может быть использовано в химической промышленности. Способ промышленного производства чистого MgCO3 включает измельчение содержащей оливин горной породы и контакт измельченной породы с водой и CO2. На первой стадии, проводимой под давлением, происходит реакция растворения согласно уравнению Mg2SiO4(s)+4H+=2Mg2++SiO2(aq)+2H2O. Затем на второй стадии проводят осаждение при более высокой величине рН. При этом происходят следующие реакции: Mg2++HCO3 -=MgCO3(s)+H+ и Mg2++СО3 2-=MgCO3(s). Присутствие ионов НСО3 - и H+ является, главным образом, результатом взаимодействия СO2 и воды. Изобретение позволяет производить чистый карбонат магния из горной породы, связывая при этом свободный углекислый газ. 18 з.п. ф-лы, 4 ил., 2 табл.
1. Способ промышленного производства чистого MgCO3, включающий поставку оливинсодержащей горной породы, измельчение этой породы для увеличения ее поверхности, контакт измельченной породы с водой и CO2, отличающийся тем, что этот способ осуществляют по крайней мере в две стадии, а именно первая стадия, осуществляемая под давлением, при одном рН, на которой реакция растворения обычно проходит согласно уравнению:
Mg2SiO4(s)+4H+=2Mg2++SiO2(aq)+2H2O,
а затем на второй стадии проводят осаждение при более высоком рН и реакцию на второй стадии обычно представляют уравнениями:
Mg2++HCO3=MgCO3(s)+H+ и
Mg2++CO3 2-=MgCO3(s),
при этом присутствие ионов НСО3 - и Н+ является, главным образом, результатом взаимодействия СO2 и воды.
2. Способ по п.1, отличающийся тем, что оливинсодержащую горную породу измельчают обычно до размера частиц менее 3 мм, более предпочтительно менее приблизительно 0,5 мм и самое предпочтительное менее 0,1 мм.
3. Способ по п.1, отличающийся тем, что величина рН на первой стадии находится в диапазоне 3-5, а величина рН на второй стадии при осаждении карбоната магния в диапазоне 5-13.
4. Способ по п.1, отличающийся тем, что железо, присутствующее в сырье, осаждают в виде гидроксида железа на первой стадии.
5. Способ по п.1, отличающийся тем, что первую стадию проводят в одной реакционной камере, а осаждение карбоната магния проводят в другой реакционной камере, в которую поступает только жидкая фракция из первой реакционной камеры, тогда как непрореагировавший реагент и осажденные побочные продукты из первой реакционной камеры выгружают.
6. Способ по п.5, отличающийся тем, что при переходе от первой реакционной камеры ко второй давление понижают, чтобы высвободить часть СО2 из раствора, и соответственно, повысить уровень рН.
7. Способ по п.5, отличающийся тем, что во второй реакционной камере создают более высокую температуру, чем в первой реакционной камере, для облегчения осаждения MgCO3.
8. Способ по любому из предыдущих пунктов, отличающийся тем, что дополнительно проводят третью стадию, на которой осаждают аморфный диоксид кремния (SiO2).
9. Способ по п.8, отличающийся тем, что SiO2 осаждают из реакционной смеси после осаждения MgCO3 и при более низкой температуре.
10. Способ по п.5, отличающийся тем, что давление в первой реакционной камере находится в диапазоне от 2 до 17 МПа (от 20 до 170 бар) и наиболее предпочтительно от 5 до 15 МПа (от 50 до 150 бар).
11. Способ по п.5, отличающийся тем, что температура в первой реакционной камере находится в диапазоне от 50 до 220°С, наиболее предпочтительно от 100 до 170°С.
12. Способ по п.5, отличающийся тем, что давление во второй реакционной камере находится в диапазоне от 0,1 до 15 МПа (от 1 до 150 бар), более предпочтительно от 2 до 13 МПа (от 20 до 130 бар) и самое предпочтительное от 5 до 8 МПа (от 50 до 80 бар).
13. Способ по п.5, отличающийся тем, что температура во второй реакционной камере находится в диапазоне от 100 до 300°С, наиболее предпочтительно от 140 до 250°С.
14. Способ по п.1, отличающийся тем, что оливинсодержащей горной породой является дунит.
15. Способ по п.1, отличающийся тем, что поток жидкости протекает непрерывно.
16. Способ по п.15, отличающийся тем, что весь процесс полностью непрерывен.
17. Способ по п.1, отличающийся тем, что реакция растворения протекает без применения сильных минеральных кислот и сильных органических кислот.
18. Способ по п.5, отличающийся тем, что горную породу измельчают до размера частиц менее 0,1 мм, давление в первой реакционной камере находится в диапазоне от 5 до 15 МПа (от 50 до 150 бар), давление во второй реакционной камере находится в диапазоне от 5 до 8 МПа (от 50 до 80 бар), величина рН в первой реакционной камере находится в диапазоне от 3 до 5, величина рН во второй реакционной камере находится в диапазоне от 5 до 13, температура в первой реакционной камере находится в диапазоне от 100 до 170°С, температура во второй реакционной камере находится в диапазоне от 140 до 250°С, в способе не используют никакой кислоты, кроме растворенного в воде CO2, и способ непрерывен.
19. Способ по п.1, отличающийся тем, что полученный MgCO3 имеет чистоту в диапазоне от 99,275 до 99,440%.
| US 2005180910 A1, 18.08.2005 | |||
| O'CONNOR W.K | |||
| et al., Carbon dioxide sequestration by direct mineral carbonation: process mineralogy of feed and products | |||
| Minerals & Metallurgical processing, 2002, vol.19, no.2, p.95-101 | |||
| Способ получения обезвоженного карбоната магния | 1988 |
|
SU1704626A3 |
| US 2004219090 Al, 04.11.2004 | |||
| УСТРОЙСТВО Для ПРОГРАММНОГО УПРАВЛЕНИЯ | 0 |
|
SU248036A1 |
| ХИМИЧЕСКАЯ ЭНЦИКЛОПЕДИЯ | |||
| / Под ред. | |||
Авторы
Даты
2011-12-27—Публикация
2006-11-23—Подача