ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к ряду новых лигандов меланокортиновых рецепторов, применяемых при лечении заболеваний, реагирующих на модуляцию таких рецепторов. Изобретение также относится к фармацевтическим композициям, включающим такие пептидные аналоги, а также к их применению в профилактике или лечении патологических состояний, опосредованных этими рецепторами.
УРОВЕНЬ ТЕХНИКИ
Меланокортины являются семейством регуляторных пептидов, которые образуются в результате посттрансляционного процессинга прогормона проопиомеланокортина (POMC, длина 131 аминокислота). POMC процессируется с образованием трех классов гормонов: меланокортинов, включая, помимо прочих, α-MSH (меланоцитостимулирующий гормон), β-MSH и γ-MSH, адренокортикотропного гормона (ACTH), различных эндорфинов (например липотропин) (Cone, R.D. et al., Recent Prog. Horm. Res., 51:287-317 (1996); а также Cone, R.D. et al., Ann. N.Y. Acad. Sci., 31:342-63 (1993)) и их пептидных фрагментов. Меланокортины были обнаружены во множестве нормальных тканей человека, включая мозг, надпочечники, кожу, яички, селезенку, почки, яичники, легкие, щитовидную железу, печень, толстую кишку, тонкую кишку и поджелудочную железу (Tatro, J. B. et al., Endocrinol., 121:1900-7 (1987); Mountjoy, K. G. et al., Science, 257:1248-51 (1992); Chhajlani, V. et al., FEBS Lett., 309:417-20 (1992); Gantz, I. et al., J. Biol. Chem., 268:8246-50 (1993) и Gantz, I. et al., J. Biol. Chem., 268:15174-9 (1993)).
Меланокортиновые пептиды, как установили, выполняют множество разнообразных физиологических функций, включая контроль поведения и памяти, влияние на нейротрофические и антипиретические свойства, а также влияние на модуляцию иммунной системы. Помимо своего известного воздействия на функции коры надпочечников (адренокортикотропный гормон, ACTH) и на меланоциты (меланоцитостимулирующий гормон, MSH), меланокортины, как установили, также управляют сердечно-сосудистой системой, анальгезией, терморегуляцией и секрецией других нейрогуморальных агентов, включая пролактин, лютеинизирующий гормон и биогенные амины (De Wied, D. et al., Methods Achiev. Exp. Pathol., 15:167-199 (1991); De Wied, D. et al., Physiol. Rev., 62:977-1059 (1982); Guber, K. A. et al., Am. J. Physiol. 257:R681-R94 (1989); Walker, J.M. et al., Science, 210:1247-9 (1980); Murphy, M. T. et al., Science, 221:192-3 (1983); Ellerkmann, E. et al., Endocrinol., 130:133-8 (1992), а также Versteeg, D. H. G. et al., Life Sci., 38:835-40 (1986)).
Также было показано, что сайты связывания меланокортинов распределены во многих типах различных тканей, включая слезные и подчелюстные железы, поджелудочную железу, жировую ткань, мочевой пузырь, двенадцатиперстную кишку, селезенку, ткани мозга и гонадные ткани, а также злокачественные меланомы. На данный момент описано пять меланокортиновых рецепторов (MC-R). Они включают меланоцит-специфичный рецептор (MC1-R), кортикоадренальный рецептор АКТГ (MC2-R), рецептор меланокортина-3 (MC3-R), меланокортина-4 (MC4-R) и меланокортина-5 (MC5-R). Все меланокортиновые рецепторы реагируют на класс пептидных гормонов - меланоцитстимулирующих гормонов (МСГ) (Cone, R. D. et al., Ann. N. Y. Acad. Sci., 680:342-63 (1993); и Cone, R. D. et al., Recent Prog. Horm. Res., 51:287-318 (1996)).
MC1-R, известный в уровне техники как рецептор меланоцитстимулирующего гормона (MSH-R), рецептор меланотропина или рецептор меланокортина-1, является трансмембранным белком размером 315 аминокислот, принадлежащим к семейству серпентиновых рецепторов, связанных с G-белками. MC1-R является рецептором и для МСГ, и для АКТГ. Активность MC1-R опосредована G-белками, которые активируют аденилатциклазу. Рецепторы MC1-R обнаружены в меланоцитах и ткани коры надпочечников, а также в других различных тканях, таких как надпочечники, лейкоциты, легкие, лимфатические узлы, яичники, мужские половые железы, гипофиз, плацента, селезенка и матка. MC2-R, также называемый рецептором адренокортикотропного гормона (ACTH-R), является трансмембранным белком размером 297 аминокислот, который присутствует в меланоцитах и ткани коры надпочечников. MC2-R опосредует кортикотропный эффект АКТГ. У людей MC3-R является трансмембранным белком размером 360 аминокислот, который присутствует в ткани мозга; у мышей и крыс MC3-R является трансмембранным белком размером 323 аминокислоты. MC4-R является трансмембранным белком размером 332 аминокислоты, который экспрессируется в мозге, а также в плацентарной ткани и тканях кишечника. MC5-R является трансмембранным белком размером 325 аминокислот, который экспрессируется в надпочечниках, желудке, легких и селезенке, а также, на очень низких уровнях, в мозге. MC5-R также экспрессируется в трех слоях коры надпочечников, преимущественно в альдостерон-продуцирующих клетках клубочковой зоны.
Пять известных меланокортиновых рецепторов отличаются, однако, по своим функциям. Например, MC1-R представляет собой рецептор, связанный с G-белком, который регулирует пигментацию в ответ на α-МСГ, активный агонист MC1-R. Агонизм рецептора MC1-R приводит к возбуждению меланоцитов, которые выделяют эумеланин, а также увеличивает риск развития рака кожи. Агонизм MC1-R может также вызывать неврологические эффекты. Стимуляция активности MC2-R может привести к возникновению карциномы ткани надпочечников. Недавнее фармакологическое исследование позволило установить, что центральные MC4-R рецепторы являются главными медиаторами анорексических и орексигенных эффектов, описанных для агонистов и антагонистов меланокортина, соответственно. Эффекты агонизма MC3-R и MC5-R пока не изучены.
Рецепторы меланокортина (MC-R) представляли большой интерес в качестве мишеней для разработки новых терапевтических средств, направленных на лечение нарушений массы тела, таких как ожирение и кахексия. И генетические, и фармакологические исследования указывают на центральные MC4-R рецепторы как на основную мишень (Giraudo, S. Q. et al., Brain Res., 809:302-6 (1998); Farooqi, I. S. et al., N.E. J. Med., 348:1085-95 (2003); MacNeil, D. J. et al., Euro. J. Pharm., 44:141-57 (2002); MacNeil, D. J. et al., Euro. J. Pharm., 450:93-109 (2002); Kask, A. et al., NeuroReport, 10:707-11 (1999); Huszer, D. et al., Cell, 131-41 (1997); Klebig, M. L. et al., Proc. Natl. Acad. Sci., 92:4728-32 (1995); Karbon, E. et al., Abstr. 19th Ann. Winter Neuropeptide Conf., (1998); Fan, W. et al., Nature, 385:165-8 (1997); Seely, R. J., Nature, 390:349 (1997); Comuzzie, A. G., Nat. Gen., 15:273-6 (1997); Chagnon, Y. C., Mol. Med., 3(10):663-73 (1997); WO 97/47316 (Lee et al., 1997); а также Shutter, J. R., Gen. & Dev., 11:593-602 (1997)). Стимуляция MC-4 рецептора его эндогенным лигандом, α-МСГ, индуцирует сигнал насыщения. Предполагается, что с помощью эффективных агонистов MC-4 рецептора может быть подавлен аппетит и достигнуто снижение веса.
Сегодняшний прогресс в отношении рецептор-селективных агонистов и антагонистов свидетельствует о терапевтическом потенциале активации меланокортиновых рецепторов, в особенности MC4-R.
Агонисты, антагонисты или другие соединения-лиганды, активирующие один или несколько меланокортиновых рецепторов, могут применяться для лечения при широком спектре показаний у нуждающегося в этом субъекта, или с риском их развития, включая острые и хронические воспалительные заболевания, такие как генерализованное воспаление (патент США 6613874 (Mazur et al., 2003) и Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), воспалительная болезнь кишечника (патент США 6713487 (Yu et al., 2004) и Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), воспаление мозга (Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), сепсис (патент США 6613874 (Mazur et al., 2003), патент США 6713487 (Yu et al., 2004) и Catania, A. et al., Pharm. Rev., 56:1-29 (2004)) и септический шок (патент США 6613874 (Mazur et al., 2003) и Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), заболевания с аутоиммунным фактором, такие как ревматоидный артрит (патент США 6713487 (Yu et al., 2004) и Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), подагрический артрит (Catania, A. et al., Pharm. Rev., 56:1-29 (2004) и Getting, S. J. et al., Curr. Opin. Investig. Drugs, 2:1064-9 (2001)), а также рассеянный склероз (патент США 6713487 (Yu et al., 2004)), нарушения обмена веществ и заболевания, сопровождаемые увеличением массы тела, такие как ожирение (патент США 6613874 (Mazur et al., 2003); патент США 6600015 (Chen et al., 2003); Fehm, H. L. et al., J. Clin. Endo. и Metab., 86:1144-8 (2001); Hansen, М. J. et al., Brain Res., 1039:137-45 (2005); Ye, Z. et al., Peptides, 26:2017-25 (2005); Farooqi, I. S. et al., N.E. J Med., 348:1085-95 (2003); MacNeil, D. J. et al., Eu. J. Pharm., 44:141-57 (2002); MacNeil, D. J. et al., Euro. J. Pharm., 450:93-109 (2002); Kask, A. et al., NeuroReport, 10:707-11 (1999); Schwartz, M. W., J. Clin. Invest., 108:963-4 (2001); Gura, T., Science, 287:1738-40 (2000); Raffin-Sanson, M. L., Euro. J. Endo., 144:207-8 (2001); а также Hamilton, B. S. et al., Obesity Res.,10:182-7 (2002)), пищевые расстройства (патент США 6720324 (Marzabadi et al., 2004); Fehm, H. L. et al., J. Clin. Endo. & Metab., 86:1144-8 (2001); и Pontillo, J. et al., Bioorganic & Med. Chem. Ltrs., 15:2541-6 (2005)), а также синдром Прадера-Вилли (GE, Y. et al., Brain Res., 957:42-5 (2002)), метаболические заболевания и патологические состояния, сопровождаемые потерей массы тела, такие как анорексия (патент США 6613874 (Mazur et al., 2003) и Wisse, B. R. et al., Endocrinology, 142:3292-301 (2001)), булимия (патент США 6720324 (Marzabadi et al., 2004)), истощение при СПИДе (Marsilje, T. H. et al., Bioorg. Med. Chem. Lett., 14:3721-5 (2004); и Markison, S. et al., Endocrinology, 146:2766-73 (2005)), кахексия (патент США 6613874 (Mazur et al., 2003); Lechan, R. M. et al., Endocrinology, 142:3288-91 (2001); и Pontillo, J. et al., Bioorganic & Med. Chem. Ltrs., 15:2541-6 (2005)), онкологическая кахексия (патент США 6639123 (Van der Ploeg et al., 2003)) и истощение у ослабленных пожилых людей (патент США 6639123 (Van der Ploeg et al., 2003)), диабет (патент США 6713487 (Yu et al., 2004)) и патологические состояния, связанные с диабетом, и осложнения диабета, такие как ретинопатия (патент США 6525019 (D'Amato, 2003), опухолевая пролиферация (патент США 6713487 (Yu et al., 2004)), например рак кожи (Буря, R. A., Melanoma Res., 12:405-16 (2002); и Bastiens, М. T. et al., Am. J. Hum. Genet., 68:884-94 (2001)), и рак простаты (Luscombe, C. J. et al., British J. Cancer, 85:1504-9 (2001)), репродуктивные или половые заболевания, такие как эндометриоз (патент США 6713487 (Yu et al., 2004)), а также маточное кровотечение у женщин (патент США 6613874 (Mazur et al., 2003)), половая дисфункция (патент США 6720324 (Marzabadi et al., 2004); Van der Ploeg, L. H. T. et al., PNAS, 99:11381-6 (2002), Molinoff, P. B. et al., Ann. N. Y. Acad. Sci., 994:96-102 (2003), и Hopps, C. V. et al., B. J. U. Int'l., 92:534-8 (2003)), эректильная дисфункция ((патент США 6613874 (Mazur et al., 2003); Diamond, L. E. et al., Urology, 65:755-9 (2005); Wessells, H. et al., Int'l. J. Impotence Res., 12:S74-9 (2000); Andersson, K-E. et al., Int'l. J. Impotence Res., 14:S82-S92 (2002); Bertolini, A. et al., Sexual Behavior: Pharmacology and Biochemistry, Raven Press, NY, p 247-57 (1975); Wessells, H. et al., Neuroscience, 118:755-62 (2003); Wessells, H. et al., Urology, 56:641-6 (2000); Shadiack, A. M. et al., Soc. for Neuroscience Abst, (2003); Wessells, H. et al., J. Urology, 160:389-93 (1998); Rosen, R. C. et al., Int'l. J. Impotence Res., 16:135-42 (2004); and Wessells, H. et al., Peptides, 26:1972-7 (2005)) и сниженное половое влечение у женщин (патент США 6713487 (Yu et al., 2004); и Fourcroy, J. L., Drugs, 63:1445-57 (2003)), заболевания или нарушения в результате терапии или повреждения организма, например, при отторжении трансплантата (патент США 6713487 (Yu et al., 2004); и Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), ишемия и реперфузионное повреждение (Mioni, C. et al., Euro. J. Pharm., 477:227-34 (2003); и Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), терапия повреждения спинного мозга и для ускорения заживления ран (Sharma H. S. et al., Acta. Nerochir. Suppl., 86:399-405 (2003); Sharma H. S., Ann. N. Y. Acad. Sci., 1053: 407-21 (2005); и патент США 6525019 (D'Amato, 2003)), а также потеря веса, вызванная химиотерапией, лучевой терапией, временной или постоянной иммобилизацией (Harris, R. B. et al., Physiol. Behav., 73:599-608 (2001)), или диализом, сердечно-сосудистые заболевания или патологические состояния, такие как геморрагический шок (Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), кардиогенный шок (патент США 6613874 (Mazur et al., 2003)), гиповолемический шок (патент США 6613874 (Mazur et al., 2003)), сердечно-сосудистые нарушения (патент США 6613874 (Mazur et al., 2003)) и сердечная кахексия (Markison, S. et al., Endocrinology, 146:2766-73 (2005)), заболевания или патологические состояния легких, такие как острый респираторный дистресс-синдром (патент США 6350430 (Dooley et al., 2002); и Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), хроническая обструктивная болезнь легких (патент США 6713487 (Yu et al., 2004)), астма (патент США 6713487 (Yu et al., 2004)) и фиброз легких, для повышения иммунной толерантности (Luger, T. A. et al., Pathobiology, 67:318-21 (1999)), а также для противодействия угрозам иммунной системе, например, связанным с некоторыми типами аллергий (патент США 6713487 (Yu et al., 2004)), или отторжение трансплантата (патент США 6713487 (Yu et al., 2004)); и Catania, A. et al., Pharm. Rev., 56:1-29 (2004)), лечение дерматологических заболеваний и патологических состояний, таких как псориаз (патент США 6713487 (Yu et al., 2004)), снижение пигментации кожи (патент США 6713487 (Yu et al., 2004); и Ye, Z. et al., Peptides, 26:2017-25 (2005)), акне (Hatta, N. et al., J. Invest. Dermatol., 116:564-70 (2001); и Bohm, M. et al., J. Invest. Dermatol., 118:533-9 (2002)), келоидное образование (патент США 6525019 (D'Amato, 2003)) и рак кожи (Sturm, R.A., Melanoma Res., 12:405-16 (2002); и Bastiens, М. T. et al., Am. J. Hum. Genet., 68:884-94 (2001)), поведенческие, центральной нервной системы или нервные заболевания и нарушения, такие как тревожное рассторойство (патент США 6720324 (Marzabadi et al., 2003); и Pontillo, J. et al., Bioorganic & Med. Chem. Ltrs., 15:2541-6 (2005)), депрессия (Chaki, S. et al., Peptides, 26:1952-64 (2005), Bednarek, M. A. et al., Expert Opinion Ther. Patents, 14:327-36 (2004); и патент США 6720324 (Marzabadi et al., 2003)), память и дисфункция памяти (патент США 6613874 (Mazur et al., 2003); и Voisey, J. et al., Curr. Drug Targets, 4:586-97 (2003)), модуляция ощущения боли (патент США 6613874 (Mazur et al., 2003); Bertolini, A. et al., J. Endocrinol. Invest., 4:241-51 (1981); и Vrinten, D. et al., J. Neuroscience, 20:8131-7 (2000)) и терапия нейропатической боли (Pontillo, J. et al., Bioorganic & Med. Chem. Ltrs., 15:2541-6 (2005)), нарушения и заболевания, связанные с употреблением алкоголя, алкогольной зависимостью и/или алкоголизмом (WO 05/060985 (Marsh et al., 2005); и Navarro, M. et al., Alcohol Clin. Exp. Res., 29:949-57 (2005)), и нарушения и заболевания почек, такие как лечение почечной кахексии (Markison, S. et al., Endocrinology, 146:2766-73 (2005)) или натрийурез (патент США 6613874 (Mazur et al., 2003)).
Соединения-лиганды, активирующие один или несколько меланокортиновых рецепторов, могут применяться для модуляции большого разнообразия нормализующих или гомеостатических функций у субъекта, испытывающего в этом потребность, включая секрецию тироксина (патент США 6613874 (Mazur et al., 2003)), синтез и секрецию альдостерона (патент США 6613874 (Mazur et al., 2003)), температуру тела (патент США 6613874 (Mazur et al., 2003)), кровяное давление (патент США 6613874 (Mazur et al., 2003)), частоту сердечных сокращений (патент США 6613874 (Mazur et al., 2003)), сосудистый тонус (патент США 6613874 (Mazur et al., 2003)), мозговое кровообращение (патент США 6613874 (Mazur et al., 2003)), уровни глюкозы в крови (патент США 6613874 (Mazur et al., 2003)), костный метаболизм, образование или развитие костной ткани (Dumont, L. M. et al., Peptides, 26:1929-35 (2005)), вес яичников (патент США 6613874 (Mazur et al., 2003)), развитие плаценты (патент США 6613874 (Mazur et al., 2003)), секреция пролактина и ФСГ (патент США 6613874 (Mazur et al., 2003)), внутриутробный рост плода (патент США 6613874 (Mazur et al., 2003)), роды (патент США 6613874 (Mazur et al., 2003)), сперматогенез (патент США 6613874 (Mazur et al., 2003)), секреция кожного сала и феромонов (патент США 6613874 (Mazur et al., 2003)), нейропротекция (патент США 6639123 (Van der Ploeg et al., 2003)) и рост нервов (патент США 6613874 (Mazur et al., 2003)), а также стимуляция модуляции (патент США 6613874 (Mazur et al., 2003)), обучение (патент США 6613874 (Mazur et al., 2003)) и другие поведения (патент США 6613874 (Mazur et al., 2003)).
Гидантоин (C3H2N2O2), также известный как гликолилмочевина или под своим названием IUPAC - имидазол-2,4(3H,5H)-дион, является кристаллическим гетероциклическим органическим соединением, которое можно рассматривать как циклический продукт реакции двойной конденсации гликолевой кислоты и мочевины или аллантоина, продукта окисления (C4H6N4O3) мочевой кислоты, которая является конечным метаболическим продуктом окисления пурина у позвоночных. Гидантоин, имеющий следующую химическую структуру:
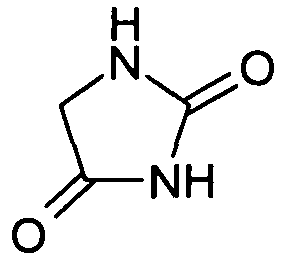
подобен имидазолидину, гидроген-насыщенному аналогу имидазола за исключением того, что имеет карбонильные группы во 2-м и 4-м положениях кольца. Он имеет молекулярную массу 100,076 г/моль, малорастворим в воде и имеет точку плавления 216-224°C. Гидантоин и его производные обладают антибактериальным, противогрибковым, противопротозойным и антигельминтным свойствами. Гидантоин традиционно являлся компонентом антиконвульсантов, применяемых при лечении судорог, связанных с эпилепсией. Предполагается, что гидантоины подавляют патологические нервные импульсы в центральной нервной системе. Фенитоин, другой антиконвульсант, синтезируемый из гидантоина, используют в качестве миорелаксанта и для лечения тяжелой невралгии тройничного нерва.
Авторы изобретения обнаружили класс соединений, которые обладают высокой аффинностью к меланокортиновым рецепторам, в частности селективны к MC-4 подтипу по сравнению с рецепторами других подтипов, в особенности к MC-5 подтипу. В частности, авторы изобретения обнаружили, что пептиды, модифицированные гидантоином, демонстрировали повышенную аффинность к рецептору подтипа MC-4. Таким образом, цель настоящего изобретения состоит в обеспечении химических соединений, которые активируют или являются антагонистами рецептора подтипа MC-4. Другая цель настоящего изобретения состоит в обеспечении лигандов меланокортиновых рецепторов, которые обладают более высокой стабильностью и селективностью к меланокортиновым рецепторам, чем нативные лиганды меланокортиновых рецепторов. Еще одна цель изобретения состоит в обеспечении способа введения указанных соединений для лечения различных заболеваний и/или нарушений, связанных либо с избыточной, либо с недостаточной выработкой меланокортиновых пептидов.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Авторы изобретения обнаружили новый класс циклических пептидных аналогов, модифицированных гидантоиновой группой, которые являются лигандами меланокортиновых рецепторов и селективны в отношении рецептора подтипа MC-4. Одной из уникальных структурных особенностей данного нового класса является использование неприродных или синтетических аминокислотных остатков в N-концевой области. Подобные замены вносят вклад не только в селективность соединения, но также и в аффинность связывания с целевым рецептором. Указанные новые соединения связываются с рецептором MC-4 с низкой наномолярной аффинностью и демонстрируют увеличенный период полувыведения в плазме по сравнению с α-МСГ. Исследования с использованием самцов крыс линии Спраг-Доули указывают, что данные новые соединения эффективно подавляют потребление пищи и вызывают снижение массы тела.
В частности настоящее изобретение направлено на соединения согласно формуле (I), (II) или (III), а также соответствующие фармацевтически приемлемые соли, гидраты, сольваты или пролекарства, применяемые в качестве модуляторов одного или нескольких меланокортиновых рецепторов. Изобретение также охватывает их применение, особенно в качестве лекарственных средств, для лечения конкретных, идентифицируемых заболеваний и/или патологических состояний. Согласно первому аспекту изобретение обеспечивает соединение формулы (I), его фармацевтически приемлемые соли, гидраты, сольваты и/или пролекарства:
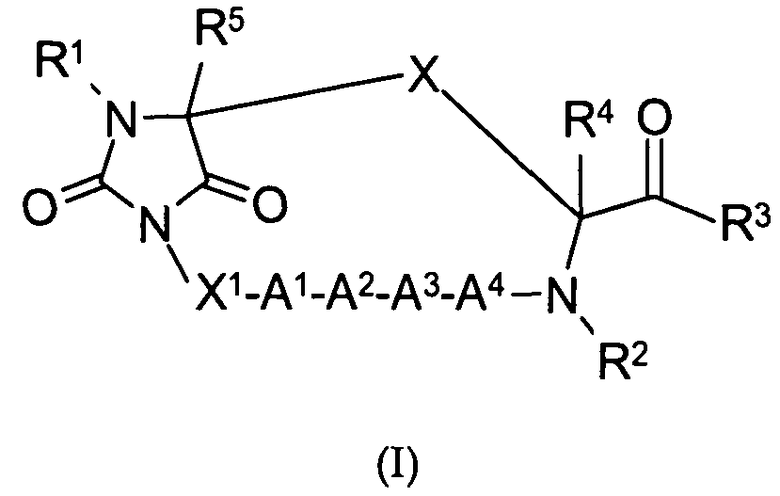
в котором гидантоиновая группа образована в результате конденсации аминогруппы X1, то есть
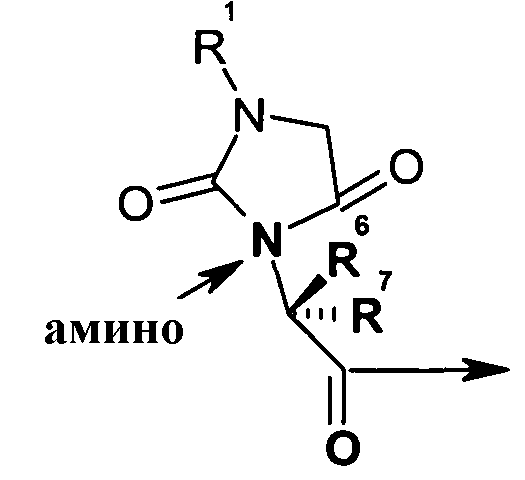
с амино и карбоксильной группами одной из аминокислот, включающих X, то есть
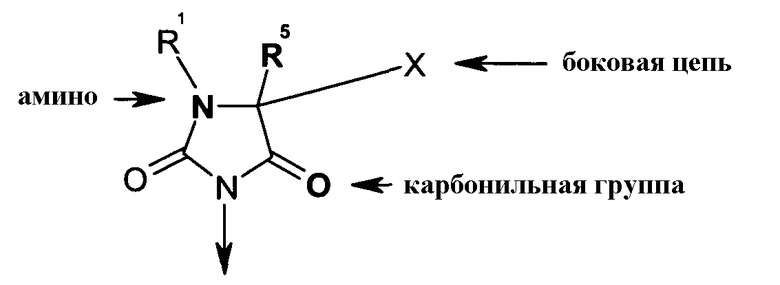
вместе с карбонильной группой, то есть
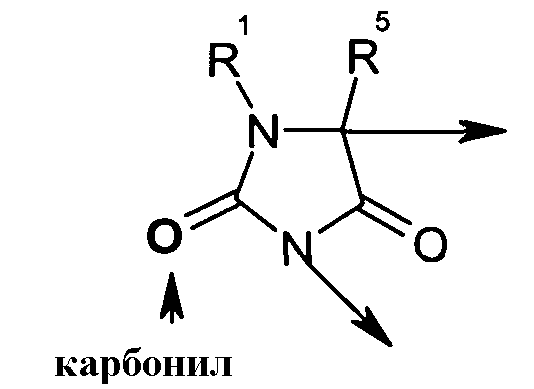 .
.
В сокращенном обозначении, используемом авторами изобретения для идентификации варианта осуществления формулы (I), например, цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:1) "Гидантоин(C(O)-(AA1-AA2)" относится к аминокислотам, которые формируют гидантоиновую структуру. В указанном выше варианте осуществления, "C(O)" относится к карбонильной группе, расположенной между двумя атомами азота имидазолинильного гетероциклического кольца. Указанная первой аминокислота "AA1" в данном примере представляет собой Cys и отдает свою N-концевую амино и C-концевую карбоксильную группы, формируя отмеченную часть гидантоиновой группы, как показано ниже:
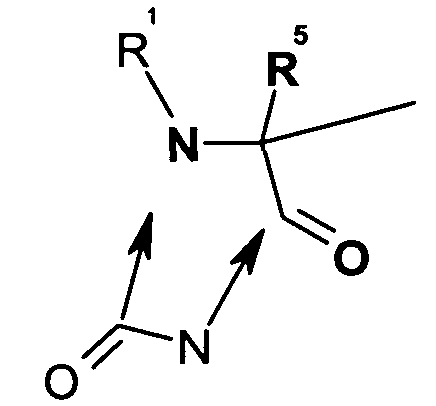
(часть гидантоиновой группы, не являющаяся частью AA1, отсутствует). В наглядном примере AA2 является D-Ala, где его N-концевая аминогруппа включает часть гидантоиновой структуры, выделенную жирным ниже,
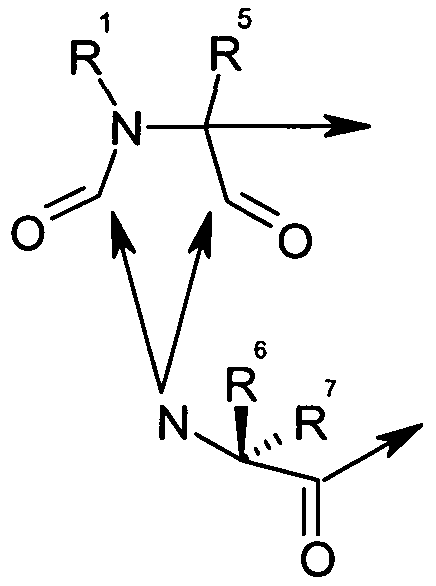
R7 является метилом, а R6 является водородом.
В предпочтительном варианте осуществления соединений согласно формуле (I), в дальнейшем называемых соединениями Группы I, X выбран из группы, состоящей из -CH2-S-S-CH2-, -C(CH3)2-S-S-CH2-, -CH2-S-S-C(CH3)2-, -C(CH3)2-S-S-C(CH3)2-, -(CH2)2-S-S-CH2-, -CH2-S-S-(CH2)2-, -(CH2)2-S-S-(CH2)2-, -C(CH3)2-S-S-(CH2)2-, -(CH2)2-S-S-C(CH3)2-, -(CH2)t-C(O)-NR8-(CH2)r- и -(CH2)r-NR8-C(O)-(CH2)t-;
каждый R1 и R2 независимо является H, (C1-C10)алкилом или замещенным (C1-C10)алкилом;
R3 представляет собой -ОН или -NH2;
каждый R4 и R5 независимо является H, (C1-C10)алкилом или замещенным (C1-C10)алкилом;
X1 представляет собой  ;
;
A1 представляет собой His, 2-Pal, 3-Pal, 4-Pal, (X1,X2,X3,X4,X5)Phe, Taz, 2-Thi, 3-Thi или отсутствует;
A2 представляет собой D-Bal, D-1-Nal, D-2-Nal, D-Phe или D-(X1,X2,X3,X4,X5)Phe;
A3 представляет собой Arg, hArg, Dab, Dap, Lys или Orn;
A4 представляет собой Bal, 1-Nal, 2-Nal, (X1,X2,X3,X4,X5)Phe или Trp;
каждый R6 и R7, независимо от своего положения, является H, (C1-C10)алкилом, (C1-C10)гетероалкилом, арил(C1-C5)алкилом, замещенным (C1-C10)алкилом, замещенным (C1-C10)гетероалкилом или замещенным арил(C1-C5)алкилом при условии, что R6 и R7 могут быть объединены с образованием кольца;
R8 является H, (C1-C10)алкилом или замещенным (C1-C10)алкилом;
r, независимо от своего положения, является 1, 2, 3, 4 или 5; и
t, независимо от своего положения, является 1 или 2.
Предпочтительное соединение вышеуказанной формулы, в дальнейшем называемое соединениями Группы I(A), является соединением, в котором X выбран из группы, состоящей из -CH2-S-S-CH2- и -(CH2)2-S-S-CH2-;
r, независимо от своего положения, является 1, 2, 3, 4 или 5;
t, независимо от своего положения, является 1 или 2;
каждый R1, R2, R4 и R5 является H;
X1 выбран из группы, состоящей из
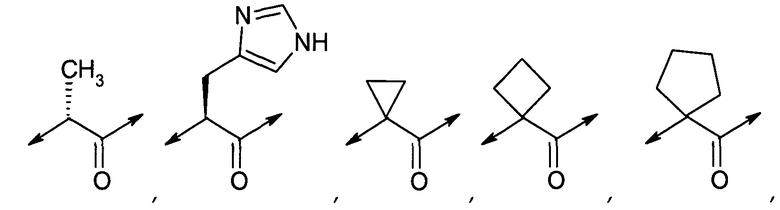
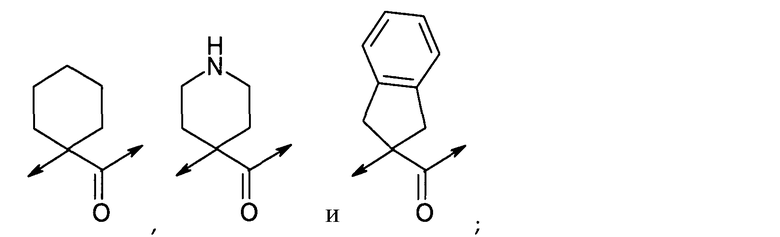
A1 представляет собой His или отсутствует;
A2 представляет собой D-1-Nal, D-2-Nal или D-Phe;
A3 представляет собой Arg; и
A4 представляет собой Bal, 1-Nal, 2-Nal или Trp.
Предпочтительным соединением Группы IA, далее называемым соединением Группы I(B), является соединение, в котором:
X1 представляет собой 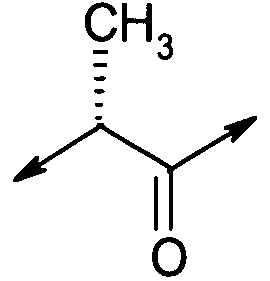 ;
;
A2 представляет собой D-Phe или D-2-Nal; и
A4 представляет собой Trp.
Характерные варианты осуществления класса соединений Группы IB, в дальнейшем назваемые соединениями Группы I(C), являются следующими:
цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:1),
цикло[Гидантоин(C(O)-(hCys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:2),
цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-2-Nal-Arg-Trp-Cys]-NH2; (SEQ ID NO:1) или
цикло[Гидантоин(C(O)-(hCys-D-Ala))-His-D-2-Nal-Arg-Trp-Cys]-NH2; (SEQ ID NO:2),
при этом наиболее предпочтительным соединением из данной Группы I является цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH2 (SEQ ID NO:1) или его фармацевтически приемлемая соль.
В другом аспекте настоящей заявки изобретение направлено на класс соединений, в дальнейшем называемых соединениями Группы I(D), в которых X выбран из группы, состоящей из -(CH2)t-C(O)-NR6-(CH2)r- и -(CH2)r-NR6-C(O)-(CH2)t-.
r, независимо от своего положения, является 1, 2, 3, 4 или 5;
t, независимо от своего положения, является 1 или 2;
каждый R1, R2, R4 и R5 является H;
R3 является NH2;
X1 выбран из группы, состоящей из
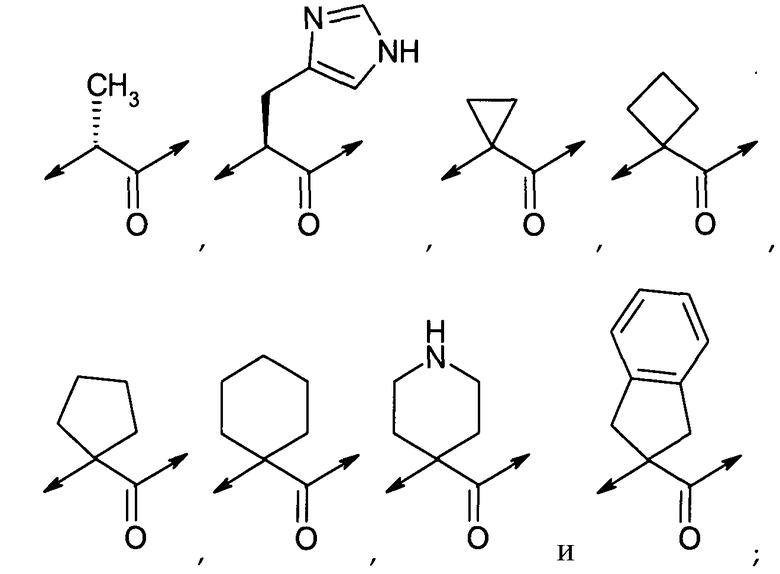
A1 представляет собой His или отсутствует;
A2 представляет собой D-1-Nal, D-2-Nal или D-Phe;
A3 представляет собой Arg; и
A4 представляет собой Bal, 1-Nal, 2-Nal или Trp;
или их фармацевтически приемлемую соль.
Подкласс соединений Группы II, соединения Группы I(E), являются такими соединениями, в которых X является -(CH2)t-C(O)-NR6-(CH2)r-;
t является 1; и
r является 1;
X1 выбран из группы, состоящей из:
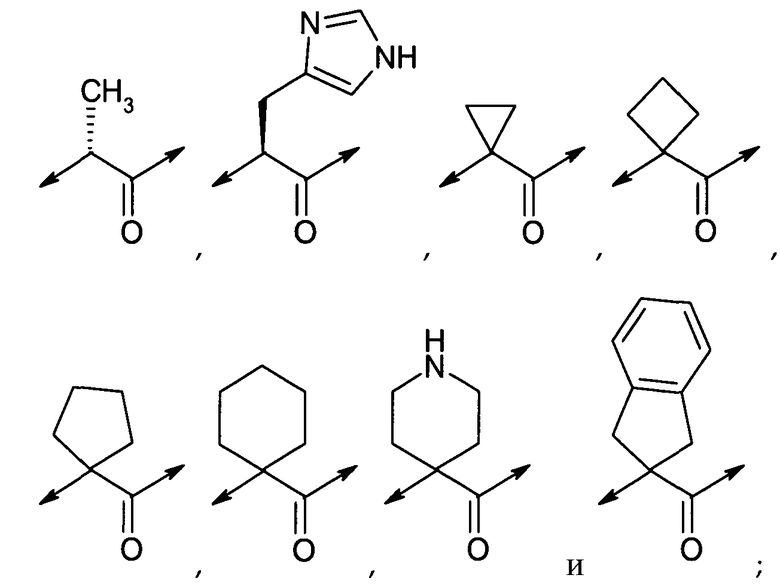
A1 представляет собой His;
A2 представляет собой D-Phe;
A3 представляет собой Arg; и
A4 представляет собой Bal, 1-Nal, 2-Nal или Trp, или их фармацевтически приемлемые соли.
Предпочтительный подкласс соединений Группы IIA, в дальнейшем называемый соединениями Группы I(F), является такими соединениями согласно формуле (I), в которых:
X1 представляет собой 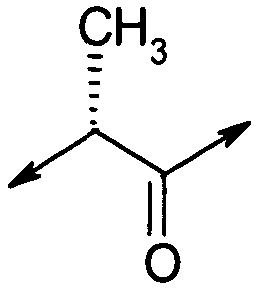 ; и
; и
R6 представляет собой метил, этил, пропил или бутил, предпочтительно либо метил, либо пропил; или их фармацевтически приемлемая соль. Конкретные примеры, относимые к соединениям Группы I(G), включают:
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Lys]-NH2; (SEQ ID NO:3),
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Orn]-NH2; (SEQ ID NO:4),
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Dab]-NH2; (SEQ ID NO:4), или
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH2; (SEQ ID NO:4),
предпочтительно, цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Orn]-NH2; (SEQ ID NO:4) или цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH2; (SEQ ID NO:4), или их фармацевтически приемлемые соли.
В другом подклассе Группы I,
X1 представляет собой 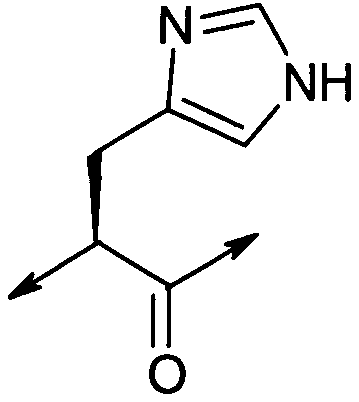 ;
;
A2 представляет собой D-2-Nal или D-Phe;
R6 представляет собой метил, этил, пропил или бутил, предпочтительно пропил; или их фармацевтически приемлемые соли, которые упоминаются как соединения Группы I(H), которые включают следующие соединения Группы I(I): цикло[Гидантоин(C(O)-(Asp-His))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:5) или цикло[Гидантоин(C(O)-(Asp-His))-D-Phe-Arg-Trp-Lys]-NH2; (SEQ ID NO:5), или их фармацевтически приемлемые соли.
В предпочтительных соединениях Группы ID A2 представляет собой D-2-Nal (Группа I(J)), как например в цикло[Гидантоин(C(O)-(Asp-His))-D-2-Nal-Arg-Trp-Lys]-NH2 (SEQ ID NO:5) (Группа I(K)), или их фармацевтически приемлемую соль.
В еще одном подклассе соединений Группы I, известных как соединения Группы I(L),
X1 выбран из группы, состоящей из:

A2 представляет собой D-2-Nal или D-Phe; и
R6 представляет собой метил, этил, пропил или бутил, предпочтительно пропил;
или фармацевтически приемлемую соль. Конкретные примеры соединений Группы IH, или соединений Группы I(M), являются следующими:
цикло[Гидантоин(C(O)-(Asp-A3c))-D-Phe-Arg-Trp-Lys]-NH2; (SEQ ID NO:6)
цикло[Гидантоин(C(O)-(Asp-A5c))-D-Phe-Arg-Trp-Lys]-NH2; (SEQ ID NO:7)
цикло[Гидантоин(C(O)-(Asp-A6c))-D-Phe-Arg-Trp-Lys]-NH2; (SEQ ID NO:8)
цикло[Гидантоин(C(O)-(Asp-A3c))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:6)
цикло[Гидантоин(C(O)-(Asp-A5c))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:7) или
цикло[Гидантоин(C(O)-(Asp-A6c))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:8)
или их фармацевтически приемлемые соли. Наиболее предпочтительными являются соединения, в которых A2 является D-2-Nal, а R6 является метилом, этилом, пропилом или бутилом, предпочтительно пропилом; или их фармацевтически приемлемая соль (класс Группы I(N)), которые включают следующие примеры Группы I(O):
цикло[Гидантоин(C(O)-(Asp-A3c))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:6)
цикло[Гидантоин(C(O)-(Asp-A5c))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:7) или
цикло[Гидантоин(C(O)-(Asp-A6c))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:8)
или их фармацевтически приемлемую соль.
В другой подгруппе (Группа I(P)) соединений Группы I:
X1 выбран из группы, состоящей из:

A2 представляет собой D-2-Nal или D-Phe;
R6 представляет собой метил, этил, пропил или бутил, предпочтительно пропил;
или их фармацевтически приемлемую соль. Предпочтительными примерами соединений следующей Группы I(Q) являются:
цикло[Гидантоин(C(O)-(Asp-Aic))-D-Phe-Arg-Trp-Lys]-NH2; (SEQ ID NO:9)
цикло[Гидантоин(C(O)-(Asp-Apc))-D-Phe-Arg-Trp-Lys]-NH2; (SEQ ID NO:10)
цикло[Гидантоин(C(O)-(Asp-Aic))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:9) или
цикло[Гидантоин(C(O)-(Asp-Apc))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:10)
или их фармацевтически приемлемая соль, причем наиболее предпочтительными соединениями данного подкласса являются соединения, в которых A2 является D-2-Nal, а R6 является метилом (Группа I(R)), как в цикло[Гидантоин-(C(O)-(Asp-Aic))-D-2-Nal-Arg-Trp-Lys]-NH2; (SEQ ID NO:9) и цикло[Гидантоин-(C(O)-(Asp-Apc))-D-2-Nal-Arg-Trp-Lys]-NH2 (SEQ ID NO:10) (Группа I(S)).
В еще одном варианте осуществления соединений формулы (I) (класс Группы I(T)),
X представляет собой -(CH2)t-C(O)-NR6-(CH2)r-;
t является 1; и
r является 2;
X1 представляет собой 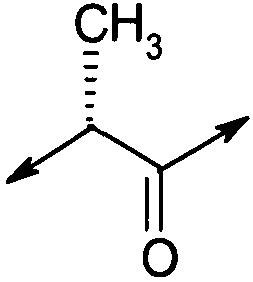 ;
;
A1 представляет собой His;
A2 представляет собой D-Phe;
A3 представляет собой Arg;
A4 представляет собой Trp; и
R6 представляет собой метил, этил, пропил или бутил;
или их фармацевтически приемлемые соли. Конкретные примеры (Группа I(U)) включают:
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Orn]-NH2; (SEQ ID NO:11)
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Dab]-NH2; (SEQ ID NO:11) или
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH2, (SEQ ID NO:11)
или их фармацевтически приемлемую соль, в особенности цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH2 (SEQ ID NO:11) (Группа I(V)), или его фармацевтически приемлемую соль.
В другом подклассе (Группа I(W)),
X1 представляет собой 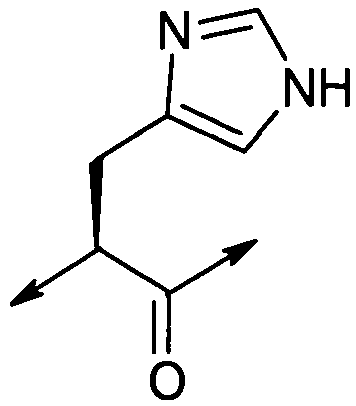 ;
;
A1 отсутствует;
A2 представляет собой D-Phe;
A3 представляет собой Arg; и
R6 представляет собой метил, этил, пропил или бутил;
или их фармацевтически приемлемую соль, при этом предпочтительным является цикло[Гидантоин(C(O)-(Glu-His))-D-Phe-Arg-Trp-Dap]-NH2 (SEQ ID NO:12) (Группа I(X)), или его фармацевтически приемлемая соль.
Фармацевтически приемлемая соль соединения формулы (I) может быть легко получена путем смешивания раствора соединения формулы (I) и нужной кислоты или основания, при необходимости. Соль может выпасть в виде осадка из раствора, а затем выделена с помощью фильтрации или путем отгонки растворителя.
Согласно первому аспекту изобретение обеспечивает соединение формулы (II), его фармацевтически приемлемые соли, гидраты, сольваты и/или пролекарства:
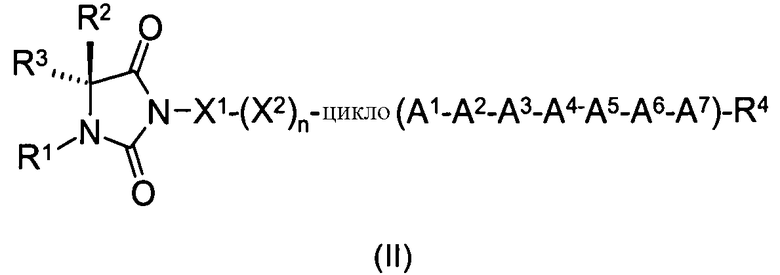
где гидантоиновая группа образована в результате конденсации аминогруппы X1, то есть
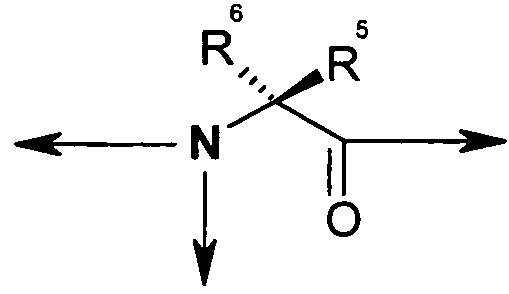
со следующим:
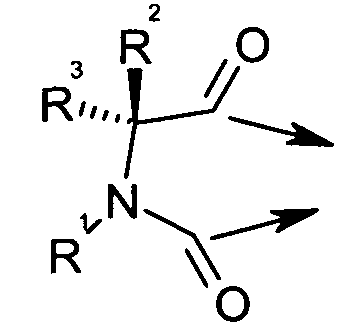
с образованием гидантоиновой структуры следующим образом:
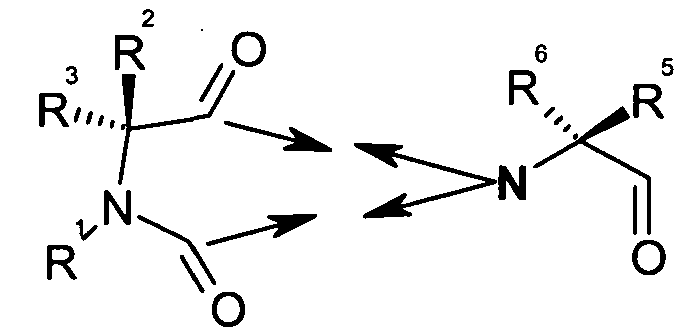
В предпочтительном варианте осуществления соединений согласно формуле (II), в дальнейшем называемых соединениями Группы II,
X1 представляет собой 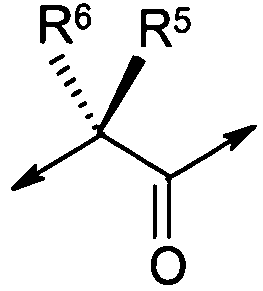 ;
;
X2 представляет собой 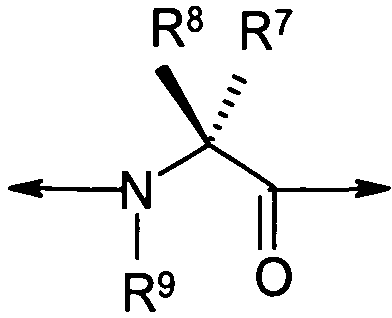 ;
;
A1 представляет собой Asp, Cys, D-Cys, Dab, Dap, Glu, Lys, Orn, Pen или D-Pen;
A2 является L- или D-аминокислотой;
A3 представляет собой His, 2-Pal, 3-Pal, 4-Pal, (X1,X2,X3,X4,X5)Phe, Taz, 2-Thi или 3-Thi;
A4 представляет собой D-Bal, D-1-Nal, D-2-Nal, D-Phe или D-(X1,X2,X3,X4,X5)Phe;
A5 представляет собой Arg, hArg, Dab, Dap, Lys или Orn;
A6 представляет собой Bal, 1-Nal, 2-Nal, (X1,X2,X3,X4,X5)Phe или Trp;
A7 представляет собой Asp, Cys, D-Cys, Dab, Dap, Glu, Lys, Orn, Pen или D-Pen;
R1 представляет собой H, (C1-C10)алкил или замещенный (C1-C10)алкил;
каждый R2 и R3 независимо представляет собой H, (C1-C10)алкил, (C1-C10)гетероалкил, арил(C1-C5)алкил, замещенный (C1-C10)алкил, замещенный (C1-C10)гетероалкил или замещенный арил(C1-C5)алкил, или R2 и R3 могут быть объединены с образованием циклической группы;
R4 представляет собой CO2H или C(O)NH2;
каждый R5 и R6 независимо представляет собой H, (C1-C10)алкил, (C1-C10)гетероалкил, арил(C1-C5)алкил, замещенный (C1-C10)алкил, замещенный (C1-C10)гетероалкил или замещенный арил(C1-C5)алкил, или R5 и R6 могут быть объединены с образованием циклической группы;
каждый R7 и R8 независимо представляет собой H, (C1-C10)алкил, (C1-C10)гетероалкил, арил(C1-C5)алкил, замещенный (C1-C10)алкил, замещенный (C1-C10)гетероалкил или замещенный арил(C1-C5)алкил; или R7 и R8 могут быть объединены с образованием циклической группы;
R9 представляет собой H, (C1-C10)алкил или замещенный (C1-C10)алкил; и
n, независимо от своего положения, является 1, 2, 3, 4, 5, 6 или 7;
или их фармацевтически приемлемую соль.
Предпочтительный класс соединений согласно формуле (II), в дальнейшем называемых примерами Группы II(A), является такими соединениями, в которых A2 представляет собой D-Ala, Asn, Asp, Gln или Glu;
каждый R5 и R6 независимо представляет собой H, (C1-C10)алкил, (C1-C10)гетероалкил, замещенный (C1-C10)алкил или замещенный (C1-C10)гетероалкил, или R5 и R6 могут быть объединены с образованием циклической группы; и
каждый R7 и R8 независимо представляет собой H, (C1-C10)алкил, (C1-C10)гетероалкил, замещенный (C1-C10)алкил или замещенный (C1-C10)гетероалкил;
или их фармацевтически приемлемую соль.
Каждый R1, R2, R3 и R9 независимо представляет собой H; и
R4 представляет собой C(O)NH2;
A1 представляет собой Cys;
A2 представляет собой D-Ala или Glu;
A3 представляет собой His;
A4 представляет собой D-2-Nal или D-Phe;
A5 представляет собой Arg;
A6 представляет собой Trp; и
A7 представляет собой Cys или Pen;
или их фармацевтически приемлемые соли.
Предпочтительным подклассом соединений Группы IIA (Группа II(B)) являются соединения, в которых:
каждый R1, R2, R3 и R9 независимо представляет собой H;
R4 представляет собой C(O)NH2;
каждый R5 и R6 независимо представляет собой H, метил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил или (CH2)-NH-C(N)-NH2; R7 представляет собой H;
R8 является метилом;
R9 представляет собой H;
или их фармацевтически приемлемые соли. Предпочтительные соединения Группы IIB (Группа II(C)) включают:
Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:13)
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:14)
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:15)
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:16)
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:17)
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; (SEQ ID NO:18)
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; (SEQ ID NO:19)
Гидантоин(C(O)-(Ala-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:20)
Гидантоин(C(O)-(D-Ala-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:21)
Гидантоин(C(O)-(Aib-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:22)
Гидантоин(C(O)-(Val-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:23)
Гидантоин(C(O)-(Ile-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:24)
Гидантоин(C(O)-(Leu-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:25)
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-Glu-His-D-2-Nal-Arg-Trp-Cys)-NH2; (SEQ ID NO:15)
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-Glu-His-D-2-Nal-Arg-Trp-Cys)-NH2; (SEQ ID NO:14)
Гидантоин(C(O)-(D-Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:26)
Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:13)
Гидантоин(C(O)-(D-Arg-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:27)
Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:28)
Гидантоин(C(O)-(D-Arg-Gly))-цикло(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; (SEQ ID NO:27) или
Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; (SEQ ID NO:28), или их фармацевтически приемлемые соли.
Более предпочтительными (Группа II (D)) являются соединения Группы IIC, в которых A4 представляет собой D-Phe, как например в следующих примерах (Группа II(E)):
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:14)
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:15)
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:16)
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:17)
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; (SEQ ID NO:18)
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2; (SEQ ID NO:19)
Гидантоин(C(O)-(Ala-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:20)
Гидантоин(C(O)-(D-Ala-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:21)
Гидантоин(C(O)-(Aib-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:22)
Гидантоин(C(O)-(Val-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:23)
Гидантоин(C(O)-(Ile-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:24)
Гидантоин(C(O)-(Leu-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:25)
Гидантоин(C(O)-(D-Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:26)
Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:13)
Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:28) или
Гидантоин(C(O)-(D-Arg-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:27) или их фармацевтически приемлемые соли, в особенности Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2 (SEQ ID NO:13) (Группа II(F)) или его фармацевтически приемлемая соль.
Второй предпочтительный подкласс формулы (II) (Группа II (G)) включает соединения, в которых:
каждый R1, R2, R3 и R9 независимо представляет собой H; и
R4 представляет собой C(O)NH2;
каждый R5 и R6 независимо представляет собой H, метил, изопропил, изобутил или объединены с образованием циклогексила или CH2-циклогексила;
R7 представляет собой H;
R8 представляет собой n-пропил;
R9 представляет собой H;
A1 представляет собой Cys;
A2 представляет собой D-Ala или Glu;
A3 представляет собой His;
A4 представляет собой D-2-Nal или D-Phe;
A5 представляет собой Arg;
A6 представляет собой Trp; и
A7 представляет собой Cys или Pen;
или их фармацевтически приемлемые соли. Примеры из подкласса, называемого как соединения Группы II(H), включают следующие:
Гидантоин(C(O)-(Ala-Nle))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:29)
Гидантоин(C(O)-(Val-Nle))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:30)
Гидантоин(C(O)-(Gly-Nle))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:31)
Гидантоин(C(O)-(A6c-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:32)
Гидантоин(C(O)-(Gly-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:33)
Гидантоин(C(O)-(Ala-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:34)
Гидантоин(C(O)-(D-Ala-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:35)
Гидантоин(C(O)-(Val-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:36)
Гидантоин(C(O)-(Leu-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:37)
Гидантоин(C(O)-(Cha-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:38) или
Гидантоин(C(O)-(Aib-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:39), или их фармацевтически приемлемые соли. Более предпочтительные соединения Группы III(H) (в дальнейшем Группа II(I)) включают примеры, в которых:
A2 представляет собой D-Ala;
A4 представляет собой D-Phe; и
A7 представляет собой Cys;
или их фармацевтически приемлемые соли. Конкретные соединения из указанного предпочтительного класса (Группа II(J)) включают:
Гидантоин(C(O)-(A6c-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:32)
Гидантоин(C(O)-(D-Ala-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:35)
Гидантоин(C(O)-(Val-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:36)
Гидантоин(C(O)-(Leu-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:37)
Гидантоин(C(O)-(Cha-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:38) или
Гидантоин(C(O)-(Aib-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:39), или их фармацевтически приемлемые соли.
Третьим предпочтительным подклассом соединений согласно формуле (II) является класс Группы II(K), включающий следующие требования:
A1 представляет собой Cys;
A2 представляет собой D-Ala или Glu;
A3 представляет собой His;
A4 представляет собой D-2-Nal или D-Phe;
A5 представляет собой Arg;
A6 представляет собой Trp; и
A7 представляет собой Cys или Pen;
каждый R1, R2, R3, R6, R7 и R9 независимо представляет собой H;
R8 представляет собой (CH2)3-NH-C(N)-NH2;
при условии, что R4 представляет собой C(O)NH2, а R5 представляет собой H, либо R5 представляет собой C(O)NH2, а R4 представляет собой H; или их фармацевтически приемлемые соли. Предпочтительные соединения Группы II(L), которые находятся в пределах данного подкласса, включают:
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:40)
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-Glu-His-D-2-Nal-Arg-Trp-Cys)-NH2; (SEQ ID NO:40)
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:41)
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; (SEQ ID NO:41)
Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:42)
Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:42)
Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:43) и
Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2; (SEQ ID NO:43) или их фармацевтически приемлемые соли.
Более предпочтительными (подкласс Группы II(M)) являются Соединения Группы II, в которых A4 представляет собой D-Phe, как в следующих предпочтительных примерах (Группа II(N)):
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:40)
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:41)
Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:42) и
Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:43), или их фармацевтически приемлемые соли.
Еще одним предпочтительным вариантом осуществления формулы (II), известной как Группа II(O), является Гидантоин(C(O)-(Nle-крыло))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2; (SEQ ID NO:44) или его фармацевтически приемлемая соль.
Фармацевтически приемлемая соль соединения формулы (II) может быть легко получена путем смешивания раствора соединения формулы (II) и нужной кислоты или основания, при необходимости. Соль может выпасть из раствора в виде осадка и выделена с помощью фильтрации или может быть получена при отгонке растворителя.
Настоящее изобретение также относится к классу циклических пептидных аналогов, которые являются лигандами меланокортиновых рецепторов, имеющими структуру согласно формуле (III), как показано ниже:

где гидантоиновая группа образована в результате конденсации аминогруппы одной из аминокислот, которые составляют X, то есть "AA2"
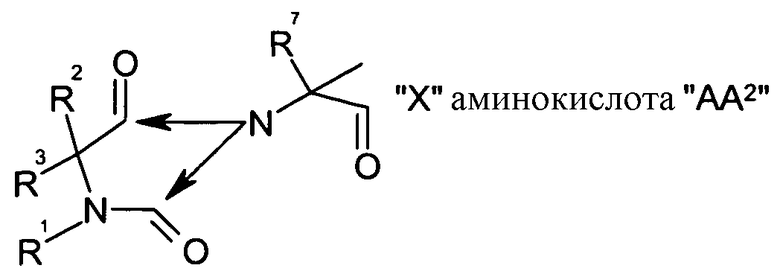
со второй аминокислотой, то есть "AA1", составляющий X,
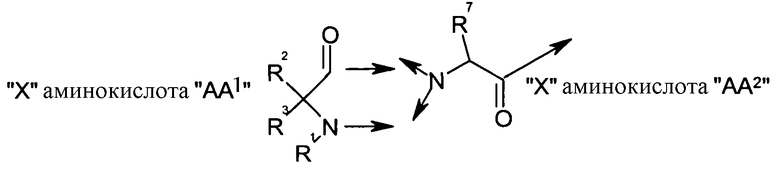
вместе с карбонильной группой, то есть C(O), следующим образом:
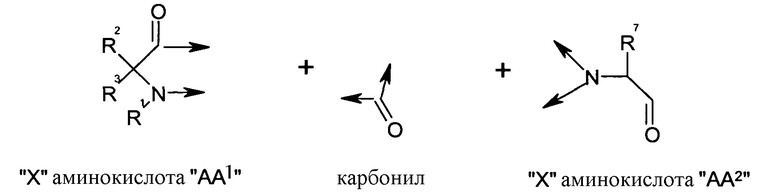 .
.
В кратком обозначении, используемом для идентификации варианта осуществления формулы (III), такого как цикло[Гидантоин(C(O)-(Ala-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:45) "Гидантоин(C(O)-(AA1-AA2)" обозначает аминокислоты, формирующие гидантоиновую структуру. Карбонильная группа, расположенная между двумя атомами азота имидазолинильного гетероциклического кольца, обозначена как "C(O)". "AA1" является частью гидантоиновой структуры, при этом один из R2 или R3 (в зависимости от стереоизомерии примера) является боковой цепью, а другой является водородом, расположенным на α-атоме углерода. "AA2" является аминокислотой, N-конец которой входит в гидантоиновую структуру. Для данного примера, цикло[Гидантоин(C(O)-(Ala-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:45) гидантоин образован следующим образом:

Что касается переменных формулы (III):
X выбран из группы, состоящей из -CH2-S-S-CH2-, -C(CH3)2-S-S-CH2-, -CH2-S-S-C(CH3)2-, -C(CH3)2-S-S-C(CH3)2-, -(CH2)2-S-S-CH2-, -CH2-S-S-(CH2)2, -(CH2)2-S-S-(CH2)2-, -C(CH3)2-S-S-(CH2)2-, -(CH2)2-S-S-C(CH3)2-, -(CH2)t-C(O)-NR8-(CH2)r- и -(CH2)r- NR8-C(O)-(CH2)t -;
каждый R1 и R5 независимо является H, (C1-C10)алкилом или замещенным (C1-C10)алкилом;
R4 представляет собой -OH или -NH2;
каждый R6 и R7 независимо является H, (C1-C10)алкилом или замещенным (C1-C10)алкилом;
каждый R2 и R3 независимо является H, (C1-C10)алкилом, (C1-C10)гетероалкилом, арил(C1-C5)алкилом, замещенным (C1-C10)алкилом, замещенным (C1-C10)гетероалкилом или замещенным арил(C1-C5)алкилом, или R2 и R3 могут быть объединены с образованием кольца;
A1 является L- или D-аминокислотой или отсутствует;
A2 представляет собой His, 2-Pal, 3-Pal, 4-Pal, (X1,X2,X3,X4,X5)Phe, Taz, 2-Thi или 3-Thi;
A3 представляет собой D-Bal, D-1-Nal, D-2-Nal, D-Phe или D-(X1,X2,X3,X4,X5)Phe;
A4 представляет собой Arg, hArg, Dab, Dap, Lys или Orn;
A5 представляет собой Bal, 1-Nal, 2-Nal, (X1,X2,X3,X4,X5)Phe или Trp;
r, независимо от своего положения, является 1, 2, 3, 4 или 5; и
t, независимо от своего положения, является 1 или 2;
или их фармацевтически приемлемые соли.
В предпочтительном варианте осуществления соединений согласно формуле (III), в дальнейшем называемых соединениями Группы III,
A1 представляет собой Ala, D-Ala, Asn, Asp, Gln, Glu или Gly; или их фармацевтически приемлемую соль.
В другом предпочтительном варианте осуществления (подкласс Группы III(A)),
X выбран из группы, состоящей из -CH2-S-S-CH2-, -C(CH3)2-S-S-CH2- и -(CH2)2-S-S-CH2-;
A1 представляет собой D-Ala или Glu;
A2 представляет собой His;
A3 представляет собой D-Phe;
A4 представляет собой Arg;
A5 представляет собой Trp;
каждый R1, R5, R6 и R7 независимо представляет собой H;
каждый R2 и R3 независимо представляет собой H, (C1-C10)алкил, (C1-C10)гетероалкил, замещенный (C1-C10)алкил или замещенный (C1-C10)гетероалкил, или R2 и R3 могут быть объединены с образованием циклической группы; и
R4 представляет собой NH2;
или их фармацевтически приемлемую соль.
В более предпочтительной подгруппе Группы III(A) (подкласс Группы III(B)) каждый R2 и R3 независимо является H, метилом, н-пропилом, изопропилом, н-бутилом, изобутилом, втор-бутилом, трет-бутилом или (CH2)-NH-C(N)-NH2; или их фармацевтически приемлемой солью. Конкретными примерами Группы III(B) являются соединения Группы III(C):
цикло[Гидантоин(C(O)-(Nle-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:46)
цикло[Гидантоин(C(O)-(Ala-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:45)
цикло[Гидантоин(C(O)-(D-Ala-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:47)
цикло[Гидантоин(C(O)-(Aib-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:48)
цикло[Гидантоин(C(O)-(Val-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:49)
цикло[Гидантоин(C(O)-(Abu-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:50)
цикло[Гидантоин(C(O)-(Leu-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:51)
цикло[Гидантоин(C(O)-(Ile-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:52)
цикло[Гидантоин(C(O)-(Cha-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:53)
цикло[Гидантоин(C(O)-(A6c-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:54)
цикло[Гидантоин(C(O)-(Phe-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:55)
цикло[Гидантоин(C(O)-(Gly-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:56) или
цикло[Гидантоин(C(O)-(Gly-Cys))-Glu-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:57)
или их фармацевтически приемлемые соли.
В другом подклассе Группы III каждый R2 и R3 независимо является H, метилом, изопропилом, изобутилом, втор-бутилом или они могут быть объединены с образованием циклогексила (далее подкласс Группы III(D)); или их фармацевтически приемлемыми солями, из которых предпочтительными являются следующие примеры (Группа III(E)):
цикло[Гидантоин(C(O)-(Aib-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:48)
цикло[Гидантоин(C(O)-(Val-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:49)
цикло[Гидантоин(C(O)-(Leu-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:51)
цикло[Гидантоин(C(O)-(Ile-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:52)
цикло[Гидантоин(C(O)-(A6c-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:54) или
цикло[Гидантоин(C(O)-(Gly-Cys))-Glu-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:57)
или их фармацевтически приемлемые соли.
В еще одном предпочтительном подклассе Группы III, в дальнейшем Группа III(F), A1 представлет собой Glu, а каждый R2 и R3 независимо является H, или их фармацевтически приемлемые соли, при этом предпочтительным примером является следующее соединение (Группа III (G)) цикло[Гидантоин(C(O)-(Gly-Cys))-Glu-His-D-Phe-Arg-Trp-Cys]-NH2; (SEQ ID NO:57) или его фармацевтически приемлемая соль.
Фармацевтически приемлемая соль соединения формулы (III) может быть легко получена путем смешивания раствора соединения формулы (III) и нужной кислоты или основания, при необходимости. Соль может выпасть из раствора в виде осадка, может быть выделена с помощью фильтрации или может быть получена при отгонке растворителя.
Во избежание недоразумений, если не указано иное, термин "замещенный" означает замещенный одной или несколькими определенными группами. В случае, когда группы могут быть выбраны из множества альтернативных групп, выбранные группы могут являться одинаковыми или различными. Во избежание недоразумений, термин независимо означает, что когда более чем один заместитель выбран из множества возможных заместителей, такие заместители могут являться одинаковыми или различными.
Фармацевтически приемлемые соли соединений изобретения содержат основную группу, например соли присоединения нетоксичных кислот, образованные с неорганическими кислотами, такими как хлороводородная, бромоводородная, йодоводородная, серная и фосфорная кислоты, с карбоновыми кислотами или с органическими сульфокислотами. Примеры включают следующие соли: HCl, HBr, HI, сульфат или бисульфат, нитрат, фосфат или гидрофосфат, ацетат, бензоат, сукцинат, сахарат, фумарат, малеат, лактат, цитрат, тартрат, глюконат, камсилат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат и памоат. Соединения изобретения могут также давать фармацевтически приемлемые соли металлов, в частности соли нетоксичных щелочных и щелочноземельных металлов, с основаниями. Примеры включают соли натрия, калия, алюминия, кальция, магния, цинка и диэтаноламина (Berge, S. M. et al., J. Pharm. Sci., 66:1-19 (1977); Gould, P.L., Int'l J. Pharmaceutics, 33:201-17 (1986); и Bighley, L.D. et al., Encyclo. Pharma. Tech., Marcel Dekker Inc, New York, 13:453-97 (1996)).
Фармацевтически приемлемые сольваты соединений изобретения включают соответствующие гидраты. Также в объем изобретения и различных солей изобретения включены соответствующие полиморфы. В дальнейшем соединения, их фармацевтически приемлемые соли, их сольваты или полиморфы, определенные в любом аспекте изобретения (за исключением промежуточных соединений в химических процессах), упоминаются "как соединения изобретения".
Соединения изобретения могут обладать одним или несколькими хиральными центрами и, таким образом, существовать в виде множества стереоизомерных форм. Все стереоизомеры и их смеси включены в объем настоящего изобретения. Рацемические соединения могут или быть выделены с помощью препаративной ВЭЖХ и колонки с хиральной неподвижной фазой, или разделены с получением индивидуальных энантиомеров с использованием методов, известных специалистам в данной области. Кроме того, хиральные промежуточные соединения могут быть разделены, а затем использоваться для получения хиральных соединений изобретения.
Соединения изобретения могут существовать в одной или нескольких таутомерных формах. Все таутомеры и их смеси включены в объем настоящего изобретения. Например, указание в формуле изобретения 2-гидроксипиридинила также охватывает его таутомерную форму - α-пиридонил.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I) (которая в дальнейшем включает формулы I(A) - I(X)), формулы (II) (которая в дальнейшем включает формулы II(A) - II(P)) или формулы (III) (которая в дальнейшем включает формулы III(A) - IIII(G)), или их фармацевтически приемлемые соли вместе с фармацевтически приемлемым носителем или разбавителем.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, где указанное соединение является агонистом или антагонистом меланокортинового рецептора.
В другом аспекте, настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, где указанное соединение является селективным агонистом рецептора меланокортина-4.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, и фармацевтически приемлемый носитель или разбавитель, где указанное соединение является селективным агонистом рецептора меланокортина-4 с функциональной активностью, характеризуемой EC50, которая является, по меньшей мере, в 15 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-1 человека, рецептора меланокортина-3 человека и рецептора меланокортина-5 человека.
В еще одном аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, где указанное соединение является селективным агонистом рецептора меланокортина-4 с функциональной активностью, характеризуемой EC50, которая является, по меньшей мере, в 17 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-3 человека, по меньшей мере, в 90 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-3 человека, по меньшей мере, в 200 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-5 человека, или по меньшей мере, в 3000 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-5 человека.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения острого или хронического воспалительного заболевания или патологического состояния, такого как генерализованное воспаление, воспалительная болезнь кишечника, воспаление мозга, сепсис и септический шок.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения заболевания или патологического состояния с аутоиммунным фактором, такого как ревматоидный артрит, подагрический артрит и рассеянный склероз.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения заболевания или патологического состояния, связанного с нарушением обмена веществ, сопровождаемого увеличением массы тела, такого как ожирение, пищевые расстройства и синдром Прадера-Вилли. В дополнительном аспекте заболеванием или патологическим состоянием, подвергаемым лечению, является ожирение. В еще одном дополнительном аспекте заболеванием или патологическим состоянием, подвергаемым лечению, является пищевое расстройство.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для уменьшения потребления пищи, для снижения массы тела или для того и другого.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для уменьшения потребления пищи, но без негативного влияния на массу тела. В еще одном аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для уменьшения потребления пищи с одновременным повышением массы тела.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения заболевания или патологического состояния, связанного с нарушением обмена веществ, сопровождаемого снижением массы тела, такого как анорексия, булимия, истощение при СПИДе, кахексия, раковая кахексия и истощение у ослабленных пожилых людей. В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для повышения потребления пищи, для повышения массы тела или для того и другого.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения онкологического заболевания или состояния, такого как рак кожи и раковая кахексия.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения репродуктивного или полового патологического состояния, такого как эндометриоз, маточное кровотечение, половая дисфункция, эректильная дисфункции и сниженное половое влечение у женщин.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения заболевания или патологического состояния, являющегося следствием лечения или повреждения организма, такого как отторжение трансплантата, ишемия и реперфузионное повреждение, ранение и повреждение спинного мозга, а также потеря веса в результате медицинской манипуляции, выбранной из группы, состоящей из химиотерапии, лучевой терапии, временной или постоянной иммобилизации и диализа.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения сердечно-сосудистого заболевания или патологического состояния, такого как геморрагический шок, кардиогенный шок, гиповолемический шок, сердечно-сосудистые нарушения и сердечная кахексия.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения заболевания или нарушения работы легких, такого как острый респираторный дистресс-синдром, фиброз легких, хроническая обструктивная болезнь легких и астма.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для повышения иммунной толерантности и лечения аллергических заболеваний.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения дерматологического заболевания или патологического состояния, такого как псориаз, снижение пигментации кожи, акне и келоидное образование.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения поведенческого, центральной нервной системы или нервного заболевания или патологического состояния, такого как тревожное расстройство, депрессия, нарушение памяти и нейропатическая боль.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для лечения заболевания или нарушения работы почек, такого как почечная кахексия и натрийурез.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для модуляции веса яичников, развития плаценты, секреции пролактина, секреции ФСГ, внутриутробного развития эмбриона, родов, сперматогенеза, секреции тироксина, синтеза и секреции альдостерона, температуры тела, кровяного давления, частоты сердечных сокращений, сосудистого тонуса, мозгового кровообращения, уровня глюкозы в крови, секреции кожного сала, секреции феромонов, мотивации, обучения и поведения, ощущения боли, нейропротекции и роста нервов.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для модуляции метаболизма кости, образования костной ткани и развития кости.
В другом аспекте настоящее изобретение обеспечивает фармацевтическую композицию, включающую эффективное количество соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, а также фармацевтически приемлемый носитель или разбавитель, которая может применяться для предотвращения потребления алкоголя, для уменьшения потребления алкоголя, для лечения алкоголизма или для преодоления алкогольной зависимости. В дополнительном аспекте соединением композиции, которая может применяться для предотвращения потребления алкоголя, для уменьшения потребления алкоголя, для лечения алкоголизма или для лечения алкогольной зависимости является селективный агонист рецептора меланокортина-4. В еще одном дополнительном аспекте соединением композиции, которая может применяться для предотвращения потребления алкоголя, является селективный агонист рецептора меланокортина-4, или его фармацевтически приемлемая соль, с функциональной активностью, характеризуемой EC50, которая является, по меньшей мере, в 15 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортин-1 человека, рецептора меланокортина-3 человека и рецептора меланокортина-5 человека. В еще одном аспекте соединением композиции, которая может применяться для предотвращения потребления алкоголя, является селективный агонист рецептора меланокортина-4, или его фармацевтически приемлемая соль, с функциональной активностью, характеризуемой EC50, которая является, по меньшей мере, в 17 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-3 человека, которая является, по меньшей мере, в 90 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-3 человека, которая является, по меньшей мере, в 200 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-5 человека, или которая является, по меньшей мере, в 3000 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-5 человека.
В другом аспекте настоящее изобретение обеспечивает применение терапевтически эффективного количества соединения-агониста рецептора меланокортина-4 формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, для изготовления лекарственного средства, которое может применяться для предотвращения потребления алкоголя, для уменьшения потребления алкоголя, для лечения алкоголизма или для лечения алкогольной зависимости у субъекта, испытывающего потребность в таком лечении.
В еще одном аспекте настоящее изобретение обеспечивает способ индуцирования агонистического или антагонистического эффекта меланокортинового рецептора у субъекта, испытывающего в этом потребность, который включает введение указанному субъекту эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ выявления индуцирования агонистического или антагонистического эффекта меланокортинового рецептора у субъекта, испытывающего в этом потребность, который включает введение указанному субъекту эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, где указанным соединением является селективный агонист рецептора меланокортина-4.
В другом аспекте настоящее изобретение обеспечивает способ индуцирования агонистического или антагонистического эффекта меланокортинового рецептора у субъекта, испытывающего в этом потребность, который включает введение указанному субъекту эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, где указанным соединением является селективный агонист рецептора меланокортина-4 с функциональной активностью, характеризуемой EC50, которая является, по меньшей мере, в 15 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-1 человека, рецептора меланокортина-3 человека и рецептора меланокортина-5 человека.
В еще одном аспекте настоящее изобретение обеспечивает способ индуцирования агонистического или антагонистического эффекта меланокортинового рецептора у субъекта, испытывающего в этом потребность, который включает введение указанному субъекту эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли, где указанным соединением является селективный агонист рецептора меланокортина-4 с функциональной активностью, характеризуемой EC50, которая является, по меньшей мере, в 17 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-3 человека, которая является, по меньшей мере, в 90 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-3 человека, которая является, по меньшей мере, в 200 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортин-5 человека, или которая является, по меньшей мере, в 3000 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-5 человека.
В другом аспекте настоящее изобретение обеспечивает способ лечения острого или хронического воспалительного заболевания или патологического состояния, такого как генерализованное воспаление, воспалительная болезнь кишечника, воспаление мозга, сепсис и септический шок, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения заболевания или патологического состояния с аутоиммунным фактором, такого как ревматоидный артрит, подагрический артрит и рассеянный склероз, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения метаболического заболевания или патологического состояния, сопровождаемого увеличением массы тела, такого как ожирение, пищевые расстройства и синдром Прадера-Вилли, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли. В дополнительном аспекте предыдущего способа заболеванием или состоянием, подвергаемым лечению, является ожирение. В еще одном аспекте предыдущего способа заболеванием или состоянием, подвергаемым лечению, является пищевое расстройство.
В другом аспекте настоящее изобретение обеспечивает способ уменьшения потребления пищи, уменьшения массы тела или комбинацию перечисленного, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ уменьшения потребления пищи без негативного влияния на массу тела посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли. В еще одном аспекте предыдущего способа настоящее изобретение обеспечивает способ уменьшения потребления пищи с одновременным повышением массы тела, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ увеличения потребления питания, повышения массы тела или комбинацию перечисленного, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения метаболического заболевания или патологического состояния, сопровождаемого снижением массы тела, такого как анорексия, булимия, истощение при СПИДе, кахексия, раковая кахексия и истощение у ослабленных пожилых людей, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения онкологического заболевания или патологического состояния, такого как рак кожи и раковая кахексия, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения репродуктивного или полового нарушения, такого как эндометриоз, маточное кровотечение, половая дисфункция, эректильная дисфункция и снижение полового влечения у женщин, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения заболевания или патологического состояния, являющегося следствием лечения или повреждения организма, такого как отторжение трансплантата, ишемия и реперфузионное повреждение, ранение и повреждение спинного мозга, а также потеря веса в результате медицинской манипуляции, выбранной из группы, состоящей из химиотерапии, лучевой терапии, временной или постоянной иммобилизации и диализа, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения сердечно-сосудистого заболевания или патологического состояния, такого как геморрагический шок, кардиогенный шок, гиповолемический шок, сердечно-сосудистые нарушения и сердечная кахексия, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения заболевания или нарушения работы легких, такого как острый респираторный дистресс-синдром, фиброз легких, хроническая обструктивная болезнь легких и астма, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ повышения иммунной толерантности или лечения аллергических заболеваний, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения дерматологического заболевания или патологического состояния, такого как псориаз, снижение пигментации кожи, акне и келоидное образование, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения поведенческого, центральной нервной системы или нервного заболевания или патологического состояния, такого как тревожное расстройство, депрессия, нарушение памяти и нейропатическая боль, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ лечения заболевания или нарушения работы почек, такого как почечная кахексия и натрийурез, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ модуляции нормализации или гомеостатической активности, такой как вес яичников, развитие плаценты, секреция пролактина, секреция ФСГ, внутриутробное развитие эмбриона, роды, сперматогенез, секреция тироксина, синтез и секреция альдостерона, температура тела, кровяное давление, частота сердечных сокращений, сосудистый тонус, мозговое кровообращение, уровень глюкозы в крови, секреция кожного сала, секреция феромонов, мотивация, обучение и поведение, ощущение боли, нейропротекция и рост нервов, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ модуляции нормализации или гомеостатической активности, такой как метаболизм кости, образование костной ткани и развитие кости, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли.
В другом аспекте настоящее изобретение обеспечивает способ предотвращения потребления алкоголя, уменьшения потребления алкоголя, лечения алкоголизма или лечения алкогольной зависимости, посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемой соли. В дополнительном аспекте предыдущего способа соединением является селективный агонист рецептора меланокортина-4. В другом дополнительном аспекте данного предыдущего способа соединением композиции, которая может применяться для предотвращения потребления алкоголя, является селективный агонист рецептора меланокортина-4, или его фармацевтически приемлемая соль, с функциональной активностью, характеризуемой EC50, которая является, по меньшей мере, в 15 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-1 человека, рецептора меланокортина-3 человека и рецептора меланокортина-5 человека. В еще одном аспекте предыдущего способа соединением композиции, которая может применяться для предотвращения потребления алкоголя, является селективный агонист рецептора меланокортина-4 или его фармацевтически приемлемая соль, с функциональной активностью, характеризуемой EC50, которая является, по меньшей мере, в 17 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-3 человека, которая является, по меньшей мере, в 90 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-3 человека, которая является, по меньшей мере, в 200 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-5 человека, или которая является, по меньшей мере, в 3000 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-5 человека.
В дополнительном аспекте настоящее изобретение обеспечивает применение терапевтически эффективного количества агониста рецептора меланокортина-4 или соединения-антагониста согласно формуле (I), формуле (II) или формуле (III), или его фармацевтически приемлемой соли, для изготовления лекарственного средства, которое может применяться для лечения заболевания и/или патологического состояния, выбранного из группы, состоящей из острых и хронических воспалительных заболеваний, таких как генерализованное воспаление, воспалительная болезнь кишечника, воспаление мозга, сепсис и септический шок; заболеваний с аутоиммунным фактором, таких как ревматоидный артрит, подагрический артрит и рассеянный склероз; заболеваний и патологических состояний, связанных с нарушением обмена веществ, сопровождаемых увеличением массы тела, таких как ожирение, пищевые расстройства и синдром Прадера-Вилли; заболеваний и патологических состояний, связанных с нарушением обмена веществ, сопровождаемых снижением массы тела, таких как анорексия, булимия, истощение при СПИДе, кахексия, раковая кахексия и истощение у ослабленных пожилых людей; диабета, патологических состояний, связанных с диабетом, и осложнений диабета, таких как ретинопатия; опухолевой пролиферации, такой как рак кожи и рак простаты; репродуктивных или половых нарушений, таких как эндометриоз и маточное кровотечение у женщин, половая дисфункция, эректильная дисфункция и сниженное половое влечение у женщин; заболеваний или патологических состояний, являющихся следствием лечения или повреждения организма, таких как отторжение трансплантата, ишемии и реперфузионного повреждения, поражения спинного мозга и ранения, а также потери веса, вызванной химиотерапией, лучевой терапией, временной или постоянной иммобилизацией, или диализом; сердечно-сосудистых заболеваний или патологических состояний, таких как геморрагический шок, кардиогенный шок, гиповолемический шок, сердечно-сосудистые нарушения и сердечная кахексия; заболеваний или нарушений работы легких, таких как острый респираторный дистресс-синдром, хроническая обструктивная болезнь легких, астма и фиброз легких; для повышения иммунной толерантности и устранения угроз иммунной системе, например, связанных с некоторыми аллергическими заболеваниями или отторжением трансплантата; лечения дерматологических заболеваний и патологических состояний, таких как псориаз, снижение пигментации кожи, акне, келоидное образование и рак кожи; поведенческих, центральной нервной системы и нервных нарушений, таких как тревожные расстройства, депрессии, нарушение памяти и нейропатическая боль; а также заболеваний и патологических состояний, связанных с нарушением функции почек, например, для лечения почечной кахексии и натрийуреза.
В дополнительном аспекте настоящее изобретение обеспечивает применение терапевтически эффективного количества агониста рецептора меланокортина-4 или соединения-антагониста согласно формуле (I), формуле (II) или формуле (III), или его фармацевтически приемлемой соли, для изготовления лекарственного средства, которое может применяться для модуляции нормализации или гомеостатических функций, таких как вес яичников, развитие плаценты, секреция пролактина, секреция ФСГ, внутриутробное развитие эмбриона, роды, сперматогенез, секреция тироксина, синтез и секреция альдостерона, температура тела, кровяное давление, частота сердечных сокращений, сосудистый тонус, мозговое кровообращение, уровни глюкозы в крови, секреция кожного сала, секреция феромонов, мотивация, обучение и поведение, ощущение боли, нейропротекция, рост нервов, метаболизм кости, образование костной ткани и развитие кости.
Следует понимать, что также рассматриваются терапевтические воздействия, направленные как на нормальные физиологические, так и на патофизиологические процессы, в которых задействованы меланокортиновые рецепторы.
Дополнительные объекты, преимущества и признаки настоящего изобретения становятся очевидными из последующего описания и прилагаемой формулы в совокупности с сопровождающими фигурами.
Соединения формулы (I), формулы (II) и формулы (III) являются лигандами, по меньшей мере, одного из меланокортиновых рецепторов (MC1-R, MC2-R, MC3-R, MC4-R и MC5-R), предпочтительно MC4-R, причем при выборе их тестировали на предмет способности действовать в качестве лиганда в in vitro анализе, описанном ниже.
КРАТКОЕ ОПИСАНИЕ ФИГУР
Фигура 1: Суммарное среднее различие потребления пищи у крыс через 1 час и через 4 часа после введения различных концентраций Соединения A по сравнению с пустой основой.
Фигура 2A. Суммарное среднее различие потребления пищи у крыс после введения различных концентраций Соединений C и D по сравнению с пустой основой.
Фигура 2B. Суммарное среднее различие потребления пищи у крыс после введения различных концентраций Соединений A, B, C, D, E и F по сравнению с пустой основой.
Фигура 3A. Суммарное среднее различие потребления пищи у крыс после введения 4,5 мкмоль/кг/день Соединения A по сравнению с пустой основой.
Фигура 3B. Суммарное среднее различие потребления пищи у крыс после введения 4,5 мкмоль/кг/день Соединения A по сравнению с пустой основой.
Фигура 4A. Суммарное среднее различие потребления пищи у крыс после введения 300 нмоль/кг/день Соединений A, C и D по сравнению с пустой основой.
Фигура 4B. Суммарное среднее различие потребления пищи у крыс после введения 300 нмоль/кг/день Соединений A, C и D по сравнению с пустой основой.
Перечень условных обозначений для Фиг.1-4B:
(SEQ ID NO:11)
(SEQ ID NO:26)
(SEQ ID NO:13)
(SEQ ID NO:42)
(SEQ ID NO:40)
(SEQ ID NO:14)
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ОПРЕДЕЛЕНИЯ ТЕРМИНОВ, СОКРАЩЕНИЙ И АКРОНИМОВ
Ниже приведены определения терминов, используемых в настоящем описании. Исходное определение, приведенное далее для группы или термина, относится к той же группе или термину по всему тексту настоящего описания, отдельно или как часть другой группы, если не указано иное. Если не определено иное, все технические и научные термины, используемые в настоящем описании, имеют стандартное значение, известное специалистам в области техники, к которой относится настоящее изобретение.
Термин "алкил" относится к нормальным или разветвленным углеводородным группам, содержащим 1-12 атомов углерода, предпочтительно 1-8 атомов углерода. Наиболее предпочтительны низшие алкильные группы, то есть алкильные группы, содержащие 1-4 атома углерода. Когда применительно к алкильной или другой группе используется подстрочный индекс, подстрочный индекс относится к числу атомов углерода, которое может содержать данная группа.
Термин "замещенный алкил" относится к алкильной группе, определенной выше, которая содержит один, два или три заместителя, выбранных из группы, состоящей из галогено, амино, циано, кето (=O), -ORa, -SRa, NRaRb, -(C=O)Ra, -CO2Ra, -C(=O)NRaRb, -NRaC(=O)Rb, NRaCO2Rb, -OC(=O)Ra, -OC(=O)NRaRb, -NRcC(=O)NRaRb, NRaSO2Rd, SO2Rd, SO3Rd, циклоалкила, арила, гетероарила или гетероцикла, где группы Ra, Rb и Rc выбраны из водорода, (C1-C6)алкила, арила, гетероарила, гетероцикла, циклоалкила или (C1-C6)алкила, замещенного галогеном, гидрокси, метокси, нитро, амино, циано, -(C=O)H, -CO2H, -(C=O)алкила, -CO2алкила, -NH(алкила), -NH(циклоалкила), -N(алкила)2, карбокси, ацила, -C(=O)H, -C(=O)фенила, -CO2-алкила, циклоалкила, -(C=O)NH2, -(C=O)NH(алкила), -(C=O)NH(циклоалкила), -(C=O)N(алкила)2, -C(=O)-(CH2)1-2NH2, -C(=O)-(CH2)1-2NH(алкила), -C(=O)-(CH2)1-2N(алкила)2, -NH-CH2-карбокси, -NH-CH2-CO2-алкила, фенила, бензила, фенилэтил или фенилокси. Группа Rd может быть выбрана из тех же групп, что и Ra, Rb и Rc, за исключением водорода. В альтернативе группы Ra и Rb могут вместе образовать гетероарильное или гетероциклическое кольцо. Следует понимать, что когда замещенная алкильная группа замещена арилом, циклоалкилом, гетероарилом или гетероциклилом, такие кольца определены ниже и, таким образом, могут иметь один - три заместителя, как описано ниже в определениях для указанных терминов.
Когда термин "алкил" используется в качестве суффикса после другой конкретно указанной группы, например арилалкил или гетероарилалкил, данный термин определяет с большей конкретностью, по меньшей мере, один из заместителей, который содержит замещенный алкил. Например, арилалкил относится к арилу, присоединенному через алкил или, другими словами, к замещенной алкильной группе, содержащей от 1 до 12 атомов углерода и, по меньшей мере, один заместитель, который является арилом (например, бензилом или бифенилом). "Низший арилалкил" относится к замещенным алкильным группам, содержащим 1-4 атома углерода и, по меньшей мере, один арильный заместитель.
Термин "алкенил" относится к нормальным или разветвленным углеводородным группам, содержащим 2-12 атомов углерода и, по меньшей мере, одну двойную связь. Наиболее предпочтительны алкенильные группы, содержащие 2-6 атомов углерода и имеющие одну двойную связь.
Термин "алкинил" относится к нормальным или разветвленным углеводородным группам, содержащим 2-12 атомов углерода и, по меньшей мере, одну тройную связь. Наиболее предпочтительны алкинильные группы, содержащие 2-6 атомов углерода и имеющие одну тройную связь. Замещенный алкенил или алкинил содержат один, два или три заместителя, как определено выше для алкильных групп.
Термин "алкилен" относится к бивалентным, нормальным или разветвленным углеводородным группам, содержащим 1-12 атомов углерода, предпочтительно 1-8 атомов углерода, например {-CH2-}n, где n равно 1-12, предпочтительно 1-8. Наиболее предпочтительны низшие алкиленовые группы, то есть алкиленовые группы, содержащие 1-4 атомов углерода. Термины "алкенилен" и "алкинилен" относятся к бивалентным радикалам алкенильных и алкинильных групп, соответственно, как определено выше. Замещенные алкиленовые, алкениленовые и алкиниленовые группы могут иметь заместители, как определено выше для замещенных алкильных групп.
Термин "алкокси" относится к группе ORe, в которой Re является алкилом, замещенным алкилом, алкенилом, замещенным алкенилом, алкинилом, замещенным алкинилом, гетероциклом или циклоалкилом. Таким образом, алкокси включает такие группы как метокси, этокси, циклопропилокси, пирролидинилокси и т.д. Термин "арилокси" относится к группам O(арил) или O(гетероарил), в которых арил и гетероарил определены ниже.
Термин "алкилтио" относится к алкильной или замещенной алкильной группе, как определено выше, присоединенной через один или несколько атомов серы (-S-), например -S(алкил) или -S(алкил-Ra).
Термин "алкиламино" относится к алкильной или замещенной алкильной группе, как определено выше, присоединенной через одну или несколько азотсодержащих (-NRf-) групп, в которых Rf является водородом, алкилом, замещенным алкилом или циклоалкилом.
Термин "ацил" относится к алкильной или замещенной алкильной группе, как определено выше, присоединенной через одну или несколько карбонильных {-C(=O)-} групп. Когда термин ацил используется совместно с другой группой, как в ациламино, он относится к карбонильной группе {-C(=O)}, связанной со второй указанной группой. Таким образом, ациламино относится к -C(=O)NH2, замещенный ациламино относится к группе -C(=O)NRR, и ациларил относится к -C(=O)(арил).
Термин "аминоацил" относится к группе -NRfC(=O)Rg, в которой Rg является водородом, алкилом или замещенным алкилом, а Rf определен выше для алкиламино групп.
Термин "галогено" или "галоген" относится к атомам хлора, брома, фтора и иода. Если не указано иное, любая галогеналкильная, галогеналкокси или галогеналкилтио группа содержит один или несколько атомов галогенов, которые могут являться одинаковыми или различными.
Термин "карбокси", если используется отдельно, относится к группе CO2H. Карбоксиалкил относится к группе CO2R, в которой R является алкилом или замещенным алкилом.
Термин "сульфонил" относится к сульфоксидной группе (то есть, -S(O)1-2-), связанной с органическим радикалом, включающим алкильную, алкенильную, алкинильную, замещенную алкильную, замещенную алкенильную или замещенную алкинильную группы, как определено выше. Органический радикал, к которому присоединена сульфоксидная группа, может являться моновалентным (например, -SO2-алкил) или бивалентным (например, -SO2-алкилен и т.д.).
Термин "циклоалкил" относится к замещенным и незамещенным моноциклическим или бициклическим углеводородным группам, содержащим 3-9 атомов углерода, которые являются, соответственно, полностью насыщенными или частично ненасыщенными, включая конденсированное арильное кольцо, например индан. Циклоалкильная группа может быть замещена одним или несколькими (например, одним - тремя) заместителями, выбранными из алкила, замещенного алкила, аминоалкила, галогена, циано, нитро, трифторметила, гидрокси, алкокси, алкиламино, сульфонила, -SO2(арила), -CO2H, -CO2-алкила, -C(=O)H, кето, -C(=O)-(CH2)1-2NH2, -C(=O)-(CH2)1-2NH(алкила), -C(=O)-(CH2)1-2N(алкила)2, ацила, арила, гетероцикла, гетероарила или другого циклоалкильного кольца, содержащего 3-7 атомов углерода. Термин "циклоалкилен" относится к циклоалкилу, формирующему связь или спейсер между двумя другими группами, то есть циклоалкилен представляет собой циклоалкил, который связан, по меньшей мере, с двумя другими группами. Термин циклоалкил включает насыщенные или частично ненасыщенные карбоциклические кольца, содержащие углерод-углеродный мостик из трех - четырех атомов углерода или включающие присоединенное к ним бензольное кольцо. Если циклоалкильная группа замещена другим кольцом, указанное другое кольцо может содержать один - два заместителя, выбранных из Rk, где Rk является низшим алкилом, гидрокси, низшим алкокси, амино, галогеном, циано, трифторметилом, трифторметокси, нитро и низшим алкилом, замещенным одним - двумя гидрокси, низшим алкокси, амино, галогеном, циано, трифторметилом, трифторметокси и/или нитро.
Термин "арил" относится к замещенному и незамещенному фенилу, 1-нафтилу и 2-нафтилу, предпочтительно фенилу. Арил может иметь ноль, один, два или три заместителя, выбранных из группы, состоящей из алкила, замещенного алкила, алкокси, алкилтио, галогено, гидрокси, нитро, циано, амино, трифторметила, трифторметокси, сульфонила, -SO2(арила), -NH(алкила), -NH(циклоалкила), -N(алкила)2, карбокси, ацила, -C(=O)H, -C(=O)фенила, -CO2-алкила, циклоалкила, -(C=O)NH2, -(C=O)NH(алкила), -(C=O)NH(циклоалкила), -(C=O)N(алкила)2, -NH-CH2-карбокси, -NH-CH2-CO2-алкила, -C(=O)-(CH2)1-2NH2, -C(=O)-(CH2)1-2NH(алкила), -C(=O)-(CH2)1-2N(алкила)2, фенила, бензила, фенилэтила, фенилокси, фенилтио, гетероцикло, гетероарила или (C3-C7)циклоалкильного кольца. Термин "арилен" относится к арилу, определенному выше, который формирует связь или спейсер между двумя другими группами, то есть арилен представляет собой арил, который связан, по меньшей мере, с двумя другими группами. Когда арильная группа замещена другим кольцом, указанное другое кольцо может иметь один - два заместителя, выбранные из Rk, где Rk определен выше.
Термин "гетероцикло" или "гетероцикл" относится к замещенным и незамещенным неароматическим 3-7-членным моноциклическим группам, 7-11-членным бициклическим группам и 10-15-членным трициклическим группам, которые содержат, по меньшей мере, один гетероатом (O, S или N), по меньшей мере, в одном из колец. Каждое кольцо гетероциклической группы, содержащее гетероатом, может содержать один или два атома кислорода или серы и/или от одного до четырех атомов азота при условии, что общее количество гетероатомов в каждом кольце равно четырем или меньше, а также при условии, что кольцо содержит, по меньшей мере, один атом углерода. Конденсированные кольца, которые составляют бициклические и трициклические группы, могут содержать только атомы углерода и могут являться насыщенными, частично насыщенными или ненасыщенными. Атомы азота и серы необязательно могут быть окислены, а атомы азота необязательно также могут быть кватернизированы. Гетероциклическая группа может быть присоединена по любому доступному атому азота или углерода. Гетероциклическое кольцо может содержать один, два или три заместителя, выбранных из группы, состоящей из галогено, амино, циано, алкила, замещенного алкила, трифторметила, трифторметокси, сульфонила, -SO2(арила), -NH(алкила, -NH(циклоалкила), -N(алкила)2, алкокси, алкилтио, гидрокси, нитро, фенила, бензила, фенилэтила, фенилокси, фенилтио, карбокси, -CO2-алкила, циклоалкила, -C(=O)H, ацила, -(C=O)NH2, -(C=O)NH(алкила), -(C=O)NH(циклоалкила), -(C=O)N(алкила)2, -NH-CH2-карбокси, -NH-CH2-CO2-алкила, -C(=O)-(CH2)1-2NH2, -C(=O)-(CH2)1-2NH(алкила), -C(=O)-(CH2)1-2N(алкила)2, гетероцикло, гетероарила, (C3-C7)циклоалкильного кольца, кето, =N-OH, =N-O-низшего алкила или пяти- или шестичленного кеталя, то есть 1,3-диоксолана или 1,3-диоксана. Когда гетероциклическая группа замещена другим кольцом, указанное другое кольцо может содержать один - два заместителя, выбранные из Rk, где Rk определен выше. Примеры моноциклических групп включают азетидинил, пирролидинил, оксетанил, имидазолинил, оксазолидинил, изоксазолинил, тиозолидинил, изотиазолидинил, тетрагидрофуранил, пиперидинил, пиперазинил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, 2-оксоазепинил, азепинил, 4-пиперидонил, тетрагидропиранил, морфолинил, тиаморфолинил, тиаморфолинил сульфоксид, тиаморфолинилсульфон, 1,3-диоксолан и тетрагидро-1,1-диоксотиенил и т.п. Примеры бициклических гетероциклических групп включают хинуклидинил.
Термин "гетероарил" относится к замещенным и незамещенным ароматическим 5- или 6-членным моноциклическим группам, 9- или 10-членным бициклическим группам и 11-14-членным трициклическим группам, которые содержат, по меньшей мере, один гетероатом (O, S или N), по меньшей мере, в одном из колец. Каждое кольцо гетероарильной группы, содержащее гетероатом, может содержать один или два атома кислорода или серы и/или от одного до четырех атомов азота при условии, что общее количество гетероатомов в каждом кольце равно четырем или меньше, причем каждое кольцо содержит, по меньшей мере, один атом углерода. Конденсированные кольца, которые составляют бициклические и трициклические группы, могут содержать только атомы углерода и могут являться насыщенными, частично насыщенными или ненасыщенными. Атомы азота и серы необязательно могут быть окислены, а атомы азота необязательно также могут быть кватернизированны. Гетероарильные группы, которые являются бициклическими или трициклическими, должны включать, по меньшей мере, одно полностью ароматическое кольцо, тогда как другое конденсированное кольцо или кольца могут являться ароматическими или неароматическими. Гетероарильная группа может быть присоединена по любому доступному атому азота или углерода любого кольца. Гетероарильная кольцевая система может содержать один, два или три заместителя, выбранные из группы, состоящей из галогено, амино, циано, алкила, замещенного алкила, трифторметила, трифторметокси, сульфонила, -SO2(арила), -NH(алкила), -NH(циклоалкила), -N(алкила)2, алкокси, алкилтио, гидрокси, нитро, фенила, бензила, фенилэтила, фенилокси, фенилтио, карбокси, -CO2-алкила, циклоалкила, -C(=O)H, ацила, -(C=O)NH2, -(C=O)NH(алкила), -(C=O)NH(циклоалкила), -(C=O)N(алкила)2, -NH-CH2-карбокси, -NH-CH2-CO2-алкила, -C(=O)-(CH2)1-2NH2, -C(=O)-(CH2)1-2NH(алкила), -C(=O)-(CH2)1-2N(алкила)2, гетероцикло, гетероарила или (C3-C7)циклоалкильного кольца. Гетероциклическое кольцо может содержать гетероатом серы, замещенный одним или несколькими атомами кислорода (=O). Примеры моноциклических гетероарильных групп включают пирролил, пиразолил, пиразолинил, имидазолил, оксазолил, изоксазолил, тиазолил, тиадиазолил, изотиазолил, фуранил, тиенил, оксадиазолил, пиридил, пиразинил, пиримидинил, пиридазинил, триазинил и т.п. Примеры бициклических гетероарильных групп включают индолил, бензотиазолил, бензодиоксолил, бензоксазолил, бензотиенил, хинолинил, тетрагидроизохинолинил, изохинолинил, бензимидазолил, бензопиранил, индолизинил, бензофуранил, хромонил, кумаринил, бензопиранил, циннолинил, хиноксалинил, индазолил, пирролопиридил, фуропиридинил, дигидроизоиндолил, тетрагидрохинолинил и т.п. Примеры трициклических гетероарильных групп включают карбазолил, бензидолил, фенантроллинил, акридинил, фенантридинил, ксантенил и т.п.
Когда в настоящем описании упоминается конкретно указанная гетероциклическая или гетероарильная группа, такая как азетидинильная, имидазолильная, пиперазинильная и т.д., указанное кольцо необязательно может содержать один или несколько (предпочтительно один - три) заместителей, выбранных из заместителей, перечисленных выше для гетероарильной и гетероциклической групп, при необходимости.
Когда в настоящем описании упоминается конкретно указанная группа, содержащая, по меньшей мере, одно гетероциклическое, гетероарильное или карбоциклическое кольцо, "присоединенное" к ней, это означает, что два заместителя, присоединенные к одному и тому же, к смежным или несмежным атомам конкретно указанной группы, могут соединяться, формируя второе или третье кольцо (то есть дополнительное кольцо может быть сконденсировано, соединено мостиком или присоединено посредством спиросвязи). Каждое кольцо указанных бициклических или трициклических групп необязательно может быть замещено, при этом соответствующие заместители выбраны из перечисленных выше для циклоалкильной, арильной, гетероциклильной и гетероарильной групп. Таким образом, имидазол, к которому присоединено, по меньшей мере, одно кольцо, может включать конденсированный с арилом имидазол, такой как бензимидазол, имеющий один или несколько (предпочтительно один - три) заместителей, конденсированный с гетероарилом имидазол, такой как пиридоимидазол, имеющий один или несколько (предпочтительно один - три) заместителей, и т.д.
Кроме того, специалист в данной области может сделать соответствующие замены различных групп соединений формулы (I), (II) или (III) согласно настоящему изобретению, не отступая от сущности и объема изобретения. Из всего текста настоящего описания могут быть выбраны соответствующие группы и заместители в целях получения стабильных молекул и соединений.
Соединения формулы (I), (II) или (III) образуют соли, которые также включены в объем настоящего изобретения. Ссылка на соединение любой из формул (I), (II) или (III), приведенных в настоящей заявке, как следует понимать, включает ссылку на соответствующие соли, если не указано иное. Термин "соль (соли)", используемый в настоящей заявке, обозначает кислотные и/или основные соли, образованные с неорганическими и/или органическими кислотами и основаниями. Кроме того, когда соединение любой из формулы (I), (II) или (III) содержит как основную группу, такую как, помимо прочих, амин или пиридин, или имидазольное кольцо, так и кислотную группу, такую как, помимо прочих, карбоксильную, могут образовываться цвиттерионы ("внутренние соли"), которые также включены в рамки тармина "соль (соли)", используемого в настоящей заявке. Фармацевтически приемлемые (то есть нетоксичные, физиологически приемлемые) соли являются предпочтительными, хотя другие соли также рассматриваются включенными в рамки изобретения, например они могут применяться в стадиях выделения или очистки, которые могут использоваться в процессе получения. Соли соединений любой из формул (I), (II) или (III) могут быть получены, например, путем взаимодействия соединения формулы (I), (II) или (III) с некоторым количеством кислоты или основания, таким как эквивалентное количество, в такой среде, как, например среда, в которой соль осаждается, или в водной среде, с последующей лиофилизацией.
Соединения любой из формул (I), (II) или (III), которые содержат основную группу, такую как, помимо прочих, амин или пиридин, или имидазольное кольцо, могут образовывать соли с различными органическими и неорганическими кислотами. Примеры солей присоединения кислот включают ацетаты (например, образованные с уксусной кислотой или тригалогензамещенной уксусной кислотой, например, трифторуксусной кислотой), адипаты, альгинаты, аскорбаты, аспартаты, бензоаты, бензолсульфонаты, бисульфаты, бораты, бутираты, цитраты, камфораты, камфорсульфонаты, циклопентанпропионаты, диглюконаты, додецилсульфаты, этансульфонаты, фумараты, глюкогептаноаты, глицерофосфаты, гемисульфаты, гептаноаты, гексаноаты, гидрохлориды (образованные с хлороводородной кислотой), гидробромиды (образованные с бромоводородом), гидроиодиды, 2-гидроксиэтансульфонаты, лактаты, малеаты (образованные с малеиновой кислотой), метансульфонаты (образованные с метансульфоновой кислотой), 2-нафталинсульфонаты, никотинаты, нитраты, оксалаты, пектинаты, персульфаты, 3-фенилпропионаты, фосфаты, пикраты, пивалаты, пропионаты, салицилаты, сукцинаты, сульфаты (например, образованные с серной кислотой), сульфонаты (такие как упомянутые в настоящем описании), тартраты, тиоцианаты, толуолсульфонаты, такие как тозилаты, ундеканоаты и т.п.
Соединения любой из формул (I), (II) или (III), которые содержат кислотную группу, такие как, помимо прочих, карбоксильную, могут образовывать соли с различными органическими и неорганическими основаниями. Примеры основных солей включают соли аммония, соли щелочных металлов, такие как соли натрия, лития и калия, соли щелочноземельных металлов, такие как соли кальция и магния, соли с органическими основаниями (например, органическими аминами), такими как бензатины, дициклогексиламины, гидрабамины [образованные с N,N-бис(дегидро-абиетил)этилендиамин], N-метил-D-глюкамины, N-метил-D-глюкамиды, т-бутиламины, а также соли с аминокислотами, такими как аргинин, лизин и т.п. Группы, содержащие основный атом азота, могут быть кватернизированы такими реагентами, как галогениды низших алкилов (например, метил-, этил-, пропил- и бутилхлориды, бромиды и иодиды), диалкилсульфатами (например, диметил-, диэтил-, дибутил- и диамилсульфатами), галогенидами с длинной цепью (например, децил-, лаурил-, миристил- и стеарилхлоридами, бромидами и иодидами), арилкилгалогенидами (например, бензил- и фенэтилбромидом) и другими. Пролекарства и сольваты соединений настоящего изобретения также рассматриваются в настоящей заявке. Термин "пролекарство", используемый в настоящей заявке, обозначает соединение, которое при введении субъекту, подвергается химическому превращению в метаболических или химических процессах с образованием соединения любой из формул (I), (II) или (III), и/или их соли, и/или их сольвата. Сольватами соединений формулы (I), (II) или (III) предпочтительно являются гидраты.
Соединения любой из формулы (I), (II) или (III), а также их соли, могут существовать в таутомерной форме (например, в виде амида или иминоэфира). Все такие таутомерные формы рассматриваются в настоящей заявке как часть настоящего изобретения.
Все стереоизомеры настоящих соединений, такие как, например, стереоизомеры, которые могут существовать из-за наличия асимметричных углеродов, включая энантиомерные формы (которые могут существовать даже в отсутствие асимметричного углерода), а также диастереомерные формы, рассматриваются и включены в объем настоящего изобретения. Индивидуальные стереоизомеры соединений настоящего изобретения могут, например, по существу не содержать других изомеров или могут находиться в форме смеси, например, в виде рацематов со всеми другими, или выбранными другими, стереоизомерами. Хиральные центры настоящего изобретения могут иметь S или R конфигурацию, как определено в соответствии с Рекомендациями IUPAC 1974.
Термины "полипептид", "пептид" и "белок" попеременно используются в настоящем описании и относяся при этом к полимеру, состоящему из аминокислотных остатков. Термины относятся к аминокислотным полимерам, в которых один или более аминокислотных остатков являются искусственным химическим миметиком природной аминокислоты, а также к природным аминокислотным полимерам и синтетическим аминокислотным полимерам. Номенклатура, используемая для обозначения пептидов, является стандартной номенклатурой, используемой в данной области, в соответствии с которой аминогруппа на N-конце расположена слева, а карбоксильная группа на C-конце расположена справа.
Термин "аминокислота" относится к природным и синтетическим аминокислотам, а также аналогам аминокислот и миметикам аминокислот, которые функционируют аналогично природным аминокислотам. Если не указано иное, за исключением N-концевой аминокислоты все сокращенные обозначения (например, Ala) аминокислот в настоящем описании соответствуют структуре -NH-C(R)(R')-CO-, где каждый R и R' независимо является водородом или боковой цепью аминокислоты (например, для Ala R = CH3, а R' = H), или R и R' могут соединяться, формируя кольцевую систему. Для N-концевой аминокислоты сокращенное обозначение соответствует структуре
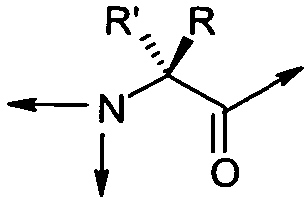
Природные аминокислоты представляют собой аминокислоты, кодируемые генетическим кодом, а также теми аминокислотами, которые затем модифицируются. Термин "аналог аминокислоты" относится к соединению, которое имеет такую же основную химическую структуру, как и природная аминокислота, то есть, α-атом углерода, который связан с водородом, карбоксильной группой, аминогруппой и группой R, например, гомосерин и норлейцин. Такие аналоги имеют модифицированные группы R (например, норлейцин) или модифицированные пептидные основные цепи, но при этом сохраняют такую же основную химическую структуру, как и природная аминокислота. "Миметики аминокислот" относятся к химическим соединениям, обладающим структурой, которая отличается от общей химической структуры аминокислоты, но при этом функционируют аналогично природной аминокислоте.
Аминокислоты могут быть указаны в настоящей заявке либо под своими стандартными трехбуквенными символами, либо однобуквенными символами, рекомендованными Комиссией по Биохимической Номенклатуре IUPAC-IUB.
Номенклатура и сокращения
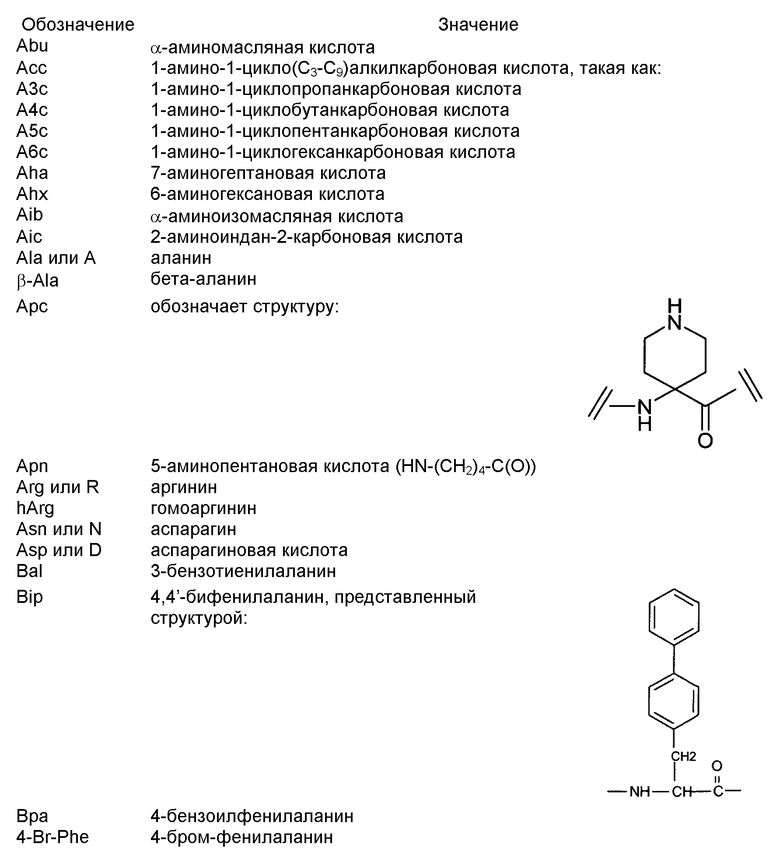

Буква "D" перед вышеуказанным трехбуквенным сокращенным обозначением, например как в "D-Nal" или "D-Phe", обозначает D-форму аминокислоты. Буква "L" перед трехбуквенным сокращенным обозначением аминокислоты обозначает природную L-форму аминокислоты. В рамках настоящего описания, если не указано иное, отсутствие "D" или "L" обозначения указывает, что сокращенное обозначение соответствет L-форме. Когда используется обычное однобуквенное сокращенное обозначение, заглавные буквы относятся к L-форме, а строчные буквы относятся к D-форме, если не указано иное.
Обозначение "NH2", например, в Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2, (SEQ ID NO:58) указывает, что C-конец пептида амидирован. Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys), (SEQ ID NO:59) или, альтернативно, Ac-Nle-c(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-OH, (SEQ ID NO:60) указывает, что C-конец является свободной кислотой.
"-c(Cys-Cys)-" или "-цикло(Cys-Cys)-" обозначает структуру:
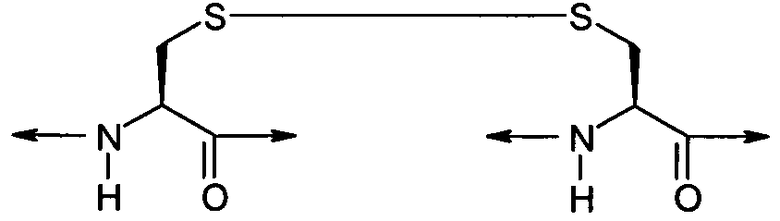
"-c(Cys-Pen)-" или "-цикло(Cys-Pen)-" обозначает структуру:
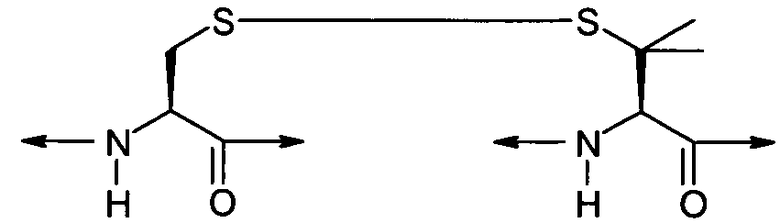
"-c(Asp-Lys)-" или "-цикло(Asp-Lys)-" обозначает структуру:
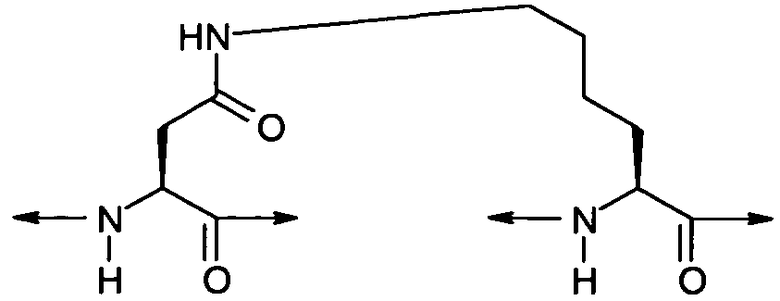
Заявители разработали следующее сокращенное обозначение, используемое при обозначении конкретных вариантов осуществления и/или видов:
"Гидантоин C(O)-(Aa-Ab)" обозначает структуру: 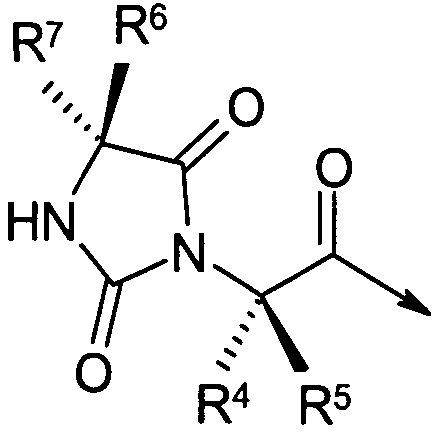 ,
,
где аминокислота "Aa" имеет структуру: 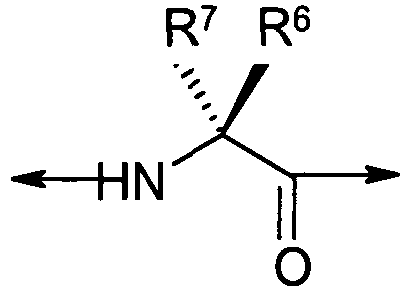 , а
, а
аминокислота "Ab" имеет структуру: 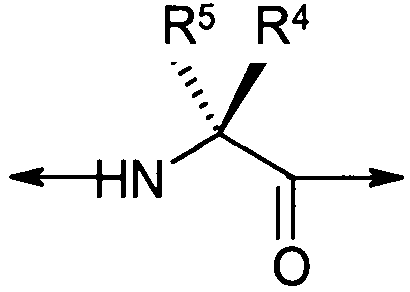 .
.
Например, соединение, обозначенное как "цикло[Гидантоин(C(O)-(Cys-Ab))-A1-A2-A3-A4-Cys]-", имеет следующую структуру:
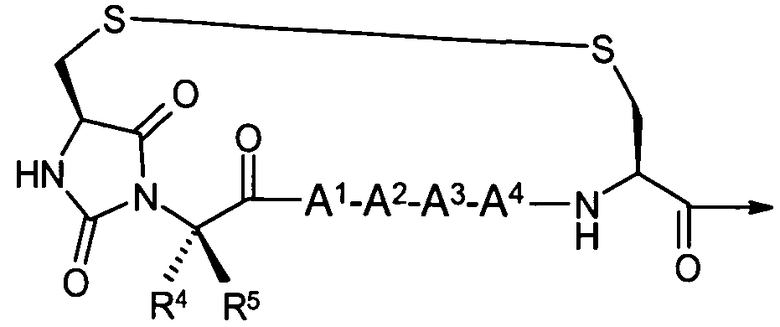 ,
,
тогда как соединение, обозначенное как "цикло[Гидантоин(C(O)-(Ab-Cys))-A1-A2-A3-A4-Cys]-", имеет структуру:
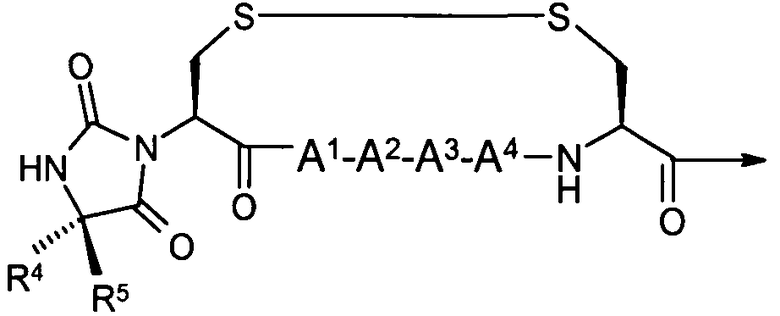 .
.
Для большей ясности "цикло[Гидантоин(C(O)-(Asp-Ab))-A1-A2-A3-A4-Lys]-" обозначает следующее соединение:
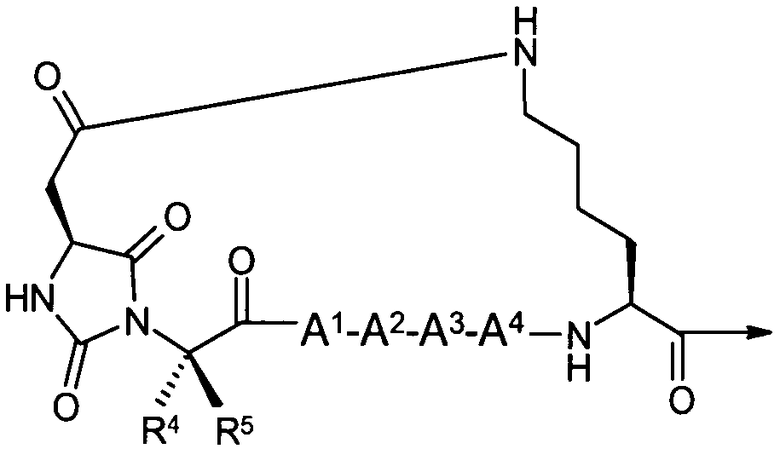 ,
,
тогда как "цикло[Гидантоин(C(O)-(Dap-Ab))-A1-A2-A3-A4-Asp]-" имеет следующую формулу:
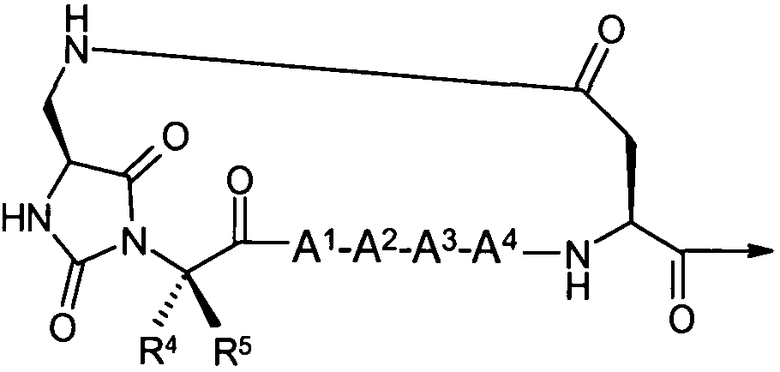 .
.
Используемые в настоящем описании "агонист MC-3", "агонист MC-4", "агонист MC-5" относятся к соединению, обладающему аффинностью к рецептору MC-3, рецептору MC-4 или рецептору MC-5, соответственно, что приводит к появлению измеримой биологической активности в клетках, тканях или организмах, которые содержат рецепторы MC-3, MC-4 или MC-5. Анализы, которые демонстрируют MC-3/MC-4/MC-5 агонистическую активность соединений, известны в уровне техники.
Используемые в настоящем описании "антагонист MC-3", "антагонист MC-4" и "антагонист MC-5" относятся к соединениям, обладающим аффинностью к рецептору MC-3, рецептору MC-4 или рецептору MC-5, соответственно, и блокирующим стимуляцию, вызываемую известным агонистом MC. Анализы, которые демонстрируют MC-3/MC-4/MC-5 антагонистическую активность соединений, известны специалистам в данной области.
Используемые в настоящем описании "рецептор MC-3", "рецептор MC-4" и " рецептор MC-5" означают известные рецепторы MC-3, MC-4 и MC-5, их сплайс-варианты, а также неописанные рецепторы. Рецептор MC-3 описан Gantz et al., выше (MC-3 человека); Desarnaud et al., выше (MC-3 мыши); а также Reyfuss, L. et al., "Identification of a Receptor for Gamma Melanotropin and Other Proopiomelanocortin Peptides in the Hypothalamus and Limbic System", Proc. Natl. Acad. Sci. USA, 90:8856-60 (1993). Рецептор MC-4 описан Gantz et al., выше (MC-4 человека); Alvaro, J. D. et al., "Morphine Down-Regulates Melanocortin-4 Receptor Expression in Brain Regions that Mediate Opiate Addiction", Mol-Pharmacol., 50(3):583-91 (1996); и Takeuchi, S. et al., "Melanocortin Receptor Genes in the Chicken-Tissue Distributions", Gen-Comp-Endocrinol., 112(2):220-31 (1998).
Используемый в настоящем описании "измеримый" означает, что биологический эффект является воспроизводимым и существенно отличается от базовой дисперсии анализа.
"Фармацевтически приемлемая соль" является катионной солью, образованной по любой кислотной (карбоксильной) группе, или анионной солью, образованной по любой основной (например, амино) группе, и известна в уровне техники, как описано в WO 87/05297 (Johnston et al., 1987), включенной в настоящую заявку путем ссылки. Предпочтительные катионные соли включают соли щелочных металлов (таких как натрий и калий) и соли щелочноземельных металлов (таких как магний и кальций), а также органические соли. Предпочтительные анионные соли включают галогениды (такие как хлориды), сульфонаты, карбоксилаты, фосфаты и т.п. Безусловно, среди таких солей рассматриваются соли дополнения, которые могут вводить оптический центр, когда таковой не присутствует. Например, из соединений изобретения может быть получен хиральный тартрат, причем данное определение включает подобные хиральный соли. Квалифицированный специалист способен получить любое число солей при наличии информации в уровне техники. Кроме того, квалифицированный специалист может предпочесть одну соль другой по соображениям растворимости, стабильности, легкости введения в лекарственную форму и т.п. Определение и оптимизация таких солей находятся в пределах практических навыков квалифицированного специалиста.
Фраза "специфично (или селективно) связывается" с меланокортиновым рецептором в случае, когда относится к белку или пептиду, относится к реакции связывания, которая служит показателем присутствия белка в гетерогенной популяции белков и других биологических веществ. Таким образом, в заданных условиях иммуноанализа указанные пептиды связываются со специфичным меланокортиновым рецептором с большей скоростью, чем фон, и практически не связываются в существенном количестве с другими белками, присутствующими в пробе. Как правило, интенсивность специфичной или селективной реакции, по меньшей мере, в два раза выше по сравнению с фоновым сигналом или шумом и обычно интенсивнее фона более чем в 10-100 раз.
Используемый в настоящем описании термин "селективный" означает наличие преимущества в активации специфичного рецептора по сравнению с другими рецепторами, которое может быть определено количественно на основе анализов с использованием цельных клеток, тканей или организмов, которые демонстрируют активность рецептора, например, системы цАМФ иммуноферментного анализа (ИФА). Селективность соединения определяют при сравнении его значений EC50 на соответствующих контрольных рецепторах. Используемый в настоящем описании термин "селективный по сравнению с другими MC рецепторами" означает селективный по сравнению со всеми другими рецепторами MC-R. Например, соединение, имеющее EC50 8 нМ для рецептора MC-4 и EC50≥80 нМ для рецепторов MC-1, MC-2, MC-3 и MC-5, обладает показателем селективности для MC-4 рецептора по отношению к другим MC рецепторам, по меньшей мере, 1:10. Кроме того, следует понимать, что селективность может также относиться к одному из рецепторов MC-1, MC-2 или MC-5 в отдельности. Например, соединение, имеющее EC50 8 нМ для рецептора MC-4 и EC50 80 нМ для рецептора MC-1, обладает показателем селективности для MC-4 рецептора по отношению к рецептору MC-1 1:10. Такое соединение является селективным по сравнению с рецептором MC-1, независимо от его значения EC50 для MC-2 или MC-5.
Используемые в настоящем описании термины "лечить" и "лечение" включают паллиативное, терапевтическое и профилактическое лечение.
Способы получения
Пептиды настоящего изобретения могут быть получены с помощью стандартного твердофазного синтеза пептидов. См., например, Stewart, J. M., et al., Solid Phase Synthesis (Pierce Chemical Co., 2d ed. 1984). Исходные материалы коммерчески доступны или могут быть легко получены средним специалистом в данной области с помощью известных способов. Растворители, температура, давление и другие условия реакции могут быть легко подобраны средним специалистом в данной области.
Заместители R2 и R3 вышеуказанной обобщенной формулы могут быть присоединены к свободному амину N-концевой аминокислоты стандартными методами, известными из уровня техники. Например, алкильные группы, например (C1-C30)алкил, могут быть присоединены с использованием восстановительного алкилирования. Гидроксиалкильные группы, например, (C1-C30)гидроксиалкил, также могут быть присоединены с использованием восстановительного алкилирования, при котором свободную гидроксильную группу защищают т-бутиловым эфиром. Ацильные группы, например COE1, могут быть присоединены посредством присоединения свободной кислоты, например E1COOH, к свободному амину N-концевой аминокислоты посредством смешивания подготовленной смолы с 3 молярными эквивалентами свободной кислоты и диизопропилкарбодиимида в метиленхлориде в течение одного часа. Если свободная кислота содержит свободную гидроксильную группу, как, например, п-гидроксифенилпропионовая кислота, то присоединение следует выполнять в присутствии дополнительных 3 молярных эквивалентов HOBT.
Когда R1 представляет собой -NH2, синтез пептида начинается с Fmoc-аминокислоты, которая присоединена к смоле Rink Amide MBHA. Если R1 представляет собой -OH, синтез пептида начинается с Fmoc-аминокислоты, которая присоединена к смоле Wang.
В синтезе пептида согласно настоящему изобретению, содержащего A6c и/или Aib, время присоединения для указанных остатков и остатка непосредственно после них составляет 2 часа.
Обозначенные стадии могут быть изменены с целью повышения выхода целевого продукта. Квалифицированный специалист осведомлен, что правильный выбор реагентов, растворителей и температур является важным компонентом в любом успешном синтезе. Определение оптимальных условий является стандартной процедурой, причем квалифицированный специалист может получить разнообразные соединения, используя приведенное ниже описание.
Необходимо понимать, что квалифицированный специалист в области органической химии может легко выполнить стандартные манипуляции с органическими соединениями без дополнительного пояснения, то есть проведение подобных манипуляций полностью входит в компетенцию и соответствует практическим навыкам квалифицированного специалиста. Указанные манипуляции включают, помимо прочих, восстановление карбонильных соединений до соответствующих спиртов, окисление гидроксилов и т.п., ацилирование, нуклеофильное и электрофильное замещение ароматических соединений, а также эфиризацию, этерификацию, омыление и т.п.
Квалифицированный специалист также с готовностью сумеет оценить, что некоторые реакции лучше всего проводить, когда потенциально реакционноспособные функциональные группы на молекуле блокированы или защищены, избегая, таким образом, протекания каких-либо побочных реакций и/или повышая выход реакции. Нельзя не отметить, что предпочтительно использовать защитную группу для любых реакционноспособных функциональных групп, таких как карбоксил, гидроксил и т.п. Это является стандартной практикой, полностью входящей в компетенцию квалифицированного специалиста. Указанные реакции можно найти в литературе, при этом они также полностью входят в компетенцию квалифицированного специалиста.
Некоторые сокращенные обозначения, используемые в процессе описания синтеза типичных примеров, приведенных ниже, имеют следующее определение:
Типичные примеры синтеза типичных соединений настоящего изобретения описаны в Примерах 1-5. В описанных способах получения пептида согласно настоящему изобретению использованы способы, известные квалифицированным специалистам. Другие способы также известны квалифицированным специалистам. Примеры приведены исключительно в целях пояснения и никонм образом не должны ограничивать объем настоящего изобретения.
Пример 1: цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH 2 (SEQ ID NO:1)
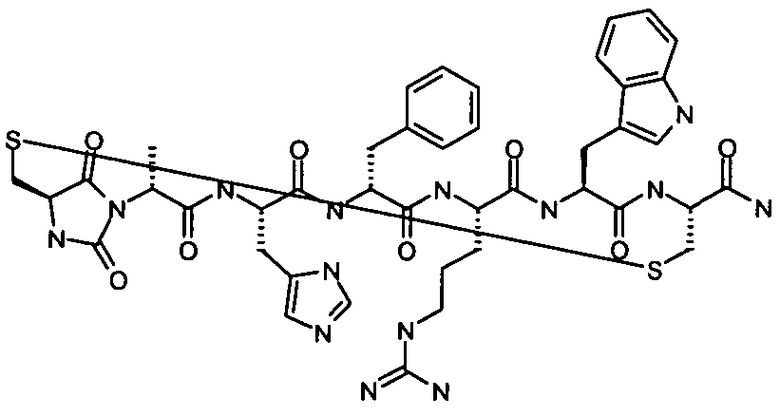
Гидантоинсодержащий циклический пептид-амид, цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH2 (SEQ ID NO:1) синтезировали, используя Fmoc-метод на синтезаторе пептидов Apex (AAPPTEC; Louisville, KY, USA). Вначале 135 мг 0,78 ммоль/г (0,105 ммоль) смолы Rink Amide MBHA (Novabiochem; San Diego, CA, USA) вносили в реакционную ячейку и перед синтезом выдерживали в 1,5 мл диметилформамида (ДМФА). Цикл 1: смолу обрабатывали двумя частями по 1,5 мл 25% пиперидина в ДМФА в течение 5 минут и 25 минут соответственно, затем 4× промывали 1,5 мл ДМФА; каждая промывка состояла из добавления 1,5 мл растворителя, перемешивания в течение 1 минуты и слива растворителя в течение 1 минуты. Стоковые растворы аминокислот готовили в N-метилпирролидиноне (NMP) в виде 0,45 М растворов, содержащих 0,45 M N-гидроксибензотриазола (HOBT). Диизопропилкарбодиимид (DIC) готовили в виде 1,3 М раствора в NMP. К деблокированной смоле добавляли 1,45 мл (0,7 ммоль) первой аминокислоты, Fmoc-цистеина(Trt)-ОН (Novabiochem; San Diego, CA, USA) вместе с 0,5 мл (0,65 ммоль) DIC. Через час непрерывного перемешивания реагенты удаляли со смолы и повторяли стадию присоединения. После ацилирования аминокислот смолу промывали двумя аликвотами ДМФА по 1,5 мл, каждая промывка длилась 1 минуту. Процесс синтеза пептида (деблокирование/промывка/ацилирование/промывка) повторяли в течение 2-7 циклов, которые проводили по аналогичной методике, описанной для цикла 1. В частности использовали следующие аминокислоты, Цикл 2: Fmoc-Trp (Boc)-OH (Genzyme; Cambridge, MA, USA); Цикл 3: Fmoc-Arg (Pbf)-OH (Novabiochem; San Diego, CA, USA); Цикл 4: Fmoc-D-Phe-OH (Genzyme; Cambridge, MA, USA); Цикл 5: Fmoc-His(Trt)-OH (Novabiochem; San Diego, CA, USA); Цикл 6: Fmoc-D-Ala-OH (Genzyme; Cambridge, MA, USA); и Цикл 7: Fmoc-Cys (Trt)-OH (Novabiochem; San Diego, CA, USA). N-концевой Fmoc удаляли 25% пиперидином в ДМФА с последующей четырехкратной промывкой ДМФА по 1,5 мл с продолжительностью каждой промывки 1 минута.
Смолу с синтезированным пептидом обрабатывали несколькими миллилитрами смеси 1,4-диоксан/вода (9:1), сушили, а затем обрабатывали 5,6 мл (80 эк.) 1,5 M диизопропилэтиламина (DIPEA) в смеси диоксан/вода (9:1) с последующим добавление 1 мл 0,32 М (3,0 эк.) фенилхлорформиата в смеси диоксан/вода (9:1). Раствор перемешивали в течение 1 часа, сушили и несколько раз промывали смесью диоксан/вода, а затем несколько раз этиловым эфиром. Затем смолу обрабатывали 0,5 М DIPEA в ДМФА и перемешивали в течение двух часов. После этого смолу снова промывали смесью диоксан/вода, а затем этиловым эфиром.
К полученной смоле с синтезированным пептидом добавляли 5 мл реагента следующего состава: 2% триизопропилсилана (TIS), 5% воды, 5% (мас./об.) дитиотреитол (DTT), 88% трифторуксусной кислоты (ТФУ); после чего смесь оставляли перемешиваться в течение 3,5 часов. Образовавшийся фильтрат собирали в 40 мл холодного безводного этилового эфира. Смесь центрифугировали в течение 10 минут при 3500 об/мин в охлаждаемой центрифуге. Эфир сливали с осадка, а пептид ресуспендировали в свежем эфире. Промывку эфиром проводили в общей сложности 3 раза. После заключительной промывки эфиром пептид оставляли сушиться на воздухе до отсутствия остатка эфира.
Пептид растворяли в 10% ацетонитриле и анализировали с помощью масс-спектрометрии и обращенно-фазовой ВЭЖХ с использованием колонки 30×4,6 см C18 (Vydac; Hesperia, CA, USA) в градиенте ацетонитрила 2-60% (0,1% ТФУ) в течение 30 минут. Данный анализ выявил наличие продукта с чистотой >42%, остальная часть преимущественно являлась продуктом, не содержащим гидантоин. Масс-спектральный анализ с использованием ионизации электрораспылением выявил основной продукт с массой 947,42 Да, которая соответствует целевому востановленному продукту. Неочищенный продукт (~95 мг) растворяли в концентрации 2 мг/мл в 5%-ной уксусной кислоте. К полученному раствору по каплям добавляли 0,5 М иод в метаноле при энергичном перемешивании, пока смесь не окрашивалась в бледно-желтый цвет. Раствор энергично перемешивали еще в течение 10 минут. Избыток иода удаляли, добавляя 1,0 М тиосульфат натрия при непрерывном перемешивании, пока смесь не становилась бесцветной. Пептид повторно анализировали с помощью масс-спектрометрии и ВЭЖХ. Масс-спектральный анализ показал наличие основного продукта с массой 944,44, что указывает на успешное окисление пептида. Раствор пептида концентрировали до объема ~10 мл, используя центробежный испаритель, а затем очищали с помощью препаративной ВЭЖХ, оборудованной колонкой C18, используя аналогичный градиент элюирования. Чистоту очищенного продукта повторно анализировали с помощью ВЭЖХ (> 95%) и масс-спектрометрии (945,1 Да), а затем лиофилизировали. После лиофилизации получили 13,6 мг очищенного продукта с выходом 13,7%.
Пример 2: цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH 2 (SEQ ID NO:11)
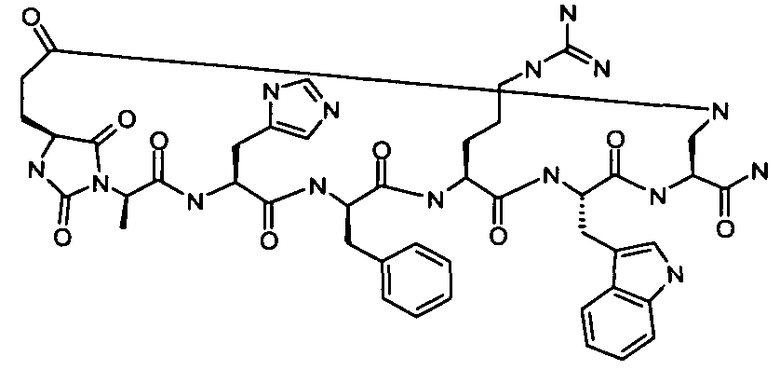
Гидантоинсодержащий пептидолактам цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH2 (SEQ ID NO:11) синтезировали с использованием Fmoc-метода на синтезаторе пептидов Apex (AAPPTEC, Louisville, KY, USA). Вначале 135 мг 0,78 ммоль/г (0,105 ммоль) смолы Rink Amide MBHA (Novabiochem; San Diego, CA, USA) вносили в реакционную ячейку и выдерживали в 1,5 мл диметилформамида (ДМФА). Цикл 1: смолу обрабатывали двумя частями 25% пиперидина в ДМФА по 1,5 мл в течение 5 и 10 минут, соответственно, после чего промывали ДМФА 4× по 1,5 мл, каждая промывка включала добавление 1,5 мл растворителя, перемешивание в течение 1 минуты и слив в течение 1 минуты. Стоковые растворы аминокислот готовили в N-метилпирролидиноне (NMP) в виде 0,45 М растворов, содержащих 0,45 М N-гидроксибензотриазола (HOBT). Диизопропилкарбодиимид (DIC) готовили в виде 1,3 М раствора в NMP. К деблокированной смоле добавляли 1,45 мл (0,62 ммоль) первой аминокислоты, Fmoc-Dap(Mtt)-OH (Novabiochem; San Diego, CA, USA) вместе с 0,5 мл (0,62 ммоль) DIC. Через час непрерывного перемешивания реагенты сливали и повторяли стадию присоединения. После ацилирования аминокислот смолу промывали двумя аликвотами ДМФА по 1,5 мл, по 1 минуте. Процесс синтеза пептида (деблокирование/промывка/ацилирование/промывка) повторяли в течение 2-7 циклов, которые были идентичны циклу 1, описанному выше. Использовали следующие аминокислоты в соответствии с циклами, как указано: Цикл 2: Fmoc-trp(Boc)-OH (Genzyme; Cambridge, MA, USA); Цикл 3: Fmoc-Arg(Pbf)-OH (Genzyme; Cambridge, MA, USA); Цикл 4: Fmoc-D-Phe-OH (Novabiochem; San Diego, CA, USA); Цикл 5: Fmoc-His(Trt)-OH (Genzyme; Cambridge, MA, USA); Цикл 6: Fmoc-D-Ala-OH (Genzyme; Cambridge, MA, USA) и Цикл 7: Fmoc-Glu (O-2-PhiPr)-OH (Bachem, King of Prussia, PA). N-концевой Fmoc удаляли 25% пиперидином в ДМФА с последующей четырехкратной промывкой 1,5 мл ДМФА по 1 минуте, затем трехкратной промывкой дихлорметаном (DCM) по 1 минуте.
Смолу обрабатывали 80 эк. 1,5 М диизопропилэтиламина (DIPEA) в DCM, а затем 2,0 эк. п-нитрофенилхлорформиата в DCM. Раствор перемешивали в течение 2 часов, сушили и несколько раз промывали ДМФА. Затем смолу обрабатывали 10 эк. DIPEA в ДМФА и перемешивали в течение 30 минут. Смолу промывали ДМФА, а затем DCM.
Mtt (метилтритильную) защитную группу боковой цепи диаминопропионовой кислоты (Dap), а также O-2-PhiPr (O-2-фенилизопропильную) защитную группу боковой цепи глутаминовой кислоты (Glu) удаляли путем 10 промывок 5 мл 5% триизопропилсилана (TIS) и 1% трифторуксусной кислоты (ТФУ) в DCM в течение 3-5 минут каждая. После заключительной промывки смолу снова промывали вначале DCM, а затем дважды ДМФА. Смолу дважды обрабатывали DIPEA (10 эк.) в ДМФА по 2 минуты, после чего 4× промывали ДМФА. Аликвота смолы (<1 мг) дала положительный тест Кайзера (положительный контроль: темно-синий цвет). Затем смолу обрабатывали 10 эк. 0,5 М HOBT, 10 эк. 0,5 М PyAop, 20 эк. 2 М DIPEA и 0,5 эк. 0,45 М DMAP в течение 8 часов с постоянным перемешиванием. Последующий тест Кайзера был слабоположительным, что указывало на неполное образование лактама. Второй цикл синтеза лактама включал дабавление 10 эк. 0,5 М HOAT, 2 эк. 0,5 М HATU, 20 эк. 1 М DIPEA и 0,5 эк. 0,45 М DMAP с постоянным перемешиванием в течение 4 часов. Последующий тест Кайзера на присутствие свободного амина был отрицательным (отсутствие синего цвета). Смолу однократно промывали ДМФА, а затем три раза DCM.
К смоле добавляли приблизительно 5 мл реагента следующего состава: 2% TIS, 5% воды, 5% (мас./об.) дитиотреитола (DTT) и 88% ТФУ, после чего смесь оставляли перемешиваться в течение 3,5 часов. Фильтрат собирали в 40 мл холодного безводного этилового эфира. Смесь центрифугировали в течение 10 минут при 3500 об/мин в охлаждаемой центрифуге. Эфир сливали с осадка, а пептид ресуспендировали в свежем эфире. Промывку эфиром проводили в общей сложности 3 раза. После заключительной промывки эфиром пептид оставляли сушиться на воздухе до отсутствия остатка эфира. Полученный пептид растворяли в 10%-ном ацетонитриле и анализировали с помощью масс-спектрометрии. Выявили одиночный продукт с массой 938,7 Да, соответствующий целевому гидантоин-лактамному пептиду. Неочищенный продукт (~90 мг) очищали с помощью препаративной ВЭЖХ, оборудованной колонкой C18, используя подходящий градиент элюирования. Чистоту очищенного продукта повторно анализировали с помощью ВЭЖХ (>95%) и лиофилизировали, получив 24 мг продукта, выход при этом составил 25%.
Пример 3: цикло[Гидантоин(C(O)-(Gly-Cys))-Glu-His-D-Phe-Arg-Trp-Cys]-NH 2 (SEQ ID NO:57)
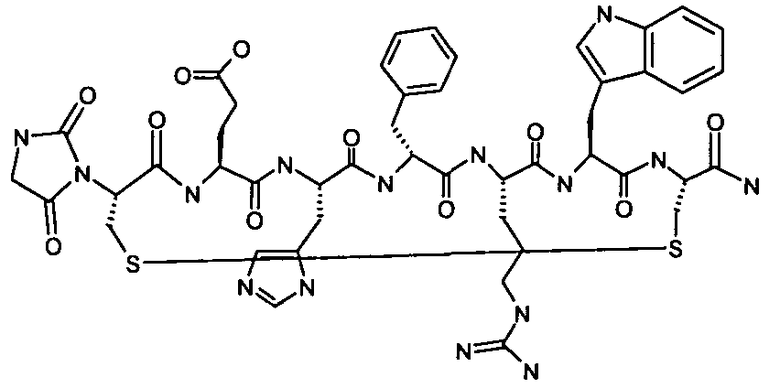
Гидантоин-содержащий циклический пептид-амид цикло[Гидантоин(C(O)-(Gly-Cys))-Glu-His-D-Phe-Arg-Trp-Cys]-NH2 (SEQ ID NO:57) синтезировали с использованием Fmoc-метода на синтезаторе пептидов Apex (AAPPTEC, Louisville, KY, USA). Перед началом синтеза в реакционную ячейку вносили 220 мг 0,91 ммоль/г (0,20 ммоль) смолы Rink Amide MBHA (Polymer Laboratories, Amherst, MA, USA) и выдерживали ее в 3,0 мл диметилформамида (ДМФА). Цикл 1: смолу обрабатывали двумя частями 25% пиперидина в ДМФА по 3 мл в течение 5 и 10 минут, соответственно, после чего промывали ДМФА 4× по 3 мл, каждая промывка включала добавление 3 мл растворителя, перемешивание в течение 1 минуты и слив в течение 1 минуты. Стоковые растворы аминокислот готовили в N-метилпирролидиноне (NMP) в виде 0,45 М растворов, содержащих 0,45 М N-гидроксибензотриазола (HOBT). HBTU [гексафторфосфат 2-(1H-бензо-триазол-1-ил)-1,1,3,3-тетраметилурония] готовили в виде 0,45 М раствора в NMP, а диизопропилэтиламин (DIPEA) готовили в виде 2,73 М раствора в NMP. К деблокированной смоле добавляли 2 мл первой аминокислоты (0,9 ммоль), Fmoc-Cys(Trt)-OH (Novabiochem; San Diego, CA, USA) вместе с 2 мл (0,9 ммоль) HBTU и 1,5 мл (4,1 ммоль) DIPEA. Через час непрерывного перемешивания реагенты сливали и повторяли стадию присоедиения. После ацилирования аминокислот смолу промывали двумя аликвотами по 3 мл ДМФА по 1 минуте. Процесс синтеза пептида (деблокирование/промывка/ацилирование/промывка) повторяли в течение 2-8 циклов, которые были идентичны циклу 1, описанному выше. Использовались следующие аминокислоты: Цикл 2: Fmoc-Trp(Boc)-OH (Genzyme; Cambridge, MA, USA); Цикл 3: Fmoc-Arg(Pbf)-OH (Novabiochem; San Diego, CA, USA); Цикл 4: Fmoc-D-Phe-OH (Genzyme; Cambridge, MA, USA); Цикл 5: Fmoc-His(Trt)-OH (Novabiochem; San Diego, CA, USA); Цикл 6: Fmoc-Glu-OH (Genzyme; Cambridge, MA, USA); Цикл 7: Fmoc-Cys(Trt)-OH (Novabiochem; San Diego, CA, USA) и Цикл 8: Fmoc-Gly-OH (Novabiochem; San Diego, CA, USA). N-концевой Fmoc удаляли 25% пиперидином в ДМФА, как описано ранее, с последующей четырехкратной промывкой ДМФА по 3 мл, по 1 минуте.
Смолу обрабатывали 80 эк. 1,5 M DIPEA в дихлорметане (DCM), а затем добавляли 1,1 эк. п-нитрофенилхлорформиат в DCM. Раствор перемешивали в течение 2 часов, сушили и несколько раз промывали ДМФА. Затем смолу обрабатывали 10 эк. DIPEA в ДМФА и перемешивали в течение 30 минут. Смолу снова промывали ДМФА, а затем DCM.
К смоле добавляли 5 мл реагента следующего состава и перемешивали в течение 3 ½ часов: 2% триизопропилсилан (TIS), 5% воды, 5% (мас./об.) дитиотреитола (DTT) и 88% трифторуксусной кислоты (ТФУ). Образовавшийся фильтрат собирали в 40 мл холодного безводного диэтилового эфира. Смесь центрифугировали в течение 10 минут при 3500 об/мин в охлаждаемой центрифуге. Эфир сливали с осадка, а собранный пептид ресуспендировали в свежем эфире. Промывку эфиром проводили 3 раза. После заключительной промывки эфиром пептид сушили на воздухе, чтобы удалить остаток эфира.
Высушенный пептид растворяли в 10%-ном ацетонитриле и анализировали с помощью масс-спектрометрии и обращенно-фазовой ВЭЖХ, используя колонку C18 30×4,6 см (Vydac; Hesperia, CA, USA) с градиентом ацетонитрила 2-60% (0,1% ТФУ) в течение 30 минут. Анализ ВЭЖХ выявил продукт, имевший 30% чистоту. Остальную часть составлял продукт, не содержащий гидантоин. Масс-спектральный анализ с использованием ионизации электрораспылением выявил основной продукт с массой 1062 Да, соответствующий целевому восстановленному продукту. Неочищенный продукт (~200 мг) растворяли до концентрации 2 мг/мл в 5%-ной уксусной кислоте. К полученному раствору по каплям добавляли 0,5 М иод в метаноле при энергичном перемешивании, пока смесь не окрашивалась в бледно-желтый цвет. Раствор энергично перемешивали в течение еще 10 минут. Избыток иода удаляли, добавляя 1,0 М тиосульфат натрия при непрерывном перемешивании, пока смесь не становилась бесцветной. Пептид повторно анализировали с помощью масс-спектрометрии и ВЭЖХ. Масс-спектральный анализ показал наличие основного продукта с массой 1060,4 Да, что указывает на успешное окисление пептида. Раствор пептида концентрировали до объема ~10 мл, используя центробежный испаритель, а затем очищали с помощью препаративной ВЭЖХ, оборудованной колонкой C18, используя аналогичный градиент элюирования. Чистоту очищенного продукта повторно анализировали с помощью ВЭЖХ (>95%) и масс-спектрометрии (1059,7 Да), а затем лиофилизировали. После лиофилизации получили 16,8 мг очищенного продукта, выход составил 7,9%.
Пример 4: Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH 2 (SEQ ID NO:42)
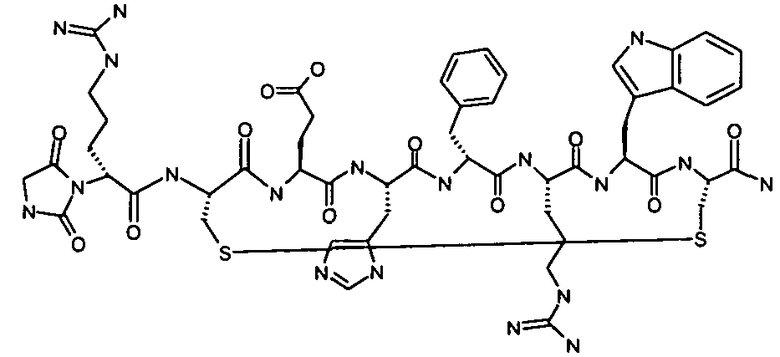
Гидантоинсодержащий циклический пептид-амид, Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2, (SEQ ID NO:42) синтезировали, используя Fmoc-метод, на синтезаторе пептидов Apex (APAPPTEC, Louisville, KY, USA).
Перед началом синтеза озаглавленного соединения 220 мг 0,91 ммоль/г (0,20 ммоль) смолы Rink Amide MBHA (Polymer Laboratories, Amherst, MA, USA) вносили в реакционную ячейку для выдерживания в 3,0 мл диметилформамида (ДМФА). Цикл 1 : смолу обрабатывали двумя частями 25% пиперидина в ДМФА по 3 мл в течение 5 и 10 минут, соответственно, после чего промывали ДМФА 4× по 3 мл, каждая промывка включала добавление 3 мл растворителя, перемешивание в течение 1 минуты и слив в течение 1 минуты. Стоковые растворы аминокислот готовили в N-метилпирролидиноне (NMP) в виде 0,45 М растворов, содержащих 0,45 М N-гидроксибензотриазола (HOBT). HBTU [гексафторфосфат 2-(1H-бензо-триазол-1-ил)-1,1,3,3-тетраметилурония] готовили в виде 0,45 М раствора в NMP. Диизопропилэтиламин (DIPEA) готовили в виде 2,73 М раствора в NMP. К деблокированной смоле добавляли 2 мл первой аминокислоты (0,9 ммоль), то есть Fmoc-Cys(Trt)-OH (Novabiochem, San Diego, CA, USA), вместе с 2 мл (0,9 ммоль) HBTU и 1,5 мл (4,1 ммоль) DIPEA. Через час непрерывного перемешивания реагенты сливали и повторяли стадию присоединения. После ацилирования аминокислот смолу промывали двумя аликвотами по 3 мл ДМФА по 1 минуте. Процесс синтеза пептида, то есть деблокирование, промывка, ацилирование и промывка, как описано выше для цикла 1, повторяли в течение 2-9 циклов. В каждом отдельном цикле использовали следующие аминокислоты, как указано далее: Цикл 2: Fmoc-Trp (Boc)-OH (Genzyme; Cambridge, MA, USA); Цикл 3: Fmoc-Arg(Pbf)-OH (Novabiochem; San Diego, CA, USA); Цикл 4: Fmoc-D-Phe-OH (Genzyme; Cambridge, MA, USA); Цикл 5: Fmoc-His(Trt)-OH (Novabiochem; San Diego, CA, USA); Цикл 6: Fmoc-Glu-OH (Genzyme; Cambridge, MA, USA); Цикл 7 : Fmoc-Cys (Trt)-OH (Novabiochem; San Diego, CA, USA); Цикл 8: Fmoc-D-Arg(Pbf)-OH (Genzyme; Cambridge, MA, USA) и Цикл 9: Fmoc-Gly-OH (Novabiochem; San Diego, CA, USA). N-концевую защитную группу Fmoc снимали 25% раствором пиперидина в ДМФА, как описано ранее, с последующей четырехкратной промывкой ДМФА по 3 мл, длительность каждой промывки составляла 1 минуту.
Смолу обрабатывали 80 эк. 1,5 M DIPEA в дихлорметане (DCM), а затем добавляли 1,1 эк. п-нитрофенилхлорформиата в DCM. Реакционную смесь перемешивали в течение 2 часов, растворитель удаляли, а полученный продукт несколько раз промывали ДМФА. Смолу обрабатывали 10 эк. DIPEA в ДМФА и перемешивали в течение приблизительно 30 минут. Смолу промывали ДМФА, а затем DCM.
К смоле добавляли 5 мл реагента следующего состава: 2% триизопропилсилана (TIS), 5% воды, 5% (мас./об.) дитиотреитола (DTT) и 88% трифторуксусной кислоты (ТФУ). Раствор перемешивали в течение 3,5 часов. Фильтрат собирали в 40 мл холодного безводного этилового эфира. Смесь центрифугировали в течение 10 минут при 3500 об/мин в охлаждаемой центрифуге. Эфир сливали с осадка, а собранный пептид ресуспендировали в свежем эфире. Промывку эфиром повторяли еще 3 раза. После заключительной промывки эфиром пептид сушили на воздухе, чтобы удалить остатки эфира.
Пептид растворяли в 10%-ном ацетонитриле и анализировали с помощью масс-спектрометрии и обращенно-фазовой ВЭЖХ с использованием 30×4,6 см колонки C18 (Vydac; Hesperia, CA, USA) в градиенте ацетонитрила 2-60% (0,1% ТФУ) в течение 30 минут. Описанный анализ показал, что чистота продукта составляла ~30%, при этом остальную часть в основном составлял продукт, не содержащий гидантоин. Масс-спектральный анализ с использованием ионизации электрораспылением выявил наличие основного продукта с массой 1218 Да, которая совпадает с ожидаемой массой восстановленного продукта. Неочищенный продукт (~200 мг) растворяли до концентрации 2 мг/мл в 5%-ной уксусной кислоте. К полученному раствору по каплям добавляли 0,5 М иод в метаноле при энергичном перемешивании, пока смесь не окрашивалась в бледно-желтый цвет. Раствор энергично перемешивали в течение 10 минут. Избыток иода удаляли, добавляя 1,0 М тиосульфат натрия при непрерывном перемешивании, пока смесь не становилась бесцветной. Пептид повторно анализировали с помощью масс-спектрометрии и ВЭЖХ. Масс-спектральный анализ показал наличие основного продукта с массой 1216,4 Да, что указывает на успешное окисление пептида. Раствор пептида концентрировали до объема ~10 мл, используя центробежный испаритель, а затем очищали с помощью препаративной ВЭЖХ, оборудованной колонкой C18, используя аналогичный градиент элюирования. Чистоту очищенного продукта повторно анализировали с помощью ВЭЖХ (>95%) и масс-спектрометрии (1216,4 Да), а затем лиофилизировали. После лиофилизации получили 18,4 мг очищенного продукта, выход составил 7,5%.
Пример 5: Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH 2 (SEQ ID NO:13)
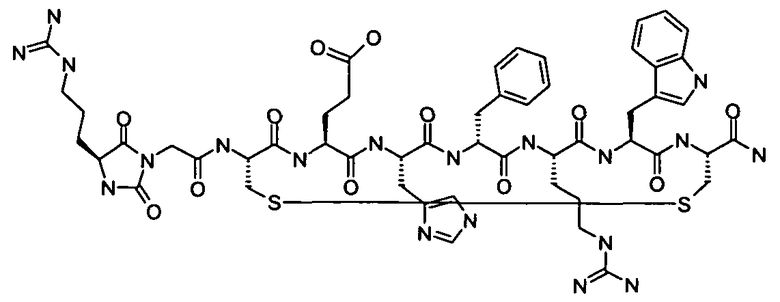
Пептид Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2 (SEQ ID NO:13) синтезировали, используя Fmoc-метод, на синтезаторе пептидов Apex (AAPPTEC, Louisville, KY, USA). В десять отдельных реакционных ячеек синтезатора вносили аликвоты по 270 мг из 0,74 ммоль/г (0,20 ммоль) смолы Rink Amide MBHA (Novabiochem; San Diego, CA, USA) и выдерживали в 3,0 мл диметилформамида (ДМФА). Цикл 1: смолу обрабатывали двумя частями 25% пиперидина в ДМФА по 3 мл в течение 5 и 10 минут, соответственно, после чего промывали ДМФА 4× по 3 мл. Каждая промывка включала добавление 3 мл растворителя, перемешивание в течение 1 минуты и слив в течение 1 минуты. Стоковые растворы аминокислот готовили в N-метилпирролидиноне (NMP) в виде 0,45 М растворов, содержащих 0,45 М N-гидроксибензотриазола (HOBT). Диизопропилкарбодиимид (DIC) готовили в виде 0,5 М раствора в NMP. К деблокированной смоле добавляли 2,25 мл первой аминокислоты (1,0 ммоль), то есть Fmoc-Cys(Trt)-OH (Novabiochem; San Diego, CA, USA), вместе с 2,0 мл (1,0 ммоль) DIC. Через час непрерывного перемешивания реагенты сливали и повторяли стадию присоедиения. После ацилирования аминокислоты смолу промывали двумя аликвотами ДМФА по 3,0 мл с длительностью каждой промывки 1 минута. Вышеописанные стадии цикла 1, то есть деблокирование, промывка, ацилироавние и промывка, повторяли в течение 2-9 циклов с использованием следующих аминокислот: цикл 2: Fmoc-Trp(Boc)-OH (Genzyme; Cambridge, MA, USA); цикл 3: Fmoc-Arg(Pbf)-OH (Novabiochem; San Diego, CA, USA); цикл 4: Fmoc-D-Phe-OH (Genzyme; Cambridge, MA, USA); цикл 5: Fmoc-His(Trt)-OH (Novabiochem; San Diego, CA, USA); цикл 6: Fmoc-Glu(OtBu)-OH (Genzyme; Cambridge, MA, USA); цикл 7: Fmoc-Cys(Trt)-OH, (Novabiochem; San Diego, CA, USA); цикл 8: Fmoc-Gly-OH (Novabiochem; San Diego, CA, USA) и цикл 9: Fmoc-Arg(Pbf)-OH (Genzyme; Cambridge, MA, USA). N-концевую Fmoc-защиту снимали 25% раствором пиперидина в ДМФА с последующей четырехкратной промывкой 3,0 мл ДМФА по 1 минуте. Смолу промывали четыре раза 3,0 мл DCM, каждая промывка продолжалась в течение приблизительно 1 минуты. Смолу из всех 10 ячеек объединяли. Отбирали небольшую аликвоту смешанной смолы, с пептида, связанного на смоле, удаляли защиту, затем пептид снимали со смолы, что позволило определить полноту синтеза главной цепи линейного пептида с помощью МС и ВЭЖХ анализа.
Смолу с пептидом переносили в реакционную емкость объемом 500 мл с пористым стеклянным фильтром на дне. Смолу выдерживали в нескольких децилитрах ДМФА в течение нескольких минут, после чего растворитель удаляли. Затем добавляли раствор, включающий 45 мл (86 эк.) 3,8 М диизопропилэтиламина (DIPEA) в дихлорметане (DCM), после чего по каплям добавляли 15,5 мл 0,3 М (2,3 эк.) фенилхлорформиата в DCM. Реакционную емкость мягко вращали на орбитальном шейкере в течение 3 часов с легким барботированием током азота. DCM периодически добавляли в течение 3 часов перемешивания, компенсируя потерю DCM в результате испарения. Затем жидкую фазу удаляли. Смолу несколько раз промывали ДМФА и обрабатывали в течение 10 минут раствором 10 эк. DIPEA в ДМФА, который позже удаляли. Обработка основанием (DIPEA) привела к образованию гидантоиновой группы с одновременным образованием п-нитрофенола, обнаруживаемого по окрашиванию растворителя в желтый цвет. Обработку основанием в течение 10 минут повторяли, пока выделение п-нитрофенола не прекращалось (отсутствие желтого окрашивания). Смолу промывали ДМФА, а затем DCM.
К полученной гидантоин-пептидил-смоле добавляли 80 мл реагента следующего состава: 6% триизопропилсилана (TIS), 2% воды, 5% (мас./об.) дитиотреитола (DTT) и 87% трифторуксусной кислоты (ТФУ), после чего смесь перемешивали в течение 4,5 часов. Фильтрат собирали в 1000 мл холодного безводного диэтилового эфира, затем смесь центрифугировали в течение 30 минут в охлаждаемой центрифуге при 4200 об/мин. Эфир удаляли фильтрованием. Пептид ресуспендировали в свежем эфире и подвергали второму центрифугированию. Эфир удаляли фильтрованием, а пептид сушили на воздухе, чтобы удалить остатки эфира.
Пептид растворяли в 10%-ном ацетонитриле и анализировали с помощью масс-спектрометрии и обращенно-фазовой ВЭЖХ, анализ выполняли в течение 30 минут с УФ детектированием при 220 нм, используя колонку Luna C18(2), 5 100Å 250×4,6 мм (Phenomenex; Torrance, CA, USA), в градиенте ацетонитрила 2-80% (0,1% ТФУ). Данный анализ выявил один основной продукт, который обладал более чем 70%-ной чистотой. Остальную часть продукта составлял продукт, не содержащий гидантоин. Массу анализировали с помощью метода ионизации электрораспылением, получив ионы 407,2, 610,0 и 1218,4, соответствующие ионам MH+3, MH+2 и MH+1, соответственно, массы 1218,4 Да, что соответствует целевому линейному продукту. Неочищенный продукт (~2,4 г) растворяли до концентрации 2 мг/мл в 5%-ной уксусной кислоте. К полученному раствору по каплям добавляли 0,5 М иод в метаноле при энергичном перемешивании, пока смесь не окрашивалась в бледно-желтый цвет. Раствор энергично перемешивали в течение 10 минут. Избыток иода удаляли, добавляя 1,0 М тиосульфат натрия при непрерывном перемешивании, пока смесь не становилась бесцветной. Пептид повторно анализировали с помощью масс-спектрометрии, которая выявила основной продукт, имеющий массу 1216,4 Да, что указывает на успешное окисление пептида до дисульфидного продукта. Раствор пептида концентрировали до объема ~500 мл, используя центробежный испаритель, а затем очищали с помощью препаративной ВЭЖХ, оборудованной колонкой Luna C18(2), 5
100Å 250×4,6 мм (Phenomenex; Torrance, CA, USA), в градиенте ацетонитрила 2-80% (0,1% ТФУ). Данный анализ выявил один основной продукт, который обладал более чем 70%-ной чистотой. Остальную часть продукта составлял продукт, не содержащий гидантоин. Массу анализировали с помощью метода ионизации электрораспылением, получив ионы 407,2, 610,0 и 1218,4, соответствующие ионам MH+3, MH+2 и MH+1, соответственно, массы 1218,4 Да, что соответствует целевому линейному продукту. Неочищенный продукт (~2,4 г) растворяли до концентрации 2 мг/мл в 5%-ной уксусной кислоте. К полученному раствору по каплям добавляли 0,5 М иод в метаноле при энергичном перемешивании, пока смесь не окрашивалась в бледно-желтый цвет. Раствор энергично перемешивали в течение 10 минут. Избыток иода удаляли, добавляя 1,0 М тиосульфат натрия при непрерывном перемешивании, пока смесь не становилась бесцветной. Пептид повторно анализировали с помощью масс-спектрометрии, которая выявила основной продукт, имеющий массу 1216,4 Да, что указывает на успешное окисление пептида до дисульфидного продукта. Раствор пептида концентрировали до объема ~500 мл, используя центробежный испаритель, а затем очищали с помощью препаративной ВЭЖХ, оборудованной колонкой Luna C18(2), 5 100Å 250×21,2 мм (Phenomenex; Torrance, CA, USA), с элюрованием в градиенте ацетонитрила 10-50% (0,1% ТФУ) в течение 40 минут с УФ-детектированием при 290 нм. Чистоту очищенного продукта повторно анализировали с помощью ВЭЖХ (>99%). Дополнительный масс-спектрометрический анализ выявил продукт с массой 1216,2 Да, что совпадает с расчетной молекулярной массой целевого пептида 1216,4 Да. После лиофилизации получили 334 мг очищенного продукта, выход составил 14%.
100Å 250×21,2 мм (Phenomenex; Torrance, CA, USA), с элюрованием в градиенте ацетонитрила 10-50% (0,1% ТФУ) в течение 40 минут с УФ-детектированием при 290 нм. Чистоту очищенного продукта повторно анализировали с помощью ВЭЖХ (>99%). Дополнительный масс-спектрометрический анализ выявил продукт с массой 1216,2 Да, что совпадает с расчетной молекулярной массой целевого пептида 1216,4 Да. После лиофилизации получили 334 мг очищенного продукта, выход составил 14%.
С использованием примеров, описанных выше, могут быть синтезированы дополнительные соединения, включающие, помимо прочих, следующие соединения:
цикло[Гидантоин(C(O)-(Asp-His))-D-2-Nal-Arg-Trp-Lys]-NH2, (SEQ ID NO:5), который имеет следующую структуру:
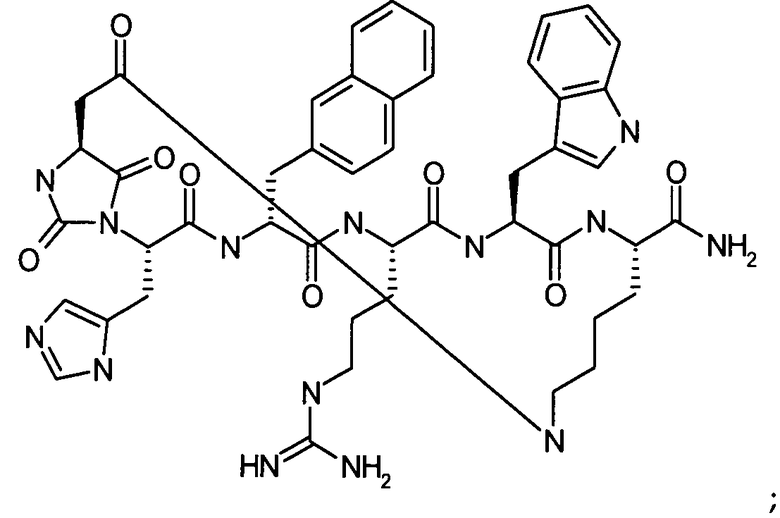
цикло[Гидантоин(C(O)-(Glu-His))-D-Phe-Arg-Trp-Lys]-NH2, (SEQ ID NO:61), который имеет следующую структуру:
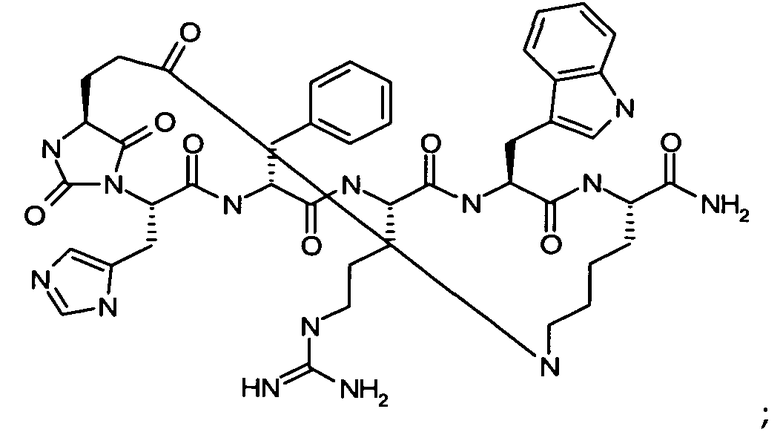
цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:1), который имеет следующую структуру:
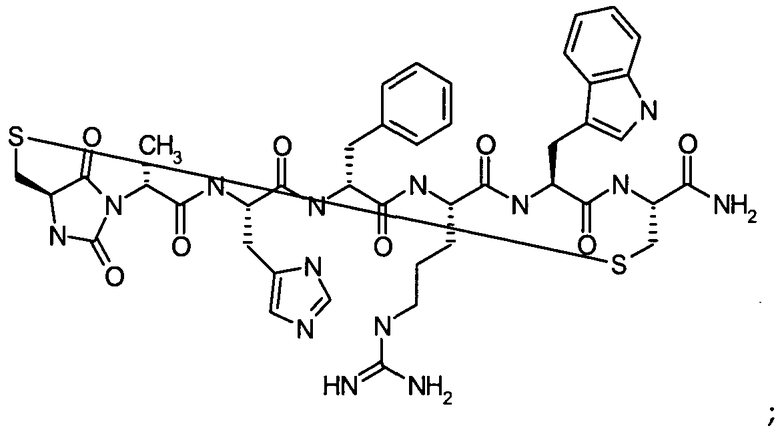
цикло [Гидантоин (C(О)-(Asp-His))-D-Phe-Arg-Trp-Lys]-NH2, (SEQ ID NO:5), который имеет следующую структуру:
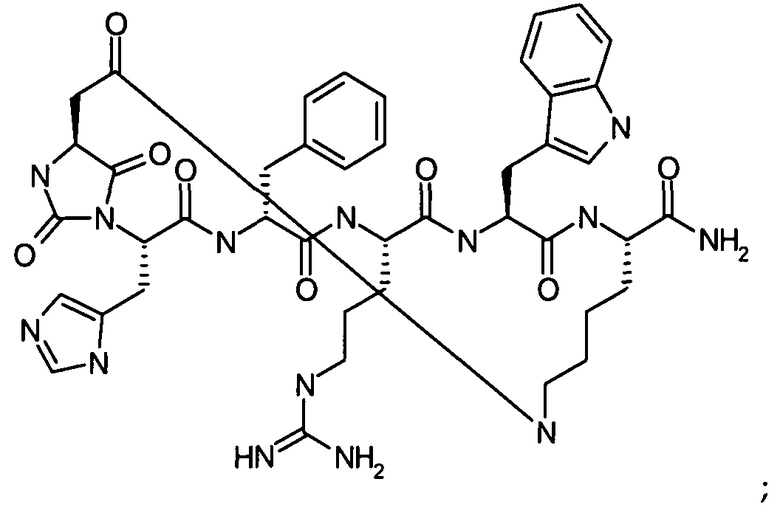
цикло[Гидантоин(C(O)-(Asp-Aic))-D-Phe-Arg-Trp-Lys]-NH2, (SEQ ID NO:9), который имеет следующую структуру:
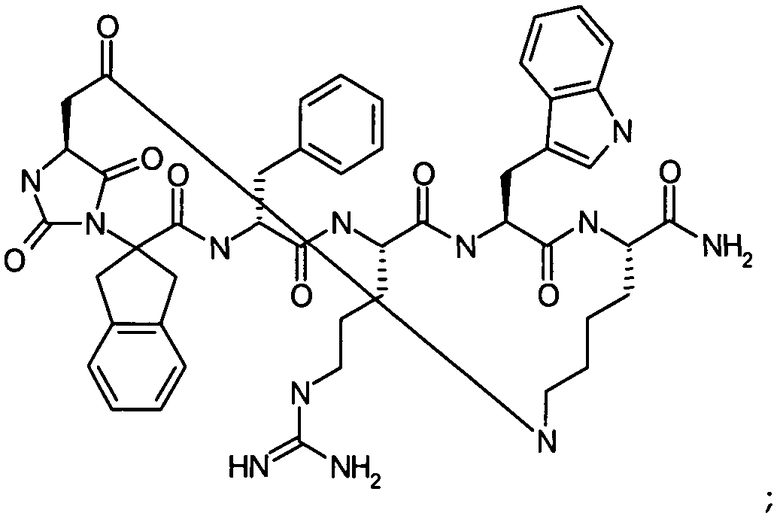
цикло[Гидантоин(C(O)-(Asp-A5c))-D-Phe-Arg-Trp-Lys]-NH2, (SEQ ID NO:7), который имеет следующую структуру:
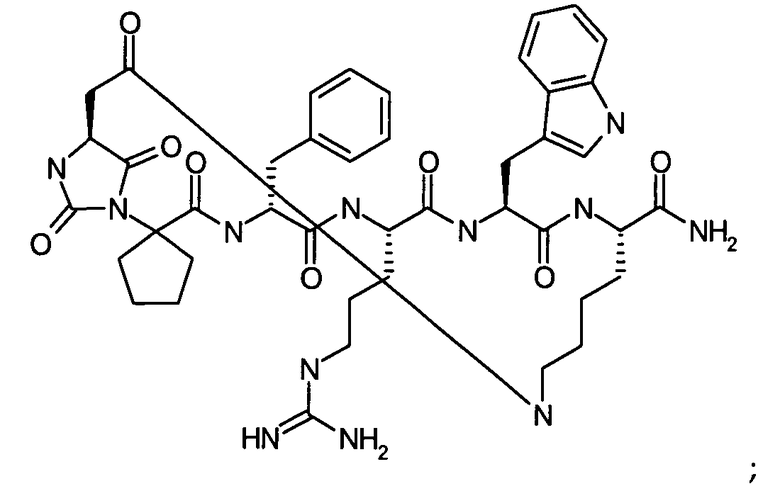
цикло[Гидантоин(C(O)-(Asp-A6c))-D-Phe-Arg-Trp-Lys]-NH2, (SEQ ID NO:8), который имеет следующую структуру:
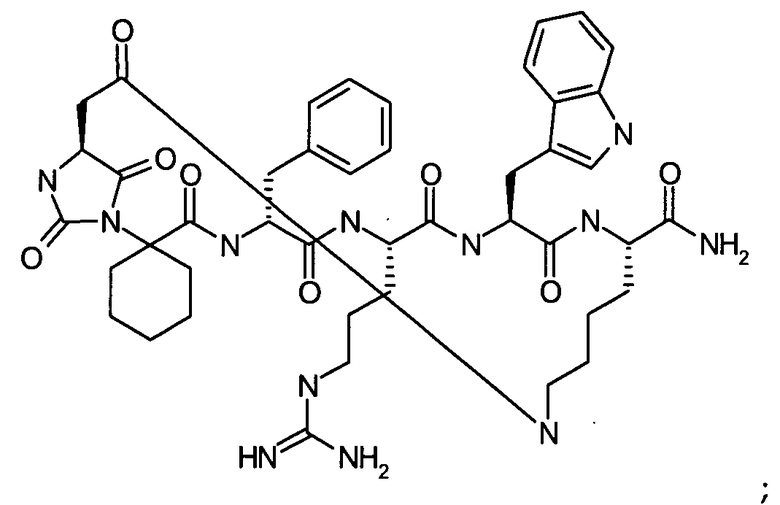
цикло[Гидантоин(C(O)-(Asp-Apc))-D-Phe-Arg-Trp-Lys]-NH2, (SEQ ID NO:10), который имеет следующую структуру:
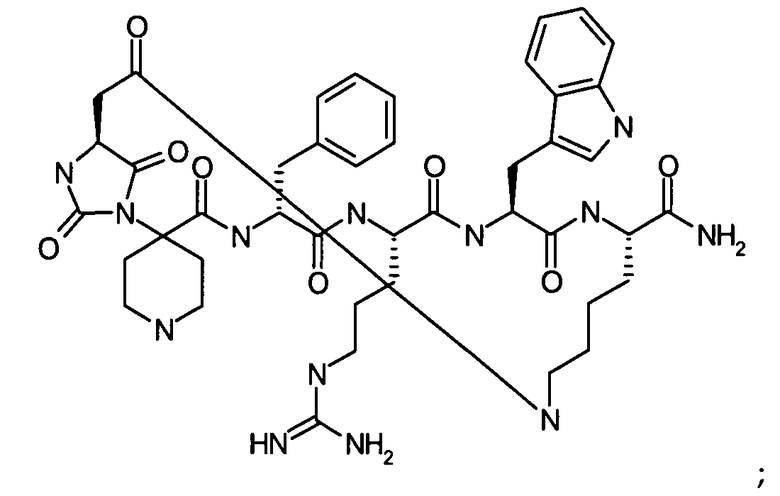
цикло[Гидантоин(C(O)-(Asp-A3c))-D-Phe-Arg-Trp-Lys]-NH2, (SEQ ID NO:6), который имеет следующую структуру:
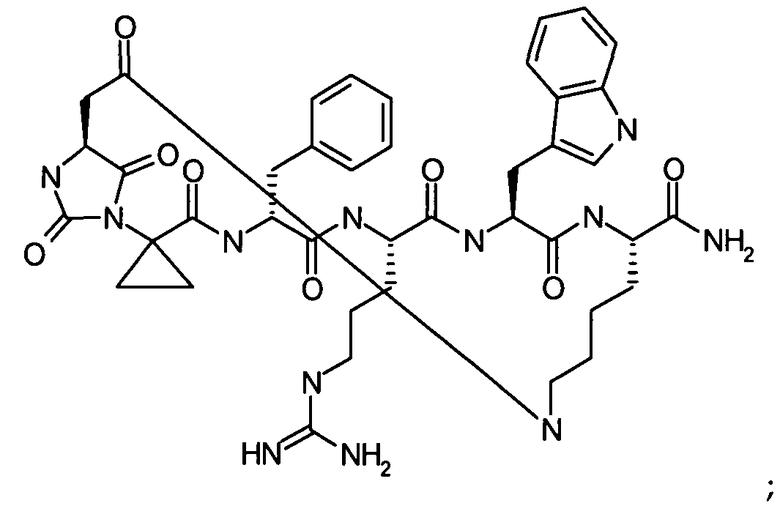
цикло[Гидантоин(C(O)-(Asp-Aic))-D-2-Nal-Arg-Trp-Lys]-NH2, (SEQ ID NO:9), который имеет следующую структуру:

цикло[Гидантоин(C(O)-(Asp-A5c))-D-2-Nal-Arg-Trp-Lys]-NH2, (SEQ ID NO:7), который имеет следующую структуру:
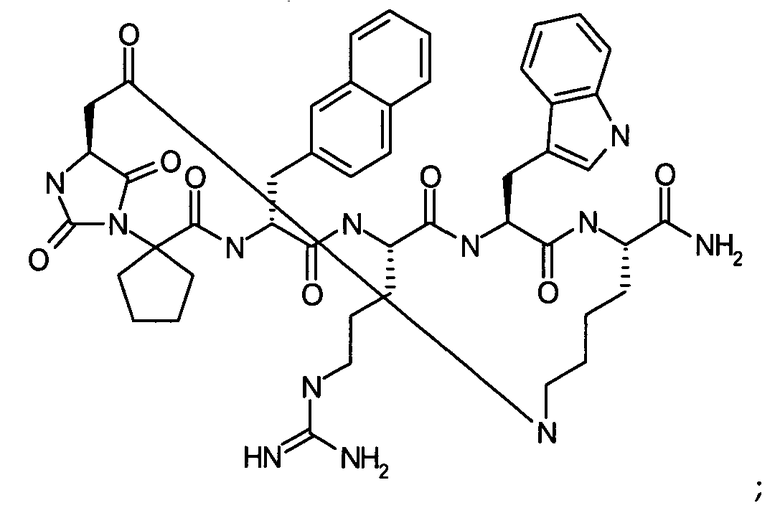
цикло[Гидантоин(C(O)-(Asp-A6c))-D-2-Nal-Arg-Trp-Lys]-NH2, (SEQ ID NO:8), который имеет следующую структуру:

цикло[Гидантоин(C(O)-(Asp-Apc))-D-2-Nal-Arg-Trp-Lys]-NH2, (SEQ ID NO:10), который имеет следующую структуру:
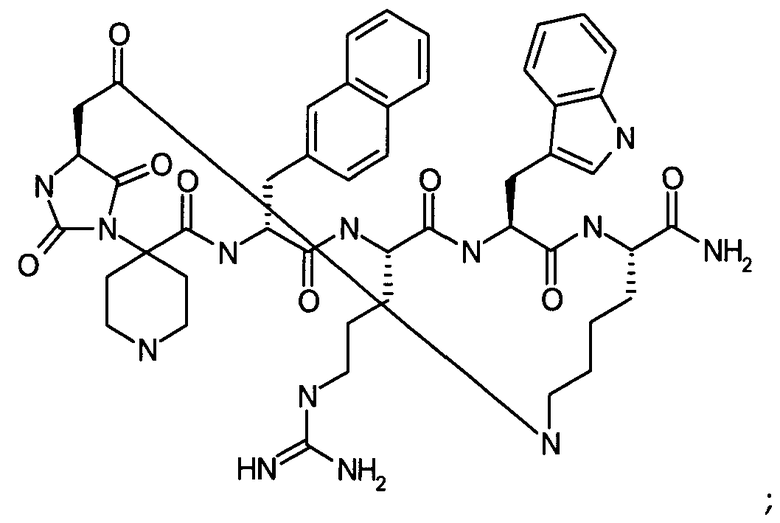
цикло[Гидантоин(C(O)-(Asp-A3c))-D-2-Nal-Arg-Trp-Lys]-NH2, (SEQ ID NO:6), который имеет следующую структуру:
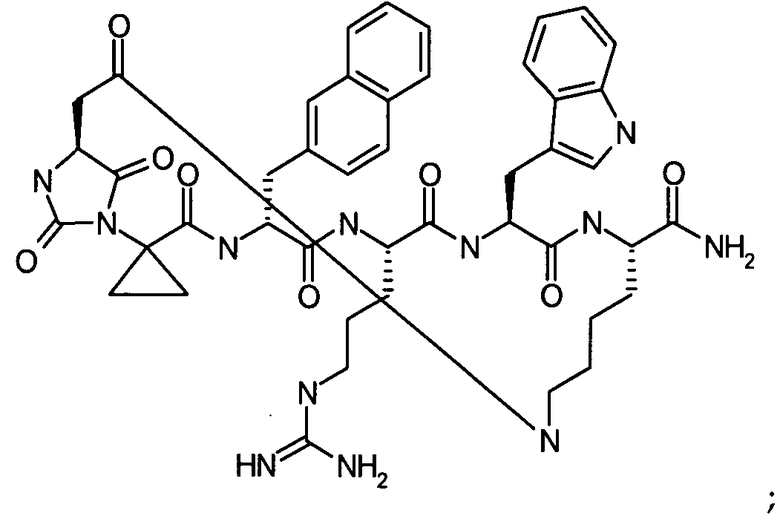
цикло [Гидантоин (C)(O)-(hCys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:2), который имеет следующую структуру:
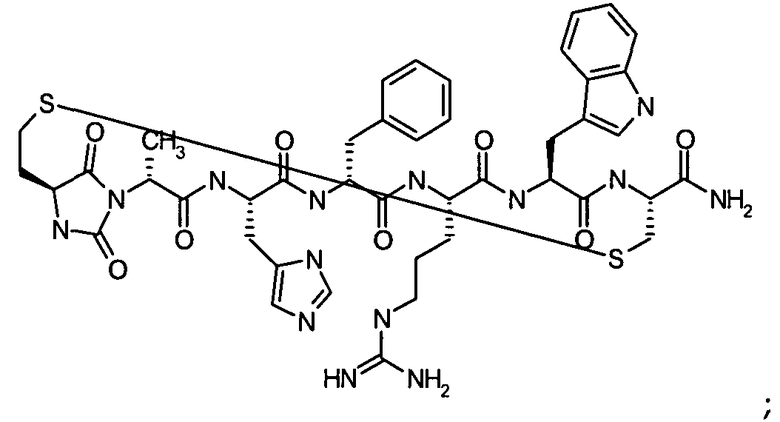
[Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:62), который имеет следующую структуру:
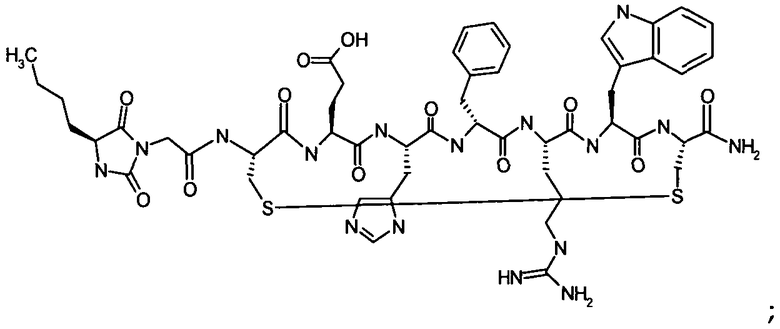
[Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:63), который имеет следующую структуру:
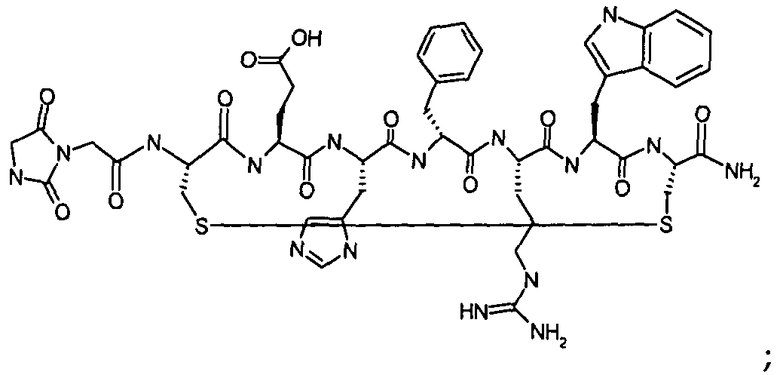
[Гидантоин(C(O)-(Ala-Nle))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:64), который имеет следующую структуру:
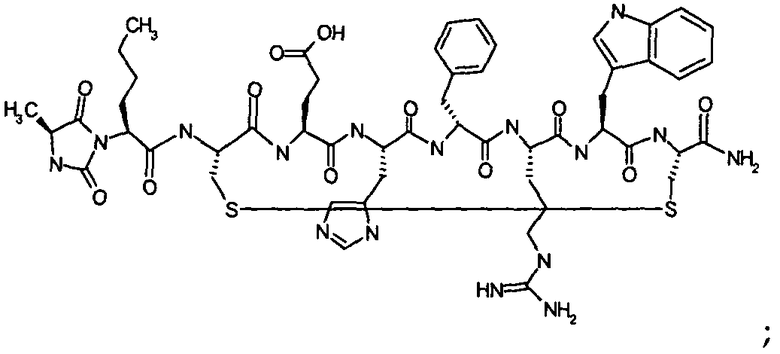
[Гидантоин(C(O)-(Val-Nle))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:65), который имеет следующую структуру:
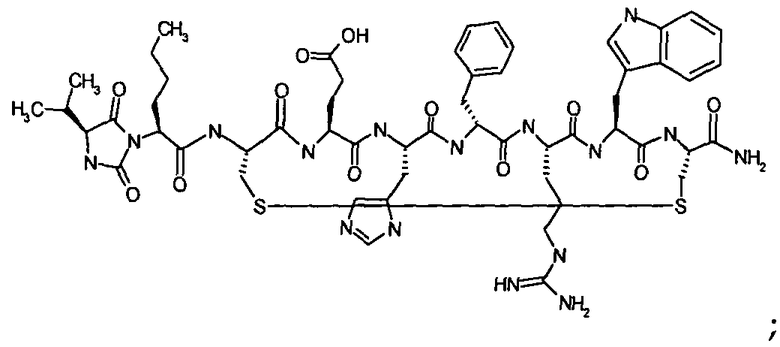
[Гидантоин(C(O)-(Nle-Ala))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:66), который имеет следующую структуру:
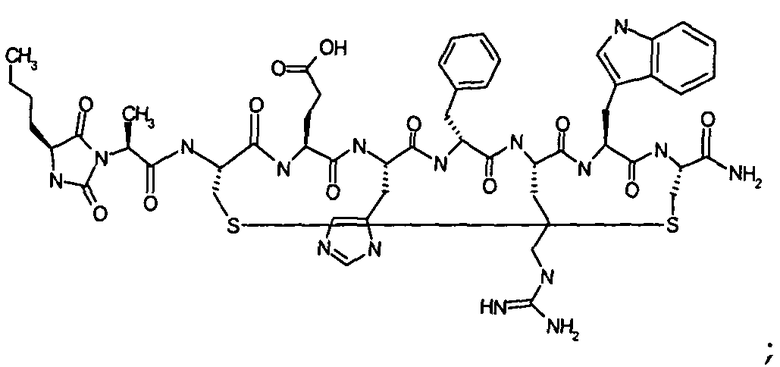
[Гидантоин(C(O)-(Gly-Nle))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:67), который имеет следующую структуру:
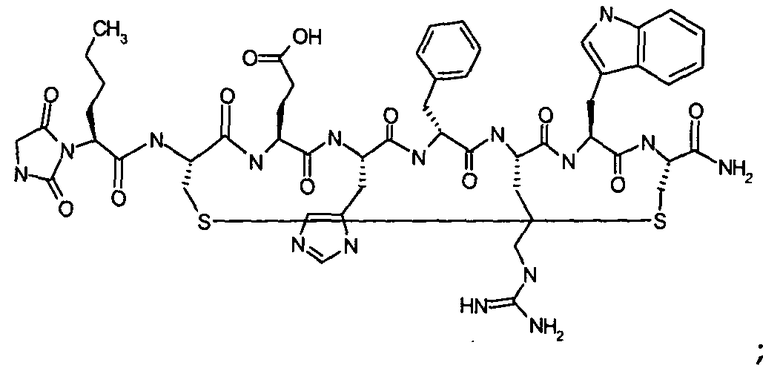
цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-2-Nal-Arg-Trp-Cys)-NH2, (SEQ ID NO:1), который имеет следующую структуру:
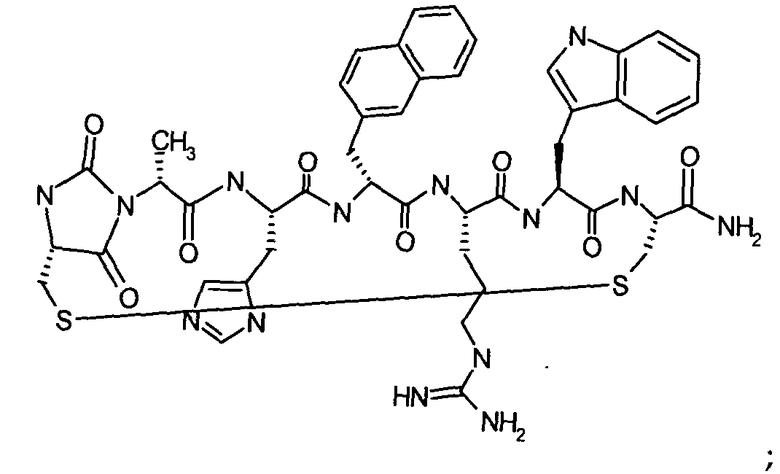
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Lys]-NH2, (SEQ ID NO:68), который имеет следующую структуру:
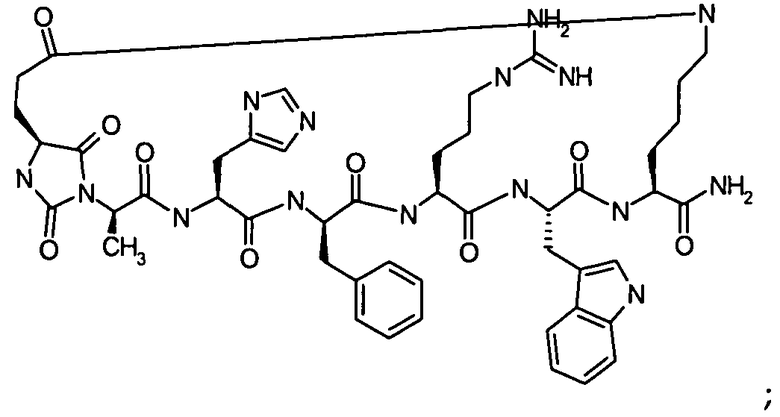
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Orn]-NH2, (SEQ ID NO:11), который имеет следующую структуру:
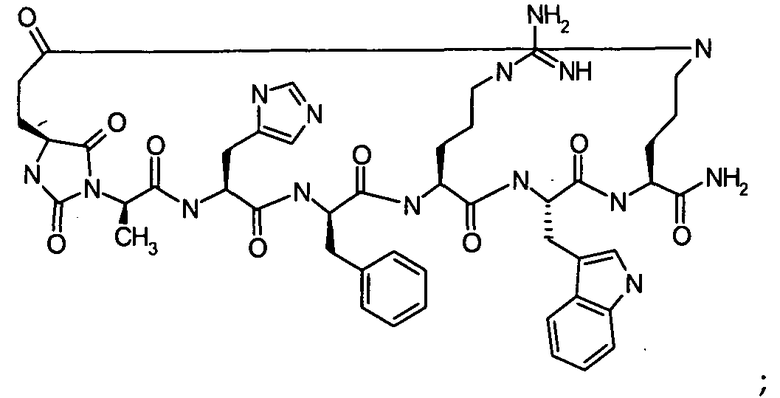
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Dab]-NH2, (SEQ ID NO:11), который имеет следующую структуру:
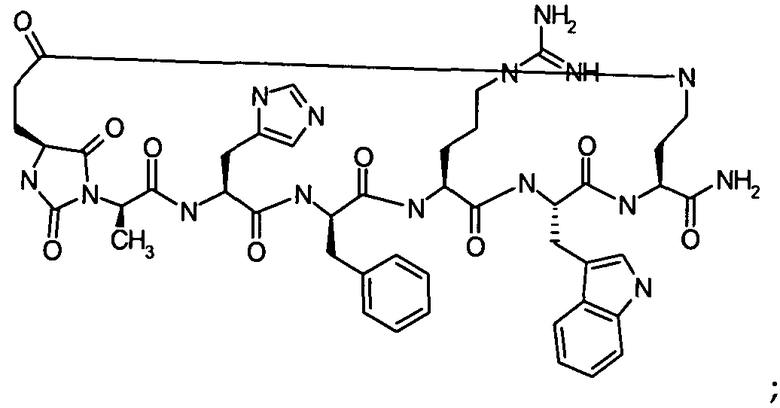
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH2, (SEQ ID NO:11), который имеет следующую структуру:
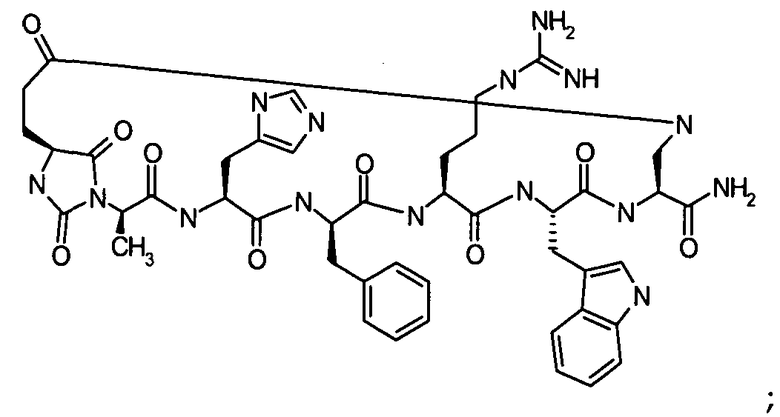
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Lys]-NH2, (SEQ ID NO:3), который имеет следующую структуру:
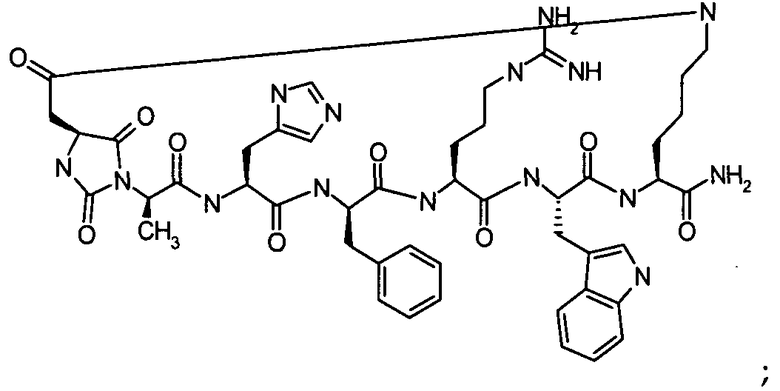
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Orn]-NH2, (SEQ ID NO:4), который имеет следующую структуру:
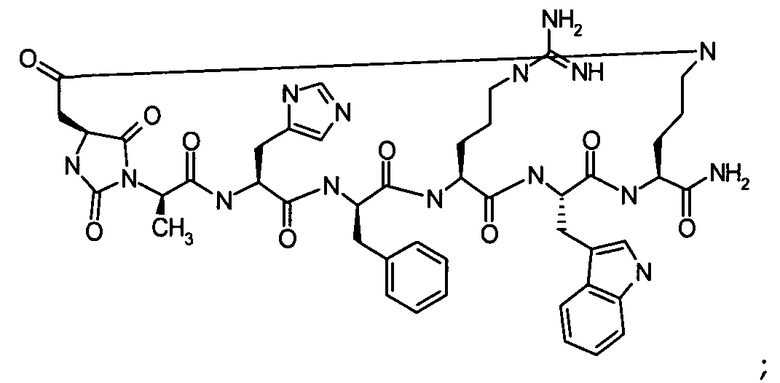
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Dab]-NH2, (SEQ ID NO:4), который имеет следующую структуру:
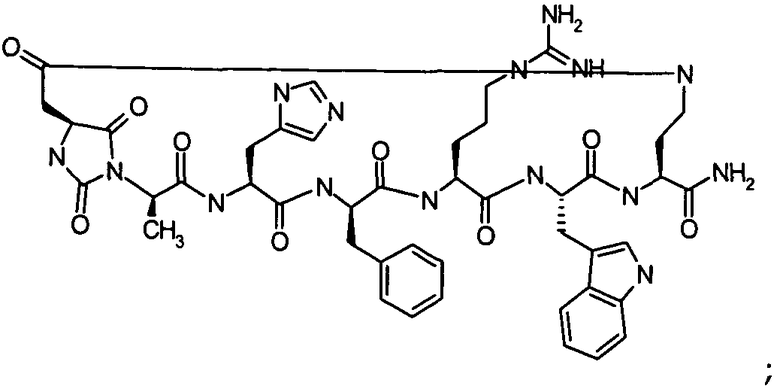
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH2, (SEQ ID NO:4), который имеет следующую структуру:

[Гидантоин(C(O)-(A6c-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:69), который имеет следующую структуру:
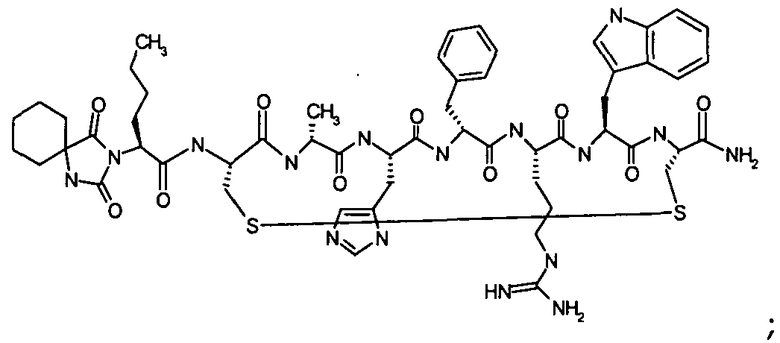
цикло[Гидантоин(C(O)-(Nle-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:46), который имеет следующую структуру:
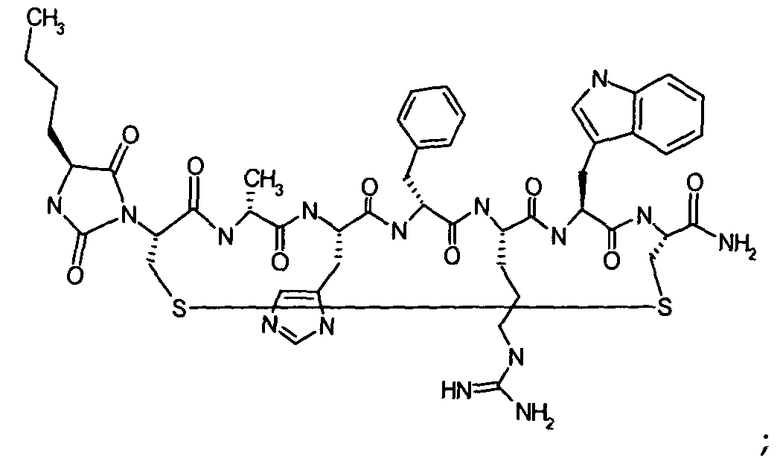
цикло[Гидантоин(C(O)-(Ala-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:45), который имеет следующую структуру:
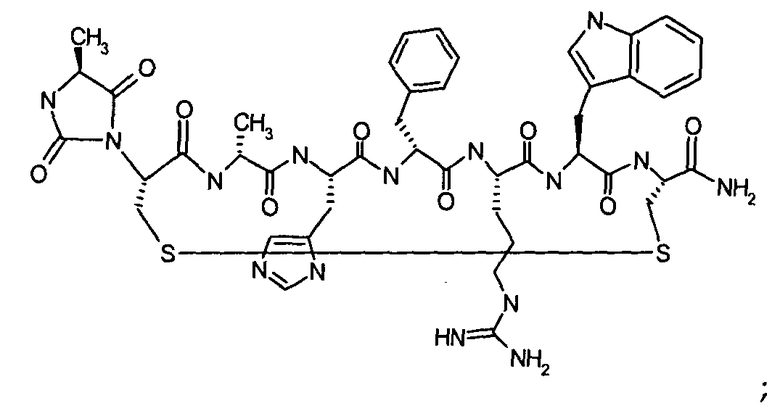
цикло[Гидантоин(C(O)-(D-Ala-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:47), который имеет следующую структуру:
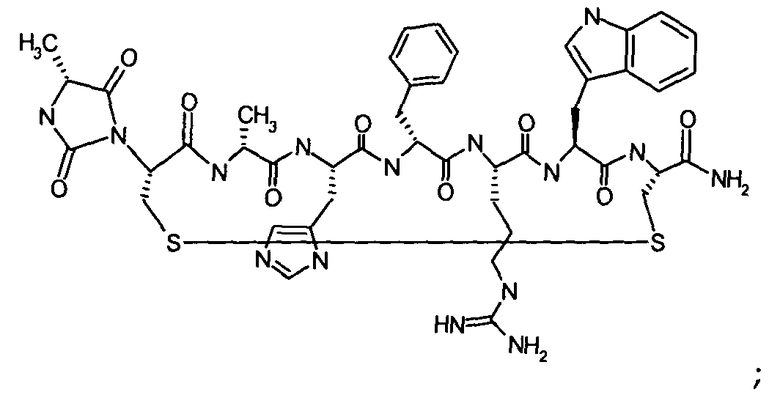
цикло[Гидантоин(C(O)-(Aib-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:48), который имеет следующую структуру:
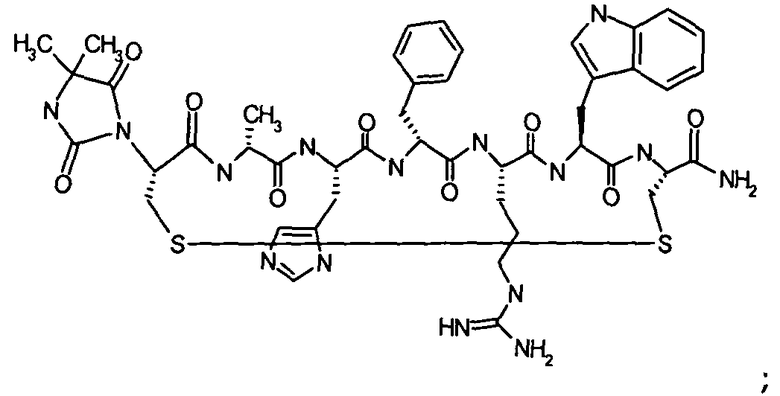
цикло[Гидантоин(C(O)-(Val-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:49), который имеет следующую структуру:
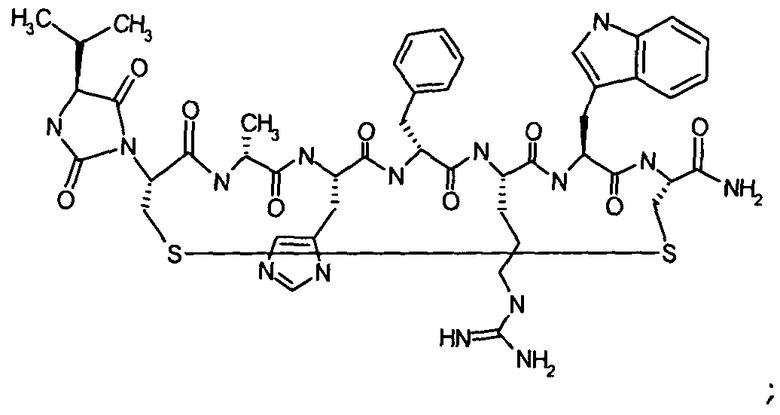
цикло[Гидантоин(C(O)-(Abu-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:50), который имеет следующую структуру:
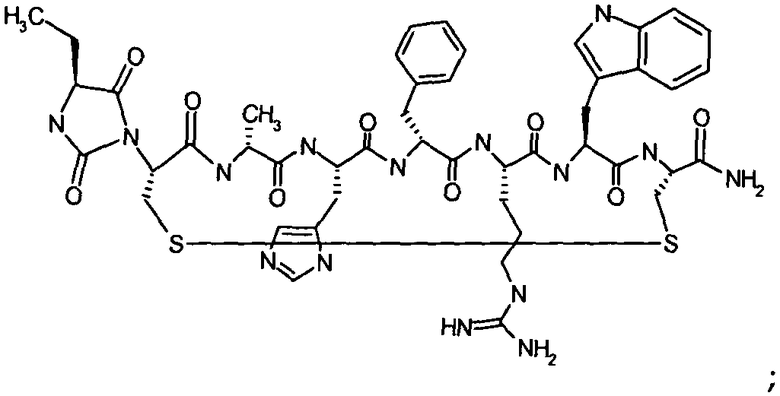
цикло[Гидантоин(C(O)-(Leu-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:51), который имеет следующую структуру:
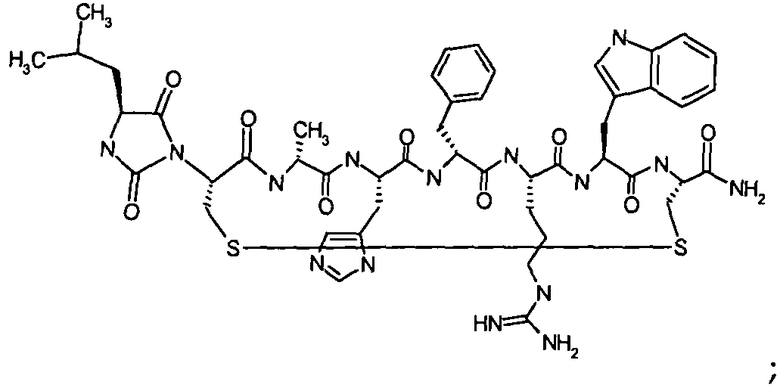
цикло[Гидантоин(C(O)-(Ile-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:52), который имеет следующую структуру:
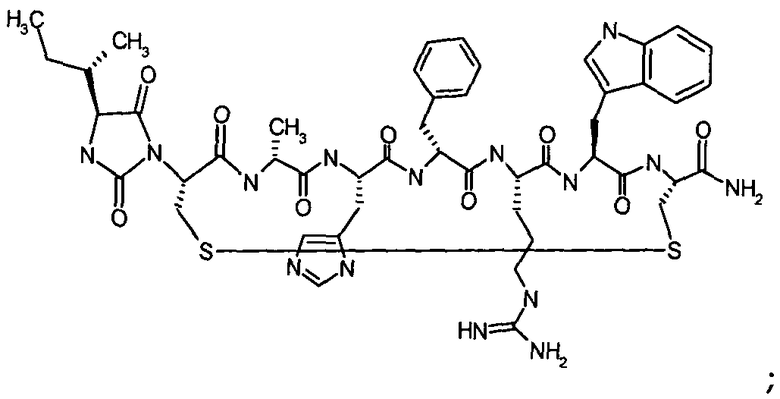
цикло[Гидантоин(C(O)-(Cha-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:53), который имеет следующую структуру:
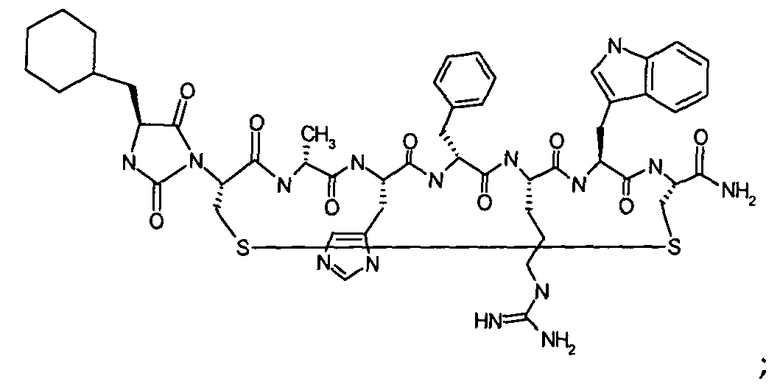
цикло[Гидантоин(C(O)-(A6c-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:54), который имеет следующую структуру:
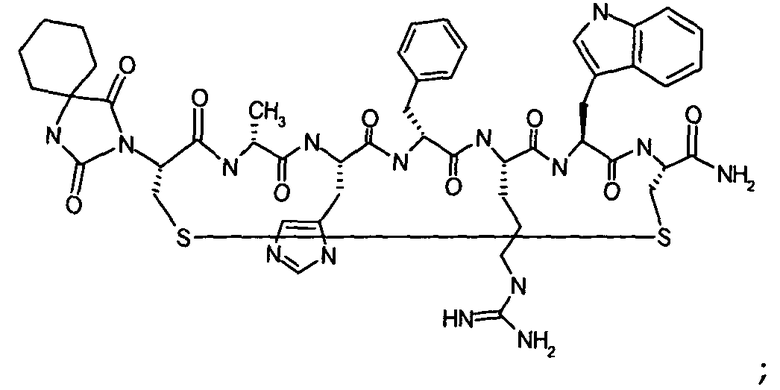
цикло[Гидантоин(C(O)-(Phe-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:54), который имеет следующую структуру:
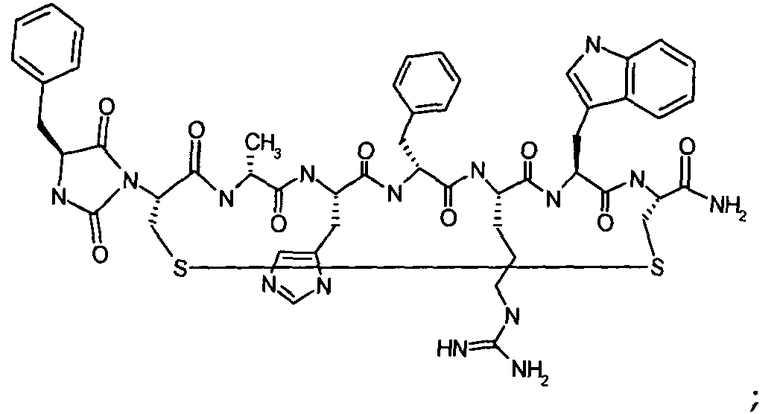
[Гидантоин(C(O)-(Gly-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:70), который имеет следующую структуру:
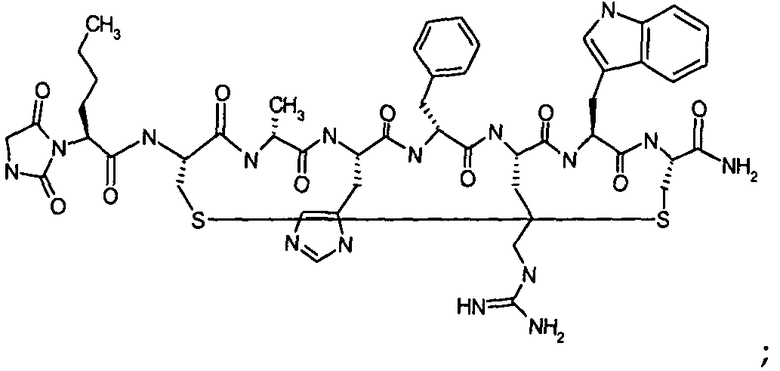
[Гидантоин(C(O)-(Ala-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:71), который имеет следующую структуру:
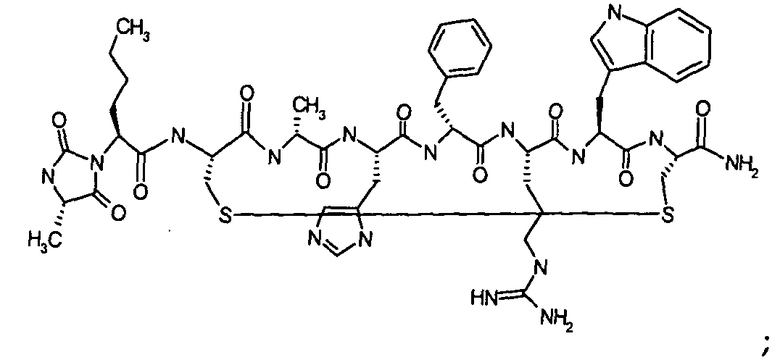
[Гидантоин(C(O)-(D-Ala-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:72), который имеет следующую структуру:
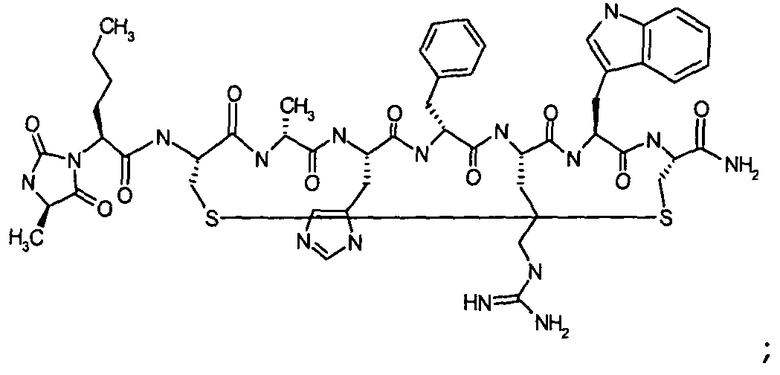
[Гидантоин(C(O)-(Val-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:73), который имеет следующую структуру:
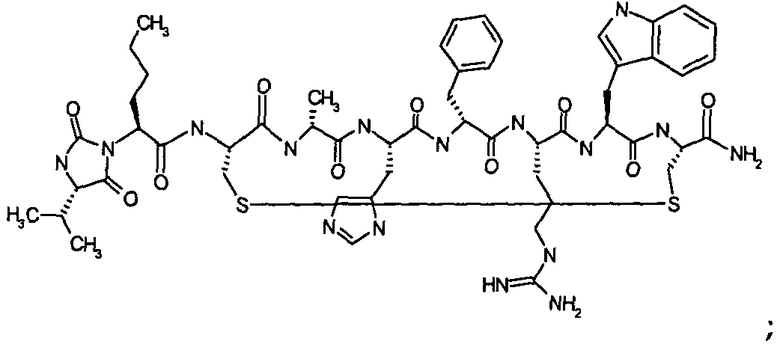
[Гидантоин(C(O)-(Leu-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:74), который имеет следующую структуру:
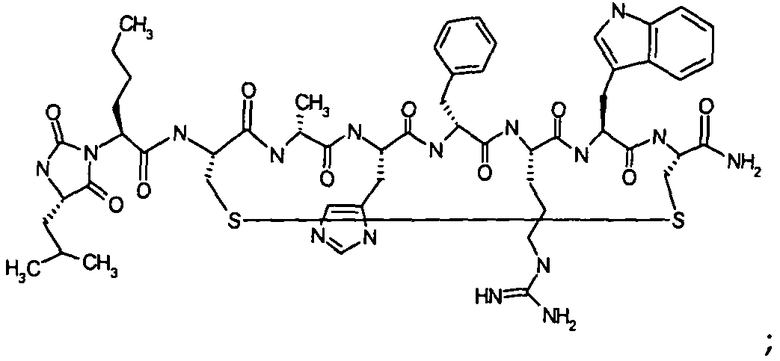
[Гидантоин(C(O)-(Cha-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:75), который имеет следующую структуру:
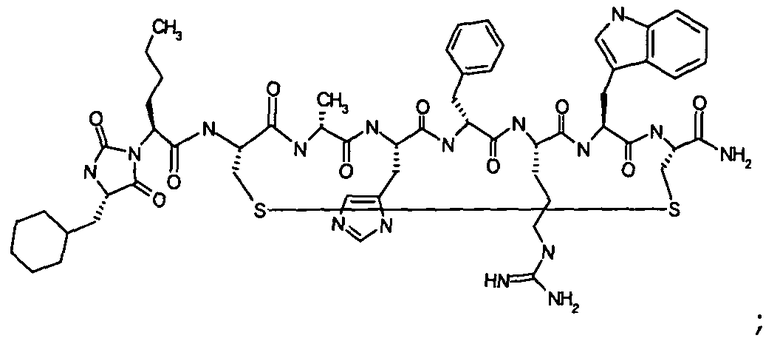
[Гидантоин(C(O)-(Aib-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:76), который имеет следующую структуру:
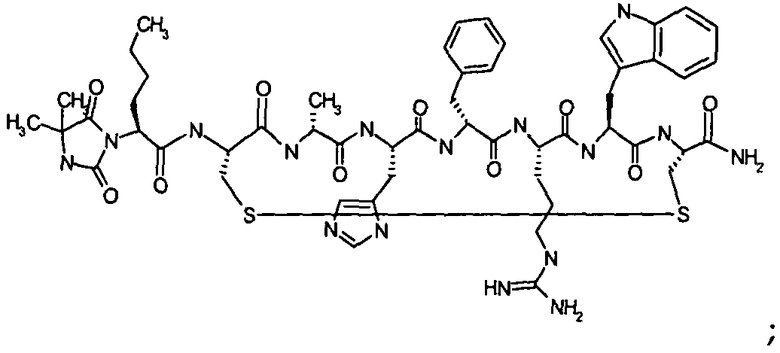
цикло[Гидантоин(C(O)-(Gly-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:56), который имеет следующую структуру:
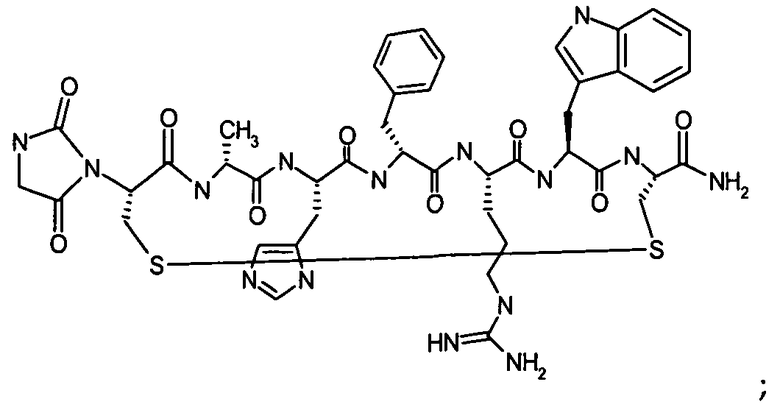
[Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:77), который имеет следующую структуру:
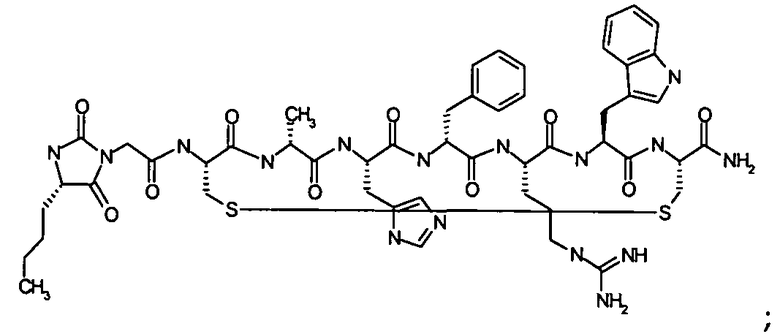
[Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:78), который имеет следующую структуру:
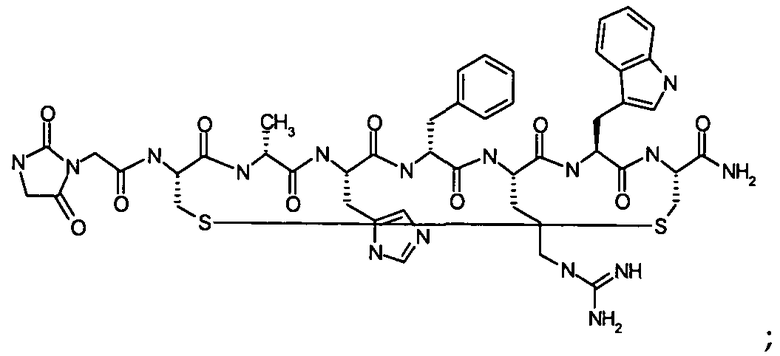
[Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)]-NH2, (SEQ ID NO:79), который имеет следующую структуру:
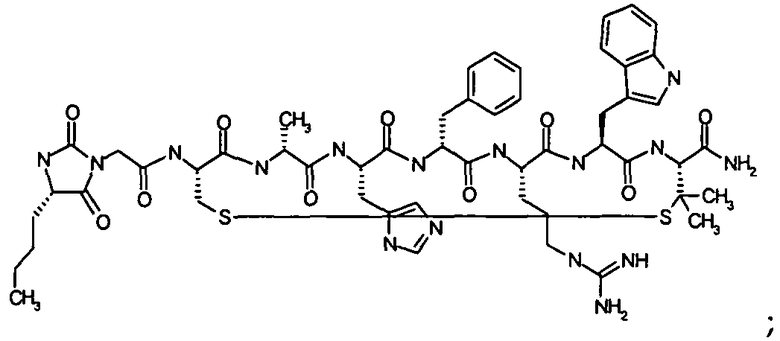
[Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)]-NH2, (SEQ ID NO:80), который имеет следующую структуру:
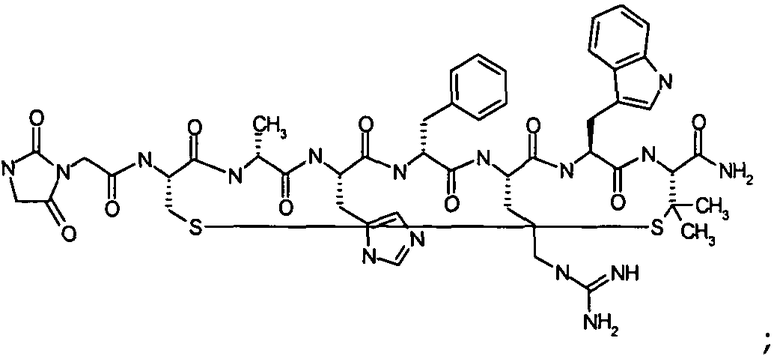
[Гидантоин(C(O)-(Ala-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:81), который имеет следующую структуру:
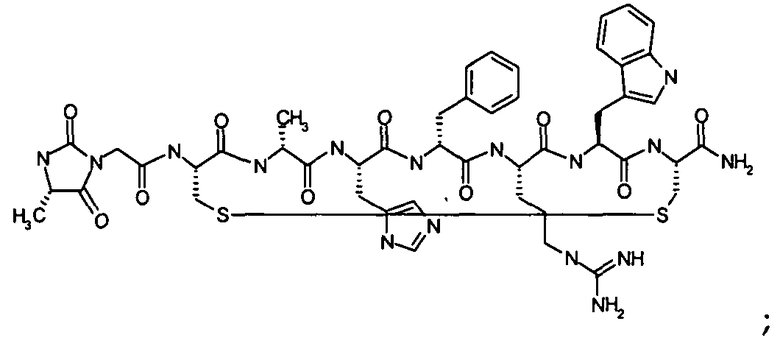
[Гидантоин(C(O)-(D-Ala-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:82), который имеет следующую структуру:

[Гидантоин(C(O)-(Aib-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:83), который имеет следующую структуру:
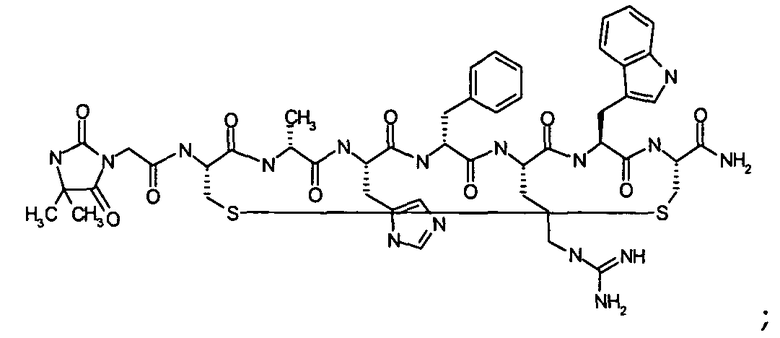
[Гидантоин(C(O)-(Val-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:84), который имеет следующую структуру:
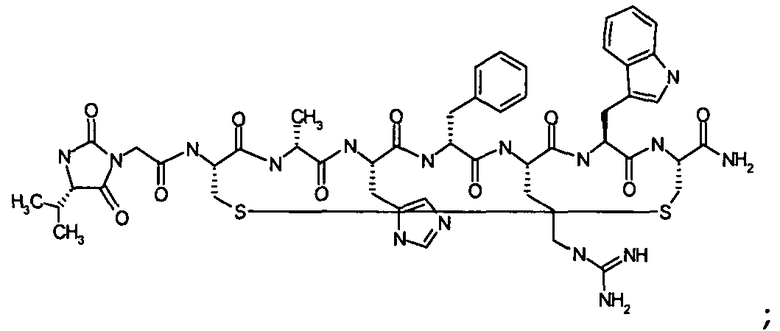
[Гидантоин(C(O)-(Ile-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg- Trp-Cys)]-NH2, (SEQ ID NO:85), который имеет следующую структуру:
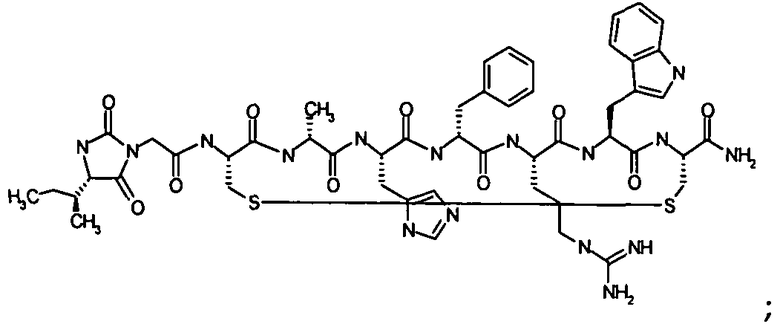
[Гидантоин(C(O)-(Leu-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:86), который имеет следующую структуру:
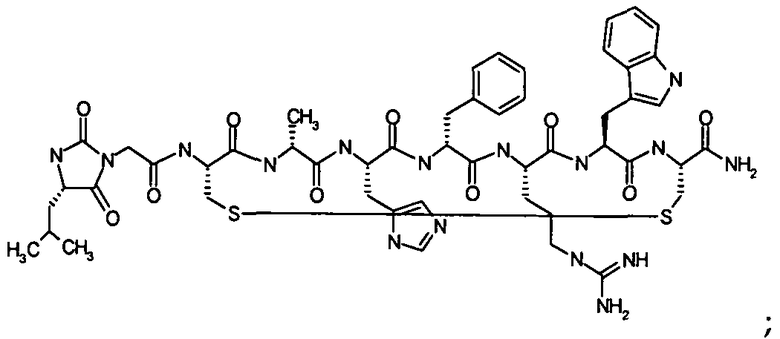
[Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-Glu-His-D-2-Nal-Arg-Trp-Cys)]-NH2, (SEQ ID NO:63), который имеет следующую структуру:
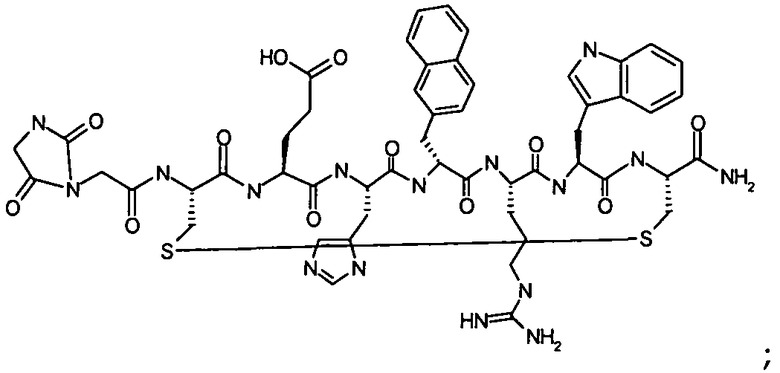
[Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-Glu-His-D-2-Nal-Arg-Trp-Cys)]-NH2, (SEQ ID NO:62), который имеет следующую структуру:

[Гидантоин(C(O)-(D-Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:87), который имеет следующую структуру:

цикло[Гидантоин(C(O)-(Gly-Cys))-Glu-His-D-Phe-Arg-Trp-Cys]-NH2, (SEQ ID NO:57), который имеет следующую структуру:
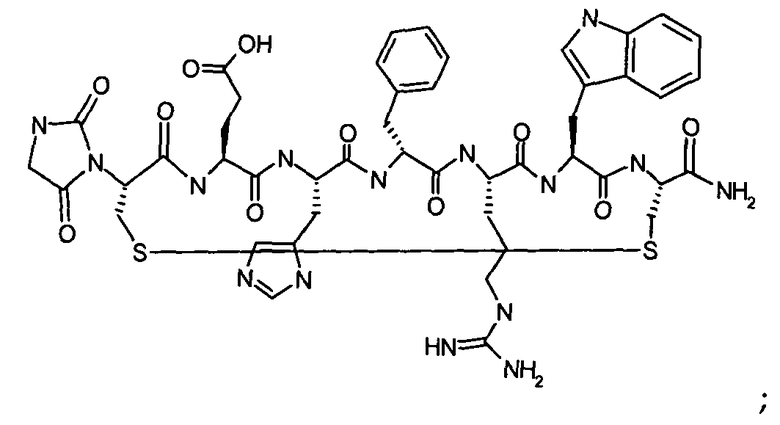
[Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:88), который имеет следующую структуру:
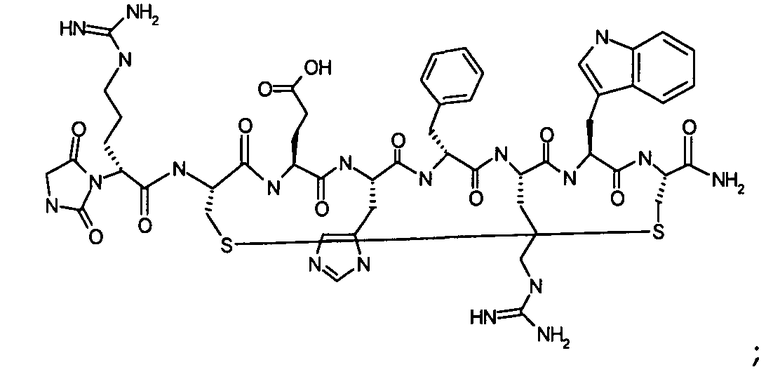
[Гидантоин(C)(O)-(Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:89), который имеет следующую структуру:
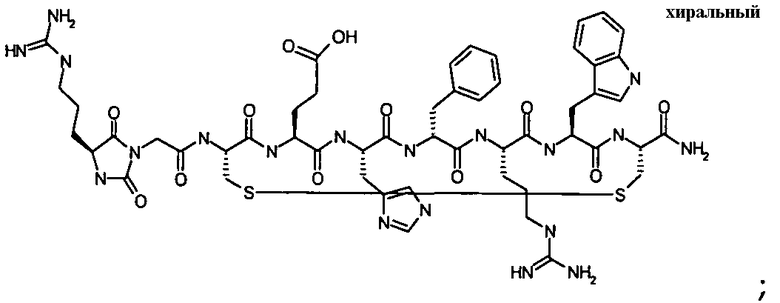
[Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:90), который имеет следующую структуру:
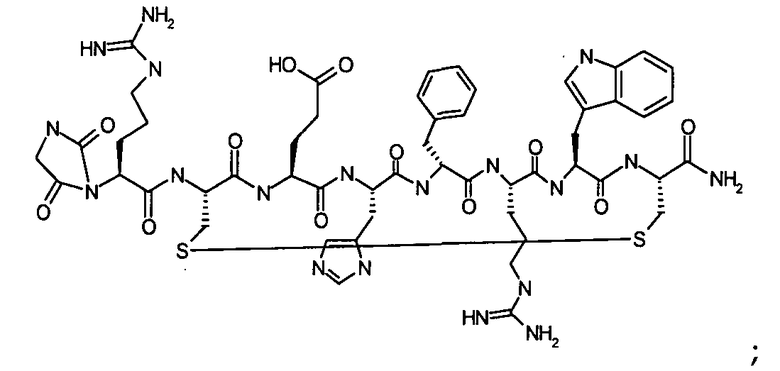
[Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:91), который имеет следующую структуру:
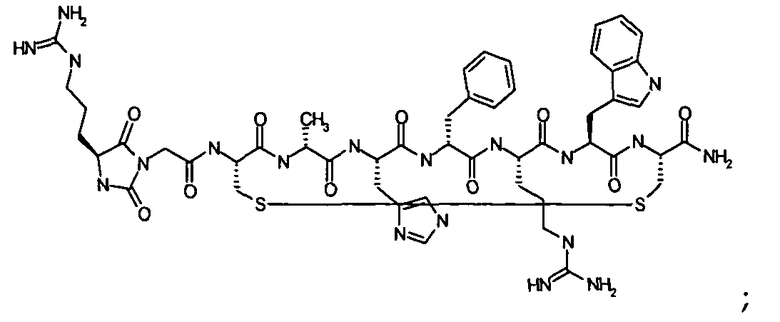
[Гидантоин(C(O)-(D-Arg-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:92), который имеет следующую структуру:
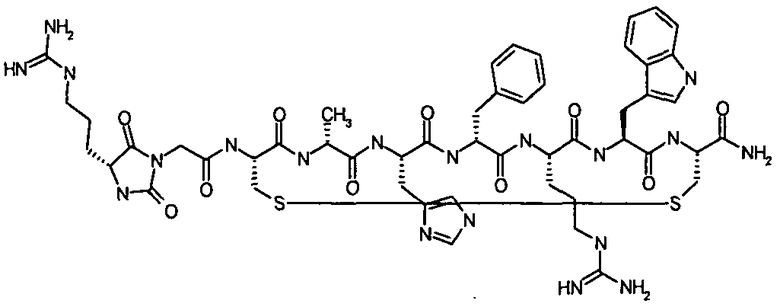 ;
;
[Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:93), который имеет следующую структуру:
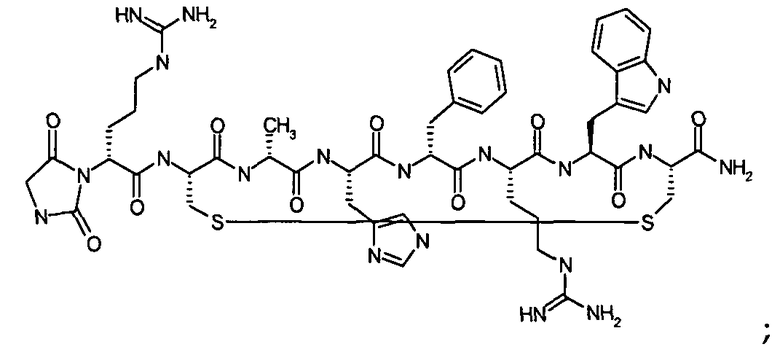
[Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)]-NH2, (SEQ ID NO:94), который имеет следующую структуру:
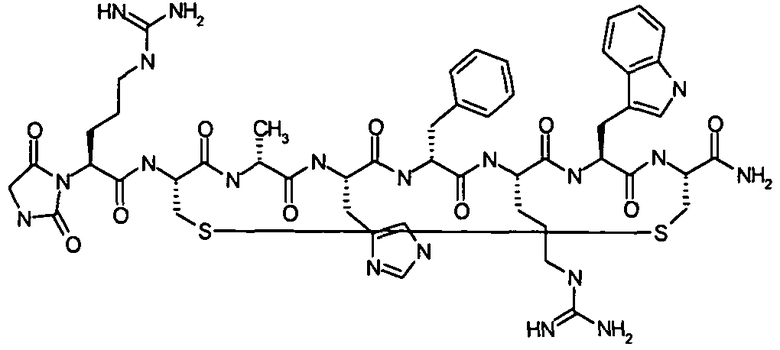 и
и
[Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)]-NH2, (SEQ ID NO:91), который имеет следующую структуру:
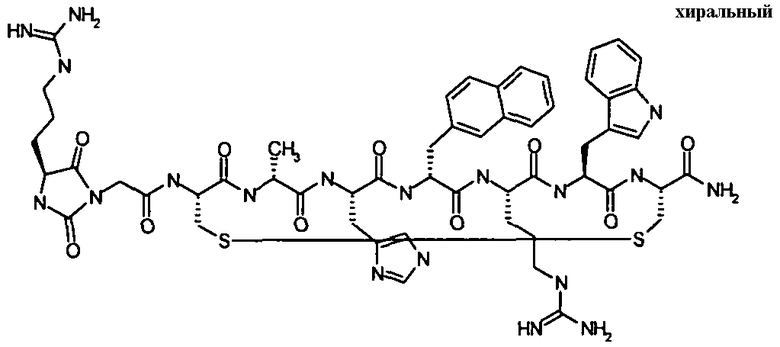 .
.
Выбор таких соединений осуществляли с помощью аналитической ВЭЖХ и масс-спектрометрии с электрораспылением, чтобы гарантировать идентичность и чистоту, результаты приведены в Таблице 1 ниже.
(SEQ ID NO:36)
(SEQ ID NO:37)
(SEQ ID NO:17)
Меланокортинфункциональная активность и селективность
Соединения настоящего изобретения из всех других меланокортиновых рецепторов взаимодействуют предпочтительно (то есть селективно) с MC-4. Селективность особенно важна, когда соединения вводят людям или животным, чтобы минимизировать число побочных эффектов, связанных с их введением. Селективность соединения к MC-4 определяется в настоящей заявке как отношение EC50 соединения для рецептора MC-1 (EC50-MC-1), деленное на EC50 соединения для рецептора MC-3 (EC50-MC-3)/MC-4(EC50-MC-4), при этом значения EC50 измеряют, как описано выше. Формулы являются следующими:
MC-3 селективность = [EC 50 -MC-1]/[EC 50 -MC-3]
MC-4 селективность = [EC 50 -MC-1]/[EC 50 -MC-4]
Соединение определяется в настоящей заявке как "селективное к рецептору MC-3", когда вышеуказанное отношение "MC-3-селективность" равно, по меньшей мере, приблизительно 10, предпочтительно, по меньшей мере, приблизительно 100, и более предпочтительно, по меньшей мере, приблизительно 500. Соединение определяется в настоящей заявке как "селективное к рецептору MC-4", когда вышеуказанное отношение "MC-4-селективность" равно, по меньшей мере, приблизительно 10, предпочтительно, по меньшей мере, приблизительно 100, и более предпочтительно, по меньшей мере, приблизительно 500.
Специалист, квалифицированный в данной области, осведомлен, что для оценки активности связывания соединений согласно настоящему изобретению с молекулами меланокортиновых рецепторов могут применяться методики, подобные описанным в настоящей заявке.
Биоанализ на циклический АМФ
Уровни внутриклеточного циклического АМФ (цАМФ) определяли с помощью электрохемилюминесцентного (ЭХЛ) анализа (Meso Scale Discovery®, Gaithersburg, MD; называемого в дальнейшем как "MSD"). Клетки CHO-K1, стабильно экспрессирующие подтипы рецептора hMC, суспендировали в RMPI 1640® аналитическом буфере (буфер RMPI 1640 содержит 0,5 мМ изобутилметилксантина (IBMX) и 0,2% белковую смесь (MSD блокатор A)). Трансгенные клетки CHO-K1, стабильно экспрессирующие подтипы 1, 3, 4 или 5 рецептора hMC, вносили в лунки при плотности приблизительно 7000 клеток в лунке в 384-луночный планшет Multi-Array® (MSD), содержащий интегрированные угольные электроды и покрытый анти-цАМФ антителом. Увеличивающиеся концентрации тестируемых соединений добавляли в лунки, после чего клетки инкубировали в течение приблизительно 40 минут приблизительно при 37°C. После указанного инкубирования добавляли лизирующий буфер (раствор хлорида натрия, забуференный HEPES, с MgCl2 и Triton X-100®, рН 7,3), содержащий 0,2% белковую смесь и 2,5 нМ TAGTM цАМФ, меченного рутением (MSD), а затем клетки инкубировали в течение приблизительно 90 минут при комнатной температуре. В конце второго периода инкубирования добавляли буфер для считывания (Трис-буфер, содержащий сореагент ЭХЛ и Triton X-100, рН 7,8), при этом уровни цАМФ в лизатах клеток немедленно определяли посредством ЭХЛ-детекции с помощью блока образования изображений планшет-ридера Sector Imager 6000® (MSD). Данные анализировали, используя компьютерный нелинейный регрессионный анализ (XL fit; IDBS), и выражали либо в значениях EC50, либо в значениях Kb.
EC50 обозначает концентрацию соединения-агониста, необходимую для обеспечения 50% от максимальной ответной реакции, например 50% от максимального уровня цАМФ, определяемого с помощью анализа, описанного выше.
Выбор соединений осуществляли с использованием вышеуказанных анализов, при этом данные биоанализа на цАМФ для выбранных соединений приведены в Таблицах 2A, 2B и 2C.
hMC1
hMC3
hMC4
hMC5
hMC1
hMC3
hMC4
hMC5
Анализы связывания радиолиганда
Клеточные мембраны, используемые в in vitro анализе связывания рецептора, получали из трансгенных клеток CHO-K1, стабильно экспрессирующих подтипы 1, 3, 4 или 5 рецептора hMC-R. Клетки CHO-K1, экспрессирующие нужный тип рецептора hMC-R, разрушали ультразвуком (Branson®, в режиме 7, приблизительно 30 секунд) в охлажденном до 0°С 50 мМ Трис-HCl, pH 7,4, а затем центрифугировали при 39000 g в течение 10 минут, приблизительно при 4°C. Осадки ресуспендировали в том же буфере и центрифугировали при 50000 g в течение 10 минут, приблизительно при 4°C. Промытые осадки, содержащие клеточные мембраны, хранили приблизительно при -80°C.
Конкурентное ингибирование связывания [125I](Tyr2)-(Nle4-D-Phe7)α-MSH ([125I]-NDP-α-MSH, Amersham Biosciences®) выполняли в полипропиленовых 96-луночных планшетах. Клеточные мембраны (1-10 мкг белка на лунку), полученные, как описано выше, инкубировали в 50 мМ Трис-HCl, pH 7,4, содержащем 0,2% бычьего сывороточного альбумина (BSA), 5 мМ MgCl2, 1 мМ CaCl2 и 0,1 мг/мл бацитрацина, с увеличивающимися концентрациями тестируемого соединения и 0,1-0,3 нМ [125I]-NDP-α-MSH в течение приблизительно 90-120 минут приблизительно при 37°C. Связанный лиганд [125I]-NDP-α-MSH отделяли от свободного [125I]-NDP-α-MSH с помощью фильтрации через стекловолоконные фильтровальные пластины GF/C (Unifilter®; Packard), пропитанные 0,1% (мас./об.) полиэтиленимином (PEI), используя коллектор Packard Filtermate®. Фильтры промывали три раза 50 мМ Трис-HCl, pH 7,4, при температуре приблизительно 0-4°C, а затем измеряли радиоактивность, используя сцинтилляционный счетчик Packard Topcount®. Данные связывания анализировали с помощью компьютерного нелинейного регрессионного анализа (XL fit; IDBS).
Выбор предпочтительных вариантов осуществления проводили с использованием вышеуказанного анализа и констант связывания (Ki, в нМ), приведенных в Таблицах 3A, 3B и 3C.
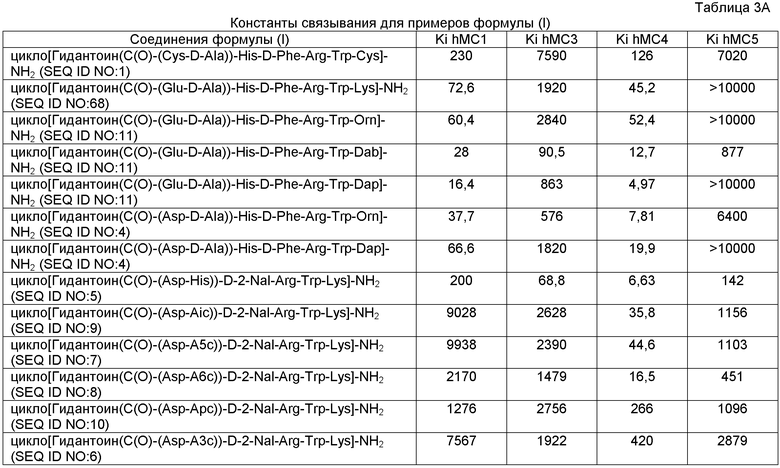
Анализы in vivo
Воздействие лигандов меланокортиновых рецепторов настоящего изобретения на потребление пищи и/или массу тела могут быть и были проанализированы согласно следующим методикам. Специалист, квалифицированный в данной области, осведомлен, что методики, подобные описанным в настоящей заявке, могут использоваться для оценки воздействия соединений согласно изобретению на потребление пищи и/или массу тела.
Короткие эксперименты по кормлению (с ограничением пищи)
Самцов крыс линии Спраг-Доули (250 г) помещали в отдельные клетки и держали при световом режиме 12:12 часов света:темноты. В течение 18 часов до начала эксперимента крысы не получали корм, вода была доступна без ограничения. В момент времени 0 крысам подкожно (п/к) вводили выбранные соединения в выбранных дозах, например 500 или 100 нмоль/кг, или основу и давали корм. Индивидуальное потребление пищи измеряли приблизительно через 1, 2, 3, 4, 5 и 6 часов после инъекции.
Короткие эксперименты по кормлению (без ограничения пищи)
Самцов крыс линии Спраг-Доули (250 г) помещали в отдельные клетки и держали при световом режиме 12:12 часов света:темноты. В течение эксперимента пища и вода были доступны без ограничения. В момент времени 0 крысам п/к вводили соединение в дозах 8 мкмоль/кг либо основу. Индивидуальное потребление пищи измеряли приблизительно через 0,5, 1, 1,5, 2, 3 и 4 часа после инъекции. Данные для выбранных соединений изобретения приведены на Фигуре 1.
Длительные эксперименты по кормлению
Самцов крыс линии Спраг-Доули (250 г) помещали в отдельные клетки и держали при световом режиме 12:12 часов света:темноты, пища и вода были доступны без ограничения. Крысам 3× в день вводили (08.00, 12.00 и 16.00) п/к соединение в различных дозах или основу, в течение 7 дней. Индивидуальную массу тела и потребление пищи регистрировали ежедневно. Данные для выбранных соединений изобретения приведены на Фигурах 2A, 2B, 3A, 3B, 4A и 4B.
Способы применения и композиции
Основанное на способности лигандов агонистически или антагонистически взаимодействовать с рецептором MC-4 и/или MC-3 настоящее изобретение также относится к применению лигандов настоящего изобретения в способах лечения ожирения, а также других нарушений массы тела (например, анорексии, булимии, истощения при СПИДе, истощения у ослабленных пожилых людей, синдрома Прадера-Вилли) и кахексии (например, раковой кахексии, почечной кахексии, сердечной кахексии). Изобретение также относится к лечению заболеваний, связанных с поведением (например, мотивации, тревоги, депрессии, нейропатической боли), памятью (включая обучение), нарушением работы сердечно-сосудистой системы (например, сердечной кахексии), нарушением работы легких (например, острого респираторного дистресс-синдрома, фиброза легких, хронической обструктивной болезни легких, астмы), воспалением (например, ревматоидного артрита, подагрического артрита, рассеянного склероза), сепсисом и септическим, кардиогенным и гиповолемическим шоком, половой дисфункцией (например, эндометриоза, маточного кровотечения), нарушением эрекции, атрофией мускулатуры, нарушением развития кости, роста нервов, защиты и восстановления (повреждения спинного мозга), нарушением внутриутробного развития эмбриона, и т.п. Кроме того, соединения формул (I), (II) или (III) могут улучшить состояние пациента при повреждающих факторах (например, при отторжении трансплантата, ишемии и реперфузионном повреждении, ранении) или при потере веса, обусловленной режимом лечения (например, при химиотерапии, лучевой терапии, временной или постоянной иммобилизации, диализе). С применением заявленных соединений обеспечивается модуляция нормальных функций тела (например, развития яичников и плаценты, секреции пролактина и ФСГ, родов, сперматогенеза, секреции тироксина, синтеза альдостерона, температуры тела, кровяного давления, частоты сердечных сокращений, сосудистого тонуса, мозгового кровообращения, уровня глюкозы в крови, секреции кожного сала и феромонов).
Настоящее изобретение обеспечивает способ предотвращения потребления алкоголя для снижения потребления алкоголя, для лечения алкоголизма или лечения алкогольной зависимости посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора, вызываемой введением эффективного количества соединения формулы (I), (II) или (III), или его фармацевтически приемлемой соли. Соединения формулы (I), (II) или (III) могут применяться для предотвращения потребления алкоголя и являются селективными агонистами рецептора меланокортина-4 или их фармацевтически приемлемой солью, функциональная активность которых характеризуется EC50, которая является, по меньшей мере, в 15 раз более, по меньшей мере, в 17 раз более, по меньшей мере, в 90 раз более, по меньшей мере, в 200 раз более или, по меньшей мере, в 3000 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-1 человека, рецептора меланокортина-3 человека и рецептора меланокортина-5 человека.
Термин лечение, используемый в настоящей заявке, означает, что введение соединения настоящего изобретения, действующего через рецептор MC-3 или MC-4, приводит, как минимум, к смягчению болезненного состояния. Таким образом, термин включает предотвращение развития болезненного состояния у млекопитающего, в особенности, когда млекопитающее предрасположено к возникновению такого заболевания, которое до настоящего момента не диагностировали; замедление развития болезненного состояния и/или облегчение или полное устранение болезненного состояния.
Соединения настоящего изобретения, таким образом, могут быть введены в фармацевтические композиции, предназначенные для применения в лечении или профилактике указанных патологических состояний. Применяют стандартные фармацевтические способы приготовления лекарственных форм, такие как описанные в последнем издании Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, Pa., и Peptide and Protein Drug Delivery, Marcel Dekker, N.Y., 1991.
Композиции настоящего изобретения включают: a) безопасное и эффективное количество соединения формулы (I), (II) или (III); и b) фармацевтически приемлемый наполнитель.
"Безопасное и эффективное количество" соединения формулы (I), (II) или (III) является количеством, которое эффективно взаимодействует с рецептором MC-4 и/или MC-3, в организме животного, предпочтительно млекопитающего, более предпочтительно человека, без развития нежелательных побочных эффектов (таких как токсичность, раздражение или аллергическая реакция), и соответствует разумному отношению выгоды/риска при применении в соответствии с настоящим изобретением. Конкретное "безопасное и эффективное количество", безусловно, изменяется в зависимости от таких факторов, как конкретное состояние, подвергаемое лечению, физическое состояние пациента, продолжительность лечения, характер сопутствующей терапии (при наличии таковой), конкретная используемая лекарственная форма, используемый наполнитель, растворимость используемого соединения формулы (I), (II) или (III), а также схема приема, требуемая для композиции.
В дополнение к рассматриваемому соединению, композиции рассматриваемого изобретения содержат один или несколько фармацевтически приемлемых наполнителей. Термин "фармацевтически приемлемый наполнитель", используемый в настоящей заявке, обозначает один или несколько совместимых твердых или жидких компонентов, которые подходят для введения животному, предпочтительно млекопитающему, более предпочтительно человеку. Термин "совместимый", используемый в настоящей заявке, означает, что компоненты композиции могут быть смешаны с рассматриваемым соединением, а также друг с другом таким способом, что между ними не происходит какого-либо взаимодействия, которое может существенно снизить фармацевтическую эффективность композиции при обычных способах применения. Фармацевтически приемлемые наполнители, безусловно, должны обладать достаточно высокой чистотой и достаточно низкой токсичностью, чтобы подходить для введения животному, которое подвергается лечению, предпочтительно млекопитающему, более предпочтительно человеку.
Некоторые примеры веществ, которые могут служить в качестве фармацевтически приемлемых наполнителей или их компонентов, включают сахара, такие как лактоза, глюкоза и сахароза; крахмалы, такие как кукурузный крахмал и картофельный крахмал; целлюлозу и ее производные, такие как натриевую соль карбоксиметилцеллюлозы, этилцеллюлозу и метилцеллюлозу; порошковую трагакантовую камедь; солод; желатин; тальк; твердые скользящие вещества, такие как стеариновая кислота и стеарат магния; растительные масла, такие как арахисовое масло, хлопковое масло, кунжутное масло, оливковое масло, кукурузное масло и теобромовое масло (масло какао); полиолы, такие как пропиленгликоль, глицерин, сорбит, маннит и полиэтиленгликоль; агар; альгиновую кислоту; смачивающие добавки и скользящие вещества, такие как лаурилсульфат натрия; красители; ароматизаторы; вспомогательные вещества для таблетирования, стабилизаторы; антиоксиданты; консерванты; апирогенную воду; изотонический раствор; а также буферы, такие как фосфатный, цитратный и ацетатный.
Выбор фармацевтически приемлемых наполнителей, которые применяются вместе с рассматриваемым соединением, в основном определяется тем, каким путем необходимо вводить соединение. Если рассматриваемое соединение нужно вводить посредством инъекции, то предпочтительным фармацевтически приемлемым наполнителем является стерильная вода, физиологический раствор или их смеси, уровень pH которых предпочтительно доведен приблизительно до 4-10 фармацевтическим буфером; также может потребоваться совместимое суспендирующее вещество.
В частности фармацевтически приемлемые наполнители для системного введения включают сахара, крахмалы, целлюлозу и ее производные, солод, желатин, тальк, сульфат кальция, лактозу, растительные масла, синтетические масла, полиолы, альгиновую кислоту, фосфатные, ацетатные и цитратные буферные растворы, эмульгаторы, изотонический раствор, а также апирогенную воду. Предпочтительные наполнители для парентерального введения включают пропиленгликоль, этилолеат, пирролидон, этанол и кунжутное масло. Предпочтительно фармацевтически приемлемый наполнитель, в композициях для парентерального введения, составляет, по меньшей мере, приблизительно 90% от полного веса композиции.
Композиции настоящего изобретения предпочтительно приготавливаются в дозированной лекарственной форме. Используемый в настоящей заявке термин "дозированная лекарственная форма" является композицией настоящего изобретения, содержащей некоторое количество соединений формулы (I), (II) или (III), которые подходят для введения животному, предпочтительно млекопитающему, более предпочтительно человеку, в разовой дозе, согласно рекомендуемой медицинской практике. Указанные композиции предпочтительно содержат приблизительно от 1 мг до приблизительно 750 мг, более предпочтительно приблизительно от 3 мг до приблизительно 500 мг, наиболее предпочтительно приблизительно от 5 мг до приблизительно 300 мг, соединения формулы (I), (II) или (III).
Композиции настоящего изобретения могут находиться в любой из множества форм, подходящих (например) для перорального, ректального, местного, назального, глазного, трансдермального, легочного или парентерального введения. В зависимости от конкретного требуемого пути введения может применяться множество различных фармацевтически приемлемых наполнителей, известных из уровня техники. Они включают твердые или жидкие наполнители, разбавители, гидротропы, поверхностно-активные вещества и инкапсулирующие вещества. Могут быть включены дополнительные фармацевтически-активные материалы, которые по существу не влияют на ингибирующую активность соединения формулы (I), (II) или (III). Количество наполнителя, используемого вместе с соединениями формулы (I), (II) или (III), является достаточным, чтобы обеспечивать требуемое количество материала при введении разовой дозы соединения. Методики и композиции, используемые для приготовления лекарственных форм, применяемых в способах настоящего изобретения, описаны в следующих источниках, включенных в настоящее описание путем отсылки: Modern Pharmaceutics, Chapters 9 and 10 (Banker & Rhodes, editors, 1979); Lieberman et al., Pharmaceutical Dosage Forms: Tablets (1981); и Ansel, Introduction to Pharmaceutical Dosage Forms 2d Edition (1976).
Могут применяться различные лекарственные формы для перорального применения, включая такие твердые формы, как таблетки, капсулы, лекарственные формы, состоящие из множества частиц, гели, пленки, суппозитории, эликсиры, гранулы и нефасованные порошки. Указанные формы для перорального применения включают безопасное и эффективное количество, обычно, по меньшей мере, приблизительно 5%, а предпочтительно приблизительно от 25% до приблизительно 50%, соединения формулы (I), (II) или (III). Таблетки могут быть прессованными, тритурационными, с кишечнорастворимым покрытием, покрытыми глазурью, пленкой или многократно прессованными, могут содержать подходящие связующие вещества, скользящие вещества, разбавители, дезинтегрирующие агенты, красители, ароматизаторы, добавки, повышающие текучесть, а также плавители. Жидкие лекарственные формы для перорального применения включают водные растворы, эмульсии, суспензии, растворы и/или суспензии, приготовленные из нешипучих гранул, а также шипучие препараты, приготовленные из шипучих гранул, содержащих подходящие растворители, консерванты, эмульгаторы, суспендирующие добавки, разбавители, подсластители, плавители, красители и ароматизаторы.
Фармацевтически приемлемый наполнитель, подходящий для приготовления дозированных лекарственных форм для перорального введения, известен в уровне техники. Таблетки обычно включают стандартные, фармацевтически совместимые вспомогательные добавки, такие как инертные разбавители, например карбонат кальция, двухосновный фосфат кальция, карбонат натрия, цитрат натрия, маннит, лактозу и целлюлозу; связующие вещества, такие как крахмал, желатин, поливинилпирролидон, гидроксипропилметилцеллюлозу (ГПМЦ), гидроксипропилцеллюлозу (ГПЦ), гуммиарабик и сахарозу; дезинтегрирующие агенты, такие как крахмал (предпочтительно кукурузный, картофельный или маниоковый), натриевую соль крахмалгликолята, альгиновую кислоту, комплексные силикаты и кроскармелозу; скользящие вещества, такие как стеарат магния, стеариновая кислота, глицерилбегенат и тальк. Для улучшения текучести порошковой смеси могут использоваться глиданты, такие как диоксид кремния. Для улучшения цвета могут быть добавлены красители, такие как красители FD&C (красители для продуктов питания, лекарственных и косметических средств). Подсластители и ароматизаторы, такие как аспартам, сахарин, ментол, мята и фруктовые ароматы, являются полезными добавками для жевательных таблеток. Капсулы обычно включают один или несколько твердых разбавителей, описанных выше. Выбор компонентов-наполнителей зависит от второстепенных признаков, таких как вкус, стоимость и стабильность при хранении, которые не являются критическими в рамках настоящего изобретения, и легко может быть сделан специалистом, квалифицированным в данной области.
Композиции для перорального введения также включают жидкие растворы, эмульсии, суспензии и т.п. Фармацевтически приемлемые наполнители, подходящие для приготовления таких композиций, известны из уровня техники. Стандартные компоненты наполнителей для сиропов, эликсиров, эмульсий и суспензий включают этанол, глицерин, пропиленгликоль, полиэтиленгликоль, сироп сахарозы, сорбит и воду. Что касается суспензий, стандартные суспендирующие агенты включают метилцеллюлозу, натриевую соль карбоксиметилцеллюлозы, трагакантовую камедь и альгинат натрия; стандартные смачивающие агенты включают лецитин и полисорбат 80; и стандартные консерванты включают метилпарабен, пропилпарабен и бензоат натрия. Жидкие композиции для перорального введения могут также содержать один или несколько компонентов, таких как подсластители, ароматизаторы и красители, описанные выше.
Дозированные лекарственные формы с модифицированным и импульсным высвобождением могут содержать наполнители, такие как предназначенные для немедленного, пролонгированного, модифицированного, замедленного, импульсного или регулируемого высвобождения в желудочно-кишечном тракте вблизи желаемого участка местного применения, или в различное время, чтобы продлить действие, вместе с дополнительными наполнителями, которые действуют как модификаторы скорости высвобождения, наносимыми стандартными способами обычно с использованием pH- или времязависимых покрытий, и/или вводимых в рабочую часть установки. Модификаторы скорости высвобождения включают, помимо прочих, гидроксипропилметилцеллюлозу, фталат гидроксипропилметилцеллюлозы, метилцеллюлозу, натриевую соль карбоксиметилцеллюлозы, этилцеллюлозу, ацетат целлюлозы, фталат ацетат целлюлозы, поливинилацетат фталат, полиэтиленоксид, ксантановую камедь, карбомер, сополимер метакрилата аммония, гидрогенизированное касторовое масло, карнаубский воск, парафин, фталат ацетат целлюлозы, фталат гидроксипропилметилцеллюлозы, сополимер метакриловой кислоты и смеси перечисленного. Дозированные лекарственные формы с модифицированным и импульсным высвобождением могут содержать один или комбинацию наполнителей, модифицирующих скорость высвобождения. Наполнители, модифицирующие скорость высвобождения, могут присутствовать как внутри дозированной лекарственной формы, то есть в сердцевине, так и снаружи дозированной лекарственной формы, то есть на поверхности или покрытии.
Соединения изобретения могут быть также введены в форме быстрораспадающихся или быстрорастворимых дозированных лекарственных форм (FDDF). Такие лекарственные формы могут содержать следующие компоненты: аспартам, ацесульфам калия, лимонную кислоту, натриевую соль кроскармелозы, кросповидон, D-аскорбиновую кислоту, этилакрилат, этилцеллюлозу, желатин, гидроксипропилметилцеллюлозу, стеарат магния, маннит, метилметакрилат, мятный ароматизатор, полиэтиленгликоль, пирогенный диоксид кремния, диоксид кремния, натриевую соль крахмалгликолята, стеарилфумарат натрия, сорбит, ксилит. Термины "распадающийся" или "растворимый", используемые в настоящей заявке при описании FDDF, зависят от растворимости используемого лекарственного вещества, то есть, когда лекарственное вещество является нерастворимым, может быть приготовлена быстрораспадающаяся дозированная лекарственная форма, а когда лекарственное вещество является растворимым, может быть приготовлена быстрорастворимая дозированная лекарственная форма.
Поскольку соединения настоящего изобретения по природе являются пептидами, предпочтительным способом введения является парентеральное введение (более предпочтительно внутривенная инъекция) в виде разовой дозированной лекарственной формы. Предпочтительные разовые дозированные лекарственные формы включают суспензии и растворы, включающие безопасное и эффективное количество соединения формулы I, (II) или (III). Для такого парентерального введения их лучше всего применять в форме стерильного водного раствора, который может содержать другие вещества, например достаточное количество солей или глюкозы, чтобы раствор являлся изотоническим с кровью. Водные растворы должны быть надлежащим образом забуферены (предпочтительно до pH от 3 до 9), при необходимости. Приготовление в стерильных условиях подходящих лекарственных форм для парентерального введения легко осуществляется с использованием стандартных фармацевтических методов, известных квалифицированным специалистам.
Другие композиции, применяемые для достижения системной доставки рассматриваемых соединений, включают сублингвальные, буккальные и назальные дозированные лекарственные формы. Такие композиции обычно включают одно или несколько растворимых наполнителей, таких как сахароза, сорбит и маннит; и связующих веществ, таких как гуммиарабик, микрокристаллическая целлюлоза, карбоксиметилцеллюлоза и гидроксипропилметилцеллюлоза. Также могут быть включены глиданты, скользящие вещества, подсластители, красители, антиоксиданты и ароматизаторы, описанные выше. При интраназальном введении или ингаляции соединения формулы (I), (II) или (III) предпочтительно доставляются посредством порошкового ингалятора или в форме аэрозольной струи, поступающей из аэрозольного баллона, насоса, спрея, распылителя или небулайзера, с или без использования подходящего пропеллента, например дихлордифторметана, трихлорфторметана, дихлортетрафторэтана, гидрофторалкана, такого как 1,1,1,2-тетрафторэтан (HFA 134A®) или 1,1,1,2,3,3,3-гептафторпропан (HFA 227EA®), диоксида углерода или другого подходящего газа. В случае аэрозольного баллона разовая доза может быть определена с помощью клапана, выпускающего дозированное количество. Аэрозольный баллон, насос, спрей, распылитель или небулайзер могут содержать раствор или суспензию активного соединения, например, используя смесь этанола и пропеллента в качестве растворителя, которая может дополнительно содержать смазку, например сорбитан триолеат. Капсулы и картриджи (изготовленные, например, из желатина), предназначенные для применения в ингаляторе или инсуффляторе, могут содержать порошковую смесь соединения изобретения и подходящей порошковой основы, такой как лактоза или крахмал.
Аэрозоль или сухие порошковые композиции предпочтительно устроены так, что каждая дозированная доза или "пшик" содержит от 1 до 50 мг соединения изобретения для доставки пациенту. Полная ежедневная доза аэрозоля находится в диапазоне от 1 до 50 мг, которую можно вводить как разовую дозу или, как правило, в виде дробных доз в течение дня.
В альтернативе соединения изобретения можно вводить в форме суппозиториев или вагинальных суппозиториев, или они могут быть нанесены местно в форме геля, гидрогеля, лосьона, раствора, крема, мази или присыпки. Соединения изобретения могут быть также введены дермально или трансдермально, например при помощи пластыря. Их можно также вводить легочным, вагинальным или ректальным путями.
Их можно также вводить глазным путем, в особенности для лечения заболеваний глаз. Для глазного применения соединения могут быть приготовлены в форме микронизированной суспензии в изотоническом, с доведенным значением pH, стерильном физиологическом растворе или, предпочтительно, в форме раствора в изотоническом, с доведенным значением pH, стерильном физиологическом растворе, необязательно в комбинации с консервантом, таким как хлорид бензалкония. В альтернативе они могут быть приготовлены в форме мази, такой как вазелин.
В целях местного применения на коже соединения изобретения могут быть приготовлены в форме подходящей мази, содержащей активное соединение, суспендированное или растворенное в, например, смеси с одним или несколькими из следующих веществ: минеральное масло, вазелиновое масло, белый вазелин, пропиленгликоль, полиоксиэтилен-полиоксипропиленовое соединение, эмульгирующий воск и вода. В альтернативе они могут быть приготовлены в форме подходящего лосьона или крема, суспендированы или растворены, например, в смеси одного или нескольких следующих веществ: минеральная нефть, сорбитан моностеарат, полиэтиленгликоль, жидкий парафин, полисорбат 60, воск из сложных эфиров цетилового спирта, цетиариловый спирт, 2-октилдодеканол, бензиловый спирт и вода.
Соединения изобретения могут также применяться в комбинации с циклодекстрином. Циклодекстрины, как известно, формируют комплексы включения и аддукты с молекулами лекарственного вещества. Образование комплекса циклодекстрина с лекарственным веществом может изменить растворимость, скорость растворения, биодоступность и/или стабильность молекулы лекарственного вещества. Комплексы циклодекстрина с лекарственным веществом обычно применяют в большинстве дозированных лекарственных форм и путей введения. В качестве альтернативы прямому комплексообразованию с лекарственным веществом циклодекстрин может использоваться как вспомогательная добавка, например, как носитель, разбавитель или солюбилизатор. Альфа-, бета- и гамма-циклодекстрины широко применяются, а соответствующие примеры описаны в WO 91/11172 (Stella et al., 1991), WO 94/02518 (Stella et al., 1994) и WO 98/55148 (Vandecruys, 1998).
В целях лечения сердечно-сосудистых заболеваний, в частности гипертонии, соединения изобретения могут быть объединены с одним или несколькими активными компонентами, выбранными из следующего списка:
a) блокаторы рецептора ангиотензина (ARB), такие как лозартан, валзартан, телмизартан, кандезартан, ирбезартан, эпрозартан и олмесартан;
b) блокаторы кальциевых каналов (CCB), такие как амлодипин;
c) статины, такие как аторвастатин;
d) ингибиторы PDE5, такие как силденафил, тадалафил, варденафил, 5-[2-этокси-5-(4-этилпиперазин-1-илсульфонил)-пиридин-3-ил]-3-этил-2-[2-метоксиэтил]-2,6-дигидро-7H-пиразоло-[4,3-d]пиримидин-7-он; 5-(5-ацетил-2-бутокси-3-пиридинил)-3-этил-2-(1-этил-3-азетидинил)-2,6-дигидро-7H-пиразоло[4,3-d]пиримидин-7-он и пиразоло[4,3-d] пиримидин-4-оны, раскрытые в WO 00/27848, в особенности N-[[3-(4,7-дигидро-1-метил-7-оксо-3-пропил-1H-пиразоло[4,3-d]-пиримидин-5-ил)-4-пропоксифенил]-сульфонил]-1-метил-2-пирролидинпропанамид [DA-8159 (Пример 68 из WO 00/27848 (Yoo et al., 2000))];
e) бета-блокаторы, такие как атенолол или карведилол;
f) ингибиторы АПФ, такие как хинаприл, эналаприл и лизиноприл;
g) альфа-блокаторы, такие как доксазозин;
h) селективные антагонисты рецептора альдостерона (САРА), такие как эплеренон или спиронолактон;
i) агонисты I1 имидазолиновых рецепторов, такие как рилменидин или моноксидин; и
j) антагонисты эндотелинового рецептора и ингибиторы эндотелинпревращающего фермента.
Композиции настоящего изобретения необязательно могут включать другие активные вещества. Если вводят комбинацию активных веществ, то их можно вводить одновременно, отдельно или последовательно.
Способы введения
Как указано, композиции настоящего изобретения можно вводить местно или системно. Системное применение включает любой способ введения соединений формулы (I), (II) или (III) в ткани тела, например внутрисуставное, интратекальное, перидуральное, внутримышечное, трансдермальное, внутривенное, внутрибрюшинное, подкожное, сублингвальное, ректальное, назальное, легочное и пероральное введение. Соединения формулы (I), (II) или (III) настоящего изобретения предпочтительно вводят системно, более предпочтительно, парентерально и, наиболее предпочтительно, посредством внутривенной инъекции.
Конкретная дозировка вводимого соединения, а также продолжительность лечения, независимо от того, является ли лечение местным или системным, взаимозависимы. Дозировка и схема лечения также зависят от таких факторов, как конкретное применяемое соединение формула (I), (II) или (III), показания для лечения, способность соединения формулы (I), (II) или (III) достигать минимальных ингибирующих концентраций в сайте ингибируемой металлопротеазы, персональные признаки пациента (например, вес), согласие со схемой лечения, а также присутствие и тяжесть каких-либо побочных эффектов лечения.
Как правило, при системном введении взрослому человеку (весом приблизительно 70 килограммов), в день вводят от приблизительно 0,003 мг до приблизительно 300 мг, более предпочтительно от приблизительно 0,03 мг до приблизительно 100 мг, соединения формулы (I), (II) или (III). Следует понимать, что указанные диапазоны доз приведены только лишь в качестве примера и что ежедневное введение может быть скорректировано в зависимости от вышеуказанных факторов.
Как известно из уровня техники и соблюдается на практике, все лекарственные формы для парентерального введения должны быть стерильными. Для млекопитающих, в особенности людей (при условии, что масса тела равна приблизительно 70 килограммов), предпочтительные индивидуальные дозы составляют от приблизительно 0,001 мг до приблизительно 100 мг.
Предпочтительным способом системного введения является внутривенная доставка. Предпочтительные индивидуальные дозы при использовании данного способа доставки составляют от приблизительно 0,01 мг до приблизительно 100 мг, предпочтительно от приблизительно 0,1 мг до приблизительно 100 мг.
Учитывая все вышеизложенное, безусловно, соединения настоящего изобретения можно вводить по отдельности или в виде смеси, при этом композиции могут также включать дополнительные лекарственные вещества или наполнители в зависимости от показаний.
Соединение настоящего изобретения может быть доставлено в предпочтительный участок в организме при помощи подходящей системы доставки лекарственного средства. Системы доставки лекарственного средства известны из уровня техники. Например, методика доставки лекарственного средства, подходящая для соединений настоящего изобретения, включает конъюгирование соединения с активной молекулой, способной проникать через биологический барьер (Zlokovic, B. V., Pharma. Res., 12:1395-406 (1995)). Конкретный пример включает присоединение соединения согласно настоящему изобретению к фрагментам инсулина с обеспечением возможности транспорта через гематоэнцефалический барьер (Fukuta, M. et al., Pharma. Res., 11:1681-8 (1994)). По поводу общих обзоров технологий доставки лекарственных средств, подходящих для соединений настоящего изобретения, см. Zlokovic, B. V., Pharma. Res ., 12:1395-406 (1995) и Pardridge, W. M., Pharmacol. Toxicol., 71:3-10 (1992).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ МЕЛАНОКОРТИНОВ ДЛЯ ЛЕЧЕНИЯ ЧУВСТВИТЕЛЬНОСТИ К ИНСУЛИНУ | 2008 |
|
RU2453328C2 |
| ЛИГАНДЫ РЕЦЕПТОРОВ МЕЛАНОКОРТИНОВ | 2006 |
|
RU2439079C2 |
| ЛИГАНДЫ РЕЦЕПТОРОВ МЕЛАНОКОРТИНОВ | 2006 |
|
RU2380372C2 |
| ЛИГАНДЫ РЕЦЕПТОРОВ МЕЛАНОКОРТИНОВ | 2006 |
|
RU2401841C2 |
| СПОСОБ ЛЕЧЕНИЯ НАРУШЕНИЙ, АССОЦИИРОВАННЫХ С ПУТЕМ РЕЦЕПТОРА МЕЛАНОКОРТИНА 4 | 2016 |
|
RU2785889C1 |
| АНАЛОГИ АЛЬФА- и ГАММА-MSH | 2013 |
|
RU2668791C2 |
| ПЕПТИДНЫЕ КОМПОЗИЦИИ | 2014 |
|
RU2725150C2 |
| ПРОЛЕКАРСТВЕННЫЕ КОМПОЗИЦИИ С ВЫСОКОЙ СТЕПЕНЬЮ ПРОНИКНОВЕНИЯ НА ОСНОВЕ ПЕПТИДОВ И РОДСТВЕННЫХ ПЕПТИДАМ СОЕДИНЕНИЙ | 2010 |
|
RU2627065C2 |
| АНАЛОГИ ПЕПТИДА ЛГ-РФ, ИХ ПРИМЕНЕНИЕ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1998 |
|
RU2212247C2 |
| ПЕПТИДНЫЕ ВЕКТОРЫ | 2004 |
|
RU2361876C2 |





















































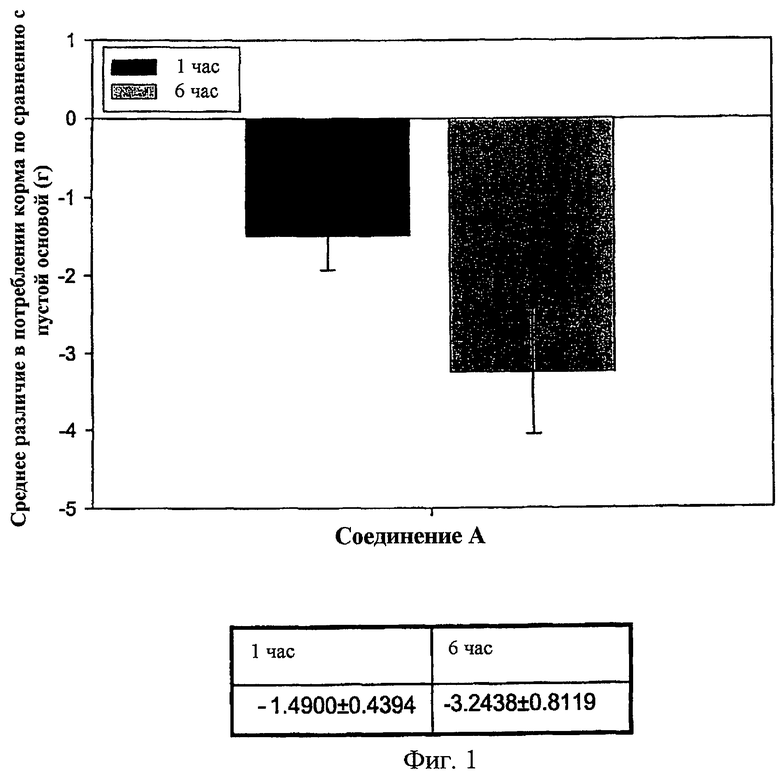

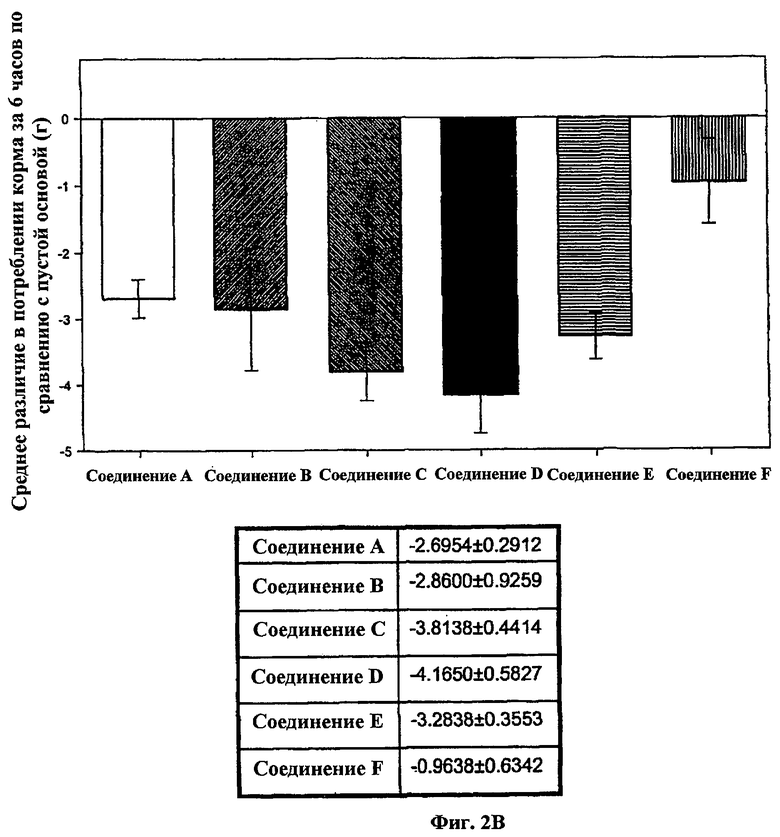
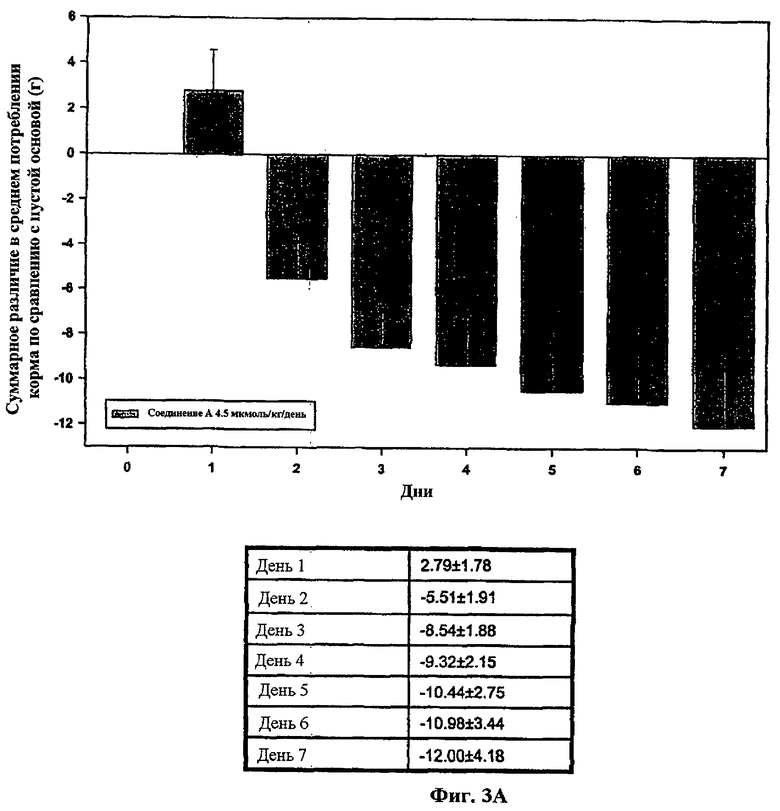
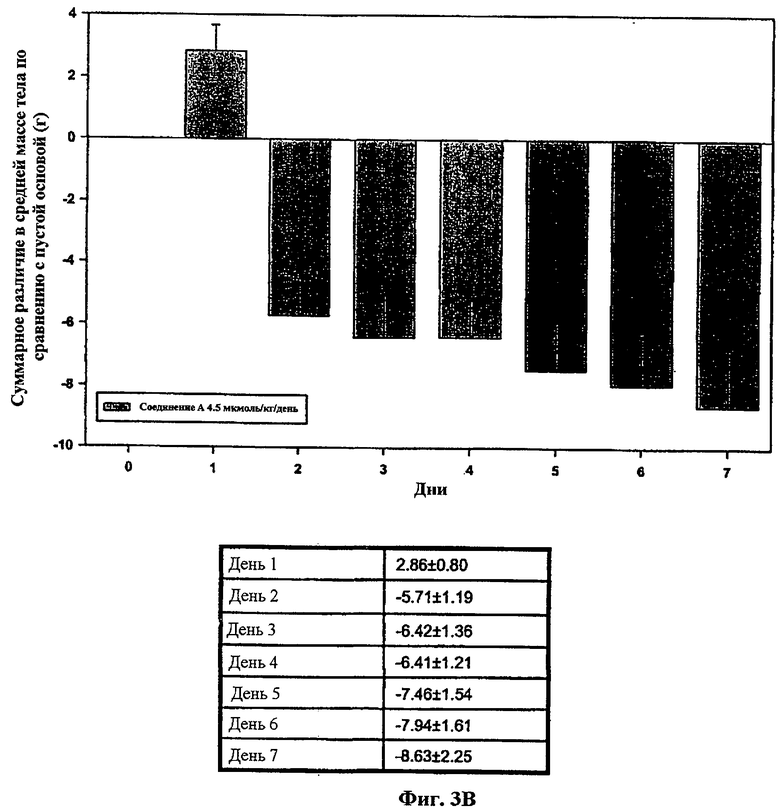
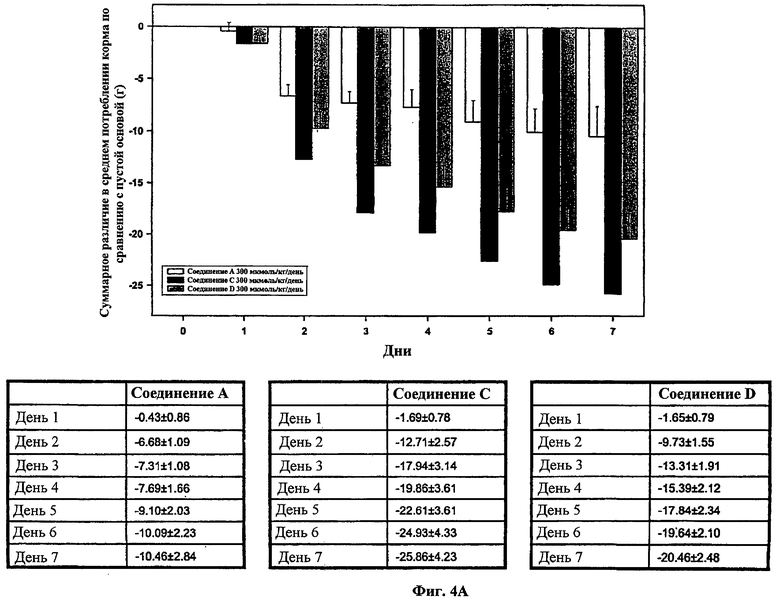
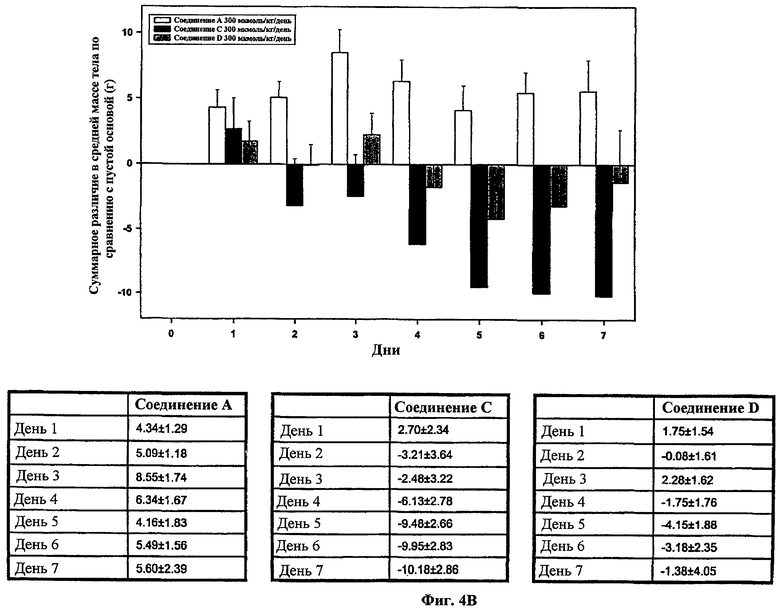
Настоящее изобретение относится к пептидным лигандам меланокортиновых рецепторов, в частности рецептора меланокортина-4, и предназначены для лечения заболеваний, реагирующих на активацию данного рецептора, например ожирения, сахарного диабета и половой дисфункции. 10 н. и 3 з.п. ф-лы, 7 ил., 7 табл., 5 пр.
1. Соединение формулы:
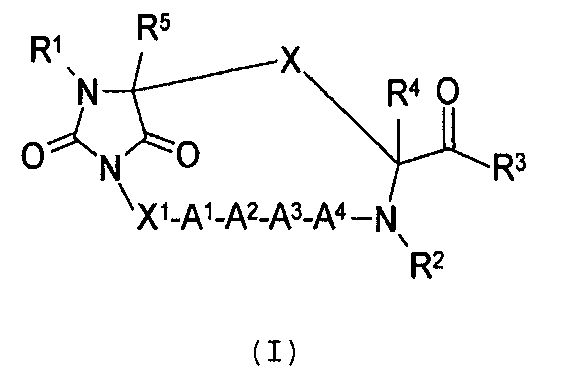
в котором X выбран из группы, состоящей из -CH2-S-S-CH2-, -(CH2)2-S-S-CH2, -(CH2)t-C(O)-NR8-(CH2)r- и -(CH2)r-NR8-C(O)-(CH2)t;
каждый R1 и R2 представляет собой Н;
R3 представляет собой -NH2;
каждый R4 и R5 представляет собой Н;
X1 представляет собой
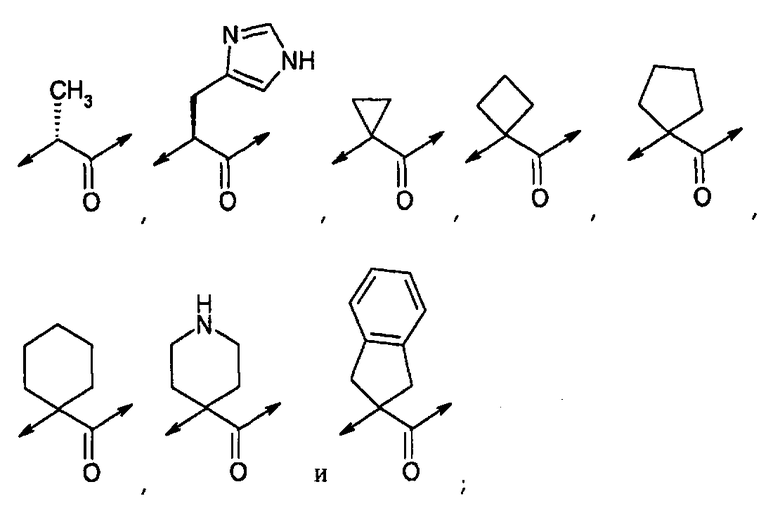
А1 представляет собой His или отсутствует;
А2 представляет собой D-1-Nal, D-2-Nal или D-Phe;
А3 представляет собой Arg;
А4 представляет собой Bal, 1-Nal, 2-Nal или Trp;
R8 представляет собой Н или (C1-С10)алкил;
r независимо от своего положения является 1, 2, 3, 4 или 5; и
t независимо от своего положения является 1 или 2; или
его фармацевтически приемлемая соль.
2. Соединение формулы (II):
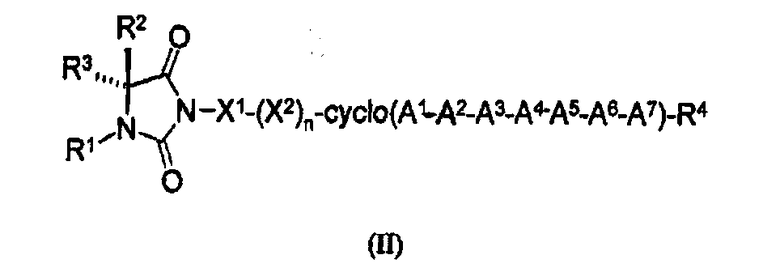
в котором
X1 представляет собой 
X2 представляет собой 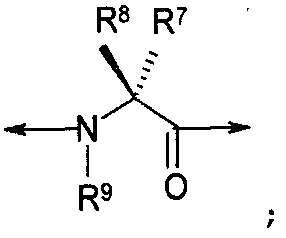
А1 представляет собой Cys;
А2 является D-Ala или Glu;
А3 представляет собой His;
А4 представляет собой D-2-Nal или D-Phe;
А5 представляет собой Arg;
А6 представляет собой Trg;
А7 представляет собой Cys или Pen;
R1 представляет собой Н;
каждый R2 и R3 представляет собой Н;
R4 представляет собой C(O)NH2;
каждый R5 и R6 представляет собой Н, метил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил или (CH2)-NH-C(N)-NH2 или R5 и R6 могут быть объединены с образованием циклогексила или СН2-циклогексила;
R7 представляет собой Н и R8 представляет собой метил;
R9 представляет собой Н; и
n независимо от своего положения является 1, 2, 3, 4, 5, 6 или 7; или
его фармацевтически приемлемая соль.
3. Соединение формулы (III)
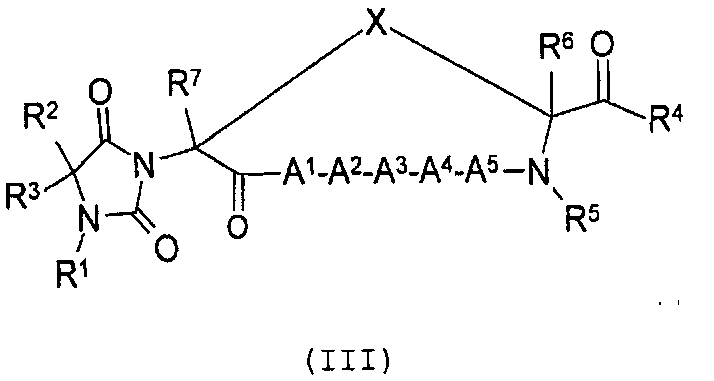
в которой X выбран из группы, состоящей из -CH2-S-S-CH2-, -C(CH3)2-S-S-
СН2- и -(CH2)2-S-S-CHr;
каждый R1 и R5 представляет собой Н;
R2 и R3 независимо представляют собой Н, метил, изопропил, изобутил или втор-бутил, или R2 и R3 могут быть объединены с образованием циклогексила;
R4 представляет собой -ОН или -NH2;
каждый R6 и R7 представляет собой Н;
А1 представляет собой D-Ala или Glu;
А2 представляет собой His;
А3 представляет собой D-Phe;
А4 представляет собой Arg;
А5 представляет собой Trp;
r независимо от своего положения является 1, 2, 3, 4 или 5; и
t независимо от своего положения является 1 или 2; или
его фармацевтически приемлемая соль.
4. Аналог меланокортина, который представляет собой соединение:
цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(hCys-D-Ala))-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Cys-D-Ala))-His-D-2-Nal-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(hCys-D-Ala))-His-D-2-Nal-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Orn]-NH2;
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Dab]-NH2;
цикло[Гидантоин(C(O)-(Asp-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH2;
цикло[Гидантоин(C(O)-(Asp-His))-D-2-Nal-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-His))-D-Phe-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-A3c))-D-Phe-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-A5c))-D-Phe-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-A6c))-D-Phe-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-A3c))-D-2-Nal-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-A5c))-D-2-Nal-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(С(O)-(Asp-A6c))-D-2-Nal-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-Aic))-D-Phe-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(С(O)-(Asp-Apc))-D-Phe-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-Aic))-D-2-Nal-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Asp-Apc))-D-2-Nal-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Lys]-NH2;
цикло[Гидантоин(С(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Orn]-NH2;
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Dab]-NH2;
цикло[Гидантоин(C(O)-(Glu-D-Ala))-His-D-Phe-Arg-Trp-Dap]-NH2;
цикло[Гидантоин(C(O)-(Glu-His))-D-Phe-Arg-Trp-Dap]-NH2;
цикло[Гидантоин(C(O)-(Glu-His))-D-Phe-Arg-Trp-Lys]-NH2;
Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Nle-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2;
Гидантоин(C(O)-(Gly-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Pen)-NH2;
Гидаптоин(C(O)-(Ala-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(С(O)-(D-Ala-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(С(O)-(Aib-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Val-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Ile-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Leu-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(О)-(Gly-Gly))-цикло(Cys-Glu-His-D-2-Nal-Arg-Trp-Cys)-NH2;
Гидантоин(C(О)-(Nle-Gly))-цикло(Cys-Glu-His-D-2-Nal-Arg-Trp-Cys)-NH2;
Гидантоин(C(О)-(D-Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(О)-(D-Arg-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(О)-(D-Arg-Gly))-цикло(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Arg-Gly))-цикло(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Ala-Nle))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Val-Nle))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-Nle))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(A6c-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Ala-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(D-Ala-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Val-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Leu-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Cha-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Aib-Nle))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-Glu-His-D-2-Nal-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-Arg))-цикло(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(О)-(Gly-D-Arg))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(О)-(Gly-D-Arg))-цикло(Gys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Gly-D-Arg))-цикло(Cys-D-Ala-His-D-2-Nal-Arg-Trp-Cys)-NH2;
Гидантоин(C(O)-(Nle-Ala))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2;
цикло[Гидантоин(C(O)-(Nle-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Ala-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(D-Ala-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Aib-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Val-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Abu-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-Leu-Cys))-D--Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Ile-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Cha-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(A6c-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Phe-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2;
цикло[Гидантоин(C(O)-(Gly-Cys))-D-Ala-His-D-Phe-Arg-Trp-Cys]-NH2 или
цикло[Гидантоин(C(O)-(Gly-Cys))-Glu-His-D-Phe-Arg-Trp-Cys]-NH2;
или его фармацевтически приемлемую соль.
5. Соединение формулы:
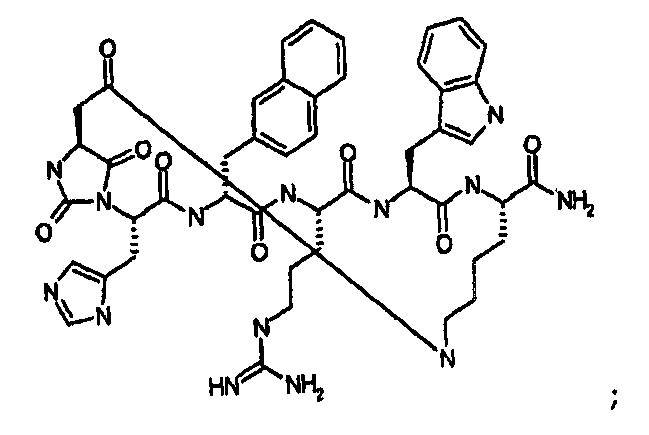
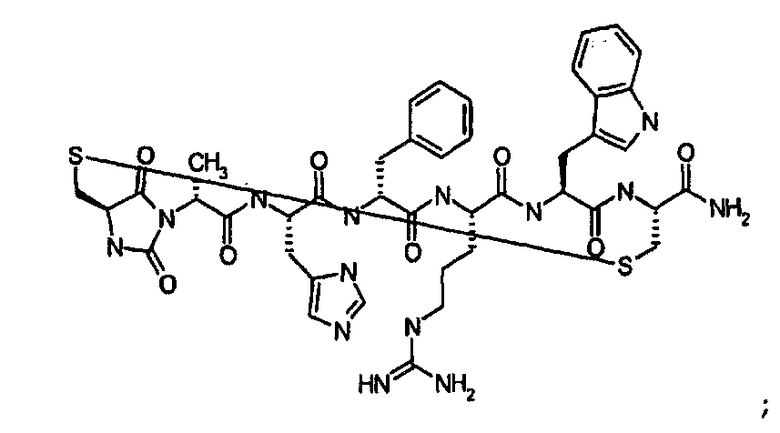
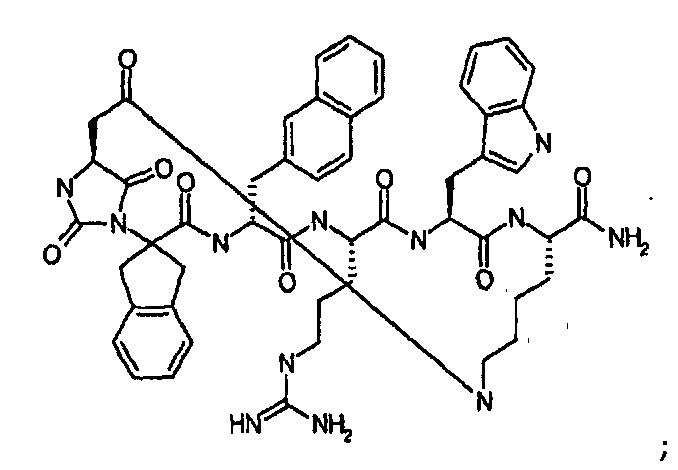
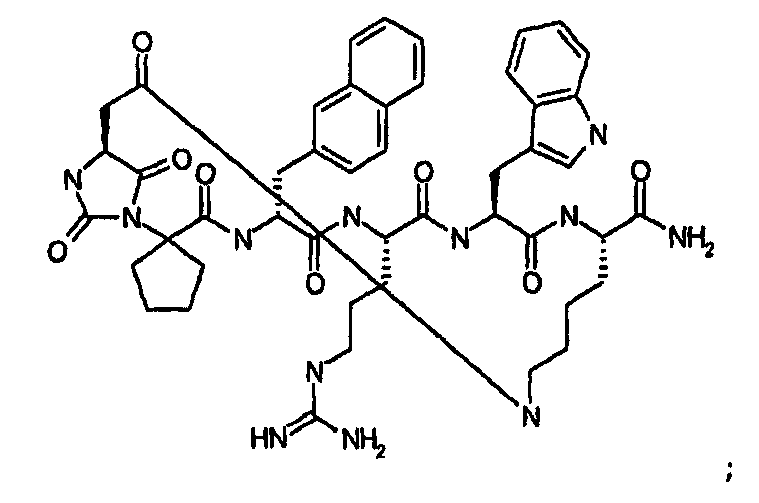
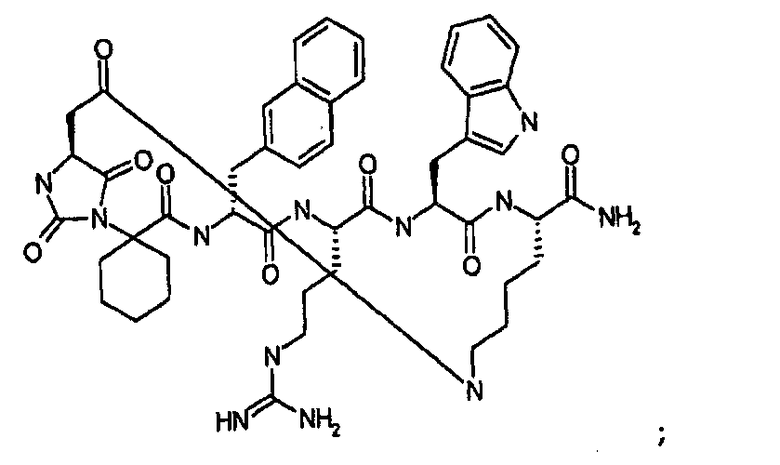
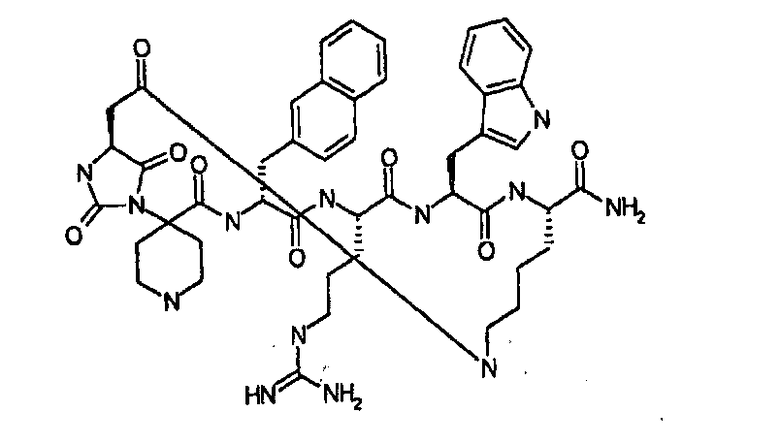
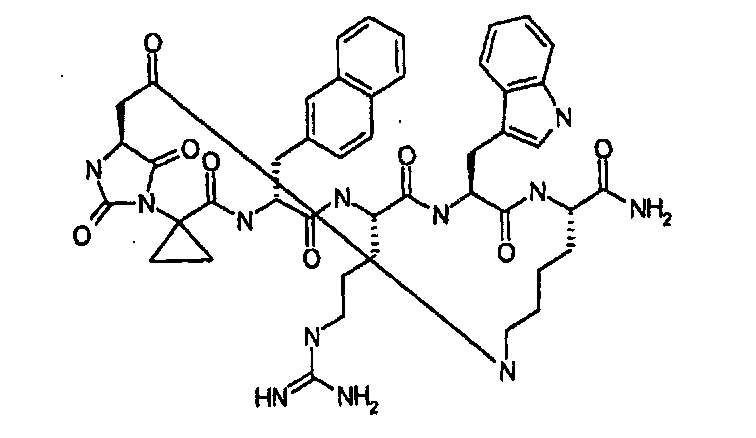
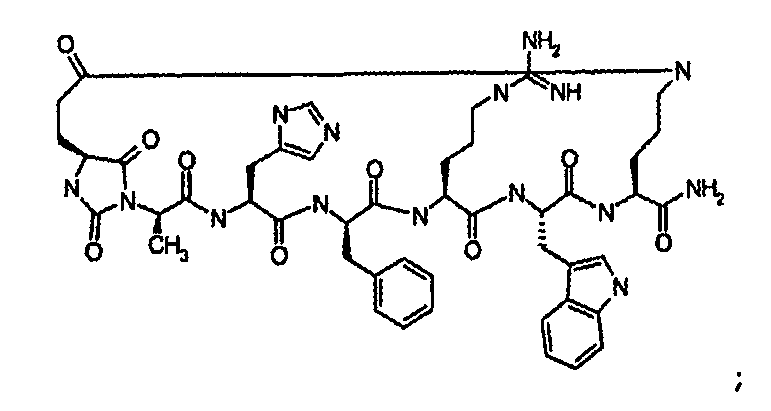
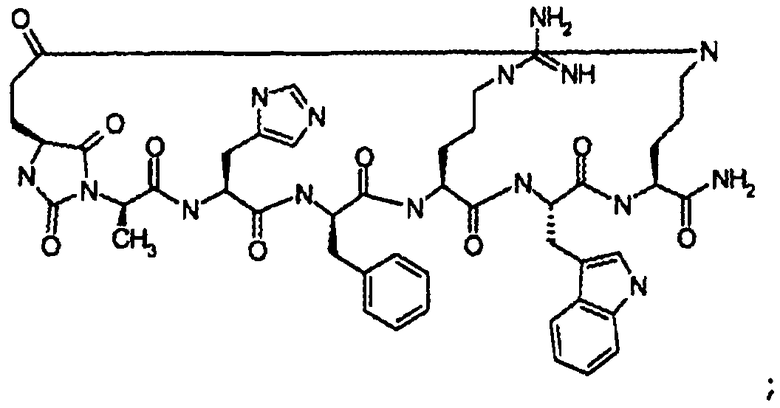
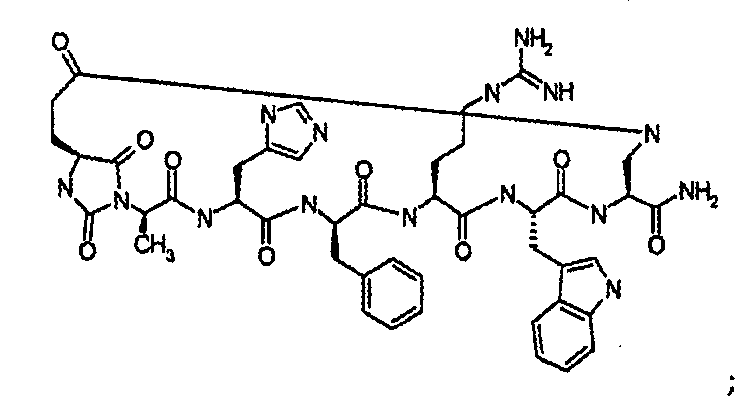

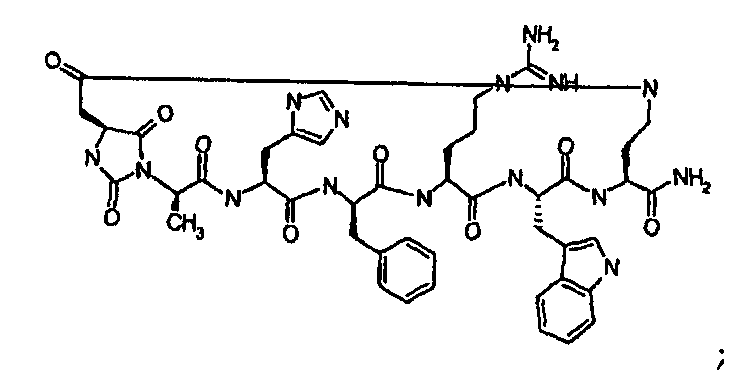
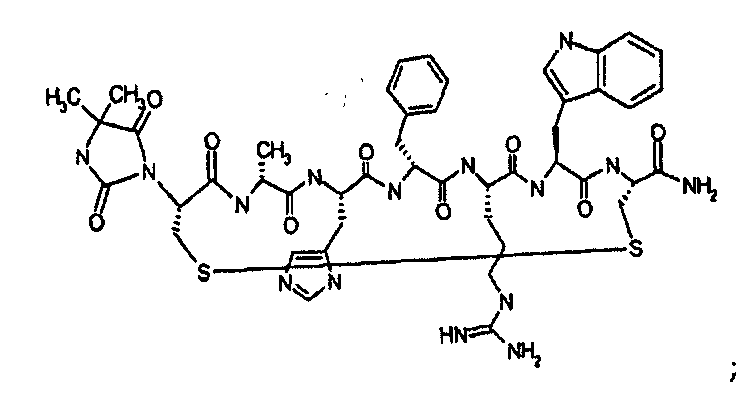
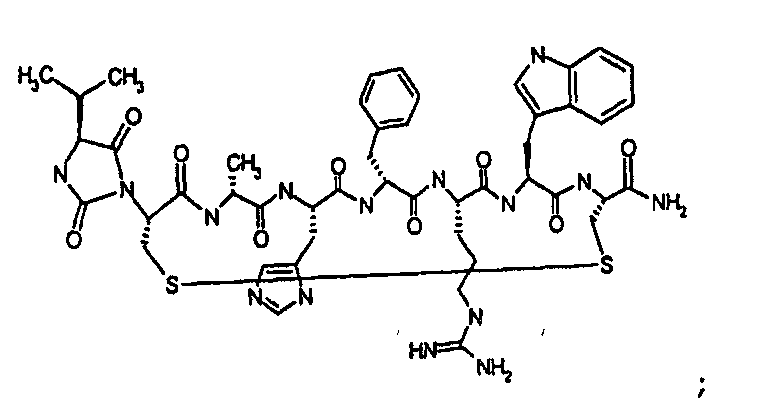
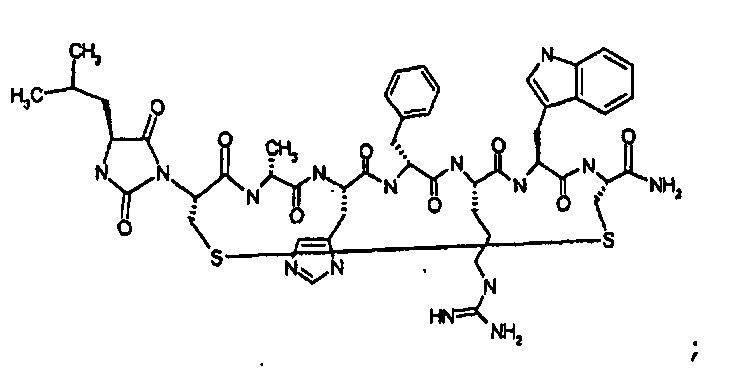
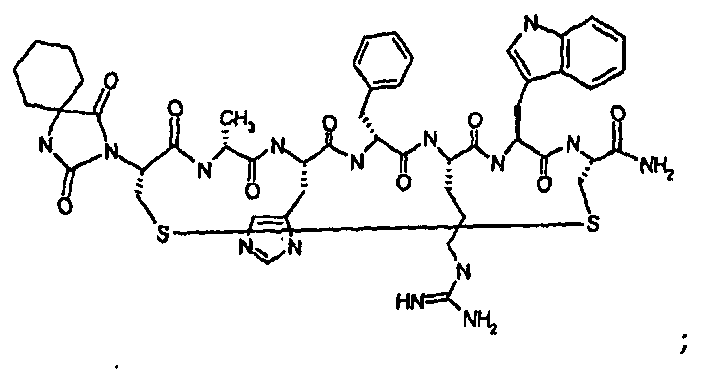 или
или
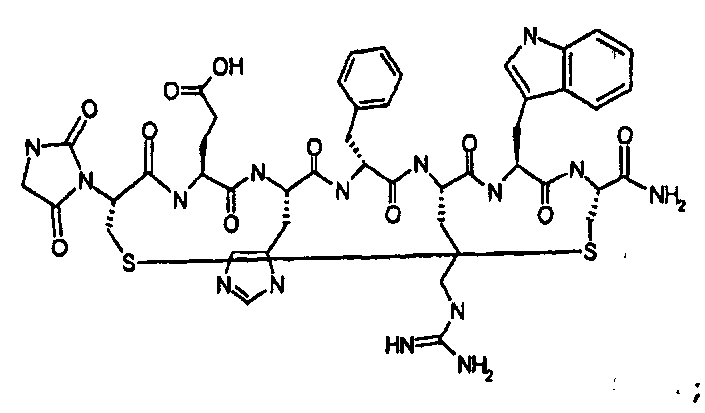
или его фармацевтически приемлемая соль.
6. Соединение по п.5, где указанным соединением является:
Гидантоин(С(O)-(Arg-Gly))-цикло(Cys-Glu-His-D-Phe-Arg-Trp-Cys)-NH2 или его фармацевтически приемлемая соль.
7. Фармацевтическая композиция, обладающая активностью агониста рецептора мелакортина-4, включающая терапевтически эффективное количество соединения по любому из пп.1-6 или его фармацевтически приемлемой соли, и фармацевтически приемлемый носитель или разбавитель.
8. Фармацевтическая композиция по п.7, где указанное соединение или его фармацевтически приемлемая соль является селективным агонистом рецептора меланокортина-4 с функциональной активностью, характеризуемой ЕС50, которая является, по меньшей мере, в 15 раз более селективной в отношении рецептора меланокортина-4 человека, чем в отношении рецептора меланокортина-1 человека, рецептора меланокортина-3 человека и рецептора меланокортина-5 человека.
9. Способ лечения ожирения или пищевого расстройства, снижения аппетита, снижения массы тела или снижения аппетита и массы тела, или лечения анорексии, булимии, СПИДа, истощения у ослабленных пожилых людей, кахексии или раковой кахексии посредством индукции агонистического или антагонистического эффекта меланокортинового рецептора путем взаимодействия указанного рецептора с соединением по пп.1-6 или его фармацевтически приемлемой солью, или с композицией по п.7 или 8.
10. Применение терапевтически эффективного количества агониста или антагониста рецептора меланокортина-4 по любому из пп.1-6 или его фармацевтически приемлемой соли для изготовления лекарственного средства, применяемого при лечении заболевания или патологического состояния, выбранного из группы, состоящей из:
генерализованного воспаления, воспалительной болезни кишечника, воспаления мозга, сепсиса и септического шока;
ревматоидного артрита, подагрического артрита и рассеянного склероза;
метаболического заболевания или патологического состояния, сопровождаемого увеличением веса, ожирения, пищевых расстройств и синдрома Прадера-Вилли;
метаболического заболевания или патологического состояния, сопровождаемого потерей веса, анорексии, булимии, истощения при СПИДе, кахексии, раковой кахексии и истощения у ослабленных пожилых людей;
рака кожи и раковой кахексии;
эндометриоза, маточного кровотечения, половой дисфункции, эректильной дисфункции и пониженного полового влечения у женщин;
отторжения трансплантата, ишемии и реперфузионного повреждения, ранения и повреждения спинного мозга, а также потери веса в результате медицинской процедуры, выбранной из группы, состоящей из химиотерапии, лучевой терапии, временной или постоянной иммобилизации и диализа;
геморрагического шока, кардиогенного шока, гиповолемического шока, сердечно-сосудистых заболеваний и сердечной кахексии; острого респираторного дистресс-синдрома, фиброза легких, хронической обструктивной болезни легких и астмы;
повышенной иммунной толерантности;
аллергии;
псориаза, сниженной пигментации кожи, акне и келойдного образования; тревожного расстройства, депрессии, нарушения памяти и нейропатической боли и
почечной кахексии и натрийуреза.
11. Применение по п.10, где указанное лекарственное средство снижает аппетит, снижает массу тела или снижает аппетит и снижает массу тела.
12. Применение терапевтически эффективного количества агониста или антагониста рецептора меланокортина-4 по любому из пп.1-6 или его фармацевтически приемлемой соли для изготовления лекарственного средства, применяемого при модуляции веса яичников, развития плаценты, секреции пролактина, секреции ФСГ, внутриматочного развития эмбриона, родов, сперматогенеза, секреции тироксина, синтеза и секреции альдостерона, температуры тела, кровяного давления, частоты сердечных сокращений, сосудистого тонуса, мозгового кровообращения, уровня глюкозы в крови, секреции кожного сала, секреции феромонов, мотивации, обучения и поведения, восприятия боли, нейропротекции, роста нервов, метаболизма кости, формирования костной ткани и развития кости.
13. Применение терапевтически эффективного количества агониста или антагониста рецептора меланокортина-4 по любому из пп.1-6 или его фармацевтически приемлемой соли для изготовления лекарственного средства, применяемого для предотвращения потребления алкоголя, снижения потребления алкоголя, лечения алкоголизма или лечения алкогольной зависимости.
| СЕЛЕКТИВНЫЕ ЦИКЛОПЕПТИДЫ | 2001 |
|
RU2239642C1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
Авторы
Даты
2012-05-10—Публикация
2008-05-23—Подача