Первые заявки
Настоящая заявка испрашивает приоритет по заявке США №60/615764, поданной 4 октября 2004 и заявке США №60/698357, поданной 11 июля 2005, обе из которых включены в настоящую заявку в качестве ссылки.
Предпосылки создания изобретения
Область изобретения
Настоящее изобретение касается композиций и способов доставки биологически активных агентов в клетки. Предпочтительно изобретение относится к катионным липополимерам, включающим полиэтиленимин (PEI), биодеградируемую группу и относительно гидрофобную группу, и к способам использования таких липополимеров для доставки биологически активных агентов, таких как ДНК, РНК, олигонуклеотитды, белки, пептиды и медикаменты.
Описание уровня техники
Известно множество методов доставки биологически активных агентов в клетки, включая использование вирусных трансфецирующих систем и невирусных трансфецирующих систем. Вирусные системы в основном обладают более высокой эффективностью трансфекции, чем не вирусные системы, но возникают вопросы относительно безопасности вирусных систем. См. Verma LM и Somia N., Nature 389 (1997), стр 239-242; Marhsall E. Science 286 (2000), стр 2244-2245. Кроме того, приготовление вирусного векторного препарата имеет тенденцию быть сложным и дорогим процессом. Хотя не вирусные трансфецирующие системы вообще менее эффективны, чем вирусные системы, на них обращается большое внимание, потому что они, как полагают, являются более безопасными и проще в приготовлении, чем вирусные системы.
Множество невирусных трансфецирующих систем включает использование катионных полимеров, которые представляют собой комплексы с биологически активными агентами. Примеры катионных полимеров, которые использовались как генные носители, включают поли (L-лизин) (PLL), полиэтиленимин (PEI), хитозан, РАМАМ дендримеры и поли (2-димети-ламино)этилметакрилат (pDMAEMA). К сожалению, эффективность трансфекции с PLL обычно незначительна и высоко молекулярный PLL показал существенную токсичность по отношению к клетке. В некоторых случаях PEI обеспечивает эффективную генную трансфекцию без необходимости в эндосомолитических или нацеливающих агентах. См. Boussif О., Lezoualc'h F., Zanta M.A., Mergny M.D., Scherman D., Demeneix В., Behr J.P., Proc Natl Acad Sci USA, Aug.1, 1995, 92 (16) 7297-301. В качества систем для доставки гена были изучены различные полиамидоаминные дендримеры. См. Eichman J.D., Bielinska A.U., Kukowska-Latallo J.F., Baker J.R., Pharm. Sci. Technol. Today 2000 July; 3(7): 232-245. К сожалению, как PEI, так и дендримеры, как сообщается, оказались токсичными для клеток, ограничивая тем самым потенциальное использование PEI как инструмента для доставки гена в применении к человеку. Кроме того, стоимость полиамидоаминных дендримеров, пригодных для генной трансфекции на практическом уровне, относительно высока.
Сообщалось о генных носителях, изготовленных с деградируемыми катионными полимерами для доставки гена в клетки млекопитающих с пониженной цитотоксичностью. См. Lim Y.В., Kim S.M., Lee Y., Lee W.К., Yang Т.О., Lee M.J., Suh H., Park J.S., J. Chem. Soc, 123 (10), 2460-2461, 2001. К сожалению, эти деградируемые системы также показали более низкую эффективность переноса гена по сравнению с не деградируемыми полимерами. Чтобы улучшить трансфеционную эффективность низко молекулярного PEI Gosselin и др. сообщил, о возможности получения высоко молекулярного PEI, используя дисульфидсодержащие линкеры. См. Gosselin, Micheal A., Guo, Menjin, и Lee, Robert J. Bioconjugate Chem. 2001. 12: 232-245. PEI полимеры, полученные с использованием дитиобис(сукцинимидилпропионата) (DSP) и диметил-3,3'-дитиобиспропионимидата-2НСl (DTBP), показали сопоставимую эффективность генной трансфекции и более низкую цитотоксичность. Однако, дисульфидсодержащие линкеры дороги, что делает получение этой системы в крупном масштабе трудным и нежелательным. Полимеры, содержащие дисульфидные линкеры, деградируют только в условиях восстановления, что ограничивает применение этих полимеров в других условиях.
Lynn и другие описали способ синтеза биодеградируемых катионных полимеров, используя диакрилаты как линкерные молекулы между катионными соединениями. См. Lynn, David A.; Anderson, Daniel G.; Putnam, David; и Langer, Robert. J. Am. Chem. Soc. 2001, 123, 8155-8156. Однако, полученные полимеры не образуют хороших комплексов со многими биологически активными агентами. Синтез этих полимеров требует нескольких дней, а количество полезного продукта, который может использоваться для доставки гена, невелико. Согласно способам Lynn и др. было получено более ста катионных полимеров, но только два из этих полимеров показали действительную эффективность для генной трансфекции. Эти факторы делают получение высокомолекулярных полимеров этим методом трудно достижимым.
Таким образом, остается потребностью в катионных полимерах, которые могут безопасно и эффективно облегчать доставку биологически активных агентов к клеткам.
Краткое изложение сущности изобретения
В одном воплощении изобретения описывается полимер, включающий повторяющееся звено, выбранное из группы, состоящей из формулы (Iа) и формулы (Ib):

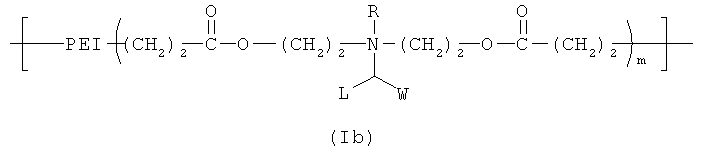
где РЕI означает полиэтилениминное повторяющееся звено; R выбирают из группы, состоящей из электронной пары, водорода, С2-С10 алкила, C2-С10 гетероалкила, С5-С30 арила, и С2-С30 гетероарила; L выбирают из группы, состоящей из С2-С50 алкила, С2-C50 гетероалкила, С2-C50 алкенила, С2-С50 гетероалкенила, С2-С50 арила; С2-C50 гетероарила; C2-C50 алкинила, С2-C50 гетероалкинила, C5-C50 арила; C2-C50 гетероарила; С2-С50 карбоксиалкенила и С2-C50 карбоксигетероалкенила; W - представляет собой катионную часть, включающую от приблизительно 2 до приблизительно 50 атомов углерода; и m представляет собой целое число в диапазоне приблизительно от 1 до приблизительно 30.
Повторяющееся звено, выбранное из группы, состоящей из формулы (Iа) и формулы (Ib), может упоминаться здесь как повторяющееся звено формулы (I). Таким образом, например, полимер, включающий повторяющееся звено, выбранное из группы, состоящей из формулы (Iа) и формулы (Ib), может упоминаться здесь как полимер, включающий повторяющееся звено формулы (I) или как полимер формулы (I). Полимер, включающий повторяющееся звено формулы (I) может упоминаться здесь как катионный липополимер.
В предпочтительных воплощениях изобретения PEI в формулах (Iа) и (Ib) представлен повторяющимся звеном формулы (II)

где х - целое число в диапазоне приблизительно от 1 до приблизительно 100, и y - целое число в диапазоне приблизительно от 1 до приблизительно 100. Для специалиста в данной области очевидно, что атом азота в повторяющемся звене формулы (I) может нести катионный заряд и таким образом может образовывать ионную связь с различными отрицательно заряженными остатками, например, с анионами, такими как хлорид, бромид, йодид, сульфат и т.д. Можно получить и хранить до использования многочисленные полимеры формулы (I), и таким образом другое воплощение изобретения касается библиотеки полимеров, включающей множество полимеров, каждый из которых индивидуально включает повторяющееся звено формулы (I), где по крайней мере один параметр, выбранный из группы, состоящей из R, L, PEI, W и m, различен по крайней мере у двух из полимеров.
В другом воплощении изобретения полимер, включающий повторяющееся звено формулы (I), дополнительно включает биомолекулу, которая образует комплекс с полимером. Биомолекула может иметь одну или больше анионных групп и может образовывать ионную связь с повторяющимся звеном формулы (I). Примеры биомолекул, имеющих одну или более анионных групп, включают нуклеиновые кислоты (например, ДНК, однонитевая РНК, двунитевая РНК, рибозим, ДНК-РНК гибридизатор, siPHK, антисмысловая ДНК и антисмысловой олигонукотитд), белки, пептиды, липиды и углеводы.
В другом воплощении изобретения полимер, включающий повторяющееся звено формулы (I), дополнительно включает биомолекулу, усиливающий доставку агент, способный внедряться в эукариотическую клетку, и/или диагностическую визуализирующую композицию, которая образует комплекс с полимером. Усиливающий доставку агент может облегчать одну или более функций в эукариотической клетке, например, рецепторное распознавание, интернализация, переход биомолекулы из эндосомы клетки, ядерной локализации, высвобождение биомолекулы и система стабилизации.
Полимер, включающий повторяющееся звено формулы (I), который дополнительно включает биомолекулу и который может дополнительно включать усиливающий доставку агент, способный внедряться в эукариотическую клетку, и/или диагностическую визуализирующую композицию, которая образует комплекс с полимером, полезен для трансфекции эукариотических клеток. Таким образом, другое воплощение изобретения касается способа трансфекции эукариотических клеток, включающего контактирование клетки с таким полимером (включающим повторяющееся звено формулы (I) и биомолекулу, необязательно дополнительно включающим усиливающий доставку агент и/или диагностическую визуализирующую композицию), чтобы таким образом доставить биомолекулу в клетку. Способ может включать лечение млекопитающего, включающее идентификацию млекопитающего, нуждающегося в генной терапии, и введение такого полимера млекопитающему. В предпочтительном воплощении изобретения биомолекула - представляет собой siPHK, где siPHK эффективна для снижения экспрессии интересующего гена.
Другое воплощение изобретения касается медицинской диагностической системы, включающей лиганд, который распознает специфический рецептор эукариотической клетки, и полимер, где полимер включает повторяющееся звено формулы (I) и биомолекулу и дополнительно может включать усиливающий доставку агент, способный внедряться в эукариотическую клетку, и/или диагностическую визуализирующую композицию, которая образует комплекс с полимером.
Другое воплощение изобретения касается фармацевтической композиции, включающей: сенсибилизирующий агент и полимер, где полимер включает повторяющееся звено формулы (I) и биомолекулу и дополнительно может включать усиливающий доставку агент, способный внедряться в эукариотическую клетку, и/или диагностическую визуализирующую композицию, которая образует комплекс с полимером. Сенсибилизирующий агент может представлять собой соединение, которое меняет свойства при выдержке на свету или под действием других стимулирующих факторов, и таким образом облегчает доставку биомолекулы (например, увеличивая скорость разложения полимера). Сенсибилизирующий агент сам может быть биомолекулой, которая меняет активность под действием стимулирующих факторов.
Более детально эти и другие воплощения изобретения описаны ниже.
Краткое описание чертежей
Фиг.1 иллюстрирует типичные GFP сигналы в клетках 293 после трансфекции липополимерами (5А, 5В и 5С) и липофектамином 2000.
Фиг.2 иллюстрирует типичные GFP сигналы в клетках 208 F после трансфекции липополимерами (5А, 5В и 5С) и липофектамином 2000.
Фиг.3 показывает диаграмму относительного уровня флуоресценции клеток 208 F и 293 после трансфекции липополимерами (5А, 5В и 5С) и липофектамином 2000 ("липо"),
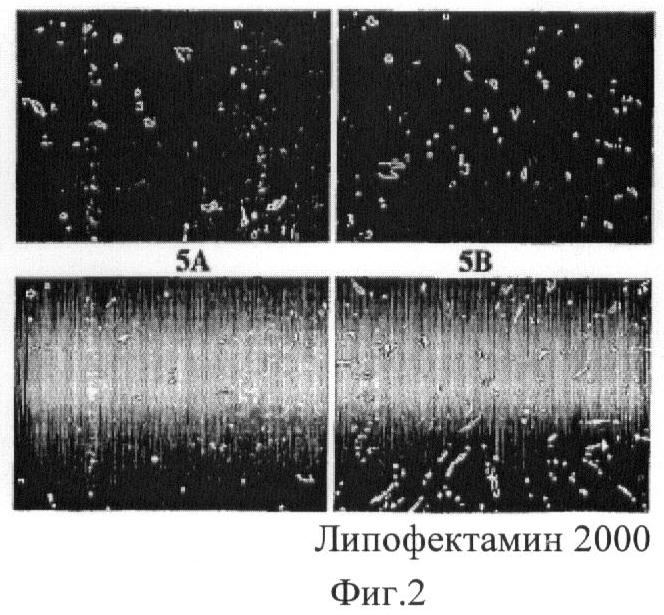
Фиг.4 иллюстрирует типичные GFP сигналы в клетках HT-GFP после доставки siPHK липополимерами (5А, 5В и 5С) и липофектамином 2000.
Фиг.5 иллюстрирует типичный GFP сигнал в клетках HeLa-GFP после доставки siPHK липополимерами (5А, 5В и 5С) и липофектамином 2000.
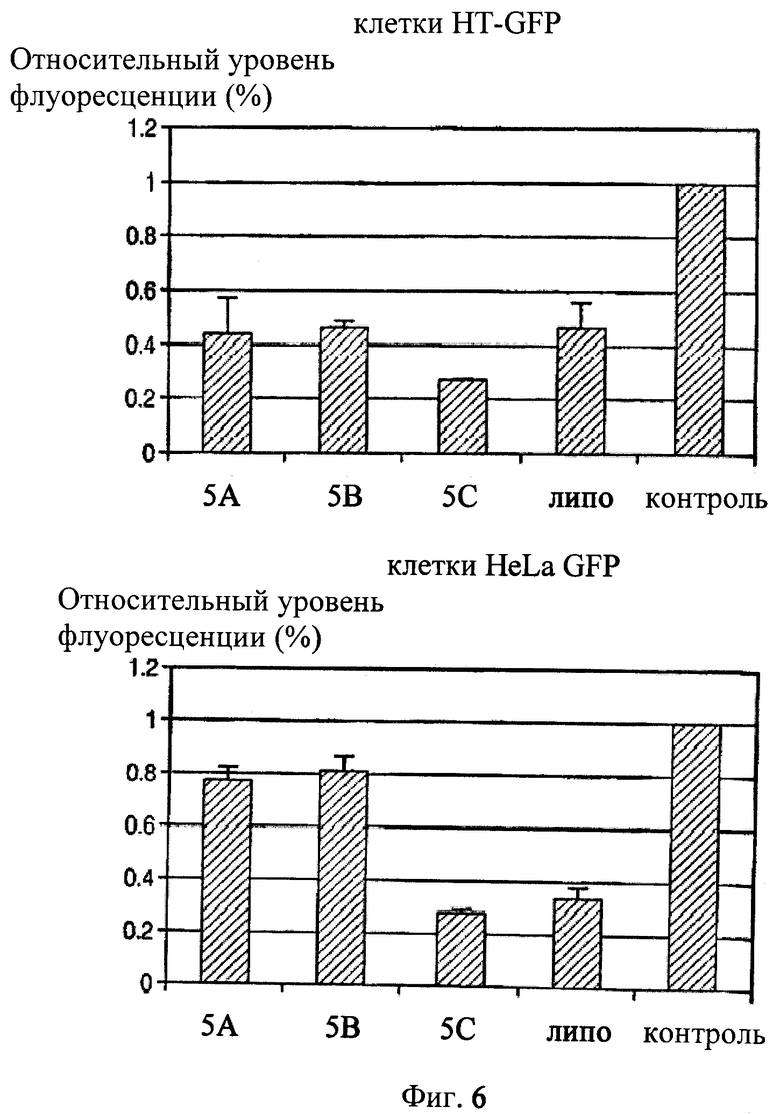
Фиг.6 показывает диаграммы относительного уровня флуоресценции клеток HT-GFP и HeLa GFP после доставки siPHK липополимерами (5А, 5В и 5С) и липофектамином 2000 («липо»).
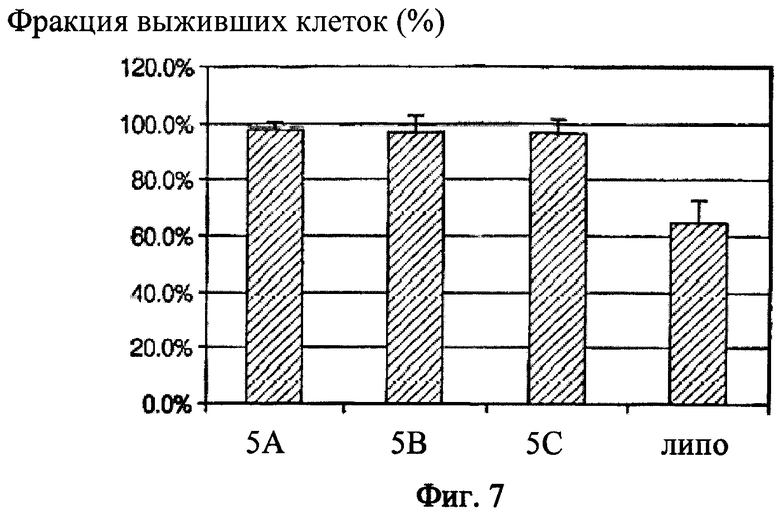
Фиг.7 показывает диаграмму фракцию выживаемости клеток после доставки siPHK липополимерами (5А, 5В и 5С) и липофектамином 2000 («липо»).
Фиг.8 показывает диаграмму относительного уровня флуоресценции гена HT-GFP после доставки различной siPHK катионными липопорлимерами (5А, 5В и 5С).
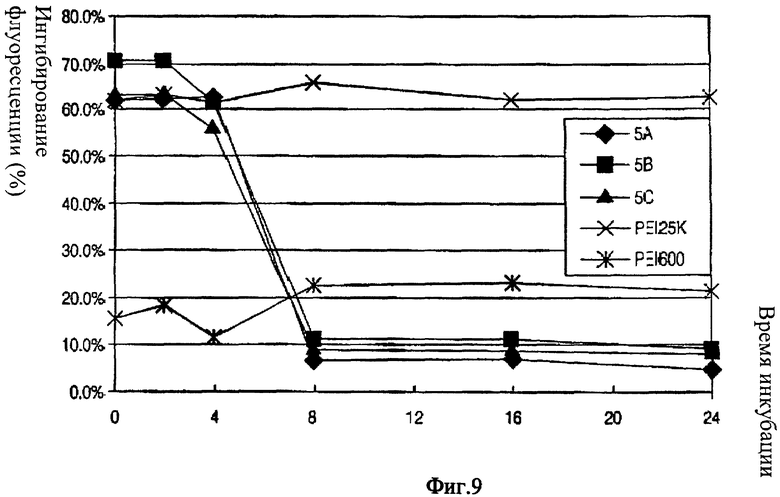
Фиг.9 показывает диаграмму относительных единиц флуоресценции комплексов антисмысловые олигонуклеотиды/липополимеры по сравнению с раствором свободных олигонуклетидов.
Фиг.10 иллюстрирует результаты гель электрофореза связывания полимера 6 с ДНК.
Фиг.11 иллюстрирует типичные GFP сигналы клеток 293 после трансфекции с помощью 7А и липофектамина 2000.
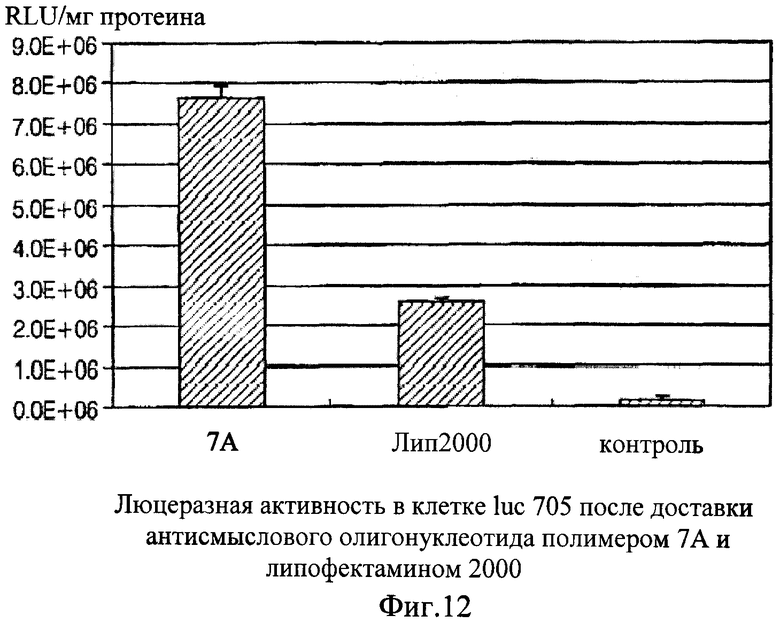
Фиг.12 показывает диаграмму люциферазной активности в luc 705-клетке после доставки антисмыслового олигонуклеотида полимером 7А и липофектамином 2000.
Фиг.13 показывает диаграмму люциферазной активности в СНО-АА8 luc после доставки siPHK, опосредованной полимером 7А и липофектамином 2000.
Фиг.14 показывает диаграмму, иллюстрирующую фракцию выживаемости клеток после трансфекции с использованием 7А и липофектамина.
Фиг.15 показывает диаграмму GFP трансфецирующей эффективности 7А после инкубации в opti MEM в течение различных периодов времени.
Детальное описание изобретения
В соответствии с изобретением описываются катионные липополимеры, включающие полиэтилениминную биодеградируемую группу и относительно гидрофобную "липо" группу. Предпочтительно катионные липополимеры включают повторяющееся звено, выбранное из группы, состоящей из формулы (Iа) и формулы (Ib):


Используемый здесь термин "формула (I)" относится как к формуле (Iа), так и к формуле (Ib). В формуле (I) PEI означает полиэтиленимин (например, полимер, включающий повторяющиеся звенья, представленные указанной выше формулой (II), эфирные линкеры представляют собой биодеградируемые группы, L представляет относительно гидрофобную "липо" группу и m находится в диапазоне приблизительно от 1 до приблизительно 30. Например, в некоторых воплощениях изобретения L выбирают из группы, состоящей из С2-С10 алкила, С2-С10 гетероалкила, C2-C50 алкенила, С2-С50 гетероалкенила, C5-C50 арила; C2-C50 гетероарила; С2-С50 алкинила, C2-C50 гетероалкинила, C2-C50 арила; С2-С50 гетероарила; С2-C50 карбоксиалкенила и С2-C50 карбоксигетероалкенила. В предпочтительных воплощениях изобретения L выбирают из группы, состоящей из С12-C18 жирных кислот, холестерина и их производных. R в формуле (I) может представлять электронную пару или атом водорода.
Специалисту в данной области очевидно, что, когда R представляет электронную пару, повторяющееся звено в формуле (I) представляет собой катион при низком рН. R в формуле (I) может также представлять относительно гидрофобную липо группу, такую как С2-С10 алкил, C2-С10 гетероалкил, С5-С30 арил или С2-С30 гетероарил, в этих случаях атом азота несет катионный заряд, в основном при широком диапазоне рН.
Катионные липополимеры, включающие повторяющееся звено формулы (I), могут быть получены реакцией диакрилатного мономера формулы (III) с полиэтиленимином (РЕ1), как показано на Схеме А ниже:
Схема А

В формуле (III) R и L имеют те же значения, которые описаны выше для катионного липополимера, включающего повторяющееся звено формулы (I). Схема А иллюстрирует получение полимера, включающего повторяющееся звено формулы (Iа). Имеется ввиду, что полимер, включающий повторяющееся звено формулы (Ib), может быть получен аналогичным способом из соответствующего диакрилатного мономера, содержащего группу W. PEI предпочтительно содержит повторяющиеся звенья формулы (II), в которой x является целым числом в диапазоне приблизительно от 1 до приблизительно 100, и y представляет целое число в диапазоне приблизительно от 1 до приблизительно 100.

Приведенная в Схеме А реакция может осуществляться смешиванием PEI и диакрилата (III) во взаимном растворителе, таком как этанол, при перемешивании, предпочтительно при комнатной температуре в течение нескольких часов с последующим упариванием растворителя с выделением полученного полимера. Настоящее изобретение не связано с теорией, но полагают, что реакция между PEI и диакрилатом (III) включает реакцию Михаэльса между одной или более аминогруппами PEI и двойными связями диакрилата. См. J.March, Advanced Organic Chemistry 3rd Ed., стр 711-712 (1985). Приведенный в Схеме А диакрилат может быть получен в соответствии с приведенными ниже примерами.
Широкое разнообразие полимеров, включающих повторяющееся звено формулы (I), может быть получено в соответствии со Схемой А, изменяя молекулярный вес и структуру PEI, размер и тип R, W и L групп диакрилата (III) и соотношении диакрилата (III) к PEI. Могут использоваться смеси различных диакрилатов и/или смеси различных PEI. PEI может быть многофункциональным и таким образом может быть способен к реакции с двумя или более диакрилатами. Для получения поперечно-сшитых катионных липополимеров можно использовать сшивающие агенты, и/или регулировать соотношения многофункционального PEI и диакрилата (III). Молекулярный вес PEI находится предпочтительно в диапазоне приблизительно от 600 до приблизительно 25000 дальтон. Молярное соотношение PEI к диакрилату находится предпочтительно в диапазоне приблизительно от 1:2 до приблизительно 1:20. Средневесовой молекулярный вес катионного липополимера может быть в диапазоне приблизительно от 500 дальтон до приблизительно 1000000 дальтон, предпочтительно в диапазоне приблизительно от 2000 дальтон до приблизительно 200000 дальтон. Молекулярный вес может быть определен с помощью гель-хроматографии с использованием PEG стандартов или электрофорезом на агарозном геле. В другом воплощении изобретения описывается библиотека полимеров, обеспечивающая получение множества катионных липополимеров, в которых R, L, W, PEI и/или m различны по крайней мере у двух из полимеров.
Катионный липополимер предпочтительно является деградируемым, более предпочтительно биодеградируемым, например, механизмом деградации, выбранным из группы, состоящей из гидролиза, ферментативного расщепления, восстановления, фоторасщепления и ультразвукового расщепления. Настоящее изобретение не ограничивается в соответствии с теорией, но полагают, что деградация катионного липополимера формулы (I) внутри клетки происходит за счет ферментативного расщепления и/или гидролиза эфирных линкеров.
Катионные липополимеры могут образовывать комплексы с биомолекулами и таким образом являются полезными в качестве носителей для доставки биомолекул в клетки. Примеры биомолекул, которые образуют комплексы с катионными липополимерами формулы (I), включают нуклеиновые кислоты, белки, пептиды, липиды и углеводы. Примеры нуклеиновых кислот включают ДНК, однонитевую РНК, двунитевую РНК, рибозим, ДНК-РНК гибридизатор и антисмысловую ДНК, например, антисмысловой олигонуклеотид. Предпочтительной нуклеиновой кислотой является siPHK. Катионные липополимеры, которые включают биомолекулу, которая образует комплекс с полимером, могут быть получены смешиванием катионных липополимеров и биомолекул во взаимном растворителе, преимущественно методами, описанными ниже в примерах.
Катионные липополимеры, которые включают биомолекулу, которая образует комплекс с полимером, могут далее включать усиливающий доставку агент, способный внедряться в эукариотическую клетку. Усиливающий доставку агент может быть растворен или смешан с комплексом или может быть соединен (например, ковалентно или комплексно) с катионным липополимероа. Усиливающие доставку агенты представляют собой вещества, которые облегчают транспорт биомолекулы в клетку, обычно увеличивая транспортировку комплекса биомолекула/носитель сквозь мембрану, снижая деградацию в течение транспортировки и/или облегчая высвобождение биомолекулы из носителя. Транспортировка биомолекулы, такой как ген, в клетку предпочтительно включает высвобождение биомолекулы из носителя после того, как комплекс биомолекула/носитель пересек клеточную мембрану, мембрану эндосомы мембрану и ядерную мембрану. Например, в случае нуклеиновой кислоты, комплекс нуклеиновая кислота/носитель сначала проходит сквозь клеточную мембрану. После завершения этого с помощью эндоцитоза происходит интернализация комплекса нуклеиновая кислота/носитель. Носитель вместе с грузом нуклеиновой кислоты обволакивается клеточной мембраной с образованием кармана, и карман впоследствии защемляется. Результатом этого является клеточная эндосома, представляющая собой большую мембранно-связанную структуру, охватывающую груз нуклеиновой кислоты и носитель. Затем комплекс нуклеиновая кислота-носитель проникает через эндосомальную мембрану в цитоплазму, избегая ферментативной деградации в цитоплазме, и пересекает ядерную мембрану. В ядре груз нуклеиновой кислоты отделяется от носителя.
В основном усиливающие доставку агенты делятся на две категории: вирусные системы доставки и невирусные системы доставки. Поскольку человеческие вирусы развили обсужденные выше пути преодоления барьеров для транспорта в ядро, вирусы или вирусные компоненты полезны для транспортировки нуклеиновых кислот в клетки. Примером вирусного компонента, полезного в качестве усилителя доставки, является пептид гемагглютинин (НА-пептид). Этот вирусный пептид облегчает транспортировку биомолекул в клетки за счет разрушения эндосомы. При кислом рН эндосомы этот белок вызывает высвобождение биомолекулы и носителя в цитозоль. Квалифицированным специалистам в данной области известны другие примеры полезных в качестве усилителей доставки вирусных компонентов.
Невирусными усилителями доставки обычно являются усилители доставки на основе полимера или на основе липида. Главным образом они являются поликатионными для того, чтобы сбалансировать отрицательный заряд нуклеиновой кислоты. Поликатионные полимеры показали себя перспективными не вирусными усилителями доставки гена частично благодаря их способности конденсировать ДНК плазмид до неограниченного размера и безопасности по отношению к вирусным векторам. Примеры включают пептиды с участками, богатыми основными аминокислотами типа олиго-лизина, олиго-аргинина или их комбинации и PEI. Как полагают, эти поликатионные полимеры облегчают транспортировку за счет конденсации ДНК. Варианты поликатионов с разветвленной цепью, такие как PEI и звездчатые дендримеры, могут способствовать как конденсации ДНК, так и эндосомальному высвобождению. См. Boussif et al. (1995) Proc. Natl. Acad. Sci. USA vol.92: 7297-7301. PEI может быть получен в виде сильно разветвленного полимера с концевыми аминогруппами, которые ионизируются при рН 6,9, и внутренними аминогруппами, которые ионизируются при рН 3,9. Благодаря такой организации PEI может вызывать изменение рН в везикуле, что ведет к раздуванию везикулы и, в конечном счете, высвобождению из эндосомального защемления.
Другой способ усиления доставки заключается во включении в катионный липополимер лиганда, который распознается рецептором на клетке, которая является мишенью доставки биомолекулярного груза. Тогда доставка биомолекулы в клетку может инициироваться за счет рецепторного распознавания. В этом контексте термин "лиганд" относится к биомолекуле, которая может связываться с определенным белком рецептора, расположенного на поверхности клетки-мишени или в ее ядре или в цитозоле. В воплощении изобретения лиганд может представлять собой антитело, гормон, феромон или нейромедиатор, или любую биомолеку, способную действовать подобно лиганду, который связывается с рецептором. Антитело представляет собой любой белок, продуцированный В лимфоцитом в ответ на антиген. Когда лиганд связывается со специфическим клеточным рецептором, стимулируется эндоцитоз. Примерами лигандов, которые используются с различными типами клеток для усиления транспортировки биомолекулы, являются галактоза, трансферрин, гликопротеин, волокнистый аденовирус, эпидермальный фактор роста, капсид вируса папилломы человека, фибробластовый фактор роста и фолиевая кислота. В случае фолатного рецептора связанный лиганд интернализуется благодаря фотоцитозу, когда рецептор связывает лиганд, окружающая мембрана закрывает от поверхности клетки и интернализованный материал проходит через везикулярную мембрану в цитоплазму. См. Gottschallc et al. (1994) Gene Ther 1: 185-191.
Различные усиливающие доставку агенты, как полагают, функционируют благодаря разрушению эндосомы. Например, в дополнение к описанному выше НА-белку дефектно-вирусные частицы также использовались как эндосомолитические агенты. См. Gotten et al. (July 1992) Proc. Natl. Acad. Sci. USA vol.89: pages 6094-6098. Невирусные агенты обычно являются или амфифильными, или на основе липидов.
Высвобождение биомолекул типа ДНК в цитоплазму клетки может усиливаться агентами, которые опосредуют эндосомальное разрушение, снижают деградацию или обходят этот процесс. Хлорохин, который увеличивает рН эндосомы, использовался для снижения деградации эндоцитозного материала, ингибируя лизосомальные гидролитические ферменты. См. Wagner et al. (1990) Proc. Natl. Acad. Sci. USA vol.87: 3410-3414. Поликатионы с разветвленной цепью типа PEI и звездчатые дендримеры также промотируют эндосомальное высвобождение, как указано выше.
Эндосомальную деградацию можно обойти, введением подзвеньев токсинов, таких как токсин Diptheria и экзотоксин Pseudomonas, в качестве компоненты рекомбинантных белков, которые могут быть введены в комплекс катионный липополимер /биомолекула. См. Uherek et al. (1998) J Biol. Chem. vol.273: 8835-8841. Эти компоненты промотируют челночное движение нуклеиновой кислоты через эндосомальную мембрану и назад через эндоплазматическую сеть.
В цитоплазме транспортировка биомолекулярного груза к ядру может быть усилена введением в нуклеиновую кислоту-носитель локализованного на ядре сигнала. Например, может использоваться определенная аминокислотная последовательность, которая функционирует как сигнал ядерной локализации (NLS). Полагают, что NLS на комплексе биомолекула/носитель взаимодействует с определенным ядерным транспортным белком рецептора, локализованного в цитозоле. Как только комплекс биомолекула/носитель сформирован, рецепторный белок в комплексе, как полагают, осуществляет многократные контакты с ядерными порами, транспортируя таким образом комплекс через ядерные поры. После того, как комплекс биомолекула/носитель достигает своего назначения, он распадается, высвобождая груз и другие компоненты. Для транспортировки в ядра может использоваться последовательность Pro-Lys-Lys-Lys-Arg-Lys-Val от SV40 большого Т-антигена. Полагается, что эта короткая последовательность от SV40 большого Т-антигена может обеспечить сигнал, который вызывает транспортировку связанных макромолекул в ядро.
Катионный липополимер может далее включать диагностическое визуализирующее соединение, такое как флуоресцентный, радиоактивный или рентгеноконтрастный краситель, который образует комплекс с полимером. Комплекс может быть образован смешиванием катионного липополимера и диагностического визуализирующего соединения во взаимном растворителе. После введения млекопитающему полимер (комплексный с диагностическим визуализирующим соединением) может быть прослежен с использованием известных методов, таких как PET, MRI, CT, SPECT и т.д. (см. Molecular Imaging of Gen Expression and Protein In Vivo With PET and SPECT, Vijay Sharma, PhD, Gary D.Luker, MD, and David Piwnica-Worms, MD. Ph.D., JOURNAL OF MAGNETIC RESONANCE IMAGING 16: 336-351 (2002)).
Другое воплощение изобретения касается фармацевтической композиции, включающей: сенсибилизирующий агент и полимер, где полимер включает повторяющееся звено формулы (I) и биомолекулу и дополнительно может включать усиливающий доставку агент, способный внедряться в эукариотическую клетку, и/или диагностическую визуализирующую композицию, которая образует комплекс с полимером. Сенсибилизирующий агент может представлять собой соединение, которое меняет свойства при выдержке на свету или под действием других стимулирующих факторов, и таким образом облегчает доставку биомолекулы (например, увеличивая скорость разложения полимера). Сенсибилизирующий агент сам может быть биомолекулой, которая меняет активность под действием стимулирующих факторов. Сенсибилизирующий агент может представлять собой лекарство, которое активизируется под действием света. Подходящие активизируемые светом лекарства включают, но не ограничиваются ими, флуоресцеин, мероцианин, ксантен и его производные и фотореактивные пиррол-производные макроциклы и их производные. Подходящие фотореактивные пиррол-производные макроциклы включают, но не ограничиваются ими, встречающиеся в природе или синтетические порфирины, природные или синтетические хлорины, природные или синтетические бактериохлорины, синтетические изобактериохлорины, фталоцианины, нафталоцианины и расширенные макроциклические системы на основе пиррола, такие как порфицены, сапфирины и тексапирины.
Пример 1

Оксалил хлорид (13,5 мл, 152 ммол) добавляют к раствору олеиновой кислоты 1 (10,7 г, 38 ммол) в дихлорметане (ДХМ, 200 мл) и N,N-диметилформамиде (ДФА, три капли) при 0°С. Реакционную смесь перемешивают в течение приблизительно 1 часа и затем дают нагреться до комнатной температуры. Через 1 час раствор разбавляют толуолом и перегоняют. Остаток растворяют в дихлорметане (200 мл) и охлаждают до 0°С. Добавляют к раствору диэтаноламин (10,9 мл, 114 ммол), 4-(диметил-амино)пиридин (490 мг, 4 ммол) и триэтиламин (21 мл, 152 ммол). Раствор перемешивают при 0°С в течение 30 минут и затем ведут процесс при комнатной температуре в течение ночи. Реакционную смесь растворяют в дихлорметане и промывают 1 N НСl и водным NaHCO3. Органическую фазу сушат (Nа2SO4) и концентрируют при пониженном давлении. Сырой остаток очищают на колонке с силикагелем (10:1 этилацетат:метанол) и получают 13,5 г (99,9%) соединения 2 в виде бесцветного масла.
Пример 2

Триэтиламин (8,1 г, 80 ммол), ДМАП (0,5 г, 4 ммол) и 2 (7,1 г, 20 ммол) растворяют в 200 мл дихлорметана при комнатной температуре. Систему продувают аргоном и охлаждают раствор на ледяной бане. Добавляют по каплям акрилоил хлорид (5,4 г, 60 ммол) в 25 мл дихлорметана. После добавления дают нагреться до комнатной температуры и перемешивают в течение ночи. Реакционную смесь разбавляют дихлорметаном и промывают водой и водным NаНСО3. Органическую фазу сушат (Nа2SO4) и концентрируют при пониженном давлении. Сырой остаток очищают на колонке с силикагелем (1:3 этилацетат:гексан) и получают 7,5 г (81%) соединения 3 в виде бесцветного масла.
Пример 3
Синтез катионного липополимера выполняют в соответствии со схемой А взаимодействием полиэтиленимина, имеющего молекулярный вес 600 (PEI-600), с соединением 3 следующим образом: взвешивают приблизительно 0,6 г PEI-600 (Aldrich) и помещают в небольшую ампулу, добавляют 10 мл этанола. После того, как PEI-600 полностью растворился, в раствор PEI быстро добавляют при перемешивании 3,7 г (8,0 ммол) 3 в 10 мл этанола. Реакционную смесь перемешивают в течение 2 часов при комнатной температуре. После удаления органического растворителя при пониженном давлении получают прозрачную, вязкую жидкость. Спектр 1Н-ЯМР показал, что двойная углерод-углеродная акрильная связь полностью исчезла. Молекулярный вес полученного полимера определен с помощью электрофореза на агарозном геле. Это общий метод, который служит моделью для других синтетических методов, включающих подобные соединения, и может использоваться для синтеза ряда деградируемых катионных липополимеров.
Пример 4
Катионный липополимер был получен, как описано в Примере 3, за исключением того, что после перемешивания реакционной смеси в течение 2 часов при комнатной температуре (25°С), реакционную смесь нейтрализуют добавлением 2,5 мл 4М НСl в эфире. Белый осадок 5С отфильтровывают, промывают этанолом и сушат при комнатной температуре при пониженном давлении. Полученный полимер 5С был характеризован с помощью спектра ЯМР и электрофореза на агарозном геле. Полимеры 5А и 5В были получены аналогично: 5А: PEI1800, m=12; 5В: РЕI600, m=3; 5С: РЕI600, m=8. Это общий метод, который служит моделью для других синтетических методов, включающих подобные соединения, и может использоваться для синтеза ряда деградируемых катионных липополимеров.
Пример 5
Клеточные культуры: клетки НЕК 293Т, 208F, НТ 1080-EGFP и HeLa-EGFP поддерживали в DMEM, содержащем 10% FBS, 100 ед/мл пенициллина и 100 мкг/мл стрептомицина при температуре 37°С, 5% CO2 и 100% влажности; в этой среде клетки имели время удвоения около 20 часов и каждые 3-4 дня их разделяли во избежание слияния.
Пример 6
Приготовление плазмидной ДНК: плазмида pEGFP-N1 была куплена у BD Sciences Clontech company. Она кодирует отливающий красным вариант дикого типа GFP, который был оптимизирован для более яркой флюоресценции и сильной экспрессии в клетках млекопитающих. GFP-белок контролируется через прямой ранний промотор CMV (PCMV IE). Плазмиды были амплифицированы в DH5α E. coli и очищены с помощью набора Qiagen Plasmid Max Preparation, и всегда имели соотношение А260/А280 больше, чем 1,7.
Пример 7
Трансфекция in vitro. Клетки 293 and 208F помещали в 96-ячеечные чашки для тканевых культур (5×104 клеток/ячейка для клеток 293 и 1×104 клеток/ячейка для клеток 208F) и инкубировали в течение ночи в DMEM с 10% FBS. Критическим условием для осуществления трансфекции являлось тщательное соблюдение порядка смешивания плазмидно-полимерного комплекса. В каждую ячейку, содержащую 7,5 мкл раствора плазмиды pEGFP-N с концентрацией по ДНК 0,6 мкг, добавляли аликвоту 7,5 мкл липополимерного раствора в различных концентрациях и полностью перемешивали. ДНК и липополимерную смесь инкубировали в течение 15 мин при комнатной температуре для того, чтобы сформировались ДНК-липополимерные комплексы. Комплексы были добавлены в каждую ячейку с клетками, и их инкубировали при температуре 37°С, 5% СO2 в течение 24 часов. Трансфецирующую активность EGFP-гена определяли по GFP-анализу сигналов. Липофектамин использовали как положительный контроль в соответствии с протоколом производителя.
Пример 8
Наблюдение GFP-сигнала: Зеленый флюоресцирующий сигнал трансфецированных клеток по примеру 3, наблюдали с помощью флуоресцентного микроскопа (Olympus, фильтр 520 нм). Клетки фотографировали, используя 10х объектив. Процент клеток, подающих GFP-сигнал в трансфецированных культурах, был определен из подсчета трех полей, содержащих оптимальные количества полимерных катионов. Трансфецирующая активность липофектамина 2000 была около 60% в 293 ячейках, эффективность 5А, 5В и 5С была около 25%, 55% и 40% соответственно, но флуоресцентная плотность 5А и 5С была немного ниже (см. фиг.1). Эффективность трансфекции генов упомянутых выше липополимеров также выявляли в клетках 208F, в которых GFP положительные клетки составляли приблизительно около 40%, 45%, 25% и 50%, соответственно, после трансфекции, вызванной 5А, 5В, 5С и липофектамином 2000 (см. фиг.2). Хотя липополимеры были не столь хороши, как липофектамин 2000, трансфецирующая эффективность 5 В была очень близка к липофектамину 2000, ведущему трансфецирующему реагенту из имеющихся на рынке. Полученные результаты показали, что липополимеры имеют потенциал трансфецирующих реагентов для различных клеточных линий.
Чтобы определить трансфецирующую активность количественно, с помощью устройства для считывания флуоресценции микроплат (FLX 800, Bio-TEK Instruments Co Ltd) была определена относительная единица флуоресценции трансфецированных клеток. Относительная единица флуоресценции (RFU) липофектамин-2000-трансфецированных клеток линии 293, была равна 14596, что примерно в 2,3 раза больше, чем определено для 5В-трансфецированных клеток (6318), в тоже время RFU для липофектамин 2000- и 5С-трансфецированных клеток линии 208F составили 2544 и 1954 соответственно, продемонстрировав, что в различных клетках трансфецирующий агент показывает различную активность и новые липополимеры могут иметь большую эффективность в отдельных клеточных линиях, чем уже имеющиеся (см. фиг.3).
Пример 9
Исследования по доставке siPHK: эффективность доставки siPHK была определена в опытах на клетках HT1080-EGFP и HeLa EGFP, которые происходили от клеток НТ 1080 и HeLa и имели относительно стабильную экспрессию гена EGFP. SiPHK таргетированные EGFP-ген и ген люциферазы синтезированы Dharmacon Research Inc. SiPHK таргетированные EGFP-ген и ген люциферазы представляли собой двунитевую РНК длиной в 21 нуклеотид, с последовательностями смысловых цепей ААС GAG AAG CGC GAU CAC AUG и AAG UGC GCU GCU GGU GCC ААС соответственно.
За 24 часа перед трансфекцией по 1,5×104 клеток HT1080-EGFP и HeLa-EGFP было помещено в 96-ячеечные плашки. В отдельные ячейки добавили аликвоты объемом 7,5 мкл раствора липополимера в различных концентрациях и 7,5 мкл раствора ДНК, содержащем 2,0 pmol siPHK, затем компоненты тщательно перемешивали. Для того чтобы сформировался siPHK-комплекс, смесь ДНК и липополимеров инкубировали 15 мин при комнатной температуре. Комплексы были добавлены к каждой ячейке и смесь инкубировали при 37°С, 5% CO2 в течение 48 часов. Липофектамин был использован как положительный контроль в соответствии с протоколом, представленным производителем. Эффективность доставки siPHK была определена анализом GFP-сигналов.
Как в клетках HT-GFP, так и в клетках HeLa GFP, 5С показал очень высокую способность к доставке siPHK. В обоих случаях GFP-сигнал легко был ингибирован после доставки в клетки siPHK, вызванной 5С. GFP-сигнал у HT-GFP и HeLa-GFP клеток, которым посредством 5С ввели siPHK, был ниже, чем у клеток, которым siPHK ввели посредством липофектамина 2000. Эти результаты показывают, что 5С имел более высокую эффективность по доставке siPHK, чем липофектами 2000 в обеих клеточных линиях (фиг.4 и фиг.5). С другой стороны образцы 5А и 5В также оказались эффективными при доставке siPHK даже при том, что их эффективность была ниже, чем у липофектамина 2000. RFU определен посредством устройства для считывания флуоресценции микроплат и полученные результаты показали, что относительный уровень флуоресценции клеток HT1080-EGFP и HeLa EGFP, которым с помощью 5С доставили siPHK, составляет только 27-28% от тех, которым не доставляли реагентную группу, это ниже, чем у клеток, которым доставили siPHK посредством липофектамина 2000, которые показывают относительный уровень флуоресценции в пределах от 3 до 46%, относительно уровня флуоресценции в тех случаях, когда такая доставка не производилась. Другими словами, ингибирующая эффективность экспрессии EGFP-гена в клетках, которым его доставляли посредством 5С, была около 72-73%, что немного выше, чем в таких опытах, выполненных с помощью липофектамина 2000, который показал ингибирующую активность на уровне 54-67%. Полученные результаты показывают, что 5С имеет более высокую эффективность при доставке siPHK, чем липофектамин 2000.
Пример 10
Проверка цитотоксичности: Цитотоксичность катионных генных носителей была оценена на клетках млекопитающих, путем использования 3-[4,5 диметилтиазол-2-ил]-2,5-дифенилтетразолиум бромида (МТТ). Через 48 часов после доставки siPHK по методам, описанным в примере 9, по 10 мкл раствора МТТ (5.0 мг/мл в PBS, Sigma) было добавлено в каждую ячейку, и их содержимое было инкубировано при температуре 37°С в течение 3-х часов. Затем среда была удалена и в каждую ячейку было добавлено 200 мкл DMSO (ДМСО) для растворения кристаллов формазана, образованных в результате жизнедеятельности клеток. Абсорбцию раствора измеряли при 570 nm. Жизнеспособность клеток оценивали, используя следующее уравнение: жизнеспособность (%)=(AbS570 (образец)/AbS570 (контроль)}. Контроль показал, что не любой реагент или siPHK может быть добавлен к клеткам. Полученные результаты показали, что цитотоксичность всех трех образцов, 5А, 5В и 5С, была очень низкой после доставки в оптимальных условиях siPHK, выживало более 95% клеток, в тоже время выживаемость клеток была около 65% после доставки siPHK с помощью липофектамина 2000. Так как клетки HeLa были чувствительны к цитотоксичному действию трансфецирующих реагентов, эти результаты предполагают, что новые липополимеры имеют очень низкую цитотоксичность.
Пример 11
Специфичность липополимерной доставки siPHK: для определения, действительно ли ингибитор GFP сигнала является причиной цитотоксичности или такое действие оказывает другой неспецифический фактор, была изучена специфичность доставки siPHK. SiPHK, нацеленная на GFP и Luc ген, была доставлена в клетки HT-GFP с помощью 5А, 5В 5С. GFP сигнал наблюдали в течение 48 часов после доставки. Было найдено, что 5В и 5А имеют низкую способность к доставке, так как GFP сигнал обнаруживался не всегда. 5С показал очень высокую способность к доставке, потому что в 72% GFP был ингибирован в течение 48 после доставки siPHK (нацеленной на ген GFP). Но с другой стороны, когда использовали siPHK, нацеленную на luc-ген, были установлены не все ингибиторы.
Полученные результаты показывают, что GFP сигнал специфически ингибируется доставкой siPHK, а не ингибиторами, оказывающими цитотоксическое действие.
Пример 12
Исследования деградации: Для выявления биодеградации, липополимеры были разведены «opti MEM» до конечной концентрации 320 мкг/мл и инкубированы при 37°С в течение 2, 4, 8, 24 часов соответственно. ДНК-связывающий аффинитет образцов был определен с помощью FITC-меченных антисмысловых олигонуклеотидов. 100 мкл полимеров было добавлено к 100 мкл раствора, содержащего олигонуклеотиды (2 мкмоль/л) в 96 ячейках плашки и перемешаны, полученную смесь инкубировали в течение 15 мин. После чего определяли флуоресценцию с помощью устройства для считывания флуоресценции микроплат (чувствительность = 45).
Относительная единица флуоресценции свободного раствора олигонуклеотидов (раствор олигонуклеотидов, смешанный со 100 мкл «opti MEM» раствора) была около 5200 RFU, для PEI 25K или PEI 600-1823 RFU и 4350 RFU соответственно. Полученные результаты показали, что PEI 25K, обладающий высокой ДНК-связывающей активностью, сильно ингибирует флуоресценцию (около 64% ингибиции), тогда как PEI 600, обладающий очень низким аффинитетом к ДНК, показывает очень низкое ингибирование флуоресценции (18%). Что касается полимеров, основанных на катионных липидах, их ингибирующая активность находилась в пределах от 65% до 70%, что указывает на их способность связывать ДНК с высоким аффинитетом.
После инкубирования при температуре 37°C с «opti MEM» в течение 24 часов, оба, PEI 25K и PEI600, показали незначительное изменение в ДНК-связывающей аффинности, так как почти не изменился сигнал флюоресценции по сравнению с исходными образцами, что показывает, что PEI 25K не является легко деградирующим соединением. Однако, после инкубирования при 37°С в течение 8 часов, ингибирующая активность 5А, 5В и 5С по флюоресценции ступенчато снизилась приблизительно на 10% ниже, чем у PEI 600. Эти результаты показывают, что липополимеры деградировали в «opti MEM».
Пример 13
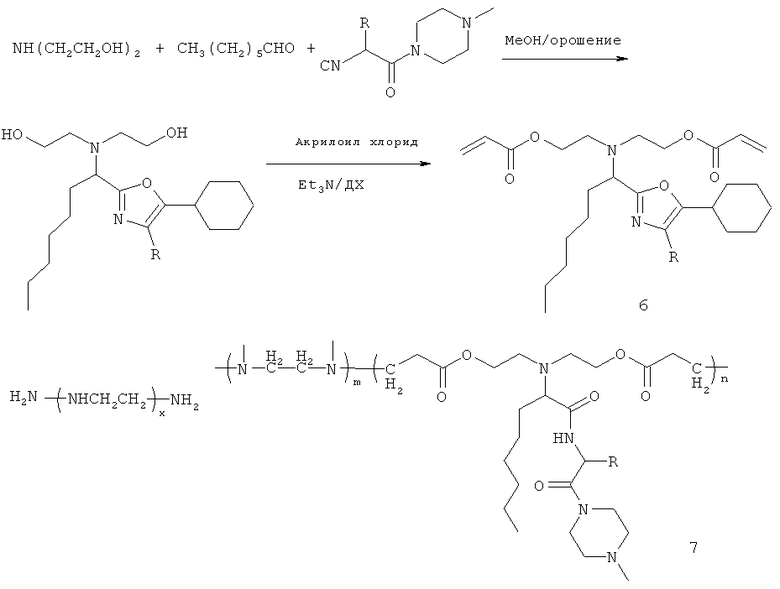
Взвешивают пентаэтиленгексамин (ПЭГА) (43 мг, 0,19 ммол) (Aldrich), помещают в небольшую ампулу и добавляют 2 мл этанола. После того, как РЕНА полностью растворился, в раствор РЕНА быстро добавляют при перемешивании соединение 6 (n×100 мг, n×0,19 ммол). Реакционную смесь перемешивают в течение 2 часов при комнатной температуре (25°С). Затем реакционную смесь нейтрализуют добавлением 1 мл 4М НСl в эфире. Белый осадок отфильтровывают, промывают этанолом и сушат при комнатной температуре при пониженном давлении.
Полученный полимер 7 охарактеризован с помощью спектра ЯМР и электрофореза на агарозном геле.
Аналогично были получены другие поперечносшитые, деградируемые, катионные липополимеры, изменяя отношение РЕНА к 6 следующим образом: 7А: РЕНА/6=1/1; 7В: РЕНА/6=2/1; 7С: РЕНА/6=3/1; 7D: РЕНА/6=4/1; 7Е: РЕНА/6=5/1; и 7F: РЕНА/6=6/1.
Пример 14
Клеточная культура: клетки НЕК 293 и HeLa 705 поддерживали в среде DMEM, содержащей 10% FBS, 100 ед/мл пенициллина и 100 мкг/мл стрептомицина при температуре 37°С, 5% СО2 и 100% влажности. СНО-АА8 luc культивировали в среде MEM, содержащей 10% FBS и антибиотики, другие условия были такими как и при культивировании клеток 293 и HeLa 705. Клетки имели время удваивания около 20 часов и каждые 3-4 дня их разделяли во избежание слияния.
Приготовление плазмидной ДНК: плазмида pEGFP-N1 куплена у BD Sciences Clontech company. Она кодирует отливающий красным вариант дикого типа GFP, который был оптимизирован для более яркой флюоресценции и сильной экспрессии в клетках млекопитающих. GFP-белок контролируется через прямой ранний промотор CMV (PCMV IE). Плазмида pCMV-luc сконструирована таким же образом. Плазмиды были амплифицированы в DH5α Е. соli и очищены с помощью набора Qiagen Plasmid Max Preparation, и всегда имели соотношение А260/А280 больше, чем 1.7.
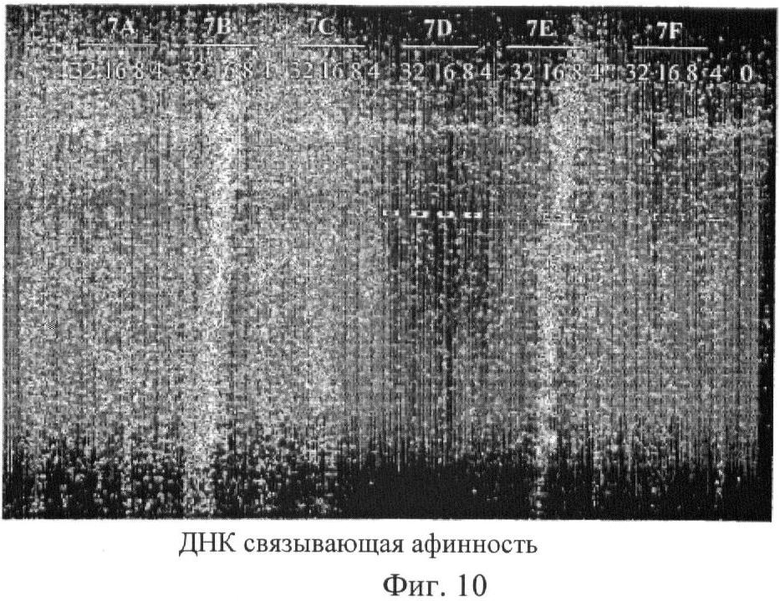
ДНК-связывающий полимер 7: Серии образцов полимера 7 и ДНК были разведены по отдельности в «opti MEM», и затем 10 мкл раствора полимера 7 были добавлены в раствор ДНК (20 мг/мл) и подвергнуты встряхиванию. Соотношения полимер/ДНК были 32:1, 16:1, 8:1 и 10:1. Смесь инкубировали при комнатной температуре в течение 15 мин до формирования полимер/ДНК комплексов. После этого, к пробе было добавлено 5 мкл DNA-загружающего буфера и 15 мкл смеси из каждой пробирки было нанесено на 0.3% агарозный гель. Пробы были подвергнуты электрофорезу при 100 V в течение около 30 мин и затем гель был визуализирован под ультрафиолетовым освещением. Результаты исследования ДНК-связывающей аффинности показаны на фиг.10.
Большинство образцов показали низкую ДНК-связывающую аффинность. Например, когда соотношение полимер/ДНК было 32:1, электрофоретическая подвижность проб 7В, 7С, 7D, 7Е и 7F/DNA смесей была такой же, как и у свободной ДНК (количество полимера - 0). Однако, когда соотношение полимер/ДНК было 32:1 и 16:1, электрофоретическая подвижность плазмид была замедленной, как это показано для пробы 7А, что в данном случае свидетельствует об ДНК-связывающей аффинности.
Пример 15
Трансфекция генов in vitro: клетки 293 были помещены в 96-ячеечную чашку для клеточных культур (5×104 клеток/ячейка) и их инкубировали в течение ночи в DMEM с 10% FBS. В каждую ячейку помещали аликвоту 7,5 мкл раствора липополимера 7 в различных концентрациях и затем добавляли 7,5 мкл раствора ДНК, содержащего 0,6 мкг ДНК плазмиды pEGFP-N1 и тщательно перемешивали. Смесь ДНК и липополимера 7 была инкубирована 15 мин при комнатной температуре для формирования ДНК-липополимерных комплексов. Комплексы были добавлены в каждую ячейку и ячейки инкубировали в течение 24 час при температуре 37°С и 5% СО2. Трансфецирующую активность гена EGFP определяли по анализу сигналов GFP. Липофектамин был использован как положительный контроль соответственно протоколу производителя. Зеленый флуоресцирующий сигнал в трансфецированных клетках наблюдали с помощью флуоресцентного микроскопа (Olympus, фильтр на 520 нм). Клетки фотографировали с использованием объектива с 10-кратным увеличением. Для определения оптимального количества катионного полимера подсчитывали в трех полях зрения процент клеток с GFP-сигналом в трансфецированных культурах.
Через приблизительно 24 часа после трансфекции около 28% 7А трансфецированных клеток 293 показали наличие сигнала, что говорит об эффективной трансфекции. Полученный результат показывает, что липополимер 7А является трансфецирующим агентом (фиг.11).
Пример 16
Доставка антисмысловых олигонуклеотидов: Др. KoIe из University of Northern Carolina разработал систему на основе гена люциферазы 705 для функциональных исследований доставки антисмысловых олигонуклеотидов. В этой системе человеческий бета-глобулин с мутацией в 705 был вставлен в последовательность между кДНК люциферазы.
Эта плазмида была перенесена в клетки HeLa для стабильной экспрессии генов, клеточная линия была обозначена как HeLa luc 705. Обычно клетки проявляют низкую люциферазную активность, так как они экспрессируют неправильный протеин люциферазы. Однако, антисмысловой олигонуклеотид, связываясь с последоватеьностью 705, блокирует ошибочный сайт сплайсинга и протеин люциферазы продуцируется биологически активным.
Люцифераза 705 является новой как функциональная модель для доставки антисмысловых олигонуклеотидов: наиболее высокая активность люциферазы показывает наиболее высокую эффективность доставки антисмыслового олигонуклеотиад.
Эффективность полимера 7 для доставки антисмысловых олигонуклеотидов была оценена на клеточной линии Luc 705. Конечная концентрация олигонуклеотида, нацеленного на luc 705, была 1,0 мкмоль/л, концентрация полимеров была 320 и 160 мкг/мл (такая же, как и количество полимеров, когда соотношение полимер/ДНК было 16:1 и 8:1 во время трансфекции). Активность люциферазы была определена через 24 часа после трансфекции.
Фон люциферазной активности у клеток 705 был около 1,6×105 RLU/мг протеина. Люциферазная активность антисмысловых олигонуклеотидов, доставленных в клетку с помощью 7А, оказалась очень возросшей, почти в 50 раз большей, чем в клетках, в которые ее не доставляли. Доставочная эффективность липофектамина 2000 была меньшей, люциферазная активность возросла только в 15 раз по сравнению с нетрансфецированными клетками. Полученные результаты показали, что липидный полимер 7А имеет более высокую эффективность по доставке антисмысловых олигонуклеотидов в клетки, чем липофектамин 2000 (фиг.12).
Пример 17
SiPHK-доставочную эффективность липополимеров определяли на линиях клеток CHO-AAS-luc. CHO-AA8 Luc являются Tet-off клеточными линиями, в которых экспрессия люциферазного гена контролируется посредством Dox. Экспрессия люциферазного гена отключается, когда к клеткам добавляют Dox, и он начинает экспрессироваться после того, как Dox удалят.
В исследованиях доставки siPHK белок гена-мишени может быть эффективно определен, потому что, если время полу-жизни продолжительна, протеин может быть идентифицирован даже тогда, когда ген-мишень уже отключен, в этом случае оказываются предпочтительными клетки CHO-AA8 Luc. Экспрессия гена люциферазы может быть выключена добавлением Dox для уменьшения фонового протеина. В течение доставки siPHK Dox может быть удален посредством замены среды и ген люциферазы начинает экспрессироваться в это время, если siPHK была удачно доставлена в клетку, высокий уровень люциферазной активности может быть ингибирован siPHK.
СНО АА8 luc были засеяны в 96 ячеек плашки со средой Dox. Через 18-24 часов был приготовлен комплекс siPHK-кассета/полимер 7. Финальная концентрация полимеров была 320 и 160 мкг/мл (такая же концентрация, как и 16:1 и 8:1, использованные при трансфекции генов). Количество siPHK-кассеты было 150 нг/мл. После замены среды клетки были промыты PBS, комплексы siPHK/полимер 7 были добавлены к клеткам. Затем клетки были инкубированы при температуре 37°С в течение 48 ч, после чего выявляли активность люциферазы.
Люциферазная активность в контроле (слепой опыт) была около 107 RLU/мг протеина, после доставки в клетки кассеты siPHK с помощью 7А и липофектамина 2000, люциферазная активность была в значительной степени ингибирована - до 2,47 и 3.49×106 RLU/мг протеина соответственно. Эти результаты показали возможность использования 7А для эффективной доставки кассеты siPHK в клетки и их значительно большую эффективность при доставке, чем у липофектамина (фиг.13).
Пример 18
Цитотоксичность катионного липополимера 7, как генного носителя, была оценена в опытах на клетках млекопитающих путем использования 3-[4,5 диметилтиазол-2-ил]-2,5-дифенилтетразолиум бромида (МТТ). Через 48 час после трансфекции генов по методу, описанному выше, 10 мкл раствора МТТ (5.0 мг/мл в PBS, Sigma) было добавлено в каждую ячейку и затем инкубировано при температуре 37°С в течение 3 часов. Затем среда была удалена и в каждую ячейку было добавлено 200 мкл DMSO (ДМСО) для растворения кристаллов формазана, образованных живыми клетками. Абсорбция раствора была измерена при 570 nm. Жизнеспособные клетки были подсчитаны по уравнению: жизнеспособные (%) = {абсорбция при 570(sample/абсорбция при 570(controi)}. Полученные результаты показали, что цитотоксичность 7А была очень низкой, более чем 95% клеток выжило после доставки siPHK в оптимальных условиях, в тоже время выживаемость клеток после доставки siPHK с помощью липофектамина 2000 была около 75%. Эти результаты показывают, что 7А обладает очень низкой цитотоксичностью (фиг.14).
Пример 19
Биодеградация полимера 7: полимер 7А был разбавлен «opti MEM» до финальной концентрации 320 мкг/мл. Серии образцов были инкубированы при температуре 37°С в течение 4 часов, 8 часов и 24 часов, затем были отобраны образцы для исследований по генному переносу в клетки 293, засеянные в 96-ячеечные плашки. Трансфекция была выполнена по протоколу, описанному выше. GFP-сигнал выявляли через 24 часа после трансфекции.
GFP-ген трансфекционная эффективность 7А была около 25% и значительного снижения трансфецирующей эффективности после того, как пробы были инкубированы в течение 4 часов, выявлено не было,
Трансфецирующая эффективность значительно снижалась после инкубирования образца в течение 8 часов, и она почти полностью исчезала после инкубирования образца в течение 24 часов. Полученные результаты показывают, что 7А биодеградирует под воздействием нейтральных условий (фиг.15).
Различные упущения, выявленные квалифицированным специалистом, их дополнения и модификации, могут быть внесены в композиции и методы, описанные выше, без изменения возможностей самого изобретения; и все такие модификации и изменения будут находиться в рамках изобретения, как это заявлено в пунктах формулы.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОРАЗРУШАЕМЫЕ КАТИОННЫЕ ПОЛИМЕРЫ | 2007 |
|
RU2451525C2 |
| КОМПОЗИЦИЯ ДЛЯ ДОСТАВКИ НУКЛЕИНОВЫХ КИСЛОТ В КЛЕТКИ МЛЕКОПИТАЮЩИХ | 2010 |
|
RU2423147C1 |
| ЛЕЧЕНИЕ ЗАБОЛЕВАНИЙ КИШЕЧНИКА | 2006 |
|
RU2418594C2 |
| ЛЕЧЕНИЕ НАРУШЕНИЙ ЦНС | 2007 |
|
RU2426544C2 |
| КОМПОЗИЦИЯ ДЛЯ ВВЕДЕНИЯ НУКЛЕИНОВОЙ КИСЛОТЫ В КЛЕТКИ | 2015 |
|
RU2715227C2 |
| rac-N-[2,3-ДИ(ТЕТРАДЕЦИЛОКСИ)ПРОП-1-ИЛ]ПИРИДИНИЙ БРОМИД В КАЧЕСТВЕ АГЕНТА ДЛЯ ДОСТАВКИ НУКЛЕИНОВЫХ КИСЛОТ В КЛЕТКИ МЛЕКОПИТАЮЩИХ | 2009 |
|
RU2405772C1 |
| Способ получения амфифильных блок-сополимеров N,N-диметиламиноэтилметакрилата для доставки нуклеиновых кислот в живые клетки | 2014 |
|
RU2617059C2 |
| КОМПОЗИЦИИ ПОЛИЭТИЛЕНИМИН: ДНК ДЛЯ АЭРОЗОЛЬНОЙ ДОСТАВКИ | 2000 |
|
RU2242970C2 |
| СРЕДСТВО ДЛЯ ВНУТРИКЛЕТОЧНОЙ ДОСТАВКИ НУКЛЕИНОВЫХ КИСЛОТ В КЛЕТКИ МЛЕКОПИТАЮЩИХ | 2014 |
|
RU2572575C1 |
| ИНДУКЦИЯ ОСТЕОГЕНЕЗА ПУТЕМ ВНЕДРЕНИЯ РНК, КОДИРУЮЩЕЙ КОСТНЫЙ МОРФОГЕНЕТИЧЕСКИЙ БЕЛОК (КМБ) | 2015 |
|
RU2718590C2 |









Настоящее изобретение относится к катионному липополимеру, включающему полиэтилениминную биодеградируемую группу и относительно гидрофобную группу «липо» группу, или его комплекс с биомолекулой, и состоящий из повторяющихся звеньев, выбранных из группы, состоящей из формулы (Iа) и формулы (Ib)


где PEI означает полиэтилениминное повторяющееся звено; R - электронная пара; L - выбирают из группы, состоящей из C12-C18 жирных кислот, холестерина и их производных, С2-С50 алкила, С2-С50 карбоксиалкенила, C2-C50 карбоксигетероалкенила; W - представляет собой катионную часть, включающую от 2 до 50 атомов углерода; и m - представляет собой целое число в диапазоне от 1 до 30. Также описаны способы доставки биомолекулы к эукариотической клетке, включающие контактирование клетки с вышеуказанным полимером. Технический результат - получение полимеров, которые могут безопасно и эффективно облегчать доставку биологически активных агентов к клеткам. 3 н. и 17 з.п. ф-лы, 15 ил.
1. Катионный липополимер, включающий полиэтилениминную биодеградируемую группу и относительно гидрофобную группу «липо» группу, или его комплекс с биомолекулой, и состоящий из повторяющихся звеньев, выбранных из группы, состоящей из формулы (Iа) и формулы (Ib)


где PEI означает полиэтилениминное повторяющееся звено;
R - электронная пара;
L - выбирают из группы, состоящей из C12-C18 жирных кислот, холестерина и их производных, C2-C50 алкила, C2-C50 карбоксиалкенила, C2-C50 карбоксигетероалкенила;
W - представляет собой катионную часть, включающую от 2 до 50 атомов углерода; и
m - представляет собой целое число в диапазоне от 1 до 30.
2. Катионный липополимер по п.1, где PEI представлен повторяющимся звеном формулы (II)

где x - целое число в диапазоне от 1 до 100, и y - целое число в диапазоне от 1 до 100.
3. Катионный липополимер по п.1, где полимер включает повторяющееся звено формулы (Iа).
4. Катионный липополимер по п.3, в котором L выбирают из группы, содержащей C12-C18 жирные кислоты, холестерин, и их производные.
5. Катионный липополимер по п.4, в котором L имеет следующую структуру:
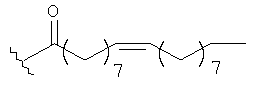
6. Катионный липополимер по п.5, в котором полиэтилениминное повторяющееся звено имеет молекулярный вес в диапазоне от 600 Да до 25000 Да.
7. Катионный липополимер по п.5, в котором полиэтилениминное повторяющееся звено имеет молекулярный вес 600 Да.
8. Катионный липополимер по п.1, в котором полимер включает повторяющееся звено формулы (Ib).
9. Катионный липополимер по п.1, в котором W включает аминогруппу и углеродсодержащую группу, выбранную из группы, состоящей из С2-С50 алкила и C2-C50 гетероалкила.
10. Катионный липополимер по п.1, где L есть С2-С50 алкил.
11. Катионный липополимер по п.1, в котором L выбирают из группы, состоящей из C12-C18 жирных кислот и их производных.
12. Катионный липополимер по п.11, в котором L имеет следующую структуру:

13. Катионный липополимер по п.1, где полиэтилениминное повторяющееся звено имеет молекулярный вес в диапазоне от 600 Да до 25000 Да.
14. Катионный липополимер по п.1, в котором полиэтилениминное повторяющееся звено имеет молекулярный вес 600 Да.
15. Катионный липополимер по п.1, в котором полимер содержит повторяющееся звено, представленное формулой (Iа), в которой PEI означает полиэтилениминное повторяющееся звено; R является электронной парой; L является С2-С50 карбоксиалкенилом; и m представляет целое число в диапазоне от 1 до 30.
16. Катионный липополимер по п.1, в котором биомолекулу выбирают из группы, состоящей из нуклеиновой кислоты, белка, пептида, липида и углевода.
17. Катионный липополимер по п.16, в котором нуклеиновую кислоту выбирают из группы, состоящей из ДНК, siRNA, и антисмыслового олигонуклеотида.
18. Способ доставки биомолекулы к эукариотической клетке, включающий контактирование клетки с полимером по п.1 для доставки биомолекулы в клетку, при этом биомолекулой является нуклеиновая кислота.
19. Способ по п.18, дополнительно включающий перемещение клетки.
20. Способ доставки биомолекулы к эукариотической клетке, включающий контактирование клетки с полимером по п.1.
| Грохот | 1985 |
|
SU1279682A1 |
| US 6696038 В1, 24.02.2004 | |||
| АДСОРБИРУЮЩЕЕ ИЗДЕЛИЕ, ВКЛЮЧАЮЩЕЕ ГИДРОФИЛЬНЫЕ И ГИДРОФОБНЫЕ УЧАСТКИ | 2005 |
|
RU2375081C1 |
Авторы
Даты
2012-01-20—Публикация
2005-09-16—Подача