Область техники, к которой относится изобретение
Изобретение относится к новому химическому соединению, а именно 4-(1-(4-(4-метоксифенилтио)-2,5-диоксо-2,5-дигидро-1Н-пирро-3-ил)-1H-индол-3-ил)бутил карбамимидотиоату, способу его применения в терапии рака толстой кишки, рака молочной железы, меланомы, лейкоза.
Уровень техники
Онкологические заболевания являются одной из основных причин смертности, уступая в этом отношении лишь сердечно-сосудистым заболеваниям. К сожалению, существующие химиотерапевтические подходы во многих случаях неэффективны и обладают серьезными побочными эффектами. По этой причине поиск новых противоопухолевых препаратов является актуальной задачей.
Одним из наиболее перспективных современных направлений в противоопухолевой терапии является блокирование сигнальных событий в опухолевой клетке, регулируемых серин-треониновыми протеинкиназами. Ингибирование указанных протеинкиназ нарушает пролиферацию, смену фаз клеточного цикла (включая митоз) и выживание при экзогенных токсических воздействиях, приводя к гибели клетки.
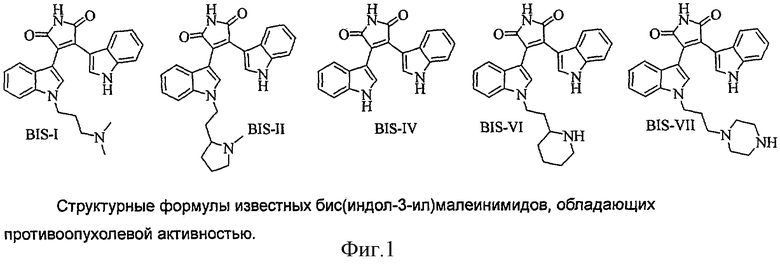
Среди серин-треониновых протеинкиназ, являющихся перспективными мишенями онкологических заболеваний, можно выделить следующие ферменты. Во-первых, это протеинкиназа С альфа (РКСα), которая играет важнейшую роль в механизмах ответа клетки на многие виды стресса, в том числе на противоопухолевые препараты (Sabbah M, Emami S, Redeuilh G, Julien S, Pruvost G, Zimber A, Ouelaa R, Bracke M, De Wever O, Gespach C. Molecular signature and therapeutic perspective of the epithelial-to-mesenchymal transitions in epithelial cancers. Drug Resist. Updat. 2008.11 (4-5):123-151). Во-вторых, это циклин-зависимые киназы 2 и 4 (CDK2 и CDK4), являющиеся регуляторами клеточного цикла (Johansson M, Persson JL. Cancer therapy: targeting cell cycle regulators. Anticancer Agents Med Chem. 2008. 8(7):723-731). В-третьих, это протоонкогенная серин-треониновая киназа РIМ-1, повышенная активность которой приводит к злокачественной трансформации нормальных клеток (Mumenthaler SM, Ng PY, Hodge A, Bearss D, Berk G, Kanekal S, Redkar S, Taverna P, Agus DB, Jain A. Pharmacologic inhibition of Pim kinases alters prostate cancer cell growth and resensitizes chemoresistant cells to taxanes. Mol Cancer Ther. 2009 Oct; 8(10):2882-93). Известен ряд химических соединений, принадлежащих к классу индолилмалеинимидов, более точно - производных бис(индол-3-ил)малеинимида, таких как BIS-I, BIS-II, BIS-IV, BIS-VI, BIS-VII (фиг.1), являющихся ингибиторами серин-треониновых протеинкиназ. Исследованы и способы их получения (Davis et al. J. Med.Chem. 1992, v.35, N.1, p.177-184, US 6133452, US 5545636, US 2005004201, EP 0657458 A1, WO 02/38561 A1) и противоопухолевая. Вместе с тем, противоопухолевая активность данных соединений (Prеtе SP, Rossi L, Correale РР, Turriziani M, Baier S, Tamburrelli G, De Vecchis L, Bonmassar E, Aquino A. Combined effects of protein kinase inhibitors and 5-fluorouracil on CEA expression in human colon cancer cells. Pharmacol Res. 2005 Aug; 52(2): 167-73; Robey RW, Shukla S, Steadman K, Obrzut T, Finley EM, Ambudkar SV, Bates SE. Inhibition of ABCG2-mediated transport by protein kinase inhibitors with a bisindolylmaleimide or indolocarbazole structure. Mol Cancer Ther. 2007 Jun;6(6):1877-85), а также их известных на сегодняшний день аналогов (Shchekotikhin А.Е., Dezhenkova L.G., Susova O.Yu., Glazunova V.A., Luzikov Yu.N., Sinkevich Yu.N., Buyanov V.N., Shtil AA, Preobrazhenskaya M.N. Naphthoindole-based analogues of tryptophan and tryptamine: synthesis and cytotoxic properties. Bioorganic and Medicinal Chemistry, 2007, 15, 2651-2659) недостаточно высока, для того чтобы применять их в качестве самостоятельных химиотерапевтических препаратов при лечении рака толстой кишки, рака молочной железы, меланомы, лейкоза и других онкологических заболеваний. Вместе с тем, класс индолилмалеинимидов, благодаря своему структурному разнообразию, является перспективным для поиска новых соединений с повышенной противоопухолевой активностью и, возможно, также с пониженной общей токсичностью.
Решение подобной задачи видится в обогащении традиционных методов органического синтеза и медицинской химии современными методами молекулярного моделирования, позволяющими моделировать взаимодействие новых, еще не синтезированных соединений с заданными белками (например, выбранными серин-треониновыми киназами).
Раскрытие изобретения
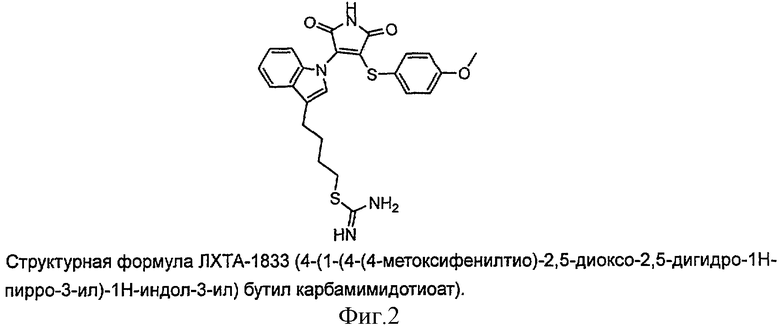
Настоящее изобретение представляет собой новое химическое соединение ЛХТА-1833 (4-(1-(4-(4-метоксифенилтио)-2,5-диоксо-2,5-дигидро-1H-пирро-3-ил)-1H-индол-3-ил)бутил карбамимидотиоат), структурная формула которого представлена на фиг.2.
Соединение ЛХТА-1833 было нйдено с помощью методов молекулярного моделирования, проводившихся по следующей схеме. Сначала генерировалась виртуальная библиотека различных (индол-1-ил)малеинимидов, содержащих различные заместители в 3-м положении индольного фрагмента, а также различные заместители при втором некарбонильном атоме углерода малеинимида. Далее в полученной библиотеке с помощью методов молекулярного моделирования отыскивались соединения, которые, по данным расчетов, демонстрировали ингибирование ферментов PKCα, CDK2, CDK4, PIM-1. Далее, на основе структур отобранных соединений генерировалась новая виртуальная библиотека соединений, которые, по мнению авторов изобретения, должны были обладать повышенным сродством к обозначенным ферментам. Процедура моделирования и конструирования повторялась до тех пор, пока не были отобраны удовлетворительные на взгляд авторов изобретения соединения. Далее, отобранные по результатам молекулярного моделирования соединения синтезировались и испытывались в in vitro моделях опухолевых заболеваний. В проведенных in vitro испытаниях соединение ЛХТА-1833 продемонстрировало высокую противоопухолевую активность. Таким образом, новое соединение ЛХТА-1833, раскрываемое в настоящем патенте, может применяться в терапии рака толстой кишки, рака молочной железы, меланомы, лейкоза и других онкологических заболеваний, в патогенезе которых участвуют серин-треониновые протеинкиназы, в частности PKCα, CDK2, CDK4, PIM-1.
Новизна раскрываемого изобретения состоит в том, что в сравнении с известными индолилмаиеинимидами соединение ЛХТА-1833 имеет ряд структурных особенностей, повышающих его сродство с целевыми ферментами (PKCα, CDK2, CDK4, PIM-1), и, следовательно, повышающих его противоопухолевую активность. А именно: изменен способ соединения индольного ядра с малеимидным фрагментом, а другой остаток индола, присутствующий в известных бис(индол-3-ил)малеинимидах, замещен на 4-метокситиофенильный остаток. В оставшемся индольном фрагменте в 3-м положении введен фрагмент бутил карбамимидотиоата. Эти модификации критичны для проявления противоопухолевой активности ЛХТА-1833.
Осуществление изобретения
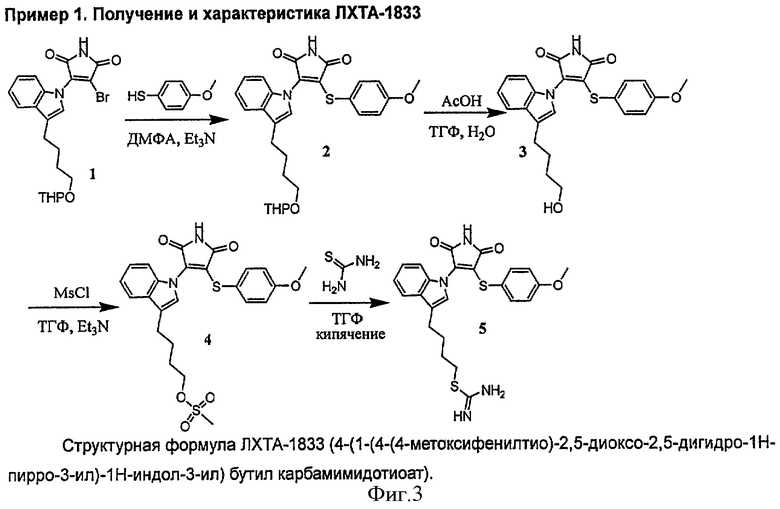
1. Синтез 3-(3-(4-гидроксибутил)-1H-индол-1-ил)-4-(4-метоксифенилтио)-1H-пиррол-2,5-диона (3). 3-Бромо-4-(3-(4-(тетрагидро-2Н-пиран-2-илокси)бутил)-1H-индол-1-ил)-1H-пиррол-2,5-дион (1 г, 2.1 ммоль) растворяют в ДМФА (5 мл), добавляют триэтиламин (0,35 мл) и 4-метокситиофенол (300 мг). Реакционную смесь перемешивают 1 ч при комнатной температуре. Реакционную смесь разбавляют этилацетатом (50 мл), промывают 0,1н HCl (2×30 мл), водой (2×30 мл), сушат и упаривают. Полученный продукт конденсации 2 используют без очистки на следующей стадии. Продукт 2 растворяют в уксусной кислоте (10 мл), добавляют воду (5 мл) и тетрагидрофуран (3 мл), нагревают до 50°С при перемешивании в течение 2-3 ч. Реакционную смесь упаривают на роторном испарителе, остаток растворяют в этилацетате (50 мл), раствор промывают раствором бикарбоната натрия (2×30 мл), сушат и упаривают. Остаток хроматографируют на силикагеле (н-гептан-этилацетат 2:1). Фракции, содержащие целевое вещество, упаривают. Получают 3-(3-(4-гидроксибутил)-1H-индол-1-ил)-4-(4-метоксифенилтио)-1H-пиррол-2,5-дион (3) с выходом 71% в виде аморфного вещества оранжевого цвета.
2. Синтез 4-(1-(4-(4-метоксифенилтио)-2,5-диоксо-2,5-дигидро-1Н-пиррол-3-ил)-1H-индол-3-ил)бутил метансульфоната (4). К раствору 3 в ТГФ добавляют триэтиламин (1 эквивалент), прикапывают раствор MsCl (метансульфонилхлорида) (1 эквивалент) в ТГФ при перемешивании в течение 2-х часов. Затем разбавляют EtOAc и промывают водой, насыщенным водным раствором NaCl, сушат и упаривают. Продукт отделяют методом колоночной хроматографии в системе (н-Гептан: EtOAc, 5:1). Остаток хроматографируют на силикагеле (н-гептан-этилацетат 2:1). Фракции, содержащие целевое вещество, упаривают. Получают 4 с выходом 80% в виде аморфного вещества оранжевого цвета.
3. Синтез ЛХТА-1833 4-(1-(4-(4-метоксифенилтио)-2,5-диоксо-2,5-дигидро-1H-пирро-3-ил)-1H-индол-3-ил)бутил карбамимидотиоата (5). Мезилат 4 (200 мг, 0,4 ммоль) растворяют в ТГФ (10 мл) добавляют тиомочевину (50 мг) и кипятят при перемешивании 6 ч, охлаждают до комнатной температуры и разбавляют н-бутанолом, промывают водой, насыщенным водным раствором NaCl. Сушат и упаривают. Продукт отделяют методом колоночной хроматографии на силикагеле, элюент-этилацетат. Фракции, содержащие целевое вещество, упаривают. Получают 5 в виде аморфного вещества оранжевого цвета (105 мг, 0.22 ммоль, 55%).
120.5, 122.1, 124.3, 126.8, 128.3, 131.9 (2С), 132.6, 135.1, 159.0, 167.6, 168.5
Пример 2. Противоопухолевая активность ЛХТА-1833 в испытаниях in vitro
Исследование цитотоксичности ЛХТА-1833 на опухолевых и нормальных клетках проводили методом, основанным на способности живых клеток восстанавливать бромид 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолия в формазан (МТТ-тест). Клетки рассевали на 96-луночные планшеты (Costar, США) (5-10×103 клеток в 190 мкл культуральной среды). В лунки вносили исследуемое соединение до конечных концентраций 0.1-6.4 мкМ или соответствующие количества растворителя диметилсульфоксида (контроль). Объем вносимого вещества не превышал 5% объема среды в лунках. Каждую концентрацию препарата изучали в 2-3 повторностях. Культуры инкубировали при 37°С, 5% СO2 до 72 часов. По окончании инкубации в лунки вносили 20 мкл 0,5% водного раствора МТТ (Sigma), и планшеты помещали в CO2-инкубатор на 2 часа. О жизнеспособности клеток судили по цветной реакции, развивающейся при восстановлении МТТ в формазан дегидрогеназами митохондрий. Окраску регистрировали на спектрофотометре при длине волны возбуждения 540 нм. Оптическую плотность в лунках, где клетки инкубировались только с диметилсульфоксидом (контроль), принимали за 100%.
Показатели оптической плотности в лунках с каждой концентрацией испытуемых препаратов усредняли и вычисляли процент выживших клеток при той или иной концентрации исследуемого соединения.
Данные по цитотоксичности ЛХТА-1833 для опухолевых и нормальных клеток представлены в таблице 2. Результаты выражены как IC50 (мкМ) (концентрация соединения, вызывающая гибель 50% клеток) после 72-часовой инкубации клеток. Средние 3-х повторностей и стандартные отклонения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ПРОИЗВОДНЫХ 4-ЗАМЕЩЕННЫХ-3-(3-ДИАЛКИЛАМИНОМЕТИЛ-ИНДОЛ-1-ИЛ)МАЛЕИМИДОВ | 2006 |
|
RU2388759C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 4-(1Н-ИНДОЛ-3-ИЛ)-БУТ-3-ЕН-2-ОНА | 2009 |
|
RU2409564C1 |
| Производное 1'-бромо-2',3',4'-триметоксибензо[5',6':4,5]-(aR, 1S)-1-ацетамидо-6,7-дигидроциклогепта-[3,4-f]-1Н-индола и его применение | 2016 |
|
RU2630303C1 |
| Замещенные N-{ 3-[4-(1-метил-1Н-индол-3-ил)пиримидин-2-иламино]-4-метоксифенил} -амиды в качестве модуляторов EGFR, предназначенные для лечения рака | 2015 |
|
RU2606949C9 |
| Способ получения 1-(2-пропаргил)-1Н-нафто[2,3-d][1,2,3]триазол-4,9-дион-4-оксим-2-оксида | 2022 |
|
RU2791249C1 |
| Этиловый эфир (E)-2-амино-5-(2-(нафталин-2-ил)-2-оксоэтилиден)-4-оксо-1-(3-циано-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)-4,5-дигидро-1H-пиррол-3-карбоновой кислоты, обладающий противоопухолевой активностью в отношении колоректального рака | 2024 |
|
RU2836297C1 |
| ПРОИЗВОДНОЕ 1",2",3"-ТРИМЕТОКСИБЕНЗО[5",6":5',4']1H-(aR,1S)-1-АЦЕТАМИДО-6',7'-ДИГИДРОЦИКЛОГЕПТА[2',3'-f]-2,3-ДИГИДРОФУРАНА И ЕГО ПРИМЕНЕНИЕ | 2018 |
|
RU2678440C1 |
| НОВАЯ СОЛЬ 3-[(3-{ [4-(4-МОРФОЛИНИЛМЕТИЛ)-1Н-ПИРРОЛ-2-ИЛ]МЕТИЛЕН} -2-ОКСО-2,3-ДИГИДРО-1Н-ИНДОЛ-5-ИЛ)МЕТИЛ]-1,3-ТИАЗОЛИДИН-2,4-ДИОНА, ЕЕ ПОЛУЧЕНИЕ И СОДЕРЖАЩИЕ ЕЕ КОМПОЗИЦИИ | 2014 |
|
RU2680826C9 |
| КОНЪЮГАТЫ ТРИТЕРПЕНОВЫХ КИСЛОТ И (Е)-4-(1Н-ИНДОЛ-3-ИЛВИНИЛ)-ПИРИДИНИЙ БРОМИДА С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2786134C2 |
| Фотохромные 3-(2,5-диметилтиофен-3-ил)-4-(1-алкил-2-диметил-5-метокси-1Н-индол-3-ил)фуран-2,5-дионы с модулируемой флуоресценцией | 2017 |
|
RU2668221C1 |
Изобретение относится к новому соединению 4-(1-(4-(4-метоксифенилтио)-2,5-диоксо-2,5-дигидро-1Н-пирро-3-ил)-1Н-индол-3-ил)бутил карбамимидотиоату (соединение ЛХТА-1833), который может быть использован в терапии рака толстой кишки, рака молочной железы, меланомы, лейкоза. 2 н.п. ф-лы, 2 табл., ил.3.
1. Индивидуальное химическое соединение ЛХТА-1833 (4-(1-(4-(4-метоксифенилтио)-2,5-диоксо-2,5-дигидро-1Н-пирро-3-ил)-1Н-индол-3-ил) бутил карбамимидотиоат).
2. Применение химического соединение ЛХТА-1833 (4-(1-(4-(4-метоксифенилтио)-2,5-диоксо-2,5-дигидро-1Н-пирро-3-ил)-1Н-индол-3-ил) бутилкарбамимидотиоата) в терапии рака толстой кишки, рака молочной железы, меланомы, лейкоза.
| US 5545636 А, 13.08.1996 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| US 7439363 B2, 21.10.2008 | |||
| Способ изготовления магнитопроводов ферритовых магнитных головок | 1976 |
|
SU657458A1 |
| ЗАМЕЩЕННЫЕ ПИРРОЛЫ | 2000 |
|
RU2261862C2 |
Авторы
Даты
2012-01-27—Публикация
2009-11-27—Подача