Изобретение относится к области биотехнологии, микробиологии и фармацевтической промышленности. Конкретно изобретение относится к субстанции Фортеплазе, содержащей рекомбинантный белок с аминокислотной последовательностью стафилокиназы. Данная субстанция может быть использована для получения лекарственного средства, обладающего фибринолитическими свойствами.
Сырьем для получения субстанции Фортеплазе является супернатант, содержащий рекомбинантный белок с аминокислотной последовательностью стафилокиназы (РБСФ), полученный при культивировании штамма Escherichia coli MZ09, регистрационный номер В-10417 ВКПМ. Супернатант получают центрифугированием культуральной жидкости, затем его хранят в замороженном состоянии.
Рекомбинантный белок состоит из 138 аминокислот (последовательность белка представлена SEQ ID NO:1). Эмпирическая формула C711H1372N168O350S1. Молекулярная масса 15,5 кДа.
Субстанция представляет собой в сухом виде белый аморфный порошок, при растворении 10 мг субстанции в 10 мл 0,9% раствора натрия хлорида становится бесцветной прозрачной жидкостью.
Отличить субстанцию можно по следующим признакам:
1. Образует зоны лизиса в фибриновом геле вследствие активации плазминогена.
2. При электрофорезе в полиакриламидном геле на электрофореграмме присутствует одна окрашенная полоса рекомбинантного белка с аминокислотной последовательностью стафилокиназы, соответствующая молекулярной массе 15,5 кДа.
3. Идентификацию белковых компонентов в субстанции Фортеплазе можно осуществить методом иммуноблотинга. В основе метода лежат перенос белка после проведения электрофореза в ПААГ на твердую подложку (нитроцеллюлозный фильтр), последующая обработка белковой полосы на фильтре специфическими антителами и окраска связавшихся антител с помощью ферментативной цветной реакции.
4. Легко растворима в 0,9% растворе натрия хлорида для инъекций. Время растворения содержимого 1 флакона (10 мг) менее 60 сек.
5. Значение pH для восстановленного раствора должно быть от 5,5 до 7,5.
6. Удельную ферментативную активность (Ауд) в МЕ/мг рассчитывают по формуле:
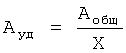
где Х - содержание белка во флаконе, мг;
Аобщ - общая ферментативная активность анализируемого препарата, ME.
Удельная ферментативная активность должна быть от 134100 до 163900 МЕ/мг белка.
7. Содержание иммунореактивных белков Е.coli в субстанции не должно превышать 10 p.p.m. (нг/мг).
Воду очищенную приготавливают на установке обратного осмоса AquaHard RQ 2500 (или аналогичную) и проводят деконтаминацию воды УФ-облучением.
Используемую посуду тщательно моют. Стеклянную бактериологическую посуду закрывают фольгой или пергаментной бумагой и стерилизуют сухим жаром в сушильно-стерилизационном шкафу при температуре 170-180°C в течение 2-2,5 часов.
Буферные растворы готовят в пластиковых емкостях с мешалкой следующим образом.
Приготовление уравновешивающего буферного раствора 0,02 М аммоний ацетата, pH 6,0 (УБ-1).
На весах отвешивают 0,0385±0,001 кг аммония ацетата.
В промытую пластиковую тарированную емкость заливают 25 литров воды очищенной и при постоянном перемешивании засыпают навеску аммония ацетата. Перемешивают до полного растворения навески. Берут пробу и определяют pH. Требуемое значение рН-6,0±0,2. Добавлением уксусной кислоты доводят величину pH до требуемого значения. Очищенной водой доводят объем до 30 литров и, еще раз тщательно перемешав буферный раствор, контролируют величину pH.
Приготовление элюирующего буферного раствора 0,02 М аммоний ацетата, 0,4 М натрия хлористого, pH 6,0 (ЭБ-1).
На весах отвешивают 0,0385±0,001 кг аммония ацетата и 0,7±0,001 кг натрия хлористого.
В промытую пластиковую тарированную емкость заливают 25 литров воды очищенной и при постоянном перемешивании засыпают навеску аммония ацетата и натрия хлористого. Перемешивают до полного растворения навесок. Берут пробу и определяют pH. Требуемое значение рН-6,0±0,2. Добавлением уксусной кислоты доводят величину pH до требуемого значения. Очищенной водой доводят объем до 30 литров и, еще раз тщательно перемешав раствор, контролируют величину pH.
Приготовление уравновешивающего буферного раствора 0,01 М Трис, 0,0002 М ЭДТА, pH 8,0 (УБ-2).
На аналитических весах отвешивают 0,0605=0,0001 кг Трис и 0,00029±0,00001 кг двунатриевой соли этилендиаминтетрауксусной кислоты (ЭДТА).
В промытую пластиковую тарированную емкость заливают 48 литров воды очищенной и при постоянном перемешивании засыпают навеску Трис и ЭДТА. Перемешивают до полного растворения навесок. Берут пробу и определяют pH. Требуемое значение pH 8,0±0,2. Добавлением уксусной кислоты доводят величину pH до требуемого значения. Очищенной водой доводят объем до 50 литров и, еще раз тщательно перемешав раствор, контролируют величину pH.
Приготовление элюирующего буферного раствора 0,01 М Трис, 0,0002 М ЭДТА, 1 М натрий хлористый, pH 8,0 (ЭБ-2).
На аналитических весах отвешивают 0,0605±0,0001 кг Трис и 0,00029±0,00001 кг двунатриевой соли этилендиаминтетрауксусной кислоты (ЭДТА). На технических весах отвешивают 2,925±0,001 кг натрия хлористого.
В промытую пластиковую тарированную емкость заливают 48 литров воды очищенной и при постоянном перемешивании засыпают навески Трис, натрия хлористого и ЭДТА. Перемешивают до полного растворения навесок. Берут пробу и определяют pH. Требуемое значение pH 8,0±0,2. Добавлением соляной кислоты доводят величину pH до требуемого значения. Очищенной водой доводят объем до 50 литров и, еще раз тщательно перемешав раствор, контролируют величину pH.
Замороженный супернатант РБСФ не менее чем за 12 часов до начала хроматографической очистки на СМ-сефарозе извлекают из морозильника и оставляют в хранилище при комнатной температуре для размораживания. Затем проводят хроматографическую очистку и выделение РБСФ из супернатанта.
Все технологические операции по очистке РБСФ с использованием колонок выполняют на хроматографическом препаративном комплексе «Axioma» низкого давления.
Хроматографическую очистку РБСФ осуществляют последовательно в 2 этапа - хроматографическая очистка на СМ-сефарозе и хроматографическая очистка на DEAE-сефарозе.
Хроматографическая очистка на СМ-сефарозе.
Для проведения работы используют препаративную стеклянную колонку «Axioma» ПСК-146-500 (или аналогичную), в которую загружают 5 л сорбента СМ-сефарозы.
В реактор объемом 60 л со сливным краном, расположенным снизу, загружают 5 л сорбента, заливают его десятикратным объемом очищенной воды и перемешивают (5±1) мин. Через (30±5) мин после остановки мешалки жидкость над осадком декантируют перистальтическим насосом. Операцию повторяют 2 раза.
В реактор с промытым сорбентом заливают 45 л очищенной воды, добавляют 5 л раствора УБ-1. Суспензию сорбента в УБ-1 при постоянном перемешивании подают через перистальтический насос на колонку. Заполнение колонки проводят в соответствии с инструкцией «Подготовка колонки с СМ-сефарозой к работе».
Хроматографическая очистка
Для хроматографической очистки используют препаративный хроматографический комплекс «Axioma». Принцип работы комплекса изложен в инструкции по эксплуатации прибора.
При помощи гибких шлангов формируют линию подачи растворов на колонку через хроматографический модуль.
При этом:
- шланг от клапана коллектора фракций «F1» опускают в воронку самотечной производственной канализации;
- для сбора материала используют клапаны коллектора фракций, соединив их шлангом с емкостями для сбора фракций;
- подсоединяют к клапанам ввода хроматографа три шланга, два из них на линейке клапанов А, один на линейке В. Клапаны распределительного коллектора соединяют шлангами с емкостями с буферами. Клапан для подачи раствора супернатанта РБСФ соединяют шлангом с емкостью с супернатантом РБСФ. Выход из хроматографического модуля соединительным шлангом подсоединяют к верхнему адаптеру колонки, а нижний адаптер колонки соединяется с клапаном на линейке В.
Запускают программу. В начале процесса клапаны должны быть открыты так, чтобы на колонку подавался уравновешивающий буфер УБ-1 по шлангу. Включают насос со скоростью подачи жидкости (0,9±0,1) л/мин. После уравновешивания колонки (35±5) л буфера на нее подают 20 л супернатанта РБСФ, переключая соответствующий клапан хроматографа.
Далее колонку с сорбентом промывают буферным раствором до падения оптической плотности при 280 нм до (0,2±0,05) оптических единиц.
Устанавливают автоматический режим управления процессом, выбрав в меню кнопку «AUTO». В открывшемся окне набирают номер цикла (протокола). Выставляют необходимые пределы измерения, программируют заданный градиент. Сорбированный материал снимают градиентом натрия хлористого (от 0 до 0,4 М) в том же буфере ЭБ-1, подающимся через клапан из реактора со скоростью 0,4 л/мин. Сбор фракций происходит автоматически.
Из каждой фракции (емкости) отбирают пробы и проводят контроль методом ПААГ-электрофореза с додецилсульфатом натрия.
Фракции, содержащие по результатам электрофореза РБСФ, объединяют, отбирают (2,5±0,01) мл пробы в пробирку и проводят спектрофотометрический контроль.
Показатели раствора РБСФ должны удовлетворять следующим требованиям:
- оптическая плотность при длине волны λ=280 нм (l=1 см) - не менее 1,0 оптической единицы (ОЕ);
- отношение OD280/OD254 - не менее 2,0.
Фракции объединяют и емкость с раствором передают на дальнейшую переработку.
Регенерация СМ-сефарозы
После каждого цикла очистки проводят регенерацию колонки с использованием 0,1 М гидроокиси натрия.
Один из распределительных клапанов хроматографического модуля подсоединяют к емкости с щелочью. Пропускают через колонну 15 л раствора щелочи, затем проводят отмывку очищенной водой до достижения значений pH (7,5±0,5) единиц.
Хроматографическая очистка РБСФ на DEAE-сефарозе
Подготовка сорбента
В тарированную емкость загружают 3 л сорбента, заливают его десятикратным объемом очищенной воды и перемешивают (5±1) мин. Через (30±5) мин жидкость над осадком декантируют перистальтическим насосом. Операцию повторяют 2 раза.
В емкость с промытым сорбентом заливают 10 л очищенной воды, добавляют 5 л раствора УБ-2. Суспензию сорбента в УБ-2 при постоянном перемешивании подают через перистальтический насос на колонку ПСК-100-500. Заполнение колонки проводят в соответствии с инструкцией.
Хроматографическая очистка
При помощи гибких шлангов соединяют верхний и нижний адаптеры колонки соответственно с входным и выходным клапанами хроматографического комплекса в соответствии с инструкцией по работе.
Запускают программу по ручному управлению работой хроматографа. В начале процесса клапаны должны быть открыты так, чтобы на колонку подавался уравновешивающий буфер (УБ-2). Включают насос и со скоростью подачи 0,4±0,005 л/мин начинают подачу УБ-2 на колонку. После уравновешивания колонки пропусканием через нее 6±1 л буфера УБ-2, переключают клапан и на колонку с DEAE-сефарозой подают раствор РБСФ.
Далее колонку с DEAE-сефарозой промывают буферным раствором (УБ-2) до падения оптической плотности при 280 нм до (0,2±0,05) оптических единиц.
Отработанные буферные растворы после выхода из хроматографического комплекса направляют в контейнер для отходов.
Затем переключают хроматографический комплекс на автоматический режим управления процессом. В открывшемся окне набирают номер протокола. Выставляют необходимые пределы измерения оптической плотности, pH и проводимости. Программируют градиент и время работы хроматографического комплекса.
Сорбированный на колонке РБСФ элюируют градиентом натрия хлористого (от 0 до 1 М) в том же буфере (УБ-2), подающемся на колонку со скоростью 0,2 л/мин. Сбор фракций происходит в автоматическом режиме. Согласно заданной программе происходит переключение клапанов коллектора.
Из каждой фракции (емкости) отбирают пробы и передают в производственную лабораторию для контроля чистоты РБСФ во фракциях методом электрофореза в ПААГ с додецилсульфатом натрия.
Фракции, пригодные для дальнейшей работы, должны содержать по результатам электрофореза чистый РБСФ (наличие одной окрашенной полосы белка, соответствующей молекулярной массе 15,5 кДа).
Содержание белка (Сб) рассчитывают по формуле:
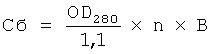 (мг/мл)
(мг/мл)
где OD280 - оптическая плотность анализируемого образца при длине волны 280 нм;
1,1 - коэффициент поглощения (соответствует оптической плотности раствора с концентрацией белка 1 мг в 1 мл при толщине слоя, равной 1 см при длине волны 280 нм, мл (мг×см);
n - разбавление фракции раствора РБСФ в кювете;
В - толщина слоя, см (=1 для кюветы с толщиной оптического слоя 1 см).
Фракции чистого РБСФ с концентрацией не менее (0,5±0,01) мг/мл объединяют, перемешивают, отбирают (2,0±0,1) мл объединенной фракции и передают в контрольную лабораторию.
Показатели объединенной фракции должны удовлетворять следующим характеристикам:
- OD280 (l=1 см) - не менее 3 оптических единиц;
- отсутствие посторонних примесей по результатам ПААГ электрофореза.
Регенерация колонки
Цикл очистки DEAE-сефарозы проводят после 10 рабочих разделений. Сорбент в колонке промывают 6 л раствора 0,1 М гидроокиси натрия.
Пропускают через колонку 6 л раствора щелочи, затем проводят отмывку водой очищенной до достижения значений pH 7,5±0,5.
Переключают клапан и начинают подачу на колонку уравновешивающего буфера УБ-2. После того как величина pH раствора на выходе из колонки сравняется с pH УБ-2 и достигнет значения pH 8,0±0,2, процесс уравновешивания прекращают, колонка готова к работе.
Перевод РБСФ в 0,3% раствор Nad на колонке с сефадексом G-25.
Подготовка колонки с сефадексом G-25
Для проведения работы используют препаративную стеклянную колонку «Axioma» ПСК-146-700 (или аналогичную). Размеры колонки: диаметр 200 мм, высота 500 мм.
В тарированную емкость загружают 2 кг сорбента, заливают его 50 л очищенной воды и перемешивают вручную (5±1) мин. Оставляют на ночь для набухания сорбента.
Утром декантируют воду и заливают набухший сорбент 15 л 0,3% натрия хлористого.
Суспензию сефадекс G-25 в 0,3% растворе натрия хлористого при постоянном перемешивании подают через перистальтический насос на колонку. Заполнение колонки проводят в соответствии с инструкцией «Подготовка колонки с сефадексом G-25 к работе».
Перевод РБСФ в 0,3% натрий хлористый
Для перевода РБСФ в 0,3% натрий хлористый используют метод фильтрации через колонку с сефадексом G-25, уравновешенным 0,3% натрием хлористым.
При помощи гибких шлангов соединяют верхний и нижний адаптеры колонки с сефадексом G-25 соответственно с входным и выходным клапанами хроматографического комплекса в соответствии с инструкцией по работе.
Запускают программу по ручному управлению работой хроматографического комплекса. В начале процесса клапаны должны быть открыты так, чтобы на колонку подавался 0,3% раствор хлористого натрия. Включают насос со скоростью подачи 0,3% хлористого натрия 0,1±0,005 л/мин. После уравновешивания колонки пропусканием через нее 10±1 л 0,3% раствора хлористого натрия на колонку с сефадексом G-25 подают раствор РБСФ.
После нанесения всего РБСФ переключают клапан и начинают подачу на колонку 0,3% натрия хлористого. Начинают собирать фракции, когда поглощение при 280 нм на выходе из колонки будет выше 0,5 ОЕ и перестают собирать, когда поглощение при 280 нм на выходе раствора из колонки упадет до 0,3 ОЕ.
Из каждой фракции (емкости) отбирают пробы и передают в производственную лабораторию для контроля чистоты РБСФ методом электрофореза в ПААГ с додецилсульфатом натрия.
Фракции, содержащие по результатам электрофореза чистый белок РБСФ (одна полоса при 15,5 кДа), объединяют, отбирают (2,5±0,01) мл пробы в пробирку и проводят спектрофотометрический контроль.
Показатели раствора РБСФ должны удовлетворять следующим требованиям:
- оптическая плотность при длине волны λ=280 нм (l=1 см) - не менее 1,0 оптической единицы.
При положительном заключении контрольной лаборатории емкости с раствором очищенного РБСФ объединяют в одной емкости и передают на стерилизующую фильтрацию и лиофильную сушку.
Регенерация колонки
После каждого цикла колонку с сефадексом G-25 отмывают 0,3% раствором натрия хлористого до поглощения при 280 нм не более 0,05 и показатели датчика проводимости на входе и выходе из колонки должны быть равными. Колонка готова к работе.
Лиофильная сушка, фасовка и маркировка
Раствор РБСФ перемешивают и фильтруют через фильтр для стерильной фильтрации с размером пор 0,2 мкм в стерильную приемную емкость. Отбирают пробу для проверки стерильности и разливают в стерильные кюветы для сушки слоем высотой не более 1-1,5 см. Кюветы закрывают стерильной салфеткой, помещают в морозильник на минус 40°С и замораживают в течение 24 часов.
Кюветы извлекают из морозильника и быстро переносят в предварительно охлажденную лиофильную сушку для сушки в асептических условиях. Снимают салфетку и в соответствии с инструкцией по сушке в течение 40-48 часов получают лиофильно высушенную стерильную субстанцию Фортеплазе.
Кюветы накрывают стерильной салфеткой и переносят в стерильный бокс с ламинарным шкафом с вертикальным потоком.
В предварительно взвешенные стерильные банки стерильным шпателем переносят лиофильно высушенную субстанцию Фортеплазе, укупоривают и после этого взвешивают наполненные банки с точностью до 0,1 г. По разности между весом пустой и заполненной банки определяют вес сухой субстанции Фортеплазе в упаковке. Заполняют этикетку, на которой указаны название субстанции, дата изготовления, номер серии, количество в граммах, условия хранения и срок годности. Передают упаковку на карантинное хранение.
При положительном заключении по качеству субстанции препарат поступает на склад.
Субстанцию Фортеплазе хранят в защищенном от света месте при температуре 2-25°С.
Срок хранения 3 года.
Краткая схема производственного процесса и внутрипроизводственного контроля получения субстанции Фортеплазе:

Проводят оценку пирогенности и аномальной токсичности с использованием следующих доз.
Тест-доза для проверки на пирогенность 0,133 мг субстанции в 0,5 мл 0,9% раствора натрия хлорида для инъекций на 1 кг массы тела кролика. Вещество апирогенно.
Тест-доза для проверки на токсичность 312 мкг Фортеплазе в 0,5 мл 0,9% раствора натрия хлорида для инъекций на мышь. Вещество нетоксично.
Субстанцию Фортеплазе используют для приготовления лекарственного препарата, обладающего фибринолитическими свойствами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА ФОРТЕЛИЗИН, ОБЛАДАЮЩЕГО ФИБРИНОЛИТИЧЕСКИМИ СВОЙСТВАМИ, И ЕГО ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ИНФАРКТА МИОКАРДА | 2011 |
|
RU2448158C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕННО-ИНЖЕНЕРНОГО ИНСУЛИНА ЧЕЛОВЕКА | 2006 |
|
RU2322504C1 |
| СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИНСУЛИНА ЧЕЛОВЕКА | 1999 |
|
RU2141531C1 |
| СПОСОБ ХРОМАТОГРАФИЧЕСКОГО ВЫДЕЛЕНИЯ И ОЧИСТКИ БЕЛКОВ, ПЕПТИДОВ И ИХ КОМПЛЕКСОВ | 1997 |
|
RU2122549C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОВОИНГИБИТОРА | 1997 |
|
RU2129438C1 |
| ШТАММ БАКТЕРИЙ Escherichia coli - ПРОДУЦЕНТ БЕЛКА ТЕПЛОВОГО ШОКА 70 И СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА БЕЛКА ТЕПЛОВОГО ШОКА ЧЕЛОВЕКА | 2013 |
|
RU2564120C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬФА-ФОТОПРОТЕИНА | 1995 |
|
RU2100031C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКООЧИЩЕННОГО КРИСТАЛЛИЧЕСКОГО ИНСУЛИНА ЛЮБОГО ПРОИСХОЖДЕНИЯ | 2011 |
|
RU2453331C1 |
| СПОСОБ ВЫДЕЛЕНИЯ И ОЧИСТКИ АЛЬФА-ФЕТОПРОТЕИНА | 2005 |
|
RU2302424C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА АЛЬФА-ФЕТОПРОТЕИНА | 1998 |
|
RU2123009C1 |

Изобретение относится к биотехнологии и фармакологии. Размораживают супернатант, содержащий рекомбинантный белок с аминокислотной последовательностью стафилокиназы (РБСФ). Выделяют и хроматографически очищают РБСФ на СМ-сефарозе. Производят хроматографическую очистку РБСФ на DEAE-сефарозе. Затем переводят РБСФ в раствор 0,3% NaCl. Осуществляют стерилизацию, фасовку, лиофильную сушку и маркировку субстанции. Изобретение расширяет арсенал средств с фибринолитическими свойствами.
Способ получения лиофилизированной субстанции, содержащей рекомбинантный белок с аминокислотной последовательностью стафилокиназы SEQ ID NO: 1, включающий размораживание супернатанта рекомбинантного белка с аминокислотной последовательностью стафилокиназы (РБСФ), полученного при культивировании штамма Escherichia coli MZ09, регистрационный номер В-10417 ВКПМ, хроматографическую очистку и выделение РБСФ на СМ-сефарозе с последующей хроматографической очисткой на DEAE-сефарозе, перевод РБСФ в 0,3%-ный раствор NaCl, стерилизацию, фасовку и лиофильную сушку субстанции.
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ТРОМБОЛИТИЧЕСКИМ И ФИБРИНОЛИТИЧЕСКИМ ДЕЙСТВИЕМ | 2002 |
|
RU2216348C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ФИБРИНОЛИТИЧЕСКИМ ДЕЙСТВИЕМ | 2007 |
|
RU2323001C1 |
Авторы
Даты
2012-04-20—Публикация
2011-03-17—Подача