Изобретение относится к получению азометинов - производных аминов 2-фенилбензоксазола и дигидроксибензальдегидов, которые обладают интенсивной люминесценцией при λ 372-505 нм при возбуждении светом с длиной волны λ 344 нм.
Полученные соединения могут быть использованы в качестве мономеров для синтеза люминесцентных жестко-гибких сополиэфиров. Интенсивная люминесценция, проявляемая ими, позволяет вводить эти мономеры наряду с нелюминесцирующими бис-фенолами при проведении поликонденсации с дихлорангидридами дикислот в малых количествах, таких, чтобы полимер содержал не более 1-ного молекулярного звена с бензоксазольным фрагментом на 200-300 молекулярных звеньев, не содержащих гетероароматический бензоксазольный фрагмент.
Образование азометиновых соединений, или оснований Шиффа, зависит от активности исходных реагентов, т.е. от основности аминогрупп (нуклеофильности) в аминах и активности альдегидной группы. В случае, если активность обоих компонентов достаточно высока, реакция образования азометинов протекает легко в одном из органических растворителей, в нейтральной или даже в слабощелочной среде [Вейгандт-Хильгетаг. Методы эксперимента в органической химии / Под ред. Суворова Н.Н. - М.: Химия, 1968. 944 с.]. Известен широкий ряд азометинов на основе первичных ароматических аминов, не содержащих гетероцикл, и замещенных бензальдегидов. При использовании в качестве аминной компоненты малоосновного амина реакцию активируют за счет повышенной температуры и проводят процесс в высококипящих растворителях - м-крезоле, n-хлорфеноле или в в неполярных растворителях - толуоле, бензоле, ксилоле с азеотропной отгонкой образующейся воды [Imine Oligomers and Polymers / M.Grigogas, C.O.Catanescu // J. of Macromol. Science. Part C: Polymer Reviews. - 2004. - V. C44, №2. - P.131-173.]. Такие азометины не обладают люминесцентными свойствами.
Известны новые электропроводящие кремнийсодержащие полисалицилиденазометины на основе салицилового альдегида и ароматических ди- и тетраминов [Синтез и спектральные характеристики кремнийсодержащих полисалицилиденазометинов на основе ароматических ди- и тетрааминов / Н.М.Геллер, А.Г.Иванов, Л.Б. Надеждина, В.В.Шаманин. Журн. прикл. химии. - 2008. - Т.81, №8. - С 521-530]. Эти соединения обладают электропроводящими свойствами, но и у них отсутствует люминесценция.
Технической задачей и положительным результатом заявляемого изобретения является синтез новых гетероароматических бензоксазолсодержащих азометинов, которые обладают рядом полезных свойств: интенсивной люминесценцией, содержат две функциональные гидроксигруппы, за счет которых могут использоваться как бифункциональные мономеры для получения люминесцирующих полимеров, а также в качестве люминесцентных меток для различных материалов.
Сущностью и основными отличительными признаками заявляемого изобретения является то, что осуществлен синтез серии новых люминесцентных азометинов на основе аминов 2-фенилбензоксазола, содержащих аминогруппы как в бензоксзольном, так и в фенильном фрагменте молекулы, и 2,5- и 3,4-дигидроксибензальдегидов в алифатических спиртах - метиловом, этиловом, изопропиловом в присутствии кислотного катализатора. При этом люминесцентные азометины содержат вещество общей формулы:
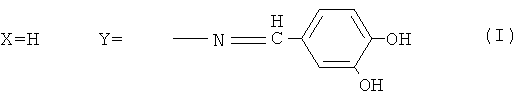

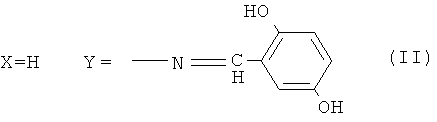
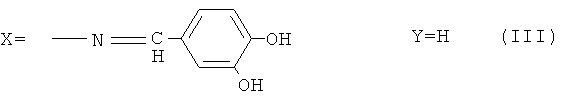
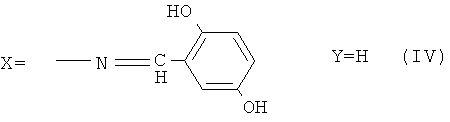
Кислотными катализаторами в этой реакции являются соляная, дихлоруксусная, муравьиная кислоты. Температура реакции от 20 до 60°С, при этом для получения соответствующего азометина выбирают следующее соотношение указанных компонентов, мас.%: амин - 2 фенилбензотиазола - 1.62-1.78; дигидрокси-замещенный бензальдегид 1.09-1.0; кислотный катализатор 0.03-0.06; полярный растворитель - остальное.
Использование метилового, этилового и изопропилового спирта в качестве растворителя, кислотных катализаторов, проведение реакции конденсации при 20-60°С позволило получить новые азометины с выходом 75-90%, а использование в качестве реагента бензотиазолсодержащих аминов придало им люминесцентные свойства.
Пример 1. Реакцию получения азометина (I) проводили при мольном соотношении альдегида и амина 1.0:1.1, при этом раствор 1.0 г (7.2 ммоль) 3,4-дигидроксибензальдегида в 40 мл метанола с добавлением 0.02 мл раствора концентрированной соляной кислоты прикалывали к раствору 1.78 г (7.92 ммоль) 2-(4-аминофенил)бензотиазола в 90 мл метанола. В течение 5 ч реакционную массу перемешивали при 50°С. Выпавший осадок отфильтровывали, промывали, сушили. Выход 2.0 г (80%), вещество (I) кристаллизовали из изопропанола. Чистота полученного продукта подтверждена данными ТСХ: одно пятно Rf 0.71 (адсорбент - Sorbfil, элюент - толуол: этилацетат - 1:1, растворитель - ДМФА), т.пл. 194-195°С. ИК-спектр, (KBr, v см-1): 1618.67 (-CH=N-) азометиновой группы.
Пример 2. Реакцию получения азометина (I) проводили аналогично примеру 1 при мольном соотношении альдегида и амина 1.1:1.0, при этом в реакцию вводили раствор 1.09 г (7.92 ммоль) 3,4-дигидроксибензальдегида в 40 мл метанола с добавлением 0.02 мл раствора концентрированной соляной кислоты и 1.62 г (7.2 ммоль) 2-(4-аминофенил)бензотиазола в 90 мл метанола. Выход 2.0 г (80%), вещество (I), кристаллизовали из изопропанола. Чистота полученного продукта подтверждена данными ТСХ: одно пятно Rf 0.71 (адсорбент - Sorbfil, элюент - толуол: этилацетат - 1:1, растворитель - ДМФА), т.пл. 194-195°С. ИК-спектр, (KBr, v см-1): 1618.67 (-CH=N-) азометиновой группы.
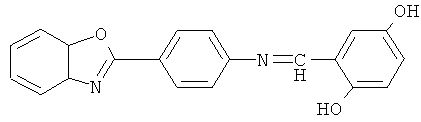
Пример 3. Реакцию получения азометина (II) проводили при мольном соотношении альдегида и амина 1.0:1.1, при этом раствор 1.0 г (7.2 ммоль) 2,5-дигидроксибензальдегида в 40 мл метанола с добавлением 0.02 мл раствора концентрированной соляной кислоты прикалывали к раствору 1.78 г (7.92 ммоль) 2-(4-аминофенил)бензотиазола в 90 мл метанола. В течение 5 ч реакционную массу перемешивали при 50°С. Выпавший осадок отфильтровывали, промывали, сушили. Выход 1.58 г (63%), вещество (II), кристаллизовали из изопропанола. Чистота полученного продукта подтверждена данными ТСХ: одно пятно Rf 0. 86 (адсорбент - Sorbfil, элюент - толуол: этилацетат - 1:1, растворитель - ДМФА)., т.пл. 237-240°С. ИК-спектр, (KBr, v см-1): 1621.06 (-CH=N-) азометиновой группы.
Пример 4. Реакцию получения азометина (II) проводили аналогично примеру 3 при мольном соотношении альдегида и амина 1.1:1.0, при этом в реакцию вводили раствор 1.09 г (7.92 ммоль) 2,5-дигидроксибензальдегида в 40 мл метанола с добавлением 0.02 мл раствора концентрированной соляной и 1.62 г (7.2 ммоль) 2-(4-аминофенил)бензотиазола в 90 мл метанола. Выход 2.0 г (63%) вещества (II), которое кристаллизовали из изопропанола. Чистота полученного продукта подтверждена данными ТСХ: одно пятно Rf 0. 86 (адсорбент - Sorbfil, элюент - толуол: этилацетат - 1:1, растворитель - ДМФА)., т.пл. 237-240°С. ИК-спектр, (KBr, v см-1): 1621.06 (-CH=N-) азометиновой группы.
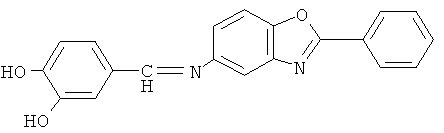
Пример 5. Реакцию получения азометина (III) проводили при мольном соотношении альдегида и амина 1.0:1.1, при этом раствор 1.0 г (7.2 ммоль) 3,4-дигидроксибензальдегида в 40 мл метанола с добавлением 0.02 мл раствора концентрированной соляной кислоты прикалывали к раствору 1.78 г (7.92 ммоль) 5-амино-2-фенилбензотиазола в 90 мл метанола. В течение 5 ч реакционную массу перемешивали при 50°С. Выпавший осадок отфильтровывали, промывали, сушили. Выход 2.0 г (80%), вещество (III) кристаллизовали из изопропанола. Чистота полученного продукта подтверждена данными ТСХ: одно пятно Rf 0.84 (адсорбент - Sorbfil, элюент - толуол: этилацетат - 1:1, растворитель - ДМФА), т.пл. 230°С. ИК-спектр, (KBr, v см-1): 1618.67 (-CH=N-) азометиновой группы.
Пример 6. Реакцию получения азометина (III) проводили аналогично примеру 5 при мольном соотношении альдегида и амина 1.1: 1.0, при этом раствор 1.09 г (7.92 ммоль) 3,4-дигидроксибензальдегида в 40 мл метанола с добавлением 0.02 мл раствора концентрированной соляной кислоты прикалывали к раствору 1.62 г (7.2 ммоль) 5-амино-2-фенилбензотиазола в 90 мл метанола. Выход 2.0 г (80%), вещество (III), кристаллизовали из изопропанола. Чистота полученного продукта подтверждена данными ТСХ: одно пятно Rf 0.84 (адсорбент - Sorbfil, элюент - толуол: этилацетат - 1:1, растворитель - ДМФА), т.пл. 230°С. ИК-спектр, (KBr, v см-1): 1618.67 (-CH=N-) азометиновой группы.
Пример 7. Реакцию получения азометина (IV) проводили при мольном соотношении альдегида и амина 1.0:1.1, при этом раствор 1.0 г (7.2 ммоль) 2,5-дигидроксибензальдегида в 40 мл метанола с добавлением 0.02 мл раствора концентрированной соляной кислоты прикалывали к раствору 1.78 г (7.92 ммоль) 5-амино-2-фенилбензотиазола в 90 мл метанола. В течение 5 ч реакционную массу перемешивали при 50°С. Выпавший осадок отфильтровывали, промывали, сушили. Выход 2.08 г (83%), вещество (IV), кристаллизовали из изопропанола. Чистота полученного продукта подтверждена данными ТСХ: одно пятно Rf 0.84 (адсорбент - Sorbfil, элюент - толуол: этилацетат - 1:1, растворитель - ДМФА), т.пл. 228-230°С. ИК-спектр, (KBr, v см-1): 1618.17 (-CH=N-) азометиновой группы.
Пример 8. Реакцию получения азометина (IV) проводили аналогично примеру 5 при мольном соотношении альдегида и амина 1.1:1.0, при этом раствор 1.09 г (7.92 ммоль) 2,5-дигидроксибензальдегида в 40 мл метанола с добавлением 0.02 мл раствора концентрированной соляной кислоты прикалывали к раствору 1.62 г (7.2 ммоль) 5-амино-2-фенилбензотиазола в 90 мл метанола. Выход 2.08 г (83%), вещество (IV), кристаллизовали из изопропанола. Чистота полученного продукта подтверждена данными ТСХ: одно пятно Rf 0.84 (адсорбент - Sorbfil, элюент - толуол: этилацетат - 1:1, растворитель - ДМФА), т.пл. 228-230°С. ИК-спектр, (KBr, v см-1): 1618.17 (-CH=N-) азометиновой группы.
Пример 9. Реакцию получения азометинов (I-IV) проводили аналогично примерам 1-8 при мольном соотношении альдегида и амина от 1.0:1.1 до 1.1:1.0, используя в качестве катализатора дихлоруксусную кислоту в количествах, аналогичных примерам 1-8. Выходы и константы (т.пл., величина Rf) для соединений (I-IV) совпадали со значениями, приведенными в примерах 1-8.
Пример 10. Реакцию получения азометинов (I-IV) проводили аналогично примерам 1-8 при мольном соотношении альдегида и амина от 1.0:1.1 до 1.1:1.0, используя в качестве катализатора муравьиную кислоту в количествах, аналогичных примерам 1-8. Выходы и константы (т.пл., величина Rf) для соединений (I-IV) совпадали со значениями, приведенными в примерах 1-8.
В условиях примеров 1-8 исследовали регламент получения соединений I-IV при мольном соотношении альдегида и амина и дозировке компонентов за обоими указанными пределами их количеств в реакционной массе (мас.%). При этом наблюдалось значительное уменьшение выхода и понижение качества получаемых соединений за счет остающихся исходных компонентов. Это требовало длительной и тщательной очистки азометинов, что, в конечном итоге, резко понижало их выход, а остающиеся примеси приводили к тушению люминесценции.
Варьирование природы кислотного катализатора, в частности использование менее слабых органических кислот: уксусной, замещенных бензойных кислот, показало, что именно предлагаемые в заявке соляная, дихлоруксусная, муравьиная кислоты приводили к наилучшим результатам по чистоте и качеству получаемого люминесцентного азометина.
Полученные данные свидетельствуют о правильности и точности выбора соотношений компонентов и условий проведения реакции при получении заявляемых соединений. Все заявляемые соединения обладают интенсивной люминесценцией при возбуждении светом с λ 339-344 нм. В таблице приведены люминесцентные характеристики полученных азометинов.
Таким образом, заявлены новые люминесцентные азометины - производные аминов 2-фенилбензотиазола и дигидроксибензальдегидов, которые могут быть использованы в качестве мономеров для получения самоорганизующихся люминесцентных полимеров, люминесцентных меток для различных органических композитов.
НМ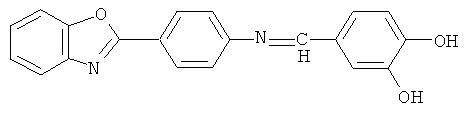

| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЮМИНЕСЦЕНТНЫЕ АЗОМЕТИНЫ БЕНЗОТИАЗОЛЬНОГО РЯДА | 2011 |
|
RU2459814C1 |
| Азометины на основе α-аминопиридина, обладающие гемолитической активностью | 2015 |
|
RU2631114C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХИРАЛЬНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ ЛИГАНДОВ НА ОСНОВЕ 1,2-ДИАМИНОЦИКЛОГЕКСАНА | 2013 |
|
RU2533424C1 |
| Новые 3,4-гидроксиамины пинановой структуры | 2016 |
|
RU2631871C1 |
| Селенсодержащие комплексы типа Ховейды-Граббса второго поколения и способ их получения | 2023 |
|
RU2807891C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОСТЫХ ПОЛИФТОРАЛКИЛОВЫХ ЭФИРОВ | 2007 |
|
RU2346926C1 |
| Способ получения хиральных монотерпеновых сульфинамидов | 2017 |
|
RU2650681C1 |
| МЕДНЫЕ КОМПЛЕКСЫ ПИРИДИНИЛМЕТИЛЕНАМИНО-БЕНЗО-15-КРАУНЫ-5 И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2661871C1 |
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ ОРГАНИЧЕСКОЕ ЛЮМИНЕСЦЕНТНОЕ ВЕЩЕСТВО | 2007 |
|
RU2368641C2 |
| ЦИНКОВЫЕ И КАДМИЕВЫЕ КОМПЛЕКСЫ ТЕТРАДЕНТАТНЫХ АЗОМЕТИНОВ 2-ТОЗИЛАМИНОБЕНЗАЛЬДЕГИДА, ОБЛАДАЮЩИЕ ЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2532642C1 |
Изобретение относится к соединениям общей формулы
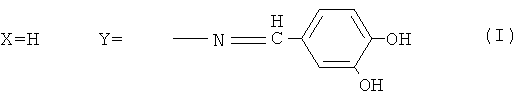




Технический результат - новые люминесцентные азометины, используемые в качестве мономеров для синтеза люминесцентных жестко-гибких сополиэфиров, а также в качестве люминесцентных меток для различных органических композитов. 4 з.п. ф-лы, 1 табл., 8 пр.
1. Люминесцентные азометины, содержащие вещество общей формулы
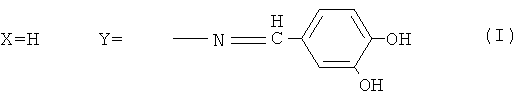




получаемые реакцией конденсации аминов 2-фенилбензоксазола и дигидроксибензальдегидов в полярном растворителе в присутствии кислотных катализаторов.
2. Люминесцентные азометины по п.1, отличающиеся тем, что в качестве полярного растворителя используют метиловый, этиловый, изопропиловый спирты, при этом в качестве дигидроксибензальдегидов используют 2,5-дигидроксибензальдегид и 3,4-дигидроксибензальдегид.
3. Люминесцентные азометины по п.1, отличающиеся тем, что в качестве кислотного катализатора используют соляную, дихлоруксусную, муравьиную кислоты.
4. Люминесцентные азометины по п.1, отличающиеся тем, что мольное соотношение амина 2-фенилбензоксазола и дигидроксибензальдегида выбирают в пределах от 1,1:1 до 1:1,1.
5. Люминесцентные азометины по п.1, отличающиеся тем, что температуру реакционной массы поддерживают в пределах от 20 до 60°C, при этом для получения соответствующего азометина выбирают следующее соотношение указанных компонентов, мас.%:
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Laliteshwar P | |||
| Singh et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| - Der Pharma Chemica, 2010, 2(4), p.206-212 | |||
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ ОРГАНИЧЕСКОЕ ЛЮМИНЕСЦЕНТНОЕ ВЕЩЕСТВО | 2007 |
|
RU2368641C2 |
| Иванов А.Г | |||
| и др | |||
| Синтез новых светочувствительных кремнийсодержащих полисалицилиденазометинов | |||
| Высокомолекулярные соединения, Серия Б, | |||
Авторы
Даты
2012-07-10—Публикация
2010-07-28—Подача