Изобретение относится к новым соединениям в ряду металлохелатов тетрадентатных азометиновых лигандов 2-тозиламинобензальдегида и алифатических диаминов, а именно к комплексам цинка и кадмия тетрадентатных азометинов 2-тозиламинобензальдегида и диоксидиаминов формулы I

I
где m=2-4, n=2-4, M=Zn, Cd
Металлокомплексные соединения I могут быть использованы в качестве электролюминесцентого слоя при создании светоизлучающих органических диодов (OLED) белого и видимого света. Одной из важных характеристик для таких соединений является высокие квантовые выходы фотолюминесценции. Особенно востребованными являются металлохелаты, излучающие в синей области спектра.
Известен бис[(2-тозиламино)бензилиден-N-алкилиминаты]цинка общей формулы II
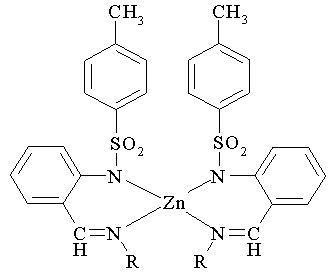
II, где R=C1-C6 - алкил
Соединения II проявляют люминесцентные свойства в синей области спектра, их квантовые выходы составляют порядка 0,3, а термостабильность порядка 260°C [патенты RU № 2295527, C07F 3/06, 2007 г. и № 2395512, C07F 3/06, 2007 г.].
Известен бис[(2-тозиламино)бензилиден-N-алкилиминаты]цинка общей формулы III:
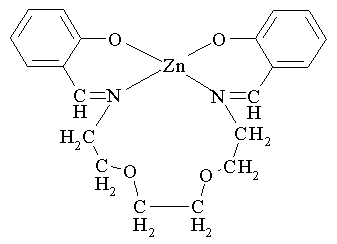
III
Соединение III проявляет фотолюминесцентные свойства в синей области спектра: полоса поглощения λ = 368 нм, полоса электролюминесценции λ = 455 нм. Оно использовалось при создании OLEDs с яркостью 730 кд/м2, что соответствует квантовой эффективности 1.2 кд/А при напряжении 6.3 В [Yu T., Su W., Li W., Hong Z., Hua K. et al. Inorg. Chim. Acta. 2006. V. 359. P. 2246-2251]. Соединение термостабильно до температуры 315°C.
Наиболее близким по выполнению и достигаемому результату является N,N'-бис[(2-тозиламинобензилиден) -1, 3-диамино-2-пропанол] цинка формулы IV:
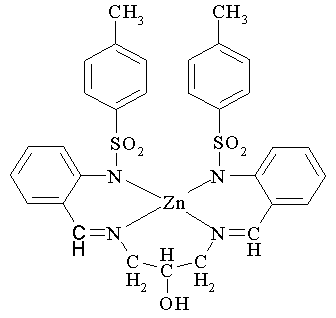
IV
Соединение IV проявляет люминесцентные свойства (полоса флуоресценции λ = 430 нм (ацетонитрил), квантовый выход φ = 0.14). Сведения о его термостабильности не приводятся [M.R. Bermejo, M. Vazquez, J. Sanmartin et al. New J. Chem. 2002. V. 26. P. 1365-1370].
Задачей изобретения является расширение серии люминесцирующих комплексов цинка и кадмия, излучающих в синей области спектра и обладающих высокой термостабильностью и летучестью.
Техническим результатом изобретения являются новые соединения в ряду металлохелатов тетрадентатных азометиновых лигандов 2-тозиламинобензальдегида и алифатических диаминов, проявляющие фотолюминесцентные свойства в синей области спектра с более высокими квантовыми выходами люминесценции, обладающие высокой термостабильностью и летучестью в условиях вакуумного напыления.
Технический результат изобретения достигается соединениями общей формулы I.
Изобретение удовлетворяет критерию изобретательского уровня, так как в ряду металлохелатов тетрадентатных азометиновых лигандов 2-тозиламинобензальдегида и алифатических диаминов не известна взаимосвязь между строением соединений и их люминесцентными свойствами.
Азометины, использованные для синтеза комплексов I, получают конденсацией 2-тозиламинобензальдегида и соответствующих аминов. Хелаты получают взаимодействием лигандов с солями металлов (хс) и электрохимическим способом (эс).
Ниже приведены примеры получения соединений.
Пример 1. N,N-бис(2-тозиламинобензаль)-3,6-диокса-1,8-октандиамин (лиганд для Iа, где M= Zn, и Iб, где M = Cd, m= n=2). К раствору 0.55 г (2 ммоль) 2-тозиламинобензальдегида в 30 мл абсолютного толуола прибавляют 0.148 г (1 ммоль) 1,8-диамино-3,6-диоксаоктана в 10 мл абсолютного толуола. Смесь кипятят в течение 2-х часов. Отгоняют растворитель, осадок отфильтровывают и перекристаллизовывают. Светло-желтые кристаллы. Выход 80 %. Тпл = 134-135°С. Найдено, %: C 61.82; H 5.64; N 8.52; S 9.84. Для C34H38N4O6S2, вычислено, %: C 61.61; H 5.78; N 8.45; S 9.68.
1H ЯМР спектр, DMSO d 6, δ, м.д.: 2.22 (6 H, c, CH3), 3.60 (4H, c, CH2), 3.69 (8H, c, CH2), 7.01-7.63 (16H, м, CAr-H), 8.36 (2H, c, CH=N), 13.06 (2H, уш. с., NH).
ИК-спектр (порошок), ν, см-1: 2909 сл (CH2), 2862 сл (NH), 1638 с (CH=N), 1599 сл, 1579 сл, 1497 ср, 1434 ср, 1402 сл, 1336 с, 1305 ср, 1278 ср (as, SO2), 1207 сл, 1156 (s, SO2), 1123 c, 1091 с, 1062 сл, 1039 ср, 947 ср, 933 ср, 908 ср, 837 ср, 815 ср 756 с, 727 с, 705 сл, 658 с.
УФ-спектр (ацетонитрил), λ, нм (ε л·моль-1·см-1): 221 (75400), 257 (23900), 311 (7100). Соединение не люминесцирует.
Пример 2. N,N'-бис(2-тозиламинобензаль)-4,9-диокса-1,12-додекандиамин (лиганд для Iв, где M = Zn, n = 3, m =4) получают аналогично примеру 1 из 0.55 г (2 ммоль) 2-тозиламинобензальдегида и 0.298 г (1ммоль) 4,9-диокса-1,12-додеканамина.
Светло-желтый порошок. Выход 96 %. Тпл = 89 - 90°С. Найдено, %: С 63,65; H 6.38; N 7.82; S 8.74. Для C38H46N4O6S2, вычислено, %: С 63,48; H 6.45; N 7.79; S 8.92.
1H ЯМР спектр, DMSO d 6, δ, м.д.: 1.55 (4 Н, д, CH2), 1.86 (4 Н, м, СН2), 2.48 (6Н, с, СН3), 3.39 (8 Н, м, СН2), 3.64 (4 Н, т, СН2), 7.04 - 7.09 (2 Н, м, CAr-H), 7.29 - 7.64 (14 Н, м, CAr-H), 8.44 (2 Н, с, CH=N), 13.25 (2 Н, уш. с., NH).
ИК-спектр (порошок), ν, см-1: 2939 сл (СН2), 2858 сл, 1634 ср (CH=N), 1597 сл, 1552 сл, 1433 сл, 1338 ср (as, SO2), 1305 сл, 1280 ср, 1168 ср, 1154 ос (s, SO2), 1112 ср, 1090 ср, 940 ср, 843 ср, 813 ср, 759 с, 730 сл, 705 сл, 659 с, 614 сл.
УФ-спектр (ацетонитрил), λ, нм (ε л·моль-1·см-1): 221 (69500), 257 (21700), 311 (6200). Соединение не люминесцирует.
Комплексы цинка и кадмия Ia,б,в получают химическим и электрохимическим способами.
Пример 3. Химический способ (хс) получения: [N,N'-бис(2-тозиламинобензаль)-3, 6-диокса-1, 8-октандиамин)]цинка Ia (M = Zn, m = n = 2).
К раствору 0.33 г (0.5 ммоль) N,N'-бис(2-тозиламинобензаль)-3, 6-диокса-1, 8-диаминооктана в 20 мл метилового спирта прибавляют раствор 0.11 г (0.5 ммоль) дигидрата ацетата цинка в 5 мл метилового спирта или 0.13 г (0.5 ммоль) дигидрата ацетата кадмия. Смесь кипятят в течение 2-х часов. Выпавший при охлаждении осадок отфильтровывают, промывают и перекристаллизовывают.
Электрохимический способ (эс) получения соединений I. В электрохимическую ячейку с платиновым катодом и цинковым (или кадмиевым) анодом помещают раствор 0.33 г (0.5 ммоль) N,N'-бис(2-тозиламинобензаль)-3, 6-диокса-1, 8-октандиамина в 20 мл ацетонитрила, добавляют 0.01 г [Et4N]ClO4 в качестве токопроводящей добавки. Электросинтез осуществляют при силе тока 40 мA и напряжении 20 В в течение 1 часа при комнатной температуре. Выпавшие осадки комплексов отфильтровывают и перекристаллизовывают.
Катод (Pt): LH2 + 2 e → L-2 + H2
Анод: (Zn0 или Cd0) M - 2 e → M2+ (M = Zn, Cd)
Раствор: L2- + M2+ → ML
[N,N'-бис(2-тозиламинобензаль)-3, 6-диокса-1, 8-октандиамин]цинка. Ia (M = Zn): Белые кристаллы. Тпл > 320°. Выход: 85 % (хс), 95 % (эс). Найдено, %: C 56.30 (хс), 56.32 (эс); H 5.11 (хс), 5.13 (эс); N 7.82 (хс), 7.68 (эс); S 8.90 (хс), S 8.92 (эс); Zn 9.12 (хс), 9.15 (эс). Для C34H36N4O6S2Zn, вычислено, %: С 56.23; Н 5.00; N 7.72; S 8.83; Zn 9.00.
1H ЯМР спектр, DMSO d 6, δ, м.д.: 2.22 (6 Н, с, СН3), 3.14 (2Н, д, CH2), 3.51-3.60 (8 Н, м, СН2). 4.21-4.29 (2 Н, м, СН2), 6.84 (2Н, т, CAr-H), 7.11-7.20 (8 Н, м, CAr-H), 7.26-7.28 (2 Н, м, CAr-H), 7.91-7.92 (4 Н, д, CAr-H), 8.45 (2Н, с, CH=N).
ИК-спектр (порошок), ν, см-1: 2926 осл, 2853 сл, 1636 с (CH=N), 1599 ср, 1558 ср, 1482 ср, 1442 ср, 1414 сл, 1285 с, 1258 с (as, SO2), 1231 сл, 1198 сл, 1175 сл, 1140 ос (s, SO2), 1120 ср, 1095 ос, 1044 сл, 949 с, 921 с, 864 с, 834 ср, 815 ср, 763 с, 708 сл, 692 ос, 652 с, 588 ср, 563 ос.
Спектр поглощения (ацетонитрил), λ, нм (ε л·моль-1·см-1): 234 (76900), 270 (21100), 277 (20500), 350 (12100). Спектр флуоресценции: максимум полосы флуоресценции 433 нм (синяя область). Квантовый выход флуоресценции φ = 0.29.
Соединение легко летуче в условиях вакуумного напыления.
Пример 4. [N,N'-бис(2-тозиламинобензаль)-3, 6-диокса-1, 8-октандиамин]кадмия. Iб (M = Cd, m = n =2): Белые кристаллы. Тпл > 320°C. Выход: 70 % (хс), 82 % (эс). Найдено, %: C 52.78 (хс), 52.84 (эс); H 4.71 (хс), 4.59 (эс); N 7.422 (хс), 7.40 (эс); S 8.35 (хс), S 8.39 (эс); Cd 14.60 (хс), 14.65 (эс). Для C34H36N4O6S2Cd, вычислено, %: С 52.84; Н 4.69; N 7.25; S 8.29; Cd 14.54.
1H ЯМР спектр, DMSO d 6, δ, м.д.: 2.22 (6 Н, с, СН3), 3.13-3.15 (2Н, м, CH2), 3.51-3.60 (8 Н, м, СН2). 4.23 (2 Н, д, СН2), 6.83-6.86 (2Н, т, CAr-H), 7.11-7.20 (8 Н, м, CAr-H), 7.26-7.28 (2 Н, м, CAr-H), 7. 50-7. 92 (4 Н, м, CAr-H), 8.45 (2Н, с, CH=N).
ИК-спектр (порошок), ν, см-1: 2928 осл, 2870 осл, 2849 сл (СН2), 1635 с (CH=N), 1598 с, 1557 с, 1481 с, 1442 с, 1412 сл, 1285 с, 1257 ос (as, SO2), 1231 сл, 1198 сл, 1174 сл, 1138 (s, SO2), 1119 с, 1107 с, 1083 ос, 1044 сл, 949 с, 922 с, 904 сл, 863 ср, 833 ср, 813 ср, 768 с, 707 ср, 691 ос, 651 с, 638 с, 587 ср, 569 ос.
Спектр поглощения (ацетонитрил), λ, нм (ε л·моль-1·см-1): 234 (80000), 270 (21300), 277 (20800), 350 (12300). Спектр флуоресценции: максимум полосы флуоресценции 433 нм (синяя область). Квантовый выход флуоресценции φ = 0.25.
Соединение легко летуче в условиях вакуумного напыления.
Пример 5. [N,N'-бис(2-тозиламинобензаль)-4, 9-диокса-1, 12-додекандиамин]цинка Iв (M = Zn, m = 4, n = 3). Получен аналогично примеру 3 химическим из 0.71 г (1 ммоль) N,N'-бис(2-тозиламинобензаль)-4, 9-диокса-1, 12-додекандиамина и 0.22 г (1 ммоль) дигидрата ацетата цинка в растворе метанола или электрохимическим способом в ацетонитриле.
Белые кристаллы. Тпл > 320°C. Выход: 85 % (хс), 90 % (эс). Найдено, %: C 58.42 (хс), 58.30 (эс); H 5.70 (хс), 5.65 (эс); N 7.26 (хс), 7.20 (эс);S 8.19 (хс), S 8.27 (эс); Zn 8.40 (хс), 8.25 (эс). Для C38H44N4O6S2Zn, вычислено, %: С 58.34; Н 5.67; N 7.16; S 8.29; Zn 8.36.
1H ЯМР спектр, DMSO d 6, δ, м.д.: 1.36 (4 Н, д, СН2), 1.73 (4 Н, уш. с., СН2), 2.24 (6 Н, с, СН3), 3.25-3.33 (4 Н, м, СН2), 3.37-3.41 (4 Н, м, СН2), 6.82-6.90 (2 Н, м, CAr-H), 7.14-7.51 (10 Н, м, CAr-H), 7.92 (4 Н, т, CAr-H), 8.54 (2 Н, с, CH=N).
ИК-спектр (порошок), ν, см-1: 2934 сл, 2864 сл (CH2), 1629 c (CH=N), 1598 ср, 1557 ср, 1482 сл, 1421 сл, 1296 с, 1287 с, 1258 с (as SO2), 1198 сл, 1174 сл, 1134 ос (s SO2), 1081 ос, 946 с, 860 с, 833 ср, 812 ср, 753 ср, 708 сл, 663 ос, 575 с.
Спектр поглощения (ацетонитрил), λ, 270, 350 нм. Спектр флуоресценции: максимум полосы флуоресценции λ = 433 нм (синяя область). Квантовый выход флуоресценции φ = 0.25.
Соединение легко летуче в условиях вакуумного напыления.
Строение комплексов Ia и Iб установлено методом рентгеноструктурного анализа (РСА). Методами квантовой химии в приближении функционала плотности DFT (B3LYP/6 - 31 G(d), программа Gaussian-03) получены структурные параметры оптимизированных молекул азометиновых лигандов для комплексов Ia и Iб. В рамках метода DT-DEF рассчитаны их электронные спектры поглощения, характеристики которых оказались близкими к экспериментальным значениям.
Таким образом, предлагаемые соединения обладают более высокими квантовыми выходами (0,3 вместо 0,14), чем прототип, достаточно термостабильны (Тпл > 320°C) и легко летучи в условиях вакуумного напыления.
| название | год | авторы | номер документа |
|---|---|---|---|
| [N,N'-БИС(2-ТОЗИЛАМИНОБЕНЗИЛИДЕН)ДИАМИНОДИПРОПИЛИМИНАТ]МЕТАЛЛА, ОБЛАДАЮЩИЙ ЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2562456C1 |
| Комплексы цинка 2-(N-тозиламинобензилиден)-2'-иминоалкилпиридинов, обладающие люминесцентной активностью | 2016 |
|
RU2616979C1 |
| Комплексы цинка и кадмия N-[2-(алкилиминометил)фенил]-4-метилбензолсульфамидов, обладающие люминесцентной активностью | 2017 |
|
RU2650529C1 |
| БИС-[2-(ЗАМЕЩЁННЫЕ БЕНЗИЛИДЕН)-3',4'-ДИМЕТОКСИФЕНИЛЭТИЛИМИНАТЫ]ЦИНКА(II), ОБЛАДАЮЩИЕ ЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2602263C1 |
| ЦИНКОВЫЕ КОМПЛЕКСЫ 5-[2-ГИДРОКСИ(ТОЗИЛАМИНО)БЕНЗИЛИДЕНАМИНО]-2-(2-ТОЗИЛАМИНОФЕНИЛ)-1АЛКИЛБЕНЗИМИДАЗОЛОВ, ОБЛАДАЮЩИЕ ФОТОЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2532904C1 |
| БИС[2-(N-ТОЗИЛАМИНО)БЕНЗИЛИДЕН-4'-ДИМЕТИЛАМИНОФЕНИЛИМИНАТО]ЦИНКА(II) И ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО НА ЕГО ОСНОВЕ | 2012 |
|
RU2518893C1 |
| БИС[2-(ТОЗИЛАМИНО)БЕНЗИЛИДЕН-N-АЛКИЛ(АРИЛ, ГЕТАРИЛ)АМИНАТЫ]ЦИНКА, ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЮМИНОФОРОВ | 2006 |
|
RU2295527C1 |
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО | 2013 |
|
RU2551675C2 |
| МОЛЕКУЛЯРНЫЕ КОМПЛЕКСЫ БИС(1-ФЕНИЛ-3-МЕТИЛ-4-ФОРМИЛ-5-ПИРАЗОЛОНАТА)ЦИНКА И КАДМИЯ С АМИНОПРОИЗВОДНЫМИ АЗОТИСТЫХ ГЕТЕРОЦИКЛОВ, ОБЛАДАЮЩИЕ ЛЮМИНЕСЦЕНТНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2485128C1 |
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНОЕ УСТРОЙСТВО | 2009 |
|
RU2408648C1 |
Изобретение относится к новым металлохелатам, а именно к комплексам цинка и кадмия тетрадентатных азометинов 2-тозиламинобензальдегида и диоксидиаминов формулы I
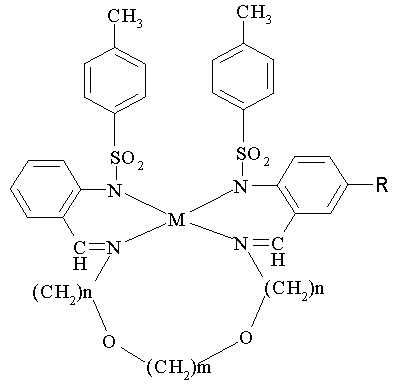
I
где m=2-4, n=2-4, M=Zn, Cd. Металлокомплексные соединения I проявляют фотолюминесцентные свойства в синей области спектра и могут быть использованы в качестве электролюминесцентого слоя при создании светоизлучающих органических диодов (OLED) белого и видимого света. 3 з.п. ф-лы, 5 пр.
1. Комплексы цинка и кадмия тетрадентатных азометинов 2-тозиламинобензальдегида и диоксидиаминов формулы I
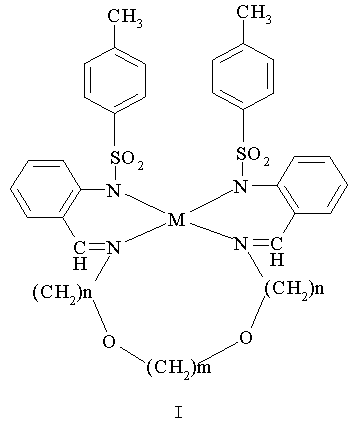
где m=2-4, n=2-4, M=Zn, Cd .
2. Комплексы цинка и кадмия по п. 1, где M = Zn, n = m = 2.
3. Комплексы цинка и кадмия по п. 1, где М = Cd, n = m = 2.
4. Комплексы цинка и кадмия по п. 1, где M = Zn, n = 3, m = 4.
| BERMEJO M.R | |||
| et al, Zinc and cadmium complexes with an achiral symmetric helicand | |||
| Crystal structure of an enantiomerically pure -Zn(II) monohelicate, New | |||
| J | |||
| Chem., 2002, v | |||
| Прибор для получения стереоскопических впечатлений от двух изображений различного масштаба | 1917 |
|
SU26A1 |
| Приспособление для подачи коробок к машинам для сборки коробок и наклеивания ярлыков | 1924 |
|
SU1365A1 |
| YU T | |||
| et al, Synthesis, crystal structure and electroluminescent properties of a Schiff base zinc complex, Inorganica Chimica Acta, 2006, v | |||
| Способ получения гидроцеллюлозы | 1920 |
|
SU359A1 |
| Микрофонно-телефонное устройство | 1925 |
|
SU2246A1 |
| БИС[2-(ТОЗИЛАМИНО)БЕНЗИЛИДЕН-N-АЛКИЛ(АРИЛ, ГЕТАРИЛ)АМИНАТЫ]ЦИНКА, ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЮМИНОФОРОВ | 2006 |
|
RU2295527C1 |
| ЭЛЕКТРОЛЮМИНЕСЦЕНТНЫЙ МАТЕРИАЛ, СОДЕРЖАЩИЙ ОРГАНИЧЕСКОЕ ЛЮМИНЕСЦЕНТНОЕ ВЕЩЕСТВО | 1998 |
|
RU2140956C1 |
Авторы
Даты
2014-11-10—Публикация
2013-07-08—Подача