Изобретение относится к области медицины, а также биохимии и физиологии, и может быть использовано для получения биологически активных веществ, способных регулировать устойчивость клеток крови к повреждающим факторам, в лабораторных и промышленных условиях.
Известен способ получения веществ, рассеивающих протонный градиент, создаваемый дыханием, и влияющих на окислительное фосфорилирование в митохондриях, взаимодействием 2-амино-4,6-динитрофенола и салицилового альдегида или п-диметилбензальдегида (патент RU 2472775 С1 от 07.06.2011). Сущность способа заключается в том, что получены различные азометины, содержащие динитрофенильный фрагмент, соединенный с различными радикалами, рассеивающие протонный градиент, создаваемый дыханием, и влияющие на окислительное фосфорилирование в митохондриях.
Известен способ получения азометинов 1,2,4-триазинов (патент RU 2146251 С1 от 18.01.1999), обладающих рострегулирующей и гербицидной активностями. Сущность метода заключается в создании новых соединений гетероциклического ряда по реакции 5-амино-3,6-диметил-1,2,4-триазина с (1) толуолом, бензальдегидом, п-толуолсульфокислотой, (2) п-хлорбензальдегидом, (3) фурфуролом, (4) валериановым альдегидом. Полученные соединения могут быть использованы в сельскохозяйственной практике для повышения урожая культур.
Известен способ получения азометинов 1,2,4-триазинов-5 (патент RU 2146252 С1 от 18.01.1999), обладающих рострегулирующей активностью. Сущность метода заключается в создании новых соединений гетероциклического ряда по реакции 3-амино-6-метил-1,2,4-триазинона-5 с (1) толуолом, бензальдегидом, п-толуолсульфокислотой, (2) п-хлорбензальдегидом, (3) фурфуролом, (4) валериановым альдегидом. Полученные соединения могут быть использованы в сельскохозяйственной практике для повышения урожая культур.
Известен способ получения азометинов бензотиазолового ряда (патент RU 2459814 С1 от 15.02.2011). Сущностью изобретения является то, что осуществлен синтез серии новых люминесцентных азометинов на основе аминов 2-фенилбензотиазола, содержащих аминогруппы как в бензотиазольном, так и в фенильном фрагменте молекулы, и 2,5- и 3,4-дигидроксибензальдегидов в алифатических спиртах - метиловом, этиловом, изопропиловом в присутствии кислотного катализатора. Полученные соединения могут быть использованы в качестве мономеров для получения самоорганизующихся люминесцентных полимеров, люминесцентных меток для различных органических композитов.
Известен способ получения люминесцентных азометинов (патент RU 2455291 С2 от 28.07.2010). Сущностью изобретения является то, что осуществлен синтез серии новых люминесцентных азометинов на основе аминов 2-фенилбензоксазола, содержащих аминогруппы как в бензоксазольном, так и в фенильном фрагменте молекулы, и 2,5- и 3,4-дигидроксибензальдегидов в алифатичесикх спиртах - метиловом, этиловом, изопропиловом в присутствии кислотного катализатора. Полученные соединения могут быть использованы для синтеза люминесцентных жестко-гибких сополимеров.
Задача изобретения - получение новых азометинов, обладающих гемолитической активностью.
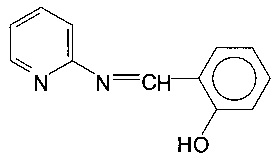
Сущность изобретения в том, что получают азометины на основе α-аминопиридина и замещенных бензальдегидов со структурной формулой
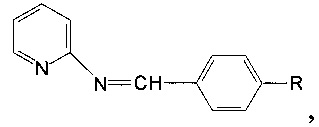
где R означает п-N(CH3)2, п-NO2, м-NO2, o-OH
обладающие гемолитической активностью и дозозависимым действием.
В предложенном изобретении получены различные азометины, содержащие бензилиденовый фрагмент, соединенный с различными радикалами, обладающие гемолитической активностью.
Изобретение относится к созданию новых соединений азометинов с общей формулой

где R означает п-N(CH3)2, п-NO2, м-NO2, о-ОН группы, которые могут найти применение в области биологии и медицины (гематологии) и может быть использовано для получения биологически активных веществ, защищающих эритроциты от гемолиза, в лабораторных и промышленных условиях.
Получают азометины реакцией α-аминопиридина с ароматическими альдегидами. Азометины - обширный класс соединений, синтезировано их достаточное множество. Среди них найдено множество соединений, обладающих биологической активностью, много лекарственных препаратов. Основное применение они находят в органическом синтезе, главным образом для получения вторичных аминов и гетероциклических соединений.
Нами синтезированы азометины на основе α-аминопиридина и замещенных бензальдегидов:
1. Азометин с гемолитической активностью, полученный взаимодействием 2-аминопиридина с 4-диметиламинобензальдегидом со структурной формулой
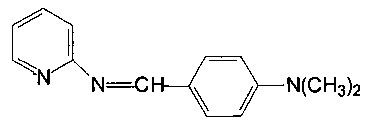
оказывающий дозозависимое ускоряющее действие на кинетику кислотного лизиса эритроцитов.
2. Азометин с гемолитической активностью, полученный взаимодействием 2-аминопиридина с 4-нитробензальдегидом со структурной формулой
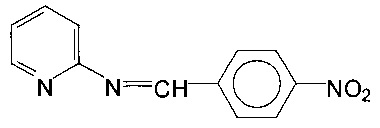
оказывающий дозозависимое ускоряющее действие на кинетику кислотного лизиса эритроцитов.
3. Азометин с гемолитической активностью, полученный взаимодействием 2-аминопиридина с 3-нитробензальдегидом со структурной формулой
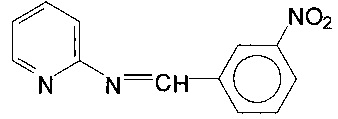
оказывающий дозозависимое угнетающее действие на кинетику кислотного лизиса эритроцитов.
4. Азометин с гемолитической активностью, полученный взаимодействием 2-аминопиридина с салициловым альдегидом со структурной формулой
оказывающий дозозависимое угнетающее действие на кинетику кислотного лизиса эритроцитов.
Получение новых соединений иллюстрируется следующими примерами.
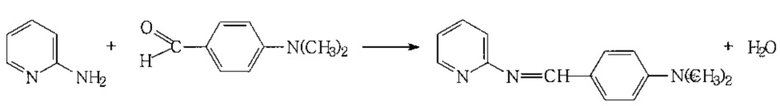
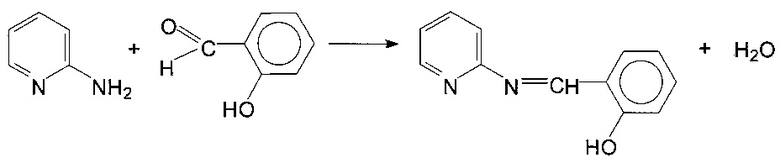
Пример 1. Синтез 2-N-(4-диметиламинобензилиден)-аминопиридина.
В колбу помещают 1 г (0,01 моль) 2-аминопиридина и 1,58 г (0,01 моль) 4-диметиламинобезальдегида в 60 мл этанола. Реакционную массу перемешивают на водяной бане при температуре 75-80°С в течение 3-х часов. По окончании реакции растворитель отгоняют. Маслообразный остаток обрабатывают гексаном, оставляют на сутки. Выпавшие кристаллы отфильтровывают, сушат на воздухе. Перекристаллизуют из гексана. Кристаллы светло-желтого цвета. Выход 1 г (46,7%), т.пл. 68°С. Растворяется в эфире, хлороформе, этиловом спирте. Не растворяется в бензоле, гексане. В ИК спектре полученного соединения обнаружены интенсивные полосы в области 1590, 1650 см-1, принадлежащие валентным колебаниям азометиновой группы (-CH=N-).
Реакция идет по схеме:
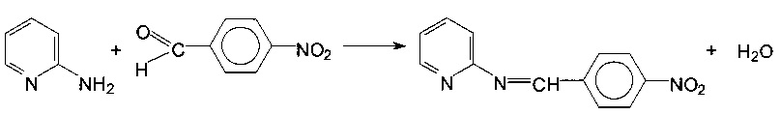
Пример 2. Синтез 2-N-(4-нитробензилиден)-аминопиридина.
В трехгорлую колбу, снабженную механической мешалкой и обратным холодильником, помещают 1 г (0,01 моль) 2-аминопиридина и 1,61 г (0,01 моль) 4-нитробезальдегида в 60 мл этанола. Реакционную массу перемешивают на водяной бане при температуре 75-80°С в течение 2-х часов. По окончании реакции растворитель отгоняют. Маслообразный остаток обрабатывают гексаном, оставляют на 2 суток. Выпавшие кристаллы отфильтровывают, сушат на воздухе. Перекристаллизуют из водного спирта (1:1). Кристаллы бледно-желтого цвета. Выход 1,45 г (60,2%), т.пл. 129°С. Растворяется в эфире, хлороформе, этиловом спирте. Не растворяется в бензоле, гексане. В ИК спектре полученного соединения обнаружены интенсивные полосы в области 1590, 1700 см-1, принадлежащие валентным колебаниям азометиновой группы (-CH=N-).
Реакция идет по схеме:
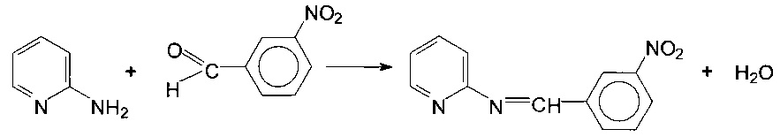
Пример 3. Синтез 2-N-(3-нитробензилиден)-аминопиридина.
В колбу помещают 1 г (0,01 моль) 2-аминопиридина и 1,61 г (0,01 моль) 3-нитробезальдегида в 60 мл этанола. Реакционную массу перемешивают на водяной бане при температуре 75-80°С в течение 2,5 часов. По окончании реакции растворитель отгоняют. Маслообразный остаток обрабатывают гексаном, оставляют на 2 суток. Выпавшие кристаллы отфильтровывают, сушат на воздухе. Перекристаллизуют из водного спирта (1:1). Кристаллы бледно-желтого цвета. Выход 1,31 г (59%), т.пл. 73°С. Растворяется в эфире, хлороформе, этиловом спирте, бензоле. Не растворяется в гексане. В ИК спектре полученного соединения обнаружены интенсивные полосы в области 1590, 1690 см-1, принадлежащие валентным колебаниям азометиновой группы (-CH=N-).
Реакция идет по схеме:
Пример 4. Синтез 2-N-салицилиден-аминопиридина.
В колбу помещают 1 г (0,01 моль) 2-аминопиридина и 1,5 мг (0,01 моль) салицилового альдегида в 60 мл этанола. Реакционную массу перемешивают на водяной бане при температуре 75-80°С в течение 2,5 часов. По окончании реакции растворитель отгоняют. Маслообразный остаток обрабатывают гексаном, оставляют на 2 суток. Выпавшие кристаллы отфильтровывают, сушат на воздухе. Перекристаллизуют из гексана. Кристаллы ярко-желтого цвета. Выход 1,71 г (81%), т.пл. 66°С. Растворяется в эфире, хлороформе, этиловом спирте, бензоле. Не растворяется в гексане. В ИК спектре полученного соединения обнаружены интенсивные полосы в области 1585, 1600 см принадлежащие валентным колебаниям азометиновой группы (-CH=N-).
Реакция идет по схеме:
Лабораторные испытания соединений.
Для регистрации влияния вновь синтезированных азометинов на ход кислотного гемолиза использовали метод кислотных эритрограмм (Леонова В.Г. Анализ эритроцитарных популяций в онтогенезе человека. - Новосибирск: Наука, 1987. - 242 с). Суспензию массы эритроцитов крысы разбавляли в 1000 раз 0,9% раствором NaCl. К 2 мл разбавленной суспензии эритроцитов добавляли 10 мкл испытуемого вещества (0.01, 0.5 и 5 мг; 0,005 мг/мл, 0,249 мг/мл, 2,49 мг/мл соответственно) в этаноле (в контрольном опыте добавляли 10 мкл этанола) и инкубировали 20 мин при 24°С. Гемолиз эритроцитов вызывали, добавляя 2 мл 0,004 н. HCl в суспензию эритроцитов (начальная оптическая плотность составляла 0,7 ед. шкалы). Регистрировали уменьшение оптической плотности при 720 нм на фотометре «Спекол 10» при 24°С вплоть до полного прекращения ее изменения. За 100% гемолиз принимали разницу между начальным и конечным значениями оптической плотности проб. Параметры кислотного гемолиза определяли из кинетических кривых гемолиза, регистрируемых как зависимость величины интегрального светорассеивания (оптической плотности) суспензии эритроцитов от времени гемолиза в кислой среде.
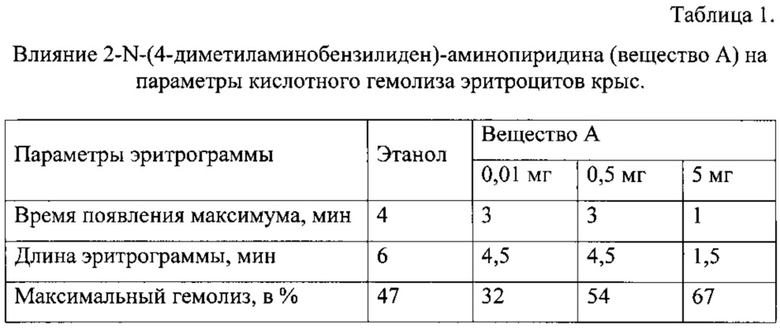
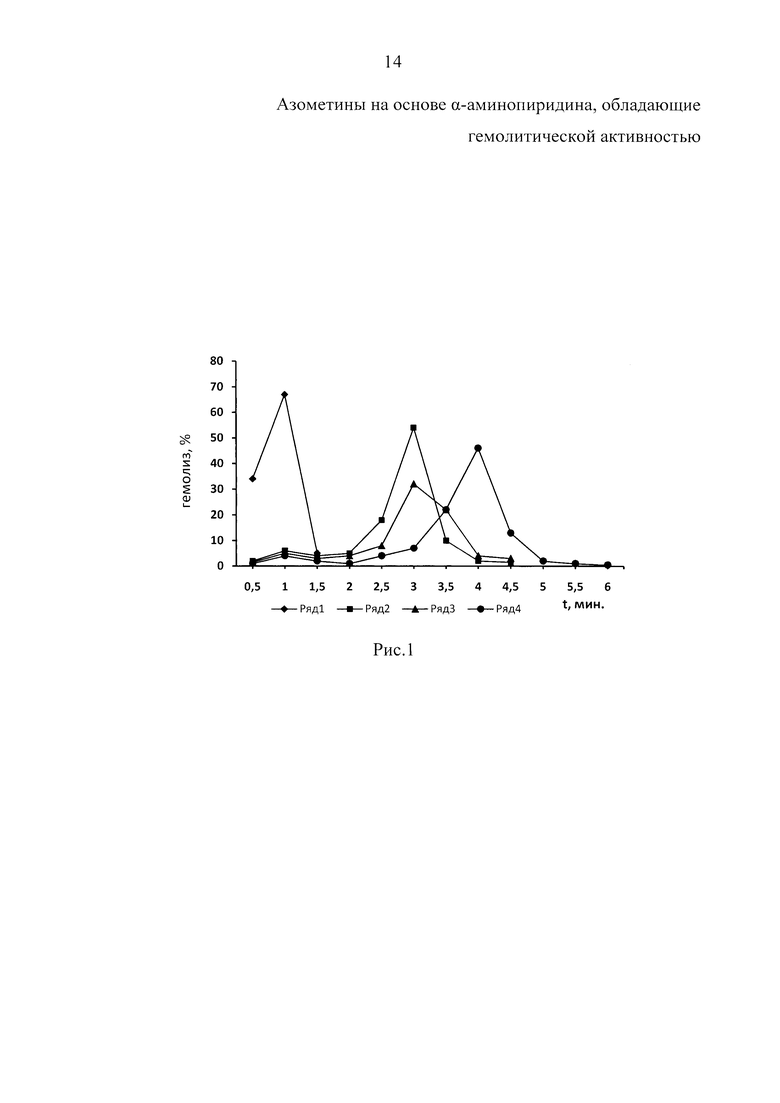
Пример 1. Изучено влияние 2-N-(4-диметиламинобензилиден)-аминопиридина (вещество А) на гемолиз эритроцитов. На рис. 1 представлены данные о влиянии различных концентраций исследуемого вещества А на гемолиз эритроцитов. Вещество стимулирует гемолиз эритроцитов. Эффект носит дозозависимый характер. С увеличением концентрации вещества гемолизирующее действие возрастает. При концентрации 5 мг происходит практически мгновенный гемолиз.
На рис. 1. представлены кислотные эритрограммы крыс в присутствии разных концентраций 2-N-(4-диметиламинобензилиден)-аминопиридина (вещество А). Концентрация вещества А: 1 ряд - 5 мг, 2 ряд - 0,5 мг, 3 ряд -0,01 мг, 4 ряд - контроль.
О стимулирующем влиянии вещества А свидетельствуют также данные таблицы 1. С увеличением концентрации вещества существенно уменьшается время появления максимума на эритрограмме, сокращается длина эритрограммы и увеличиваются максимальные значения гемолиза.
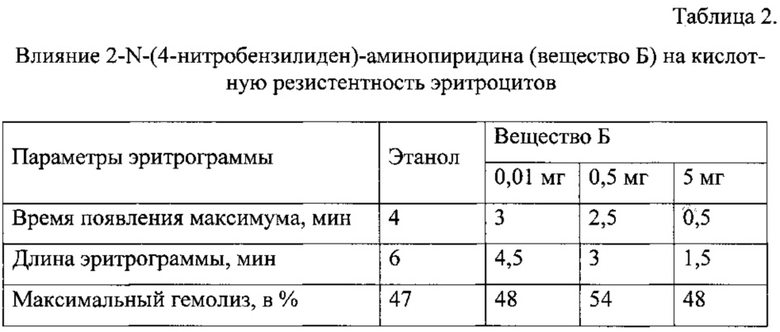
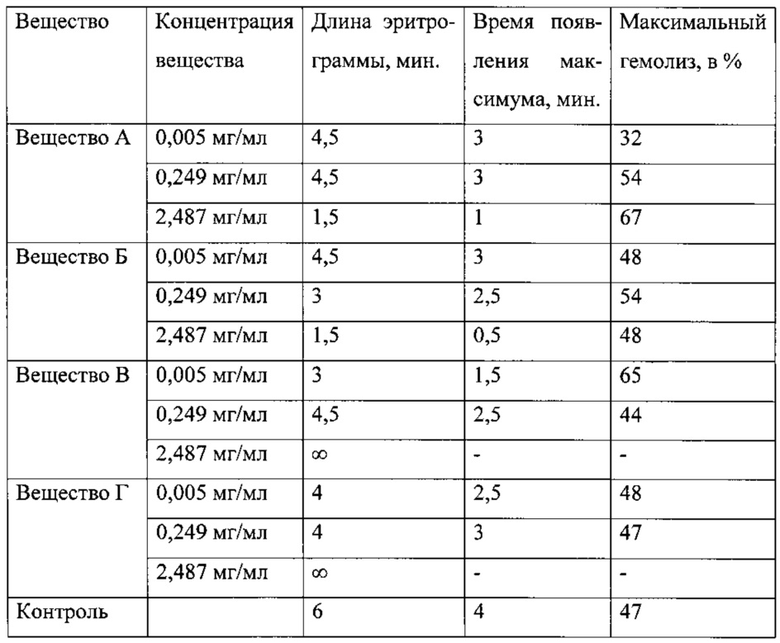
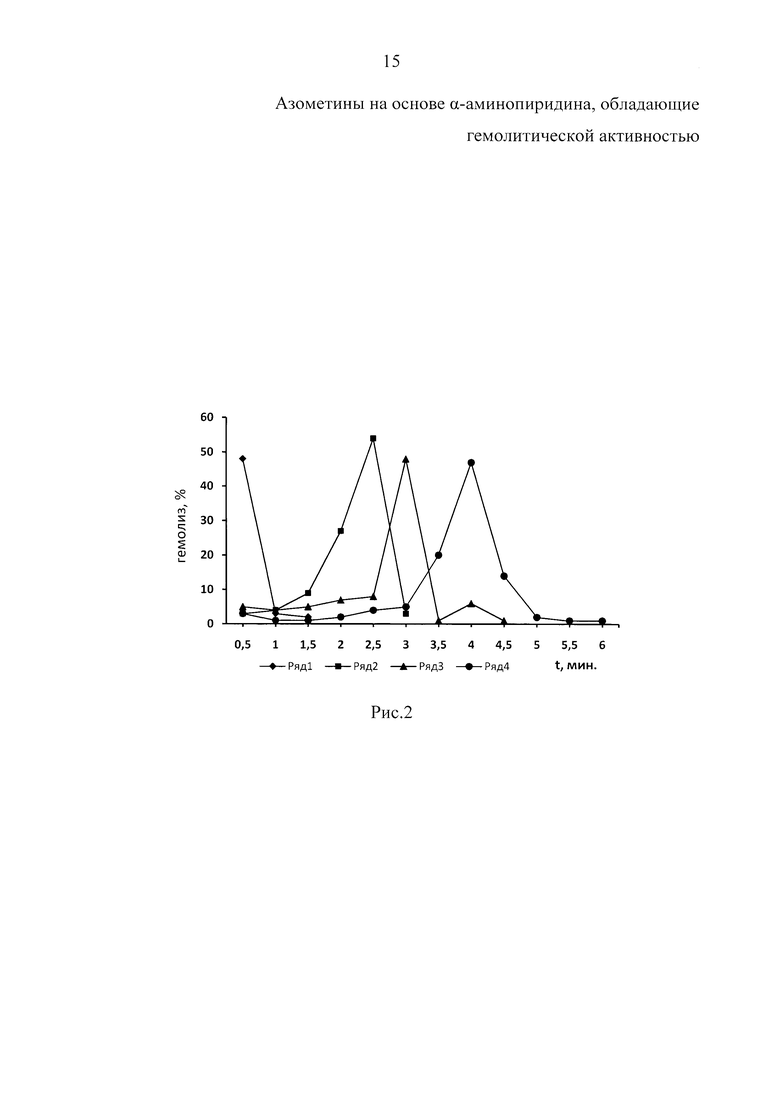
Пример 2. Изучено влияние 2-N-(4-нитробензилиден)-аминопиридина (вещество Б) на гемолиз эритроцитов. На рис. 2 представлены данные о влиянии различных концентраций исследуемого вещества Б на гемолиз эритроцитов. Вещество стимулирует гемолиз эритроцитов. Эффект носит дозозависимый характер. С увеличением концентрации вещества гемолизирующее действие возрастает.
На рис. 2. представлены кислотные эритрограммы крыс в присутствии разных концентраций 2-N-(4-нитробензилиден)-аминопиридина (вещество Б). Концентрация вещества Б: 1 ряд - 5 мг, 2 ряд - 0,5 мг, 3 ряд - 0,01 мг, 4 ряд - контроль.
О стимулирующем влиянии вещества Б на гемолиз свидетельствуют также данные таблицы 2. С увеличением концентрации вещества существенно уменьшается время появления максимума на эритрограмме и сокращается длина эритрограммы.
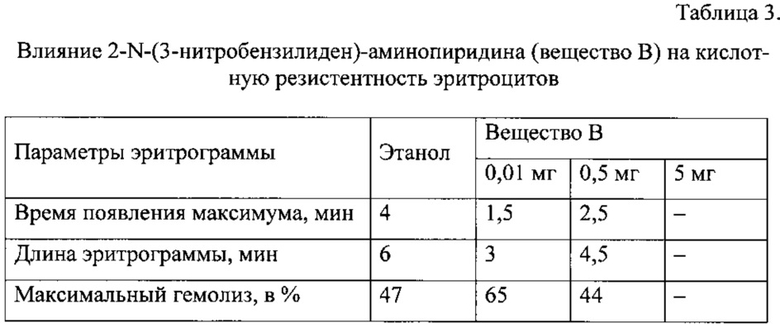
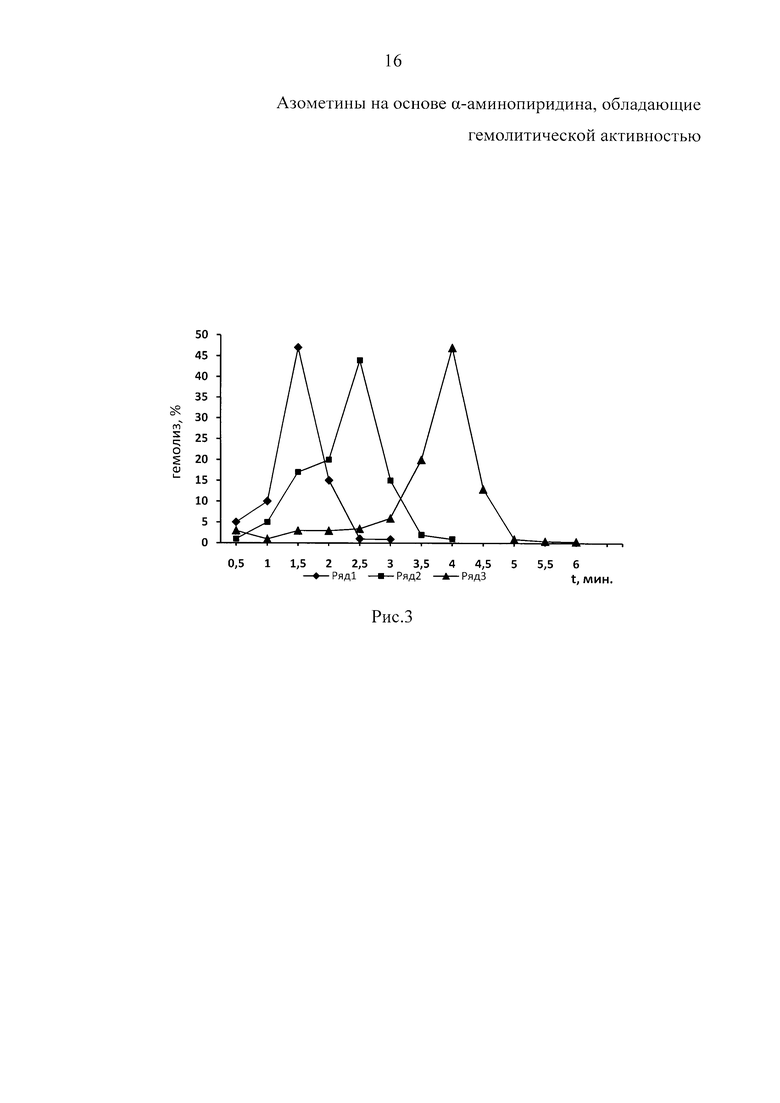
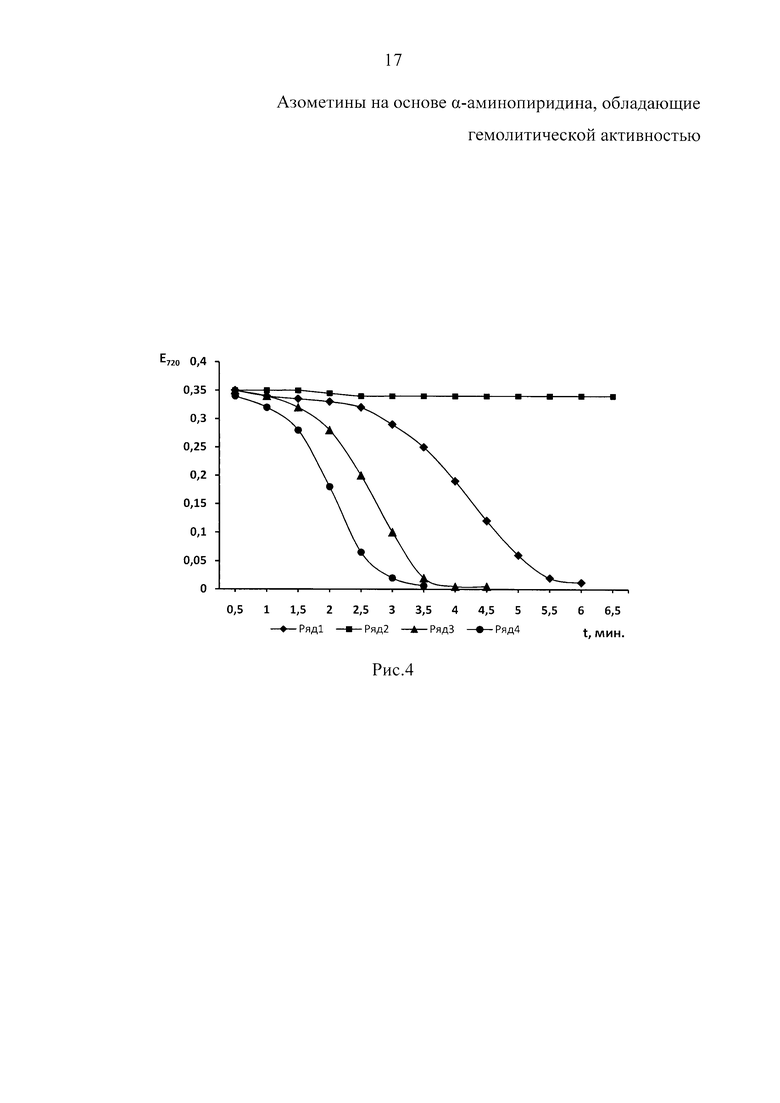
Пример 3. Изучено влияние 2-N-(3-нитробензилиден)-аминопиридина (вещество В) на гемолиз эритроцитов. На рис. 3 представлены данные о влиянии различных концентраций исследуемого вещества В на гемолиз эритроцитов. Низкие концентрации (0,01 мг) стимулируют гемолиз эритроцитов (табл. 3). При повышении концентрации вещества в 50 раз снижается гемолитическое действие вещества. Как видно на кинетических кривых кислотного лизиса эритроцитов (рис. 4), высокие концентрации вещества (5 мг) оказывают антигемолитическое действие. В присутствии 5 мг вещества В гемолиз не наступал даже через 30 мин наблюдения.
На рис. 3. представлены кислотные эритрограммы крыс в присутствии разных концентраций 2-N-(3-нитробензилиден)-аминопиридина (вещество В). Концентрация вещества В: 1 ряд - 0,5 мг, 2 ряд - 0,01 мг, 3 ряд - контроль.
На рис. 4. представлены кинетические кривые кислотного лизиса эритроцитов крыс в присутствии различных концентраций 2-N-(3-нитробензилиден)-аминопиридина (вещество В). Концентрация вещества В: 2 ряд - 5 мг, 3 ряд - 0,5 мг, 4 ряд - 0,01 мг, 1 ряд - контроль.
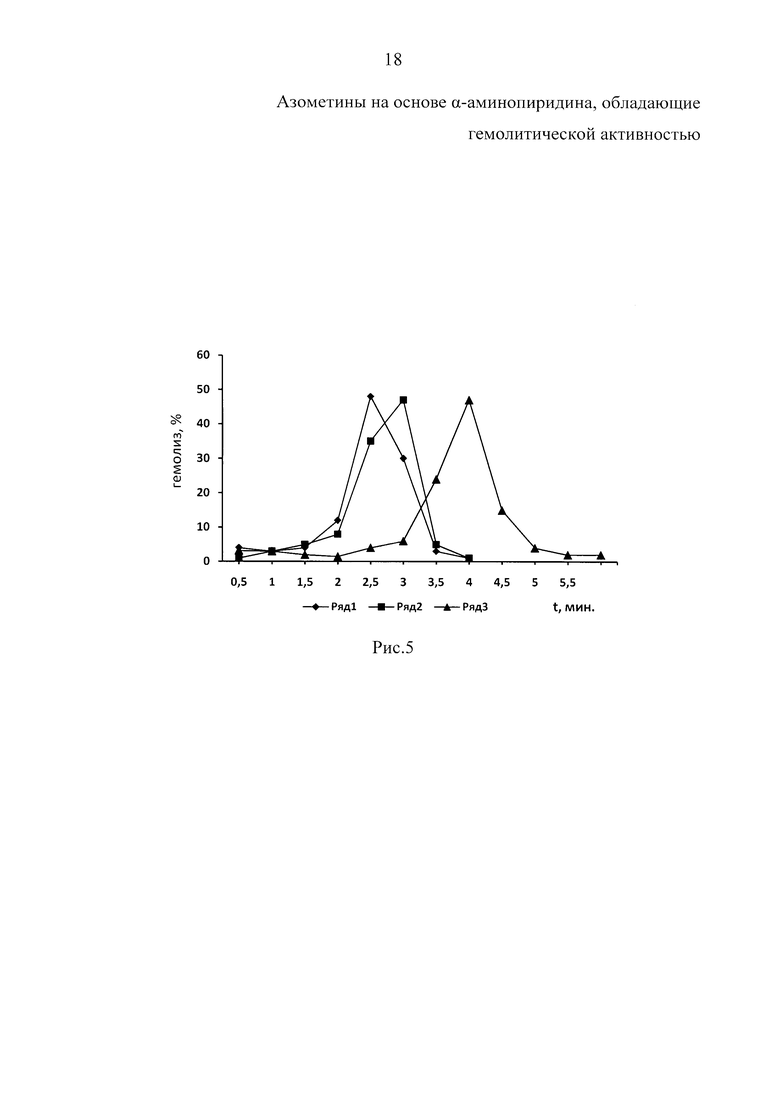
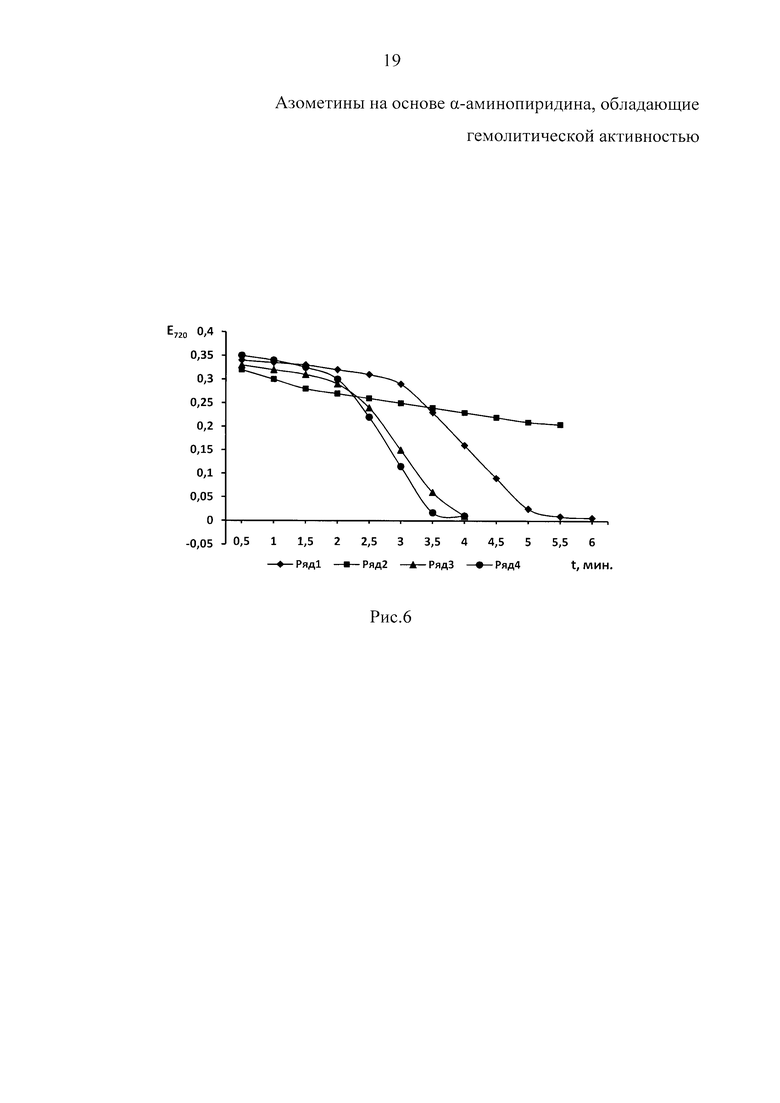
Пример 4. Изучено влияние 2-N-салицилиден-аминопиридина (вещество Г) на гемолиз эритроцитов. На рис. 5 представлены данные о влиянии различных концентраций исследуемого вещества Г на гемолиз эритроцитов. Низкие концентрации (0,01 мг) стимулируют гемолиз эритроцитов (табл. 4). При повышении концентрации вещества в 50 раз снижается гемолитическое действие вещества. Как видно на кинетических кривых кислотного лизиса эритроцитов (рис. 6), высокие концентрации вещества (5 мг) оказывают антигемолитическое действие.
На рис. 5. представлены кислотные эритрограммы крыс в присутствии разных концентраций 2-N-салицилиден-аминопиридина (вещество Г). Концентрация вещества Г: 1 ряд - 0,01 мг, 2 ряд - 0,5 мг, 3 ряд - контроль.
На рис. 6. представлены кинетические кривые кислотного лизиса эритроцитов крыс в присутствии различных концентраций 2-N-салицилиден-аминопиридина (вещество Г). Концентрация вещества Г: 1 ряд - контроль; 2 ряд - 5 мг, 3 ряд - 0,5 мг, 4 ряд - 0,01 мг.
В целом получены следующие результаты:
Известно, что под действием кислоты происходит денатурация белков мембраны эритроцитов и последующая их агрегация с образованием пор, достаточных для выхода гемоглобина (Иванов И.Т., Бенов Л.Ц. Агрегация денатурированных мембранных белков - начальный этап кислотного гемолиза // Биофизика. 1991. Т. 36, вып. 5. С. 839-843; Заводник И.Б., Пилецкая Т.П. Кислотный лизис эритроцитов человека // Биофизика. 1997. Т. 42, вып. 5, С. 1106-1112). Исходя из этого сделан вывод, что вещества А и Б, способствуют агрегации денатурированных белков мембраны эритроцитов и, соответственно, стимулируют лизис клеток, а вещества В и Г предотвращают агрегацию денатурированных мембранных белков и, следовательно, предотвращают гемолиз эритроцитов.
Устойчивость эритроцитов к гемолитическому воздействию определяется многими факторами, в том числе возрастом клеток и состоянием их клеточной мембраны. Низкие концентрации веществ А и Б, вызывающие гемолиз эритроцитов, можно использовать для оценки физико-химического состояния мембраны эритроцитов в норме и патологических состояниях у человека. Вещества В и Г обладающие антигемолитическим действием можно использовать для увеличения стабильности эритроцитов донорской крови и долговременного хранения консервированной крови.
Таким образом, синтезированные новые четыре азометина влияют на кинетику кислотного лизиса эритроцитов крыс. Два из них (вещество А и Б) дозозависимо стимулируют кислотный лизис эритроцитов. Действие веществ В и Г зависит от их концентрации: низкие концентрации стимулируют гемолиз эритроцитов, а высокие - полностью тормозят этот процесс.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРОФИЛАКТИКИ ПОВРЕЖДЕНИЯ БИОЛОГИЧЕСКИХ МЕМБРАН | 2013 |
|
RU2549449C2 |
| СПОСОБ ПОДАВЛЕНИЯ ГЕМОЛИТИЧЕСКОЙ АКТИВНОСТИ ПАТОГЕННЫХ ШТАММОВ КИШЕЧНОЙ ПАЛОЧКИ | 1999 |
|
RU2180849C2 |
| СПОСОБ ПОВЫШЕНИЯ УСТОЙЧИВОСТИ К ГЕМОЛИЗУ ЭРИТРОЦИТОВ И ВОССТАНОВЛЕНИЯ ИХ ПОВРЕЖДЕННОЙ ФОРМЫ | 1998 |
|
RU2162698C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ФУНКЦИОНАЛЬНОГО СОСТОЯНИЯ ОРГАНИЗМА ПО СТЕПЕНИ РЕЗИСТЕНТНОСТИ КРОВИ К КИСЛОТНОМУ ГЕМОЛИЗУ | 2000 |
|
RU2179315C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИГИПОКСИЧЕСКОЙ И АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ | 2001 |
|
RU2191592C1 |
| СПОСОБ ДИАГНОСТИКИ ПАТОЛОГИИ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА БОЛЬНОГО | 1994 |
|
RU2098819C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВ, СТИМУЛИРУЮЩИХ КЛЕТОЧНОЕ ДЫХАНИЕ | 2011 |
|
RU2472775C1 |
| Способ определения антиоксидантной активности веществ | 1980 |
|
SU1097264A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КИСЛОТНОЙ УСТОЙЧИВОСТИ ЭРИТРОЦИТОВ ХЛАДНОКРОВНЫХ ЖИВОТНЫХ | 2014 |
|
RU2571081C1 |
| МЕМБРАНОПРОТЕКТОРНОЕ СРЕДСТВО | 2013 |
|
RU2538803C1 |
Изобретение относится к способам получения азометинов на основе α-аминопиридина и замещенных бензальдегидов со структурной формулой
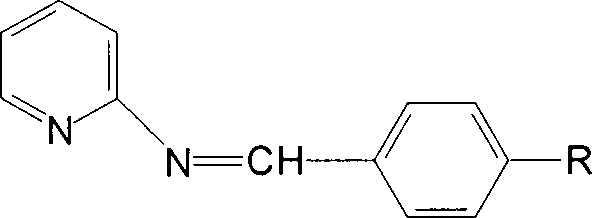
где R означает м-NO2, о-ОН группы, реакцию проводят при температуре 75-80°С в течение 2,5 часов. Полученные азометины обладают гемолитической активностью и дозозависимым действием. Технический результат изобретения - получение новых азометинов, обладающих антигемолитической активностью. 2 н.п. ф-лы, 6 ил., 4 табл., 4 пр.
1. Способ получения азометина, включающий взаимодействие 2-аминопиридина и 3-нитробезальдигида с этанолом путем перемешивания на водяной бане при температуре 75-80°С в течение 2,5 часов, затем маслообразный остаток обрабатывают гексаном, через 2 суток выпавшие кристаллы отфильтровывают и сушат на воздухе, и перекристаллизовывают из водного спирта, со структурной формулой

обладающего антигемолитической активностью и дозозависимым действием.
2. Способ получения азометина, отличающийся взаимодействием 2-аминопиридина и салицилового альдегида в этаноле, и перекристаллизацией из гексана со структурной формулой
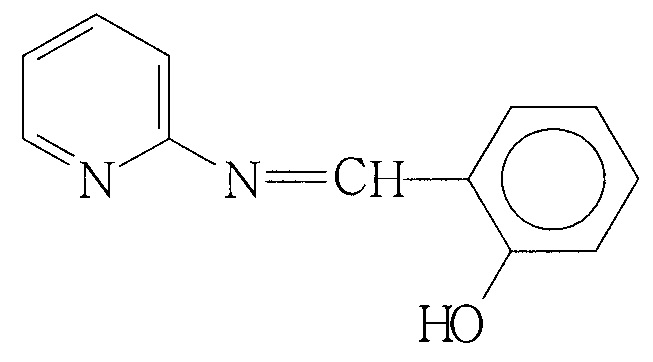
обладающего антигемолитической активностью и дозозависимым действием.
| Feist, K.; Awe, W.; Volksen, W | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| III | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Электрический поворотный выключатель | 1918 |
|
SU1823A1 |
| Feist, K.; Awe, W.; Schultz, J.; Klatt, F | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| Приспособление для разматывания лент с семенами при укладке их в почву | 1922 |
|
SU56A1 |
| Messina, Italy)."Reactivity of the azomethine group | |||
| X | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Размывочно-крепильная машина для проходки способом гидромеханизации подземных выработок | 1940 |
|
SU66385A1 |
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
| Приспособление с иглой для прочистки кухонь типа "Примус" | 1923 |
|
SU40A1 |
| Stuart; Clapp, Mary A | |||
| (Mellon Inst., Pittsburgh, PA)., "Azomethines from p-dialkylaminobenzaldehydes.", Journal of Organic Chemistry, 11, 292-5 (Unavailable) 1946 | |||
| Устройство для выработки кускового сахара | 1927 |
|
SU19174A1 |
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| Div., CIBA, Pharmaceut | |||
| Co., Summit, NJ)., "Synthesis of varied heterocyclic and substituted aryl alkyl secondary amines, related Schiff bases, and amides | |||
| ", Journal of Medicinal Chemistry, 9(4), 624-30 (English) 1966. | |||
Авторы
Даты
2017-09-19—Публикация
2015-04-01—Подача