Текст описания приведен в факсимильном виде.


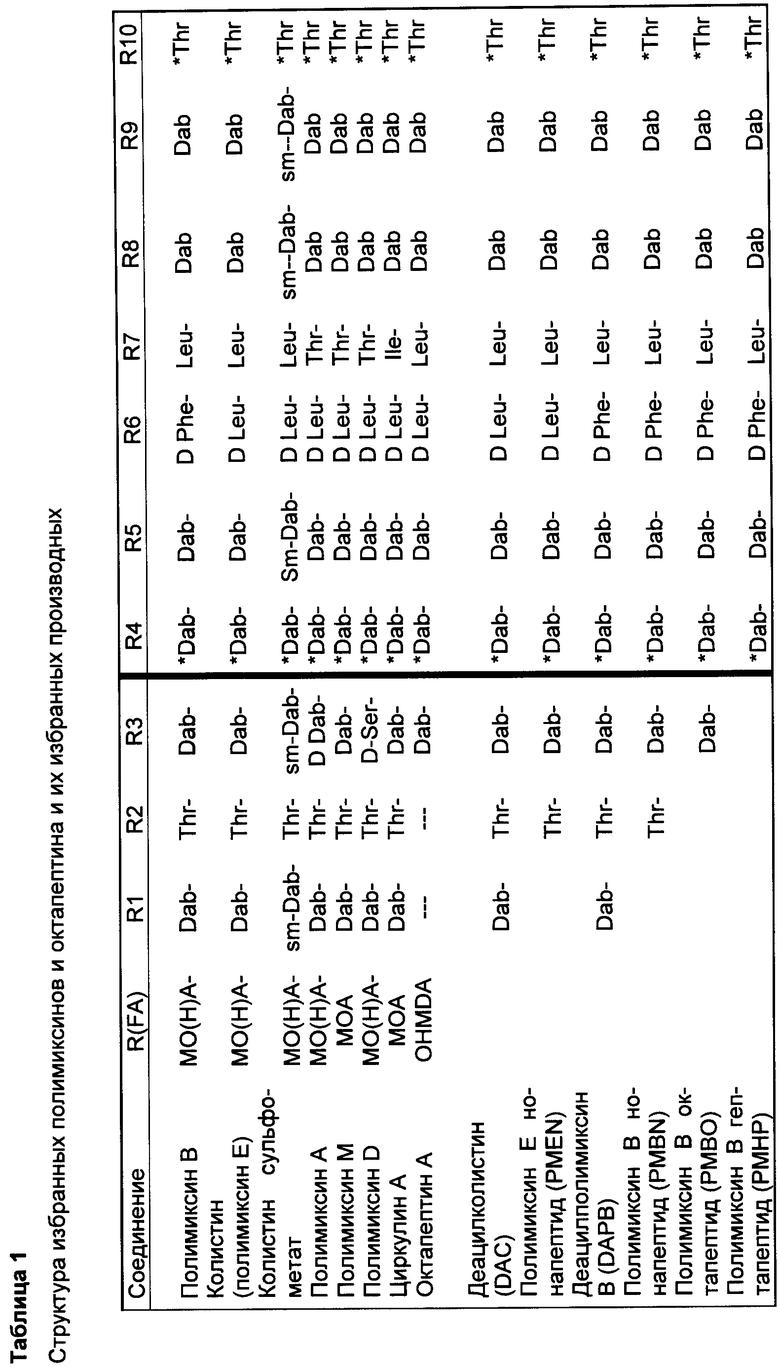





































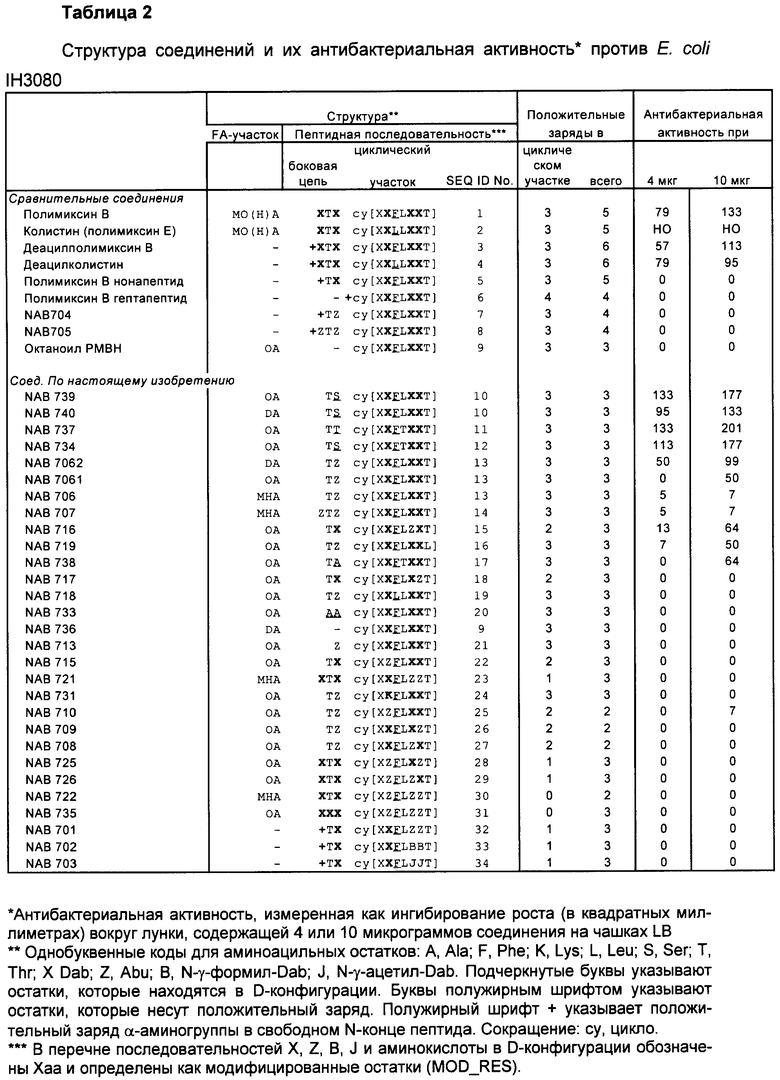





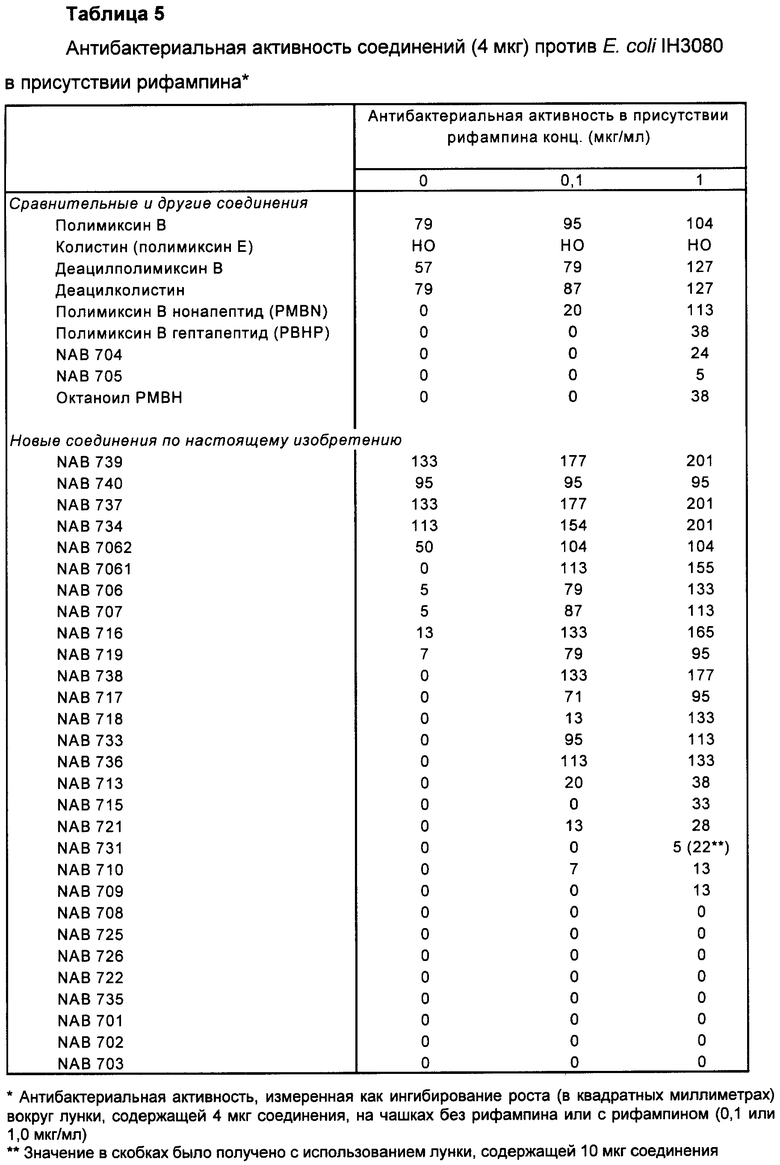




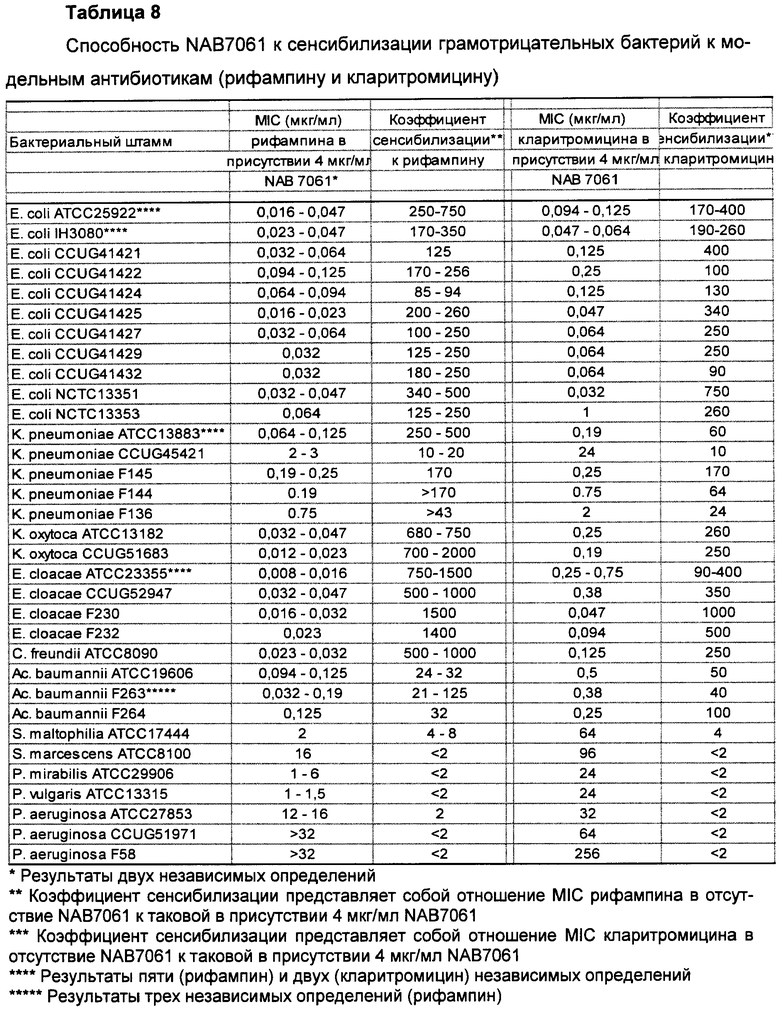








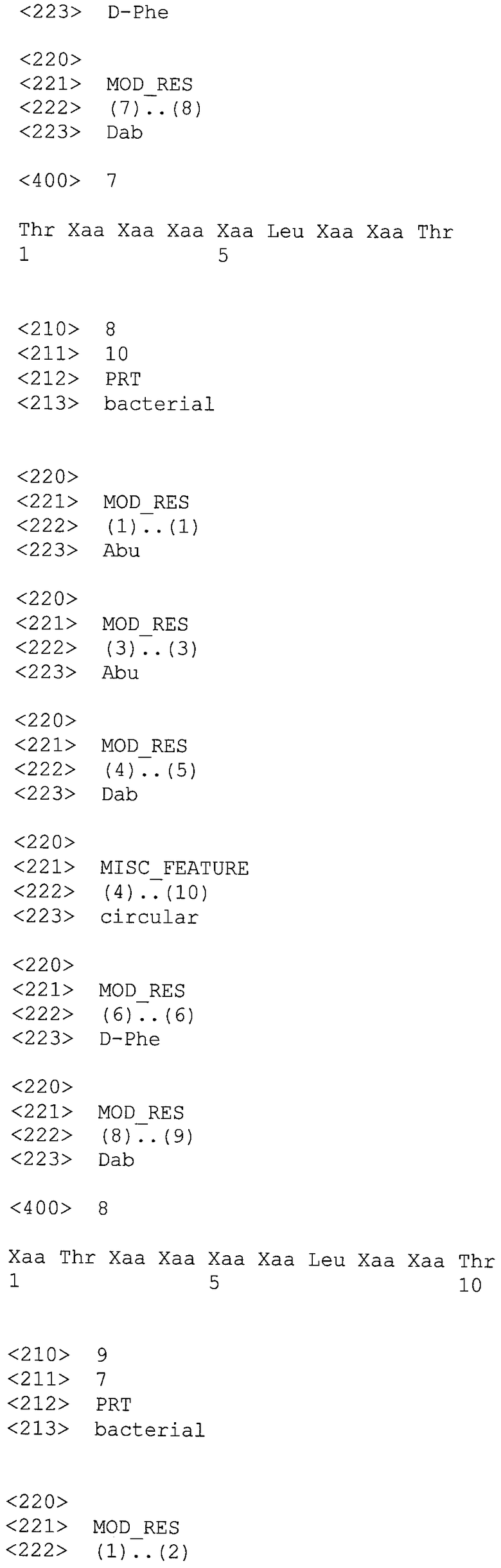
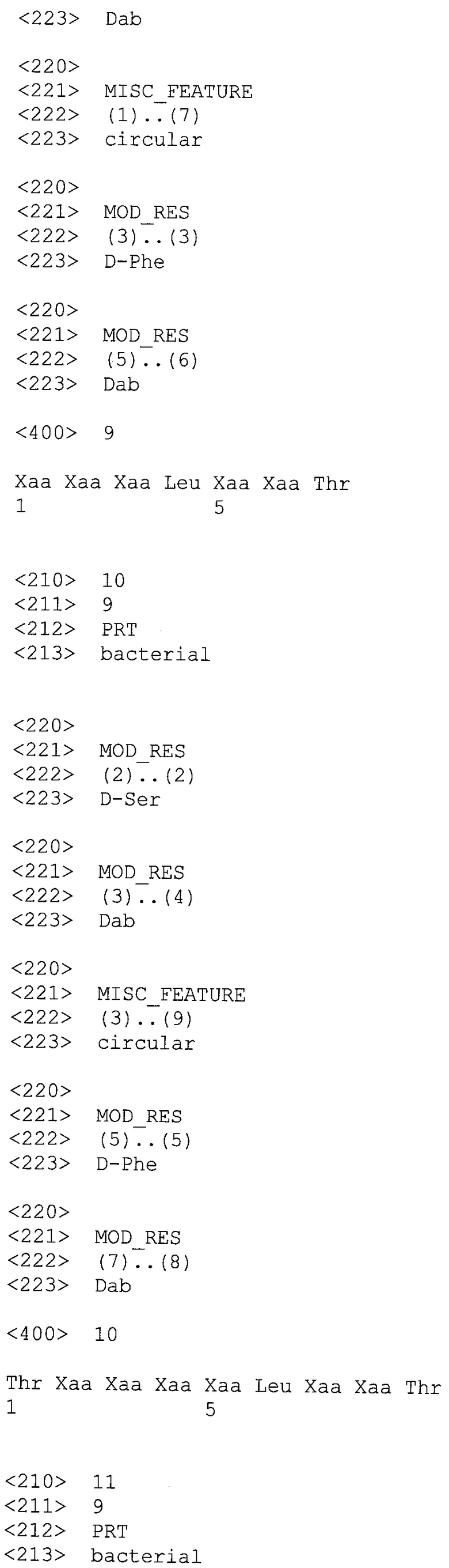








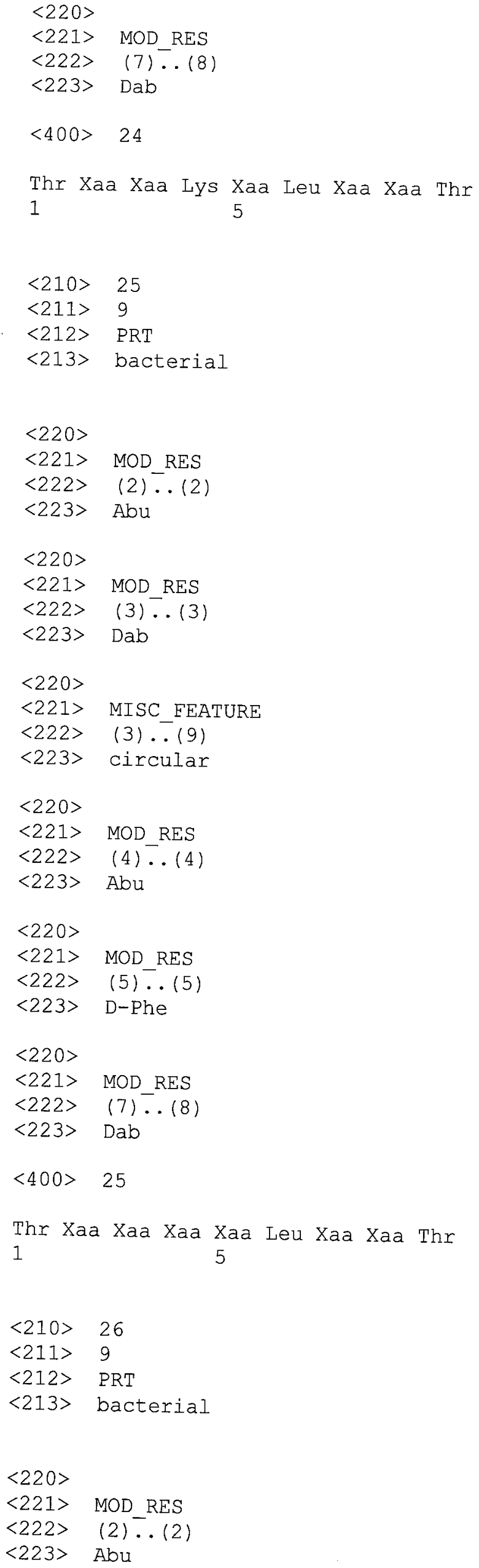



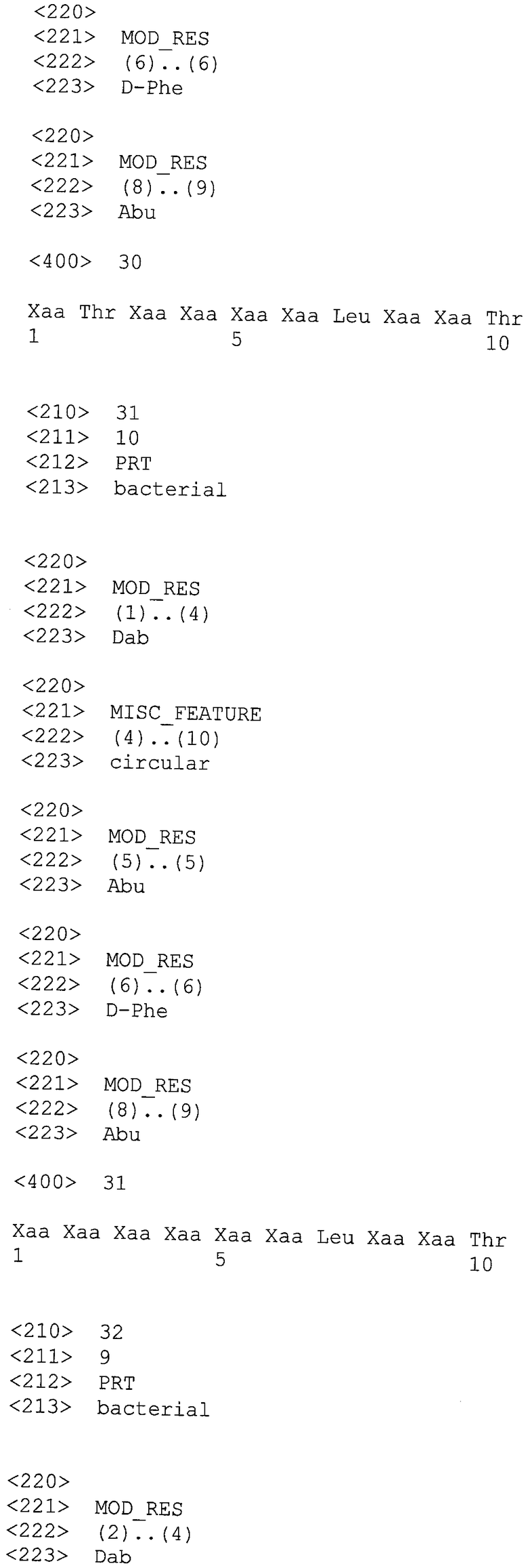


Изобретение относится к производному полимиксина, где R1, R2 и R3 являются возможными, но не обязательными и R1, R2, R3, R5, R8 и R9 представляют собой катионные или нейтральные аминокислотные остатки, выбранные таким образом, чтобы суммарное число положительных зарядов при физиологическом значении рН составляло по меньшей мере два, но не более чем три. Изобретение также относится к способу лечения, облегчения или ослабления инфекции у субъекта, вызванной грамотрицательной бактерией, путем введения терапевтически эффективного количества производного согласно изобретению указанному субъекту; к способу сенсибилизации грамотрицательных бактерий к антибактериальному агенту путем введения, одновременного или последовательного в любом порядке, терапевтически эффективного количества указанного антибактериального агента и производного согласно настоящему изобретению указанному субъекту; к способам разработки новых антибиотиков; снижения нефротоксичности, улучшения фармакокинетических свойств природных полимиксинов и октапептинов; и сенсибилизации клинически значимых бактерий к защитному механизму комплемента хозяина, присутствующего в сыворотке, а также к способу получения таких производных полимиксина. 12 н. и 24 з.п. ф-лы, 10 табл., 13 пр.
1. Производное полимиксина общей формулы (I)
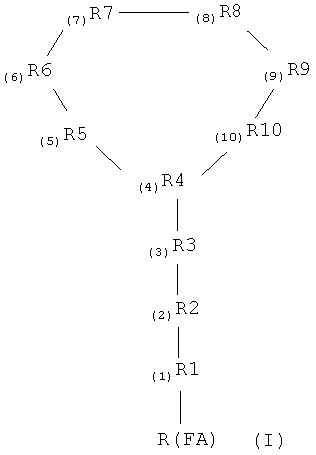
где R1, R2 и R3 являются возможными, но не обязательными; и каждый, если присутствует, представляет собой аминокислотный остаток;
R4 представляет собой аминокислотный остаток, содержащий функциональную боковую цепь, способную циклизовать указанное производное;
R6 представляет собой возможно замещенный гидрофобный аминокислотный остаток;
R7 представляет собой возможно замещенный гидрофобный аминокислотный остаток или треонин;
R5, R8 и R9 представляют собой положительно заряженные или нейтральные аминокислотные остатки;
R10 представляет собой Leu, Thr или любой негидрофобный аминокислотный остаток;
R(FA) представляет собой возможно замещенный остаток жирного ацила или алкила или гидрофобный олигопептид;
при условии, что R8 и R9 не формилированы оба, когда R(FA)-R1-R2-R3 составляет нативную боковую цепь полимиксина В; и
когда R(FA) непосредственно связан с R4, тогда R(FA) представляет собой деканоил;
где указанные аминокислотные остатки выбраны таким образом, что суммарное число положительных зарядов при физиологическом значении рН составляет по меньшей мере два, но не более чем три, и общее число положительных зарядов в боковой цепи R(FA)-R1-R2-R3 не превышает 2, так что указанное производное полимиксина все еще обладает антибактериальной активностью против грамотрицательных бактерий, и/или обладает способностью сенсибилизировать грамотрицательные бактерии к антибактериальным агентам;
или фармацевтически приемлемая соль указанного производного.
2. Производное по п.1, где указанные положительные заряды выбраны из группы, состоящей из свободных незамещенных аминогрупп и других катионных групп.
3. Производное по любому из пп.1 и 2, где R1-R10 выбраны из группы, состоящей из SEQ ID NO: 9-26.
4. Производное по любому из пп.1-3, где R(FA) выбран из группы, состоящей из октаноила, деканоила и 6-метилгептаноила.
5. Производное по любому из пп.1-4, где число указанных положительных зарядов равно трем.
6. Производное по п.5, где R1-R10 выбраны из группы, состоящей из SEQ ID NO: 9-20.
7. Производное по п.6, выбранное из группы, состоящей из OA-SEQ ID NO.10, DA-SEQ ID NO.10, OA-SEQ ID NO.11, OA-SEQ ID NO.12, DA-SEQ ID NO.13, OA-SEQ ID NO.13, MHA-SEQ ID NO.13, MHA-SEQ ID NO.14, OA-SEQ ID NO.15, OA-SEQ ID NO.16, OA-SEQ ID NO.17. OA-SEQ ID NO.18, OA-SEQ ID NO.19, OA-SEQ ID NO.20 и DA-SEQ ID NO.9.
8. Фармацевтическая композиция для лечения инфекций, вызванных грамотрицательными бактериями, содержащая эффективное количество по меньшей мере одного производного по любому из пп.1-7 и по меньшей мере один фармацевтически приемлемый носитель и/или эксципиент.
9. Фармацевтическая композиция по п.8, дополнительно содержащая антибактериальный агент, который по меньшей мере умеренно гидрофобен, или крупный антибактериальный агент, в отношении которого внешняя мембрана грамотрицательной бактерии действует как непроницаемый барьер.
10. Способ лечения, облегчения или ослабления инфекции у субъекта, вызванной грамотрицательной бактерией, при котором вводят терапевтически эффективное количество по меньшей мере одного производного по любому из пп.1-7.
11. Способ по п.10, где указанная бактерия выбрана из группы, состоящей из: Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter cloacae, Citrobacter freundii, Pseudomonas aeruginosa и Acinetobacter baumannii.
12. Способ сенсибилизации грамотрицательных бактерий к антибактериальному агенту, который по меньшей мере умеренно гидрофобен, или крупному антибактериальному агенту, в отношении которого внешняя мембрана грамотрицательной бактерии действует как непроницаемый барьер, при котором вводят, одновременно или последовательно в любом порядке, терапевтически эффективное количество указанного антибактериального агента и по меньшей мере одно производное по любому из пп.1-7.
13. Способ по п.12, где указанный антибактериальный агент выбран из группы, состоящей из макролида, линкозамина, стрептограмина, рифамицина, фузидовой кислоты, мупироцина, оксазолидинона, гликопептидного антибиотика, фторхинолона, бета-лактамового антибиотика, ингибитора синтеза фолатов.
14. Способ по п.13, где указанный антибактериальный агент выбран из группы, состоящей из кларитромицина, азитромицина, эритромицина, клиндамицина, комбинации стрептограминов квинупристин далфопристин, рифампина, фузидовой кислоты, мупироцина, оксазолидинона линезолида, ванкомицина, фторхинолона моксифлоксацина и ингибитора синтеза фолатов триметоприма.
15. Способ по п.12, где указанная бактерия выбрана из группы, состоящей из: Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter cloacae, Citrobacter freundii, Pseudomonas aeruginosa и Acinetobacter baumannii.
16. Способ разработки новых антибиотиков, включающий стадии
а) получения соединения природного полимиксина или октапептина или его производного, имеющего суммарно от 4 до 6 положительных зарядов;
б) замены от 1 до 4 остатков, несущих один или более чем один положительный заряд, остатком, не имеющим положительного заряда, или ковалентной связью, с получением посредством этого производного соединения полимиксина, имеющего 2 или 3 положительных заряда;
в) анализа указанного производного соединения на антибактериальную активность против грамотрицательных бактерий или на способность к сенсибилизации грамотрицательных бактерий к антибиотику; и
г) отбора соединений, обладающих антибактериальной активностью против грамотрицательных бактерий или способностью к сенсибилизации грамотрицательных бактерий к антибактериальному агенту.
17. Способ снижения токсичности природных полимиксинов, октапептинов и их производных, где указанный способ включает стадии:
а) получения соединения природного полимиксина или октапептина или его производного, имеющего суммарно от 4 до 6 положительных зарядов;
б) замены от 1 до 4 остатков, несущих один или более чем один положительный заряд, остатком, не имеющим положительного заряда, или ковалентной связью, с получением посредством этого производного, имеющего 2 или 3 положительных заряда; и
в) сравнения этого соединения с природным полимиксином на животной модели in vivo; и
г) отбор соединений, которые менее токсичны, чем природные полимиксины.
18. Способ по п.17, где указанная токсичность представляет собой нефротоксичность, что подтверждается на животной модели или в тесте in vitro с измерением аффинности почечных структур.
19. Способ улучшения фармакокинетических свойств природных полимиксинов, октапептинов и их производных, где указанный способ включает стадии:
а) получения соединения природного полимиксина или октапептина или его производного, имеющего суммарно от 4 до 6 положительных зарядов;
б) замены от 1 до 4 остатков, несущих один или более чем один положительный заряд, остатком, не имеющим положительного заряда, или ковалентной связью, с получением посредством этого производного, имеющего 2 или 3 положительных заряда;
где указанные улучшенные фармакокинетические свойства состоят в пролонгированном времени полужизни в сыворотке или в более низкой склонности к инактивации полианионными составляющими тканей и гноя по сравнению с исходным соединением.
20. Способ сенсибилизации клинически значимых грамотрицательных бактерий к защитному механизму комплемента хозяина, присутствующего в сыворотке, где указанные бактерии подвергают действию производного по любому из пп.1-7 во время манифестной инфекции.
21. Способ по п.20, где указанные бактерии выбраны из группы, состоящей из: Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter cloacae, Citrobacter freundii, Pseudomonas aeruginosa и Acinetobacter baumannii.
22. Применение производного по любому из пп.1-7 при изготовлении фармацевтической композиции для лечения инфекций, вызванных грамотрицательными бактериями.
23. Применение по п.22, где указанные бактерии выбраны из группы, состоящей из: Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter cloacae, Citrobacter freundii, Pseudomonas aeruginosa и Acinetobacter baumannii.
24. Применение производного по любому из пп.1-7 для изготовления фармацевтической композиции для сенсибилизации грамотрицательных бактерий к антибактериальным агентам, в отношении которых внешняя мембрана грамотрицательной бактерии служит непроницаемым барьером.
25. Применение по п.24, где указанные бактерии выбраны из группы, состоящей из: Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter cloacae, Citrobacter freundii, Pseudomonas aeruginosa и Acinetobacter baumannii.
26. Применение по п.24, где указанный антибактериальный агент выбран из группы, состоящей из макролида, линкозамина, стрептограмина, рифамицина, фузидовой кислоты, мупироцина, оксазолидинона, гликопептидного антибиотика, фторхинолона, бета-лактамового антибиотика, ингибитора синтеза фолатов.
27. Применение по п.26, где указанный антибактериальный агент выбран из группы, состоящей из кларитромицина, азитромицина, эритромицина, клиндамицина, комбинации стрептограминов квинупристин-далфопристин, рифампина, фузидовой кислоты, мупироцина, оксазолидинона линезолида, ванкомицина, фторхинолона моксифлоксацина и ингибитора синтеза фолатов триметоприма.
28. Применение производного по любому из пп.1-7 для изготовления фармацевтической композиции для сенсибилизации клинически значимых грамотрицательных бактерий к защитному механизму комплемента хозяина, присутствующего в сыворотке.
29. Применение по п.28, где указанные бактерии выбраны из группы, состоящей из: Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter cloacae, Citrobacter freundii, Pseudomonas aeruginosa и Acinetobacter baumannii.
30. Способ получения производного полимиксина формулы (I), как определено в п.1, при котором модифицируют соединение природного или синтетического полимиксина или октапептина или его производное, имеющее от 4 до 6 положительно заряженных остатков, путем замены от 1 до 4 из указанных остатков нейтральными остатками или ковалентной связью, либо преобразования от 1 до 4 из указанных остатков в нейтральные остатки с целью получения производного полимиксина формулы (I) по п.1, имеющего 2 или 3 положительно заряженных остатка.
31. Способ по п.30, при котором этот способ осуществляют в виде общего процесса синтеза.
32. Способ по п.30, при котором этот способ осуществляют в виде полусинтетического процесса.
33. Способ по п.32, при котором:
а) подвергают соединение природного или синтетического полимиксина или октапептина или его производное расщеплению с целью удаления боковой цепи указанного соединения полимиксина и выделяют циклический участок указанного соединения, и
б) подвергают сочетанию циклический участок, полученный на стадии а), с полученной синтетическим путем боковой цепью с целью получения производного полимиксина формулы (I) по п.1.
34. Способ по п.33, при котором расщепление на стадии а) осуществляют ферментативным путем.
35. Способ по п.33, при котором расщепление на стадии а) осуществляют химическим путем.
36. Способ по п.33, при котором расщепление на стадии а) осуществляют, используя сочетание как химической, так и ферментативной обработки.
| WO 2006083317 A9, 10.08.2006 | |||
| US 4510132 A, 09.04.1985 | |||
| THOMAS C.J | |||
| et al.: 'Kinetics of the interaction of endotoxin with polymyxin В and its analogs: a surface plasmon resonance analysis' FEBS LETTERS, 1999, vol.445, pages 420-424 | |||
| TSUBERY H | |||
| et al.: 'N-terminal modifications of Polymyxin В nonapeptides and their effect on antibacterial activity' |
Авторы
Даты
2012-07-10—Публикация
2007-08-10—Подача