ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к производным полимиксина и к их применениям при лечении инфекций, вызванных грамотрицательными бактериями. Производные полимиксина по настоящему изобретению особенно полезны при сенсибилизации бактерий для усиления эффектов других антибактериальных агентов.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Сепсис убивает более 215000 американцев ежегодно. По оценкам 750000 американцев инфицировано тяжелым сепсисом, и 29% из них погибает от него ежегодно. Смерти от сепсиса составляют 9% всех смертельных случаев в США. Сепсис убивает столько же американцев, сколько миокардиальные инфекции, даже больше, чем дорожно-транспортные происшествия.
От двух до трех миллионов американцев ежегодно заражается внутрибольничной инфекцией, и 10% из этих инфекций прогрессирует до сепсиса. Более чем 90000 этих пациентов погибает от сепсиса, инфицированного в больницах.
Тяжелый сепсис и септический шок (тяжелый сепсис, сочетанный с низким кровяным давлением) уносит вплоть до 135000 жизней ежегодно в отделениях интенсивной терапии (ОИТ) в Евросоюзе согласно Докладу о здоровье ОЭСР 2000. В Великобритании 5000 из 100000 пациентов, которые приобрели внутрибольничную инфекцию, ежегодно умирает от сепсиса в больницах, предназначенных для интенсивной терапии при приступах, принадлежащих организации ГСЗ (Государственной службы здравоохранения).
Потери в результате смерти от года к году возрастают в связи с тем фактом, что возросло число пациентов, предрасположенных к сепсису, таких как пожилые люди, недоношенные новорожденные и пациенты с раком, несмотря на то, что многие серьезные заболевания в большей степени излечимы, чем ранее. Также возросло применение инвазивных медицинских приборов и агрессивных методов лечения.
Грамотрицательные бактерии вызывают более чем 40% всех септицемических инфекций, и многие из грамотрицательных бактерий обладают в высокой степени множественной устойчивостью. Грамотрицательные бактерии дают более тяжелую симптоматику при терапии, чем грамположительные, поскольку они обладают уникальной структурой, наружной мембраной, в качестве их самой наружной структуры. Молекулы липополисахаридов, локализованные на наружной мембране, ингибируют более глубокую диффузию в клетку многих антибактериальных агентов, где расположены их конечные мишени. Более чем у 95% новых антибактериальных агентов, выделенных из природных источников или синтезированных химическим путем в 1972-1991 годах, отсутствовала активность против грамотрицательных бактерий (Vaara 1993).
Полимиксины представляют собой группу близкородственных антибиотических веществ, продуцируемых штаммами Paenibacillus polymyxa и родственными организмами. Эти катионные лекарства представляют собой относительно простые пептиды с молекулярными массами около 1000. Полимиксины, такие как полимиксин В, представляют собой декапептидные антибиотики, то есть они состоят из десяти (10) аминоацильных остатков. Они обладают бактерицидной активностью и особенно эффективны против грамотрицательных бактерий, таких как Escherichia coli и другие виды Enterobacteriaceae, Pseudomonas, Acinetobacter baumannii и других. Однако полимиксины обладают тяжелыми побочными эффектами, включая нефротоксичность и нейротоксичность. Поэтому эти лекарства имеют ограниченное применение в качестве терапевтических агентов в связи с высокой системной токсичностью.
Полимиксины применяют при терапии серьезных инфекций, вызванных этими бактериями, но в связи с токсичностью их применение было в широком масштабе запрещено в 70-е годы, когда были разработаны новые, лучше переносимые антибиотики. Недавнее появление штаммов грамотрицательных бактерий с множественной устойчивостью привело к необходимости терапевтического применения полимиксинов в качестве последнего средства, несмотря на их токсичность, и, поскольку многие из менее токсичных антибиотиков уже утратили свою эффективность против конкретных штаммов указанных бактерий, применение полимиксинов снова возросло.
Соответственно, в настоящее время полимиксины возвращены в терапевтический арсенал, хотя, вследствие их токсичности, в весьма ограниченном масштабе. Их системное (то есть не местное) применение, однако, в широком масштабе ограничено терапией инфекций, угрожающих жизни, вызванных множественно устойчивыми штаммами Ps. aeruginosa и A. baumannii, а также устойчивыми к карбо-пенемам кишечными бактериями.
Полимиксины состоят из циклической гептапептидной части и линейной части, состоящей из трипептидного участка и гидрофобного жирнокислотного хвоста, связанного с а-аминогруппой N-концевого аминокислотного остатка трипептида, и могут быть представлены общей формулой:
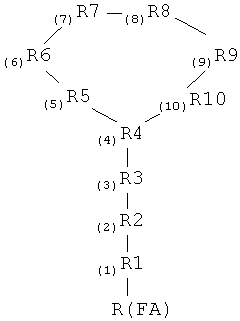
где R1-R3 представляют собой участок трипептидной боковой цепи; R4-R10 представляют собой гептапептидный кольцевой участок; R(FA) представляет собой гидрофобный жирнокислотный хвост, связанный с а-аминогруппой N-концевого аминокислотного остатка трипептида.
Полимиксиновая группа включает следующие полимиксины: A1, A2, B1-B6, ИЛ-полимиксин B1, C, D1, D2, E1, E2, F, K1, K2, M, P1, P2, S и T (Storm et al. 1977; Srinivasa and Ramachandran 1979). Все полимиксины являются поликатионными и обладают пятью (5) положительными зарядами за исключением полимиксинов D, F и S, которые обладают четырьмя (4) положительными зарядами. Следует отметить, что модифицированные полимиксины, у которых отсутствует жирнокислотная часть R(FA), но которые несут R1-R10, имеют один дополнительный положительный заряд по сравнению с природными полимиксинами, из которых они образованы, за счет свободной а-аминогруппы в N-конце производного. Соответственно, например, такое производное полимиксина В или полимиксина Е в сумме несет шесть (6) положительных зарядов.
Клинически применяемый полимиксин В и полимиксин Е отличаются друг от друга только по остатку R6, который представляет собой остаток D-фенилаланила в полимиксине В и остаток D-лейцила в полимиксине Е.
Циркулин А и В также классифицируют как полимиксины (Storm et al. 1977). Они отличаются от других полимиксинов только тем, что несут остаток изолейцила в положении R7, тогда как другие полимиксины имеют либо остаток треонила, либо остаток лейцила в указанном положении. Обзор структур некоторых полимиксинов см. в таблице 1.
Полимиксин В представлен приведенной ниже формулой:
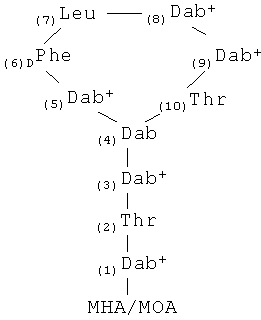
Имеющийся в продаже полимиксин В представляет собой смесь, где R-FA преимущественно представляет собой 6-метилоктаноил (6-МОА, в полимиксине В1), но также может представлять собой родственный жирный ацил, такой как 6-метилгептаноил (6-МНА, в полимиксине В2), октаноил (в полимиксине В3) или гептаноил (в полимиксине В4) (Sakura et al. 2004). Все эти варианты в равной степени эффективны против грамотрицательных бактерий E. coli (Sakura et al. 2004). Также аналогично в полимиксине Е1 (колистине А) и в циркулине A R-FA представляет собой 6-МОА, и в полимиксине Е2 (колистине В) и в циркулине В R-FA представляет собой 6-МНА. Различные исследователи присоединили различные гидрофобные группировки, включая различные остатки жирного ацила, к N-концу производных полимиксина и его аналогов, и показано, что полученные в результате производные обладают сильной антибактериальной активностью (Chihara ef al. 1973, Sakura et al. 2004 и публикация патента США №2006004185). Даже производное, которое несет объемный гидрофобный остаток 9-флуоренилметоксикарбонила в качестве R-FA, является почти столь же эффективным, что и полимиксин В, при ингибировании роста E. coli и других грамотрицательных бактерий (Tsubery et al. 2001).
Для биологической активности гептапептидная кольцевая структура является существенной (Storm et al. 1997). Производное с октапептидным кольцом значительно менее активно в качестве антибиотика.
Получены множественные модификации полимиксинов и множественные подобные полимиксинам синтетические молекулы, и с некоторыми ограничениями они сохранили свою биологическую активность. Эти модификации включают, но не ограничены ими, модификации в боковой цепи, а также молекулы, в которых характерный гидрофобный аминокислотный остаток (такой как D-Phe или Leu) заменен другим гидрофобным аминокислотным остатком, или в которых катионный Dab заменен другим катионным аминоацильным остатком, таким как остаток Lys, Arg или орнитина (Storm et а/. 1997, Tsubery et al. 2000а, Tsubery et al. 2002, публикация патента США №2004082505, Sakura ef al. 2004, публикация патента США №2006004185).
Другие модификации, которые приводят в результате к соединениям, обладающим по меньшей мере частичной микробиологической активностью, включают, но не ограничены ими, алканоиловые эфиры, где OH-группы остатков треонила образуют эфиры с алканоилами, такими как пропионил и бутирил (патент США №3450687).
Октапептины близки полимиксинам, но имеют ковалентную связь вместо остатков R1-R2 (Таблица 1). В данном изобретении положения R пронумерованы в соответствии с таковыми в природных полимиксинах и, таким образом, только аминоацильный остаток в боковой цепи октапептинов определен как R3. Соответственно, октапептины представляют собой октапептиды, тогда как все природные полимиксины представляют собой декапептиды, и они обладают только четырьмя (4) положительными зарядами. Остатки R-FA среди различных октапептинов (А1, А2, A3, В1, В2, В3, С1) включают следующие: 3-OH-8-метилдекановую кислоту, 3-OH-8-метилнонановую кислоту и β-OH-6-метилоктановую кислоту. Производные, которые имеют жирнокислотный остаток, содержащий от 6 до 18 атомов углерода, обладают сильной антибактериальной активностью против E. coli (Storm et al. 1977).
Первой мишенью полимиксинов в грамотрицательных бактериях является их наружная мембрана (НМ), которая представляет собой эффективный барьер проницаемости против многих токсичных агентов, таких как антибиотики большого размера (Mw более чем 700 Д), а также гидрофобные антибиотики. Посредством связывания с молекулами липополисахаридов (ЛПС), расположенными на внешней поверхности НМ, полимиксины повреждают структуру и функцию НМ и в результате пермеабилизуют (то есть делают проницаемой) НМ как для самого полимиксина, так и для многих других токсичных агентов (Nikaido and Vaara 1985, Vaara 1992, Nikaido 2003). Конечной и летальной мишенью (бактерицидной мишенью) полимиксинов считают цитоплазматическую мембрану (внутреннюю мембрану) бактерий.
Многочисленные усилия сделаны по снижению токсичности полимиксинов. В результате обработки полимиксина Е (колистина) формальдегидом и бисульфитом натрия получают колистин сульфометат, в котором свободные аминогруппы пяти остатков диаминомасляной кислоты частично замещены сульфометильными группами (Таблица 1). Препараты состоят из неопределенных смесей моно-, ди-, три-, тетра- и пентазамещенных соединений. В сульфометилированных препаратах, когда они только что растворены в воде, первоначально отсутствует как антибактериальная активность, так и токсичность исходной молекулы, но, когда эти соединения начинают разлагаться в растворе, в крови или в тканях с образованием менее замещенных производных и свободного колистина, как антибактериальная активность, так и токсичность частично возвращаются. Кроме того, степень исходного сульфометилирования, очевидно, варьирует между имеющимися в продаже фармацевтическими препаратами. Опубликовано множество других путей блокирования всех свободных аминогрупп. Примеры включают, но не ограничены ими, образование нестабильных шиффовых оснований с аминокислотами (Storm et al. 1977).
Полимиксин Е нонапептид (PMEN, колистин нонапептид, Таблица 1), полученный путем ферментативной обработки полимиксина Е, и в котором отсутствуют R-FA и R1, как было показано в 1973 г., является менее токсичным, чем исходное соединение, в анализе на острую токсичность (немедленную смерть преимущественно вследствие прямой нервно-мышечной блокады) у мышей (Chihara et al. 1973). Однако у него также отсутствует антибактериальная активность, которая измерена на основании его способности к ингибированию бактериального роста (Chirara et al. 1973). Роль линейной части может вносить вклад в антибактериальную активность полимиксинов.
Vaara и Vaara, с другой стороны, показали, что полимиксин В нонапептид (PMBN, Таблица 1) сохраняет активность пермеабилизации НМ грамотрицательных бактерий (Vaara and Vaara 1983а, b, с; патент США 4510132; Vaara 1992). Соответственно, даже, несмотря на то, что у него отсутствует прямая антибактериальная активность (то есть способность к ингибированию бактериального роста), он способен сенсибилизировать (то есть делать чувствительными, как также называют, делать восприимчивыми) бактерии ко многим антибактериальным агентам, таким как гидрофобные антибиотики, а также антибиотики большого размера и некоторые другие токсичные агенты.
PMBN также сенсибилизирует бактерии к бактерицидной активности системы комплемента человека, присутствующей в свежей сыворотке человека в качестве защитной системы первой линии против паразитов (Vaara and Vaara 1983а, Vaara et al. 1984, Vaara 1992). Кроме того, он сенсибилизирует бактерии к объединенной бактерицидной активности сывороточного комплемента и полиморфно-ядерных лейкоцитов человека (Rose et al. 1999).
PMBN подобен PMEN в том, что он является менее токсичным в анализе на острую токсичность у мышей, чем немодифицированные полимиксины. В других токсикологических анализах по нескольким критериям доказано, что PBMN является менее токсичным, чем его исходное соединение, но это производное полимиксина все же считают слишком нефротоксичным для клинического применения (Vaara 1992).
PMBN несет пять (5) положительных зарядов. В последующих исследованиях выявлено, достаточно неожиданно, что PMEN, также несущий пять (5) положительных зарядов, а также деацилполимиксин В и деацилполимиксин Е, оба несущие шесть (6) положительных зарядов, являются эффективными агентами для сенсибилизации бактерий к другим антибиотикам (Viljanen et al. 1991, Vaara 1992). Кроме того, показано, что дополнительно структурно редуцированное производное полимиксина В октапептид (РМВО) сохраняет очень эффективную пермеабилизи-рующую активность, тогда как полимиксин В гептапептид (РМВН) является менее активным (Kimura et al. 1992). PMBN, PMEN и PMBO имеют пять (5) положительных зарядов, тогда как РМВН имеет только четыре (4) положительных заряда. Это различие может объяснить более слабую активность PMBH.
Группой исследователей Ofek, Tsubery и Friedkin недавно описаны подобные полимиксинам пептиды, которые были связаны с хемотаксическими пептидами, такими как fMLF, которые привлекают полиморфно-ядерные лейкоциты (публикация патента США №2004082505, Tsubery et al. 2005). Эти описанные пептиды fMLF-PMBN, MLF-PMBN, fMLF-PMEN, fMLF-PMBO и MLF-PMBO все несут четыре (4) положительных заряда, которые сенсибилизируют грамотрицательные бактерии к антибиотикам, даже хотя не было опубликовано сравнительных исследований с возрастающими концентрациями соединений (Tsubery et al. 2005).
В целях исследования структурных и функциональных свойств полимиксинов в нескольких работах, среди других соединений, раскрыты производные полимиксина, имеющие менее чем четыре (4) положительных заряда.
Teuber (1970) описана обработка полимиксина В уксусным ангидридом, в результате которой получен препарат, содержащий как полимиксин В, так и его моно-, ди-, три-, тетра- и пента-N-ацетилированые формы. Teuber также выделил каждую группу и не количественно показал, используя анализ диффузии в агаре, что у пентаацетилированных и тетраацетилированных форм отсутствует способность к остановке роста Salmonella typhimurium, тогда как ди- и моноацетилированные формы обладают такой способностью. Триацетилированная форма обладает некоторой способностью.
Srinivasa и Ramachandran (1978) выделили частично формилированные производные полимиксина В и показали, что диформилированное производное, а также триформилированное производное ингибировали рост Pseudomonas aeruginosa. Этими авторами не раскрыта способность этих соединений к сенсибилизации бактерий к антибиотикам. Кроме того, в 1980 г. они показали, что свободные аминогруппы триформилполимиксина В в остатках R1 и R3, а также свободные аминогруппы диформилполимиксина В в остатках R1, R3 и R5 являются существенными, тогда как свободные аминогруппы в R8 и R9 являются несущественными для ингибирования роста (Srinivasa and Ramachandran, 1980а).
Укороченное производное полимиксина В октаноилполимиксин В гептапептид раскрыто Sakura et al. (2004). Присоединение остатка октаноила к N-концу остатка R4 полимиксина В гептапептида приводит в результате к соединению, имеющему только три (3) положительных заряда. Sakura et al. обнаружили, что октаноилполимиксин В гептапептид ингибирует рост бактерий только при очень высокой концентрации (128 мкг/мл), тогда как другие производные, такие как октаноилполимиксин В октапептид и октаноилполимиксин В нонапептид, оба имеющие четыре (4) заряда, являются очень эффективными агентами по ингибированию бактериального роста.
В публикации патента США №2006004185 недавно раскрыты некоторые производные полимиксина и промежуточные соединения, которые можно использовать для синтеза новых пептидных антибиотиков. Описанные антибактериальные соединения обладали четырьмя (4) или пятью (5) положительными зарядами.
Кроме того, близкородственные соединения полимиксин В и полимиксин В1 также раскрыты Okimura et al. (2007) и de Visser er al. (2003). Okimura et al. исследовали химическое преобразование природного полимиксина В и колистина в их N-концевые производные, и de Visser et al. исследовали твердофазный синтез полимиксина B1 и его аналогов посредством метода надежно связанного линкера. Антибактериальные соединения, описанные в этих работах, обладали четырьмя (4) или пятью (5) положительными зарядами.
Все еще существует крайняя необходимость в производных полимиксина, которые сенсибилизируют бактерии для усиления эффектов других антибактериальных агентов, для эффективных терапий бактериальных инфекций, в частности, инфекций, вызванных грамотрицательными бактериями с множественной устойчивостью.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к производному полимиксина, где суммарное число положительных зарядов при физиологическом значении pH равно трем, и где это производное имеет жирнокислотный хвост (то есть R(FA) или D), содержащий от 1 до 5 атомов углерода. Обнаружено, что некоторые производные полимиксина по изобретению, имеющие жирнокислотные хвосты из 1-5 атомов углерода, могут обладать улучшенными фармакокинетическими свойствами по сравнению с нативными полимиксинами, октапептинами и производными полимиксина с более длинными жирнокислотными хвостами. Примеры этих фармакокинетических свойств включают, но не ограничены ими, более длительное время полужизни в сыворотке, повышенный почечный клиренс и/или повышенное выделение с мочой.
Настоящее изобретение относится, по меньшей мере частично, к производным полимиксина формулы (I):
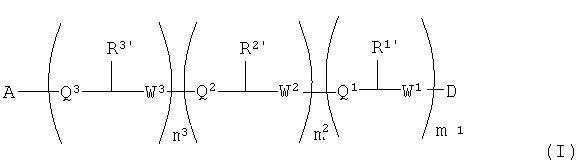
где:
A представляет собой кольцевую группировку полимиксина;
D представляет собой концевую группировку, содержащую от 1 до 5 атомов углерода;
m1, m2 и m3 каждое независимо равно 0 или 1;
Q1, Q2 и Q3 каждый независимо представляет собой CH2, C=O или C=S;
W1, W2 и W3 каждый независимо представляет собой NR4, O или S;
R1, R2, и R3 каждый независимо представляет собой боковые цепи природных или неприродных аминокислот, алкил, алкенил, арилалкил, арил, алкокси, алкоксикарбонил, арилоксикарбонил, алкиламино или алкинил; и
R4 представляет собой атом водорода или алкил,
и к их фармацевтически приемлемым пролекарствам и солям, при условии, что (1) когда A представляет собой кольцо октапептина, m1 и m2 равны 0, m3 равно 1, W3 представляет собой NH, Q3 представляет собой C=O, и R3 представляет собой боковую цепь диаминомасляной кислоты (Dab), тогда D не представляет собой C2-C5 ацил, и (2) когда D представляет собой ацетил, бутаноил или пентаноил, тогда R3 не представляет собой боковую цепь Dab.
Изобретение также направлено на производные полимиксина формулы (II):
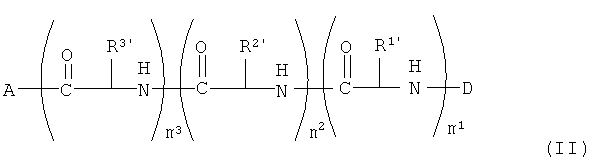
где
A представляет собой кольцевую группировку полимиксина;
D представляет собой R12-C(=O), R12-C(=S) или R12';
m1, m2 и m3 каждый независимо равны 0 или 1, при условии, что по меньшей мере одно из m1, m2 и m3 равно 1;
R1', R2,n R3' каждый независимо представляет собой боковые цепи природных или неприродных аминокислот, алкил, алкенил, арилалкил, арил, алкокси, алкоксикарбонил, арилоксикарбонил, алкиламино или алкинил; и
R12 представляет собой C1-C4 алкил, C2-C4 алкенил или C2-C4 алкинил,
R12' представляет собой C1-C5 алкил, C2-C5 алкенил или C2-C5 алкинил, и их фармацевтически приемлемые пролекарства и соли, при условии, что (1) когда A представляет собой кольцо октапептина, m1 и m2 равны 0, m3 равно 1, и R3' представляет собой боковую цепь диаминомасляной кислоты (Dab), и D представляет собой R12-C=O, тогда R12 не представляет собой C1-С5 алкил, и (2) когда D представляет собой ацетил, бутаноил или пентаноил, тогда R3' не представляет собой боковую цепь Dab.
В другой форме осуществления изобретение также включает производные полимиксина формулы (III):
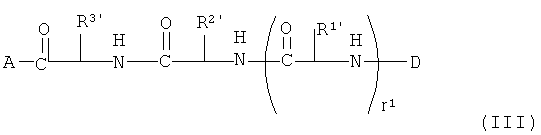
где
A представляет собой кольцевую группировку полимиксина В или полимиксина Е;
D представляет собой R12-C(=O), R12-C(=S) или R12';
m1 равно 0 или 1;
R1', R2' и R3' каждый независимо представляет собой боковые цепи природных или неприродных аминокислот, алкил, алкенил, арилалкил, арил, алкокси, алкоксикарбонил, арилоксикарбонил, алкиламино или алкинил, где по меньшей мере один из R2' и R3' содержит карбамильную, гидроксильную или карбоксилатную группу; и
R12 представляет собой C1-C4 алкил,
R12' представляет собой C1-C5 алкил,
и их фармацевтически приемлемые пролекарства и соли, при условии, что, когда D представляет собой ацетил, бутаноил или пентаноил, тогда R3' представляет собой не боковую цепь Dab.
Еще в одной другой форме осуществления изобретение также включает производные полимиксина формулы (IV):
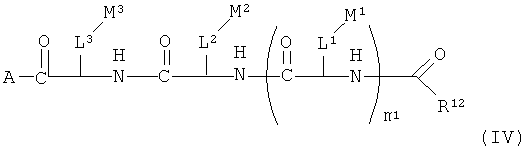
где
A представляет собой кольцевую группировку полимиксина В или полимиксина Е;
m1 равно 0 или 1;
L1, L2 и L3 каждый независимо представляет собой C1-C3 алкил или ковалентную связь;
M1, M2 и M3 каждый независимо представляет собой H, C(=O)NH2, C(=O)OH или -OH;
R12 представляет собой C1-C4 алкил,
и их фармацевтически приемлемые пролекарства и соли, при условии, что, когда R12 представляет собой метил, пропил или бутил, тогда L3-M3 представляет собой не боковую цепь Dab, и где указанное производное имеет три положительных заряда при физиологическом pH.
В другой форме осуществления изобретение также включает производные полимиксина формулы (V):
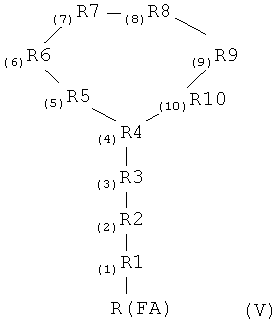
где R4 представляет собой аминокислотный остаток, содержащий функциональную боковую цепь, способную к циклизации молекулы;
R6 и R7 каждый независимо выбран из возможно, но не обязательно замещенных гидрофобных аминокислотных остатков;
R10 представляет собой Leu или любой не гидрофобный аминокислотный остаток; и
где R1 является возможным, но не обязательным; и где R1, R2, R3, R5, R8 и R9 каждый представляет собой независимо выбранный аминокислотный остаток; и где R(FA) представляет собой возможно, но не обязательно замещенный алкано-ильный или алкильный остаток, имеющий суммарно от 1 до 5 атомов углерода; или его фармацевтически приемлемая соль или пролекарство, при условии, что (1) когда R1 и R2 отсутствуют, R3, R4. R5, R8 и R9 представляют собой Dab, R6 представляет собой D-Leu, R7 представляет собой L-Leu или L-Phe, и R10 представляет собой Thr, или когда R1 и R2 отсутствуют, R3, R4. R5, R8, и R9 представляют собой Dab, R6 представляет собой D-Phe, R7 представляет собой L-Leu и R10 представляет собой Thr, тогда R(FA) представляет собой не незамещенный алканоильный остаток, и (2) когда R(FA) представляет собой ацетил, бутаноил или пентаноил, тогда R3 представляет собой не Dab.
Более конкретно настоящее изобретение относится к производному, где R2-R10 выбраны из группы, состоящей из Thr-DSer-cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-] [=SEQ ID NO: 10] и Thr-DAsn-cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-] [=SEQ ID NO: 39].SEQ ID NO: 10 соответствует SEQ ID NO: 1, и SEQ ID NO: 39 соответствует SEQ ID NO: 2 в прилагаемом перечне последовательностей.
Изобретение также относится к комбинированному продукту, содержащему два или более производных согласно настоящему изобретению, и к фармацевтической композиции, содержащей такое производное(ые) или их комбинацию и фармацевтически приемлемые носители и эксципиенты.
Кроме того, настоящее изобретение относится к способу сенсибилизации грамотрицательных бактерий к антибактериальному агенту, при котором вводят, одновременно или последовательно в любом порядке, терапевтически эффективное количество указанного антибактериального агента и производного согласно настоящему изобретению, где указанный антибактериальный агент может быть выбран из группы, состоящей из кларитромицина, азитромицина, эритромицина и других макролидов, кетолидов, клиндамицина и других линкозаминов, стрептограминов, рифампина, рифабутина, рифалазила и других рифамицинов, фузидовой кислоты, мупироцина, оксазолидинонов, ванкомицина, далбаванцина, телаванцина, оритаванцина и других гликопептидных антибиотиков, фторхинолонов, бацитрацина, производных тетрациклина, беталактамовых антибиотиков, новобиоцина, плевромутилинов, ингибиторов синтеза фолатов, ингибиторов деформилазы и ингибиторов бактериального выкачивающего насоса.
Также предложены способы разработки новых антибиотиков а также сенсибилизации клинически значимых грамотрицательных бактерий к защитному механизму комплемента хозяина, присутствующему в сыворотке.
В настоящем изобретении также предложены применения производного полимиксина согласно настоящему изобретению при получении лекарства для сенсибилизации грамотрицательных бактерий, таких как, например, Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter cloacae, Citrobacter freundii, и Acinetobacter baumannii, против антибактериальных агентов; и для сенсибилизации грамотрицательных бактерий к защитному механизму комплемента хозяина, присутствующему в сыворотке.
Настоящее изобретение также относится к способам лечения грамотрицательных инфекций у субъекта, включающим введение субъекту производного по изобретению (например, производного формул (I-(V)) в комбинации с антибактериальным агентом, так, что субъекта лечат от инфекции.
Наконец, настоящее изобретение относится к способу получения производного полимиксина согласно настоящему изобретению, включающему (А) модифицирование природного или синтетического соединения полимиксина или октапептина или его производного, несущего от 4 до 5 положительно заряженных остатков и концевую группировку (D), содержащую от 1 до 5 атомов углерода, путем замены от 1 до 2 из указанных положительно заряженных остатков нейтральными остатками или ковалентной связью, или путем преобразования от 1 до 2 из указанных положительно заряженных остатков в нейтральные остатки с целью получения производного полимиксина формулы (I), несущего 3 положительно заряженных остатка и концевую группировку (D), содержащую от 1 до 5 атомов углерода, или (Б) модифицирование природного или синтетического соединения полимиксина или октапептина или его производного, несущего от 4 до 5 положительно заряженных остатков и концевую группировку (D), содержащую более 5 атомов углерода, путем замены от 1 до 2 из указанных положительно заряженных остатков нейтральными остатками или ковалентной связью, или путем преобразования от 1 до 2 из указанных положительно заряженных остатков в нейтральные остатки, и путем замены указанной концевой группировки (D), имеющей более 5 атомов углерода, концевой группировкий (D), содержащей суммарно от 1 до 5 атомов углерода, с целью получения производного полимиксина формулы (1), несущего 3 положительно заряженных остатка и концевую группировку (D), содержащую суммарно от 1 до 5 атомов углерода, или (В) модифицирование природного или синтетического соединения полимиксина или октапептина или его производного, несущего от 4 до 6 положительно заряженных остатков, и в котором отсутствует концевая группировка (D), путем замены от 1 до 3 из указанных остатков нейтральными остатками или ковалентной связью, или преобразования от 1 до 3 из указанных остатков в нейтральные остатки, и путем введения концевой группировки (D), содержащей суммарно от 1 до 5 атомов углерода, с целью получения производного полимиксина формулы (I) по п.1, несущего 3 положительно заряженных остатка и R(FA), имеющую суммарно от 1 до 5 атомов углерода. В одной форме осуществления изобретения концевая группировка D представляет собой R12-C(=O), R12-C(=S) или R12', где R12 и R12' определены здесь ниже. В другой форме осуществления изобретения концевая группировка D представляет собой R(FA), который представляет собой возможно, но не обязательно замещенный алканоильный или алкильный остаток, имеющий суммарно от 1 до 5 атомов углерода.
ОПРЕДЕЛЕНИЯ
"Физиологическое значение pH", как используют здесь, относится к значению pH более чем 7,0 и ниже 7,6, такое как значение pH в интервале от 7,1 до 7,5, например, в интервале от 7,2 до 7,4.
"Положительный заряд", как используют здесь, обозначает положительные заряды при вышеуказанных физиологических значениях pH.
"Катионная" молекула, как используют здесь, относится к молекуле, которая содержит один или более чем один положительный заряд.
"Аминокислотный остаток", как используют здесь, относится к любому природному, неприродному или модифицированному аминокислотному остатку, либо в L-, либо в D-конфигурации.
"Эквивалентные остатки", как используют здесь, подразумевают как включающие очевидные модификации, например, аминокислот, приводящие в результате к неприродным аминокислотам или их производным, но сохраняющие структурную и/или функциональную способность замененного остатка.
"Природный полимиксин(ы)", как используют здесь, относится к полимиксинам и циркулинам.
"Производное полимиксина" относится, для цели данного изобретения, к синтетическим или полусинтетическим производным природных полимиксинов или октапептинов, который имеют циклическую гептапептидную (или гептапептидную кольцевую) часть R4-R10 и боковую цепь, связанную с N-концевым аминоацильным остатком R4. Боковая цепь может состоять из R(FA)-триаминоацил(R1-R3), R(FA)-диаминоацил(R2-R3), R(FA)-моноаминоацил(R3) или из одной R(FA).
"R(FA)" или "жирнокислотный хвост," как используют здесь, относится к жирнокислотной части, то есть к алканоильной части структуры полимиксина, связанной с N-концевым аминокислотным остатком линейной пептидной части (боковой цепи) полимиксина или, в отсутствие линейной пептидной части, с аминокислотным остатком R4 (аминокислотой в положении 4 циклической пептидной части полимиксина). Кроме того, для цели настоящего изобретения R(FA) может также представлять собой родственную гидрофобную группу, такую как алкил. В некоторых формах осуществления изобретения жирнокислотный хвост может в некоторых случаях представлять собой концевую группировку, выбранную из группы, состоящей из R12-(C=O); R12-SO2-; R12-(C=NH)-; R12-NH-(C=S)-; R12-NH-(C=O)-; R12-NH-(C=NH)-;R12-O-(C=S)-; R12-O-(C=O); R12-P(O)OH-; R12-(C=S) и R12', где R12 и R12' представляют собой алкил, алкенил, алкинил, арил или арилалкил.
"Соединения", как используют здесь, включают все стереохимические изомеры указанного соединения.
"Сенсибилизирующую активность" или "способность к сенсибилизации", как используют здесь, подразумевают как включающую любую способность повышать чувствительность бактерии, делать бактерию чувствительной или делать ее восприимчивой к антибактериальному агенту.
"Кольцевая группировка полимиксина" или "A" включает кольцевую часть полимиксина А, полимиксина В, ИЛ-полимиксин-В1, полимиксина D, полимиксина Е, полимиксина F, полимиксина М, полимиксина S, полимиксина Т, циркулина А, октапептина А, октапептина В, октапептина С, октапептина D и их производных. Примеры производных включают группировки с модификациями, которые по существу не влияют на способность кольцевой группировки к осуществлению предназначенной ей функции, то есть в качестве антибиотика, и/или на ее способность к сенсибилизации бактерии к одному или более чем одному антибактериальному агенту. Термин "кольцевая группировка полимиксина В" относится к кольцевой части полимиксина В (то есть cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-]). Другие примеры кольцевых группировок полимиксина включают группировки формулы:
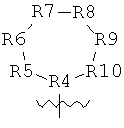
где
R4 представляет собой аминокислотный остаток, содержащий функциональную боковую цепь, способную к циклизации молекулы;
R5, R8 и R9 представляют собой независимо выбранные аминокислотные остатки;
R6 и R7 представляют собой возможно, но не обязательно замещенные гидрофобные аминокислотные остатки; и
R10 представляет собой Leu или любой не гидрофобный аминокислотный остаток. Другие примеры R4-R10 более подробно обсуждены в формуле (V).
Термин "кольцо октапептина" относится к кольцевой части нативного октапептина А (то есть cy[Dab-Dab-DLeu-LLeu-Dab-Dab-Leu-], то есть соединения, где R4, R5, R8 и R9 представляют собой Dab, R6 представляет собой DLeu, R7 представляет собой LLeu и R10 представляет собой Leu), октапептина В (то есть cy[Dab-Dab-DLeu-LPhe-Dab-Dab-Leu-], то есть соединения, где R4, R5, R8 и R9 представляют собой Dab, R6 представляет собой DLeu, R7 представляет собой LPhe и R10 представляет собой Leu) и октапептина С (то есть cy[Dab-Dab-DPhe-LLeu-Dab-Dab-Leu-], то есть соединения, где R4, R5, R8 и R9 представляют собой Dab, R6 представляет собой DPhe, R7 представляет собой LLeu и R10 представляет собой Leu).
Термин "пролекарство" включает группировки, которые расщепляются in vivo с получением активного соединения производного полимиксина по изобретению. Пролекарства включают группировки, которые маскируют или иначе нейтрализуют положительные заряды (например, -NH3 + или другие протонированные соединения) при физиологическом pH. Как только пролекарство вводят субъекту, пролекарственные группировки или группировки, маскирующие заряд, расщепляются или иначе удаляются с получением активного производного полимиксина по изобретению, возможно, но не обязательно с тремя положительными зарядами при физиологическом pH.
Термин "группировка, маскирующая заряд", включает группировки, которые обратимо нейтрализуют положительные заряды на производных. Предпочтительно эти группировки расщепляются или иначе диссоциируют с положительными зарядами соединения полимиксина после его введения субъекту. Примеры группировок, нейтрализующих заряд, включают сульфоалкил (например, сульфометилированные производные). Другие группировки, маскирующие положительный заряд, включают, но не ограничены ими, хлорид, бромид, йодид, нитрат, сульфат, бисульфат, фосфат, кислый фосфат, изоникотинат, ацетат, лактат, салицилат, цитрат, кислый цитрат, тартрат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкуронат, сахарат, формиат, бензоат, глутамат, метансульфонат, этансульфонат, бензолсульфонат, пара-толуолсульфонат и памоат (то есть 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)).
Термин "субъект" включает организмы, способные страдать бактериальными инфекциями, примеры субъектов включают млекопитающих, например, лошадей, коров, свиней, овец, коз, кошек, собак, кроликов, хорьков, обезьян и предпочтительно людей.
Сокращения
Жирные кислоты: ЖК, остаток жирного ацила; 6-МОА и МОА, остаток 6-метилоктаноила; 6-МНА и МНА, остаток 6-метилгептаноила; МО(Н)А, смесь 6-метилоктаноила, 6-метилгептаноила и родственных остатков жирного ацила, встречающихся в полимиксине В; OHMDA, 3-OH-8-метилдекановая кислота; OA, октаноил; DA, деканоил; Ac, ацетил; Me, метил.
Аминокислоты: Dab, остаток α,γ-диамино-н-бутирила; fDab, остаток N-γ-формилдиамино-н-бутирила; acDab, остаток N-γ-ацетилдиамино-н-бутирила; Abu, остаток α-аминобутирила; Asn, остаток аспартила; Thr, остаток треонила; Ser, остаток серинила; Phe, остаток фенилаланила; Leu, остаток лейцила; lle, остаток изолейцила; Ala, остаток аланила; sm-Dab, остаток γ-сульфометилированного α,γ-диамино-н-бутирила. Однобуквенные коды для модифицированных аминоацильных остатков: X, Dab; Z, Abu; B, N-γ-fDab; J, N-γ-acDab.
Пептиды: DAPB, деацилполимиксин В; DAC, деацилколистин; PMBN, полимиксин В нонапептид; PMEN, полимиксин Е нонапептид; РМВО, полимиксин В октапептид; РМНР, полимиксин В гептапептид.
Другие: су, цикло (для обозначения циклической части пептида, заключенной в скобки); f, формил; ас, ацетил; sm, сульфометил; MS, метансульфонат; ЛПС, липополисахарид; НМ, наружная мембрана; MIC, минимальная ингибиторная концентрация; КОЕ, колониеобразующая единица. Символ * используют здесь для отметки остатков, между которыми гептапептидная кольцевая часть соединения замкнута, оставляя остальную часть молекулы в виде боковой цепи.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Теперь обнаружено, что некоторые соединения, подобные полимиксинам, содержащие только три (3) положительных заряда и имеющие только короткий хвост жирного ацила R(FA) или концевую группировку (D) (суммарно не более 5 атомов углерода все же обладают способностью к сенсибилизации грамотрицательных бактерий к антибактериальным агентам, таким как антибиотики, полусинтетические антибиотики и химиотерапевтические агенты, а также защитные факторы хозяина, такие как система комплемента свежей сыворотки человека.
Поскольку эти новые соединения не обладают более чем тремя (3) положительными зарядами, они, по аналогии с производными полимиксина, описанными в заявке на патент США, серийный №11/891,629, могут быть менее токсичными в целом и в меньшей степени нефротоксичными в частности, чем полимиксины и их известные производные. Подобным образом, настоящим изобретенные соединения могут высвобождать меньше гистамина из тканей хозяина, чемполимиксин, и обладают преимущественными фармакокинетическими свойствами по сравнению с полимиксином В, колистином и их ранее описанными производными. Кроме того, короткоцепочечная R(FA) или концевая группировка (D) могут сделать новые соединения менее токсичными в анализах на острую токсичность, по аналогии с полимиксином В нонапептидом и колистином нонапептидом, у которых полностью отсутствует часть жирного ацила. Кроме того, новые соединения могут обладать фармакокинетическими свойствами, которые дают преимущество по сравнению с производными полимиксина, которые имеют длинную R(FA) или концевую группировку (D) более чем с пятью атомами углерода.
В одной форме осуществления изобретение относится к производным полимиксина формулы (I):
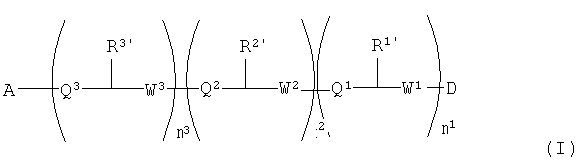
где
A представляет собой кольцевую группировку полимиксина;
D представляет собой концевую группировку, содержащую от 1 до 5 атомов углерода;
m1, m2 и m3 каждое независимо равно 0 или 1;
Q1, Q2 и Q3 каждый независимо представляет собой CH2, C=O или C=S;
W1, W2 и W3 каждый независимо представляет собой NR4, O или S;
R1', R2' и R3' каждый независимо представляет собой боковые цепи природных или неприродных аминокислот, алкил, алкенил, арилалкил, арил, алкокси, алкоксикарбонил, арилоксикарбонил, алкиламино или алкинил; и
R4 представляет собой атом водорода или алкил,
и к их фармацевтически приемлемым пролекарствам и солям, при условии, что (1) когда A представляет собой кольцо октапептина, m1 и m2 равны 0, m3 равно 1, W3 представляет собой NH, Q3 представляет собой C=O и R3' представляет собой боковая цепь диаминомасляной кислоты (Dab), тогда D представляет собой не C2-C5 ацил, и (2) когда D представляет собой ацетил, бутаноил или пентаноил, тогда R3 представляет собой не боковую цепь Dab.
В некоторых формах осуществления соединения по изобретению (например, производные любой из формул (I)-(V)) могут иметь по меньшей мере два, но не более чем три положительных заряда при физиологическом pH. В другой форме осуществления соединения имеют три положительных заряда при физиологическом pH.
Примеры пролекарств этих производных включают производные с группировками, маскирующими заряд, которые нейтрализуют три положительных заряда при введении субъекту, которые удаляются in vivo с получением соединения с тремя положительными зарядами. Примеры группировок, маскирующих заряд, включают сульфоалкильные группировки, такие как сульфометил.
Предпочтительно производные имеют три положительных заряда при физиологическом pH, как определено выше. В некоторых формах осуществления изобретения, R1', R2' и R3' не содержат положительно заряженных функциональных групп при физиологическом pH. R1', R2' и R3' могут содержать, например, одну, либо две, либо более гидроксильных, карбоксилатных, карбамильных, тиоловых, сульфатных, сульфонильных или фосфатных групп.
В одной форме осуществления m1 равно 0, и m2 и m3 каждое равно 1. В другой Q2 и Q3 каждый представляет собой C=O, и W2 и W3 каждый представляет собой NH.
В некоторых формах осуществления R2' замещен одной или более чем одной группой, выбранной из гидроксильной, карбамильной, карбоксилатной, тиоловой, сульфатной, сульфонильной или фосфатной групп. Предпочтительно R2' замещен карбамильной, гидроксильной или карбоксилатной группой. Примеры R2' включают замещенный алкил и боковые цепи аланина, аминомасляной кислоты, аспарагина, аспарагиновой кислоты, диаминомасляной кислоты, глутаминовой кислоты, глутамина, серина или треонина либо в D-, либо в L-конфигурации. Предпочтительно, R2' представляет собой D-аланин, L-серин или L-треонин.
В некоторых формах осуществления, R3' замещен одной или более чем одной группой выбранной из карбамильной, гидроксильной, карбоксилатной, тиоловой, сульфатной, сульфонильной или фосфатной групп. Предпочтительно R3' замещен алкилом и может быть замещен карбамильной, гидроксильной или карбоксилатной группой. R3' может представлять собой боковую цепь аланина, аминомасляной кислоты, аспарагина, аспарагиновой кислоты, диаминомасляной кислоты, глутаминовой кислоты, глутамина, серина или треонина либо в D-, либо в L-конфигурации. Предпочтительно, R3' представляет собой D-аспарагин, L- или D-серин.
Примеры A включают кольцевую группировку полимиксина В (то есть cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-] и полимиксина Е (то есть cy[Dab-Dab-DLeu-Leu-Dab-Dab-Thr-]).
В следующей форме осуществления концевая группировка выбрана из группы, состоящей из R12-(C=O); R12-SO2-; R12-(C=NH)-; R12-NH-(C=S)-; R12-NH-(C=O)-; R12-NH-(C=NH)-; R12-O-(C=S)-; R12-O-(C=O); R12-P(O)OH-; R12-(C=S) или R12', где R12 и R12' каждый представляет собой алкил, циклоалкил, алкенил, алкинил, арил или арилалкил. В некоторых формах осуществления D представляет собой R12-(C=O) или R12-(C=S) и R12 представляет собой метил, этил, пропил или бутил. Конкретные примеры D включают ацетил, пропионил, бутаноил и пентаноил.
В другой форме осуществления изобретение также относится к производным полимиксина формулы (II):
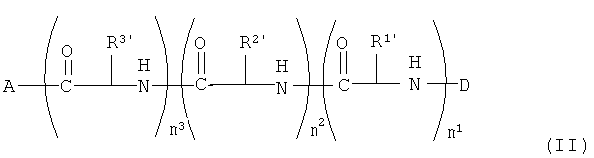
где
A представляет собой кольцевую группировку полимиксина;
D представляет собой R12-C(=O), R12-C(=S) или R12';
m1, m2 и m3 каждое независимо равно 0 или 1, при условии, что по меньшей мере одно из m1, m2 и m3 равно 1;
R1', R2' и R3' каждый независимо представляет собой боковые цепи природных или неприродных аминокислот, алкил, алкенил, арилалкил, арил, алкокси, алкоксикарбонил, арилоксикарбонил, алкиламино или алкинил; и
R12 представляет собой C1-C4 алкил, C2-C4 алкенил или C2-C4 алкинил,
R12' представляет собой C1-C5 алкил, C2-C5 алкенил или C2-C5 алкинил,
и к их фармацевтически приемлемым пролекарствам и солям, при условии, что (1) когда А представляет собой колько октапептина, m1 и m2 равны 0, m3 равно 1 и R3' представляет собой боковую цепь диаминомасляной кислоты (Dab) и D представляет собой R12-C=O, тогда R12 представляет собой не C1-C5 алкил и (2) когда D представляет собой ацетил, бутаноил или пентаноил, тогда R3' представляет собой не боковую цепь Dab.
Предпочтительно производное формулы (II) имеет три положительных заряда при физиологическом pH. В следующей форме осуществления m1 может быть равно 0 и/или m2 и m3 может быть каждое равно 1. В следующей форме осуществления R2' и/или R3' может каждый независимо представлять собой замещенный алкил (например, замещенный карбамильной, гидроксильной или карбоксилатной группой). Кроме того, R2' и/или R3' может каждый представлять собой боковую цепь серина или треонина (включая обе, D и L, конфигурации). Примеры R2' включают боковые цепи D-аланина, L-серина и L-треонина. Примеры R3' включают боковые цепи D-аспарагина, L- и D-серина.
В следующей форме осуществления R12 представляет собой алкил и D может представлять собой ацетил, пропионил, бутаноил или пентаноил.
В другой следующей форме осуществления изобретение также относится к производным полимиксина формулы (III):
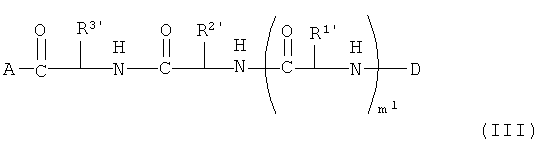
где
A представляет собой кольцевую группировку полимиксина В или полимиксина Е;
D представляет собой R12-C(=O), R12-C(=S) или R12';
m1 равно 0 или 1;
R1', R2' и R3' каждый независимо представляет собой боковые цепи природных или неприродных аминокислот, алкил, алкенил, арилалкил, арил, алкокси, алкоксикарбонил, арилоксикарбонил, алкиламино или алкинил, где по меньшей мере один из R2' и R3' содержит карбамильную, гидроксильную или карбоксилатную группу; и
R12 представляет собой C1-C4 алкил,
R12' представляет собой C1-C5 алкил,
и к их фармацевтически приемлемым пролекарствам и солям, при условии, что, когда D представляет собой ацетил, бутаноил или пентаноил, тогда R3' представляет собой не боковую цепь Dab.
Предпочтительно соединения по изобретению имеют три положительных заряда при физиологическом pH, m1 равно 0, R2' и R3' оба представляют собой замещенный алкил, и/или D представляет собой ацетил, пропионил, бутаноил или пентаноил.
Еще в другой форме осуществления изобретения также характеризуется производными полимиксина формулы (IV):
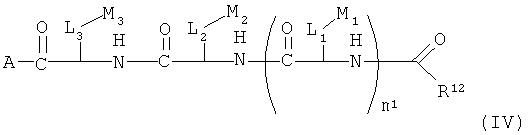
где
A представляет собой кольцевую группировку полимиксина В или полимиксина Е;
m1 равно 0 или 1;
L1, L2 и L3 каждый независимо представляет собой C1-C3 алкил или ковалентную связь;
M1, M2 и M3 каждый независимо представляет собой H, C(=O)NH2, C(=O)OH или -OH;
R12 представляет собой C1-C4 алкил,
и их фармацевтически приемлемыми пролекарствами и солями, при условии, что, когда R12 представляет собой метил, пропил или бутил, тогда L3-M3 представляет собой не боковую цепь Dab.
Предпочтительно m1 равно 0. Примеры L2 включают разветвленный алкил (например, -CH(CH3)-). Примеры M2 включают OH. Другие примеры L2 включают -CH2-, и другие примеры M2 включают OH и H. В другой форме осуществления, L3 представляет собой -CH2-, и M3 представляет собой OH. Еще в одной другой форме осуществления L3 представляет собой -CH2-CH2- и M3 представляет собой C(=O)NH2. Предпочтительно соединения формулы (IV) имеют три положительных заряда при физиологическом pH.
Настоящее изобретение, таким образом, относится к производному полимиксина, которое может быть представлено общей формулой (V):
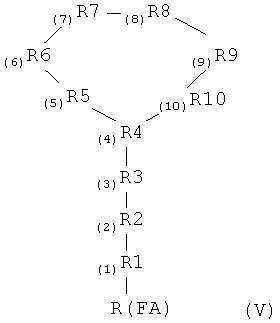
где
R4 представляет собой аминокислотный остаток, содержащий функциональную боковую цепь, способную к циклизации молекулы;
R6 и R7 представляют собой возможно, но не обязательно замещенные гидрофобные аминокислотные остатки;
R10 представляет собой Leu или любой не гидрофобный аминокислотный остаток; и
где R1 может отсутствовать; и
где R1, R2, R3, R5, R8 и R9 каждый представляет собой независимо выбранные аминокислоты; и
где R(FA) представляет собой возможно, но не обязательно замещенный алканоильный или алкильный остаток, имеющий суммарно от 1 до 5 атомов углерода;
или к его фармацевтически приемлемому пролекарству или соли, при условии, что (1) когда R1 и R2 отсутствуют, R3, R4. R5, R8 и R9 представляют собой Dab, R6 представляет собой D-Leu, R7 представляет собой L-Leu или L-Phe, и R10 представляет собой Thr, или когда R1 и R2 отсутствуют, R3, R4. R5, R8 и R9 представляют собой Dab, R6 представляет собой D-Phe, R7 представляет собой L-Leu и R10 представляет собой Thr, тогда R(FA) представляет собой не незамещенный алканоильный остаток, и (2) когда R(FA) представляет собой ацетил, бутаноил или пентаноил, тогда R3 представляет собой не Dab.
В производном согласно настоящему изобретению R(FA) может представляет собой любой остаток, который имеет низкую молекулярную массу и от 1 до 5 атомов углерода. Основной ролью короткоцепочечного R(FA) является блокирование свободной N-концевой аминогруппы пептида и, следовательно, элиминация одного положительного заряда пептида.
Предпочтительно соединения формулы (V) могут иметь три положительных заряда при физиологическом pH. Кроме того, R1, R2, R3, R5, R8 и R9 могут быть специально выбраны так, чтобы соединения имели три положительных заряда при физиологическом pH.
R(FA) предпочтительно выбран из группы, состоящей из остатков карбоновых кислот, то есть алканоильных групп, или алкильных групп, имеющих суммарно от 1 до 5 атомов углерода. R(FA) предпочтительно выбран из группы, состоящей из метильных, формильных и ацетильных остатков. Другие полезные остатки могут быть выбраны из пропаноильных, бутаноильных, изобутаноильных, валероильных и изовалероильных остатков. Остатки могут быть разветвленными, прямоцепочечными или циклическими.
R(FA) может также представлять собой ненасыщенный остаток, содержащий одну или более чем одну двойную или тройную связь.
R(FA) может быть замещен заместителями, легко распознаваемыми специалистами в данной области техники, при условии, что R(FA) имеет не более чем от 1 до 5 атомов углерода. Заместители могут включать алкил, гидрокси и алкокси. Алкил предпочтительно представляет собой метил, этил или пропил. Алкокси предпочтительно представляет собой метокси, этокси или пропокси. Специалист в данной области техники может легко распознать эквиваленты этих предпочтительных остатков R(FA) и их заместителей.
В природных полимиксинах и октапептинах R1 представляет собой Dab или отсутствует (то есть заменен ковалентной связью). Примеры известных производных, которые обладают антибактериальной активностью, включают те, где R1 представляет собой Ala или ковалентную связь.
В производном согласно настоящему изобретению R1, если присутствует, может представлять собой любой аминокислотный остаток при условии, что суммарное число положительных зарядов в указанном производном не превышает три, и что суммарное число положительных зарядов в участке боковой цепи не превышает один, и предпочтительно отсутствует.
В природных полимиксинах и октапептинах R2 представляет собой Thr или отсутствует (то есть заменен ковалентной связью). Примеры известных производных, которые обладают антибактериальной активностью, включают те, где R2 представляет собой O-ацетил-Thr, O-пропионил-Thr, O-бутирил-Thr или ковалентную связь.
В производном согласно настоящему изобретению R2 может представлять собой любой аминокислотный остаток, предпочтительно гидрофильный или относительно гидрофильный, при условии, что суммарное число положительных зарядов в указанном производном не превышает три, и что суммарное число положительных зарядов в участке боковой цепи не превышает один. Примеры R2 включают аланин, аминомасляную кислоту, аспарагин, аспарагиновую кислоту, диаминомасляную кислоту, глутаминовую кислоту, глутамин, серии или треонин либо в D-, либо в L-конфигурации, Специалисту в данной области техники также понятно, что эквивалентным остатком Thr является Ser.
В природных полимиксинах и октапептинах R3 представляет собой Dab, DDab или DSer.
В производном согласно настоящему изобретению R3 может представлять собой любой аминокислотный остаток, предпочтительно гидрофильный или относительно гидрофильный, при условии, что суммарное число положительных зарядов в указанном производном не превышает три, и что суммарное число положительных зарядов в участке боковой цепи не превышает один, и предпочтительно выбран из группы, состоящей из аланина, аминомасляной кислоты, аспарагина, аспарагиновой кислоты, диаминомасляной кислоты, глутаминовой кислоты, глутамина, серина или треонина либо в D-, либо в L-конфигурации.
Специалист в данной области техники может легко распознать другие гидрофильные или относительно гидрофильные остатки, чем эти предпочтительные остатки R1, R2 и R3, и может выбрать такие из группы, состоящей, например, из аргинина, N□метиларгинина, α-метиласпартата, цистеина, гистидина, гидроксилизина, лизина, метионина, орнитина, пенициламина, пролина, фосфосерина, фос-фотреонина и тирозина.
Специалист в данной области техники может легко отметить, что один из остатков R1, R2 и R3 может не быть гидрофильным или относительно гидрофильным при условии, что два других остатка являются такими. Соответственно, R1, R2 и R3 могут быть выбраны из группы, состоящей, например, из ковалентной связи, аланина, 2-аминоадипиновой кислоты, α-н-масляной кислоты, N-(4-аминобутил)глицина, α-аминомасляной кислоты, γ-аминомасляной кислоты, γ-аминокапроновой кислоты, аминоциклопропанкарбоксилата, аминоизомасляной кислоты, аминонорборнилкарбоксилата, α-амино-н-валериановой кислоты, аргинина, Nω-метиларгинина, аспарагина, аспарагина, α-метиласпартата, аспарагиновой кислоты, N-бензилглицина, N-(2-карбамилэтил)глицина, N-(карбамилэтил)глицина, 1-карбокси-1(2,2-дифенилэтиламино)циклопропана, цистеина, Nα-метилдиамино-н-масляной кислоты, Nγ-ацетилдиамино-н-масляной кислоты, Nγ-формилдиамино-н-масляной кислоты, Nγ-метилдиамино-н-масляной кислоты, N-(N-2,2-дифенилэтил)карбамилметилглицина, N-(N-3,3-дифенилпропил)карбамилметил(1)глицина, N-(3,3-дифенилпропил)глицина, глутаминовой кислоты, глутамина, глицина, трет-бутилглицина, 2-амино-4-гуанидиномасляной кислоты, N(3-гуанидинопропил)глицина, гистидина, гомофенилаланина, изодесмозина, изолейцина, лейцина, норлейцина, гидроксилизина, Nα-метиллизина, лизина, Nα-метилгидроксилизина, Nα-метиллизина, Nε-ацетилгидроксилизина, Nε-ацетиллизина, Nε-формилгидроксилизина, Nε-формиллизина, Nε-метилгидроксилизина, Nε-метиллизина, метионина, α-метил-γ-аминобутирата, α-метиламиноизобутирата, α-метилциклогексилаланина, α-нафтилаланина, норлейцина, норвалина, α-метилорнитина, Nα-метилорнитина, Nδ-ацетилорнитина, Nδ-формилорнитина, Nδ-метилорнитина, орнитина, пенициламина, фенилаланина, гидроксипролина, пролина, Nα-метилдиамино-н-пропионовой кислоты, Nβ-ацетилдиамино-н-пропионовой кислоты, Nβ-формилдиамино-н-пропионовой кислоты, Nβ-метилдиамино-н-пропионовой кислоты, фосфосерина, серина, фосфотреонина, треонина, триптофана, тирозина, норвалина и валина.
В природных полимиксинах и октапептинах R4 представляет собой Dab. Примеры синтетических производных, которые обладают антибактериальной активностью, включают те, где R4 представляет собой Lys.
В производном согласно настоящему изобретению R4 представляет собой аминокислотный остаток, содержащий функциональную боковую цепь, способную к циклизации молекулы, и может быть выбран из группы эквивалентных остатков, состоящей из Lys, гидроксилизина, орнитина, Glu, Asp, Dab, диаминопропионовой кислоты, Thr, Ser и Cys, предпочтительно Dab.
В природных полимиксинах и октапептинах R5, R8 и R9 представляют собой Dab. Примеры синтетических производных, которые обладают антибактериальной активностью, включают те, где R5, R8 и R9 могут представлять собой Lys или 2-амино-4-гуанидиномасляную кислоту.
В производном согласно настоящему изобретению R5, R8 и R9 могут представлять собой положительно заряженный или нейтральный аминокислотный остаток, предпочтительно Dab или Abu, при условии, что суммарное число положительных зарядов в указанном производном не превышает три.
Специалист в данной области техники может легко распознать эквивалентные остатки этих предпочтительных остатков и может выбрать такие остатки из группы, состоящей, например, из диаминомасляной кислоты, диаминопропионовой кислоты, лизина, гидроксилизина, орнитина, 2-амино-4-гуанидиномасляной кислоты, глицина, аланина, валина, лейцина, изолейцина, фенилаланина, D-фенилаланина, метионина, треонина, серина, α-амино-н-масляной кислоты, α-амино-н-валериановой кислоты, α-аминокапроновой кислоты, Nε-формиллизина, Nε-ацетиллизина, Nε-метиллизина, Nε-формилгидроксилизина, Nε-ацетилгидроксилизина, Nε-метилгидроксилизина, L-Nα-метилгидроксилизина, Nγ-формилдиамино-н-масляной кислоты, Nγ-ацетилдиамино-н-масляной кислоты, Nγ-метилдиамино-н-масляной кислоты, Nβ-формилдиамино-н-пропионовой кислоты, D-Nβ-формилдиамино-н-пропионовой кислоты, Nβ-ацетилдиамино-н-пропионовой кислоты, Nβ-метилдиамино-н-пропионовой кислоты, Nδ-формилорнитина, Nδ-ацетилорнитина и Nδ-метилорнитина.
В природных полимиксинах и октапептинах R6 представляет собой DPhe или DLeu и R7 представляет собой Leu, lle, Phe или Thr. Синтетические производные, которые обладают антибактериальной активностью, включают те, где R6 представляет собой DTrp и где R7 представляет собой Ala.
В производном согласно настоящему изобретению R6 представляет собой возможно замещенный гидрофобный аминокислотный остаток, предпочтительно DPhe или DLeu, и R7 представляет собой возможно замещенный гидрофобный остаток, предпочтительно Leu, Thr или lle.
Специалист в данной области техники может легко распознать эквивалентные остатки этих предпочтительных остатков и может выбрать такие остатки из группы, состоящей, например, из фенилаланина, α-амино-н-масляной кислоты, триптофана, лейцина, метионина, валина, норвалина, норлейцина, изолейцина и тирозина. Специалисту в данной области техники также понятно, что эквивалентным остатком треонина является серии.
В природных полимиксинах и октапептинах R10 представляет собой Thr и Leu. Примеры известных производных, которые обладают антибактериальной активностью, включают те, где R10 представляет собой O-ацетил-Thr, O-пропионил-Thr или O-бутирил-Thr.
В производном согласно настоящему изобретению R10 представляет собой Leu или любой не гидрофобный аминокислотный остаток при условии, что суммарное число положительных зарядов в указанном производном не превышает три. Предпочтительно R10 представляет собой Thr или Leu.
Специалисту в данной области техники также понятно, что эквивалентным остатком треонина является серии.
Три (3) положительных заряда, присутствующих в производном согласно изобретению могут быть локализованы в гептапептидной кольцевой части; либо два (2) положительных заряда могут быть локализованы в гептапептидной кольцевой части, тогда как один оставшийся положительный заряд локализован в боковой цепи.
В одной форме осуществления производные согласно настоящему изобретению могут быть выбраны из группы производных, где R2-R10 выбраны из группы, состоящей из Thr-DSer-cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-], то есть SEQ ID NO: 10; и Thr-DAsn-cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-], то есть SEQ ID NO: 39.
В других формах осуществления производные согласно настоящему изобретению могут быть выбраны из группы, состоящей из: ацетил-Thr-DSer-cyPab-Dab-DPhe-Leu-Dab-Dab-Thr-], то есть Ac-SEQ ID NO: 10; и ацетил-Thr-DAsn-cyfDab-Dab-DPhe-Leu-Dab-Dab-Thr-], то есть Ac-SEQ ID NO: 39.
Как показано в разделе примеров данной заявки, соединения согласно настоящему изобретению, несущие только три (3) положительных заряда и имеющие R(FA), содержащий только от 1 до 5 атомов углерода, могут быть очень эффективными агентами для сенсибилизации грамотрицательных бактерий к антибактериальным агентам.
Для сенсибилизирующей активности по меньшей мере два (2) и более, предпочтительно три (3) положительных заряда локализованы в гептапептидном кольце.
В работах Teuber (1970), Srinivasa and Ramachandran (1980a) и Sakura et al. (2004) раскрыты, среди других производных полимиксина, производные, имеющие только два (2) или три (3) положительных заряда. Однако эти соединения несут более длинную жирнокислотную часть R(FA), чем 5 атомов углерода. С другой стороны, полимиксин В нонапептид и колистин нонапептид, оба известных ранее эффективных агента для сенсибилизации грамотрицательных бактерий к антибиотикам, не имеют полноразмерной части R(FA), но несут пять (5) положительных зарядов.
В некоторых формах осуществления изобретения производные полимиксина формул I-V можно вводить субъекту в форме пролекарства. Это пролекарство может содержать одну или более чем одну группировку, маскирующую заряд, которая маскирует положительные заряды соединения до момента после введения его субъекту.
В настоящем изобретении в одном аспекте предложены новые производные полимиксина, несущие только три (3) положительных заряда, и R(FA), содержащий только от 1 до 5 атомов углерода, и способные сенсибилизировать один или более чем один вид грамотрицательных бактерий к антибиотику или антибактериальному агенту.
Восприимчивость бактерий к антибактериальному агенту можно определить двумя микробиологическими методами. В быстрой, но грубой методике используют имеющиеся в продаже диски фильтровальной бумаги, которые пропитаны определенным количеством антибактериального агента. Эти диски помещают на поверхность чашек с агаром, которые инокулированы суспензией тестируемого организма, и на чашках наблюдают зоны ингибирования роста. Более точная методика, тест на восприимчивость в разведении бульона, включает подготовку пробирок, содержащий серийные разведения лекарства в жидкой культуральной среде, затем инокуляции тестируемого организма в эти пробирки. Самую низкую концентрацию лекарства, которая ингибирует рост бактерий после пригодного периода инкубации, указывают как минимальную ингибиторную концентрацию (MIC).
Производные согласно настоящему изобретению могут сенсибилизировать клинически значимые грамотрицательные бактерии к антибактериальным агентам, где указанные грамотрицательные бактерии могут представлять собой бактерии, принадлежащие к видам рода Acinetobacter, Aeromonas, Alcaligenes, Bordetella, Branhamella, Campylobacter, Citrobacter, Enterobacter, Escherichia, Francisella, Fusobacterium, Haemophilus, Helicobacter, Klebsiella, Legionella, Moraxella, Pasteurella, Plesiomonas, Pseudomonas, Salmonella, Serratia, Shigella и Yersinia. Эти бактерии могут представлять собой, например, Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter cloacae, Enterobacter aerogenes, другие виды Enterobacter, Citrobacter freundii, Pseudomonas aeruginosa, другие виды Pseudomonas, Acinetobacter baumannii, а также многие другие виды неферментативных грамотрицательных бактерий. Эти бактерии также включают Helicobacter pylori, а также другие клинически значимые грамотрицательные бактерии.
Бактериальные инфекции, подлежащие лечению, включают, например, бактериемию, септицемию, инфекцию кожи и мягких тканей, пневмонию, менингит, инфекции в пельвиоперитонеальной области, инфекцию инородного тела, лихорадку у гематологического пациента, инфекцию, связанную с капельницей или другим катетером, канюлей и/или устройством, инфекцию в желудочно-кишечном тракте, в глазу или в ухе, поверхностную кожную инфекцию и колонизацию желудочно-кишечного тракта, слизистых оболочек и/или кожи потенциально токсичными бактериями.
Бактериальные инфекционные заболевания включают (но не ограничены ими) тяжелые внутрибольничные инфекции, инфекции пациентов с иммунной недостаточностью, инфекции пациентов после трансплантации органов, инфекции в отделениях интенсивной терапии (ОИТ), тяжелые инфекции ожоговых ран, тяжелые бытовые инфекции, инфекции пациентов с муковисцидозом, а также инфекции, вызванные грамотрицательными бактериями с множественной устойчивостью.
Настоящее изобретение также направлено на комбинации двух или более чем двух производных согласно настоящему изобретению для комбинированного лечения. Эти комбинации могут включать производные, обладающие способностью к сенсибилизации различных видов или штаммов грамотрицательных бактерий к антибактериальным агентам.
Другой аспект настоящего изобретения направлен на фармацевтические композиции, содержащие производные полимиксина согласно настоящему изобретению, их пролекарственные и солевые формы, их избранные комбинации и возможно антибактериальный агент, включенный в препарат вместе с одним или более чем одним фармацевтически приемлемым носителем и эксципиентом. Они способствуют обработке активных соединений с получением препаратов, которые можно применять фармацевтически, и включают, например, разбавители, наполнители, буферные агенты, загустители, смачивающие агенты, диспергирующие агенты, солюбилизаторы, суспендирующие агенты, эмульгаторы, связующие агенты, стабилизаторы, разрыхлители, инкапсулирующие агенты, покрытия, агенты для включения, смазывающие агенты, красители и корригенты, а также абсорбенты, усилители всасывания, увлажнители, консерванты и тому подобное, хорошо известные специалистам в данной области техники.
Фармацевтические композиции включают композиции, где активные ингредиенты содержатся в количестве, эффективном для достижения предназначенной цели. Более конкретно терапевтически эффективное количество в связи с настоящим изобретением означает количество соединения, эффективное для сенсибилизации грамотрицательных бактерий к антибактериальным агентам. Определение терапевтически эффективного количества находится в пределах компетенции специалиста в области медицины.
Композиции можно готовить способами, хорошо известными в данной области техники, например, путем общепринятого смешивания, растворения, инкапсуляции, включения, лиофилизации, эмульгирования и грануляции. Соответствующий препарат зависит от выбранного пути введения, и препарат фармацевтической композиции можно готовить для немедленного высвобождения или медленного высвобождения (например, с целью продления терапевтического эффекта и/или улучшения переносимости). Кроме того, препараты могут быть общепринято представлены в стандартной лекарственной форме способами, известными в области фармацевтики.
Фармацевтические композиции согласно настоящему изобретению включают (но не ограничены ими) композиции, предназначенные для внутривенного, внутримышечного, перорального или местного введения, а также вводимые в виде суппозитория или ингаляционного аэрозоля. Композиции включают внутривенные, внутримышечные, внутрибрюшинные, подкожные, костномозговые, подоболочечные, внутрижелудочковые, интраназальные или внутриглазные инъекции, ингаляционные аэрозоли, а также композиции, предназначенные для ректальной, пероральной, интравагинальной, чресслизистой или чрескожной доставки.
Для парентерального введения (например, путем болюсной инъекции, быстрых инфузий или медленных инфузий) препараты соединений согласно данному изобретению, а также вышеописанных комбинаций можно готовить в виде их подходящих солевых или эфирных форм в стерильных водных растворах, предпочтительно в физиологически совместимых жидкостях, таких как физиологически раствор, 5% декстроза, раствор Рингера и раствор Хэнкса. Препарат может также включать органические растворители, такие как пропиленгликоль, полиэтиленгликоль или родственные соединения, а также консерванты и сурфактанты.
Фармацевтически приемлемые соли присоединения кислоты могут быть получены из неорганических и органических кислот. Соли, образованные из неорганических кислот, включают соли соляной кислоты, бромисто-водородной кислоты, серной кислоты, азотной кислоты, фосфорной кислоты и тому подобные. Соли, образованные из органических кислот, включают соли уксусной кислоты, пропионовой кислоты, гликолевой кислоты, пировиноградной кислоты, щавелевой кислоты, яблочной кислоты, малоновой кислоты, янтарной кислоты, малеиновой кислоты, фумаровой кислоты, винной кислоты, лимонной кислоты, бензойной кислоты, коричной кислоты, миндальной кислоты, метансульфоновой кислоты, этансульфоновой кислоты, пара-толуолсульфоновой кислоты, салициловой кислоты и тому подобные.
Кроме того, фармацевтические композиции для парентерального введения могут представлять собой суспензии или эмульсии в масляных или водных носителей и могут содержать агенты для препаратов, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Подходящие липофильные носители и растворители включают жирные масла, такие как натуральные и/или синтетические эфиры жирных кислот, такие как этилолеат и триглицериды, или липосомы. суспензии могут содержать вещества, которые повышают вязкость суспензии, такие как натрийкарбоксиметилцеллюлоза, сорбит или декстран.
Парентеральные композиции могут быть представлены в герметичных контейнерах, содержащих однократную дозу или многократные дозы, таких как ампулы и флаконы, и их можно хранить в высушенном вымораживанием (лиофилизированном) состоянии, требующем только добавления стерильного жидкого эксципиента, например, воды для инъекций, непосредственно перед применением.
Для перорального введения препараты твердых форм включают, например, препараты в виде порошков, таблеток, пилюль, драже, пастилок, капсул, крахмальных капсул и микрогранул. Фармацевтические препараты можно готовить, используя твердый эксципиент, возможное измельчение полученной в результате смеси и обработку смеси гранул после добавления подходящих вспомогательных веществ, если желательно, с получением таблеток или сердцевин драже. Твердый носитель/эксципиент может представлять собой одно или более чем одно вещество, которое может также действовать в качестве разбавителя, солюбилизатора, смазывающего агента, суспендирующего агента, связующего агента, консерванта, корригента, увлажняющего агента, разрыхлителя для таблеток или материала для инкапсуляции. Подходящие носители включают, но не ограничены ими, карбонат магния, стеарат магния, тальк, декстрозу, лактозу, пектин, крахмал, желатин, трагакант, метилцеллюлозу, натрийкарбоксиметилцеллюлозу, легкоплавкий воск, масло какао и тому подобное.
Жидкие препараты, пригодные для перорального введения, включают, например, водные растворы, сиропы, эликсиры, водные суспензии, эмульсии и гели. Водные растворы можно готовить путем растворения активного компонента в воде и добавления подходящих стабилизирующих агентов и загустителей, а также красителей и корригентов. Водные суспензии можно готовить путем диспергирования тонкоизмельченного активного компонента в воде с вязким веществом, таким как натуральные или синтетические камеди, смолы, метилцеллюлоза, натрийкарбоксиметилцеллюлоза и другие хорошо известные суспендирующие агенты. Эмульсии можно готовить в растворах в водном пропиленгликоле, либо они могут содержать эмульгирующие агенты, такие как лецитин, сорбитана моноолеат или аравийскую камедь.
Препараты соединений согласно изобретению или вышеописанных комбинаций можно также готовить для местного введения. Активные соединения смешивают в стерильных условиях с фармацевтически приемлемыми носителями/эксципиентами, включающими любые необходимые буферные агенты и консерванты. Препараты в виде мазей, кремов и лосьонов можно, например, готовить с водной или масляной основой с добавлением подходящих эмульгирующих, диспергирующих, суспендирующих, загущающих, стабилизирующих агентов или красителей. Общепринято используемые эксципиенты включают животные и растительные жиры и масла, воски, парафины, крахмал, производные целлюлозы, трагакант и полиэтиленгликоль.
Другие местные препараты включают, но не ограничены ими, глазные капли и чрескожные пластыри.
Для чрескожного, а также чресслизистого введения в препарате можно использовать усилители проницаемости, известные в данной области техники.
Для введения путем ингаляции соединения согласно данному изобретению и вышеописанные комбинации доставляют в форме, представленной в виде аэрозольного спрея, из респиратора, корпуса под давлением или небулайзера с использованием подходящего пропеллента, например, дихлордифторметана, трихлорфторметана, дихлортетрафторэтана или диоксида углерода. В случае аэрозоля под давлением стандартную дозу можно определить путем обеспечения клапана для доставки отмеренного количества. Препараты в виде капсул и картриджей, например, из желатина для применения в ингаляторе или инсуффляторе можно готовить с содержанием порошкообразной смеси соединения и подходящей порошковой основы, такой как лактоза или крахмал.
Препараты соединений согласно данному изобретению и вышеописанных комбинаций можно также готовить в виде ректальных композиций, таких как удерживающие клизмы или суппозитории, используя общепринятые основы суппозиториев, такие как масло какао, другие глицериды, полиэтиленгликоль или воск для суппозиториев.
Настоящее изобретение также относится к способу применения настоящих производных полимиксина или комбинации таких производных в виде части клинической терапии (или превентивного профилактического режима) субъектов людей или животных, страдающих инфекционным заболеванием (то есть грамотрицательной бактериальной инфекцией), и включает введение указанному субъекту терапевтически эффективной дозы по меньшей мере одного производного согласно настоящему изобретению в комбинации с антибактериальным агентом.
Настоящее изобретение также относится к способу сенсибилизации грамотрицательных бактерий к антибактериальному агенту, где производное согласно настоящему изобретению вводят одновременно или последовательно в любом порядке с терапевтически эффективным количеством указанного антибактериального агента.
Производное по настоящему изобретению и антибактериальный агент можно вводить вместе в виде одного препарата или различными путями. Например, производное полимиксина можно вводить внутривенно, тогда как антибактериальный агент вводят внутримышечно, внутривенно, подкожно, перорально или внутрибрюшинно. Альтернативно производное можно вводить внутримышечно или внутрибрюшинно, тогда как антибактериальный агент вводят внутривенно, внутримышечно или внутрибрюшинно, либо производное можно вводить в аэрозольной или распыляемой форме, тогда как антибактериальный агент вводят, например, внутривенно. Производное и антибактериальные агенты можно вводить одновременно или последовательно, насколько их дают способом, который дает достаточную возможность достижения обоими активных концентраций в области инфекции.
"Терапевтическая эффективность" основана на успешном исходе заболевания и не требует того, чтобы производное согласно настоящему изобретению в комбинации с антибактериальным агентом, уничтожало 100% бактерий, вовлеченных в инфекцию. Успешное лечение зависит от достижения уровня антибактериальной активности в области инфекции, достаточного для ингибирования бактерий таким образом, чтобы баланс перевешивал в пользу хозяина. Когда защитные механизмы хозяина максимально эффективны, необходимый антибактериальный эффект может быть умеренным. Уменьшение нагрузки организма даже на один логарифм (основание 10) может дать возможность собственным защитным механизмам хозяина контролировать инфекцию. Кроме того, повышение раннего бактерицидного/бактериостатического эффекта может быть важнее, чем долговременный бактерицидный/бактериостатический эффект. Эти ранние события составляют значимую и принципиальную часть терапевтического успеха, поскольку они дают время для активации защитных механизмов хозяина. Повышение скорости бактерицидного действия может быть особенно важно для инфекций, таких как менингит, инфекции костей или суставов.
Терапевтическая эффективность антибактериального агента зависит от чувствительности вида бактерий к указанному антибактериальному агенту при клинически релевантной концентрации производного согласно данному изобретению. Эффект соединений согласно настоящему изобретению по улучшению терапевтической эффективности антибактериальных агентов in vivo можно продемонстрировать в животных моделях in vivo, таких как анализы перитонита мышей или бактериемии кроликов, и ее можно предсказать на основании ряда тестов in vitro, включая (1) определения минимальной ингибиторной концентрации (MIC) антибактериального агента, необходимой для ингибирования роста грамотрицательной бактерии в течение 24 часов, (2) определения эффекта антибактериального агента на кинетическую кривую роста грамотрицательной бактерии и (3) титрования MIC в двух направлениях серийных разведений антибактериального агента, одного или в комбинации с серийными разведениями соединения(й). Примерные модели или тесты хорошо известны в данной области техники.
Используя in vitro определения MIC через 24 часа, можно показать, что производное согласно настоящему изобретению снижает MIC антибактериального агента. При этом результате ожидают, что одновременное введение соединения in vivo должно повышать чувствительность грамотрицательной бактерии к антибактериальному агенту. Можно также показать, что соединение согласно настоящему изобретению снижает MIC антибактериального агента от интервала, в котором организм считают клинически устойчивым, до интервала, в котором организм считают клинически чувствительным. При этом результате ожидают, что одновременное введение in vivo одного или более чем одного соединения согласно настоящему изобретению с антибактериальным агентом должно привести к обратному развитию устойчивости и эффективно преобразовать организм, устойчивый к антибиотику, в организм, чувствительный к антибиотику.
Путем измерения эффекта антибактериальных агентов на кривые роста in vitro грамотрицательных бактерий в присутствии или в отсутствие соединения согласно настоящему изобретению можно показать, что соединение усиливает ранний антибактериальный эффект антибактериальных агентов в пределах периода, предпочтительно меньшего, чем 24 часа. Усиление ранних бактерицидных эффектов/эффектов ингибирования роста важно при определении исхода лечения.
При титровании в двух направлениях комбинирование соединения согласно настоящему изобретению с антибактериальными агентами может привести в результате к "синергическому" дробному индексу ингибиторной концентрации (FICI). Способ титрования в двух направлениях основан на аддитивности, которая предполагает, что результат, наблюдаемый при множественных лекарствах, представляет собой сумму отдельных эффектов тестируемых лекарств; согласно этой системе FICI менее чем 0,5 оценивают как синергизм, 1 оценивают как аддитивность, и более чем 1, но менее чем 2 оценивают как инертность.
Антибактериальные агенты, пригодные для применения в комбинации с производными согласно настоящему изобретению, включают, например, макролиды, такие как кларитромицин, азитромицин и эритромицин, кетолиды, линкозамины, такие как клиндамицин, стрептограмины, рифамицины, такие как рифампин, рифабутин и рифалазил, фузидовую кислоту, мупироцин, оксазолидиноны, гликопептидные антибиотики, такие как ванкомицин, далбаванцин, телаванцин и оритаванцин, фторхинолоны, производные тетрациклина, гидрофобные производные пенициллинов, цефалоспорины, монобактамы, карбапенемы, пенемы и другие бета-лактамовые антибиотики, новобиоцин, плевромутилины, ингибиторы синтеза фолатов, ингибиторы деформилазы и ингибиторы бактериального выкачивающего насоса. Специалист в области лечения грамотрицательных инфекций может легко распознать дополнительные клинически релевантные антибактериальные агенты, которые могут быть полезны. Предпочтительно указанные антибактериальные агенты выбраны из группы гидрофобных или умеренно гидрофобных антибактериальных агентов, против которых наружная мембрана грамотрицательных бактерий действует как эффективный барьер проницаемости.
Изобретение также включает применение настоящих соединений или их комбинаций для сенсибилизации клинически значимых бактерий, перечисленных здесь, к защитному механизму комплемента хозяина (присутствующему в свежей сыворотке человека и животного) путем действия на указанные бактерии таких соединений во время манифестной (клинической) инфекции или подозреваемой инфекции. Защита хозяина может осуществляться, например, путем комбинированного действия комплемента и полиморфоядерных лейкоцитов.
Специалист в области медицины может легко оптимизировать эффективные дозировки и режимы введения для соединений согласно настоящему изобретению, а также для антибиотиков при одновременном введении, учитывая факторы, хорошо известные в данной области техники, включая тип субъекта, получающего дозировку, возраст, массу, пол и медицинское показание субъекта, путь введения, функцию почек и печени субъекта, желаемый эффект, конкретное применяемое соединение согласно настоящему изобретению и переносимость его субъектом. Дозировки всех противомикробных агентов следует регулировать у пациентов с нарушением функции почек или печеночной недостаточностью вследствие сниженного метаболизма и/или выделения лекарств у пациентов с этими состояниями. Дозировки у детей следует также снижать, как правило, в соответствии с массой тела.
Суммарная суточная доза производного согласно настоящему изобретению, вводимая человеку или животному, может варьировать, например, в количествах от 0,1 до 100 мг на кг массы тела, предпочтительно от 0,25 до 25 мг на кг массы тела.
Специалисту в данной области техники также должно быть понятно, что оптимальный курс лечения, то есть число доз, даваемых в сутки, в течение определенного числа суток следует определять в соответствии с природой и степенью состояния, подлежащего лечению, формой, путем и местом введения, а также с конкретным пациентом, подлежащим лечению, и что такие оптимумы могут быть определены с помощью общепринятых методик.
Также предложен способ анализа соединения согласно настоящему изобретению, где указанное соединение представляет собой производное природного полимиксина или октапептина, где указанное производное имеет только 3 положительных заряда и концевую группировку (D), содержащую от 1 до 5 атомов углерода в противоположность встречающемуся в природе соединению, от которого оно образовано, на способность сенсибилизировать опасную грамотрицательную бактерию к антибактериальным агентам и/или комплементу, присутствующему в сыворотке, где указанный способ включает стадию приведения бактерии в контакт с указанным производным природного полимиксина или октапептина и идентификации производных, обладающих сенсибилизирующей активностью в отношении указанной бактерии.
В следующем аспекте предложен способ разработки новых антибиотиков, включающий стадии
(а) получения соединения природного полимиксина или октапептина или его производного, несущего суммарно от 4 до 6 положительных зарядов и концевую группировку (D), содержащую от 1 до 5 атомов углерода,
(б) замены от 1 до 3 остатков, несущих один или более чем один положительный заряд, остатком, не имеющим положительного заряда, или ковалентной связью, образуя таким путем производное полимиксина, несущее 3 положительных заряда и концевую группировку (D), содержащую от 1 до 5 атомов углерода,
(в) анализа указанного производного полимиксина на способность сенсибилизировать грамотрицательные бактерии к антибактериальному агенту; и
(г) отбора соединений, обладающих способностью сенсибилизировать грамотрицательные бактерии к антибактериальному агенту.
В одной форме осуществления способа по изобретению концевая группировка (D) представляет собой R12-C(=O), R12-(C=S) или R12', где R12 и R12' являются такими, как определено выше. В другой форме осуществления изобретения, концевая группировка (D) представляет собой R(FA), который возможно, но не обязательно замещен алканоильным или алкильным остатком, имеющим суммарно от 1 до 5 атомов углерода.
В следующем аспекте изобретения предложен способ разработки новых антибиотиков, включающий стадии
(а) получения соединения природного полимиксина или октапептина или его производного, несущего суммарно 4 или 5 положительных зарядов или суммарно 6 положительных зарядов, как в деацилполимиксинах, и концевую группировку (D), содержащую более 5 атомов углерода,
(б) замены от 1 до 3 остатков, несущих один или более чем один положи- тельный заряд, остатком, не имеющим положительного заряда, или ковалентной связью, образуя таким путем соединение производного полимиксина, имеющее 3 положительных заряда,
(в) замены концевой группировки (D), содержащей более 5 атомов углерода, концевой группировкой (D), содержащей от 1 до 5 атомов углерода, образуя таким путем соединение производного полимиксина, имеющее 3 положительных заряда и концевую группировку (D), содержащую от 1 до 5 атомов углерода,
(г) анализа указанного производного полимиксина на способность сенсибилизировать грамотрицательные бактерии к антибактериальному агенту; и
(д) отбора соединений, обладающих способностью сенсибилизировать грамотрицательные бактерии к антибактериальному агенту.
В одной форме осуществления способа по изобретению концевая группировка (D) представляет собой R12-C(=O), R12-(C=S) или R12', где R12 и R12' являются такими, как определено выше. В другой форме осуществления изобретения, концевая группировка (D) представляет собой R(FA), который возможно, но не обязательно замещен алканоильным или алкильным остатком, имеющим суммарно от 1 до 5 атомов углерода.
Еще в одном следующем аспекте настоящего изобретения предложен способ разработки новых антибиотиков, включающий стадии
а) получение соединения полимиксина или октапептина или его производного, имеющего суммарно от 4 до 6 положительных зарядов и не имеющего концевой группировки (D),
б) замены от 1 до 3 остатков, несущих один или более чем один положи- тельный заряд, остатком, не имеющим положительного заряда, или ковалентной связью, образуя таким путем производное полимиксина, имеющее 3 положительных заряда;
в) введения концевой группировки (D), содержащей от 1 до 5 атомов углерода, образуя таким путем соединение полимиксина, имеющее 3 положительных заряда и концевую группировку (D), содержащую от 1 до 5 атомов углерода;
г) анализа указанного производного полимиксина на способность сенсибилизировать грамотрицательные бактерии к антибактериальному агенту; и
д) отбора соединений, обладающих способностью сенсибилизировать грамотрицательные бактерии к антибактериальному агенту.
В одной форме осуществления способа по изобретению концевая группировка (D) представляет собой R12-C(=O), R12-(C=S) или R12', где R12 и R12' являются такими, как определено выше. В другой форме осуществления изобретения, концевая группировка (D) представляет собой R(FA), который возможно, но не обязательно замещен алканоильным или алкильным остатком, имеющим суммарно от 1 до 5 атомов углерода.
В соответствии с настоящим изобретением также предложено полусинтетическое производное полимиксина, которое может быть получено путем химической или ферментативной обработки встречающихся в природе полимиксинов или октапептинов, соответственно, или тех их вариантов, которые производятся генетически модифицированными организмами. Химические обработки включают, но не ограничены ими, обработки ацетангидридом, муравьиной кислотой, гидразином и щавелевой кислотой. Ферментативные обработки включают, но не ограничены ими, обработки ферментами, такими как деацилаза полимиксинов, фицин, папаин, бромелаин, субтилопептидазы, субтилизин, гидролаза колистинов и Нагарсе.
Предпочтительные соединения согласно одному воплощению являются в меньшей степени катионными, чем природные полимиксины или октапептины, имеют только три (3) положительных заряда и R(FA), имеющий от 1 до 5 атомов углерода, и:
(а) способны сенсибилизировать грамотрицательные бактерии, такие как Escherichia coli, Klebsiella pneumoniae, Klebsiella oxytoca, Enterobacter cloacae, Citrobacter freundii и Acinetobacter baumannii, к антибиотикам и/или
(б) менее токсичны, чем клинически применяемые полимиксины, по данным на животной модели in vivo, и/или
(в) обладают меньшей нефротоксичностью, чем клинически применяемые полимиксины, по данным на животной модели и/или в тесте in vitro, в котором измеряют сродство этих соединений к почечным структурам, и/или
(г) способны вызывать меньшее высвобождение гистамина из тканей, чем клинически применяемые полимиксины, при введении местным путем или при ингаляции в виде аэрозоля, и/или
(д) обладают более благоприятной фармакокинетикой, так как обладают более длительным временем полужизни в сыворотке, повышенным почечным клиренсом, повышенным выделением с мочой и/или, поскольку в меньшей степени инактивируются полианионными компонентами тканей и гноя, чем клинически при- меняемые полимиксины.
В следующей форме осуществления соединения по изобретению обладают одним или более чем одним более благоприятным фармакокинетическим свойством по сравнению с нативными полимиксинами или октапептинами (например, полимиксином А, полимиксином В, ИЛ-полимиксин-B1, полимиксином D, полимиксином Е, полимиксином F, полимиксином М, полимиксином S, полимиксином Т, циркулином А, октапептином А, октапептином В, октапептином С или октапептином D). Примеры таких благоприятных фармакокинетических свойств включают более длительное время полужизни в сыворотке, повышенный почечный клиренс или повышенное выделение с мочой по сравнению с нативными полимиксинами или октапептинами (такими как полимиксин Е).
В следующей форме осуществления соединения по изобретению могут иметь более высокий процент выделения с мочой введенной дозы за 24 часа, чем полимиксин Е (колистин). В другой следующей форме осуществления выделение с мочой на основе экспериментов с крысами составляет примерно 1% или выше, примерно 5% или выше, примерно 10% или выше, примерно 15% или выше, примерно 20% или выше, примерно 25% или выше, примерно 30% или выше, примерно 35% или выше, примерно 40% или выше, примерно 45% или выше или примерно 50% или выше. Напротив, выделение с мочой полимиксина Е (колистина) было определено как примерно 0,18±0,14% дозы за 24 часа (Li et al., 2003) с использованием такой же дозы и методики.
В другой следующей форме осуществления соединения по изобретению могут обладать более высоким почечным клиренсом, чем полимиксин Е (колистин), при введении одного и того же пути и дозировки. В следующей форме осуществления соединения по изобретению обладают почечным клиренсом на основе экспериментов с крысами выше, чем примерно 0,1 мл/мин/кг, выше, чем примерно 0,5 мл/мин/кг, выше, чем примерно 1,0 мл/мин/кг, выше, чем примерно 2,0 мл/мин/кг, выше, чем примерно 2,5 мл/мин/кг, выше, чем примерно 3,0 мл/мин/кг или выше, чем примерно 3,5 мл/мин/кг. В другой следующей форме осуществления почечный клиренс соединений по изобретению может быть по меньшей мере в 10 раз, по меньшей мере в 50 раз, по меньшей мере в 100 раз, по меньшей мере в 150 раз, по меньшей мере в 200 раз, по меньшей мере в 250 раз или по меньшей мере в 300 раз выше, чем полимиксина Е, при введении такой же дозы и пути введения.
В другой следующей форме осуществления соединения по изобретению могут также обладать одним или более чем одним благоприятным фармакокинетическим свойством по сравнению с подобными соединениями с более длинными жирнокислотными хвостами (то есть концевой группировкой или R(FA), имеющей более пяти атомов углерода). Как показано в Примере 8, NAB741 обладает повышенным почечным клиренсом и повышенным выделением с мочой по сравнению с NAB739. Эти соединения химически идентичны за исключением того, что NAB741 имеет ацетильную концевую группировку, a NAB739 имеет октаноильную концевую группировку.
Способы синтеза соединений согласно настоящему изобретению включают, но не ограничены ими, описанные здесь ниже. Для конкретного соединения, которое нужно синтезировать, специалист в данной области техники способен выбрать подходящий способ.
1. Полусинтетические производные полимиксинов и октапептинов, которые несут неизмененный гептапептидный участок и модифицированную ацилом-аминоацилом боковую цепь, могут быть получены с помощью методик, описанных ниже:
Защита свободных аминогрупп в исходном веществе (полимиксине или октапептине, либо их модификациях) способами, известными специалистам в данной области техники. Эта защита может быть достигнута путем использования остатков, таких как трет-бутоксикарбонил (tBoc), флуоренилметоксикарбонил (Fmoc), бензилоксикарбонил (CBZ, Z), аллилоксикарбонил (ALOC), 3-пиридил-N-оксид-метоксикарбонил (как описано в публикации патента GB 1323962), путем использования шиффовых оснований, таких как бензальдегид, способом, описанным в публикации японского патента 7115630/1971, или тому подобных, которые могут быть удалены с помощью общепринятых условий, совместимых с природой продукта.
В условиях, где слабая растворимость в воде иногда создает проблему при последующих стадиях, защита может быть получена путем использования отрицательно заряженных блокирующих групп, таких как сульфокислотное производное Fmoc или карбоново-кислотное производное Fmoc, где этот способ описан в публикации патента США 2006004185. Растворимость в воде можно также усилить путем присоединения подходящей удаляемой, отрицательно заряженной, очень гидрофобной блокирующей группы к OH-группе треонина.
Затем соединение подвергают ферментативной обработке ферментами, такими как деацилаза полимиксинов, гидролаза полимиксинов, папаин, фицин, бромелаин, субтилопептидаза, Нагарсе или другие ферменты, которые удаляют концевой участок боковой цепи или даже всю боковую цепь соединений полимиксина или октапептина. Эту обработку, возможно, можно осуществлять с помощью методики расщепления по Эдману. В полученном в результате соединении отсутствует вся боковая цепь, и оно состоит только из циклического гептапептидного участка, но имеет свободную N-концевую альфа-аминогруппу.
Альтернативно полимиксины и октапептины, которые имеют аминогруппы, защищенные кислотоустойчивыми группами, такими как бензилоксикарбонил, можно обработать щавелевой кислотой или муравьиной кислотой с получением защищенных деацилпроизводных способом, описанным Kurihara et al. (1974). Эту методику осуществляют путем дополнительной ферментативной обработки, как описано выше, и/или путем расщепления по Эдману с получением гептапептида.
Затем подходящий остаток присоединяют к свободному альфа-амино положению гептапептидного кольцевого участка. Этот остаток может содержать ацил или родственный остаток (R(FA), имеющий суммарно от 1 до 5 атомов углерода), такой как метильный, ацетильный, пропионильный, бутаноильный, изобутаноильный, валероильный или изовалероильный остаток, а также аминокислотные остатки, предпочтительно вплоть до трех и предпочтительно два остатка. Например, одно полусинтетическое соединение с ацильной группой и двумя аминокислотными остатками может быть получено путем присоединения к вышеописанному гептапептиду синтетического остатка (ацил)-треонил-D-треонила. Это может быть достигнуто с помощью общепринятых общих методик, известных специалистам в области органической химии, где эти методики включают использование остатков, сшитых с N-гидроксисукцинимидом, как описано в US 2006004185. При данном конкретном синтезе методика может включать использование N-ацетилтреонил-D-серинил-N-гидроксисукцинимида.
2. Ацилированные полимиксины нонапептиды, несущие три (3) свободных аминогруппы. Полимиксин D имеет только четыре (4) положительных заряда и имеет DSer в положении R3. Свободные аминогруппы полимиксина D могут быть защищены вышеописанными способами. Это осуществляют путем ферментативной обработки и возможной стадии расщепления по Эдману с получением нонапептида, который можно затем ацилировать ацилизотиоцианатом (способом, хорошо известным специалистам в данной области техники и описанным в US 2006004185), хлорангидридом (способом, хорошо известным специалистам в данной области техники и описанным в Chihara et al. 1974) или путем использования остатков, сшитых с N-гидроксисукцинимидом (способом, хорошо известным специалистам в данной области техники и описанным в US 2006004185). Наконец, защитные группы удаляют. Ацилированный полимиксин D нонапептид несет только три (3) свободных аминогруппы, все в гептапептидной кольцевой части.
Аналогично может быть получен ацилированный полимиксин S нонапептид. Он несет только три (3) свободных аминогруппы.
3. Полностью синтетические производные полимиксина и октапептина могут быть получены самыми общепринятыми способами, известными специалистам в данной области техники. Такие способы включают методики синтеза в жидкой фазе, а также методики твердофазного синтеза, описанные, например, Sakura et al. (2004), Tsubery et al. (2000a, 2000b, 2002, 2005) и Ofek et al. (2004). Эти способы включают, например, использование защитных агентов, таких как Fmoc, tBoc и CBZ при стратегических положениях, а также стадии циклизации, где используют DPPA (дифенилфосфоразидат) или смесь бензотриазол-1-илокси-трис-пирролидинофосфония гексафторфосфата (РуВор), N-гидроксибензотриазола (HoBt) и N-метилморфолина (NMM). Fmoc-производные многих нетривиальных аминокислот, а также D-аминокислот имеются в продаже. Амино-конец последнего аминокислотного остатка оставляют незащищенным, чтобы обеспечить прямое взаимодействие при методике ацилирования с кислотами, такими как пропионовая кислота, масляная кислота, изомасляная кислота, валериановая кислота и изовалериановая кислота.
4. Ацилирование свободной N-концевой альфа-аминогруппы вышеописанных промежуточных соединений (параграфы 1-3) можно также осуществлять путем использования ангидридов, таких как уксусный ангидрид (см. Пример 1), пропионовый ангидрид, масляный ангидрид и валериановый ангидрид, путем использования условий, хорошо известных специалистам в данной области техники. N-формилирование можно осуществлять путем использования пара-нитрофенилформиата в N-метилпирролидине и условий, хорошо известных специалистам в данной области техники. N-метилирование можно осуществлять путем использования смеси муравьиной кислоты и уксусного ангидрида в диметилформамиде и условий, хорошо известных специалистам в данной области техники.
ЭКВИВАЛЕНТЫ
Специалистам в данной области техники понятны или могут быть установлены с использованием не более чем обычного экспериментирования различные эквиваленты конкретных методик, описанных в данной заявке. Такие эквиваленты считают находящимися в пределах объема настоящего изобретения и охваченными нижеследующей формулой изобретения. Содержания всех ссылок, патентов и заявок на патенты, цитируемых на протяжении всей данной заявки, включены в данную заявку посредством ссылки. Соответствующие компоненты, процессы и способы этих патентов, заявок и других документов могут быть выбраны для настоящего изобретения и его форм осуществления.
ПЕРЕЧЕНЬ ССЫЛОК
Все ссылки, цитируемые в настоящей заявке, включены здесь путем ссылки в полном объеме.
Chihara S, Tobita T, Yahata M, Ito A, Koyama Y. 1973. Enzymatic degradation of colistin. Isolation and identification of α-N-Acyl α,γ-diaminobutyric acid and colistin nonapeptide. Agr Biol Chem 37: 2455-2463.
Chihara S, Ito A, Yahata M, Tobita T, Koyama Y. 1974. Chemical synthesis, isolation and characterization of α-N-fattyacyl colistin nonapeptide with special reference to the correlation between antimicrobial activity and carbon number of fattyacyl moiety. Agric Biol Chem 38: 521-529.
de Visser PC, Kriek NMAJ, van Hooft PAV, Van Schepdael A, Filippov DV, van der Marel GA, Overkleeft HS, van Boom JH, Noort D. 2003. Solid-phase synthesis of polymyxin B1 and analogues via a safety-catch approach. J. Peptide Res. 61: 298-306.
Kimura Y, Matsunaga H, Vaara M. 1992. Polymyxin В octapeptide and polymyxin В heptapeptide are potent outer membrane permeability-increasing agents. J Antibiot 45: 742-749.
Kurihara T, Takeda H, Ito H, Sato H, Shimizu M, Kurosawa A. 1974. Studies on the compounds related to colistin. IX. On the chemical deacylation of colistin and colistin derivatives. Yakugaku Zasshi 94: 1491-1494.
Li J, Milne RW, Nation RL, Turnidge JB, Smeaton TC, and Coulthard K. 2003. Use of high-performance liquid chromatography to study the pharmacokinetics of colistin sulfate in rats following intravenous administration. Antimicrob Agents Chemother 47: 1766-1770.
Li J, Milne RW, Nation RL, Turnidge JB, Smeaton TC, and Coulthard K. 2004. Pharmacokinetics of colistin methanesulphonate and colistin in rats following an intravenous dose of colistin methanesulphonate. J Antimicrob Chemother 53: 837-840.
Nagai J, Saito M, Adachi Y, Yumoto R, Takano M. 2006. Inhibition of gentamicin binding to rat renal brush-border membrane by megalin ligands and basic peptides. J Control Release 112: 43-50.
Nikaido H. 2003. Molecular basis of bacterial outer membrane per-meability revisited. Microbiol Molec Biol Rev 67: 593-656.
Nikaido H, Vaara M. 1985. Molecular basis of bacterial outer mem-brane permeability. Microbiol Rev 49: 1-32.
Okimura K, Ohki K, Sato Y, Ohnishi K, Uchida Y, Sakura N. 2007. Chemical conversion of natural polymyxin В and colistin to their N-terminal derivatives. Bull. Chem. Soc. Jpn. 80 (No. 3): 543-552.
Rose F, Heuer KU, Sibelius U, Hombach-Klonisch S, Ladislau K, Seeger W, Grimminger F. 1999. Targeting lipopolysaccharides by the non-toxic polymyxin В nonapeptide sensitizes resistant E. coli to the bactericidal effect of human neutrophils. J Infect Dis 182: 191-199.
Sakura N, Itoh T, Uchida Y, Ohki K, Okimura K, Chiba K, Sato Y, Sawanishi H. 2004. The contribution of the N-terminal structure of polymyxin В peptides to antimicrobial and lipopolysaccharide binding activity. Bull Chem Soc Jpn 77: 1915-1924.
Srinivasa BD, Ramachandran LK. 1978. Chemical modification of peptide antibiotics: Part VI - Biological activity of derivatives of polymyxin B. Ind J Biochem Biophys 14: 54-58.
Srinivasa BD, Ramachandran LK. 1979. The polymyxins. J Scient Industr Res 38: 695-709.
Srinivasa BD, Ramachandran LK. 1980. Essential amino groups of polymyxin B. Ind J Biochem Biophys 17: 112-118.
Storm DR, Rosenthal KS, Swanson PE. 1977. Polymyxin and related peptide antibiotics. Annu Rev Biochem 46: 723-63.
Teuber M. 1970. Preparation of biologically active mono-N-acetyl(14C)-derivatives of the membrane-specific polypeptide antibiotic po-lymyxin B. Z Naturforsch 25b: 117.
Tsubery H, Ofek I, Cohen S, Fridkin M. 2000a. Structure-function studies of polymyxin В nonapeptide: Implications to sensitization of Gram-negative bacteria. J. Med Chem 43: 3085-3092.
Tsubery H, Ofek I, Cohen S, Fridkin M. 2000b. The functional association of polymyxin В with bacterial lipopolysaccharide is stereospecific: Studies on polymyxin В nonapeptide. Biochemistry 39: 11837-11844.
Tsubery H, Ofek I, Cohen S, Fridkin M. 2001. N-terminal modifications of polymyxin В nonapeptide and their effect on antibacterial activity. Pep-tides 22: 1675-1681.
Tsubery H, Ofek I, Cohen S, Eisenstein M, Fridkin M. 2002. Modulation of the hydrophobic domain of polymyxin В nonapeptide: effect on outer-membrane permeabilization and lipopolysaccharide neutralization. Molecular Pharmacology 62: 1036-42.
Tsubery H, Yaakov H, Cohen S, Giterman T, Matityahou A, Fridkin M, Ofek I. 2005. Neopeptide antibiotics that function as opsonins and membrane-permeabilizing agents for gram-negative bacteria. Antimicrob Agents Chemother 49: 3122-3128.
Vaara M. 1992. Agents that increase the permeability of the outer membrane. Microbiol Rev 56: 395-411.
Vaara M. 1993. Antibiotic-supersusceptible mutants of Escherichia coli and Salmonella typhimurium. Antimicrob Agents Chemother 37: 2255-2260.
Vaara M, Vaara T. 1983a. Sensitization of Gram-negative bacteria to antibiotics and complement by a nontoxic oligopeptide. Nature (London) 303: 526-528.
Vaara M, Vaara T. 1983b. Polycations sensitize enteric bacteria to antibiotics. Antimicrob Agents Chemother 24: 107-113.
Vaara M, Vaara T. 1983c. Polycations as outer membrane-disorganizing agents. Antimicrob Agents Chemother 24: 114-122.
Vaara M, Viljanen P, Vaara T, Mäkelä P. 1984. An outer membrane disorganizing peptide PMBN sensitizes E. coli strains to serum bactericidal action. J Immunol 132: 2582-2589.
Viljanen P, Matsunaga H, Kimura Y, Vaara M. 1991. The outer membrane permeability-increasing action of deacylpolymyxins. J Antibiotics 44: 517-523.
ПРИМЕРЫ
Приведенные ниже примеры иллюстрируют некоторые воплощения настоящего изобретения и не должны быть истолкованы как ограничивающие объем изобретения.
Пример 1
Пептидный синтез
Производные полимиксина ("NAB пептиды" или "NAB соединения") синтезировали путем общепринятой твердофазной химии, используя стандартную стратегию защиты Fmoc. Аминокислота на С-конце имеется в продаже в виде присоединенной к твердой фазе, и при отщеплении от смолы кислотой образует С-концевую карбоновую кислоту.
Стратегия при защите представляла собой использование трех уровней ортогональной защиты, временной защиты Fmoc для альфа-амино функциональных групп, групп, которые удаляются во время стадии кислотного гидролиза, и полупостоянной защиты для закрытия реакционных функциональных групп боковой цепи, когда происходит реакция циклизации. После отщепления пептида от смолы С-концевая карбоновая кислота взаимодействует с функциональной группой амино на боковой цепи одной из аминокислот с образованием циклического пептида. После стадии циклизации полупостоянные защитные группы удаляют с получением NAB пептида.
Соответственно, альфа-амино функциональная группа аминокислоты была защищена флуоренилметоксикарбонилом (Fmoc), и Fmoc удаляли 20% пиперидином в диметилформамиде (ДМФ) при каждом цикле. Аминокислота, которая вовлечена при циклизации, например диаминомасляная кислота, была защищена трет-бутоксикарбонилом (tBoc), группой, разлагаемой кислотой, которую удаляли на стадии отщепления. Функциональную группу аспарагина защищали путем тритилирования. Все другие аминокислоты, которые имеют функциональные группы боковой цепи, были защищены группой, которая стабильна на стадии кислотного гидролиза, то есть бензилоксикарбонилом (Z). Для аминокислот фенилаланин и лейцин естественно не требуется защита боковой цепи. Аминоконец не был защищен; это обеспечивает прямое взаимодействие при методике ацилирования.
Стадии синтеза проводили в имеющемся в продаже автоматическом синтезаторе, в котором использовали O-(6-хлорбензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат (HCTU) в качестве активатора.
Ацилирование проводили путем использования четырехкратного молярного избытка каждой аминокислоты или жирной кислоты, четырехкратного молярного избытка активатора HCTU (см. выше) и восьмикратного молярного избытка N-метилморфолина. Время реакции составляло 30 мин.
Аминокислоты покупали в уже защищенном виде у стандартных поставщиков.
Пептид отделяли от смолы путем взаимодействия с раствором 95% трифторуксусной кислоты и 5% воды в течение 2 часов при комнатной температуре с получением частично защищенного продукта. Полученный в результате пептид осаждали диэтиловым эфиром.
Используемая смесь для циклизации представляла собой бензотриазол-1-илокси-трис-пирролидинофосфония гексафторфосфат (РуВор), N-гидроксибензотриазол (HoBt) и N-метилморфолин (NMM) при молярном избытке 2, 2 и 4, соответственно. Пептид растворяли в диметилформамиде, добавляли смесь для циклизации и давали возможность взаимодействовать в течение 2 часов. Циклизованный, защищенный пептид осаждали добавлением холодного диэтилового эфира. Какой-либо остаточный PyBop удаляли промыванием пептида водой.
Ацетилирование осуществляли путем использования уксусного ангидрида-диизопропилэтиламина - ДМФ (1:1:18 об/об/об).
Остальные защитные группы боковой цепи (Z) удаляли путем каталитической дегидрогенизации. Пептид растворяли в смеси уксусной кислоты, метанола и воды (5:4:1) в атмосфере водорода и в присутствии катализатора палладия на угле.
Пептид очищали хроматографией с обращенной фазой, используя общепринятые градиенты ацетонитрила: воды: трифторуксусной кислоты. Продукт высушивали путем лиофилизации.
Выход составлял 10-20 мг, представляя примерно 10%-20% от теоретического, вычисленного на основании молярного количества (примерно 100 микромоль) первого аминоацильного остатка, связанного со смолой.
Чистота по оценкам путем ВЭЖХ с обращенной фазой составляла более чем 90%. В пределах ошибки эксперимента полученные массы соответствовали ожидаемым на основании теоретических значений.
Пример 2
Активность соединений против Escherichia coli и Pseudomonas aeruginosa
Оба пептида, синтезированные в Примере 1, несущие по меньшей мере - только три (3) положительных заряда, исследовали на их способность сенсибилизировать Е. coli к модельному антибиотику рифампину. Тестирование проводили, используя чашки с агаром LB (LB Agar Lennox, Difco, BD, Sparks, MD, U.S.A), который содержит возрастающие концентрации (0,1 мкг/мл, 0,3 мкг/мл, 1 мкг/мл) рифампина (Sigma-Aldrich, St. Louis, MO, U.S.A), а также путем использования контрольных чашек с агаром LB, который не содержал рифампин.
Индикаторный организм Е. coli IH3080 (K1:O18) представлял собой инкапсулированный штамм, исходно выделенный у новорожденного, страдающего менингитом (Vaara et al. 1984), и полученный из Национального института здравоохранения, Хельсинки, Финляндия.
Из ночной культуры IH3080 на агаре LB готовили суспензию примерно 108 клеток/мл в 0,9% NaCl. Затем аликвоты этой суспензии переносили пипеткой на чашки с агаром, и чашки мягко встряхивали для равномерного распределения суспензии по всей поверхности чашки. Затем не абсорбированную часть суспензии удаляли с использованием пастеровской пипетки. После высыхания поверхности на чашках просверливали маленькие лунки (диаметром 2 мм) (пять лунок на чашку) путем использования узкой металлической трубки с острыми краями, одноразового наконечника автоматической пипетки и вакуумного всасывания. Альтернативно для рассева инокулума использовали кисточку. Затем образцы (4 мкл и 10 мкл) раствора пептида в 0,9% NaCl (при концентрациях 1 мкг/мл и 0,1 мкг/мл) переносили пипеткой в лунки, и жидкости образца давали возможность абсорбироваться. Контроли включали 0,9% раствор NaCl без тестируемого соединения. Затем чашки инкубировали в течение 18 ч при 37°C, после чего измеряли диаметры зон ингибирования роста вокруг каждой лунки; диаметр самой лунки не вычитали. Наконец диаметры переводили в площади поверхности ингибирования роста (в квадратных мм).
В таблице 2 показана активность новых соединений против Е. coli IH3080 по сравнению с активностью контрольных соединений. Даже, несмотря на то, что у обоих отсутствовала прямая антибактериальная активность NAB739, они сенсибилизировали при концентрации 4 мкг/мл мишень к столь низкой концентрации рифампина, как 0,1 мкг/мл. Интересно, что NAB747 обладал прямой антибактериальной активностью против P. aeruginosa АТСС 27853. В лунке, содержащей 10 мкг пептида, он вызывал зону ингибирования с площадью поверхности 50 кв.мм. При 4 мкг соответствующее значение составляло 20 кв.мм.
Пример 3
NAB741 сенсибилизирует Е. coli, Klebsiella pneumoniae и Enterobacter cloacae к широкому ряду антибактериальных агентов
Минимальные ингибиторные концентрации (MIC) репрезентативной группы клинически применяемых противомикробных агентов были определены для Двух штаммов Е. coli (АТСС25922 и IH3080), K. pneumoniae АТСС13883 и Е. cloacae АТСС23355 путем использования агаровой среды Мюллера-Хинтона (продукт №Lab039; LabM Ltd., Бери, Ланкашир, СК) в присутствии NAB741 (4 мкг/мл), а также в его отсутствие. MIC определяли путем использования E-Strips (Biodisk Ltd., Солна, Швеция) согласно инструкциям изготовителя. Используемая концентрация NAB741 сама по себе не ингибировала рост бактерий-мишеней. MIC NAB741 для всех этих штаммов составляла >16 мкг/мл.
Результаты показаны в таблице 3. NAB741 при концентрации 4 мкг/мл был способен сенсибилизировать тестируемые штаммы к рифампину с коэффициентом в интервале от более 64 до более 2000. Коэффициент сенсибилизации определяют как отношение MIC антибиотика в отсутствие NAB741 к таковой в присутствии 4 мкг/мл NAB741. Крайне высокие коэффициенты сенсибилизации наблюдали также к кларитромицину (24-340), мупироцину (8-192), азитромицину (16-32), для некоторых из штаммов к фузидовой кислоте (128-170), и для Е. cloacae к ванкомицину (170). Все эти антибактериальные агенты обладают значительной гидрофобностью или большим размером (ванкомицин) и известно, что они исключаются интактной НМ грамотрицательных бактерий, но проникают через поврежденную НМ.
Пример 4
Чувствительность семи различных штаммов грамотрицательных бактерий к рифампину и кларитромицину в присутствии NAB741 (4 мкг/мл)
Минимальные ингибиторные концентрации (MIC) рифампина и кларитромицина для репрезентативной группы различных штаммов клинически релевантных грамотрицательных бактерий определяли способом Е-теста, как в Примере 3, и путем использования агара Мюллера-Хинтона с NAB741 (4 мкг/мл) или без него. Данная концентрация NAB741 сама по себе не ингибирует рост бактерий-мишеней. Пять штаммов имеют происхождение из АТСС. Acinetobacter baumannii F264 покупали от Mobidiag Ltd., Хельсинки, Финляндия. Источник Е. coli IH3080 приведен в Примере 2.
Результаты показаны в таблице 4. В ней показано, что NAB741 обладает заметной активностью даже против Acinetobacter baumannii.
Пример 5
NAB741 сенсибилизирует устойчивый к меропенему штамм Acinetobacter baumannii к меропенему
Минимальные ингибиторные концентрации (MIC) меропенема для двух штаммов A. baumannii определяли способом Е-теста, как в Примере 4, и путем использования агара Мюллера-Хинтона с NAB741 (4 мкг/мл) и без него. Данная концентрация NAB741 сама по себе не ингибирует рост бактерий-мишеней. Коэффициент сенсибилизации определяли, как в Примере 4. Результаты показаны в таблице 5. NAB461 сенсибилизировал устойчивый к меропенему штамм F264 к меропенему с коэффициентом более 4.
Пример 6
NAB741 сенсибилизирует Е. coli к комплементу в свежей нормальной сыворотке
Способность NAB741 к сенсибилизации инкапсулированного, гладкого штамма Е. coli к бактерицидному действию нормальной сыворотки морской свинки (GPS) исследовали способом, описанным Vaara et al. (1984). Е. coli IH3080 (018, K1) выращивали в жидкой среде LB (LB broth Lennox, Difco, BD, Спаркс, Мэриленд, США) при 37°C в ротационном шейкере до ранней логарифмической фазы роста, промывали ФСБ (фосфатно-солевым буферным раствором, 8,0 г NaCl, 0,2 г KCl, 1,44 г Na2HPO4×2H2O и 0,2 г KH2PO4 на литр) и ресуспендировали в ФСБ примерно до 109 клеток/мл). GPS использовали в качестве источника комплемента. Сыворотку хранили при -70°C до использования. Для инактивации комплемента сыворотку инкубировали при 56°C в течение 30 мин.
Экспериментальная методика была следующей. 10% GPS в ФСБ инокулировали примерно 500 КОЕ (колониеобразующих единиц) бактерий на мл и переносили пипеткой в 0,2 мл аликвотах в лунки микротитрационных планшетов. Лунки уже содержали возрастающие количества NAB7061 в 0,020 мл 0,9% NaCl. Планшет инкубировали при 37°C в течение 2 ч, после чего каждую лунку опорожняли в чашки LB. Чашки инкубировали в течение ночи при 37°C и считали развившиеся колонии.
Результаты представлены в таблице 6. NAB741 сам по себе значимо не снижает счет КОЕ в отсутствие GPS или в присутствии инактивированной нагреванием 10% GPS. Однако столь низкая концентрация NAB741, как 2 мкг/мл, была достаточна для снижения счета КОЕ с коэффициентом примерно 100 в присутствии 10% свежей GPS. Соответственно, NAB741 действует синергично с бактерицидным механизмом комплемента, присутствующим в свежей сыворотке, как и PMBN, агент, хорошо известный как обладающий этим свойством.
Пример 7
Получение и биологическая активность NAB739 метансульфоната натриевой соли
NAB739 ацетат (100 мг) растворяли в воде (2 мл) и добавляли нейтральный раствор формальдегида (400 микролитров 30% водного формальдегида [доведенный до pH 7,2 1 н. Na-HCO3]). Затем добавляли 1 н. раствор NaHCO3 (2 мл), и выпавшее в осадок производное NAB739 формальдегид фильтровали и промывали водой. Влажное твердое вещество суспендировали в воде (5 мл) и добавляли метабисульфит натрия (100 мг). Через несколько минут получили прозрачный раствор и лиофилизировали. Хлопьевидное белое твердое вещество экстрагировали теплым ацетоном (7,5 мл) и высушивали в вакууме. Выход составлял 56 мг. Анализ продукта с помощью ИЭР масс-спектрометрии выявил преобладающий пик молекулярной массы 1075,3, что указывает на то, что большая часть производного была сульфометилирована при каждом из трех остатков Dab соединения NAB739. Также был видим минорный пик, представляющий собой NAB739, случайным образом блокированный при двух из трех остатков Dab.
Для измерения антибактериальной активности водных растворов NAB739 метансульфоната натрия готовили три различных раствора: 1) Раствор (1 мг/мл) готовили в 0,9% NaCl непосредственно перед экспериментом, 2) раствор (1 мг/мл) готовили в 0,9% NaCl за 24 ч до эксперимента и держали при 37°C, 3) раствор (1 мг/мл) готовили в 0,9% NaCl за 48 ч до эксперимента и держали при 37°C. Свежеприготовленный раствор NAB739 ацетата служил в качестве контрольного соединения.
Тестируемая бактерия представляла собой Е. coli IH3080. Ее выращивали в бульоне LB (LB broth Lennox, Difco, BD, Sparks, MD, U.S.A.) при 37°C в ротационном шейкере в ранней логарифмической фазе роста, промывали ФСБ и ресуспендировали в ФСБ примерно при 10е9 клеток/мл. ФСБ инокулировали примерно 500 КОЕ (колониеобразующих единиц) бактерий на мл и переносили пипеткой в аликвотах 0,2 мл в лунки микротитрационного планшета. Планшеты уже содержали возрастающие концентрации NAB739 метансульфоната или контрольного соединения в 0,020 мл 0,9% NaCl. Планшет инкубировали при 37°C в течение 1 ч, после чего каждую лунку опорожняли на чашки LB. Планшет инкубировали в течение ночи при 37°C и считали проявленные колонии.
Результаты показаны в таблице 7. Свежий раствор NAB739 метансульфоната обладал значительно меньшей антибактериальной активностью, чем контрольное соединение NAB739. Выдерживание раствора NAB739 метансульфоната при 37°C в течение 24 ч перед использованием несколько повышало активность, тогда как выдерживание в течение 48 ч привело в результате к активности, почти равной активности, наблюдаемой с контрольным соединением. Эти результаты указывают на то, что NAB739 метансульфонат по аналогии с колистином метансульфонатом медленно разлагается в водных растворах с образованием вещество с большей антибактериальной активностью, то есть в меньшей степени сульфометилированных веществ, и в конечном счете свободного NAB739.
Подобным образом, получают метансульфонатные производные NAB741, NAB745, NAB747 и другие соединения, как описано в данной заявке. Эти пролекарства разлагаются in vivo с образованием соединений, которые обладают способностью сенсибилизировать бактерии-мишени к другим антибактериальным агентам и сывороточным комплементам.
Пример 8
Сравнение основных фармакокинетических свойств NAB741 и NAB739
Исследования проводили, в основном, путем использования способов, описанных Li et al. (2003, 2004). Каждую крысу (n=4 для обоих соединений, линия Спраг-Доули, самцы) анестезировали, используя изофлуран, и полиэтиленовую канюлю вставляли в яремную вену. Каждую крысу помещали в метаболическую клетку и давали возможность выздороветь от процедуры в течение ночи. Тестируемое соединение (ацетат, 1 мг/кг) вводили в виде болюса (в 200 мкл стерильного 0,9% физиологического раствора) через канюлю, после чего промывали 0,8 мл физиологического раствора. Девять образцов крови (0, 10, 20, 30, 60, 90, 120, 180 и 240 мин), каждый 200 мкл, собирали вручную через канюлю. При сборе образцов первые 100 мкл крови вытягивали и держали в шприце. После отбора действительного образца другим шприцом содержимое первого шприца возвращали в крысу вместе с 400 мкл гепаринизированного физиологического раствора. Образцы крови центрифугировали для получения плазмы. Образцы мочи собирали на 0-4 ч, 4-6 ч и 6-24 ч интервалах. Образцы плазмы и мочи хранили при -80°C.
Образцы анализировали, используя жидкостную хроматографию и масс-спектрометрию с интерфейсом ионизации электрораспылением (ЖХ/МС ионизация электрораспылением). К образцу 100 мкл добавляли 10 мкл внутреннего стандарта (NAB739, 80 мкг/мл) и 200 мкл плазмы (образцы плазмы) или 100 мкл (образцы мочи) ацетонитрила, смесь перемешивали на вортексе в течение 1 мин и центрифугировали при 10000 g в течение 10 мин. Для хроматографии использовали ВЭЖХ колонку С18 (50×2 мм), 0,1% муравьиную кислоту в качестве растворителя А, 0,1% ацетонитрил в качестве растворителя В, скорость тока 0,2 мл/мин и следующий градиент: 5%-30% В за 6 мин, 30%-90% В за 0,5 min, 90% В держали в течение 2,5 мин, 90%-5% В за 1 мин. Элюент между 5,90-7,00 мин и 9,00-10,1 мин направляли в систему МС, используя переключающий клапан. Положительные протонированные молекулярные ионы NAB741 при m/z 496,7 и 331,4 и NAB739 при m/z=538,8 и 359,6 и проводили мониторинг. NAB741 элюировали при 6,65±0,05 мин, и NAB739 элюировали при 9,45±0,05 мин. Фармакокинетический анализ без компартментализации соединений в плазме проводили, используя программное обеспечение WinNonlin (версия 4,0, Mountain View, CA, USA), с моделью NA201 (ввод i.v. болюса для данных плазмы).
Основные фармакокинетические параметры, определенные для NAB741, были такими, как приведено ниже: время полужизни (мин), 32,7±2,41; объем распределения (мл/кг), 243±24,0; клиренс (мл/мин/кг), 7,39±0,85; выделение с мочой (% дозы за 24 ч), 50,9±13,6; и почечный клиренс (мл/мин/кг), 3,78±1,11.
Основные фармакокинетические параметры, определенные для NAB739, соединения, во всем остальном идентичного NAB741, но имеющего октаноильный остаток вместо ацетильного остатка в качестве его концевой группировки, были такими, как приведено ниже: время полужизни (мин), 69,0±21,9; объем распределения (мл/кг), 222±20,5; клиренс (мл/мин/кг), 2,63±0,54; выделение с мочой (% дозы за 24 ч), 19,4±7,38; и почечный клиренс (мл/мин/кг), 0,53±0,30.
Соответствующие параметры для колистина, как определено Li et al. (2003) путем использования идентичной дозировки и методики введения, являются такими, как приведено ниже: время полужизни (мин), 74,6±13,2; объем распределения (мл/кг), 496±60; клиренс (мл/мин/кг), 5,2±0,4; выделение с мочой (% дозы за 24 ч), 0,18±0,14; и почечный клиренс (мл/мин/кг), 0,010±0,008.


Настоящее изобретение относится к производному полимиксина, которое имеет суммарно три положительных заряда при физиологическом pH и где концевая группировка (D) этого производного содержит суммарно от 1 до 5 атомов углерода, его способу получения; к комбинированному продукту, содержащему по меньшей мере два таких производных; фармацевтической композиции, содержащей производное полимиксина; способу сенсибилизации грамотрицательных бактерий к антибактериальному агенту; способу разработки новых антибиотиков. Изобретение также относится к применению производного полимиксина при получении лекарства для сенсибилизации грамотрицательных бактерий к антибактериальным агентам. 11 н. и 12 з.п. ф-лы, 7 табл., 8 пр.
1. Производное полимиксина общей формулы (V),
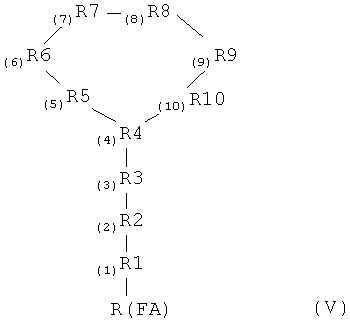
где R4 представляет собой аминокислотный остаток, содержащий функциональную боковую цепь, способную к циклизации молекулы;
R6 представляет собой независимо выбранный, возможно, но необязательно замещенный гидрофобный аминокислотный остаток;
R7 представляет собой независимо выбранный, возможно, но необязательно замещенный гидрофобный аминокислотный остаток или Thr;
R10 представляет собой Leu или любой не гидрофобный аминокислотный остаток; и
где R1 является возможным, но необязательным; и
где R1, R2, R3, R5, R8 и R9 представляют собой аминокислотные остатки; и
где R1, R2, R3, R5, R8 и R9 выбраны таким образом, что производное полимиксина имеет три положительных заряда при физиологическом рН; и
где R(FA) представляет собой возможно, но необязательно замещенный алканоильный или алкильный остаток, имеющий суммарно от 1 до 5 атомов углерода;
или его фармацевтически приемлемые соли.
2. Производное по п.1, где указанные R1, R2 и R3 выбраны таким образом, чтобы суммарное значение положительного заряда боковой цепи производного полимиксина не превышало один.
3. Производное по п.1, где R(FA) представляет собой остаток, имеющий от 1 до 3 атомов углерода.
4. Производное по п.1, где R(FA) представляет собой ацетил.
5. Производное по п.1, где R1-R10 выбран из группы, состоящей из Thr-DSer-cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-] и Thr-DAsn-cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-].
6. Производное по п.5, выбранное из группы, состоящей из Ac-Thr-DSer-cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-] и Ac-Thr-DAsn-cy[Dab-Dab-DPhe-Leu-Dab-Dab-Thr-].
7. Производное по п.1, которое представляет собой пролекарство, содержащее одну или более чем одну сульфоалкильную группировку, маскирующую положительный заряд.
8. Производное по п.7, где указанная сульфоалкильная группировка представляет собой сульфометил.
9. Производное по п.1, которое обладает более низкой токсичностью, чем полимиксин В.
10. Производное по п.1, которое повышает бактериальную чувствительность ко второму антибактериальному агенту или комплементу сыворотки.
11. Производное по п.10, где вторым антибактериальным агентом является рифампин, кларитромицин, мупироцин, азитромицин, фузидовую кислоту или ванкомицин.
12. Производное по п.1, где указанное производное обладает одним или более чем одним благоприятным фармакокинетическим свойством, выбранным из более длительного времени полужизни в сыворотке, повышенного почечного клиренса или повышенного выделение с мочой по сравнению с нативными полимиксинами, октапептинами или производными полимиксина с концевыми группировками более чем с пятью атомами углерода.
13. Комбинированный продукт для сенсибилизации грамотрицательных бактерий к антибактериальному агенту, содержащий два или более производных по любому из пп.1-12.
14. Фармацевтическая композиция для сенсибилизации грамотрицательных бактерий к антибактериальному агенту, содержащая по меньшей мере одно производное по любому из пп.1-12 в эффективном количестве и по меньшей мере один фармацевтически приемлемый носитель и/или эксципиент.
15. Фармацевтическая композиция по п.14, дополнительно содержащая второй антибактериальный агент, который по меньшей мере является средне гидрофобным или высоко антибактериальным агентом, внешняя мембрана грамотрицательных бактерий для которого является проницаемым барьером.
16. Способ сенсибилизации грамотрицательных бактерий к антибактериальному агенту, который по меньшей мере является средне гидрофобным или высоко антибактериальным агентом, внешняя мембрана грамотрицательных бактерий для которого является проницаемым барьером, при котором вводят, одновременно или последовательно в любом порядке, терапевтически эффективное количество указанного антибактериального агента и производного по любому из пп.1-12 или комбинации по п.13.
17. Способ разработки новых антибиотиков по любому из пп.1-12, включающий стадии:
а) получения соединения природного полимиксина или октапептина или его производного, имеющего суммарно от 4 до 6 положительных зарядов и концевую группировку R(FA), содержащую суммарно от 1 до 5 атомов углерода;
б) замены от 1 до 3 остатков, несущих один или более чем один положительный заряд, остатком, не имеющим положительного заряда, или ковалентной связью, с получением посредством этого производного соединения полимиксина, имеющего 3 положительных заряда и концевую группировку R(FA), содержащую суммарно от 1 до 5 атомов углерода;
в) анализа указанного производного полимиксина на способность к сенсибилизации грамотрицательных бактерий к антибактериальному агенту; и
г) отбора соединений, обладающих способностью к сенсибилизации грамотрицательных бактерий к антибактериальному агенту.
18. Способ разработки новых антибиотиков по любому из пп.1-12, включающий стадии:
а) получения соединения природного полимиксина или октапептина или его производного, имеющего суммарно от 4 до 6 положительных зарядов и концевую группировку R(FA), имеющую более 5 атомов углерода;
б) замены от 1 до 3 остатков, несущих один или более чем один положительный заряд, остатком, не имеющим положительного заряда, или ковалентной связью, с получением посредством этого производного соединения полимиксина, имеющего 3 положительных заряда;
в) замены указанной концевой группировки R(FA), имеющей более 5 атомов углерода, концевой группировкой R(FA), содержащей суммарно от 1 до 5 атомов углерода, с получением посредством этого производного соединения полимиксина, имеющего 3 положительных заряда и концевую группировку R(FA), содержащую суммарно от 1 до 5 атомов углерода;
в) анализа указанного производного полимиксина на способность к сенсибилизации грамотрицательных бактерий к антибактериальному агенту; и
г) отбора соединений, обладающих способностью к сенсибилизации грамотрицательных бактерий к антибактериальному агенту.
19. Способ разработки новых антибиотиков по любому из пп.1-12, включающий стадии:
а) получения соединения природного полимиксина или октапептина или его производного, имеющего суммарно от 4 до 6 положительных зарядов и не имеющего концевой группировки R(FA),
б) замены от 1 до 3 остатков, несущих один или более чем один положительный заряд, остатком, не имеющим положительного заряда, или ковалентной связью, с получением посредством этого производного соединения полимиксина, имеющего 3 положительных заряда;
в) введения концевой группировки R(FA), содержащей от 1 до 5 атомов углерода, с получением посредством этого производного соединения полимиксина, имеющего 3 положительных заряда и концевую группировку R(FA), содержащую суммарно от 1 до 5 атомов углерода;
в) анализа указанного производного полимиксина на способность к сенсибилизации грамотрицательных бактерий к антибактериальному агенту; и
г) отбора соединений, обладающих способностью к сенсибилизации грамотрицательных бактерий к антибактериальному агенту.
20. Способ сенсибилизации клинически значимых грамотрицательных бактерий к защитному механизму комплемента хозяина, присутствующего в сыворотке, где указанные бактерии подвергают действию производного по любому из пп.1-12 во время манифестной инфекции.
21. Применение производного по любому из пп.1-12 при получении лекарства для сенсибилизации грамотрицательных бактерий к антибактериальным агентам.
22. Применение производного по любому из пп.1-12 при получении лекарства для сенсибилизации грамотрицательных бактерий к защитному механизму комплемента хозяина, присутствующего в сыворотке.
23. Способ получения производного полимиксина формулы (V), как определено в п.1, включающий
(А) модифицирование природного или синтетического соединения полимиксина или октапептина или его производного, имеющего от 4 до 5 положительно заряженных остатков и концевую группировку R(FA), содержащую суммарно от 1 до 5 атомов углерода, путем замены от 1 до 2 из указанных остатков нейтральными остатками или ковалентной связью, либо преобразования от 1 до 2 из указанных остатков в нейтральные остатки с целью получения производного полимиксина формулы (V) по п.1, имеющего 3 положительно заряженных остатка и концевую группировку R(FA), содержащую суммарно от 1 до 5 атомов углерода; или
(Б) модифицирование природного или синтетического соединения полимиксина или октапептина или его производного, имеющего от 4 до 5 положительно заряженных остатков и концевую группировку R(FA), имеющую более 5 атомов углерода, путем замены от 1 до 3 из указанных остатков нейтральными остатками или ковалентной связью, либо преобразования от 1 до 3 из указанных остатков в нейтральные остатки и путем замены указанной концевой группировки R(FA), содержащей более 5 атомов углерода, концевой группировкой R(FA), содержащей суммарно от 1 до 5 атомов углерода, с целью получения производного полимиксина формулы (V) по п.1, имеющего 3 положительно заряженных остатка и концевую группировку R(FA), содержащую суммарно от 1 до 5 атомов углерода; или
(В) модифицирование природного или синтетического соединения полимиксина или октапептина или его производного, имеющего от 4 до 5 положительно заряженных остатков и не имеющего концевой группировки R(FA), путем замены от 1 до 3 из указанных остатков нейтральными остатками или ковалентной связью, либо преобразования от 1 до 3 из указанных остатков в нейтральные остатки и путем введения концевой группировки R(FA), содержащей суммарно от 1 до 5 атомов углерода, с целью получения производного полимиксина формулы (V) по п.1, имеющего 3 положительно заряженных остатка и концевую группировку R(FA), содержащую суммарно от 1 до 5 атомов углерода.
| ПРОИЗВОДНЫЕ ПОЛИМИКСИНА И ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2455311C2 |
| WO 2006083317 A2, 10.08.2006 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| OKIMURA К ET AL: "Chemical conversion of natural polymyxin В and colistin to their N-terminal derivatives" BULLETIN OF THE | |||
Авторы
Даты
2013-09-10—Публикация
2009-02-05—Подача