Изобретение относится к области вирусологии и биотехнологии и касается выделения штамма вируса иммунодефицита человека первого типа.
Создание лечебной и (или) профилактической вакцины против вируса иммунодефицита человека первого типа (ВИЧ-1) является актуальной проблемой современной вирусологии, так как вакцина служит наиболее эффективным средством в борьбе с вирусными инфекциями. К настоящему времени более 30 препаратов как возможных кандидатов вакцинных препаратов были использованы в клинических испытаниях, но ни один из них не показал эффективного протективного эффекта. Исследования по созданию новых вакцинных препаратов активно продолжаются (1, 2). Они создаются на базе штаммов ВИЧ-1, которые широко используются в научных исследованиях во всем мире.
Другим направлением профилактики ВИЧ-инфекции является создание антиретровирусных препаратов. В настоящее время в клинике применяется около 28 препаратов, действующих на различных стадиях инфекционного цикла вируса. Наиболее многочисленную группу составляют препараты, подавляющие активность обратной транскриптазы и протеазы. Среди них первым с 1987 г.начал применяться азидотимидин (zidovudine, Retrovir) (АЗТ). Его действие направлено против обратной транскриптазы. Несмотря на большие успехи антиретровирусной терапии существует большая проблема, связанная с появлением в процессе лечения вариантов вируса с мутациями, снижающими чувствительность вируса к химиопрепаратам и, как следствие, ухудшение эффективности лечения. Эти мутации называются основными (3). При их появлении необходима смена лекарственной схемы. Кроме мутаций, с которыми связана высокая степень резистентности к определенным химиопрепаратам (основными мутациями), могут существовать варианты вируса с другими фенотипическими мутациями, которые также могут иметь отношение к химиотерапии. Эти мутации называются вторичными и впервые были обнаружены у пациентов в процессе лечения (3). Кроме того, наряду с высокой степенью изменчивости вируса в процессе пасеирования в человеческой популяции под действием факторов иммунной системы, для вируса характерна региональная изменчивость. Эти мутации сами по себе не влияют на эффективность известных в настоящее время антиретровирусных препаратов, но могут усиливать резистентность вируса к некоторым химиопрепаратам при появлении или наличии основной мутации. Характерная особенность российских вариантов вируса заключается в том, что более 50% из них содержат вторичные мутации V77I в Протеазе и/или A62V в Обратной транскриптазе (4,5). В связи с этим использование штаммов, полученных от пациентов, проживающих на территории Российской Федерации, представляется перспективным для создания профилактических и лечебных препаратов, а также для создания более чувствительных диагностических тест-систем. К тому же выделение штаммов ВИЧ-1, имеющих как первичные, так и вторичные мутации, с которыми связана резистентность к различным химиопрепаратам, может быть полезна для скрининга и испытания новых химиопрепаратов и оценки их эффективности против вирусов с различными мутациями.
Задачей настоящего изобретение явилось получение нового оригинального штамма обладающего рядом вирусологических свойств, позволяющих рассматривать его как удобную биотехнологическую природную модель для разработки диагностических и вакцинных препаратов, а также для скрининга различных соединений и испытания лекарственных препаратов.
Новый оригинальный авторский штамм 316RU вируса иммунодефицита человека ВИЧ-1/Россия, который циркулирует на территории России, получен от пациента, принимающего курсами специфическую химиотерапию в течение 3-х лет, имеет одну основную и четыре вторичных мутации, может быть использован для приготовления диагностических тест-систем, моделирования молекулярно-генетических экспериментальных вакцинных препаратов и для изучения антивирусного действия различных соединений, в том числе для оценки противовирусной активности лекарственных препаратов. Штамм депонирован в Государственную коллекцию вирусов, действующую на базе Федерального государственного бюджетного учреждения «Научно-исследовательский институт вирусологии им. Д.И.Ивановского» Министерства здравоохранения и социального развития Российской Федерации (ФГУ «НИИ вирусологии им. Д.И.Ивановского» Минздравсоцразвития России), и имеет регистрационный номер ГКВ-1033.
Штамм обладает высокой репродуктивной активностью для штаммов ВИЧ-1 и легко размножается в неопластических суспензионных Т-лимфоидных клетках человека МТ-4. О продукции вируса можно легко судить по ярко выраженному цитопатическому действию, выражающемуся в цитолизе и гибели через 7-10 дней после заражения инфицированных клеток. Продуктивная активность штамма составляет 4.0 lg ТЦД50. Штамм хорошо хранится при -70°С.
Идентификация штамма ВИЧ-1/Россия/3161RU осуществлена рядом независимых методов, в качестве контроля использовали эталонный культуральный штамм ВИЧ-1/IIIB.
Культуральные свойства.
Штамм вируса выделен из лимфоцитов периферической крови пациента с диагнозом ВИЧ-инфекция. Пациент относится к группе риска лиц, практикующих внутривенное использование наркотических препаратов. Пациент в течение 3-х лет принимал в качестве антиретровирусной терапии АЗТ.
Штамм был получен путем 4-х последовательных сокультиваций мононуклеарных клеток периферической крови пациента с ВИЧ-инфекцией в присутствии интерлейкина-2 человека с первичными культурами мононуклеарных клеток доноров, предварительно стимулированных фитогемагглютинином в течение 3-х дней. В дальнейшем штамм был адаптирован к неопластическим суспензионным Т-клеткам человека МТ-4. Штамм прошел 50 пассажей в клетках МТ-4.
Репродукция.
Штамм вируса реплицируется в мононуклеарных клетках периферической крови, неопластической клеточной культуре Т-клеток человека МТ-4. Репродукция вируса сопровождается характерным цитопатическим действием в виде цитолиза и гибели клеток через 7-10 дней после инфекции.
Штамм ВИЧ-1/Россия/316RU и может поддерживаться длительное время при пассировании в МТ-4 клетках. Через 7-10 дней после инфицирования клеток вируссодержащей культуральной жидкостью инфицированная клеточная взвесь добавляется к свежей клеточной суспензии в соотношении 1:10, или замораживается и хранится при - 70 С длительное время. После размораживания используется для заражения свежей клеточной суспензии в соотношении 1:10.
Инфекционный титр вируса определяли методом конечных разведении и оценивали по 50% тканевой цитопатической дозе вируса на клетках МТ-4 в сравнении с эталонным штаммом ВИЧ-1/IIIВ (Фиг.1).
Антигенные свойства.
Вирус иммунодефицита человека 1-го типа относится к семейству Retro viridae, подсемейство Orthoretrovirinae, род Lentivirus, подгруппа Primat lentivirus. Вирусы этой группы являются оболочечными РНК-содержащими вирусами с размером частиц около 100-150 нм. В составе частиц в мажорных количествах обнаруживают не менее 6 основных структурных антигенов, обладающих в различной степени иммуногенными свойствами, которые и в инфицированных вирусом клетках и вируссодержащей культуральной жидкости могут быть выявлены с помощью различных иммунобиологических методов.
Иммунофлуоресценция.
Исследование методом непрямой иммунофлюоресценции с использованием сыворотки пациента с ВИЧ-инфекцией, содержащей антитела к ВИЧ-1, показало наличие в инфицированной клеточной культуре через 6 дней после инфекции наличие ВИЧ-1 антигена в 40-50% инфицированных клетках.
Иммуноблот.
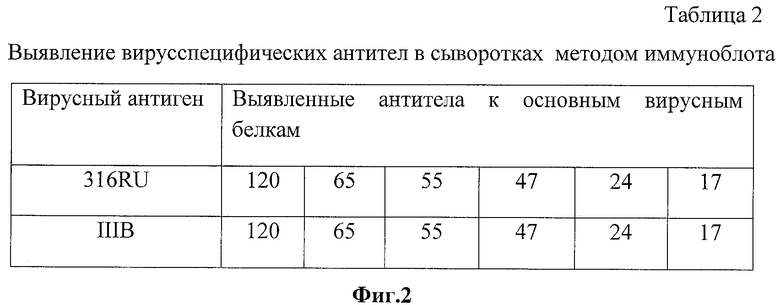
Исследования в иммуноблоте 100-кратного концентрата вируса из культуральной жидкости инфицированных вирусом клеток позволили заключить, что вирус содержит основные структурные антигены, характерные для ВИЧ-1: gp120, p53-55, gp41, p24, р17, р9 (Фиг.2).
Анализ нуклеотидной и белковой последовательности гена ро1.
Исследовали ДНК продукт гена ро1, кодирующего белки Протеазы и Обратной транскриптазы, путем автоматического секвенирования. Для получения ДНК продукта использовали вируссодержащую культуральную жидкость, полученную на 8-ой день после заражения клеток МТ-4. Получение РНК вируса, реакцию обратной транскрипции, полимеразную цепную реакцию и циклическое секвенирование проводили с использованием коммерческой тест-системы ViroSeq V2.1 (Abbott, USA). Секвенирование позволило изучить аминокислотную последовательность всего белка Протеазы - 99 аминокислотных остатков (ако)- и основную часть Обратной транскриптазы - 320 ако. Для определения подтипа гена ро1 вируса была использована база Стендфордского Университета - Stanford University HIV DRAG RESISTANCE DATABASE, а также был проведен фенотипический анализ гена с использованием программ BioEdit и MEGA4 отдельно по генам протеазы и обратной транскриптазы с использованием стандартных референс последовательностей для всех известных в настоящее время подтипов ВИЧ-1. Оба анализа показали, что по генам протеазы и обратной транскриптазы вирус принадлежит к подтипу В. Протеаза содержит вторичные мутации L63P и V77I, Обратная транскриптаза содержит основную мутацию T215F и вторичные мутации D67N и K70R.
Штамм имеет следующую аминокислотную последовательность белка Протеазы:

Иммуногенные свойства.
Трехкратная иммунизация кроликов очищенным препаратом вирусных частиц приводит к возникновению у лабораторных животных специфического иммунного ответа. С помощью иммуноблота можно выявить антитела к основным структурным белкам ВИЧ-1: gp120, gp41, p55, P24, p17 (Фиг.3).
Сыворотка крови лабораторных животных способна нейтрализовать другие штаммы ВИЧ-1 субтипа В, например эталонный штамм ВИЧ-1/IIIB (Фиг.4).
Пример 1. Диагностика антител сыворотки крови ВИЧ-инфицированных пациентов методом иммуноблота.
Материал для исследования антител к ВИЧ-1 представлен 10 стандартными сыворотками, содержащими анти-ВИЧ антитела ко всем основным структурным белкам вируса и предварительно охарактеризованными в коммерческой тест-системе фирмы «Био-рад» (Австрия). В качестве антигена использовали штамм ВИЧ-1/Россия/316RU и эталонный штамм ВИЧ-1/IIIВ. Концентрированные и очищенные лизаты антигенов вирусов были получены по стандартной методике. Результаты исследования представлены в табл.2. (Фиг.2). Обнаружено, что антиген ВИЧ-1/Россия/316RU выявляет антитела ко всем основным структурным белкам ВИЧ-1.
Пример 2. Демонстрация использования штамма ВИЧ-1/Россия/ГКВ1033/ 316RU для получения специфических антител, способных нейтрализовать ВИЧ-1. Для сравнения использовали эталонный штамм ВИЧ-1/IIIB.
Трехкратную иммунизацию кроликов очищенными препаратами вирусных частиц проводили внутримышечно с интервалом в 4 недели с использованием полного адьюванта Фрейнда при первой иммунизации. Анализ сывороток проводили с использованием коммерческих тест-систем фирмы «Био-рад» (Австрия). Результаты анализа кроличьих сывороток, полученных после иммунизации представлены в табл.3 (Фиг.3). Выявлено, что препарат антигена, приготовленного из штамма ВИЧ-1/Россия/316RU, обладает иммуногенной активностью, сравнимой с иммуногенной активностью эталонного штамма ВИЧ-1/IIIВ.
Анализ нейтрализующей активности вирусспецифических антител, полученных к штамму ВИЧ-1/Россия/316RU? показал, что они способны нейтрализовать репликацию эталонного штамма ВИЧ-1/IIIВ в клетках МТ-4 (Фиг.4).
Пример 3. Применение штамма ВИЧ-1/Россия/316RU для изучения активности противовирусных препаратов. Для сравнения брали эталонный штамм ВИЧ-1/IIIВ.
Использовали стандартную лабораторную модель и методику исследования, применяемые для скрининга противовирусных препаратов и для оценки противовирусной активности различных соединений. Клетки МТ-4 заражали штаммом ВИЧ-1/Россия/316RU и штаммом ВИЧ-1/IIIB. Зараженные клетки инкубировали в присутствии двух ингибиторов Обратной транскриптазы ВИЧ-1 - азидотимидина и индинавира. Первый относится к нуклеозидным ингибиторам Обратной транскриптазы, второй - к ингибиторам Протеазы. Как показали исследования, чувствительность к азидотимидину у штамма ВИЧ-1/Россия/316RU по сравнению со штаммом ВИЧ-1/IIIB снижена в 12 раз. Чувствительность к индинавиру несущественно снижена (Фиг.5).
Предлагаемый оригинальный штамм вируса ВИЧ-1/Россия/316RU обладает высокой репликативной активностью и адаптирован к чувствительной неопластической клеточной линии МТ-4, характеризуется высокой антигенной активностью. Штамм имеет мутации в обратной транскриптазе (D67N, K70R, T215F) и протеазе (L63P, V77I), которые могут изменять его чувствительность к химиопрепаратам. Приготовленные на его основе препараты могут найти применение в вирусологической практике при разработке и создании противовирусных вакцин и диагностики ВИЧ-инфекции. Штамм может использоваться для испытания противовирусных препаратов и для оценки противовирусной активности различных соединений.
Список литературы
1. С.L.Boutwell, M.M.Rolland, J.Т.Herbeck et al. Viral Evolution and Escape during Acute HIV-1 Infection. J Infect Dis, 2010, 202 (Suppl 2), p.S323-326.
2. M.J.McElrath. Immune Responses to HIV Vaccines and PotentialImpact on Control of Acute HIV-1 Infection. J Infect Dis, 2010, 202 (Suppl 2), p. S323-326.
3. Snanford University. HIV DRUG RESISTANCE DATABASE. http://hivdb6.stanford.edu.
4. Roudinskii N.I., Sukhanova A.L., Kazennova E.V. et al. Diverrsity of human immunodeficiency virus type 1 subtype A and CRF03 AB protease in Eastern Europe: Selection of the V77I variant and its rapid spread in injecting drug user populations. J. Virol. 2004, vol.2, p.11276-11287.
5. Л.М.Селимова, Л.В.Серебровская, Л.А.Иванова и др. Показатели CD4+ и CD8+ Т-лимфоцитов пациентов, инфицированных вариантами вируса иммунодефицита человека 1-го типа подтипа А, несущими мутации V77I и A62V в обратной транскриптазе. Вопросы вирусологии, 2010, 55(2), с.22-26.
| название | год | авторы | номер документа |
|---|---|---|---|
| ШТАММ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1-ГО ТИПА ИВ710 СУБТИПА А РЕЗИСТЕНТНЫЙ К АНТИРЕТРОВИРУСНЫМ ПРЕПАРАТАМ ДЛЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2012 |
|
RU2513692C1 |
| ШТАММ HOMINIS IMMUNODEFICITI VIRUS (HIV-I) ВИЧ-1 /РОССИЯ/ГМ-12-95 (RU 1295) СУБТИПА В ДЛЯ ДИАГНОСТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 1996 |
|
RU2121502C1 |
| ШТАММ A1.RU.09RU2255 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА СУБТИПА А, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2421516C1 |
| ШТАММ 02_AG.RU.09RU2204 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2415931C1 |
| ШТАММ 02_AG.RU.09RU3124 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2420574C1 |
| ШТАММ А1.RU.09RU2065 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА СУБТИПА А, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2420572C1 |
| ШТАММ A1.RU.09RU2225 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА СУБТИПА А, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2420573C1 |
| ШТАММ 02_AG.RU.09RU2308 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2421517C1 |
| ШТАММ 02_AG.RU.09RU2273 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2421515C1 |
| ШТАММ 02_AG.RU.09RU2383 ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА 1 ТИПА РЕКОМБИНАНТНОГО СУБТИПА 02_AG, ИСПОЛЬЗУЕМЫЙ ДЛЯ ДИАГНОСТИКИ И ИЗУЧЕНИЯ ЭФФЕКТИВНОСТИ ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКИХ И ВАКЦИННЫХ ПРЕПАРАТОВ | 2010 |
|
RU2420576C1 |




Изобретение относится к области вирусологии и биотехнологии и касается штамма вируса иммунодефицита человека первого типа (ВИЧ-1). Штамм получен от пациента, принимающего специфическую химиотерапию в течение 3-х лет, имеет одну основную и четыре вторичных мутации, которые могут изменять его чувствительность к химиопрепаратам. Штамм депонирован в Государственную коллекцию вирусов на базе Федерального государственного бюджетного учреждения «Научно-исследовательский институт вирусологии им. Д.И.Ивановского» Министерства здравоохранения и социального развития Российской Федерации под номером ГКВ №1033. Представленный штамм может быть использован как биотехнологическая природная модель для разработки диагностических и вакцинных препаратов, а также для скрининга различных соединений и испытания лекарственных препаратов. 5 ил., 3 пр.
Штамм Hominis immunodeficiti virus ВИЧ-1/Россия/316RU подтипа В по гену роl депонированный под номером ГКВ №1033 в Государственную коллекцию вирусов на базе Федерального государственного бюджетного учреждения «Научно-исследовательский институт вирусологии им. Д.И. Ивановского» Министерства здравоохранения и социального развития Российской Федерации, для приготовления диагностических и вакцинных препаратов и для оценки противовирусной активности различных соединений, содержащий следующую аминокислотную последовательность, соответствующую с 1-й по 419-ю позиции белков гена pol:
Протеаза -
PQITLWQRPLVTIRIGGQLKEALLDTGADDTVLEEMNLPGRWKPKMIGG IGGFIKVRQYDQIPIEICGHKAIGTVLIGPTPVNIIGRNLLTQLGCTLNF -
Обратная транскриптаза -
PISPIETVPVKLKPGMDGPRVKQWPLTEEKIKALVEICTEMEKEGKISKIGPENPYNTPVFAIKKKNSTRWRKLVDFRELNKRTQDFWEVQLGIPHPAGLKKRKSVTVLDVGDAYFSVPLDKDFRKYTAFTIPSINNETPGIRYQYNVLPQGWKGSPAIFQCSMTKILEPFRKQNPDIVIYQYMDDLYVGSDLEIGQHRTKIEELRQHLLRWGFFTPDKKHQKEPPFLWMGYELHPDKWTVQPIVLPEKDSWTVNDIQKLVGKLNWASQIYPGIQVRQLCKLLRGTKALTEVIPLTEEAELELAENREILKEPVHGVYYDP.
| Штамм вируса иммунодефицита человека 1-типа для приготовления диагностических препаратов | 1990 |
|
SU1768637A1 |
| ШТАММ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА I ТИПА, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ ДИАГНОСТИЧЕСКИХ ТЕСТ-СИСТЕМ | 1992 |
|
RU2046138C1 |
| M.JULIANA McELRATH, Immune Responses to HIV Vaccines and Potential Impact on Control of Acute HIV-1 Infection, Journal of Infectious Diseases, 2010, Vol.202, No.2, p.p.323-326. | |||
Авторы
Даты
2012-07-27—Публикация
2011-01-20—Подача