ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к области биотехнологии, конкретно к защитным генам растений, кодирующим биологически активные пептиды с антифунгальной активностью.
УРОВЕНЬ ТЕХНИКИ
Ущерб, наносимый мировому сельскому хозяйству со стороны патогенов культурных растений (грибов, бактерий, вирусов и вироидов) и насекомых-вредителей (две главные причины ущерба), оценивается трлн. рублей ежегодно. Потери достигают половины урожая. Методы, применяемые с целью снижения убытков, в основном сводятся к использованию синтетических пестицидов, многие из которых являются экологически агрессивными веществами. Использование химических средств защиты растений представляет значительную опасность для окружающей среды, биологические средства более безопасны.
Альтернативой длительной селекции полезных признаков, например устойчивости к тем или иным факторам среды, служит генная инженерия. Ее применение для трансформации растений открывает новые возможности создания культур, обладающих широкой устойчивостью к патогенам, вредителям, а также абиотическому стрессу (засухе, засоленности почвы и др.). Пионерские работы по получению резистентных сортов сельскохозяйственных культур с использованием технологий рекомбинантных ДНК были выполнены около 25 лет назад [Andrews R.E., Faust R.M., Wabiko H., Raymond K.C., Bulla L.A. The biotechnology of Bacillus thuringiensis. // Crit. Rev. Biotech. - 1987.- Vol.6.- P. 163-232. Vaeck M., Reynaerts A., Höfte H., Jansens S., De Beuckeleer M., Dean C., Zabeau M., Van Montagu M., Leemans J. Transgenic plants protected from insect attack. // Nature - 1987. - Vol.328. - P.33-37]. С использованием гена инсектицидного белка бактерии Bacillus thuringiensis были получены трансгенные растения табака, устойчивые по отношению к паразитическим личинкам бабочки Manducta sexta. С тех пор гены энтомотоксинов из В. thuringiensis были перенесены и экспрессированы в десятках видов растений, приобретших устойчивость к некоторым вредителям [Schuler Т.Н., Poppy G.M., Kerry B.R., Denholm I. Insect-resistant transgenic plants. // Trends Biotech. - 1998. - Vol.16. - P. 168-175. Romeis J., Meissle M., Bigler F. Transgenic crops expressing Bacillus thuringiensis toxins and biological control. // Nat. Biotechnol. - 2006. - Vol.24 - P.63-71]. Значительная часть мирового урожая приходится сегодня на долю Bt-трансформированных продуктов [James С.Global Status of Commercialized Biotech/GM Crops: 2010. // ISAAA Brief - 2010. - No.42]. Тем не менее, до сих пор обсуждается вопрос безопасности Bt-содержащих продуктов для человека, не совсем ясны экологические последствия глобального распространения трансгенных растений, содержащих гены энтомотоксинов В. thuringiensis, а в последнее время остро стоит проблема выработки насекомыми устойчивости к токсинам [Sanahuja G., Banakar R., Twyman R.M., Capell Т., Christou P. Bacillus thuringiensis: a century of research, development and commercial applications. // Plant Biotechnol. J. - 2011. - Vol.9. - P.283-300]. Кроме того, видимое нарушение межвидового барьера получает отрицательный отклик в современном обществе. Стоит отметить, что инженерия устойчивости к заболеваниям оказалась более сложной задачей, нежели повышение сопротивляемости насекомым.
По-видимому, наиболее перспективными подходами к получению устойчивых сортов являются те, что направлены на усиление собственных защитных свойств растительного организма. К соединениям, продуцируемым растениями для защиты от патогенов, относятся так называемые фитоалексины и фитоантисипины - вещества различной химической природы, а также некоторые белки и пептиды [Sels J., Mathys J., De Coninck B.M., Cammue B.P., De Bolle M.F. Plant pathogenesis-related (PR) proteins: a focus on PR peptides. // Plant Physiol. Biochem. - 2008. - Vol.46. - P.941-950]. Перспективным является получение устойчивых сортов с измененной экспрессией собственных защитных генов или же перенесение генов из одного растения в другое, например из дикорастущего в культурное, поскольку известно, что в ходе селекции и отбора сельскохозяйственные растения, приобретая одни полезные признаки, теряли другие. Наибольший интерес вызывают полипептидные соединения, обладающие защитными свойствами, ввиду возможности их прямого использования для получения трансгенных растений [Carlini C.R., Grossi-de-Sá M.F. Plant toxic proteins with insecticidal properties. A review on their potentialities as bioinsecticides. // Toxicon - 2002. - Vol.40. - P.1515-1539].
К заявляемой нуклеотидной последовательности sm-аmр наиболее близок ген пептида Аr-АМР из амаранта Amaranthus retroflexus [Lipkin A., Anisimova V., Nikonorova A., Babakov A., Krause E., Bienert M., Grishin E., Egorov T. An antimicrobial peptide Ar-AMP from amaranth (Amaranthus retroflexus L.) seeds. // Phytochemistry. - 2005. - Vol.66. - P. 2426-2431]. Ar-AMP относится к тому же обширному семейству цистеин-богатых хитин-связывающих пептидов. В структуре кодирующей части гена (мРНК) выделяют области, соответствующие сигнальному пептиду, зрелому Ar-AMP и С-концевой пропоследовательности. Наиболее существенное отличие заявляемой последовательности sm-amp состоит в одновременном кодировании двух зрелых пептидов.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Изобретение решает задачу расширения ассортимента защитных генов растений, доступных для использования в сельскохозяйственной биотехнологии с целью инженерии устойчивости культурных растений к факторам внешней среды.
Поставленная задача решается за счет структуры новой нуклеотидной последовательности sm-amp, кодирующей антифунгальные пептиды звездчатки Stellaria media:

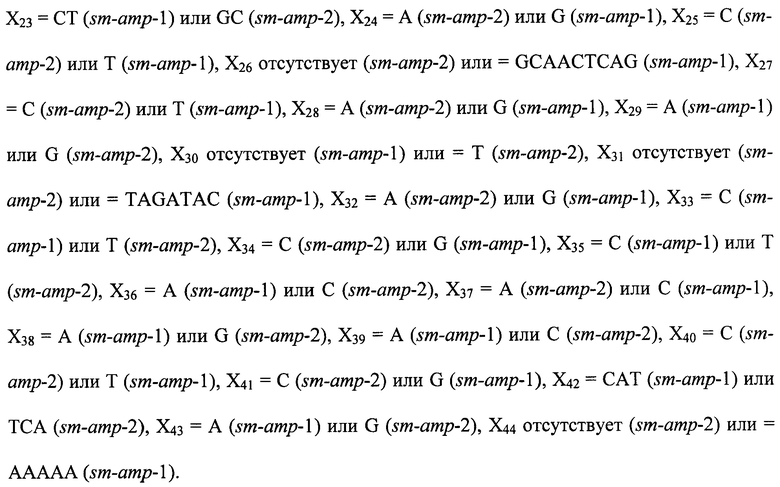
Нуклеотидная последовательность sm-amp соответствует кДНК (мРНК), полученной из природного источника - сорного растения звездчатки средней или мокрицы Stellaria media (L.) Vill., которая относится к семейству гвоздичные Caryophyllaceae, классу двудольные Dicotyledones (Magnoliopsida), отделу покрытосеменные или цветковые растения Magnoliophyta (Angiospermae).
Нуклеотидная последовательность sm-amp кодирует белки-предшественники антифунгальных пептидов pSm-AMP-1 и pSm-AMP-2 длиной 163-167 аминокислотных остатков, имеющие следующие составные элементы: N-концевой сигнальный пептид (22 остатка), первый зрелый пептид (Sm-AMP-1.1a или Sm-AMP-2.1a, 35 остатков), короткую спейсерную пропоследовательность (10 остатков), второй зрелый пептид (Sm-AMP-1.2a или Sm-AMP-2.2a, 32-33 остатка) и протяженную С-концевую пропоследовательность (64-67 остатков). Заявляемая нуклеотидная последовательность sm-amp кодирует пептиды Sm-AMP-1.1a, Sm-AMP-1.2a, Sm-AMP-2.1a, Sm-AMP-2.2a и их производные длиной 30-35 аминокислотных остатков, проявляющие выраженную антифунгальную активность в отношении многих грибов-патогенов растений, в том числе Alternaria consortiale, Fusarium culmorum, Helminthosporium sativum (syn. Bipolaris sorokiniana, Drechslera sorokiniana), Thielatiopsis basicola, в микромолярных концентрациях.
Изобретение иллюстрируют следующие примеры.
Пример 1.
Получение кДНК звездчатки Stellaria media, кодирующей антифунгальные пептиды
Тотальную РНК выделяют из растительного материала при помощи Тризола (Trizol; Life Technologies, США) в соответствии со стандартным протоколом, предлагаемым производителем. 1 мкг тотальной РНК используют для синтеза первой цепи кДНК в соответствии с протоколом Smart (BD Biosciences Clontech, США).
кДНК амплифицируют посредством ПЦР с праймером Smart PCR (BD Biosciences Clontech). Основываясь на аминокислотной последовательности пептидов Sm-Amp-1.1a (H2N-SGPNGQCGPGWGGCRGGLCCSQYGYCGSGPKYCAH-COOH) и Sm-Amp-2.2c (H2N-AAGQCYRGRCSGGLCCSKYGYCGSGPAYCG-COOH), конструируют и синтезируют на автоматическом синтезаторе праймеры для амплификации 3'-концевой части кДНК.
Для sm-amp-1: 5'-CAGTGTGG(T/G)CC(T/C/G)GG(T/C/A/G)TGGGG-3'.
Для sm-amp-2: 5'-GCTGCTGG(T/C/G)CA(A/G)TG(T/C)TA(T/C)CG-3'.
Далее, используя праймеры фирмы BD Biosciences Clontech для 3' RACE-PCR и выше приведенные специфичные праймеры, амплифицируют 3'-фрагменты кДНК sm-amp-1 и sm-amp-2. Амплифицированные фрагменты клонируют в вектор и секвенируют на автоматическом секвенаторе.
На основе установленных нуклеотидных последовательностей фрагментов кДНК конструируют и синтезируют праймеры для амплификации 5'-фрагментов кДНК sm-amp-1 и sm-amp-2:
sm-amp-1-R1: 5'-AATCTCAGAAAGAGGAGTGTTG-3';
sm-amp-1-R2: 5'-CACAATATCCATATTGGGAGC-3';
sm-amp-2-R1: 5'-CCTGGCACATGCCTAGTCC-3';
sm-amp-2-R2: 5'-CGCTCCCACAATATCCATATTT-3'.
Используя праймеры фирмы BD Biosciences Clontech для 5' RACE-PCR и выше приведенные специфичные праймеры, путем последовательной двуступенчатой ПЦР амплифицируют 5'-фрагменты кДНК. Амплифицированные фрагменты клонируют в вектор и секвенируют.
Результирующие нуклеотидные последовательности sm-аmр1 и sm-amp-2, кодирующие pSm-AMP-1 и pSm-AMP-2, получают путем объединения перекрывающихся последовательностей 5'- и 3'-фрагментов кДНК:
sm-amp-1 (826 нуклеотидов):


sm-amp-1 и sm-amp-2 являются близкородственными последовательностями (~92% идентичных нуклеотидов) и могут быть объединены общей формулой.
Пример 2.
Строение кодирующей части генов антифунгальных пептидов звездчатки Stellaria media
sm-amp-1 и sm-amp-2 кодируют близкородственные (~86% идентичных аминокислотных остатков) белки-предшественники (препробелки) pSm-AMP-1 и pSm-АМР-2, соответственно. Их аминокислотные последовательности получают с помощью in silico трансляции нуклеотидных последовательностей sm-amp:
pSm-AMP-1 (167 остатков):

pSm-AMP-1 содержит следующие составные части: N-концевой сигнальный пептид (22 остатка), зрелый пептид Sm-AMP-1.1a (H2N-SGPNGQCGPGWGGCRGGLCCSQYGYCGSGPKYCAH-COOH; 35 остатков), короткую спейсерную пропоследовательность (10 остатков), зрелый пептид Sm-AMP-1.2a (H2N-DAGRCSGRGTCSGGRCCSKYGYCGTGPAYCGLG-COOH; 33 остатка) и протяженную С-концевую пропоследовательность (67 остатков).
Аналогично pSm-AMP-2 содержит следующие составные части: N-концевой сигнальный пептид (22 остатка), зрелый пептид Sm-AMP-2.1a (Н2N-YDPNGKCGRQYGKCRAGQCCSQYGYCGSGSKYCAH-COOH; 35 остатков), короткую спейсерную пропоследовательность (10 остатков), зрелый пептид Sm-AMP-2.2a (H2N-AAGQCYRGRCSGGLCCSKYGYCGSGPAYCGLG-COOH; 32 остатка) и протяженную С-концевую пропоследовательность (64 остатка).
Таким образом, sm-amp-1 одновременно кодирует зрелые пептиды Sm-AMP-1.1a и Sm-AMP-1.2a (и их производные), а sm-amp-2 - Sm-AMP-2.1a и Sm-AMP-2.2a (и их производные).
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕН ЗВЕЗДЧАТКИ Stellaria media, КОДИРУЮЩИЙ АНТИМИКРОБНЫЙ ПЕПТИД Sm-AMP-X | 2013 |
|
RU2531505C1 |
| ГЕНЫ ПШЕНИЦЫ Triticum kiharae, КОДИРУЮЩИЕ АНТИМИКРОБНЫЕ ПЕПТИДЫ | 2011 |
|
RU2483109C1 |
| ПЕПТИД, ОБЛАДАЮЩИЙ АНТИФУНГАЛЬНОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2352580C1 |
| ПЕПТИД ЗВЕЗДЧАТКИ STELLARIA MEDIA L., ОБЛАДАЮЩИЙ АНТИФУНГАЛЬНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2603058C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА pSM-ZsGreen, КОДИРУЮЩАЯ БЕЛКИ SOX2 И С-MYC ЧЕЛОВЕКА И ФЛУОРЕСЦЕНТНЫЙ БЕЛОК ZsGreen, ПРЕДНАЗНАЧЕННАЯ ДЛЯ ПОЛУЧЕНИЯ ИНДУЦИРОВАННЫХ ПЛЮРИПОТЕНТНЫХ СТВОЛОВЫХ КЛЕТОК ЧЕЛОВЕКА | 2011 |
|
RU2477314C1 |
| ИНСЕКТИЦИДНЫЕ БЕЛКИ, ВЫДЕЛЕННЫЕ ИЗ ВИДОВ БАКТЕРИЙ Bacillus, И ИХ ПРИМЕНЕНИЕ | 2004 |
|
RU2382822C2 |
| ПОЛИПЕПТИДЫ С ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ И КОДИРУЮЩИЕ ИХ ПОЛИНУКЛЕОТИДЫ | 2005 |
|
RU2393224C2 |
| СПОСОБЫ УСИЛЕНИЯ ДЕГРАДАЦИИ ИЛИ ПРЕВРАЩЕНИЯ ЦЕЛЛЮЛОЗНОГО МАТЕРИАЛА | 2006 |
|
RU2441912C2 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА pAd-SM, КОДИРУЮЩАЯ БЕЛКИ SOX2 И C-MYC ЧЕЛОВЕКА, ЯВЛЯЮЩАЯСЯ ОСНОВОЙ ДЛЯ ПОЛУЧЕНИЯ ВИРУЛЕНТНЫХ АДЕНОВИРУСОВ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ПОЛУЧЕНИЯ ИНДУЦИРОВАННЫХ ПЛЮРИПОТЕНТНЫХ КЛЕТОК ЧЕЛОВЕКА | 2012 |
|
RU2495127C2 |
| МОДУЛЯЦИЯ УРОВНЯ ПРЕДШЕСТВЕННИКОВ АРОМАТА КОФЕ В СЫРЫХ (НЕОБЖАРЕННЫХ) КОФЕЙНЫХ ЗЕРНАХ | 2004 |
|
RU2348693C2 |
Изобретение относится к области биотехнологии, к защитным генам растений, кодирующим биологически активные пептиды с антифунгальной активностью. Изобретение решает задачу расширения ассортимента защитных генов растений, доступных для использования в сельскохозяйственной биотехнологии с целью создания устойчивости культурных растений к факторам внешней среды за счет структуры новой нуклеотидной последовательности sm-amp, кодирующей антифунгальные пептиды звездчатки Stellaria media.
Нуклеотидная последовательность, кодирующая антифунгальные пептиды звездчатки Slellaria media':
5'-X1ATААACATАААССТТАСАТАСААAAGCTAGTCACАХ2AAAААТСАAGTGAAAATGTTGAACATGAAGAGCTTTGCACTTX3TTATGCTATTCGCCACCCTAGTAGGGGTGACAATAGCATX4CGX5CCX6AATGGCX7AGTGТGGТСХ8ТХ9GGТХ10АТGТСGТGХ11СGGХ12СХ13GТGТТGСТСССААТATGGATATTGTGGTTC AGGCX14CTAAGTACTGX15GCCCACAACACTCCTCTTTCTGAGATTGAGCCTACTGX16CGCX17GGCCX18GTGTX19TX20CGCGGAAX21ATGTAGTGGTGGGCX22TTGTTGCTCCAAATATGGATATTGTGGGAX23GGCCCTGCGTACTGCGGACTAGGCATGTGCCAGGGCAGCTGTGCCTGATATGCCTAATCACCCAGCTCAGATCCAAGCTCGGACTGAAGCTGCTCAGGCTGAAGCTCAGGCTGAGGCTTATAACCAX24GCAAATGAAGCTGCTCAAGTTGAGGCTTATTAX25CAGX26GCTCAGACACAGGCTCAACCTCAGGTTGAGCCTGCTGTX27ACCAAAGCTCCTTGAAAGCTGGCX28TAX29CTATGGGTTACGTGGCAAATAAACTTTGCTGGTTAATTGTAGTTAATTAGX30TTCAAGGTTAAATCGATTGCATGCATGTTAGTACGX31TAGATAGATGGTTAAATAAGTTATGC ATGC AAGTGTX32CTTTGX33TTATX34TTTTGTTX35GTCATTTTCCTTTAX36TGTAATAGX37TCGATCGTATTTCX38ATCATAX39ACAAGTCTAX40GGAATGAAATAAAGAGTGCCACX41TTX42TX43AAAAAAAAAAAAAAAAAAAAАХ44-3',
где X1 отсутствует (у sm-amp-1) или=АТС (sm-amp-2), Х2=А (sm-amp-1) или СТ (sm-amp-2), Х3=С (sm-amp-2) или G (sm-amp-1), Х4=А (sm-amp-2) или С (sm-amp-1), Х5=АС (sm-amp-2) или GT (sm-amp-1), Х6=А (sm-amp-2) или С (sm-amp-1), Х7=А (sm-amp-2) или С (sm-amp-1), X8=CGGGC (sm-amp-1) или GTCAG (sm-amp-2), X9=AT (sm-amp-2) или GG (sm-amp-1), Х10=АА (sm-amp-2) или GG (sm-amp-1), Х11=С (sm-amp-2) или G (sm-amp-1), X12=A (sm-amp-2) или G (sm-amp-1), X13=A (sm-amp-2) или T (sm-amp-1), X14=C (sm-amp-1) или T (sm-amp-2), X15=C (sm-amp-1) или T (sm-amp-2), X16=A (sm-amp-1) или С (sm-amp-2), X17=A (sm-amp-2) или T (sm-amp-1), X18=A (sm-amp-2) или G (sm-amp-1), X19=AG (sm-amp-1) или ТА (sm-amp-2), X20 отсутствует (sm-amp-2) или =GGA (sm-amp-1), X21=C (sm-amp-1) или G (sm-amp-2), X22=G (sm-amp-1) или T (sm-amp-2), X23=CT (sm-amp-1) или GC (sm-amp-2), X24=A (sm-amp-2) или G (sm-amp-1), X25=C (sm-amp-2) или T (sm-amp-1), X26 отсутствует (sm-amp-2) или =GCAACTCAG (sm-amp-1), X27=C (sm-amp-2) или T (sm-amp-1), X28=A (sm-amp-2) или G (sm-amp-1), X29=A (sm-amp-1) или G (sm-amp-2), X30 отсутствует (sm-amp-1) или =T (sm-amp-2), X31 отсутствует (sm-amp-2) или =TAGATAC (sm-amp-1), X32=A (sm-amp-2) или G (sm-amp-1), X33=C (sm-amp-1) или T (sm-amp-2), X34=C (sm-amp-2) или G (sm-amp-1), X35=C (sm-amp-1) или T (sm-amp-2), X36=A (sm-amp-1) или С (sm-amp-2), X37=A (sm-amp-2) или С (sm-amp-1), X38=A (sm-amp-1) или G (sm-amp-2), X39=A (sm-amp-1) или С (sm-amp-2), X40=C (sm-amp-2) или T (sm-amp-1), X41=C (sm-amp-2) или G (sm-amp-1), X42=CAT (sm-amp-1) или ТСA (sm-amp-2), X43=A (sm-amp-1) или G (sm-amp-2), X44 отсутствует (sm-amp-2) или =AAAAA (sm-amp-1).
| ПЕПТИД, ОБЛАДАЮЩИЙ АНТИФУНГАЛЬНОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2352580C1 |
| Shukurov R.R | |||
| et al | |||
| Increase of Resistance of Arabidopsis thaliana Plants to Phytopathogenic Fungi Expressing Hevein-like Peptides from Weed Plant Stellaria media | |||
| Russian Agricultural Sciences, 2010, Vol.36, No | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Broekaert WF et al | |||
| Antimicrobial peptides from Amaranthus caudatus seeds with sequence homology | |||
Авторы
Даты
2012-07-27—Публикация
2011-01-21—Подача