ОБЛАСТЬ ТЕХНИКИ
Данный способ относится к подсчету, сегментации и идентификации объектов, таких как частицы вирусов, изображенных на изображении, таком как электронная микрофотография.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
В прошлом было сделано множество попыток классифицировать и анализировать структуры клеток, которые содержат вирусы и другие компоненты. Для описания, сегментации и классификации вирусов были разработаны различные методы анализа изображений, в которых использовалась доступная технология получения изображений. Например, использовалась низкотемпературная электронная микроскопия, но она не достаточно хорошо показывала структуры клеток и частиц вирусов. Также оказалось сложно объективно, повторяемо и надежно описать компоненты клеток, чтобы точно определить стадию зрелости компонентов клеток.
Конкретнее, упорядочение структуры вируса представляет собой сложный процесс и является предметом интенсивного изучения. Вирусы используют клетку-хозяина, чтобы создавать свои вторичные вирусные частицы, подвергаясь сложному процессу созревания и внутриклеточного переноса. Этот процесс можно наблюдать при высоком увеличении с использованием электронного микроскопа, что позволяет визуально дифференцировать различные типы вирусных частиц в различных клеточных компартментах. К важным вопросам, еще требующим решения, относятся идентификация протеинов вирусов, которые участвуют на каждом шаге процесса упорядочения структуры вируса, а также механизм, лежащий в основе внутриклеточной транслокации и локализации различных типов вирусных частиц во время созревания вируса. К структурным аспектам созревания вируса в общем случае трудно подойти, хотя такие методы визуализации, как томография и низкотемпературные электронные микроскопы, внесли свой вклад в обширную информацию о структурах вирусов. Данные методы дают информацию о стабильных и часто зрелых вирусных частицах. Имеются генетические инструменты, чтобы создать мутанты основных компонентов белка вируса, и структурные эффекты можно наблюдать с помощью электронного микроскопа (ЭМ). Однако отсутствуют необходимые инструменты для характеристики структурных эффектов, в особенности промежуточных и неясных форм частиц, и для их правильного и объективного количественного описания.
Это частично объясняет, почему предшествующие способы анализа не были очень эффективными, и возникает потребность в более эффективных способах анализа структуры клетки и вирусных частиц. Возникает потребность в инструментах для анализа изображений, чтобы характеризовать и количественно описывать созревание вирусной частицы и внутриклеточный перенос с целью облегчить объективное изучение различных состояний упорядочения структуры вируса. Также имеется потребность в эффективном способе идентификации и количественного описания вирусных частиц, видимых на изображении.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ДАННОГО ИЗОБРЕТЕНИЯ
Способ, предложенный в данном изобретении, дает решение обозначенных выше проблем. Этот способ можно использовать для внутриклеточного подсчета и сегментации вирусных частиц на изображениях, таких как электронные микрофотографии. Создается изображение, на котором имеется множество объектов. Идентифицируются все круглые и эллиптические объекты на изображении. Круглые и эллиптические объекты разделяются на группы. Определяется профиль плотности по радиусу для круглых частиц. Также определяются эллиптические объекты, которые могут быть сформированы при заданном профиле плотности по радиусу круглых вирусных частиц. Вирусные частицы идентифицируются среди групп рассортированных круглых и эллиптических объектов путем анализа профилей плотности по радиусу объектов в отобранной группе. Например, данный способ можно использовать для внутриклеточного подсчета и сегментации частиц цитомегаловируса человека, обработанных si-PHK, на просвечивающих микрофотографиях.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1А - схематический пример изображения (А), инвариантного относительного вращения;
Фиг.1В - схематический пример изображения (В), инвариантного относительного угла;
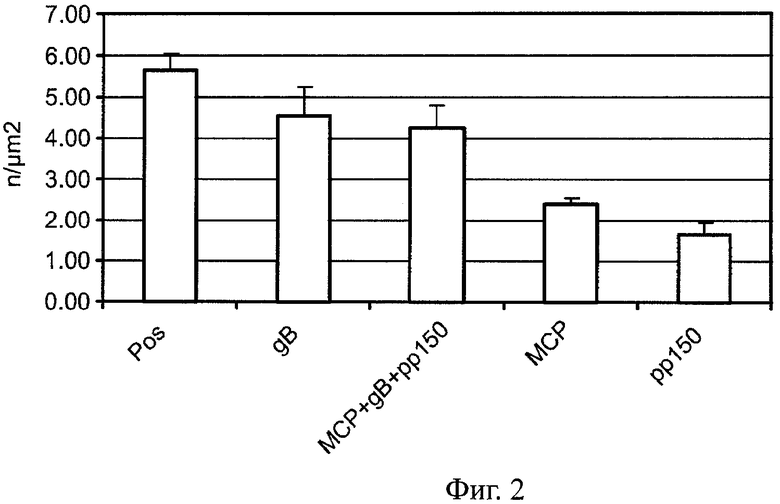
Фиг.2 - графическая иллюстрация измерений плотности для пяти множеств изображений;
Фиг.3 - схематический вид профилей плотности по радиусу от всех множеств изображений, помещенных в ЛПВ (линейное векторное пространство);
Фиг.4 - схематическое изображение усредненных профилей по радиусу со стандартным отклонением, показанным штрихпунктирными линиями вокруг среднего, для подмножества А;
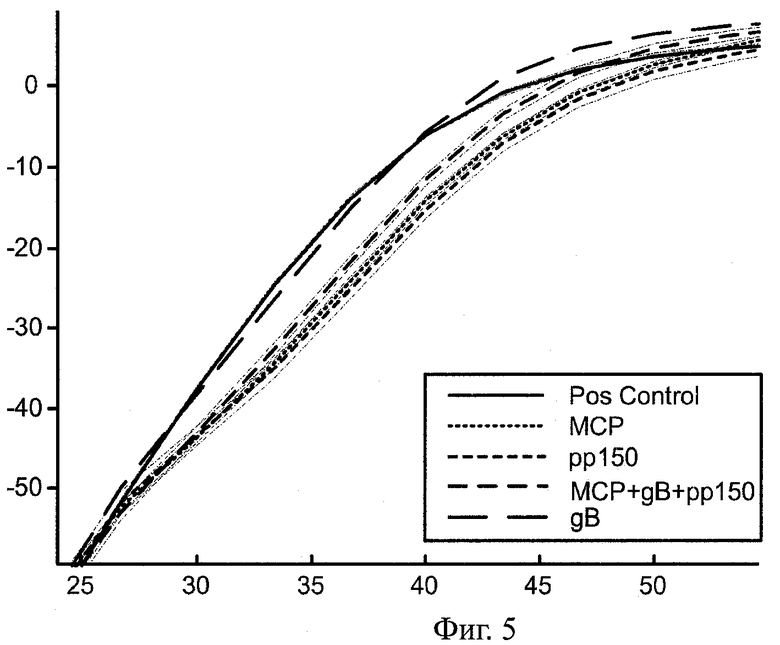
Фиг.5 - схематическое изображение усредненных профилей по радиусу со стандартным отклонением, показанным штрихпунктирными линиями вокруг среднего, для подмножества В; и
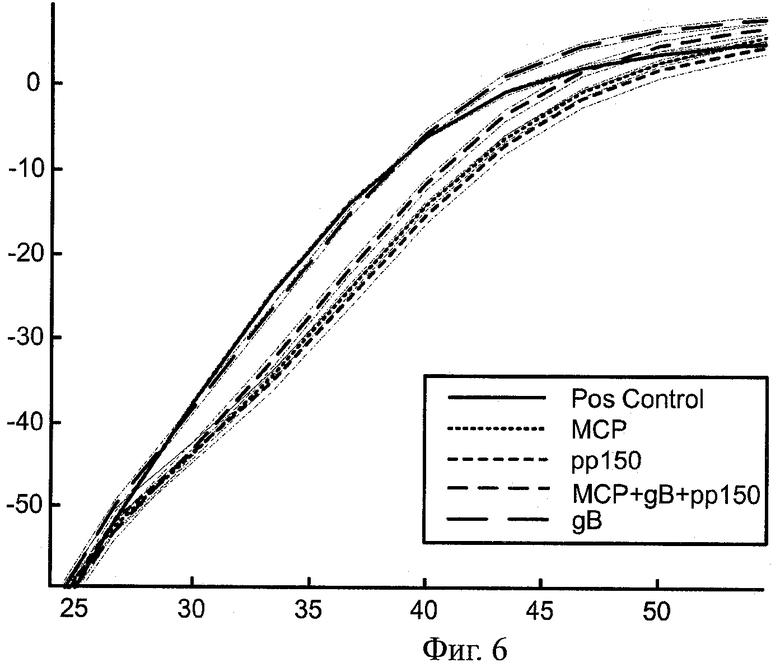
Фиг.6 - схематическое изображение крупным планом Фиг.5 при значениях радиуса между 30 и 40 нм.
ПОДРОБНОЕ ОПИСАНИЕ
Способ, предлагаемый в данном изобретении, можно использовать для поиска, сегментации и идентификации частиц/объектов на изображениях, таких как объекты, изображенные на просвечивающих электронных микрофотографиях. Идентифицированные объекты на изображениях могут относиться к вирусным частицам и другим частицам, которые имеют круглую или эллиптическую форму. Эллиптические формы можно определить как имеющие максимальный радиус и минимальный радиус, в то время, как совершенно круглые формы имеют один радиус каждая. Предпочтительно, чтобы данный способ определял, какие объекты эллиптической формы могут быть сформированы в диапазоне радиусов анализируемых вирусных частиц. Например, если вирусная частица имеет радиус 100 единиц, то максимальный радиус и минимальный радиус эллиптических форм может быть, например, на 20% больше (т.е. 120 единиц) и на 20% меньше (т.е. 80 единиц), чем радиус вирусной частицы, когда эта вирусная частица круглая. Если максимальный радиус или минимальный радиус находятся вне допустимого диапазона радиусов, то данный объект будет считаться неприемлемым и не будет идентифицирован как вирусная частица. Затем круглые и эллиптические формы сортируются и группируются таким образом, что одинаковые диапазоны радиусов относятся к одной группе. Затем в объединенных в группы формах объектов идентифицируются и количественно описываются вирусные частицы. Также возможно идентифицировать вирусные частицы, которые находятся между двумя различными стадиями зрелости, т.е. которые находятся в стадии зрелости, которая находится между двумя различными группами зрелости. Вирусные частицы могут иметь заданный заранее профиль плотности по радиусу, и математическое уравнение, такое как преобразование Фурье, можно использовать для того, чтобы определить, какие объекты эллиптической формы являются вирусными частицами, на основании заданного заранее профиля плотности по радиусу, который является типичным для вирусных частиц. В предпочтительном случае отсутствует необходимость использовать инструкции, в которых изображены профили плотности по радиусу вирусных частиц на определенных стадиях зрелости, поскольку поврежденные вирусные частицы или вирусные частицы, которые находятся между двумя различными стадиями зрелости, приведенных в инструкции, могут быть не обнаружены при использовании инструкции.
Может оказаться возможным определить распределение диапазонов радиусов или профилей плотности по радиусу в группах, как показано на Фиг.3 и подробно описано ниже. Также, как будет описано ниже, вирусные частицы могут быть подвергнуты воздействию химического вещества, такого как фармацевтический препарат, и шаги данного способа, согласно данному изобретению, могут быть выполнены снова на основе видоизмененного изображения для того, чтобы определить, как изменилось распределение размеров частиц или профили плотности по радиусу в результате воздействия химического вещества или лечения. Таким образом, становится возможным определить эффективность воздействия химического вещества на вирусные частицы.
Также становится возможным использовать метод si-PHK для того, чтобы заблокировать некоторые строительные блоки, например, путем повреждения протеинов рр150 и блокирования создания частиц ЦМВ внутри вирусных частиц. После подобной обработки si-PHK можно проанализировать воздействие на вирусные частицы и морфологические/структурные изменения вирусных частиц. Кроме того, также можно изучать количество поврежденных вирусных частиц.
Также оказывается возможным использовать способ, предложенный в данном изобретении, для того, чтобы идентифицировать вирусные частицы путем анализа профилей плотности по радиусу и решить, какие вирусные частицы имеются на изображении. После обнаружения всех круглых и эллиптических объектов на изображении и распределения объектов по группам на основе их радиальных характеристик следующим шагом может быть идентификация радиальных характеристик конкретной вирусной частицы. Любая группа объектов с радиальными характеристиками, находящимися внутри заданного диапазона радиусов вирусной частицы, например внутри диапазона радиусов, равного 80±3 единицы, может, таким образом, использоваться для идентификации вирусных частиц. Благодаря использованию диапазона радиальных характеристик также могут быть включены деформированные или эллиптические частицы. Частицы, имеющие радиусы вне допустимого диапазона, исключаются и классифицируются как не являющиеся вирусными частицами. Если внутри требуемого интервала радиусов имеется много типов вирусных частиц, становится возможным воздействовать на эти вирусные частицы химическим или медицинскими препаратами, а затем снова использовать указанный способ, чтобы определить, как вирусные частицы реагируют на воздействие. На основании этой реакции становится возможным опознать, что представляет собой данная вирусная частица. Например, становится возможным увеличить число копий ДНК, например, используя методы PCR (полимеразная цепная реакция), что создает эталонное описание, которое можно использовать для идентификации вирусной частицы. Таким образом, можно использовать дополнительное испытание, чтобы проверить или подтвердить идентификацию вирусной частицы.
Таким образом, способ, предлагаемый в данном изобретении, можно использовать для поиска, сегментации и идентификации вирусных частиц на просвечивающих электронных микрофотографиях, как будет подробно описано ниже. Капсиды вирусных частиц являются приблизительно круглыми объектами с одинаковой плотностью протеинов на фиксированных радиусах от центра, так называемыми объектами, инвариантными относительно вращения, что лучше всего показано на Фиг.1А. Для того чтобы создать меру инвариантности относительно вращения, требуется наличие "противоположной" характеристики, с которой можно сравнить инвариантность относительно вращения. Объект, обладающий инвариантностью относительно угла, может быть использован для этой цели, поскольку он имеет одинаковую плотность протеина при фиксированном угле от центра, что лучше всего показано на Фиг.1В.
Спектр Фурье функции (f), значения которой определяются радиусом r, с соответствующей частотой Фурье (wr), от центра, и углом (t), с соответствующей частотой Фурье (wt), взятым от любого фиксированного направления наружу от центра, может служить иллюстрацией объекта, обладающего инвариантностью относительно вращения, и объекта, обладающего инвариантностью относительно угла. Функция, обладающая полной инвариантностью относительно вращения, содержит всю энергию при wt=0; а объект, обладающий полной инвариантностью относительно угла, содержит всю свою энергию при wr=0; все объекты, расположенные между ними, содержат энергию в обоих частотных диапазонах. Таким образом, достаточно хорошей мерой является сравнение разности этих энергий, что дает априорную меру с пороговым уровнем этой меры, который является единственной неизвестной константой, которая может быть получена путем отрицательного контроля.
Мера плотности вирусных структур на просвечивающих электронных микрофотографиях будет описана ниже. Мера плотности, предназначенная для сравнения количества вирусных структур на различных изображениях, вводится как некоторое количество объектов (n) на единицу площади А изображения.
d=n/A
Сегментация различных вирусных структур будет описана ниже. Профиль плотности по радиусу каждого обнаруженного объекта/частицы служит в качестве хорошего приближения вирусной частицы. Помещение профилей в линейное векторное пространство (ЛВП) с основанием, связанным с главными осями профилей, вычисленными при помощи разложения по сингулярным значениям (РСЗ), дает визуальное понимание того, как ведут себя группы различных вирусных структур. Используя эту информацию, возможно выделить различные группы и подсчитать по отдельности и выделить структурные различия при использовании лекарственных препаратов путем вычисления усредненной структуры в каждом множестве изображений.
Приблизительно 500 Мбайт изображений, как показано в приведенной ниже Таблице 1, инфицированных клеток при использовании четырех различных siPHK. были получены при помощи электронного микроскопа при разрешении 3,3 нм/пиксел. Это изображение обрабатывалось при помощи меры инвариантности относительно вращения. Контрольный радиус для инвариантности относительно вращения был установлен равным 15 пикселов (около 50 нм), и объекты на изображении получались при локальных максимумах радиусов, равных 15 пикселам, а мера инвариантности по радиусу превышала уровень, равный 15. При получении профилей плотности по радиусу среднее каждого профиля исключалось для того, чтобы компенсировать различие в уровнях яркости на различных изображения. Среднее бралось по радиусу, равному 100 пикселей, т.е. около 330 нм.
В Таблице 2 приведены средние значения и стандартные отклонения среднего для вычисленных плотностей. Сравнение результатов, полученных с использованием изображений рр150 и МСР, с положительным контролем посредством t-критерия Стьюдента, дает значения р, равные 7,21·10-13 и 2,19·10-11 соответственно, которые позволяют отклонить гипотезу о том, что плотности получены из распределений с равным средним.
Фиг.2 представляет собой графическую иллюстрацию измерений плотности для пяти множеств изображений (Положительный контроль, МСР, gB, MCP+gB+pp150 и рр150) с одним стандартным отклонением. МСР и рр150 показывают значительно меньшие плотности, чем положительный контроль.
Сегментация вирусных структур описывается ниже. Профили плотности по радиусу были построены в ЛВП, что лучше всего показано на Фиг.3, на которой показана информация по двум основным осям. На Фиг.3 показаны профили плотности по радиусу для всех множеств изображений, помещенных в ЛВП. На изображении видны две значительно отделенные друг от друга группы, обозначенные А и В, которые будут описаны подробнее ниже. Важной отличительной чертой является то, что также показаны частицы между двумя группами. Например, эти частицы могут быть на таких стадиях зрелости, которые находятся между стадиями зрелости, представленными скоплениями. Часто особенно важно изучать частицы, находящиеся между скоплениями или группами частиц, когда вирусные частицы подверглись воздействию фармацевтического препарата, с тем, чтобы можно было определить влияние этого препарата.
Усредненные профили плотности по радиусу для каждого множества (положительный контроль, МСР, рр150, gB и MCP+gB+pp150) для скопления А показаны на Фиг.4. Это раскрывает общеизвестную классификацию А (пустые оболочки вирусов) промежуточных форм зрелости НСМV(ЦМВЧ). Вследствие того, что количество обнаруженных объектов данного типа мало, объекты имеют малые энергии как по радиусу, так и по углу, и во множестве присутствует большое количество невирусных структур, невозможно получить значимую информацию помимо информации о том, что стенка капсиды расположена приблизительно на расстоянии 40 нм от центра.
Усредненные профили плотности по радиусу для каждого множества (положительный контроль, МСР, рр150, gB и MCP+gB+pp150) для скопления В показаны на Фиг.5. Это раскрывает общеизвестные классификации В (капсиды с полупрозрачным ядром) и С (зрелые капсиды с плотным ядром) промежуточных форм зрелости НСМV(ЦМВЧ). Множества, относящиеся к положительному контролю и gB, отличаются от множеств, относящихся к МСР, рр150 и MCP+gB+pp150, при радиусах, находящихся между 30 и 40 нм, что лучше всего показано в начальной и конечной зонах Фиг.6 и в центре.
Как следствие этого, возможно разработать модель вирусных частиц на просвечивающих электронных микрофотографиях. Использование характеристики, инвариантной относительно угла, в качестве меры для сравнения с характеристикой, инвариантной относительно вращения, можно заменить отношением энергии функции, которую можно описать объектом, инвариантным относительно вращения, к полной энергии. Однако если полная энергия очень мала, то это отношение может стать при расчетах численно нестабильным.
Чтобы решить эту проблему, можно использовать пороговый уровень. Использование заданного порогового уровня является источником субъективности. Однако на этом уровне было подсчитано очень мало ложных структур. Но при этом группа отрицательного контроля могла бы служить для установки порогового уровня, а также чтобы увидеть воздействие молекул siPHK.
Любое ортогональное преобразование профилей плотности, включая главные оси, сохраняет расстояние и скалярное произведение в линейном векторном пространстве L2. Следовательно, группирование различных подструктур происходит независимо относительно выбора базиса.
Пример
Ниже описывается пример материалов и способов, которые можно использовать. Легочные фибробласты эмбриона человека (HF) выдерживались в несодержащей бикарбонатов минимальной основной среде с солями Хенка (Hank′s salts) (GIBCO BRL), дополненной 25 мМ HEPES [4-(2 гидроксиэтил)-1-пиперазин этансульфоновая кислота], 10% инактивированной теплом эмбриональной сывороткой теленка, L-глютамином (2 мМ), пенициллином (100 U/мл) и стрептомицином (100 мг/мл) (GIBCO BRL, Гранд Айлэнд, Нью-Йорк, США). Клетки выращивались в колбах с тканевой культурой площадью 175 см2 (Корнинг, Нью-Йорк, США) и использовались максимально за 17 переносов. Клетки инфицировались цитомегаловирусом человека (HCMV) при кратности инфицирования (MOI), равной 1. Содержащая вирус надосадочная жидкость собралась на 7 или 10 день после инфицирования. Затем содержащая вирус надосадочная жидкость очищалась от остатков клеток путем центрифугирования на малой скорости и замораживалась при -70°С до момента ее использования. Монослои легочных фибропласт человека (HF), выращенные на пластинах с 96 чашками или на предметных стеклах с лунками, инфицировались штаммом AD169 вируса HCMV с кратностью инфицирования, равной 1.
Клетки эндотелия легочной артерии человека (НРАЕС) были получены из Clonetics, Калифорния, США. Клетки выдерживались в ЕВМ-2 (Clonetics, Калифорния, США) с факторами роста при 37°С и 5% содержании СО2. За один час до инфицирования среда изменялась на ЕВМ, содержащую 5% эмбриональной сыворотки теленка, и клетки выращивались в этой среде во время всего процесса инфицирования. Клетки выращивались в покрытых 0,2% желатином колбах с тканевой культурой площадью 175 см2 (Falcon) или на предметных стеклах с 8 лунками (Nalge Nunc International) и использовались в экспериментах до восьмого переноса.
Клетки эндотелия аллантоисной вены человека (HUVEC) выращивались в среде EGM (Clonetics, Калифорния, США). За один час до инфицирования среда изменялась на ЕВМ, содержащую 5% эмбриональной сыворотки теленка, и клетки выращивались в этой среде во время процесса инфицирования. Клетки выращивались в колбах с тканевой культурой площадью 175 см2 (Falcon) и на предметных стеклах с 8 лунками (Nalge Nunc International) и использовались в экспериментах до восьмого переноса. Затем клетки инфицировались штаммом ТВ 40, предназначенным для эндотелия, при кратности инфицирования, равной 1.
Клетки гладких мышц выделялись из аортальных трансплантатов, получаемых от пациентов, перенесших хирургическую операцию по поводу аневризмы аорты со вставкой аортального трансплантата, или из аортальных трансплантатов или трансплантатов подвздошных сосудов, взятых от доноров трансплантатов. Клетки выделялись путем первоначального удаления клеток эндотелия путем соскабливания клеток острым инструментом. Затем сосуд разделялся на два различных слоя, внутренний слой (соответствующий внутренней выстилке сосуда) и наружный слой (соответствующий промежуточному слою сосуда), путем осторожного разделения двух сосудов при помощи пинцета. Аортальный трансплантат разделялся на мелкие кусочки по 1 мм и выращивался в чашках для культивирования клеток в среде SMGM 2 (Clonetics) с добавлением SmGM-2 Single Quotes (hEGF 0,5 мкг/мл, 0,5 мл; инсулин 5 мг/мл, 0,5 мл; hFGF-b - 1 мкг/мл, 1 мл; FBS 25 мл; GA-1000, 0,5 мл) приблизительно в течение двух недель до тех пор, пока не начиналась миграция клеток гладких мышц с эксплантата. Клетки выращивались в колбах с тканевой культурой площадью 175 см2 (Falcon). Для того, чтобы определить чистоту культуры SMC, клетки выращивались на предметных стеклах с лунками и фиксировались в 3% формальдегиде в течение 45 минут при 4°С и становились проницаемыми после обработок в 0,3% растворе Triton X в течение 5 минут. После фиксации клетки окрашивались для выявления конъюгированного FITC анти-актина, специфического для клеток гладких мышц (SIGMA), и оценивать при помощи флуоресцентной микроскопии. Клетки фиксировались смесью метанола и ацетона (1:1) при 4°С в течение 5 минут и окрашивались при помощи конъюгированного FITC анти-фактора фон Виллебранда (Anti-vWF) и специфического для клеток эндотелия фактора фон Виллебранда и оценивать при помощи флуоресцентной микроскопии. В экспериментах использовался контроль изотипов для антител. Культуры были на 100% положительными по отношению к анти а-актину и отрицательны по отношению к фактору фон Виллебранда.
Для того чтобы изучить с помощью электронного микроскопа инфицированные вирусом клетки, неинфицированные клетки и клетки, инфицированные цитомегаловирусом человека (кратность инфицирования равна 1), собирались на 3, 5, 7 и 10 дни после инфицирования и фиксировались в 2% глютаральдегиде в 0,1 М буфера из какодилата натрия, содержащего 0,1 М сахарозы и 3 mM CaCl2, с рН 7,4 при комнатной температуре в течение 30 минут. Затем эти клетки соскабливались при помощи деревянной палочки и переносились в пробку Эппендорфа и далее фиксировались в течение ночи в холодильнике. После фиксации клетки промывались в буферном растворе 0,15 М какодилата натрия, содержащем 3 mM CaCl2, при рН 7,4 и центрифугировались. Затем гранулы вторично фиксировались в 2% тетроксиде осмия, растворенного в 0,07М буферного раствора какодилата натрия, содержащего 1,5 mМ CaCl2, с рН 7,4 при 4°С в течение двух часов, дегидратировались последовательно в эталоне и ацетоне и заделывались в LX-112 (Ледд, Берлингтон, Вермонт, США). Контраст на препаратах достигался посредством уранилацетата с последующим использованием цитрата свинца, а исследование проводилось на просвечивающем электронном микроскопе Tecnai 10 (FEI, Нидерланды) при 80 кВ. Цифровое изображение выполнялось цифровой камерой Mega View II (Soft Imaging System, GmbH, Мюнстер, Германия).
Обработка электронных микрофотографий описывается ниже. Контраст на препаратах достигался посредством уранилацетата с последующим использованием цитрата свинца, а исследование проводилось на просвечивающем электронном микроскопе Tecnai 10 (FEI, Нидерланды) при 80 кВ. Цифровое изображение выполнялось цифровой камерой Mega View II (Soft Imaging System, GmbH, Мюнстер, Германия) или электронные микрофотографии выполнялись, проявлялись и сканировались для оцифровки. Микрофотографии оцифровывались в 8-битовые изображения при помощи сканера с плоским основанием HP ScanJet 6200C с размерами пикселей, равными либо 2×2 нм, либо 3×3 нм, что соответствует радиусам капсид, приблизительно равным 25 или 17 пикселей соответственно, на оцифрованных микрофотографиях. Каждое оцифрованное изображение имеет размер, приблизительно равный 1000×1000 пикселей (1М байт). Разрешение было достаточным, чтобы различать три исследуемых здесь класса капсид, но сильно текстурированный фон делает задачу идентификации капсид очень сложной. Автоматизированное рабочее место DEC alpha 433, выполняющее программу Нр Tru64 UNIX, использовалось для разработки и оценки способа, предложенного в данном изобретении. Реализация и испытания осуществлялись при помощи программного обеспечения Matlab 7.0.1 (the MathWorks, Inc., Нетик, Миннесота, США). Полученные цифры профилей уровней серого обрабатывались в Corel Draw 10 (Corel Corporation, Оттава, Канада) и Photoshop CS (Adobe Systems Inc, Сан-Хосе, Калифорния, США).
Хотя данное изобретение было описано в соответствии с предпочтительными составами и вариантами выполнения, следует понимать, что можно произвести в них некоторые замены и изменения, не выходя за пределы сущности объема следующих пунктов патентных притязаний.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИДЕНТИФИКАЦИЯ И КЛАССИФИКАЦИЯ ВИРУСНЫХ ЧАСТИЦ НА ТЕКСТУРИРОВАННЫХ ЭЛЕКТРОННЫХ МИКРОФОТОГРАФИЯХ | 2006 |
|
RU2409855C2 |
| КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЧАСТИЦЫ HCMV | 2008 |
|
RU2505314C2 |
| СПОСОБ АНАЛИЗА КЛЕТОЧНЫХ СТРУКТУР И ИХ КОМПОНЕНТОВ | 2006 |
|
RU2420593C2 |
| ВИРУСНАЯ ЧАСТИЦА, ВЫСВОБОЖДАЮЩАЯСЯ ПОСЛЕ ИНФИЦИРОВАНИЯ КЛЕТОК МЛЕКОПИТАЮЩИХ ЦИТОМЕГАЛОВИРУСОМ ЧЕЛОВЕКА (HCMV), СОДЕРЖАЩАЯ СЛИТЫЙ БЕЛОК, И ЕЕ ПРИМЕНЕНИЕ | 2011 |
|
RU2623172C2 |
| СТАБИЛИЗИРОВАННЫЕ КАПСИДЫ FMDV | 2014 |
|
RU2663004C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ЦИТОМЕГАЛОВИРУСА | 2012 |
|
RU2737530C1 |
| УСЛОВНО РЕПЛИЦИРУЮЩИЙСЯ ЦИТОМЕГАЛОВИРУС В КАЧЕСТВЕ ВАКЦИНЫ ПРОТИВ CMV | 2012 |
|
RU2670012C1 |
| СПОСОБЫ ДЕТЕКЦИИ АНТИЦИТОМЕГАЛОВИРУСНЫХ НЕЙТРАЛИЗУЮЩИХ АНТИТЕЛ | 2013 |
|
RU2660712C2 |
| ТЕСТ-СИСТЕМА ДЛЯ ОДНОВРЕМЕННОЙ ДЕТЕКЦИИ ГУМОРАЛЬНЫХ МАРКЕРОВ ИНФИЦИРОВАНИЯ ГЕРПЕСВИРУСАМИ ЧЕЛОВЕКА | 2019 |
|
RU2724897C1 |
| РОТАВИРУСНЫЕ ЧАСТИЦЫ С ХИМЕРНЫМИ ПОВЕРХНОСТНЫМИ БЕЛКАМИ | 2014 |
|
RU2698049C2 |



Изобретение относится к подсчету, сегментации и идентификации объектов. Техническим результатом является расширение функциональных возможностей за счет создания инструментов для характеристики структурных эффектов, в особенности промежуточных и неясных форм частиц, и для их правильного и объективного количественного описания. Данный способ предназначен для внутриклеточного подсчета и сегментации частиц вирусов на изображении. Создается изображение, на котором имеется множество объектов. Определяется диапазон радиусов частиц вирусов. Идентифицируются круглые объекты на изображении, радиус которых находится внутри определенного диапазона радиусов. Определяются эллиптические объекты, которые могут быть сформированы в заданном диапазоне радиусов. Сортируются круглые и эллиптические объекты, идентифицированные по группам. Идентифицируются частицы вирусов среди круглых и эллиптических объектов. Например, данный способ можно использовать для внутриклеточного подсчета и сегментации частиц цитомегаловируса человека, обработанных si-PHK, на просвечивающих электронных микрофотографиях. 3 з.п. ф-лы, 7 ил., 2 табл.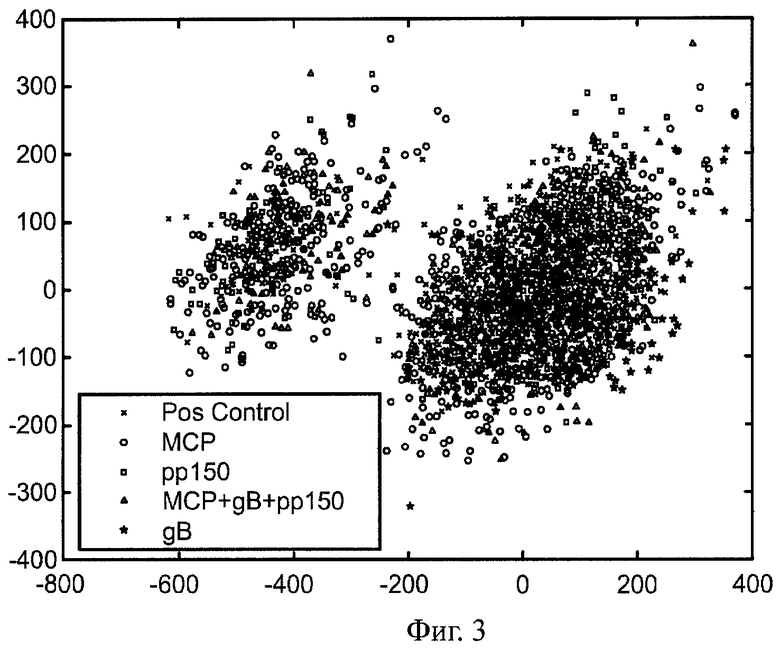
1. Способ внутриклеточного подсчета и сегментации вирусных частиц на изображении, содержащий:
создание изображения, на котором имеется множество объектов;
идентификацию круглых объектов на изображении;
сортировку идентифицированных круглых объектов по группам, имеющим одинаковые диапазоны радиусов;
определение распределения профилей плотности по радиусу для идентифицированных круглых объектов;
идентификацию эллиптических объектов, которые могут сформироваться при установленном распределении профилей плотности по радиусу;
сортировку идентифицированных эллиптических объектов по группам, имеющим одинаковые диапазоны радиусов; и
идентификацию вирусных частиц среди отсортированных круглых и эллиптических объектов на основе распределения профилей плотности по радиусу объектов в отобранной группе круглых и эллиптических объектов;
воздействие на вирусные частицы фармацевтическим препаратом;
сортировку вирусных частиц по группам после воздействия на них фармацевтическим препаратом;
анализ различий между распределением профилей плотности по радиусу у вирусных частиц до воздействия и распределением профилей плотности по радиусу у вирусных частиц после воздействия фармацевтическим препаратом.
2. Способ по п.1, содержащий, кроме того, анализ изменений в распределении размеров объектов на изображении в результате воздействия.
3. Способ по п.1, содержащий, кроме того, определение разности количества объектов в группе до и после воздействия химическим веществом.
4. Способ по п.1, содержащий, кроме того, анализ морфологических структур вирусных частиц.
| US 20050051725 А1, 10.03.2005 | |||
| US 20030201393 A1, 30.10.2003 | |||
| УСТРОЙСТВО ДЛЯ СЪЕМКИ ИЗОБРАЖЕНИЙ | 1998 |
|
RU2207626C2 |
| СПОСОБ СКАНИРОВАНИЯ РИСУНКА КОЖНЫХ ЛИНИЙ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2000 |
|
RU2168206C1 |
Авторы
Даты
2012-09-10—Публикация
2008-04-25—Подача