Изобретение относится к области органической химии и биотехнологии и может быть использовано при получении водорастворимых производных фуллеренов С60, с биологической активностью, в частности, для создания средств лечения заболеваний, связанных с окислительным стрессом (аллергия, астма, дерматиты, ишемические болезни), препаратов для фотодинамической терапии опухолей, радиопротекторов, антиоксидантных компонентов косметических средств и носителей для доставки лекарств в клетки.
Главная проблема в использовании фуллерена в медицине - его практически полная нерастворимость в водных средах - 0,02 нг/л [Ruoff R.S., Tse D.S., Malhotra R., Lorents D.C. Solubility of fullerene (C60) in a variety of solvents. J. Phys. Chem., 1993; 97: 3379-3383; Безмельницын В. H., Елецкий А. В., Окунь М. В. Фуллерены в растворах. Успехи физ. наук, 1998; 168: 1195-1120]. Среди множества способов решения этой проблемы выделяют три наиболее приемлемые пути: получение водных нанодисперсий кристаллического фуллерена, создание прочных комплексов с гидрофильными соединениями и введение гидрофильных групп в ядро (аддукты).
Большинство способов образования стабильных водных дисперсий фуллерена основано на переносе фуллерена из органического раствора (бензол, толуол, тетрагидрофуран) в водную фазу с применением ультразвука и постепенным удалением органического растворителя с помощью вакуума либо продувкой инертным газом [Deguchi Sh., Mukai S.-A. Top-down preparation of dispersions of C60 nanoparticles in organic solvents. Chemistry Letters, 2006; 35(4): 396-397; Andrievsky G.V., Kosevich M.V., Vovk О.M., Shelkovsky V.S., Vashcenko L.A. On the production of an aqueous colloidal solution of fullerenes. J. Chem. Soc, 1995; 12: 1281-1282]. В результате образуется стабильный коллоидный раствор желто-коричневого цвета, содержащий гидратированные кластеры из молекул С60, размер которых зависит от особенностей метода и колеблется в нанометровом диапазоне (25-500 нм).
Известно также получение водных дисперсий путем прямого механического диспергирования порошка фуллерита в водной среде очень длительное время [Labille J., Brant J.A., Villieras F., Pelletier M, Wiesner M.R., Bottero J.-Y. Affinity of C60 fullerenes with water. Fullerenes, Nanotubes, and Carbon Nanostructures, 2006,
14(2-3):307-314].
Такие дисперсии в различных публикациях обозначаются по-разному: nC60, нано-C60, C60FWS, С60@{H2O}n, микронизированный фуллерен, молекулярно-коллоидный фуллерен (МКФ), гидратированный фуллерен (ГФ или HyFn). Наличие отрицательного заряда на поверхности кластеров играет важную роль в стабилизации водных дисперсий фуллерена. Поскольку фуллереновые наночастицы в водных дисперсиях несут слабый заряд, они легко агрегируют при изменении рН и ионной силы среды. Свойства таких дисперсий (размер частиц, стабильность, рН коагуляции и др.) сильно зависят от метода их приготовления, их нельзя высушивать, сроки хранения дисперсий неизвестны (возникают проблемы со стандартизацией) и их стоимость достаточно высока. Как исходный продукт для получения аддуктов фуллерена они малопригодны из-за высокой стоимости их изготовления, низкой концентрации фуллереновых частиц и склонности к коагуляции при изменении среды.
Для образования комплексов с гидрофильными веществами, как правило, используют циклодекстрины (ЦД, циклические сахара, состоящие из 6-8 остатков глюкозы). Так, фуллерен переходит в раствор при кипячении кристаллов фуллерита с водным раствором γ-циклодекстрина с преимущественным мольным соотношением С60:ЦД=1:2. Фуллерен внутри комплекса находится в свободной и гидратированной формах. Хотя такой комплекс можно подвергать гель-хроматографии, он все же будет медленно распадаться. Т.е. стабильность таких комплексов недостаточна для длительных манипуляций, и в среде всегда будут находиться в равновесном состоянии свободные компоненты [Andersson Т., Nilsson К., Sundahl М., Westman G., Wennerström О. C60 embedded in γ-cyclodextrin: a water-soluble fullerene. J. Chem. Soc, Chem. Commun., 1992; 604-605]. Комплексы подобного типа формируют также каликсарены и другие «корзиноподобные» соединения [Пиотровский Л.Б., Киселев О.И. Фуллерены в биологии. СПб: Росток; 2006].
Из амфифильных полимеров, способных образовывать водорастворимые нековалентные ассоциаты с С60, наиболее популярен биосовместимый полимер поливинилпирролидон (ПВП). Растворы фуллерена в поливинилпирролидоне имеют коричневый цвет, а содержание фуллерена в них достигает 0,5-1% в зависимости от молекулярной массы ПВП [Yamakoshi Y.N., Yagami Т., Fukuhara К., Sueyoshi S., Miyata N. Solubilization of fullerenes into water with polyvinylpyrrolidone applicable to biological tests. J. Chem. Soc. Chem. Commun., 1994; 517-518; Пиотровский Л.Б., Киселев О.И. Фуллерены в биологии. СПб: Росток; 2006]. Для повышения растворимости фуллерена также используют водорастворимые белки.
Комплексы фуллерена с липосомами имеют упорядоченную стабильную структуру и привлекательны как средство для доставки препаратов в клетки и как трансмембранный якорь. Комбинация фуллеренов и липидных мембран образует комплексы в виде стабильных монослойных пленок, обладающих интересными электрохимическими эффектами [Nakanishi Т., Ariga К., Morita М., Kozai Н., Taniguchi N., Murakami Н., Sagara Т., Nakashima N. Electrochemistry of fullerene C60 embedded in Langmuir-Blodgett films of artificial lipids on electrodes. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2006; 284-285: 607-612]. [Braun et al. 2000].
Однако прочность нековалентных комплексов (ассоциатов) фуллерена сильно зависит от среды, в которой они находятся, такие продукты не являются индивидуальными веществами, поэтому применение их как исходных реагентов для получения широкого спектра водорастворимых аддуктов фуллерена неприемлемо.
Более универсальный и широко применяемый метод солюбилизации фуллерена - его химическая модификация гидрофильными соединениями. Фуллерен содержит 30 слабосопряженных двойных связей и ведет себя как электронодефицитный полиолефин, поэтому основным типом его химических превращений являются реакции по двойной связи - реакции нуклеофильного и радикального присоединения (циклоприсоединения). Такие реакции очень удобны для функционализации фуллерена. Большинство образующихся в результате этих процессов аддуктов имеют достаточную стабильность и это позволяет применять дальнейшие химические модификации для создания новых биологически активных веществ.
Наиболее известными реакциями в химии фуллерена являются реакции циклоприсоединения, известного в органической химии как диеновый синтез Дильса-Альдера, где С60 всегда выступает в роли диенофила [Юровская М.А. Методы получения производных фуллерена С60. Соросовский образовательный журнал, 2000; 5:26-30; Сидоров Л.Н., Юровская М.А., Борщевский А.Я. Трушков И.В., Иоффе И.Н. Фуллерены (учебное пособие для вузов), М: Экзамен; 2005]. Такие реакции позволяют вводить в ядро С60 практически любые функциональные группы. Множество разнообразных «диенов» протестировано в реакции взаимодействия с фуллереном и в большинстве случаев отмечено образование моноаддуктов.
Известны также реакции одностадийного присоединения первичных и вторичных аминов (Hirsch A., Li Q., Wudl F. Globe-trotting hydrogens on the surface of the fullerene compounds C60H6N[(CH2CH2)2O]6. Angew. Chem. Int. Ed., 1991). Такие реакции протекают достаточно сложно и идут по радикальному механизму, т.е. с образованием анион-радикалов, при этом реакция сопровождается присоединением кислорода. По такому же механизму протекают реакции прямого присоединения аминокислот и дипептидов к фуллерену (Романова В.С, Цыряпкин В.А., Ляховецкий Ю.А., Парнес З.Н., Вольпин М.Е. Присоединение аминокислот и дипептидов к фуллерену С60 с образованием моноаддуктов. Известия РАН, сер. химическая, 1994; 1154-1155). При этом имеет место введение в реакцию стерически незатрудненных аминов (линейных или циклических), в результате чего образуются продукты полиприсоединения. Поскольку для их получения используют природные аминокислоты, данный класс соединений фуллурена вполне физиологичен, и их низкая токсичность была подтверждена рядом биологических тестов [Масалова О.В., Шепелев А.В., Атанадзе С.Н., Парнес З.Н., Романова В.С, Вольпина О.М., Семилетов Ю.А., Кущ А.А. Иммуностимулирующее действие водорастворимых производных фуллерена - перспективных адъювантов для вакцин нового поколения. Докл. РАН, 1999; 369(3): 411-413; Меджидова М.Г., Абдуллаева М.В., Федорова Н.Е., Романова В.С, Кущ А.А. Противовирусная активность аминокислотных производных фуллерена при цитомегаловирусной инфекции in vitro. Антибиотики и химиотерапия, 2004; 49(8-9): 13-20, 8-10; Андреев С.М., Бабахин А.А., Петрухина А.О., Романова В.С, Парнес З.Н., Петров Р.В. Иммуногенные и аллергенные свойства конъюгатов фуллерена с аминокислотами и белком. Докл. РАН, 2000; 390(2): 261-264].
Главной проблемой синтеза водорастворимых аддуктов фуллерена с гидрофильными соединениями (аминокислоты, пептиды) является несовместимость по растворимости компонентов реакции: очень гидрофобного фуллерена и гидрофильных аминокислот. Фуллерен для растворения требует апротонной неполярной среды, а аминокислоты - полярной водной среды. Гетерогенность реакционной системы увеличивает длительность реакционного процесса и уменьшает выход целевого продукта; применяемое при этом нагревание может приводить к рацемизации присоединяемого адденда (аминокислоты, пептида и т.п.).
Известен способ получения водорастворимого производного фуллерена (патент США US6613771, МПК С07С 211/50, НПК 514/256, оп.2003), который предполагает использование любых алкиловых или арил-алкиловых заместителей, в частности тех, которые замещаются азотом или кислородом, содержащим от 1 до 20 атомов углерода. Однако такой способ достаточно сложен, при этом полученное в результате соединение имеет низкую растворимость в воде (<1 мг/мл), а потому известный способ не находит широкого применения при производстве производных фуллерена.
Наиболее близким из известных к описываемому изобретению является способ получения аминокислотных и дипептидных производных фуллерена (Патент РФ №2124022, МПК С07К9/00, оп.1998 г), в котором для реакции с фуллереном используют натриевые или калиевые соли аминокапроновой, аминомасляной кислот и др. в форме комплексов с 18-краун-6, причем система гетерогенная: о-дихлорбензол - вода и нагрев при 60°С 6-8 часов, после чего растворители отгоняют, остаток обрабатывают насыщенным раствором хлористого калия и водой. Известный способ синтеза предполагает применение двухфазной системы, нагрева, что отражается на низком выходе целевого продукта (не более 5% в расчете на фуллерен). Кроме того, в известном способе используют токсичный о-дихлорбензол, который является ирритантом, оказывающим наркотическое действие, повреждающим центральную нервную систему, печень почки. Также имеет место фактор высокой температуры, что в случае оптически активных соединений (аминокислоты, пептиды, аминосахара) может приводить к их рацемизации. Кроме того, указанный способ ограничен применением солей аминокислот и краун-эфира, который повышает гидрофобность аминокислот. Для соединений, где отсутствует карбоксильная группа (аминосахара, полигидроксиламины), этот метод неприемлем.
Технический результат настоящего изобретения состоит в повышении производительности, технологичности и универсальности способа синтеза водорастворимых аддуктов фуллерена, расширении спектра получаемых продуктов и повышении их безопасности.
Указанный технический результат достигается тем, что в способе получения водорастворимых аддуктов фуллерена путем смешивания дисперсии фуллерена С60 с гидрофильными соединениями, где гидрофильное соединение выбирают из ряда: аминокислота, аминосахар, гидроксилированный амин, белок, которые предварительно переводят в триметилсилильное (ТМС) производное путем смешивания с триметилсилилирующим реагентом (N,O-бис(триметилсилил)-ацетамидом в среде полярного апротонного растворителя, после чего полученный раствор триметисилильного производного (ТМС) смешивают с дисперсией фуллерена в полярном апротонном растворителе и перемешивают смесь при комнатной температуре от 2 до 24 часов.
При этом полярный апротонный растворитель выбирают из ряда соединений, характеризующихся высокой диэлектрической проницаемостью, например, N-метил-2-пирролидон (МП), диметилсульфоксид (ДМСО), диметилформамид (ДМФА), диметилацетамид (ДМАА).
Предпочтительно гидрофильное соединение X выбирать из природных L-аминокислот.
В качестве гидрофильного соединения X может быть использован N-трис-(гидроксиметил)аминометан, или аминосахар, или природный белок.
В процессе превращения гидрофильного соединения в триметилсилильное (ТМС или (CH3)3Si) производное в присутствии ТМС-донора в среде полярного апротонного растворителя все подвижные протоны гидрофильного соединения замещаются на триметилсилильную группу (ТМС-группу) и образуемое ТМС-аминосоединение (ТМС-Х) переходит в раствор. Последующее добавление фуллерена и выдерживание реакционной смеси в течение определенного времени (от 2 до 24 часов) при комнатной температуре приводит к образованию целевого аддукта. Поскольку реакция идет с доступом кислорода воздуха, одновременно происходит присоединение атома кислорода с образованием эпокиси. На этой стадии образуемый продукт находится в среде апротонного растворителя, откуда его выделяют путем разбавления водой с последующим диализом. Вода расщепляет все связи, образованные ТМС с X, заменяя ТМС-группы на атомы водорода, при этом остатки ТМС образуют гексаметилдисилоксан (ГМДС). Поэтому перед диализом из водной смеси необходимо удалить ГМДС, обычно или путем испарения в вакууме, или экстракцией этилацетатом или серным эфиром. Тот факт, что молекулы получаемых соединений не проходят через диализную мембрану, говорит о том, что вещества находятся в коллоидном (агрегированном) состоянии. Это же подтверждают и данные измерения размеров частиц в получаемых растворах. Растворы, содержащие частицы до 200 нм, практически прозрачны для человеческого глаза. Данный размер характерен для белков и вирусов, что имеет большое значение в биологическом плане, позволяя им транспортироваться внутрь клетки по тому или иному механизму. Этот аспект также важен и для фармацевтических препаратов, если они находятся в нанодисперсном состоянии, такая форма резко увеличивает их биодоступность. Раствор после диализа высушивают лиофильно, получая конечный продукт в виде сухого порошка, цвет - от светло-коричневого до черного.
Изобретение проиллюстрировано рисунками, схемами и графиками фиг.1- 7, где представлено на:
фиг.1 - Схема синтеза аддукта фуллерена с α-аминокислотой,
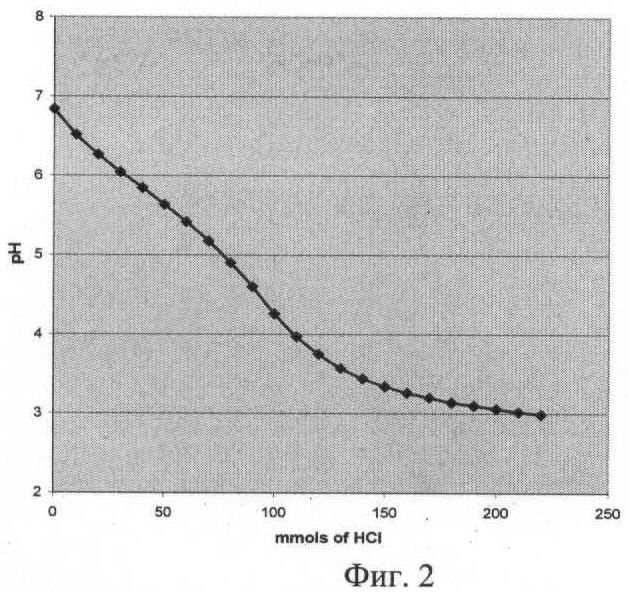
фиг.2 - Кривая титрования натриевой соли С60-Аср соляной кислотой,
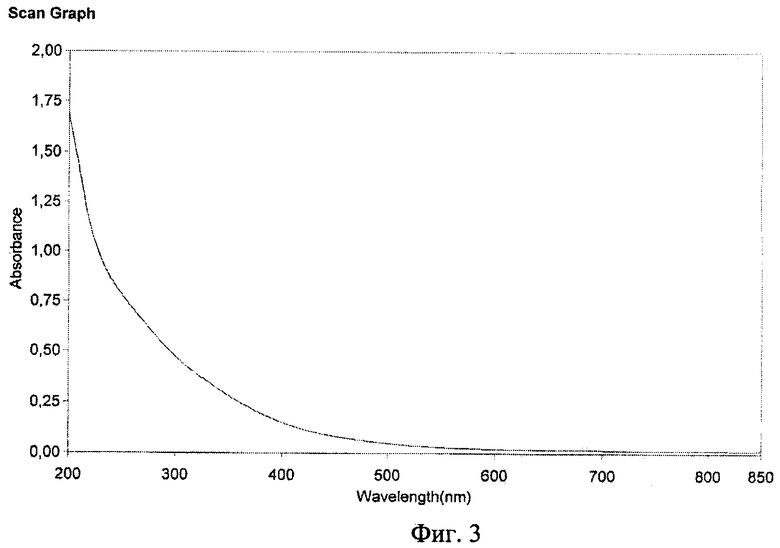
фиг.3 - Электронный спектр C60-Lys в воде,
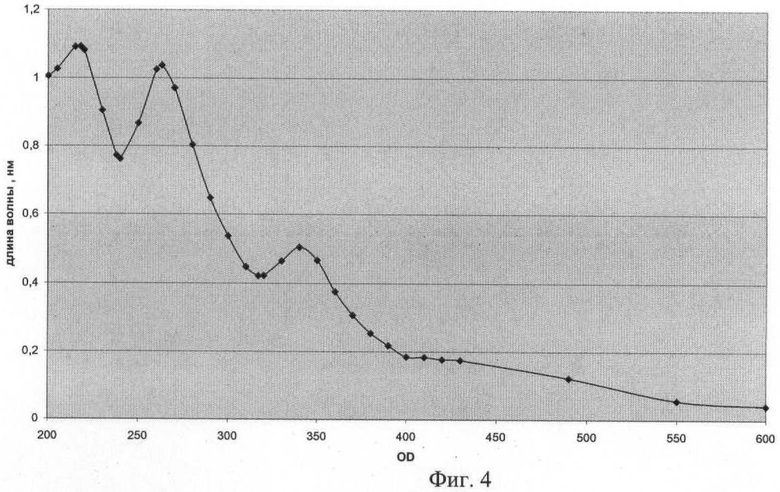
фиг.4 - Электронный спектр водной наносуспензии фуллерена С60,
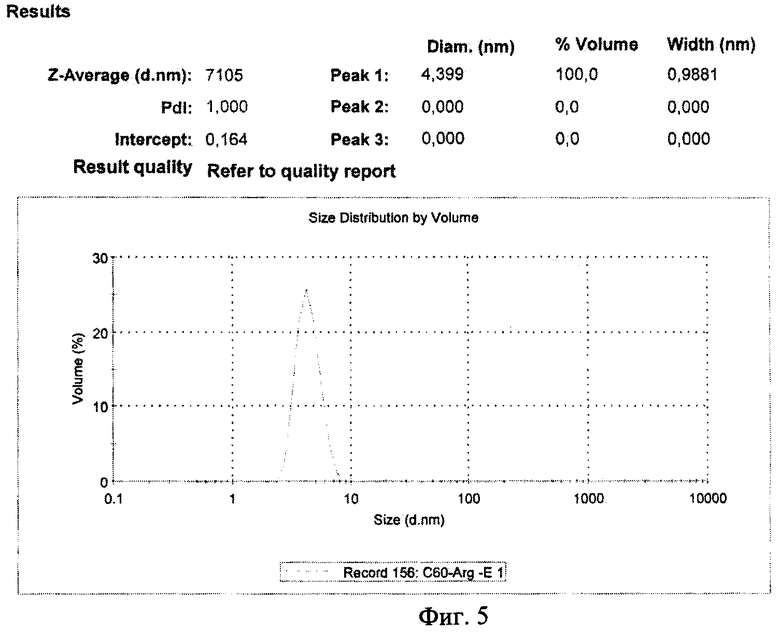
фиг.5 - Результаты анализа размера частиц C60-(Arg)6,
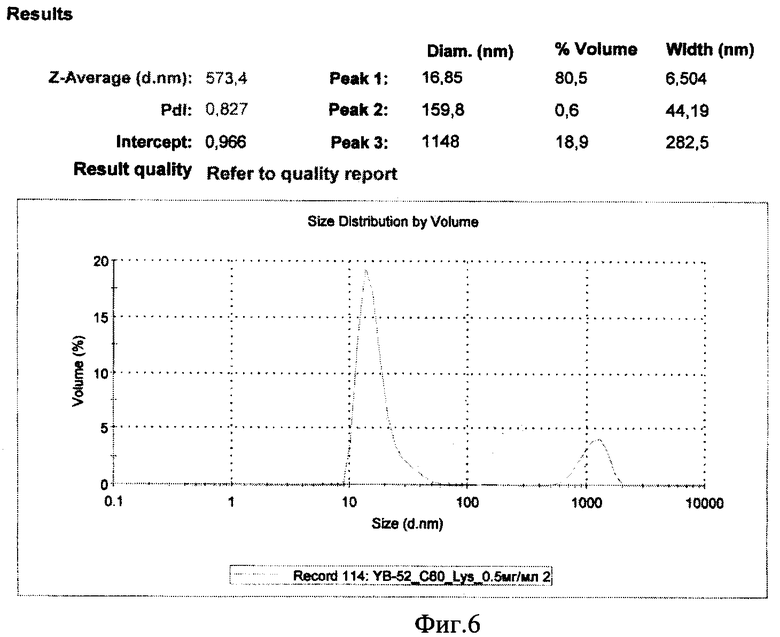
фиг.6 - Результаты анализа объемного распределения размера наночастиц C60-Lys в воде,
фиг.7 - Электронный спектр аддукта С60 с яичным альбумином (Ova).
Иллюстрация способа в соответствии с изобретением приведена на примере и схеме синтеза аддукта фуллерена с -аминокислотой:

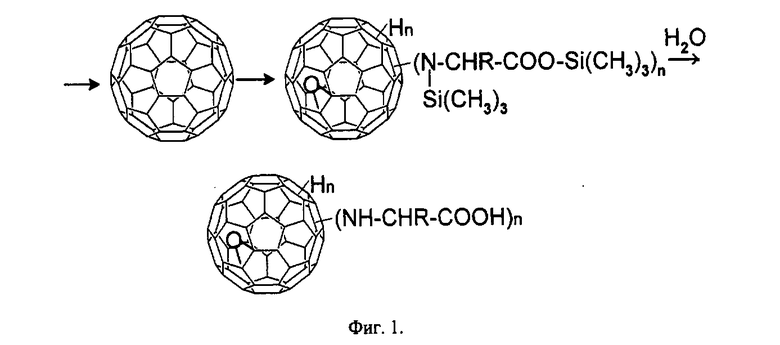
На первой стадии аминокислота в нерастворимой цвиттерионой форме (кристаллическая форма) реагирует с БТСА, образуя ТМС-аминокислоту, которая растворима в апротонном растворителе. Затем ТМС-аминокислота взаимодействует с фуллереном, давая продукт присоединения, т.е. аддукт, который еще содержит ТМС-группы. Гидролиз водой отщепляет ТМС и приводит к целевому продукту.
Практически все ТМС-производные аминокислот, пептидов и аминосахаров обладают липофильными свойствами, поэтому способны растворяться в апротонных растворителях, в том числе и тех, которые пригодны для растворения фуллерена. В качестве растворителя можно использовать полярные апротонные растворители с высокой диэлектрической проницаемостью, способные смешиваться с водой, такие как N-метил-2-пирролидон, диметилсульфоксид, диметилформамид, диметилацетамид. Для ввода ТМС можно применять N,O-бис-(триметилсилил)-ацетамид, N-метил-триметилсилилацетамид, N,O-бис(триметилсилил)-трифторацетамид, выступающие хорошими донорами ТМС и плохими нуклеофилами. Замена протона в первичной аминогруппе на ТМС лишь частично снижает ее нуклеофильность, сохраняя ее реакционно-способность с электрофилами [Рогожин С.В., Давидович Ю.А., Андреев С.М., Миронова Н.В., Юртанов А.И. Получение триметилсилил-производных аминокислот и пептидов для пептидного синтеза. Известия АН СССР, сер. хим., 1975, 23 (8): 1789-1792; Андреев С.М., Миронова Н.В., Давидович Ю.А., Рогожин С.В. О реакционной способности триметилсилильных производных аминокислот в реакциях с активированными эфирами. Изв. АН СССР, сер. хим., 1978, №8]. Указанный метод пригоден для получения аддуктов фуллерена с любым первичным амином, содержащим подвижный протон, т.е. является универсальным, пригодным для введения в фуллерен различных классов аминосоединений: аминокислот, пептидов, аминосахаров, полиаминов с гидрофильным группами.
Использование ТМС-группы предпочтительно тем, что практически мгновенно отщепляется от амино-, гидроксильных и карбоксильных групп при обработке водой. При получении фуллеренового аддукта единственный побочный продукт, нерастворимый в воде, гексаметилдисилоксан, легко удаляется в вакууме (т.кип. 100°С при 760 мм рт.ст.) или путем экстракции этилацетатом или серным эфиром. Все другие побочные продукты (ацетамид, аминокислоты, пептиды, аминосахара, не вступившие в реакцию) растворимы в воде и удобно отделяются диализом. В диализате остается только целевой продукт, который выделяется после удаления воды лиофилизацией.
Количество присоединяемых аминокислот на молекулу фуллерена зависит от соотношения компонентов и свойства гидрофильного соединения (X). Метод предусматривает применение 10-100-кратного мольного избытка компонента X по отношению к фуллерену. Содержание X в фуллерене может составлять от 2 до 12 молей на моль фуллерена, при этом сам фуллерен, как правило, реагирует на 100% от взятого в реакцию фуллерена.
Аминокислотные производные фуллерена (АПФ) растворимы в водной среде, образуя коллоидную систему из наночастиц (нанодисперсию). Растворимость в водной среде определяется в большой мере содержанием в фуллерене гидрофильного соединения X.
Полученные в соответствии с изобретением соединения представляют собой твердые темно-коричневые порошки, растворимые в водных средах в определенной зоне рН, которая зависит от наличия в структуре аддукта ионогенных групп и констант их диссоциации (рК). Например, аддукт фуллерена с аргинином, C60-(Arg)6 (поликатион), содержит высокоосновные гуанидиновые группы (рК>11), поэтому хорошо растворим при рН ниже 9, образуя солевую форму. С другой стороны, аддукт фуллерена с ε-аминокапроновой кислотой, С60-Аср (полианион), хорошо растворим в форме щелочной соли (рН>7). Количество присоединяемого адденда может быть определено путем кислотно-основного титрования. На фиг.2 показана кривая титрования натриевой соли С60-Аср соляной кислотой. Точку эквивалентности определяют по перегибу полученной кривой, расчет показывает, что данный образец содержит примерно 2 моля Аср на моль фуллерена.
В отличие от свободного фуллерена его аминокислотные аддукты практически нерастворимы в ароматических углеводородах (бензол, толуол), но хорошо растворимы в ДМФА, ДМСО, N-метипирролидоне. В ИК-спектрах аддуктов наблюдается сильная полоса поглощения около 1100 см-1, характерная для С60-аминопроизводных, электронные спектры растворов всех аддуктов аминокислот выглядят как ниспадающая кривая с небольшими перегибами (фиг.2), и сильно отличается от спектра водной суспензии чистого фуллерена (фиг.3). Рассчитанный молярный коэффициент экстинкции (ε) для С60-(Аср)2 при 340 нм имеет величину 18250 (вода рН 10), в ДМФА - около 7000, тогда как для чистого фуллерена в форме водной наносуспензии она равна 68000.
Тип и количество аминокислоты, присоединенной к фуллерену, оказывает существенное влияние на гидродинамический размер частиц в формируемой дисперсии. Так, анализ размера частиц С60-ε-Аср и C60-Lys в водном растворе при рН около 7 (20 мкг/мл), измеренный методом динамического светорассеяния (Nanosizer ZS Malvern), показывает для С60-ε-Аср (дианион) средний диаметр в пределах 50 нм (не показано). Тогда как наночастицы C60-(Arg)6 (гексакатион), обладающие сильным позитивным зарядом, имеют средний размер 4-5 нм (фиг.4).
Ниже представлены примеры реализации способа в соответствии с изобретением, где в примерах 1-7 приведено описание синтеза конкретных аддуктов фуллеренов.
Пример 1. Фуллерен-L-лизин (C60-Lys)
К суспензии 510 мг (3,5 ммолей) L-лизина в 7 мл N-метилпирролидона (МП) добавляют 2,57 мл (10,5 ммоля) N,O-бис(триметилсилил)ацетамида (БТСА), полученную смесь перемешивают в течение порядка 2-х часов до получения полупрозрачного раствора, затем в него вносят 50 мг (0.07 ммоля) фуллерена С60 и перемешивают полученную суспензию 18 часов при комнатной температуре. Фуллерен при этом переходит в раствор, по истечении первого часа цвет суспензии меняется от буро-зеленого до коричневого. Затем к смеси добавляют 90 мл дистиллированной воды, смесь перемешивают 15 мин, добавляют 30 мл этил ацетата и перемешивают и отделяют этилацетатный слой, содержащий побочный ГМДС. Водную фазу подкисляют до рН 3, полученный раствор диализуют против дистиллированной воды, диализат фильтруют через фильтр 0,2 µ и раствор подвергают лиофильной сушке. Выход коричневого порошка 81 мг (89% в расчете на присоединение 4 молекул лизина). Данные УФ-спектр: 2 очень слабых плеча при 250 и 340 нм, ИК-спектр, сильные полосы: 1706, 1636, 1506, 1453, 1403, 1350, 1110 и 1044 см-1. Кислотно-основное титрование показывают наличие в препарате примерно четырех молекул лизина на молекулу фуллерена. Анализ объемного распределения размера наночастиц С60-Lys в воде, представленный на графиках фиг.5, указывает на их средний размер в районе 17 нм.
Пример 2. Фуллерен-L-лизин (C60-Lys)
К суспензии 1,82 мг (10 ммолей) L-лизина в 20 мл диметилсульфоксида (ДМСО) добавляют 8,8 мл (36 ммоля) БТСА, полученную смесь перемешивают до получения полупрозрачного раствора (~3 часа), затем вносят 50 мг (0.07 ммоля) фуллерена С60 и перемешивают 20 часов при комнатной температуре (цвет суспензии приобретает коричневый оттенок). Затем к смеси добавляют 50 мл дистиллированной воды, смесь перемешивают 30 мин, добавляют 30 мл этилацетата, перемешивают и отделяют этилацетатный слой. Полученный раствор диализуют против дист. воды и диализат фильтруют через фильтр 0,2 µ и раствор подвергают лиофильной сушке. Выход коричневого порошка 53 мг. Данные УФ-спектра и ИК-спектров аналогичны спектрам в примере 1. Результаты кислотно-основного титрования показывают наличие в препарате примерно 5 молекул лизина на молекулу фуллерена.
Пример 3. Получение фуллерен-L-аргинина (C60-Arg)
К суспензии 1,74 мг мг (10 ммолей) L-аргинина в 20 мл ДМСО добавляют 8,8 мл (36 ммоля) БТСА, полученную смесь перемешивают до получения желтоватого раствора (примерно 3 часа) и затем вносят 144 мг (0,2 ммоля) фуллерена С60 и перемешивают 18 часов при комнатной температуре. Затем к смеси добавляют 90 мл дистиллированной воды, смесь перемешивают 15 мин и упаривают в вакууме на роторном испарителе при температуре 40°С для удаления гексаметилдисилоксана. Оставшуюся водную фазу подкисляют до рН 3, полученный раствор диализуют против дист. воды, диализат фильтруют через фильтр 0,2 µ и раствор высушивают лиофильно. Выход темно-коричневого порошка 370 мг. Тест Бейлыптейна на хлор (ион хлора, связанный с аминогруппой C60-Arg) - позитивный. УФ-спектр: слабое плечо при 330-350 нм. ИК-спектр: Кислотно-основного титрования показывают содержание около 6 молекул аргинина на молекулу фуллерена. Результаты Н1-ЯМР соответствуют ожидаемому спектру.
Пример 4. Получение фуллерен-ε-аминокапроновой кислоты (С60-Аср)
К суспензии 1,31 г (10 ммолей) ε-аминокапроновой кислоты (Аср) в 20 мл диметилацетамида (ДМАА) добавляют 4,89 мл (20 ммоля) БТСА, полученную смесь перемешивают 4 часа и затем вносят 50 мг (0,07 ммоля) фуллерена С60 и перемешивают 15 часов при комнатной температуре. Полученный коричневый раствор разбавляют 100 мл дистиллированной воды, смесь перемешивают 15 мин, удаляют в вакууме гексаметилдисилоксан и оставшуюся водную фазу подщелачивают до рН 9-10. Раствор диализуют против дист. воды, фильтруют через фильтр 0, 2 µ и высушивают лиофильно. Выход коричневого порошка 57,8 мг. УФ-спектр: слабое плечо при 330-350 нм. Кислотно-основного титрования показывают содержание 2 молекул Аср на молекулу фуллерена.
Пример 5. Получение фуллерен-D-галактозамина (С60-GalN)
К суспензии 250 мг (1,16 ммолей) гидрохлорида D-галактозамина в 20 мл N-метилпирролидона (МП) добавляют 128 мкл (1,16 ммоля) N-метилморфолина, затем добавляют 1.36 мл (5.57 ммоля) БТСА, полученную смесь перемешивают до получения полупрозрачного раствора, вносят 50 мг (0.07 ммоля) фуллерена С60 и перемешивают 18 часов при комнатной температуре. Удаляют в вакууме гексаметилдисилоксан, затем к остатку добавляют 50 мл дистиллированной воды, смесь перемешивают 30 мин. Полученный раствор диализуют против дист. воды, диализат фильтруют через фильтр 0,2 µ и раствор подвергают лиофильной сушке. Выход целевого продукта - 72 мг, содержание GalN, определенное по данным элементного анализа, составило 3, 3 моля/моль фуллерена.
Пример 6. Получение фуллерен-овальбумина (С60-Ova)
К суспензии 100 мг (2,2 мкмоля) белка овальбумина (Ova) в 20 мл МП добавляют 1 мл (4 ммоля) БТСА, полученную смесь перемешивают при комнатной температуре до получения раствора (~5 часов) и затем вносят 3,2 мг (4,4 мкмоля) фуллерена С60 в виде раствора в 10 мл МП. Смесь перемешивают 18 часов при комнатной температуре (цвет меняется от светло-фиолетового до светло-коричневого) и затем к смеси добавляют 50 мл дистиллированной воды, перемешивают 30 мин и полученный желтый раствор диализуют против дист. воды. Диализат фильтруют через фильтр 0,2 µ и лиофильно высушивают. Выход светло-коричневого порошка 98 мг. УФ-спектр водного раствора С60-Ova свидетельствует о наличии в белке фуллерена ввиду характерного поглощения в области 320-350 нм.
Пример 7. Получение фуллерен-трис-(гидроксиметил)аминометан (C60-Tris)
К суспензии 0,84 г (6,95 ммоля) трис-(гидроксиметил)аминометана (Tris) в 20 мл МП добавляют 3,39 мл (13.9 ммоля) БТСА, в полученный раствор вносят 100 мг (0.139 ммоля) фуллерена С60 и перемешивают 18 часов при комнатной температуре. Удаляют в вакууме гексаметилдисилоксан, затем к остатку добавляют 50 мл дистиллированной воды, смесь перемешивают 30 мин. Полученный раствор диализуют против дист. воды, диализат фильтруют через фильтр 0,2 µ и раствор подвергают лиофильной сушке. Выход водорастворимого коричневого порошка 145 мг. Содержание Tris, определенное по данным элементного анализа, составило 2,1 моля/моль фуллерена.
Таким образом, изобретение позволяет получать водорастворимые аддукты фуллерена с аддендами из очень широкого класса соединений, перспективных для создания препаратов с антиоксидантными свойствами, препаратов для лечения аллергии, воспалительных и нейродегенеративных заболеваний, что резко отличает предлагаемый способ от известных способов. Кроме того, изобретение позволяет значительно упростить способ получения производных фуллеренов за счет проведения процесса в гомогенной среде и при комнатной температуре. При этом использование нетоксичных растворителей повышает экологическую безопасность производства производных фуллеренов. Известно, что из-за токсичности хлорбензола производители продуктов, технология получения которых требует использования хлорбензолов, ведут интенсивный поиск более экологичных заменителей или пытаются минимизировать количество хлорбензола в процессе производства.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ВОДНЫХ НАНОДИСПЕРСИЙ ФУЛЛЕРЕНА | 2013 |
|
RU2548971C2 |
| Способ получения аддуктов легких фуллеренов с L-аминокислотами | 2024 |
|
RU2837394C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДНО-СОЛЕВЫХ ДИСПЕРСИЙ ФУЛЛЕРЕНА | 2015 |
|
RU2630561C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ И СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКОГО ЗАБОЛЕВАНИЯ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2005 |
|
RU2323722C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВЫСОКОКОНЦЕНТРИРОВАННОГО ВОДНОГО РАСТВОРА ФУЛЛЕРЕНА | 2018 |
|
RU2679257C1 |
| СПОСОБ ПОЛУЧЕНИЯ АДДУКТОВ СМЕСИ ФУЛЛЕРЕНОВ ФРАКЦИИ С50-С92 И РЕГУЛЯТОР РОСТА РАСТЕНИЙ НА ИХ ОСНОВЕ | 2014 |
|
RU2581658C2 |
| ГЕРБИЦИД НА ОСНОВЕ АДДУКТОВ ФУЛЛЕРЕНОВ | 2014 |
|
RU2596031C2 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕШАННЫХ ФУЛЛЕРЕНОЛОВ | 2011 |
|
RU2473462C2 |
| Фунгицид на основе аддуктов фуллеренов | 2017 |
|
RU2668556C1 |
| Применение водно-солевого раствора фуллерена Cв качестве терапевтического средства при заболеваниях атопическим дерматитом | 2016 |
|
RU2641091C1 |


Изобретение относится к области органической химии и биотехнологии. Предложен способ получения аддуктов фуллерена путем смешивания дисперсии фуллерена С60 с гидрофильными соединениями, где в качестве гидрофильного соединения используют аминокислоту, или аминосахар, или полигидроксиламин, или белок, которые предварительно переводят в триметилсилильное (ТМС) производное путем смешивания с триметилсилилирующим реагентом (N,O-бис(триметилсилил)-ацетамидом в среде полярного апротонного растворителя, после чего полученный раствор триметисилильного производного (ТМС) смешивают с дисперсией фуллерена в полярном апротонном растворителе и перемешивают смесь при комнатной температуре от 2 до 24 часов. 4 з.п. ф-лы, 7 ил., 7 пр.

1. Способ получения аддуктов фуллерена путем смешивания дисперсии фуллерена С60 с гидрофильными соединениями, отличающийся тем, что в качестве гидрофильного соединения используют аминокислоту, или аминосахар, или полигидроксиламин, или белок, которые предварительно переводят в триметилсилильное (ТМС) производное путем смешивания с триметилсилилирующим реагентом (N,O-бис(триметилсилил)-ацетамидом в среде полярного апротонного растворителя, после чего полученный раствор триметисилильного производного (ТМС) смешивают с дисперсией фуллерена в полярном апротонном растворителе и перемешивают смесь при комнатной температуре от 2 до 24 ч.
2. Способ по п.1, отличающийся тем, что из полярных апротонных растворителей выбирают растворители с высокой диэлектрической проницаемостью, N-метил-2-пирролидон, диметилсульфоксид или диметилформамид.
3. Способ по п.1, отличающийся тем, что гидрофильное соединение X выбирают из природных L-аминокислот.
4. Способ по п.1, отличающийся тем, что в качестве гидрофильного соединения X используют аминосахар.
5. Способ по п.1, отличающийся тем, что в качестве гидрофильного соединения X используют природный белок.
| RU 2213049 С1, 27.09.2003 | |||
| АДЪЮВАНТЫ | 1997 |
|
RU2129436C1 |
| RU 21240022 C1, 27.12.1998 | |||
| Колосоуборка | 1923 |
|
SU2009A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(N-ФЕНИЛАМИНО)-1,2-ДИГИДРО[60]ФУЛЛЕРЕНА | 2006 |
|
RU2310646C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(N,N-ДИФЕНИЛАМИНО)-1,2-ДИГИДРО[60]ФУЛЛЕРЕНА | 2006 |
|
RU2309941C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-(4-ХИНОЛИНАМИНО)-1,2-ДИГИДРО[60]ФУЛЛЕРЕНА | 2006 |
|
RU2313521C1 |
| СРЕДСТВО ДЛЯ ИНГИБИРОВАНИЯ ВИЧ И ЦМВ-ИНФЕКЦИЙ И СПОСОБ ИХ ИНГИБИРОВАНИЯ | 2002 |
|
RU2196602C1 |
| АНДРЕЕВ С.M | |||
| и др | |||
| О генерации антител к фуллерену С// Иммунология | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
Авторы
Даты
2012-09-27—Публикация
2010-12-09—Подача