Область техники, к которой относится изобретение
Настоящее изобретение, в общем, касается лечения инфекционных заболеваний, в частности эффективных способов лечения оппортунистических грибковых заболеваний.
Предшествующий уровень техники
Мукормикоз является опасным для жизни заболеванием, которое вызывается грибками из класса Zygomycetes, отряда Mucorales. Принадлежащие к отряду Mucorales грибки распадаются на 6 семейств, причем все они могут вызывать мукормикоз (Ibrahim et al., Zygomycosis, p.241-251. In W.E.Dismukes, P.G.Pappas and J.D.Sobel (ed.), Clinical Mycology, Oxford University Press, New York (2003); Kwon-Chung K.J. and J.E.Bennett, Mucormycosis, p.524-559, Medical Mycology, Lea & Febiger, Philadelphia (1992); Ribes et al., Zygomycetes in Human Disease, Clin. Microbiol. Rev. 13: 236-301 (2000)). Однако чаще всего возбудителями инфекции являются грибки, принадлежащие к семейству Mucoraceae, в особенности вид Rhizopus oryzae (Rhizopus arrhizus) (Ribes et al., supra). Также отмечается все больше случаев мукормикоза, вызванного Cunninghamella spp. из семейства Cunninghamellaceae (Cohen-Abbo et al., Clinical Infectious Diseases 17: 173-77 (1993); Kontoyianis et al., Clinical Infectious Diseases 18: 925-28 (1994); Kwon-Chung et al., American Journal of Clinical Pathology 64: 544-48 (1975); Ventura et al., Cancer 58: 1534-36 (1986)). Остальные 4 семейства отряда Mucorales не так часто являются возбудителями заболевания (Bearer et al., Journal of Clinical Microbiology 32: 1823-24 (1994); Kamalam and Thambiah, Sabouraudia 18: 19-20 (1980); Kemna et al., Journal of Clinical Microbiology 32: 843-45 (1994); Lye et al., Pathology 28: 364-65 (1996); Ribes et al., supra)).
Возбудители мукормикоза являются оппортунистическими патогенами, которые почти неизменно поражают организм хозяина с ослабленной иммунной системой (Spellberg et al., Clin. Microbiol. Rev. 18: 556-69 (2005)). Больные диабетическим кетоацидозом особенно подвержены мукормикозам, и у них эти инфекции возникают чаще, чем инфекции, вызванные другими грибками. Тем не менее, при наличии других иммунологических нарушений, располагающих к возникновению мукормикоза, включая нейтропению и кортикостероидную терапию, мукормикоз встречается реже, чем другие оппортунистические грибковые инфекции, к примеру, вызванные Candida и Aspergillus spp. В целом, по данным недавнего демографического исследования, встречаемость мукормикоза составляет 1,7 случаев на миллион человек в год, что означает примерно 500 случаев в год в США (Rees et al., Clinical Infectious Diseases 27: 1138-47 (1998)). Тем не менее, у пациентов с высоким уровнем риска, к примеру, подвергающихся аллогенной трансплантации костного мозга, встречаемость мукормикоза достигает 2-3% (Maertens et al., Bone Marrow Transplantation 24: 307-12 (1999); Marty et al., N. Engl. J. Med. 350: 950-52 (2004)). Более того, в недавнем обзоре отмечено заметное повышение встречаемости мукормикоза за последние двадцать лет (Gleissner et al., Leuk. Lymphoma 45: 1351-60 (2004)). Аналогичное возрастание отмечено крупными центрами по пересадке стволовых клеток. Например, сообщалось о возрастании встречаемости мукормикоза более чем в два раза за последние двадцать лет (Marr et al., Clin. Infect. Dis. 34: 909-17 (2002); Kontoyianis et al., Clin. Infect. Dis. 30: 851-56 (2000)). Учитывая широкую распространенность диабета, рака и трансплантации органов у стареющего населения США, следует ожидать, что возрастание встречаемости мукормикоза будет и впредь продолжаться в обозримом будущем.
Имеющиеся способы лечения инвазивного мукормикоза включают стремление устранить лежащие в его основе предрасполагающие факторы, входящую в практику хирургическую обработку пораженного участка и вспомогательную противогрибковую терапию (Edwards J., Jr., Zygomycosis, p.1192-1199. In P.Hoeprich and M.Jordan (ed.), Infectious Disease, 4th ed., J.B.Lippincott Co., Philadelphia (1989); Ibrahim et al. (2003), supra; Kwon-Chung and Bennett, supra; Sugar A.M., Agent of Mucormycosis and Related Species, p.2311-2321. In G.Mandell, J.Bennett and R.Dolin (ed.), Principles and Practices of Infectious Diseases, 4th ed., Churchill Livingstone, New York (1995)). Единственным противогрибковым средством, принятым для лечения инвазивного мукормикоза, остается амфотерицин В (AmB) (Id.). Поскольку грибок сравнительно устойчив к АmВ, то требуются высокие дозы, которые часто вызывают нефротоксичность и другие неблагоприятные эффекты (Sugar, supra). К тому же в отсутствие хирургического удаления инфицированного очага (к примеру, удаления глаза у больных риноцеребральным мукормикозом), одна лишь противогрибковая терапия редко ведет к излечению (Edwards J. (1989), supra; Ibrahim et al. (2003), supra)). Даже при сочетании хирургической обработки с высокими дозами AmB смертность от мукормикоза превышает 50% (Sugar, supra). У больных диссеминированной формой смертность достигает 100% (Husain et al., Clin. Infect. Dis. 37: 221-29 (2003)). Вследствие такой недопустимо высокой смертности и чрезвычайной болезненности вызывающего сильное обезображивание хирургического лечения становится необходимой разработка новых методов лечения и профилактики инвазивного мукормикоза.
Нефротоксичность AmB побудила врачей-клиницистов заимствовать липидные композиции AmB, которые менее нефротоксичны, чем AmB, и могут применяться в более высоких дозах на более продолжительный срок (Ibrahim et al. (2003), supra)). В нескольких случаях было зафиксировано успешное лечение больных мукормикозом с помощью липидных композиций амфотерицина до 15 мг/кг/день (Cagatay et al., BMC Infect. Dis. 1: 22 (2001); Ericsson et al., Clinical Infectious Diseases 16: 585-56 (1993); Walsh et al., Antimicrob. Agents Chemother. 45: 3487-96 (2001)). Тем не менее, смертность у пациентов, получавших липидные композиции амфотерицина, остается высокой, что подчеркивает потребность в новых терапевтических средствах для этого смертельного заболевания.
Практически все микробные патогены нуждаются в железе для роста и вирулентности (Howard D.H., Clin. Microbiol. Rev. 12: 394-404 (1999)). В организме млекопитающих для микроорганизмов доступно очень мало железа в сыворотке крови, так как оно прочно связано с такими белками-переносчиками, как трансферрин (Artis et al., Diabetes 31: 1109-14 (1982)). Секвестрация железа в сыворотке является главным защитным механизмом, в частности, против R. oryzae (Artis et al., supra). Этот организм плохо растет в сыворотке, но торможение роста устраняется при добавлении экзогенного железа (Artis et al., supra; Boelaert et al., Journal of Clinical Investigations 91: 1979-86 (1993)).
Больные с повышенным уровнем доступного железа в сыворотке особенно подвержены инфекции R. oryzae и другими Zymomycetes, но в меньшей степени, чем другими патогенными грибками, как то Candida или Aspergillus (Ibrahim et al. (2003), supra; Sugar, supra)). Например, у больных, получавших хелатор железа - дефероксамин, заметно возрастает встречаемость инвазивного мукормикоза, что связано с уровнем смертности >80% у этих больных (Boelaert et al., Kidney International 45: 667-71 (1994)). Хотя дефероксамин действует как хелатор железа на организм человека, его действие на R. oryzae выглядит совсем наоборот. Дефероксамин вызывает предрасположенность пациентов к инфекции Rhizopus, действуя в качестве сидерофора, поставляющего грибку ранее недоступное железо (Boelaert et al. (1993), supra)). Rhizopus получает железо из комплекса железо-дефероксамин посредством внутриклеточного транспорта восстановленного железа без интернализации дефероксамина (de Locht et al., Biochemical Pharmacology 47: 1843-50 (1994)). Этот транспорт реализуется высокоаффинными пермеазами железа. Следовательно, повышение доступного железа в сыворотке является фактором риска для патогенеза мукормикоза. Однако хелатирующие железо соединения могут действовать как сидерофоры для патогена, поэтому в общем случае они не могут применяться для лечения.
Таким образом, существует потребность в соединениях и способах, способных уменьшить риск патогенеза мукормикоза и обеспечить эффективный режим лечения. Настоящее изобретение удовлетворяет эту потребность, а также обеспечивает различные преимущества.
Сущность изобретения
Изобретением предусмотрены композиции, включающие по меньшей мере одно хелатирующее железо соединение и по меньшей мере одно противогрибковое средство. Композиции могут содержать хелатирующие железо соединения - деферипрон или деферасирокс. Противогрибковое средство, входящее в композицию, может представлять собой полиеновое противогрибковое средство, азоловое противогрибковое средство или эхинокандиновое противогрибковое средство. Изобретением также предусмотрен способ лечения или предотвращения грибковых заболеваний. Способ включает введение индивидууму, страдающему или подверженному грибковому заболеванию, терапевтически эффективного количества по меньшей мере одного хелатирующего железо соединения на протяжении достаточного времени для уменьшения тяжести грибкового заболевания, причем хелатирующее железо соединение не является сидерофором или ксеносидерофором в отношении грибкового заболевания. Способ лечения или предотвращения грибковых заболеваний, предусмотренный изобретением, также может включать введение индивидууму, страдающему или подверженному грибковому заболеванию, терапевтически эффективного количества по меньшей мере одного хелатирующего железо соединения и по меньшей мере одного противогрибкового средства. Изобретением также предусмотрен способ, включающий профилактическое введение по меньшей мере одного хелатирующего железо соединения либо по меньшей мере одного хелатирующего железо соединения и по меньшей мере одного противогрибкового средства еще до возникновения грибкового заболевания.
Краткое описание фигур
На фиг.1 представлена зависимость между Def и железом и выживаемостью мышей DKA, инфицированных R. oryzae. Мышам (n≥20 по каждой обработке) давали деферипрон (Def) либо Def+FeCl3 (60 мг/кг) для устранения эффекта хелатирования железа. В качестве контроля включали мышей, получавших LAmB. Обработку начинали через 24 ч после инфицирования. * означает р<0,003 по сравнению с инфицированными без обработки или неинфицированными без обработки + FeCl3.
На фиг.2 представлено, как Exjade™ (деферасирокс) улучшает выживаемость мышей с диабетическим кетоацидозом, инфицированных R. oryzae. Мышей (n=6 для плацебо и n=7 для Exjade) инфицировали путем инъекции в хвостовую вену 2,2×104 спор R. oryzae 99-892 (клинический изолят, полученный из легких инфицированного пациента). Через 24 ч после инфицирования мышам гаважем вводили плацебо либо 1, 3 или 10 мг/кг Exjade два раза в день на протяжении 7 дней. * означает р<0,05 по сравнению с плацебо.
На фиг.3 представлена выживаемость мышей DKA, инфицированных R. oryzae и получавших различные режимы обработки Def. Мышей (n=6 на группу) через 24 ч после инфицирования обрабатывали Def в дозе 50, 100 или 200 мг/кг каждый день (qd) или через день (qod), в совокупности 4 дозы. * означает р<0,05 по сравнению с инфицированными без обработки.
На фиг.4 представлено лечение экспериментального мукормикоза с помощью комбинации Def и LAmB. Мышей (n=11 для инфицированных без обработки и Def и n=6 для LAmB и Def+LAmB) инфицировали R.oryzae, а затем через 24 ч обрабатывали Def, LAmB или комбинацией обоих препаратов, в совокупности 4 дозы. * означает р<0,005 по сравнению с инфицированными мышами без обработки.
На фиг.5 представлена выживаемость мышей с нейтропенией, инфицированных R.oryzae и получавших для профилактики Def, LAmB или оба препарата. Мышей (n=9) в день -1 обрабатывали Def qod, LAmB qd или обоими препаратами, в совокупности 4 дозы. * означает р<0,05 для LAmB или LAmB+Def по сравнению с инфицированными без обработки.
На фиг.6 представлена обсемененность грибком R. oryzae головного мозга мышей DKA (n=6), получавших деферипрон, LAmB или плацебо. Мышей инфицировали 3,8×103 спор и через 54 ч извлекали мозги после обработки двумя дозами одного из препаратов. Данные выражали в виде медианы ± межквартильного размаха. Ось у отражает нижний предел обнаружения метода. * означает р<0,036 по сравнению с плацебо согласно критерию Стила для множественных сравнений.
На фиг.7 представлен замороженный срез некротической слизистой оболочки носа, окрашенный метанамином серебра, на котором видны грибки с широкими лентообразными гифами без перегородок, характерными для Mucorales. Увеличение × 840.
На фиг.8 показано, что деферасирокс индуцирует экспрессию гена rFTR1 у Rhizopus oryzae. В частности, на фиг.8(а) представлена детектируемая методом ОТ-ПЦР экспрессия гена rFTR1 в мицелии R. oryzae при инкубации в богатых железом условиях, в условиях хелатирования железа (деферасирокс) или устранения хелатирования железа (деферасирокс, насыщенный FeCl3). Экспрессия 18S-рДНК включена для проверки качества экстракции РНК. На фиг.8(b) представлена диаграмма, показывающая стратегию конструирования вектора для экспрессии GFP R. oryzae. Промотор означает либо rFtr1p, либо Act1p. На фиг.8(с) представлена экспрессия GFP в R. oryzae под управлением rFtr1p или Act1p (при определении методами конфокальной микроскопии и проточной цитометрии) при культивировании R. oryzae в богатой железом среде, в содержащей деферасирокс среде или в среде, содержащей деферасирокс, насыщенный FeCl3. Экспрессию GFP выявляли по зеленой флуоресценции клеток методом конфокальной микроскопии, а процент флуоресцентных клеток в канале FL1 (ось у) - методом проточной цитометрии.
На фиг.9(а) представлена выживаемость мышей с диабетическим кетоацидозом (n>7 на группу), инфицированных R. oryzae 99-892 (2,2×104) и обработанных различными дозами деферасирокса. Мышам давали плацебо (гидроксипропилцеллюлозный носитель), деферасирокс или деферасирокс+железо (FeCl3, 10 мг/кг) для устранения эффекта хелатирования железа. * означает р<0,05 для выживаемости. На фиг.9(b) представлена выживаемость мышей с диабетическим кетоацидозом (n=24 в трех отдельных опытах с близкими результатами), инфицированных R. oryzae 99-880 (инокулировали в среднем 1,3×103 спор) и через 24 ч получавших деферасирокс 10 мг/кг два раза в день на протяжении 7 дней. * означает р<0,003 по сравнению с плацебо.
На фиг.10(а) представлена обсемененность грибком мозга и почек мышей с диабетическим кетоацидозом (n=11 на группу), инфицированных R. oryzae 99-892 (4,2×104 спор) и получавших плацебо, деферасирокс (10 мг/кг два раза в день) или деферасирокс + железо. На 4-й день после продолжавшейся 3 дня обработки извлекали органы. Данные выражали в виде медианы ± межквартильного размаха. Ось у отражает нижний предел обнаружения метода. На фиг.10(b) представлены окрашенные гематоксилином и эозином срезы почек мышей с диабетическим кетоацидозом, инфицированных R. oryzae 99-892 и получавших деферасирокс, деферасирокс + FeCl3 или плацебо, как указано в 10(а). Стрелками отмечены гифы R. oryzae в ткани. Увеличение × 400. * означает р<0,002 для обсемененности тканей грибком по сравнению с плацебо или деферасирокс + FeCl3.
На фиг.11 показано, что хелатирование железа повышает частотность лимфоцитов Th1 и Th2 в селезенке и повышает уровень провоспалительных цитокинов по сравнению с мышами, перегруженными железом. В частности, на фиг.11(а) представлена частотность лимфоцитов Th1 и Th2 в селезенке мышей с диабетическим кетоацидозом (n=11), инфицированных 3,1×104 спор R. oryzae 99-892 и через 24 ч получавших плацебо, деферасирокс или деферасирокс + FeCl3. На фиг.11(b) представлены результаты анализа цитокинов методом Cytometric Bead Array™ в целых органах тех же мышей (n=11), что указаны в 11(а), которых забивали и извлекали селезенку и почки через 4 дня после инфицирования. Данные в 11(а) и (b) выражали в виде медианы ± межквартильного размаха. * означает р<0,02 по сравнению с плацебо или деферасирокс + FeCl3. ** означает р<0,05 по сравнению и ¥ означает р<0,07 по сравнению с деферасирокс + FeCl3.
На фиг.12 представлена эффективность против мукормикоза самого дефера-сирокса, самого LAmB и комбинации деферасирокса вместе с LAmB. А именно, на графике представлена выживаемость мышей с диабетическим кетоацидозом (n>16 в двух отдельных опытах с близкими результатами), инфицированных R. oryzae 99-880 (инокулировали в среднем 1,5×103 спор) и получавших только деферасирокс, только LAmB или комбинацию деферасирокса (10 мг/кг два раза в день на протяжении 7 дней) с LAmB (15 мг/кг на протяжении 4 дней).
На фиг.13 представлена эффективность в уменьшении инфицированности органов-мишеней самого деферасирокса, самого LAmB и комбинации деферасирокса вместе с LAmB. В частности, на графике представлена обсемененность грибком R. oryzae тканей мозга и почек мышей (n>7), инфицированных R. oryzae 99-880. У этих мышей обработка начиналась через 24 ч после инфицирования и состояла из плацебо, деферасирокса (10 мг/кг два раза в день), LAmB (15 мг/кг/день) или комбинации обоих препаратов. Органы извлекали на 3-й день после продолжавшейся 2 дня обработки. Данные выражали в виде медианы ± межквартильного размаха. Ось у отражает нижний предел обнаружения метода. * означает р<0,003 по сравнению с плацебо. ** означает р<0,003 по сравнению с плацебо, деферасироксом или LAmB. ¥ означает р<0,01 по сравнению с плацебо или деферасироксом.
На фиг.14 представлена эффективность деферасирокса при лечении инфекций R. oryzae у мышей с нейтропенией. Обработанных циклофосфамидом мышей (n=19 в двух отдельных опытах с близкими результатами) инфицировали 2,7×103 спор R. oryzae 99-892. Через 24 ч после инфицирования мышам вводили плацебо или деферасирокс (10 мг/кг) каждый день (qd) или через день (qod), в совокупности 5 доз. * означает р=0,037 по сравнению с плацебо.
Раскрытие сущности изобретения
Настоящее изобретение направлено на применение хелатирующих железо соединений для лечения или уменьшения тяжести грибковых заболеваний. Выбираются такие хелатирующие железо соединения, которые обладают слабой сидерофорной или ксеносидерофорной активностью в отношении искомого грибкового заболевания. В некоторых воплощениях выбираются такие хелатирующие железо соединения, которые практически лишены сидерофорной или ксеносидерофорной активности в отношении искомого грибкового заболевания. В отличие от хелаторов железа, действующих как сидерофоры или ксеносидерофоры, поставляющие ранее недоступное железо грибку, несидерофорные или нексеносидерофорные хелатирующие железо соединения не обладают способствующей этому или транспортной активностью. Поэтому хелаторы железа по изобретению могут применяться для удаления железа из окружающей среды. Одно из преимуществ хелатирования железа для провогрибковой терапии состоит в том, что оно уменьшает доступность важного минерала, в котором нуждаются многие микробные патогены для роста и/или вирулентности.
В одном воплощении изобретение касается терапевтической композиции, содержащей хелатирующее железо соединение и противогрибковое средство. Хелатирующим железо соединением может быть деферипрон (1,2-диметил-3-гидроксипирид-4-1) или деферасирокс (4-[3,5-бис-(2-гидроксифенил)-1Н-1,2,4-триазол-1-ил]-бензойная кислота). И деферипрон, и деферасирокс применялись в терапии для лечения состояний перегруженности железом, поэтому они безопасны и эффективны при хелатирующей железо терапии для лечения или профилактики грибковых заболеваний. Для комбинирования с хелаторами железа по изобретению можно выбрать известные в этой области противогрибковые средства. Комбинирование полезно для применения при лечении или профилактике грибковых заболеваний.
В другом воплощении изобретение касается способа лечения или профилактики грибковых заболеваний. Способ включает введение индивидууму одного или нескольких хелатирующих железо соединений, обладающих активностью несидерофорного или нексеносидерофорного хелатирования железа в отношении искомого вида грибка. Способ также может включать совместное введение противогрибкового средства для усиления эффективности по сравнению с одним лишь хелатором железа. Хелатирующим железо соединением может быть деферипрон или деферасирокс либо оно выбирается из других хелатирующих железо соединений, известных в этой области. Способы изобретения особенно полезны для терапевтического и профилактического лечения, так как хелатирование железа направлено на удаление минерала, важного для грибкового патогенеза.
Изобретением предусмотрены композиции, включающие по меньшей мере одно хелатирующее железо соединение и по меньшей мере одно противогрибковое средство.
Большинство грибковых систем нуждаются в железе для роста, жизнеспособности и/или вирулентности. Грибы выработали целый ряд механизмов для приобретения, захвата и способов хранения, обеспечивающих достаточное поступление этого важного металла. Композиции изобретения направлены на удаление этого важного минерала из среды организма хозяина для нейтрализации грибковых патогенов. Композиции изобретения включают хелатирующее железо соединение для истощения доступного железа и торможения роста, жизнеспособности и/или вирулентности грибкового патогена.
Композиции изобретения включают комбинирование по меньшей мере одного хелатирующего железо соединения вместе с по меньшей мере одним противогрибковым средством. При включении хелатирующего железо соединения вместе с противогрибковым средством объединяются противогрибковые активности, нацеленные на два различных пути, используемые грибками для роста, жизнеспособности и/или вирулентности. Нацеленность на два или несколько различных грибковых путей обеспечивает эффективное терапевтическое лечение грибковых заболеваний, так как вероятность избежания патогеном обоих намеченных путей является низкой.
В настоящем изобретении термин "хелатирующее железо соединение" или "хелатор железа" служит для обозначения соединений, связывающих железо между двумя или несколькими отдельными участками связывания с образованием хелатного кольца или колец. Хелатирующее железо соединение, связанное или образовавшее комплекс с железом, далее именуется хелатом железа. Хелатирующее железо соединение может быть бидентатным, то есть связывать железо с помощью двух отдельных участков связывания. Хелатирующие железо соединения по изобретению также могут быть тридентатными, тетрадентатными или мультидентатными высшего порядка, то есть связывать железо с помощью трех, четырех и больше отдельных участков связывания, соответственно. Хелатирующие железо соединения по изобретению включают хелатирующие соединения, которые могут связываться с железом во всех степенях окисления, включая, к примеру, железо(-II), железо(-I), железо(0), железо(I), железо(II), железо(III), железо(IV) и/или железо(V). Хелатирующая железо терапия означает применение хелатора железа для связывания железа in vivo с образованием хелата железа, при этом железо теряет свое токсическое действие или вредное физиологическое действие. С другой стороны, хелатированное железо становится недоступным для вызывающего инфекцию организма.
К хелатирующим железо соединениям, применимым в композициях изобретения, относятся любые хелаторы или другие молекулы, способные связывать и предотвращать использование железа искомым грибком или грибками. Конкретные примеры хелатирующих железо соединений, включаемых в композиции изобретения, включают, к примеру, деферипрон и деферасирокс. Эти типичные хелатирующие железо соединения особенно полезны, так как они в различных странах апробированы для терапевтических показаний, не связанных с грибковыми заболеваниями, поэтому они хорошо изучены, безопасны и нетоксичны для человека.
Термин "деферипрон" в настоящем изобретении служит для обозначения хелатирующего железо соединения, имеющего структуру 1,2-диметил-3-гидроксипирид-4-1. Деферипрон (Def) также известен как L1, CP20, Ferriprox или Keifer. Деферипрон является представителем хелаторов железа из класса α-кетогидроксипиридинов и коммерчески доступен, к примеру, от фирмы Apotex Inc. (Weston, Ontario, Канада).
Термин "деферасирокс" в настоящем изобретении служит для обозначения хелатирующего железо соединения, имеющего структуру 4-[3,5-бис-(2-гидроксифенил)-1Н-1,2,4-триазол-1-ил]-бензойной кислоты с молекулярной массой 373,4 дальтон. Деферасирокс также известен как Exjade и ICL 670 и является представителем тридентатных хелаторов железа из класса N-замещенных бис-гидроксифенилтриазолов. Деферасирокс коммерчески доступен, к примеру, от фирмы Novartis Corp. (Basel, Швейцария), например, под торговой маркой Exjade®. В соответствии с настоящим изобретением термины "деферасирокс", "ICL670", "Exjade" относятся к активному ингредиенту 4-[3,5-бис-(2-гидроксифенил)-1Н-1,2,4-триазол-1-ил]-бензойной кислоты, например самой 4-[3,5-бис-(2-гидроксифенил)-1Н-1,2,4-триазол-1-ил]-бензойной кислоте или ее фармацевтически приемлемой соли. Деферасирокс, способ его получения и применение описаны, к примеру, в патентах США №№6,465,504 В1 и 6,595,750 В2 и в европейском патенте №ЕР 0914118. Фармацевтические препараты, содержащие 4-[3,5-бис-(2-гидроксифенил)-1Н-1,2,4-триазол-1-ил]-бензойную кислоту или ее фармацевтически приемлемую соль, описаны, к примеру, в международной патентной заявке WO 2004/035026.
Другие хелатирующие железо соединения также могут быть включены в композиции изобретения. Такие другие хелатирующие железо соединения хорошо известны в этой области и к ним относятся, к примеру, природные сидерофоры и ксеносидерофоры типа тех, что описаны ниже, а также не встречающиеся в природе соединения, такие как деферипрон и деферасирокс.
Примерами не встречающихся в природе хелатирующих железо соединений являются такие представители хелаторов из класса гидроксипиридин-4-онов (НРО), как деферипрон, такие представители хелаторов из класса N-замещенных бис-гидроксифенилтриазолов, как деферасирокс, диэтилентриаминпентауксусная кислота (DTPA) и дефероксамин. Деферипрон, деферасирокс и любые из вышеприведенных примеров хелатирующих железо соединений, а также другие, хорошо известные в этой области, могут быть включены в композиции изобретения, содержащие хелатирующие железо соединения.
Сидерофоры и ксеносидерофоры включают, к примеру, гидроксаматы и поликарбоксилаты. Гидроксаматы содержат группировку N-δ-гидроксиорнитина и обычно подразделяются на 4 типичные семейства. Одно семейство включает родоторуловую кислоту, представляющую собой дикетопиперазин N-δ-ацетил-L-N-δ-гидроксиорнитина. В нее же включают и такие производные, как дигидроксамат, называемый димерумовой кислотой. Второе семейство включает копрогены, которые содержат группировку N-δ-ацил-N-δ-гидрокси-L-орнитина. Копрогены можно рассматривать и как тригидроксаматные производные родоторуловой кислоты с линейной структурой. Третье семейство включает феррихромы, которые состоят из циклических пептидов, содержащих трипептид N-δ-ацил-N-δ-гидроксиорнитина в комбинации с глицином, серином или аланином. Четвертое типичное семейство включает фузаринины, также именуемые фузигенами, которые могут представлять собой линейные или же циклические гидроксаматы. Фузаринин представляет собой соединение, характеризующееся N-ацилированием N-гидроксиорнитина ангидромевалоновой кислотой.
Поликарбоксилаты состоят из содержащего лимонную кислоту поликарбоксилата, называемого ризоферрином. Молекула содержит два остатка лимонной кислоты, соединенные с диаминобутаном. Ризоферрин широко распространен среди представителей типа Zygomycota, отмечен он и в отряде Mucorales, и в отряде Entomophthorales. Другие категории сидерофоров, применимых в качестве хелатирующих железо соединений в композициях изобретения, включают, к примеру, сидерофоры из класса фенолятов-катехолатов, гемин и β-кетоальдегидные фитотоксины.
Количество хелатирующего железо соединения, входящего в композицию по изобретению, может варьировать, но обычно оно составляет терапевтически эффективное количество либо количество, которое может быть восстановлено или разбавлено до терапевтически эффективного количества. Например, эффективные количества хелатирующих железо соединений по изобретению будут описаны ниже при обращении к способам изобретения. Количества одного, некоторых или всех хелатирующих железо соединений вводятся в композицию изобретения в соответствии с этими типичными эффективными количествами.
Хелатирующее железо соединение может вводиться в композицию изобретения также и в количестве, превышающем терапевтически эффективное количество для краткосрочного или долгосрочного хранения, а конечный потребитель может разбавить композицию перед применением до требуемого терапевтически эффективного количества. С другой стороны, хелатирующее железо соединение, входящее в композицию по изобретению, может подвергаться лиофилизации или вырабатываться в виде порошка или иной твердой формы, а конечный потребитель может восстановить сухую композицию перед применением до требуемого терапевтически эффективного количества.
Сухие или концентрированные формы или лекарственные формы, содержащие эффективное количество составных частей, могут содержать хелатирующее железо соединение и противогрибковое средство сами по себе или вместе с любыми желательными наполнителями, поверхностно-активными веществами, тонификаторами, солями или буферами. Разбавление или восстановление может проводиться в фармацевтически приемлемой среде, которой состав доводится до требуемого терапевтически эффективного количества по меньшей мере одного хелатирующего железо соединения и по меньшей мере одного противогрибкового средства и включает любые дополнительные наполнители, поверхностно-активные вещества, тонификаторы, соли или буфера. Лекарственные формы хорошо известны и применяются в фармацевтике. Любые такие известные формы и компоненты лекарственных форм применимы для композиций по изобретению. Лекарственные формы, наполнители, их применение, составление и характеристики хорошо известны в данной области и описаны, к примеру, в Remington: The Science and Practice of Pharmacy, supra; Williams et al., Foye's Principles of Medicinal Chemistry, 5th Ed., Lippincott, Williams & Wilkins (2002); Allen et al., Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems, 8th Ed., Lippincott, Williams & Wilkins (2004). Точно так же поверхностно-активные вещества, их применение, составление и характеристики хорошо известны в данной области и описаны, к примеру, в Holmberg et al., Surfactants and Polymers in Aqueous Solution, supra; Surfactants: A Practical Handbook, K.Robert Lange, ed., supra; и Vogel A.I., Vogel's Textbook of Practical Organic Chemistry, supra.
Композиции изобретения также включают по меньшей мере одно противогрибковое средство. Термин "противогрибковое средство" или "антигрибковое" в настоящем изобретении служит для обозначения средства, которое уничтожает грибки либо подавляет или предотвращает рост, жизнеспособность и/или вирулентность грибков. Типичные категории противогрибковых средств включают полиеновые противогрибковые средства, азоловые противогрибковые средства и эхинокандиновые противогрибковые средства. Конкретные примеры полиеновых противогрибковых средств включают амфотерицин В-дезоксихолат, липосомный амфотерицин В, липидный комплекс амфотерицина В и амфотек. Конкретные примеры азоловых противогрибковых средств включают посаконазол, ворикоазол, флуконазол и итраконазол. Конкретные примеры эхинокандиновых противогрибковых средств включают каспофунгин-ацетат и микафунгин. Многие другие противогрибковые средства известны в этой области и охватываются значением этого термина в настоящем изобретении.
Комбинации из по меньшей мере одного хелатирующего железо соединения и по меньшей мере одного противогрибкового средства нужно выбирать в зависимости от конкретного грибкового заболевания. Например, липидный комплекс амфотерицина В может быть хорошим противогрибковым средством, к примеру, против зигомикоза, (мукормикоза), аспергиллоза и/или кандидамикоза, и его можно комбинировать с таким хелатирующим железо соединением, как деферипрон или деферасирокс. Аналогичным образом одно из приведенных выше противогрибковых средств или другое, известное в этой области, может быть эффективным или терапевтически желательным против другого конкретного заболевания, и одно из них можно комбинировать с хелатирующим железо соединением для получения композиции изобретения. Таким образом, композиции по изобретению являются гибкими по входящим в их состав хелатирующим железо соединениям и входящим в их состав противогрибковым средствам и позволяют всевозможные комбинации и перетасовки при комбинировании по меньшей мере одного хелатирующего железо соединения и по меньшей мере одного противогрибкового средства, к примеру, в одной лекарственной форме.
Соответственно, в одном воплощении изобретением предусмотрены композиции, содержащие по меньшей мере одно хелатирующее железо соединение и по меньшей мере одно противогрибковое средство. Хелатирующее железо соединение может быть выбрано, к примеру, из не встречающихся в природе хелатирующих железо соединений, описанных ранее, типичными примерами которых являются такие представители хелаторов из класса гидроксипиридин-4-онов (НРО), как деферипрон, такие представители хелаторов из класса N-замещенных бис-гидроксифенилтриазолов, как деферасирокс, диэтилентриамин-пентауксусная кислота (DTPA) и дефероксамин. Хелатирующее железо соединение также может быть выбрано, к примеру, из сидерофоров и/или ксеносидерофоров, типичными примерами которых являются, к примеру, гидроксаматы, поликарбоксилаты, сидерофоры из класса фенолятов-катехолатов, гемин и β-кетоальдегидные фитотоксины, описанные ранее.
Противогрибковое средство может быть выбрано, к примеру, из полиеновых противогрибковых средств, таких как амфотерицин В-дезоксихолат, липосомный амфотерицин В, липидный комплекс амфотерицина В или амфотек. Противогрибковое средство также может быть выбрано, к примеру, из азоловых противогрибковых средств, таких как посаконазол, ворикоазол, флуконазол или итраконазол. Противогрибковое средство также может быть выбрано, к примеру, из эхинокандиновых противогрибковых средств, таких как каспофунгин-ацетат или микафунгин. Примером композиции по изобретению, содержащей одно хелатирующее железо соединение в качестве по меньшей мере одного хелатирующего железо соединения и содержащей одно противогрибковое средство в качестве по меньшей мере одного противогрибкового средства, может быть деферасирокс и липидный комплекс амфотерицина В.
Как и количество хелатирующего железо соединения, входящего в композицию изобретения, количество противогрибкового средства также может варьировать, но обычно оно составляет терапевтически эффективное количество либо количество, которое может быть восстановлено или разбавлено до терапевтически эффективного количества. Например, эффективные количества противогрибковых средств по изобретению будут описаны ниже на примере полиеновых противогрибковых средств. Количества одного, некоторых или всех противогрибковых средств вводятся в композицию изобретения в соответствии с этими типичными эффективными количествами для полиеновых противогрибковых средств или в соответствии с хорошо известными эффективными количествами для других противогрибковых средств, таких как азоловые противогрибковые средства или эхинокандиновые противогрибковые средства. Точно так же, как описано в отношении хелатирующих железо соединений, входящих в композицию изобретения, противогрибковое средство тоже может вводить в композицию изобретения в концентрированном виде для краткосрочного или долгосрочного хранения, а конечный потребитель может разбавить композицию перед применением до требуемого терапевтически эффективного количества. Кроме того, противогрибковое средство, входящее в композицию по изобретению, может вырабатываться в лиофилизированном виде или в виде порошка или иной твердой формы, а конечный потребитель может восстановить сухую композицию перед применением до требуемого терапевтически эффективного количества.
Сухие или концентрированные формы или лекарственные формы, содержащие эффективное количество составных частей, могут содержать хелатирующее железо соединение и противогрибковое средство сами по себе или вместе с любыми желательными наполнителями, поверхностно-активными веществами, тонификаторами, солями или буферами. Разбавление или восстановление может проводиться, как описано ранее и приведено, к примеру, в Remington: The Science and Practice of Pharmacy, supra; Williams et al., Foye's Principles of Medicinal Chemistry, 5th Ed., Lippincott, Williams & Wilkins (2002); Allen et al., Ansel's Pharmaceutical Dosage Forms and Drug Delivery Systems, 8th Ed., Lippincott, Williams & Wilkins (2004); Holmberg et al., Surfactants and Polymers in Aqueous Solution, supra; Surfactants: A Practical Handbook, K.Robert Lange, ed., supra; и Vogel A.I., Vogel's Textbook of Practical Organic Chemistry, supra.
Композиции изобретения могут дополнительно содержать два или несколько хелатирующих железо соединений. Включение двух или нескольких хелатирующих железо соединений позволяет воздействовать на множественные грибковые заболевания и/или обеспечивает включение целого ряда аффинностей к железу в хелатирующий железо компонент по изобретению. Включение хелатирующих железо соединений с различным сродством к железу может оказаться терапевтически благоприятным для дополнительного предотвращения ускользания грибковых патогенов.
Композиции изобретения в общем случае содержат порядка 1-8, предпочтительно 2-7, более предпочтительно 3-6 или еще более предпочтительно 4-5 хелатирующих железо соединений. В композициях изобретения можно использовать и больше или промежуточное число хелатирующих железо соединений. Например, можно получить композиции по изобретению, содержащие практически любое нужное число различных хелатирующих железо соединений, в том числе, к примеру, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 или больше.
Композиции изобретения могут дополнительно содержать два или несколько противогрибковых средств. Как и при включении двух или нескольких хелатирующих железо соединений, включение двух или нескольких противогрибковых средств также позволяет воздействовать на множественные грибковые заболевания и/или обеспечивает воздействие на различные грибковые механизмы, используемые для роста, жизнеспособности и вирулентности. Включение нескольких противогрибковых средств тоже может оказаться терапевтически благоприятным для дополнительного предотвращения ускользания грибковых патогенов.
Аналогичным образом, композиции изобретения в общем случае содержат порядка 1-8, предпочтительно 2-7, более предпочтительно 3-6 или еще более предпочтительно 4-5 противогрибковых средств. В композициях изобретения можно использовать и больше или промежуточное число противогрибковых средств. Таким образом, можно получить композиции по изобретению, содержащие практически любое нужное число различных противогрибковых средств, в том числе, к примеру, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 или больше.
Типичные композиции включают деферасирокс и одно или несколько из числа амфотерицина В-дезоксихолата, липосомного амфотерицина В, липидного комплекса амфотерицина В, амфотека, посаконазола, ворикоазола, флуконазола, итраконазола, каспофунгин-ацетата или микафунгина. Деферипрон и деферасирокс и одно или несколько из числа амфотерицина В-дезоксихолата, липосомного амфотерицина В, липидного комплекса амфотерицина В, амфотека, посаконазола, ворикоазола, флуконазола, итраконазола, каспофунгин-ацетата или микафунгина. Особенно полезные композиции включают, к примеру, деферасирокс и/или деферипрон и одно, два, три или несколько противогрибковых средств, выбранных из каждой категории, соответствующей полистовым противогрибковым средствам, азоловым противогрибковым средствам и эхинокандиновым противогрибковым средствам. Таким образом, изобретением предусмотрены любые комбинации из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 или больше хелатирующих железо соединений вместе с любой комбинацией из 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 или больше противогрибковых средств. Такие композиции, содержащие несколько хелатирующих железо соединений и/или несколько противогрибковых средств, могут быть составлены, как описано ранее.
Композиции изобретения также могут включать фармацевтически приемлемую среду. В настоящем изобретении термин "фармацевтически приемлемая среда" служит для обозначения того, что среда, которую смешивают с хелатирующим железо соединением изобретения, обладает достаточной чистотой и качеством для применения на людях. Фармацевтически приемлемая среда охватывает такие лекарственные формы, которые практически свободны от загрязняющих частиц и организмов. Следовательно, этот термин охватывает среды, совместимые с хелатирующими железо соединениями изобретения, и является безопасной и нетоксичной при введении людям. Такие фармацевтически приемлемые среды хорошо известны в этой области.
Изобретением также предусмотрен способ лечения или профилактики грибковых заболеваний. Способ включает введение индивидууму, страдающему или подверженному грибковому заболеванию, терапевтически эффективного количества по меньшей мере одного хелатирующего железо соединения на протяжении достаточного времени для уменьшения тяжести грибкового заболевания, причем хелатирующее железо соединение не является сидерофором или ксеносидерофором в отношении грибкового заболевания.
Изобретением дополнительно предусмотрен способ лечения или профилактики грибковых заболеваний, который включает введение индивидууму, страдающему или подверженному грибковому заболеванию, терапевтически эффективного количества по меньшей мере одного хелатирующего железо соединения и по меньшей мере одного противогрибкового средства на протяжении достаточного времени для уменьшения тяжести грибкового заболевания, причем хелатирующее железо соединение не является сидерофором или ксеносидерофором в отношении грибкового заболевания.
Способы изобретения включают хелатирующую железо терапию саму по себе или вместе с противогрибковой терапией. В первом способе применяется лекарственная форма, включающая по меньшей мере одно хелатирующее железо соединение. В последнем способе применяется лекарственная форма, включающая по меньшей мере одно хелатирующее железо соединение и по меньшей мере одно противогрибковое средство. Такие формы выбираются и получаются, как описано ранее в отношении композиций изобретения. Следовательно, композиция по изобретению может быть получена без по меньшей мере одного противогрибкового средства для применения в хелатирующей железо терапии самой по себе или же она может быть получена с по меньшей мере одним противогрибковым средством для применения в комбинированной хелатирующей железо и противогрибковой терапии. Первая композиция по изобретению также может быть получена без по меньшей мере одного противогрибкового средства, а вторая композиция по изобретению может быть получена без по меньшей мере одного хелатирующего железо соединения. Первый и второй препараты затем могут применяться одновременно, последовательно или поочередно для комбинированной хелатирующей железо и противогрибковой терапии. Таким образом, описанные выше положения и указания в отношении композиции по изобретению могут аналогичным образом использоваться для выбора и получения лекарственной формы, содержащей по меньшей мере одно хелатирующее железо соединение само по себе, лекарственной формы, содержащей по меньшей мере одно противогрибковое средство, или комбинации, содержащей и то, и другое.
Для применения в способах изобретения хелатирующее железо соединение в лекарственной форме, содержащей по меньшей мере одно хелатирующее железо соединение, первом или втором препарате, содержащем по меньшей мере одно хелатирующее железо соединение, и/или композиции по изобретению нужно выбирать таким образом, чтобы оно не являлось сидерофором или ксеносидерофором в отношении грибкового заболевания или грибкового возбудителя заболевания.
Термин "сидерофор" в настоящем изобретении служит для обозначения хелатора железа, способствующего накоплению железа микроорганизмом. Например, в условиях нехватки железа многие грибки синтезируют сидерофоры, которые функционируют в накоплении железа посредством связывания и захвата железа. Сидерофоры обычно являются низкомолекулярными соединениями (например, имеют мол. вес менее 2000) и могут проявлять функции клеточного захвата и/или хранения железа. Сидерофоры синтезируются использующим их организмом. По сравнению с термином "хелатор железа", который обычно применяется безотносительно к конкретному организму или виду, термином "сидерофор" в настоящем изобретении обозначаются хелаторы железа в связи с или в отношении организма или вида, вырабатывающего и использующего этот сидерофор. Соответственно, хотя хелатирующие железо сидерофоры связывают железо и снижают его уровень во внеклеточной среде, однако поскольку они способствуют захвату и использованию железа патогеном, то они обладают низкой терапевтической пользой при использовании для хелатирующей железо терапии в отношении заболеваний, вызванных вырабатывающими сидерофоры организмами. Синтез сидерофоров и их применение описаны, к примеру, в Howard D.H., Clinical Microbiology Reviews 12: 394-404 (1999).
Термин "ксеносидерофор" в настоящем изобретении служит для обозначения сидерофоров, которые не вырабатываются использующим их грибком или организмом. Термином "ксеносидерофор" обозначаются хелаторы железа в связи с или в отношении использующего их организма или вида. Аналогично сидерофорам, ксеносидерофоры обладают терапевтической ценностью при использовании для хелатирующей железо терапии в отношении заболеваний, вызванных не использующими их организмами. Синтез сидерофоров и ксеносидерофоров и их применение описаны, к примеру, в Howard D.H., FEMS Immunology and Medical Microbiology 40: 95-100 (2004).
Таким образом, хелатирующее железо соединение, соответственно не являющееся сидерофором или ксеносидерофором в отношении заданного грибкового заболевания, означает такой сидерофор, который не вырабатывается или не используется грибком-возбудителем грибкового заболевания, либо такой ксеносидерофор, который не используется грибком-возбудителем грибкового заболевания.
Хелатирующие железо лекарственные формы, композиции, в том числе препараты первой и второй составных частей, а также способы изобретения применимы для лечения, уменьшения тяжести, предотвращения и излечения грибковых заболеваний. Особенно полезное применение хелатирующих железо лекарственных форм, композиций и способов изобретения включает профилактическое применение еще до возникновения грибкового заболевания.
Термином "лечить" или "лечение" в настоящем изобретении обозначается улучшение клинического симптома, свидетельствующего о грибковом заболевании. Улучшение клинического симптома включает, к примеру, снижение или уменьшение по меньшей мере одного симптома грибкового заболевания у подлежащего лечению индивидуума по сравнению с уровнем до лечения или по сравнению с индивидуумом, страдающим грибковым заболеванием. Термин "лечить" также включает уменьшение тяжести патологического состояния, хронического осложнения или оппортунистической грибковой инфекции, связанных с грибковым заболеванием. Такие патологические состояния, хронические осложнения или оппортунистические инфекции приводятся ниже на примере мукормикоза. Мукормикоз и другие такие же патологические состояния, хронические осложнения и оппортунистические инфекции описаны, к примеру, в Merck Manual, Sixteenth Edition, 1992; и Spellberg et al., Clin. Microbiol. Rev. 18: 556-69 (2005).
Симптомы грибковых заболеваний, которые могут быть облегчены способом изобретения, включают, к примеру, жар, озноб, потение ночью, анорексию, похудание, недомогание, депрессию и легочные, кожные и другие повреждения. Другие симптомы или характерные проявления включают, к примеру, диссеминацию из первичного очага, острые или подострые высыпания, прогрессирующую пневмонию, фунгемию, проявления внелегочной диссеминации, хронический менингит, прогрессирующий диссеминированный гистоплазмоз в виде генерализованного поражения ретикулоэндотелиальной системы (печени, селезенки, костного мозга) и бластомикоз в виде одиночных или множественных поражений кожи. Эффективное лечение лиц с грибковыми заболеваниями, к примеру, приводит к уменьшению одного или нескольких таких симптомов у больного. Многие другие клинические симптомы грибковых заболеваний хорошо известны в этой области и их можно использовать в качестве меры улучшения или уменьшения тяжести грибковых заболеваний с помощью описанных в изобретении способов.
Диагноз грибкового заболевания может быть подтвержден путем выделения грибка возбудителя, к примеру, из мокроты, мочи, крови, костного мозга или образцов из зараженных тканей. Например, грибковые инфекции с большой степенью надежности можно диагностировать методами гистопатологии, исходя из отличительных морфологических характеристик поражающих грибков и/или методами иммуногистохимии и т.п., избирательными в отношении идентификации антигенов. Оценка активности инфекции также может основываться на культурах, выделенных из многих разных участков, жаре, числе лейкоцитов, клинических и лабораторных параметрах, касающихся конкретных пораженных органов (например, анализе функции печени), и иммуносерологических анализах. Клиническая значимость положительных культур из мокроты может подтверждаться проверкой на инвазию тканей. Такое подтверждение может оказаться особенно полезным в отношении организмов-комменсалов, таких как Candida albicans, или в отношении тех организмов, которые преобладают в окружающей среде, таких как Aspergillus sp.
Термином "предотвращать" или "предотвращение" в настоящем изобретении обозначается предупреждение клинического симптома, свидетельствующего о грибковом заболевании. Предупреждение клинического симптома включает, к примеру, поддержание нормальных физиологических показателей у индивидуума, подвергающегося риску заражения грибком или грибками до возникновения открытых симптомов заболевания или до постановки диагноза заболевания. Следовательно, термин "предотвращать" включает профилактическое лечение индивидуумов для ограждения их от возникновения грибкового заболевания. Предотвращение грибкового заболевания у индивидуума также включает подавление или приостановление развития грибкового заболевания. Подавление или приостановление развития заболевания означает, к примеру, подавление или приостановление появления аномальных физиологических показателей или клинических симптомов типа тех, что описаны выше и/или хорошо известны в этой области. Таким образом, эффективное предотвращение грибкового заболевания должно включать поддержание нормальной температуры тела, веса, психологического состояния, а также отсутствие описанных выше поражений или иных патологических проявлений у лица, предрасположенного к грибковому заболеванию. Лица, предрасположенные к грибковым заболеваниям, включают индивидуумов со СПИДом, азотемией, сахарным диабетом, бронхоэктазией, эмфиземой, туберкулезом, лимфомой, лейкемией или ожогами, либо индивидуумы с историей подверженности грибковым заболеваниям. Подавление или приостановление развития заболевания также включает, к примеру, подавление или приостановление прогрессирования одного или нескольких патологических состояний, хронических осложнений или подверженности оппортунистической инфекции в связи с грибковым заболеванием.
Способы изобретения применимы для лечения и/или предотвращения широкого круга грибковых заболеваний. Термин "грибковое заболевание" в настоящем изобретении служит для обозначения ненормального состояния, вызванного грибковой инфекцией. Грибковые инфекции, или микозы, у людей и животных включают, к примеру, поверхностные грибковые инфекции, поражающие наружные слои кожи; грибковые инфекции слизистых оболочек, включая рот (молочница), вагинальную и анальную области, как то инфекции, вызванные Candida albicans; и грибковые инфекции, поражающие глубокие слои кожи и внутренние органы и способные вызвать серьезные, зачастую смертельные болезни. Грибковые инфекции хорошо известны в этой области и включают, к примеру, зигомикоз, аспергиллоз, криптококкоз, кандидамикоз, гистоплазмоз, кокцидиомикоз, паракокцидиомикоз, фузариоз (гиалогифомикоз), бластомикоз, пенициллиоз или споротрихоз. Эти и другие грибковые инфекции описаны, к примеру, в Merck Manual, Sixteenth Edition, 1992; и Spellberg et al., Clin. Microbiol. Rev. 18: 556-69 (2005). Типичные грибковые заболевания, описанные выше, дополнительно описаны ниже.
В настоящем изобретении термин "зигомикоз" служит для обозначения грибкового заболевания, которое вызывается грибками из класса Zygomycetes, включающего отряды Mucorales и Entomophthorales. Entomophthorales вызывают подкожные и слизисто-кожные инфекции, известные как энтомофторомикозы, которые в основном поражают иммунокомпетентных лиц в развивающихся странах.
В настоящем изобретении термин "мукормикоз" служит для обозначения грибкового заболевания, которое вызывается грибками из отряда Mucorales. Мукормикоз является опасной для жизни грибковой инфекцией, которая почти неизменно поражает лица с ослабленной иммунной системой как в развивающихся, так и в промышленно развитых странах. Принадлежащие к отряду Mucorales грибки распадаются на 6 семейств, причем все они могут вызывать и кожные, и глубокие инфекции. Принадлежащие к семейству Мuсоrасеае виды выделяют из больных мукормикозом чаще, чем виды любого другого семейства. Среди Мuсоrасеае частым возбудителем инфекции является Rhizopus oryzae (Rhizopus arrhizus). Другие типичные виды семейства Мuсоrасеае, вызывающие сходный круг инфекций, включают, к примеру, Rhizopus microsporus var. rhizopodiformis, Absidia corymbifera, Apophysomyces elegans, Mucor spp., Rhizomucor pusillus и Cunninghamella spp. (семейство Cunninghamellaceae). Мукормикоз хорошо известен в этой области и включает, к примеру, риноцеребральный мукормикоз, легочный мукормикоз, желудочно-кишечный мукормикоз, диссеминированный мукормикоз, костный мукормикоз, мукормикоз средостения, мукормикоз трахеи, мукормикоз почек, мукормикоз брюшины, мукормикоз верхней полой вены или мукормикоз наружного уха.
В настоящем изобретении термин "кандидамикоз" служит для обозначения грибкового заболевания, которое вызывается грибками из рода Candida. Кандидамикоз может возникать на коже и слизистых оболочках рта, дыхательных путей и/или влагалища, а также проникать в кровоток, особенно у лиц с ослабленной иммунной системой. Кандидамикоз также известен как кандидоз или монилиаз. Типичными видами рода Candida являются, к примеру, Candida albicans, Candida krusei, Candida tropicalis, Candida glabrata и Candida parapsilosis.
В настоящем изобретении термин "аспергиллоз" служит для обозначения группы заболеваний, которые вызываются родом Aspergillus. Симптомы включают, к примеру, жар, кашель, боли в груди и/или нарушение дыхания. Больные с ослабленной иммунной системой или страдающие легочными заболеваниями особенно подвержены аспергиллозу. Типичными формами этого грибкового заболевания являются аллергический аспергиллоз, который поражает больных астмой, кистическим фиброзом и синуситом; острый инвазивный аспергиллоз, который все чаще встречается у больных с ослабленным иммунитетом, как то больных раком, больных, подвергающихся химиотерапии, и больных СПИДом; диссеминированный инвазивный аспергиллоз, который распространяется по всему организму; и оппортунистическая инфекция Aspergillus, которая характеризуется воспалением и поражением уха и других органов. Род Aspergillus содержит около 200 грибков. Виды Aspergillus, вызывающие инвазивные заболевания, включают, к примеру, Aspergillus fumigatus и Aspergillus flavus. Виды Aspergillus, вызывающие аллергические заболевания, включают, к примеру, Aspergillus fumigatus и Aspergillus clavatus. Другие типичные инфекционные виды Aspergillus включают, к примеру, Aspergillus terreus и Aspergillus nidulans.
В настоящем изобретении термин "криптококкоз" служит для обозначения грибкового заболевания, которое вызывается родом Cryptococcus. Криптококкоз, также известный как болезнь Буссе-Бушке, обычно проявляется в виде системной инфекции, которая может поражать любой орган в организме, в том числе, к примеру, легкие, кожу или другие органы, но чаще всего встречается в центральной нервной системе - головном мозге и оболочках мозга. Криптококкоз является оппортунистической инфекцией при СПИДе, хотя повышенному риску также подвергаются больные лимфомой Ходжкина и другими лимфомами или саркоидозом, а также больные, подвергающиеся долгосрочной кортикостероидной терапии. Симптомы включают, к примеру, боли в груди, сухой кашель, вздутие живота, головные боли, нечеткое зрение и спутанность сознания. Типичными формами этого грибкового заболевания являются кожный криптококкоз, который встречается в ранах, легочный криптококкоз и криптококковый менингит. Криптококковый менингит может возникать при диссеминации Cryptococcus neoformans из наблюдаемой или незамеченной легочной инфекции у больных с ослабленным иммунитетом. У иммунокомпетентных людей инфекции обычно вызывает С. gattii. Одним из полезных методов диагностики является выявление криптококкового антигена (капсулярного) при культивировании спинномозговой жидкости, мокроты и мочи. При тяжелых инфекциях и культуры крови могут быть положительными.
В настоящем изобретении термин "гистоплазмоз" служит для обозначения грибкового заболевания, которое вызывается родом Histoplasma, включая инфекционное заболевание, вызванное вдыханием спор Histoplasma capsulatum. Гистоплазмоз также известен как болезнь Дарлинга. Заболевание может быть бессимптомным, но может прогрессировать в острую пневмонию или гриппообразное заболевание, которое прежде всего поражает легкие. Гистоплазмоз может распространяться и на другие органы и системы в организме. Как и при других диссеминированных формах грибковых заболеваний, такой диссеминированный гистоплазмоз может оказаться смертельным. Симптомы могут появиться в пределах от 3 до 17 дней после контакта. Однако при недиссеминированной форме инфицированные лица обычно не проявляют видимых признаков болезни. Острое респираторное заболевание может характеризоваться респираторными симптомами, общим плохим самочувствием, жаром, болями в груди и сухим или непродуктивным кашлем. К тому же при флюорографии грудной клетки выявляется отчетливая картина. Хроническое легочное заболевание похоже на туберкулез и может обостряться за несколько месяцев или лет.
В настоящем изобретении термин "кокцидиомикоз" служит для обозначения грибкового заболевания, которое вызывается родом Coccidioides. Значение этого термина охватывает инфекционные респираторные заболевания, вызванные Coccidioides immitis или С. posadasii, в частности при вдыхании спор, которые характеризуются различными респираторными симптомами. Кокцидиомикоз также известен как кокцидиоидомикоз и калифорнийская лихорадка. Системный кокцидиомикоз может распространяться из дыхательных путей, к примеру, на кожу, кости и центральную нервную систему. Проявления заболевания колеблются от полного отсутствия симптомов до системной инфекции и смерти. Например, симптоматическая инфекция (около 40% случаев) может проявляться как гриппообразное заболевание с жаром, кашлем, головной болью, сыпью и миалгией (мышечной болью). У некоторых больных не происходит выздоровления и возникает хроническая легочная инфекция или обширная диссеминированная инфекция (которая поражает оболочки мозга, мягкие ткани, суставы и кости). Может возникнуть тяжелое легочное заболевание, к примеру, у ВИЧ-инфицированных и других больных с ослабленной иммунной системой.
В настоящем изобретении термин "паракокцидиомикоз" служит для обозначения грибкового заболевания, которое вызывается родом Paracoccidioides, включая, к примеру, хронический микоз, вызванный Paracoccidioides brasiliensis. Паракокцидиомикоз характеризуется первичным поражением легких с диссеминацией во многие внутренние органы, выраженными язвенными гранулемами слизистых оболочек щек и носа, переходящими на кожу, и генерализованным воспалением лимфатических узлов. Паракокцидиомикоз также известен как паракокцидиоидомикоз, болезнь Альмейды, болезнь Лутца-Сплендора-Альмейды, паракокцидиоидальная гранулема и Южно-Американский бластомикоз.
В настоящем изобретении термин "фузариоз" или "гиалогифомикоз" служит для обозначения грибкового заболевания, которое вызывается родом Fusarium. Вызывающие заболевание виды Fusarium включают, к примеру, F. solani, F. oxysporum и F. moniliforme. Инфекция включает кератит, онихомикоз и иногда перитонит и целлюлит. Факторы риска для диссеминированного фузариоза включают тяжелую иммуносупрессию (нейтропения, лимфопения, реакция "трансплантат против хозяина", кортикостероиды), колонизацию и поражение тканей. У иммунокомпетентных пациентов фактором риска для фузариоза является разрушение тканей (вызванное травмой, тяжелыми ожогами или чужеродным телом). Клиническая картина включает рефракторную лихорадку, поражения кожи и синопульмонарные инфекции. У многих пациентов диагноз устанавливается по поражениям кожи, которые предшествуют фунгемии примерно на 5 дней. Диагноз диссеминированного фузариоза устанавливается, к примеру, по культуре крови и другим известным методам, описанным выше и ниже.
В настоящем изобретении термин "бластомикоз" служит для обозначения грибкового заболевания, которое вызывается родом Blastomyces, в общем возникает как респираторная инфекция и обычно распространяется на легкие, кости и кожу. Бластомикоз характеризуется множественными воспалительными поражениями кожи, слизистых оболочек или внутренних органов. Возбудителем преимущественно является один вид - Blastomyces dermatitidis. Симптомы бластомикоза включают, к примеру, гриппообразное заболевание с жаром, ознобом, миалгией, головной болью и непродуктивным кашлем; острое заболевание похоже на бактериальную пневмонию с симптомами сильного жара, озноба, продуктивного кашля и плевритной боли в груди; хроническое заболевание похоже на туберкулез или рак легких с симптомами слабого жара, продуктивного кашля, ночной потливости и похудания; быстрое, прогрессирующее и тяжелое заболевание, которое проявляется в виде ARDS с жаром, одышкой, тахипноэ и диффузными легочными инфильтратами; поражения кожи; литические поражения костей; простатит и/или поражение гортани, вызывающее хриплость.
В настоящем изобретении термин "пенициллиоз" служит для обозначения грибкового заболевания, которое вызывается родом Penicillium. Типичным видом служит Penicillium marneffei, который является преимущественным возбудителем оппортунистических грибковых инфекций у лиц с ослабленной иммунной системой. Диагноз может быть установлен по идентификации грибков из клинических образцов. Биопсии поражений кожи, лимфатических узлов и костного мозга могут показать наличие микроорганизмов при гистопатологии. Симптомы включают, к примеру, жар, поражения кожи, анемию, генерализованную лимфаденопатию и увеличение печени.
В настоящем изобретении термин "споротрихоз" служит для обозначения грибкового заболевания, которое вызывается родом Sporotrix, включая вид S. schenckii. Заболевание проявляется в виде хронической инфекции, характеризующейся узелками или язвочками в лимфатических узлах и коже. Споротрихозная инфекция может распространяться через кровь на другие области, включая, к примеру, суставы, легкие, глаза, а также мочеполовую и центральную нервную систему. В общем, диссеминированный споротрихоз возникает у лиц с ослабленной иммунной системой, таких как больные СПИДом, раком, больные, подвергающиеся химиотерапии, и реципиенты трансплантатов при иммунодепрессивной терапии.
В настоящем изобретении термины "эффективное количество" или "терапевтически эффективное количество" служат для обозначения такого количества хелатирующего железо соединения, противогрибкового средства или того и другого по изобретению, которое необходимо для уменьшения степени, величины или скорости распространения грибкового заболевания при введении индивидууму. Следовательно, эффективное количество в применении к хелатирующему железо соединению означает такое количество хелатирующего железо соединения, которое достаточно для ослабления по меньшей мере одного симптома, связанного с данным грибковым заболеванием.
Дозировка хелатирующего железо соединения, противогрибкового средства или того и другого по изобретению, необходимая для обеспечения терапевтической эффективности, зависит, к примеру, от подлежащего лечению грибкового заболевания, сродства хелатирующего железо соединения к железу, степени распространенности и концентрации железа, а также веса и состояния индивидуума и предыдущего или параллельного лечения. Надлежащее количество, составляющее эффективную дозу для конкретного применения способа, может быть установлено специалистами в этой области с помощью приведенных в нем правил. Например, это количество может быть экстраполировано из анализов in vitro или in vivo, как описано ниже. Специалисты должны понимать, что нужно отслеживать состояние пациента на протяжении всего курса терапии, а вводимое количество композиции можно корректировать в соответствии с реакцией на лечение.
Типичные эффективные количества хелатирующих железо соединений включают, к примеру, концентрации в пределах от 0,3 до 3,0 мкг/мл, но могут включать и такие низкие концентрации, как 0,01 мкг/мл или меньше, и такие высокие, как 10 мкг/мл или больше. Вводимые количества противогрибкового средства хорошо известны в этой области и охватываются значением термина "эффективное количество".
В доклинических исследованиях деферасирокса, к примеру, практически никакой токсичности не наблюдалось при дозах вплоть до 400 мг/кг/день у перегруженных железом мартышек (Nick et al., Adv. Exp. Med. Biol. 509: 185-203 (2002)). Однако при хроническом введении его мартышкам в отсутствие перегруженности железом наблюдалась сильная токсичность при дозах 80 мг/кг, подтверждая, что деферасирокс хуже переносится в отсутствие перегруженности железом (Id.). Тем не менее, даже в отсутствие перегруженности железом у мартышек не отмечалось токсичности после 39-недельного лечения дозами вплоть до 40 мг/кг/день, а при подостром лечении (4 недели) дозы вплоть до 65 мг/кг/день хорошо переносились без каких-либо неблагоприятных эффектов. В клинических исследованиях на перегруженных железом пациентах (Nisbet-Brown et al., Lancet 361: 1597-1602 (2003); Galanello et al., J. Clin. Pharmacol. 43: 565-572 (2003); Cappellini et al., Blood 107: 3455-3462 (2006)) деферасирокс очень хорошо переносился при дозах вплоть до 40 мг/кг/день на протяжении до 12 дней, а при хроническом введении на протяжении месяцев и лет - вплоть до 30 мг/кг/день.
В общем, хелатирующее железо соединение включают в лекарственную форму для хелатирующей железо терапии, форму для первой или второй составной части и/или композицию изобретения при концентрации 0,01-10 мкг/мл, 0,01-8 мкг/мл, 0,02-6 мкг/мл, предпочтительно 0,3-3,0 мкг/мл, более предпочтительно 0,6-2,0 мкг/мл, еще более предпочтительно 0,8-1,0 мкг/мл или около 0,9 мкг/мл. Также можно использовать меньшие, большие или промежуточные концентрации и/или количества хелатирующего железо соединения в лекарственных формах для хелатирующей железо терапии, формах для первой или второй составной части и/или композициях изобретения. Например, в лекарственную форму или композицию можно включать одно или несколько хелатирующих железо соединений, составляющих менее 0,1 мкг/мл. Аналогичным образом лекарственная форма или композиция может содержать одно или несколько хелатирующих железо соединений в концентрации более 10 мкг/мл, особенно при составлении для хранении. Соответственно, можно получить лекарственную форму или композицию, применимую в способах изобретения, содержащую практически любую желательную концентрацию или количество одного или нескольких хелатирующих железо соединений, включая, к примеру, 0,01, 0,02, 0,03, 0,04, 0,05, 0,06, 0,07, 0,08, 0,09, 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 мкг/мл или больше.
Типичные эффективные количества противогрибковых средств включают, к примеру, количества, приведенные ниже в отношении полиеновых противогрибковых средств. Например, амфотерицин В-дезоксихолат обычно вводится, к примеру, в дозах менее 10 мг/кг массы тела, а при внутривенном введении может включать скорости введения 0,25-1,0 мг/кг/день. Липосомный амфотерицин В (L-AmB) обычно вводится, к примеру, в дозах 1-5 мг/кг. Липосомный амфотерицин В также может вводиться и в таких высоких дозах, как 15 мг/кг/день, особенно при заболеваниях головного мозга. Липидный комплекс амфотерицина В (ABLC) обычно вводится в дозе 5 мг/кг, но может составлять и 0,5-15 мг/кг. Амфотек обычно вводится в однократных дозах 50-100 мг. Аналогичным образом, при комбинированной терапии с помощью хелатирующего железо соединения и противогрибкового средства вышеприведенные количества могут вводиться вместе или же количество одного соединения и/или средства либо обоих можно увеличить или уменьшить. Эффективные количества азоловых противогрибковых средств и эхинокандиновых противогрибковых средств хорошо известны специалистам в этой области и обычно охватывают дозировки в вышеприведенных пределах.
Учитывая приведенные выше положения и указания, специалисты в этой области должны понимать, что вышеприведенные эффективные количества можно модулировать, к примеру, в отношении типа и количества другого активного ингредиента. Например, если дозировка по меньшей мере одного хелатирующего железо соединения попадает в интервал высоких доз, приведенных выше, то при желании можно уменьшить количество одного или нескольких из по меньшей мере одного противогрибкового средства и все-таки получить эффективное количество. Аналогичным образом, если дозировка по меньшей мере одного противогрибкового средства попадает в интервал высоких доз или превышает те, что приведены выше, то при желании можно уменьшить количество одного или нескольких из по меньшей мере одного хелатирующего железо соединения. Дозировки двух или нескольких хелатирующих железо соединений и/или дозировки двух или нескольких противогрибковых средств также можно модулировать относительно друг друга. В способе изобретения можно использовать и все другие модуляции таких комбинированных эффективных количеств.
Подразумевается, что модификации, не затрагивающие существенным образом действие различных воплощений данного изобретения, также попадают под определение изобретения, приведенное в нем. Соответственно, следующие примеры предназначаются для иллюстрации, но не ограничения настоящего изобретения.
Сведения, подтверждающие возможность осуществления изобретения
ПРИМЕР I
Хелатирующая железо терапия для уменьшения тяжести грибковых заболеваний
В данном примере описаны предварительные исследования, показывающие, что деферипрон и Exjade™ могут уменьшать патогенез мукормикоза.
На животных моделях было показано, что введение дефероксамина или свободного железа ухудшает выживаемость животных, инфицированных Rhizopus, но в меньшей степени Candida albicans, что подчеркивает уникальную потребность в железе для патогенности Rhizopus (Abe et al., Mycopathologia 110: 87-91 (1990); Boelaert et al. (1993), supra; Boelaert et al. (1994), supra; Van Cutsem and Boelaert, Kidney International 36: 1061-68 (1989)). Кроме того, опыты in vitro по захвату радиомеченого железа из дефероксамина в сыворотку показали, что Rhizopus накапливает в 8 раз и 40 раз больше железа, чем Aspergillus fumigatus и С. albicans, соответственно (Boelaert et al. (1993), supra)). Такой повышенный захват железа у Rhizopus линейно коррелирует с его ростом в сыворотке (Boelaert et al. (1993), supra)). Повышение роста в сыворотке может объяснить особую склонность Zygomycetes к прямому проникновению и прорастанию через кровеносные сосуды, что вызывает предрасположенность к тромбозу и некрозу тканей при заболевании (Edwards (1989), supra; Ibrahim et al. (2003), supra; Ventura et al., supra)).
Как описано ранее, больные диабетическим кетоацидозом также подвергаются большому риску возникновения риноцеребрального мукормикоза. У этих больных также повышен уровень доступного железа в сыворотке, вероятно, вследствие высвобождения железа из связывающих белков на фоне ацидоза (Artis et al., supra). Сыворотки от больных диабетическим кетоацидозом поддерживали рост R. oryzae на фоне кислого рН (7,3-6,88), но не на фоне щелочного рН (7,78-8,38). Оказалось, что сыворотки, не поддерживающие рост R. oryzae при кислом рН, содержат меньше доступного железа, чем сыворотки, поддерживающие рост грибка. Более того, добавление экзогенного железа в сыворотки способствовало сильному росту R. oryzae в кислых условиях, но не при рН>7,4. Наконец, при воспроизведении кислых условий снижалась способность к связыванию железа у сывороток от нормальных добровольцев, свидетельствуя, что ацидоз временно нарушает способность трансферрина к связыванию железа. Следовательно, повышенная восприимчивость к мукормикозу у больных диабетическим кетоацидозом, вероятно, по крайней мере частично обусловлена повышением доступного железа в сыворотке при диабетическом кетоацидозе.
Роль метаболизма железа в патогенезе мукормикоза дает возможность использовать эффективные хелаторы железа для противогрибковой терапии, в том числе и вспомогательной противогрибковой терапии. В отличие от дефероксамина, другие хелаторы железа не дают возможности микроорганизму захватывать железо и не поддерживают рост in vitro в присутствии железа (например, см. Boelaert et al. (1994), supra)). Более того, хотя дефероксамин вызывал значительное ухудшение при диссеминированной инфекции R. oryzae у морских свинок, один из других хелаторов не оказывал влияния на инфекцию in vivo, а остальные хелаторы увеличивали более чем в два раза среднее время жизни инфицированных морских свинок (табл.1).
Приведенные данные in vitro и in vivo свидетельствуют, что деферипрон может быть использован для эффективного лечения заболевания мукормикозом. В табл.1 представлены результаты предварительного исследования, в котором деферипрон значительно повышал среднее время жизни инфицированных животных. Эти предварительные опыты также показали, что деферипрон очень активен in vitro против R. oryzae, проявляя фунгистатический эффект через 24 ч и фунгицидный эффект через 48 ч инкубации [минимальная ингибирующая концентрация (MIC) и минимальная фунгицидная концентрация (MFC) обе равны 6,25 мкг/мл через 48 ч]. У инфицированных мышей DKA липосомный амфотерицин В (LAmB), который является обычным лекарством против мукормикоза, или деферипрон (Def) улучшали 28-дневную выживаемость по сравнению с плацебо (выживаемость составила 52% в случае LAmB, 30% в случае Def и 0% в случае плацебо, лог-ранговый критерий: р<0,003 для LAmB или Def против плацебо, р=0,15 для LAmB против Def). Эффективность Def устранялась при введении мышам FeCl3, подтверждая, что механизм защитного действия Def заключается в хелатировании железа (фиг.1). Это средство, т.е. деферипрон, разрешено для клинического применения в качестве хелатора железа в Европе и Индии и доступно на сострадательной основе при перегруженности железом в США.
Другой хелатор железа, Exjade™ (Novartis), разрешен для клинического применения на перегруженных железом пациентах в США. Этот препарат тестировали против R. oryzae in vitro и на животной модели - мышах с диабетическим кетоацидозом. Мыши, инфицированные летальной дозой R. oryzae и получавшие Exjade™ в дозах 1, 3 или 10 мг/кг два раза в день, проявляли большее время жизни, чем мыши, получавшие плацебо [28-дневная выживаемость составила 0% в случае плацебо и 29% при 1 мг/кг Exjade (р=0,03), 40% при 3 мг/кг Exjade (р=0,049) и 57% при 10 мг/кг Exjade (p=0,01), всюду лог-ранговый критерий] (фиг.2). Эти опыты свидетельствуют об эффективности применения Exjade™ при лечении мукормикоза. Эти опыты дополнительно свидетельствуют, что вышеуказанные хелаторы железа могут быть применимы для лечения других грибковых заболеваний, включая мукормикоз у лиц с нейтропенией, а также другие инфекции, такие как диссеминированный кандидамикоз и аспергиллоз.
ПРИМЕР II
Хелатирующая железо терапия для лечения мукормикоза
В этом примере представлено сравнение эффективности деферипрона и липо-сомного амфотерицина В (LAmB) при лечении мукормикоза у мышей с диабетическим кетоацидозом (DKA) или профилактике против мукормикоза у мышей с нейтропенией.
R. oryzae является обычным возбудителем мукормикоза (Ibrahim et al. (2003), supra). Больные с повышенным уровнем доступного железа в сыворотке, как то диабетики с кетоацидозом, подвергаются большому риску возникновения инфекции мукормикоза (Artis et al., supra). Кроме того, хелатирующая железо терапия дефероксамином вызывает у больных предрасположенность к этим инфекциям. Дефероксамин действует в качестве ксеносидерофора, поставляя прежде недоступное железо грибку (Boelaert et al. (1993), supra)). Поэтому оценивали применение такого хелатора железа, который не может использоваться грибком для извлечения железа из организма хозяина, на эффективность против мукормикоза. Def является таким хелатором железа, который не может использоваться грибком Rhizopus для извлечения железа (Boelaert et al. (1994), supra)).
Сначала в этом исследовании оценивали действие деферипрона против R. oryzae in vitro. Вкратце, выделяли R. oryzae 99-880 из абсцесса головного мозга больного диабетом. Микроорганизм выращивали на агаре с картофельной декстрозой (PDA) в течение 3 дней при 37°С. В некоторых экспериментах R. oryzae подвергали голоданию по железу путем культивирования на PDA в присутствии 1 мМ аскорбиновой кислоты и феррозина. Спорангиоспоры собирали в лишенный эндотоксинов PBS, содержащий 0,01% твин-80, промывали с помощью PBS, а затем просчитывали на гемацитометре для приготовления конечного инокулята. Для тестирования на чувствительность определяли минимальную ингибирующую концентрацию (MIC) и минимальную фунгицидную концентрацию (MFC) для Def и дефероксамина по методу Espinel-Ingroff (J. Clin. Microbiol. 39:954 (2001)).
Результаты представлены ниже в табл.2. Деферипрон действовал как фунгистатик против R. oryzae через 24 ч (MIC и MFC=3,12 и 100 мкг/мл, соответственно), но проявлял фугицидность через 48 ч инкубации (MIC и MFC=6,25 мкг/мл). Напротив, дефероксамин, который поставляет железо R. oryzae, не ингибировал рост R. oryzae (MIC и MFC>100 мкг/мл через 24 или 48 ч), и в самом деле при визуальном осмотре рост в лунках, содержащих дефероксамин, оказался сильнее, чем в контрольных лунках (не содержащих хелаторов железа).
После подтверждения его действия против R. oryzae in vitro использовали модель на мышах DKA для оценки роли деферипрона при лечении диссеминированной инфекции R. oryzae in vivo. Вкратце, перед инфицированием in vivo у самцов мышей BALB/c (≥20 г) вызывали диабет с помощью однократной инъекции 210 мг/кг стрептозотоцина в 0,2 мл цитратного буфера внутрибрюшинно за 10 дней до заражения грибком. Через 7 дней после обработки стрептозотоцином у всех мышей была подтверждена гликозурия и кетонурия. Мышей инфицировали через хвостовую вену соответствующим инокулятом R. oryzae. Для проверки инокулята делали разведения и штриховали на чашки с PDA, а после инкубации в течение 24 ч при комнатной температуре подсчитывали колонии. Первичным показателем эффективности служило время до наступления смерти. В качестве вторичного показателя определяли обсемененность мозга (главного органа-мишени) грибком при гомогенизации путем прокачивания пипеткой органов, помещенных в мешочки Whirl-Pak (Nasco, Fort Atkinson, WI), содержащие 2 мл физраствора. Делали серийные разведения гомогената в 0,85% физрастворе, а затем количественно культивировали на PDA. Значения выражали в log10KOE на г ткани. Все процедуры с участием мышей были одобрены институтским комитетом по использованию и содержанию животных в соответствии с директивами Национальных институтов здравоохранения по размещению и содержанию животных.
Препараты и режимы терапии: LAmB, разведенный в 5% растворе декстрозы, получали из Gilead Sciences и вводили внутривенно в дозе 15 мг/кг раз в день через хвостовую вену. Деферипрон (Apotex Research Inc.) растворяли в свободной от железа воде и вводили внутрибрюшинно в дозе 50, 100 или 200 мг/кг раз в день или через день. Обработку начинали через 24 ч после инфицирования и продолжали в совокупности 4 дозы. Контрольные группы получали растворитель - 5% раствор декстрозы.
В некоторых экспериментах вместе с деферипроном вводили насыщающую дозу свободного железа с тем, чтобы устранить эффект хелатирования железа. Известно, что деферипрон образует молекулярные комплексы с трехвалентным железом (Fe3+) при соотношении железа к деферипрону 1:3. Исходя из известных молекулярных весов хлорида железа (III) (FeCl3, молекулярный вес 162,22 г/моль) и деферипрона (молекулярный вес 139 г/моль) было рассчитано, что введение дозы FeCl3 в 60 мг/кг приведет к значительному избытку железа при дозе деферипрона в 100 мг/кг на мышь весом 18 г: число молей Fe3+=(0,060 г/кг × 0,018 [вес мыши] / 162,22 г/моль)=6,5×10-6 моль, а число молей деферипрона = (0,1 г/кг × 0,018 [вес мыши] / 139 г/моль)=1,3×10-5 моль. Молярное отношение Fe3+ к деферипрону составляет 1:2, что больше, чем нужно для достижения насыщающего соотношения 1:3.
Статистический анализ выполняли с помощью непараметрического лог-рангового критерия при определении отличий по времени жизни мышей. Отличия по обсемененности тканей грибком в инфицированных органах устанавливали по непараметрическому критерию Стила для множественных сравнений. Значения р<0,05 считались значимыми.
Сначала устанавливали зависимость доза-эффект, используя дозы, основанные на неопубликованных наблюдениях изготовителя (50, 100 или 200 мг/кг раз в день или через день). Мышей инфицировали 4,3×103 спор R. oryzae и через 24 ч после инфицирования начинали обработку деферипроном, в совокупности 4 дозы. Результаты представлены на фиг.3 и фиг.1, которые свидетельствуют, что деферипрон защищал мышей DKA от инфекции R. oryzae. При дозировке деферипрона в 100 мг/кг через день выживаемость мышей DKA улучшалась по сравнению с плацебо (р=0,027, фиг.3). Повышение дозы, включая 100 мг/кг раз в день или 200 мг/кг раз в день или через день, не давало улучшения выживаемости, как и дозировки в 50 мг/кг раз в день или через день.
Как описано ранее в Примере 1, эффективность деферипрона также сравнивали с обычным способом лечения мукормикоза, т.е. LAmB в высоких дозах. Была выбрана дозировка LAmB в 15 мг/кг раз в день, так как мы показали, что эта доза обеспечивает большую защиту на модели у мышей DKA, чем 1 мг/кг амфотерицина В-дезоксихолата. К тому же для проверки того, что защитный механизм деферипрона заключается в хелатировании железа, также оценивали эффективность деферипрона вместе с насыщающей дозой (60 мг/кг) свободного железа в виде FeCl3. FeCl3 вводили внутривенно каждый раз, когда животным давали деферипрон.
LAmB или деферипрон при дозировке 100 мг/кг через день улучшал 28-дневную выживаемость по сравнению с плацебо (фиг.1, р<0,003, лог-ранговый критерий для LAmB или деферипрона против плацебо). Не было статистических отличий по выживаемости между мышами, получавшими LAmB, и мышами, получавшими деферипрон (р=0,15). Эффективность деферипрона полностью устранялась при введении хлорида железа (III) (фиг.1).
В дополнительных опытах также оценивали лечение экспериментального мукормикоза с помощью комбинации LAmB и Def. Вкратце, мышей (n=11 для инфицированных без обработки и Def и n=6 для LAmB и Def+LAmB) инфицировали R. oryzae, а затем через 24 ч вводили Def, LAmB или комбинацию из обоих препаратов, в совокупности 4 дозы. Результаты представлены на фиг.4 и свидетельствуют об усилении эффективности при комбинировании обоих препаратов (* означает р<0,005 по сравнению с инфицированными мышами без обработки).
Аналогичным образом оценивали выживаемость мышей с нейтропенией, инфицированных R.oryzae и подвергнутых профилактике с помощью Def, LAmB или обоих препаратов. Мышей (n=9) в день -1 обрабатывали Def через день, LAmB раз в день или обоими препаратами, в совокупности 4 дозы. Эти результаты представлены на фиг.5 и также свидетельствуют об усилении эффективности при комбинировании противогрибкового лечения с хелатированием железа (* означает р<0,05 для LAmB или LAmB+Def по сравнению с инфицированными без обработки). Например, профилактика с помощью Def обеспечила выживаемость в 22% по сравнению с 0% у мышей, получавших плацебо (р>0,05); a LAmB и LAmB+Def обеспечивали выживаемость в 100% (р 0,05 против плацебо для обоих).
В качестве дополнительного маркера эффективности также исследовали влияние терапии деферипроном на обсемененность грибком головного мозга, поскольку мозг является главным органом-мишенью на этой животной модели. Мышей инфицировали 3,8×103 спор, а затем обрабатывали двумя дозами LAmB (раз в день) или деферипрона (через день). В предыдущих опытах контрольные мыши начинали погибать еще до введения второй дозы деферипрона. Для того чтобы протестировать хотя бы две дозы деферипрона через день перед определением обсемененности ткани грибком, в этих опытах деферипрон вводили через 30 мин и 48 ч после инфицирования, а LAmB вводили через 24 ч и 48 ч после инфицирования. Мозги извлекали примерно через 54 ч после инфицирования. Результаты представлены на фиг.6 и свидетельствуют о том, что оба препарата снижали обсемененность мозга грибком по сравнению с плацебо (р≤0,036).
Вышеприведенные результаты свидетельствуют о том, что хелатирующая железо терапия с помощью Def эффективна при лечении экспериментального мукормикоза мышей, а также обладает профилактическим эффектом, в том числе и при нейтропении. В частности, Def ингибировал рост R.oryzae in vitro, тогда как дефероксамин - нет. Def обладает значительной эффективностью при лечении мукормикоза на DKA-модели, и эта эффективность сравнима с терапией высокими дозами LAmB. Вероятно, эффективность Def обусловлена его способностью хелатировать железо, поскольку введение свободого железа устраняло защитный эффект. Профилактика с помощью Def, по-видимому, не препятствует защитному эффекту LAmB на модели мукормикоза у мышей с нейтропенией.
ПРИМЕР III
Применение деферасирокса для терапевтического лечения мукормикоза
В этом примере представлено применение деферасирокса - хелатирующего железо реагента в качестве спасательной терапии риноцеребрального мукормикоза.
Деферасирокс (Exjade®) является новым первоклассным пероральным хелатором железа, недавно получившим разрешение FDA США для лечения перегруженности железом при посттрансфузионной анемии. В данном исследовании описано применение деферасирокса в качестве спасательной терапии для больных риноцеребральным мукормикозом, не поддающихся максимальной стандартной противогрибковой терапии.
Мужчина 40 лет с диабетическим кетоацидозом попал в отделение скорой помощи посторонней больницы с полиурией, полидипсией, болью в области левого ресничного узла и парезом левого черепного нерва (CN) VI. Компьютерная томография (СТ) головы показала только синусит левой клиновидной и решетчатой пазухи. За первые 24 часа состояние больного прогрессировало до полной левой офтальмоплегии. Был заподозрен риноцеребральный мукормикоз, и ему начали вводить липидный комплекс амфотерицина В (ABLC) в дозе 5 мг/кг/день, вместе с подобранными эмпирически противобактериальными средствами для лечения синусита. На 2-й день пребывания в больнице его подвергли эндоскопическому исследованию клиновидной и решетчатой пазухи. Не было обнаружено некротических тканей или струпа, а множественные биопсии показали неспецифическое воспаление. Посев на грибки оказался отрицательным, а специальное окрашивание не выявило никаких организмов. Посев на бактерии дал только редкие Entarobacter aerogenes.
В течение следующих 12 дней у больного возникла слепота и усилился проптоз в левом глазу. Ему продолжали вводить ABLC и не делали никакой хирургии. Серийная магнитно-резонансная интраскопия (MRI) глазниц и мозга показала прогрессирование левостороннего пансинусита, а также утолщение и аномальное увеличение левых наружных глазных мышц.
Больной был переведен в наш институт для дальнейшего лечения на 14-й день пребывания в больнице. Сразу же по прибытии он был подвергнут экзентерации левой глазницы с энуклеацией и всестороннему очищению и резекции пазух. Полученные во время операции данные включали ишемию глазного яблока с обширным окружающим некрозом наружных глазных мышц. Патологические образцы свидетельствовали о Mucorales (фиг.7), но посев на грибки оказался отрицательным. Больному начали вводить липосомный амфотерицин В (LAmB) в дозе 15 мг/кг/день и каспофунгин в дозе 70 мг/кг/день (исходя из опубликованных данных на мышах, свидетельствующих о синергизме между полиенами и эхинокандинами). СТ головы, проведенная через 2 дня после экзентерации глазницы, показала тромбоз левой пещеристой пазухи; этот результат был подтвержден при последующей интраскопии MRI.
Несмотря на отсутствие новых неврологических данных, интраскопия MRI на 36-й день пребывания в больнице показала прогрессирование тромбоза левой пещеристой пазухи с замедлением кровотока в левой внутренней сонной артерии и увеличением нового черепного нерва (CN) V, что согласуется с прогрессированием мукормикоза. Противогрибковая терапия была продолжена. На 71-й день пребывания в больнице MRI мозга показала новое увеличение в супраселлярной цистерне, и впервые возникло повреждение ствола мозга в области моста с обступающим отеком. Учитывая локализацию повреждения на внешней стороне моста, ввели дозу амфотерицина в полость цистерны, но больной отказался от дальнейших доз. Состояние больного в клиническом и неврологическом отношении оставалось без изменений. Поскольку последующая интраскопия показала стабилизацию, на 86-й день пребывания в больнице он был выписан с условием продолжения монотерапии LAmB три раза в неделю амбулаторно.
Заболевание в клиническом и неврологическом отношении оставалось неизменным на протяжении нескольких месяцев. Вследствие ухудшения почечной недостаточности (Cr 3,5-4,0 от исходного 0,8), через 10 недель после выписки доза LAmB была снижена до 10 мг/кг два раза в неделю, а затем уменьшена до одного раза в неделю через 4 месяца после выписки. Еще через месяц повторная MRI показала новое увеличение с обступающим отеком в левой средней части ножки мозга и левом мостомозжечковом углу, что свидетельствует о прогрессировании болезни.
Исходя из данных по экспериментальному хелатору железа - деферипрону, а также неопубликованных наблюдений по деферасироксу на мышах, стали давать деферасирокс в дозе 1000 мг в день per os на протяжении 7 дней. И продолжали вводить LAmB. В последний день применения деферасирокса у больного возникла эритематозная, слегка зудящая, сплошная пятнисто-узловатая сыпь на туловище и конечностях, весьма похожая на лекарственную сыпь. Прурит пролечили дифенгидрамином. Других неблагоприятных эффектов не наблюдалось. Повторная MRI мозга через 1 неделю после применения деферасирокса показала разрешение отека в левой ножке мозга. Последующая интраскопия через 5 недель показала отсутствие новых повреждений. Вследствие ухудшения почечной недостаточности (Cr ~ 5,5) и на фоне стабильности радиографических данных при повторной интраскопии LAmB был отменен. Через 10 мес. после первоначального диагноза больной не обнаруживал симптомов и неврологических повреждений.
Описанный больной явно не излечился от инвазивного мукормикоза, несмотря на всестороннюю хирургию и месяцы противогрибковой терапии, так как у него появились новые радиографические данные, свидетельствующие о прогрессирующем мукормикозе после 7 месяцев лечения максимально допустимыми дозами LAmB. Однако после 7 дней лечения деферасироксом отмечалось существенное радиографическое улучшение. Через 2 месяца после применения деферасирокса всякая противогрибковая терапия была прекращена. После этого больной не обнаруживал клинических симптомов и оставался радиографически стабильным, без каких-либо признаков прогрессирования болезни. Больной хорошо переносил деферасирокс, за исключением легкой реакции на препарат, которую можно было отнести на счет хелатора.
Мы описали случай запущенного мукормикоза с поражением ствола мозга и пещеристой пазухи после заметного опоздания в проведении надлежащей хирургии и с несомненно успешным исходом после применения деферасирокса для спасательной терапии. Точный эффект лечения деферасироксом несколько затемнен проводившейся одновременно полиеновой терапией. Однако до добавления деферасирокса больной явно не поддавался очень агрессивной полиеновой терапии. Учитывая обнадеживающие результаты в данном случае, а также ограниченный набор альтернатив и плохой прогноз при мукормикозе, несмотря на текущие противогрибковые терапии, дополнительное изучение хелатирования железа при лечении мукормикоза будет оправдано.
ПРИМЕР IV Эффекты деферасирокса на Mucorales in vitro
В этом примере представлены эффекты деферасирокса на экспрессию гена высокоаффинной пермеазы железа (rFTR1) у Rhizopus oryzae. В этом примере также представлена чувствительность к деферасироксу нескольких клинических изолятов Mucorales.
Далее следует описание материалов и методов, использовавшихся в процедурах, описанных в этом или последующих примерах.
R. oryzae и условия культивирования
R. oryzae 99-880 является клиническим изолятом из абсцесса мозга больного диабетом. R. oryzae 99-892 является клиническим изолятом из легких. R. oryzae M16 является нулевым мутантом по pyrF (pyrF кодирует орнитин-5'-фосфатдекарбоксилазу - фермент, необходимый для синтеза урацила), который получен из R. oryzae 99-880 путем химического мутагенеза. Этот мутант устойчивый ауксотрофный фенотип по урацилу даже при посеве более 1×109 спор. Микроорганизмы выращивали на агаре с картофельной декстрозой (PDA) [состав на 1 л: 4 г картофельного крахмала, 20 г декстрозы, 15 г агара] в течение 4 дней при 37°С. Для M16 в PDA добавляли 100 мкг/мл урацила. В некоторых экспериментах R. oryzae подвергали голоданию по железу путем культивирования на дрожжевой азотистой основе (YNB) (Difco/Becton Dickinson, Sparks, MD) с добавлением полной добавочной среды без урацила (CSM-Ura), т.е. YNB+CSM-Ura) [состав на 100 мл: 1,7 г YNB без аминокислот, 20 г глюкозы, 0,77 г CSM-Ura] в присутствии 1 мМ аскорбиновой кислоты и феррозина. Спорангиоспоры собирали в лишенный эндотоксинов PBS, содержащий 0,01% твин-80, промывали с помощью PBS и просчитывали на гемацитометре для приготовления конечного инокулята.
Анализ экспрессии гена высокоаффинной пермеазы железа R. oryzae (rFTR1)
Пробы R. oryzae 99-880, взятые из конфлуэнтной чашки с PDA, культивировали в картофельном бульоне с декстрозой (PDB) в течение ночи при 37°С со встряхиванием. Мицелии собирали асептически и переносили в колбы со свежим PDB, содержащим 350 мкМ FeCl3 (чтобы подавить экспрессию rFTRl), 350 мкМ FeCl3+2 мМ деферасирокса для проверки хелатирования железа или 2 мМ деферасирокса + 6 мМ FeCl3 для сверхнасыщения добавленного деферасирокса. Колбы инкубировали в течение 1 ч при 37°С со встряхиванием. Мицелий собирали фильтрованием и растирали в жидком азоте в ступке с помощью пестика. Тотальную РНК экстрагировали с помощью набора RNEasy Plabt Mini™ kit (Qiagen) в буфере RLC. РНК подвергали обратной транскрипции с праймером олиго(dТ) с помощью системы Superscript™ First-Strand Synthesis System (Invitrogen) для получения первой нити кДНК. Продукты разбавляли и использовали в реакции ПЦР для детектирования экспрессии FTR1 R. oryzae и гена 18S-рДНК. Праймеры для ПЦР имели следующие последовательности: смысловой праймер 5'-TCAGAGAAGGACTTGAAGC-3' и антисмысловой праймер 5'-TAAGTAGCCGTATTGTTCC-3' для амплификации rFTR1 R. oryzae; смысловой праймер 5'-CATGGTTGAGATTGTAAGATAG-3' и антисмысловой праймер 5'-AGTCAATGGACGTGGAGTC-3' для гена 18S-pHHK. Продукты ПЦР разделяли на 2% агарозном геле, содержащем 0,1 мкг/мл этидия бромида. Оба набора праймеров предназначались для амплификации полос в 400 п.о.
Метод зеленого флуоресцентного белка (GFP) как репортера
Подвергали ПЦР-амплификации находящийся выше от ORF rFTR1 фрагмент в 1,5 т.п.о. с помощью следующей пары праймеров: смысловой праймер 5'-GCTCTAGATCAGTCTCAACACCATCAATT-3' и антисмысловой праймер 5'-TGCGGCCGTGCTTTTTAGTTCTCCTTGGA-3'. Также подвергали ПЦР-амплификации служащий в качестве контроля фрагмент в 2,1 т.п.о., содержащий экспрессирующийся конститутивно промотор актина, с помощью следующий пары праймеров: смысловой праймер 5'-GCTCTAGATGGTATTATCGATTTAGA-3' и антисмысловой праймер 5'-TACGGCCGCATACCGGAACCGTTATCG-3'. Амплифицированные фрагменты лигировали по сайтам XbaI и EagI в плазмиду pyr225b (35). GFP амплифицировали из pGFPB21-43.31 (36) и клонировали в плазмиду ниже от одного из промоторов по сайтам EagI-SacI. Наконец, фрагмент 2,1 т.п.о., представляющий собой ORF pyrF и его нативный промотор, клонировали в плазмиду по сайтам SpeI-ClaI в качестве селекционного маркера. Плазмиды, содержащие GFP под управлением rFTR1p или ACT1p, вводили в R. oryzae M16 путем трансформации методом бомбардирования микрочастицами (BioRad). Селекцию трансформантов проводили на чашках со средой YNB+CSM-Ura путем культивирования при 37°С в течение 5-7 дней после бомбардирования. Затем изоляты тестировали на ауксотрофность по урацилу путем пересева трансформантов на чашки, содержащие минимальную среду без урацила, и инкубации их при 37°С. Очищенных трансформантов, прошедших селекцию на лишенных урацила чашках, анализировали методом Southern-гибридизации.
Экспрессию rFTR1p и ACT1p исследовали на трансформантах, культивируемых в богатой железом среде (т.е. YNB+CSM-Ura) или в обедненных железом условиях (т.е. YNB+CSM-Ura с добавлением 2 мМ деферасирокса). Кроме того, для устранения эффекта деферасирокса трансформантов культивировали в YNB+CSM-Ura с добавлением 2 мМ деферасирокса и сверхнасыщения 6 мМ FeCl3. Наконец, в качестве отрицательного контроля использовали M16, трансформированных пустой плазмидой (pyr225b-pyrF без GFP). Вышеуказанные среды инокулировали спорами (1×104/мл) и инкубировали в течение ночи при 37°С. На предметное стекло наносили каплю культуры и визуализировали экспрессию GFP в R. oryzae с помощью конфокального микроскопа Leica DMRXE с возбуждением при 488 нм. Кроме того, также использовали по 1 мл из каждой культуры для количественного измерения излучаемой флуоресценции на приборе FACSCaliber™ (Becton Dickison), снабженном аргоновым лазером, излучающим при 488 нм. Споры засекали по прямому и боковому рассеянию света и измеряли флуоресценцию в канале FL1.
Тестирование на чувствительность
Минимальную ингибирующую концентрацию (MIC) и минимальную фунгицидную концентрацию (MFC) для деферасирокса определяли по методу Espinel-Ingroff, используя споры R. oryzae, подвергнутые голоданию по железу (Espinel-Ingroff (2001), supra)). Фунгицидность задавали как ≤4-кратное отличие между MIC и MFC.
Режимы обработки
Деферасирокс (Novartis Pharmaceuticals, Basel, Швейцария) суспендировали в 0,5% гидроксипропилцеллюлозе (Klucel) и вводили гаважем в дозе 1, 3 или 10 мг/кг раз в день (qd) или через день (qod). Обработку начинали через 24 ч после инфицирования и продолжали в совокупности 5 или 7 доз. Контрольные группы получали растворитель - 5% раствор декстрозы и 0,5% Klucel. В некоторых опытах вместе с деферасироксом вводили насыщающую дозу свободного железа. Известно, что деферасирокс образует молекулярные комплексы с трехвалентным железом (Fe3+) при соотношении железа к деферасироксу 1:2. Исходя из известных молекулярных весов хлорида железа (III) (FeCl3, молекулярный вес 162,22 г/моль) и деферасирокса (молекулярный вес 373,4 г/моль) было рассчитано, что введение дозы FeCl3 в 2,8 мг/кг приведет к значительному избытку Fe3+ при дозе деферасирокса в 10 мг/кг на мышь весом 18 г: число молей Fe3+=(0,0028 г/кг × 0,018 [вес мыши] / 162,22 г/моль)=3×10-7 моль, а число молей деферасирокса = (0,01 г/кг × 0,018 [вес мыши] / 373,4 г/моль)=5×10-7 моль. Молярное отношение Fe3+ к деферасироксу составляет 1:1,7, что больше, чем нужно для достижения насыщающего соотношения 1:2. LAmB, разведенный в 5% растворе декстрозы, получали из Gilead Sciences (Foster City, CA) и вводили в дозе 15 мг/кг раз в день через хвостовую вену на протяжении 4 дней.
Статистический анализ
Использовали непараметрический лог-ранговый критерий для определении отличий по времени жизни мышей. Отличия по обсемененности тканей грибком, частотности лимфоцитов в селезенке и содержанию цитокинов в инфицированных органах устанавливали по U-критерию Манна-Уитни. Значения р<0,05 считались значимыми.
Ранее было показано (Fu et al., FEMS Microbiol. Lett. 235: 169-176 (2004)), что голодание по железу вызывает быструю экспрессию гена высокоаффинной пермеазы железа (rFTRl) у Rhizopus oryzae, самого частого возбудителя мукормикоза. Поэтому для проверки того, что деферасирокс эффективно хелатирует железо из R. oryzae, изучали влияние обработки деферасироксом in vitro на экспрессию rFTR1 R. oryzae. Споры R. oryzae 99-880 инкубировали в течение ночи в среде PDB. На следующий день мицелий переносили в PDB с добавлением 350 мкМ FeCl3 (много железа), 350 мкМ FeCl3+2 мМ деферасирокса (мало железа) или 2 мМ деферасирокса + сверхнасыщение 6 мМ FeCl3. Из спор, культивированных при каждых условиях в течение 1 ч при 37°С, экстрагировали РНК и выполняли ОТ-ПЦР для оценки экспрессии гена. Ген rFTR1 экспрессировался в присутствии деферасирокса, но не в среде с добавлением FeCl3 и не в присутствии деферасирокса и сверхнасыщения FeCl3 (фиг.8а).
Для проверки экспрессии rFTR1p и активности промотора rFTR1 в условиях хелатирования ген, кодирующий зеленый флуоресцентный белок (GFP), клонировали за промотором rFTR1 (фиг.8b). Споры R. oryzae M16, трансформированные конструкцией rFTR1::GFP или ACT1p::GFP (конститутивный отрицательный контроль), инкубировали в течение ночи в средах с деферасироксом, деферасироксом+сверхнасыщающим FeCl3 или богатой железом среде. Фиг.8с показывает, что в отличие от GFP под контролем промотора АСТ1, который экспрессировался конститутивно вне зависимости от условий культивирования, GFP под контролем промотора rFTR1 экспрессировался или проявлял активность только на фоне условий хелатирования железа (деферасирокс). Как показала конфокальная микроскопия, M16, трансформированные конститутивной конструкцией ACT1p::GFP, флуоресцировали независимо от условий культивирования. Напротив, M16, трансформированные rFTR1::GFP, флуоресцировали только в присутствии деферасирокса. Аналогичным образом, по данным проточной цитометрии флуоресцировали менее 1% нетрансфомированных или трансформированных rFTR1::GFP спор, культивированных в богатых железом условиях. И наоборот, флуоресцировали 43% спор, трансформированных rFTR1::GFP и культивированных в присутствии деферасирокса. В совокупности эти данные подтверждают, что деферасирокс вызывал реакцию голодания по железу у R. oryzae.
Далее определяли чувствительность к деферасироксу у многих клинических изолятов Mucorales (табл.3). Значения MIC90 деферасирокса против Mucor, Rhizopus spp. (кроме oryzae) и R. oryzae составляли от 3,12 до 6,25 мкг/мл. Значения MFC были близки к значениям MIC, а деферасирокс оказался фунгицидом для 28/29 (97%) изолятов. Отметим, что небольшой рост наблюдался в первые 12 часов даже при чрезвычайно высоких концентрациях деферасирокса. Однако эти грибки погибали к 24 часам даже при низких концентрациях деферасирокса, свидетельствуя о том, что фунгицидное действие деферасирокса зависит скорее от времени, чем от концентрации. Более того, значения MIC и MFC деферасирокса против этих изолятов были существенно ниже клинически достижимых высших (~38 мкг/мл) и низших (~17 мкг/мл) уровней препарата в сыворотке крови в стационарном состоянии при введении в разрешенной FDA начальной дозе (20 мг/кг/день).
Этот пример, наряду со свидетельством того, что деферасирокс вызывает реакцию голодания по железу у R. oryzae, показал и то, что деферасирокс является фунгицидом для многих клинических изолятов из двух разных родов семейства Mucorales.
ПРИМЕР V
Эффективность деферасирокса против R. oryzae in vivo
В этом примере представлена эффективность деферасирокса in vivo при лечении мышей, инфицированных Mucorales.
Далее следует описание материалов и методов, использовавшихся в процедурах, описанных в этом или последующих примерах.
Модели на мышах
Для инфицирования in vivo у самцов мышей BALB/c (>20 г) вызывали диабет с помощью однократной инъекции 210 мг/кг стрептозотоцина в 0,2 мл цитратного буфера внутрибрюшинно за 10 дней до заражения грибком. Через 7 дней после обработки стрептозотоцином у всех мышей была подтверждена гликозурия и кетонурия. Для модели на мышах с нейтропенией им делали однократные инъекции циклофосфамида (Bristol Myer Squibb) в дозе 200 мг/кг внутрибрюшинно за 2 дня до заражения R. oryzae. Такая схема обработки приводила к панцитопении с - 2-го дня по 5-й день относительно инфицирования, причем восстановление числа клеток начиналось на 6-й день после инфицирования. Мышей инфицировали через хвостовую вену соответствующим инокулятом R. oryzae. Для проверки инокулята делали разведения и штриховали на чашки с PDA, содержащие 0,1% тритона, и подсчитывали колонии после инкубации в течение 24 ч при 37°С. Первичным показателем эффективности служило время до наступления смерти. В качестве вторичного показателя определяли обсемененность мозга (главного органа-мишени) грибком при гомогенизации путем прокачивания пипеткой органов, помещенных в мешочки Whirl-Pak™ (Nasco, Fort Atkinson, WI), содержащие 1 мл физраствора. Делали серийные разведения гомогената в 0,85% физрастворе, а затем количественно культивировали на PDA. Значения выражали в log10KOE на г ткани. Наконец, для гистопатологического анализа из мышей извлекали зараженные органы и фиксировали в 10% цинк-формалине. Фиксированные ткани заключали в парафин, а срезы в 5 мкм окрашивали гематоксилином и эозином для исследования методом световой микроскопии. Все процедуры с участием мышей были одобрены институтским комитетом по использованию и содержанию животных в соответствии с директивами Национальных институтов здравоохранения по размещению и содержанию животных.
Чтобы установить, будет ли активность деферасирокса in vitro претворяться в эффективность in vivo, использовали модель диссеминированного мукормикоза на мышах с диабетическим кетоацидозом. Мышей с диабетическим кетоацидозом инфицировали через хвостовую вену 2,2×104 спор R. oryzae 99-892. Начиная со следующего дня после инфицирования, мышам гаважем вводили 1, 3 или 10 мг/кг деферасирокса в 0,5% гидроксипропилцеллюлозе (Klucel) два раза в день (bid) на протяжении 7 дней. Мыши отрицательного контроля получали носитель - гидроксипропилцеллюлозу (плацебо) или деферасирокс+насыщающий FeCl3 (вводили подкожно). Дополнительный отрицательный контроль состоял из неинфицированных мышей, получавших FeCl3. Деферасирокс в дозе 1, 3 или 10 мг/кг bid значительно улучшал выживаемость по сравнению с контролями (фиг.9а).
В отдельном эксперименте деферасирокс оказался эффективным против второго клинического изолята R.oryzae - изолята 99-880. Мышей с диабетическим кетоацидозом инфицировали через хвостовую вену 1,3×103 спор более вирулентного R. oryzae 99-880 и обрабатывали, как описано выше, деферасироксом в дозе 10 мг/кг bid или плацебо на протяжении 7 дней. Деферасирокс значительно улучшал время до наступления смерти инфицированных R. oryzae мышей по сравнению с плацебо (фиг.9b).
Чтобы определить влияние деферасирокса на обсемененность тканей грибком, мышей с диабетическим кетоацидозом инфицировали через хвостовую вену 4,2×104 спор R. oryzae 99-892. Мышей обрабатывали деферасироксом (10 мг/кг bid), деферасироксом+насыщающим FeCl3 или плацебо. Обработку начинали через 16 ч после инфицирования и продолжали каждый день на протяжении 3 дней. На 4-й день извлекали почки и мозги, гомогенизировали и подвергали количественному культивированию. Деферасирокс вызывал снижение обсемененности грибком и мозга, и почек (главных органов-мишеней) более чем в 10 раз по сравнению с мышами, получавшими плацебо или деферасирокс + насыщающий FeCl3 (фиг.10а). По данным гистопатологии, в почках обработанных деферасироксом мышей не было видно гиф (как показано стрелками на фиг.10b), тогда как в почках мышей, получавших плацебо или деферасирокс+насыщающий FeCl3, повсеместно были нитчатые грибки. Более того, у мышей, обработанных насыщающим железом, отмечалось поразительное отсутствие притока нейтрофилов к местам инфекции, тогда как в почках мышей, обработанных деферасироксом, отмечался заметный приток нейтрофилов (фиг.10b).
Наряду со свидетельством прямых противогрибковых эффектов деферасирокса, данный пример показывает, что защитный эффект деферасирокса устраняется при введении свободного железа, подтверждая, что защитный механизм препарата заключается в хелатировании железа.
ПРИМЕР VI
Эффекты хелатирования железа и избытка железа на иммунные реакции организма хозяина
В этом примере представлено сравнение между эффектами деферасирокса и деферасирокса + FeCl3 на иммунные реакции организма хозяина.
Далее следует описание материалов и методов, использовавшихся в процедурах, описанных в этом или последующих примерах.
Частотность лимфоцитов в селезенке и анализ цитокинов на целых органах
Частотность лимфоцитов в селезенке определяли, как описано ранее (Spellberg et al., Infect. Immun. 71: 5756-5764 (2003)). Вкратце, гомогенаты селезенки пропускали через фильтры на 70 мкм, после чего лизировали эритроциты с помощью 0,15 М NH4Cl. Клетки фиксировали буфером Cytofix™ (BD Pharmingen), пермеабилизировали буфером Cytoperm (BD Pharmingen) и окрашивали с помощью 10 мкг/мл конъюгированного с FITC антитела к CD4 мыши (клон RM4-5), конъюгированного с РЕ антитела к IFN-γ мыши (клон XMG1.2) или контроля на изотип (клон R-34), конъюгированного с аллофикоцианином (АРС) антитела к IL-4 мыши (клон 11В11) или контроля на изотип (клон R3-34), либо конъюгированного с АРС антитела к IL-10 мыши (клон JES5-16E3) или контроля на изотип (клон А95-1) (все от BD Pharmingen). В отдельных опытах определяли частотность регуляторных Т-клеток CD4+CD25+foxp3 с помощью набора Mouse Regulatory T cell Staining™ Kit (eBiosciences) согласно рекомендациям изготовителя. Частотность апоптоза определяли с помощью набора Annexin FITC Apoptosis™ Kit (BD Pharmingen).
Клетки отмывали и выполняли трехцветную проточную цитометрию на приборе Becton-Dickinson FACScan™, откалиброванном по шарикам CaliBRITE™ (BD Pharmingen) с помощью программы FACSComp™ согласно рекомендациям изготовителя. Во время сбора данных лимфоциты CD4+засекали по сцепленности прямого и бокового рассеяния света с флуоресцентными свойствами FIТС-антитела к CD4. Сбор данных по каждому образцу выполняли до полного анализа 10000 лимфоцитов CD4+.
Анализ цитокинов на целых органах
Селезенки и почки гомогенизировали в 1 мл PBS. Гомогенаты центрифугировали при максимальной скорости в настольной центрифуге при 4°С. Супернатанты подвергали анализу на цитокины с помощью набора Cytometric Bead Array Murine Inflammatory Cytokine™ Kit (BD Phanningen) согласно рекомендациям изготовителя.
Ввиду изменений притока воспалительных клеток в почках мышей, получавших насыщающий FeCl3 в сравнении с хелатированием железа, в этом примере определяли влияние терапии деферасироксом на ответы Th1/Th2 и воспалительных цитокинов у инфицированных мышей. Мышей с диабетическим кетоацидозом инфицировали 3,1×104 спор R. oryzae 99-892, как описано выше, и обрабатывали деферасироксом, деферасироксом + FeCl3 или плацебо. На 4-й день после инфицирования селезенки и почки подвергали обработке для определения внутриклеточных цитокинов и на целых органах. Деферасирокс вызывал значительное повышение частотности спленоцитов Th1 и Th2 по сравнению с мышами, получавшими насыщающий FeCl3 или плацебо (фиг.11а). Частотности спленоцитов CD4+IL-10+ или CD4+CD25+foxp3+ не проявляли значительных отличий между группами (данные не приводятся). Также не было значительных отличий по апоптозу спленоцитов между группами (данные не приводятся).
У обработанных деферасироксом мышей уровни канонических провоспалительных цитокинов TNF и IFN-7 в селезенке были существенно выше, чем у мышей, получавших насыщающий FeCl3 или плацебо (фиг.11b). У мышей, обработанных деферасироксом, также были существенно повышены уровни IFN-γ в почках (фиг.11b).
Это исследование показывает, что деферасирокс неспецифически стимулирует подавленные воспалительные реакции у мышей с диабетическим кетоацидозом, повышая частотность лимфоцитов Th1 и Th2, а также уровни воспалительных цитокинов в селезенке и почках. Более того, устранение хелатирования при введении сверхнасыщающей дозы железа ведет к уменьшению числа нейтрофилов в инфицированных почках.
ПРИМЕР VII
Применение деферасирокса (Exjade®) в комбинации с липосомным амфотерицином В для терапевтического лечения мукормикоза мышей
В этом примере представлены эффекты комбинированной терапии с помощью хелатора железа - деферасирокса (Exjade®) и липосомного амфотерицина В (LAmB) для лечения мукормикоза.
Как описано ранее, клинические данные и модели на животных свидетельствуют, что повышение уровня доступного железа в сыворотке вызывает предрасположенность организма хозяина к мукормикозу. Как свидетельствуют вышеприведенные примеры, хелатирующая железо терапия деферасироксом улучшает выживаемость мышей с диабетическим кетоацидозом, инфицированных R. oryzae, самым распространенным возбудителем мукормикоза. Для того чтобы подтвердить эффективность деферасирокса во вспомогательной терапии, эффективность комбинирования деферасирокса с LAmB сравнивали с каждым из них поодиночке на животной модели при лечении мукормикоза мышей.
Методы, обработку животных проводили и/или реагенты готовили, как описано ранее. Вкратце, мышей BALB/c с вызванным стрептозотоцином DKA инфицировали через хвостовую вену 2,0×103 спор R. oryzae. Через 24 ч после инфицирования начинали обработку: (1) LAmB (15 мг/кг внутривенно) раз в день, в совокупности 4 дозы; (2) деферасирокс (10 мг/кг per os) два раза в день, в совокупности 7 доз; или (3) LAmB + деферасирокс в вышеуказанных дозах. Контролем служили мыши, получавшие плацебо - носитель. Показателями служили время до наступления смерти и колониеобразующие единицы (KOE).
Результаты данного исследования представлены на фиг.12 и 13. На фиг.12 представлена эффективность для монотерапии одним деферасироксом или одним LAmB, а также для комбинированной терапии деферасироксом вместе с LAmB при лечении мукормикоза. Результаты показывают, что обе монотерапии улучшали выживаемость по сравнению с плацебо (выживаемость составила 25% и 28% для деферасирокса и LAmB, соответственно, и 0% для плацебо, р 0,003). Комбинированная терапия заметно улучшала и время до наступления смерти, и выживаемость в целом инфицированных мышей с DKA (n>16 на группу) по сравнению со всеми другими группами (выживаемость составила 70% при комбинированной терапии, р<0,008 для всех сравнений, лог-ранговый критерий).
Результаты этих обработок в отношении органов-мишеней представлены на фиг.13. Результаты свидетельствуют, что ни один препарат сам по себе не вызывал снижения KOE в мозге (главном органе-мишени) по сравнению с плацебо. Однако комбинированная терапия деферасироксом вместе с LAmB снижала KOE в мозге более чем на 2 лог-единицы по сравнению со всеми другими группами (р<0,04). Только LAmB и комбинированная терапия вызывали снижение КОЕ в почках (второстепенном органе-мишени) по сравнению с мышами, получавшими плацебо (р<0,01).
Это исследование показывает, что хелатирующая железо терапия и LAmB в высоких дозах могут быть одинаково эффективными при лечении экспериментального мукормикоза при DKA. Комбинированная терапия LAmB и деферасироксом оказалась более эффективной, чем каждый препарат сам по себе. Эти данные дополнительно подтверждают терапевтическую эффективность применения такого хелатора железа, как деферасирокс в качестве вспомогательной терапии вместе с липидной композицией амфотерицина В при лечении заболеваний мукормикозом. Вышеприведенные результаты также свидетельствуют, что комбинирование хелатора железа деферасирокса (Exjade®) с липосомным амфотерицином В дает синергический эффект при лечении мукормикоза на животной модели.
ПРИМЕР VIII
Эффективность деферасирокса на инфицированных мышах с нейтропенией
В этом примере представлена эффективность деферасирокса при лечении мышей с нейтропенией, инфицированных R. oryzae.
Чтобы установить, будет ли деферасирокс также эффективен на фоне нейтропении, мышей подвергали миелодеструкции с помощью циклофосфамида. Чере 2 дня мышей инфицировали 2,7×103 спор R. oryzae 99-892. Предварительные опыты доза-эффект показали, что, в противоположность модели с диабетическим кетоацидозом, оптимальные результаты достигались при дозировке деферасирокса через день, а не каждый день (данные не приводятся), как было описано ранее в отношении другого хелатора железа - деферипрона. Обработка деферасироксом (10 мг/кг по два раза через день, начиная с 24 ч после инфицирования, в совокупности 5 доз) значительно улучшала время до наступления смерти по сравнению с плацебо (фиг.14). В противоположность этому, деферасирокс при дозировке два раза в день не вызывал значительного улучшения времени до наступления смерти по сравнению с плацебо.
Это исследование показывает, что для максимальной эффективности деферасирокса на мышах с нейтропенией требовалась менее частая дозировка, чем на модели у мышей с диабетическим кетоацидозом, причем деферасирокс оказался несколько более эффективным на мышах с диабетическим кетоацидозом, чем на мышах с нейтропенией.
ПРИМЕР IX
Оценка специфической токсичности деферасирокса на мышах с нейтропенией
В этом примере представлены результаты оценки токсичности на мышах с нейтропенией, получавших ежедневные дозы деферасирокса.
Далее следует описание материалов и методов, использовавшихся в процедурах, описанных в этом примере.
Исследования токсичности деферасирокса
Токсичность деферасирокса оценивали на мышах с нейтропенией. Нейтропению у мышей вызывали, как описано выше, и обрабатывали их деферасироксом в дозе 10 мг/кг два раза в день или через день на протяжении 7 дней. Мышей из 3 разных групп (т.е. плацебо, деферасирокс каждый день и деферасирокс через день) забивали на 3-й или 8-й день, брали кровь и отсылали в Charles River Laboratories для исследования. Кроме того, делали мазки костного мозга из бедренной кости, а образцы тканей фиксировали в цинк-формалине, заключали в парафин, делали срезы в 5 мкм и окрашивали гематоксилином и эозином. Полученные препараты изучал дипломированный ветеринарный патолог в Charles River Laboratories.
Поскольку дозировка деферасирокса через день оказалась оптимальной на модели с нейтропенией, мы постарались идентифицировать любую потенциальную токсичность, вызванную ежедневной дозировкой деферасирокса, на мышах с нейтропенией. У мышей вызывали нейтропению с помощью циклофосфамида, как описано выше, но не инфицировали их. Мышей обрабатывали деферасироксом в дозе 10 мг/кг два раза в день на протяжении 7 дней, 10 мг/кг по два раза через день, в совокупности 4 дозы, или плацебо. На 3-й или 8-й день делали терминальное кровопускание и проводили полный анализ форменных элементов крови, химический анализ сыворотки и тесты на функцию печени. Делали гистопатологию на широком круге органов, включая мозг, сердце, легкие, печень, желчный пузырь, селезенку, почки, желудочно-кишечный тракт (в том числе желудок, тонкий кишечник и толстый кишечник) и костный мозг (мазки и сердцевина). Не было выявлено никаких отличий по числу лейкоцитов, абсолютному числу нейтрофилов, числу тромбоцитов, уровню гемоглобина, химическому анализу сыворотки (включая креатинин, азот мочевины крови и электролиты) или тестам на функцию печени (включая AST, ALT и билирубин) между тремя группами в какой-либо момент времени. По данным гистопатологии не установлено никакой органоспецифической токсичности, относимой на счет деферасирокса, включая отсутствие признаков нарушений гематопоэза. В частности, не было признаков обострения или замедленного восстановления от деструкции костного мозга при химиотерапии, как и не было признаков дисфункции почек или печени по лабораторным анализам либо специфической токсичности для органов при гистопатологическом исследовании.
Это исследование показывает, что уменьшение активности при ежедневной дозировке деферасирокса на мышах с нейтропенией не могло быть обусловлено токсическим действием деферасирокса на таких мышей, поскольку не было обнаружено никаких признаков токсичности.
По всей настоящей заявке делались ссылки на различные публикации в скобках. При этом содержание этих публикаций во всей полноте включено в настоящее изобретение путем ссылки для более полного описания современного уровня в той области, к которой относится данное изобретение.
Несмотря на то что изобретение было описано на примере раскрытых воплощений, специалисты в этой области должны понимать, что конкретные примеры и исследования, изложенные выше, служат только для раскрытия изобретения. Следует иметь в виду, что можно совершать различные модификации, не отходящие от духа изобретения. Соответственно, изобретение ограничивается только нижеследующей формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИСПОЛЬЗОВАНИЕ СОЕДИНЕНИЙ ПРИ ЛЕЧЕНИИ ГРИБКОВЫХ ИНФЕКЦИЙ | 2021 |
|
RU2805930C1 |
| СОЕДИНЕНИЯ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ГРИБКОВЫХ ИНФЕКЦИЙ | 2021 |
|
RU2824066C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ПЕРЕГРУЗКИ ОРГАНИЗМА ЖЕЛЕЗОМ ИЛИ ГЕМАХРОМАТОЗА | 2014 |
|
RU2557959C1 |
| НОВОЕ ПРОТИВОГРИБКОВОЕ СОЕДИНЕНИЕ 2-(3,4-ДИМЕТИЛ-2,5-ДИГИДРО-1H-ПИРРОЛ-2-ИЛ)-1-МЕТИЛЭТИЛА ПЕНТАНОАТ | 2002 |
|
RU2294923C2 |
| НОВАЯ ЛЕКАРСТВЕННАЯ ФОРМА ДЛЯ ЛЕЧЕНИЯ ГРИБКОВОЙ ИНФЕКЦИИ | 2010 |
|
RU2481100C2 |
| Фармацевтическая композиция для лечения грибковых поражений слизистых оболочек | 2016 |
|
RU2705098C2 |
| ПРИМЕНЕНИЕ АПО-ФОРМЫ ЛАКТОФЕРРИНА ЧЕЛОВЕКА В КАЧЕСТВЕ АНТИГИПОКСАНТА И СТАБИЛИЗАТОРА ГИПОКСИЯ-ИНДУЦИБЕЛЬНОГО ФАКТОРА-1 АЛЬФА | 2011 |
|
RU2465004C1 |
| Противогрибковый полусинтетический полиеновый антибиотик, его водорастворимые соли и фармацевтические композиции на их основе | 2018 |
|
RU2688658C1 |
| ПРОТИВОГРИБКОВЫЕ АГЕНТЫ | 2015 |
|
RU2727520C2 |
| ЛЕЧЕНИЕ ГРИБКОВОЙ ИНФЕКЦИИ ПРОТИВОГРИБКОВЫМИ ПРЕПАРАТАМИ ИЗ ГРУППЫ ПОЛИЕНОВ ИЛИ ИНГИБИТОРОВ β-ГЛЮКАНСИНТАЗЫ В КОМБИНАЦИИ С АНТИ-hsp90-АНТИТЕЛАМИ | 2001 |
|
RU2262952C2 |
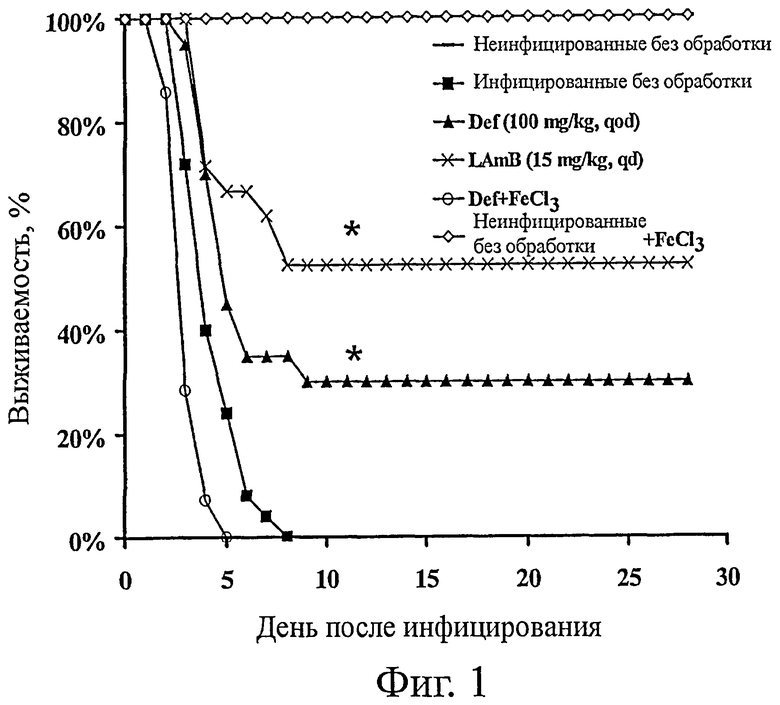
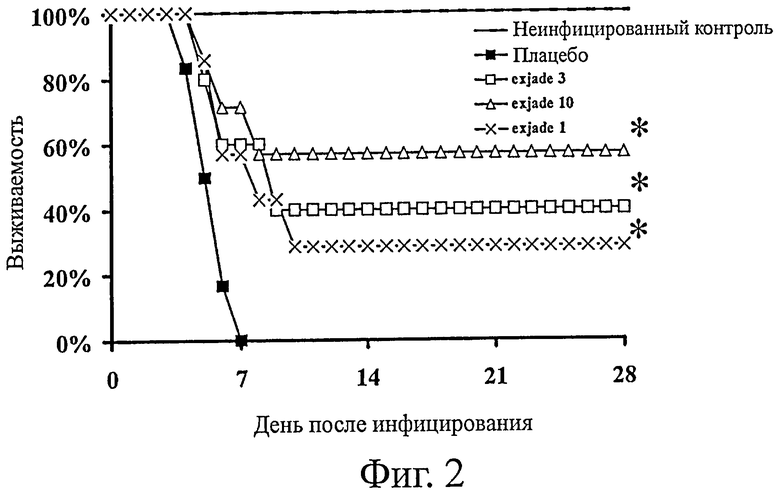
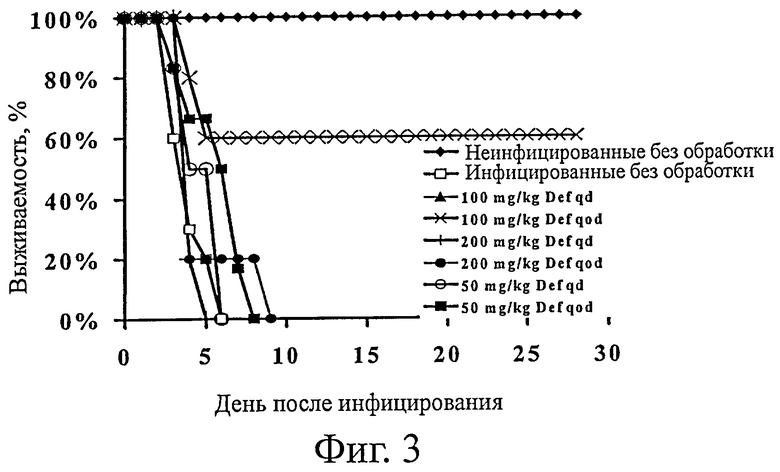
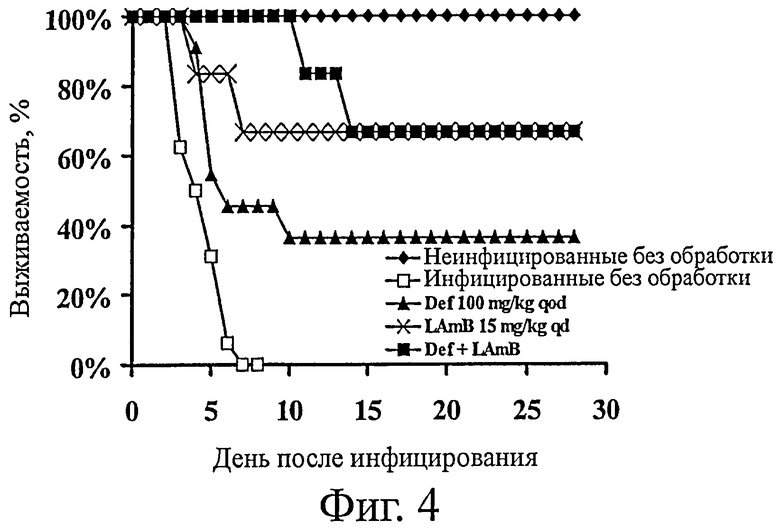
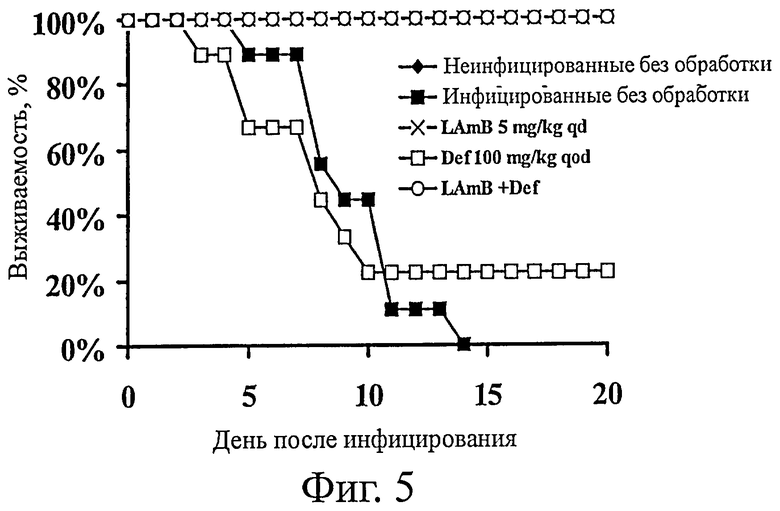
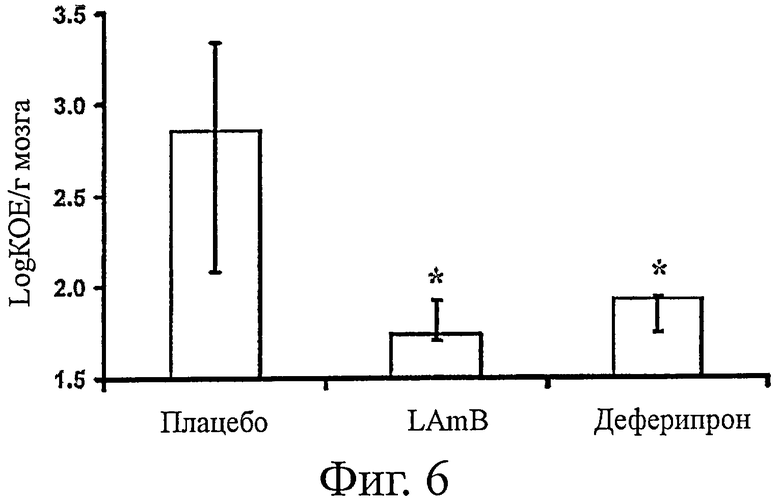
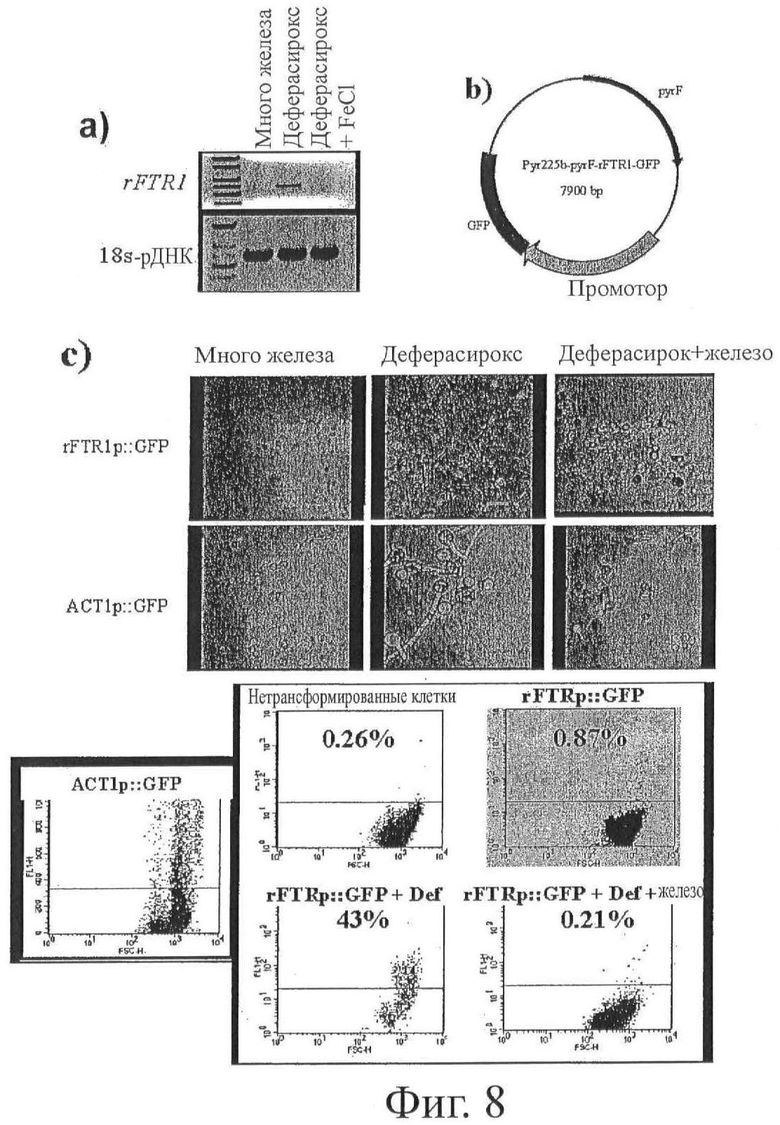
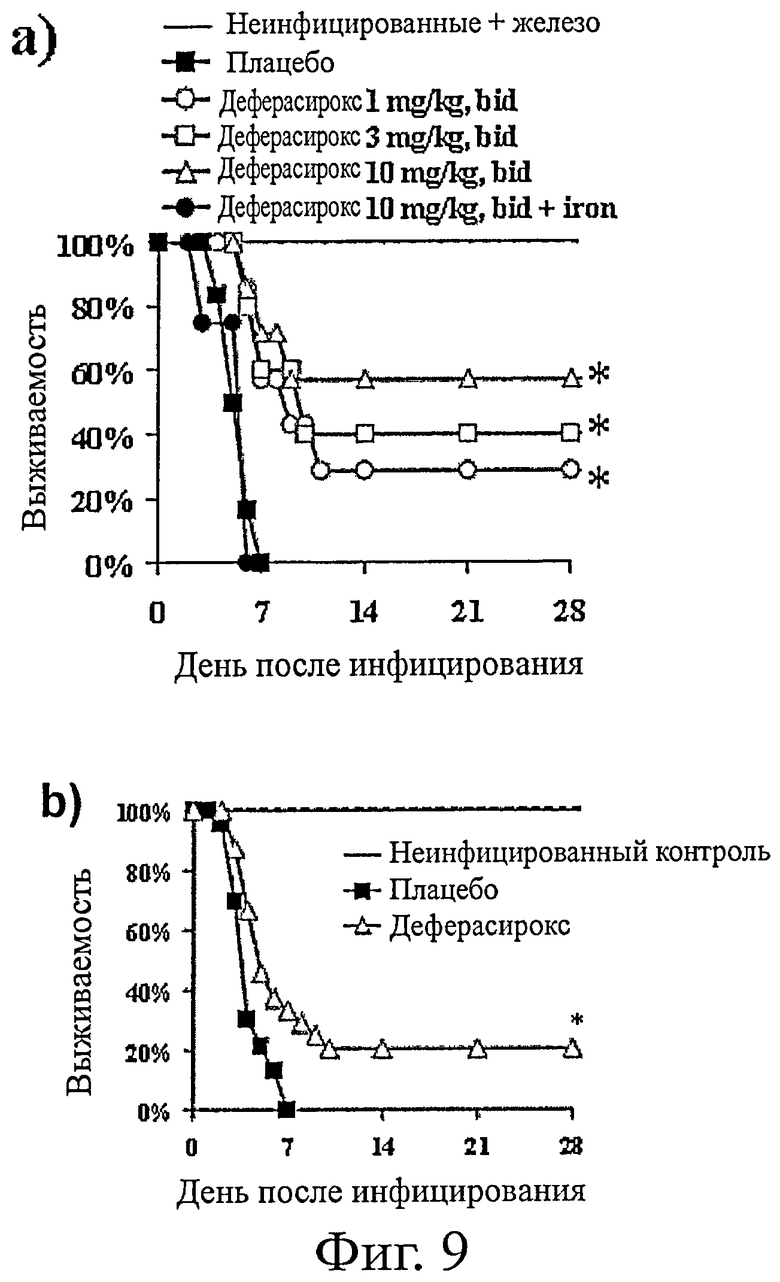
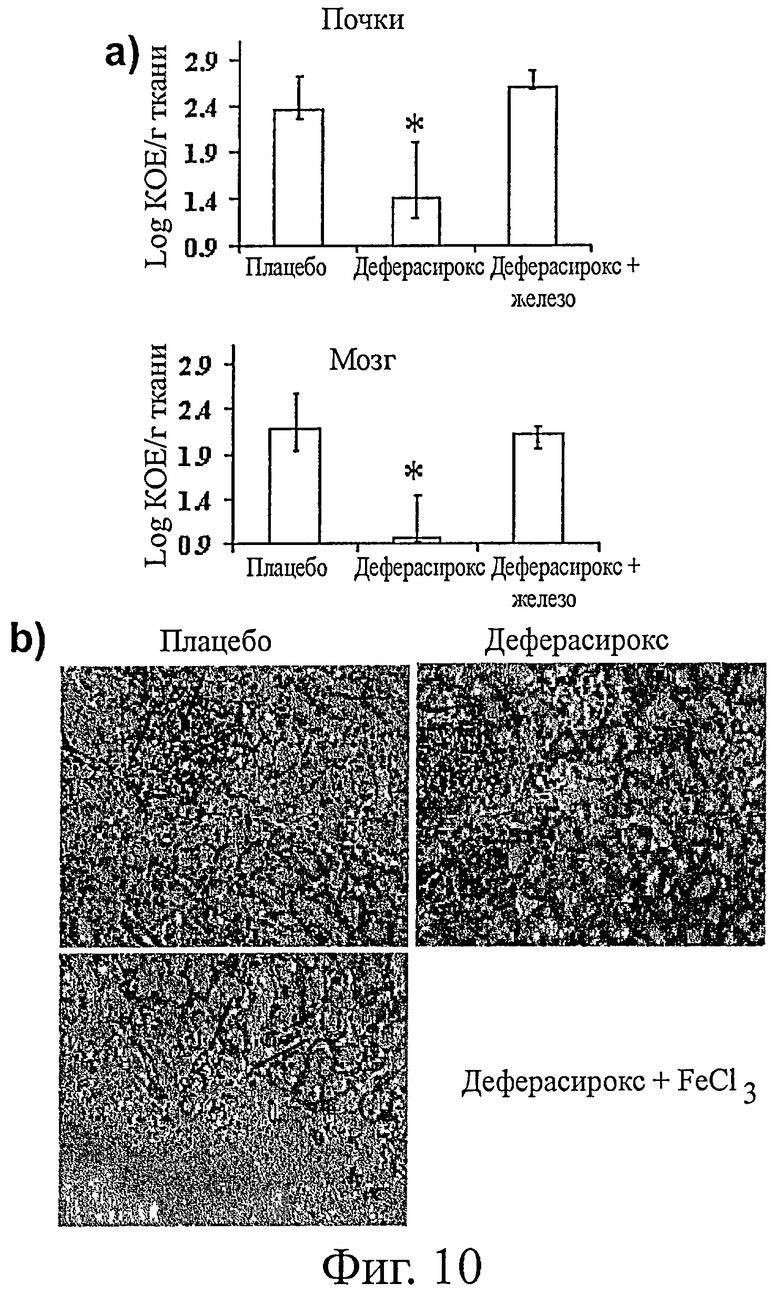
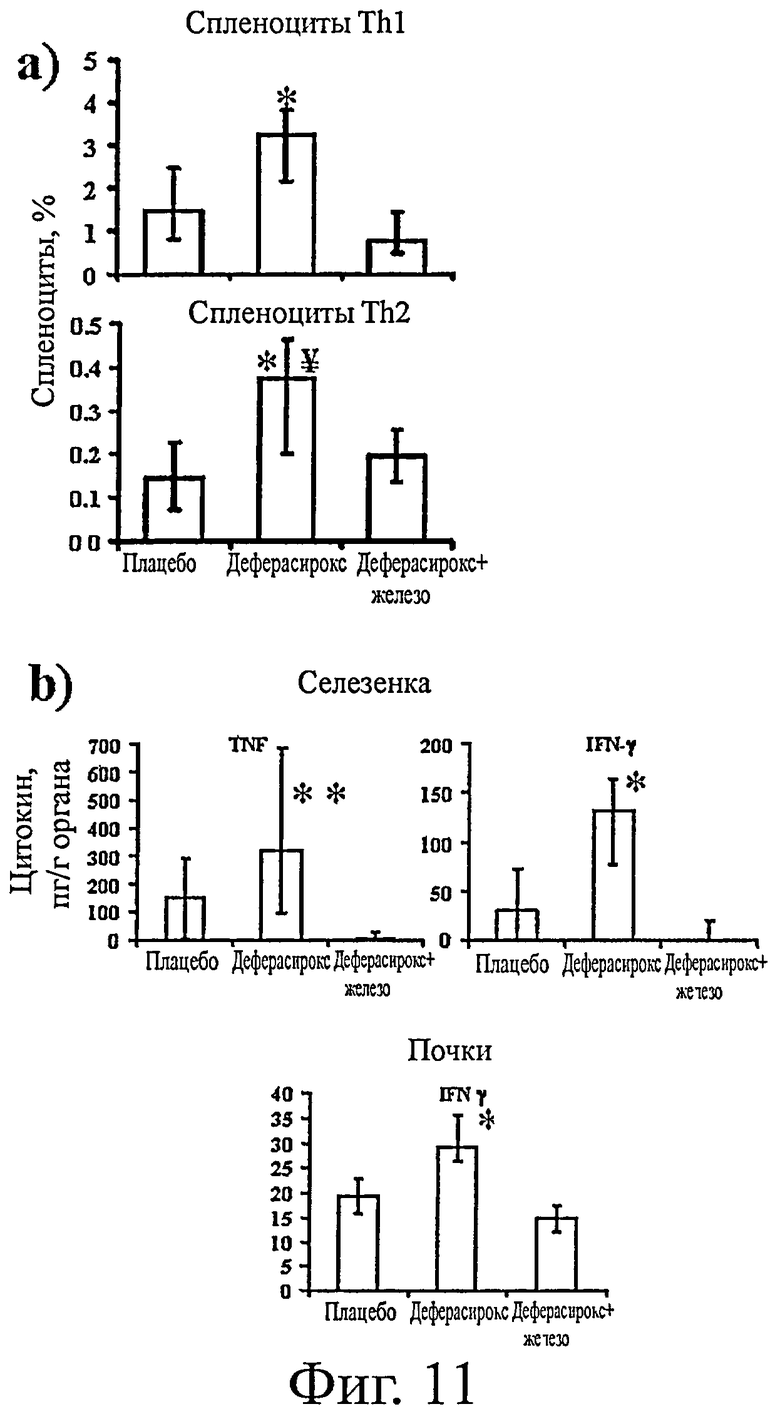
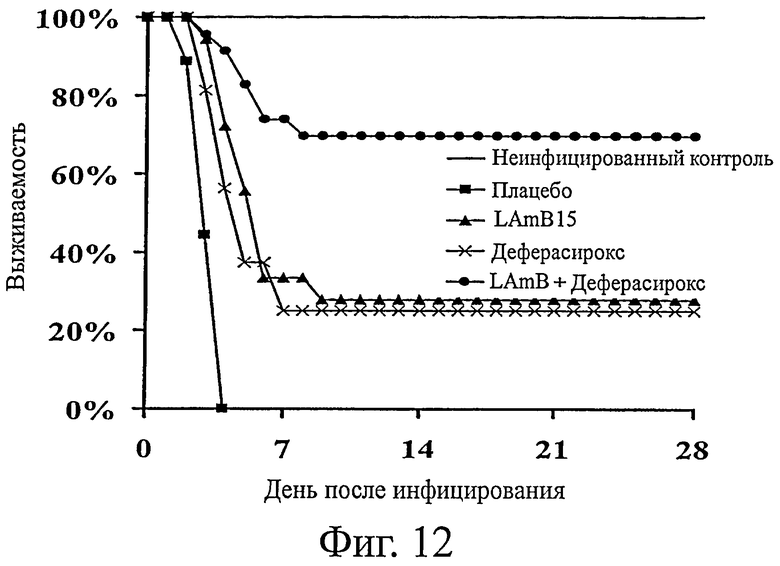
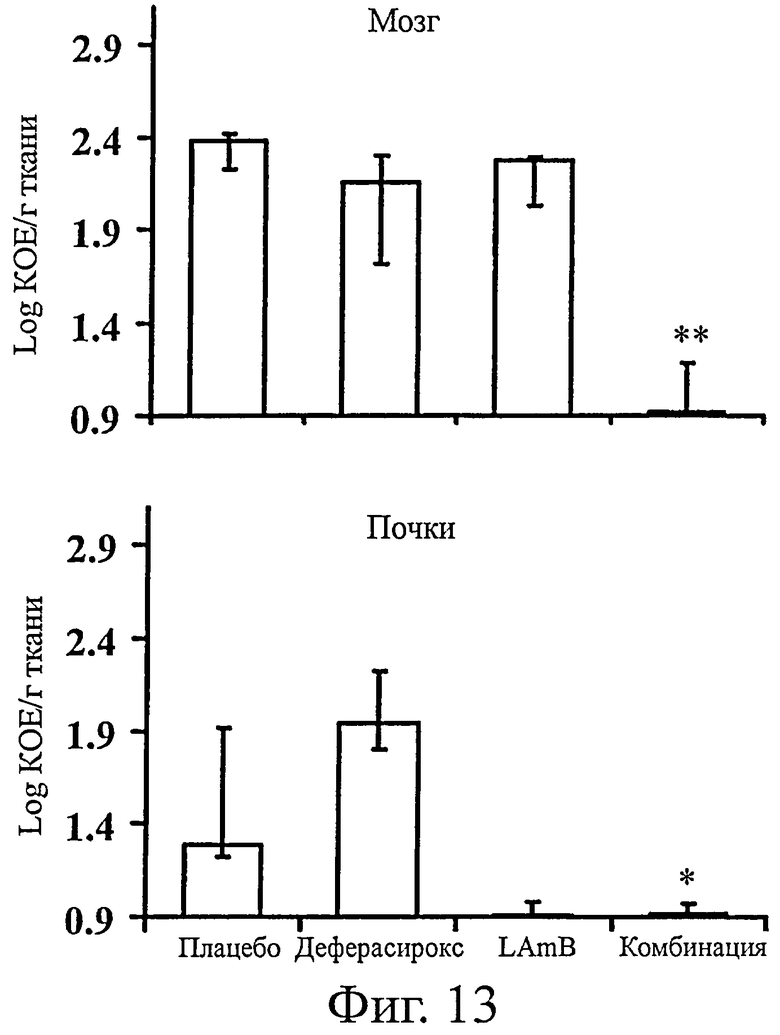
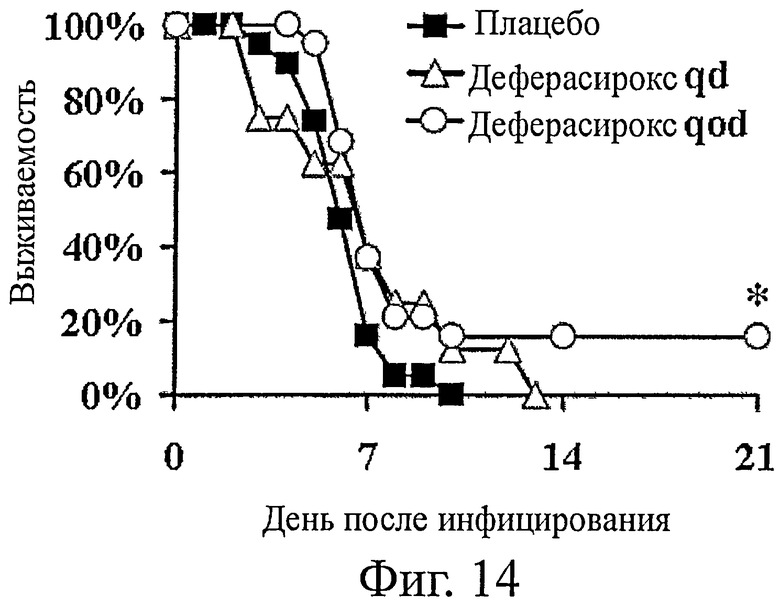
Изобретение касается применения композиций для изготовления лекарственного средства для лечения или предотвращения мукормикоза. Композиции включают по меньшей мере одно хелатирующее железо соединение. Также композиции могут дополнительно включать по меньшей мере одно противогрибковое средство. В качестве хелатирующих железо соединений выбирают соединения, не являющиеся сидерофором или ксеносидерофором в отношении данного грибкового заболевания, а именно деферипрон и деферасирокс. Противогрибковые средства, входящие в композиции, могут включать полиеновые, азоловые или эхинокандиновые противогрибковые средства. Изобретение используют для лечения или уменьшения тяжести грибковых заболеваний. 2 н. и 21 з.п. ф-лы, 3 табл., 9 пр., 14 ил.
1. Применение терапевтически эффективного количества по меньшей мере одного хелатирующего железо соединения для изготовления лекарственного средства для лечения или предотвращения мукормикоза, где хелатирующее железо соединение не является сидерофором или ксеносидерофором в отношении мукормикоза.
2. Применение по п.1, в котором мукормикоз включает риноцеребральный мукормикоз, легочный мукормикоз, желудочно-кишечный мукормикоз, диссеминированный мукормикоз, костный мукормикоз, мукормикоз средостения, мукормикоз трахеи, мукормикоз почек, мукормикоз брюшины, мукормикоз верхней полой вены или мукормикоз наружного уха.
3. Применение по п.2, в котором мукормикоз связан с возбудителем инфекции из отряда Mucorales.
4. Применение по п.3, в котором возбудитель из отряда Mucorales выбран из рода Rhizopus, в том числе Rhizopus oryzae (Rhizopus arrhizus), Rhizopus microsporus var. rhizopodiformis, Absidia corymbifera, Apophysomyces elegans, Mucor spp., Rhizomucor pusillus и Cunninghamella spp.(семейства Cunninghamellaceae).
5. Применение по п.1, в котором хелатирующее железо соединение включает деферипрон или деферасирокс.
6. Применение по п.1, дополнительно включающий два или несколько хелатирующих железо соединений, причем каждое хелатирующее железо соединение не является сидерофором или ксеносидерофором в отношении мукормикоза.
7. Применение по п.6, в котором два или несколько хелатирующих железо соединений включают деферипрон и деферасирокс.
8. Применение по п.1, в котором предотвращение включает профилактическое применение по меньшей мере одного хелатирующего железо соединения еще до возникновения мукормикоза.
9. Применение терапевтически эффективного количества по меньшей мере одного хелатирующего железо соединения и по меньшей мере одного противогрибкового средства для изготовления лекарственного средства для лечения или предотвращения мукормикоза, где хелатирующее железо соединение не является сидерофором или ксеносидерофором в отношении мукормикоза.
10. Применение по п.9, в котором мукормикоз включает риноцеребральный мукормикоз, легочный мукормикоз, желудочно-кишечный мукормикоз, диссеминированный мукормикоз, костный мукормикоз, мукормикоз средостения, мукормикоз трахеи, мукормикоз почек, мукормикоз брюшины, мукормикоз верхней полой вены или мукормикоз наружного уха.
11. Применение по п.10, в котором мукормикоз связан с возбудителем инфекции из отряда Mucorales.
12. Применение по п.11, в котором возбудитель из отряда Mucorales выбран из рода Rhizopus, в том числе Rhizopus oryzae (Rhizopus arrhizus), Rhizopus microsporus var. rhizopodiformis, Absidia corymbifera, Apophysomyces elegans, Mucor spp., Rhizomucor pusillus и Cunninghamella spp. (семейства Cunninghamellaceae).
13. Применение по п.9, в котором хелатирующее железо соединение включает деферипрон или деферасирокс.
14. Применение по п.9, в котором противогрибковое средство включает полиеновое противогрибковое средство, азоловое противогрибковое средство или эхинокандиновое противогрибковое средство.
15. Применение по п.14, в котором полиеновое противогрибковое средство выбрано из амфотерицина В-дезоксихолата, липосомного амфотерицина В, липидного комплекса амфотерицина В или амфотека.
16. Применение по п.14, в котором азоловое противогрибковое средство выбрано из посаконазола, ворикоазола, флуконазола и итраконазола.
17. Применение по п.14, в котором эхинокандиновое противогрибковое средство выбрано из каспофунгина-ацетата и микафунгина.
18. Применение по п.9, дополнительно включающий два или несколько хелатирующих железо соединений, причем каждое хелатирующее железо соединение не является сидерофором или ксеносидерофором в отношении мукормикоза.
19. Применение по п.18, в котором два или несколько хелатирующих железо соединений включают деферипрон и деферасирокс.
20. Применение по п.9, дополнительно включающий два или несколько противогрибковых средств.
21. Применение по п.20, в котором два или несколько противогрибковых средств выбраны из полиеновых противогрибковых средств, азоловых противогрибковых средств и эхинокандиновых противогрибковых средств.
22. Применение по п.21, в котором противогрибковые средства выбраны из амфотерицина В-дезоксихолата, липосомного амфотерицина В, липидного комплекса амфотерицина В, амфотека, посаконазола, ворикоазола, флуконазола, итраконазола, каспофунгина-ацетата и микафунгина.
23. Применение по п.9, в котором предотвращение включает профилактическое введение по меньшей мере одного хелатирующего железо соединения и по меньшей мере одного противогрибкового средства еще до возникновения мукормикоза.
| WO 2004045609 A2, 03.06.2004 | |||
| Weiss H.Markus et al | |||
| Пневматический прибор для заправки нити в челнок | 1924 |
|
SU670A1 |
| Drag metabolism and disposition, v.34, №6, June 2006 (2006-06), p.971-975 | |||
| Abstract | |||
| WO | |||
Авторы
Даты
2012-10-20—Публикация
2007-07-13—Подача