Область техники
Настоящее изобретение относится к новой функции лизил-тРНК-синтетазы. Более конкретно, изобретение относится к способу контроля метастазирования злокачественных опухолей или миграции злокачественных клеток посредством модуляции клеточного уровня лизил-тРНК-синтетазы, к применению вектора экспрессии, содержащего конструкцию, ингибирующую экспрессию KRS, для профилактики или лечения злокачественной опухоли, к применению средства, ингибирующего активность KRS для профилактики или лечения злокачественной опухоли, к способу скрининга средства, модулирующего метастазирование злокачественной опухоли или миграцию злокачественных клеток, к способу скрининга средства, ингибирующего взаимодействие между KRS и 67LR.
Предшествующий уровень техники
Опухоль развивается в результате бесконтрольной беспорядочной патологической клеточной пролиферации. В частности, если такая опухоль демонстрирует деструктивный рост, инвазивность и метастазирование, то ее рассматривают как злокачественную. Инвазивность представляет собой инфильтрацию или разрушение окружающих тканей и, в частности, в результате такого поведения разрушается базальный слой тканей, что приводит к локальному распространению и иногда к попаданию опухоли в систему кровообращения. Под метастазированием понимают распространение опухолевых клеток из исходного места возникновения в другие области по лимфатическим или кровеносным сосудам. В широком смысле метастазирование также означает непосредственное распространение опухолевых клеток через серозную полость тела или другое пространство.
В настоящее время для лечения злокачественной опухоли широко применяют хирургическое вмешательство, лучевую терапию и химиотерапию, самостоятельно или совместно. Хирургическое вмешательство представляет собой способ удаления пораженной ткани. Таким образом, с помощью хирургического вмешательства можно эффективно удалить опухоль в конкретной области, например в случае молочной железы, опухолей кишечника и кожи. Однако опухоль, расположенная в позвоночнике, или лечение рассеянной опухоли, например лейкоз, невозможно вылечить посредством хирургического вмешательства.
Химиотерапия блокирует репликацию или метаболизм клеток, и ее используют для лечения рака молочной железы, рака легких и рака яичка. Однако из пациентов со злокачественными опухолями, которые получали лечение посредством химиотерапии, были отмечены тяжелые побочные эффекты при системной химиотерапии. Обычными, но неприятными примерами таких побочных эффектов являются тошнота и рвота. Побочные эффекты химиотерапии могут оказывать влияние на жизнь пациента, так как быстро снижают его адаптивность. Кроме того, одним из основных побочных эффектов химиотерапии также является DLT (лимитирующая дозу токсичность), которую следует учитывать при введении лекарственного средства. Примером DLT для противораковых средств является мукозит, например, который представляет собой антиметаболическое цитотоксическое средство, 5-фторурацил, и метотрексат, противоопухолевый антибиотик, например доксорубицин. Если у пациента серьезные побочные эффекты химиотерапии, то его необходимо госпитализировать и вводить обезболивающие средства, снижающие боль. Таким образом, побочные эффекты химиотерапии и лучевой терапии при лечении пациентов со злокачественными опухолями являются серьезной проблемой.
Генотерапия представляет собой способ лечения или профилактики заболеваний, вызываемых генетической изменчивостью клеток человека, например различных генетических нарушений, злокачественных опухолей, сердечно-сосудистых заболеваний, инфекционных заболеваний и аутоиммунных заболеваний, на основе преимуществ способа рекомбинации ДНК, так пациенту для коррекции генетического дефекта или для активации или добавления функций клеток вводят терапевтический ген. Более точно, при генотерапии лечение заболевания проходит за счет нацеливания терапевтического гена на орган-мишень, индуцируя в клетках экспрессию терапевтического или нормального белка. Преимуществами генотерапии является превосходная специфичность и повышение степени и скорости восстановления, которые трудно регулировать при введении других лекарственных средств, которые обеспечивают длительное введение. Генотерапия не предназначена для лечения симптомов заболевания, но предназначена для лечения или устранения причины заболевания. Для успешной терапии важно доставить терапевтический ген в клетку-мишень, улучшив тем самым степень его экспрессии, что является основным подходом в генотерапии.
Необходимым медиатором для встраивания терапевтического гена в клетку-мишень является переносчик гена. Идеальный переносчик гена не должен оказывать негативного влияния на человека, должен активно продуцироваться, эффективно переносить ген в клетку-мишень и непрерывно экспрессировать ген. Получение переносчика гена является главным способом в генотерапии. Наиболее характерными переносчиками генов, широко используемыми для генотерапии в настоящее время, являются вирусные переносчики, такие как носители из аденовирусов, аденоассоциированных вирусов, ретровирусов, и невирусные носители, такие как липосомы, полиэтиленамин и тому подобное.
В качестве генотерапевтической стратегии для контроля опухолевых клеток использовали способы с применением гена опухолевого супрессора, с применением компетентного по репликации онколитического вируса, с применением "суицидального" гена и с применением иммунорегуляторного гена и тому подобное. Способ использования гена опухолевого супрессора представляет собой лечение злокачественной опухоли посредством специфической доставки пациенту гена опухолевого супрессора, такого как p53, туда, где ген является дефектным или измененным. Кроме того, способ использования компетентного по репликации онколитического вируса представляет собой лечение злокачественной опухоли, используя нарушенную активность гена опухолевого супрессора в опухолевых тканях, посредством переноса вирусного переносчика гена, способного к специфическому росту в опухолевых клетках организма человека. Эти два способа представляют собой стратегии непосредственного уничтожения опухолевых клеток. Альтернативно, к ним относят способ с использованием "суицидального" гена. Характерным примером терапии "суицидальным" геном является лечение заболевания посредством доставки гена HSV-TK и химических средств против злокачественных опухолей, таких как ганцикловир, которые могут индуцировать гибель опухолевых клеток. С другой стороны, способ введения иммунорегуляторного гена представляет собой вид непрямых способов лечения, благодаря которым в живой организм вводят один или несколько генов, таких как интерлейкин 12, интерлейкин 4, интерлейкин 7, гамма-интерферон и фактор некроза опухоли и тому подобное для того, чтобы индуцировать распознавание T-клетками опухолевых клеток или апоптоз посредством блокирования белка, связанного с развитием опухоли. С другой стороны, к таким непрямым способам лечения также относится способ уничтожения опухолевых клеток посредством блокировки доставки питательных веществ, посредством экспрессии ингибирующих ангиогенез факторов, таких как ангиостатин или эндостатин и тому подобное.
Метастазирование является критическим показателем летальности злокачественной опухоли. Рецептор ламинина 67 кДа (67LR) представляет собой рецептор неинтегринового типа, встроенный в плазматическую мембрану и связанный с инвазией и метастазированием злокачественной опухоли (Nelson, J. et al., The 67 kDa laminin receptor: structure, function and role in disease. Biosci. Rep. 28, 33-48 (2008)). 67LR образуется в результате димеризации своего предшественника, размером 37 кДа (37LRP), хотя подробности молекулярного взаимодействия в этом процессе преобразования не изучены. 37LRP идентичен рибосомальной субъединице p40, которая вовлечена в образование полисомы (Auth, D. & Brawerman, G. A 33-kDa polypeptide with homology to the laminin receptor: component of translation machinery. Proc. Natl. Acad. Sci. USA 89, 4368-4372 (1992)). В злокачественных опухолях часто отмечают высокие уровни 67LR (Nelson, J. et al., The 67 kDa laminin receptor: structure, function and role in disease. Biosci. Rep. 28, 33-48 (2008); Menard, S., Castronovo, V., Tagliabue, E. & Sobel, M. E. New insights into the metastasis-associated 67 kD laminin receptor. J. Cell. Biochem. 67, 155-165 (1997)). Однако регуляторный и молекулярный механизм присутствия на мембране 67LR еще не были определены. В настоящей работе авторы настоящего изобретения обнаружили, что лизил-тРНК-синтетаза (KRS) усиливает клеточную миграцию и метастазирование злокачественной опухоли, стабилизируя 67LR на плазматической мембране.
KRS относится к аминоацил-тРНК-синтетазам (ARS), которые связывают узнаваемые ими аминокислоты и тРНК для синтеза белка. Эти древние ферменты кроме каталитической активности обладают множеством других функций (Park, S. G., Ewalt, K. L. & Kim, S. Functional expansion of aminoacyl-tRNA synthetases and their interacting factors: new perspectives on housekeepers. Trends Biochem. Sci. 30, 569-574 (2005)). Кроме того, некоторые ARS млекопитающих, в том числе KRS, образуют молекулярный комплекс (Lee, S. W., Cho, B. H., Park, S. G. & Kim, S. Aminoacyl-tRNA synthetase complexes: beyond translation. J. Cell. Sci. 117, 3725-3734 (2004); Han, J. M., Kim, J. Y. & Kim, S. Molecular network and functional implications of macromolecular tRNA synthetase complex. Biochem. Biophys. Res. Commun. 303, 985-993 (2003)), который служит молекулярным резервуаром (Ray, P. S., Arif, A. & Fox, P. Macromolecular complexes as depots for releasable regulatory proteins. Trends Biochem. Sci. 32, 158-164 (2007)) и контролирует большое число функций составляющих белков. KRS человека содержит уникальный N-концевой участок, участвующий во взаимодействиях с РНК и другими белками (Rho, S. B. et al. Genetic dissection of protein-protein interactions in multi-tRNA synthetase complex. Proc. Natl. Sci. Acad. USA 96, 4488-4493 (1999); Francin, M., Kaminska, M., Kerjan, P. & Mirande. M. The N-terminal domain of mammalian Lysyl-tRNA synthetase is a functional tRNA-binding domain. J. Biol. Chem. 211, 1762-1769 (2002)).
Техническая проблема
Для определения значимости этого пептида для функциональной разносторонности KRS человека авторы настоящего изобретения выделили N-концевой пептид KRS человека длиной 116 аминокислот и использовали его в качестве затравки для скрининга связывающихся с ним белков из библиотеки кДНК клеток HeLa с использованием дрожжевой двухгибридной системы. В этой работе на основании скрининга авторы настоящего изобретения в качестве одного из потенциальных связывающихся белков идентифицировали 37LRP/p40 и исследовали функциональное значение взаимодействия KRS и рецептора ламинина. Для определения значимости этого пептида в отношении функциональной разносторонности KRS человека, авторы настоящего изобретения выделили N-концевой пептид KRS человека из 116 аминокислот и использовали его в качестве затравки для скрининга связывающихся с ним белков из библиотеки кДНК клеток HeLa с использованием дрожжевой двухгибридной системы. В этой работе на основании скрининга авторы настоящего изобретения в качестве одного из потенциальных связывающихся белков идентифицировали 37LRP/p40 и исследовали функциональное значение взаимодействия KRS и рецептора ламинина.
В результате авторы настоящего изобретения обнаружили, что лизил-тРНК-синтетаза (KRS) усиливает клеточную миграцию и метастазирование опухоли, стабилизируя 67LR в плазматической мембране, оказывая воздействие на метастазирование злокачественной опухоли или миграцию злокачественных клеток посредством рецептора ламинина в плазматическую мембрану, таким образом, достигнув настоящее изобретение.
Целью настоящего изобретения является получение нового применения лизил-тРНК-синтетазы в отношении метастазирования злокачественной опухоли или миграции злокачественных клеток.
Для достижения указанной выше цели настоящее изобретение относится к способу контроля метастазирования злокачественной опухоли посредством модуляции клеточного уровня лизил-тРНК-синтетазы.
Для достижения другой цели настоящее изобретение относится к способу контроля миграции злокачественных клеток посредством модуляции клеточного уровня лизил-тРНК-синтетазы.
Для достижения еще одной цели настоящее изобретение относится к композиции для профилактики и лечения злокачественной опухоли, которая содержит вектор экспрессии, содержащий в качестве эффективного компонента промотор и функционально связанный с ним полинуклеотид или антитело против KRS, где полинуклеотид кодирует антисмысловую РНК или миРНК против полинуклеотида KRS.
Для достижения еще одной цели настоящее изобретение относится к способу профилактики и лечения злокачественной опухоли, включающему введение индивиду, при необходимости, эффективного количества вектора экспрессии, содержащего промотор и функционально связанный с ним полинуклеотид или антитело против KRS, где полинуклеотид кодирует антисмысловую РНК или миРНК против полинуклеотида KRS.
Для достижения еще одной цели настоящее изобретение относится к применению вектора экспрессии, содержащего промотор и функционально связанный с ним полинуклеотид или антитело против KRS для получения средства против злокачественной опухоли, где полинуклеотид кодирует антисмысловую РНК или миРНК против полинуклеотида KRS.
Для достижения еще одной цели настоящее изобретение относится к композиции для профилактики и лечения злокачественной опухоли, содержащей в качестве активного компонента средство, ингибирующее активность KRS.
Для достижения еще одной цели настоящее изобретение относится к способу профилактики и лечения злокачественной опухоли, включающему введение индивиду, при необходимости, эффективного количества средства, ингибирующего активность KRS.
Для достижения еще одной цели настоящее изобретение относится к применению средства, ингибирующего активность KRS для получения терапевтического средства против злокачественной опухоли.
В другом аспекте настоящее изобретение относится к способу скрининга средства, регулирующего метастазирование злокачественной опухоли или миграцию злокачественных клеток, включающему:
(a) приведение тестируемого средства в контакт с KRS в присутствии тестируемого средства;
(b) измерение активности KRS и выбор тестируемого средства, изменяющего активность KRS; и
(c) тестирование того, может ли выбранное средство регулировать метастазирование опухоли или миграцию злокачественных клеток.
В другом аспекте настоящее изобретение относится к способу скрининга средства, ингибирующего взаимодействие между KRS и 67LR, включающему:
(a) приведение тестируемого средства в контакт с KRS и рецептором ламинина (67LR) в присутствии тестируемого средства; и
(b) тестирование того, может ли выбранное средство регулировать взаимодействие между KRS и рецептором ламинина.
В другом аспекте настоящее изобретение относится к способу диагностики рака легких или рака молочной железы, включающему:
(a) анализ сверхэкспрессии 67LR в образце; и
(b) анализ сверхэкспрессии KRS в образце со сверхэкспрессией 67LR.
Техническое решение
Ниже в настоящем документе приведено подробное описание настоящего изобретения.
В настоящем изобретении авторы настоящего изобретения сначала определили, что KRS оказывает воздействие на метастазирование злокачественной опухоли или миграцию злокачественных клеток. То есть авторы настоящего изобретения определили, что KRS оказывает воздействие на метастазирование злокачественной опухоли или миграцию злокачественных клеток благодаря рецептору ламинина в плазматической мембране.
Определение
Если не определено иначе все технические и научные термины, используемые в настоящем документе, имеют то же значение, которое известно среднему специалисту в данной области, к которой принадлежит изобретение. Общие определения большинства из терминов, используемых в настоящем изобретении, предоставлены специалисту в следующих ссылках: Singleton et al., DICTIONARY OF MICROBIOLOGY AND MOLECULAR BIOLOTY (2d ed. 1994); THE CAMBRIDGE DICTIONARY OF SCIENCE AND TECHNOLOGY (Walker ed., 1988); и Hale & Marham, THE HARPER COLLINS DICTIONARY OF BIOLOGY. Кроме того, для удобства читателя в практическом осуществлении изобретения предоставлены приведенные ниже определения.
Как используется в настоящем документе "экспрессия" относится к образованию белка или нуклеиновой кислоты в клетках.
Как используется в настоящем документе "клетка-хозяин" относится к прокариотической или эукариотической клетке, содержащей гетерологичную ДНК, которую вводят в клетку любым способом, например посредством электропорации, осаждения фосфатом кальция, микроинъекции, трансформации, инфицирования вирусами и/или тому подобное.
Термин "выделенный" означает, что вещество извлекают из его исходного окружения (например, из природной среды, если оно является природным). Например, природные нуклеиновая кислота, полипептид или клетка, находящиеся у живущего животного, не являются выделенными, но те же полинуклеотид, полипептид или клетка, отделенные от некоторых или всех совместно находящихся в природной системе веществ, являются выделенными, даже если их затем обратно вводят в природную систему. Такие нуклеиновые кислоты могут представлять собой часть вектора, и/или такие нуклеиновые кислоты или полипептиды могут составлять часть композиции и могут являться выделенными в том смысле, что вектор или композиция не являются частью их природного окружения.
Термин "модулирует" в отношении видов биологической активности KRS относится к изменению клеточного уровня KRS. Модуляция видов биологической активности KRS может представлять собой положительную регуляцию (т.е. активацию или стимуляцию) или отрицательную регуляцию (т.е. ингибирование или супрессию). Например, модуляция может вызывать изменение клеточного уровня KRS, стабильности белка, ферментативной модификации (например, фосфорилирования) KRS, характеристик связывания (например, связывания с регуляторным элементом транскрипции мишени) или любого другого биологического, функционального или иммунологического свойств KRS. Изменение активности может происходить, например, вследствие повышения или снижения экспрессии гена KRS, стабильности мРНК, кодирующей белок KRS, эффективности трансляции, или вследствие изменения других видов биологической активности фактора транскрипции KRS (например, регулирующего экспрессию отвечающего за KRS гена). Способ действия модулятора KRS может быть прямым, например, за счет связывания с белком KRS или с генами, кодирующими белок KRS. Изменение также может быть непрямым, например, вследствие связывания и/или модификации (например, ферментативно) другой молекулы, которая модулирует KRS другим способом (например, киназа, специфически фосфорилирующая KRS).
Термин "полипептид" в настоящем документе попеременно используют с терминами "полипептиды" и "белок(ки)", и он относится к полимеру из аминокислотных остатков как, например, обычно в природных белках.
Термин "полипептид KRS" относится к полипептиду, известному как лизил-тРНК-синтетаза. Указанный полипептид KRS может представлять собой полипептид с аминокислотной последовательностью с SEQ ID NO:1 (инвентарный номер GenBank NP_005539,1). И KRS по изобретению содержит его функциональные эквиваленты.
Термин "функциональные эквиваленты" относится к полипептиду, содержащему аминокислотную последовательность, которая по меньшей мере на 70% гомологична аминокислотной последовательности (т.е. идентична), предпочтительно, по меньшей мере на 80%, а более предпочтительно, по меньшей мере на 90%, например, на 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% и 100% гомологична аминокислотной последовательности, который обладает по существу одинаковой физиологической активностью с полипептидом с последовательностью SEQ ID NO:1. "По существу одинаковая физиологическая активность" означает взаимодействие с рецептором ламинина плазматической мембраны и регуляцию метастазирования опухоли или миграции клеток опухоли. Функциональные эквиваленты могут включать, например, пептиды, получаемые в результате добавления, замены или делеции любой аминокислоты из SEQ ID NO:1. Аминокислотные замены предпочтительно являются консервативными заменами. Примеры консервативных замен природных аминокислот являются следующими: алифатические аминокислоты (Gly, Ala, Pro), гидрофобные аминокислоты (Ile, Leu, Val), ароматические аминокислоты (Phe, Tyr, Trp), кислые аминокислоты (Asp, Glu), основные аминокислоты (His, Lys, Arg, Gln, Asn) и серосодержащие аминокислоты (Cys, Met). Кроме того, функциональные эквиваленты также включают варианты с делецией любой аминокислотной последовательности в KRS по изобретению. Аминокислотные делеции или замены, предпочтительно, расположены в областях, которые напрямую не вовлечены в физиологическую активность полипептида по изобретению. И аминокислотные делеции, предпочтительно, расположены в областях, которые не вовлечены в физиологическую активность KRS. Кроме того, функциональные эквиваленты также включают варианты с добавлением нескольких аминокислот на обоих концах аминокислотной последовательности KRS или внутри последовательности. Кроме того, функциональные эквиваленты по изобретению также включают производные полипептидов, содержащие модификации некоторых из химических структур полипептида по изобретению при сохранении основного каркаса и физиологической активности полипептида по изобретению. Примеры этих модификаций включают структурные модификации для изменения стабильности, хранимости, летучести или растворимости полипептида по изобретению.
Идентичность или гомология последовательностей определены в настоящем документе как доля аминокислотных остатков в кандидатной последовательности, которая идентична аминокислотной последовательности KRS (SEQ ID NO:1), после выравнивания последовательностей и внесения, если необходимо, пропусков для достижения максимального процента идентичности последовательностей, и не рассматривая любые консервативные замены (как описано выше) как составляющие идентичности последовательностей. Ни одно из N-концевых, C-концевых или внутренних удлинений, делеций или вставок в аминокислотную последовательность KRS не следует рассматривать как влияющую на идентичность или гомологию последовательностей. Таким образом, идентичность последовательностей можно определить стандартными способами, которые широко используют для сравнения сходства положения аминокислот двух полипептидов. Используя компьютерную программу, например BLAST или FASTA, два полипептида выравнивают для оптимального совпадения их соответствующих аминокислот (или по всей длине одной или обеих последовательностей, или по предопределенной части одной или обеих последовательностей). В программах предусмотрены штраф за введение пропуска по умолчанию и штраф за пропуск по умолчанию, и в сочетании с компьютерной программой можно использовать оценочную матрицу, такую как PAM 250 (стандартная оценочная матрица; см. Dayhoff et al., in Atlas of Protein Sequence and Structure, vol. 5, supp. 3 (1978)). Например, процент идентичности можно рассчитать, как указано ниже. Общее количество идентичных совпадений умножают на 100, а затем делят на сумму длины более длинной последовательности в пределах подбираемого участка и числа пропусков, внесенных в более длинную последовательность для выравнивания двух последовательностей.
Полипептид по настоящему изобретению может быть получен путем выделения из природных веществ или способами генетической инженерии. Например, молекулу ДНК, кодирующую KRS или его функциональные эквиваленты (например, SEQ ID NO:2 (инвентарный номер GenBank D32053)), конструируют любым общепринятым способом. Молекулу ДНК можно синтезировать, проводя ПЦР с использованием подходящих праймеров. Альтернативно, молекулу ДНК также можно синтезировать стандартным известным в данной области способом, например, с применением автоматического ДНК-синтезатора (коммерчески доступный в Biosearch или Applied Biosystems). Сконструированную молекулу ДНК вставляют в вектор, содержащий по меньшей мере одну контролирующую экспрессию последовательность (например, промотор, энхансер), которая функционально связана с последовательностью ДНК так, чтобы контролировать экспрессию молекулы ДНК, и полученным рекомбинантным вектором экспрессии трансформируют клетки-хозяева. Трансформированные клетки культивируют в среде и условиях, подходящих для экспрессии последовательности ДНК, и из среды для культивирования выделяют по существу чистый полипептид, кодируемый последовательностью ДНК. Выделение чистого полипептида можно проводить известным в данной области способом, например хроматографией. В отношении этого термин "по существу чистый полипептид" означает полипептид по изобретению, который по существу не содержит любых других белков, происходящих из клеток-хозяев. Относительно способа генетической инженерии для синтеза полипептида по изобретению читатель может обратиться к следующей литературе: Maniatis et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory 1982; Sambrook et al., Molecular Cloning; A Laboratory Manual, Cold Spring Harbor Press, N.Y., Second (1998) and Third (2000) Editions; Gene Expression Technology, Method in Enzymology, Genetics and Molecular Biology, Method in Enzymology, Guthrie & Fink (eds.), Academic Press, San Diego, Calif. 1991; и Hitzeman et al., J. Biol. Chem., 255, 12073-12080, 1990.
Альтернативно полипептид по изобретению можно легко синтезировать химически известным в данной области способом (Creighton, Proteins: Structures and Molecular Principles, W.H. Freeman and Co., NY, 1983). В качестве типичного способа, они не ограничиваются, но включают жидко- или твердофазный синтез, конденсацию фрагментов, химические реакции с F-MOC или T-BOC (Chemical Approaches to the Synthesis of Peptides and Proteins, Williams et al., Eds., CRC Press, Boca Raton Florida, 1997; A Practical Approach, Atherton & Sheppard, Eds., IRL Press, Oxford, England, 1989).
Рецептор ламинина по изобретению (67LR) массой 67 кДа представляет собой встроенный в плазматическую мембрану, неинтегриновый рецептор, и, например, он может иметь любую нуклеотидную последовательность или аминокислотную последовательность из представленных в инвентарных номерах GenBank NM_002295, S37431, AF284768, S37431, AF284768, J03799, XP 370865, XP 001083023.
Термины "нуклеиновая кислота", "последовательность ДНК" или "полинуклеотид" относятся к полимеру из дезоксирибонуклеотидов или рибонуклеотидов в одно- или двухцепочечной форме, и, если не ограничено иным образом, включает известные аналоги природных нуклеотидов, которые гибридизуются с нуклеиновыми кислотами сходным с природными нуклеотидами образом.
Термин "нуклеотид, кодирующий KRS или ее функциональные эквиваленты" может включать нуклеиновую кислоту, кодирующую полипептид с аминокислотной последовательностью SEQ ID NO:1, или полипептид, который гомологичен аминокислотной последовательности указанного полипептида по меньшей мере на 70%. Нуклеиновая кислота включает ДНК, кДНК или РНК. Полинуклеотид может иметь нуклеотидную последовательность, кодирующую аминокислотную последовательность SEQ ID NO:1, или аминокислотную последовательность с гомологией с SEQ ID NO:1 по меньшей мере 70%. Предпочтительно, полинуклеотид содержит нуклеотидную последовательность SEQ ID NO. 2. Нуклеиновая кислота может быть выделена из природного источника или получена известным в данной области способом генной инженерии.
Термин "аналог" используют в настоящем документе для обозначения молекулы, которая структурно сходна с эталонной молекулой, но которая модифицирована целенаправленным или контролируемым способом, посредством замены конкретного заместителя эталонной молекулы альтернативным заместителем. Специалист в настоящей области может ожидать, что по сравнению с эталонной молекулой аналог будет иметь такую же, сходную или улучшенную активность. Синтез и скрининг аналогов с идентификацией вариантов известных соединений с улучшенными свойствами (такими как повышенная аффинность связывания с молекулой-мишенью) представляет собой подход, который хорошо известен в области фармацевтической химии.
Термин "гомологичный", если он относится к белкам и/или белковым последовательностям, означает, что они получены из природного источника или искусственно, на основе общего белка-предшественника или общей белковой последовательности-предшественника. Подобным образом, нуклеиновые кислоты и/или последовательности нуклеиновых кислот являются гомологичными, если они получены из природного источника или искусственно, из общей нуклеиновой кислоты-предшественника или общей последовательности-предшественника нуклеиновой кислоты.
Как используют в настоящем документе, термин "эффективное количество" относится к количеству, демонстрирующему эффект изменения биологической активности KRS (например, уровней в клетках и тому подобное), отличный от нормальных клеток или тканей, или эффект ингибирования убиквитинилирования KRS.
Как используют в настоящем документе, "приведение в контакт" имеет его нормальное значение и относится к комбинированию двух или более средств (например, двух полипептидов) или комбинированию средств и клеток (например, белка и клетки). Приведение в контакт можно проводить in vitro, например, комбинируя два или более средств или комбинируя тестируемое средство и клетку или клеточный лизат в тестовой пробирке или другом контейнере. Приведение в контакт также можно проводить в клетке или in situ, например, приводя в контакт два полипептида в клетке посредством коэкспрессии в клетке или в клеточном лизате рекомбинантных полинуклеотидов, кодирующих два полипептида.
Термин "средство" или "тестируемое средство" включает любое вещество, молекулу, элемент, соединение, структуру или их сочетание. В качестве неограничивающих примеров он включает, например, белок, полипептид, малую органическую молекулу, полисахарид, полинуклеотид и т.п. Оно может представлять собой природный продукт, синтетическое соединение или химическое соединение, или сочетание двух или более веществ. Если не указано иначе, термины "средство", "вещество" и "соединение" можно использовать взаимозаменяемо. Более конкретно, тестируемые средства, которые можно идентифицировать способами по настоящему изобретению, включают полипептиды, миметики бета-изгибов, полисахариды, фосфолипиды, гормоны, простагландины, стероиды, ароматические соединения, гетероциклические соединения, бензодиазепины, олигомерные N-замещенные глицины, олигокарбаматы, полипептиды, сахариды, жирные кислоты, стероиды, пурины, пиримидины, производные, структурные аналоги или их сочетания. Некоторые тестируемые средства представляют собой синтетические молекулы и другие природные молекулы. Тестируемые средства получают из широкого множества источников, включающего библиотеки синтетических или природных соединений. Комбинаторные библиотеки можно получать из многих типов соединений, которые можно синтезировать поэтапным способом. Большие комбинаторные библиотеки соединений можно конструировать способом кодируемых синтетических библиотек (ESL), описанном в WO 95/12608, WO 93/06121, WO 94/08051, WO 95/35503 и WO 95/30642. Пептидные библиотеки также можно получать способами фагового дисплея (см., например, Devlin, WO 91/18980). Библиотеки природных соединений в форме бактериальных, грибковых, растительных и животных экстрактов можно получать из коммерческих источников или собирать в полевых условиях. Для получения структурных аналогов известные фармакологические средства можно подвергать направленным или случайным химическим модификациям, таким как ацилирование, алкилирование, этерификация, амидирование.
Тестируемые средства могут представлять собой природные белки или их фрагменты. Такие тестируемые средства можно получать из природного источника, например клетки или тканевого лизата. Также можно получать библиотеки полипептидных средств, например из библиотеки кДНК, коммерчески доступной или получаемой общепринятыми способами. Тестируемые средства также могут представлять собой пептиды, например пептиды из аминокислот в количестве приблизительно от 5 до приблизительно 30, с предпочтительным количеством аминокислот приблизительно от 5 до приблизительно 20 и особенно предпочтительным количеством приблизительно от 7 до приблизительно 15. Пептиды могут представлять собой продукты расщепления природных белков, случайные пептиды или "смещенные" случайные пептиды.
Тестируемые средства также могут представлять собой "нуклеиновые кислоты". Тестируемые средства в виде нуклеиновых кислот могут представлять собой природные нуклеиновые кислоты, случайные нуклеиновые кислоты или "смещенные" случайные нуклеиновые кислоты. Например, продукты расщепления прокариотических или эукариотических геномов можно использовать аналогично, как описано выше для белков.
В некоторых предпочтительных способах тестируемые средства представляют собой низкомолекулярные соединения (например, молекулы с молекулярной массой не более чем приблизительно 1000). Предпочтительно, для скрининга таких низкомолекулярных соединений адаптируют и используют высокопроизводительные анализы. Для такого скрининга доступен ряд анализов, например, как описано в Schultz (1998) Bioorg. Med. Chem. Lett. 8:2409-2414; авторы настоящего изобретения (1997) Mol. Divers. 3:61-70; Fernandes (1998) Curr. Opin. Chem. Biol. 2:597-603; и Sittampalam (1997) Curr. Opin. Chem. Biol. 1:384-91.
Библиотеки тестируемых средств для скрининга способами по настоящему изобретению также можно получать на основе структурного анализа KRS, ее фрагментов или ее аналогов. Такой структурный анализ обеспечивает идентификацию тестируемых средств, которые с большей вероятностью связываются с KRS. Трехмерные структуры KRS можно исследовать рядом способов, например, посредством кристаллической структуры и молекулярного моделирования. В литературе хорошо известны способы исследования структуры белков с применением рентгеноструктурной кристаллографии. См. Physical Bio-chemistry, Van Holde, K. E. (Prentice-Hall, New Jersey 1971), pp. 221-239 и Physical Chemistry with Applications to the Life Sciences, D. Eisenberg & D. C. Crothers (Benjamin Cummings, Menlo Park 1979). Другие средства для разработки тестируемых средств для скрининга KRS предоставляют компьютерное моделирование структур KRS. Способы молекулярного моделирования описаны в литературе, например, в патенте США № 5612894, озаглавленном "System and method for molecular modeling utilizing a sensitivity factor", и в патенте США № 5583973 "Molecular modeling method and system". Кроме того, структуру белков также можно определять посредством нейтронографии и ядерного магнитного резонанса (ЯМР). См., например, Physical Chemistry, 4th Ed. Moore, W. J. (Prentice-Hall, New Jersey 1972), и NMR of Proteins and Nucleic Acids, K. Wuthrich (Wiley-Interrscience, New York 1986).
Ниже в настоящем документе приведено подробное описание настоящего изобретения.
Авторы настоящего изобретения выявили, что KRS по изобретению взаимодействует с 67LR посредством транслокации KRS в плазматическую мембрану и, таким образом, усиливает миграцию клеток опухоли (или злокачественной опухоли), таким образом, оказывая влияние на метастазирование злокачественной опухоли. Кроме того, авторы настоящего изобретения также выявили, что сверхэкспрессия KRS или ингибирование экспрессии KRS может модулировать метастазирование клеток опухоли (или злокачественной опухоли) в экспериментах in vivo с использованием мышей.
Таким образом, настоящее изобретение относится к способу контроля метастазирования злокачественной опухоли посредством изменения клеточного уровня лизил-тРНК-синтетазы.
Подробнее, если клеточный уровень лизил-тРНК-синтетазы по изобретению снижен, метастазирование злокачественной опухоли может подавляться, а если клеточный уровень лизил-тРНК-синтетазы по изобретению увеличен, метастазирование злокачественной опухоли может индуцироваться.
Снижение или увеличение клеточного уровня регулируется различными хорошо известными в данной области способами, как описано выше. Например, но не ограничиваясь этим, клеточный уровень можно контролировать посредством регуляции транскрипции или посттранскрипционной регуляции. Регуляцию транскрипции можно проводить способом увеличения экспрессии гена, известным в данной области, например, способом увеличения экспрессии гена, посредством получения рекомбинантного вектора экспрессии, содержащего полинуклеотид, кодирующий KRS или ее функциональный эквивалент, функционально связанные с промотором, или способом вставки рядом с геном регулирующей экспрессию последовательности для увеличения экспрессии гена, кодирующего KRS или ее функциональный эквивалент, или способом ингибирования экспрессии гена, например, способом ингибирования активности промотора или функции белка, посредством индукции мутации в областях промотора или гена, способом экспрессии смыслового гена, или миРНК или микроРНК.
Посттранскрипционную регуляцию можно проводить способом увеличения или снижения экспрессии белка, известным в данной области, например способом увеличения или снижения стабильности мРНК гена, кодирующего KRS или ее функциональный эквивалент, способом увеличения или снижения стабильности белка или полипептида, или способом увеличения или снижения активности белка или полипептида.
В качестве конкретного примера указанных выше способов можно индуцировать одновременную супрессию посредством трансформации с использованием последовательности ДНК, кодирующей РНК, действующей на мРНК, такую как интрон типа 1, РНК типа M1, типа головки молотка или типа шпильки или типа микроРНК, или посредством трансформации с использованием ДНК с той же, как у гена-мишени или сходной последовательностью.
Предпочтительно, в настоящем изобретении способ контроля клеточного уровня KRS или ее функционального эквивалента можно осуществлять способом повышения или снижения экспрессии полинуклеотида, кодирующего полипептид. Способ повышения или снижения могут использовать специалисты в данной области, например, посредством получения рекомбинантного вектора экспрессии, содержащего полинуклеотид, кодирующий KRS или ее функциональный эквивалент, функционально связанные с промотором, для увеличения экспрессии полинуклеотида, или посредством получения рекомбинантного вектора экспрессии, содержащего полинуклеотид антисмысловой РНК или полинуклеотид миРНК против полинуклеотида, кодирующего KRS или ее функциональный эквивалент, функционально связанные с промотором, для подавления экспрессии полинуклеотида. Предпочтительно, полинуклеотид, кодирующий KRS или ее функциональный эквивалент, может иметь нуклеотидную последовательность, представленную SEQ ID.NO:2.
Кроме того, настоящее изобретение относится к способу контроля миграции злокачественных клеток посредством изменения клеточного уровня лизил-тРНК-синтетазы, и модуляция клеточного уровня является такой же, как описано выше.
Кроме того, если экспрессия KRS по изобретению супрессирована, то метастазирование опухоли (или злокачественной опухоли) ингибировано, настоящее изобретение относится к композиции для профилактики и лечения злокачественной опухоли, в качестве эффективного ингредиента содержащей вектор экспрессии, содержащий промотор и структурный ген, подавляющий экспрессию KRS, функционально связанный с ним, или антитело против KRS. Структурный ген, подавляющий экспрессию KRS, может представлять собой антисмысловую РНК или миРНК против полинуклеотида, кодирующего KRS.
Заболевания, в отношении которых композиция по изобретению может быть эффективна, представляют собой злокачественные опухоли. Злокачественные опухоли включают, но ими не ограничиваются, рак толстого кишечника, рак легких, рак печени, рак желудка, рак пищевода, рак поджелудочной железы, рак желчного пузыря, рак почки, рак мочевого пузыря, рак предстательной железы, рак семенников, рак шейки матки, карциному эндометрия, хориокарциному, рак яичников, рак молочной железы, рак щитовидной железы, опухоль головного мозга, злокачественную опухоль головы или шеи, злокачественную меланому, лимфому, апластическую анемию.
"Промотор" означает последовательность ДНК, регулирующую экспрессию последовательности нуклеиновой кислоты, функционально связанной с промотором, в конкретной клетке-хозяине, а термин "функционально связанный" означает, что один фрагмент нуклеиновой кислоты связан с другим фрагментом нуклеиновой кислоты так, что его функция или экспрессия находятся под влиянием другого фрагмента нуклеиновой кислоты. Кроме того, промотор может содержать последовательность оператора для контроля транскрипции, последовательность, кодирующую подходящий участок связывания рибосомы мРНК, и последовательности, контролирующие терминацию транскрипции и трансляции. Кроме того, он может представлять собой конститутивный промотор, который конститутивно индуцирует экспрессию гена-мишени, или индуцибельный промотор, который индуцирует экспрессию гена-мишени в конкретном участке и в конкретный момент времени, и их примеры включают промотор SV40, промотор CMV, промотор CAG (Hitoshi Niwa et al., Gene, 108:193-199, 1991; Monahan et al., Gene Therapy, 7:24-30, 2000;), промотор 35S CaMV (Odell et al., Nature 313:810-812, 1985), промотор Rsyn7 (патентная заявка США № 08/991601), промотор актина риса (McElroy et al., Plant Cell 2:163-171, 1990), промотор убиквитина (Christensen et al., Plant Mol. Biol. 12:619-632, 1989), промотор ALS (патентная заявка США № 08/409297). Подходящие промоторы также описаны в патенте США № 5608149; 5608144; 5604121; 5569597; 5466785; 5399680; 5268463; и 5608142 и тому подобное.
При этом настоящее изобретение относится к способу профилактики и лечения злокачественной опухоли, включающему введение индивиду, при необходимости, эффективного количества вектора экспрессии, содержащего промотор и структурный ген, подавляющий экспрессию KRS, функционально связанный с ним, или антитело против KRS. Так как структурный ген описан выше, настоящее изобретение относится к способу профилактики и лечения злокачественной опухоли, включающему введение индивиду, при необходимости, эффективного количества вектора экспрессии, содержащего в качестве эффективного ингредиента промотор и функционально связанный с ним полинуклеотид или антитело против KRS, где полинуклеотид кодирует антисмысловую РНК или миРНК против полинуклеотида KRS.
Как используют в настоящем документе, "эффективное количество" относится к количеству вектора экспрессии по изобретению, эффективному для лечения опухоли, а "индивид" относится к животным, предпочтительно человеку, а также он может представлять собой клетки, ткани, органы, полученные у животных. Индивид может представлять собой больного.
Кроме того, настоящее изобретение относится к использованию вектора экспрессии, содержащего промотор и структурный ген, подавляющий экспрессию KRS, функционально связанный с ним, или антитело против KRS, для получения средства против злокачественной опухоли. Более конкретно, настоящее изобретение относится к применению вектора экспрессии, содержащего промотор и функционально связанный с ним полинуклеотид или антитело против KRS, для получения средства против злокачественной опухоли, где полинуклеотид кодирует антисмысловую РНК или миРНК против полинуклеотида KRS. Относительно указанного выше промотор, KRS, вектор экспрессии, злокачественные опухоли, к которым все это применимо, являются такими, как можно видеть из указанного ранее.
Как используют в настоящем документе, термин антитело против KRS означает специфическую белковую молекулу, которая направлена к антигенной области, относящейся к антигенной области KRS. Относительно задач настоящего изобретения антитело относится к антителу, специфически связывающему KRS, и оно включает все поликлональные, моноклональные и рекомбинантные антитела.
Антитела против KRS можно легко получать общепринятыми способами, известными специалисту в данной области. Поликлональные антитела можно получать широко известным в данной области способом, который включает инъекцию белка KRS животному и взятие образцов крови животного с получением сыворотки, содержащей антитела. Такие поликлональные антитела можно получать у различных животных-хозяев, например козы, кролика, овцы, обезьяны, лошади, свиньи, коровы и собаки.
Моноклональные антитела можно получать широко известным в данной области способом, таким как гибридомный способ (Kohler and Milstein, European Journal of Immunology, 6:511-519(1976)) или способ фаговой библиотеки антител (Clackson et al., Nature, 352:624-628(1991); и Marks et al., J. Mol. Biol., 222:58, 1-597(1991)).
В гибридомном способе используют клетки иммунологически подходящих животных-хозяев, таких как мыши, которым в качестве антигена инъецируют диагностический маркерный белок рака легких, и клеточную линию злокачественной опухоли или миеломы в качестве другой группы. Клетки двух групп сливают друг с другом широко известным в данной области способом, например с применением полиэтиленгликоля, и продуцирующие антитела клетки размножают стандартным способом тканевой культуры. После получения однотипных клеточных колоний посредством субклонирования с использованием способа лимитирующих разведений, гибридомы, способные продуцировать антитела, специфичные к диагностическому маркерному белку рака легких, стандартным способом культивируют в крупном масштабе in vitro или in vivo. Моноклональные антитела, полученные посредством гибридом, можно использовать в неочищенной форме, но для того, чтобы получить наилучший результат их предпочтительно использовать после того, как они станут высокоочищенными, используя широко известный в данной области способ. Способ фаговой библиотеки антител включает конструирование фаговой библиотеки антител in vitro, получая гены антител (одноцепочечный вариабельный фрагмент (scFv)) к ряду внутриклеточных маркеров рака легких и экспрессируя их в форме слитого белка на поверхности фагов, и выделение моноклональных антител, связывающихся со специфичными для рака легких белками из библиотеки. Антитела, полученные указанными выше способами, выделяют с использованием электрофореза в геле, диализа, высаливания, ионообменной хроматографии, аффинной хроматографии и тому подобное.
Кроме того, антитела по настоящему изобретению включают полные формы, содержащие две полноразмерные легкие цепи и две полноразмерные тяжелые цепи, а также функциональные фрагменты молекул антител. Функциональные фрагменты молекул антител относятся к фрагментам, сохраняющим по меньшей мере антигенсвязывающую функцию и включают Fab, F(ab'), F(ab')2 и Fv.
Кроме того, также авторы настоящего изобретения обнаружили, что в случае снижения клеточного уровня KRS, происходит подавление метастазирования злокачественной опухоли, таким образом, обеспечивая профилактику и лечение злокачественной опухоли, и настоящее изобретение относится к композициям для профилактики и лечения злокачественной опухоли, содержащим в качестве эффективного ингредиента ингибитор активности KRS. Кроме того, настоящее изобретение относится к способу профилактики и лечения злокачественной опухоли, включающему введение индивиду, при необходимости, эффективного количества ингибитора активности KRS и применение ингибитора активности KRS для получения средства против злокачественной опухоли. Тип злокачественной опухоли, индивид, эффективное количество и тому подобное являются такими же, как описано выше.
Ингибитор активности KRS означает средство для подавления экспрессии KRS, т.е. подавления экспрессии на уровне мРНК или белка, например, он может представлять собой антисмысловую РНК или миРНК против KRS, или конкурентный ингибитор или неконкурентный ингибитор для подавления активности экспрессированного KRS, например, антитела против KRS, но не ограничиваться ими.
В случае снижения клеточного уровня KRS, так как она ингибирует метастазирование злокачественной опухоли с профилактикой и лечением злокачественной опухоли, композицию, способ и применение по изобретению можно использовать самостоятельно, а также можно использовать в виде комбинаций с хорошо известным в данной области способом профилактики и лечения злокачественной опухоли. Т.е. так как композиция, способ и тому подобное по изобретению могут подавлять метастазирование злокачественной опухоли, если их использовать совместно с хорошо известными лекарственными средствами против злокачественных опухолей или способами профилактики и лечения злокачественных опухолей, они подавляют метастазирование злокачественной опухоли и могут быть эффективны в отношении полного восстановления, включая лечение основной области опухоли.
Противоопухолевое средство или способ профилактики и лечения, которые можно использовать в комбинации с полипептидом по настоящему изобретению, могут представлять собой любое, используемое для лечения опухоли. Например, можно включать паклитаксел, доксорубицин, винкристин, даунорубицин, винбластин, даунорубицин D, доцетаксел, этопозид, тенипозид, бизантрен, гомогаррингтонин, гливек (STI-571), цисплатин, 5-фторурацил, адриамицин, метотрексат, бусульфан, хлорамбуцил, циклофосфамид, мелфалан, азотистый иприт, нитрозомочевину и тому подобное. Количество пептида по настоящему изобретению, вводимого в композицию по настоящему изобретению, может быть различным в зависимости от вида и количества лекарственного средства против злокачественной опухоли, с которым связывают пептид.
Специалист в данной области может соответствующим образом осуществлять комбинирование средств и формировать композицию или способ по настоящему изобретению в зависимости от вида и количества лекарственного средства против злокачественной опухоли.
Вектор экспрессии, средство, ингибирующее активность антитела против KRS или KRS, по изобретению, можно вводить перорально или парентерально. Пероральное введение может включать сублингвальный способ. Способы парентерального введения не ограничены, но включают способы инъекции, такие как подкожный, внутримышечный и внутривенный, и способ капельного введения. Вектор экспрессии, средство, ингибирующее активность антитела против KRS или KRS, по изобретению можно получать в различных видах фармацевтических композиций посредством смешивания с фармацевтически приемлемыми носителями. Как используется в настоящем документе, термин "фармацевтически приемлемый" означает то, что является физиологически приемлемым и если его вводят людям, как правило, не вызывает аллергических реакций, таких как желудочно-кишечные расстройства и головокружения, или сходных с ними реакций. В случае перорального состава можно использовать связывающее средство, смазочное средство, средство, способствующее растворению, эксципиент, растворитель, диспергирующее средство, стабилизатор, суспендирующее средство, краситель и ароматизатор. В случае инъекционного состава можно использовать буфер, консервант, обезболивающее средство, растворитель, средство придания изотоничности и стабилизатор, а в случае парентерального состава можно использовать основание, эксципиент, смазочное средство и консервант. Фармацевтическую композицию, содержащую вектор экспрессии, средство, ингибирующее активность антитела против KRS или KRS, по изобретению можно получать в различных видах, смешивая с фармацевтически приемлемыми носителями. Например, в случае перорального состава, его можно составлять в виде таблетки, пастилки, капсулы, эликсира, суспензии, сиропа и вафли, а в случае инъекционного состава его можно получать в виде ампулы для однократного дозирования или ампулы для множественного дозирования.
Общее эффективное количество вектора экспрессии, средства, ингибирующего активность антитела против KRS или KRS, по изобретению можно вводить индивиду в виде однократной дозы или можно вводить с использованием протокола дробного лечения, при котором в течение более длительного периода времени вводят несколько доз. У композиции, содержащей вектор экспрессии, средство, ингибирующее активность антитела против KRS или KRS, по изобретению, в зависимости от тяжести заболевания и/или заболевшего индивида количество эффективного компонента можно варьировать, но, как правило, можно вводить от 0,1 мкг до 100 мг, а предпочтительно, от 1 мкг до 10 мг и несколько раз в сутки. Однако специалисту в данной области известно, что концентрация вектора экспрессии или средства по изобретению, ингибирующего активность KRS, необходимая для получения эффективной дозы у индивида, зависит от многих факторов, в том числе возраста, массы тела, общего состояния, тяжести заболевания, питания и системы выведения индивида, пути введения, количества вводимых лекарственных средств и тому подобное. Принимая во внимание эти факторы, любой специалист в данной области может определить подходящую эффективную дозу вектора экспрессии или средства, ингибирующего активность KRS, по изобретению. Конкретного ограничения на состав, маршрут введения и способ введения фармацевтической композиции по настоящему изобретению не накладывается при условии, что композиция демонстрирует действие по настоящему изобретению.
Композиции по изобретению можно вводить пациентам в количестве, которое эффективно для профилактики заболевания. Как правило, эффективное количество композиции по изобретению составляет приблизительно от 0,0001 до 100 мг/кг массы тела/сутки. Предпочтительно от 0,01 до 1 мг/кг массы тела/сутки. Его можно соответствующим образом определить, учитывая различные факторы, такие как возраст, масса тела, состояние здоровья, пол, тяжесть заболевания, диета и система выделения индивида, нуждающегося в лечении, а также время введения и способ введения.
При этом указанный вектор экспрессии можно вводить в клетку-мишень любым известным в данной области способом, таким как инфекция, трансфекция или трансдукция.
Способ переноса генов с использованием плазмидного вектора экспрессии представляет собой способ переноса плазмидной ДНК непосредственно в клетки млекопитающих, который представляет собой одобренный FDA способ, применимый для людей (Nabel, E. G., et al., Science, 249:1285-1288, 1990). В отличие от вирусных векторов преимуществом плазмидной ДНК является тот факт, что она является гомогенно очищенной. Плазмидные векторы экспрессии, которые можно использовать в настоящем изобретении, включают экспрессирующие плазмиды млекопитающих, известные в данной области. Например, они не ограничены, но, как правило, включают pRK5 (европейский патент № 307247), pSV16B (публикация PCT № 91/08291) и pVL1392 (PharMingen). Плазмидный вектор экспрессии, содержащий указанный полинуклеотид, можно вводить в клетки-мишени любым известным в данной области способом, включая в качестве неограничивающих примеров, способы транзиторной трансфекции, микроинъекции, трансдукции, слияния клеток, осаждения фосфатом кальция, опосредованной липосомами трансфекции, опосредованной DEAE-декстраном трансфекции, опосредованной полибреном трансфекции, электропорации, генной пушки и другие известные способы введения ДНК в клетки (Wu et al., J. Bio. Chem., 267:963-967, 1992; Wu and Wu, J. Bio. Chem., 263:14 621-14 624, 1988).
Кроме того, вирусные векторы экспрессии, содержащие указанный полинуклеотид, включают в качестве неограничивающих примеров ретровирус, аденовирус, вирус герпеса, вирус оспы птиц и тому подобное. Ретровирусный вектор конструируют так, что вирусный вектор, в котором все вирусные гены удалены или модифицированы, может продуцировать в инфицированных клетках невирусные белки. Основными преимуществами ретровирусного вектора для генотерапии являются то, что он трансфицирует большое количество генов в реплицирующиеся клетки, точно интегрирует трансфицированные гены в клеточную ДНК и не индуцирует длительных инфекций после трансфекции генов (Miller, A.D., Nature, 357:455-460, 1992). Ретровирусный вектор, одобренный FDA, получали с использованием амфотропных упаковывающих ретровирусы клетки PA317 (Miller, A. D. and Buttimore, C., Molec. Cell Biol., 6:2895-2902, 1986). Неретровирусные векторы включают аденовирусы, как описано выше (Rosenfeld et al., Cell, 68:143-155, 1992; Jaffe et al., Nature Genetics, 1:372-378, 1992; Lemarchand et al., Proc. Natl. Acad. Sci. USA, 89:6482-6486, 1992). Основными преимуществами аденовирусов является то, что они трансфицируют большое количество фрагментов ДНК (геномы из 36 т.п.н.) и способны инфицировать нереплицирующиеся клетки с очень высоким титром. Кроме того, также пригодным для генотерапии человека может являться вирус герпеса (Wolfe, J.H., et al., Nature Genetics, 1:379-384, 1992). Кроме того, можно использовать другие известные подходящие вирусные векторы.
Кроме того, вектор, способный ингибировать экспрессию KRS, можно вводить любым известным способом. Например, вектор можно вводить местно, парентерально, перорально, интраназально, внутривенно, внутримышечно или подкожно или любыми другими подходящими путями. В частности, вектор можно непосредственно вводить путем инъекции в интересующую злокачественную опухоль или опухолевую клетку в эффективном количестве для обработки опухолевых клеток ткани-мишени. В частности, для злокачественной опухоли или опухоли, присутствующей в полости тела, такой как глаз, желудочно-кишечный тракт, мочеполовые пути, легочная и бронхиальная система и тому подобное, фармацевтическую композицию по изобретению можно непосредственно инъецировать в полый орган, пораженный злокачественной опухолью или опухолью, с применением иглы, катетера или других направляющих трубок. Для определения локализации ткани-мишени и направления иголки или трубки катетера можно использовать любое эффективное визуализирующее устройство, такое как рентгеновская установка, фонограф или волоконно-оптическая система визуализации. Кроме того, для лечения злокачественной опухоли или опухоли, которую нельзя достичь напрямую или выделить анатомически, фармацевтическую композицию по изобретению можно вводить в систему кровообращения.
Настоящее изобретение также относится к способу скрининга средства, модулирующего метастазирование злокачественной опухоли или миграцию злокачественных клеток, включающему:
(a) приведение тестируемого средства в контакт с KRS в присутствии тестируемого средства;
(b) измерение активности KRS и выбор тестируемого средства, изменяющего активность KRS; и
(c) тестирование того, может ли выбранное средство регулировать метастазирование опухоли или миграцию злокачественных клеток.
Для практического осуществления настоящего изобретения можно использовать различные способы биохимии и молекулярной биологии или хорошо известные в данной области анализы. Такие способы описаны, например, в Sambrook et al., Sambrook et al., Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Press, N.Y., второе (1989) и третье (2000) издания; и Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, Inc., New York (1987-1999).
Предпочтительно, тестируемое средство вначале анализируют на его способность модулировать биологическую активность KRS (первый этап анализа). В частности, на первом этапе можно идентифицировать модулирующие средства, модулирующие биологическую активность указанного полипептида, анализируя биологическую активность выделенной KRS в присутствии тестируемого средства. Более предпочтительно, настоящее изобретение может включать:
(a) приведение тестируемых средств в контакт с KRS в присутствии тестируемого средства; и
(b) измерение активности KRS и выбор тестируемого средства, изменяющего активность KRS.
На первом этапе можно анализировать модуляцию различных видов биологической активности KRS. Например, можно анализировать активность тестируемого средства в отношении модуляции уровня экспрессии KRS, например транскрипции или трансляции. Также можно анализировать активность тестируемого средства в отношении изменения клеточного уровня или стабильности KRS, например посттрансляционной модификации или протеолиза.
На первом этапе анализа идентифицируют тестируемые средства, которые увеличивают биологическую активность KRS, затем тестируемые средства подвергают дальнейшему тестированию на способность модулировать активность рецептора ламинина (67LR) в присутствии KRS (второй этап тестирования). Например, тестируемые средства затем подвергают дальнейшему тестированию на способность модулировать метастазирование злокачественной опухоли или миграцию клеток опухоли.
Как указано выше, модулирующие KRS средства, идентифицированные в настоящем изобретении, могут модулировать метастазирование злокачественной опухоли или миграцию клеток опухоли. Если тестируемое средство, идентифицированное на первом этапе тестирования, модулирует клеточный уровень (например, посредством изменения активности транскрипции) модулирующих KRS средств, оно будет модулировать метастазирование злокачественной опухоли или миграцию клеток опухоли.
С другой стороны, если тестируемое средство модулирует активность, отличную от клеточного уровня KRS, то для подтверждения, что его модулирующий эффект на KRS действительно может приводить к модуляции метастазирования злокачественной опухоли или миграции клеток опухоли, необходим дополнительный этап тестирования. Например, тестируемому средству, модулирующему активность фосфорилирования KRS, для подтверждения того, что модуляция активности фосфорилирования KRS может приводить к модуляции метастазирования злокачественной опухоли или миграции клеток опухоли, необходимо дополнительное тестирование.
На первом этапе и на втором этапе можно использовать интактную KRS и ее субъединицы или фрагменты, аналоги или функциональные производные. Фрагменты, которые можно использовать в этих анализах, как правило, сохраняют один или несколько видов биологической активности KRS. Предпочтительно, фрагменты AIMP2 могут содержать 1-72 аминокислотных остатка SEQ ID NO:1, а также для скрининга тестируемых средств можно использовать слитые белки, содержащие такие фрагменты или аналоги. Функциональные производные KRS, как правило, содержат делеции и/или вставки, и/или замены аминокислот, сохраняя при этом один или несколько видов биологической активности, и, таким образом, их также можно использовать в практическом осуществлении способов скрининга по настоящему изобретению.
Для идентификации тестируемых средств, которые модулируют KRS, можно использовать ряд хорошо известных способов. Предпочтительно, тестируемые средства подвергают скринингу посредством системы анализа на основе клеток. Например, в характерном анализе на основе клеток (т.е. на втором этапе скрининга) измеряют активность репортерного гена (т.е. ферментативную активность) в присутствии тестируемого средства, а затем сравнивают с активностью репортерного гена в отсутствие тестируемого средства. Репортерный ген может кодировать любой детектируемый полипептид (полипептид ответа или репортерный полипептид), известный в данной области, например, детектируемый посредством флуоресценции или фосфоресценции или на основании обладания им ферментативной активности. Детектируемый полипептид ответа может представлять собой, например, люциферазу, альфа-глюкуронидазу, альфа-галактозидазу, хлорамфениколацетилтрансферазу, зеленый флуоресцентный белок, улучшенный зеленый флуоресцентный белок и секретируемую щелочную фосфатазу человека.
В основанных на клетках анализах тестируемое средство (например, пептид или полипептид) также можно экспрессировать с помощью вектора, отличного от вектора, который уже присутствует в клетке-хозяине. В определенных способах библиотека тестируемых средств закодирована библиотекой таких векторов (например, библиотека кДНК; см. пример ниже). Такие библиотеки можно получать известными в данной области способами (см., например, Sambrook et al. и Ausubel et al., выше) или получать из ряда коммерческих источников.
Кроме клеточных анализов, описанных выше, также можно проводить скрининг не основанными на клетках способами. Эти способы включают, например, анализ связывания ДНК со сдвигом подвижности, анализы метилирования и интерференции урацила, анализ футпринтинга с применением ДНКазы и гидроксидных радикалов, анализ поляризации флуоресценции и сшивку УФ или химическими кросс-линкерами. Для общего обзора см., например, Ausubel et al., выше (глава 12, DNA-Protein Interactions). Один из способов выделения совместно связанных белков, включая связывающие нуклеиновые кислоты и ДНК/РНК белки, включает использование сшивания УФ или химическими кросс-линкерами, включая например, расщепляемые кросс-линкеры дитиобис(сукцинимидилпропионат) и 3,3'-дитиобис(сульфосукцинимидилпропионат); см., например, McLaughlin, Am. J. Hum. Genet., 59:561-569, 1996; Tang, Biochemistry, 35:8216-8225, 1996; Lingner, Proc. Natl. Acad. Sci. U.S.A., 93:10712, 1996; и Chodosh, Mol. Cell. Biol., 6:4723-4733, 1986.
Первый этап анализа. Скрининг тестируемых средств, которые модулируют KRS
Для скрининга тестируемых средств на модуляторы KRS можно использовать ряд систем анализа. Как указано выше, в скрининге можно использовать систему анализа in vitro или систему анализа на основе клеток. На этом этапе скрининга тестируемые средства можно подвергать скринингу на связывание с KRS, изменение клеточного уровня KRS или изменение других видов биологической активности KRS.
1) Скрининг тестируемых средств, которые связывают KRS
На первом этапе скрининга применяют определенные способы, которыми определяют связывание тестируемого средства с KRS. Например, его можно анализировать рядом способов, включая, например, анализы связывания меченых белков in vitro, анализы изменения электрофоретической подвижности, иммунологические анализы связывания белков, функциональные анализы (анализы фосфорилирования и тому подобное) и тому подобное. См., например, патенты США №№ 4366241; 4376110; 4517288 и 4837168; а также Bevan et al., Trends in Biotechnology 13:115-122, 1995; Ecker et al., Bio/Technology 13:351-360, 1995; и Hodgson, Bio/Technology 10:973-980, 1992. Тестируемое средство можно идентифицировать посредством детекции прямого связывания с KRS, например коиммунопреципитации с KRS посредством антитела против KRS. Тестируемое средство также можно идентифицировать посредством детекции сигнала, указывающего на то, что средство связывается с KRS, например гашение флуоресценции.
Для идентификации тестируемых средств, которые специфически связываются с KRS, подходящий формат обеспечивают анализы конкурентного связывания. В таких форматах тестируемые средства подвергают скринингу в конкуренции с соединениями, для которых уже известно, что они связываются с KRS. Известное связывающееся соединение может представлять собой синтетическое соединение. Оно также может представлять собой антитело, которое специфически распознает полипептид KRS, например моноклональное антитело, направленное против KRS. Если тестируемое средство ингибирует связывание соединения, для которого известно, что оно связывает KRS, тогда тестируемое средство также связывает KRS.
Известно множество разновидностей анализов конкурентного связывания, например: твердофазный прямой или непрямой радиоиммунологический анализ (RIA), твердофазный прямой или непрямой иммуноферментный анализ (EIA), анализ конкурентного связывания по типу сэндвича (см. Stahli et al., Methods in Enzymology 9:242-253 (1983)); твердофазный прямой EIA с биотином-авидином (см. Kirkland et al., J. Immunol. 137:3614-3619 (1986)); твердофазный прямой анализ с мечеными веществами, твердофазный прямой анализ с мечеными веществами по типу сэндвича (см. Harlow and Lane, "Antibodies, A Laboratory Manual," Cold Spring Harbor Press (1988)); твердофазный прямой RIA с меткой с использованием метки 125I (см. Morel et al., Mol. Immunol. 25(1):7-15 (1988)); твердофазный прямой биотин-авидин EIA (Cheung et al., Virology 176:546-552 (1990)); и прямой RIA с мечеными веществами (Moldenhauer et al., Scand. J. Immunol. 32:77-82 (1990)). Как правило, в таком анализе предусмотрено использование очищенного полипептида, связанного с твердой поверхностью или с клетками, несущими любой из них, немеченого тестируемого средства и меченого эталонного соединения. Конкурентное ингибирование измеряют, определяя количество метки, связанной с твердой поверхностью или с клетками, в присутствии тестируемого средства. Как правило, тестируемое средство находится в избытке. Модулирующие средства, идентифицированные анализом конкурентного связывания, включают средства, связывающиеся с тем же эпитопом, что и эталонное соединение, и средства, связывающиеся со смежным эпитопом, находящимся в достаточной близости к эпитопу, связанному эталонным соединением, чтобы возникло стерическое препятствие. Как правило, когда конкурирующее средство присутствует в избытке, оно ингибирует специфическое связывание эталонного соединения с общим полипептидом, являющимся общей мишенью, по меньшей мере на 50 или 75%.
Анализы скрининга можно проводить в нерастворимом или растворимом формате. Одним из примеров анализов в нерастворимом формате является иммобилизация KRS или ее фрагментов на твердофазном матриксе. Затем твердофазный матрикс приводят в контакт с тестируемыми средствами в течение интервала, достаточного для того, чтобы позволить тестируемым средствам связаться. После отмывки любого несвязавшегося вещества с твердофазного матрикса, наличие средства, связанного с твердой фазой, позволяет идентифицировать средство. Способы могут включать этап элюции связанного средства с твердофазного матрикса, таким образом, проводя выделение средства. Альтернативно, иммобилизации KRS, с твердым матриксом связывают тестируемые средства, а затем добавляют KRS.
Анализы в растворимом формате включают определенные способы скрининга комбинаторных библиотек, описанные выше. В анализах в растворимых форматах ни тестируемые средства, ни KRS не связаны с твердой поверхностью. Связывание KRS или ее фрагмента с тестируемым средством можно определять, например, по изменениям флуоресценции KRS, или тестируемых средств, или обоих. Флуоресценция может быть собственной или ее можно придать посредством мечения любого компонента флуорофором.
В определенных анализах связывания для облегчения идентификации, детекции и количественного определения полипептида в конкретных условиях KRS, тестируемое средство или третью молекулу (например, антитело против KRS) можно предоставлять в виде меченых структур, т.е. ковалентно связанных или соединенных с детектируемой меткой или группой или сшиваемой группой. Эти детектируемые группы могут содержать детектируемую полипептидную группу, например поддающийся анализу фермент или эпитоп антитела. Альтернативно детектируемую группу можно выбирать из ряда других детектируемых групп или меток, таких как радиоактивные метки (например, 125I, 32P, 35S) или хемилюминесцентные или флуоресцентные группы. Подобным образом детектируемая группа может представлять собой субстрат, кофактор, ингибитор или аффинный лиганд.
2) Скрининг тестируемых средств, модулирующих другие виды активности KRS
Связывание тестируемого средства с KRS обеспечивает указание на то, что средство может являться модулятором KRS. Это также позволяет предположить, что средство может модулировать активность рецептора ламинина с модуляцией метастазирования злокачественной опухоли или миграции клеток опухоли. Таким образом, тестируемое средство, которое связывается с KRS, можно дополнительно тестировать на способность модулировать активность рецептора ламинина.
Альтернативно тестируемое средство, которое связывается с KRS, можно дополнительно тестировать для определения его активности в отношении KRS. Существование, характер и степень такой активности можно тестировать посредством анализа активности. Такой анализ активности может подтверждать, что связывание тестируемого средства с KRS действительно обладает модулирующей активностью в отношении KRS. Чаще такие анализы активности можно использовать независимо для идентификации тестируемых средств, модулирующих различные виды активности KRS (т.е. без первого анализа их способности связываться с KRS). В основном такие способы включают добавление тестируемого средства к образцу, содержащему KRS, в присутствии или отсутствии других молекул или реагентов, которые необходимы для тестирования биологической активности KRS и определения изменения биологической активности KRS. В дополнение к анализам для скрининга средств, модулирующих ферментативную активность или другие виды биологической активности KRS, анализы активности также включают скрининг in vitro и скрининг in vivo на изменения экспрессии или клеточного уровня KRS.
Второй этап тестирования. Скрининг средств, модулирующих метастазирование опухоли или миграцию клеток опухоли
После идентификации того, что модулирующее средство связывается KRS и/или модулирует биологическую активность (включая клеточный уровень) KRS, его можно дополнительно тестировать на способность модулировать метастазирование опухоли или миграцию клеток опухоли. Модуляцию метастазирования опухоли или миграцию клеток опухоли модулирующим средством, как правило, тестируют в присутствии KRS. Когда применяют систему скрининга на основе клеток, KRS можно экспрессировать с вектора экспрессии, который введен в клетку-хозяина. Альтернативно, клетка-хозяин в системе скрининга может обеспечивать KRS эндогенно.
Настоящее изобретение также относится к способу скрининга средства, ингибирующего взаимодействие между KRS и 67LR, включающему:
(a) приведение тестируемого средства в контакт с KRS и рецептором ламинина (67LR) в присутствии тестируемого средства; и
(b) тестирование того, может ли выбранное средство регулировать взаимодействие между KRS и рецептором ламинина.
Указанное средство может представлять собой средство, стимулирующее или усиливающее взаимодействие между KRS и рецептором ламинина (67LR), или, напротив, оно может представлять собой средство, ингибирующее или ухудшающее взаимодействие.
Этап (b) может включать детекцию относительных изменений уровня взаимодействия между KRS и полипептидом 67LR в клетках или их клеточном лизате, содержащих тестируемое средство, по сравнению с уровнем взаимодействия между KRS и 67LR в клетках или их клеточном лизате, не содержащих тестируемого средства.
Способ идентификации можно проводить любым обычным способом, известным в данной области, таким как анализы связывания меченых белков in vitro (анализы осаждения in vitro), EMSA (анализы изменения электрофоретической подвижности), иммунологические анализы связывания белков, функциональные анализы (анализы фосфорилирования и тому подобное), анализ в дрожжевой двухгибридной системе, анализы неиммунной иммунопреципитации, иммунопреципитация/анализы блоттинга авторов настоящего изобретения, анализы иммуносолокализации.
Например, анализы в дрожжевой двухгибридной системе можно проводить с использованием дрожжей, экспрессирующих AIMP2 и p53, или части или гомологи этих белков, слитые с ДНК-связывающим доменом репрессора бактерий LexA или GAL4 дрожжей и доменом трансактивации белка дрожжей GAL4 соответственно (Kim, M. J. et al., Nat. Gent., 34:330-336, 2003). Взаимодействие между AIMP2 и p53 реконструирует трансактиватор, индуцирующий экспрессию репортерного гена под контролем промотора с регуляторной последовательностью, связывающейся с ДНК-связывающим доменом LexA или GAL4.
Как описано выше, репортерный ген может представлять собой известный в данной области ген, кодирующий детектируемый полипептид. Например, можно использовать хлорамфениколацетилтрансферазу (CAT), люциферазу, β-галактозидазу, β-глюкозидазу, щелочную фосфатазу, зеленый флуоресцентный белок (GFP) и тому подобное. Если тестируемое средство облегчает или усиливает взаимодействие между AIMP2 и p53 или частями или гомологами этих белков, экспрессия репортерного гена по сравнению с экспрессией в обычных условиях увеличивается. С другой стороны, если тестируемое средство ингибирует или снижает взаимодействие, репортерный ген не экспрессируется или экспрессируется в меньшей степени, чем в обычных условиях.
Кроме того, можно выбирать репортерный ген, кодирующий белок, который обеспечивает рост дрожжей (т.е. если репортерный ген не экспрессируется, рост дрожжей ингибирован). Например, можно использовать ауксотрофные гены, кодирующие ферменты, вовлеченные в биосинтез для получения аминокислот или азотистых оснований (например, такие гены дрожжей, как ADE3, HIS3 и тому подобное или сходные гены других видов). Если тестируемое средство ингибирует или снижает экспрессию AIMP2 и p53 или частей или гомологов этих белков, репортерный ген не экспрессируется или экспрессируется в меньшей степени. Таким образом, в таких условиях рост дрожжей останавливается или замедляется. Такое воздействие на экспрессию репортерного гена можно наблюдать глазами или с применением различных устройств (например, микроскопа).
Кроме того, в качестве результата анализа сверхэкспрессии 67LR и KRS, проводимого у пациентов с раком легких или раком молочной железы, выявлено, что в случае сверхэкспрессии 67LR связь между сверхэкспрессией KRS и раком легких или раком молочной железы является высокой (таблица 1). Таким образом, настоящее изобретение относится к способу диагностики рака легких или рака молочной железы, состоящему из:
(a) анализа сверхэкспрессии 67LR в образце;
и
(b) анализа сверхэкспрессии LRS в образце со сверхэкспрессией 67LR.
При заборе образцов для диагностики и при обработке для диагностики и анализа сверхэкспрессии 67LR и KRS можно использовать способы молекулярной биологии, хорошо известные в данной области, и способы, описанные выше.
Ниже описаны фигуры настоящего изобретения.
На фиг.1-6 показано специфическое взаимодействие между KRS человека и рецептором ламинина. На фиг.1 взаимодействие между полноразмерной KRS человека и 37LRP/p40 определяли посредством анализа в дрожжевой двухгибридной системе. В качестве положительного и отрицательного контроля использовали, соответственно, AIMP1 и AIMP2, два компонента комплекса с несколькими ARS. На положительное взаимодействие указывает формирование синих колоний на среде для дрожжей, содержащей X-gal. На фиг.2, 37LRP синтезировали посредством трансляции in vitro в присутствии [35S]-метионина и подвергали осаждению с GST-KRS или GST. 37LRP, совместно осаждаемый с GST-KRS, детектировали посредством радиоавтографии. На фиг.3, пептидные области KRS и 37LRP, вовлеченные в их взаимодействие, определяли посредством анализа в дрожжевой двухгибридной системе, как указано выше. 37LRP содержит 296 аминокислот, где N-концевой цитоплазматический (аминокислоты 54-113) и C-концевой внеклеточный (аминокислоты 137-210) домены разделены трансмембранным доменом (аминокислоты 113-137). За N-концевым уникальным участком (приблизительно 70 аминокислот) KRS человека (597 аминокислот) следуют антикодонсвязывающий с OB-укладкой (аминокислоты 70-214) и каталитические домены (аминокислоты 220-574). На фиг.4 клетки A549, трансфицированные Myc-KRS, лизировали и подвергали анализу иммуноблоттингом с антителами против Myc и против рецептора ламинина. Myc-KRS иммунопреципитировали антителами против Myc, и совместно осаждаемые 67LR и 37LRP определяли иммуноблоттингом. Для специфического блоттинга 37LRP и 67LR авторы настоящего изобретения использовали поликлональные антитела H-141 и F-18 (Santacruz), соответственно (WCL:полный клеточный лизат). На фиг.5 трансфицированные лизатами Myc-KRS клетки A549 подвергали вестерн-блоттингу с указанными антителами. Клетки разделяли на цитоплазматические и мембранные фракции и иммунопреципитировали антителами против Myc, и совместно осаждаемые 37LRP и 67LR определяли вестерн-блоттингом. В качестве контроля использовали IgG. На фиг.6 при обработке 10 мкг/мл ламинина в течение 1 часа авторы настоящего изобретения подтвердили, что связывание 67LR и KRS увеличивалось. Для его идентификации проводили иммунопреципитацию с распознающим 67LR антителом (abcam, каталожный № ab2508), а уровень IgG слева представляет собой общий IgG кролика, и его использовали в качестве контроля. Затем проводили SDS PAGE, затем проводили перенос на мембрану из PVDF и проводили иммуноблоттинг с распознающими KRS и 67LR антителами соответственно.
На фиг.7-12 показано, что ламинин индуцировал транслокацию в мембрану и фосфорилирование KRS. На фиг.7 клетки A549 обрабатывали ламинином (10 мкг/мл) и уровень 67LR, 37LRP и KRS определяли вестерн-блоттингом в указанные моменты времени. В качестве маркеров цитоплазмы и мембраны использовали Hsp90 и кадгерин соответственно. На фиг.8 клетки A549, необработанные или в течение 1 часа обработанные ламинином, подвергали иммунофлуоресцентному окрашиванию антителами против 67LR (MLuC5, Santacruz, sc-59732) (красный) и против KRS (зеленый). На фиг.9 клетки A549 в течение 3 часов обрабатывали U73122 (U), стауроспорином (ST) и LY294002 (LY), который ингибирует PLC-гамма, PKC и PI3K соответственно, затем в течение 1 часа ламинином и проверяли, как эти ингибиторы киназ будут влиять на уровень 67LR и KRS в мембране и цитоплазме. На фиг.10 клетки A549 трансфицировали Myc-KRS и инкубировали в течение 24 часов. Клетки обрабатывали указанными химическими веществами, а затем ламинином, как указано выше. Myc-KRS иммунопреципитировали и подвергали иммуноблоттингу с антителами против p-Thr, -Ser, и -Tyr. На фиг.11 клетки A549 трансфицировали Myc-KRS и культивировали в течение 24 часов. Трансфектанты предварительно в течение 3 часов обрабатывали LY294002, а затем в течение 1 часа обрабатывали ламинином. Myc-KRS иммунопреципитировали и совместное осаждение 67LR определяли вестерн-блоттингом. В качестве контроля для иммунопреципитации использовали IgG. На фиг.12 клетки A549 культивировали в отсутствии и в присутствии ламинина и LY294002, как указано. EPRS (глутамилпролил-тРНК-синтетазу) иммунопреципитировали специфическим антителом (AbCam) и коиммунопреципитацию KRS определяли вестерн-блоттингом (верхняя панель). Иммуноистощенный супернатант (ID) подвергали вестерн-блоттингу с антителами против KRS и EPRS.
На фиг.13-17 показано, что KRS стабилизирует мембраносвязанный 67LR. На фиг.13 клетки A549 трансфицировали контрольной миРНК или миРНК KRS и инкубировали в отсутствие и в присутствии ламинина. Затем клетки разделяли на цитоплазматическую и мембранную фракции, и вестерн-блоттингом определяли уровни 67LR и KRS в каждой фракции. В качестве маркеров плазматической мембраны и цитоплазмы использовали кадгерин (cad) и hsp90 соответственно. На фиг.14 посредством проточной цитометрии с использованием антител против LR (MLuC5) подвергали мониторингу уровень мембраносвязанного 67LR в клетках A549. Клетки трансфицировали пустым вектором или плазмидой с KRS и инкубировали в течение 24 часов (верхняя панель). Для того чтобы увидеть влияние супрессии KRS на уровень 67LR клетки трансфицировали миРНК KRS или контрольной миРНК и инкубировали в течение 48 час (нижняя панель). На фиг.15 клетки A549, трансфицированные EV или KRS, отбирали с G418 в течение недели, и посредством иммунофлуоресцентного окрашивания с антителом против LR (MLuC5) определяли клеточное распределение 67LR. Расположенный на мембране LR помечен белыми стрелками. На фиг.16 клетки A549 обрабатывали циклогексимидом для ингибирования синтеза белка de novo и вестерн-блоттингом определяли влияние уровней KRS на уровень 67LR в мембране и цитоплазме. На фиг.17 посредством эксперимента с вытеснением метки определяли важность KRS для стабильности 67LR в клетке. Клетки 293 трансфицировали миРНК KRS или контрольной миРНК и в течение 1 часа вводили радиоактивный метионин. 67LR иммунопреципитировали с антителом, специфически распознающим 67LR (F-18, Santacruz), разделяли посредством SDS-PAGE и подвергали радиоавтографии. Супрессию KRS специфичной к ней миРНК подтверждали вестерн-блоттингом, а контролем загрузки являлся тубулин.
На фиг.18-22 показано, что KRS усиливает клеточную миграцию и метастазирование злокачественной опухоли посредством 67LR. На фиг.18 клетки A549 трансфицировали указанными плазмидами, инкубировали в отсутствие и в присутствии ламинина и их влияние на клеточную миграцию определяли, определяя мигрирующие клетки в камере transwell, как описано. Подсчитывали количество клеток, проходящих через мембрану, и они представлены на каждой панели. Эксперименты проводили три раза. На фиг.19 клетки, обработанные, как указано выше, использовали для определения активности и уровня MMP-2 посредством зимографии и вестерн-блоттинга соответственно. На фиг.20 клетки карциномы молочной железы 4T-1 трансфицировали указанными миРНК и подкожно инъецировали обратно мышам Balb/C. Через 21 сутки выделяли легкие мышей и подсчитывали опухолевые узлы, превосходящие 1 мм в диаметре. На фиг.21 две различные линии клеток 4T-1, стабильно экспрессирующие экзогенно введенную KRS (KRS-1 и -2), инокулировали также, как указано выше, а опухолевые узлы подсчитывали через 30 суток после инъекции. В качестве контроля использовали клетки 4T-1 с пустым вектором. На фиг.22 сравнивали уровни экспрессии KRS и 67LR в раковых тканях легкого (верхняя панель) и молочной железы (нижняя панель) посредством иммуногистохимического окрашивания соответствующими им антителами. Иммуногистохимическому окрашиванию антителами против KRS и против 67LR подвергали 39 образцов тканей рака легкого и 40 образцов тканей рака молочной железы, и их уровни экспрессии сравнивали с уровнями экспрессии в нормальной ткани (9 образцов для каждой ткани). Также здесь показаны характерные пары пациентов с одинаковой злокачественной опухолью, демонстрирующие сверхэкспрессию KRS и 67LR. Результаты статистического анализа корреляции уровней KRS и 67LR представлены в таблице 1.
На фиг.23 показано, что уровень 67LR в мембране зависит от экспрессии KRS. Клетки 293, трансфицированные указанными плазмидами, разделяли на цитоплазматическую и мембранную фракции, и в каждой фракции вестерн-блоттингом с соответствующими антителами определяли уровни 67LR, 37LRP и KRS.
На фиг.24-27 показано влияние внутриклеточной и внеклеточной KRS на клеточную миграцию, синтез белка и клеточный цикл. На фиг.24 миграцию клеток A549, инкубированных в отсутствие ламинина, определяли, измеряя мигрирующие клетки в камере Transwell. На фиг.25 для того, чтобы увидеть хемотаксическую активность KRS, в нижнюю камеру помещали среду без сыворотки, содержащую указанную концентрацию KRS, и клетки A549 инкубировали в верхней камере камеры Transwell. Через 6 часов инкубации подсчитывали количество мигрировавших клеток. На фиг.26 уровень KRS в клетках A549 при введении миРНК и экзогенной KRS снижался и повышался (нижние панели фиг.26 и 27). Трансфицированные клетки инкубировали в течение 48 и 24 часов, соответственно, и содержали без питательных веществ в среде без метионина в течение 1 часа и в течение 2 часов вводили радиоактивно меченый метионин. После отмывки клетки инкубировали в течение 4 часов и лизировали в лизирующем растворе 0,5% Triton X-100, и включившуюся радиоактивность определяли посредством подсчета импульсов в жидкой фазе. На фиг.27 клетки A549, трансфицированные, как указано, фиксировали и окрашивали йодистым пропидием и посредством проточной цитометрии определяли их клеточный цикл.
На фиг.28-30 показано влияние супрессии KRS на метастазирование злокачественной опухоли. На фиг.28 влияние миРНК KRS и миРНК DRS на экспрессию их соответствующих белков-мишеней определяли вестерн-блоттингом. В качестве контроля загрузки использовали тубулин. На фиг.29 трансфицированные миРНК клетки (1×106) инъецировали, как описано в способах, и влияние супрессии KRS и DRS на первичный рост опухоли определяли, измеряя массы и объемы опухолей через 21 сутки после инокуляции. Каждая группа состояла из 5 мышей. На фиг.30 легкие, выделенные выше, фиксировали в 10% формалине. Показаны количество и размер узлов метастазирующих опухолей.
На фиг.31-33 показано влияние сверхэкспрессии KRS на метастазирование злокачественной опухоли. На фиг.31 в клеточных линиях KRS-1 и -2 вестерн-блоттингом определяли сверхэкспрессию. На фиг.32 также сравнивали влияние сверхэкспрессии KRS на первичный рост опухоли, как указано выше. На фиг.33, влияние сверхэкспрессии KRS на метастазирование злокачественной опухоли определяли через 30 суток после инокуляции. Каждая группа состояла из 4 мышей.
Описание фигур
Фиг.1 представляет собой результат, подтверждающий взаимодействие между KRS человека и 37LRP/p40 с применением анализа в дрожжевой двухгибридной системе.
Фиг.2 представляет собой результат, подтверждающий взаимодействие между KRS человека и 37LRP с применением анализа осаждения.
Фиг.3 представляет собой результат, подтверждающий наличие области взаимодействия между KRS человека и 37LRP.
Фиг.4 представляет собой результат анализа иммуноблоттингом с подтверждением связывания KRS с 67LR и 37LRP в клетках A549, трансфицированных Myc-KRS, с применением антител против Myc и против рецептора ламинина.
Фиг.5 представляет собой результат анализа вестерн-блоттингом с подтверждением связывания KRS с 67LR и 37LRP в лизатах трансфицированных Myc-KRS клеток A549.
Фиг.6 представляет собой результат иммунопреципитации с подтверждением связывания 67LR и KRS в зависимости от обработки ламинином.
Фиг.7 представляет собой результат вестерн-блоттинга с подтверждением уровня 67LR, 37LRP и KRS в зависимости от обработки ламинином.
Фиг.8 представляет собой результат иммунофлуоресцентного окрашивания с анализом уровня экспрессии 67LR и KRS в клетках A549 в зависимости от обработки ламинином.
Фиг.9 представляет собой результат, подтверждающий влияние ингибиторов киназ на уровень экспрессии 67LR и KRS в мембране и цитоплазме.
Фиг.10 представляет собой результат иммуноблоттинга с определением уровня фосфорилирования в экспрессирующих KRS клетках A549, когда ингибитор ламинина и киназы до фосфорилирования обрабатывали с использованием антител против p-Thr, -Ser и -Tyr.
Фиг.11 представляет собой результат вестерн-блоттинга с определением связывания фосфорилированной KRS с 67LR в экспрессирующих KRS клетках A549.
Фиг.12 представляет собой результат вестерн-блоттинга с подтверждением влияния ламинина на связывание KRS и EPRS.
Фиг.13 представляет собой результат вестерн-блоттинга с подтверждением уровней 67LR и KRS в клетках A549, трансфицированных контрольной миРНК или миРНК KRS.
Фиг.14 представляет собой результат проточной цитометрии с подтверждением уровня мембраносвязанного 67LR в клетках A549.
Фиг.15 представляет собой результат иммунофлуоресцентного окрашивания с подтверждением клеточного распределения 67LR в клетках A549 с EV (пустой вектор) или KRS.
Фиг.16 представляет собой результат вестерн-блоттинга с подтверждением влияния уровня KRS на уровень 67LR в мембране и цитоплазме в клетках A549 с ингибированием синтеза белка de novo.
Фиг.17 представляет собой результат эксперимента с вытеснением метки, подтверждающий важность KRS для стабильности 67LR в клетке.
Фиг.18 представляет собой результат, подтверждающий воздействие на клеточную миграцию при ингибировании экспрессии KRS и/или 67LR.
Фиг.19 представляет собой результат зимографии и вестерн-блоттинга с определением активности и уровня MMP-2 при ингибировании экспрессии KRS и/или 67LR.
На фиг.20 показано количество опухолевых узлов при ингибировании экспрессии KRS у мышей с трансплантированными клетками 4T-1.
На фиг.21 показано количество опухолевых узлов при усилении экспрессии KRS у мышей с трансплантированными клетками 4T-1.
Фиг.22 представляет собой результат иммуногистохимического окрашивания с подтверждением уровней экспрессии KRS и 67LR в тканях рака легкого и молочной железы.
Фиг.23 представляет собой результат вестерн-блоттинга с подтверждением того, что уровень 67LR в мембране зависит от экспрессии KRS.
Фиг.24 представляет собой результат измерения миграции клеток A549 в отсутствие ламинина.
Фиг.25 представляет собой результат измерения хемотаксической активности KRS при клеточной миграции.
Фиг.26 представляет собой результат, подтверждающий наличие уровня KRS и общего синтеза белка в клетках A549 при введении миРНК и экзогенной KRS.
Фиг.27 представляет собой результат, подтверждающий наличие уровня KRS и клеточный цикл в клетках A549 при введении миРНК и экзогенной KRS.
Фиг.28 представляет собой результат вестерн-блоттинга с подтверждением влияния миРНК KRS и миРНК DRS на экспрессию их белков-мишеней.
Фиг.29 представляет собой результат, подтверждающий влияние супрессии KRS и DRS на первичный рост опухоли при трансплантации опухолевых клеток.
Фиг.30 представляет собой результат, подтверждающий количество и размер метастатических опухолевых узлов при трансплантации опухолевых клеток.
Фиг.31 представляет собой результат вестерн-блоттинга с подтверждением сверхэкспрессии KRS в клеточных линиях KRS-1 и -2.
Фиг.32 представляет собой результат, подтверждающий влияние сверхэкспрессии KRS на первичный рост опухоли при трансплантации опухолевых клеток.
Фиг.33 представляет собой результат, подтверждающий количество и размер метастатических опухолевых узлов при трансплантации опухолевых клеток.
Способ по изобретению
Далее в настоящем документе настоящее изобретение подробно описано посредством примеров. Однако следует понимать, что эти примеры приведены только с целью иллюстрации и не предназначены для ограничения объема настоящего изобретения.
Экспериментальный способ
1. Клеточная культура и материалы
A549 и HEK293 приобретали в ATCC. Клеточная линия карциномы молочной железы мышей 4T-1 любезно предоставлена Dr. Seong Jin Kim (Gachun Medical School). Для культивирования клеток использовали RPMI (для клеток A549 и 4T-1) и модифицированную Дульбекко среду Игла (для других клеточных линий), содержащие 10% эмбриональную телячью сыворотку и 1% антибиотики. pcDNA3.1, кодирующую 37LRP, была любезно предоставлена Dr. Hirofumi Tachibana (Kyushu University). Меченые Myc KRS и DRS человека клонировали по участку EcoRI/XhoI pcDNA3. кДНК KRS мыши получали посредством ОТ-ПЦР и клонировали по участку HindIII/XhoI pcDNA3.1. миРНК, направленные против KRS и DRS мыши и человека, приобретали в Invitrogen. Последовательности миРНК могут быть предоставлены после запроса. В качестве реагентов для трансфекции использовали репортерный ген (GTS) и липофектамин 2000 (Invitrogen). LY294002, U73122 и стауроспорин приобретали в Calbiochem, а циклогексимид и ламинин (саркома Энгельбрата-Хольма-Сварма мыши) в Sigma.
2. Иммунопреципитация и блоттинг авторов настоящего изобретения.
Клетки лизировали буфером с 20 мМ Tris-HCl (pH 7,4), содержащим 150 мМ NaCl, 0,5% Triton X-100, 0,1% SDS и ингибитор протеазы. Белковые экстракты инкубировали в агарозе с нормальным IgG и белом G в течение 2 часов, а затем центрифугировали для удаления неспецифических связывающих IgG белков. Затем авторы настоящего изобретения смешивали супернатанты с очищенным антителом против 67LR (F-18, Santacruz), инкубировали в течение 2 часов при 4°C при перемешивании, и добавляли агарозу с белком A. После трехкратной отмывки охлажденным на льду лизирующим буфером осадок растворяли в буфере для образцов с SDS и разделяли посредством SDS-PAGE. Для определения связывания KRS и LR в различных клеточных фракциях авторы настоящего изобретения трансфицировали pcDNA3.1-Myc-KRS и разделяли фракцию плазматической мембраны и цитоплазматическую фракцию с применением набора ProteoExtract (Calbiochem) по инструкциям производителя, а коиммунопреципитацию проводили, как указано выше. Для анализа уровней белков белки, экстрагированные из клеток, разделяли посредством 10% SDS-PAGE. Если не указано иначе, антитело против LR (Abeam, ab2508) использовали для одновременного иммуноблоттинга 37LRP и 67LR. Антитела для hsp90 и Pan-кадгерина приобретали в Santacruz.
3. Проточная цитометрия
Для изучения клеточного цикла культивируемые клетки трансфицировали или обрабатывали указанным вектором или химическими веществами, фиксировали 70% этанолом в течение 1 часа при 4°C и дважды отмывали ледяным PBS. Затем клетки окрашивали йодистым пропидием (50 мкг/мл), цитратом натрия 0,1%, NP40 0,3% и РНКазой A (50 мкг/мл) в течение 40 мин и подвергали проточной цитометрии (FACS Calibur, Beckton-Dickinson). Для каждого образца анализировали 20000 клеток с использованием программного обеспечения Cell Quest Pro. Для анализа количества 67 кДа LR на клеточной поверхности 1×106 клеток инкубировали с IgG или антителом против LR (MLuC5, 1 мкг), распознающим внеклеточный домен 67LR, а затем со вторичным антителом с FITC. После отмывки PBS образцы сканировали посредством FACS.
4. Иммунофлуоресцентное и иммуногистохимическое окрашивание
Клетки A549 фиксировали на 9 мм покровном стекле 70% метиловым спиртом и недолго отмывали холодным фосфатно-солевым буфером (PBS). После инкубации с блокирующим буфером, содержащим 1% CAS, 3% BSA и 0,5% Triton X-100 в течение 30 мин, клетки инкубировали с антителом против KRS (Abcam) и MLuC-5 (Santacruz) в течение 1 часа. Затем в течение 30 минут при комнатной температуре добавляли Alexa 488 и 568 (Invitrogen). После отмывки холодным PBS в течение 30 мин образцы обследовали посредством лазерной сканирующей микроскопии. Стеклянные чипы тканей рака молочной железы и легких приобретали в Super-Biochip (Korea) и подвергали иммуногистохимическому окрашиванию соответствующими им антителами для определения уровня экспрессии 67LR и KRS, как описано (Park, S. G. et al., Human lysyl-tRNA synthetase is secreted to trigger pro-inflammatory response, Proc. Natl. Acad. Sci. USA 102, 6356-6361 (2005)). Для оценки корреляции экспрессии 67LR и KRS проводили статистические анализы с использованием критерия Пирсона χ2 и t-критерия Стьюдента. Значимыми считали значения P<0,05. Все статистические анализы проводили с использованием программного обеспечения SPSS v11.5 (SPSS, Chicago, Ill).
5. Эксперимент с вытеснением метки
Клетки 293 трансфицировали миРНК KRS или контрольной миРНК (Invitrogen) с применением липофектамина 2000. Затем клетки инкубировали в среде без метионина в течение 1 часа и добавляли [35S]-метионин (50 Ки/мл) и инкубировали в течение 1 часа. После отмывки радиоактивного метионина свежей средой, 67LR иммунопреципитировали специфическим антителом (Santacruz), разделяли 12% SDS-PAGE и подвергали радиоавтографии с применением BAS (FLA-3000, FujiFilm). Количество 67LR количественно определяли посредством программы Multi-gauge (V3.0, FujiFilm).
6. Анализ в двухгибридной дрожжевой системе
кДНК, кодирующие различные фрагменты KRS человека, получали посредством ПЦР с соответствующими праймерами. Продукт ПЦР KRS расщепляли EcoRI и XhoI и лигировали в соответствующие участки pEG202 (для конструирования слитых с LexA белков) и pJG4-5 (для конструирования слитых с B42 белков). кДНК, кодирующие фрагменты 37LRP, были любезно предоставлены Dr. Barbara J. Ballermann (University of Alberta), и их субклонировали по участкам EcoRI и XhoI pJG4-5. Взаимодействие между двумя видами слитых белов анализировали по образованию синих колоний в содержащей X-gal дрожжевой среде.
7. Анализ связывания in vitro
Авторы настоящего изобретения экспрессировали GST-KRS или GST в штамме Escherichia coli Rosetta (DE3), смешивали белковые экстракты с глутатион-сефарозой в буфере PBS, содержащем 1% Triton X-100 и 0,5% N-лаурилсаркозин при 4°C в течение 2 часов. Авторы настоящего изобретения синтезировали 37LRP человека посредством трансляции in vitro в присутствии [35S]-метионина с использованием pcDNA3-37LRP в качестве матрицы с использованием системы TNT Quick coupled Transcription/Translation (Promega). Синтезированный 37LRP добавляли к указанной выше смеси с белком GST, инкубировали при 4°C в течение 4 часов с перемешиванием в буфере PBS, содержащем 1% Triton X-100, 0,5% N-лаурилсаркозин, 1 мМ DTT, 2 мМ ЭДТА и 300 М фенилметилсульфонилфторид, и шесть раз отмывали тем же буфером, содержащим 0,5% Triton X-100. Затем авторы настоящего изобретения элюировали белки, связанные с сефарозными гранулами буфером для образцов с SDS, разделяли SDS-PAGE и подвергали радиоавтографии.
8. Анализ клеточной миграции
Клеточную миграцию определяли с применением 24-луночных камер Transwell с поликарбонатными мембранами (размер пор 8,0 мкм, Costar), как описано ранее (Park, S. G. et al., Human lysyl-tRNA synthetase is secreted to trigger pro-inflammatory response, Proc. Natl. Acad. Sci. USA 102, 6356-6361 (2005)). Клетки A549 суспендировали в среде RPMI без сыворотки и добавляли в верхнюю камеру при 1×105 клеток на лунку. В нижнюю лунку помещали каждый из очищенного KRS человека при указанных концентрациях, ламинина (10 мкг/мл) или желатина (10 мкг/мл), и клеткам позволяли мигрировать в течение 6 часов при 37°C в CO2-инкубаторе. Клетки фиксировали 70% метиловым спиртом в PBS в течение 30 мин и трехкратно отмывали PBS. Клетки окрашивали гематоксилином (Sigma) в течение 10 мин и отмывали дистиллированной водой. Немигрировавшие клетки удаляли с верхней поверхности мембраны ватной палочкой. Мембраны вырезали из камеры и закрепляли с применением Gel Mount (Biomeda, Foster City, CA). Мигрировавшие клетки (клетки, прикрепленные к нижней поверхности мембраны) подсчитывали в четырех случайно выбранных областях в полях зрения под большим увеличением (×20).
9. Зимография
Клетки A549, трансфицированные плазмидами, кодирующими указанные миРНК и рекомбинантную KRS (или DRS), инкубировали в течение 48 и 24 часов соответственно, и высевали (1×105 клетки/лунку) в RPMI, содержащую 10% FBC. После выдерживания клеток без поступления питательных веществ в среде RPMI без сыворотки в течение 2 часов добавляли 10 мкг/мл ламинина и инкубировали в течение 24 часов. 20 л среды для культивирования смешивали с 5× буфером FOD (0,125 M Tris-HCl, pH 6,8, содержащий 4% SDS, 20% глицерин и 0,01% бромфеноловый синий) и подвергали 10% SDS-PAGE, содержащему 1 мг/мл желатина. Гель дважды промывали 2,5% Triton X-100 каждый раз в течение 20 мин, затем дважды дистиллированной водой каждый раз в течение 20 мин и инкубировали в реакционном буфере (50 мМ Tris-HCl, pH 7,5, содержащем 10 мМ CaCl2, 150 мМ NaCl, 1 М ZnCl2, 1% Triton X-100, 0,002% азид натрия) в течение 24 час при 37°C. Гель промывали дистиллированной водой и окрашивали кумасси синим R250 и удаляли окраску 35% метанолом.
10. Эксперимент по метастазированию злокачественной опухоли in vivo
Клетки карциномы молочной железы мышей 4T-1 трансфицировали миРНК KRS, миРНК DRS или контрольной миРНК и инкубировали в течение 24 часов. Клетки (1×106) подкожно инокулировали в спину самок мышей Balb/c в возрасте 6 недель. Влияние миРНК на экспрессию их мишеней тестировали у оставшихся клеток через 48 часов после трансфекции, а также в первичных опухолях вестерн-блоттингом с соответствующими им антителами через период от 3 до 10 суток после инокуляции с интервалами 2 суток. Рост опухоли контролировали, три раза в неделю измеряя размер опухоли. Также в то же время измеряли общую массу тела. Мышей умерщвляли через 21 сутки после инокуляции, и у животного вырезали первичные опухоли и легкие. Легкие фиксировали в 10% формалине в течение двадцати четырех часов. Подсчитывали количество и размер метастатических опухолевых узлов в легких, а опухолевые узлы более 1 мм в диаметре записывали раздельно. Также первичные опухоли взвешивали. Для анализа влияния сверхэкспрессии KRS на метастазирование злокачественной опухоли в клетки 4T-1 трансфицировали вектор KRS мыши или пустой вектор, и стабильных трансфектантов отбирали посредством инкубации в присутствии G418 в течение 3 недель. Затем авторы настоящего изобретения отделяли несколько одиночных колоний и вестерн-блоттингом сравнивали уровень экспрессии KRS. Выбрали две различных колонии (KRS-1 и -2), экспрессировавших KRS с более высоким уровнем, чем контрольные клетки, и их использовали для инокуляции. Все процедуры проводили, как указано выше, за исключением того, что мышей умерщвляли через 30 суток после инокуляции.
Экспериментальные результаты и обсуждение
Специфическое взаимодействие между полноразмерными KRS и 37LRP подтверждали посредством анализа в дрожжевой двухгибридной системе. LexA-KRS позволял получать синие колонии при спаривании с B42-37LRP, а также AIMP2, известным партнером KRS (Kim, J.Y. et al. p38 is essential for the assembly and stability of macromolecular tRNA synthetase complex: Implications for its physiological significance, Proc. Natl. Acad. Sci. USA 99, 7912-7916 (2002)), но не с AIMP1 (фиг.1). Для анализа связывания in vitro меченный [35S]-метионином 37LRP смешивали или с GST-KRS, или с GST, осаждали глутатион-сефарозой и подвергали радиоавтографии. 37LRP совместно осаждался с GST-KRS, но не с GST (фиг.2). Делеционное картирование посредством анализа в дрожжевой двухгибридной системе позволило определить, что в их ассоциацию вовлечены N-концевой участок KRS человека и C-концевой внеклеточный домен LR (фиг.3).
Так как цитоплазматический 37LRP преобразуется в мембраносвязанный 67LR, авторы настоящего изобретения проверяли, связывается ли KRS различным образом с 37LPR и 67LR. В клетки карциномы легкого A549 вводили Myc-KRS и иммунопреципитировали антителом против Myc. Блоттинг авторов настоящего изобретения всего клеточного лизата продемонстрировал, что 67LR существует на меньшем уровне, чем 37LRP (фиг.4 справа). Однако Myc-KRS преимущественно связывался с 67LR, а не с 37LRP (фиг.4 слева). Затем авторы настоящего изобретения разделяли клетки A549 на цитоплазматическую фракцию и фракцию плазматической мембраны и определяли взаимодействие Myc-KRS с 67LR и 37LRP. 37LRP и 67LR в основном детектировали в цитоплазме и плазматической мембране соответственно (фиг.5, справа), тогда как KRS присутствовала в обеих фракциях, хотя основную долю наблюдали в цитоплазме. Когда обе фракции подвергали иммунопреципитации антителом к Myc, в основном совместно с KRS осаждался мембраносвязанный 67LR, хотя также осаждалось небольшое количество 37LRP в цитоплазме (фиг.5 слева), что указывает на предпочтительное взаимодействие между находящимся в мембране 67LR и KRS.
Затем авторы настоящего изобретения исследовали, изменяется ли клеточное распределение KRS при обработке клеток A549 ламинином посредством фракционирования клеток и иммунофлуоресцентного окрашивания. После обработки ламинином уровень KRS и 67LR в мембране постепенно увеличивался с небольшими изменениями цитоплазматического уровня KRS и 37LRP или их экспрессии (фиг.7 и данные не показаны). Иммунофлуоресцентное окрашивание также продемонстрировало сдвиг 67LR и KRS в направлении мембраны при обработке ламинином (фиг.8, красный и зеленый соответственно). Затем авторы настоящего изобретения исследовали, включает ли транслокация KRS в мембрану посттрансляционную модификацию. Известно, что ламинин активирует несколько различных киназ, таких как фосфоинозитол-3-OH-киназа (PI3K) (Shaw, L. M., Rabinovitz, I., Wang, H. H., Toker, A. & Mericurio. A.M. Activation of phosphoinositide 3-OH kinase by the alpha6beta4 integrin promotes carcinoma invasion. Cell 91, 949-960 (1997)), протеинкиназа C (PKC) (Li, Y. Q. et al. Protein kinase C mediates the signal for interferon-gamma mRNA expression in cytotoxic T cells after their adhesion to laminin. Immunology 93, 455-461 (1998)) и фосфолипаза C-гамма (PLC-гамма) (Vossmeyer, D., Hofmann, W., Loster, K., Reutter, W. & Danker, K. Phospholipase C-gamma binds alphalbetal integrin and modulates alphalbetal integrin-specific adhesion. J. Biol. Chem. 277, 4636-4643 (2002); Kanner, S. B., Grosmaire, L. S., Ledbetter, J. A. & Damle, N. K. Beta 2-integrin LFA-1 signaling through phospholipase C-gamma 1 activation. Proc. Natl. Acad. Sci. USA 90, 7099-7103 (1993)). Для того чтобы увидеть, вовлечена ли любая из этих киназ в зависимую от ламинина транслокацию KRS в мембрану, авторы настоящего изобретения блокировали каждую из этих киназ соответствующими им ингибиторами и проверяли, как эта обработка будет влиять на транслокацию KRS в мембрану. Зависимое от ламинина увеличение KRS и 67LR в мембранной фракции блокировалось в присутствии LY294002, ингибитора PI3K, тогда как клетки, обработанные U73122 или стауроспорином, все еще демонстрировали зависимую от ламинина индукцию 67LRS, как у контрольных клеток (фиг.9 верхняя панель и данные не показаны). Ни одна из этих киназ не влияла на уровень KRS в цитоплазме (фиг.9 нижняя панель). Эти результаты означают, что PI3K должна быть вовлечена в индуцированное ламинином фосфорилирование KRS. Фактически количество фосфорилированной по треонину и серину, но не по тирозину KRS при обработке ламинином увеличивалось, но блокировалось в присутствии LY294002, тогда как стауроспорин не оказывал такого эффекта (фиг.10). Затем авторы настоящего изобретения проверяли, могло ли индуцированное ламинином фосфорилирование KRS быть необходимым для ее взаимодействия с 67LR. Обработка LY294002 супрессировала индуцированную ламинином ассоциацию KRS с 67LR (фиг.11). Так как цитоплазматическая KRS прикреплена к комплексу с несколькими ARS, авторы настоящего изобретения также проверяли, может ли зависимое от ламинина фосфорилирование KRS влиять на ее ассоциацию с комплексом с несколькими ARS посредством коиммунопреципитации KRS с глутамилпролил-тРНК-синтетазой (EPRS), другим ферментным компонентом комплекса. В отсутствие соединения LY обработка ламинином снижала ассоциацию KRS с EPRS с одновременным увеличением KRS в иммуноистощенной растворимой фракции (фиг.12 левые полосы в верхней и нижней панелях). В отличие от этого связывание KRS с EPRS при предварительной обработке соединением LY294002 при обработке ламинином не затрагивалось (фиг.12 правые полосы на верхней и нижней панелях), что позволяет предположить, что фосфорилирование KRS необходимо для зависимой от ламинина диссоциации KRS из комплекса.
Затем авторы настоящего изобретения проверяли, влияет ли KRS на уровень 67LR в мембране клеток A549. Уровень 67LR при обработке ламинином возрастал, но влияние ламинина исчезало, когда KRS супрессировали специфичной к ней миРНК (фиг.13 слева), что указывает на важность KRS при зависимом от ламинина увеличении 67LR. Авторы настоящего изобретения также подвергали мониторингу мембраносвязанный 67LR посредством проточной цитометрии. Уровень 67LR в мембране возрастал и снижался, когда клетки трансфицировали KRS и миРНК KRS соответственно (фиг.14). Клеточное распределение рецептора ламинина сравнивали у клеток A549, трансфицированных EV или KRS посредством иммунофлуоресцентного окрашивания. Рецептор ламинина по сравнению с окрашиванием в контрольных клетках в областях плазматической мембраны в клетках со сверхэкспрессией KRS окрашивался более плотно (фиг.15). Положительную корреляцию уровней KRS и 67LR дополнительно подтверждали, измеряя 67LR в мембране и цитоплазме в соответствии с вариацией уровня KRS (фиг.23).
Затем авторы настоящего изобретения исследовали, как KRS увеличивает уровень 67LR в мембране. KRS может стимулировать синтез 67LR посредством транскрипции или преобразования из 37LRP. Однако трансфекция KRS не увеличивала транскрипцию LR (данные не показаны), за исключением ее потенциальной роли в регуляции транскрипции LR. Кроме того, так как KRS продемонстрировала плохое связывание с 37LRP в цитоплазме (фиг.4 и 5), маловероятно, что она стимулирует процесс преобразования 37LRP в 67LR. Авторы настоящего изобретения также проверяли, может ли KRS опосредовать ацилирование жирных кислот 37LRP, т.к. известно, что данная модификация необходима для преобразования 37LRP в 67LR (Landowski, T. H., Dratz, E.,A. & Starkey, J. R. Studies of the structure of the metastasis-associated 67 kDa laminin binding protein: fatty acid acylation and evidence supporting dimerization of the 32 kDa gene product to form the mature protein. Biochemistry 34, 11276-11287 (1995); Buto, S. et al., Formation of the 67-kDa laminin receptor by acylation of the precursor. J. Cell. Biochem. 69, 244-251 (1998)). В анализе авторов изобретения KRS не влиял на ацилирование каких-либо жирных кислот 37LRP (данные не показаны). Так как KRS может увеличивать клеточную стабильность мембраносвязанного 67LR, авторы настоящего изобретения проверяли, может ли KRS препятствовать эндоцитозу мембраносвязанного 67LR. Для того чтобы увидеть эту возможность, авторы настоящего изобретения останавливали синтез белка de novo циклогексимидом и проверяли, будет ли KRS влиять на уровень 67LR в мембране и цитоплазме. Когда экспрессию KRS супрессировали ее специфической миРНК, уровень 67LR в мембране снижался с одновременным увеличением 67LR в цитоплазматической фракции (фиг.16 слева). Наоборот, сверхэкспрессия KRS увеличивала уровень 67LR в мембране, как указано выше (фиг.16 справа). На основе этих результатов, по-видимому, KRS продлевает нахождение 67LR в мембране, блокируя ее обратное возвращение в цитоплазму. Авторы настоящего изобретения дополнительно исследовали влияние KRS на кругооборот 67LR посредством эксперимента с вытеснением метки. В начале синтеза белка проводили мечение радиоактивным метионином, а затем блокировали его циклогексимидом. Затем проводили мониторинг исчезновения 67LR посредством радиоавтографии с временными интервалами. Количество 67LR быстро снижалось, когда KRS супрессировали ее миРНК, тогда как ее уровень в клетках с контрольной миРНК хорошо сохранялся в течение этого же временного интервала (фиг.17). Таким образом, по-видимому, KRS продлевает время полужизни 67LR посредством ее ассоциации с 67LR в плазматической мембране, таким образом, ингибируя эндоцитоз 67LR, хотя процесс разрушения 67LR нуждается в дополнительном исследовании.
Затем авторы настоящего изобретения исследовали, влияет ли уровень экспрессии KRS на зависимую от ламинина миграцию клеток A549 с использованием анализа на мембране Transwell. Миграция контрольных клеток при обработке ламинином в среднем увеличивалась приблизительно в 6 раз (фиг.24 и 18). Однако клеточная миграция, зависимая от ламинина, при супрессии KRS ее специфичной миРНК снижалась (фиг.18, контрольная миРНК и миРНК KRS). Наоборот, сверхэкспрессия KRS дополнительно увеличивала клеточную миграцию, индуцированную обработкой ламинином (фиг.18, EV и KRS). Однако влияние KRS на клеточную миграцию, когда рецептор ламинина супрессировали его миРНК, снижалось (фиг.18 миРНК LR, нижняя панель). Так как KRS также секретируется в некоторых злокачественных клетках в виде цитокина (Park, S. G. et al., Human lysyl-tRNA synthetase is secreted to trigger pro-inflammatory response, Proc. Natl. Acad. Sci. USA 102, 6356-6361 (2005)), авторы настоящего изобретения проверяли, может ли внеклеточная KRS влиять на клеточную миграцию. Когда клетки A549 обрабатывали очищенной KRS в различных концентрациях, она немного влияла на клеточную миграцию (фиг.25), исключая внеклеточное действие KRS в этом анализе. Кроме того, супрессия или сверхэкспрессия KRS в течение экспериментов не влияла на синтез клеточных белков и клеточный цикл (фиг.26 и 27), что указывает на то, что зависимая от KRS клеточная миграция не является результатом ее влияния на какой-либо из этих процессов. Так как обработка ламинином приводит к активации MMP-2 (матриксная металлопротеиназа-2) (Givant-Horwitz, V., Davidson, B. & Reich, R. Laminin-induced signaling in tumor cells; the role of the M(r) 67,000 laminin receptor. Cancer Res. 64, 3572-3579 (2004)), авторы настоящего изобретения проверяли влияние KRS на зависимую от ламинина активацию MMP-2 с использованием анализа зимографии in vitro. Активность MMP-2 под действием ламинина усиливалась, что блокировалось в присутствии миРНК KRS (фиг.19 слева), но дополнительно усиливалось при сверхэкспрессии KRS (фиг.19 справа). KRS не влияла на уровень экспрессии MMP-2 (фиг.19 снизу).
Так как KRS может индуцировать клеточную миграцию посредством 67LR, который участвует в метастазировании злокачественных опухолей, авторы настоящего изобретения проверяли, влияет ли также уровень экспрессии KRS на метастазирование злокачественной опухоли с применением клеток карциномы молочной железы мыши 4T-1, которые на высоком уровне метастазируют в легкое. Авторы настоящего изобретения супрессировали KRS или DRS (аспартил-тРНК-синтетаза), другой компонент комплекса с несколькими ARS, с их специфичными миРНК и сравнивали, как негативная регуляция KRS и DRS может влиять на метастазирование злокачественной опухоли. После подтверждения эффекта супрессии миРНК KRS и миРНК DRS вестерн-блоттингом (фиг.28), каждые из этих линий клеток и клетки с контрольной миРНК подкожно инъецировали в кожу спины мышей Balb/c. Все из трех инъецированных линий клеток развивались в опухоли, по наблюдениям авторов настоящего изобретения сходного размера и объема (фиг.29), что позволяет предполагать, что уровень KRS не влияет на рост первичных опухолей. Легкие выделяли через 21 сутки после инокуляции, и в группах сравнивали количество метастатических опухолевых узлов (более 1 мм в диаметре). Количество метастатических узлов при супрессии KRS по сравнению с количеством метастатических узлов, полученных с контрольными клетками или клетками с супрессией DRS, значимо снижалось (фиг.21 и 33). С другой стороны, авторы настоящего изобретения проверяли, будет ли сверхэкспрессия KRS усиливать метастазирование злокачественной опухоли, применяя тот же способ, как указано выше. Авторы настоящего изобретения сначала получили клеточные линии 4T-1, стабильно сверхэкспрессирующие KRS, посредством трансфекции кодирующей KRS плазмиды и скрининга с G418. Сверхэкспрессию KRS в полученных клеточных линиях подтверждали вестерн-блоттингом, и авторы настоящего изобретения отобрали две различных клеточных линии (KRS-1 и KRS-2), экспрессирующих KRS в больших количествах, по сравнению с клетками, трансфицированными пустым вектором (фиг.31). Эти клетки также давали первичные опухоли сходных массы и размера (фиг.32). Когда авторы настоящего изобретения исследовали легкие через 30 суток после инокуляции клеток, обе линии сверхэкспрессирующих KRS клеток давали большее количество узлов в сравнении с контрольными клетками (фиг.21 и 33). Все эти результаты позволяют предположить, что KRS может индуцировать метастазирование злокачественных опухолей in vivo.
Так как часто наблюдают специфичную для злокачественных опухолей сверхэкспрессию рецептора ламинина (Fontanini, G. et al., 67-Kilodalton laminin receptor expression correlates with worse prognostic indicators in non-small cell lung carcinomas. Clin. Cancer Res. 3, 227-231 (1997), Viacava, P. et al., The spectrum of 67-kD laminin receptor expression in breast carcinoma progression. J. Pathol. 182, 36-44 (1997)), авторы настоящего изобретения анализировали, ассоциирована ли сверхэкспрессия 67LR также со сверхэкспрессией KRS посредством иммуногистохимического окрашивания 67LR и KRS тканей рака легкого и молочной железы в качестве примером. Среди 39 протестированных образцов тканей рака легких сверхэкспрессию 67LR наблюдали в 21 случае (54%), в которых в 19 случаях также был увеличен уровень KRS (приблизительно 90%) (таблица 1 и фиг.22 верхняя панель). Подобным образом, сверхэкспрессию 67LR продемонстрировали в 21 случае из 40 протестированных пациентов с раком молочной железы. В этих случаях, во всех 21 случаях также показали увеличенные уровни KRS (таблица 1 и фиг.22 нижняя панель). В обоих случаях показана тесная связь экспрессии этих двух белков, хотя следует определить, действительно ли их совместная экспрессия при злокачественной опухоли связана с метастазированием.
На данном этапе это можно рассматривать, как описание таблицы 1. Таблица 1 представляет собой корреляцию экспрессии 67LR и KRS в тканях злокачественных опухолей. Для тестирования того, ассоциирован ли уровень экспрессии 67LR с уровнем экспрессии KRS, микрочипы тканей пациентов с раком легкого и молочной железы подвергали иммуногистохимическому окрашиванию их соответствующими антителами, и определяли уровни относительной экспрессии двух белков. Для иммунодетекции 67LR использовали антитело MLuC5. Уровень экспрессии определяли по интенсивности окрашивания образца и классифицировали на 4 группы (показатель 0, 1, 2 и 3). При конечной оценке образцы разделяли на нормальную (с показателем 0 или 1) и сверхэкспрессирующую группу (с показателем 2 или 3). Статистические анализы для оценки корреляции экспрессии 67LR и KRS проводили с использованием критерия Пирсона χ2 и t-критерия Стьюдента. Значимыми считали значения P<0,05. Все статистические анализы проводили с использованием программного обеспечения SPSS v11.5 (SPSS, Chicago, Ill).
Многие трансляционные факторы, включая рибосомальные компоненты, являются плейотропными (Wool, I. G. Extraribosomal functions of ribosomal proteins Trends Biochem. Sci. 21, 164-165 (1996)) и ассоциированными с различными видами образования опухолей (Lee, S. W., Kang, Y. S. & Kim, S. Multifunctional proteins in tumorigenesis: Aminoacyl-tRNA synthetases and translational components. Curr. Proteomics 3, 233-247 (2006)). В данном документе авторы настоящего изобретения продемонстрировали, что два трансляционных фактора, KRS и p40/37LRP, действуют совместно в отношении клеточной миграции и метастазирования злокачественных опухолей in vivo (фиг.18 и 22). В настоящее время авторы настоящего изобретения не знают, является ли потенциальная ассоциация этих двух белков эволюционным совпадением или имеет другое физиологическое обоснование в синтезе белка, которое необходимо понято в будущем. Среди компонентов комплекса с несколькими ARS, KRS является наиболее стабильным белком, и она необходима для стабильности других компонентов (Han, J. M. et al., Hierarchical Network between the components of the multi-tRNA synthetase complex: Implications for complex formation. J. Biol. Chem. 281, 38663-38667 (2006)), что подразумевает ее потенциал для стабилизации ассоциированных белков. В настоящем документе авторы настоящего изобретения показали, что KRS также увеличивает стабильность 67LR в клетке (фиг.17).
Ассоциация KRS с 67LR может иметь различные функциональные последствия. В физиологических условиях часть цитоплазматической KRS фосфорилирована и мобилизуется на плазматическую мембрану под действием различных постстимуляторных сигналов или сигналов на выживание для связывания с 67LR, который опосредует сигнал ламинина. В злокачественных клетках уровень KRS в мембране может аномально увеличиваться или вследствие его сверхэкспрессии или вследствие его конститутивной транслокации в мембрану, являющейся результатом гиперактивированных расположенных выше по каскаду киназ, таких как PI3K. Вероятно, этот избыток KRS направляется в плазматическую мембрану, т.е. или образует комплекс с 67LR, или секретируется. Кроме того, стоит отметить, что разрегулируемая активация PI3K часто ассоциирована с ростом опухоли и метастазированием (Wymann, M. P. & Marone, R. Phosphoinositide 3-kinase in disease: timing, location, and scaffolding. Curr. Opin. Cell Biol. 17, 141-149 (2005)), и ламинин способствует инвазии злокачественной опухоли посредством PI3K (Baba, Y. et al., Laminin-332 promotes the invasion of oesophageal squamous cell carcinoma via PI3K activation. Br. J. Cancer 98, 974-980 (2008)). Конститутивная активация PI3K может приводить к фосфорилированию KRS, которая может мобилизоваться на мембрану. Любое или оба из этих состояний могут вносить вклад в увеличение уровня 67LR в плазматической мембране, таким образом, усиливая сигнал ламинина на метастазирование злокачественной опухоли. Ведутся большие исследования, направленные на контроль метастазирования злокачественной опухоли. В связи с этим активность KRS при метастазировании злокачественной опухоли посредством 67LR может предоставлять ранее неисследованную область для диагностики и терапии злокачественных опухолей.
Промышленная применимость
Как можно видеть из указанного выше, авторы настоящего изобретения выявили, что KRS по изобретению взаимодействует с 67LR посредством транслокации KRS в плазматическую мембрану, и таким образом усиливает миграцию клеток опухоли (или злокачественной опухоли), таким образом, влияя на метастазирование злокачественной опухоли. Кроме того, авторы изобретения посредством экспериментов in vivo с использованием мышей также выявили, что сверхэкспрессия KRS или ингибирование экспрессии KRS может модулировать метастазирование клеток опухоли (или злокачественной опухоли). Таким образом, с использованием KRS по изобретению можно контролировать метастазирование злокачественных опухолей и миграцию злокачественных клеток, кроме того, можно контролировать клеточный метаболизм, связанный с рецептором ламинина (67LR) плазматической мембраны. Связь между KRS и рецептором ламинина, выявленная в настоящем изобретении, может оказаться очень полезной при лечении, профилактике и/или диагностике различных связанных с ней заболеваний.




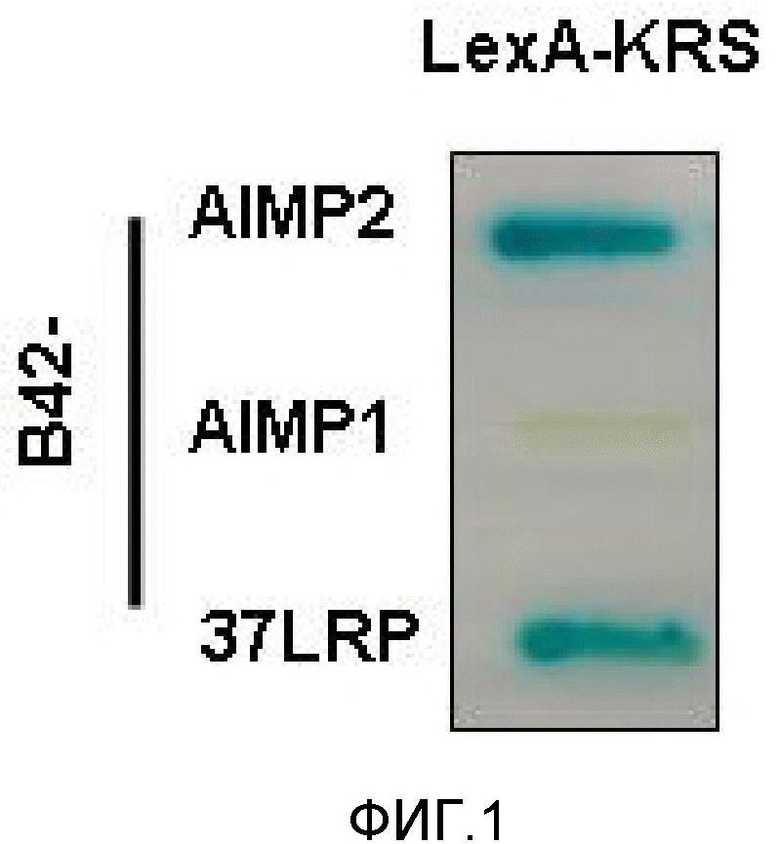
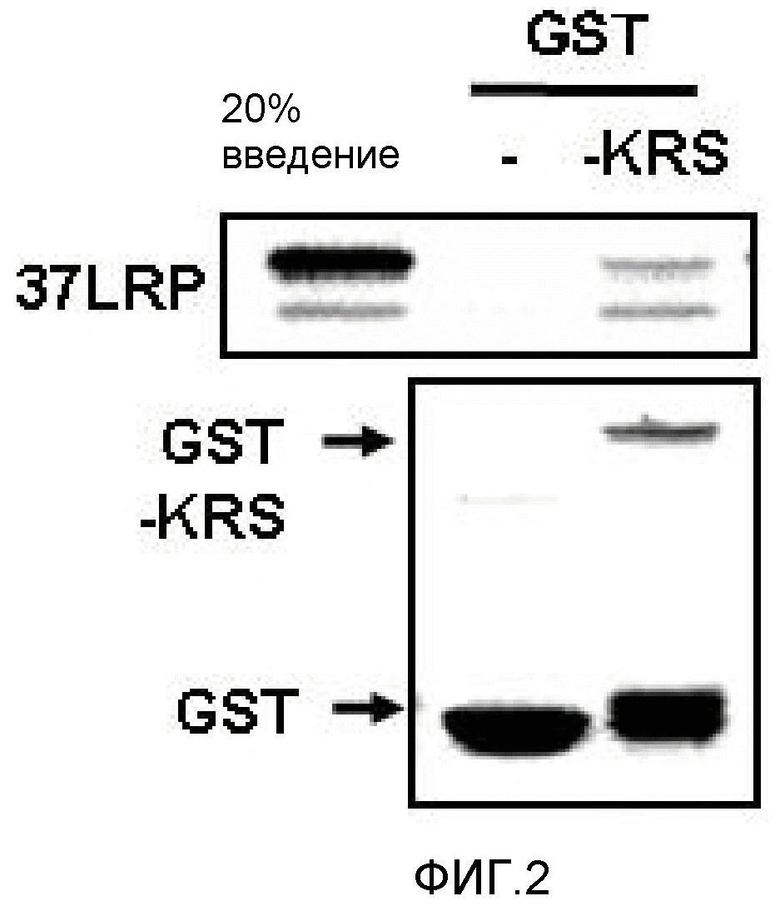
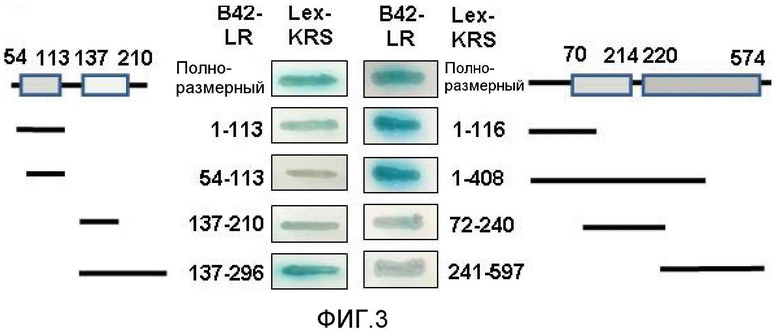
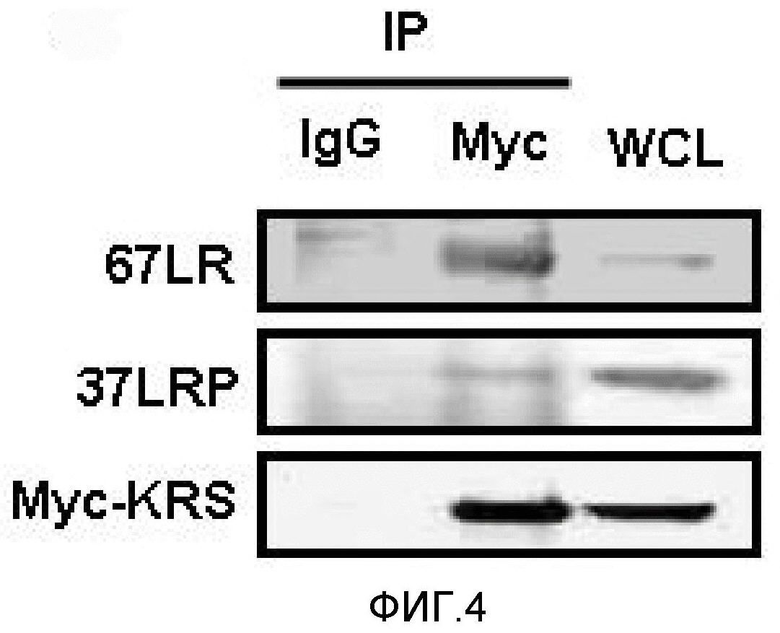
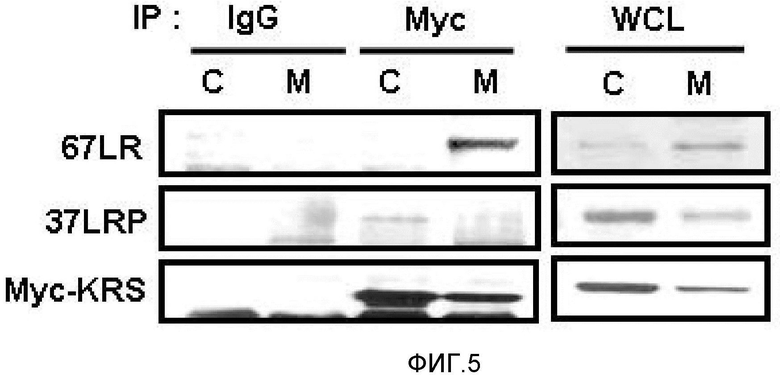
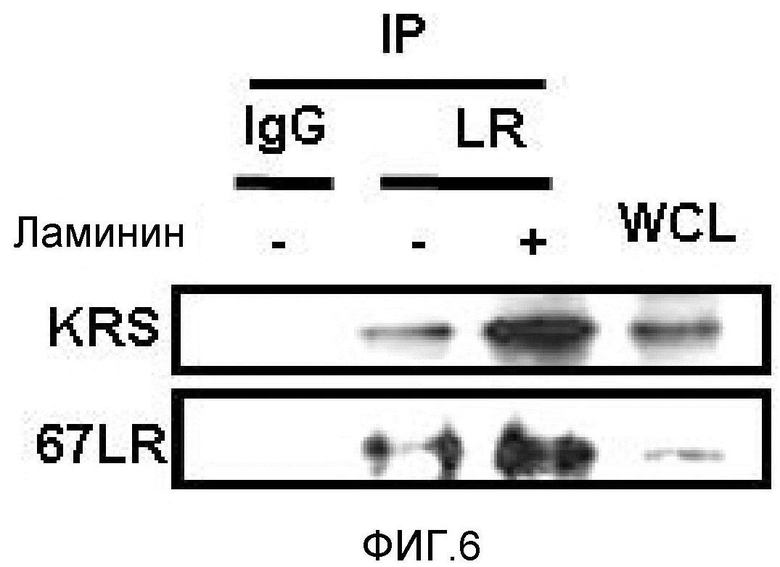
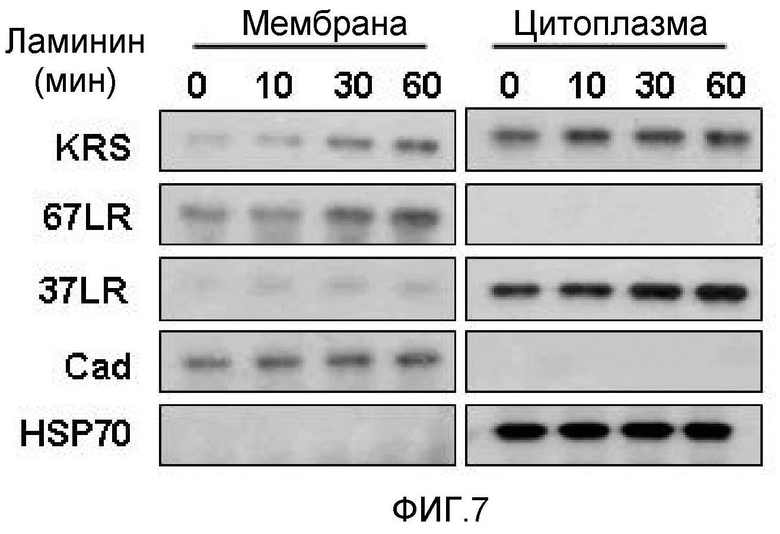
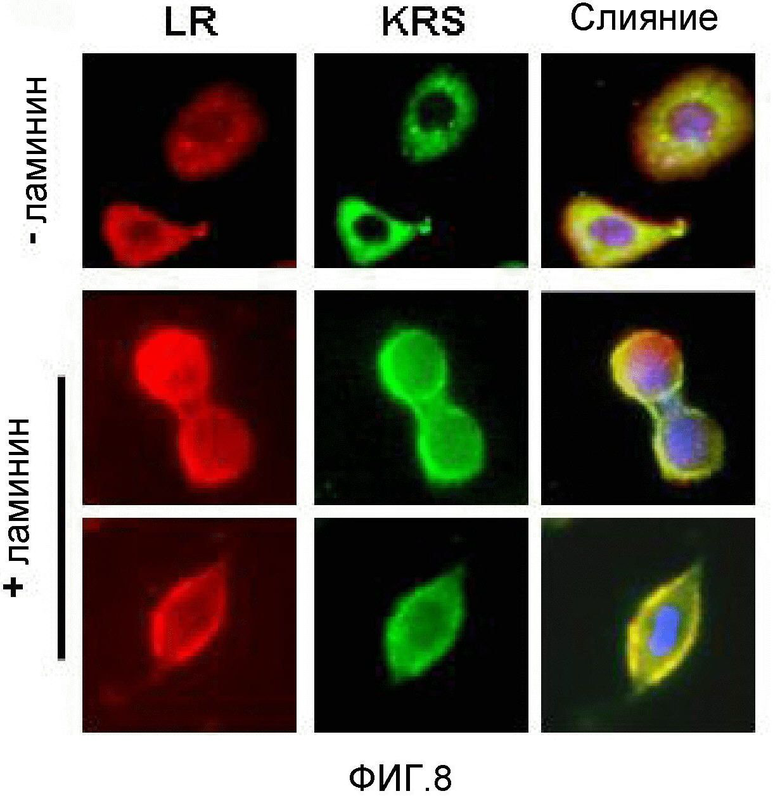
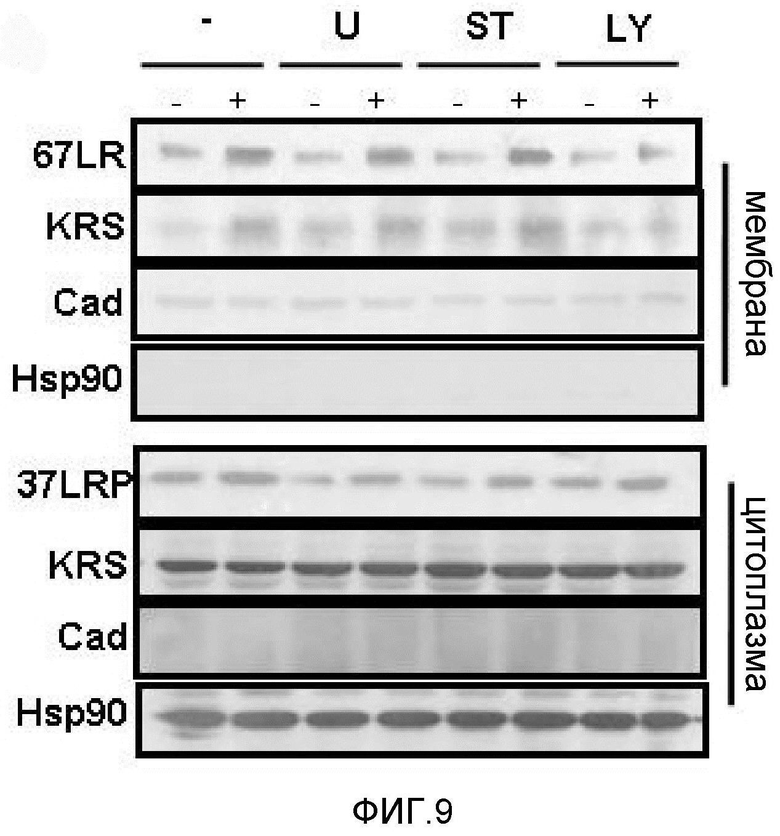
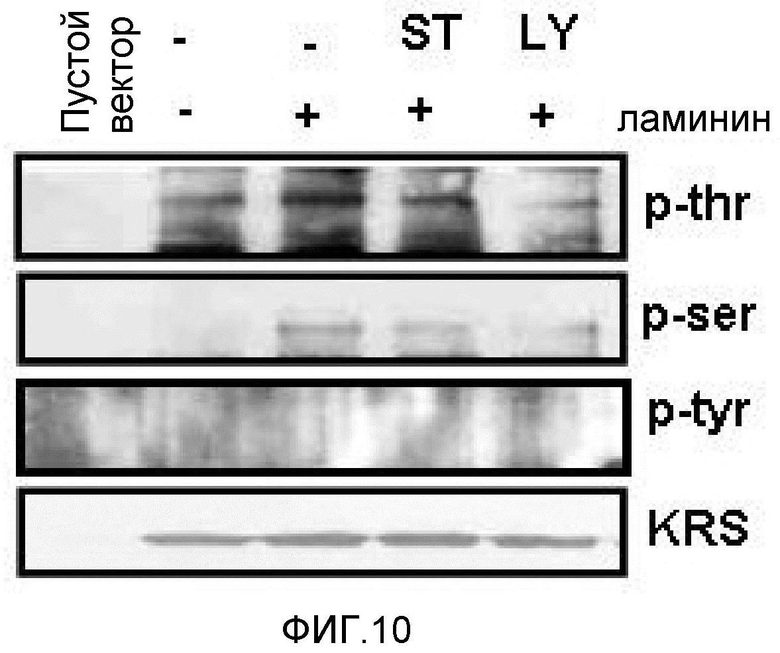
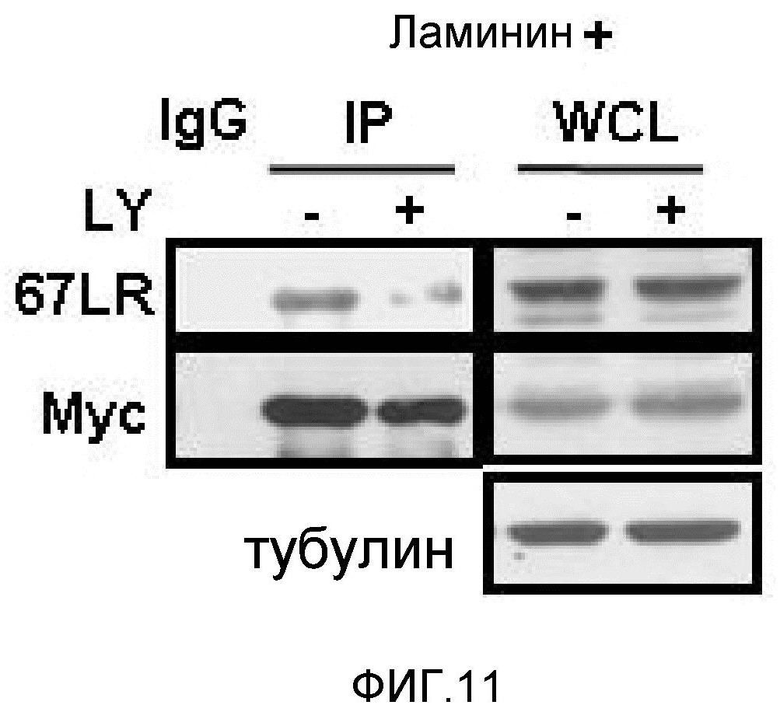
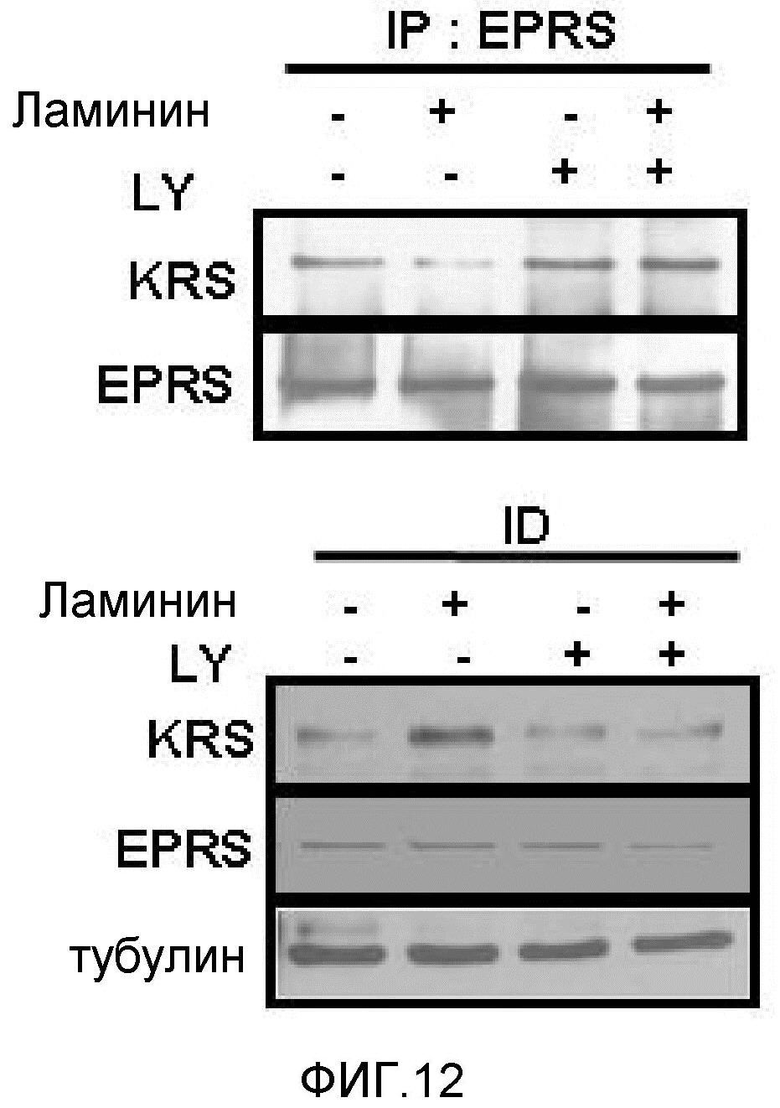
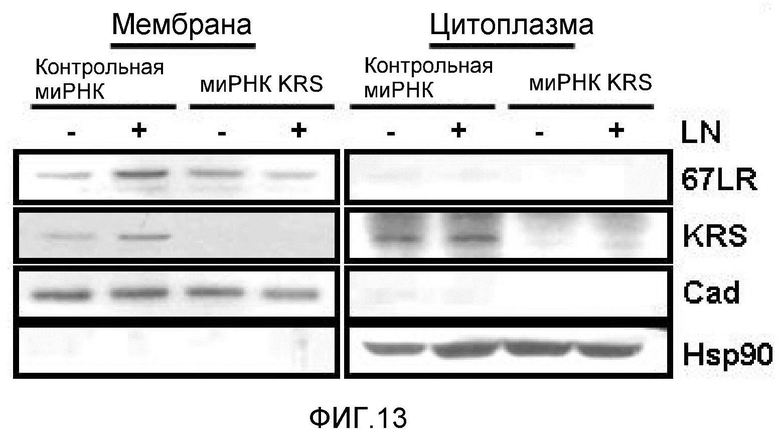
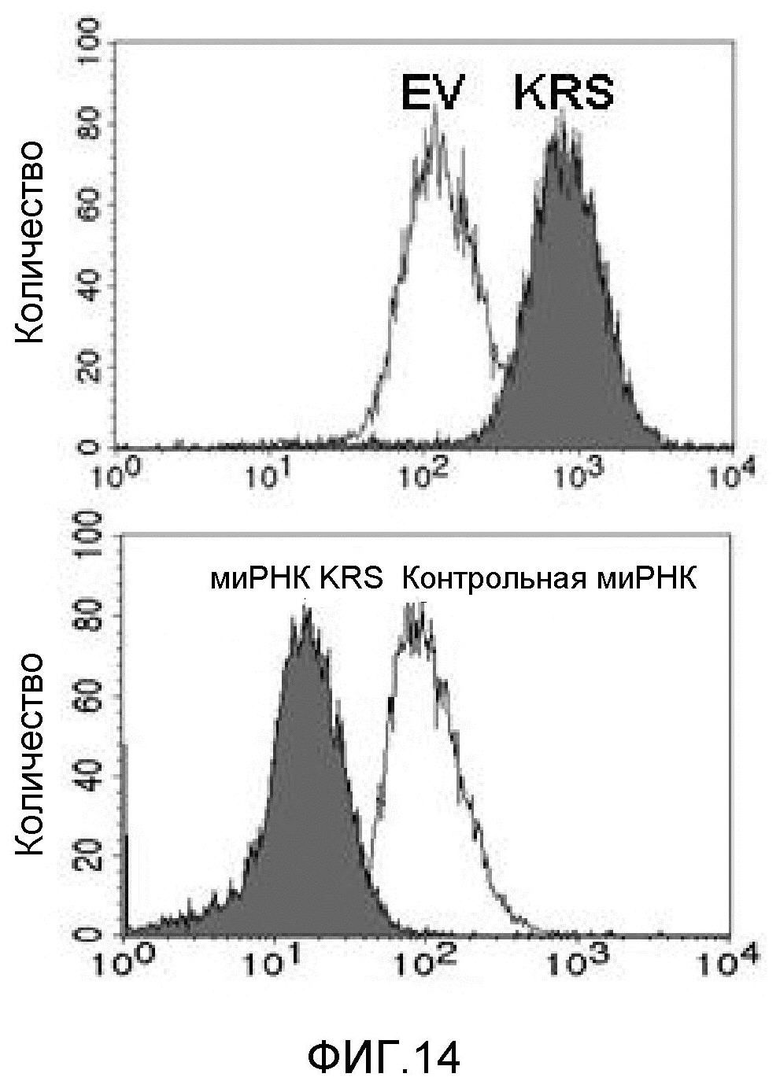
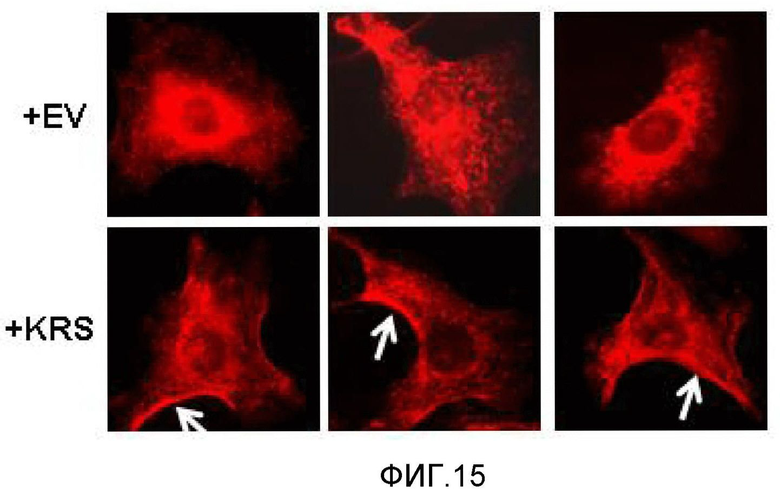
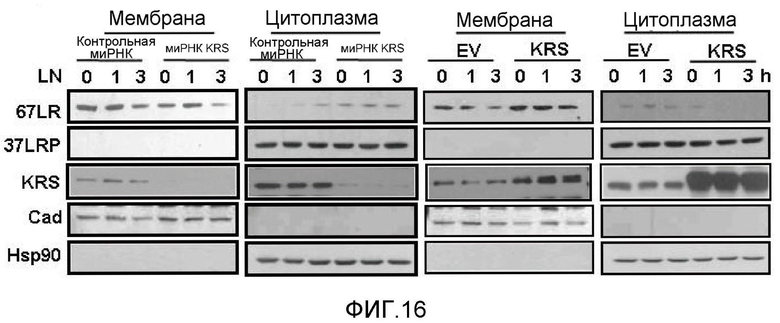
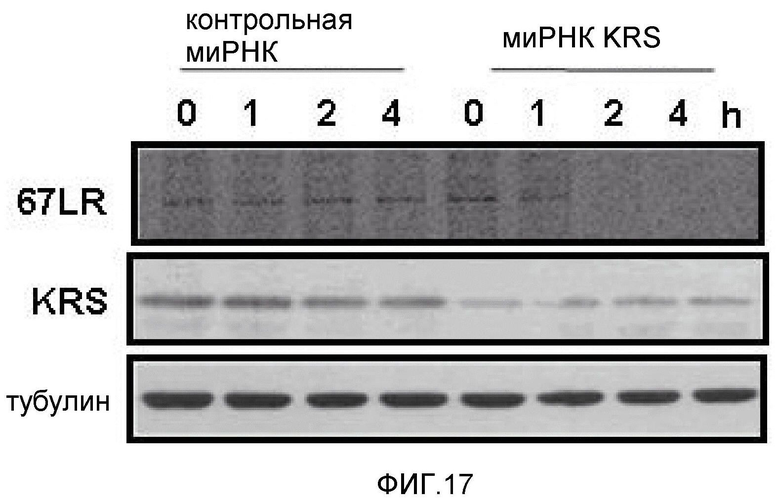
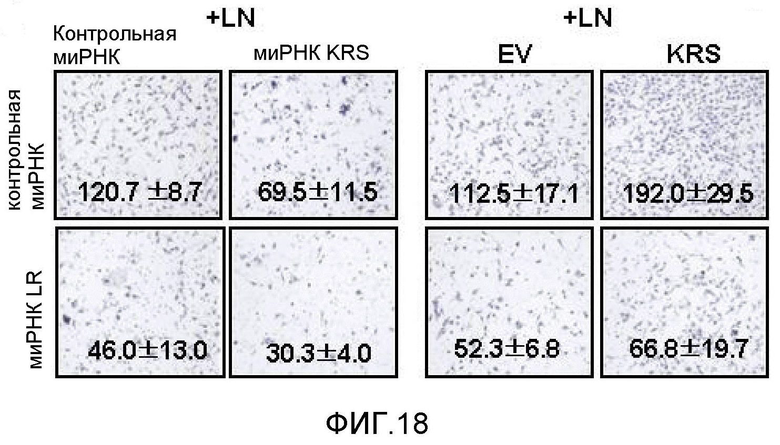
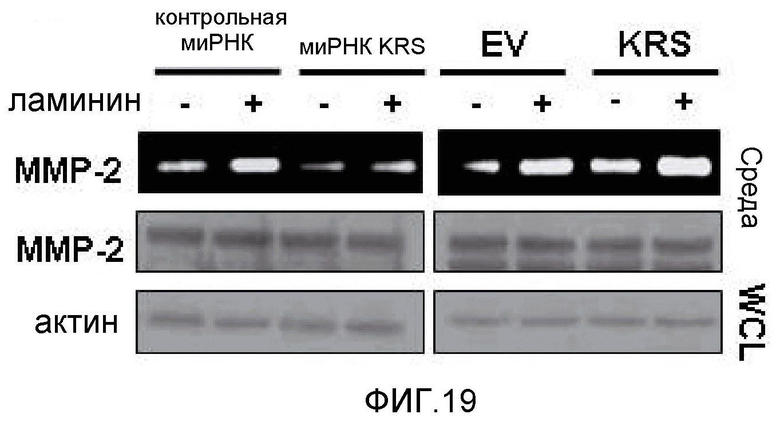
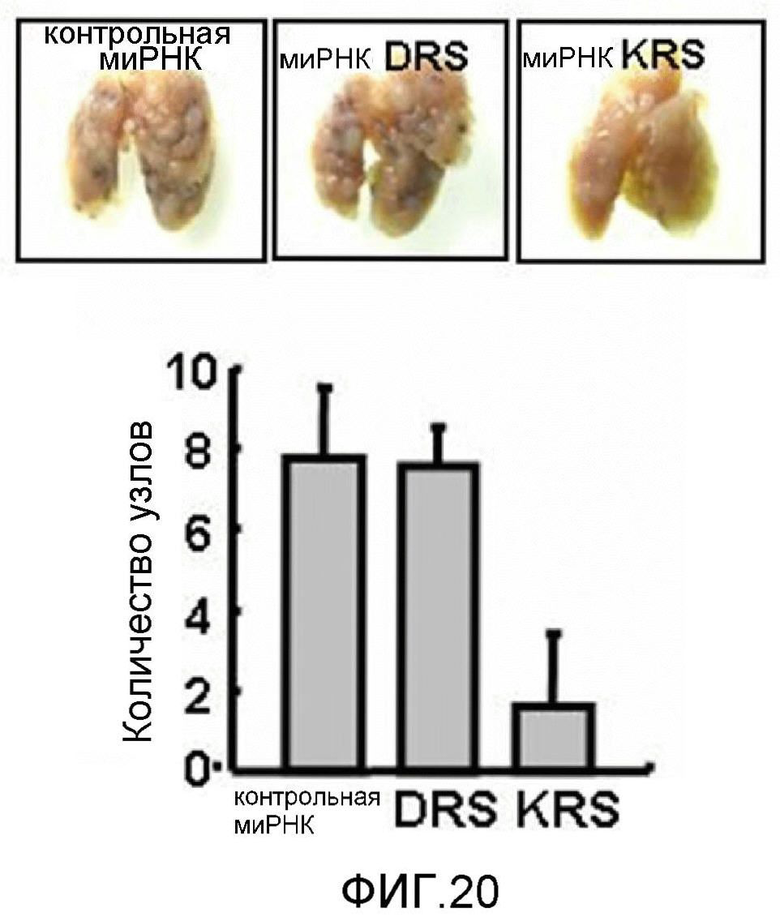
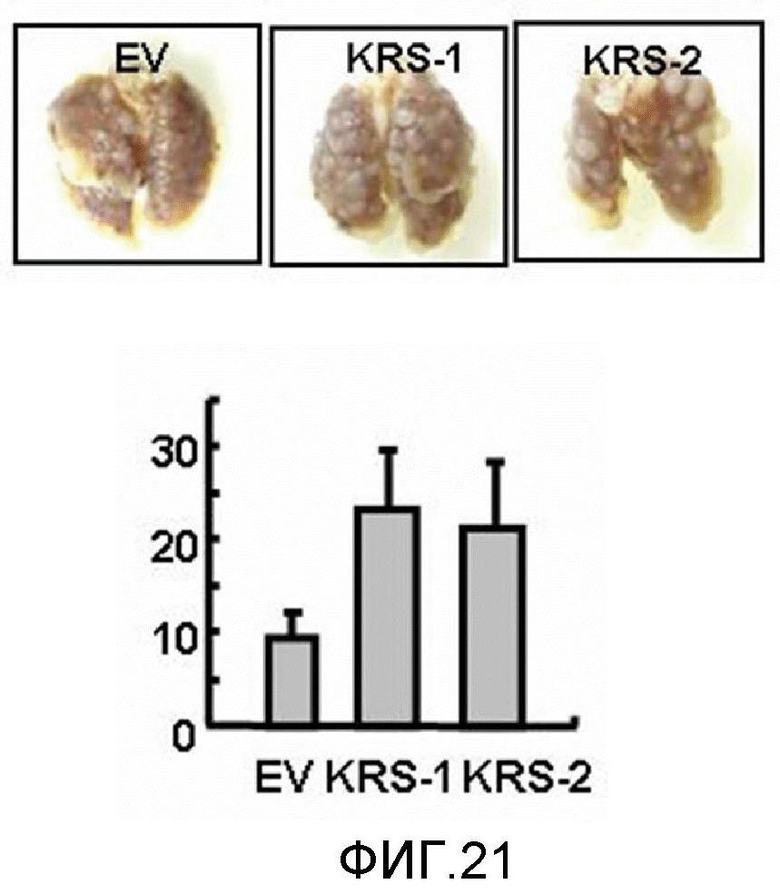
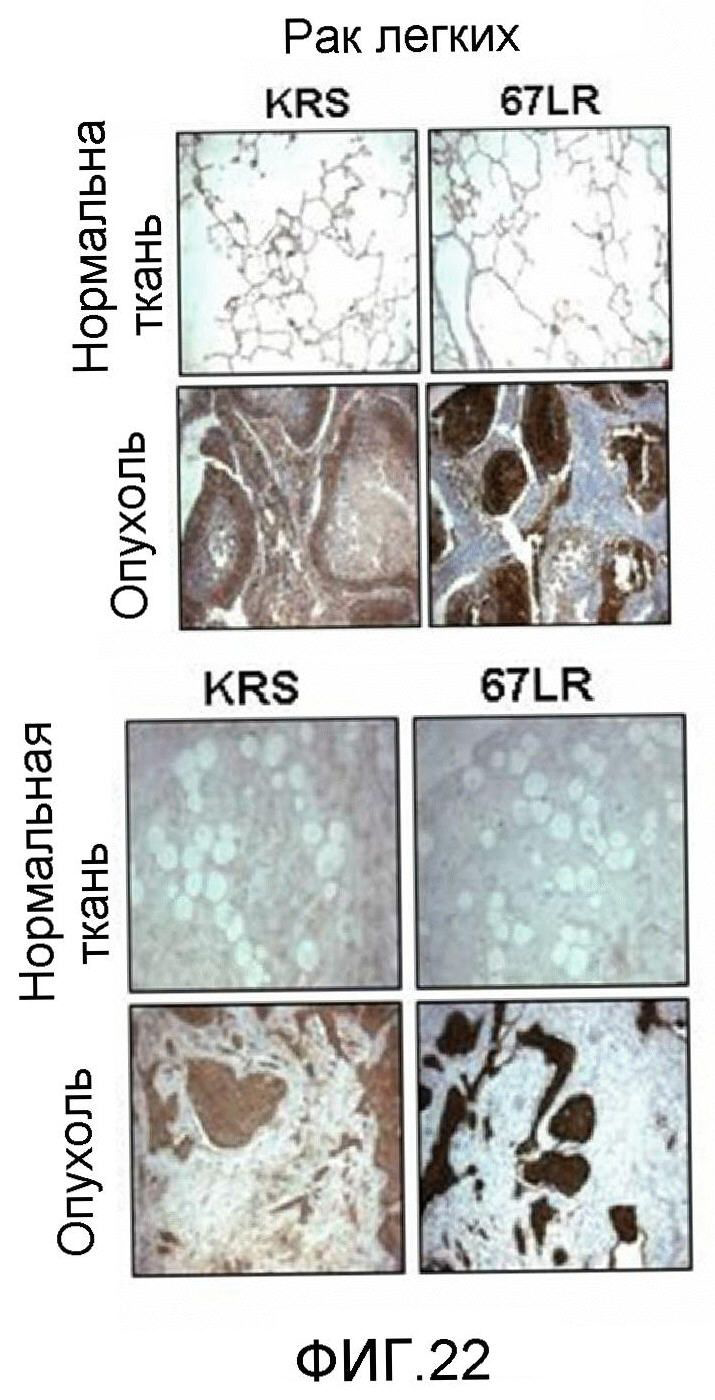
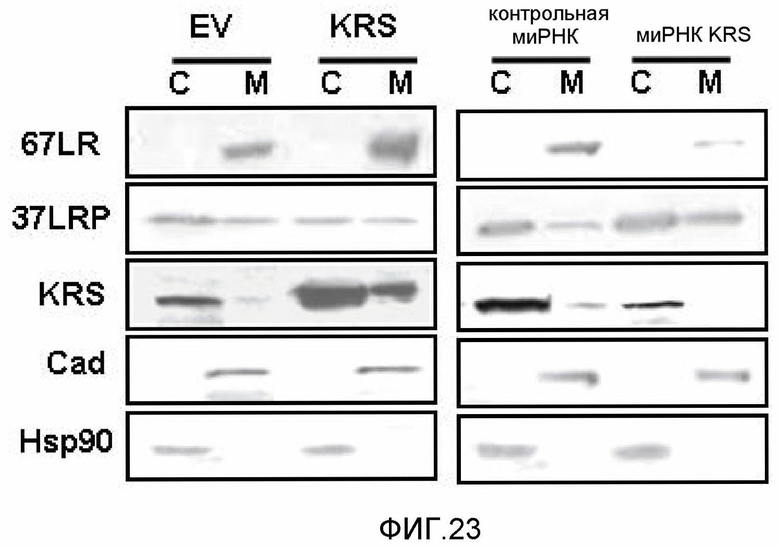
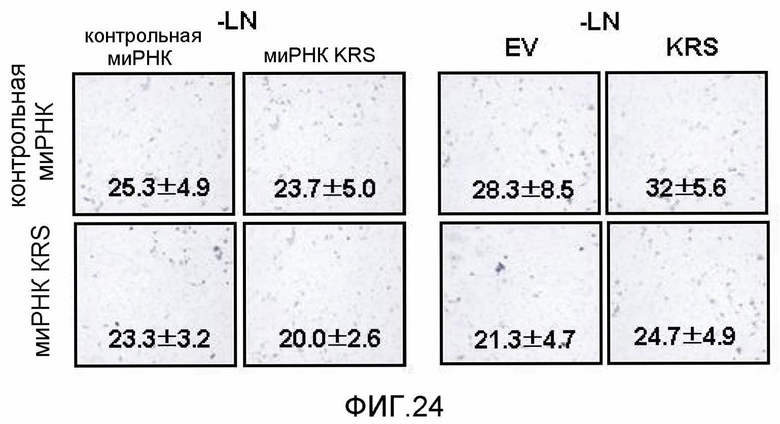
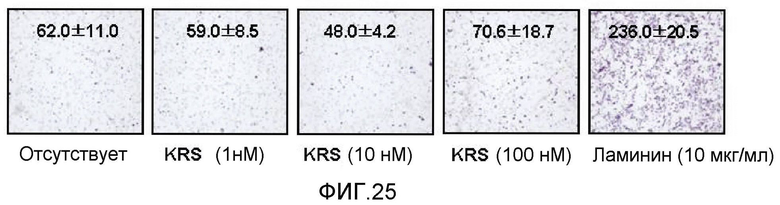
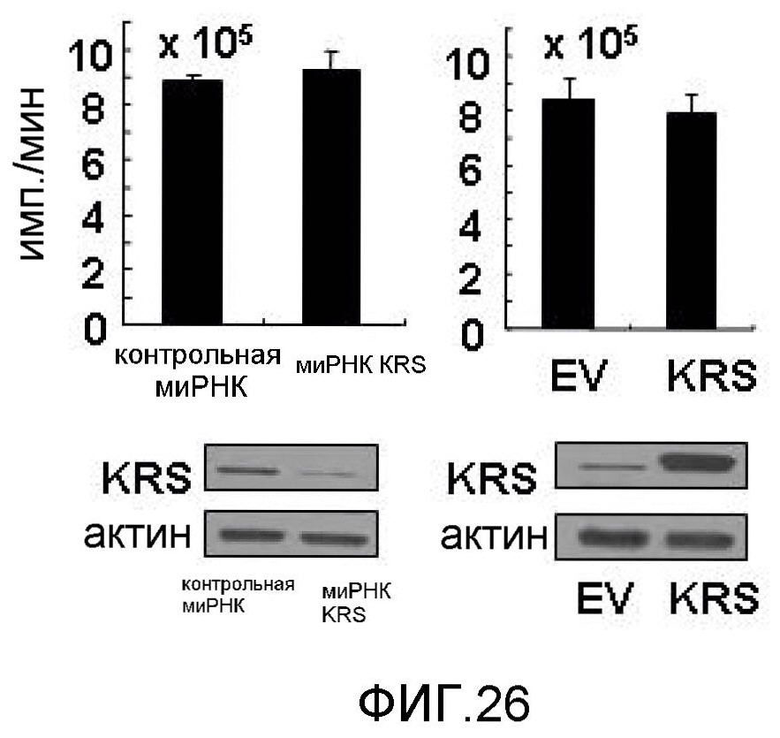
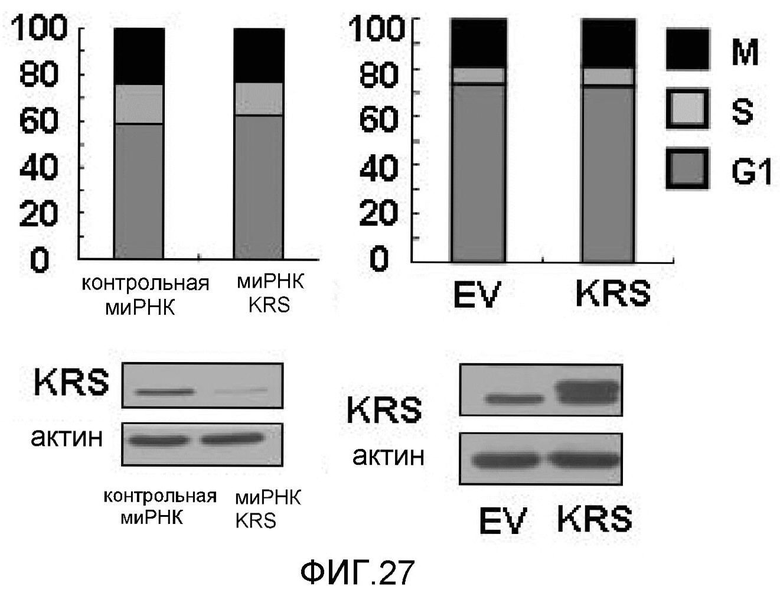
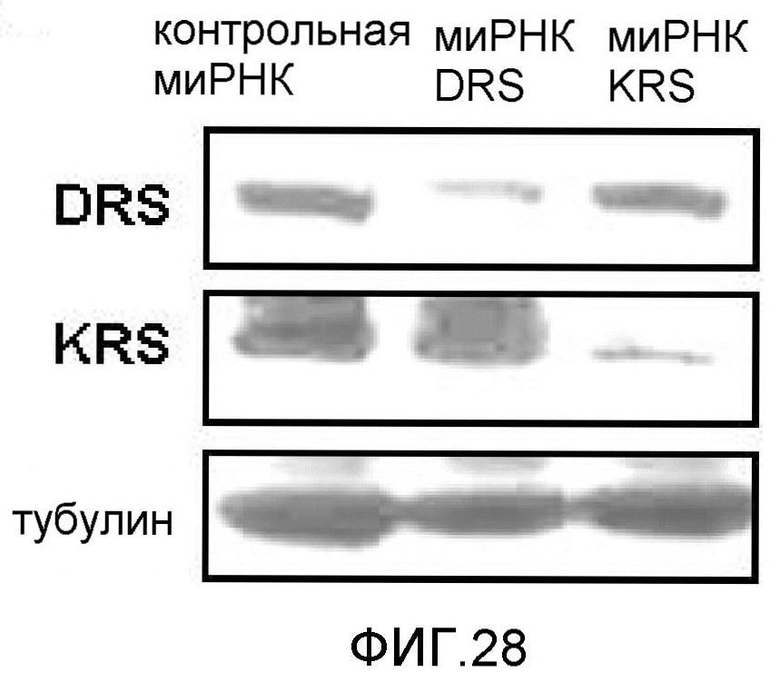
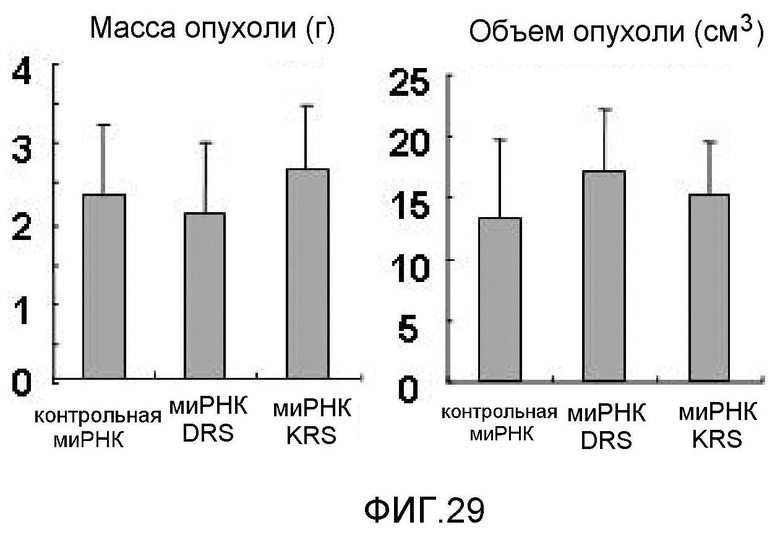
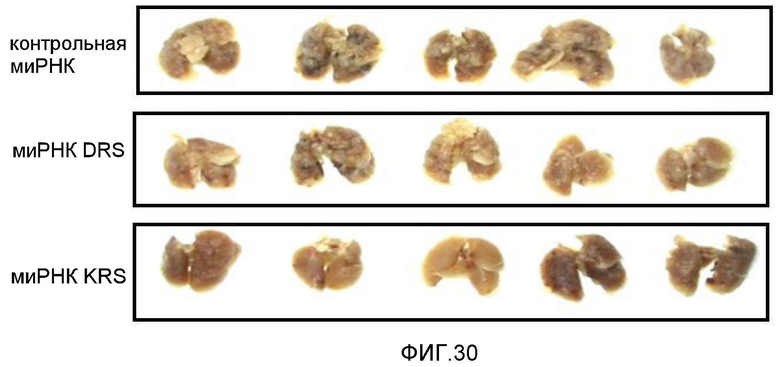
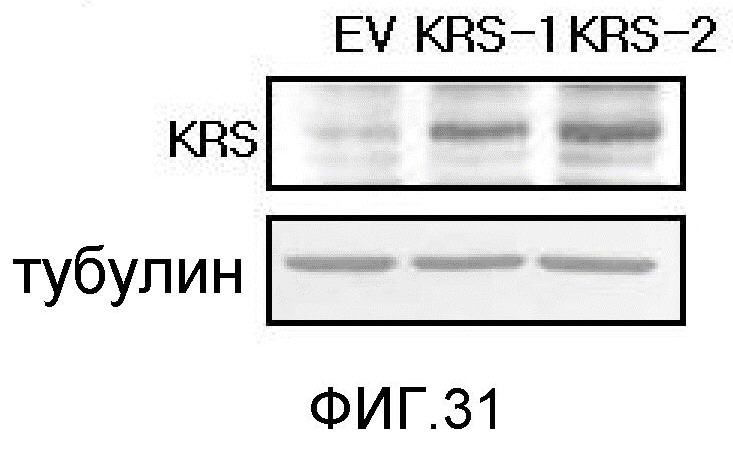
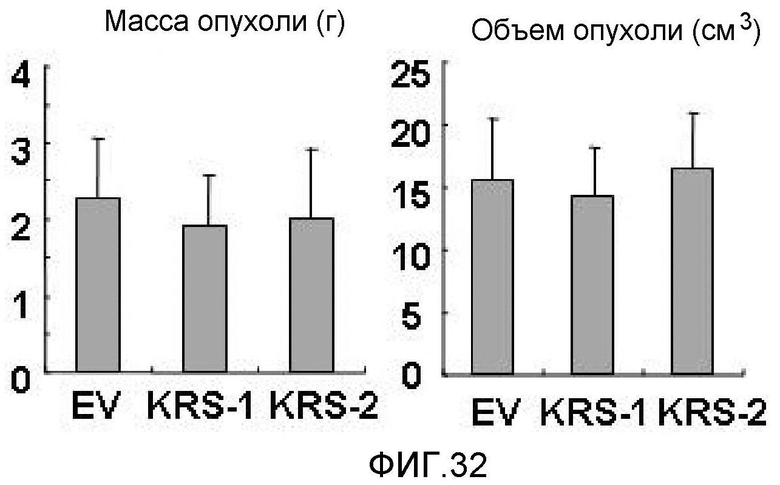
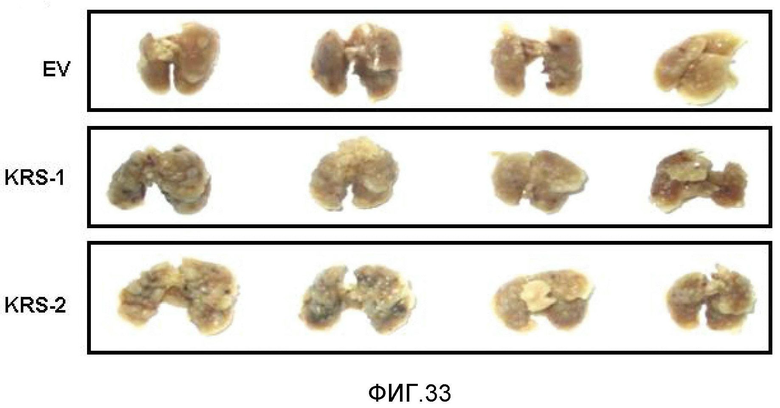
Изобретение относится к области биотехнологии, конкретно к исследованию функций лизил-тРНК-синтетазы (KRS), и может быть использовано в медицине. Предложен способ ингибирования метастазирования злокачественной опухоли или миграции злокачественных клеток посредством снижения клеточного уровня KRS. Для этого используют вектор экспрессии, содержащий промотор и функционально связанный с ним полинуклеотид, кодирующий антисмысловую РНК или миРНК против полинуклеотида KRS, или антитело против KRS. Настоящее изобретение позволяет эффективно ингибировать метастазирование злокачественной опухоли посредством ингибирования функции KRS, отвечающей за усиление миграции клеток опухоли и проявляющейся при транслокации KRS в мембрану и взаимодействии с рецептором ламинина (67LR). 5 н. и 3 з.п. ф-лы, 33 ил., 1 табл.
1. Способ ингибирования метастазирования злокачественной опухоли посредством снижения клеточного уровня лизил-тРНК-синтетазы (KRS).
2. Способ ингибирования метастазирования по п.1, где лизил-тРНК-синтетаза состоит из аминокислотной последовательности SEQ ID NO: 1.
3. Способ ингибирования миграции злокачественных клеток посредством снижения клеточного уровня лизил-тРНК-синтетазы (KRS).
4. Способ по п.3, где лизил-тРНК-синтетаза состоит из аминокислотной последовательности SEQ ID NO:1.
5. Композиция для ингибирования метастазирования злокачественной опухоли или миграции злокачественных клеток, содержащая в качестве эффективного ингредиента вектор экспрессии, содержащий промотор и функционально связанный с ним полинуклеотид, или антитело против KRS, где полинуклеотид кодирует антисмысловую РНК или миРНК против полинуклеотида KRS.
6. Композиция по п.5, где злокачественная опухоль выбрана из группы, состоящей из рака толстого кишечника, рака легких, рака печени, рака желудка, рака пищевода, рака поджелудочной железы, рака желчного пузыря, рака почки, рака мочевого пузыря, рака предстательной железы, рака семенников, рака шейки матки, карциномы эндометрия, хориокарциномы, рака яичников, рака молочной железы, рака щитовидной железы, опухоли головного мозга, злокачественной опухоли головы или шеи, злокачественной меланомы, лимфомы, апластической анемии.
7. Способ ингибирования метастазирования злокачественной опухоли или миграции злокачественных клеток, включающий введение индивиду, при необходимости, эффективного количества вектора экспрессии, содержащего промотор и функционально связанный с ним полинуклеотид, или антитела против KRS, где полинуклеотид кодирует антисмысловую РНК или миРНК против полинуклеотида KRS.
8. Применение вектора экспрессии, содержащего промотор и функционально связанный с ним полинуклеотид, или антитела против KRS для получения средства для ингибирования метастазирования злокачественной опухоли или миграции злокачественных клеток, где полинуклеотид кодирует антисмысловую РНК или миРНК против полинуклеотида KRS.
| SANG GYU PARK ET AL., Aminoacyl tRNA synthetases and their connections to disease, PROCEEDINGS OF THE NATIONAL ACADEMY OF SCIENCES, 2008, v.105, n.32, p.11043-11049 | |||
| SANG GYU PARK ET AL, Human lysyl-tRNA synthetase is secreted to trigger proinflammatory response, PROCEEDINGS OF THE NATIONAL ACADEMY OF SCIENCES, 2005, v.102, n.18, p.6356-6361 | |||
| SANG |
Авторы
Даты
2012-10-27—Публикация
2008-08-18—Подача