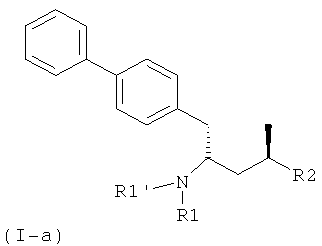
Настоящее изобретение относится к получению соединения формулы (I)

или его соли, в котором R1 и R1' независимо являются водородом или защитной группой для аминогруппы, a R2 является карбоксильной группой или сложноэфирной группой, включающий взаимодействие соединения формулы (II),

или его соли, в котором R1, R1' и R2 отвечают вышеприведенному определению, с водородом в присутствии катализатора на основе переходного металла и хирального лиганда, где переходный металл выбран из 7, 8 или 9 группы периодической системы.
Помимо этого настоящее изобретение относится к продуктам, получаемым с помощью упомянутого способа, и к их применению в получении ингибиторов нейтральной эндопептидазы (НЭП). Кроме того, настоящее изобретение относится к применению катализатора на основе переходного металла в получении ингибиторов НЭП или их пролекарств, в частности ингибиторов НЭП, содержащих в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты.
Эндогенные атриальные натрийуретические пептиды (АНП), также именуемые атриальными натрийуретическими факторами (АНФ) несут у млекопитающих мочегонную, натрийуретическую и сосудорасширяющую функцию. Природные пептиды АНФ метаболически инактивированы, в частности, разрушающим ферментом, который, как было обнаружено, соответствует ферменту нейтральной эндопептидазы (НЭП, ЕС 3.4.24.11), который также ответственен, например, за метаболическую инактивацию энкефалинов.
В соответствующей области известны биарил-замещенные производные фосфоновой кислоты, применимые в качестве ингибиторов нейтральной эндопептидазы (НЭП), например в качестве ингибиторов разрушающего АНФ фермента у млекопитающих, с целью продления и усиления диуретических, натрийуретических и сосудорасширяющих свойств АНФ у млекопитающих посредством ингибирования их деградации до менее активных метаболитов. Вследствие этого ингибиторы НЭП особенно применимы для лечения состояний и расстройств, чувствительных к ингибированию нейтральной эндопептидазы (ЕС 3.4.24.11), в частности сердечно-сосудистых расстройств, таких как повышенное давление, почечная недостаточность, включая отек и отложение солей, отек легких и застойную сердечную недостаточность.
Способы получения ингибиторов НЭП известны. Эти способы включают, как правило, стадию гидрирования при посредстве палладиевого катализатора на угле.
Патент США 5217996 описывает биарил-замещенные производные амида 4-аминомасляной кислоты, применимые в качестве ингибиторов нейтральной эндопептидазы (НЭП), например в качестве ингибиторов фермента, разрушающего АНФ, у млекопитающих. Патент США 5217996 описывает этиловый эфир N-(3-карбокси-1-оксопропил)-(4S)-(n-фенилфенилметил)-4-амино-(2R)-метилбутановой кислоты в качестве предпочтительного варианта осуществления. Для получения данного соединения этиловый эфир N-трет-бутоксикарбонил-(4R)-(n-фенилфенилметил)-4-амино-(2R)-метил-2-бутеновой кислоты 1 (II-а) (4,2 г) гидрируют в присутствии палладия на угле, что приводит к этиловому эфиру N-трет-бутоксикарбонил-(4R)-(n-фенилфенилметил)-4-амино-(2R)-метилбутановой кислоты в виде смеси диастереомеров 1(I-а):1(I-б) в соотношении 80:20.
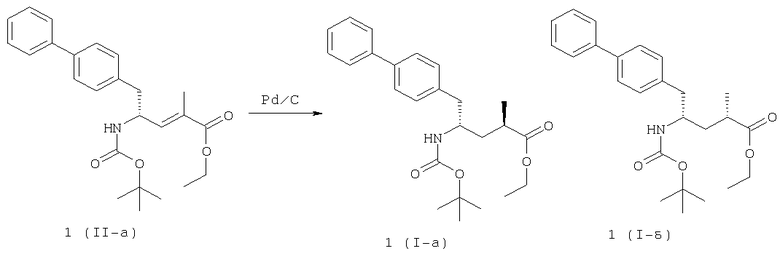
1(I-a):1(I-б) 80:20
В патенте США 5250522 описаны фосфонометил-биарил-замещенные производные аминокислот, проявляющие НЭП-ингибирующую активность. Предпочтительным вариантом осуществления является этиловый эфир (S)-5-(бифенил-4-ил)-4-[(диметилфосфонометил)амино]-2-пентеновой кислоты. На промежуточной стадии получения данного ингибитора НЭП этиловый эфир (S)-4-(трет-бутоксикарбониламино)-5-(бифенил-4-ил)пентеновой кислоты гидрируют с помощью палладиевого катализатора на угле, что приводит к этиловому эфиру (S)-4-(трет-бутоксикарбониламино)-5-(бифенил-4-ил)пентановой кислоты.
Некоторые дипептиды дикарбоновых кислот, являющиеся ингибиторами нейтральной эндопептидазы (НЭП), описаны в G.M.Kasander и др., J. Med. Chem. 1995, 38, 1689-1700, "Dicarboxylic Acid Dipeptide Neutral Endopeptidase Inhibitors" (Дипептиды дикарбоновых кислот - ингибиторы нейтральной эндопептидазы). В ходе получения данных ингибиторов задействовано катализируемое палладием гидрирование.
Объектом настоящего изобретения является разработка альтернативной стадии гидрирования в способе получения ингибиторов НЭП или их пролекарств, в частности разработка альтернативного процесса получения соединений формулы (I) или его солей, каковые могут быть использованы в качестве промежуточных соединений при получении ингибиторов НЭП или их пролекарств, в частности ингибиторов НЭП, содержащих в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты.
Еще одним объектом настоящего изобретения является разработка способа получения соединений согласно формулам (I-а) и (I-б) или их солей, в которых R1, R1' и R2 отвечают вышеприведенным определениям, с высоким диастереомерным соотношением предпочтительно выше 88:12.

Еще одним объектом настоящего изобретения является разработка способа получения высокого диастереомерного соотношения между соединениями согласно формуле (I-a) или их солями и соединениями согласно формуле (I-б) или их солями предпочтительно выше 88:12, более предпочтительно выше 90:10. Объектом настоящего изобретения является разработка способа, при котором соединения согласно формуле (I-б) или их соли могут быть полностью удалены, а соединения согласно формуле (I-а) или их соли могут быть получены в чистом виде.
Еще одним объектом настоящего изобретения является разработка способа получения высокого диастереомерного соотношения между соединениями согласно формуле (I-б) или их солями и соединениями согласно формуле (I-а) или их солями предпочтительно выше 88:12, более предпочтительно выше 90:10. Объектом настоящего изобретения является разработка способа, при котором соединения согласно формуле (I-а) или их соли могут быть полностью удалены, а соединения согласно формуле (I-б) или их соли могут быть получены в чистом виде.
Еще одним объектом настоящего изобретения является разработка способа получения соединений согласно формулам (I-в) и (I-г) или их солей, в которых R1, R1' и R2 отвечают вышеприведенным определениям, с высоким диастереомерным соотношением предпочтительно выше 88:12.


Еще одним объектом настоящего изобретения является разработка способа получения высокого диастереомерного соотношения между соединениями согласно формуле (I-в) или их солями и соединениями согласно формуле (I-г) или их солями предпочтительно выше 88:12, более предпочтительно выше 90:10. Объектом настоящего изобретения является разработка способа, при котором соединения согласно формуле (I-в) или их соли могут быть полностью удалены, а соединения согласно формуле (I-г) или их соли могут быть получены в чистом виде.
Еще одним объектом настоящего изобретения является разработка стадии гидрирования в способе получения ингибиторов НЭП или их пролекарств, в частности ингибиторов НЭП, содержащего в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты, в котором стадия гидрирования предпочтительно характеризуется высоким выходом и предпочтительно ведет к продуктам, характеризуемым высокой степенью чистоты, предпочтительно к продуктам в диастереомерном соотношении выше 88:12.
Цели настоящего изобретения могут быть достигнуты посредством использования специального катализатора и специального хирального лиганда на стадии гидрирования в получении ингибитора НЭП, в частности ингибитора НЭП, содержащего в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты. Предпочтительно специальный катализатор и специальный хиральный лиганд применяются в реакции гидрирования соединения согласно формуле (II) или его солей, в частности в реакции гидрирования соединения согласно формуле (II-а) или его солей,

в котором R1, R1' и R2 отвечают вышеприведенным определениям.
Еще в одном варианте осуществления настоящего изобретения специальный катализатор и специальный хиральный лиганд применяются в реакции гидрирования соединения согласно формуле (II-б),

или его солей, в котором R1, R1' и R2 отвечают вышеприведенным определениям.
Таким образом, предметом настоящего изобретения является способ получения соединения согласно формуле (I),

или его соли, в котором R1 и R1' независимо являются водородом или защитной группой для аминогруппы, а R2 является карбоксильной группой или сложноэфирной группой, включающий взаимодействие соединения согласно формуле (II),

или его соли, в котором R1, R1' и R2 отвечают вышеприведенным определениям, с водородом в присутствии катализатора на основе переходного металла и хирального лиганда, в которых переходный металл выбран из 7, 8 или 9 группы периодической системы.
В формулах (I) и (II) термин " " обозначает ковалентную связь, где стереохимия связь определяется либо (S)-конфигурацией, либо (R)-конфигурацией соответствующего хирального центра.
" обозначает ковалентную связь, где стереохимия связь определяется либо (S)-конфигурацией, либо (R)-конфигурацией соответствующего хирального центра.
Как следствие, соединения согласно формуле (II) или их соли являются хиральными соединениями и относятся к соединениям согласно формуле (II-а) или их солям или соединениям согласно формуле (II-б) или их солям.
В соответствии с этим соединения согласно формуле (I) или их соли являются хиральными соединениями и относятся к соединениям согласно формулам (I-а), (I-б), (I-в) и (I-г) или их солям.
Настоящее изобретение относится к способу диастереоселективного гидрирования соединения формулы (II) водородом в присутствии катализатора на основе переходного металла и хирального лиганда. Исходное вещество формулы (II) является хиральным, поэтому хиральность как субстрата, так и лиганда влияет на диастереоселективность посредством явления, называемого «двойной диастереодифференциацией» («согласованная» и «несогласованная» двойная асимметрическая индукция).
Степень фациальной селективности, наблюдаемая при гидрировании хирального соединения формулы (II) в отсутствии каких-либо других хиральных элементов, является степенью субстратного контроля.
Если фациальная селективность субстрата совпадает с фациальной селективностью лиганда («согласованная» двойная асимметрическая индукция), можно ожидать повышения диастереоселективности гидрирования водородом в присутствии катализатора на основе переходного металла и хирального лиганда. Однако если фациальная селективность субстрата не совпадает с фациальной селективностью лиганда («несогласованная» двойная асимметрическая индукция), высокой диастереоселективности ожидать нельзя.
Как было обнаружено, при задействовании способа согласно настоящему изобретению гидрирование соединения формулы (II) может быть осуществлено с высокой диастереоселективностью вне зависимости от степени субстратного контроля. Поэтому даже если степень субстратного контроля высока (например, диастереомерное соотношение вплоть до 80 к 20), способ по настоящему изобретению предоставляет средства к получению любого из возможных диастереомерных продуктов с высокой диастереоселективностью. Таким образом, преимуществом настоящего изобретения является возможность стереоконтролируемого гидрирования соединений формулы (II) вне зависимости от стереохимии исходного соединения формулы (II). Описываемый в контексте способ может, таким образом, обеспечить получение любого из соединений (I-а), (I-б), (I-в) и (I-г) с высоким диастереомерным избытком. В соответствии с этим при задействовании способа по настоящему изобретению гидрирование соединения формулы (II-a) может привести как к (I-а), так и к (I-б) с высоким диастереомерным избытком. Сходным образом, гидрирование соединения формулы (II-б) может привести как к (I-в), так и к (I-г) с высоким диастереомерным избытком.
Соединения формулы (I) содержат в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту. Известны ингибиторы НЭП, которые содержат в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту, такие как N-(3-карбокси-1-оксопропил)-(4S)-n-фенилфенилметил)-4-амино-(2R)-метилбутановая кислота. Таким образом, настоящее изобретение предоставляет новый асимметрический подход к получению ингибиторов НЭП. Что более важно, данный подход осуществляется с высокой степенью стереоконтроля.
В формулах (I) и (II) R1 и R1' независимо являются водородом или защитной группой для аминогруппы.
Предпочтительным является, если R1 является защитной группой для аминогруппы. Также предпочтительным является, если R1' является водородом. Таким образом, в предпочтительном варианте осуществления настоящего изобретения R1 является одной из нижеописанных защитных групп для аминогруппы, а R1' является водородом. Альтернативно R1 и R1' могут совместно образовывать циклическую структуру (и образуют таким образом бифункциональную циклическую защитную группу для аминогруппы).
Термин «защитная группа для аминогруппы» включает любую группу, способную обратимо защищать аминофункцию. Подходящие защитные группы для аминогруппы общепринято применяются в химии пептидов и описаны, например, в стандартных обзорных работах, таких как J.F.W.McOmie. Protective Groups in Organic Chemistry (Защитные группы в органической химии), Plenum Press, Лондон и Нью-Йорк, 1973, в Т.W.Greene и Р.G.M.Wuts, "Protective Groups in Organic Synthesis" (Защитные группы в органическом синтезе), 4-е издание, Wiley, Нью-Йорк, 2007, в "The Peptides" (Пептиды), т.3 (под ред. Е.Gross и J.Meienhofer), Academic Press, Лондон и Нью-Йорк, 1981, и в Methoden der organischen Chemie (Методы органической химии), Houben Weyl, 4-е издание, т.15/1, Georg Thieme Verlag, Штуттгарт, 1974.
Предпочтительные защитные группы включают, например, (С1-С2)алкил, моно-, ди- или тризамещенный фенилом, такой как бензил, (или) бензгидрил или тритил, в которых фенильный цикл является незамещенным или замещенным одним или более, например, двумя или тремя остатками, например, выбранными из группы, включающей (С1-С7)алкил, гидроксигруппу, (С1-С7)алкоксигруппу, (С2-С8)алканоилоксигруппу, галоид, нитрогруппу, цианогруппу и CF3, а также фенил(С1-С2)алкоксикарбонильную группу и аллил или циннамил. Особенно предпочтительными являются бензилоксикарбонильная группа (Cbz), 9-флуоренилметилоксикарбонильная группа (Fmoc), бензилоксиметил (ВОМ), пивалоилоксиметил (РОМ), трихлорэтоксикарбонильная группа (Troc), 1-адамантилоксикарбонильная группа (Adoc), но также могут быть использованы бензил, кумил, бензгидрил, тритил, аллил, (С1-С10)алкенилоксикарбонильная группа, такая как «alloc» (аллилоксикарбонильная группа). Защитная группа также может быть силилом, таким как триалкилсилил, в особенности триметилсилил, трет-бутилдиметилсилил, триэтилсилил, триизопропилсилил, триметилсилилэтоксиметил (SEM), а также может быть сульфонильной группой, такой как метансульфонильная группа, трифторметансульфонильная группа и бензилсульфонильная группа, или сульфенильной группой, такой как бензолсульфенильная группа.
R1 и/или R1' также могут быть сукцинимидильной группой или ацетальной группой.
Примеры R1 и/или R1' также включают (С1-С10)алкенилоксикарбонильную группу, (С6-С10)арил(С1-С6)алкил, (С1-С6)алкилкарбонильную группу, (С6-С10)арилкарбонильную группу, (С1-С6)алкоксикарбонильную группу и (С6-С10)арил(С1-С6)алкоксикарбонильную группу. В предпочтительном варианте осуществления настоящего изобретения R1 является (С6-С10)арил(С1-С6)алкил-оксикарбонильной группой, (С1-С6)алкоксикарбонильной группой, аллилоксикарбонильной группой или (С6-С10)арил(С1-С6)алкилом, как то бензил или трет-бутоксикарбонильная группа (ВОС).
В особенно предпочтительном варианте осуществления настоящего изобретения R1 является трет-бутоксикарбонильной группой (ВОС). Более предпочтительным является, если R1 является трет-бутоксикарбонильной группой (ВОС), а R1' является водородом.
В другом особенно предпочтительном варианте осуществления настоящего изобретения R1 и/или R1' независимо являются водородом или выбраны из бензильной группы, сукцинимидильной группы, ацетальной группы, силильной группы или оксикарбонильной группы.
В еще одном особенно предпочтительном варианте осуществления настоящего изобретения R1 и/или R1' независимо являются водородом или защитной группой для аминогруппы, выбранной из группы, включающей (С1-С6)алкил, моно-, ди- или тризамещенный (С6-С10)арилом, где арильный цикл является незамещенным или замещенным одним, двумя или тремя остатками, выбранными из группы, включающей (С1-С7)алкил, гидроксигруппу, (С1-С7)алкоксигруппу, галоид, нитрогруппу, цианогруппу и CF3, а также (С6-С10)арил(С1-С6)алкил, кумил, фенил(С1-С2)алкоксикарбонильную группу, аллил, циннамил, 9-флуоренилметилоксикарбонильную группу (Fmoc), бензилоксиметил (ВОМ), пивалоилоксиметил (РОМ), трихлорэтоксикарбонильную группу (Troc), 1-адамантилоксикарбонильную группу (Adoc), (С1-С10)алкенилоксикарбонильную группу, силил, сульфонильную группу, сульфенильную группу, сукцинимидильную группу, (С2-С6)алканоил, (С6-С10)арилкарбонильную группу, (С1-С6)алкоксикарбонильную группу и (С6-С10)арил(С1-С6)алкоксикарбонильную группу.
В формулах (I) и (II) термин «сложноэфирная группа» включает любую сложноэфирную или карбоксильную группу, общеизвестную в соответствующей области, например группы-COOR3, в которых R3 выбран из группы, включающей (С1-С6)алкил, такой как метил, этил или трет-бутил, (С1-С6)алкокси(С1-С6)алкил, гетероциклил, такой как тетрагидрофуранил, (С6-С10)арилокси(С1-С6)алкил, такой как бензилоксиметил (ВОМ), силил, такой как триметилсилил, трет-бутилдиметилсилил и трет-бутилдифенилсилил, циннамил, аллил, (С1-С6)алкил, моно-, ди- или тризамещенный галоидом, силилом, цианогруппой или (С1-С6)арилом, где арильный цикл является незамещенным или замещенным одним, двумя или тремя остатками, выбранными из группы, включающей (С1-С7)алкил, гидроксигруппу, (С1-С7)алкоксигруппу, галоид, нитрогруппу, цианогруппу и CF3 или (С1-С2)алкил, замещенный 9-флуоренилом.
В предпочтительном варианте осуществления настоящего изобретения R2 является -COOR3, где R3 является (С1-С6)алкильным остатком. В частности, R3 является этильной группой.
В особенно предпочтительном варианте осуществления настоящего изобретения R2 является СООН.
Кроме того, в предпочтительном варианте осуществления настоящего изобретения R1 является трет-буоксикарбонильной группой. В другом предпочтительном варианте осуществления настоящего изобретения R1 является трет-буоксикарбонильной группой. В обоих предпочтительных вариантах осуществления настоящего изобретения R1' предпочтительно является водородом.
Вышеприведенные определения R1, R1' и R2 также относятся к формулам (I-а), (I-б), (I-в), (I-г), (II-а) и (II-б).
Реакцию соединения согласно формуле (II) или его соли с водородом осуществляют в присутствии катализатора на основе переходного металла, в котором переходный металл выбран из групп 7, 8 или 9 периодической системы. Таким образом, катализатор на основе переходного металла содержит, например, марганец (Mn), рений (Re), железо (Fe), рутений (Ru), осмий (Os), кобальт (Со), родий (Rh) и/или иридий (Ir).
В предпочтительном варианте осуществления настоящего изобретения катализатор на основе переходного металла содержит родий, иридий или рутений. В более предпочтительном варианте осуществления настоящего изобретения катализатор на основе переходного металла содержит родий или рутений. В особенно предпочтительном варианте осуществления настоящего изобретения катализатор на основе переходного металла содержит рутений.
Как правило, катализатор на основе переходного металла является металлоорганическим комплексом, содержащим один или более из вышеупомянутых атомов металлов и подходящие лиганды.
Подходящие лиганды для металлорганических комплексов являются, как правило, σ-донорными лигандами, σ-донорными/π-акцепторными лигандами или σ,π-донорными/π-акцепторными лигандами. Примерами подходящего типа лигандов являются, среди прочего, монооксид углерода, галогенид-анионы, фосфины, алкенилы, алкинилы, арилы и их смеси.
Примерами предпочтительных лигандов для металлоорганического комплекса являются норборнадиен (nbd), циклооктадиен (cod), цимен, в частности, n-цимен, и иодид-анион.
Комплексы могут содержать один атом переходного металла. В предпочтительных вариантах осуществления настоящего изобретения комплексы могут содержать два или более атома переходного металла, необязательно включая связь металл-металл. В предпочтительном варианте осуществления настоящего изобретения два атома металла связаны через два мостиковых галогенид-аниона.
Примерами предпочтительных катализаторов на основе переходного металла являются [RuI2(n-цимен)]2, [Rh(nbd)2BF4] и [Ir(cod)2Cl]2. Более предпочтительными являются [RuI(n-цимен)]2 и [Rh(nbd)2BF4].
Особенно предпочтительным катализатором на основе переходного металла является [Rh(nbd)2BF4] {=тетрафторборат бис(норборнадиен)родия(I)}
Другим особенно предпочтительным катализатором на основе переходного металла является [RuI2(n-пимен)]2 (=димер дииод(n-цимен)рутения(II)):

Как правило, термин "хиральный лиганд" включает любой лиганд, подходящий для построения металлоорганических комплексов и включающий хиральный центр.
В предпочтительном варианте осуществления настоящего изобретения хиральный лиганд включает хиральный фосфин.
Кроме того, является предпочтительным, если хиральный лиганд включает хиральный ферроцен. Также является предпочтительным, если хиральный лиганд включает ферроценовую структуру, в которой циклопентадиенильный (Ср) лиганд ферроцена замещен хиральной группой.
В предпочтительном варианте осуществления настоящего изобретения хиральный лиганд выбран из лигандов Josiphos, Walphos, Taniaphos, Solphos, Mandyphos, Butiphane или их смесей. Лиганды Josiphos, Walphos, Taniaphos и Mandyphos отвечают формулам:
Josiphos
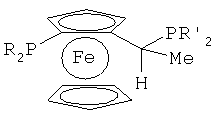
Walphos

Taniaphos

Solphos

Mandyphos
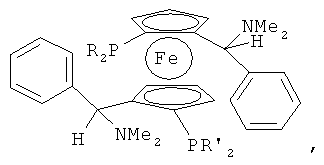
в которых R и R' таковы, как это описано в международной заявке на изобретение WO 2006/003196, европейском патенте ЕР-В1-612758, международных заявках на изобретение WO 2006/017045, WO 2006/117369 и, в особенности, как описано в приведенных в контексте примерах.
Примерами подходящих хиральных лигандов являются:
Хиральные лиганды со структурой Mandyphos:
SL-M001-1: (αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дифенилфосфино)ферроцен (также известный как (R)-(S)-NMe2-PPh2-Mandyphos)

SL-M004-1: (αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (также известный как (R)-(S)-NMe2-P(3,5-Me-4-MeOPh)2-Mandyphos)

SL-M004-2: (αS,αS)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (также известный как (S)-(R)-NMe2-P(3,5-Me-4-MeOPh)2-Mandyphos)



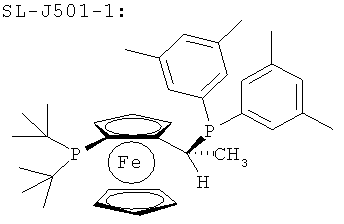
Хиральные лигады со структурой Josiphos:









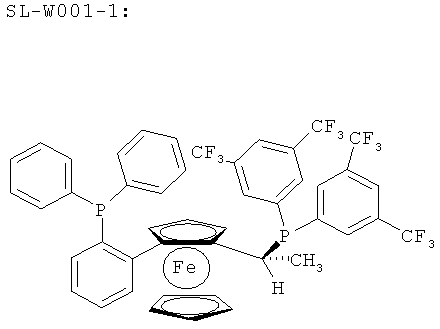
Хиральные лиганды со структурой Walphos:



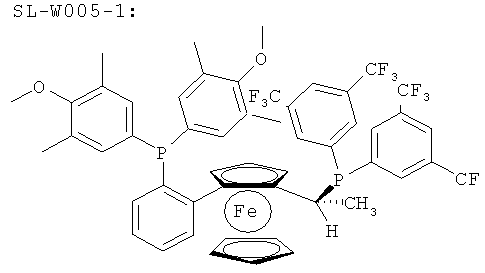

Примерами подходящих хиральных лигандов являются

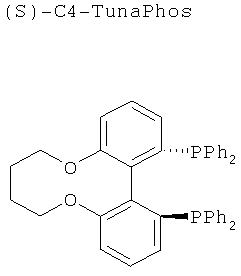








Получение лиганда (S)-C4-TunaPhos описано в J. Org. Chem., 2000, 65, 6223 (пример 4). Лиганд (R)-(+)-BINAP может быть приобретен у коммерческих источников, таких как Aldrich. Все остальные упомянутые выше лиганды (Mandyphos, Josiphos, Walphos, Solphos, и т.п.) коммерчески доступны от компании Solvias AG (Базель, Швейцария).
Предпочтительными хиральными лигандами являются:
(αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дифенилфосфино)ферроцен (=Mandyphos SL-M001-1),
(αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (=Mandyphos SL-M004-1),
(αS,αS)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (=Mandyphos SL-M004-2),
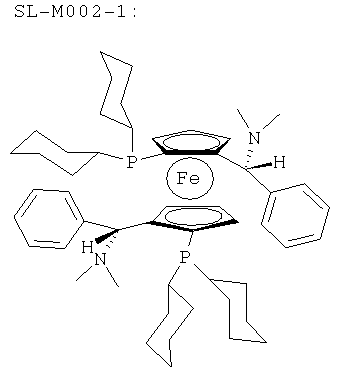
(αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дициклогексилфосфино)ферроцен (=SL-M002-1),
(R)-N,N'-Диметил-7,7'-бис(дифенилфосфино)-3,3',4,4'-тетрагидро-8,8'-би-2H-1,4-бензоксазин (=Solphos SL-A001-1),
(R)-1-[(S)-2-Дициклогексилфосфино)ферроценил]этилдициклогексилфосфин (=SL-J003-1),
(R)-1-[(S)-2-Дициклогексилфосфино)ферроценил]этилди-трет-бутилфосфин (=SL-J009-1),
(S)-1-[(S)-2-(2'-Дифенилфосфинофенил)ферроценил]этилди(бис-3,5-трифторметилфенил)фосфин (=SL-W001-2),
(R)-1-[(R)-2-(2'-Дифенилфосфинофенил)ферроценил]этилдициклогексилфосфин (=SL-W003-1),
(R)-1-[(S)-2-Дициклогексилфосфино)ферроценил]этилдициклогексилфосфин (=Josiphos SL-J002-1) и/или
(R)-1-[(R)-2-(2'-Дициклогексилфосфинофенил)ферроценил]этилди(бис(3,5-трифторметил)фенил)фосфин (=Walphos SL-W008-1).
Более предпочтительными хиральными лигандами являются:
(αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дифенилфосфино)ферроцен (=Mandyphos SL-M001-1),
(αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (=Mandyphos SL-M004-1),
(αS,αS)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (=Mandyphos SL-M004-2),
(R)-1-[(S)-2-Дициклогексилфосфино)ферроценил]этилдициклогексилфосфин (=Josiphos SL-J002-1) и/или
(R)-1-[(R)-2-(2'-Дициклогексилфосфинофенил)ферроценил]этилди(бис-(3,5-трифторметил)фенил)-фосфин (=Walphos SL-W008-1).
Еще более предпочтительными хиральными лигандами являются:
(αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дифенилфосфино)ферроцен (=Mandyphos SL-M001-1),
(αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (=Mandyphos SL-M004-1) и/или
(αS,αS)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (=Mandyphos SL-M004-2).
Наиболее предпочтительными хиральными лигандами являются:
(αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дифенилфосфино)ферроцен (=Mandyphos SL-M001-1) и/или
(αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (=Mandyphos SL-M004-1).
Особенно предпочтительным в качестве хирального лиганда является
(αR,αR)-2,2'-Бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (=Mandyphos SL-M004-1).
В одном из вариантов осуществления настоящего изобретения предпочтительными являются следующие комбинации катализатора на основе переходного металла и хирального лиганда: родиевый катализатор и лиганд Mandyphos, Walphos, Josiphos или Solphos, более предпочтительно Rh(nbd)2BF4 и лиганд Mandyphos, Walphos, Josiphos или Solphos, еще более предпочтительно, родиевый катализатор и Mandyphos SL-M004-1, Josiphos SL-J003-1, Josiphos SL-J009-1, Walphos SL-W001-2, Walphos SL-W003-1, Walphos SL-W008-1 или Solphos SL-A001-1, еще более предпочтительно Rh(nbd)2BF4 и Mandyphos SL-M004-1, Josiphos SL-J003-1, Josiphos SL-J009-1, Walphos SL-W001-2, Walphos SL-W003-1, Walphos SL-W008-1 или Solphos SL-A001-1.
В другом варианте осуществления настоящего изобретения предпочтительными являются следующие комбинации катализатора на основе переходного металла и хирального лиганда: родиевый катализатор и Walphos SL-W008-1, еще более предпочтительно Rh(nbd)2BF4 и Walphos SL-W008-1. При задействовании данных комбинаций катализатора на основе переходного металла и хирального лиганда в результате взаимодействия соединения формулы (II-а) или его соли получают композицию, содержащую соединения согласно формулам (I-а) и (I-б) или их соли, в которой мольное соотношение между (I-а) и (I-б) составляет по крайней мере 88:12.
В другом варианте осуществления настоящего изобретения предпочтительными являются следующие комбинации катализатора на основе переходного металла и хирального лиганда: родиевый катализатор и Mandyphos SL-M004-1, Josiphos SL-J003-1, Josiphos SL-J009-1, Walphos SL-W001-2, Walphos SL-W003-1 или Solphos SL-A001-1, еще более предпочтительно Rh(nbd)2BF4 и Mandyphos SL-M004-1, Josiphos SL-J003-1, Josiphos SL-J009-1, Walphos SL-W001-2, Walphos SL-W003-1 или Solphos SL-A001-1. При задействовании данных комбинаций катализатора на основе переходного металла и хирального лиганда в результате взаимодействия соединения формулы (II-а) или его соли получают композицию, содержащую соединения согласно формулам (I-а) и (I-б) или их соли, в которой мольное соотношение между (I-б) и (I-а) составляет по крайней мере 65:35, более предпочтительно по крайней мере 73:27.
В другом варианте осуществления настоящего изобретения предпочтительными являются следующие комбинации катализатора на основе переходного металла и хирального лиганда: родиевый катализатор и лиганд Mandyphos или Walphos, более предпочтительно [Rh(nbd)2BF4] и лиганд Mandyphos или Walphos, равно как и родиевый катализатор и SL-M004-2 или SL-W008-1, наиболее предпочтительно [Rh(nbd)2BF4] и SL-M004-2 или [Rh(nbd)2BF4] и SL-W008-1.
В еще одном варианте осуществления настоящего изобретения предпочтительными являются следующие комбинации катализатора на основе переходного металла и хирального лиганда: рутениевый катализатор и лиганд Mandyphos или Josiphos, более предпочтительно [RuI2(n-цимен)]2 и лиганд Mandyphos или Josiphos, еще более предпочтительно рутениевый катализатор и SL-M001-1, SL-M002-1, SL-M004-1, SL-M004-2 или SL-J002-1, еще более предпочтительно [RuI2(n-цимен)]2 и SL-M001-1, SL-M002-1, SL-M004-1, SL-M004-2 или SL-J002-1.
В другом варианте осуществления настоящего изобретения предпочтительными являются следующие комбинации катализатора на основе переходного металла и хирального лиганда: рутениевый катализатор и Mandyphos SL-M004-2 или SL-M002-1, предпочтительно [RuI2(n-цимен)]2 и Mandyphos SL-M004-2 или SL-M002-1. При задействовании данных комбинаций катализатора на основе переходного металла и хирального лиганда в результате взаимодействия соединения формулы (II-а) или его соли получают композицию, содержащую соединения согласно формулам (I-а) и (I-б) или их соли, в которой мольное соотношение между (I-б) и (I-а) составляет по крайней мере 65:35, более предпочтительно, по крайней мере 73:27, наиболее предпочтительно, по крайней мере, 94:6.
В еще одном предпочтительном варианте осуществления настоящего изобретения имеют место следующие комбинации катализатора на основе переходного металла и хирального лиганда: рутениевый катализатор и Mandyphos SL-M001-1, Mandyphos SL-M004-1 или Josiphos SL-J002-1; предпочтительно [RuI2(n-цимен)]2 и Mandyphos SL-M001-1, Mandyphos SL-M004-1 или Josiphos SL-J002-1. При задействовании данных комбинаций катализатора на основе переходного металла и хирального лиганда в результате взаимодействия соединения формулы (II-а) или его соли получают композицию, содержащую соединения согласно формулам (I-а) и (I-б) или их соли, в которой мольное соотношение между (I-а) и (I-б) составляет по крайней мере 88:12, более предпочтительно, по крайней мере, 98:2.
В еще одном предпочтительном варианте осуществления настоящего изобретения имеют место следующие комбинации катализатора на основе переходного металла и хирального лиганда: рутениевый катализатор и Mandyphos SL-M004-1, предпочтительно [RuI2(п-цимен)]2 и Mandyphos SL-M004-1. При задействовании данных комбинаций катализатора на основе переходного металла и хирального лиганда в результате взаимодействия соединения формулы (II-б или его соли получают композицию, содержащую соединения согласно формулам (I-в) и (I-г) или их соли, в которой мольное соотношение между (I-в) и (I-г) составляет по крайней мере 88:12, более предпочтительно по крайней мере 92:8.
В еще одном варианте осуществления настоящего изобретения предпочтительными являются следующие комбинации катализатора на основе переходного металла и хирального лиганда: рутениевый катализатор и лиганд Mandyphos или Josiphos, более предпочтительно [RuI2(n-цимен)]2 и лиганд Mandyphos или Josiphos, равно как и рутениевый катализатор и SL-M001-1, SL-М004-1 или SL-J002-1, наиболее предпочтительно [RuI2(n-цимен)]2 и SL-M001-1, SL-M004-1 или SL-J002-1.
В частности, предпочтительным является сочетание [RuI2(n-цимен)]2 и Mandyphos SL-M004-1.
Условия взаимодействий в способе по настоящему изобретению предпочтительно выбирают таким образом, чтобы взаимодействие осуществлялось в режиме гомогенного катализа. Как правило, термин «гомогенный катализ» обозначает режим катализа, при котором катализатор находится в той же фазе (например, твердой, жидкой и газовой), что и реагенты.
Предпочтительно способ по настоящему изобретению не осуществляют в режиме гетерогенного катализа. Как правило, термин «гетерогенный катализ» обозначает режим катализа, при котором катализатор находится в иной фазе, нежели реагенты. При гетерогенном катализе обычно задействована поверхность для протекания на ней химических реакций.
В настоящем изобретении могут быть применены растворители, общеизвестные в соответствующей области. Предпочтительно применяют растворитель, способный к растворению катализатора на основе переходного металла и хирального лиганда. Предпочтительно применяют полярный растворитель, например, одноатомный спирт. Более предпочтительно растворитель является метанолом или этанолом. Более предпочтительно применяют этанол. Количество задействуемого растворителя может быть таким, чтобы концентрация реагента находилась в диапазоне от 1 до 30% масс./об. (масса/объем), предпочтительно от 3 до 25% масс./об., более предпочтительно от 10 до 25% масс./об., наиболее предпочтительно от 20 до 25% масс./об.
В предпочтительном варианте осуществления настоящего изобретения
гидрирование осуществляют при температуре между 0°С и 80°С,
предпочтительно между комнатной температурой и 80°С, более
предпочтительно между комнатной температурой и 60°С, еще более
предпочтительно между комнатной температурой и 45°С, наиболее
предпочтительно между комнатной температурой и 35°С.
Гидрирование обычно осуществляют при температуре между 0°С и 60°С, предпочтительно между 30°С и 50°С, более предпочтительно между 35°С и 45°С.
Давление напускаемого водорода обычно находится в пределах между 5 бар и 30 бар, предпочтительно между 10 бар и 25 бар, более предпочтительно между 12 бар и 20 бар. Время взаимодействия обычно находится в пределах между 1 часом и 25 часами, более предпочтительно между 6 часами и 24 часами, еще более предпочтительно между 5 часами и 20 часами. Наиболее предпочтительно время взаимодействия обычно находится в пределах от 1 часа до 25 часов, предпочтительно от 5 часов до 20 часов.
В предпочтительном варианте осуществления настоящего изобретения давление водорода находится в пределах от 5 бар до 25 бар, предпочтительно от 5 бар до 20 бар, более предпочтительно от 10 бар до 20 бар, еще более предпочтительно от 15 до 20 бар. Наиболее предпочтительно давление водорода составляет 20 бар.
Задействуемое, как правило, в данном способе количество катализатора на основе переходного металла по отношению к субстрату (II) может находиться в пределах от 0,001 до 5 мольных %, предпочтительно от 0,001 до 1 мольного %, более предпочтительно от 0,003 до 0,3 мольного %, еще более предпочтительно от 0,005 до 0,1 мольного %, наиболее предпочтительно от 0,01 до 0,05 мольного %.
Как правило, в процессе по настоящему изобретению соотношение между субстратом и катализатором (=соотношение S/C) составляет 100 или более, предпочтительно 500 или более, более предпочтительно 1000 или более. В предпочтительном варианте осуществления настоящего изобретения верхняя граница соотношения S/C составляет 25000, более предпочтительно 30000.
В настоящем изобретении термин «соотношение между субстратом и катализатором» относится к мольному соотношению исходного соединения согласно формуле (II) или его соли и «активного катализатора» (образуемого посредством смешения катализатора на основе переходного металла и хирального лиганда).
Как правило, активный катализатор получают посредством смешения от 0,9 до 1,2, предпочтительно от 1,0 до 1,1, более предпочтительно от 1,0 до 1,05 моля хирального лиганда с 1,0 моля атомов переходного металла, содержащихся в катализаторе на основе переходного металла. Например, если задействован димерный катализатор на основе переходного металла, предпочтительно два моля хирального лиганда вводят во взаимодействие с одним молем катализатора на основе переходного металла с целью получения «активного катализатора».
Как правило, хиральный лиганд добавляют к реакционной смеси в растворе, приготовленном с тем же растворителем, что и применяемый для взаимодействия.
В способе по настоящему изобретению предпочтительно осуществляют взаимодействие с соединением согласно формуле (II) или его солью в оптически активной форме. Это означает, что в способе по настоящему изобретению соединение согласно формуле (II-а) или его соль,
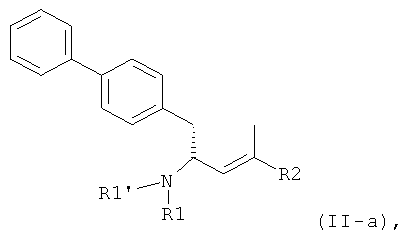
в которых R1, R1' и R2 отвечают вышеприведенным определениям, или согласно формуле (II-б) или его соль,

в которых R1, R1' и R2 отвечают вышеприведенным определениям, может быть применено в качестве исходного соединения.
Предпочтительно в качестве исходного соединения применяют соединение (II-а) или его соль. Синтез исходного соединения (II) или его соли, в котором R1 является ВОС, R1' является водородом, а R2 является COOEt, известен в соответствующей области.
Пример возможного синтеза исходного вещества (II-а) или его соли, в котором R1 является ВОС, R1' является водородом, a R2 является СООН, приведен на нижеследующей схеме реакции:

ТЕМПО - 2,2,6,6-тетраметилпиперидин-1-оксил
Если в качестве исходного соединения применяют соединение (II-а) или его соль, могут быть получены соединения согласно формуле (I-а)

и формулы (I-б) или их соли,

в которых R1, R1' и R2 отвечают вышеприведенным определениям.
Если в качестве исходного соединения применяют соединение (II-б) или его соль, могут быть получены соединения согласно формуле (I-в)

и формулы (I-г) или их соли,

в которых R1, R1' и R2 отвечают вышеприведенным определениям.
Соотношения между соединениями согласно формуле (I-а) и (I-б) и формуле (I-в) и (I-г), соответственно, или их солями зависит, как правило, от выбранных условий взаимодействия, например, от катализатора на основе переходного металла, от хирального лиганда, от соотношения S/C и/или от растворителя.
Предпочтительно в способе по настоящему изобретению получают соединения согласно формуле (I-а) или их соли.
В одном из предпочтительных вариантов осуществления способа по настоящему изобретению получают композицию, содержащую соединения согласно формулам (I-a) и (I-б) или их соли, в которой мольное соотношение между соединениями согласно формуле (I-a) или их солями и соединениями согласно формуле (I-б) или их солями составляет по крайней мере 88:12, предпочтительно выше 90:10, более предпочтительно выше 99 к 1. Наиболее предпочтительно мольное соотношение между соединениями согласно формуле (I-a) или их солями и соединениями согласно формуле (I-б) или их солями составляет по крайней мере 88:12, предпочтительно от 90:10 до 99,9:0,1. В предпочтительном варианте осуществления способ по настоящему изобретению приводит к соединениям согласно формулам (I-a) и (I-б) или их солям, в которых R1 и R1' независимо являются водородом или защитной группой для аминогруппы, a R2 является СООН.
Как следствие, еще одним объектом настоящего изобретения является смесь, содержащая соединения согласно формулам (I-a) и (I-б) или их соли, в которой мольное соотношение между (I-a) и (I-б) составляет по крайней мере 88:12, предпочтительно выше 90:10, более предпочтительно выше 99 к 1. Наиболее предпочтительно смесь содержит согласно формулам (I-a) и (I-б) или их соли с мольным соотношением между (I-a) и (I-б), по крайней мере, 88:12, предпочтительно от 90:10 до 99,9:0,1. В предпочтительном варианте осуществления настоящего изобретения смесь содержит соединения согласно формулам (I-a) и (I-б) или их соли, в которых R1 и R1' независимо являются водородом или защитной группой для аминогруппы, а R2 является СООН.
В одном из предпочтительных вариантов осуществления способа по настоящему изобретению получают композицию, содержащую соединения согласно формулам (I-a) и (I-б) или их соли, в которой:
- мольное соотношение между соединениями согласно формуле (I-a) или их солями и соединениями согласно формуле (I-б) или их солями составляет по крайней мере 88:12, предпочтительно по крайней мере 90:10, более предпочтительно по крайней мере 99 к 1,
- сочетания катализатора на основе переходного металла и хирального лиганда отвечают вышеописанным, предпочтительно: родиевый катализатор и лиганд Mandyphos, Walphos, Josiphos или Solphos, более предпочтительно Rh(nbd)2BF4 и лиганд Mandyphos, Walphos, Josiphos или Solphos, еще более предпочтительно родиевый катализатор и лиганд Walphos, еще более предпочтительно родиевый катализатор и Walphos SL-W008-1, наиболее предпочтительно Rh(nbd)2BF4 и Walphos SL-W008-1.
В другом предпочтительном варианте осуществления способа по настоящему изобретению получают композицию, содержащую соединения согласно формулам (I-a) и (I-б) или их соли, в которой:
- мольное соотношение между соединениями согласно формуле (I-a) или их солями и соединениями согласно формуле (I-б) или их солями составляет по крайней мере 88:12, предпочтительно по крайней мере 90:10, более предпочтительно по крайней мере 99 к 1,
- сочетания катализатора на основе переходного металла и хирального лиганда отвечают вышеописанным, предпочтительно: рутениевый катализатор и лиганд Mandyphos или Josiphos, более предпочтительно [RuI2(n-цимен)]2 и лиганд Mandyphos или Josiphos, еще более предпочтительно, рутениевый катализатор и SL-M001-1, SL-M004-1 или SL-J002-1, еще более предпочтительно, [RuI2(n-цимен)]2 и SL-M001-1, SL-M004-1 или SL-J002-1, наиболее предпочтительно, [RuI2(n-цимен)]2 и SL-M001-1 или SL-M004-1.
В одном из вариантов осуществления способа по настоящему изобретению получают композицию, содержащую соединения согласно формулам (I-a) и (I-б) или их соли, в которой:
- мольное соотношение между соединениями согласно формуле (I-б) или их солями и соединениями согласно формуле (I-a) или их солями составляет по крайней мере 65:35, более предпочтительно по крайней мере 73:27, наиболее предпочтительно по крайней мере 94 к 6.
В предпочтительном варианте осуществления способа по настоящему изобретению получают композицию, содержащую соединения согласно формулам (I-a) и (I-б) или их соли, в которой:
- мольное соотношение между соединениями согласно формуле (I-б) или их солями и соединениями согласно формуле (I-a) или их солями составляет по крайней мере 65:35, более предпочтительно по крайней мере 73:27, наиболее предпочтительно по крайней мере 94 к 6.
- сочетания катализатора на основе переходного металла и хирального лиганда отвечают вышеописанным, предпочтительно: родиевый катализатор и лиганд Mandyphos, Walphos, Josiphos или Solphos, более предпочтительно Rh(nbd)2BF4 и лиганд Mandyphos, Walphos, Josiphos или Solphos, еще более предпочтительно родиевый катализатор и Mandyphos SL-M004-1, Josiphos SL-J003-1, Josiphos SL-J009-1, Walphos SL-W001-2, Walphos SL-W003-1, или Solphos SL-A001-1, еще более предпочтительно Rh(nbd)2BF4 и Mandyphos SL-M004-1, Josiphos SL-J003-1, Josiphos SL-J009-1, Walphos SL-W001-2, Walphos SL-W003-1, или Solphos SL-A001-1, наиболее предпочтительно Rh(nbd)2BF4 и Mandyphos SL-M004-1, Walphos SL-W001-2 или Solphos SL-A001-1.
В другом предпочтительном варианте осуществления способа по настоящему изобретению получают композицию, содержащую соединения согласно формулам (I-a) и (I-б) или их соли, в которой:
- мольное соотношение между соединениями согласно формуле (I-б) или их солями и соединениями согласно формуле (I-a) или их солями составляет по крайней мере 65:35, более предпочтительно по крайней мере 73:27, наиболее предпочтительно по крайней мере 94 к 6.
- сочетания катализатора на основе переходного металла и хирального лиганда отвечают вышеописанным, предпочтительно: рутениевый катализатор и лиганд Mandyphos или Josiphos, более предпочтительно [RuI2(n-цимен)]2 и лиганд Mandyphos или Josiphos, еще более предпочтительно рутениевый катализатор и лиганд Mandyphos, еще более предпочтительно рутениевый катализатор и SL-M002-1 или SL-M004-2, еще более предпочтительно [RuI2(n-цимен)]2 и SL-M002-1 или SL-M004-2, наиболее предпочтительно [RuI2(n-цимен)]2 и SL-M004-2.
В одном из вариантов осуществления способа по настоящему изобретению получают композицию, содержащую соединения согласно формулам (I-в) и (I-г) или их соли, в которой
- мольное соотношение между соединениями согласно формуле (I-в) или их солями и соединениями согласно формуле (I-г) или их солями составляет по крайней мере 88: 12, предпочтительно выше 90:10, более предпочтительно по крайней мере 92:8.
В предпочтительном варианте осуществления способа по настоящему изобретению получают композицию, содержащую соединения согласно формулам (I-в) и (I-г) или их соли, в которой
- мольное соотношение между соединениями согласно формуле (I-в) или их солями и соединениями согласно формуле (I-г) или их солями составляет по крайней мере 88:12, предпочтительно выше 90:10, более предпочтительно по крайней мере 92:8,
- сочетания катализатора на основе переходного металла и хирального лиганда отвечают вышеописанным, предпочтительно: рутениевый катализатор и лиганд Mandyphos или Josiphos, более предпочтительно [RuI2(n-цимен)]2 и лиганд Mandyphos или Josiphos, еще более предпочтительно рутениевый катализатор и лиганд Mandyphos, еще более предпочтительно рутениевый катализатор и SL-M004-1, наиболее предпочтительно, [RuI2(n-цимен)]2 и SL-М004-1.
Способ по настоящему изобретению может включать дополнительную необязательную стадию, на которой соединения согласно формуле (I-a) или их соли выделяют из вышеописанной смеси посредством кристаллизации.
В предпочтительном варианте осуществления стадии кристаллизации смесь, содержащую соединения согласно формулам (I-a) и (I-б) или их соли [предпочтительно с мольным соотношением между (I-a) и (I-б) по крайней мере 88:12] растворяют в подходящем полярном первом растворителе, например в одноатомном спирте, предпочтительно этаноле, или в сложном эфире, предпочтительно изопропилацетате. В другом варианте осуществления вслед за этим может быть добавлен подходящий менее полярный второй растворитель. Предпочтительно в качестве второго растворителя применяют углеводороды, например гептан. Таким образом, предпочтительная система, включающая первый и второй растворители, является смесью изопропилацетата и гептана.
Стадия кристаллизации приводит к соединениям соединения согласно формуле (I-a) или их солям в кристаллической форме. Поэтому объектом настоящего изобретения являются соединения или их соли согласно формуле (I-а) в кристаллической форме. Кроме того, объектом настоящего изобретения также являются соединения или их соли согласно формулам (I-б), (I-в) и (I-г) в кристаллической форме.
В предпочтительном варианте осуществления настоящего изобретения кристаллические продукты по настоящему изобретению образуют кристаллы моноклинной сингонии. Также является предпочтительным, если кристаллические продукты по настоящему изобретению характеризуются пространственной группой симметрии P21. В предпочтительном варианте осуществления настоящего изобретения кристаллические продукты по настоящему изобретению характеризуются следующими параметрами элементарной ячейки, измеренными при температуре 100 К:
Как правило, те же самые предпочтительные варианты осуществления, что и описанные выше для способа по настоящему изобретению, применимы ко всем соединениям и смесям по настоящему изобретению. Это, в частности, относится к остаткам R1, R1' и R2 формул (I) и (II) способа по настоящему изобретению.
Таким образом, предпочтительными являются соединения согласно формуле (I-a) или их соли в кристаллической форме, в которых R2 является СООН или RCOOEt, в частности, в которых R2 является СООН. Кроме того, R1 предпочтительно является ВОС, а R1' предпочтительно является водородом.
Помимо этого объектом настоящего изобретения являются соединения согласно формуле (I-a)

или их соли, в которых R1 и R1' независимо являются водородом или защитной группой для аминогруппы, а R2 является карбоксильной группой или сложноэфирной группой при том условии, что R2 не является COOEt, когда R1 является ВОС, а R1' является водородом. Предпочтительно R2 является СООН.
Кроме того, объектом настоящего изобретения являются соединения согласно формулам (I-б), (I-в) и/или (I-г) или их соли, в которых R1 и R1' независимо являются водородом или защитной группой для аминогруппы, а R2 является карбоксильной группой или сложноэфирной группой. Предпочтительно R2 является СООН или COOEt, более предпочтительно R2 является СООН.
Продукты способа по настоящему изобретению могут быть применены в синтезе ингибиторов НЭП или их пролекарств, в частности они могут быть применены в синтезе ингибиторов НЭП, содержащих в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты.
Термин «ингибитор НЭП» описывает соединение, ингибирующее активность фермента нейтральной эндопептидазы (НЭП, ЕС 3.4.24.11).
Термин «пролекарство» описывает фармакологическое вещество, которое вводят в неактивной (или менее активной) форме. После ведения пролекарство метаболизируется в организме in vivo в активное соединение.
Таким образом, вариант осуществления способа по настоящему изобретению включает одну или более дополнительную стадию, на которых соединение согласно формуле (I) или его соль дополнительно вводят во взаимодействие с целью получения ингибитора НЭП или его пролекарства, в частности ингибитора НЭП или его пролекарства, содержащего в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты.
В настоящем изобретении термин «ингибитор НЭП» или «пролекарство ингибитора НЭП» относится к веществам как таковым или к их солям, предпочтительно к их фармацевтически приемлемым солям. Примерами являются соли натрия, калия, магния, кальция или аммония. Предпочтительными являются соли кальция.
Предпочтительно соединения согласно формуле (I-a) или их соли вводят в дальнейшее взаимодействие с целью получение ингибитора НЭП или его пролекарства, в частности ингибитора НЭП или его пролекарства, содержащего в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты. Особенно предпочтительным является соединение согласно формуле (I-a) или его соль, в котором R1 является ВОС, R1' является водородом, a R2 является СООН.
В предпочтительном варианте осуществления настоящего изобретения соединение согласно формуле (I-a) или его соль вводят в дополнительное взаимодействие с целью получения пролекарства ингибитора НЭП - этилового эфира N-(3-карбокси-1-оксопропил)-(4S)-n-фенилфенилметил)-4-амино-(2R)-метилбутановой кислоты (известной в соответствующей области как AHU 377) или его соли.
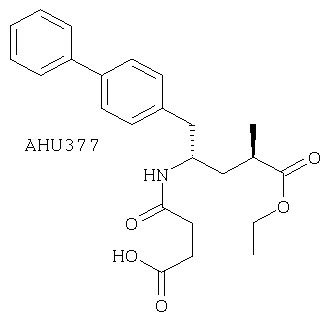
В целом, настоящее изобретение включает в свой объем любую фармацевтически приемлемую соль этилового эфира N-(3-карбокси-1-оксопропил)-(4S)-n-фенилфенилметил)-4-амино-(2R)-метилбутановой кислоты, среди которых предпочтительной является соль кальция.
Пролекарство ингибитора НЭП этиловый эфир N-(3-карбокси-1-оксопропил)-(4S)-n-фенилфенилметил)-4-амино-(2R)-метилбутановой кислоты необязательно вводят в дальнейшее взаимодействие с целью получения активного ингибитора НЭП N-(3-карбокси-1-оксопропил)-(4S)-n-фенилфенилметил)-4-амино-(2R)-метилбутановой кислоты.
В предпочтительном варианте осуществления настоящего изобретения синтез этилового эфира N-(3-карбокси-1-оксопропил)-(4S)-n-фенилфенилметил)-4-амино-(2R)-метилбутановой кислоты начинается с соединения согласно формуле (I-a) или его соли. Предпочтительно синтез начинается с соединения формулы (I-a), в котором R1 предпочтительно является ВОС, R1' предпочтительно является водородом, а R2 предпочтительно является СООН. Предпочтительно данные взаимодействия включают следующие стадии:
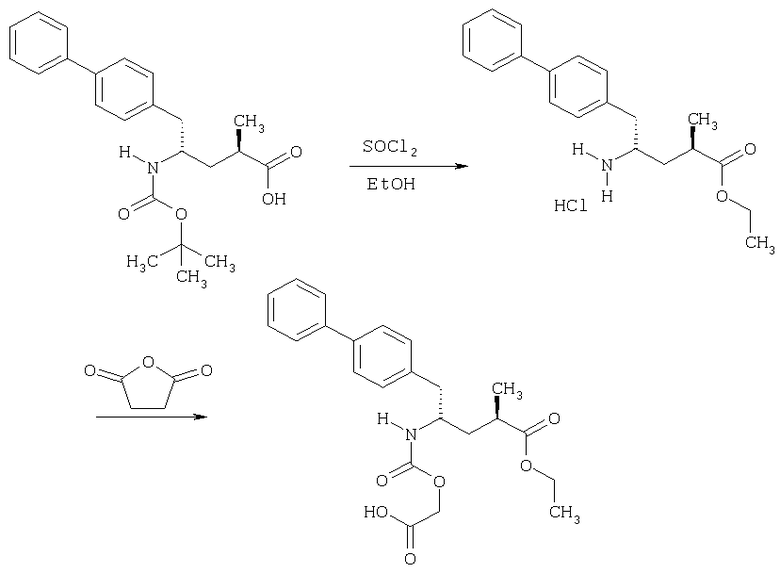
и необязательно следующие дополнительные стадии:

Как описано выше, способ по настоящему изобретению может быть применен в синтезе ингибиторов НЭП или их пролекарств, в частности ингибиторов НЭП или их пролекарств, содержащего в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты. Таким образом, еще одним объектом настоящего изобретения является применение катализатора на основе переходного металла и хирального лиганда в синтезе ингибитора НЭП или его пролекарства, в частности ингибитора НЭП или его пролекарства, содержащего в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты, где переходный металл выбран из групп 7, 8 или 9 периодической системы.
В целом, те же самые предпочтительные варианты осуществления, что и обсужденные выше для способа по настоящему изобретению, относятся к применению по настоящему изобретению. Это, в частности, относится к описанию, касающемуся предпочтительных катализаторов на основе переходных металлов, хиральных лигандов и их сочетаний.
Предпочтительно катализатор на основе переходного металла и хиральный лиганд применяют на стадии гидрирования в синтезе ингибитора НЭП, в частности ингибитора НЭП или его пролекарства, содержащего в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты. В предпочтительном варианте осуществления настоящего изобретения стадия гидрирования приводит к двум диастереомерам с диастереомерным соотношением по крайней мере 88:12, более предпочтительно от 90:10 до 99,9:0,1. В предпочтительном варианте осуществления настоящего изобретения стадия гидрирования приводит к двум диастереомерам согласно формулам (I-a) и (I-б) с диастереомерным соотношением по крайней мере 88:12, более предпочтительно от 90:10 до 99,9:0,1. В другом предпочтительном варианте осуществления настоящего изобретения стадия гидрирования приводит к двум диастереомерам соединений согласно формулам (I-a) и (I-б) или их солей, в которых R1 и R1' отвечают вышеприведенным определениям, с диастереомерным соотношением по крайней мере 88:12, предпочтительно по крайней мере 90:10, более предпочтительно по крайней мере 99:1.
В другом предпочтительном варианте осуществления настоящего изобретения катализатор на основе переходного металла и хиральный лиганд, как они определены выше, применяют в синтезе пролекарства ингибитора НЭП этилового эфира N-(3-карбокси-1-оксопропил)-(4S)-n-фенилфенилметил)-4-амино-(2R)-метилбутановой кислоты или его соли.
Общие определения употребляемы выше и ниже имеют, если иное не оговорено специально, нижеследующие значения.
Алкил, как радикал или часть радикала, является неразветвленной или разветвленной (один или, если то желаемо и возможно, более раз) углеродной цепью, в особенности (С1-С7)алкилом, в частности (С1-С4)алкилом.
Термин «(C1-C7)» определяет остаток, содержащий до 7 атомов углерода включительно, в особенности до 4 атомов углерода включительно, причем таковой остаток является разветвленным (один или более раз) или неразветвленным и присоединен через концевой или неконцевой атом углерода.
Арил является, например, (С6-С10)арилом предпочтительно является моно- или полициклическим, в особенности моноциклическим, бициклическим или трициклическим арильным остатком, содержащим от 6 до 10 атомов углерода.
Незамещенный или замещенный гетероциклил является моно- или полициклической, предпочтительно моно-, би- или трициклической, наиболее предпочтительно моноциклической, ненасыщенной, частично насыщенной, насыщенной или ароматической системой циклов, предпочтительно содержащей от 3 до 22 (более предпочтительно от 3 до 14) кольцевых атомов и содержащая один или более предпочтительно от одного до четырех, гетероатомов, независимо выбранных из азота, кислорода, серы, S(=O)- или S-(=O)2, и является незамещенным или замещенным одним или более заместителями, например числом до трех, предпочтительно независимо выбранными из заместителей, упомянутых выше для циклоалкила. Если гетероциклил является ароматической системой циклов, он также именуется гетероарилом.
Галоид или галоген предпочтительно является фтором, хлором, бромом или иодом, наиболее предпочтительно фтором, хлором или бромом.
Галоидалкил является, например, галоид(С1-С7)алкилом, в частности галоид(С1-С4)алкилом, таким как трифторметил, 1,1,2-трифтор-2-хлорэтил или хлорметил. Предпочтительный галоид(С1-С7)алкил является трифторметилом.
Алкоксигруппа является, например, (С1-С7)алкоксигруппой и является, например, метоксигруппой, этоксигруппой, н-пропилоксигруппой, изопропилоксигруппой, н-бутилоксигруппой, изобутилоксигруппой, втор-бутилоксигруппой, трет-бутилоксигруппой, включая также соответствующие пентилоксигруппы, гексилоксигрупы и гептилоксигруппы. Предпочтительной является (С1-С4)алкоксигруппа.
Алканоил является, например, (С2-С7)алканоилом и является, например, ацетилом [-С(=O)Ме], пропионилом, бутирилом, изобутирилом или пивалоилом. Предпочтительным является (С2-С5)алканоил, в особенности ацетил.
Ацетил является -С(=O)(С1-С7)алкилом, предпочтительно -С(=O)Ме.
Алкоксиалкил может быть линейным или разветвленным. Алкоксигруппа предпочтительно содержит от 1 до 4, в особенности 1 или 2 атома углерода, а алкильная группа предпочтительно содержит от 1 до 4 атомов углерода. Примерами являются метоксиметил, 2-метоксиэтил, 3-метоксипропил, 4-метоксибутил, 5-метоксипентил, 6-метоксигексил, этоксиметил, 2-этоксиэтил, 3-этоксипропил, 4-этоксибутил, 5-этоксипентил, 6-этоксигексил, пропилоксиметил, бутилоксиметил, 2-пропилоксиэтил и 2-бутилоксиэтил.
Силил является группой -SiRR'R”, в которой R, R' и R” независимо друг от друга являются (С1-С7)алкилом, арилом или фенил(С1-С4)алкилом.
Сульфонильная группа является (С1-С7)алкилсульфонильной группой, такой как метилсульфонильная группа, (фенил- или нафтил)-(С1-С7)алкилсульфонильной группой, такой как фенилметансульфонильная группа, [(С1-С7)алкил-, фенил-, галоид(С1-С7)алкил-, галоид-, оксо(С1-С7)алкил-, (С1-С7)алкилокси-, фенил(С1-С7)алкокси, галоид(С1-С7)алкилокси-, фенокси-, (С1-С7)алканоиламино-, (С1-С7)алкилсульфонил-, циано- и/или (С1-С7)алкилсульфонил-]-(моно-, ди- или три-)замещенной) (фенил- или нафтил)-(С1-С7)алкилсульфонильной группой или (незамещенной или [(С1-С7)алкил-, фенил-, галоид(низш.)алкил-, галоид-, оксо(С1-С7)алкил-, (С1-С7)алкилокси-, фенил(С1-С7)алкокси, галоид(С1-С7)алкилокси-, фенокси-, (С1-С7)алканоиламино-, (С1-С7)алкилсульфонил-, циано- и/или (С1-С7)алкилсульфонил-]-(моно-, ди- или три-)замещенной) (фенил- или нафтил)-сульфонильной группой, в которой заместители, если их наличествует более одного, независимо выбраны из упомянутых. Особенно предпочтительными являются (С1-С7)алкилсульфонильная группа, такая как метилсульфонильная группа, и (фенил- или нафтил)-(С1-С7)алкилсульфонильная группа, такая как фенилметансульфонильная группа.
Сульфенильная группа является (незамещенной или замещенной) (С6-С10)арил(С1-С7)алкилсульфенильной группой или (незамещенной или замещенной) (С6-С10)арилсульфенильной группой, в которой заместители, если их наличествует более одного, например от одного до четырех заместителей, независимо выбраны из нитрогруппы, галоида, галоид(С1-С7)алкила и (С1-С7)алкилоксигруппы.
Алкенил может являться линейным или разветвленным алкилом, содержащим двойную связь и предпочтительно включающим от 2 до 12 атомов углерода, особенно предпочтительно от 2 до 8 атомов углерода. Особенно предпочтительным является линейный (С2-С4)алкенил. Некоторыми из примеров алкильных групп являются этил и изомеры пропила, бутила, пентила, гексила, гептила, октила, нонила, децила, ундецила, додецила, тетрадецила, гексадецила октацила и эйкозила, каждый из которых содержит двойную связь, особенно предпочтительным является аллил.
Соли являются, в особенности, фармацевтически приемлемыми солями или, в общем случае, солями любого из упоминаемых в контексте промежуточных соединений, если только соли не исключаются по причинам химического свойства, как то должно быть понятно специалисту в соответствующей области. Они могут быть образованы в случае присутствия солеобразующих групп, таких как кислотные группы или основные группы, хотя бы частично способных к существованию в диссоциированной форме, например в диапазоне рН от 4 до 10 в водных растворах, или могут быть выделены, в особенности, в твердом, в особенности, в кристаллическом виде.
Подобные соли образуются из соединений или любых упоминаемых в контексте промежуточных соединений, содержащих основный атом азота (например, имино- или аминогруппу), например, в форме кислотно-аддитивных солей, предпочтительно с органическими или неорганическими кислотами, в особенности, как фармацевтически приемлемые соли. Подходящими неорганическими кислотами являются, например, галоидводородные кислоты, такие как соляная кислота, серная кислота или фосфорная кислота. Подходящими органическими кислотами являются, например, карбоновые кислоты, фосфокислоты, сульфокислоты или сульфаминовые кислоты, например уксусная кислота, пропионовая кислота, молочная кислота, фумаровая кислота, янтарная кислота, лимонная кислота, аминокислоты, такие как глутаминовая кислота или аспартамовая кислота, малеиновая кислота, гидроксималеиновая кислота, метилмалеиновая кислота, бензойная кислота, метан- или этансульфокислота, этан -1,2-дисульфокислота, бензолсульфокислота, 2-нафталинсульфокислота, 1,5-нафталиндисульфокислота, N-циклогексилсульфаминовая кислота, N-метил-, N-этил- или N-пропилсульфаминовая кислота или другие органические протонные кислоты, такие как аскорбиновая кислота.
В присутствии отрицательно заряженных радикалов, таких как карбоксильная группа или сульфогруппа, соли могут также быть образованы с основаниями, как, например, соли металлов или аммония, такие как соли щелочных металлов или щелочноземельных металлов, например соли натрия, калия, магния или кальция или соли аммония с аммиаком или подходящими органическими аминами, такими как третичные моноамины, например, триэтиламин или три(2-гидроксиэтил)амин, или гетероциклическими основаниями, например, N-этилпиперидином или N,N'-диметилпиперазином.
Если в одной и той же молекуле присутствуют кислотная группа и основная группа, любое из упомянутых в контексте промежуточных соединений может также образовывать внутренние соли.
Для целей выделения или очистки любого из упомянутых в контексте промежуточных соединений возможно также использование фармацевтически неприемлемых солей, например, пикратов или перхлоратов.
Ввиду тесного родства между соединениями и промежуточными веществами в свободной форме и в форме их солей, включая те соли, которые могут быть применены в качестве промежуточных веществ, например, для очистки или идентификации соединений или их солей, следует понимать, что любое выше- или нижеприведенное упоминание «соединений», «исходных веществ» и «промежуточных соединений» равно относится и к одной или более их соли или смеси соответствующего соединения, промежуточного соединения или исходного вещества в свободной форме и одной или более его соли, причем подразумевается, что каждое из упомянутого также включает любой сольват или соль любого или любых из них, как то будет уместно и целесообразно, если иное не оговорено специально. Могут быть получены разные кристаллические формы, которые, таким образом, также включены сюда.
Если для соединений, исходных веществ, промежуточных соединений, солей, фармацевтических препаратов, заболеваний, расстройств и тому подобного употреблена форма множественного числа, следует понимать, что имеется в виду одно (предпочтительное) или более отдельное соединение(соединения), соль(соли), фармацевтический препарат(препараты), заболевание(заболевания), расстройство (расстройства) и тому подобное, если же употребляется форма единственного числа или неопределенный артикль, это лишь предпочтительно подразумевает единственность, но не исключает множественности.
Настоящее изобретение проиллюстрировано нижеследующими примерами.
Примеры
Пример 1: (E)-(R)-5-бифенил-4-yl-4-трет-бутоксикарбониламино-2-метилпент-2-еновая кислота

Этиловый эфир (Е)-(R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпент-2-еновой кислоты (CAS #149709-59-1) гидролизуют с помощью гидроксида лития в этаноле, что приводит к (E)-(R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпент-2-еновой кислоте в виде твердого вещества белого цвета. δН (400 МГц; ДМСО (диметилсульфоксид)) 1,31 (9Н, s, (СН3)3), 1,59 (3Н, s, 1-СН3), 2,68 (1Н, dd, J 6,8, 13,2, 5-HA), 2,86 (1Н, m, 5-HB), 4,44 (1Н, m, 4-H), 6,51 (1Н, d, J 79,2, 3-H), 7,16 (1Н, d, J 8,0, NH), 7,26 (2H, d, J 78,0, Ar-орто-H(Ph)), 7,31 (1Н, t, J 7,6, Ar-(Ph)-пара-H), 7,40 (2H, t, J 8,0, Ar-(Ph)-мета-H), 7,54 (2H, d, J 8,0, Ar-мета-H(Ph), 7,60 (2H, d, J 7,6, Ar-(Ph)-орто-H), 12,26 (1Н, s, СО2Н); m/z (+ИЭР (ионизация электрораспылением)) 404 ([MNa]+, 17%), 382 ([MH]+, 2), 326 (10), 264 (100), 167 (13).
Пример 2: (2R,4S)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпентановая кислота в кристаллической форме [2(I-а)]

К суспензии (E)-(R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпент-2-еновой кислоты [2(II-а)] (200 г, 524,3 ммоля) в обезгаженном этаноле (900 мл) добавляют при температуре 40°С раствор димера дииод(и-цимен)рутения(II) (0,052 г, 0,0524 ммоля) и (αR,αR')-2,2'-бис(α-N,N-диметиламинофенилметил)-(5,5)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфин]ферроцена (=Mandyphos SL-M004-1) (0,116 г, 0,110 ммоля) в обезгаженном этаноле (100 мл). Раствор обезгаживают под вакуумом и напускают водород с давлением 20 бар. Смесь перемешивают при температуре 40°С в течение 6 часов. После этого сосуд продувают водородом. Удаляют этанол (700 мл) посредством отгонки. Добавляют изопропилацетат (600 мл). Удаляют растворитель (600 мл) посредством отгонки. Добавляют изопропилацетат (600 мл). Удаляют растворитель (600 мл) посредством отгонки. Добавляют изопропилацетат (300 мл) и кипятят раствор с обратным холодильником. Добавляют фракцию гептанов (1200 мл) и охлаждают смесь до комнатной температуры. Твердое вещество собирают посредством фильтрования и промывают смесью фракции гептанов и изопропилацетата 2:1 (360 мл). Твердое вещество сушат в течение ночи при температуре 50°С под вакуумом (при давлении 1-50 мбар), что приводит к указанному в заглавии соединению в виде белого/грязно-белого твердого вещества [Соотношение 2(I-a):2(I-б) 99:1, по данным анализа методом высокоэффективной жидкостной хроматографии (ВЭЖХ)]. tпл. 146-147°С; δН (500 МГц; ДМСО) 1,07 (3Н, d, J 7,0, 1-СН3), 1,34 (9Н, s, (СН3)3), 1,38 (1Н, m, 3-НА), 1,77 (1Н, m, 3-НВ), 2,43 (1Н, m, 2-Н), 2,70 (2Н, d, J 7,0, 5-Н), 3,69 (1Н, m, 4-Н), 6,74 (1Н, d, J 9,0, NH), 7,27 (2Н, d, J 8,0, Ar-орто-H(Ph)), 7,36 (1Н, t, J7,0, Ar-(Ph)-пара-H), 7,46 (2Н, t, J 7,5, Ar-(Ph)-мета-Н), 7,57 (2Н, d, J 8,0, Ar-мета-H(Ph), 7,64 (2Н, d, J 7,5, Ar-(Ph)-орто-H), 12,01 (1H, s, CO2H); 8 с (500 МГц, ДМСО) 18,1 (1-СН3), 28,3 [(СН3)3], 35,9 (2-С), 37,9 (3-С), 40,7 (5-С), 50,0 (4-С), 77,4 [(С(СН3)3], 126,3, 126,5, 127,2, 128,9, 129,8 (Ar-CH), 137,7 (Ar-unco-C(Ph)), 138,3 (Ar-пара-C(Ph)), 140,1 (Ar-(Ph)-unco-С), 155,2 (NCO), 177,2 (CO2H); m/z (+ИЭР) 406 ([MNa]+, 6%), 384 ([MH]+, 31), 328 (100), 284 (19); найдено: [МН]+, 384,21691. C23H30N4 требует МП 384,21693.
На фигуре 1 представлена структура кристаллической (2R,4S)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпентановой кислоты, определенная с помощью рентгенодиффракционного анализа. Кристаллы характеризуются следующими параметрами элементарной ячейки, измеренными при температуре 100 К:
Альтернативные методики (способы 1-5) получения 2(I-a)
Общая методика для способов 1-5
К суспензии (Е)-(R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпент-2-еновой кислоты [2(II-а)] (300 мг, 0,79 ммоля) в обезгаженном этаноле или метаноле (6 мл) добавляют при комнатной температуре раствор катализатора на основе переходного металла (соотношение S/C 100) и хирального лиганда (соотношение S/C 100; 1,05 экв. по отношению к металлу) в обезгаженном этаноле или метаноле (4 мл). Раствор обезгаживают под вакуумом и напускают водород при давлении 10 или 15 в течение 24 часов. После этого растворитель отгоняют под вакуумом, что приводит к соответствующему продукту.
Способ 1: Хиральный лиганд {(R)-1-[(R)-2-(2'-дициклогексилфосфинофенил)ферроценил]этилди(бис(3,5-трифторметил)фенил)фосфин = SL-W008-1}; катализатора на основе переходного металла {тетрафторборат бис(норборнадиен)родия(1)}; МеОН; 15 бар; соотношение 2(I-a):2(I-б) 89:11 (по данным ВЭЖХ-анализа).
Способ 2: Хиральный лиганд {(R)-1-[(R)-2-(2'-дициклогексилфосфинофенил)ферроценил]этилди(бис(3,5-трифторметил)фенил)фосфин = SL-W008-1}; катализатор на основе переходного металла {тетрафторборат бис(норборнадиен)родия(1)}; МеОН; 10 бар; соотношения 2(I-a):2(I-б) 89:11 (по данным ВЭЖХ-анализа).
Способ 3: Хиральный лиганд {(R)-1-[(S)-2-дифенилфосфино)ферроценил]этилди-трет-бутилфосфин = SL-J002-1}; катализатор на основе переходного металла {димер дииод(n-цимен)рутения(II)}; EtOH; 15 бар; соотношение 2(I-a):2(I-б) 90:10 (по данным ВЭЖХ-анализа).
Способ 4: Хиральный лиганд {(αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(5,5)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфин]ферроцен = SL-M004-1}; катализатор на основе переходного металла {димер дииод(n-цимен)рутения(II}; EtOH; 15 бар; соотношение 2(I-a):2(I-б) 99:1 (по данным ВЭЖХ-анализа).
Способ 5: Хиральный лиганд {(αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(5,5)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен = SL-M001-1}; катализатор на основе переходного металла {димер дииод(n-цимен)рутения(II)}; EtOH; 15 бар; соотношение 2(I-a):2(I-б) 98:2 (по данным ВЭЖХ-анализа).
(2S,4S)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпентановая кислота [2(I-б)]

К суспензии (E)-(R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпент-2-еновой кислоты [2(II-а)] (10 г, 26,1 ммоля) в обезгаженном этаноле (90 мл) добавляют порциями в продолжение всех 5 суток взаимодействия раствор димер дииод(n-цимен)рутения(II) (0,156 г, 0,16 ммоля) и (αS,αS)-2,2'-бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфин]ферроцена (=Mandyphos SL-M004-2) (0,348 г, 0,33 ммоля) в обезгаженном этаноле (30 мл). Раствор обезгаживают под вакуумом и напускают водород при давлении 5,5 бар. Смесь нагревают до температуры 60°С и перемешивают при данной температуре в течение 5 суток. После этого сосуд продувают азотом. Растворитель отгоняют под вакуумом. Получаемое таким образом твердое вещество растворяют в изопропилацетате (34 мл) и кипятят с обратным холодильником. Добавляют фракцию гептанов (68 мл) и охлаждают смесь до комнатной температуры. Твердое вещество собирают посредством фильтрования и промывают смесью гептана и изопропилацетата 2:1 (20 мл). Твердое вещество сушат в течение ночи при температуре 50°С под вакуумом (давление 1-50 мбар), что приводит к указанному в заглавии соединению [соотношение 2(I-a):2(I-б) 6:94, по данным ВЭЖХ-анализа] в виде твердого вещества серого цвета. δН (500 МГц; ДМСО) 1,06 (3Н, d, J 7,0, 1-СН3), 1,32 (9Н, s, (СН3)3), 1,42 (1Н, m, 3-НА), 1,78 (1Н, m, 3-НВ), 2,39 (1Н, m, 2-Н), 2,73 (2Н, d, J 7,0, 5-Н), 3,73 (1Н, m, 4-Н), 6,75 (1Н, d, J 9,5, NH), 7,29 (2H, d, J 8,0, Ar-орто-H(Ph)), 7,35 (1Н, t, J 7,0, Ar-(Ph)-пара-H), 7,46 (2H, t, J 7,5, Ar-(Ph)-мета-H), 7,57 (2H, d, J 8,0, Ar-мета-H(h)), 7,64 (2H, d, J 7,5, Ar-(Ph)-орто-H), 12,01 (1Н, s, СО2Н); δС (500 МГц, ДМСО) 16,2 (1-СН3), 28,2 [(СН3)3], 35,7 (2-С), 37,9 (3-С), 40,7 (5-С), 49,2 (4-С), 77,4 [(С(СН3)3], 126,3, 126,5, 127,2, 128,9, 129,7 (Ar-CH), 137,8 (Ar-unco-C(Ph)), 138,4 (Ar-пара-C(Ph)), 140,1 (Ar-(Ph)-unco-С), 155,3 (NCO), 177,6 (CO2H); m/z (+ИЭР) 406 ([MNa]+, 4%), 384 ([MH]+, 44), 328 (100), 284 (22); найдено: [MH]+, 384,21696, C23H30NO4 требует МН 384,21693.
(2S,4S)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпентановая кислота [2(I-б)] (способ 2)
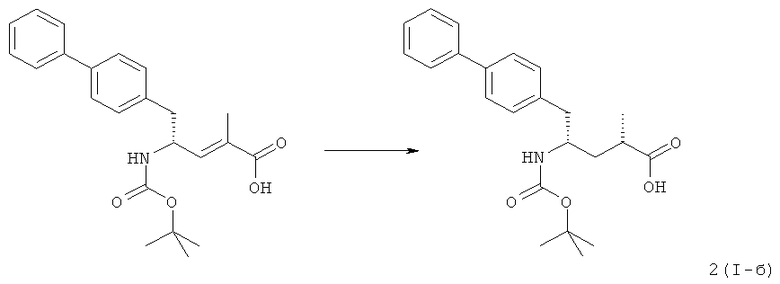
К суспензии (Е)-(R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпент-2-еновой кислоты [2(II-а)] (20 г, 52 ммоля) в обезгаженном этаноле (100 мл) добавляют раствор димера дииод(n-цимен)рутения(II) (0,215 г, 0,22 ммоля) и (αS,αS)-2,2'-бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфин]ферроцена (=Mandyphos SL-M004-2) (0,50 г, 0,47 ммоля) в обезгаженном этаноле (15 мл). Раствор обезгаживают под вакуумом и напускают водород при давлении 20 бар. Смесь перемешивают при температуре 25°С в течение 15 часов. Затем сосуд продувают азотом. Растворитель отгоняют под вакуумом. Получаемое таким образом твердое вещество сушат в течение ночи при температуре 50°С под вакуумом (давление 1-50 мбар), что приводит к указанному в заглавии соединению [соотношение 2(I-a):2(I-б) 7:93, по данным ВЭЖХ-анализа].
Альтернативные методики (способы 1'-8') получения 2(I-б):
Общая методика для способов 1'-8'
К суспензии (Е)-(R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпент-2-еновой кислота [2(II-а)] (300 мг, 0,79 ммоля) в обезгаженном этаноле или метаноле (6 мл) при комнатной температуре добавляют раствор катализатора на основе переходного металла (соотношение S/C 100) и хирального лиганда (соотношение S/C 100; 1,05 экв. по отношению к металлу) в обезгаженном этаноле или метаноле (4 мл). Раствор обезгаживают под вакуумом и напускают водород при давлении 15 бар в течение 24 часов. После этого отгоняют растворитель под вакуумом, что приводит к соответствующему продукту.
Способ 1': Хиральный лиганд {(R)-N,N'-диметил-7,7'-бис(дифенилфосфино)-3,3',4,4'-тетрагидро-8,8'-би-2H-1,4-бензоксазин = Solphos SL-A001-1}; катализатор на основе переходного металла {тетрафторборат бис(норборнадиен)родия(I)}; МеОН; 15 бар; соотношение 2(I-a):2(I-б) 26:74 (по данным ВЭЖХ-анализа).
Способ 2': Хиральный лиганд {(R)-1-[(S)-2-дициклогексилфосфино)ферроценил]этилдициклогексилфосфин = SL-J003-1}; катализатор на основе переходного металла {тетрафторборат бис(норборнадиен)родия(I)}; EtOH; 15 бар; соотношение 2(I-a):2(I-б) 34:66 (по данным ВЭЖХ-анализа).
Способ 3': Хиральный лиганд {(R)-1-[(S)-2-дициклогексилфосфино)ферроценил]этилди-трет-бутилфосфин = SL-J009-1}; катализатор на основе переходного металла {тетрафторборат бис(норборнадиен)родия(I)}; МеОН; 15 бар; соотношение 2(I-a):2(I-б) 35:65 (по данным ВЭЖХ-анализа).
Способ 4': Хиральный лиганд {(αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(5,5)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфин]ферроцен = SL-M004-1}; катализатор на основе переходного металла {тетрафторборат бис(норборнадиен)родия(I)}; МеОН; 15 бар; соотношение 2(I-a):2(I-б) 27:73 (по данным ВЭЖХ-анализа).
Способ 5': Хиральный лиганд {(S)-1-[(S)-2-(2'-дифенилфосфинофенил)ферроценил]этилди(бис-3,5-трифторметилфенил)фосфин = SL-W001-2}; катализатор на основе переходного металла {тетрафторборат бис(норборнадиен)родия(1)}; МеОН; 15 бар; соотношение 2(I-a):2(I-б) 27:73 (по данным ВЭЖХ-анализа).
Способ 6': Хиральный лиганд {(R)-1-[(R)-2-(2'-дифенилфосфинофенил)ферроценил]этилдициклогексилфосфин = SL-W003-1};
катализатор на основе переходного металла {тетрафторборат бис(норборнадиен)родия(I)}; МеОН; 15 бар; соотношение 2(I-a):2(I-б) 33:67 (по данным ВЭЖХ-анализа).
Способ 7': Хиральный лиганд {(αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(5,5)-1,1'-бис(дициклогексилфосфино)ферроцен = SL-M002-1}; катализатор на основе переходного металла {димер дииод(n-цимен)рутения(II)}; EtOH; 15 бар; соотношение 2(I-a):2(I-б) 25:75 (по данным ВЭЖХ-анализа).
Способ 8': Хиральный лиганд {(αS,αS)-2,2'-бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфин]ферроцен = SL-M004-2}; катализатор на основе переходного металла {димер дииод(n-цимен)рутения(II)}; EtOH; 15 бар;
Соотношение 2(I-a):2(I-б) 6:94 (по данным ВЭЖХ-анализа).
Пример 3: (2S,4R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпентановая кислота [3(I-г)]

К суспензии (E)-(S)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпент-2-еновой кислоты 3(II-б) (10 г, 26,2 ммоля) и триэтиламина (3,6 мл, 26,2 ммоля) в изопропилацетате добавляют палладий на угле (1 г, 10% содержание). После этого напускают водород в течение 5 часов. После отфильтровывания катализатора отгоняют растворитель под вакуумом, что приводит к указанному в заглавии соединению {соотношение 3(I-г):3(I-в) 80:20; соотношение 3(I-г):3(I-в) 99,9: 0,1 после перекристаллизации; по данным ВЭЖХ-анализа}.
Перекристаллизация: 94,5 г смеси 3(I-г):3(I-в) 80:20 суспендируют в изопропилацетате (190 мл) и кипятят с обратным холодильником до образования раствора. Добавляют фракцию гептанов (378 мл) и охлаждают смесь до комнатной температуры. Вещество собирают посредством фильтрования и промывают 180 мл смеси гептана и изопропилацетата (2:1), что приводит к смеси 3(I-г):3(I-в) 91,7:8,3. Данную смесь снова суспендируют в изопропилацетате (280 мл) и кипятят с обратным холодильником. Добавляют фракцию гептанов (560 мл) и охлаждают смесь до комнатной температуры. Вещество собирают посредством фильтрования и промывают 180 мл смеси гептана и изопропилацетата (2:1), что приводит к смеси 3(I-г):3(I-в) 99,9:0,1. δН (400 МГц; ДМСО) 1,07 (3Н, d, J 7,1, 1-СН3), 1,34 (9Н, s, (СН3)3), 1,37 (1Н, m, 3-НА), 1,76 (1Н, m, 3-НВ), 2,43 (1Н, m, 2-H), 2,69 (2Н, d, J 6,8, 5-H), 3,68 (1Н, m, 4-H), 6,72 (1Н, d, J 8,8, NH), 7,25 (2Н, d, J 8,2, Ar-орто-H(Ph)), 7,34 (1Н, m, Ar-(Ph)-пара-H), 7,45 (2Н, m, Ar-(Ph)-мета-H), 7,57 (2Н, d, J8,2, Ar-мета-H(Ph), 7,64 (2Н, d, J 7,9, Ar-(Ph)-орто-H), 11,97 (1Н, s, CO2H); m/z (+ИЭР) 384 ([MH]+, 66%), 328 (100), 284 (12).
(2R,4R)-5-бифенил-4-ил-4-трет-бутоксикарбониламино-2-метилпентановая кислота [3(I-в)]
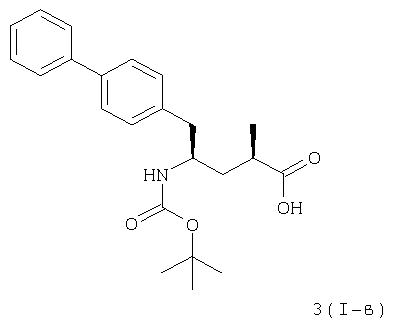
К суспензии (Е)-(S)-5-бифенил-4-yl-4-трет-бутоксикарбониламино-2-метилпент-2-еновой кислоты 3(II-б) (10 г, 26,2 ммоля) в обезгаженном этаноле (80 мл) добавляют при температуре 40°С раствор димера дииод(n-цимен)рутения(II) (125 мг) и (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(5',5')-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфин]ферроцена (290 мг) в обезгаженном этаноле (20 мл). Раствор обезгаживают под вакуумом и напускают водород при давлении 5.5 бар. Смесь перемешивают при температуре 40°С в течение 24 часов. После этого продувают сосуд азотом. Раствор концентрируют под вакуумом, что приводит к указанному в заглавии соединению {соотношение 3(I-г):3(I-в) 8:92; по данным ВЭЖХ-анализа}.
δН (400 МГц; ДМСО) 1,04 (3Н, d, J 78,0), 1,32 (9Н, s), 1,41 (1Н, m), 1,76 (1H, m), 2,36 (1H, m), 2,70 (1H, m), 2,72 (1H, m), 3,70 (1H, m), 6,69 (1H, d, J 8,0), 7,23 (2H, d, J 8,0), 7,32 (1H, m), 7,43 (2H, t, J 8,0), 7,54 (2H, d, J 8,0), 7,60 (2H, d, J 8,0), 12,01 (1H, s); m/z (-ИЭР) 382 ([M-H]-, 100), 308 (8).
Условия ВЭЖХ:
Колонка: HP Hypersil, BDS-C 18, 5 мкм, 125×4.6 мм. Подвижная фаза А (Н2О+0,1% трифторуксусной кислоты); Подвижная фаза Б (ацетонитрил + 0,1% трифторуксусной кислоты). Градиент: 0 мин (99% А; 1% Б); 10 мин (100% Б); 12 мин (100% Б). Скорость потока: 1 мл/мин. Длина волны: 254 нм.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЙ СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНЫХ СОЕДИНЕНИЙ, ИСПОЛЬЗУЕМЫХПРИ ПОЛУЧЕНИИИНГИБИТОРОВ NEP | 2011 |
|
RU2573824C2 |
| СПОСОБ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5-БИФЕНИЛ-4-ИЛ-2-МЕТИЛПЕНТАНОВОЙ КИСЛОТЫ | 2009 |
|
RU2513521C2 |
| СПОСОБ И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5-БИФЕНИЛ-4-ИЛ-2-МЕТИЛПЕНТАНОВОЙ КИСЛОТЫ | 2013 |
|
RU2636936C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОМЕРНО И ДИАСТЕРЕОМЕРНО ОБОГАЩЕННЫХ ЦИКЛОБУТАНАМИНОВ И -АМИДОВ | 2018 |
|
RU2793738C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПРОПИОНОВОЙ КИСЛОТЫ | 2010 |
|
RU2544989C2 |
| ЗАМЕЩЕННЫЕ ФЕРРОЦЕНИЛДИФОСФИНЫ В КАЧЕСТВЕ ЛИГАНДОВ ДЛЯ ГОМОГЕННЫХ КАТАЛИЗАТОРОВ ГИДРИРОВАНИЯ | 2004 |
|
RU2352577C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПРОПИОНОВОЙ КИСЛОТЫ | 2011 |
|
RU2575345C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВОРИКОНАЗОЛА И ЕГО АНАЛОГОВ | 2013 |
|
RU2619928C2 |
| СПОСОБ | 2014 |
|
RU2671972C1 |
| РЕАКЦИИ СОЧЕТАНИЯ, КОТОРЫЕ МОГУТ БЫТЬ ИСПОЛЬЗОВАНЫ ПРИ ПОЛУЧЕНИИ ПРОИЗВОДНЫХ (1Н-ТЕТРАЗОЛ-5-ИЛ)БИФЕНИЛА | 2005 |
|
RU2426728C2 |

Изобретение относится к способу получения соединения формулы 
или его соли, где R1 и R1' независимо являются водородом или защитной группой для аминогруппы, a R2 - карбоксильной или сложноэфирной группой. Способ включает взаимодействие соединения формулы 
или его соли, где R1, R1' и R2 определены выше, с водородом в присутствии катализатора на основе переходного металла и хирального лиганда. Переходный металл выбран из 8 или 9 группы периодической системы, а хиральный лиганд является хиральным фосфином. Изобретение относится также к применению катализатора на основе переходного металла и хирального лиганда в способе получения соединения формулы (I), используемом в синтезе ингибитора нейтральной эндопептидазы (НЭП) или его пролекарства. 2 н. и 34 з.п. ф-лы, 1 ил., 3 пр.
1. Способ получения соединения формулы (I)

или его соли, в которой R1 и R1' независимо являются водородом или защитной группой для аминогруппы, a R2 является карбоксильной группой или сложноэфирной группой, включающий взаимодействие соединения формулы (II)

или его соли, в которой R1, R1' и R2 отвечают вышеприведенным определениям, с водородом в присутствии катализатора на основе переходного металла и хирального лиганда, где переходный металл выбран из 8 или 9 группы Периодической системы и хиральный лиганд является хиральным фосфином.
2. Способ по п.1, в котором взаимодействие осуществляют в режиме гомогенного катализа.
3. Способ по п.1 или 2, в котором катализатор на основе переходного металла включает родий или рутений.
4. Способ по любому из предшествующих пунктов, в котором катализатор на основе переходного металла включает димерный комплекс, предпочтительно, димерный комплекс рутения.
5. Способ по любому из предшествующих пунктов, в котором катализатор на основе переходного металла включает димер дииод(n-цимен)рутения(II) (=[RuI2(n-цимен)]2).
6. Способ по любому из пп.1-3, в котором катализатор на основе переходного металла включает тетрафторборат бис(норборнадиен)родия(I) (=Rh(nbd)2BF4).
7. Способ по любому из предшествующих пунктов, в котором хиральный лиганд является лигандом Mandyphos, Walphos, Josiphos или Solphos.
8. Способ по любому из предшествующих пунктов, в котором хиральный лиганд выбран из (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дифенилфосфино)ферроцена (= Mandyphos SL-M001-1), (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дициклогексилфосфино)-ферроцена (= Mandyphos SL-M002-1), (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)-фосфино]ферроцена (= Mandyphos SL-M004-1), (αS,αS)-2,2'-бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)-фосфино]ферроцена (= Mandyphos SL-M004-2), (R)-1-[(S)-2-дициклогексилфосфино)ферроценил]этилдициклогексилфосфина (= Josiphos SL-J002-1), (R)-1-[(S)-2-дициклогексилфосфино)ферроценил]этилдицикло-гексилфосфина (= Josiphos SL-J003-1), (R)-1-[(S)-2-дициклогексилфосфино)ферроценил]этилди-трет-бутилфосфина (= Josiphos SL-J009-1), (S)-1-[(S)-2-(2'-дифенилфосфинофенил)ферроценил]этилди(бис-3,5-трифторметилфенил)фосфина (= Walphos SL-W001-2), (R)-1-[(R)-2-(2'-дифенилфосфинофенил)ферроценил]этилдициклогексилфосфина (= Walphos SL-W003-1), (R)-1-[(R)-2-(2'-дициклогексилфосфинофенил)ферроценил]-этилди(бис(3,5-трифторметил)фенил)фосфина (= Walphos SL-W008-1) или (R)-N,N'-диметил-7,7'-бис(дифенилфосфино)-3,3',4,4'-тетрагидро-8,8'-би-2H-1,4-бензоксазина (= Solphos SL-A001-1).
9. Способ по п.3, в котором катализатор на основе переходного металла включает родий и в котором хиральный лиганд выбран из (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метокси-фенил)фосфино]ферроцена (= Mandyphos SL-M004-1), (R)-1-[(S)-2-дициклогексилфосфино)ферроценил]этилдициклогексилфосфина (= Josiphos SL-J003-1), (R)-1-[(S)-2-дициклогексилфосфино)ферроценил]этилди-трет-бутилфосфина (= Josiphos SL-J009-1), (S)-1-[(S)-2-(2'-дифенилфосфинофенил)ферроценил]этилди(бис-3,5-трифторметилфенил)-фосфина (= Walphos SL-W001-2), (R)-1-[(R)-2-(2'-дифенилфосфинофенил)ферроценил]этилдициклогексилфосфина (= Walphos SL-W003-1), (R)-1-[(R)-2-(2'-дициклогексилфосфинофенил)ферроценил]-этилди(бис(3,5-трифторметил)фенил)фосфина (= Walphos SL-W008-1) или (R)-N,N'-диметил-7,7'-бис(дифенилфосфино)-3,3',4,4'-тетрагидро-8,8'-би-2H-1,4-бензоксазина (= Solphos SL-A001-1).
10. Способ по п.9, в котором катализатор на основе переходного металла включает тетрафторборат бис(норборнадиен)родия(I) (=Rh(nbd)2BF4).
11. Способ по п.9 или 10, в котором хиральным лигандом является (R)-1-[(R)-2-(2'-дициклогексилфосфинофенил)ферроценил]
этилди(бис(3,5-трифторметил)фенил)фосфин (= Walphos SL-W008-1).
12. Способ по п.3, в котором катализатор на основе переходного металла включает рутений и в котором хиральный лиганд выбран из (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дифенилфосфино)ферроцена (= Mandyphos SL-M001-1), (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дициклогексилфосфино)ферроцена (= Mandyphos SL-M002-1), (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцена (= Mandyphos SL-M004-1), (αS,αS)-2,2'-бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцена (= Mandyphos SL-M004-2) или (R)-1-[(S)-2-дициклогексилфосфино)ферроценил]этилдициклогексилфосфина (= JosiphosSL-J002-1).
13. Способ по п.12, в котором катализатор на основе переходного металла включает димер дииод(n-цимен)рутения(II) (=[RuI2(n-цимен)]2).
14. Способ по п.12 или 13, в котором хиральный лиганд выбран из (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дифенил-фосфино)ферроцена (= Mandyphos SL-M001-1), (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)-фосфино]ферроцена (= Mandyphos SL-M004-1) или (R)-1-[(S)-2-дициклогексилфосфино)ферроценил]этилдициклогексилфосфина (= Josiphos SL-J002-1).
15. Способ по п.12 или 13, в котором хиральным лигандом является (αS,αS)-2,2'-бис(α-N,N-диметиламинофенилметил)-(R,R)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (= Mandyphos SL-M004-2).
16. Способ по п.12 или 13, в. котором хиральным лигандом является (αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен (= Mandyphos SL-M004-1).
17. Способ по любому из предшествующих пунктов, в котором мольное соотношение между соединением формулы (II) или его солью и «активным катализатором» (S/C) составляет 100 или выше, предпочтительно от 1000 до 30000.
18. Способ по любому из предшествующих пунктов, в котором напускают водород при давлении от 5 до 25 бар.
19. Способ по любому из предшествующих пунктов, в котором R1 и R1' независимо являются водородом или защитной группой для аминогруппы, выбранной из группы, включающей (С1-С6)алкил, моно-, ди- или тризамещенный (С6-С10)арилом, где арильный цикл является незамещенным или замещенным одним, двумя или тремя остатками, выбранными из группы, включающей (С1-С7)алкил, гидроксигруппу, (С1-С7)алкоксигруппу, галоид, нитрогруппу, цианогруппу и CF3, а также (С6-С10)арил(С1-С6)алкил, кумил, фенил(С1-С2)алкоксикарбонил, аллил, циннамил, 9-флуоренил-метилоксикарбонильную группу (Fmoc), бензилоксиметил (ВОМ), пивалоилоксиметил (РОМ), трихлорэтоксикарбонильную группу (Troc), 1-адамантилоксикарбонильную группу (Adoc), (С1-С10)алкенил-оксикарбонильную группу, силил, сульфонильную группу, сульфенильную группу, сукцинимидильную группу, (С2-С6)алканоил, (С6-С10)арил-карбонильную группу, (С1-С6)алкоксикарбонильную группу и (С6-С10)арил(С1-С6)алкоксикарбонильную группу.
20. Способ по любому из предшествующих пунктов, в котором R1 является трет-бутоксикарбонильной группой.
21. Способ по любому из предшествующих пунктов, в котором R2 является -СООН или -COOR3, где R3 является (С1-С6)алкилом.
22. Способ по любому из предшествующих пунктов, в котором вводят во взаимодействие соединение формулы (II-а) или его соль
 ,
,
в которой R1 и R1' независимо являются водородом или защитной группой для аминогруппы, а R2 является карбоксильной группой или сложноэфирной группой.
23. Способ по п.22, в котором образуется соединение формулы (I-а) или его соль
 ,
,
в которой R1 и R1' независимо являются водородом или защитной группой для аминогруппы, a R2 является карбоксильной группой или сложноэфирной группой.
24. Способ по п.22, в котором образуется соединение формулы (1-6) или его соль
 ,
,
в которой R1 и R1' независимо являются водородом или защитной группой для аминогруппы, а R2 является карбоксильной группой или сложноэфирной группой.
25. Способ по п.22, в котором образуется смесь, включающая соединения формул (I-а) и (I-б) или их соли, и в котором мольное соотношение между соединением формулы (I-а) и соединением формулы (I-б) составляет по крайней мере 88:12.
26. Способ по п.22, в котором образуется смесь, включающая соединения формул (I-а) и (I-б) или их соли, и в котором мольное соотношение между соединением формулы (I-б) или его солью и соединением формулы (I-а) или его солью составляет по крайней мере 65:35.
27. Способ по п.25, в котором соединения формулы (I-а) или их соли выделяют из смеси посредством кристаллизации.
28. Способ по п.25, в котором в качестве растворителей используют изопропилацетат и гептан.
29. Способ по любому из предшествующих пунктов, в котором вводят во взаимодействие соединение формулы (II-б) или его соль
 ,
,
в которой R1 и R1' независимо являются водородом или защитной группой для аминогруппы, a R2 является карбоксильной группой или сложноэфирной группой.
30. Способ по п.29, в котором образуется соединение формулы (I-в) или его соль

в которой R1 и R1' независимо являются водородом или защитной группой для аминогруппы, а R2 является карбоксильной группой или сложноэфирной группой.
31. Способ по п.29, в котором образуется соединение формулы (I-г) или его соль
 ,
,
в которой R1 и R1' независимо являются водородом или защитной группой для аминогруппы, a R2 является карбоксильной группой или сложноэфирной группой.
32. Способ по п.29, в котором образуется смесь, включающая соединения формул (I-в) и (I-г) или их соли и в котором мольное соотношение между соединением формулы (I-в) или его солью и соединением формулы (I-г) или его солью составляет по крайней мере 88:12.
33. Применение катализатора на основе переходного металла и хирального лиганда в способе по п.1, используемом в синтезе ингибитора НЭП или его пролекарства.
34. Применение по п.33, в котором ингибитор НЭП или его пролекарство содержит в качестве остова γ-амино-δ-бифенил-α-метилалкановую кислоту или сложный эфир кислоты.
35. Применение по п.33 или 34, в котором реакция приводит к двум диастереомерам с диастереомерным соотношением по крайней мере 88:12.
36. Применение по любому из пп.33-35, в котором пролекарство ингибитора НЭП является этиловым эфиром N-(3-карбокси-1-оксопропил)-(4S)-n-фенилфенилметил)-4-амино-(2R)-метилбутановой кислоты или его солыо.
| KSANDER G.M | |||
| et al | |||
| Dicarboxylic Acid Dipeptide Neutral Endopeptidase Inhibitors // J | |||
| MED | |||
| CHEM | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| US 5217996 A, 08.06.1993 | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| RU 98123562 A, 27.12.2000. | |||
Авторы
Даты
2012-12-10—Публикация
2007-09-11—Подача