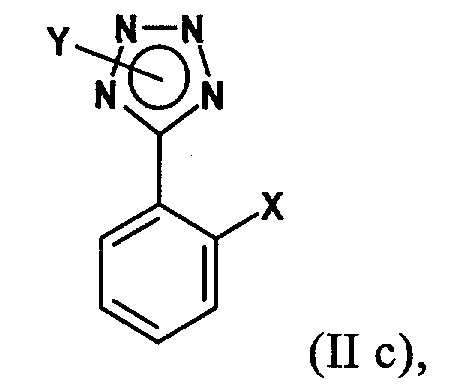
Настоящее изобретение относится к способу получения промежуточных продуктов, которые можно использовать при получении ARB (также называемых антагонистами рецепторов ангиотензина II или антагонистами рецепторов AT1), включающих в качестве общей структурной особенности тетразоловое кольцо. ARB могут быть использованы, например, для лечения гипертонии и связанных с этим заболеваний и состояний.
Можно упомянуть, например, ARB, которые выбирают из группы, включающей валзартан (см. ЕР 443983), лозартан (см. ЕР 253310), кандезартан (см. ЕР 459136), эпрозартан (см. ЕР 403159), ирбезартан (см. ЕР 454511), олмезартан (см. ЕР 503785) и тазозартан (см. ЕР 539086), а также их фармацевтически приемлемые соли.
Более конкретно все эти ARB включают следующий общий структурный элемент формулы (А):
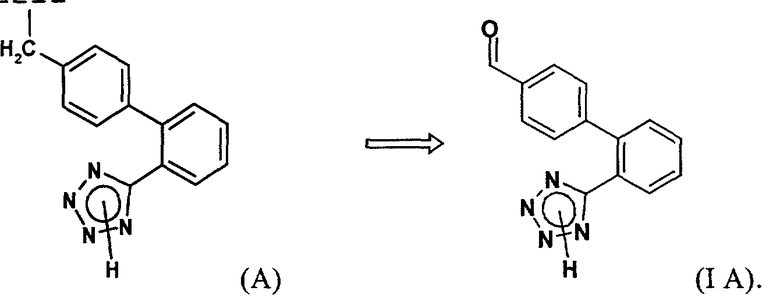
При получении вышеупомянутых антагонистов рецепторов ангиотензина II решающей стадией является получение альдегида формулы (IА), соответствующего упомянутому элементу формулы (А). В данной области техники рекомендованы различные арил-арильные реакции сочетания с образованием бифенильного остатка в альдегиде формулы (IА).
В ЕР 550313 описано получение защищенного 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегида, включающее катализируемую переходным металлом реакцию сочетания защищенного 5-(2-иодфенил)-2Н-тетразола с цинкорганическим реагентом или арилборной кислотой. Образование стехиометрических количеств отходов цинковой соли в первом случае, осуществление нескольких химических стадий, необходимых для получения арилборной кислоты, во втором случае и образование стехиометрических количеств иодидных отходов в обоих случаях рассматривают как недостатки.
В US 5468867 описано получение защищенного 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегида, включающее металлирование арилгалогенида металлорганическим основанием, таким как литийалкильный реагент, с последующей реакцией сочетания, например, с защищенным 5-(2-метоксифенил)-2Н-тетразолом. Недостаток этого способа состоит в образовании стехиометрических количеств реакционноспособных галоидсодержащих отходов.
Целью настоящего изобретения является разработка нового синтеза соединений формул (I) и (IС)
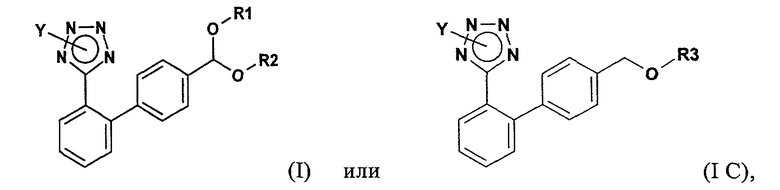
в которых Y обозначает защищающую тетразол группу, R1 и R2 независимо друг от друга обозначают С1-С10алкил или R1 и R2 совместно образуют C2-С10алкилен, а R3 обозначает защищающую гидроксил группу; который (1) свободен от описанных выше недостатков, (2) позволяет использовать такие защищающие тетразол группы, которые легко удаляют в присутствии кислоты Бренстеда, (3) не требует больших избытков реагентов, (4) дает минимальное количество отходов, преимущественно не стехиометрические количества реакционноспособных или создающих экологические проблемы отходов, и (5) является экономически привлекательным.
Соединения формул (I) и (I С) могут быть легко превращены в соединения формулы (I А) и, следовательно, являются важными промежуточными продуктами для получения ARB, обладающих структурной особенностью, соответствующей формуле (А), как это изложено, например, в заявке РСТ № WO 04/026847.
Было установлено, что способ в соответствии с настоящим изобретением удовлетворяет по меньшей мере указанным выше целям.
В одном варианте настоящее изобретение относится к способу получения соединения формулы (I)
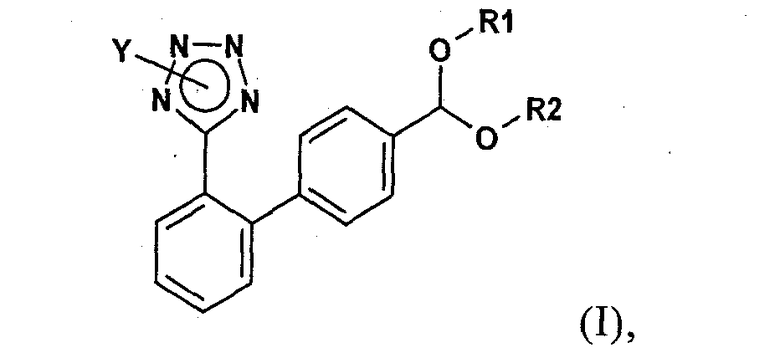
в которой Y обозначает защищающую тетразол группу, a R1 и R2 независимо друг от друга обозначают C1-С10алкил или R1 и R2 совместно образуют С2-С10алкилен, включающему (а) реакцию соединения формулы (II а)
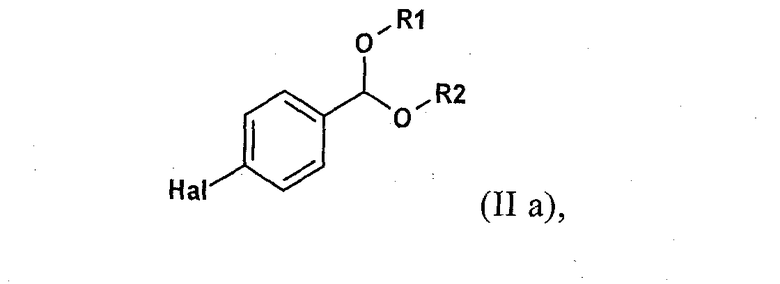
в которой Hal обозначает атом хлора, брома или иода, с активной формой магния в соответствующем растворителе; (б) реакцию полученного арилмагнийгалогенидного соединения формулы (IIb)
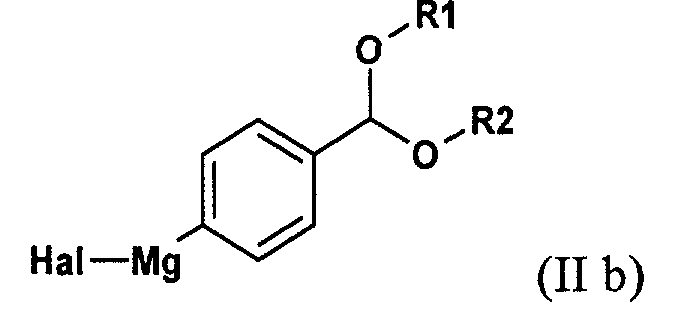
в присутствии катализатора с переходным металлом и каталитически эффективного количества соли металла как добавки с соединением формулы (IIс)
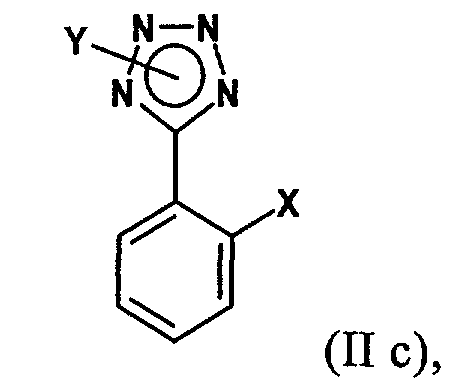
в которой Х обозначает заместитель, который, когда он связан с фенильным кольцом, не способен существенно замещаться при комнатной температуре арилмагнийгалогенидным реагентом формулы (IIb) в отсутствие катализатора, и, если необходимо, выделение полученного соединения формулы (I).
В другом варианте объектом настоящего изобретения является способ получения соединения формулы (IС)
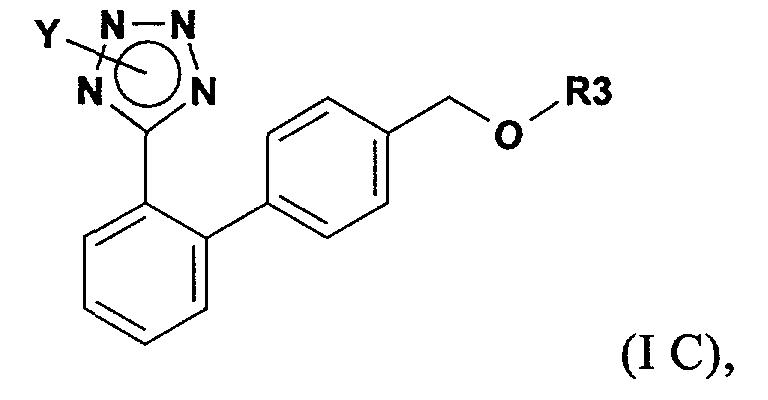
в которой Y обозначает защищающую тетразол группу, а R3 обозначает защищающую гидроксил группу; включающий (а') реакцию соединения формулы (IIIа)
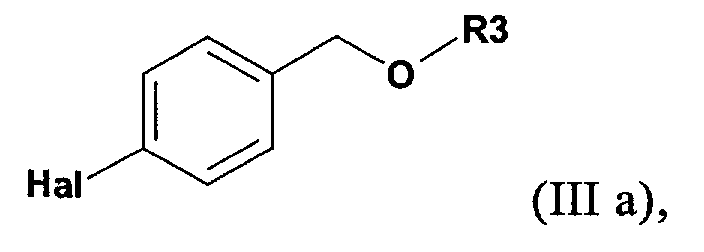
в которой Hal обозначает атом хлора, брома или иода, с активной формой магния в соответствующем растворителе; (б') реакцию полученного арилмагнийгалогенидного соединения формулы (IIIb)
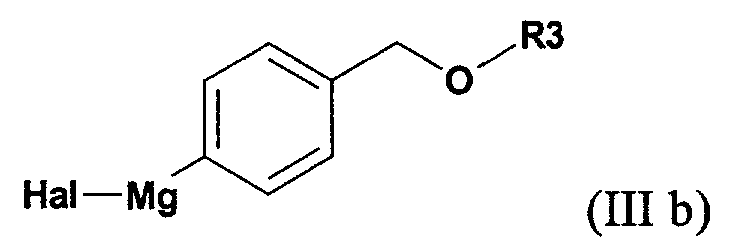
в присутствии катализатора с переходным металлом и каталитически эффективного количества соли металла как добавки с соединением формулы (IIс)
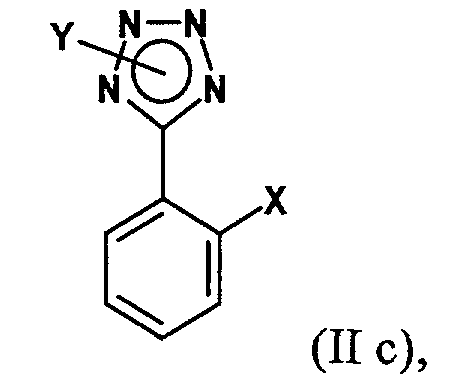
в которой Х обозначает заместитель, который, когда он связан с фенильным кольцом, не способен существенно замещаться при комнатной температуре арилмагнийгалогенидным реагентом формулы (IIIb) в отсутствие катализатора, и, если необходимо, выделение полученного соединения формулы (IС).
Еще одним объектом настоящего изобретения является объединение стадий (а) и/или (б) или стадий (а') и/или (б') с последующей стадией (в) удаления защитной группы с получением в результате соединения формулы (IА) или (IВ)
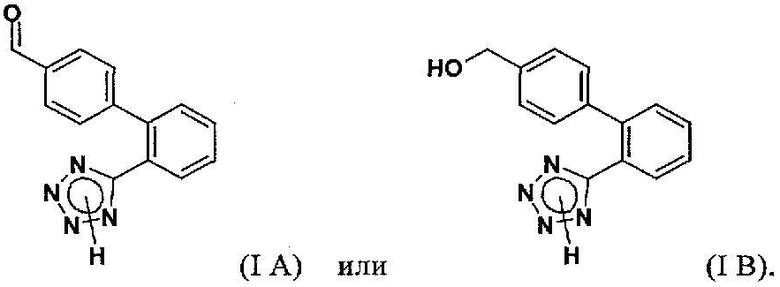
Полученное соединение соответственно формулы (IА) или (IВ) в дальнейшем выделяют, и его можно использовать в качестве промежуточного продукта при получении ARB, как они представлены в настоящем описании выше. Для специалистов в данной области техники совершенно очевидно, что соединение формулы (IВ) может быть легко превращено в соединение формулы (IА) обработкой окислителем в соответствии с методами, хорошо известными в данной области техники.
Реакции, описанные выше и ниже в вариантах, проводят, например, в отсутствие или обычно в присутствии подходящего растворителя или разбавителя, или их смеси, причем реакцию, в зависимости от необходимости, проводят с охлаждением, при комнатной температуре или с подогревом, например в температурном диапазоне от примерно -80°С до точки кипения реакционной среды, предпочтительно от примерно -10 до примерно 140°С, и, если необходимо, в закрытом сосуде под давлением, в атмосфере инертного газа и/или в безводных условиях.
Целью введения защитных групп, например Y и R3, является защита функциональных групп, например соответственно тетразольной и гидроксильной групп, от нежелательных реакций с реакционными компонентами в условиях, создаваемых для осуществления способа по настоящему изобретению. Выбор защитных групп специалистам в данной области техники известен и зависит от природы функциональной группы, которая должна быть защищена, и реакционных условий.
Хорошо известные защитные группы, которые удовлетворяют этим условиям, и их введение и удаление описаны, например, в работах McOmie, "Protective Groups in Organic Chemistry", Plenum Press, London, NY (1973), и Green и Wuts, "Protective Groups in Organic Chemistry", John Wiley и Sons, Inc., NY (1999).
Защищающую тетразол группу (Y) выбирают, например, из ряда, включающего трет-С4-С7алкил, такой как трет-бутил; метил, который замещен одним, двумя или тремя заместителями, выбранными из С1-С7алкила и C1-С7алкокси, например 1-этоксиэтил, 1-метокси-1-метилэтил; 2-тетрагидропиранил; 2-тетрагидрофуранил; С1-С2алкил, который моно-, ди- или тризамещен фенилом, таким как бензил, бензгидрил и тритил, у которого фенильное кольцо не замещено или замещено одним или несколькими, например двумя или тремя, заместителями, в частности теми, которые выбраны из ряда, включающего трет-С1-С7алкил, С1-С7алкокси, С2-С8алканоилокси; пиперонил; 1-метил-1-фенилэтил; флуоренил; метилтиометил; силил, такой как три-С1-С4алкилсилил, например триметилсилил, триэтилсилил или трет-бутилдиметилсилил, или ди-С1-С4алкилфенилсилил, например диметилфенилсилил; С1-С7алкилсульфонил; арилсульфонил, такой как фенилсульфонил, у которого фенильное кольцо не замещено или замещено одним или несколькими, например двумя или тремя, заместителями, в частности теми, которые выбраны из ряда, включающего С1-С7алкил, С1-С7алкокси, С2-С8алканоилокси; С2-С8алканоил, такой как ацетил и валероил; и эстерифицированная карбоксигруппа, такая как С1-С7алкоксикарбонил, например метокси-, этокси- или трет-бутилоксикарбонил. Подобным же образом защищающей тетразол группой (Y) может также служить катион, например, щелочного металла или щелочно-земельного металла, в частности Li(I), Na(I), K(I), Rb(I), Cs(I), Mg(II), Ca(II) и Sr(II).
Примерами предпочтительных защитных групп Y являются трет-бутил, бензил, п-метоксибензил, 3,4-диметоксибензил, 1-метил-1-фенилэтил, трифенилметил, (п-метоксифенил)бифенилметил, бензилоксиметил, метоксиметил, этоксиметил, 1-бутоксиэтил, 1-этоксиэтил, 2-тетрагидропиранил, 2-тетрагидрофуранил, 1-метокси-1-метилэтил, 1-метоксициклогексил, 1-этоксициклогексил, триметилсилил и триэтилсилил.
Особенно предпочтительными защитными группами Y являются 1-бутоксиэтил, 1-этоксиэтил, 2-тетрагидропиранил и 2-тетрагидрофуранил.
Защищающую гидроксил группу (R3) выбирают, например, из ряда, включающего трет-С4-С7алкил, такой как трет-бутил; метил, который замещен одним, двумя или тремя заместителями, выбранными из С1-С7алкила и С1-С7алкокси, например 1-этоксиэтил, 1-метокси-1-метилэтил; 2-тетрагидропиранил; 2-тетрагидрофуранил; С1-С2алкил, который моно-, ди- или тризамещен фенилом, таким как бензил, бензгидрил и тритил, у которого фенильное кольцо не замещено или замещено одним или несколькими, например двумя или тремя, заместителями, в частности теми, которые выбраны из ряда, включающего трет-С1-С7алкил, С1-С7алкокси, С2-С8алканоилокси; пиперонил; 1-метил-1-фенилэтил; флуоренил; метилтиометил; силил, такой как три-C1-С4алкилсилил, например триметилсилил, триэтилсилил или трет-бутилдиметилсилил, или ди-С1-С4алкилфенилсилил, например диметилфенилсилил; 2,2-диметилпропаноил (т.е. пивалоил) и эстерифицированная карбоксигруппа, такая как трет-бутилоксикарбонил и бензилоксикарбонил.
Примерами предпочтительных защитных групп R3 являются 2-тетрагидропиранил, 2-тетрагидрофуранил, 1-бутоксиэтил и 1-этоксиэтил.
Общие термины, использованные выше и в дальнейшем, во всех случаях, если не указано иное, приведены в следующих значениях.
С1-С10алкил представляет собой, например, С1-С7алкильный, такой как метальный, этильный, н-пропильный, изопропильный, н-бутильный, изобутильный, втор-бутильный, трет-бутильный и соответствующий пентильный, гексильный и гептильный остатки. Предпочтителен С1-С4алкил, преимущественно метил или этил.
С2-С10алкилен представляет собой, например, С2-С6алкилен, такой как этилен, пропилен, бутилен, 1,2-диметилэтилен, 2,2-диметилпропилен и 1,4-диметил-1,4-бутилен. Предпочтителен С2-С4алкилен, преимущественно, этилен или пропилен.
Hal обозначает, в частности, атом хлора или брома.
С1-С7алкокси представляет собой, например, метокси, этокси, н-пропилокси, изопропилокси, н-бутилокси, изобутилокси, втор-бутилокси, трет-бутилокси или соответствующий пентилокси-, гексилокси- или гептилоксиостаток. Предпочтителен С1-С4алкокси. Особенно предпочтительны метокси, этокси и бутокси.
С2-С8алканоил представляет собой, например, С2-С5алканоил, такой как ацетил, пропионил, бутирил, валероил или пивалоил. Особенно предпочтителен ацетил.
Стадии (а) и (а')
Активной формой магния является, например, магниевая стружка такого типа, как обычно используемая для таких превращений, магниевая крошка, порошкообразный магний или магниевые стержни.
Более того активной формой магния является магний, который активируют каталитически эффективным количеством иода, брома, 1,2-дибромэтана, гидридный реагент или арилмагнийгалогенидный реагент, который необходимо приготовить.
Приемлемое количество магния составляет от 1,0 до 1,8 молярного эквивалента, предпочтительно от 1,0 до 1,2 молярного эквивалента, относительно количества используемого соединения формулы (IIа) или (IIIа).
Эту реакцию проводят, например, в приемлемом инертном растворителе или смеси растворителей. Инертные растворители обычно не взаимодействуют с соответствующим исходным материалом формулы (IIа) или (IIIа).
Соответствующие растворители представляют собой эфирные растворители, такие как этиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, бутиловый эфир, 1,2-диметоксиэтан, 1,2-диэтоксиэтан, смесь двух или большего числа этих растворителей и смесь одного из этих растворителей и ароматического растворителя, такого как толуол и ксилол. Предпочтительным растворителем является тетрагидрофуран.
Предпочтительная приемлемая реакционная температура находится в пределах от 0 до 75°С, более предпочтительно в пределах от 10 до 35°С.
Стадии (б) и (б')
Стадию (б) или (б') реакции сочетания осуществляют в присутствии катализатора с переходным металлом. Приемлемым переходным металлом является, например, никель, палладий, платина, кобальт, марганец или медь. Эффективной солью переходного металла является, например, хлорид, бромид, иодид, гидроксид, оксид, ацетат, гидроксиацетат, пропионат, сукцинат, трифторацетат, ацетилацетонат, нитрат, цианид, сульфат, трифторметансульфонат, метансульфонат, бензолсульфонат или п-толуолсульфонат никеля(II), палладия(II), платины(II), кобальта(II), марганца(II), меди(I) или меди(II).
Предпочтительный приемлемый катализатор с переходным металлом представляет собой комплекс переходного металла или соли переходного металла и одного, двух или до четырех координационных лигандов. Катализатор с переходным металлом может быть предварительно приготовлен или он может быть генерирован in situ в реакционной смеси. Приемлемый катализатор с переходным металлом может также представлять собой переходный металл не в форме комплекса, а в своей элементной форме или соль переходного металла не в форме комплекса. Некомплексная форма переходного металла или его соль может быть нанесена на уголь, диоксид кремния, оксид алюминия или диатомовую землю.
Приемлемыми лигандами являются олефины, такие как 1,5-циклооктадиен; три(С1-С4алкил)амины, такие как триэтиламин и этилдиизопропиламин; N-С1-С4алкилпиперидины, такие как N-метилпиперидин; N,N,N',N'-тетраметилэтилендиамин; гетероциклические амины и диамины, такие как пиридин, N-метилимидазол, 2,2'-дипиридил, 1,10-фенантролин, у которого кольцо не замещено или замещено одним или несколькими, например двумя или тремя, С1-С4алкильными остатками, как, например, в коллидине; линейные и циклические простые эфиры, содержащие два или большее число, например три или четыре, атома кислорода, такие как 1,2-диметоксиэтан, 1,2-диэтоксиэтан, ди(этиленгликоль)диметиловый эфир и 1,2-диметоксибензол.
Особенно приемлемые лиганды представляют собой те, которые содержат один или два атома трехвалентного фосфора, например трифенилфосфин, три(орто-толил)фосфин и три(пара-толил)фосфин, три(С1-С8алкил)фосфины, такие как триметилфосфин, триэтилфосфин, трибутилфосфин, три(1,1-диметилэтил)фосфин, три(С4-С7-циклоалкил)фосфины, такие как трициклопентилфосфин и трициклогексилфосфин, три(С1-С6алкил)фосфиты, такие как триметилфосфит, триэтилфосфит и три(1-метилэтил)фосфит, три(С4-С7-циклоалкил)фосфиты, такие как трициклопентилфосфит и трициклогексилфосфит, 1,2-бис-(бифенилфосфино)этан (т.е. ДФФЭ), 1,3-бис-(бифенилфосфино)пропан (т.е. ДФФП), 1,4-бис-(бифенилфосфино)бутан (т.е. ДФФБ), 1,1'-бис-(бифенилфосфино)ферроцен (т.е. ДФФФ), 1,1'-бис-(ди-[2-пропил]фосфино)ферроцен, 1,1'-бис-(ди-трет-бутилфосфино)ферроцен, 1,2-бис-(бифенилфосфино)бензол, 2,2'-бис-(бифенилфосфино)-1,1'-бифенил (т.е. БИФЕФ), 2,2'-бис-(бифенилфосфино)-1,1'-бинафтил (т.е. ДИНАФ), бис-(2-бифенилфосфинофенил)эфир (т.е. ДФЭфос), 9,9-диметил-4,5-бис-(бифенилфосфино)ксантен (т.е. КСАНТФОС).
Соли переходных металлов дериватизируют из вышеуказанных переходных металлов.
Предпочтительными солями переходных металлов являются хлорид никеля(II), бромид никеля(II) и ацетилацетонат никеля(II). Особенно предпочтительная соль переходного металла представляет собой хлорид никеля (II).
Предпочтительными лигандами являются трифенилфосфин, 1,2-бис-(бифенилфосфино)этан (т.е. ДФФЭ), 1,3-бис-(бифенилфосфино)пропан (т.е. ДФФП), 1,1'-бис-(бифенилфосфино)ферроцен (т.е. ДФФФ). Особенно предпочтительный лиганд представляет собой 1,2-бис-(бифенилфосфино)этан (т.е. ДФФЭ).
Предпочтительными катализаторами являются дихлорбис-(трифенилфосфин)никель(II), дихлор[1,2-бис-(бифенилфосфино)этан]никель(II), дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II). Особенно предпочтительный катализатор представляет собой дихлор[1,2-бис-(бифенилфосфино)этан]никель(II).
Количество используемого никелевого катализатора в предпочтительном варианте находится в пределах от 0,05 до 2 мол.% относительно исходного материала с N-защищенным тетразолом формулы (IIс), предпочтительно в пределах от 0,2 до 1,5 молярного %.
Также предпочтительными солями переходных металлов являются хлорид палладия(II), бромид палладия(II) и ацетат палладия(II). Особенно предпочтительная соль переходного металла представляет собой хлорид палладия(II).
Предпочтительными лигандами являются трифенилфосфин, 1,3-бис-(бифенилфосфино)пропан (т.е. ДФФП), 1,1'-бис-(бифенилфосфино)ферроцен (т.е. ДФФФ). Особенно предпочтительный лиганд представляет собой 1,1'-бис-(бифенилфосфино)ферроцен (т.е. ДФФФ).
Предпочтительными палладиевыми катализаторами являются дихлорбис-(трифенилфосфин)палладий(II), дихлор[1,3-бис-(бифенилфосфино)пропан]палладий(II) и дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или его дихлорметановый продукт присоединения. Особенно предпочтительный палладиевый катализатор представляет собой дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или его дихлорметановый продукт присоединения.
Количество используемого палладиевого катализатора в предпочтительном варианте находится в пределах от 0,01 до 1 мол.% относительно исходного материала с N-защищенным тетразолом (IIс), предпочтительно в пределах от 0,05 до 0,3 мол.%.
Реакция сочетания на стадии (б) или (б') может включать соль металла как добавку. Функция соли металла как добавки, которую используют в каталитически эффективных количествах, состоит в содействии протеканию реакции сочетания. В сравнении с реакциями сочетания с арилцинковыми реагентами применение каталитически эффективных количеств такой соли металла как добавки приводит к образованию меньшего количества отходов. Кроме того, в присутствии соли металла как добавки могут быть достигнуты более высокие значения степени превращения исходного материала (IIс). Эффективная соль металла как добавка представляет собой соль меди(I), меди(II), цинка(II), серебра(I), кадмия(II), ртути(II), алюминия(III), галлия(III), индия(III), олова(IV), титана(IV) или циркония(IV). Примерами таких солей служат соответствующие хлорид, бромид, иодид, карбонат, гидроксид, оксид, С1-С7алканоаты, такие как ацетат и пропионат, С1-С7алкоксиды, такие как метоксид и этоксид, трифторацетат, ацетилацетонат, нитрат, цианид, сульфат, трифторметансульфонат, метансульфонат, бензолсульфонат и пара-толуолсульфонат.
Предпочтительными солями металлов как добавок являются соли цинка(II), такие как хлорид цинка(II) и бромид цинка(II). Особенно предпочтительная соль металла как добавка представляет собой хлорид цинка(II).
Количество используемой соли металла как добавки в предпочтительном варианте находится в пределах от 0,1 до 8 мол.% относительно исходного материала с N-защищенным тетразолом формулы (IIс), предпочтительно в пределах от 0,5 до 6 мол.%.
Заместитель Х представляет собой заместитель, который не способен существенно замещаться при комнатной температуре арилмагнийгалогенидным реагентом формулы (IIb) или (IIIb) в отсутствие катализатора с переходным металлом. Так, в частности, Х обозначает, например, атом хлора или брома. Предпочтительный заместитель Х представляет собой атом хлора.
Когда Х обозначает атом хлора, предпочтительным переходным металлом катализатора служит никель.
Когда Х обозначает атом брома, предпочтительным переходным металлом катализатора служит палладий.
Независимо от выбора катализатора реакцию проводят, например, в приемлемом инертном растворителе или смеси растворителей. Инертные растворители обычно не взаимодействуют с соответствующими исходными материалами формул (IIb), (IIIb) и (IIс).
Соответствующий растворитель для реакции представляет собой эфирный растворитель, такой как этиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, бутиловый эфир, 1,2-диметоксиэтан и 1,2-диэтоксиэтан; биполярный апротонный растворитель, такой как 1-метил-2-пирролидинон (т.е. N-МП) и 1,3-диметил-3,4,5,6-тетрагидро-2(1Н)пиримидинон (т.е. ДМПМ); ароматический растворитель, такой как толуол и ксилол, или смесь двух или большего числа растворителей, выбранных из вышеприведенных групп. Предпочтительным растворителем является тетрагидрофуран.
Реакцию в предпочтительном варианте проводят при температуре в пределах от -10 до 60°С, предпочтительно в пределах от 10 до 35°С.
Как изложено в настоящем описании выше, объектом настоящего изобретения является способ получения защищенного 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегида формулы (I), что проиллюстрировано следующей схемой реакции:
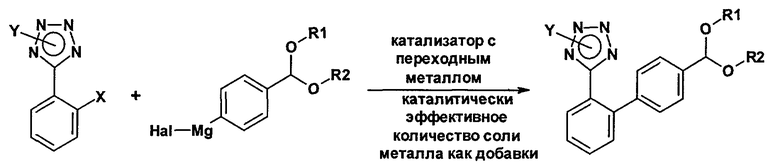
включающий реакцию сочетания N-защищенного фенилтетразола (X обозначает Cl или Br; Y обозначает защищающую тетразол группу) с арилмагнийгалогенидом (Hal обозначает Cl, Br, I; R1, R2 обозначают С1-С10алкил или совместно С2-С10алкилен) в присутствии катализатора с переходным металлом, который находится в форме комплекса, не в форме комплекса или представляет собой нанесенный на носитель металлический никель, палладий, платину, кобальт, марганец или медь или ее соответствующую соль, и необязательно каталитически эффективного количества соли металла как добавки, такой как соль меди(I), меди(II), цинка(II), серебра(I), кадмия(II), ртути(II), алюминия(III), галлия(III), индия(III), олова(IV), титана(IV) или циркония(IV), в присутствии инертного растворителя или смеси инертных растворителей.
Аналогичным образом объектом настоящего изобретения является способ получения защищенного спирта формулы (IС), что проиллюстрировано приведенной ниже схемой реакции
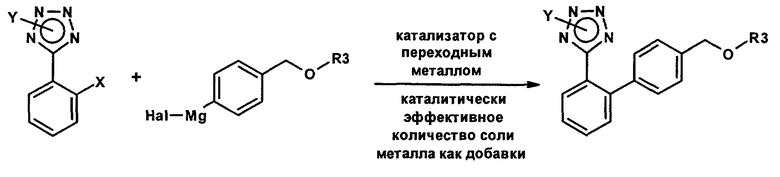
включающий реакцию сочетания N-защищенного фенилтетразола (X обозначает Cl или Br; Y обозначает защищающую тетразол группу) с арилмагнийгалогенидом (Hal обозначает Cl, Br, I; R3 обозначает защищающую гидроксил группу) в присутствии катализатора с переходным металлом, который находится в форме комплекса, не в форме комплекса или представляет собой нанесенный на носитель металлический никель, палладий, платину, кобальт, марганец или медь или ее соответствующую соль, и необязательно каталитически эффективного количества соли металла как добавки, такой как соль меди(I), меди(II), цинка(II), серебра(I), кадмия(II), ртути(II), алюминия(III), галлия(III), индия(III), олова(IV), титана(IV) или циркония(IV), в присутствии инертного растворителя или смеси инертных растворителей.
Предпочтительный Hal обозначает, например, Br.
Предпочтительные R1 и R2 обозначают, например, метил.
Предпочтительный R3 обозначает, например, 2-тетрагидропиранил.
Предпочтительный Х обозначает, например, Cl.
Когда Х обозначает атом хлора, предпочтительный катализатор с переходным металлом представляет собой комплекс никеля(0) или никеля(II), например комплекс соли никеля(II), который координирован по меньшей мере одним фосфорорганическим соединением, содержащим трехвалентный фосфор. Предпочтительны комплексы никеля(II), включающие два фосфорорганических лиганда. Особенно предпочтительны комплексы никеля(II) с фосфорорганическими лигандами, которые содержат два атома трехвалентного фосфора, такие как дихлор[1,2-бис-(бифенилфосфино)этан]никель(II) (т.е. NiСl2(ДФФЭ)). Предпочтительная соль металла как добавка представляет собой, например, соль цинка(II), такую как ZnCl2 и ZnBr2.
Предпочтительные растворители представляют собой эфирные растворители, особенно тетрагидрофуран.
Когда Х обозначает атом хлора, в представленном выше способе соединения формулы (I) могут быть получены без соли металла как добавки (например, ZnCl2), т.е. с катализом реакции сочетания только никелевым катализатором.
Когда Х обозначает атом брома, предпочтительный катализатор с переходным металлом представляет собой палладиевый комплекс, например комплекс палладия(0) или комплекс соли палладия(II) с по меньшей мере одним фосфорорганическим соединением, содержащим трехвалентный фосфор. Предпочтительны комплексы палладия(II), включающие два фосфорорганических лиганда. Особенно предпочтительны комплексы палладия(II) с фосфорорганическими лигандами, которые содержат два атома трехвалентного фосфора, такие как дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) (т.е. РdСl2(ДФФФ)) или его дихлорметановый продукт присоединения.
Предпочтительная соль металла как добавка представляет собой, например, соль цинка(II), такую как ZnCl2 и ZnBr2.
По одному из объектов настоящего изобретения другой вариант выполнения настоящего изобретения представляет собой способ получения соединения формулы (I)
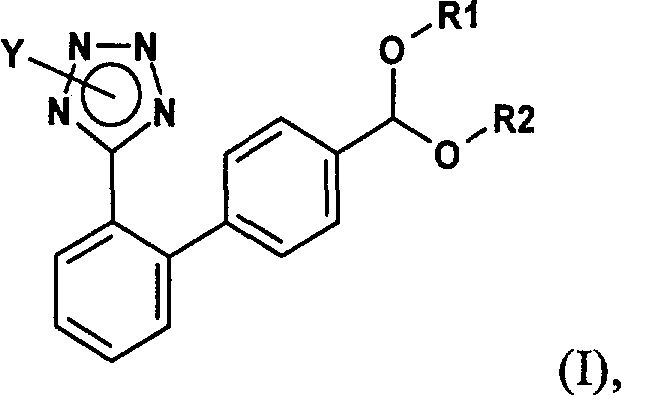
в которой Y обозначает защищающую тетразол группу, a R1 и R2 независимо друг от друга обозначают С1-С10алкил или R1 и R2 совместно образуют С2-С10алкилен; включающий (а) реакцию соединения формулы (IIа)
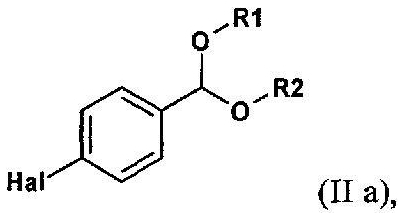
в которой Hal обозначает атом хлора, брома или иода, с активной формой магния в соответствующем растворителе; (б) реакцию полученного арилмагнийгалогенидного соединения формулы (IIb)
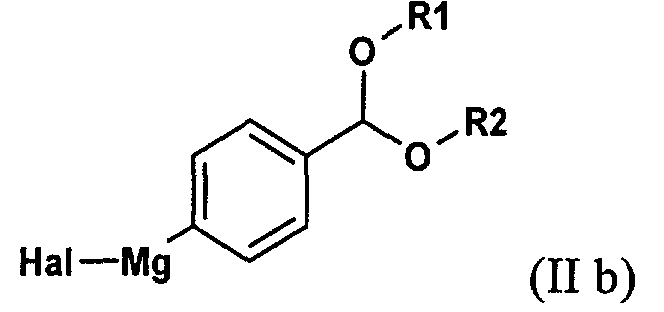
в присутствии катализатора с переходным металлом с соединением формулы (IIс)
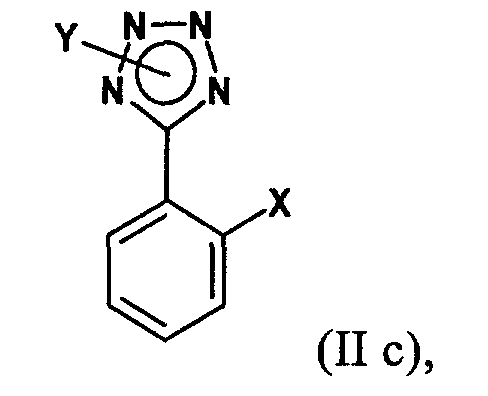
в которой Х обозначает атом хлора, в отсутствие соли металла как добавки и, если необходимо, выделение полученного соединения формулы (I).
И тем не менее другим объектом настоящего изобретения является способ получения соединения формулы (IС)
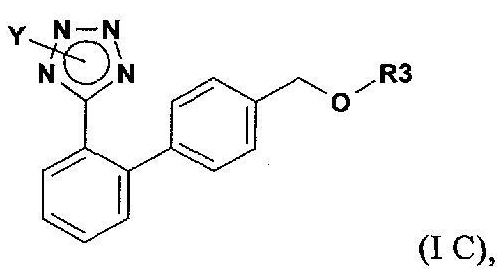
в которой Y обозначает защищающую тетразол группу, а R3 обозначает защищающую гидроксил группу; включающий (а') реакцию соединения формулы (IIIа)
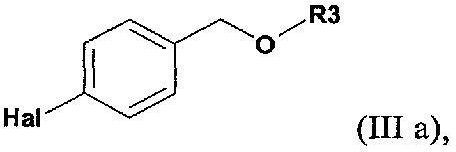
в которой Hal обозначает атом хлора, брома или иода, с активной формой магния в соответствующем растворителе; (б') реакцию полученного арилмагнийгалогенидного соединения формулы (IIIb)
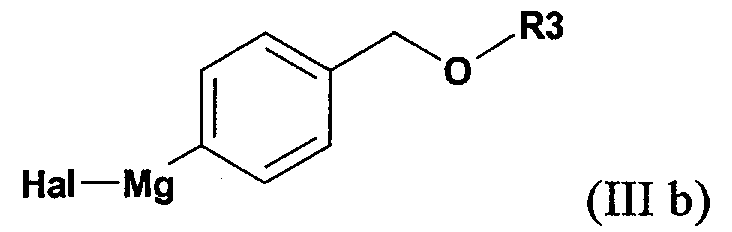
в присутствии катализатора с переходным металлом с соединением формулы (IIс)
в которой Х обозначает атом хлора, в отсутствие соли металла как добавки и, если необходимо, выделение полученного соединения формулы (IС).
Еще одним вариантом выполнения настоящего изобретения является реакционная стадия соответственно (б) или (б'), т.е. особая реакция соединения формулы соответственно (IIb) или (IIIb) с соединением формулы (IIс), в которой Х обозначает атом хлора. В ходе проведения этой реакции для получения соединения формулы соответственно (I) или (IС) нет необходимости, что неожиданно, во введении каталитически эффективного количества соли металла как добавки.
В случае, в котором как соль переходного металла, так и соль металла как добавку не включают, сколько-нибудь значительного количества соединения формулы соответственно (I) или (IС) из исходного материала формулы (IIс), в которой Х обозначает атом хлора, не получают.
Стадия выделения
Выделение соединения формулы (I) или (IС) осуществляют в соответствии с обычными методами выделения, такими как кристаллизация полученного соединения формулы (I) или (IС) из реакционной смеси, при желании или необходимости после обработки, преимущественно экстракцией или хроматографией реакционной смеси, или по любым сочетаниям методов.
Стадия (в)
Для этой цели защитные группы у полученного соединения формулы (I) или (IС) стадии соответственно (б) или (б') удаляют последовательно или в одну стадию в условиях гидролиза, предпочтительно в присутствии кислоты Бренстеда.
Стадию (в) осуществляют, например, растворением соединения формулы (I) или (IС) в воде или смеси воды и соответствующего органического растворителя и последующей обработкой кислотой предпочтительно при повышенной температуре.
Соответствующие органические растворители представляют собой простые эфиры, такие как тетрагидрофуран, 1,4-диоксан, бутиловый эфир, нитрилы, такие как ацетонитрил, спирты, такие как метанол, этанол, 1-пропанол, 2-пропанол, 1-бутанол, изопропилацетат, толуол, ксилол, уксусную кислоту или муравьиную кислоту. Предпочтительными растворителями являются метанол и этанол.
Приемлемыми кислотами являются кислоты Бренстеда, такие как серная кислота, соляная кислота, фосфорная кислота, метансульфоновая кислота, этансульфоновая кислота, пара-толуолсульфоновая кислота, бензойная кислота, уксусная кислота, муравьиная кислота, а также нанесенные на полимеры кислоты Бренстеда (например, кислые ионообменные смолы).
Предпочтительными кислотами являются серная кислота и соляная кислота.
Используемое количество кислоты в предпочтительном варианте находится в пределах от 0,05 до 2,0 экв. относительно соединения формулы (I) или (IС), более предпочтительно в пределах от 0,1 до 1,2 экв.
Реакцию проводят при температуре в пределах от 0°С до точки кипения растворителя, предпочтительно в пределах от 25 до 70°С.
Выделение соединения формулы (IА) или (IВ) осуществляют в соответствии с обычными методами выделения, такими как кристаллизация соединения формулы (IА) или (IВ) из реакционной смеси и, если желательно или необходимо, после обработки, преимущественно экстракцией или хроматографией реакционной смеси, или по любым сочетаниям методов. Так, например, кристаллизацию продукта осуществляют отгонкой всего или части органического растворителя, добавлением воды, охлаждением смеси или сочетанием этих технических приемов.
Некоторые исходные материалы формул (IIа) и (IIIа) в данной области техники известны и могут быть получены в соответствии с методами, хорошо известными в данной области техники. Так, например, соединение формулы (IIа) может быть получено обычной катализируемой кислотой ацетализацией 4-галобензальдегида в присутствии спирта или диола. В частности, получение соединения формулы (IIа) с Hal, обозначающим атом брома, и R1 и R2, обозначающими метил, изложено в Journal of Organic Chemistry, 1991, 56, 4280. Соответствующее соединение с R1 и R2, обозначающими этил, может быть получено в этаноле в присутствии триэтилортоформиата и кислотного катализатора. Соединение формулы (IIIа) может быть получено, например, обычной катализируемой кислотой реакцией 4-галобензилового спирта с подходящим алкилирующим агентом, таким как 3,4-дигидро-2Н-пиран. Так, например, получение соединения формулы (IIIа), в которой Hal обозначает атом брома, а R3 обозначает тетрагидропиран-2-ил, изложено в Tetrahedron, 1983, 39, 2531.
Некоторые исходные материалы формулы (IIс) с разными защитными группами Y в данной области техники известны. Некоторые примеры получения приведены в ЕР 788487.
Изобретение, описанное выше, иллюстрируют следующие примеры, однако их не следует рассматривать как ограничивающие в какой-либо степени его объем, например, конкретными реакционными условиями.
Пример 1
Получение 5-(4'-[1,3]диоксан-2-илбифенил-2-ил)-2-(1-метил-1-фенилэтил)-2Н-тетразола
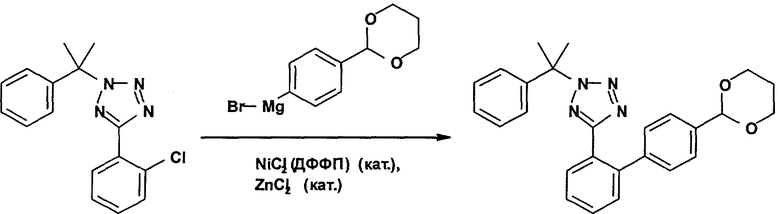
К магниевой стружке (0,882 г) в безводных условиях добавляют 12 мл раствора 2-(4-бромфенил)-[1,3]диоксана (8,02 г; 33 ммоля) в безводном тетрагидрофуране (33 мл). Эту смесь нагревают до примерно 50°С и добавляют пять капель 1,2-дибромэтана. После начала реакции смесь нагревают до температуры кипения и в течение 40 мин, добавляют оставшийся раствор 2-(4-бромфенил)-[1,3]диоксана. Далее приготовленную смесь перемешивают при 60°С в течение одного часа и, наконец, ей дают остыть до комнатной температуры. В соответствии с титрованием концентрация 4-([1,3]диоксан-2-ил)фенилмагнийбромида в растворе над избытком магниевой стружки составляет 0,50 М.
В другой колбе дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II) (0,022 г; 0,04 ммоля) суспендируют в трет-бутилметиловом эфире (3 мл) и охлаждают до примерно 0°С, после чего добавляют 0,5 М раствора хлорида цинка в тетрагидрофуране (0,40 мл; 0,20 ммоля) и раствора 5-(2-хлорфенил)-2-(1-метил-1-фенилэтил)-2Н-тетразола (1,20 г; 4,0 ммоля) в трет-бутилметиловом эфире (1,2 мл). В интенсивно перемешиваемую образовавшуюся суспензию при примерно 0°С в течение одного часа добавляют 9,6 мл вышеупомянутого 0,5 М раствора 4-([1,3]диоксан-2-ил)фенилмагнийбромида (4,8 ммоля). Полученному темно-коричневому раствору дают нагреться и в дальнейшем перемешивают при комнатной температуре в течение 20 ч. Эту смесь охлаждают до примерно 0°С, гасят реакцию 10 мл 3,8%-ного раствора аммонийхлорида в воде и разбавляют этилацетатом (25 мл). Водную фазу отделяют и экстрагируют этилацетатом (25 мл). Объединенные органические фазы промывают 0,5 М раствором гидроксида натрия в воде (10 мл) и 10%-ным раствором хлорида натрия в воде (10 мл). Объединенные органические фазы выпаривают под вакуумом. Раствор полученного бледно-зеленого твердого вещества в небольшом количестве этилацетата фильтруют и выпаривают. Полученный бледно-зеленый твердый продукт очищают хроматографией в колонке на силикагеле, элюируя смесью 1:10 трет-бутилметилового эфира и толуола с получением в виде бесцветных кристаллов 5-(4'-[1,3]диоксан-2-илбифенил-2-ил)-2-(1-метил-1-фенилэтил)-2Н-тетразола.
1Н-ЯМР (400 МГц, d6-ДМСО): 1,47-1,52 (m, 1H), 2,01 (s, 6H), 2,02-2,07 (m, 1H), 3,96-4,02 (m, 2H), 4,17-4,21 (m, 2H), 5,55 (s, 1H), 6,95-6,98 (m, 2H), 7,10-7,13 (m, 2H), 7,32-7,39 (m, 5H), 7,51-7,53 (m, 1H), 7,56-7,61 (m, 1H), 7,65-7,69 (m, 1H), 7,78-7,80 (m, 1H).
Диапазон плавления 102-106°С.
Пример 2
Получение 5-(4'-диэтоксиметилбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразола
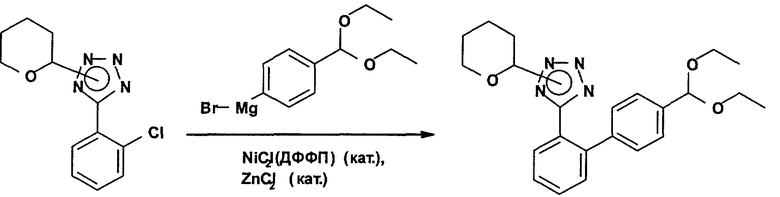
К магниевой стружке (2,92 г) в безводных условиях добавляют одну пятую раствора 1-бром-4-(диэтоксиметил)бензола (25,9 г; 100 ммолей) в безводном тетрагидрофуране (80 мл). Эту смесь нагревают до примерно 40°С и добавляют 1,2-дибромэтана (0,09 мл; 1,0 ммоля). После начала реакции в течение одного часа добавляют оставшийся раствор 1 -бром-4-(диэтоксиметил)бензола. Приготовленную смесь в дальнейшем перемешивают при 40°С в течение двух часов и при комнатной температуре в течение 30 мин и, наконец, разбавляют добавлением безводного тетрагидрофурана (25 мл). В соответствии с титрованием концентрация 4-(диэтоксиметил)фенилмагнийбромида в растворе над избытком магниевой стружки составляет 0,46 М.
В другой колбе дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II) (0,027 г; 0,05 ммоля) суспендируют в трет-бутилметиловом эфире (3,8 мл) и охлаждают до примерно 0°С, после чего добавляют 0,5 М раствора хлорида цинка в тетрагидрофуране (0,50 мл; 0,25 ммоля) и раствора смеси 5-(2-хлорфенил)-2-(тетрагидропиран-2-ил)-2Н-тетразола и 5-(2-хлорфенил)-1-(тетрагидропиран-2-ил)-1Н-тетразола (1,32 г; 5,0 ммоля) в трет-бутилметиловом эфире (1,3 мл). В интенсивно перемешиваемую образовавшуюся суспензию при примерно 0°С в течение одного часа добавляют 13 мл 0,46 М раствора вышеупомянутого 4-(диэтоксиметил)фенилмагнийбромида (6,0 ммоля). Полученный черно-желтый раствор перемешивают при примерно 0°С в течение 5 ч, дают нагреться и в дальнейшем перемешивают при комнатной температуре в течение 19 ч. Эту смесь охлаждают до примерно 0°С и гасят реакцию 7,5%-ным раствором аммонийхлорида в воде (10 мл). Водную фазу отделяют и экстрагируют этилацетатом (25 мл). Объединенные органические фазы промывают водой (10 мл), 7,5%-ным раствором карбоната натрия в воде (10 мл) и 10%-ным раствором хлорида натрия в воде (10 мл). Объединенные органические фазы выпаривают под вакуумом. Раствор полученного коричнево-желтого продукта в виде масла в небольшом количестве этилацетата фильтруют и выпаривают. Полученное вещество в виде масла (2,68 г) очищают хроматографией в колонке на силикагеле, элюируя смесью 1:4 этилацетата и гексана (в присутствии 0,2 об.% триэтиламина) с получением в виде бесцветного масла основного изомера (N2-изомер) 5-(4'-диэтоксиметилбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразола.
1H-ЯМР N2-изомера (400 МГц, CDCl3): 1,24 (t, J=7,2 Гц, 6Н), 1,60-1,67 (m, 3Н), 1,86-2,03 (m, 2Н), 2,11-2,17 (m, 1Н), 3,50-3,73 (m, 6Н), 5,49 (s, 1Н), 5,97-5,99 (m, 1Н), 7,17-7,20 (m, 2Н), 7,37-7,39 (m, 2Н), 7,43-7,56 (m, 3Н), 7,90-7,92 (m, 1Н).
Пример 3
Получение 5-(4'-[1,3]диоксан-2-илбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразола и 5-(4'-[1,3]диоксан-2-илбифенил-2-ил)-1-(тетрагидропиран-2-ил)-1H-тетразола
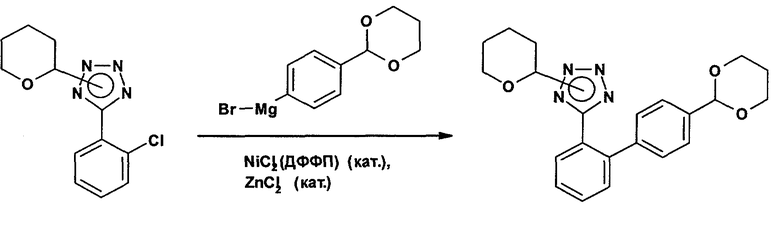
Суспензию магниевой стружки (2,68 г) в безводном тетрагидрофуране (20 мл) охлаждают до 10°С и добавляют пять капель 1,2-дибромэтана. При 10°С с интенсивным перемешиванием добавляют 2 мл раствора 2-(4-бромфенил)-[1,3]диоксана (24,3 г; 100 ммолей) в безводном тетрагидрофуране (80 мл). После начала реакции в течение 90 мин добавляют оставшийся раствор 2-(4-бромфенил)-[1,3]диоксана. Приготовленную смесь в дальнейшем перемешивают при примерно 16°С в течение 2 ч и при 25°С в течение 75 мин. Концентрация 4-([1,3]диоксан-2-ил)фенилмагнийбромида в растворе над избытком магниевой стружки составляет примерно 0,90 M. В другой колбе дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II) (0,054 г; 0,10 ммоля) суспендируют в 1,2-диметоксиэтане (7,7 мл) и охлаждают до примерно 0°С, после чего добавляют 0,5 М раствор хлорида цинка в тетрагидрофуране (1,0 мл; 0,50 ммоля) и раствор смеси 5-(2-хлорфенил)-2-(тетрагидропиран-2-ил)-2Н-тетразола и 5-(2-хлорфенил)-1-(тетрагидропиран-2-ил)-1Н-тетразола (2,65 г; 10,0 ммоля) в 1,2-диметоксиэтана (2,7 мл). В интенсивно перемешиваемую образовавшуюся суспензию при примерно 0°С в течение одного часа добавляют 13,4 мл раствора 0,90 М вышеупомянутого 4-([1,3]диоксан-2-ил)фенилмагнийбромида (12,0 ммоля). Полученному коричнево-желтому раствору дают нагреться и в дальнейшем перемешивают при комнатной температуре в течение 3 ч. Эту смесь охлаждают до примерно 0°С и гасят реакцию 7,5%-ным раствором аммонийхлорида в воде (20 мл). Водную фазу отделяют и экстрагируют этилацетатом (50 мл). Объединенные органические фазы промывают водой (20 мл), 7,5%-ным раствором карбоната натрия в воде (20 мл) и водой (20 мл). Объединенные органические фазы выпаривают под вакуумом. Раствор полученного продукта в виде масла в небольшом количестве этилацетата фильтруют и выпаривают. Полученное вещество в виде масла очищают хроматографией в колонке на силикагеле, элюируя смесью 1:2 этилацетата и гексана с получением в виде бесцветного масла основного изомера (N2-изомер) 5-(4'-[1,3]диоксан-2-илбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразола и в виде бесцветных кристаллов небольшого изомера (N1-изомер) 5-(4'-[1,3]диоксан-2-илбифенил-2-ил)-1-(тетрагидропиран-2-ил)-1Н-тетразола.
1H-ЯМР N2-изомера (400 МГц, CDCl3): 1,42-1,47 (m, 1H), 1,57-1,65 (m, 3H), 1,79-1,87 (m, 1H), 1,96-2,03 (m, 1H), 2,10-2,27 (m, 2H), 3,60-3,69 (m, 2H), 3,95-4,01 (m, 2H), 4,23-4,27 (m, 2H), 5,48 (s, 1H), 5,98 до 6,00 (m, 1H), 7,18-7,21 (m, 2H), 7,38-7,42 (m, 3H), 7,46-7,54 (m, 2H), 7,89-7,91 (m, 1H).
1H-ЯМР N1-изомера (400 МГц, CDCl3)): 0,98-1,02 (m, 1H), 1,31-1,36 (m, 1H), 1,42-1,47 (m, 2H), 1,51-1,61 (m, 1H), 1,87-1,96 (m, 2H), 2,14-2,26 (m, 1H), 3,25-3,31 (m, 1H), 3,70-3,75 (m, 1H), 3,93-4,00 (m, 2H), 4,22-4,27 (m, 2H), 4,84-4,87 (m, 1H), 5,45 (s, 1H), 7,12-7,15 (m, 2H), 7,40-7,42 (m, 2H), 7,50-7,68 (m, 4H).
Диапазон плавления N1-изомера 125-127°С.
Пример 4
Получение 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегида
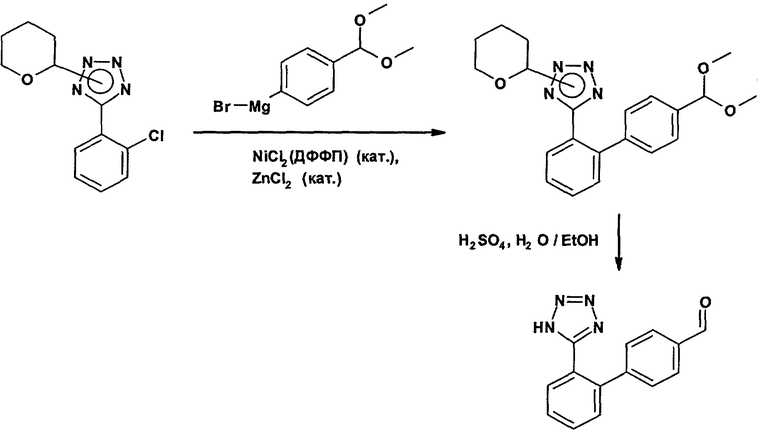
Суспензию магниевой стружки (6,31 г) в безводном тетрагидрофуране (59 мл) охлаждают до 14°С, обрабатывают 1 М раствором диизобутилалюмогидрида в тетрагидрофуране (2,35 мл, 2,4 ммоля) и перемешивают в течение 20 мин. При 14°С с интенсивным перемешиванием добавляют 1-бром-4-диметоксиметилбензола (2,72 г; 11,7 ммоля). После начала реакции в течение 45 мин добавляют еще 1-бром-4-диметоксиметилбензола (51,79 г; 223 ммоля) и одновременно смесь разбавляют двумя порциями безводного тетрагидрофурана (59 мл каждая). Приготовленную смесь в дальнейшем перемешивают при примерно 25°С в течение 2,5 ч. Концентрация 4-(диметоксиметил)фенилмагнийбромида в растворе над избытком магниевой стружки составляет примерно 1,0 М. В другой колбе смесь 5-(2-хлорфенил)-2-(тетрагидропиран-2-ил)-2Н-тетразола и 5-(2-хлорфенил)-1-(тетрагидропиран-2-ил)-1Н-тетразола (98,2%-ное содержание; 53,91 г; 200 ммолей) в инертной атмосфере растворяют в безводном тетрагидрофуране (37 мл) и добавляют дихлор[1,2-бис-(бифенилфосфино)этан]никеля(II) (0,862 г; 1,60 ммоля) и 0,5 М раствора хлорида цинка в тетрагидрофуране (6,0 мл; 3,0 ммоля). Интенсивно перемешиваемую образовавшуюся суспензию охлаждают до примерно 14°С и в течение одного часа добавляют 1,0 М раствора вышеупомянутого 4-(диметоксиметил)фенилмагнийбромида (229 мл; 230 ммолей), одновременно поддерживая внешним охлаждением температуру ниже 25°С. Темно-коричневую реакционную смесь перемешивают при комнатной температуре в течение 17,5 ч. После этого превращают больше 99% исходного материала и в смесь добавляют метанола (8,0 мл).
Под пониженным давлением отгоняют часть растворителей (примерно 156 мл). Добавляют этанола (в общей сложности 307 мл), одновременно отгоняя дополнительное количество растворителей. В образовавшуюся коричневую смесь при 50°С в течение 10 мин добавляют смесь 2 М водного раствора серной кислоты (32 мл; 64 ммоля) и воды (75 мл). Эту смесь в дальнейшем перемешивают при 50°С в течение 50 мин, при 60°С в течение 1,5 ч и при 35°С в течение ночи. Смесь перемешивают при 60°С с активированным углем (5,3 г) и ускорителем фильтрования (2,7 г) в общей сложности в течение 40 мин и затем фильтруют при примерно 55°С. Оранжевый фильтрат концентрируют отгонкой под пониженным давлением примерно 202 мл растворителей. После добавления воды (48 мл) при 50°С образовавшейся перемешиваемой суспензии в течение ночи дают остыть до комнатной температуры и в дальнейшем перемешивают при примерно 10°С в течение 90 мин. Твердые частицы собирают фильтрованием, промывают смесью 1:2 этанола и воды и сушат под пониженным давлением при примерно 60°С с получением в виде бледно-желтого кристаллического твердого вещества 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегида.
Диапазон плавления 188,6-189,9°С.
Пример 5
Получение 5-(4'-диэтоксиметилбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразола
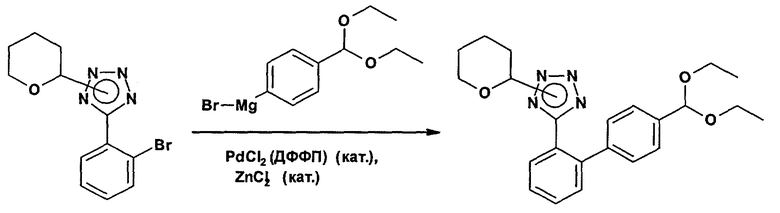
В суспензию магниевой стружки (5,11 г) в безводном тетрагидрофуране (40 мл) добавляют 1,2-дибромэтана (0,106 мл; 1,2 ммоля). Суспензию охлаждают до 12°С и добавляют 6 мл раствора 1-бром-4-(диэтоксиметил)бензола (53,6 г; 200 ммолей) в безводном тетрагидрофуране (120 мл) и вторую порцию 1,2-дибромэтана (0,106 мл; 1,2 ммоля). После начала реакции в течение 90 мин добавляют оставшийся раствор 1-бром-4-(диэтоксиметил)бензола. Приготовленную смесь в дальнейшем перемешивают при температуре от 20 до 25°С в течение 2,5 ч. Эту смесь разбавляют безводным тетрагидрофураном до общего объема 250 мл. Концентрация 4-(диэтоксиметил)фенилмагнийбромида в растворе над избытком магниевой стружки составляет примерно 0,78 М. В другой колбе в дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II)дихлорметановый продукт присоединения (0,012 г; 0,015 ммоля) добавляют 0,5 М раствора хлорида цинка в тетрагидрофуране (0,6 мл; 0,30 ммоля) и раствора смеси 5-(2-бромфенил)-2-(тетрагидропиран-2-ил)-2Н-тетразолаи 5-(2-бромфенил)-1-(тетрагидропиран-2-ил)-1Н-тетразола (4,99 г; 14,3 ммоля) в тетрагидрофуране (30 мл). В перемешиваемый образовавшийся желто-оранжевый раствор при комнатной температуре в течение двух часов добавляют 22,2 мл 0,78 М раствора вышеупомянутого 4-(диэтоксиметил)фенилмагнийбромида (17,3 ммоля). Полученный оранжевый раствор в дальнейшем перемешивают при комнатной температуре в течение 18 ч. После этого исходный материал больше не мог бы быть обнаружен тонкослойной хроматографией. Эту смесь охлаждают до примерно 0°С и добавляют раствор бикарбоната натрия (2,0 г) в воде (25 мл) и этилацетата (30 мл). Водную фазу отделяют и экстрагируют этилацетатом (40 мл). Объединенные органические фазы промывают раствором бикарбоната натрия (2,0 г) в воде (25 мл) и дважды водой (25 мл), после чего их выпаривают под вакуумом. Полученный продукт в виде оранжевого масла очищают хроматографией в колонке на силикагеле, элюируя смесью 1:4 этилацетата и гексана (в присутствии 0,3 об.% триэтиламина) с получением в виде бледно-желтого масла основного изомера (N2-изомер) 5-(4'-диэтоксиметилбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразола.
1Н-ЯМР N2-изомера (400 МГц, СDСl3): 1,24 (t, J=7,2 Гц, 6Н), 1,59-1,67 (m, 3Н), 1,85-2,03 (m, 2Н), 2,11-2,18 (m, 1Н), 3,50-3,74 (m, 6Н), 5,49 (s, 1Н), 5,97-5,99 (m, 1Н), 7,17-7,20 (m, 2Н), 7,38-7,40 (m, 2Н), 7,43-7,56 (m, 3Н), 7,90-7,92 (m, 1H).
Пример 6
Получение 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегида
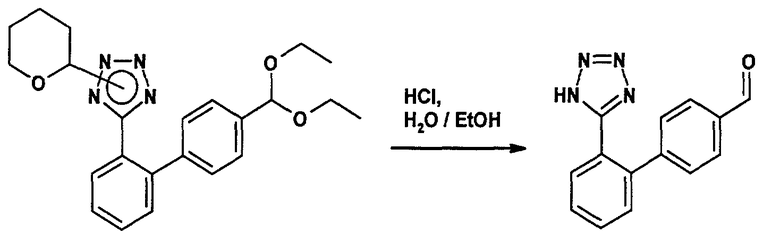
К 5-(4'-диэтоксиметилбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразолу (0,408 г; 1,00 ммоля) добавляют 94%-ного этанола (2,5 мл) и 2 н. водного раствора соляной кислоты (0,5 мл; 1,0 ммоля). Полученный раствор в течение 3 ч выдерживают при 45°С. После добавления воды (примерно 2 мл) смеси дают остыть до комнатной температуры и затем перемешивают при температуре от 0 до 5°С в течение 30 мин. Полученную суспензию фильтруют и твердые частицы промывают небольшим количеством воды и сушат под вакуумом при 40°С с получением в виде белого кристаллического порошка 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегида.
Температура плавления 187,5-190,0°С.
Пример 7
Получение 5-(4'-диметоксиметилбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразола в присутствии никелевого катализатора и в отсутствие цинковой соли
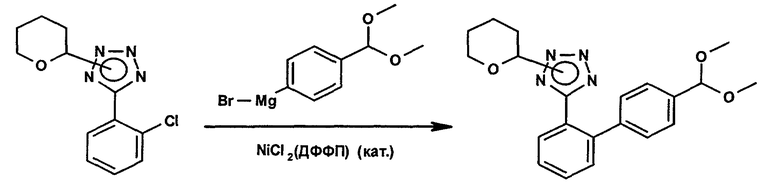
Суспензию магниевой стружки (2,35 г) в безводном тетрагидрофуране (66 мл) охлаждают до 14°С, обрабатывают 1 М раствором диизобутилалюмогидрида в тетрагидрофуране (1,8 мл; 1,8 ммоля) и перемешивают в течение 20 мин. При 14°С с интенсивным перемешиванием добавляют 1-бром-4-диметоксиметилбензола (1,02 г; 4,4 ммоля). После начала реакции в течение 50 мин добавляют дополнительно 1-бром-4-диметоксиметилбензола (19,32 г; 83,6 ммоля). Приготовленную смесь в дальнейшем перемешивают при примерно 25°С в течение 2,5 ч. Концентрация 4-(диметоксиметил)фенилмагнийбромида в растворе над избытком магниевой стружки составляет примерно 0,96 М. В другой колбе смесь 5-(2-хлорфенил)-2-(тетрагидропиран-2-ил)-2Н-тетразола и 5-(2-хлорфенил)-1-(тетрагидропиран-2-ил)-1Н-тетразола (94%-ное содержание; 4,22 г; 15,0 ммоля) в инертной атмосфере растворяют в безводном тетрагидрофуране (2,8 мл) и добавляют дихлор[1,2-бис-(бифенилфосфино)этан]никеля(II) (80,8 мг; 0,15 ммоля). Интенсивно перемешиваемую образовавшуюся суспензию охлаждают до примерно 15°С и в течение одного часа добавляют 0,96 М раствора вышеупомянутого 4-(диметоксиметил)фенилмагнийбромида (18 мл; 17,3 ммоля), одновременно поддерживая внешним охлаждением температуру ниже 25°С. Темно-коричневую реакционную смесь перемешивают при комнатной температуре в течение 22,5 ч. После этого превращают примерно 94% исходного материала. В эту смесь добавляют метанола (1,2 мл; 30 ммолей), после чего изопропилацетата (35 мл), раствора аммонийхлорида (0,4 г) в воде (10 мл) и воды (10 мл). Слои разделяют. Органический слой промывают водой (10 мл), три раза раствором бикарбоната натрия (1,0 г) в воде (12 мл) и дважды водой (10 мл), после чего его выпаривают под вакуумом. Полученный продукт в виде коричневого масла очищают хроматографией в колонке на силикагеле, элюируя смесью 1:4 этилацетата и гексана (в присутствии 0,3 об.% триэтиламина) с получением в виде бледно-желтого масла основного изомера (N2-изомер) 5-(4'-диметоксиметилбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразола.
1Н-ЯМР N2-изомера (400 МГц, CDCl3): 1,59-1,68 (m, 3H), 1,86-1,93 (m, 1H), 1,96-2,04 (m, 1H), 2,12-2,20 (m, 1H), 3,34 (s, 6H), 3,65-3,76 (m, 2H), 5,38 (s, 1H), 5,95-5,98 (m, 1H), 7,18-7,21 (m, 2H), 7,36-7,38 (m, 2H), 7,44-7,56 (m, 3H), 7,90-7,92 (m, 1H).
Пример 8
Попытка получения 5-(4'-диметоксиметилбифенил-2-ил)-2-(тетрагидропиран-2-ил)-2Н-тетразола в отсутствие катализатора
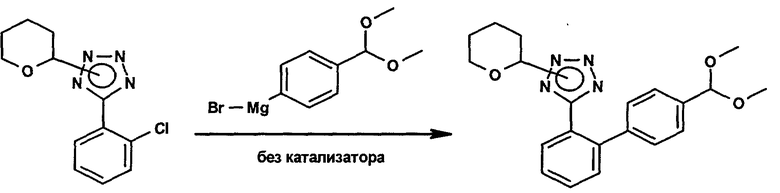
Смесь 5-(2-хлорфенил)-2-(тетрагидропиран-2-ил)-2Н-тетразола и 5-(2-хлорфенил)-1-(тетрагидропиран-2-ил)-1Н-тетразола (94%-ное содержание; 4,22 г; 15,0 ммоля; в таких же количествах, как использованные в примере 7) в инертной атмосфере растворяют в безводном тетрагидрофуране (2,8 мл). Интенсивно перемешиваемую образовавшуюся суспензию охлаждают до примерно 15°С и в течение одного часа добавляют 0,96 М раствора 4-(диметоксиметил)фенилмагнийбромида (18 мл; 17,3 ммоля; в таком же количестве, как использованное в примере 7), одновременно поддерживая внешним охлаждением температуру ниже 25°С. Коричневую реакционную смесь перемешивают при комнатной температуре в течение 22 ч. После этого проводят ВЭЖХ анализ образца, который, как обычно, гидролизуют разбавленной водной соляной кислотой. Анализ показывает наличие главным образом непревращенного исходного материала (определенного как 5-(2-хлорфенил)-1Н-тетразол) и меньше 0,25% по площади продукта реакции С-С-сочетания (определен как 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегид). Наконец, когда в смесь добавляют метанола (1,2 мл; 30 ммолей), отмечают необычно сильную экзотермию, которая указывает на то, что по прошествии общего времени реакции 23 ч все еще присутствует большая часть 4-(диметоксиметил)фенилмагнийбромида.
Пример 9
Получение 2-(тетрагидропиран-2-ил)-5-[4'-(тетрагидропиран-2-илоксиметил)бифенил-2-ил]-2Н-тетразола
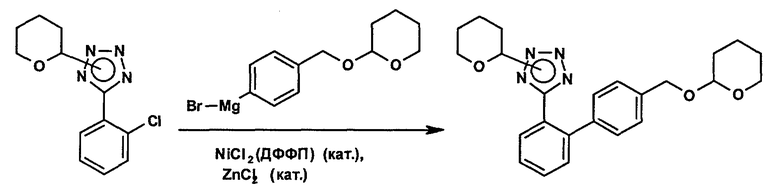
Суспензию магниевой стружки (0,48 г) в безводном тетрагидрофуране (13,5 мл) охлаждают до 14°С, обрабатывают раствором диизобутилалюмогидрида в толуоле (0,24 мл; 0,36 ммоля) концентрацией 25 мас.% и перемешивают в течение 20 мин. При 14°С с интенсивным перемешиванием добавляют 2-(4-бромбензилокси)тетрагидропирана (94,5%-ное содержание; 0,26 г; 0,90 ммоля). После начала реакции в течение 40 мин дополнительно добавляют 2-(4-бромбензилокси)тетрагидропирана (94,5%-ное содержание; 4,91 г; 17,1 ммоля). Приготовленную смесь в дальнейшем перемешивают при примерно 25°С в течение 2,5 ч. Теоретическая концентрация 4-(тетрагидропиран-2-илоксиметил)фенилмагнийбромида в растворе над избытком магниевой стружки составляет примерно 0,95 М. В другой колбе в инертной атмосфере в безводном тетрагидрофуране (2,8 мл) растворяют смесь 5-(2-хлорфенил)-2-(тетрагидропиран-2-ил)-2Н-тетразола и 5-(2-хлорфенил)-1-(тетрагидропиран-2-ил)-1Н-тетразола (94%-ное содержание; 4,22 г; 15,0 ммоля) и добавляют дихлор[1,2-бис-(бифенилфосфино)этан]никеля(II) (80,8 мг; 0,15 ммоля) и 0,5 М раствора хлорида цинка в тетрагидрофуране (0,45 мл; 0,23 ммоля). Интенсивно перемешиваемую образовавшуюся суспензию охлаждают до примерно 15°С и в течение одного часа добавляют раствора вышеупомянутого 4-(тетрагидропиран-2-илоксиметил)фенилмагнийбромида (19 мл; 18 ммолей), одновременно поддерживая внешним охлаждением температуру ниже 25°С.Коричневую реакционную смесь перемешивают при комнатной температуре в течение 17,5 ч. После этого, в соответствии с ВЭЖХ анализом, превращают примерно 97% исходного материала. В эту смесь добавляют метанола (1,2 мл; 30 ммолей), после чего изопропилацетата (40 мл), раствора аммонийхлорида (0,4 г) в воде (10 мл) и воды (10 мл). Слои разделяют. Органический слой промывают водой (10 мл) и три раза раствором бикарбоната натрия (1,0 г) в воде (12 мл). Водный слой экстрагируют изопропилацетатом (50 мл). Объединенные органические слои дважды промывают водой (10 мл) и выпаривают под вакуумом. Полученный продукт в виде зеленоватого масла очищают хроматографией в колонке на силикагеле, элюируя смесью 1:4 этилацетата и гексана (в присутствии 0,3 об.% триэтиламина), с получением в виде бесцветного масла основного изомера (N2-изомер) 2-(тетрагидропиран-2-ил)-5-[4'-(тетрагидропиран-2-илоксиметил)бифенил-2-ил]-2Н-тетразола.
МС (ESI+): m/z=421 [М+Н]+и m/z=438 [М+NH4]+.
Пример 10
Получение [2'-(1Н-тетразол-5-ил)бифенил-4-ил]метанола
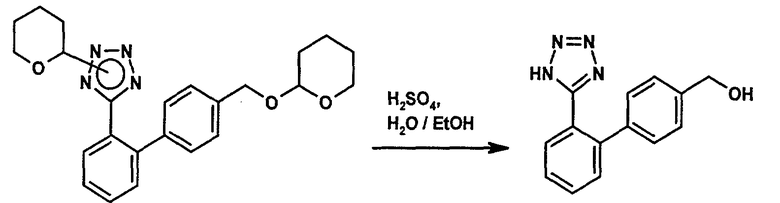
К 2-(тетрагидропиран-2-ил)-5-[4'-(тетрагидропиран-2-илоксиметил)бифенил-2-ил]-2Н-тетразолу (3,36 г; 8,00 ммоля) добавляют 94%-ного этанола (12 мл) и 2 М водного раствора серной кислоты (1,0 мл; 2,0 ммоля). Полученную смесь выдерживают при 45°С в течение 3,5 ч. Медленно добавляют воды (16 мл) и смеси дают остыть до комнатной температуры. Добавлением 2 М водного раствора гидроксида натрия (0,6 мл) рН реакционной смеси доводят до значения от 2 до 3. Смесь концентрируют под пониженным давлением, разбавляют изопропилацетатом (15 мл) и три раза промывают водой (3 мл). Органический экстракт концентрируют под пониженным давлением до объема примерно 4 мл и медленно добавляют трет-бутилметилового эфира (в общей сложности 8 мл). Эту смесь перемешивают в течение ночи, разбавляют небольшим количеством изопропилацетата и в дальнейшем перемешивают в течение 4,5 ч. Суспендированный белый твердый материал отфильтровывают, промывают небольшим количеством изопропилацетата и сушат под пониженным давлением с получением [2'-(1Н-тетразол-5-ил)бифенил-4-ил]метанола. Фильтрат концентрируют под пониженным давлением и медленно добавляют трет-бутилметилового эфира (3 мл) и гептана (0,5 мл). Смесь перемешивают при комнатной температуре в течение ночи и при температуре от 0 до 5°С в течение 1 ч. Суспендированный белый твердый продукт отфильтровывают, промывают небольшим количеством изопропилацетата и сушат под пониженным давлением с получением второй порции [2'-(1Н-тетразол-5-ил)бифенил-4-ил]метанола.
Диапазон плавления 132,4-134,6°С.
Пример 11
Получение 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегида
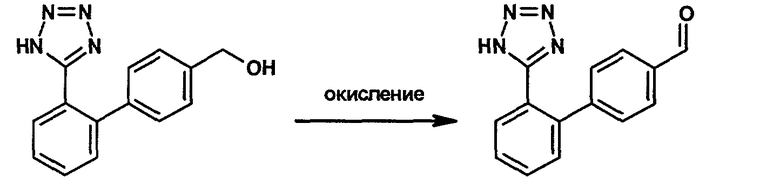
Смесь [2'-(1Н-тетразол-5-ил)бифенил-4-ил]метанола (1,03 г; 4,0 ммоля), триэтиламина (2,80 мл; 20 ммолей) и диметилсульфоксида (2 мл) охлаждают до 12°С и в течение 10 мин добавляют раствор пиридинового комплекса триоксида серы (1,27 г; 8,0 ммоля) в диметилсульфоксиде (6,4 мл). Полученный прозрачный раствор перемешивают при комнатной температуре в течение почти 48 ч, во время которых добавляют еще триэтиламина (0,28 мл; 2,0 ммоля). Эту смесь разбавляют этилацетатом (10 мл), охлаждают до температуры от 0 до 5°С и медленно обрабатывают 2 М водным раствором соляной кислоты (15 мл). Водный слой отделяют и экстрагируют этилацетатом (10 мл). Объединенные органические слои разбавляют этилацетатом (10 мл), промывают 2 М водным раствором соляной кислоты (15 мл), дважды 1 М водным раствором соляной кислоты (10 мл) и 10%-ным водным раствором хлорида натрия (10 мл). Органический экстракт концентрируют при 45°С под пониженным давлением до объема от примерно 4 до 5 мл. Образующуюся суспензию перемешивают при комнатной температуре в течение 45 мин и при температуре от 0 до 5°С в течение одного часа с последующим ее фильтрованием. Твердые частицы промывают холодным этилацетатом (2 мл) и сушат при 45°С под пониженным давлением с получением в виде белого кристаллического твердого вещества 2'-(1Н-тетразол-5-ил)бифенил-4-карбальдегида. Вторая порция может быть получена концентрированием маточного раствора до объема примерно 1 мл и отфильтровыванием образующегося твердого вещества.
Диапазон плавления 188,2-189,3°С.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ БЛОКАТОРА АНГИОТЕНЗИНОВОГО РЕЦЕПТОРА | 2003 |
|
RU2412173C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВАЛСАРТАНА | 2003 |
|
RU2348619C2 |
| СПОСОБЫ КРОСС-СОЧЕТАНИЯ | 2017 |
|
RU2777977C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОМЕРНО И ДИАСТЕРЕОМЕРНО ОБОГАЩЕННЫХ ЦИКЛОБУТАНАМИНОВ И -АМИДОВ | 2018 |
|
RU2793738C2 |
| СПОСОБ ПОЛУЧЕНИЯ (E)-N-(3-ТРЕТ-БУТИЛ-5-(2,4-ДИОКСО-3,4-ДИГИДРОПИРИМИДИН-1(2Н)-ИЛ)-2-МЕТОКСИ-СТИРИЛ)ФЕНИЛ)МЕТАНСУЛЬФОНАМИДА И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ЕГО ПОЛУЧЕНИЯ | 2010 |
|
RU2524573C2 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРОВ 5-ЛИПОКСИГЕНАЗЫ, ИМЕЮЩИХ РАЗЛИЧАЮЩИЕСЯ ГЕТЕРОЦИКЛИЧЕСКИЕ СИСТЕМЫ | 2000 |
|
RU2177005C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОРИКОНАЗОЛА И ЕГО АНАЛОГОВ | 2013 |
|
RU2619928C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-ЗАМЕЩЕННЫХ АНТРАЦИКЛИНОНОВ | 1989 |
|
RU2071463C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИАРИЛЗАМЕЩЕННОЙ 4-АМИНОМАСЛЯНОЙ КИСЛОТЫ ИЛИ ЕЕ ПРОИЗВОДНЫХ И ИХ ПРИМЕНЕНИЕ В ИЗГОТОВЛЕНИИ ИНГИБИТОРОВ НЭП | 2007 |
|
RU2469019C2 |
| АНАЛОГ ПИРИДИНО[1,2-А]ПИРИМИДОНА, ИСПОЛЬЗУЕМЫЙ В КАЧЕСТВЕ ИНГИБИТОРА mTOR/PI3K | 2015 |
|
RU2658912C1 |
Описывается улучшенный способ получения бифенилпроизводных тетразола формул (I) и (IA)
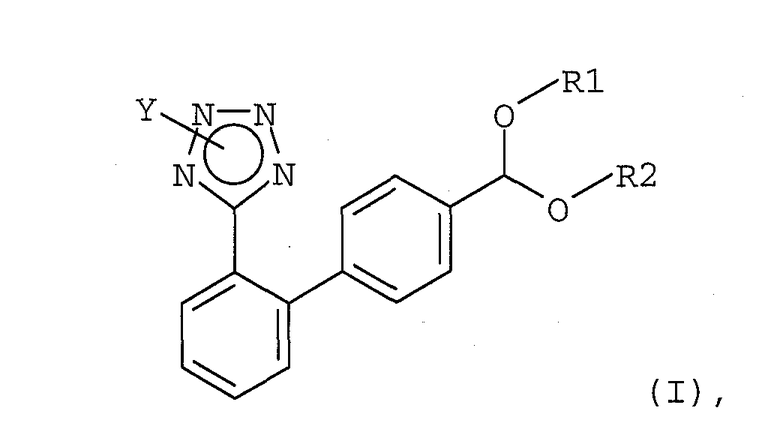
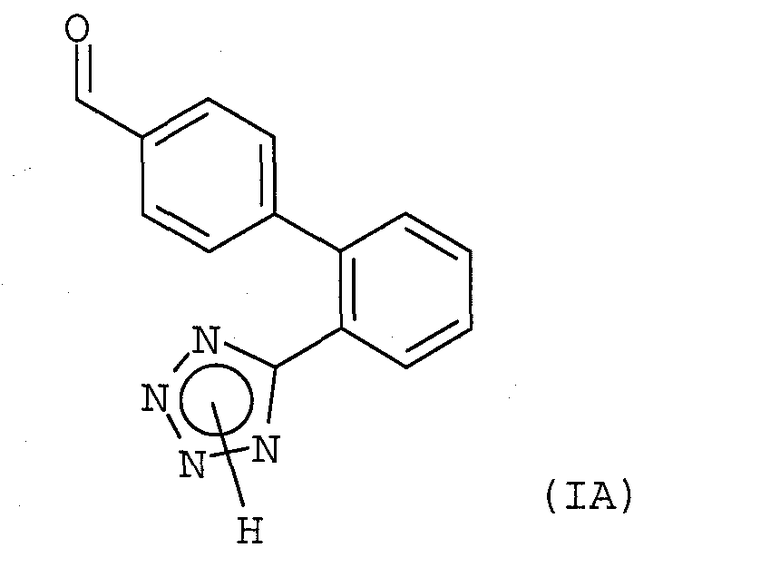
являющихся промежуточными продуктами в синтезе ARB (антагонистов рецепторов ангиотензина II или антагонистов рецепторов AT1), включающих в качестве общей структурной компоненты (1Н-тетразол-5-ил)бифенильное кольцо. Способ заключается во взаимодействии соединения (IIb) с соединением (IIc) в присутствии катализатора с переходным металлом и каталитически эффективного количества соли металла как добавки с последующим, в случае необходимости, снятием гидроксизащитной группы и/или защитной группы на тетразольном кольце и окислением гидроксигруппы до альдегида. 6 н. и 17 з.п. ф-лы.
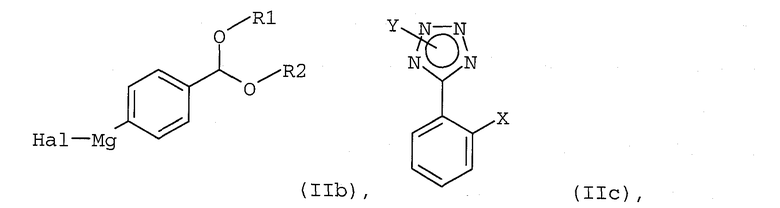
1. Способ получения соединения формулы (I)
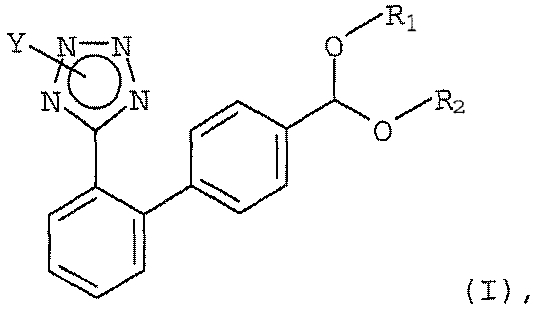
в которой Y обозначает защищающую тетразол группу, выбранную из ряда, включающего 2-тетрагидропиранил и 2-тетрагидрофуранил, a R1 и R2 независимо друг от друга обозначают C1-С10алкил или R1 и R2 совместно образуют С2-С10алкилен; включающий реакцию арилмагнийгалогенидного соединения формулы (IIb)
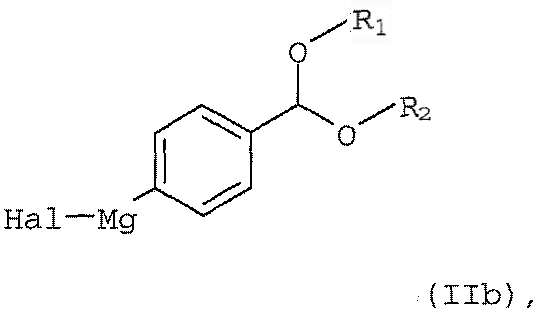
в которой Hal обозначает атом хлора, брома или иода,
в присутствии катализатора с переходным металлом и каталитически эффективного количества соли металла как добавки, где
катализатор с переходным металлом представляет собой комплекс
переходного металла или соли переходного металла и одного, двух или до четырех координационных лигандов, выбранных из ряда, включающего трифенилфосфин, три(орто-толил)фосфин, три(пара-толил)фосфин, триметилфосфин, триэтилфосфин, трибутилфосфин, три(1,1-диметилэтил)фосфин, трициклопентилфосфин, трициклогексилфосфин, триметилфосфит, триэтилфосфит, три(1-метилэтил)фосфит, трициклопентилфосфит, трициклогексилфосфит, 1,2-бис-(бифенилфосфино)этан, 1,3-бис-(бифенилфосфино)пропан, 1,4-бис-(бифенилфосфино)бутан, 1,1'-бис-(бифенилфосфино)ферроцен, 1,1'-бис-(ди[2-пропил]фосфино)ферроцен, 1,1'-бис-(дитрет-бутилфосфино)ферроцен, 1,2-бис-(бифенилфосфино)бензол, 2,2'-бис-(бифенилфосфино)-1,1'-бифенил, 2,2'-бис-(бифенилфосфино)-1,1'-бинафтил, бис-(2-бифенилфосфинофенил)эфир и 9,9-диметил-4,5-бис-(бифенилфосфино)ксантен, а соль переходного металла выбирают из ряда, включающего хлорид никеля(II), бромид никеля(II) и ацетилацетонат никеля(II), хлорид палладия(II), бромид палладия(II) и ацетат палладия(II);
катализатор с переходным металлом выбирают из ряда, включающего дихлорбис-(трифенилфосфин)никель(II), дихлор[1,2-бис-(бифенилфосфино)этан]никель(II) и дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II), дихлорбис-(трифенилфосфин)палладий(II), дихлор[1,3-бис-(бифенилфосфино)пропан]палладий(II) и дихлор[ 1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или дихлорметановый продукт его присоединения;
катализатор с переходным металлом представляет собой переходный металл не в форме комплекса, который выбирают из ряда, включающего никель и палладий; или в котором катализатор с переходным металлом представляет собой соль переходного металла не в форме комплекса, которую выбирают из ряда, включающего хлорид, бромид, иодид, гидроксид, оксид, ацетат, гидроксиацетат, пропионат, сукцинат, трифторацетат, ацетилацетонат, нитрат, цианид, сульфат, трифторметансульфонат, метансульфонат, бензолсульфонат и п-толуолсульфонат никеля(II), и палладия(II); а
соль металла как добавка представляет собой соль цинка(II);
с соединением формулы (II с)
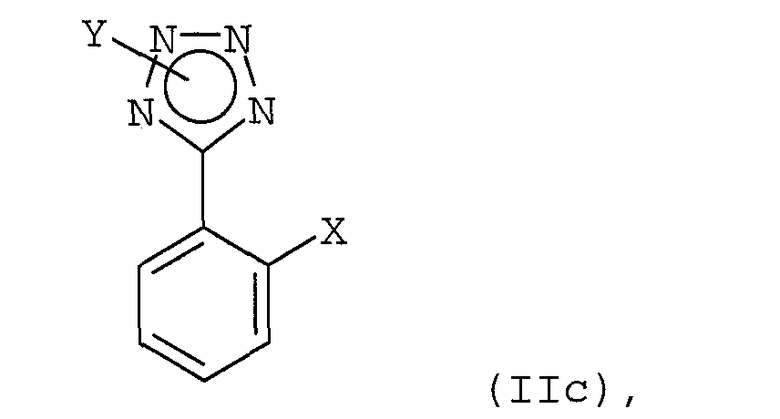
в которой Х обозначает атом хлора или брома; и выделение полученного соединения формулы (I).
2. Способ по п.1, в котором арилмагнийгалогенидный реагент формулы (IIb) получают реакцией соединения формулы (IIа)
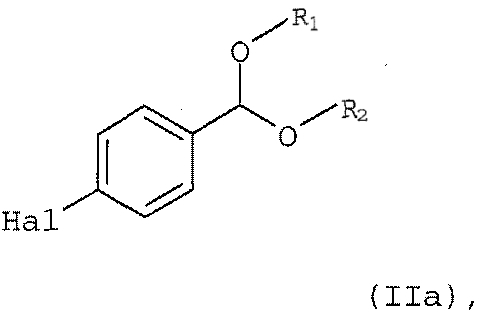
в которой R1, R2 и Hal имеют значения, указанные в п.1, с активной формой магния в соответствующем растворителе.
3. Способ по п.1 или 2, в котором заместитель Y представляет собой 2-тетрагидропиранил.
4. Способ по п.1 или 2, в котором катализатор с переходным металлом выбирают из ряда, включающего дихлорбис-(трифенилфосфин)никель(II), дихлор[1,2-бис-(бифенилфосфино)этан]никель(II) и дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II).
5. Способ по п.1 или 2, в котором катализатор с переходным металлом выбирают из ряда, включающего дихлорбис-(трифенилфосфин)палладий(II), дихлор[1,3-бис-(бифенилфосфино)пропан]палладий(II) и дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или дихлорметановый продукт его присоединения.
6. Способ по п.1 или 2, в котором катализатор с переходным металлом представляет собой дихлор[1,2-бис-(бифенилфосфино)этан]никель(II).
7. Способ по п.1 или 2, в котором катализатор с переходным металлом представляет собой дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или дихлорметановый продукт его присоединения.
8. Способ по п.1 или 2, в котором соль металла как добавка представляет собой хлорид цинка(II) или бромид цинка(II).
9. Способ получения соединения формулы (IA)
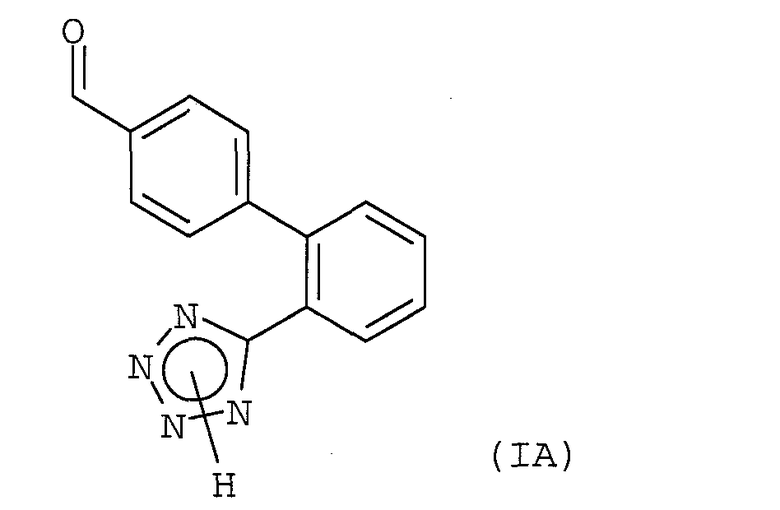
включающий реакцию арилмагнийгалогенидного соединения формулы (IIb)
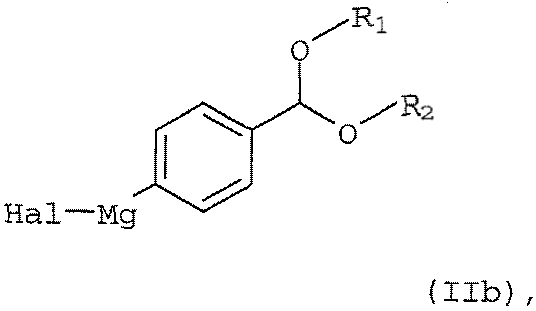
в которой Hal обозначает атом хлора, брома или иода, a R1 и R2 независимо друг от друга обозначают C1-С10алкил или R1 и R2 совместно образуют С2-С10алкилен, в присутствии катализатора с переходным металлом и каталитически эффективного количества соли металла как добавки, где катализатор с переходным металлом представляет собой комплекс переходного металла или соли переходного металла и одного, двух или до четырех координационных лигандов, выбранных из ряда, включающего трифенилфосфин, три(орто-толил)фосфин, три(пара-толил)фосфин, триметилфосфин, триэтилфосфин, трибутилфосфин, три(1,1-диметилэтил)фосфин, трициклопентилфосфин, трициклогексилфосфин, триметилфосфит, триэтилфосфит, три(1-метилэтил)фосфит, трициклопентилфосфит, трициклогексилфосфит, 1,2-бис-(бифенилфосфино)этан, 1,3-бис-(бифенилфосфино)пропан, 1,4-бис-(бифенилфосфино)бутан, 1,1'-бис-(бифенилфосфино)ферроцен, 1,1'-бис-(ди[2-пропил]фосфино)ферроцен, 1,1'-бис-(дитрет-бутилфосфино)ферроцен, 1,2-бис-(бифенилфосфино)бензол, 2,2'-бис-(бифенилфосфино)-1,1'-бифенил, 2,2'-бис-(бифенилфосфино)-1,1'-бинафтил, бис-(2-бифенилфосфинофенил)эфир и 9,9-диметил-4,5-бис-(бифенилфосфино)ксантен, а соль переходного металла выбирают из ряда, включающего хлорид никеля(II), бромид никеля(II) и ацетилацетонат никеля(II), хлорид палладия(II), бромид палладия(II) и ацетат палладия(II);
катализатор с переходным металлом выбирают из ряда, включающего дихлорбис-(трифенилфосфин)никель(II), дихлор[1,2-бис-(бифенилфосфино)этан]никель(II) и дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II), дихлорбис-(трифенилфосфин)палладий(II), дихлор[1,3-бис-(бифенилфосфино)пропан] палладий(II) и дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или дихлорметановый продукт его присоединения;
катализатор с переходным металлом представляет собой переходный металл не в форме комплекса, который выбирают из ряда, включающего никель и палладий; или в котором катализатор с переходным металлом представляет собой соль переходного металла не в форме комплекса, которую выбирают из ряда, включающего хлорид, бромид, иодид, гидроксид, оксид, ацетат, гидроксиацетат, пропионат, сукцинат,
трифторацетат, ацетилацетонат, нитрат, цианид, сульфат, трифторметансульфонат, метансульфонат, бензолсульфонат и п-толуолсульфонат никеля(II), и палладия(II); а
соль металла как добавка представляет собой соль цинка(II);
с соединением формулы (IIс)
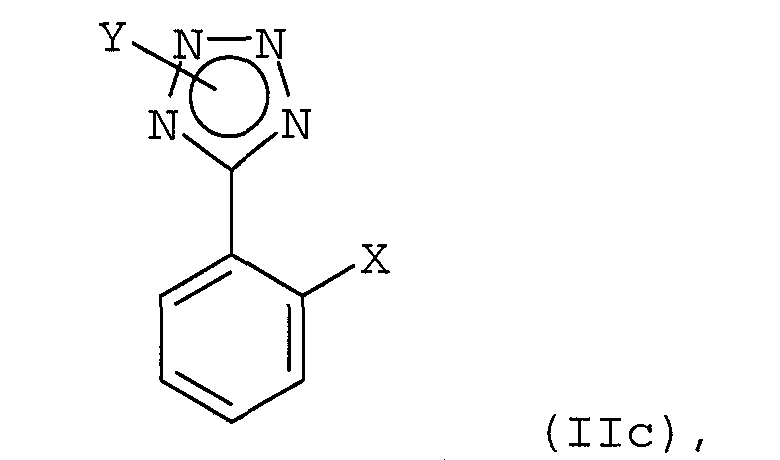
в которой Х обозначает атом хлора или брома, Y обозначает защищающую тетразол группу, выбранную из ряда, включающего 2-тетрагидропиранил и 2-тетрагидрофуранил, с получением соединения формулы (I)
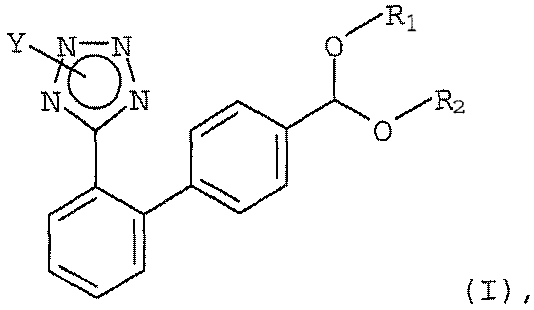
в которой Y обозначает защищающую тетразол группу, выбранную из ряда, включающего 2-тетрагидропиранил и 2-тетрагидрофуранил, a R1 и R2 независимо друг от друга обозначают C1-С10алкил или R1 и R2 совместно образуют С2-С10алкилен; и удаление защитной группы у соединения формулы (I) с получением соединения формулы (IA).
10. Способ по п.9, в котором заместитель Y представляет собой 2-тетрагидропиранил.
11. Способ получения соединения формулы (IС)
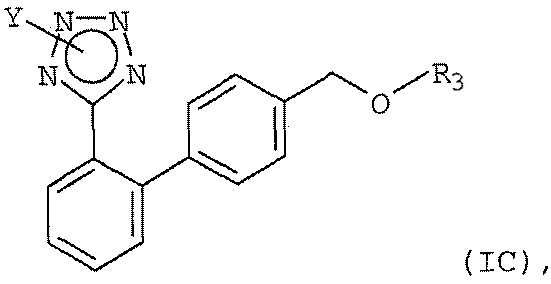
в которой Y обозначает защищающую тетразол группу, выбранную из ряда, включающего 2-тетрагидропиранил и 2-тетрагидрофуранил, а R3 выбран из группы, состоящей из 2-тетрагидропиранила или 2-тетрагидрофуранила; включающий реакцию арилмагнийгалогенидного соединения формулы (IIIb)
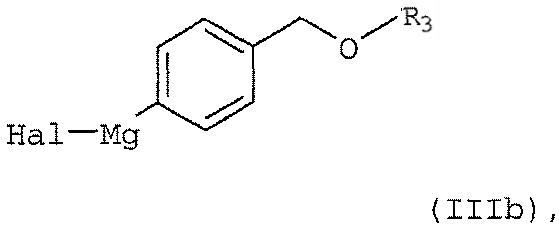
в которой Hal обозначает атом хлора, брома или иода, а R3 выбран из группы, состоящей из 2-тетрагидропиранила или 2-тетрагидрофуранила, в присутствии катализатора с переходным металлом и каталитически эффективного количества соли металла как добавки, где
катализатор с переходным металлом представляет собой комплекс переходного металла или соли переходного металла и одного, двух или до четырех координационных лигандов, выбранных из ряда, включающего трифенилфосфин, три(орто-толил)фосфин, три(пара-толил)фосфин, триметилфосфин, триэтилфосфин, трибутилфосфин, три(1,1-диметилэтил)фосфин, трициклопентилфосфин, трициклогексилфосфин, триметилфосфит, триэтилфосфит, три(1-метилэтил)фосфит, трициклопентилфосфит, трициклогексилфосфит, 1,2-бис-(бифенилфосфино)этан, 1,3 -бис-(бифенилфосфино)пропан, 1,4-бис-(бифенилфосфино)бутан, 1,1'-бис-(бифенилфосфино)ферроцен, 1,1'-бис-(ди[2-пропил]фосфино)ферроцен, 1,1'-бис-(дитрет-бутилфосфино)ферроцен, 1,2-бис-(бифенилфосфино)бензол, 2,2'-бис-(бифенилфосфино)-1,1'-бифенил, 2,2'-бис-(бифенилфосфино)-1,1'-бинафтил, бис-(2-бифенилфосфинофенил)эфир и 9,9-диметил-4,5-бис-(бифенилфосфино)ксантен, а соль переходного металла выбирают из ряда, включающего хлорид никеля(II), бромид никеля(II) и ацетилацетонат никеля(II), хлорид палладия(II), бромид палладия(II) и ацетат палладия(II);
катализатор с переходным металлом выбирают из ряда, включающего дихлорбис-(трифенилфосфин)никель(II), дихлор[1,2-бис-(бифенилфосфино)этан]никель(II) и дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II), дихлорбис-(трифенилфосфин)палладий(II), дихлор[1,3-бис-(бифенилфосфино)пропан]палладий(II) и дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или дихлорметановый продукт его присоединения;
катализатор с переходным металлом представляет собой переходный металл не в форме комплекса, который выбирают из ряда, включающего никель и палладий; или в котором катализатор с переходным металлом представляет собой соль переходного металла не в форме комплекса, которую выбирают из ряда, включающего хлорид, бромид, иодид, гидроксид, оксид, ацетат, гидроксиацетат, пропионат, сукцинат, трифторацетат, ацетилацетонат, нитрат, цианид, сульфат, трифторметансульфонат, метансульфонат, бензолсульфонат и п-толуолсульфонат никеля(II), и палладия(II); а
соль металла как добавка представляет собой соль цинка(II);
с соединением формулы (IIс)
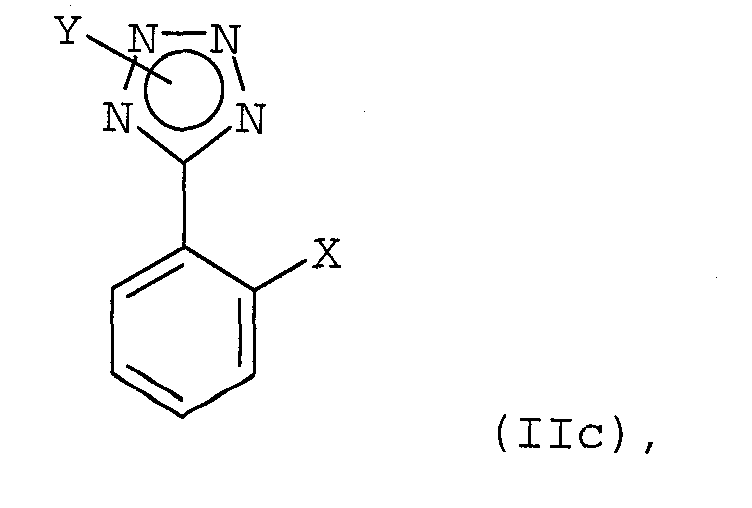
в которой Х обозначает атом хлора или брома, Y обозначает защищающую тетразол группу, выбранную из ряда, включающего 2-тетрагидропиранил и 2-тетрагидрофуранил; и выделение полученного соединения формулы (IC).
12. Способ по п.11, в котором арилмагнийгалогенидный реагент формулы (IIIb) получают реакцией соединения формулы (IIIa)
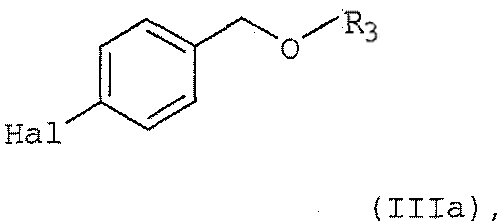
в которой R3 и Hal имеют значения, указанные в п.11, с активной формой магния в соответствующем растворителе.
13. Способ по п.11 или 12, в котором заместитель Y представляет собой 2-тетрагидропиранил.
14. Способ по п.11 или 12, в котором катализатор с переходным металлом выбирают из ряда, включающего дихлорбис-(трифенилфосфин)никель(II), дихлор[1,2-бис-(бифенилфосфино)этан]никель(II) и дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II).
15. Способ по п.11 или 12, в котором катализатор с переходным металлом выбирают из ряда, включающего дихлорбис-(трифенилфосфин)палладий(II), дихлор[1,3-бис-(бифенилфосфино)пропан]палладий(II) и дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или дихлорметановый продукт его присоединения.
16. Способ по п.11 или 12, в котором катализатор с переходным металлом представляет собой дихлор[1,2-бис-(бифенилфосфино)этан]никель(II).
17. Способ по п.11 или 12, в котором катализатор с переходным металлом представляет собой дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или дихлорметановый продукт его присоединения.
18. Способ по п.11 или 12, в котором соль металла как добавка представляет собой хлорид цинка(II) или бромид цинка(II).
19. Способ получения соединения формулы (IB)
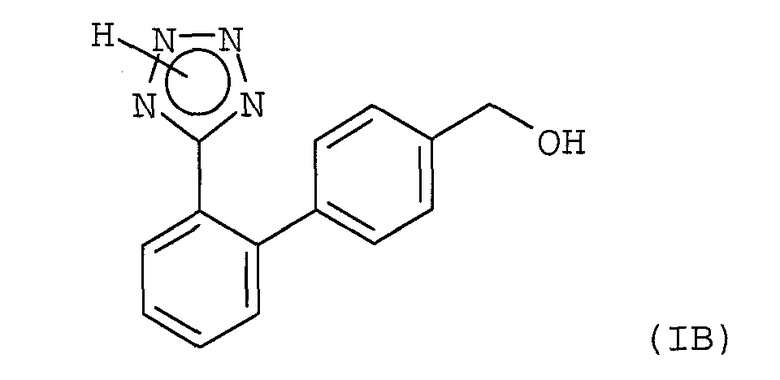
включающий реакцию арилмагнийгалогенидного соединения формулы (IIIb)
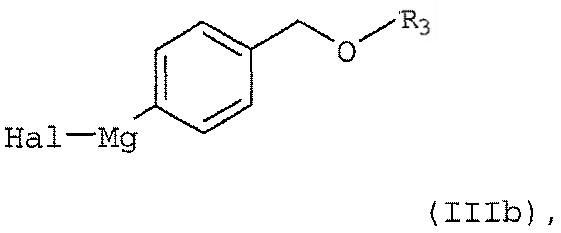
в которой Hal обозначает атом хлора, брома или иода, а R3 выбран из группы, состоящей из 2-тетрагидропиранила или 2-тетрагидрофуранила, в присутствии катализатора с переходным металлом и каталитически эффективного количества соли металла как добавки, где
катализатор с переходным металлом представляет собой комплекс переходного металла или соли переходного металла и одного, двух или до четырех координационных лигандов, выбранных из ряда, включающего трифенилфосфин, три(орто-толил)фосфин, три(пара-толил)фосфин, триметилфосфин, триэтилфосфин, трибутилфосфин, три(1,1-диметилэтил)фосфин, трициклопентилфосфин, трициклогексилфосфин, триметилфосфит, триэтилфосфит, три(1-метилэтил)фосфит, трициклопентилфосфит, трициклогексилфосфит, 1,2-бис-(бифенилфосфино)этан, 1,3-бис-(бифенилфосфино)пропан, 1,4-бис-(бифенилфосфино)бутан, 1,1'-бис-(бифенилфосфино)ферроцен, 1,1'-бис-(ди[2-пропил]фосфино)ферроцен, 1,1'-бис-(дитрет-бутилфосфино)ферроцен, 1,2-бис-(бифенилфосфино)бензол, 2,2'-бис-(бифенилфосфино)-1,1'-бифенил, 2,2'-бис-(бифенилфосфино)-1,1'-бинафтил, бис-(2-бифенилфосфинофенил)эфир и 9,9-диметил-4,5-бис-(бифенилфосфино)ксантен, а соль переходного металла выбирают из ряда, включающего хлорид никеля(II), бромид никеля(II) и ацетилацетонат никеля(II), хлорид палладия(II), бромид палладия(II) и ацетат палладия(II);
катализатор с переходным металлом выбирают из ряда, включающего дихлорбис-(трифенилфосфин)никель(II), дихлор[1,2-бис-(бифенилфосфино)этан]никель(II) и дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II), дихлорбис-(трифенилфосфин)палладий(II), дихлор[1,3-бис-(бифенилфосфино)пропан]палладий(II) и дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или дихлорметановый продукт его присоединения;
катализатор с переходным металлом представляет собой переходный металл не в форме комплекса, который выбирают из ряда, включающего никель и палладий; или в котором катализатор с переходным металлом представляет собой соль переходного металла не в форме комплекса, которую выбирают из ряда, включающего хлорид, бромид, иодид, гидроксид, оксид, ацетат, гидроксиацетат, пропионат, сукцинат, трифторацетат, ацетилацетонат, нитрат, цианид, сульфат, трифторметансульфонат, метансульфонат, бензолсульфонат и п-толуолсульфонат никеля(II), и палладия(II); а
соль металла как добавка представляет собой соль цинка(II);
с соединением формулы (IIс)
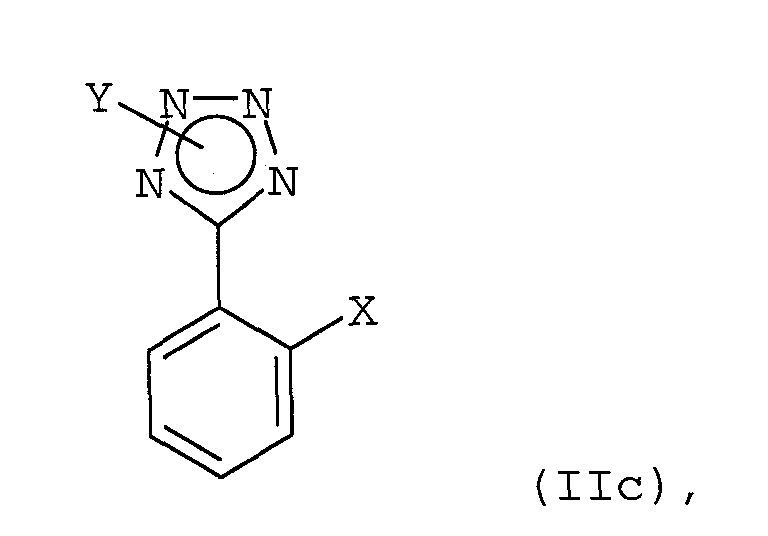
в которой Х обозначает атом хлора или брома, Y обозначает защищающую тетразол группу, выбранную из ряда, включающего 2-тетрагидропиранил и 2-тетрагидрофуранил;
с получением соединения формулы (IС)
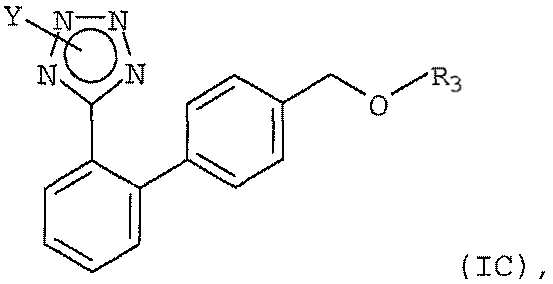
в которой Y обозначает защищающую тетразол группу, выбранную из ряда, включающего 2-тетрагидропиранил и 2-тетрагидрофуранил, а R3 выбран из группы, состоящей из 2-тетрагидропиранила или 2-тетрагидрофуранила; и удаление защитной группы у соединения формулы (IC) с получением соединения формулы (IB).
20. Способ по п.19, в котором заместитель Y представляет собой 2-тетрагидропиранил.
21. Способ получения соединения формулы (IA)
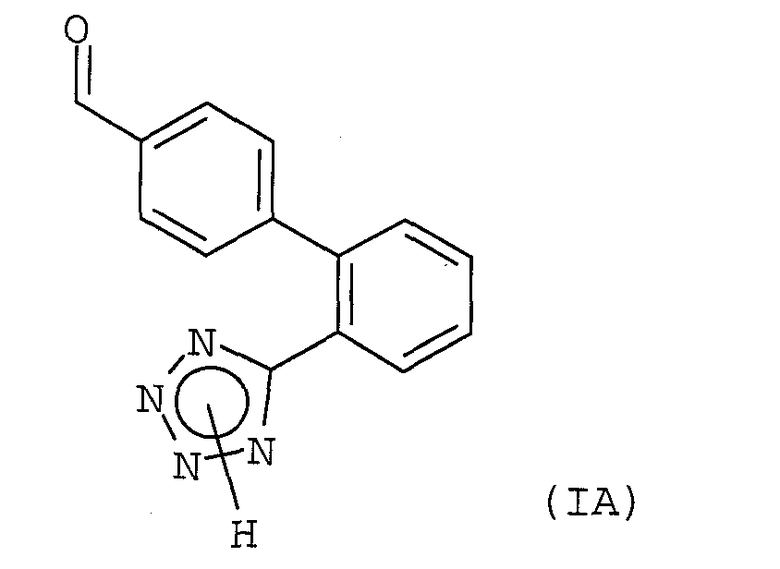
включающий реакцию арилмагнийгалогенидного соединения формулы (IIIb)
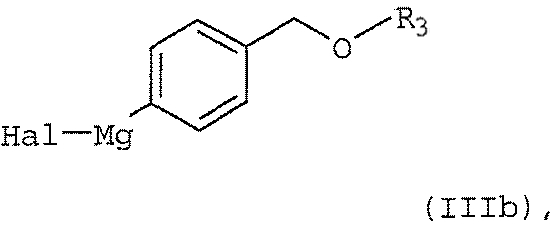
в которой Hal обозначает атом хлора, брома или иода, а R3 выбран из группы, состоящей из 2-тетрагидропиранила или 2-тетрагидрофуранила, в присутствии катализатора с переходным металлом и каталитически эффективного количества соли металла как добавки, где
катализатор с переходным металлом представляет собой комплекс переходного металла или соли переходного металла и одного, двух или до четырех координационных лигандов, выбранных из ряда, включающего трифенилфосфин, три(орто-толил)фосфин, три(пара-толил)фосфин, триметилфосфин, триэтилфосфин, трибутилфосфин, три(1,1-диметилэтил)фосфин, трициклопентилфосфин, трициклогексилфосфин, триметилфосфит, триэтилфосфит, три(1-метилэтил)фосфит, трициклопентилфосфит, трициклогексилфосфит, 1,2-бис-(бифенилфосфино)этан, 1,3-бис-(бифенилфосфино)пропан, 1,4-бис-(бифенилфосфино)бутан, 1,1'-бис-(бифенилфосфино)ферроцен, 1,1'-бис-(ди[2-пропил]фосфино)ферроцен, 1,1'-бис-(дитрет-бутилфосфино)ферроцен, 1,2-бис-(бифенилфосфино)бензол, 2,2'-бис-(бифенилфосфино)-1,1'-бифенил, 2,2'-бис-(бифенилфосфино)-1,1'-бинафтил, бис-(2-бифенилфосфинофенил)эфир и 9,9-диметил-4,5-бис-(бифенилфосфино)ксантен, а соль переходного металла выбирают из ряда, включающего хлорид никеля(II), бромид никеля(II) и ацетилацетонат никеля(II), хлорид палладия(II), бромид палладия(II) и ацетат палладия(II);
катализатор с переходным металлом выбирают из ряда, включающего дихлорбис-(трифенилфосфин)никель(II), дихлор[1,2-бис-(бифенилфосфино)этан)никель(II) и дихлор[1,3-бис-(бифенилфосфино)пропан]никель(II), дихлорбис-(трифенилфосфин)палладий(II), дихлор[1,3-бис-(бифенилфосфино)пропан]палладий(II) и дихлор[1,1'-бис-(бифенилфосфино)ферроцен]палладий(II) или дихлорметановый продукт его присоединения;
катализатор с переходным металлом представляет собой переходный металл не в форме комплекса, который выбирают из ряда, включающего никель и палладий; или в котором катализатор с переходным металлом представляет собой соль переходного металла не в форме комплекса, которую выбирают из ряда, включающего хлорид, бромид, иодид, гидроксид, оксид, ацетат, гидроксиацетат, пропионат, сукцинат, трифторацетат, ацетилацетонат, нитрат, цианид, сульфат, трифторметансульфонат, метансульфонат, бензолсульфонат и п-толуолсульфонат никеля(II), и палладия(II); а
соль металла как добавка представляет собой соль цинка(II);
с соединением формулы (IIс)
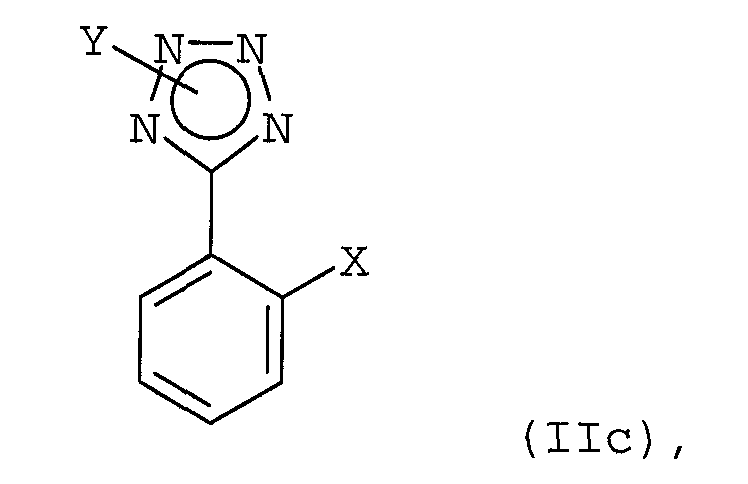
в которой Х обозначает атом хлора или брома, Y обозначает защищающую тетразол группу, выбранную из ряда, включающего 2-тетрагидропиранил и 2-тетрагидрофуранил;
с получением соединения формулы (IС)
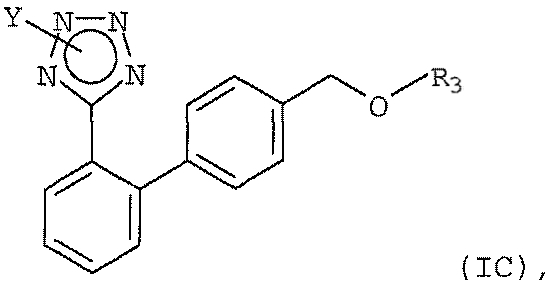
в которой Y обозначает защищающую тетразол группу, выбранную из ряда, включающего 2-тетрагидропиранил и 2-тетрагидрофуранил, а R3 выбран из группы, состоящей из 2-тетрагидропиранила или 2-тетрагидрофуранила; удаление защитной группы у соединения формулы (IC) с получением соединения формулы (IB)
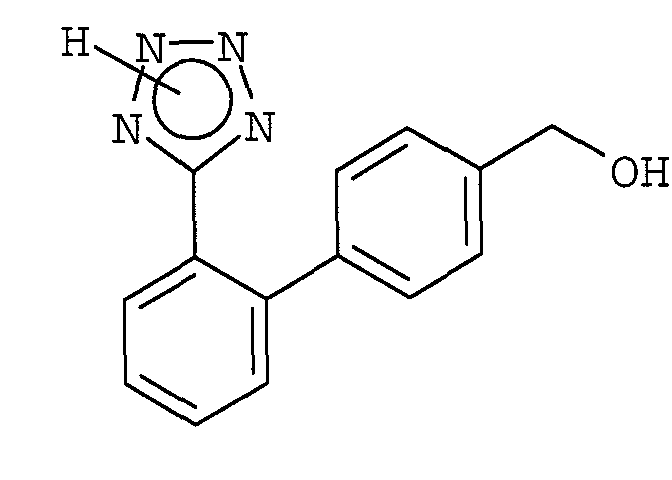
и обработка соединения формулы (IB) окислителем в присутствии подходящего растворителя с получением соединения формулы (IA).
22. Соединение формулы (IC)

в которой Y выбирают из ряда, включающего 2-тетрагидропиранил или 2-тетрагидрофуранил, а R3 выбирают из ряда, включающего 2-тетрагидропиранил или 2-тетрагидрофуранил.
23. Соединение по п.22, в котором заместитель Y представляет собой 2-тетрагидропиранил.
| СОЕДИНИТЕЛЬНОЕ УСТРОЙСТВО ВЕЛОСИПЕДНОГО КОЛЕСА (ВАРИАНТЫ) | 2015 |
|
RU2688503C2 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Journal of Medicinal Chemistry, American Chemical Society, v.35, № 22, p.4027-4038 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2011-08-20—Публикация
2005-02-01—Подача