Данная заявка заявляет приоритет согласно статье 35, Свод Законов США §119 (е) предварительной заявки Соединенных Штатов №61/125011, поданной 22 апреля 2008 года, описание которой данной ссылкой полностью включается в данное описание.
ОБЛАСТЬ ТЕХНИКИ
[0001] Данное изобретение относится к способу производства продуктов лития высокой чистоты, в особенности моногидрата гидроксида лития, для использования в коммерческих применениях, в частности в применениях для аккумуляторных батарей.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
[0002] Моногидрат гидроксида лития (LiOH H2O) может быть получен посредством водной реакции каустификации между гашеной известью (Са(ОН)2) и карбонатом лития (Li2CO3). Гашеная известь может быть сформирована из оксида кальция (СаО), который гидратируется водой (H2O). Это производит приблизительно 3% водный раствор LiOH, который потом концентрируют до насыщенного раствора и кристаллизуют посредством стандартной промышленной практики. Реакции приведены ниже:
[0003] СаО+Н2O=Са(ОН)2+тепло
[0004] Li2CO3+Са(ОН)2=2LiOH (водный)+СаСО3
[0005] 2LiOH (водный)=2LiOH H2O (моногидрат гидроксида лития)
[0006] Источник лития может основываться как на рассоле, так и на руде. Как исходный материал карбонат лития может быть получен как из природного, так и из искусственного источника. В конечном итоге на чистоту конечного продукта будут влиять качество исходных материалов, карбоната лития, извести и качество воды, используемой для приготовления водных растворов.
[0007] Моногидрат гидроксида лития все чаще используется в различных применениях для аккумуляторных батарей. Применение для аккумуляторных батарей обычно требует очень низких уровней загрязняющих примесей, в особенности натрия, кальция и хлоридов. Получение продукта гидроксида лития с низким уровнем кальция является сложным при использовании соединения на основе кальция, такого как известь в качестве основания, без выполнения одного или нескольких этапов очистки. Эти дополнительные этапы очистки увеличивают время и стоимость производства желаемого продукта гидроксида лития.
[0008] Дополнительно натуральные рассолы в основном содержат лишь очень небольшие количества лития несмотря на то, что иногда встречаются натуральные "концентрированные" рассолы, содержащие до около 0,5% лития. Большинство из этих натуральных рассолов, однако, связаны с высокими концентрациями магния или других металлов, что делает извлечение лития нерентабельным. Таким образом, производство моногидрата гидроксида лития из натуральных рассолов представляет собой очень трудную задачу не только из-за экономических показателей работы с очень низкими концентрациями лития, которые встречаются в природе; дополнительно сложность вызывает отделение соединений лития с пригодной степенью чистоты от близких по своим химическим свойствам материалов, которыми обычно загрязнены соли лития, например солей натрия. Также чрезвычайно сложно произвести в значительной степени чистый моногидрат гидроксида лития, используя типичные способы, которые используют соединение, содержащее кальций, например гашеную известь, при производстве. Тем не менее потребность в литии быстро растет, и требуются новые способы производства продуктов лития высокой чистоты, в особенности моногидрата гидроксида лития.
[0009] В патенте США №7157065 В2 раскрываются, помимо всего прочего, способы и устройство для производства карбоната лития и хлорида лития с низким содержанием натрия из рассола с концентрацией лития до около 6,0 весовых процентов. Также раскрыты способы и устройство прямого извлечения технического сорта хлорида лития из концентрированного рассола.
[0010] Предыдущие попытки извлечь соединения лития из натуральных рассолов и/или получить из них продукты лития описаны в литературе.
[0011] В патенте США №4036713 раскрывается способ производства гидроксида лития высокой чистоты из рассола, природного или другого источника, содержащего литий и другие щелочные и щелочноземельные металлы главным образом в качестве галогенидов. Источник лития предварительно концентрируют так, чтобы содержание лития составляло около 2-7% для отделения большей части щелочных и щелочноземельных металлов, отличных от лития, посредством осаждения; рН такого концентрированного рассола затем увеличивают от около 10,5 до около 11,5, предпочтительно используя продукт способа, гидроксид лития используют для осаждения главным образом всех любых сохранившихся загрязняющих примесей магния и добавляют карбонат лития для удаления загрязняющих примесей кальция для обеспечения очищенного рассола; указанный очищенный рассол затем подвергают электролизу как анолит в ячейке, имеющей катионоизбирательную проницаемую мембрану, отделяющую анолит от католита, последний является водой или водным гидроксидом лития, при этом ионы лития перемещаются сквозь мембрану для образования главным образом чистого водного гидроксида лития в католите, продукта, из которого могут быть отделены кристаллические соединения лития высокой чистоты, такие как моногидрат гидроксида лития или карбонат лития.
[0012] В источнике The Kirk-Othmer Encyclopedia of Chemical Technology, Second Edition, Supplement Volume, страницы 438-467, описаны рассолы Большого Соленого озера штата Юта и известные попытки извлечь из них различные химические частицы, представляющие промышленную ценность. Чрезвычайно интересно отметить, что рассолы из этого источника значительно различаются по составу не только от места к месту в озере, но и от года к году. Данная ссылка описывает много различных способов, которые были предложены для извлечения частиц лития, представляющих промышленную ценность, из этих рассолов, включающих выпаривание-кристаллизацию-термическое разложение; ионообмен; комплексообразование лития и алюминия и экстракцию растворителем. Видно, что все предложенные выше способы являются сложными и дорогостоящими и неспособны обеспечить продукты достаточно высокой чистоты для использования в большинстве коммерческих применений.
[0013] В патенте США №2004018 описан известный из уровня техники способ отделения солей лития из смесей с солями других щелочных и щелочноземельных металлов, в котором смешанные соли первоначально преобразовывают в сульфаты и затем обрабатывают сульфатом алюминия для удаления основной массы калия в качестве осадка. Затем добавляют регулируемые количества растворимого карбоната в раствор, чтобы вначале удалить карбонаты магния и кальция, а затем провести осаждение и отделение карбоната лития от других оставшихся в растворе карбонатов щелочных металлов. Rosett и другие предпочитают, однако, работать с хлоридами, которые получены посредством обработки смешанных солей соляной кислотой. Полученный раствор концентрируют посредством кипячения, пока точка кипения является такой, что при охлаждении максимально возможное количество смешанных хлоридов щелочных металлов осаждается, оставляя хлорид лития в растворе. Затем раствор может быть дополнительно концентрирован до такой точки, что при охлаждении хлорид лития осадится в виде моногидрата.
[0014] Патент США №2726138 относится к способу приготовления так называемого хлорида лития высокой чистоты посредством сначала концентрирования сырого водного раствора, содержащего около 2% общего количества хлоридов лития, натрия и калия, до концентрации около 40-44% хлорида лития посредством выпаривания при повышенных температурах для того, чтобы при охлаждении до 25-50°С хлориды натрия и калия выделялись, оставляя больше растворимого хлорида лития в растворе. Затем полученный раствор экстрагируют с инертным органическим растворителем для хлорида лития.
[0015] Патент США №3523751 относится к осаждению карбоната лития из раствора хлорида лития посредством добавления карбоната натрия. Дополнительно он попутно раскрывает, что растворы гидроксида лития легко карбонизируются для осаждения карбоната лития. Кроме того, отмечается, что реакция раствора хлорида лития с карбонатом натрия приводит к осаждению карбоната лития.
[0016] Патент США №3597340 относится к извлечению моногидрата гидроксида лития из водных хлористых рассолов, содержащих и хлорид лития, и хлорид натрия, посредством электролизации рассолов в диафрагменной ячейке, которая поддерживает разделение между анолитом и католитом; диафрагма выполнена из листа стандартного асбестового волокна.
[0017] В патенте США №3652202 описывается способ приготовления карбоната щелочного металла из карбонизированного водного щелока гидроксида щелочного металла ячейки, приготовленного посредством электролиза хлорида щелочного металла в электролитической ячейке приведением в контакт карбонизированного щелока ячейки с аттапульгитовой глиной и впоследствии кристаллизации карбоната щелочного металла из обработанной щелоком ячейки.
[0018] В патенте США №3268289 описывается концентрированно рассолов Большого Соленого озера при помощи испарения солнечной теплотой и средств для повышения отношения хлорида лития к хлориду магния в концентрированном рассоле. В документе говорится, что полученный рассол затем может быть обработан различными способами, такими как удаление магния в электролитической ячейке или окисление магния до оксида магния.
[0019] В патенте США №3755533 описывается способ отделения солей лития от других солей металлов посредством комплексообразования с мономерными или полимерными органическими хелатными добавками.
[0020] Вышеупомянутые способы производства лития из натуральных рассолов или смесей солей щелочных и щелочноземельных металлов включают сложные или дорогостоящие процессы отделения и не обеспечивают, в основном, продукты лития достаточной чистоты для использования в некоторых промышленных применениях.
ЦЕЛИ ИЗОБРЕТЕНИЯ
[0021] Таким образом, целью данного изобретения является обеспечение относительно простого и экономичного способа извлечения частиц лития, имеющих промышленную ценность, в виде соединения лития высокой чистоты, которое также является легко преобразуемым в другие соединения лития высокой чистоты.
[0022] Другой целью данного изобретения является обеспечение улучшенного электролитического способа для концентрации частиц лития, имеющих промышленную ценность, который является высокоэффективным и который может функционировать на продолжении длительных периодов времени благодаря отсутствию мешающих катионов.
[0023] Конкретной целью изобретения является получение водного раствора гидроксида лития высокой чистоты, из которого такие ценные продукты, как кристаллический моногидрат гидроксида лития и карбонат лития, могут быть легко отделены.
[0024] Эти и другие цели изобретения, которые станут более понятными ниже, достигаются посредством следующих способов.
[0025] Важно, хотя уровни кальция и магния рассолов натрия были уменьшены до уровней в диапазоне ppb на фактически обычных основаниях, уровни кальция и магния в рассолах лития очень тяжело уменьшить до таких уровней, однако не полагается, что они не могут быть уменьшены до уровней 150 ppb или меньше (в целом), что является значительным преимуществом данного изобретения. Таким образом, рассолы лития, имеющие в целом уровень меньше чем 150 ppb, предпочтительно меньше чем 50 ppb каждый, являются важной целью данного изобретения как способы получения таких рассолов.
КРАТКОЕ ИЗЛОЖЕНИЕ СУТИ ИЗОБРЕТЕНИЯ
[0026] Данное изобретение относится к способу производства продуктов лития высокой чистоты, в особенности моногидрата гидроксида лития. Способ является применимым ко всем литийсодержащим водным рассолам, однако натуральные водные рассолы являются предпочтительными. Также может использоваться содержащая литий руда как источник, обеспечивающий полученный из нее литийсодержащий рассол.
[0027] Используемые источники рассола могут содержать множество загрязняющих примесей, т.е. отличных от лития ионов, таких как магния, кальция, натрия, калия и т.п. Перед ионообменной очисткой такие загрязняющие примеси предпочтительно удаляют или уменьшают их содержание посредством подходящих способов, известных из уровня техники для удаления или уменьшения содержания соответствующей загрязняющей примеси.
[0028] После удаления или уменьшения содержания загрязняющих примесей рассол с или без удаления загрязняющих примесей затем концентрируют относительно содержания лития. Предпочтительно рассол концентрируют до содержания лития около 2-7% по весу и предпочтительно от 2,8 до 6,0% по весу или до около 12-44% по весу и предпочтительно 17-36% по весу, рассчитанного как хлорид лития, что является причиной того, что большая часть всего присутствующего натрия и калия выделяется из раствора.
[0029] Далее рН такого концентрированного рассола регулируют до около 10,5-11,5 и предпочтительно около 11 для осаждения ди- или тривалентных ионов, таких как ионы железа, магния и кальция. Это может быть выполнено, например, при помощи регулировки посредством добавления гидроксида лития и карбоната лития в количествах, стехиометрически равных содержанию железа, кальция и магния. Регулирование рН предпочтительно выполнено посредством добавления основания, предпочтительно содержащего литий основания, такого как гидроксид лития и карбонат лития, которые являются предпочтительно восстановленными продуктами способа. В результате регулирования рН значительное количество железа, кальция и магния удаляется из концентрированного рассола с отрегулированным рН.
[0030] Содержание кальция и магния, так же как и других ди- и тривалентных ионов, может затем быть дополнительно уменьшено посредством ионообмена, так что конечный результат представляет собой рассол, содержащий меньше чем 150 ppb кальция и магния в целом.
[0031] Данный более очищенный рассол затем подвергается электролизу для выхода раствора гидроксида лития, содержащего меньше чем 150 ppb общего количества кальция и магния. Полупроницаемая мембрана, которая выборочно пропускает катионы, используется в процессе электролиза, при этом ионы лития перемещаются сквозь мембрану для образования главным образом чистого водного гидроксида лития в католите, продукта, из которого могут быть образованы кристаллические соединения лития высокой чистоты, такие как моногидрат гидроксида лития или карбонат лития.
[0032] Чрезвычайно предпочтительный способ согласно данному изобретению относится к способу производства кристаллов моногидрата гидроксида лития посредством очистки содержащего литий рассола, который также содержит натрий и необязательно калий, для уменьшения общей концентрации кальция и магния до меньше чем 150 ppb; электролиза рассола для образования раствора гидроксида лития, содержащего меньше чем 150 ppb общего количества кальция и магния, с газообразным хлором и газообразным водородом в качестве побочных продуктов; и концентрирования и кристаллизации раствора гидроксида лития для получения кристаллов моногидрата гидроксида лития.
[0033] Другой предпочтительный способ по данному изобретению относится к способу производства соляной кислоты посредством очистки содержащего литий рассола, который также содержит натрий и необязательно калий, для уменьшения общей концентрации кальция и магния до меньше чем 150 ppb; электролиза рассола для образования раствора гидроксида лития, содержащего меньше чем 150 ppb общего количества кальция и магния, с газообразным хлором и газообразным водородом в качестве побочных продуктов; и производства соляной кислоты посредством сжигания газообразного хлора с избыточным водородом.
[0034] Другой предпочтительный способ данного изобретения относится к способу производства и моногидрата гидроксида лития, и соляной кислоты посредством очистки содержащего литий рассола, который также содержит натрий и необязательно калий, для уменьшения общей концентрации кальция и магния до меньше чем 150 ppb; электролиза рассола для образования раствора гидроксида лития, содержащего меньше чем 150 ppb общего количества кальция и магния, с газообразным хлором и газообразным водородом в качестве побочных продуктов; и концентрирования и кристаллизации раствора гидроксида лития для получения кристаллов моногидрата гидроксида лития; и производства соляной кислоты посредством сжигания газообразного хлора с избыточным водородом.
[0035] Еще один предпочтительный вариант осуществления изобретения относится к способу производства кристаллов моногидрата гидроксида лития посредством концентрирования содержащего литий рассола, который также содержит натрий и необязательно калий, для осаждения натрия и необязательно калия из рассола; необязательной очистки рассола для удаления или для уменьшения концентраций бора, магния, кальция, сульфата и любых сохранившихся натрия или калия; регулировки рН рассола до около 10,5-11 для дополнительного удаления любых катионов, отличных от лития; дополнительной очистки рассола посредством ионообмена для уменьшения общей концентрации кальция и магния до меньше чем 150 ppb; электролиза рассола для образования раствора гидроксида лития, содержащего меньше чем 150 ppb общего количества кальция и магния, с газообразным хлором и газообразным водородом в качестве побочных продуктов; и концентрирования и кристаллизации раствора гидроксида лития для получения кристаллов моногидрата гидроксида лития.
[0036] В предпочтительном варианте осуществления раствор гидроксида лития способа преобразован в продукт лития высокой чистоты и более предпочтительно карбонат лития высокой чистоты, содержащий меньше чем 150 ppb кальция и магния в целом.
[0037] В чрезвычайно предпочтительном варианте осуществления кристаллы моногидрата гидроксида лития центрифугированы и восстановлены. Центрифугированные или другим способом восстановленные кристаллы могут быть необязательно высушены, после чего следует упаковка сухого материала.
[0038] Предпочтительно рассол концентрируют до концентрации лития от около 2% до около 7%, предпочтительно 6,5% и более предпочтительно 2,8-6,0% по весу перед электролизом.
[0039] В еще одном предпочтительном варианте осуществления содержащий литий рассол концентрируют посредством испарения солнечной теплотой.
[0040] Содержание бора в рассоле может быть необязательно уменьшено, например, посредством процесса органической экстракции или посредством ионообмена.
[0041] Содержание магния предпочтительно уменьшают добавлением извести или управляемой реакцией с известью или гашеной известью, однако использование извести является предпочтительным. Содержание кальция предпочтительно уменьшают добавлением щавелевой кислоты для осаждения оксалата кальция. Кальций и магний могут также быть удалены посредством ионообмена или посредством комбинации любых известных из уровня техники средств для уменьшения содержания этих ионов в рассоле лития.
[0042] Содержание сульфата может быть необязательно уменьшено, например, посредством добавления бария для осаждения сульфата бария.
[0043] Содержание натрия может быть уменьшено посредством фракционной кристаллизации или других средств, если желательно или при необходимости.
[0044] Для электролиза электроды предпочтительно изготовлены из материала с высокой коррозионной устойчивостью. В чрезвычайно предпочтительном варианте осуществления электроды имеют титановое и никелевое покрытие. В другом предпочтительном варианте осуществления на этапе электролиза электрохимическая ячейка расположена в конфигурации с "псевдонулевым зазором". Чрезвычайно предпочтительно, что на этапе электролиза используют монополярную мембранную ячейку, например монополярную мембрану Ineos ChlorFM1500.
[0045] В предпочтительных вариантах осуществления электрод со стороны катода имеет многопластинчатую конструкцию в форме фонаря для вызова турбулентности и высвобождения газа на протяжении гидролиза.
[0046] Предпочтительный способ по данному изобретению относится к производству соляной кислоты посредством (а) концентрирования содержащего литий рассола, который также содержит натрий и необязательно калий, для осаждения натрия и необязательно калия из рассола; очистки рассола для удаления или уменьшения концентраций бора, если необходимо, магния, кальция, сульфата и любого оставшегося натрия или калия; регулирования рН рассола до около 10,5-11 для дополнительного удаления любых катионов, отличных от лития; дополнительной очистки рассола посредством ионообмена для уменьшения общей концентрации кальция и магния до меньше чем 150 ppb; электролиза рассола для образования раствора гидроксида лития, содержащего меньше чем 150 ppb общего количества кальция и магния, с образованием газообразного хлора и газообразного водорода в качестве побочных продуктов; и производства соляной кислоты посредством сжигания газообразного хлора с избыточным водородом. Любые варианты осуществления могут быть включены в данный способ при желании, например для уменьшения присутствия нежелательных ионов, например кальция и магния.
Также изобретение относится к моногидрату гидроксида лития, содержащего меньше чем 150 ppb в целом общего количества Са и Mg и предпочтительно меньше чем 50 ppb общего количества и более предпочтительно меньше чем 15 ppb в целом общего количества.
Другой аспект изобретения относится к водному гидроксиду лития, содержащему меньше чем 150 ppb общего количества Са и Mg и предпочтительно меньше чем 50 ppb общего количества и более предпочтительно меньше чем 15 ppb в целом общего количества.
Продукты или другие продукты производства, например аккумуляторные батареи, которые включают вышеуказанный моногидрат гидроксида лития и/или водные растворы гидроксида лития, также являются аспектом изобретения.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0047] На фигуре изображена блок-схема предпочтительного способа согласно данному изобретению.
ПОДРОБНОЕ ОПИСАНИЕ
[0048] Данное изобретение в основном относится к способу производства или моногидрата гидроксида лития, или соляной кислоты, или того и другого посредством очистки содержащего литий рассола, который также содержит натрий и необязательно калий, для уменьшения общей концентрации кальция и магния до меньше чем 150 ppb; электролиза рассола для образования раствора гидроксида лития, содержащего меньше чем 150 ppb общего количества кальция и магния, с газообразным хлором и газообразным водородом в качестве побочных продуктов; и затем выполнения, по меньшей мере, одного из следующих этапов, на которых концентрируют раствор гидроксида лития для образования кристаллов моногидрата гидроксида лития или дополнительно производят соляную кислоту посредством сжигания газообразного хлора с избыточным водородом.
[0049] В предпочтительных вариантах осуществления способ производства моногидрата гидроксида лития и соляной кислоты согласно данному изобретению обычно включает этапы, на которых: концентрируют содержащий литий рассол посредством, например, испарения солнечной теплотой или нагреванием; предпочтительно снижают содержание любых загрязняющих примесей бора, которые могут содержаться в рассоле, посредством, например, процесса органической экстракции или процесса ионообмена, если желательно; уменьшают содержание магния, если имеется, посредством управляемой реакции с известью и/или гашеной известью для осаждения гидроксида магния, как желательно; сначала уменьшают содержание любого кальция, например, посредством обработки щавелевой кислотой для осаждения оксалата кальция, если желательно. Содержание сульфата может быть уменьшено посредством обработки, например, барием, если желательно. Уровень натрия в рассоле может быть уменьшен посредством, например, фракционной кристаллизации. Важно, чтобы уровни Са и Mg были уменьшены до меньше чем 150 ppb (в целом общего количества) и более предпочтительно до меньше чем 50 ppb (в целом общего количества) и наиболее предпочтительно меньше чем 15 ppb (в целом общего количества) посредством ионообмена, отдельно или совместно с другими процессами, например посредством осаждения, такого как описано выше.
[0050] Далее результирующий очищенный литийсодержащий водный раствор, имеющий менее чем 150 ppb Са и Mg (в целом общего количества), электрохимически разделяют на раствор гидроксида лития с газообразным хлором и газообразным водородом в качестве побочных продуктов. Далее вода может необязательно быть электрохимически образована посредством отделения воды с целью выхода потока газообразного водорода. Потоки газообразного хлора и газообразного водорода необязательно осушают.
[0051] Затем соляная кислота может быть получена посредством сжигания газообразного хлора с избыточным водородом и последующей мокрой очистки результирующего потока газа очищенной водой.
[0052] Затем раствор гидроксида лития может быть концентрирован или модифицирован другим способом для получения кристаллов моногидрата гидроксида лития, например, посредством вакуумного охлаждения или испарения для выхода продукта моногидрата гидроксида лития, который является достаточно чистым для применения в аккумуляторных батареях, например, содержащего меньше чем 150 ppb Ca и Mg (в целом общего количества) и предпочтительно меньше чем 50 ppb общего количества и наиболее предпочтительно меньше чем 15 ppb (в целом общего количества).
[0053] Центрифугирование кристаллов, необязательно с промывкой, увеличивает чистоту, но не является необходимым.
[0054] Кристаллы могут необязательно быть высушены, предпочтительно после промывки, для выхода кристалла чистого моногидрата и последующей упаковки высушенного материала.
[0055] Используемый исходный рассол будет, само собой разумеется, иметь различное содержание ионов в зависимости от источника, так что способ будет соответственно изменяться. Например, перед ионообменной очисткой обычно будет необходимо очистить рассол для удаления или уменьшения концентраций нежелательных ионов, например, Ca, Mg, В, Fe, Na, сульфата и т.д. Такие процессы удаления известны из уровня техники, кроме того, также могут использоваться процессы, отличные от уже известных. В предпочтительном варианте осуществления специалист, осуществляющий способ по данному изобретению, будет использовать содержащий литий рассол, который будет обычно содержать другие щелочные и щелочноземельные металлы, прежде всего в качестве ионизированных галогенидных солей. В начале рассол может быть концентрирован посредством любых подходящих средств до концентрации лития от около 2 до около 7% по весу, благодаря чему большая часть всего присутствующего натрия и калия выделяется из рассолов в качестве галогенидов, которые не растворимы в галогенидном растворе лития этой концентрации, т.е. от около 12 до около 44%, рассчитанной как хлорид лития. С другой стороны, хотя возможно электролизировать рассол подходящего насыщения хлорида лития, т.е. около 44% (7,1% лития), предпочтительным является не использовать настолько концентрированные рассолы, так как возрастает тенденция перемещения хлорида сквозь мембрану. Таким образом, более целесообразным является использование в качестве анолита рассола, содержащего около 2-5% лития или от около 12% до около 30% хлорида лития для наилучших результатов и выхода.
[0056] После отделения солей натрия и калия рН рассола регулируют до значения в диапазоне от около 10,5 до около 11,5, предпочтительно около 11, и добавляют карбонат лития, чтобы вызвать осаждение для уменьшения содержания любых оставшихся кальция и/или магния и любого присутствующего железа или устранить присутствие этих ионов. Данное регулирование рН может быть выполнено посредством любых подходящих средств, но предпочтительным является осуществление регулирования добавлением гидроксида лития и карбоната лития, оба из которых могут быть легко получены из продукта процесса, как будет видно ниже. Добавление гидроксида лития и карбоната лития в количествах, стехиометрически равных содержанию железа, кальция и магния, вызывает главным образом полное удаление этих катионов в качестве нерастворимых гидроксидов железа и магния и карбоната кальция.
[0057] Далее полученный рассол, из которого главным образом все катионы, отличные от лития, были удалены или практически удалены до желаемых переделов, предпочтительно нейтрализуют предпочтительно соляной кислотой или другой подходящей минеральной или органической кислотой и обрабатывают ионообменной смолой для дальнейшего уменьшения уровней кальция и магния. Затем данный более очищенный рассол подвергается электролизу для выхода раствора гидроксида лития, содержащего меньше чем 150 ppb общего количества Са и Mg, и может быть выпарен или нагрет для кристаллизации моногидрата гидроксида лития такой же чистоты, который может быть использован, например, в применениях для аккумуляторных батарей.
[0058] Продукт данного способа, главным образом чистый водный гидроксид лития, содержащий меньше чем 150 ppb общего количества Са и Mg, более предпочтительно меньше чем 50 ppb (общего количества) и наиболее предпочтительно меньше чем 15 ppb (общего количества), легко преобразовывается в другие продукты лития высокой чистоты коммерческого пользования как раствор или после его осаждения для выхода соли моногидрата. Например, раствор может быть обработан двуокисью углерода для предпочтительного осаждения карбоната лития высокой чистоты. Альтернативно, водный гидроксид лития может быть выпарен или частично, или полностью для получения моногидрата гидроксида лития высокой чистоты.
[0059] Чрезвычайно предпочтительная технология заключается в частичном выпаривании раствора для кристаллизации моногидрата гидроксида лития высокой чистоты и повторном использовании оставшегося раствора со свежеприготовленным раствором, со сливом, поскольку кристаллический моногидрат гидроксида лития, полученный данным образом, имеет большую чистоту, чем чистота, которая может быть получена другим способом. Продукты лития, полученные таким образом, имеют очень высокую чистоту и фактически будут включать максимальное остаточное содержание хлорида 0,05%, при этом содержание хлорида 0,01% является более типичным. Это является очень важным во многих применениях, например, где гидроксид лития используется в смазочных материалах, которые должны включать минимальное содержание хлоридионов из-за их коррозионного потенциала. Кроме того, если хлорид не устранен, как, например, в ячейке, использующей стандартную промышленную монополярную мембрану, очень сложным является получить гидроксид лития высокой чистоты посредством повторной кристаллизации.
[0060] Причина, по которой необходимо в способе по данному изобретению уменьшить до минимума концентрацию катионов, отличных от лития, в рассоле, который будет подвергнут электролизу, заключается в обеспечении производства гидроксида лития высокой чистоты, хотя также это необходимо потому, что некоторые катионы, как, например, кальция, магния и железа, имеют тенденцию осаждаться в мембране с избирательной катионной проницаемостью как нерастворимые гидроксиды кальция, магния и железа. Такие осаждения, само собой разумеется, являются крайне нежелательными, поскольку это не только уменьшает способность мембраны пропускать ионы лития, но также значительно сокращает срок службы мембраны электролизной ячейки и, следовательно, возможный период непрерывной работы ячейки, увеличивая стоимость осаждения.
[0061] Способ по данному изобретению может проводиться на любых натуральных или искусственных рассолах лития. Исходный рассол будет также обычно содержать в качестве загрязняющей примеси одну или более из следующих: магний, кальций, бор, рубидий и другие, обычно в растворимой форме и часто в качестве, соответствующей хлористой соли. Понятно, что этапы способа, необходимые для удаления таких загрязняющих примесей, будут изменять с присутствием или отсутствием загрязняющей примеси. Таким образом, если нет загрязняющей примеси или если содержание такое, что конечный продукт будет удовлетворять требованиям для отдельного применения, тогда этап удаления не требуется в отношение этой загрязняющей примеси.
[0062] На таких этапах удаления будут использоваться способы, которые уже известны или станут доступными из уровня техники.
[0063] После выполнения необходимых этапов удаления все еще может оставаться содержание загрязняющих примесей, так что могут использоваться последующие этапы удаления, которые могут быть такими же или отличными от предыдущего этапа удаления.
[0064] Способ по данному изобретению является широко применимым ко всем литийсодержащим водным рассолам. Подходящие рассолы встречаются в природе как в качестве грунтовой воды в родниках или шахтах, так и в качестве поверхностной воды в океанах и озерах, как, например, рассолы, естественно встречающиеся в Неваде, Аргентине и Чили. Также рассолы могут быть искусственно получены посредством реакции соляной кислоты с минералами лития для получения содержащих хлорид лития рассолов. Соляная кислота для этой цели может быть получена посредством реакции побочных продуктов водорода и хлора этапа электролиза данного изобретения. Обычно такие рассолы содержат очень низкие концентрации лития порядка 50-500 ppm или даже меньше, хотя могут встречаться рассолы, содержащие вплоть до 0,5% лития. Хотя теоретически способ по изобретению может быть осуществлен с рассолом любой концентрации, от очень низкой до насыщенной, очевидно, что менее экономически целесообразной является работа с рассолами, имеющими очень низкое содержание лития, из-за времени и размеров оборудования, которое будет необходимо. По этой причине является желательным в качестве предварительного этапа концентрировать слабые рассолы натурального происхождения до тех пор, пока концентрация лития не возрастет до, по меньшей мере, от около 0,04% до около 1% и предпочтительно, по меньшей мере, около 0,1%.
[0065] Содержание лития в слабых рассолах может быть увеличено любым подходящим способом несмотря на то, что в настоящее время отмечаются некоторые виды процессов выпаривания по причине сложности химического отделения компонентов смеси солей, обычно находящихся в рассолах. Хотя выпаривание может быть осуществлено любым известным способом, предпочтительным является простое хранение рассолов в отстойниках и обеспечение концентрирования посредством испарения солнечной теплотой в течение периода времени. Такое испарение солнечной теплотой направлено на отделение части хлоридов натрия и калия, которые являются менее растворимыми, чем хлорид лития. Кроме того, из-за абсорбции двуокиси углерода из воздуха часть содержания магния может также быть удалена из базовых рассолов данным образом в качестве карбоната магния.
[0066] Когда таким образом концентрацию лития в слабых рассолах привели к около 0,04-1% или предпочтительно, по меньшей мере, около 0,1%, рН рассола желательно, но необязательно регулировали до значения в диапазоне от около 10,5 до около 11,5, предпочтительно около 11, для содействия в удалении катионных загрязняющих примесей, т.е. катионов, отличных от лития, в частности магния, если данный элемент присутствует в значительных количествах. Это может быть выполнено добавлением любого подходящего щелочного материала, такого как известь, карбонат натрия или гидроксид кальция, первоочередным является низкая стоимость. Далее рассол может быть дополнительно концентрирован испарением солнечной теплотой, обычно до содержания около 0,5-1% лития (т.е. около 3,1-6,2% хлорида лития). Ввиду того что абсорбция диоксида углерода из воздуха может уменьшить рН до около 9, оно должно быть снова отрегулировано до 10,5-11,5 добавлением извести, гидроксида кальция или карбоната натрия для уменьшения остаточного магния и кальция в растворе до около 0,1%.
[0067] Затем рассол еще дальше дополнительно концентрируют любыми подходящими средствами, такими как испарение солнечной теплотой или, более быстро, погружным горением в соответствии с технологиями, известными из уровня техники. В ходе этого процесса рассолы могут снова абсорбировать диоксид углерода из атмосферы, тем самым возможно повторное снижение рН до около 9. Таким образом, рассол уменьшается в объеме до концентрации от около 2 до около 7% лития, т.е. от около 12 до около 44% хлорида лития. Концентрация хлорида лития удобно вычисляется посредством умножения концентрации лития на коэффициент 6,1. Хлориды натрия и калия являются главным образом менее растворимыми в рассоле, чем хлорид лития, так что главным образом весь натрий и весь калий будут удалены, когда концентрация лития превысит около 40%. Сам по себе хлорид лития достигнет насыщения в водном растворе при содержании лития около 7,1% или около 44% хлорида лития при окружающей температуре. Это, таким образом, является верхним пределом, до которого концентрация рассолов является практически применимой без осаждения хлорида лития с присутствующими загрязняющими примесями. Как отмечено выше, ввиду того что значительные количества натрия и калия остаются в растворе до тех пор, пока концентрация лития не достигнет около 35%, что является фактическим нижним пределом этапа испарительного концентрирования данного способа, если не удалять катионы натрия и калия посредством повторной кристаллизации гидроксидов для того, чтобы получить литий высокой чистоты.
[0068] Ввиду того что таким образом концентрированный и очищенный рассол будет дополнительно очищен посредством электролиза, предпочтительным является удаление любых оставшихся мешающих катионов. В предпочтительном варианте осуществления рассол, который будет подвержен электролизу, разбавляют, если необходимо, до содержания лития от около 2 до 5% (около 12-30% хлорида лития) для ограничения перемещений ионов хлорида при электролизе, при этом электрические КПД фактически выше при таких концентрациях. Само собой разумеется, данное разбавление не является необходимым, если концентрация лития на этапе концентрирования не превышает 5%. Удаление главным образом всех оставшихся мешающих катионов, которые являются обычно в первую очередь кальцием и магнием и, возможно, железом, выполняют посредством повторного повышения рН рассола до около 10,5-11,5, предпочтительно около 11. Это может быть выполнено добавлением любого подходящего щелочного материала, но для того, чтобы получить наилучшее разделение без загрязнения, предпочтительным является добавление стехиометрических количеств гидроксида лития и карбоната лития. Таким образом, главным образом все мешающие катионы будут удалены как гидроксид магния, карбонат кальция или в качестве гидроксидов железа. Гидроксид лития и карбонат лития для этого являются легко доступными из продукта данного способа, как будет описано ниже.
[0069] Как указанно выше, рассол, который будет подвергнут электролизу, должен быть главным образом свободным от мешающих катионов, хотя на практике небольшие количества ионов щелочных металлов, как, например, калия и натрия, могут быть допустимы при условии, что количество, которое будет оставаться в растворе при повторной кристаллизации, не превышает около 5% по весу. Содержание катионов, которые будут всерьез мешать электролизу из-за осаждения в катионопроницаемой мембране, таких как железа, кальция и магния, должно, однако, быть уменьшено до очень низких уровней. Общее содержание таких ионов предпочтительно не должно превышать около 0,004%, хотя могут допускаться концентрации вплоть до их пределов растворимости в католите. Такие повышенные концентрации могут быть использованы, если необходимо, с уменьшением срока службы мембраны ячейки. Содержание анионов, отличных от ионов хлорида, в рассоле, который будет подвержен электролизу, не должно превышать около 5%.
[0070] Католит может состоять из любого подходящего материала, содержащего достаточно ионов для прохождения тока. Хотя вода отдельно может быть использована с учетом изложенных выше ограничений, предпочтительно обеспечивать необходимую ионизацию продуктом, который производится, т.е. гидроксидом лития. Исходная концентрация гидроксида лития может изменяться от только достаточной для того, чтобы ячейка работала, до концентрации насыщения при преобладающих условиях давления и температуры. Однако ввиду того, что обычно нежелательно допускать осаждение гидроксида лития в ячейке и в особенности необходимо избегать осаждения гидроксида внутри мембраны, насыщения избегают. Кроме того, ввиду того что доступные катионоизбирательные мембраны не идеальны и пропускают некоторые анионы, чем выше концентрации гидроксильных ионов в католите, тем больше таких ионов переходит сквозь мембрану в анолит, что является нежелательным, так как такие ионы реагируют с ионами хлорида с образованием окисей хлора, таким образом уменьшая выход производства хлора в качестве побочного продукта и уменьшая существующую эффективность ячейки в целом.
[0071] Даже если эффективность описанного здесь способа является высокой, предпочтительный процесс будет повторно использовать истощенный раствор хлорида лития, который укрепляют свежеприготовленным очищенным рассолом лития. Этот повторно используемый рассол обрабатывают для удаления любых окисей хлора, которые могут образовываться, используя способы, известные специалистам в данной области техники. Таким образом, способ сохраняет свою высокую эффективность, а также использует в максимальной степени дорогостоящий литиевый поток.
[0072] Любые подходящие полупроницаемые электролизные мембраны, которые избирательно пропускают катионы и препятствуют прохождению анионов, могут использоваться в данном способе. Такие мембраны хорошо известны для специалистов в области электролиза. Подходящие коммерческие электролизные мембраны включают серию, доступную от E.I. DuPont de Nemours & Co. под маркой Nafion. Такая катионопроницаемая мембрана с избирательной проницаемостью размещается между рассолом анолита, который будет подвержен электролизу, и католитом, описанным выше, для поддержания физического разделения между двумя жидкостями.
[0073] Электрический ток от около 100 А/фут2 до около 300 А/фут2 проходит сквозь мембрану в католит при электролизе. Предпочтительно диапазон значений тока составляет от 150 А/фут2 до 250 А/фут2. Предпочтительно, чтобы уровень кальция и магния поддерживался на уровне между <20-<30 ppb в целом Са и Mg в зависимости от плотности тока для того, чтобы избежать обрастания мембраны.
[0074] В ходе электролиза хлорид-ионы в анолите переходят к аноду и разряжаются для получения газообразного хлора, который может быть извлечен в качестве побочного продукта и использован для получения соляной кислоты среди прочих химических реагентов, как описано ниже, или посредством других процессов. Гидроксильные ионы в католите, хотя и притягиваются к аноду, главным образом не проходят в анолит из-за непроницаемости мембраны для таких анионов. Ионы лития, которые входят в католит, ассоциируются сами с гидроксил-ионами, полученными из воды в католите, таким образом, освобождая ионы водорода, которые разряжаются возле катода с образованием водорода, который также может быть отобран как побочный продукт и использован, например, с результирующим хлором для производства НСl. Альтернативно, газообразный водород может быть использован как источник тепла для выработки энергии.
[0075] В ходе способа хлорид лития в рассоле анолита преобразуется в гидроксид лития в католите; эффективность преобразования составляет фактически 100% на основании хлорида лития, залитого в анодную камеру ячейки. Электролиз может производиться непрерывно, пока концентрация гидроксида лития не достигнет желаемого уровня, который может доходить до 14% или до чуть более низкого насыщения. Этот водный гидроксид лития имеет очень высокую чистоту и будет предпочтительно содержать не более чем около 0,5% по весу катионов, отличных от лития, наиболее предпочтительно меньше чем 0,4% по весу и наиболее предпочтительно меньше чем 0,2 вес.%. Моногидрат гидроксида лития будет также предпочтительно содержать меньше чем 0,05 вес.% анионов, отличных от гидроксила, наиболее предпочтительно меньше чем 0,04 вес.% и наиболее предпочтительно меньше чем 0,02 вес.%. Особенно должно быть отмечено, что содержание хлоридов не должно превышать 0,04 вес.%, наиболее предпочтительно меньше чем 0,03 вес.%, наиболее предпочтительно меньше чем 0,02 вес.%. В частности, в соответствии со способом по изобретению получают данную чистоту моногидрата гидроксида лития без необходимости в дополнительных этапах обработки, хотя другие этапы обработки могут быть использованы для дополнительной очистки продукта при желании.
[0076] Водный гидроксид лития высокой чистоты, обеспеченный посредством способа по данному изобретению, может быть использован, как есть, или он может быть легко преобразован в другие коммерчески пригодные продукты лития высокой чистоты. Например, водный гидроксид лития может быть обработан двуокисью углерода для осаждения карбоната лития высокой чистоты, содержащего не более чем 0,05% хлорида и обычно только около 0,01%.
[0077] Альтернативно, водный гидроксид лития может быть преобразован в кристаллический моногидрат гидроксида лития высокой чистоты посредством простого испарения раствора до сухого состояния. Более сложные технологии кристаллизации могут быть применены, используя частичную кристаллизацию, повторное использование и слив, для получения кристаллического моногидрата гидроксида лития очень высокой чистоты.
[0078] Из приведенного выше можно видеть, что часть продукта водного гидроксида лития может, таким образом, быть преобразована для обеспечения карбоната лития и гидроксида лития, используемых на более ранних этапах данного способа для удаления содержания железа, кальция и магния концентрированных рассолов.
[0079] Также из приведенного выше очевидно, что новый способ впервые обеспечивает метод получения частиц лития, имеющих промышленную ценность, из натуральных рассолов высокой чистоты в виде продуктов, непосредственно используемых в коммерческих применениях без дополнительной очистки, и что извлечение лития из концентрированных рассолов составляет главным образом 100%.
[0080] Дополнительно, как только раствор гидроксида лития, кристаллы моногидрата и раствор соляной кислоты будут получены, они могут быть использованы в качестве исходного материала для других литийсодержащих соединений в дополнения к продаже на рынке. Это может быть выполнено, например, посредством использования чистого сжатого газа СO2 для реакции с раствором гидроксида лития для осаждения карбоната лития высокой чистоты, который может также быть использован в некоторых применениях для аккумуляторных батарей.
[0081] Альтернативой является использование данного раствора гидроксида лития для промывки газов сгорания, образуемых в результате сжигания ископаемого топлива, что приводит к образованию менее чистого карбоната, однако также снижаются выбросы парниковых газов.
[0082] Другой пример представляет собой использование ультрачистого гидроксида лития и соляной кислоты, которые получены в результате способа по данному изобретению в качестве реагентов для преобразования раствора хлорида лития очень высокой чистоты, который впоследствии будет подвергнут кристаллизации и использован для производства металлического лития, который требует чрезвычайно низких уровней загрязняющих примесей (например, для компонентов аккумуляторных батарей).
[0083] Дальнейшие примеры включают использование раствора гидроксида лития по данному изобретению для формирования гипохлорита лития, который является признанным дезинфицирующим средством, производства фторидов и бромидов лития высокой чистоты и других содержащих литий соединений, полученных посредством кислотно-основных реакций.
[0084] Установлена необходимость высокой чистоты для раствора хлорида лития, в способе по данному изобретению используют ионообменную смолу, которая является эффективной в уменьшении содержания ионов кальция и магния до уровней, которые меньше чем 200 ppb в целом. Как показано, эти уровни будут приемлемыми в электрохимических ячейках хлорида лития и могут быть достигнуты, используя высокоемкий макропористый слабокислый катионит с равномерным точным распределением гранул. Смола может быть регенерирована соляной кислотой и гидроксидом лития в последующих процессах для экономии эксплуатационных затрат.
[0085] Результирующий очищенный раствор хлорида лития содержит между 15 и 30 вес.% раствора лития (в виде хлорида лития) со следующим типичным составом загрязняющих примесей:
[0086] Должно быть отмечено, что эти низкоуровневые составы требуют повышенной степени осторожности для избежания загрязнений, приводящих к ложному высокому показанию. Аналитические методы, обычно используемые в области хлоридов натрия и щелочей, не подходят.
[0087] Далее этот очищенный рассол подвергают электролизу в электрохимической ячейке. Типичная электрохимическая ячейка имеет три (3) основных элемента, анод, проницаемая мембрана и катод. В способе по данному изобретению будет использоваться катионообменная мембрана на основе перфторсульфоновой кислоты, например одна из мембран семейства DuPont's' Nafion®.
[0088] Из-за коррозионной способности растворов и в особенности хлорида лития электроды предпочтительно выполнены из материала с высокой коррозионной устойчивостью. Предпочтительно электроды имеют титановое и никелевое покрытие. Предпочтительная конструкция ячейки имеет конфигурацию, называемую "псевдонулевым зазором", например, Ineos FMO1 с плоским пластинчатым анодом с вызывающей турбулентность сеткой на стороне анолита как для вызова турбулентности, так и для удержания мембраны на расстоянии от поверхности анода. Эта конструкция является более предпочтительной, чем более традиционная конструкция с нулевым зазором для избежания преждевременного повреждения или разрушения покрытия анода из-за области с потенциально высоким градиентом рН участка, непосредственно примыкающей к аноду.
[0089] Предпочтительно электрод со стороны катода имеет многопластинчатую конструкцию в форме фонаря для возникновения турбулентности и высвобождения газа.
[0090] Полная и полуреакции на электродах следующие:
[0095] Обычные рабочие условия описанной выше ячейки приведены ниже:
[0096] Специалисту в данной области будет понятно, что это является примерным и неограничивающим и будет зависеть от вариантов этапов способа, используемого оборудования, желаемого конечного продукта и других факторов.
[0097] Используя теплоту фазового перехода раствора католита, моногидрат гидроксида лития может быть получен посредством, например, обычной кристаллизации охлаждением под вакуумом; используя доступное стандартное промышленное оборудование, созданное для таких целей.
[0098] Продукт моногидрата гидроксида лития данного изобретения является достаточно чистым для того, чтобы быть использованным в применениях для аккумуляторных батарей, и представляет собой более совершенный результат по сравнению с другими способами получения гидроксида лития, которые требуют дополнительной промывки или других этапов обработки для достижения чистоты, необходимой для использования в аккумуляторных батареях.
[0099] Хлор и водород, образованные в результате работы электрохимических ячеек, могут быть обезвожены и необязательно слегка сжаты. Между хлором и водородом происходит экзотермическая реакция для образования газообразного хлористого водорода. Оба газа проходят через форсунку и воспламеняются внутри соответственно сконструированной камеры сгорания, охлаждаемой водой. Полученный газообразный хлористый водород охлаждается и адсорбируется водой для получения соляной кислоты желаемой концентрации. Качество используемой для адсорбции воды будет определять чистоту результирующей кислоты. Альтернативно, специалист в данной области техники может получить другие химические соединения из этих потоков.
[00100] Дополнительные этапы способа могут быть добавлены к общим этапам изобретения. Например, может быть необходимым время от времени удалять жидкость из электролитической ячейки, если, например, концентрации ионов превысят диапазон, необходимый для получения желаемого продукта моногидрата гидроксида лития или, например, для поддержания корректного функционирования электродов.
[00101] ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНОГО ВАРИАНТА ОСУЩЕСТВЛЕНИЯ
[00102] Обратимся к фигуре, которая раскрывает предпочтительный вариант осуществления способа по данному изобретению, при этом обеспечивают содержащий хлорид лития рассол (1), который может быть натуральным или может быть доступным иным образом, например из руды. Данный рассол подвергают первичному этапу (2) очистки для снижения количеств нежелательных ионов или других загрязняющих примесей. Это этап может быть завершен, например, выпадением в осадок магния, бора, бария и кальция или натрия в качестве нерастворимых солей посредством способов, описанных выше, или иным способом, известным из уровня техники, например базовой регулировкой рН рассола для выпадения в осадок гидроксидов нежелательных ионов. Затем данный рассол может быть использован для других способов, использующих такой рассол (3), или, что более имеет отношение к данному применению, может быть подвергнут вторичному этапу (4) очистки с ионообменом, как было описано выше. В конечном итоге общий вес Са и Mg в рассоле перед электролизом составляет меньше чем 150 ppb в результате любой комбинации химических процессов, процессов испарения солнечной теплотой и/или ионообменных процессов.
[00103] Затем рассол, имеющий меньше чем в целом общего количества 150 ppb ионов Са и Mg, подвергают электролизу (5) с катионоизбирательной проницаемой мембраной для отделения анолита от католита. Ионы лития проходят сквозь мембрану для образования водного католита, содержащего главным образом чистый водный гидроксид лития.
[00104] Выпрямитель (21) присоединен к источнику переменного тока (не показан) и обеспечивает постоянный ток на анод и катод электролитической ячейки (5). Предпочтительно охлаждающая вода циркулирует через выпрямитель для удаления избыточного тепла и улучшения эффективности функционирования выпрямителя. Ячейки запускаются при 1,5 кА/м2, и затем происходит повышение до рабочих условий 2-3 кА/м2 согласно необходимому производственному параметру. Это выполняется при рабочем напряжении 3-3,5 вольт, снова в соответствии с производственными параметрами. Со временем при уменьшении эффективности ячейки необходимая плотность тока будет возрастать, так же как и необходимое напряжение для тех же производственных требований.
[00105] Анолит (14) может быть повторно использован в процессе посредством добавления НСl как из внешнего источника, так и из данного процесса и может быть возращен в сырьевой поток (1) хлорида лития. Предпочтительно анолит очищается (15) перед смешиванием с сырьевым потоком (1) хлорида лития. В предпочтительном варианте осуществления анолит покидает ячейки с концентрацией <20 вес.% и более предпочтительно <19.5 вес.%. Этот отработанный анолит может содержать хлораты и/или гипохлорит вследствие перехода сквозь мембрану иона ОН-. Эти ионы будут предпочтительно нейтрализованы добавлением НСl к повторно используемому отработанному анолиту, а также к свежему анолиту.
[00106] В результате гидролиза образуются газообразный хлор (6) и газообразный водород (7) в качестве побочных продуктов. Затем они могут быть объединены в блоке синтеза соляной кислоты для получения соляной кислоты, которая затем идет на хранение (9). Абсорбер хлора (10) предпочтительно предназначен для работы при аварийных ситуациях в соответствии с хорошо известной техникой безопасности и будет абсорбировать газообразный хлор в случае проблемы с синтетической магистралью НСl.
[00107] В данном предпочтительном варианте осуществления скруббер (12) остаточных газов принимает деминерализованную воду, например, от технологического потока или напрямую, принимает газообразный водород и/или газообразный хлор, подводимые к блоку синтеза (8) НСl для удаления загрязняющих примесей из газовых потоков, таких как остаточный газообразный хлор, не вступивший в реакцию с водородом в блоке синтеза НСl. Блок (12) обеспечивает соответствие нормам выброса в атмосферу.
[00108] Католит (13) представляет собой водный содержащий гидроксид лития раствор, имеющий меньше чем 150 ppb в целом кальция и магния в качестве загрязняющей примеси. Затем гидроксид лития может быть отделен от католита посредством, например, концентрирования каустического средства и/или кристаллизации (16) для осаждения моногидрата гидроксида лития, и далее эти кристаллы могут быть центрифугированы и необязательно высушены (17), моногидрат гидроксида или карбонат лития может быть отделен. Пар может быть использован для процесса очистки кристаллов. Далее в соответствии с требованиями восстановленные кристаллы моногидрата гидроксида лития хранят в их конечной упаковке (18).
[00109] В данном предпочтительном варианте осуществления католит может быть охлажден (19), например, при помощи добавления холодной воды перед восстановлением кристаллов моногидрата гидроксида лития или католит может быть возращен для дальнейшего электролиза (20).
[00110] Технологический конденсат может быть получен из конденсации испарений или в результате работы ячейки, или в результате испарения воды в процессе кристаллизации. Для избежания высоких концентраций ионов ОН- и увеличения переноса ионов Li сквозь мембрану технологический конденсат добавляют до уровней, приводящих к оптимальной эффективности ячейки.
[00111] В альтернативном варианте осуществления католит (13) может быть использован непосредственно в других процессах (22) без восстановления гидроксида лития в качестве кристаллов.
[00112] После концентрирования каустического средства и/или сушки (16) кристаллов оставшийся раствор, который может содержать невосстановленный литий, может быть удален (24) и повторно использован в качестве каустической добавки (25) в сырьевой поток (1) для повторной обработки для восстановления любого неиспользованного лития в качестве гидроксида. Это также поможет отрегулировать рН сырьевого потока анолита, который будет кислотным из-за добавления кислоты, предпочтительно соляной кислоты, полученной на протяжении способа (26).
[00113] Все присутствующие в данном описании ссылки, патенты, патентные заявки, публикации и другие цитаты полностью включаются в него ссылкой для любых целей.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МОНОГИДРАТА ГИДРОКСИДА ЛИТИЯ БИПОЛЯРНЫМ ЭЛЕКТРОДИАЛИЗОМ ИЗ РАССОЛОВ ХЛОРКАЛЬЦИЕВОГО ТИПА И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2024 |
|
RU2834791C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОГИДРАТА ГИДРОКСИДА ЛИТИЯ ВЫСОКОЙ СТЕПЕНИ ЧИСТОТЫ ИЗ МАТЕРИАЛОВ, СОДЕРЖАЩИХ КАРБОНАТ ЛИТИЯ ИЛИ ХЛОРИД ЛИТИЯ | 2019 |
|
RU2751710C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА ЛИТИЯ ВЫСОКОЙ СТЕПЕНИ ЧИСТОТЫ ИЗ ПРИРОДНЫХ РАССОЛОВ | 1998 |
|
RU2157338C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРООКИСИ ЛИТИЯ ИЗ РАССОЛОВ И УСТАНОВКА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1998 |
|
RU2193008C2 |
| Способ получения моногидрата гидроксида лития из рассолов | 2019 |
|
RU2713360C2 |
| Способ получения моногидрата гидроксида лития из рассолов и установка для его осуществления | 2016 |
|
RU2656452C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОГИДРАТА ГИДРОКСИДА ЛИТИЯ ВЫСОКОЙ СТЕПЕНИ ЧИСТОТЫ ИЗ МАТЕРИАЛОВ, СОДЕРЖАЩИХ КАРБОНАТ ЛИТИЯ | 2001 |
|
RU2196735C1 |
| Способ получения моногидрата гидроксида лития высокой степени чистоты из материалов, содержащих соли лития | 2021 |
|
RU2769609C2 |
| ВОССТАНОВЛЕНИЕ ЛИТИЯ ИЗ ВОДНЫХ РАСТВОРОВ | 2009 |
|
RU2470878C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛОВ КАРБОНАТА НАТРИЯ | 2007 |
|
RU2466934C2 |
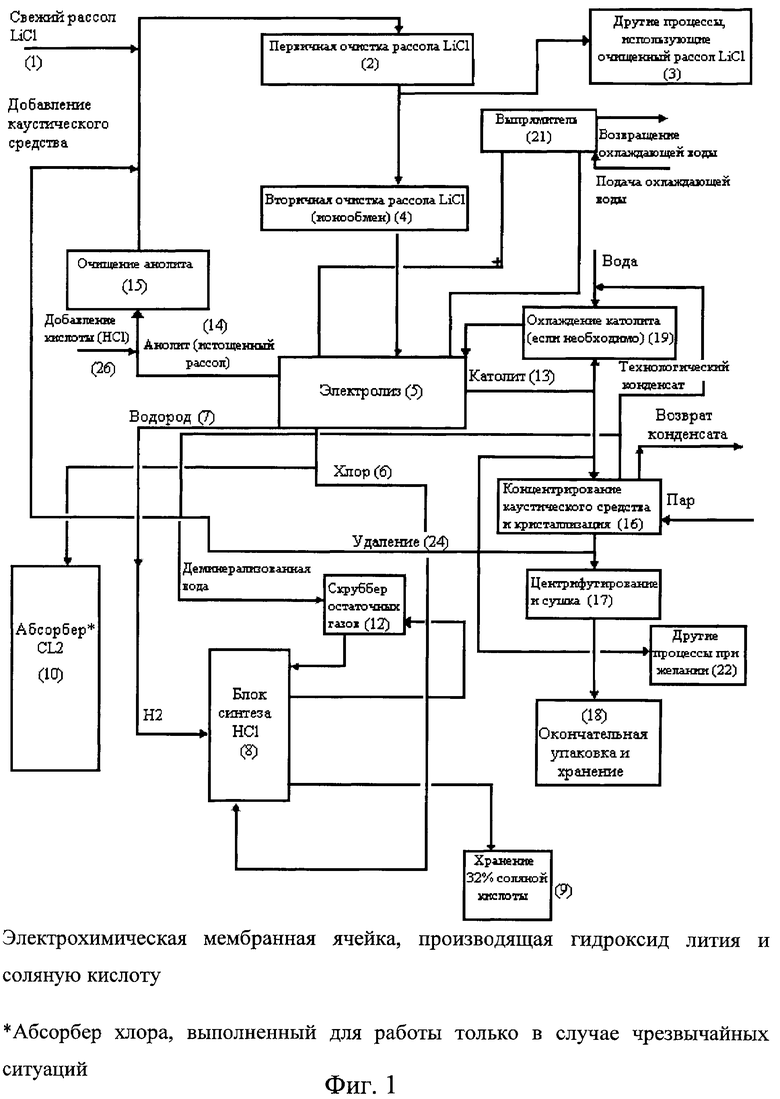
Изобретение может быть использовано в химической промышленности для получения кристаллического моногидрата гидроксида лития, применяемого в аккумуляторных батареях, и карбоната лития. Способ производства кристаллов моногидрата гидроксида лития и соляной кислоты включает очищение рассола, содержащего литий, посредством ионообмена для уменьшения концентраций ионов кальция и магния. Рассол подвергают электролизу для образования раствора гидроксида лития, содержащего меньше чем 150 частей на миллиард общего количества кальция и магния, с получением в качестве побочных продуктов газообразного хлора и водорода. Соляную кислоту производят посредством сжигания полученного газообразного хлора с избыточным водородом. Раствор гидроксида лития концентрируют и кристаллизуют для получения кристаллов моногидрата гидроксида лития. Изобретение позволяет получить высокочистый водный раствор гидроксида лития, из которого легко может быть выделен кристаллический моногидрат гидроксида лития, а также в качестве побочного продукта соляную кислоту. 7 н. и 42 з.п. ф-лы, 1 ил., 2 табл.
1. Способ производства кристаллов моногидрата гидроксида лития, включающий этапы, на которых:
(a) концентрируют содержащий литий рассол, который также содержит натрий и необязательно калий, для осаждения натрия и необязательно калия из рассола;
(b) необязательно очищают рассол для удаления или уменьшения концентраций бора, магния, кальция, сульфата и любого оставшегося натрия или калия;
(c) регулируют рН рассола до около 10,5-11 для дополнительного удаления любых катионов, отличных от лития;
(d) дополнительно очищают рассол посредством ионообмена для уменьшения общей концентрации кальция и магния до меньше, чем 150 млрд-1;
(e) проводят электролиз рассола для образования раствора гидроксида лития, содержащего меньше, чем 150 млрд-1 общего количества кальция и магния, с газообразным хлором и газообразным водородом в качестве побочных продуктов; и
(f) концентрируют и кристаллизуют раствор гидроксида лития для получения кристаллов моногидрата гидроксида лития.
2. Способ по п.1, отличающийся тем, что указанный раствор гидроксида лития на этапе (f) преобразовывают в продукты лития высокой чистоты, предпочтительно карбонат лития высокой чистоты.
3. Способ по п.1, отличающийся тем, что дополнительно содержит центрифугирование кристаллов моногидрата гидроксида лития.
4. Способ по п.3, отличающийся тем, что дополнительно содержит сушку указанных центрифугированных кристаллов и последующую упаковку высушенного материала.
5. Способ по п.1, отличающийся тем, что рассол концентрируют до концентрации лития от около 2% до около 7% перед электролизом.
6. Способ по п.1, отличающийся тем, что содержащий литий рассол, как на этапе (а) концентрируют посредством испарения солнечной теплотой.
7. Способ по п.1, отличающийся тем, что количество бора в рассоле, как на этапе (b) уменьшают посредством процесса органической экстракции или ионообмена.
8. Способ по п.1, отличающийся тем, что количество магния в рассоле, как на этапе (b) уменьшают посредством управляемой реакции с известью или гашеной известью.
9. Способ по п.1, отличающийся тем, что количество магния в рассоле, как на этапе (b) уменьшают посредством управляемой реакции с известью и гашеной известью.
10. Способ по п.1, отличающийся тем, что количество кальция в рассоле, как на этапе (b) уменьшают посредством обработки щавелевой кислотой.
11. Способ по п.1, отличающийся тем, что количество сульфата в рассоле, как на этапе (b) уменьшают посредством обработки барием.
12. Способ по п.1, отличающийся тем, что количество натрия в рассоле, как на этапе (b) уменьшают посредством фракционной кристаллизации.
13. Способ по п.1, отличающийся тем, что рН рассола регулируют до значения около 11.
14. Способ по п.1, отличающийся тем, что рН рассола регулируют добавлением гидроксида лития и карбоната лития в количествах, стехиометрически равных содержанию железа, кальция и магния.
15. Способ по п.1, отличающийся тем, что рН рассола регулируют добавлением гидроксида лития и карбоната лития, которые получены из продуктов способа по п.1.
16. Способ по п.1, отличающийся тем, что общую концентрацию кальция и магния в рассоле уменьшают до меньше, чем 150 млрд-1 посредством ионообмена.
17. Способ по п.1, отличающийся тем, что на этапе электролиза используют полупроницаемые мембраны, которые избирательно пропускают катионы и препятствуют прохождению анионов.
18. Способ по п.1, отличающийся тем, что на этапе электролиза электроды изготовлены из материала с высокой коррозионной устойчивостью.
19. Способ по п.1, отличающийся тем, что на этапе электролиза электроды имеют титановое и никелевое покрытие.
20. Способ по п.1, отличающийся тем, что на этапе электролиза электрохимическую ячейку располагают в конфигурации с псевдо нулевым зазором.
21. Способ по п.1, отличающийся тем, что на этапе электролиза используют монополярную мембранную ячейку, предпочтительно монополярную мембрану Ineos Chlor FM1 500.
22. Способ по п.1, отличающийся тем, что на этапе электролиза электрод со стороны катода имеет многопластинчатую конструкцию в форме фонаря для возникновения турбулентности и высвобождения газа.
23. Способ производства соляной кислоты, при этом способ включает этапы, на которых:
(a) концентрируют содержащий литий рассол, который также содержит натрий и необязательно калий, для осаждения натрия и необязательно калия из рассола;
(b) необязательно очищают рассол для удаления или уменьшения концентраций бора, магния, кальция, сульфата и любого оставшегося натрия или калия;
(c) регулируют рН рассола до около 10,5-11 для дополнительного удаления любых катионов, отличных от лития;
(d) дополнительно очищают рассол посредством ионообмена для уменьшения общей концентрации кальция и магния до меньше, чем 150 млрд-1;
(e) электролизируют рассол для образования раствора гидроксида лития, содержащего меньше, чем 150 млрд-1 общего количества кальция и магния с газообразным хлором и газообразным водородом в качестве побочных продуктов; и
(f) производят соляную кислоту посредством сжигания газообразного хлора с избыточным водородом.
24. Способ по п.23, отличающийся тем, что указанный раствор гидроксида лития на этапе (е) преобразовывают в продукты лития высокой чистоты, предпочтительно карбонат лития высокой чистоты.
25. Способ по п.24, отличающийся тем, что дополнительно содержит концентрирование и кристаллизацию раствора гидроксида лития для получения кристаллов моногидрата гидроксида лития.
26. Способ по п.25, отличающийся тем, что дополнительно содержит сушку указанных кристаллов.
27. Способ по п.23, отличающийся тем, что рассол концентрируют до концентрации лития от около 2% до около 7% перед электролизом.
28. Способ по п.23, отличающийся тем, что содержащий литий рассол, как на этапе (а) концентрируют посредством испарения солнечной теплотой.
29. Способ по п.23, отличающийся тем, что количество бора в рассоле, как на этапе (b) уменьшают посредством процесса органической экстракции.
30. Способ по п.23, отличающийся тем, что количество магния в рассоле, как на этапе (b) уменьшают посредством управляемой реакции с известью или гашеной известью.
31. Способ по п.23, отличающийся тем, что количество магния в рассоле, как на этапе (b) уменьшают посредством управляемой реакции с известью.
32. Способ по п.23, отличающийся тем, что количество кальция в рассоле, как на этапе (b) уменьшают посредством обработки щавелевой кислотой.
33. Способ по п.23, отличающийся тем, что количество сульфата в рассоле, как на этапе (b) уменьшают посредством обработки барием.
34. Способ по п.23, отличающийся тем, что количество натрия в рассоле, как на этапе (b) уменьшают посредством фракционной кристаллизации.
35. Способ по п.23, отличающийся тем, что рН рассола регулируют до значения около 11.
36. Способ по п.23, отличающийся тем, что рН рассола регулируют добавлением гидроксида лития и карбоната лития в количествах, стехиометрически равных содержанию железа, кальция и магния.
37. Способ по п.23, отличающийся тем, что рН рассола регулируют добавлением гидроксида лития и карбоната лития, которые получены из продуктов способа по п. 1.
38. Способ по п.23, отличающийся тем, что общую концентрацию кальция и магния в рассоле уменьшают до меньше, чем 150 млрд-1 посредством ионообмена.
39. Способ по п.23, отличающийся тем, что на этапе электролиза используют полупроницаемые мембраны, которые избирательно пропускают катионы и препятствуют прохождению анионов.
40. Способ по п.23, отличающийся тем, что на этапе электролиза электроды изготовлены из материала с высокой коррозионной устойчивостью.
41. Способ по п.23, отличающийся тем, что на этапе электролиза электроды имеют титановое и никелевое покрытие.
42. Способ по п.23, отличающийся тем, что на этапе электролиза электрохимическую ячейку располагают в конфигурации с псевдо нулевым зазором.
43. Способ по п.23, отличающийся тем, что на этапе электролиза используют монополярную мембранную ячейку, предпочтительно Ineos Chlor FM1 500 или другую коммерчески доступную монополярную мембранную ячейку.
44. Способ по п.23, отличающийся тем, что на этапе электролиза электрод со стороны катода имеет многопластинчатую конструкцию в форме фонаря для возникновения турбулентности и высвобождения газа.
45. Способ производства кристаллов моногидрата гидроксида лития, включающий этапы, на которых:
(a) очищают содержащий литий рассол, который также содержит натрий и необязательно калий, для уменьшения общей концентрации кальция и магния до меньше, чем 150 млрд-1;
(b) электролизируют рассол для образования раствора гидроксида лития, содержащего меньше, чем 150 млрд-1 общего количества кальция и магния, с газообразным хлором и газообразным водородом в качестве побочных продуктов; и
(c) концентрируют и кристаллизуют раствор гидроксида лития для получения кристаллов моногидрата гидроксида лития.
46. Способ производства соляной кислоты, при этом способ включает этапы, на которых:
(a) очищают содержащий литий рассол, который также содержит натрий и необязательно калий, для уменьшения общей концентрации кальция и магния до меньше, чем 150 млрд-1;
(b) электролизируют рассол для образования раствора гидроксида лития, содержащего меньше, чем 150 млрд-1 общего количества кальция и магния, с газообразным хлором и газообразным водородом в качестве побочных продуктов; и
(c) производят соляную кислоту посредством сжигания газообразного хлора с избыточным водородом.
47. Способ производства и моногидрата гидроксида лития, и соляной кислоты, при этом способ включает этапы, на которых:
(a) очищают содержащий литий рассол, который также содержит натрий и необязательно калий, для уменьшения общей концентрации кальция и магния до меньше, чем 150 млрд-1;
(b) электролизируют рассол для образования раствора гидроксида лития, содержащего меньше, чем 150 млрд-1 общего количества кальция и магния, с газообразным хлором и газообразным водородом в качестве побочных продуктов; и
(c) концентрируют и кристаллизуют раствор гидроксида лития для получения кристаллов моногидрата гидроксида лития; и
(d) производят соляную кислоту посредством сжигания газообразного хлора с избыточным водородом.
48. Моногидрат гидроксида лития, содержащий меньше, чем 150 млрд-1 в целом общего количества Са и Mg и, предпочтительно меньше, чем 50 млрд-1 общего количества, и, более предпочтительно меньше, чем 15 млрд-1 в целом общего количества.
49. Водный гидроксид лития, содержащий меньше, чем 150 млрд-1 общего количества Са и Mg и, предпочтительно меньше, чем 50 млрд-1 общего количества, и, более предпочтительно меньше, чем 15 млрд-1 в целом общего количества.
| US 4036713 А, 19.07.1977 | |||
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА ЛИТИЯ ИЛИ ЕГО СОЛЕЙ С ВЫСОКОЙ СТЕПЕНЬЮ ЧИСТОТЫ ИЗ ПРИРОДНЫХ РАССОЛОВ | 1994 |
|
RU2090503C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИДА ЛИТИЯ ВЫСОКОЙ СТЕПЕНИ ЧИСТОТЫ ИЗ ПРИРОДНЫХ РАССОЛОВ | 1998 |
|
RU2157338C2 |
| US 20070160516 C1, 12.07.2007 | |||
| US 3597340 A1, 03.08.1971. | |||
Авторы
Даты
2012-12-27—Публикация
2009-04-09—Подача