Описание
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ НАСТОЯЩЕЕ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к органической аминовой соли 6-фтор-3-гидрокси-2-пиразинкарбонитрила, которая является пригодной в качестве промежуточного соединения для получения фармацевтических препаратов, и способу получения данной аминовой соли.
УРОВЕНЬ ТЕХНИКИ
6-фтор-3-гидрокси-2-пиразинкарбоксамид (в настоящем изобретении называемый T-705) представляет собой соединение, которое является пригодным для предупреждения и лечения заболеваний, в частности гриппа. Известно, что T-705 можно получить, например, из 6-фтор-3-гидрокси-2-пиразинкарбонитрила (патентный документ 1).
В качестве способа получения 6-фтор-3-гидрокси-2-пиразинкарбонитрила, например, известны следующие (1) и (2) способы: (1) способ, в котором 3,6-дифтор-2-пиразинкарбонитрил реагирует с бензиловым спиртом и продукт реакции дебензилируют; и (2) способ, в котором 3,6-дифтор-2-пиразинкарбонитрил подвергают реакции с водой (патентный документ 1).
Данные известные способы, однако, имеют некоторые недостатки, например недостатки, упомянутые ниже: (A) промежуточный продукт 3-бензилокси-6-фтор-2-пиразинкарбонитрил является лабильным соединением; (B) трудные операции, такие как экстракция, колоночная хроматография и удаление растворителя отгонкой, являются необходимыми; (C) генерируется вредный водород при подкислении реакционной среды; (D) выход является низким.
Кроме того, не легко выделить 6-фтор-3-гидрокси-2-пиразинкарбонитрил из реакционной смеси с высоким выходом простой операцией, т.к. соединение является растворимым в воде и многих органических растворителях.
Патентный документ 1: международная публикация No. 01/60834
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ЗАДАЧИ, РЕШАЕМЫЕ НАСТОЯЩИМ ИЗОБРЕТЕНИЕМ
Более подходящее промежуточное соединение для получения T-705 и способ получения промежуточного соединения чрезвычайно необходимы.
СПОСОБЫ РЕШЕНИЯ УКАЗАННЫХ ПРОБЛЕМ
В данных обстоятельствах авторы настоящего изобретения продолжили интенсивные исследования данного объекта и, как результат, обнаружили, что органическая аминовая соль 6-фтор-3-гидрокси-2-пиразинкарбонитрила обладает превосходной степенью кристалличности и может служить в качестве промежуточного соединения для получения T-705. Они также обнаружили, что органическую аминовую соль 6-фтор-3-гидрокси-2-пиразинкарбонитрила можно легко получить с высоким выходом реакцией 3,6-дифтор-2-пиразинкарбонитрила с водой в присутствии основания и, затем, добавлением органического амина. Данные находки привели их к созданию настоящего изобретения.
ПРЕИМУЩЕСТВА НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Органические аминовые соли гидрокси-2-пиразинкарбонитрила согласно настоящему изобретению обладают превосходной степенью кристалличности, и их можно выделить из реакционной смеси с высоким выходом простой операцией, и они являются пригодными в качестве промежуточного соединения для получения T-705. Кроме того, способ получения органических аминовых солей 6-фтор-3-гидрокси-2-пиразинкарбонитрила согласно настоящему изобретению имеет ряд преимуществ, а именно: (1) в способе не применяется лабильное промежуточное соединение; (2) не требуются трудные операции, такие как экстракция, колоночная хроматография и удаление растворителя отгонкой; (3) не образуется вредный водород; (4) выход является высоким; и (5) полученные органические аминовые соли имеют высокую частоту. Данный способ настоящего изобретения, следовательно, является пригодным в качестве способа для промышленного получения органических аминовых солей 6-фтор-3-гидрокси-2-пиразинкарбонитрила.
ЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Настоящее изобретение будет объяснено подробно ниже.
В настоящем описании настоящего изобретения "органические амины" обозначают следующее, если не указано особо: третичные амины, такие как триметиламин, триэтиламин, трипропиламин, трибутиламин, трибензиламин и N,N-диметилциклогексиламин; вторичные амины, такие как диметиламин, диэтиламин, дипропиламин, дибутиламин, дибензиламин, N-бензилметиламин и дициклогексиламин; первичные амины, такие как этиламин, пропиламин, бутиламин, бензиламин, анилин; и пиридин и подобные.
В органических аминовых солях 6-фтор-3-гидрокси-2-пиразинкарбонитрила, представленных в качестве соединений настоящего изобретения, следующие соединения являются предпочтительными.
Соединения, содержащие в качестве органического амина вторичный амин, в частности дипропиламин, дибутиламин, дициклогексиламин, дибензиламин и N-бензилметиламин, являются предпочтительными, и соединения, содержащие дициклогексиламин, являются особенно предпочтительными.
Предпочтительный способ получения согласно настоящему изобретению показан ниже.
Способ получения органической аминовой соли 6-фтор-3-гидрокси-2-пиразинкарбонитрила реакцией 3,6-дифтор-2-пиразинкарбонитрила с водой в присутствии основания и, затем, добавлением органического амина, где применяют вторичный амин в качестве органического амина, является предпочтительным. Более предпочтительным является способ, в котором в качестве вторичного амина применяют дипропиламин, дибутиламин, дициклогексиламин, дибензиламин или N-бензилметиламин. Способ, в котором применяют дициклогексиламин, является даже более предпочтительным.
Далее объясняется способ получения согласно настоящему изобретению.
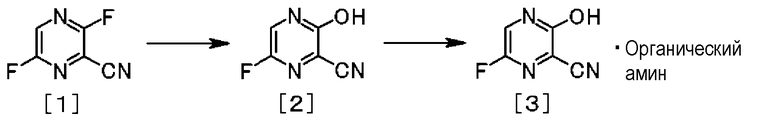
Органическую аминовую соль соединения формулы [3] можно получить реакцией соединения формулы [1] с водой в присутствии основания для получения соединения формулы [2] и, затем, дополнительной реакцией его с органическим амином.
Данный способ настоящего изобретения будет описан подробно ниже.
[Стадия 1]
Соединение формулы [2] можно получить реакцией соединения формулы [1] с водой в присутствии основания.
Данную реакцию обычно проводят в присутствии растворителя. Можно применять все виды растворителей, поскольку они не оказывают никакого нежелательного эффекта на реакцию. Примеры данных растворителей включают нитрилы, такие как ацетонитрил; ароматические углеводороды, такие как бензол, толуол и ксилол; эфиры, такие как диоксан, тетрагидрофуран, диметиловый эфир этиленгликоля и диметиловый эфир диэтиленгликоля; кетоны, такие как ацетон и 2-бутанон; спирты, такие как этанол, пропанол, 2-пропанол и бутанол; амиды, такие как N,N-диметилформамид и N,N-диметилацетамид; и сульфоксиды, такие как диметилсульфоксид. Можно применять смеси данных растворителей. Предпочтительными растворителями для применения в настоящем изобретении являются ароматические углеводороды, эфиры, амиды и сульфоксиды. Среди данных растворителей амиды и сульфоксиды являются более предпочтительными, N,N-диметилформамид даже еще более предпочтительным. Количество применяемого растворителя конкретно не описывают, но его желательно применяют в количестве в 1-50 раз (об./вес), предпочтительно в 1-15 раз (об./вес) больше количества соединения формулы [1].
Применяемые основания в вышеуказанной реакции не зависят от конкретных описаний при условии, что они являются реагентами, обычно применяемыми для гидроксилирования в реакциях нуклеофильного замещения соединений, содержащих ароматический атом галогена. Примеры данных оснований включают органические основания, такие как диизопропилэтиламин и триэтиламин; гидроксиды четвертичного аммония, такие как гидроксид бензилтриметиламмония; карбоксилаты, такие как формиат калия, формиат натрия, муравьиная кислота-триэтиламин, ацетат калия, ацетат натрия, уксусная кислота-триэтиламин, пропионат натрия, гексаноат натрия, бензоат натрия и бензойная кислота-триэтиламин; и неорганические основания, такие как гидроксид натрия, гидроксид калия, карбонат натрия, карбонат калия, бикарбонат натрия, бикарбонат калия, гидрофосфат дикалия, фосфат трикалия. Карбоксилаты являются предпочтительными для применения в качестве основания. Формиат калия, муравьиная кислота-триэтиламин, ацетат калия и уксусная кислота-триэтиламин являются более предпочтительными. В настоящем изобретении основание применяют в количестве 1 моль или более, желательно 1-10 молей на один моль соединения формулы [1].
Карбоксилаты можно получить в реакционной системе.
Количество применяемой воды для реакции специально не определено; достаточно применять воду в количестве один моль или более, желательно 1-50 моль на один моль соединения формулы [1].
В случае применения карбоксилата, можно получить соединение формулы [2] реакцией соединения формулы [1] с карбоксилатом в отсутствии воды и, затем, проведением реакции с водой.
Температуру реакции специально не определяют, но требуется, чтобы она не была выше 200°C, желательно от 0 до 150°C.
Продолжительность реакции также не описана в настоящем изобретении; продолжительность от 5 минут до 50 часов является достаточной для данной реакции. Предпочтительная продолжительность реакции составляет от 5 минут до 24 часов.
Соединение формулы [2] можно выделять и очищать, но желательно обеспечить применение в следующей реакции без выделения.
[Стадия 2]
Органическую аминовую соль соединения формулы [3] можно получить, подвергая соединение формулы [2] реакции с органическим амином.
Данную реакцию обычно проводят в присутствии растворителя. Можно применять любой тип растворителя для реакции, при условии, что их присутствие не препятствует протеканию реакции любым способом. Примерами данных растворителей являются нитрилы, такие как ацетонитрил; ароматические углеводороды, такие как бензол, толуол и ксилол; эфиры, такие как диоксан, тетрагидрофуран, диметиловый эфир этиленгликоля и диметиловый эфир диэтиленгликоля; кетоны, такие как ацетон и 2-бутанон; спирты, такие как метанол, этанол, пропанол, 2-пропанол и бутанол; амиды, такие как N,N-диметилформамид, сульфоксиды, такие как диметилсульфоксид; и воду. Также являются пригодными смеси данных растворителей. Предпочтительной для применения в настоящем изобретении является смесь, по меньшей мере, одного растворителя, выбранного из ароматических углеводородов, кетонов, спиртов, амидов и сульфоксидов с водой. Смесь ароматического углеводорода, кетона или амида с водой является особенно предпочтительной, и смесь толуола, ацетона или N,N-диметилформамида с водой является более предпочтительной. Количество растворителя, применяемое в настоящем изобретении, неопределенно, но желательно в 1-100 раз (об./вес), предпочтительно в 1-50 раз (об./вес) больше количества соединения формулы [2].
Количество органического амина, применяемого в реакции также не определенно, но применение органического амина в количестве один моль или более одного моля соединения формулы [2] является достаточным. Желательно применять органический амин в количестве 1-2 моля на один моль соединения формулы [2].
Температуру реакции специально не определяют, но требуется, чтобы она была не выше 150°C, желательно от 0 до 100°C.
Продолжительность реакции также не определяют в настоящем изобретении; продолжительность от одной минуты до 50 часов является достаточной для реакции. Предпочтительная продолжительность реакцию составляет от одной минуты до 24 часов.
Данную реакцию желательно проводить в основных условиях. Например, желательно добавлять в реакционную смесь основание, выбранное из аммиачной воды, гидроксида калия, гидроксида натрия, ацетата калия и ацетата натрия.
Органические аминовые соли соединения формулы [3], полученные вышеописанным способом получения, можно выделять фильтрацией и собиранием твердого остатка.
Соединение формулы [1], применяемое в качестве продукта настоящего изобретения, можно получить из 3,6-дихлор-2-пиразинкарбонитрила или подобных, например, способом, описанным в патентном документе 1. 3,6-дихлор-2-пиразинкарбонитрил можно получить объединением по существу известных способов (патентный документ 1). Например, вышеуказанное соединение можно получить реакцией 3-гидрокси-6-нитро-2-пиразинкарбоксамида или 6-бром-3-гидрокси-2-пиразинкарбоксамида с галогенирующим агентом, таким как хлорокись фосфора. В данных способах получения соединение формулы [1] и 3,6-дихлор-2-пиразинкарбонитрил можно выделить и очистить, но их можно непосредственно применять в следующей реакции без выделения.
В способе получения соединения формулы [3] из соединения формулы [1] выход способа получения, описанный в патентном документе 1, составлял 46% (патентный документ 1; пример II-5(a)).
В отличие от этого, в способе получения органической аминовой соли соединения формулы [3] из соединения формулы [1] выход способа получения настоящего изобретения составлял 83% (пример 1-1).
Таким образом, способ получения настоящего изобретения имеет больший выход и является пригодным в качестве способа получения.
Соединения формулы [2] и соединения формулы [3] включают таутомер 6-фтор-3-оксо-3,4-дигидро-2-пиразинкарбонитрила. Настоящее изобретение включает данный таутомер, и в настоящем изобретении можно применять гидраты, сольваты и все кристаллические формы.
Примеры
Настоящее изобретение будет объяснено посредством примеров, а также примеров получения, но данные примеры предназначены просто в качестве иллюстрации и не подразумевается, что они ограничивают настоящее изобретение любым способом.
DMCO-d6: диметилсульфоксид-d6
Пример 1-1
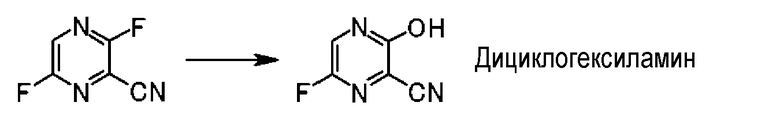
К 17,5 мл N,N-диметилформамидного раствора 5,0 г 3,6-дифтор-2-пиразинкарбонитрила добавляли по каплям 3,8 мл водного раствора 7,83 г ацетата калия при 25-35°C и раствор перемешивали при той же температуре в течение 2 часов. Добавляли 0,38 мл аммиачной воды к реакционной смеси и затем 15 мл воды и добавляли 0,38 г активированного угля. Нерастворимые вещества отфильтровывали и остаток на фильтре промывали 11 мл воды. Фильтрат и промывки объединяли, pH данного раствора доводили до 9,4 аммиачной водой и добавляли 15 мл ацетона и 7,5 мл толуола. Затем добавляли по каплям 7,71 г дициклогексиламина и раствор перемешивали при 20-30°C в течение 45 минут. Затем добавляли по каплям 15 мл воды, раствор охлаждали до 10°C и осадок фильтровали и собирали, получая 9,44 г дициклогексиламина 6-фтор-3-гидрокси-2-пиразинкарбонитрила в виде светло-желтоватого твердого остатка.
1H-ЯМР (DMCO-d6) δ значения: 1,00-1,36 (10H, м), 1,56-1,67 (2H, м), 1,67-1,81 (4H, м), 1,91-2,07 (4H, м), 3,01-3,18 (2H, м), 8,03-8,06 (1H, м), 8,18-8,89 (1H, уширенный)
Пример 1-2
Добавляли 4,11 мл уксусной кислоты при 5-15°C к 17,5 мл N,N-диметилформамидного раствора 5,0 г 3,6-дифтор-2-пиразинкарбонитрила. Затем добавляли по каплям 7,27 г триэтиламина и раствор перемешивали в течение 2 часов. Добавляли к реакционной смеси 3,8 мл воды и 0,38 мл аммиачной воды и затем добавляли 15 мл воды и 0,38 г активированного угля. Нерастворимые вещества отфильтровывали и остаток на фильтре промывали 11 мл воды. Фильтрат и промывки объединяли, pH данного раствора доводили до 9,2 аммиачной водой и добавляли к раствору 15 мл ацетона и 7,5 мл толуола, с последующим добавлением по каплям 7,71 г дициклогексиламина. Затем, добавляли по каплям 15 мл воды, раствор охлаждали до 10°C и осадок фильтровали и собирали, получая 9,68 г дициклогексиламина 6-фтор-3-гидрокси-2-пиразинкарбонитрила в виде слегка желтоватого белого твердого остатка.
Примеры 2-5
Соединения, показанные в таблице 1, получали тем же способом, как в примере 1-1.
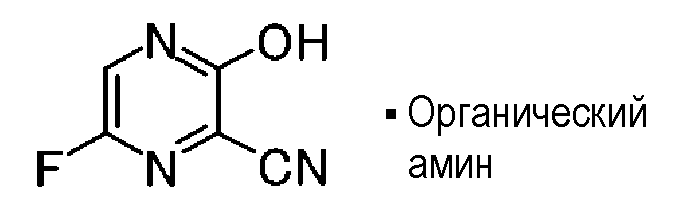
Дипропиламиновая соль 6-фтор-3-гидрокси-2-пиразинкарбонитрила
1H-ЯМР (DMCO-d6) δ значения: 0,39 (6H, т, J=7,5 Гц), 1,10 (4H, секс, J=7,5 Гц), 2,30-2,38 (4H, м), 7,54 (1H, д, J=8,3 Гц)
Дибутиламиновая соль 6-фтор-3-гидрокси-2-пиразинкарбонитрил-2-пиразинкарбонитрила
1H-ЯМР (DMCO-d6) δ значения: 0,36 (6H, т, J=7,3 Гц), 0,81 (4H, секс, J=7,3 Гц), 0,99-1,10 (4H, м), 2,32-2,41 (4H, м), 7,53 (1H, д, J=8,3 Гц)
Дибензиламиновая соль 6-фтор-3-гидрокси-2-пиразинкарбонитрила
1H-ЯМР (DMCO-d6) δ значения: 4,17 (4H, с), 7,34-7,56 (10H, м), 8,07 (1H, д, J=8,3 Гц)
N-бензилметиламиновая соль 6-фтор-3-гидрокси-2-пиразинкарбонитрила
1H-ЯМР (DMCO-d6) δ значения: 2,57 (3H, с), 4,14 (2H, с), 7,37-7,53 (5H, м), 8,02-8,08 (1H, м)
Пример получения 1

300 мл толуола добавляли к 600 мл водного раствора 37,5 г гидроксида натрия. Затем добавляли 150 г дициклогексиламиновой соли 6-фтор-3-гидрокси-2-пиразинкарбонитрила при 15-25°C и раствор перемешивали при той же температуре в течение 30 минут. Водный слой отделяли и промывали толуолом и затем добавляли 150 мл воды, с последующим добавлением по каплям 106 г 30% раствора пероксида водорода при 15-30°C и перемешиванием в течение 1 часа при 20-30°C. Затем добавляли 39 мл хлороводородной кислоты, добавляли затравку при 40-50°C и дополнительно добавляли по каплям 39 мл хлороводородной кислоты при той же температуре. Раствор охлаждали до 10°C, осадок фильтровали и собирали, получая 65,6 г 6-фтор-3-гидрокси-2-пиразинкарбоксамида в виде слегка желтоватого белого твердого остатка.
1H-ЯМР (DMCO-d6) δ значения: 8,50 (1H, с), 8,51 (1H, д, J=7,8 Гц), 8,75 (1H, с), 13,41 (1H, с)
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Органические аминовые соли 6-фтор-3-гидрокси-2-пиразинкарбонитрила настоящего изобретения обладают превосходной степенью кристалличности и являются пригодными в качестве промежуточного соединение для получения 6-фтор-3-гидрокси-2-пиразинкарбоксамида.
Изобретение относится к органической аминовой соли 6-фтор-3-гидрокси-2-пиразинкарбонитрила, в которой органический амин представляет собой вторичный амин, например дипропиламин, дибутиламин, дициклогексиламин, дибензиламин или N-бензилметиламин. Изобретение также относится к способу получения указанной соли. Технический результат - получена новая органическая аминовая соль 6-фтор-3-гидрокси-2-пиразинкарбонитрила, которая обладает превосходной степенью кристалличности и является пригодной в качестве промежуточного соединения для получения 6-фтор-3-гидрокси-2-пиразинкарбоксамида. 2 н. и 4 з.п. ф-лы, 1 табл., 5 пр.
1. Органическая аминовая соль 6-фтор-3-гидрокси-2-пиразинкарбонитрила, в которой органический амин представляет собой вторичный амин.
2. Органическая аминовая соль по п.1, в которой вторичный амин представляет собой дипропиламин, дибутиламин, дициклогексиламин, дибензиламин или N-бензилметиламин.
3. Органическая аминовая соль по п.1, в которой вторичный амин представляет собой дициклогексиламин.
4. Способ получения органической аминовой соли 6-фтор-3-гидрокси-2-пиразинкарбонитрила, который включает реакцию 3,6-дифтор-2-пиразинкарбонитрила с водой в присутствии основания и затем образование соли с органическим амином, в котором органический амин представляет собой вторичный амин.
5. Способ по п.4, в котором вторичный амин представляет собой дипропиламин, дибутиламин, дициклогексиламин, дибензиламин или N-бензилметиламин.
6. Способ по п.4, в котором вторичный амин представляет собой дициклогексиламин.
| ПРОИЗВОДНЫЕ ПИРАЗИНА ИЛИ ИХ СОЛИ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ДАННЫЕ СОЕДИНЕНИЯ, И ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ИХ ПОЛУЧЕНИЯ | 2001 |
|
RU2297414C2 |
| JP 2004043371 A, 12.02.2004 | |||
| СПОСОБ ПОЛУЧЕНИЯ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ КАРБОНОВЫХ КИСЛОТ, СОДЕРЖАЩИХ ГИДРОКСИЛЬНУЮ ГРУППУ, ИЛИ ИХ РАСТВОРИМЫХ СОЛЕЙ, ШТАММ БАКТЕРИЙ, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ БИОТРАНСФОРМАЦИИ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ КАРБОНОВЫХ КИСЛОТ В АЗОТСОДЕРЖАЩИЕ ГЕТЕРОЦИКЛИЧЕСКИЕ КАРБОНОВЫЕ КИСЛОТЫ, СОДЕРЖАЩИЕ ГИДРОКСИЛЬНУЮ ГРУППУ. | 1993 |
|
RU2122029C1 |
Авторы
Даты
2012-12-27—Публикация
2008-09-25—Подача