Область техники
Данное изобретение относится к фторсодержащему сераорганическому соединению и пестицидной композиции, содержащей соединение.
Уровень техники
До настоящего времени было разработано и применяется на практике множество пестицидных композиций для борьбы с членистоногими вредителями. Также, в JP-A 2005-179321 описано определенное галогенсодержащее сераорганическое соединение.
Описание изобретения
Объектом данного изобретения является новое соединение, оказывающее превосходное контролирующее действие на членистоногих вредителей, и его применение.
Авторы данного изобретения провели активные исследования для получения соединения, оказывающего превосходное контролирующее действие на членистоногих вредителей. В результате они обнаружили, что фторсодержащее сераорганическое соединение, представленное формулой (I), оказывает превосходное контролирующее действие на членистоногих вредителей, таких как вредные насекомые или вредные клещи. Таким образом, было получено данное изобретение.
То есть в данном изобретении представлено:
(1) Фторсодержащее сераорганическое соединение, представленное формулой (I):
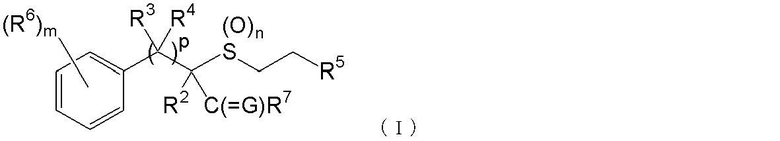
где G является атомом кислорода или атомом серы;
R2 является атомом галогена, атомом водорода или C1-C4 углеводородной цепью, которая может быть замещена атомом галогена;
R3 и R4 независимо являются C1-C4 углеводородной цепью или атомом водорода;
R5 является атомом фтора или C1-C5 галогеналкилом, содержащим, по крайней мере, один атом фтора;
R6 является атомом галогена, цианогруппой, нитрогруппой или -(G1)q-R8 группой;
R7 является аминогруппой, С1-C4 алкиламиногруппой, которая может быть необязательно замещена атомом галогена, ди(C1-C4 алкил)аминогруппой, которая может быть необязательно замещена атомом галогена, или С2-C5 циклической аминогруппой;
R8 является C1-C4 углеводородной цепью, которая может быть необязательно замещена атомом галогена;
m равно целому числу от 0 до 5, при условии, что R6 необязательно являются одинаковыми или отличными друг от друга, если m равно от 2 до 5;
n равно целому числу от 0 до 2;
p равно 0 или 1;
q равно 0 или 1; и
G1 является атомом кислорода, атомом серы, -SO- группой или -SO2- группой (далее обозначенной как «соединение в соответствии с данным изобретением»);
(2) Фторсодержащее сераорганическое соединение по (1), где p равно 0;
(3) Фторсодержащее сераорганическое соединение по (1) или (2), где G является атомом кислорода;
(4) Фторсодержащее сераорганическое соединение по (1) или (2), где G является атомом кислорода и R7 является аминогруппой;
(5) Фторсодержащее сераорганическое соединение по любому из (1)-(4), где R2 является атомом галогена;
(6) Фторсодержащее сераорганическое соединение по любому из (1) до (5), где n равно 2;
(7) Пестицидная композиция, содержащая фторсодержащее сераорганическое соединение по любому из (1)-(6) в качестве активного ингредиента; и
(8) Способ контроля членистоногих вредителей, который включает нанесение эффективного количества фторсодержащего сераорганического соединения по любому из (1)-(6) на членистоногих вредителей или место, где обитают членистоногие вредители.
Иллюстративный вариант осуществления данного изобретения
Выражение "C1-C4" или подобное в данном описании означает общее количество атомов углерода, составляющих каждую группу заместителя.
Примеры «атома галогена» включают атом фтора, атом хлора и атом брома.
Примеры “C1-C4 углеводородной цепи, которая может быть необязательно замещена атомом галогена» включают C1-C4 алкильную группу, которая может быть необязательно замещена атомом галогена, такую как метильная группа, этильная группа, пропильная группа, 1-метилэтильная группа (далее иногда обозначенная как изо-пропильная группа), 1,1-диметилэтильная группа (далее иногда обозначенная как трет-бутильная группа), хлорметильная группа, фторметильная группа, дифторметильная группа, трифторметильная группа, 2,2,2-трифторэтильная группа, 1,1,2,2-тетрафторэтильная группа или 1,1,2,2,2-пентафторэтильная группа; C2-C4 алкенильную группу, которая может быть необязательно замещена атомом галогена, такую как винильная группа, 2,2-дифторвинильная группа, 1,2,2-трифторвинильная группа, 1-пропенильная группа, 2-пропенильная группа, 3,3-дифтор-2-пропенильная группа, 1-метил-2-пропенильная группа, 2-метил-2-пропенильная группа, 1-бутенильная группа или 2-бутенильная группа; и C2-C4 алкинильную группу, которая может быть необязательно замещена атомом галогена, такую как этинильная группа, 1-пропинильная группа, 3,3,3-трифтор-1-пропинильная группа, 2-пропинильная группа, 1-метил-2-пропинильная группа, 1-бутинильная, 2-бутинильная или 3-бутинильная группа.
Примеры “C1-C4 углеводородной цепи” включают C1-C4 алкильную группу, такую как метильная группа, этильная группа, пропильная группа, 1-метилэтильная группа (далее иногда обозначенная как изо-пропильная группа) или 1,1-диметилэтильная группа (далее иногда обозначенная как трет-бутильная группа); C2-C4 алкенильную группу, такую как винильная группа, 1-пропенильная группа, 2-пропенильная группа, 1-метил-2-пропенильная группа, 2-метил-2-пропенильная группа, 1-бутенильная группа или 2-бутенильная группа; и C2-C4 алкинильную группу, такую как этинильная группа, 1-пропинильная группа, 2-пропинильная группа, 1-метил-2-пропинильная группа, 1-бутинильная группа, 2-бутинильная группа или 3-бутинильная группа.
Примеры “C1-C5 галогеналкильной группы, содержащей, по меньшей мере, один атом фтора” включают фторметильную группу, дифторметильную группу, трифторметильную группу, 1-фторэтильную группу, 2-фторэтильную группу, 1,1-дифторэтильную группу, 2,2-дифторэтильную группу, 2,2,2-трифторэтильную группу, 1,1,2,2,2-пентафторэтильную группу, 1-фторпропильную группу, 1,1-дифторпропильную группу, 2-фторпропильную группу, 2,2-дифторпропильную группу, 3-фторпропильную группу, 3,3-дифторпропильную группу, 3,3,3-трифторпропильную группу, 1,1,2,2,3,3,3-гептафторпропильную группу, 2,2,3,3,3-пентафторпропильную группу, 2,2,2-трифтор-(1-трифторметил)этильную группу, 1,2,2,2-тетрафтор-трифтор-(1-трифторметил)этильную группу, 2,2,3,3-тетрафторпропильную группу, 1-фторбутильную группу, 1,1-дифторбутильную группу, 2-фторбутильную группу, 2,2-дифторбутильную группу, 3-фторбутильную группу, 3,3-дифторбутильную группу, 4-фторбутильную группу, 4,4-дифторбутильную группу, 4,4,4-трифторбутильную группу, 3,3,4,4,4-пентафторбутильную группу, 2,2,3,4,4-пентафторбутильную группу, 2,2,3,3,4,4,4-гептафторбутильную группу, 1-фторпентильную группу, 1,1-дифторпентильную группу, 2-фторпентильную группу, 2,2-дифторпентильную группу, 3-фторпентильную группу, 3,3-дифторпентильную группу, 4-фторпентильную группу, 4,4-дифторпентильную группу, 5-фторпентильную группу, 5,5-дифторпентильную группу, 5,5,5-трифторпентильную группу, 4,4,5,5,5-пентафторпентильную группу, 3,3,4,4,5,5,5-гептафторпентильную группу, 2,2,3,3,4,4,5,5-октафторпентильную группу и 2,2,3,3,4,4,5,5,5-нонафторпентильную группу.
Примеры “-(G1)q-R8 группы”, где q равно 0, включают метильную группу, этильную группу, 1-метилэтильную группу, 1-этилэтильную группу, 1,1-диметилэтильную группу, пропильную группу, 1-метилпропильную группу, бутильную группу, фторметильную группу, хлорметильную группу, бромметильную группу, йодметильную группу, дифторметильную группу, хлордифторметильную группу, бромдифторметильную группу, трифторметильную группу, дихлорметильную группу, трихлорметильную группу, 1-хлорэтильную группу, 1-бромэтильную группу, 1-фторэтильную группу, 2-хлорэтильную группу, 2-бромэтильную группу, 2-фторэтильную группу, 2,2-дифторэтильную группу, 2,2,2-трифторэтильную группу, 2,2,2-трихлорэтильную группу, пентафторэтильную группу, 2,2,2-трифтор-1-хлорэтильную группу, 3-фторпропильную группу, 3-хлорпропильную группу, 1-фтор-1-метилэтильную группу, 1-хлор-1-метилэтильную группу, 2-хлор-1,1-диметилэтильную группу, 2-фтор-1,1-диметилэтильную группу, гептафторпропильную группу, 1,1,2,2,3,3-гексафторпропильную группу, 4-хлорбутильную группу, 4-фторбутильную группу, винильную группу, 1-метилвинильную группу, 1-пропенильную группу, 1-метил-1-пропенильную группу, 2-метил-1-пропенильную группу, 2-пропенильную группу, 1-метил-2-пропенильную группу, 2-метил-2-пропенильную группу, 2,2-дифторвинильную группу, 2-хлор-2-пропенильную группу, 3,3-дихлор-2-пропенильную группу, 2-бром-2-пропенильную группу, 3,3-дибром-2-пропенильную группу, 2-фтор-2-пропенильную группу, 3,3-дифтор-2-пропенильную группу, этинильную группу, 1-пропинильную и 3,3,3-трифтор-1-пропинильную группу.
Примеры “-(G1)q-R8 группы”, где q равно 1 и G1 является атомом кислорода, включают метоксигруппу, этоксигруппу, пропоксигруппу, трифторметоксигруппу, бромдифторметоксигруппу, дифторметоксигруппу, хлордифторметоксигруппу, пентафторэтоксигруппу, 2,2,2-трифторэтоксигруппу и 1,1,2,2-тетрафторэтоксигруппу.
Примеры “-(G1)q-R8 группы”, где q равно 1 и G1 является атомом серы, включают метилтиогруппу, этилтиогруппу, трифторметилтиогруппу, хлордифторметилтиогруппу, бромдифторметилтиогруппу, дибромфторметилтиогруппу, 2,2,2-трифторэтилтиогруппу, 1,1,2,2-тетрафторэтилтиогруппу и пентафторэтилтиогруппу.
Примеры “-(G1)q-R8 группы”, в которой q равно 1 и G1 является -SO-группой, включают метилсульфинильную группу, этилсульфинильную группу и трифторметилсульфинильную группу.
Примеры “-(G1)q-R8 группы”, где q равно 1 и G1 является -SO2-группой, включают метилсульфонильную группу, этилсульфонильную группу и трифторметилсульфонильную группу.
Примеры “C1-C4 алкиламиногруппы, которая может быть необязательно замещена атомом галогена” включают N-метиламино группу, N-этиламино группу, N-пропиламино группу, N-(1-метилэтил)амино группу, и N-(2,2,2-трифторэтил)амино группу.
Примеры “ди(C1-C4 алкильной)аминогруппы, которая может быть необязательно замещена атомом галогена” включают N,N-диметиламиногруппу, N-этил-N-метиламиногруппу, N,N-диэтиламиногруппу, N-метил-N-пропиламиногруппу, N-этил-N-пропиламиногруппу, N,N-дипропиламиногруппу, N-метил-N-(1-метилэтил)аминогруппу, N-этил-N-(1-метилэтил)аминогруппу, N,N-ди(1-метилэтил)аминогруппу, N-метил-N-(2,2,2-трифторэтил)аминогруппу и N-этил-N-(2,2,2-трифторэтил)аминогруппу.
Примеры “C2-C5 циклической аминогруппы” включают 1-азиридиногруппу, 1-азетидинильную группу, 1-пирролидинильную группу, 1-пиперидинильную группу и 1-морфолинильную группу.
Конкретные примеры соединения в соответствии с данным изобретением включают:
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом кислорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом кислорода и R7 является C1-C4 алкиламиногруппой, которая необязательно замещена атомом галогена, или ди(C1-C4 алкил)аминогруппу, которая необязательно замещена атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом кислорода и R7 является аминогруппой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом серы;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом серы и R7 является C1-C4 алкиламиногруппой, которая может быть необязательно замещена атомом галогена, или ди(C1-C4 алкил)аминогруппой, которая может быть необязательно замещена атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом серы и R7 является аминогруппой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R2 является C1-C4 алкильной группой, которая может быть необязательно замещена атомом галогена, C2-C4 алкенильной группой, которая может быть необязательно замещена атомом галогена, C2-C4 алкинильной группой, которая может быть необязательно замещена атомом галогена, атомом галогена или атомом водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R2 является атомом водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R2 является атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R2 является атомом фтора или хлора;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R2 является C1-C4 углеводородной цепью, которая может быть необязательно замещена атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R2 является C1-C4 алкильной группой, которая может быть необязательно замещена атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R2 является метильной группой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R2 является C2-C4 алкенильной группой, которая может быть необязательно замещена атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R2 является C2-C4 алкинильной группой, которая может быть необязательно замещена атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R3 и R4 независимо являются C1-C4 алкильной группой или атомом водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R3 и R4 являются атомами водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R3 и R4 являются C1-C4 углеводородной цепью;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R3 и R4 являются C1-C4 алкильной группой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R3 является C1-C4 алкильной группой и R4 является атомом водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R3 является метильной группой и R4 является атомом водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R5 является атомом фтора;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R5 является C1-C5 галогеналкильной группой, содержащей, по меньшей мере, один атом фтора;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R5 является фторметильной группой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R5 является трифторметильной группой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R5 является 1,1,2,2,2-пентафторэтильной группой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R5 является 1,1,2,2,3,3,3-гептафторпропильной группой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где R6 является атомом галогена, цианогруппой, нитрогруппой, C1-C4 алкильной группой, которая может быть необязательно замещена атомом галогена, C2-C4 алкенильной группой, которая может быть необязательно замещена атомом галогена, C2-C4 алкинильной группой, которая может быть необязательно замещена атомом галогена, C1-C4 алкоксигруппой, которая может быть необязательно замещена атомом галогена, C1-C4 алкилтиогруппой, которая может быть необязательно замещена атомом галогена, C1-C4 алкилсульфинильной группой, которая может быть необязательно замещена атомом галогена или C1-C4 алкилсульфонильной группой, которая может быть необязательно замещена атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 0;
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 1;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 1;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 1 и R6 является атомом хлора в качестве заместителя в положении 4;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 1 и R6 является атомом галогена в качестве заместителя в положении 4;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 1 и R6 является трифторметильной группой в качестве заместителя в положении 4;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 1 и R6 является этинильной группой в качестве заместителя в положении 4;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 1 и R6 является нитрогруппой в качестве заместителя в положении 4;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 1 и R6 является цианогруппой в качестве заместителя в положении 4;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 2;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 2 и один из R6 является атомом галогена в качестве заместителя в положении 4;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 3;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 3 и один из R6 является атомом галогена в качестве заместителя в положении 4;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 3 и все R6 являются атомами галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 4;
фторсодержащее сераорганическое соединение, представленное формулой (I), где m равно 5;
фторсодержащее сераорганическое соединение, представленное формулой (I), где n равно 0;
фторсодержащее сераорганическое соединение, представленное формулой (I), где n равно 1;
фторсодержащее сераорганическое соединение, представленное формулой (I), где n равно 2;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом кислорода, R7 является аминогруппой и R2 является атомом водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом кислорода, R7 является аминогруппой и R2 является метильной группой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом кислорода, R7 является аминогруппой и R2 является атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом кислорода, R7 является аминогруппой и R2 является атомом фтора или хлора;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом серы, R7 является аминогруппой и R2 является атомом водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом серы, R7 является аминогруппой и R2 является метильной группой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом серы, R7 является аминогруппой и R2 является атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где G является атомом серы, R7 является аминогруппой и R2 является атомом фтора или хлора;
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 0, G является атомом кислорода, R7 является аминогруппой и R2 является атомом водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 0, G является атомом кислорода, R7 является аминогруппой и R2 является метильной группой;
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 0, G является атомом кислорода, R7 является аминогруппой и R2 является атомом галогена;
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 0, G является атомом кислорода, R7 является аминогруппой и R2 является атомом фтора или хлора;
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 0, G является атомом серы, R7 является аминогруппой и R2 является атомом водорода;
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 0, G является атомом серы, R7 является аминогруппой, и R2 представляет собой метильную группу;
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 0, G является атомом серы, R7 является аминогруппой и R2 является атомом галогена; и
фторсодержащее сераорганическое соединение, представленное формулой (I), где p равно 0, G является атомом серы, R7 является аминогруппой и R2 является атомом фтора или хлора.
Далее в данном изобретении представлено промежуточное соединение для получения соединения в соответствии с данным изобретением (далее обозначенное как промежуточное соединение в соответствии с данным изобретением), которое применяют в способе получения соединения в соответствии с данным изобретением, описанным ниже, способом, описанным ниже, и которое представлено формулой (II):
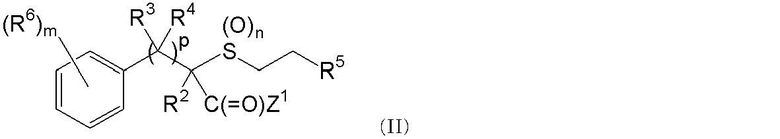
где Z1 представляет атомом галогена, гидроксильную группу или C1-C5 алкоксигруппу;
R2 является C1-C4 углеводородной цепью, которая может быть необязательно замещена атомом галогена, атомом галогена или атомом водорода;
R3 и R4 независимо являются C1-C4 углеводородной цепью или атомом водорода;
R5 является C1-C5 галогеналкильной группой, содержащей, по меньшей мере, один атом фтора, или атомом фтора;
R6 является атомом галогена, цианогруппой, нитрогруппой или -(G1)q-R8 группой;
R8 является C1-C4 углеводородной цепью, которая может быть необязательно замещена атомом галогена;
m равно целому числу от 0 до 5, при условии, что R6 необязательно могут быть одинаковыми или отличными друг от друга, если m равно от 2 до 5;
n равно целому числу от 0 до 2;
p равно 0 или 1;
q равно 0 или 1; и
G1 является атомом кислорода, атомом серы, -SO-группой или -SO2-группой.
Конкретные примеры промежуточного соединения в соответствии с данным изобретением включают:
соединение, представленное формулой (II), где Z1 является атомом галогена;
соединение, представленное формулой (II), где Z1 является гидроксильной группой;
соединение, представленное формулой (II), где Z1 является C1-C5 алкоксигруппой;
соединение, представленное формулой (II), где Z1 является метоксигруппой;
соединение, представленное формулой (II), где R2 является атомом водорода;
соединение, представленное формулой (II), где R2 является атомом галогена;
соединение, представленное формулой (II), где R2 является атомом фтора или хлора;
соединение, представленное формулой (II), где R2 является C1-C4 углеводородной цепью, которая может быть необязательно замещена атомом галогена;
соединение, представленное формулой (II), где R2 является C1-C4 алкильную группой, которая может быть необязательно замещена атомом галогена;
соединение, представленное формулой (II), где R2 является метильной группой;
соединение, представленное формулой (II), где R2 является C2-C4 алкенильной группой, которая может быть необязательно замещена атомом галогена;
соединение, представленное формулой (II), где R2 является C2-C4 алкинильной группой, которая может быть необязательно замещена атомом галогена;
соединение, представленное формулой (II), где R3 и R4 являются атомами водорода;
соединение, представленное формулой (II), где R3 и R4 являются C1-C4 углеводородной цепью;
соединение, представленное формулой (II), где R3 и R4 являются C1-C4 алкильными группами;
соединение, представленное формулой (II), где R3 является алкильной группой и R4 является атомом водорода;
соединение, представленное формулой (II), где R3 является метильной группой и R4 является атомом водорода;
соединение, представленное формулой (II), где R5 является атомом фтора;
соединение, представленное формулой (II), где R5 является C1-C5 галогеналкоксигруппой, содержащей, по меньшей мере, один атом фтора;
соединение, представленное формулой (II), где R5 является фторметильной группой;
соединение, представленное формулой (II), где R5 является трифторметильной группой;
соединение, представленное формулой (II), где R5 является 1,1,2,2,2-пентафторэтильной группой;
соединение, представленное формулой (II), где R5 является 1,1,2,2,3,3,3-гептафторпропильной группой;
соединение, представленное формулой (II), где p равно 0;
соединение, представленное формулой (II), где p равно 1;
соединение, представленное формулой (II), где m равно 1;
соединение, представленное формулой (II), где m равно 1 и R6 является атомом хлора в качестве заместителя в положении 4;
соединение, представленное формулой (II), где m равно 1 и R6 является атомом галогена в качестве заместителя в положении 4;
соединение, представленное формулой (II), где m равно 1 и R6 является трифторметильной группой в качестве заместителя в положении 4;
соединение, представленное формулой (II), где m равно 1 и R6 является этинильной группой в качестве заместителя в положении 4;
соединение, представленное формулой (II), где m равно 1 и R6 является нитрогруппой в качестве заместителя в положении 4;
соединение, представленное формулой (II), где m равно 1 и R6 является цианогруппой в качестве заместителя в положении 4;
соединение, представленное формулой (II), где m равно 2;
соединение, представленное формулой (II), где m равно 2 и один из R6 является атомом галогена в качестве заместителя в положении 4;
соединение, представленное формулой (II), где m равно 3;
соединение, представленное формулой (II), где m равно 3 и один из R6 является атомом галогена в качестве заместителя в положении 4;
соединение, представленное формулой (II), где m равно 3 и все R6 являются атомами галогена;
соединение, представленное формулой (II), где m равно 4;
соединение, представленное формулой (II), где m равно 5;
соединение, представленное формулой (II), где n равно 0;
соединение, представленное формулой (II), где n равно 1; и
соединение, представленное формулой (II), где n равно 2.
Затем представлены способы получения соединения в соответствии с данным изобретением.
Способ получения 1
Соединение, представленное формулой (I-2) (далее обозначенное как соединение (I-2)), которое является соединением в соответствии с данным изобретением, где R2 является C1-C4 углеводородной цепью, которая может быть необязательно замещена атом галогена, может быть получено взаимодействием соединения, представленного формулой (I-1) (далее обозначенного как соединение (I-1)) с соединением, представленным формулой (a) (далее обозначенным как соединение (a)), как показано ниже:
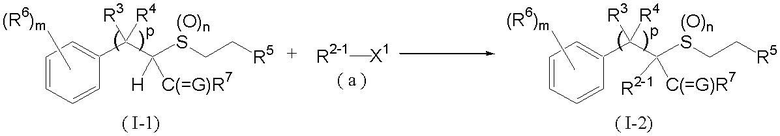
где R3, R4, R5, R6, R7, G, p, m и n такие, как определены выше, R2-1 является C1-C4 алкильной группой, C2-C4 алкенильной группой, которая может быть необязательно замещена атомом галогена, или C2-C4 алкинильной группой, которая может быть необязательно замещена атомом галогена, и X1 является уходящей группой, такой как атом хлора, атом брома, атом йода, метансульфонильная группа, п-толуолсульфонильная группа или трифторметансульфонильная группа.
Реакцию обычно проводят в присутствии основания в растворителе.
Примеры растворителей, применяемых в реакции в соответствии с данным изобретением, включают простые эфиры, такие как диэтиловый эфир, тетрагидрофуран или диметоксиэтан, амиды кислот, такие как N,N-диметилформамид, органические соединения серы, такие как диметилсульфоксид или сульфолан, алифатические углеводороды, такие как гексан или гептан, ароматические углеводороды, такие как толуол или ксилол, галогенированные углеводороды, такие как 1,2-дихлорэтан или хлорбензол, вода и их смеси.
Примеры основания, применяемого в данной реакции, включают неорганические основания, такие как гидрид натрия, гидроксид натрия, гидроксид калия или карбонат калия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, и органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (I-1).
Количество соединения (a), применяемого в данной реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (I-1).
Температура реакции обычно составляет от -50 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (I-2) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси с органическим растворителем с последующей концентрацией. Выделенное соединение (I-2) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 2
Соединение, представленное формулой (I-3) (далее обозначенное как соединение (I-3)), которое является соединения в соответствии с данным изобретением, где R2 является атомом галогена, может быть получено взаимодействием соединения (I-1) с галогенирующим агентом (b) в присутствии основания, как показано ниже:
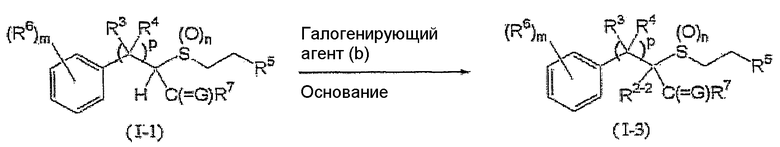
где R3, R4, R5, R6, R7, G, p, m и n такие, как определены выше, и R2-2 является атомом галогена.
Реакцию обычно проводят в присутствии основания в растворителе.
Примеры растворителя, применяемого в реакции, включают простые эфиры, такие как диэтиловый эфир, тетрагидрофуран или диметоксиэтан, амиды кислоты, такие как N,N-диметилформамид, органические соединения серы, такие как диметилсульфоксид и сульфолан, алифатические углеводороды, такие как гексан или гептан, ароматические углеводороды, такие как толуол или ксилол, галогенированные углеводороды, такие как 1,2-дихлорэтан или хлорбензол, воду и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидроксид натрия, гидроксид калия или карбонат калия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, и органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (I-1).
Примеры галогенирующего агента (b), применяемого в реакции, включают галогенированные углеводороды, такие как четыреххлористый углерод или гексахлорэтан, галогены, такие как фтор, хлор, бром или йод, N-галогенированный сукцинимид, такой как N-хлорсукцинимид, N-бромсукцинимид или N-йодсукцинимид, соли N-фторпиридиния, такие как трифторметансульфонат 1-фтор-2,4,6-триметилпиридиния или бистетрафторборат 1,1'-дифтор-2,2'-бипиридиния, и неорганические соли, такие как хлорид меди (II) или бромид меди (II).
Количество галогенирующего агента (b), применяемого в реакции, составляет обычно от 1 до 10 молей на 1 моль соединения (I-1).
Температура реакции обычно составляет от -100 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (I-3) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-3) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 3
Соединение (I-3) может быть получено взаимодействием соединения (I-1) с галогенирующим агентом (c), как показано ниже:
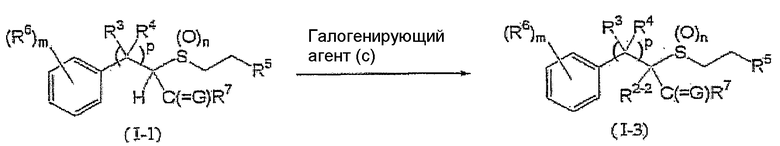
где R3, R4, R5, R6, R7, R2-2, G, p, m и n такие, как определены выше.
Реакцию обычно проводят без растворителя или в растворителе.
Примеры растворителя, применяемого в реакции, включают галогенированные углеводороды, такие как хлороформ, четыреххлористый углерод, 1,2-дихлорэтан, дихлорметан и дихлорбензол, ароматические углеводороды, такие как толуол или ксилол, алифатические нитрилы, такие как ацетонитрил или пропионитрил, алифатические карбоновые кислоты, такие как уксусная кислота, сероуглерод, воды и их смеси.
Примеры галогенирующего агента (c), применяемого в реакции, включают галогены, такие как фтор, хлор, бром или йод, гидрогалогенид, такой как гидрофторид, гидрохлорид, гидробромид или гидройодид, соединения серагалогенидов, такие как тионилхлорид, тионилбромид или сульфурилхлорид, и соединения фосфоргалогенидов, такие как треххлористый фосфор, трехбромистый фосфор, пятихлористый фосфор или хлорокись фосфора.
Количество галогенирующего агента (c), применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (I-1).
Температура реакции обычно составляет от -100 до 200°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (I-3) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-3) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 4
Соединение, представленное формулой (I-4) (далее обозначенное как соединение (I-4)), которое является соединением в соответствии с данным изобретением, где G является атомом кислорода, может быть получено взаимодействием соединения, представленного формулой (f) (далее обозначенного как соединение (f)), с соединением, представленным формулой (g) (далее обозначенным как соединение (f)), как показано ниже:
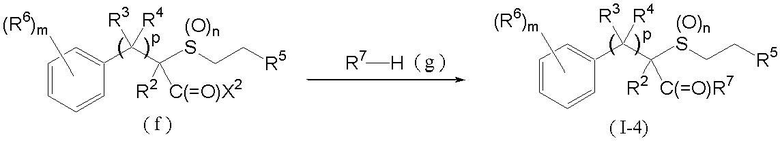
где R2, R3, R4, R5, R6, R7, p, m и n такие, как определены выше, и X2 является атомом галогена.
Реакцию обычно проводят в растворителе в присутствии основания.
Примеры растворителя, применяемого в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир или тетрагидрофуран, органические соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, вода, и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидроксид натрия, гидроксид калия или карбонат калия, или органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (f).
Количество соединения (g), применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (f).
Температура реакции обычно составляет от -20 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (I-4) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-4) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 5
Соединение (I-4) может быть получено взаимодействием соединения, представленного формулой (d) (далее обозначенного как соединение (d)) с соединением (g), как показано ниже:
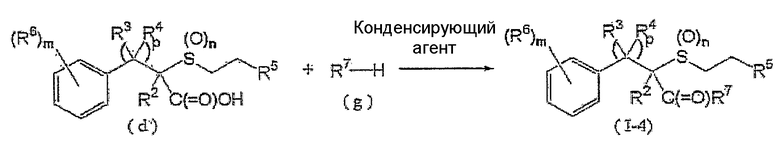
где R2, R3, R4, R5, R6, R7, p, m и n такие, как определены выше.
Реакцию обычно проводят в присутствии конденсирующего агента в растворителе.
Примеры растворителя, применяемого в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир или тетрагидрофуран, органические соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, и ароматические углеводороды, такие как толуол или ксилол.
Примеры конденсирующего агента, применяемого в реакции, включают дициклогексилкарбодиимид, N-(3-диметиламинопропил)-N'-этилкарбодиимид и карбонилдиимидазол.
Количество конденсирующего агента, применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (d).
Количество соединения (g), применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (d).
Температура реакции обычно составляет от -20 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (I-4) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-4) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 6
Соединение, представленное формулой (I-1-1) (далее обозначенное как соединение (I-1-1)), которое является соединением в соответствии с данным изобретением, где R2 является атомом водорода и p равно 1, может быть получено взаимодействием соединения, представленного формулой (h) (далее обозначенного как соединение (h)), с соединением, представленным формулой (i) (далее обозначенным как соединение (i)), как показано ниже:
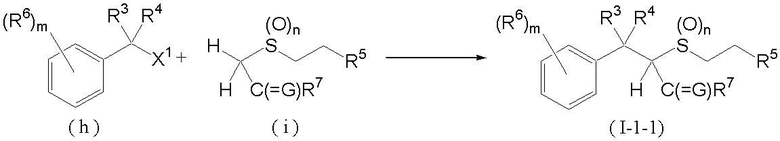
где R3, R4, R5, R6, R7, G, X1, m и n такие, как определены выше.
Реакцию обычно проводят в присутствии основания в растворителе.
Примеры растворителя, применяемого в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир или тетрагидрофуран, органические соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, вода, и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидроксид натрия, гидроксид калия или карбонат калия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, амиды щелочных металлов, такие как диизопропиламид лития, или органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (i).
Количество соединения (h), применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (i).
Температура реакции обычно составляет от -100 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (I-1-1) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-1-1) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 7
Соединение (I-4) может быть получено, например, взаимодействием соединения, представленного формулой (q) (далее обозначенного как соединение (q)) с соединением (g), как показано ниже:
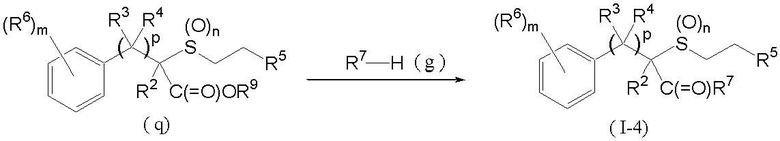
где R2, R3, R4, R5, R6, R7, p, m и n такие, как определены выше, и R9 является C1-C5 алкильной группой.
Реакцию обычно проводят в растворителе.
Примеры растворителя, применяемые в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир или тетрагидрофуран, органические соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, и спирты, такие как метанол или этанол.
Количество соединения (g), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (q).
Температура реакции обычно составляет от -20 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (I-4) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-4) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 8
Соединение, представленное формулой (I-6) (далее обозначенное как соединение (I-6)), которое является соединением в соответствии с данным изобретением, где G является атомом серы, может быть получено взаимодействием соединения (I-4) с сульфирующим агентом (k), как показано ниже:
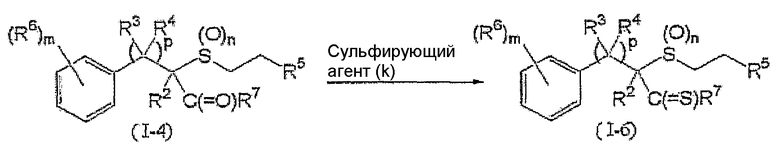
где R2, R3, R4, R5, R6, R7, p, m и n такие, как определены выше.
Реакцию обычно проводят в растворителе.
Примеры растворителя, применяемые в реакции, включают галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, и ароматические углеводороды, такие как толуол или ксилол.
Примеры сульфирующего агента (k), применяемого в реакции, включают неорганическое соединения серы, такие как сероводород или дифосфорпентасульфид, и органические соединения серы, такие как 2,4-бис(4-метоксифенил)-1,3-дитиа-2,4-дифосфетан 2,4-дисульфид.
Количество сульфирующего агента (k), применяемого в реакции, обычно составляет от 0,5 до 10 молей на 1 моль соединения (I-4).
Температура реакции обычно составляет от 0 до 250°C, и время реакции обычно составляет от 1 до 72 часов.
После завершения реакции соединение (I-6) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-6) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 9
Соединение, представленное формулой (I-7) (далее обозначенное как соединение (I-7)), которое является соединением в соответствии с данным изобретением, где n равно 0, может быть получено взаимодействием соединения, представленного формулой (l) (далее обозначенного как соединение (l)) с соединением, представленным формулой (m) (далее обозначенным как соединение (m)), как показано ниже:

где R2, R3, R4, R5, R6, R7, G, X1, p и m такие, как определены выше.
Реакцию обычно проводят в присутствии основания в растворителе.
Примеры растворителя, применяемые в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир или тетрагидрофуран, органическое соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, спирты, такие как метанол или этанол, воду, и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидрид калия, гидроксид натрия, гидроксид калия или карбонат калия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, амиды щелочных металлов, такие как диизопропиламид лития, и органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (l).
Количество соединения (m), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (l).
Температура реакции обычно составляет от -20 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (I-7) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-7) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 10
Соединение (I-7) может быть получено взаимодействием соединения, представленного формулой (n) (далее обозначенного как соединение (n)) с соединением, представленным формулой (o) (далее обозначенным как соединение (o)), как показано ниже:
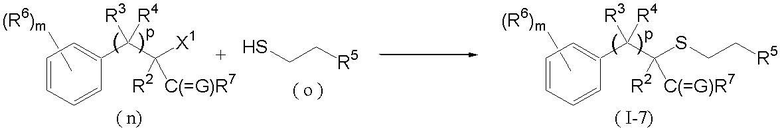
где R2, R3, R4, R5, R6, R7, G, X1, p и m такие, как определены выше.
Реакцию обычно проводят в присутствии основания в растворителе.
Примеры растворителя, применяемые в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир или тетрагидрофуран, органические соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, спирты, такие как метанол или этанол, воду, и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидрид калия, гидроксид натрия, гидроксид калия или карбонат калия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, амиды щелочных металлов, такие как диизопропиламид лития, или органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (n).
Количество соединения (o), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (n).
Температура реакции обычно составляет от -20 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (I-7) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-7) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ получения 11
Соединение, представленное формулой (I-8) (далее обозначенное как соединение (I-8)), которое является соединением в соответствии с данным изобретением, где n равно 1 или 2, может быть получено взаимодействием соединения (I-7) с окисляющим агентом (x), как показано ниже:
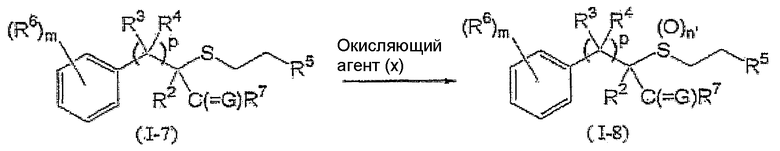
где R2, R3, R4, R5, R6, R7, G, p и m такие, как определены выше, и n' равно 1 или 2.
Реакцию обычно проводят в растворителе.
Примеры растворителя, применяемые в реакции, включают галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, алифатические карбоновые кислоты, такие как уксусная кислота или трифторуксусная кислота, спирты, такие как метанол или этанол, вода, и их смеси.
Примеры окисляющего агента (x), применяемого в реакции, включают органические перекиси, такие как пероксиуксусная кислота, трифторпероксиуксусная кислота или м-хлорпербензойная кислота, галогены, такие как хлор или бром, галогенсодержащие имиды, такие как N-хлорсукцинимид, галогениды, такие как перхлорная кислота (или ее соль) или йодная кислота (или ее соль), перманганаты, такие как перманганаты калия, хроматы, такие как хромат калия, и перекись водорода.
Количество окисляющего агента (x), применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (I-7).
Температура реакции обычно составляет от -50 до 200°C, и время реакции обычно составляет от 1 до 72 часов.
После завершения реакции соединение (I-8) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (I-8) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Далее описаны ссылочные способы получения промежуточного соединения в соответствии с данным изобретением.
Ссылочный способ 1
Соединение (d) может быть получено гидролизом соединения (q), как показано ниже:
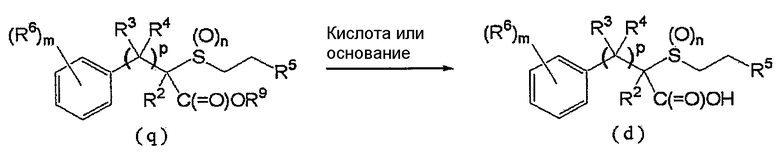
где R2, R3, R4, R5, R6, R9, р, m и n такие, как определены выше.
Реакцию обычно проводят в органическом растворителе в присутствии кислоты или основания, и воды.
Примеры растворителей, применяемых в реакции, включают амиды кислоты, простые эфиры, такие как диэтиловый эфир или тетрагидрофуран, органические соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, алифатические углеводороды, такие как уксусная кислота или муравьиная кислота, спирты, такие как метанол или этанол, и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидроксид натрия или гидроксид калия.
Примеры кислоты, применяемой в реакции, включают неорганические кислоты, такие как хлористоводородная кислота или серная кислота.
Количество кислоты или основания, применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (q).
Температура реакции обычно составляет от -20 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (d) может быть выделено, например, экстрагированием реакционной смеси органическим растворителем после, при необходимости, добавления воды и/или кислоты к реакционной смеси, с последующей концентрацией. Выделенное соединение (d) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Ссылочный способ 2
Соединение, представленное формулой (q-2) (далее обозначенное как соединение (q-2)), которое является соединением (q), где R2 является C1-C4 углеводородной цепью, которая может быть необязательно замещена атомом галогена, может быть получено взаимодействием соединения, представленного формулой (q-1) (далее обозначенного как соединение (q-1)), которое является соединением (q), где R2 является атомом водорода, с соединением (a) как показано ниже:
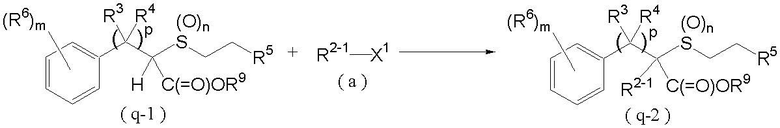
где R2-1, R3, R4, R5, R6, R9, X1, p, m и n такие, как определены выше.
Реакцию обычно проводят в присутствии основания в растворителе.
Примеры растворителя, применяемого в реакции, включают простые эфиры, такие как диэтиловый эфир, тетрагидрофуран или диметоксиэтан, амиды кислоты, такие как N,N-диметилформамид, органические соединения серы, такие как диметилсульфоксид или сульфолан, алифатические углеводороды, такие как гексан или гептан, ароматические углеводороды, такие как толуол или ксилол, галогенированные углеводороды, такие как 1,2-дихлорэтан или хлорбензол, вода, и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидроксид натрия, гидроксид калия или карбонат калия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, или органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (q-1).
Количество соединения (a), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (q-1).
Температура реакции обычно составляет от -50 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (q-2) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (q-2) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Ссылочный способ 3
Соединение, представленное формулой (q-3) (далее обозначенное как соединение (q-3)), которое является соединением (q), где R2 является атомом галогена, может быть получено взаимодействием соединения (q-1) с галогенирующим агентом (b) в присутствии основания, такого как показано ниже:
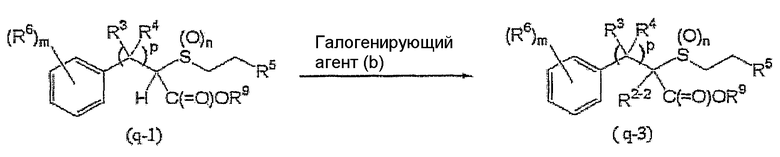
где R2-2, R3, R4, R5, R6, R9, p, m и n такие, как определены выше.
Реакцию обычно проводят в органическом растворителе в присутствии основания.
Примеры растворителя, применяемого в реакции, включают простые эфиры, такие как диэтиловый эфир, тетрагидрофуран или диметоксиэтан, амиды кислоты, такие как N,N-диметилформамид, органические соединения серы, такие как диметилсульфоксид или сульфолан, алифатические углеводороды, такие как гексан или гептан, ароматические углеводороды, такие как толуол или ксилол, галогенированные углеводороды, такие как 1,2-дихлорэтан или хлорбензол, вода, и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидроксид натрия, гидроксид калия или карбонат калия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, или органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (q-1).
Примеры галогенирующего агента (b), применяемого в реакции, включают галогенированные углеводороды, такие как четыреххлористый углерод или гексахлорэтан, галогены, такие как фтор, хлор, бром или йод, N-галогенированный сукцинимид, такой как N-хлорсукцинимид, N-бромсукцинимид или N-йодсукцинимид, соли N-фторпиридиния, такие как трифторметансульфонат 1-фтор-2,4,6-триметилпиридиния или бистетрафторборат 1,1'-дифтор-2,2'-бипиридиния, и неорганические соли, такие как хлорид меди (II) или бромид меди (II).
Количество галогенирующего агента (b), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (q-1).
Температура реакции обычно составляет от -100 до 100°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (q-3) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (q-3) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Ссылочный способ 4
Соединение (q-3) может быть получено взаимодействием соединения (q-1) с галогенирующим агентом (c), как показано ниже:
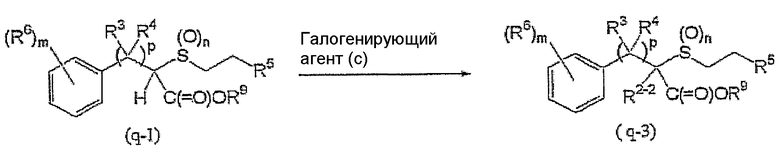
где R2-2, R3, R4, R5, R6, R9, p, m и n такие, как определены выше.
Реакцию обычно проводят с или без растворителя.
Примеры растворителя, применяемого в реакции, включают галогенированные углеводороды, такие как хлороформ, четыреххлористый углерод, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, алифатические нитрилы, такие как ацетонитрил или пропионитрил, алифатические карбоновые кислоты, такие как уксусная кислота, сероводород, воду, и их смеси.
Примеры галогенирующего агента (c), применяемого в реакции, включают галогены, такие как фтор, хлор, бром или йод, гидрогалогениды, такие как гидрохлорид, гидрофторид, гидробромид или гидройодид, соединения серагалогенидов, такие как тионилхлорид, тионилбромид или сульфурилхлорид, и соединения фосфоргалогенидов, такие как треххлористый фосфор, трехбромистый фосфор, пятихлористый фосфор или хлорокись фосфора.
Количество галогенирующего агента (c), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (q-1).
Температура реакции обычно составляет от -100 до 200°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (q-3) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (q-3) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Ссылочный способ 5
Соединение, представленное формулой (q-4) (далее обозначенное как соединение (q-4)), которое является соединением (q), где R2 является C1-C4 углеводородной цепью или атомом водорода и p равно 0, может быть получено взаимодействием соединения, представленного формулой (r) (далее обозначенного как соединение (r)) с соединением, представленным формулой (s) (далее обозначенным как соединение (s)), как показано ниже:
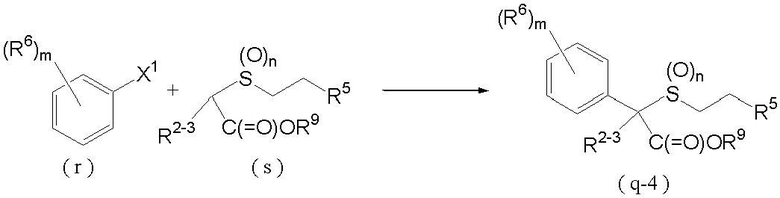
где R5, R6, R9, X1, m, n и X такие, как определены выше, и R2-3 является C1-C4 углеводородной цепью или атомом водорода.
Реакцию обычно проводят в органическом растворителе в присутствии основания.
Примеры растворителя, применяемого в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир, 1,4-диоксан или тетрагидрофуран, и органические соединения серы, такие как диметилсульфоксид или сульфолан.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидрид калия, гидроксид натрия, гидроксид калия, карбонат калия или карбонат цезия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, и амиды щелочных металлов, такие как диизопропиламид лития.
Количество основания, применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (s).
Количество соединения (r), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (s).
Температура реакции обычно составляет от -20 до 200°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (q-4) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (q-4) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Ссылочный способ 6
Соединение (q-4) может быть получено взаимодействием соединения (r) с соединением (s) в присутствии металлического катализатора (y) как показано ниже:

где R2-3, R5, R6, R9, X1, m и n такие, как определены выше.
Реакцию обычно проводят в органическом растворителе в присутствии основания и катализатора.
Примеры растворителя, применяемого в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир, 1,4-диоксан или тетрагидрофуран, или органические соединения серы, такие как диметилсульфоксид или сульфолан.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидрид калия, гидроксид натрия, гидроксид калия, карбонат калия или карбонат цезия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, и амиды щелочного металла, такие как диизопропиламид лития.
Количество основания, применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (s).
Количество соединения (r), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (s).
Примеры металлического катализатора (y), применяемого в реакции, включают комплексы палладия, такие как тетракис(трифенилфосфин)палладий (0) или трис(дибензилиденацетон)дипалладий (0), комплекс хлороформа и галогениды меди (I), такие как бромид (I) или йодид меди (I).
Количество металлического катализатора (y), применяемое в соответствии с данным изобретением, обычно составляет от 0,001 до 0,5 моля на 1 моль соединения (s).
Температура реакции обычно составляет от -20 до 200°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (q-4) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (q-4) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Ссылочный способ 7
Соединение, представленное формулой (q-5) (далее обозначенное как соединение (q-5)), которое является соединением (q), где R2 является C1-C4 углеводородной цепью или атомом водорода и p равно 1, может быть получено взаимодействием соединения (s) с соединением (h) как показано ниже:
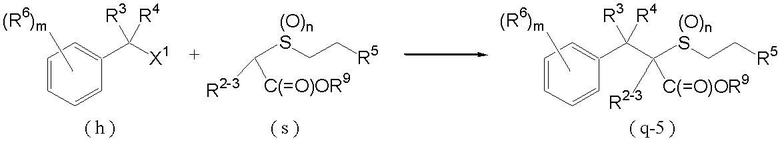
где R2-3, R3, R4, R5, R6, R9, X1, m и n такие, как определены выше.
Реакцию обычно проводят в органическом растворителе в присутствии основания.
Примеры растворителя, применяемого в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир, 1,4-диоксан или тетрагидрофуран, органические соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, спирты, такие как метанол или этанол, воду и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидрид калия, гидроксид натрия, гидроксид калия, карбонат калия или карбонат цезия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, амиды щелочных металлов, такие как диизопропиламид лития или органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (s).
Количество соединения (h), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (s).
Температура реакции обычно составляет от -100 до 150°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (q-5) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (q-5) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Ссылочный способ 8
Соединение, представленное формулой (q-6) (далее обозначенное как соединение (q-6)), которое является соединением (q), где n равно 0, и соединение, представленное формулой (q-7) (далее обозначенное как соединение (q-7)), которое является соединением (q), где n равно 1 или 2, может быть получено следующим способом:
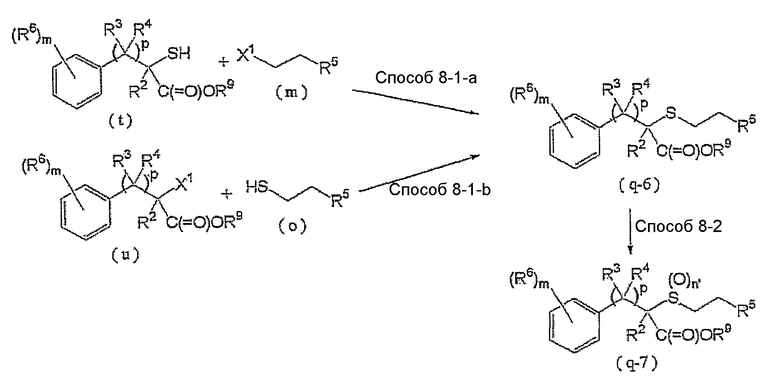
где R2, R3, R4, R5, R6, R9, G, X1, p, m и n такие, как определены выше.
Способ 8-1-a:
Соединение (q-6) может быть получено взаимодействием соединения, представленного формулой (t) (далее обозначенного как соединение (t)) с соединением (m).
Реакцию обычно проводят в растворителе в присутствии основания.
Примеры растворителя, применяемого в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир, 1,4-диоксан или тетрагидрофуран, органические соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, спирты, такие как метанол или этанол, воду и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидрид калия, гидроксид натрия, гидроксид калия, карбонат калия или карбонат цезия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, и органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (t).
Количество соединения (m), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (t).
Температура реакции обычно составляет от -20 до 150°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (q-6) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (q-6) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ 8-1-b:
Соединение (q-6) также может быть получено взаимодействием соединения, представленного формулой (u) (далее обозначенного как соединение (u)) с соединением (o).
Реакцию обычно проводят в растворителе в присутствии основания.
Примеры растворителя, применяемого в реакции, включают амиды кислоты, такие как N,N-диметилформамид, простые эфиры, такие как диэтиловый эфир, 1,4-диоксан или тетрагидрофуран, органические соединения серы, такие как диметилсульфоксид или сульфолан, галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, ароматические углеводороды, такие как толуол или ксилол, спирты, такие как метанол или этанол, воду и их смеси.
Примеры основания, применяемого в реакции, включают неорганические основания, такие как гидрид натрия, гидрид калия, гидроксид натрия, гидроксид калия, карбонат калия или карбонат цезия, алкоксиды щелочных металлов, такие как метоксид натрия или трет-бутоксид калия, и органические основания, такие как триэтиламин, 1,4-диазабицикло[2.2.2]октан или 1,8-диазабицикло[5.4.0]-7-ундецен.
Количество основания, применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (u).
Количество соединения (o), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (u).
Температура реакции обычно составляет от -20 до 150°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (q-6) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (q-6) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Способ 8-2:
Соединение (q-7) может быть получено взаимодействием соединения (q-6) с окисляющим агентом (x).
Реакцию обычно проводят в растворителе.
Примеры растворителя, применяемого в реакции, включают галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, органические углеводороды, такие как толуол или ксилол, алифатические карбоновые кислоты, такие как уксусная кислота или трифторуксусная кислота, спирты, такие как метанол или этанол, воду и их смеси.
Примеры окисляющего агента (x), применяемого в реакции, включают органические перекиси, такие как пероксиуксусная кислота, трифторпероксиуксусная кислота или м-хлорпербензойная кислота, галогены, такие как хлор или бром, галогенсодержащие имиды, такие как N-хлорсукцинимид, галогениды, такие как перхлорная кислота (или ее соль) или йодная кислота (или ее соль), перманганаты, такие как перманганат калия, хроматы, такие как хромат калия, и перекись водорода.
Количество окисляющего агента (x), применяемое в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (q-6).
Температура реакции обычно составляет от -50 до 200°C, и время реакции обычно составляет от 1 до 72 часов.
После завершения реакции соединение (q-7) может быть выделено, например, выливанием реакционной смеси в воду и экстрагированием полученной смеси органическим растворителем с последующей концентрацией. Выделенное соединение (q-7) может быть далее очищено хроматографией, перекристаллизацией или подобными, при необходимости.
Ссылочный способ 9
Соединение (f) может быть получено взаимодействием соединения (d) с галогенирующим агентом (e), как показано ниже:

где R2, R3, R4, R5, R6, X2, p, m и n такие, как определены выше.
Реакцию проводят без растворителя или в растворителе.
Примеры растворителя, применяемого в реакции, включают галогенированные углеводороды, такие как хлороформ, дихлорметан, 1,2-дихлорэтан или хлорбензол, и ароматические углеводороды, такие как толуол или ксилол.
Примеры галогенирующего агента (e) включают оксалилхлорид, тионилхлорид, тионилбромид, треххлористый фосфор, трехбромистый фосфор и пентахлорид фосфора.
Количество галогенирующего агента (е), применяемого в реакции, обычно составляет от 1 до 10 молей на 1 моль соединения (d).
Температура реакции обычно составляет от -20 до 150°C, и время реакции обычно составляет от 1 до 24 часов.
После завершения реакции соединение (f) может быть выделено, например, концентрацией и подобными. Выделенное соединение (f) может быть далее очищено дистилляцией или подобными, при необходимости.
Примеры членистоногих вредителей, на которых соединение в соответствии с данным изобретением оказывает контролирующее действие, включают вредных насекомых и вредный клещей, и более конкретно, следующие виды членистоногих.








Хотя пестицидная композиция в соответствии с данным изобретением может быть соединением в соответствии с данным изобретением сама по себе, пестицидная композиция в соответствии с данным изобретением обычно содержит соединение в соответствии с данным изобретением в комбинации с твердым носителем, жидким носителем и/или газообразным носителем, и, при необходимости, поверхностно-активное вещество или другие фармацевтические добавки, и принимает форму эмульгируемого концентрата, масляного раствора, шампуня, текучей композиции, тонкоизмельченного порошка, смачиваемого порошка, гранул, пасты, микрокапсул, пены, аэрозоля, композиции с двуокисью углерода, таблетки, композиции с полимером или подобными. Пестицидная композиция в соответствии с данным изобретением может быть переработана с получением отравленной приманки, противомоскитной спирали, электрического противомоскитного мата, дымящего пестицида, фумигатора или пластин, и затем использоваться по назначению.
Пестицидная композиция в соответствии с данным изобретением обычно содержит от 0,1 до 95 мас.% соединения в соответствии с данным изобретением.
Примеры твердых носителей включают тонкоизмельченный порошок или гранулы глины (например, каолина, диатомовой земли, бентонита, глины Фубасами, кислой глины и т.д.), синтетическую гидрированную окись кремния, тальк, керамику, другие неорганические минералы (например, серицит, кварц, серу, активированный уголь, карбонат кальция, гидроокись кремния и т.д.), химические удобрения (например, сульфат аммония, фосфат аммония, нитрат аммония, хлорид аммония, мочевину и т.д.) и подобные.
Примеры жидкого носителя включают ароматические или алифатические углеводороды (например, ксилол, толуол, алкилнафталин, фенилксилилэтан, керосин, легкое масло, гексан, циклогексан и т.д.), галогенированные углеводороды (например, хлорбензол, дихлорметан, дихлорэтан, трихлорэтан и т.д.), спирты (например, метанол, этанол, изопропиловый спирт, бутанол, гексанол, этиленгликоль и т.д.), простые эфиры (например, диэтиловый эфир, диметиловый эфир этиленгликоля, монометиловый эфир диэтиленгликоля, моноэтиловый эфир диэтиленгликоля, монометиловый эфир пропиленгликоля, тетрагидрофуран, диоксан и т.д.), сложные эфиры (например, этилацетат, бутилацетат и т.д.), кетоны (например, ацетон, метилэтилкетон, метилизобутилкетон, циклогексанон и т.д.), нитрилы (например, ацетонитрил, изобутиронитрил и т.д.), сульфоксиды (например, диметилсульфоксид и т.д.), амиды кислоты (например, N,N-диметилформамид, N,N-диметилацетамид и т.д.), растительные масла (например, соевое масло, хлопковое масло и т.д.), растительные эфирные масла (например, масло апельсина, масло иссопа, масло лимона и т.д.), воду и подобные.
Примеры газообразного носителя включают бутан, хлорфторуглерод, СНГ (сжиженный нефтяной газ), диметиловый эфир, двуокись углерода и подобные.
Примеры поверхностно-активного вещества включают соли алкилсульфата, соли алкилсульфоната, соли алкиларилсульфоната, простые эфиры алкиларила и их полиоксиэтилированные производные, простые эфиры полиэтиленгликоля, сложные эфиры многоатомного спирта и производные сахарного спирта.
Примеры других фармацевтических добавок включают связующий агент, диспергатор, стабилизатор и подобные, и конкретные примеры их включают казеин, желатин, полисахариды (например, крахмал, аравийскую камедь, производные целлюлозы, альгиновую кислоту и т.д.), производные лигнина, бентонит, сахариды, синтетические водорастворимые полимеры (например, поливиниловый спирт, поливинилпирролидон, полиакриловую кислоту и т.д.), PAP (фосфат изопропиловой кислоты), BHT (2,6-ди-трет-бутил-4-метилфенол), BHA (смесь 2-трет-бутил-4-метоксифенола и 3-трет-бутил-4-метоксифенола), растительные масла, минеральные масла, жирные кислоты и сложные эфиры жирных кислот.
Примеры основного материала для полимерных композиций включают винилхлоридные полимеры, полиуретан и подобные. К основному материалу, при необходимости, добавляют пластификатор, такой как фталат (например, диметилфталат, диоктилфталат и т.д.), адипат, стеариновую кислоту или подобные. Полимерную композицию получают пластификацией соединения в соответствии с данным изобретением в основном материале с применением обычного аппарата для пластификации, с последующей формовкой, такой как литьевое прессование, профилирование, прессование или подобные. Полученная полимерная композиция может иметь форму пластины, пленки, ленты, сетки, нитки или подобную, которую получают дальнейшим формованием, разрезанием или подобными методами, при необходимости. Такие полимерные композиции могут применяться, например, в форме ошейников для животных, клипс для ушей животных, табличек, крышек или плодовых опор.
Примеры основного материала для отравленных приманок включают зерновой порошок, растительное масло, сахар, кристаллическую целлюлозу и подобные. К этому основному материалу может быть добавлен, при необходимости, антиоксидант, такой как дибутилгидрокситолуол или нордигидрогваяретовая кислота, консервант, такой как дегидроуксусная кислота, агент для предотвращения случайного поедания детьми или домашними животными, такой как порошок жгучего перца, добавка, привлекающая вредителей, такая как запах сыра, запах лука или арахисовое масло, или подобные.
Пестицидная композиция в соответствии с данным изобретением может наноситься, например, непосредственно на членистоногих вредителей и/или на место обитания членистоногих вредителей (например, растения, животных, почву и т.д.).
Пестицидная композиция в соответствии с данным изобретением может применяться на посевных площадях, таких как культивируемые площади, затопляемые рисовые поля, лужайки и фруктовые сады. Пестицидная композиция в соответствии с данным изобретением может контролировать членистоногих вредителей на посевных площадях, не вызывая лекарственного повреждения сельскохозяйственных культур, которые культивируют на посевных площадях, в некоторых случаях.
Примеры таких сельскохозяйственных культур перечислены ниже.
Сельскохозяйственные культуры: кукуруза, рис, пшеница, овес, рожь, ячмень, сорго, хлопок, соя, арахис, гречиха, сахарная свекла, рапс, подсолнечник, сахарный тростник, табак и т.д..
Овощи: пасленовые овощи (баклажан, томат, паприка, жгучий перец, картофель и т.д.), тыквенные овощи (огурец, тыква, цуккини, арбуз, дыня и т.д.), крестоцветные овощи (дайкон, турнепс, хрен, кольраби, китайская капуста, капуста, горчица сарептская, брокколи, цветная капуста и т.д.), сложноцветные овощи (лопух, хризантема увенчанная, артишок, латук и т.д.), лилейные овощи (лук-татарка, лук, чеснок, спаржа и т.д.), зонтичные овощи (морковь, петрушка, сельдерей, пастернак и т.д.), маревые овощи (шпинат, листовая свекла и т.д.), губоцветные овощи (японский базилик, мята, базилик и т.д.), земляника, сладкий картофель, ямс, аронник и т.д..
Цветы или декоративные растения.
Декоративно-лиственные растения.
Фруктовые деревья: семечковые фрукты (яблоко, обычная груша, груша песчаная, китайская айва, айва и т.д.), косточковые фрукты (персик, слива, нектарин, слива китайская, вишня, абрикос, слива домашняя и т.д.), цитрусовые растения (мандарин уншиу, апельсин, лимон, лайм, грейпфрут и т.д.), орехи (каштан, грецкий орех, фундук, миндаль, фисташка, кешью, макадамия и т.д.), ягодные кустарники (голубика, клюква, черная смородина, малина и т.д.), виноград, хурма, олива, мушмула японская, банан, кофе, финик, кокос и т.д..
Деревья, отличные от фруктовых деревьев: чай, тутовое дерево, цветущие деревья и кустарники, уличные деревья (ясень, береза, кизил, эвкалипт, гинкго, сирень, клен, дуб, тополь, багряник, китайское амбровое дерево, платан, дзелькова, японская туя, ель, тсуга разнолистная, можжевельник твердый, сосна, ель, тис) и т.д.
Указанные выше сельскохозяйственные культуры включают такие, у которых имеется резистентность к HPPD ингибитору, такому как изоксафлутол, ALS ингибитору, такому как имазетапир или тифенсульфурон-метил, ингибитору EPSP синтезирующего фермента, ингибитору глутамин синтезирующего фермента, ингибитору ацетил CoA карбоксилазы или гербициду, такому как бромоксинил, придаваемая классическими методами селекции или методами генной инженерии.
Примеры сельскохозяйственных растений, которым резистентность придается классическими методами селекции, включают канолу Clearfield (зарегистрированный товарный знак), которая резистентна к имидазолиноновым гербицидам, таким как имазетапир, и сою STS, которая резистентна к сульфонилмочевинному гербициду - ингибитору ALS, такому как тифенсульфурон-метил, а также кукуруза SR, которая резистентна к ингибитору ацетил CoA карбоксилазы, такому как гербициды на основе оксима триона или гербициды арилоксифеноксипропионовой кислоты. Например, сельскохозяйственные растения, которым придана резистентность к ингибитору ацетил CoA карбоксилазы, описаны в Proc. Natl. Acad. Sci. USA, 1990, vol. 87, p.7175-7179. Кроме того, мутированная ацетил CoA карбоксилаза, которая резистентна к ингибитору ацетил CoA карбоксилазы, описана в Weed Science, vol. 53, p.728-746, 2005. Когда ген, кодирующий мутированную ацетил CoA карбоксилазу, вводят в сельскохозяйственное растение методом генной инженерии, или когда мутацию, связанную с приданием резистентности ацетил CoA карбоксилазе, вводят в ген, кодирующий ацетил CoA карбоксилазу сельскохозяйственного растения, может быть получено сельскохозяйственное растение, резистентное к ингибитору ацетил CoA карбоксилазы. Далее, нуклеиновые кислоты для введения основной замещающей мутации могут быть введены в клетки сельскохозяйственного растения химерапластикой (см. Gura T. 1999, Repairing the Genome's Spelling Mistakes, Science 285: 316-318) для того, чтобы вызвать сайт-направленную мутацию замещения аминокислоты в гене, который поражается ингибитором ацетил CoA карбоксилазы или гербицидом в сельскохозяйственном растении, и таким образом может быть получено сельскохозяйственное растение, резистентное к ингибитору ацетил CoA карбоксилазы или гербициду.
Примеры сельскохозяйственных растений, которым придается резистентность методом генной инженерии, включают сорта кукурузы, которые резистентны к глифосату и глуфосинату. Некоторые из таких сортов кукурузы продают под торговым наименованием RoundupReady (зарегистрированный товарный знак) и LibertyLink (зарегистрированный товарный знак).
Указанные выше сельскохозяйственные растения включают такие, которым способность вырабатывать инсектицидный токсин, например, селективный токсин, который вырабатывается Bacillus, придается методом генной инженерии.
Примеры инсектицидного токсина, который вырабатывается такими генно-модифицированными растениями, включает инсектицидные белки, полученные из Bacillus cereus и Bacillus popilliae; δ-эндотоксины, полученные из Bacillus thuringiensis, такие как Cry1Ab, Cry1Ac, Cry1F, Cry1Fa2, Cry2Ab, Cry3A, Cry3Bb1 или Cry9C; инсектицидные белки, полученные из Bacillus thuringiensis, такие как VIP 1, VIP 2, VIP 3 или VIP 3A; инсектицидные белки, полученные из нематод; токсины, вырабатываемые животными, такими как токсины скорпиона, токсины паука, токсины пчелы или специфические к насекомым нервные токсины; токсины грибов; растительный лектин; агглутинин; ингибиторы протеазы, такие как ингибиторы трипсина, ингибиторы серинпротеазы, ингибиторы пататина, цистатина или папаина; инактивирующие рибосому белки (RIP), такие как рицин, кукурузные-RIP, абрин, сапорин или бриодин; стероидные метаболизирующие ферменты, такие как 3-гидроксистероидная протеаза, экдистероид-UDP-глюкозилтрансфераза или холестериноксидаза; ингибиторы экдизона; HMG-CoA редуктаза; ингибиторы ионных каналов, такие как ингибиторы натриевого канала или ингибиторы кальциевого канала; эстераза ювенильного гормона; рецепторы диуретического гормона; стилбенсинтаза; бибензилсинтаза; хитиназа; и глюканаза.
Инсектицидный токсин, который вырабатывают такие генетически модифицированные растения, также включает гибридные токсины различных инсектицидных белков, например, δ-эндотоксинов, таких как Cry1Ab, Cry1Ac, Cry1F, Cry1Fa2, Cry2Ab, Cry3A, Cry3Bb1 или Cry9C, и инсектицидных белков, таких как VIP 1, VIP 2, VIP 3 или VIP 3A, и токсинов, в которых часть аминокислот, составляющих инсектицидный белок, исключена или модифицирована. Гибридный токсин получают объединением различных доменов инсектицидных белков методом генной инженерии. Примером токсина, в котором часть аминокислот, составляющих инсектицидный белок, исключена, является Cry1Ab, в котором часть аминокислот исключена. Примером токсина, в котором часть аминокислот, составляющих инсектицидный белок, модифицирована, является токсин, в котором одна или более аминокислот природного токсина замещена.
Инсектицидный токсин и генетически модифицированное сельскохозяйственное растение, обладающее способностью вырабатывать инсектицидный токсин, описаны, например, в EP-A-0374753, WO 93/07278, WO 95/34656, EP-A-0427529, EP-A-451878, WO 03/052073, и подобных.
Генетически модифицированное сельскохозяйственное растение, обладающее способностью вырабатывать инсектицидный токсин, особенно резистентно к поражению жесткокрылыми вредителями, двукрылыми вредителями или чешуекрылыми вредителями.
Генетически модифицированные растения, которые имеют один или более резистентных к вредителям генов и, следовательно, вырабатывают один или более инсектицидных токсинов, также известны, и некоторые из них доступны коммерчески. Примеры подходящих генетически модифицированных растений включают YieldGard (зарегистрированный товарный знак) (сорт кукурузы, экспрессирующий Cry1Ab токсин), YieldGard Rootworm (зарегистрированный товарный знак) (сорт кукурузы, экспрессирующий Cry3Bb1 токсин), YieldGard Plus (зарегистрированный товарный знак) (сорт кукурузы, экспрессирующий Cry1Ab и Cry3Bb1 токсины), Herculex I (зарегистрированный товарный знак) (сорт кукурузы, экспрессирующий Cry1Fa2 токсин и фосфинотрицин N-ацетилтрансферазу (PAT) для придания резистентности к глуфосинату), NuCOTN33B (зарегистрированный товарный знак) (сорт хлопка, экспрессирующий Cry1Ac токсин), Bollgard I (зарегистрированный товарный знак) (сорт хлопка, экспрессирующий Cry1Ac токсин), Bollgard II (зарегистрированный товарный знак) (сорт хлопка, экспрессирующий Cry1Ac и Cry2Ab токсины), VIPCOT (зарегистрированный товарный знак) (сорт хлопка, экспрессирующий VIP токсин), NewLeaf (зарегистрированный товарный знак) (сорт картофеля, экспрессирующий Cry3A токсин), NatureGard Agrisure GT Advantage (зарегистрированный товарный знак) (GA21 глифосат-резистентный признак), Agrisure CB Advantage (зарегистрированный товарный знак) (признак Bt11 кукурузного мотылька (CB)), Protecta (зарегистрированный товарный знак), и подобные.
Указанные выше сельскохозяйственные культуры включают такие, которым способность вырабатывать антипатогенное вещество придается методом генной инженерии.
Примеры антипатогенных веществ включают PR белки (PRP, описанные в EP-A-0392225); ингибиторы ионных каналов, такие как ингибиторы натриевых каналов или ингибиторы кальциевых каналов (например, KP1, KP4, KP6 токсины и т.д., вырабатываемые вирусами); стилбенсинтазу; бибензилсинтазу; хитиназу; глюканазу; вещества, вырабатываемые микроорганизмами, такими как пептидный антибиотики, или факторы белка, вовлеченные в резистентность растения к болезням (описанные в WO 03/000906); и подобные. Такие антипатогенные вещества и генетически модифицированные растения, которые вырабатывают антипатогенные вещества, описаны в EP-A-0392225, WO 05/33818, EP-A-0353191 и подобные.
Если пестицидную композицию в соответствии с данным изобретением применяют для контроля вредителей в сельском хозяйстве и лесоводстве, наносимое количество обычно составляет от 1 до 10000 г/га, предпочтительно от 10 до 500 г/га соединения в соответствии с данным изобретением в качестве активного ингредиента. Если пестицидная композиция в соответствии с данным изобретением имеет форму эмульгируемого концентрата, смачиваемого порошка, текучей композиции или микроинкапсулированной композиции, ее обычно применяют после разведения водой до получения концентрации соединения в соответствии с данным изобретением в качестве активного ингредиента от 0,01 до 1000 ч./млн. Если пестицидная композиция в соответствии с данным изобретением имеет форму порошка или гранул, ее обычно применяют как есть. Пестицидная композиция в соответствии с данным изобретением может распыляться непосредственно на растения, защищаемые от членистоногих вредителей. Альтернативно, почва может быть обработана пестицидной композицией в соответствии с данным изобретением для контроля членистоногих вредителей, живущих в почве. Семенные лунки до посадки или посадочные лунки или ножка растения при посадке также могут быть обработаны пестицидной композицией в соответствии с данным изобретением. Далее, пластины, содержащие пестицидную композицию в соответствии с данным изобретением, могут наматываться вокруг растений, располагаться рядом с растениями, класться на поверхность почвы у ножки растения или наноситься подобными методами.
Если пестицидную композицию в соответствии с данным изобретением применяют для контроля эпидемии, наносимое количество обычно составляет от 0,001 до 10 мг/м3 соединения в соответствии с данным изобретением в качестве активного ингредиента для нанесения на площадь, и от 0,001 до 100 мг/м2 активного ингредиента для нанесения по плану. Пестицидную композицию в соответствии в форме эмульгируемого концентрата, смачиваемого порошка или текучей композиции обычно применяют после разведения водой до содержания активного ингредиента от 0,001 до 10000 ч./млн. Пестицидную композицию в форме масляного раствора, аэрозольной композиции, дымящего пестицида или отравленной приманки обычно наносят как есть.
Если пестицидную композицию в соответствии с данным изобретением применяют для контроля внешних паразитов домашнего скота, такого как корова, лошадь, свинья, овца, коза или курица, или мелких животных, таких как собака, кошка, крыса или мышь, она может наноситься методом, известным в ветеринарии. Более конкретно, при необходимости системного контроля пестицидную композицию в соответствии с данным изобретением вводят, например, в виде таблетки, смеси с кормом, суппозитория или инъекции (например, внутримышечно, подкожно, внутривенно, внутрибрюшинно и т.д.). Если необходим не системный контроль, методы применения пестицидной композиции в соответствии с данным изобретением включают распыление, обработку заливкой или точечную обработку пестицидной композицией в форме масляного раствора или водной жидкости, мытье животного пестицидной композицией в форме шампуня, и ношение животным ошейника или клипсы, содержащих пестицидную композицию в форме полимерной композиции. При введении животному количество соединения в соответствии с данным изобретением обычно составляет от 0,1 до 1000 мг на 1 кг массы тела животного.
Пестицидная композиция в соответствии с данным изобретением может применяться в смеси или в сочетании с другими инсектицидами, нематоцидами, акарицидами, фунгицидами, гербицидами, регуляторами роста растений, синергистами, удобрениями, почвоулучшителями, кормом для животных и подобными.
Примеры активного ингредиента такого инсенктицида включают
(1) фосфорорганические соединения:
ацефат, фосфид алюминия, бутатиофос, кадузафос, хлорэтоксифос, хлорфенвинфос, хлорпирифос, хлорпирифос-метил, цианофос (CYAP), диазинон, DCIP (дихлордиизопропиловый эфир), дихлофентион (ECP), дихлорвос (DDVP), диметоат, диметилвинфос, дисульфотон, EPN, этион, этопрофос, этримфос, фентион (MPP), фенитротион (MEP), фостиазат, формотион, гидрофосфид, изофенфос, изоксатион, малатион, месульфенфос, метидатион (DMTP), монокротофос, налед (BRP), оксидепрофос (ESP), паратион, фозалон, фосмет (PMP), пиримифос-метил, пиридафентион, хиналфос, фентоат (PAP), профенофос, пропафос, протиофос, пирахлорфос, салитион, сульпрофос, тебупиримфос, темефос, тетрахлорвинфос, тербуфос, тиометон, трихлорфон (DEP), вамидотион, форат, кадузафос и подобные;
(2) соединения карбамата:
аланикарб, бендиокарб, бенфуракарб, BPMC, карбарил, карбофуран, карбосульфан, клоэтокарб, этиофенкарб, фенобукарб, фенотиокарб, феноксикарб, фуратиокарб, изопрокарб (MIPC), метолкарб, метомил, метиокарб, NAC, оксамил, пиримикарб, пропоксур (PHC), XMC, тиодикарб, ксилилкарб, алдикарб и подобные;
(3) синтетические пиретроидные соединения:
акринатрин, аллетрин, бета-цифлутрин, бифентрин, циклопротрин, цифлутрин, цигалотрин, циперметрин, эмпентрин, дельтаметрин, эсфенвалерат, этофенпрокс, фенпропатрин, фенвалерат, флуцитринат, флуфенопрокс, флуметрин, флувалинат, галфенпрокс, имипротрин, перметрин, праллетрин, пиретрины, ресметрин, сигма-циперметрин, силафлуофен, тефлутрин, тралометрин, трансфлутрин, тетраметрин, фенотрин, цифенотрин, альфа-циперметрин, зета-циперметрин, лямбда-цигалотрин, гамма-цигалотрин, фураметрин, тау-флувалинат, метофлутрин, 2,3,5,6-тетрафтор-4-метилбензил 2,2-диметил-3-(1-пропенил)циклопропанкарбоксилат, 2,3,5,6-тетрафтор-4-(метоксиметил)бензил 2,2-диметил-3-(2-метил-1-пропенил)циклопропанкарбоксилат, 2,3,5,6-тетрафтор-4-(метоксиметил)бензил 2,2-диметил-3-(2-циано-1-пропенил)циклопропанкарбоксилат, 2,3,5,6-тетрафтор-4-(метоксиметил)бензил 2,2,3,3-тетраметилциклопропанкарбоксилат и подобные;
(4) соединения нереистоксина:
картап, бенсультап, тиоциклам, моносультап, бисультап и подобные;
(5) соединения неоникотиноида:
имидаклоприд, нитенпирам, ацетамиприд, тиаметоксам, тиаклоприд, динотефуран, клотианидин и подобные;
(6) соединения бензоилмочевины:
хлорфлуазурон, бистрифлурон, диафентиурон, дифлубензурон, флуазурон, флуциклоксурон, флуфеноксурон, гексафлумурон, луфенурон, новалурон, новифлумурон, тефлубензурон, трифлумурон, триазурон и подобные;
(7) соединения фенилпиразола:
ацетопрол, этипрол, фипронил, ванилипрол, пирипрол, пирафлупрол и подобные;
(8) инсектициды на основе Bt токсина:
живые споры, полученные из Bacillus thuringiesis и кристаллические токсины, полученные из них, а также их смеси;
(9) соединения гидразина:
хромафенозид, галофенозид, метоксифенозид, тебуфенозид и подобные;
(10) хлорорганические соединения:
алдрин, диелдрин, диенохлор, эндосульфан, метоксихлор и подобные;
(11) натуральные инсектициды:
машинное масло, сульфат никотина и подобные;
(12) другие инсектициды:
авермектин-B, бромпропилат, бупрофезин, хлорфенапир, циромазин, D-D (1,3-дихлорпропен), эмамектин-бензоат, феназаквин, флупиразофос, гидропрен, метопрен, индоксакарб, метоксадиазон, милбемицин-A, пиметрозин, пиридалил, пирипроксифен, спиносад, сульфлурамид, толфенпирад, триазамат, флубендиамид, лепимектин, мышьяковая кислота, бенклотиаз, цианамид кальция, полисульфид кальция, хлордан, DDT, DSP, флуфенерим, флоникамид, флуримфен, форметанат, метам-аммоний, метам-натрий, метилбромид, олеат калия, протрифенбут, спиромесифен, сера, метафлумизон, спиротетрамат, пирифлуквиназон, спинеторам, хлорантранилипрол, тралопирил, соединение, представленное формулой (A):
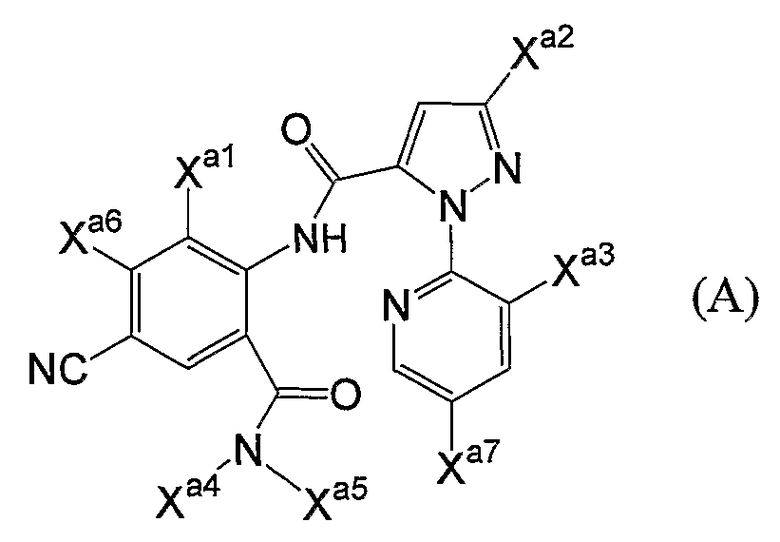
где Xa1 является метильной группой, атомом хлора, атомом брома или атомом фтора, Xa2 является атомом фтора, атомом хлора, атомом брома, C1-C4 галогеналкильной группой или C1-C4 галогеналкоксигруппой, Xa3 является атомом фтора, атомом хлора или атомом брома, Xa4 является необязательно замещенной C1-C4 алкильной группой, необязательно замещенной C3-C4 алкенильной группой, необязательно замещенной C3-C4 алкинильной группой, необязательно замещенной C3-C5 циклоалкилалкильной группой или атомом водорода, Xa5 является атомом водорода или метильной группой, Xa6 является атомом водорода, атомом фтора или атомом хлора, и Xa7 является атомом водорода, атомом фтора или атомом хлора;
соединение, представленное формулой (B):
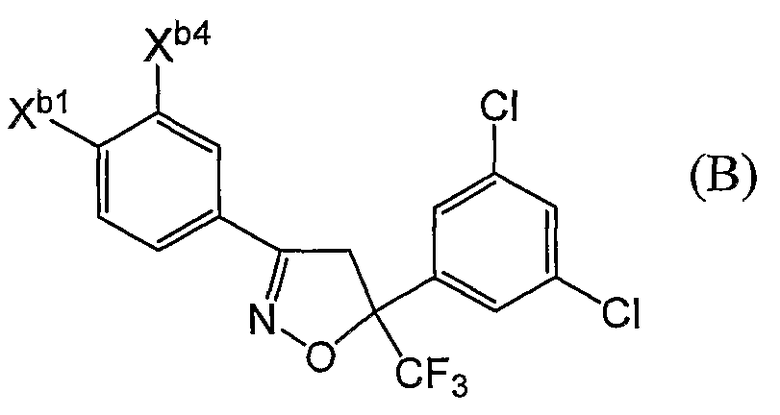
где Xb1 является Xb2-NH-C(=O) группой, Xb2-C(=O)-NH-CH2 группой, Xb3-S(O) группой, необязательно замещенной пиррол-1-ильной группой, необязательно замещенной имидазол-1-ильной группой, необязательно замещенной пиразол-1-ильной группой или необязательно замещенной 1,2,4-триазол-1-ильной группой, Xb2 является необязательно замещенной C1-C4 галогеналкильной группой, такой как 2,2,2-трифторэтильная группа, или необязательно замещенной C3-C6 циклоалкильной группой, такой как циклопропильная группа, и Xb3 является необязательно замещенной C1-C4 алкильной группой, такой как метильная группа, и Xb4 является атомом водорода, атомом хлора, цианогруппой или метильной группой;
соединение, представленное формулой (C):
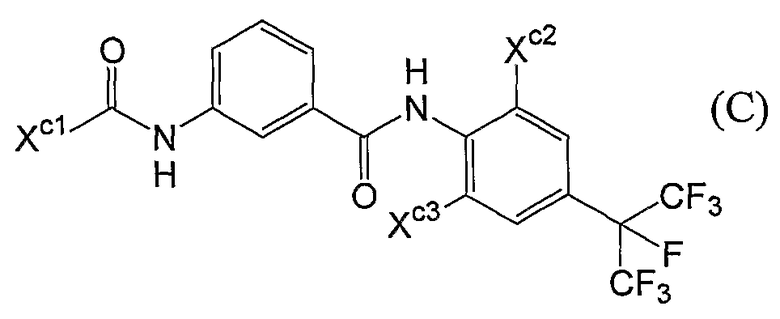
где Xc1 является необязательно замещенной C1-C4 алкильной группой, такой как 3,3,3-трифторпропильная группа, необязательно замещенной C1-C4 алкоксигруппой, такой как 2,2,2-трихлорэтоксигруппа, или необязательно замещенной фенильной группой, такой как 4-цианофенильная группа, или необязательно замещенной пиридильной группой, такой как 2-хлор-3-пиридильная группа, Xc2 является метильной группой или трифторметилтиогруппой, и Xc3 является метильной группой или атомом галогена; и подобные.
Примеры активного ингредиента акарицида включают ацеквиноцил, амитраз, бензоксимат, бифеназат, бромпропилат, хинометионат, хлорбензилат, CPCBS (хлорфенсон), клофентезин, цифлуметофен, кельтан (дикофол), этоксазол, фенбутатина оксид, фенотиокарб, фенпироксимат, флуакрипирим, флупроксифен, гекситиазокс, пропаргит (BPPS), полинактины, пиридабен, пиримидифен, тебуфенпирад, тетрадифон, спиродиклофен, спиромезифен, спиротетрамат, амидофлумет, циенопирафен и подобные.
Примеры нематоцида включают DCIP, фостиазат, гидрохлорид левамизола, метилизотиоцианат, тартрат морантела, имициафос и подобные.
Примеры активного ингредиента таких фунгицидов включают соединения стробилурина, такие как азоксистробин; фосфаторганические соединения, такие как толклофос-метил; соединения азола, такие как трифлумизол, пефуразоат или дифеноконазол; фталид, флутоланил, валидамицин, пробеназол, дикломезин, пенцикурон, дазомет, казугамицин, IBP, пироквилон, оксолиновую кислоту, трициклазол, феримзон, мепронил, EDDP, изопротиолан, карпропамид, диклоцимет, фураметпир, флудиоксонил, процимидон и диэтофенкарб.
Примеры
Далее данное изобретение описано более подробно в примерах получения, примерах композиции и примерах эксперимента, которыми данное изобретение не ограничено.
Сначала представлены примеры получения соединения в соответствии с данным изобретением.
Пример получения 1
К раствору 0,5 г метил 2-фтор-2-(3,4,5-трифторфенил)-2-(3,3,3-трифторпропилсульфонил)ацетата в 20 мл метанола добавляют 0,6 мл 7M раствора аммиака в метаноле при комнатной температуре, и смесь перемешивают при той же температуре в течение 14 часов. Реакционную смесь концентрируют при пониженном давлении. Остаток очищают хроматографией на колонке с получением 0,35 г 2-фтор-2-(3,3,3-трифторпропилсульфонил)-2-(3,4,5-трифторфенил)ацетамида (далее обозначенного как данное соединение (1)).
Данное соединение (1):
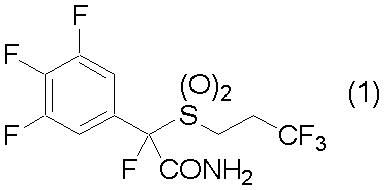
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,56-7,65 (2H, м), 6,57 (1H, ушир.с), 5,91 (1H, ушир.с), 3,56-3,73 (2H, м), 3,23-3,48 (2H, м).
Пример получения 2
К раствору 1,0 г метил 2-(3,4,5-трифторфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата в 2,0 мл метанола добавляют 8,0 мл 7M раствора аммиака в метаноле при комнатной температуре, и смеси перемешивают при той же температуре в течение 48 часов. Реакционную смесь концентрируют при пониженном давлении. Остаток очищают хроматографией на колонке с получением 0,20 г 2-(3,4,5-трифторфенил)-2-(3,3,3-трифторпропилсульфонил)пропанамида (далее обозначенного как данное соединение (2)).
Данное соединение (2):
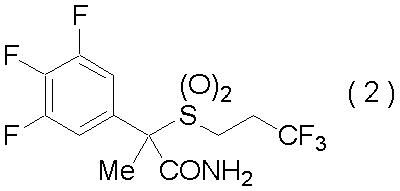
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,36 (2H, дд), 6,41 (1H, ушир.с), 6,15 (1H, ушир.с), 3,26-3,58 (2H, м), 2,50-2,74 (2H, м) 2,08 (3H, с).
Пример получения 3
К раствору 0,8 г метил 2-(4-хлор-3-фторфенил)-2-фтор-2-(3,3,3-трифторпропилсульфонил)ацетата в 20 мл метанола добавляют 1,5 мл 7M раствора аммиака в метаноле при комнатной температуре, и смесь перемешивают при той же температуре в течение 16 часов. Реакционную смесь концентрируют при пониженном давлении. Остаток очищают хроматографией на колонке с получением 0,60 г 2-(4-хлор-3-фторфенил)-2-фтор-2-(3,3,3-трифторпропилсульфонил)ацетамида (далее обозначенного как данное соединение (3)).
Данное соединение (3):
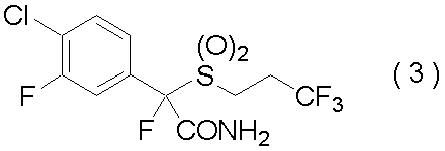
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,74 (1H, дд), 7,64 (1H, дд), 7,55 (1H, дд), 6,60 (1H, ушир.с), 6,02 (1H, ушир.с), 3,21-3,46 (2H, м), 2,49-2,69 (2H, м)
Пример получения 4
К раствору 0,6 г метил 2-(4-хлорфенил)-2-фтор-2-(3,3,3-трифторпропилсульфонил)ацетата в 30 мл метанола добавляют 0,7 мл 7M раствора аммиака в метаноле при комнатной температур, и смесь перемешивают при той же температуре в течение 10 часов. Реакционную смесь концентрируют при пониженном давлении. Остаток очищают хроматографией на колонке с получением 0,40 г 2-(4-хлорфенил)-2-фтор-2-(3,3,3-трифторпропилсульфонил)ацетамида (далее обозначенного как данное соединение (4)).
Данное соединение (4):
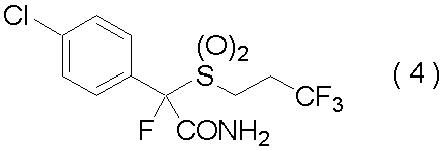
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,86 (2H, д), 7,49 (2H, д), 6,57 (1H, ушир.с), 5,92 (1H, ушир.с), 3,20-3,45 (2H, м), 2,43-2,68 (2H, м).
Пример получения 5
К раствору 0,4 г метил 2-фтор-2-(4-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)ацетата в 30 мл метанола добавляют 0,4 мл 7M раствора аммиака в метаноле при комнатной температур, и смесь перемешивают при той же температуре в течение 4 дней. Реакционную смесь концентрируют при пониженном давлении. Остаток очищают хроматографией на колонке с получением 0,25 г 2-фтор-2-(3,3,3-трифторпропилсульфонил)-2-(4-трифторметилфенил)ацетамида (далее обозначенного как данное соединение (5)).
Данное соединение (5):
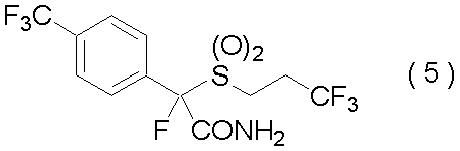
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 8,06 (2H, д), 7,78 (2H, д), 6,58 (1H, ушир.с), 5,92 (1H, ушир.с), 3,22-3,48 (2H, м), 2,52-2,68 (2H, м).
Пример получения 6
К раствору 1,69 г 2-(4-хлорфенил)-2-(3,3,3-трифторпропилсульфанил)уксусной кислоты и 0,81 г тионилхлорида в 15 мл толуола добавляют одну каплю N,N-диметилформамида при комнатной температуре, и смесь перемешивают при 80°C в течение часа. Реакционную смесь концентрируют. Остаток растворяют в 10 мл тетрагидрофурана и туда добавляют 4,0 мл 28% водного раствора аммиака при комнатной температуре. Смесь перемешивают при той же температуре в течение 0,5 часа с последующим экстрагированием этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 1,52 г 2-(4-хлорфенил)-2-(3,3,3-трифторпропилсульфанил)ацетамида (далее обозначенного как данное соединение (6)).
Данное соединение (6):
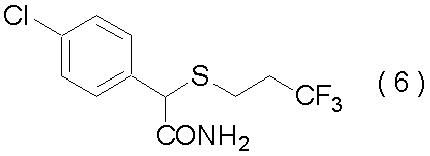
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,36-7,34 (4H, м), 6,30 (1H, ушир.с), 5,89 (1H, ушир.с), 4,54 (1H, с), 2,81-2,69 (2H, м), 2,46-2,31 (2H, м).
Пример получения 7
К раствору 0,40 г 2-(4-хлорфенил)-2-(3,3,3-трифторпропилсульфанил)ацетамида в 10 мл хлороформа добавляют 0,76 г мета-хлорпербензойной кислоты (67%) при комнатной температуре. Смесь перемешивают при комнатной температуре в течение 3 часов и затем кипятят с обратным холодильником в течение 10 часов. Реакционную смесь последовательно промывают водным раствором сульфита натрия и водным насыщенным раствором гидрокарбоната натрия, сушат над безводным сульфатом натрия и затем концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,30 г 2-(4-хлорфенил)-2-(3,3,3-трифторпропилсульфонил)ацетамида (далее обозначенного как данное соединение (7)).
Данное соединение (7):
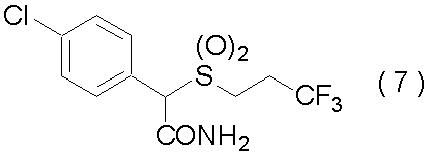
1H-ЯМР (ДМСО-D6, ТМС): δ (ч./млн) 7,76 (1H, ушир.с), 7,64-7,61 (2H, м), 7,56-7,53 (2H, м), 5,42 (1H, с), 3,57-3,54 (1H, м), 3,33-3,29 (1H, м), 2,81-2,56 (2H, м).
Пример получения 8
К раствору 0,33 г метил 2-хлор-3-(4-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата в 3,0 мл метанола добавляют 1,0 мл 7M раствора аммиака в метаноле при комнатной температуре, и смесь перемешивают при той же температуре в течение 28 часов. Реакционную смесь концентрируют при пониженном давлении. Остаток очищают хроматографией на колонке с получением 0,20 г 2-хлор-3-(4-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропанамида (далее обозначенного как данное соединение (8)).
Данное соединение (8):
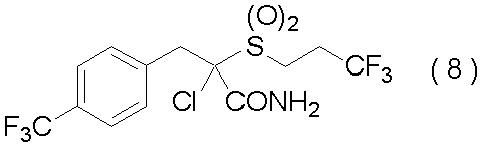
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,61 (2H, д), 7,44 (2H, д), 6,67 (1H, ушир.с), 5,77 (1H, ушир.с), 4,13 (1H, д), 3,93-3,85 (1H, м), 3,56-3,48 (1H, м), 3,41 (1H, д), 2,83-2,76 (2H, м).
Пример получения 9
К раствору 0,23 г 2-хлор-3-(3-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата в 3,0 мл метанола добавляют 0,8 мл 7M раствора аммиака в метаноле при комнатной температуре, и смесь перемешивают при той же температуре в течение 2 часов. Реакционную смесь концентрируют при пониженном давлении. Остаток очищают хроматографией на колонке с получением 0,13 г 2-хлор-3-(3-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропанамида (далее обозначенного как данное соединение (9)).
Данное соединение (9):
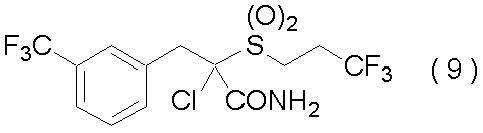
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,61-7,59 (2H, м), 7,52-7,45 (2H, м), 6,67 (1H, ушир.с), 5,89 (1H, ушир.с), 4,13 (1H, д), 3,91-3,87 (1H, м), 3,56-3,48 (1H, м), 3,41 (1H, д), 2,81-2,77 (2H, м).
Пример получения 10
К раствору 0,61 г метил 2-хлор-3-(2-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата в 3,0 мл метанола добавляют 5,2 мл 7M раствора аммиака в метаноле при комнатной температуре, и смесь перемешивают при той же температуре в течение 2 часов. Реакционную смесь концентрируют при пониженном давлении. Остаток очищают хроматографией на колонке с получением 0,20 г 2-хлор-3-(2-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропанамида (далее обозначенного как данное соединение (10)).
Данное соединение (10):

1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,72 (1H, д), 7,52-7,50 (1H, м), 7,45-7,43 (2H, м), 6,95 (1H, ушир.с), 6,41 (1H, ушир.с), 4,28 (1H, д), 3,87-3,80 (2H, м), 3,58-3,50 (1H, м), 2,82-2,76 (2H, м).
Затем показаны конкретные примеры соединения в соответствии с данным изобретением.
Соединение, представленное формулой (I-1):
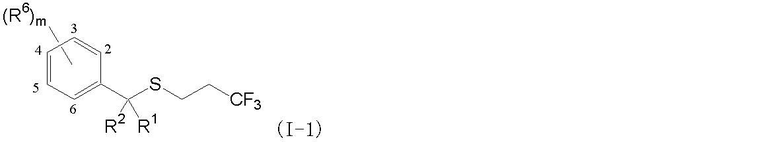
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-2):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-3):
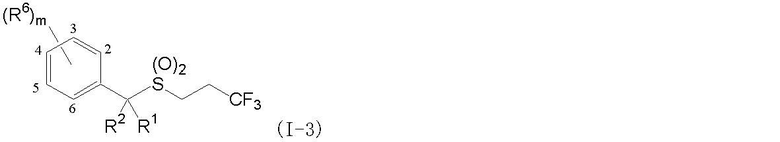
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-4):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-5):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-6):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-7):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-8):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-9):
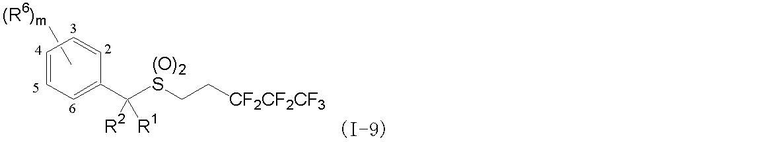
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-10):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-11):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-12):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-13):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-14):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-15):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-16):
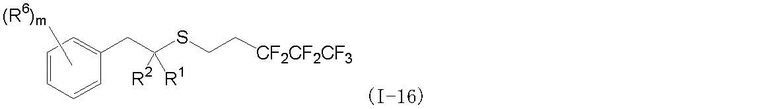
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-17):
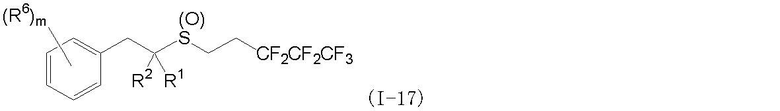
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-18):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-19):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-20):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-21):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-22):
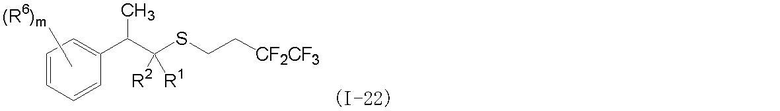
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-23):
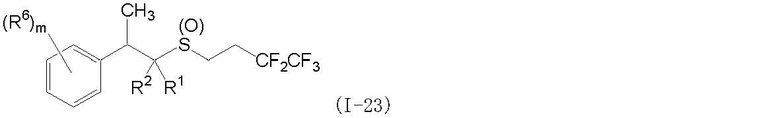
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-24):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-25):
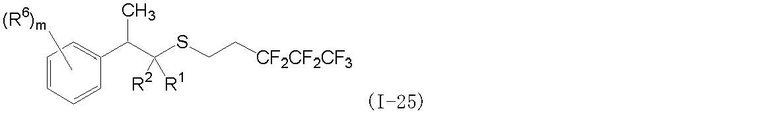
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-26):
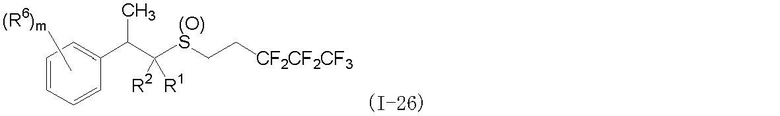
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-27):
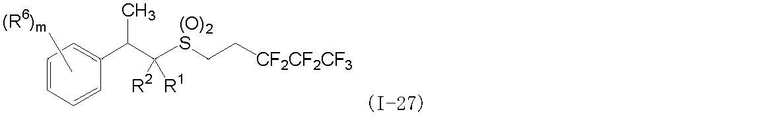
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-28):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-29):
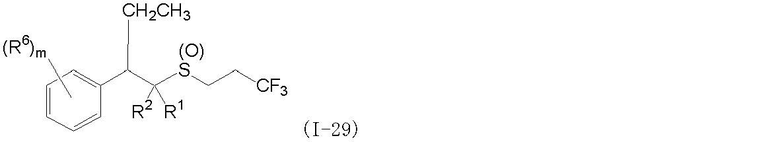
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-30):
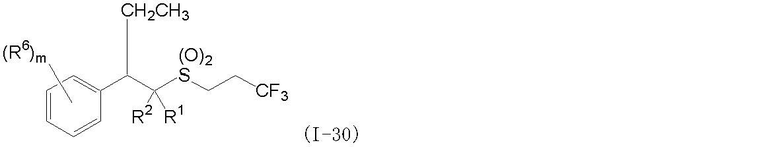
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-31):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-32):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-33):
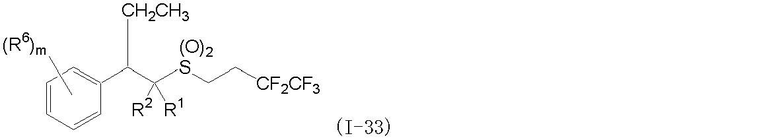
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-34):
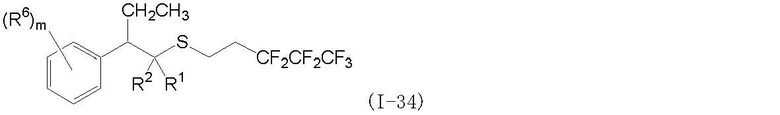
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-35):
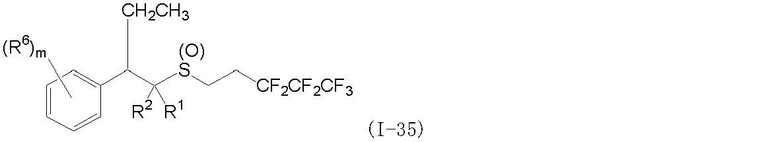
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-36):
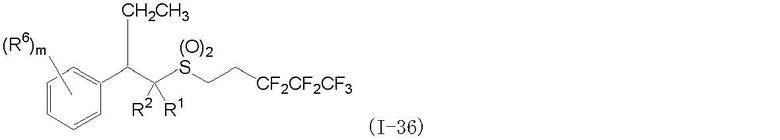
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-37):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-38):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-39):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-40):
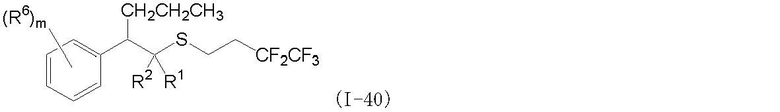
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-41):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-42):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-43):
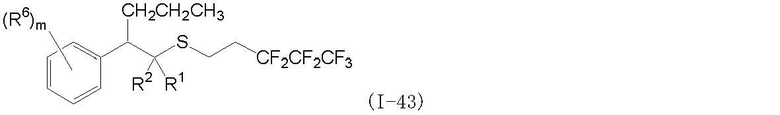
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-44):
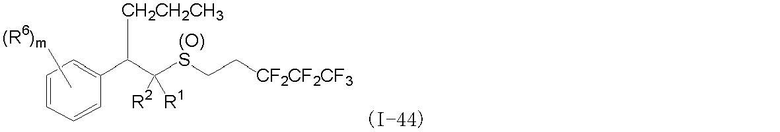
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-45):
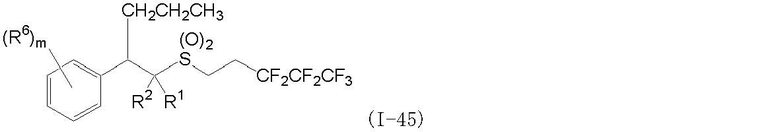
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-46):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-47):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-48):
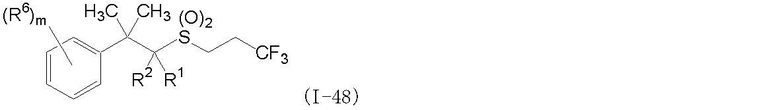
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-49):
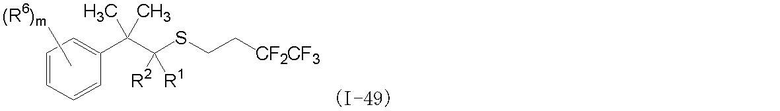
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-50):
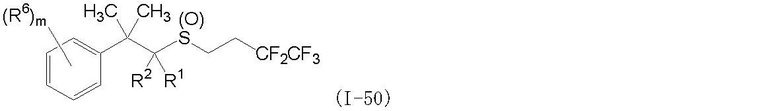
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-51):
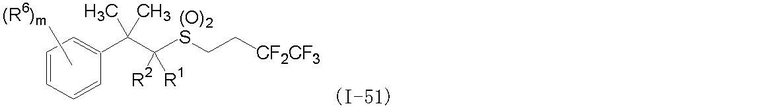
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-52):

где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-53):
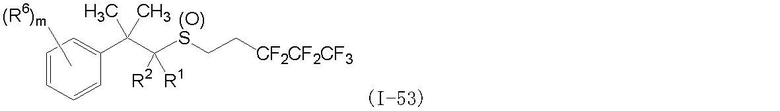
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Соединение, представленное формулой (I-54):
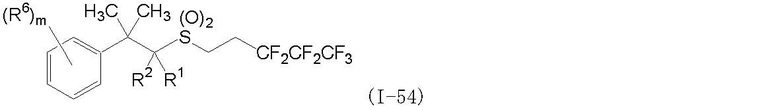
где R2, R1 и (R6)m являются любым из показанных ниже сочетаний.
Сочетания R2, R1 и (R6)m для соединений, представленных указанными выше формулами (I-1)-(I-54) представлены ниже (см. в конце описания).
Среди соединений, определенных указанными выше формулами (I-1)-(I-54) и указанными выше сочетаниями R1, R2 и (R6)m, например, соединением, определенным формулой (I-1) и сочетанием № 855 (обозначенным как соединение (I-1-855)) и соединением, определенным формулой (I-12) и сочетанием № 723 (обозначенным как соединение (I-12-723)), являются следующие соединения.
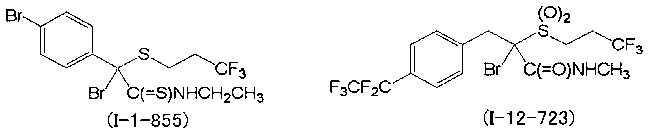
Далее представлены ссылочные примеры получения промежуточных соединений в соответствии с данным изобретением.
Ссылочный пример получения 1
К раствору 0,5 г 5-бром-1,2,3-трифторбензола и 0,72 г метил (3,3,3-трифторпропилсульфонил)ацетата в 20 мл 1,4-диоксана добавляют 0,28 г гидрида натрия (60% дисперсия в парафиновом масле), 49 мг трис(дибензилиденацетон)(хлороформ)дипалладия(0) и 75 мг трифенилфосфина при комнатной температуре, и смесь перемешивают при 80°C в течение 48 часов. К реакционной смеси добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,54 г метил (3,4,5-трифторфенил)-(3,3,3-трифторпропилсульфонил)ацетата, представленного следующей формулой:
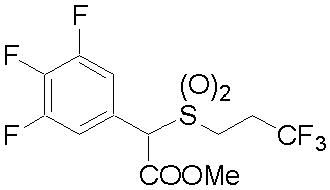
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,29 (2H, дд), 4,95 (1H, с), 3,91 (3H, с), 3,18-3,56 (2H, м), 2,48-2,76 (2H, м).
Ссылочный пример получения 2
К суспензии 0,11 г гидрида натрия (60% дисперсия в парафиновом масле) в 30 мл тетрагидрофурана добавляют 1,0 г метил (3,4,5-трифторфенил)-(3,3,3-трифторпропилсульфонил)ацетата при комнатной температуре. Смесь перемешивают при комнатной температуре в течение 0,5 часа и в нее добавляют 0,79 г трифторметансульфоната 1-фтор-2,4,6-триметилпиридиния. Реакционную смесь перемешивают при той же температуре в течение 2 часов, и туда добавляют 10% хлористоводородную кислоту и затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,99 г метил фтор-(3,4,5-трифторфенил)-(3,3,3-трифторпропилсульфонил)ацетата, представленного формулой:
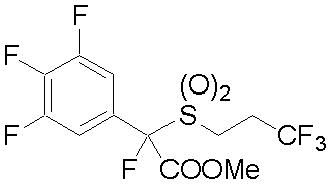
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,50 (2H, дд), 4,00 (3H, с) 3,33-3,46 (2H, м), 2,61-2,76 (2H, м).
Ссылочный пример получения 3
К суспензии 0,11 г гидрида натрия (60% дисперсия в парафиновом масле) в 30 мл N,N-диметилформамида добавляют 1,0 г метил (3,4,5-трифторфенил)-(3,3,3-трифторпропилсульфонил)ацетата при комнатной температуре. Смесь перемешивают при комнатной температуре в течение 0,5 часа и к ней добавляют 0,39 г метилйодида. Реакционную смесь перемешивают при той же температуре в течение 48 часов и к ней добавляют 10% хлористоводородную кислоту и затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,92 г метил 2-(3,4,5-трифторфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата, представленного формулой:
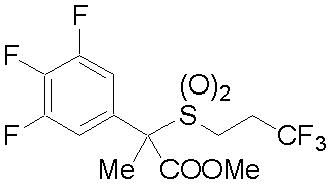
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,20 (2H, дд), 3,94 (3H, с), 3,05-3,70 (2H, м), 2,39-2,73 (2H, м), 2,04 (3H, с).
Ссылочный пример получения 4
К раствору 3,0 г 2-фтор-4-йодхлорбензола и 3,6 г метил (3,3,3-трифторпропилсульфонил)ацетата в 100 мл 1,4-диоксана добавляют 1,40 г гидрида натрия (60% дисперсия в парафиновом масле), 242 мг (дибензилиденацетон)(хлороформ)дипалладия(0) и 368 мг трифенилфосфина при комнатной температуре, и смесь перемешивают при 80°C в течение 5 дней. К реакционной смеси добавляют 10% хлористоводородную кислоту и затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 1,8 г метил (4-хлор-3-фторфенил)-(3,3,3-трифторпропилсульфонил)ацетата, представленного формулой:
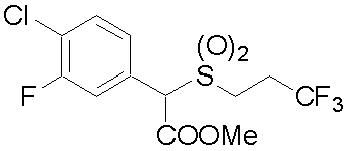
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,43-7,53 (2H, м), 7,31 (1H, дд), 5,02 (1H, с), 3,90 (3H, с), 3,17-3,58 (2H, м), 2,44-2,77 (2H, м).
Ссылочный пример получения 5
К суспензии 0,11 г гидрида натрия (60% дисперсия в парафиновом масле) в 30 мл тетрагидрофурана добавляют 1,0 г метил (4-хлор-3-фторфенил)-(3,3,3-трифторпропилсульфонил)ацетат при комнатной температуре. Смесь перемешивают при комнатной температуре в течение 0,5 часа и к ней добавляют 0,79 г трифторметансульфоната 1-фтор-2,4,6-триметилпиридиния. Реакционную смесь перемешивают при той же температуре в течение 2 часов и к ней добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,99 г метил (4-хлор-3-фторфенил)-фтор-(3,3,3-трифторпропилсульфонил)ацетата, представленного формулой:
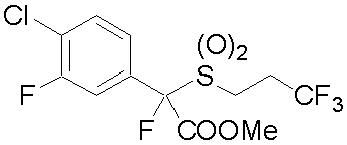
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,52-7,66 (3H, м), 4,00 (3H, с), 3,28-3,38 (2H, м), 2,58-2,73 (2H, м).
Ссылочный пример получения 6
К раствору 2,8 г 4-йодхлорбензола и 3,56 г метил (3,3,3-трифторпропилсульфонил)ацетата в 100 мл 1,4-диоксана добавляют 1,4 г гидрида натрия (60% дисперсия в парафиновом масле), 242 мг трис(дибензилиденацетон)(хлороформ)дипалладия(0) и 368 мг трифенилфосфина при комнатной температуре, и смесь перемешивают при 80°C в течение 48 часов. К реакционной смеси добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 2,6 г метил (4-хлорфенил)-(3,3,3-трифторпропилсульфонил)ацетат, представленного формулой:
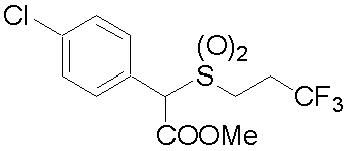
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,53 (2H, д), 7,44 (2H, д), 5,05 (1H, с), 3,88 (3H, с), 3,15-3,55 (2H, м), 2,40-2,73 (2H, м).
Ссылочный пример получения 7
К суспензии 81 мг гидрида натрия (60% дисперсия в парафиновом масле) в 30 мл тетрагидрофурана добавляют 0,7 г метил (4-хлорфенил)-(3,3,3-трифторпропилсульфонил)-ацетат при комнатной температуре. Смесь перемешивают при комнатной температуре в течение 0,5 часа и к ней добавляют 0,59 г трифторметансульфоната 1-фтор-2,4,6-триметилпиридиния. Реакционную смесь перемешивают при той же температуре в течение 2 часов, и к ней добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,67 г метил (4-хлорфенил)-фтор-(3,3,3-трифторпропилсульфонил)ацетата, представленного формулой:
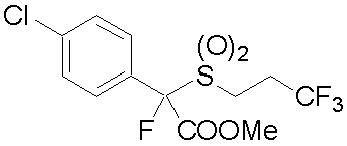
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,74 (2H, дд), 7,49 (2H, дд), 3,99 (3H, с), 3,24-3,38 (2H, м), 2,52-2,72 (2H, м).
Ссылочный пример получения 8
К раствору 5,0 г 4-трифторметилйодбензола и 5,6 г метил (3,3,3-трифторпропилсульфонил)ацетата в 100 мл 1,4-диоксана добавляют 2,21 г гидрида натрия (60% дисперсия в парафиновом масле), 579 мг трис(дибензилиденацетон)(хлороформ)дипалладия(0) и 381 мг трифенилфосфина при комнатной температуре, и смесь перемешивают при 80°C в течение 20 часов. К реакционной смеси добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 4,2 г метил (4-трифторметилфенил)-(3,3,3-трифторпропилсульфонил)ацетата, представленного формулой:

1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,73 (4H, с), 5,11 (1H, с), 3,90 (3H, с), 3,15-3,58 (2H, м), 2,43-2,75 (2H, м).
Ссылочный пример получения 9
К суспензии 106 мг гидрида натрия (60% дисперсия в парафиновом масле) в 30 мл тетрагидрофурана добавляют 1,0 г метил (4-трифторметилфенил)-(3,3,3-трифторпропилсульфонил)-ацетата при комнатной температуре. Смесь перемешивают при комнатной температуре в течение 0,5 часа и к ней добавляют 0,77 г трифторметансульфоната 1-фтор-2,4,6-триметилпиридиния. Реакционную смесь перемешивают при той же температуре в течение 10 часов и к ней добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,92 г метил фтор-(4-трифторметилфенил)-(3,3,3-трифторпропилсульфонил)ацетата, представленного формулой:
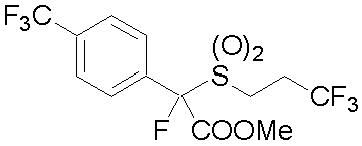
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,96 (2H, д), 7,78 (2H, д) 4,00 (3H, с), 3,28-3,42 (2H, м), 2,56-2,80 (2H, м).
Ссылочный пример получения 10
К раствору 1,78 г S-(3,3,3-трифторпропил)бензолтиоата в 30 мл тетрагидрофурана по каплям добавляют 1,5 мл метоксида натрия (28% раствор в метаноле) при комнатной температуре, и затем добавляют 2,0 г метил бром-(4-хлорфенил)ацетата при комнатной температуре. Смесь перемешивают при той же температуре в течение 4 часов. К реакционной смеси добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 2,2 г метил (4-хлорфенил)-(3,3,3-трифторпропилсульфанил)ацетата, представленного формулой:
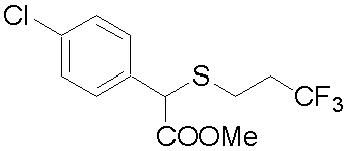
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,40 (2H, дд), 7,34 (2H, дд) 4,57 (1H, с), 3,76 (3H, с), 2,61-2,78 (2H, м) 2,25-2,42 (2H, м).
Ссылочный пример получения 11
К раствору 1,88 г метил (4-хлорфенил)-(3,3,3-трифторпропилсульфанил)ацетата в 10 мл метанола добавляют 5,0 мл 10% водного раствора гидроксида натрия при комнатной температуре, и смесь перемешивают при той же температуре в течение 0,5 часа. К реакционной смеси добавляют 12% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 1,70 г (4-хлорфенил)-(3,3,3-трифторпропилсульфанил)уксусной кислоты, представленной формулой:

1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,41-7,35 (4H, м), 4,56 (1H, с), 2,80-2,67 (2H, м), 2,41-2,26 (2H, м).
Ссылочный пример получения 12
К суспензии 349 мг гидрида натрия (55% дисперсия в парафиновом масле) в 6,0 мл тетрагидрофуран добавляют по каплям раствор 1,87 г метил (3,3,3-трифторпропилсульфонил)ацетата в 3,0 мл тетрагидрофурана при комнатной температуре, и смесь перемешивают при той же температуре в течение 0,5 часа. Туда добавляют раствор 1,91 г 4-трифторметилбензилбромида в 6,0 мл тетрагидрофурана. Реакционную смесь перемешивают при комнатной температуре в течение 4 часов, и туда добавляют 12% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 1,80 г метил 3-(4-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата, представленного формулой:
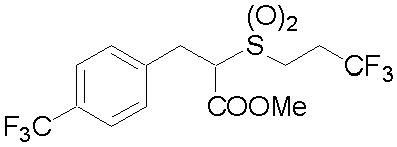
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,60 (2H, д), 7,35 (2H, д), 4,11 (1H, дд), 3,76 (3H, с), 3,57-3,33 (4H, м), 2,80-2,66 (2H, м).
Ссылочный пример получения 13
К суспензии 104 мг гидрида натрия (55% дисперсия в парафиновом масле) в 3,0 мл тетрагидрофурана добавляют раствор 0,85 г метил 3-(4-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата в 5,0 мл тетрагидрофурана при комнатной температуре. Смесь перемешивают при комнатной температуре в течение 0,5 часа, и к ней добавляют раствор 0,42 г N-хлорсукцинимида в 6,0 мл тетрагидрофурана при комнатной температуре. Реакционную смесь перемешивают при той же температуре в течение 19 часов и туда добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,33 г метил 2-хлор-3-(4-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата, представленного формулой:
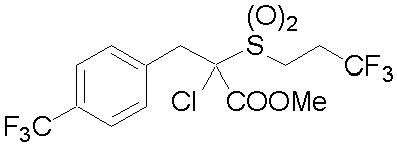
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,60 (2H, д), 7,47 (2H, д), 4,05 (1H, д), 3,91 (3H, с), 3,81-3,72 (1H, м), 3,55 (1H, д), 3,54-3,50 (1H, м), 2,80-2,71 (2H, м).
Ссылочный пример получения 14
К суспензии 0,16 г гидрида натрия (55% дисперсия в парафиновом масле) в 6,0 мл тетрагидрофурана добавляют по каплям раствор 0,95 г метил (3,3,3-трифторпропилсульфонил)ацетата в 3,0 мл тетрагидрофурана при комнатной температуре, и смесь перемешивают при той же температуре в течение 0,5 часа. В смесь добавляют 0,94 г 3-трифторметилбензилбромида в 6,0 мл тетрагидрофуране. Реакционную смесь перемешивают при комнатной температуре в течение 3 часов, и туда добавляют 12% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,38 г метил 3-(3-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата, представленного формулой:
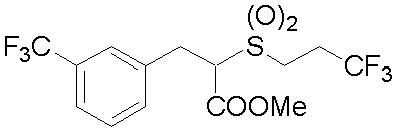
1H-ЯМР(CDCl3, ТМС): δ (ч./млн) 7,57-7,56 (1H, м), 7,50-7,41 (3H, м), 4,10 (1H, дд), 3,75 (3H, с), 3,54 (1H, дд), 3,52-3,45 (1H, м), 3,44 (1H, дд), 3,42-3,32 (1H, м), 2,79-2,67 (2H, м).
Ссылочный пример получения 15
К суспензии 47 мг гидрида натрия (55% дисперсия в парафиновом масле) в 3,0 мл тетрагидрофурана добавляют раствор 0,38 г метил 3-(3-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата в 5,0 мл тетрагидрофурана при комнатной температуре, и смесь перемешивают при комнатной температуре в течение 0,5 часа. К смеси добавляют 0,14 г N-хлорсукцинимида в 6,0 мл тетрагидрофурана при комнатной температуре. Реакционную смесь перемешивают при той же температуре в течение 2 часов, и к ней добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,31 г метил 2-хлор-3-(3-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата, представленного формулой:
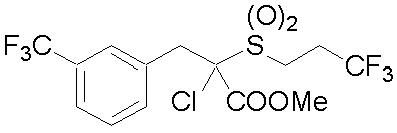
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,58-7,48 (4H, м), 4,05 (1H, д), 3,90 (3H, с), 3,79-3,76 (1H, м), 3,55 (1H, д), 3,54-3,50 (1H, м), 2,82-2,69 (2H, м).
Ссылочный пример получения 16
К суспензии 349 мг гидрида натрия (55% дисперсия в парафиновом масле) в 6,0 мл тетрагидрофурана добавляют по каплям раствор 1,87 г метил (3,3,3-трифторпропилсульфонил)ацетата в 3,0 мл тетрагидрофурана при комнатной температуре, и затем смесь перемешивают при той же температуре в течение 0,5 часа. К смеси добавляют раствор 1,99 г 2-трифторметилбензилбромида в 6,0 мл тетрагидрофурана. Реакционную смесь перемешивают при комнатной температуре в течение 4 часов, и к ней добавляют 12% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 1,79 г метил 3-(2-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата, представленного формулой:
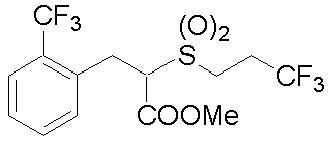
1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,70 (1H, д), 7,51 (1H, т), 7,42 (1H, т), 7,37 (1H, д), 4,16 (1H, дд), 3,76 (3H, с), 3,73 (1H, дд), 3,55-3,32 (3H, м), 2,75-2,69 (2H, м).
Ссылочный пример получения 17
К суспензии 206 мг гидрида натрия (55% дисперсия в парафиновом масле) в 3,0 мл тетрагидрофурана добавляют раствор 1,21 г метил 3-(2-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата в 5,0 мл тетрагидрофурана при комнатной температуре, и смесь перемешивают при комнатной температуре в течение 0,5 часа. К смеси добавляют раствор 0,82 г N-хлорсукцинимида в 6,0 мл тетрагидрофурана при комнатной температуре. Реакционную смесь перемешивают при той же температуре в течение 7 часов, и к ней добавляют 10% хлористоводородную кислоту, затем экстрагируют этилацетатом. Органический слой сушат над безводным сульфатом натрия и концентрируют при пониженном давлении. Остаток очищают хроматографией на силикагеле с получением 0,72 г метил 2-хлор-3-(2-трифторметилфенил)-2-(3,3,3-трифторпропилсульфонил)пропаноата, представленного формулой:

1H-ЯМР (CDCl3, ТМС): δ (ч./млн) 7,73-7,71 (1H, м), 7,53-7,51 (1H, м), 7,45-7,38 (2H, м), 4,26 (1H, д), 3,91 (3H, с), 3,88 (1H, д), 3,82-3,78 (1H, м), 3,59-3,55 (1H, м), 2,84-2,71 (2H, м).
Затем представлен пример композиции. Термин «часть(и)» означает массовую часть(и). Соединения в соответствии с данным изобретением представлены соединениями, номера которых указаны выше.
Пример композиции 1
Девять частей любого из данных соединений (1)-(10) растворяют в смеси 37,5 частей ксилола и 37,5 частей N,N-диметилформамида. К смеси добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 2
Пять частей данного соединения (1) и 4 части соединения, выбранного из представленной ниже группы [A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Группа [A]:
фосфид алюминия, бутатиофос, кадузафос, хлорэтоксифос, хлорфенвинфос, хлорпирифос, хлорпирифос-метил, цианофос (CYAP), диазинон, DCIP (дихлордиизопропиловый эфир), дихлофентион (ECP), дихлорвос (DDVP), диметоат, диметилвинфос, дисульфотон, EPN, этион, этопрофос, этримфос, фентион (MPP), фенитротион (MEP), фостиазат, формотион, гидрофосфид, изофенфос, изоксатион, малатион, мезулфенфос, метидатион (DMTP), монокротофос, налед (BRP), оксидепрофос (ESP), паратион, фозалон, фосмет (PMP), пиримфос-метил, пиридафентион, квиналфос, фентоат (PAP), профенофос, пропафос, протиофос, пираклофос, салитион, сульпрофос, тебупиримфос, темефос, тетрахлорвинфос, тербуфос, тиометон, трихлорфон (DEP), вамидотион, форат, кадузафос;
аланикарб, бендиокарб, бенфуракарб, BPMC, карбарил, карбофуран, карбосульфан, клоэтокарб, этиофенкарб, фенобукарб, фенотиокарб, феноксикарб, фуратиокарб, изопрокарб (MIPC), метолкарб, метомил, метиокарб, NAC, оксамил, пиримикарб, пропоксур (PHC), XMC, тиодикарб, ксилилкарб, алдикарб;
акринатрин, аллетрин, бета-цифлутрин, бифентрин, циклопротрин, цифлутрин, цигалотрин, эмпентрин, дельтаметрин, эсфенвалерат, этофенпрокс, фенвалерат, флуцитринат, флуфенопрокс, флуметрин, флувалинат, галфенпрокс, имипротрин, праллетрин, пиретрины, ресметрин, сигма-циперметрин, силафлуофен, тефлутрин, тралометрин, трансфлутрин, тетраметрин, лямбда-цигалотрин, гамма-цигалотрин, фураметрин, тау-флувалинат, 2,3,5,6-тетрафтор-4-метилбензил 2,2-диметил-3-(1-пропенил)циклопропанкарбоксилат, 2,3,5,6-тетрафтор-4-(метоксиметил)бензил 2,2-диметил-3-(2-метил-1-пропенил)циклопропанкарбоксилат, 2,3,5,6-тетрафтор-4-(метоксиметил)бензил 2,2-диметил-3-(2-циано-1-пропенил)циклопропанкарбоксилат, 2,3,5,6-тетрафтор-4-(метоксиметил)бензил 2,2,3,3-тетраметилциклопропанкарбоксилат;
картап, бенсультап, тиоциклам, моносультап, бисультап;
имидаклоприд, нитенпирам, ацетамиприд, тиаметоксам, тиаклоприд;
хлорфлуазурон, бистрифлурон, диафентиурон, дифлубензурон, флуазурон, флуциклоксурон, флуфеноксурон, гексафлумурон, луфенурон, новалурон, новифлумурон, тефлубензурон, трифлумурон, триазурон;
ацетопрол, фипронил, ванилипрол, пирипрол, пирафлупрол;
хромафенозид, галофенозид, метоксифенозид, тебуфенозид;
алдрин, диелдрин, диенохлор, эндосульфан, метоксихлор;
сульфат никотина;
авермектин-B, бромпропилат, бупрофезин, хлорфенапир, циромазин, D-D (1,3-дихлорпропен), эмамектин-бензоат, феназаквин, флупиразофос, гидропрен, метопрен, индоксакарб, метоксадиазон, милбемицин-A, пиметрозин, пиридалил, спиносад, сульфлурамид, толфенпирад, триазамат, флубендиамид, лепимектин, мышьяковая кислота, бенклотиаз, цианамид кальция, полисульфид кальция, хлордан, ДДТ, DSP, флуфенерим, флоникамид, флуримфен, форметанат, метам-аммоний, метам-натрий, метилбромид, олеат калия, протрифенбут, спиромесифен, сера, метафлумизон, спиротетрамат, пирифлуквиназон, спинеторам, хлорантранилипрол, тралопирил,
соединение, представленное формулой (A):
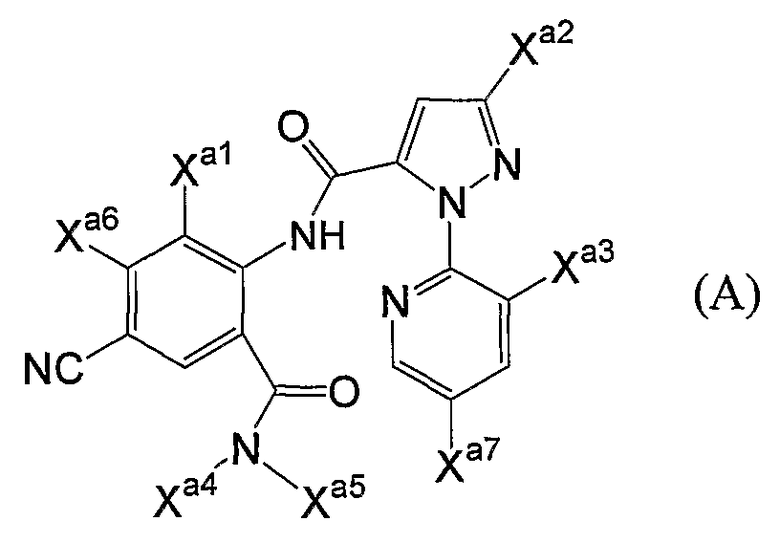
где Xa1 является метильной группой, атомом хлора, атомом брома или атомом фтора, Xa2 является атомом фтора, атомом хлора, атомом брома, C1-C4 галогеналкильной группой или C1-C4 галогеналкоксигруппой, Xa3 является атомом фтора, атомом хлора или атомом брома, Xa4 является необязательно замещенной C1-C4 алкильной группой, необязательно замещенной C3-C4 алкенильной группой, необязательно замещенной C3-C4 алкинильной группой, необязательно замещенной C3-C5 циклоалкилалкильной группой или атомом водорода, Xa5 является атомом водорода или метильной группой, Xa6 является атомом водорода, атомом фтора или атомом хлора, и Xa7 является атомом водорода, атомом фтора или атомом хлора,
соединение, представленное формулой (B):
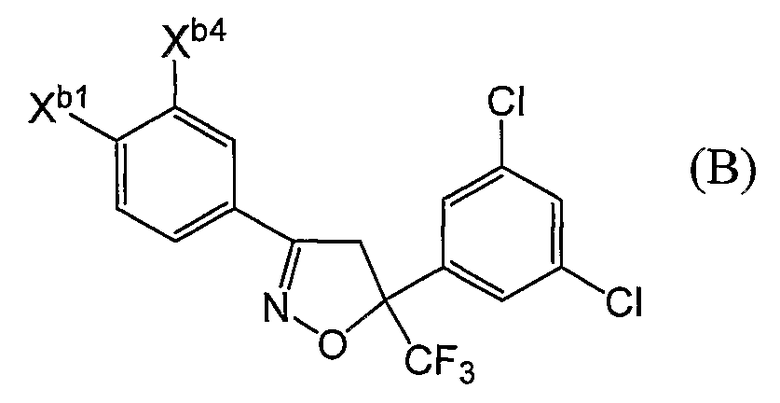
где Xb1 является Xb2-NH-C(=O) группой, Xb2-C(=O)-NH-CH2 группой, Xb3-S(O) группой, необязательно замещенной пиррол-1-ильной группой, необязательно замещенной имидазол-1-ильной группой, необязательно замещенной пиразол-1-ильной группой или необязательно замещенной 1,2,4-триазол-1-ильной группой, Xb2 является необязательно замещенной C1-C4 галогеналкильной группой, такой как 2,2,2-трифторэтильная группа, или необязательно замещенной C3-C6 циклоалкильной группой, такой как циклопропильная группа, Xb3 является необязательно замещенной C1-C4 алкильной группой, такой как метильная группа, и Xb4 является атомом водорода, атомом хлора, цианогруппой или метильной группой,
соединение, представленное формулой (C):

где Xc1 является необязательно замещенной C1-C4 алкильной группой, такой как 3,3,3-трифторпропильная группа, необязательно замещенной C1-C4 алкоксигруппой, такой как 2,2,2-трихлорэтоксигруппа, или необязательно замещенной фенильной группой, такой как 4-цианофенильная группа, или необязательно замещенной пиридильной группой, такой как 2-хлор-3-пиридильная группа, Xc2 является метильной группой или трифторметилтиогруппой, и Xc3 является метильной группой или атомом галогена,
ацеквиноцил, амитраз, бензоксимат, бифеназат, бромпропилат, хинометионат, хлорбензилат, CPCBS (хлорфенсон), клофентезин, цифлуметофен, кельтан (дикофол), фенбутатина оксид, фенотиокарб, фенпироксимат, флуакрипирим, флупроксифен, гекситиазокс, пропаргит (BPPS), пиридабен, пиримидифен, тебуфенпирад, тетрадифон, спиродиклофен, спиромезифен, спиротетрамат, амидофлумет и циенопирафен.
Пример композиции 3
Пять частей данного соединения (2) и 4 части соединения, выбранного из группы
[A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 4
Пять частей данного соединения (3) и 4 части соединения, выбранного из группы
[A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 5
Пять частей данного соединения (4) и 4 части соедиенния, выбранного из группы
[A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 6
Пять частей данного соединения (5) и 4 части соединения, выбранного из группы
[A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 7
Пять частей данного соединения (6) и 4 части соединения, выбранного из группы
[A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 8
Пять частей данного соединения (7) и 4 части соединения, выбранного из группы
[A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 9
Пять частей данного соединения (8) и 4 части соединения, выбранного из группы
[A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 10
Пять частей данного соединения (9) и 4 части соединения, выбранного из группы
[A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 11
Пять частей данного соединения (10) и 4 части соединения, выбранного из группы [A], растворяют в 37,5 частях ксилола и 37,5 частях N,N-диметилформамида. К раствору добавляют 10 частей стирилфенилового эфира полиоксиэтилена и 6 частей додецилбензолсульфоната кальция и тщательно смешивают с получением эмульгируемого концентрата.
Пример композиции 12
Пять частей SORPOL 5060 (зарегистрированное торговое наименование для TOHO Chemical Industry Co., LTD.) добавляют к 40 частям любого из данных соединений (1)-(10) и тщательно смешивают. Затем добавляют 32 части CARPLEX #80 (зарегистрированное торговое наименование для Shionogi & Co., Ltd., порошок синтетической безводной окиси кремния) и 23 части 300 меш диатомовой земли, и смешивают в миксере с получением смачиваемого порошка.
Пример композиции 13
Три части любого из данных соединений (1)-(10), 5 частей порошка синтетического водного оксида кремния, 5 частей додецилбензолсульфоната натрия, 30 частей бентонита и 57 частей глины тщательно смешивают. К этой смеси добавляют подходящее количество воды. Смесь далее перемешивают, гранулируют с применением гранулятора и затем сушат на воздухе с получением гранул.
Пример композиции 14
4,5 части любого из данных соединений (1)-(10), 1 часть порошка синтетического водного оксида кремния, 1 часть Dorires B (производства Sankyo) в качестве хлопьеобразующего агента, и 7 частей глины тщательно смешивают в ступе и затем в миксере. К полученной смеси добавляют 86,5 частей измельченной глины и тщательно смешивают с получением тонкоизмельченного порошка.
Пример композиции 15
Десять частей любого из данных соединений (1)-(10), 35 частей смеси белой сажи с аммониевой солью сульфата полиоксиэтиленалкилового эфира (массовое соотношение 50/50) и 55 частей воды смешивают и измельчают методом мокрого измельчения с получением композиции.
Пример композиции 16
0,5 части любого из данных соединений (1)-(10) растворяют в 10 частях дихлорметана. Этот раствор смешивают с 89,5 частями Isopar M (изопарафин: зарегистрированное торговое наименование для Exxon Chemical) с получением масляного раствора.
Пример композиции 17
0,1 части любого из данных соединений (1)-(10) и 49,9 частей NEO-TIOZOL (Chuo Kasei Co., Ltd.) помещают в аэрозольный баллончик. К баллончику крепят аэрозольный клапан, и затем в баллончик загружают 25 частей диметилового эфира и 25 частей LPG. К баллончику прикрепляют привод с получением масляного аэрозоля.
Пример композиции 18
Аэрозольный контейнер загружают 0,6 части любого из данных соединений (1)-(10), 0,01 части BHT, 5 частей ксилола, смесь 3,39 частей дезодорированного керосина и 1 часть эмульгирующего агента [Atmos 300 (зарегистрированное торговое наименование для Atmos Chemical Ltd.)] и 50 частей дистиллированной воды. Клапан прикрепляют к контейнеру, и контейнер затем загружают 40 частями газа-вытеснителя (LPG) через клапан при повышенном давлении с получением водного аэрозоля.
Пример композиции 19
Пять частей любого из данных соединений (1)-(10) растворяют в 80 частях моноэтилового эфира диэтиленгликоля. К смеси добавляют 15 частей пропиленкарбоната с получением жидкой композиции для точечного нанесения.
Пример композиции 20
Десять частей любого из данных соединений (1)-(10) растворяют в 70 частях моноэтилового эфира диэтиленгликоля. К смеси добавляют 20 частей 2-октилдодеканола с получением жидкой композиции для обмывания.
Пример композиции 21
К 0,5 части любого из данных соединений (1)-(10) добавляют 60 частей NIKKOL TEALS-42 (42% водный раствор лаурилсульфата триэтаноламина, Nikko Chemicals) и 20 частей пропиленгликоля. Смесь хорошо перемешивают с получением гомогенного раствора. К нему добавляют 19,5 частей воды и тщательно перемешивают с получением гомогенного шампуня.
Пример композиции 22
Пористую керамическую пластину длиной 4,0 см, шириной 0,4 см и толщиной 1,2 см пропитывают раствором 0,1 г любого из данных соединений (1)-(10) в 2 мл пропиленгликоля с получением нагреваемого дымящего пестицида.
Пример композиции 23
Пять частей любого из данных соединений (1)-(10) и 95 частей этилен-метилметакрилатного сополимера (доля метилметакрилата в сополимере: 10 мас.%, ACRYFT WD301, Sumitomo Chemical) плавят и смешивают в герметично закрытой месильной машине под давлением (Moriyama Manufacturing Co., Ltd.). Полученный перемешанный продукт экструдируют через пресс-форму с применением экструдера с получением формованного бруска длиной 15 см и диаметром 3 мм.
Пример композиции 24
Пять частей любого из данных соединений (1)-(10) и 95 частей гибкого поливинилхлоридного полимера плавят и перемешивают в герметично закрытой месильной машине под давлением (Moriyama Manufacturing Co., Ltd.). Полученный перемешанный продукт экструдируют через пресс-форму с применением экструдера с получением формованного бруска длиной 15 см и диаметром 3 мм.
Далее представлены экспериментальные примеры, показывающие эффективность соединения в соответствии с данным изобретением в качестве активного ингредиента пестицидной композиции.
Экспериментальный пример 1
Композицию любого из данных соединений (1)-(10), полученных по методике примера композиции 15, разводят таким образом, что концентрация активного ингредиента составляет 500 ч./млн. с получением тестируемого раствора.
Одновременно, 50 г культурной почвы, Bonsol №2 (производства Sumitomo Chemical Co., Ltd.), помещают в полиэтиленовый стакан и туда сажают 10-15 семян риса. Растения риса выращивают до появления второго листа и затем срезают таким образом, чтобы все растения имели одинаковую высоту, 5 см. Тестируемый раствор распыляют на рисовые растения в количестве 20 мл/стакан. После распыления тестируемого раствора рисовые растения сушат, рисовые растения помещают в пластиковый стакан для предотвращения ухода тестируемых гусениц. Тридцать личинок первой стадии зрелости рисовой дельфациды выпускают в стакан и стакан накрывают крышкой. Затем стакан помещают в теплицу при 25°C на 6 дней. Затем изучают количество рисовых дельфацид, паразитирующих на рисовых растениях.
В результате на растениях, обработанных любым из представленных соединений (1), (2), (3), (4), (5) и (6), количество паразитов составляло 3 или менее.
Экспериментальный пример 2
Композицию любого из данных соединений (1)-(10), полученных по методике примера композиции 15, разводят таким образом, что концентрация активного ингредиента составляет 55,6 ч./млн. с получением тестируемого раствора.
Одновременно, 50 г культурной почвы, Bonsol №2 (производства Sumitomo Chemical Co., Ltd.), помещают в полиэтиленовый стакан с пятью отверстиями диаметром 5 мм на дне и туда сажают 10-15 семян риса. Растения риса выращивают до появления второго листа и затем обрабатывают 45 мл тестируемого раствора, позволяя растениям абсорбировать тестируемый раствор со дна стакана. Рисовые растения помещают в теплицу при 25°С на 6 дней и затем срезают таким образом, чтобы все растения имели одинаковую высоту, 5 см. Тридцать личинок первой стадии зрелости рисовой дельфациды выпускают в теплицу при 25°C на 6 дней. Затем изучают количество рисовых дельфацид, паразитирующих на рисовых растениях.
В результате на растениях, обработанных любым из представленных соединений (1), (2), (3), (4), (5), (6) и (7) количество паразитов составляло 3 или менее.
Экспериментальный пример 3
Композицию любого из данных соединений (1)-(10), полученных по методике примера композиции 15, разводят водой таким образом, что концентрация активного ингредиента составляет 500 ч./млн. с получением тестируемого раствора.
Фильтровальную бумагу диаметром 5,5 см расстилают на дне полиэтиленового стакана диаметром 5,5 см и на фильтровальную бумагу по каплям добавляют 0,7 мл тестируемого раствора. В качестве приманки на фильтровальную бумагу равномерно кладут 30 мг сахарозы. В полиэтиленовый стакан выпускают 10 взрослых самок Musca domestica и стакан закрывают крышкой. Через 24 часа определяют количество выживших Musca domestica и рассчитывают процент гибели вредителей.
В результате обработка любым их представленных соединений (1), (3), (4) и (5) показала процент гибели 90% или более. Обработка любым из данных соединений (2) и (10) показала процент гибели 40% или более.
Экспериментальный пример 4
Композицию любого из данных соединений (1)-(10), полученных по методике примера композиции 15, разводят водой таким образом, что концентрация активного ингредиента составляет 500 ч./млн. с получением тестируемого раствора.
Фильтровальную бумагу диаметром 5,5 см расстилают на дне полиэтиленового стакана диаметром 5,5 см, и на фильтровальную бумагу по каплям добавляют 0,7 мл тестируемого раствора. В качестве приманки на фильтровальную бумагу равномерно кладут 30 мг сахарозы. В полиэтиленовый стакан выпускают 2 взрослых самцов Blattalla germanica и стакан закрывают крышкой. Через 6 дней определяют количество выживших Blattalla germanica и рассчитывают процент гибели вредителей.
В результате обработка любым их представленных соединений (1), (2), (3), (4) и (5) показала процент гибели 100%. Обработка данным соединением (9) показала процент гибели 50% или более.
Экспериментальный пример 5
Композицию любого из данных соединений (1)-(10), полученных по методике примера композиции 15, разводят водой таким образом, что концентрация активного ингредиента составляет 500 ч./млн. с получением тестируемого раствора.
К 100 мл ионообменной воды добавляют 0,7 мл тестируемого раствора (концентрация активного ингредиента: 3,5 ч./млн.). В раствор выпускают 20 личинок в последней стадии развития Culex pipiens pallens. Через один день определяют количество выживших Culex pipiens pallens и рассчитывают процент гибели вредителей.
В результате обработка любым их представленных соединений (1), (3), (4), (5), (6) и (10) показала процент гибели 95% или более. Обработка любым из данных соединений (6), (7) и (9) показала процент гибели 10% или более.
Экспериментальный пример 6
В этом экспериментальном примере, в качестве сравнительного соединения применяют соединение, описанное в JP-A 2005-179321 (Соединение № 37 в таблице 2) и представленное формулой:
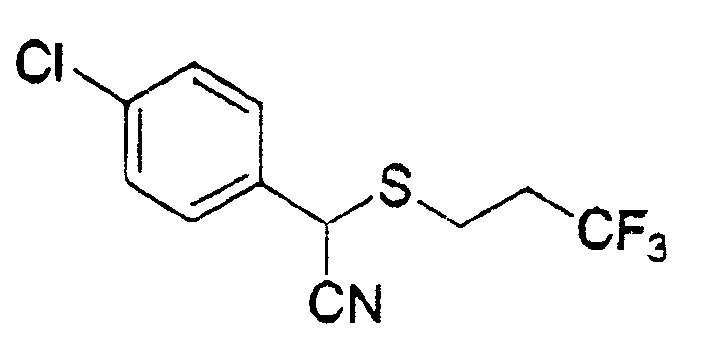
(далее обозначенное как сравнительное соединение (1)).
Каждую композицию данного соединения (6) и сравнительного соединения (1) получают по методике примера композиции 15. Композицию разводят таким образом, что концентрация активного ингредиента составляет 175 ч./млн. с получением тестируемого раствора.
Одновременно, 50 г культурной почвы, Bonsol №2 (производства Sumitomo Chemical Co., Ltd.), помещают в полиэтиленовый стакан и туда сажают 10-15 семян риса. Растения риса выращивают до появления второго листа, и затем срезают таким образом, чтобы все растения имели одинаковую высоту, 5 см. Тестируемый раствор распыляют на рисовые растения в количестве 20 мл/стакан. После распыления тестируемого раствора рисовые растения сушат, рисовые растения помещают в пластиковый стакан для предотвращения ухода тестируемых гусениц. Тридцать личинок первой стадии зрелости рисовой дельфациды выпускают в стакан, и стакан накрывают крышкой. Затем стакан помещают в теплицу при 25°C на 6 дней. Затем изучают количество рисовых дельфацид, паразитирующих на рисовых растениях.
В результате на растениях, обработанных любым из представленных соединений (6), количество паразитов составляло 3 или менее. На растениях, обработанных сравнительным соединением (1), количество паразитирующих вредителей было 21 или более.
Промышленная применимость
Соединение в соответствии с данным изобретением обладает превосходным контролирующим действием на членистоногих вредителей, и таким образом, может применяться в качестве активного ингредиента для пестицидной композиции.


































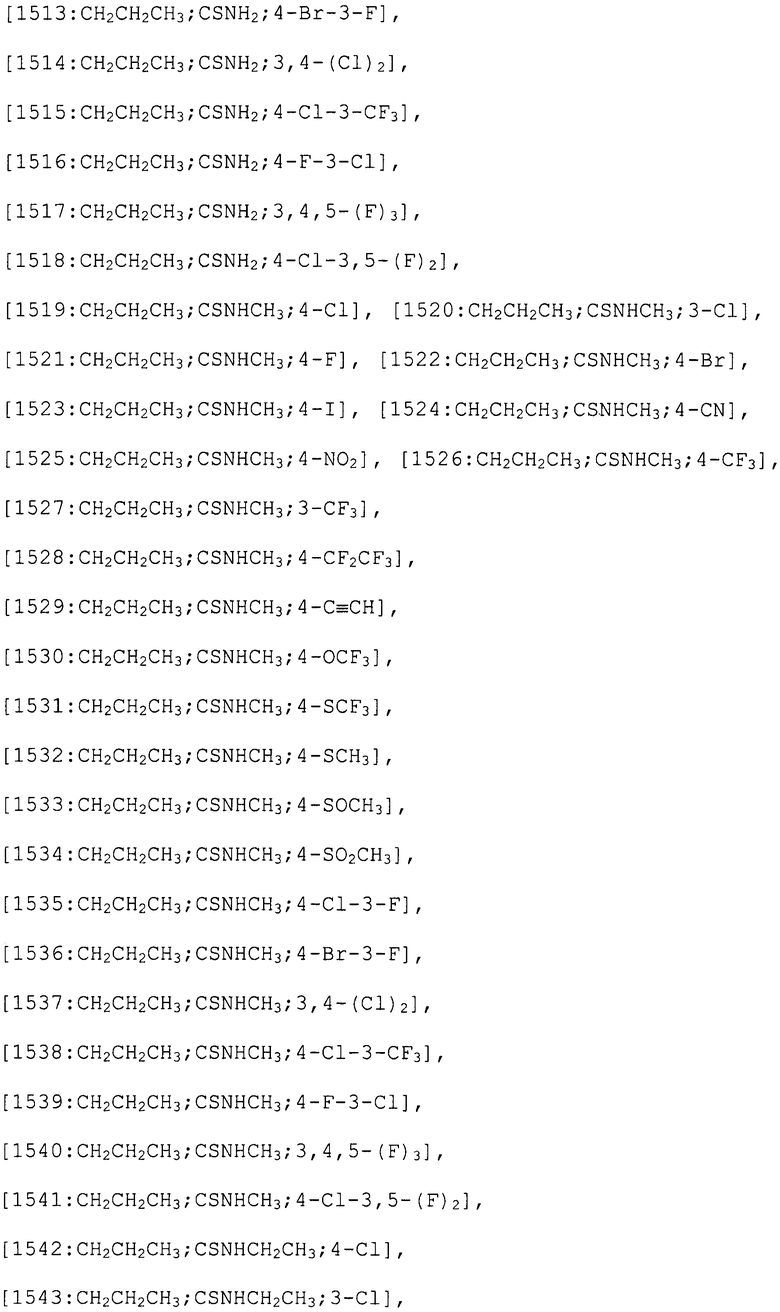










Изобретение относится к фторсодержащему сераорганическому соединению, представленному формулой (I):
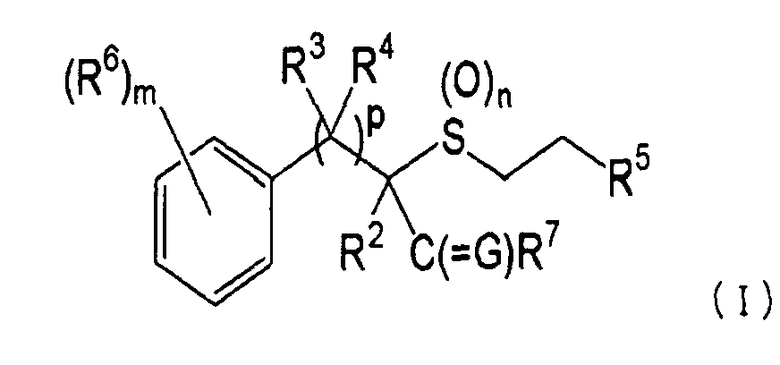 , где G является атомом кислорода; R2 является атомом галогена, атомом водорода, или С1-С4 алкилом; R3 и R4 независимо являются атомом водорода; R5 является С1-С5 гапогеналкильной группой, содержащей, по меньшей мере, один атом фтора; R6 является атомом галогена или -(G1)q-R8 группой; R7 является аминогруппой; R8 является С1-С4 алкилом, который замещен атомом галогена; m равно целому числу от 1 до 3, при условии, что R6 необязательно являются одинаковыми или отличными друг от друга, если m равно от 2 до 3; n равно целому числу 0 или 2; p равно 0; q равно 0; и G1 является атомом кислорода, атомом серы, -SO-группой или -SO2-группой. Изобретение также относится к пестицидной композиции на основе указанных соединений. Технический результат: получены новые соединения, которые могут найти применение в сельском хозяйстве для борьбы с членистоногими вредителями. 3 н. и 2 з.п. ф-лы, 10 пр.
, где G является атомом кислорода; R2 является атомом галогена, атомом водорода, или С1-С4 алкилом; R3 и R4 независимо являются атомом водорода; R5 является С1-С5 гапогеналкильной группой, содержащей, по меньшей мере, один атом фтора; R6 является атомом галогена или -(G1)q-R8 группой; R7 является аминогруппой; R8 является С1-С4 алкилом, который замещен атомом галогена; m равно целому числу от 1 до 3, при условии, что R6 необязательно являются одинаковыми или отличными друг от друга, если m равно от 2 до 3; n равно целому числу 0 или 2; p равно 0; q равно 0; и G1 является атомом кислорода, атомом серы, -SO-группой или -SO2-группой. Изобретение также относится к пестицидной композиции на основе указанных соединений. Технический результат: получены новые соединения, которые могут найти применение в сельском хозяйстве для борьбы с членистоногими вредителями. 3 н. и 2 з.п. ф-лы, 10 пр.
1. Фторсодержащее сераорганическое соединение, представленное формулой (I):
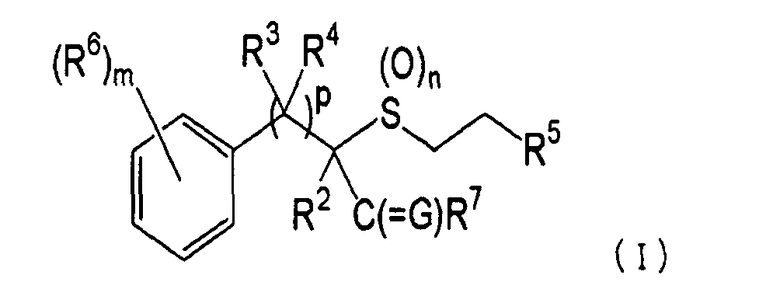
где G является атомом кислорода;
R2 является атомом галогена, атомом водорода, или С1-С4 алкилом;
R3 и R4 независимо являются атомом водорода;
R5 является С1-С5 галогеналкильной группой, содержащей, по меньшей мере, один атом фтора;
R6 является атомом галогена или -(G1)q-R8 группой;
R7 является аминогруппой;
R8 является С1-С4 алкилом, который замещен атомом галогена;
m равно целому числу от 1 до 3, при условии, что R6 необязательно являются одинаковыми или отличными друг от друга, если m равно от 2 до 3;
n равно целому числу 0 или 2;
p равно 0;
q равно 0; и
G1 является атомом кислорода, атомом серы, -SO-группой или -SO2-группой.
2. Фторсодержащее сераорганическое соединение по п.1, где R2 является атомом галогена.
3. Фторсодержащее сераорганическое соединение по п.1, где n равно 2.
4. Пестицидная композиция, содержащая фторсодержащее сераорганическое соединение по любому из пп.1-3 в качестве активного ингредиента и носитель.
5. Способ борьбы с членистоногими вредителями, который включает нанесение эффективного количества фторсодержащего сераорганического соединения по любому из пп.1-3 на членистоногих вредителей или место обитания членистоногих вредителей.
| JP 2005179321 А, 07.07.2005 | |||
| ПРОИЗВОДНОЕ БЕНЗИЛСУЛЬФИДА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПЕСТИЦИД | 1996 |
|
RU2170728C2 |
Авторы
Даты
2013-03-27—Публикация
2008-07-25—Подача