Область изобретения
Настоящее изобретение относится к визуализирующим агентам, подходящим для оптической визуализации in vivo, которые включают конъюгаты бензопирилиевых красителей с группировками, обеспечивающими направленную доставку к биологической мишени, такими как пептиды. Также раскрыты фармацевтические композиции и наборы и способы визуализации in vivo.
Предшествующий уровень техники
В US 6750346 раскрыты совместимые с лазером маркерные красители для ближней инфракрасной области спектра (NIR) формул А, В или С:
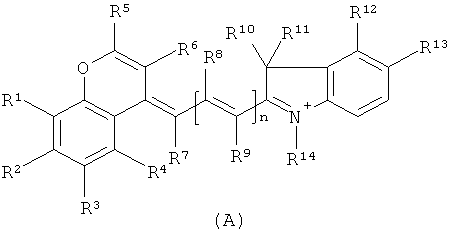 ,
,
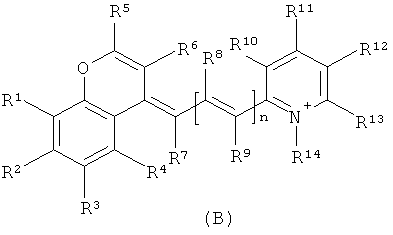 ,
,
 ,
,
где:
n равно 1, 2 или 3;
R1-R14 являются одинаковыми или разными и выбраны из Н, Cl, Br; алифатической или одноядерной ароматической группы из до 12 атомов углерода, которая может содержать в качестве замещаемой группы в дополнение к С и Н до 4 атомов кислорода и 0, 1 или 2 атома азота, или атом серы, или атом серы и азота; или может представлять собой аминофункциональную группу, имеющую атом азота, с которым происходит связывание, Н или по меньшей мере один заместитель, имеющий до 8 атомов углерода, при этом указанный заместитель выбран из группы, состоящей из С, Н и до двух сульфокислотных групп.
Красители, описанные в US 6750346, выбраны таким образом, что предпочтительно по меньшей мере один из R1-R14 содержит солюбилизирующую или ионизируемую группу. Считают, что такие группы включают: циклодекстрин, сахар, 
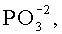
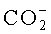
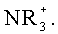
В US 6924372 раскрыты асимметрические полиметиновые красители формулы D или Е:
 ,
,
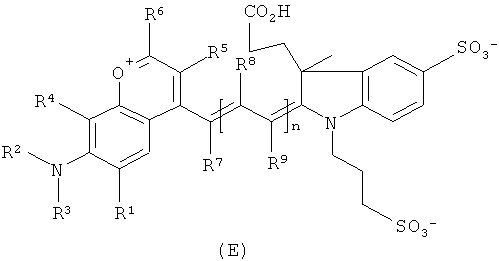 ,
,
где:
n равно 0, 1, 2 или 3;
R1-R9 являются одинаковыми или разными и могут представлять собой Н, остатки алкил-, трет-алкил, арил-, карбоксиарил-, дикарбоксиарил, гетероарил-, циклоалкил-, гетероциклоалкил-, алкилокси-, алкилмеркапто- (где "алкил" и "циклоалкил" также включают остатки с олефиновой связью), арилокси-, арилмеркапто-, гетероарилокси-, гетероарилмеркапто-, гидрокси-, нитро- или циано и R1 и R2, R2 и R3, R3 и R4, R5 и R7 могут образовывать одно или более чем одно алифатическое, гетероалифатическое или ароматическое кольцо.
По меньшей мере один из заместителей R1-R9, описанных в US 6924372, возможно может представлять собой солюбилизирующий или ионизирующий заместитель (например, 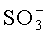

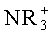
Lisy et al. (J. Biomed. Optics, 11(6), 064014 (2006)) раскрыт способ диагностики перитонита с использованием оптической визуализации в ближней инфракрасной области спектра и меченых моноцитов или макрофагов. Моноциты-макрофаги могут быть мечены in vitro красителем DY-676 (Dyomics GmbH). Введение самого красителя DY-676 в животную модель перитонита in vivo привело к повышенной флуоресценции в области перитонита. Авторы сделали вывод, что мечение моноцитов-макрофагов имело место in vivo.
В Lisy et al. (Invest. Radiol., 42(4), 235-241 (2007)) раскрыты бимодальные контрастные агенты для магнитно-резонансной визуализации (MRI) и оптической визуализации, которые включают наночастицы, меченные флуоресцентными магнетосомами. Флуоресцентные магнетосомные наночастицы использовали для мечения макрофагов посредством фагоцитоза. Краситель, использованный для мечения магнетосом, представлял собой DY-676.
Веб-сайт Dyomics GmbH (www.dyomics.com) содержит бесплатную копию I.Hilger (FSU Jena), озаглавленную "Visualisation of Arthritis in a Rat by Accumulation of DY-676 in Joints". Никаких дополнительных подробностей не приведено.
В WO 2007/139815 раскрыты способы визуализации и терапевтические способы, в которые вовлечены клетки-предшественники. Раскрыты конъюгаты следующей формулы:
AB-X,
где:
AB включает витамин или аналог, который связывается с CD133+ Flk1+ эндотелиальными клетками-предшественниками;
Х представляет собой количественно измеряемый маркер.
Количественно измеряемый маркер может представлять собой, например, радиоактивный зонд или флуоресцентный зонд. Утверждают, что подходящими флуоресцентными зондами являются: флуоресцеин, родамин, техасский красный (Texas Red), фикоэритрин, Орегон зеленый (Oregon Green), Alexa Fluor 488…, Су3, Су5, Су7 и тому подобное. В примере 30 WO 2007/139815 раскрыт единственный бензопирилиевый краситель (DyLight™ 680), конъюгированный с фолатом посредством 5-мерного пептидного линкера (Asp-Arg-Asp-Asp-Cys).
Настоящее изобретение
Согласно настоящему изобретению предложены визуализирующие агенты, подходящие для оптической визуализации in vivo, которые включают конкретный класс бензопирилиевого красителя, конъюгированного с группировкой, обеспечивающей направленную доставку к биологической мишени (ВТМ). В качестве части таких ковалентно-связанных ВТМ-конъюгатов авторы настоящего изобретения идентифицировали сульфонированные бензопирилиевые красители, подходящие для применений в оптической визуализации in vivo.
Бензопирилиевые красители (BzpM) по настоящему изобретению обладают комбинацией свойств, которые делают их полезными для применений в оптической визуализации in vivo:
(1) способностью к конъюгации с молекулами, обеспечивающими направленную доставку к биологической мишени (ВТМ);
(2) растворимостью в воде;
(3) поглощением и эмиссией в красной, дальней красной или ближней инфракрасной области электромагнитного спектра;
(4) высокими коэффициентами экстинкции;
(5) низким связыванием с белками плазмы крови;
(6) высокой фотостабильностью и яркостью;
(7) высокой стабильностью красителя и конъюгата краситель-ВТМ в крови;
(8) быстрым выведением из крови in vivo;
(9) отсутствием потенциально опасных метаболитов (согласно Meteor/Derek анализам).
Подробное описание изобретения
В первом аспекте настоящего изобретения предложена фармацевтическая композиция, содержащая визуализирующий агент, подходящий для оптической визуализации in vivo организма млекопитающего, вместе с биосовместимым носителем, причем указанная композиция находится в форме, подходящей для введения млекопитающему, где указанный визуализирующий агент включает конъюгат формулы I:
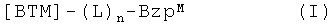 ,
,
где:
ВТМ представляет собой группировку, обеспечивающую направленную доставку к биологической мишени;
n представляет собой целое число величиной 0 или 1;
L представляет собой синтетическую линкерную группу формулы -(А)m-, где m представляет собой целое число величиной от 1 до 20, и каждый А независимо представляет собой -CR2-, -CR=CR-, -C≡C-, -CR2CO2-, -CO2CR2-, -NRCO-, -CONR-, -NR(C=O)NR-, -NR(C=S)NR-, -SO2NR-, -NRSO2-, -CR2OCR2-, -CR2SCR2-, -CR2NRCR2-, С4-8циклогетероалкиленовую группу, С4-8циклоалкиленовую группу, С5-12ариленовую группу или С3-12гетероариленовую группу, аминокислоту, сахар или монодисперсный полиэтиленгликолевый (ПЭГ) строительный блок; где каждый R независимо выбран из Н, С1-4алкила, С2-4алкенила, С2-4алкинила, С1-4алкоксиалкила или С1-4гидроксиалкила;
BzpM представляет собой бензопирилиевый краситель формулы II
 ,
,
где:
Y1 представляет собой группу формулы Ya или Yb
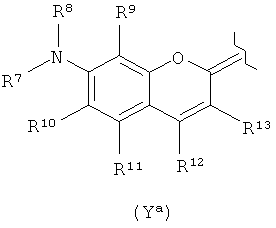
 ,
,
R1-R4 и R9-R13 независимо выбраны из Н, -SO3M1, Hal, Ra или С3-12арила, где каждый М1 независимо представляет собой Н или Bc, и Bc представляет собой биосовместимый катион;
R5 представляет собой Н, С1-4алкил, C1-6карбоксиалкил, С3-12арил-сульфонил, Cl или R5 вместе с одним из R6, R14, R15 или R16 возможно может образовывать 5- или 6-членное ненасыщенное алифатическое, ненасыщенное гетероалифатическое или ароматическое кольцо;
R6 и R16 независимо представляют собой группы Ra;
R7 и R8 независимо представляют собой С1-4алкил, С1-4сульфоалкил или C1-6гидроксиалкил или возможно вместе с одним или обоими R9 и/или R10 могут образовывать 5- или 6-членное N-содержащее гетероциклическое или гетероарильное кольцо;
Х представляет собой -CR14R15-, -O-, -S-, -Se-, -NR16- или -СН=СН-, где R14-R16 независимо представляют собой группы Ra;
Ra представляет собой С1-4алкил, С1-4сульфоалкил, C1-6карбоксиалкил или C1-6гидроксиалкил;
w равно 1 или 2;
J представляет собой биосовместимый анион;
при условии, что BzpM содержит по меньшей мере один сульфокислотный заместитель, выбранный из групп R1-R16.
Под термином "визуализирующий агент" понимают соединение, подходящее для оптической визуализации, представляющей интерес области целого (то есть интактного) организма млекопитающего in vivo. Предпочтительно, млекопитающим является человек. Визуализация может быть инвазивной (например, проводимой во время операции или эндоскопической) или неинвазивной. Визуализация возможно может быть использована для содействия биопсии (например, через биопсийный канал в эндоскопическом инструменте) или резекции опухоли (например, во время интраоперационных процедур посредством идентификации границ опухоли).
Под термином "оптическая визуализация" понимают любой способ, который формирует изображение для детекции, определения стадии или диагностики заболевания, слежения за развитием заболевания или для слежения за лечением заболевания, основанный на взаимодействии со светом в диапазоне от зеленой до ближней инфракрасной области спектра (длина волны 500-1200 нм). Оптическая визуализация также включает все способы, начиная от непосредственной визуализации без использования какого-либо устройства и включая применение устройств, таких как различные оптические приборы, катетеры и оборудование для оптической визуализации, например, управляемое с помощью компьютера оборудование для томографических изображений. Способы и методики измерения включают: люминесцентную визуализацию; эндоскопию; флуоресцентную эндоскопию; оптическую когерентную томографию; визуализацию пропускания (transmittance imaging); визуализацию пропускания с временным разрешением (time resolved transmittance imaging); конфокальную визуализацию; нелинейную микроскопию; фотоакустическую визуализацию; акустико-оптическую визуализацию; спектроскопию; отражательную спектроскопию; интерферометрию; когерентную интерферометрию; диффузную оптическую томографию и опосредованную флуоресценцией диффузную оптическую томографию (системы непрерывной волны, временной области и частотной области) и измерение рассеяния света, поглощения, поляризации, люминесценции, продолжительности флуоресценции, квантового выхода и гашения, но не ограничиваются ими. Дополнительные подробности этих методик представлены в: Tuan Vo-Dinh (редактор): "Biomedical Photonics Handbook" (2003), CRC Press LCC; Mycek & Pogue (редакторы): "Handbook of Biomedical Fluorescence" (2003), Marcel Dekker, Inc.; Splinter & Hopper: "An Introduction to Biomedical Optics" (2007), CRC Press LCC.
Свет в диапазоне от зеленой до ближней инфракрасной области спектра соответствует длине волны 500-1200 нм, предпочтительно длине волны 550-1000 нм, наиболее предпочтительно 600-800 нм. Метод оптической визуализации предпочтительно представляет собой флуоресцентную эндоскопию. Организмом млекопитающего в шестом аспекте предпочтительно является организм человека. Предпочтительными воплощениями визуализирующего агента являются агенты, описанные для первого аспекта (выше). В частности, предпочтительно, чтобы используемый краситель BzpM был флуоресцентным.
Под термином "биосовместимый носитель" понимают текучую среду, особенно жидкость, в которой визуализирующий агент можно суспендировать или растворять таким образом, чтобы композиция была физиологически приемлемой, то есть ее можно было вводить в организм млекопитающего без токсичности или чрезмерного дискомфорта. Биосовместимым носителем является подходящим образом инъецируемая жидкость-носитель, такая как стерильная, апирогенная вода для инъекций; водный раствор, такой как физиологический раствор (который предпочтительно может быть сбалансирован таким образом, чтобы конечный продукт для инъекции был изотоническим); водный раствор одного или более регулирующих тоничность веществ (например, солей катионов плазмы с биосовместимыми противоионами), сахаров (например, глюкозы или сахарозы), спиртов сахаров (например, сорбита или маннита), гликолей (например, глицерина) или других неионных высокомолекулярных спиртов (например, полиэтиленгликолей, пропиленгликолей и тому подобного). Предпочтительно, биосовместимым носителем является апирогенная вода для инъекций или изотонический физиологический раствор.
Под термином "конъюгат" понимают, что ВТМ, группа (L)n и краситель BzpM соединены ковалентными связями.
Хотя конъюгат формулы I подходит для визуализации in vivo, он также может находить применения in vitro (например, в анализах количественного определения ВТМ в биологических образцах или для визуализации ВТМ в образцах тканей). Предпочтительно, визуализирующий агент используют для визуализации in vivo.
Под термином "сульфокислотный заместитель" понимают заместитель формулы -SO3M1, где М1 представляет собой Н или Bc, и Bc представляет собой биосовместимый катион. Заместитель -SO3M1 ковалентно связан с атомом углерода, и этот атом углерода может быть арильным (то есть сульфоарильным, как например, когда R1 или R2 представляет собой -SO3M1) или алкильным (то есть в сульфоалкильной группе). Под термином "биосовместимый катион" (Bc) понимают положительно заряженный противоион, который образует соль с ионизированной, отрицательно заряженной группой (в данном случае сульфонатной группой), где указанный положительно заряженный противоион также является нетоксичным и, следовательно, подходит для введения в организм млекопитающего, особенно организм человека. Примеры подходящих биосовместимых катионов включают: катионы щелочных металлов натрия или калия; щелочноземельных металлов кальция и магния и ион аммония. Предпочтительными биосовместимыми катионами являются катионы натрия и калия, наиболее предпочтительно натрия.
Под термином "биосовместимый анион" (J) понимают отрицательно заряженный противоион, который образует соль с ионизированной, положительно заряженной группой (в данном случае: индолиниевой группой), где указанный отрицательно заряженный противоион также является нетоксичным и, следовательно, подходит для введения в организм млекопитающего, особенно организм человека. Противоион (J-) представляет собой анион, который присутствует в эквимолярном количестве, уравновешивая, таким образом, положительный заряд на красителе BzpM. Соответственно, анион (J) является одно- или многозарядным при условии, что присутствует в уравновешивающем заряд количестве. Анион подходящим образом происходит из неорганической или органической кислоты. Примеры подходящих анионов включают: галогенид-ионы, такие как хлорид или бромид; сульфат; нитрат; цитрат; ацетат; фосфат и борат. Предпочтительным анионом является хлорид.
Под термином "группировка, обеспечивающая направленную доставку к биологической мишени" (ВТМ), понимают соединение, которое после введения в организм млекопитающего in vivo избирательно поглощается или располагается в конкретном месте организма указанного млекопитающего. Такие места, например, могут быть вовлечены в конкретное болезненное состояние и быть индикаторами того, как функционирует орган, или проходит метаболический процесс. Группировка, обеспечивающая направленную доставку к биологической мишени, предпочтительно включает 3-100-мерные пептиды, пептидные аналоги, пептоиды или пептидные миметики, которые могут быть линейными пептидами или циклическими пептидами, или их комбинациями; или субстраты ферментов, антагонисты ферментов или ингибиторы ферментов; синтетические рецептор-связывающие соединения; олигонуклеотиды или олиго-ДНК- или олиго-РНК-фрагменты.
Под термином "пептид" понимают соединение, содержащее две или более чем две аминокислоты, как они определены ниже, соединенные пептидной связью (то есть амидной связью, соединяющей амин одной аминокислоты с карбоксилом другой). Термин "пептидный миметик" или "миметик" относится к биологически активным соединениям, которые имитируют биологическую активность пептида или белка, но уже не являются пептидными по своей химической природе, то есть они уже не содержат никаких пептидных связей (то есть амидных связей между аминокислотами). В данном описании термин пептидный миметик используют в более широком смысле для включения молекул, которые уже не являются полностью пептидными по своей природе, таких как псевдопептиды, полупептиды и пептоиды. Термин "пептидный аналог" относится к пептидам, содержащим один или более чем один аминокислотный аналог, как они описаны ниже. Смотри также "Synthesis of Peptides and Peptidomimetics", M.Goodman et al., Houben-Weyl E22c, Thieme.
Под термином "аминокислота" понимают L- или D-аминокислоту, аминокислотный аналог (например, нафтилаланин) или аминокислотный миметик, которые могут быть природными или иметь чисто синтетическое происхождение и могут быть оптически чистыми, то есть представлять собой единичный энантиомер и, следовательно, быть хиральными, или смесь энантиомеров. В данном описании используют традиционные трехбуквенные или однобуквенные сокращения для аминокислот. Предпочтительно, аминокислоты по настоящему изобретению являются оптически чистыми. Под термином "аминокислотный миметик" понимают синтетические аналоги природных аминокислот, которые представляют собой изостеры, то есть разработаны с целью имитации пространственной и электронной структуры природного соединения. Такие изостеры хорошо известны специалистам в данной области техники и включают депсипептиды, ретроинверсопептиды, тиоамиды, циклоалканы или 1,5-дизамещенные тетразолы (смотри M.Goodman, Biopolymers, 24, 137 (1985)), но не ограничиваются ими.
Подходящие субстраты, антагонисты или ингибиторы ферментов включают глюкозу и аналоги глюкозы, такие как фтордезоксиглюкоза; жирные кислоты или ингибиторы эластазы, ангиотензина II или металлопротеиназы. Предпочтительным непептидным антагонистом ангиотензина II является лозартан. Подходящие синтетические рецептор-связывающие соединения включают эстрадиол, эстроген, прогестин, прогестерон и другие стероидные гормоны; лиганды для дофаминового D-1 или D-2 рецептора или транспортера дофамина, такие как тропаны; и лиганды для серотонинового рецептора. Если рецептор-связывающим соединением является фолат, то линкерная группа предпочтительно не будет содержать 5-мерный пептид Asp-Arg-Asp-Asp-Cys. В наиболее предпочтительном случае рецептор-связывающее соединение не представляет собой фолат.
Бензопирилиевый краситель (BzpM) формулы II представляет собой флуоресцентный краситель или хромофор, который можно детектировать либо непосредственно, либо опосредованно в процедуре оптической визуализации с использованием света в диапазоне от зеленой до ближней инфракрасной области спектра (длина волны 500-1200 нм, предпочтительно 550-1000 нм, более предпочтительно 600-800 нм). Предпочтительно, BzpM обладает флуоресцентными свойствами.
Предусматривается, что одна из ролей линкерной группы -(А)m- в формуле I заключается в дистанцировании BzpM от связывающего сайта ВТМ. Это особенно важно, поскольку BzpM является относительно объемным, поэтому возможны неблагоприятные стерические взаимодействия. Этого можно достичь посредством комбинирования гибкости (например, простых алкильных цепей), чтобы BzpM обладал степенью свободы для размещения в стороне от сайта связывания, и/или жесткости, например, циклоалкильного или арильного спейсера, который ориентирует BzpM в сторону от сайта связывания. Для модификации биораспределения визуализирующего агента также можно использовать природу линкерной группы. Так, например, введение в линкер простых эфирных групп поможет минимизировать связывание с белками плазмы. Если -(А)m- включает полиэтиленгликолевый (ПЭГ) строительный блок или пептидную цепь из 1-10 аминокислотных остатков, то такая линкерная группа может функционировать в качестве модифицирующей фармакокинетику и скорости клиренса из крови визуализирующего агента in vivo. Такие линкерные группы-"биомодификаторы" могут ускорять клиренс визуализирующего агента из фоновой ткани, такой как мышца или печень, и/или из крови, способствуя тем самым получению лучшего диагностирующего изображения вследствие меньших фоновых помех. Линкерная группа-биомодификатор также может быть использована для способствования конкретному пути экскреции, например через почки, в противоположность экскреции через печень.
Под термином "сахар" понимают моно-, ди- или трисахарид. Подходящие сахара включают: глюкозу, галактозу, мальтозу, маннозу и лактозу. В сахар возможно могут быть введены функциональные группы для обеспечения легкого сочетания с аминокислотами. Так, например, глюкозаминное производное аминокислоты можно конъюгировать с другими аминокислотами посредством пептидных связей. Одним из примеров этого является глюкозаминное производное аспарагина (имеющееся в продаже от NovaBiochem):

Формула I означает, что группировка -(L)n[BzpM] может быть присоединена по любому подходящему положению ВТМ. Такие подходящие положения для группировки -(L)n[BzpM] выбраны таким образом, что они располагаются в стороне от части ВТМ, которая ответственна за связывание с активным сайтом in vivo. Группировка [BTM]-(L)n- в формуле I может быть присоединена по любому подходящему положению BzpM формулы II. Группировка [ВТМ]-(L)n- либо занимает место существующего заместителя (например, одной из групп R1-R16), либо ковалентно присоединена к существующему в BzpM заместителю. Группировка [BTM]-(L)n- предпочтительно присоединена через карбоксиалкильный заместитель в BzpM.
Подходящими визуализирующими агентами по изобретению являются агенты, у которых BzpM имеет формулу IIa или IIb:
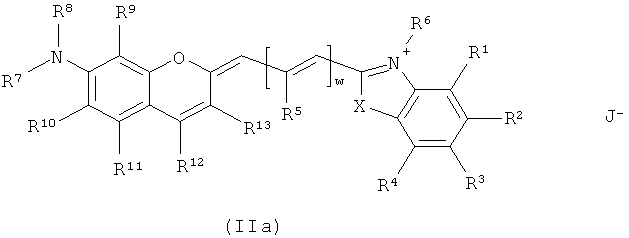 ,
,
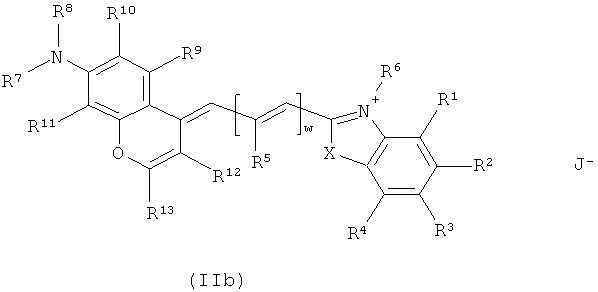 ,
,
где X, w, J и R1-R13 являются такими, как определено для формулы II.
Когда R5 вместе с одним из R6/R14-R16 образует 5- или 6-членное ненасыщенное алифатическое, ненасыщенное гетероалифатическое или ароматическое кольцо, такие подходящие ароматические кольца включают: фенильное, фурановое, тиазольное, пиридильное, пиррольное или пиразольное кольца. Подходящие ненасыщенные кольца содержат по меньшей мере С=С, куда присоединен R5.
Когда R7 и/или R8 вместе с одним или обоими из R9 и/или R10 образуют 5- или 6-членное N-содержащее гетероциклическое или гетероарильное кольцо, такие подходящие кольца включают: тиазольное, пиридильное, пиррольное или пиразольное кольца или их частично гидрогенизированные версии, предпочтительно пиридильное или дигидропиридильное.
В альтернативном воплощении красители формулы IIb возможно могут быть выбраны таким образом, что по меньшей мере один из R1-R4 представляет собой F или -(CF2)f-F, где f представляет собой целое число величиной от 1 до 4.
Фармацевтическая композиция поставляется в подходящих флаконах или сосудах, которые включают герметично закрытый контейнер, позволяющий поддерживать стерильную чистоту, плюс, возможно, инертный заполняющий свободное пространство газ (например, азот или аргон), в то же время допускающий добавление и отбор растворов с помощью шприца или канюли. Таким предпочтительным контейнером является флакон с герметизирующей прокладкой, у которого газонепроницаемая крышка обжата дополнительным укупорочным средством (обычно из алюминия). Крышка подходит для однократного или многократного прокалывания иглой для подкожных инъекций (например, обжатая крышка с герметизирующей прокладкой) с поддержанием при этом стерильной чистоты. Такие контейнеры имеют дополнительное преимущество, заключающееся в том, что крышка при желании может выдерживать вакуум (например, для замены заполняющего свободное пространство газа или дегазирования растворов) и может выдерживать изменения давления, например, уменьшения давления без возможности проникновения газов из внешней окружающей среды, таких как кислород или водяной пар.
Предпочтительные контейнеры для многократных доз включают одиночный большой флакон (например, объемом от 10 до 30 см3), который содержит многократные предназначенные для пациента дозы, с помощью которого однократные предназначенные для пациента дозы могут, таким образом, быть отобраны в шприцы клинической марки с различными интервалами времени в течение срока годности препарата в соответствии с клинической ситуацией. Предварительно заполненные шприцы сконструированы для включения однократной дозы для человека или "стандартной дозы" и поэтому предпочтительно представляют собой шприц одноразового применения или другой шприц, подходящий для клинического применения. Фармацевтические композиции по настоящему изобретению предпочтительно имеют дозировку, подходящую для одного пациента, и предоставлены в подходящем шприце или контейнере, как описано выше.
Фармацевтическая композиция возможно может содержать дополнительные эксципиенты, такие как антимикробный консервант, рН-регулирующий агент, наполнитель, стабилизатор или регулирующий осмоляльность агент. Под термином "антимикробный консервант" понимают агент, который ингибирует рост потенциально вредных микроорганизмов, таких как бактерии, дрожжи или плесневые грибы. Антимикробный консервант также может демонстрировать некоторые бактерицидные свойства в зависимости от используемой дозировки. Основная роль антимикробного консерванта(ов) по настоящему изобретению состоит в ингибировании роста любого такого микроорганизма в фармацевтической композиции. Однако антимикробный консервант также возможно может быть использован для ингибирования роста потенциально вредных микроорганизмов в одном или более компонентах наборов, применяемых для приготовления указанной композиции перед введением. Такие наборы описаны во втором аспекте (ниже). Подходящий(е) антимикробный(е) консервант(ы) включает(ют): парабены, то есть метил-, этил-, пропил- или бутилпарабен или их смеси; бензиловый спирт; фенол; крезол; цетримид и тиомерсал. Предпочтительными антимикробными консервантами являются парабены.
Термин "рН-регулирующий агент" означает соединение или смесь соединений, полезных для обеспечения нахождения рН композиции в пределах, приемлемых (приблизительно рН от 4,0 до 10,5) для введения человеку или млекопитающему. Такие подходящие рН-регулирующие агенты включают фармацевтически приемлемые буферы, такие как трицин, фосфат или ТРИС (то есть трис(гидроксиметил)аминометан), и фармацевтически приемлемые основания, такие как карбонат натрия, бикарбонат натрия или их смеси. Когда композицию применяют в форме набора, рН-регулирующий агент возможно может быть представлен в отдельном флаконе или контейнере, так что пользователь набора может осуществить регулирование рН в качестве части многостадийной процедуры.
Под термином "наполнитель" понимают фармацевтически приемлемый увеличивающий объем агент, который может облегчить работу с материалом в процессе его получения и лиофилизации. Подходящие наполнители включают неорганические соли, такие как хлорид натрия, и водорастворимые сахара или спирты сахаров, такие как сахароза, мальтоза, маннит или трегалоза.
Фармацевтические композиции по первому аспекту могут быть приготовлены в асептических условиях производства (то есть в чистой комнате) с получением желаемого стерильного апирогенного продукта. Предпочтительно, чтобы ключевые компоненты, особенно ассоциируемые реагенты, плюс те части оборудования, которые приводят в контакт с визуализирующим агентом (например, флаконы), были стерильны. Компоненты и реагенты можно стерилизовать способами, известными в данной области техники, включая: стерильную фильтрацию, окончательную стерилизацию с использованием, например, гамма-облучения, автоклавирование, обработку сухим жаром или химическую обработку (например, этиленоксидом). Некоторые компоненты предпочтительно стерилизовать заранее, с тем чтобы выполнять минимальное количество необходимых манипуляций. Тем не менее, для предосторожности предпочтительно включить по меньшей мере стадию стерильной фильтрации в качестве конечной стадии приготовления фармацевтической композиции.
Фармацевтическую композицию по первому аспекту предпочтительно приготавливают из набора, как описано ниже для второго аспекта.
Предпочтительные признаки
Удобно, чтобы молекулярная масса визуализирующего агента составляла до 30000 дальтон включительно. Молекулярная масса предпочтительно находится в диапазоне от 1000 до 20000 дальтон, наиболее предпочтительно от 2000 до 18000 дальтон, причем особенно предпочтителен диапазон от 2500 до 16000 дальтон.
ВТМ может иметь синтетическое или природное происхождение, но предпочтительно является синтетической. Термин "синтетический" имеет свое традиционное значение, то есть изготовленный человеком в отличие от выделенного из природных источников, например из организма млекопитающего. Преимущество таких соединений заключается в том, что их изготовление и профиль примесей можно полностью контролировать. Таким образом, моноклональные антитела и их фрагменты природного происхождения находятся вне объема термина "синтетический", как он использован в данном описании.
ВТМ предпочтительно выбрана из: 3-100-мерного пептида, субстрата фермента, антагониста фермента или ингибитора фермента. Наиболее предпочтительно ВТМ представляет собой 3-100-мерный пептид или пептидный аналог. Если ВТМ представляет собой пептид, то предпочтительно представляет собой 4-30-мерный пептид и наиболее предпочтительно 5-28-мерный пептид.
Группировка [BTM]-(L)n- в формуле I предпочтительно присоединена к BzpM формулы II по положениям R5, R6, R14, R15 или R16, более предпочтительно по R6, R14, R15 или R16, наиболее предпочтительно по R6, R14 или R15. Для облегчения присоединения релевантный заместитель R5, R6, R14, R15 или R16 предпочтительно представляет собой C1-6карбоксиалкил, более предпочтительно С3-6карбоксиалкил, с карбоксигруппой, используемой в качестве активного сложного эфира.
Бензопирилиевый краситель (BzpM) предпочтительно имеет по меньшей мере 2 сульфокислотных заместителя, более предпочтительно 2-6 сульфокислотных заместителя, наиболее предпочтительно 2-4 сульфокислотных заместителя. Предпочтительно, по меньшей мере одним из сульфокислотных заместителей является С1-4сульфоалкильная группа. Такие сульфоалкильные группы предпочтительно расположены по положениям R6, R7, R8, R14, R15 или R16; более предпочтительно по R6, R7, R8, R14 или R15; наиболее предпочтительно по R6 вместе с одним или обоими из R7 и R8 из формулы II. Сульфоалкильные группы из формулы II предпочтительно имеют формулу -(СН2)kSO3M1, где М1 представляет собой Н или Bc, k представляет собой целое число величиной от 1 до 4, и Bc представляет собой биосовместимый катион (как определено выше). k предпочтительно равно 3 или 4.
В формуле II w предпочтительно равно 1. R5 предпочтительно представляет собой Н или С1-4карбоксиалкил и наиболее предпочтительно представляет собой Н. Х предпочтительно представляет собой -CR14R15- или -NR16- и наиболее предпочтительно представляет собой -CR14R15-.
Предпочтительные красители BzpM имеют формулу III:
 ,
,
где Y1, R1-R4, R6, R14, R15 и J являются такими, как определено для формулы II.
Подходящие красители формулы III имеют формулу IIIa или IIIb:
 ,
,
 .
.
Предпочтительными группами R1-R4 и R6-R13 из формул III, IIIa и IIIb являются группы, описанные выше для формул IIa и IIb. В формулах III, IIIa и IIIb R14 и R15 предпочтительно выбраны таким образом, что один представляет собой группу Rb, а другой представляет собой группу Rc. Rb представляет собой С1-2алкил, наиболее предпочтительно метил. Rc представляет собой С1-4алкил, C1-6карбоксиалкил или С1-4сульфоалкил, предпочтительно С3-6карбоксиалкил или -(СН2)kSO3M1, где k выбран равным 3 или 4.
Предпочтительно, красители формулы III имеют C1-6карбоксиалкильный заместитель, позволяющий облегчить ковалентное присоединение к ВТМ.
В формуле II или III, когда R7 и/или R8 вместе с одним или обоими из R9 и/или R10 образуют 5- или 6-членное N-содержащее гетероциклическое или гетероарильное кольцо, такими предпочтительными кольцами являются пиридильное или дигидропиридильное. Предпочтительная группа Y1, в которой группа R8 циклизована с R10, имеет формулу Yc:
 .
.
Предпочтительная группа Y1, в которой как группа R7, так и группа R8 циклизованы, имеет формулу Yd:
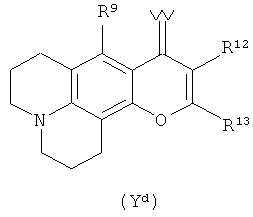 ,
,
где:
R7, R9 и R11-R13 являются такими, как определено выше;
каждый X1 независимо представляет собой Н или С1-4алкил.
В формуле Yc предпочтительно, когда:
каждый X1 представляет собой СН3;
R9 представляет собой R11, который представляет собой Н;
R12 представляет собой Н;
R12 представляет собой СН3 или -С(СН3)3, более предпочтительно -С(СН3)3.
В формуле Yd предпочтительно, когда:
R9 представляет собой Н;
R12 представляет собой Н;
R12 предпочтительно представляет собой СН3 или -С(СН3)3, более предпочтительно -С(СН3)3.
Предпочтительно, чтобы группа -NR7R8 из формулы III либо:
1) существовала в форме открытой цепи, то есть группы R7/R8 были не циклизованы с одной или обеими R9/R10. Такие предпочтительные группы R7 и R8 независимо выбраны из С1-4алкила или С1-4сульфоалкила, наиболее предпочтительно этила или С3-4сульфоалкила;
2) была циклизована с получением циклического заместителя Y1 формулы Yc или Yd, более предпочтительно формулы Yc.
Форма открытой цепи (1) является наиболее предпочтительной.
Особенно предпочтительные красители формулы III имеют формулы IIIc, IIId или IIIe:
 ,
,
 ,
,
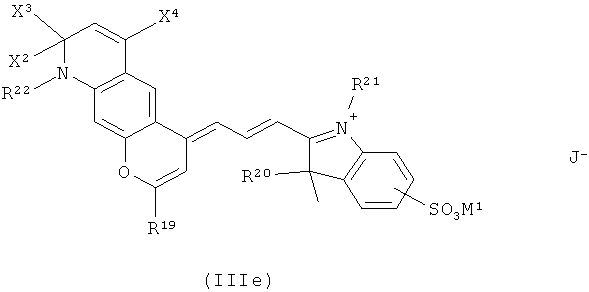 ,
,
где:
M1 и J являются такими, как определено выше;
R17 и R18 независимо выбраны из С1-4алкила или С1-4сульфоалкила;
R19 представляет собой Н или С1-4алкил;
R20 представляет собой С1-4алкил, С1-4сульфоалкил или C1-6карбоксиалкил;
R21 представляет собой С1-4сульфоалкил или C1-6карбоксиалкил;
R22 представляет собой С1-4алкил, С1-4сульфоалкил или C1-6карбоксиалкил;
X2, X3 и X4 независимо представляют собой Н или С1-4алкил.
Красители формул IIId, IIIe и IIIf предпочтительно выбраны таким образом, что один или более чем один из R20-R22 представляет собой С1-4сульфоалкил.
Конкретными предпочтительными красителями формулы IIId являются DY-631 и DY-633:
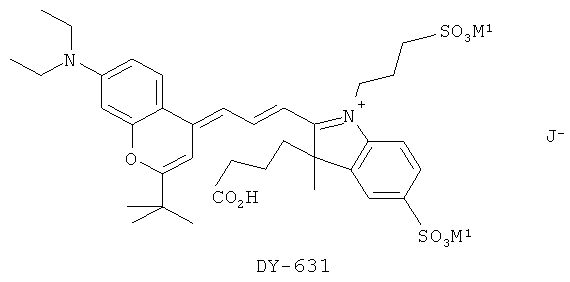 ,
,
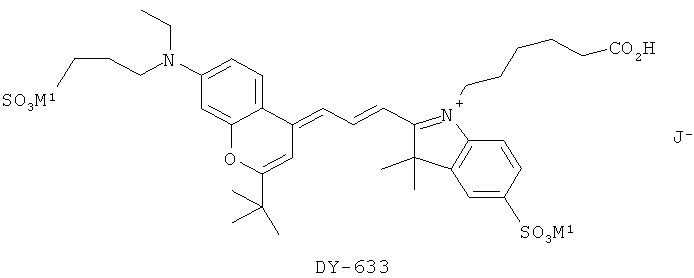 .
.
Конкретным предпочтительным красителем формулы IIIe является DY-652:
 .
.
Конкретными предпочтительными красителями являются DY-631 и DY-652, причем DY-652 является наиболее предпочтительным.
Когда ВТМ представляет собой пептид, такие предпочтительные пептиды включают:
- соматостатин, октреотид и аналоги;
- пептиды, связывающиеся с рецептором ST, где ST означает термостабильный токсин, продуцируемый Е.coli и другими микроорганизмами;
- ламининовые фрагменты, например YIGSR, PDSGR, IKVAV, LRE и KCQAGTFALRGDPQG;
- N-формил-содержащие пептиды для направленной доставки к сайтам скопления лейкоцитов;
- тромбоцитарный фактор 4 (PF4) и его фрагменты;
- RGD(Arg-Gly-Asp)-содержащие пептиды, которые могут, например, иметь мишенью ангиогенез (R.Pasqualini et al., Nat. Biotechnol. 1997 Jun, 15(6): 542-6; Е.Ruoslahti, Kidney Int. 1997 May, 51(5): 1413-7);
- пептидные фрагменты α2-антиплазмина, фибронектина или бета-казеина, фибриногена или тромбоспондина. Аминокислотные последовательности α2-антиплазмина, фибронектина, бета-казеина, фибриногена и тромбоспондина можно найти в следующих ссылках: предшественник α2-антиплазмина (M.Tone et al., J. Biochem, 102, 1033, (1987)); бета-казеин (L.Hansson et al., Gene, 139, 193, (1994)); фибронектин (A.Gutman et al., FEBS Lett., 207, 145, (1996)); предшественник тромбоспондина-1 (V.Dixit et al., Proc. Natl. Acad. Sci., USA, 83, 5449, (1986); R.F.Doolittle, Ann. Rev. Biochem., 53, 195, (1984));
- пептиды, являющиеся субстратами или ингибиторами ангиотензина, например:
ангиотензин II: Asp-Arg-Val-Tyr-Ile-His-Pro-Phe (Е.С.Jorgensen et al., J. Med. Chem., 1979, Vol.22, 9, 1038-1044),
[Sar,Ile]-ангиотензин II: Sar-Arg-Val-Tyr-Ile-His-Pro-Ile (R.K.Turker et al., Science, 1972, 177, 1203);
- ангиотензин I: Asp-Arg-Val-Tyr-Ile-His-Pro-Phe-His-Leu.
Когда ВТМ представляет собой пептид, то один или оба конца пептида, предпочтительно оба, конъюгированы с ингибирующей метаболизм группой (MIG). Оба конца пептида, защищенные таким способом, важны для применений при визуализации in vivo, поскольку иначе можно ожидать быстрого метаболизма с последующей потерей аффинности селективного связывания для пептида ВТМ. Под термином "ингибирующая метаболизм группа" (MIG) понимают биосовместимую группу, которая ингибирует или подавляет ферментативный, особенно пептидазный, такой как карбоксипептидазный, метаболизм пептида ВТМ либо по амино-концу, либо по карбокси-концу. В частности, такие группы важны для применений in vivo, они хорошо известны специалистам в данной области техники, и их подходящим образом выбирают для амино-конца пептида из:
N-ацилированных групп -NH(С=O)RG, где ацильная группа -(С=O)RG имеет RG, выбранный из: C1-6алкильных, С3-10арильных групп, или содержит полиэтиленгликолевый (ПЭГ) строительный блок. Подходящие ПЭГ-группы описаны для линкерной группы (L) ниже. Такие предпочтительные ПЭГ-группы представляют собой биомодификаторы формул Bio1 или Bio2 (ниже). Такими предпочтительными аминоконцевыми группами MIG являются ацетил, бензилоксикарбонил или трифторацетил, наиболее предпочтительно ацетил.
Подходящие ингибирующие метаболизм группы для карбоксильного конца пептида включают: карбоксамид, сложный трет-бутиловый эфир, сложный бензиловый эфир, сложный циклогексиловый эфир, аминоспирт или полиэтиленгликолевый (ПЭГ) строительный блок. Подходящей группой MIG для карбоксиконцевого аминокислотного остатка пептида ВТМ является группа, где концевой амин аминокислотного остатка N-алкилирован С1-4алкильной группой, предпочтительно метильной группой. Такими предпочтительными группами MIG являются карбоксамид или ПЭГ, наиболее предпочтительно такими группами является карбоксамид.
Если один или оба конца пептида защищены группой MIG, то группировка -(L)n[BzpM] возможно может быть присоединена к группе MIG. Предпочтительно, чтобы по меньшей мере один конец пептида не имел группы MIG, с тем чтобы присоединение группировки -(L)n[BzpM] по этому положению давало соединения формул IVa или IVb соответственно:
 ;
;
 ;
;
где:
Z1 присоединен к N-концу пептида ВТМ и представляет собой Н или MIG;
Z2 присоединен к С-концу пептида ВТМ и представляет собой ОН, OBc или MIG,
где Bc представляет собой биосовместимый катион (как определено выше).
В формулах IVa и IVb Z1 и Z2 предпочтительно оба независимо представляют собой MIG. Такими предпочтительными группами MIG для Z1 и Z2 являются группы, описанные выше для концов пептида. В то время как ингибирования метаболизма пептида ВТМ по любому концу пептида также можно достичь посредством присоединения группировки -(L)n[BzpM], сама группировка -(L)n[BzpM] находится вне определения MIG по настоящему изобретению.
Пептид ВТМ возможно может содержать по меньшей мере один дополнительный аминокислотный остаток, обладающий боковой цепью, подходящей для облегчения конъюгации с BzpM, и образующий часть остатков А линкерной группы (L). Такие подходящие аминокислотные остатки включают остатки Asp или Glu для конъюгации с амин-функционализированными красителями BzpM, или остаток Lys для конъюгации с карбокси-функционализированным красителем BzpM или красителем BzpM, функционализированным активным сложным эфиром. Дополнительный(е) аминокислотный(е) остаток(и) для конъюгации с BzpM соответственно расположен(ы) в стороне от связывающего участка пептида ВТМ и предпочтительно расположен(ы) или на С-, или на N-конце. Предпочтительно, аминокислотным остатком для конъюгации является остаток Lys.
В тех случаях, когда имеется синтетическая линкерная группа (L), она предпочтительно содержит концевые функциональные группы, облегчающие конъюгацию с [ВТМ] и BzpM. Такие подходящие группы (Qa) описаны ниже. Когда L содержит пептидную цепь из 1-10 аминокислотных остатков, эти аминокислотные остатки предпочтительно выбраны из глицина, лизина, аргинина, аспарагиновой кислоты, глутаминовой кислоты или серина. Когда L содержит ПЭГ-группировку, то она предпочтительно содержит единицы, полученные в результате олигомеризации монодисперсных ПЭГ-подобных структур формул Bio1 или Bio2:
 ,
,
17-амино-5-оксо-6-аза-3,9,12,15-тетраоксагептадекановую кислоту формулы Bio1, где p равно целому числу от 1 до 10. Альтернативно, можно использовать ПЭГ-подобную структуру на основе производного пропионовой кислоты формулы Bio2:
 ,
,
где p является таким, как определено для формулы Bio1, и q равно целому числу от 3 до 15.
В формуле Bio2 p предпочтительно равно 1 или 2 и q предпочтительно равно от 5 до 12.
Когда линкерная группа не содержит ПЭГ или пептидную цепь, предпочтительные группы L имеют основную цепь из связанных атомов, образующих группировку -(А)m- из 2-10 атомов, наиболее предпочтительно 2-5 атомов, особенно предпочтительно из 2 или 3 атомов. Минимальная основная цепь линкерной группы из 2 атомов предоставляет преимущество, заключающееся в том, что BzpM хорошо отделен, так что любое нежелательное взаимодействие минимизировано.
Пептиды ВТМ, которые отсутствуют в продаже, могут быть синтезированы твердофазным пептидным синтезом, как описано в Р.Lloyd-Williams, F.Albericio and E.Girald; Chemical Approaches to the Synthesis of Peptides and Proteins, CRC Press, 1997.
Визуализирующие агенты могут быть получены следующим образом.
Для облегчения конъюгации BzpM с ВТМ к BzpM подходящим образом присоединяют реакционно-способную функциональную группу (Qa). Группа Qa предназначена для взаимодействия с комплементарной функциональной группой ВТМ, в результате чего образуется ковалентная связь между BzpM и ВТМ. Комплементарная функциональная группа ВТМ может составлять неотъемлемую часть ВТМ или может быть введена в результате получения производного с использованием бифункциональной группы, как известно в данной области техники. В Таблице 1 показаны примеры реакционно-способных групп и их комплементарных аналогов.
Под термином "активированный сложный эфир" или "активный сложный эфир" понимают сложноэфирное производное карбоновой кислоты, которое предназначено быть лучшей уходящей группой и, следовательно, давать возможность для более легкого взаимодействия с нуклеофилом, таким как амины. Примерами подходящих активных сложных эфиров являются: N-гидроксисукцинимидный (NHS), пентафторфенольный, пентафтортиофенольный, пара-нитрофенольный и гидроксибензотриазольный. Предпочтительными активными сложными эфирами являются N-гидроксисукцинимидный или пентафторфенольный эфиры.
Примеры функциональных групп, присутствующих в ВТМ, таких как белки, пептиды, нуклеиновые кислоты, углеводы и тому подобных, включают: гидрокси, амино, сульфгидрил, карбонил (включая альдегид и кетон) и тиофосфат. Подходящие группы Qa могут быть выбраны из карбоксила; активированных сложных эфиров; изотиоцианата; малеимида; галогеноацетамида; гидразида; винилсульфона, дихлортриазина и фосфорамидита. Предпочтительно, Qa представляет собой активированный сложный эфир карбоновой кислоты, изотиоцианат, малеимид или галогеноацетамид.
Когда комплементарная группа представляет собой амин или гидроксил, Qa предпочтительно представляет собой активированный сложный эфир; предпочтительные сложные эфиры являются такими, как описано выше. Таким предпочтительным заместителем на BzpM является активированный сложный эфир 5-карбоксипентильной группы. Когда комплементарная группа представляет собой тиол, Qa предпочтительно представляет собой малеимидную или йодацетамидную группу.
Общие способы конъюгации красителей с биологическими молекулами описаны Licha et al. (Topics Curr. Chem., 222, 1-29 (2002); Adv. Drug Deliv. Rev., 57, 1087-1108 (2005)). Пептидные, белковые и олигонуклеотидные субстраты для применения в данном изобретении могут быть мечены по концевому положению или, альтернативно, по одному или более внутренним положениям. Обзоры и примеры мечения белков с использованием реагентов мечения, представляющих собой флуоресцентные красители, приведены в "Non-Radioactive Labelling, a Practical Introduction", Garman, A.J. Academic Press, 1997; "Bioconjugation - Protein Coupling Techniques for the Biomedical Sciences", Aslam, M. and Dent, A., Macmillan Reference Ltd, (1998). Доступные протоколы достижения сайт-специфического мечения синтезированного пептида приведены, например, в Hermanson, G.T, "Bioconjugate Techniques", Academic Press (1996).
Предпочтительно, способ получения визуализирующего агента включает или:
(1) взаимодействие аминной функциональной группы в ВТМ с соединением формулы J1-(L)n-[BzpM]; или
(2) взаимодействие функциональной группы карбоновой кислоты или активированного сложного эфира в ВТМ с соединением формулы J2-(L)n-[BzpM];
(3) взаимодействие тиольной группы в ВТМ с соединением формулы:
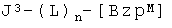 ,
,
где ВТМ, MIG, L, n и BzpM являются такими, как определено выше, и
J1 представляет собой группу карбоновой кислоты, активированного сложного эфира, изотиоцианатную или тиоцианатную группу;
J2 представляет собой аминную группу;
J3 представляет собой малеимидную группу.
J2 предпочтительно представляет собой первичную или вторичную аминную группу, наиболее предпочтительно первичную аминную группу. На стадии (3) тиольная группа в ВТМ предпочтительно представляет собой цистеиновый остаток.
На стадиях (1)-(3) ВТМ возможно может иметь другие функциональные группы, которые потенциально способны к взаимодействию с производным BzpM, защищенным подходящими защитными группами, так что химическая реакция протекает избирательно только в желаемом месте. Под термином "защитная группа" понимают группу, которая ингибирует или подавляет нежелательные химические реакции, но которая предназначена быть достаточно реакционно-способной, чтобы она могла отщепляться от рассматриваемой функциональной группы в условиях, достаточно мягких для того, чтобы не модифицировать остальную часть молекулы. После снятия защиты получают целевой продукт. Аминные защитные группы хорошо известны специалистам в данной области техники, и их подходящим образом выбирают из: Boc (где Boc представляет собой трет-бутилоксикарбонил), Fmoc (где Fmoc представляет собой флуоренилметоксикарбонил), трифторацетила, аллилоксикарбонила, Dde (то есть 1-(4,4-диметил-2,6-диоксоциклогексилиден)этила) или Npys (то есть 3-нитро-2-пиридинсульфенила). Подходящими тиол-защитными группами являются Trt (тритил), Acm (ацетамидометил), трет-Bu (трет-бутил), трет-бутилтио, метоксибензил, метилбензил или Npys (3-нитро-2-пиридин-сульфенил). Применение дополнительных защитных групп описано в "Protective Groups in Organic Synthesis", Theodora W.Greene and Peter G.M.Wuts (John Wiley & Sons, 1991). Предпочтительными аминными защитными группами являются Boc и Fmoc, наиболее предпочтительно - Boc. Предпочтительными тиол-защитными группами являются Trt и Acm.
Бензопирилиевые красители (BzpM), функционализированные подходящим образом для конъюгации с ВТМ, имеются в продаже у Dyomics (Dyomics GmbH, Winzerlaer Str. 2A, D-07745 Jena, Germany; www.dyomics.com), у которых реакционно-способная функциональная группа (Qa) представляет собой сложный NHS-эфир, малеимид, амино или карбоновую кислоту. Предшественники, подходящие для синтеза бензопирилиевых красителей, также могут быть получены, как описано в US 5405976. Способы конъюгации оптических репортерных красителей с аминокислотами и пептидами описаны Licha (смотри выше), а также Flanagan et al. (Bioconj. Chem., 8, 751-756 (1997)); Lin et al. (там же, 13, 605-610 (2002)) и Zaheer (Mol. Imaging, 1(4), 354-364 (2002)). Способы конъюгации линкерной группы (L) с ВТМ включают аналогичные химические реакции, что и с самими красителями (смотри выше), и они известны в данной области техники.
Во втором аспекте настоящего изобретения предложен набор для приготовления фармацевтической композиции по первому аспекту, где указанный набор содержит конъюгат формулы I в стерильной твердой форме, такой, что после восстановления стерильным источником биосовместимого носителя происходит растворение с получением желаемой фармацевтической композиции. "Конъюгат" и "биосовместимый носитель" вместе с их предпочтительными воплощениями являются такими, как описано в первом аспекте.
Что касается набора, то конъюгат вместе с другими возможными эксипиентами, которые описаны выше, может быть представлен в виде лиофилизированного порошка в подходящем флаконе или контейнере. Порошок предназначен для дальнейшего восстановления желаемым биосовместимым носителем с получением фармацевтической композиции в стерильной апирогенной форме, готовой для введения млекопитающему.
Предпочтительной стерильной твердой формой конъюгата является лиофилизированное твердое вещество. Стерильная твердая форма предпочтительно поставляется в контейнере фармацевтической марки, как описано для фармацевтической композиции (выше). Когда набор является лиофилизированным, композиция возможно может содержать криопротектор, выбранный из сахарида, предпочтительно маннита, мальтозы или трицина.
В третьем аспекте настоящего изобретения предложен конъюгат формулы I:
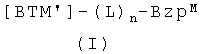 ,
,
где L и n являются такими, как определено для первого аспекта, и BzpM имеет формулу II, определенную выше; ВТМ' представляет собой ВТМ, определенную в первом аспекте, которая является синтетической и выбрана из:
(1) 3-100-мерного пептида;
(2) субстрата фермента, антагониста фермента или ингибитора фермента;
(3) рецептор-связывающего соединения;
(4) олигонуклеотида;
(5) олиго-ДНК- или олиго-РНК-фрагмента.
Термин "синтетический" имеет определение, приведенное выше. Предпочтительными воплощениями BzpM формулы II в конъюгате являются такие, которые описаны выше в первом аспекте. Предпочтительными аспектами ВТМ' (1)-(5) являются такие, которые описаны выше в первом аспекте для этих типов ВТМ. ВТМ' предпочтительно представляет собой 3-100-мерный пептид.
Конъюгаты по третьему аспекту полезны в приготовлении фармацевтических композиций визуализирующего агента по изобретению. Конъюгаты могут быть получены, как описано в первом аспекте.
В четвертом аспекте настоящего изобретения предложен способ оптической визуализации in vivo организма млекопитающего, включающий применение фармацевтической композиции по первому аспекту для получения изображений мест локализации ВТМ in vivo.
Термин "оптическая визуализация" является таким, как определено в первом аспекте (выше).
В способе по четвертому аспекту предпочтительно, чтобы фармацевтическая композиция визуализирующего агента была предварительно введена в организм указанного млекопитающего. Под "предварительным введением" понимают то, что стадия, включающая участие врача-клинициста, когда пациенту дают визуализирующий агент, например в виде внутривенной инъекции, уже проведена до визуализации. Это воплощение включает применение конъюгата, определенного в первом аспекте, в изготовлении диагностирующего агента для оптической визуализации in vivo болезненных состояний организма млекопитающего, в которые вовлечена ВТМ.
Предпочтительным способом оптической визуализации по четвертому аспекту является визуализация на основе отражения флуоресценции (FRI). В FRI-методе визуализирующий агент по настоящему изобретению вводят диагностируемому субъекту и после этого тканевую поверхность субъекта облучают возбуждающим светом - возбуждением непрерывной волны (CW). Свет возбуждает краситель BzpM визуализирующего агента. Флуоресценцию от визуализирующего агента, которая генерируется под действием возбуждающего света, детектируют с использованием детектора флуоресценции. Отраженный свет предпочтительно фильтруют для отделения компонента флуоресценции (исключительно или частично). От флуоресцентного света формируют изображение. Обычно проводят минимальную обработку (не используют никакого процессора для расчета оптических параметров, таких как продолжительность, квантовый выход и так далее), и изображение отображает картину интенсивности флуоресценции. Визуализирующий агент разработан для концентрирования в области заболевания, чтобы давать более высокую интенсивность флуоресценции. Таким образом, область заболевания дает положительный контраст в картине интенсивности флуоресценции. Изображение предпочтительно получают с использованием CCD-камеры (камера с зарядовой связью) или CCD-элемента (элемент с зарядовой связью), чтобы иметь возможность визуализации в режиме реального времени.
Длина волны возбуждения варьируется в зависимости от конкретного используемого красителя BzpM, но обычно находится в диапазоне 500-1200 нм для красителей по настоящему изобретению. Аппарат для генерирования возбуждающего света может представлять собой традиционный источник возбуждающего света, такой как: лазер (например, ионный лазер, лазер на красителях или полупроводниковый лазер); галогеновый источник света или ксеноновый источник света. Для получения оптимальной длины волны возбуждения возможно могут быть использованы различные оптические фильтры. Предпочтительный FRI-способ включает следующие стадии:
(1) облучения, представляющей интерес тканевой поверхности организма млекопитающего возбуждающим светом;
(2) детекции флуоресценции от визуализирующего агента, которая генерируется возбуждением BzpM, с использованием детектора флуоресценции;
(3) возможно, фильтрации света, детектируемого детектором флуоресценции, для отделения компонента флуоресценции;
(4) формирования изображения, представляющей интерес указанной тканевой поверхности в результате флуоресцентного света со стадий (2) или (3).
Возбуждающий свет со стадии (1) по своей природе предпочтительно представляет собой непрерывную волну (CW). На стадии (3) детектируемый свет предпочтительно фильтруют. Особенно предпочтительным FRI-способом является флуоресцентная эндоскопия.
В альтернативном способе визуализации по шестому аспекту используют FDPM (миграцию фотонов в диапазоне частот). Этот способ обладает преимуществами по сравнению со способами непрерывной волны (CW) в тех случаях, когда важна большая глубина детекции красителя внутри ткани (Sevick-Muraca et al., Curr. Opin. Chem. Biol., 6, 642-650 (2002)). Для такого типа визуализации с использованием частотной/временной области благоприятно, если BzpM обладает флуоресцентными свойствами, которые можно модулировать в зависимости от глубины поражения ткани, изображение которого получают, и типа используемого измерительного оборудования.
FDPM-способ состоит в следующем:
(а) в подвергании светорассеивающей биологической ткани организма указанного млекопитающего, имеющей гетерогенный состав, воздействию света от источника света с предварительно определенной изменяющейся во времени интенсивностью для возбуждения визуализирующего агента, причем указанная ткань многократно рассеивает возбуждающий свет;
(б) в детекции эмиссии многократно рассеянного тканью света в ответ на указанное подвергание воздействию;
(в) в количественном определении характеристики флуоресценции во всей ткани в результате эмиссии путем установления ряда величин с использованием процессора, каждая из которых соответствует уровню характеристики флуоресценции в разном положении внутри ткани, причем уровень характеристики флуоресценции изменяется в зависимости от гетерогенного состава ткани; и
(г) в генерировании изображения ткани путем составления карты гетерогенного состава ткани в соответствии с величинами стадии (в).
Характеристика флуоресценции со стадии (в) предпочтительно соответствует поглощению визуализирующего агента и предпочтительно дополнительно включает построение карты ряда количественных характеристик, соответствующих коэффициентам поглощения и рассеяния ткани до введения визуализирующего агента. Характеристика флуоресценции со стадии (в) предпочтительно соответствует по меньшей мере одному из: продолжительности флуоресценции, квантовой эффективности флуоресценции, выходу флуоресценции и поглощению визуализирующего агента. Характеристика флуоресценции предпочтительно не зависит от интенсивности эмиссии и не зависит от концентрации визуализирующего агента.
Количественное определение на стадии (в) предпочтительно включает: (1) установление оценочных значений величин, (2) определение рассчитанной эмиссии как функции оценочного значения, (3) сравнение рассчитанной эмиссии с эмиссией, полученной в результате указанной детекции, для определения ошибки, (4) установление измененного оценочного значения характеристики флуоресценции как функции ошибки. Количественное определение предпочтительно включает определение величин на основании математического соотношения, моделирующего многократное светорассеивающее поведение ткани. Способ по первому варианту предпочтительно дополнительно включает мониторинг метаболического свойства ткани in vivo посредством детекции изменения указанной характеристики флуоресценции.
Оптическую визуализацию по четвертому аспекту предпочтительно используют для облегчения регулирования (management) болезненного состояния организма млекопитающего. Под термином "регулирование" понимают использование в: детекции, определении стадии, диагностике, мониторинге прогрессирования заболевания или мониторинге лечения. Болезненное состояние соответствующим образом представляет собой такое состояние, в которое вовлечена ВТМ визуализирующего агента. Применения визуализации предпочтительно включают поверхностную визуализацию с использованием камеры, эндоскопию и хирургические указания. Дополнительные подробности подходящих способов оптической визуализации приведены в обзоре Sevick-Muraca et al. (Curr. Opin. Chem. Biol., 6, 642-650 (2002)).
В пятом аспекте настоящего изобретения предложен способ детекции, определения стадии, диагностики, мониторинга прогрессирования заболевания или мониторинга лечения болезненного состояния организма млекопитающего, включающий способ оптической визуализации in vivo по четвертому аспекту.
Настоящее изобретение проиллюстрировано неограничивающими Примерами, подробно описанными ниже. В Примере 1 приведен синтез пептида, обеспечивающего направленную доставку к биологической мишени, (Пептида 1), который связывается с cMet. В Примере 2 приведены способы конъюгации красителей BzpM по изобретению с пептидами, в частности, с Пептидом 1. В Примере 3 приведены данные, демонстрирующие, что пептидные конъюгаты Пептида 1 по изобретению сохраняют аффинность в отношении cMet, то есть, что конъюгированный краситель не препятствует биологическому связыванию и селективности. Были продемонстрированы приемлемое низкое связывание с альбумином сыворотки человека и высокая стабильность в плазме. В Примере 4 показано, что пептидные конъюгаты по изобретению демонстрируют полезные соотношения опухоль: фон на животной модели колоректального рака. В Примере 5 описано использование прогнозирующего программного обеспечения для красителей по изобретению и продемонстрировано, что в красителях по изобретению отсутствуют потенциально опасные in vivo метаболиты. В Примере 6 описано тестирование токсичности Соединения 6, показывающее, что ожидаемая клиническая доза хорошо переносилась и не вызывала каких-либо связанных с лекарственным средством неблагоприятных эффектов.
где Rd представляет собой -(СН2)3SO3H, Re представляет собой -(СН2)3CO2H и Rf представляет собой -(СН2)5CO2H.
DY-752 имеет те же кольца и картину замещения, что и DY-652, но обладает пентаметиновой связью (т.е. w равен 2 и R5 представляет собой Н) вместо триметиновой связи в DY-652.
Сокращения
Используют традиционные трехбуквенные и однобуквенные сокращения аминокислот.
Пример 1. Синтез Пептида 1
Использовали 26-мерный бициклический пептид, содержащий 2 Cys-Cys связи (Cys4-16 и 6-14), имеющий следующую последовательность:
Ac-Ala-Gly-Ser-Cys-Tyr-Cys-Ser-Gly-Pro-Pro-Arg-Phe-Glu-Cys-Trp-Cys-Tyr-Glu-Thr-Glu-Gly-Thr-Gly-Gly-Gly-Lys-NH2 ("Пептид 1").
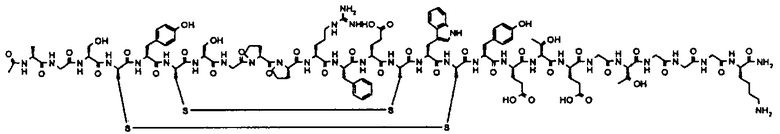
Стадия (а): синтез защищенного линейного предшественника Пептида 1
Линейный пептид-предшественник имеет следующую последовательность:
Ac-Ala-Gly-Ser-Cys-Tyr-Cys(Acm)-Ser-Gly-Pro-Pro-Arg-Phe-Glu-Cys(Acm)-Trp-Cys-Tyr-Glu-Thr-Glu-Gly-Thr-Gly-Gly-Gly-Lys-NH2.
Проводили сборку пептидильной смолы H-Ala-Gly-Ser(tBu)-Cys(Trt)-Tyr(tBu)-Cys(Acm)-Ser(tBu)-Gly-Pro-Pro-Arg(Pbf)-Phe-Glu(OtBu)-Cys(Acm)-Trp(Boc)-Cys(Trt)-Tyr(tBu)-Glu(OtBu)-Thr(ψMe,Mepro)-Glu(OtBu)-Gly-Thr(tBu)-Gly-Gly-Gly-Lys(Вос)-Полимер на пептидном синтезаторе Applied Biosystems 433A с использованием Fmoc-химии, начиная с 0,1 ммоль смолы Rink Amide Novagel. На стадиях сочетания применяли избыток предварительно активированных аминокислот 1 ммоль (используя HBTU). В последовательность вводили Glu-Thr-псевдопролин (Novabiochem 05-20-1122). Смолу переносили в аппарат с азотным барботированием и обрабатывали раствором уксусного ангидрида (1 ммоль) и NMM (1 ммоль) в DCM (5 мл) в течение 60 мин. Раствор ангидрида удаляли фильтрованием, смолу промывали DCM и сушили в потоке азота.
Одновременное удаление защитных групп боковых цепей и отщепление пептида от смолы осуществляли в TFA (10 мл), содержащей 2,5% TIS (триизопропилсилан), 2,5% 4-тиокрезола и 2,5% воды в течение 2 часов и 30 мин. Смолу удаляли фильтрованием, TFA удаляли в вакууме и к остатку добавляли диэтиловый эфир. Образовавшийся осадок промывали диэтиловым эфиром и сушили на воздухе, что позволило получить 264 мг неочищенного пептида.
Очистка препаративной HPLC (градиент: 20-30% В в течение 40 мин, где А = H2O/0,1% TFA и В = ACN/0,1% TFA, скорость потока: 10 мл/мин, колонка: С18 (2) (5 мкм; 250×21,20 мм) Phenomenex Luna, детектирование: УФ 214 нм, время удерживания продукта: 30 мин) неочищенного пептида позволила получить 100 мг чистого линейного предшественника Пептида 1. Чистый продукт анализировали аналитической HPLC (градиент: 10-40% В в течение 10 мин, где А = H2O/0,1% TFA и В = ACN/0,1% TFA, скорость потока: 0,3 мл/мин, колонка: С18 (2) (3 мкм; 50×2 мм) Phenomenex Luna, детектирование: УФ 214 нм, время удерживания продукта: 6,54 мин). Снятие дополнительной характеристики продукта осуществляли с использованием масс-спектрометрии с электрораспылением (

Стадия (b): образование дисульфидного мостика Cys4-16
Cys4-16; Ac-Ala-Gly-Ser-Cys-Tyr-Cys(Acm)-Ser-Gly-Pro-Pro-Arg-Phe-Glu-Cys(Acm)-Trp-Cys-Tyr-Glu-Thr-Glu-Gly-Thr-Gly-Gly-Gly-Lys-NH2.
Линейный предшественник со стадии (а) (100 мг) растворяли в смеси 5% DMSO/вода (200 мл) и рН раствора доводили до 6 с использованием аммиака. Реакционную смесь перемешивали в течение 5 суток. Затем рН раствора доводили до 2 с использованием TFA и большую часть растворителя удаляли выпариванием в вакууме. Для очистки продукта остаток (40 мл) порциями вводили в колонку для препаративной HPLC.
Очистка препаративной HPLC (градиент: 0% В в течение 10 мин, затем 0-40% В в течение 40 мин, где А = H2O/0,1% TFA и В = ACN/0,1% TFA, скорость потока: 10 мл/мин, колонка: С18 (2) (5 мкм; 250×21,20 мм) Phenomenex Luna, детектирование: УФ 214 нм, время удерживания продукта: 44 мин) остатка позволила получить 72 мг чистого моноциклического предшественника Пептида 1.
Чистый продукт (в виде смеси изомеров Р1-Р3) анализировали аналитической HPLC (градиент: 10-40% В в течение 10 мин, где А = H2O/0,1% TFA и В = ACN/0,1% TFA, скорость потока: 0,3 мл/мин, колонка: С18 (2) (3 мкм; 50×2 мм) Phenomenex Luna, детектирование: УФ 214 нм, время удерживания продукта: 5,37 мин (Р1); 5,61 мин (Р2); 6,05 мин (Р3)). Снятие дополнительной характеристики продукта осуществляли с использованием масс-спектрометрии с электрораспылением (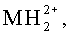

Стадия (с): образование дисульфидного мостика Cys6-14 (Пептид 1)
Моноциклический предшественник со стадии (b) (72 мг) растворяли в смеси 75% АсОН/вода (72 мл) в защитной среде азота. Добавляли 1 М HCl (7,2 мл) и 0,05 М I2 в АсОН (4,8 мл) в указанном порядке и смесь перемешивали в течение 45 мин. Добавляли 1 М аскорбиновую кислоту (1 мл), что делало смесь бесцветной. Большую часть растворителей выпаривали в вакууме, остаток (18 мл) разбавляли смесью вода/0,1% TFA (4 мл) и продукт очищали с использованием препаративной HPLC. Очистка препаративной HPLC (градиент: 0% В в течение 10 мин, затем 20-30% В в течение 40 мин, где А = H2O/0,1% TFA и В = ACN/0,1% TFA, скорость потока: 10 мл/мин, колонка: С18 (2) (5 мкм; 250×21,20 мм) Phenomenex Luna, детектирование: УФ 214 нм, время удерживания продукта: 43-53 мин) остатка позволила получить 52 мг чистого Пептида 1. Чистый продукт анализировали аналитической HPLC (градиент: 10-40% В в течение 10 мин, где А = H2O/0,1% TFA и В = ACN/0,1% TFA, скорость потока: 0,3 мл/мин, колонка: С18 (2) (3 мкм; 50×2 мм) Phenomenex Luna, детектирование: УФ 214 нм, время удерживания продукта: 6,54 мин). Снятие дополнительной характеристики продукта осуществляли с использованием масс-спектрометрии с электрораспылением (MH2 2+, рассчитано: 1391,5; 
Пример 2. Синтез конъюгатов пептида с бензопирилиевыми красителями
Общий способ конъюгации
К раствору Пептида 1 (из Примера 1; 4 мг; 1,4 мкмоль) в DMF (0,5 мл) добавляли раствор NHS-эфира BzpM (1 мг; 1 мкмоль) и сим.-коллидин (8 мкл; 60 мкмоль) в DMF (0,5 мл). Реакционную смесь нагревали (с помощью микроволнового излучения) при 60°С в течение 1 ч; затем выдерживали при КТ (комнатная температура) в течение ночи. Реакционную смесь далее разбавляли смесью 20% ACN/вода/0,1% TFA (7 мл) и продукт очищали с использованием препаративной HPLC.
Очистка и снятие характеристик
Очистка препаративной HPLC (градиент: 20-40% В в течение 40 мин, где А = H2O/0,1% TFA и В = ACN/0,1% TFA, скорость потока: 10 мл/мин, колонка: С18 (2) (5 мкм; 250×21,2 мм) Phenomenex Luna, детектирование: УФ 214 нм) неочищенного пептида позволила получить чистый конъюгат [Пептид 1]-BzpM. Чистый продукт анализировали аналитической HPLC (градиент: 10-40% В в течение 5 мин, где А = H2O/0,1% TFA и В = ACN/0,1% TFA, скорость потока: 0,6 мл/мин, колонка: С18 (2) (3 мкм; 20×2 мм) Phenomenex Luna, детектирование: УФ 214 нм). Снятие дополнительных характеристик продукта осуществляли с использованием масс-спектрометрии с электрораспылением.
Полученные соединения приведены в Таблице 3.

Пример 3. Анализ поляризации флуоресценции in vitro
Анализ поляризации флуоресценции использовали для изучения аффинности связывания визуализирующего агента с мишенью cMet, а также связывающих свойств в отношении белков плазмы. Принцип метода поляризации флуоресценции кратко может быть описан следующим образом.
Монохроматический свет проходит через горизонтальный поляризационный фильтр и возбуждает флуоресцентные молекулы в образце. Только те молекулы, которые при ориентации надлежащим образом в вертикальной плоскости поляризации (vertically polarized plane) поглощают свет, становятся возбужденными и впоследствии излучают свет. Излучаемый свет измеряют как в горизонтальной, так и в вертикальной плоскостях. Величина анизотропии (А) представляет собой отношение интенсивностей света, соответствующее уравнению:
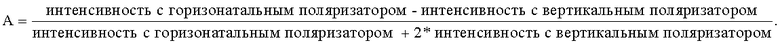
Измерения анизотропии флуоресценции проводили в 384-луночных микропланшетах в объеме 10 мкл в буфере для связывания (PBS; 0,01% Твин-20; рН 7,5) с использованием планшетного ридера поляризации флуоресценции Tecan Safire (Tecan, US) для возбуждения при 635 нм и эмиссии при 678 нм. Концентрацию меченного красителем пептида поддерживали постоянной (5 нМ), а концентрацию химерной конструкции c-Met/Fc человека (R&D Systems) варьировали в диапазоне 0-250 нМ. Для осуществления связывания смеси уравновешивали в микропланшете в течение 10 мин при 30°С. Наблюдаемое изменение анизотропии аппроксимировали к уравнению:
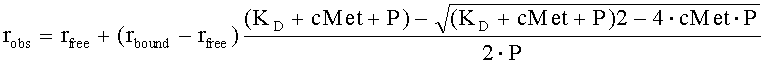
где robs представляет собой наблюдаемую анизотропию, rfree представляет собой анизотропию свободного пептида, rbound представляет собой анизотропию связанного пептида, KD представляет собой константу диссоциации, cMet представляет собой суммарную концентрацию c-Met и Р представляет собой суммарную концентрацию меченного красителем пептида. Согласно уравнению подразумевается, что синтетический пептид и рецептор образуют обратимый комплекс в растворе со стехиометрией 1:1. Подгонку данных выполняли методом нелинейной регрессии, используя программное обеспечение SigmaPlot для получения величины KD (связывание в одном центре).
Соединения 1-6 тестировали в отношении связывания с c-Met человека (химерной конструкцией с Fc). Результаты (смотри Таблицу 4) показали, что KD всех протестированных соединений вследствие связывания с c-Met человека лежат в области наномолярных концентраций.
Изменение величины поляризации использовали для оценки связывания соединения с альбумином сыворотки человека, поскольку небольшое изменение величины поляризации ассоциировано со слабым связыванием, подходящим для применения in vivo. Связывание белков плазмы (РРВ) подтверждали измерениями на Biacore. Стабильность визуализирующего агента в плазме подтверждали, измеряя количество соединения, остающегося после инкубации в мышиной плазме в течение 2 часов при 37°С.

Пример 4. Тестирование соединений 2-6 in vivo
(а) Животная модель
В исследовании использовали самок бестимусных мышей BALB с/А (Bom). Использование животных было одобрено местной комиссией по этическим нормам поведения. Бестимусные мыши BALB с/А представляют собой линию инбредных мышей с ослабленным иммунитетом и с высокой частотой возникновения человеческих опухолей по сравнению с другими линиями бестимусных мышей. Возраст мышей при получении составлял 8 недель, а масса тела в начале исследования составляла приблизительно 20 граммов. Животных размещали в отдельных вентилируемых клетках (IVC, Scanbur BK) с фильтруемым через фильтр HEPA воздухом. Животным предоставляли доступ без ограничения к корму "Rat and Mouse nr. 3 Breeding" (Scanbur BK) и водопроводной воде, подкисленной добавлением HCl до молярной концентрации 1 мМ (рН 3,0).
НТ-29-Клетка рака толстой кишки происходит из карциномы толстой кишки человека, и известно, что экспрессирует c-Met (Zeng et al., Clin. Exp. Metastasis, 21, 409-417 (2004)). Доказано, что данная клеточная линия является канцерогенной при подкожной инокуляции бестимусным мышам (Flatmark et al., Eur. J. Cancer 40, 1593-1598 (2004)).
Клетки НТ-29 выращивали в среде Маккоя 5а (Sigma, № М8403), дополненной 10%-ной фетальной сывороткой теленка и пенициллином/стрептомицином. Концентрированные препараты готовили из пассажа номер четыре (Р4) и замораживали для хранения в жидком азоте в количестве 107 клеток/флакон в соответствующих культуральных средах, содержащих 5% DMSO. В день проведения трансплантации клетки быстро размораживали в водяной бане при 37°С (приблизительно 2 мин), промывали и ресуспендировали в смеси PBS/2% сыворотки (центрифугирование при 1200 об/мин в течение 10 мин). Тщательное перемешивание клеток во флаконах обеспечивали каждый раз, когда клетки всасывали в дозирующий шприц. Клеточную суспензию объемом 0,1 мл вводили посредством подкожной (s.c.) инъекции в плечо и спину, используя иглу с тонким каналом (25 G). После этого животных возвращали в их клетки и опухолям давали возможность расти в течение 13-17 суток. Животным предоставляли период акклиматизации в течение по меньшей мере 5 суток перед процедурой инокуляции.
(б) Процедура
Все тестируемые вещества восстанавливали, используя PBS из лиофилизированного порошка. Для получения плоскостного изображения, которое использовали для коррекции неоднородностей освещения, использовали небольшую стопку белой бумаги для принтера.
Чтобы обездвижить животное во время процедуры оптической визуализации, животных анестезировали изофлураном (обычно 1,3-2%), применяя коаксиальную открытую маску, до обеспечения легкой хирургической стадии наркоза, используя кислород в качестве газа-носителя. Небольшой кусочек кожи (3-5 мм) удаляли над частями опухоли и прилегающей мышцы, используя хирургические щипцы и тонкие ножницы, пока животное находилось под наркозом. Это делали для того, чтобы измерить сигнал от опухоли и мышцы без помех со стороны лежащей сверху кожной ткани. Рану закрывали, применяя жидкий, нефлуоресцентный аэрозоль для наложения повязки (bandage spray) (3М, MN, USA).
Дыхание и температуру тела животного регистрировали, используя систему BioVet (m2m Imaging Corp, NJ, USA), применяя пневматический датчик под животным и ректальный температурный зонд. Система BioVet также позволяла осуществлять внешний обогрев с использованием обогревающего мата с установкой температуры на 40°С для поддержания нормальной температуры тела в продолжение процедуры визуализации (2 часа). В хвостовую вену помещали катетер Venflon для введения контрастного агента. Каждому животному делали одну инъекцию контрастного агента. Объем вводимого инъекцией тестируемого соединения составлял 0,1 мл, вслед за этим незамедлительно осуществляли промывку 0,2 мл физиологического раствора. Картины флуоресценции регистрировали непосредственно перед инъекцией (p.i.) и затем каждые 30 секунд в течение 2 часов.
(в) Визуализация
Визуализацию осуществляли посредством клинического лапароскопа, приспособленного для использования источника света с целью возбуждения репортерного соединения и системы фильтрования для извлечения компонентов флуоресценции. Для возбуждения репортерной молекулы использовали 635 нм лазер. В качестве детектора использовали CCD-камеру Hamamatsu ORCA ERG. Камера работала в режиме биннинга 2×2 с коэффициентом усиления 0. Стандартное время экспонирования для визуализации толстой кишки составляло 4 с. Распределение интенсивностей на изображении корректировали на предмет неоднородностей освещения с использованием калибровочных данных системы. Подсчитывали отношение мишени к фону для представляющих интерес областей, расположенных поверх экспонированной опухоли и нормальной фоновой мышечной ткани.
(г) Результаты
Тестируемые Соединения характеризовались следующими средними соотношениями опухоль: мышца (Таблица 5).
Пример 5. Прогноз метаболизма и токсичности
Средства программного обеспечения Derek и Meteor получали от Lhasa Ltd (22-23 Blenheim Terrace, Leeds LS2 9HD, UK). Derek используют для прогноза токсичности новых химических соединений на основе известной зависимости токсичности от структуры. Аналогичным образом с использованием Meteor предсказывают возможные метаболиты новых химических соединений. Оба программных средства основываются на опубликованных и неопубликованных (но подтвержденных) данных для химических соединений. Вводили химическую структуру красителя DY-652. Ни одного потенциально опасного метаболита in vivo предсказано не было.
Пример 6. Тестирование токсичности соединения 6
Проводили исследование предельной дозы острой токсичности с целью изучения толерантности к соединению 6 в дозе, в 100 раз превышающей дозу, используемую при доклинической визуализации (50 нмоль/кг массы тела).
Соединение вводили самцам крыс посредством внутривенной инъекции и животных умерщвляли на 1-е, 14-е, 21-е и 28-е сутки после инъекции (p.i.). При вскрытии проводили осмотр основных органов на макроскопическую патологию и почки помещали в забуференный до нейтрального значения формалин для последующей гистологической оценки. Непосредственно после инъекции наблюдали слабое голубое окрашивание кожи и умеренное голубое окрашивание мочи, которое исчезало в течение 1-х суток p.i. Почки при вскрытии были диффузно зелеными на 1-е сутки p.i. Световая микроскопия показала отсутствие связанных с соединением 6 изменений. Другие наблюдаемые незначительные изменения были несущественными и общими для молодых лабораторных крыс. Сильное окрашивание флуоресцентным веществом кровеносных сосудов почки наблюдали на 1-е сутки p.i. Окрашивание уменьшалось к 14-м суткам p.i. и становилось неотличимым от контроля на 21-е сутки p.i.
Никаких доказательств дегенерации, некроза или воспаления не было отмечено ни у одного из обработанных животных, что подтверждает низкую нефротоксичность соединения. Было сделано заключение, что однократное внутривенное введение соединения 6 самцам крыс в дозе, в 100 раз превышающей применяемую клиническую дозу, хорошо переносилось и не вызывало каких-либо побочных эффектов, связанных с лекарственным веществом.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОПТИЧЕСКИЕ АГЕНТЫ ВИЗУАЛИЗАЦИИ | 2008 |
|
RU2475266C2 |
| МЕЧЕНЫЕ ПЕПТИДЫ, СВЯЗЫВАЮЩИЕ ФАКТОР РОСТА ГЕПАТОЦИТОВ (HGF), ДЛЯ ВИЗУАЛИЗАЦИИ | 2008 |
|
RU2473361C9 |
| КОМПОЗИЦИИ ПЕПТИДНЫХ РАДИОАКТИВНЫХ ИНДИКАТОРОВ | 2011 |
|
RU2594167C2 |
| СОСТАВ ДЛЯ ОПТИЧЕСКОЙ ВИЗУАЛИЗАЦИИ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2019 |
|
RU2802481C2 |
| ПЕПТИДНЫЕ СОЕДИНЕНИЯ | 2005 |
|
RU2393167C2 |
| СПОСОБ ВИЗУАЛИЗАЦИИ | 2008 |
|
RU2505316C2 |
| УСОВЕРШЕНСТВОВАННЫЕ КОНЪЮГАТЫ N4 ХЕЛАТООБРАЗУЮЩИХ АГЕНТОВ | 2005 |
|
RU2360701C2 |
| КОНТРАСТНЫЙ АГЕНТ, НАЦЕЛЕННЫЙ НА РЕЦЕПТОР УРОКИНАЗНОГО АКТИВАТОРА ПЛАЗМИНОГЕНА | 2005 |
|
RU2394837C2 |
| МОДИФИЦИРОВАННЫЕ ЦИАНИНОВЫЕ КРАСИТЕЛИ И ИХ КОНЪЮГАТЫ | 2020 |
|
RU2833355C2 |
| МЕЧЕНЫЕ МОЛЕКУЛЯРНЫЕ ВИЗУАЛИЗИРУЮЩИЕ АГЕНТЫ, СПОСОБЫ ПОЛУЧЕНИЯ И СПОСОБЫ ПРИМЕНЕНИЯ | 2010 |
|
RU2523411C2 |
Изобретение относится к визуализирующим агентам, подходящим для оптической визуализации in vivo организма млекопитающего. Визуализирующий агент включает конъюгат формулы (I) бензопирилиевого красителя через линкерную группу с 3-100-мерным синтетическим пептидом, обеспечивающим направленную доставку к биологической мишени. Также раскрыты фармацевтическая композиция, включающая указанный конъюгат формулы (I), набор для приготовления указанной фармацевтической композиции и способы визуализации in vivo организма млекопитающего. Изобретение обеспечивает эффективную оптическую визуализацию in vivo организма млекопитающего с регулированием его болезненного состояния. 5 н. и 19 з.п. ф-лы, 5 табл., 6 пр.
1. Фармацевтическая композиция, содержащая визуализирующий агент, подходящий для оптической визуализации in vivo организма млекопитающего, вместе с биосовместимым носителем, причем указанная композиция находится в форме, подходящей для введения млекопитающему, где указанный визуализирующий агент включает конъюгат формулы I:
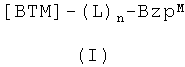
где ВТМ представляет собой 3-100-мерный синтетический пептид;
n представляет собой целое число величиной 0 или 1;
L представляет собой синтетическую линкерную группу формулы -(А)m-, где m представляет собой целое число величиной от 1 до 20, и каждый А независимо представляет собой -CR2-, -CR=CR-, -C≡C-, -CR2CO2-, -CO2CR2-, -NRCO-, -CONR-, -NR(C=O)NR-, -NR(C=S)NR-, -SO2NR-, -NRSO2-, -CR2OCR2-, -CR2SCR2-, -CR2NRCR2-, С4-8циклогетероалкиленовую группу, С4-8циклоалкиленовую группу, С5-12ариленовую группу или С3-12гетероариленовую группу, аминокислоту, сахар или монодисперсный полиэтиленгликолевый (ПЭГ) строительный блок; где каждый R независимо выбран из Н, С1-4алкила, С2-4алкенила, С2-4алкинила, С1-4алкоксиалкила или С1-4гидроксиалкила;
BzpM представляет собой бензопирилиевый краситель формулы II:

где Y1 представляет собой группу формулы Ya или Yb


R1-R4 и R9-R13 независимо выбраны из Н, -SO3M1, Hal, Ra или С3-12арила, где каждый М1 независимо представляет собой Н или Bc, и Bc представляет собой биосовместимый катион;
R5 представляет собой Н, С1-4алкил, C1-6карбоксиалкил, С3-12арилсульфонил, Cl, или R5 вместе с одним из R6, R14 или R15 возможно может образовывать 5- или 6-членное ненасыщенное алифатическое, ненасыщенное гетероалифатическое или ароматическое кольцо;
R6 представляет собой группу Rа;
R7 и R8 независимо представляют собой С1-4алкил, С1-4сульфоалкил или C1-6гидроксиалкил или возможно вместе с одним или обоими R9 и/или R10 могут образовывать 5- или 6-членное N-содержащее гетероциклическое или гетероарильное кольцо;
Х представляет собой -CR14R15-, где R14 и R15 независимо представляют собой группы Ra;
Ra представляет собой С1-4алкил, С1-4сульфоалкил, C1-6карбоксиалкил или C1-6гидроксиалкил;
w равно 1 или 2;
J представляет собой биосовместимый анион;
при условии, что BzpM содержит по меньшей мере один сульфокислотный заместитель, выбранный из групп R1-R4 и из групп R6-R15.
2. Композиция по п.1, где BzpM имеет формулу IIa:

3. Композиция по п.1, где BzpM имеет формулу IIb:

4. Композиция по п.1, где BzpM содержит от 2 до 4 сульфокислотных заместителей.
5. Композиция по п.1, где BzpM содержит по меньшей мере один С1-4сульфоалкильный заместитель.
6. Композиция по п.5, где сульфоалкильный заместитель имеет формулу
-(CH2)kSO3M1, где М1 представляет собой Н или Bc, и k представляет собой целое число величиной от 1 до 4.
7. Композиция по п.1, где w равно 1.
8. Композиция по п.1, где R5 представляет собой Н.
9. Композиция по п.1, где BzpM имеет формулу III:

где Y1, R1-R4, R6, R14, R15 и J являются такими, как определено в п.1.
10. Композиция по п.9, которая содержит формулу IIIc, IIId или IIIe:



где М1 является таким, как определено в п.1;
R17 и R18 независимо выбраны из С1-4алкила или С1-4сульфоалкила;
R19 представляет собой Н или С1-4алкил;
R20 представляет собой С1-4алкил, С1-4сульфоалкил или C1-6карбоксиалкил;
R21 представляет собой С1-4сульфоалкил или C1-6карбоксиалкил;
R22 представляет собой С1-4алкил, С1-4сульфоалкил или C1-6карбоксиалкил;
X2, X3 и X4 независимо представляют собой Н или С1-4алкил.
11. Композиция по п.1, которая содержит формулы IVa или IVb:
 ;
;
 ;
;
где Z1 присоединен к N-концу пептида ВТМ и представляет собой Н или MIG;
Z2 присоединен к С-концу пептида ВТМ и представляет собой ОН, OBc или MIG,
где Bc является таким, как определено в п.1, и
MIG представляет собой ингибирующую метаболизм группу, представляющую собой биосовместимую группу, которая ингибирует или подавляет ферментативный метаболизм пептида ВТМ.
12. Композиция по п.11, где каждый из Z1 и Z2 независимо представляет собой MIG.
13. Композиция по любому из пп.1-12, которая имеет дозировку, подходящую для одного пациента, и предоставлена в подходящем шприце или контейнере.
14. Набор для приготовления фармацевтической композиции по любому из пп.1-13, содержащий конъюгат формулы I, как определено в пп.1-12, в стерильной твердой форме, такой, что после восстановления стерильным источником биосовместимого носителя происходит растворение с получением желаемой фармацевтической композиции.
15. Набор по п.14, где стерильная твердая форма представляет собой лиофилизированное твердое вещество.
16. Конъюгат формулы I:

где L и n являются такими, как определено в п.1, BzpM является таким, как определено в любом из пп.1-10, и ВТМ' представляет собой ВТМ, как определено в п.1.
17. Способ оптической визуализации in vivo организма млекопитающего, включающий применение фармацевтической композиции по любому из пп.1-13 для получения изображений мест локализации ВТМ in vivo.
18. Способ по п.17, где фармацевтическая композиция предварительно введена в организм указанного млекопитающего.
19. Способ по п.18, включающий стадии:
(1) облучения представляющей интерес тканевой поверхности организма млекопитающего возбуждающим светом;
(2) детекции флуоресценции от визуализирующего агента, которая генерируется возбуждением BzpM, с использованием детектора флуоресценции;
(3) возможно, фильтрации света, детектируемого детектором флуоресценции, для отделения компонента флуоресценции;
(4) формирования изображения представляющей интерес указанной тканевой поверхности в результате флуоресцентного света со стадий (2) или (3).
20. Способ по п.19, где возбуждающий свет со стадии (1) по своей природе представляет собой непрерывную волну (CW).
21. Способ по п.18, включающий:
(а) подвергание светорассеивающей биологической ткани организма указанного млекопитающего, имеющей гетерогенный состав, воздействию света от источника света с предварительно определенной изменяющейся во времени интенсивностью для возбуждения визуализирующего агента, причем указанная ткань многократно рассеивает возбуждающий свет;
(б) детекцию эмиссии многократно рассеянного тканью света в ответ на указанное подвергание воздействию;
(в) количественное определение характеристики флуоресценции во всей ткани в результате эмиссии путем установления ряда величин с использованием процессора, каждая из которых соответствует уровню характеристики флуоресценции в разном положении внутри ткани, причем уровень характеристики флуоресценции изменяется в зависимости от гетерогенного состава ткани; и
(г) генерирование изображения ткани путем составления карты гетерогенного состава ткани в соответствии с величинами стадии (в).
22. Способ по п.17, где способ оптической визуализации представляет собой флуоресцентную эндоскопию.
23. Способ по любому из пп.17-22, где оптическую визуализацию in vivo применяют для оказания помощи в детекции, определении стадии, диагностике, мониторинге прогрессирования заболевания или мониторинге лечения болезненного состояния организма млекопитающего.
24. Способ регулирования болезненного состояния организма млекопитающего, выбранный из группы, включающей способ детекции, определения стадии, диагностики, мониторинга прогрессирования заболевания или мониторинга лечения болезненного состояния организма млекопитающего, включающий способ оптической визуализации in vivo по любому из пп.17-23.
| Захват манипулятора | 1985 |
|
SU1281405A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| LISY M-R | |||
| et al | |||
| Journal of Biomedical Optics, 02.01.2007, v.11, №6, p.64014-1-64014-9 | |||
| RU 2004106155 A, 10.07.2005 | |||
| СОЕДИНЕНИЯ НА ОСНОВЕ ПЕПТИДОВ ДЛЯ НАПРАВЛЕННОЙ ДОСТАВКИ К РЕЦЕПТОРАМ ИНТЕГРИНОВ | 2002 |
|
RU2303042C2 |
| ЭФИРЫ 5-АМИНОЛЕВУЛИНОВОЙ КИСЛОТЫ КАК ФОТОЧУВСТВИТЕЛЬНЫЕ АГЕНТЫ В ФОТОХИМИОТЕРАПИИ | 2001 |
|
RU2246483C2 |
| ЦИКЛОПЕПТИДЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1996 |
|
RU2157379C2 |
| ДИАРИЛЬНЫЕ СОЕДИНЕНИЯ С МОСТИКОВОЙ СВЯЗЬЮ | 2002 |
|
RU2297409C2 |
| RU 2004129766 A, 10.08.2005. | |||
Авторы
Даты
2013-06-10—Публикация
2008-07-29—Подача