Настоящее изобретение относится к области органической химии и касается, в частности, способа получения 2,4-динитро- и 2,4,6-тринитробензойных кислот. Данные соединения представляют несомненный практический интерес. Из 2,4-динитро- и 2,4,6-тринитробензойных кислот разработаны способы получения разнообразных гетероциклических систем, являющихся ценными полупродуктами для синтеза биологически активных молекул, исходных соединений в синтезе красителей и ароматических конденсационных полимеров [A.V.Samet, V.N.Marshalkin, K.A.Kislyi, N.B.Chemysheva, Y.A.Strelenko, V.V.Semenov, “Synthetic utilization of polynitroaromatic compounds. 3. Preparation of substituted dibenz [b,f] [1,4] oxazepine-11(10H)-ones from 2,4,6-trinitrobenzoic acid via nucleophilic displacement of nitro groups” // J.Org.Chem., 2005, 70, 9371-9376; К.Ф.Кислый, А.В.Самет, В.В.Семенов, “4,6-Динитроантраниловая кислота и бензоконденсированные 6-членные гетероциклы на ее основе” // ЖОрХ, 2006, 42, 307-308]. Одним из важных направлений утилизации 2,4,6-тринитротолуола, выплавляемого из боеприпасов после окончания срока их хранения, является окисление его до 2,4,6-тринитробензойной кислоты, декарбоксилирование которой в мягких условиях гладко приводит к симтринитробензолу [Е.Ю.Орлова, Химия и технология бризантных взрывчатых веществ, «Химия», Ленинград, 1973, с.180; Shevelev S.A., Tartakovsky V.A., Rusanov A.L. // Conversion of demilitarized TNT to higher value products in "Combustion of Energetic Materials // Ed. K.K.Kuo, L.T.DeLuca. N.Y.: Begell House, Inc., 2002, p.62].
В литературе описаны способы получения 2,4-динитро- и 2,4,6-тринитробензойных кислот окислением соответствующих производных толуола с использованием химических и электрохимического методов. Последние представляются более предпочтительными с экологической точки зрения.
Известно, что широко используемым лабораторным способом получения 2,4,6-тринитробензойной кислоты является окисление 2,4,6-тринитротолуола солями хрома (VI) в концентрированной серной кислоте при 40-55°С [А.Б.Тронов, Н.В.Чернобровин, Н.В.Пупова, «Окисление 2,4,6-тринитробензола до 2,4,6-тринитробензойной кислоты». Труды Алтайского Политехнического института, 1968, №2, с.68-73]. Этот способ модифицируют добавлением уксусной кислоты [Haba Michio, Hatachi Akihisa, “Oxidation of alkyl-substituted aromatic nitro compounds by chromate”, JP 49048420, JP 1970-28018] или используют в качестве окислителя хромовый ангидрид [”Verfahren zur Darstellung von Trinitrobenzoësäure aus Trinitrotoluol” 'Deutsches. Pat. 127325, 1901 (kl. 12o)]. Выход 2,4,6-тринитробензойной кислоты во всех случаях достаточно высокий -от 70 до 98%. При этом, однако, образуется большое количество токсичных и трудно утилизируемых отходов.
Известен способ получения 2,4,6-тринитробензойной кислоты окислением 2,4,6-тринитротолуола азотной кислотой при температуре 180-190°С под давлением 35-40 атм. [A.Astrat'ev, V.Marchukov, V.Suschev, A.Aleksandrov, “Oxidation with aqueous nitric acid: from technology development to pilot process optimization” // Abstracts of 218-th ACS National Meeting, USA, New Orleans, LA, August 22-26, 1999, Abstract №50]. Конверсия 2,4,6-тринитротолуола в оптимальных условиях составляет 40%, выход 2,4,6-тринитробензойной кислоты в расчете на конвертированный 2,4,6-тринитротолуол - 75% (степень чистоты получаемой 2,4,6-тринитробензойной кислоты не приведена). В публикации не указано, замкнуты ли кислотные и щелочные циклы соответственно для получения 2,4,6-тринитробензойной кислоты и ее выделения из смеси продуктов окисления 2,4,6-тринитротолуола. Неясно, насколько безопасно высокотемпературное окисление при утилизации тротила из боеприпасов.
Известен электрохимический способ получения 2,4-динитробензойной кислоты путем электроокисления 2,4-динитротолуола на свинцовом аноде в 50% H2SO4, содержащей 2% CrO3, при температуре 75°С [O.W.Brown, A.E.Brown, “The electrolytic preparation of 2,4-dinitrobenzoic acid from 2,4-dinitrotoluene”, Trans. Electrochem. Soc., 1939, v.75, p.393]. В этих условиях выход 2,4-динитробензойной кислоты по веществу составляет 74%. Однако невысокие значения конверсии (51%) и выхода по току (43%), а также необходимость утилизации анолита, содержащего соединения хрома, являются очевидным недостатком этого способа получения целевого соединения.
Известен, и принятый нами за прототип, способ получения 2,4-динитро- и 2,4,6-тринитробензойных кислот прямым электроокислением 2,4,6-тринитротолуола и 2,4-динитротолуола [F.Sachs, R.Kempf, “Ueber den 2,4-Dinitrobenzaldehyd (II Mittheiliung) Ber., 1902 bd35, 2704-2717]. Электролиз проводили на свинцовом электроде в диафрагменном электролизере в 30% серной кислоте в гальваностатическом режиме при температуре 60°С. Выход по веществу соответствующих полинитробензойных кислот составил около 25%, а по току (согласно проведенному нами расчету - не более 1%). Прямое окисление полинитротолуолов непосредственно на электроде (аноде) не нашло практического применения из-за его низкой эффективности.
Задачей настоящего изобретения является создание практически безотходного способа получения 2,4-динитро- и 2,4,6-тринитробензойных кислот с высоким выходом по веществу и току на примере окисления трудно окисляемых соединений - 2,4-динитро- и 2,4,6-тринитротолуолов.
Поставленная задача достигается предлагаемым способом получения 2,4-динитро- или 2,4,6-тринитробензойных кислот путем электроокисления соответствующих полинитротолуолов в диафрагменном электролизере, снабженном катодом и анодом, в гальваностатическом режиме, в кислой среде, согласно изобретению, электроокисление проводят в присутствии азотнокислого кобальта на платиновом аноде в концентрированной азотной кислоте при температуре 30-40°С и плотности тока 180-700 А·м-2.
Электроокисление проводят с использованием электролизера, снабженного платиновым анодом и катодом, объемом 0,1 л. Анолитом служит раствор соли кобальта (медиатор) в 60-80% азотной кислоте. Католит - 10-15 мл 60%-ного раствора HNO3, помещают в керамический стакан, расположенный по центру ячейки и закрепленный в электролизере с помощью крышки из фторопласта с отверстиями. В качестве катода используют платиновую сетку, а в качестве анода - платиновую пластину.
Около 60% от образующейся 2,4,6-тринитробензойной кислоты выпадает после электролиза в виде белого осадка, оставшуюся в растворе 2,4,6-тринитробензойную кислоту, при необходимости, выделяют экстракцией этилацетатом из разбавленного водой анолита. Для замыкания цикла фильтрат использовали для электроокисления следующей порции полинитротолуола. В случае 2,4-динитротолуола целевая 2,4-динитробензойная кислота также выпадает в виде белого осадка при электролизе из относительно разбавленных растворов азотной кислоты, поэтому ее выделяют экстракцией эфиром при разбавлении анолита водой.
Процесс протекает по следующей схеме:
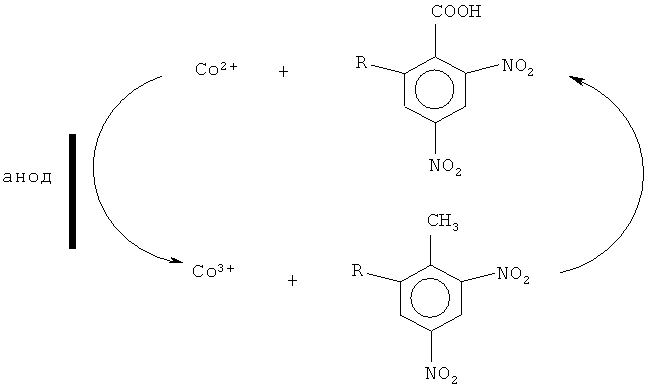
Известно, что для увеличения окислительной способности среды необходимо использовать концентрированные кислоты и высокие концентрации окислителя. Однако использование концентрированной серной кислоты в электросинтезе невозможно из-за низкой проводимости среды. А регенерация хрома (3+) в хром (6+) протекает только в разбавленной серной кислоте. Нами использована система, обладающая большим окислительным потенциалом: соль кобальта в концентрированной азотной кислоте. Электрохимическая регенерация соли кобальта (3+) позволяет не только повысить эффективность окисления, но и дает возможность многократного использования анолита, что не создает существенных проблем при его утилизации.
Проведение электролиза в 80%-ной HNO3 увеличивает выход кислот: 2,4,6-тринитробензойной кислоты до 90%, а 2,4-динитробензойной кислоты - до 94%.
Для обеспечения достаточно высокой скорости взаимодействия полинитросоединений с медиатором и нивелирования образования побочных продуктов электроокисление проводят при температуре 30-40°С. Увеличение температуры анолита до 60°С приводит к снижению выхода целевых кислот. Замечено, что выход 2,4-динитробензойной кислоты более чувствителен к изменению температуры электроокисления, чем выход 2,4,6-тринитробензойной кислоты.
При пропускании теоретического количества электричества (Qтеор), рассчитанного для 6-электронного окисления 2,4,6-тринитротолуола, его конверсия составляет 50-60%. Более высокая конверсия (около 92%) достигается при значении Qтеор=2,4. Однако при этом выход 2,4,6-тринитробензойной кислоты уменьшается на 20-25%. При пропускании Qтеор=1,5-1,7 и 70%-ной конверсии 2,4,6-тринитротолуола удалось достичь 97%-го выхода 2,4,6-тринитробензойной кислоты.
Полная конверсия 2,4-динитротолуола достигается при значении количества пропущенного электричества, близком к удвоенному значению Qтеор. При большем времени электролиза выход 2,4-динитробензойной кислоты падает из-за ее разрушения в условиях длительного эксперимента.
На основании полученных данных были определены оптимальные и наиболее технологически приемлемые условия получения полинитробензойных кислот методом электроокисления полинитротолуолов в присутствии соли кобальта в 60-80% HNO3, при плотности тока 180-700 Ам-2 и температуре 30-40°С.
Количество пропущенного электричества 1,7-2,0 Qтеор. В этих условиях при 70%-ной конверсии 2,4,6-тринитротолуола выход 2,4,6-тринитробензойной кислоты составляет 97%. В случае 2,4-динитротолуола при его полной конверсии выход 2,4-динитробензойной кислоты равняется 78%.
Техническим результатом предлагаемого изобретения является создание безотходного способа получения полинитробензойных кислот при атмосферном давлении и невысоких температурах среды 30-40°С с высоким выходом аналитически чистых кислот.
Изобретение соответствует критерию «новизна», так как в известной научно-технической и патентной литературе отсутствует полная совокупность признаков, характеризующих предлагаемое изобретение.
В литературе известно эффективное использование редокс-систем в подходящих растворителях при электросинтезе замещенных ароматических кислот из замещенных толуолов, имеющих не более одной электроноакцепторной группы в кольце. В качестве редокс-пар, окисленная форма которых регенерируется на аноде, предлагаются Ce4+/Ce3+, Co3+/Co2+, Mn+3/Mn2+ в метансульфоновой кислоте [V.Devadoss, M.Noel, K.Jayaraman, C.Ahmed Basha, “Electrochemical behavior Mn3+/Mn2+ Co3+/2+, Ce4+/3+ redox mediators in methanesulfonic asid” J.Appl. Electrochemistry. 33 (2003) 319-323],
Co3+/Co2+ в уксусной кислоте [G.Falgayrac, A/Savall, “Electro chemical activation of the catalytic effect of cobalt in autoxidation of toluene in acetic acid”, J.Appl. Electrochemistry. 29 (1999) 253-258], Ce4+/Ce3+ в хлорной кислоте [K.Kramer, P.M.Robertson, N.Ibl, “Indirect electrolytic oxidation of some aromatic derivatives”, J.Appl. Electrochemistry. 10 (1980) 29-36].
Система Co3+/Co2+ в 20% (3,5N) азотной кислоте обладает наибольшим из перечисленных выше окислительным потенциалом. Однако окисление производных толуола в этих условиях приводит к образованию соответствующих альдегидов, а не кислот, и применимо только в случае сравнительно легко окисляемых ароматических соединений [H.Wendt, H.Schneider, “Reaction kinetic and reaction techniques for mediated oxidation of methylarenes to aromatic ketones” // J.Appl. Electrochemistry. 16 (1986) 134-146]. В связи с этим использование таких редокс-систем в случае трудно окисляемых полинитротолуолов представлялось далеко не очевидным, что потребовало нахождение условий селективного проведения электроокисления такого рода соединений. О чем свидетельствует тот факт, что до настоящего времени не был предложен эффективный и технологически приемлемый электрохимический способ получения полинитробензойных кислот.
Таким образом, можно сделать вывод, что предлагаемое изобретение соответствует критерию «изобретательский уровень», так как заявленное изобретение не вытекает для специалиста явным образом из известного уровня техники.
Настоящее изобретение промышленно применимо, так как его можно использовать для получения ценных полупродуктов в синтеза биологически активных веществ, исходных соединений в производстве красителей и ароматических конденсационных полимеров, а также на производствах при утилизации 2,4,6-тринитротолуола, выплавляемого из боеприпасов.
Изобретение иллюстрируется следующими примерами, не ограничивающими его объем.
Пример 1.
Раствор 1,55 г Co(NO3)2·6H2O в 15 мл 80% HNO3 помещают в анодное пространство электрохимической ячейки. В катодное пространство, отделенное от анодного керамической мембраной, заливают 10 мл азотной кислоты той же концентрации, анод - платиновая пластина площадью около 15 см2, катод - платиновая сетка. Нитрат кобальта (II) до нитрата кобальта (III) окисляют на аноде в течение 10-15 мин до начала выделения кислорода, при этом окраска раствора изменяется с малиновой на темно-зеленую. В полученный раствор соли кобальта (III) добавляют 2,25 г 2,4,6-тринитротолуола порциями по 0,2 г через 8-10 мин и пропускают ток 1А. Плотность тока 700 Ам-2, количество пропущенного электричества 2,25 А·ч (1,4 Qтеор.). Температуру анолита поддерживают около 40°С. После электролиза анолит охлаждают до 15°С. Выпавший осадок 2,4,6-тринитробензойной кислоты отфильтровывают, промывают ледяной водой и сушат. Вес выделенной в виде осадка кислоты 1,35 г (60%). Промывные воды и фильтрат объединяют, разбавляют водой до 100-120 мл, выпавший осадок не прореагировавшего 2,4,6-тринитротолуола отделяют, сушат и взвешивают для определения конверсии. Фильтрат после отделения 2,4,6-тринитротолуола экстрагируют этилацетатом (3×30 мл), промывают водой, сушат безводным Na2SO4, упаривают органический растворитель и получают 0,91 г смеси 2,4,6-тринитротолуола и 2,4,6-тринитробензойной кислоты, в которой, согласно ПМР-спектру, содержится 83% 2,4,6-тринитробензойной кислоты. Общий выход 2,4,6-тринитробензойной кислоты по веществу составляет 93%, выход по току 59%, конверсия 2,4,6-тринитротолуола - 85%.
Пример 2.
Электроокисление проводят так же как и в примере 1, но используют 60% HNO3 и пропускают 4,75 А·ч (3Qтеор). Общий выход 2,4,6-тринитробензойной кислоты по веществу составляет 63%, выход по току 20%, конверсия 2,4,6-тринитротолуола - 95%.
Пример 3.
Электроокисление 1 г 2,4,6-тринитротолуола проводят так же как и в примере 1, но используют 3,0 г Co(NO3)2·6H2O в 15 мл 72% HNO3 и пропускают 1,2 А·ч электричества (1,7Qтеор). Общий выход 2,4,6-тринитробензойной кислоты по веществу составляет 97%, выход по току 37%, конверсия 2,4,6-тринитротолуола - 70%.
Пример 4.
Проводят электролиз 1,5 г Co(NO3)2·6H2O в 15 мл 72% HNO3 для получения раствора трехвалентного кобальта, как описано в примере 1. 1 г 2,4,6-тринитротолуола добавляют к полученному раствору и ведут электролиз при токе 1А, плотность тока 700 Ам-2, количество электричества пропущено 1,1 А·ч (1,5Qтеор.) при температуре 40°С. После охлаждения до 15°С анолита отделяют осадок 2,4,6-тринитробензойной кислоты, а фильтрат возвращают в электролизер и добавляют 1 г 2,4,6-тринитротолуола, проводят еще один цикл электроокисления при тех же условиях и отделяют образующийся осадок 2,4,6-тринитробензойной кислоты, а фильтрат возвращают в электролизер и добавляют 1 г 2,4,6-тринитротолуола. После трех циклов электроокисления обрабатывают анолит, как описано в примере 1. Суммарный выход по веществу выделенной кислоты в виде осадка составляет 89%, аналитический выход - 96%, выход по току - 45% при конверсии 72%.
Пример 5.
Проводят электролиз 10 г Co(NO3)2·6H2O в 20 мл 60% HNO3 для получения раствора трехвалентного кобальта, как описано выше. В электрохимическую ячейку загружают 1 г 2,4-динитротолуола и пропускают 1,77 А·ч (2Qтеор) при плотности тока 180 Ам-2 и температуре 25-30°С. После электролиза выпавший осадок 2,4-динитробензойной кислоты отделяют фильтрованием, промывают ледяной водой и сушат (0,56 г). Фильтрат разбавляют водой и экстрагируют 2,4-динитробензойную кислоту эфиром. Суммарный выход по веществу 2,4-динитробензойной кислоты составляет 78%, выход по току - 38%, конверсия 2,4-динитротолуола - 100%.
Пример 6.
Раствор 5 г Co(NO3)2·6H2O в 10 мл 80% HNO3 помещают в анодное пространство электрохимической ячейки и проводят электролиз на платиновом электроде 25 мин. Добавляют 0,5 г 2,4 динитротолуола и пропускают 0,44 А·ч - теоретически необходимое количество электричества для окисления 2,4-динитротолуола до 2,4-динитробензойной кислоты при плотности тока 180 Ам-2 и температуре 35-40°С. Анолит разбавляют водой до объема 200 мл и экстрагируют эфиром 2,4-динитротолуол. Выход 2,4-динитробензойной кислоты по веществу составляет 94%, выход по току - 77%, конверсия 2,4-динитротолуола 82%.
Пример 7.
Готовят раствор трехвалентного кобальта в 20 мл 60% HNO3, как описано выше, электролизом 10 г Co(NO3)2·6H2O. В электрохимическую ячейку загружают 1 г 2,4-динитротолуола и пропускают 1,33 А·ч (1,5Qтеор) при плотности тока 360А·м-2 и температуре 30-35°С. После электролиза анолит обрабатывают, как описано в примере 5. Суммарный выход по веществу 2,4-динитробензойной кислоты состовляет 77%, выход по току - 43%, конверсия 2,4-динитротолуола - 83%.
Пример 8.
Электроокисление 1 г 2,4,6-тринитротолуола проводят так же как и в примере 1, но используют 1,56 г Co(NO3)2·6H2O в 15 мл 72% HNO3 и пропускают 1,27 А·ч электричества (1,8Qтеор) при плотности тока 500Ам-2. Общий выход 2,4,6-тринитробензойной кислоты по веществу составляет 98% выход по току 38%, конверсия 2,4,6-тринитротолуола - 70%.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НИТРАТА ЦЕРИЯ (IV) | 2015 |
|
RU2603642C1 |
| СПОСОБ ПОЛУЧЕНИЯ НИТРАТА ЦЕРИЯ (IV) ЭЛЕКТРОХИМИЧЕСКИМ ОКИСЛЕНИЕМ НИТРАТА ЦЕРИЯ (III) | 2015 |
|
RU2578717C1 |
| СОВМЕЩЕННЫЙ СПОСОБ ПОЛУЧЕНИЯ 4-АМИНО-2,6-ДИНИТРО- И 2,4,6-ТРИАМИНОТОЛУОЛОВ | 2008 |
|
RU2368598C1 |
| ЭЛЕКТРОКАТАЛИТИЧЕСКИЙ СПОСОБ СИНТЕЗА УГЛЕВОДОРОДОВ И СПИРТОВ НА ОСНОВЕ РАСТИТЕЛЬНОГО СЫРЬЯ | 2011 |
|
RU2471890C1 |
| СПОСОБ ЭЛЕКТРОХИМИЧЕСКОГО ОКИСЛЕНИЯ ЦЕРИЯ | 2016 |
|
RU2623542C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭТИЛОВОГО ЭФИРА П-АМИНОБЕНЗОЙНОЙ КИСЛОТЫ (АНЕСТЕЗИН) | 2006 |
|
RU2302405C1 |
| Способ электроокисления ионов церия (III) | 2018 |
|
RU2673809C1 |
| Способ получения диметилдисульфона | 2017 |
|
RU2641302C1 |
| Способ получения хинолиновой кислоты | 1961 |
|
SU140062A1 |
| СПОСОБ РЕГЕНЕРАЦИИ ХРОМАТНОГО РАСТВОРА ПАССИВИРОВАНИЯ ЦИНКА | 2018 |
|
RU2685840C1 |
Изобретение относится к способу получения 2,4-динитро- или 2,4,6-тринитробензойных кислот, которые находят применение в качестве полупродуктов в синтезе биологически активных веществ, исходных соединений в производстве красителей и ароматических конденсационных полимеров. Предлагаемый способ получения 2,4-динитро- или 2,4,6-тринитробензойных кислот включает электроокисление соответствующих полинитротолуолов в диафрагменном электролизере, снабженном катодом и анодом, в гальваностатическом режиме, в кислой среде. Способ характеризуется тем, что электроокисление проводят в присутствии азотнокислого кобальта на платиновом аноде в концентрированной азотной кислоте при температуре 30-40°С и плотности тока 180-700 А·м-2. Способ позволяет получать 2,4-динитро- или 2,4,6-тринитробензойные кислоты с высоким выходом по веществу и току. 8 пр.
Способ получения 2,4-динитро- или 2,4,6-тринитробензойных кислот путем электроокисления соответствующих полинитротолуолов в диафрагменном электролизере, снабженном катодом и анодом, в гальваностатическом режиме, в кислой среде, отличающийся тем, что электроокисление проводят в присутствии азотнокислого кобальта на платиновом аноде в концентрированной азотной кислоте при температуре 30-40°С и плотности тока 180-700 А·м-2.
| F.SACHS et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| (II | |||
| Mittheilung), BERICHTE DER DEUTSCHEN CHEMISCHEN GESELLSCHAFT, 1902, Vol.35, pp.2704-2717 | |||
| Способ превращения провитаминов группы Д в витамины Д | 1955 |
|
SU102762A1 |
| H.WENDT et al | |||
| Reaction kinetics and reaction techniques for mediated oxidation of methylarenes to aromatic ketones, J | |||
| APPL | |||
| ELECTROCHEMISTRY, 1986, Vol.16, pp.134-146. | |||
Авторы
Даты
2013-06-20—Публикация
2012-04-18—Подача