Взаимодействие содержащих рутений или соединения рутения катализаторов с сернистыми соединениями во многих типичных сферах практического использования указанных катализаторов приводит к необратимому снижению их активности, что согласно общему мнению следует объяснить их отравлением. Настоящее изобретение относится к способу, в соответствии с которым содержание серы в содержащем рутений или соединения рутения катализаторе, отравленном серой в виде сернистых соединений, путем реализуемой в неокислительных условиях целенаправленной обработки содержащим хлороводород потоком может быть уменьшено настолько, что активность подобного катализатора повышается до активности аналогичного катализатора, не отравленного серой в виде сернистых соединений. Успех подобной регенерации может быть продемонстрирован на примерах каталитического окисления хлороводорода кислородом и окисления монооксида углерода кислородом.
Типичной сферой применения содержащего рутений или соединения рутения катализатора является получение хлора путем газофазного окисления хлороводорода кислородом:
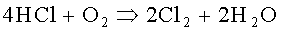
Речь при этом идет о равновесной реакции. При повышении ее температуры положение равновесия смещается не в сторону образования целевого конечного продукта. В связи с этим предпочтительным является использование обладающих максимально высокой активностью катализаторов, которые способствуют протеканию указанной реакции при пониженной температуре.
Первые катализаторы окисления хлороводорода содержали в качестве активного компонента хлорид меди, соответственно оксид меди, и были описаны Диконом еще в 1868 году. Однако при пониженных температурах (ниже 400°С) они обладали весьма незначительной активностью. Хотя активность указанных катализаторов и удавалось увеличить за счет повышения температуры реакции, однако летучесть активного компонента обусловливала их быстрое деактивирование.
Поскольку несмотря на интенсивные усилия исследователей до 60-х годов двадцатого столетия не удавалось достичь существенного прогресса в рассматриваемой области, названный по имени первооткрывателя способ Дикона был оттеснен на задний план хлор-щелочным электролизом. До 90-х годов практически весь хлор производили путем электролиза водных растворов хлорида натрия [Ullmann Encyclopedia of industrial chemistry, seventh release, 2006]. Однако поскольку мировая потребность в хлоре в настоящее время растет более интенсивно по сравнению со спросом на раствор едкого натра, способ Дикона не утратил своей привлекательности, так как он позволяет повторно использовать для получения хлора хлороводород, который в значительных объемах образуется в качестве сопутствующего продукта, например, при фосгенировании аминов.
Существенный прогресс в сфере окисления хлороводорода был достигнут благодаря открытию возможности использования рутения, или соответственно соединений рутения, в качестве каталитически активных компонентов, которая впервые была описана в 1965 году в немецком патенте DE 1567788. С тех пор был достигнут существенный прогресс, обусловленный в первую очередь тем, что удалось найти надлежащий носитель. Особенно пригодным носителем оказался диоксид титана, использование которого описано, например, в европейской заявке на патент ЕР 743277 А1, а также диоксид олова, об использовании которого сообщается, например, в немецкой заявке на патент DE 102006024543 А1.
К другим типичным сферам использования содержащих рутений или соединения рутения катализаторов относятся (селективное) окисление монооксида углерода и очистка отходящего воздуха. В заявке США на патент US 7247592 B2 описан содержащий рутений, соответственно соединения рутения, катализатор селективного окисления монооксида углерода. Из заявки США на патент US 7318915 B2 известно о применении содержащих рутений, или соответственно соединения рутения, катализаторов для комбинированного применения в сфере обработки отходящего воздуха. Описываемый в этом документе катализатор окисляет монооксид углерода и летучие углеводороды, и одновременно происходит восстановление нитрозных газов.
Известно также о многих других сферах использования содержащих рутений или соединения рутения катализаторов. Содержащие рутений или соединения рутения катализаторы часто играют ключевую роль, в частности, при синтезе органических исходных материалов из нефтяных фракций, природного газа или угля.
Крупной проблемой использования содержащих рутений или соединения рутения катализаторов несомненно является их чувствительность по отношению к сере. Присутствие серы в исходном потоке может быть обусловлено, например, использованием содержащего серу сырья (например, нефтяных фракций, природного газа, угля) или реализацией некоторых предшествующих катализу процессов (например, сушки газа серной кислотой или серосодержащим активированным углем). Как известно, например, из международной заявки WO 2007066810 А1, решающее значение для продолжительности службы содержащего рутений, или соответственно соединения рутения, катализатора окисления хлороводорода имеет содержание серы в исходном потоке, которое необходимо снижать до уровня менее 2 м.д. В соответствии с цитируемой публикацией для снижения содержания серы используют различные оксиды, с которыми присутствующие в исходном потоке серосодержащие компоненты вступают во взаимодействие. Недостатком подобного способа является возможность попадания летучих хлоридов этих элементов на катализатор, а также проскок сернистых соединении при возникновении их пиковых концентраций.
Ранее уже были описаны способы регенерации содержащих рутений, соответственно соединения рутения катализаторов, отравленных серой в виде сернистых соединений, однако подобные способы страдают различными недостатками. Так, например, из заявки Великобритании на патент GB 744049 А известно, что содержащие рутений или соответственно соединения рутения катализаторы, отравленные серой в виде сернистых соединений, могут быть регенерированы путем промывки. При этом в качестве примеров промывочной жидкости в цитируемой публикации указывают воду, этанол, уксусную кислоту, циклогексан, бензол и ацетон. Однако промывка катализатора всегда бывает сопряжена с риском уноса части его активных компонентов промывочной жидкостью. Подобный унос может являться результатом протекания физико-химических процессов (например, химических реакций в сочетании с абсорбцией, а также растворимости), а также механических процессов (например, истирания). Кроме того, подобная промывка, как правило, требует предварительной выгрузки подлежащего промывке катализатора из используемого для осуществления целевой реакции реактора.
В заявке Великобритании на патент GB 1278119 А описана регенерация содержащего рутений, соответственно соединения рутения катализатора, отравленного серой в виде сернистых соединений, которую осуществляют путем восстанавливающей обработки катализатора безводным потоком водорода при температуре от 430 до 595°С и давлении, находящемся в интервале от 3 до 24 бар, а также некоторых других операций окисления и восстановления. Подобное сочетание восстанавливающих условий с высокими температурами обеспечивает максимально полное восстановление присутствующих в катализаторе оксидов рутения до металлического рутения, включая самые глубокие слои. Однако подобная обработка сопровождается резкими изменениями в содержащем рутений, или соответственно соединения рутения катализаторе, которые могут оказаться нежелательными для некоторых сфер его применения. Кроме того, подобная обработка требует использования герметичных реакторов, трубопроводов и арматуры, в связи с чем подвергаемый ей катализатор, как правило, подлежит выгрузке.
Таким образом, до последнего времени не существует пригодного для несложного практического использования способа, позволяющего в мягких условиях выполнять регенерацию содержащего рутений или соединения рутения катализатора, отравленного серой в виде сернистых соединений. Использование всех известных до настоящего времени способов регенерации указанных катализаторов сопряжено с риском частичной потери рутения или нежелательного изменения структуры катализатора. Вследствие этого медленное отравление содержащего рутений или соединения рутения катализатора серой в виде сернистых соединений продолжает оставаться фактором, ограничивающим срок службы указанного катализатора во многих сферах его применения. Наиболее неблагоприятной является мгновенная необратимая потеря активности катализатора вследствие самопроизвольного возникновения пикового содержания серы, возможность которого обусловлена, например, нестационарным режимом пуска. Оба указанных фактора таят в себе огромный экономический риск, поскольку повторное использование содержащегося в отработанном катализаторе рутения является весьма трудоемкой операцией, реализация которой может сопровождаться частичной потерей рутения.
С учетом вышеизложенного в основу настоящего изобретения была положена задача предложить эффективный и простой способ регенерации содержащего рутений или соединения рутения катализатора, отравленного серой в виде сернистых соединений, с возможностью его реализации в щадящем режиме.
Неожиданно было обнаружено, что содержание серы в содержащем рутений или соединения рутения катализаторе, отравленном серой в виде сернистых соединений, путем целенаправленной обработки указанного катализатора содержащим галогеноводород, в частности хлороводород, газовым потоком, реализуемой в неокислительных условиях при необходимости при повышенной температуре, может быть уменьшено до такой степени, что активность указанного катализатора возрастает, достигая активности аналогичного катализатора, который не был отравлен серой в виде сернистых соединений.
Объектом настоящего изобретения является способ регенерации содержащего рутений или соединения рутения катализатора, отравленного серой в виде сернистых соединений, отличающийся тем, что катализатор подвергают обработке содержащим галогеноводород, в частности хлороводород, газовым потоком, реализуемой в неокислительных условиях при необходимости при повышенной температуре.
В дальнейшем вместо словесного оборота «регенерация содержащего рутений или соединения рутения катализатора, отравленного серой» для краткости используют также такие термины, как «регенерация катализатора», «регенерация» или подобные обозначения. Предлагаемый в изобретении способ пригоден для регенерации катализаторов как на основе металлического рутения, так и на основе соединений рутения. Предпочтительными соединениями рутения являются индивидуальные галогениды рутения, в частности хлориды рутения, оксидгалогениды рутения, в частности оксидхлориды рутения, или оксиды рутения, или смеси указанных соединений рутения. При этом для регенерации содержащих хлор соединений рутения предпочтительно используют хлороводород.
В соответствии с настоящим изобретением катализатор считают отравленным в том случае, если каталитическая активность, определяемая по конверсии на отравленном серой в виде сернистых соединений, содержащем рутений или соединения рутения катализаторе (рабочем катализаторе) в дифференциальном диапазоне конверсии катализируемой реакции (конверсия <=10%), понизилась, в частности, по меньшей мере на 5%, предпочтительно по меньшей мере на 10%, особенно предпочтительно по меньшей мере на 20%. В возможном предпочтительном варианте с целью определения потери активности катализатора от поступающего в реактор основного потока отделяют небольшой боковой поток, который пропускают через отдельный слой состоящего из аналогичного материала катализатора, на котором благодаря выбору соответствующего времени контакта достигают дифференциальную конверсию. В возможном предпочтительном варианте небольшую часть отобранного из реактора содержащего рутений или соединения рутения рабочего катализатора преобразуют в отдельный слой, на котором реализуют модельную реакцию и определяют потерю каталитической активности в дифференциальном диапазоне конверсии посредством выбора соответствующего времени контакта.
Сернистыми соединениями, которые вызывают отравление (деактивирование) содержащих рутений или соединения рутения катализаторов, предпочтительно могут являться одно или несколько соединений, выбранных из группы, включающей H2SO4, H2SO3, SO3, SO2, COS, H2S, а также соли H2SO4 и H2SO3. В результате протекающей на поверхности катализатора реакции указанные сернистые соединения в окислительных условиях предпочтительно превращаются в оксиды серы, которые соединяются с поверхностью катализатора предпочтительно через мостиковые атомы кислорода или посредством химических связей «сера-металл». В восстанавливающих условиях сера соединяется с поверхностью катализатора предпочтительно посредством химических связей «сера-металл». Предлагаемый в изобретении способ позволяет вновь перевести находящуюся в виде сернистых соединений серу, иммобилизованную на поверхности катализатора вследствие протекающей на ней реакции, в летучие сернистые соединения, которые в дальнейшем могут быть удалены с поверхности катализатора.
Регенерацию катализатора, в частности, осуществляют при температуре до 600°С. В предпочтительном варианте регенерацию катализатора осуществляют в температурном интервале от 200 до 500°С, в то время как в особенно предпочтительном варианте ее осуществляют в температурном интервале от 300 до 450°С.
Регенерирующий поток содержит галогеноводород, предпочтительно хлороводород, причем содержание галогеноводорода предпочтительно составляет от 0,1 до 100% об. В предпочтительном варианте осуществления изобретения содержание галогеноводорода в регенерирующем потоке составляет от 1 до 30% об., особенно предпочтительно от 5 до 25% об. Другими компонентами регенерирующего потока, в частности, могут являться инертные газы, например, такие как азот или аргон. Вместо свободного галогеноводорода можно использовать также вещества, соответственно смеси веществ, которые в указанных выше условиях регенерации выделяют свободный галогеноводород, то есть, в частности, хлороводород, фтороводород, бромоводород или иодоводород, или вещества, соответственно смеси веществ, содержащиеся в которых функциональные атомы водорода и галогена в указанных выше условиях регенерации проявляют сравнимое со свободным галогеноводородом действие. Примером последних может служить фосген.
Поток регенерационного газа содержит лишь незначительное количество кислорода, в частности составляющее не более 1% об., предпочтительно не более 0,2% об., особенно предпочтительно не более 0,1% об. В особенно предпочтительном варианте осуществления изобретения регенерирующий поток вообще не содержит кислорода.
Как показывает опыт, указанные выше используемые для регенерации газы нередко содержат технически обусловленные примеси (их содержание по порядку величины составляет менее 1000 м.д.), например хлор и воду, присутствие которых не оказывает отрицательного воздействия на регенерацию. Целесообразным является предварительное удаление вредных примесей (например, серы в виде сернистых соединений или кислорода) из регенерационного газа.
Длительность регенерации предпочтительно составляет от 0,5 до 100 часов. В случае слишком длительной регенерации может произойти непреднамеренное снижение содержания рутения в катализаторе, обусловленное образованием летучих соединений этого металла. Оптимальная длительность регенерации катализатора, в частности, зависит от количества присутствующей в нем серы, температуры регенерации и содержания хлороводорода в регенерирующем потоке. Регенерацию катализатора можно осуществлять в одну стадию или в течение нескольких временных интервалов. Регенерацию предпочтительно осуществляют в течение нескольких временных интервалов, между которыми определяют содержание серы и/или активность катализатора.
В особенно предпочтительном варианте катализатор во время регенерации остается в реакторе, в котором осуществляют также и каталитическую целевую реакцию. В соответствии с возможной предпочтительной реализацией подобного варианта регенерацию выполняют в потоке регенерирующего газа, противоположном его обычному направлению, что позволяет избежать попадания отделенных от катализатора содержащих серу компонентов в слабо отравленные или неотравленные слои катализатора.
Предпочтительным является использование предлагаемого в изобретении способа для регенерации содержащих рутений или соединения рутения катализаторов газофазного окисления хлороводорода кислородом, поскольку в этом случае уже имеется необходимая для обращения с хлороводородом аппаратура, а катализатор должен сохранять стойкость к хлороводороду также и в процессе регенерации.
Предпочтительным является использование предлагаемого в изобретении способа для регенерации катализаторов, активный компонент которых состоит главным образом из рутения или соединений рутения на носителе. Особенно предпочтительным является использование предлагаемого в изобретении способа для регенерации содержащих рутений или соединения рутения катализаторов, носитель которых преимущественно обладает структурой рутила. Особенно предпочтительным является также использование предлагаемого в изобретении способа для регенерации содержащих рутений или соединения рутения катализаторов, носитель которых содержит диоксид титана, оксид алюминия, оксид циркония, диоксид олова или их смеси. Предпочтительным является использование предлагаемого в изобретении способа для регенерации катализатора синтеза изоцианатов, осуществляемого на нескольких взаимосвязанных стадиях, включая стадию катализируемого окисления хлороводорода, некоторые из которых в принципе известны, например из европейской заявки на патент ЕР 1867631 А1.
Предпочтительным является комбинирование предлагаемого в изобретении способа со способом каталитического газофазного окисления, известным как процесс Дикона. Речь при этом идет о сопровождаемой образованием водяного пара экзотермической равновесной реакции окисления хлороводорода кислородом до хлора. Температура указанной реакции обычно составляет от 150 до 500°С, давление обычно находится в интервале от 1 до 25 бар. Поскольку речь идет о равновесной реакции, ее целесообразно осуществлять при как можно более низкой температуре, при которой катализатор еще обладает достаточной активностью. Кроме того, кислород целесообразно использовать в сверхстехиометрических количествах по отношению к хлороводороду. Обычным является, например, использование кислорода в избытке от двухкратного до четырехкратного. Поскольку опасаться снижения селективности не следует, может оказаться экономически благоприятным осуществление процесса при относительно высоком давлении и соответственно при более длительном времени пребывания по сравнению с нормальным давлением.
Каталитическое окисление хлороводорода можно осуществлять в адиабатическом, а также предпочтительно в изотермическом или почти изотермическом режиме, периодически, однако предпочтительно непрерывно, в псевдоожиженном или неподвижном слое катализатора, предпочтительно в неподвижном слое катализатора, особенно предпочтительно в трубчатых реакторах, на гетерогенных катализаторах при температуре от 180 до 500°С, предпочтительно от 200 до 400°С, особенно предпочтительно от 220 до 350°С, и давлении от 1 до 25 бар (от 1000 до 25000 гпа), предпочтительно от 1,2 до 20 бар, особенно предпочтительно от 1,5 до 17 бар, и в частности от 2,0 до 15 бар.
Устройствами, в которых обычно осуществляют каталитическое окисление хлороводорода, являются реакторы со стационарным слоем катализатора или реакторы с псевдоожиженным слоем катализатора. Каталитическое окисление хлороводорода предпочтительно можно осуществлять также в несколько стадий.
Конверсия хлороводорода при однократном пропускании реагентов через реактор предпочтительно находится в интервале от 15 до 90%, предпочтительно от 40 до 90%, особенно предпочтительно от 50 до 90%. Непревращенный хлороводород после разделения продуктов реакции можно частично или полностью возвращать на стадию каталитического окисления хлороводорода.
В случае адиабатического или почти адиабатического режима каталитического окисления хлороводорода можно использовать также (при дополнительном промежуточном охлаждении) несколько последовательно соединенных реакторов, число которых может составлять от 2 до 10, предпочтительно от 2 до 6, особенно предпочтительно от 2 до 5, и в частности от 2 до 3. Хлороводород вместе с кислородом можно полностью подавать в первый реактор или распределять его по отдельным реакторам. Последовательное соединение отдельных реакторов может быть реализовано также в одном аппарате. В подобном случае предоставляется возможность простой реализации предпочтительного метода очистки катализатора в виде технологии in situ, в соответствии с которой один реактор каскада реакторов исключают из процесса Дикона и содержащийся в нем катализатор подвергают предлагаемой в изобретении регенерации.
Другой предпочтительный вариант исполнения устройства, пригодного для реализации процесса Дикона, предусматривает использование структурированного насыпного слоя катализатора, каталитическая активность которого возрастает в направлении потока. Соответствующее структурирование насыпного слоя катализатора может быть достигнуто благодаря разной пропитке носителя катализатора активной массой или благодаря разному разбавлению катализатора инертным материалом. В качестве инертного материала можно использовать, например, кольца, цилиндры или шарики из диоксида титана, диоксида циркония или их смесей, а также из оксида алюминия, стеатита, керамики, стекла, графита или специальной стали. В случае предпочтительного использования формованных частиц катализатора частицы инертного материала предпочтительно должны обладать аналогичными наружными размерами.
Предпочтительные катализаторы, пригодные для осуществления процесса Дикона, содержат оксиды рутения, хлориды рутения или другие соединения рутения. Пригодными материалами носителя являются, например, диоксид кремния, графит, диоксид титана со структурой рутила или анатаза, диоксид циркония, оксид алюминия или их смеси, предпочтительно диоксид титана, диоксид циркония, оксид алюминия или их смеси, особенно предпочтительно γ-оксид алюминия, δ-оксид алюминия или смеси этих модификаций оксида алюминия. Пригодные катализаторы могут быть получены, например, путем нанесения хлорида рутения(III) на носитель и последующей сушки или сушки с прокаливанием. Пригодные катализаторы помимо соединения рутения могут содержать также соединения других благородных металлов, например золота, палладия, платины, осмия, иридия, серебра, меди или рения. Пригодные катализаторы могут содержать также оксид хрома(III).
В качестве используемых для легирования катализаторов промоторов пригодны щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, предпочтительно литий, натрий и калий, особенно предпочтительно калий, щелочноземельные металлы, такие как магний, кальций, стронций и барий, предпочтительно магний и кальций, особенно предпочтительно магний, редкоземельные металлы, такие как скандий, иттрий, лантан, церий, празеодим и неодим, предпочтительно скандий, иттрий, лантан и церий, особенно предпочтительно лантан и церий, или их смеси.
Придание катализаторам надлежащей формы можно выполнять после или предпочтительно до пропитки материала носителя. Пригодными являются формованные частицы катализатора любой конфигурации, причем предпочтительными являются таблетки, кольца, цилиндры, звезды, колеса или шары, особенно предпочтительно кольца, цилиндры или стренги со звездообразным сечением. Формованные частицы катализатора в дальнейшем могут быть подвергнуты сушке, осуществляемой при температуре от 100 до 400°С, предпочтительно от 100 до 300°С, например, в атмосфере азота, аргона или воздуха, и при необходимости прокаливанию. Формованные частицы катализатора предпочтительно сначала сушат при температуре от 100 до 150°С, а затем прокаливают при температуре от 200 до 400°С.
Другим возможным применением предлагаемого в изобретении способа является регенерация катализатора, используемого в качестве «жертвенного» слоя, предшествующего обычному катализатору основной реакции, в частности реакции Дикона, и защищающего последний в первую очередь от сернистых соединений, а также от других каталитических ядов.
Приведенные ниже примеры служат для более подробного пояснения настоящего изобретения.
Примеры
Часть 1. Приготовление катализаторов
В качестве носителя гранулированных рутениевых катализаторов для большей наглядности использовали SnO2, соответственно TiO2.
Пример 1а
200 г гранулированного SnO2 в виде шариков диаметром около 1,9 мм (фирма Alfa Aesar) пропитывали раствором 9,99 г n-гидратированного хлорида рутения в 33,96 мл воды, после чего в течение одного часа осуществляли перемешивание. Влажное твердое вещество в течение 4 часов сушили при 60°С в муфельной печи в атмосфере воздуха, а затем в течение 16 часов прокаливали при 250°С.
Пример 1b
100 г гранулированного TiO2 в виде цилиндров диаметром около 2 мм и длиной от 2 до 10 мм (фирма Saint-Gobain) пропитывали раствором n-гидратированного хлорида рутения в воде таким образом, чтобы содержание рутения составляло 3% масс. Полученные влажные гранулы в течение ночи сушили при 60°С, в сухом состоянии в атмосфере азота погружали в раствор NaOH и 25%-ный раствор гидразингидрата в воде и выдерживали в течение одного часа. Затем упаривали избыточную воду. Влажные гранулы сушили в течение 2 часов при 60°С, после чего последовательно промывали четырьмя порциями воды по 300 г каждая. Полученные влажные гранулы в течение 20 минут сушили при 120°С в муфельной печи в атмосфере воздухе, а затем в течение 3 часов прокаливали при 350°С.
Часть 2. Отравление катализаторов сернистыми соединениями
Для большей наглядности часть приготовленных указанным выше образом гранул катализатора подвергали целенаправленному отравлению серой в виде сернистых соединений (COS, или соответственно SO2). Обозначение отравленных катализаторов и наиболее важные параметры процесса отравления приведены также в таблице 1.
Пример 2а
5 г приготовленных согласно примеру 1а гранул катализатора помещали в кварцевую реакционную трубку диаметром 10 мм, через которую при 330°С в течение одного часа пропускали газовую смесь, состоящую из хлороводорода (5 л/ч), кислорода (20 л/ч), азота (25 л/ч) и COS (0,05 л/ч).
Пример 2b
5 г приготовленных согласно примеру 1а гранул катализатора помещали в кварцевую реакционную трубку диаметром 10 мм, через которую при 330°С в течение одного часа пропускали газовую смесь, состоящую из хлороводорода (5 л/ч), кислорода (20 л/ч), азота (25 л/ч) и SO2 (0,05 л/ч).
Пример 2с
5 г приготовленных согласно примеру 1b гранул катализатора помещали в кварцевую реакционную трубку диаметром 10 мм, через которую при 330°С в течение одного часа пропускали газовую смесь, состоящую из хлороводорода (5 л/ч), кислорода (20 л/ч), азота (25 л/ч) и COS (0,05 л/ч).
Пример 2d
5 г приготовленных согласно примеру 1b гранул катализатора помещали в кварцевую реакционную трубку диаметром 10 мм, через которую при 330°С в течение одного часа пропускали газовую смесь, состоящую из хлороводорода (5 л/ч), кислорода (20 л/ч), азота (25 л/ч) и SO2 (0,05 л/ч).
Пример 3. Поинтервальная регенерация рутениевых катализаторов на SnO2 в качестве носителя, отравленных серой в виде сернистых соединений (COS и SO2)
Ниже описано поинтервальное выполнение регенерации (с временными интервалами от i до v) и соответствующие технологические операции.
По 1 г гранул катализаторов из примеров 1а, 2а и 2b загружали соответственно в три кварцевые реакционные трубки диаметром 10 мм, через которые соответственно в течение 16 часов пропускали газовую смесь 1 (10 л/ч), состоящую из хлороводорода (1 л/ч), кислорода (4 л/ч) и азота (5 л/ч), после чего с целью регенерации через соответствующие реакционные трубки в течение определенного интервала времени пропускали газовую смесь 2 (6 л/ч), состоящую из хлороводорода (1 л/ч) и азота (5 л/ч). После каждого временного интервала регенерации вновь переходили на газовую смесь 1 (10 л/ч) и по истечении примерно одного часа пропускания указанной смеси с целью контроля результатов регенерации газовый поток продуктов реакции каждого из реакторов дважды в течение примерно 15 минут пропускали через 20-процентный раствор иодида калия. После этого с целью определения количества вводимого в указанный раствор хлора образовавшийся йод оттитровывали 0,1н. стандартным раствором тиосульфата (двойное определение). На основании результатов определения количества хлора по приведенной ниже формуле вычисляли показатель RZA - выход хлора в расчете на единицу объема и единицу времени (смотри таблицу 3а):
RZA = г (хлор) × г-1 (катализатор) × ч-1 (время).
Непосредственно после регенерации гранулы катализатора выгружали из соответствующих реакционных трубок, растирали в ступке и методом RFA определяли содержание рутения и серы (смотри таблицу 3b). Аналогичным образом анализировали также не подвергнутые регенерации гранулы катализатора.
Показатель RZA отравленных серой катализаторов (2а, 2b) после каждого интервала регенерации возрастал, причем после последнего интервала регенерации (v) он соответствовал показателю RZA неотравленного сравнительного катализатора (1а). Очевидно, что регенерация в течение совокупности всех временных интервалов полностью компенсирует потерю RZA, обусловленную отравлением катализаторов серой в виде сернистых соединений. Успеха достигали при регенерации рутениевых катализаторов на носителе, отравленных как COS, так и SO2. В обоих случаях прирост показателя RZA явным образом коррелирует со значительным снижением содержания серы в катализаторах. Существенных потерь рутения не обнаружено.
Пример 4. Поинтервальная регенерация отравленных серой в виде сернистых соединений (COS и SO2) рутениевых катализаторов на TiO2 в качестве носителя
Ниже описано поинтервальное выполнение регенерации (с временными интервалами от i до iii) и соответствующие технологические операции.
По 1 г гранул катализаторов из примеров 1b, 2с и 2d загружали соответственно в три кварцевые реакционные трубки диаметром 10 мм, через которые соответственно в течение 16 часов пропускали газовую смесь 1 (10 л/ч), состоящую из хлороводорода (1 л/ч), кислорода (4 л/ч) и азота (5 л/ч), после чего с целью регенерации через соответствующие реакционные трубки в течение определенного интервала времени пропускали газовую смесь 2 (6 л/ч), состоящую из хлороводорода (1 л/ч) и азота (5 л/ч). После каждого временного интервала регенерации вновь переходили на газовую смесь 1 (10 л/ч) и по истечении примерно одного часа пропускания указанной смеси с целью контроля результатов регенерации газовый поток продуктов реакции каждого из реакторов дважды в течение примерно 15 минут пропускали через 20%-ный раствор йодида калия. После этого с целью определения количества вводимого в указанный раствор хлора образовавшийся йод оттитровывали 0,1н. стандартным раствором тиосульфата (двойное определение). На основании результатов определения количества хлора по приведенной ниже формуле вычисляли показатель RZA - выход хлора в расчете на единицу объема и единицу времени (смотри таблицу 4а):
RZA = г (хлор) × г-1 (катализатор) × ч-1 (время).
Непосредственно после регенерации гранулы катализатора выгружали из соответствующих реакционных трубок, растирали в ступке и методом RFA определяли содержание рутения и серы (смотри таблицу 4b). Аналогичным образом анализировали также не подвергнутые регенерации гранулы катализатора.
Показатель RZA отравленных серой катализаторов (2с, 2d) после каждого интервала регенерации возрастал, причем после последнего интервала регенерации (интервала iii) он соответствовал показателю RZA неотравленного сравнительного катализатора (1b). Очевидно, что регенерация в течение совокупности всех временных интервалов полностью компенсирует потерю RZA, обусловленную отравлением катализаторов серой в виде сернистых соединений. Успеха достигали при регенерации рутениевых катализаторов на носителе, отравленных как COS, так и SO2. Использование другого носителя (TiO2 вместо SnO2), очевидно, не оказывает отрицательного влияния на результаты регенерации. Прирост показателя RZA явным образом коррелирует со значительным снижением содержания серы в катализаторах. Существенных потерь рутения не обнаружено.
Пример 5. Одностадийная регенерация рутениевых катализаторов на носителе (SnO2), отравленных серой в виде соединения серы (SO2)
Гранулированные катализаторы 1а и 2b (соответственно 1 г и 0,42 г) загружали в соответствующие кварцевые реакционные трубки диаметром 10 мм, через которые пропускали газовую смесь 1 (10 л/ч), состоящую из хлороводорода (1 л/ч), кислорода (4 л/ч) и азота (5 л/ч), после чего с целью регенерации в течение 16 часов, или соответственно 63 часов, при 330°С, или соответственно 380°С, пропускали газовую смесь 2 (6 л/ч), состоящую из хлороводорода (1 л/ч) и азота (5 л/ч). После указанной регенерации вновь переходили на газовую смесь 1 (10 л/ч). До и после указанной регенерации с целью контроля ее результатов газовый поток продуктов реакции каждого из реакторов дважды в течение примерно 15 минут пропускали через 20%-ный раствор йодида калия. После этого с целью определения количества вводимого в указанный раствор хлора образовавшийся йод оттитровывали 0,1н. стандартным раствором тиосульфата (двойное определение). На основании результатов определения количества хлора по приведенной ниже формуле вычисляли показатель RZA - выход хлора в расчете на единицу объема и единицу времени (смотри таблицу 5а):
RZA = г (хлор) × г-1 (катализатор) × ч-1 (время).
Непосредственно после регенерации гранулы катализатора выгружали, растирали в ступке и методом RFA определяли содержание рутения и серы (смотри таблицу 5b). Аналогичным образом анализировали также не подвергнутые регенерации гранулы катализатора.
Повышение показателя RZA отравленного серой катализатора (2b) после выполненной при 380°С в течение 16 часов регенерации значительно выше по сравнению с регенерацией, выполненной в течение 63 часов при 330°С. Повышение температуры регенерации с 330 до 380°С, очевидно, оказывает существенное положительное влияние на результат регенерации и необходимую для ее осуществления длительность. Очевидным является отсутствие необходимости осуществления поинтервальной регенерации, поскольку и после единственного цикла регенерации, в случае ее реализации при 380°С в течение 16 часов, показатель RZA почти соответствует показателю RZA неотравленного сравнительного катализатора (1а) и полностью соответствует ему в случае 63-часовой регенерации при 380°С. Однако в случае очень длительной регенерации катализатора (например, в течение 63 часов при 380°С) наблюдаются значительные потери содержащегося в нем рутения.
Сравнительный пример 6. Изменение активности рутениевого катализатора на носителе (SnO2), отравленного серой в виде соединения серы (SO2), без регенерации
По 1 г гранулированного катализатора 1а и 2а загружали в соответствующие кварцевые реакционные трубки диаметром 10 мм, через которые в течение 63 часов при 330°С пропускали газовую смесь 1 (10 л/ч), состоящую из хлороводорода (1 л/ч), кислорода (4 л/ч) и азота (5 л/ч). По истечении 1 часа и 62 часов с целью контроля изменения показателя RZA газовый поток продуктов реакции каждого из реакторов дважды в течение примерно 15 минут пропускали через 20%-ный раствор йодида калия. Для определения количества вводимого в указанный раствор хлора образовавшийся йод оттитровывали 0,1н. стандартным раствором тиосульфата (двойное определение). На основании результатов определения количества хлора по приведенной ниже формуле вычисляли показатель RZA - выход хлора в расчете на единицу объема и единицу времени (смотри таблицу 6):
RZA = г (хлор) × г-1 (катализатор) × ч-1 (время).
Показатель RZA катализатора, отравленного серой в виде сернистого соединения, оставался неизменным: следовательно, в условиях пропускания газовой смеси 1 (реализации процесса Дикона) регенерация катализатора отсутствовала. Отсюда следует, что окислительные условия, очевидно, непригодны для осуществления предлагаемого в изобретении способа регенерации.
Пример 7. Влияние регенерации рутениевых катализаторов на носителе, отравленных серой в виде соединения серы (SO2), на их активность в окислении монооксида углерода
По 0,42 г гранулированных катализаторов 1а, 2b и регенерированного согласно примеру 3 катализатора загружали в три соответствующие кварцевые реакционные трубки диаметром 10 мм, через которые при температуре, варьируемой в интервале от 200 до 280°С, пропускали газовую смесь 3 (9 л/ч), состоящую из монооксида углерода (0,25 л/ч), диоксида углерода (0,05 л/ч), кислорода (4 л/ч) и азота (4,7 л/ч). После примерно двухчасового пропускания указанной газовой смеси при каждой из выбранных температур газовый поток продуктов реакции каждого из реакторов соответственно в течение получаса пропускали через газовую ловушку (200 мл). Непосредственно после этого газовую ловушку отсоединяли и определяли состав ее содержимого методом газовой хроматографии. На основании определенных концентраций монооксида углерода и диоксида углерода по приведенной ниже формуле вычисляли конверсию монооксида углерода (смотри таблицу 7):
конверсия СО [%]={1-COt[%]}/СО0[%]}×100,
причем COt/CO2t означает отношение текущих концентраций CO/CO2, тогда как СО0/CO20 означает отношение концентраций СО/СO2 на входе в реактор.
Для всех полученных результатов в хорошем приближении соблюдался массовый баланс (COt+CO2t=СО0+CO20).
Присутствующий в исходном потоке монооксид углерода на катализаторе (2b), отравленном серой в виде сернистых соединений, во всем температурном диапазоне от 200 до 280°С лишь частично превращается в диоксид углерода, в то время как применение неотравленного сравнительного катализатора (1а), а также регенерированного согласно примеру 3 катализатора позволяет достичь почти полного превращения монооксида углерода уже при 220°С. В пределах точности определения активность регенерированного рутениевого катализатора на носителе идентична активности неотравленного сравнительного катализатора.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОРЫ НА ОСНОВЕ ОКСИДА РУТЕНИЯ ДЛЯ КОНВЕРСИИ ДИОКСИДА СЕРЫ В ТРИОКСИД СЕРЫ | 2006 |
|
RU2422357C2 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРА КАТАЛИТИЧЕСКИМ ОКИСЛЕНИЕМ ХЛОРИСТОГО ВОДОРОДА И СПОСОБ ПОЛУЧЕНИЯ ИЗОЦИАНАТОВ | 2008 |
|
RU2480402C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГАЗООБРАЗНОГО ХЛОРА ПУТЕМ КАТАЛИТИЧЕСКОГО ОКИСЛЕНИЯ ХЛОРОВОДОРОДА | 2015 |
|
RU2670301C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРА ИЗ ХЛОРОВОДОРОДА С ПОМОЩЬЮ ВОЛЬФРАМСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 2012 |
|
RU2485046C1 |
| КАТАЛИЗАТОР И СПОСОБ ИЗГОТОВЛЕНИЯ ХЛОРА ПУТЕМ ОКИСЛЕНИЯ ХЛОРОВОДОРОДА В ГАЗОВОЙ ФАЗЕ | 2008 |
|
RU2469790C2 |
| ТЕРМОСТОЙКИЙ КАТАЛИЗАТОР ДЛЯ ГАЗОФАЗНОГО ОКИСЛЕНИЯ | 2007 |
|
RU2440186C2 |
| УСТОЙЧИВЫЙ К ВОЗДЕЙСТВИЮ ТЕМПЕРАТУРЫ КАТАЛИЗАТОР ДЛЯ ОКИСЛЕНИЯ ХЛОРОВОДОРОДА В ГАЗОВОЙ ФАЗЕ | 2008 |
|
RU2486006C2 |
| СПОСОБ КОНВЕРСИИ ХЛОРОВОДОРОДА ДЛЯ ПОЛУЧЕНИЯ ХЛОРА | 2010 |
|
RU2448038C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРА КАТАЛИТИЧЕСКИМ ОКИСЛЕНИЕМ ХЛОРИСТОГО ВОДОРОДА | 2009 |
|
RU2409516C1 |
| СПОСОБ ПОЛУЧЕНИЯ ХЛОРА КАТАЛИТИЧЕСКИМ ОКИСЛЕНИЕМ ХЛОРИСТОГО ВОДОРОДА МОЛЕКУЛЯРНЫМ КИСЛОРОДОМ | 2009 |
|
RU2417945C1 |
Данное изобретение касается способа регенерации катализатора, в соответствии с которым содержание серы в содержащем рутений или соединения рутения катализаторе, отравленном серой в виде сернистых соединений, путем целенаправленной обработки содержащим галогеноводород, в частности хлороводород, газовым потоком, осуществляемой в неокислительных условиях при необходимости при повышенной температуре, может быть уменьшено настолько, что активность подобного катализатора повышается до активности аналогичного катализатора, не отравленного серой в виде сернистых соединений. Описан способ катализируемого газофазного окисления хлороводорода кислородом с применением катализатора на основе рутения или соединений рутения, при этом катализатор после снижения его каталитической активности до заданного значения подвергают регенерации согласно описанному выше способу. Технический эффект - содержание серы в катализаторе может быть сокращено настолько, что активность обработанного катализатора возрастает до уровня, характерного для аналогичного содержащего рутений или соединения рутения катализатора, не деактивированного серой в виде сернистых соединений. 2 н. и 10 з.п. ф-лы, 7 табл., 7 пр.
1. Способ регенерации содержащего рутений или соединения рутения катализатора, отравленного серой в виде сернистых соединений, отличающийся тем, что катализатор при необходимости при повышенной температуре подвергают обработке в неокислительных условиях газовым потоком, содержащим галогеноводород, в частности хлороводород.
2. Способ по п.1, отличающийся тем, что регенерацию осуществляют при температуре до 600°С, предпочтительно от 200 до 500°С, особенно предпочтительно от 300 до 450°С.
3. Способ по п.1, отличающийся тем, что регенерацию осуществляют при давлении до 20 бар, предпочтительно до 5 бар, особенно предпочтительно до 1,5 бар.
4. Способ по п.1, отличающийся тем, что регенерацию осуществляют при содержании галогеноводорода от 0,1 до 100 об.%, предпочтительно от 1 до 30 об.%, особенно предпочтительно от 5 до 25 об.%.
5. Способ по п.1, отличающийся тем, что содержащим рутений или соединения рутения катализатором является катализатор на основе галогенидов рутения, в частности хлоридов рутения, оксидгалогенидов рутения, в частности оксидхлоридов рутения, или оксидов рутения, присутствующих в катализаторе в виде отдельных соединений или в виде смеси.
6. Способ по п.1, отличающийся тем, что регенерацию осуществляют в течение промежутка времени от 0,5 до 100 ч.
7. Способ по п.1, отличающийся тем, что регенерацию катализатора осуществляют в том же реакционном объеме, в котором его применяют для осуществления катализируемой им реакции.
8. Способ по п.7, отличающийся тем, что поток регенерационного газа пропускают в направлении, противоположном направлению потока компонентов катализируемой катализатором реакции.
9. Способ по п.1, отличающийся тем, что катализатором является катализатор газофазного окисления хлороводорода кислородом.
10. Способ по п.1, отличающийся тем, что регенерацию осуществляют поинтервально, причем между соответствующими временными интервалами определяют содержание серы и/или активность катализатора.
11. Способ по одному из пп.1-10, отличающийся тем, что сернистыми соединениями являются одно или несколько соединений, выбранных из группы, включающей H2SO4, H2SO3, SO3, SO2, COS, H2S, а также соли H2SO4 и H2SO3.
12. Способ катализируемого газофазного окисления хлороводорода кислородом с применением катализатора на основе рутения или соединений рутения, отличающийся тем, что катализатор подвергают регенерации по одному из пп.1-11 после снижения его каталитической активности до заданного значения.
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| US 4072628 A, 07.02.1978 | |||
| EP 0743277 A, 20.11.1996 | |||
| Контактная группа | 1975 |
|
SU535619A2 |
| СПОСОБ РЕГЕНЕРАЦИИ КАТАЛИЗАТОРА ДЛЯ ПОЛУЧЕНИЯ ВИНИЛАЦЕТАТА | 0 |
|
SU291408A1 |
| СПОСОБ ПОВЕРХНОСТНОГО МОДИФИЦИРОВАНИЯ РЕЗИН | 1999 |
|
RU2169159C2 |
| Контактная группа | 1975 |
|
SU535619A2 |
| ЕР 743277 А1, 20.11.1996. | |||
Авторы
Даты
2013-06-27—Публикация
2009-03-10—Подача