Изобретение относится к области медицины, а именно к экспериментальной хирургии и патофизиологии, и может быть использовано для коррекции иммунных нарушений.
Известно, что удаление селезенки, относящейся к наиболее крупным периферическим лимфоидным органам, вызывает изменение пула периферических иммунокомпетентных клеток, вследствие чего нарушается клеточное звено иммунитета, что приводит к угнетению фагоцитарной активности клеток крови и развитию иммунодефицита.
Известны различные способы коррекции нарушения иммунитета, как в клинике, так и в эксперименте.
Так, известен способ коррекции иммунодефицита в клинике путем внутривенного введения препарата Ронколейкин® в суточной дозе от 125 до 500 тыс ME. Курс лечения составляет 4-8 внутривенных инфузий. (Скляр Л.Ф., Маркелова Е.В. Клинико-иммунологическая эффективность применения Ронколейкина® при лечении хронического вирусного гепатита С. // Здравоохранение Урала. - 2002 - №5 Т.11 - с.39-43).
Основным недостатком известного способа является то, что при спленэктомии происходит одномоментная потеря огромного количества иммунокомпетентных клеток, вследствие чего иммуностимуляция Ронколейкином затруднена.
К недостаткам данного способа следует также отнести и его внутривенное введение, т.к. такое применение препарата в эксперименте затруднено в связи с использованием мелких лабораторных животных. В связи с небольшим весом и размерами вен животных имеется сложность в подборе дозы от 125 до 500 тыс. ME при 8-ми кратном внутривенном введении препарата, что сопряжено с дополнительным воздействием на животное (стресс, наркозные препараты, повреждение вен, болевой синдром, кровотечение). Эти дополнительные факторы не позволяют стандартизировать полученные результаты.
Кроме этого, по данным авторов заявляемого способа, не известно использование Ронколейкина для коррекции нарушений иммунитета после спленэктомии.
Наиболее близким по технической сущности к предлагаемому является способ коррекции иммунных нарушений после спленэктомии путем подкожного введения криоконсервированных клеток селезенки (Прокопьев М.В. Применение ксенотрансплантации криоконсервированных клеток селезенки для коррекции постспленэктомического гипоспленизма (экспериментальное исследование): дис.… канд. мед. наук. - Иркутск, 2001. - С.29).
Известный способ осуществляют следующим образом. Животным через час после спленэктомии выполняют подкожное введение 1 мл взвеси, содержащей 2×106 клеток селезенки. Введение проводят в область передней брюшной стенки. При этом инъекционную иглу вводят на всю длину в толщу подкожной жировой клетчатки параллельно коже. Затем при порционном введении взвеси клеток проводят постепенное подтягивание иглы на себя. Этим достигают равномерного распределения ксенотрансплантата в подкожной жировой клетчатке.
К недостаткам данного способа следует отнести низкую активацию фагоцитоза, т.к. трансплантированные ксеногенные клетки не восстанавливают Т-клеточное звено иммунитета у аспленизированных животных. Кроме этого, за счет использования ксеногенных клеток, время эффективного их воздействия ограничено, так как существует риск их отторжения.
Задачей заявляемого изобретения является разработка способа коррекции иммунных нарушений в эксперименте.
Техническим результатом предлагаемого способа является повышение эффективности коррекции иммунных нарушений, за счет восстановления процессов фагоцитоза и Т-клеточного звена иммунитета у аспленизированных животных.
Технический результат заявляемого способа достигается тем, что коррекция иммунных нарушений, вызванных полной аспленизацией животного, в эксперименте включает однократное введение в раннем послеоперационном периоде взвеси культивированных клеток.
Основным отличием предлагаемого способа является то, что аспленизированным крысам линии Вистар вводят 1 мл взвеси суточной культуры аллогенных мононуклеарных клеток костного мозга здоровых крыс, содержащей 2,4×108 клеток.
Отличие заявляемого способа так же заключается и в том, что аллотрансплантацию суточной культуры мононуклеарных клеток костного мозга проводят внутрибрюшинно.
Сопоставительный анализ заявляемого технического решения с прототипом позволяет сделать вывод о соответствии заявляемого технического решения критерию изобретения «новизна».
Авторами предлагаемого способа установлено, что аллотрансплантация суточной культуры мононуклеарных клеток костного мозга, в активной фазе их жизнедеятельности, обеспечивает активацию фагоцитоза и Т-клеточного звена иммунной системы, угнетенного спленэктомией. Введение взвеси аллогенных мононуклеарных клеток костного мозга в концентрации 2,4×108 в 1 мл обеспечивает активацию иммунной системы, что подтверждает выживаемость экспериментальных животных после тотальной аспленизации. Так, на 10-е сутки эксперимента выживаемость крыс, которым была выполнена трансплантация аллогенных мононуклеарных клеток костного мозга составила 58,4%. Летальность в этой группе животных наблюдалась с 5-х по 8-е сутки после спленэктомии, в то время как в группе животных без коррекции иммунных нарушений летальность к 10-м суткам составила 100%.
Авторами заявляемого способа опытным путем определен оптимальный путь введения мононуклеарных клеток костного мозга. Исследования показали, что наилучшие иммунологические показатели получены у животных после однократного внутрибрюшинного введения взвеси культивированных мононуклеарных клеток, в сравнении с их внутривенным и подкожным введением. Так при внутрибрюшинном введении аллогенных культивированных мононуклеарных клеток костного мозга летальность экспериментальных животных составила 41,6%, при внутривенной их трансплантации - 83,3%, при подкожном введении - 75%.
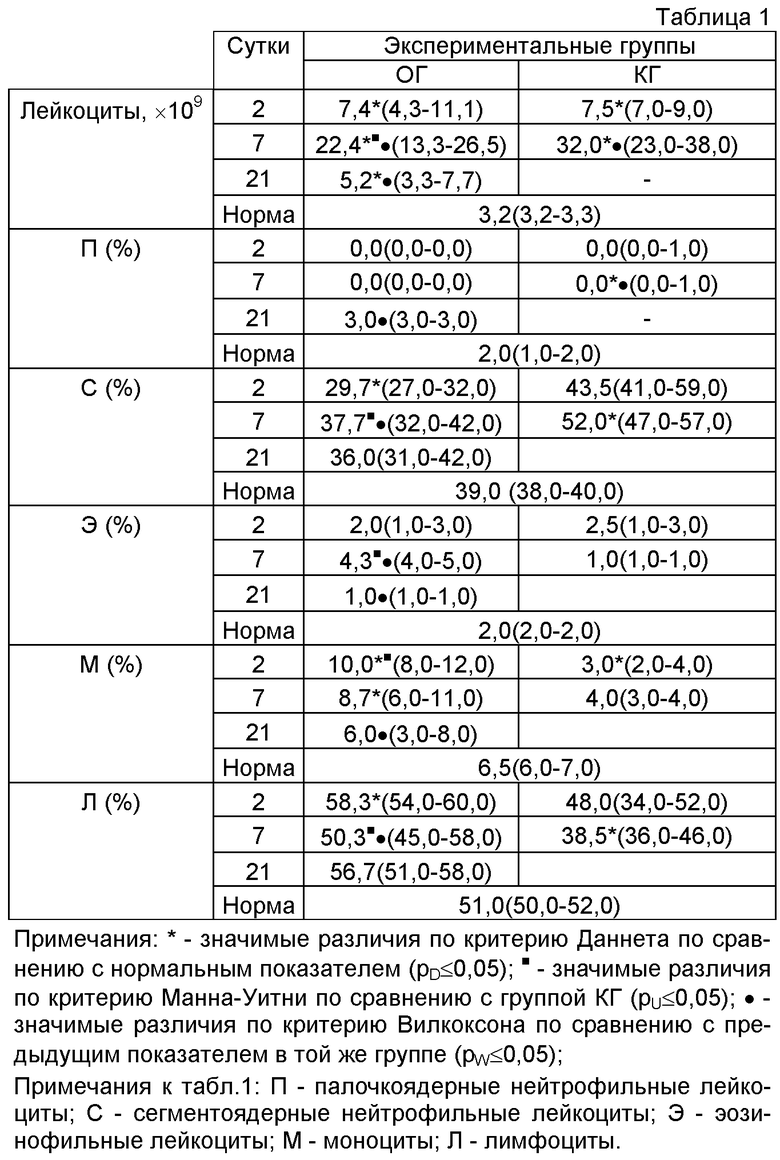
При исследовании показателей воспалительной реакции организма в условиях иммунных нарушений и трансплантации мононуклеарных клеток костного мозга установлена нормализация показателей к 21-м суткам (лейкоциты 5,2 (3,3-7,7)×109; лимфоциты 56,7 (51,0-58,0)%, тогда как в контроле выявлены прогрессирующие расстройства (см. Приложение к описанию, табл.1). Показатели фагоцитоза в условиях иммунных нарушений и трансплантации мононуклеарных клеток костного мозга существенно возрастали на 7-е сутки: фагоцитарный индекс (ФИ)=76,0 (65,0-80,0); фагоцитарное число (ФЧ)=3,4 (3,4-4,5); НСТсп 6,6 (6,0-7,0); спонтанный тест восстановления нитросинего тетразолия (НСТ-сп)=20,0 (19,0-21,5) (см. Приложение к описанию, табл.2), при стабильно низких показателях в группе контроля. При оценке Т-клеточного звена иммунитета в условиях иммунных нарушений и трансплантации мононуклеарных клеток костного мозга установлено увеличение количества T-зрелых лимфоцитов и Т-хелперов, снижение цитотоксических супрессорных клеток, тогда как в контроле отмечали снижение количества T-зрелых лимфоцитов и Т-хелперов, увеличение цитотоксических супрессорных клеток (см. Приложение к описанию, табл.3).
Следовательно, предлагаемый способ обеспечивает достижение усматриваемого заявителем технического результата, а именно - повышение эффективности коррекции иммунных нарушений после полной аспленизации животного в эксперименте, за счет активации процессов фагоцитоза, Т-клеточного звена иммунитета и ограничения воспаления.
Проведенный анализ известных технических решений показал отсутствие сведений о влиянии отличительных признаков заявляемого способа на достижение усматриваемого заявителем технического результата. Это позволяет считать предлагаемое изобретение соответствующим критерию «изобретательский уровень».
Способ, составляющий заявляемое изобретение предназначен для использования в медицине. Возможность его осуществления подтверждена описанными в заявке приемами и средствами. Следовательно, заявляемое изобретение соответствует условию патентоспособности «промышленная применимость».
Предлагаемый способ осуществляют следующим образом.
Состояние иммунодефицита у экспериментального животного получают проведением спленэктомии с удалением всех обнаруженных добавочных очагов селезеночной ткани, т.е. проведением полной аспленизации. После чего экспериментальному животному (крысе) вводят однократно внутрибрюшинно 1 мл взвеси суточной культуры аллогенных мононуклеарных клеток костного мозга здоровых крыс, содержащей 2,4×108 клеток.
Предлагаемый способ поясняется примером конкретного выполнения.
В эксперименте были использованы животные крысы-самцы линии Wistar в возрасте не менее 6 месяцев, весом 200-250 г. Животных содержали в условиях вивария при свободном доступе к воде и пище соответственно нормативам ГОСТа «Содержание экспериментальных животных в питомниках НИИ» (виварий I категории, вет. удостоверение 238 №0015220 от 28 ноября 2011 г, служба ветеринарии Иркутской области). Опыты на животных проводили в соответствии с правилами гуманного обращения с животными, которые регламентированы «Правилами проведения работ с использованием экспериментальных животных», утвержденных Приказом МЗ СССР №742 от 13.11.84 г. «Об утверждении правил проведения работ с использованием экспериментальных животных» и №48 от 23.01.85 г. «О контроле за проведением работ с использованием экспериментальных животных».
У всех экспериментальных животных, в стерильных условиях, под общим обезболиванием была выполнена спленэктомия с удалением всех обнаруженных очагов резидуальной ткани (полная аспленизация).
Опытную группу (ОГ) составили 56 животных, которым через час после полной аспленизации внутрибрюшинно однократно вводили 1 мл клеточной взвеси, содержащей 2,4×108 суточной культуры мононуклеарных клеток костного мозга. В качестве трансплантата были использованы мононуклеарные клетки костного мозга здоровых крыс линии Wistar, а именно их суточная культура в концентрации 2,4×108 в 1 мл. Жизнеспособность клеток составила 99,8%.
Контрольной группе (КГ) животных (n=56) через час после аспленизации выполняли внутрибрюшинно инъекцию 1 мл физиологического раствора.
Проведено исследование общего анализа крови и иммунологических показателей у всех животных. Забор анализов выполняли на 2-е, 5-е и 7-е сутки послеоперационного периода. За норму приняты показатели, полученные у 6-ти здоровых животных.
Иммунологические методы исследования. Для определения параметров фагоцитарной реакции нейтрофилов крови использовали убитые при 80-90°С, клетки дрожжей Saccharomyces cerevisiae. Оценивали фагоцитарную активность по проценту фагоцитов из числа сосчитанных нейтрофилов (ФИ) и по фагоцитарному числу (ФЧ) - среднее число дрожжей, поглощенных одним нейтрофилом.
Для оценки степени антигенной раздраженности не активированных in vitro гранулоцитов крови исследовали спонтанный тест восстановления нитросинего тетразолия (НСТ-сп), выражая результаты в процентах. Активированный тест восстановления нитросинего тетразолия (НСТ-инд) в %%, определяли для оценки функционального резерва кислородзависимого механизма бактерицидности фагоцитов.
Лабораторные методы исследования крови. Подсчитывали количество эритроцитов, лейкоцитов, лейкоцитарную формулу крови по общепринятым методикам.
Проточная цитометрия выполнена на двулазерном проточном флуориметре Facs Calibur BD (США) с использованием крысиных моноклональных антител к CD3+, CD4+, CD8+ (фирмы Coltak).
При исследовании показателей воспалительной реакции организма у животных контрольной группы (табл.1) отмечали лейкоцитоз, с максимальным увеличением на 7-е сутки до 32,0 (23,0-38,0), возрастало количество сегментоядерных нейтрофилов 52,0 (47,0-57,0) и снижалось общее количество лимфоцитов. Летальность животных контрольной группы составила 100%.
При исследовании показателей воспалительной реакции организма в условиях иммунных нарушений и трансплантации мононуклеарных клеток костного мозга выявлено существенное (pW≤0,05) снижение лейкоцитоза и нормализация количества лейкоцитов и форменных элементов крови к двадцать первым суткам исследования, по сравнению с контрольной группой. В группе контроля наблюдали прогрессирующие расстройства, характерные для иммунодефицита. Показано, что трансплантация мононуклеарных клеток костного мозга способствует ограничению воспалительной реакции.
Результаты исследования показателей неспецифической резистентности организма, а именно - фагоцитоза, представлены в табл.2.
В условиях иммунных нарушений и трансплантации мононуклеарных клеток костного мозга выявляли активацию фагоцитарной активности, существенно повышались показатели ФИ, ФЧ, НСТсп, НСТинд (pW≤0,05; pD≤0,05; pU≤0,05). Активация фагоцитоза отмечалась до 21-х суток исследования, отметим, что показатели НСТсп, НСТинд снижались до нормальных значений.
Для оценки T-клеточного звена иммунитета изучали субпопуляции иммунокомпетентных клеток при аспленизации и трансплантации культуры мононуклеарных клеток костного мозга, контролировали количество лейкоцитов, лимфоцитов и фракции Т-лимфоцитов в периферической крови. Полученные результаты представлены в нижеприведенной таблице (табл.3).
В контрольной группе на вторые сутки исследования процент зрелых лимфоцитов достоверно снижался, так же отмечали существенное понижение Т-хелперов (pD≤0,05). Отметим несущественное нарастание цитотоксических супрессорных клеток.
На 5-е сутки, изучаемые показатели сохранялись пониженными, однако процент цитотоксических супрессорных клеток существенно возрастал (pD=0,001), достигая максимальных значений.
Таким образом, аспленизация животных приводит к выраженным изменениям выбранных показателей к 7-м суткам, с развитием иммунодефицита, что проявляется снижением количества Т-зрелых лимфоцитов и Т-хелперов, увеличением цитотоксических супрессорных клеток.
В опытной группе установлено, что на вторые сутки исследования процент зрелых лимфоцитов достоверно увеличивался, так же отмечали существенное понижение Т-хелперов (pD≤0,05). Отметим нормальную величину цитотоксических супрессорных клеток. На 5-е сутки изучаемые показатели становились нормальными, однако процент цитотоксических супрессорных клеток существенно возрастал (pD=0,004).
К 21-м суткам исследования изучаемые показатели иммунных нарушений нормализовались.
Выявлено, что аспленизация животных приводит к выраженным изменениям с развитием иммунодефицита, что проявляется лейкоцитозом, угнетением фагоцитоза, снижением количества T-зрелых лимфоцитов и Т-хелперов, увеличением цитотоксических супрессорных клеток. Трансплантация суточной культуры мононуклеарных клеток аллогенного костного мозга, введенная внутрибрюшинно, способствует предупреждению иммунных нарушений после спленэктомии в раннем послеоперационном периоде, с нормализацией показателей к 21-м суткам. Коррекция иммунных нарушений происходит за счет активации фагоцитоза, увеличения количества Т-зрелых лимфоцитов, Т-хелперов и нормализации числа цитотоксических супрессорных клеток.
Таким образом, заявляемый способ позволяет достичь указанного технического результата - повысить эффективность коррекции иммунных нарушений, за счет восстановления процессов фагоцитоза и T-клеточного звена иммунитета у аспленизированных животных, что приводит к ограничению воспалительной реакции организма и снижению летальности.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЛЕЧЕНИЯ ВНЕБОЛЬНИЧНОЙ ПНЕВМОНИИ У ДЕТЕЙ | 2012 |
|
RU2529782C2 |
| ВЕЩЕСТВО И СПОСОБ МОДУЛЯЦИИ ПРОЛИФЕРАЦИИ И ДИФФЕРЕНЦИРОВКИ РЕГУЛЯТОРНЫХ, СТВОЛОВЫХ И ДРУГИХ СОМАТИЧЕСКИХ КЛЕТОК | 2014 |
|
RU2620069C2 |
| СПОСОБ КОРРЕКЦИИ ДИСФУНКЦИИ ФАКТОРОВ ВРОЖДЕННОГО И АДАПТИВНОГО ИММУНИТЕТА ПРИ ХРОНИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ В ЭКСПЕРИМЕНТЕ | 2015 |
|
RU2616213C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИММУНОСТИМУЛИРУЮЩИМ И ГЕМОСТИМУЛИРУЮЩИМ ДЕЙСТВИЕМ | 2009 |
|
RU2414223C1 |
| Способ лечения острой печеночной недостаточности | 2018 |
|
RU2701792C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ УСТОЙЧИВОСТИ ОРГАНИЗМА К СТРЕССОРНОМУ ВОЗДЕЙСТВИЮ | 2006 |
|
RU2322675C1 |
| СПОСОБ ЛЕЧЕНИЯ ПЕЧЕНОЧНОЙ НЕДОСТАТОЧНОСТИ | 2017 |
|
RU2655528C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЙ (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ БИОТРАНСПЛАНТАТА (ВАРИАНТЫ), БИОТРАНСПЛАНТАТ (ВАРИАНТЫ) | 2006 |
|
RU2322248C2 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИММУНОЗАВИСИМЫХ ОСЛОЖНЕНИЙ У КАРДИОХИРУРГИЧЕСКИХ БОЛЬНЫХ В ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ | 2006 |
|
RU2326679C1 |
| СРЕДСТВО ДЛЯ ИММУНОКОРРЕКЦИИ ОРГАНИЗМА ЖИВОТНЫХ | 2008 |
|
RU2382650C1 |
Изобретение относится к медицине, в частности к экспериментальной хирургии и патофизиологии, и может быть использовано для коррекции иммунных нарушений. Для моделирования иммунных нарушений крысам линии Вистар проводят полную аспленизацию. В раннем послеоперационном периоде вводят внутрибрюшинно 1 мл взвеси суточной культуры аллогенных мононуклеарных клеток костного мозга здоровых крыс, содержащей 2,4×108 клеток. Способ позволяет повысить эффективность коррекции иммунодефицита за счет активации Т-клеточного звена иммунитета и процессов фагоцитоза. 3 табл.
Способ коррекции иммунных нарушений, вызванных полной аспленизацией животного в эксперименте, включающий однократное введение в раннем послеоперационном периоде взвеси культивированных клеток, отличающийся тем, что аспленизированным крысам линии Вистар вводят внутрибрюшинно 1 мл взвеси суточной культуры аллогенных мононуклеарных клеток костного мозга здоровых крыс, содержащей 2,4·108 клеток.
| ПРОКОПЬЕВ М.В | |||
| Применение ксенотрансплантации криоконсервированных клеток селезенки для коррекции постспленэктомического гипоспленизма: Автореф | |||
| дисс | |||
| к.м.н | |||
| - Иркутск, 2001, с.1-29 | |||
| СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2006 |
|
RU2325934C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ ЗАБОЛЕВАНИЙ (ВАРИАНТЫ), СПОСОБ ПОЛУЧЕНИЯ БИОТРАНСПЛАНТАТА (ВАРИАНТЫ), БИОТРАНСПЛАНТАТ (ВАРИАНТЫ) | 2006 |
|
RU2322248C2 |
| СПОСОБ ПРОФИЛАКТИКИ ПОСТСПЛЕНЭКТОМИЧЕСКОГО СИНДРОМА В ЭКСПЕРИМЕНТЕ | 2003 |
|
RU2247567C2 |
| US 20020142462 A1, 03.10.2002 | |||
| US 20080279861 A1, 13.11.2008 | |||
| БЕРСЕНЕВ А.В | |||
| Клеточная | |||
Авторы
Даты
2013-07-27—Публикация
2012-02-28—Подача