Область техники, к которой относится изобретение
Настоящее изобретение относится к новому фенилимидазольному соединению.
Уровень техники
Современное общество называют обществом чревоугодия, и число людей с диагностированной гиперлипидемией, ожирением и тому подобным резко растет. Состояния, такие как гиперлипидемия, ожирение и тому подобное, являются чрезвычайно опасными, поскольку эти состояния могут вызывать сахарный диабет и являться причиной артериосклероза и других заболеваний, таких как инфаркт миокарда и ишемический инсульт, которые приписываются артериосклерозу.
Соответственно, с целью профилактики и лечения гиперлипидемии, ожирения и тому подобного был проведен целый ряд исследований фармацевтических продуктов, химиотерапии и тому подобного для облегчения этих состояний. Химиотерапия, используемая для активации LPL (липопротеинлипазы), и химиотерапевтические средства для этого являются примерами таких исследований. Считается, что активация LPL эффективна при профилактике и лечении гиперлипидемии, ожирения и тому подобного (например, непатентные документы 1-6).
Документы, известные из уровня техники
Непатентные документы
[Непатентный документ 1] LPL Activation and Arteriosclerosis: J. Clin. Invest., 92, 411 (1993)
[Непатентный документ 2] LPL Activation and Cataract: Biol. Pharm. Bull., 19, 1570 (1996)
[Непатентный документ 3] LPL Activation and Cachexia: Anticancer Research, 19, 4099 (1999)
[Непатентный документ 4] LPL Activity and Nephrosis: Metabolism, 49, 588 (2000)
[Непатентный документ 5] LPL Activation and Hyperlipidemia: Diabetes, 44, 414 (1995)
[Непатентный документ 6] LPL Activation and Obesity: Diabetologia, 43, 875 (2000)
Сущность изобретения
Цель настоящего изобретения
Главной целью настоящего изобретения является предоставление фармацевтического продукта (химиотерапевтического средства), эффективного при профилактике и лечении гиперлипидемии, ожирения и тому подобного.
Средства достижения цели
С целью предоставления фармацевтического продукта (химиотерапевтического средства), эффективного при профилактике и лечении гиперлипидемии, ожирения и тому подобного, авторы настоящего изобретения провели интенсивные исследования для разработки соединения, обладающего LPL-активирующей функцией, в частности LPL-активирующей функцией, специфичной для скелетных мышц. В процессе проведения указанных исследований авторы изобретения успешно синтезировали фенилимидазольное соединение, представленное общей формулой (1), показанной ниже, и обнаружили, что соединение обладает искомыми свойствами. Настоящее изобретение было сделано на основе этих знаний.
Настоящее изобретение относится к следующим изобретениям в соответствии с пунктами 1-30.
Пункт 1. Фенилимидазольное соединение, представленное следующей общей формулой (1):
[Хим. 1]
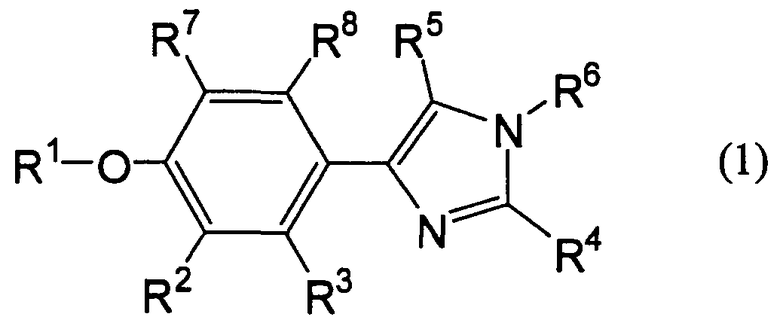
где R1 представляет собой атом водорода, фенил-низшую алкильную группу или пиридил-низшую алкильную группу, и бензольное кольцо и пиридиновое кольцо необязательно замещены 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп. Один из R2 и R3 представляет собой атом водорода, а другой представляет собой низшую алкоксигруппу. R4 представляет собой низшую алкильную группу, фурильную группу, тиенильную группу или фенильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, карбоксильной группы, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп. R5 и R6 являются одинаковыми или разными и представляют собой атом водорода или низшую алкильную группу. R7 и R8 являются одинаковыми или разными и представляют собой атом водорода или низшую алкоксигруппу. Однако если R1 представляет собой незамещенную фенил-низшую алкильную группу, R2 представляет собой низшую алкоксигруппу, R3 представляет собой атом водорода, R4 представляет собой незамещенную фенильную группу или фенильную группу, содержащую 1 или 2 галогензамещенные низшие алкильные группы, и R5 представляет собой атом водорода, то R6 не является атомом водорода.
Пункт 2. Фенилимидазольное соединение в соответствии с пунктом 1, где в общей формуле (1) R7 и R8 представляют собой атом водорода.
Пункт 3. Фенилимидазольное соединение в соответствии с пунктом 1 или 2, где в общей формуле (1) R4 представляет собой тиенильную группу.
Пункт 4. Фенилимидазольное соединение в соответствии с пунктом 1 или 2, где в общей формуле (1) R4 представляет собой фурильную группу.
Пункт 5. Фенилимидазольное соединение в соответствии с пунктом 1 или 2, где в общей формуле (1) R4 представляет собой фенильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, карбоксильной группы, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп.
Пункт 6. Фенилимидазольное соединение в соответствии с пунктом 1 или 2, где в общей формуле (1) R1 представляет собой незамещенную фенил-низшую алкильную группу или фенил-низшую алкильную группу, замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп.
Пункт 7. Фенилимидазольное соединение в соответствии с пунктом 6, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из бензила, 4-цианобензила, 3-цианобензила, 2-цианобензила, 4-хлорбензила, 4-трифторметилбензила, 4-хлор-2-фторбензила и 4-бром-2-фторбензила.
Пункт 8. Фенилимидазольное соединение в соответствии с пунктом 6, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из бензила, 4-цианобензила, 3-цианобензила, 2-цианобензила, 4-хлорбензила и 4-бром-2-фторбензила.
Пункт 9. Фенилимидазольное соединение в соответствии с пунктом 1, 2 или 6, где в общей формуле (1) R4 представляет собой тиенильную группу, фурильную группу или фенильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп.
Пункт 10. Фенилимидазольное соединение в соответствии с пунктом 1, 2 или 6, где в общей формуле (1) R4 представляет собой группу, выбранную из группы, состоящей из 2-тиенила, 3-тиенила, 3-фурила, фенила, 4-фторфенила, 3-фторфенила, 3-фтор-4-метилфенила, 3,4-дифторфенила, 4-трифторметилфенила, 3-трифторметилфенила, 2-трифторметилфенила, 4-хлорфенила, 3-хлорфенила, 3,4-дихлорфенила, 3,5-дихлорфенила, 3-хлор-4-фторфенила, 3-метоксифенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонилфенила, 4-карбоксифенила, 4-(1,1-диметилэтил)фенила, 1-метилэтила и 4-метилфенила.
Пункт 11. Фенилимидазольное соединение в соответствии с пунктом 10, где в общей формуле (1) R4 представляет собой группу, выбранную из группы, состоящей из 2-тиенила, 3-тиенила, 3-фурила, фенила, 4-фторфенила, 3-фторфенила, 3,4-дифторфенила, 4-трифторметилфенила, 3-трифторметилфенила, 2-трифторметилфенила, 4-хлорфенила, 3-хлорфенила, 3,4-дихлорфенила, 3,5-дихлорфенила, 3-хлор-4-фторфенила, 3-метоксифенила, 4-метоксикарбонилфенила, 4-(1,1-диметилэтил)фенила, 1-метилэтила и 4-метилфенила.
Пункт 12. Фенилимидазольное соединение в соответствии с пунктом 1 или 2, где в общей формуле (1) R1 представляет собой пиридил-низшую алкильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп.
Пункт 13. Фенилимидазольное соединение в соответствии с пунктом 12, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из 5-трифторметил-2-пиридилметила, 2-пиридилметила, 3-пиридилметила, 5-хлор-2-пиридилметила и 5-циано-2-пиридилметила.
Пункт 14. Фенилимидазольное соединение в соответствии с пунктом 1 или 2, где в общей формуле (1) R1 представляет собой пиридил-низшую алкильную группу, необязательно замещенную галогензамещенной низшей алкильной группой.
Пункт 15. Фенилимидазольное соединение в соответствии с пунктом 14, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из 2-пиридилметила и 6-трифторметил-3-пиридилметила.
Пункт 16. Фенилимидазольное соединение в соответствии с пунктом 1 или 2, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из бензила, 4-хлорбензила и 4-бром-2-фторбензила, и R4 представляет собой группу, выбранную из группы, состоящей из 4-трифторметилфенила, 4-фторфенила, 3,4-дифторфенила, 4-хлорфенила, 3,4-дихлорфенила и 4-метилфенила.
Пункт 17. Фенилимидазольное соединение в соответствии с пунктом 1, выбранное из следующих соединений:
4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-(4-бензилокси-3-метоксифенил)-2-(3-тиенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(4-фторфенил)-1H-имидазол;
4-(4-бензилокси-3-метоксифенил)-2-(4-фторфенил)-5-метил-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-3-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-хлорфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]-2-(2-тиенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(3-тиенил)-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-[3-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-метилфенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дихлорфенил)-1H-имидазол.
Пункт 18. Фенилимидазольное соединение в соответствии с пунктом 1, выбранное из следующих соединений:
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(4-фторфенил)-1H-имидазол;
4-(4-бензилокси-3-метоксифенил)-2-(4-фторфенил)-5-метил-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-хлорфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-метилфенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дихлорфенил)-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол.
Пункт 19. Фармацевтическая композиция, содержащая в качестве активного ингредиента соединение в соответствии с любым из пунктов 1-18.
Пункт 20. Активатор LPL, содержащий в качестве активного ингредиента соединение в соответствии с любым из пунктов 1-18.
Пункт 21. Средство для профилактики и лечения гиперлипидемии, содержащее в качестве активного ингредиента соединение в соответствии с любым из пунктов 1-18.
Пункт 22. Антиартериосклеротическое средство, содержащее в качестве активного ингредиента соединение в соответствии с любым из пунктов 1-18.
Пункт 23. Средство от ожирения, содержащее в качестве активного ингредиента соединение в соответствии с любым из пунктов 1-18.
Пункт 24. Способ активации LPL, включающий введение эффективного количества соединения в соответствии с любым из пунктов 1-18.
Пункт 25. Способ профилактики или лечения гиперлипидемии, включающий введение эффективного количества соединения в соответствии с любым из пунктов 1-18.
Пункт 26. Способ профилактики или лечения артериосклероза, включающий введение эффективного количества соединения в соответствии с любым из пунктов 1-18.
Пункт 27. Способ профилактики или лечения ожирения, включающий введение эффективного количества соединения в соответствии с любым из пунктов 1-18.
Пункт 28. Применение соединения в соответствии с любым из пунктов 1-18 в качестве лекарственного средства.
Пункт 29. Применение соединения в соответствии с любым из пунктов 1-18 для получения активатора LPL.
Пункт 30. Соединение в соответствии с любым из пунктов 1-18 для применения при активации LPL.
Эффекты изобретения
Фенилимидазольное соединение по настоящему изобретению обладает активирующим действием в отношении липопротеинлипазы (LPL) и эффективно в качестве активатора LPL для профилактики и лечения гиперлипидемии, ожирения и т.п.
Наилучший способ осуществления изобретения
Далее в этом документе подробно описано фенилимидазольное соединение по настоящему изобретению.
Каждая группа, описанная в общей формуле (1) и где-либо еще в настоящем описании, описана более подробно, как изложено ниже. В настоящем описании термин «низший», используемый для каждой содержащей атом углерода группы, относится к группе, содержащей от 1 до 6 атомов углерода.
Примеры низших алкильных групп включают неразветвленные или разветвленные C1-6алкильные группы, такие как метил, этил, пропил, 1-метилэтил, бутил, 2-метилпропил, 1,1-диметилэтил, пентил, гексил и т.п.
Примеры низших алкоксигрупп включают C1-6алкоксигруппы, такие как метокси, этокси, пропокси, 1-метилэтокси, бутокси, 2-метилпропокси, 1,1-диметилэтокси, пентилокси, гексилокси и т.п.
Примеры атомов галогена включают фтор, хлор, бром, йод и т.п.
Примеры фурильных групп включают 2-фурил, 3-фурил и т.п.
Примеры тиенильных групп включают 2-тиенил, 3-тиенил и т.п.
Примеры галогензамещенных низших алкильных групп включают галогеналкильную группу, которая содержит неразветвленную или разветвленную C1-6алкильную группу, замещенную по меньшей мере одним атомом галогена, выбранным из группы, состоящей из атомов фтора, хлора, брома и йода. Их предпочтительным примером является пергалогеналкильная группа, и их наиболее предпочтительным примером является перфторалкильная группа. Их конкретные примеры включают трифторметил, пентафторэтил, гептафторпропил, нонафторбутил, ундекафторпентил, тридекафторгексил и т.п.
Примеры низших алкоксикарбонильных групп включают неразветвленную или разветвленную C1-6алкоксикарбонильную группу, такую как метоксикарбонил, этоксикарбонил, пропоксикарбонил, 1-метилэтоксикарбонил, бутоксикарбонил, 2-метилпропоксикарбонил, 1,1-диметилэтоксикарбонил, пентилоксикарбонил, гексилоксикарбонил и т.п.
Примеры фенил-низших алкильных групп, необязательно замещенных 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп, включают следующие: бензил, 1-фенилэтил, 2-фенилэтил, 3-фенилпропил, 4-фенилбутил, 5-фенилпентил, 6-фенилгексил, 2-хлорбензил, 3-хлорбензил, 4-хлорбензил, 2-бромбензил, 3-бромбензил, 4-бромбензил, 2-йодбензил, 3-йодбензил, 4-йодбензил, 2-фторбензил, 3-фторбензил, 4-фторбензил, 2,4-дихлорбензил, 2,3-дихлорбензил, 3,5-дихлорбензил, 3,4-дихлорбензил, 2,5-дихлорбензил, 2,6-дихлорбензил, 2,4-дифторбензил, 2,4-дибромбензил, 2,4-дийодбензил, 4-бром-2-фторбензил, 2-бром-4-фторбензил, 4-бром-2-фторбензил, 4-хлор-2-фторбензил, 2-цианобензил, 3-цианобензил, 4-цианобензил, 2,4-дицианобензил, 3,5-дицианобензил, 4-бром-2-цианобензил, 2-бром-4-цианобензил, 4-хлор-2-цианобензил, 2-хлор-4-цианобензил, 4-бром-2-цианобензил, 2-бром-4-цианобензил, 4-фтор-2-цианобензил, 2-фтор-4-цианобензил, 1-(4-хлорофенил)этил, 2-(4-хлорфенил)этил, 3-(4-хлорфенил)пропил, 4-(4-хлорфенил)бутил, 5-(4-хлорфенил)пентил, 6-(4-хлорфенил)гексил, 1-(4-цианофенил)этил, 2-(4-цианофенил)этил, 3-(4-цианофенил)пропил, 4-(4-цианофенил)бутил, 5-(4-цианофенил)пентил, 6-(4-цианофенил)гексил, 1-(4-бром-2-фторфенил)этил, 2-(4-бром-2-фторфенил)этил, 3-(4-бром-2-фторфенил)пропил, 4-(4-бром-2-фторфенил)бутил, 5-(4-бром-2-фторфенил)пентил, 6-(4-бром-2-фторфенил)гексил, 2-трифторметилбензил, 3-трифторметилбензил, 4-трифторметилбензил, 1-(4-трифторметилфенил)этил, 2-(4-трифторметилфенил)этил, 3-(4-трифторметилфенил)пропил, 4-(4-трифторметилфенил)бутил, 5-(4-трифторметилфенил)пентил, 6-(4-трифторметилфенил)гексил, 2-бром-4-трифторметилбензил, 2-циано-4-трифторметилбензил и т.п.
Примеры пиридил-низших алкильных групп, необязательно замещенных 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп, включают следующие: 2-пиридилметил, 3-пиридилметил, 4-пиридилметил, (3-трифторметил-2-пиридил)метил, (4-трифторметил-2-пиридил)метил, (5-трифторметил-2-пиридил)метил, (6-трифторметил-2-пиридил)метил, (2-трифторметил-3-пиридил)метил, (4-трифторметил-3-пиридил)метил, (5-трифторметил-3-пиридил)метил, (6-трифторметил-3-пиридил)метил, (2-трифторметил-4-пиридил)метил, (3-трифторметил-4-пиридил)метил, (5-пентафторэтил-2-пиридил)метил, (5-гептафторпропил-2-пиридил)метил, (5-нонафторбутил-2-пиридил)метил, (5-ундекафторпентил-2-пиридил)метил, (5-тридекафторгексил-2-пиридил)метил, 1-(5-трифторметил-2-пиридил)этил, 2-(5-трифторметил-2-пиридил)этил, 3-(5-трифторметил-2-пиридил)пропил, 4-(5-трифторметил-2-пиридил)бутил, 5-(5-трифторметил-2-пиридил)пентил, 6-(5-трифторметил-2-пиридил)гексил, (3-бром-2-пиридил)метил, (4-бром-2-пиридил)метил, (5-бром-2-пиридил)метил, (6-бром-2-пиридил)метил, (2-бром-3-пиридил)метил, (4-бром-3-пиридил)метил, (5-бром-3-пиридил)метил, (6-бром-3-пиридил)метил, (2-бром-4-пиридил)метил, (3-бром-4-пиридил)метил, (5-хлор-2-пиридил)метил, (6-хлор-3-пиридил)метил, (5-фтор-2-пиридил)метил, (6-фтор-3-пиридил)метил, (3-циано-2-пиридил)метил, (4-циано-2-пиридил)метил, (5-циано-2-пиридил)метил, (6-циано-2-пиридил)метил, (2-циано-3-пиридил)метил, (4-циано-3-пиридил)метил, (5-циано-3-пиридил)метил, (6-циано-3-пиридил)метил, (2-циано-4-пиридил)метил, (3-циано-4-пиридил)метил, 1-(5-хлор-2-пиридил)этил, 2-(5-хлор-2-пиридил)этил, 3-(5-хлор-2-пиридил)пропил, 4-(5-хлор-2-пиридил)бутил, 5-(5-хлор-2-пиридил)пентил, 6-(5-хлор-2-пиридил)гексил и т.п.
Примеры фенильных групп, необязательно замещенных 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, карбоксильной группы, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп, включают в дополнение к фенильной группе следующие: 2-хлорфенил, 3-хлорфенил, 4-хлорфенил, 2-бромфенил, 3-бромфенил, 4-бромфенил, 2-йодфенил, 3-йодфенил, 4-йодфенил, 2-фторфенил, 3-фторфенил, 4-фторфенил, 3,4-дифторфенил, 2,4-дихлорфенил, 2,3-дихлорфенил, 3,5-дихлорфенил, 3,4-дихлорфенил, 2,5-дихлорфенил, 2,6-дихлорфенил, 2,4-дифторфенил, 2,4-дибромфенил, 3,4-дибромфенил, 2,4-дийодфенил, 4-бром-2-фторфенил, 2-бром-4-фторфенил, 4-бром-2-хлорфенил, 3-хлор-4-фторфенил, 2-метилфенил, 3-метилфенил, 4-метилфенил, 4-этилфенил, 4-пропилфенил, 4-(1-метилэтил)фенил, 4-бутилфенил, 4-(2-метилпропил)фенил, 4-(1,1-диметилэтил)фенил, 4-пентилфенил, 4-гексилфенил, 2,4-диметилфенил, 2,3-диметилфенил, 3,5-диметилфенил, 3,4-диметилфенил, 2,5-диметилфенил, 2,6-диметилфенил, 2-метоксифенил, 3-метоксифенил, 4-метокисфенил, 4-этоксифенил, 4-пропоксифенил, 4-(1-метилэтокси)фенил, 4-бутосифенил, 4-(2-метилпропокси)фенил, 4-(1,1-диметилэтокси)фенил, 4-пентилоксифенил, 4-гексилоксифенил, 2,4-диметоксифенил, 2,3-диметоксифенил, 3,5-диметоксифенил, 3,4-диметоксифенил, 2,5-диметоксифенил, 2,6-диметоксифенил, 2-трифторметилфенил, 3-трифторметилфенил, 4-трифторметилфенил, 4-пентафторэтилфенил, 4-гептафторпропилфенил, 4-нонафторбутилфенил, 4-ундекафторпентилфенил, 4-тридекафторгексилфенил, 2,4-бистрифторметилфенил, 2,3-бистрифторметилфенил, 3,5-бистрифторметилфенил, 3,4-бистрифторметилфенил, 2,5-бистрифторметилфенил, 2,6-бистрифторметилфенил, 4-метокси-2-метилфенил, 4-метокси-3-метилфенил, 3-метокси-5-метилфенил, 4-хлор-2-метилфенил, 4-хлор-3-метилфенил, 3-хлор-5-метилфенил, 3-фтор-5-метилфенил, 3-фтор-4-метилфенил, 3-бром-5-метилфенил, 3-йод-5-метилфенил, 2-метил-4-трифторметилфенил, 3-метил-4-трифторметилфенил, 3-метил-5-трифторметилфенил, 2-хлор-4-метоксифенил, 3-хлор-4-метоксифенил, 3-хлор-5-метоксифенил, 4-метокси-2-трифторметилфенил, 4-метокси-3-трифторметилфенил, 3-метокси-5-трифторметилфенил, 4-хлор-2-трифторметилфенил, 4-хлор-3-трифторметилфенил, 3-хлор-5-трифторметилфенил, 2-карбоксифенил, 3-карбоксифенил, 4-карбоксифенил, 2-метоксикарбонилфенил, 3-метоксикарбонилфенил, 4-метоксикарбонилфенил, 4-этоксикарбонилфенил, 4-пропоксикарбонилфенил, 4-бутоксикарбонилфенил, 4-пентилоксикарбонилфенил, 4-гексилоксикарбонилфенил и т.п.
В общей формуле (1) предпочтительный R1 представляет собой незамещенную фенил-низшую алкильную группу или фенил-низшую алкильную группу, замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп. Конкретные примеры предпочтительного R1 включают бензил, 4-цианобензил, 3-цианобензил, 2-цианобензил, 4-хлорбензил, 4-трифторметилбензил, 4-хлор-2-фторбензил и 4-бром-2-фторбензил и т.п. Конкретные примеры более предпочтительного R1 включают бензил, 4-цианобензил, 3-цианобензил, 2-цианобензил, 4-хлорбензил, 4-бром-2-фторбензил и т.п.
Другой предпочтительный R1 представляет собой пиридил-низшую алкильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп. Конкретные примеры предпочтительного R1 включают 5-трифторметил-2-пиридилметил, 2-пиридилметил, 3-пиридилметил, 5-хлор-2-пиридилметил, 5-циано-2-пиридилметил и т.п.
Другой предпочтительный R1 представляет собой пиридил-низшую алкильную группу, необязательно замещенную галогензамещенной низшей алкильной группой. Конкретные примеры предпочтительного R1 включают 2-пиридилметил, 6-трифторметил-3-пиридилметил и т.п.
В общей формуле (1) предпочтительный R4 представляет собой фурильную группу, тиенильную группу или фенильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, карбоксильной группы, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп. Более предпочтительный R4 представляет собой фурильную группу, тиенильную группу или фенильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп.
Конкретные примеры предпочтительного R4 включают 2-тиенил, 3-тиенил, 3-фурил, фенил, 4-фторфенил, 3-фторфенил, 3-фтор-4-метилфенил 3,4-дифторфенил, 4-трифторметилфенил, 3-трифторметилфенил, 2-трифторметилфенил, 4-хлорфенил, 3-хлорфенил, 3,4-дихлорфенил, 3,5-дихлорфенил, 3-хлор-4-фторфенил, 3-метоксифенил, 4-метоксифенил, 3,4-диметоксифенил, 4-метоксикарбонилфенил, 4-карбоксифенил, 4-(1,1-диметилэтил)фенил, 1-метилэтил, 4-метилфенил и т.п. Конкретные примеры более предпочтительного R4 включают 2-тиенил, 3-тиенил, 3-фурил, фенил, 4-фторфенил, 3-фторфенил, 3,4-дифторфенил, 4-трифторметилфенил, 3-трифторметилфенил, 2-трифторметилфенил, 4-хлорфенил, 3-хлорфенил, 3,4-дихлорфенил, 3,5-дихлорфенил, 3-хлор-4-фторфенил, 3-метоксифенил, 4-метоксикрабонилфенил, 4-(1,1-диметилэтил)фенил, 1-метилэтил, 4-метилфенил и т.п.
В общей формуле (1) предпочтительные R4 и R5 представляют собой атомы водорода.
В общей формуле (1) предпочтительные R7 и R8 представляют собой атомы водорода.
Предпочтительное фенилимидазольное соединение, представленное общей формулой (1), представляет собой соединение, в котором R1 представляет собой группу, выбранную из группы, состоящей из бензила, 4-хлорбензила и 4-бром-2-фторбензила; и R4 представляет собой группу, выбранную из группы, состоящей из 4-трифторметилфенила, 4-фторфенила, 3,4-дифторфенила, 4-хлорфенила, 3,4-дихлорфенила и 4-метилфенила.
Конкретные примеры более предпочтительного фенилимидазольного соединения, представленного общей формулой (1), включают следующие соединения:
4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-(4-бензилокси-3-метоксифенил)-2-(3-тиенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(4-фторфенил)-1H-имидазол;
4-(4-бензилокси-3-метоксифенил)-2-(4-фторфенил)-5-метил-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-3-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-хлорфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]-2-(2-тиенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(3-тиенил)-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-[3-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-метилфенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дихлорфенил)-1H-имидазол.
Конкретные примеры особенно предпочтительного фенилимидазольного соединения, представленного общей формулой (1), включают следующие соединения:
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(4-фторфенил)-1H-имидазол;
4-(4-бензилокси-3-метоксифенил)-2-(4-фторфенил)-5-метил-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-хлорфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-метилфенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дихлорфенил)-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол.
Способ получения соединения (1) по настоящему изобретению
Фенилимидазольное соединение по настоящему изобретению может быть получено различными способами.
Их предпочтительный пример является следующим.
Схема реакций 1
[Хим. 2]
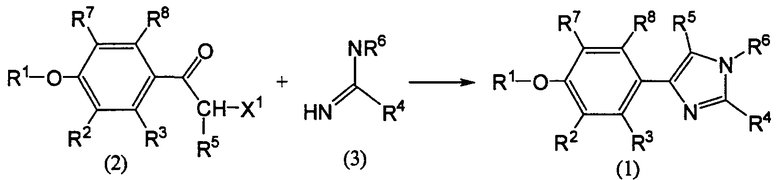
где значения R1, R2, R3, R4, R5, R6, R7 и R8 определены выше. X1 представляет собой атом галогена.
Как представлено на описанной выше схеме реакций 1, соединение (1) по настоящему изобретению может быть получено путем циклизации соединения (2) и соединения (3).
Реакцию циклизации проводят путем взаимодействия по существу эквимолярных количеств соединения (2) и соединения (3) в инертном растворителе, таком как тетрагидрофуран (ТГФ), 1,4-диоксан, вода или смесь указанных растворителей, в присутствии щелочи, такой как гидрокарбонат натрия, гидрокарбонат калия, карбонат натрия и т.п., при температуре от комнатной температуры до 100°C в течение 0,5-10 часов. На 1 моль соединения (2) используют 1-5 моль щелочи.
Соединение (2), которое используют в качестве исходного вещества в схеме реакций 1, может быть получено путем реакции галогенирования, представленной ниже на схеме реакций 2.
Схема реакций 2
[Хим. 3]
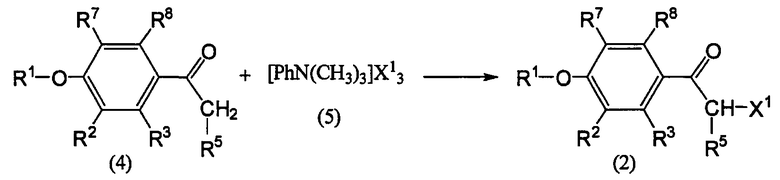
где значения R1, R2, R3, R5, R7, R8 и X1 определены выше.
Целевое соединение (2) может быть получено путем взаимодействия соединения (4) и тригалогенида триметилфениламмония (5), например, в инертном растворителе, таком как тетрагидрофуран (ТГФ), 1,4-диоксан и т.п., при 0°C-50°C в течение 5-20 часов. На 1 моль соединения (4) используют 1-1,3 моль тригалогенида триметилфениламмония (5).
Кроме того, на схеме реакций 2 соединение (4a), включенное в используемое в качестве исходного вещества соединение (4), представляет собой соединение, в котором R1 представляет собой фенил-низшую алкильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп; и соединение (4b), включенное в соединение (4), представляет собой соединение, в котором R1 представляет собой пиридил-низшую алкильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп. Указанные соединения (4a) и (4b) могут быть получены способами, представленными ниже на схеме реакций 3, схеме реакций 4 соответственно.
Схема реакций 3
[Хим. 4]
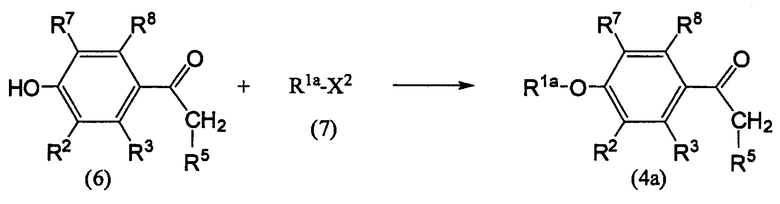
где R1a представляет собой фенил-низшую алкильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп, или пиридил-низшую алкильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп; и значения R2, R3, R5, R7 и R8 определены выше. X2 представляет собой атом галогена.
Упомянутое выше известное соединение (6) может быть преобразовано в соединение (4a) путем его взаимодействия с галогенидом (7).
Реакцию проводят в инертном растворителе, таком как N,N-диметилформамид (ДМФА), N,N-диметилацетамид (DMA), диметилсульфоксид (ДМСО) и т.п., в присутствии щелочи, такой как карбонат калия, карбонат натрия и т.п., и реакция завершается при температуре от комнатной температуры до 100°C в течение приблизительно от 5 до приблизительно 30 часов. На 1 моль соединения (6) используют 1-2 моль галогенида (7) и на 1 моль соединения (6) используют 1-3 моль щелочи.
Схема реакций 4
[Хим. 5]
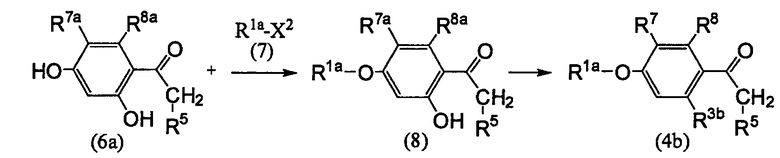
где R3b представляет собой низшую алкоксигруппу, R7a и R8a являются одинаковыми или разными и представляют собой атом водорода или гидроксигруппу, и значения R1a, R2, R3, R5, R7, R8 и X2 определены выше.
Упомянутое выше известное соединение (6a) подвергают взаимодействию с галогенидом (7), преобразуют в соединение (8), а затем алкилируют. Таким образом, соединение (4b) может быть получено из соединения (6a). Взаимодействие соединения (6a) с галогенидом (7) проводят в тех же реакционных условиях, что и реакцию, представленную выше на схеме реакций 3.
Реакцию алкилирования полученного соединения (8) проводят в инертном растворителе, таком как N,N-диметилформамид (ДМФА), N,N-диметилацетамид (DMA), диметилсульфоксид (ДМСО) и т.п., в присутствии щелочи, такой как карбонат калия, карбонат натрия и т.п., с использованием низшего алкилгалогенида, такого как йодметан, йодэтан, 1-йодпропан, 1-йодбутан, 1-йодпентан, 1-йодгексан и т.п., и реакция завершается при 0°C-50°C в течение приблизительно от 10 до приблизительно 100 часов. На 1 моль соединения (8) используют 1-3 эквивалента щелочи, и на 1 моль соединения (8) используют 1-2 эквивалента низшего алкилгалогенида.
Некоторые из соединений по настоящему изобретению способны к образованию фармакологически приемлемых солей присоединения кислоты, например гидрохлорида, нитрата, сульфата, гидробромида, фосфата, карбоната, ацетата, лактата, цитрата и т.п. Эти соли присоединения кислоты также могут быть получены в соответствии с известными способами. Настоящее изобретение также включает эти соли присоединения кислоты.
Следует заметить, что некоторые из соединений по настоящему изобретению могут включать оптические изомеры, содержащие атом углерода в качестве центра асимметрии. Настоящее изобретение включает все рацематы, которые представляют собой смеси таких оптических изомеров, и оптически активные формы (т.е. оптические изомеры). Вышеупомянутые оптические изомеры могут быть разделены с использованием различных известных способов разделения.
Целевое соединение в каждом способе, представленном на любой описанной выше схеме реакций, и соединение по настоящему изобретению могут быть легко выделены и очищены общепринятыми способами разделения. Примеры таких способов разделения включают адсорбционную хроматографию, препаративную тонкослойную хроматографию, перекристаллизацию, экстракцию растворителем и т.п.
Соединение по настоящему изобретению (включая его соль; то же самое применяется ниже) обладает активирующим действием в отношении липопротеинлипазы (LPL) и эффективно в качестве активатора LPL для профилактики и лечения гиперлипидемии, артериосклероза, ожирения и тому подобного. Соответственно, настоящее изобретение также относится к средству для профилактики и лечения гиперлипидемии, антиартериосклеротическому средству, средству от ожирения и тому подобного.
Настоящее изобретение также относится к фармацевтической композиции, содержащей соединение по настоящему изобретению. Такая фармацевтическая композиция обычно применяется в форме общего фармацевтического препарата. Примеры фармацевтически приемлемых носителей, используемых для фармацевтического препарата по настоящему изобретению, включают наполнители, разбавители, связующие вещества, увлажнители, разрыхлители, поверхностно-активные вещества, смазки и подобные разбавители и эксципиенты, которые обычно используются в соответствии с применением фармацевтических препаратов. Указанные носители соответствующим образом выбирают в соответствии со стандартной лекарственной формой конечного фармацевтического препарата.
В зависимости от терапевтической цели для вышеупомянутого фармацевтического препарата может быть соответствующим образом выбран набор стандартных лекарственных форм. Типичными примерами являются таблетки, пилюли, порошки, растворы, суспензии, эмульсии, гранулы, капсулы, суппозитории, инъецируемые формы (растворы, суспензии и т.п.), мази и т.п.
В качестве вышеупомянутых фармацевтически приемлемых носителей для получения таблеток могут быть использованы, например, следующие: лактоза, сахароза, хлорид натрия, глюкоза, мочевина, крахмал, карбонат кальция, каолин, кристаллическая целлюлоза, кремниевая кислота, фосфат калия и другие эксципиенты; вода, этанол, пропанол, простой сироп, растворы глюкозы, растворы крахмала, растворы желатина, карбоксиметилцеллюлоза, гидроксипропилцеллюлоза, метилцеллюлоза, поливинилпирролидон и другие связующие вещества; карбоксиметилцеллюлоза натрия, карбоксиметилцеллюлоза кальция, гидроксипропилцеллюлоза с низкой степенью замещения, сухой крахмал, альгинат натрия, порошок агара, порошок ламинарина, бикарбонат натрия, карбонат кальция и другие разрыхлители; сложные эфиры жирных кислот полиоксиэтиленсорбитана, лаурилсульфат натрия, моноглицериды стеариновой кислоты и другие поверхностно-активные вещества; сахароза, стеарин, масло какао, гидрированные масла и другие ингибиторы разрыхления; четвертичные аммониевые основания, лаурилсульфат натрия и другие ускорители всасывания; глицерин, крахмал и другие увлажнители; крахмал, лактоза, каолин, бентонит, коллоидная кремниевая кислота и другие адсорбенты; очищенный тальк, стеарат, порошок борной кислоты, полиэтиленгликоль и другие смазки и т.п. Кроме того, при необходимости, такие таблетки могут быть покрыты типичными покровными веществами для приготовления, например, таблеток в сахарной оболочке, таблеток в желатиновой оболочке, таблеток с кишечнорастворимым покрытием, таблеток с пленочной оболочкой, двухслойных или многослойных таблеток и т.п.
В качестве фармацевтически приемлемых носителей для получения пилюль могут быть использованы, например, следующие: глюкоза, лактоза, крахмал, масло какао, гидрированные растительные масла, каолин, тальк и другие эксципиенты; порошок аравийской камеди, порошок трагаканта, желатин, этанол и другие связующие вещества; ламинарин, агар и другие разрыхлители и т.п.
В качестве фармацевтически приемлемых носителей для получения суппозиториев могут быть использованы, например, следующие: полиэтиленгликоль, масло какао, высшие спирты, сложные эфиры высших спиртов, желатин, полусинтетические глицериды и т.п.
Капсулы приготавливают в соответствии с известными способами, обычно путем смешивания соединений по настоящему изобретению с вышеупомянутыми фармацевтически приемлемыми носителями и помещения смеси в твердую желатиновую капсулу, мягкую желатиновую капсулу или т.п.
Для приготовления инъецируемых форм, таких как растворы, эмульсии, суспензии и тому подобное, инъецируемые формы стерилизуют и предпочтительно придают им изотоничность по отношению к крови. В качестве разбавителей для получения таких инъецируемых форм могут быть использованы, например, следующие: вода, этанол, макрогол, пропиленгликоль, этоксилированный изостеариловый спирт, полиоксилированный изостеариловый спирт, сложные эфиры жирных кислот полиоксиэтиленсорбитана и т.п. В этом случае фармацевтический препарат может содержать хлорид натрия, глюкозу или глицерин в количестве, достаточном для приготовления изотонического раствора, а также может содержать обычные солюбилизаторы, буферы, успокаивающие средства и т.п.
В качестве разбавителей для получения мазей, таких как пасты, кремы, гели и тому подобное, могут быть использованы, например, следующие: белый вазелин, парафин, глицерин, производные целлюлозы, полиэтиленгликоль, силикон, бентонит и т.п.
Кроме того, при необходимости, препарат по настоящему изобретению может содержать красители, консерванты, ароматизаторы, отдушки, подсластители и тому подобное, и/или другие лекарственные средства и может быть приготовлен в виде фармацевтического препарата.
Количество соединений (соединений - активных ингредиентов) по настоящему изобретению, содержащихся в препарате по настоящему изобретению, конкретно не ограничивается и соответствующим образом выбирается из широкого диапазона. Как правило, их пропорция в фармацевтическом препарате составляет приблизительно от 0,5 до приблизительно 90 мас.%, предпочтительно приблизительно от 1 до приблизительно 85 мас.%.
Способ введения описанного выше фармацевтического препарата конкретно не ограничивается и определяется формой препарата, возрастом пациента, полом и другими условиями, тяжестью заболевания и т.п. Например, таблетки, пилюли, растворы, суспензии, эмульсии, гранулы и капсулы вводят перорально. Инъецируемые формы вводят внутривенно, внутримышечно, внутрикожно, подкожно или интраперитонеально, по отдельности или в сочетании с обычно инъецируемыми трансфузиями, такими как растворы глюкозы, растворы аминокислот и т.п. Суппозитории вводят ректально.
Дозу описанного выше фармацевтического препарата выбирают соответствующим образом в соответствии со способом применения, возрастом пациента, полом и другими условиями, тяжестью заболевания и т.п. Количество соединений по настоящему изобретению, то есть активных ингредиентов, составляет обычно приблизительно от 0,5 до приблизительно 20 мг, предпочтительно приблизительно от 1 до приблизительно 10 мг на кг массы тела взрослого человека в сутки. Препарат можно вводить один раз в сутки или от 2 до 4 раз в сутки отдельными дозами.
Кроме того, настоящее изобретение представляет собой способ активации LPL у пациентов, нуждающихся в лечении путем активации LPL, причем способ включает введение пациентам эффективного количества по меньшей мере одного соединения по настоящему изобретению.
В дополнение, настоящее изобретение относится к способу профилактики или лечения гиперлипидемии у пациентов, нуждающихся в профилактике или лечении гиперлипидемии, причем способ включает введение пациентам эффективного количества по меньшей мере одного соединения по настоящему изобретению.
Кроме того, настоящее изобретение относится к способу профилактики или лечения артериосклероза у пациентов, нуждающихся в профилактике или лечении артериосклероза, причем способ включает введение пациентам эффективного количества по меньшей мере одного соединения по настоящему изобретению.
Кроме того, настоящее изобретение относится к способу профилактики или лечения ожирения у пациентов, нуждающихся в лечении ожирения, причем способ включает введение пациентам эффективного количества по меньшей мере одного соединения по настоящему изобретению.
Кроме того, настоящее изобретение относится к применению соединений по настоящему изобретению для получения LPL-активирующей композиции; к применению соединений по настоящему изобретению для получения композиции для профилактики или лечения гиперлипидемии и к применению соединений по настоящему изобретению для получения композиции против ожирения.
Примеры
Далее в этом документе настоящее изобретение описывается более подробно со ссылкой на справочные примеры, примеры и т.п. Тем не менее настоящее изобретение ими не ограничивается.
Справочный пример 1
Получение 2-бром-1-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]этанона
К ДМФА (80 мл) добавляли 1-(4-гидрокси-3-метоксифенил)этанон (25,0 г, 0,15 моль) и карбонат калия (15,4 г, 0,11 моль). К смеси добавляли 4-бром-1-(бромметил)-2-фторбензол (50,2 г, 0,19 моль), перемешивали смесь при комнатной температуре в течение 2 часов, а затем перемешивали при 60°C в течение 16 часов. Добавляли метанол (40 мл) к этому реакционному раствору, который перемешивали при 60°C в течение 1 часа, а затем разбавляли водой (200 мл). Выпавшие в осадок кристаллы фильтровали и промывали водой и гексаном. Кристаллы сушили в условиях вакуума при 60°C в течение 3 часов с получением 1-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]этанона (52,7 г).
Затем полученное выше соединение (52,0 г) растворяли в ТГФ (170 мл) и при охлаждении на льду добавляли трибромид триметилфениламмония (57,2 г, 0,15 моль). Смесь перемешивали при охлаждении на льду в течение 1 часа, а затем перемешивали при комнатной температуре в течение 14 часов. К этому раствору добавляли воду (200 мл), выпавшие в осадок кристаллы фильтровали и промывали метанолом с получением целевых соединений (59,7 г). Ниже в таблице 1 представлены структура и температура плавления полученного соединения.
Справочные примеры 2-7
Каждое из соединений, перечисленных в таблице 1, получали способом, аналогичным описанному в справочном примере 1.
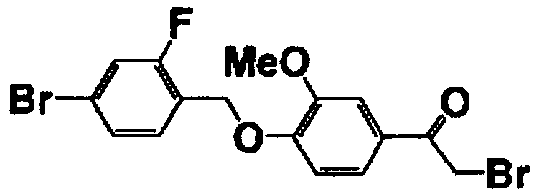
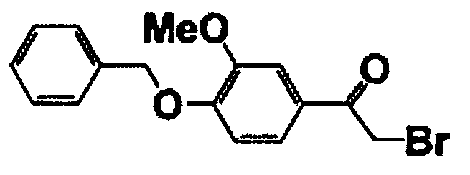
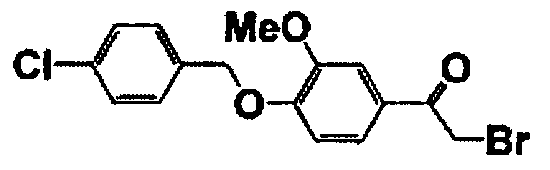
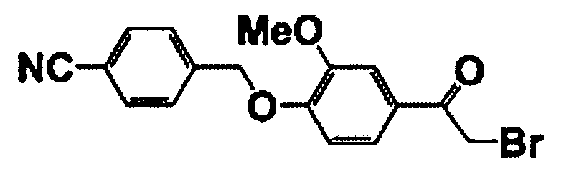
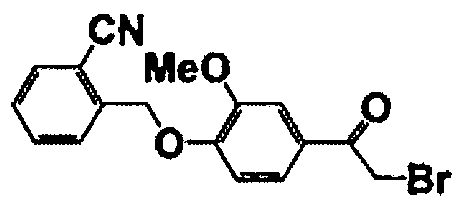
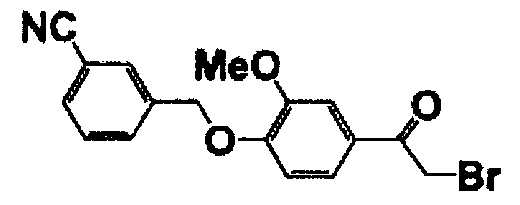
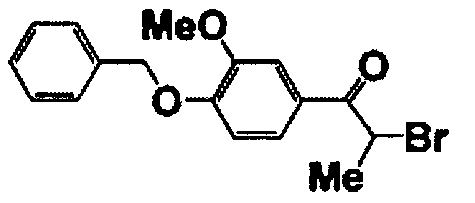
Справочный пример 8
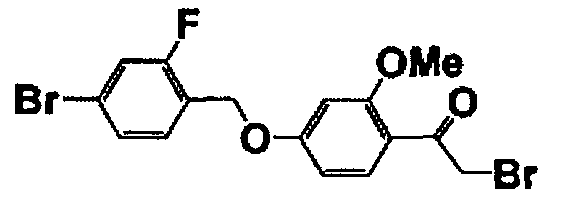
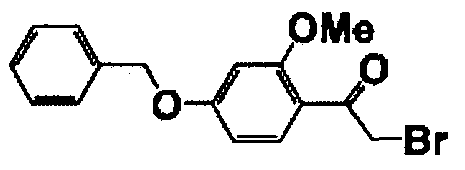
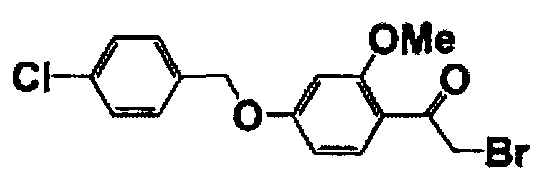
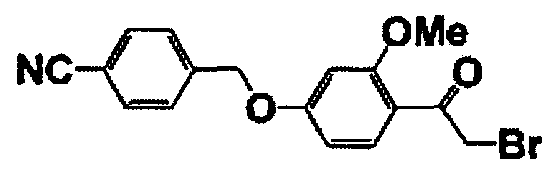
Получение 2-бром-1-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]этанона
1-(2,4-Дигидроксифенил)этанон (25,3 г, 0,17 моль) и 4-бром-1-бромметил-2-фторбензол (44,6 г, 0,17 моль) растворяли в ДМФА (150 мл). При охлаждении на льду к раствору добавляли карбонат калия (11,8 г, 0,09 моль), перемешивали смесь при охлаждении на льду, а затем перемешивали при комнатной температуре в течение 12 часов. При охлаждении на льду к смеси снова добавляли карбонат калия (11,8 г, 0,09 моль), перемешивали смесь при охлаждении на льду в течение 30 минут, а затем перемешивали при комнатной температуре в течение 12 часов. К этой реакционной смеси добавляли метанол (100 мл) и перемешивали смесь при 80°C в течение 1 часа. После этого к смеси добавляли воду (150 мл), выпавшие в осадок кристаллы фильтровали и промывали метанолом. Кристаллы сушили в условиях вакуума при 60°C в течение 2 часов с получением 1-[4-(4-бром-2-фторбензилокси)-2-гидроксифенил]этанона (43,5 г, выход: 75%).
Затем полученное выше соединение (43,5 г, 0,13 моль) и карбонат калия (21,6 г, 0,16 моль) добавляли к ДМФА (100 мл), при охлаждении на льду к смеси по каплям добавляли йодметан (27,3 г, 0,19 моль), перемешивали смесь при охлаждении на льду в течение 1 часа, а затем перемешивали при комнатной температуре в течение 48 часов. К этому реакционному раствору добавляли метанол (100 мл) и перемешивали смесь при 80°C в течение 2 часов. После этого к смеси добавляли воду (150 мл), выпавшие в осадок кристаллы фильтровали и промывали метанолом. Кристаллы сушили в условиях вакуума при 60°C в течение 1 часа с получением 1-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]этанона (42,1 г, выход: 92%).
Полученное соединение (42,0 г) растворяли в ТГФ (100 мл) и при охлаждении на льду добавляли к смеси трибромид триметилфениламмония (44,7 г, 0,12 моль). Смесь перемешивали в течение 1 часа при охлаждении на льду, а затем перемешивали при комнатной температуре в течение 13 часов. К этому раствору добавляли воду (100 мл) и метанол (100 мл), выпавшие в осадок кристаллы фильтровали и перекристаллизовывали из этилацетата (100 мл) и метанола (200 мл) с получением целевого соединения (46,8 г). Ниже в таблице 2 представлены структура и температура плавления полученного соединения.
Справочные примеры 9-12
Каждое из соединений, перечисленных в таблице 2, получали способом, аналогичным описанному в справочном примере 8.
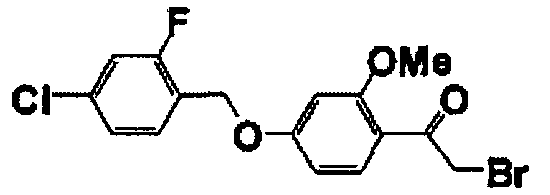
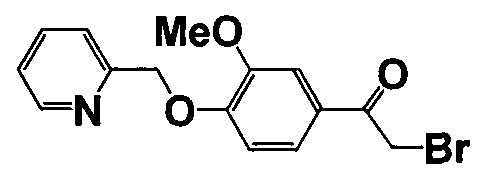
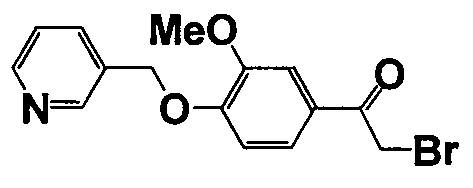
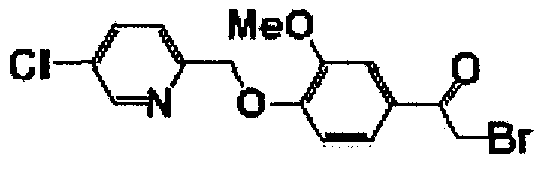
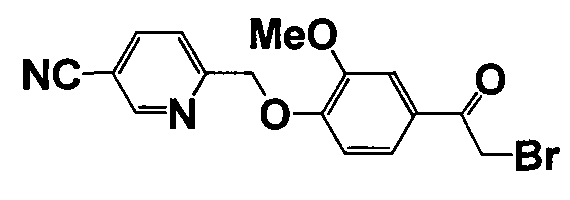
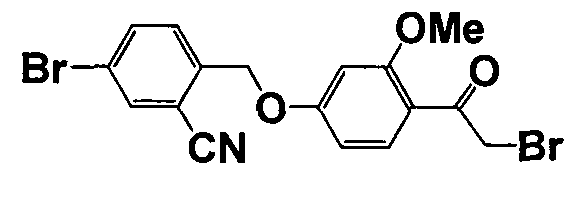
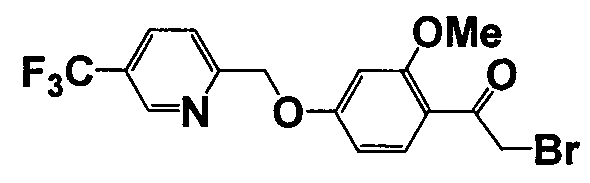
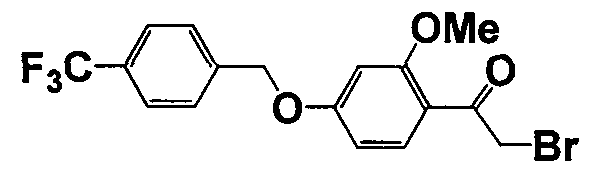
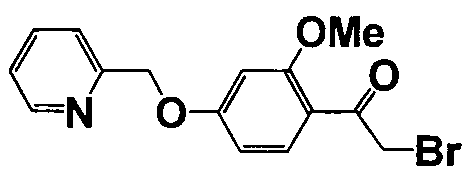
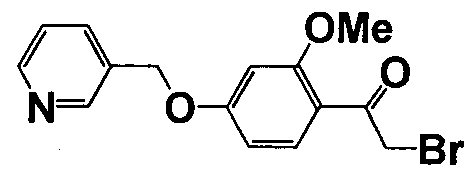
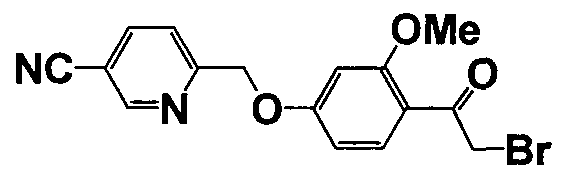
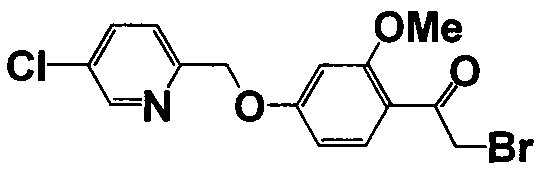
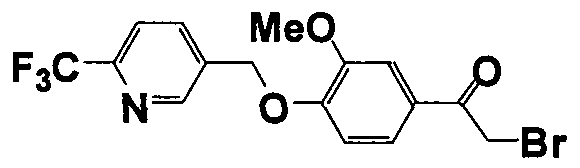
Справочные примеры 13-27
Каждое из соединений, перечисленных в таблице 3, получали способом, аналогичным описанному в справочном примере 1 или 8, с использованием соответствующих исходных веществ. В таблице 3 представлены структуры полученных соединений.
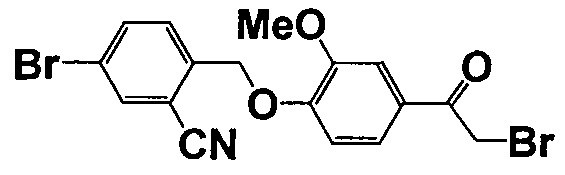
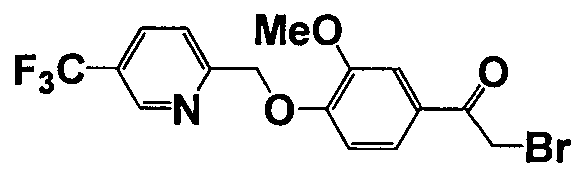
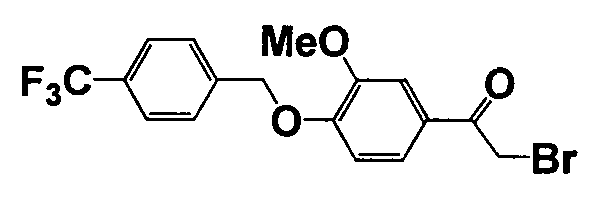
Пример 1
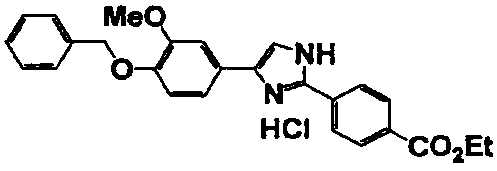
Получение гидрохлорида 4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]2-[4-(трифторметил)фенил]-1H-имидазола
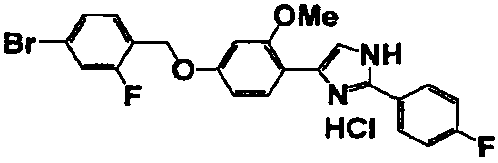
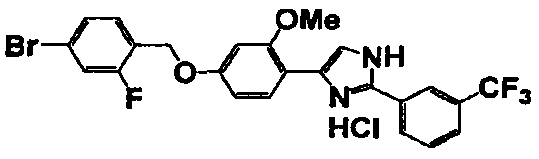
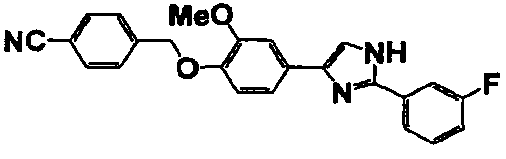
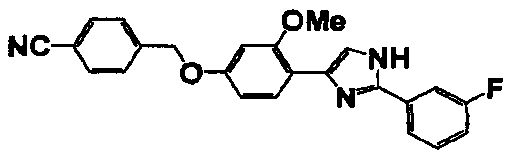
Гидрокарбонат калия (2,8 г, 28,0 ммоль), соединение справочного примера 1 (3,0 г, 6,9 ммоль) и дигидрат гидрохлорида п-трифторметилбензамидина (1,6 г, 6,9 ммоль) добавляли к смеси воды (4 мл) и ТГФ (12 мл) и перемешивали смесь при 60°C в течение 16 часов. Реакционный раствор охлаждали до комнатной температуры, добавляли к раствору этилацетат (70 мл) и перемешивали раствор в течение 30 минут. Этот раствор последовательно промывали водой и насыщенным солевым раствором и сушили безводным сульфатом магния. После выпаривания растворителя при пониженном давлении добавляли диэтиловый эфир и фильтровали выпавшие в осадок кристаллы. Кристаллы сушили в условиях вакуума при 70°C в течение 1 часа с получением целевого соединения (3,0 г). В таблице 4 представлены структура и свойства полученного соединения.
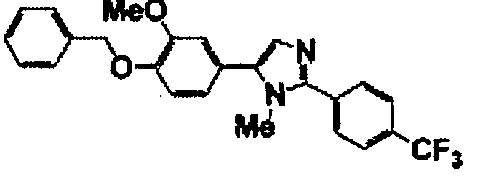
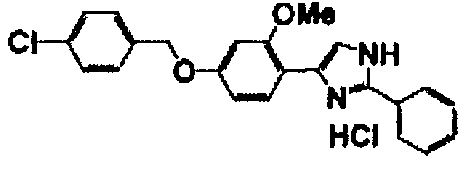
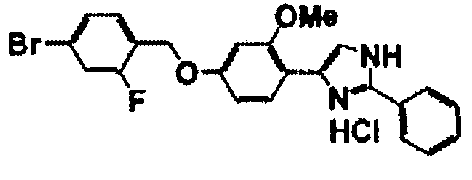
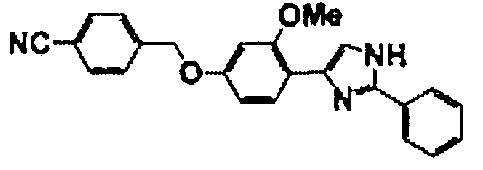
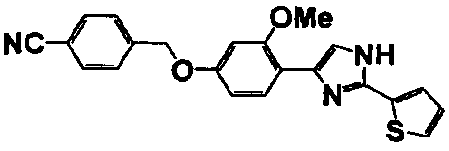
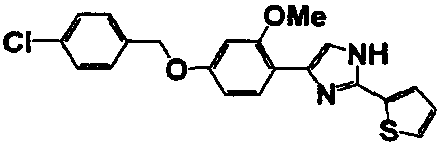
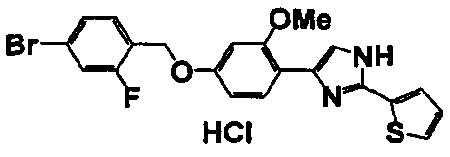
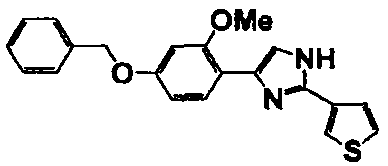
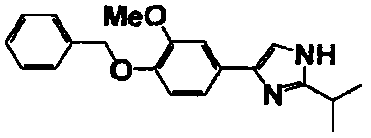
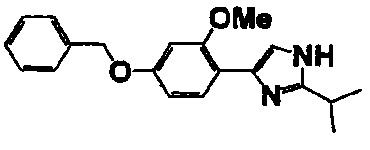
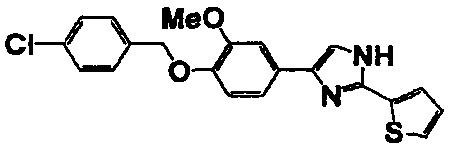
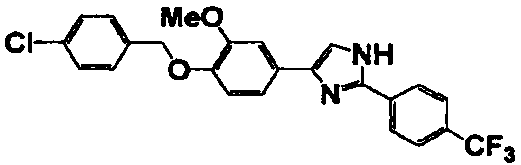
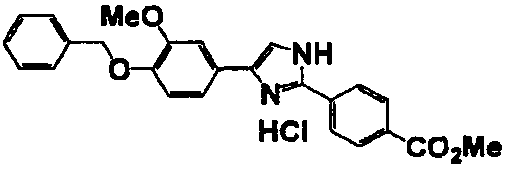
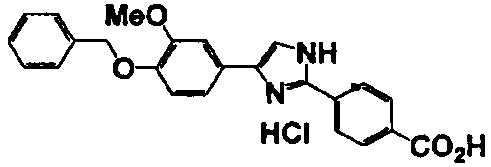
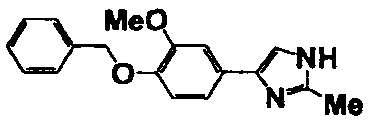
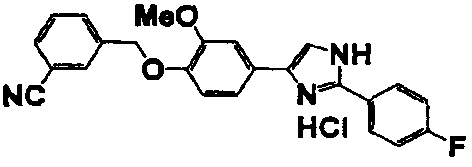
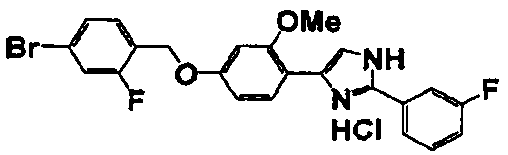
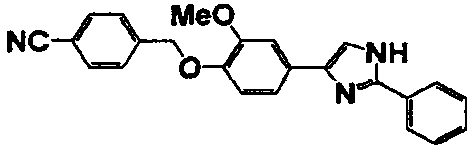
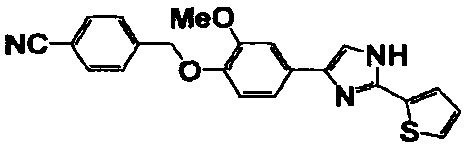
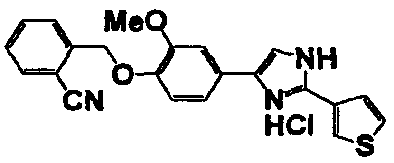
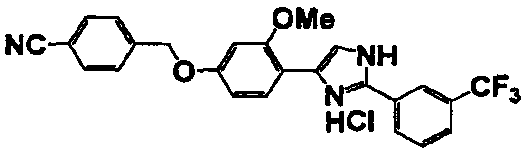
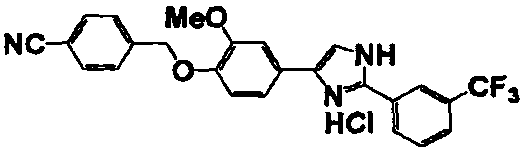
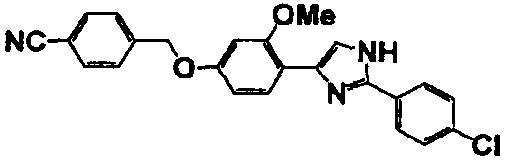
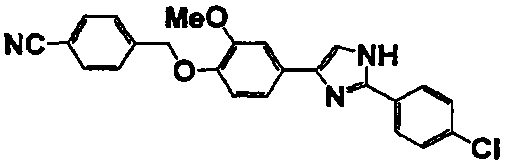
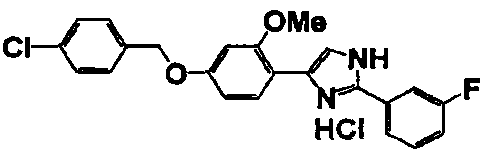
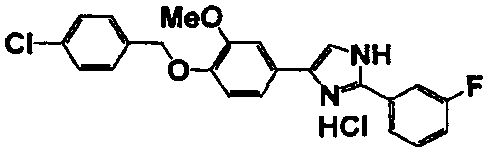
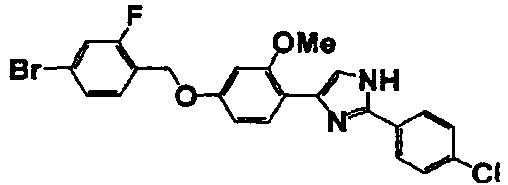
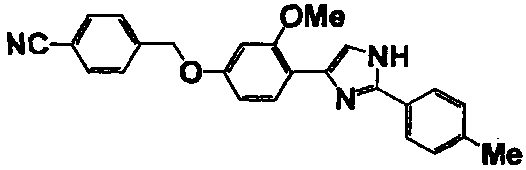
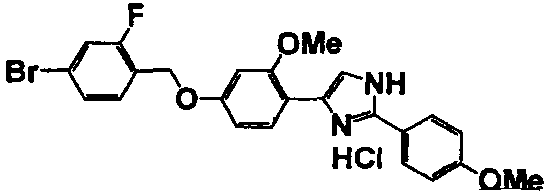
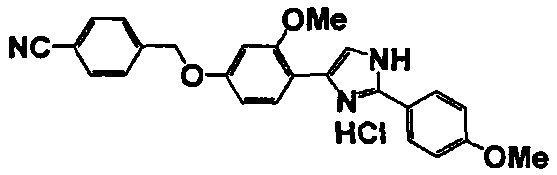
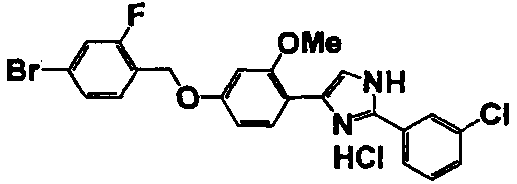
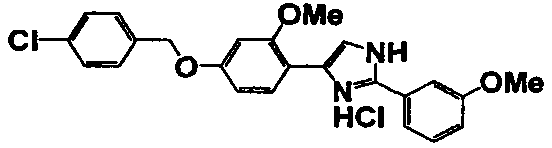
Примеры 2-101
Соединение по настоящему изобретению получали способом, аналогичным описанному в примере 1, используя в качестве исходных веществ соединения справочных примеров 1-12, известный 2-бром-1-(4-гидрокси-3-метоксифенил)этанон или т.п. В таблице 4 представлены структуры и свойства полученных соединений.
(°C)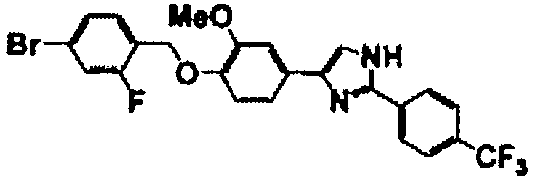
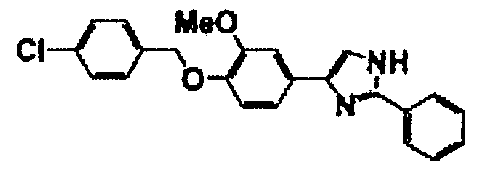
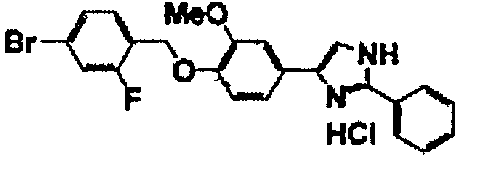
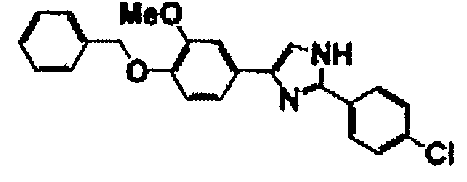
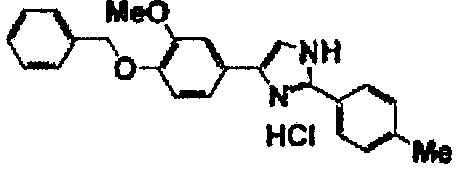
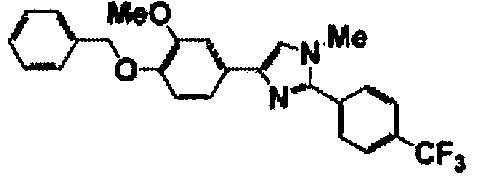
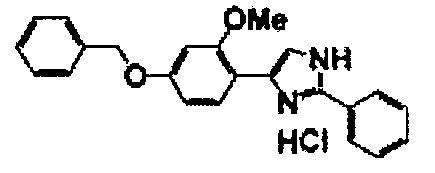
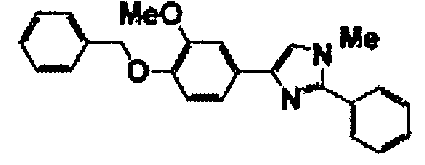
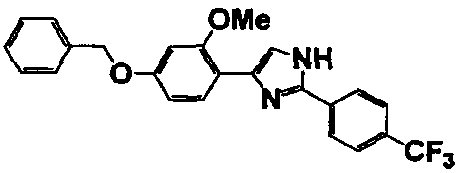
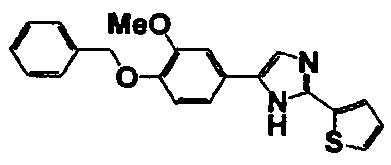
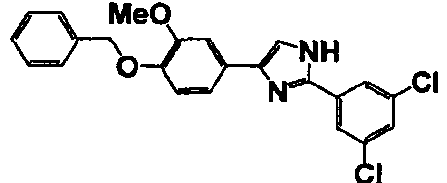
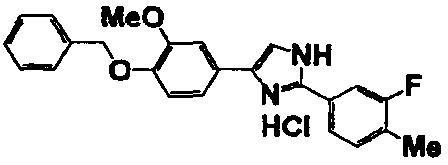
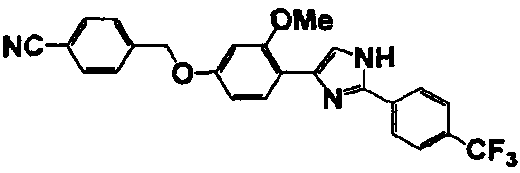
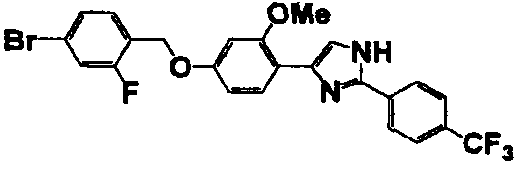
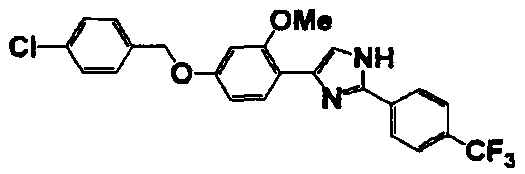
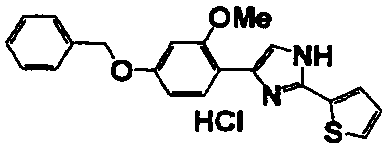
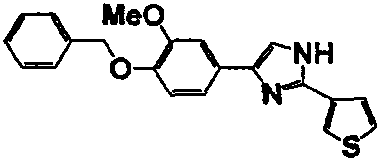
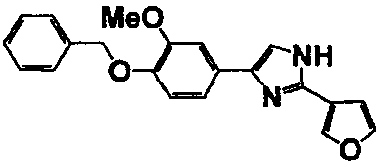
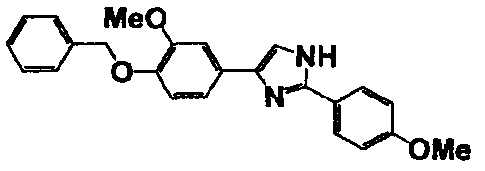
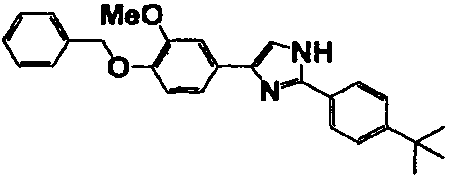
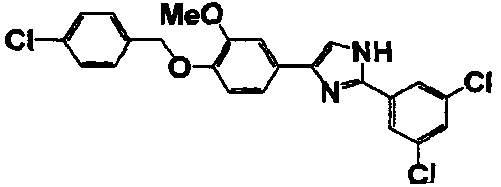
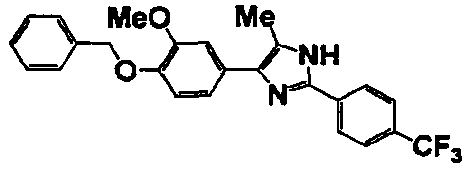
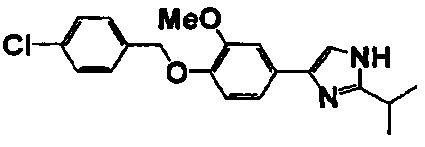
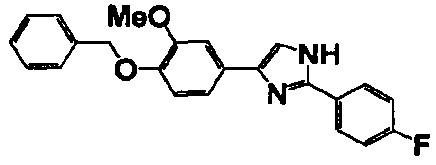
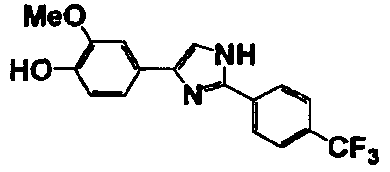
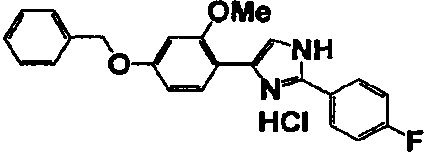
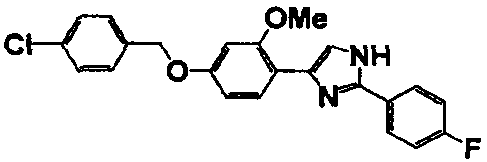
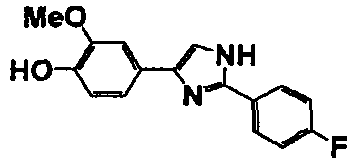
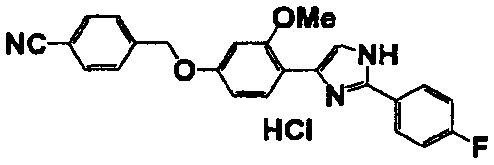
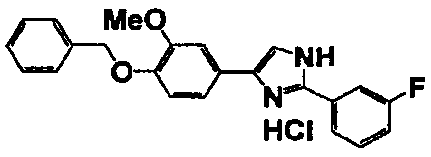
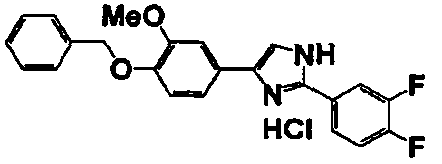
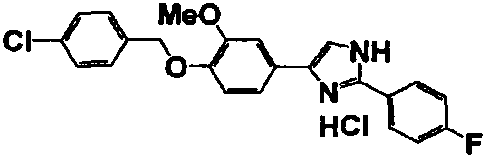
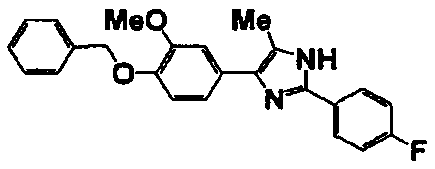
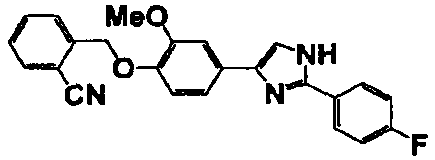
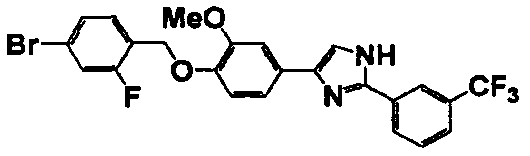
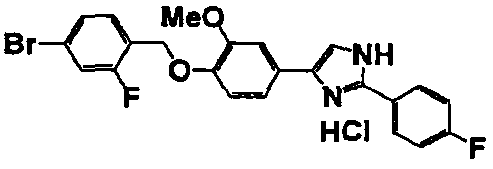
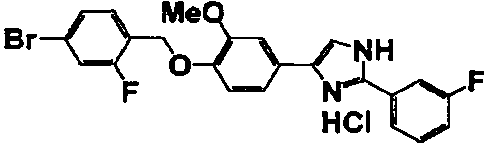
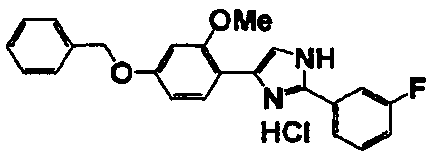
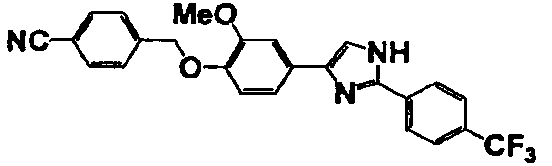
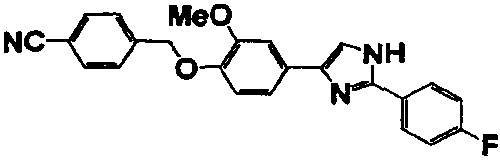
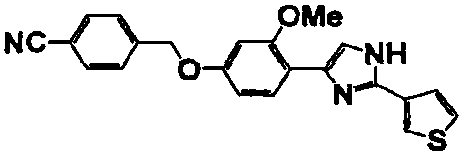
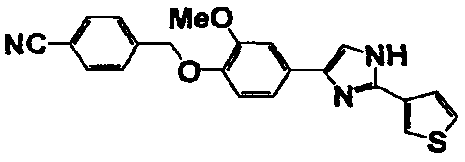
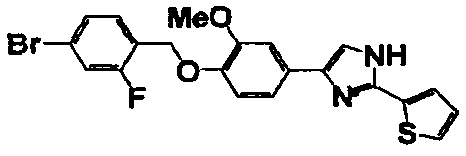
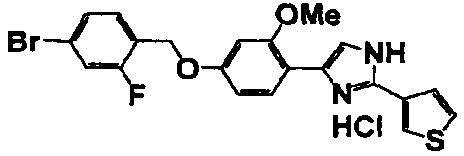
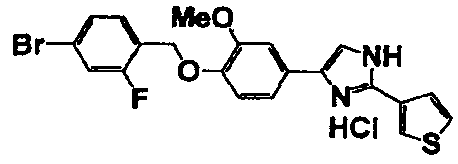
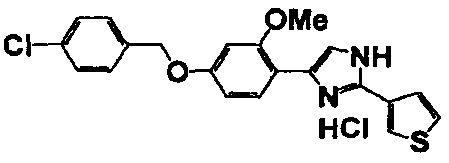
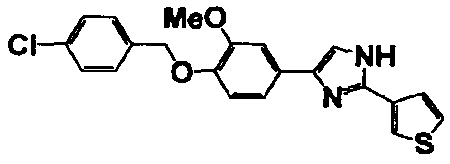
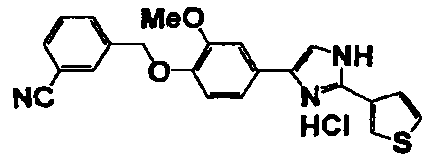
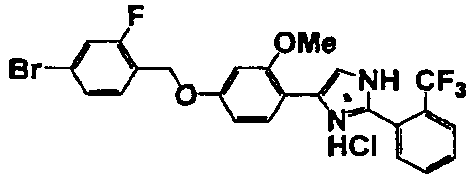
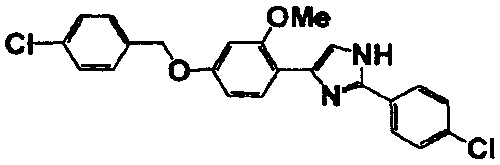
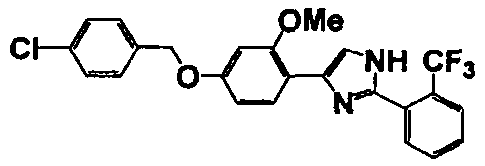
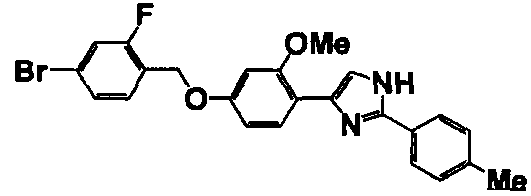
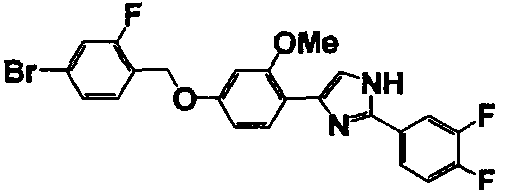
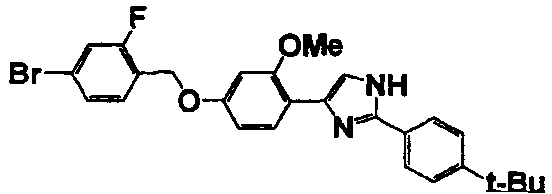
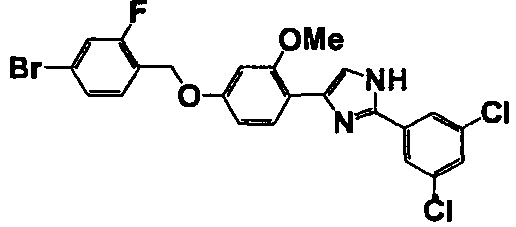
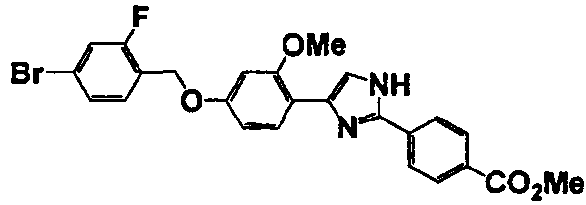
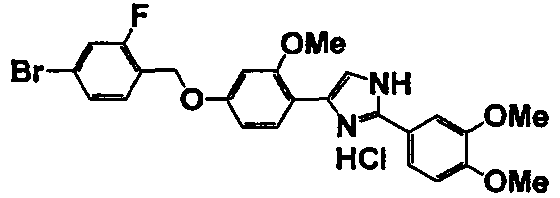
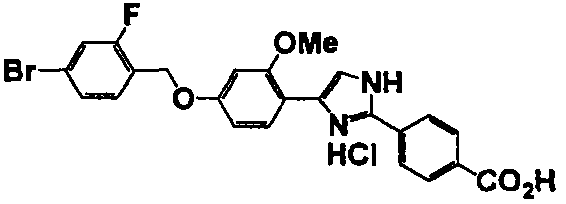
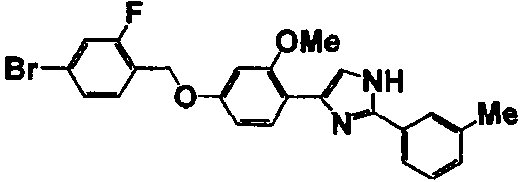
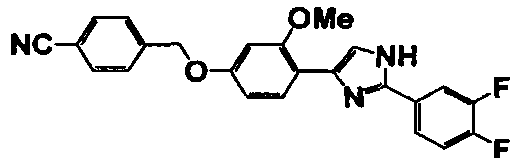
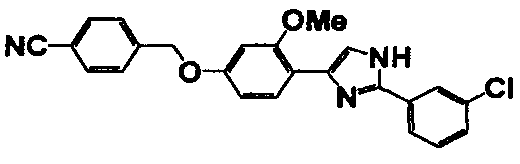
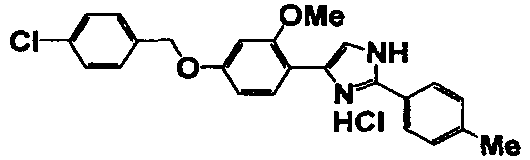
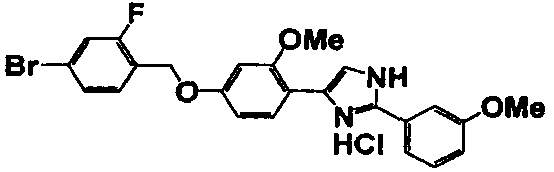
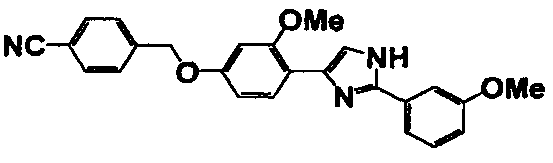
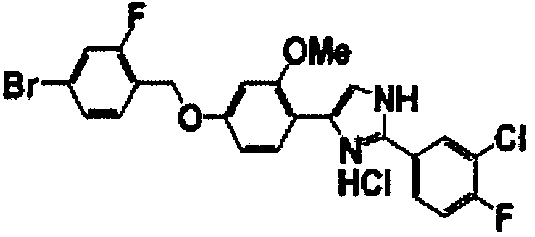
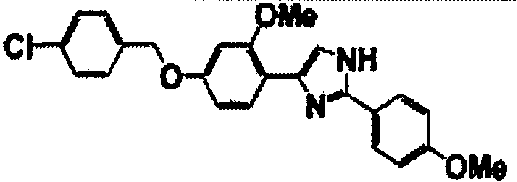
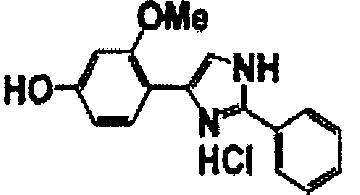
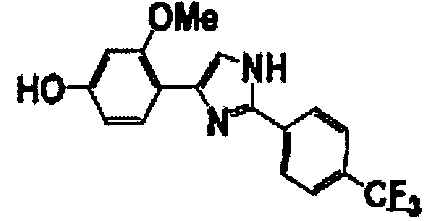
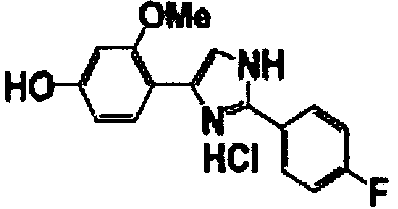
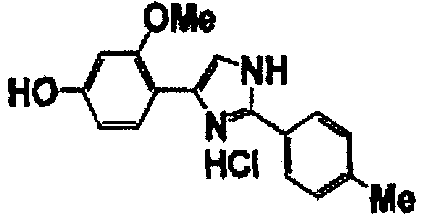
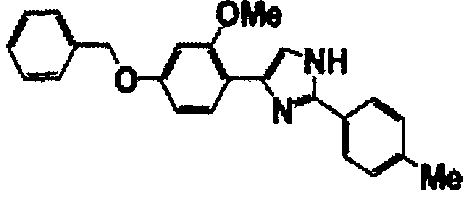
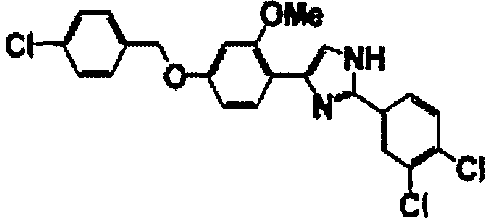
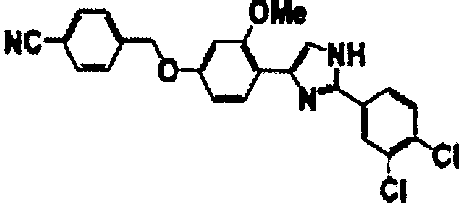
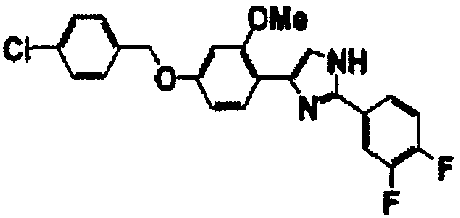
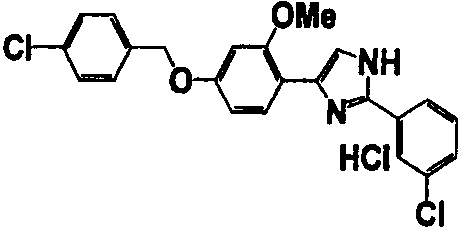
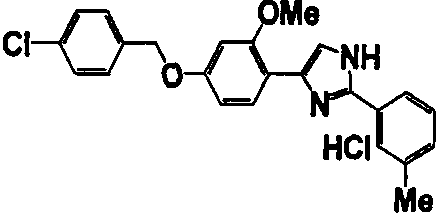
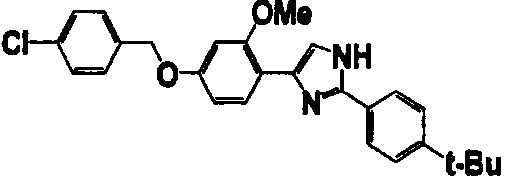
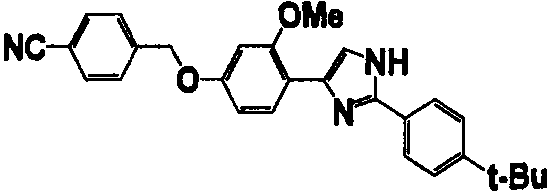
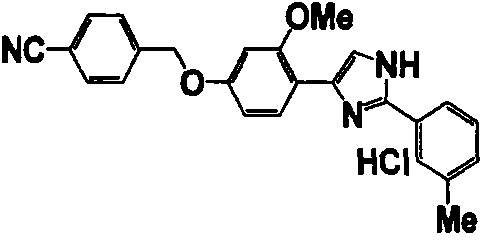
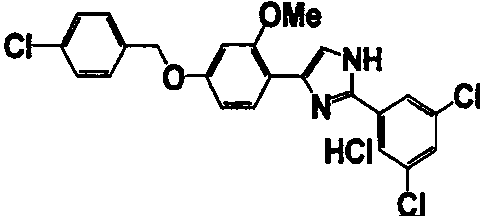
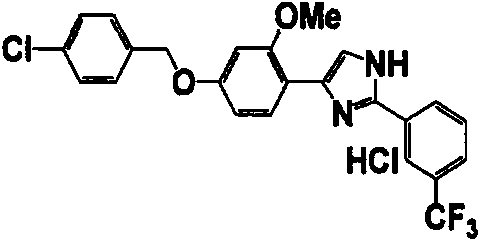
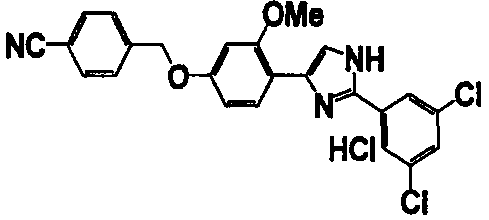
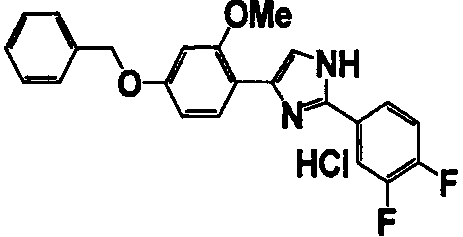
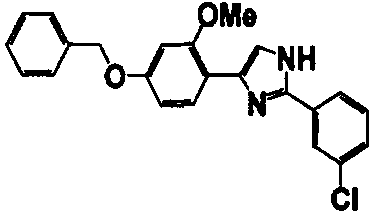
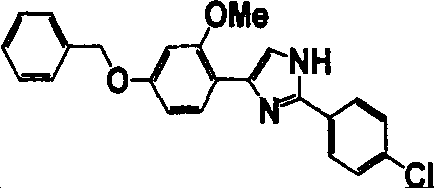
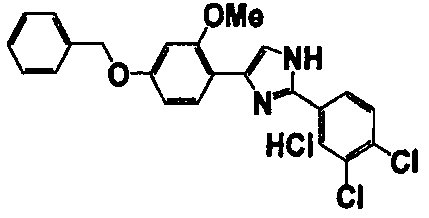
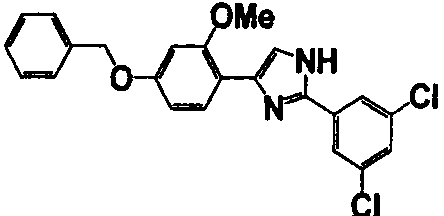
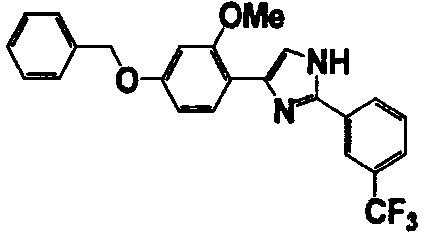
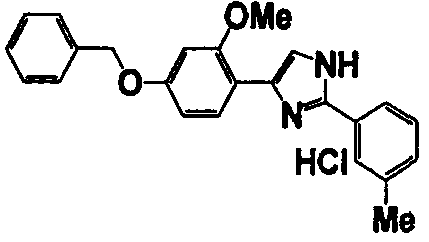
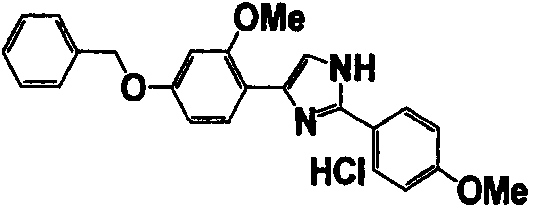
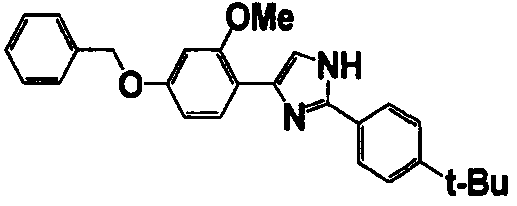
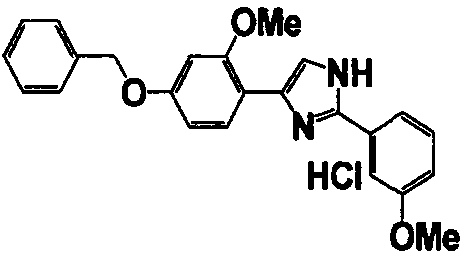
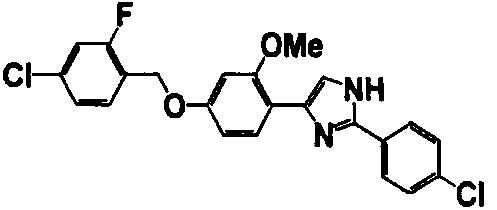
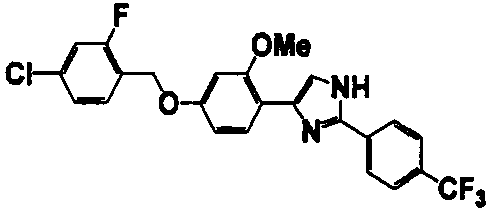
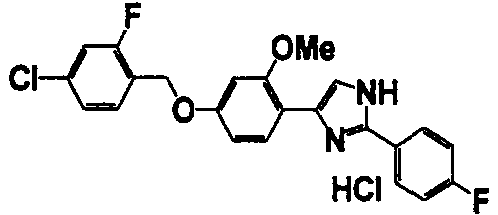
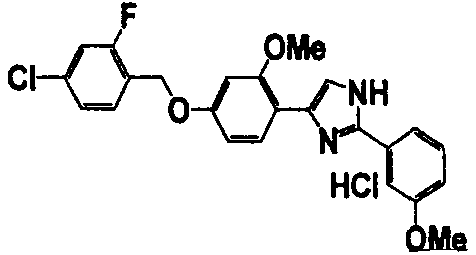
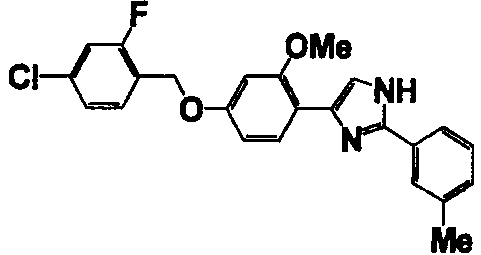
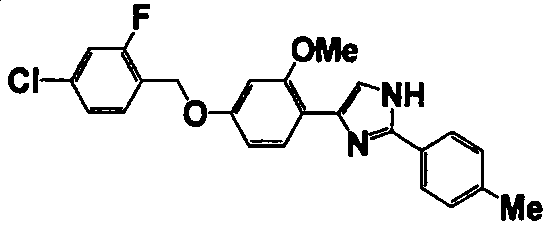
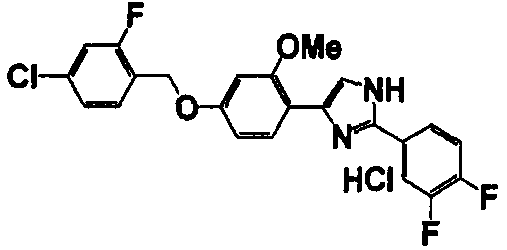
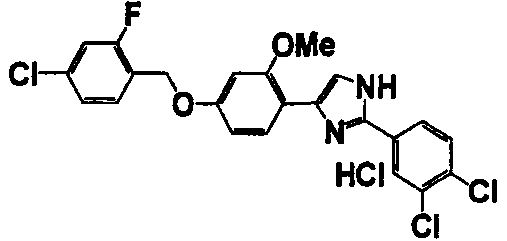
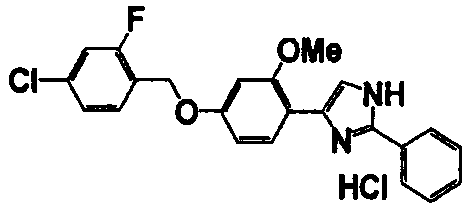
Примеры 102-139
Соединение по настоящему изобретению получали способом, аналогичным описанному в примере 1, используя соединения справочных примеров или соответствующие исходные вещества. В таблице 5 представлены структуры и свойства полученных соединений.
(°C)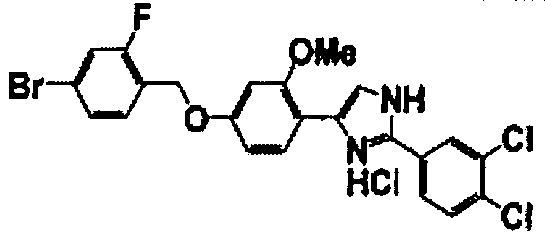
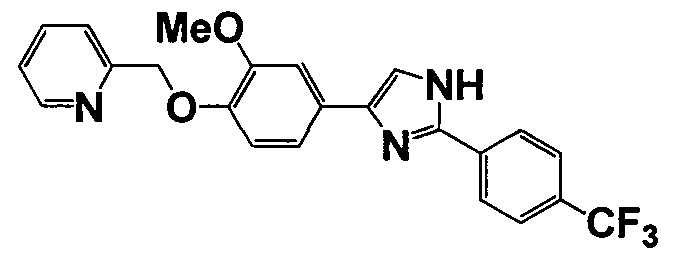
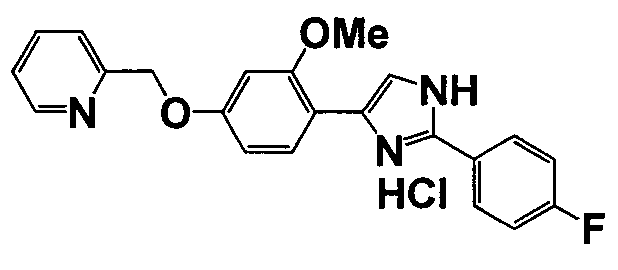
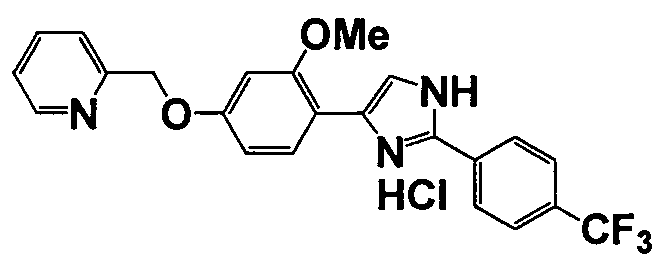
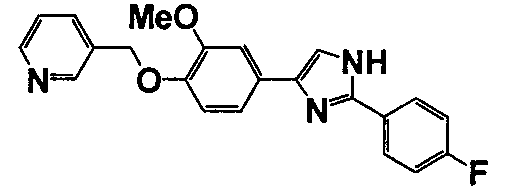
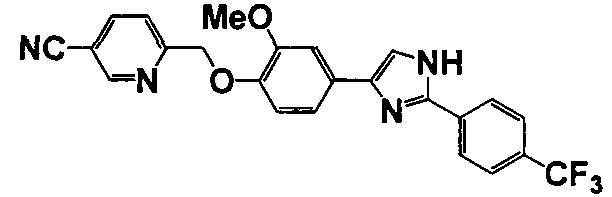
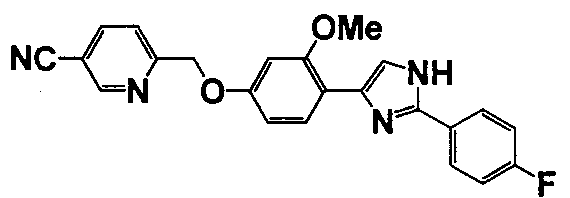
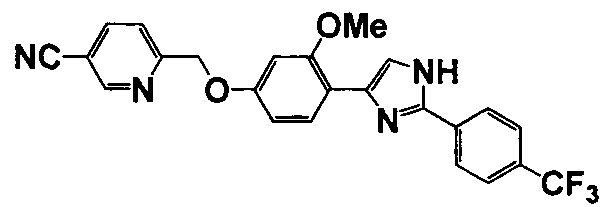
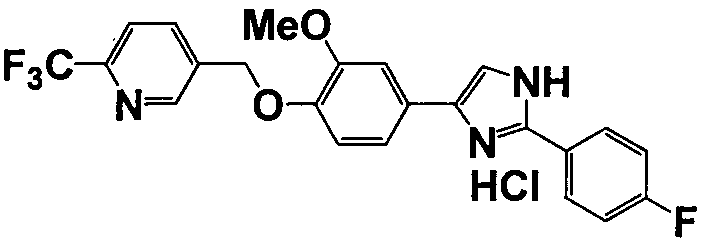
Примеры 140-188
Соединение по настоящему изобретению получали способом, аналогичным описанному в примере 1, используя соответствующие исходные вещества. В таблице 6 представлены структуры полученных соединений.
№
(°C)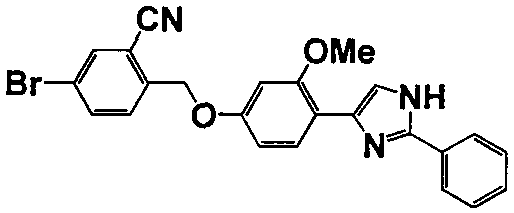
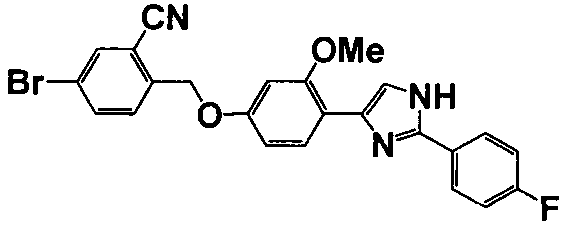
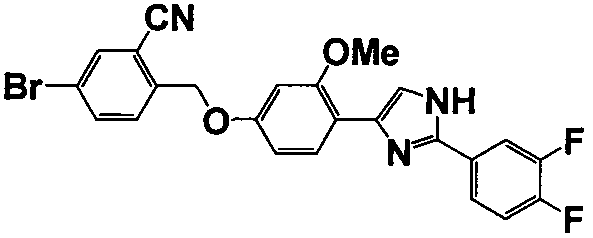
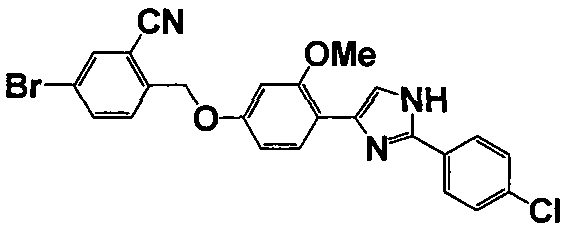
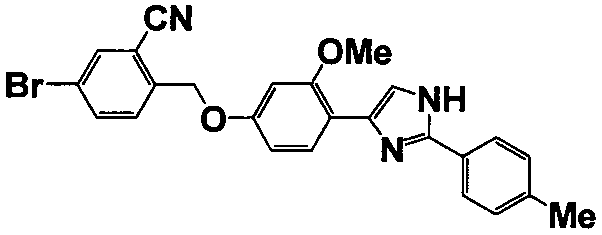
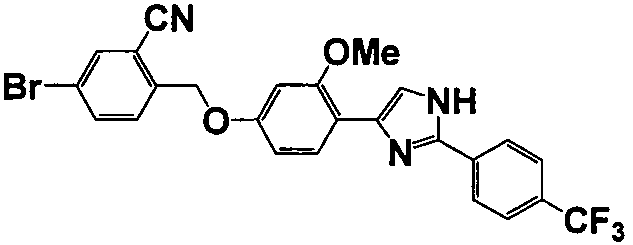
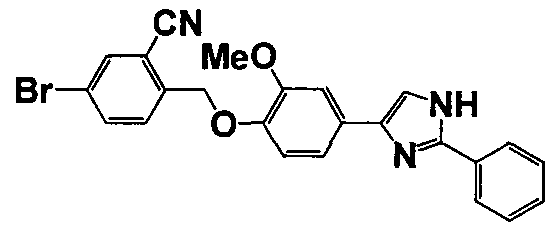
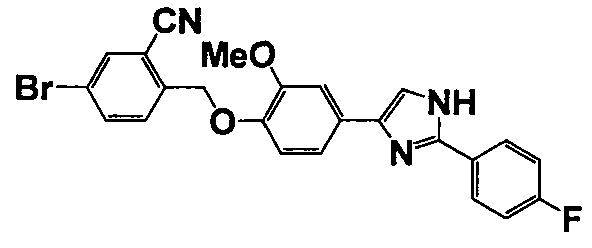
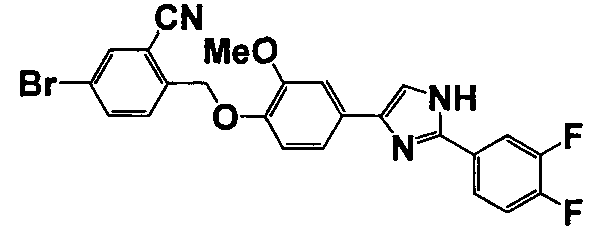
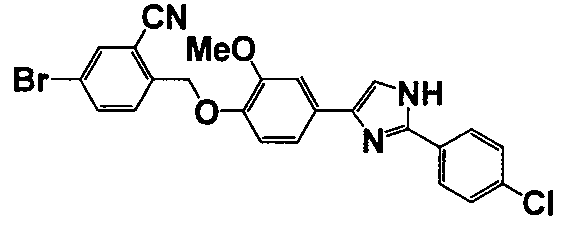
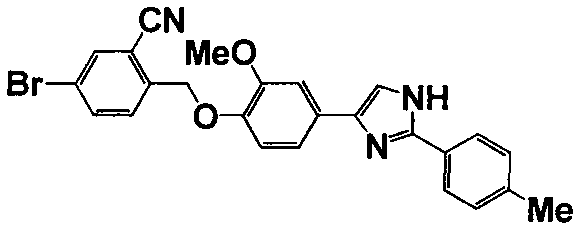
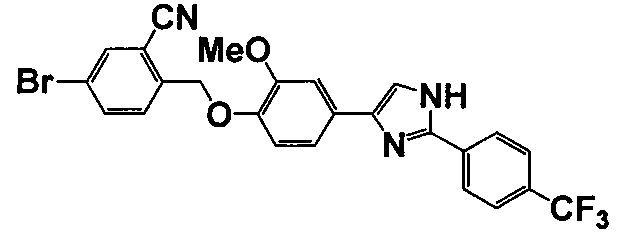
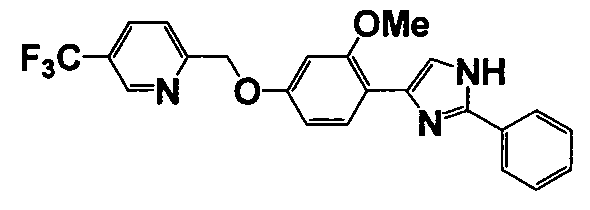
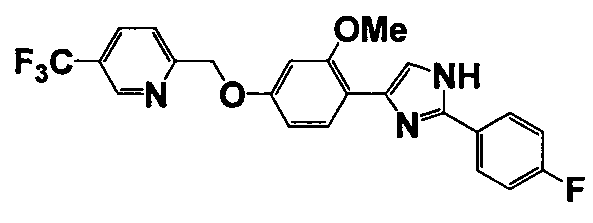
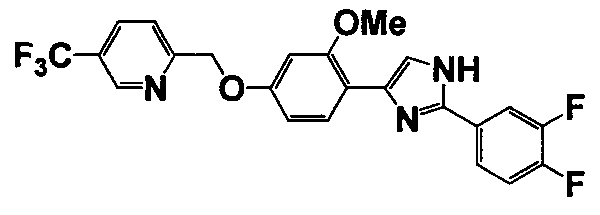
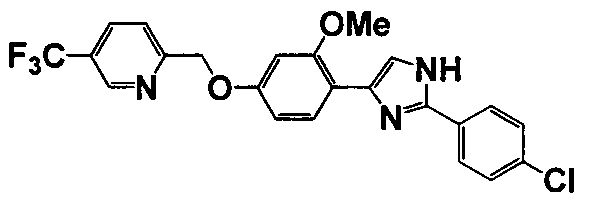
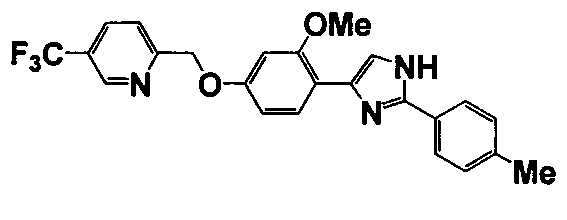
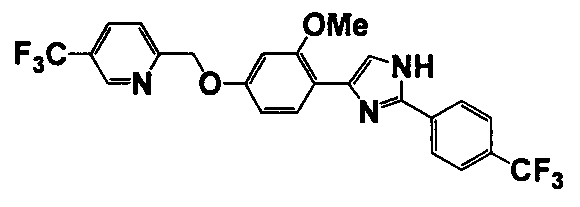
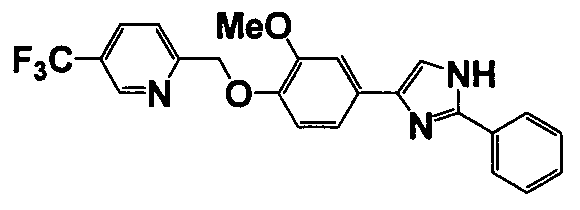
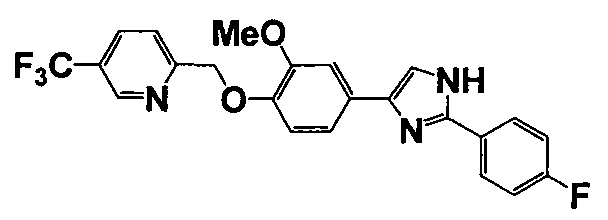
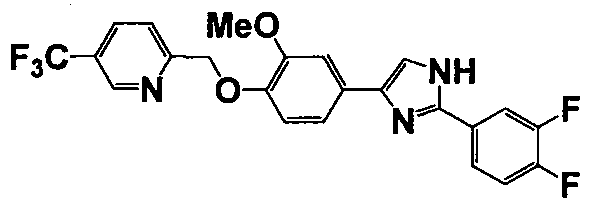
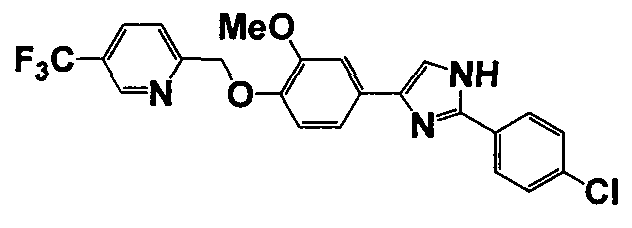
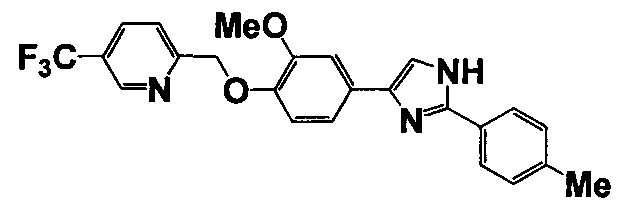
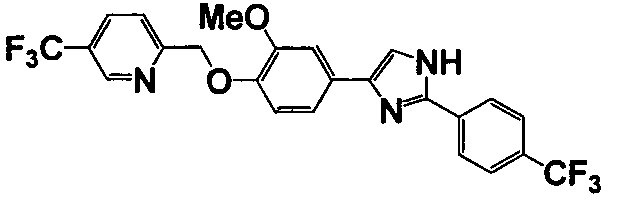
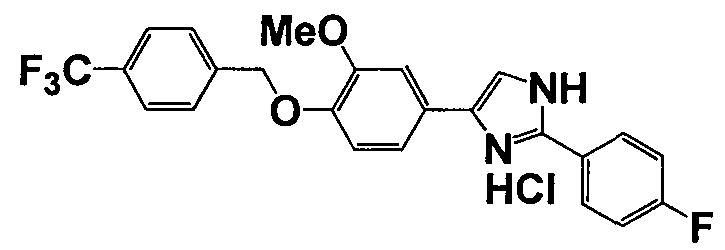
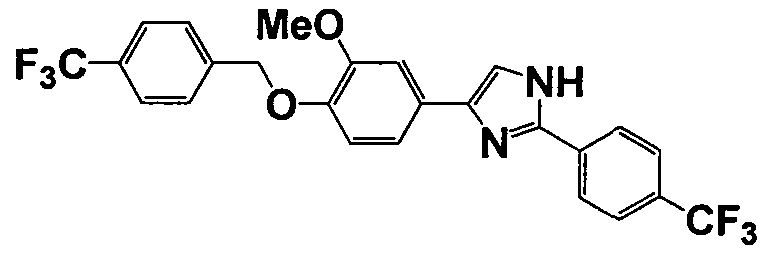
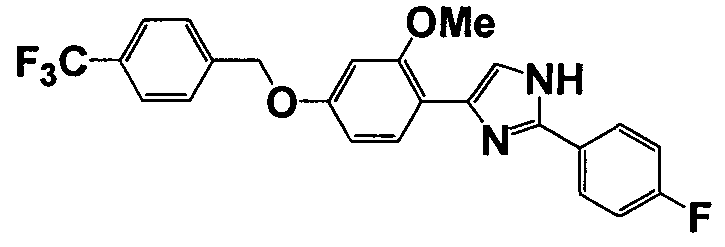
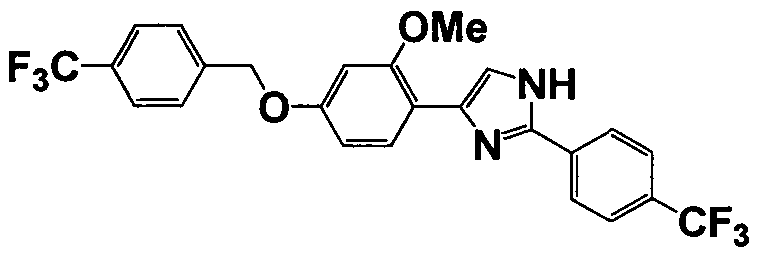
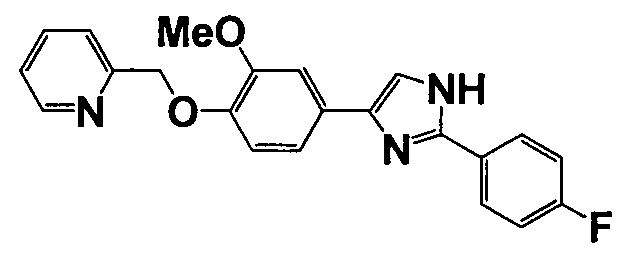
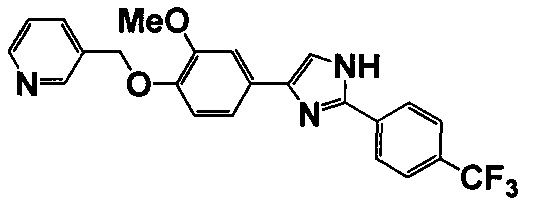
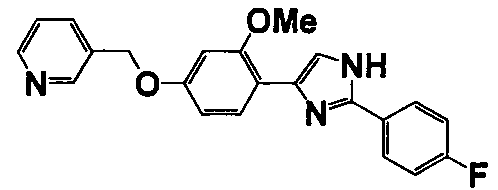
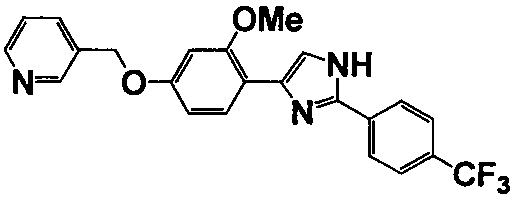
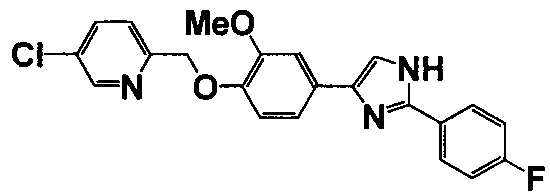
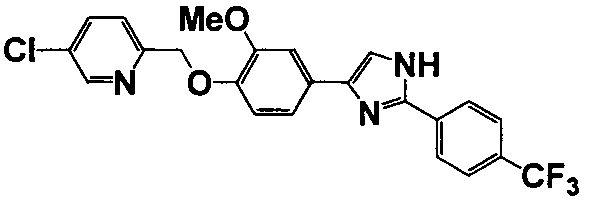
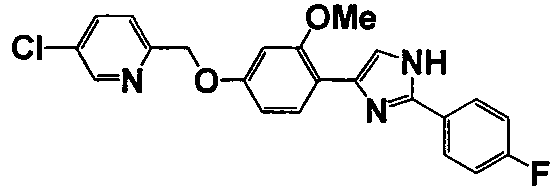
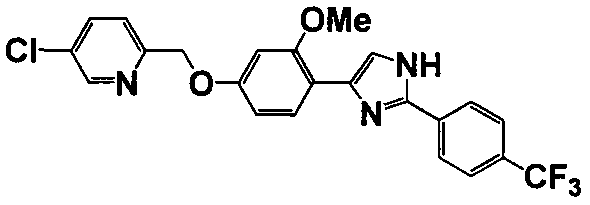
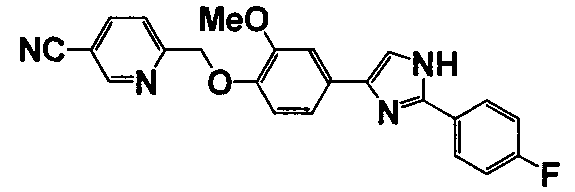
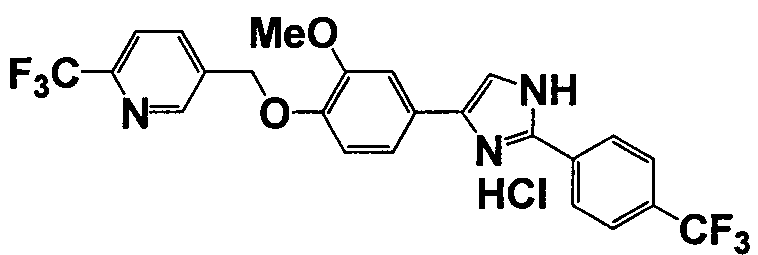
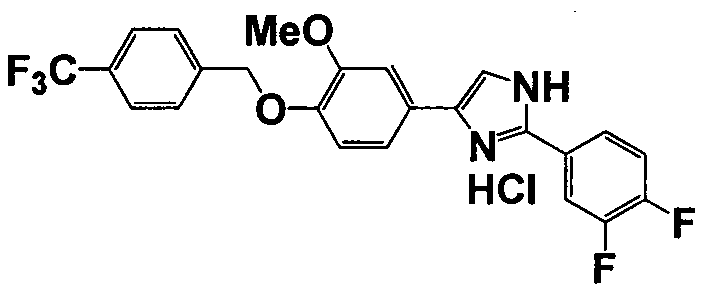
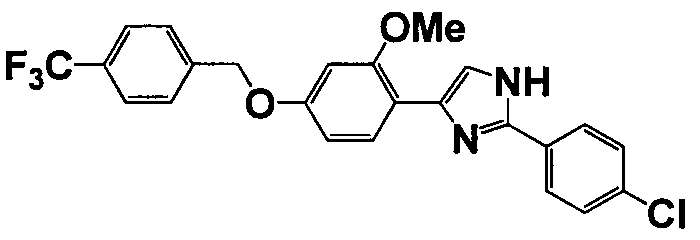
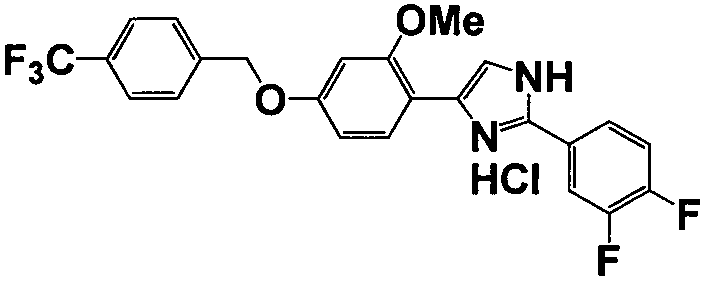
Тестовый пример 1
Тест для подтверждения эффекта активации LPL в клетках скелетных мышц человека и клетках скелетных мышц мыши
Посеянные в планшеты, выращенные и дифференцированные клетки скелетных мышц человека (скелетные мышечные миобласты человека) или клетки скелетных мышц мыши (клетки C2C12) обрабатывали содержащей 0,3% диметилсульфоксида питательной средой, в которой было растворено соединение по настоящему изобретению (концентрация: 10 мкМ или 30 мкМ). Среду удаляли спустя 8 часов после обработки, к клеткам добавляли 10 мМ Tris-HCl буфер (150 мМ NaCl, 10 мкг/мл; содержащий гепарин-натрий) и инкубировали клетки при 37°C в присутствии 5% CO2 в течение 10 минут. Активность LPL в надосадочной жидкости измеряли с использованием набора для анализа активности LPL (производства Roar Biomedical Inc.). Активность LPL оценивали по увеличению интенсивности флуоресценции в течение 10-70 минут после смешивания надосадочной жидкости с субстратом для LPL. Среднее значение увеличения интенсивности флуоресценции клеток, обработанных содержащей 0,3% диметилсульфоксида питательной средой по настоящему изобретению, использовали как среднее значение в контрольной группе. Следует отметить, что соединения примеров 18, 19, 32, 45 и 57 тестировали с использованием клеток скелетных мышц человека, а другие соединения тестировали с использованием клеток скелетных мышц мыши.
Степень увеличения (%) рассчитывали из измеренных значений активности LPL в контрольной группе и экспериментальной группе по следующей формуле:
Степень увеличения активности LPL (%)=[(среднее значение в экспериментальной группе)-(среднее значение в контрольной группе)]/(среднее значение в контрольной группе)×100
Результаты представлены в таблице 7.
В таблице 7 отмечено увеличение активности LPL, вызванное соединением по настоящему изобретению.
Тестовый пример 2
Тест для подтверждения улучшающего липиды действия и эффекта ингибирования прироста массы тела
Использовали крыс SD в возрасте 8 недель (Japan Charles River: средняя масса тела приблизительно 350 г). В экспериментальной группе перорально вводили 5 мл/кг массы тела 5% водной суспензии аравийской камеди, которую приготавливали так, чтобы доза соединения по настоящему изобретению составляла 100 мг/кг массы тела. В контрольной группе перорально вводили 5 мл/кг массы тела 5% водной суспензии аравийской камеди (не содержащей каких-либо соединений по настоящему изобретению). Крыс делили на группы в соответствии с массой тела в возрасте 8 недель так, чтобы в каждой группе было 5 крыс. Тестируемые соединения перорально вводили ежесуточно в определенное время в течение 5 суток или 2 недель, начиная с возраста 9 недель. В течение периода перорального введения регулярно измеряли массу тела и наблюдали эффект ингибирования прироста массы тела. Спустя 4 часа после последнего введения тестируемого соединения отбирали кровь из вены, отделяли плазму от собранной крови и проводили биохимические исследования крови (триглицериды, холестерин-HDL (холестерин липопротеинов высокой плотности)).
Степень ингибирования прироста массы тела (%) рассчитывали из измеренной массы тела крыс в контрольной группе и экспериментальной группе по следующей формуле (результаты представлены в таблице 8):
Степень ингибирования прироста массы тела (%)=[(среднее значение в контрольной группе)-(среднее значение в экспериментальной группе)]/(среднее значение в контрольной группе)×100
Проводили биохимические исследования крови крыс в контрольной группе и экспериментальной группе. Значения степени изменения (%) рассчитывали по следующим формулам из измеренных значений, полученных из биохимических исследований крови (результаты представлены в таблице 8):
Степень снижения содержания триглицеридов (%)=[(среднее значение в контрольной группе)-(среднее значение в экспериментальной группе)]/(среднее значение в контрольной группе)×100
Степень увеличения содержания HDL-холестерина (%)=[(среднее значение в экспериментальной группе)-(среднее значение в контрольной группе)]/(среднее значение в контрольной группе)×100
Эффект на прирост массы тела
Данные в таблице 8 подтверждают, что соединение по настоящему изобретению обладает эффектом ингибирования прироста массы тела у нормальных крыс.
Данные в таблице 9 подтверждают, что соединение по настоящему изобретению обладает эффектом снижения содержания триглицеридов в крови и эффектом увеличения содержания HDL-холестерина (хорошего холестерина). Избыточное увеличение содержания триглицеридов в крови может вызвать гиперлипидемию и артериосклероз. С другой стороны, увеличение содержания HDL-холестерина может ингибировать наступление гиперлипидемии и артериосклероза. Соответственно, эти результаты показывают, что соединение по настоящему изобретению эффективно для профилактики и лечения гиперлипидемии и артериосклероза.
Тестовый пример 3
Тест для подтверждения действия против ожирения у мышей с алиментарным ожирением
Использовали мышей AKR/J. Мышам обеспечивали рацион с высоким содержанием жира (60% ккал жира), при этом развивалась модель диетического ожирения. В экспериментальной группе мышам с ожирением перорально вводили 5 мл/кг массы тела 5% водной суспензии аравийской камеди, которую приготавливали так, чтобы доза соединения по настоящему изобретению составляла 20 мг/кг массы тела. В контрольной группе вводили 5 мл/кг массы тела 5% водной суспензии аравийской камеди, не содержащей каких-либо соединений по настоящему изобретению. Мышей делили на группы в соответствии с массой тела. Тестируемую суспензию вводили ежесуточно в определенное время в течение 4 недель. В течение периода перорального введения измеряли массу тела и подтверждали эффект ингибирования прироста массы тела. Степень снижения массы тела (%) рассчитывали из измеренной массы тела мышей в контрольной группе и экспериментальной группе по следующей формуле (результаты представлены в таблице 10):
Степень снижения массы тела (%)=[(среднее значение в контрольной группе)-(среднее значение в экспериментальной группе)]/(среднее значение в контрольной группе)×100
Эффект у мышей с алиментарным ожирением
В таблице 10 отмечен эффект снижения массы тела, также наблюдаемый на модели мышей, страдающих ожирением. Соответственно, было подтверждено, что соединение по настоящему изобретению эффективно для снижения ожирения.
Пример приготовления 1
Приготовление таблеток
С использованием в качестве активного ингредиента соединения, полученного в примере 18, приготавливали таблетки (10000 таблеток), каждая из которых содержала 300 мг соединения, в соответствии со следующей рецептурой:
соединение, полученное в примере 18 - 3000 г;
лактоза (продукт Japanese Pharmacopeia) - 335 г;
кукурузный крахмал (продукт Japanese Pharmacopeia) - 165 г;
карбоксиметилцеллюлоза кальция (продукт Japanese Pharmacopeia) - 125 г;
метилцеллюлоза (продукт Japanese Pharmacopeia) - 60 г;
стеарат магния (продукт Japanese Pharmacopeia) - 15 г.
В соответствии с вышеуказанной рецептурой соединение, полученное в примере 18, лактозу, кукурузный крахмал и карбоксиметилцеллюлозу кальция надлежащим образом смешивали. Смесь гранулировали с использованием водного раствора метилцеллюлозы, просеивали через сито 24-меш, смешивали со стеаратом магния и прессовали в таблетки, получая тем самым желаемые таблетки.
Пример приготовления 2
Приготовление капсул
С использованием в качестве активного ингредиента соединения, полученного в примере 57, приготавливали твердые желатиновые капсулы (10000 капсул), каждая из которых содержала 200 мг соединения, в соответствии со следующей рецептурой:
соединение, полученное в примере 57 - 2000 г;
кристаллическая целлюлоза (продукт Japanese Pharmacopeia) - 300 г;
кукурузный крахмал (продукт Japanese Pharmacopeia) - 170 г;
тальк (продукт Japanese Pharmacopeia) - 20 г;
стеарат магния (продукт Japanese Pharmacopeia) - 10 г.
В соответствии с вышеуказанной рецептурой каждый из компонентов измельчали в мелкодисперсный порошок, порошки смешивали с получением однородной смеси и загружали в желатиновые капсулы желаемого размера для перорального введения, получая тем самым желаемые капсулы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЕ СУЛЬФОНАМИДА ИЛИ ЕГО СОЛЬ | 2007 |
|
RU2425029C2 |
| СЛОЖНОЭФИРНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2003 |
|
RU2293721C2 |
| N-((ГЕТ)АРИЛМЕТИЛ)-ГЕТЕРОАРИЛ-КАРБОКСАМИДНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ПЛАЗМЕННОГО КАЛЛИКРЕИНА | 2015 |
|
RU2707870C2 |
| N-((ГЕТ)АРИЛМЕТИЛ)-ГЕТЕРОАРИЛ-КАРБОКСАМИДНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ПЛАЗМЕННОГО КАЛЛИКРЕИНА | 2015 |
|
RU2821520C2 |
| ПРОИЗВОДНЫЕ ДИАМИНОВ | 2002 |
|
RU2319699C2 |
| ИНГИБИТОРНЫЕ СОЕДИНЕНИЯ | 2013 |
|
RU2673079C2 |
| ПРОИЗВОДНЫЕ ДИАМИНА | 2002 |
|
RU2314303C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ПИПЕРИДИНА | 2006 |
|
RU2417985C2 |
| КОМПОЗИЦИИ ДЛЯ АКТИВАЦИИ ЛИПОПРОТЕИНЛИПАЗЫ, ВКЛЮЧАЮЩИЕ ПРОИЗВОДНЫЕ БЕНЗОЛА | 2008 |
|
RU2466725C2 |
| ПИКОЛИНАМИДНЫЕ СОЕДИНЕНИЯ С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2687160C2 |
Настоящее изобретение относится к области органической химии, а именно к новым производным фенилимидазола общей формулы (1), где R1 представляет собой атом водорода, фенил-низшую алкильную группу или пиридил-низшую алкильную группу, причем бензольное кольцо и пиридиновое кольцо необязательно замещены 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп; один из R2 и R3 представляет собой атом водорода, а другой представляет собой низшую алкоксигруппу; R4 представляет собой низшую алкильную группу, фурильную группу, тиенильную группу или фенильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, карбоксильной группы, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп; R5 и R6 являются одинаковыми или разными и представляют собой атом водорода или низшую алкильную группу; R7 и R8 являются одинаковыми или разными и представляют собой атом водорода или низшую алкоксигруппу; при условии, что если R1 представляет собой незамещенную фенил-низшую алкильную группу, R2 представляет собой низшую алкоксигруппу, R3 представляет собой атом водорода, R4 представляет собой незамещенную фенильную группу или фенильную группу, содержащую 1 или 2 галогензамещенные низшие алкильные группы, и R5 представляет собой атом водорода, то R6 не является атомом водорода. Также изобретение относится к активатору LPL, средству для профилактики и лечения гиперлипидемии, антиартериосклеротическому средству и средству от ожирения на основе соединения формулы (1). Технический результат: получены новые производные фенилимидазола, полезные для активации LPL. 5 н. и 18 з.п. ф-лы, 10 табл., 7 пр.
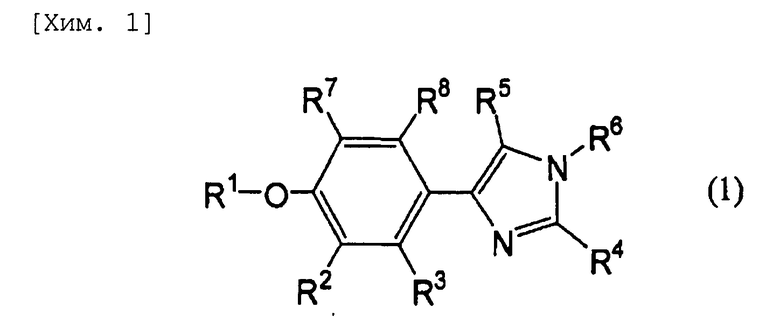
1. Фенилимидазольное соединение, представленное следующей общей формулой (1):

где R1 представляет собой атом водорода, фенил-низшую алкильную группу или пиридил-низшую алкильную группу, причем бензольное кольцо и пиридиновое кольцо необязательно замещены 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп; один из R2 и R3 представляет собой атом водорода, а другой представляет собой низшую алкоксигруппу; R4 представляет собой низшую алкильную группу, фурильную группу, тиенильную группу или фенильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, карбоксильной группы, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп; R5 и R6 являются одинаковыми или разными и представляют собой атом водорода или низшую алкильную группу; R7 и R8 являются одинаковыми или разными и представляют собой атом водорода или низшую алкоксигруппу; при условии, что если R1 представляет собой незамещенную фенил-низшую алкильную группу, R2 представляет собой низшую алкоксигруппу, R3 представляет собой атом водорода, R4 представляет собой незамещенную фенильную группу или фенильную группу, содержащую 1 или 2 галогензамещенные низшие алкильные группы, и R5 представляет собой атом водорода, то R6 не является атомом водорода.
2. Фенилимидазольное соединение по п.1, где в общей формуле (1) R7 и R8 представляют собой атом водорода.
3. Фенилимидазольное соединение по п.1 или 2, где в общей формуле (1) R4 представляет собой тиенильную группу.
4. Фенилимидазольное соединение по п.1 или 2, где в общей формуле (1) R4 представляет собой фурильную группу.
5. Фенилимидазольное соединение по п.1 или 2, где в общей формуле (1) R4 представляет собой фенильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, карбоксильной группы, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп.
6. Фенилимидазольное соединение по п.1 или 2, где в общей формуле (1) R1 представляет собой незамещенную фенил-низшую алкильную группу или фенил-низшую алкильную группу, замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп.
7. Фенилимидазольное соединение по п.6, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из бензила, 4-цианобензила, 3-цианобензила, 2-цианобензила, 4-хлорбензила, 4-трифторметилбензила, 4-хлор-2-фторбензила и 4-бром-2-фторбензила.
8. Фенилимидазольное соединение по п.6, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из бензила, 4-цианобензила, 3-цианобензила, 2-цианобензила, 4-хлорбензила и 4-бром-2-фторбензила.
9. Фенилимидазольное соединение по п.1 или 2, где в общей формуле (1) R4 представляет собой тиенильную группу, фурильную группу или фенильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из низших алкильных групп, низших алкоксигрупп, атомов галогена, низших алкоксикарбонильных групп и галогензамещенных низших алкильных групп.
10. Фенилимидазольное соединение по п.1 или 2, где в общей формуле (1) R4 представляет собой группу, выбранную из группы, состоящей из 2-тиенила, 3-тиенила, 3-фурила, фенила, 4-фторфенила, 3-фторфенила, 3-фтор-4-метилфенила, 3,4-дифторфенила, 4-трифторметилфенила, 3-трифторметилфенила, 2-трифторметилфенила, 4-хлорфенила, 3-хлорфенила, 3,4-дихлорфенила, 3,5-дихлорфенила, 3-хлор-4-фторфенила, 3-метоксифенила, 4-метоксифенила, 3,4-диметоксифенила, 4-метоксикарбонилфенила, 4-карбоксифенила, 4-(1,1-диметилэтил)фенила, 1-метилэтила и 4-метилфенила.
11. Фенилимидазольное соединение по п.10, где в общей формуле (1) R4 представляет собой группу, выбранную из группы, состоящей из 2-тиенила, 3-тиенила, 3-фурила, фенила, 4-фторфенила, 3-фторфенила, 3,4-дифторфенила, 4-трифторметилфенила, 3-трифторметилфенила, 2-трифторметилфенила, 4-хлорфенила, 3-хлорфенила, 3,4-дихлорфенила, 3,5-дихлорфенила, 3-хлор-4-фторфенила, 3-метоксифенила, 4-метоксикарбонилфенила, 4-(1,1-диметилэтил)фенила, 1-метилэтила и 4-метилфенила.
12. Фенилимидазольное соединение по п.1 или 2, где в общей формуле (1) R1 представляет собой пиридил-низшую алкильную группу, необязательно замещенную 1 или 2 заместителями, выбранными из группы, состоящей из атомов галогена, цианогруппы и галогензамещенных низших алкильных групп.
13. Фенилимидазольное соединение по п.12, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из 5-трифторметил-2-пиридилметила, 2-пиридилметила, 3-пиридилметила, 5-хлор-2-пиридилметила и 5-циано-2-пиридилметила.
14. Фенилимидазольное соединение по п.1 или 2, где в общей формуле (1) R1 представляет собой пиридил-низшую алкильную группу, необязательно замещенную галогензамещенными низшими алкильными группами.
15. Фенилимидазольное соединение по п.14, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из 2-пиридилметила и 6-трифторметил-3-пиридилметила.
16. Фенилимидазольное соединение по п.1 или 2, где в общей формуле (1) R1 представляет собой группу, выбранную из группы, состоящей из бензила, 4-хлорбензила и 4-бром-2-фторбензила, и R4 представляет собой группу, выбранную из группы, состоящей из 4-трифторметилфенила, 4-фторфенила, 3,4-дифторфенила, 4-хлорфенила, 3,4-дихлорфенила и 4-метилфенила.
17. Фенилимидазольное соединение по п.1, выбранное из следующих соединений:
4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-(4-бензилокси-3-метоксифенил)-2-(3-тиенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(4-фторфенил)-1H-имидазол;
4-(4-бензилокси-3-метоксифенил)-2-(4-фторфенил)-5-метил-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-3-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-хлорфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-3-метоксифенил]-2-(2-тиенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(3-тиенил)-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-[3-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-метилфенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дихлорфенил)-1H-имидазол.
18. Фенилимидазольное соединение по п.1, выбранное из следующих соединений:
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-[4-(трифторметил)фенил]-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(4-фторфенил)-1H-имидазол;
4-(4-бензилокси-3-метоксифенил)-2-(4-фторфенил)-5-метил-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-хлорфенил)-1H-имидазол;
4-[4-(4-бром-2-фторбензилокси)-2-метоксифенил]-2-(4-метилфенил)-1H-имидазол;
4-[4-(4-хлорбензилокси)-2-метоксифенил]-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дифторфенил)-1H-имидазол;
4-(4-бензилокси-2-метоксифенил)-2-(3,4-дихлорфенил)-1H-имидазол;
4-[4-(4-цианобензилокси)-2-метоксифенил]-2-(4-фторфенил)-1H-имидазол.
19. Активатор LPL, содержащий в качестве активного ингредиента соединение по любому из пп.1-18.
20. Средство для профилактики и лечения гиперлипидемии, содержащее в качестве активного ингредиента соединение по любому из пп.1-18.
21. Антиартериосклеротическое средство, содержащее в качестве активного ингредиента соединение по любому из пп.1-18.
22. Средство от ожирения, содержащее в качестве активного ингредиента соединение по любому из пп.1-18.
23. Соединение по п.1 или 2 для использования при активации LPL.
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| US 4665023 A1, 12.05.1987 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИМИДАЗОЛА | 0 |
|
SU350792A1 |
| УСТРОЙСТВО ДЛЯ АВТОМАТИЧЕСКОЙ ОТКАЧКИ КОНДЕНСАТА ИЗ ДРИППОВ ИЛИ СЕПАРАТОРОВ | 0 |
|
SU217319A1 |
| Способ получения производных имидазола | 1973 |
|
SU489330A3 |
Авторы
Даты
2013-11-10—Публикация
2010-02-03—Подача