Область техники, к которой относится изобретение
Настоящее изобретение относится к новым соединениям, которые ингибируют активированный фактор Х свертывания крови (далее сокращенно называемый «FXa»), проявляя сильный противосвертывающий эффект, и могут быть введены перорально, и к антикоагулянтам или средствам для профилактики и/или лечения тромбоза или эмболии, которые содержат такое новое соединение в качестве активного компонента.
Предпосылки создания изобретения
При нестабильной стенокардии, инфаркте головного мозга, эмболии головного мозга, инфаркте миокарда, инфаркте легких, эмболии легких, болезни Бюргера, тромбозе глубоких вен, синдроме диссеминированного внутрисосудистого коагулирования, тромбообразовании после замены клапана, реокклюзии после ангиопластики и образовании тромбов при экстракорпоральном кровообращении основным фактором является состояние гиперкоагуляции. Поэтому существует потребность в создании очень хороших антикоагулянтов, обладающих хорошей дозозависимостью, большой продолжительностью действия, низким риском кровотечения и малыми побочными эффектами и быстрым достижением достаточной эффективности даже при пероральном введении (Thrombosis Research, Vol. 68, pp. 507-512, 1992).
На основе исследования антикоагулянтов с различным механизмом действия возникло предположение, что ингибиторы FXa являются многообещающими антикоагулянтами. Система свертывания крови содержит ряд реакций, приводящих к образованию большого количества тромбина вследствие процесса амплификации многостадийными ферментативными реакциями с образованием нерастворимого фибрина. В эндогенной системе активированный фактор IX активируется в фактор Х на фосфолипидной мембране в присутствии активированного фактора VIII и ионов кальция после многостадийных реакций после активации фактора контакта. В экзогенной системе активированный фактор VII активирует фактор Х в присутствии тканевого фактора. В частности, активация фактора Х в FXa в свертывающей системе является решающей реакцией при образовании тромбина. Активированный фактор Х (FXa) ограниченно разлагает протромбин с образованием тромбина в обеих системах. Поскольку выработанный тромбин активирует факторы свертывания в верхнем течении, образование тромбина еще более усиливается. Как описано выше, поскольку свертывающая система в верхнем течении FXa разделяется на эндогенную систему и экзогенную систему, продуцирование FXa не может быть в достаточной мере ингибировано ингибирующими ферментами в свертывающей системе в верхнем течении FXa, что приводит к вырабатыванию тромбина. Так как свертывающая система содержит самоамплификационные реакции, ингибирование свертывающей системы может быть более эффективно обеспечено ингибированием FXa в верхнем течении тромбина, чем ингибированием тромбина (Thrombosis Research, Vol. 15, pp. 617-629, 1979).
Другим превосходным качеством ингибиторов FXa является большая разница между эффективной дозой в модели тромбоза и дозой, удлиняющей время кровотечения в экспериментальной геморрагической модели. Исходя из результатов указанного эксперимента, ингибиторы FXa считают антикоагулянтами с низким риском кровотечения.
Уже были сообщения о различных соединениях, служащих в качестве ингибиторов FXa. Известно, что антитромбин III и антитромбин III-зависимые пентасахариды по существу не могут ингибировать протромбиназные комплексы, которые играют важную роль в тромбообразовании в живом организме (Thrombosis Research, Vol. 68, pp. 507-512, 1992; Journal of Clinical Investigation Vol. 71, pp. 1383-1389, 1983; Mebio, Vol. 14, the August number, pp. 92-97). Кроме того, они не эффективны при пероральном введении. Клещевой противосвертывающий пептид (ТАР) (Science, Vol. 248, pp. 593-596, 1990) и антистазин (AST) (Journal of Biological Chemisry, Vol. 263, pp. 10162-10167, 1988), выделенные из клещей или пиявок, которые являются кровососущими, также ингибируют FXa и оказывают антитромботический эффект против венозного тромбоза и артериального тромбоза. Однако указанные соединения являются высокомолекулярными пептидами и непригодны для перорального введения. Как описано выше, уже была проведена работа по созданию антитромбин III-независимых низкомолекулярных ингибиторов FXa, непосредственно ингибирующих факторы свертывания.
Таким образом, задачей настоящего изобретения является создание нового соединения, обладающего сильным FXa-ингибирующим эффектом и оказывающего быстрый, достаточный и устойчивый антитромботический эффект при пероральном введении.
Описание изобретения
Авторы настоящего изобретения исследовали синтез и фармакологические эффекты новых ингибиторов FXa. В результате были найдены производные диамина, их соли и их сольваты и N-оксиды, которые проявляют сильный FXa-ингибирующий эффект и противосвертывающий эффект. Было также найдено, что указанные соединения быстро, устойчиво и сильно ингибируют FXa и оказывают сильный противосвертывающий и противотромботический эффекты при пероральном введении и, следовательно, полезны как профилактические и лечебные лекарственные средства для различных заболеваний, обусловленных тромбоэмболией, что и привело к созданию настоящего изобретения.
В соответствии с настоящим изобретением предлагается соединение, представленное общей формулой (1):
Q1-Q2-Т0-N(R1)-Q3-N(R2)-Т1-Q4 (1)
где
R1 и R2 независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу;
Q1 представляет насыщенную или ненасыщенную 5- или 6-членную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q2 представляет одинарную связь, насыщенную или ненасыщенную 5- или 6-членную двухвалентную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную двухвалентную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q3 представляет следующую группу:
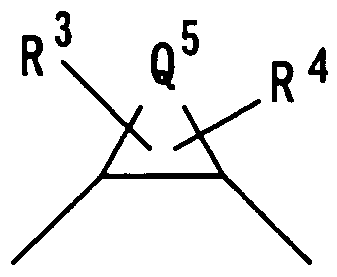
в которой Q5 означает алкиленовую группу, имеющую 1-8 углеродных атомов, алкениленовую группу, имеющую 2-8 углеродных атомов, или группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, ―NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-, и R3 и R4 являются заместителями у углеродного атома(ов), атома(ов) азота или атомов серы кольца, содержащего Q5, и независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу, алкенильную группу, алкинильную группу, атом галогена, галогеналкильную группу, цианогруппу, цианоалкильную группу, аминогруппу, аминоалкильную группу, N-алкиламиноалкильную группу, N,N-диалкиламиноалкильную группу, ацильную группу, ацилалкильную группу, ациламиногруппу, которая может быть замещенной, алкоксииминогруппу, гидроксииминогруппу, ациламиноалкильную группу, алкоксигруппу, алкоксиалкильную группу, гидроксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, алкоксикарбонильную группу, алкоксикарбонилалкильную группу, алкоксикарбонилалкиламиногруппу, карбоксиалкиламиногруппу, алкоксикарбониламиногруппу, алкоксикарбониламиноалкильную группу, карбамоильную группу, N-алкилкарбамоильную группу, которая может содержать заместитель в алкильной группе, N,N-диалкилкарбамоильную группу, которая может иметь заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильную группу, N-алкенилкарбамоилалкильную группу, N-алкенил-N-алкилкарбамоильную группу, N-алкенил-N-алкилкарбамоилалкильную группу, N-алкоксикарбамоильную группу, N-алкил-N-алкоксикарбамоильную группу, N-алкоксикарбамоилалкильную группу, N-алкил-N-алкоксикарбамоилалкильную группу, карбазоильную группу, которая может быть замещенной 1-3 алкильными группами, алкилсульфонильную группу, алкилсульфонилалкильную группу, 3-6-членную гетероциклическую карбонильную группу, которая может быть замещенной, карбамоилалкильную группу, N-алкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), карбамоилоксиалкильную группу, N-алкилкарбамоилоксиалкильную группу, N,N-диалкилкарбамоилоксиалкильную группу, 3-6-членную гетероциклическую карбонилалкильную группу, которая может быть замещенной, 3-6-членную гетероциклическую карбонилоксиалкильную группу, которая может быть замещенной, арильную группу, аралкильную группу, гетероарильную группу, гетероарилалкильную группу, алкилсульфониламиногруппу, арилсульфониламиногруппу, алкилсульфониламиноалкильную группу, арилсульфониламиноалкильную группу, алкилсульфониламинокарбонильную группу, арилсульфониламинокарбонильную группу, алкилсульфониламинокарбонилалкильную группу, арилсульфониламинокарбонилалкильную группу, оксогруппу, карбамоилоксигруппу, аралкилоксигруппу, карбоксиалкилоксигруппу, ацилоксигруппу, ацилоксиалкильную группу, арилсульфонильную группу, алкоксикарбонилалкилсульфонильную группу, карбоксиалкилсульфонильную группу, алкоксикарбонилацильную группу, алкоксиалкилоксикарбонильную группу, гидроксиацильную группу, алкоксиацильную группу, галогенацильную группу, карбоксиацильную группу, аминоацильную группу, ацилоксиацильную группу, ацилоксиалкилсульфонильную группу, гидроксиалкилсульфонильную группу, алкоксиалкилсульфонильную группу, 3-6-членную гетероциклическую сульфонильную группу, которая может быть замещенной, N-алкиламиноацильную группу, N,N-диалкиламиноацильную группу, N,N-диалкилкарбамоилацильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкилсульфонильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), алкилсульфонилацильную группу, аминокарботиоильную группу, N-алкиламинокарботиоильную группу, N,N-диалкиламинокарботиоильную группу или алкоксиалкил(тиокарбонильную) группу, или R3 и R4 вместе друг с другом означают алкиленовую группу, имеющую 1-5 углеродных атомов, алкениленовую группу, имеющую 2-5 углеродных атомов, алкилендиоксигруппу, имеющую 1-5 углеродных атомов, или карбонилдиоксигруппу;
Q4 представляет арильную группу, которая может быть замещенной, арилалкенильную группу, которая может быть замещенной, арилалкинильную группу, которая может быть замещенной, гетероарильную группу, которая может быть замещенной, гетероарилалкенильную группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Т0 представляет карбонильную или тиокарбонильную группу; и
Т1 представляет карбонильную группу, сульфонильную группу, группу -С(=О)-С(=О)-N(R')-, группу -С(=S)-С(=О)-N(R')-, группу -С(=О)-С(=S)-N(R')-, группу -С(=S)-С(=S)-N(R')-, где R' означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-А1-N(R")-, где А1 означает алкиленовую группу, имеющую 1-5 углеродных атомов, которая может быть замещенной, и R" означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-NH-, группу -С(=S)-NH-, группу -С(=О)-NH-NH-, группу -С(=О)-А2-С(=О)-, где А2 означает одинарную связь или алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-А3-С(=О)-NH-, где А3 означает алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-С(=NORа)-N(Rb)-, группу -С(=S)-С(=NORа)-N(Rb)-, где Rа означает атом водорода, алкильную группу или алканоильную группу и Rb означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-N=N-, группу -С(=S)-N=N-, группу -С(=NORс)-С(=О)-N(Rd)-, где Rс означает атом водорода, алкильную группу, алканоильную группу, арильную группу или аралкильную группу и Rd означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=N-N(Rе)(Rf)-С(=О)-N(Rg)-, где Rе и Rf независимо друг от друга означают атом водорода, алкильную группу, алканоильную группу или алкил(тиокарбонильную) группу и Rg означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, или тиокарбонильную группу; его соль, сольват или N-оксид.
В соответствии с настоящим изобретением предлагаются также лекарственное средство, ингибитор активированного фактора Х свертывания крови, антикоагулянт, средство для профилактики и/или лечения тромбоза или эмболии и средство для профилактики и/или лечения инфаркта головного мозга, эмболии головного мозга, инфаркта миокарда, стенокардии, инфаркта легких, эмболии легких, болезни Бюргера, тромбоза глубоких вен, синдрома диссеминированного внутрисосудистого коагулирования, тромбообразования после замены клапана или сустава, тромбообразования и реокклюзии после ангиопластики, синдрома системной воспалительной реакции (SIRS), синдрома заболевания многих органов (MODS), образования тромбов при экстракорпоральном кровообращении или свертывания крови при ее сборе, каждое из которых содержит соединение, представленное общей формулой (1), его соль, сольват или N-оксид.
Кроме того, предлагается промежуточное соединение, полезное для получения соединения, представленного общей формулой (1).
Далее, в соответствии с настоящим изобретением предлагается применение соединения, представленного общей формулой (1), его соли, сольвата или N-оксида для изготовления лекарственного средства.
И еще в соответствии с настоящим изобретением предлагается способ лечения тромбоза или эмболии, который включает введение эффективного количества соединения, представленного общей формулой (1), его соли, сольвата или N-оксида.
Наилучший способ осуществления изобретения
Далее описаны заместители в производных диамина по настоящему изобретению, представленных общей формулой (1).
<О группе Q4>
Группа Q4 означает арильную группу, которая может быть замещенной, арилалкенильную группу, которая может быть замещенной, арилалкинильную группу, которая может быть замещенной, гетероарильную группу, которая может быть замещенной, гетероарилалкенильную группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной.
В группе Q4 арильная группа может включать арильные группы, имеющие 6-14 углеродных атомов, например, фенильную, нафтильную, антрильную и фенантрильную группы. Арилалкенильная группа означает группу, образованную арильной группой, имеющей 6-14 углеродных атомов, и алкениленовой группой, имеющей 2-6 углеродных атомов, и ее примеры могут включать стирильную группу. Арилалкинильная группа означает группу, образованную арильной группой, имеющей 6-14 углеродных атомов, и алкиниленовой группой, имеющей 2-6 углеродных атомов, и ее примеры могут включать фенилэтинильную группу.
Гетероарильная группа означает одновалентную ароматическую группу, имеющую по крайней мере один гетероатом, выбранный из атомов кислорода, серы и азота, и ее примеры могут включать 5- или 6-членные гетероарильные группы, например, пиридильную, пиридазинильную, пиразинильную, фурильную, тиенильную, пирролильную, тиазолильную, оксазолильную, пиримидинильную и тетразолильную группы. Гетероарилалкенильная группа означает группу, образованную описанной выше гетероарильной группой и алкениленовой группой, имеющей 2-6 углеродных атомов, и ее примеры могут включать тиенилэтенильную и пиридилэтенильную группы.
Насыщенная или ненасыщенная бициклическая или трициклическая конденсированная углеводородная группа означает одновалентную группу, образованную от насыщенного или ненасыщенного бициклического или трициклического конденсированного углеводорода. Насыщенный или ненасыщенный бициклический или трициклический конденсированный углеводород означает бициклический или трициклический конденсированный углеводород, образованный конденсацией 2 или 3 насыщенных или ненасыщенных 5- или 6-членных циклических углеводородов, одинаковых или отличающихся друг от друга. В данном случае примеры насыщенных или ненасыщенных 5- или 6-членных циклических углеводородов могут включать циклопентан, циклопентен, циклогексан, циклогексен, циклогексадиен и бензол. Конкретные примеры насыщенной или ненасыщенной бициклической или трициклической конденсированной углеводородной группы могут включать инденильную, инданильную, тетрагидронафтильную и нафтильную группы. Между прочим, положение насыщенной или ненасыщенной бициклической или трициклической конденсированной углеводородной группы, присоединенной к Т1 в общей формуле (1), особо не ограничивается.
Насыщенная или ненасыщенная бициклическая или трициклическая конденсированная гетероциклическая группа означает одновалентную группу, образованную от насыщенного или ненасыщенного бициклического или трициклического конденсированного гетероциклического кольца. Насыщенное или ненасыщенное бициклическое или трициклическое конденсированное гетероциклическое кольцо означает следующее гетероциклическое кольцо (1), (2) или (3):
(1): бициклическое или трициклическое конденсированное гетероциклическое кольцо, образованное конденсацией 2 или 3 насыщенных или ненасыщенных 5-7-членных гетероциклических колец, одинаковых или отличающихся друг от друга;
(2): бициклическое или трициклическое конденсированное гетероциклическое кольцо, образованное конденсацией насыщенного или ненасыщенного 5-7-членного гетероциклического кольца с 1 или 2 насыщенными или ненасыщенными 5- или 6-членными циклическими углеводородами; или
(3): трициклическое конденсированное гетероциклическое кольцо, образованное конденсацией 2 насыщенных или ненасыщенных 5-7-членных гетероциклических колец с насыщенным или ненасыщенным 5- или 6-членным циклическим углеводородом.
Положение насыщенной или ненасыщенной бициклической или трициклической конденсированной гетероциклической группы, присоединенной к Т1 в общей формуле (1), особо не ограничивается.
Насыщенное или ненасыщенное 5-7-членное гетероциклическое кольцо означает гетероциклическое кольцо, содержащее по крайней мере один гетероатом, выбранный из атомов кислорода, серы и азота, и его конкретные примеры могут включать фуран, пиррол, тиофен, пиразол, имидазол, оксазол, оксазолидин, тиазол, тиадиазол, фуразан, пиран, пиридин, пиримидин, пиридазин, пирролидин, пиперазин, пиперидин, оксазин, оксадиазин, морфолин, тиазин, тиадиазин, тиоморфолин, тетразол, триазол, триазин, тиадиазин, оксадиазин, азепин, диазепин, триазепин, тиазепин и оксазепин. Насыщенный или ненасыщенный 5- или 6-членный циклический углеводород означает такой же насыщенный или ненасыщенный 5- или 6-членный циклический углеводород, как указанный при описании насыщенной или ненасыщенной бициклической или трициклической конденсированной углеводородной группы. Конкретные примеры насыщенной или ненасыщенной бициклической или трициклической конденсированной гетероциклической группы могут включать бензофурильную, изобензофурильную, бензотиенильную,
индолильную, индолинильную, изоиндолильную, изоиндолинильную,
индазолильную, хинолильную, дигидрохинолильную,
4-оксодигидрохинолильную (дигидрохинолин-4-он),
тетрагидрохинолильную, изохинолильную, тетрагидроизохинолильную,
хроменильную, хроманильную, изохроманильную,
4Н-4-оксобензопиранильную,
3,4-дигидро-4Н-4-оксобензопиранильную,
4Н-хинолизинильную, хиназолинильную, дигидрохиназолинильную,
тетрагидрохиназолинильную, хиноксалинильную,
тетрагидрохиноксалинильную, циннолинильную,
тетрагидроциннолинильную, индолизинильную,
тетрагидроиндолизинильную, бензотиазолильную,
тетрагидробензотиазолильную, бензоксазолильную,
бензоизотиазолильную, бензоизоксазолильную, бензимидазолильную,
нафтиридинильную, тетрагидронафтиридинильную, тиенопиридильную,
тетрагидротиенопиридильную, тиазолопиридильную,
тетрагидротиазолопиридильную, тиазолопиридазинильную,
тетрагидротиазолопиридазинильную, пирролопиридильную,
дигидропирролопиридильную, тетрагидропирролопиридильную,
пирролопиримидинильную, дигидропирролопиримидинильную,
пиридохиназолинильную, дигидропиридохиназолильную,
пиридопиримидинильную, тетрагидропиридопиримидинильную,
пиранотиазолильную, дигидропиранотиазолильную, фуропиридильную,
тетрагидрофуропиридильную, оксазолопиридильную,
тетрагидрооксазолопиридильную, оксазолопиридазинильную,
тетрагидрооксазолопиридазинильную, пирролотиазолильную,
дигидропирролотиазолильную, пирролооксазолильную,
дигидропирролооксазолильную, тиенопирролильную,
тиазолопиримидинильную, 4-оксотетрагидроциннолинильную,
1,2,4-бензотиадиазинильную,
1,1-диокси-2Н-1,2,4-бензотиадиазинильную,
1,2,4-бензоксадиазинильную, циклопентапиранильную,
тиенофуранильную, фуропиранильную, пиридоксазинильную,
пиразолоксазолильную, имидазотиазолильную, имидазопиридильную,
тетрагидроимидазопиридильную, пиразинопиридазинильную,
бензоизохинолильную, фуроциннолильную,
пиразолотиазолопиридазинильную,
тетрагидропиразолотиазолопиридазинильную,
гексагидротиазолопиридазинопиридазинильную,
имидазотриазинильную, оксазолопиридильную, бензоксепинильную,
бензоазепинильную, тетрагидробензоазепинильную,
бензодиазепинильную, бензотриазепинильную, тиеноазепинильную,
тетрагидротиеноазепинильную, тиенодиазепинильную,
тиенотриазепинильную, тиазолоазепинильную,
тетрагидротиазолоазепинильную,
4,5,6,7-тетрагидро-5,6-тетраметилентиазолопиридазинильную и
5,6-триметилен-4,5,6,7-тетрагидротиазолопиридазинильную группы.
Нет особого ограничения на форму конденсирования конденсированной гетероциклической группы. Например, нафтиридинильная группа может быть любой из 1,5-, 1,6-, 1,7-, 1,8-, 2,6- и 2,7-нафтиридинильных групп, тиенопиридильная группа может быть любой из тиено[2,3-b]пиридильной, тиено[2,3-c]пиридильной, тиено[3,2-b]пиридильной, тиено[3,2-c]пиридильной, тиено[3,4-b]пиридильной и тиено[3,4-с]пиридильной групп, тиенопирролильная группа может быть любой из тиено[2,3-b]пирролильной и тиено[3,2-b]пирролильной групп, тиазолопиридильная группа может быть любой из тиазоло[4,5-b]пиридильной, тиазоло[4,5-c]пиридильной, тиазоло[5,4-b]пиридильной, тиазоло[5,4-c]пиридильной, тиазоло[3,4-а]пиридильной и тиазоло[3,2-а]пиридильной групп, тиазолопиридазинильная группа может быть любой из тиазоло[4,5-с]пиридазинильной, тиазоло[4,5-d]пиридазинильной, тиазоло[5,4-с]пиридазинильной и тиазоло[3,2-b]пиридазинильной групп, пирролопиридильная группа может быть любой из пирроло[2,3-b]пиридильной, пирроло[2,3-c]пиридильной, пирроло[3,2-b]пиридильной, пирроло[3,2-c]пиридильной, пирроло[3,4-b]пиридильной и пирроло[3,4-с]пиридильной групп, пиридопиримидинильная группа может быть любой из пиридо[2,3-d]пиримидинильной, пиридо[3,2-d]пиримидинильной, пиридо[3,4-d]пиримидинильной, пиридо[4,3-d]пиримидинильной, пиридо[1,2-с]пиримидинильной и пиридо[1,2-а]пиримидинильной групп, пиранотиазолильная группа может быть любой из пирано[2,3-d]тиазолильной, пирано[4,3-d]тиазолильной, пирано[3,4-d]тиазолильной и пирано[3,2-d]тиазолильной групп, фуропиридильная группа может быть любой из фуро[2,3-b]пиридильной, фуро[2,3-c]пиридильной, фуро[3,2-b]пиридильной, фуро[3,2-c]пиридильной, фуро[3,4-b]пиридильной и фуро[3,4-с]пиридильной групп, оксазолопиридильная группа может быть любой из оксазоло[4,5-b]пиридильной, оксазоло[4,5-c]пиридильной, оксазоло[5,4-b]пиридильной, оксазоло[5,4-c]пиридильной, оксазоло[3,4-а]пиридильной и оксазоло[3,2-а]пиридильной групп, оксазолопиридазинильная группа может быть любой из оксазоло[4,5-с]пиридазинильной, оксазоло[4,5-d]пиридазинильной, оксазоло[5,4-с]пиридазинильной и оксазоло[3,4-b]пиридазинильной групп, пирролотиазолильная группа может быть любой из пирроло[2,1-b]тиазолильной, пирроло[1,2-c]тиазолильной, пирроло[2,3-d]тиазолильной, пирроло[3,2-d]тиазолильной и пирроло[3,4-d]тиазолильной групп, пирролооксазолильная группа может быть любой из пирроло[2,1-b]оксазолильной, пирроло[1,2-c]оксазолильной, пирроло[2,3-d]оксазолильной, пирроло[3,2-d]оксазолильной и пирроло[3,4-d]оксазолильной групп, бензоазепинильная группа может быть любой из 1Н-1-бензоазепинильной, 1Н-2-бензоазепинильной и 1Н-3-бензоазепинильной групп или может представлять собой бензоазепинильную группу типа дигидрооксопроизводного, такую как 4,5-дигидро-1-оксо-1Н-2-бензоазепинильная группа, бензодиазепинильная группа может быть любой из 1Н-1,3-бензодиазепинильной, 1Н-1,4-бензодиазепинильной и 1Н-1,5-бензодиазепинильной групп или может представлять собой бензодиазепинильную группу типа дигидрооксопроизводного, такую как 4,5-дигидро-4-оксо-1Н-1,3-бензодиазепинильная группа, бензотриазепинильная группа может быть любой из 1Н-1,3,4-бензотриазепинильной и 1Н-1,3,5-бензотриазепинильной групп или может представлять собой бензотриазепинильную группу типа дигидрооксопроизводного, такую как 4,5-дигидро-5-оксо-1Н-1,3,4-бензотриазепинильная группа, и тиеноазепинильная группа может быть любой из тиено[2,3-b]азепинильной, тиено[2,3-с]азепинильной, тиено[2,3-d]азепинильной, тиено[3,2-с]азепинильной и тиено[3,2-b]азепинильной групп или может представлять собой тиеноазепинильную группу типа дигидрооксопроизводного, такую как 5,6,7,8-тетрагидро-4-оксо-4Н-тиено[3,2-c]азепинильная группа. Тиенодиазепинильная и тиенотриазепинильная группы также могут быть любой формы конденсации или могут представлять собой указанные группы типа дигидрооксопроизводного. Бензотиазепинильная группа может быть любой из 1Н-1-бензотиазепинильной, 1Н-2-бензотиазепинильной и 1Н-3-бензотиазепинильной групп или может представлять собой бензотиазепинильную группу типа дигидрооксопроизводного, такую как 4,5-дигидро-1-оксо-1Н-2-бензотиазепинильная группа, и бензоксазепинильная группа может быть любой из 1Н-1-бензоксазепинильной, 1Н-2-бензоксазепинильной и 1Н-3-бензоксазепинильной групп или может представлять собой бензоксазепинильную группу типа дигидрооксопроизводного, такую как 4,5-дигидро-1-оксо-1Н-2-бензоксазепинильная группа. Могут быть допустимы и иные, чем указанные, формы конденсации.
Каждая из описанных выше арильных групп, гетероарильных групп, арилалкенильных групп, гетероарилалкенильных групп, насыщенных или ненасыщенных бициклических или трициклических конденсированных углеводородных групп и насыщенных или ненасыщенных бициклических или трициклических конденсированных гетероциклических групп может иметь 1-3 заместителя. Примеры заместителей могут включать гидроксильную группу, атомы галогена, такие как атом фтора, атом хлора, атом брома и атом йода, галогеналкильные группы с 1-6 углеродными атомами, замещенные 1-3 атомами галогена, аминогруппу, цианогруппу, аминоалкильные группы, нитрогруппу, гидроксиалкильные группы (например, гидроксиметильную группу, 2-гидроксиэтильную группу и т.д.), алкоксиалкильные группы (например, метоксиметильную группу, 2-метоксиэтильную группу и т.д.), карбоксильную группу, карбоксиалкильные группы (например, карбоксиметильную группу, 2-карбоксиэтильную группу и т.д.), алкоксикарбонилалкильные группы (например, метоксикарбонилметильную группу, этоксикарбонилметильную группу и т.д.), ацильные группы (например, алканоильные группы, такие как формильная группа, ацетильная группа и пропионильная группа), амидиногруппу, гидроксиамидиногруппу, неразветвленные, разветвленные или циклические алкильные группы, имеющие 1-6 углеродных атомов (например, метильную группу, этильную группу и т.д.), неразветвленные, разветвленные или циклические алкоксигруппы, имеющие 1-6 углеродных атомов (например, метоксигруппу, этоксигруппу и т.д.), амидиногруппы, замещенные алкоксикарбонильной группой, имеющей 2-7 углеродных атомов (например, метоксикарбониламидиногруппу, этоксикарбониламидиногруппу и т.д.), неразветвленные, разветвленные или циклические алкенильные группы, имеющие 2-6 углеродных атомов (например, винильную группу, аллильную группу и т.д.), неразветвленные или разветвленные алкинильные группы, имеющие 2-6 углеродных атомов (например, этинильную группу, пропинильную группу и т.д.), неразветвленные, разветвленные или циклические алкоксикарбонильные группы, имеющие 2-6 углеродных атомов (например, метоксикарбонильную группу, этоксикарбонильную группу и т.д.), карбамоильную группу, моно- или диалкилкарбамоильные группы, замещенные неразветвленными, разветвленными или циклическими алкильными группами, имеющими 1-6 углеродных атомов, у атома(ов) азота (например, метилкарбамоильную группу, этилкарбамоильную группу, диметилкарбамоильную группу, этилметилкарбамоильную группу и т.д.), моно- или диалкиламиногруппы, замещенные 1 или 2 неразветвленными, разветвленными или циклическими алкильными группами, имеющими 1-6 углеродных атомов (например, этиламино-, диметиламино- и метилэтиламиногруппы), и 5- или 6-членные азотсодержащие гетероциклические группы (например, пирролидиногруппу, пиперидиногруппу, пиперазиногруппу, морфолиногруппу и т.д.).
В качестве группы Q4 из описанных выше групп следующие 12 групп (а)-(l) являются предпочтительными. А именно:
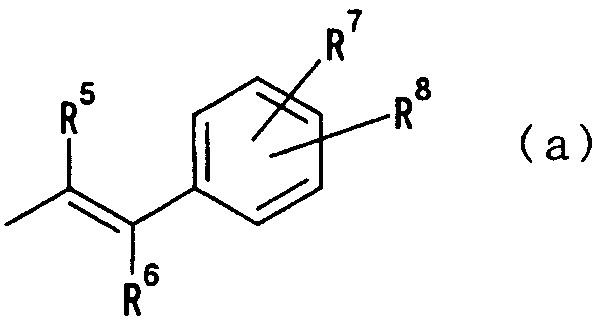
где R5 и R6 независимо друг от друга представляют атом водорода, цианогруппу, атом галогена, алкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, алкоксикарбонильную группу, алкоксикарбонилалкильную группу или фенильную группу, которая может быть замещена цианогруппой, гидроксильной группой, атомом галогена, алкильной группой или алкоксигруппой, и R7 и R8 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу;
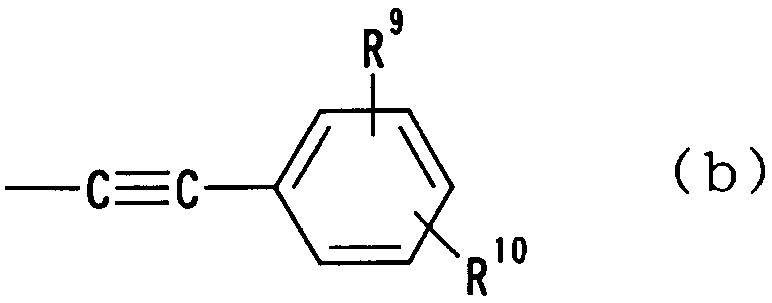
где R9 и R10 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу;
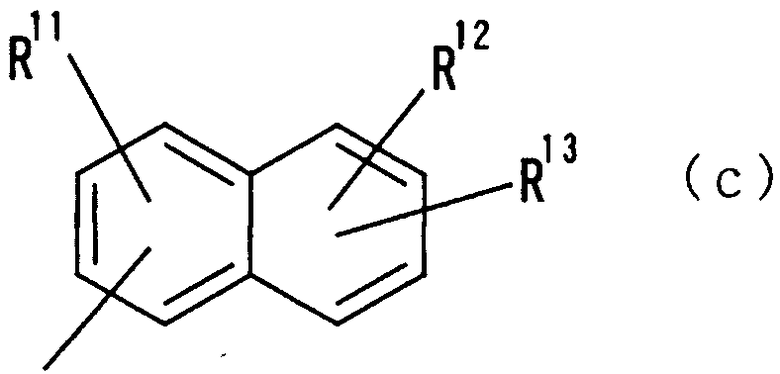
где R11, R12 и R13 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу;
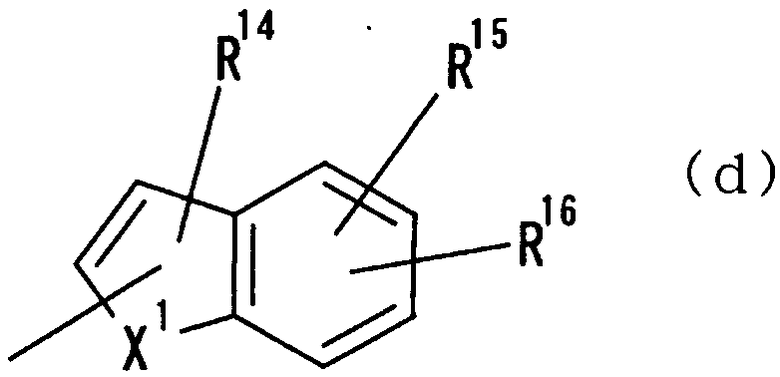
где Х1 представляет СН2, СН, NH, NOH, N, O или S и R14, R15 и R16 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу;
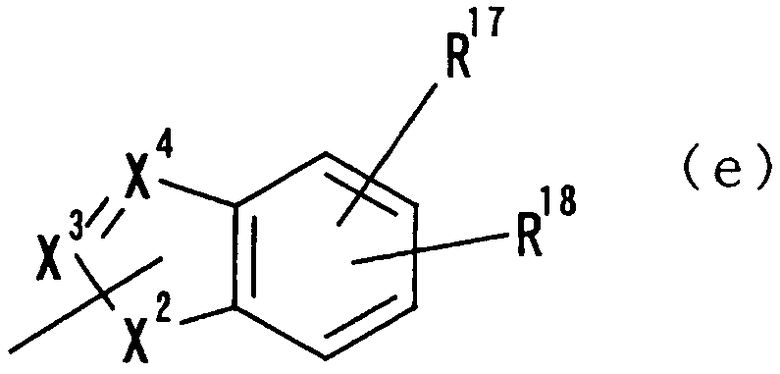
где Х2 представляет NH, N, O или S, Х3 представляет N, С или СН, Х4 представляет N, С или СН и R17 и R18 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу, исключая случаи, когда Х3 и Х4 являются комбинациями С и СН и оба представляют С или СН;
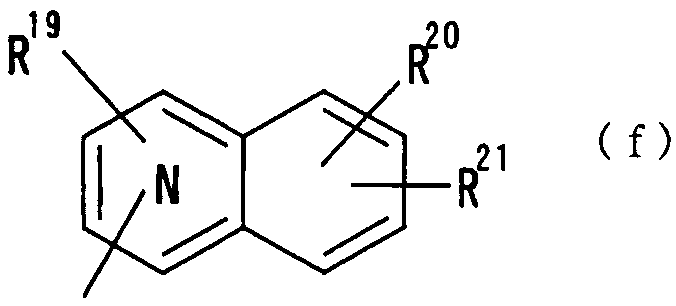
где N показывает, что 1 или 2 углеродных атома кольца, замещенных группой R19, уже были замещены атомом азота, и R19, R20 и R21 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу;
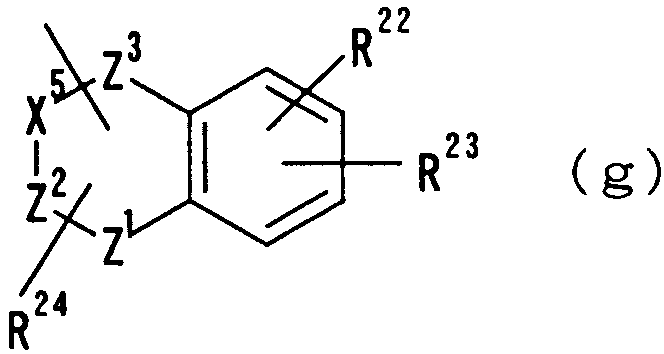
где Х5 представляет СН2, СН, N или NH, Z1 представляет N, NH или О, Z2 представляет СН2, СН, С или N, Z3 представляет СН2, СН, S, SO2 или С=О, Х5-Z2 указывает, что Х5 и Z2 связаны друг с другом одинарной связью или двойной связью, R22 и R23 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу и R24 представляет атом водорода или алкильную группу.
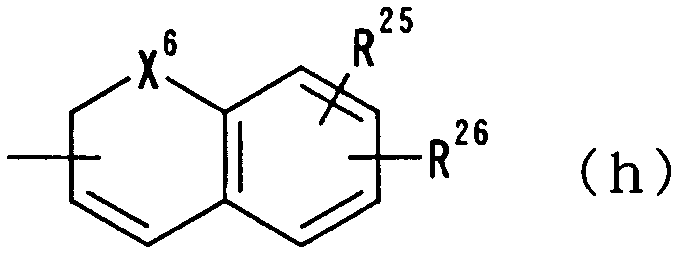
где Х6 представляет О или S и R25 и R26 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу;
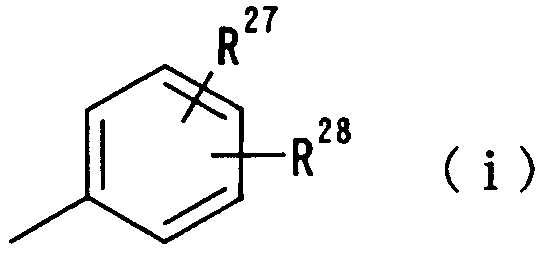
где R27 и R28 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу;
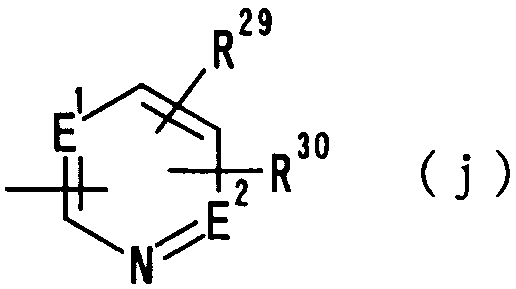
где Е1 и Е2 независимо друг от друга представляют N или CN и R29 и R30 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу;
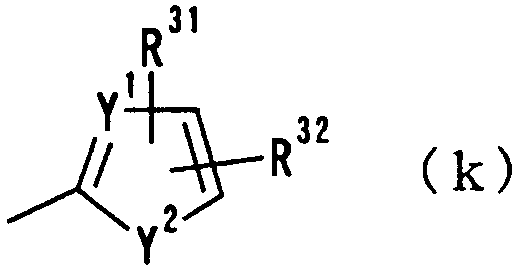
где Y1 представляет СН или N, Y2 представляет -N(R33)-, где R33 означает атом водорода или алкильную группу, имеющую 1-6 углеродных атомов, О или S и R31 и R32 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу; и
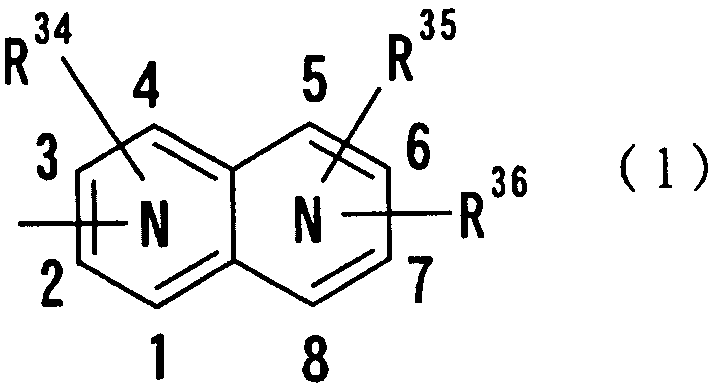
где цифры 1-8 обозначают положения, каждый N показывает, что какой-нибудь один из углеродных атомов положений 1-4 и какой-нибудь один из углеродных атомов положений 5-8 замещены атомом азота, и R34, R35 и R36 независимо друг от друга представляют атом водорода, гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу, гидроксиалкильную группу, алкоксигруппу, алкоксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, ацильную группу, карбамоильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу, алкоксикарбонильную группу, амидиногруппу или алкоксикарбонилалкильную группу.
Ниже дано описание указанных групп.
В описании R5-R36 атом галогена является атомом фтора, хлора, брома или йода, алкильная группа является неразветвленной, разветвленной или циклической алкильной группой, имеющей 1-6 углеродных атомов, алкенильная группа является неразветвленной, разветвленной или циклической алкенильной группой, имеющей 2-6 углеродных атомов, алкинильная группа является неразветвленной или разветвленной алкинильной группой, имеющей 2-6 углеродных атомов, гидроксиалкильная группа означает описанную выше С1-С6алкильную группу, замещенную гидроксильной группой, алкоксигруппа является неразветвленной, разветвленной или циклической алкоксигруппой, имеющей 1-6 углеродных атомов, алкоксиалкильная группа означает описанную выше С1-С6алкильную группу, замещенную описанной выше С1-С6алкоксигруппой, карбоксиалкильная группа означает описанную выше С1-С6алкильную группу, замещенную карбоксильной группой, ацильная группа представляет алканоильную группу (включая формил), имеющую 1-6 углеродных атомов, ароильную группу, такую как бензоильная или нафтоильная группа, или арилалканоильную группу с описанной выше С6-C14арильной группой, замещенной указанной выше С1-С6алканоильной группой, N-алкилкарбамоильная группа означает карбамоильную группу с описанной выше С1-С6алкильной группой, замещенной атомом азота, N,N-диалкилкарбамоильная группа означает карбамоильную группу с двумя описанными выше С1-С6алкильными группами, замещенными атомом азота, алкоксикарбонильная группа является группой, состоящей из описанной выше С1-С6алкоксигруппы и карбонильной группы, алкоксикарбонилалкильная группа означает описанную выше С1-С6алкильную группу, замещенную описанной выше С1-С6алкоксикарбонильной группой, и галогеналкильная группа означает описанную выше С1-С6алкильную группу, замещенную 1-3 атомами галогена. Кстати, в приведенном выше описании не налагается особого ограничения на положение замещения.
В следующей группе:
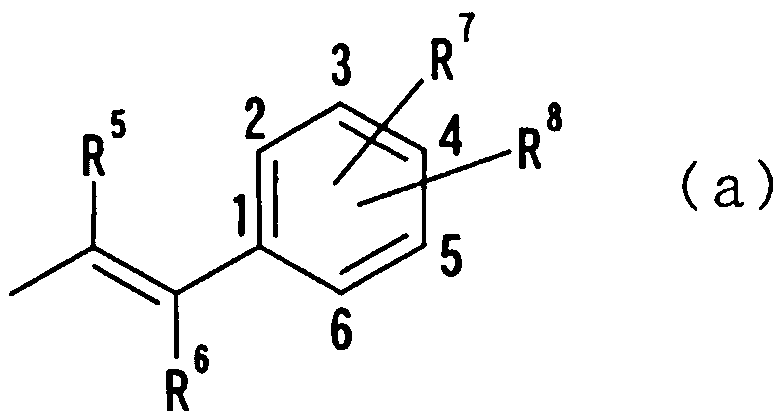
где R5, R6, R7 и R8 имеют такие же значения, как определено выше, и цифры 1-6 указывают положения, R5 и R6 независимо друг от друга предпочтительно представляют атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Более предпочтительно R5 и R6 представляют атомы водорода или алкильные группы. В случае алкильной группы предпочтительной является метильная группа. Предпочтительно, чтобы один из R7 и R8 представлял атом водорода, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В этом случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы особенно предпочтительной является этинильная группа. В качестве конкретных предпочтительных примеров группы, представленной показанной выше формулой, можно назвать хлорстирильную, фторстирильную, бромстирильную и этинилстирильную группы. Особенно предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в приведенной выше формуле является, хотя особо не ограничивается, положение 4. В качестве конкретных предпочтительных примеров можно назвать 4-хлорстирильную, 4-фторстирильную, 4-бромстирильную и 4-этинилстирильную группы.
В следующей группе:
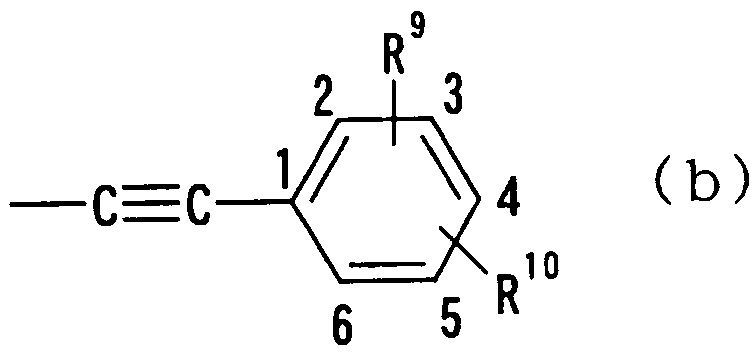
где R9 и R10 имеют такие же значения, как определено выше, и цифры 1-6 указывают положения, R9 и R10 независимо друг от друга предпочтительно представляют атом водорода, атом галогена, алкильную группу или алкинильную группу. Более предпочтительно R9 представляет атом водорода, а R10 представляет атом водорода, атом галогена, алкильную группу или алкинильную группу. В данном случае атом галогена представляет предпочтительно атом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы особенно предпочтительной является этинильная группа. В качестве конкретных предпочтительных примеров группы, представленной показанной выше формулой, можно назвать хлорфенилэтинильную, фторфенилэтинильную, бромфенилэтинильную и этинилфенилэтинильную группы. Особенно предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в указанной формуле является, хотя особо не ограничивается, положение 4. В качестве конкретных предпочтительных примеров можно назвать 4-хлорфенилэтинильную, 4-фторфенилэтинильную, 4-бромфенилэтинильную и 4-этинилфенилэтинильную группы.
В следующей группе:
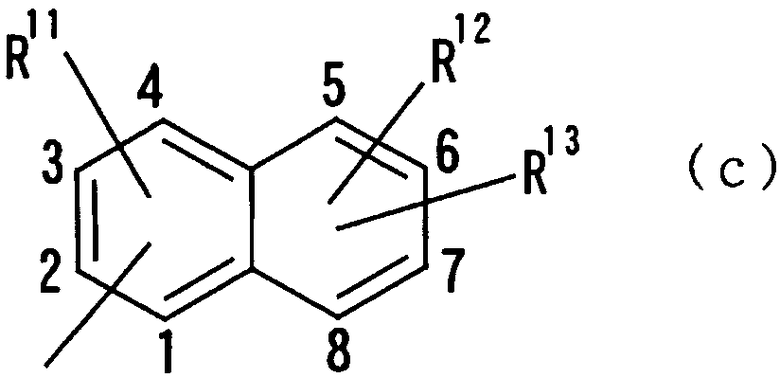
где R11, R12 и R13 имеют такие же значения, как определено выше, и цифры 1-8 указывают положения, R11, R12 и R13 предпочтительно представляют, независимо друг от друга, атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. R11 предпочтительно представляет атом водорода, алкильную группу, атом галогена или гидроксильную группу, причем особенно предпочтительным является атом водорода. Предпочтительно, чтобы один из R12 и R13 представлял атом водорода, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В этом случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы предпочтительной является этинильная группа. В случае нафтильной группы 2-нафтильная группа является более предпочтительной, чем 1-нафтильная группа. В случае 2-нафтильной группы предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в указанной формуле является, хотя особо не ограничивается, положение 6 или 7, причем наиболее предпочтительным является положение 6. Указанные нафтильные группы предпочтительно замещены атомом хлора, фтора или брома, алкинильной группой или подобным, причем особенно предпочтительной является группа, имеющая заместители, такие как атом хлора, фтора или брома, алкинильная группа или тому подобное, в указанном выше положении в приведенной формуле. В качестве конкретных предпочтительных примеров можно назвать 6-хлор-2-нафтильную, 6-фтор-2-нафтильную, 6-бром-2-нафтильную, 6-этинил-2-нафтильную, 7-хлор-2-нафтильную, 7-фтор-2-нафтильную, 7-бром-2-нафтильную и 7-этинил-2-нафтильную группы.
В следующей группе:
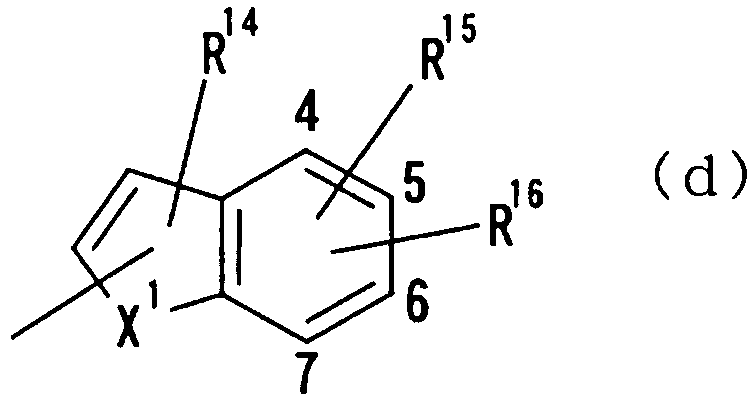
где Х1, R14, R15 и R16 имеют такие же значения, как определено выше, и цифры 4-7 указывают положения, Х1 представляет предпочтительно NH, NOH, N, O или S, особенно предпочтительно NH, O или S. R14 предпочтительно представляет атом водорода, атом галогена, ацильную группу, N-алкилкарбамоильную группу, N,N-диалкилкарбамоильную группу или алкильную группу, а R15 и R16 предпочтительно представляют, независимо друг от друга, атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Предпочтительно, чтобы один из R15 и R16 представлял атом водорода или атом галогена, предпочтительно атом фтора или атом хлора, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В этом случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы предпочтительной является этинильная группа. Положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в указанной формуле предпочтительно является, хотя особо не ограничивается, положение 4, 5 или 6. В качестве конкретных предпочтительных примеров группы, представленной показанной выше формулой, можно назвать такие группы, как 5-хлориндолильная, 5-фториндолильная,
5-броминдолильная, 5-этинилиндолильная, 5-метилиндолильная,
5-хлор-4-фториндолильная, 5-хлор-3-фториндолильная,
5-фтор-3-хлориндолильная, 5-этинил-3-фториндолильная,
5-хлор-3-(N,N-диметилкарбамоил)индолильная,
5-фтор-3-(N,N-диметилкарбамоил)индолильная,
5-хлор-3-формилиндолильная, 5-фтор-3-формилиндолильная,
6-хлориндолильная, 6-фториндолильная, 6-броминдолильная,
6-этинилиндолильная, 6-метилиндолильная, 5-хлорбензотиенильная,
5-фторбензотиенильная, 5-бромбензотиенильная,
5-этинилбензотиенильная, 5-метилбензотиенильная,
5-хлор-4-фторбензотиенильная, 6-хлорбензотиенильная,
6-фторбензотиенильная, 6-бромбензотиенильная,
6-этинилбензотиенильная, 6-метилбензотиенильная,
5-хлорбензофурильная, 5-фторбензофурильная,
5-бромбензофурильная, 5-этинилбензофурильная,
5-метилбензофурильная, 5-хлор-4-фторбензофурильная,
6-хлорбензофурильная, 6-фторбензофурильная, 6-бромбензфурильная,
6-этинилбензофурильная и 6-метилбензофурильная группы. Положение описанной выше замещающей группы, присоединенной к Т1, особо не ограничивается, но предпочтительным является положение 2 или положение 3 в формуле (d). В частности, более предпочтительными являются 5-хлориндол-2-ильная, 5-фториндол-2-ильная,
5-броминдол-2-ильная, 5-этинилиндол-2-ильная,
5-метилиндол-2-ильная, 5-хлор-4-фториндол-2-ильная,
5-хлор-3-фториндол-2-ильная, 3-бром-5-хлориндол-2-ильная,
3-хлор-5-фториндол-2-ильная, 3-бром-5-фториндол-2-ильная,
5-бром-3-хлориндол-2-ильная, 5-бром-3-фториндол-2-ильная,
5-хлор-3-формилиндол-2-ильная, 5-фтор-3-формилиндол-2-ильная,
5-бром-3-формилиндол-2-ильная, 5-этинил-3-формилиндол-2-ильная,
5-хлор-3-(N,N-диметилкарбамоил)индол-2-ильная,
5-фтор-3-(N,N-диметилкарбамоил)индол-2-ильная,
5-бром-3-(N,N-диметилкарбамоил)индол-2-ильная,
5-этинил-3-(N,N-диметилкарбамоил)индол-2-ильная,
6-хлориндол-2-ильная, 6-фториндол-2-ильная,
6-броминдол-2-ильная, 6-этинилиндол-2-ильная,
6-метилиндол-2-ильная, 5-хлориндол-3-ильная,
5-фториндол-3-ильная, 5-броминдол-3-ильная,
5-этинилиндол-3-ильная, 5-метилиндол-3-ильная,
5-хлор-4-фториндол-3-ильная, 6-хлориндол-3-ильная,
6-фториндол-3-ильная, 6-броминдол-3-ильная,
6-этинилиндол-3-ильная, 6-метилиндол-3-ильная,
5-хлорбензотиофен-2-ильная, 5-фторбензотиофен-2-ильная,
5-бромбензотиофен-2-ильная, 5-этинилбензотиофен-2-ильная,
5-метилбензотиофен-2-ильная, 5-хлор-4-фторбензотиофен-2-ильная,
6-хлорбензотиофен-2-ильная, 6-фторбензотиофен-2-ильная,
6-бромбензотиофен-2-ильная, 6-этинилбензотиофен-2-ильная,
6-метилбензотиофен-2-ильная, 5-хлорбензотиофен-3-ильная,
5-фторбензотиофен-3-ильная, 5-бромбензотиофен-3-ильная,
5-этинилбензотиофен-3-ильная, 5-метилбензотиофен-3-ильная,
5-хлор-4-фторбензотиофен-3-ильная, 6-хлорбензотиофен-3-ильная,
6-фторбензотиофен-3-ильная, 6-бромбензотиофен-3-ильная,
6-этинилбензотиофен-3-ильная, 6-метилбензотиофен-3-ильная,
5-хлорбензофуран-2-ильная, 5-фторбензофуран-2-ильная,
5-бромбензофуран-2-ильная, 5-этинилбензофуран-2-ильная,
5-метилбензофуран-2-ильная, 5-хлор-4-фторбензофуран-2-ильная,
6-хлорбензофуран-2-ильная, 6-фторбензофуран-2-ильная,
6-бромбензофуран-2-ильная, 6-этинилбензофуран-2-ильная,
6-метилбензофуран-2-ильная, 5-хлорбензофуран-3-ильная,
5-фторбензофуран-3-ильная, 5-бромбензофуран-3-ильная,
5-этинилбензофуран-3-ильная, 5-метилбензофуран-3-ильная,
5-хлор-4-фторбензофуран-3-ильная, 6-хлорбензофуран-3-ильная,
6-фторбензофуран-3-ильная, 6-бромбензофуран-3-ильная,
6-этинилбензофуран-3-ильная и 6-метилбензофуран-3-ильная группы,
и особенно предпочтительными являются 5-хлориндол-2-ильная,
5-фториндол-2-ильная, 5-броминдол-2-ильная,
5-этинилиндол-2-ильная, 5-метилиндол-2-ильная,
5-хлор-4-фториндол-2-ильная, 6-хлориндол-2-ильная,
6-фториндол-2-ильная, 6-броминдол-2-ильная,
6-этинилиндол-2-ильная, 6-метилиндол-2-ильная,
5-хлор-3-фториндол-2-ильная, 3-бром-5-хлориндол-2-ильная,
3-хлор-5-фториндол-2-ильная, 3-бром-5-фториндол-2-ильная,
5-бром-3-хлориндол-2-ильная, 5-бром-3-фториндол-2-ильная,
5-хлор-3-формилиндол-2-ильная, 5-фтор-3-формилиндол-2-ильная,
5-бром-3-формилиндол-2-ильная, 5-этинил-3-формилиндол-2-ильная,
5-хлор-3-(N,N-диметилкарбамоил)индол-2-ильная,
5-фтор-3-(N,N-диметилкарбамоил)индол-2-ильная,
5-бром-3-(N,N-диметилкарбамоил)индол-2-ильная,
5-этинил-3-(N,N-диметилкарбамоил)индол-2-ильная,
5-хлорбензотиофен-2-ильная, 5-фторбензотиофен-2-ильная,
5-бромбензотиофен-2-ильная, 5-этинилбензотиофен-2-ильная,
5-метилбензотиофен-2-ильная, 5-хлор-4-фторбензотиофен-2-ильная,
6-хлорбензотиофен-2-ильная, 6-фторбензотиофен-2-ильная,
6-бромбензотиофен-2-ильная, 6-этинилбензотиофен-2-ильная,
6-метилбензотиофен-2-ильная, 5-хлорбензофуран-2-ильная,
5-фторбензофуран-2-ильная, 5-бромбензофуран-2-ильная,
5-этинилбензофуран-2-ильная, 5-метилбензофуран-2-ильная,
5-хлор-4-фторбензофуран-2-ильная, 6-хлорбензофуран-2-ильная,
6-фторбензофуран-2-ильная, 6-бромбензофуран-2-ильная,
6-этинилбензофуран-2-ильная и 6-метилбензофуран-2-ильная группы.
В следующей группе:
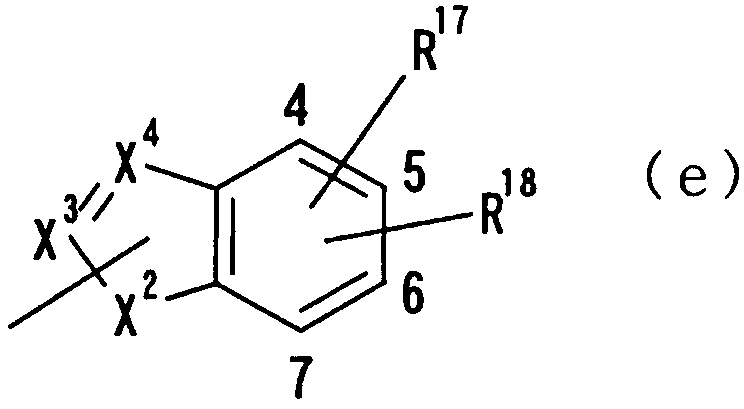
где Х2, Х3, Х4, R17 и R18 имеют такие же значения, как определено выше, и цифры 4-7 указывают положения, Х2 представляет предпочтительно NH, O или S, любой из Х3 и Х4 представляет предпочтительно СН или С, и особенно предпочтительно С. R17 и R18 предпочтительно представляют, независимо друг от друга, атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Предпочтительно, чтобы один из R17 и R18 представлял собой атом водорода, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В данном случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы предпочтительной является этинильная группа. Предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в указанной формуле является, хотя особо не ограничивается, положение 5 или 6. В качестве конкретных предпочтительных примеров группы, представленной показанной выше формулой, можно назвать такие группы, как 5-хлориндазолильная,
5-фториндазолильная, 5-броминдазолильная,
5-этинилиндазолильная, 6-хлориндазолильная, 6-фториндазолильная,
6-броминдазолильная, 6-этинилиндазолильная,
5-хлорбензимидазолильная, 5-фторбензимидазолильная,
5-бромбензимидазолильная, 5-этинилбензимидазолильная,
6-хлорбензимидазолильная, 6-фторбензимидазолильная,
6-бромбензимидазолильная, 6-этинилбензимидазолильная,
5-хлорбензотиазолильная, 5-фторбензотиазолильная,
5-бромбензотиазолильная, 5-этинилбензотиазолильная,
6-хлорбензотиазолильная, 6-фторбензотиазолильная,
6-бромбензотиазолильная, 6-этинилбензотиазолильная,
5-хлорбензоксазолильная, 5-фторбензоксазолильная,
5-бромбензоксазолильная, 5-этинилбензоксазолильная,
6-хлорбензоксазолильная, 6-фторбензоксазолильная,
6-бромбензоксазолильная, 6-этинилбензоксазолильная,
5-хлорбензизотиазолильная, 5-фторбензизотиазолильная,
5-бромбензизотиазолильная, 5-этинилбензизотиазолильная,
6-хлорбензизотиазолильная, 6-фторбензизотиазолильная,
6-бромбензизотиазолильная, 6-этинилбензизотиазолильная,
5-хлорбензизоксазолильная, 5-фторбензизоксазолильная,
5-бромбензизоксазолильная, 5-этинилбензизоксазолильная,
6-хлорбензизоксазолильная, 6-фторбензизоксазолильная,
6-бромбензизоксазолильная и 6-этинилбензизоксазолильная группы. Положение описанной выше замещающей группы, присоединенной к Т1, особо не ограничивается. Более предпочтительными являются
5-хлориндазол-3-ильная, 5-фториндазол-3-ильная,
5-броминдазол-3-ильная, 5-этинилиндазол-3-ильная,
6-хлориндазол-3-ильная, 6-фториндазол-3-ильная,
6-броминдазол-3-ильная, 6-этинилиндазол-3-ильная,
5-хлорбензимидазол-2-ильная, 5-фторбензимидазол-2-ильная,
5-бромбензимидазол-2-ильная, 5-этинилбензимидазол-2-ильная,
6-хлорбензимидазол-2-ильная, 6-фторбензимидазол-2-ильная,
6-бромбензимидазол-2-ильная, 6-этинилбензимидазол-2-ильная,
5-хлорбензотиазол-2-ильная, 5-фторбензотиазол-2-ильная,
5-бромбензотиазол-2-ильная, 5-этинилбензотиазол-2-ильная,
6-хлорбензотиазол-2-ильная, 6-фторбензотиазол-2-ильная,
6-бромбензотиазол-2-ильная, 6-этинилбензотиазол-2-ильная,
5-хлорбензоксазол-2-ильная, 5-фторбензоксазол-2-ильная,
5-бромбензоксазол-2-ильная, 5-этинилбензоксазол-2-ильная,
6-хлорбензоксазол-2-ильная, 6-фторбензоксазол-2-ильная,
6-бромбензоксазол-2-ильная, 6-этинилбензоксазол-2-ильная,
5-хлорбензизотиазол-3-ильная, 5-фторбензизотиазол-3-ильная,
5-бромбензизотиазол-3-ильная, 5-этинилбензизотиазол-3-ильная,
6-хлорбензизотиазол-3-ильная, 6-фторбензизотиазол-3-ильная,
6-бромбензизотиазол-3-ильная, 6-этинилбензизотиазол-3-ильная,
5-хлорбензизоксазол-3-ильная, 5-фторбензизоксазол-3-ильная,
5-бромбензизоксазол-3-ильная, 5-этинилбензизоксазол-3-ильная,
6-хлорбензизоксазол-3-ильная, 6-фторбензизоксазол-3-ильная,
6-бромбензизоксазол-3-ильная и 6-этинилбензизоксазол-3-ильная группы, и особенно предпочтительными являются
5-хлорбензимидазол-2-ильная, 5-фторбензимидазол-2-ильная,
5-бромбензимидазол-2-ильная, 5-этинилбензимидазол-2-ильная,
6-хлорбензимидазол-2-ильная, 6-фторбензимидазол-2-ильная,
6-бромбензимидазол-2-ильная, 6-этинилбензимидазол-2-ильная,
5-хлорбензотиазол-2-ильная, 5-фторбензотиазол-2-ильная,
5-бромбензотиазол-2-ильная, 5-этинилбензотиазол-2-ильная,
6-хлорбензотиазол-2-ильная, 6-фторбензотиазол-2-ильная,
6-бромбензотиазол-2-ильная, 6-этинилбензотиазол-2-ильная,
5-хлорбензоксазол-2-ильная, 5-фторбензоксазол-2-ильная,
5-бромбензоксазол-2-ильная, 5-этинилбензоксазол-2-ильная,
6-хлорбензоксазол-2-ильная, 6-фторбензоксазол-2-ильная,
6-бромбензоксазол-2-ильная и 6-этинилбензоксазол-2-ильная группы. Из них еще более предпочтительными являются 5-хлорбензимидазол-2-ильная, 5-фторбензимидазол-2-ильная, 5-бромбензимидазол-2-ильная и 5-этинилбензимидазол-2-ильная группы.
В следующей группе:
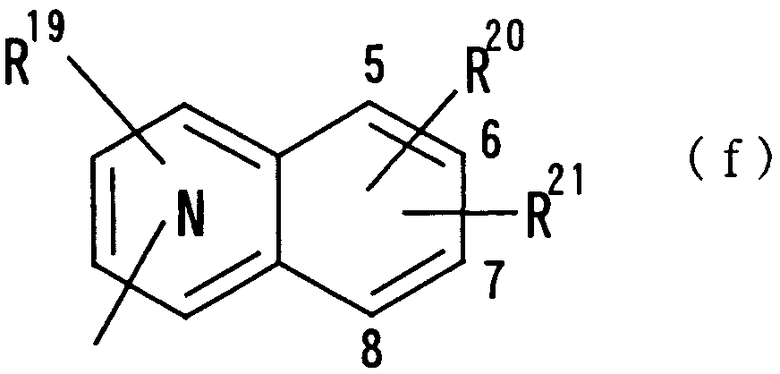
где N показывает, что 1 или 2 углеродных атома кольца, замещенного группой R19, уже замещены атомом азота, R19, R20 и R21 имеют такие же значения, как определено выше, и цифры 5-8 указывают положения, R19, R20 и R21 предпочтительно представляют, независимо друг от друга, атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. R19 особенно предпочтительно представляет атом водорода. Предпочтительно, чтобы один из R20 и R21 представлял собой атом водорода, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В этом случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы предпочтительной является этинильная группа. Предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в указанной формуле является, хотя особо не ограничивается, положение 6 или 7. В качестве конкретных предпочтительных примеров таких групп можно назвать хинолинильную, изохинолинильную и циннолинильную группы. Более предпочтительными являются 6-хлорхинолинильная,
6-фторхинолинильная, 6-бромхинолинильная, 6-этинилхинолинильная,
6-хлоризохинолинильная, 6-фторизохинолинильная,
6-бромизохинолинильная, 6-этинилизохинолинильная,
7-хлорциннолинильная, 7-фторциннолинильная, 7-бромциннолинильная
и 7-этинилциннолинильная группы, а особенно предпочтительными являются 6-хлорхинолин-2-ильная, 6-фторхинолин-2-ильная,
6-бромхинолин-2-ильная, 6-этинилхинолин-2-ильная,
6-хлорхинолин-3-ильная, 6-фторхинолин-3-ильная,
6-бромхинолин-3-ильная, 6-этинилхинолин-3-ильная,
7-хлорхинолин-2-ильная, 7-фторхинолин-2-ильная,
7-бромхинолин-2-ильная, 7-этинилхинолин-2-ильная,
7-хлорхинолин-3-ильная, 7-фторхинолин-3-ильная,
7-бромхинолин-3-ильная, 7-этинилхинолин-3-ильная,
6-хлоризохинолин-3-ильная, 6-фторизохинолин-3-ильная,
6-бромизохинолин-3-ильная, 6-этинилизохинолин-3-ильная,
7-хлоризохинолин-3-ильная, 7-фторизохинолин-3-ильная,
7-бромизохинолин-3-ильная, 7-этинилизохинолин-3-ильная,
7-хлорциннолин-3-ильная, 7-фторциннолин-3-ильная,
7-бромциннолин-3-ильная и 7-этинилциннолин-3-ильная группы. Из них еще более предпочтительными являются 6-хлорхинолин-2-ильная,
6-фторхинолин-2-ильная, 6-бромхинолин-2-ильная,
6-этинилхинолин-2-ильная, 7-хлорхинолин-3-ильная,
7-фторхинолин-3-ильная, 7-бромхинолин-3-ильная,
7-этинилхинолин-3-ильная, 7-хлоризохинолин-3-ильная,
7-фторизохинолин-3-ильная, 7-бромизохинолин-3-ильная,
7-этинилизохинолин-3-ильная, 7-хлорциннолин-3-ильная,
7-фторциннолин-3-ильная, 7-бромциннолин-3-ильная и
7-этинилциннолин-3-ильная группы.
В следующей группе:
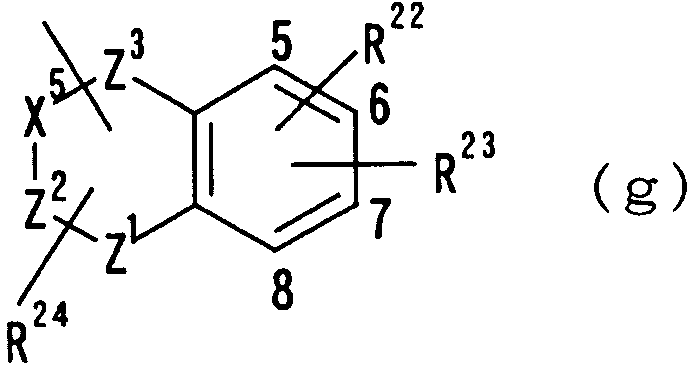
где цифры 5-8 указывают положения, Х5 представляет СН2, СН, N или NH, Z1 представляет N, NH или О, Z2 представляет СН2, СН, С или N, Z3 представляет СН2, СН, S, SO2 или С=О, Х5-Z2 указывает, что Х5 и Z2 связаны друг с другом одинарной связью или двойной связью, и R22, R23 и R24 имеют такие же значения, как определено выше, R22 и R23 предпочтительно представляют, независимо друг от друга, атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Предпочтительно, чтобы один из R22 и R23 представлял собой атом водорода, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В этом случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы предпочтительной является этинильная группа. Предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в указанной формуле является, хотя особо не ограничивается, положение 6 или 7. R24 предпочтительно представляет атом водорода или алкильную группу, и метильная группа является предпочтительной в случае алкильной группы. В качестве R24 особенно предпочтительным является атом водорода. В качестве конкретных предпочтительных примеров группы, представленной показанной выше формулой, можно назвать 4-оксодигидрохинолинильную, тетрагидрохинолинильную, 4-оксодигидрохиназолин-2-ильную, 4-оксотетрагидроциннолинильную, 4-оксобензопиранильную, 4-оксобензотиадиазинильную, 1,1-диокси-4-оксобензотиадиазинильную и бензоксадиазинильную группы. В качестве их конкретных предпочтительных примеров можно назвать такие группы, как 6-хлор-4-оксодигидрохинолинильная,
6-фтор-4-оксодигидрохинолинильная,
6-бром-4-оксодигидрохинолинильная,
6-этинил-4-оксодигидрохинолинильная,
7-хлор-4-оксодигидрохинолинильная,
7-фтор-4-оксодигидрохинолинильная,
7-бром-4-оксодигидрохинолинильная,
7-этинил-4-оксодигидрохинолинильная,
6-хлор-4-оксо-1,4-дигидрохиназолинильная,
6-фтор-4-оксо-1,4-дигидрохиназолинильная,
6-бром-4-оксо-1,4-дигидрохиназолинильная,
6-этинил-4-оксо-1,4-дигидрохиназолинильная,
7-хлор-4-оксо-1,4-дигидрохиназолинильная,
7-фтор-4-оксо-1,4-дигидрохиназолинильная,
7-бром-4-оксо-1,4-дигидрохиназолинильная,
7-этинил-4-оксо-1,4-дигидрохиназолинильная,
6-хлор-1,2,3,4-тетрагидрохинолинильная,
6-фтор-1,2,3,4-тетрагидрохинолинильная,
6-бром-1,2,3,4-тетрагидрохинолинильная,
6-этинил-1,2,3,4-тетрагидрохинолинильная,
7-хлор-1,2,3,4-тетрагидрохинолинильная,
7-фтор-1,2,3,4-тетрагидрохинолинильная,
7-бром-1,2,3,4-тетрагидрохинолинильная,
7-этинил-1,2,3,4-тетрагидрохинолинильная,
6-хлор-1,2,3,4-тетрагидро-4-оксоциннолинильная,
6-фтор-1,2,3,4-тетрагидро-4-оксоциннолинильная,
6-бром-1,2,3,4-тетрагидро-4-оксоциннолинильная,
6-этинил-1,2,3,4-тетрагидро-4-оксоциннолинильная,
7-хлор-1,2,3,4-тетрагидро-4-оксоциннолинильная,
7-фтор-1,2,3,4-тетрагидро-4-оксоциннолинильная,
7-бром-1,2,3,4-тетрагидро-4-оксоциннолинильная,
7-этинил-1,2,3,4-тетрагидро-4-оксоциннолинильная,
6-хлор-4Н-4-оксобензопиранильная,
6-фтор-4Н-4-оксобензопиранильная,
6-бром-4Н-4-оксобензопиранильная,
6-этинил-4Н-4-оксобензопиранильная,
7-хлор-4Н-4-оксобензопиранильная,
7-фтор-4Н-4-оксобензопиранильная,
7-бром-4Н-4-оксобензопиранильная,
7-этинил-4Н-4-оксобензопиранильная,
6-хлор-1,1-диокси-2Н-1,2,4-бензотиадиазинильная,
6-фтор-1,1-диокси-2Н-1,2,4-бензотиадиазинильная,
6-бром-1,1-диокси-2Н-1,2,4-бензотиадиазинильная,
6-этинил-1,1-диокси-2Н-1,2,4-бензотиадиазинильная,
7-хлор-1,1-диокси-2Н-1,2,4-бензотиадиазинильная,
7-фтор-1,1-диокси-2Н-1,2,4-бензотиадиазинильная,
7-бром-1,1-диокси-2Н-1,2,4-бензотиадиазинильная,
7-этинил-1,1-диокси-2Н-1,2,4-бензотиадиазинильная,
6-хлор-2Н-1,2,4-бензоксадиазинильная,
6-фтор-2Н-1,2,4-бензоксадиазинильная,
6-бром-2Н-1,2,4-бензоксадиазинильная,
6-этинил-2Н-1,2,4-бензоксадиазинильная,
7-хлор-2Н-1,2,4-бензоксадиазинильная,
7-фтор-2Н-1,2,4-бензоксадиазинильная,
7-бром-2Н-1,2,4-бензоксадиазинильная и
7-этинил-2Н-1,2,4-бензоксадиазинильная группы; причем предпочтительными являются
6-хлор-4-оксо-1,4-дигидрохинолин-2-ильная,
6-фтор-4-оксо-1,4-дигидрохинолин-2-ильная,
6-бром-4-оксо-1,4-дигидрохинолин-2-ильная,
6-этинил-4-оксо-1,4-дигидрохинолин-2-ильная,
7-хлор-4-оксо-1,4-дигидрохинолин-2-ильная,
7-фтор-4-оксо-1,4-дигидрохинолин-2-ильная,
7-бром-4-оксо-1,4-дигидрохинолин-2-ильная,
7-этинил-4-оксо-1,4-дигидрохинолин-2-ильная,
6-хлор-4-оксо-1,4-дигидрохиназолин-2-ильная,
6-фтор-4-оксо-1,4-дигидрохиназолин-2-ильная,
6-бром-4-оксо-1,4-дигидрохиназолин-2-ильная,
6-этинил-4-оксо-1,4-дигидрохиназолин-2-ильная,
7-хлор-4-оксо-1,4-дигидрохиназолин-2-ильная,
7-фтор-4-оксо-1,4-дигидрохиназолин-2-ильная,
7-бром-4-оксо-1,4-дигидрохиназолин-2-ильная,
7-этинил-4-оксо-1,4-дигидрохиназолин-2-ильная,
6-хлор-1,2,3,4-тетрагидрохинолин-2-ильная,
6-фтор-1,2,3,4-тетрагидрохинолин-2-ильная,
6-бром-1,2,3,4-тетрагидрохинолин-2-ильная,
6-этинил-1,2,3,4-тетрагидрохинолин-2-ильная,
6-хлор-1,2,3,4-тетрагидро-4-оксоциннолин-2-ильная,
6-фтор-1,2,3,4-тетрагидро-4-оксоциннолин-2-ильная,
6-бром-1,2,3,4-тетрагидро-4-оксоциннолин-2-ильная,
6-этинил-1,2,3,4-тетрагидро-4-оксоциннолин-2-ильная,
7-хлор-1,2,3,4-тетрагидро-4-оксоциннолин-2-ильная,
7-фтор-1,2,3,4-тетрагидро-4-оксоциннолин-2-ильная,
7-бром-1,2,3,4-тетрагидро-4-оксоциннолин-2-ильная,
7-этинил-1,2,3,4-тетрагидро-4-оксоциннолин-2-ильная,
6-хлор-4Н-4-оксобензопиран-2-ильная,
6-фтор-4Н-4-оксобензопиран-2-ильная,
6-бром-4Н-4-оксобензопиран-2-ильная,
6-этинил-4Н-4-оксобензопиран-2-ильная,
7-хлор-4Н-4-оксобензопиран-2-ильная,
7-фтор-4Н-4-оксобензопиран-2-ильная,
7-бром-4Н-4-оксобензопиран-2-ильная,
7-этинил-4Н-4-оксобензопиран-2-ильная,
6-хлор-1,1-диокси-2Н-1,2,4-бензотиадиазин-3-ильная,
6-фтор-1,1-диокси-2Н-1,2,4-бензотиадиазин-3-ильная,
6-бром-1,1-диокси-2Н-1,2,4-бензотиадиазин-3-ильная,
6-этинил-1,1-диокси-2Н-1,2,4-бензотиадиазин-3-ильная,
7-хлор-1,1-диокси-2Н-1,2,4-бензотиадиазин-3-ильная,
7-фтор-1,1-диокси-2Н-1,2,4-бензотиадиазин-3-ильная,
7-бром-1,1-диокси-2Н-1,2,4-бензотиадиазин-3-ильная,
7-этинил-1,1-диокси-2Н-1,2,4-бензотиадиазин-3-ильная,
6-хлор-2Н-1,2,4-бензоксадиазин-3-ильная,
6-фтор-2Н-1,2,4-бензоксадиазин-3-ильная,
6-бром-2Н-1,2,4-бензоксадиазин-3-ильная,
6-этинил-2Н-1,2,4-бензоксадиазин-3-ильная,
7-хлор-2Н-1,2,4-бензоксадиазин-3-ильная,
7-фтор-2Н-1,2,4-бензоксадиазин-3-ильная,
7-бром-2Н-1,2,4-бензоксадиазин-3-ильная и
7-этинил-2Н-1,2,4-бензоксадиазин-3-ильная группы. Среди них особенно предпочтительными являются
6-хлор-4-оксо-1,4-дигидрохинолин-2-ильная,
6-фтор-4-оксо-1,4-дигидрохинолин-2-ильная,
6-бром-4-оксо-1,4-дигидрохинолин-2-ильная,
6-этинил-4-оксо-1,4-дигидрохинолин-2-ильная,
6-хлор-4-оксо-1,4-дигидрохиназолин-2-ильная,
6-фтор-4-оксо-1,4-дигидрохиназолин-2-ильная,
6-бром-4-оксо-1,4-дигидрохиназолин-2-ильная и
6-этинил-4-оксо-1,4-дигидрохиназолин-2-ильная группы.
В следующей группе:
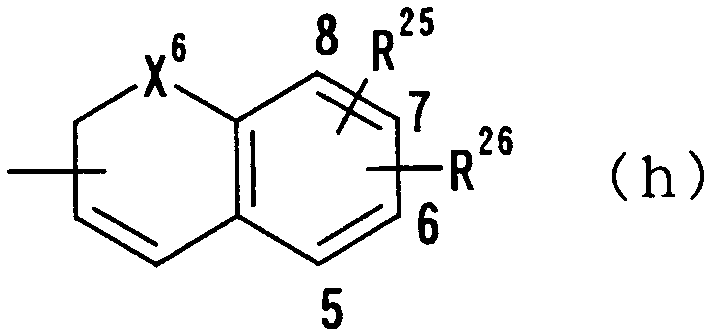
где Х6 представляет О или S, R25 и R26 имеют такие же значения, как определено выше, и цифры 5-8 указывают положения, Х6 представляет предпочтительно O, и R25 и R26 предпочтительно представляют, независимо друг от друга, атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Предпочтительно, чтобы один из R25 и R26 представлял собой атом водорода, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В данном случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы предпочтительной является этинильная группа. Предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в указанной формуле является, хотя особо не ограничивается, положение 6 или 7. В качестве конкретных предпочтительных примеров группы, представленной показанной выше формулой, могут быть названы 6-хлор-2Н-хромен-3-ильная, 6-фтор-2Н-хромен-3-ильная, 6-бром-2Н-хромен-3-ильная, 6-этинил-2Н-хромен-3-ильная, 7-хлор-2Н-хромен-3-ильная, 7-фтор-2Н-хромен-3-ильная, 7-бром-2Н-хромен-3-ильная и 7-этинил-2Н-хромен-3-ильная группы, и особенно предпочтительными являются 7-хлор-2Н-хромен-3-ильная, 7-фтор-2Н-хромен-3-ильная, 7-бром-2Н-хромен-3-ильная и 7-этинил-2Н-хромен-3-ильная группы.
В следующей группе:
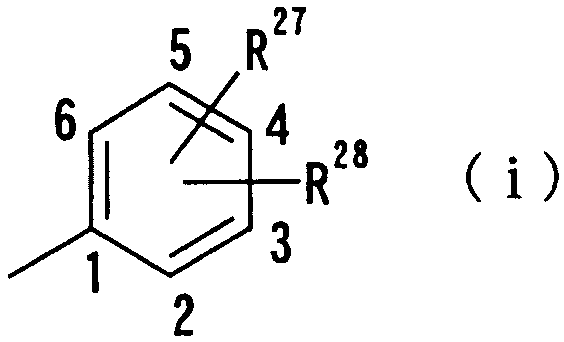
где R27 и R28 имеют такие же значения, как определено выше, и цифры 1-6 указывают положения, предпочтительно, чтобы один из R27 и R28 представлял собой атом водорода или атом галогена, а другой - атом водорода, цианогруппу, нитрогруппу, аминогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу, галогеналкильную группу или N,N-диалкилкарбамоильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В данном случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы предпочтительной является этинильная группа. В качестве конкретных примеров группы, представленной показанной выше формулой, можно назвать фенильную, хлорфенильную, фторфенильную, бромфенильную, этинилфенильную и хлорфторфенильную группы. Особенно предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в указанных группах является, хотя особо не ограничивается, положение 3 или 4 в показанной выше формуле в случае одного заместителя или комбинация положения 4 и положения 2 или 3 в показанной выше формуле в случае двух заместителей. В качестве конкретных предпочтительных примеров группы, представленной показанной выше формулой, можно назвать фенил, 4-хлорфенил, 4-фторфенил, 4-бромфенил, 4-этинилфенил, 3-хлорфенил, 3-фторфенил, 3-бромфенил, 3-этинилфенил, 3-хлор-4-фторфенил, 4-хлор-3-фторфенил, 4-хлор-2-фторфенил, 2-хлор-4-фторфенил, 4-бром-2-фторфенил, 2-бром-4-фторфенил, 2,4-дихлорфенил, 2,4-дифторфенил, 2,4-дибромфенил, 4-хлор-3-метилфенил, 4-фтор-3-метилфенил, 4-бром-3-метилфенил, 4-хлор-2-метилфенил, 4-фтор-2-метилфенил, 4-бром-2-метилфенил, 3,4-дихлорфенил, 3,4-дифторфенил и 3,4-дибромфенил.
В следующей группе:
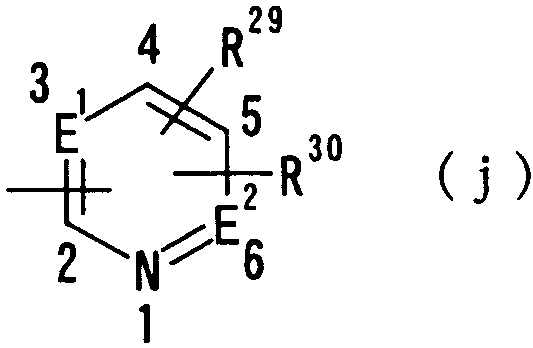
где Е1, Е2 R29 и R30 имеют такие же значения, как определено выше, и цифры 1-6 указывают положения, предпочтительно, чтобы один из R29 и R30 представлял собой атом водорода или атом галогена, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В данном случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы особенно предпочтительной является этинильная группа. В качестве конкретных примеров группы, представленной показанной выше формулой, можно назвать пиридильную, пиримидильную и пиридазинильную группы. Особенно предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в указанных группах является, хотя особо не ограничивается, положение 4 или 5 в показанной выше формуле в случае, когда связь показанной группы с группой Т1 находится в положении 2 в представленной выше формуле. В качестве конкретных предпочтительных примеров могут быть названы 2-пиридильная, 3-пиридильная, 4-пиридильная,
4-хлор-2-пиридильная, 4-фтор-2-пиридильная,
4-бром-2-пиридильная, 4-этинил-2-пиридильная,
4-хлор-3-пиридильная, 4-фтор-3-пиридильная,
4-бром-3-пиридильная, 4-этинил-3-пиридильная,
5-хлор-2-пиридильная, 5-фтор-2-пиридильная,
5-бром-2-пиридильная, 5-этинил-2-пиридильная,
4-хлор-5-фтор-2-пиридильная, 5-хлор-4-фтор-2-пиридильная,
5-хлор-3-пиридильная, 5-фтор-3-пиридильная,
5-бром-3-пиридильная, 5-этинил-3-пиридильная,
5-хлор-2-пиримидильная, 5-фтор-2-пиримидильная,
5-бром-2-пиримидильная, 5-этинил-2-пиримидильная,
4-хлор-3-пиридазинильная, 4-фтор-3-пиридазинильная,
4-бром-3-пиридазинильная, 4-этинил-3-пиридазинильная,
6-хлор-3-пиридазинильная, 6-фтор-3-пиридазинильная,
6-бром-3-пиридазинильная и 6-этинил-3-пиридазинильная группы. Особенно предпочтительными являются 2-пиридильная,
3-пиридильная, 4-пиридильная, 4-хлор-2-пиридильная,
4-фтор-2-пиридильная, 4-бром-2-пиридильная,
4-этинил-2-пиридильная, 4-хлор-3-пиридильная,
4-фтор-3-пиридильная, 4-бром-3-пиридильная,
4-этинил-3-пиридильная, 5-хлор-2-пиридильная,
5-фтор-2-пиридильная, 5-бром-2-пиридильная,
5-этинил-2-пиридильная, 4-хлор-5-фтор-2-пиридильная,
5-хлор-4-фтор-2-пиридильная, 5-хлор-3-пиридильная,
5-фтор-3-пиридильная, 5-бром-3-пиридильная,
5-этинил-3-пиридильная, 6-хлор-3-пиридазинильная,
6-фтор-3-пиридазинильная, 6-бром-3-пиридазинильная,
6-этинил-3-пиридазильная, 4-хлор-3-пиридазинильная,
4-фтор-3-пиридазинильная, 4-бром-3-пиридазинильная и
4-этинил-3-пиридазинильная группы. Среди них еще более предпочтительными являются 2-пиридильная, 3-пиридильная,
4-пиридильная, 5-хлор-2-пиридильная, 5-фтор-2-пиридильная,
5-бром-2-пиридильная, 5-этинил-2-пиридильная,
5-хлор-4-фтор-2-пиридильная, 4-хлор-5-фтор-2-пиридильная,
4-хлор-3-пиридазинильная, 4-фтор-3-пиридазинильная,
4-бром-3-пиридазинильная и 4-этинил-3-пиридазинильная группы.
В следующей группе:
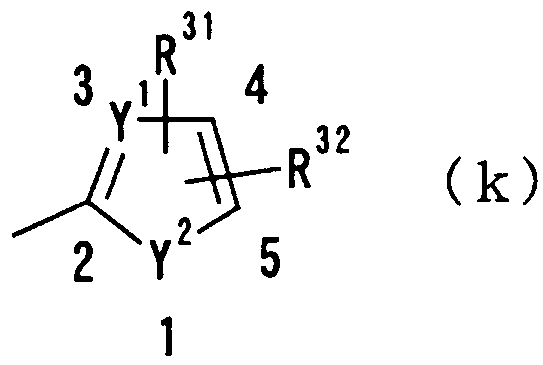
где Y1, Y2 R31 и R32 имеют такие же значения, как определено выше, и цифры 1-5 указывают положения, предпочтительно, чтобы один из R31 и R32 представлял собой атом водорода или атом галогена, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В данном случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы особенно предпочтительной является этинильная группа. В качестве конкретных примеров группы, представленной показанной выше формулой, можно назвать тиенильную, пирролильную, фурильную, оксазолильную и тиазолильную группы. Особенно предпочтительным положением, замещенным атомом галогена, алкильной группой или алкинильной группой, в таких группах является, хотя особо не ограничивается, положение 4 или 5 в представленной выше формуле. В качестве конкретных предпочтительных примеров таких групп могут быть названы 4-хлор-2-тиенильная, 4-фтор-2-тиенильная,
4-бром-2-тиенильная, 4-этинил-2-тиенильная,
4-хлор-2-пирролильная, 4-фтор-2-пирролильная,
4-бром-2-пирролильная, 4-этинил-2-пирролильная,
4-хлор-2-фурильная, 4-фтор-2-фурильная, 4-бром-2-фурильная,
4-этинил-2-фурильная, 5-хлор-2-тиенильная, 5-фтор-2-тиенильная,
5-бром-2-тиенильная, 5-этинил-2-тиенильная,
5-хлор-2-тиазолильная, 5-фтор-2-тиазолильная,
5-бром-2-тиазолильная, 5-этинил-2-тиазолильная,
5-хлор-2-оксазолильная, 5-фтор-2-оксазолильная,
5-бром-2-оксазолильная и 5-этинил-2-оксазолильная группы. Особенно предпочтительными являются 5-хлор-2-тиазолильная,
5-фтор-2-тиазолильная, 5-бром-2-тиазолильная и
5-этинил-2-тиазолильная группы.
В следующей группе:
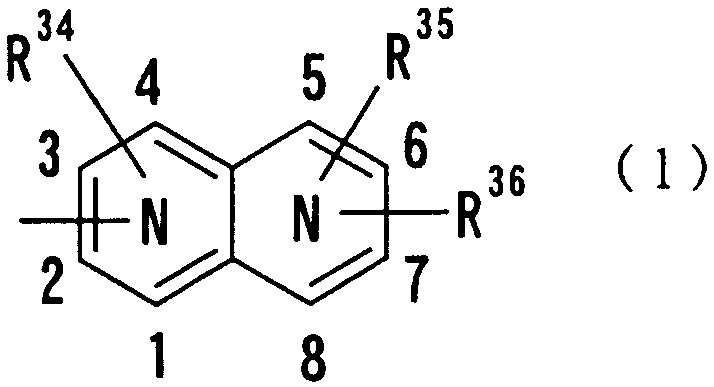
где цифры 1-8 указывают положения, каждый N показывает, что какой-нибудь один из 4 углеродных атомов в положениях 1-4 и какой-нибудь один из 4 углеродных атомов в положениях 5-8 замещены атомом азота, и R34-R36 имеют такие же значения, как определено выше, положение каждого атома азота может быть в любой позиционной связи и R34 предпочтительно представляет атом водорода или атом галогена. Предпочтительно, чтобы один из R35 и R36 представлял собой атом водорода или атом галогена, а другой - атом водорода, цианогруппу, атом галогена, алкильную группу, алкенильную группу, алкинильную группу или галогеналкильную группу. Особенно предпочтительно, чтобы другая группа представляла собой атом водорода, атом галогена, алкильную группу или алкинильную группу. В данном случае атом галогена предпочтительно является атомом фтора, хлора или брома. В случае алкильной группы предпочтительной является метильная группа. В случае алкинильной группы предпочтительной является этинильная группа. Положение, замещенное атомом галогена, алкильной группой или алкинильной группой, особо не ограничивается. В качестве предпочтительных примеров конкретных групп, представленных показанной выше формулой, могут быть названы
6-хлор-1,5-нафтиридин-2-ильная, 6-фтор-1,5-нафтиридин-2-ильная,
6-бром-1,5-нафтиридин-2-ильная,
6-этинил-1,5-нафтиридин-2-ильная,
7-хлор-1,5-нафтиридин-2-ильная, 7-фтор-1,5-нафтиридин-2-ильная,
7-бром-1,5-нафтиридин-2-ильная,
7-этинил-1,5-нафтиридин-2-ильная,
6-хлор-1,5-нафтиридин-3-ильная, 6-фтор-1,5-нафтиридин-3-ильная,
6-бром-1,5-нафтиридин-3-ильная,
6-этинил-1,5-нафтиридин-3-ильная,
7-хлор-1,5-нафтиридин-3-ильная, 7-фтор-1,5-нафтиридин-3-ильная,
7-бром-1,5-нафтиридин-3-ильная,
7-этинил-1,5-нафтиридин-3-ильная,
6-хлор-1,7-нафтиридин-2-ильная, 6-фтор-1,7-нафтиридин-2-ильная,
6-бром-1,7-нафтиридин-2-ильная,
6-этинил-1,7-нафтиридин-2-ильная,
6-хлор-1,7-нафтиридин-3-ильная, 6-фтор-1,7-нафтиридин-3-ильная,
6-бром-1,7-нафтиридин-3-ильная,
6-этинил-1,7-нафтиридин-3-ильная,
6-хлор-1,8-нафтиридин-2-ильная, 6-фтор-1,8-нафтиридин-2-ильная,
6-бром-1,8-нафтиридин-2-ильная,
6-этинил-1,8-нафтиридин-2-ильная,
7-хлор-1,8-нафтиридин-2-ильная, 7-фтор-1,8-нафтиридин-2-ильная,
7-бром-1,8-нафтиридин-2-ильная,
7-этинил-1,8-нафтиридин-2-ильная,
6-хлор-1,8-нафтиридин-3-ильная,
6-фтор-1,8-нафтиридин-3-ильная, 6-бром-1,8-нафтиридин-3-ильная,
6-этинил-1,8-нафтиридин-3-ильная,
7-хлор-1,8-нафтиридин-3-ильная, 7-фтор-1,8-нафтиридин-3-ильная,
7-бром-1,8-нафтиридин-3-ильная,
7-этинил-1,8-нафтиридин-3-ильная,
6-хлор-2,5-нафтиридин-3-ильная, 6-фтор-2,5-нафтиридин-3-ильная,
6-бром-2,5-нафтиридин-3-ильная,
6-этинил-2,5-нафтиридин-3-ильная,
7-хлор-2,5-нафтиридин-3-ильная, 7-фтор-2,5-нафтиридин-3-ильная,
7-бром-2,5-нафтиридин-3-ильная,
7-этинил-2,5-нафтиридин-3-ильная,
7-хлор-2,6-нафтиридин-3-ильная, 7-фтор-2,6-нафтиридин-3-ильная,
7-бром-2,6-нафтиридин-3-ильная,
7-этинил-2,6-нафтиридин-3-ильная,
6-хлор-2,8-нафтиридин-3-ильная, 6-фтор-2,8-нафтиридин-3-ильная,
6-бром-2,8-нафтиридин-3-ильная,
6-этинил-2,8-нафтиридин-3-ильная,
7-хлор-2,8-нафтиридин-3-ильная, 7-фтор-2,8-нафтиридин-3-ильная,
7-бром-2,8-нафтиридин-3-ильная и
7-этинил-2,8-нафтиридин-3-ильная группы. Особенно предпочтительные примеры конкретных групп включают
7-хлор-2,5-нафтиридин-3-ил, 7-фтор-2,5-нафтиридин-3-ил,
7-бром-2,5-нафтиридин-3-ил, 7-этинил-2,5-нафтиридин-3-ил.
Кроме описанных выше 12 групп (а)-(l), предпочтительной является тиенопирролильная группа, которая может быть замещенной. Данная группа может содержать 1-3 заместителя, и примеры заместителей включают гидроксильную группу, нитрогруппу, аминогруппу, цианогруппу, атомы галогена, алкильные группы, алкенильные группы, алкинильные группы, галогеналкильные группы, гидроксиалкильные группы, алкоксигруппы, алкоксиалкильные группы, карбоксильную группу, карбоксиалкильные группы, ацильные группы, карбамоильную группу, N-алкилкарбамоильные группы, N,N-диалкилкарбамоильные группы, алкоксикарбонильные группы, амидиногруппу и алкоксикарбонилалкильные группы. Из них предпочтительными являются цианогруппа, атомы галогена, алкильные группы, алкенильные группы, алкинильные группы и галогеналкильные группы. В качестве конкретных предпочтительных примеров таких групп можно назвать 2-хлортиено[2,3-b]пиррол-5-ильную, 2-фтортиено[2,3-b]пиррол-5-ильную, 2-бромтиено[2,3-b]пиррол-5-ильную и 2-этинилтиено[2,3-b]пиррол-5-ильную группы.
<О группе Q1>
В настоящем изобретении Q1 означает насыщенную или ненасыщенную 5- или 6-членную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной.
В качестве примеров насыщенной или ненасыщенной 5- или 6-членной циклической углеводородной группы можно назвать циклопентильную, циклопентенильную, циклогексильную, циклогексенильную и фенильную группы. Предпочтительными являются циклопентильная, циклогексильная и фенильная группы, из которых особенно предпочтительной является фенильная группа.
Насыщенная или ненасыщенная 5-7-членная гетероциклическая группа означает одновалентную гетероциклическую группу, имеющую по крайней мере один гетероатом, выбранный из атомов кислорода, серы и азота, и ее конкретные примеры могут включать фурильную, пирролильную, тиенильную, пиразолильную, имидазолильную, пиразолинильную, оксазолильную, оксазолинильную, тиазолильную, тиазолинильную, тиадиазолильную, фуразанильную, пиранильную, пиридильную, пиримидильную, пиридазинильную, пирролидинильную, пиперазинильную, пиперидинильную, оксазинильную, оксадиазинильную, морфолинильную, тиазинильную, тиадиазинильную, тиоморфолинильную, тетразолильную, триазолильную, триазинильную, азепинильную, диазепинильную и триазепинильную группы. Предпочтительными являются тиенильная, пиразолильная, имидазолильная, оксазолильная, тиазолильная, тиадиазолильная, фуразанильная, пиридильная, пиримидильная, пиридазинильная, пирролидинильная, пиперазинильная, пиперидинильная, морфолинильная, тиадиазинильная и триазолильная группы, и особенно предпочтительными являются тиенильная, тиазолильная, пиразолильная, имидазолильная, пиридильная, пиримидильная, пиридазинильная, пирролидинильная, пиперазинильная и пиперидинильная группы. Из указанных гетероциклических групп азотсодержащие гетероциклические группы могут быть в форме N-оксида.
Насыщенная или ненасыщенная бициклическая или трициклическая конденсированная углеводородная группа означает такую же насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, как определено в описании Q4 в общей формуле (1). В качестве ее конкретных примеров можно назвать инденильную, инданильную, нафтильную, тетрагидронафтильную, антрильную и фенантрильную группы, из которых предпочтительными являются инденильная, инданильная, нафтильная и тетрагидронафтильная группы.
Насыщенная или ненасыщенная бициклическая или трициклическая конденсированная гетероциклическая группа означает такую же насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, как определено в описании Q4 в общей формуле (1). В качестве ее конкретных примеров можно назвать бензофурильную, изобензофурильную,
бензотиенильную, индолильную, индолинильную, изоиндолильную,
изоиндолинильную, индазолильную, хинолильную,
дигидрохинолильную,
4-оксодигидрохинолильную (дигидрохинон-4-он),
тетрагидрохинолильную, изохинолильную, тетрагидроизохинолильную,
хроменильную, хроманильную, изохроманильную,
4Н-4-оксобензопиранильную,
3,4-дигидро-4Н-4-оксобензопиранильную, 4Н-хинолизинильную,
хиназолинильную, дигидрохиназолинильную,
тетрагидрохиназолинильную, хиноксалильную,
тетрагидрохиноксалильную, циннолинильную,
тетрагидроциннолинильную, индолизинильную,
тетрагидроиндолизинильную, бензотиазолильную,
тетрагидробензотиазолильную, бензоксазолильную,
бензизотиазолильную, бензизоксазолильную, бензимидазоильную,
нафтиридинильную, тетрагидронафтиридинильную, тиенопиридильную,
тетрагидротиенопиридильную, тиазолопиридильную,
тетрагидротиазолопиридильную, тиазолопиридазинильную,
тетрагидротиазолопиридазинильную, пирролопиридильную,
дигидропирролопиридильную, тетрагидропирролопиридильную,
пирролопиримидинильную, дигидропирролопиримидинильную,
пиридохиназолильную, дигидропиридохиназолильную,
пиридопиримидинильную, тетрагидропиридопиримидинильную,
пиранотиазолильную, дигидропиранотиазолильную, фуропиридильную,
тетрагидрофуропиридильную, оксазолопиридильную,
тетрагидрооксазолопиридильную, оксазолопиридазинильную,
тетрагидрооксазолопиридазинильную, пирролотиазолильную,
дигидропирролотиазолильную, пирролооксазолильную,
дигидропирролооксазолильную, тиенопирролильную,
тиазолопиримидинильную, дигидротиазолопиримидинильную,
4-оксотетрагидроциннолинильную, 1,2,4-бензотиадиазинильную,
1,1-диокси-2Н-1,2,4-бензотиадиазинильную,
1,2,4-бензоксадиазинильную, циклопентапиранильную,
тиенофуранильную, фуропиранильную, пиридоксазинильную,
пиразолоксазолильную, имидазотиазолильную, имидазопиридильную,
тетрагидроимидазопиридильную, пиразинопиридазинильную,
бензизохинолильную, фуроциннолильную,
пиразолотиазолопиридазинильную,
тетрагидропиразолотиазолопиридазинильную,
гексагидротиазолопиридазинопиридазинильную,
имидазотриазинильную, оксазолопиридильную, бензоксепинильную,
бензазепинильную, тетрагидробензазепинильную,
бензодиазепинильную, бензотриазепинильную, тиеноазепинильную,
тетрагидротиеноазепинильную, тиенодиазепинильную,
тиенотриазепинильную, тиазолоазепинильную,
тетрагидротиазолоазепинильную,
4,5,6,7-тетрагидро-5,6-тетраметилентиазолопиридазинильную и
5,6-триметилен-4,5,6,7-тетрагидротиазолопиридазинильную группы. Предпочтительными являются бензотиазолильная,
тетрагидробензотиазолильная, тиенопиридильная,
тетрагидротиенопиридильная, тиенопирролильная,
тиазолопиридильная, тетрагидротиазолопиридильная,
тиазолопиридазинильная, тетрагидротиазолопиридазинильная,
пирролопиримидинильная, дигидропирролопиримидинильная,
пиранотиазолильная, дигидропиранотиазолильная, фуропиридильная,
тетрагидрофуропиридильная, оксазолопиридильная,
тетрагидрооксазолопиридильная, пирролопиридильная,
дигидропирролопиридильная, тетрагидропирролопиридильная,
оксазолопиридазинильная, тетрагидрооксазолопиридазинильная,
пирролотиазолильная, дигидропирролотиазолильная,
пирролооксазолильная, дигидропирролооксазолильная,
тиазолопиримидинильная, дигидротиазолопиримидинильная,
бензазепинильная, тетрагидробензазепинильная,
тиазолоазепинильная, тетрагидротиазолоазепинильная,
тиеноазепинильная, тетрагидротиеноазепинильная,
4,5,6,7-тетрагидро-5,6-тетраметилентиазолопиридазинильная и
5,6-триметилен-4,5,6,7-тетрагидротиазолопиридазинильная группы, из которых особенно предпочтительными являются
тетрагидробензотиазолильная, тетрагидротиенопиридильная,
тетрагидротиазолопиридильная, тетрагидротиазолопиридазинильная,
дигидропирролопиримидинильная, дигидропиранотиазолильная,
тетрагидрооксазолопиридильная, дигидропирролотиазолильная,
4,5,6,7-тетрагидро-5,6-тетраметилентиазолопиридазинильная и
5,6-триметилен-4,5,6,7-тетрагидротиазолопиридазинильная группы.
Не налагается особого ограничения на форму конденсации конденсированной гетероциклической группы. Например, тиенопиридин может быть любым из тиено[2,3-b]пиридина, тиено[2,3-c]пиридина, тиено[3,2-b]пиридина, тиено[3,2-c]пиридина, тиено[3,4-b]пиридина и тиено[3,4-с]пиридина, из которых предпочтительными являются тиено[2,3-c]пиридин и тиено[3,2-c]пиридин. Тиенопирролил может быть любым из тиено[2,3-b]пирролила и тиено[3,2-b]пирролила. Тиазолопиридин может быть любым из тиазоло[4,5-b]пиридина, тиазоло[4,5-c]пиридина, тиазоло[5,4-b]пиридина, тиазоло[5,4-c]пиридина, тиазоло[3,4-а]пиридина и тиазоло[3,2-а]пиридина, из которых предпочтительными являются тиазоло[4,5-c]пиридин и тиазоло[5,4-c]пиридин. Тиазолопиридазин может быть любым из тиазоло[4,5-с]пиридазина, тиазоло[4,5-d]пиридазина, тиазоло[5,4-с]пиридазина и тиазоло[3,2-b]пиридазина, из которых предпочтительным является тиазоло[4,5-d]пиридазин. Пирролопиридин может быть любым из пирроло[2,3-b]пиридина, пирроло[2,3-c]пиридина, пирроло[3,2-b]пиридина, пирроло[3,2-c]пиридина, пирроло[3,4-b]пиридина и пирроло[3,4-с]пиридина, из которых предпочтительными являются пирроло[2,3-с]пиридин и пирроло[3,2-c]пиридин. Пирролопиримидин может быть любым из пирроло[3,4-d]пиримидина, пирроло[3,2-d]пиримидина и пирроло[2,3-d]пиримидина, из которых предпочтительным является пирроло[3,4-d]пиримидин. Пиридопиримидин может быть любым из пиридо[2,3-d]пиримидина, пиридо[3,2-d]пиримидина, пиридо[3,4-d]пиримидина, пиридо[4,3-d]пиримидина, пиридо[1,2-с]пиримидина и пиридо[1,2-а]пиримидина, из которых предпочтительными являются пиридо[3,4-d]пиримидин и пиридо[4,3-d]пиримидин. Пиранотиазол может быть любым из пирано[2,3-d]тиазола, пирано[4,3-d]тиазола, пирано[3,4-d]тиазола и пирано[3,2-d]тиазола, из которых предпочтительными являются пирано[4,3-d]тиазол и пирано[3,4-d]тиазол. Фуропиридин может быть любым из фуро[2,3-b]пиридина, фуро[2,3-c]пиридина, фуро[3,2-b]пиридина, фуро[3,2-c]пиридина, фуро[3,4-b]пиридина и фуро[3,4-с]пиридина, из которых предпочтительными являются фуро[2,3-c]-пиридин и фуро[3,2-с]пиридин. Оксазолопиридин может быть любым из оксазоло[4,5-b]пиридина, оксазоло[4,5-c]пиридина, оксазоло[5,4-b]пиридина, оксазоло[5,4-c]пиридина, оксазоло[3,4-а]пиридина и оксазоло[3,2-а]пиридина, из которых предпочтительными являются оксазоло[4,5-c]пиридин и оксазоло[5,4-с]пиридин. Оксазолопиридазин может быть любым из оксазоло[4,5-с]пиридазина, оксазоло[4,5-d]пиридазина, оксазоло[5,4-с]пиридазина и оксазоло[3,4-b]пиридазина, из которых предпочтительным является оксазоло[4,5-d]пиридазин. Пирролотиазол может быть любым из пирроло[2,1-b]тиазола, пирроло[1,2-c]тиазола, пирроло[2,3-d]тиазола, пирроло[3,2-d]тиазола и пирроло[3,4-d]тиазола, из которых предпочтительным является пирроло[3,4-d]тиазол. Пирролооксазол может быть любым из пирроло[2,1-b]оксазола, пирроло[1,2-c]оксазола, пирроло[2,3-d]оксазола, пирроло[3,2-d]оксазола и пирроло[3,4-d]оксазола, из которых предпочтительным является пирроло[3,4-d]оксазол. Бензоазепин может быть любым из 1Н-1-бензоазепина, 1Н-2-бензоазепина и 1Н-3-бензоазепина, из которых предпочтительным является 1Н-3-бензоазепин. Тиазоло[4,5-c]азепин может быть любым из 4Н-тиазоло[4,5-c]азепина, 4Н-тиазоло[4,5-d]азепина и 4Н-тиазоло[5,4-c]азепина, из которых предпочтительным является 4Н-тиазоло[4,5-d]азепин. Тиено[2,3-c]азепин может быть любым из 4Н-тиено[2,3-d]азепина и 4Н-тиено[3,2-c]азепина, из которых предпочтительным является 4Н-тиено[2,3-d]азепин.
Из указанных гетероциклических групп азотсодержащие гетероциклические группы могут быть в форме N-оксида. Кстати, положение указанной выше замещающей группы, присоединенной к Q2, особо не ограничивается.
Каждая из описанных выше насыщенных или ненасыщенных 5- или 6-членных циклических углеводородных групп, насыщенных или ненасыщенных 5-7-членных гетероциклических групп, насыщенных или ненасыщенных бициклических или трициклических конденсированных углеводородных групп и насыщенных или ненасыщенных бициклических или трициклических конденсированных гетероциклических групп может иметь 1-3 заместителя. Примеры заместителей могут включать гидроксильную группу; атомы галогена, такие как атом фтора, атом хлора, атом брома и атом йода; галогенметильные группы, имеющие 1-3 атома галогена; аминогруппу; цианогруппу; амидиногруппу; гидроксиамидиногруппу; неразветвленные, разветвленные или циклические алкильные группы, имеющие 1-6 углеродных атомов (далее называемые как С1-С6алкильные группы, которые означают неразветвленные, разветвленные и циклические алкильные группы; например, неразветвленные или разветвленные С1-С6алкильные группы, такие как метильная группа, этильная группа, изопропильная группа и трет-бутильная группа; С3-С6циклоалкильные группы, такие как циклопропильная группа, циклобутильная группа, циклопентильная группа и 1-метилциклопропильная группа; и С3-С6циклоалкил-С1-С6алкильные группы, такие как циклопропилметильная группа); гидрокси-С1-С6алкильные группы (такие как гидроксиэтильная и 1,1-диметил-2-гидроксиэтильные группы); С1-С6алкоксигруппы (например, метоксигруппу, этоксигруппу и тому подобное); С1-С6алкокси-С1-С6алкильные группы; карбоксильную группу; С2-С6карбоксиалкильные группы (например, карбоксиметильную группу и тому подобное); С2-С6алкоксикарбонилС1-С6алкильные группы (например, метоксикарбонилметильную группу, трет-бутоксикарбонилметильную группу и тому подобное); амидиногруппы, замещенные С2-С6алкоксикарбонильной группой; С2-С6алкенильные группы (например, винильную группу, аллильную группу и тому подобное); С2-С6алкинильные группы (например, этинильную группу, пропинильную группу и тому подобное); С2-С6алкоксикарбонильные группы (например, метоксикарбонильную группу, этоксикарбонильную группу, трет-бутоксикарбонильную группу и тому подобное); амино-С1-С6алкильные группы (например, аминометильную группу, аминоэтильную группу и тому подобное); С1-С6алкиламино-С1-С6алкильные группы (например, N-метиламинометильную группу, N-этиламинометильную группу и тому подобное); ди(С1-С6алкил)амино-С1-С6алкильные группы (например, N,N-диметиламинометильную группу, N,N-диэтиламинометильную группу, N-этил-N-метиламиноэтильную группу и тому подобное); С2-С6алкоксикарбониламино-С1-С6алкильные группы (например, метоксикарбониламиноэтильную группу, трет-бутоксикарбониламиноэтильную группу и тому подобное); С1-С6алканоильные группы (например, формильную группу, ацетильную группу, метилпропионильную группу, циклопентанкарбонильную группу и тому подобное); С1-С6алканоиламино-С1-С6алкильные группы (например, ацетиламинометильную группу и тому подобное); С1-С6алкилсульфонильные группы (например, метансульфонильную группу и тому подобное); С1-С6алкилсульфониламино-С1-С6алкильные группы (например, метансульфониламинометильную группу и тому подобное); карбамоильную группу; С1-С6алкилкарбамоильные группы (например, метилкарбамоильную группу, этилкарбамоильную группу, изопропилкарбамоильную группу, трет-бутилкарбамоильную группу и тому подобное); N,N-ди(С1-С6алкил)карбамоильные группы (например, диметилкарбамоильную группу, диэтилкарбамоильную группу, метилэтилкарбамоильную группу и тому подобное); С1-С6алкиламиногруппы (например, N-метиламиногруппу, N-этиламиногруппу и тому подобное); ди(С1-С6алкил)аминогруппы (например, N,N-диметиламиногруппу, N,N-диэтиламиногруппу, N-этил-N-метиламиногруппу и тому подобное); 5- или 6-членные гетероциклические группы, содержащие один из атомов азота, кислорода и серы или два, одинаковых или различных, из указанных атомов (например, пирролидинильную группу, пиперидинильную группу, пиперазинильную группу, морфолинильную группу, пиридильную группу, пиримидинильную группу, тетрагидропиранильную группу и тому подобное); указанные выше 5- или 6-членные гетероциклические-С1-С4алкильные группы (например, морфолинометильную группу и тому подобное); и указанные выше 5- или 6-членные гетероциклические-амино-С1-С4алкильные группы (например, N-(оксазол-2-ил)аминометильную группу и тому подобное).
В качестве конкретных примеров Q1 можно назвать бициклические гетероциклические группы, такие как
5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ильная,
4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ильная,
5-циклопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ильная,
5-карбоксиметил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ильная,
5-бутил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ильная,
5-(4-пиридил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ильная,
5-метил-4,5,6,7-тетрагидротиазоло[4,5-c]пиридин-2-ильная,
6-метил-4,5,6,7-тетрагидротиено[2,3-c]пиридин-2-ильная,
5-метил-4,5,6,7-тетрагидрооксазоло[5,4-c]пиридин-2-ильная,
5-метил-4,6-дигидро-5Н-пирроло[3,4-d]тиазол-2-ильная,
5,7-дигидро-6-метилпирроло[3,4-d]пиримидин-2-ильная,
5,6-диметил-4,5,6,7-тетрагидротиазоло[4,5-d]пиридазин-2-ильная,
5,6-диметил-4,5,6,7-тетрагидрооксазоло[4,5-d]пиридазин-2-ильная, 5-диметиламино-4,5,6,7-тетрагидробензо[d]тиазол-2-ильная,
5-(4-пиридил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ильная и
6,7-дигидро-4Н-пирано-[4,3-d]тиазол-2-ильная группы; и 5- или 6-членные гетероциклические группы, такие как пиридильные группы, такие как 4-пиридил и 2 пиридил; дигидрооксазолильные группы, такие как 4,5-дигидрооксазол-2-ил; 4-[N-(4,5-дигидрооксазол-2-ил)-N-метиламинометил]тиофен-2-ильную, 4-[N-(4,5-дигидрооксазол-2-ил)-N-метиламинометил]-3-хлортиофен-2-ильную, 5-(N-метиламинометил)тиазол-2-ильную, 5-(N-метиламинометил)тиофен-2-ильную, 5-(N,N-диметиламинометил)тиазол-2-ильную, 5-(N,N-диметиламинометил)тиофен-2-ильную и 5-(N,N-диметиламинометил)пиридин-2-ильную группы. Между прочим, Q1 не ограничивается указанными примерами.
<О группе Q2>
Группа Q2 означает одинарную связь, насыщенную или ненасыщенную 5- или 6-членную двухвалентную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную двухвалентную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной.
В группе Q2 насыщенная или ненасыщенная 5- или 6-членная двухвалентная циклическая углеводородная группа означает двухвалентную группу, образованную от насыщенного или ненасыщенного 5- или 6-членного циклического углеводорода, определенного в описании Q4 в общей формуле (1). В качестве ее конкретных примеров можно назвать циклогексиленовую, циклогексениленовую и фениленовую группы, из которых предпочтительными являются циклогексиленовая и фениленовая группы.
Насыщенная или ненасыщенная 5-7-членная двухвалентная гетероциклическая группа означает двухвалентную группу, образованную от насыщенного или ненасыщенного 5-7-членного гетероциклического кольца, определенного в описании Q4 в общей формуле (1). В качестве ее конкретных примеров можно назвать двухвалентные группы, образованные от фурана, пиррола, тиофена, пиразола, имидазола, оксазола, оксазолидина, тиазола, тиадиазола, фуразана, пирана, пиридина, пиримидина, пиридазина, пирролидина, пиперазина, пиперидина, оксазина, оксадиазина, морфолина, тиазина, тиадиазина, тиоморфолина, тетразола, триазола, триазина, азепина, диазепина и триазепина. Из них предпочтительные примеры включают двухвалентные группы, образованные от пиразола, имидазола, оксазола, тиазола, тиадиазола, фуразана, пиридина, пиримидина, пиридазина, пирролидина, пиперазина, пиперидина, триазола, триазина, азепина, диазепина и триазепина.
Насыщенная или ненасыщенная двухвалентная бициклическая или трициклическая конденсированная углеводородная группа означает двухвалентную группу, образованную от насыщенной или ненасыщенной бициклической или трициклической конденсированной углеводородной группы, определенной в описании Q4 в общей формуле (1). В качестве конкретных ее примеров можно указать двухвалентные группы, образованные от индена, индана, нафталина, тетрагидронафталина, антрацена, фенантрена и подобного. В качестве предпочтительных ее примеров можно назвать двухвалентные группы, образованные от индана и нафталина.
Насыщенная или ненасыщенная двухвалентная бициклическая или трициклическая конденсированная гетероциклическая группа означает двухвалентную группу, образованную от насыщенного или ненасыщенного бициклического или трициклического конденсированного гетероциклического кольца, определенного в описании Q4 в общей формуле (1). В качестве ее конкретных примеров можно указать двухвалентные группы, образованные от
бензофурана, бензотиофена, индола, изоиндола, индазола,
хинолина, тетрагидрохинолина, изохинолина,
тетрагидроизохинолина, хиназолина, дигидрохиназолина,
тетрагидрохиназолина, хиноксалина, тетрагидрохиноксалина,
циннолина, тетрагидроциннолина, индолизина,
тетрагидроиндолизина, бензотиазола, тетрагидробензотиазола,
нафтиридина, тетрагидронафтиридина, тиенопиридина,
тетрагидротиенопиридина, тиазолопиридина,
тетрагидротиазолопиридина, тиазолопиридазина,
тетрагидротиазолопиридазина, пирролопиридина,
дигидропирролопиридина, тетрагидропирролопиридина,
пирролопиримидина, дигидропирролопиримидина,
дигидропиридохиназолина, пиранотиазола, дигидропиранотиазола,
фуропиридина, тетрагидрофуропиридина, оксазолопиридина,
тетрагидрооксазолопиридина, оксазолопиридазина,
тетрагидрооксазолопиридазина, пирролотиазола,
дигидропирролотиазола, пирролооксазола, дигидропирролооксазола и
бензоазепина. В качестве ее предпочтительных примеров можно назвать двухвалентные группы, образованные от бензофурана, бензотиофена, индола, индазола, хинолина, изохинолина, тетрагидроизохинолина, бензотиазола, нафтиридина, тиенопиридина, тиазолопиридина, тетрагидротиазолопиридина, тиазолопиридазина, пирролопиридина, тетрагидропирролопиридина, пиридопиримидина, пиранотиазола, дигидропиранотиазола, фуропиридина, оксазолопиридина, оксазолопиридазина, пирролотиазола, дигидропирролотиазола, пирролооксазола и дигидропирролооксазола. Не налагается особого ограничения на форму конденсации конденсированной гетероциклической группы. Например, нафтиридин может быть любым из 1,5-, 1,6-, 1,7-, 1,8-, 2,6- и 2,7-нафтиридина, тиенопиридин может быть любым из
тиено[2,3-b]пиридина, тиено[2,3-c]пиридина,
тиено[3,2-b]пиридина, тиено[3,2-c]пиридина, тиено[3,4-b]пиридина
и тиено[3,4-с]пиридина, тиазолопиридин может быть любым из
тиазоло[4,5-b]пиридина, тиазоло[4,5-c]пиридина,
тиазоло[5,4-b]пиридина, тиазоло[5,4-c]пиридина,
тиазоло[3,4-а]пиридина и тиазоло[3,2-а]пиридина,
тиазолопиридазин может быть любым из тиазоло[4,5-с]пиридазина,
тиазоло[4,5-d]пиридазина, тиазоло[5,4-с]пиридазина и
тиазоло[3,2-b]пиридазина, пирролопиридин может быть любым из
пирроло[2,3-b]пиридина, пирроло[2,3-c]пиридина,
пирроло[3,2-b]пиридина, пирроло[3,2-c]пиридина,
пирроло[3,4-b]пиридина и пирроло[3,4-с]пиридина,
пирролопиримидин может быть любым из пирроло[3,4-d]пиримидина,
пирроло[3,2-d]пиримидина и пирроло[2,3-d]пиримидина,
пиридопиримидин может быть любым из пиридо[2,3-d]пиримидина,
пиридо[3,2-d]пиримидина и пиридо[3,4-d]пиримидина, пиранотиазол
может быть любым из пирано[2,3-d]тиазола, пирано[4,3-d]тиазола,
пирано[3,4-d]тиазола и пирано[3,2-d]тиазола, фуропиридин может быть любым из фуро[2,3-b]пиридина, фуро[2,3-c]пиридина,
фуро[3,2-b]пиридина, фуро[3,2-c]пиридина, фуро[3,4-b]пиридина и
фуро[3,4-с]пиридина, оксазолопиридин может быть любым из
оксазоло[4,5-b]пиридина, оксазоло[4,5-c]пиридина,
оксазоло[5,4-b]пиридина, оксазоло[5,4-c]пиридина,
оксазоло[3,4-а]пиридина и оксазоло[3,2-а]пиридина,
оксазолопиридазин может быть любым из оксазоло[4,5-с]пиридазина,
оксазоло[4,5-d]пиридазина, оксазоло[5,4-с]пиридазина и
оксазоло[3,4-b]пиридазина, пирролотиазол может быть любым из
пирроло[2,1-b]тиазола, пирроло[1,2-c]тиазола,
пирроло[3,2-d]тиазола и пирроло[3,4-d]тиазола и пирролооксазол
может быть любым из пирроло[2,1-b]оксазола,
пирроло[1,2-c]оксазола, пирроло[2,3-d]оксазола,
пирроло[3,2-d]оксазола и пирроло[3,4-d]оксазола. Допустимы и иные, чем указанные, формы конденсации.
Каждая из описанных выше насыщенных или ненасыщенных 5- или 6-членных двухвалентных циклических углеводородных групп, насыщенных или ненасыщенных 5-7-членных двухвалентных гетероциклических групп, насыщенных или ненасыщенных двухвалентных бициклических или трициклических конденсированных углеводородных групп и насыщенных или ненасыщенных двухвалентных бициклических или трициклических конденсированных гетероциклических групп может иметь 1-3 заместителя. Примеры заместителей могут включать гидроксильную группу, атомы галогена, такие как атомы фтора, хлора, брома и йода, галогеналкильные группы, имеющие 1-3 атома галогена, аминогруппу, цианогруппу, аминоалкильные группы, амидиногруппу, гидроксиамидиногруппу, неразветвленные, разветвленные или циклические алкильные группы, имеющие 1-6 углеродных атомов (например, метильную группу, этильную группу и т.д.), неразветвленные, разветвленные или циклические алкоксигруппы, имеющие 1-6 углеродных атомов (например, метоксигруппу, этоксигруппу и т.д.), амидиногруппу, замещенную неразветвленными, разветвленными или циклическими алкоксикарбонильными группами, имеющими 2-7 углеродных атомов (например, метоксикарбониламидиногруппу, этоксикарбониламидиногруппу и т.д.), неразветвленные, разветвленные или циклические алкенильные группы, имеющие 2-6 углеродных атомов (например, винильную группу, аллильную группу и т.д.), неразветвленные или разветвленные алкинильные группы, имеющие 2-6 углеродных атомов (например, этинильную группу, пропинильную группу и т.д.), неразветвленные, разветвленные или циклические алкоксикарбонильные группы, имеющие 2-6 углеродных атомов (например, метоксикарбонильную группу, этоксикарбонильную группу и т.д.), и карбамоильную группу.
Предпочтительными группами в описанном выше Q2 являются одинарная связь, насыщенная или ненасыщенная 5- или 6-членная двухвалентная циклическая углеводородная группа, которая может быть замещенной, насыщенная или ненасыщенная 5-7-членная двухвалентная гетероциклическая группа, которая может быть замещенной, и насыщенная или ненасыщенная двухвалентная бициклическая или трициклическая конденсированная гетероциклическая группа, которая может быть замещенной. Особенно предпочтительными являются одинарная связь, насыщенные или ненасыщенные двухвалентные 5- или 6-членные циклические углеводородные группы, насыщенные или ненасыщенные 5-7-членные двухвалентные гетероциклические группы.
Когда Q1 представляет насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной, группа Q2 предпочтительно является одинарной связью. То, что Q2 представляет одинарную связь в описанной выше комбинации, означает, что общая формула (1):
Q1-Q2-Т0-N(R1)-Q3-N(R2)-Т1-Q4, (1)
где R1, R2, Q1, Q2, Q3, Q4, Т0 и Т1 имеют такие же значения, как определено выше, принимает вид следующей общей формулы (1'):
Q1-Т0-N(R1)-Q3-N(R2)-Т1-Q4, (1')
где Q1 представляет указанную бициклическую или трициклическую конденсированную углеводородную группу или бициклическую или трициклическую конденсированную гетероциклическую группу, и R1, R2, Q3, Q4, Т0 и Т1 имеют такие же значения, как определено выше.
В частности, предпочтительными являются те соединения, в которых группа Q1 представляет собой тиенопиридильную группу, которая может быть замещенной, тетрагидротиенопиридильную группу, которая может быть замещенной, тиазолопиридильную группу, которая может быть замещенной, тетрагидротиазолопиридильную группу, которая может быть замещенной, тиазолопиридазинильную группу, которая может быть замещенной, тетрагидротиазолопиридазинильную группу, которая может быть замещенной, пиранотиазолильную группу, которая может быть замещенной, дигидропиранотиазолильную группу, которая может быть замещенной, фуропиридильную группу, которая может быть замещенной, тетрагидрофуропиридильную группу, которая может быть замещенной, оксазолопиридильную группу, которая может быть замещенной, тетрагидрооксазолопиридильную группу, которая может быть замещенной, пирролопиридильную группу, которая может быть замещенной, дигидропирролопиридильную группу, которая может быть замещенной, тетрагидропирролопиридильную группу, которая может быть замещенной, пирролопиримидильную группу, которая может быть замещенной, дигидропирролопиримидильную группу, которая может быть замещенной, оксазолопиридазинильную группу, которая может быть замещенной, тетрагидрооксазолопиридазинильную группу, которая может быть замещенной, пирролотиазолильную группу, которая может быть замещенной, дигидропирролотиазолильную группу, которая может быть замещенной, пирролооксазолильную группу, которая может быть замещенной, дигидропирролооксазолильную группу, которая может быть замещенной, бензотиазолильную группу, которая может быть замещенной, тетрагидробензотиазолильную группу, которая может быть замещенной, тиазолопиримидинильную группу, которая может быть замещенной, дигидротиазолопиримидинильную группу, которая может быть замещенной, бензоазепинильную группу, которая может быть замещенной, тетрагидробензоазепинильную группу, которая может быть замещенной, тиазолоазепинильную группу, которая может быть замещенной, тетрагидротиазолоазепинильную группу, которая может быть замещенной, тиеноазепинильную группу, которая может быть замещенной, тетрагидротиеноазепинильную группу, которая может быть замещенной, 4,5,6,7-тетрагидро-5,6-тетраметилентиазолопиридазинильную группу, которая может быть замещенной, или 5,6-триметилен-4,5,6,7-тетрагидротиазолопиридазинильную группу, которая может быть замещенной, и Q2 представляет одинарную связь.
Когда Q1 представляет насыщенную или ненасыщенную 5- или 6-членную циклическую углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную 5-7-членную гетероциклическую группу, которая может быть замещенной, группа Q2 предпочтительно представляет насыщенную или ненасыщенную 5- или 6-членную двухвалентную циклическую углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную 5-7-членную двухвалентную гетероциклическую группу, которая может быть замещенной. В качестве предпочтительных примеров группы Q1-Q2 можно указать такие группы, как
4-(4-пиридил)фенильная, 4-(2-пиридил)фенильная,
5-(4-пиридил)тиазолильная, 1-(4-пиридил)пиперидильная,
4-(4-пиридил)пиперидильная,
4-гидрокси-1-(4-пиридил)пиперидин-4-ильная, бифенилильная,
4-(2-аминосульфонилфенил)фенильная, 4-(2-амидинофенил)фенильная,
4-(2-метилсульфонилфенил)фенильная,
4-(2-аминометилфенил)фенильная, 4-(2-карбамоилфенил)фенильная,
4-(2-имидазолил)фенильная, 4-(1-метил-2-имидазолил)фенильная,
4-(2,3,4,5-тетрагидропиримидин-2-ил)фенильная,
4-(1-метил-2,3,4,5-тетрагидропиримидин-2-ил)фенильная,
4-(5-тетразолил)фенильная, 1-(4-пиридил)пиперидин-4-ильная,
3-(4-пиперидил)изоксазолин-5-ильная,
3-(4-амидинофенил)изоксазолин-5-ильная,
3-(4-пиперидил)изоксазолидин-5-ильная,
3-(4-амидинофенил)изоксазолидин-5-ильная,
2-(4-пиперидил)-1,3,4-тиадиазол-5-ильная,
2-(4-аминофенил)-1,3,4-оксадиазол-5-ильная,
4-(4-пиперидил)пиперидин-1-ильная,
4-(4-пиперидил)пиперазин-1-ильная,
4-(4-пиперазинил)пиперазин-1-ильная,
1-(4-пиримидинил)пиперидин-1-ильная,
1-(2-метилпиримидин-4-ил)пиперидин-4-ильная,
1-(4-пиримидинил)пирролидин-3-ильная,
1-(4-метилпиримидин-6-ил)пиперазин-4-ильная,
1-(2-метилпиримидин-4-ил)пирролидин-4-ильная,
1-(6-хлорпиримидин-4-ил)пиперидин-4-ильная,
5-(4-хлорфенил)тиофен-2-ильная, 2-(4-хлорфенил)тиазол-4-ильная,
3-(4-хлорфенил)-1Н-пиррол-2-ильная, 4-(4-пиримидинил)фенильная и
4-(4-имидазолил)фенильная группы.
<О группе Q3>
Группа Q3 представляет следующую группу:
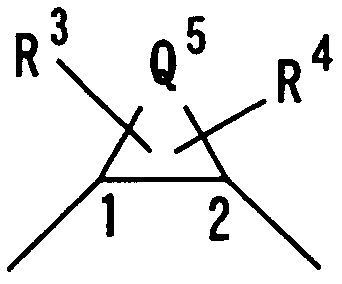
где Q5 означает алкиленовую группу, имеющую 1-8 углеродных атомов, алкениленовую группу, имеющую 2-8 углеродных атомов, или группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, ―NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-, цифры 1 и 2 указывают положения и R3 и R4 являются заместителями у углеродного атома(ов), атома(ов) азота или атомов серы кольца, содержащего Q5, и независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу, алкенильную группу, алкинильную группу, атом галогена, галогеналкильную группу, цианогруппу, цианоалкильную группу, аминогруппу, аминоалкильную группу, N-алкиламиноалкильную группу, N,N-диалкиламиноалкильную группу, ацильную группу, ацилалкильную группу, ациламиногруппу, которая может быть замещенной, алкоксииминогруппу, гидроксииминогруппу, ациламиноалкильную группу, алкоксигруппу, алкоксиалкильную группу, гидроксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, алкоксикарбонильную группу, алкоксикарбонилалкильную группу, алкоксикарбонилалкиламиногруппу, карбоксиалкиламиногруппу, алкоксикарбониламиногруппу, алкоксикарбониламиноалкильную группу, карбамоильную группу, N-алкилкарбамоильную группу, которая может содержать заместитель в алкильной группе, N,N-диалкилкарбамоильную группу, которая может иметь заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильную группу, N-алкенилкарбамоилалкильную группу, N-алкенил-N-алкилкарбамоильную группу, N-алкенил-N-алкилкарбамоилалкильную группу, N-алкоксикарбамоильную группу, N-алкил-N-алкоксикарбамоильную группу, N-алкоксикарбамоилалкильную группу, N-алкил-N-алкоксикарбамоилалкильную группу, карбазоильную группу, которая может быть замещенной 1-3 алкильными группами, алкилсульфонильную группу, алкилсульфонилалкильную группу, 3-6-членную гетероциклическую карбонильную группу, которая может быть замещенной, карбамоилалкильную группу, N-алкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), карбамоилоксиалкильную группу, N-алкилкарбамоилоксиалкильную группу, N,N-диалкилкарбамоилоксиалкильную группу, 3-6-членную гетероциклическую карбонилалкильную группу, которая может быть замещенной, 3-6-членную гетероциклическую карбонилоксиалкильную группу, которая может быть замещенной, арильную группу, аралкильную группу, гетероарильную группу, гетероарилалкильную группу, алкилсульфониламиногруппу, арилсульфониламиногруппу, алкилсульфониламиноалкильную группу, арилсульфониламиноалкильную группу, алкилсульфониламинокарбонильную группу, арилсульфониламинокарбонильную группу, алкилсульфониламинокарбонилалкильную группу, арилсульфониламинокарбонилалкильную группу, оксогруппу, карбамоилоксигруппу, аралкилоксигруппу, карбоксиалкилоксигруппу, ацилоксигруппу, ацилоксиалкильную группу, арилсульфонильную группу, алкоксикарбонилалкилсульфонильную группу, карбоксиалкилсульфонильную группу, алкоксикарбонилацильную группу, алкоксиалкилоксикарбонильную группу, гидроксиацильную группу, алкоксиацильную группу, галогенацильную группу, карбоксиацильную группу, аминоацильную группу, ацилоксиацильную группу, ацилоксиалкилсульфонильную группу, гидроксиалкилсульфонильную группу, алкоксиалкилсульфонильную группу, 3-6-членную гетероциклическую сульфонильную группу, которая может быть замещенной, N-алкиламиноацильную группу, N,N-диалкиламиноацильную группу, N,N-диалкилкарбамоилацильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкилсульфонильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), алкилсульфонилацильную группу, аминокарботиоильную группу, N-алкиламинокарботиоильную группу, N,N-диалкиламинокарботиоильную группу или алкоксиалкил(тиокарбонильную) группу или R3 и R4 вместе друг с другом означают алкиленовую группу, имеющую 1-5 углеродных атомов, алкениленовую группу, имеющую 2-5 углеродных атомов, алкилендиоксигруппу, имеющую 1-5 углеродных атомов, или карбонилдиоксигруппу.
Следующая группа описана далее подробно:

где Q5, R3 и R4 имеют такие же значения, как определено выше, и цифры 1 и 2 указывают положения.
Часть циклической структуры, содержащей группу Q5, представляет 3-10-членную двухвалентную циклическую углеводородную группу, которая может иметь двойную связь, или 5-12-членную двухвалентную гетероциклическую группу, содержащую 1 или 2 гетероатома, предпочтительно 3-8-членную двухвалентную циклическую углеводородную группу или 5-8-членную двухвалентную гетероциклическую группу, и более предпочтительно 5-7-членную двухвалентную циклическую углеводородную группу или 5-7-членную двухвалентную гетероциклическую группу. Из них предпочтительной является группа, в которой Q5 является алкиленовой группой, имеющей 3-6 углеродных атомов, или группой -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или 1 и А имеет такие же значения, как определено выше. Особенно предпочтительной является группа, в которой Q5 представляет алкиленовую группу, имеющую 4 углеродных атома.
Указанная циклическая углеводородная группа или гетероциклическая группа может иметь структуру как цис-, так и транс-формы относительно положения 1 и положения 2. Однако в случае 5-членного кольца предпочтительной является транс-форма, а в случае 6- или 7-членного кольца предпочтительными являются и цис-форма, и транс-форма.
Далее заместители R3 и R4 описаны подробно. Атом галогена означает атом фтора, хлора, брома или йода. Примеры алкильной группы включают неразветвленные, разветвленные или циклические С1-С6алкильные группы (например, метильную группу, циклопропильную группу, изобутильную группу и тому подобное). Примеры галогеналкильной группы включают алкильные группы, замещенные 1-3 галогенами (например, хлорметильную группу, 1-бромэтильную группу, трифторметильную группу и тому подобное). Примеры цианоалкильной группы включают С1-С6алкильные группы, замещенные цианогруппой (например, цианометильную группу, 1-цианоэтильную группу и тому подобное). Примеры алкенильной группы включают неразветвленные или разветвленные алкенильные группы, имеющие 2-6 углеродных атомов и двойную связь (например, винильную группу, аллильную группу и тому подобное). Примеры алкинильной группы включают неразветвленные или разветвленные алкинильные группы, имеющие 2-6 углеродных атомов и тройную связь (например, этинильную группу, пропинильную группу и тому подобное). Примеры ацильной группы включают С1-С6алканоильные группы (например, формильную группу, ацетильную группу и тому подобное), С7-С15ароильные группы, такие как бензоильная группа и нафтоильная группа, и арилалканоильные группы, которые являются С1-С6алканоильными группами, замещенными С6-С14арильной группой (например, фенацетильную группу и тому подобное). Примеры ацилалкильной группы включают С1-С6алкильные группы, замещенные ацильной группой (например, ацетилметильную группу и тому подобное). Примеры алкоксигруппы включают неразветвленные, разветвленные или циклические С1-С6алкоксигруппы (например, метоксигруппу, циклопропоксигруппу, изопропоксигруппу и тому подобное). Примеры алкоксиалкильной группы включают С1-С6алкильные группы, замещенные С1-С6алкоксигруппой (например, метоксиметильную группу, этоксиметильную группу и тому подобное). Примеры гидроксиалкильной группы включают С1-С6алкильные группы, замещенные гидроксильной группой (например, гидроксиметильную группу, 1-гидроксиэтильную группу и тому подобное). Примеры карбоксиалкильной группы включают С1-С6алкильные группы, замещенные карбоксильной группой (например, карбоксиметильную группу, 1-карбоксиэтильную группу и тому подобное). Примеры алкоксикарбонильной группы включают группы, состоящие из С1-С6алкоксигруппы и карбонильной группы (например, метоксикарбонильную группу, этоксикарбонильную группу и тому подобное). Примеры алкоксикарбонилалкильной группы включают С1-С6алкильные группы, замещенные С1-С6алкоксикарбонильной группой (например, метоксикарбонилэтильную группу, этоксикарбонилэтильную группу и тому подобное). Примеры карбамоилалкильной группы включают С1-С6алкильные группы, замещенные карбамоильной группой (например, карбамоилметильную группу, карбамоилэтильную группу и тому подобное).
Примеры гетероарильной группы включают такие же гетероарильные группы, как определено в описании Q4 в общей формуле (1). Примеры гетероарилалкильной группы включают С1-С6алкильные группы, замещенные гетероарильной группой (например, тиенилметильную группу, пиридилэтильную группу и тому подобное). Примеры арильной группы включают арильные группы, имеющие 6-14 углеродных атомов, такие как фенильная группа и нафтильная группа. Арильные группы могут иметь 1-3 заместителя, выбранных из С1-С6алкильных групп, С1-С6алканоильных групп, гидроксильной группы, нитрогруппы, цианогруппы, атомов галогена, С2-С6алкенильных групп, С2-С6алкинильных групп, С1-С6галогеналкильных групп, С1-С6алкоксигрупп, карбоксигруппы, карбамоильной группы, С1-С6алкоксикарбонильных групп и тому подобное. Примеры аралкильных групп включают С1-С6алкильные группы, замещенные С6-С14арильными группами (например, бензильную группу, фенетильную группу и тому подобное). Между прочим, в приведенном выше описании не налагается особого ограничения на положение замещения. Примеры ациламиногруппы, которая может быть замещенной, включают аминогруппы, замещенные С1-С6ацильной группой (например, формиламиногруппу, ацетиламиногруппу и тому подобное), и ацильные группы, имеющие 1 или несколько заместителей, выбранных из атомов галогена, гидроксильной группы, С1-С6алкоксигрупп, аминогруппы, N-С1-С6алкиламиногрупп, N,N-ди-С1-С6алкиламиногрупп, карбоксильной группы, С2-С6алкоксикарбонильных групп и тому подобное (например, 2-метоксиацетиламиногруппу, 3-аминопропиониламиногруппу и тому подобное). Примеры ациламиноалкильной группы включают С1-С6алкильные группы, замещенные С1-С6ациламиногруппой (например, формиламинометильную группу, ацетиламинометильную группу и тому подобное). Примеры аминоалкильной группы включают С1-С6алкильные группы, замещенные аминогруппой (например, аминометильную группу, 1-аминоэтильную группу и тому подобное). Примеры N-алкиламиноалкильной группы включают амино-С1-С6алкильные группы, замещенные С1-С6алкильной группой у атома азота (например, N-метиламинометильную группу, N-метиламиноэтильную группу и тому подобное). Примеры N,N-диалкиламиноалкильной группы включают амино-С1-С6алкильные группы, соответственно замещенные двумя С1-С6алкильными группами у атомов азота (например, N,N-диметиламинометильную группу, N-этил-N-метиламиноэтильную группу и тому подобное). Примеры N-алкенилкарбамоильной группы включают карбамоильные группы, замещенные неразветвленной или разветвленной С2-С6алкенильной группой (например, аллилкарбамоильную группу и тому подобное). Примеры N-алкенилкарбамоилалкильной группы включают С1-С6алкильные группы, замещенные N-С2-С6алкенилкарбамоильной группой (например, аллилкарбамоилэтильную группу и тому подобное). Примеры N-алкенил-N-алкилкарбамоильной группы включают N-С2-С6алкенилкарбамоильные группы, замещенные неразветвленной или разветвленной С1-С6алкильной группой у атома азота (например, N-аллил-N-метилкарбамоильную группу и тому подобное). Примеры N-алкенил-N-алкилкарбамоилалкильной группы включают N-С2-С6алкенилкарбамоилалкильные группы, замещенные неразветвленной или разветвленной С1-С6алкильной группой у атома азота (например, N-аллил-N-метилкарбамоилметильную группу и тому подобное). Примеры N-алкоксикарбамоильной группы включают карбамоильные группы, замещенные неразветвленной или разветвленной С1-С6алкоксигруппой (например, метоксикарбамоильную группу и тому подобное). Примеры N-алкоксикарбамоилалкильной группы включают неразветвленные или разветвленные С1-С6алкильные группы, замещенные N-С1-С6алкоксикарбамоильной группой (например, метоксикарбамоилметильную группу и тому подобное). Примеры N-алкил-N-алкоксикарбамоильной группы включают карбамоильные группы, замещенные неразветвленной или разветвленной С1-С6алкоксигруппой и С1-С6алкильной группой (например, N-этил-N-метоксикарбамоильную группу и тому подобное). Примеры N-алкил-N-алкоксикарбамоилалкильной группы включают неразветвленные или разветвленные С1-С6алкильные группы, замещенные N-С1-С6алкил-N-С1-С6алкоксикарбамоильной группой (например, N-этил-N-метоксикарбамоилметильную группу и тому подобное). Примеры карбазоильной группы, которая может быть замещенной 1-3 алкильными группами, включают карбазоильную группу, а также карбазоильные группы, замещенные 1-3 неразветвленными или разветвленными С1-С6алкильными группами (например, 1-метилкарбазоильную группу, 1,2-диметилкарбазоильную группу и тому подобное). Примеры алкилсульфонильной группы включают неразветвленные, разветвленные или циклические С1-С6алкилсульфонильные группы (например, метансульфонильную группу и тому подобное). Примеры алкилсульфонилалкильной группы включают неразветвленные или разветвленные С1-С6алкильные группы, замещенные С1-С6алкилсульфонильной группой (например, метансульфонилметильную группу и тому подобное). Примеры алкоксииминогруппы включают С1-С6алкоксииминогруппы (например, метоксииминогруппу, этоксииминогруппу и тому подобное). Примеры алкоксикарбонилалкиламиногруппы включают аминогруппы, замещенные С1-С6алкоксикарбонилалкильной группой (например, метоксикарбонилметиламиногруппу, этоксикарбонилпропиламиногруппу и тому подобное). Примеры карбоксиалкиламиногруппы включают аминогруппы, замещенные карбокси-С1-С6алкильной группой (например, карбоксиметиламиногруппу, карбоксиэтиламиногруппу и тому подобное). Примеры алкоксикарбониламиногруппы включают аминогруппы, замещенные С1-С6алкоксикарбонильной группой (например, метоксикарбониламиногруппу, трет-бутоксикарбониламиногруппу и тому подобное). Примеры алкоксикарбониламиноалкильной группы включают алкильные группы, замещенные С1-С6алкоксикарбониламиногруппой (например, метоксикарбониламинометильную группу, трет-бутоксикарбониламиноэтильную группу и тому подобное). N-алкилкарбамоильная группа, которая может иметь заместитель в алкильной группе, означает карбамоильную группу, замещенную неразветвленной, разветвленной или циклической С1-С6алкильной группой, которая может быть замещена гидроксильной группой, аминогруппой, N-С1-С6алкиламиногруппой, амидиногруппой, атомом галогена, карбоксильной группой, цианогруппой, карбамоильной группой, С1-С6алкоксигруппой, С1-С6алканоильной группой, С1-С6алканоиламиногруппой, С1-С6алкилсульфониламиногруппой или тому подобное, и ее примеры включают N-метилкарбамоильную группу, N-этилкарбамоильную группу, N-изопропилкарбамоильную группу, N-циклопропилкарбамоильную группу, N-(2-гидроксиэтил)карбамоильную группу, N-(2-фторэтил)карбамоильную группу, N-(2-цианоэтил)карбамоильную группу, N-(2-метоксиэтил)карбамоильную группу, N-карбоксиметилкарбамоильную группу, N-(2-аминоэтил)карбамоильную группу, N-(2-амидиноэтил)карбамоильную группу и тому подобное. N,N-диалкилкарбамоильная группа, которая может иметь заместитель в алкильной(ых) группе(ах), означает карбамоильную группу, замещенную 2 неразветвленными, разветвленными или циклическими С1-С6алкильными группами, которые могут быть замещенными гидроксильной группой, аминогруппой, N-С1-С6алкиламиногруппой, амидиногруппой, атомом галогена, карбоксильной группой, цианогруппой, карбамоильной группой, С1-С6алкоксигруппой, С1-С6алканоильной группой, С1-С6алканоиламиногруппой, С1-С6алкилсульфониламиногруппой или тому подобное, и ее примеры включают N,N-диметилкарбамоильную группу, N,N-диэтилкарбамоильную группу, N-этил-N-метилкарбамоильную группу, N-изопропил-N-метилкарбамоильную группу, N-(2-гидроксиэтил)-N-метилкарбамоильную группу, N,N-бис(2-гидроксиэтил)карбамоильную группу, N,N-бис(2-фторэтил)карбамоильную группу, N-(2-цианоэтил)-N-метилкарбамоильную группу, N-(2-метоксиэтил)-N-метилкарбамоильную группу, N-карбоксиметил-N-метилкарбамоильную группу, N,N-бис(2-аминоэтил)карбамоильную группу и тому подобное. Примеры N-алкилкарбамоилалкильной группы, которая может иметь заместитель в алкильной(ых) группе(ах), включают неразветвленные или разветвленные С1-С6алкильные группы, замещенные N-алкилкарбамоильной группой, которая может иметь заместитель в С1-С6алкильной группе (например, N-метилкарбамоилметильную группу, N-(2-гидроксиэтил)карбамоилметильную группу и тому подобное). Примеры N,N-диалкилкарбамоилалкильной группы, которая может иметь заместитель в алкильной(ых) группе(ах), включают неразветвленные или разветвленные С1-С6алкильные группы, замещенные N,N-диалкилкарбамоильной группой, которая может иметь заместитель в С1-С6алкильной(ых) группе(ах) (например, N,N-диметилкарбамоилметильную группу, N-(2-гидроксиэтил)-N-метилкарбамоилметильную группу и тому подобное). 3-6-Членная гетероциклическая карбонильная группа, которая может быть замещенной, представляет собой группу, состоящую из насыщенного или ненасыщенного гетероциклического кольца и карбонильной группы. Гетероциклическое кольцо означает 3-6-членное гетероциклическое кольцо, которое содержит по крайней мере 1-3 гетероатома (атом азота, атом кислорода, атом серы и т.д.). Гетероциклическое кольцо может иметь заместитель, такой как гидроксигруппа, атом галогена, аминогруппа, С1-С6алкильная группа или тому подобное. В качестве ее конкретных примеров можно назвать азиридинилкарбонильную группу, азетидинилкарбонильную группу, 3-гидроксиазетидинилкарбонильную группу, 3-метоксиазетидинилкарбонильную группу, пирролидинилкарбонильную группу, 3-гидроксипирролидинилкарбонильную группу, 3-фторпирролидинилкарбонильную группу, пиперидинилкарбонильную группу, пиперазинилкарбонильную группу, морфолинилкарбонильную группу, тетрагидропиранилкарбонильную группу, пиридилкарбонильную группу, фуроильную группу и тиофенкарбонильную группу. Примеры 3-6-членной гетероциклической карбонилалкильной группы, которая может быть замещенной, включают С1-С6алкильные группы, замещенные 3-6-членной гетероциклической карбонильной группой, которая может быть замещенной (например, азетидинилкарбонилметильную группу, пирролидинилкарбонилэтильную группу и тому подобное). Примеры 3-6-членной гетероциклической карбонилоксиалкильной группы, которая может быть замещенной, включают С1-С6алкильные группы, замещенные 3-6-членной гетероциклической карбонилоксигруппой, которая состоит из 3-6-членной гетероциклической карбонильной группы и атома кислорода (например, пиперидинилкарбонилоксиэтильную группу, морфолинилкарбонилоксиметильную группу и тому подобное).
Примеры карбамоилоксиалкильной группы включают С1-С6алкильные группы, замещенные карбамоилоксигруппой, состоящей из карбамоильной группы и атома кислорода (например, карбамоилоксиметильную группу, карбамоилоксиэтильную группу и тому подобное). Примеры N-алкилкарбамоилоксиалкильной группы включают С1-С6алкильные группы, замещенные N-алкилкарбамоилоксигруппой, состоящей из N-алкилкарбамоильной группы, которая может иметь заместитель в С1-С6алкильной группе, и атома кислорода (например, N-метилкарбамоилоксиметильную группу, N-метилкарбамоилоксиэтильную группу и тому подобное). Примеры N,N-диалкилкарбамоилоксиалкильной группы включают С1-С6алкильные группы, замещенные N,N-диалкилкарбамоилоксигруппой, состоящей из N,N-диалкилкарбамоильной группы, которая может иметь заместитель в алкильной(ых) группе(ах), и атома кислорода (например, N,N-диметилкарбамоилоксиметильную группу, N-этил-N-метилкарбамоилоксиэтильную группу и тому подобное). Примеры алкилсульфониламиногруппы включают аминогруппы, замещенные алкилсульфонильной группой, имеющей С1-С6алкильную группу (например, метилсульфониламиногруппу, изопропилсульфониламиногруппу и тому подобное). Примеры арилсульфониламиногруппы включают аминогруппы, замещенные арилсульфонильной группой, имеющей арильную группу (например, фенилсульфониламиногруппу, нафтилсульфониламиногруппу и тому подобное). Примеры алкилсульфониламиноалкильной группы включают С1-С6алкильные группы, замещенные С1-С6алкилсульфониламиногруппой (например, метилсульфониламинометильную группу, метилсульфониламиноэтильную группу и тому подобное). Примеры арилсульфониламиноалкильной группы включают С1-С6алкильные группы, замещенные арилсульфониламиногруппой (например, фенилсульфониламинометильную группу, нафтилсульфониламиноэтильную группу и тому подобное). Примеры алкилсульфониламинокарбонильной группы включают группы, состоящие из С1-С6алкилсульфониламиногруппы и карбонильной группы (например, метилсульфониламинокарбонильную группу, изопропилсульфониламинокарбонильную группу и тому подобное). Примеры арилсульфониламинокарбонильной группы включают группы, состоящие из арилсульфониламиногруппы и карбонильной группы (например, фенилсульфониламинокарбонильную группу, нафтилсульфониламинокарбонильную группу и тому подобное). Примеры алкилсульфониламинокарбонилалкильной группы включают С1-С6алкильные группы, замещенные С1-С6алкилсульфониламинокарбонильной группой (например, метилсульфониламинокарбонилметильную группу, изопропилсульфониламинокарбонилметильную группу и тому подобное). Примеры арилсульфониламинокарбонилалкильной группы включают С1-С6алкильные группы, замещенные арилсульфониламинокарбонильной группой (например, фенилсульфониламинокарбонилметильную группу, нафтилсульфониламинокарбонилметильную группу и тому подобное). Ацилоксигруппа означает группу, состоящую из ацильной группы и атома кислорода (например, формилоксигруппу, ацетилоксигруппу и тому подобное). Примеры ацилоксиалкильной группы включают С1-С6алкильные группы, замещенные ацилоксигруппой (например, формилоксиметильную группу, ацетилоксиметильную группу и тому подобное). Примеры аралкилоксигруппы включают С1-С6алкоксигруппы, замещенные арильной группой (например, бензилоксигруппу, нафтилметоксигруппу и тому подобное). Примеры карбоксиалкилоксигруппы включают алкоксигруппы, замещенные карбоксильной группой (например, карбоксиметоксигруппу, карбоксиэтоксигруппу и тому подобное).
Примеры арилсульфонильной группы включают С6-С14арилсульфонильные группы (например, фенилсульфонильную группу, нафтилсульфонильную группу и тому подобное). Примеры алкоксикарбонилалкилсульфонильной группы включают группы, состоящие из С1-С6алкоксикарбонилалкильной группы и сульфонильной группы (например, метоксикарбонилэтилсульфонильную группу, этоксикарбонилэтилсульфонильную группу и тому подобное). Примеры карбоксиалкилсульфонильной группы включают группы, состоящие из карбоксиалкильной группы и сульфонильной группы (например, карбоксиметилсульфонильную группу, карбоксиэтилсульфонильную группу и тому подобное). Примеры алкоксикарбонилацильной группы включают группы, состоящие из алкоксикарбонилалкильной группы и карбонильной группы (например, метоксикарбонилметилкарбонильную группу, этоксикарбонилметилкарбонильную группу и тому подобное). Примеры алкоксиалкилоксикарбонильной группы включают алкоксикарбонильные группы, замещенные С1-С6алкоксигруппой (например, метоксиметилоксикарбонильную группу, метоксиэтилоксикарбонильную группу и тому подобное). Примеры гидроксиацильной группы включают ацильные группы (включая С1-С6алканоил и ароил), замещенные гидроксильной группой (например, гликолоильную группу, лактоильную группу, бензилоильную группу и тому подобное). Примеры алкоксиацильной группы включают ацильные группы, замещенные С1-С6алкоксигруппой (например, метоксиацетильную группу, этоксиацетильную группу и тому подобное). Примеры галогенацильной группы включают группы, состоящие из галогеналкильной группы и карбонильной группы (например, хлорметилкарбонильную группу, трифторметилкарбонильную группу и тому подобное). Примеры карбоксиацильной группы включают ацильные группы, замещенные карбоксильной группой (например, карбоксиацетильную группу, 2-карбоксипропионильную группу и тому подобное). Примеры аминоацильной группы включают ацильные группы (включая С1-С6алканоил и ароил), замещенные аминогруппой (например, аминометилкарбонильную группу, 1-аминоэтилкарбонильную группу и тому подобное). Примеры ацилоксиацильной группы включают группы, состоящие из ацилоксиалкила и карбонильной группы (например, формилоксиметилкарбонильную группу, ацетилоксиметилкарбонильную группу и тому подобное). Примеры ацилоксиалкилсульфонильной группы включают группы, состоящие из ацилоксиалкила и сульфонильной группы (например, формилоксиметилсульфонильную группу, ацетилоксиметилсульфонильную группу и тому подобное). Примеры гидроксиалкилсульфонильной группы включают группы, состоящие из С1-С6гидроксиалкильной группы и сульфонильной группы (например, гидроксиметилсульфонильную группу, 1-гидроксиэтилсульфонильную группу и тому подобное). Примеры алкоксиалкилсульфонильной группы включают группы, состоящие из С1-С6алкоксиалкильной группы и сульфонильной группы (например, метоксиметилсульфонильную группу, этоксиэтилсульфонильную группу и тому подобное). Примеры 3-6-членной гетероциклической сульфонильной группы, которая может быть замещенной, включают группы, состоящие из 3-6-членной гетероциклической группы, которая может быть замещенной, и сульфонильной группы (например, азиридинилсульфонильную группу, азетидинилсульфонильную группу, пирролидинилсульфонильную группу, пиперидилсульфонильную группу, пиперазинилсульфонильную группу, морфолинилсульфонильную группу, тетрагидропиранилсульфонильную группу и тому подобное). Примеры N-алкиламиноацильной группы включают аминоацильные группы, замещенные С1-С6алкильной группой у атома азота (например, N-метиламиноацетильную группу, N-этиламиноацетильную группу и тому подобное). Примеры N,N-диалкиламиноацильной группы включают аминоацильные группы, замещенные двумя С1-С6алкильными группами у атомов азота (например, N,N-диметиламиноацетильную группу, N-этил-N-метиламиноацетильную группу и тому подобное). Примеры N,N-диалкилкарбамоилацильной группы, которая может иметь заместитель в алкильной(ых) группе(ах), включают ацильные группы, замещенные N,N-диалкилкарбамоильной группой, которая может иметь заместитель в С1-С6алкильной(ых) группе(ах) (например, N,N-диметилкарбамоилацетильную группу, N,N-диэтилкарбамоилацетильную группу, N-этил-N-метилкарбамоилацетильную группу и тому подобное). Примеры N,N-диалкилкарбамоилалкилсульфонильной группы, которая может иметь заместитель в алкильной(ых) группе(ах), включают группы, состоящие из N,N-диалкилкарбамоильной группы, которая может иметь заместитель в С1-С6алкильной(ых) группе(ах), и сульфонильной группы (например, N,N-диметилкарбамоилметилсульфонильную группу, N-(2-гидроксиэтил)-N-метилкарбамоилметилсульфонильную группу и тому подобное). Примеры алкилсульфонилацильной группы включают ацильные группы, замещенные алкилсульфонильной группой, содержащей С1-С6алкильную группу (например, метилсульфонилацетильную группу, изопропилсульфонилацетильную группу и тому подобное).
Аминокарботиоильная группа является группой, представленной формулой -С(=S)-NH2, и N-алкиламинокарботиоильная группа означает аминотиокарбонильную группу, замещенную одной из описанных выше алкильных групп, и ее примеры включают (метиламино)карботиоильную группу, (этиламино)карботиоильную группу и тому подобное. N,N-диалкиламинокарботиоильная группа означает аминотиокарбонильную группу, замещенную двумя описанными выше алкильными группами, и ее примеры включают (диметиламино)карботиоильную группу, (диэтиламино)карботиоильную группу и (этилметиламино)карботиоильную группу. Алкоксиалкил(тиокарбонильная) группа означает группу, состоящую из описанной выше алкоксиалкильной группы и тиокарбонильной группы, и ее примеры включают 2-этоксиэтантиоильную группу и тому подобное.
Алкиленовая группа означает неразветвленную или разветвленную алкиленовую группу, имеющую 1-5 углеродных атомов, и ее примеры включают метиленовую группу, этиленовую группу, пропиленовую группу и тому подобное. Алкениленовая группа является алкениленовой группой, имеющей 2-5 углеродных атомов и двойную связь, и ее примеры включают виниленовую группу, пропениленовую группу и тому подобное. Примеры алкилендиоксигруппы включают алкилендиоксигруппы, имеющие 1-5 углеродных атомов, такие как метилендиоксигруппа, этилендиоксигруппа и пропилендиоксигруппа. Карбонилдиоксигруппа является группой, представленной формулой -О-С-(=О)-О-. Между прочим, в приведенном выше описании не налагается особого ограничения на положение замещения.
Среди указанных заместителей, представленных символами R3 и R4, предпочтительными являются атом водорода, гидроксильная группа, алкильная группа, алкенильная группа, алкинильная группа, атом галогена, галогеналкильная группа, аминогруппа, гидроксииминогруппа, алкоксииминогруппа, аминоалкильная группа, N-алкиламиноалкильная группа, N,N-диалкиламиноалкильная группа, ацильная группа, ацилалкильная группа, ациламиногруппа, которая может быть замещенной, ациламиноалкильная группа, алкоксигруппа, алкоксиалкильная группа, гидроксиалкильная группа, карбоксильная группа, карбоксиалкильная группа, алкоксикарбонильная группа, алкоксикарбонилалкильная группа, алкоксикарбониламиногруппа, алкоксикарбониламиноалкильная группа, карбамоильная группа, N-алкилкарбамоильная группа, которая может иметь заместитель в алкильной группе, N,N-диалкилкарбамоильная группа, которая может иметь заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильная группа, N-алкенилкарбамоилалкильная группа, N-алкенил-N-алкилкарбамоильная группа, N-алкенил-N-алкилкарбамоилалкильная группа, N-алкоксикарбамоильная группа, N-алкил-N-алкоксикарбамоильная группа, N-алкоксикарбамоилалкильная группа, N-алкил-N-алкоксикарбамоилалкильная группа, карбазоильная группа, которая может быть замещенной 1-3 алкильными группами, алкилсульфонильная группа, алкилсульфонилалкильная группа, 3-6-членная гетероциклическая карбонильная группа, которая может быть замещенной, 3-6-членная гетероциклическая карбонилоксиалкильная группа, которая может быть замещенной, карбамоилалкильная группа, карбамоилоксиалкильная группа, N-алкилкарбамоилоксиалкильная группа, N,N-диалкилкарбамоилоксиалкильная группа, N-алкилкарбамоилалкильная группа, которая может иметь заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильная группа, которая может иметь заместитель в алкильной(ых) группе(ах), алкилсульфониламиногруппа, алкилсульфониламиноалкильная группа, оксогруппа, ацилоксигруппа, ацилоксиалкильная группа, арилсульфонильная группа, алкоксикарбонилалкилсульфонильная группа, карбоксиалкилсульфонильная группа, алкоксикарбонилацильная группа, карбоксиацильная группа, алкоксиалкилоксикарбонильная группа, галогенацильная группа, N,N-диалкиламиноацильная группа, ацилоксиацильная группа, гидроксиацильная группа, алкоксиацильная группа, алкоксиалкилсульфонильная группа, N,N-диалкилкарбамоилацильная группа, N,N-диалкилкарбамоилалкилсульфонильная группа, алкилсульфонилацильная группа, аминокарботиоильная группа, N-алкиламинокарботиоильная группа, N,N-диалкиламинокарботиоильная группа, алкоксиалкил(тиокарбонильная) группа и тому подобное. Также предпочтительными являются алкиленовая группа, алкениленовая группа, алкилендиоксигруппа, карбонилдиоксигруппа и тому подобное, образованные заместителями R3 и R4 вместе друг с другом.
Предпочтительно, чтобы R3 был атомом водорода, а R4 одним из заместителей, указанных выше в качестве предпочтительных групп. В данном случае примеры группы, более предпочтительной в качестве R4, включают атом водорода, гидроксильную группу, алкильную группу, атом галогена, гидроксииминогруппу, N-алкиламиноалкильную группу, N,N-диалкиламиноалкильную группу, ацильную группу, ациламиногруппу, которая может быть замещенной, ациламиноалкильную группу, алкоксигруппу, алкоксиалкильную группу, гидроксиалкильную группу, карбоксильную группу, алкоксикарбонильную группу, алкоксикарбонилалкильную группу, алкоксикарбониламиногруппу, карбамоильную группу, N-алкилкарбамоильную группу, которая может иметь заместитель в алкильной группе, N,N-диалкилкарбамоильную группу, которая может иметь заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильную группу, N-алкенилкарбамоилалкильную группу, N-алкенил-N-алкилкарбамоильную группу, N-алкенил-N-алкилкарбамоилалкильную группу, N-алкоксикарбамоильную группу, N-алкил-N-алкоксикарбамоильную группу, N-алкил-N-алкоксикарбамоилалкильную группу, карбазоильную группу, которая может быть замещенной 1-3 алкильными группами, алкилсульфонильную группу, алкилсульфонилалкильную группу, 3-6-членную гетероциклическую карбонильную группу, которая может быть замещенной, 3-6-членную гетероциклическую карбонилоксиалкильную группу, которая может быть замещенной, карбамоилалкильную группу, N,N-диалкилкарбамоилоксиалкильную группу, N-алкилкарбамоилалкильную группу, которая может иметь заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильную группу, которая может иметь заместитель в алкильной(ых) группе(ах), алкилсульфониламиногруппу, алкилсульфониламиноалкильную группу,
ацилоксигруппу, арилсульфонильную группу, алкоксикарбонилалкилсульфонильную группу, карбоксиалкилсульфонильную группу, алкоксикарбонилацильную группу, карбоксиацильную группу, алкоксиалкилоксикарбонильную группу, галогенацильную группу, N,N-диалкиламиноацильную группу, ацилоксиацильную группу, гидроксиацильную группу, алкоксиацильную группу, алкоксиалкилсульфонильную группу, N,N-диалкилкарбамоилацильную группу, N,N-диалкилкарбамоилалкилсульфонильную группу, алкилсульфонилацильную группу, аминокарботиоильную группу, N-алкиламинокарботиоильную группу, N,N-диалкиламинокарботиоильную группу, алкоксиалкил(тиокарбонильную) группу и тому подобное.
Из них особенно предпочтительными примерами R4 является атом водорода, гидроксильная группа, алкильная группа, N,N-диалкиламиноалкильная группа, ациламиногруппа, которая может быть замещенной, ациламиноалкильная группа, алкоксигруппа, алкоксиалкильная группа, гидроксиалкильная группа, алкоксикарбонильная группа, алкоксикарбониламиногруппа, карбамоильная группа, N-алкилкарбамоильная группа, которая может иметь заместитель в алкильной группе, N,N-диалкилкарбамоильная группа, которая может иметь заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильная группа, N-алкенилкарбамоилалкильная группа, N-алкенил-N-алкилкарбамоильная группа, N-алкенил-N-алкилкарбамоилалкильная группа, N-алкил-N-алкоксикарбамоильная группа, карбазоильная группа, которая может быть замещена 1-3 алкильными группами, алкилсульфонильная группа, алкилсульфонилалкильная группа, 3-6-членная гетероциклическая карбонильная группа, которая может быть замещенной, N,N-диалкилкарбамоилоксиалкильная группа, N-алкилкарбамоилалкильная группа, которая может иметь заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильная группа, которая может иметь заместитель в алкильной(ых) группе(ах), алкилсульфониламиногруппа, алкилсульфониламиноалкильная группа, ацилоксигруппа, ацильная группа, алкоксиалкилоксикарбонильная группа, галогенацильная группа, N,N-диалкиламиноацильная группа, гидроксиацильная группа, алкоксиацильная группа, аминокарботиоильная группа, N-алкиламинокарботиоильная группа, N,N-диалкиламинокарботиоильная группа, алкоксиалкил(тиокарбонильная) группа и тому подобное.
В качестве конкретных предпочтительных примеров R3 и R4 можно назвать атом водорода, гидроксильную группу,
метильную группу, этильную группу, изопропильную группу,
N,N-диметиламинометильную группу,
N,N-диметиламиноэтильную группу,
N,N-диэтиламинометильную группу, ацетиламиногруппу,
метоксиацетиламиногруппу, ацетиламинометильную группу,
ацетиламиноэтильную группу, метоксигруппу, этоксигруппу,
метоксиметильную группу, метоксиэтильную группу,
гидроксиметильную группу, 2-гидроксиэтильную группу,
1-гидрокси-1-метилэтильную группу, метоксикарбонильную группу,
этоксикарбонильную группу, метоксикарбониламиногруппу,
этоксикарбониламиногруппу, N-аллилкарбамоильную группу,
N-аллилкарбамоилметильную группу,
N-аллил-N-метилкарбамоильную группу,
N-аллил-N-метилкарбамоилметильную группу,
N-метокси-N-метилкарбамоильную группу,
N,N-диметилкарбазоильную группу,
N,N,N'-триметилкарбазоильную группу, метансульфонильную группу,
метансульфонилметильную группу, этансульфонилметильную группу,
N-метилкарбамоильную группу, N-этилкарбамоильную группу,
N-пропилкарбамоильную группу, N-изопропилкарбамоильную группу, N-трет-бутилкарбамоильную группу,
N-циклопропилкарбамоильную группу,
N-циклопропилметилкарбамоильную группу,
N-(1-этоксикарбонилциклопропил)карбамоильную группу,
N-(2-гидроксиэтил)карбамоильную группу,
N-(2-фторэтил)карбамоильную группу,
N-(2-метоксиэтил)карбамоильную группу,
N-(карбоксиметил)карбамоильную группу,
N-(2-аминоэтил)карбамоильную группу,
N-(2-амидиноэтил)карбамоильную группу,
N,N-диметилкарбамоильную группу, N,N-диэтилкарбамоильную группу,
N-этил-N-метилкарбамоильную группу,
N-изопропил-N-метилкарбамоильную группу,
N-метил-N-пропилкарбамоильную группу,
N-(2-гидроксиэтил)-N-метилкарбамоильную группу,
N-(2-фторэтил)-N-метилкарбамоильную группу,
N,N-бис(2-гидроксиэтил)карбамоильную группу,
N,N-бис(2-фторэтил)карбамоильную группу,
N-(2-метоксиэтил)-N-метилкарбамоильную группу,
N-карбоксиметил-N-метилкарбамоильную группу,
N,N-бис(2-аминоэтил)карбамоильную группу,
азетидинокарбонильную группу,
3-метоксиазетидинокарбонильную группу,
3-гидроксиазетидинокарбонильную группу,
пирролидинокарбонильную группу,
3-гидроксипирролидинокарбонильную группу,
3-фторпирролидинокарбонильную группу,
3,4-диметоксипирролидинокарбонильную группу,
пиперидинокарбонильную группу, пиперазинокарбонильную группу,
морфолинокарбонильную группу,
(тетрагидропиран-4-ил)карбонильную группу, бензоильную группу,
пиридилкарбонильную группу, N-метилкарбамоилметильную группу,
N-метилкарбамоилэтильную группу,
N-этилкарбамоилметильную группу,
N-(2-фторэтил)карбамоилметильную группу,
N-(2-метоксиэтил)карбамоилметильную группу,
N,N-диметилкарбамоилметильную группу,
N,N-диметилкарбамоилэтильную группу,
N-(2-фторэтил)-N-метилкарбамоилметильную группу,
N-(2-метоксиэтил)-N-метилкарбамоилметильную группу,
N,N-диметилкарбамоилоксиметильную группу,
2-(N-этил-N-метилкарбамоилокси)этильную группу,
метилсульфониламиногруппу, этилсульфониламиногруппу,
метилсульфониламинометильную группу,
метилсульфониламиноэтильную группу,
ацетильную группу, пропионильную группу, изобутирильную группу,
2-метоксиэтоксикарбонильную группу, трифторацетильную группу,
N,N-диметиламиноацетильную группу,
N-этил-N-метиламиноацетильную группу, гидроксиацетильную группу,
1,1-диметил-2-гидроксиэтилкарбонильную группу,
метоксиацетильную группу,
1,1-диметил-2-метоксиэтилкарбонильную группу,
аминокарботиоильную группу, (диметиламино)карботиоильную группу,
2-метоксиэтентиоильную группу и тому подобное.
Как описано выше, предпочтительно, чтобы R3 был атомом водорода, а R4 одним из указанных конкретных заместителей, предпочтительно N,N-диалкилкарбамоильной группой, которая может иметь заместитель в алкильной(ых) группе(ах), особенно предпочтительно N,N-диметилкарбамоильной группой. Однако R3 и R4 нисколько не ограничиваются указанными конкретными заместителями.
<О группе Т0>
Группа Т0 представляет карбонильную группу или тиокарбонильную группу, причем предпочтительной является карбонильная группа.
<О группе Т1>
Группа Т1 представляет карбонильную группу, сульфонильную группу, группу -С(=О)-С(=О)-N(R')-, группу -С(=S)-С(=О)-N(R')-, группу -С(=О)-С(=S)-N(R')-, группу -С(=S)-С(=S)-N(R')-, где R' означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-А1-N(R")-, где А1 означает алкиленовую группу, имеющую 1-5 углеродных атомов, которая может быть замещенной, и R" означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-NH-, группу -С(=S)-NH-, группу -С(=О)-NH-NH-, группу -С(=О)-А2-С(=О)-, где А2 означает одинарную связь или алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-А3-С(=О)-NH-, где А3 означает алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-С(=NORа)-N(Rb)-, группу -С(=S)-С(=NORа)-N(Rb)-, где Rа означает атом водорода, алкильную группу или алканоильную группу и Rb означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-N=N-, группу -С(=S)-N=N-, группу -С(=NORс)-С(=О)-N(Rd)-, где Rс означает атом водорода, алкильную группу, алканоильную, арильную или аралкильную группу и Rd означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=N-N(Rе)(Rf)-С(=О)-N(Rg)-, где Rе и Rf независимо друг от друга означают атом водорода, алкильную группу, алканоильную группу или алкил(тиокарбонильную) группу и Rg означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, или тиокарбонильную группу.
В описанной выше группе алкиленовая группа, имеющая 1-5 углеродных атомов, в А1, А2 и А3 означает неразветвленную, разветвленную или циклическую алкиленовую группу, имеющую 1-5 углеродных атомов, и ее примеры включают метиленовую, этиленовую, пропиленовую, циклопропиленовую, 1,3-циклопентиленовую группу и тому подобное. Алкильная группа в R',R", Rа, Rb, Rс, Rd, Re, Rf и Rg означает неразветвленную, разветвленную или циклическую алкильную группу, имеющую 1-6 углеродных атомов, и ее примеры включают метильную, этильную группы и тому подобное. Алкоксигруппа означает неразветвленную, разветвленную или циклическую алкоксигруппу, имеющую 1-6 углеродных атомов, и ее примеры включают метокси-, этоксигруппу и тому подобное.
В Rа, Rс, Re и Rf алканоильная группа означает группу, состоящую из неразветвленной, разветвленной или циклической алкильной группы, имеющей 1-6 углеродных атомов, и карбонильной группы, и ее примеры включают ацетильную, пропионильную группы и тому подобное.
В Rс арильная группа означает арильную группу, имеющую 6-14 углеродных атомов, и ее примеры включают фенильную, нафтильную группы и тому подобное. Аралкильная группа означает неразветвленную, разветвленную или циклическую алкильную группу, имеющую 1-6 углеродных атомов, замещенную арильной группой, имеющей 6-14 углеродных атомов, и ее примеры включают бензильную, фенетильную группы и тому подобное.
В качестве Т1 предпочтительными являются карбонильная группа, группа -С(=О)-С(=О)-N(R')-, группа -С(=S)-С(=О)-N(R')-, группа -С(=О)-С(=S)-N(R')-, группа -С(=S)-С(=S)-N(R')- и группа -С(=О)-СН2-N(R")- и особенно предпочтительными карбонильная группа, группа -С(=О)-С(=О)-N(R')-, группа -С(=S)-С(=О)-N(R')-, группа -С(=О)-С(=S)-N(R')- и группа -С(=S)-С(=S)-N(R')-.
<О группе R1 и группе R2>
R1 и R2 представляют, независимо друг от друга, атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, предпочтительно атом водорода или алкильную группу, и более предпочтительно атом водорода.
В R1 и R2 алкильная группа означает неразветвленную, разветвленную или циклическую алкильную группу, имеющую 1-6 углеродных атомов, и ее примеры включают метильную, этильную группы и тому подобное. Алкоксигруппа означает неразветвленную, разветвленную или циклическую алкоксигруппу, имеющую 1-6 углеродных атомов, и ее примеры включают метоксигруппу, этоксигруппу и тому подобное. R1 и R2 независимо друг от друга представляют предпочтительно атом водорода или алкильную группу, более предпочтительно оба представляют атом водорода.
Когда Т1 представляет карбонильную или сульфонильную группу и Q5 в группе Q3 представляет алкиленовую группу, имеющую 1-8 углеродных атомов, или алкениленовую группу, имеющую 2-8 углеродных атомов, Q4 предпочтительно представляет группу (b), (f), (g), (h), (i), (j), (k) и (l) из описанных выше 12 групп, при условии, что N в группе (f) показывает, что 2 углеродных атома кольца, замещенного R19, уже замещены атомом азота.
Когда Т1 представляет карбонильную или сульфонильную группу и Q5 в группе Q3 представляет алкиленовую группу, имеющую 1-8 углеродных атомов, или алкениленовую группу, имеющую 2-8 углеродных атомов, заместитель в группе Q5 предпочтительно представляет N-алкилкарбамоильную или N,N-диалкилкарбамоильную группу.
Когда Т1 представляет группу -С(=О)-С(=О)-N(R')-, группу -С(=S)-С(=О)-N(R')-, группу -С(=О)-С(=S)-N(R')- или группу -С(=S)-С(=S)-N(R')- и Q5 в группе Q3 представляет алкиленовую группу, имеющую 1-8 углеродных атомов, или алкениленовую группу, имеющую 2-8 углеродных атомов, Q4 предпочтительно представляет группу (i), (j) или (k) из описанных выше 12 групп.
Когда Т1 представляет группу -С(=О)-С(=О)-N(R')-, группу -С(=S)-С(=О)-N(R')-, группу -С(=О)-С(=S)-N(R')- или группу -С(=S)-С(=S)-N(R')- и Q5 в группе Q3 представляет алкиленовую группу, имеющую 1-8 углеродных атомов, или алкениленовую группу, имеющую 2-8 углеродных атомов, заместитель в группе Q5 предпочтительно представляет N-алкилкарбамоильную или N,N-диалкилкарбамоильную группу.
Особенность соединений по настоящему изобретению, представленных общей формулой (1), их солей, сольватов и N-оксидов заключается в комбинации группы Т1 и группы Q3. Комбинация грубо делится на следующие два случая (I) и (II):
(I) случай, когда Т1 представляет карбонильную, сульфонильную или тиокарбонильную группу и Q3 представляет следующую группу:

где Q5 означает группу -(СН2)m-СН2-А-СН2-(СН2)n-, в которой m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, ―NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-; и
(II) случай, когда Т1 представляет группу -С(=О)-С(=О)-N(R')-, группу -С(=S)-С(=О)-N(R')-, группу -С(=О)-С(=S)-N(R')- или группу -С(=S)-С(=S)-N(R')-, в которой R' означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, -С(=О)-А1-N(R")-, где А1 означает алкиленовую группу, имеющую 1-5 углеродных атомов, которая может быть замещенной, и R" означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-NH-, группу -С(=S)-NH-, группу -С(=О)-NH-NH-, группу -С(=О)-А2-С(=О)-, в которой А2 означает одинарную связь или алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-А3-С(=О)-NH-, в которой А3 означает алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-С(=NORа)-N(Rb)-, группу -С(=S)-С(=NORа)-N(Rb)-, в которой Rа означает атом водорода, алкильную группу или алканоильную группу и Rb означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-N-N-, группу -С(=S)-N=N-, группу -С(=NORс)-С(=О)-N(Rd)-, в которой Rс означает атом водорода, алкильную группу, алканоильную группу, арильную группу или аралкильную группу и Rd означает атом водорода, гидроксигруппу, алкильную группу или алкоксигруппу, группу -С(=N-N(Rе)(Rf)-С(=О)-N(Rg)-, в которой Rе и Rf независимо друг от друга представляют атом водорода, алкильную группу, алканоильную группу или алкил(тиокарбонильную) группу и Rg означает атом водорода, гидроксигруппу, алкильную группу или алкоксигруппу, или тиокарбонильную группу и Q3 представляет следующую группу:

где Q5 означает алкиленовую группу, имеющую 1-8 углеродных атомов, алкениленовую группу, имеющую 2-8 углеродных атомов, или группу -(СН2)m-СН2-А-СН2-(СН2)n-, в которой m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, ―NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-.
В случаях (I) и (II) в качестве предпочтительных примеров можно назвать следующие (i) и (ii) соответственно:
(i) пример, где группа R1 и группа R2 представляют, независимо друг от друга, атом водорода или алкильную группу, группа Q1 представляет насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной, группа Q2 представляет одинарную связь, группа Q5 в группе Q3 представляет группу -(СН2)m-СН2-А-СН2-(СН2)n-, в которой m и n независимо друг от друга равны 0 или 1 и А имеет такие же значения, как определено выше, группа Q4 выбрана из 9 групп (а)-(h) и (l) из описанных выше 12 групп, группа Т0 представляет карбонильную группу или тиокарбонильную группу и группа Т1 представляет карбонильную группу или сульфонильную группу; и
(ii) пример, где в общей формуле (1) группы R1 и R2 представляют, независимо друг от друга, атом водорода или алкильную группу, группа Q1 представляет насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной, группа Q2 представляет одинарную связь, группа Q5 в группе Q3 представляет алкиленовую группу, имеющую 3-6 углеродных атомов, или группу -(СН2)m-СН2-А-СН2-(СН2)n-, в которой m и n независимо друг от друга равны 0 или 1 и А имеет такие же значения, как определено выше, группа Q4 выбрана из 3 групп (i), (j) и (k) из описанных выше 12 групп, группа Т0 представляет карбонильную группу или тиокарбонильную группу и группа Т1 представляет группу -С(=О)-С(=О)-N(R')-, группу -С(=S)-С(=О)-N(R')-, группу -С(=О)-С(=S)-N(R')- или группу -С(=S)-С(=S)-N(R')-.
В соединениях по настоящему изобретению, представленных общей формулой (1), могут присутствовать стереоизомеры или оптические изомеры, произведенные от асимметрического углеродного атома. Все указанные стереоизомеры, оптические изомеры и их смеси включены в объем настоящего изобретения.
Не налагается особого ограничения на соли соединений по настоящему изобретению, представленных общей формулой (1), лишь бы они были фармацевтически приемлемыми солями. Конкретные их примеры включают соли минеральных кислот, такие как гидрохлориды, гидробромиды, гидроиодиды, фосфаты, нитраты и сульфаты; бензоаты; органические сульфонаты, такие как метансульфонаты, 2-гидроксиэтансульфонаты и п-толуолсульфонаты; и органические карбоксилаты, такие как ацетаты, пропаноаты, оксалаты, малонаты, сукцинаты, глутараты, адипаты, тартраты, малеаты, малаты и манделаты. В случае, когда соединения, представленные общей формулой (1), имеют кислотную группу, они могут быть солями ионов щелочных металлов или ионов щелочноземельных металлов. Не налагается особого ограничения на их сольваты, лишь бы они были фармацевтически приемлемыми сольватами. В качестве их конкретных примеров можно назвать гидраты и сольваты с этанолом. Когда в общей формуле (1) присутствует атом азота, такие соединения могут быть преобразованы в их N-оксиды.
Предпочтительными соединениями по настоящему изобретению являются соединения, описанные в следующих примерах, и их соли, а также следующие соединения и их соли:
1) 3-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)[1,6]нафтиридин-7-карбоксамид;
2) 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-4-фторциннолин-3-карбоксамид;
3) 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-4а,8а-дигидро-4Н-1,2,4-бензоксадиазин-3-карбоксамид;
4) N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-6-фтор-4-оксо-1,4-дигидрохинолин-2-карбоксамид;
5) 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-5-оксо-4,5-дигидро-1Н-1,3,4-бензотриазепин-2-карбоксамид;
6) 6-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-4-оксо-3,4-дигидро-2(1Н)-циннолинкарбоксамид;
7) 6-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-1,2,3,4-тетрагидрохинолин-2-карбоксамид;
8) N-{(1R,2S,5S)-2-{[3-(3-хлорфенил)-2-пропионил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид;
9) N-{(1R,2S,5S)-2-[(4-хлорбензоил)амино]-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид;
10) N-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-6-метил-5,6,7,8-тетрагидро-4Н-тиазоло[4,5-d]азепин-2-карбоксамид;
11) 5-хлор-N-[(1S,2R,4S)-4-[(диметиламино)карбонил]-2-({[5-(3-пирролидинилокси)тиазол-2-ил]карбонил}амино)циклогексил]индол-2-карбоксамид;
12) N1-(4-хлорфенил)-N2-((1S,2R)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
13) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
14) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R)-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамид;
15) N1-(4-хлорфенил)-N2-((1S,2R)-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамид;
16) N1-(5-хлорпиридин-2-ил)-N2-((1R,2R)-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклопентил)этандиамид;
17) N1-(4-хлорфенил)-N2-((1R,2R)-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклопентил)этандиамид;
18) N1-(4-хлорфенил)-N2-((1R,2R)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогептил)этандиамид;
19) N1-(5-хлорпиридин-2-ил)-N2-((1R,2R)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогептил)этандиамид;
20) N1-(5-хлорпиридин-2-ил)-N2-((1R,2R)-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогептил)этандиамид;
21) N1-(4-хлорфенил)-N2-((1R,2R)-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогептил)этандиамид;
22) N1-(5-хлор-6-метилпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
23) N1-(5-хлор-3-метилпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
24) N1-(5-хлор-4-метилпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
25) N1-(4-хлор-3-гидроксифенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
26) N1-(4-хлор-2-гидроксифенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
27) N1-[4-хлор-2-(фторметил)фенил]-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
28) N1-[4-хлор-2-(метоксиметил)фенил]-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
29) N-{(1R,2S,5S)-2-({[1-(4-хлоранилино)циклопропил]карбонил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
30) N1-(5-хлорпиридин-2-ил)-N2-((1R,2R,4R)-4-(гидроксиметил)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклопентил)этандиамид;
31) N1-(5-хлорпиридин-2-ил)-N2-((1R,2R,4S)-4-(гидроксиметил)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклопентил)этандиамид;
32) N1-((3R,4S)-1-ацетил-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)-N2-(5-хлорпиридин-2-ил)этандиамид;
33) N1-(5-хлорпиридин-2-ил)-N2-((3R,4S)-1-(метилсульфонил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамид;
34) N1-{(1S,2R,4S)-2-{[(3-хлорбензотиофен-2-ил)карбонил]амино}-4-[(диметиламино)карбонил]циклогексил)-N2-(5-хлорпиридин-2-ил)этандиамид;
35) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карботиоил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
36) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карботиоил]амино}циклогексил)этандиамид;
37) N1-(5-хлорпиридин-2-ил)-N2-((3R,4S)-1-(2-метоксиэтантиоил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамид;
38) N1-(5-хлорпиридин-2-ил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карботиоил]амино}пиперидин-4-ил)этандиамид;
39) N-[(3R,4S)-4-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоэтантиоил}амино)-1-(2-метоксиацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
40) N-[(3R,4S)-4-({2-[(5-хлорпиридин-2-ил)амино]-2-тиоксоацетил}амино)-1-(2-метоксиацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
41) N1-(4-хлорфенил)-N2-((3R,4S)-1-(2-метоксиэтантиоил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамид;
42) N1-(4-хлорфенил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карботиоил]амино}пиперидин-4-ил)этандиамид;
43) N-[(3R,4S)-4-({2-[(4-хлоранилино)-2-оксоэтантиоил]амино}-1-(2-метоксиацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
44) N-[(3R,4S)-4-({2-[(4-хлорфенил)амино]-2-тиоксоацетил}амино)-1-(2-метоксиацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
45) N1-((1S,2R,4S)-4-(1-азетидинилкарбонил)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)-N2-(5-хлорпиридин-2-ил)этандиамид;
46) N1-(5-хлорпиридин-2-ил)-N2-[(1S,2R,4S)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}-4-(1-пирролидинилкарбонил)циклогексил]этандиамид;
47) N1-(5-хлорпиридин-2-ил)-N2-[(1S,2R,4S)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}-4-(1-пиперидинилкарбонил)циклогексил]этандиамид;
48) N1-(5-хлорпиридин-2-ил)-N2-[(1S,2R,4S)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}-4-(4-морфолинилкарбонил)циклогексил]этандиамид;
49) N1-(5-хлорпиридин-2-ил)-N2-[(1S,2R,4S)-4-[(метиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил]этандиамид;
50) N1-{(1R,2S,5S)-2-({2-[(6-хлорпиридазин-3-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
51) N1-(4-бромфенил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамид;
52) N1-(5-хлорпиридин-2-ил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[4-(пиридин-4-ил)бензоил]амино}пиперидин-4-ил)этандиамид;
53) N1-(5-хлорпиридин-2-ил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-({[2-(пиридин-4-ил)пиримидин-5-ил]карбонил}амино)пиперидин-4-ил)этандиамид;
54) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-({[2-(пиридин-4-ил)пиримидин-5-ил]карбонил}амино)циклогексил)этандиамид;
55) N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-2-оксоэтан(метокси)имидоил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
56) N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-2-(метоксиимино)ацетил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
57) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(4,4,5-триметил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамид;
58) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(4,4-этилен-5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамид;
59) N-{(1R,2S,5S)-2-{[(Е)-2-(4-хлорфенил)этенил]сульфонил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
60) N-{(1R,2S,5S)-2-{[(4-хлорбензил)сульфонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
61) N-{(1R,2S,5S)-2-[(2-{[(4-хлорфенил)сульфонил]амино}ацетил)амино]-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
62) N-{(1R,2S,5S)-2-({2-[(5-хлорпиримидин-2-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
63) N-{(1R,2S,5S)-2-({2-[(5-хлорпиразин-2-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
64) N-[(1R,2S,5S)-5-[(диметиламино)карбонил]-2-({2-[(5-фтор-2-тиенил)амино]-2-оксоэтантиоил}амино)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
65) N-{(1R,2S,5S)-2-{[2-(3-амино-4-хлоранилино)-2-оксоэтантиоил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
66) N1-(4-хлортиазол-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
67) N1-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)-N2-(3-фторфенил)этандиамид;
68) N1-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)-N2-фенилэтандиамид;
69) N1-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)-N2-(пиридин-2-ил)этандиамид;
70) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5,6,6-триметил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамид;
71) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(4,4,5,6,6-пентаметил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамид;
72) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(2-метил-2,3-дигидротиазоло[5,4-d]изоксазол-5-ил)карбонил]амино}циклогексил)этандиамид;
73) N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(2-метил-2,3-дигидротиазоло[4,5-d]изоксазол-5-ил)карбонил]амино}циклогексил)этандиамид;
74) N1-(5-хлор-2-фурил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
75) N1-(5-хлороксазол-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
76) N1-(5-хлор-1Н-имидазол-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид;
77) N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-1-этоксиимино-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
78) N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-1-феноксиимино-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
79) N-{(1R,2S,5S)-2-{[1-бензилоксиимино-2-(4-хлоранилино)-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
80) N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-1-гидразоно-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
81) N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-1-(2-метилгидразоно)-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
82) N-{(1R,2S,5S)-2-({2-(5-хлорпиридин-2-ил)амино}-1-(2,2-диметилгидразоно)-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
83) N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-1-метилимино-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
84) N-{(1R,2S,5S)-2-{[1-(2-ацетилгидразоно)-2-(4-хлоранилино)-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид;
85) N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-1-[(2-этантиоилгидразоно)-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид; и
86) N-{(1R,2S,5S)-2-{[(Е)-3-(5-хлорпиридин-2-ил)-2-пропеноил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамид.
Ниже описаны способы получения производных (1) диамина по настоящему изобретению.
[Способ 1 получения]
Соединение, представленное общей формулой (1), его соль, сольват или N-оксид можно получить, например, следующим способом:
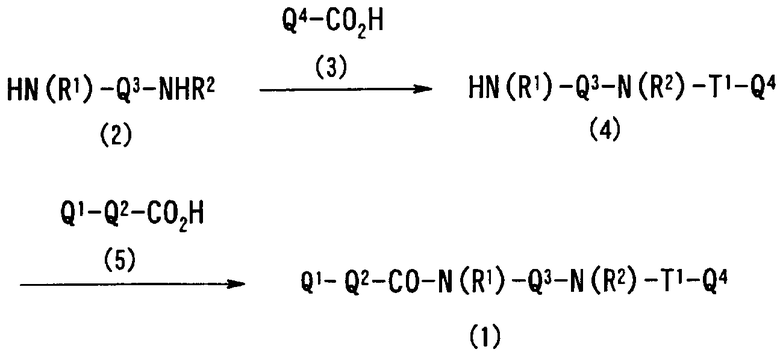
где Q1, Q2, Q3, Q4, R1 и R2 имеют такие же значения, как определено выше, и Т1 представляет карбонильную группу.
Смешанный ангидрид кислоты, галогенангидрид, активированный сложный эфир или тому подобное, являясь производным карбоновой кислоты (3), может при взаимодействии с диамином (2) давать соединение (4). Полученное соединение (4) может, взаимодействуя с карбоновой кислотой (5) в тех же самых условиях, давать соединение (1) по настоящему изобретению. На описанных выше стадиях можно использовать реагенты и условия, обычно используемые в синтезе пептидов. Смешанный ангидрид кислоты может быть получен, например, взаимодействием хлорформиата, такого как этилхлорформиат или изобутилхлорформиат, с карбоновой кислотой (3) в присутствии основания. Галогенангидрид может быть получен обработкой карбоновой кислоты (3) галогенангидридом, таким как тионилхлорид или оксалилхлорид. Активированный сложный эфир включает различные виды сложных эфиров. Такой эфир может быть получен, например, взаимодействием фенола, такого как п-нитрофенол, N-гидроксибензотриазол или N-гидроксисукцинимид, с карбоновой кислотой (3) с использованием конденсирующего агента, такого как N,N'-дициклогексилкарбодиимид или гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида. Активированный сложный эфир может быть также получен взаимодействием карбоновой кислоты (3) с пентафторфенилтрифторацетатом или подобным, взаимодействием карбоновой кислоты (3) с гексафторфосфитом 1-бензотриазолилокситрипирролидинофосфония, взаимодействием карбоновой кислоты (3) с диэтилцианофосфонатом (метод Shioiri), взаимодействием карбоновой кислоты (3) с трифенилфосфином и 2,2'-дипиридилдисульфидом (метод Mukaiyama) или подобным. Полученный таким образом смешанный ангидрид кислоты, галогенангидрид или активированный сложный эфир карбоновой кислоты (3) может, взаимодействуя с диамином (2) при (-78°C)-(150°C) в присутствии подходящего основания в инертном растворителе, давать соединение (4). Полученное соединение (4) может взаимодействовать со смешанным ангидридом, галогенангидридом или активированным сложным эфиром карбоновой кислоты (5) в тех же самых условиях с получением соединения (1) по настоящему изобретению. Реагенты и условия реакции при взаимодействии соединения (4) с карбоновой кислотой (5) такие же, как при взаимодействии диамина (2) с карбоновой кислотой (3).
В качестве конкретных примеров основания, используемого на каждой из описанных выше стадий, можно назвать карбонаты щелочных или щелочноземельных металлов, такие как карбонат натрия и карбонат калия, алкоксиды щелочных металлов, такие как этоксид натрия и бутоксид калия, гидроксиды щелочных металлов, такие как гидроксид натрия и гидроксид калия, и гидриды щелочных или щелочноземельных металлов, такие как гидрид натрия и гидрид калия; металлоорганические основания, примерами которых являются алкиллитий, такой как н-бутиллитий, и диалкиламинолитий, такой как диизопропиламид лития; металлоорганические основания, примером которых является бис(силил)амин, такой как бис(триметилсилил)амид лития; и органические основания, такие как пиридин, 2,6-лутидин, коллидин, 4-диметиламинопиридин, триэтиламин, N-метилморфолин, диизопропилэтиламин и диазабицикло[5.4.0]ундец-7-ен (DBU).
Примеры инертного растворителя, используемого в данной реакции, включают растворители типа алкилгалогенида, такие как дихлорметан, хлороформ и тетрахлорид углерода, растворители типа простого эфира, такие как тетрагидрофуран, 1,2-диметоксиэтан и диоксан, ароматические растворители, такие как бензол и толуол, и амидные растворители, такие как N,N-диметилформамид, N,N-диметилацетамид и N-метилпирролидин-2-он. Кроме указанных растворителей в некоторых случаях можно использовать сульфоксидный растворитель, такой как диметилсульфоксид или сульфолан, кетонный растворитель, такой как ацетон или метилэтилкетон, или тому подобное.
[Способ 2 получения]
Соединение (1) по настоящему изобретению может быть получено также следующим способом:
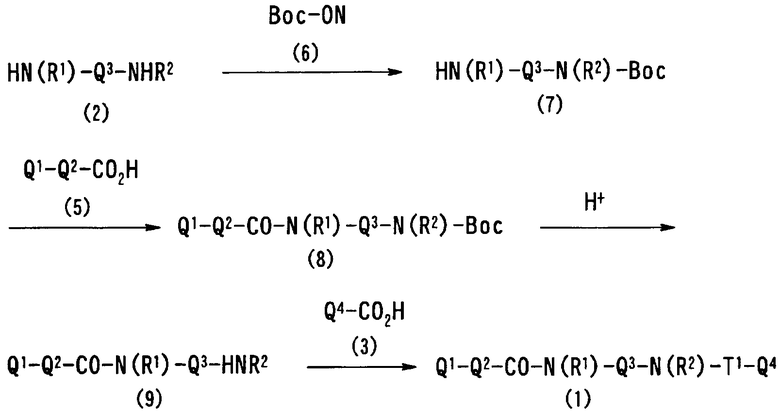
где Q1, Q2, Q3, Q4, R1 и R2 имеют такие же значения, как определено выше, Т1 представляет карбонильную группу, Boc представляет трет-бутоксикарбонильную группу и Boc-ON представляет 2-(трет-бутоксикарбонилоксиимино)-2-фенилацетонитрил.
Как описано выше, диамин (2) обрабатывают, используя Boc-ON, (6), с получением соединения (7), в котором одна из двух аминогрупп защищена трет-бутоксикарбонильной группой. Полученное соединение (7), взаимодействуя с карбоновой кислотой (5), дает соединение (8). Соединение (8) затем обрабатывают кислотой с получением соединения (9). Затем соединение (9), взаимодействуя с карбоновой кислотой (3), дает соединение (1) по настоящему изобретению. Соединение (7) может быть получено проведением реакции при температуре от -10°C до 40°C в присутствии триэтиламина в растворителе, таком как дихлорметан. Взаимодействие соединения (7) со смешанным ангидридом, галогенангидридом или активированным эфиром карбоновой кислоты (5) осуществляют с использованием таких же реагентов и условий реакции, как описано в способе 1 получения, в результате чего может быть получено соединение (8). Полученное соединение (8) обрабатывают трифторуксусной кислотой или подобным при температуре от -20°C до 70°C, в результате чего может быть получен амин (9). При взаимодействии полученного амина (9) с карбоновой кислотой (3) могут быть использованы такие же реагенты и условия, как описано в способе 1 получения.
Между прочим, трет-бутоксикарбонильная группа соединения (7) может быть заменена другими аминозащитными группами. В этом случае реагент (6) также заменяют другими реагентами, при этом необходимо использовать соответствующие реагентам условия реакции и тому подобное. В качестве примеров других защитных групп для аминогрупп можно назвать алканоильные группы, такие как ацетильная группа, алкоксикарбонильные группы, такие как метоксикарбонильная и этоксикарбонильная группы, арилметоксикарбонильные группы, такие как бензилоксикарбонильная, п-метоксибензилоксикарбонильная и п- или о-нитробензилоксикарбонильная группы, арилметильные группы, такие как бензил- и трифенилметильная группы, ароильные группы, такие как бензоильная группа, и арилсульфонильные группы, такие как 2,4-динитробензолсульфонильная и о-нитробензолсульфонильная группы. Указанные защитные группы могут быть выбраны для использования в соответствии с природой и т.п. соединения, аминогруппу которого нужно защищать. При удалении такой защитной группы можно использовать реагенты и условия, соответствующие защитной группе.
[Способ 3 получения]
Соединение (1) по настоящему изобретению может быть получено взаимодействием диамина (2) с сульфонилгалогенидом (10) с последующей конденсацией продукта реакции с карбоновой кислотой (5):
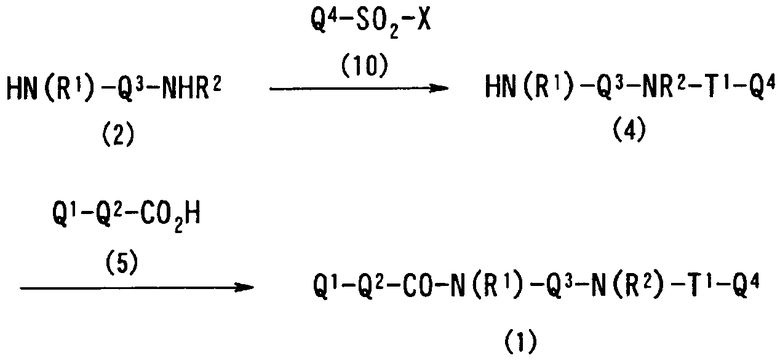
где Q1, Q2, Q3, Q4, R1 и R2 имеют такие же значения, как определено выше, Т1 представляет сульфонильную группу и Х представляет атом галогена.
Диамин (2), взаимодействуя с сульфонилгалогенидом (10) при температуре от -10°C до 30°C в присутствии основания, такого как триэтиламин, в инертном растворителе, дает соединение (4). Инертный растворитель и основание могут быть надлежащим образом выбраны для использования из тех, что описаны в способе 1 получения. Полученное соединение (4) конденсируют с карбоновой кислотой (5), используя реагенты и условия, описанные в способе 1 получения, в результате чего может быть получено соединение (1) по настоящему изобретению. Сульфонилгалогенид (10) может быть синтезирован в подходящем основании известным способом (WO96/10022, WO00/09480) или соответствующим ему способом.
[Способ 4 получения]
Соединение (1) по настоящему изобретению может быть получено также следующим способом:
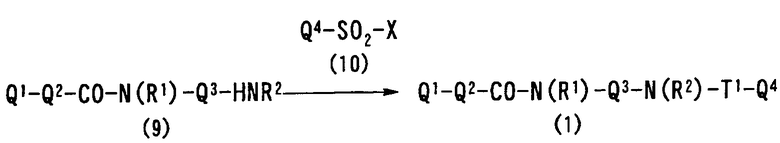
где Q1, Q2, Q3, Q4, R1, R2 и Х имеют такие же значения, как определено выше, и Т1 представляет сульфонильную группу.
В частности, амин (9) может, взаимодействуя с сульфонилгалогенидом (10) при температуре от -10°C до 30°C в присутствии основания в инертном растворителе, давать соединение (1). Инертный растворитель и основание могут быть надлежащим образом выбраны для использования из тех, что описаны в способе 1 получения.
[Способ 5 получения]
В соединениях (1) по настоящему изобретению присутствуют геометрические изомеры транс-формы и цис-формы, связанные с положением 1 и положением 2, когда Q3 представляет следующую группу:

где R3, R4 и Q5 имеют такие же значения, как определено выше, и цифры 1 и 2 указывают положения.
Способы получения соединений (1), имеющих транс-форму и цис-форму, описаны ниже.
<Способ получения транс-формы>
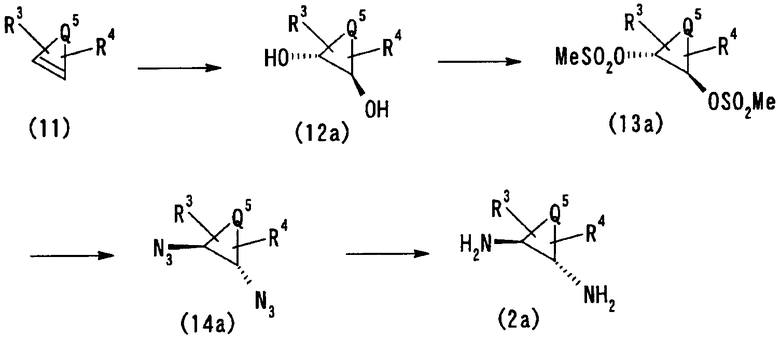
где Q5, R3 и R4 имеют такие же значения, как определено выше.
В качестве примера получения транс-диола (12а) из циклического алкена (11) известно превращение, например, циклогексена в транс-циклогександиол (Organic Synthesis, 1995, Vol. III, p. 217). В качестве примера получения транс-диамина (2а) из транс-диола (12а) известно превращение транс-циклопентандиола в транс-циклопентандиамин (WO98/30574). Транс-диамин (2а) может быть получен из циклического алкена (11) в соответствии с указанными сообщениями.
Транс-диамин (2а), полученный описанным выше способом, может быть превращен в транс-соединение (1) любым из описанных выше способов 1-4.
<Способ получения цис-формы>
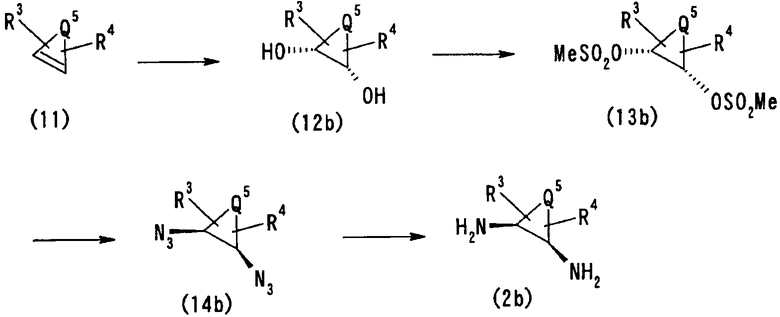
где Q5, R3 и R4 имеют такие же значения, как определено выше.
В качестве примера получения цис-диола (12b) из циклического алкена (11) известно превращение, например, циклогексена в цис-циклогександиол (J. Org. Chem., 1998, Vol. 63, p. 6094). В качестве примера получения цис-диамина (2b) из цис-диола (12а) известно превращение цис-циклопентандиола в цис-циклопентандиамин (WO98/30574). Цис-диамин (2b) может быть получен из циклического алкена (11) в соответствии с указанными сообщениями.
Цис-диамин (2b), полученный описанным выше способом, может быть превращен в цис-соединение (1) любым из описанных выше способов 1-4.
[Способ 6 получения]
Как описано выше, в соединениях (1) по настоящему изобретению может присутствовать либо цис-форма, либо транс-форма, образованная в Q3, и, следовательно, присутствуют геометрические изомеры. Кроме того, в соответствующих геометрических изомерах могут присутствовать оптические изомеры. Способ получения оптически активного вещества описан ниже:
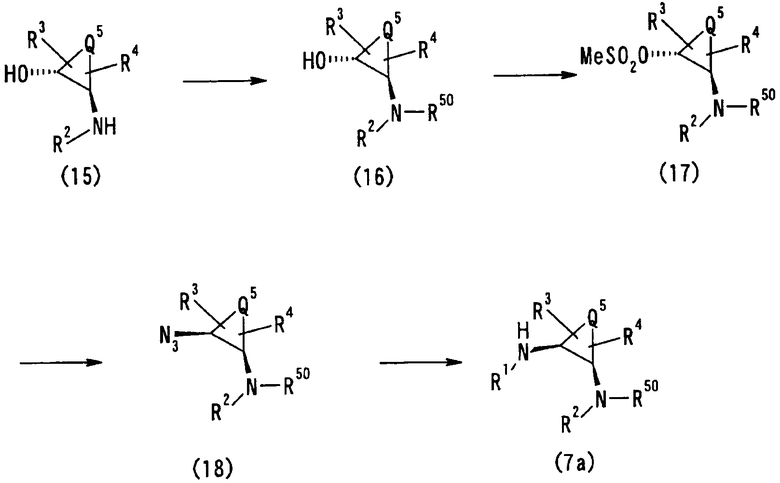
где Q5, R1, R2, R3 и R4 имеют такие же значения, как определено выше, и R50 представляет защитную группу для аминогруппы.
Что касается способа получения оптически активного аминоспиртового производного (15) 1,2-транс-формы, известен, например, способ получения оптически активного 1,2-транс-2-аминоциклопентанола из циклопентеноксида или способ получения оптически активного 1,2-транс-2-аминоциклогексанола из циклогексеноксида (Tetrahedron: Asymmetry, 1996, Vol. 7, p. 843; J. Org. Chem., 1985, Vol. 50, p. 4154; J. Med. Chem., 1998, Vol. 41, p. 38). При взаимодействии аминогруппы оптически активного аминоспирта (15), полученного указанным уже известным способом или с использованием указанного способа, с подходящим защитным реагентом может быть получено соединение (16). В качестве защитной группы, соответствующей R50 в соединении (16), из обычных защитных групп ацильного типа предпочтительной является алкоксикарбонильная группа, такая как метоксикарбонильная, этоксикарбонильная, трет-бутоксикарбонильная группа и тому подобное, арилметоксикарбонильная группа, такая как бензилоксикарбонильная, п-метоксибензилоксикарбонильная, п- или о-нитробензилоксикарбонильная группа и тому подобное, или арилсульфонильная группа, такая как 2,4-динитробензолсульфонильная, о-нитробензолсульфонильная или тому подобное. При защите аминогруппы, например, трет-бутоксикарбонильной группой аминоспирт (15) может взаимодействовать с ди-трет-бутилдикарбонатом при температуре от -78°C до 50°C в инертном растворителе с получением соединения (16). Подходящий инертный растворитель может быть выбран для использования из тех, что описаны в способе 1 получения.
Соединение (16) может взаимодействовать с метансульфонилхлоридом при температуре от -78°C до 50°C в присутствии основания в инертном растворителе с получением соединения (17). Подходящий инертный растворитель может быть выбран для использования из тех, что описаны в способе 1 получения. В качестве основания предпочтительным является органическое основание, такое как пиридин, 2,6-лутидин, коллидин, 4-диметиламинопиридин, триэтиламин, N-метилморфолин, диизопропилэтиламин и диазабицикло[5.4.0]ундец-7-ен (DBU) и тому подобное.
Соединение (17) может взаимодействовать с азидом натрия при температуре от -10°C до 150°C в подходящем растворителе с получением соединения (18). Подходящим растворителем является амидный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид или N-метилпирролидин-2-он, спиртовой растворитель, такой как метанол или этанол, растворитель типа простого эфира, такой как тетрагидрофуран, 1,2-диметоксиэтан или диоксан, ароматический растворитель, такой как толуол, галогенид углерода, такой как дихлорметан, хлороформ или тетрахлорид углерода, ацетон, диметилсульфоксид или смешанный растворитель, полученный из какого-либо указанного растворителя, смешанного с водой.
Существует много способов, подходящих для превращения производного (18) азида в соединение (7а), таких как гидрирование с использованием палладиевого катализатора, катализатора на основе никеля Ренея или платинового катализатора, реакция с использованием восстановителя, такого как литийалюминийгидрид, боргидрид натрия или боргидрид цинка, реакция с использованием цинка в присутствии хлорида никеля или хлорида кобальта, реакция с использованием трифенилфосфина и тому подобное. Подходящие условия реакции могут быть выбраны в соответствии с природой соединения. Например, азидное производное (18) гидрируют при температуре от -10°C до 70°C с использованием 1-20% палладия на углероде в качестве катализатора в подходящем растворителе, в результате чего может быть получено соединение (7а). Давление водорода может быть выше атмосферного давления. В качестве растворителя подходящим является спиртовой растворитель, такой как метанол или этанол, растворитель типа простого эфира, такой как тетрагидрофуран, 1,2-диметоксиэтан или диоксан, амидный растворитель, такой как N,N-диметилформамид, N,N-диметилацетамид или N-метилпирролидин-2-он, растворитель типа сложного эфира, такой как этилацетат, уксусная кислота, хлористоводородная кислота, вода, смешанный растворитель из указанных растворителей и тому подобное.
Оптически активный амин (7а), полученный описанным выше способом, может быть превращен в оптически активное соединение (1) в соответствии с описанным выше способом 2 получения. Аналогичным способом может быть также получен антипод (1) оптически активного вещества (1), полученного из оптически активного амина (7а).
Оптически активное соединение (1) может быть получено разделением рацемического соединения (1) путем пропускания через колонку с оптически активным носителем. Можно также разделять промежуточное соединение (2), (4), (7), (8) или (9) для получения рацемического соединения (1) путем пропускания через колонку с оптически активным носителем с выделением оптически активного промежуточного соединения (2), (4), (7), (8) или (9) и затем получения оптически активного соединения (1) любым из способов получения 1-4. В качестве способа выделения оптически активного соединения (1), оптически активного промежуточного соединения (2), (4), (7), (8) или (9) можно использовать способ фракционной кристаллизации соли с оптически активной карбоновой кислотой или, наоборот, способ фракционной кристаллизации соли с оптически активным основанием.
[Способ 7 получения]
Из числа соединений (1) по настоящему изобретению ниже подробно описан способ получения соединения (1с), содержащего гетероатом(ы) в группе Q3.
Соединение, представленное общей формулой (1с), его соль, сольват или N-оксид можно получить, например, следующим способом:
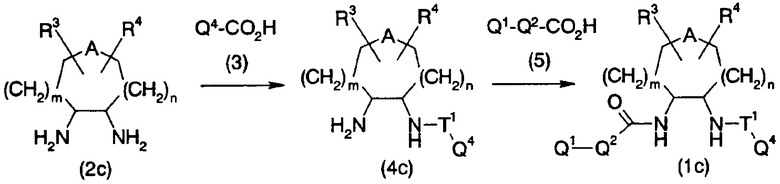
где Q1, Q2, Q3, Q4, R3, R4, А, m и n имеют такие же значения, как определено выше, и Т1 представляет карбонильную группу.
Смешанный ангидрид кислоты, галогенангидрид, активированный сложный эфир или тому подобное, являясь производным карбоновой кислоты (3), может при взаимодействии с соединением (2с) давать соединение (4с). Полученное соединение (4с) может, взаимодействуя с карбоновой кислотой (5) в тех же самых условиях, давать соединение (1с) по настоящему изобретению.
На описанных выше стадиях можно использовать реагенты и условия, обычно используемые в пептидном синтезе. Смешанный ангидрид кислоты может быть получен, например, взаимодействием хлорформиата, такого как этилхлорформиат или изобутилхлорформиат, с карбоновой кислотой (3) в присутствии основания. Галогенангидрид может быть получен обработкой карбоновой кислоты (3) галогенангидридом, таким как тионилхлорид или оксалилхлорид. Активированный сложный эфир включает различные виды сложных эфиров. Такой эфир может быть получен, например, взаимодействием фенола, такого как п-нитрофенол, N-гидроксибензотриазола или N-гидроксисукцинимида с карбоновой кислотой (3) с использованием конденсирующего агента, такого как N,N'-дициклогексилкарбодиимид или гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида. Активированный сложный эфир может быть также получен взаимодействием карбоновой кислоты (3) с пентафторфенилтрифторацетатом или подобным, взаимодействием карбоновой кислоты (3) с гексафторфосфитом 1-бензотриазолилокситрипирролидинофосфония, взаимодействием карбоновой кислоты (3) с диэтилцианофосфонатом (метод Shioiri), взаимодействием карбоновой кислоты (3) с трифенилфосфином и 2,2'-дипиридилдисульфидом (метод Mukaiyama) или подобным. Полученный таким образом смешанный ангидрид кислоты, галогенангидрид или активированный сложный эфир карбоновой кислоты (3) может, взаимодействуя с диамином (2с) при температуре в пределах температур от охлаждения до нагревания в присутствии подходящего основания в инертном растворителе, давать соединение (4с). Полученное соединение (4с) может взаимодействовать со смешанным ангидридом, галогенангидридом или активированным сложным эфиром карбоновой кислоты (5) в тех же самых условиях с получением соединения (1с) по настоящему изобретению. Реагенты и условия реакции при взаимодействии соединения (4с) с карбоновой кислотой (5) такие же, как при взаимодействии диамина (2с) с карбоновой кислотой (3).
В качестве конкретных примеров основания, используемого на каждой из описанных выше стадий, можно назвать карбонаты щелочных или щелочноземельных металлов, такие как карбонат натрия и карбонат калия, алкоксиды щелочных металлов, такие как этоксид натрия и бутоксид калия, гидроксиды щелочных металлов, такие как гидроксид натрия и гидроксид калия, и гидриды щелочных или щелочноземельных металлов, такие как гидрид натрия и гидрид калия; металлоорганические основания, примерами которых являются алкиллитий, такой как н-бутиллитий, и диалкиламинолитий, такой как диизопропиламид лития; металлоорганические основания, примером которых является бис(силил)амин, такой как бис(триметилсилил)амид лития; и органические основания, такие как пиридин, 2,6-лутидин, коллидин, 4-диметиламинопиридин, триэтиламин, N-метилморфолин, диизопропилэтиламин и диазабицикло[5.4.0]ундец-7-ен (DBU).
Примеры инертного растворителя, используемого в данной реакции, включают растворители типа алкилгалогенида, такие как метиленхлорид и хлороформ, растворители типа простого эфира, такие как тетрагидрофуран и 1,4-диоксан, ароматические растворители, такие как бензол и толуол, и амидные растворители, такие как N,N-диметилформамид. Кроме указанных растворителей в некоторых случаях можно использовать сульфоксидный растворитель, такой как диметилсульфоксид, кетонный растворитель, такой как ацетон, или тому подобное.
На описанных выше стадиях получения соединения (1с) целесообразно применять такие процессы, как введение и удаление защитной группы и превращение функциональной группы.
В качестве защитной группы для аминогруппы нужно только использовать защитную группу, которую обычно используют в качестве защитной группы для аминогруппы в синтезе органических соединений, в частности, в пептидном синтезе. В качестве ее примеров можно назвать алкоксикарбонильные группы, такие как трет-бутоксикарбонильная, метоксикарбонильная и этоксикарбонильная группы, арилметоксикарбонильные группы, такие как бензилоксикарбонильная, п-метоксибензилоксикарбонильная и п- или о-нитробензилоксикарбонильная группы, арилметильные группы, такие как бензильная, 4-метоксибензильная и трифенилметильная группы, алканоильные группы, такие как формильная и ацетильная группа, ароильные группы, такие как бензоильная группа, и арилсульфонильные группы, такие как 2,4-динитробензолсульфонильная и о-нитробензолсульфонильная группы.
В качестве защитной группы для гидроксильной группы нужно только использовать защитную группу для гидроксильной группы, которую обычно используют в синтезе органических соединений. В качестве ее примеров можно назвать алкоксиметильные группы, такие как метоксиметильная группа, арилметильные группы, такие как бензильная, 4-метоксибензильная и трифенилметильная группы, алканоильные группы, такие как ацетильная группа, ароильные группы, такие как бензоильная группа, и трет-бутилдифенилсилилоксигруппу. Карбоксильная группа может быть защищена как сложный эфир алкильной группой, такой как трет-бутильная группа, или арилметильной группой, такой как бензильная группа. Введение и удаление защитной группы можно осуществлять методом, известным в данной области.
Соединение (1с) по настоящему изобретению может быть превращено в различные производные путем преобразования его функциональной группы. Например, соединение, в котором А представляет атом азота, не содержащий заместителя, может быть превращено в амидное соединение ацилированием с использованием смешанного ангидрида кислоты, галогенангидрида, активированного сложного эфира или подобного обычными методами органической химии, производное сульфонамида - взаимодействием с сульфонилгалогенидом, N-алкильное соединение - взаимодействием с алкилгалогенидом, N-арильное соединение - взаимодействием с арилгалогенидом или производное карбамата - взаимодействием с изоцианатом. Кстати, соединение, в котором А представляет атом азота без заместителя, может быть получено, например, обработкой кислотой соединения (1с), полученного из диамина (2с), где А уже защищен трет-бутоксикарбонильной группой, по способу 7 получения.
Соединения по настоящему изобретению, полученные таким образом, могут быть выделены и очищены общеизвестными методами, например, экстракцией, осаждением, фракционной хроматографией, фракционной кристаллизацией, перекристаллизацией и т.д. Соединения по настоящему изобретению могут быть преобразованы в требуемые соли в соответствии с обычными реакциями солеобразования.
В соединениях по настоящему изобретению присутствуют оптические изомеры, произведенные от асимметрического атома углерода. Такой оптически активный изомер может быть получен способом получения из оптически активного диамина (2с) и, кроме того, способом образования оптически активного амина или кислоты и соли из рацемического соединения (1с) и его фракционной кристаллизации, способом его разделения колоночной хроматографией с использованием оптически активного носителя.
Соединение (1с), в котором Т1 представляет сульфонильную группу, может быть получено заменой карбоновой кислоты (3) сульфонилгалогенидом (10) в реакции соединения (2с) с карбоновой кислотой (3).
[Способ 8 получения]
Соединение (1с) по настоящему изобретению может быть также получено следующим способом:
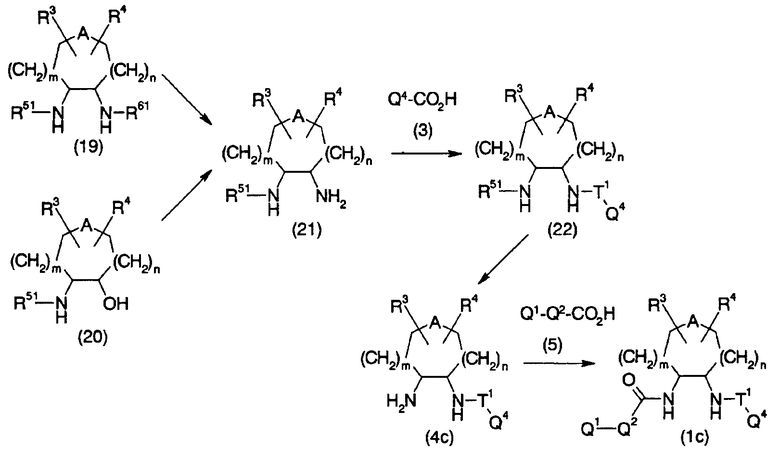
где Q1, Q2, Q3, Q4, R3, R4, А, m и n имеют такие же значения, как определенно выше, Т1 представляет карбонильную группу и R51 и R61 представляют защитные группы для аминогруппы.
Соединение (21) может быть получено удалением защитной группы R61 соединения (19), полученного защитой аминогрупп соединения (2с). Не налагается особого ограничения на защитные группы для аминогрупп, показанные как R51 и R61, лишь бы они были группами, обычно используемыми для защиты аминогруппы. Однако в качестве их типичных примеров можно назвать защитные группы для аминогруппы, описанные в способе 7 получения. В данном случае требуется, чтобы R51 и R61 были защитными группами, способными удаляться с использованием отличающихся друг от друга методов или условий. В качестве их типичных примеров можно назвать комбинацию, в которой R51 представляет трет-бутоксикарбонильную группу и R61 представляет бензилоксикарбонильную группу. Указанные защитные группы могут быть выбраны для использования в соответствии с природой и т.п. соединения, аминогруппу которого нужно защитить. При удалении такой защитной группы могут быть использованы реагенты и условия, соответствующие защитной группе.
Соединение (21) может быть также получено превращением гидроксильной группы в аминоспиртовом производном (20) в аминогруппу. В качестве примера получения аминоспиртового производного (20) известно превращение метионина в 3-гидрокси-4-аминотиопиран-1,1-диоксид (Tetrahedron Lett., Vol. 37, p. 7457, 1996).
В качестве способа превращения гидроксильной группы в аминоспиртовом производном (20) в аминогруппу можно назвать способ, в котором аминоспиртовое производное (20) может взаимодействовать с метансульфонилхлоридом, п-толуолсульфонилхлоридом, трифторметансульфоновым ангидридом или подобным, полученный продукт может затем взаимодействовать с аммиаком, первичным арилалкиламином, таким как бензиламин, п-метоксибензиламин или 2,4-диметоксибензиламин, вторичным арилалкиламином, таким как дибензиламин, или гидроксиламином, таким как N-бензилгидроксиламин или N,О-дибензилгидроксиламин, после чего при необходимости бензильная группа или тому подобное удаляется с получением диамина (21). Аминоспиртовое производное (20) может быть также превращено в диамин (21) взаимодействием с фталимидом или сукцинимидом в соответствии с реакцией с трифенилфосфином и этилазодикарбоксилатом (метод Mukaiyama) или подобным и затем обработкой продукта реакции гидразином или N-метилгидразином. Когда А в формуле представляет SO2 и n равно 0, диамин (21) может быть получен добавлением аммиака, первичного арилалкиламина, такого как бензиламин, п-метоксибензиламин или 2,4-диметоксибензиламин, вторичного арилалкиламина, такого как дибензиламин, или гидроксиламина, такого как N-бензилгидроксиламин или N,О-дибензилгидроксиламин, к α,β-ненасыщенному циклическому сульфону, образованному при взаимодействии аминоспиртового производного (20) с метансульфонилхлоридом, п-толуолсульфонилхлоридом, трифторметансульфоновым ангидридом или подобным, с последующей обработкой продукта реакции подходящим основанием, или непосредственным взаимодействием аминоспиртового производного (20) с трифенилфосфином и этилазодикарбоксилатом и удалением бензильной группы или подобного, при необходимости.
Полученный диамин (21) может взаимодействовать с карбоновой кислотой (3) с образованием соединения (22). Затем удаляют защитную группу R51 с получением соединения (4с). Соединение (4с) может взаимодействовать с карбоновой кислотой (5), образуя соединение (1с) по настоящему изобретению. Реагенты и условия реакции при взаимодействии соединения (21) с карбоновой кислотой (3) и взаимодействии соединения (4с) с карбоновой кислотой (5) могут быть такими же, как описано в способе 7 получения.
Аналогично, соединение (1с), в котором Т1 представляет сульфонильную группу, может быть получено заменой карбоновой кислоты (3) сульфонилхлоридом (10) при взаимодействии соединения (21) с карбоновой кислотой (3).
[Способ 9 получения]
Описан типичный способ получения промежуточного соединения (2с) для получения, описанного в способе 7 получения:
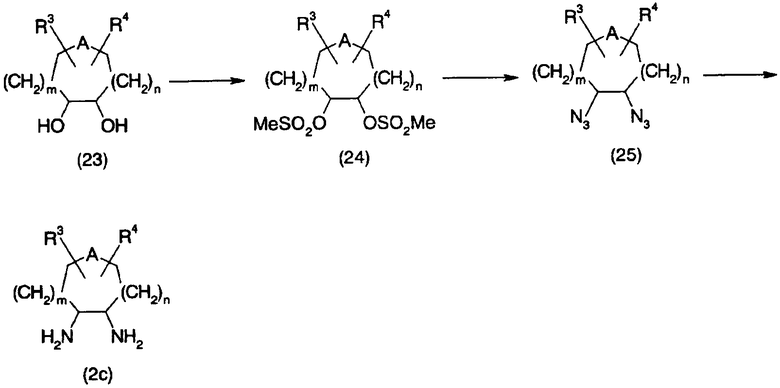
где R3, R4, А, m и n имеют такие же значения, как определено выше.
В качестве способов получения производного диола (23) известны, например, превращение 1,2,3,6-тетрагидропиридина в 1-бензилоксикарбонил-3,4-цис-дигидроксипирролидин (выложенная заявка на патент Японии № 138264/1995), превращение L-винной кислоты в (R,R)-тетрагидрофурандиол или (R,R)-N-бензилпирролидиндиол (Tetrahedron: Asymmetry, Vol. 8, p. 1861, 1997). Производное диола (23) может быть получено с использованием уже известного способа как такового или с использованием такого способа и удалением защитной группы, или преобразованием функциональной группы, при необходимости.
Производное диола (23) может, взаимодействуя с метансульфонилхлоридом при температуре в пределах от температуры охлаждения до комнатной температуры в присутствии основания в инертном растворителе, давать соединение (24). Инертный растворитель может быть подходящим образом выбран для использования из тех, что описаны в способе 7 получения. Однако особенно предпочтительными являются растворители типа алкилгалогенида, такие как метиленхлорид и хлороформ, и эфирные растворители, такие как тетрагидрофуран и 1,4-диоксан. В качестве основания предпочтительным является органическое основание, такое как пиридин, 2,6-лутидин, 4-диметиламинопиридин, триэтиламин, N-метилморфолин, диизопропилэтиламин и диазабицикло[5.4.0]ундец-7-ен (DBU).
Соединение (24) может взаимодействовать с азидом натрия при температуре в пределах температур от охлаждения до нагревания в подходящем растворителе с образованием азидного производного (25). Подходящим растворителем является амидный растворитель, такой как N,N-диметилформамид или N-метилпирролидин-2-он, спиртовой растворитель, такой как метанол или этанол, эфирный растворитель, такой как тетрагидрофуран или 1,4-диоксан, ароматический растворитель, такой как бензол или толуол, галогенид углерода, такой как метиленхлорид или хлороформ, диметилсульфоксид, ацетон или тому подобное. Такой растворитель может быть смешан с водой.
Существует много способов, подходящих для превращения азидного производного (25) в соединение (2с), таких как гидрирование с использованием палладиевого катализатора, катализатора на основе никеля Ренея или платинового катализатора, реакция с использованием восстановителя, такого как литийалюминийгидрид или боргидрид натрия, реакция с использованием цинка в присутствии хлорида никеля или хлорида кобальта и реакция с использованием трифенилфосфина. Подходящие реагенты и условия реакции могут быть выбраны в соответствии с природой соединения. Давление водорода может превышать атмосферное давление. В качестве растворителя подходящим является спиртовой растворитель, такой как метанол или этанол, эфирный растворитель, такой как тетрагидрофуран или 1,4-диоксан, амидный растворитель, такой как N,N-диметилформамид или N-метилпирролидин-2-он, растворитель типа сложного эфира, такой как этилацетат, уксусная кислота, хлористоводородная кислота, вода, смешанный растворитель из указанных растворителей. Соединение (1с) по настоящему изобретению может быть получено из производного диамина (2с), полученного описанным выше способом, в соответствии со способом 7 получения.
Когда производное диола (23) представляет собой транс-3,4-дигидрокситетрагидрофуран или транс-1-замещенный 3,4-дигидроксипирролидин, присутствуют оптически активные вещества. Указанные оптически активные производные диола (23) могут быть превращены в оптически активные производные (2c) диамина и затем в оптически активные соединения (1с) по настоящему изобретению в соответствии со способом 7 получения.
[Способ 10 получения]
Описан типичный способ получения оптически активных соединений (30), (31) и (32), входящих в соединение (19), описанное в способе 8 получения. При этом положение асимметрического углеродного атома на показанной ниже схеме получения указано в качестве примера:
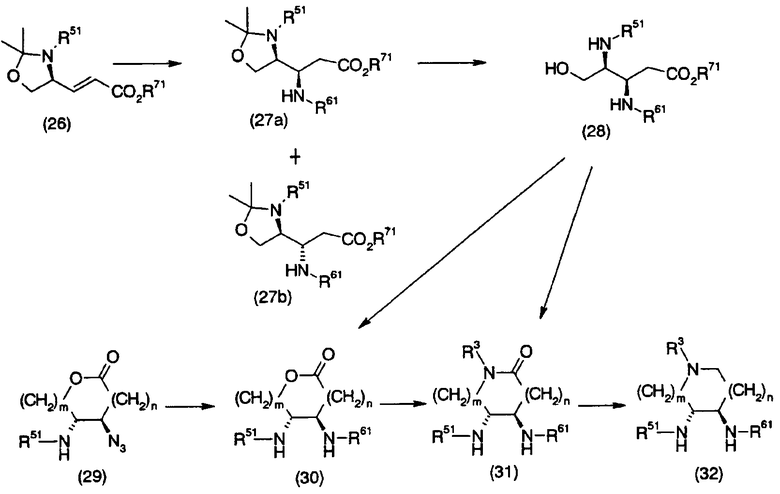
где m, n, R3, R51 и R61 имеют такие же значения, как определено выше, и R71 представляет защитную группу для карбоксильной группы.
Оптически активное α,β-ненасыщенное сложноэфирное производное (26) может быть получено согласно способу, описанному в литературе (J. Org. Chem. Vol. 61, p. 581, 1996; J. Org. Chem. Vol. 57, p. 6279, 1992, и т.д.), или с использованием такого способа. Оптически активное α,β-ненасыщенное производное (26) сложного эфира может взаимодействовать с амином при температуре в пределах температур от охлаждения до нагревания в подходящем растворителе с образованием диастереомеров (27а) и (27b). Амин может быть подходящим образом выбран для использования из тех, что описаны в способе 8 получения. Растворитель желательно является органическим растворителем, не реагирующим на субстрат, продукт или реагент, в частности, спиртовым растворителем, таким как метанол или этанол, или эфирным растворителем, таким как тетрагидрофуран, 1,2-диметоксиэтан или 1,4-диоксан. Диастереомеры (27а) и (27b) могут быть также получены взаимодействием α,β-ненасыщенного сложноэфирного производного (26) с металлоорганическим основанием, таким как N-бензил(триметилсилил)амид лития, с использованием способа, описанного в литературе (J. Org. Chem. Vol. 63, p. 7263, 1998). Диастереомеры могут быть разделены для использования, например, диастереомера (27а) в следующей реакции.
Соединение (27а) обрабатывают кислотой при температуре в пределах температур от охлаждении до нагревания в подходящем растворителе с образованием соединения (28). Примеры используемой кислоты включают хлористоводородную кислоту, серную кислоту, кислоты Льюиса, такие как трифторид бора, трифторуксусную кислоту и п-толуолсульфоновую кислоту. В качестве растворителя используют воду или спиртовой растворитель, такой как метанол или этанол. Такой растворитель может быть смешанным растворителем с водой. В данной реакции защитная группа R61 может быть в некоторых случаях удалена. В этом случае такое соединение требуется подвергать взаимодействию с подходящим защитным реагентом для аминогруппы, при необходимости.
Соединение (28) может быть обработано кислотой при температуре в пределах температур от охлаждения до нагревания в подходящем растворителе с образованием оптически активного соединения (30). Используемая кислота может быть подходящим образом выбрана для использования из кислот, указанных выше, причем особенно предпочтительной является кислота Льюиса, такая как трифторид бора, или п-толуолсульфоновая кислота. В качестве растворителя в реакции используют эфирный растворитель, такой как 1,4-диоксан или тетрагидрофуран, или ароматические растворители, такие как бензол или толуол. Соединение (30) может быть также получено из азидного производного (29). В качестве примеров получения оптически активного азидного производного (29) известны превращение L-аспарагиновой кислоты в (R,R)-(3S,4S)-3-амино-4-азид-5-оксотетрагидрофуран (Can. J. Chem., Vol. 71, p. 1047, 1993) и тому подобное. Оптически активное азидное производное (29) можно получить, используя уже известный способ как таковой или используя такой способ и удаляя защитную группу или превращая функциональную группу, при необходимости. Азид в азидном производном (29) может быть восстановлен до аминогруппы и полученный продукт может быть подвергнут взаимодействию с подходящим защитным реагентом для аминогруппы с образованием соединения (30). Реагенты и условия реакции, используемые при восстановлении азида (29), могут быть такими же, как описано в способе превращения азидного производного (25) в соединение (2с).
Содержащая гидроксильную группу часть соединения (28) может быть превращена в аминогруппу и затем обработана основанием с получением соединения (31). Преобразование гидроксильной группы в соединении (28) в аминогруппу может быть осуществлено, например, по способу 8 получения. Соединение (31) может также быть получено обработкой спиртового производного (28) окислителем и затем восстановительным аминированием полученного альдегидного производного. Конкретные предпочтительные примеры окислителя, используемого в описанной выше реакции, включают хлорхромат пиридиния (РСС), дихромат пиридиния (PDC) и комплексы триоксида серы и пиридина. Примеры амина включают первичные алкиламины, такие как аммиак, метиламин и этиламин, и первичные аралкиламины, такие как бензиламин, п-метоксибензиламин и 2,4-диметоксибензиламин. В качестве способа восстановления существуют способ гидрирования с палладиевым катализатором, катализатором на основе никеля Ренея или платиновым катализатором, реакция с использованием восстановителя, такого как боргидрид натрия, триацетоксиборгидрид натрия или цианоборгидрид натрия, причем подходящие реагенты и условия реакции могут быть выбраны в соответствии с природой соединения. Основание, используемое в описанном выше способе, может быть подходящим образом выбрано для использования из тех оснований, которые описаны в способе 7 получения. Соединение (31) можно также получить, используя соединение (30) и амин в соответствии со способом, описанным в литературе (Tetrahedron Lett., Vol. 41, p. 1141, 2000; Heterocycles, Vol. 53, p. 173, 2000), или с использованием такого способа. Примеры используемого амина включают первичные алкиламины, такие как аммиак, метиламин и этиламин, и первичные арилалкиламины, такие как бензиламин и п-метоксибензиламин.
Соединение (31) может быть обработано восстановителем при температуре в пределах температур от охлаждения до нагревания в растворителе с образованием соединения (32). Примеры восстановителя включают боран-тетрагидрофурановые комплексы, боран-метилсульфидные комплексы и литийалюминийгидрид. Однако подходящие реагенты и условия реакции могут быть выбраны в соответствии с природой соединения. Растворитель желательно является органическим растворителем, не реагирующим на субстрат, продукт или реагент, в частности, эфирным растворителем, таким как тетрагидрофуран или 1,4-диоксан.
Оптически активные вещества (1с) соединений по настоящему изобретению могут быть образованы из соединений (30), (31) и (32), полученных способами, описанными выше.
Одно из оптически активных веществ на описанной выше схеме получения уже было описано в качестве примера. Однако другие оптически активные вещества, отличающиеся по конформации друг от друга, также могут быть получены по аналогичным схемам получения с использованием соответствующих исходных веществ, отличающихся по конформации друг от друга.
[Способ 11 получения]
Соединение (1), в котором Т1 представляет группу -СО-СО-N(R')-, где R' имеет такое же значение, как определено выше, может быть получено по следующей схеме:

где Q1, Q2, Q3, Q4, R1, R2 и R' имеют такие же значения, как определено выше, Т1 представляет группу -СО-СО-N(R')-, где R' имеет такое же значение, как определено выше.
Галогенангидрид, активированный сложный эфир или тому подобное, образованный из карбоновой кислоты (33), может взаимодействовать с диамином (2) с получением соединения (4). Полученное соединение (4) может взаимодействовать с карбоновой кислотой (5) в тех же самых условиях, что дают соединение (1) по настоящему изобретению. На описанных выше стадиях реакции могут быть использованы реагенты и условия, обычно используемые в пептидном синтезе. Галогенангидрид может быть получен обработкой карбоновой кислоты (33) галогенангидридом, таким как тионилхлорид или оксалилхлорид. Активированный сложный эфир включает различные виды сложных эфиров. Такой сложный эфир может быть получен, например, взаимодействием фенола, такого как п-нитрофенол, N-гидроксибензотриазола или N-гидроксисукцинимида с карбоновой кислотой (33) с использованием конденсирующего агента, такого как N,N'-дициклогексилкарбодиимид или гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида. Активированный сложный эфир может быть также получен взаимодействием карбоновой кислоты (33) с пентафторфенилтрифторацетатом или подобным, взаимодействием карбоновой кислоты (33) с гексафторфосфитом 1-бензотриазолилокситрипирролидинофосфония, взаимодействием карбоновой кислоты (33) с диэтилцианофосфонатом (метод Shioiri), взаимодействием карбоновой кислоты (33) с трифенилфосфином и 2,2'-дипиридилдисульфидом (метод Mukaiyama) и подобным. Полученный таким образом смешанный ангидрид кислоты, галогенангидрид или активированный сложный эфир карбоновой кислоты (33) может взаимодействовать с диамином (2) при температуре от -78°C до 150°C в присутствии подходящего основания в инертном растворителе с получением соединения (4). Полученное соединение (4) может взаимодействовать со смешанным ангидридом кислоты, галогенангидридом или активированным сложным эфиром карбоновой кислоты (5) в тех же самых условиях с получением соединения (1) по настоящему изобретению. Реагенты и условия реакции при взаимодействии соединения (4) с карбоновой кислотой (5) такие же, как при взаимодействии диамина (2) с карбоновой кислотой (33). Основания и растворители, используемые на описанных выше соответствующих стадиях, могут быть подходящим образом выбраны из тех, что описаны в способе получения 1.
Когда получают соединение (1), где Q3 представляет следующую группу:

где R3, R4 и Q5 имеют такие же значения, как определено выше, и цифры 1 и 2 указывают положения, а соотношение между положением 1 и положением 2 представляет транс-форму или цис-форму, нужно лишь использовать диамин (2а) или (2b), описанный в способе 5 получения.
Когда получают соединение (1), где Q5 содержит гетероатом, такой как атом азота, атом кислорода или атом серы, нужно лишь заменить карбоновую кислоту (3) карбоновой кислотой (33) в реакции соединения (2с) с карбоновой кислотой (3), как описано в способе 7 получения. А именно, соединение (1), где Q5 содержит гетероатом, т.е. соединение (1с), может быть получено по следующей схеме реакций:
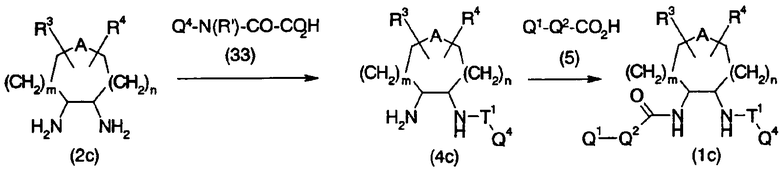
где Q1, Q2, Q4, R3, R4, R', А, m и n имеют такие же значения, как определено выше, и Т1 представляет группу -СО-СО-N(R')-, где R' имеет такое же значение, как определено выше.
[Способ 12 получения]
Соединение (1), где Т1 представляет группу -СО-СО-N(R')-, где R' имеет такое же значение, как определено выше, может быть также получено по следующей схеме:
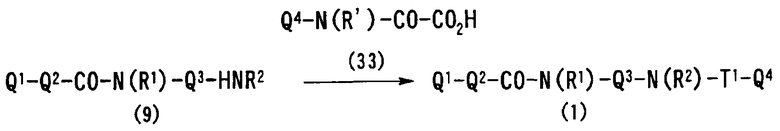
где Q1, Q2, Q3, Q4, R1, R2 и R' имеют такие же значения, как определено выше, и Т1 представляет группу -СО-СО-N(R')-, где R' имеет такое же значение, как определено выше.
В реакции амина (9) с карбоновой кислотой (33) можно использовать те же самые реагенты и условия, которые описаны в способе 1 получения.
Используемый в данной реакции амин (9) может быть также получен по следующей схеме, показанной в качестве схемы получения амина (41) в дополнение к схеме, описанной в способе 2 получения:
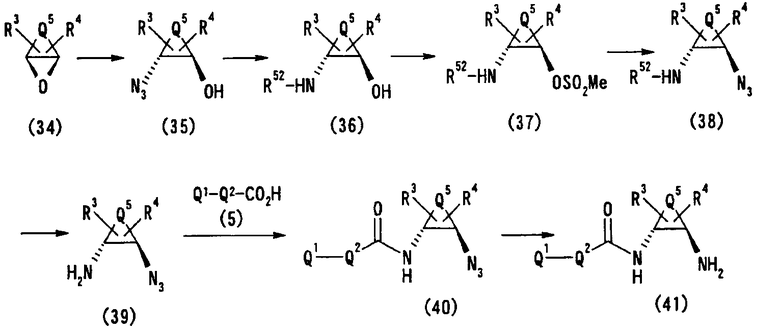
где R3, R4, Q1, Q2 и Q5 имеют такие же значения, как определено выше, и R52 представляет защитную группу для аминогруппы.
Соединение (34) на показанной выше схеме может быть получено обработкой циклоалкена пербензойной кислотой или ее производным в растворителе, таком как метиленхлорид, для его эпоксидирования. Условиями данной реакции могут быть обычные условия эпоксидирования алкена. Соединение (34) может быть также получено способом, описанным в J. Org. Chem., Vol. 61, pp. 8687-8691 (1996), или соответствующим ему способом.
Соединение (34) может взаимодействовать с азидом натрия в соответствии со способом, известным в данной области, с получением азида (35). Азид (35) может быть каталитически восстановлен и аминогруппа полученного соединения может быть защищена, в результате чего будет получено соединение (36). В качестве примеров защитной группы для аминогруппы в данной реакции можно указать те, которые описаны в способе 2 получения. Соединение (36) может быть превращено в азид (38) подобно способу, описанному в способе 5 получения, и защитная группа для его аминогруппы может быть удалена, в результате чего будет получено соединение (39). Соединение (39) может взаимодействовать с карбоновой кислотой (5) с получением соединения (40). Соединение (40) может быть затем каталитически восстановлено, что дает соединение (41).
[Способ 13 получения]
Соединение (1), где Т1 представляет группу -СО-СО-N(R')-, где R' имеет такое же значение, как определено выше, может быть также получено заменой взаимодействия соединения (9) с карбоновой кислотой (3) на схеме, описанной в способе 2 получения, взаимодействием соединения (9) с соединением (33):
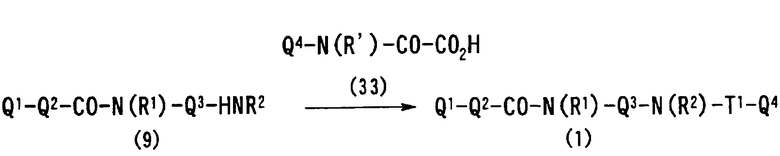
где Q1, Q2, Q3, Q4, R1, R2 и R' имеют такие же значения, как определено выше, и Т1 представляет группу -СО-СО-N(R')-, где R' имеет такое же значение, как определено выше.
Условия реакции могут быть такими же, как описано в способе 2 получения.
Когда получают соединение (1), где Q3 представляет следующую группу:

где R3, R4 и Q5 имеют такие же значения, как определено выше, и цифры 1 и 2 указывают положения и Q5 содержит гетероатом, такой как атом азота, атом кислорода или атом серы, нужно лишь заменить карбоновую кислоту (3) карбоновой кислотой (33) в реакции между соединением (21) и карбоновой кислотой (3), как описано в способе 8 получения. А именно, соединение (1), где Q5 содержит гетероатом, т.е. соединение (1с), может быть получено по следующей схеме реакций:
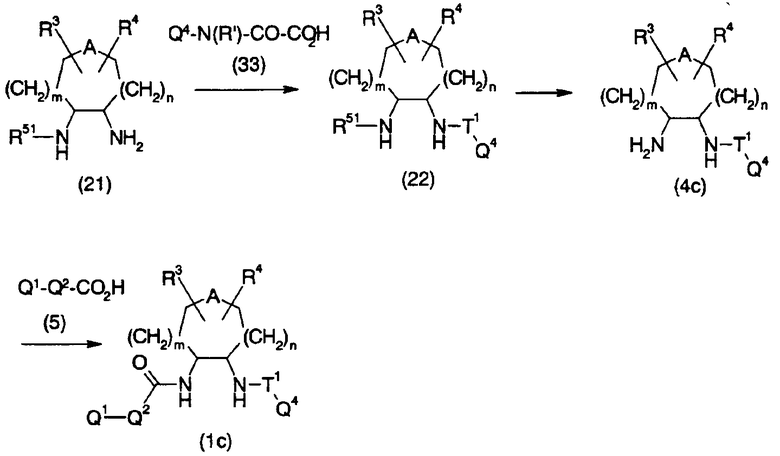
где Q1, Q2, Q4, R3, R4, R', А, m и n имеют такие же значения, как определено выше, и Т1 представляет группу -СО-СО-N(R')-, где R' имеет такое же значение, как определено выше, и R51 представляет защитную группу для аминогруппы.
[Способ 14 получения]
Соединение (1), где Т1 представляет группу -СО-А1-N(R")-, где R" представляет атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу и А1 представляет алкиленовую группу, имеющую 1-5 углеродных атомов, которая может быть замещенной, может быть получено взаимодействием соединения (9), описанного в способе 2 получения, с Q4-N(R")-А1-СО2Н (42) при температуре от -55°C до 50°C с использованием конденсирующего агента в инертном растворителе. В качестве примеров конденсирующего агента можно указать N,N'-дициклогексилкарбодиимид и гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида. В качестве примеров инертного растворителя можно указать растворители типа алкилгалогенида, такие как метиленхлорид, хлороформ и тетрахлорид углерода, эфирные растворители, такие как тетрагидрофуран, 1,2-диметоксиэтан и диоксан, ароматические растворители, такие как бензол и толуол, и амидные растворители, такие как N,N-диметилформамид.
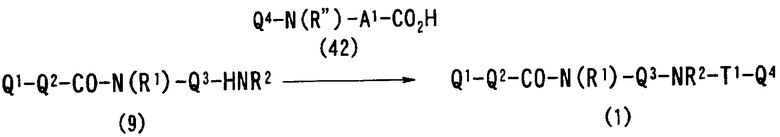
где Q1, Q2, Q3, Q4, R1, R2 и R" имеют такие же значения, как определено выше, и Т1 представляет группу -СО-А1-N(R")-, где R" представляет атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу и А1 представляет алкиленовую группу, имеющую 1-5 углеродных атомов, которая может быть замещенной.
Соединение (42), описанное в способе получения, приведенном выше, может быть получено, например, взаимодействием ариламина, такого как 4-хлоранилин, со сложным эфиром бромалкановой кислоты при 40-120°C в присутствии основания, такого как карбонат калия, в растворителе, таком как ацетонитрил или N,N-диметилформамид, с последующим гидролизом сложного эфира со щелочью, такой как гидроксид лития, гидроксид калия или гидроксид натрия. Соединение (42) может быть использовано в реакции в форме соли, такой как калиевая соль.
[Способ 15 получения]
Соединение (1), где Т1 представляет группу -С(=О)-NH- или группу -С(=S)-NH-, может быть получено взаимодействием соединения (9), описанного в способе 2 получения, с изоцианатом (Q4-N=С=О) или изотиоцианатом (Q4-N=С=S) при температуре от -20°C до 50°C в инертном растворителе. Типичные примеры инертного растворителя описаны в способе 14 получения. Когда изоцианат или изотиоцианат коммерчески недоступны, они могут быть синтезированы обычными способами.
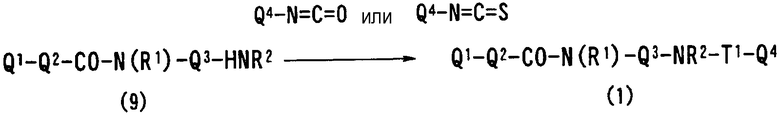
где Q1, Q2, Q3, Q4, R1 и R2 имеют такие же значения, как определено выше, и Т1 представляет группу -С(=О)-NH- или группу -С(=S)-NH-.
[Способ 16 получения]
Соединение (1), где Т1 представляет группу -СО-NH-NH-, может быть получено взаимодействием соединения (9), описанного в способе 2 получения, с Q4-NH-NH=СО2Ph (43) при температуре от комнатной до 150°C в инертном растворителе в присутствии основания, при необходимости. В качестве типичных примеров инертного растворителя можно назвать ацетонитрил и N,N-диметилформамид, а также те растворители, которые описаны в способе 14 получения. В качестве примеров основания можно назвать пиридин, 2,6-лутидин, коллидин, 4-диметиламинопиридин, триэтиламин, N-метилморфолин, диизопропилэтиламин и диазабицикло[5.4.0]ундец-7-ен (DBU).
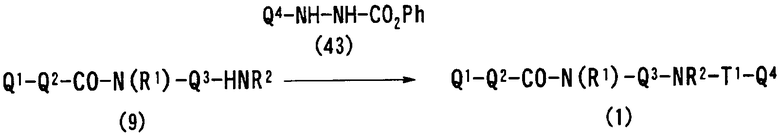
где Q1, Q2, Q3, Q4, R1 и R2 имеют такие же значения, как определено выше, и Т1 представляет группу -СО-NH-NH-.
Соединение (43), описанное в способе получения, приведенном выше, может быть получено, например, взаимодействием арилгидразина, такого как 4-хлорфенилгидразин, с дифенилкарбонатом при температуре от комнатной до 120°C в растворителе, таком как ацетонитрил, N,N-диметилформамид, метиленхлорид, хлороформ, тетрагидрофуран, 1,2-диметоксиэтан, диоксан, бензол или толуол.
[Способ 17 получения]
Соединение (1), где Т1 представляет группу -СО-А2-СО-, где А2 представляет одинарную связь или алкиленовую группу, имеющую 1-5 углеродных атомов, может быть получено взаимодействием соединения (9), описанного в способе 2 получения, с Q4-СО-А2-СО2Н (44) при температуре от -50°C до 50°C с использованием конденсирующего агента в инертном растворителе. В качестве примеров конденсирующего агента можно указать N,N'-дициклогексилкарбодиимид и гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида. В качестве примеров растворителя можно указать те, которые описаны в способе 16 получения.
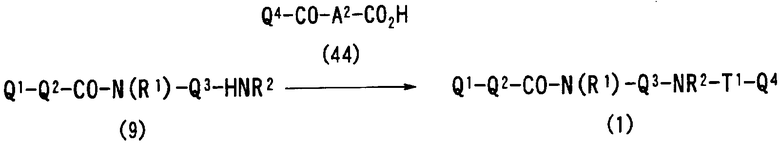
где Q1, Q2, Q3, Q4, R1 и R2 имеют такие же значения, как определено выше, и Т1 представляет группу -СО-А2-СО-, где А2 представляет одинарную связь или алкиленовую группу, имеющую 1-5 углеродных атомов.
Когда А2 представляет одинарную связь, соединение (44), описанное в способе получения, приведенном выше, может быть получено, например, гидролизом соединения (например, Q4-СО-СО2Et), полученного по Фриделю-Крафтсу взаимодействием ароматического углеводорода, такого как хлорбензол, или ароматического гетероциклического соединения, такого как тиофен, с хлороксоацетатом (например, ClCO-CO2Et) с использованием щелочи, такой как гидроксид лития, гидроксид калия или гидроксид натрия.
Когда А2 представляет метиленовую группу, соединение (44) может быть получено, например, гидролизом производного сложного кетоэфира (например, Q4-СО-СН2-СО2Et), полученного взаимодействием арилкарбнилхлорида, такого как 4-хлорбензоилхлорид, или гетероарилкарбонилхлорида, такого как тиофенкарбонилхлорид, с монокарбоксилатом калия моноэфира малоновой кислоты в присутствии хлорида магния и триэтиламина с использованием щелочи, такой как гидроксид лития, гидроксид калия или гидроксид натрия. Производное сложного кетоэфира можно использовать для взаимодействия с соединением (9) в форме карбоновой кислоты, полученной гидролизом после превращения ее карбонильной группы в этиленкеталь. Когда А2 представляет алкиленовую группу, имеющую по крайней мере 2 углеродных атома, соединение (44) может быть получено, например, гидролизом производного сложного кетоэфира (например, Q4-СО-А2-СО2Et), полученного по Фриделю-Крафтсу взаимодействием ароматического углеводорода, такого как бензол, или ароматического гетероциклического соединения, такого как тиофен, с монохлорангидридом моноэфира алкилендикарбоновой кислоты, с использованием щелочи, такой как гидроксид лития, гидроксид калия или гидроксид натрия.
[Способ 18 получения]
Соединение (1), где Т1 представляет группу -СО-А3-СО-NH-, где А3 представляет алкиленовую группу, имеющую 1-5 углеродных атомов, может быть получено взаимодействием соединения (9), описанного в способе 2 получения, с Q4-NH-СО-А3-СО2Н (45) при температуре от 50°C до 50°C с использованием конденсирующего агента в инертном растворителе. В качестве примеров конденсирующего агента можно указать N,N'-дициклогексилкарбодиимид и гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида. Примеры инертного растворителя включают растворители типа алкилгалогенида, такие как метиленхлорид, хлороформ и тетрахлорид углерода, эфирные растворители, такие как тетрагидрофуран, 1,2-диметоксиэтан и диоксан, ароматические растворители, такие как бензол и толуол, и амидные растворители, такие как N,N-диметилформамид.
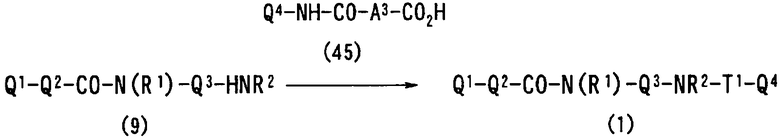
где Q1, Q2, Q3, Q4, R1 и R2 имеют такие же значения, как определено выше, и Т1 представляет группу -СО-А3-СО-, где А3 представляет алкиленовую группу, имеющую 1-5 углеродных атомов.
Соединение (45) может быть получено гидролизом соединения (например, Q4-NH-СО-А3-СО2Et), полученного взаимодействием ариламина, такого как 4-хлоранилин, или гетероариламина, такого как аминопиридин, соответствующий Q4-NH2, с монокарбоксилатом калия моноэфира алкилендикарбоновой кислоты при температуре от -50°C до 50°C с использованием конденсирующего агента в инертном растворителе со щелочью, такой как гидроксид лития, гидроксид калия или гидроксид натрия.
[Способ 19 получения]
Соединение (1), где Т1 представляет группу -CS-CO-N(R')-, где R' имеет такое же значение, как определено выше, может быть получено по следующей схеме:
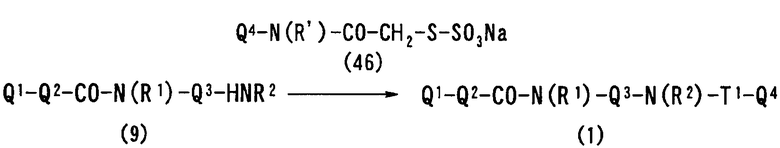
где Q1, Q2, Q3, Q4, R1, R2 и R' имеют такие же значения, как определено выше, и Т1 представляет группу -CS-СО-N(R')-, где R' имеет такое же значение, как определено выше.
В частности, тиосульфат натрия (46) и соединение (9) могут быть растворены или диспергированы в растворителе и нагреты с получением соединения (1) по настоящему изобретению. Температура реакции составляет предпочтительно 80-200°C, особенно предпочтительно примерно 150°C. В качестве растворителя, используемого в данной реакции, можно назвать воду, спирты, такие как метанол и этанол, основные растворители, такие как пиридин и N-метилморфолин, растворители типа алкилгалогенида, такие как метиленхлорид и хлороформ, эфирные растворители, такие как тетрагидрофуран, 1,2-диметоксиэтан и диоксан, и амидные растворители, такие как N,N-диметилформамид. Указанные растворители могут быть подходящим образом смешаны во время использования. В качестве примеров смешанных растворителей можно назвать смешанный растворитель метанол/метиленхлорид. В данной реакции растворитель необязательно кипятить с обратным холодильником. Например, при использовании смешанного растворителя метанола/метиленхлорид реакционный раствор (или реакционную смесь) нагревают при внешней температуре 150°C, чтобы отогнать растворитель, и затем остаток нагревают при той же температуре.
[Способ 20 получения]
Соединение (1), где Т1 представляет группу -СО-CS-N(R')-, где R' имеет такое же значение, как определено выше, может быть получено по следующей схеме:
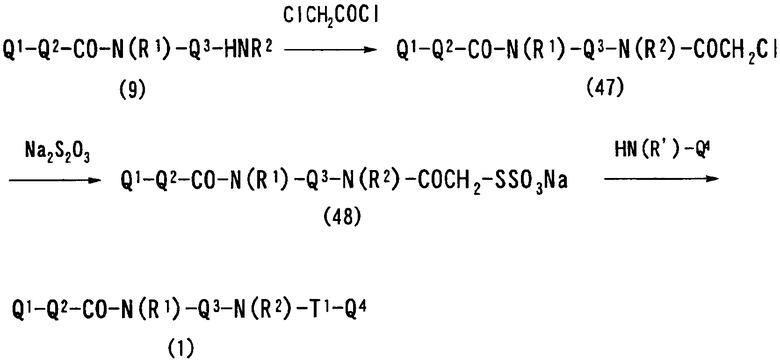
где Q1, Q2, Q3, Q4, R1, R2 и R' имеют такие же значения, как определено выше, и Т1 представляет группу -СО-CS-N(R')-, где R' имеет такое же значение, как определено выше.
В частности, соединение (9) может взаимодействовать с хлорацетилхлоридом в присутствии основания с получением соединения (47). Соединение (47) может быть нагрето вместе с тиосульфатом натрия в растворителе с получением производного тиосульфата натрия (48). Полученное таким образом производное тиосульфата натрия (48) может быть нагрето с амином, т.е. HN(R')-Q4, с получением соединения (1) по настоящему изобретению.
Для получения соединения (47) из соединения (9) можно использовать условия, растворитель и т.п., обычно используемые для взаимодействия амина с хлорангидридом. Чтобы получить соединение (48) из соединения (47), нужно лишь нагревать соединение (47) вместе с тиосульфатом натрия при температуре кипения с обратным холодильником в течение примерно 1 часа в растворителе, таком как этанол. Когда соединение (47) является солью хлористоводородной кислоты или подобным, реакция может быть осуществлена в присутствии основания, такого как гидрокарбонат натрия. Условия получения соединения (48) не ограничиваются приведенными в данном описании и можно подходящим образом изменять температуру и виды растворителя и основания. Условия взаимодействия соединения (48) с NH(R')-Q4 являются такими же, как описано в способе 19 получения.
[Способ 21 получения]
Соединение (1), где Т0 представляет тиокарбонильную группу (-CS-)-, может быть получено по следующей схеме:
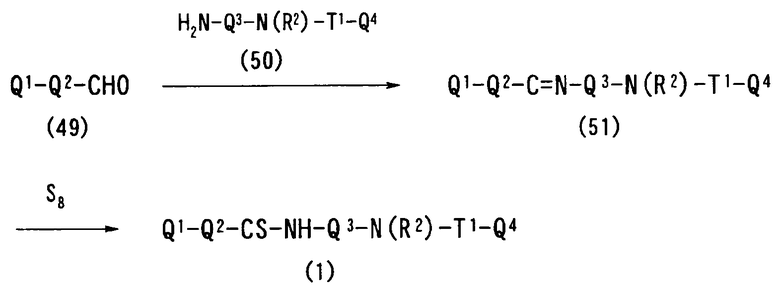
где Q1, Q2, Q3, Q4 и R2 имеют такие же значения, как определено выше, и Т1 представляет группу -SO2-, -CO-, -CO-NH-, -CS-NH-, -CO-NH-NH-, -CO-CO-N(R'), где R' имеет такое же значение, как определено выше, -CO-CS-N(R'), где R' имеет такое же значение, как определено выше, -CS-CO-N(R')-, где R' имеет такое же значение, как определено выше, -CS-CS-N(R')-, где R' имеет такое же значение, как определено выше, -CO-А1-N(R")-, где А1 и R" имеют такие же значения, как определено выше, -СО-А2-СО-, где А2 имеет такое же значение, как определено выше, -СО-А3-СО-NH-, где А3 имеет такое же значение, как определено выше, или -СО-А3-СО-, где А3 имеет такое же значение, как определено выше.
В частности, соединение (49) может быть подвергнуто реакции дегидратации с амином (50) в присутствии кислотного катализатора, такого как п-толуолсульфоновая кислота, с получением соединения (51). Соединение (51) может быть нагрето с порошком серы в растворителе, таком как смешанный растворитель метанол/метиленхлорид, с получением соединения (1) по настоящему изобретению. Для получения соединения (51) из соединения (49) и амина (50) могут быть использованы условия, обычно используемые для получения основания Шиффа. В частности, нагревание при температуре кипения с обратным холодильником может быть проведено в присутствии кислотного катализатора в бензоле или толуоле в условиях, обеспечивающих удаление воды из реакционной системы, например, с использованием ловушки Дина-Старка. Для удаления воды из реакционной системы можно также использовать молекулярные сита.
Ниже представлены важные промежуточные соединения, описанные в способах 1-21 получения соединений (1) по настоящему изобретению.
1) Соединения, описанные в способах 1, 3 и 11 и представленные следующей общей формулой (4):
HN(R1)-Q3-N(R2)-Т1-Q4, (4)
где R1, R2, Q3 и Q4 имеют такие же значения, как определено выше, и Т1 представляет карбонильную группу, сульфонильную группу или группу -СО-СО-N(R'), где R' имеет такое же значение, как определено выше, важны в качестве промежуточных соединений для получения соединений (1) по настоящему изобретению.
Среди описанных выше промежуточных соединений предпочтительными являются соединения, где Т1 представляет группу -С(=О)-С(=О)-N(R'), где R' означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, и соединения, в которых Т1 в приведенной выше формуле представляет карбонильную группу и Q3 представляет следующую группу:

где R3 и R4 имеют такие же значения, как определено выше, Q5 означает группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, -NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-.
2) Соединения, описанные в способах 2, 4 и 12 и представленные следующей общей формулой (9):
Q1-Q2-С(=О)-N(R1)-Q3-NHR2, (9)
где R1, R2, Q1, Q2 и Q3 имеют такие же значения, как определено выше, важны в качестве промежуточных соединений для получения соединений (1) по настоящему изобретению.
Среди описанных выше промежуточных соединений предпочтительными являются соединения, где Q3 представляет следующую группу:

где R3 и R4 имеют такие же значения, как определено выше, и Q5 означает группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, -NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-.
3) Следующие соединения (4с), описанные в способах 7, 11 и 13 получения, важны в качестве промежуточных соединений для получения соединений (1) по настоящему изобретению:
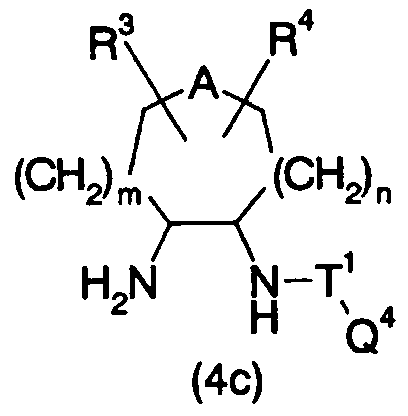
где Q4, R3, R4, А, m и n имеют такие же значения, как определено выше, и Т1 представляет карбонильную группу, сульфонильную группу или группу -СО-СО-N(R'), где R' имеет такое же значение, как определено выше.
Среди описанных выше промежуточных соединений предпочтительными являются соединения, где Т1 в приведенной выше формуле представляет группу -СО-СО-N(R'), где R' имеет такое же значение, как определено выше, и соединения, где Т1 представляет карбонильную группу и А представляет атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, -NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-.
4) Следующие соединения (22), описанные в способах 8 и 13 получения, важны в качестве промежуточных соединений для получения соединений (1) по настоящему изобретению:
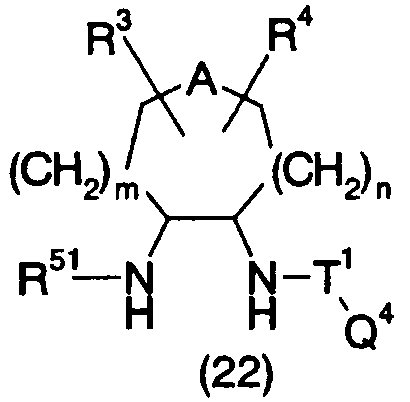
где Q4, R3, R4, А, m и n имеют такие же значения, как определено выше, Т1 представляет карбонильную группу, сульфонильную группу или группу -СО-СО-N(R'), где R' имеет определенное выше значение, и R51 представляет защитную группу для аминогруппы.
Среди описанных выше промежуточных соединений предпочтительными являются соединения, где Т1 в приведенной выше формуле представляет группу -СО-СО-N(R'), где R' имеет определенное выше значение, и соединения, где Т1 представляет карбонильную группу и А представляет атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, O-NH-, -NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-.
5) Следующие оптически активные соединения (7а), описанные в способе 6 получения, важны в качестве промежуточных соединений для получения соединений (1) по настоящему изобретению:
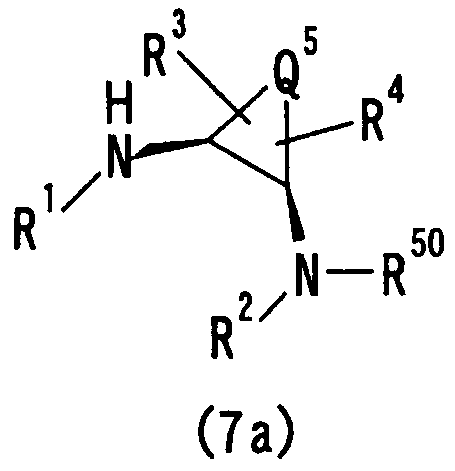
где Q5, R1, R3 и R4 имеют такие же значения, как определено выше, и R50 представляет защитную группу для аминогруппы.
Среди описанных выше промежуточных соединений предпочтительными являются соединения, где Q5 в приведенной выше формуле представляет группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, -NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-.
6) Следующие соединения (21), описанные в способе 8 получения, важны в качестве промежуточных соединений для получения соединений (1) по настоящему изобретению:
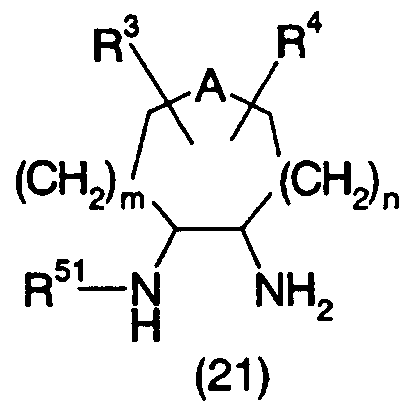
где R3, R4, А, m и n имеют такие же значения, как определено выше, и R51 представляет защитную группу для аминогруппы.
Среди описанных выше промежуточных соединений предпочтительными являются соединения, в которых А в приведенной выше формуле представляет атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, -NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-.
7) Следующие соединения (21), описанные в способе 10 получения, важны в качестве промежуточных соединений для получения соединений (1) по настоящему изобретению. В частности, следующие оптически активные (транс-форма) соединения (30), (31) и (32):
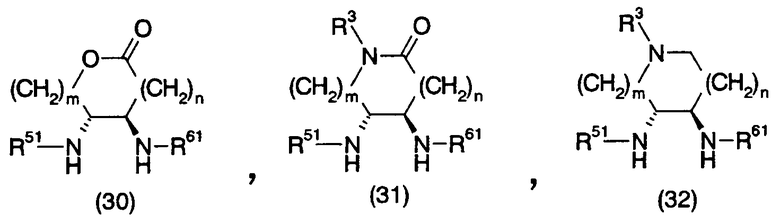
где R3, m и n имеют такие же значения, как определено выше, и R51 и R61 представляют защитные группы для аминогруппы, энантиомеры (30а), (31а) и (32а) указанных выше соединений, полученные аналогичным образом:
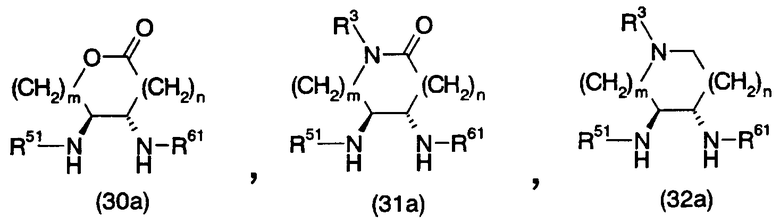
где R3, m и n имеют такие же значения, как определено выше, и R51 и R61 представляют защитные группы для аминогруппы, имеющие цис-форму соединения (30b), (31b) и (32b):
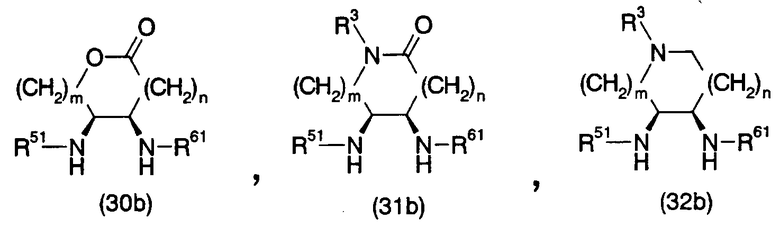
где R3, m и n имеют такие же значения, как определено выше, и R51 и R61 представляют защитные группы для аминогруппы, и их энантиомеры (30с), (31с) и (32с):
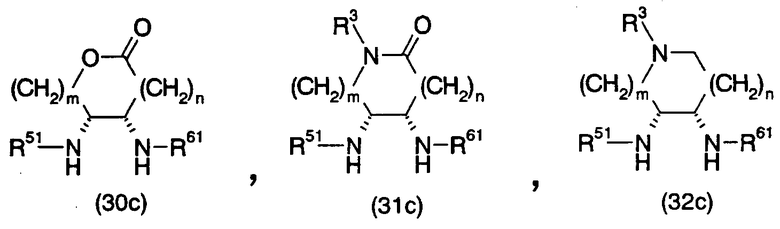
где R3, m и n имеют такие же значения, как определено выше, и R51 и R61 представляют защитные группы для аминогруппы, важны в качестве промежуточных соединений для получения соединений (1) по настоящему изобретению.
Производные диамина по настоящему изобретению оказывают сильное ингибирующее действие на активированный фактор Х свертывания крови и потому полезны в качестве лекарственных средств для млекопитающих, включая человека, антикоагулянтов, средств для профилактики и/или лечения тромбоза или эмболии, средств для профилактики и/или лечения тромботических заболеваний и средств для профилактики и/или лечения инфаркта головного мозга, эмболии головного мозга, инфаркта миокарда, стенокардии, инфаркта легких, эмболии легких, болезни Бюргера, тромбоза глубоких вен, синдрома диссеминированного внутрисосудистого коагулирования, тромбообразования после замены клапана или сустава, тромбообразования и реокклюзии после ангиопластики, синдрома системной воспалительной реакции (SIRS), синдрома заболевания многих органов (MODS), образования тромбов при экстракорпоральном кровообращении или свертывания крови при ее сборе.
Когда соединение по настоящему изобретению применяют в качестве лекарственного средства для организма человека, доза находится в пределах от 1 мг до 1 г, предпочтительно 10-300 мг, в сутки для взрослого человека. Доза для животного колеблется в соответствии с целью (лечение или профилактика) введения, видом и размером животного, подлежащего лечению, видом возбудителя инфекции и состоянием подлежащего лечению заболевания. Однако обычно она находится в диапазоне 0,1-200 мг, предпочтительно 0,5-100 мг, на кг массы в сутки. При этом введение может быть одноразовым в сутки или может быть разделено на 2-4 раза в сутки. При необходимости суточная доза может превышать указанные выше пределы.
Медицинские композиции, содержащие соединение по настоящему изобретению, можно изготавливать, выбрав подходящую лекарственную форму, соответствующую способу введения, в соответствии со способом изготовления выбранной лекарственной формы. В качестве примеров лекарственных форм медицинских композиций, содержащих соединение по настоящему изобретению в качестве основного компонента, можно указать таблетки, порошки, гранулы, капсулы, растворы, сиропы, эликсиры, масляные или водные суспензии для перорального применения.
В случае инъекционного раствора можно при его изготовлении использовать стабилизатор, консервант и средство, способствующее растворению. Раствор, который может содержать указанные вспомогательные вещества, в некоторых случаях может быть также приготовлен в твердой форме, которую помещают в сосуд и затем сушат методом лиофилизации или подобным для последующего приготовления инъекционного раствора перед применением. В сосуд можно также помещать дозу или дозы инъекционного раствора.
В качестве примеров лекарственных форм для наружного применения можно назвать растворы, суспензии, эмульсии, мази, гель, кремы, лосьоны, аэрозоли и пластыри.
Твердый препарат может, кроме соединения по настоящему изобретению, содержать фармацевтически приемлемые добавки. Например, для получения препарата могут быть подходящим образом подобраны и смешаны наполнители, разбавители, связывающие вещества, разрыхлители, ускорители растворения, увлажняющие вещества и т.д.
В качестве примеров лекарственных форм жидкого препарата можно назвать растворы, суспензии и эмульсии. В некоторых случаях они могут содержать суспендирующее средство, эмульгатор и/или тому подобное.
Соединения по настоящему изобретению подробно описаны ниже в следующих пунктах (А)-(Е).
(А): Соединение, представленное общей формулой (1):
Q1-С(=О)-N(R1)-Q2-N(R2)-Т1-Q3, (1)
где
R1 и R2 независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу;
Q1 представляет насыщенную или ненасыщенную 5- или 6-членную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-6-членную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q2 представляет следующую группу:
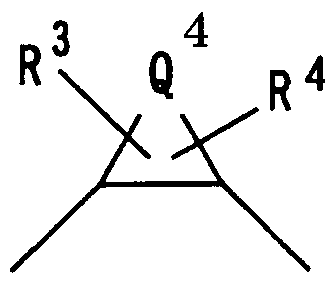
где Q4 означает алкиленовую группу, имеющую 1-8 углеродных атомов, алкениленовую группу, имеющую 2-8 углеродных атомов, или группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом серы, -SO-, -SO2-, -NH-, -O-NH-, ―NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-, и цифры 1 и 2 указывают положения; и R3 и R4 являются заместителями у углеродного атома(ов), атома(ов) азота или атомов серы кольца, содержащего Q4, и независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу, алкенильную группу, алкинильную группу, атом галогена, галогеналкильную группу, цианогруппу, цианалкильную группу, аминогруппу, аминоалкильную группу, N-алкиламиноалкильную группу, N,N-диалкиламиноалкильную группу, ацильную группу, ацилалкильную группу, ациламиногруппу, которая может быть замещенной, алкоксииминогруппу, гидроксииминогруппу, ациламиноалкильную группу, алкоксигруппу, алкоксиалкильную группу, гидроксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, алкоксикарбонильную группу, алкоксикарбонилалкильную группу, алкоксикарбонилалкиламиногруппу, карбоксиалкиламиногруппу, алкоксикарбониламиногруппу, алкоксикарбониламиноалкильную группу, карбамоильную группу, N-алкилкарбамоильную группу, которая может содержать заместитель в алкильной группе, N,N-диалкилкарбамоильную группу, которая может иметь заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильную группу, N-алкенилкарбамоилалкильную группу, N-алкенил-N-алкилкарбамоильную группу, N-алкенил-N-алкилкарбамоилалкильную группу, N-алкоксикарбамоильную группу, N-алкил-N-алкоксикарбамоильную группу, N-алкоксикарбамоилалкильную группу, N-алкил-N-алкоксикарбамоилалкильную группу, карбазоильную группу, которая может быть замещенной 1-3 алкильными группами, алкилсульфонильную группу, алкилсульфонилалкильную группу, 3-6-членную гетероциклическую карбонильную группу, которая может быть замещенной, карбамоилалкильную группу, N-алкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), карбамоилоксиалкильную группу, N-алкилкарбамоилоксиалкильную группу, N,N-диалкилкарбамоилоксиалкильную группу, 3-6-членную гетероциклическую карбонилалкильную группу, которая может быть замещенной, 3-6-членную гетероциклическую карбонилоксиалкильную группу, которая может быть замещенной, арильную группу, аралкильную группу, гетероарильную группу, гетероарилалкильную группу, алкилсульфониламиногруппу, арилсульфониламиногруппу, алкилсульфониламиноалкильную группу, арилсульфониламиноалкильную группу, алкилсульфониламинокарбонильную группу, арилсульфониламинокарбонильную группу, алкилсульфониламинокарбонилалкильную группу, арилсульфониламинокарбонилалкильную группу, оксогруппу, карбамоилоксигруппу, аралкилоксигруппу, карбоксиалкилоксигруппу, ацилоксигруппу, ацилоксиалкильную группу, арилсульфонильную группу, алкоксикарбонилалкилсульфонильную группу, карбоксиалкилсульфонильную группу, алкоксикарбонилацильную группу, алкоксиалкилоксикарбонильную группу, гидроксиацильную группу, алкоксиацильную группу, галогенацильную группу, карбоксиацильную группу, аминоацильную группу, ацилоксиацильную группу, ацилоксиалкилсульфонильную группу, гидроксиалкилсульфонильную группу, алкоксиалкилсульфонильную группу, 3-6-членную гетероциклическую сульфонильную группу, которая может быть замещенной, N-алкиламиноацильную группу, N,N-диалкиламиноацильную группу, N,N-диалкилкарбамоилацильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкилсульфонильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), алкилсульфонилацильную группу или тому подобное, или R3 и R4 вместе друг с другом означают алкиленовую группу, имеющую 1-5 углеродных атомов, алкениленовую группу, имеющую 2-5 углеродных атомов, алкилендиоксигруппу, имеющую 1-5 углеродных атомов, или карбонилдиоксигруппу;
Q3 представляет арильную группу, которая может быть замещенной, арилалкенильную группу, которая может быть замещенной, гетероарильную группу, которая может быть замещенной, гетероарилалкенильную группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной; и
Т1 представляет карбонильную или сульфонильную группу;
его соль, сольват или N-оксид.
(В): Соединение, представленное общей формулой (1):
Q1-Q2-С(=О)-N(R1)-Q3-N(R2)-Т1-Q4, (1)
где
R1 и R2 независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу;
Q1 представляет насыщенную или ненасыщенную 5- или 6-членную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-6-членную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q2 представляет одинарную связь, насыщенную или ненасыщенную 5- или 6-членную двухвалентную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-6-членную двухвалентную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q3 представляет следующую группу:

где Q5 означает алкиленовую группу, имеющую 1-8 углеродных атомов, алкениленовую группу, имеющую 2-8 углеродных атомов, или группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, ―NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-; и R3 и R4 являются заместителями у углеродного атома(ов), атома(ов) азота или атома(ов) серы кольца, содержащего Q5, и независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу, алкенильную группу, алкинильную группу, атом галогена, галогеналкильную группу, цианогруппу, цианалкильную группу, аминогруппу, аминоалкильную группу, N-алкиламиноалкильную группу, N,N-диалкиламиноалкильную группу, ацильную группу, ацилалкильную группу, ациламиногруппу, которая может быть замещенной, алкоксииминогруппу, гидроксииминогруппу, ациламиноалкильную группу, алкоксигруппу, алкоксиалкильную группу, гидроксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, алкоксикарбонильную группу, алкоксикарбонилалкильную группу, алкоксикарбонилалкиламиногруппу, карбоксиалкиламиногруппу, алкоксикарбониламиногруппу, алкоксикарбониламиноалкильную группу, карбамоильную группу, N-алкилкарбамоильную группу, которая может содержать заместитель в алкильной группе, N,N-диалкилкарбамоильную группу, которая может иметь заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильную группу, N-алкенилкарбамоилалкильную группу, N-алкенил-N-алкилкарбамоильную группу, N-алкенил-N-алкилкарбамоилалкильную группу, N-алкоксикарбамоильную группу, N-алкил-N-алкоксикарбамоильную группу, N-алкоксикарбамоилалкильную группу, N-алкил-N-алкоксикарбамоилалкильную группу, карбазоильную группу, которая может быть замещенной 1-3 алкильными группами, алкилсульфонильную группу, алкилсульфонилалкильную группу, 3-6-членную гетероциклическую карбонильную группу, которая может быть замещенной, карбамоилалкильную группу, N-алкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), карбамоилоксиалкильную группу, N-алкилкарбамоилоксиалкильную группу, N,N-диалкилкарбамоилоксиалкильную группу, 3-6-членную гетероциклическую карбонилалкильную группу, которая может быть замещенной, 3-6-членную гетероциклическую карбонилоксиалкильную группу, которая может быть замещенной, арильную группу, аралкильную группу, гетероарильную группу, гетероарилалкильную группу, алкилсульфониламиногруппу, арилсульфониламиногруппу, алкилсульфониламиноалкильную группу, арилсульфониламиноалкильную группу, алкилсульфониламинокарбонильную группу, арилсульфониламинокарбонильную группу, алкилсульфониламинокарбонилалкильную группу, арилсульфониламинокарбонилалкильную группу, оксогруппу, карбамоилоксигруппу, аралкилоксигруппу, карбоксиалкилоксигруппу, ацилоксигруппу, ацилоксиалкильную группу, арилсульфонильную группу, алкоксикарбонилалкилсульфонильную группу, карбоксиалкилсульфонильную группу, алкоксикарбонилацильную группу, алкоксиалкилоксикарбонильную группу, гидроксиацильную группу, алкоксиацильную группу, галогенацильную группу, карбоксиацильную группу, аминоацильную группу, ацилоксиацильную группу, ацилоксиалкилсульфонильную группу, гидроксиалкилсульфонильную группу, алкоксиалкилсульфонильную группу, 3-6-членную гетероциклическую сульфонильную группу, которая может быть замещенной, N-алкиламиноацильную группу, N,N-диалкиламиноацильную группу, N,N-диалкилкарбамоилацильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкилсульфонильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), алкилсульфонилацильную группу или тому подобное, или R3 и R4 вместе друг с другом означают алкиленовую группу, имеющую 1-5 углеродных атомов, алкениленовую группу, имеющую 2-5 углеродных атомов, алкилендиоксигруппу, имеющую 1-5 углеродных атомов, или карбонилдиоксигруппу;
Q4 представляет арильную группу, которая может быть замещенной, арилалкенильную группу, которая может быть замещенной, гетероарильную группу, которая может быть замещенной, гетероарилалкенильную группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной; и
Т1 представляет карбонильную, сульфонильную группу или группу -С(=О)-С(=О)-N(R')-, где R' означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу;
его соль, сольват или N-оксид.
(С): Соединение, представленное общей формулой (1):
Q1-Q2-С(=О)-N(R1)-Q3-N(R2)-Т1-Q4, (1)
где
R1 и R2 независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу;
Q1 представляет насыщенную или ненасыщенную 5- или 6-членную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q2 представляет одинарную связь, насыщенную или ненасыщенную 5- или 6-членную двухвалентную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную двухвалентную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q3 представляет следующую группу:

в которой Q5 означает алкиленовую группу, имеющую 1-8 углеродных атомов, алкениленовую группу, имеющую 2-8 углеродных атомов, или группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, ―NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-; и R3 и R4 являются заместителями у углеродного атома(ов), атома(ов) азота или атома(ов) серы кольца, содержащего Q5, и независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу, алкенильную группу, алкинильную группу, атом галогена, галогеналкильную группу, цианогруппу, цианалкильную группу, аминогруппу, аминоалкильную группу, N-алкиламиноалкильную группу, N,N-диалкиламиноалкильную группу, ацильную группу, ацилалкильную группу, ациламиногруппу, которая может быть замещенной, алкоксииминогруппу, гидроксииминогруппу, ациламиноалкильную группу, алкоксигруппу, алкоксиалкильную группу, гидроксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, алкоксикарбонильную группу, алкоксикарбонилалкильную группу, алкоксикарбонилалкиламиногруппу, карбоксиалкиламиногруппу, алкоксикарбониламиногруппу, алкоксикарбониламиноалкильную группу, карбамоильную группу, N-алкилкарбамоильную группу, которая может содержать заместитель в алкильной группе, N,N-диалкилкарбамоильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильную группу, N-алкенилкарбамоилалкильную группу, N-алкенил-N-алкилкарбамоильную группу, N-алкенил-N-алкилкарбамоилалкильную группу, N-алкоксикарбамоильную группу, N-алкил-N-алкоксикарбамоильную группу, N-алкоксикарбамоилалкильную группу, N-алкил-N-алкоксикарбамоилалкильную группу, карбазоильную группу, которая может быть замещенной 1-3 алкильными группами, алкилсульфонильную группу, алкилсульфонилалкильную группу, 3-6-членную гетероциклическую карбонильную группу, которая может быть замещенной, карбамоилалкильную группу, N-алкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), карбамоилоксиалкильную группу, N-алкилкарбамоилоксиалкильную группу, N,N-диалкилкарбамоилоксиалкильную группу, 3-6-членную гетероциклическую карбонилалкильную группу, которая может быть замещенной, 3-6-членную гетероциклическую карбонилоксиалкильную группу, которая может быть замещенной, арильную группу, аралкильную группу, гетероарильную группу, гетероарилалкильную группу, алкилсульфониламиногруппу, арилсульфониламиногруппу, алкилсульфониламиноалкильную группу, арилсульфониламиноалкильную группу, алкилсульфониламинокарбонильную группу, арилсульфониламинокарбонильную группу, алкилсульфониламинокарбонилалкильную группу, арилсульфониламинокарбонилалкильную группу, оксогруппу, карбамоилоксигруппу, аралкилоксигруппу, карбоксиалкилоксигруппу, ацилоксигруппу, ацилоксиалкильную группу, арилсульфонильную группу, алкоксикарбонилалкилсульфонильную группу, карбоксиалкилсульфонильную группу, алкоксикарбонилацильную группу, алкоксиалкилоксикарбонильную группу, гидроксиацильную группу, алкоксиацильную группу, галогенацильную группу, карбоксиацильную группу, аминоацильную группу, ацилоксиацильную группу, ацилоксиалкилсульфонильную группу, гидроксиалкилсульфонильную группу, алкоксиалкилсульфонильную группу, 3-6-членную гетероциклическую сульфонильную группу, которая может быть замещенной, N-алкиламиноацильную группу, N,N-диалкиламиноацильную группу, N,N-диалкилкарбамоилацильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкилсульфонильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), алкилсульфонилацильную группу или тому подобное, или R3 и R4 вместе друг с другом означают алкиленовую группу, имеющую 1-5 углеродных атомов, алкениленовую группу, имеющую 2-5 углеродных атомов, алкилендиоксигруппу, имеющую 1-5 углеродных атомов, или карбонилдиоксигруппу;
Q4 представляет арильную группу, которая может быть замещенной, арилалкенильную группу, которая может быть замещенной, арилалкинильную группу, которая может быть замещенной, гетероарильную группу, которая может быть замещенной, гетероарилалкенильную группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной; и
Т1 представляет карбонильную, сульфонильную группу, группу -С(=О)-С(=О)-N(R')-, где R' означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-А1-N(R")-, где А1 означает алкиленовую группу, имеющую 1-5 углеродных атомов, которая может быть замещенной, и R" означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-NH-, группу -С(=S)-NH-, группу -С(=О)-NH-NH-, группу -С(=О)-А2-С(=О)-, где А2 означает одинарную связь или алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-А3-С(=О)-NH-, где А3 означает алкиленовую группу, имеющую 1-5 углеродных атомов, или тиокарбонильную группу;
его соль, сольват или N-оксид.
(D): Соединение, представленное общей формулой (1):
Q1-Q2-Т0-N(R1)-Q3-N(R2)-Т1-Q4, (1)
где
R1 и R2 независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу;
Q1 представляет насыщенную или ненасыщенную 5- или 6-членную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q2 представляет одинарную связь, насыщенную или ненасыщенную 5- или 6-членную двухвалентную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную двухвалентную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q3 представляет следующую группу:

где Q5 означает алкиленовую группу, имеющую 1-8 углеродных атомов, алкениленовую группу, имеющую 2-8 углеродных атомов, или группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, ―NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-; и R3 и R4 являются заместителями у углеродного атома(ов), атома(ов) азота или атома(ов) серы кольца, содержащего Q5, и независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу, алкенильную группу, алкинильную группу, атом галогена, галогеналкильную группу, цианогруппу, цианалкильную группу, аминогруппу, аминоалкильную группу, N-алкиламиноалкильную группу, N,N-диалкиламиноалкильную группу, ацильную группу, ацилалкильную группу, ациламиногруппу, которая может быть замещенной, алкоксииминогруппу, гидроксииминогруппу, ациламиноалкильную группу, алкоксигруппу, алкоксиалкильную группу, гидроксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, алкоксикарбонильную группу, алкоксикарбонилалкильную группу, алкоксикарбонилалкиламиногруппу, карбоксиалкиламиногруппу, алкоксикарбониламиногруппу, алкоксикарбониламиноалкильную группу, карбамоильную группу, N-алкилкарбамоильную группу, которая может содержать заместитель в алкильной группе, N,N-диалкилкарбамоильную группу, которая может иметь заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильную группу, N-алкенилкарбамоилалкильную группу, N-алкенил-N-алкилкарбамоильную группу, N-алкенил-N-алкилкарбамоилалкильную группу, N-алкоксикарбамоильную группу, N-алкил-N-алкоксикарбамоильную группу, N-алкоксикарбамоилалкильную группу, N-алкил-N-алкоксикарбамоилалкильную группу, карбазоильную группу, которая может быть замещенной 1-3 алкильными группами, алкилсульфонильную группу, алкилсульфонилалкильную группу, 3-6-членную гетероциклическую карбонильную группу, которая может быть замещенной, карбамоилалкильную группу, N-алкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), карбамоилоксиалкильную группу, N-алкилкарбамоилоксиалкильную группу, N,N-диалкилкарбамоилоксиалкильную группу, 3-6-членную гетероциклическую карбонилалкильную группу, которая может быть замещенной, 3-6-членную гетероциклическую карбонилоксиалкильную группу, которая может быть замещенной, арильную группу, аралкильную группу, гетероарильную группу, гетероарилалкильную группу, алкилсульфониламиногруппу, арилсульфониламиногруппу, алкилсульфониламиноалкильную группу, арилсульфониламиноалкильную группу, алкилсульфониламинокарбонильную группу, арилсульфониламинокарбонильную группу, алкилсульфониламинокарбонилалкильную группу, арилсульфониламинокарбонилалкильную группу, оксогруппу, карбамоилоксигруппу, аралкилоксигруппу, карбоксиалкилоксигруппу, ацилоксигруппу, ацилоксиалкильную группу, арилсульфонильную группу, алкоксикарбонилалкилсульфонильную группу, карбоксиалкилсульфонильную группу, алкоксикарбонилацильную группу, алкоксиалкилоксикарбонильную группу, гидроксиацильную группу, алкоксиацильную группу, галогенацильную группу, карбоксиацильную группу, аминоацильную группу, ацилоксиацильную группу, ацилоксиалкилсульфонильную группу, гидроксиалкилсульфонильную группу, алкоксиалкилсульфонильную группу, 3-6-членную гетероциклическую сульфонильную группу, которая может быть замещенной, N-алкиламиноацильную группу, N,N-диалкиламиноацильную группу, N,N-диалкилкарбамоилацильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкилсульфонильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), или алкилсульфонилацильную группу, или R3 и R4 вместе друг с другом означают алкиленовую группу, имеющую 1-5 углеродных атомов, алкениленовую группу, имеющую 2-5 углеродных атомов, алкилендиоксигруппу, имеющую 1-5 углеродных атомов, или карбонилдиоксигруппу;
Q4 представляет арильную группу, которая может быть замещенной, арилалкенильную группу, которая может быть замещенной, арилалкинильную группу, которая может быть замещенной, гетероарильную группу, которая может быть замещенной, гетероарилалкенильную группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Т0 представляет карбонильную или тиокарбонильную группу; и
Т1 представляет карбонильную группу, сульфонильную группу, группу -С(=О)-С(=О)-N(R')-, группу -С(=S)-С(=О)-N(R')-, группу -С(=О)-С(=S)-N(R')-, группу -С(=S)-С(=S)-N(R')-, где R' означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-А1-N(R")-, где А1 означает алкиленовую группу, имеющую 1-5 углеродных атомов, которая может быть замещенной, и R" означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-NH-, группу -С(=S)-NH-, группу -С(=О)-NH-NH-, группу -С(=О)-А2-С(=О)-, где А2 означает одинарную связь или алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-А3-С(=О)-NH-, где А3 означает алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-С(=NORа)-N(Rb)-, группу -С(=S)-С(=NORа)-N(Rb)-, где Rа означает атом водорода, алкильную группу или алканоильную группу и Rb означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-N=N-, группу -С(=S)-N=N-, или тиокарбонильную группу;
его соль, сольват или N-оксид.
(Е): Соединение, представленное общей формулой (1):
Q1-Q2-Т0-N(R1)-Q3-N(R2)-Т1-Q4, (1)
где
R1 и R2 независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу;
Q1 представляет насыщенную или ненасыщенную 5- или 6-членную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q2 представляет одинарную связь, насыщенную или ненасыщенную 5- или 6-членную двухвалентную циклическую углеводородную группу, которая может быть замещенной, насыщенную или ненасыщенную 5-7-членную двухвалентную гетероциклическую группу, которая может быть замещенной, насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную двухвалентную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Q3 представляет следующую группу:

в которой Q5 означает алкиленовую группу, имеющую 1-8 углеродных атомов, алкениленовую группу, имеющую 2-8 углеродных атомов, или группу -(СН2)m-СН2-А-СН2-(СН2)n-, где m и n независимо друг от друга равны 0 или целому числу 1-3 и А означает атом кислорода, атом азота, атом серы, -SO-, -SO2-, -NH-, -O-NH-, ―NH-NH-, -S-NH-, -SO-NH- или -SO2-NH-; и R3 и R4 являются заместителями у углеродного атома(ов), атома(ов) азота или атома(ов) серы кольца, содержащего Q5, и независимо друг от друга представляют атом водорода, гидроксильную группу, алкильную группу, алкенильную группу, алкинильную группу, атом галогена, галогеналкильную группу, цианогруппу, цианалкильную группу, аминогруппу, аминоалкильную группу, N-алкиламиноалкильную группу, N,N-диалкиламиноалкильную группу, ацильную группу, ацилалкильную группу, ациламиногруппу, которая может быть замещенной, алкоксииминогруппу, гидроксииминогруппу, ациламиноалкильную группу, алкоксигруппу, алкоксиалкильную группу, гидроксиалкильную группу, карбоксильную группу, карбоксиалкильную группу, алкоксикарбонильную группу, алкоксикарбонилалкильную группу, алкоксикарбонилалкиламиногруппу, карбоксиалкиламиногруппу, алкоксикарбониламиногруппу, алкоксикарбониламиноалкильную группу, карбамоильную группу, N-алкилкарбамоильную группу, которая может содержать заместитель в алкильной группе, N,N-диалкилкарбамоильную группу, которая может иметь заместитель в алкильной(ых) группе(ах), N-алкенилкарбамоильную группу, N-алкенилкарбамоилалкильную группу, N-алкенил-N-алкилкарбамоильную группу, N-алкенил-N-алкилкарбамоилалкильную группу, N-алкоксикарбамоильную группу, N-алкил-N-алкоксикарбамоильную группу, N-алкоксикарбамоилалкильную группу, N-алкил-N-алкоксикарбамоилалкильную группу, карбазоильную группу, которая может быть замещенной 1-3 алкильными группами, алкилсульфонильную группу, алкилсульфонилалкильную группу, 3-6-членную гетероциклическую карбонильную группу, которая может быть замещенной, карбамоилалкильную группу, N-алкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), карбамоилоксиалкильную группу, N-алкилкарбамоилоксиалкильную группу, N,N-диалкилкарбамоилоксиалкильную группу, 3-6-членную гетероциклическую карбонилалкильную группу, которая может быть замещенной, 3-6-членную гетероциклическую карбонилоксиалкильную группу, которая может быть замещенной, арильную группу, аралкильную группу, гетероарильную группу, гетероарилалкильную группу, алкилсульфониламиногруппу, арилсульфониламиногруппу, алкилсульфониламиноалкильную группу, арилсульфониламиноалкильную группу, алкилсульфониламинокарбонильную группу, арилсульфониламинокарбонильную группу, алкилсульфониламинокарбонилалкильную группу, арилсульфониламинокарбонилалкильную группу, оксогруппу, карбамоилоксигруппу, аралкилоксигруппу, карбоксиалкилоксигруппу, ацилоксигруппу, ацилоксиалкильную группу, арилсульфонильную группу, алкоксикарбонилалкилсульфонильную группу, карбоксиалкилсульфонильную группу, алкоксикарбонилацильную группу, алкоксиалкилоксикарбонильную группу, гидроксиацильную группу, алкоксиацильную группу, галогенацильную группу, карбоксиацильную группу, аминоацильную группу, ацилоксиацильную группу, ацилоксиалкилсульфонильную группу, гидроксиалкилсульфонильную группу, алкоксиалкилсульфонильную группу, 3-6-членную гетероциклическую сульфонильную группу, которая может быть замещенной, N-алкиламиноацильную группу, N,N-диалкиламиноацильную группу, N,N-диалкилкарбамоилацильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), N,N-диалкилкарбамоилалкилсульфонильную группу, которая может содержать заместитель в алкильной(ых) группе(ах), или алкилсульфонилацильную группу, или R3 и R4 вместе друг с другом означают алкиленовую группу, имеющую 1-5 углеродных атомов, алкениленовую группу, имеющую 2-5 углеродных атомов, алкилендиоксигруппу, имеющую 1-5 углеродных атомов, или карбонилдиоксигруппу;
Q4 представляет арильную группу, которая может быть замещенной, арилалкенильную группу, которая может быть замещенной, арилалкинильную группу, которая может быть замещенной, гетероарильную группу, которая может быть замещенной, гетероарилалкенильную группу, которая может быть замещенной, насыщенную или ненасыщенную бициклическую или трициклическую конденсированную углеводородную группу, которая может быть замещенной, или насыщенную или ненасыщенную бициклическую или трициклическую конденсированную гетероциклическую группу, которая может быть замещенной;
Т0 представляет карбонильную или тиокарбонильную группу; и
Т1 представляет карбонильную группу, сульфонильную группу, группу -С(=О)-С(=О)-N(R')-, группу -С(=S)-С(=О)-N(R')-, группу -С(=О)-С(=S)-N(R')-, группу -С(=S)-С(=S)-N(R')-, где R' означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-А1-N(R")-, где А1 означает алкиленовую группу, имеющую 1-5 углеродных атомов, которая может быть замещенной, и R" означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-NH-, группу -С(=S)-NH-, группу -С(=О)-NH-NH-, группу -С(=О)-А2-С(=О)-, где А2 означает одинарную связь или алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-А3-С(=О)-NH-, где А3 означает алкиленовую группу, имеющую 1-5 углеродных атомов, группу -С(=О)-С(=NORа)-N(Rb)-, группу -С(=S)-С(=NORа)-N(Rb)-, где Rа означает атом водорода, алкильную группу или алканоильную группу и Rb означает атом водорода, гидроксильную группу, алкильную группу или алкоксигруппу, группу -С(=О)-N=N-, группу -С(=S)-N=N-, или тиокарбонильную группу;
его соль, сольват или N-оксид.
Далее настоящее изобретение описано следующими ссылочными примерами, примерами и примерами испытаний. Но настоящее изобретение не ограничивается данными примерами.
[Ссылочный пример 1]
трет-Бутил пиридин-4-илкарбамат
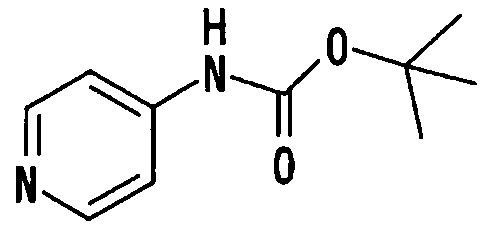
4-Аминопиридин (10 г) растворяли в тетрагидрофуране (500 мл), к раствору добавляли ди-трет-бутилдикарбонат (25,5 г) и смесь перемешивали при комнатной температуре в течение 10 минут. Полученную реакционную смесь концентрировали при пониженном давлении и выпавшие в осадок твердые частицы промывали гексаном с получением указанного в заголовке соединения (16,9 г).
1Н-ЯМР (CDCl3) δ: 1,53 (9Н, с), 6,86 (1Н, шир.с), 7,30 (2Н, дд, J=1,5, 4,9Гц), 8,44 (2Н, дд, J=1,5, 4,9Гц).
МС (FAB) m/z: 195 (М+Н)+.
[Ссылочный пример 2]
трет-Бутил 3-сульфанилпиридин-4-илкарбамат
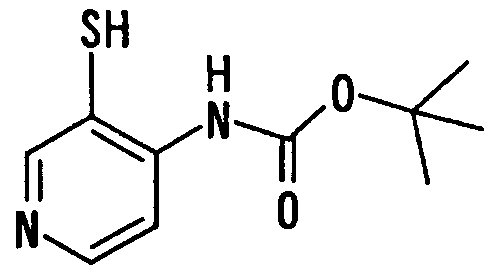
Соединение (61,6 г), полученное в ссылочном примере 1, растворяли в тетрагидрофуране (2000 мл) и раствор перемешивали при -78°C в течение 10 минут. К раствору добавляли по каплям гексановый раствор (1,59 моль/л, 500 мл) н-бутиллития и смесь перемешивали 10 минут и затем 2 часа при охлаждении льдом. Затем реакционную смесь охлаждали до -78°C, добавляли порошок серы (12,2 г) и полученную смесь нагревали до комнатной температуры и перемешивали в течение 1 часа. В реакционную смесь добавляли воду (1000 мл) для отделения водного слоя. Затем к водному слою добавляли 3N хлористоводородную кислоту, доводя рН водного слоя до 3-4, добавляли метиленхлорид для отделения органического слоя. Органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 50:1) с получением указанного в заголовке соединения (33,2 г).
1Н-ЯМР (ДМСО-d6) δ: 1,52 (9Н, с), 7,89 (1Н, д, J=6,4Гц), 7,99 (1Н, д, J=6,4Гц), 8,20 (1Н, с), 9,91 (1Н, шир.с).
МС (FAB) m/z: 227 (М+Н)+.
[Ссылочный пример 3]
Тиазоло[5,4-c]пиридин
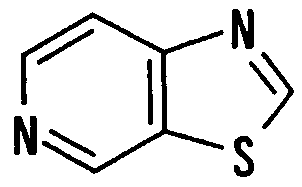
Соединение (33,2 г), полученное в ссылочном примере 2, растворяли в муравьиной кислоте (250 мл) и раствор кипятили с обратным холодильником в течение 3 дней. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли 5N водный раствор (100 мл) гидроксида калия и диэтиловый эфир для отделения органического слоя. Органический слой сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 25:1) с получением указанного в заголовке соединения (9,03 г).
1Н-ЯМР (CDCl3) δ: 8,05 (1Н, д, J=5,4Гц), 8,70 (1Н, д, J=5,4Гц), 9,23 (1Н, с), 9,34 (1Н, с).
МС (FAB) m/z: 137 (М+Н)+.
[Ссылочный пример 4]
5-Метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин
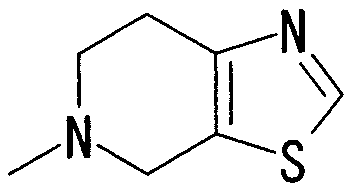
Соединение (1,61 г), полученное в ссылочном примере 3, растворяли в N,N-диметилформамиде (50 мл), к раствору добавляли метилиодид (1,50 мл) и полученную смесь перемешивали при 80°C в течение 4 часов. Реакционную смесь концентрировали при пониженном давлении и остаток растворяли в метаноле (100 мл), добавляли боргидрид натрия (1,53 г) и полученную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли насыщенный водный раствор карбоната калия и диэтиловый эфир для отделения органического слоя. Органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 25:1) с получением указанного в заголовке соединения (1,28 г).
1Н-ЯМР (CDCl3) δ: 2,52 (3Н, с), 2,83 (2Н, т, J=5,9Гц), 2,98 (2Н, т, J=5,9Гц), 3,70 (2Н, с), 8,63 (1Н, с).
МС (FAB) m/z: 155 (М+Н)+.
[Ссылочный пример 5]
5-Метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксилат лития
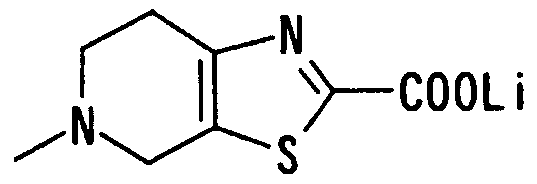
Соединение (6,43 г), полученное в ссылочном примере 4, растворяли в абсолютном тетрагидрофуране (200 мл), к раствору добавляли по каплям при -78°C раствор н-бутиллития (1,47N гексановый раствор, 34,0 мл) и полученную смесь перемешивали в течение 40 минут. После барботирования через реакционную смесь газообразного диоксида углерода при -78°C в течение 1 часа реакционную смесь нагревали до комнатной температуры и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения (9,42 г).
1Н-ЯМР (ДМСО-d6) δ: 2,37 (3Н, с), 2,64-2,77 (4Н, м), 3,54 (2Н, с).
МС (FAB) m/z: 199 (М+Н)+.
[Ссылочный пример 6]
трет-Бутил 2-амино-6,7-дигидротиазоло[5,4-c]пиридин-5[4Н]-карбоксилат
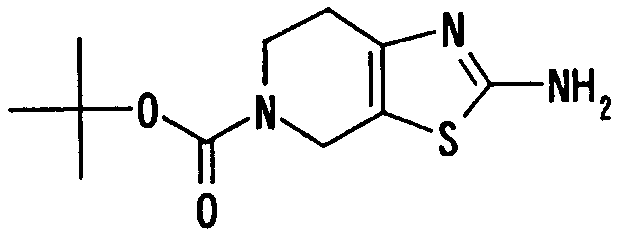
1-трет-Бутоксикарбонил-4-пиперидон (40,0 г) растворяли в циклогексане (80 мл) и к раствору добавляли моногидрат п-толуолсульфоновой кислоты (191 мг) и пирролидин (17,6 мл). Смесь кипятили с обратным холодильником в течение 2 часов, удаляя воду с помощью ловушки Дина-Старка. Затем реакционную смесь концентрировали при пониженном давлении, остаток растворяли в метаноле (60 мл) и добавляли порошок серы (6,42 г). К раствору медленно добавляли по каплям при охлаждении льдом метанольный раствор (10 мл) цианамида (8,44 г) и смесь перемешивали при комнатной температуре в течение 5 часов. Выпавшее в осадок твердое вещество отфильтровывали с получением указанного в заголовке соединения (31,0 г).
1Н-ЯМР (ДМСО-d6) δ: 1,41 (9Н, с), 2,44 (2Н, т, J=5,6Гц), 3,57 (2Н, т, J=5,6Гц), 4,29 (2Н, с), 6,79 (2Н, с).
МС (EI) m/z: 255 (М+).
[Ссылочный пример 7]
трет-Бутил 2-бром-6,7-дигидротиазоло[5,4-c]пиридин-5[4Н]-карбоксилат
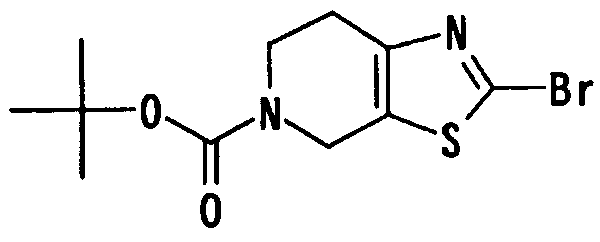
Бромид меди(II) (1,05 г) суспендировали в N,N-диметилформамиде (20 мл), добавляли при охлаждении льдом трет-бутилнитрит (0,696 мл) и соединение (1,00 г), полученное в ссылочном примере 6, и реакционную смесь нагревали и перемешивали при 40°C в течение 30 минут. Реакционную смесь концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:5) с получением указанного в заголовке соединения (568 мг).
1Н-ЯМР (CDCl3) δ: 1,48 (9Н, с), 2,85 (2Н, шир.с), 3,72 (2Н, шир.с), 4,56 (2Н, шир.с).
МС (FAB) m/z: 319 (М+Н)+.
[Ссылочный пример 8]
Трифторацетат 2-бром-4,5,6,7-тетрагидротиазоло[5,4-c]пиридина
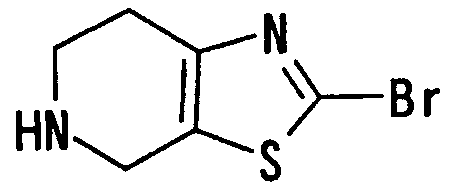
Соединение (890 мг), полученное в ссылочном примере 7, растворяли в метиленхлориде (2 мл), к раствору добавляли трифторуксусную кислоту (15 мл) и смесь перемешивали при комнатной температуре в течение 30 секунд. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли диэтиловый эфир. Выпавшее в осадок твердое вещество отфильтровывали с получением указанного в заголовке соединения (867 мг).
1Н-ЯМР (ДМСО-d6) δ: 2,98 (2Н, т, J=6,1Гц), 3,45 (2Н, т, J=6,1Гц), 4,35 (2Н, с), 9,53 (2Н, шир.с).
МС (FAB) m/z: 219 (М+Н)+.
[Ссылочный пример 9]
2-Бром-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин
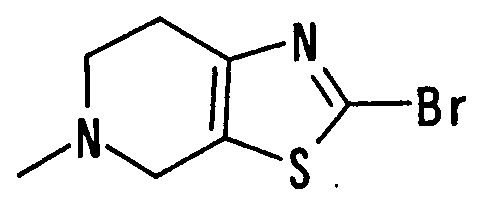
Соединение (422 мг), полученное в ссылочном примере 8, суспендировали в метиленхлориде (10 мл) и добавляли триэтиламин (0,356 мл) для получения раствора. К раствору последовательно добавляли уксусную кислоту (0,216 мл), водный раствор (35% раствор, 0,202 мл) формальдегида и триацетоксиборгидрид (428 мг) натрия и полученную смесь перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли насыщенный водный раствор (100 мл) гидрокарбоната натрия, метиленхлорид (100 мл) и 3N водный раствор (3 мл) гидроксида натрия для разделения жидкости. Затем органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3) с получением указанного в заголовке соединения (286 мг).
1Н-ЯМР (CDCl3) δ: 2,49 (3Н, с), 2,79 (2Н, т, J=5,7Гц), 2,85-2,93 (2Н, м), 3,58 (2Н, т, J=1,8Гц).
МС (FAB) m/z: 233 (М+Н)+.
[Ссылочный пример 10]
5-Метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксилат лития
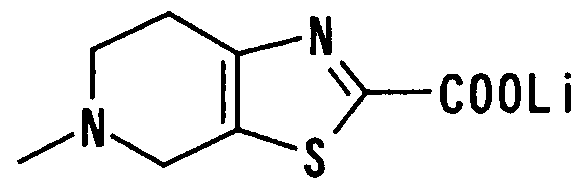
Соединение (531 мг), полученное в ссылочном примере 9, растворяли в абсолютном диэтиловом эфире (20 мл), добавляли по каплям при -78°C н-бутиллитий (1,54N гексановый раствор, 1,63 мл) и смесь перемешивали в течение 30 минут при охлаждении льдом. После барботирования через реакционную смесь диоксида углерода при -78°C в течение 10 минут смесь нагревали до комнатной температуры. Реакционную смесь концентрировали при пониженном давлении с получением указанного в заголовке соединения (523 мг).
1Н-ЯМР (ДМСО-d6) δ: 2,37 (3Н, с), 2,64-2,85 (4Н, м), 3,54 (2Н, с).
[Ссылочный пример 11]
Этил 2-[(Е)-2-фенилэтенил]оксазол-4-карбоксилат
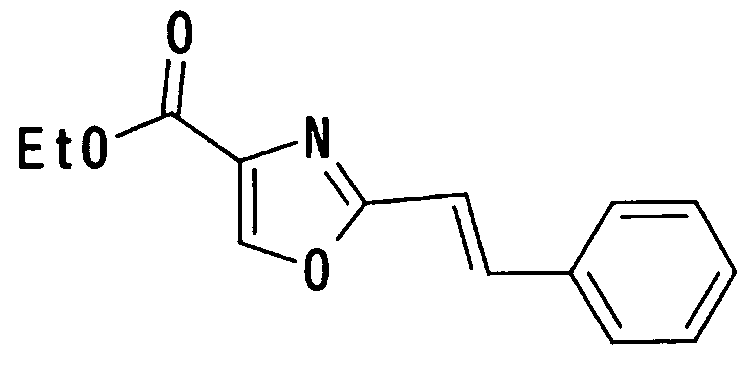
Синтез проводили в соответствии с методикой (Panek et al. J. Org. Chem., 1996, Vol. 61, p. 6496). Гидрокарбонат натрия (22,8 г) и этилбромпируват (10,5 мл) добавляли к раствору циннамамида (10,0 г) в тетрагидрофуране (250 мл) при комнатной температуре и смесь кипятили с обратным холодильником в течение 48 часов. Реакционной смеси давали остыть до комнатной температуры, фильтровали через Целит и затем концентрировали при пониженном давлении с получением остатка. Трифторуксусный ангидрид (30 мл) добавляли к раствору полученного остатка в тетрагидрофуране (30 мл) при 0°C и смесь постепенно нагревали до комнатной температуры. Затем смесь перемешивали 63 часа, добавляли к реакционной смеси насыщенный водный раствор (500 мл) гидрокарбоната натрия и этилацетат (150 мл) и отделяли водный слой. Водный слой экстрагировали этилацетатом (150 мл). Органические слои объединяли, промывали насыщенным водным раствором хлорида натрия (150 мл), сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 5:1 → 3:1) с получением указанного в заголовке соединения (10,9 г).
1Н-ЯМР (CDCl3) δ: 1,41 (3Н, т, J=7,0Гц), 4,42 (2Н, кв, J=7,0Гц), 6,96 (1Н, д, J=16,6Гц), 7,30-7,40 (3Н, м), 7,53 (2Н, д, J=6,8Гц), 7,63 (1Н, д, J=16,6Гц), 8,20 (1Н, с).
[Ссылочный пример 12]
2-[(Е)-2-Фенилэтенил]оксазол-4-карбальдегид
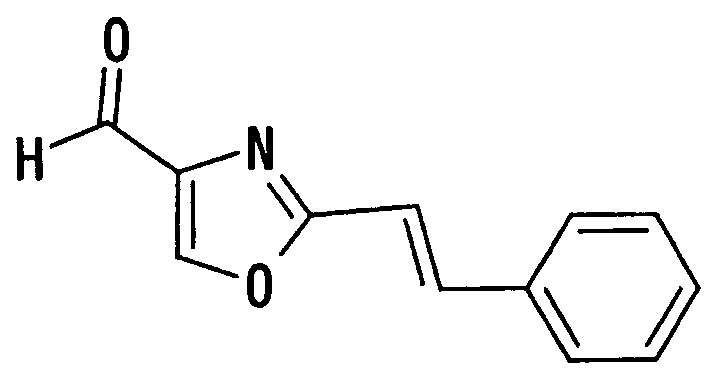
Гидрид диизобутилалюминия (1,0N гексановый раствор, 66 мл) добавляли по каплям к раствору соединения (8,57 г), полученного в ссылочном примере 11, в метиленхлориде (80 мл) при -78°C. Через 15 минут добавляли по каплям метанол (11 мл) и смесь нагревали до комнатной температуры в течение 1 часа. Реакционную смесь фильтровали через Целит и полученное пастообразное вещество растворяли в этилацетате (200 мл), добавляли насыщенный водный раствор (200 мл) хлорида аммония и отделяли водный слой. Водный слой затем экстрагировали метиленхлоридом (2 х 100 мл). Полученные органические слои отделяли и промывали насыщенным водным раствором (100 мл) гидрокарбоната натрия и насыщенным водным раствором хлорида натрия (100 мл), объединяли с фильтратом, полученным фильтрованием через Целит, и затем сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:этилацетат = 5:1 → метиленхлорид:метанол = 10:1) с получением указанного в заголовке соединения (5,86 г).
1Н-ЯМР (CDCl3) δ: 6,96 (1Н, д, J=16,6Гц), 7,35-7,45 (3Н, м), 7,56 (2Н, д, J=6,4Гц), 7,67 (1Н, д, J=16,6Гц), 8,26 (1Н, с), 9,98 (1Н, с).
МС (FAB) m/z: 200 (М+Н)+.
[Ссылочный пример 13]
2-[(Е)-2-Фенилэтенил]-4-винилоксазол
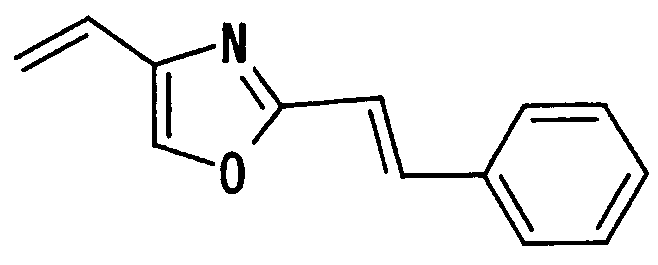
н-Бутиллитий (1,54N гексановый раствор, 14,2 мл) добавляли по каплям к раствору бромида метилтрифенилфосфония (8,16 г) в тетрагидрофуране (80 мл) при 0°C и смесь перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь охлаждали снова до 0°C, добавляли раствор соединения (3,64 г), полученного в ссылочном примере 12, в тетрагидрофуране (20 мл) и смесь нагревали до комнатной температуры. После перемешивания в течение 2 часов добавляли воду (200 мл) и этилацетат (100 мл) и отделяли водный слой. Водный слой экстрагировали этилацетатом (50 мл). Затем органические слои объединяли, промывали насыщенным водным раствором хлорида натрия (100 мл), сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1 → 3:1) с получением указанного в заголовке соединения (2,84 г).
1Н-ЯМР (CDCl3) δ: 5,33 (1Н, дд, J=1,5, 10,7Гц), 5,98 (1Н, дд, J=1,5, 17,6Гц), 6,56 (1Н, дд, J=10,7, 17,6Гц), 6,95 (1Н, д, J=16,6Гц), 7,31-7,42 (3Н, м), 7,49-7,56 (4Н, м).
МС (FAB) m/z: 198 (М+Н)+.
[Ссылочный пример 14]
2-{2-[(Е)-2-Фенилэтенил]оксазол-4-ил}-1-этанол
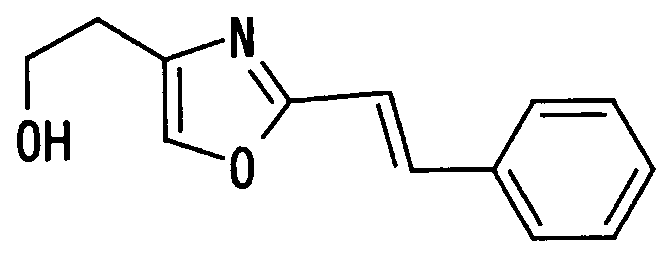
9-Борабицикло[3.3.1]нонан (0,5N тетрагидрофурановый раствор, 158 мл) добавляли к раствору соединения (13,0 г), полученного в ссылочном примере 13, в тетрагидрофуране (500 мл) и смесь перемешивали при комнатной температуре в течение 15 часов. Воду (10 мл), 3N водный раствор (80 мл) гидроксида натрия и водный пероксид водорода (80 мл) последовательно добавляли по каплям к реакционной смеси при 0°C и смесь перемешивали при комнатной температуре в течение 6 часов. Затем к полученной реакционной смеси добавляли воду (600 мл) и этилацетат (200 мл) для отделения водного слоя и водный слой экстрагировали этилацетатом (200 мл). Затем органические слои отделяли, промывали насыщенным водным раствором хлорида натрия (200 мл), сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 2:1 → только этилацетат) с получением указанного в заголовке соединения (14,1 г).
1Н-ЯМР (CDCl3) δ: 2,69 (1Н, шир.с), 2,80 (2Н, т, J=5,6Гц), 3,90-3,97 (2Н, м), 6,91 (1Н, д, J=16,6Гц), 7,30-7,42 (4Н, м), 7,43-7,56 (3Н, м).
МС (FAB) m/z: 216 (М+Н)+.
[Ссылочный пример 15]
2-(2-{2-[(Е)-2-Фенилэтенил]оксазол-4-ил}этил)-1Н-изоиндол-1,3(2Н)-дион
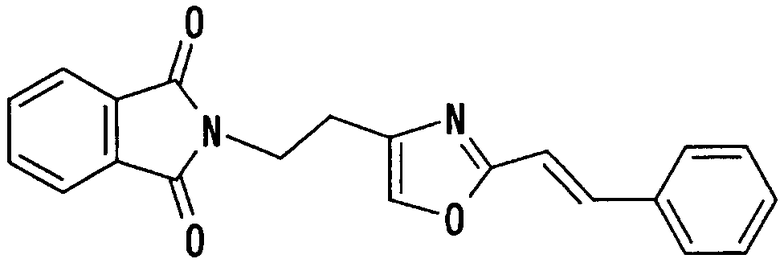
Фталимид (200 мг), трифенилфосфин (357 мг) и диэтилазодикарбоксилат (0,214 мл) добавляли к раствору соединения (292 мг), полученного в ссылочном примере 14, в тетрагидрофуране (15 мл) при комнатной температуре и смесь перемешивали 4 часа. Растворитель реакционной смеси отгоняли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1) с получением указанного в заголовке соединения (447 мг).
1Н-ЯМР (CDCl3) δ: 2,98 (2Н, т, J=7,2Гц), 4,03 (2Н, т, J=7,2Гц), 6,88 (1Н, д, J=16,6Гц), 7,28-7,45 (5Н, м), 7,48 (2Н, д, J=7,3Гц), 7,71 (2Н, дд, J=2,9, 5,4Гц), 7,84 (2Н, дд, J=2,9, 5,4Гц).
МС (FAB) m/z: 345 (М+Н)+.
[Ссылочный пример 16]
трет-Бутил 2-{2-[(Е)-2-фенилэтенил]оксазол-4-ил}этилкарбамат
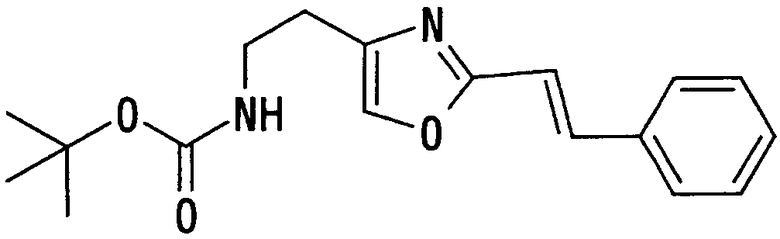
После добавления моногидрата гидразина (1,50 мл) к раствору соединения (6,40 г), полученного в ссылочном примере 15, в этаноле (150 мл) при комнатной температуре смесь перемешивали в течение 1 часа, снова добавляли моногидрат гидразина (0,500 мл) при комнатной температуре и смесь перемешивали 2 часа. Метиленхлорид (150 мл), насыщенный водный раствор (150 мл) гидрокарбоната натрия и ди-трет-бутилдикарбонат (13,4 г) добавляли к реакционной смеси при комнатной температуре. После перемешивания в течение 30 минут водный слой отделяли и экстрагировали метиленхлоридом (50 мл). Полученные органические слои объединяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 2:1 → 1:1) с получением указанного в заголовке соединения (5,06 г).
1Н-ЯМР (CDCl3) δ: 1,45 (9Н, с), 2,75 (2Н, т, J=6,6Гц), 3,46 (2Н, дт, J=5,9, 6,6Гц), 4,92 (1Н, шир.с), 6,91 (1Н, д, J=16,6Гц), 7,29-7,45 (4Н, м), 7,48 (1Н, д, J=16,6Гц), 7,52 (2Н, д, J=7,3Гц).
МС (FAB) m/z: 315 (М+Н)+, 259 (М-изобутен+Н)+, 315 (М-Вос+Н)+.
[Ссылочный пример 17]
трет-Бутил 2-[(Е)-2-фенилэтенил]-6,7-дигидрооксазоло[5,4-c]пиридин-5(4Н)-карбоксилат
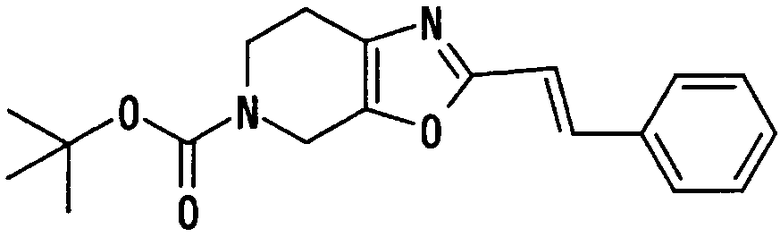
Параформ (54,5 мг) и п-толуолсульфоновую кислоту (7,2 мг) добавляли к раствору соединения (190 мг), полученного в ссылочном примере 16, в толуоле (15 мл) при комнатной температуре. После кипячения с обратным холодильником в течение 1 часа реакционной смеси давали остыть и этилацетат (15 мл) и насыщенный водный раствор (15 мл) гидрокарбоната натрия добавляли к реакционной смеси, чтобы отделить водный слой. После экстрагирования водного слоя этилацетатом (10 мл) полученные органические слои объединяли, сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1 → 2:1) с получением указанного в заголовке соединения (153 мг).
1Н-ЯМР (CDCl3) δ: 1,50 (9Н, с), 2,67 (2Н, шир.с), 3,73 (2Н, шир.с), 4,55 (2Н, с), 6,90 (1Н, д, J=16,1Гц), 7,29-7,42 (3Н, м), 7,46 (1Н, д, J=16,1Гц), 7,52 (2Н, д, J=7,3Гц).
МС (FAB) m/z: 327 (М+Н)+, 271 (М-изобутен+Н)+, 227 (М-Вос+Н)+.
[Ссылочный пример 18]
трет-Бутил 2-формил-6,7-дигидрооксазоло[5,4-c]пиридин-5(4Н)-карбоксилат
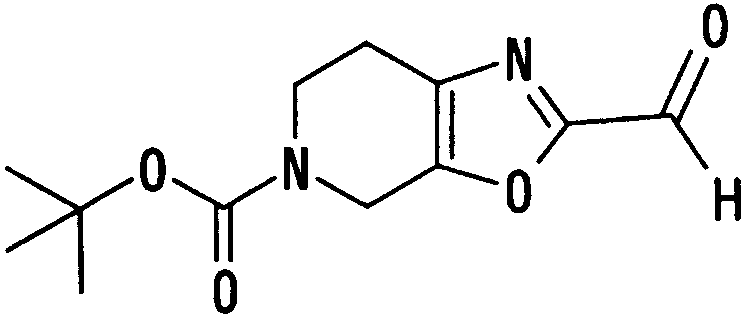
Ацетон (8,0 мл), воду (4,0 мл), N-оксид N-метилморфолина (577 мг) и 0,039М водный раствор (3,20 мл) тетроксида осмия добавляли к раствору соединения (803 мг), полученного в ссылочном примере 17, в тетрагидрофуране (16 мл) при комнатной температуре и смесь перемешивали в течение ночи. Этилацетат (50 мл) и 10% водный раствор (50 мл) тиосульфата натрия добавляли к реакционной смеси, чтобы отделить водный слой. Затем водный слой экстрагировали этилацетатом (30 мл). Затем полученные органические слои объединяли, сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Метанол (8,0 мл), воду (8,0 мл) и метапериодат натрия (790 мг) добавляли к раствору остатка в тетрагидрофуране (16 мл). После перемешивания в течение 3 часов этилацетат (30 мл) и воду (50 мл) добавляли к реакционной смеси, чтобы отделить водный слой. Водный слой экстрагировали этилацетатом (20 мл). После объединения полученных органических слоев, промывания насыщенным водным раствором (50 мл) гидрокарбоната натрия и сушки над безводным сульфатом натрия отгоняли растворитель при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1 → 2:1) с получением указанного в заголовке соединения (234 мг). Так как полученный альдегид был неустойчивым, его сразу же использовали в следующей реакции.
1Н-ЯМР (CDCl3) δ: 1,49 (9Н, с), 2,77 (2Н, шир.с), 3,77 (2Н, шир.с), 4,62 (2Н, с), 9,70 (1Н, с).
[Ссылочный пример 19]
5-трет-Бутил 2-метил-6,7-дигидрооксазоло[5,4-c]пиридин-2,5(4Н)-дикарбоксилат
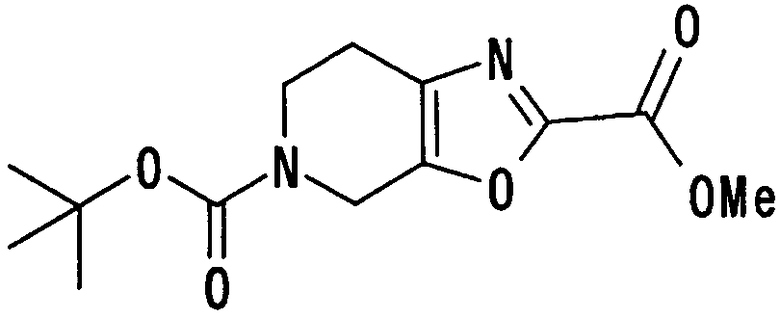
Цианид натрия (220 мг) и диоксид марганца (780 мг) добавляли к раствору соединения (225 мг), полученного в ссылочном примере 18, в метаноле (9,0 мл) при комнатной температуре. После перемешивания в течение 30 минут реакционную смесь фильтровали через Целит с этилацетатом. Фильтрат промывали водой (50 мл) и насыщенным водным раствором хлорида натрия (50 мл) и сушили над безводным сульфатом натрия. Затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:2 → 1:1) с получением указанного в заголовке соединения (120 мг).
1Н-ЯМР (CDCl3) δ: 1,49 (9Н, с), 2,73 (2Н, шир.с), 3,74 (2Н, шир.с), 4,01 (3Н, с), 4,59 (2Н, с).
МС (FAB) m/z: 283 (М+Н)+.
[Ссылочный пример 20]
Метил 5-метил-4,5,6,7-тетрагидрооксазоло[5,4-c]пиридин-2-карбоксилат
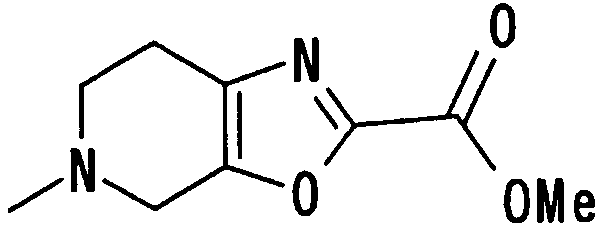
Трифторуксусную кислоту (15 мл) добавляли к раствору соединения (500 мг), полученного в ссылочном примере 19, в метиленхлориде (15 мл) при комнатной температуре и смесь перемешивали 10 минут. Реакционную смесь концентрировали при пониженном давлении и к полученному остатку добавляли при комнатной температуре метиленхлорид (20 мл), триэтиламин (0,495 мл), уксусную кислоту (205 мл), формалин (0,230 мл) и триацетоксиборгидрид натрия (570 мг). После перемешивания в течение 15 минут добавляли метиленхлорид (20 мл) и насыщенный водный раствор (50 мл) гидрокарбоната натрия, чтобы отделить органический слой. Водный слой экстрагировали метиленхлоридом (3 х 20 мл). Затем полученные органические слои объединяли и сушили над безводным сульфатом натрия, растворитель отгоняли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 20:1 → 10:1) с получением указанного в заголовке соединения (257 мг).
1Н-ЯМР (CDCl3) δ: 2,52 (3Н, с), 2,72-2,78 (2Н, м), 2,78-2,83 (2Н, м), 3,61 (2Н, т, J=1,7Гц), 4,00 (3Н, с).
МС (FAB) m/z: 197 (М+Н)+, 165 (М-ОСН3)+.
[Ссылочный пример 21]
5-Метил-4,5,6,7-тетрагидрооксазоло[5,4-c]пиридин-2-карбоксилат лития
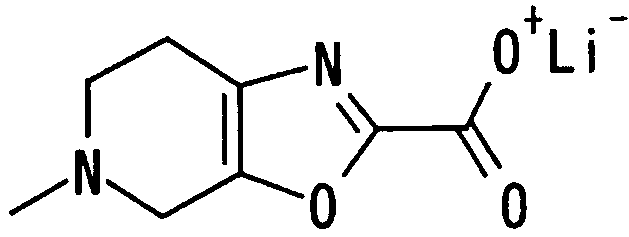
Воду (6,0 мл) и гидроксид лития (99,7 мг) добавляли к раствору соединения (800 мг), полученного в ссылочном примере 20, в тетрагидрофуране (24 мл) при комнатной температуре и смесь перемешивали в течение 10 минут. Реакционную смесь концентрировали при пониженном давлении с получением указанного в заголовке соединения (825 мг).
1Н-ЯМР (ДМСО-d6) δ: 2,37 (3Н, с), 2,47 (2Н, т, J=5,6Гц), 2,64 (2Н, т, J=5,6Гц), 3,43 (2Н, с).
[Ссылочный пример 22]
Метил 5-хлор-6-фториндол-2-карбоксилат
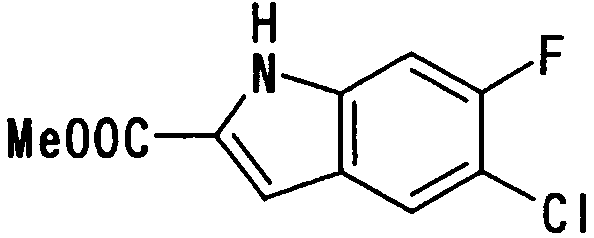
Смесь метил 3-хлор-4-фтор-α-азидоциннамата (выложенная заявка № 149723/1995 на патент Японии) (1,85 г) и ксилола (140 мл) кипятили с обратным холодильником в течение 1 часа и затем отгоняли растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид) с получением указанного в заголовке соединения (491 мг).
1Н-ЯМР (CDCl3) δ: 3,95 (3Н, с), 7,13-7,15 (1Н, м), 7,20 (1Н, дд, J=9,3, 0,49Гц), 7,71 (1Н, д, J=7,3Гц), 8,93 (1Н, шир.с).
МС (FAB) m/z: 227 М+.
[Ссылочный пример 23]
5-Хлор-6-фториндол-2-карбоновая кислота
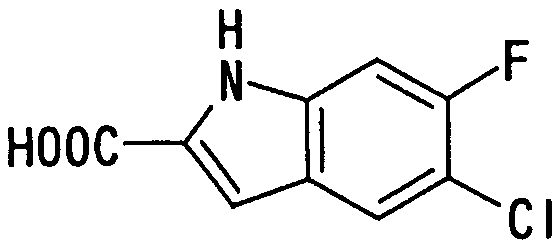
Соединение (461 мг), полученное в ссылочном примере 22, растворяли в смешанном растворителе из тетрагидрофурана (15 мл), метанола (10 мл) и воды (10 мл), добавляли при комнатной температуре гидроксид лития (283 мг) и смесь перемешивали 4 часа. Растворитель отгоняли при пониженном давлении и к остатку добавляли 1N хлористоводородную кислоту для слабого его подкисления. Полученный порошок отфильтровывали и сушили с получением указанного в заголовке соединения (422 мг).
1Н-ЯМР (CDCl3) δ: 7,08-7,10 (1Н, м), 7,34 (1Н, д, J=9,5Гц), 7,88 (1Н, д, J=7,6Гц), 12,04 (1Н, с), 13,16 (1Н, с).
МС (FAB) m/z: 213 (М+).
[Ссылочный пример 24]
5-(Пиридин-4-ил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин
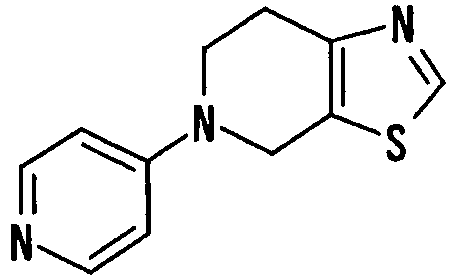
1) Дифосфорпентасульфид (500 мг) суспендировали в формамиде (3000 мл) при охлаждении льдом и суспензию перемешивали в течение ночи. К реакционной смеси добавляли воду и диэтиловый эфир, органический слой отделяли, сушили над безводным сульфатом магния и отгоняли растворитель с получением масла. После растворения масла в н-бутаноле (350 мл) и добавления к раствору этил 3-хлор-4-оксо-1-пиперидинкарбоксилата (150 г), синтезированного способом, описанным в литературе (Tetrahedron, 1983, Vol. 39, p. 3767), полученную смесь перемешивали при 100°C в течение 2,5 часов. Реакционную смесь фильтровали через Целит. Фильтрат промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид → этилацетат:гексан = 1:2) с получением этил 6,7-дигидротиазоло[5,4-c]пиридин-5-(4Н)-карбоксилата (79,0 г).
1Н-ЯМР (CDCl3) δ: 1,30 (3Н, т, J=7,3Гц), 2,96 (2Н, шир.с), 3,82 (2Н, шир.с), 4,19 (2Н, кв, J=7,3Гц), 4,73 (2Н, шир.с), 8,68 (1Н, с).
МС (FAB) m/z: 213 (М+Н)+.
2) К полученному выше продукту реакции (33,5 г) добавляли 3,5N водный раствор (250 мл) гидроксида натрия и смесь кипятили с обратным холодильником в течение ночи. Затем реакционную смесь охлаждали до комнатной температуры, добавляли ди-трет-бутилдикарбонат (103 г) при охлаждении льдом и смесь перемешивали в течение ночи при комнатной температуре. К реакционной смеси добавляли 3N хлористоводородную кислоту, доводя рН до 1-2, затем добавляли метиленхлорид. После отделения органического слоя его промывали последовательно водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Затем органический слой концентрировали при пониженном давлении, полученный остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:2) с получением трет-бутил 6,7-дигидротиазоло[5,4-c]пиридин-5-(4Н)-карбоксилата (21,1 г).
1Н-ЯМР (CDCl3) δ: 1,49 (9Н, с), 2,94 (2Н, шир.с), 3,76 (2Н, шир.с), 4,68 (2Н, с), 8,67 (1Н, с).
МС (FAB) m/z: 241 (М+Н)+.
3) Трифторуксусную кислоту (25 мл) добавляли к раствору соединения (5,00 г), полученного на стадии 2), в метиленхлориде (25 мл) при комнатной температуре. После перемешивания смеси в течение 10 минут реакционную смесь концентрировали при пониженном давлении и к полученному остатку при комнатной температуре добавляли 4-бромпиридин (5,20 г), N,N-диметилформамид (30 мл) и триэтиламин (15,5 мл) и смесь перемешивали при 150°C в течение 2 дней, затем давали ей остыть до комнатной температуры. Бесцветные осадки отделяли фильтрованием и фильтрат концентрировали при пониженном давлении. Затем к остатку добавляли метиленхлорид (50 мл) и насыщенный водный раствор (100 мл) гидрокарбоната натрия и полученный водный слой насыщали хлоридом натрия. После отделения органического слоя полученный водный слой экстрагировали метиленхлоридом (5 х 30 мл). Полученные органические слои объединяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1 → 8:1) с получением указанного в заголовке соединения (2,97 г).
1Н-ЯМР (CDCl3) δ: 3,07 (2Н, т, J=5,9Гц), 3,81 (2Н, т, J=5,9Гц), 4,61 (2Н, с), 6,74 (2Н, т, J=6,5Гц), 8,30 (2Н, т, J=6,5Гц), 8,70 (1Н, с).
МС (ESI) m/z: 218 (М+Н)+.
[Ссылочный пример 25]
2-Хлор-6,7-дигидро-4Н-пирано[4,3-d]тиазол
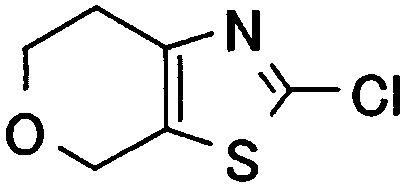
1) Тетрагидро-4Н-пиран-4-он (5,0 г) растворяли в циклогексане (20 мл) и к раствору добавляли пирролидин (4,35 мл) и моногидрат п-толуолсульфоновой кислоты (48 мг), затем смесь кипятили с обратным холодильником в течение 70 минут, удаляя при этом воду с помощью ловушки Дина-Старка. Реакционную смесь охлаждали до комнатной температуры и супернатант отбирали и концентрировали при пониженном давлении. Остаток растворяли в метаноле (15 мл) и к раствору добавляли при охлаждении льдом порошок серы (1,60 г). Через 15 минут добавляли по каплям в течение 20 минут метанольный раствор (10 мл) цианамида (2,10 г) и смесь перемешивали 3 дня. Отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1 → 10:1 → 4:1) с получением 6,7-дигидро-4Н-пирано[4,3-d]тиазол-2-иламина (3,97 г).
1Н-ЯМР (CDCl3) δ: 2,66-2,70 (2Н, м), 3,97 (2Н, т, J=5,6Гц), 4,63 (2Н, с), 4,94 (2Н, шир.с).
МС (FAB) m/z: 157 (М+Н)+.
2) Хлорид меди(II) (4,10 г) растворяли в ацетонитриле (50 мл) и к раствору добавляли трет-бутилнитрит (3,93 г) одной порцией при охлаждении льдом. Через 10 минут к смеси добавляли примерно за 1 час соединение (3,97 г), полученное по описанной выше реакции, и реакционную смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь нагревали до 65°C и непрерывно перемешивали в течение 2 часов. После добавления в реакционную смесь силикагеля (20 г) отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1) с получением указанного в заголовке соединения (1,78 г).
1Н-ЯМР (CDCl3) δ: 2,85-2,89 (2Н, м), 4,02 (2Н, т, J=5,6Гц), 4,73 (2Н, с).
МС (FAB) m/z: 175 (М+Н)+.
[Ссылочный пример 26]
6,7-Дигидро-4Н-пирано[4,3-d]тиазол-2-карбоксилат лития
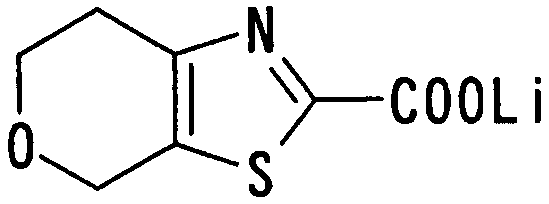
1) Соединение (1,78 г), полученное в ссылочном примере 25, растворяли в метаноле (30 мл) и к раствору добавляли 10% палладий на углероде (300 мг) и ацетат натрия (830 мг). Смесь перемешивали 5 дней в токе водорода при 5 атм. После отделения катализатора фильтрованием растворитель концентрировали и остаток подвергали колоночной хроматографии на силикагеле (гексан:этилацетат = 2:1) с получением 6,7-дигидро-4Н-пирано[4,3-d]тиазола (1,14 г).
1Н-ЯМР (CDCl3) δ: 2,97-3,01 (2Н, м), 4,04 (2Н, т, J=5,6Гц), 4,87 (2Н, с), 8,69 (1Н, с).
МС (FAB) m/z: 142 (М+Н)+.
2) После растворения продукта (1,14 г), полученного, как описано выше, в диэтиловом эфире (30 мл) и охлаждения до -78°С добавляли к раствору 1,6М бутиллитий (6,6 мл) и смесь перемешивали. Через 20 минут проводили барботирование диоксидом углерода в течение 15 минут. Реакционную смесь нагревали до комнатной температуры и концентрировали при пониженном давлении с получением указанного в заголовке соединения (1,65 г).
1Н-ЯМР (ДМСО-d6) δ: 2,83 (2Н, т, J=5,6Гц), 3,92 (2Н, т, J=5,6Гц), 4,73 (2Н, с).
[Ссылочный пример 27]
Тиазоло[4,5-c]пиридин
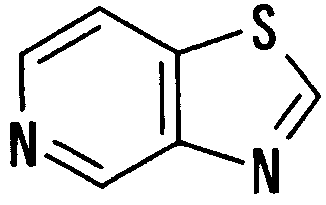
3-(трет-Бутоксикарбониламино)-4-меркаптопиридин (выложенная заявка № 321691/1992 на патент Японии) (9,20 г) растворяли в муравьиной кислоте (60 мл) и раствор кипятили с обратным холодильником в течение 4 часов. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли 5N водный раствор (100 мл) гидроксида калия и диэтиловый эфир для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. К остатку добавляли диэтиловый эфир и выпавшие в осадок твердые частицы отфильтровывали с получением указанного в заголовке соединения (3,97 г).
1Н-ЯМР (CDCl3) δ: 7,93 (1Н, д, J=5,4Гц), 8,60 (1Н, д, J=5,4Гц), 9,07 (1Н, с), 9,46 (1Н, с).
[Ссылочный пример 28]
5-Метил-4,5,6,7-тетрагидротиазоло[4,5-c]пиридин

Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 27, подобно способу ссылочного примера 4.
1Н-ЯМР (CDCl3) δ: 2,52 (3Н, с), 2,77 (2Н, т, J=5,4Гц), 2,92-3,00 (2Н, м), 3,69 (2Н, т, J=2,0Гц), 8,61 (1Н, с).
МС (FAB) m/z: 155 (М+Н)+.
[Ссылочный пример 29]
5-Метил-4,5,6,7-тетрагидротиазоло[4,5-c]пиридин-2-карбоксилат лития
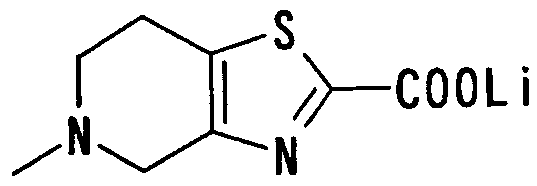
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 28, подобно способу ссылочного примера 5.
1Н-ЯМР (ДМСО-d6) δ: 2,38 (3Н, с), 2,64 (2Н, шир.с), 2,80 (2Н, шир.с), 3,44 (2Н, шир.с).
[Ссылочный пример 30]
2-Хлор-N,N-диметил-4,5,6,7-тетрагидробензотиазол-6-амин
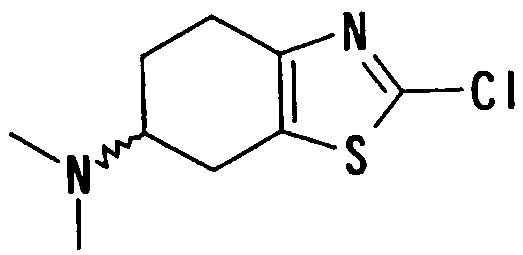
2-Хлор-4,7-дигидро-1,3-бензотиазол-6(5Н)-он (Helv. Cim. Acta., 1994, Vol. 77, p. 1256) (2,0 г) растворяли в метаноле (100 мл) и, добавив ацетат аммония (8,2 г) и цианоборгидрид натрия (4,0 г), смесь кипятили с обратным холодильником в течение 20 часов. К реакционной смеси добавляли хлористоводородную кислоту для разложения избыточного цианоборгидрида натрия, затем отгоняли при пониженном давлении растворитель. Остаток подщелачивали 1N раствором гидроксида натрия и затем экстрагировали метиленхлоридом. Полученный органический слой сушили над безводным сульфатом магния и отгоняли при пониженном давлении растворитель с получением бледно-желтого масла. Полученное масло растворяли в метаноле (50 мл), добавляли водный раствор (4,29 г) формальдегида и цианоборгидрид натрия (3,49 г) и смесь перемешивали при комнатной температуре в течение 12 часов. Растворитель отгоняли при пониженном давлении, к остатку добавляли метиленхлорид и органический слой промывали насыщенным водным раствором гидрокарбоната натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 10:1) с получением указанного в заголовке соединения (740 мг).
1Н-ЯМР (CDCl3) δ: 1,71-1,78 (1Н, м), 2,10-2,19 (1Н, м), 2,35 (6Н, с), 2,66-2,94 (5Н, м).
МС (FAB) m/z: 217 (М+Н)+.
[Ссылочный пример 31]
6-(Диметиламино)-4,5,6,7-тетрагидробензотиазол-2-карбоксилат лития
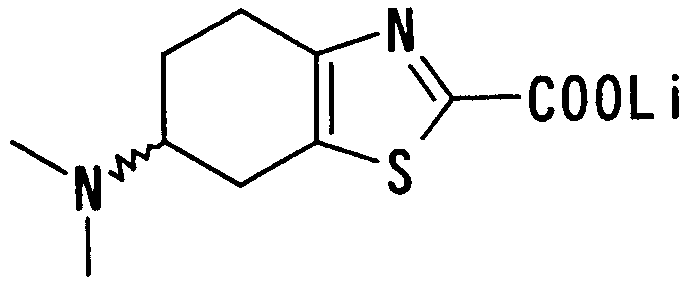
После растворения соединения (750 мг), полученного в ссылочном примере 30, в диэтиловом эфире (15 мл) и охлаждения раствора до -78°C добавляли 1,5N трет-бутиллитий (3,5 мл), смесь перемешивали 20 минут и затем барботировали диоксид углерода в течение примерно 15 минут. Реакционную смесь нагревали до комнатной температуры и концентрировали при пониженном давлении с получением указанного в заголовке соединения.
1Н-ЯМР (ДМСО-d6) δ: 1,75-1,78 (1Н, м), 1,98-2,07 (1Н, м), 2,50 (6Н, с), 2,64-2,88 (5Н, м).
[Ссылочный пример 32]
трет-Бутил 2-амино-4,6-дигидро-5Н-пирроло[3,4-d]тиазол-5-карбоксилат
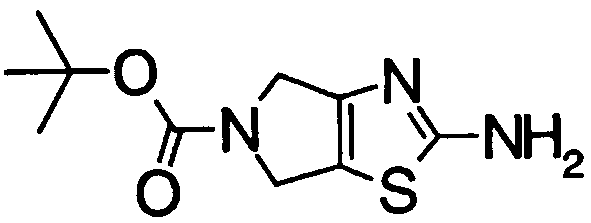
1-трет-Бутоксикарбонил-3-пирролидон (1,58 г) растворяли в циклогексане (10 мл), добавляли моногидрат п-толуолсульфоновой кислоты (8,12 мг) и пирролидин (607 мг) и смесь кипятили с обратным холодильником в течение 1,5 часов, удаляя при этом воду с помощью ловушки Дина-Старка. Супернатант отбирали и концентрировали при пониженном давлении, затем остаток растворяли в метаноле (5 мл) и добавляли порошок серы (274 мг). Смесь перемешивали 15 минут при охлаждении льдом. Метанольный раствор (2 мл) цианамида (377 мг) медленно по каплям добавляли к реакционной смеси и смесь перемешивали в течение ночи при комнатной температуре. Смесь кипятили с обратным холодильником еще 2 часа, реакционную смесь концентрировали и добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:39) с получением указанного в заголовке соединения (248 мг).
1Н-ЯМР (CDCl3) δ: 1,50 (9Н, с), 4,34-4,37 (1Н, м), 4,40-4,45 (1Н, м), 4,49-4,55 (2Н, м), 4,99 (2Н, м).
[Ссылочный пример 33]
трет-Бутил 2-бром-4,6-дигидро-5Н-пирроло[3,4-d]тиазол-5-карбоксилат
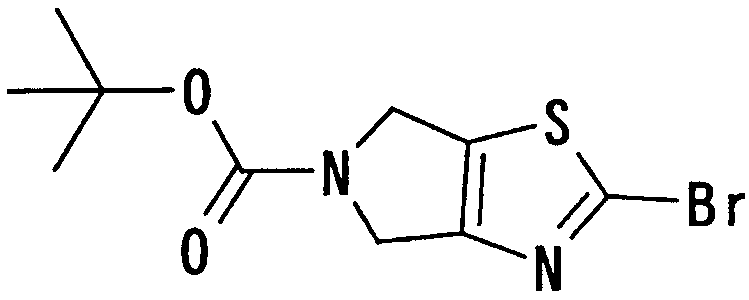
Бромид меди(II) (445 мг) суспендировали в N,N-диметилформамиде и добавляли по каплям при комнатной температуре трет-бутилнитрит (256 мг). Затем N,N-диметилформамидный раствор (1 мл) соединения (400 мг), полученного в ссылочном примере 32, добавляли при охлаждении льдом и реакционную смесь нагревали и перемешивали при 60°C в течение 1,5 часов. К реакционной смеси добавляли диэтиловый эфир и насыщенный водный раствор хлорида натрия и полученный органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанного в заголовке соединения (174 мг).
1Н-ЯМР (CDCl3) δ: 1,51 (9Н, с), 4,52-4,55 (1Н, м), 4,57-4,67 (3Н, м).
МС (FAB) m/z: 305 (М+Н)+.
[Ссылочный пример 34]
(5-трет-Бутоксикарбонил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксилат лития
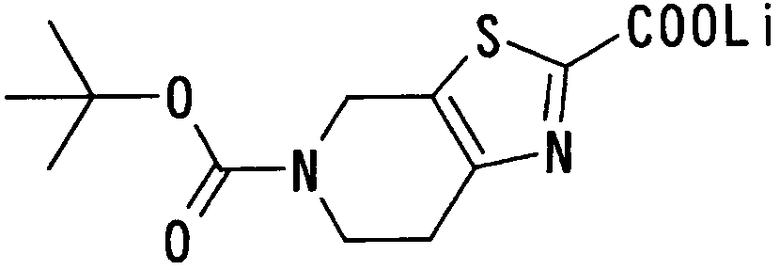
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 7, подобно способу ссылочного примера 10.
1Н-ЯМР (ДМСО-d6) δ: 1,42 (9Н, с), 2,69-2,77 (2Н, м), 3,60-3,68 (2Н, м), 4,51-4,58 (2Н, м).
[Ссылочный пример 35]
Метил 2-бром-4-(2-метокси-2-оксоэтил)тиазол-5-карбоксилат
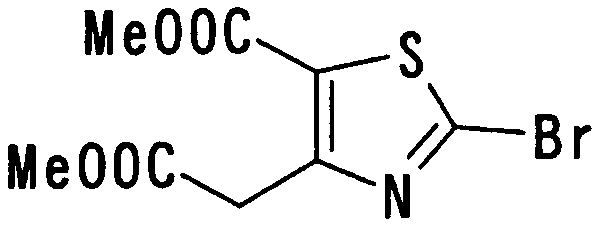
Хлорид меди(II) (26,8 г) добавляли к раствору трет-бутилнитрита (15,5 г) в ацетонитриле (500 мл) одной порцией при охлаждении льдом. К реакционной смеси добавляли по каплям за 45 минут раствор метил 2-амино-5-метоксикарбонилтиазол-4-ацетата (Yakugaku Zasshi, 1966, Vol. 86, p. 300) (23,0 г) в ацетонитриле (500 мл) и полученную смесь перемешивали в течение 1 часа при охлаждении льдом и 30 минут при комнатной температуре. Растворитель концентрировали и к остатку добавляли 10% хлористоводородную кислоту и диэтиловый эфир для отделения органического слоя. Органический слой сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанного в заголовке соединения (25,9 г).
1Н-ЯМР (CDCl3) δ: 3,73 (3Н, с), 3,87 (3Н, с), 4,21 (2Н, с).
[Ссылочный пример 36]
2-[5-(Гидроксиметил)тиазол-4-ил]-1-этанол
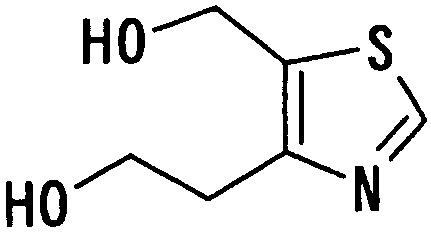
Раствор соединения (23,4 г), полученного в ссылочном примере 35, в тетрагидрофуране (500 мл) добавляли по каплям за 1 час к суспензии литийалюминийгидрида (9,03 г) в тетрагидрофуране (500 мл) при охлаждении льдом. После перемешивания в течение еще 1 часа при охлаждении льдом последовательно добавляли воду (9 мл), 35% водный раствор (9 мл) гидроксида натрия и воду (27 мл) и смесь перемешивали при комнатной температуре в течение 1 часа. После добавления к реакционной смеси безводного сульфата магния и перемешивания полученной смеси удаляли фильтрованием через Целит нерастворимое вещество и фильтрат концентрировали. Остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 7:93) с получением указанного в заголовке соединения (8,64 г).
1Н-ЯМР (CDCl3) δ: 3,01 (2Н, т, J=5,5Гц), 3,30 (1Н, шир.с), 3,57 (1Н, шир.с), 3,90 (2Н, шир.с), 4,75 (2Н, шир.с), 8,66 (1Н, с).
МС (ESI) m/z: 160 (М+Н)+.
[Ссылочный пример 37]
2-(5-{[(Метилсульфонил)окси]метил}тиазол-4-ил)этилметансульфонат
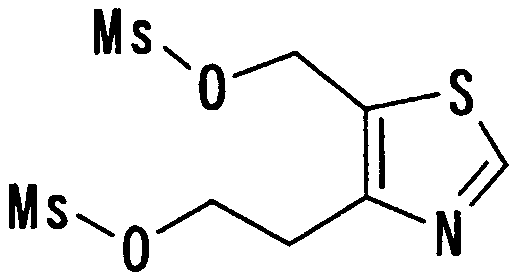
Метиленхлоридный раствор метансульфонилхлорида (12,6 мл) добавляли по каплям к раствору соединения (8,64 г), полученного в ссылочном примере 36, и триэтиламина (45,4 мл), в метиленхлориде (500 мл) за 20 минут при -78°C. После перемешивания реакционной смеси в течение 15 минут при -78°C и в течение 1 часа при 0°C добавляли воду для отделения органического слоя. Органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (13,4 г).
1Н-ЯМР (CDCl3) δ: 2,93 (3Н, с), 3,03 (3Н, с), 3,28 (2Н, т, J=6,3Гц), 4,61 (2Н, т, J=6,3Гц), 5,44 (2Н, с), 8,84 (1Н, с).
[Ссылочный пример 38]
5-(1-Метилциклопропил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин
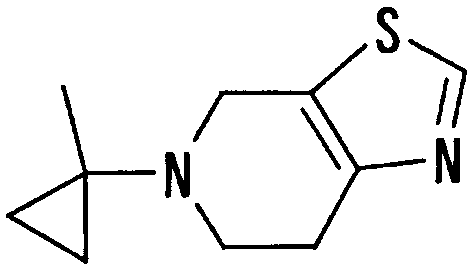
Гидрохлорид 1-метилциклопропиламина (J. Org. Chem., 1989, Vol. 54, p. 1815) (1,89 г) добавляли к метиленхлориду (20 мл), содержащему соединение, полученное в ссылочном примере 37 (4,46 г), при охлаждении льдом и смесь перемешивали при комнатной температуре в течение ночи. Дополнительно добавляли гидрохлорид 1-метилциклопропиламина (1,89 г) и смесь перемешивали 20 часов при комнатной температуре и 5 часов при кипении с обратным холодильником. К реакционной смеси добавляли метиленхлорид и воду, чтобы отделить органический слой. Органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:49) с получением указанного в заголовке соединения (944 мг).
1Н-ЯМР (CDCl3) δ: 0,40-0,50 (2Н, м), 0,68-0,73 (2Н, м), 1,16 (3Н, с), 2,88-2,94 (2Н, м), 3,03 (2Н, т, J=5,7 Гц), 3,89 (2Н, шир.с), 8,60 (1Н, с).
МС (ESI) m/z: 195 (М+Н)+.
[Ссылочный пример 39]
5-(1-Метилциклопропил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксилат лития
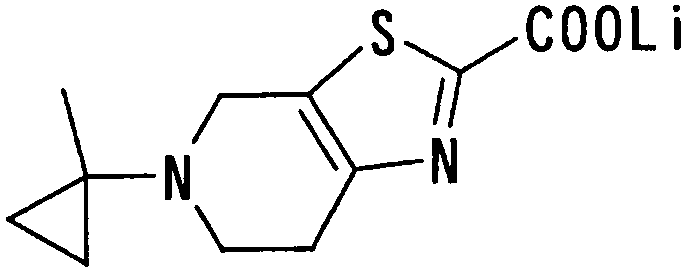
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 38, подобно способу ссылочного примера 5.
1Н-ЯМР (ДМСО-d6) δ: 0,39 (2Н, шир.с), 0,56 (2Н, шир.с), 1,10 (3Н, шир.с), 2,66 (2Н, шир.с), 2,89 (2Н, шир.с), 3,75 (2Н, шир.с).
[Ссылочный пример 40]
2-[6,7-Дигидротиазоло[5,4-c]пиридин-5(4Н)-ил]-2-метил-1-пропанол
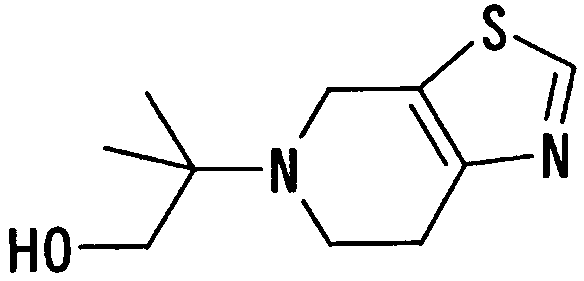
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 37, и 2-амино-2-метил-1-пропанола подобно способу ссылочного примера 38.
1Н-ЯМР (CDCl3) δ: 1,15 (6Н, с), 2,91 (4Н, с), 3,45 (2Н, с), 3,87 (2Н, с), 8,63 (1Н, с).
[Ссылочный пример 41]
5-(2-{[трет-Бутил(дифенил)силил]окси}-1,1-диметилэтил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин
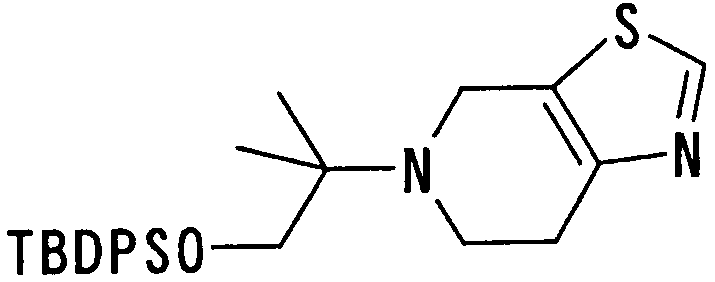
трет-Бутилхлордифенилсилан (1,93 г) и имидазол (994 мг) добавляли к раствору соединения, полученного в ссылочном примере 40 (1,24 г), в N,N-диметилформамиде (5 мл) при комнатной температуре и смесь перемешивали в течение ночи. Добавляли к реакционной смеси воду и диэтиловый эфир, чтобы отделить органический слой. Органический слой сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 1:2) с получением указанного в заголовке соединения (2,46 г).
1Н-ЯМР (CDCl3) δ: 1,07 (9Н, с), 1,15 (6Н, с), 2,83-2,90 (2Н, м), 2,93-3,00 (2Н, м), 3,63 (2Н, с), 3,97 (2Н, с), 7,35-7,48 (6Н, м), 7,63-7,70 (4Н, м), 8,58 (1Н, с).
МС (ESI) m/z: 451 (М+Н)+.
[Ссылочный пример 42]
5-(2-{[трет-Бутил(дифенил)силил]окси}-1,1-диметилэтил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксилат лития
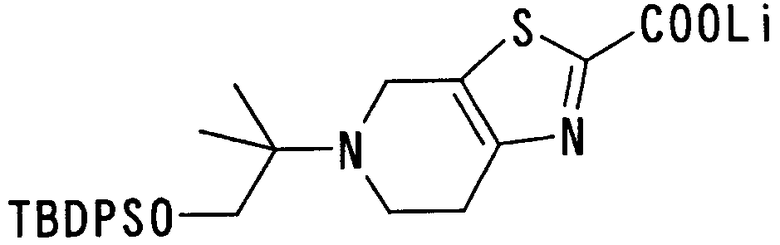
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 41, подобно способу ссылочного примера 5.
1Н-ЯМР (ДМСО-d6) δ: 1,01 (9Н, с), 1,11 (6Н, с), 2,55-2,65 (2Н, м), 2,80-2,90 (2Н, м), 3,57 (2Н, с), 3,80 (2Н, шир.с), 7,40-7,52 (6Н, м), 7,60-7,65 (4Н, м).
[Ссылочный пример 43]
4,7,8,10-Тетрагидро-6Н-пиразоло[1,2-a]тиазоло[4,5-d]пиридазин
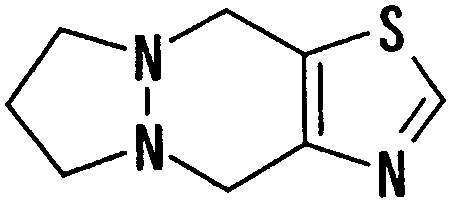
1) 4,5-Диметилтиазол (5,00 г), N-бромсукцинимид (15,7 г) и α,α'-азобисизобутиронитрил (362 мг) растворяли в этилендихлориде (500 мл) при комнатной температуре и раствор кипятили с обратным холодильником в течение 1 часа. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (гексан:диэтиловый эфир = 1:4) с получением 4,5-бис(бромметил)тиазола (5,24 г).
1Н-ЯМР (CDCl3) δ: 4,64 (2Н, с), 4,74 (2Н, с), 8,75 (1Н, с).
2) 4,5-Бис(бромметил)тиазол (1,37 г) и гидрохлорид 1,2-триметиленгидразина (WO9532965) (732 мг) суспендировали в этаноле (15 мл) при охлаждении льдом и добавляли по каплям триэтиламин (2,82 мл) за 5 минут. После перемешивания смеси при комнатной температуре в течение 2 часов отгоняли растворитель и к остатку добавляли метиленхлорид (50 мл) и насыщенный водный раствор гидрокарбоната натрия, чтобы отделить органический слой. Органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 3:47) с получением указанного в заголовке соединения (358 мг).
1Н-ЯМР (CDCl3) δ: 2,10-2,25 (2Н, м), 3,01 (4Н, шир.с), 3,95 (2Н, с), 3,99 (2Н, шир.с), 8,64 (1Н, с).
МС (FAB) m/z: 182 (М+Н)+.
[Ссылочный пример 44]
4,7,8,10-Тетрагидро-6Н-пиразоло[1,2-а]тиазоло[4,5-d]пиридазин-2-карбоксилат лития

Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 43, подобно способу ссылочного примера 5.
1Н-ЯМР (ДМСО-d6) δ: 1,90-2,10 (2Н, м), 2,60-3,10 (4Н, шир.с), 3,65-4,00 (4Н, м).
[Ссылочный пример 45]
4,6,7,8,9,11-Гексагидропиридазино[1,2-а]тиазоло[4,5-d]пиридазин
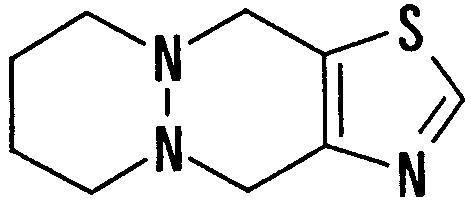
Указанное в заголовке соединение получали из 4,5-бис(бромметил)тиазола (2,20 г), полученного в 1) ссылочного примера 43, и гидрохлорида 1,2-тетраметиленгидразина (US 5726126) подобно способу ссылочного примера 43.
1Н-ЯМР (CDCl3) δ: 1,77 (4Н, шир.с), 2,20-3,50 (4Н, шир.), 3,92 (4Н, шир.с), 8,65 (1Н, с).
МС (FAB) m/z: 196 (М+Н)+.
[Ссылочный пример 46]
4,6,7,8,9,11-Гексагидропиридазино[1,2-а]тиазоло[4,5-d]пиридазин-2-карбоксилат лития:
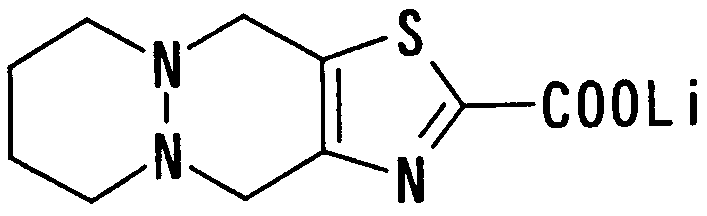
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 45, подобно способу ссылочного примера 5.
[Ссылочный пример 47]
трет-Бутил 2-(метилсульфанил)-5,7-дигидро-6Н-пирроло[3,4-d]пиримидин-6-карбоксилат
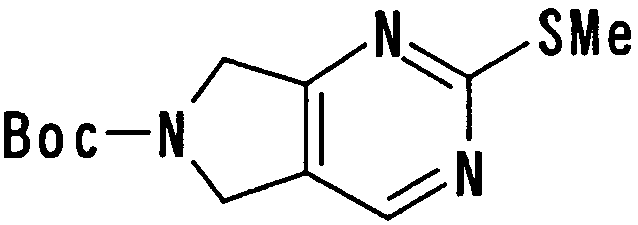
1-трет-Бутоксикарбонил-3-пирролидон (4,57 г) добавляли к диметилацеталю N,N-диметилформамида (30 мл) при комнатной температуре и смесь нагревали в течение 1 часа при 140°C. Дав реакционной смеси остыть до комнатной температуры, ее концентрировали при пониженном давлении. К остатку добавляли гексан и выпавший в осадок желтый порошок отфильтровывали. Полученный порошок растворяли в этаноле (100 мл), к полученному раствору при комнатной температуре добавляли сульфат метилизотиомочевины (9,24 г) и этоксид натрия (4,52 г) и смесь кипятили с обратным холодильником в течение 24 часов. К реакционной смеси добавляли насыщенный водный раствор хлорида натрия и диэтиловый эфир, чтобы отделить органический слой. Органический слой сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:99) с получением указанного в заголовке соединения (1,10 г).
1Н-ЯМР (CDCl3) δ: 1,51 (9Н, с), 2,57 (3Н, м), 4,15-4,45 (4Н, м), 8,39 (1/2Н, с), 8,43 (1/2Н, с).
МС (FAB) m/z: 268 (М+Н)+.
[Ссылочный пример 48]
трет-Бутил 2-(метилсульфонил)-5,7-дигидро-6Н-пирроло[3,4-d]пиримидин-6-карбоксилат
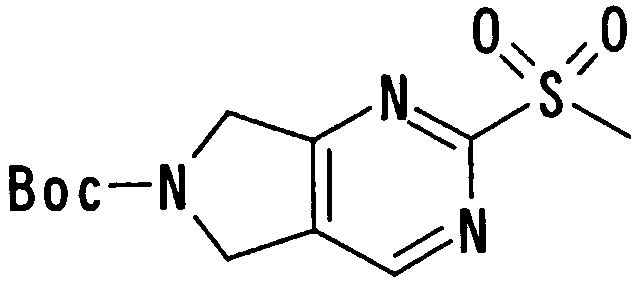
м-Хлорпербензойную кислоту (1,99 г) добавляли к метиленхлоридному раствору (20 мл) соединения (1,08 г), полученного в ссылочном примере 47, при охлаждении льдом и смесь перемешивали в течение 5 часов. Добавляли насыщенный водный раствор сульфита натрия, насыщенный водный раствор гидрокарбоната натрия и метиленхлорид, чтобы отделить органический слой. Затем органический слой сушили над безводным сульфатом натрия. Отгоняли при пониженном давлении растворитель, к остатку добавляли гексан и отфильтровывали выпавший в осадок порошок с получением указанного в заголовке соединения (1,09 г).
1Н-ЯМР (CDCl3) δ: 1,53 (9Н, с), 3,36 (3Н, м), 4,77-4,90 (4Н, м), 8,77 (1/2Н, с), 8,81 (1/2Н, с).
МС (FAB) m/z: 300 (М+Н)+.
[Ссылочный пример 49]
трет-Бутил 2-циано-5,7-дигидро-6Н-пирроло[3,4-d]пиримидин-6-карбоксилат
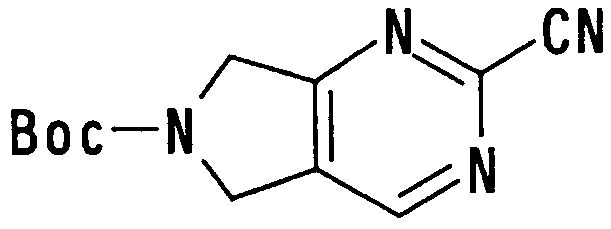
Цианид тетрабутиламмония (1,04 г) добавляли к раствору соединения (1,05 г), полученного в ссылочном примере 48, в метиленхлориде (30 мл) при комнатной температуре и смесь перемешивали при комнатной температуре в течение 1 часа. Добавляли к реакционной смеси 1N гидроксид натрия, чтобы отделить органический слой, и органический слой сушили над безводным сульфатом натрия. Отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:ацетон = 20:1) с получением указанного в заголовке соединения (776 мг).
1Н-ЯМР (CDCl3) δ: 1,52 (9Н, с), 4,70-4,85 (4Н, м), 8,68-8,77 (1Н, м).
МС (FAB) m/z: 247 (М+Н)+.
[Ссылочный пример 50]
6-трет-Бутил 2-метил-5,7-дигидро-6Н-пирроло[3,4-d]пиримидин-2,6-дикарбоксилат
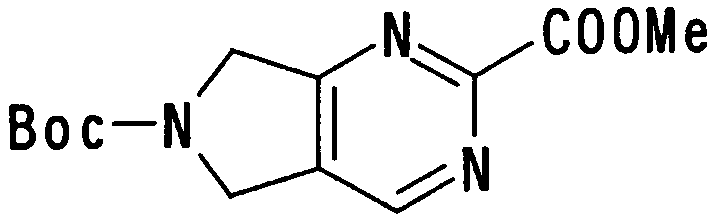
Концентрированную хлористоводородную кислоту (5 мл) добавляли к раствору соединения (776 мг), полученного в ссылочном примере 49, в метаноле (10 мл) при комнатной температуре и смесь перемешивали при 100°C в течение 1 часа. Дав реакционной смеси остыть, ее концентрировали при пониженном давлении и остаток растворяли в метаноле (10 мл). Триэтиламин (2,20 мл) и ди-трет-бутилдикарбонат (1,37 г) добавляли к раствору при комнатной температуре и перемешивали в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид и насыщенный водный раствор хлорида натрия, чтобы отделить органический слой, и органический слой сушили над безводным сульфатом натрия. Отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 3:97) с получением указанного в заголовке соединения (317 мг).
1Н-ЯМР (CDCl3) δ: 1,53 (9Н, с), 4,09 (3Н, с), 4,75-4,85 (4Н, м), 8,81 (1/2Н, с), 8,85 (1/2Н, с).
МС (FAB) m/z: 280 (М+Н)+.
[Ссылочный пример 51]
5,6-Диметил-4,5,6,7-тетрагидротиазоло[4,5-d]пиридазин-2-карбоксилат лития
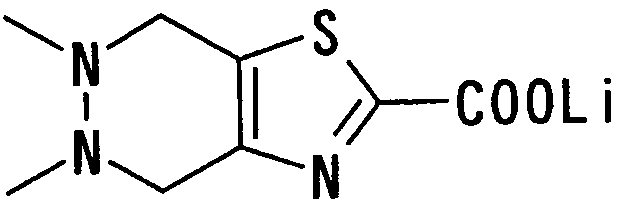
1) После растворения 4,5-бис(бромметил)тиазола (600 мг), полученного в 1) ссылочного примера 43, в этаноле (20 мл) и добавления гидрохлорида 1,2-диметилгидразина (294 мг) при охлаждении льдом добавляли одной порцией триэтиламин (1,23 мл) и смесь перемешивали 30 минут при комнатной температуре и 30 минут при 50°C. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:19) с получением 5,6-диметил-4,5,6,7-тетрагидротиазоло[4,5-d]пиридазина (90 мг).
1Н-ЯМР (CDCl3) δ: 2,43 (3Н, с), 2,56 (3Н, с), 3,92 (2Н, с), 4,06 (2Н, шир.с), 8,68 (1Н, с).
МС (FAB) m/z: 170 (М+Н)+.
2) Указанное в заголовке соединение получали из 5,6-диметил-4,5,6,7-тетрагидротиазоло[4,5-d]пиридазина подобно способу ссылочного примера 5.
1Н-ЯМР (ДМСО-d6) δ: 2,28 (3Н, с), 2,39 (3Н, с), 3,66 (2Н, шир.с), 3,88 (2Н, шир.с).
[Ссылочный пример 52]
4-Нитрофенил 5-хлориндол-2-карбоксилат
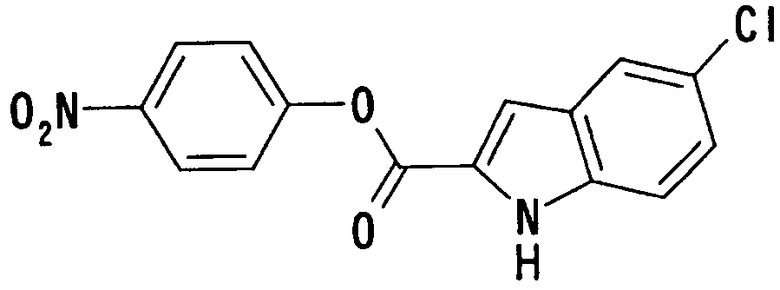
После суспендирования 5-хлориндол-2-карбоновой кислоты (20 г) в метиленхлориде (1500 мл) и добавления N,N-диметилформамида (2 мл) добавляли по каплям при комнатной температуре тионилхлорид (11 мл). Реакционную смесь кипятили с обратным холодильником в течение ночи и затем концентрировали при пониженном давлении. Остаток растворяли в метиленхлориде (1000 мл) и триэтиламин (84,7 мл) и п-нитрофенол (14,2 г) добавляли к смеси при охлаждении льдом. После перемешивания в течение 1 часа при комнатной температуре реакционную смесь концентрировали при пониженном давлении и к остатку добавляли этилацетат и 0,2N хлористоводородную кислоту, чтобы отделить органический слой. Органический слой последовательно промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (29,9 г).
1Н-ЯМР (CDCl3) δ: 7,35 (1Н, дд, J=9,0, 1,7Гц), 7,39-7,42 (2Н, м), 7,45 (2Н, дд, J=7,3, 1,7Гц), 7,73 (1Н, д, J=1,0Гц), 8,35 (2Н, дд, J=7,3, 1,7Гц), 9,09 (1Н, шир.с).
МС (FD) m/z: 316 (М)+.
[Ссылочный пример 53]
6-Хлор-2-хинолинкарбонитрил
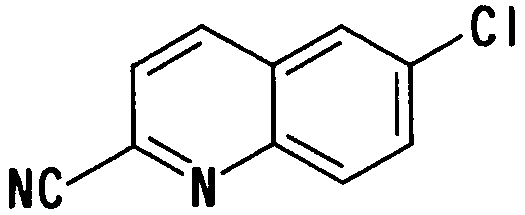
6-Хлориндолин (2,50 г) растворяли в метиленхлориде (25 мл), добавляли м-хлорпербензойную кислоту (3,71 г) при охлаждении льдом и смесь перемешивали при комнатной температуре в течение 1 часа. После разбавления реакционной смеси метиленхлоридом разбавленную смесь промывали водным раствором тиосульфата натрия и водным раствором гидроксида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении, остаток растворяли в метиленхлориде (40 мл), затем добавляли триметилсилилцианид (2,0 мл) и N,N-диметилкарбамоилхлорид (1,50 мл) и полученную смесь кипятили с обратным холодильником в течение 9 часов. Затем добавляли дополнительно триметилсилилцианид (1,0 мл) и N,N-диметилкарбамоилхлорид (0,80 мл) и смесь кипятили с обратным холодильником в течение 16 часов, затем реакционную смесь разбавляли метиленхлоридом, добавляли 10% водный раствор (40 мл) карбоната калия и смесь перемешивали 30 минут. Органический слой отделяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. К остатку добавляли метиленхлорид и выпавшие в осадок кристаллы отфильтровывали, получая указанное в заголовке соединение (1,77 г). Далее маточный раствор очищали колоночной хроматографией на силикагеле (метиленхлорид) с получением указанного в заголовке соединения (0,80 г).
1Н-ЯМР (ДМСО-d6) δ: 7,94 (1Н, дд, J=9,0, 2,2Гц), 8,09 (1Н, д, J=8,5Гц), 8,15 (1Н, д, J=9,0Гц), 8,29 (1Н, д, J=2,2Гц), 8,63 (1Н, д, J=8,5Гц).
МС (FAB) m/z: 189 (М+Н)+.
[Ссылочный пример 54]
6-Хлор-2-хинолинкарбоновая кислота
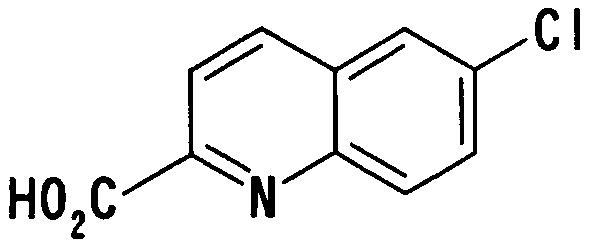
Соединение (1,73 г), полученное в ссылочном примере 53, растворяли в концентрированной хлористоводородной кислоте (40 мл) и раствор кипятили с обратным холодильником в течение 19 часов. Реакционную смесь охлаждали до комнатной температуры и осадок отфильтровывали и затем промывали водой с получением указанного в заголовке соединения (1,81 г).
1Н-ЯМР (ДМСО-d6) δ: 7,87 (1Н, дд, J=9,0, 2,4Гц), 8,10-8,20 (2Н, м), 8,24 (1Н, д, J=2,2Гц), 8,52 (1Н, д, J=8,5Гц).
МС (FAB) m/z: 208 (М+Н)+.
[Ссылочный пример 55]
Метил 3-(4-хлорфенил)-2-(формиламино)пропионат
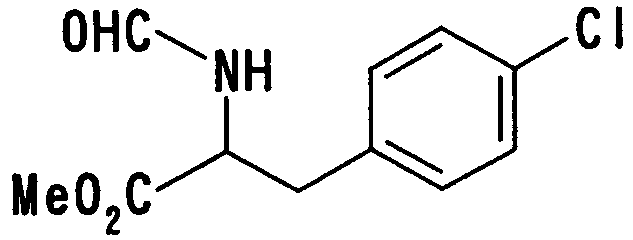
Гидрохлорид сложного метилового эфира (±)-(4-хлорфенил)аланина (2,00 г) суспендировали в метиленхлориде (20 мл), добавляли гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (1,60 г), моногидрат 1-гидроксибензотриазола (1,23 г), N-метилморфолин (1,90 мл) и муравьиную кислоту (0,30 мл) и смесь перемешивали в течение 15 минут. После 3-кратного повторения процесса дополнительного добавления муравьиной кислоты (0,30 мл) при перемешивании смеси в течение 15 минут реакционную смесь разбавляли метиленхлоридом. Органический слой промывали водой и затем сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 40:1) с получением указанного в заголовке соединения (1,21 г).
1Н-ЯМР (CDCl3) δ: 3,10 (1Н, дд, J=13,9, 5,6Гц), 3,18 (1Н, дд, J=13,9, 5,9Гц), 3,75 (3Н, с), 4,95 (1Н, м), 6,07 (1Н, шир.), 7,05 (2Н, д, J=8,3Гц), 7,27 (2Н, д, J=8,3Гц), 8,18 (1Н, с).
МС (FAB) m/z: 242 (М+Н)+.
[Ссылочный пример 56]
Метил 7-хлор-3-изохинолинкарбоксилат
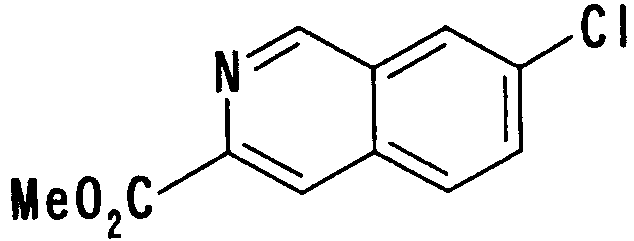
Соединение (1,45 г), полученное в ссылочном примере 55, растворяли в метиленхлориде (40 мл) и добавляли по каплям оксалилхлорид (0,57 мл). После перемешивания смеси при комнатной температуре в течение 30 минут добавляли хлорид железа (1,17 г) при температуре окружающей среды около -10°C и смесь перемешивали при комнатной температуре в течение 4 дней. Добавляли 1N хлористоводородную кислоту и полученную смесь разбавляли метиленхлоридом, чтобы отделить органический слой. Органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток растворяли в метаноле (38 мл), добавляли концентрированную серную кислоту (2 мл) и смесь кипятили с обратным холодильником в течение 20 часов. К реакционной смеси добавляли водный раствор гидрокарбоната натрия, полученную смесь экстрагировали метиленхлоридом и экстракт сушили над безводным сульфатом натрия. Отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 2:1 → этилацетат) с получением указанного в заголовке соединения (0,25 г).
1Н-ЯМР (CDCl3) δ: 4,07 (3Н, с), 7,74 (1Н, дд, J=8,8, 2,0Гц), 7,94 (1Н, д, J=8,8Гц), 8,06 (1Н, д, J=2,0Гц), 8,59 (1Н, с), 9,28 (1Н, с).
[Ссылочный пример 57]
Гидрохлорид 7-хлор-3-изохинолинкарбоновой кислоты
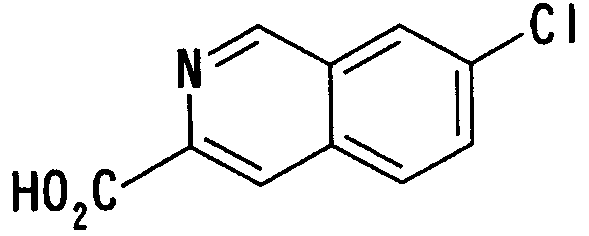
Соединение (0,23 г), полученное в ссылочном примере 56, растворяли в концентрированной хлористоводородной кислоте (10 мл) и кипятили смесь с обратным холодильником в течение 18 часов. Температуру реакционной смеси снижали до комнатной температуры и осадок отфильтровывали, а затем промывали водой с получением указанного в заголовке соединения (0,21 г).
1Н-ЯМР (ДМСО-d6) δ: 7,96 (1Н, м), 8,29 (1Н, д, J=8,5Гц), 8,44 (1Н, с), 8,72 (1Н, с), 9,45 (1Н, д, J=6,6Гц).
МС (FAB) m/z: 208 (М+Н)+.
[Ссылочный пример 58]
(3R)-1-Бензил-3-(трет-бутилдифенилсилилокси)пирролидин
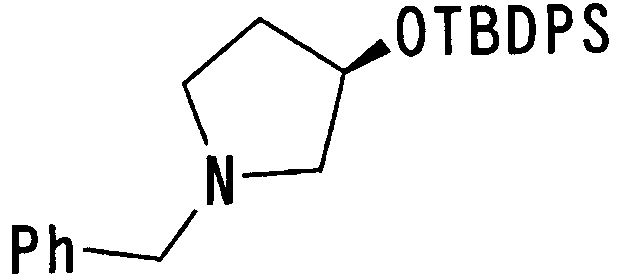
(3R)-1-Бензил-3-гидроксипирролидин (500 мкл) и имидазол (466 мг) растворяли в N,N-диметилформамиде (15 мл), добавляли при охлаждении льдом трет-бутилдифенилсилилхлорид (1,57 мл) и смесь перемешивали при комнатной температуре в течение 9 дней. Отгоняли при пониженном давлении растворитель и к остатку добавляли метиленхлорид и воду для разделения жидкостей, затем полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток подвергали флэш-хроматографии на силикагеле (гексан:этилацетат = 3:1) с получением указанного в заголовке соединения (1,27 г).
1Н-ЯМР (CDCl3) δ: 1,05 (9Н, с), 1,70-1,85 (1Н, м), 1,90-2,00 (1Н, м), 2,45-2,65 (3Н, м), 2,70-2,80 (1Н, м), 3,50-3,70 (2Н, м), 4,35-4,45 (1Н, м), 7,20-7,45 (11Н, м), 7,60-7,70 (4Н, м).
МС (ESI) m/z: 416 (M+H)+.
[Ссылочный пример 59]
N-[(1R*,2S*)-2-Аминоциклопропил]-5-хлориндол-2-карбоксамид
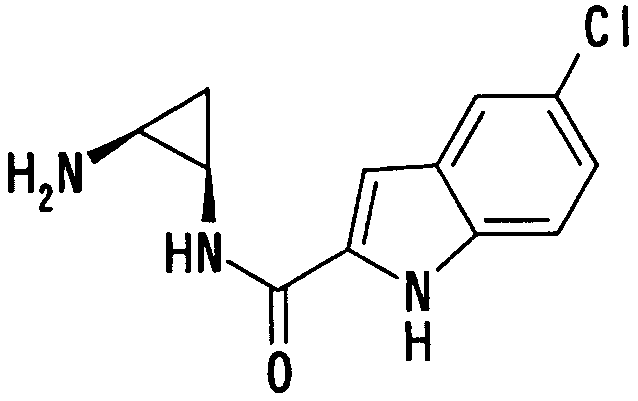
Моногидрат 1-гидроксибензотриазола (377 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (642 мг) и диизопропилэтиламин (1,95 мл) добавляли к раствору гидрохлорида цис-1,2-циклопропандиамина (J. Med. Chem., 1998, Vol. 41, pp. 4723-4732) (405 мг) и 5-хлориндол-2-карбоновой кислоты (546 мг) в N,N-диметилформамиде (10 мл) при комнатной температуре и смесь перемешивали в течение 50 часов. После концентрирования реакционной смеси при пониженном давлении добавляли метиленхлорид (50 мл) и насыщенный водный раствор (200 мл) гидрокарбоната натрия и отделяли фильтрованием выпавшее в осадок бесцветное твердое вещество. Фильтрат экстрагировали метиленхлоридом. Полученные органические слои объединяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель с получением остатка. Остаток очищали колоночной флэш-хроматографией на силикагеле (метиленхлорид:метанол = 100:7 → 10:1) с получением указанного в заголовке соединения (110 мг).
1Н-ЯМР (ДМСО-d6) δ: 0,44 (1H, дд, J=10,7, 4,4Гц), 1,11 (1H, дд, J=14,0, 7,4Гц), 2,63-2,70 (1H, м), 3,07-3,16 (1H, м), 6,77 (1H, с), 6,97 (1H, шир.с), 7,23 (1H, дд, J=8,9, 1,8Гц), 7,36 (1H, д, J=8,9Гц), 7,60 (1H, с), 9,32 (1H, с),
МС (FAB) m/z: 250 (М+Н)+.
[Ссылочный пример 60]
N-[(1R*,2S*)-2-Аминоциклобутил]-5-хлориндол-2-карбоксамид
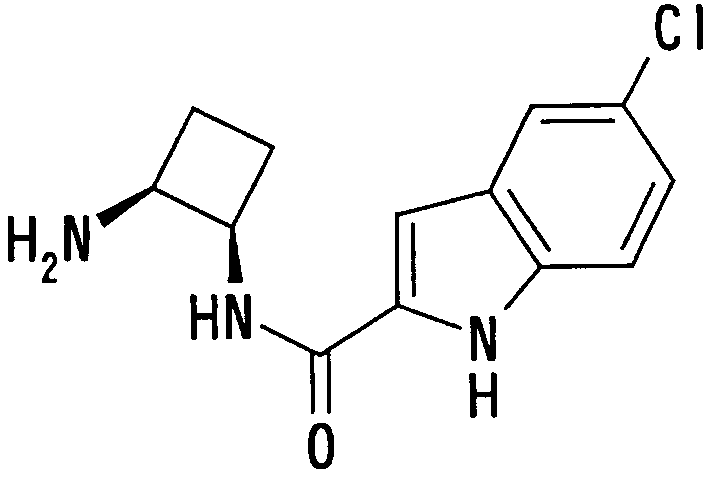
Указанное в заголовке соединение получали из гидрохлорида цис-1,2-циклобутандиамина (J. Am. Chem. Soc., 1942, Vol. 64, pp. 2696-2700) подобно способу ссылочного примера 59.
1Н-ЯМР (ДМСО-d6) δ: 1,55-2,20 (4H, м), 3,52-3,62 (1H, м), 4,35-4,50 (1H, м), 7,16 (1H, дд, J=8,7, 2,1Гц), 7,19 (1H, с), 7,42 (1H, д, J=8,7Гц), 7,70 (1H, д, J=2,1Гц), 8,36 (1H, д, J=7,8Гц), 11,77 (1H, шир.с).
МС (ESI) m/z: 264 (М+Н)+.
[Ссылочный пример 61]
трет-Бутил (1R*,2R*)]-2-аминоциклопентилкарбамат
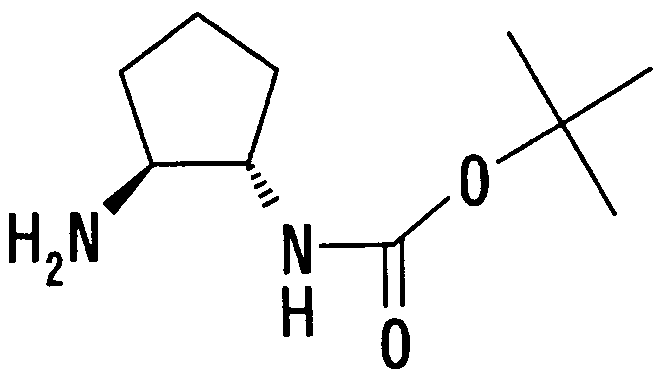
(±)-транс-1,2-Циклопентандиамин (WO98/30574) (692 мг) растворяли в метиленхлориде (10 мл), к раствору добавляли триэтиламин (1,1 мл) и 2-(трет-бутоксикарбонилоксиимино)-2-фенилацетонитрил (493 мг) и смесь перемешивали при 0°C в течение 1 часа. Затем дополнительно добавляли 2-(трет-бутоксикарбонилоксиимино)-2-фенилацетонитрил (493 мг) и смесь перемешивали при комнатной температуре в течение 7 часов. К реакционной смеси добавляли воду, чтобы отделить органический слой. Органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Остаток очищали колоночной флэш-хроматографией на силикагеле (метиленхлорид:метанол = 9:1) с получением указанного в заголовке соединения (395 мг).
1Н-ЯМР (CDCl3) δ: 1,25-1,40 (2Н, м), 1,49 (9Н, с), 1,59-1,77 (2Н, м), 1,92-2,08 (1Н, м), 2,10-2,17 (1Н, м), 2,98 (1Н, кв, J=7,2Гц), 3,48-3,53 (1Н, м), 4,49 (1Н, шир.с).
МС (ESI) m/z: 201 (М+Н)+.
[Ссылочный пример 62]
Гидрохлорид N-[(1R*,2R*)-2-аминоциклопентил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
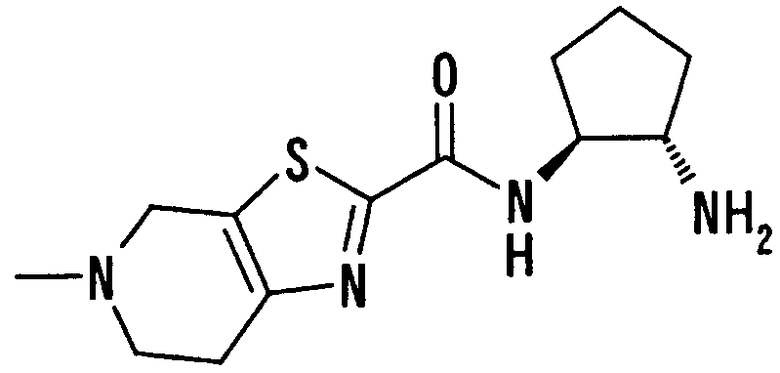
Соединение (175 мг), полученное в ссылочном примере 61, растворяли в N,N-диметилформамиде (3 мл) и к раствору добавляли 5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксилат лития (чистота: 90%, 258 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (252 мг) и моногидрат 1-гидроксибензотриазола (60 мг). Смесь перемешивали при комнатной температуре в течение 2 дней. Пользуясь насосом, отгоняли при пониженном давлении растворитель и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия, чтобы отделить органический слой. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной флэш-хроматографией на силикагеле (метиленхлорид:метанол = 47:3). Полученное бледно-желтое масло растворяли в этанольном растворе (5 мл) хлористоводородной кислоты и раствор перемешивали при комнатной температуре в течение 1 часа. Затем добавляли этилацетат и отгоняли при пониженном давлении растворитель. К остатку добавляли этилацетат и отфильтровывали образовавшийся осадок с получением указанного в заголовке соединения (120 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,63-1,73 (4H, м), 1,99-2,06 (2H, м), 2,91 (3H, с), 3,09-3,14 (1H, м), 3,25-3,70 (4H, м), 4,27-4,32 (1H, м), 4,42-4,46 (1H, м), 4,68-4,71 (1H, м), 8,20-8,23 (3H, м), 9,09 (1H, д, J=8,3Гц), 11,82-12,01 (1H, м)
МС (ESI) m/z: 281 (М+Н)+.
[Ссылочный пример 63]
Гидрохлорид N-[(1R*,2R*)-2-аминоциклопентил]-5-хлор-1Н-индол-2-карбоксамида

Соединение (1,40 г), полученное в ссылочном примере 61, растворяли в N,N-диметилформамиде (15 мл) и к раствору добавляли 5-хлориндол-2-карбоновую кислоту (1,64 г), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (2,68 г) и моногидрат 1-гидроксибензотриазола (473 мг). Смесь перемешивали при комнатной температуре в течение 23 часов. Отгоняли при пониженном давлении растворитель и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия и отфильтровывали осадок. Осадок промывали этилацетатом, метиленхлоридом и метанолом. С другой стороны, отделяли фильтрат для получения органического слоя, который отбирали и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной флэш-хроматографией на силикагеле (метиленхлорид:метанол = 19:1) с получением бледно-желтого твердого вещества. Бледно-желтое твердое вещество объединяли с осадком, полученным фильтрованием, растворяли в метиленхлориде (10 мл), добавляли трифторуксусную кислоту (10 мл) и смесь перемешивали при комнатной температуре в течение 3 часов. Растворитель отгоняли при пониженном давлении, к остатку добавляли метиленхлорид и 1N водный раствор гидроксида натрия и отфильтровывали осадок. Органический слой фильтрата отделяли и сушили над безводным сульфатом натрия. Отфильтрованные осадки добавляли к полученному раствору, затем добавляли 4N диоксановый раствор (20 мл) хлористоводородной кислоты. Растворитель отгоняли при пониженном давлении и к остатку добавляли метиленхлорид (10 мл) и 4N диоксановый раствор (10 мл) хлористоводородной кислоты. Снова отгоняли растворитель при пониженном давлении. К остатку добавляли этилацетат и отфильтровывали образовавшийся осадок, получая указанное в заголовке соединение (1,83 г).
1Н-ЯМР (ДМСО-d6) δ: 1,60-1,75 (4H, м), 2,05-2,10 (2H, м), 3,49 (1H, кв, J=7,6Гц), 4,27 (4H, квинтет, J=7,6Гц), 7,17 (1H, д, J=8,6Гц), 7,19 (1H, с), 7,42 (1H, д, J=8,6Гц), 7,70 (1H, с), 8,24 (3H, шир.с), 8,85 (1H, д, J=7,3Гц), 11,91 (1H, с).
МС (ESI) m/z: 278 (M+H)+.
[Ссылочный пример 64]
трет-Бутил (1R*,2R*)-2-аминоциклогексилкарбамат
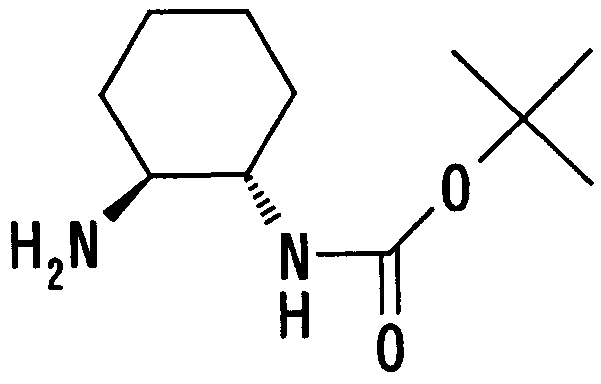
Указанное в заголовке соединение получали из (±)-транс-1,2-циклогександиамина подобно способу ссылочного примера 61.
Т.пл. 79-81°C.
1Н-ЯМР (CDCl3) δ: 1,05-1,34 (4Н, м), 1,45 (9Н, с), 1,68-1,75 (2Н, м), 1,92-2,02 (2Н, м), 2,32 (1Н, дт, J=10,3, 3,9Гц), 3,08-3,20 (1Н, м), 4,50 (1Н, шир.с).
МС (FAB) m/z: 215 (М+Н)+.
[Ссылочный пример 65]
Трифторацетат (гидрохлорид) N-[(1R*,2R*)-2-аминоциклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
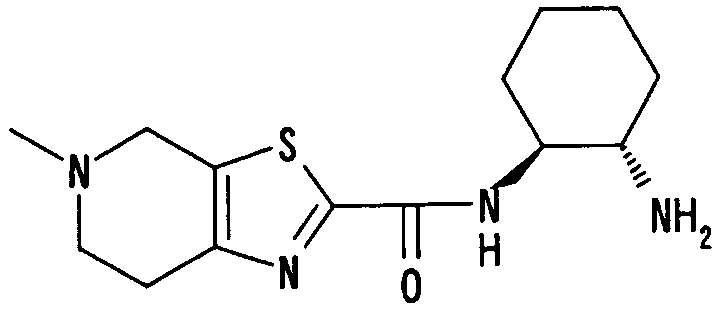
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 64, подобно способу ссылочного примера 62.
1Н-ЯМР (ДМСО-d6) δ: 1,10-1,80 (7Н, м), 1,95-2,05 (1Н, м), 2,97 (3Н, с), 3,00-3,20 (3Н, м), 3,63 (2Н, шир.с), 3,72-3,88 (1Н, м), 4,61 (2Н, шир.с), 7,98 (3Н, с), 8,89 (1Н, д, J=9,2Гц).
МС (FAB) m/z: 295 (М+Н)+.
Гидрохлорид получали аналогичным образом.
[Ссылочный пример 66]
трет-Бутил (1R*,2S*)-2-аминоциклогексилкарбамат
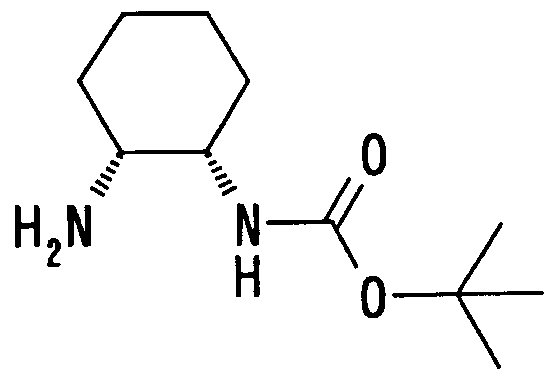
Указанное в заголовке соединение получали из цис-1,2-циклогександиамина подобно способу ссылочного примера 61.
1Н-ЯМР (CDCl3) δ: 1,30-1,70 (17Н, м), 2,98-3,05 (1Н, м), 3,60 (1Н, шир.с), 4,98 (1Н, шир.с).
МС (FAB) m/z: 215 (М+Н)+.
[Ссылочный пример 67]
Гидрохлорид (трифторацетат) N-[(1R*,2S*)-2-аминоциклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
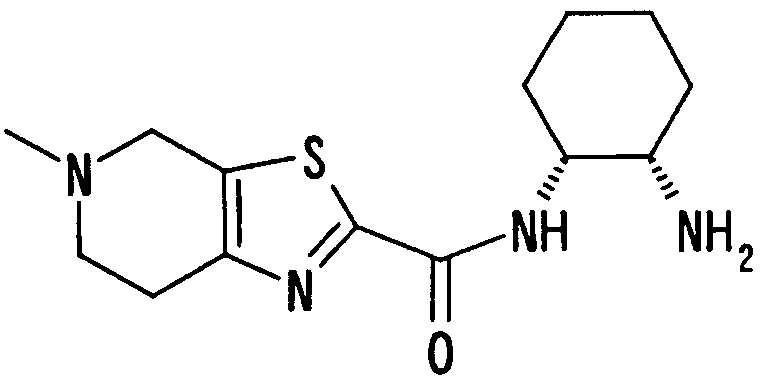
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 66, подобно способу ссылочного примера 62.
1Н-ЯМР (ДМСО-d6) δ: 1,30-1,90 (8Н, м), 2,92 (3Н, с), 3,05-3,79 (5Н, м), 4,23 (1Н, шир.с), 4,34-4,79 (2Н, м), 8,01-8,34 (3Н, м), 8,30-8,49 (1Н, м), 11,90-12,30 (1Н, м).
МС (FAB) m/z: 295 (М+Н)+.
Трифторацетат получали аналогичным образом.
[Ссылочный пример 68]
трет-Бутил (1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексилкарбамат
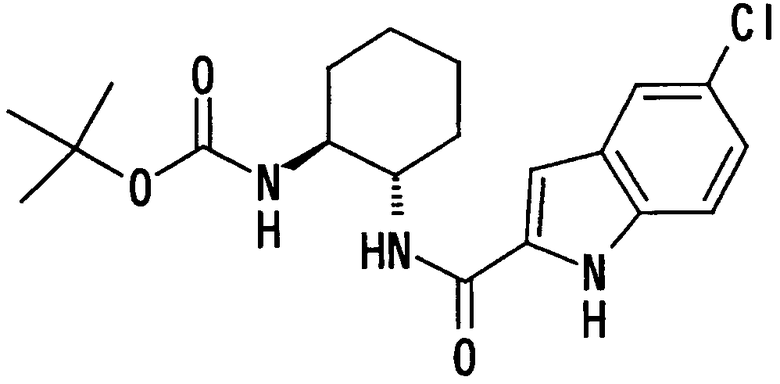
5-Хлориндол-2-карбоновую кислоту (2,88 г), моногидрат 1-гидроксибензотриазола (2,08 г) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (2,95 г) добавляли к раствору соединения (3,00 г), полученного в ссылочном примере 64, в N,N-диметилформамиде (10 мл) при комнатной температуре. После перемешивания в течение 3 дней реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид (30 мл), насыщенный водный раствор гидрокарбоната натрия (150 мл) и воду (150 мл). Отфильтровывали образовавшийся бесцветный осадок и сушили его с получением указанного в заголовке соединения (5,21 г).
1Н-ЯМР (ДМСО-d6) δ: 1,10-1,45 (4H, м), 1,21 (9H, с), 1,68 (2H, д, J=8,1Гц), 1,86 (2H, т, J=16,2Гц), 3,22-3,42 (1H, м), 3,69 (1H, шир.с), 6,66 (1H, д, J=8,5Гц), 7,02 (1H, с), 7,15 (1H, дд, J=8,5, 2,0Гц), 7,41 (1H, д, J=8,5Гц), 7,67 (1H, д, J=2,0Гц), 8,15 (1H, д, J=8,1Гц), 11,73 (1H, шир.с).
МС (ESI) m/z: 392 (M+H)+.
[Ссылочный пример 69]
Гидрохлорид N-[(1R*,2R*)-2-аминоциклогексил]-5-хлориндол-2-карбоксамида
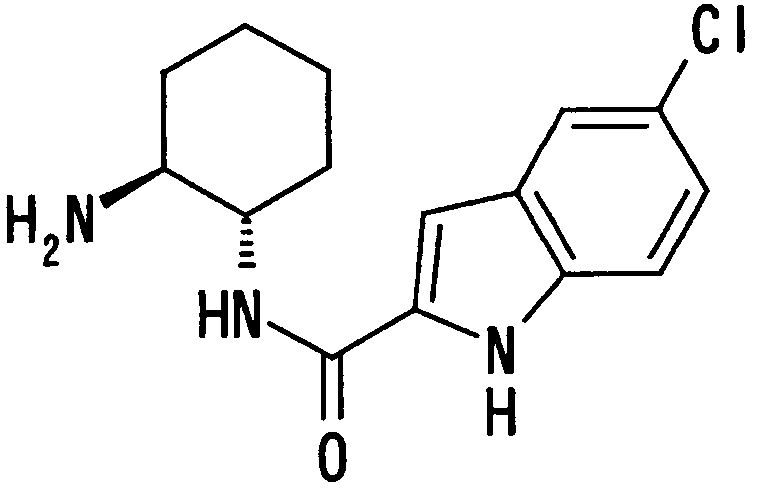
Этанольный раствор (100 мл) хлористоводородной кислоты добавляли к раствору соединения (5,18 г), полученного в ссылочном примере 68, в метиленхлориде (100 мл) при комнатной температуре. После перемешивания в течение 2 дней реакционную смесь концентрировали при пониженном давлении, к полученному остатку добавляли диэтиловый эфир (300 мл) и образовавшийся бесцветный осадок отфильтровывали и сушили с получением указанного в заголовке соединения (4,30 г).
1Н-ЯМР (ДМСО-d6) δ: 1,20-1,36 (2H, м), 1,36-1,50 (2H, м), 1,60 (2H, шир.с), 1,90 (1H, д, J=13,0Гц), 2,07 (1H, д, J=13,7Гц), 3,06 (1H, шир.с), 3,83-3,96 (1H, м), 7,15-7,24 (2H, м), 7,45 (1H, д, J=8,6Гц), 7,73 (1H, с), 8,00 (3H, шир.с), 8,60 (1H, д, J=8,3Гц), 11,86 (1H, с).
МС (ESI) m/z: 292 (M+H)+.
[Ссылочный пример 70]
трет-Бутил (1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексилкарбамат
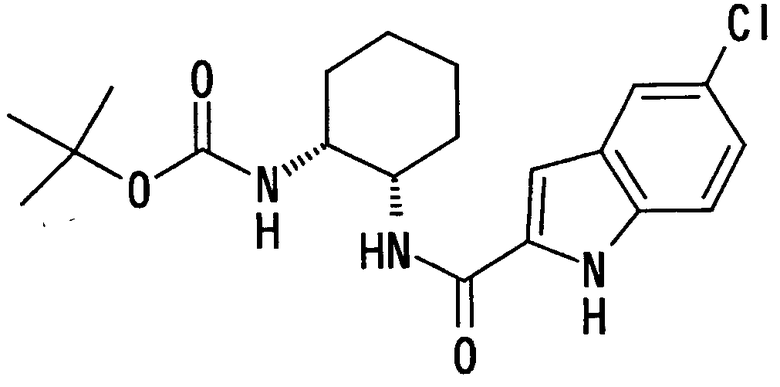
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 66, подобно способу ссылочного примера 68.
1Н-ЯМР (ДМСО-d6) δ: 1,20-1,45 (11H, м), 1,45-1,70 (4H, м), 1,70-1,85 (2H, м), 3,76 (1H, шир.с), 4,08 (1H, шир.с), 6,64 (1H, д, J=7,6Гц), 7,12 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,43 (1H, д, J=8,8Гц), 7,69 (1H, д, J=2,0Гц), 7,85 (1H, д, J=6,9Гц), 11,80 (1H, шир.с).
МС (ESI) m/z: 392 (M+H)+.
[Ссылочный пример 71]
Гидрохлорид N-[(1R*,2S*)-2-аминоциклогексил]-5-хлориндол-2-карбоксамида
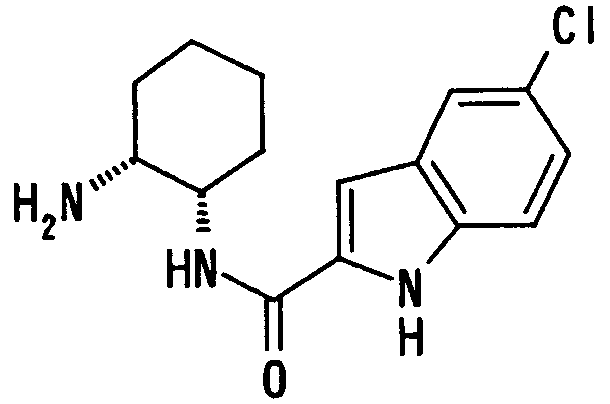
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 70, подобно способу ссылочного примера 69.
1Н-ЯМР (ДМСО-d6) δ: 1,30-1,50 (2H, м), 1,55-1,95 (6H, м), 3,41 (1H, шир.с), 4,32 (1H, шир.с), 7,19 (1H, дд, J=8,7, 2,0Гц), 7,33 (1H, с), 7,45 (1H, д, J=8,7Гц), 7,60-7,90 (4H, м), 8,17 (1H, д, J=7,1Гц), 11,91 (1H, с).
МС (FAB) m/z: 292 (М+Н)+.
[Ссылочный пример 72]
(1R*,2R*)-1,2-Циклогептандиол
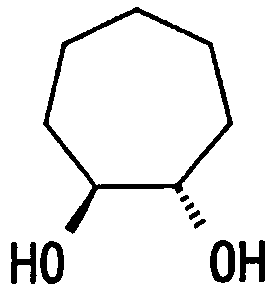
Циклогептен (3,85 г) добавляли порциями к 30% водному пероксиду водорода (45 мл) и 88% муравьиной кислоте (180 мл) и смесь перемешивали при 40-50°C в течение 1 часа и затем при комнатной температуре в течение ночи. Отгоняли при пониженном давлении растворитель и к остатку для его подщелачивания добавляли 35% водный раствор гидроксида натрия. Затем остаток перемешивали при 40-50°C в течение 10 минут и добавляли этилацетат для разделения жидкостей. Полученный водный слой экстрагировали 4 раза этилацетатом. Полученные органические слои отделяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (4,56 г).
1Н-ЯМР (CDCl3) δ: 1,44-1,56 (6Н, м), 1,63-1,70 (2Н, м), 1,83-1,91 (2Н, м), 2,91 (2Н, шир.с), 3,40-3,44 (2Н, м).
МС (FAB) m/z: 131 (М+Н)+.
[Ссылочный пример 73]
Гидрохлорид (1R*,2R*)-1,2-циклогептандиамина
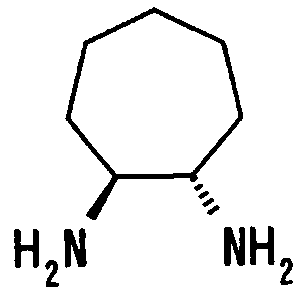
Соединение (4,56 г), полученное в ссылочном примере 72, растворяли в метиленхлориде (35 мл), добавляли триэтиламин (29 мл) и смесь охлаждали до -78°C. К смеси добавляли по каплям метансульфонилхлорид (8,13 мл). Медленно добавляли метиленхлорид (10 мл) и смесь перемешивали 20 минут при той же температуре и затем 1,5 часа при 0°C. К реакционной смеси добавляли воду для разделения жидкостей и полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении с получением масла. Полученное масло растворяли в N,N-диметилформамиде (90 мл), добавляли азид натрия (13,65 г) и смесь перемешивали при 65°C в течение 18 часов. К реакционной смеси добавляли эфир и воду для разделения жидкостей. Полученный эфирный слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении с получением масла.
Полученное масло растворяли в этаноле (70 мл), добавляли 10% палладий на углероде (содержащий 50% воды, 4 г) и смесь перемешивали 4 дня в атмосфере водорода (3,5 атм). После отделения палладия на углероде фильтрованием к фильтрату добавляли 1N этанольный раствор (70 мл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. Остаток растворяли в метаноле, добавляли этилацетат и снова отгоняли при пониженном давлении растворитель. Образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (3,57 г).
1Н-ЯМР (ДМСО-d6) δ: 1,44 (4Н, шир.с), 1,73-1,81 (6Н, м), 3,43 (2Н, шир.с), 8,63 (6Н, шир.с).
МС (ESI) m/z: 129 (М+Н)+.
[Ссылочный пример 74]
N-[(1R*,2R*)-2-Аминоциклогептил]-5-хлориндол-2-карбоксамид

Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 73, подобно способу ссылочного примера 59.
1Н-ЯМР (ДМСО-d6) δ: 1,49-1,52 (4H, м), 1,72-1,91 (6H, м), 4,04-4,10 (1H, м), 7,17-7,23 (2H, м), 7,44 (1H, д, J=8,8Гц), 7,72 (1H, д, J=2,0Гц), 7,96 (2H, шир.с), 8,75 (1H, д, J=8,5Гц), 11,89 (1H, шир.с).
МС (ESI) m/z: 306 (М+Н)+.
[Ссылочный пример 75]
(1R*,2S*)-1,2-Циклооктандиол
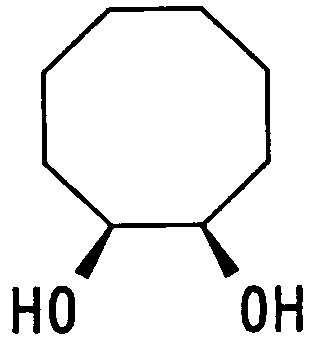
Циклооктен (4,41 г) растворяли в ацетонитриле (45 мл) и воде (15 мл), к раствору добавляли N-оксид N-метилморфолина (5,15 г) и микрокапсулированный тетроксид осмия (1 г, содержащий 10% тетроксид осмия) и смесь перемешивали при 40-50°C в течение 21 часа. Нерастворившийся микрокапсулированный тетроксид осмия удаляли фильтрованием, промывали ацетонитрилом и фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной флэш-хроматографией на силикагеле (гексан:этилацетат = 1:1) с получением указанного в заголовке соединения (4,97 г).
1Н-ЯМР (CDCl3) δ: 1,48-1,58 (6Н, м), 1,64-1,75 (4Н, м), 1,86-1,96 (2Н, м), 2,28 (2Н, д, J=2,9Гц), 3,90 (2Н, д, J=8,3Гц).
МС (FAB) m/z: 145 (М+Н)+.
[Ссылочный пример 76]
(1R*,2S*)-1,2-диазидоциклооктан
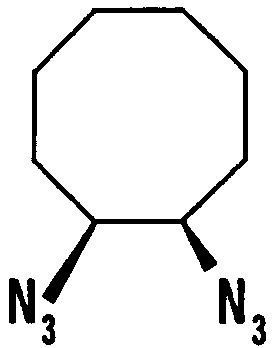
После растворения цис-1,2-циклооктандиола (4,82 г) в метиленхлориде (60 мл) и добавления к раствору триэтиламина (27,7 мл) сосуд продували аргоном, затем смесь охлаждали до -78°C и добавляли к ней по каплям метансульфонилхлорид (7,7 мл, 100 ммоль). Смесь перемешивали в течение 1 часа при той же температуре и затем в течение 1 часа при 0°C. К реакционной смеси добавляли воду для разделения жидкостей и полученный органический слой промывали водой, 0,5N хлористоводородной кислотой, водой и насыщенным водным раствором гидрокарбоната натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток растворяли в N,N-диметилформамиде (80 мл), добавляли азид натрия (13,0 г) и смесь перемешивали при 65°C в течение 19 часов. К реакционной смеси добавляли эфир и воду для разделения жидкостей. Полученный эфирный слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной флэш-хроматографией на силикагеле (гексан:этилацетат = 6:1) с получением указанного в заголовке соединения (4,85 г).
1Н-ЯМР (CDCl3) δ: 1,49-1,64 (6Н, м), 1,67-1,78 (2Н, м), 1,81-1,97 (4Н, м), 3,74-3,76 (2Н, м).
[Ссылочный пример 77]
Гидрохлорид (1R*,2S*)-1,2-циклооктандиамина
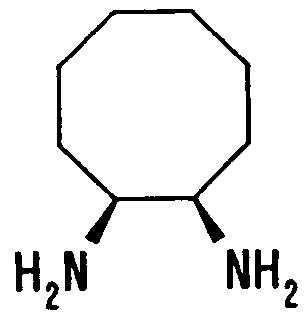
Соединение (4,85 г), полученное в ссылочном примере 76, растворяли в этаноле (55 мл), к раствору добавляли 10% палладий на углероде (содержащий 50% воды, 3,0 г) и смесь перемешивали в течение 21 часа в атмосфере водорода (4,5 атм). После отделения катализатора фильтрованием к фильтрату добавляли 1N этанольный раствор (50 мл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли этилацетат и образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (4,14 г).
1Н-ЯМР (ДМСО-d6) δ: 1,51 (6Н, шир.с), 1,69 (2Н, шир.с), 1,79-1,99 (4Н, м), 3,68-3,70 (2Н, м), 8,66 (6Н, шир.с).
МС (ESI) m/z: 143 (М+Н)+.
[Ссылочный пример 78]
N-[(1R*,2S*)-2-Аминоциклооктил]-5-хлориндол-2-карбоксамид
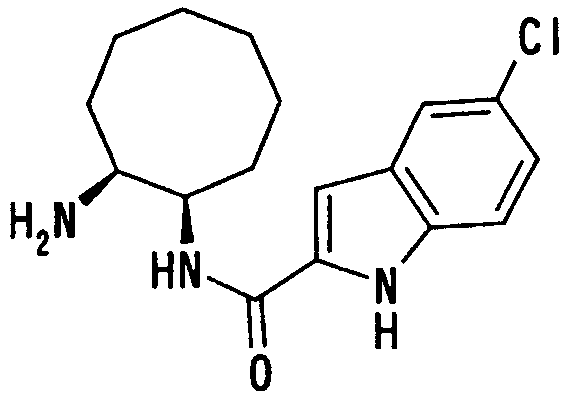
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 77, подобно способу ссылочного примера 59.
МС (ESI) m/z: 320 (М+Н)+.
[Ссылочный пример 79]
(1R*,2R*)-4-Метокси-1,2-циклопентандиол (смесь стереоизомеров положения 4)
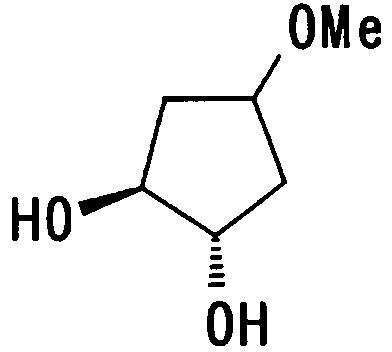
60% Гидрид натрия (800 мг) добавляли порциями к раствору 3-циклопентен-1-ола (1,68 г) и метилиодида (1,25 мл) в тетрагидрофуране (20 мл) при охлаждении льдом и смесь перемешивали в течение ночи при комнатной температуре. Воду и диэтиловый эфир добавляли к реакционной смеси, чтобы отделить органический слой, органический слой сушили над безводным сульфатом магния, отгоняли при пониженном давлении растворитель с получением при охлаждении льдом неочищенного 4-метокси-1-циклопентена.
88% Муравьиную кислоту (90 мл) и 30% пероксид водорода (3,17 мл) добавляли к полученному таким образом 4-метокси-1-циклопентену и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли 35% водный раствор гидроксида натрия для подщелачивания реакционной смеси, затем смесь перемешивали при 50°C в течение 10 минут. Реакционную смесь охлаждали до комнатной температуры, экстрагировали этилацетатом и органический слой сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:19) с получением указанного в заголовке соединения (1,21 г).
1Н-ЯМР (CDCl3) δ: 1,65-1,85 (2Н, м), 2,15-2,30 (2Н, м), 3,28 (3Н, с,), 3,90-4,00 (2Н, м), 4,26 (1Н, шир.с).
[Ссылочный пример 80]
(1R*,2R*)-1,2-Диазидо-4-метоксициклопентан (смесь стереоизомеров положения 4)
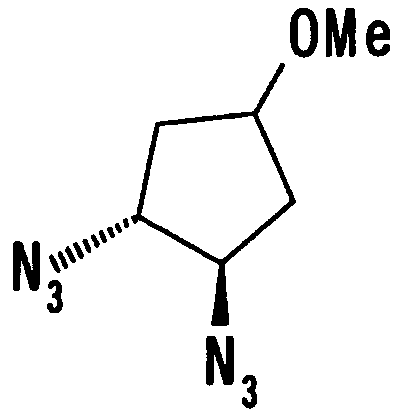
Соединение (1,21 г), полученное в ссылочном примере 79, и триэтиламин (7,66 мл) растворяли в метиленхлориде (20 мл) и к раствору добавляли по каплям за 20 минут при -78°C метансульфонилхлорид (2,13 мл). По окончании капельного добавления смесь нагревали до 0°C и перемешивали 80 минут с получением неочищенного (1R*,2R*)-1,2-бис(метансульфонилокси)-4-метоксициклопентана. Полученный продукт растворяли в N,N-диметилформамиде (20 мл), добавляли азид натрия (3,57 г) и смесь нагревали и перемешивали при 65°C в течение 22 часов. Добавляли дополнительно азид натрия (3,57 г) и перемешивали смесь при 70°C в течение 2 дней. Реакционной смеси давали остыть и добавляли воду и диэтиловый эфир для отделения органического слоя. Органический слой сушили над безводным сульфатом магния. Отгоняли растворитель и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 2:1) с получением указанного в заголовке соединения (584 мг).
1Н-ЯМР (CDCl3) δ: 1,65-1,80 (2Н, м), 2,05-2,18 (1Н, м), 2,25-2,40 (1Н, м), 3,21 (3Н, с,), 3,55-3,65 (1Н, м), 3,75-3,90 (2Н, м).
[Ссылочный пример 81]
Гидрохлорид (1R*,2R*)-4-метокси-1,2-циклопентандиамина (смесь стереоизомеров положения 4)
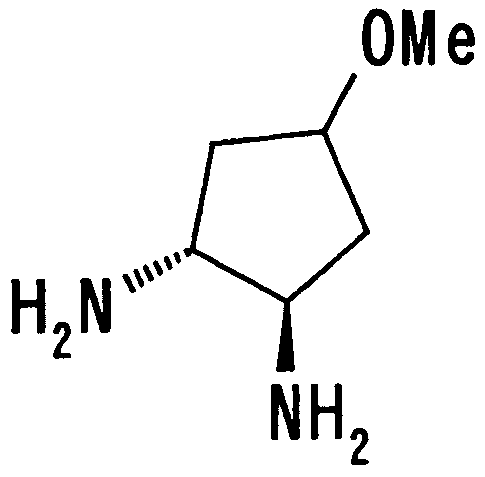
Соединение (584 мг), полученное в ссылочном примере 80, растворяли в этаноле, добавляли 10% палладий на углероде (321 мг) и гидрировали при нормальной температуре и нормальном давлении в течение 2 дней. После удаления катализатора фильтрованием реакционную смесь концентрировали и к остатку добавляли 1N этанольный раствор хлористоводородной кислоты и этилацетат. Смесь концентрировали с получением указанного в заголовке соединения (488 мг).
1Н-ЯМР (CDCl3) δ: 1,72-1,83 (1Н, м), 1,91-2,03 (1Н, м), 2,07-2,18 (1Н, м), 2,37-2,50 (1Н, м), 3,19 (3Н, с,), 3,55-3,75 (2Н, шир.), 3,85-3,95 (1Н, м), 8,60-8,90 (6Н, шир.).
МС (ESI) m/z: 261 (2M+H)+.
[Ссылочный пример 82]
N-[(1R*,2R*)-2-Амино-4-метоксициклопентил]-5-хлориндол-2-карбоксамид (смесь стереоизомеров положения 4)
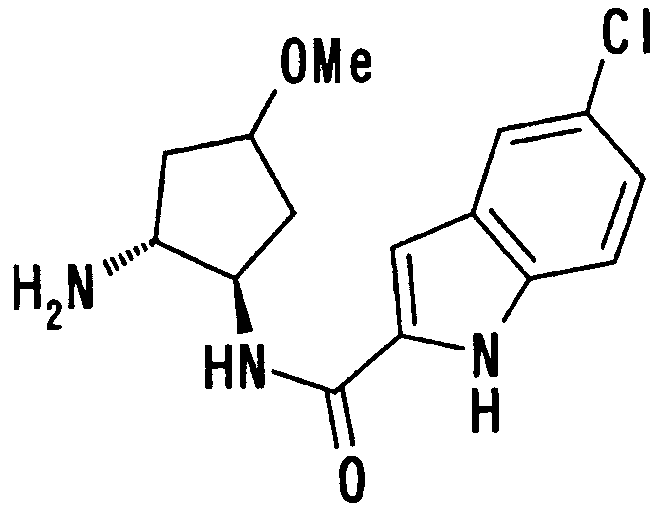
Соединение (470 мг), полученное в ссылочном примере 81, суспендировали в N,N-диметилформамиде (5 мл) и добавляли триэтиламин (0,966 мл) и п-нитрофенил 5-хлориндол-2-карбоксилат (805 мг). Смесь перемешивали при комнатной температуре в течение 4 дней. Растворитель отгоняли при пониженном давлении, добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей и затем органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:9) с получением указанного в заголовке соединения (268 мг).
[Ссылочный пример 83]
(1R*,2R*)-4-[(Бензилокси)метил]-1,2-циклопентандиол (смесь стереоизомеров положения 4)
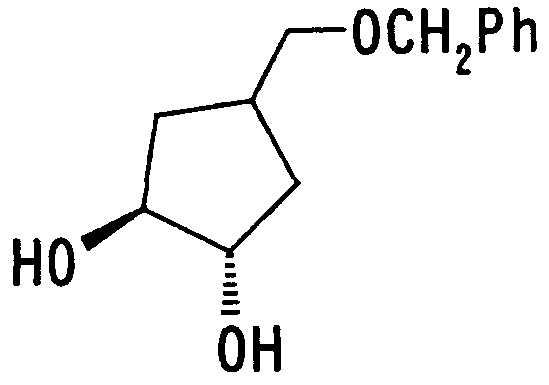
Указанное в заголовке соединение получали бензилированием 4-гидроксиметил-1-циклопентена (J. Heterocycl. Chem., 1989, Vol. 26, p. 451) бензилбромидом и последующим взаимодействием продукта со смесью муравьиная кислота-пероксид водорода подобно способу ссылочного примера 79.
1Н-ЯМР (CDCl3) δ: 1,44-1,52 (1H, м), 1,77-1,85 (1H, м), 1,89-1,97 (1H, м), 2,25-2,35 (1H, м), 2,46-2,58 (1H, м), 3,40-3,50 (2H, м), 3,89 (1H, шир.с), 4,08 (1H, шир.с), 4,54 (2H, с), 7,27-7,39 (5H, м)
МС (FAB) m/z: 223 (М+Н)+.
[Ссылочный пример 84]
(1R*,2R*)-4-[(Бензилокси)метил]-1,2-циклопентандиамин (смесь стереоизомеров положения 4)
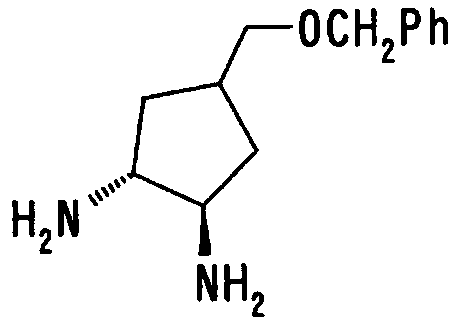
(1R*,2R*)-4-Бензилоксиметил-1,2-диазидоциклопентан получали из соединения, полученного в ссылочном примере 83, подобно способу ссылочного примера 80. Указанное в заголовке соединение получали подобно способу ссылочного примера 81 из указанного продукта без его очистки.
[Ссылочный пример 85]
N-{(1R*,2R*)-2-Амино-4-[(бензилокси)метил]циклопентил}-5-хлориндол-2-карбоксамид (смесь стереоизомеров положения 4)
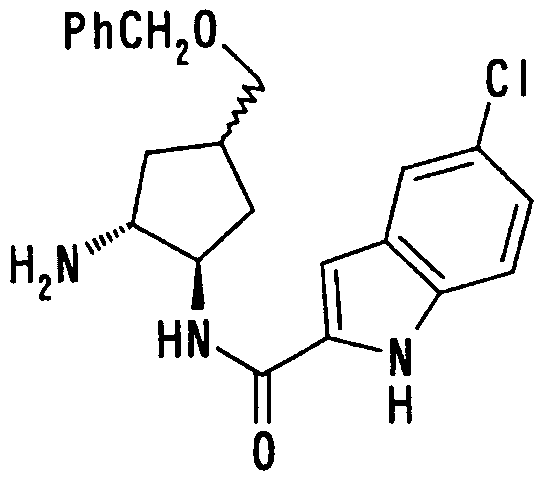
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 84, подобно способу ссылочного примера 59.
1Н-ЯМР (ДМСО-d6) δ: 1,07-1,15 (0,5H, м), 1,26-1,35 (0,5H, м), 1,47-1,55 (0,5H, м), 1,61-1,79 (1H, м), 1,83-1,92 (0,5H, м), 1,99-2,10 (0,5H, м), 2,12-2,20 (0,5H, м), 2,27-2,40 (1H, м), 3,10-3,20 (1H, м), 3,33-3,39 (2H, м), 3,81-3,92 (1H, м), 4,48 (2H, с), 7,13-7,20 (2H, м), 7,22-7,39 (5H, м), 7,43 (1H, д, J=8,5Гц), 7,69 (1H, д, J=2,2Гц), 8,34 (1H, т, J=7,1Гц).
МС (FAB) m/z: 398 (М+Н)+.
[Ссылочный пример 86]
Этил (1R*,3R*,6S*)-7-оксабицикло[4.1.0]гептан-3-карбоксилат
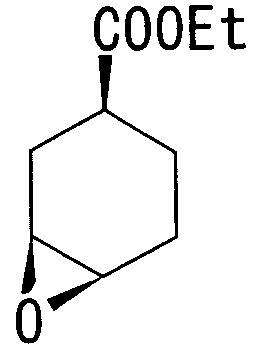
(1R*,4R*,5R*)-4-Йод-6-оксабицикло[3.2.1]октан-7-он (J. Org. Chem., 1996, Vol. 61, p. 8687) (14,3 г) растворяли в этаноле (130 мл), добавляли при охлаждении льдом 2N водный раствор (34,5 мл) гидроксида натрия и смесь перемешивали затем при комнатной температуре в течение 7 часов. Затем растворитель отгоняли при пониженном давлении и добавляли к остатку воду и экстрагировали метиленхлоридом, экстракт сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 83:17) с получением указанного в заголовке соединения (6,54 г).
1Н-ЯМР (CDCl3) δ: 1,25 (3Н, т, J=7,1Гц), 1,50-1,70 (2Н, м), 1,71-1,82 (1Н, м), 2,08-2,28 (4Н, м), 3,16 (2Н, с), 4,12 (2Н, кв, J=7,1Гц).
[Ссылочный пример 87]
Этил (1R*,3S*,4S*)-3-азидо-4-гидроксициклогексанкарбоксилат
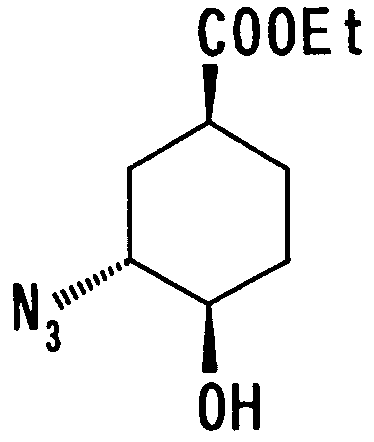
Соединение (13,6 г), полученное в ссылочном примере 86, растворяли в N,N-диметилформамиде (100 мл), добавляли последовательно при комнатной температуре хлорид аммония (6,45 г) и азид натрия (7,8 г) и смесь затем перемешивали при 75°C в течение 12 часов. Растворитель концентрировали до примерно 1/3 и остаток разбавляли водой и этилацетатом при перемешивании смеси в течение 3 минут. Полученный органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанного в заголовке соединения (15,8 г).
1Н-ЯМР (CDCl3) δ: 1,28 (3Н, т, J=7,1Гц), 1,37-1,67 (2Н, м), 1,86-1,95 (1Н, м), 2,04-2,18 (2Н, м), 2,32-2,43 (1Н, м), 2,68-2,78 (1Н, м), 3,40-3,60 (2Н, м), 4,17 (2Н, кв, J=7,1Гц).
[Ссылочный пример 88]
Этил (1R*,3S*,4S*)-3-[(трет-бутоксикарбонил)амино]-4-гидроксициклогексанкарбоксилат
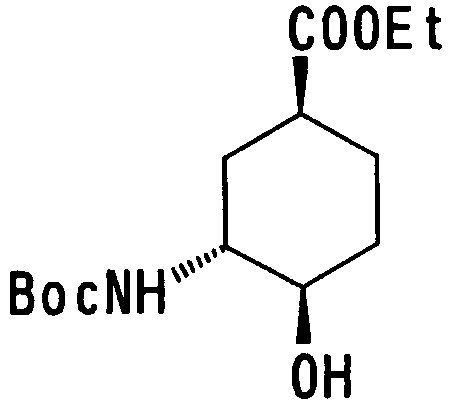
Соединение (100 мг), полученное в ссылочном примере 87, и ди-трет-бутилдикарбонат (133 мг) растворяли в этилацетате (12 мл), добавляли каталитическое количество 10% палладия на углероде и смесь перемешивали при комнатной температуре в течение 12 часов в атмосфере водорода. Затем нерастворимое вещество удаляли фильтрованием, отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1) с получением указанного в заголовке соединения (145 мг).
1Н-ЯМР (CDCl3) δ: 1,28 (3H, т, J=7,1Гц), 1,45 (9H, с), 1,38-1,57 (2H, м), 1,86-1,95 (1H, м), 2,05-2,17 (1H, м), 2,29-2,39 (2H, м), 2,61-2,68 (1H, м), 3,25-3,66 (3H, м), 4,17 (2H, кв, J=7,1Гц), 4,53 (1H, шир.с).
[Ссылочный пример 89]
Этил (1R*,3S*,4R*)-4-азидо-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат и этил (1R*,3S*,4S*)-4-азидо-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
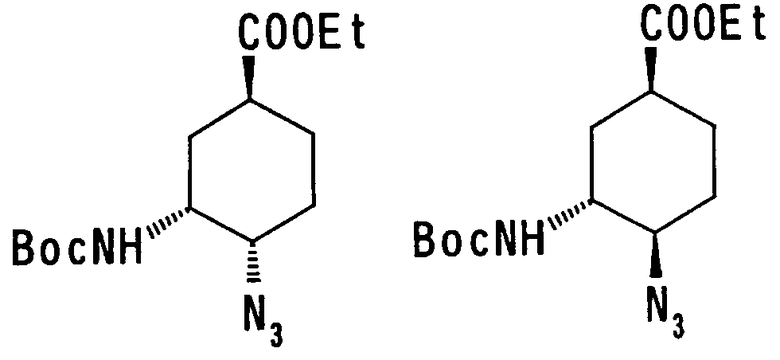
После растворения соединения (16 г), полученного в ссылочном примере 88, и триэтиламина (38 мл) в метиленхлориде (150 мл) и охлаждения раствора до -78°C добавляли по каплям метансульфонилхлорид (13 мл) при той же температуре. После перемешивания в течение 15 минут при той же температуре смесь нагревали до 0°C и перемешивали 30 минут, а затем 2 часа при комнатной температуре. Добавляли 0,1N хлористоводородную кислоту и смесь разбавляли метиленхлоридом, затем полученный органический слой отделяли, промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении с получением неочищенного этил (1R*,3S*,4S*)-3-[(трет-бутоксикарбонил)амино]-4-[(метансульфонил)окси]циклогексанкарбоксилата.
Полученный продукт растворяли в N,N-диметилформамиде (100 мл) и добавляли при комнатной температуре азид натрия (18 г). Смесь нагревали до 75°C и перемешивали 12 часов. Концентрировали растворитель до 1/3, остаток разбавляли водой и этилацетатом и перемешивали смесь в течение 3 минут. Полученный органический слой отделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанных в заголовке соединений [(1R*,3S*,4R*)-форма (6,74 г) и (1R*,3S*,4S*)-форма (1,32 г)].
(1R*,3S*,4R*)-форма:
1Н-ЯМР (CDCl3) δ: 1,26 (3Н, т, J=7,1Гц), 1,45 (9Н, с), 1,38-2,33 (6Н, м), 2,57-2,68 (1Н, м), 3,77-4,20 (4Н, м), 4,63 (1Н, шир.с).
(1R*,3S*,4S*)-форма:
1Н-ЯМР (CDCl3) δ: 1,27 (3Н, т, J=7,1Гц), 1,46 (9Н, с), 1,53-2,30 (6Н, м), 2,50-2,65 (1Н, м), 3,42-3,72 (2Н, м), 4,15 (2Н, кв, J=7,1Гц), 4,67 (1Н, шир.с).
[Ссылочный пример 90]
Этил (1R*,3S*,4R*)-4-амино-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
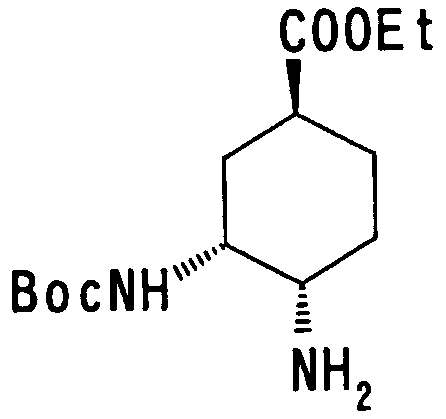
Этил (1R*,3S*,4R*)-4-азидо-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат (5,4 г), полученный в ссылочном примере 89, растворяли в смешанном растворителе из этанола (10 мл) и этилацетата (10 мл), добавляли каталитическое количество 10% палладия на углероде и смесь перемешивали при комнатной температуре в течение 20 часов в атмосфере водорода. После удаления фильтрованием нерастворимого вещества растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (4,7 г).
[Ссылочный пример 91]
Этил (1R*,3S*,4R*)-3-[(трет-бутоксикарбонил)амино]-4-{[(5-хлориндол-2-ил)карбонил]амино}циклогексанкарбоксилат
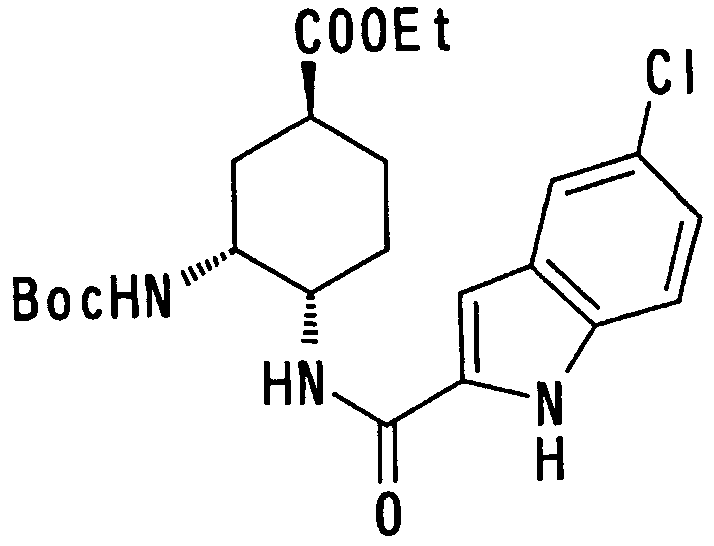
Соединение (4,62 г), полученное в ссылочном примере 90, растворяли в метиленхлориде (50 мл), добавляли при комнатной температуре 5-хлориндол-2-карбоновую кислоту (3,63 г), моногидрат 1-гидроксибензотриазола (2,43 г) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (3,45 г) и смесь перемешивали в течение 12 часов. После добавления 0,1N хлористоводородной кислоты смесь экстрагировали метиленхлоридом, полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 2:3) с получением указанного в заголовке соединения (5,3 г).
1Н-ЯМР (CDCl3) δ: 1,26 (3H, т, J=7,1Гц), 1,43 (9H, с), 1,35-2,46 (7H, м), 3,91-4,02 (1H, м), 4,10-4,22 (2H, м), 4,79 (1H, шир.с), 6,79 (1H, с), 7,18-7,40 (2H, м), 7,59 (1H, с), 8,00 (1H, шир.с), 9,13 (1H, шир.с).
[Ссылочный пример 92]
Этил (1S*,3S*,6R*)-7-оксабицикло[4.1.0]гептан-3-карбоксилат
(1S*,4S*,5S*)-4-Йод-6-оксабицикло[3.2.1]октан-7-он (J. Org. Chem., 1996, Vol. 61, p. 8687) (89,3 г) суспендировали в этаноле (810 мл), добавляли 2N водный раствор (213 мл) гидроксида натрия и смесь перемешивали затем при комнатной температуре в течение 3 часов. После отгонки при пониженном давлении растворителя добавляли к остатку воду и экстрагировали метиленхлоридом, экстракт сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 17:3) с получением указанного в заголовке соединения (41,3 г).
[α]D 25 = -58° (C = 1,0, хлороформ).
[Ссылочный пример 93]
Этил (1S,3R,4R)-3-азидо-4-гидроксициклогексанкарбоксилат
Соединение (41 г), полученное в ссылочном примере 92, растворяли в N,N-диметилформамиде (300 мл), последовательно добавляли хлорид аммония (19,3 г) и азид натрия (23,5 г) при комнатной температуре и затем смесь перемешивали при 76°C в течение 13 часов. Реакционную смесь фильтровали, фильтрат концентрировали, в осадок продукта, ранее уловленный фильтром, добавляли воду для растворения выделенного продукта. Раствор экстрагировали этилацетатом. Полученный органический слой промывали водой и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (51,5 г).
[α]D 25 = +8° (C = 1,0, хлороформ).
[Ссылочный пример 94]
Этил (1S,3R,4R)-3-[(трет-бутоксикарбонил)амино]-4-гидроксициклогексанкарбоксилат
Соединение (51,2 г), полученное в ссылочном примере 93, и ди-трет-бутилдикарбонат (68,1 г) растворяли в этилацетате (1000 мл), добавляли 5% палладий на углероде (5,0 г) и смесь перемешивали в течение ночи при комнатной температуре при давлении водорода 7 кг/см2. После удаления нерастворимого вещества фильтрованием отгоняли при пониженном давлении растворитель, остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1 → 3:1) и добавляли гексан для отверждения продукта с получением указанного в заголовке соединения (46,9 г).
[α]D 25 = +25° (C = 1,0, хлороформ).
[Ссылочный пример 95]
Этил (1S,3R,4S)-4-азидо-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат и этил (1S,3R,4R)-4-азидо-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
Соединение (53,5 г), полученное в ссылочном примере 94, и триэтиламин (130 мл) растворяли в метиленхлориде (500 мл) и при охлаждении, при температуре от -10°C до -15°C в течение 20 минут добавляли по каплям метансульфонилхлорид (42 мл). После перемешивания в течение 20 минут при той же температуре смесь нагревали до комнатной температуры за 2 часа. Реакционную смесь охлаждали до 0°C, добавляли по каплям 0,5N хлористоводородную кислоту (800 мл) и смесь экстрагировали метиленхлоридом. Полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении с получением неочищенного этил (1S,3R,4R)-3-[(трет-бутоксикарбонил)амино]-4-[(метансульфонил)окси]циклогексанкарбоксилата.
Полученный выше неочищенный продукт растворяли в N,N-диметилформамиде (335 мл), добавляли азид натрия (60,5 г) и смесь перемешивали при 67°C-75°C в течение 16 часов. Реакционную смесь фильтровали, фильтрат концентрировали, отгоняя 250 мл растворителя, осадок продукта, уловленный фильтром, растворяли в воде и экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанных в заголовке соединений [(1S,3R,4S)-форма (18,4 г) и (1S,3R,4R)-форма (3,3 г)].
(1S,3R,4S)-форма: [α]D 25 = +62°(C = 1,0, хлороформ).
(1S,3R,4R)-форма: [α]D 25 = -19° (C = 1,0, хлороформ).
[Ссылочный пример 96]
Этил (1S,3R,4S)-4-амино-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
Соединение (4,0 г), полученное в ссылочном примере 95, растворяли в смешанном растворителе из этанола (150 мл) и этилацетата (150 мл), добавляли 5% палладий на углероде (0,5 г) и смесь перемешивали при комнатной температуре в течение 17 часов в атмосфере водорода (5 кг/см2). После удаления фильтрованием нерастворимого вещества отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (4,2 г).
[Ссылочный пример 97]
Этил (1S,3R,4S)-3-[(трет-бутоксикарбонил)амино]-4-{[(5-хлориндол-2-ил)карбонил]амино}циклогексанкарбоксилат
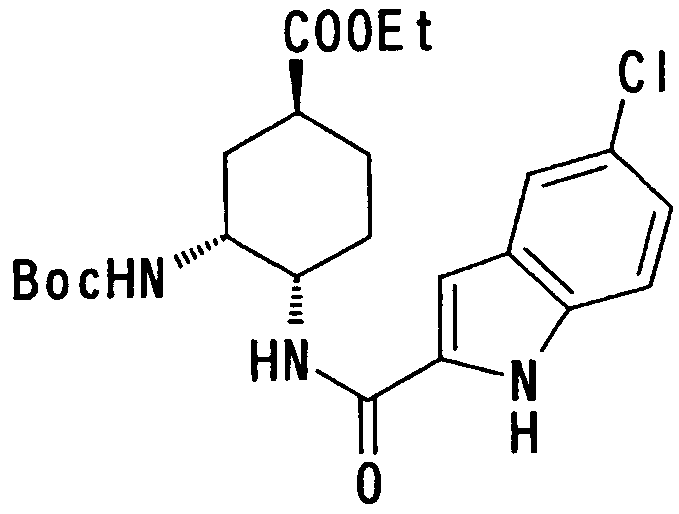
Соединение (4,2 г), полученное в ссылочном примере 96, растворяли в метиленхлориде (50 мл), добавляли при комнатной температуре 5-хлориндол-2-карбоновую кислоту (3,33 г), моногидрат 1-гидроксибензотриазола (2,52 г) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (3,15 г) и смесь перемешивали в течение 12 часов. После добавления к реакционной смеси 0,1N хлористоводородной кислоты смесь экстрагировали метиленхлоридом, полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:1) с получением указанного в заголовке соединения (4,36 г).
[α]D 25 = -27° (C = 1,0, хлороформ).
[Ссылочный пример 98]
Этил (1R*,3S*,4R*)-3-[(трет-бутоксикарбонил)амино]-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
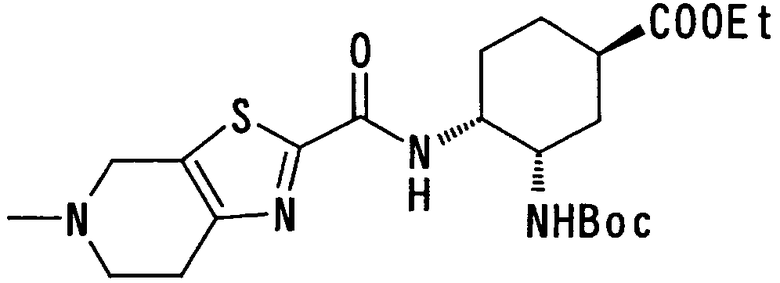
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 90, и соединения, полученного в ссылочном примере 10, подобно способу ссылочного примера 91.
[Ссылочный пример 99]
Бензил 3-циклогексен-1-карбоксилат
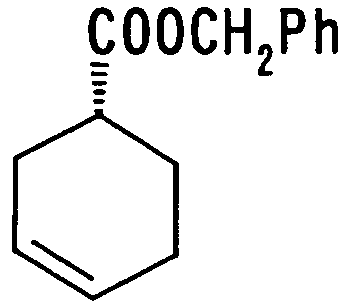
(±)-3-Циклогексен-1-карбоновую кислоту (50 г) растворяли в N,N-диметилформамиде (550 мл), добавляли при охлаждении льдом триэтиламин (170 мл) и бензилбромид (61 мл) и смесь перемешивали при комнатной температуре в течение 12 часов. Добавляли воду, проводили экстракцию этилацетатом и полученный органический слой промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1) с получением указанного в заголовке соединения (70,8 г).
1Н-ЯМР (CDCl3) δ: 1,66-1,76 (1Н, м), 2,00-2,13 (3Н, м), 2,27-2,29 (2Н, м), 2,58-2,65 (1Н, м), 5,13 (2Н, с), 5,66 (2Н, шир.с), 7,29-7,38 (5Н, м).
[Ссылочный пример 100]
Бензил (1R*,3S*,6S*)-7-оксабицикло[4.1.0]гептан-3-карбоксилат
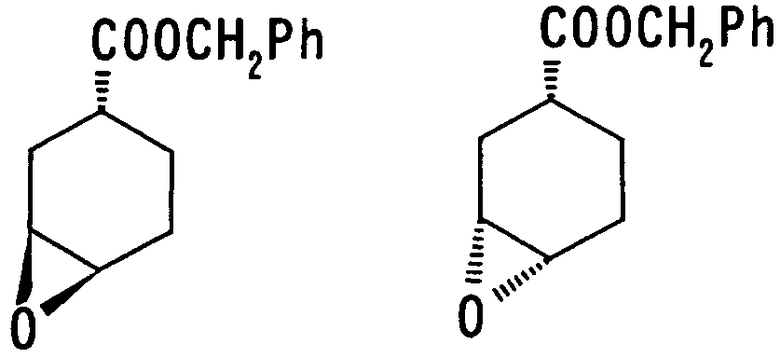
Соединение (40 г), полученное в ссылочном примере 99, растворяли в метиленхлориде (500 мл), добавляли при охлаждении льдом м-хлорпербензойную кислоту (86 г) и смесь перемешивали 2 часа. После добавления 10% водного раствора тиосульфата натрия и перемешивания в течение 20 минут органический слой отделяли, промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:9) с получением указанного в заголовке соединения (23,4 г) и бензил (1R*,3R*,6S*)-7-оксабицикло[4.1.0]гептан-3-карбоксилата (12,1 г).
1Н-ЯМР (CDCl3) δ: 1,39-1,49 (1H, м), 1,75-1,82 (1H, м), 1,90-2,04 (3H, м), 2,30 (1H, дд, J=14,9, 4,9Гц), 2,54-2,61 (1H, м), 3,12-3,14 (1H, м), 3,22-3,24 (1H, м), 5,12 (2H, с), 7,30-7,39 (5H, м),
МС (FAB) m/z: 233 (M+H)+.
[Ссылочный пример 101]
Бензил (1R*,3S*,4S*)-4-азидо-3-гидроксициклогексанкарбоксилат
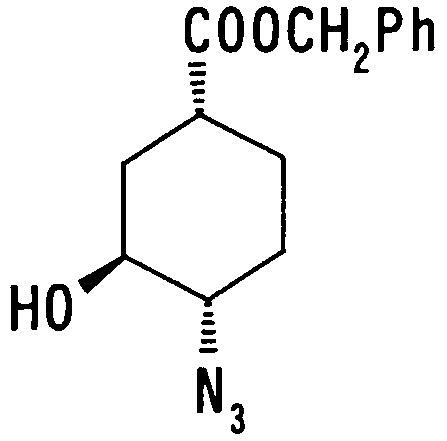
Соединение (52,3 г), полученное в ссылочном примере 100, растворяли в N,N-диметилформамиде (1000 мл), добавляли хлорид аммония (21,9 г) и азид натрия (18,1 г) и смесь нагревали до 70°C и перемешивали 24 часа. Растворитель отгоняли при пониженном давлении, добавляли воду и экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (61,8 г).
1Н-ЯМР (CDCl3) δ: 1,51-1,66 (2Н, м), 1,91-1,98 (1Н, м), 2,07-2,10 (1Н, м), 2,27-2,32 (1Н, м), 2,51-2,52 (1Н, м), 2,81-2,86 (1Н, м), 3,30-3,36 (1Н, м), 3,70-3,75 (1Н, м), 5,13 (2Н, с), 7,30-7,39 (5Н, м).
[Ссылочный пример 102]
Бензил (1R*,3S*,4S*)-4-[(трет-бутоксикарбонил)амино]-3-гидроксициклогексанкарбоксилат
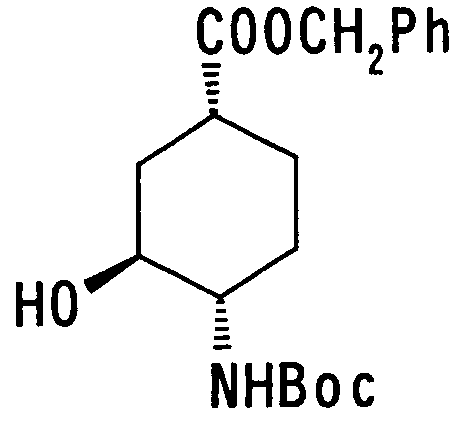
Соединение (5,27 г), полученное в ссылочном примере 101, растворяли в тетрагидрофуране (25 мл), добавляли трифенилфосфин (5,53 г) и воду (0,55 мл) и смесь перемешивали при комнатной температуре в течение 20 часов. К реакционной смеси добавляли ди-трет-бутилдикарбонат (4,82 г), продолжая перемешивать еще 2 часа. Отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 2:1) с получением указанного в заголовке соединения (6,22 г).
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 1,59-1,66 (2H, м), 1,88-2,00 (2H, м), 2,29-2,32 (1H, м), 2,80-2,85 (1H, м), 3,02 (1H, шир.с), 3,42 (1H, шир.с), 3,59-3,65 (1H, м), 4,56 (1H, шир.с), 5,12 (2H, кв, J=12,5Гц), 7,30-7,38 (5H, м).
МС (FAB) m/z: 350 (M+H)+.
[Ссылочный пример 103]
Метил (1R*,3S*,4S*)-4-[(трет-бутоксикарбонил)амино]-3-гидроксициклогексанкарбоксилат
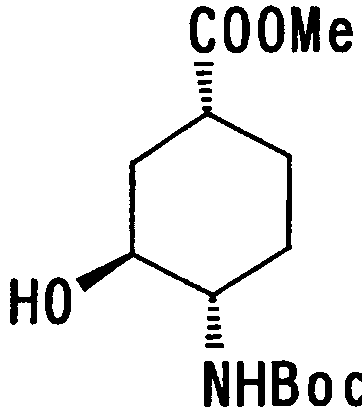
Соединение (2,54 г), полученное в ссылочном примере 102, растворяли в этилацетате (15 мл) и к раствору добавляли каталитическое количество 10% палладия на древесном угле. Смесь перемешивали в токе водорода при комнатной температуре в течение 20 часов. Катализатор отфильтровывали и фильтрат концентрировали при пониженном давлении с получением (1R*,3S*,4S*)-4-[(трет-бутоксикарбонил)амино]-3-гидроксициклогексанкарбоновой кислоты в виде бесцветного масла. Масло растворяли в смеси метанола (8 мл) и толуола (15 мл), к раствору добавляли при охлаждении льдом 2N гексановый раствор (10 мл) триметилсилилдиазометана и полученную смесь перемешивали 30 минут при комнатной температуре. После удаления при пониженном давлении растворителя полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 1:1) с получением указанного в заголовке соединения (1,82 г).
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 1,36-2,32 (7H, м), 2,74-2,82 (1H, м), 3,04 (1H, шир.с), 3,33-3,47 (1H, м), 3,55-3,65 (1H, м), 3,68 (3H, с), 4,56 (1H, шир.с).
МС (FAB) m/z: 274 (M+H)+.
[Ссылочный пример 104]
Метил (1R*,3R*,4S*)-3-азидо-4-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат и метил (1R*,3S*,4S*)-3-азидо-4-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
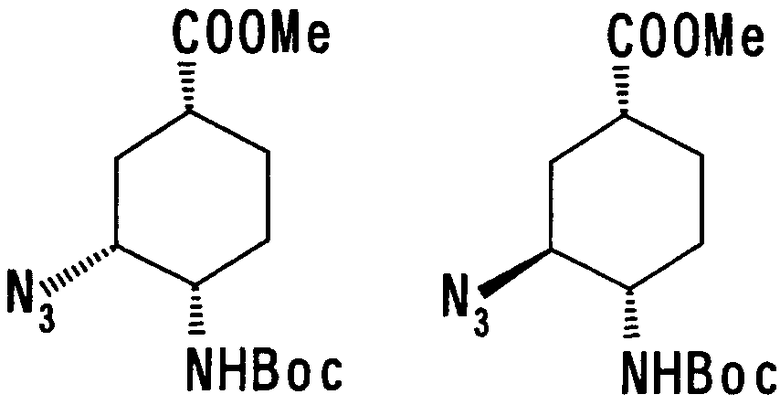
Соединение (1,81 г), полученное в ссылочном примере 103, растворяли в метиленхлориде (36 мл) и добавляли при -78°C триэтиламин (4,6 мл) и метансульфонилхлорид (1,63 мл). Через 30 минут смесь нагревали до 0°C и перемешивали в течение 30 минут. Добавляли 1N хлористоводородную кислоту, смесь экстрагировали метиленхлоридом и полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении с получением неочищенного метил (1R*,3S*,4S*)-4-[(трет-бутоксикарбонил)амино]-3-[(метилсульфонил)окси]циклогексанкарбоксилата.
Неочищенный продукт, полученный выше, растворяли в N,N-диметилформамиде (23 мл), добавляли азид натрия (1,29 г) и смесь нагревали до 70°C и перемешивали 12 часов. В реакционную смесь добавляли воду, экстрагировали этилацетатом и полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной флэш-хроматографией на силикагеле (этилацетат:гексан = 3:17) с получением метил (1R*,3S*,4S*)-3-азидо-4-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилата (85 мг) и метил (1R*,3R*,4S*)-3-азидо-4-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилата (590 мг).
(1R*,3R*,4S*)-форма: 1Н-ЯМР (CDCl3) δ: 1,45 (9Н, с), 1,35-2,35 (7Н, м), 2,45-2,55 (1Н, м), 3,73 (3Н, с), 3,67-3,84 (2Н, м), 4,70 (1Н, шир.с).
МС (FAB) m/z: 299 (M+H)+.
(1R*,3S*,4S*)-форма: 1Н-ЯМР (CDCl3) δ: 1,45 (9Н, с), 1,56-2,25 (7Н, м), 2,68-2,80 (1Н, м), 3,70 (3Н, с), 3,48-3,68 (2Н, м), 4,56 (1Н, шир.с).
МС (FAB) m/z: 299 (M+H)+.
[Ссылочный пример 105]
Метил (1R*,3R*,4S*)-3-амино-4-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
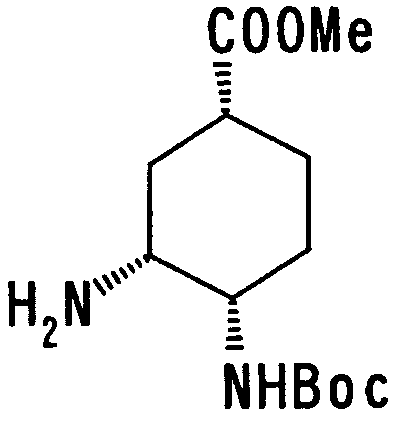
(1R*,3R*,4S*)-соединение (230 мг), полученное в ссылочном примере 104, растворяли в этилацетате (8 мл), добавляли каталитическое количество 10% палладия на углероде и смесь перемешивали при комнатной температуре в течение 20 часов в атмосфере водорода. Нерастворимое вещество удаляли фильтрованием и фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (220 мг).
[Ссылочный пример 106]
Метил (1R*,3R*,4S*)-4-[(трет-бутоксикарбонил)амино]-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
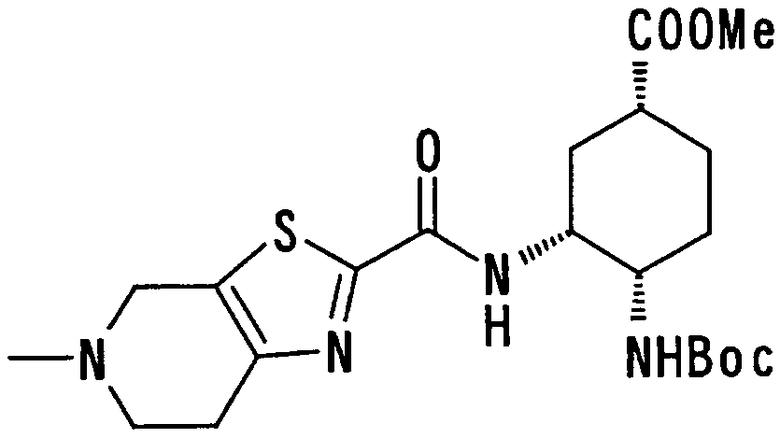
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 105, и соединения, полученного в ссылочном примере 10, подобно способу ссылочного примера 91.
1Н-ЯМР (CDCl3) δ: 1,46 (9H, с), 1,53-1,95 (5H, м), 2,17-2,24 (1H, м), 2,50 (3H, с), 2,50-2,53 (1H, м), 2,80-2,96 (4H, м), 3,67 (3H, с), 3,69-3,74 (1H, м), 4,10 (2H, шир.с), 4,88 (1H, шир.с).
МС (FAB) m/z: 453 (M+H)+.
[Ссылочный пример 107]
Метил (1R*,3R*,4S*)-4-[(трет-бутоксикарбонил)амино-3-{[(5-хлориндол-2-ил)карбонил]амино}циклогексанкарбоксилат
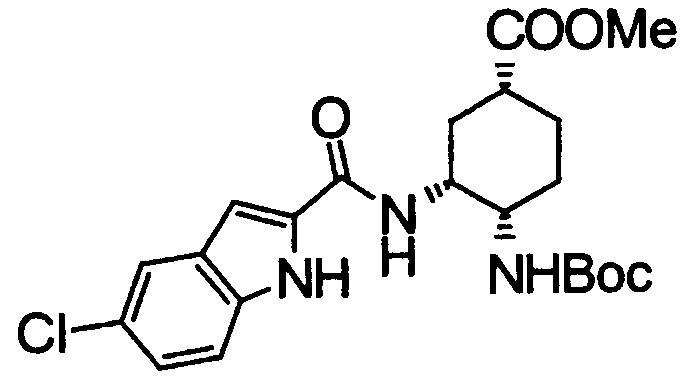
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 105, подобно способу ссылочного примера 91.
1Н-ЯМР (CDCl3) δ: 1,33 (9H, с), 1,42-2,47 (6H, м), 2,78-2,88 (1H, м), 3,70 (3H, с), 3,86-4,15 (2H, м), 4,65-4,75 (1H, м), 6,86 (1H, шир.с), 7,18-7,38 (2H, м), 7,57-7,61 (1H, м), 8,32 (1H, шир.с).
МС (ESI) m/z: 450 (М+Н)+.
[Ссылочный пример 108]
Бензил (1S,3R,6R)-7-оксабицикло[4.1.0]гептан-3-карбоксилат
1) Бензил (1R)-3-циклогексен-1-карбоксилат получали из (1R)-3-циклогексен-1-карбоновой кислоты (J. Am. Chem. Soc., 1978, Vol. 100, p. 5199) подобно способу ссылочного примера 99.
2) Указанное в заголовке соединение получали из описанного выше продукта подобно способу ссылочного примера 100.
МС (FAB) m/z: 233(М+Н)+.
[Ссылочный пример 109]
Бензил (1R,3S,4S)-4-[(трет-бутоксикарбонил)амино]-3-гидроксициклогексанкарбоксилат
1) Бензил-(1R,3S,4S)-4-азидо-3-гидроксициклогексанкарбоксилат получали из соединения, полученного в ссылочном примере 108, подобно способу ссылочного примера 101.
2) Указанное в заголовке соединение получали из описанного выше продукта подобно способу ссылочного примера 102.
МС (FAB) m/z: 350(М+Н)+.
[Ссылочный пример 110]
Бензил (1R,3R,4S)-3-азидо-4-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
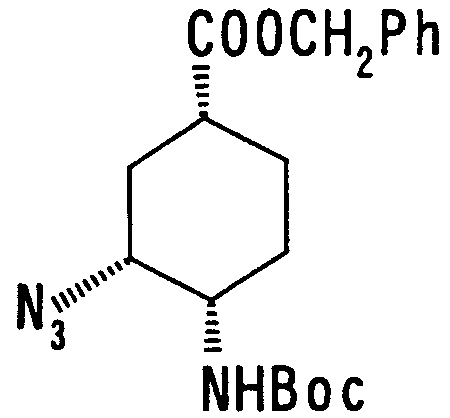
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 109, подобно способу ссылочного примера 104.
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,52-1,66 (2H, м), 1,83-2,01 (3H, м), 2,20-2,28 (1H, м), 2,51-2,54 (1H, м), 3,77 (2H, шир.с), 4,70 (1H, шир.с), 5,15 (2H, АВкв, J=12,2Гц), 7,33-7,38 (5H, м).
МС (FAB) m/z: 375 (M+H)+.
[Ссылочный пример 111]
Метил (1R,3R,4S)-3-азидо-4-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
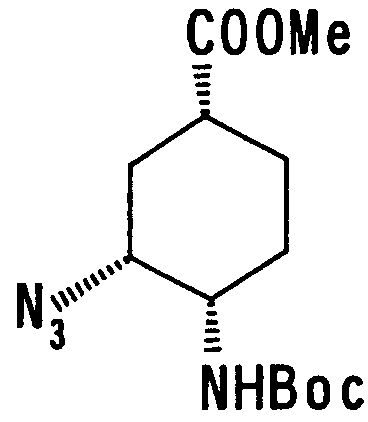
Соединение (3,5 г), полученное в ссылочном примере 110, растворяли в тетрагидрофуране (130 мл) и к раствору добавляли при охлаждении льдом воду (16 мл) и гидроксид лития (291 мг). Через 10 минут смесь нагревали до комнатной температуры, продолжая перемешивание. Через 20 минут реакцию прекращали, отгоняли при пониженном давлении растворитель и полученный остаток подвергали колоночной хроматографии на силикагеле (метанол:метиленхлорид = 1:20) с получением (1R,3R,4S)-3-азидо-4-[(трет-бутоксикарбонил)амино]циклогексанкарбоновой кислоты (3,34 г) в виде бледно-желтого масла. Полученный продукт растворяли в метаноле (18 мл) и толуоле (64 мл), добавляли при охлаждении льдом 2N гексановый раствор (6,1 мл) триметилсилилдиазометана. Через 10 минут смесь нагревали до комнатной температуры и перемешивали в течение 2 часов. Затем растворитель отгоняли при пониженном давлении, остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанного в заголовке соединения (3,35 г).
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,57-1,63 (2H, м), 1,82-1,85 (1H, м), 1,95-1,99 (2H, м), 2,20-2,28 (1H, м), 2,48-2,51 (1H, м), 3,73 (3H, с), 3,78 (2H, шир.с), 4,70-4,72 (1H, м).
МС (FAB) m/z: 299 (М+Н)+.
[Ссылочный пример 112]
Метил (1R,3R,4S)-4-[(трет-бутоксикарбонил)амино]-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
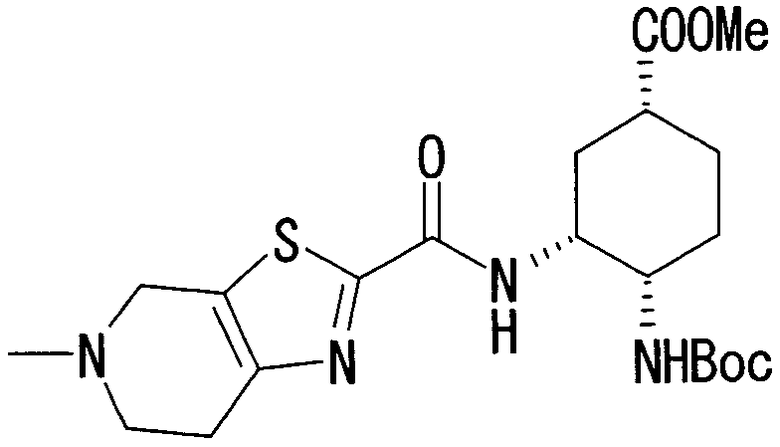
1) Метил (1R,3R,4S)-3-амино-4-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат получали из соединения, полученного в ссылочном примере 111, подобно способу ссылочного примера 105.
2) Указанное в заголовке соединение получали из описанного выше продукта и соединения, полученного в ссылочном примере 10, подобно способу ссылочного примера 106.
МС (FAB) m/z: 453(М+Н)+.
[Ссылочный пример 113]
трет-Бутил (1R*,2S*,5S*)-5-аминокарбонил-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексилкарбамат
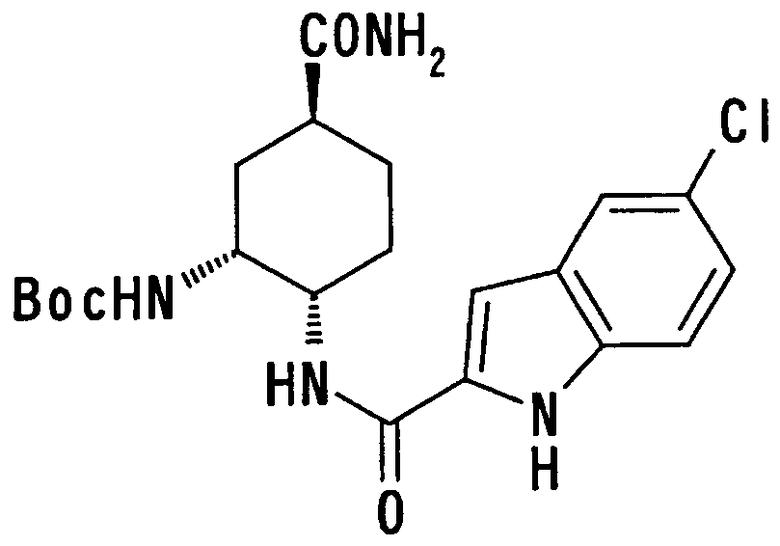
Соединение (590 мг), полученное в ссылочном примере 91, растворяли в смешанном растворителе из этанола (3 мл) и тетрагидрофурана (6 мл), добавляли при комнатной температуре 1N водный раствор (2,5 мл) гидроксида натрия и смесь перемешивали 12 часов. Растворитель отгоняли с получением (1R*,3S*,4R*)-3-[(трет-бутоксикарбонил)амино]-4-{[(5-хлориндол-2-ил)карбонил]амино}циклогексанкарбоксилата натрия. Полученный продукт суспендировали в N,N-диметилформамиде (4 мл), добавляли при комнатной температуре ди-трет-бутилдикарбонат (654 мг) и гидрокарбонат аммония (1 г) и смесь перемешивали 18 часов. Растворитель отгоняли при пониженном давлении, добавляли воду и смесь экстрагировали хлороформом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 47:3) с получением указанного в заголовке соединения (82 мг).
МС (ESI) m/z: 435(М+Н)+.
[Ссылочный пример 114]
Бензил (1R,6S)-6-{[(бензилокси)карбонил]амино}-3-циклогексен-1-илкарбамат
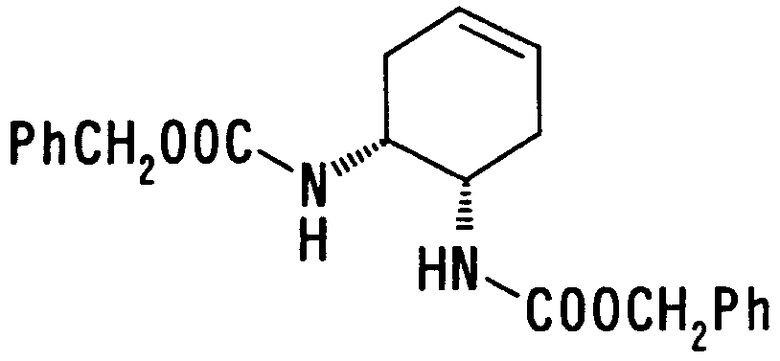
Гидрохлорид 4-циклогексен-1,2-диамина (4,0 г) растворяли в смешанном растворителе из воды (20 мл) и ацетонитрила (20 мл), добавляли бензилхлорформиат (7,66 мл) и карбонат калия (14,9 г) и смесь перемешивали при комнатной температуре в течение 3 дней. Реакционную смесь вливали в воду и экстрагировали метиленхлоридом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид) с получением указанного в заголовке соединения (8,22 г).
1Н-ЯМР (CDCl3) δ: 2,03 (2Н, м), 2,53 (2Н, д, J=17,1Гц), 3,77 (2Н, м), 5,03 (2Н, кв, J=12,3Гц), 5,09 (2Н, кв, J=12,3Гц), 5,59 (2Н, с), 7,32 (10Н, м).
МС (ESI) m/z: 381 (M+H)+.
[Ссылочный пример 115]
Бензил (1R*,2S*)-2-{[(бензилокси)карбонил]амино}-5-гидроксициклогексилкарбамат
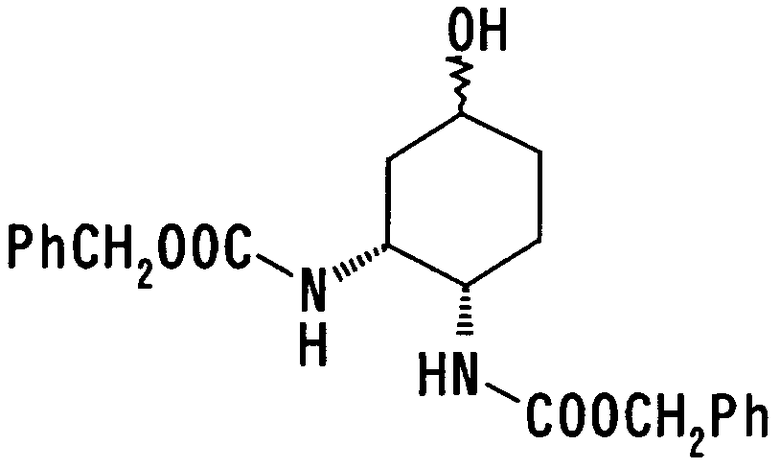
Соединение (10 г), полученное в ссылочном примере 114, растворяли в абсолютном тетрагидрофуране (70 мл), добавляли при 0°C боран-диметилсульфидный комплекс (7,4 мл) и смесь постепенно нагревали до комнатной температуры и перемешивали в течение 14 часов. В реакционную смесь добавляли лед для разложения избыточного борана, добавляли 1N водный раствор (80 мл) гидроксида натрия и 30% водный пероксид водорода (80 мл) и смесь перемешивали в течение 1 часа. Реакционную смесь экстрагировали этилацетатом, полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 2:1) с получением указанного в заголовке соединения (9,2 г).
1Н-ЯМР (CDCl3) δ: 1,98 (1Н, м), 2,08 (1Н, м), 2,30 (1Н, м), 3,43 (2Н, м), 3,73 (1Н, м), 5,06 (6Н, м), 7,32 (10Н, с).
МС (ESI) m/z: 399 (M+H)+.
[Ссылочный пример 116]
Бензил (1R*,2S*)-2-{[(бензилокси)карбонил]амино}-5-оксоциклогексилкарбамат
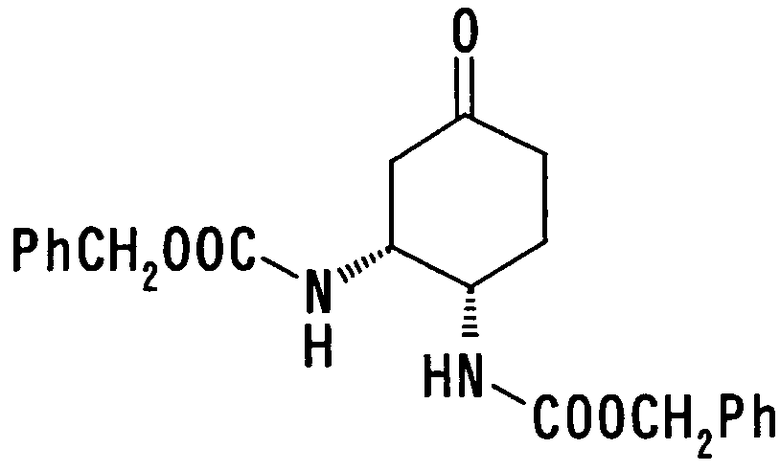
Диметилсульфоксид (8,2 мл) добавляли к раствору оксалилхлорида (9,9 мл) в метиленхлориде (90 мл) при -60°C и к смеси добавляли одной порцией раствор соединения (9,2 г), полученного в ссылочном примере 115, в тетрагидрофуране (90 мл). Через 1 час повышали температуру смеси до -40°C и добавляли одной порцией триэтиламин (26 мл). Смесь нагревали до комнатной температуры и перемешивали 3 часа. Реакционную смесь вливали в воду и экстрагировали метиленхлоридом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:1) с получением указанного в заголовке соединения (8,0 г).
1Н-ЯМР (CDCl3) δ: 2,27-2,43 (4Н, м), 2,78 (1Н, дд, J=14,4, 3,9Гц), 3,86 (2Н, м), 5,08 (4Н, м), 5,22 (2Н, м), 7,32 (10Н, м).
МС (ESI) m/z: 397 (M+H)+.
[Ссылочный пример 117]
Бензил (1R*,2S*)-2-{[(бензилокси)карбонил]амино}-5,5-диметоксициклогексилкарбамат
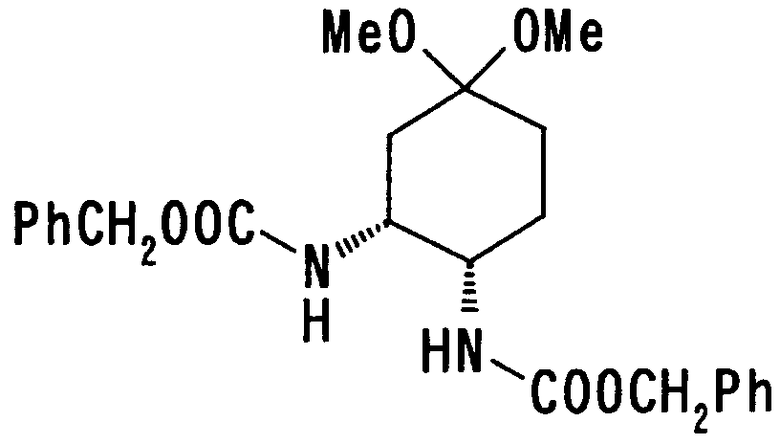
Соединение (3,89 г), полученное в ссылочном примере 116, растворяли в смешанном растворителе из метанола (15 мл) и тетрагидрофурана (15 мл), добавляли 2,2-диметоксипропан (10,7 мл) и п-толуолсульфоновую кислоту (187 мг) и смесь перемешивали при комнатной температуре в течение 3 часов. Растворитель концентрировали, добавляли насыщенный водный раствор гидрокарбоната натрия и смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:2) с получением указанного в заголовке соединения (3,54 г).
1Н-ЯМР (CDCl3) δ: 1,30-1,41 (4Н, м), 1,93 (1Н, м), 2,38 (1Н, м), 3,19 (6Н, с), 3,46 (1Н, м), 3,59 (1Н, м), 5,03 (2Н, кв, J=12,5Гц), 5,09 (2Н, кв, J=12,5Гц), 7,32 (10Н, с).
[Ссылочный пример 118]
N-[(1R*,2S*)-2-Амино-4,4-диметоксициклогексил]-5-хлориндол-2-карбоксамид и N-[(1R*,2S*)-2-амино-5,5-диметоксициклогексил]-5-хлориндол-2-карбоксамид
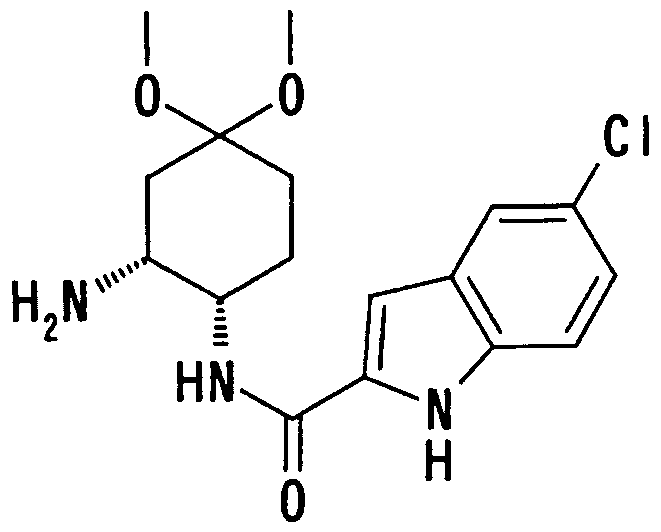
Соединение (1,45 г), полученное в ссылочном примере 117, растворяли в метаноле (12 мл), добавляли 10% палладий на углероде (290 мг) и смесь перемешивали при комнатной температуре в течение 20 часов в атмосфере водорода. Дополнительно добавляли 10% палладий на углероде (290 мг) и метанол (10 мл) и смесь перемешивали 8 часов. Реакционную смесь фильтровали через целит, маточный раствор концентрировали и остаток растворяли в N,N-диметилформамиде (10 мл). Добавляли 5-хлориндол-2-карбоновую кислоту (320 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (377 мг), моногидрат 1-гидроксибензотриазола (301 мг) и N-метилморфолин (360 мл) и смесь перемешивали при комнатной температуре в течение 14 часов. Реакционную смесь вливали в водный раствор гидрокарбоната натрия и экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и остаток выделяли и очищали препаративной тонкослойной хроматографией на силикагеле (метиленхлорид:метанол = 93:7) с получением N-[(1R*,2S*)-2-амино-4,4-диметоксициклогексил]-5-хлориндол-2-карбоксамида (или N-[(1R*,2S*)-2-амино-5,5-диметоксициклогексил]-5-хлориндол-2-карбоксамида) (98 мг) и N-[(1R*,2S*)-2-амино-5,5-диметоксициклогексил]-5-хлориндол-2-карбоксамида (или N-[(1R*,2S*)-2-амино-4,4-диметоксициклогексил]-5-хлориндол-2-карбоксамида) (105 мг).
N-[(1R*,2S*)-2-Амино-4,4-диметоксициклогексил]-5-хлориндол-2-карбоксамид:
1Н-ЯМР (CDCl3) δ: 1,45-1,50 (2H, м), 2,06-2,10 (2H, м), 2,34 (1H, д, J=13,1Гц), 2,78 (1H, дт, J=2,9, 13,1Гц), 3,18 (3H, с), 3,23 (3H, с), 3,75-3,77 (1H, м), 6,24 (1H, д, J=8,3Гц), 6,79 (1H, с), 7,23 (1H, дд, J=8,8, 2,0Гц), 7,35 (1H, д, J=8,8Гц), 7,60 (1H, д, J=8,8Гц), 9,53 (1H, шир.с).
МС (ESI) m/z: 352 (М+Н)+.
N-[(1R*,2S*)-2-Амино-5,5-диметоксициклогексил]-5-хлориндол-2-карбоксамид:
1Н-ЯМР (CDCl3) δ: 1,83-1,87 (1H, м), 1,97-2,01 (1H, м), 2,39 (1H, шир., J=13,2Гц), 2,86-2,90 (1H, м), 3,22-3,28 (10H, м), 4,00-4,02 (1H, м), 6,77 (1H, с), 7,23 (1H, д, J=8,5Гц), 7,37 (1H, д, J=8,5Гц), 7,61 (1H, с), 9,49 (1H, шир.с).
МС (ESI) m/z: 352 (М+Н)+.
[Ссылочный пример 119]
Бензил (7R*,8S*)-7-{[(бензилокси)карбонил]амино}-1,4-диоксаспиро[4.5]дец-8-илкарбамат
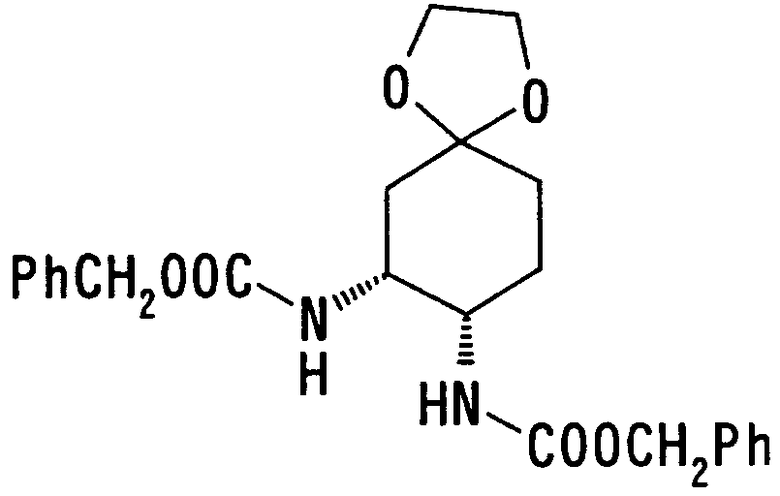
Соединение (4,0 г), полученное в ссылочном примере 116, растворяли в абсолютном тетрагидрофуране (30 мл), добавляли этиленгликоль (5,6 мл) и п-толуолсульфоновую кислоту (192 мг) и смесь перемешивали при комнатной температуре в течение 17 часов. Реакционную смесь вливали в насыщенный водный раствор гидрокарбоната натрия и экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:1) с получением указанного в заголовке соединения (4,23 г).
1Н-ЯМР (CDCl3) δ: 1,65-1,71 (4Н, м), 2,00 (1Н, м), 2,11 (1Н, м), 3,49 (1Н, м), 3,73 (1Н, м), 3,93 (4Н, с), 5,03 (2Н, кв, J=12,2Гц), 5,08 (2Н, кв, J=12,2Гц), 7,32 (10Н, с).
МС (ESI) m/z: 441 (M+H)+.
[Ссылочный пример 120]
N-[(7R*,8S*)-7-Амино-1,4-диоксаспиро[4.5]дец-8-ил]-5-хлориндол-2-карбоксамид и N-[(7R*,8S*)-8-амино-1,4-диоксаспиро[4.5]дец-7-ил]-5-хлориндол-2-карбоксамид
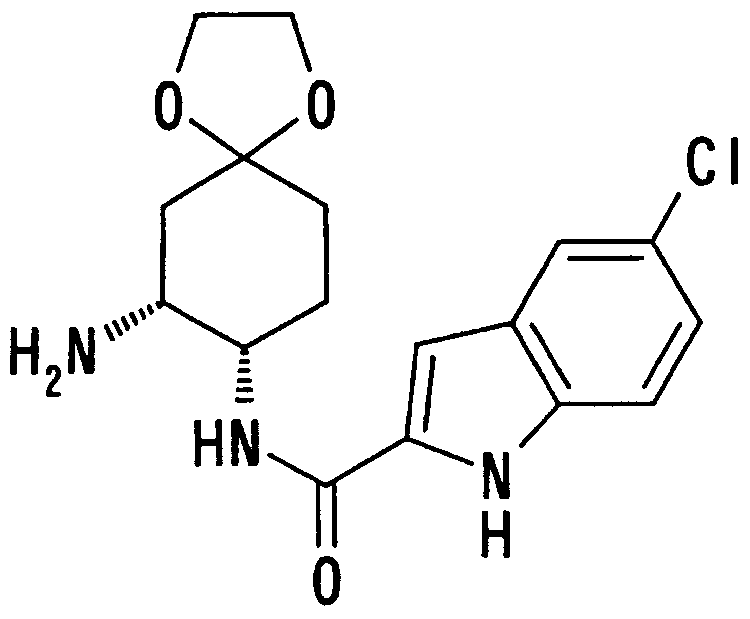
N-[(7R*,8S*)-7-Амино-1,4-диоксаспиро[4.5]дец-8-ил]-5-хлориндол-2-карбоксамид (или N-[(7R*,8S*)-8-амино-1,4-диоксаспиро[4.5]дец-7-ил]-5-хлориндол-2-карбоксамид) и N-[(7R*,8S*)-8-амино-1,4-диоксаспиро[4.5]дец-7-ил]-5-хлориндол-2-карбоксамид (или N-[(7R*,8S*)-7-амино-1,4-диоксаспиро[4.5]дец-8-ил]-5-хлориндол-2-карбоксамид) получали из соединения, полученного в ссылочном примере 119, подобно способу ссылочного примера 118.
N-[(7R*,8S*)-7-Амино-1,4-диоксаспиро[4.5]дец-8-ил]-5-хлориндол-2-карбоксамид (или N-[(7R*,8S*)-8-амино-1,4-диоксаспиро[4.5]дец-7-ил]-5-хлориндол-2-карбоксамид):
1Н-ЯМР (CDCl3) δ: 1,68-1,81 (4H, м), 2,11 (2H, м), 2,87 (1H, тд, J=3,9, 11,2Гц), 3,77 (1H, м), 3,97 (4H, с), 6,27 (1H, д, J=7,6Гц), 6,80 (1H, с), 7,24 (1H, д, J=9,0Гц), 7,35 (1H, д, J=9,0Гц), 7,61 (1H, с), 9,47 (шир.с, 1H).
МС (ESI) m/z: 350 (M+H)+.
N-[(7R*,8S*)-8-амино-1,4-диоксаспиро[4.5]дец-7-ил]-5-хлориндол-2-карбоксамид (или N-[(7R*,8S*)-7-амино-1,4-диоксаспиро[4.5]дец-8-ил]-5-хлориндол-2-карбоксамид):
1Н-ЯМР (CDCl3) δ: 1,65 (2H, м), 1,88 (1H, м), 1,96 (1H, м), 2,31 (1H, дд, J=12,9, 3,2Гц), 2,96 (1H, м), 3,98 (1H, м), 4,02 (4H, с), 4,12 (1H, м), 6,77 (1H, с), 7,06 (1H, шир.с), 7,23 (1H, дд, J=8,8, 2,0Гц), 7,37 (1H, д, J=8,8Гц), 7,62 (1H, д, J=2,0Гц), 9,49 (1H, шир.с).
МС (ESI) m/z: 350 (M+H)+.
[Ссылочный пример 121]
трет-Бутил (1R,6S)-6-[(трет-бутоксикарбонил)амино]-3-циклогексен-1-илкарбамат
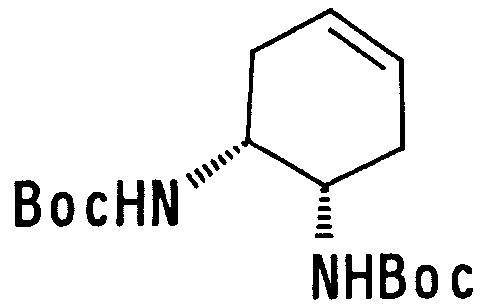
Гидрохлорид цис-4-циклогексен-1,2-диамина (4,0 г) растворяли в смешанном растворителе из воды (40 мл) и ацетонитрила (40 мл), добавляли ди-трет-бутоксикарбонат (11,8 г) и триэтиламин (12 мл) и смесь перемешивали при комнатной температуре в течение 4,5 часов. Реакционную смесь вливали в воду, смесь экстрагировали метиленхлоридом и полученный метиленхлоридный слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанного в заголовке соединения (6,12 г).
1Н-ЯМР (CDCl3) δ: 1,44 (18Н, с), 1,98 (2Н, дд, J=9,3, 15,9Гц), 2,48 (2Н, шир.д, J=15,9Гц), 3,66 (2Н, шир.с), 4,88 (2Н, шир.с), 5,58 (2Н, д, J=2,7Гц).
[Ссылочный пример 122]
трет-Бутил (1R*,2S*)-2-[(трет-бутоксикарбонил)амино]-5-гидроксициклогексилкарбамат (смесь стереоизомеров)
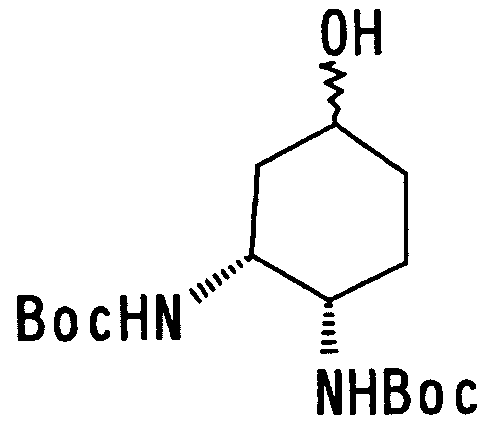
Соединение (6,1 г), полученное в ссылочном примере 121, растворяли в абсолютном тетрагидрофуране (40 мл), добавляли при охлаждении льдом боран-диметилсульфидный комплекс (2,22 мл). Смесь перемешивали 16 часов, постепенно нагревая до комнатной температуры. В реакционную смесь добавляли лед, добавляли 1N водный раствор гидроксида натрия и 30% водный пероксид водорода (50 мл) и смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь экстрагировали этилацетатом и полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:2 → 2:1) с получением указанного в заголовке соединения (6,1 г).
1Н-ЯМР (CDCl3) δ: 1,42 (9Н, с), 1,43 (9Н, с), 1,83-1,67 (5Н, м), 2,15 (1Н, м), 1,22 (1Н, с), 3,34 (1Н, м), 3,78 (1Н, м), 4,15 (1Н, с), 4,98 (1Н, кв, J=9,0Гц), 5,02 (1Н, кв, J=9,0Гц).
МС (ESI) m/z: 331 (M+H)+.
[Ссылочный пример 123]
трет-Бутил (1R*,2S*)-2-[(трет-бутоксикарбонил)амино]-5-оксоциклогексилкарбамат
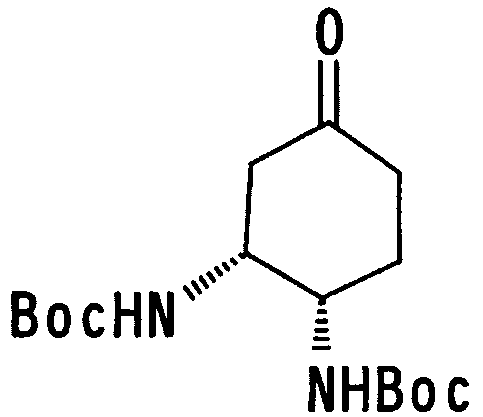
Оксалилхлорид (8,2 мл) и диметилсульфоксид (6,8 мл) растворяли в метиленхлориде (100 мл) при -60°C, к раствору добавляли весь раствор соединения (смесь стереоизомеров) (6,32 г), полученного в ссылочном примере 122, в тетрагидрофуране (80 мл) и смесь перемешивали в течение 1 часа. Температуру смеси повышали до -40°C и добавляли к смеси триэтиламин (21 мл). Смесь нагревали до комнатной температуры. Через 3 часа реакционную смесь вливали в воду и экстрагировали метиленхлоридом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:1) с получением указанного в заголовке соединения (3,8 г).
1Н-ЯМР (CDCl3) δ: 1,43 (9Н, с), 1,44 (9Н, с), 2,24-2,36 (3Н, м), 2,39-2,44 (2Н, м), 2,75 (1Н, дд, J=14,6, 2,9Гц), 3,66-3,81 (2Н, м), 4,95-4,90 (1Н, м), 4,97-5,03 (1Н, м).
МС (ESI) m/z: 329 (M+H)+.
[Ссылочный пример 124]
трет-Бутил (1R*,2S*)-2-[(трет-бутоксикарбонил)амино]-5-(метоксиимино)циклогексилкарбамат
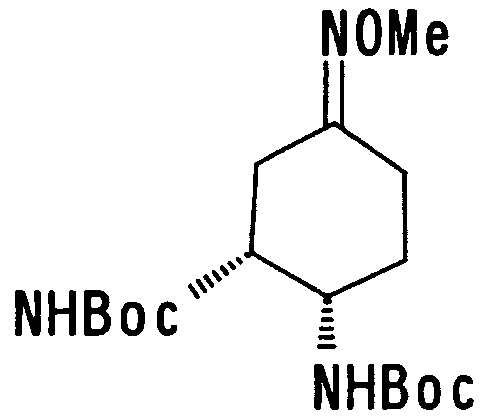
Соединение (1,5 г), полученное в ссылочном примере 123, растворяли в метаноле (30 мл), добавляли гидрохлорид О-метилгидроксиламина (572 мг) и пиридин (737 мл) и смесь перемешивали при комнатной температуре в течение 17 часов. Реакционную смесь концентрировали, добавляли воду и смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанного в заголовке соединения (1,52 г).
1Н-ЯМР (CDCl3) δ: 1,44 (18Н, с), 1,64 (1Н, м), 2,16 (2Н, м), 2,44 (1Н, м), 3,45-3,63 (3Н, м), 3,82 (3Н, с), 4,93 (1Н, м).
МС (ESI) m/z: 358 (M+H)+.
[Ссылочный пример 125]
трет-Бутил (1R*,2S*)-2-[(трет-бутоксикарбонил)амино]-5-{[трет-бутил(дифенил)силил]окси}циклогексилкарбамат (стереоизомер А)
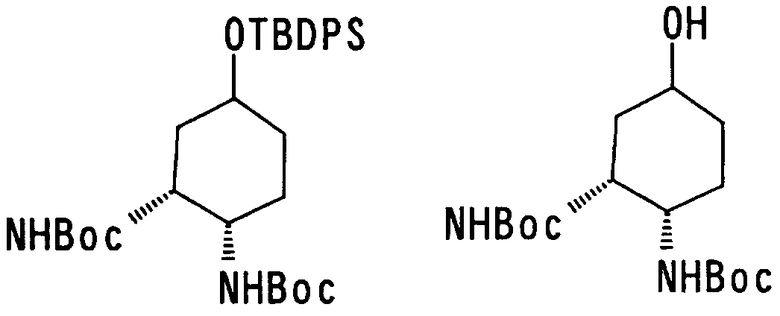
Указанное в заголовке соединение получали из соединения (смесь стереоизомеров), полученного в ссылочном примере 122, подобно способу ссылочного примера 58, и извлекали трет-бутил (1R*,2S*)-2-[(трет-бутоксикарбонил)амино]-5-гидроксициклогексилкарбамат (стереоизомер В).
1Н-ЯМР (CDCl3) δ: 1,03 (9Н, с), 1,39 (9Н, с), 1,40 (9Н, с), 1,72 (1Н, м), 1,86 (1Н, м), 2,13 (1Н, м), 3,24 (2Н, м), 3,65 (1Н, м), 4,83 (1Н, м), 7,37 (10Н, м).
[Ссылочный пример 126]
Бензил (1R*,2S*)-2-{[(бензилокси)карбонил]амино}-5-гидрокси-5-метилциклогексилкарбамат
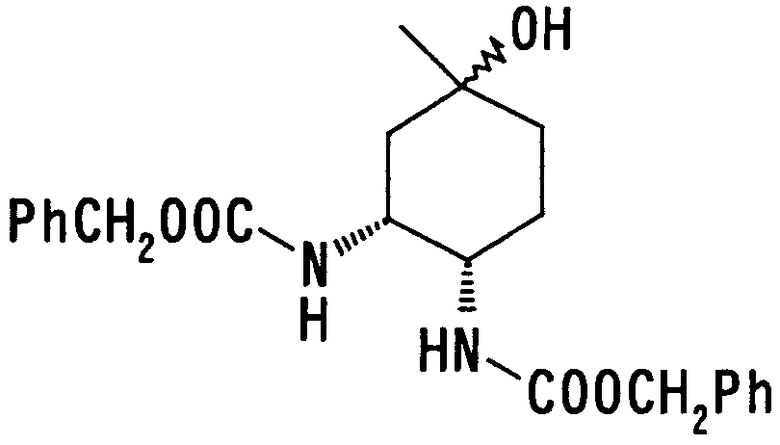
Безводный хлорид церия (6,4 г) суспендировали в тетрагидрофуране (50 мл) и суспензию охлаждали до -78°C в атмосфере аргона. К суспензии добавляли раствор метиллития (1,14N раствор в диэтиловом эфире, 22,5 мл) и смесь перемешивали при -78°C в течение 30 минут. Добавляли по каплям при -78°C тетрагидрофурановый раствор (50 мл) соединения (3,0 г), полученного в ссылочном примере 116, и смесь перемешивали 30 минут. Реакционную смесь вливали в 3% водный раствор (100 мл) уксусной кислоты, добавляли диэтиловый эфир (50 мл) и смесь перемешивали при комнатной температуре в течение 10 минут. Реакционную смесь экстрагировали этилацетатом и полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Отгоняли при пониженном давлении растворитель и остаток очищали два раза колоночной хроматографией на силикагеле (метанол:хлороформ = 0:100-1:19) с получением указанного в заголовке соединения (стереоизомер А) (780 мг) и указанного в заголовке соединения (стереоизомер В) (1,1 г).
Стереоизомер А:
1Н-ЯМР (CDCl3) δ: 1,26 (3Н, с), 1,27-2,08 (6Н, м), 3,48 (1Н, шир.с), 3,59 (1Н, шир.с), 5,02-5,09 (5Н, м), 5,33 (1Н, шир.с), 7,30-7,32 (10Н, с).
МС (FAB) m/z: 413 (M+H)+.
Стереоизомер В:
1Н-ЯМР (CDCl3) δ: 1,25 (3Н, с), 1,29-2,07 (6Н, м), 3,39 (1Н, шир.с), 3,82 (1Н, шир.с), 5,02-5,23 (6Н, м), 7,30 (10Н, с).
МС (FAB) m/z: 413 (M+H)+.
[Ссылочный пример 127]
(3R*,4S*)-3,4-Диамино-1-метилциклогексанол (стереоизомер А)
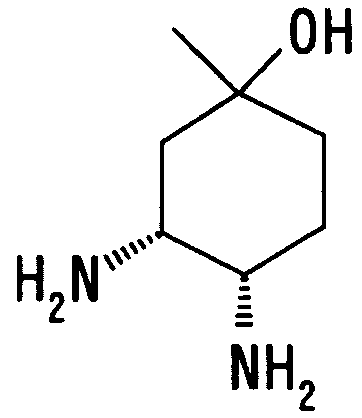
10% Палладий на углероде (350 мг) суспендировали в метанольном растворе (100 мл) соединения (стереоизомер А) (780 мг), полученного в ссылочном примере 126, и суспензию перемешивали 5 часов в атмосфере водорода. Катализатор удаляли фильтрованием и фильтрат концентрировали при пониженном давлении. Остаток растворяли в метиленхлориде (100 мл) и затем раствор сушили над безводным сульфатом натрия и отгоняли растворитель с получением указанного в заголовке соединения (стереоизомер А) (190 мг).
1Н-ЯМР (CDCl3) δ: 1,22 (3Н, с), 1,25-2,48 (11Н, м), 2,62 (1Н, шир.с), 2,78 (1Н, шир.с).
[Ссылочный пример 128]
Смесь N-[(1R*,2S*)-2-амино-4-гидрокси-4-метилциклогексил]-5-хлориндол-2-карбоксамида (стереоизомер А) и N-[(1R*,2S*)-2-амино-5-гидрокси-5-метилциклогексил]-5-хлориндол-2-карбоксамида (стереоизомер А)
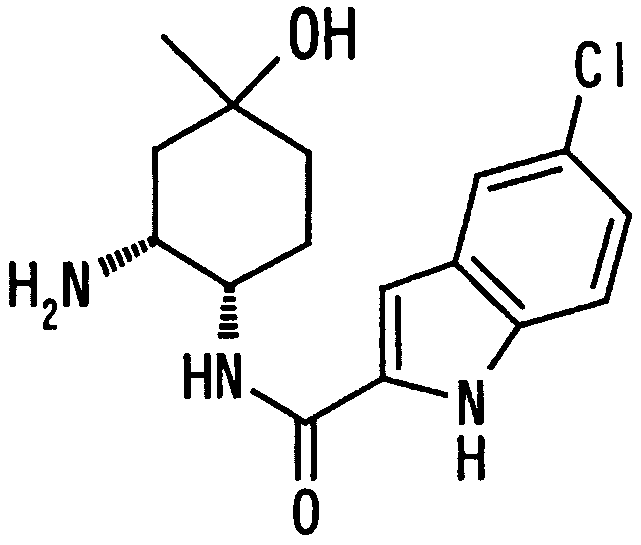
Указанное в заголовке соединение получали из соединения (стереоизомер А), полученного в ссылочном примере 127, и 5-хлориндол-2-карбоновой кислоты подобно способу ссылочного примера 59.
1Н-ЯМР (CDCl3) δ: 1,32 (3Н, с), 1,34-2,29 (6Н, м), 4,42-4,70 (4Н, шир.), 7,13 (2Н, с), 7,50 (2Н, с), 8,00 (1Н, с), 11,0 (1Н, шир.).
[Ссылочный пример 129]
трет-Бутил (1R*,2R*,5S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-(гидроксиметил)циклогексилкарбамат
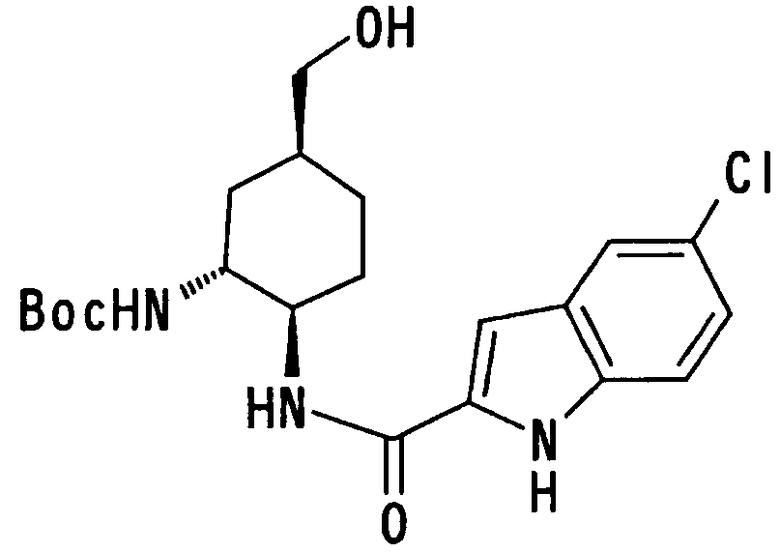
1) Этил (1R*,3S*,4S*)-3-[(трет-бутоксикарбонил)амино]-4-{[(5-хлориндол-2-ил)карбонил]амино}циклогексанкарбоксилат получали из (1R*,3S*,4S*)-формы, полученной в ссылочном примере 89, подобно способу, описанному в ссылочных примерах 90 и 91.
1Н-ЯМР (CDCl3) δ: 1,22-1,72 (6H, м), 2,15-2,28 (2H, м), 2,41-2,49 (1H, м), 2,85 (1H, шир.с), 3,62-3,75 (1H, м), 3,78-3,92 (1H, м), 4,12-4,28 (2H, м), 4,56-4,63 (1H, м), 6,88 (1H, шир.с), 7,20 (1H, дд, J=8,8 и 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,52-7,57 (1H, м), 7,59 (1H, д, J=2,0Гц), 9,24 (1H, с).
МС (ESI) m/z: 464 (М+Н)+.
2) Полученный выше продукт (735 мг) растворяли в метиленхлориде (10 мл), добавляли при -78°C 1N гексановый раствор (5 мл) гидрида диизобутилалюминия и смесь перемешивали 3 часа и затем 30 минут при 0°C. Добавляли при -78°C насыщенный водный раствор хлорида аммония, смесь экстрагировали метиленхлоридом и полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 19:1) с получением указанного в заголовке соединения (480 мг).
1Н-ЯМР (CDCl3) δ: 1,20-2,30 (7Н, м), 3,60-3,86 (4Н, м), 4,64 (1Н, шир.с), 6,87 (1Н, с), 7,20-7,48 (3Н, м), 9,15 (1Н, шир.с).
МС (ESI) m/z: 422 (M+H)+.
[Ссылочный пример 130]
(1R*,3R*,6S*)-3-(Метоксиметил)оксабицикло[4.1.0]гептан
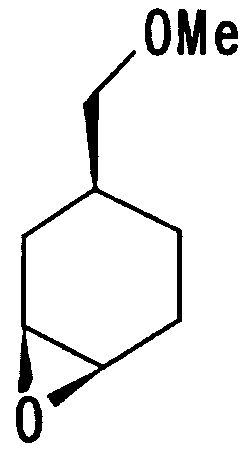
1) (1R*,4R*,5R*)-4-Йод-6-оксабицикло[3.2.1]октан-7-он (2,8 г) растворяли в смешанном растворителе из тетрагидрофурана (27 мл) и воды (3 мл), добавляли концентрированную хлористоводородную кислоту (0,1 мл) и смесь кипятили с обратным холодильником в течение 1 часа. Растворитель отгоняли при пониженном давлении с получением (1R*,3R*,4R*)-3-гидрокси-4-йодциклогексанкарбоновой кислоты (3,23 г) в виде бесцветного твердого вещества.
2) Продукт (3,22 г), полученный по описанной выше реакции, растворяли в тетрагидрофуране (50 мл), добавляли при охлаждении льдом боран-диметилсульфидный комплекс (2М тетрагидрофурановый раствор, 47 мл) и смесь перемешивали при комнатной температуре в течение 12 часов. Растворитель отгоняли при пониженном давлении, остаток растворяли в изопропаноле (10 мл), добавляли 1N водный раствор (12 мл) гидроксида натрия и смесь перемешивали 12 часов. Растворитель концентрировали до примерно 1/5, затем реакционную смесь разбавляли водой и метиленхлоридом и перемешивали ее в течение 10 минут. Органический слой отделяли, последовательно промывали насыщенным водным раствором хлорида аммония и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:2) с получением (1R*,3R*,6S*)-7-оксабицикло[4.1.0]гепт-3-илметанола (1,25 г) в виде бесцветного масла.
3) Продукт (4,63 г), полученный по реакции, описанной в пункте 2), растворяли в тетрагидрофуране (50 мл), добавляли к раствору при -78°C бис(триметилсилил)амид калия (0,5N толуольный раствор, 80 мл). После перемешивания при той же температуре в течение 10 минут добавляли метилиодид (2,93 мл). После нагревания смеси до 0°C ее перемешивали 1 час, гасили насыщенным водным раствором хлорида аммония и затем разбавляли диэтиловым эфиром. Органический слой отделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанного в заголовке соединения (3,7 г).
1Н-ЯМР (CDCl3) δ: 0,89-1,63 (5Н, м), 1,80-2,05 (2Н, м), 1,89-3,06 (4Н, м), 3,16 (3Н, с).
[Ссылочный пример 131]
(1R*,2R*,4S*)-2-Азидо-4-(метоксиметил)циклогексанол
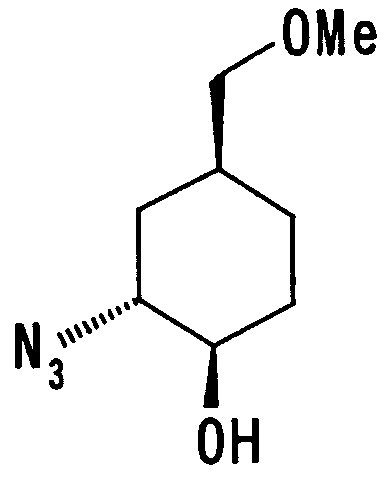
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 130, подобно способу ссылочного примера 87.
1Н-ЯМР (CDCl3) δ: 1,45-1,70 (5Н, м), 1,77-1,95 (2Н, м), 1,98-2,08 (1Н, м), 3,30 (2Н, д, J=6,8Гц), 3,35 (3Н, с), 3,45-3,65 (2Н, м).
[Ссылочный пример 132]
трет-Бутил (1R*,2R*,5S*)-2-гидрокси-5-(метоксиметил)циклогексилкарбамат
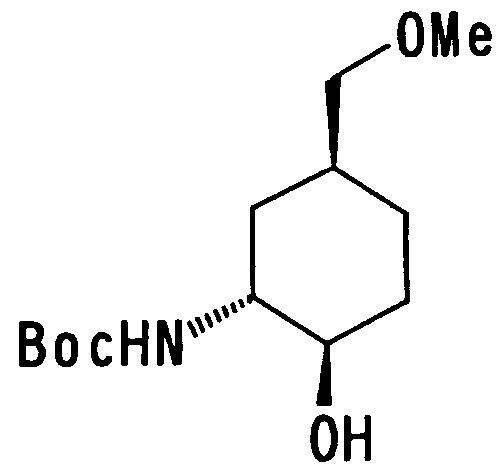
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 131, подобно способу ссылочного примера 88.
1Н-ЯМР (CDCl3) δ: 1,35-2,01 (16Н, м), 3,05 (1Н, шир.с), 3,32 (2Н, д, J=7,1Гц), 3,34 (3Н, с), 3,44-3,62 (2Н, м), 4,59 (1Н, шир.с).
[Ссылочный пример 133]
трет-Бутил (1R*,2S*,5S*)-2-азидо-5-(метоксиметил)циклогексилкарбамат
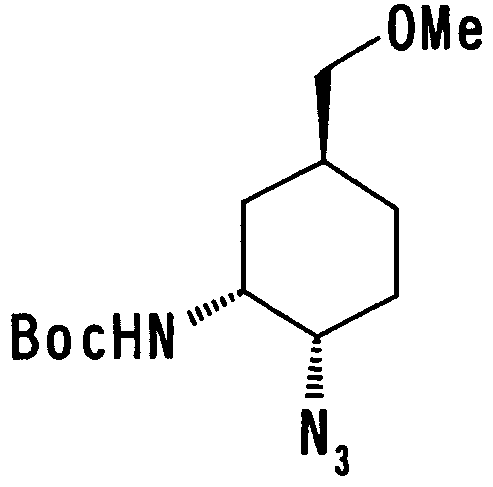
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 132, подобно способу ссылочного примера 89.
1Н-ЯМР (CDCl3) δ: 1,31-1,93 (16Н, м), 3,27 (2Н, д, J=6,4Гц), 3,32 (3Н, с), 3,57-3,70 (1Н, м), 3,67 (1Н, шир.с), 3,95 (1Н, шир.с).
[Ссылочный пример 134]
трет-Бутил (1R*,2S*,5S*)-2-амино-5-(метоксиметил)циклогексилкарбамат
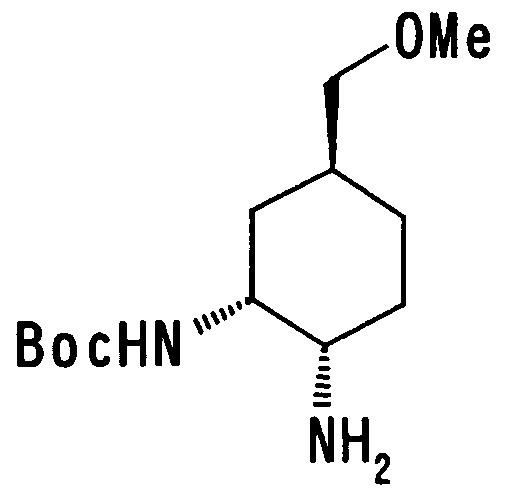
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 133, подобно способу ссылочного примера 90.
[Ссылочный пример 135]
трет-Бутил (1R*,2S*,5S*)-2-{[(5-[хлориндол-2-ил)карбонил]амино}-5-(метоксиметил)циклогексилкарбамат
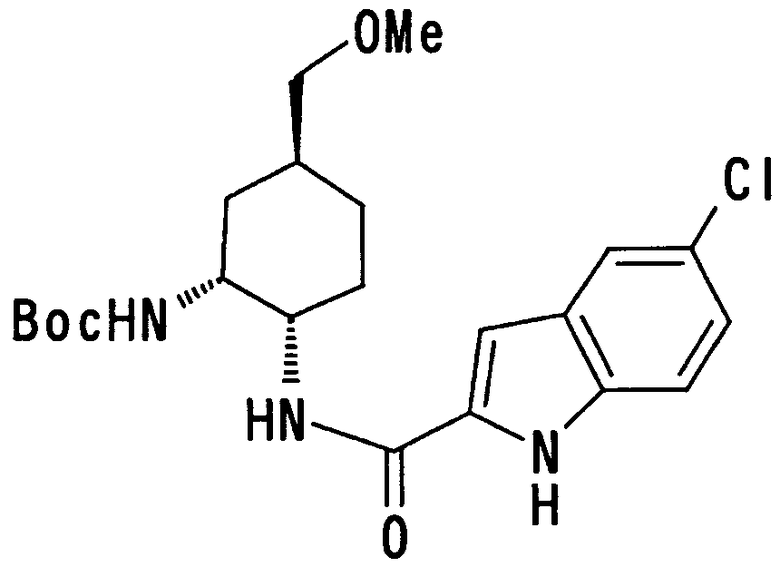
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 134, и 5-хлориндол-2-карбоновой кислоты подобно способу ссылочного примера 91.
1Н-ЯМР (CDCl3) δ: 1,12-2,31 (16H, м), 3,14-3,30 (2H, м), 3,34 (3H, с), 3,92 (1H, шир.с), 4,13 (1H, шир.с), 4,88 (1H, шир.с), 6,82 (1H, с), 7,21 (1H, шир.д, J=8,8Гц), 7,33 (1H, д, J=8,8Гц), 7,60 (1H, с), 8,09 (1H, шир.с), 9,42 (1H, шир.с).
МС (ESI) m/z: 436 (M+H)+.
[Ссылочный пример 136]
трет-Бутил (1R*,2S*,5S*)-2-{[(5-[хлориндол-2-ил)карбонил]амино}-5-(гидроксиметил)циклогексилкарбамат
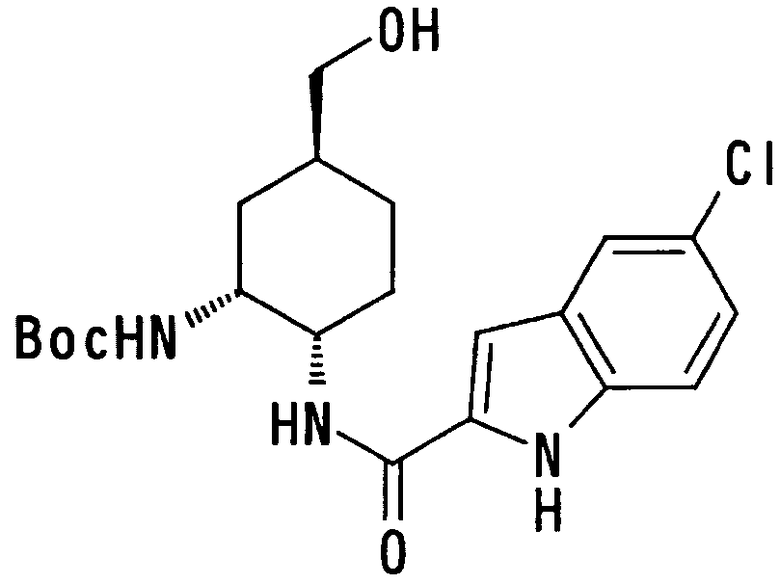
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 91, подобно способу ссылочного примера 129.
1Н-ЯМР (CDCl3) δ: 0,78-2,30 (16H, м), 3,41-3,59 (3H, м), 3,86-3,95 (1H, м), 4,12-4,20 (1H, м), 4,82-4,91 (1H, м), 6,81 (1H, с), 7,17-7,40 (2H, м), 7,60 (1H, с), 8,03 (1H, шир.с), 9,18 (1H, шир.с).
МС (ESI) m/z: 422 (M+H)+.
[Ссылочный пример 137]
трет-Бутил (1R*,2S*,5S*)-5-(азидометил)-2-{[(5-[хлориндол-2-ил)карбонил]амино}циклогексилкарбамат
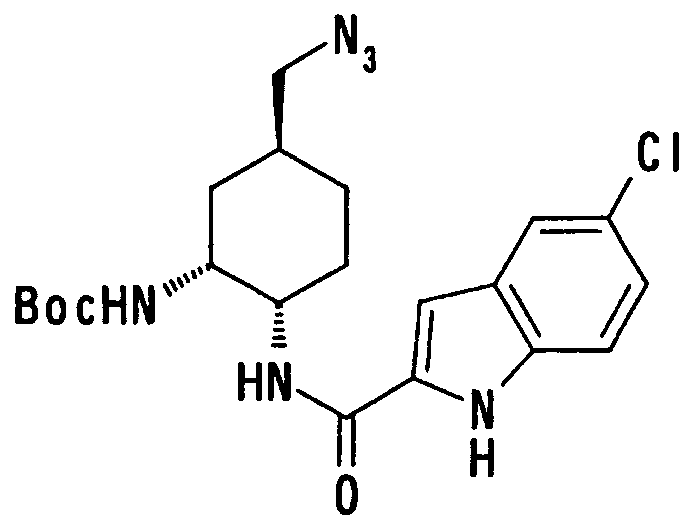
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 136, подобно способу ссылочного примера 80.
[Ссылочный пример 138]
трет-Бутил 3-циклогексен-1-илкарбамат
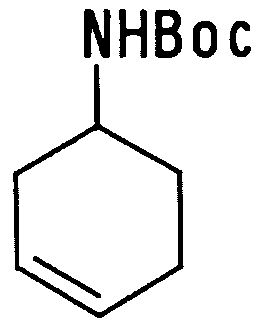
3-Циклогексен-1-карбоновую кислоту (25,3 г) растворяли в трет-бутаноле (250 мл), добавляли триэтиламин (28 мл) и дифенилфосфорилазид (43,0 мл) и смесь перемешивали 1 час при комнатной температуре и 2 дня при 90°C. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид) и затем снова очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 20:1) с получением указанного в заголовке соединения (24,9 г).
1Н-ЯМР (CDCl3) δ: 1,45 (9Н, с), 1,45-1,60 (1Н, м), 1,80-1,90 (2Н, м), 2,05-2,20 (2Н, м), 2,35-2,45 (1Н, м), 3,78 (1Н, шир.), 4,56 (1Н, шир.), 5,55-5,65 (1Н, м), 5,65-5,75 (1Н, м).
[Ссылочный пример 139]
трет-Бутил (3R*,4S*)-3,4-дигидроксициклогексилкарбамат
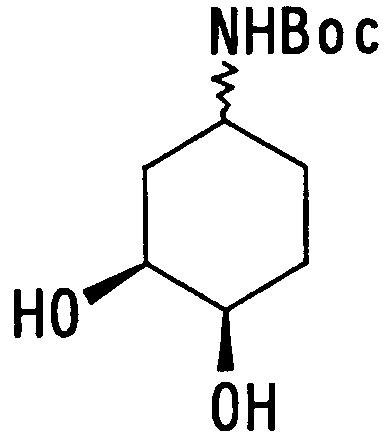
Соединение (1,24 г), полученное в ссылочном примере 138, растворяли в смешанном растворителе из ацетонитрила (15 мл) и воды (5 мл), добавляли N-оксид N-метилморфолина (0,90 г) и микрокапсулированный 10% тетроксид осмия (1 г) и смесь перемешивали примерно при 80°C в течение суток. После удаления фильтрованием нерастворимого вещества фильтрат концентрировали при пониженном давлении. Полученный таким образом остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1) с получением указанного в заголовке соединения (1,28 г).
1Н-ЯМР (CDCl3) δ: 1,15-1,30 (1/2Н, м), 1,35-2,00 (15Н, м), 2,15-2,30 (3/2Н, м), 2,40-2,60 (1Н, м), 3,64 (1Н, шир.), 3,75-3,90 (3/2Н, м), 4,00 (1/2Н, шир.).
МС (FAB) m/z: 232 (M+H)+.
[Ссылочный пример 140]
трет-Бутил (3R*,4S*)-3,4-диазидоциклогексилкарбамат (стереоизомер А и стереоизомер В)
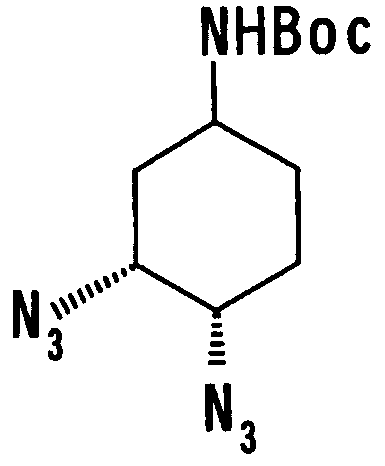
Указанные в заголовке соединения (стереоизомер А и стереоизомер В) получали из соединения, полученного в ссылочном примере 139, подобно способу ссылочного примера 80.
Стереоизомер А:
1Н-ЯМР (CDCl3) δ: 1,45 (9Н, с), 1,40-1,55 (1Н, м), 1,55-1,80 (3Н, м), 1,95-2,15 (2Н, м), 3,53 (1Н, м), 3,59 (1Н, шир.), 3,80 (1Н, м), 4,70 (1Н, шир.).
Стереоизомер В:
1Н-ЯМР (CDCl3) δ: 1,27 (1Н, м), 1,44 (9Н, с), 1,40-1,55 (1Н, м), 1,80-2,00 (2Н, м), 2,00-2,15 (1Н, м), 2,21 (1Н, м), 3,48 (1Н, м), 3,77 (1Н, шир.), 3,89 (1Н, шир.), 4,34 (1Н, шир.).
[Ссылочный пример 141]
Этил (1S,3R,4S)-4-{[(бензилокси)карбонил]амино}-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
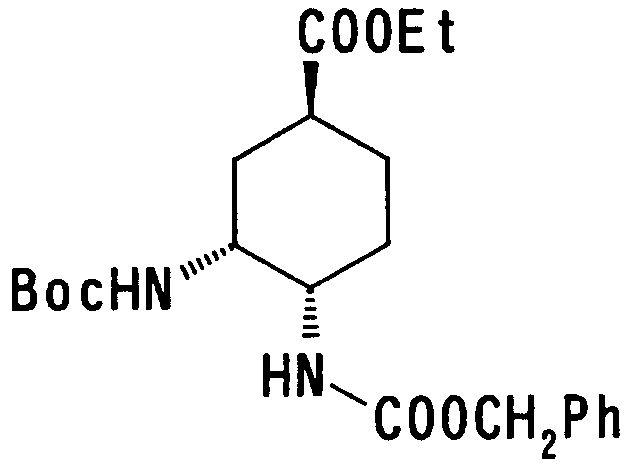
Соединение (3,10 г), полученное в ссылочном примере 96, растворяли в тетрагидрофуране (50 мл) и добавляли насыщенный водный раствор (50 мл) гидрокарбоната натрия. После добавления по каплям бензилоксикарбонилхлорида (1,71 мл) к реакционной смеси при охлаждении льдом смесь перемешивали при комнатной температуре в течение 4 дней. К реакционной смеси добавляли этилацетат (200 мл) и воду (200 мл) и жидкости разделяли. Полученный органический слой сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель. Выпавшие в осадок твердые частицы отфильтровывали с получением указанного в заголовке соединения (3,24 г).
1Н-ЯМР (CDCl3) δ: 1,24 (3H, т, J=7,1Гц), 1,29-1,44 (1H, м), 1,44 (9H, с), 1,51-1,64 (1H, м), 1,72-2,10 (4H, м),2,27-2,43 (1H, м), 3,60-3,73 (1H, м), 4,00-4,18 (3H, м), 4,62 (1H, шир.с), 5,01-5,13 (2H, м), 5,26 (1H, шир.с), 7,27-7,38 (5H, м).
[Ссылочный пример 142]
(1S,3R,4S)-4-{[(Бензилокси)карбонил]амино}-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоновая кислота
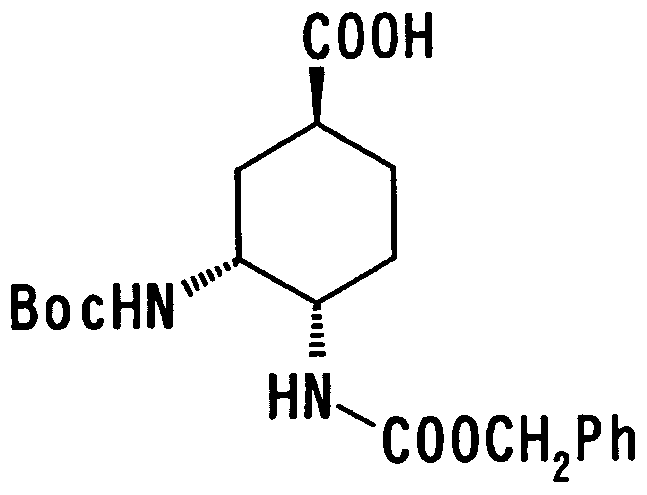
Соединение (620 мг), полученное в ссылочном примере 141, растворяли в тетрагидрофуране (20 мл), добавляли водный раствор (10 мл) моногидрата гидроксида лития (93 мг) и смесь перемешивали при комнатной температуре в течение 16 часов. Дополнительно добавляли к реакционной смеси моногидрат гидроксида лития (217 мг) и смесь перемешивали при комнатной температуре в течение 2 часов, затем реакционную смесь нейтрализовали 1N хлористоводородной кислотой и экстрагировали метиленхлоридом. Органический слой промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (600 мг).
1Н-ЯМР (CDCl3) δ: 1,22-2,20 (6Н, м), 1,44 (9Н, с), 2,45 (1Н, шир.с), 3,60-3,80 (1Н, шир.), 4,09 (1Н, шир.с), 4,66 (1Н, шир.с), 5,00-5,20 (2Н, м), 5,26 (1Н, шир.с), 7,20-7,40 (5Н, м).
МС (ESI) m/z: 393 (M+H)+.
[Ссылочный пример 143]
Бензил (1S,2R,4S)-2-[(трет-бутоксикарбонил)амино]-4-[(диметиламино)карбонил]циклогексилкарбамат
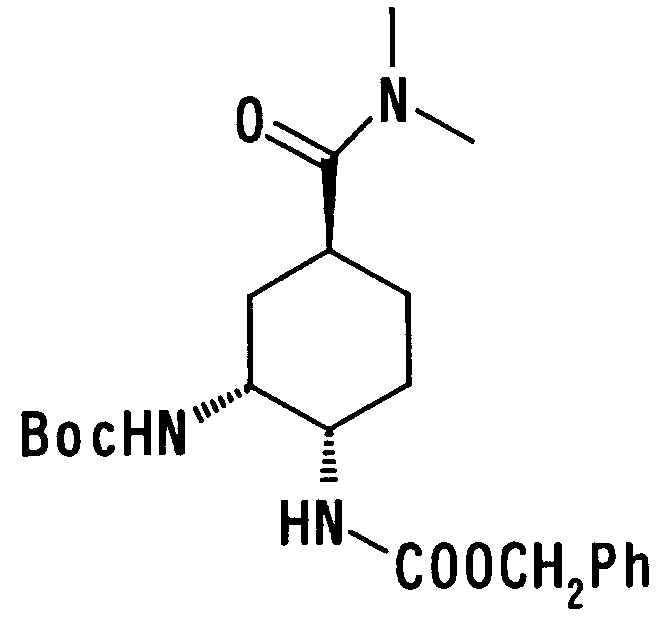
После суспендирования соединения (600 мг), полученного в ссылочном примере 142, и гидрохлорида диметиламина (240 мг) в метиленхлориде (50 мл) в суспензию добавляли подходящее для получения раствора количество тетрагидрофурана. К полученному раствору добавляли триэтиламин (0,41 мл), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (422 мг) и моногидрат 1-гидроксибензотриазола (338 мг) и смесь перемешивали при комнатной температуре в течение 1 часа. Добавляли дополнительно к реакционной смеси гидрохлорид диметиламина (480 мг) и триэтиламин (0,82 мл) и смесь перемешивали при комнатной температуре еще 18 часов. Реакционную смесь вливали в воду, чтобы отделить органический слой. Органический слой промывали 1N хлористоводородной кислотой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 3:47 → 2:23) с получением указанного в заголовке соединения (620 мг).
1Н-ЯМР (CDCl3) δ: 1,20-1,50 (2H, м), 1,44 (9H, с), 1,50-2,10 (4H, м), 2,60 (1H, шир.т, J=11,6Гц), 2,93 (3H, с), 3,02 (3H, с), 3,70 (1H, шир.с), 4,14 (1H, шир.с), 4,65 (1H, шир.с), 5,00-5,30 (3H, м), 7,26-7,40 (5H, м).
МС (ESI) m/z = 420 (М+Н)+.
[Ссылочный пример 144]
трет-Бутил (1R,2S,5S)-2-амино-5-[(диметиламино)карбонил]циклогексилкарбамат
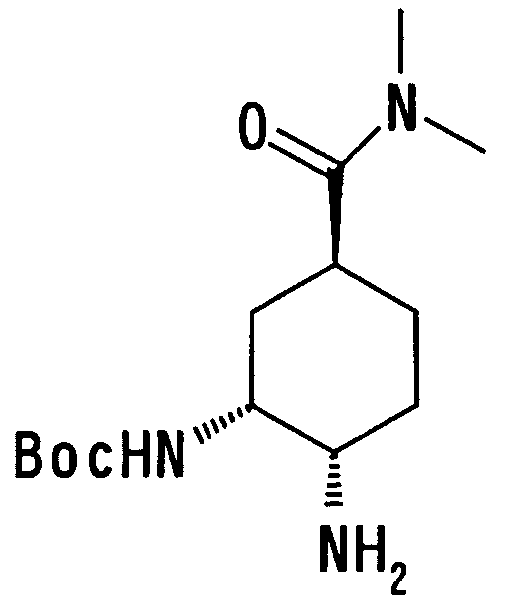
10% Палладий на углероде (57 г) добавляли к раствору соединения (190 г), полученного в ссылочном примере 143, в метаноле (8000 мл) и смесь перемешивали 3 часа при давлении водорода (7 атм). После удаления катализатора фильтрованием фильтрат концентрировали при пониженном давлении. К остатку добавляли толуол и смесь концентрировали при пониженном давлении, затем добавляли гексан (2500 мл) для отверждения продукта. Продукт отфильтровывали и сушили, получая указанное в заголовке соединение (121 г).
1Н-ЯМР (CDCl3) δ: 1,20-1,77 (6Н, м), 1,45 (9Н, с), 2,20-2,35 (1Н, шир.), 2,63-2,74 (1Н, м), 2,92 (3Н, с), 3,02 (3Н, с), 3,02-3,11 (2Н, м), 3,74-3,82 (1Н, м), 4,88-5,00 (1Н, шир.).
МС (ESI) m/z: 286 (M+H)+.
[Ссылочный пример 145]
трет-Бутил (1R,2S,5S)-2-{[(6-хлорхинолин-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
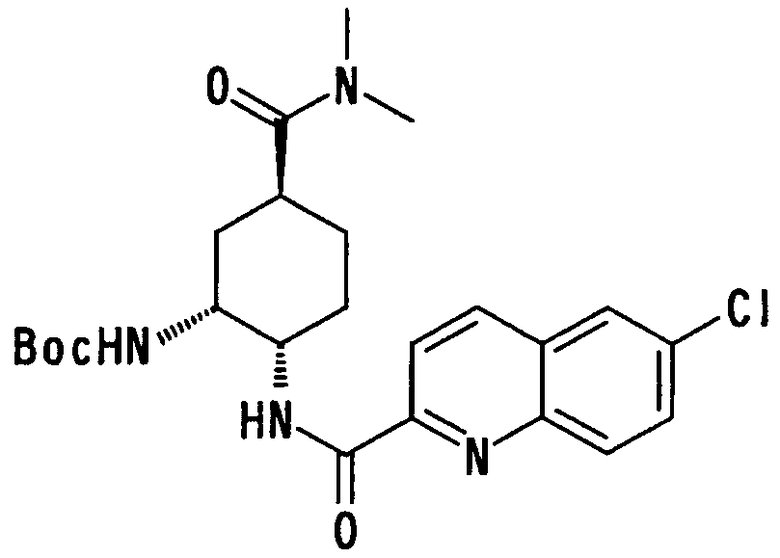
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и соединения, полученного в ссылочном примере 54, подобно способу ссылочного примера 91.
1Н-ЯМР (CDCl3) δ: 1,41 (9H, шир.), 1,50-1,70 (1H, м), 1,75-1,95 (2H, м), 1,95-2,25 (3H, м), 2,65-2,80 (1H, м), 2,96 (3H, с), 3,07 (3H, с), 4,15-4,30 (1H, м), 4,30-4,40 (1H, м), 4,95 (1H, шир.), 7,66 (1H, д, J=8,8Гц), 7,84 (1H, с), 8,00 (1H, д, J=8,8Гц), 8,19 (1H, д, J=8,6Гц), 8,30 (1H, д, J=8,6Гц).
МС (FAB) m/z: 475 (M+H)+.
[Ссылочный пример 146]
трет-Бутил (1R,2S,5S)-2-{[(7-хлорхинолин-3-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
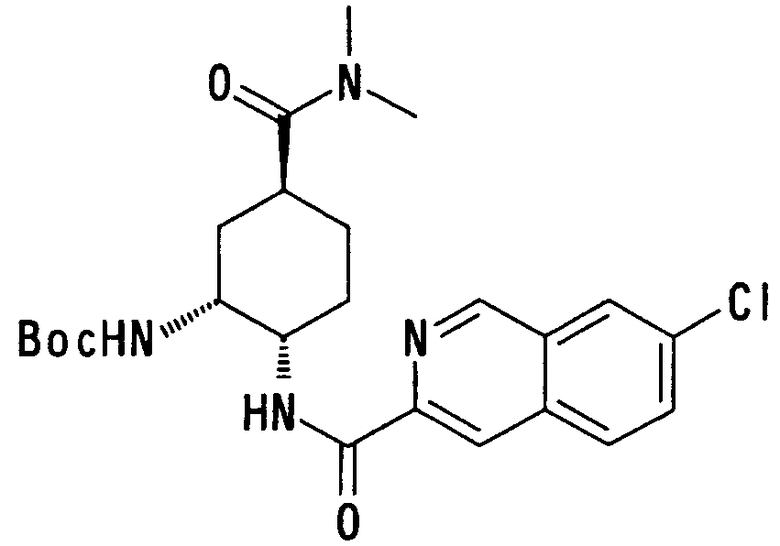
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и соединения, полученного в ссылочном примере 57, подобно способу ссылочного примера 91.
1Н-ЯМР (CDCl3) δ: 1,30-1,65 (10H, шир.), 1,75-1,90 (2H, м), 1,90-2,25 (3H, м), 2,65-2,90 (1H, шир.), 2,96 (3H, с), 3,08 (3H, с), 4,20-4,30 (1H, м), 4,30-4,40 (1H, м), 4,93 (1H, шир.), 7,68 (1H, м), 7,90 (1H, шир.), 7,99 (1H, с), 8,35-8,70 (2H, м), 9,01 (1H, шир.).
МС (FAB) m/z: 475 (М+Н)+.
[Ссылочный пример 147]
2-Бром-5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин
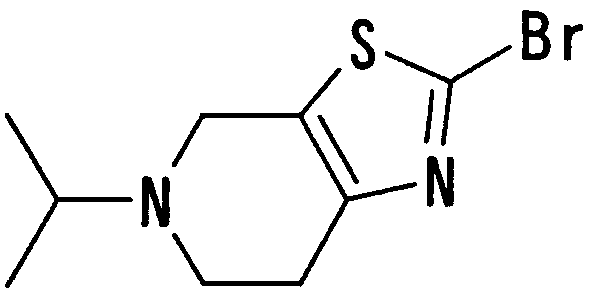
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 8, подобно способу ссылочного примера 9.
1Н-ЯМР (CDCl3) δ: 1,13 (6Н, д, J=6,5Гц), 2,86 (4Н, с), 2,89-3,00 (1Н, м), 3,70 (2Н, с).
[Ссылочный пример 148]
5-Изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксилат лития
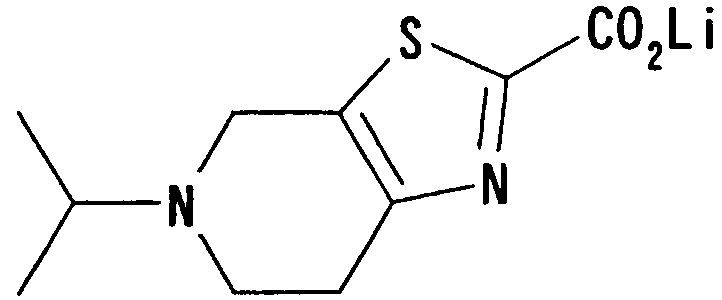
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 147, подобно способу ссылочного примера 10.
1Н-ЯМР (ДМСО-d6) δ: 1,05 (6Н, д, J=6,4Гц), 2,68-2,70 (2Н, м), 2,75-2,77 (2Н, м), 2,87-2,93 (1Н, м), 3,66 (2Н, с).
[Ссылочный пример 149]
4-Нитрофенил 5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксилат
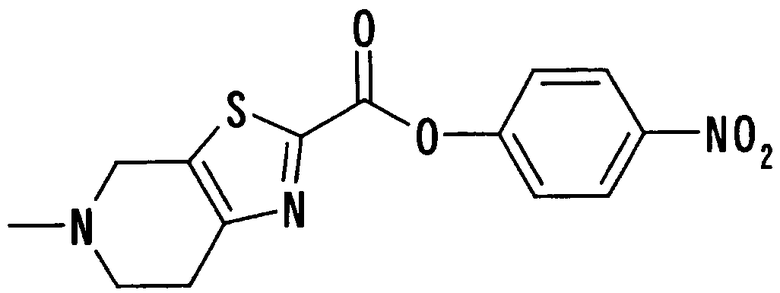
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 10, и п-нитрофенола подобно способу ссылочного примера 52.
1Н-ЯМР (CDCl3) δ: 2,55 (3Н, с), 2,88 (2Н, т, J=5,7Гц), 3,06-3,12 (2Н, м), 3,80 (2Н, с), 7,46 (2Н, д, J=9,3Гц), 8,32 (2Н, д, J=9,3Гц).
МС (ESI) m/z: 320 (M+H)+.
[Ссылочный пример 150]
Бензил 3-оксоциклобутанкарбоксилат
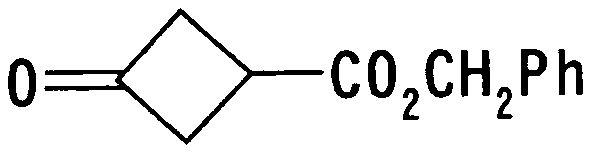
Триэтиламин (2,0 мл) и бензилбромид (1,2 мл) добавляли к раствору 3-оксоциклобутанкарбоновой кислоты (J. Org. Chem., Vol. 53, pp. 3841-3843, 1981) (995 мг) в тетрагидрофуране (5,0 мл) и смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь разбавляли этилацетатом и промывали последовательно 1N хлористоводородной кислотой, насыщенным водным раствором гидрокарбоната натрия и насыщенным раствором соли и сушили над безводным сульфатом натрия. Затем отгоняли при пониженном давлении растворитель и полученный остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:6) с получением указанного в заголовке соединения (886 мг).
1Н-ЯМР (CDCl3) δ: 3,22-3,33 (3Н, м), 3,37-3,48 (2Н, м), 5,19 (2Н, с), 7,31-7,42 (5Н, м).
МС (FAB) m/z: 205 (M+H)+.
[Ссылочный пример 151]
Бензил 3-гидроксициклобутанкарбоксилат
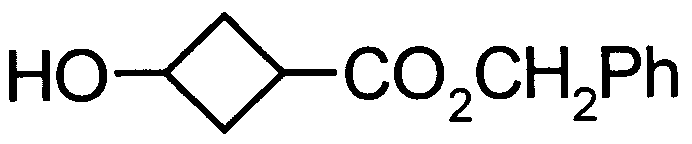
Боргидрид натрия (76 мг) добавляли к раствору соединения (781 мг), полученного в ссылочном примере 150, в смешанном растворителе из тетрагидрофурана (10 мл) и метанола (0,5 мл) при 0°C и смесь перемешивали при той же температуре в течение 30 минут. Реакционную смесь разбавляли этилацетатом и промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия в указанном порядке и сушили над безводным сульфатом натрия. Затем отгоняли при пониженном давлении растворитель и полученный остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:2) с получением указанного в заголовке соединения (770 мг).
1Н-ЯМР (CDCl3) δ: 2,13-2,27 (3Н, м), 2,55-2,71 (3Н, м), 4,14-4,23 (1Н, м), 5,12 (2Н, с), 7,28-7,39 (5Н, м).
МС (FAB) m/z: 207 (M+H)+.
[Ссылочный пример 152]
3-Гидроксициклобутанкарбоновая кислота
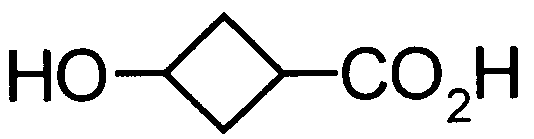
10% Палладий на углероде (108 мг) добавляли к раствору соединения (706 мг), полученного в ссылочном примере 151, в этаноле (10 мл) и смесь перемешивали при комнатной температуре в течение 3 часов в атмосфере водорода. Удалив фильтрованием через целит катализатор, фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (399 г).
1Н-ЯМР (CD3OD) δ: 2,00-2,21 (2Н, м), 2,41-2,61 (3Н, м), 4,01-4,13 (1Н, м).
[Ссылочный пример 153]
Бензил 3-метоксициклобутанкарбоксилат
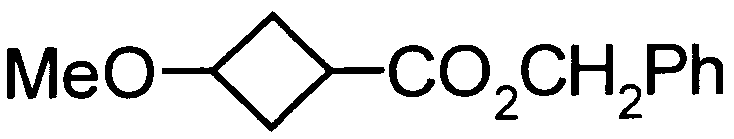
Метилиодид (194 мкл) и оксид серебра (237 мг) добавляли к раствору соединения (317 мг), полученного в ссылочном примере 151, в N,N-диметилформамиде (3 мл) и смесь перемешивали при 45°C в течение 1 часа. К реакционной смеси дополнительно добавляли метилиодид (194 мкл) и оксид серебра (226 мг) и смесь перемешивали при 45°C в течение 16 часов. Удалив фильтрованием катализатор, фильтрат концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:10) с получением указанного в заголовке соединения (152 мг).
1Н-ЯМР (CDCl3) δ: 2,14-2,24 (2Н, м), 2,44-2,54 (2Н, м), 2,59-2,72 (1Н, м), 3,21 (3Н, с), 3,73-3,81 (1Н, м), 5,11 (2Н, с), 7,22-7,39 (5Н, м).
МС (ESI) m/z: 221 (M+H)+.
[Ссылочный пример 154]
3-Метоксициклобутанкарбоновая кислота
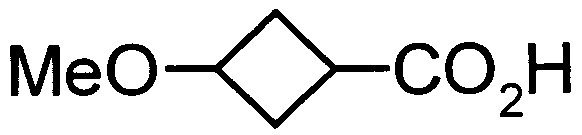
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 153, подобно способу ссылочного примера 152.
1Н-ЯМР (CDCl3) δ: 2,17-2,27 (2Н, м), 2,48-2,58 (2Н, м), 2,62-2,73 (1Н, м), 3,25 (3Н, с), 3,76-3,86 (1Н, м), 8,60-9,30 (1Н, шир.).
[Ссылочный пример 155]
Метил 3-метокси-2-(метоксиметил)пропионат
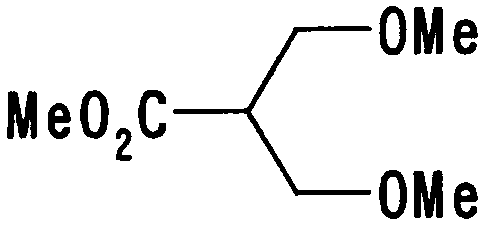
Метоксид натрия (1,21 г) добавляли к раствору метил 2-(бромметил)акрилата (1,0 мл) в метаноле (10 мл) и смесь кипятили с обратным холодильником в течение 26 часов. После охлаждения реакционную смесь разбавляли диэтиловым эфиром, отфильтровывали осадок и фильтрат концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанного в заголовке соединения (726 мг).
1Н-ЯМР (CDCl3) δ: 2,90-2,96 (1H, м), 3,34 (6H, с), 3,57 (2H, дд, J=9,3, 5,9Гц), 3,64 (2H, дд, J=9,3, 6,6Гц), 3,73 (3H, с).
13C-ЯМР (CDCl3) δ: 172,71, 70,31, 59,91, 46,49.
МС (ESI) m/z: 163 (M+H+).
[Ссылочный пример 156]
Тетрагидро-2Н-пиран-4-карбоновая кислота
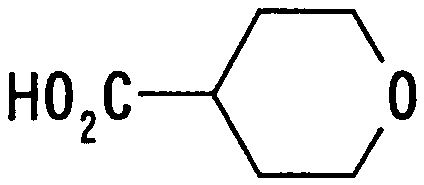
Диметил тетрагидро-4Н-пиран-4,4-дикарбоксилат (4,04 г) добавляли к 20% хлористоводородной кислоте (20 мл) и смесь кипятили с обратным холодильником в течение 19 часов. К реакционной смеси добавляли воду и экстрагировали диэтиловым эфиром. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. После отверждения полученного осадка гексаном полученные твердые частицы отфильтровывали и промывали с получением указанного в заголовке соединения (2,63 г).
1Н-ЯМР (CDCl3) δ: 1,75-1,95 (4Н, м), 2,55-2,65 (1Н, м), 3,40-3,52 (2Н, м), 3,93-4,05 (2Н, м).
[Ссылочный пример 157]
Метил 3-{[трет-бутил(дифенил)силил]окси}-2,2-диметилпропионат
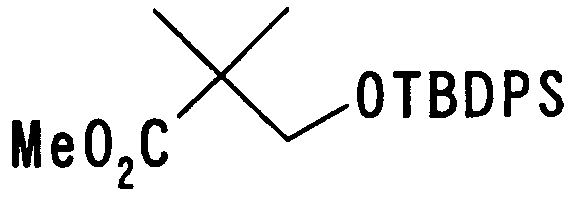
Указанное в заголовке соединение получали из метил 2,2-диметил-3-гидроксипропионата подобно способу ссылочного примера 41.
1Н-ЯМР (CDCl3) δ: 1,03 (9Н, с), 1,20 (6Н, с), 3,64-3,68 (5Н, м), 7,38-7,44 (6Н, м), 7,63-7,65 (4Н, м).
[Ссылочный пример 158]
3-{[трет-Бутил(дифенил)силил]окси}-2,2-диметилпропионовая кислота
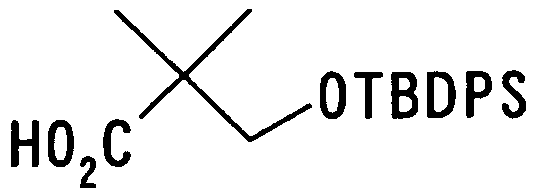
Воду (0,24 мл) добавляли к суспензии, состоящей из трет-бутоксида калия (5,32 г) и диэтилового эфира (100 мл), при охлаждении льдом и смесь перемешивали в течение 5 минут. К смеси добавляли соединение (2,22 г), полученное в ссылочном примере 157, и полученную смесь перемешивали в течение ночи при комнатной температуре. К реакционной смеси добавляли воду и смесь подкисляли 1N хлористоводородной кислотой и экстрагировали 3 раза диэтиловым эфиром. Полученный органический слой сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и полученный остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:6) с получением указанного в заголовке соединения (735 мг).
1Н-ЯМР (CDCl3) δ: 1,04 (9Н, д, J=0,7Гц), 1,22 (6Н, с), 3,65 (2Н, с), 7,36-7,45 (6Н, м), 7,64-7,66 (4Н, м).
[Ссылочный пример 159]
Метил 3-метокси-2,2-диметилпропионат
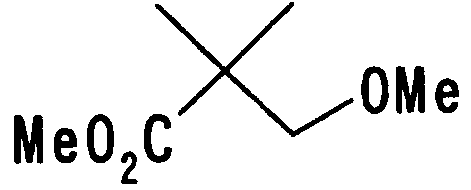
Раствор метил 3-гидрокси-2,2-диметилпропионата (25,0 г) в тетрагидрофуране (300 мл) добавляли по каплям к суспензии, состоящей из 60% масляной суспензии гидрида натрия (8,32 г) и тетрагидрофурана (100 мл), при охлаждении льдом и смесь перемешивали при 60°C в течение 1 часа. К реакционной смеси добавляли метилиодид (53,7 г) и полученную смесь перемешивали при комнатной температуре в течение 2 часов. Осторожно добавляли воду и дважды экстрагировали метиленхлоридом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и полученное масло дистиллировали с получением указанного в заголовке соединения (12,8 г).
Температура кипения: 140-142°C (обычное давление).
1Н-ЯМР (CDCl3) δ: 1,19 (6Н, д, J=1,0Гц), 3,33 (3Н, д, J=1,0Гц), 3,38 (2Н, д, J=1,0Гц), 3,69 (3Н, д, J=1,0Гц).
[Ссылочный пример 160]
3-Метокси-2,2-диметилпропионовая кислота
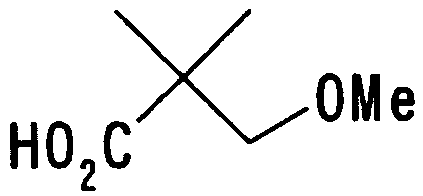
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 159, подобно способу ссылочного примера 158.
1Н-ЯМР (CDCl3) δ: 1,22 (6Н, д, J=0,7Гц), 3,38 (3Н, д, J=0,7Гц), 3,40 (2Н, д, J=0,7Гц).
[Ссылочный пример 161]
1-(Метоксикарбонил)циклопропанкарбоновая кислота
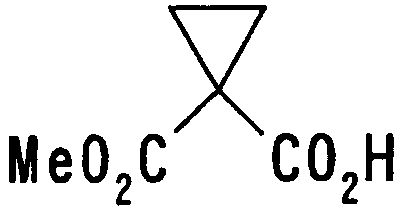
Диметил 1,1-циклопропанкарбоксилат (25 г) растворяли в метаноле (250 мл) и раствор охлаждали льдом. Затем добавляли по каплям 1N водный раствор гидроксида натрия (158 мл) и полученную смесь нагревали до комнатной температуры и перемешивали в течение ночи. После отгонки метанола остаток промывали хлороформом и водный слой охлаждали льдом, доводили до рН 2 концентрированной хлористоводородной кислотой и экстрагировали этилацетатом. Экстракт сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (16,8 г).
1Н-ЯМР (CDCl3) δ: 1,76-1,80 (2Н, м), 1,82-1,88 (2Н, м), 3,79 (3Н, с), 12,73 (1Н, шир.).
[Ссылочный пример 162]
Метил 1-(гидроксиметил)циклопропанкарбоксилат
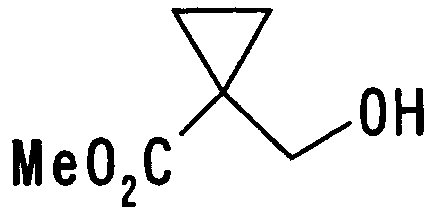
Соединение (9,0 г), полученное в ссылочном примере 161, и триэтиламин (9,7 мл) растворяли в тетрагидрофуране (180 мл) и раствор охлаждали до -10°C, добавляли к нему по каплям изобутилхлорформиат (9,1 мл) и полученную смесь перемешивали в течение 1 часа. С другой стороны, растворяли боргидрид натрия (7,1 г) в смеси тетрагидрофуран (100 мл)-вода (25 мл) и охлаждали льдом. После удаления нерастворимого вещества фильтрованием добавляли по каплям заранее приготовленный раствор и полученную смесь перемешивали при той же температуре в течение 1 часа. Реакционную смесь вливали в охлажденный 10% водный раствор лимонной кислоты и экстрагировали этилацетатом. Экстракт промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, затем отгоняли растворитель при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:9-2:1) с получением указанного в заголовке соединения (4,25 г).
1Н-ЯМР (CDCl3) δ: 0,87-0,93 (2Н, м), 1,28-1,30 (2Н, м), 3,63 (2Н, с), 3,70 (3Н, с).
[Ссылочный пример 163]
Метил 1-(бромметил)циклопропанкарбоксилат

Трифенилфосфин (10 г) и тетрабромид углерода (16 г) добавляли к раствору соединения (4,20 г), полученного в ссылочном примере 162, в метиленхлориде (168 мл) при комнатной температуре в атмосфере азота. Через 2 минуты к смеси добавляли насыщенный водный раствор гидрокарбоната натрия. Полученный органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:19) с получением указанного в заголовке соединения (2,15 г).
1Н-ЯМР (CDCl3) δ: 1,00-1,05 (2Н, м), 1,52-1,59 (2Н, м), 3,61 (2Н, с), 3,73 (3Н, с).
[Ссылочный пример 164]
трет-Бутил (4S)-4-[(E)-3-этокси-3-оксо-1-пропенил]-2,2-диметил-1,3-оксазолидин-3-карбоксилат
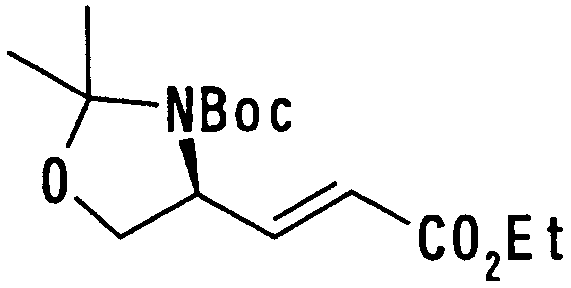
Смешанный раствор, состоящий из трет-бутил (4R)-4-формил-2,2-диметил-1,3-оксазолидин-3-карбоксилата (11,7 г), (карбоэтоксиметилен)трифенилфосфорана (20,7 г) и толуола (100 мл), нагревали и перемешивали при 100°C в течение 18 часов. Реакционную смесь концентрировали и полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 8:1) с получением указанного в заголовке соединения (17 г).
1Н-ЯМР (CDCl3) δ: 1,29 (3Н, т, J=6,6Гц), 1,43-1,56 (15Н, м), 3,80 (1Н, дд, J=9,0, 2,4Гц), 4,09 (1Н, дд, J=9,0, 6,6Гц), 4,11-4,23 (2Н, м), 4,30-4,61 (1Н, м), 5,83-6,02 (1Н, м), 6,74-6,89 (1Н, м).
[Ссылочный пример 165]
трет-Бутил (4S)-4-[1-(бензиламино)-3-этокси-3-оксопропил]-2,2-диметил-1,3-оксазолидин-3-карбоксилат
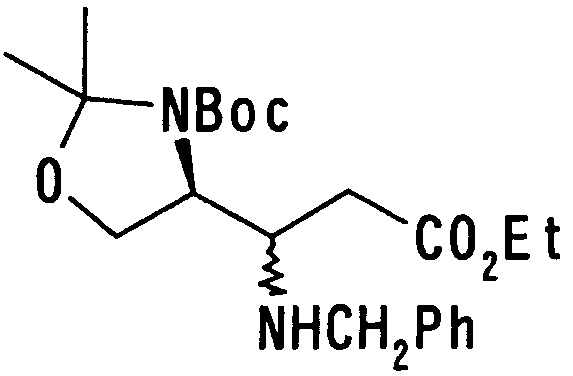
Смешанный раствор, состоящий из соединения (22,2 г), полученного в ссылочном примере 164, бензиламина (16 г) и этанола (100 мл), кипятили с обратным холодильником в течение 2 дней. Реакционную смесь концентрировали и полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 8:1) с получением указанного в заголовке соединения (26 г).
1Н-ЯМР (CDCl3) δ: 1,25 (3Н, т, J=6,6Гц), 1,42-1,63 (15Н, м), 2,24-2,33 (0,5Н, м), 2,40-2,50 (1Н, м), 2,63-2,74 (0,5Н, м), 3,41-3,52 (1Н, м), 3,67-3,80 (1Н, м), 3,83 (2Н, с), 3,89-4,00 (1Н, м), 4,03-4,22 (4Н, м), 7,23-7,45 (5Н, м).
[Ссылочный пример 166]
трет-Бутил (4S)-4-(1-амино-3-этокси-3-оксопропил)-2,2-диметил-1,3-оксазолидин-3-карбоксилат
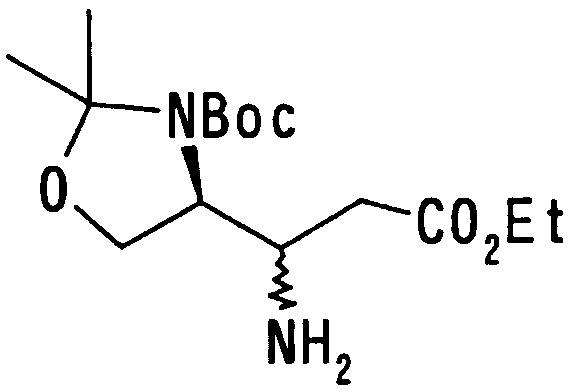
10% Палладий на углероде (10 г) добавляли к раствору соединения (13,6 г), полученного в ссылочном примере 165, в этаноле (200 мл) и смесь перемешивали 2 дня в атмосфере водорода. Нерастворимое вещество удаляли через слой целита и фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (10,5 г).
1Н-ЯМР (ДМСО-d6) δ: 1,19 (1,5Н, т, J=6,6Гц), 1,20 (1,5Н, т, J=6,6Гц), 1,32-1,50 (15Н, м), 2,63-2,81 (2Н, м), 3,22-3,34 (2Н, м), 3,93 (1Н, дд, J=10,0, 6,8Гц), 4,08 (2Н, кв, J=6,6Гц), 4,20-4,30 (1Н, м).
[Ссылочный пример 167]
трет-Бутил (4S)-4-(1-{[(бензилокси}карбонил]амино)-3-этокси-3-оксопропил)-2,2-диметил-1,3-оксазолидин-3-карбоксилат
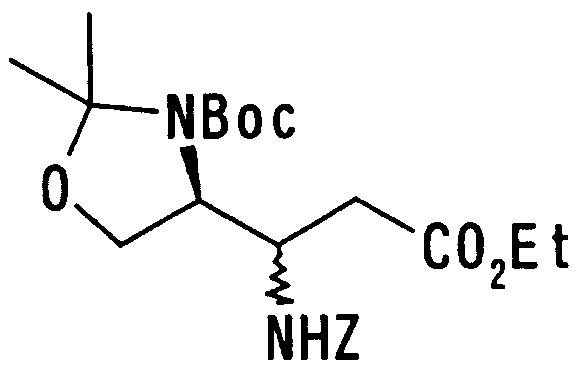
Соединение (3,0 г), полученное в ссылочном примере 166, суспендировали в 9% водном растворе (56 мл) гидрокарбоната натрия и к суспензии добавляли по каплям при охлаждении льдом раствор N-(бензилоксикарбонилокси)сукцинимида (2,3 г) в диоксане (12 мл). Полученную смесь перемешивали 3 часа при постепенном повышении при этом температуры системы до комнатной температуры. Реакционную смесь разбавляли этилацетатом, промывали водой, 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ) с получением указанного в заголовке соединения (3,8 г).
1Н-ЯМР (CDCl3) δ: 1,23 (3Н, т, J=6,6Гц), 1,48 (9Н, с), 1,56 (6Н, с), 2,40-2,51 (2Н, м), 2,63-2,70 (2Н, м), 3,92-4,04 (1Н, м), 4,06-4,10 (2Н, м), 4,14-4,22 (1Н, м), 5,09 (2Н, с), 7,30-7,43 (5Н, м).
[Ссылочный пример 168]
Этил (3S,4S)-3-{[(бензилокси}карбонил]амино)-4-[(трет-бутоксикарбонил)амино]-5-гидроксивалерат (низкополярное соединение) и этил (3R,4S)-3-{[(бензилокси}карбонил]амино)-4-[(трет-бутоксикарбонил)амино]-5-гидроксивалерат (высокополярное соединение)
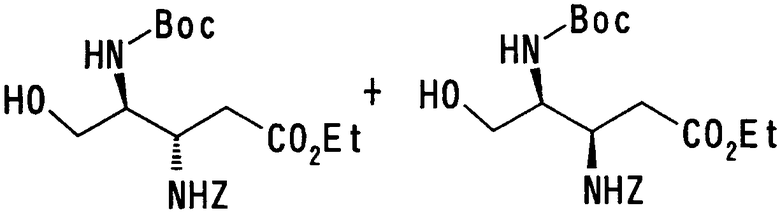
Трифторуксусную кислоту (100 мл) добавляли по каплям к раствору соединения (30 г), полученного в ссылочном примере 167, в метиленхлориде (100 мл) при охлаждении льдом и смесь перемешивали 3 часа при постепенном повышении температуры системы до комнатной температуры. Реакционную смесь концентрировали при пониженном давлении и полученный остаток растворяли в метиленхлориде (100 мл). К полученному раствору при охлаждении льдом добавляли по каплям последовательно триэтиламин (20 мл) и раствор ди-трет-бутилдикарбоната (19 г) в метиленхлориде (100 мл) и смесь перемешивали 4 часа при постепенном повышении температуры системы до комнатной температуры. Реакционную смесь концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 2:1) с получением указанного в заголовке низкополярного соединения (7,6 г) и указанного в заголовке высокополярного соединения (10 г).
Низкополярное соединение:
1Н-ЯМР (CDCl3) δ: 1,24 (3H, т, J=6,6Гц), 1,42 (9H, с), 2,63 (2H, д, J=4,4Гц), 3,30-3,41 (1H, м), 3,50 (1H, т, J=9,7Гц), 3,65 (1H, т, J=9,7Гц), 3,75 (1H, д, J=11,7Гц), 3,90-4,00 (1H, м), 4,03-4,23 (2H, м), 5,12 (2H, с), 5,13-5,25 (1H, м), 5,79-6,02 (1H, м), 7,32-7,41 (5H, м).
Высокополярное соединение:
1Н-ЯМР (CDCl3) δ: 1,22 (3H, т, J=6,6Гц), 1,41 (9H, с), 2,50-2,70 (2H, м), 3,20-3,31 (1H, м), 3,43-3,51 (1H, м), 3,56-3,70 (1H, м), 3,74-3,78 (1H, м), 4,00-4,19 (2H, м), 4,23-4,30 (1H, м), 4,78-4,89 (1H, м), 5,10 (2H, с), 5,56-5,67 (1H, м), 7,31-7,40 (5H, м).
[Ссылочный пример 169]
(3R,4S)-4-[(Метилсульфонил)окси]тетрагидро-3-фуранилметансульфонат
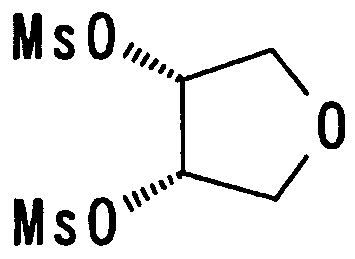
Триэтиламин (12,0 мл) и метансульфонилхлорид (3,6 мл) последовательно добавляли по каплям к раствору 1,4-ангидроэритрита (5,0 г) в метиленхлориде (50 мл) при охлаждении льдом и смесь перемешивали в течение 10 минут при охлаждении льдом. Реакционную смесь разбавляли метиленхлоридом и промывали 10% хлористоводородной кислотой, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (9,2 г).
1Н-ЯМР (CDCl3) δ: 3,15 (6Н, с), 3,99 (2Н, дд, J=11,2, 2,5Гц), 4,16 (2Н, дд, J=11,2, 4,6Гц), 5,10-5,20 (2Н, м).
[Ссылочный пример 170]
(3R,4S)-3,4-Диазидотетрагидрофуран
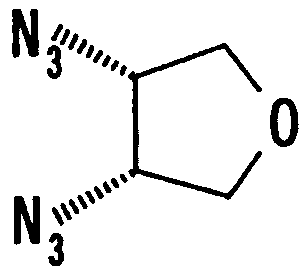
Соединение (9,2 г), полученное в ссылочном примере 169, растворяли в N,N-диметилформамиде (50 мл), добавляли азид натрия (18 г) и полученную смесь нагревали и перемешивали при 100°C в течение 18 часов. Реакционную смесь разбавляли этилацетатом и промывали насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (3,8 г).
1Н-ЯМР (CDCl3) δ: 3,83 (2Н, дд, J=8,6, 2,0Гц), 3,96-4,12 (4Н, м).
[Ссылочный пример 171]
Дигидрохлорид (3R,4S)-тетрагидро-3-4-фурандиамина
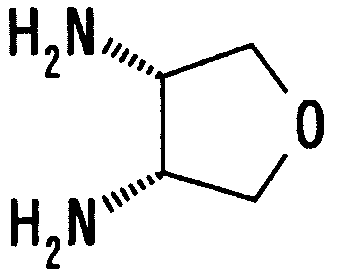
Соединение (3,8 г), полученное в ссылочном примере 170, растворяли в этаноле (50 мл), к раствору добавляли 10% палладий на углероде (1,0 г) и смесь перемешивали 18 часов в атмосфере водорода. Нерастворимое вещество удаляли через слой целита и фильтрат концентрировали при пониженном давлении. К полученному остатку добавляли 1N этанольный раствор хлористоводородной кислоты, получая гидрохлорид. Гидрохлорид перекристаллизовывали из смешанного растворителя этанол/диэтиловый эфир с получением указанного в заголовке соединения (2,0 г).
1Н-ЯМР (CDCl3) δ: 3,90 (2Н, дд, J=9,0, 3,7Гц), 4,01-4,13 (4Н, м), 8,84 (6Н, с).
[Ссылочный пример 172]
N-[(3R*,4S*)-4-Аминотетрагидро-3-фуранил]-5-хлориндол-2-карбоксамид
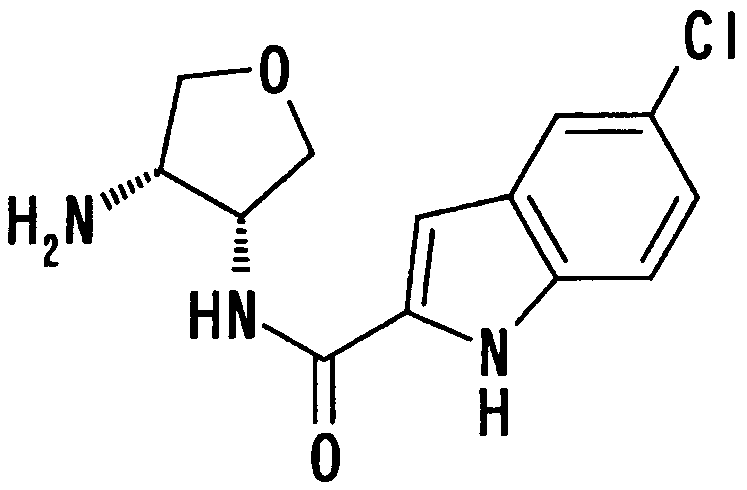
5-Хлориндол-2-карбоновую кислоту (0,29 г), моногидрат 1-гидроксибензотриазола (0,2 г) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (0,6 г) последовательно добавляли к раствору соединения (0,5 г), полученного в ссылочном примере 171, в N,N-диметилформамиде (10 мл) и смесь нагревали и перемешивали при 50°C в течение суток. Реакционную смесь концентрировали и полученный остаток разбавляли смешанным растворителем хлороформ/метанол (9:1) и промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 95:5) с получением указанного в заголовке соединения (0,2 г).
1Н-ЯМР (CDCl3) δ: 1,80-1,92 (1H, м), 3,62 (1H, дд, J=9,3, 4,2Гц), 3,68-3,80 (2H, м), 4,06 (1H, дд, J=9,3, 5,6Гц), 4,21 (1H, дд, J=9,3, 6,8Гц), 4,36-4,52 (2H, м), 6,87 (1H, с), 7,24 (1H, дд, J=8,8, 2,0Гц), 7,36 (1H, д, J=8,8Гц), 7,44-7,56 (1H, м), 7,62 (1H, д, J=2,0Гц), 9,41 (1H, с).
[Ссылочный пример 173]
трет-Бутил (4R)-4-[(E)-3-этокси-3-оксо-1-пропенил]-2,2-диметил-1,3-оксазолидин-3-карбоксилат
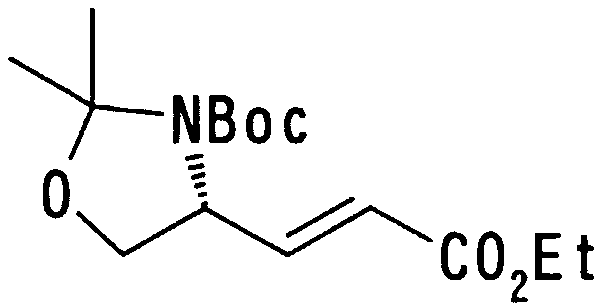
Указанное в заголовке соединение получали из трет-бутил (4S)-4-формил-2,2-диметил-1,3-оксазолидин-3-карбоксилата подобно способу ссылочного примера 164.
1Н-ЯМР (CDCl3) δ: 1,29 (3H, т, J=6,6Гц), 1,40-1,60 (15H, м), 3,80 (1H, дд, J=9,0, 2,4Гц), 4,09 (1H, дд, J=9,0, 6,6Гц), 4,11-4,21 (2H, м), 4,32-4,64 (1H, м), 5,78-6,01 (1H, м), 6,67-6,89 (1H, м).
[Ссылочный пример 174]
трет-Бутил (4R)-4-[1-(бензиламино)-3-этокси-3-оксопропил]-2,2-диметил-1,3-оксазолидин-3-карбоксилат
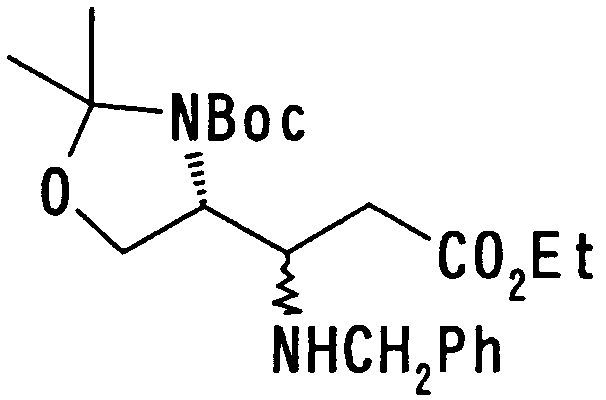
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 173, подобно способу ссылочного примера 165.
1Н-ЯМР (CDCl3) δ: 1,25 (3H, т, J=6,6Гц), 1,40-1,61 (15H, м), 2,21-2,32 (0,5H, м), 2,40-2,51 (1H, м), 2,61-2,72 (0,5H, м), 3,43-3,50 (1H, м), 3,67-3,80 (1H, м), 3,83 (2H, с), 3,90-4,03 (1H, м), 4,04-4,22 (4H, м), 7,20-7,40 (5H, м).
[Ссылочный пример 175]
трет-Бутил (4R)-4-(1-{[(5-хлориндол-2-ил)карбонил]амино}-3-этокси-3-оксопропил)-2,2-диметил-1,3-оксазолидин-3-карбоксилат
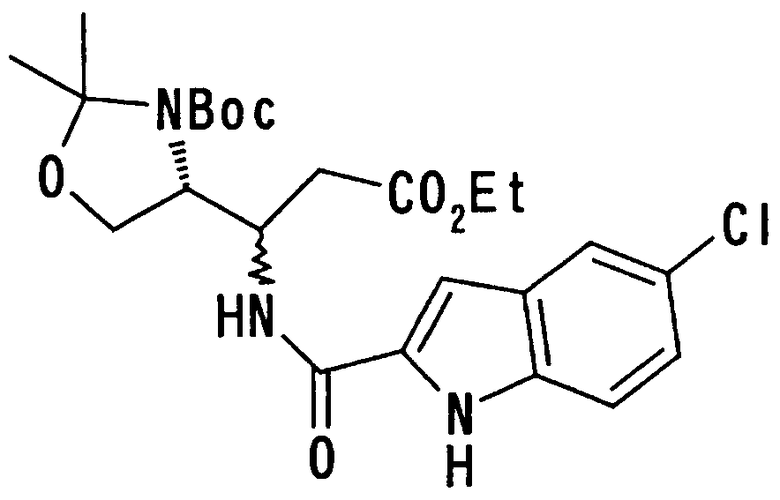
Указанное в заголовке соединение получали восстановлением соединения, полученного в ссылочном примере 174, подобно способу ссылочного примера 166, с удалением бензильной группы и затем конденсацией его с 5-хлориндол-2-карбоновой кислотой подобно способу ссылочного примера 172.
1Н-ЯМР (CDCl3) δ: 1,23 (1,5H, т, J=6,6Гц), 1,25 (1,5H, т, J=6,6Гц), 1,50 (4,5H, с), 1,54 (4,5H, с), 1,62 (6H, с), 2,50-2,70 (1,5H, м), 2,86 (0,5H, дд, J=16,4, 5,5Гц), 3,80-3,90 (0,5H, м), 4,00-4,31 (5H, м), 4,41-4,67 (0,5H, м), 6,85 (0,5H, с), 6,87 (0,5H, с), 7,10-7,20 (1H, м), 7,34 (0,5H, д, J=8,8Гц), 7,38 (0,5H, д, J=8,8Гц), 7,57 (0,5H, с), 7,63 (0,5H, с), 7,88 (0,5H, д, J=7,6Гц), 8,54 (0,5H, д, J=7,6Гц), 9,40 (0,5H, с), 9,54 (0,5H, с).
[Ссылочный пример 176]
трет-Бутил (3R,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}-6-оксотетрагидро-2Н-пиран-3-илкарбамат (низкополярное соединение) и трет-бутил (3R,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-6-оксотетрагидро-2Н-пиран-3-илкарбамат (высокополярное соединение)
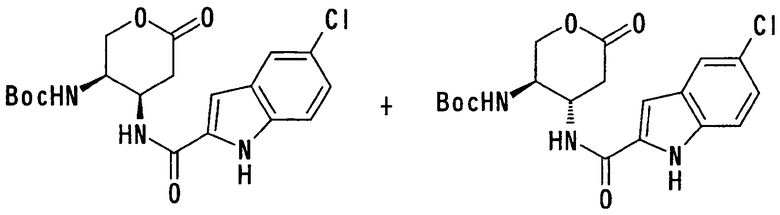
1N Водный раствор (4,0 мл) гидроксида натрия добавляли к раствору соединения (1,0 г), полученного в ссылочном примере 175, в этаноле (20 мл) и смесь перемешивали 4 часа. К реакционной смеси добавляли лимонную кислоту, доводя рН реакционной смеси до 4,0. Реакционную смесь экстрагировали этилацетатом и полученный органический слой промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении. Полученный остаток растворяли в метаноле (50 мл), к раствору добавляли моногидрат толуолсульфоновой кислоты (0,1 г) и полученную смесь перемешивали в течение 18 часов. Реакционную смесь разбавляли этилацетатом и промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 99:1) с получением указанного в заголовке низкополярного соединения (0,3 г) и указанного в заголовке высокополярного соединения (0,3 г).
Низкополярное соединение:
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 2,70 (1H, дд, J=16,5, 4,9Гц), 2,85 (1H, дд, J=16,5, 4,6Гц), 3,50-3,61 (1H, м), 3,71-3,81 (2H, м), 4,30-4,40 (1H, м), 5,30 (1H, д, J=9,5Гц), 6,89 (1H, с), 7,23 (1H, дд, J=8,8, 2,0Гц), 7,38 (1H, д, J=8,8Гц), 7,62 (1H, д, J=2,0Гц), 7,93 (1H, д, J=9,5Гц), 9,30 (1H, с).
Высокополярное соединение:
1Н-ЯМР (CDCl3) δ: 1,39 (9H, с), 2,75 (1H, дд, J=16,5, 4,9Гц), 2,82 (1H, дд, J=16,5, 4,6Гц), 3,41-3,52 (2H, м), 3,71-3,82 (1H, м), 3,85-3,94 (1H, м), 5,03 (1H, д, J=9,3Гц), 6,99 (1H, с), 7,22-7,31 (1H, м), 7,34 (1H, д, J=8,8Гц), 7,61 (1H, д, J=2,0Гц), 7,83 (1H, д, J=9,3Гц), 9,28 (1H, с).
[Ссылочный пример 177]
трет-Бутил 1,1,3-триоксогексагидро-1-тиопиран-4-илкарбамат
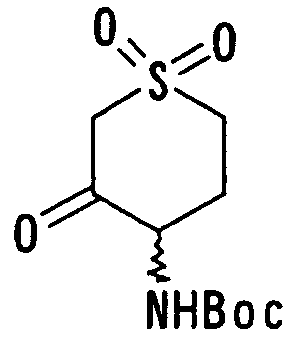
Раствор метилового эфира N-трет-бутоксикарбонил-L-метионинсульфона (60,2 г) в тетрагидрофуране (900 мл) охлаждали до -78°C, добавляли к нему по каплям 0,5М бис(триметилсилил)амид калия (толуольный раствор, 900 мл) и смесь перемешивали 2 часа при -78°C и 4,5 часа при комнатной температуре. Добавляли 1М водный раствор хлорида аммония и смесь перемешивали. Слои жидкой реакционной смеси разделяли и затем полученный органический слой промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и образовавшиеся твердые частицы отфильтровывали с получением указанного в заголовке соединения (12,4 г). Отделенный ранее водный слой экстрагировали дважды этилацетатом и полученные органические слои объединяли, промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Водные слои, использованные при промывке, также объединяли и снова экстрагировали этилацетатом и экстракт промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Этилацетатные экстракты объединяли, сушили и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения (27,7 г) (общее количество указанного в заголовке соединения: 40,1 г).
1Н-ЯМР (CDCl3) δ: 1,45 (9Н, с), 1,85-1,96 (1Н, м), 2,76-2,78 (1Н, м), 3,34-3,46 (2Н, м), 4,05 (1Н, дд, J=13,5, 3,7Гц), 4,14 (1Н, д, J=13,5Гц), 4,38-4,44 (1Н, м), 5,46 (1Н, шир.).
МС (ESI) m/z: 262 (M-H)-.
[Ссылочный пример 178]
трет-Бутил (3R*,4R*)-3-гидрокси-1,1-диоксогексагидро-1-тиопиран-4-илкарбамат
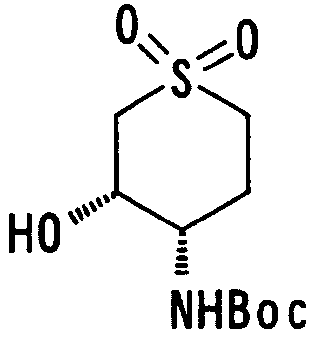
Боргидрид натрия (2,17 г) добавляли к суспензии соединения (10,1 г), полученного в ссылочном примере 177, в метаноле (200 мл) и смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь концентрировали при пониженном давлении. Добавив к остатку этилацетат и насыщенный водный раствор гидрокарбоната натрия, разделяли жидкости и полученный водный слой экстрагировали два раза этилацетатом. Полученные органические слои объединяли, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения (9,96 г).
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 2,21-2,36 (2H, м), 3,03-3,17 (2H, м), 3,26-3,28 (2H, м), 3,77-3,80 (2H, м), 4,26-4,28 (1H, м), 5,05-5,07 (1H, м).
МС (ESI) m/z: 264 (М-Н)-.
[Ссылочный пример 179]
трет-Бутил (3R*,4R*)-3-амино-1,1-диоксогексагидро-1-тиопиран-4-илкарбамат (низкополярное соединение) и трет-бутил (3R*,4S*)-3-амино-1,1-диоксогексагидро-1-тиопиран-4-илкарбамат (высокополярное соединение)
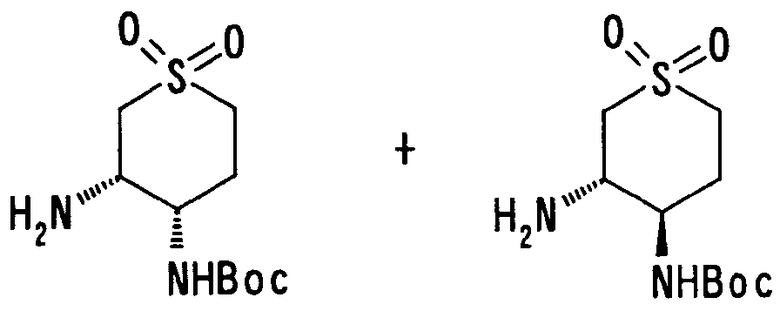
Диэтилазодикарбоксилат (6,96 г) добавляли к раствору соединения (9,66 г), полученного в ссылочном примере 178, и трифенилфосфина (10,5 г) в тетрагидрофуране (150 мл) и смесь перемешивали при комнатной температуре в течение 4,5 часов. Реакционную смесь концентрировали при пониженном давлении, затем к остатку добавляли диэтиловый эфир и образовавшиеся твердые частицы отфильтровывали. Отфильтрованные твердые частицы очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 7:3) с получением смеси (7,25 г), содержащей трет-бутил 1,1-диоксо-1,2,3,4-тетрагидропиран-4-илкарбамат в виде бесцветного твердого вещества. Маточный раствор концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 7:3) с получением смеси (9,18 г), содержащей трет-бутил 1,1-диоксо-1,2,3,4-тетрагидропиран-4-илкарбамат в виде бесцветного твердого вещества (общее количество: 16,4 г). Полученные таким образом смеси растворяли в диоксане (60 мл) и добавляли 28% водный аммиак (60 мл). Полученную смесь перемешивали при 60°C в течение 4,5 часов в герметичной пробирке. После охлаждения реакционную смесь концентрировали при пониженном давлении. После отгонки диоксана остаток экстрагировали 5 раз метиленхлоридом. Полученные органические слои объединяли и концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 94:6) с получением указанного в заголовке низкополярного соединения (2,31 г) и указанного в заголовке высокополярного соединения (4,31 г).
Низкополярное соединение:
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 2,14-2,28 (2H, м), 3,01-3,08 (3H, м), 3,23 (1H, дд, J=13,8, 3,9Гц), 3,47-3,49 (1H, м), 3,71-3,76 (1H, м), 5,32 (1H, д, J=7,3Гц).
МС (ESI) m/z: 265 (M+H+).
Высокополярное соединение:
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,94-2,01 (1H, м), 2,37-2,44 (1H, м), 2,91 (1H, дд, J=11,2, 14,1Гц), 3,04-3,07 (2H, м), 3,12-3,19 (1H, м), 3,26-3,30 (1H, м), 3,39-3,42 (1H, м), 4,62 (1H, шир.).
МС (ESI) m/z: 265 (М+Н+).
[Ссылочный пример 180]
(2S,3S)-2,3-Бис(метоксиметокси)-1,4-бутандиол
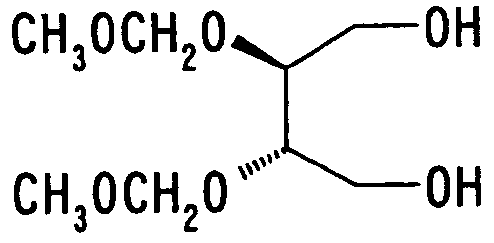
Хлорметилметиловый эфир (4,8 мл) добавляли по каплям к смешанному раствору из диэтил L-тартрата (8,6 г), диизопропилэтиламина (40 мл) и метиленхлорида (40 мл) при охлаждении льдом и смесь перемешивали 18 часов, постепенно понижая температуру системы до комнатной температуры. Реакционную смесь концентрировали и полученный остаток разбавляли этилацетатом и промывали 10% хлористоводородной кислотой, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и полученный остаток растворяли в тетрагидрофуране. Раствор добавляли по каплям к тетрагидрофурановой суспензии литийалюминийгидрида (2,2 г) при охлаждении льдом и смесь перемешивали в течение 2 часов при охлаждении льдом. Осторожно добавляли при охлаждении льдом 10% водный раствор гидросульфата натрия и смесь перемешивали в течение 1 часа, затем реакционную смесь разбавляли насыщенным водным раствором хлорида натрия и экстрагировали этилацетатом. Полученный органический слой сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (3,0 г).
1Н-ЯМР (CDCl3) δ: 1,55-1,64 (2Н, м), 3,44 (6Н, с), 3,70-3,81 (6Н, м), 4,70 (2Н, д, J=6,9Гц), 4,76 (2Н, д, J=6,9Гц).
[Ссылочный пример 181]
(3S,4S)-3,4-Бис(метоксиметокси)тетрагидрофуран
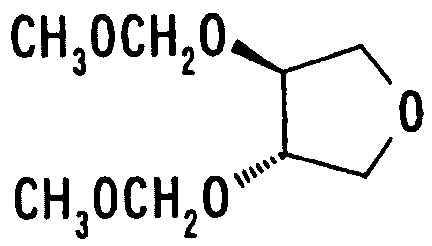
Диэтилазодикарбоксилат (2,46 мл) добавляли по каплям к смешанному раствору, состоящему из соединения (3,0 г), полученного в ссылочном примере 180, трифенилфосфина (4,5 г), тетрагидрофурана (10 мл) и толуола (40 мл), и смесь перемешивали при комнатной температуре в течение 4 дней. Реакционную смесь концентрировали при пониженном давлении, к полученному остатку добавляли смешанный растворитель (160 мл) гексан/диэтиловый эфир (1:1) и смесь перемешивали 3 часа. Затем выпавшее в осадок нерастворимое вещество отфильтровывали. Фильтрат концентрировали и полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1) с получением указанного в заголовке соединения (1,95 г).
1Н-ЯМР (CDCl3) δ: 3,38 (6Н, с), 3,80 (2Н, дд, J=9,2, 1,7Гц), 4,00 (2Н, дд, J=9,2, 4,4Гц), 4,23 (2Н, дд, J=4,4, 1,7Гц), 4,67 (2Н, д, J=6,9Гц), 4,71 (2Н, д, J=6,9Гц).
[Ссылочный пример 182]
(3S,4S)-Тетрагидро-3,4-фурандиол
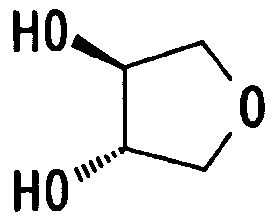
Концентрированную хлористоводородную кислоту (2,1 мл) добавляли к раствору соединения (1,95 г), полученного в ссылочном примере 181, в метаноле (6,0 мл) и смесь перемешивали 18 часов. Реакционную смесь концентрировали и полученный остаток разбавляли хлороформом и сушили над карбонатом калия, затем отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (0,52 г).
1Н-ЯМР (CDCl3) δ: 1,77 (2Н, д, J=4,7Гц), 3,73 (2Н, д, J=10,2Гц), 4,08 (2Н, дд, J=10,2, 3,7Гц), 4,18-4,34 (2Н, м).
[Ссылочный пример 183]
(3S,4S)-Тетрагидро-3,4-фурандиамин
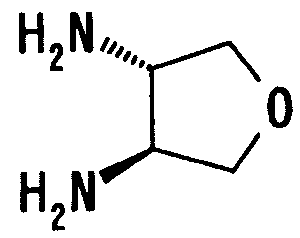
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 182, подобно способам, описанным в ссылочных примерах 169 и 171.
1Н-ЯМР (CDCl3) δ: 1,35-1,46 (4Н, м), 3,19 (2Н, дд, J=5,6, 4,1Гц), 3,50 (2Н, дд, J=9,0, 4,1Гц), 4,09 (2Н, дд, J=9,0, 5,6Гц).
[Ссылочный пример 184]
(2R,3R)-2,3-Бис(метоксиметокси)-1,4-бутандиол
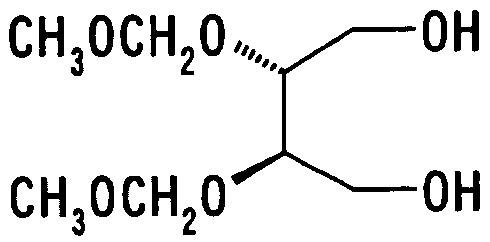
Указанное в заголовке соединение получали из диэтил D-тартрата подобно способу ссылочного примера 180.
1Н-ЯМР: Данные такие же, как у энантиомера в ссылочном примере 180.
[Ссылочный пример 185]
(3R,4R)-3,4-Бис(метоксиметокси)тетрагидрофуран

Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 184, подобно способу ссылочного примера 181.
1Н-ЯМР: Данные такие же, как у энантиомера в ссылочном примере 181.
[Ссылочный пример 186]
(3R,4R)-Тетрагидро-3,4-фурандиол
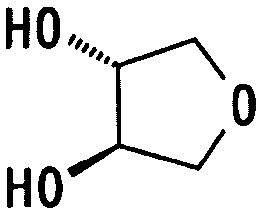
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 185, подобно способу ссылочного примера 182.
1Н-ЯМР: Данные такие же, как у энантиомера в ссылочном примере 182.
[Ссылочный пример 187]
(3R,4R)-Тетрагидро-3,4-фурандиамин
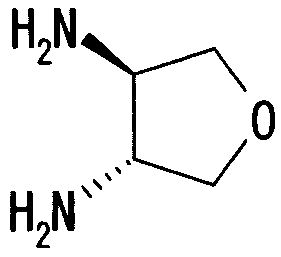
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 186, подобно способу ссылочного примера 183.
1Н-ЯМР (CDCl3) δ: Данные такие же, как у энантиомера в ссылочном примере 183.
[Ссылочный пример 188]
(3R,4R)-1-Бензил-3,4-дигидрокси-2,5-пирролидиндион
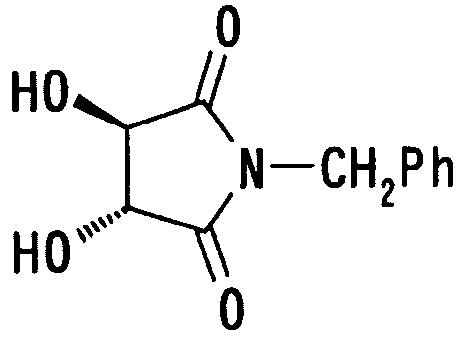
L-Винную кислоту (30 г) и бензиламин (22 мл) добавляли к ксилолу (150 мл) и смесь нагревали с обратным холодильником при 150°C в течение 3 часов с использованием ловушки Дина-Старка. После охлаждения реакционной смеси в течение ночи отфильтровывали кристаллы и промывали их ацетоном. Полученный неочищенный продукт перекристаллизовывали из этанола с получением указанного в заголовке соединения (23,2 г).
1Н-ЯМР (ДМСО-d6) δ: 4,36-4,40 (2Н, м), 4,55 (каждый 1Н, тип АВ д, J=15Гц), 6,26-6,30 (2Н, м), 7,25-7,35 (5Н, м).
[Ссылочный пример 189]
(3S,4S)-1-Бензил-3,4-пирролидиндиол
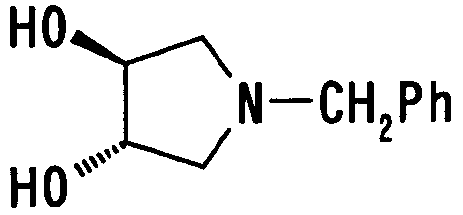
Соединение (11 г), полученное в ссылочном примере 188, растворяли в тетрагидрофуране (110 мл) и к раствору при охлаждении льдом добавляли порциями литийалюминийгидрид (5,69 г). Смесь нагревали до комнатной температуры в течение 1 часа и кипятили с обратным холодильником еще в течение ночи. После охлаждения реакционной смеси добавляли при охлаждении льдом воду (5,7 мл), 15% водный раствор (5,7 мл) гидроксида натрия и воду (17,1 мл) в указанном порядке и смесь нагревали до комнатной температуры и перемешивали в течение 1 часа. Осадок отфильтровывали через целит и концентрировали при пониженном давлении маточный раствор, затем полученный остаток перекристаллизовывали из этилацетата с получением указанного в заголовке соединения (6,35 г).
1Н-ЯМР (CDCl3) δ: 2,40-2,44 (2Н, м), 2,88-2,92 (2Н, м), 3,58 (каждый 1Н, тип АВ д, J=7,8Гц), 4,04 (2Н, т, J=4,2Гц), 7,25-7,34 (5Н, м).
[Ссылочный пример 190]
(3S,4S)-1-Бензил-4-[(метилсульфонил)окси]пирролидинилметансульфонат
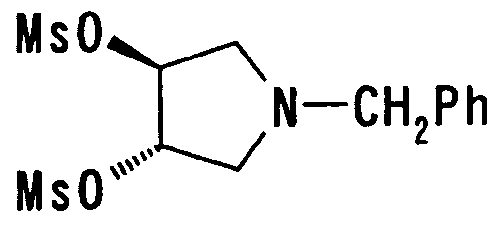
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 189, подобно способу ссылочного примера 169.
1Н-ЯМР (CDCl3) δ: 2,76 (2Н, дд, J=11, 4,6Гц), 3,08 (6Н, с), 3,64 (2Н, д, J=2,5Гц), 3,68-7,75 (2Н, м), 5,12-5,15 (2Н, м), 7,27-7,35 (5Н, м).
[Ссылочный пример 191]
трет-Бутил (3S,4S)-3,4-бис[(метилсульфонил)окси]-1-пирролидинкарбоксилат
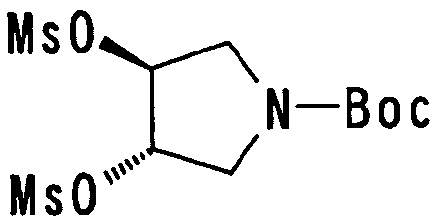
Соединение (1,57 г), полученное в ссылочном примере 190, растворяли в 1,2-дихлорэтане (16 мл), добавляли при комнатной температуре 1-хлорэтилхлорформиат (0,73 мл) и полученную смесь кипятили с обратным холодильником в течение 4 часов. Отогнав при пониженном давлении растворитель, к полученному остатку добавляли метанол (16 мл) и полученную смесь кипятили с обратным холодильником в течение 1 часа, давали остыть и концентрировали. Кристаллы, полученные перекристаллизацией из этилацетата, отфильтровывали с получением гидрохлорида (3S,4S)-3,4-бис[(метилсульфонил)окси]пирролидина (1,30 г) в виде бесцветных кристаллов. Ди-трет-бутилдикарбонат (1,15 мл) добавляли к раствору полученного таким образом гидрохлорида и триэтиламина (1,40 мл) в метиленхлориде (26 мл) и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали и остаток разбавляли этилацетатом, промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:9-1:1) с получением указанного в заголовке соединения (1,40 г).
1Н-ЯМР (CDCl3) δ: 1,47 (9Н, с), 3,12 (6Н, с), 3,70-3,73 (2Н, м), 3,79 (1Н, д, J=4,5Гц), 3,82 (1Н, д, J=4,5Гц), 5,19 (2Н, шир.).
[Ссылочный пример 192]
трет-Бутил (3R,4R)-3,4-диазидо-1-пирролидинкарбоксилат
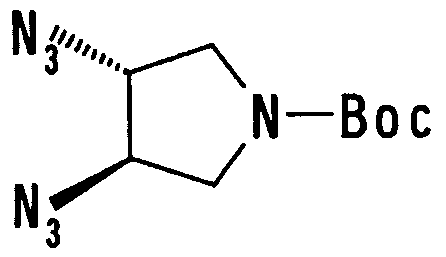
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 191, подобно способу ссылочного примера 170.
1Н-ЯМР (CDCl3) δ: 1,47 (9Н, с), 3,37-3,46 (2Н, м), 3,64-3,71 (2Н, м), 3,96 (2Н, т, J=3,2Гц).
[Ссылочный пример 193]
трет-Бутил (3R,4R)-3-амино-4-{[(5-хлориндол-2-ил)карбонил]амино}пирролидин-1-карбоксилат
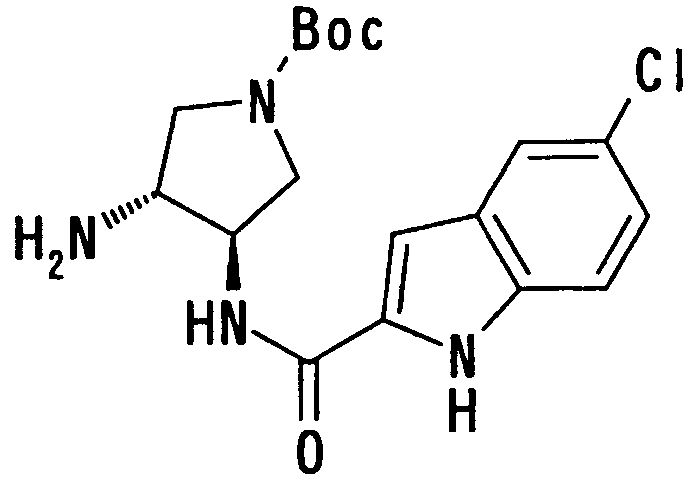
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 192, подобно способу ссылочных примеров 171 и 172.
1Н-ЯМР (ДМСО-d6) δ: 1,39 (9H, с), 2,95-3,00 (1H, м), 3,09-3,13 (1H, м), 3,52 (1H, дд, J=10, 6,5Гц), 3,68 (1H, дд, J=10, 7,8Гц), 4,04-4,09 (2H, м), 7,16 (1H, с), 7,18 (1H, с), 7,42 (1H, д, J=8,5Гц), 7,69 (1H, д, J=1,5Гц), 8,50 (1H, д, J=6,5Гц), 11,77 (1H, шир.).
[Ссылочный пример 194]
трет-Бутил (3S)-5-оксотетрагидро-3-фуранилкарбамат
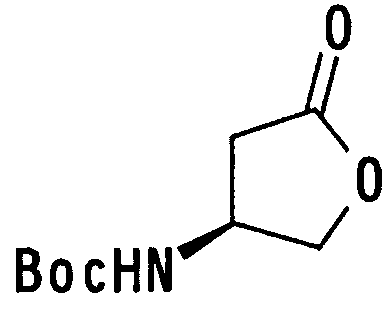
ди-трет-Бутилдикарбамат (4,1 г) и 10% палладий на углероде (0,4 г) добавляли к раствору бензил (3S)-(-)-тетрагидро-5-оксо-3-фуранилкарбамата (3,3 г) в тетрагидрофуране (20 мл) и смесь перемешивали в течение суток в атмосфере водорода. Отфильтровав через слой целита нерастворимое вещество, фильтрат концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1) с получением указанного в заголовке соединения (1,5 г).
1Н-ЯМР (CDCl3) δ: 1,45 (9Н, с), 2,45 (1Н, дд, J=17,8, 2,7Гц), 2,86 (1Н, дд, J=17,8, 7,3Гц), 4,12-4,23 (1Н, м), 4,54-4,62 (2Н, м), 4,85-4,95 (1Н, м).
[Ссылочный пример 195]
трет-Бутил (3S,4S)-4-азидо-5-оксотетрагидро-3-фуранилкарбамат
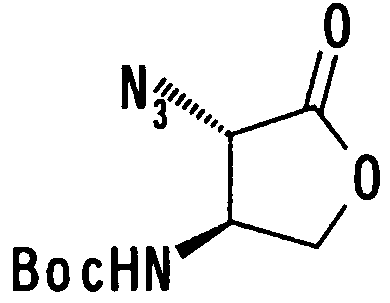
1М Бис(триметилсилил)амид лития (тетрагидрофурановый раствор, 8,65 мл) добавляли по каплям к раствору соединения (0,87 г), полученного в ссылочном примере 194, в тетрагидрофуране (20 мл) при -78°C и смесь перемешивали в течение 30 минут. Затем добавляли раствор п-толуолсульфонилазида (1,02 г) в тетрагидрофуране (10 мл) и смесь перемешивали в течение 5 минут, добавляли триметилхлорсилан (1,7 мл) и смесь перемешивали 2 часа, при постепенном повышении температуры системы до комнатной температуры. Реакционную смесь разбавляли диэтиловым эфиром, промывали 10% хлористоводородной кислотой, 5% насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1) с получением указанного в заголовке соединения (0,62 г).
1Н-ЯМР (CDCl3) δ: 1,46 (9Н, с), 4,09 (1Н, дт, J=15,3, 7,6Гц), 4,12-4,23 (1Н, м), 4,37-4,50 (1Н, м), 4,54 (1Н, дд, J=9,0, 7,6Гц), 4,81-4,90 (1Н, м).
[Ссылочный пример 196]
трет-Бутил (3S,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-5-оксотетрагидро-3-фуранилкарбамат
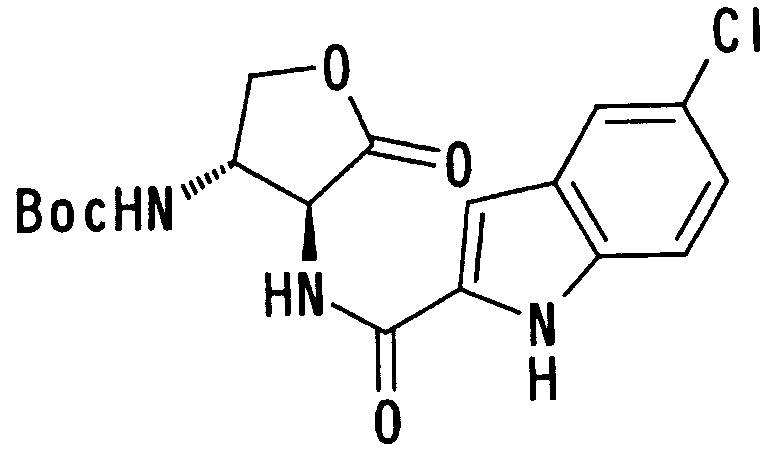
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 195, подобно способам ссылочных примеров 90 и 91.
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 4,01-4,13 (1H, м), 4,20-4,36 (1H, м), 4,78-4,93 (2H, м), 6,15 (1H, с), 6,93 (1H, с), 7,03-7,11 (1H, м), 7,20-7,28 (1H, м), 7,30 (1H, д, J=8,8Гц), 7,61 (1H, с), 9,27 (1H, с).
[Ссылочный пример 197]
трет-Бутил (3S,4S)-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}-5-оксотетрагидро-3-фуранилкарбамат
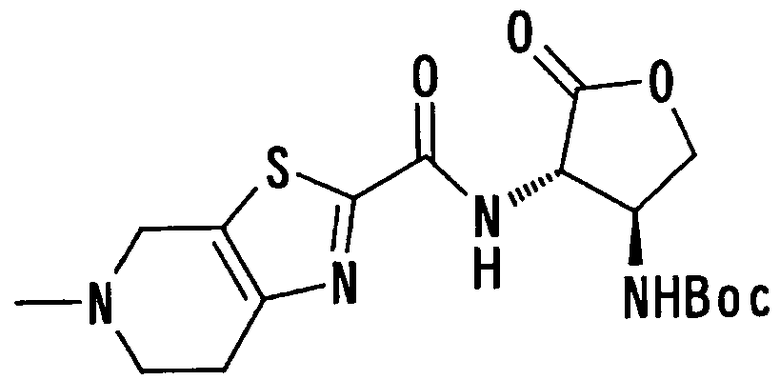
Указанное в заголовке соединение получали через трет-бутил (3S,4S)-4-амино-5-оксотетрагидро-3-фуранилкарбоксилат из соединения, полученного в ссылочном примере 195, подобно способу ссылочного примера 90, с последующим взаимодействием с соединением, полученным в ссылочном примере 10, в соответствии с условиями реакции ссылочного примера 91.
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 2,52 (3H, с), 2,83 (2H, т, J=5,9Гц), 2,79-3,02 (2H, м), 3,74 (2H, с), 4,03-5 4,12 (1H, м), 4,21-4,36 (1H, м), 4,80-4,95 (2H, м), 6,14-6,24 (1H, м), 7,76-7,85 (1H, м).
[Ссылочный пример 198]
Этил 2-[((3S)-3-[(трет-бутоксикарбонил)амино]2-{[(5-хлориндол-2-ил)карбонил]амино}-4-гидроксибутаноил)амино]ацетат
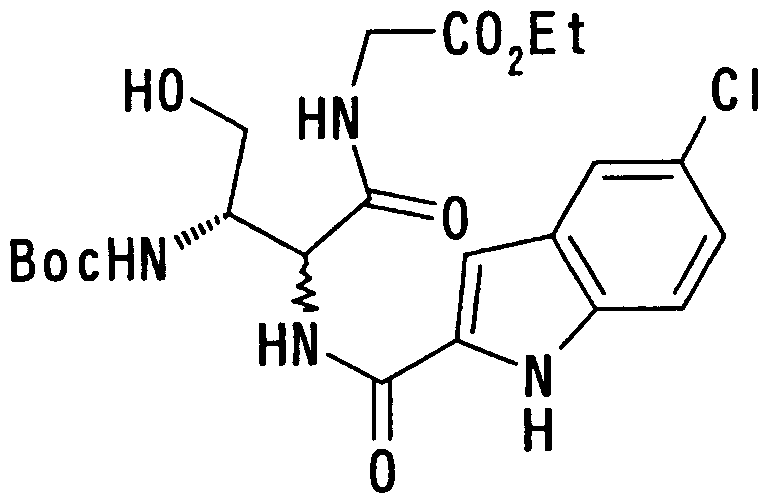
Соединение (0,4 г), полученное в ссылочном примере 196, гидрохлорид этилового эфира глицина (1,0 г) и триэтиламин (1,0 г) добавляли к этанолу (20 мл) и смесь нагревали и перемешивали при 60°C в течение 18 часов. Реакционную смесь разбавляли хлороформом и промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 98:2) с получением указанного в заголовке соединения (0,31 г).
1Н-ЯМР (ДМСО-d6) δ: 1,17 (3H, т, J=7,0Гц), 1,34 (6H, с), 1,36 (3H, с), 3,51-3,63 (0,6H, м), 3,72-3,80 (2H, м), 4,06 (2H, кв, J=7,0Гц), 4,11-4,23 (1,4H, м), 4,67-4,82 (1H, м), 4,85-4,91 (1H, м), 6,48 (0,4H, д, J=9,5Гц), 6,80 (0,6H, д, J=9,5Гц), 7,10-7,22 (2H, м), 7,42 (1H, д, J=8,8Гц), 7,72 (0,4H, д, J=2,0Гц), 7,73 (0,6H, д, J=2,0Гц), 8,23-8,31 (0,6H, м), 8,34-8,41 (0,4H, м), 8,43-8,50 (1H, м), 11,83 (1H, с).
[Ссылочный пример 199]
Гидрохлорид этил 2-((4R)-4-амино-3-{[(5-хлориндол-2-ил)карбонил]амино}-2-оксопирролидин-1-ил)ацетата
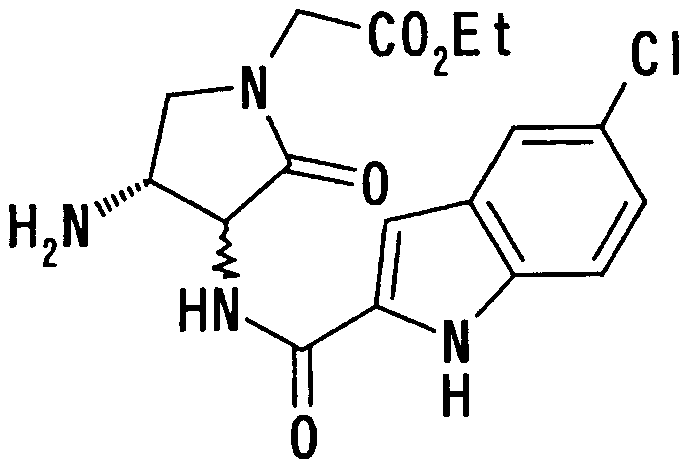
Указанное в заголовке соединение получали преобразованием соединения, полученного в ссылочном примере 198, в производное пирролидона в условиях реакции, описанных в ссылочном примере 181, и затем удалением трет-бутоксикарбонильной группы подобно способу ссылочного примера 69.
1Н-ЯМР (ДМСО-d6) δ: 1,17 (2H, т, J=7,0Гц), 1,23 (1H, т, J=7,0Гц), 3,31-3,40 (0,6H, м), 3,57 (0,4H, д, J=11,2Гц), 3,90-4,23 (4H, м), 4,42 (0,6H, дд, J=12,0, 6,1Гц), 4,50-4,60 (0,4H, м), 4,62 (0,6H, дд, J=12,0, 3,9Гц), 5,12-5,23 (0,4H, м), 7,17 (0,4H, с), 7,20 (0,4H, дд, J=8,8, 2,0Гц), 7,28 (0,6H, дд, J=8,8, 2,0Гц), 7,30 (0,6H, с), 7,44 (0,4H, д, J=8,8Гц), 7,50 (0,6H, д, J=8,8Гц), 7,75 (1H, д, J=2,0Гц), 8,20-8,33 (1H, м), 8,71-8,94 (3,6H, м), 9,22-9,35 (0,4H, м), 11,97 (0,4H, с), 12,44 (0,6H, с).
[Ссылочный пример 200]
трет-Бутил (3R,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-метил-5-оксопирролидин-3-илкарбамат
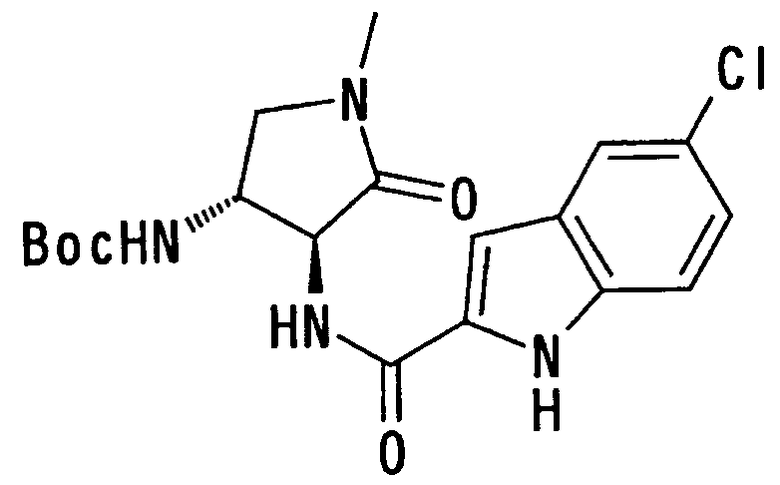
Указанное в заголовке соединение получали обработкой соединения, полученного взаимодействием соединения, полученного в ссылочном примере 196, с метиламином (40% метанольный раствор) подобно способу ссылочного примера 198, в таких же условиях, как в ссылочном примере 181.
1Н-ЯМР (CDCl3) δ: 1,43 (9Н, с), 2,90 (3Н, с), 4,26 (1Н, шир.с), 4,36 (2Н, м), 4,51-4,52 (1Н, м), 5,35 (1Н, шир.с), 6,95-6,99 (2Н, м), 7,22-7,32 (3Н, м), 7,63 (1Н, с), 8,95 (1Н, шир.с).
[Ссылочный пример 201]
N-[(3S,4R)-4-Амино-1-метил-2-оксопирролидин-3-ил]-5-хлориндол-2-карбоксамид
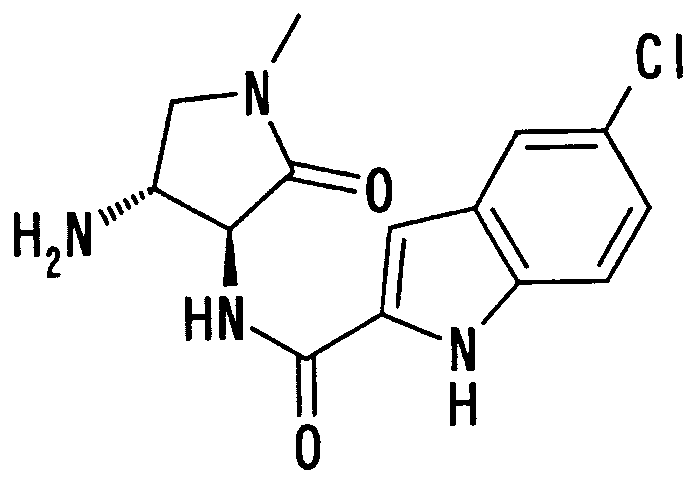
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 200, подобно способу ссылочного примера 69.
1Н-ЯМР (CDCl3) δ: 2,95 (3H, д, J=5,1Гц), 3,91-3,93 (1H, м), 4,19 (1H, д, J=3,7Гц), 4,36 (1H, дд, J=11, 1,7Гц), 4,48 (1H, дд, J=11, 2,0Гц), 6,90-6,97 (2H, м), 7,21-7,33 (2H, м), 7,62 (1H, д, J=2,0Гц), 8,90 (1H, с).
[Ссылочный пример 202]
трет-Бутил 3,6-дигидро-1(2Н)-пиридинкарбоксилат
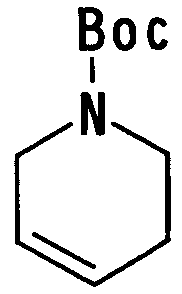
трет-Бутилдикарбонат (6,55 г) добавляли к смеси 1,2,3,6-тетрагидропиридина (2,50 г) и 10% водного раствора (3,0 мл) карбоната натрия и смесь перемешивали при комнатной температуре в течение 20 часов. К реакционной смеси добавляли воду и экстрагировали этилацетатом. Полученный органический слой промывали 0,5N хлористоводородной кислотой, водой, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия в указанном порядке и сушили над безводным сульфатом натрия. Затем отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (5,08 г).
1Н-ЯМР (CDCl3) δ: 1,47 (9Н, с), 2,12 (2Н, шир.с), 3,48 (2Н, т, J=5,6Гц), 3,88 (2Н, шир.с), 5,60 (1Н, шир.с), 5,78-5,90 (1Н, м).
[Ссылочный пример 203]
трет-Бутил (3R*,4S*)-3,4-дигидрокси-1-пиперидинкарбоксилат
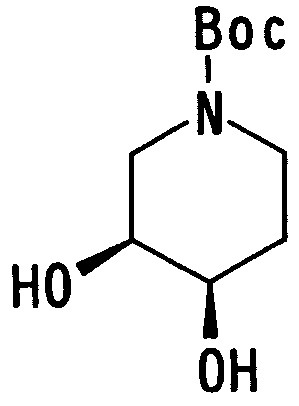
Соединение (18,45 г), полученное в ссылочном примере 202, растворяли в ацетонитриле (200 мл) и добавляли воду (38 мл), 0,039М водный раствор (82 мл) тетроксида осмия и N-оксид N-метилморфолина (23,13 г). Смесь перемешивали при комнатной температуре в течение 17 часов. Избыточный окисляющий агент обрабатывали насыщенным водным раствором сульфита натрия и экстрагировали этилацетатом. Полученный органический слой промывали водой, 0,5N хлористоводородной кислотой, водой, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия в указанном порядке, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 1:3) с получением указанного в заголовке соединения (15,0 г).
1Н-ЯМР (CDCl3) δ: 1,46 (9Н, с), 1,60-1,73 (1Н, м), 1,77-1,90 (1Н, м), 2,68 (2Н, шир.с), 2,80-3,20 (1Н, шир.), 3,22-3,32 (1Н, м), 3,42 (1Н, дд, J=14,3, 3,4Гц), 3,50-3,62 (2Н, м), 3,77 (1Н, шир.с), 3,81-3,92 (1Н, м).
[Ссылочный пример 204]
трет-Бутил (3R*,4S*)-3,4-бис[(метилсульфонил)окси]-1-пиперидинкарбоксилат
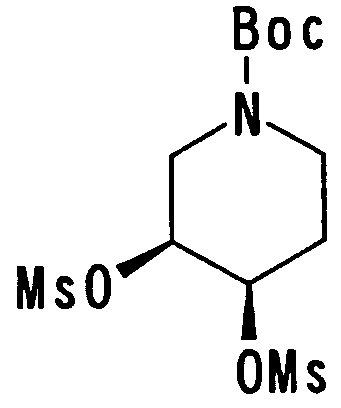
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 203, подобно способу ссылочного примера 169.
1Н-ЯМР (CDCl3) δ: 1,47 (9Н, с), 1,85-1,97 (1Н, м), 2,08-2,20 (1Н, м), 3,00-4,20 (4Н, м), 3,12 (6Н, с), 4,85 (1Н, шир.с), 4,94 (1Н, шир.с).
[Ссылочный пример 205]
трет-Бутил (3R*,4S*)-3,4-диазидо-1-пиперидинкарбоксилат
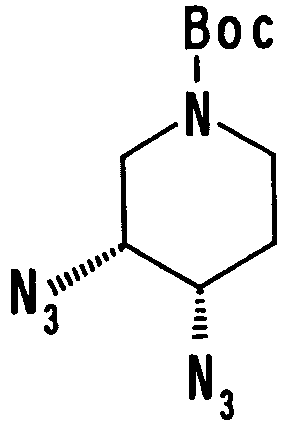
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 204, подобно способу ссылочного примера 170.
1Н-ЯМР (CDCl3) δ: 1,47 (9Н, с), 1,70-1,80 (1Н, м), 1,90-2,00 (1Н, м), 3,05-4,00 (6Н, м).
[Ссылочный пример 206]
трет-Бутил (3R*,4S*)-3,4-диамино-1-пиперидинкарбоксилат
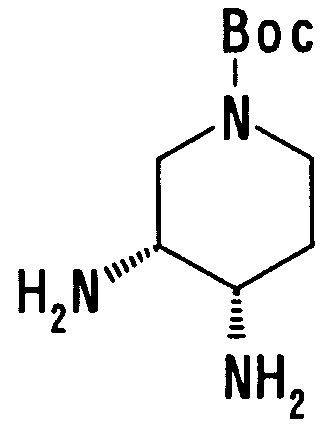
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 205, подобно способу ссылочного примера 171.
1Н-ЯМР (CDCl3) δ: 1,46 (9Н, с), 1,48-1,60 (2Н, м), 1,80-2,10 (4Н, шир.), 2,85-2,91 (2Н, м), 2,97 (1Н, шир.с), 3,09 (1Н, дд, J=13,6, 2,7Гц), 3,74 (1Н, дд, J=13,6, 4,2Гц), 3,81 (1Н, с).
[Ссылочный пример 207]
трет-Бутил (3R*,4S*)-3-амино-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-пиперидинкарбоксилат
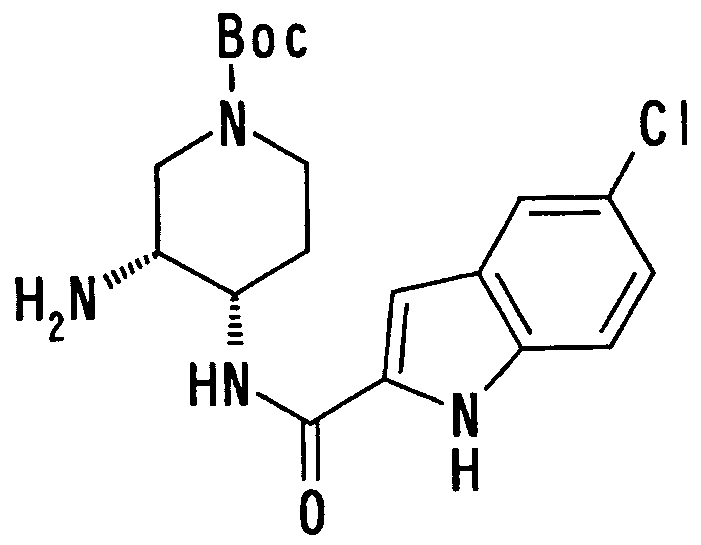
Соединение (3,23 г), полученное в ссылочном примере 206, растворяли в N,N-диметилформамиде (100 мл) и к раствору добавляли триэтиламин (2,08 мл) и соединение (3,80 г), полученное в ссылочном примере 52. Смесь перемешивали при комнатной температуре в течение 3 дней. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли воду и экстрагировали метиленхлоридом. Полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1-10:1) с получением указанного в заголовке соединения (2,70 г).
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,58 (3H, м), 1,41 (9H, с), 1,75-1,90 (1H, м), 2,95 (1H, шир.с), 2,98-3,05 (1H, м), 3,19-3,28 (1H, м), 3,74 (1H, дд, J=19,5, 15,4Гц), 3,79 (1H, шир.с), 4,04-4,12 (1H, м), 7,17 (1H, дд, J=8,7, 1,9Гц), 7,21 (1H, с), 7,42 (1H, д, J=8,7Гц), 7,68 (1H, д, J=1,9Гц), 8,00 (1H, шир.д, J=7,6Гц), 11,80 (1H, с).
[Ссылочный пример 208]
трет-Бутил (3R*,4S*)-3-амино-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}-1-пиперидинкарбоксилат
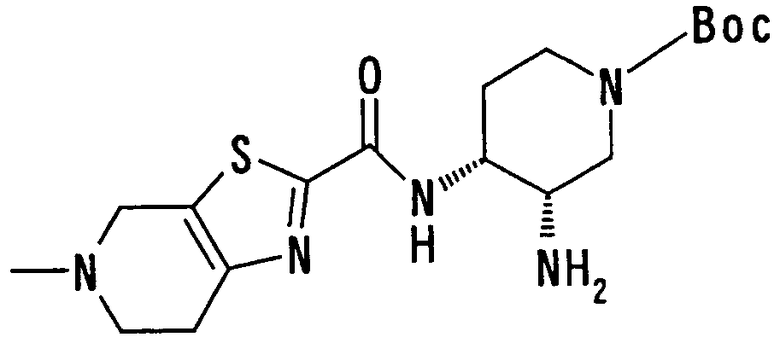
Соединение (3,23 г), полученное в ссылочном примере 206, растворяли в N,N-диметилформамиде (100 мл) и к раствору добавляли триэтиламин (2,08 мл). Затем добавляли соединение (3,83 г), полученное в ссылочном примере 149, и смесь перемешивали при комнатной температуре в течение 3 дней. Реакционную смесь концентрировали при пониженном давлении, к остатку добавляли воду и экстрагировали метиленхлоридом. Полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 10:1-5:1) с получением указанного в заголовке соединения (2,27 г).
1Н-ЯМР (CDCl3) δ: 1,30-1,62 (3H, м), 1,47 (9H, с), 1,78-1,88 (1H, м), 2,51 (3H, с), 2,81 (2H, т, J=5,9Гц), 2,85-2,98 (3H, м), 3,00-3,15 (2H, м), 3,71 (2H, с), 3,80-4,15 (3H, м), 7,79 (1H, шир.с).
[Ссылочный пример 209]
трет-Бутил (3R*,4S*)-3-амино-4-{[(5-фториндол-2-ил)карбонил]амино}-1-пиперидинкарбоксилат
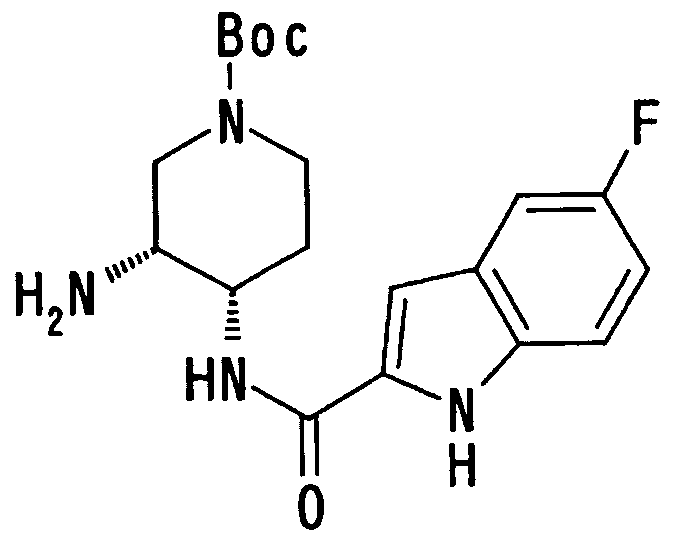
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 206, и 5-фториндол-2-карбоновой кислоты подобно способу ссылочного примера 172.
1Н-ЯМР (CDCl3) δ: 1,40-1,70 (3H, м), 1,48 (9H, с), 2,79-2,92 (1H, м), 2,99-3,14 (1H, м), 4,00-4,23 (3H, м), 6,85 (1H, с), 7,04 (1H, тд, J=9,0, 2,4Гц), 7,07-7,20 (1H, шир.), 7,27 (1H, дд, J=9,0, 2,4Гц), 7,35 (1H, д, J=9,0, 4,4Гц), 9,25-9,50 (1H, шир.).
МС (ESI)m/z: 377 (M+H)+.
[Ссылочный пример 210]
Этил (3R,4R)-5-азидо-3-{[(бензилокси)карбонил]амино}-4-[(трет-бутоксикарбонил)амино]валерат
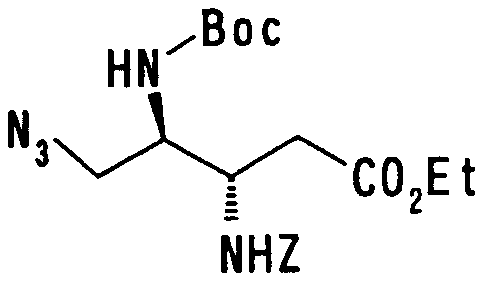
Триэтиламин (4,80 мл) и метансульфонилхлорид (1,55 мл) последовательно добавляли по каплям к раствору (3S,4S)-соединения, полученного в ссылочном примере 168 (низкополярное соединение) (7,1 г), в метиленхлориде (100 мл) при охлаждении льдом и смесь перемешивали 30 минут при охлаждении льдом. Реакционную смесь разбавляли хлороформом и промывали 10% водным раствором лимонной кислоты, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель с получением метансульфонильного производного (9,20 г). Смешанный раствор, состоящий из полученного метансульфонильного производного, азида натрия (5,64 г) и N,N-диметилформамида (100 мл), перемешивали при 80°C в течение 20 часов. Реакционную смесь разбавляли этилацетатом и промывали водой и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и полученный остаток очищали колоночной хроматографией на силикагеле (хлороформом) с получением указанного в заголовке соединения (5,42 г).
1Н-ЯМР (CDCl3) δ: 1,24 (3H, т, J=7,1Гц), 1,43 (9H, с), 2,56-2,68 (2H, м), 3,48-3,60 (2H, м), 3,88-3,97 (1H, м), 4,04-4,20 (3H, м), 4,88-4,97 (1H, шир.), 5,10 (2H, с), 5,60-5,75 (1H, шир.), 7,30-7,40 (5H, м).
МС (ESI) m/z: 436 (М+Н)+.
[Ссылочный пример 211]
Бензил (4S,5R)-5-[(трет-бутоксикарбонил)амино]-2-оксопиперидин-4-илкарбамат
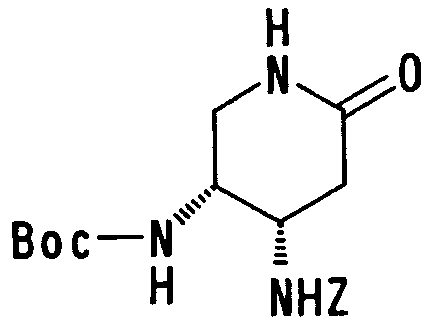
Катализатор Линдлара (2,71 г) добавляли к раствору соединения (5,42 г), полученного в ссылочном примере 210, в смешанном растворителе из этанола (150 мл) и тетрагидрофурана (10,0 мл) и смесь перемешивали 3 часа в атмосфере водорода и затем 14 часов в атмосфере азота. Нерастворимое вещество удаляли фильтрованием через слой целита и фильтрат концентрировали при пониженном давлении, затем полученный остаток растворяли в тетрагидрофуране (30 мл) и к раствору добавляли триэтиламин (3,0 мл). Смесь перемешивали при комнатной температуре в течение 1,5 часов. Реакционную смесь разбавляли этилацетатом и промывали 10% водным раствором лимонной кислоты, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 25:1) с получением указанного в заголовке соединения (2,50 г).
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 2,30-2,50 (1H, шир.), 2,65-2,90 (1H, шир.), 3,15-3,30 (1H, шир.), 3,35-3,65 (1H, шир.), 4,00-4,25 (2H, шир.), 5,11 (2H, с), 5,55-5,60 (1H, шир.), 5,65-5,90 (1H, шир.), 6,25-6,55 (1H, шир.), 7,28-7,40 (5H, м).
МС (ESI) m/z: 364 (М+Н)+.
[Ссылочный пример 212]
Бензил (3R,4S)-3-[(трет-бутоксикарбонил)амино]пиперидин-4-илкарбамат
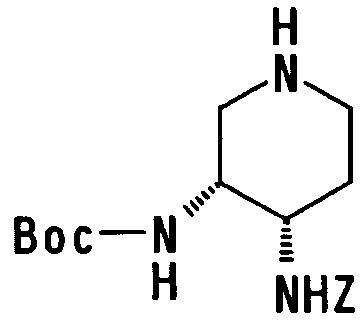
1М Боран-тетрагидрофурановый комплекс (тетрагидрофурановый раствор, 34,0 мл) добавляли по каплям к тетрагидрофурановому раствору (70 мкл) соединения (2,49 г), полученного в ссылочном примере 211, при охлаждении льдом и смесь перемешивали 20 часов при постепенном повышении температуры системы до комнатной температуры. Метанол (100 мл) добавляли к реакционной смеси и отгоняли при пониженном давлении растворитель. К остатку добавляли этанол (45 мл), воду (5 мл) и триэтиламин (10 мл) и смесь кипятили с обратным холодильником в течение 24 часов. Реакционную смесь концентрировали и полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол:вода = 7:3:1, нижний слой) с получением указанного в заголовке соединения (1,61 г).
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 1,65-1,72 (2H, м), 2,67 (1H, т, J=12,0Гц), 2,82 (12H, д, J=12,0Гц), 2,90-3,10 (1H, шир.), 3,60-3,80 (2H, м), 3,90-4,00 (1H, м), 5,00-5,20 (2H, м), 5,40-5,60 (2H, шир.), 7,25-7,74 (5H, м).
МС (FAB) m/z: 350 (М+Н)+.
[Ссылочный пример 213]
трет-Бутил (3R,4S)-1-ацетил-4-{[(бензилокси)карбонил]амино}пиперидин-3-илкарбамат
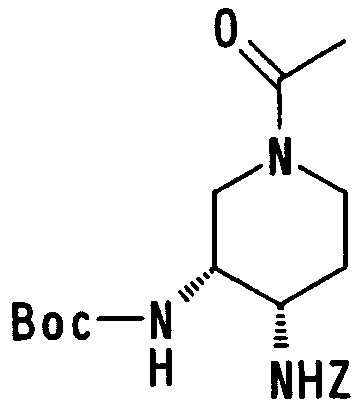
Указанное в заголовке соединение получали взаимодействием соединения, полученного в ссылочном примере 212, с ацетилхлоридом и триэтиламином в метиленхлориде.
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 1,85-2,15 (2H, м), 2,07 (1,5H, с), 2,14 (1,5H, с), 2,75-2,90 (1H, м), 3,10-3,20 (0,5H, м), 3,25-3,35 (0,5H, шир.д, J=14,2Гц), 3,65-4,05 (3H, м), 4,38-4,47 (0,5H, шир.д, J=13,0Гц), 4,54-4,63 (0,5H, м), 4,69-4,83 (1H, шир.), 4,98-5,20 (2,5H, м), 5,90-6,05 (0,5H, шир.), 7,30-7,40 (5H, м).
МС (ESI) m/z: 392 (М+Н)+.
[Ссылочный пример 214]
трет-Бутил (3R,4S)-1-ацетил-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-илкарбамат
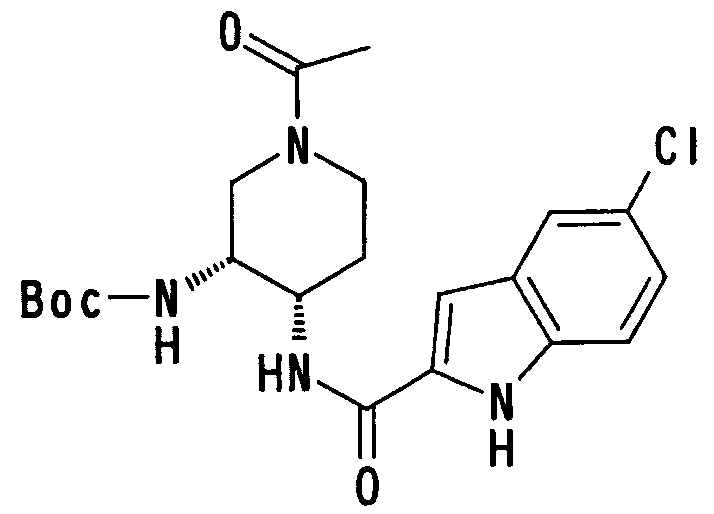
10% Палладий на углероде (532 мг) добавляли к раствору соединения (745 мг), полученного в ссылочном примере 213, в этаноле (50 мл) и смесь перемешивали при комнатной температуре в течение 16 часов в атмосфере водорода. Нерастворимое вещество удаляли фильтрованием через целит и затем фильтрат концентрировали при пониженном давлении. Полученный остаток обрабатывали 5-хлориндол-2-карбоновой кислотой (467 мг) подобно способу ссылочного примера 68 с получением указанного в заголовке соединения (650 мг).
1Н-ЯМР (CDCl3) δ: 1,52 (9H, с), 1,60-1,80 (2H, м), 2,12 (1H, с), 2,16 (2H, с), 2,30-2,45 (0,5H, м), 2,67-2,82 (0,3H, м), 2,89 (0,7H, д, J=13,7Гц), 3,23 (0,7H, т, J=12,9Гц), 3,37 (0,3H, д, J=13,7Гц), 3,81-3,95 (1H, м), 4,05-4,33 (2H, м), 4,62-4,72 (0,3H, шир.), 4,77 (0,7H, д, J=13,7Гц), 5,10-5,27 (1H, м), 6,81 (0,3H, шир.с), 6,85 (0,7H, с), 7,21 (1H, шир.д, J=8,8Гц), 7,34 (1H, д, J=8,8Гц), 7,57 (0,3H, шир.с), 7,61 (0,7H, с), 8,55-8,65 (0,5H, шир.), 9,43-9,53 (0,7H, шир.), 9,60-9,70 (0,3H, шир.).
МС (ESI) m/z: 435 (М+Н)+.
[Ссылочный пример 215]
Этил (3R,4R)-5-азидо-3-{[(бензилокси)карбонил]амино}-4-[(трет-бутоксикарбонил)амино]валерат
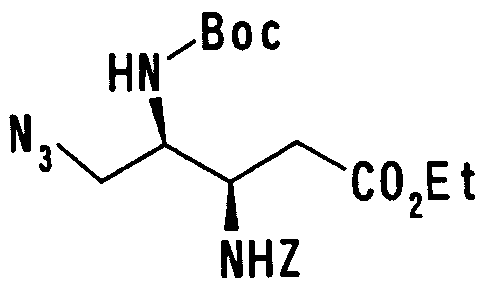
Указанное в заголовке соединение получали из (3R,4S)-соединения (высокополярное соединение), полученного в ссылочном примере 168, подобно способу ссылочного примера 210.
1Н-ЯМР (CDCl3) δ: 1,23 (3H, т, J=6,6Гц), 1,42 (9H, с), 2,51-2,63 (2H, м), 3,43-3,50 (2H, м), 3,84-3,92 (1H, м), 4,03-4,23 (3H, м), 5,10 (2H, с), 5,11-5,24 (1H, м), 5,54-5,60 (1H, м), 7,32-7,44 (5H, м).
[Ссылочный пример 216]
Бензил (4R,5R)-5-[(трет-бутоксикарбонил)амино]-2-оксопиперидин-4-илкарбамат
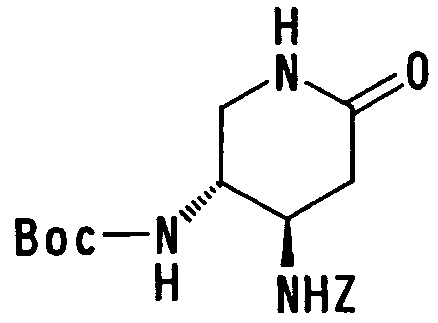
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 215, подобно способу ссылочного примера 211.
1Н-ЯМР (ДМСО-d6) δ: 1,35 (9H, с), 2,19 (1H, дд, J=17,4, 9,1Гц), 2,41-2,51 (1H, м), 2,97 (1H, т, J=9,1Гц), 3,00-3,11 (1H, м), 3,51-3,64 (1H, м), 3,67-3,73 (1H, м), 5,00 (2H, с), 6,71-6,80 (1H, м), 7,20-7,30 (5H, м), 7,44-7,52 (1H, м), 8,30 (1H, с).
[Ссылочный пример 217]
Бензил (3R,4R)-3-[(трет-бутоксикарбонил)амино]пиперидин-4-илкарбамат
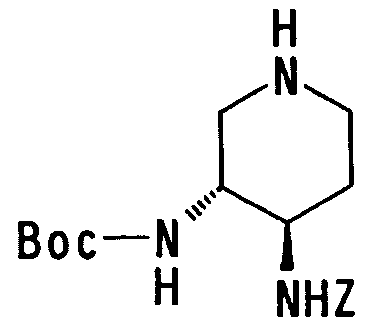
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 216, подобно способу ссылочного примера 212.
1Н-ЯМР (CDCl3) δ: 1,39 (9H, с), 2,05 (2H, д, J=12,9Гц), 2,40 (1H, т, J=11,0Гц), 2,63 (1H, т, J=12,0Гц), 3,09 (1H, д, J=12,0Гц), 3,31 (1H, д, J=11,0Гц), 3,42-3,53 (2H, м), 4,80-4,91 (1H, м), 5,09 (2H, с), 5,23-5,32 (1H, м), 7,34-7,41 (5H, м).
[Ссылочный пример 218]
трет-Бутил (3R,4R)-1-ацетил-4-{[(бензилокси)карбонил]амино}пиперидин-3-илкарбамат
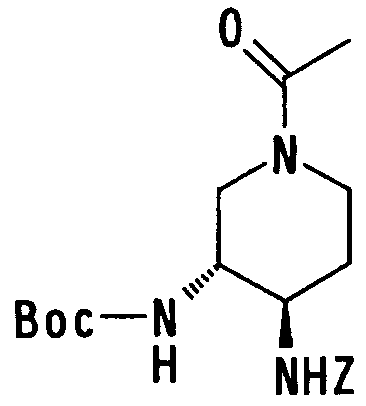
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 217, подобно способу ссылочного примера 213.
1Н-ЯМР (CDCl3) δ: 1,42 (9H, с), 1,53-1,67 (1H, м), 1,89-2,00 (1H, м), 2,09 (1,5H, с), 2,15 (1,5H, с), 2,57 (1H, т, J=12,0Гц), 2,78 (1H, т, J=12,0Гц), 3,20-3,30 (1H, м), 3,40-3,56 (2H, м), 4,23-4,31 (1H, м), 4,45-4,56 (1H, м), 5,01-5,08 (1H, м), 5,10 (2H, с), 7,32-7,44 (5H, м).
[Ссылочный пример 219]
трет-Бутил (3R,4R)-1-ацетил-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-илкарбамат
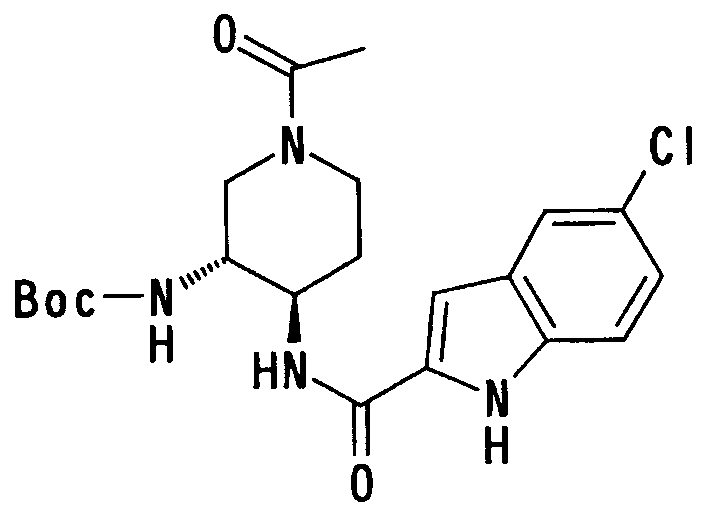
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 218, подобно способу ссылочного примера 214.
1Н-ЯМР (CDCl3) δ: 1,35 (9H, с), 1,42-1,56 (2H, м), 2,00-2,10 (1H, м), 2,12 (1,5H, с), 2,17 (1,5H, с), 2,31-2,43 (1H, м), 2,67-3,00 (1H, м), 3,55-3,63 (1H, м), 3,78-4,00 (1H, м), 4,03-4,21 (1H, м), 4,78-5,24 (2H, м), 6,91 (0,5H, с), 6,92 (0,5H, с), 7,22-7,32 (1H, м), 7,33 (1H, д, J=8,8Гц), 7,58 (1H, с), 9,45 (0,5H, с), 9,51 (0,5H, с).
[Ссылочный пример 220]
Бензил (3R,4S)-3-[(трет-бутоксикарбонил)амино]-1-(2-метоксиацетил)пиперидин-4-илкарбамат
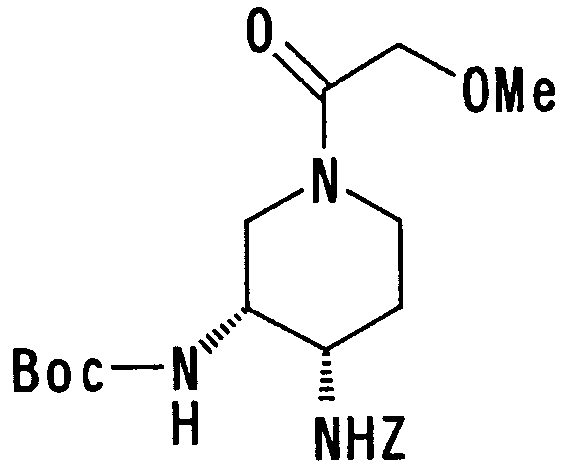
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 212, и метоксиацетилхлорида подобно способу ссылочного примера 213.
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 1,70-2,15 (2H, м), 2,70-2,85 (1H, м), 2,90-3,30 (1H, м), 3,35-3,70 (1H, м), 3,43 (3H, с), 3,75-3,90 (2H, м), 3,90-4,25 (3H, м), 4,40-4,80 (1H, м), 5,05-5,09 (1H, м), 5,10 (2H, шир.с), 7,30-7,40 (5H, м).
МС (ESI) m/z: 322 (М+Н+).
[Ссылочный пример 221]
трет-Бутил (3R,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-илкарбамат
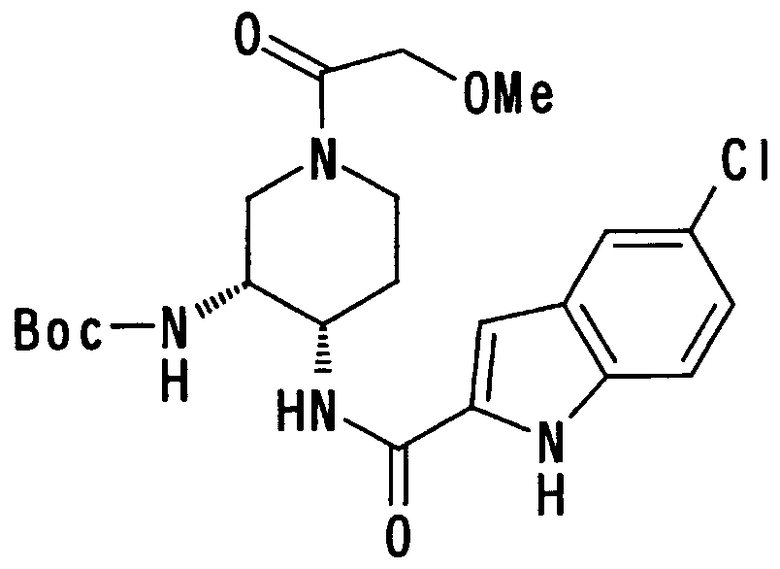
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 220, подобно способу ссылочного примера 214.
1Н-ЯМР (CDCl3) δ: 1,52 (9H, с), 1,60-1,80 (1H, м), 2,20-2,40 (1H, м), 2,70-2,80 (0,6H, м), 2,90-3,00 (0,4H, м), 3,15-3,30 (0,4H, м), 3,32-3,40 (0,6H, м), 3,46, 3,49 (всего 3H, каждый с), 3,85-4,30 (5H, м), 4,55-4,80 (1H, м), 5,11 (0,4H, шир.с), 6,05 (0,6H, шир.с), 6,86 (1H, с), 7,20 (1H, дд, J=8,7, 2,0Гц), 7,33 (1H, д, J=8,7Гц), 7,61 (1H, с), 8,40-8,60 (1H, м), 9,41 (1H, шир.с).
МС (FAB) m/z: 465 (М+Н)+.
[Ссылочный пример 222]
Бензил (3R,4R)-3-[(трет-бутоксикарбонил)амино]-1-(2-метоксиацетил)пиперидин-4-илкарбамат
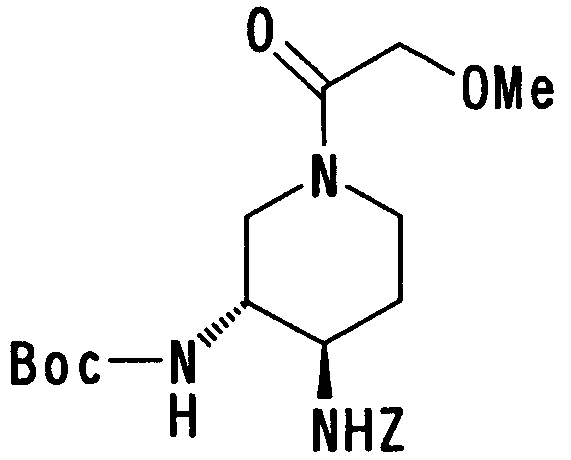
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 217, и метоксиацетилхлорида подобно способу ссылочного примера 213.
1Н-ЯМР (CDCl3) δ: 1,41 (9H, с), 1,45-1,67 (1H, м), 2,01-2,14 (1H, м), 2,63 (1H, т, J=12,0Гц), 2,75 (1H, т, J=12,0Гц), 3,20-3,30 (1H, м), 3,32-3,41 (5H, м), 3,44-3,56 (2H, м), 4,21-4,32 (1H, м), 4,50-4,63 (1H, м), 5,03-5,08 (1H, м), 5,09 (2H, с), 7,32-7,40 (5H, м).
[Ссылочный пример 223]
трет-Бутил (3R,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-илкарбамат
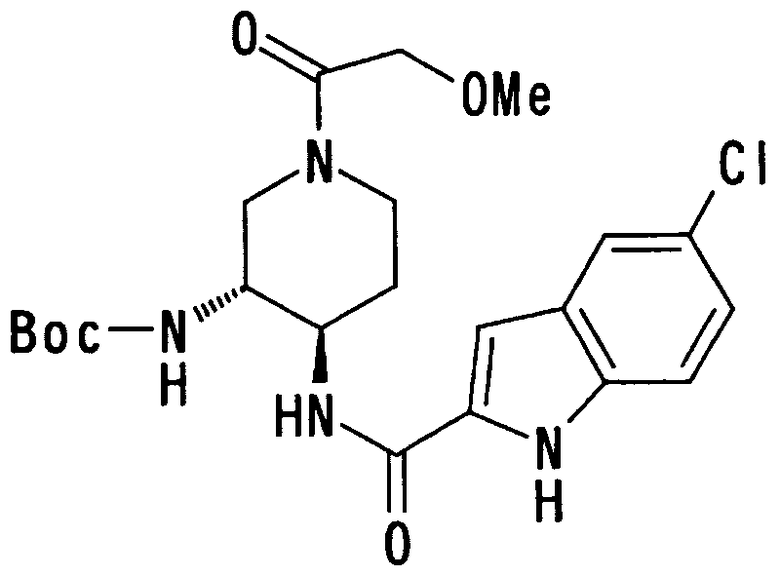
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 222, и 5-хлориндол-2-карбоновой кислоты подобно способу ссылочного примера 214.
1Н-ЯМР (CDCl3) δ: 1,35 (9H, с), 1,41-1,56 (2H, м), 2,11-2,23 (0,5H, м), 2,34-2,50 (0,5H, м), 2,78-2,89 (0,5H, м), 3,01-3,12 (0,5H, м), 3,42 (5H, с), 3,45-3,56 (1H, м), 3,78-3,89 (1H, м), 4,00-4,21 (2H, м), 4,78-5,21 (2H, м), 6,91 (0,5H, с), 6,93 (0,5H, с), 7,23 (1H, дд, J=8,8, 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,59 (1H, с), 9,37 (0,5H, с), 9,54 (0,5H, с).
[Ссылочный пример 224]
Этил (3R,4S)-3-{[(бензилокси)карбонил]амино}-4-[(трет-бутоксикарбонил)амино]-5-{[трет-бутил(дифенил)силил]окси}валерат
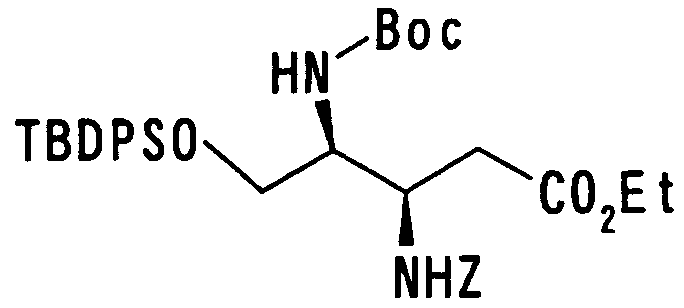
Триэтиламин (0,47 мл), имидазол (0,19 г) и трет-бутилхлордифенилсилан (0,7 мл) последовательно добавляли к раствору (3R,4S)-соединения (высокополярное соединение) (0,74 г), полученного в ссылочном примере 168, в N,N-диметилформамиде (30 мл) при охлаждении льдом и смесь перемешивали 4 суток при постепенном повышении температуры системы до комнатной температуры. Реакционную смесь разбавляли этилацетатом и промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 8:1) с получением указанного в заголовке соединения (0,85 г).
1Н-ЯМР (CDCl3) δ: 1,07 (9H, с), 1,19 (3H, т, J=7,4Гц), 1,40 (9H, с), 2,40-2,50 (1H, м), 2,60 (1H, дд, J=15,9, 4,5Гц), 3,56-3,67 (1H, м), 3,74 (1H, дд, J=11,2, 4,5Гц), 3,78-3,89 (1H, м), 4,08 (2H, кв, J=7,4Гц), 4,21-4,30 (1H, м), 4,99-5,13 (3H, м), 5,41-5,52 (1H, м), 7,40-7,53 (6H, м), 7,60-7,72 (4H, м).
[Ссылочный пример 225]
Этил (3R,4S)-4-[(трет-бутоксикарбонил)амино]-5-{[трет-бутил(дифенил)силил]окси}-3-{[(5-хлориндол-2-ил)карбонил]амино}валерат
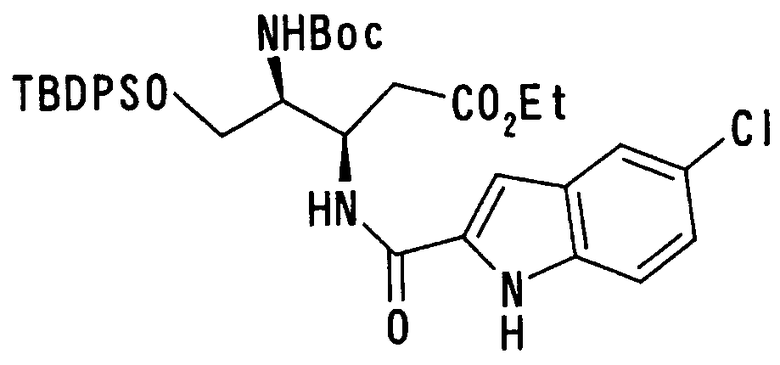
Указанное в заголовке соединение получали удалением бензилоксикарбонильной группы соединения, полученного в ссылочном примере 224, и конденсацией с 5-хлориндол-2-карбоновой кислотой подобно способу ссылочного примера 214.
1Н-ЯМР (CDCl3) δ: 1,10 (9H, с), 1,20 (3H, т, J=7,4Гц), 1,32 (9H, с), 2,40-2,52 (1H, м), 2,71 (1H, дд, J=15,9, 4,5Гц), 3,67-3,81 (2H, м), 4,00-4,20 (2H, м), 4,56-4,74 (1H, м), 5,00-5,11 (1H, м), 6,81 (1H, с), 7,21 (1H, дд, J=8,8, 2,0Гц), 7,32 (1H, д, J=8,8Гц), 7,40-7,50 (6H, м), 7,58 (1H, д, J=8,5Гц), 7,63-7,74 (5H, м), 9,01-9,14 (1H, м).
[Ссылочный пример 226]
трет-Бутил (3R*,4R*)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-4-илкарбамат
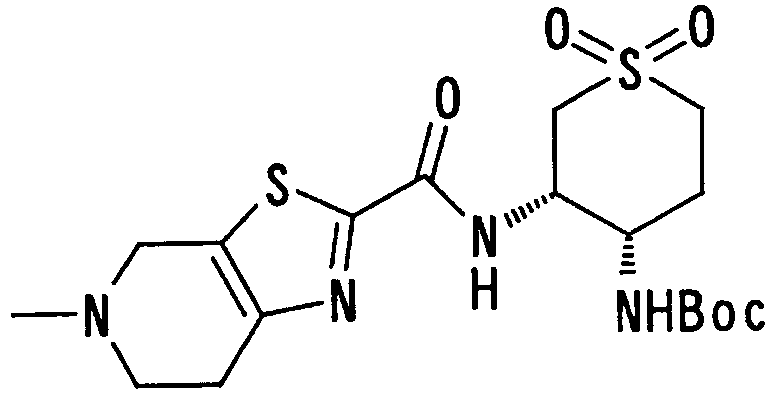
Указанное в заголовке соединение получали из (3R*,4R*)-соединения (низкополярное соединение), полученного в ссылочном примере 179, и соединения, полученного в ссылочном примере 10, подобно способу ссылочного примера 68.
1Н-ЯМР (CDCl3) δ: 1,43 (9H, с), 2,30-2,37 (2H, м), 2,51 (3H, с), 2,82-2,85 (2H, м), 2,92-2,95 (2H, м), 3,17-3,20 (4H, м), 3,40-3,43 (1H, м), 3,69-3,77 (2H, м), 3,97-3,98 (1H, м), 4,98 (1H, шир.), 5,25 (1H, шир.).
[Ссылочный пример 227]
Гидрохлорид N-[(3R*,4R*)-4-амино-1,1-диоксогексагидро-1-тиопиран-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
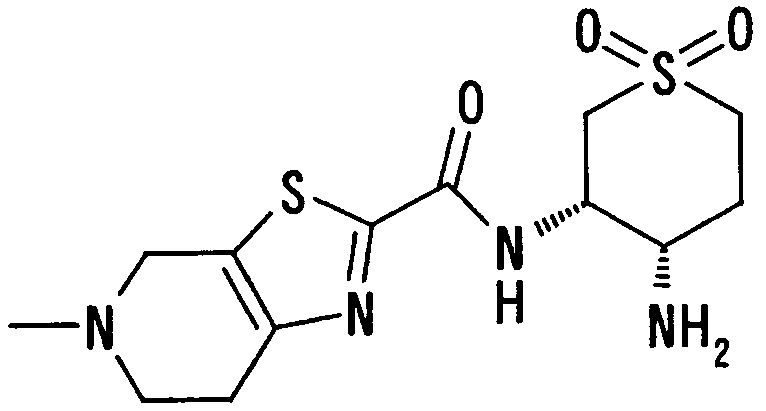
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 226, подобно способу ссылочного примера 69.
1Н-ЯМР (ДМСО-d6) δ: 2,29-2,33 (2H, м), 2,93 (3H, с), 3,16 (2H, шир.), 3,40 (2H, шир.), 3,52 (2H, шир.), 3,69-3,76 (3H, м), 4,48 (1H, шир.), 4,71-4,82 (2H, м), 8,34 (2H, шир.), 8,82 (1H, шир.).
МС (ESI) m/z: 345 (M+H)+.
[Ссылочный пример 228]
трет-Бутил (3R*,4R*)-3-{[(5-хлориндол-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-4-илкарбамат
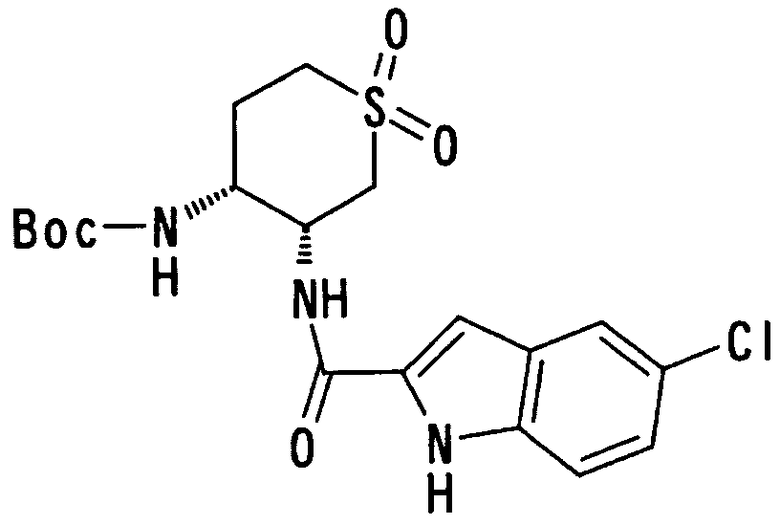
Указанное в заголовке соединение получали из (3R*,4R*)-соединения (низкополярное соединение), полученного в ссылочном примере 179, и 5-хлориндол-2-карбоновой кислоты подобно способу ссылочного примера 68.
1Н-ЯМР (ДМСО-d6) δ: 1,34 (9H, с), 2,09 (2H, шир.), 3,07 (1H, д, J=12,6Гц), 3,24-3,28 (1H, м), 3,48 (2H, шир.), 4,12 (1H, шир.), 4,53 (1H, шир.), 7,04 (1H, с), 7,16-7,1,8 (2H, м), 7,44 (1H, д, J=8,7Гц), 7,67 (1H, с), 8,37 (1H, шир.), 11,81 (1H, с).
МС (ESI) m/z: 442 (M+H)+.
[Ссылочный пример 229]
Гидрохлорид N-[(3R*,4R*)-4-амино-1,1-диоксогексагидро-1-тиопиран-3-ил]-5-хлориндол-2-карбоксамида
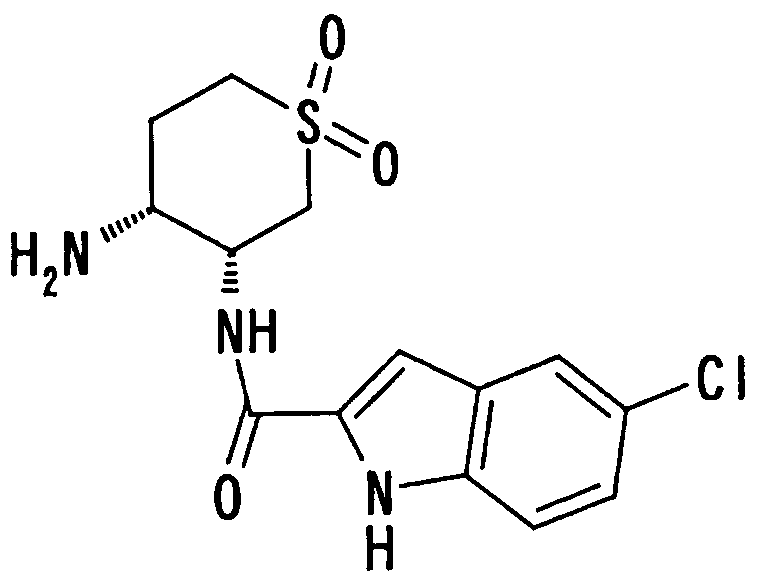
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 228, подобно способу ссылочного примера 69.
1Н-ЯМР (ДМСО-d6) δ: 2,24-2,33 (2H, м), 3,43-3,55 (3H, м), 3,60-3,66 (1H, м), 3,77 (1H, шир.), 4,75-4,79 (1H, м), 7,18-7,21 (2H, м), 7,46 (1H, д, J=8,8Гц), 7,72 (1H, д, J=1,7Гц), 8,39 (2H, шир.), 8,58 (1H, д, J=6,8Гц), 11,93 (1H, с).
МС (ESI) m/z: 342 (М+Н)+.
[Ссылочный пример 230]
трет-Бутил (3R*,4S*)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-4-илкарбамат
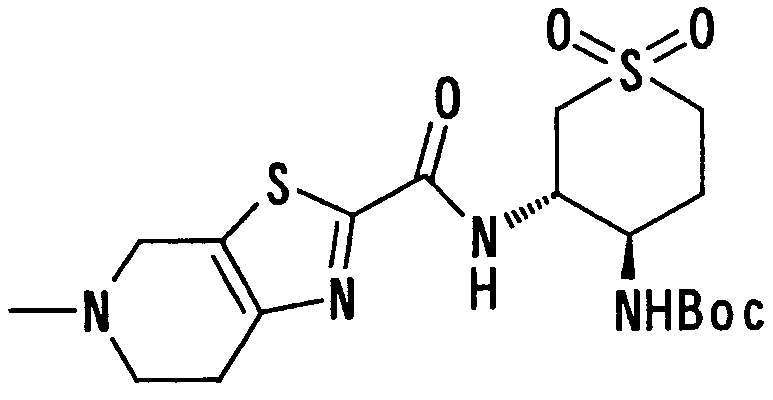
Указанное в заголовке соединение получали из (3R*,4S*)-соединения (высокополярное соединение), полученного в ссылочном примере 179, и соединения, полученного в ссылочном примере 10, подобно способу ссылочного примера 98.
1Н-ЯМР (CDCl3) δ: 1,32 (9H, с), 2,14-2,24 (1H, м), 2,33-2,38 (1H, м), 2,50 (3H, с), 2,78-2,83 (2H, м), 2,86-2,95 (2H, м), 3,08-3,14 (3H, м), 3,55 (1H, д, J=13,4Гц), 3,68 (1H, д, J=15,5Гц), 3,72 (1H, д, J=15,5Гц), 3,86-3,88 (1H, м), 4,45-4,53 (1H, м), 4,75 (1H, д, J=8,5Гц), 7,76 (1H, д, J=8,3Гц).
МС (ESI) m/z: 445 (М+Н)+.
[Ссылочный пример 231]
Гидрохлорид N-[(3R*,4S*)-4-амино-1,1-диоксогексагидро-1-тиопиран-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
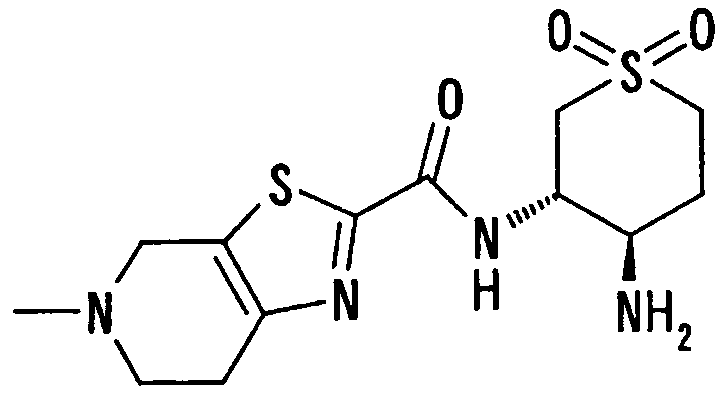
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 230, подобно способу ссылочного примера 69.
1Н-ЯМР (ДМСО-d6) δ: 2,03-2,12 (1H, м), 2,51 (1H, шир.), 2,93 (3H, с), 3,14 (2H, д, J=12,2Гц), 3,28 (2H, шир.), 3,33 (2H, шир.), 3,48 (3H, шир.), 3,72 (2H, шир.), 4,49 (2H, шир.), 4,71-4,7,4 (1H, м), 8,38 (2H, шир.), 9,21-9,24 (1H, м).
МС (ESI) m/z: 345 (M+H)+.
[Ссылочный пример 232]
трет-Бутил (3R*,4R*)-3-{[(5-фториндол-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-4-илкарбамат
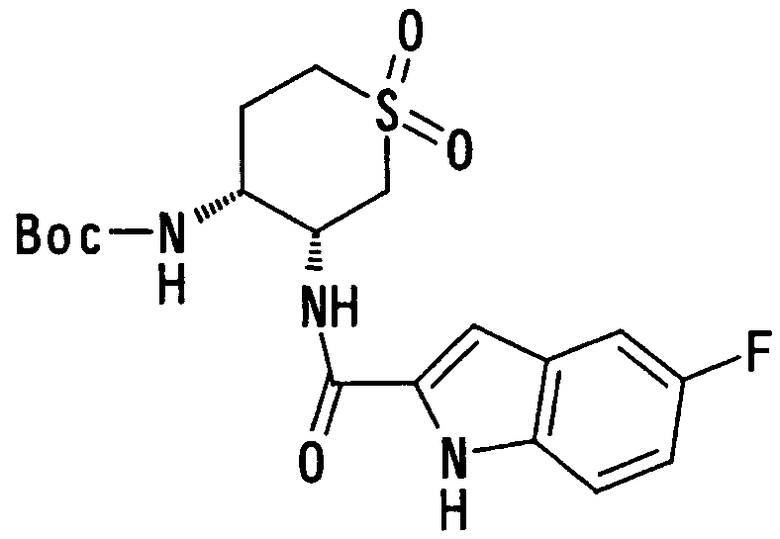
Указанное в заголовке соединение получали из (3R*,4R*)-соединения (низкополярное соединение), полученного в ссылочном примере 179, и 5-фториндол-2-карбоновой кислоты подобно способу ссылочного примера 68.
1Н-ЯМР (ДМСО-d6) δ: 1,37 (9H, с), 2,10-2,13 (2H, м), 3,06 (1H, шир.), 3,37-3,49 (3H, м), 4,13 (1H, шир.), 4,57 (1H, шир.), 6,95-7,01 (2H, м), 7,14 (1H, шир.), 7,30 (1H, д, J=8,5Гц), 7,41 (1H, дд, J=8,8, 4,5Гц), 8,28 (1H, шир.), 11,68 (1H, с).
МС (ESI) m/z: 426 (M+H)+.
[Ссылочный пример 233]
Гидрохлорид N-[(3R*,4R*)-4-амино-1,1-диоксогексагидро-1-тиопиран-3-ил]-5-фториндол-2-карбоксамида
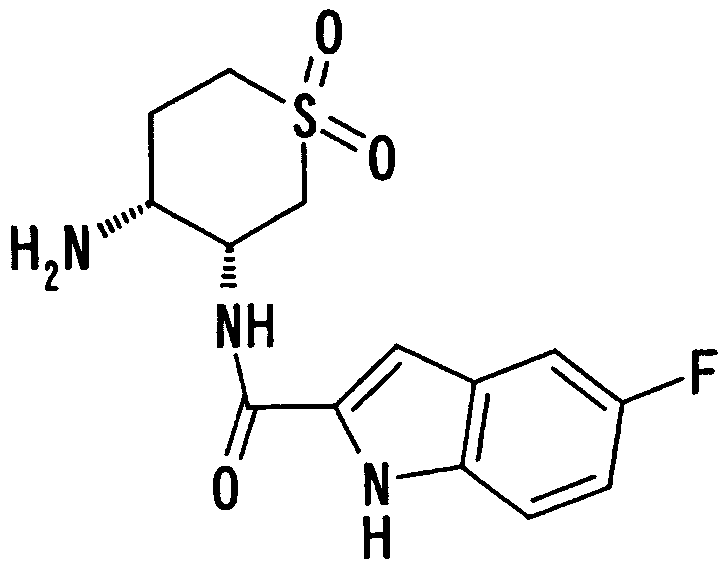
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 232, подобно способу ссылочного примера 69.
1Н-ЯМР (ДМСО-d6) δ: 2,25-2,31 (1H, м), 2,47 (1H, шир.), 3,30 (1H, шир.), 3,49-3,53 (2H, м), 3,60-3,66 (1H, м), 3,78 (1H, шир.), 4,79 (1H, шир.), 7,01-7,05 (1H, м), 7,21 (1H, с), 7,38 (1H, д, J=9,0Гц), 7,44 (1H, дд, J=8,8, 4,4Гц), 8,40 (2H, шир.), 8,56 (1H, шир.), 11,81 (1H, с).
МС (ESI) m/z: 326 (М+Н)+.
[Ссылочный пример 234]
Этил (3R)-3-{[(бензилокси)карбонил]амино}-4-[(трет-бутоксикарбонил)амино]-5-оксовалерат
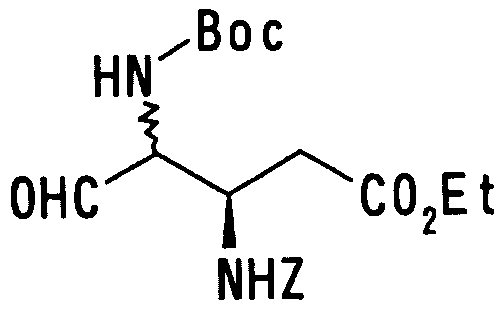
Комплекс (1,5 г) триоксида серы с пиридином постепенно добавляли к смешанному растворителю, состоящему из (3R,4S)-соединения (высокополярное соединение) (0,5 г), полученного в ссылочном примере 168, диметилсульфоксида (6,8 мл) и триэтиламина (2,6 мл), и смесь перемешивали в течение 20 минут. Реакционную смесь вливали в воду и экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида аммония, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Органический слой сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1) с получением указанного в заголовке соединения (0,51 г).
1Н-ЯМР (CDCl3) δ: 1,25 (3H, т, J=7,4Гц), 1,44 (9H, с), 2,51-2,70 (2H, м), 4,01-4,23 (2H, м), 4,45-4,67 (1H, м), 5,00-5,23 (2H, с), 5,24-5,42 (1H, м), 7,23-7,43 (5H, м), 9,63 (0,5H, с), 9,67 (0,5H, с).
[Ссылочный пример 235]
Бензил (4R)-5-[(трет-бутоксикарбонил)амино]-1-метил-2-оксопиперидин-4-илкарбамат
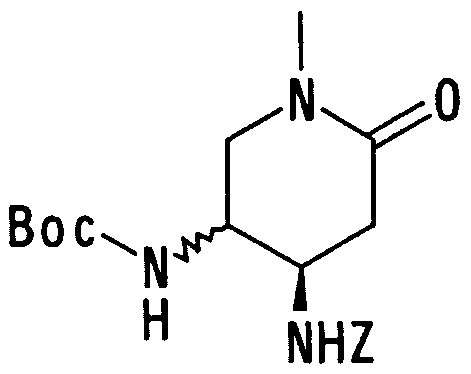
Уксусную кислоту (0,27 мл) и 2М метиламин (тетрагидрофурановый раствор, 1,0 мл) последовательно добавляли к раствору соединения (0,51 г), полученного в ссылочном примере 234, в этаноле (10 мл) при охлаждении льдом и смесь перемешивали 1 час при постепенном повышении температуры системы до комнатной температуры. Добавляли цианоборгидрид натрия (0,15 г) и смесь перемешивали 18 часов. Реакционную смесь разбавляли хлороформом и промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и полученный остаток растворяли в толуоле (20 мл). К полученному раствору добавляли триэтиламин (2 мл) и смесь кипятили с обратным холодильником в течение 2 часов. Реакционную смесь концентрировали при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 98:2) с получением указанного в заголовке соединения (0,28 г).
1Н-ЯМР (ДМСО-d6) δ: 1,36 (3,6H, с), 1,38 (5,4H, с), 2,22-2,43 (1H, м), 2,44-2,61 (1H, м), 2,72 (1,2H, с), 2,80 (1,8H, с), 3,10 (0,5H, дд, J=12,5, 8,3Гц), 3,21-3,30 (0,5H, м), 3,33-3,45 (1H, м), 3,56-3,82 (1H, м), 3,89-4,00 (1H, м), 4,94 (1H, д, J=8,1Гц), 5,00 (1,2H, с), 5,01 (0,8H, с), 6,89-7,02 (0,5H, м), 7,23-7,44 (5,5H, м).
[Ссылочный пример 236]
трет-Бутил (4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-метил-6-оксопиперидин-3-илкарбамат
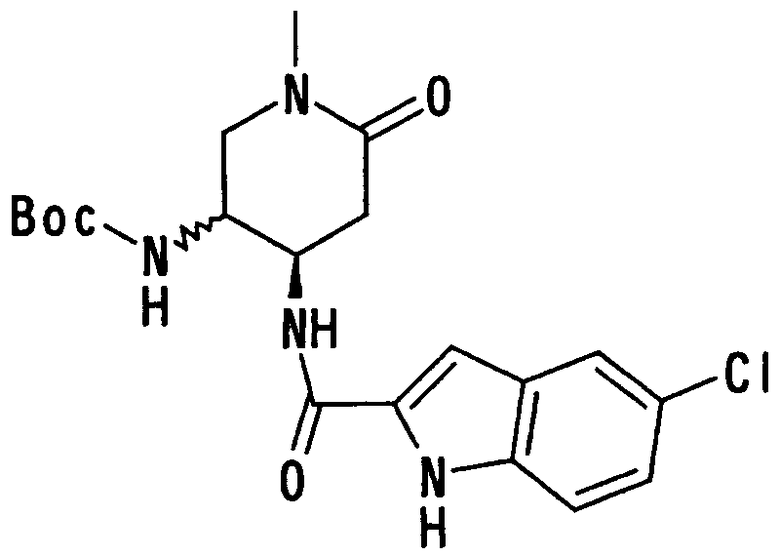
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 235, и 5-хлориндол-2-карбоновой кислоты подобно способу ссылочного примера 214.
1Н-ЯМР (ДМСО-d6) δ: 1,24 (5,4H, с), 1,35 (3,6H, с), 2,43-2,56 (2H, м), 2,80 (3H, с), 3,10-3,20 (1H, м), 3,30-3,52 (1H, м), 3,83-3,91 (0,4H, м), 4,02-4,10 (0,6H, м), 4,20-4,31 (0,6H, м), 4,43-4,54 (0,4H, м), 6,94 (0,6H, д, J=8,1Гц), 7,08 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,42 (1H, д, J=8,8Гц), 7,69 (1H, д, J=2,0Гц), 8,30 (0,4H, с), 8,36 (0,4H, д, J=7,3Гц), 8,43 (0,6H, д, J=8,3Гц), 11,75 (0,6H, с), 11,78 (0,4H, с).
[Ссылочный пример 237]
Гидрохлорид 4-(пиридин-4-ил)бензойной кислоты
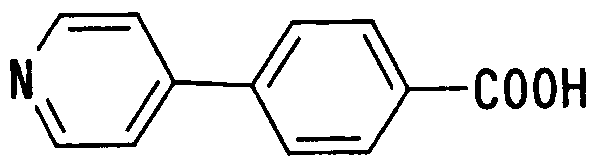
Гидрохлорид 4-бромпиридина (11,7 г) и 4-карбоксифенилборную кислоту (10,0 г) растворяли в смешанном растворителе из толуола (250 мл) и воды (250 мл), добавляли последовательно тетракис(трифенилфосфин)палладий(0) (5,0 г) и безводный карбонат натрия (25,4 г) и смесь нагревали с обратным холодильником при 120°C в течение 19 часов. После охлаждения реакционной смеси до комнатной температуры добавляли этилацетат и экстрагировали реакционную смесь водой. К водному слою для его подкисления добавляли концентрированную хлористоводородную кислоту. Водный слой промывали этилацетатом, затем концентрировали и выпавшие в осадок твердые частицы собирали с получением указанного в заголовке соединения (8,37 г).
1Н-ЯМР (ДМСО-d6) δ: 8,11 (2H, д, J=8,8Гц), 8,14 (2H, д, J=8,8Гц), 8,35 (2H, д, J=6,6Гц), 8,97 (2H, д, J=6,6Гц),
МС (FAB) m/z: 200 (М+Н)+.
[Ссылочный пример 238]
Метил 4-(пиридин-4-ил)бензоат
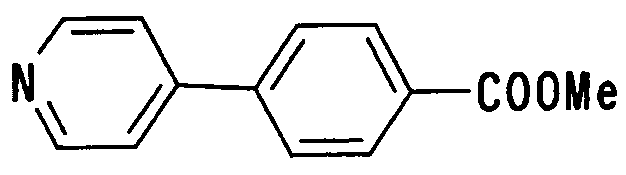
Соединение (12,4 г), полученное в ссылочном примере 237, растворяли в метаноле (200 мл), добавляли концентрированную серную кислоту при комнатной температуре и смесь кипятили с обратным холодильником в течение 3 часов. По окончании реакции отгоняли растворитель, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и смесь экстрагировали этилацетатом. Экстракт сушили над безводным сульфатом натрия, отгоняли растворитель и к остатку для его отверждения добавляли гексан с получением указанного в заголовке соединения (9,86 г).
1Н-ЯМР (CDCl3) δ: 3,96 (3H, с), 7,54 (2H, д, J=5,9Гц), 7,71 (2H, д, J=8,3Гц), 8,16 (2H, д, J=8,3Гц), 8,71 (2H, д, J=5,9Гц).
[Ссылочный пример 239]
N-Оксид 4-[4-(метоксикарбонил)фенил]пиридина
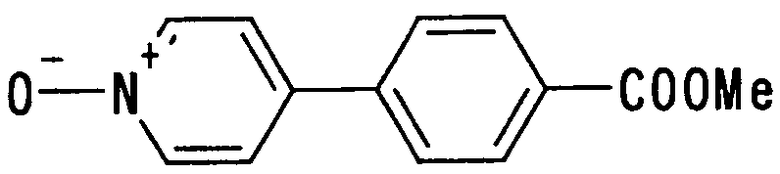
Соединение (1,49 г), полученное в ссылочном примере 238, растворяли в метиленхлориде (30 мл), добавляли 70% м-хлорпербензойную кислоту (3,46 г) и смесь перемешивали при комнатной температуре в течение 1 часа. Добавляли водный раствор сульфита натрия и разделяли жидкости. Полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли с получением указанного в заголовке соединения (1,33 г).
1Н-ЯМР (ДМСО-d6) δ: 3,88 (3H, с), 7,86 (2H, д, J=7,2Гц), 7,94 (2H, д, J=8,3Гц), 8,05 (2H, д, J=8,3Гц), 8,30 (2H, д, J=7,2Гц),
МС (FAB) m/z: 230 (М+Н)+.
[Ссылочный пример 240]
N-Оксид 4-(4-карбоксифенил)пиридина
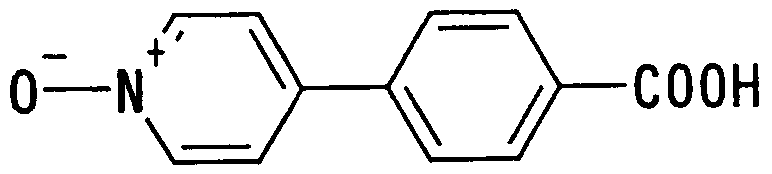
Соединение (802 мг), полученное в ссылочном примере 239, растворяли в диоксане (20 мл), добавляли 1N водный раствор (5 мл) гидроксида натрия и смесь кипятили с обратным холодильником в течение 1 часа и затем перемешивали при комнатной температуре в течение 2 часов. Для нейтрализации смеси добавляли 1N хлористоводородную кислоту (5 мл). Затем добавляли воду (5 мл) и образовавшийся осадок отфильтровывали, получая указанное в заголовке соединение (627 мг).
1Н-ЯМР (ДМСО-d6) δ: 7,85 (2H, д, J=7,2Гц), 7,91 (2H, д, J=8,3Гц), 8,03 (2H, д, J=8,3Гц), 8,30 (2H, д, J=7,2Гц).
[Ссылочный пример 241]
N-Оксид 2-(4-карбоксифенил)-1-пиридина
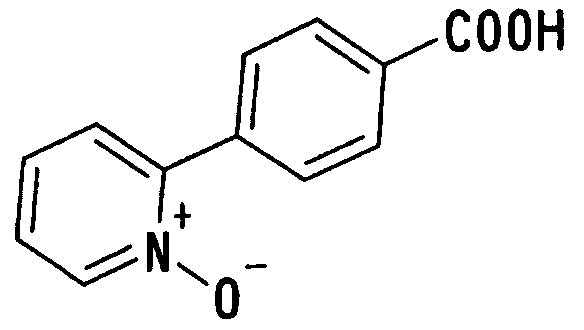
Указанное в заголовке соединение получали из 2-бромпиридина подобно способам ссылочных примеров 237, 238, 239 и 240.
1Н-ЯМР (ДМСО-d6) δ: 7,41-7,45 (2Н, м), 7,65-7,69 (1Н, м), 7,94 (2Н, д, J=8,3Гц), 8,02 (2Н, д, J=8,3Гц), 8,34-8,38 (1Н, м), 13,09 (1Н, с).
МС (FAB) m/z: 216 (M+H)+.
[Ссылочный пример 242]
Этил 2-(4-хлоранилино)-2-оксоацетат
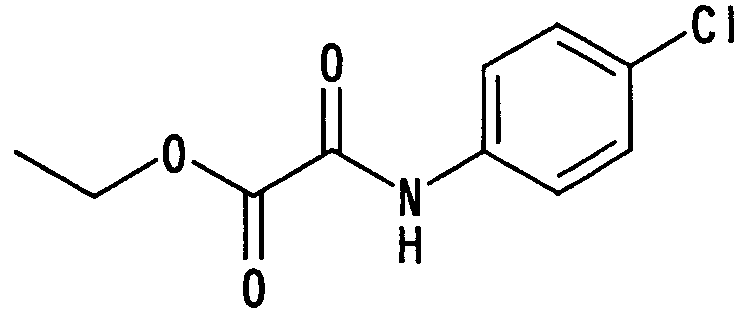
Триэтиламин (1,52 мл) и этилхлороксоацетат (1,11 мл) последовательно добавляли к раствору 4-хлоранилина (1,16 г) в метиленхлориде (26 мл) и смесь перемешивали при комнатной температуре в течение 14 часов. После добавления к реакционной смеси насыщенного водного раствора гидрокарбоната натрия для разделения жидкостей полученный органический слой последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Затем растворитель концентрировали при пониженном давлении, добавляли к остатку гексан для осаждения кристаллов и кристаллы отфильтровывали и сушили с получением указанного в заголовке соединения (1,89 г).
1Н-ЯМР (CDCl3) δ: 1,43 (3H, т, J=7,1Гц), 4,42 (2H, кв, J=7,1Гц), 7,34 (2H, д, J=8,8Гц), 7,60 (2H, д, J=8,8Гц), 8,86 (1H, шир.с).
МС (ESI)m/z: 228 (М+Н)+.
[Ссылочный пример 243]
Метил 2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетат
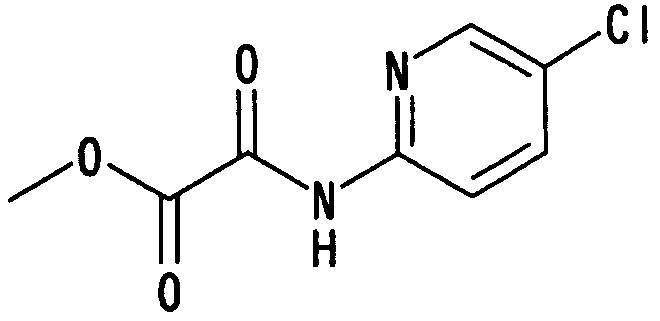
2-Амино-5-хлорпиридин (1,16 г) и триэтиламин (1,51 мл) растворяли в метиленхлориде (26 мл), к раствору добавляли этилхлороксоацетат (1,10 мл) при охлаждении льдом и смесь перемешивали при комнатной температуре в течение 14 часов. После добавления к реакционной смеси насыщенного водного раствора гидрокарбоната натрия для разделения жидкостей полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1). Полученные бледно-желтые твердые частицы растворяли в метаноле (20 мл) и раствор перемешивали при 50°C в течение 11 часов. Реакционную смесь концентрировали при пониженном давлении и выпавшие в осадок кристаллы отфильтровывали и сушили с получением указанного в заголовке соединения (0,43 г).
1Н-ЯМР (CDCl3) δ: 3,99 (3H, с), 7,73 (1H, дд, J=8,8, 2,2Гц), 8,24 (1H, д, J=8,8Гц), 8,31 (1H, д, J=2,2Гц), 9,39 (1H, шир.с).
МС (ESI) m/z: 215 (М+Н)+.
[Ссылочный пример 244]
(1S)-3-Циклогексен-1-карбоновая кислота
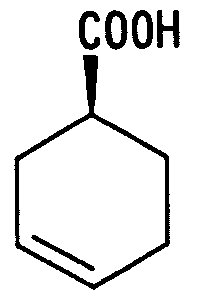
(R)-(+)-α-Метилбензиламинную соль (J. Am. Chem. Soc., Vol. 100, pp. 5199-5203, 1978) (95,0 г) (1S)-3-циклогексен-1-карбоновой кислоты растворяли в смеси этилацетата (1,6 л) и 2N хлористоводородной кислоты (1,6 л). После отделения органического слоя водный слой экстрагировали этилацетатом (500 мл х 2 раза). Полученные органические слои объединяли и промывали насыщенным водным раствором хлорида натрия (300 мл х 2 раза), отделяя органический слой. Водный слой экстрагировали этилацетатом (200 мл) и затем полученный органический слой промывали насыщенным водным раствором хлорида натрия (100 мл). Все органические слои объединяли, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения (48,3 г).
[α]25 D = -104° (c = 1, хлороформ).
1Н-ЯМР (CDCl3) δ: 1,66-1,77 (1Н, м), 2,00-2,20 (3Н, м), 2,20-2,38 (2Н, м), 2,57-2,65 (1Н, м), 5,65-5,75 (2Н, м).
[Ссылочный пример 245]
(1S,4S,5S)-4-Йод-6-оксабицикло[3.2.1]октан-7-он
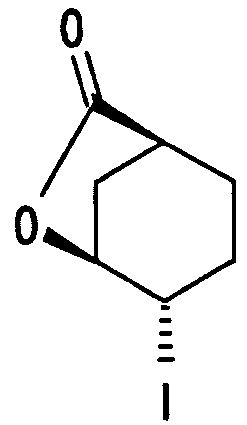
Йод (125,4 г) добавляли к смеси соединения (48,0 г), полученного в ссылочном примере 244, метиленхлорида (580 мл), иодида калия (82,1 г), гидрокарбоната натрия (42,0 г) и воды (530 мл) при температуре реакционной массы 5°C и полученную смесь перемешивали при комнатной температуре в течение 3 часов. После добавления к реакционной смеси 1N водного раствора (800 мл) тиосульфата натрия полученную смесь экстрагировали метиленхлоридом (1 л, 500 мл). Полученный органический слой промывали водным раствором (300 мл) гидрокарбоната натрия, водой (500 мл) и насыщенным водным раствором хлорида натрия (300 мл), сушили над безводным сульфатом магния и затем концентрировали. Выпавшие в осадок кристаллы отфильтровывали, промывали гексаном и затем сушили с получением указанного в заголовке соединения (89,5 г).
Т.пл. 130-131°C.
[α]25 D = -41°(c = 1, хлороформ).
1Н-ЯМР (CDCl3) δ: 1,78-1,96 (2H, м), 2,12 (1H, дд, J=16,5Гц, 5,2Гц), 2,35-2,50 (2H, м), 2,65-2,70 (1H, м), 2,80 (1H, д, J=12,2Гц), 4,45-4,55 (1H, м), 4,77-4,87 (1H, м).
[Ссылочный пример 246]
Этил (1S,3S,6R)-7-оксабицикло[4.1.0]гептан-3-карбоксилат
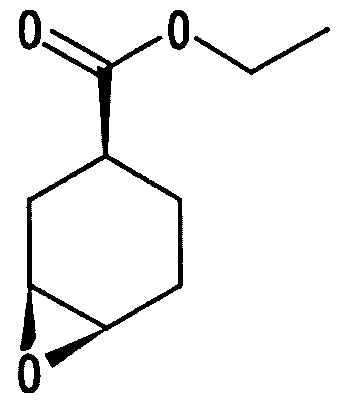
2N Водный раствор (213 мл) гидроксида натрия добавляли к суспензии соединения (89,3 г), полученного в ссылочном примере 245, в этаноле (810 мл) и смесь перемешивали при комнатной температуре в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении на горячей бане с температурой 35°C и к полученному маслу добавляли воду (500 мл) и экстрагировали метиленхлоридом (500 мл и 300 мл). Экстракт промывали водой (300 мл) и сушили над безводным сульфатом магния, затем концентрировали при пониженном давлении. Полученное масло очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 85:15) с получением указанного в заголовке соединения (41,3 г).
[α]25 D = -58°(c = 1, хлороформ).
1Н-ЯМР (CDCl3) δ: 1,25 (3H, т, J=7,2Гц), 1,50-1,70 (2H, м), 1,71-1,82 (1H, м), 2,08-2,28 (4H, м), 3,16 (2H, с), 4,12 (2H, кв, J=7,2Гц).
[Ссылочный пример 247]
Этил (1S,3R,4R)-3-азидо-4-гидроксициклогексанкарбоксилат
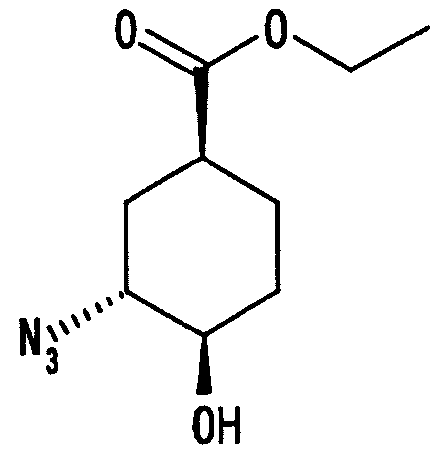
Смесь соединения (41,0 г), полученного в ссылочном примере 246, N,N-диметилформамида (300 мл), хлорида аммония (19,3 г) и азида натрия (23,5 г) перемешивали при 76°C в течение 13 часов. Нерастворимое вещество отфильтровывали, фильтрат концентрировали при пониженном давлении без отверждения, к остатку добавляли отфильтрованный продукт и смесь растворяли в воде (500 мл). Раствор экстрагировали этилацетатом (500 мл и 300 мл) и экстракт промывали водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и затем концентрировали с получением указанного в заголовке соединения (51,5 г).
[α]25 D = +8° (c = 1, хлороформ).
1Н-ЯМР (CDCl3) δ: 1,28 (3H, т, J=7,1Гц), 1,37-1,64 (3H, м), 1,86-1,95 (1H, м), 2,04-2,16 (1H, м), 2,32-2,41 (1H, м), 2,44 (1H, шир.с), 2,68-2,78 (1H, м), 3,45-3,60 (2H, м), 4,17 (2H, кв, J=7,1Гц).
[Ссылочный пример 248]
Этил (1S,3R,4R)-3-[(трет-бутоксикарбонил)амино]-4-гидроксициклогексанкарбоксилат
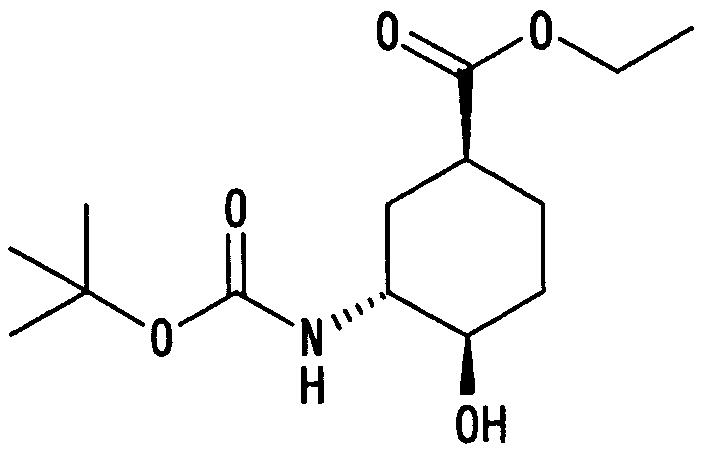
Смесь соединения (51,2 г), полученного в ссылочном примере 247, ди-трет-бутилдикарбоната (68,1 г), 5% палладия на углероде (5,0 г) и этилацетата (1000 мл) перемешивали в течение ночи при комнатной температуре под давлением водорода (7 кг/см2). Масло, полученное фильтрованием реакционной смеси и концентрированием фильтрата, очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1 → 3:1). Очищенный продукт кристаллизовали из гексана с получением указанного в заголовке соединения (46,9 г). Маточный раствор дополнительно очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 100:1) с получением указанного в заголовке соединения (6,74 г).
[α]25 D = +25° (c = 1, хлороформ).
1Н-ЯМР (CDCl3) δ: 1,28 (3H, т, J=7,1Гц), 1,38-1,57 (3H, м), 1,45 (9H, с), 1,86-1,95 (1H, м), 2,05-2,17 (1H, м), 2,29-2,39 (1H, м), 2,61-2,68 (1H, м), 3,34 (1H, шир.с), 3,39-3,48 (1H, м), 3,53-3,64 (1H, м), 4,10-4,24 (2H, м), 4,54 (1H, шир.с).
[Ссылочный пример 249]
Этил (1S,3R,4S)-4-азидо-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
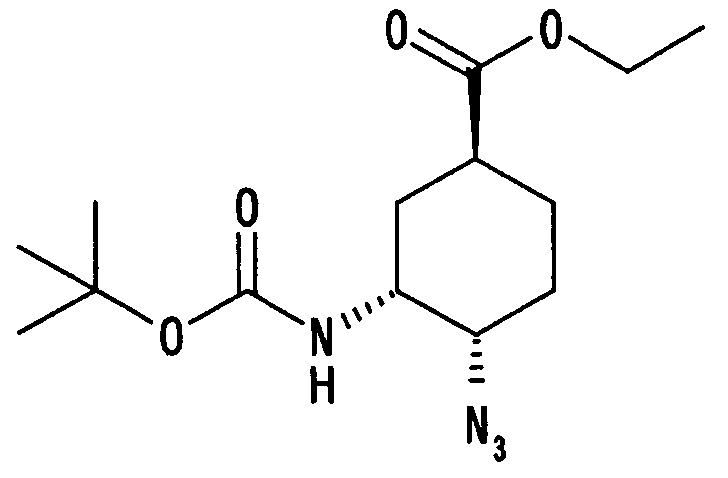
Метансульфонилхлорид (42 мл) добавляли по каплям к раствору, содержащему соединение (53,5 г), полученное в ссылочном примере 248, метиленхлорид (500 мл) и триэтиламин (130 мл), за 20 минут при температуре от -10°C до -15°C. Смесь нагревали до комнатной температуры за 2 часа и перемешивали в течение 2 часов. К реакционной смеси при 0°C добавляли по каплям для ее подкисления 0,5N хлористоводородную кислоту (800 мл) и экстрагировали метиленхлоридом (500 мл и 300 мл). Полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния и затем концентрировали при пониженном давлении. Полученные кристаллы растворяли в N,N-диметилформамиде (335 мл), добавляли азид натрия (60,5 г) и смесь перемешивали при 67°C-75°C в течение 16 часов. После фильтрования реакционной смеси фильтрат концентрировали при пониженном давлении, отгоняя 250 мл растворителя. Остаток объединяли с отфильтрованным продуктом и смесь растворяли в воде (500 мл). Раствор экстрагировали этилацетатом (1 л и 300 мл) и экстракт промывали насыщенным водным раствором хлорида натрия (400 мл и 200 мл), сушили над безводным сульфатом магния и затем концентрировали. Полученные при этом кристаллы очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1) с получением указанного в заголовке соединения (18,4 г).
[α]25 D = +62° (c = 1, хлороформ).
1Н-ЯМР (CDCl3) δ: 1,26 (3H, т, J=7,1Гц), 1,35-2,00 (15H, с), 2,60-2,68 (1H, м), 3,80-3,96 (2H, м), 4,15 (2H, кв, J=7,1Гц), 4,61 (1H, шир.с).
[Ссылочный пример 250]
(1S,3R,4S)-4-Азидо-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоновая кислота
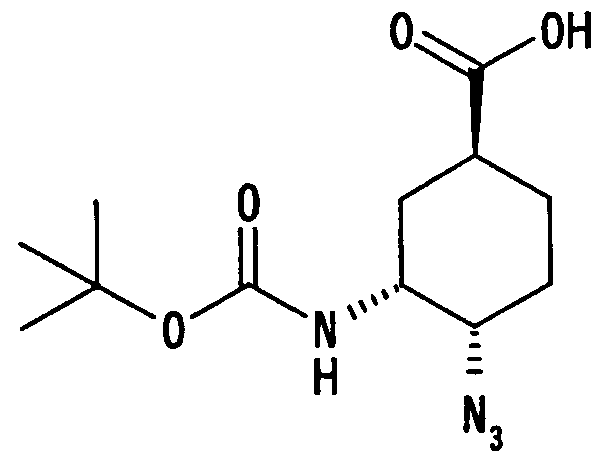
Гидроксид лития (102 мг) и воду (5 мл) добавляли к раствору соединения (1,0 г), полученного в ссылочном примере 249, в тетрагидрофуране (25 мл). После перемешивания в течение 17 часов добавляли еще гидроксид лития (50 мг) и смесь перемешивали в течение 4 часов. К реакционной смеси добавляли 1N хлористоводородную кислоту (6,3 мл) и экстрагировали этилацетатом. Полученный органический слой сушили и затем отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (980 мг).
1Н-ЯМР (CDCl3) δ: 1,30-2,20 (6H, м), 1,45 (9H, с), 2,70-2,80 (1H, м), 3,94 (2H, шир.с), 4,73 (1H, шир.с).
[Ссылочный пример 251]
трет-Бутил (1R,2S,5S)-2-азидо-5-[(диметиламино)карбонил]циклогексилкарбамат
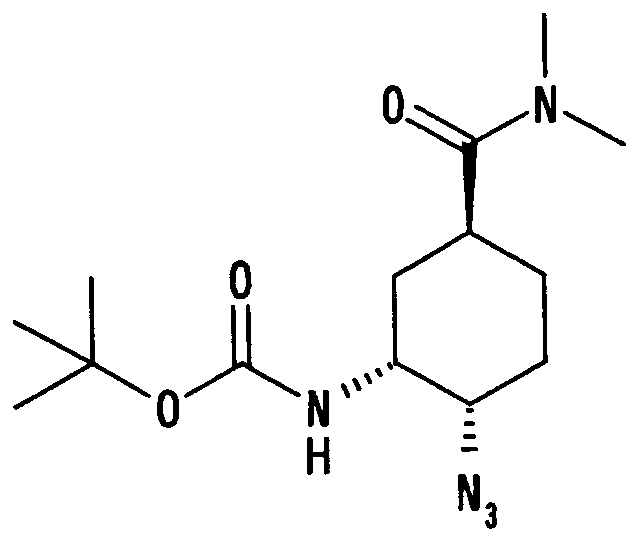
Соединение (4,77 г), полученное в ссылочном примере 250, растворяли в метиленхлориде (150 мл), к раствору добавляли гидрохлорид диметиламина (3,26 г), гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (4,60 г), моногидрат 1-гидроксибензотриазола (3,24 г) и N-метилморфолин (8,09 г) и смесь перемешивали при комнатной температуре в течение 18 часов. К реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Затем сушили полученный органический слой и отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:50) с получением указанного в заголовке соединения (4,90 г).
1Н-ЯМР (CDCl3) δ: 1,30-1,90 (4H, м), 1,45 (9H, с), 1,97-2,18 (2H, м), 2,75-2,85 (1H, м), 2,92 (3H, с), 3,02 (3H, с), 3,68-3,80 (1H, м), 4,05-4,20 (1H, м), 4,55-4,75 (1H, м).
[Ссылочный пример 252]
N-{(1R,2S,5S)-2-Азидо-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
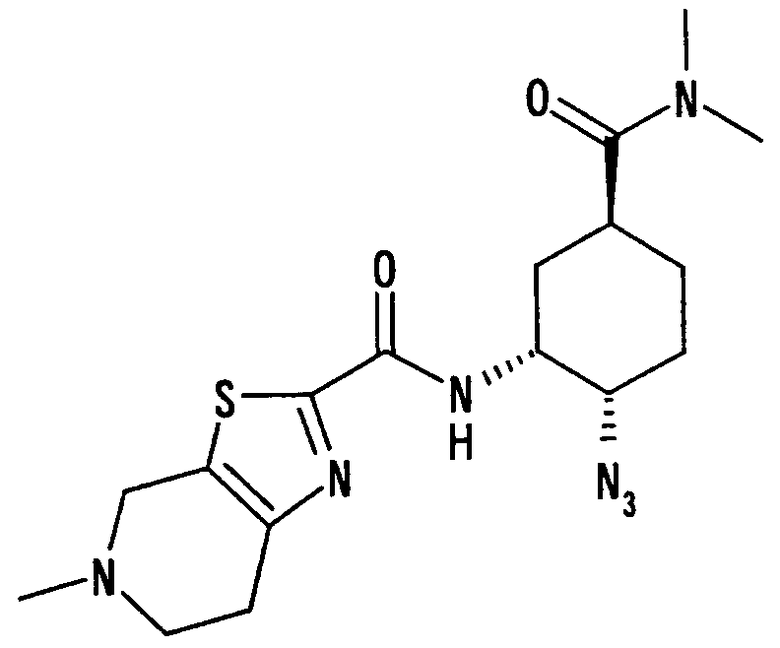
Соединение (9,13 г), полученное в ссылочном примере 251, растворяли в метиленхлориде (100 мл), к раствору добавляли этанольный раствор (100 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 1 минуты. Реакционную смесь концентрировали при пониженном давлении и полученный остаток растворяли в N,N-диметилформамиде (200 мл). К раствору добавляли соединение (7,75 г), полученное в ссылочном примере 10, моногидрат 1-гидроксибензотриазола (4,47 г), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (11,2 г) и триэтиламин (2,02 мл) и смесь перемешивали в течение ночи при комнатной температуре. Добавляли еще соединение (2,38 г), полученное в ссылочном примере 10, и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (5,60 г) и смесь перемешивали в течение 3 суток. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток затем очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 47:3) с получением указанного в заголовке соединения (7,38 г).
1Н-ЯМР (CDCl3) δ: 1,72-1,97 (4H, м), 2,10-2,27 (2H, м), 2,51 (3H, с), 2,77-3,05 (11H, м), 3,68 (1H, д, J=15,4Гц), 3,74 (1H, д, J=15,4Гц), 3,86-3,93 (1H, м), 4,54-4,60 (1H, м), 7,25 (1H, д, J=7,6Гц).
[Ссылочный пример 253]
N-{(1R,2S,5S)-2-Амино-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
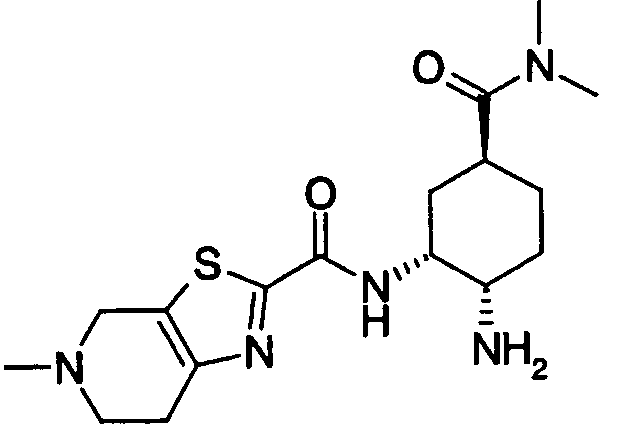
10% Палладий на углероде (6,0 г) добавляли к раствору соединения (9,0 г), полученного в ссылочном примере 252, в метаноле (300 мл) и смесь интенсивно перемешивали при комнатной температуре в течение 11 часов при давлении водорода 4 атм. Катализатор отфильтровывали и фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (7,67 г).
1Н-ЯМР (CDCl3) δ: 1,42-1,54 (1H, м), 1,66-1,89 (5H, м), 2,30-2,40 (1H, м), 2,51 (3H, с), 2,68-3,05 (6H, м), 2,92 (3H, с), 3,00 (3H, с), 3,10-3,18 (1H, м), 3,65-3,77 (2H, м), 4,21-4,28 (1H, м), 7,52 (1H, д, J=6,1Гц).
[Ссылочный пример 254]
Метил 2-(4-фторанилино)-2-оксоацетат
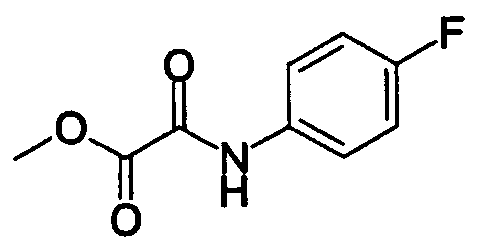
Указанное в заголовке соединение получали из 4-фторанилина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 3,98 (3Н, с), 7,00-7,14 (2Н, м), 7,55-7,68 (2Н, м), 8,85 (1Н, шир.с).
МС (ESI) m/z: 198 (M+H)+.
[Ссылочный пример 255]
Метил 2-(4-броманилино)-2-оксоацетат
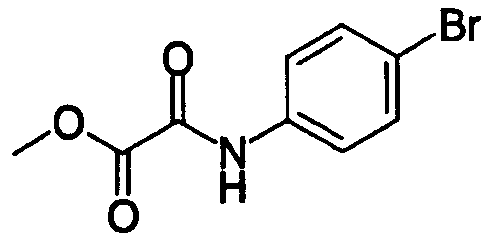
Указанное в заголовке соединение получали из 4-броманилина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 3,98 (3H, с), 7,49 (2H, д, J=9,0Гц), 7,55 (2H, д, J=9,0Гц), 8,85 (1H, шир.с).
МС (FAB)m/z: 258 М+.
[Ссылочный пример 256]
Метил 2-(4-хлор-2-метиланилино)-2-оксоацетат
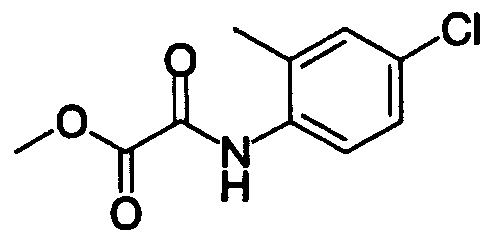
Указанное в заголовке соединение получали из 4-хлор-2-метиланилина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 2,31 (3H, с), 3,99 (3H, с), 7,15-7,30 (2H, м), 7,98 (1H, д, J=8,8Гц), 8,77 (1H, шир.).
МС (FAB) m/z: 228 (М+Н)+.
[Ссылочный пример 257]
Метил 2-(4-хлор-3-метиланилино)-2-оксоацетат
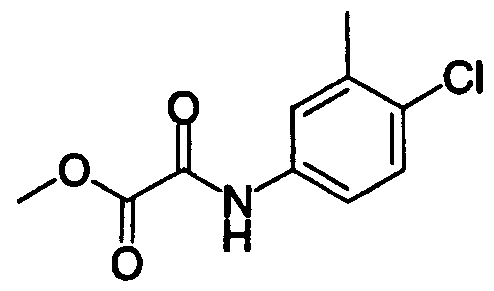
Указанное в заголовке соединение получали из 4-хлор-3-метиланилина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 2,39 (3H, с), 3,98 (3H, с), 7,33 (1H, д, J=12,5Гц), 7,44 (1H, дд, J=12,5, 2,5Гц), 7,53 (1H, д, J=2,5Гц), 8,81 (1H, шир.с).
МС (ESI)m/z: 228 (М+Н)+.
[Ссылочный пример 258]
Метил 2-(4-хлор-2-фторанилино)-2-оксоацетат
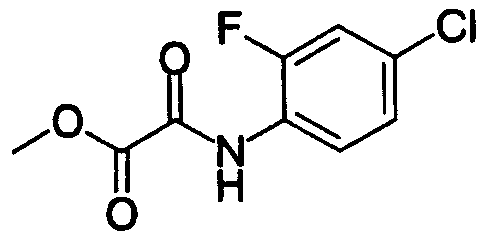
Указанное в заголовке соединение получали из 4-хлор-2-фторанилина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 3,99 (3H, с), 7,15-7,24 (2H, м), 8,33 (1H, т, J=8,4Гц), 9,05 (1H, шир.с).
МС (ESI) m/z: 232 (М+Н)+.
[Ссылочный пример 259]
Метил 2-(2,4-дифторанилино)-2-оксоацетат
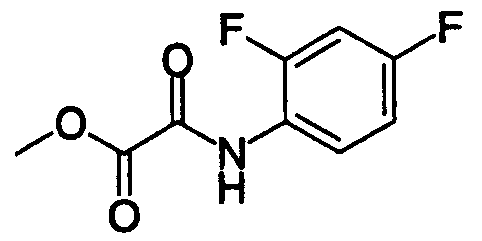
Указанное в заголовке соединение получали из 2,4-дифторанилина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 3,99 (3H, с), 6,87-7,00 (2H, м), 8,29-8,38 (1H, м), 8,99 (1H, шир.с).
МС (ESI) m/z: 215 М+.
[Ссылочный пример 260]
Метил 2-(3,4-дифторанилино)-2-оксоацетат
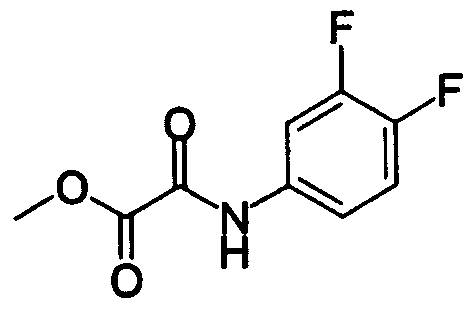
Указанное в заголовке соединение получали из 3,4-дифторанилина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 3,98 (3H, с), 7,10-7,28 (2H, м), 7,67-7,78 (1H, м), 8,83 (1H, шир.с).
МС (ESI) m/z: 215 М+.
[Ссылочный пример 261]
Метил 2-оксо-2-(пиридин-4-иламино)ацетат
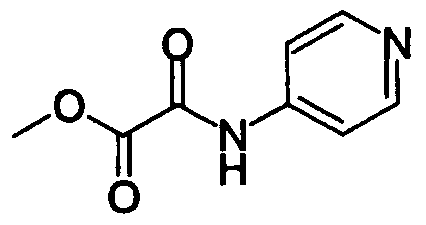
Указанное в заголовке соединение получали из 4-аминопиридина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 3,99 (3H, с), 7,58 (2H, дд, J=4,8, 1,6Гц), 8,60 (2H, дд, J=4,8, 1,6Гц), 9,04 (1H, шир.с).
МС (ESI) m/z: 181 (М+Н)+.
[Ссылочный пример 262]
Метил 2-[(5-бромпиридин-2-ил)амино]2-оксоацетат
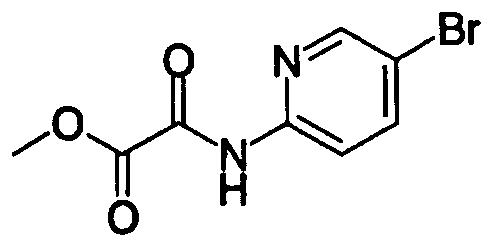
Указанное в заголовке соединение получали из 2-амино-5-бромпиридина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 3,99 (3H, с), 7,87 (1H, дд, J=8,8, 2,4Гц), 8,19 (1H, д, J=8,8Гц), 8,41 (1H, д, J=2,4Гц), 9,38 (1H, шир.с).
МС (FAB) m/z: 259 М+.
[Ссылочный пример 263]
Этил 2-[(6-хлорпиридин-3-ил)амино]-2-оксоацетат
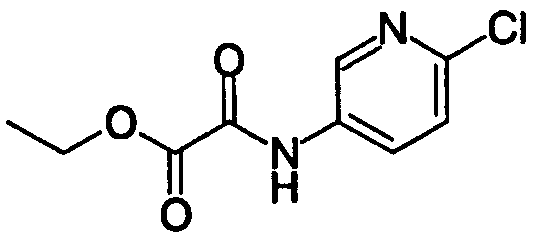
5-Амино-2-хлорпиридин (386 мг) растворяли в N,N-диметилформамиде (58 мл), к раствору добавляли 2-этокси-2-оксоацетат калия (469 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (863 мг) и моногидрат 1-гидроксибензотриазола (203 мг) и смесь перемешивали при комнатной температуре в течение 2 суток. Растворитель отгоняли при пониженном давлении, добавляли к остатку метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей и полученный органический слой сушили над безводным сульфатом натрия. Растворитель концентрировали при пониженном давлении и затем остаток очищали колоночной флэш-хроматографией на силикагеле (гексан:этилацетат = 2:1) с получением остатка (200 мг), содержащего указанное в заголовке соединение.
1Н-ЯМР (CDCl3) δ: 1,43 (3H, т, J=7,2Гц), 4,44 (2H, кв, J=7,2Гц), 7,36 (1H, д, J=8,7Гц), 8,24 (1H, дд, J=8,7, 2,7Гц), 8,55 (1H, д, J=2,7Гц), 9,03 (1H, шир.с).
[Ссылочный пример 264]
Метил 2-[(6-хлорпиридазин-3-ил)амино]-2-оксоацетат
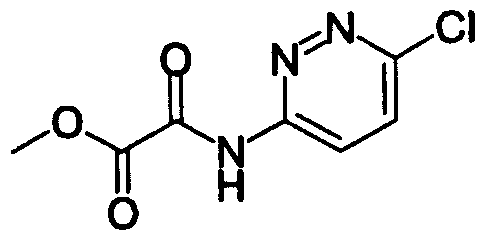
3-Амино-6-хлорпиридазин (516 мг) растворяли в пиридине (26 мл), последовательно добавляли при охлаждении льдом триэтиламин (665 мкл) и метилхлороксоацетат (441 мкл) и смесь перемешивали при комнатной температуре в течение 14 часов. После добавления к реакционной смеси воды для разделения жидкостей полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (748 мг).
1Н-ЯМР (CDCl3) δ: 4,03 (3H, с), 7,59 (1H, д, J=9,3Гц), 8,52 (1H, д, J=9,3Гц), 9,88 (1H, шир.с).
МС (FAB) m/z: 215 M+.
[Ссылочный пример 265]
Метил 2-[(5-хлортиазол-2-ил)амино]-2-оксоацетат
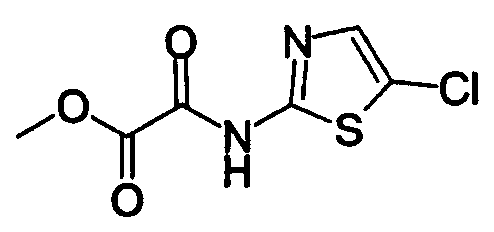
Указанное в заголовке соединение получали из 2-амино-5-хлортиазола и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 4,02 (3H, с), 7,48 (1H, с), 11,03 (1H, шир.с).
МС (ESI) m/z: 221 (M+H)+.
[Ссылочный пример 266]
2-[(5-Хлорпиридин-2-ил)амино]-2-оксоацетат лития
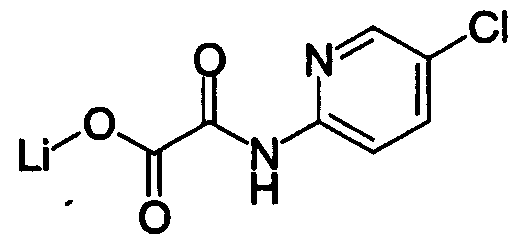
Воду (5,0 мл) и гидроксид лития (128 мг) добавляли к раствору соединения (1,12 г), полученного в ссылочном примере 243, в тетрагидрофуране (20 мл) при комнатной температуре и смесь перемешивали в течение 5 часов. Растворитель отгоняли при пониженном давлении, к полученным белым твердым частицам добавляли гексан (30 мл) и смесь перемешивали в течение 30 минут. Твердые частицы отфильтровывали и сушили, получая указанное в заголовке соединение (1,02 г).
1Н-ЯМР (ДМСО-d6) δ: 7,90 (1H, дд, J=8,9, 2,6Гц), 8,12 (1H, д, J=8,9Гц), 8,34 (1H, д, J=2,6Гц), 10,18 (1H, с).
[Ссылочный пример 267]
Этил 2-(4-хлоранилино)ацетат
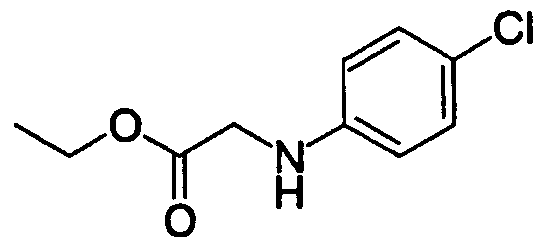
4-Хлоранилин (2,0 г) растворяли в ацетонитриле (20 мл), добавляли этилбромацетат (2,1 г) и карбонат калия (2,2 г) и смесь перемешивали при 60°C в течение 2 суток. Реакционную смесь фильтровали через слой целита и фильтрат концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (гексан:хлороформ = 2:1) с получением указанного в заголовке соединения (2,3 г).
1Н-ЯМР (CDCl3) δ: 1,30 (3H, т, J=7,3Гц), 3,86 (2H, с), 4,24 (2H, кв, J=7,3Гц), 4,26-4,35 (1H, м), 6,53 (2H, дд, J=6,6, 2,2Гц), 7,14 (2H, дд, J=6,6, 2,2Гц).
[Ссылочный пример 268]
Этил 2-(4-хлор-2-фторанилино)ацетат
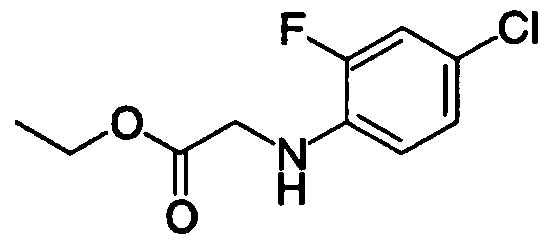
Указанное в заголовке соединение получали из 4-хлор-2-фторанилина и этилбромацетата подобно способу ссылочного примера 267.
1Н-ЯМР (CDCl3) δ: 1,29 (3H, т, J=7,3Гц), 3,91 (2H, с), 4,22 (2H, кв, J=7,3Гц), 4,42-4,51 (1H, м), 6,49 (1H, т, J=8,8Гц), 6,98 (1H, дт, J=8,8, 2,5Гц), 7,01 (1H, дд, J=11,3, 2,5Гц).
[Ссылочный пример 269]
Этил 2-[((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)амино]-2-оксоацетат
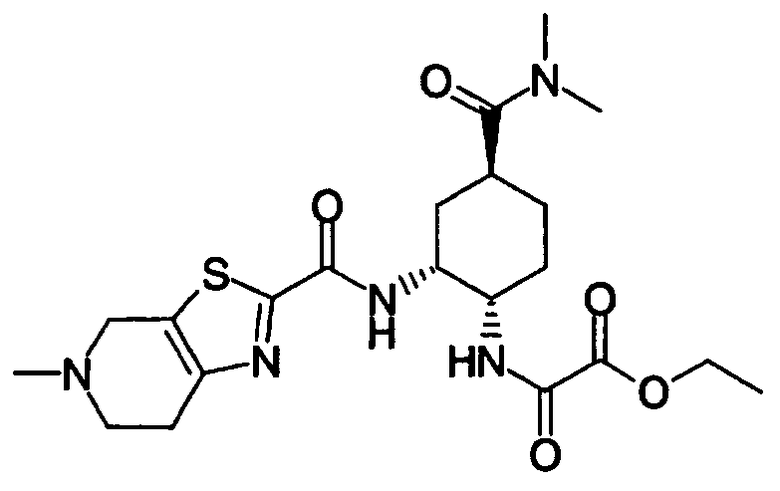
Соединение (1,5 г), полученное в ссылочном примере 253, растворяли в N,N-диметилформамиде (15 мл), к раствору добавляли 2-этокси-2-оксоацетат калия (962 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (1,18 г) и моногидрат 1-гидроксибензотриазола (227 мг) и смесь перемешивали при комнатной температуре в течение 14 часов. Растворитель отгоняли при пониженном давлении, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и затем остаток очищали колоночной флэш-хроматографией на силикагеле (метиленхлорид:метанол = 47:3) с получением указанного в заголовке соединения (1,13 г).
1Н-ЯМР (CDCl3) δ: 1,37 (3H, т, J=7,1Гц), 1,55-2,15 (6H, м), 2,52 (3H, с), 2,77-2,89 (3H, м), 2,94 (5H, шир.с), 3,06 (3H, с), 3,71 (1H, д, J=15,5Гц), 3,73 (1H, д, J=15,5Гц), 4,06-4,13 (1H, м), 4,32 (2H, кв, J=7,1Гц), 4,60-4,63 (1H, м), 7,39 (1H, д, J=8,3Гц), 7,83 (1H, д, J=7,6Гц).
МС (ESI) m/z: 466 (M+H)+.
[Ссылочный пример 270]
2-[((1S,2R,4S)-4-[(Диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)амино]-2-оксоацетат лития
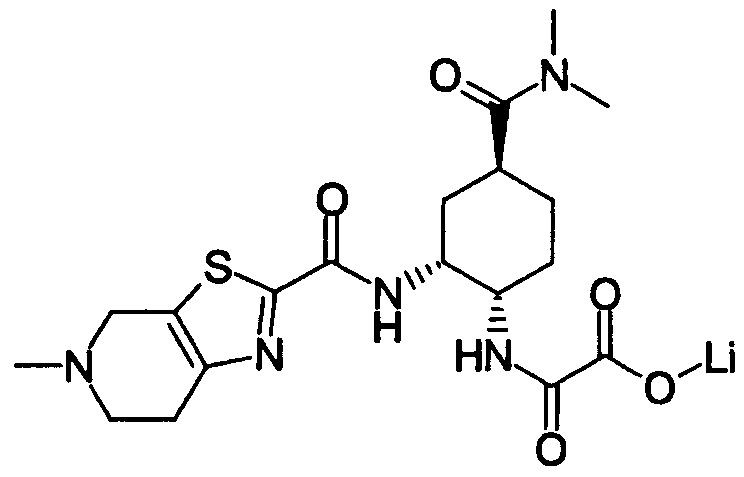
Соединение (1,13 г), полученное в ссылочном примере 269, растворяли в тетрагидрофуране (20 мл), метаноле (10 мл) и воде (10 мл), добавляли гидроксид лития (58 мг) и смесь перемешивали при комнатной температуре в течение 30 минут. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (1,10 г).
1Н-ЯМР (ДМСО-d6) δ: 1,41-1,73 (4H, м), 2,00-2,07 (2H, м), 2,39 (3H, с), 2,74-2,99 (11H, м), 3,67 (2H, с), 3,82-3,88 (1H, м), 4,28-4,30 (1H, м), 8,66-8,70 (2H, м).
[Ссылочный пример 271]
N-{(1R,2S,5S)-2-Азидо-5-[(диметиламино)карбонил]циклогексил}-5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-карбоксамид
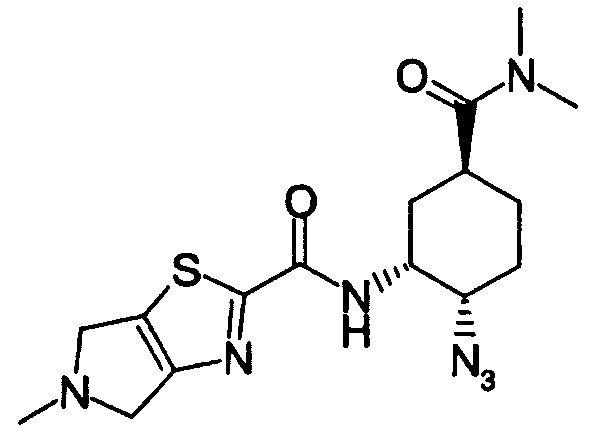
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 293, и соединения, полученного в ссылочном примере 251, подобно способу, описанному в ссылочном примере 252.
1Н-ЯМР (CDCl3) δ: 1,73-1,87 (4H, м), 2,11-2,20 (2H, м), 2,67 (3H, с), 2,85-2,90 (1H, м), 2,93 (3H, с), 3,00 (3H, с), 3,90-4,10 (5H, м), 4,57-4,62 (1H, м), 7,20-7,22 (1H, м).
МС (FAB) m/z: 378 (М+Н)+.
[Ссылочный пример 272]
N-{(1R,2S,5S)-2-Амино-5-[(диметиламино)карбонил]циклогексил}-5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-карбоксамид
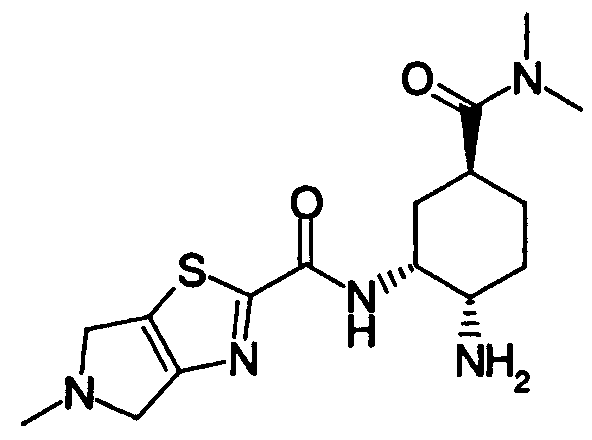
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 271, подобно способу, описанному в ссылочном примере 253.
1Н-ЯМР (CDCl3) δ: 1,67-1,97 (6H, м), 2,36-2,40 (1H, м), 2,67 (3H, с), 2,92 (3H, с), 3,00 (3H, с), 3,07-3,18 (1H, м), 3,92-3,95 (2H, м), 4,02-4,06 (2H, м), 4,23-4,26 (1H, м), 7,50-7,52 (1H, м).
[Ссылочный пример 273]
Метил 5-хлор-4-фториндол-2-карбоксилат
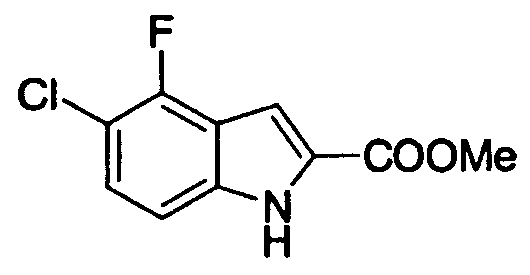
Этанол (100 мл) добавляли к гидриду натрия (содержание: 60%, 4,7 г) при 0°C в атмосфере аргона и смесь перемешивали 10 минут. После добавления к реакционной смеси 2-нитропропана (11 мл) и перемешивания смеси в течение 10 минут добавляли 1-(бромметил)-3-хлор-2-фторбензол (10 г) и смесь перемешивали при комнатной температуре в течение 3,5 часов. Осадок удаляли фильтрованием и фильтрат концентрировали при пониженном давлении. Остаток распределяли между диэтиловым эфиром и водой, органический слой последовательно промывали 1N водным раствором гидроксида натрия, водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 3:7) с получением неочищенного 3-хлор-2-фторбензальдегида (5,5 г) в виде бледно-желтого масла. Метанол (20 мл) добавляли к гидриду натрия (содержание: 60%, 1,6 г) при 0°C в атмосфере аргона и смесь перемешивали 10 минут. Реакционную смесь охлаждали до -20°C и добавляли в течение 20 минут неочищенный 3-хлор-2-фторбензальдегид (5,5 г) и раствор метил 2-азидоацетата (5,0 г) в метаноле (10 мл). Температуру реакционной смеси повышали до 0°C и после перемешивания смеси в течение 2,5 часов добавляли воду (40 мл). Реакционную смесь концентрировали при пониженном давлении, остаток экстрагировали смешанным растворителем метиленхлорид/этилацетат. Экстракт промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (толуол:гексан = 3:17) с получением неочищенного метил 2-азидо-3-[(3-хлор-2-фтор)фенил]акрилата (2,6 г). Полученный продукт растворяли в ксилоле (50 мл) и раствор перемешивали при 130°C-140°C в течение 3 часов. Реакционную смесь концентрировали и полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид), затем кристаллизовали из смеси диэтиловый эфир-гексан с получением указанного в заголовке соединения (440 мг).
1Н-ЯМР (ДМСО-d6) δ: 4,08 (3Н, с), 7,20 (1Н, с), 7,31-7,38 (2Н, м).
МС (FAB) m/z: 228 (M+H)+.
[Ссылочный пример 274]
5-Хлор-4-фториндол-2-карбоновая кислота
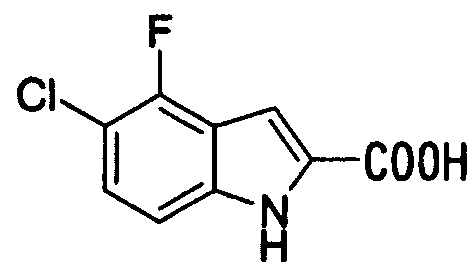
Соединение (440 мг), полученное в ссылочном примере 273, растворяли в тетрагидрофуране (10 мл), добавляли водный раствор (5 мл) гидроксида лития (160 мг) и смесь перемешивали при комнатной температуре в течение 3 часов. К реакционной смеси дополнительно добавляли водный раствор (5 мл) гидроксида лития (240 мг) и смесь перемешивали еще 1 час, затем реакционную смесь концентрировали при пониженном давлении. Остаток нейтрализовали 1N хлористоводородной кислотой и экстрагировали 3 раза этилацетатом. Полученные органические слои объединяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (390 мг).
1Н-ЯМР (ДМСО-d6) δ: 6,79 (1H, с), 7,16-7,26 (2H, м).
МС (FAB) m/z: 214 (М+Н)+.
[Ссылочный пример 275]
Этил 1-бензил-5-хлориндол-2-карбоксилат
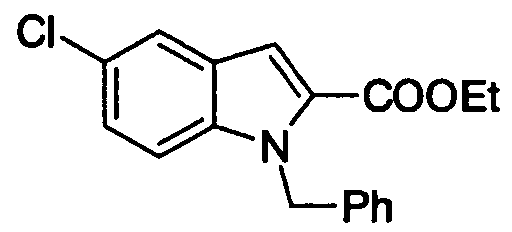
Этил 5-хлориндол-2-карбоксилат (1,4 г) растворяли в N,N-диметилформамиде (30 мл) и добавляли карбонат калия (2,9 г) и бензилхлорид (2,4 мл). Смесь нагревали и перемешивали в течение 1,5 часов на горячей бане, отрегулированной на 100°C. Реакционную смесь концентрировали при пониженном давлении и остаток вливали в ледяную воду и экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли, остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:19) и кристаллизовали из смеси диэтиловый эфир-гексан с получением указанного в заголовке соединения (1,6 г).
1Н-ЯМР (CDCl3) δ: 1,36 (3H, т, J=7,1Гц), 4,33 (2H, кв, J=7,1Гц), 5,83 (2H, с), 7,00-7,02 (2H, д), 7,20-7,38 (6H, м), 7,67 (1H, д, J=1,7Гц).
[Ссылочный пример 276]
Этил 1-бензил-5-хлор-3-фториндол-2-карбоксилат
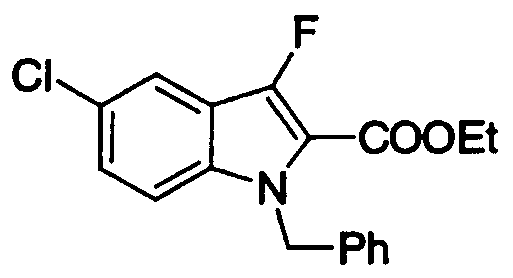
Трифлат 1-фтор-2,6-дихлорпиридиния (4,4 г) добавляли к раствору соединения (2,2 г), полученного в ссылочном примере 275, в метиленхлориде (30 мл) и смесь кипятили с обратным холодильником в течение 3 суток. Реакционную смесь распределяли между этилацетатом и водой и водный слой экстрагировали этилацетатом. Полученные органические слои объединяли, последовательно промывали 1N хлористоводородной кислотой, водой и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:24) с получением неочищенного указанного в заголовке соединения (2,8 г). Часть данного продукта очищали препаративной тонкослойной хроматографией на силикагеле с получением указанного в заголовке соединения.
1Н-ЯМР (ДМСО-d6) δ: 1,25 (3H, т, J=7,1Гц), 4,29 (2H, кв, J=7,1Гц), 5,77 (2H, с), 6,97-6,99 (2H, м), 7,18-7,28 (3H, м), 7,39 (1H, дд, J=9,0, 2,1Гц), 7,69 (1H, дд, J=9,0, 2,1Гц), 7,78 (1H, д, J=2,1Гц).
[Ссылочный пример 277]
Этил 5-хлор-3-фториндол-2-карбоксилат
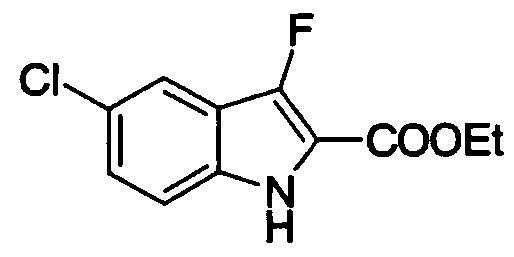
Неочищенное соединение (1,4 г), полученное в ссылочном примере 276, растворяли в анизоле (30 мл) и к раствору добавляли порциями при охлаждении льдом хлорид алюминия (2,9 г). Реакционную смесь перемешивали при комнатной температуре в течение 30 минут, добавляли еще хлорид алюминия (2,9 г) и смесь перемешивали 18 часов. Добавляли к реакционной смеси хлорид алюминия (8,0 г), перемешивали смесь в течение 5 часов, затем добавляли воду. Реакционную смесь экстрагировали этилацетатом, полученные органические слои объединяли, последовательно промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид) с получением указанного в заголовке соединения (470 мг).
1Н-ЯМР (CDCl3) δ: 1,43 (3H, т, J=7,2Гц), 4,45 (2H, кв, J=7,2Гц), 7,25-7,31 (2H, м), 7,66 (1H, д, J=0,73Гц), 8,53 (1H, шир.с).
МС (FAB) m/z: 242 (М+Н)+.
[Ссылочный пример 278]
5-Хлор-3-фториндол-2-карбоновая кислота
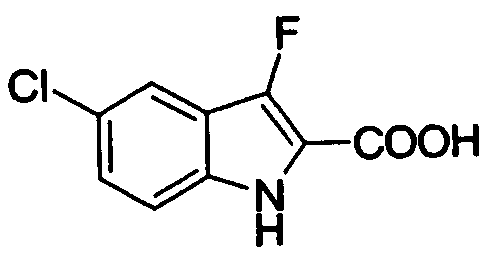
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 277, подобно способу ссылочного примера 274.
1Н-ЯМР (ДМСО-d6) δ: 7,31 (1Н, дд, J=8,8, 1,9Гц), 7,42 (1Н, дд, J=8,8, 1,9Гц), 7,70 (1Н, д, J=1,9Гц), 11,78 (1Н, с).
МС (FAB) m/z: 214 (M+H)+.
[Ссылочный пример 279]
трет-Бутил (1R,2S,5S)-{[(5-хлор-3-фториндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}карбамат
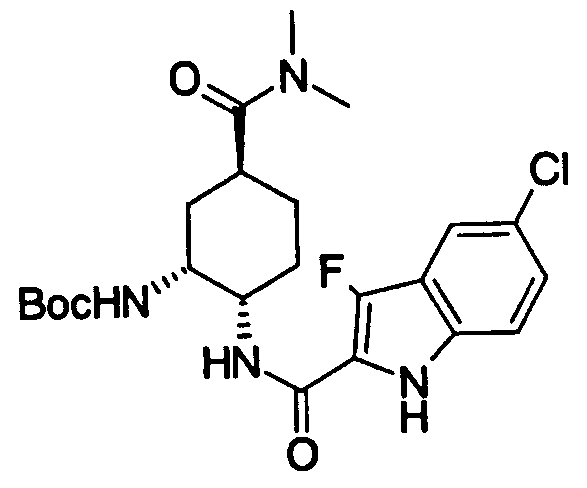
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и соединения, полученного в ссылочном примере 278, подобно способу, описанному в ссылочном примере 97.
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,73-2,11 (6H, м), 2,65 (1H, шир.с), 2,96 (3H, с), 3,07 (3H, с), 4,20 (1H, шир.с), 4,28 (1H, шир.с), 4,78 (1H, шир.), 7,23-7,30 (3H, м), 7,58 (1H, с), 9,03 (1H, с).
МС (FAB) m/z: 481 (М+Н)+.
[Ссылочный пример 280]
Этил 3-бром-5-хлориндол-2-карбоксилат
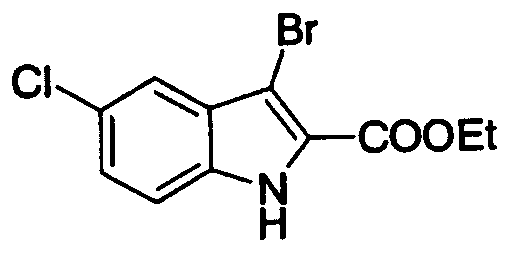
N-Бромсукцинимид (440 мг) добавляли к раствору этил 5-хлориндол-2-карбоксилата (500 мг) в N,N-диметилформамиде (10 мл). Реакционную смесь перемешивали при комнатной температуре в течение 18 часов и отгоняли при пониженном давлении растворитель. Остаток распределяли между этилацетатом и водой и водный слой экстрагировали этилацетатом. Полученные органические слои объединяли, промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли, остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 1:9) и полученный белый порошок промывали гексаном с получением указанного в заголовке соединения (680 мг).
1Н-ЯМР (CDCl3) δ: 1,42-1,48 (3H, м), 4,43-4,49 (2H, м), 7,30-7,32 (2H, м), 7,65 (1H, д, J=0,74Гц), 9,11 (1H, с)
МС (FAB) m/z; 303 (М+Н)+.
[Ссылочный пример 281]
3-Бром-5-хлориндол-2-карбоновая кислота
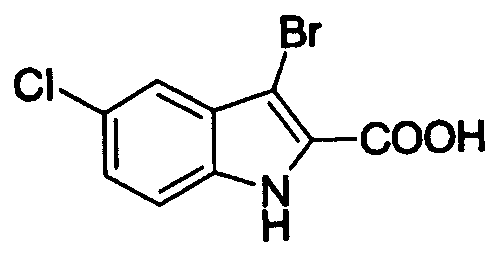
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 280, подобно способу ссылочного примера 274.
1Н-ЯМР (ДМСО-d6) δ: 7,35 (1Н, дд, J=8,8, 2,0Гц), 7,48-7,53 (2Н, м), 12,33 (1Н, с).
МС (FAB) m/z: 275 (M+H)+.
[Ссылочный пример 282]
трет-Бутил (1R,2S,5S)-2-{[(3-бром-5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
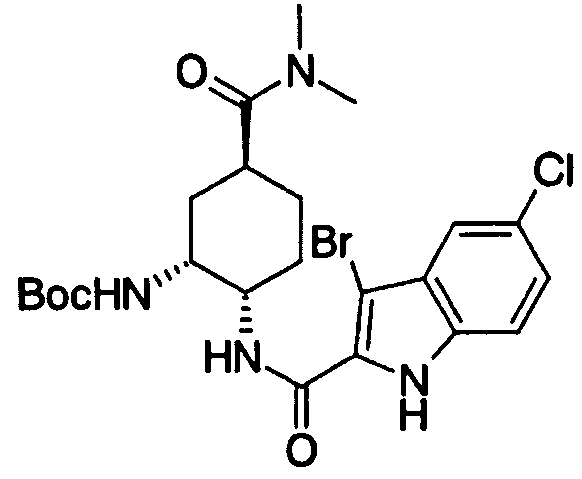
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и соединения, полученного в ссылочном примере 281, подобно способу, описанному в ссылочном примере 97.
1Н-ЯМР (CDCl3) δ: 1,42 (9H, с), 1,58-2,17 (6H, м), 2,70 (1H, шир.с), 2,96 (3H, с), 3,07 (3H, с), 4,23-4,28 (2H, м), 4,83 (1H, шир.), 7,34-7,41 (3H, м), 7,52 (1H, с), 9,76 (1H, с).
МС (FAB) m/z: 542 (М+Н)+.
[Ссылочный пример 283]
Этил 3-хлор-5-фториндол-2-карбоксилат
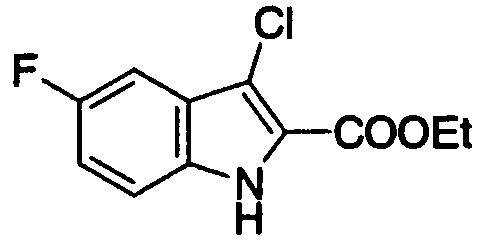
Этил 5-фториндол-2-карбоксилат (2,0 г) растворяли в N,N-диметилформамиде (20 мл) и к раствору добавляли по каплям при охлаждении льдом раствор N-хлорсукцинимида (1,4 г) в N,N-диметилформамиде (10 мл). Смесь перемешивали при комнатной температуре в течение 18 часов и реакционную смесь разбавляли этилацетатом и последовательно промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Затем полученный органический слой сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 5:1) с получением указанного в заголовке соединения (1,9 г).
1Н-ЯМР (CDCl3) δ: 1,45 (3H, т, J=7,4Гц), 4,46 (2H, кв, J=7,4Гц), 7,14 (1H, дт, J=8,0, 2,7Гц), 7,32-7,36 (2H, м), 8,91 (1H, шир.).
[Ссылочный пример 284]
3-Хлор-5-фториндол-2-карбоновая кислота
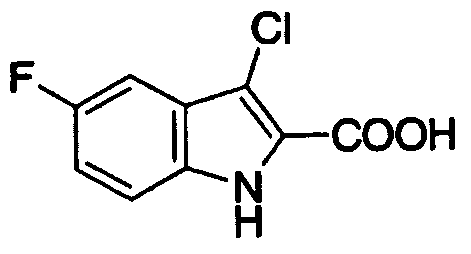
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 283, подобно способу ссылочного примера 274.
1Н-ЯМР (ДМСО-d6) δ: 7,20 (1H, дт, J=8,8, 2,4Гц), 7,31 (1H, дд, J=8,8, 2,4Гц), 7,46 (1H, дд, J=8,8, 4,4Гц), 12,12 (1H, шир.).
[Ссылочный пример 285]
Этил 5-хлор-3-формилиндол-2-карбоксилат
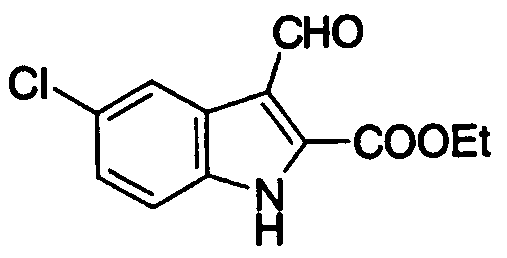
После добавления оксихлорида фосфора (2,0 мл) к N-метилформанилиду (2,9 г) и перемешивания смеси в течение 15 минут добавляли 1,2-дихлорэтан (50 мл) и этил 5-хлориндол-2-карбоксилат (4,0 г) и полученную смесь кипятили с обратным холодильником в течение 1 часа. Реакционную смесь вливали в водный раствор (28 мл) ацетата натрия (14 г) при охлаждении льдом. После перемешивания в течение 18 часов отфильтровывали нерастворимое вещество. Полученный продукт последовательно промывали водой и диэтиловым эфиром с получением указанного в заголовке соединения (3,56 г).
1Н-ЯМР (CDCl3) δ: 1,38 (3H, т, J=7,1Гц), 4,44 (2H, кв, J=7,1Гц), 7,38 (1H, дд, J=8,0, 1,4Гц), 7,56 (1H, д, J=8,0Гц), 8,19 (1H, д, J=1,4Гц), 10,53 (1H, с).
[Ссылочный пример 286]
5-хлор-3-формилиндол-2-карбоновая кислота
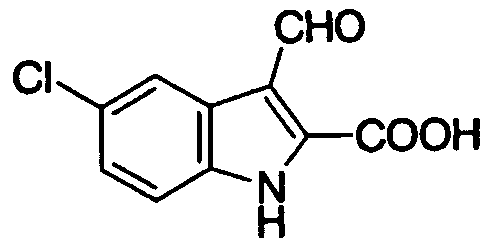
Соединение (1,0 г), полученное в ссылочном примере 285, растворяли в этаноле (10 мл), к раствору добавляли по каплям 1N водный раствор (10 мл) гидроксида натрия и смесь перемешивали при 50°C в течение 2 часов. Добавляли к реакционной смеси 1N хлористоводородную кислоту (11 мл), полученную смесь перемешивали и нерастворимое вещество отфильтровывали с получением указанного в заголовке соединения (0,86 г).
1Н-ЯМР (ДМСО-d6) δ: 7,39 (1H, д, J=8,0Гц), 7,55 (1H, д, J=8,0Гц), 8,20 (1H, с), 10,58 (1H, с), 12,90 (1H, шир.).
[Ссылочный пример 287]
5-Хлор-2-этоксикарбонилиндол-3-карбоновая кислота
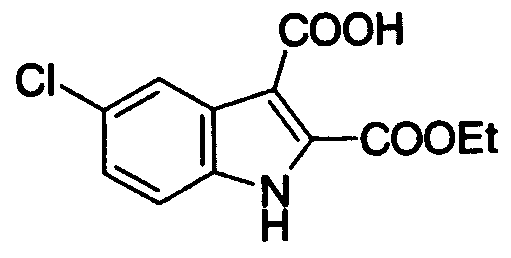
Соединение (1,5 г), полученное в ссылочном примере 286, и сульфаминовую кислоту (1,7 г) растворяли в смеси трет-бутанол (30 мл)-вода (30 мл), к раствору добавляли хлорит натрия (1,6 г) и смесь перемешивали в течение 8 часов. Реакционную смесь разбавляли водой, экстрагировали этилацетатом, экстракт последовательно промывали 1N хлористоводородной кислотой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток перекристаллизовывали из смешанного растворителя изопропиловый эфир/гексан с получением указанного в заголовке соединения (0,7 г).
1Н-ЯМР (ДМСО-d6) δ: 1,34 (3H, т, J=7,1Гц), 4,38 (2H, кв, J=7,1Гц), 7,33 (1H, дд, J=8,0, 1,4Гц), 7,52 (1H, д, J=8,0Гц), 7,97 (1H, д, J=1,4Гц), 12,75 (1H, шир.).
[Ссылочный пример 288]
Этил 5-хлор-3-[(диметиламино)карбонил]индол-2-карбоксилат
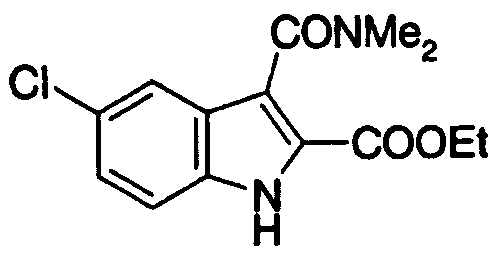
Соединение (0,7 г), полученное в ссылочном примере 287, растворяли в N,N-диметилформамиде (10 мл), к раствору добавляли гидрохлорид диметиламина (0,26 мл), моногидрат 1-гидроксибензотриазола (0,43 г) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (1,0 г) и смесь перемешивали при комнатной температуре в течение 2 суток. Затем реакционную смесь разбавляли этилацетатом и промывали 1N хлористоводородной кислотой, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия в указанном порядке, полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток перекристаллизовывали из смешанного растворителя изопропиловый эфир/гексан с получением указанного в заголовке соединения (0,6 г).
1Н-ЯМР (ДМСО-d6) δ: 1,29 (3H, т, J=7,1Гц), 2,78 (3H, с), 3,04 (3H, с), 4,30 (2H, кв, J=7,1Гц), 7,31 (1H, дд, J=8,0, 1,4Гц), 7,45 (1H, д, J=1,4Гц), 7,48 (1H, д, J=8,0Гц), 12,29 (1H, с).
[Ссылочный пример 289]
5-Хлор-3-[(диметиламино)карбонил]индол-2-карбоновая кислота
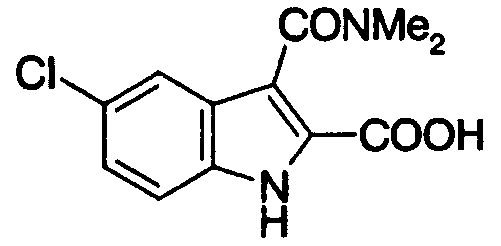
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 288, подобно способу ссылочного примера 286.
1Н-ЯМР (ДМСО-d6) δ: 2,91 (6H, с), 7,29 (1H, д, J=8,0Гц), 7,44 (1H, д, J=8,0Гц), 7,47 (1H, с), 12,16 (1H, с).
[Ссылочный пример 290]
5-(Фенилсульфонил)-5,6-дигидро-4Н-пирроло[3,4-d]тиазол
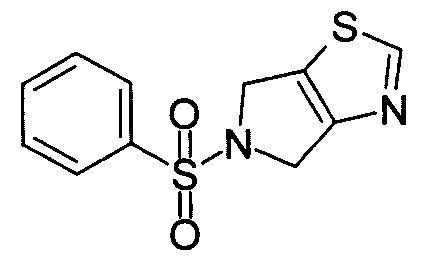
Бензолсульфонамид (638 мг) и 4,5-бис(бромметил)тиазол (M. Al. Hariri, O. Galley, F. Pautet, H. Fillion, Eur. J. Org. Chem., 1998, 593-594) (1,10 г) растворяли в N,N-диметилформамиде (10 мл), добавляли весь гидрид натрия (60% в масле, 357 мг) и смесь перемешивали при комнатной температуре в течение 3 часов. Добавляли воду и метиленхлорид, проводя разделение жидкостей. Полученный органический слой сушили над безводным сульфатом натрия, отгоняли растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:этилацетат = 9:1) с получением указанного в заголовке соединения (137 мг).
1Н-ЯМР (CDCl3) δ: 4,60-4,63 (2H, м), 4,70-4,73 (2H, м), 7,52-7,64 (3H, м), 7,88-7,92 (2H, м), 8,71 (1H, с).
МС (FAB) m/z: 267 (М+Н)+.
[Ссылочный пример 291]
Дигидробромид 5,6-дигидро-4Н-пирроло[3,4-d]тиазола
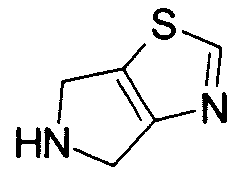
Смесь соединения (800 мг), полученного в ссылочном примере 290, фенола (800 мкл) и 47% бромистоводородной кислоты (5,00 мл) кипятили с обратным холодильником в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры добавляли этилацетат и воду, проводя разделение жидкостей. Полученный водный слой концентрировали при пониженном давлении. К остатку добавляли этилацетат и осадок отфильтровывали с получением указанного в заголовке соединения (521 мг).
1Н-ЯМР (ДМСО-d6) δ: 4,42 (2Н, шир.с), 4,56 (2Н, шир.с), 9,14 (1Н, с).
МС (FAB) m/z: 127 (M+H)+.
[Ссылочный пример 292]
5-Метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол
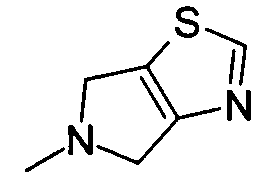
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 291, подобно способу ссылочного примера 9.
1Н-ЯМР (CDCl3) δ: 2,67 (3Н, с), 3,95-3,99 (2Н, м), 4,01-4,05 (2Н, м), 8,69 (1Н, с).
МС (ESI) m/z: 141 (M+H)+.
[Ссылочный пример 293]
5-Метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-карбоксилат лития
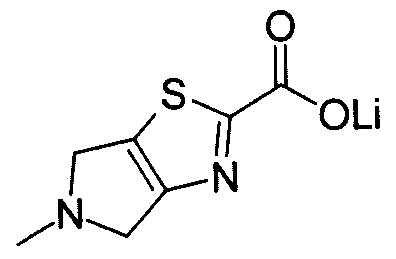
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 292, подобно способу ссылочного примера 5.
1Н-ЯМР (ДМСО-d6) δ: 2,52 (3H, с), 3,73 (2H, т, J=3,2Гц), 3,87 (2H, т, J=3,2Гц).
[Ссылочный пример 294]
трет-Бутил (1R,2S,5S)-2-[(6-хлор-2-нафтоил)амино]-5-[(диметиламино)карбонил]циклогексилкарбамат
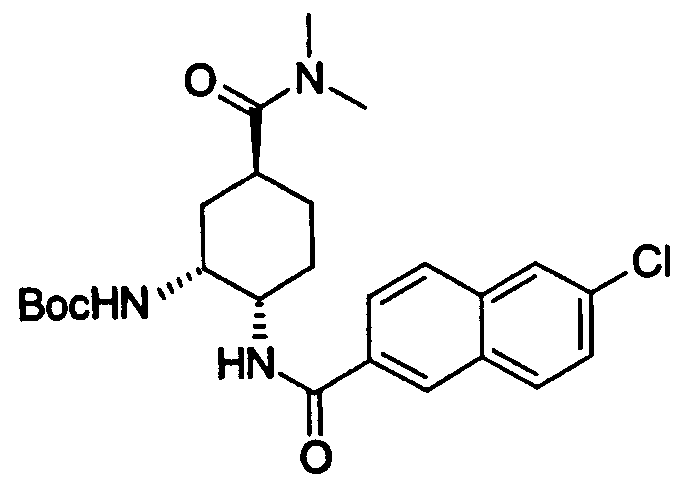
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и 6-хлорнафталин-2-карбоновой кислоты (Eur. J. Chem-Chim. Ther., 1984, Vol. 19, pp. 205-214) подобно способу, описанному в ссылочном примере 97.
1Н-ЯМР (CDCl3) δ: 1,30-2,00 (15H, м), 2,60-2,80 (1H, м), 2,96 (3H, с), 3,09 (3H, с), 4,00-4,20 (1H, м), 4,20-4,30 (1H, м), 4,75-4,95 (1H, м), 7,44 (1H, д, J=9,0Гц), 7,70-7,95 (5H, м), 8,31 (1H, с).
МС (FAB) m/z: 474 (М+Н)+.
[Ссылочный пример 295]
Этил (Е)-3-(морфолин-4-ил)-2-акрилат
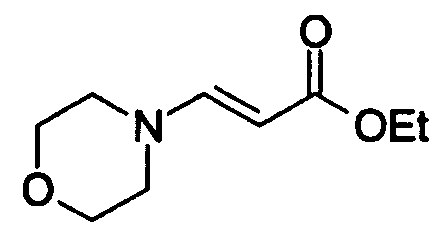
Этилпропионат (2,0 мл) растворяли в метиленхлориде (20 мл) и добавляли по каплям при охлаждении льдом морфолин (1,70 мл). После перемешивания при комнатной температуре в течение 1 часа реакционную смесь концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1) с получением указанного в заголовке соединения (3,72 г).
1Н-ЯМР (CDCl3) δ: 1,26 (3H, т, J=7,1Гц), 3,21 (4H, т, J=5,1Гц), 3,71 (4H, т, J=5,1Гц), 4,14 (2H, кв, J=7,1Гц), 4,70 (1H, д, J=13,4Гц), 7,36 (1H, д, J=13,4Гц).
МС (FAB) m/z: 186 (M+H)+.
[Ссылочный пример 296]
Тетрафторборат 3-хлорбензолдиазония
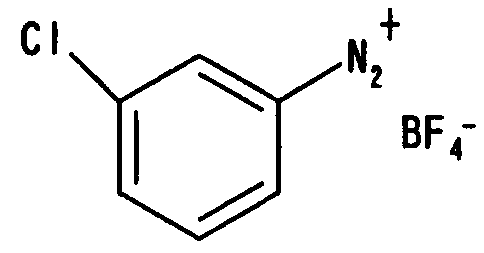
3-Хлоранилин (2,0 г) растворяли в смешанном растворителе из воды (30 мл) и концентрированной хлористоводородной кислоты (3,5 мл), добавляли при охлаждении льдом нитрит натрия (1,30 г) и смесь перемешивали в течение 10 минут. После добавления к реакционной смеси концентрированной хлористоводородной кислоты (5,3 мл) и тетрафторбората натрия (6,90 г) смесь перемешивали 30 минут при охлаждении льдом, осадок отфильтровывали и промывали водой, метанолом и диэтиловым эфиром с получением указанного в заголовке соединения (2,63 г). Полученное соединение непосредственно использовали в следующей реакции.
[Ссылочный пример 297]
Этил 7-хлорциннолин-3-карбоксилат
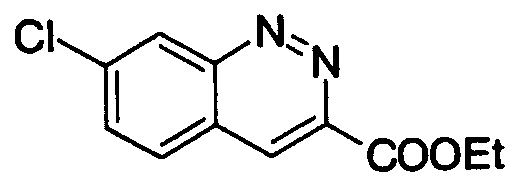
Соединение (1,45 г), полученное в ссылочном примере 295, растворяли в ацетонитриле (100 мл) и добавляли соединение (1,73 г), полученное в ссылочном примере 296. После перемешивания при комнатной температуре в течение 1 часа смесь кипятили с обратным холодильником в течение 7 суток. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид → метиленхлорид:этилацетат = 10:1, затем гексан:этилацетат = 4:1 → 1:1) с получением указанного в заголовке соединения (0,25 г).
1Н-ЯМР (CDCl3) δ: 1,53 (3H, т, J=7,1Гц), 4,62 (2H, кв, J=7,1Гц), 7,80 (1H, дд, J=8,8, 2,0Гц), 7,95 (1H, д, J=8,8Гц), 8,64 (1H, с), 8,68 (1H, д, J=2,0Гц).
[Ссылочный пример 298]
7-Хлорциннолин-3-карбоновая кислота
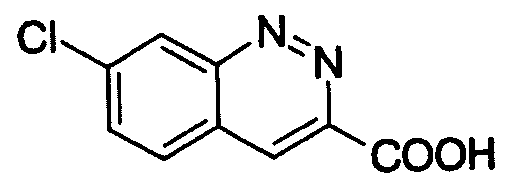
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 297, подобно способу ссылочного примера 286.
1Н-ЯМР (ДМСО-d6) δ: 8,02 (1H, дд, J=8,8, 2,0Гц), 8,34 (1H, д, J=8,8Гц), 8,70 (1H, с), 8,90 (1H, с).
МС (FAB) m/z: 209 (M+H)+.
[Ссылочный пример 299]
трет-Бутил (1R,2S,5S)-2-{[(7-хлорциннолин-3-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
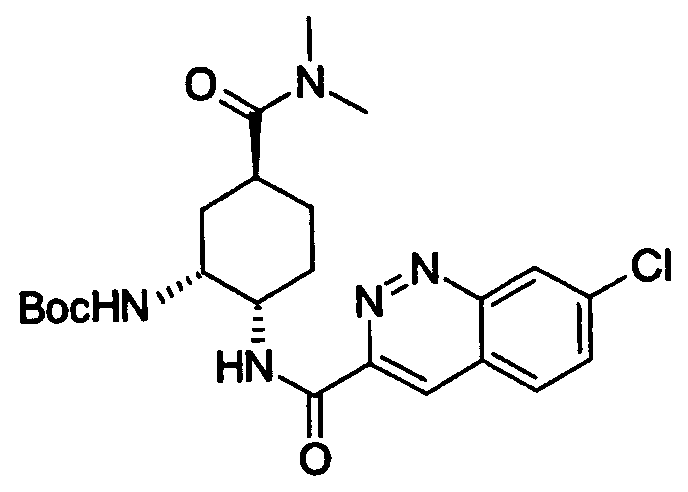
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и соединения, полученного в ссылочном примере 298, подобно способу ссылочного примера 97.
1Н-ЯМР (CDCl3) δ: 1,36 (9H, с), 1,80-2,20 (5H, м), 2,72 (1H, м), 2,96 (3H, с), 3,07 (3H, с), 3,49 (1H, д, J=3,7Гц), 4,30-4,45 (2H, м), 4,87 (1H, шир.), 7,77 (1H, дд, J=8,8, 2,0Гц), 7,96 (1H, д, J=8,8Гц), 8,59 (2H, шир.), 8,72 (1H, с),
МС (FAB) m/z: 476 (M+H)+.
[Ссылочный пример 300]
трет-Бутил (1R,2S,5S)-2-{[(5-хлор-1Н-бензимидазол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
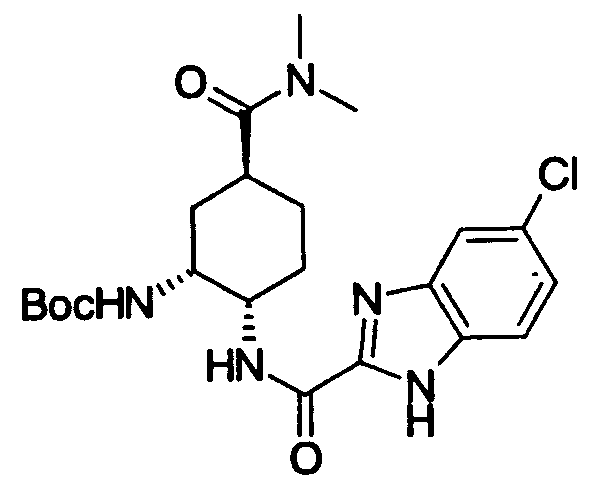
10% Палладий на углероде (50 мг) добавляли к раствору соединения (235 мг), полученного в ссылочном примере 143, в тетрагидрофуране (5,0 мл) и смесь перемешивали в течение ночи при комнатной температуре в атмосфере водорода. К раствору продукта, полученного фильтрованием реакционной смеси и концентрированием фильтрата, и 5-хлорбензимидазол-2-карбоновой кислоты (Bull. Chem. Soc. Jpn., Vol. 62, p. 2668, 1989) (165 мг) в N,N-диметилформамиде (5,0 мл) добавляли моногидрат 1-гидроксибензотриазола (100 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (171 мг) при комнатной температуре и смесь перемешивали в течение 4 суток. После концентрирования реакционной смеси добавляли метиленхлорид, насыщенный водный раствор гидрокарбоната натрия и воду, проводя разделение жидкостей, и полученный водный слой экстрагировали метиленхлоридом. Полученные органические слои объединяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной флэш-хроматографией на силикагеле (метиленхлорид:метанол = 10:1) с получением указанного в заголовке соединения (250 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,01-2,00 (6H, м), 1,34 (9H, с), 2,79 (3H, с), 2,80-2,95 (1H, м), 2,98 (3H, с), 3,89-4,06 (2H, м), 7,08 (1H, д, J=6,6Гц), 7,31 (1H, д, J=8,5Гц), 7,62 (2H, шир.с), 8,47 (1H, д, J=8,5Гц), 13,46 (1H, шир.с).
МС (ESI) m/z: 466 (M+H)+.
[Ссылочный пример 301]
Метил 3-(4-фторфенил)-2-{[(4-метилфенил)сульфонил]амино}пропионат
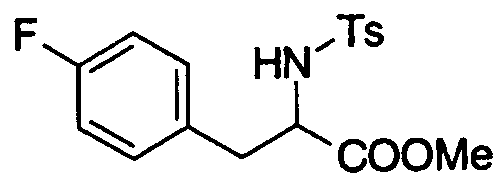
Метил 2-амино-3-(4-фторфенил)пропионат (2,01 г), п-толуолсульфонилхлорид (2,25 г) и 4-диметиламинопиридин (309 мг) растворяли в хлороформе (30 мл), добавляли пиридин (3,0 мл) и смесь кипятили с обратным холодильником в течение 4,5 часов. Добавляли еще п-толуолсульфонилхлорид (2,20 г) и смесь кипятили с обратным холодильником в течение 3,5 часов. Реакционную смесь вливали в 1N хлористоводородную кислоту (17 мл) со льдом для разделения жидкостей. Полученный органический слой последовательно промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 9:1 → 2:1) с получением указанного в заголовке соединения (2,89 г).
1Н-ЯМР (CDCl3) δ: 2,41 (3H, с), 2,90-3,10 (2H, м), 3,51 (3H, с), 4,10-4,20 (1H, м), 5,04 (1H, д, J=9,0Гц), 6,85-6,95 (2H, м), 7,00-7,10 (2H, м), 7,20-7,30 (2H, м), 7,60-7,70 (2H, м).
МС (ESI) m/z: 352 (М+Н)+.
[Ссылочный пример 302]
Метил 7-фтор-2-[(4-метилфенил)сульфонил]-1,2,3,4-тетрагидроизохинолин-3-карбоксилат
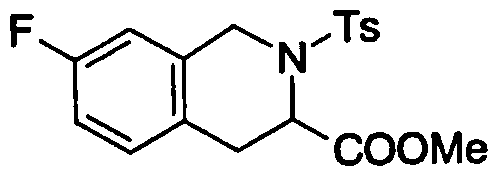
Соединение (1,50 г), полученное в ссылочном примере 301, и параформ (207 мг) растворяли в хлороформе (40 мл) и систему продували аргоном. Затем добавляли комплекс (1,20 мл) трифторборан-диэтиловый эфир и смесь перемешивали при комнатной температуре в течение 7,5 часов. Реакционную смесь вливали в насыщенный водный раствор гидрокарбоната натрия со льдом для разделения жидкостей. Затем полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1) с получением указанного в заголовке соединения (1,45 г).
1Н-ЯМР (CDCl3) δ: 2,42 (3H, с), 3,15 (2H, д, J=3,9Гц), 3,46 (3H, с), 4,45 (1H, д, J=15,9Гц), 4,69 (1H, д, J=15,9Гц), 5,01 (1H, т, J=4,4Гц), 6,70-6,80 (1H, м), 6,80-6,90 (1H, м), 7,00-7,10 (1H, м), 7,29 (2H, д, J=8,1Гц), 7,72 (2H, д, J=8,3Гц).
МС (ESI) m/z: 364 (М+Н)+.
[Ссылочный пример 303]
Метил 7-фторизохинолин-3-карбоксилат
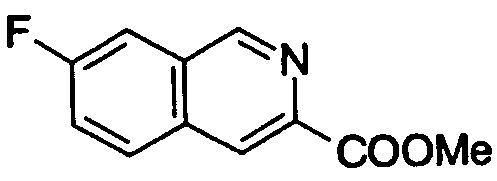
Соединение (1,45 г), полученное в ссылочном примере 302, растворяли в N,N-диметилформамиде (40 мл). В полученный раствор вводили кислород и раствор перемешивали при 100°C в течение 3,5 часов. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей, затем полученный органический слой последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 1:1) с получением указанного в заголовке соединения (0,59 г).
1Н-ЯМР (CDCl3) δ:4,07 (3H, с), 7,55-7,65 (1H, м), 7,65-7,75 (1H, м), 8,00-8,05 (1H, м), 8,61 (1H, с), 9,30 (1H, с).
МС (ESI) m/z: 206 (M+H)+.
[Ссылочный пример 304]
Гидрохлорид 7-фторизохинолин-3-карбоновой кислоты
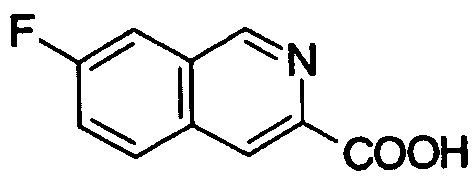
Соединение (1,45 г), полученное в ссылочном примере 303, растворяли в концентрированной хлористоводородной кислоте (18 мл) и раствор кипятили с обратным холодильником в течение 2,5 часов. Реакционную смесь охлаждали и кристаллы отфильтровывали, промывали водой и затем сушили с получением указанного в заголовке соединения (0,46 г).
1Н-ЯМР (ДМСО-d6) δ: 7,90-8,00 (1H, м), 8,15-8,25 (1H, м), 8,40-8,50 (1H, м), 8,82 (1H, с), 9,55 (1H, с).
МС (FAB) m/z: 192 (М+Н)+.
[Ссылочный пример 305]
Этил 7-хлор-2Н-хромен-3-карбоксилат
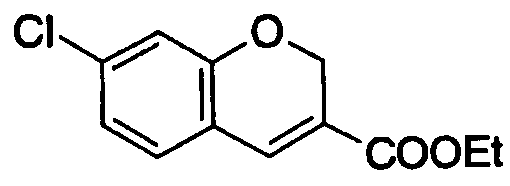
4-Хлор-2-гидроксибензальдегид (Acta. Chem. Scand., Vol. 53, p. 258, 1999) (510 мг) растворяли в тетрагидрофуране (40 мл), добавляли гидрид натрия (60% в масле, 157 мг) и смесь перемешивали при комнатной температуре в течение 2 часов. Добавляли к реакционной смеси тетрагидрофурановый раствор (10 мл) этил 2-диэтилфосфоноакрилата (J. Org. Chem., Vol. 43, p. 1256, 1978) (769 мг) и полученную смесь перемешивали при комнатной температуре в течение 2 часов и затем кипятили с обратным холодильником в течение ночи. После охлаждения реакционной смеси до комнатной температуры добавляли воду и диэтиловый эфир для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 10:1) с получением указанного в заголовке соединения (247 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,33 (3H, т, J=7,1Гц), 4,27 (2H, кв, J=7,1Гц), 4,99 (2H, д, J=1,2Гц), 6,85 (1H, д, J=1,2Гц), 6,89 (1H, дд, J=8,1, 2,0Гц), 7,04 (1H, д, J=8,1Гц), 7,38 (1H, д, J=1,0Гц).
МС (EI) m/z: 238 (М+).
[Ссылочный пример 306]
7-Хлор-2Н-хромен-3-карбоновая кислота
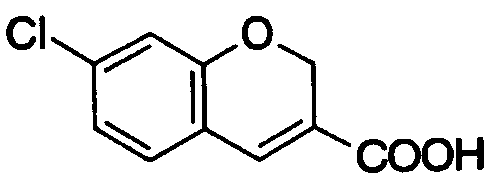
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 305, подобно способу ссылочного примера 274.
1Н-ЯМР (ДМСО-d6) δ: 4,92 (1H, д, J=2,0Гц), 6,95 (1H, д, J=2,0Гц), 7,01 (1H, дд, J=8,1, 2,2Гц), 7,35 (1H, д, J=8,1Гц), 7,44 (1H, с).
МС (EI) m/z: 210 М+.
[Ссылочный пример 307]
трет-Бутил (1R,2S,5S)-2-{[(Е)-(4-хлорфенил)-2-пропеноил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
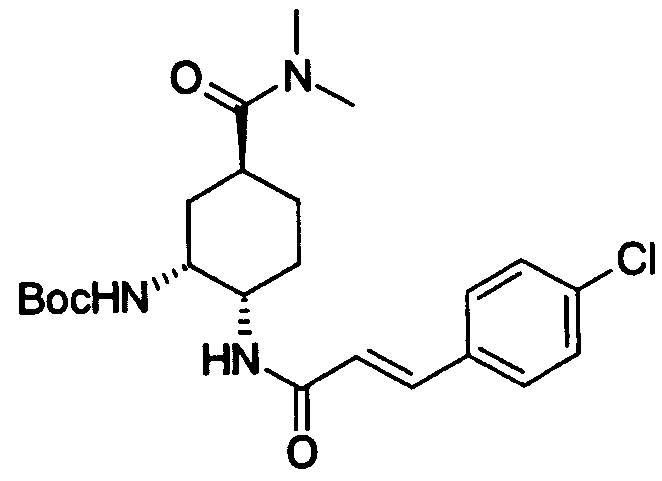
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и 4-хлоркоричной кислоты подобно способу ссылочного примера 97.
1Н-ЯМР (CDCl3) δ: 1,30-1,55 (3H, м), 1,48 (9H, с), 1,60-2,30 (4H, м), 2,57-2,70 (1H, м), 2,95 (3H, с), 3,06 (3H, с), 4,01 (1H, шир.с), 4,10-4,20 (1H, м), 4,78 (1H, шир.с), 6,30 (1H, д, J=15,6 Гц), 7,02 (1H, с), 7,31 (2H, д, J=8,5 Гц), 7,40 (2H, д, J=8,5 Гц), 7,52 (1H, д, J=15,6 Гц).
МС (ESI)m/z: 450 (М+Н)+.
[Ссылочный пример 308]
Метил 6-хлор-4-оксо-1,4-дигидрохинолин-2-карбоксилат
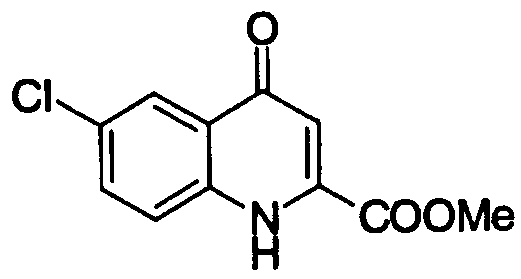
Диметилацетилендикарбоксилат (13,5 мл) добавляли к раствору 4-хлоранилина (12,76 г) в метаноле (150 мл) и смесь кипятили с обратным холодильником в течение 8 часов. Реакционную смесь концентрировали при пониженном давлении, остаток растворяли в дифениловом эфире (70 мл) и раствор кипятили с обратным холодильником при 240°C в течение 4 часов. После охлаждения реакционной смеси добавляли смешанный растворитель гексан/диэтиловый эфир и выпавшие в осадок кристаллы отфильтровывали и промывали с получением указанного в заголовке соединения (11,09 г).
1Н-ЯМР (ДМСО-d6) δ: 3,97 (3H, с), 7,76 (1H, дд, J=9,0, 2,5Гц), 7,90-8,05 (2H, м), 12,28 (1H, шир.с).
МС (ESI) m/z: 238 (М+Н)+.
[Ссылочный пример 309]
6-Хлор-4-оксо-1,4-дигидрохинолин-2-карбоновая кислота
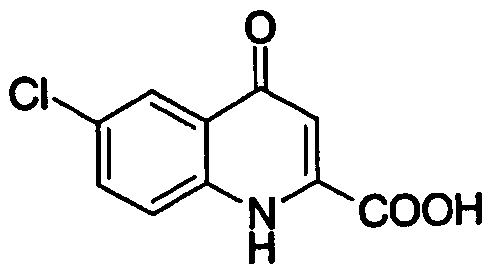
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 308, подобно способу ссылочного примера 286.
1Н-ЯМР (ДМСО-d6) δ: 6,90-7,05 (1H, м), 7,90-8,05 (2H, м), 10,10-10,30 (1H, м), 12,13 (1H, шир.с).
МС (ESI) m/z: 224 (М+Н)+.
[Ссылочный пример 310]
трет-Бутил (1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
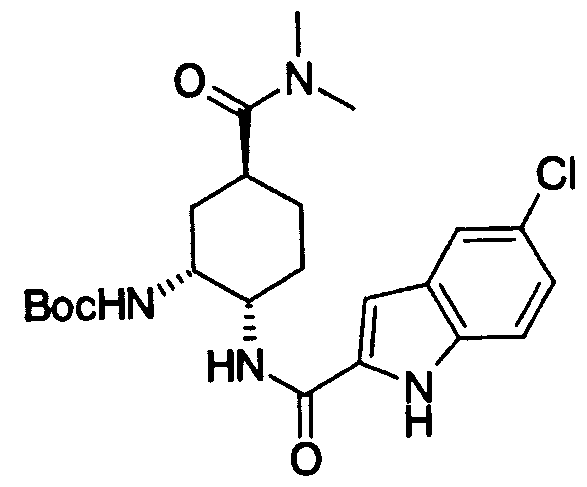
Воду (10 мл) и гидроксид лития (263 мг) добавляли к раствору соединения (5,00 г), полученного в ссылочном примере 97, в тетрагидрофуране (40 мл) и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь фильтровали, фильтрат концентрировали и к раствору полученного остатка и гидрохлорида диметиламина (1,85 г) в N,N-диметилформамиде (100 мл) добавляли при комнатной температуре моногидрат 1-гидроксибензотриазола (1,75 г), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (3,32 г) и диизопропилэтиламин (11,3 мл). Полученную смесь перемешивали в течение 2 дней. После концентрирования реакционной смеси добавляли метиленхлорид, насыщенный водный раствор гидрокарбоната натрия и воду для разделения жидкостей. Полученный водный слой экстрагировали метиленхлоридом. Органические слои объединяли и сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:ацетон = 2:1 → 1:1) с получением указанного в заголовке соединения (4,59 г).
1Н-ЯМР (CDCl3) δ: 1,60-1,76 (2H, м), 1,73 (9H, с), 1,76-1,87 (1H, м), 1,93 (1H, шир.с), 2,14 (1H, шир.с), 2,28 (1H, шир.с), 2,65 (1H, шир.с), 2,95 (3H, с), 3,05 (3H, с), 4,01 (1H, шир.с), 4,21 (1H, шир.с), 4,84 (1H, шир.с), 6,81 (1H, шир.с), 7,20 (1H, дд, J=8,8, 1,9Гц), 7,36 (1H, д, J=8,8Гц), 7,59 (1H, шир.с), 8,02 (1H, шир.с), 10,06 (1H, шир.с).
МС (FAB) m/z: 465 (М+Н)+.
[Ссылочный пример 311]
трет-Бутил (1R,2S,5S)-2-{[(5-фториндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
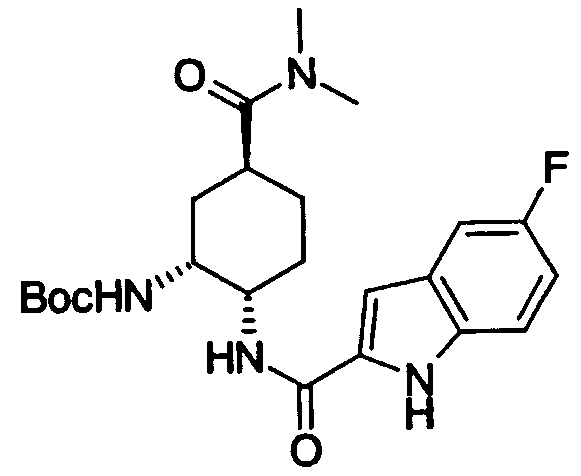
1) Этил (1S,3R,4S)-3-[(трет-бутоксикарбонил)амино]-4-{[(5-фториндол-2-ил)карбонил]амино}циклогексанкарбоксилат получали из соединения, полученного в ссылочном примере 96, и 5-фториндол-2-карбоновой кислоты подобно способу ссылочного примера 91.
1Н-ЯМР (CDCl3) δ: 1,26 (3H, т, J=7,1Гц), 1,52 (9H, с), 1,67-2,41 (7H, м), 3,97 (1H, шир.с), 4,15 (2H, кв, J=7,1Гц), 4,08-4,22 (1H, м), 6,83 (1H, с), 7,00-7,05 (1H, м), 7,32-7,36 (1H, м), 8,02 (1H, с), 9,51 (1H, с).
МС (FAB) m/z: 448 (М+Н)+.
2) Указанное в заголовке соединение получали из соединения, полученного выше, подобно способу ссылочного примера 310.
1Н-ЯМР (CDCl3) δ: 1,52 (9H, с), 1,57-1,79 (2H, м), 1,79-2,00 (2H, м), 2,14 (1H, шир.с), 2,31 (1H, шир.с), 2,65 (1H, шир.с), 2,95 (3H, с), 3,07 (3H, с), 4,02 (1H, шир.с), 4,17-4,25 (1H, м), 4,80 (1H, шир.с), 6,82 (1H, шир.с), 7,02 (1H, дт, J=2,3, 9,0Гц), 7,24 (1H, шир.с), 7,35 (1H, дд, J=9,0, 4,3Гц), 7,91 (1H, шир.с), 9,49 (1H, шир.с).
МС (FAB) m/z: 447 (M+H)+.
[Ссылочный пример 312]
Этил 2-амино-6,6-диметил-6,7-дигидротиазоло[4,5-c]пиридин-5(4Н)-карбоксилат
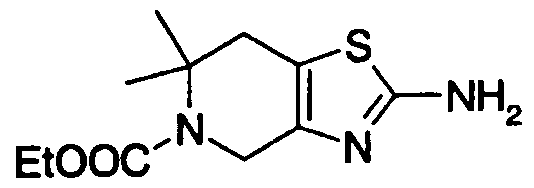
После суспендирования цианида меди(I) (918 мг) в тетрагидрофуране (50 мл) в атмосфере аргона и охлаждения суспензии до -20°C добавляли по каплям за 5 минут н-бутиллитий (1,56N гексановый раствор, 6,41 мл) и смесь перемешивали при -20°C в течение 30 минут. После охлаждения реакционной смеси до -50°C добавляли по каплям за 20 минут гидрид диизобутилалюминия (1,00М гексановый раствор) и смесь перемешивали при -50°C в течение 1 часа. Раствор этил 2,2-диметил-5-оксо-5,6-дигидро-2Н-пиридин-1-карбоксилата (Helv. Chim. Acta, Vol. 81, p. 303, 1998) (986 мг) в тетрагидрофуране (5 мл) добавляли по каплям к реакционной смеси за 5 минут и смесь перемешивали при -50°C в течение 2 часов. После повышения температуры реакционной смеси до -20°C добавляли весь бром (4,90 мл) и смесь перемешивали при -20°C в течение 30 минут. К реакционной смеси добавляли воду и этилацетат для разделения жидкостей. Полученный органический слой промывали насыщенным водным раствором сульфита натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток растворяли в N,N-диметилформамиде (10 мл), добавляли тиомочевину (760 мг) и смесь перемешивали в течение ночи при 50°C. После отгонки растворителя добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли растворитель. Остаток очищали колоночной хроматографией на силикагеле (этилацетат:гексан = 4:1) с получением указанного в заголовке соединения (412 мг).
1Н-ЯМР (CDCl3) δ: 1,25 (3H, т, J=7,1Гц), 1,54 (6H, с), 2,65-2,67 (2H, м), 4,09 (2H, кв, J=7,1Гц), 4,44-4,46 (2H, м), 4,78 (2H, шир.с).
[Ссылочный пример 313]
Этил 2-бром-6,6-диметил-6,7-дигидротиазоло[4,5-c]пиридин-5(4Н)-карбоксилат
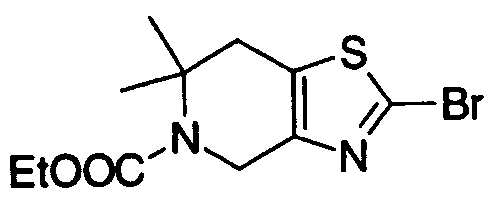
Бромид меди(II) (431 мг) суспендировали в ацетонитриле (8 мл) и добавляли по каплям при комнатной температуре трет-бутилнитрит (249 мг). После добавления к реакционной смеси при охлаждении льдом ацетонитрилового раствора (8 мл) соединения (412 мг), полученного в ссылочном примере 312, смесь нагревали до 50°C и перемешивали в течение 15 минут. Растворитель отгоняли при пониженном давлении и к остатку добавляли диэтиловый эфир и 10% хлористоводородную кислоту для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом магния и концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 6:1) с получением указанного в заголовке соединения (151 мг).
1Н-ЯМР (CDCl3) δ: 1,26 (3H, т, J=7,1Гц), 1,55 (6H, с), 2,79-2,81 (2H, м), 4,10 (2H, кв, J=7,1Гц), 4,65-4,67 (2H, м).
МС (ESI) m/z: 319 (M+H)+.
[Ссылочный пример 314]
Этил 6,6-диметил-6,7-дигидротиазоло[4,5-c]пиридин-5(4Н)-карбоксилат
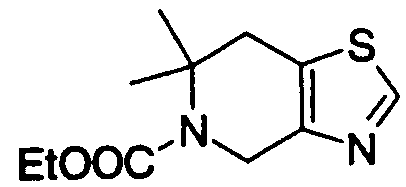
н-Бутиллитий (1,56N гексановый раствор, 1,04 мл) добавляли к раствору соединения (432 мг), полученного в ссылочном примере 313, в диэтиловом эфире (5 мл) при -78°C и смесь перемешивали при -78°C в течение 30 минут. К реакционной смеси добавляли воду и диэтиловый эфир для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом магния и отгоняли растворитель с получением указанного в заголовке соединения (307 мг).
1Н-ЯМР (CDCl3) δ: 1,28 (3H, т, J=7,1Гц), 1,55 (6H, с), 2,90 (2H, с), 4,12 (2H, кв, J=7,1Гц), 4,75 (2H, м), 8,63 (1H, с).
[Ссылочный пример 315]
6,6-Диметил-4,5,6,7-тетрагидротиазоло[4,5-c]пиридин
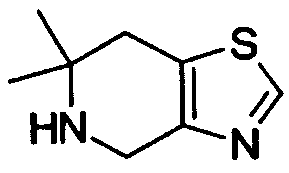
Соединение (307 мг), полученное в ссылочном примере 314, растворяли в смешанном растворителе из воды (5 мл), этанола (5 мл) и диоксана (5 мл), к полученной реакционной смеси добавляли гидроксид лития (598 мг) и смесь кипятили с обратным холодильником в течение 7 суток. Дав реакционной смеси остыть до комнатной температуры, добавляли воду и метиленхлорид для разделения жидкостей. Полученный водный слой экстрагировали 6 раз метиленхлоридом. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли растворитель с получением указанного в заголовке соединения (207 мг).
1Н-ЯМР (CDCl3) δ: 1,23 (6H, с), 2,71-2,73 (2H, м), 4,09-4,11 (2H, м), 8,61 (1H, с).
МС (ESI) m/z: 168 (М+).
[Ссылочный пример 316]
трет-Бутил 6,6-диметил-6,7-дигидротиазоло[4,5-c]пиридин-5(4Н)-карбоксилат
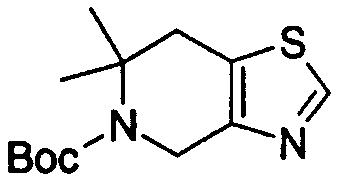
Соединение (207 мг), полученное в ссылочном примере 315, растворяли в метиленхлориде (5 мл), добавляли ди-трет-бутилдикарбонат (404 мг) и 4-(N,N-диметиламино)пиридин (151 мг) и смесь перемешивали при комнатной температуре в течение 2 часов. Добавляли еще ди-трет-бутилдикарбонат (404 мг) и смесь перемешивали в течение ночи при комнатной температуре. Добавляли еще ди-трет-бутилдикарбонат (1,00 г) и смесь перемешивали в течение 1 часа. Добавляли метиленхлорид и 10% хлористоводородную кислоту для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли растворитель. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1) с получением указанного в заголовке соединения (95,4 мг).
1Н-ЯМР (CDCl3) δ: 1,47 (9H, с), 1,52 (6H, с), 2,87 (2H, с), 4,69 (2H, с), 8,62 (1H, с).
МС (ESI) m/z: 269 (М+Н)+.
[Ссылочный пример 317]
4-Хлор-5-(1,3-диоксолан-2-ил)тиазол-2-карбоксилат лития
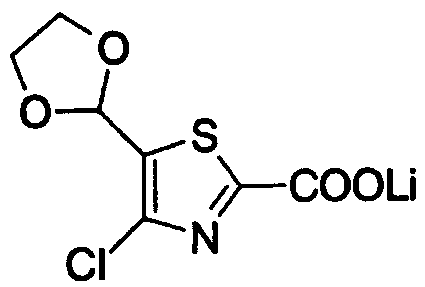
Этиленацеталь 2,4-дихлортиазол-5-карбальдегида (J. Chem. Soc. Perkin Trans. 1, 1992, p. 973) (2,26 г) растворяли в тетрагидрофуране (15 мл), добавляли н-бутиллитий (1,5N гексановый раствор, 6,8 мл) при охлаждении смесью сухой лед-ацетон и полученную смесь перемешивали 20 минут. При той же температуре вводили затем диоксид углерода. Реакционную смесь постепенно нагревали до комнатной температуры за 1,5 часа и затем концентрировали. К реакционной смеси добавляли гексан для превращения продукта в порошок. Продукт отфильтровывали и суспендировали в этилацетате и образовавшийся порошок снова отфильтровывали, получая указанное в заголовке соединение (1,65 г).
[Ссылочный пример 318]
Этил 4-хлор-5-(1,3-диоксолан-2-ил)тиазол-2-карбоксилат
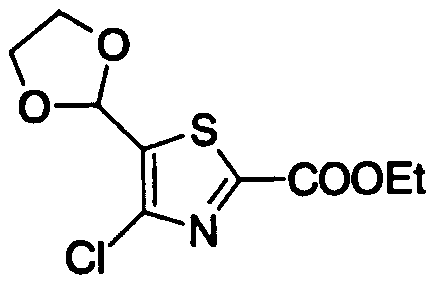
Соединение (242 мг), полученное в ссылочном примере 317, и этанол (0,2 мл) растворяли в N,N-диметилформамиде (2 мл), добавляли моногидрат 1-гидроксибензотриазола (136 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (250 мг) и смесь перемешивали при комнатной температуре в течение ночи. Растворитель отгоняли при пониженном давлении и добавляли диэтиловый эфир и разбавленную хлористоводородную кислоту для отделения органического слоя. Органический слой промывали водой и насыщенным водным раствором гидрокарбоната натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (170 мг).
1Н-ЯМР (CDCl3) δ: 1,43 (3H, т, J=7,3Гц), 4,00-4,10 (2H, м), 4,10-4,20 (2H, м), 4,48 (2H, кв, J=7,3Гц), 6,15 (1H, с).
МС (ESI) m/z: 264 (M+H)+.
[Ссылочный пример 319]
Этил 4-хлор-5-формилтиазол-2-карбоксилат
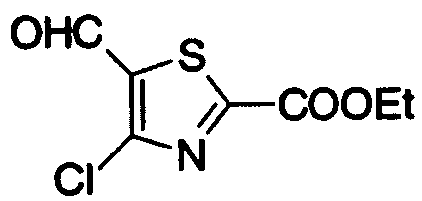
Соединение (132 мг), полученное в ссылочном примере 318, растворяли в диэтиловом эфире (5 мл), добавляли 20% хлористоводородную кислоту (0,3 мл) и смесь перемешивали при комнатной температуре в течение 7 часов. Добавляли к реакционной смеси насыщенный водный раствор гидрокарбоната натрия и экстрагировали диэтиловым эфиром. Экстракт сушили над безводным сульфатом магния и отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (110 мг).
1Н-ЯМР (CDCl3) δ: 1,46 (3H, т, J=7,1Гц), 4,52 (2H, кв, J=7,1Гц), 10,12 (1H, с).
[Ссылочный пример 320]
Этил 4-азидо-5-формилтиазол-2-карбоксилат
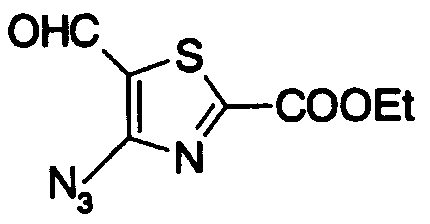
Соединение (5,15 г), полученное в ссылочном примере 319, растворяли в диметилсульфоксиде (30 мл), добавляли азид натрия (1,52 г) и смесь перемешивали при комнатной температуре в течение 2,5 часов. К реакционной смеси добавляли ледяную воду и экстрагировали диэтиловым эфиром. Экстракт промывали дважды водой и затем сушили над безводным сульфатом магния, растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 24:1) с получением указанного в заголовке соединения (1,78 г).
1Н-ЯМР (CDCl3) δ: 1,45 (3Н, т, J=7,1Гц), 4,50 (2Н, кв, J=7,1Гц), 9,95 (1Н, с).
[Ссылочный пример 321]
Этил 6-метил-6,7-дигидротиазоло[4,5-d]пиримидин-2-карбоксилат
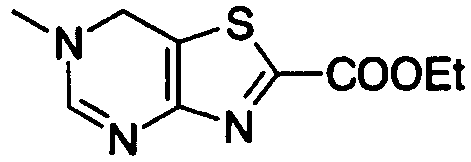
Соединение (1,56 г) полученное в ссылочном примере 320, растворяли в метиленхлориде (20 мл), добавляли уксусную кислоту (2 мл), метиламин (2N тетрагидрофурановый раствор, 21 мл) и триацетоксиборгидрид натрия (2,98 г) и смесь перемешивали. Через 1 час добавляли еще триацетоксиборгидрид натрия (2,98 г) и продолжали перемешивание в течение еще 4,5 часов. К реакционной смеси для ее подщелачивания добавляли 0,5N водный раствор (100 мл) гидроксида натрия. Затем реакционную смесь экстрагировали метиленхлоридом и экстракт сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении с получением коричневого масла (1,43 г). Полученное масло растворяли в этаноле (50 мл), добавляли 10% палладий на углероде (2,0 г) и гидрировали при нормальных температуре и давлении. Через 2,5 часа катализатор удаляли фильтрованием и фильтрат концентрировали. Остаток растворяли в метиленхлориде (30 мл), добавляли триметилортоформиат (0,7 мл) и комплекс (0,3 мл) трифторид бора-диэтиловый эфир и смесь перемешивали при комнатной температуре в течение 15 часов. К реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия и смесь экстрагировали метиленхлоридом. Экстракт сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 97:3) с получением указанного в заголовке соединения (100 мг).
1Н-ЯМР (CDCl3) δ: 1,41 (3H, т, J=7,1Гц), 2,95 (3H, с), 4,44 (2H, кв, J=7,1Гц), 4,87 (2H, с), 7,06 (1H, с).
МС (ESI) m/z: 226 (M+Н)+.
[Ссылочный пример 322]
6-Метил-6,7-дигидротиазоло[4,5-d]пиримидин-2-карбоксилат лития
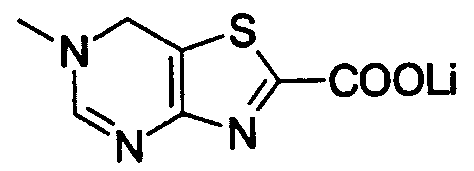
Соединение (463 мг) растворяли в тетрагидрофуране (20 мл), добавляли гидроксид лития (54,1 мг) и воду (4 мл) и смесь перемешивали при комнатной температуре в течение 4,5 часов. Растворитель отгоняли при пониженном давлении и остаток сушили с помощью вакуумного насоса с получением указанного в заголовке соединения (460 мг).
1Н-ЯМР (ДМСО-d6) δ: 2,86 (3Н, с), 4,71 (2Н, с), 7,03 (1Н, с).
[Ссылочный пример 323]
трет-Бутил (1R,2S,5S)-2-азидо-5-{[этил(метил)амино]карбонил}циклогексилкарбамат
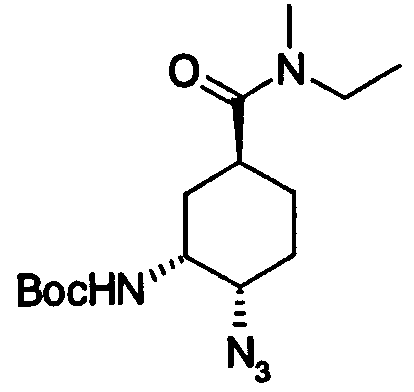
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 250, с этилметиламином.
1Н-ЯМР (CDCl3) δ: 1,08, 1,18 (всего 3H, каждый т, J=7,1Гц), 1,46 (9H, с), 1,52-1,80 (4H, м), 2,04-2,08 (2H, м), 2,71-2,77 (1H, м), 2,89, 2,98 (всего 3H, каждый с), 3,32, 3,39 (всего 2H, каждый кв, J=7,1Гц), 3,74-3,76 (1H, м), 4,09-4,11 (1H, м), 4,60 (1H, шир.с).
МС (EI) m/z: 326 (M+H)+.
[Ссылочный пример 324]
трет-Бутил (1R,2S,5S)-2-{[(7-хлоризохинолин-3-ил)карбонил]амино}-5-{[этил(метил)амино]карбонил}циклогексилкарбамат
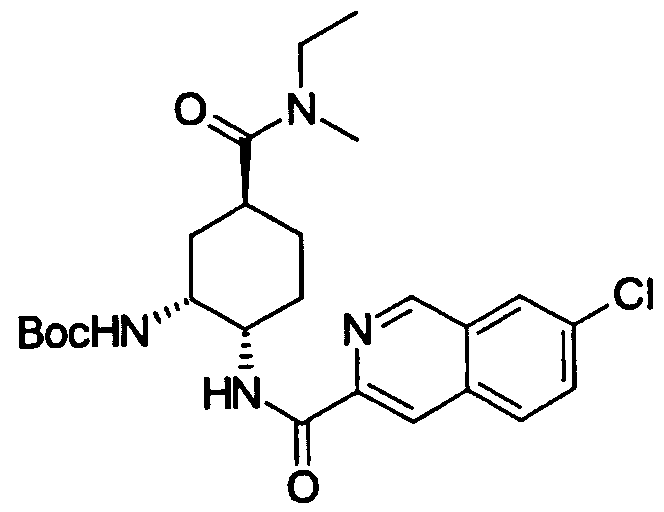
Соединение (1,44 г), полученное в ссылочном примере 323, растворяли в метаноле (20 мл), добавляли 10% палладий на углероде (150 мг) и смесь перемешивали в атмосфере водорода. Через 24 часа удаляли фильтрованием катализатор, затем концентрировали при пониженном давлении растворитель с получением бесцветного масла. Полученное масло непосредственно использовали в следующей реакции.
Полученное выше масло растворяли в метиленхлориде (30 мл), добавляли соединение (850 мг), полученное в ссылочном примере 57, гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида (1,27 г), моногидрат 1-гидроксибензотриазола (900 мг) и N-метилморфолин (1,34 г) и смесь перемешивали при комнатной температуре. Через 17 часов к реакционной смеси добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей и полученный органический слой сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:50) с получением указанного в заголовке соединения (1,61 г).
1Н-ЯМР (CDCl3) δ: 1,10, 1,22 (всего 3H, каждый т, J=7,1Гц), 1,43 (9H, с), 1,84-2,17 (6H, м), 2,66 (1H, шир.с), 2,92, 3,03 (всего 3H, каждый с), 3,35-3,44 (2H, м), 4,20-4,30 (2H, м), 5,30 (1H, шир.с), 7,70 (1H, д, J=8,6Гц), 7,92 (1H, д, J=8,6Гц), 8,00 (1H, с), 8,40 (1H, шир.с), 8,56 (1H, с), 9,03 (1H, с).
МС (FAB) m/z: 489 (M+H)+.
[Ссылочный пример 325]
N-((1S,2R,4S)-2-Амино-4-[(7-хлоризохинолин-3-ил)карбонил]-4-{[этил(метил)амино]карбонил}циклогексил)-7-хлоризохинолин-3-карбоксамид
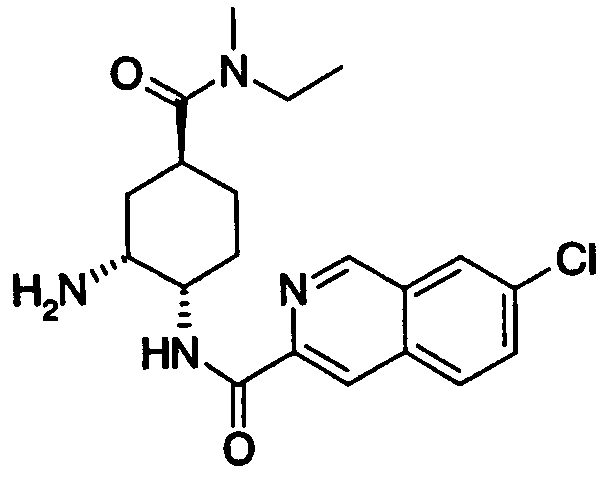
Соединение (1,60 г), полученное в ссылочном примере 324, растворяли в этанольном растворе (25 мл) хлористоводородной кислоты и раствор перемешивали при комнатной температуре в течение 30 минут. Растворитель отгоняли при пониженном давлении и к остатку добавляли метиленхлорид и 1N водный раствор гидроксида натрия для разделения жидкостей. Полученный водный слой экстрагировали метиленхлоридом и органические слои объединяли и сушили над карбонатом калия. Растворитель отгоняли при пониженном давлении, к остатку добавляли гексан и осадок отфильтровывали с получением указанного в заголовке соединения (1,22 г).
1Н-ЯМР (ДМСО-d6) δ: 1,10, 1,23 (всего 3H, каждый т, J=7,1Гц), 1,26 (2H, шир.с), 1,69-2,11 (6H, м), 2,89 (1H, шир.с), 2,93, 3,05 (всего 3H, каждый с), 3,38-3,45 (2H, м), 3,52 (1H, с), 4,18 (1H, шир.с), 7,70 (1H, дд, J=8,8, 2,0Гц), 7,94 (1H, д, J=8,8Гц), 8,02 (1H, д, J=2,0Гц), 8,50 (1H, шир.с), 8,59 (1H, с), 9,11 (1H, с).
МС (FAB) m/z: 389 (М+Н)+.
[Ссылочный пример 326]
Этил (1R*,3S*,4S*)-3-[(трет-бутоксикарбонил)амино]-4-{[трет-бутил(дифенил)силил]окси}циклогексанкарбоксилат
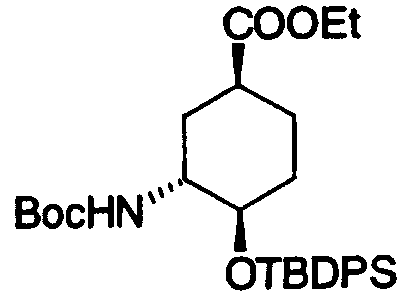
Соединение (28,0 г), полученное в ссылочном примере 88, растворяли в N,N-диметилформамиде (500 мл) и добавляли трет-бутилдифенилсилилхлорид (63,5 мл) и имидазол (19,9 г). После перемешивания смеси при комнатной температуре в течение 10 часов к реакционной смеси добавляли этилацетат и воду для разделения жидкостей. Полученный водный слой экстрагировали этилацетатом и органические слои объединяли, промывали два раза водой и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и затем остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 1:0 → 47:3) с получением указанного в заголовке соединения (52,5 г), содержащего 0,4 молекулы N,N-диметилформамида.
1Н-ЯМР (CDCl3) δ: 1,07 (9H, с), 1,27 (3H, т, J=7,1Гц), 1,38 (9H, с), 1,43-1,59 (3H, м), 1,63-1,67 (1H, м), 1,92-1,98 (1H, м), 2,25-2,32 (1H, м), 2,37-2,42 (1H, м), 3,66 (1H, шир.с), 3,80 (1H, шир.с), 4,16 (2H, кв, J=7,1Гц), 4,32 (1H, д, J=8,1Гц), 7,34-7,46 (6H, м), 7,65-7,73 (4H, м).
[Ссылочный пример 327]
трет-Бутил (1R*,2R*,5S*)-2-{[трет-бутил(дифенил)силил]окси}-5-(гидроксиметил)циклогексанкарбамат
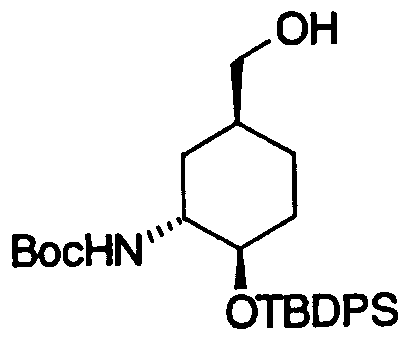
Литийалюминийгидрид (7,11 г) суспендировали в абсолютном диэтиловом эфире (100 мл) при 0°C при продувке аргоном и раствор соединения (52,5 г), полученного в ссылочном примере 326, в диэтиловом эфире (500 мл) добавляли по каплям за 30 минут. После перемешивания при 0°C в течение 30 минут к реакционной смеси добавляли по каплям метанол (100 мл). Полученную взвесь удаляли фильтрованием через целит и фильтрат концентрировали. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1) с получением указанного в заголовке соединения (29,6 г).
1Н-ЯМР (CDCl3) δ: 1,07 (9H, с), 1,32-1,74 (16H, м), 1,87 (1H, т, J=10,4Гц), 3,35-3,55 (2H, м), 3,71 (1H, шир.с), 10 3,79 (1H, шир.с), 4,36 (1H, шир.с), 7,34-7,44 (6H, м), 7,65-7,72 (4H, м).
[Ссылочный пример 328]
(1R*,3S*,4S*)-3-[(трет-Бутоксикарбонил)амино]-4-{[трет-бутил(дифенил)силил]окси}циклогексил)метилметансульфонат
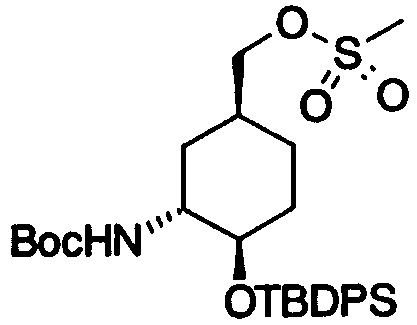
Соединение (29,5 г), полученное в ссылочном примере 327, растворяли в метиленхлориде (200 мл) и пиридине (20 мл), добавляли метансульфонилхлорид (9,5 мл) и смесь перемешивали при комнатной температуре в течение 6 часов. Растворитель отгоняли при пониженном давлении и к остатку добавляли этилацетат и воду для разделения жидкостей. Полученный водный слой экстрагировали этилацетатом и органические слои объединяли, промывали два раза водой и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 2:1) с получением указанного в заголовке соединения (29,8 г).
1Н-ЯМР (CDCl3) δ: 1,08 (9H, с), 1,38 (9H, с), 1,43-1,61 (5H, м), 1,86-1,89 (2H, м), 3,02 (3H, с), 3,77 (1H, шир.с), 3,81 (1H, шир.с), 4,10 (2H, д, J=5,4Гц), 4,32 (1H, шир.с), 7,35-7,45 (6H, м), 7,64-7, 68 (4H, м).
МС (ESI) m/z: 562 (M+H)+.
[Ссылочный пример 329]
трет-Бутил (1R*,2R*,5S*)-2-{[трет-бутил(дифенил)силил]окси}-5-(цианометил)циклогексанкарбамат
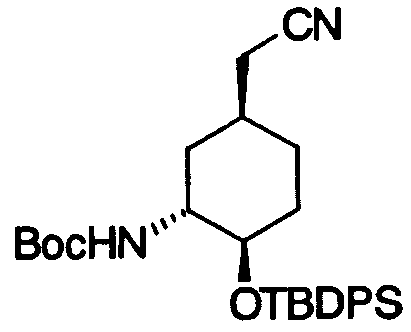
Соединение (29,8 г), полученное в ссылочном примере 328, растворяли в N,N-диметилформамиде (400 мл), добавляли цианид натрия (3,64 г) и смесь перемешивали при 80°C в течение 11 часов. К реакционной смеси добавляли этилацетат и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный водный слой экстрагировали дважды этилацетатом и органические слои объединяли, промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 5:1) с получением указанного в заголовке соединения (20,6 г).
1Н-ЯМР (CDCl3) δ: 1,08 (9H, с), 1,38 (9H, с), 1,43-1,68 (5H, м), 1,79-1,85 (1H, м), 1,88-1,95 (1H, м), 2,32 (2H, д, J=7,1Гц), 3,77 (1H, шир.с), 3,82 (1H, шир.с), 4,32 (1H, шир.д, J=6,8Гц), 7,35-7,45 (6H, м), 7,65-7,71 (4H, м).
[Ссылочный пример 330]
трет-Бутил (1R*,2R*,5S*)-2-{[трет-бутил(дифенил)силил]окси}-5-(2-оксоэтил)циклогексанкарбамат
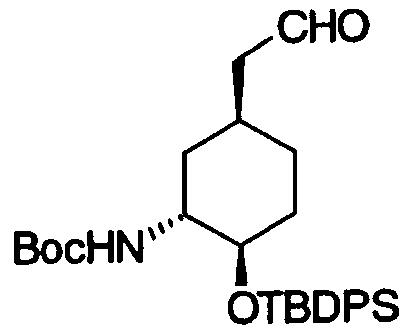
Соединение (2,00 г), полученное в ссылочном примере 329, растворяли в абсолютном метиленхлориде (20 мл) и систему продували аргоном и затем охлаждали до -78°C. К раствору добавляли по каплям гидрид диизобутилалюминия (0,95М гексановый раствор, 8,55 мл). Затем давали температуре смеси подняться до комнатной температуры и перемешивали смесь 3 часа. Реакционную смесь охлаждали до 0°C и добавляли по каплям метанол (10 мл). Полученную взвесь удаляли фильтрованием через целит и фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 1:0 → 49:1) с получением указанного в заголовке соединения (1,45 г).
1Н-ЯМР (CDCl3) δ: 1,07 (9H, с), 1,38 (9H, с), 1,43-1,54 (5H, м), 1,82-1,88 (1H, м), 2,06 (1H, шир.с), 2,42-2,43 (2H, м), 3,72 (1H, шир.с), 3,77 (1H, шир.с), 4,38 (1H, шир.с), 7,34-7,44 (6H, м), 7,65-7,68 (4H, м), 9,77 (1H, т, J=1,7Гц).
МС (FAB) m/z: 496 (М+Н)+.
[Ссылочный пример 331]
2-((1R*,3S*,4S*)-3-[(трет-Бутоксикарбонил)амино]-4-{[трет-бутил(дифенил)силил]окси}циклогексил)уксусная кислота
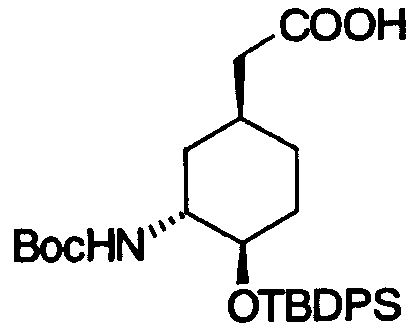
Соединение (8,40 г), полученное в ссылочном примере 330, растворяли в смешанном растворителе из воды (33 мл) и трет-бутанола (120 мл), добавляли 2-метил-2-бутен (8,08 мл), дигидрат дигидрофосфата натрия (2,64 г) и хлорит натрия (3,45 г) и смесь перемешивали при комнатной температуре в течение 1,5 часов. К реакционной смеси для ее разбавления добавляли метиленхлорид и воду. Полученный водный слой доводили 1N хлористоводородной кислотой до рН примерно 4. Жидкости разделяли и полученный водный слой экстрагировали дважды метиленхлоридом. Органические слои объединяли, сушили над безводным сульфатом магния и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 2:1 → 1:1) с получением указанного в заголовке соединения (7,62 г).
1Н-ЯМР (CDCl3) δ: 1,07 (9H, с), 1,22-1,63 (15H, м), 1,82 (1H, шир.с), 2,17 (1H, шир.с), 2,27-2,33 (1H, м), 3,69 (1H, шир.с), 3,84 (1H, шир.с), 7,00 (1H, шир.с), 7,33-7,42 (6H, м), 7,63-7,65 (4H, м).
МС (ESI) m/z: 512 (М+Н)+.
[Ссылочный пример 332]
трет-Бутил (1R*,2R*,5S*)-2-{[трет-бутил(дифенил)силил]окси}-5-[2-(диметиламино)-2-оксоэтил]циклогексанкарбамат
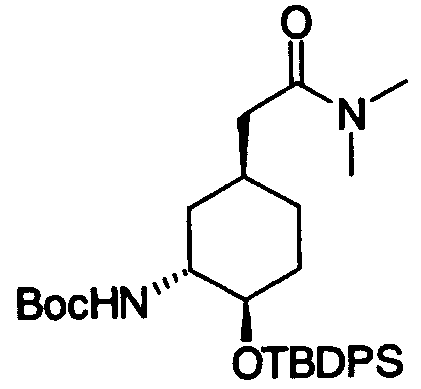
Соединение (7,62 г), полученное в ссылочном примере 331, растворяли в N,N-диметилформамиде (150 мл), добавляли гидрохлорид диметиламина (6,07 г), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (8,56 г), моногидрат 1-гидроксибензотриазола (1,01 г) и триэтиламин (10,3 мл) и смесь перемешивали при комнатной температуре в течение 4 суток. Растворитель отгоняли при пониженном давлении и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный органический слой экстрагировали метиленхлоридом и органические слои объединяли и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 1:1). Растворитель отгоняли, к остатку добавляли гексан и образовавшийся белый осадок отфильтровывали с получением указанного в заголовке соединения (6,42 г).
1Н-ЯМР (CDCl3) δ: 1,08 (9H, с), 1,38 (9H, шир.с), 1,43-1,55 (5H, м), 1,79-1,86 (1H, м), 2,03 (1H, шир.с), 2,21-2,32 (2H, с), 2,94 (3H, с), 3,03 (3H, с), 3,74 (1H, шир.с), 3,80 (1H, шир.с), 4,49 (1H, шир.с), 7,33-7,44 (6H, м), 7,64-7,69 (4H, м).
МС (ESI) m/z: 539 (M+H)+.
[Ссылочный пример 333]
трет-Бутил (1R*,2R*,5S*)-5-[2-(диметиламино)-2-оксоэтил]-2-гидроксициклогексанкарбамат
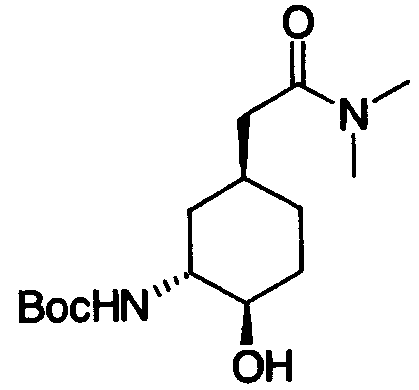
Соединение (6,36 г), полученное в ссылочном примере 332, растворяли в тетрагидрофуране (50 мл), добавляли фторид тетрабутиламмония (1N тетрагидрофурановый раствор, 17,85 мл) и смесь перемешивали при комнатной температуре в течение 13 часов. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной флэш-хроматографией на силикагеле (метиленхлорид:метанол = 24:1) с получением указанного в заголовке соединения (3,49 г).
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 1,46-1,60 (4H, м), 1,79-1,84 (2H, м), 2,28-2,35 (3H, с), 2,82 (1H, шир.с), 2,95 (3H, с), 3,01 (3H, с), 3,56 (2H, шир.с), 4,67 (1H, шир.с).
МС (ESI) m/z: 301 (M+H)+.
[Ссылочный пример 334]
((1R*,2R*,4S*)-2-[(трет-Бутоксикарбонил)амино]-4-[2-(диметиламино)-2-оксоэтил]циклогексилметансульфонат
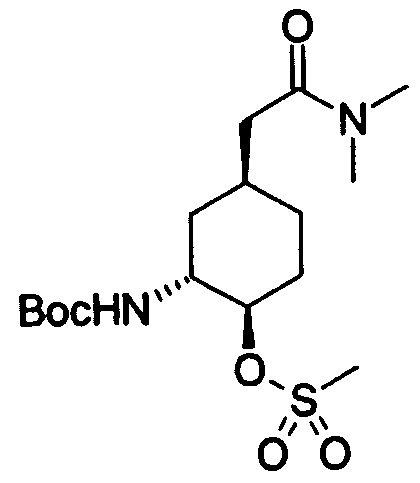
Соединение (8,05 мг), полученное в ссылочном примере 333, растворяли в метиленхлориде (50 мл), раствор охлаждали до -78°C в атмосфере аргона и добавляли по каплям метансульфонилхлорид (2,70 мл). Дав температуре смеси подняться до 0°C, смесь перемешивали 30 минут и затем ее перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду для разделения жидкостей и полученный водный слой экстрагировали метиленхлоридом. Органические слои объединяли, промывали водой и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной флэш-хроматографией на силикагеле (гексан:этилацетат = 1:1 → 0:1) с получением указанного в заголовке соединения (3,63 г).
1Н-ЯМР (CDCl3) δ: 1,43 (9H, с), 1,59-1,74 (4H, м), 1,85-2,30 (5H, м), 2,95 (3H, с), 3,00 (3H, с), 3,10 (3H, с), 3,79-3,83 (1H, м), 4,72 (1H, шир.с), 4,91 (1H, шир.с).
МС (ESI) m/z: 379 (M+H)+.
[Ссылочный пример 335]
трет-Бутил (1R*,2S*,5S*)-2-азидо-5-[2-(диметиламино)-2-оксоэтил]циклогексанкарбамат
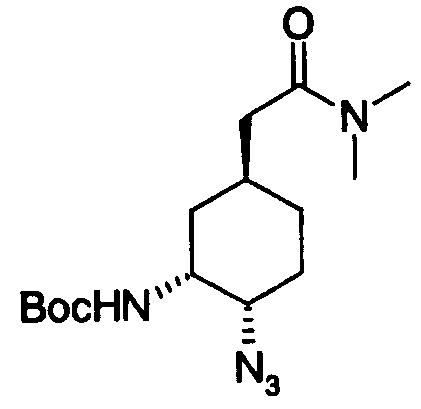
Соединение (3,62 г), полученное в ссылочном примере 334, растворяли в N,N-диметилформамиде (20 мл), добавляли азид натрия (3,11 г) и смесь перемешивали при 75°C в течение 17 часов. Реакционную смесь вливали в смешанный растворитель вода/этилацетат и жидкости разделяли. Полученный водный слой экстрагировали дважды этилацетатом и органические слои объединяли, промывали водой, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной флэш-хроматографией на силикагеле (этилацетат) с получением указанного в заголовке соединения (1,30 г).
1Н-ЯМР (CDCl3) δ: 1,14-1,21 (1H, м), 1,33-1,40 (1H, м), 1,45 (9H, с), 1,61-1,71 (1H, м), 1,78-1,91 (3H, м), 2,22-2,27 (3H, м), 2,94 (3H, с), 3,00 (3H, с), 3,60-3,62 (1H, м), 3,97 (1H, шир.с), 4,76 (1H, шир.с).
МС (ESI) m/z: 326 (M+H)+.
[Ссылочный пример 336]
Гидрохлорид N-{(1R*,2S*,4R*)-2-амино-4-[2-(диметиламино)-2-оксоэтил]циклогексил}-5-хлориндол-2-карбоксамида
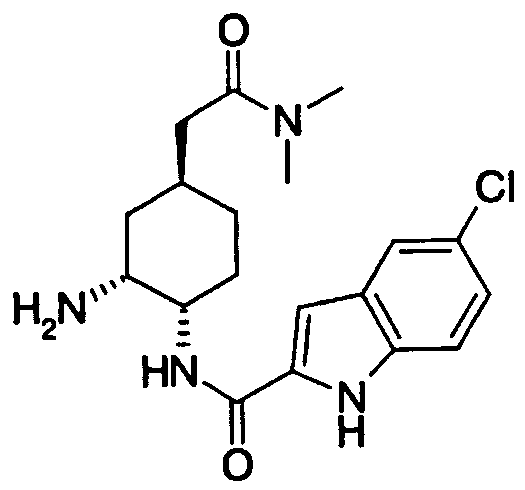
Указанное в заголовке соединение получали обработкой подобно способу ссылочного примера 69 продукта, полученного каталитическим восстановлением соединения, полученного в ссылочном примере 335, подобно способу ссылочного примера 324 и затем конденсацией его с 5-хлориндол-2-карбоновой кислотой.
1Н-ЯМР (ДМСО-d6) δ: 1,16-1,19 (1H, м), 1,51-1,56 (1H, м), 1,70-1,73 (1H, м), 1,81-1,91 (2H, м), 1,99-2,03 (1H, м), 2,19-2,30 (3H, м), 2,83 (3H, с), 2,99 (3H, с), 3,63 (1H, шир.с), 4,08 (1H, шир.с), 7,19 (1H, дд, J=8,7, 1,7Гц), 7,35 (1H, с), 7,44 (1H, д, J=8,7Гц), 7,69 (1H, д, J=1,7Гц), 8,22 (3H, шир.с), 8,62 (1H, д, J=7,1Гц), 11,91 (1H, с).
МС (ESI) m/z: 377 (М+Н)+.
[Ссылочный пример 337]
трет-Бутил (1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-(гидроксиметил)циклогексанкарбамат
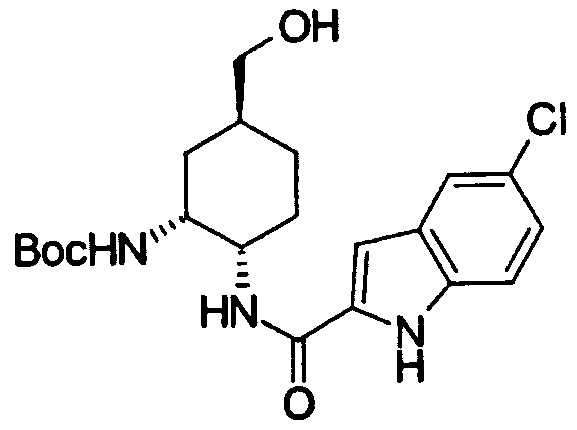
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 97, подобно способу стадии 2) ссылочного примера 129.
[Ссылочный пример 338]
((1S,3R,4S)-3-[(трет-Бутоксикарбонил)амино]-4-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)метилметансульфонат
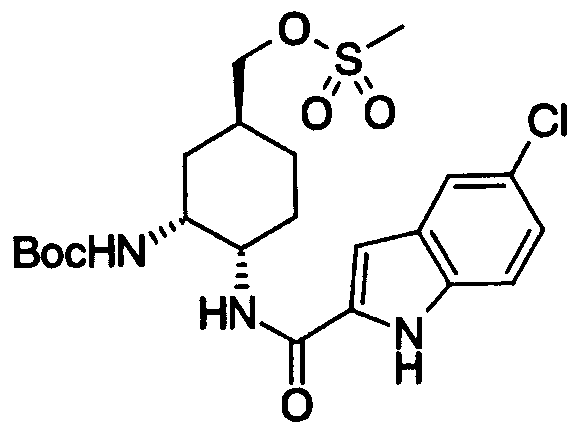
Соединение (500 мг), полученное в ссылочном примере 337, и триэтиламин (329 мл) суспендировали в смеси тетрагидрофуран (8 мл)-метиленхлорид (8 мл) и суспензию охлаждали до -78°C. К суспензии добавляли по каплям метансульфонилхлорид (138 мл), затем температуру суспензии постепенно повышали до -5°C и перемешивали суспензию при той же температуре в течение 15 часов. Реакционную смесь концентрировали, затем к остатку добавляли воду и смесь экстрагировали 3 раза метиленхлоридом. Полученные органические слои промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (654 мг).
1Н-ЯМР (CDCl3) δ: 1,57 (9H, с), 1,84-2,01 (4H, м), 2,28-2,31 (1H, м), 3,04 (3H, с), 3,68 (1H, с), 3,74-3,75 (1H, м), 3,91-3,93 (1H, м), 4,02-4,12 (2H, м), 4,18-4,20 (1H, м), 4,85 (1H, шир.с), 6,81 (1H, с), 7,21 (1H, дд, J=2,0, 8,8Гц), 7,34 (1H, д, J=8,8Гц), 7,60 (1H, с), 8,02 (1H, шир.с), 9,27 (1H, шир.с).
МС (ESI) m/z: 500 (M+H)+.
[Ссылочный пример 339]
трет-Бутил (1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(метилсульфанил)метил]циклогексанкарбамат
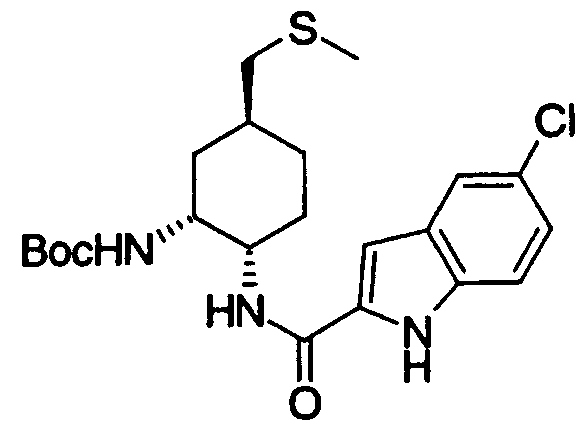
Соединение (654 мг), полученное в ссылочном примере 338, растворяли в N,N-диметилформамиде (8 мл), добавляли 15% водный раствор (1,8 мл) тиометоксида натрия и смесь перемешивали при комнатной температуре в течение 4 часов. Реакционную смесь вливали в воду и экстрагировали 3 раза этилацетатом. Полученные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и затем концентрировали. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 24:1) с получением указанного в заголовке соединения (492 мг).
1Н-ЯМР (CDCl3) δ: 1,52 (9H, с), 1,87-3,04 (13H, м), 3,91-3,94 (1H, м), 4,12-4,15 (1H, м), 4,95 (1H, шир.с), 6,81 (1H, с), 7,19 (1H, дд, J=8,8, 1,2Гц), 7,35 (1H, д, J=8,8Гц), 7,57 (1H, с), 9,82 (1H, шир.с).
МС (ESI) m/z: 452 (M+H)+.
[Ссылочный пример 340]
трет-Бутил (1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(метилсульфонил)метил]циклогексанкарбамат
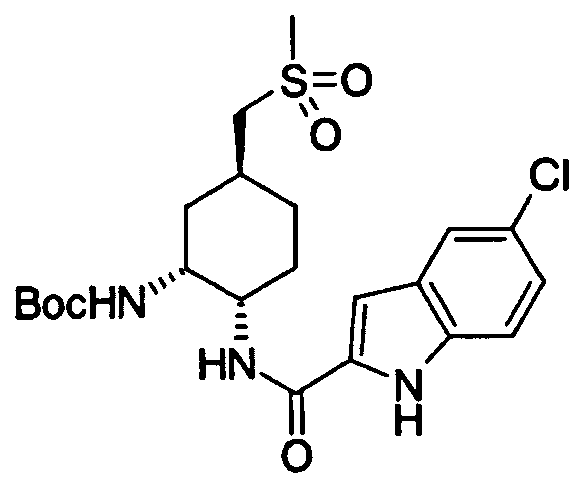
Соединение (300 мг), полученное в ссылочном примере 339, растворяли в метиленхлориде (10 мл) и к раствору добавляли при 0°C при перемешивании м-хлорпербензойную кислоту (70%, 400 мг). Продолжали перемешивание реакционной смеси в указанных условиях в течение 1 часа, затем ее вливали в воду и экстрагировали 3 раза этилацетатом. Полученные органические слои промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и затем концентрировали. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 24:1), затем жидкости разделяли с использованием насыщенного водного раствора гидрокарбоната натрия и этилацетата и полученный органический слой концентрировали с получением указанного в заголовке соединения (254 мг).
1Н-ЯМР (CDCl3) δ: 1,44-2,19 (13H, м), 2,22-2,30 (2H, м), 2,89-3,25 (7H, м), 3,93-4,15 (2H, м), 4,98 (1H, шир.с), 6,82 (1H, с), 7,21 (1H, дд, J=8,8, 2,0Гц), 7,34 (1H, д, J=8,8Гц), 7,60 (1H, шир.с), 9,54 (1H, шир.с).
[Ссылочный пример 341]
(5-Хлортиен-3-ил)метанол
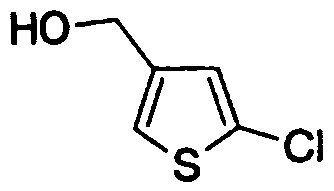
5-Хлортиофен-3-карбоновую кислоту (Monatsh. Chem., Vol. 120, p. 53, 1989) (6,93 г) растворяли в тетрагидрофуране (750 мл), добавляли триэтиламин (27,3 мл) и этилхлорформиат (18,7 мл) и смесь перемешивали при комнатной температуре в течение 2,5 часов. Добавляли по каплям за 10 минут водный раствор (41 мл) боргидрида натрия (19,3 г) и смесь перемешивали при комнатной температуре в течение 18,5 часов. После добавления к реакционной смеси для ее подкисления уксусной кислоты отгоняли при пониженном давлении растворитель. К остатку добавляли воду и метиленхлорид для разделения жидкостей. Полученный органический слой промывали водой и насыщенным водным раствором гидрокарбоната натрия. После сушки органического слоя отгоняли при пониженном давлении растворитель. Остаток очищали колоночной флэш-хроматографией на силикагеле (этилацетат:гексан = 1:4) с получением указанного в заголовке соединения (5,17 г).
1Н-ЯМР (CDCl3) δ: 1,63 (1H, т, J=5,8Гц), 4,59 (2H, д, J=5,3Гц), 6,91 (1H, д, J=1,7Гц), 6,98-6,99 (1H, м).
[Ссылочный пример 342]
5-Хлортиофен-3-карбальдегид
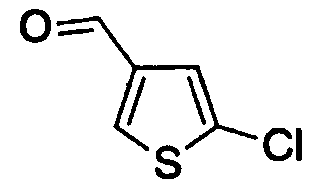
Соединение (5,17 г), полученное в ссылочном примере 341, растворяли в метиленхлориде (400 мл), добавляли диоксид марганца (51,3 г) и смесь перемешивали при комнатной температуре в течение 15 часов. После фильтрования реакционной смеси отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (2,84 г).
1Н-ЯМР (CDCl3) δ: 7,35 (1H, д, J=1,7Гц), 7,88 (1H, д, J=1,7Гц), 9,75 (1H, с).
[Ссылочный пример 343]
Этил 2-азидо-3-(5-хлортиен-3-ил)акрилат
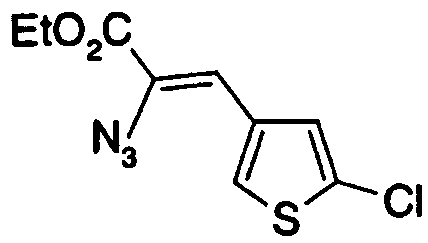
После добавления этанола (15 мл) к 20% этанольному раствору (10,7 мл) этоксида натрия и охлаждения смеси до 0°C добавляли по каплям за 30 минут смесь соединения (1,01 г), полученного в ссылочном примере 342, и этилазидоацетата (3,55 г) и полученную смесь перемешивали при 0°C в течение 3 часов. К реакционной смеси добавляли охлажденный водный раствор хлорида аммония и смесь 3 раза экстрагировали диэтиловым эфиром. Органические слои объединяли и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной флэш-хроматографией на силикагеле (этилацетат:гексан = 1:49) с получением указанного в заголовке соединения (1,04 г).
1Н-ЯМР (CDCl3) δ: 1,38 (3H, т, J=7,1Гц), 4,34 (2H, кв, J=7,1Гц), 6,75 (1H, с), 7,39 (1H, д, J=1,7Гц), 7,54 (1H, д, J=1,7Гц).
[Ссылочный пример 344]
Этил 2-хлор-6Н-тиено[2,3-b]пиррол-5-карбоксилат
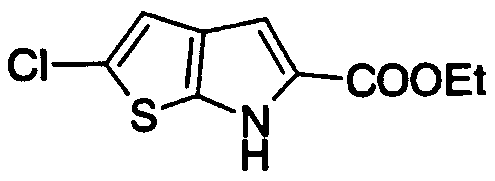
Соединение (0,97 г), полученное в ссылочном примере 343, растворяли в ксилоле (20 мл) и раствор кипятили с обратным холодильником в течение 30 минут. Дав реакционной смеси остыть, отгоняли при пониженном давлении растворитель. К остатку добавляли гексан и образовавшиеся твердые частицы отфильтровывали с получением указанного в заголовке соединения (0,608 г).
1Н-ЯМР (CDCl3) δ: 1,38 (3H, т, J=7,0Гц), 4,35 (2H, кв, J=7,0Гц), 6,90 (1H, с), 7,00 (1H, д, J=1,9Гц), 9,32 (1H, шир.).
[Ссылочный пример 345]
2-Хлор-6Н-тиено[2,3-b]пиррол-5-карбоновая кислота
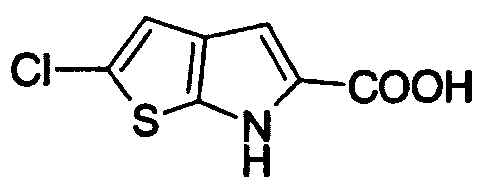
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 344, подобно способу ссылочного примера 274.
1Н-ЯМР (CD3OD): 3,35 (1Н, с), 6,94 (1Н, с), 6,96 (1Н, с).
МС (ESI) m/z: 200 (M-H)-.
[Ссылочный пример 346]
1-Хлор-4-(2,2-дибромвинил)бензол
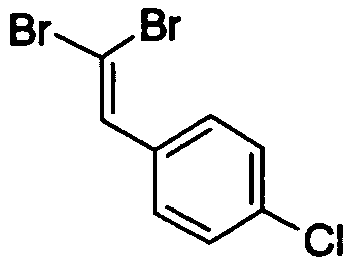
4-Хлорбензальдегид (2,81 г) растворяли в метиленхлориде (300 мл), добавляли тетрабромид углерода (13,3 г) и трифенилфосфин (21,0 г) и смесь перемешивали при комнатной температуре в течение 90 минут. После удаления фильтрованием выпавшего в осадок нерастворимого вещества фильтрат концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 20:1) с получением указанного в заголовке соединения (5,54 г).
1Н-ЯМР (CDCl3) δ: 7,33 (2Н, д, J=8,5 Гц), 7,43 (1Н, с), 7,47 (2Н, д, J=8,5 Гц).
МС (EI) m/z: 296 (M+).
[Ссылочный пример 347]
3-(4-Хлорфенил)-2-пропиоловая кислота
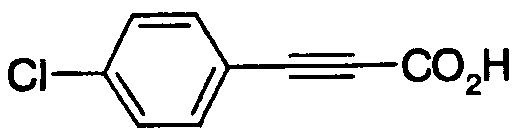
Соединение (1,0 г), полученное в ссылочном примере 346, растворяли в тетрагидрофуране (30 мл) и к раствору добавляли по каплям при -78°C в атмосфере аргона н-бутиллитий (1,59N гексановый раствор, 4,46 мл). Температуре реакционной смеси давали подняться до комнатной температуры и перемешивали смесь в течение 1 часа. Реакционную смесь снова охлаждали до -78°C, перемешивали 2 минуты в атмосфере диоксида углерода и затем нагревали до комнатной температуры. Реакционную смесь концентрировали при пониженном давлении, затем к остатку добавляли насыщенный водный раствор хлорида натрия и этилацетат для разделения жидкостей. К полученному водному слою для его подкисления добавляли 3N хлористоводородную кислоту и экстрагировали этилацетатом. Полученный органический слой сушили над безводным сульфатом натрия и концентрировали при пониженном давлении с получением указанного в заголовке соединения (453 мг).
1Н-ЯМР (ДМСО-d6) δ: 7,55 (2Н, д, J=8,5 Гц), 7,66 (2Н, д, J=8,5 Гц), 13,90 (1Н, шир.с).
МС (EI) m/z: 180 (M+).
[Ссылочный пример 348]
Этил 6-хлор-4-оксо-1,4-дигидрохиназолин-2-карбоксилат
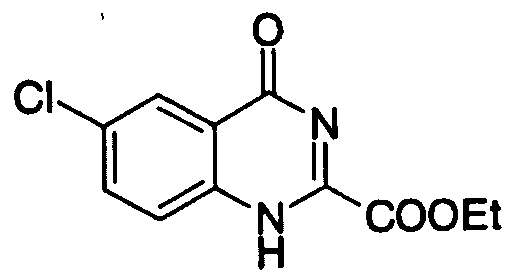
Этилхлороксоацетат (2,0 мл) добавляли к раствору 2-амино-5-хлорбензамида (2,50 г) в пиридине (15 мл) и смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь концентрировали при пониженном давлении и полученный остаток растворяли в уксусной кислоте (50 мл). К раствору добавляли уксусный ангидрид (5,0 мл) и смесь кипятили с обратным холодильником в течение 16 часов. Растворитель отгоняли при пониженном давлении и к остатку добавляли этанол. Выпавшие в осадок кристаллы отфильтровывали и промывали с получением указанного в заголовке соединения (2,71 г).
1Н-ЯМР (ДМСО-d6) δ: 1,35 (3H, т, J=7,1Гц), 4,38 (2H, кв, J=7,1Гц), 7,85 (1H, д, J=8,6Гц), 7,91 (1H, дд, J=8,6, 2,3Гц), 8,10 (1H, д, J=2,3Гц), 12,85 (1H, шир.с).
МС (ESI) m/z: 253 (M+H)+.
[Ссылочный пример 349]
6-Хлор-4-оксо-1,4-дигидрохиназолин-2-карбоновая кислота
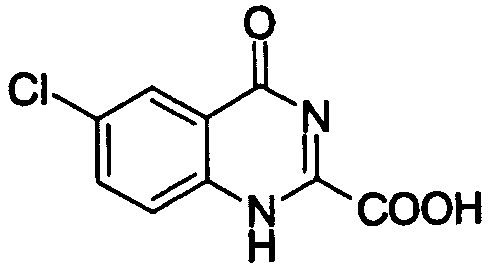
Гидроксид лития (263 мг) добавляли к раствору соединения (1,26 г), полученного в ссылочном примере 348, в смешанном растворителе из воды (5 мл) и тетрагидрофурана (25 мл) и смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь нейтрализовали 1N хлористоводородной кислотой (11 мл) при охлаждении льдом и перемешивали в течение 1 часа. Выпавшие в осадок кристаллы отфильтровывали и промывали водой с получением указанного в заголовке соединения (0,96 г).
1Н-ЯМР (ДМСО-d6) δ: 7,50-8,20 (3Н, м), 12,44 (1Н, шир.с).
МС (ESI) m/z: 265 (M+Н+CH3CN)+.
[Ссылочный пример 350]
2-Хлор-N-(4-хлорфенил)ацетамид
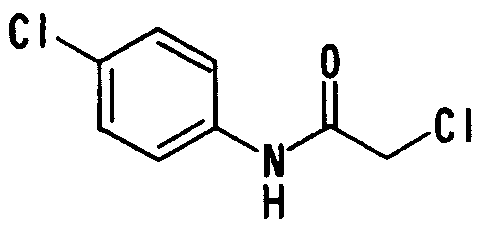
п-Хлоранилин (3,82 г) растворяли в этилацетате (30 мл), добавляли при комнатной температуре хлорацетилхлорид (2,39 мл) и смесь перемешивали в течение 1 часа. После нагревания реакционной смеси и перемешивания при 60°C в течение 3,5 часов выпавшие в осадок кристаллы отфильтровывали с получением указанного в заголовке соединения (4,78 г). Фильтрат концентрировали до примерно 1/4 и выпавшие в осадок кристаллы отфильтровывали с получением указанного в заголовке соединения (1,01 г).
1Н-ЯМР (CDCl3) δ: 4,19 (2Н, с), 7,33 (2Н, д, J=9,0Гц), 7,51 (2Н, д, J=9,0Гц), 8,22 (1Н, шир.с).
[Ссылочный пример 351]
S-[2-(4-Хлоранилино)-2-оксоэтил]тиосульфат натрия
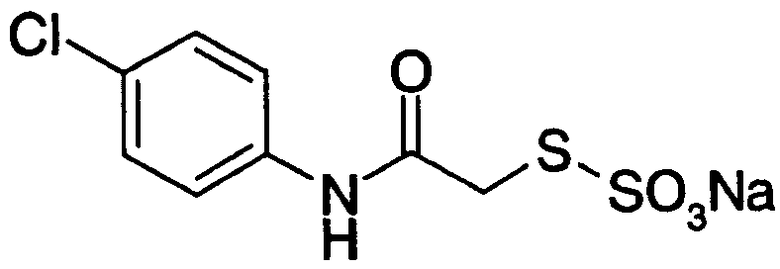
Соединение (5,79 г), полученное в ссылочном примере 350, растворяли в этаноле (140 мл), добавляли при 70°C весь водный раствор (140 мл) пентагидрата тиосульфата натрия (7,04 г) и смесь кипятили с обратным холодильником в течение 1,5 часов. Реакционную смесь концентрировали до примерно 1/10 и выпавшие в осадок кристаллы отфильтровывали с получением указанного в заголовке соединения (8,20 г).
1Н-ЯМР (ДМСО-d6) δ: 3,73 (2Н, с), 7,35 (2Н, д, J=8,8Гц), 7,57 (2Н, д, J=8,8Гц), 10,30 (1Н, с).
[Ссылочный пример 352]
Гидрохлорид 2-хлор-N-(5-хлорпиридин-2-ил)ацетамида
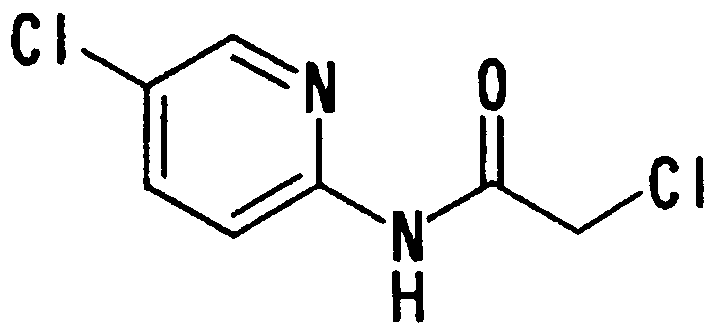
2-Амино-5-хлорпиридин (3,85 г) растворяли в этилацетате (60 мл), добавляли при комнатной температуре хлорацетилхлорид (2,39 мл) и смесь перемешивали в течение 1 часа. После нагревания реакционной смеси и перемешивания при 60°C в течение 30 минут добавляли хлорацетилхлорид (0,5 мл) и смесь перемешивали при 60°C еще 1 час. Выпавший в осадок порошок отфильтровывали с получением указанного в заголовке соединения (6,18 г).
1Н-ЯМР (ДМСО-d6) δ: 4,36 (2H, с), 7,94 (1H, дд, J=8,8, 2,7Гц), 8,09 (1H, д, J=8,8Гц), 8,40 (1H, д, J=2,7Гц), 11,03 (1H, с).
[Ссылочный пример 353]
S-{2-[(5-Хлорпиридин-2-ил)амино]-2-оксоэтил}тиосульфат натрия
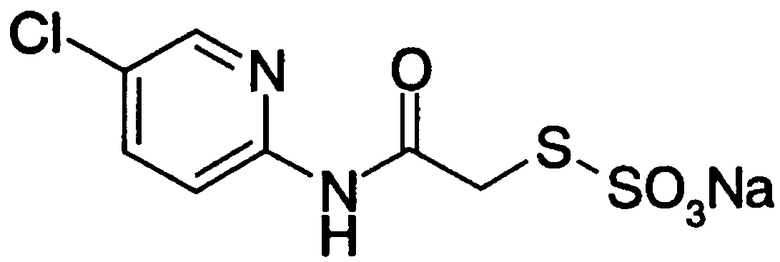
Водный раствор (130 мл) пентагидрата тиосульфата натрия (6,35 г) и гидрокарбоната натрия (2,15 г) добавляли к раствору соединения (6,18 г), полученного в ссылочном примере 352, в этаноле (130 мл) одной порцией при 80°C и перемешивании и смесь нагревали с обратным холодильником при 110°C в течение 2 часов. Реакционную смесь концентрировали при пониженном давлении до образования твердых частиц и к остатку добавляли этанол (500 мл). Полученную смесь нагревали и экстрагировали два раза. Экстракт концентрировали до примерно 1/20 и добавляли диэтиловый эфир. Выпавшее в осадок нерастворимое вещество отфильтровывали с получением указанного в заголовке соединения (6,65 г).
1Н-ЯМР (ДМСО-d6) δ: 3,77 (2H, с), 7,89 (1H, дд, J=9,0, 2,7Гц), 8,09 (1H, д, J=9,0Гц), 8,34 (1H, д, J=2,7Гц), 10,57 (1H, с).
[Ссылочный пример 354]
Гидрохлорид N-{(1R,2S,5S)-2-[(2-хлорацетил)амино]-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
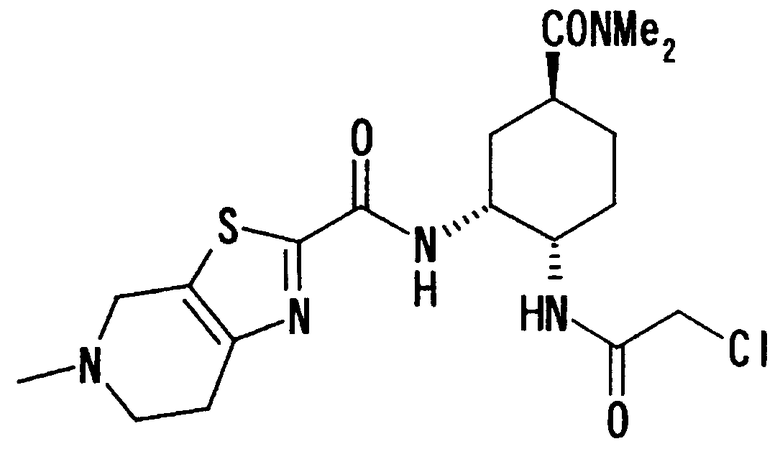
Соединение (100 мг), полученное в ссылочном примере 253, растворяли в этилацетате (10 мл), добавляли хлорацетилхлорид (21,6 мкл) и смесь нагревали и перемешивали при 60°C в течение 30 минут. Дав реакционной смеси остыть, отфильтровывали нерастворимое вещество, растворяли его в смеси метиленхлорид-метанол и отгоняли при пониженном давлении растворитель с получением неочищенного указанного в заголовке соединения (112 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,50 (1H, м), 1,55-2,00 (5H, м), 2,78 (3H, с), 2,98 (3H, с), 3,00-3,25 (5H, м), 3,17 (3H, с), 3,80-3,90 (1H, м), 3,96 (1H, д, J=12,9Гц), 4,00-4,15 (1H, м), 4,02 (1H, д, J=12,9Гц), 4,45-4,70 (2H, м), 7,85-8,00 (1H, шир.), 8,12 (1H, д, J=7,3Гц), 8,35 (1H, д, J=8,3Гц).
МС (ESI) m/z: 442 (M+H)+.
[Ссылочный пример 355]
S-{2-[((1S,2R,4S)-4-[(Диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)амино]-2-оксоэтил}тиосульфат натрия
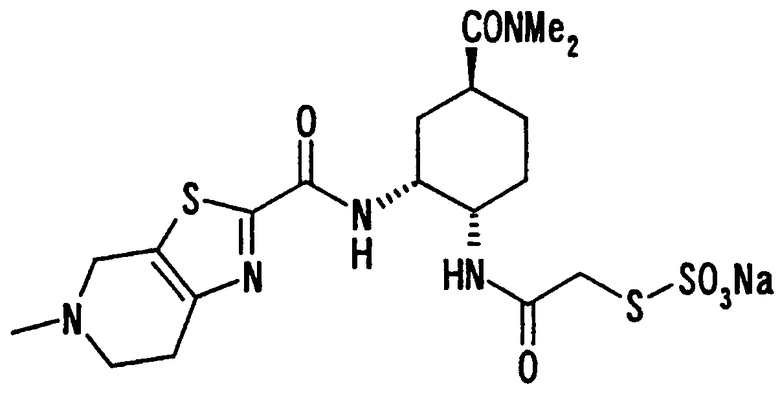
Соединение (106 мг), полученное в ссылочном примере 354, растворяли в этаноле (1,5 мл) и к полученному раствору добавляли при 90°C и перемешивании весь водный раствор (1,5 мл) пентагидрата тиосульфата натрия (55 мг) и гидрокарбоната натрия (18,6 мг). Полученную смесь кипятили с обратным холодильником в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении до образования твердых частиц и к остатку добавляли этанол (10 мл). Полученную смесь нагревали и экстрагировали. Экстракт концентрировали до примерно 1/2 и добавляли изопропиловый эфир (10 мл). Выпавшее в осадок нерастворимое вещество отфильтровывали с получением указанного в заголовке соединения (72 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,50 (1H, м), 1,55-1,90 (5H, м), 2,40 (3H, с), 2,78 (3H, с), 2,80-3,10 (5H, м), 2,96 (3H, с), 3,44 (1H, д, J=14,2Гц), 3,50 (1H, д, J=14,2Гц), 3,68 (2H, с), 3,75-3,90 (1H, м), 4,45-4,50 (1H, м), 8,01 (1H, д, J=7,4Гц), 8,15 (1H, д, J=8,3Гц).
[Ссылочный пример 356]
Метил 2-[(5-хлортиен-2-ил)амино]-2-оксоацетат
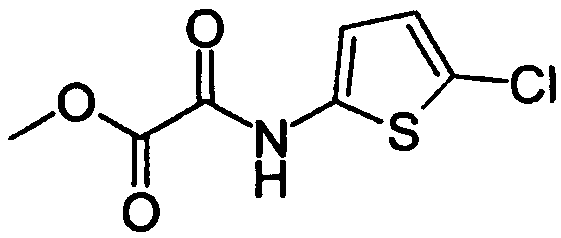
Триэтиламин (1,25 мл) и дифенилфосфорилазид (1,55 мл) добавляли к суспензии 5-хлортиофен-2-карбоновой кислоты (0,99 г) в толуоле (20 мл) и смесь перемешивали при 80°C в течение 1 часа. После охлаждения реакционной смеси до комнатной температуры добавляли трет-бутанол (2 мл) и смесь кипятили с обратным холодильником в течение 19 часов. Реакционную смесь концентрировали при пониженном давлении и к полученному остатку добавляли метиленхлорид (200 мл). Полученную смесь последовательно промывали дистиллированной водой, 10% водным раствором лимонной кислоты, дистиллированной водой, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1) с получением трет-бутил 5-хлор-2-тиенилкарбамата (1,05 г).
1Н-ЯМР (CDCl3) δ: 1,51 (9H, с), 6,21 (1H, д, J=3,1Гц), 6,60 (1H, д, J=3,1Гц), 6,91 (1H, шир.с),
МС (ESI) m/z: 234 (М+Н)+.
Полученный выше продукт (1,87 г) добавляли к 4N диоксановому раствору (40 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 4 часов, затем отгоняли при пониженном давлении растворитель. Остаток суспендировали в тетрагидрофуране (50 мл), добавляли при охлаждении льдом гидрокарбонат натрия (2,02 г) и метилхлороксоацетат (0,883 мл) и смесь перемешивали при комнатной температуре в течение 18 часов. Растворитель отгоняли при пониженном давлении, добавляли к остатку воду и метиленхлорид для разделения жидкостей, полученный органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1) и отгоняли растворитель с получением указанного в заголовке соединения (1,44 г).
1Н-ЯМР (CDCl3) δ: 3,98 (3H, с), 6,61 (1H, д, J=4,2Гц), 6,75 (1H, д, J=4,2Гц), 9,42 (1H, шир.с).
МС (FAB) m/z: 220 (М+Н)+.
[Ссылочный пример 357]
Метил 2-[(5-фторпиридин-2-ил)амино]-2-оксоацетат
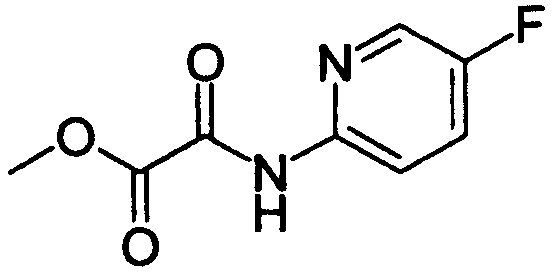
Указанное в заголовке соединение получали из 2-амино-5-фторпиридина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 3,99 (3H, с), 7,48-7,53 (1H, м), 8,21 (1H, д, J=2,9Гц), 8,27-8,31 (1H, м), 9,41 (1H, шир.с).
МС (FAB) m/z: 198 (M+H)+.
[Ссылочный пример 358]
Метил 2-[4-хлор-2-(трифторметил)анилино]-2-оксоацетат
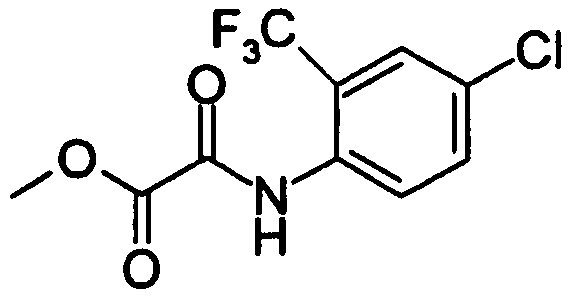
Указанное в заголовке соединение получали из 4-хлор-2-трифторанилина и метилхлороксоацетата подобно способу ссылочного примера 242.
1Н-ЯМР (CDCl3) δ: 4,01 (3Н, с), 7,58 (1Н, дд, J=8,8, 2,2Гц), 7,65 (1Н, д, J=2,2Гц), 8,34 (1Н, д, J=8,8Гц), 9,30 (1Н, шир.с).
МС (EI) m/z: 281 (M+Н)+.
[Ссылочный пример 359]
2-[4-Хлор-2-(трифторметил)анилино]-2-оксоуксусная кислота
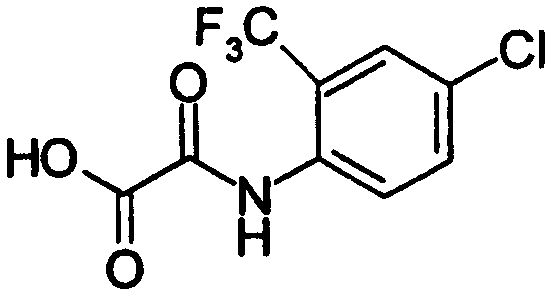
Гидроксид лития (28 мг) добавляли к раствору соединения (297 мг), полученного в ссылочном примере 358, в смешанном растворителе из тетрагидрофурана (7 мл) и воды (3 мл) и смесь перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли 1N хлористоводородную кислоту (8 мл) и метиленхлорид (20 мл) для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и остаток сушили с получением указанного в заголовке соединения (291 мг).
1Н-ЯМР (CDCl3) δ: 7,61 (1H, дд, J=8,8, 2,5Гц), 7,68 (1H, д, J=2,5Гц), 8,26 (1H, д, J=8,8Гц), 9,36 (1H, шир.с).
МС (ESI, анион) m/z: 267 (M-Н)-.
[Ссылочный пример 360]
5-Хлор-N,N-диметил-2-нитробензамид
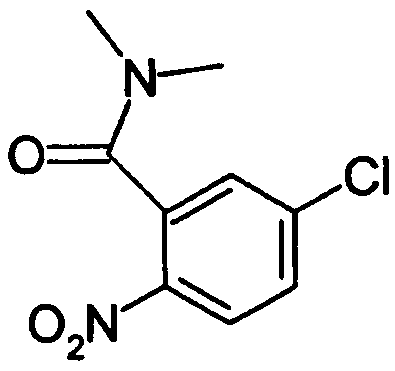
Указанное в заголовке соединение получали конденсацией 5-хлор-2-нитробензойной кислоты с диметиламином подобно способу, описанному в ссылочном примере 143.
1Н-ЯМР (CDCl3) δ: 2,86 (3H, с), 3,16 (3H, с), 7,38 (1H, д, J=2,2Гц), 7,51 (1H, дд, J=8,8, 2,2Гц), 8,15 (1H, д, J=8,8Гц).
[Ссылочный пример 361]
2-Амино-5-хлор-N,N-диметилбензамид
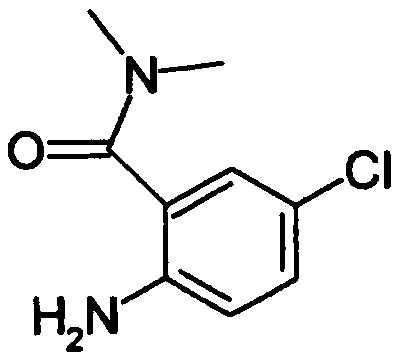
Гексагидрат хлорида железа(III) (9,93 г) и порошок цинка (8,01 г) добавляли к раствору соединения (2,8 г), полученного в ссылочном примере 360, в смешанном растворителе из N,N-диметилформамида (80 мл) и воды (40 мл) и смесь кипятили с обратным холодильником в течение 20 минут. Реакционную смесь фильтровали через целит 545 и к фильтрату добавляли этилацетат (200 мл) для разделения жидкостей. Полученный водный слой промывали этилацетатом (100 мл х 2) и полученные органические слои объединяли, промывали дистиллированной водой и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и полученный остаток подвергали колоночной хроматографии на силикагеле (метиленхлорид:гексан = 1:1 → 1:0 → метанол:метиленхлорид = 1:100) с получением указанного в заголовке соединения (2,41 г).
1Н-ЯМР (CDCl3) δ: 3,13 (6H, с), 4,33 (2H, шир.), 6,65 (1H, д, J=8,5Гц), 7,07 (1H, д, J=2,2Гц), 7,11 (1H, дд, J=8,5, 2,2Гц).
МС (ESI) m/z: 240 (M+MeCN)+.
[Ссылочный пример 362]
Метил 2-{4-хлор-2-[(диметиламино)карбонил]анилино}-2-оксоацетат
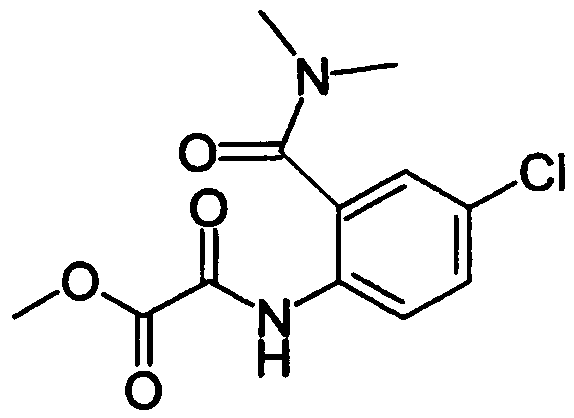
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 361, и метилхлороксоацетата подобно способу, описанному в ссылочном примере 242.
1Н-ЯМР (CDCl3) δ: 3,09 (6H, шир.), 3,96 (3H, с), 7,30 (1H, д, J=2,4Гц), 7,41 (1H, д, J=8,8, 2,4Гц), 8,34 (1H, д, J=8,8Гц), 10,46 (1H, шир.).
МС (ESI) m/z: 285 (M+H)+.
[Ссылочный пример 363]
4-Хлор-2-метоксианилин
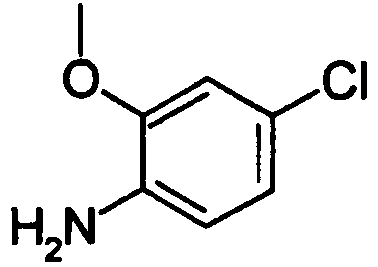
Указанное в заголовке соединение получали из 5-хлор-2-нитроанизола подобно способу, описанному в ссылочном примере 361.
1Н-ЯМР (CDCl3) δ: 3,65-3,95 (2H, шир.), 3,87 (3H, с), 6,61 (1H, д, J=8,8Гц), 6,74-6,78 (2H, м).
МС (ESI) m/z: 199 (M+MeCN+H)+.
[Ссылочный пример 364]
Метил 2-(4-хлор-2-метоксианилино)-2-оксоацетат
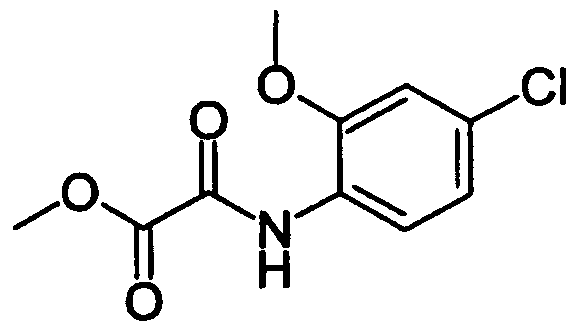
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 363, и метилхлороксоацетата подобно способу, описанному в ссылочном примере 242.
1Н-ЯМР (CDCl3) δ: 3,92 (3H, с), 3,97 (3H, с), 6,90 (1H, д, J=2,2Гц), 6,98 (1H, дд, J=8,8, 2,2Гц), 8,35 (1H, д, J=8,8Гц), 9,33-9,44 (1H, шир.).
МС (ESI) m/z: 244 (М+Н)+.
[Ссылочный пример 365]
Этил 2-(4-хлоранилино)-2-(гидроксиимино)ацетат
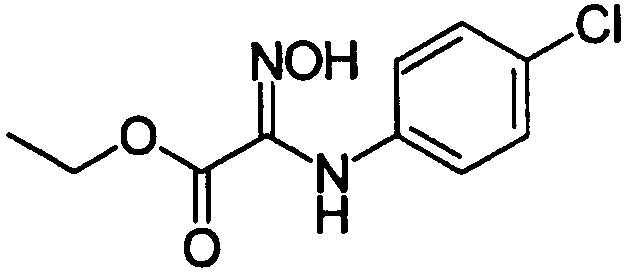
Указанное в заголовке соединение получали из 4-хлоранилина (3,03 г) и этил 2-хлор-2-гидроксииминоацетата подобно способу, описанному в литературе (Gilchrist, T. L.; Peek, M. E.; Rees, C. W.; J. Chem. Soc. Chem. Commun., 1975, 913).
1Н-ЯМР (CDCl3) δ: 1,26 (3H, т, J=7,1Гц), 1,60-1,80 (1H, шир.), 4,28 (2H, кв, J=7,1Гц), 6,85 (2H, д, J=8,6Гц), 7,24 (2H, д, J=8,6Гц), 8,15-8,45 (1H, шир.).
МС (ESI) m/z: 243 (M+H)+.
[Ссылочный пример 366]
трет-Бутил (1R,2S,5S)-2-{[2-(4-хлоранилино)-2-(гидроксиимино)ацетил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
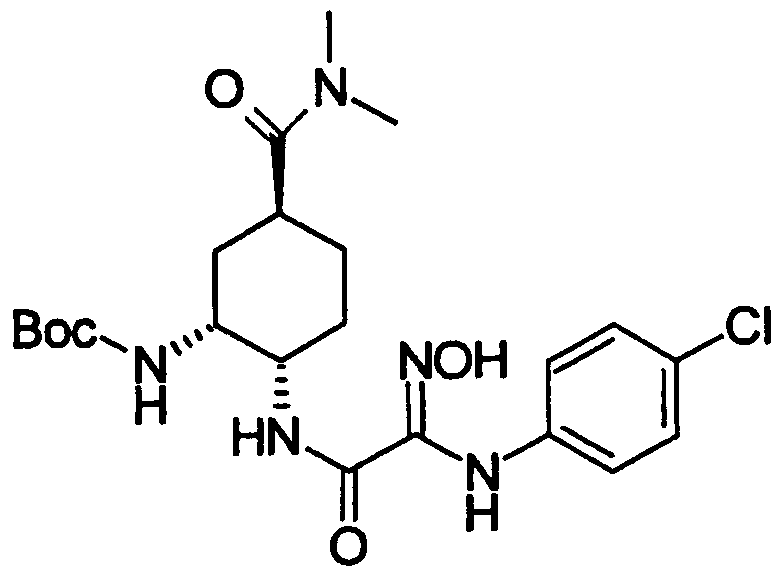
Соединение (597 мг), полученное в ссылочном примере 144, добавляли к раствору соединения (350 мг), полученного в ссылочном примере 365, в этаноле (5,0 мл) и смесь перемешивали при 70°C в течение 3 суток. Реакционную смесь концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 30:1) с получением указанного в заголовке соединения (180 мг).
1Н-ЯМР (CD3OD) δ: 1,46 (9H, с), 1,47-1,84 (6H, м), 1,88-1,95 (1H, м), 2,90 (3H, с), 3,08 (3H, с), 3,90-3,97 (1H, м), 4,11-4,17 (1H, м), 6,84 (2H, д, J=8,8Гц), 7,18 (2H, д, J=8,8Гц).
МС (ESI) m/z: 504 (M+Na)+.
[Ссылочный пример 367]
трет-Бутил (3R,4S)-4-{[2-(4-хлоранилино)-2-оксоацетил]амино}-1-(2-метоксиацетил)пиперидин-3-илкарбамат
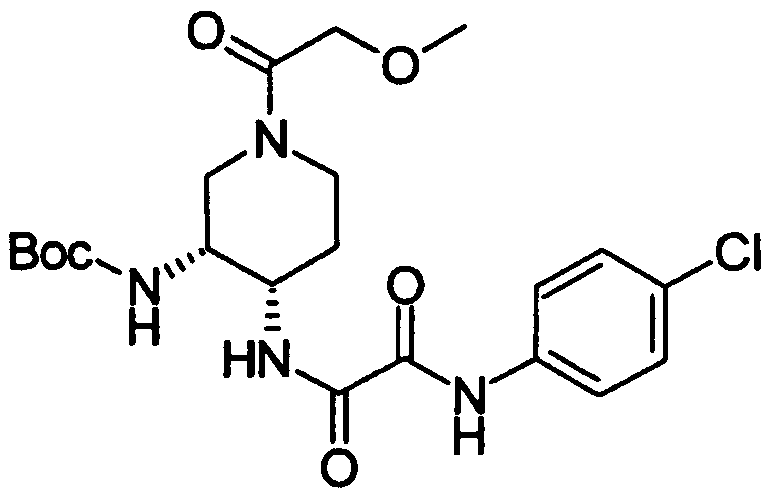
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 374, и соединения, полученного в ссылочном примере 220, подобно способу, описанному в ссылочном примере 214.
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,55-1,75 (1H, шир.), 1,94-2,07 (1H, шир.), 2,70-3,00 (1H, м), 3,10-3,37 (1H, м), 3,44 (3H, с), 3,88-4,22 (4H, м), 4,55-4,69 (1H, шир.), 4,80-4,90 (0,5H, шир.), 5,36-5,48 (0,5H, шир.), 7,20-7,30 (1H, шир.), 7,32 (2H, д, J=8,8Гц), 7,62 (2H, д, J=8,8Гц), 8,20-8,40 (1H, шир.), 9,15-9,25 (1H, шир.).
МС (ESI) m/z: 469 (M+H)+.
[Ссылочный пример 368]
трет-Бутил (3R,4S)-4-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-1-(2-метоксиацетил)пиперидин-3-илкарбамат
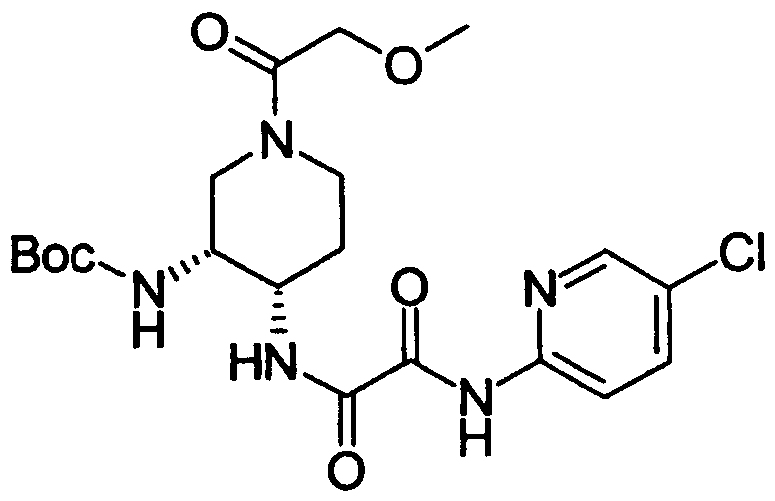
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 266, и соединения, полученного в ссылочном примере 220, подобно способу, описанному в ссылочном примере 214.
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,65-2,30 (2H, шир.), 2,68-3,02 (1H, м), 3,10-3,35 (1H, м), 3,44 (3H, с), 3,80-4,25 (4H, м), 4,45-4,70 (1H, м), 5,05-5,20 (0,5H, м), 5,80-5,93 (0,5H, м), 7,30-7,40 (1H, шир.), 7,71 (1H, шир.д, J=8,7Гц), 7,95-8,05 (0,3H, шир.), 8,19 (1H, шир.д, J=8,8Гц), 8,31 (1H, шир.с), 8,38-8,53 (0,7H, шир.), 9,74-9,84 (1H, шир.).
МС (ESI) m/z: 470 (M+H)+.
[Ссылочный пример 369]
трет-Бутил (3R,4S)-4-({2-[(5-бромпиридин-2-ил)амино]-2-оксоацетил}амино)-1-(2-метоксиацетил)пиперидин-3-илкарбамат
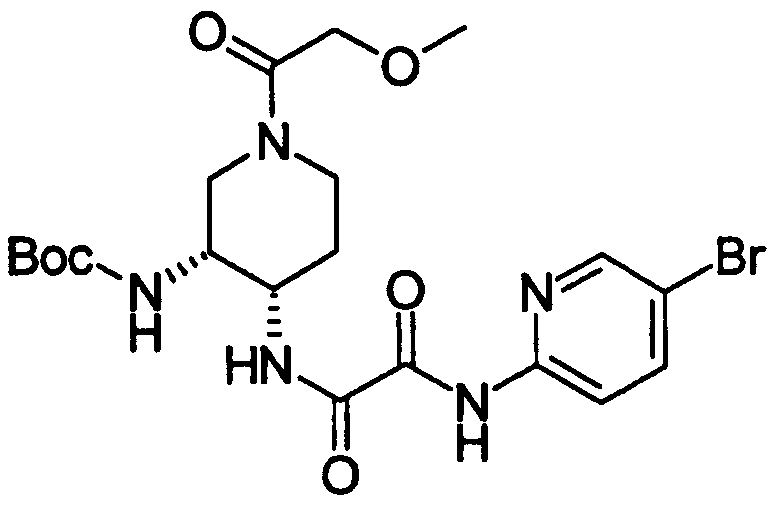
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 375, и соединения, полученного в ссылочном примере 220, подобно способу, описанному в ссылочном примере 214.
1Н-ЯМР (CDCl3) δ: 1,47 (9H, с), 1,50-1,75 (1H, м), 1,95-2,13 (1H, шир.), 2,70-2,98 (1H, м), 3,05-3,36 (1H, м), 3,45 (3H, с), 3,80-4,24 (4H, м), 4,57-4,73 (1H, шир.), 4,85-4,95 (0,25H, шир.), 5,10-5,15 (0,25H, шир.), 5,45-5,58, (0,5H, шир.), 7,30-7,38 (1H, м), 7,84 (1H, дд, J=8,8, 2,2Гц), 8,16 (1H, д, J=8,8Гц), 8,30-8,55 (1H, шир.), 8,40 (1H, д, J=2,2Гц), 9,68 (1H, шир.с).
[Ссылочный пример 370]
Этил 3-(4-хлоранилино)-3-оксопропионат
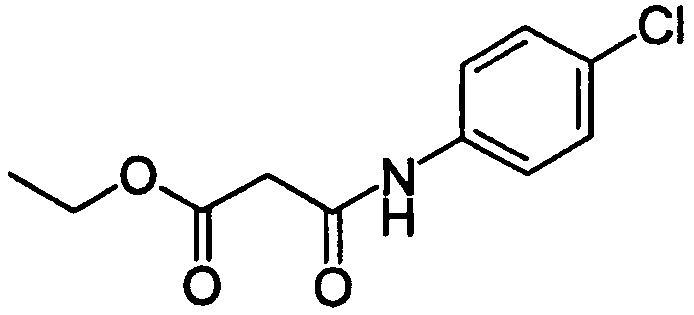
Этилмалонат калия (3,2 г), 1-гидроксибензотриазол (2,1 г) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (4,5 г) последовательно добавляли к раствору 4-хлоранилина (2,0 г) в N,N-диметилформамиде (20 мл) при комнатной температуре и смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь разбавляли этилацетатом и промывали насыщенным водным раствором гидрокарбоната натрия, 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель с получением указанного в заголовке соединения (4,0 г).
1Н-ЯМР (CDCl3) δ: 1,33 (3H, т, J=7,3Гц), 3,47 (2H, с), 4,26 (2H, кв, J=7,3Гц), 7,29 (2H, д, J=8,8Гц), 7,51 (2H, д, J=8,8Гц), 9,32 (1H, шир.с).
[Ссылочный пример 371]
3-(4-Хлоранилино)-3-оксопропионовая кислота
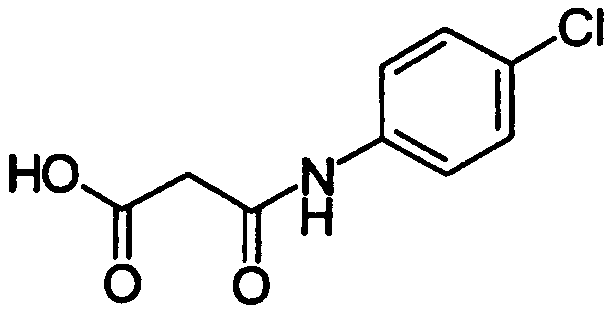
1N Водный раствор (10 мл) гидроксида натрия добавляли по каплям к раствору соединения (1,0 г), полученного в ссылочном примере 370, в этаноле (10 мл) при комнатной температуре и смесь перемешивали 2 часа. К реакционной смеси добавляли 1N хлористоводородную кислоту (10 мл), смесь перемешивали и затем выпавшее в осадок нерастворимое вещество отфильтровывали с получением указанного в заголовке соединения (0,5 г).
1Н-ЯМР (ДМСО-d6) δ: 3,34 (2H, с), 7,35 (2H, д, J=8,8Гц), 7,59 (2H, д, J=8,8Гц), 10,26 (1H, с), 12,66 (1H, шир.с).
[Ссылочный пример 372]
Этил 3-(3-хлоранилино)-3-оксопропионат
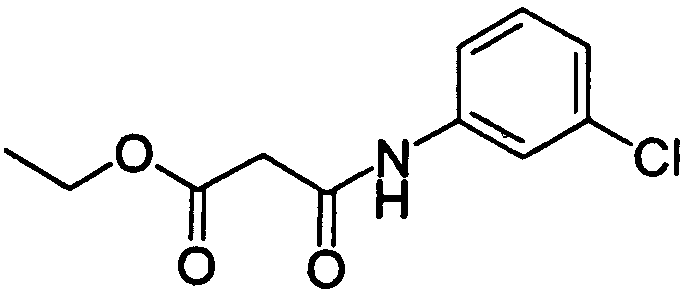
Указанное в заголовке соединение получали конденсацией 3-хлоранилина с этилмалонатом калия подобно способу, описанному в ссылочном примере 370.
1Н-ЯМР (CDCl3) δ: 1,33 (3H, т, J=7,3Гц), 3,47 (2H, с), 4,26 (2H, кв, J=7,3Гц), 7,09 (1H, д, J=8,8Гц), 7,22-7,26 (1H, м), 7,39 (1H, д, J=8,8Гц), 7,69 (1H, с), 9,35 (1H, шир.с).
[Ссылочный пример 373]
3-(3-Хлоранилино)-3-оксопропионовая кислота
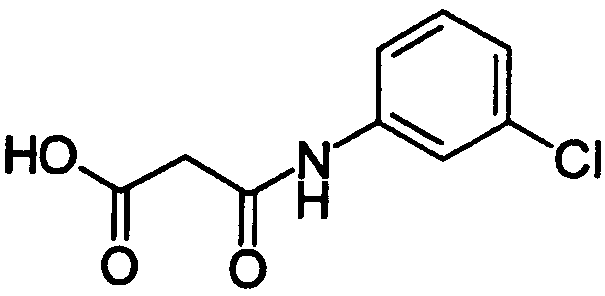
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 372, подобно способу, описанному в ссылочном примере 371.
1Н-ЯМР (ДМСО-d6) δ: 3,35 (2H, с), 7,11 (1H, д, J=8,8Гц), 7,33 (1H, т, J=8,8Гц), 7,39 (1H, д, J=8,8Гц), 7,78 (1H, с), 10,31 (1H, с), 12,67 (1H, шир.с).
[Ссылочный пример 374]
2-(4-Хлоранилино)-2-оксоуксусная кислота
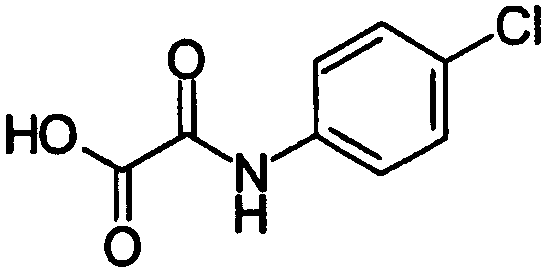
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 242, подобно способу, описанному в ссылочном примере 359.
1Н-ЯМР (ДМСО-d6) δ: 7,37 (2H, д, J=8,8Гц), 7,79 (2H, д, J=8,8Гц), 10,66 (1H, с).
[Ссылочный пример 375]
3-[(5-Бромпиридин-2-ил)амино]-2-оксоуксусная кислота
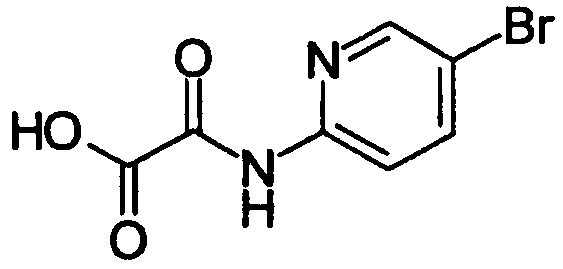
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 262, подобно способу, описанному в ссылочном примере 359.
1Н-ЯМР (ДМСО-d6) δ: 7,95-8,00 (1H, м), 8,08 (1H, дд, J=8,8, 2,0Гц), 8,50 (1H, д, J=2,0Гц), 10,74 (1H, с).
[Ссылочный пример 376]
4-Хлор-3-фторбензойная кислота
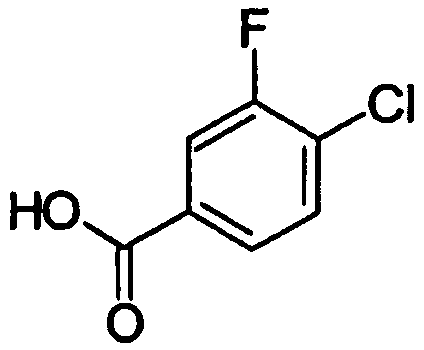
Хлорит натрия (17 г) добавляли порциями к смешанному раствору, состоящему из 4-хлор-3-фторбензальдегида (10 г), амидосерной кислоты (18 г), трет-бутилового спирта (50 мл) и воды (50 мл), при охлаждении льдом и смесь перемешивали в течение 4 суток при постепенном повышении температуры системы до комнатной температуры. Реакционную смесь разбавляли этилацетатом и промывали водой, 1N хлористоводородной кислотой и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель, затем полученный остаток перекристаллизовывали из смешанного растворителя диизопропиловый эфир/гексан с получением указанного в заголовке соединения (11,2 г).
1Н-ЯМР (ДМСО-d6) δ: 7,72 (1H, дт, J=8,3, 1,5Гц), 7,77 (1H, дт, J=8,3, 1,6Гц), 7,82 (1H, дт, J=9,7, 1,5Гц), 13,45 (1H, с).
[Ссылочный пример 377]
Метил 2-(4-хлор-3-фторанилино)-2-оксоацетат
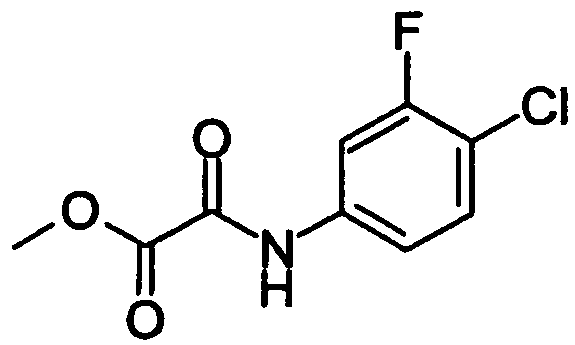
Указанное в заголовке соединение получали, подвергая соединение, полученное в ссылочном примере 376, перегруппировке Курциуса и затем конденсируя полученный продукт с метилхлороксоацетатом подобно способу, описанному в ссылочном примере 356.
1Н-ЯМР (CDCl3) δ: 3,99 (3H, с), 7,25-7,27 (1H, м), 7,39 (1H, т, J=8,5Гц), 7,72 (1H, дд, J=10,4, 2,4Гц), 8,90 (1H, шир.с).
[Ссылочный пример 378]
2-(4-Хлор-2-фторанилино)-2-оксоуксусная кислота
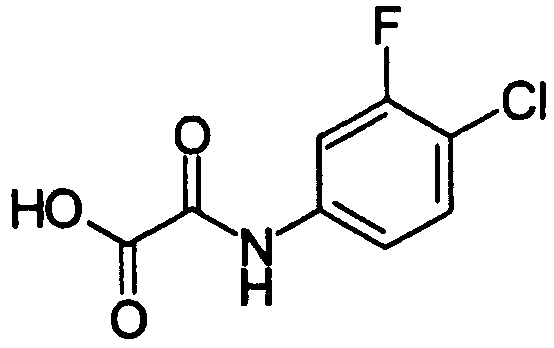
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 377, подобно способу, описанному в ссылочном примере 359.
1Н-ЯМР (ДМСО-d6) δ: 7,52 (1H, т, J=8,8Гц), 7,63 (1H, дд, J=8,8, 2,2Гц), 7,88 (1H, дд, J=12,0, 2,2Гц), 10,83 (1H, шир.с).
[Ссылочный пример 379]
Этил 3-(4-хлорфенил)-3-оксопропионат
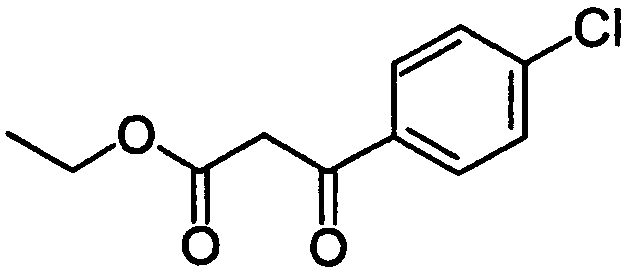
Триэтиламин (17 мл) и хлорид магния (5,5 г) добавляли к суспензии этилмалоната калия (8,2 г) в этилацетате (100 мл) при охлаждении льдом и смесь перемешивали в течение 18 часов при постепенном повышении температуры системы до комнатной температуры. С другой стороны, суспензию, состоящую из 4-хлорбензойной кислоты (5,0 г), тионилхлорида (12 мл), N,N-диметилформамида (одна капля) и толуола (100 мл), кипятили с обратным холодильником в течение 1 часа и затем реакционную смесь концентрировали. Полученный остаток растворяли в этилацетате и к реакционной смеси добавляли по каплям при охлаждении льдом заранее приготовленный раствор. Полученную смесь перемешивали 18 часов при постепенном повышении температуры системы до комнатной температуры. К реакционной смеси добавляли 10% водный раствор лимонной кислоты и смесь перемешивали 30 минут для отделения полученного органического слоя. Органический слой промывали насыщенным водным раствором хлорида натрия, затем сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток отделяли и очищали колоночной хроматографией на силикагеле (хлороформ) с получением указанного в заголовке соединения (6,4 г).
1Н-ЯМР (CDCl3) δ: 1,26 (3H, т, J=7,3Гц), 3,96 (2H, с), 4,21 (2H, кв, J=7,3Гц), 7,46 (2H, д, J=8,8Гц), 7,89 (2H, д, J=8,8Гц).
[Ссылочный пример 380]
Этил 3-(4-хлорфенил)-3-гидроксипропионат
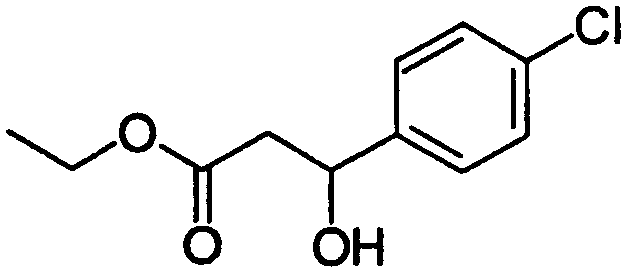
Боргидрид натрия (0,2 г) добавляли порциями при охлаждении льдом к раствору соединения (1,0 г), полученного в ссылочном примере 379, в тетрагидрофуране (10 мл) и смесь перемешивали в течение 2 часов при постепенном повышении температуры системы до комнатной температуры. К реакционной смеси добавляли 10% водный раствор лимонной кислоты и полученную смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия, затем сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток отделяли и очищали колоночной хроматографией на силикагеле (хлороформ) с получением указанного в заголовке соединения (0,56 г).
1Н-ЯМР (CDCl3) δ: 1,27 (3H, т, J=7,3Гц), 2,70 (1H, д, J=7,8Гц), 2,71 (1H, д, J=3,4Гц), 3,37 (1H, д, J=3,4Гц), 4,18 (2H, кв, J=7,3Гц), 5,09-5,13 (1H, м), 7,30-7,35 (5H, м).
[Ссылочный пример 381]
3-(4-Хлорфенил)-3-гидроксипропионовая кислота
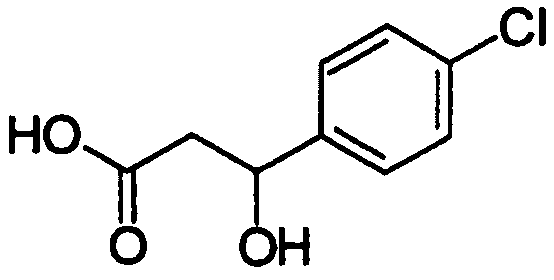
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 380, подобно способу, описанному в ссылочном примере 359.
1Н-ЯМР (ДМСО-d6) δ: 3,25-3,32 (1Н, м), 4,89-4,95 (1Н, м), 5,45-5,53 (1Н, м), 7,35-7,36 (5Н, м), 12,11-12,18 (1Н, м).
МС (ESI, анион) m/z: 198 (M-H)-.
[Ссылочный пример 382]
трет-Бутил (1R,2S,5S)-2-{[3-(4-хлорфенил)-3-гидроксипропаноил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
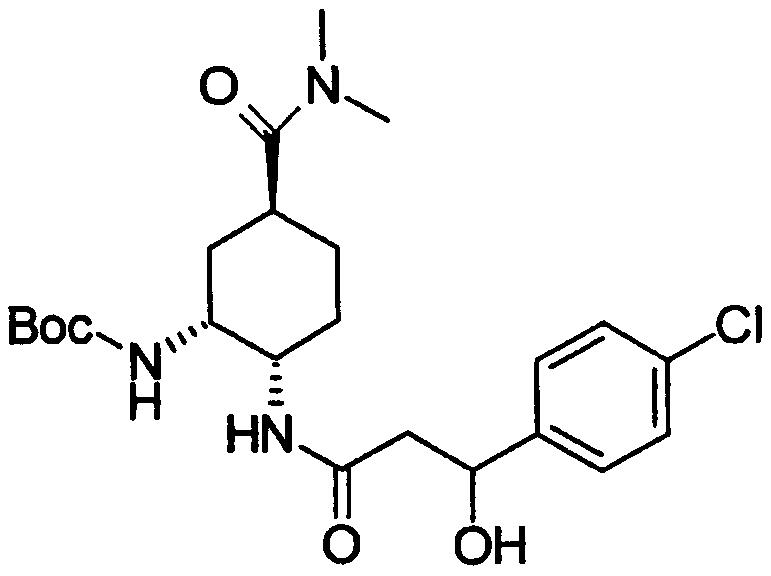
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 144, с соединением, полученным в ссылочном примере 381, подобно способу, описанному в ссылочном примере 91.
1Н-ЯМР (CDCl3) δ: 1,21-1,44 (2H, м), 1,46 (9H, с), 1,76-1,92 (2H, м), 1,95-2,10 (2H, м), 2,40-2,55 (2H, м), 2,55-2,68 (1H, м), 2,94 (3H, с), 3,05 (3H, с), 3,82-3,96 (1H, м), 4,02-4,17 (1H, м), 4,65-4,80 (2H, м), 5,03-5,13 (1H, м), 7,28-7,33 (5H, м).
МС (ESI) m/z: 468 (М+Н)+.
[Ссылочный пример 383]
трет-Бутил (1R,2S,5S)-2-{[3-(4-хлорфенил)-3-оксопропаноил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
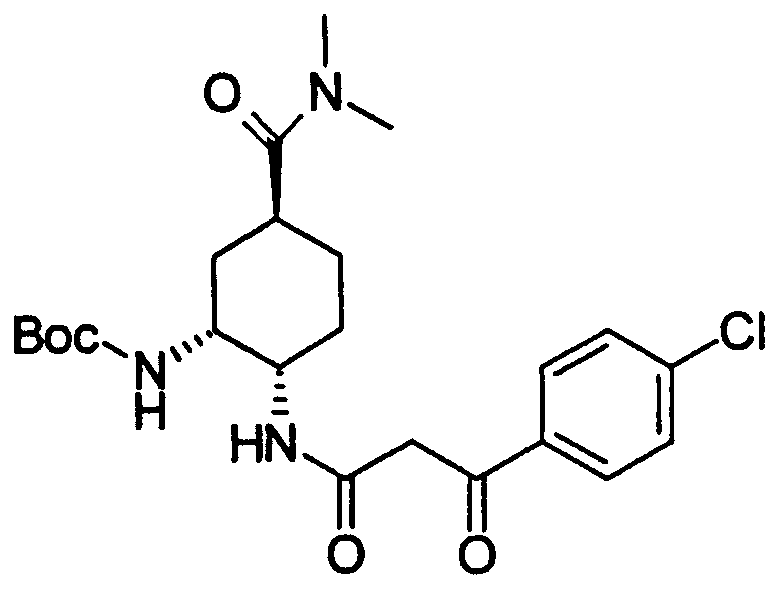
Диоксид марганца (0,47 г) добавляли к раствору соединения (0,5 г), полученного в ссылочном примере 382, в 1,4-диоксане (20 мл) при комнатной температуре и смесь перемешивали в течение 4 суток. Нерастворимое вещество удаляли фильтрованием через слой целита и полученный фильтрат концентрировали при пониженном давлении с получением указанного в заголовке соединения (0,46 г).
1Н-ЯМР (ДМСО-d6) δ: 1,28-1,39 (1H, м), 1,40 (9H, с), 1,41-1,63 (3H, м), 2,25-2,42 (2H, м), 2,76 (3H, с), 2,90-2,97 (1H, м), 2,98 (3H, с), 3,56 (2H, с), 3,89-3,97 (1H, м), 4,88-4,98 (1H, м), 6,65-6,70 (1H, м), 7,30-7,35 (4H, м), 7,33 (1H, дд, J=2,9, 1,7Гц).
МС (ESI, анион) m/z: 464 (M-H)-.
[Ссылочный пример 384]
Этил (1S,3R,4R)-4-азидо-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
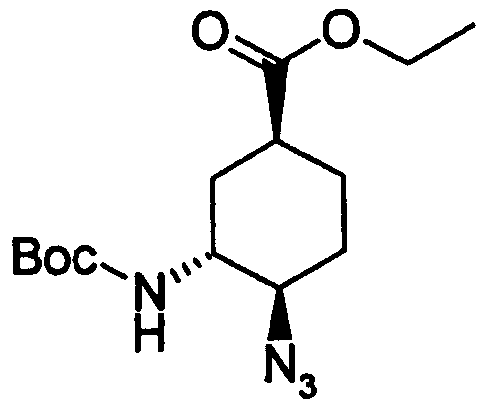
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 248, подобно способу, описанному в ссылочном примере 249.
[α]25 D = +62° (c = 1, хлороформ).
1Н-ЯМР (CDCl3) δ: 1,27 (3H, т, J=7,1Гц), 1,46 (9H, с), 1,61 (1H, с), 1,61-1,71 (2H, м), 1,81-1,90 (1H, м), 1,97-2,03 (1H, м), 2,22-2,28 (1H, м), 2,56-2,60 (1H, м), 3,54 (1H, шир.с), 3,63-3,68 (1H, м), 4,16 (2H, кв, J=7,1Гц), 4,58 (1H, шир.с).
[Ссылочный пример 385]
трет-Бутил (1R,2R,5S)-2-азидо-5-[(диметиламино)карбонил]циклогексилкарбамат
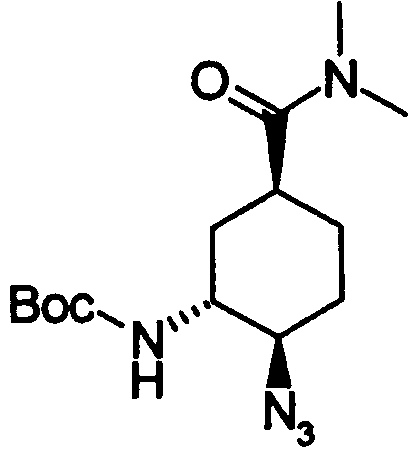
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 384, подобно способам ссылочных примеров 250 и 251.
1Н-ЯМР (CDCl3) δ: 1,46 (9H, с), 1,40-2,20 (6H, м), 2,70-2,80 (1H, м), 2,93 (3H, с), 3,03 (3H, с), 3,60-3,78 (1H, м), 3,83-3,95 (1H, м), 4,65 (1H, д, J=7,2Гц).
[Ссылочный пример 386]
трет-Бутил (1R,2R,5S)-2-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-5-[(диметиламино)карбонил]циклогексилкарбамат
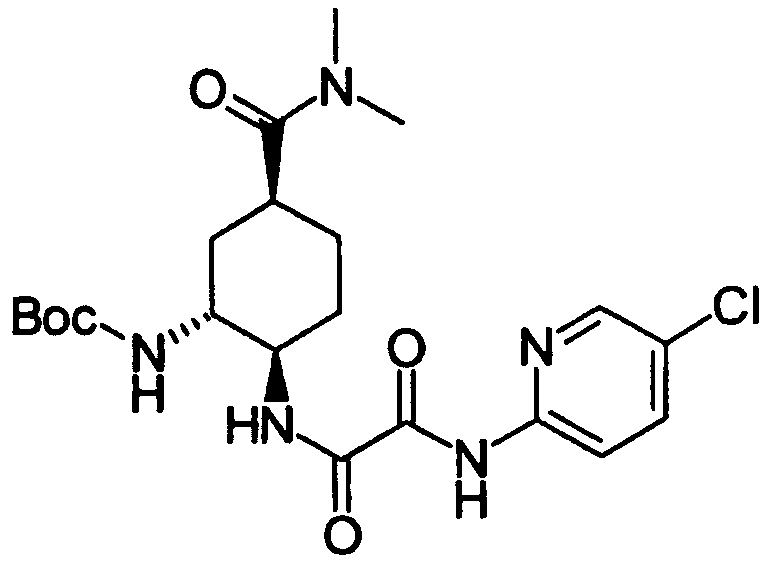
Указанное в заголовке соединение получали превращением азидной группы соединения, полученного в ссылочном примере 385, в аминогруппу подобно способу, описанному в ссылочном примере 90, и затем конденсацией полученного продукта с соединением, полученным в ссылочном примере 266, подобно способу, описанному в ссылочном примере 91.
1Н-ЯМР (CDCl3) δ: 1,13-2,25 (16H, м), 2,94 (3H, с), 3,03 (3H, с), 3,60-3,78 (1H, м), 4,13-4,31 (1H, м), 4,45-4,65 (1H, м), 7,80 (1H, дд, J=8,8, 2,4Гц), 8,03 (1H, шир.с), 8,21 (1H, д, J=8,8Гц), 8,29 (1H, д, J=2,4Гц), 9,71 (1H, с).
МС (ESI) m/z: 468 (М+Н)+.
[Ссылочный пример 387]
N-{(1R,2R,5S)-2-Азидо-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
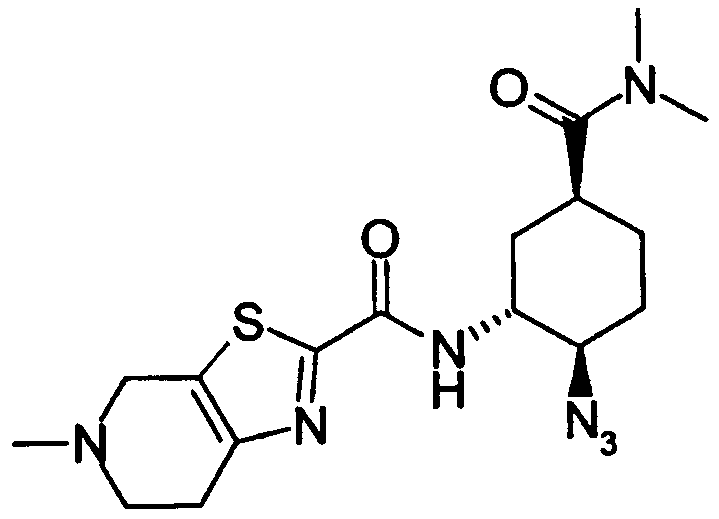
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 385, и соединения, полученного в ссылочном примере 10, подобно способу, описанному в ссылочном примере 252.
1Н-ЯМР (CDCl3) δ: 1,75-2,08 (6H, м), 2,20-2,32 (1H, м), 2,51 (3H, с), 2,75-2,97 (4H, м), 2,95 (3H, с), 3,04 (3H, с), 3,65-3,80 (3H, м), 4,27-4,39 (1H, м), 7,17-7,28 (1H, м).
МС (ESI) m/z: 392 (М+Н)+.
[Ссылочный пример 388]
трет-Бутил 4-[(2-метокси-2-оксоацетил)амино]пиперидин-1-карбоксилат
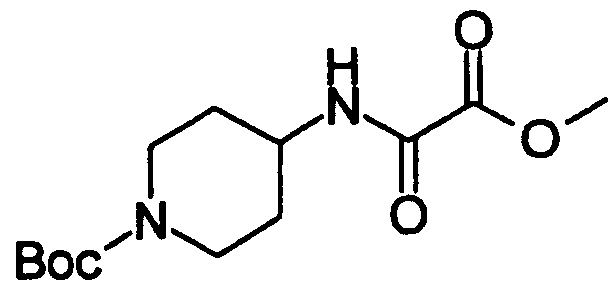
Указанное в заголовке соединение получали из (4-амино-N-трет-бутоксикарбонил)пиперидина и метилхлороксоацетата подобно способу, описанному в ссылочном примере 242.
1Н-ЯМР (ДМСО-d6) δ: 1,46 (9H, с), 1,34-1,51 (2H, м), 1,89-1,98 (2H, м), 2,82-2,96 (2H, м), 3,91 (3H, с), 3,88-4,14 (3H, м), 6,96-7,07 (1H, м).
МС (FAB) m/z: 287 (М+Н)+.
[Ссылочный пример 389]
трет-Бутил 4-{[2-({(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}амино)-2-оксоацетил]амино}пиперидин-1-карбоксилат
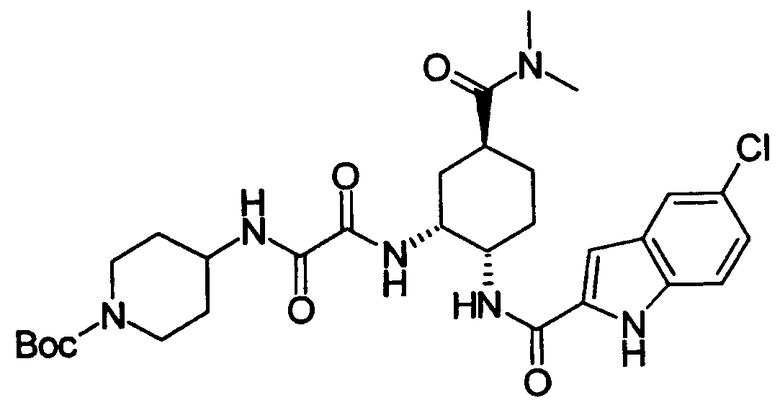
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 310, и соединения, полученного в ссылочном примере 388, подобно способу, описанному в ссылочном примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,46 (9H, с), 1,35-2,28 (11H, м), 2,70-3,18 (9H, м), 3,80-4,57 (4H, м), 6,78 (1H, с), 7,15-8,12 (6H, м), 9,45 (1H, с).
МС (FAB) m/z: 617 (М+Н)+.
[Ссылочный пример 390]
Метил 2-[(5-хлорпиридин-2-ил)(метил)амино]-2-оксоацетат
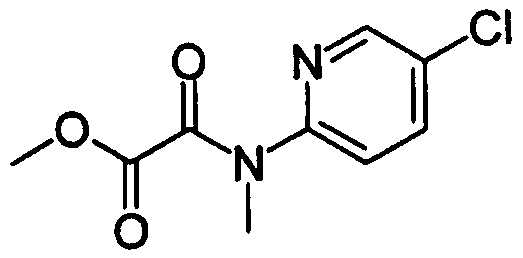
Указанное в заголовке соединение получали из 5-хлор-N-метил-2-пиридинамина и метилхлороксоацетата подобно способу, описанному в ссылочном примере 242.
1Н-ЯМР (CDCl3) δ: 3,43 (3H, с), 3,81 (3H, с), 7,08 (1H, шир.с), 7,68-7,78 (1H, м), 8,27 (1H, шир.с).
МС (ESI) m/z: 229 (M+H)+.
[Ссылочный пример 391]
Метил 2-[(5-хлорпиримидин-2-ил)амино]-2-оксоацетат
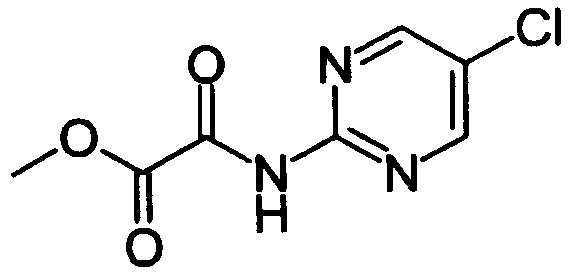
Указанное в заголовке соединение получали из 2-амино-5-хлорпиримидина и метилхлороксоацетата подобно способу, описанному в ссылочном примере 242.
1Н-ЯМР (CDCl3) δ: 4,00 (3H, с), 8,63 (2H, с), 9,58 (1H, шир.с).
МС (ESI) m/z: 215 (M+H)+.
[Ссылочный пример 392]
N-((1R,2S,5S)-2-Азидо-5-{[этил(метил)амино]карбонил}циклогексил)-5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-карбоксамид
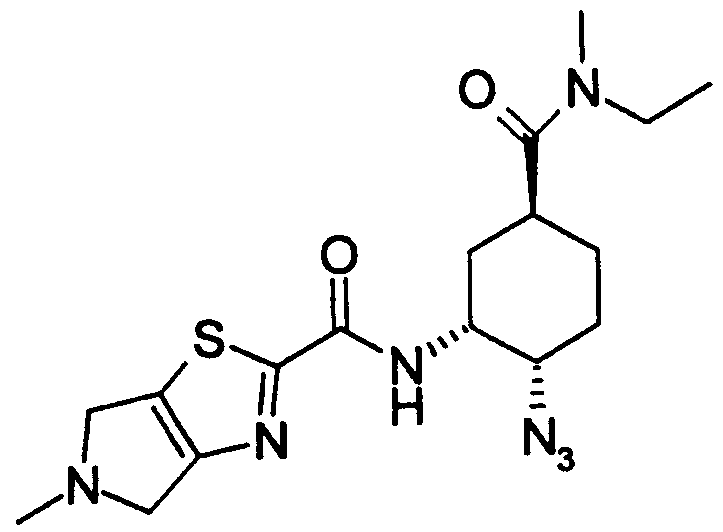
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 323, и соединения, полученного в ссылочном примере 293, подобно способу, описанному в ссылочном примере 252.
1Н-ЯМР (CDCl3) δ: 1,08, 1,15 (3H, каждый т, J=7,1Гц), 1,74-1,88 (4H, м), 2,12-2,22 (2H, м), 2,67 (3H, с), 2,81-2,86 (1H, м), 2,89, 2,96 (3H, каждый с), 3,28-3,43 (2H, м), 3,91-4,10 (5H, м), 4,60-4,62 (1H, м), 7,21 (1H, д, J=7,6Гц).
МС (ESI) m/z: 392 (М+Н)+.
[Ссылочный пример 393]
Метил 2-(4-хлор-3-метоксианилино)-2-оксоацетат
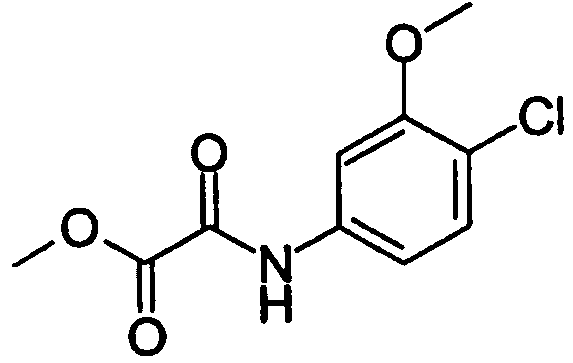
Указанное в заголовке соединение получали восстановлением 2-хлор-5-нитроанизола подобно способу, описанному в ссылочном примере 361, до аминопроизводного и затем конденсацией аминопроизводного с метилхлороксоацетатом подобно способу, описанному в ссылочном примере 242.
1Н-ЯМР (CDCl3) δ: 3,93 (3H, с), 3,98 (3H, с), 7,00 (1H, дд, J=8,5, 2,4Гц), 7,33 (1H, д, J=8,5Гц), 7,57 (1H, д, J=2,4Гц), 8,89 (1H, шир.с).
[Ссылочный пример 394]
2-(4-Хлор-3-метоксианилино)-2-оксоуксусная кислота
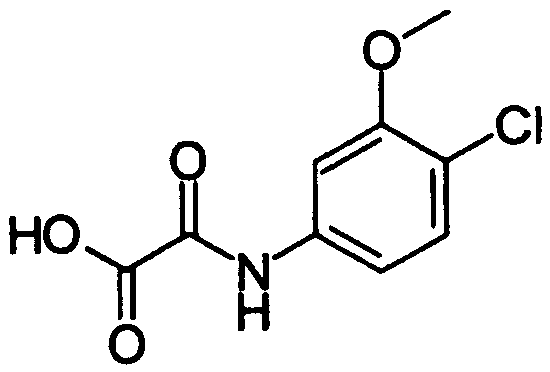
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 393, подобно способу, описанному в ссылочном примере 359.
1Н-ЯМР (ДМСО-d6) δ: 3,81 (3H, с), 7,36 (1H, д, J=8,7Гц), 7,43 (1H, д, J=8,7Гц), 7,65 (1H, д, J=2,2Гц), 10,79 (1H, с).
МС (ESI, анион) m/z: 228 (М-Н)-.
[Ссылочный пример 395]
N1-{(1S,2R,4S)-2-Амино-4-[(диметиламино)карбонил]циклогексил}-N2-(4-хлор-3-метоксифенил)этандиамид
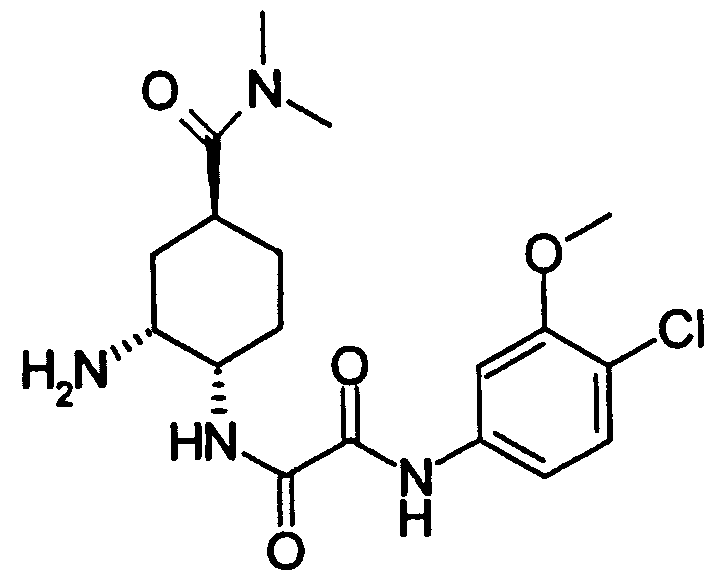
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 144, с соединением, полученным в ссылочном примере 394, подобно способу, описанному в ссылочном примере 97, обработкой полученного продукта хлористоводородной кислотой подобно способу, описанному в ссылочном примере 69, и затем нейтрализацией его 1N водным раствором гидроксида натрия.
1Н-ЯМР (CDCl3) δ: 1,48-2,00 (8H, м), 2,84-2,93 (1H, м), 2,95 (3H, с), 3,08 (3H, с), 3,33-3,35 (1H, м), 3,89-3,94 (4H, м), 7,06 (1H, дд, J=8,5, 2,2Гц), 7,32 (1H, д, J=8,5Гц), 7,56 (1H, д, J=2,2Гц), 8,05 (1H, д, J=8,5Гц), 9,43 (1H, шир.с).
МС (ESI) m/z: 397 (М+).
[Ссылочный пример 396]
Метил 2-(4-этиниланилино)-2-оксоацетат
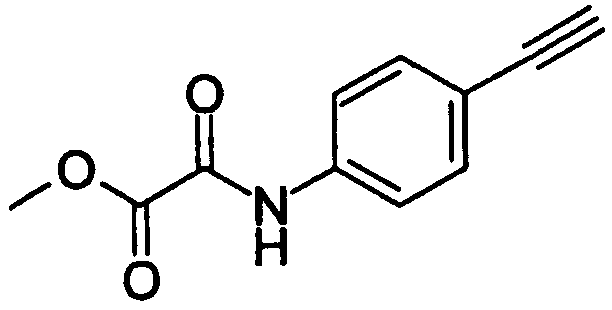
Указанное в заголовке соединение получали из 4-этиниланилина и метилхлороксоацетата подобно способу, описанному в ссылочном примере 242.
1Н-ЯМР (CDCl3) δ: 3,09 (1H, с), 3,98 (3H, с), 7,50 (2H, д, J=8,4Гц), 7,62 (2H, д, J=8,4Гц), 8,89 (1H, шир.с).
[Ссылочный пример 397]
2-(4-Этиниланилино)-2-оксоацетат натрия
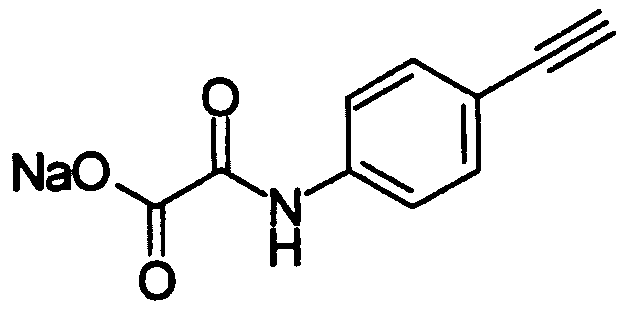
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 396, с гидроксидом натрия подобно способу, описанному в ссылочном примере 266.
1Н-ЯМР (ДМСО-d6) δ: 4,06 (1H, с), 7,39 (2H, д, J=8,4Гц), 7,80 (2H, д, J=8,4Гц), 10,33 (1H, шир.с).
[Ссылочный пример 398]
Метил 2-[(5-хлорпиразин-2-ил)амино]-2-оксоацетат

Указанное в заголовке соединение получали из 2-амино-5-хлорпиразина, синтезированного в соответствии с литературой (Sato, Nobuhiro et al., J. Heterocycl. Chem., 1982, 19(3), 673-4), и метилхлороксоацетата подобно способу, описанному в ссылочном примере 242.
1Н-ЯМР (CDCl3) δ: 4,02 (3H, с), 8,35 (1H, д, J=1,5Гц), 9,37 (1H, д, J=1,5Гц), 9,41 (1H, шир.с).
МС (FAB) m/z: 216 (M+H)+.
[Ссылочный пример 399]
2-[(5-Хлорпиразин-2-ил)амино]-2-оксоуксусная кислота
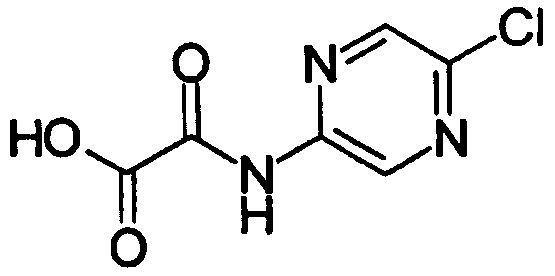
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 398, подобно способу, описанному в ссылочном примере 359.
1Н-ЯМР (ДМСО-d6) δ: 8,62 (1H, с), 9,02 (1H, шир.с), 11,30 (1H, с).
МС (EI) m/z: 201 М+.
[Ссылочный пример 400]
2-(4-Хлор-3-нитроанилино)-2-оксоуксусная кислота
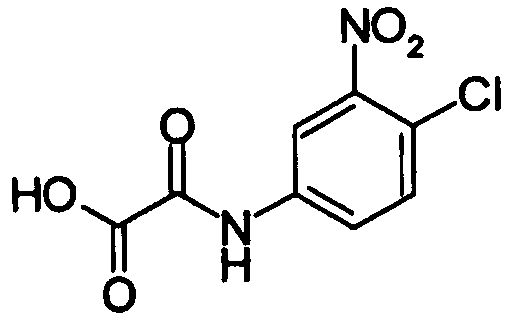
Указанное в заголовке соединение получали конденсацией 4-хлор-3-нитроанилина с метилхлороксоацетатом подобно способу, описанному в ссылочном примере 242, и затем гидролизом полученного продукта подобно способу, описанному в ссылочном примере 359.
1Н-ЯМР (ДМСО-d6) δ: 7,76 (1H, дд, J=8,8Гц), 8,04 (1H, дд, J=8,8, 2,4Гц), 8,55 (1H, д, J=2,4Гц), 11,24 (1H, с).
Не наблюдалось никакого протона, свойственного карбоновой кислоте.
МС (EI) m/z: 244 M+.
[Ссылочный пример 401]
2-(4-Хлор-2-нитроанилино)-2-оксоацетат натрия
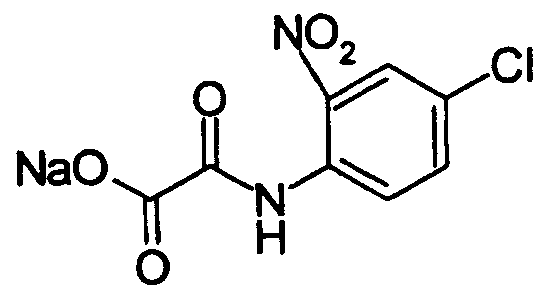
Указанное в заголовке соединение получали конденсацией 4-хлор-2-нитроанилина с метилхлороксоацетатом подобно способу, описанному в ссылочном примере 242, гидролизом полученного продукта подобно способу, описанному в ссылочном примере 266, растворением полученного остатка в метаноле, добавлением 1N водного раствора гидроксида натрия и отфильтровыванием образовавшегося осадка.
1Н-ЯМР (ДМСО-d6) δ: 7,84 (1H, дд, J=9,0, 2,5Гц), 8,20 (1H, д, J=2,5Гц), 8,67 (1H, д, J=9,0Гц), 11,89 (1H, с).
[Ссылочный пример 402]
6-Хлор-4-метил-3-пиридинамин
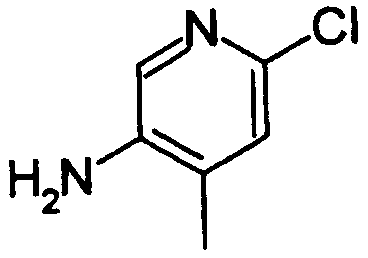
2-Хлор-4-метил-5-нитропиридин (173 мг) растворяли в этаноле (5 мл), добавляли каталитическое количество никеля Ренея в качестве катализатора и смесь перемешивали при комнатной температуре в течение 9 часов в атмосфере водорода. Катализатор удаляли фильтрованием и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:2) с получением указанного в заголовке соединения (113 мг).
1Н-ЯМР (CDCl3) δ: 2,13 (3H, с), 3,85 (2H, шир.с), 6,96 (1H, с), 7,74 (1H, с).
МС (EI) m/z: 142 M+.
[Ссылочный пример 403]
N1-(2-Аминофенил)-N2-(4-хлорфенил)этанамид
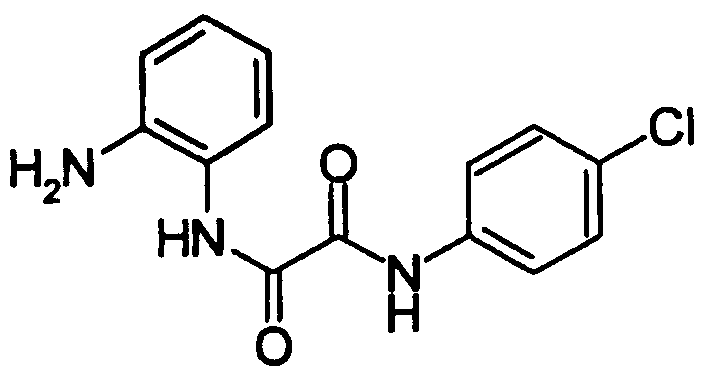
Указанное в заголовке соединение получали конденсацией 1,2-бензолдиамина с соединением, полученным в ссылочном примере 374, подобно способу, описанному в ссылочном примере 59.
1Н-ЯМР (ДМСО-d6) δ: 5,00 (2H, с), 6,59-6,63 (1H, м), 6,78 (1H, дд, J=8,1, 1,2Гц), 6,96-7,01 (1H, м), 7,25 (1H, дд, J=7,8, 1,2Гц), 7,44 (2H, д, J=8,8Гц), 7,91 (2H, д, J=8,8Гц), 10,04 (1H, с), 10,91 (1H, с).
МС (FAB): 290 (М+Н)+.
[Ссылочный пример 404]
N-((1R,2S,5S)-2-Азидо-5-{[этил(метил)амино]карбонил}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
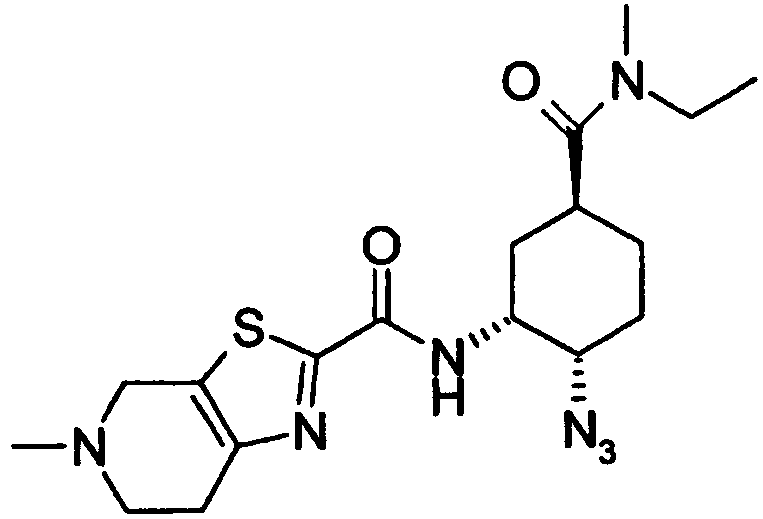
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 323, хлористоводородной кислотой, снятием защиты и затем конденсацией полученного продукта с соединением, полученным в ссылочном примере 10, подобно способу, описанному в ссылочном примере 252.
1Н-ЯМР (CDCl3) δ: 1,08 (1/2 от 3H, т, J=7,2Гц), 1,14 (1/2 от 3H, т, J=7,2Гц), 1,70-1,90 (4H, м), 2,10-2,25 (2H, м), 2,52 (3H, с), 2,78-3,00 (8H, м), 3,25-3,45 (2H, м), 3,69 (1H, д, J=13,4Гц), 3,73 (1H, д, J=13,4Гц), 3,87-3,95 (1H, м), 4,55-4,62 (1H, м), 7,26 (1H, д, J=7,6Гц).
[Ссылочный пример 405]
Фенил 2-(4-хлорфенил)-1-гидразинкарбоксилат
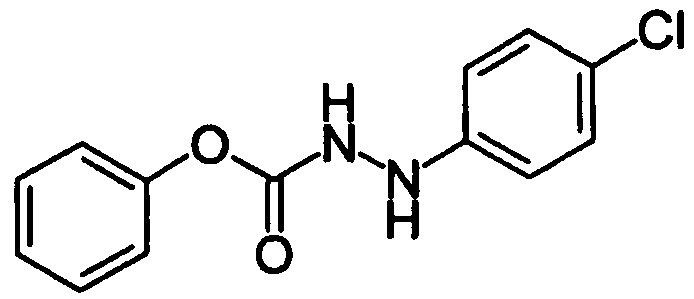
Гидрохлорид (4-хлорфенил)гидразина (3,00 г) растворяли в тетрагидрофуране (50 мл), диэтиловом эфире (50 мл) и насыщенном водном растворе гидрокарбоната натрия. Органический слой отделяли, сушили над безводным сульфатом натрия и затем концентрировали с получением (4-хлорфенил)гидразина в виде коричневого твердого вещества. Полученный продукт растворяли в бензоле (15 мл) и раствор кипятили с обратным холодильником, добавляя к нему по каплям раствор дифенилкарбоната (5,22 г) в бензоле (8,0 мл) за, по крайней мере, 30 минут. После кипения с обратным холодильником в течение 19 часов реакционной смеси давали остыть и концентрировали ее. Затем к остатку добавляли бензол (15 мл). Смесь подвергали ультразвуковой обработке с получением суспензии. После добавления к суспензии гексана (50 мл) и перемешивания смеси в течение 30 минут нерастворимое вещество отфильтровывали и сушили с получением указанного в заголовке соединения (1,05 г).
1Н-ЯМР (CDCl3) δ: 5,86 (1H, шир.с), 6,83-6,92 (3H, м), 7,17 (1H, шир.с), 7,20-7,32 (4H, м), 7,37 (2H, т, J=7,7Гц).
МС (ESI) m/z: 263 (M+H)+.
[Ссылочный пример 406]
5-трет-Бутоксикарбонил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-карбоксилат лития
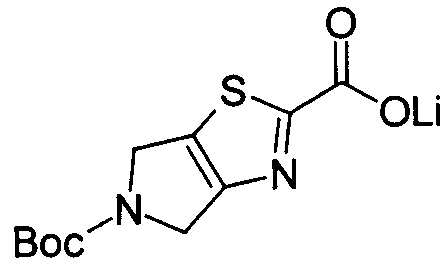
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 33, подобно способу, описанному в ссылочном примере 10.
1Н-ЯМР (ДМСО-d6) δ: 1,46 (9H, с), 4,30-4,70 (4H, м).
[Ссылочный пример 407]
Бензил 1-гидроксициклопропанкарбоксилат
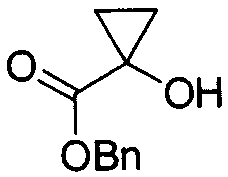
Триэтиламин (1,0 мл) и бензилбромид (650 мкл) добавляли к раствору 1-гидроксициклопропанкарбоновой кислоты (409 мг) в тетрагидрофуране (3,0 мл) и смесь перемешивали при комнатной температуре в течение 23 часов. К реакционной смеси добавляли метиленхлорид и 1N хлористоводородную кислоту для разделения смеси на два слоя. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Неочищенный продукт очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 4:1) с получением указанного в заголовке соединения (607 мг).
1Н-ЯМР (CDCl3) δ: 1,16 (2H, дд, J=7,9, 4,9Гц), 1,32 (2H, дд, J=7,9, 4,9Гц), 3,09 (0,5H, с), 3,11 (0,5H, с), 5,17 (2H, с), 7,30-7,39 (5H, м).
МС (FAB) m/z: 192 (М+Н)+.
[Ссылочный пример 408]
Бензил 1-метоксициклопропанкарбоксилат
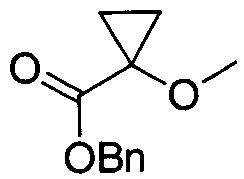
60% Гидрид натрия в масле (345 мг) и метилиодид (900 мкл) добавляли к раствору соединения (600 мг), полученного в ссылочном примере 407, в тетрагидрофуране (5,0 мл) и смесь кипятили с обратным холодильником в течение 28 часов. К реакционной смеси добавляли этилацетат и насыщенный водный раствор хлорида аммония для разделения смеси на два слоя. Органический слой промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Неочищенный продукт очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 10:1) с получением указанного в заголовке соединения (340 мг).
1Н-ЯМР (CDCl3) δ: 1,16 (2H, дд, J=7,9, 4,8Гц), 1,31 (2H, дд, J=7,9, 4,8Гц), 3,42 (3H, с), 5,18 (2H, с), 7,30-7,39 (5H, м).
МС (FAB) m/z: 207 (М+Н)+.
[Ссылочный пример 409]
1-Метоксициклопропанкарбоновая кислота
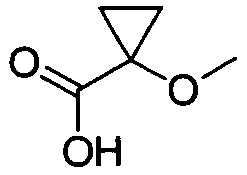
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 408, подобно способу, описанному в ссылочном примере 152.
1Н-ЯМР (CDCl3) δ: 1,23 (2H, дд, J=8,0, 4,9Гц), 1,38 (2H, дд, J=8,0, 4,9Гц), 3,45 (3H, с), 8,80-9,00 (1H, шир.).
[Ссылочный пример 410]
трет-Бутил (3R,4S)-4-({7-хлоризохинолин-3-ил}карбонил)амино}-1-(2-метоксиацетил)пиперидин-3-илкарбамат
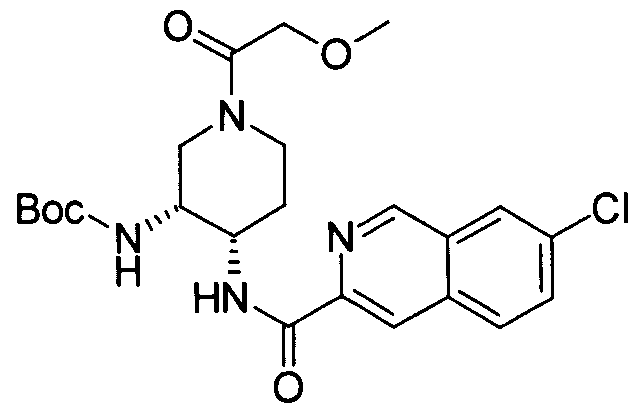
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 220, подобно способу, описанному в ссылочном примере 214.
1Н-ЯМР (CDCl3) δ: 1,46 (9H, шир.с), 1,62-1,80 (1H, м), 2,04-2,22 (1H, м), 2,95-3,32 (1H, м), 3,38-3,53 (1H, м), 3,46 (3H, с), 3,84-3,95 (1H, м), 4,02-4,27 (3H, м), 4,30-4,65 (2H, м), 4,87-4,98 (0,5H, шир.), 5,32-5,43 (0,5H, шир.), 7,71 (1H, дд, J=8,8, 2,0Гц), 7,94 (1H, д, J=8,8Гц), 8,02 (1H, с), 8,55-8,66 (0,7H, шир.), 8,58 (1H, с), 8,73-8,85 (0,3H, шир.), 9,14 (1H, шир.с).
МС (ESI) m/z: 477 (М+Н)+.
[Ссылочный пример 411]
трет-Бутил (3R,4S)-4-{[2-(4-хлор-3-фторанилино)-2-оксоацетил]амино}-1-(2-метоксиацетил)пиперидин-3-илкарбамат
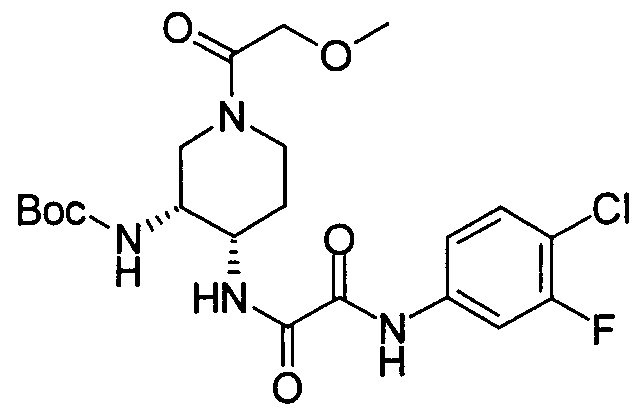
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 220, с соединением, полученным в ссылочном примере 337, подобно способу, описанному в ссылочном примере 214.
1Н-ЯМР (CDCl3) δ: 1,46 (9H, с), 1,60-1,75 (1H, м), 1,92-2,08 (1H, м), 2,68-2,80 (0,5H, м), 2,88-3,03 (0,5H, м), 3,06-3,24 (0,5H, м), 3,27-3,36 (0,5H, м), 3,45 (3H, с), 3,90-4,22 (5H, м), 4,56-4,71 (1H, м), 4,80-4,92 (0,3H, шир.), 5,44-5,54 (0,7H, шир.), 7,24 (1H, д, J=12,9Гц), 7,35 (1H, т, J=8,3Гц), 7,72 (1H, дд, J=8,3, 2,3Гц), 8,20-8,42 (1H, шир.), 9,18-9,28 (1H, шир.).
МС (ESI) m/z: 487 (М+Н)+.
[Ссылочный пример 412]
трет-Бутил (3R,4S)-4-({2-[(5-хлор-2-тиенил)амино]-2-оксоацетил}амино)-1-(2-метоксиацетил)пиперидин-3-илкарбамат
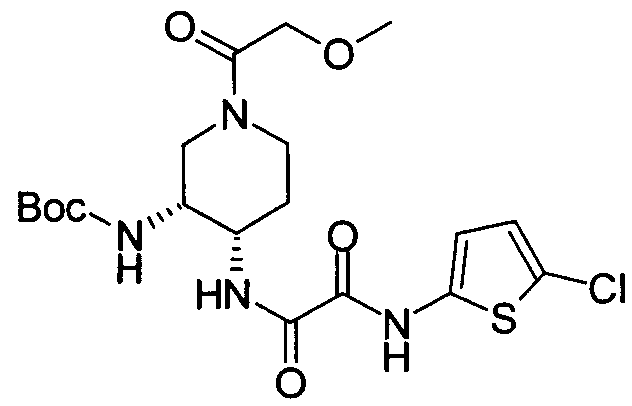
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 220, и литиевой соли карбоновой кислоты, полученной гидролизом соединения, полученного в ссылочном примере 356, подобно способу, описанному в ссылочном примере 214.
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,55-1,75 (1H, шир.), 1,90-2,10 (1H, шир.), 2,68-2,80 (0,7H, м), 2,90-3,03 (0,3H, шир.), 3,07-3,22 (0,3H, шир.), 3,25-3,35 (0,7H, шир.), 3,45 (3H, с), 3,83-4,22 (5H, м), 4,55-4,70 (1H, шир.), 4,80-4,90 (0,2H, шир.), 5,07-5,14 (0,2H, шир.), 5,44-5,55 (0,6H, шир.), 6,58-6,64 (1H, шир.), 6,73 (1H, д, J=3,9Гц), 8,05-8,27 (1H, шир.), 9,65-9,88 (1H, шир.).
МС (FAB) m/z: 475 (М+Н)+.
[Ссылочный пример 413]
Этил 5-метил-5Н-пирроло[3,4-d]тиазоло-2-карбоксилат
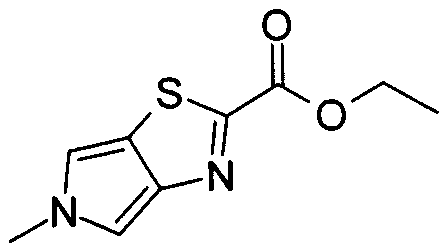
1) Этил 2-тиоксоацетат (26,75 г) добавляли к раствору 3-бром-2-бутанона (26,36 г) в этаноле (250 мл) и смесь кипятили с обратным холодильником в течение 14 часов. После охлаждения реакционной смеси ее концентрировали и добавляли этилацетат и насыщенный водный раствор хлорида натрия для разделения смеси на два слоя. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 6:1) с получением этил 4,5-диметилтиазол-2-карбоксилата (19,53 г).
1Н-ЯМР (CDCl3) δ: 1,42 (3H, т, J=7,1Гц), 2,42 (3H, с), 2,44 (3H, с), 4,45 (2H, кв, J=7,1Гц).
2) N-Бромсукцинимид (62,42 г) и 2,2'-азобисизобутиронитрил (227 мг) добавляли к раствору описанного выше продукта (19,53 г) в 1,2-дихлорэтане (500 мл) и смесь кипятили с обратным холодильником в течение 42 часов. После охлаждения реакционной смеси добавляли воду и метиленхлорид для разделения смеси на два слоя. Органический слой промывали насыщенным водным раствором хлорида натрия и затем концентрировали при пониженном давлении с получением неочищенного продукта (40,54 г) в виде темно-коричневого масла. К неочищенному продукту (8,41 г) добавляли триэтиламин (8,0 мл) и 2М тетрагидрофурановый раствор (11,0 мл) метиламина и смесь перемешивали при комнатной температуре в течение 3 суток. Реакционную смесь концентрировали при пониженном давлении, к остатку добавляли метиленхлорид и насыщенный водный раствор хлорида натрия для разделения смеси на два слоя. Органический слой промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 3:1) с получением указанного в заголовке соединения (270 мг).
1Н-ЯМР (CDCl3) δ: 1,45 (3H, т, J=7,1Гц), 3,91 (3H, с), 4,48 (2H, кв, J=7,1Гц), 6,73 (1H, д, J=1,7Гц), 7,30 (1H, д, J=1,7Гц).
МС (ESI) m/z: 211 (М+Н)+.
[Ссылочный пример 414]
Этил 6-хлор-4-оксо-4Н-хромен-2-карбоксилат
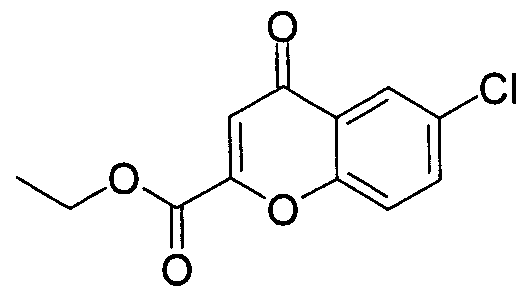
Приблизительно 60% гидрид натрия в масле (1,68 г) добавляли к этанолу (10 мл) при продувке аргоном и смесь перемешивали при комнатной температуре в течение 10 минут. После добавления диэтилоксалата (3,36 мл) добавляли по каплям этанольный раствор (20 мл) 5'-хлор-2'-гидроксиацетофенона (2,82 г). Добавляли дополнительно этанол (40 мл) и смесь кипятили с обратным холодильником в течение 1,5 часов и перемешивали при 50°C в течение 14 часов. К реакционной смеси добавляли концентрированную серную кислоту (1,5 мл) и этанол (10 мл) и полученную смесь кипятили с обратным холодильником в течение 4 часов. После охлаждения уменьшали содержание растворителя наполовину концентрированием при пониженном давлении. К концентрированной реакционной смеси добавляли толуол и 1N водный раствор (15 мл) гидроксида натрия. Проводили экстракцию этилацетатом и полученный органический слой промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 7:1), затем полученные твердые частицы промывали гексаном с получением указанного в заголовке соединения (1,20 г).
1Н-ЯМР (CDCl3) δ: 1,44 (3H, т, J=7,1Гц), 4,47 (2H, кв, J=7,1Гц), 7,12 (1H, с), 7,58 (1H, д, J=9,0Гц), 7,69 (1H, дд, J=9,0, 2,7Гц), 8,16 (1H, д, J=2,7Гц).
МС (ESI) m/z: 293 (M+MeCN+H)+.
[Ссылочный пример 415]
6-Хлор-4-оксо-4Н-хромен-2-карбоновая кислота
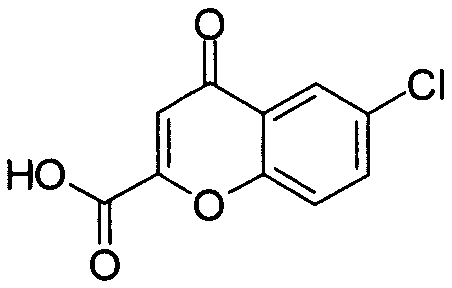
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 414, подобно способу, описанному в ссылочном примере 359.
1Н-ЯМР (CDCl3) δ: 7,12 (1H, с), 7,60 (1H, д, J=8,8Гц), 7,69 (1H, дд, J=8,8, 2,7Гц), 8,15 (1H, д, J=2,7Гц).
МС (FAB) m/z: 225 (М+Н)+.
[Ссылочный пример 416]
Этил (1S,3R,4S)-4-амино-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
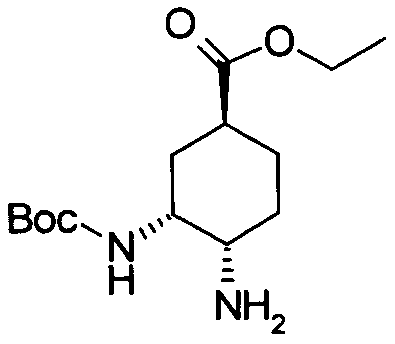
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 249, подобно способу, описанному в ссылочном примере 90.
1Н-ЯМР (CDCl3) δ: 1,20-1,80 (4H, м), 1,25 (3H, т, J=7,3Гц), 1,46 (9H, с), 1,85-2,00 (1H, м), 2,10-2,20 (1H, м), 2,30-2,45 (1H, м), 2,90-3,00 (1H, м), 3,84 (1H, шир.с), 4,12 (2H, кв, J=7,3Гц), 4,75 (1H, шир.с).
[Ссылочный пример 417]
трет-Бутил (1R,2S,5S)-2-{[(6-хлор-4-оксо-4Н-хромен-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамат
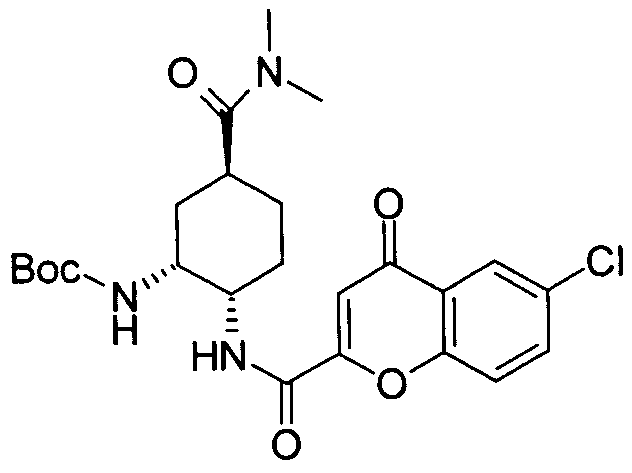
N,N-Диметилформамид (0,02 мл) добавляли к раствору соединения (213 мг), полученного в ссылочном примере 415, в тионилхлориде (2,0 мл) и смесь кипятили с обратным холодильником в течение 15 минут. Реакционную смесь концентрировали при пониженном давлении и остаток растворяли в тетрагидрофуране (4,0 мл). К раствору добавляли триэтиламин (500 мкл) и соединение (294 мг), полученное в ссылочном примере 144, и смесь перемешивали при комнатной температуре в течение 15 минут. Добавляли этилацетат и 10% водный раствор лимонной кислоты для разделения реакционной смеси на два слоя. Органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 30:1) с получением указанного в заголовке соединения (230 мг).
1Н-ЯМР (CDCl3) δ: 1,33-1,77 (3H, м), 1,50 (9H, с), 1,81-2,34 (3H, м), 2,63-2,80 (1H, м), 2,95 (3H, с), 3,10 (3H, с), 3,90-4,04 (1H, шир.), 4,18-4,31 (1H, шир.), 4,93-5,12 (1H, шир.), 7,13 (1H, с), 7,55 (1H, д, J=8,8Гц), 7,66 (1H, дд, J=8,8, 2,4Гц), 8,14 (1H, д, J=2,4Гц), 8,77-8,92 (1H, шир.).
МС (ESI) m/z: 492 (M+H)+.
[Ссылочный пример 418]
трет-Бутил (3R,4S)-4-{[(7-хлорциннолин-3-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-илкарбамат
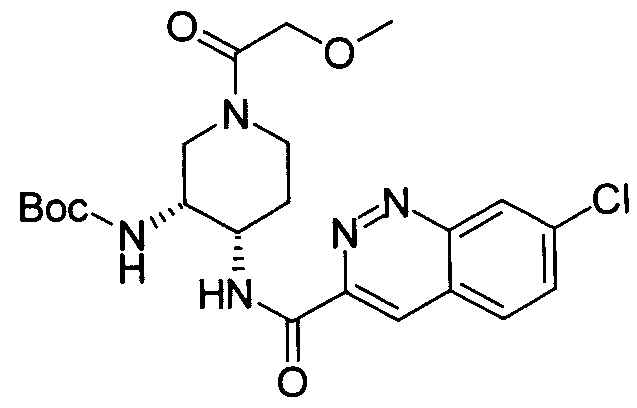
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 220, и литиевой соли карбоновой кислоты, полученной гидролизом сложного эфира, описанного в ссылочном примере 297, подобно способу, описанному в ссылочном примере 214.
1Н-ЯМР (CDCl3) δ: 1,38 (9H, с), 1,65-1,90 (1H, м), 1,90-2,15 (1H, м), 2,80-3,00 (0,6H, м), 3,00-3,15 (0,4H, м), 3,20-3,50 (1H, м), 3,46 (3H, с), 3,80-4,70 (6H, м), 4,87 (0,4H, шир.с), 5,30 (0,6H, шир.с), 7,78 (1H, д, J=8,8Гц), 7,97 (1H, д, J=8,8Гц), 8,61 (1H, с), 8,62-8,90 (1H, шир.), 8,73 (1H, с).
МС (ESI) m/z: 478 (M+H)+.
[Ссылочный пример 419]
трет-Бутил (1R,2S,5S)-2-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-5-[(диметиламино)карбонил]циклогексилкарбамат
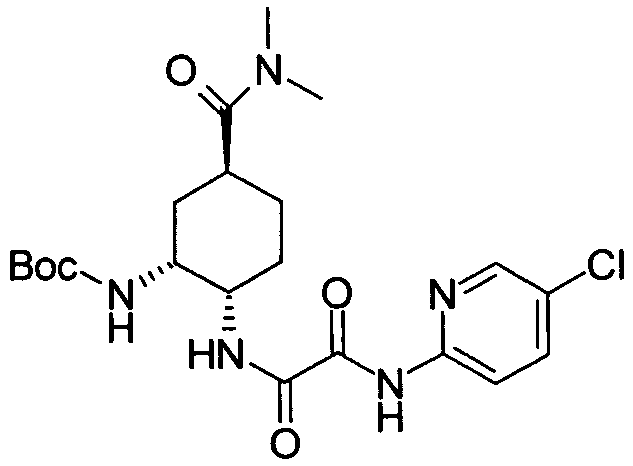
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 144, с соединением, полученным в ссылочном примере 266, подобно способу, описанному в ссылочном примере 68.
1Н-ЯМР (CDCl3) δ: 1,35-1,65 (1H, м), 1,45 (9H, с), 1,65-1,89 (2H, м), 1,90-2,10 (3H, м), 2,56-2,74 (1H, шир.), 2,95 (3H, с), 3,06 (3H, с), 3,94-4,01 (1H, м), 4,18-4,27 (1H, м), 4,70-4,90 (0,7H, шир.), 5,80-6,20 (0,3H, шир.), 7,68 (1H, дд, J=8,9, 2,6Гц), 7,83 (1H, шир.с), 8,14 (1H, шир.д, J=7,8Гц), 8,30 (1H, с), 9,72 (1H, с).
МС (ESI) m/z: 468 (М+Н)+.
[Ссылочный пример 420]
Гидрохлорид N1-{(1S,2R,4S)-2-амино-4-[(диметиламино)карбонил]циклогексил}-N2-(5-хлорпиридин-2-ил)этандиамида
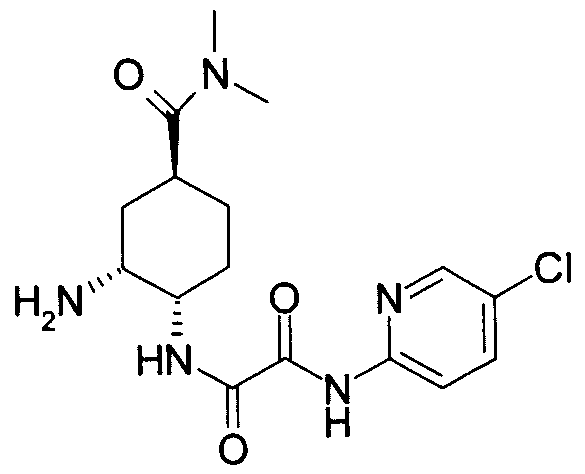
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 419, подобно способу, описанному в ссылочном примере 69.
1Н-ЯМР (ДМСО-d6) δ: 1,38-1,51 (1H, м), 1,65-1,85 (3H, м), 1,96-2,10 (2H, м), 2,81 (3H, с), 3,07 (3H, с), 3,23-3,33 (1H, м), 3,74 (1H, шир.с), 3,84-3,92 (1H, м), 8,02 (1H, дд, J=9,0, 2,5Гц), 8,07 (1H, д, J=9,0Гц), 8,34 (3H, шир.с), 8,46 (1H, д, J=2,5Гц), 8,96 (1H, д, J=6,6Гц), 10,34 (1H, с).
МС (ESI) m/z: 368 (М+Н)+.
[Ссылочный пример 421]
трет-Бутил 2-[({(1R,2S,5S)-2-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-5-[(диметиламино)карбонил]циклогексил}амино)карбонил]-6,7-дигидротиено[3,2-c]пиридин-5(4Н)-карбоксилат
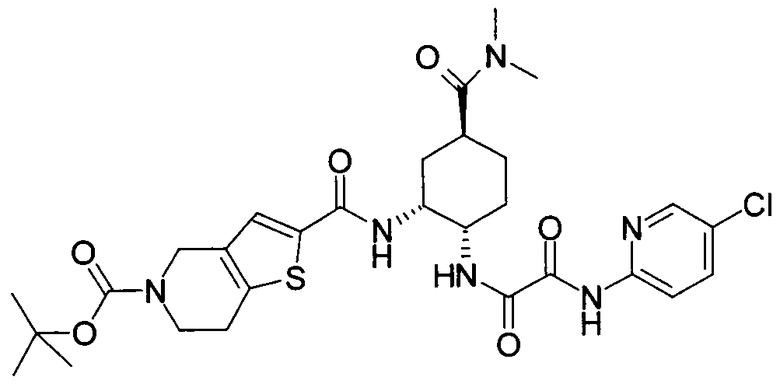
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 420, с 5-(трет-бутоксикарбонил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин-2-карбоновой кислотой (WO94/21599).
1Н-ЯМР (CDCl3) δ: 1,50 (9H, с), 1,73-1,95 (3H, м), 1,95-2,06 (1H, м), 2,08-2,20 (2H, м), 2,82 (3H, шир.с), 2,94 (3H, с), 3,03 (3H, с), 3,60-3,80 (2H, м), 3,96-4,08 (1H, м), 4,44 (2H, шир.с), 4,66 (1H, шир.с), 6,74 (1H, шир.с), 7,20-7,32 (1H, м), 7,66 (1H, дд, J=9,0, 2,4Гц), 8,13 (1H, д, J=9,0Гц), 8,13-8,25 (1H, м), 8,28 (1H, д, J=2,4Гц), 9,75 (1H, с).
МС (ESI) m/z: 633 (M+H)+.
[Ссылочный пример 422]
2-Хлор-N-(4-фторфенил)ацетамид
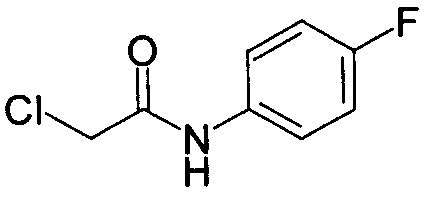
Указанное в заголовке соединение получали из п-фторанилина подобно способу, описанному в ссылочном примере 350.
1Н-ЯМР (CDCl3) δ: 4,19 (2H, с), 7,05 (2H, т, J=8,6Гц), 7,51 (2H, дд, J=9,1, 4,7Гц), 8,19 (1H, шир.с).
[Ссылочный пример 423]
S-[2-(4-Фторанилино)-2-оксоэтил]тиосульфат натрия
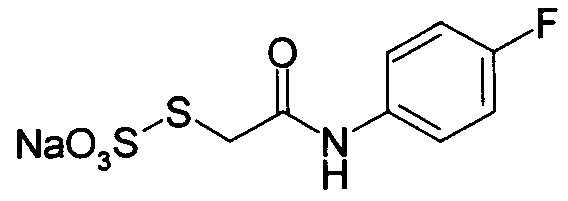
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 422, подобно способу, описанному в ссылочном примере 351.
1Н-ЯМР (ДМСО-d6) δ: 3,72 (2H, с), 7,14 (2H, т, J=9,0Гц), 7,56 (2H, дд, J=9,0, 5,1Гц), 10,21 (1H, с)
[Ссылочный пример 424]
трет-Бутил (1R,2S,5S)-5-[(диметиламино)карбонил]-2-{[2-(4-фторанилино)-2-оксоэтантиоил]амино}циклогексилкарбамат
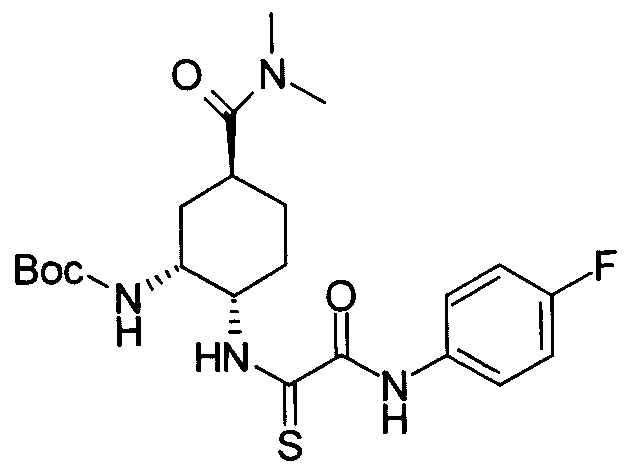
Соединение (1,1 г), полученное в ссылочном примере 144, и соединение (1,2 г), полученное в ссылочном примере 423, растворяли в N-метилморфолине (20 мл), температуру бани повышали от комнатной температуры до 140°C за 15 минут и нагревали и перемешивали смесь в течение 15 минут при указанной температуре. Дав реакционной смеси остыть, добавляли ледяную воду и отфильтровывали нерастворимое вещество. Полученный продукт очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 200:1 → 197:3) с получением указанного в заголовке соединения (1,43 г).
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,70-2,10 (5H, м), 2,10-2,30 (1H, м), 2,60-2,80 (1H, м), 2,96 (3H, с), 3,07 (3H, с), 4,30-4,50 (2H, м), 4,65-4,85 (1H, м), 7,06 (2H, т, J=8,5Гц), 7,50-7,70 (2H, м), 9,75-9,95 (1H, м), 10,13 (1H, с).
МС (ESI) m/z: 467 (М+Н)+.
[Ссылочный пример 425]
Гидрохлорид 2-хлор-N-(5-фторпиридин-2-ил)ацетамида
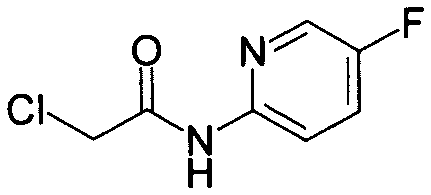
Указанное в заголовке соединение получали из 2-амино-5-фторпиридина подобно способу, описанному в ссылочном примере 352.
1Н-ЯМР (ДМСО-d6) δ: 4,35 (2H, с), 7,74-7,82 (1H, м), 8,10 (1H, дд, J=9,0, 4,2Гц), 8,36 (1H, д, J=2,9Гц).
МС (ESI) m/z: 188 (М+Н)+.
[Ссылочный пример 426]
S-{2-[(5-Фторпиридин-2-ил)амино]-2-оксоэтил}тиосульфат натрия
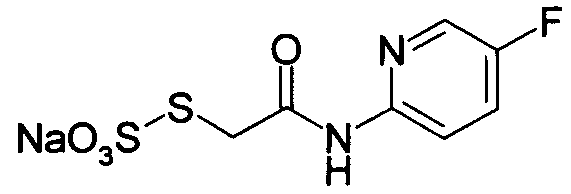
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 425, подобно способу, описанному в ссылочном примере 353.
1Н-ЯМР (ДМСО-d6) δ: 3,75 (2H, с), 7,67-7,77 (1H, м), 8,07 (1H, дд, J=9,2, 4,2Гц), 8,28 (1H, д, J=2,9Гц), 10,48 (1H, с).
[Ссылочный пример 427]
трет-Бутил (1R,2S,5S)-5-[(диметиламино)карбонил]-2-({2-[(5-фторпиридин-2-ил)амино]-2-оксоэтантиоил}амино)циклогексилкарбамат
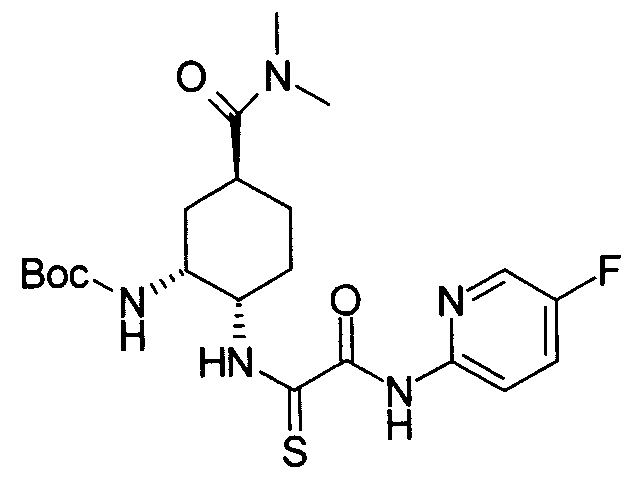
Раствор соединения (1,20 г), полученного в ссылочном примере 144, в пиридине (70 мл) нагревали до 120°C и добавляли к нему соединение (2,42 г), полученное в ссылочном примере 426. После перемешивания смеси в течение 30 минут реакционной смеси давали остыть до комнатной температуры и отгоняли при пониженном давлении растворитель. К полученному остатку добавляли метиленхлорид (100 мл), насыщенный водный раствор (100 мл) гидрокарбоната натрия и воду (50 мл) для разделения жидкостей. Затем водный слой экстрагировали метиленхлоридом. Органические слои объединяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (гексан:тетрагидрофуран = 1:1). После выдержки взвеси полученных твердых частиц в изопропиловом эфире (40 мл) в течение 1 часа их отфильтровывали и сушили с получением указанного в заголовке соединения (920 мг).
1Н-ЯМР (CDCl3) δ: 1,47 (9H, с), 1,70-2,10 (5H, м), 2,27 (1H, шир.с), 2,70 (1H, шир.с), 2,96 (3H, с), 3,08 (3H, с), 4,34-4,44 (2H, м), 4,77 (1H, шир.с), 7,44-7,51 (1H, м), 8,18-8,27 (2H, м), 9,90 (1H, шир.с), 10,57 (1H, с).
МС (ESI) m/z: 468 (М+Н)+.
[Ссылочный пример 428]
трет-Бутил (1R,2S,5S)-2-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карбонил]циклогексилкарбамат
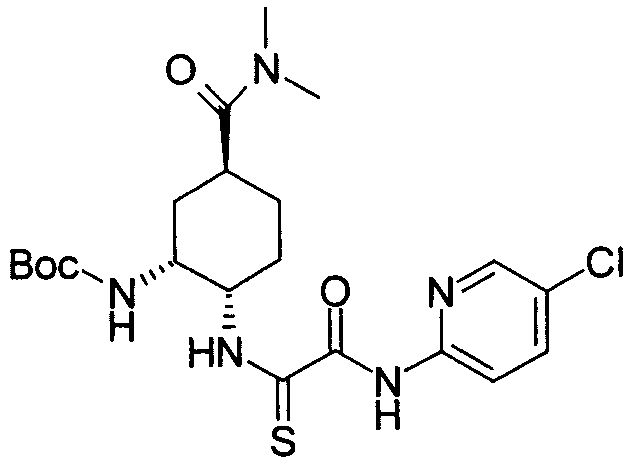
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и соединения, полученного в ссылочном примере 353, подобно способу, описанному в ссылочном примере 427.
1Н-ЯМР (CDCl3) δ: 1,43 (9H, с), 1,65-2,35 (6H, м), 2,70 (1H, шир.с), 2,95 (3H, с), 3,09 (3H, с), 4,30-4,60 (2H, м), 4,87 (1/2H, шир.с), 6,92 (1/2H, шир.с), 7,69 (1H, дд, J=8,9, 2,6Гц), 7,95-8,20 (1H, шир.), 8,29 (1H, с), 9,67 (1/2H, шир.с), 9,93 (1/2H, шир.с), 10,54 (1H, шир.с).
[Ссылочный пример 429]
2-Хлор-4,5,6,7-тетрагидробензотиазол-6-илформамид
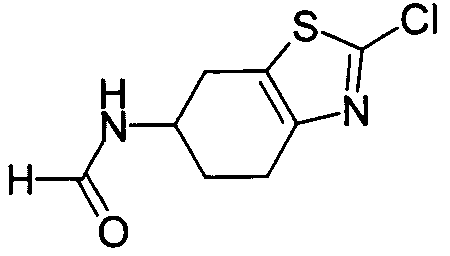
Ацетат аммония (18,58 г) и цианоборгидрид натрия (10,68 г) добавляли к раствору 2-хлор-5-оксо-4,5,6,7-тетрагидробензо[d]тиазола (Helv. Cim. Acta., 1994, Vol. 77, p. 1256) (4,53 г) в метаноле (200 мл) и смесь кипятили с обратным холодильником. Через 19 часов добавляли хлористоводородную кислоту для разложения избыточных реагентов перед концентрированием реакционной смеси при пониженном давлении. После подщелачивания остатка 1N водным раствором гидроксида натрия добавляли метиленхлорид для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом магния и отгоняли при пониженном давлении растворитель. Полученный остаток подвергали колоночной хроматографии на силикагеле (метиленхлорид:метанол = 20:1) и отгоняли растворитель с получением бледно-желтого масла (2,42 г). Полученное масло растворяли в метиленхлориде (100 мл), добавляли муравьиную кислоту (530 мкл), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (3,68 г), 1-гидроксибензотриазол (2,60 г) и N-метилморфолин (3,88 г) и смесь перемешивали при комнатной температуре. Через 20 часов добавляли к реакционной смеси метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом магния, затем отгоняли при пониженном давлении растворитель и полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1) с получением указанного в заголовке соединения (2,21 г).
1Н-ЯМР (CDCl3) δ: 1,93-2,11 (2H, м), 2,63-2,69 (1H, м), 2,83-2,89 (2H, м), 3,13 (1H, дд, J=16,2, 4,4Гц), 4,46-4,48 (1H, м), 5,76 (1H, шир.с), 8,17 (1H, с).
[Ссылочный пример 430]
трет-Бутил N-(2-хлор-4,5,6,7-тетрагидробензотиазол-6-ил)-N-метилкарбамат
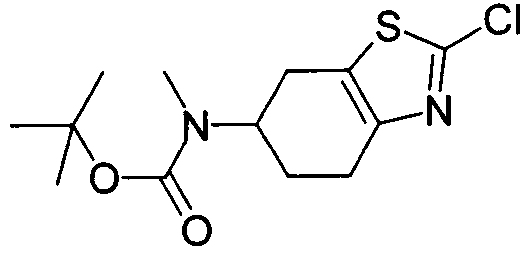
1М Тетрагидрофурановый раствор (14,6 мл) боран-тетрагидрофуранового комплекса добавляли к раствору соединения (2,11 г), полученного в ссылочном примере 429, в тетрагидрофуране (50 мл) и смесь кипятили с обратным холодильником. Через 15 часов добавляли дополнительно 1М тетрагидрофурановый раствор (6,0 мл) боран-тетрагидрофуранового комплекса и смесь кипятили с обратным холодильником. Через 4 часа добавляли этанол (10 мл) и 1N хлористоводородную кислоту (15 мл) и смесь кипятили с обратным холодильником. Через 3 часа реакционную смесь концентрировали при пониженном давлении. К остатку добавляли 1N водный раствор гидроксида натрия и метиленхлорид для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом магния и отгоняли при пониженном давлении растворитель. Полученный остаток растворяли в метиленхлориде (50 мл), добавляли триэтиламин (1,28 г) и ди-трет-бутилдикарбонат (2,21 г) и смесь перемешивали при комнатной температуре. Через 30 минут добавляли метиленхлорид и 1N хлористоводородную кислоту для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом магния и отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (гексан:этилацетат = 2:1) с получением указанного в заголовке соединения (2,26 г).
1Н-ЯМР (CDCl3) δ: 1,47 (9H, с), 1,96-1,98 (2H, м), 2,80-2,96 (7H, м), 4,40-4,50 (1H, м).
МС (FAB) m/z: 303 (М+Н)+.
[Ссылочный пример 431]
трет-Бутил N-(2-[({(1R,2S,5S)-2-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-5-[(диметиламино)карбонил]циклогексил}амино)карбонил]-4,5,6,7-тетрагидробензотиазол-6-ил)-N-метилкарбамат
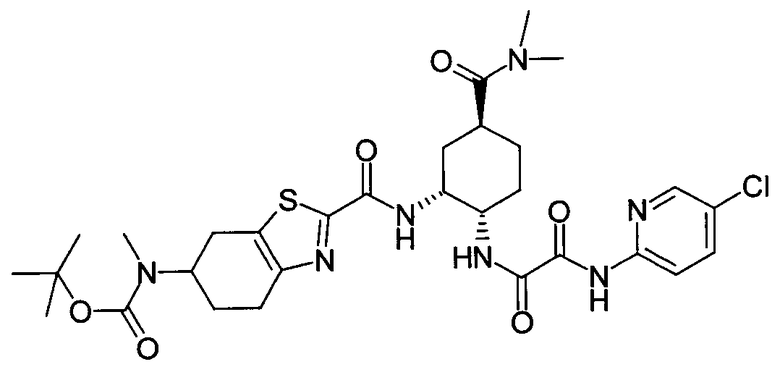
После охлаждения до -78°C раствора соединения (1,0 г), полученного в ссылочном примере 430, в смеси диэтиловый эфир (10 мл)-тетрагидрофуран (5 мл) добавляли 1,6N пентановый раствор (3,1 мл) трет-бутиллития и смесь перемешивали в течение 20 минут. Вводили диоксид углерода в течение 20 минут. Реакционную смесь нагревали до комнатной температуры и концентрировали при пониженном давлении с получением 6-[(трет-бутоксикарбонил)(метил)амино]-4,5,6,7-тетрагидробензотиазол-2-карбоксилата лития.
Литиевую соль (350,2 мг) карбоновой кислоты, полученную по описанной выше реакции, гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (287,6 мг), 1-гидроксибензотриазол (202,7 мг) и N-метилморфолин (0,319 мл) добавляли к раствору соединения (490,5 мг), полученного в ссылочном примере 420, в N,N-диметилформамиде (20 мл) и смесь перемешивали при комнатной температуре в течение 4 суток. Растворитель отгоняли при пониженном давлении и к остатку добавляли воду и метиленхлорид для разделения жидкостей. Затем полученный органический слой последовательно промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Органический слой сушили над безводным сульфатом натрия, концентрировали при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 40:1 → 20:1) с получением указанного в заголовке соединения (323,9 мг).
1Н-ЯМР (CDCl3) δ: 1,48, 1,49 (всего 9H, каждый с), 1,60-1,92 (4H, м), 1,95-2,20 (6H, м), 2,78-3,10 (3H, м), 2,83 (3H, с), 2,95 (3H, с), 3,06, 3,07 (всего 3H, каждый с), 4,05-4,15 (1H, м), 4,20-4,60 (1H, м), 4,63-4,73 (1H, м), 7,39 (1H, д, J=8,6Гц), 7,68 (1H, дт, J=8,8, 2,6Гц), 7,95-8,10 (1H, м), 8,13-8,22 (1H, м), 8,30-8,35 (1H, м), 9,72 (1H, шир.с),
МС (ESI) m/z: 662 (М+Н)+.
[Ссылочный пример 432]
Гидрохлорид N-{(1S,2R,4S)-2-амино-4-[(диметиламино)карбонил]циклогексил}-5-хлориндол-2-карбоксамида
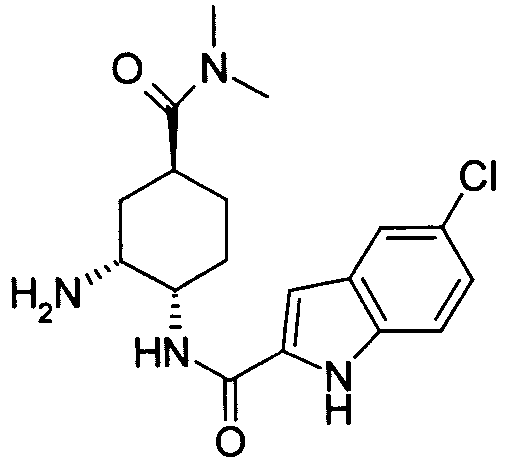
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 310, подобно способу, описанному в ссылочном примере 69.
1Н-ЯМР (ДМСО-d6) δ: 1,43-1,56 (0,5H, м), 1,72-1,97 (4,5H, м), 2,82 (3H, с), 3,06 (3H, с), 3,11-3,26 (1H, м), 3,75-3,84 (1H, м), 4,07-4,14 (1H, м), 4,22-4,41 (1H, м), 7,19 (1H, дд, J=2,0, 8,8Гц), 7,29 (1H, д, J=2,0Гц), 7,45 (1H, д, J=8,8Гц), 7,72 (1H, с), 8,07 (3H, шир.), 8,47 (1H, м), 11,85 (1H, шир.).
[Ссылочный пример 433]
2-[(5-Хлорпиридин-2-ил)амино]-2-оксоацетат лития
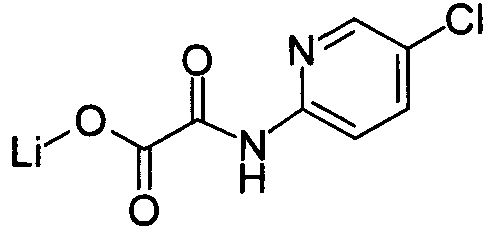
Метилхлороксоацетат (78,7 мл) добавляли по каплям к суспензии 2-амино-5-хлорпиридина (100 г) и гидрокарбоната натрия (78,4 г) в тетрагидрофуране (2000 мл) при 0°C и смесь перемешивали при комнатной температуре в течение 2 часов. После добавления реакционной смеси к смеси диэтилового эфира (2000 мл), хлорида аммония (62,4 г) и воды (1000 мл) осуществляли разделение жидкостей. Полученный водный слой экстрагировали метиленхлоридом. Органические слои объединяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель с получением метил 2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетата (162 г). Воду (450 мл) и гидроксид лития (18,2 г) добавляли к раствору полученного эфира (160 г) в тетрагидрофуране (1800 мл). После перемешивания смеси при комнатной температуре в течение 2 часов отгоняли при пониженном давлении растворитель, к полученному остатку добавляли гексан (3000 мл) и смесь перемешивали в течение 3 часов. Твердые частицы отфильтровывали и сушили. К твердым частицам (190 г) добавляли ацетонитрил (1000 мл) и смесь перемешивали в течение 1 часа. Образовавшиеся твердые частицы отфильтровывали, промывали диэтиловым эфиром (500 мл) и затем сушили с получением указанного в заголовке соединения (158 г).
1Н-ЯМР (ДМСО-d6) δ: 7,92 (1H, дд, J=9,1, 2,7Гц), 8,13 (1H, дд, J=9,1, 0,5Гц), 8,36 (1H, дд, J=2,7, 0,5Гц), 10,19 (1H, с).
[Ссылочный пример 434]
трет-Бутил (1R,2S,5S)-2-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-5-[(диметиламино)карбонил]циклогексилкарбамат
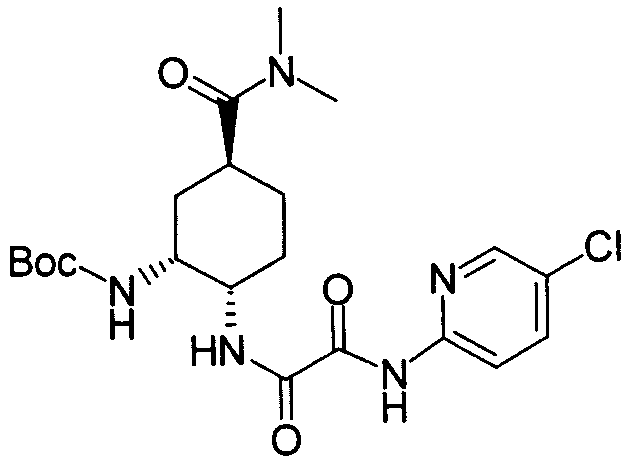
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и соединения, полученного в ссылочном примере 433, подобно способу, описанному в ссылочном примере 91.
1Н-ЯМР (CDCl3) δ: 1,25-1,55 (1H, м), 1,45 (9H, с), 1,60-2,15 (5H, м), 2,56-2,74 (1H, шир.), 2,95 (3H, с), 3,06 (3H, с), 3,90-4,01 (1H, м), 4,18-4,27 (1H, м), 4,70-4,85 (0,7H, шир.), 5,70-6,00 (0,3H, шир.), 7,70 (1H, дд, J=8,8, 2,4Гц), 7,75-8,00 (1H, шир.), 8,16 (1H, шир.д, J=8,8Гц), 8,30 (1H, д, J=2,4Гц), 9,73 (1H, с).
МС (ESI) m/z: 468 (М+Н)+.
[Ссылочный пример 435]
Гидрохлорид N1-{(1S,2R,4S)-2-амино-4-[(диметиламино)карбонил]циклогексил}-N2-(5-хлорпиридин-2-ил)этандиамида
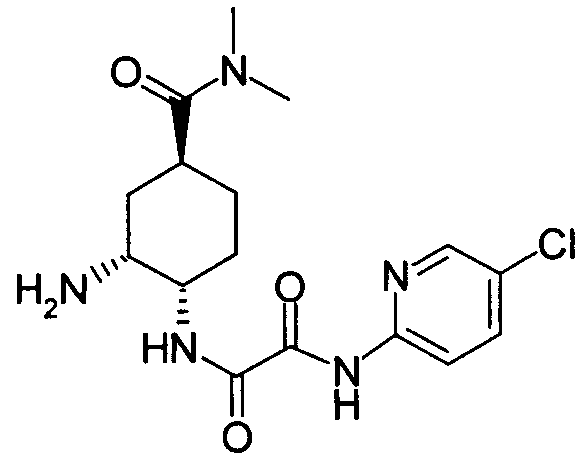
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 434, подобно способу, описанному в ссылочном примере 69.
1Н-ЯМР (ДМСО-d6) δ: 1,38-1,51 (1H, м), 1,65-1,85 (3H, м), 1,92-2,09 (2H, м), 2,80 (3H, с), 3,06 (3H, с), 3,20-3,32 (1H, м), 3,55-4,40 (2H, шир.), 8,02 (1H, дд, J=9,1, 2,5Гц), 8,07 (1H, д, J=9,1Гц), 8,15-8,40 (3H, шир.), 8,45 (1H, д, J=2,5Гц), 8,96 (1H, д, J=6,6Гц), 10,33 (1H, с).
[Ссылочный пример 436]
Бензил (1S,2R,4S)-2-[(трет-бутоксикарбонил)амино]-4-[(метиламино)карбонил]циклогексилкарбамат
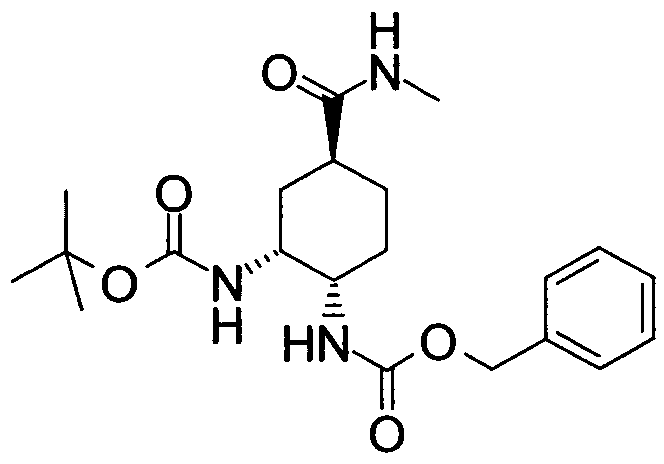
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 142, и гидрохлорида метиламина подобно способу ссылочного примера 143.
1Н-ЯМР (ДМСО-d6) δ: 1,39 (9H, с), 1,40-1,61 (4H, м), 1,63-1,73 (1H, м), 1,75-1,85 (1H, м), 2,23-2,48 (1H, м), 2,53 (3H, д, J=4,6Гц), 3,48 (1H, шир.с), 3,80-3,91 (1H, м), 5,01 (1H, 1/2АВкв, J=12,1Гц), 5,03 (1H, 1/2АВкв, J=12,1Гц), 6,28-6,40 (1H, м), 6,82-6,98 (1H, м), 7,25-7,40 (5H, м), 7,50-7,60 (1H, м).
МС (FAB) m/z: 406 (M+H)+.
[Ссылочный пример 437]
трет-Бутил (1R,2S,5S)-2-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-5-[(метиламино)карбонил]циклогексилкарбамат
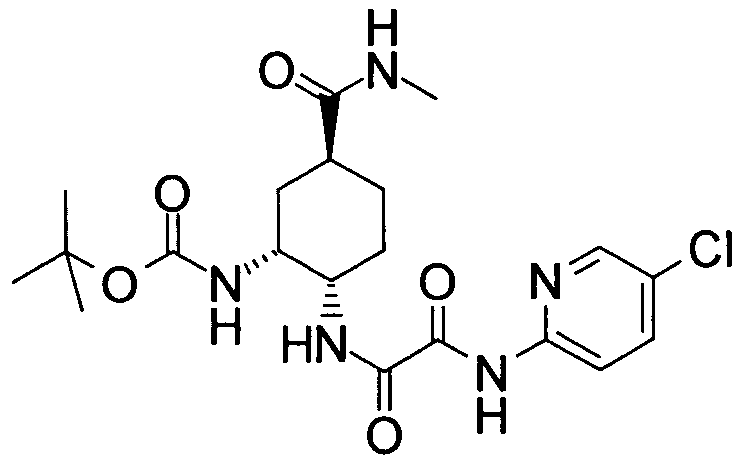
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 436, подобно способу, описанному в ссылочном примере 144, и конденсацией полученного амина с соединением, полученным в ссылочном примере 433, подобно способу, описанному в ссылочном примере 91.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,75 (3H, м), 1,39 (9H, с), 1,75-1,86 (2H, м), 1,87-1,95 (1H, м), 2,30-2,40 (1H, м), 2,55 (3H, д, J=4,6Гц), 3,79-3,90 (2H, м), 6,73-6,90 (1H, м), 7,58-7,70 (1H, м), 8,00-8,13 (2H, м), 8,46 (1H, дд, J=2,2, 1,0Гц), 8,67 (1H, д, J=7,6Гц), 10,26 (1H, с).
МС (ESI: отрицательный) m/z: 452[(M-H)-, Cl35], 454[(M-H)-, Cl37].
[Ссылочный пример 438]
Гидрохлорид 2-хлор-N-(5-метилпиридин-2-ил)ацетамида
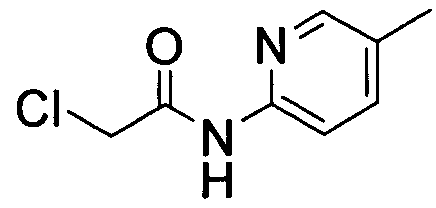
Указанное в заголовке соединение получали из 2-амино-5-пиколина подобно способу, описанному в ссылочном примере 425.
1Н-ЯМР (ДМСО-d6) δ: 2,30 (3H, с), 4,40 (2H, с), 7,83 (1H, д, J=8,8Гц), 7,91 (1H, д, J=8,5Гц), 8,21 (1H, с), 11,40 (1H, с).
[Ссылочный пример 439]
S-{2-[(5-метилпиридин-2-ил)амино]-2-оксоэтил}тиосульфат натрия
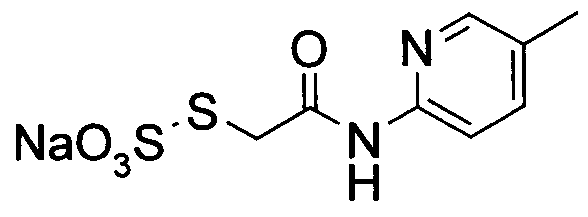
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 438, подобно способу, описанному в ссылочном примере 353.
1Н-ЯМР (ДМСО-d6) δ: 2,24 (3H, с), 3,74 (2H, с), 7,59 (1H, д, J=8,5Гц), 7,94 (1H, д, J=8,3Гц), 8,12 (1H, с), 10,26 (1H, с).
[Ссылочный пример 440]
трет-Бутил (1R,2S,5S)-5-[(диметиламино)карбонил]-2-({2-[(5-метилпиридин-2-ил)амино]-2-оксоэтантиоил}амино)циклогексилкарбамат
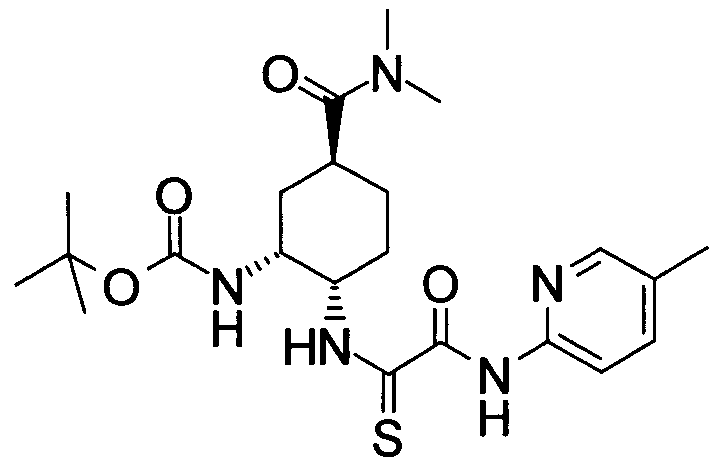
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 144, и соединения, полученного в ссылочном примере 439, подобно способу, описанному в ссылочном примере 427.
1Н-ЯМР (CDCl3) δ: 1,46 (9H, с), 1,60-2,10 (5H, м), 2,15-2,35 (1H, м), 2,31 (3H, с), 2,60-2,80 (1H, м), 2,95 (3H, с), 3,07 (3H, с), 4,30-4,45 (2H, м), 4,65-4,85 (1H, м), 7,54 (1H, дд, J=8,5, 2,0Гц), 8,06 (1H, шир.д), 8,18 (1H, с), 9,70-9,90 (1H, м), 10,48 (1H, с).
МС (ESI) m/z: 464 (M+H)+.
[Ссылочный пример 441]
трет-Бутил (3R,4S)-4-{[2-(4-хлоранилино)-2-оксоэтантиоил]амино}-1-(2-метоксиацетил)пиперидин-3-илкарбамат
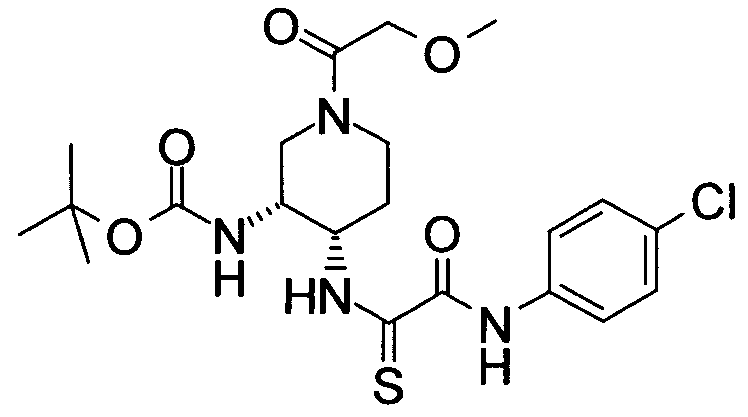
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 220, каталитическим восстановлением подобно способу, описанному в ссылочном примере 214, и конденсацией полученного амина с соединением, полученным в ссылочном примере 351, подобно способу, описанному в ссылочном примере 427.
1Н-ЯМР (CDCl3) δ: 1,46 (9H, с), 1,59-1,84 (1H, м), 2,10-2,33 (1H, м), 2,68-2,81 (0,7H, м), 2,94-2,04 (0,3H, м), 3,15-3,40 (1H, м), 3,44 (3H, с), 3,91-4,32 (4H, м), 4,45-4,58 (1H, м), 4,60-4,77 (1H, м), 5,15-5,30 (0,3H, шир.), 5,84-5,94 (0,7H, м), 7,32 (2H, д, J=8,6Гц), 7,61 (2H, д, J=8,6Гц), 10,12 (1H, с), 10,19-10,33 (1H, шир.).
МС (FAB) m/z: 485 [(M+H)+, Cl35], 487 [(M+H)+, Cl37].
[Ссылочный пример 442]
9Н-Флуорен-9-илметил (1S,2R,4S)-2-[(трет-бутоксикарбонил)амино]-4-[(диметиламино)карбонил]циклогексилкарбамат
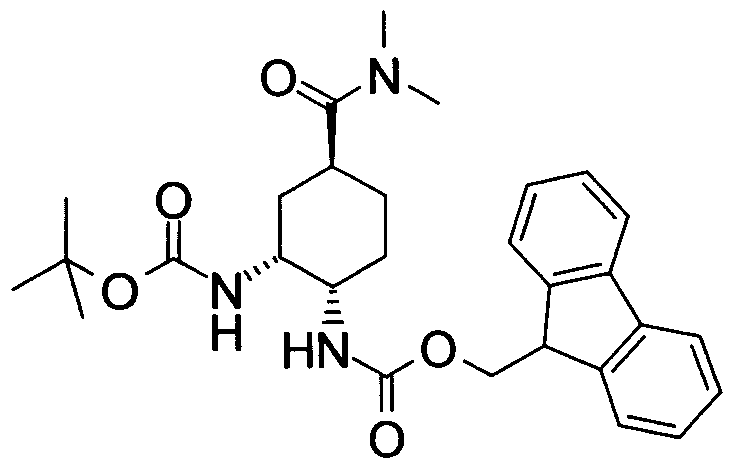
Соединение (856 мг), полученное в ссылочном примере 144, растворяли в ацетоне (10 мл), к раствору добавляли 9-флуоренилметилпентафторфенилкарбамат (1,34 г) и гидрокарбонат натрия (302 мг) и смесь перемешивали при комнатной температуре в течение 2,5 часов. Добавляли дополнительно 9-флуоренилметилпентафторфенилкарбамат (609 мг) и гидрокарбонат натрия (151 мг) и полученную смесь кипятили с обратным холодильником в течение 30 минут. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной флэш-хроматографией на силикагеле (SI-40B метиленхлорид:метанол = 93:7) с получением указанного в заголовке соединения (1,47 г).
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,30-2,05 (6H, м), 2,63 (1H, шир.с), 2,94 (3H, с), 3,04 (3H, с), 3,69 (1H, шир.с), 4,15 (1H, шир.с), 4,21 (1H, шир.с), 4,37 (2H, шир.с), 4,73 (1H, шир.с), 5,41 (1H, шир.с), 7,29 (2H, т, J=7,3Гц), 7,39 (2H, т, J=7,3Гц), 7,57 (2H, д, J=7,3Гц), 7,75 (2H, д, J=7,3Гц).
МС (ESI) m/z: 508 (M+H)+.
[Ссылочный пример 443]
9Н-Флуорен-9-илметил (1S,2R,4S)-2-[(трет-бутоксикарбонил)амино]-4-[(диметиламино)карботиоил]циклогексилкарбамат
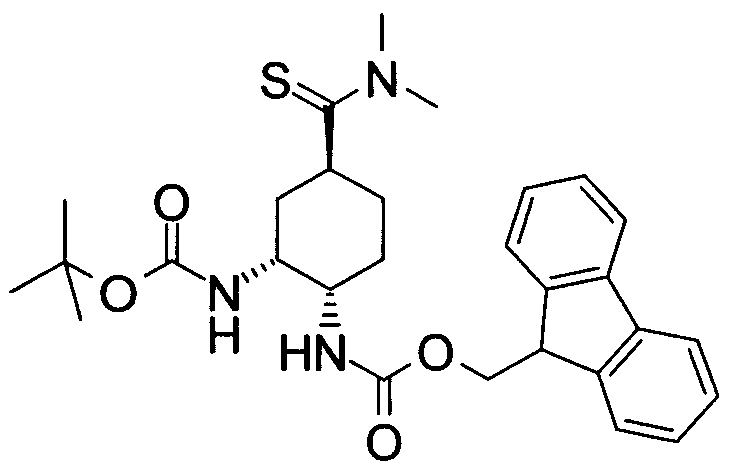
Соединение (1,26 г), полученное в ссылочном примере 442, растворяли в толуоле (50 мл), к раствору добавляли реактив Лоссона (Lawesson) (1,00 г) и смесь перемешивали при 60°C в течение 1 часа. Нерастворимое вещество удаляли фильтрованием и отгоняли при пониженном давлении растворитель. Остаток растворяли в этаноле (50 мл) и к раствору добавляли ди-трет-бутилдикарбонат (541 мг) и гидрокарбонат натрия (208 мг). Полученную смесь перемешивали при комнатной температуре в течение 1 часа, отгоняли при пониженном давлении растворитель и остаток очищали колоночной флэш-хроматографией на силикагеле (гексан:этилацетат = 1:1 → метиленхлорид:метанол = 9:1) с получением указанного в заголовке соединения (609 мг) в виде белого твердого вещества.
1Н-ЯМР (CDCl3) δ: 1,43 (9H, с), 1,43-2,10 (6H, м), 2,92 (1H, шир.с), 3,31 (3H, с), 3,47 (3H, с), 3,74 (1H, шир.с), 4,09-4,19 (2H, м), 4,38 (2H, шир.с), 4,75 (1H, шир.), 5,29 (1H, шир.с), 7,29 (2H, т, J=7,3Гц), 7,38 (2H, т, J=7,3Гц), 7,55 (2H, шир.с), 7,75 (2H, д, J=7,3Гц).
[Ссылочный пример 444]
трет-Бутил (1R,2S,5S)-2-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-5-[(диметиламино)карботиоил]циклогексилкарбамат
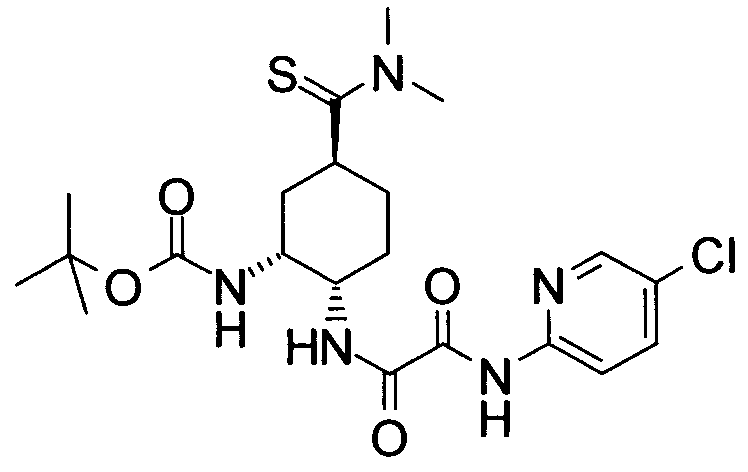
Соединение (1,11 г), полученное в ссылочном примере 443, растворяли в N,N-диметилформамиде (30 мл), к раствору добавляли пиперазин (3,0 мл) и смесь перемешивали при комнатной температуре в течение 15 минут. Растворитель отгоняли при пониженном давлении и к остатку добавляли этилацетат и воду для разделения жидкостей. Полученный водный слой экстрагировали дважды этилацетатом. Органические слои объединяли, сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток конденсировали с соединением, полученным в ссылочном примере 433, подобно способу, описанному в ссылочном примере 91, с получением указанного в заголовке соединения (629 мг).
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 1,48-2,23 (6H, м), 2,98 (1H, шир.с), 3,36 (3H, с), 3,49 (3H, с), 3,98-4,04 (1H, м), 4,22-4,25 (1H, м), 4,75 (1H, шир.с), 7,70 (1H, дд, J=8,8, 2,7Гц), 7,85 (1H, шир.с), 8,16 (1H, д, J=8,8Гц), 8,30 (1H, д, J=2,7Гц), 9,73 (1H, с).
МС (FAB) m/z: 484 [(M+H)+, Cl35], 486 [(M+H)+, Cl37].
[Ссылочный пример 445]
Дигидрохлорид N1-{(1S,2R,4S)-2-амино-4-[(диметиламино)карботиоил]циклогексил}-N2-(5-хлорпиридин-2-ил)этандиамида
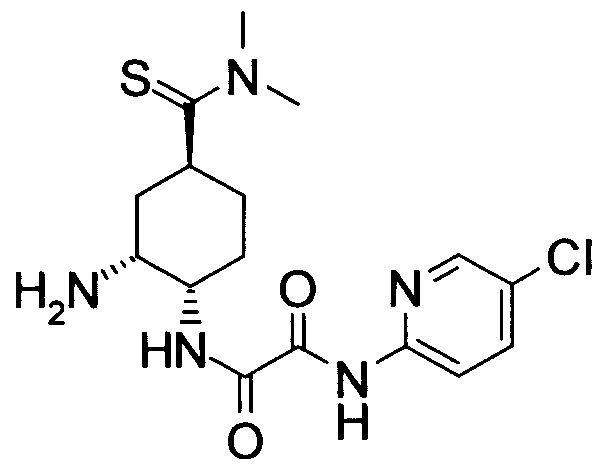
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 444, подобно способу, описанному в ссылочном примере 69.
1Н-ЯМР (ДМСО-d6) δ: 1,66-2,11 (6H, м), 3,38 (3H, с), 3,42 (3H, с), 3,52 (1H, шир.с), 3,75 (1H, шир.с), 3,88 (1H, шир.с), 8,03-8,09 (2H, м), 8,21 (3H, шир.с), 8,48 (1H, д, J=2,2Гц), 9,06 (1H, д, J=6,8Гц), 10,34 (1H, с).
МС (FAB) m/z: 384 [(M+H)+, Cl35], 386 [(M+H)+, Cl37].
[Ссылочный пример 446]
9Н-Флуорен-9-илметил (3R,4S)-3-[(трет-бутоксикарбонил)амино]-1-(2-метоксиацетил)пиперидин-4-илкарбамат
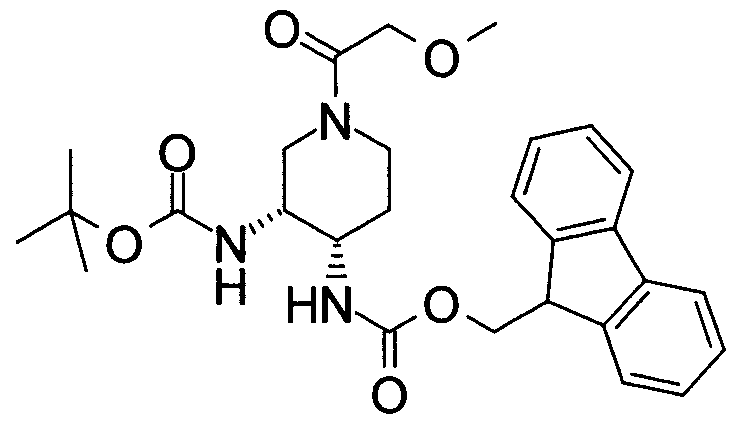
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 220, каталитическим восстановлением подобно способу, описанному в ссылочном примере 214, и обработкой полученного амина подобно способу, описанному в ссылочном примере 442.
1Н-ЯМР (CDCl3) δ: 1,48 (9H, с), 1,55-1,80 (1H, м), 1,92-2,20 (1H, м), 2,70-3,35 (2H, м), 3,44 (3H, с), 3,77-4,90 (10H, м), 5,29-5,45 (0,6H, шир.), 5,75-5,90 (0,4H, шир.), 7,26-7,34 (2H, м), 7,39 (2H, т, J=7,6Гц), 7,55-7,65 (2H, м), 7,76 (2H, д, J=7,6Гц).
МС (FAB) m/z: 510 (M+H)+.
[Ссылочный пример 447]
9Н-Флуорен-9-илметил (3R,4S)-3-[(трет-бутоксикарбонил)амино]-1-(2-метоксиэтантиоил)пиперидин-4-илкарбамат
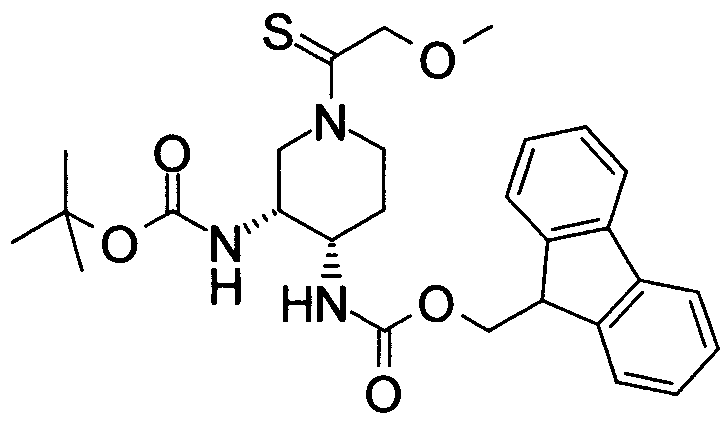
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 446, подобно способу, описанному в ссылочном примере 443.
1Н-ЯМР (CDCl3) δ: 1,48 (9H, с), 1,50-1,80 (1H, м), 2,07-2,23 (1H, м), 3,04-3,18 (0,5H, м), 3,25-3,37 (0,5H, м), 3,44 (1,5H, с), 3,47 (1,5H, с), 3,88-4,75 (9H, м), 5,00-5,70 (2H, шир.), 5,98-6,23 (1H, шир.), 7,26-7,29 (2H, м), 7,39 (2H, т, J=7,3Гц), 7,55-7,68 (2H, м), 7,77 (2H, д, J=7,3Гц).
МС (FAB) m/z: 526 (M+H)+.
[Ссылочный пример 448]
трет-Бутил (3R,4S)-4-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-1-(2-метоксиэтантиоил)пиперидин-3-илкарбамат
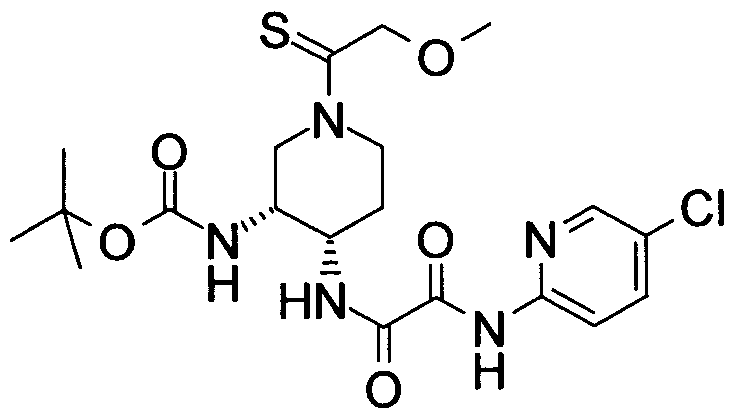
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 447, диэтиламином подобно способу, описанному в ссылочном примере 444, для снятия защиты и затем конденсацией полученного соединения с соединением, полученным в ссылочном примере 433.
1Н-ЯМР (CDCl3) δ: 1,47 (9H, с), 1,73-1,88 (1H, м), 2,07-2,22 (1H, м), 3,05-3,15 (1H, м), 3,27-3,42 (1H, м), 3,45 (1H, с), 3,48 (2H, с), 4,10-4,54 (5H, м), 5,12-5,21 (0,3H, шир.), 5,48-5,56 (0,7H, шир.), 5,61-5,74 (1H, шир.), 7,70 (1H, дд, J=8,5, 2,0Гц), 8,21 (1H, д, J=8,5Гц), 8,31 (1H, д, J=2,0Гц), 8,42-8,60 (1H, шир.), 9,72 (1H, шир.с).
МС (ESI) m/z: 486 [(M+H)+, Cl35], 488 [(M+H)+, Cl37].
[Ссылочный пример 449]
Этил (1S,3R,4S)-4-{[(аллилокси)карбонил]амино}-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
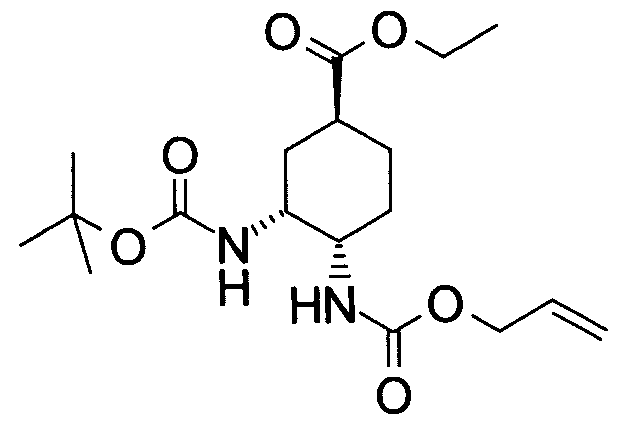
10% Палладий на углероде (10,2 г) добавляли к раствору соединения (10,0 г), полученного в ссылочном примере 141, в смешанном растворителе из тетрагидрофурана (40 мл) и этанола (40 мл) и смесь перемешивали при комнатной температуре в течение 63 часов в атмосфере водорода. После отфильтровывания катализатора полученный фильтрат концентрировали при пониженном давлении. Полученное бесцветное масло растворяли в тетрагидрофуране (25 мл) и к раствору при комнатной температуре добавляли пиридин (2,3 мл), затем добавляли по каплям при 0°C аллилхлорформиат (2,70 мл) и смесь перемешивали в течение 20 минут. После добавления льда и этилацетата к реакционной смеси и перемешивания полученной смеси в течение 5 минут добавляли 10% водный раствор лимонной кислоты для подкисления смеси. Полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 40:1) с получением указанного в заголовке соединения (6,03 г).
1Н-ЯМР (CDCl3) δ: 1,25 (3H, т, J=7,1Гц), 1,31-1,40 (1H, м), 1,45 (9H, с), 1,51-1,65 (1H, м), 1,72-1,86 (1H, м), 1,89-2,10 (3H, м), 2,25-2,50 (1H, шир.), 3,63-3,72 (1H, м), 4,03-4,15 (1H, шир.), 4,13 (2H, кв, J=7,1Гц), 4,49-4,59 (2H, м), 4,60-4,75 (1H, м), 5,20 (1H, д, J=10,5Гц), 5,22-5,32 (1H, шир.), 5,29 (1H, дд, J=17,1, 1,7Гц), 5,85-5,97 (1H, м).
МС (ESI) m/z: 371 (M+H)+.
[Ссылочный пример 450]
(1S,3R,4S)-4-{[(Аллилокси)карбонил]амино}-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоновая кислота
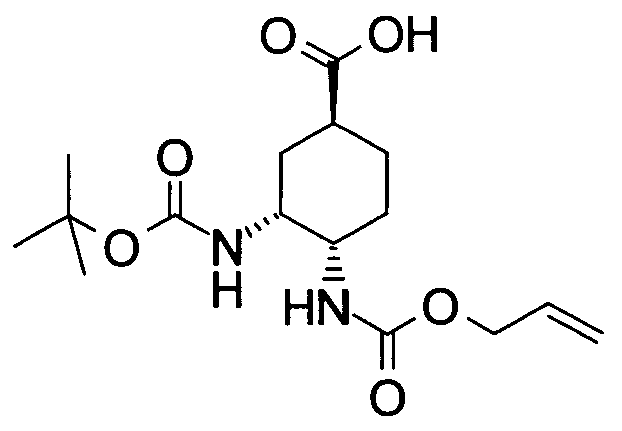
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 449, подобно способу, описанному в ссылочном примере 142.
1Н-ЯМР (CDCl3) δ: 1,35-2,15 (6H, шир.), 1,45 (9H, с), 2,35-2,65 (1H, шир.), 3,65-3,75 (1H, м), 4,00-4,15 (1H, шир.), 4,48-4,63 (2H, м), 4,63-4,80 (1H, шир.), 5,03-5,33 (1H, шир.), 5,21 (1H, д, J=10,3Гц), 5,29 (1H, дд, J=17,1, 1,5Гц), 5,86-5,97 (1H, м).
МС (ESI) m/z: 343 (M+H)+.
[Ссылочный пример 451]
2,2,2-Трихлорэтил (1S,3R,4S)-4-{[(аллилокси)карбонил]амино}-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
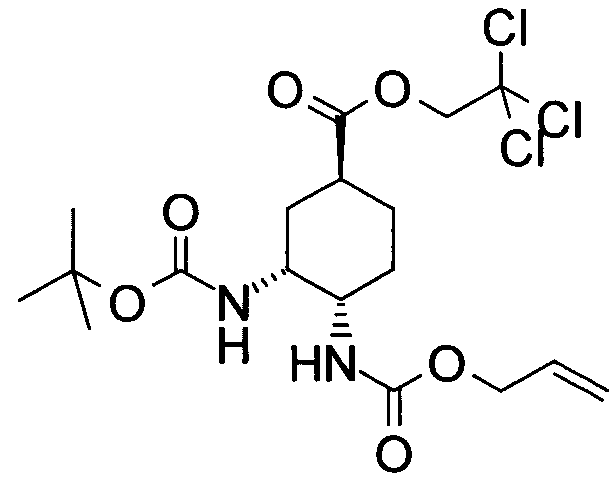
Гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (4,99 г), 1-гидроксибензотриазол (2,81 г), 2,2,2-трихлорэтанол (4,15 мл) и 4-диметиламинопиридин (4,15 г) добавляли к раствору соединения (5,93 г), полученного в ссылочном примере 450, в N,N-диметилформамиде (40 мл) и смесь перемешивали при комнатной температуре в течение 1,5 часов. Затем реакционную смесь концентрировали при пониженном давлении и добавляли к остатку этилацетат и воду. Полученный водный слой экстрагировали этилацетатом и органические слои объединяли, промывали 10% водным раствором лимонной кислоты, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 40:1) с получением указанного в заголовке соединения (8,88 г).
1Н-ЯМР (CDCl3) δ: 1,35-1,50 (1H, м), 1,46 (9H, с), 1,55-1,73 (1H, м), 1,77-2,22 (4H, м), 2,50-2,65 (1H, шир.), 3,66-3,75 (1H, м), 4,05-4,20 (1H, м), 4,50-4,60 (2H, м), 4,60-4,80 (1H, шир.), 4,71 (1H, д, J=11,8Гц), 4,77 (1H, д, J=11,8Гц), 5,18-5,34 (1H, шир.), 5,20 (1H, д, J=10,5Гц), 5,30 (1H, дд, J=17,4, 1,0Гц), 5,86-5,97 (1H, м).
МС (ESI) m/z: 473 [(M+H)+, 3xCl35], 475 [(M+H)+, 2xCl35, Cl37], 477 [(M+H)+, Cl35, 2xCl37].
[Ссылочный пример 452]
2,2,2-Трихлорэтил (1S,3R,4S)-4-амино-3-[(трет-бутоксикарбонил)амино]циклогексанкарбоксилат
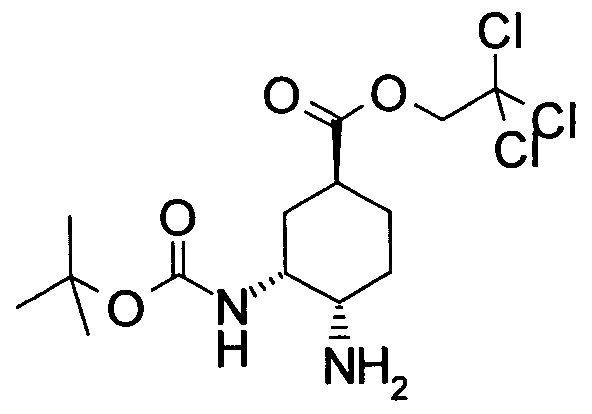
Диэтиламин (20 мл) и тетракис(трифенилфосфин)палладий (719 мг) добавляли к раствору соединения (8,83 г), полученного в ссылочном примере 451, в тетрагидрофуране (35 мл) и смесь перемешивали при комнатной температуре в течение 2,5 часов в атмосфере аргона. К реакционной смеси для ее подкисления добавляли 10% водный раствор (250 мл) лимонной кислоты и к полученной смеси добавляли диэтиловый эфир. Затем полученный водный слой промывали диэтиловым эфиром, добавляли к водному слою для его подщелачивания карбонат натрия и водный слой экстрагировали метиленхлоридом. Полученный метиленхлоридный слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении с получением указанного в заголовке соединения (4,35 г).
1Н-ЯМР (CDCl3) δ: 1,20-1,50 (3H, м), 1,46 (9H, с), 1,58-1,69 (1H, м), 1,70-1,81 (2H, м), 1,98-2,07 (1H, м), 2,22-2,31 (1H, м), 2,55-2,66 (1H, м), 2,97-3,04 (1H, м), 3,79-3,93 (1H, шир.), 4,70 (1H, д, J=12,0Гц), 4,75-4,85 (1H, шир.), 4,78 (1H, д, J=12,0Гц).
МС (ESI) m/z: 389 [(M+H)+, 3xCl35], 391 [(M+H)+, 2xCl35, Cl37], 393 [(M+H)+, Cl35, 2xCl37].
[Ссылочный пример 453]
2,2,2-Трихлорэтил (1S,3R,4S)-3-[(трет-бутоксикарбонил)амино]-4-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)циклогексанкарбоксилат
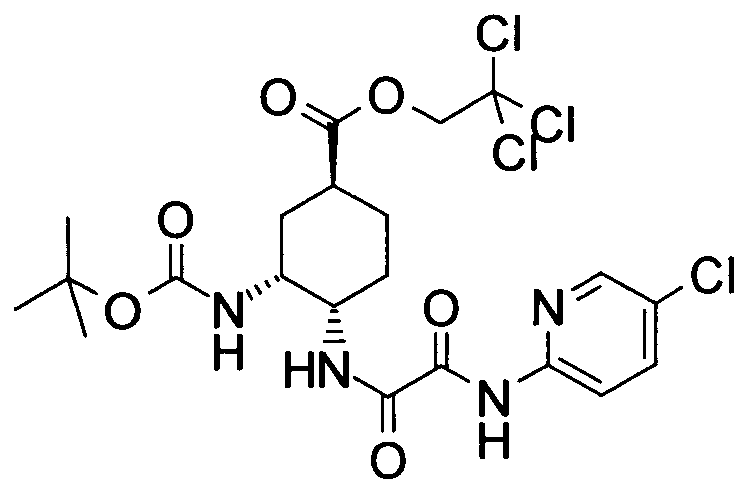
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 452, с соединением, полученным в ссылочном примере 433, подобно способу, описанному в ссылочном примере 91.
1Н-ЯМР (CDCl3) δ: 1,46 (9H, с), 1,50-1,63 (1H, м), 1,65-1,79 (2H, м), 1,87-2,08 (2H, м), 2,10-2,22 (2H, м), 2,50-2,70 (1H, шир.), 3,94-4,02 (1H, м), 4,17-4,30 (1H, шир.), 4,73 (1H, д, J=12,0Гц), 4,78 (1H, д, J=12,0Гц), 7,70 (1H, дд, J=8,8, 2,4Гц), 7,90-8,07 (1H, шир.), 8,18 (1H, д, J=8,8Гц), 8,31 (1H, д, J=2,4Гц), 9,72 (1H, шир.с).
МС (ESI) m/z: 571 [(M+H)+, 3xCl35], 573 [(M+H)+, 2xCl35, Cl37], 575 [(M+H)+, Cl35, 2xCl37].
[Ссылочный пример 454]
Метил 2-[((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)амино]-2-(метоксиимино)ацетат
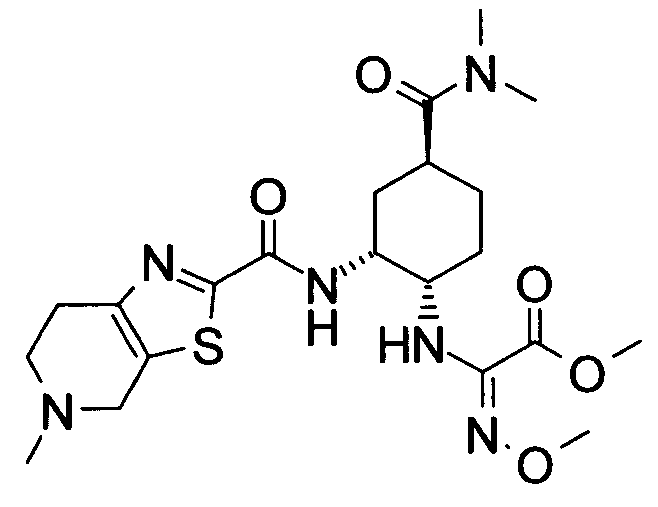
Соединение (435 мг), полученное в ссылочном примере 144, и метил 2-(метоксиимино)-2-(метилсульфонил)ацетат (WO99/67209) (233 мг) растворяли в тетрагидрофуране (5 мл), к полученному раствору добавляли триэтиламин (332 мкл) и смесь перемешивали в течение ночи при 70°C. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный масляный слой сушили над безводным сульфатом натрия. После концентрирования масляного слоя полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 91:9) с получением указанного в заголовке соединения (111 мг).
1Н-ЯМР (CDCl3) δ: 1,42-2,10 (6H, м), 2,52 (3H, с), 2,70-3,10 (11H, м), 3,71 (2H, шир.с), 3,83 (3H, с), 3,84 (3H, с), 4,22-4,35 (1H, м), 4,55-4,65 (1H, м), 5,16 (1H, д, J=8,8Гц), 7,25-7,30 (1H, м).
МС (ESI) m/z: 481 (M+H)+.
[Ссылочный пример 455]
N1-((1S,2R,4S)-4-[(Диметиламино)карботиоил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}цилогексил)-N2-{5-[2-(триметилсилил)этинил]пиридин-2-ил}этандиамид
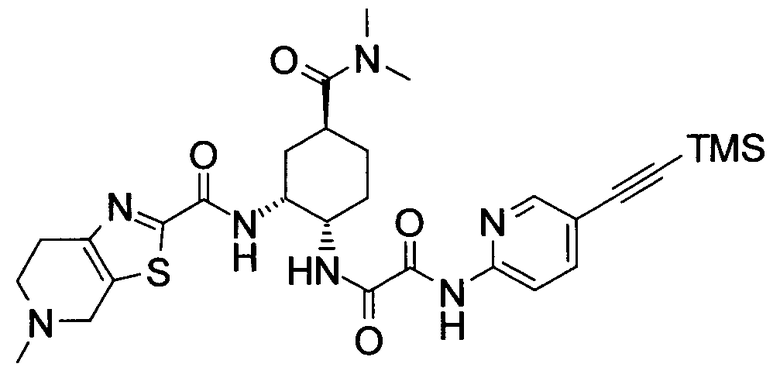
Соединение (658 г), полученное в ссылочном примере 204, растворяли в тетрагидрофуране (10 мл), N,N-диметилформамиде (10 мл) и триэтиламине (20 мл) и к раствору добавляли трифенилфосфин (87 мг), триметилсилилацетилен (471 мкл), ацетат палладия (50 мг). Полученную смесь перемешивали при 80°C в течение 14 часов в атмосфере аргона. Реакционную смесь фильтровали через целит и фильтрат тщательно промывали метиленхлоридом. К фильтрату добавляли воду для разделения жидкостей и полученный органический слой обесцвечивали активированным углем (примерно 3 г) и сушили над безводным сульфатом натрия. После фильтрования отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 93:7) с получением указанного в заголовке соединения (360 мг).
1Н-ЯМР (CDCl3) δ: 0,25 (9H, с), 1,66-2,13 (6H, м), 2,52 (3H, с), 2,78-2,96 (8H, м), 3,05 (3H, с), 3,70 (1H, д, J=15,4Гц), 3,73 (1H, д, J=15,4Гц), 4,08-4,15 (1H, м), 4,66-4,69 (1H, м), 7,42 (1H, д, J=8,4Гц), 7,77 (1H, дд, J=8,4, 2,1Гц), 8,03 (1H, д, J=8,1Гц), 8,13 (1H, д, J=8,8Гц), 8,43 (1H, д, J=2,1Гц), 9,74 (1H, с).
МС (ESI) m/z: 610 (M+H)+.
[Ссылочный пример 456]
Метил 5-метил-5,6-дигидро-4Н-тиено[2,3-c]пиррол-2-карбоксилат
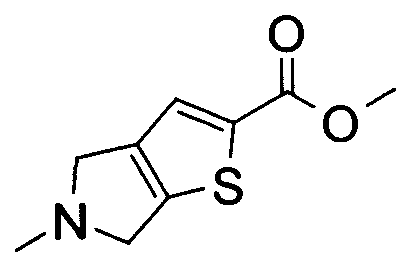
Метил 4,5-бис(хлорметил)-2-тиофенкарбоновую кислоту (D. J. Zwanenburg and Hans Wynberg, J. Org. Chem., 34, 333-340, (1969)) (520 мг) растворяли в ацетонитриле (600 мл), к раствору добавляли метиламин (40% метанольный раствор, 722 мкл) и смесь перемешивали при комнатной температуре в течение 3 суток. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 1:0 → 19:1) с получением указанного в заголовке соединения (176 мг).
1Н-ЯМР (CDCl3) δ: 2,63 (3H, с), 3,82-3,83 (2H, м), 3,86 (3H, с), 3,97-3,99 (2H, м), 7,51 (1H, с).
МС (ESI) m/z: 198 (M+H)+.
[Ссылочный пример 457]
2-Хлор-N-(6-хлорпиридазин-3-ил)ацетамид
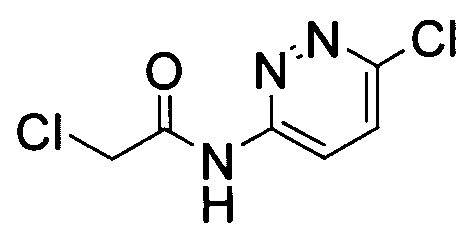
3-Амино-6-хлорпиридазин (10,4 г) растворяли в N,N-диметилформамиде (200 мл), к раствору добавляли хлорацетилхлорид (7,48 мл) и смесь перемешивали при комнатной температуре в течение 1 часа. Растворитель отгоняли при пониженном давлении и к остатку добавляли этилацетат и насыщенный водный раствор гидрокарбоната натрия. Выпавшие в осадок твердые частицы отфильтровывали и промывали этилацетатом и водой с получением указанного в заголовке соединения (9,39 г).
1Н-ЯМР (CDCl3) δ: 4,30 (2H, с), 7,56 (1H, д, J=9,3Гц), 8,51 (1H, д, J=9,3Гц), 9,68 (1H, шир.с).
[Ссылочный пример 458]
S-{2-[(6-Хлорпиридазин-3-ил)амино]-2-оксоэтил}тиосульфат натрия
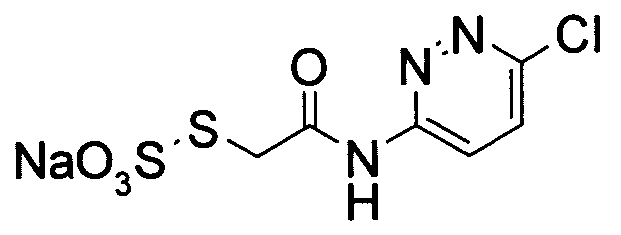
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 457, подобно способу, описанному в ссылочном примере 353.
1Н-ЯМР (ДМСО-d6) δ: 3,84 (2H, с), 7,87 (1H, д, J=9,4Гц), 8,36 (1H, д, J=9,4Гц), 11,21 (1H, шир.с).
[Ссылочный пример 459]
трет-Бутил (1R,2S,5S)-2-({2-[(6-хлорпиридазин-3-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карботиоил]циклогексилкарбамат
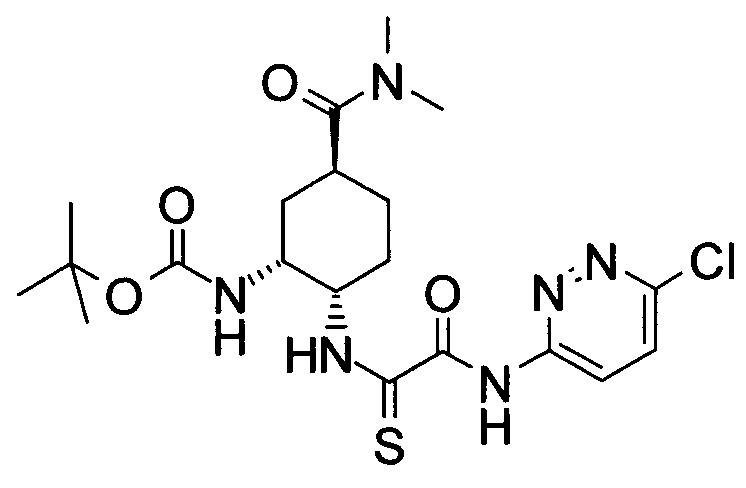
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 458, и соединения, полученного в ссылочном примере 144, подобно способу, описанному в ссылочном примере 427.
1Н-ЯМР (CDCl3) δ: 1,35-1,58 (10H, м), 1,71-1,80 (1H, м), 1,86-1,94 (2H, м), 2,09 (1H, шир.с), 2,30 (1H, шир.с), 2,96 (3H, с), 3,08 (3H, с), 4,36 (2H, шир.с), 4,79 (1H, шир.с), 5,30 (1H, шир.с), 7,54 (1H, д, J=9,0Гц), 8,47 (1H, д, J=9,0Гц), 10,03 (1H, шир.с), 11,03 (1H, с).
[Ссылочный пример 460]
Гидрохлорид (1S,3R,4S)-3-амино-4-({2-[(6-хлорпиридазин-3-ил)амино]-2-оксоэтантиоил}амино)-N,N-диметилциклогексанкарбоксамида
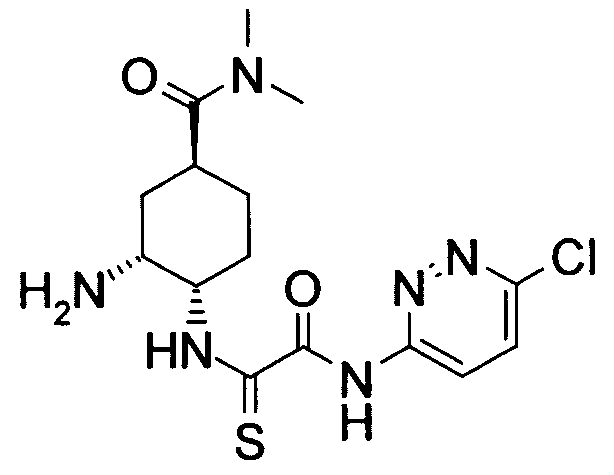
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 459, подобно способу, описанному в ссылочном примере 69.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,53 (1H, м), 1,73-1,85 (3H, м), 2,03-2,07 (1H, м), 2,15-2,24 (1H, м), 2,82 (3H, с), 3,08 (3H, с), 3,32-3,37 (1H, м), 4,06 (1H, шир.с), 4,39 (1H, шир.с), 8,01 (1H, д, J=9,3Гц), 8,37 (1H, д, J=9,3Гц), 8,43 (3H, шир.с), 11,11 (1H, д, J=6,6Гц), 11,37 (1H, с).
МС (FAB) m/z: 385 [(M+H)+, Cl35], 387 [(M+H)+, Cl37].
[Ссылочный пример 461]
2-Хлор-N-(6-хлорпиридин-3-ил)ацетамид
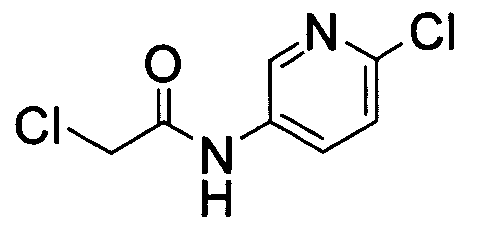
Указанное в заголовке соединение получали из 5-амино-2-хлорпиридина подобно способу, описанному в ссылочном примере 457.
1Н-ЯМР (CDCl3) δ: 4,22 (2H, с), 7,34 (1H, д, J=8,5Гц), 8,14 (1H, дд, J=8,5, 2,7Гц), 8,30 (1H, шир.с), 8,45 (1H, д, J=2,7Гц).
[Ссылочный пример 462]
S-{2-[(6-Хлорпиридин-3-ил)амино]-2-оксоэтил}тиосульфат натрия
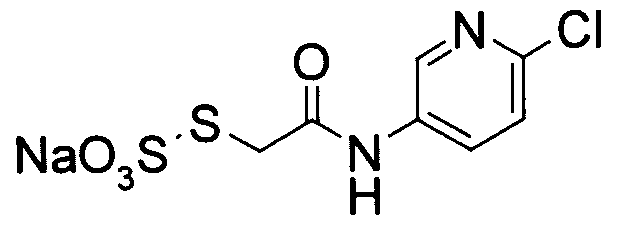
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 461, подобно способу, описанному в ссылочном примере 353.
1Н-ЯМР (ДМСО-d6) δ: 3,77 (2H, с), 7,47 (1H, д, J=8,8Гц), 8,04 (1H, дд, J=8,8, 2,7Гц), 8,57 (1H, д, J=2,7Гц), 10,51 (1H, с).
[Ссылочный пример 463]
трет-Бутил (1R,2S,5S)-2-({2-[(6-хлорпиридин-3-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карбонил]циклогексилкарбамат
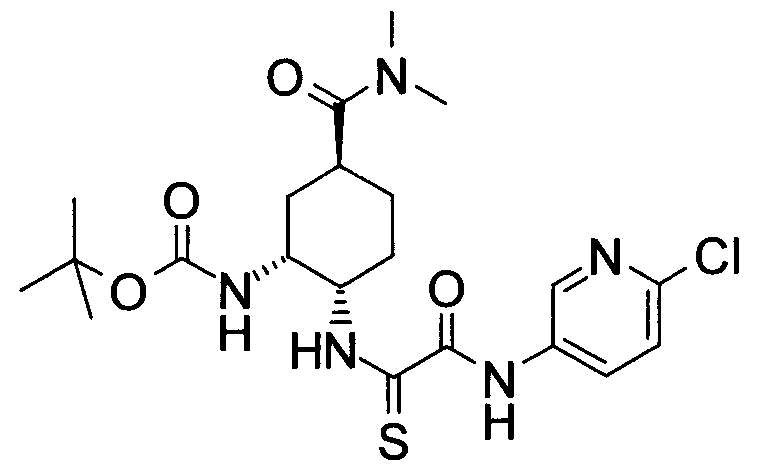
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 462, и соединения, полученного в ссылочном примере 144, подобно способу, описанному в ссылочном примере 427.
1Н-ЯМР (CDCl3) δ: 1,46 (9H, шир.с), 1,60-2,23 (6H, м), 2,68 (1H, шир.с), 2,96 (3H, с), 3,08 (3H, с), 4,34-4,38 (2H, м), 4,78 (1H, м), 7,33 (1H, д, J=8,5Гц), 8,09 (1H, шир.с), 8,63 (1H, с), 9,91 (1H, шир.с), 10,24 (1H, с).
МС (ESI) m/z: 506 [(M+Na)+, Cl35], 508 [(M+Na)+, Cl37].
[Ссылочный пример 464]
Гидрохлорид (1S,3R,4S)-3-амино-4-({2-[(6-хлорпиридин-3-ил)амино]-2-оксоэтантиоил}амино)-N,N-диметилциклогексанкарбоксамида
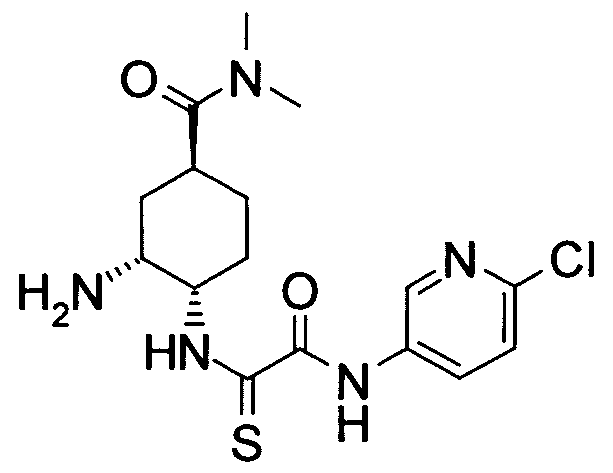
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 463, подобно способу, описанному в ссылочном примере 69.
1Н-ЯМР (ДМСО-d6) δ: 1,46-1,49 (1H, м), 1,79-1,81 (3H, м), 1,99-2,03 (1H, м), 2,14-2,16 (1H, м), 2,82 (3H, с), 3,06 (3H, с), 3,25-3,28 (1H, м), 3,99 (1H, шир.с), 4,30-4,60 (1H, шир.), 7,55 (1H, д, J=8,7Гц), 8,26 (1H, дд, J=8,7, 2,4Гц), 8,38 (3H, шир.с), 8,85 (1H, д, J=2,4Гц), 10,90 (1H, д, J=6,8Гц), 11,07 (1H, с).
МС (FAB) m/z: 384 [(M+H)+, Cl35], 386 [(M+H)+, Cl37].
[Ссылочный пример 465]
2'-Аминосульфонил-1,1'-бифенил-4-карбоновая кислота
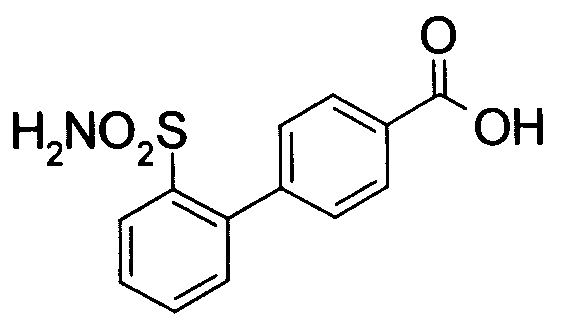
2-Бромбензолсульфонамид (800 мг) и 4-карбоксифенилбороновую кислоту (563 мг) суспендировали в смешанном растворителе из толуола (5 мл) и воды (5 мл). К суспензии добавляли последовательно тетракис(трифенилфосфин)палладий (392 мг) и безводный карбонат натрия (1,08 г) и смесь кипятили с обратным холодильником в течение ночи. После охлаждения реакционной смеси до комнатной температуры добавляли диэтиловый эфир и воду для разделения жидкостей. Полученный органический слой экстрагировали дважды водой. Все полученные водные слои объединяли и к полученному раствору добавляли для его подкисления 12N хлористоводородную кислоту. Раствор концентрировали до примерно 20 мл при пониженном давлении. Выпавший в осадок бесцветный порошок отфильтровывали и сушили при пониженном давлении с получением указанного в заголовке соединения (539 мг).
МС (EI) m/z: 277 М+.
[Пример 1]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклопропил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
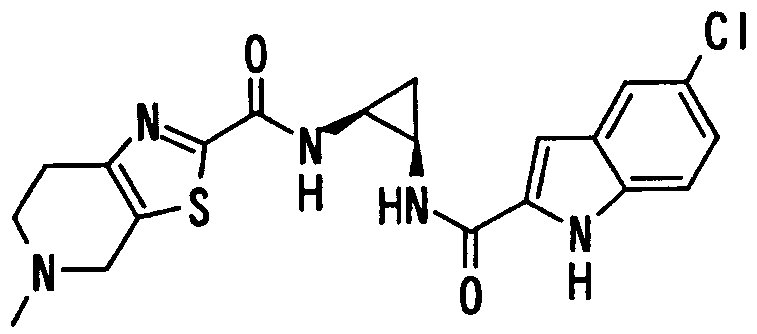
Моногидрат 1-гидроксибензотриазола (71 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (100 мг) добавляли к раствору соединения (108 мг), полученного в ссылочном примере 59, и соединения (124 мг), полученного в ссылочном примере 10, в N,N-диметилформамиде (3 мл) при комнатной температуре и смесь перемешивали в течение 8 дней. После концентрирования реакционной смеси при пониженном давлении с использованием вакуумного насоса к остатку добавляли воду (50 мл) и насыщенный водный раствор (50 мл) гидрокарбоната натрия и смесь экстрагировали метиленхлоридом. Полученные органические фракции отделяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и остаток очищали препаративной тонкослойной хроматографией на силикагеле (метиленхлорид:метанол = 10:1). После добавления к полученному таким образом аморфному веществу 1N хлористоводородной кислоты, метиленхлорида и метанола смесь концентрировали с получением указанного в заголовке соединения (72 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,15-1,35 (2H, м), 2,88 (3H, с), 2,95-3,25 (4H, м), 3,35-3,75 (2H, м), 4,32-4,45 (1H, м), 4,68 (1H, шир., J=15,4Гц), 7,08 (1H, с), 7,17 (1H, дд, J=8,6, 2,1Гц), 7,41 (1H, д, J=8,6Гц), 7,70 (1H, с), 8,50 (1H, шир., J=11,0Гц), 8,56 (1H, шир.с), 11,56 (1H, шир., J=19,3Гц), 11,86 (1H, с).
МС (FAB) m/z: 430 (М+Н)+.
[Пример 2]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклобутил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
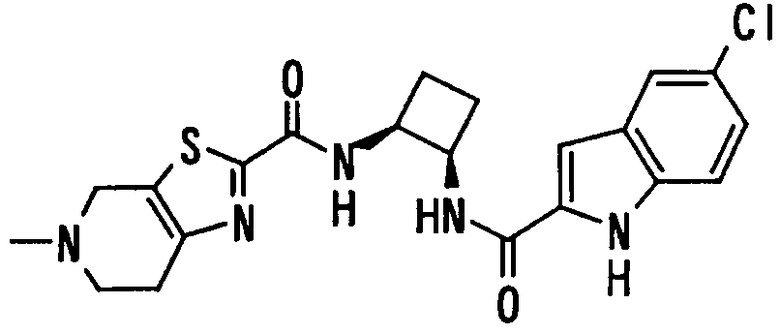
Соединение (136 мг), полученное в ссылочном примере 10, гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (255 мг) и моногидрат 1-гидроксибензотриазола (90 мг) добавляли к раствору соединения (117 мг), полученного в ссылочном примере 60, в N,N-диметилформамиде (5 мл) и смесь перемешивали в течение ночи при комнатной температуре. Затем отгоняли при пониженном давлении растворитель, используя вакуумный насос, и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный органический слой промывали насыщенным раствором хлорида натрия и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 7:93). После добавления к полученному выше соединению этилацетата и 1N этанольного раствора хлористоводородной кислоты для подкисления отгоняли при пониженном давлении растворитель. Снова добавляли этилацетат и образовавшийся осадок отфильтровывали и сушили с получением указанного в заголовке соединения (56 мг).
1Н-ЯМР (ДМСО-d6) δ: 2,00-2,35 (4H, м), 2,88 (3H, м), 3,10 (2H, шир.с), 3,20-3,75 (3H, м), 4,20-4,85 (3H, м), 7,09 (1H, с), 7,16 (1H, д, J=8,8Гц), 7,38 (1H, д, J=8,8Гц), 7,71 (1H, с), 8,63 (1H, д, J=8,3Гц), 8,85 (1H, д, J=8,6Гц), 10,85-11,20 (1H, шир.), 11,81 (1H, с).
МС (FAB) m/z: 444 (М+Н)+.
[Пример 3]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклопентил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
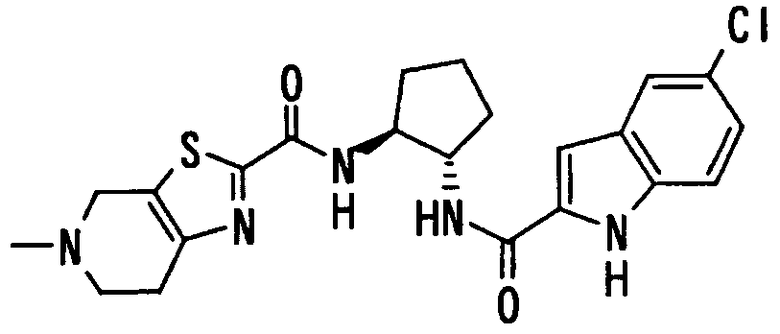
5-Хлориндол-2-карбоновую кислоту (80 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (98 мг), моногидрат 1-гидроксибензотриазола (23 мг) и триэтиламин (141 мкл) добавляли к раствору соединения (120 мг), полученного в ссылочном примере 62, в N,N-диметилформамиде (5 мл) и смесь перемешивали при комнатной температуре в течение 3 суток. Растворитель отгоняли при пониженном давлении и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 93:7). К полученному таким образом бледно-желтому твердому веществу добавляли метиленхлорид (5 мл) и 1N этанольный раствор (282 мкл) хлористоводородной кислоты, затем добавляли этилацетат и образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (109 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,64-1,74 (4H, м), 1,98-2,02 (2H, м), 2,89 (3H, с), 3,14 (2H, шир.с), 3,47-3,65 (2H, м), 4,29-4,63 (4H, м), 7,10 (1H, д, J=1,5Гц), 7,14 (1H, дд, J=8,5, 2,0Гц), 7,38 (1H, д, J=8,5Гц), 7,68 (1H, д, J=2,0Гц), 8,55 (1H, д, J=8,5Гц), 8,91 (1H, д, J=8,5Гц), 11,49 (1H, шир.с), 11,76 (1H, с).
МС (ESI) m/z: 458 (М+Н)+.
[Пример 4]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)сульфонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
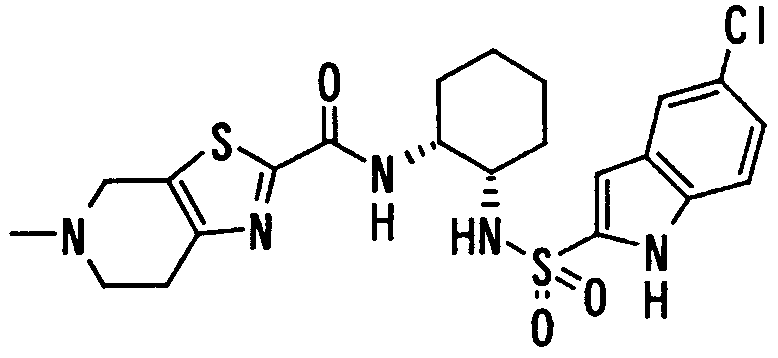
Соединение (400 мг), полученное в ссылочном примере 67, суспендировали в метиленхлориде (10 мл), добавляли триэтиламин (0,514 мл) и 5-хлор-1-фенилсульфонилиндол-2-сульфонилхлорид (выложенная заявка № 2000-119253 на патент Японии) (319 мг) и смесь перемешивали при комнатной температуре в течение 15 минут. После добавления в реакционную смесь воды для разделения жидкостей полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3) с получением бледно-желтого пенистого вещества. Полученное вещество растворяли в тетрагидрофуране (3 мл), добавляли метанол (2 мл) и 1N водный раствор (1,5 мл) гидроксида натрия и смесь кипятили с обратным холодильником в течение 2 часов. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид и 1N хлористоводородную кислоту для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3). К полученному продукту добавляли 1N хлористоводородную кислоту (1 мл) и смесь концентрировали при пониженном давлении с получением указанного в заголовке соединения (108 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,20-1,78 (8H, м), 2,94 (3H, с), 3,13 (2H, шир.с), 3,22-3,40 (1H, м), 3,44-3,70 (3H, м), 3,83-3,95 (1H, м), 4,20-4,70 (1H, м), 6,78 (1H, с), 7,18-7,30 (2H, м), 7,44 (1H, с), 7,69 (1H, шир.с), 8,09 (1H, шир.с), 11,92 (1H, с).
МС (FAB) m/z: 508 (М+Н)+.
[Пример 5]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
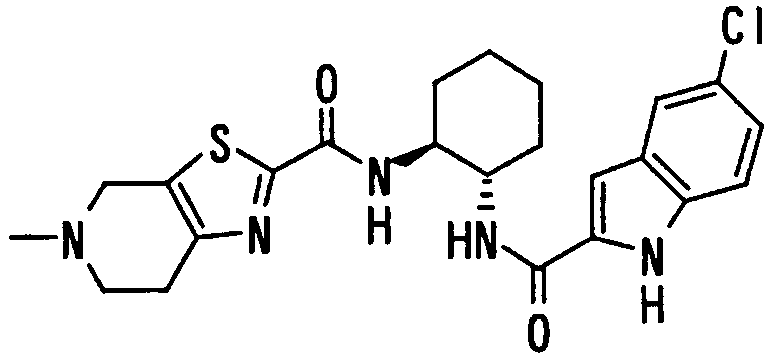
5-Хлориндол-2-карбоновую кислоту (109 мг), моногидрат 1-гидроксибензотриазола (9 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (321 мг) и триэтиламин (0,232 мл) добавляли к раствору соединения (300 мг), полученного в ссылочном примере 65, в N,N-диметилформамиде (20 мл) и смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь концентрировали при пониженном давлении с использованием вакуумного насоса и к остатку добавляли метиленхлорид и воду для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 25:1) с получением бесцветного пенистого вещества. Полученное вещество суспендировали в 1N хлористоводородной кислоте (1 мл) и суспензию концентрировали при пониженном давлении с получением указанного в заголовке соединения (203 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,25-1,40 (2H, м), 1,46-1,81 (4H, м), 1,88-1,98 (2H, м), 2,89 (3H, с), 3,00-3,76 (5H, м), 3,86-3,97 (1H, м), 4,00-4,10 (1H, м), 4,25-4,72 (1H, м), 7,03 (1H, с), 7,12 (1H, дд, J=8,5, 1,2Гц), 7,38 (1H, д, J=8,5Гц), 7,64 (1H, с), 8,28 (1H, д, J=8,5Гц), 8,54 (1H, д, J=8,5Гц), 11,70 (1H, с).
МС (FAB) m/z: 472 (М+Н)+.
[Пример 6]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
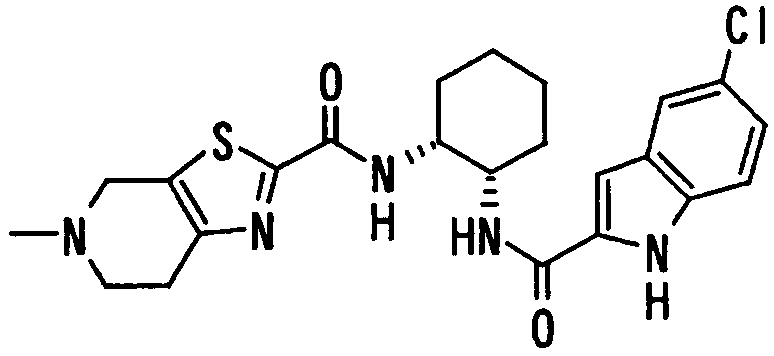
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 67, и 5-хлориндол-2-карбоновой кислоты подобно способу примера 5.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,70 (6H, м), 1,80-2,06 (2H, м), 2,89 (3H, с), 3,00-3,27 (2H, м), 3,35-3,51 (1H, м), 3,57-3,82 (1H, м), 4,15-4,30 (2H, м), 4,32-4,48 (1H, м), 4,60-4,74 (1H, м), 7,15 (1H, с), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,6Гц), 7,70 (1H, д, J=2,0Гц), 8,14 (1H, шир.с), 8,36-8,48 (1H, м), 11,51 (1H, шир.с), 11,86 (1H, с).
МС (FAB) m/z: 472 (М+Н)+.
[Пример 7]
Гидрохлорид N-{(1R*,2S*)-2-{[(6-хлорнафтоил)амино]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
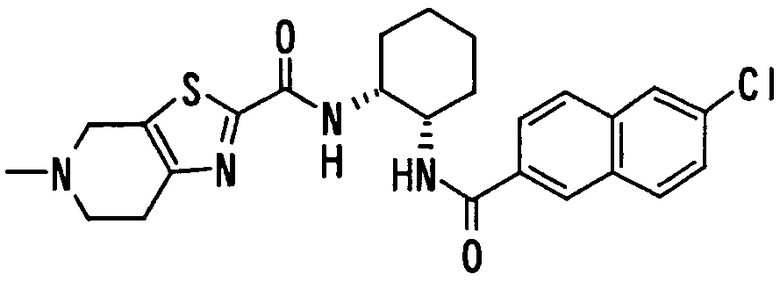
Указанное в заголовке соединение (186 мг) получали растворением соединения (275 мг), полученного в ссылочном примере 67, 6-хлорнафталин-2-карбоновой кислоты (Eur. J. Chem. Chim. Ther., 1984, Vol. 19, pp. 205-214) (148 мг), триэтиламина (0,298 мл) и моногидрата 1-гидроксибензотриазола (11 мг) в N,N-диметилформамиде (20 мл) и взаимодействием с гидрохлоридом 1-(3-диметиламинопропил)-3-этилкарбодиимида (412 мг) подобно способу примера 5.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,56 (2H, м), 1,57-1,77 (4H, м), 1,90-2,10 (2H, м), 2,90 (3H, с), 3,13 (2H, шир.с), 3,28-3,74 (2H, м), 4,26 (2H, шир.с), 4,30-4,74 (2H, м), 7,59 (1H, д, J=8,6Гц), 7,90 (1H, д, J=8,6Гц), 7,98 (1H, д, J=8,3Гц), 8,03-8,11 (2H, м), 8,25-8,58 (3H, м), 11,52 (1H, шир.с).
МС (FAB) m/z: 483 (М+Н)+.
[Пример 8]
Гидрохлорид N-((1R*,2R*)-2-{[(6-хлор-1-бензотиофен-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
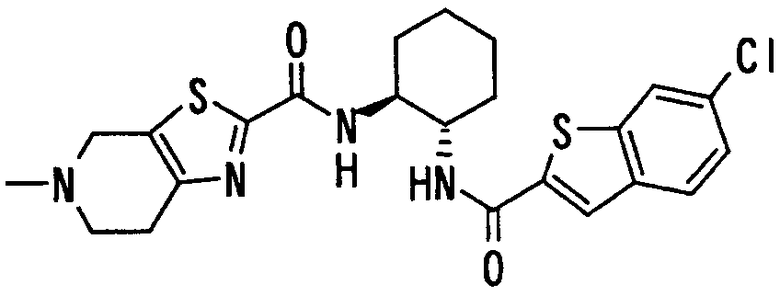
Указанное в заголовке соединение (239 мг) получали растворением соединения (255 мг), полученного в ссылочном примере 65, 6-хлорбензо[b]тиофен-2-карбоновой кислоты (выложенная заявка № 2000-119253 на патент Японии) (141 мг), триэтиламина (0,276 мл) и моногидрата 1-гидроксибензотриазола (10 мг) в N,N-диметилформамиде (20 мл) и подвергая взаимодействию с гидрохлоридом 1-(3-диметиламинопропил)-3-этилкарбодиимида (382 мг) подобно способу примера 5.
1Н-ЯМР (ДМСО-d6) δ: 1,20-1,98 (8H, м), 2,88 (3H, с), 3,00-3,72 (4H, м), 3,84-4,09 (2H, м), 4,20-4,75 (2H, м), 7,41 (1H, дд, J=8,6, 1,7Гц), 7,91 (1H, д, J=8,6Гц), 7,99 (1H, с), 8,12 (1H, с), 8,54-8,67 (2H, м), 11,53 (1H, шир.с).
МС (FAB) m/z: 489 (M+H)+.
[Пример 9]
Гидрохлорид N-((1R*,2R*)-2-{[(5-фториндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
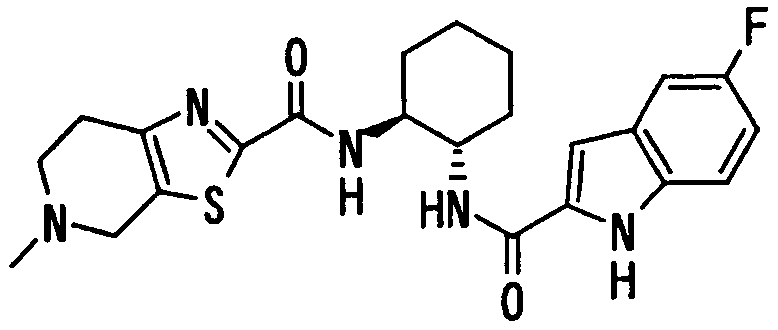
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 65, и 5-фториндол-2-карбоновой кислоты подобно способу примера 5.
1Н-ЯМР (ДМСО-d6) δ: 1,20-1,38 (2H, м), 1,40-1,57 (1H, м), 1,54-5 1,68 (1H, м), 1,71 (2H, д, J=7,3Гц), 1,88 (2H, д, J=12,0Гц), 2,86 (3H, с), 2,95-3,24 (2H, м), 3,40 (1H, шир.с), 3,63 (1H, шир.с), 3,90 (1H, шир.с), 3,97-4,10 (1H, м), 4,20-4,44 (1H, м), 4,53-4,70 (1H, м), 6,98 (1H, дд, J=9,2, 2,3Гц), 7,01 (1H, с), 7,31-7,39 (2H, м), 8,26 (1H, д, J=8,6Гц), 8,59 (1H, д, J=8,4Гц), 11,21 (1/2H, шир.с), 11,42 (1/2H, шир.с), 11,60 (1H, с).
МС (ESI) m/z: 456 (M+H)+.
[Пример 10]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлор-6-фториндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
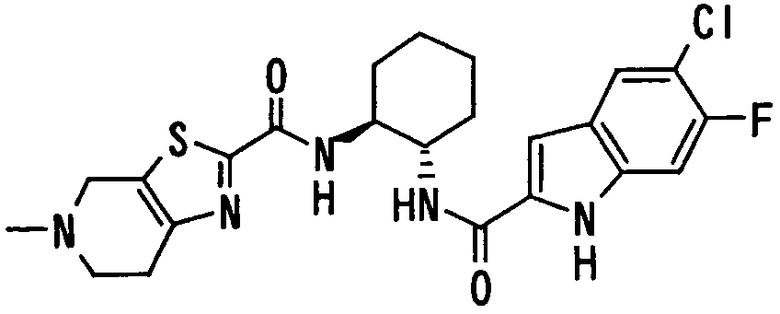
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 65, и соединения, полученного в ссылочном примере 23, подобно способу примера 5.
1Н-ЯМР (ДМСО-d6) δ: 1,20-1,40 (2H, м), 1,40-1,80 (4H, м), 1,80-2,00 (2H, м), 2,87 (3H, с), 3,01 (2H, шир.с), 3,30-3,80 (2H, м), 3,81-3,97 (2H, м), 4,20-4,80 (2H, м), 7,06 (1H, с), 7,28 (1H, д, J=10,0Гц), 7,86 (1H, д, J=7,3Гц), 8,32 (1H, д, J=8,5Гц), 8,59 (1H, д, J=8,5Гц), 11,77 (1H, с).
МС (FAB) m/z: 490 (М+Н)+.
[Пример 11]
Гидрохлорид N-((1R*,2S*)-2-{[(5-броминдол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
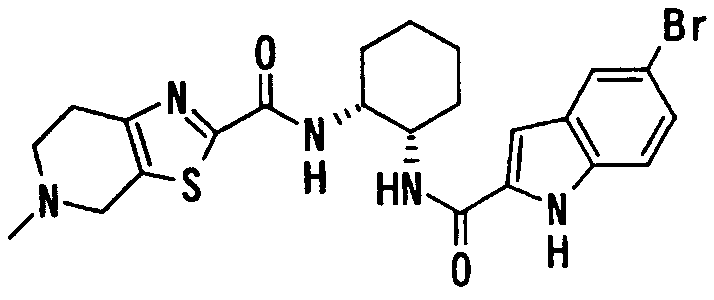
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 67, и 5-броминдол-2-карбоновой кислоты подобно способу примера 5.
1Н-ЯМР (ДМСО-d6) δ: 1,43 (2H, шир.с), 1,61 (4H, шир.с), 1,80-2,10 (2H, м), 2,88 (3H, с), 3,00-3,26 (2H, м), 3,40 (1H, шир.с), 3,65 (1H, шир.с), 4,22 (1H, шир.с), 4,26 (1H, шир.с), 4,41 (1H, шир.с), 4,67 (1H, д, J=15,6Гц), 7,14 (1H, с), 7,28 (1H, д, J=8,7Гц), 7,37 (1H, д, J=8,7Гц), 7,84 (1H, с), 8,13 (1H, шир.с), 8,33-8,52 (1H, м), 11,51 (1H, шир.с), 11,86 (1H, с).
МС (ESI) m/z: 515 (М+).
[Пример 12]
Гидрохлорид N-((1R*,2S*)-2-{[(5-этинилиндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
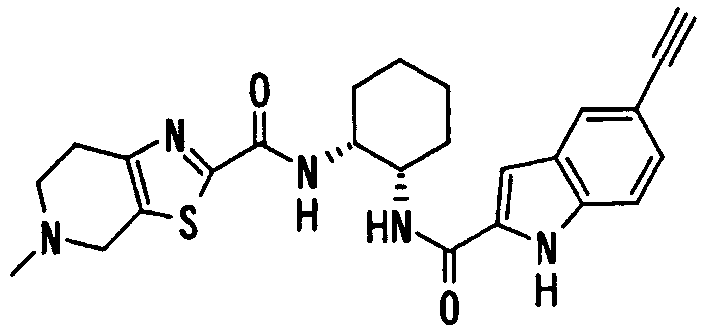
Триэтиламин (6 мл), N,N-диметилформамид (5 мл), триметилсилилацетилен (0,250 мл) и ацетат палладия (20 мг) добавляли к тетрагидрофурановому раствору (2 мл) соединения (300 мг), полученного в примере 11, и трифенилфосфина (70 мг) при комнатной температуре. После перемешивания при 90°C в течение 2 часов реакционной смеси давали остыть до комнатной температуры и добавляли к ней метиленхлорид (20 мл) и насыщенный водный раствор (30 мл) гидрокарбоната натрия для разделения жидкостей. Полученный водный слой экстрагировали метиленхлоридом (3 х 10 мл), органические слои объединяли, сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель с получением остатка. Полученный остаток очищали препаративной тонкослойной хроматографией на силикагеле (метиленхлорид:ацетон:метанол = 10:10:1) с получением бесцветных твердых частиц. Полученный продукт растворяли в метаноле (6 мл), добавляли карбонат калия (120 мг) и смесь перемешивали 1 час. К реакционной смеси добавляли метиленхлорид (20 мл) и воду (20 мл) для разделения жидкостей. Полученный водный слой экстрагировали метиленхлоридом (2 х 15 мл), органические слои объединяли и сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали препаративной тонкослойной хроматографией на силикагеле (метиленхлорид:ацетон:метанол = 10:10:1) и растворяли в смеси вода-метанол-метиленхлорид. Затем полученный раствор концентрировали с получением указанного в заголовке соединения (72 мг).
1Н-ЯМР (CDCl3) δ: 1,50-2,25 (8H, м), 2,53 (3H, с), 2,85 (2H, шир.с), 2,93 (2H, шир.с), 3,01 (1H, с), 3,74 (1H, д, J=14,1Гц), 3,77 (1H, д, J=14,1Гц), 4,21 (1H, шир.с), 4,45 (1H, шир.с), 6,91 (1H, с), 7,25-7,42 (2H, м), 7,61 (1H, шир.с), 7,80-7,97 (2H, м), 9,72 (1H, с).
МС (FAB) m/z: 462 (M+H)+.
[Пример 13]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5,6-диметил-4,5,6,7-тетрагидротиазоло[4,5-d]пиридазин-2-карбоксамида
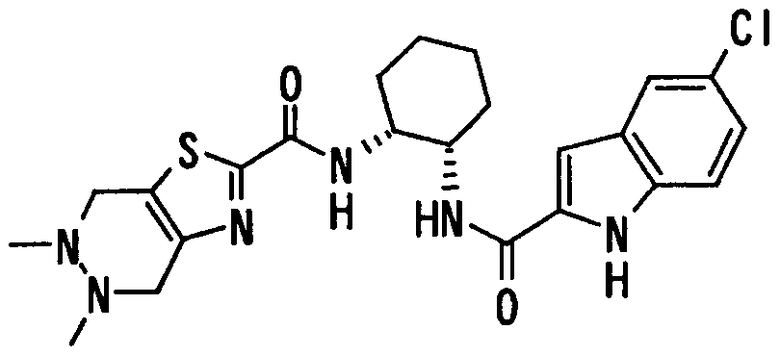
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 71, и соединения, полученного в ссылочном примере 51, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,50 (2H, м), 1,50-1,75 (4H, м), 1,80-2,10 (2H, м), 2,70 (3H, шир.с), 2,79 (3H, шир.с), 4,10-4,70 (6H, м), 7,10-7,27 (2H, м), 7,41 (1H, д, J=8,8Гц), 7,70 (1H, с), 8,12 (1H, д, J=6,8Гц), 8,47 (1H, д, J=7,6Гц), 11,85 (1H, с).
МС (FAB) m/z: 487 (М+Н)+.
[Пример 14]
N-((1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}циклогексил)-6,7-дигидро-4Н-пирано[4,3-d]тиазол-2-карбоксамид
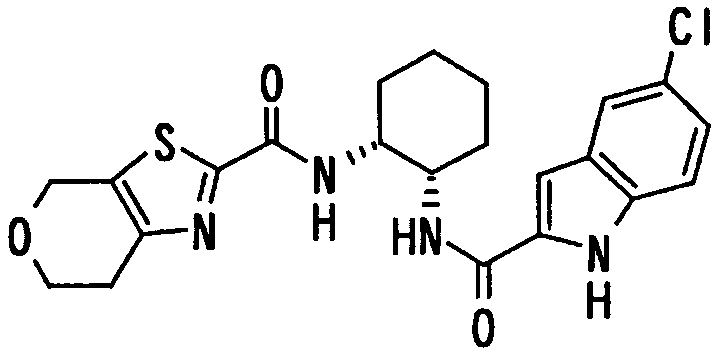
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 71, и соединения, полученного в ссылочном примере 26, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,36-1,72 (6H, м), 1,90-2,10 (2H, м), 2,80-2,87 (2H, м), 3,93 (2H, т, J=5,6Гц), 4,20-4,32 (2H, м), 4,81 (2H, с), 7,12 (1H, с), 7,15 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,67 (1H, д, J=1,7Гц), 8,11 (1H, д, J=6,6Гц), 8,36 (1H, д, J=8,3Гц), 11,78 (1H, с).
МС (FAB) m/z: 459 (M+H)+.
[Пример 15]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[4,5-с]пиридин-2-карбоксамида
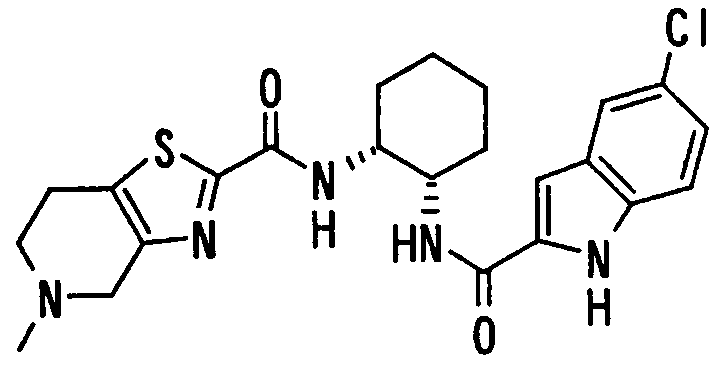
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 71, и соединения, полученного в ссылочном примере 29, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,32-1,74 (6H, м), 1,82-2,10 (2H, м), 2,92 (3H, с), 3,12-3,50 (3H, м), 3,69 (1H, шир.с), 4,13-4,39 (3H, м), 4,51 (1H, шир.с), 7,10-7,19 (2H, м), 7,41 (1H, д, J=8,6Гц), 7,68 (1H, с), 8,10 (1H, шир.с), 8,40 (1H, шир.с), 11,41 (1H, шир.с), 11,87 (1H, с).
МС (FAB) m/z: 472 (М+Н)+.
[Пример 16]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидрооксазоло[5,4-c]пиридин-2-карбоксамида
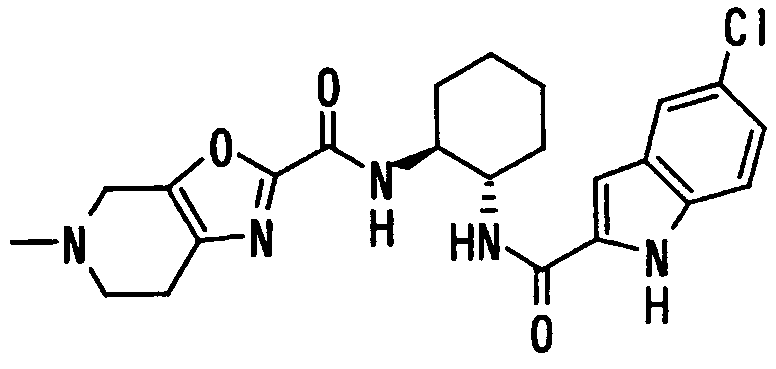
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 69, и соединения, полученного в ссылочном примере 21, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,23-1,39 (2H, м), 1,40-1,81 (4H, м), 1,82-1,98 (2H, м), 2,60-3,00 (5H, м), 3,20-3,70 (2H, м), 3,87-3,96 (1H, м), 3,98-4,10 (1H, м), 4,12-4,70 (2H, м), 7,04 (1H, д, J=1,5Гц), 7,12 (1H, дд, J=8,8, 2,0Гц), 7,38 (1H, д, J=8,8Гц), 7,65 (1H, д, J=2,0Гц), 8,33 (1H, д, J=8,6Гц), 8,72 (1H, д, J=8,6Гц), 11,61 (1H, шир.с), 11,72 (1H, с).
МС (FAB) m/z: 456 (M+H)+.
[Пример 17]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-4,5,6,7-тетрагидротиено[3,2-c]пиридин-2-карбоксамида
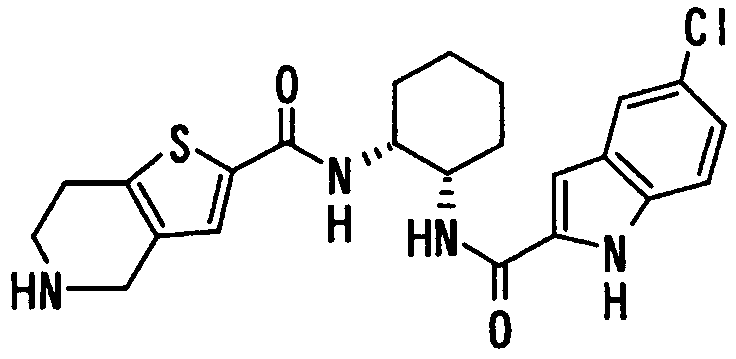
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 71, с 5-трет-бутоксикарбонил-4,5,6,7-тетрагидротиено[3,2-c]пиридин-2-карбоновой кислотой (WO94/21599) и обработкой полученного продукта хлористоводородной кислотой для снятия защиты подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,42 (2H, шир.с), 1,56-1,76 (4H, м), 1,98-2,11 (2H, м), 3,04 (2H, шир.с), 3,32-3,45 (2H, м), 4,15 (3H, шир.с), 4,26 (1H, шир.с), 7,14 (1H, дд, J=8,8, 2,0Гц), 7,23 (1H, с), 7,41 (1H, д, J=8,8Гц), 7,62 (1H, с), 7,77 (1H, с), 8,18-8,30 (2H, м), 9,42 (2H, шир.с), 11,92 (1H, с).
МС (FAB) m/z: 457 (M+H)+.
[Пример 18]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиено[3,2-c]пиридин-2-карбоксамида
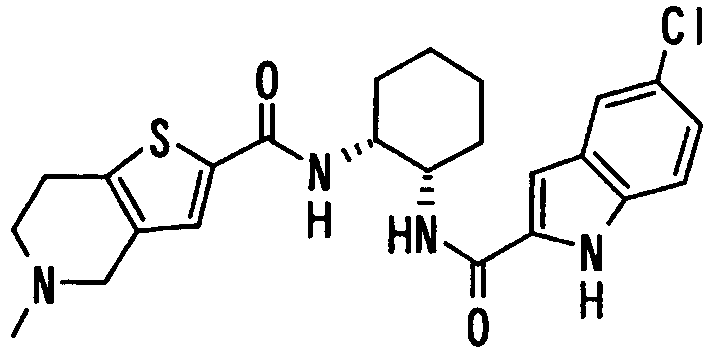
Соединение (171 мг), полученное в примере 17, суспендировали в метиленхлориде (10 мл), добавляли триэтиламин (0,104 мл) и смесь перемешивали при комнатной температуре в течение 10 минут. После добавления в реакционную смесь уксусной кислоты (0,059 мл) добавляли 35% водный раствор формальдегида (0,070 мл) и триацетоксиборгидрид натрия (118 мг) и смесь перемешивали при комнатной температуре 30 минут. После добавления к реакционной смеси 1N водного раствора (3 мл) гидроксида натрия, добавляли воду для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 50:3) с получением бесцветного пенистого вещества. Полученное вещество суспендировали в 1N хлористоводородной кислоте и суспензию концентрировали при пониженном давлении с получением указанного в заголовке соединения (85 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,40 (2H, шир.с), 1,50-1,71 (4H, м), 1,97-2,05 (2H, м), 2,87 (3H, с), 2,98-3,20 (1H, м), 3,30-3,38 (2H, м), 3,54-3,70 (1H, м), 4,05-4,42 (4H, м), 7,14 (1H, д, J=8,6Гц), 7,23 (1H, с), 7,40 (1H, д, J=8,6Гц), 7,63 (1H, с), 7,77 (1H, с), 8,17-8,27 (2H, м), 10,83 (1H, шир.с), 11,92 (1H, с).
МС (FAB) m/z: 471 (М+Н)+.
[Пример 19]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-6-(диметиламино)-4,5,6,7-тетрагидробензотиазол-2-карбоксамида
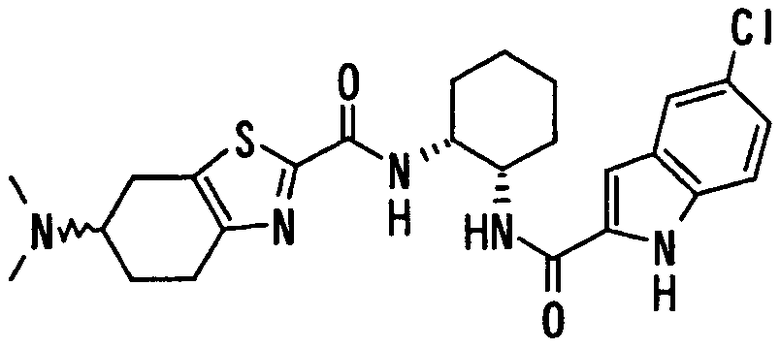
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 71, и соединения, полученного в ссылочном примере 31, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,44 (2H, шир.с), 1,52-1,68 (4H, м), 1,87-2,08 (3H, м), 2,30-2,40 (1H, м), 2,65-2,75 (1H, м), 2,77 (6H, с), 2,95-3,17 (2H, м), 3,30-3,70 (2H, м), 4,15-4,30 (2H, м), 7,10-7,20 (2H, м), 7,41 (1H, д, J=8,6Гц), 7,69 (1H, с), 8,11 (1H, д, J=5,1Гц), 8,34 (1H, д, J=8,1Гц), 10,95 (1H, шир.с), 11,83 (1H, с).
МС (FAB) m/z: 500 (М+Н)+.
[Пример 20]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-(пиридин-4-ил)-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамида
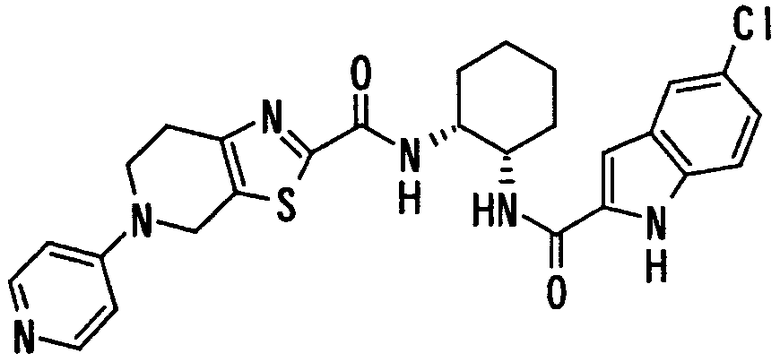
н-Бутиллитий (1,60N гексановый раствор, 0,704 мл) добавляли по каплям к раствору соединения (204 мг), полученного в ссылочном примере 24, в тетрагидрофуране (3 мл) при -78°C и смесь перемешивали при 0°C в течение 30 минут. После охлаждения реакционной смеси снова до -78°C, ее нагревали за 20 минут до комнатной температуры, барботируя диоксид углерода, и реакционную смесь концентрировали при пониженном давлении. Соединение (400 мг), полученное в ссылочном примере 71, моногидрат 1-гидроксибензотриазола (254 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (360 мг) и изопропиламин (0,491 мл) добавляли к раствору полученного остатка в N,N-диметилформамиде (6 мл) при комнатной температуре. После перемешивания в течение 3 суток реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид (30 мл), насыщенный водный раствор (100 мл) гидрокарбоната натрия и воду (100 мл) для разделения жидкостей. Полученный водный слой экстрагировали метиленхлоридом (4 х 15 мл), органические слои объединяли, сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1 → 10:1) и растворяли в смеси 1N хлористоводородная кислота-метанол-метиленхлорид. Затем полученный раствор концентрировали с получением указанного в заголовке соединения (245 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,42 (2H, шир.с), 1,60 (4H, шир.с), 1,84-1,94 (1H, м), 1,94-2,08 (1H, м), 2,97 (2H, шир.с), 3,97-4,13 (2H, м), 4,19 (1H, шир.с), 4,27 (1H, шир.с), 5,03 (2H, с), 7,13 (1H, шир.с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,32 (2H, шир.с), 7,40 (1H, д, J=8,8Гц), 7,68 (1H, д, J=2,0Гц), 8,15 (1H, шир., J=7,3Гц), 8,31 (2H, д, J=5,9Гц), 8,39 (1H, д, J=8,1Гц), 11,90 (1H, с), 14,03 (1H, шир.с).
МС (ESI) m/z: 535 (М+Н)+.
[Пример 21]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогептил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамида
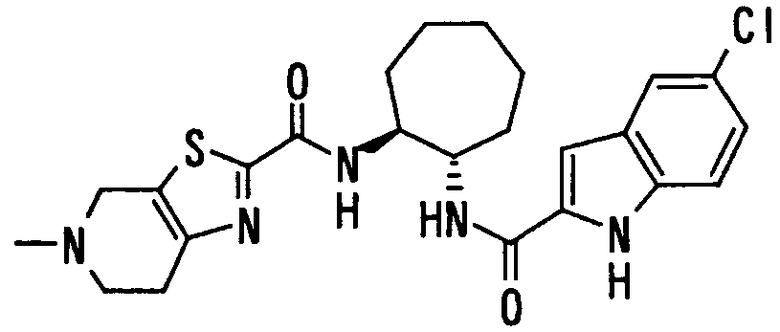
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 74, и соединения, полученного в ссылочном примере 10, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,51-1,55 (4H, м), 1,75-1,80 (6H, м), 2,88 (3H, с), 3,12 (1H, шир.с), 3,35-3,63 (4H, м), 4,10-4,13 (1H, м), 4,29-4,61 (2H, м), 7,06 (1H, с), 7,14 (1H, дд, J=8,8, 2,0Гц), 7,39 (1H, д, J=8,8Гц), 7,67 (1H, д, J=2,0Гц), 8,46 (1H, д, J=8,3Гц), 8,77 (1H, д, J=8,3Гц), 11,21-11,35 (1H, м), 11,71 (1H, с).
МС (ESI) m/z: 486 (M+H)+.
[Пример 22]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклооктил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамида
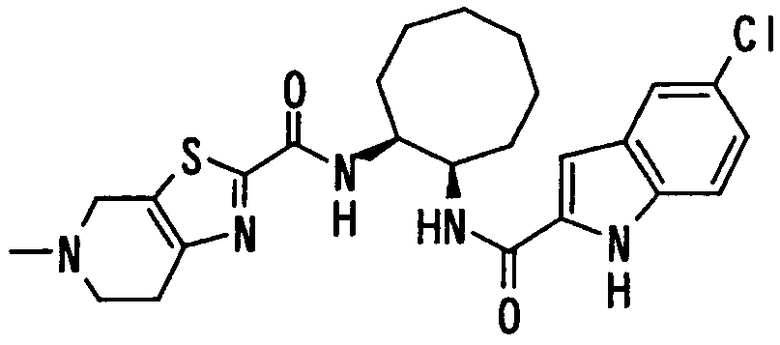
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 78, и соединения, полученного в ссылочном примере 10, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,61-2,06 (12H, м), 2,90 (3H, с), 3,08-3,17 (2H, м), 3,43-3,45 (1H, шир.с), 3,67 (1H, шир.с), 4,43 (3H, шир.с), 4,67 (1H, шир.с), 7,16-7,18 (2H, м), 7,42 (1H, д, J=8,8Гц), 7,70 (1H, с), 8,24 (1H, шир.с), 8,58 (1H, д, J=8,3Гц), 11,43, 11,63 (1H, каждый шир.с), 11,80 (1H, с).
МС (ESI) m/z: 500 (М+Н)+.
[Пример 23]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклопентил)-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамида
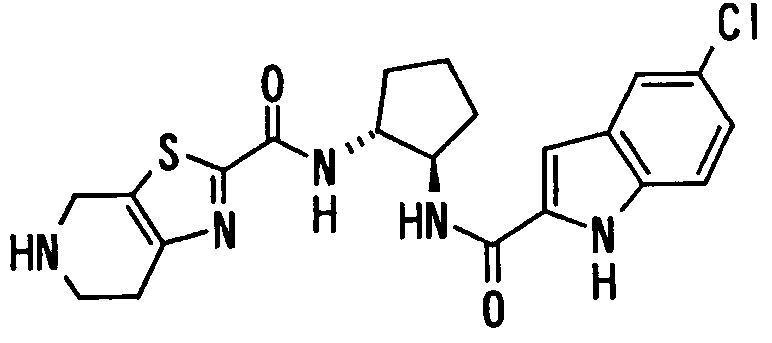
Указанное в заголовке соединение получали обработкой продукта, полученного взаимодействием соединения, полученного в ссылочном примере 63, с соединением, полученным в ссылочном примере 34, хлористоводородной кислотой подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,60-1,82 (4H, м), 1,91-2,15 (2H, м), 3,08 (2H, с), 3,37-3,49 (2H, м), 4,28-4,56 (4H, м), 7,13 (1H, с), 7,15 (1H, д, J=8,8Гц), 7,40 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,61 (1H, д, J=8,3Гц), 8,88 (1H, д, J=8,3Гц), 10,05 (2H, шир.с), 11,82 (1H, с).
МС (FAB) m/z: 444 (М+Н)+.
[Пример 24]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклопентил)-5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамида
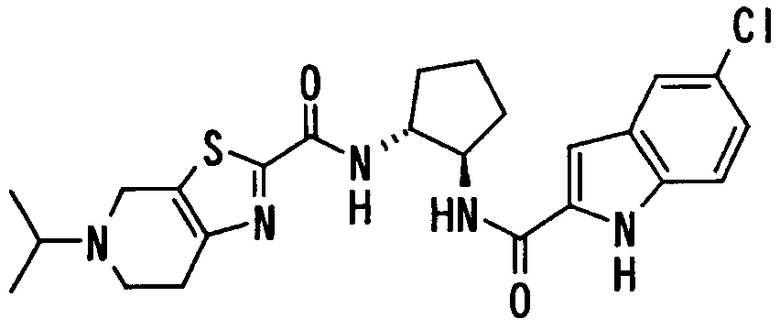
Соединение (30 мг), полученное в примере 23, суспендировали в метиленхлориде (20 мл) и добавляли триэтиламин (260 мкл), перемешивая смесь при комнатной температуре в течение 15 минут. К реакционной смеси добавляли уксусную кислоту (179 мкл) и ацетон (920 мкл) и полученную смесь перемешивали при комнатной температуре в течение 2 минут. К реакционной смеси добавляли триацетоксиборгидрид натрия (796 мг) и смесь перемешивали при комнатной температуре 5 часов. К реакционной смеси добавляли 1N водный раствор (10 мл) гидроксида натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3) с получением бесцветного пенистого вещества. Полученный продукт растворяли в метиленхлориде и добавляли 1N этанольный раствор (1 мл) хлористоводородной кислоты. Раствор концентрировали при пониженном давлении с получением указанного в заголовке соединения (205 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,27-1,39 (6H, м), 1,58-1,80 (4H, м), 1,95-2,10 (2H, м), 3,00-3,12 (1H, м), 3,25-3,45 (2H, м), 3,59-3,77 (2H, м), 4,25-4,39 (1H, м), 4,40-4,55 (2H, м), 4,57-4,65 (1H, м), 7,10 (1H, с), 7,14 (1H, д, J=8,8Гц), 7,38 (1H, д, J=8,8Гц), 7,68 (1H, с), 8,56 (1H, д, J=8,8Гц), 8,90 (1H, д, J=8,8Гц), 11,39 (1H, шир.с), 11,76 (0,5H, с), 11,80 (0,5H, с).
МС (FAB) m/z: 486 (М+Н)+.
[Пример 25]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклопентил)-5-этил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамида
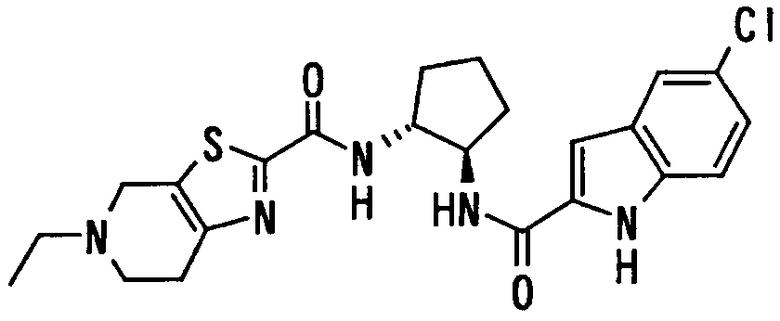
Соединение (500 мг), полученное в примере 23, растворяли в N,N-диметилформамиде (10 мл) и добавляли триэтиламин (576 мкл) и этилиодид (329 мкл), перемешивая смесь в течение ночи при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении, к остатку добавляли воду и отфильтровывали нерастворимое вещество. Полученный продукт очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3) с получением бледно-коричневого пенистого вещества. Полученное вещество суспендировали в 1N хлористоводородной кислоте и суспензию концентрировали при пониженном давлении с получением указанного в заголовке соединения (180 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,32 (3H, т, J=7,1Гц), 1,60-1,80 (4H, м), 1,96-2,10 (2H, м), 3,20-3,39 (5H, м), 3,70-3,80 (1H, м), 4,26-4,58 (3H, м), 4,68-4,79 (1H, м), 7,11 (1H, с), 7,15 (1H, дд, J=8,8, 2,0Гц), 7,39 (1H, д, J=8,8Гц), 7,69 (1H, д, J=1,5Гц), 8,55 (1H, д, J=8,5Гц), 8,92 (1H, д, J=8,5Гц), 11,38 (1H, шир.с), 11,70-11,80 (1H, м).
МС (FAB) m/z: 472 (М+Н)+.
[Пример 26]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклопентил)-5-(1-метилциклопропил)-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-карбоксамида
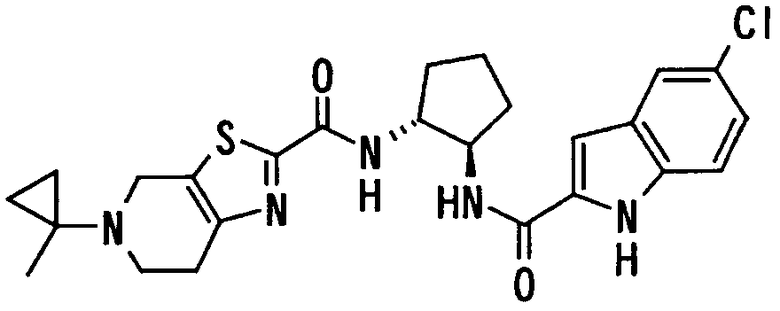
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 63, и соединения, полученного в ссылочном примере 39, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 0,81 (2H, шир.с), 1,20-1,55 (5H, шир.), 1,55-1,80 (4H, м), 1,95-2,12 (2H, м), 3,05-3,40 (2H, шир.), 3,60-3,80 (2H, шир.), 4,25-4,80 (4H, м), 7,10 (1H, с), 7,16 (1H, д, J=8,8Гц), 7,39 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,53 (1H, д, J=8,6Гц), 8,85-8,95 (1H, м), 10,60-10,90 (1H, шир.), 11,73 (1H, шир.с).
МС (FAB) m/z: 498 (M+H)+.
[Пример 27]
Гидрохлорид N-((1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-метоксициклопентил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида (стереоизомер А и стереоизомер В)
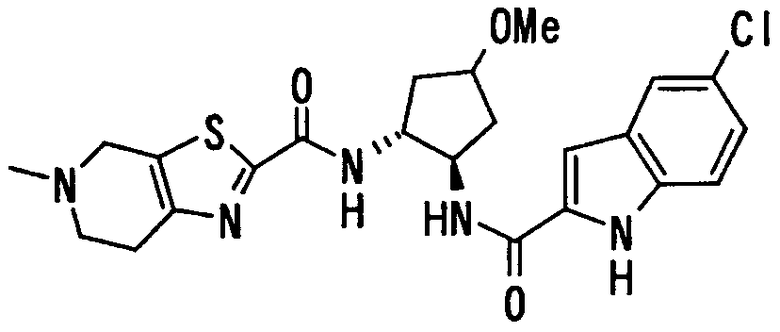
Смесь указанных в заголовке соединений, т.е. стереоизомера А и стереоизомера В, синтезировали конденсацией соединения (смесь стереоизомеров положения 4) (268 мг), полученного в ссылочном примере 82, с соединением, полученным в ссылочном примере 10, подобно способу примера 2. Изомеры выделяли колоночной хроматографией на силикагеле и затем преобразовывали в гидрохлориды с получением указанных в заголовке соединений [стереоизомер А (75 мг) и стереоизомер В (70 мг)].
Стереоизомер А:
1Н-ЯМР (ДМСО-d6) δ: 1,70-2,15 (4H, м), 2,90 (3H, с), 3,00-3,90 (8H, м), 4,10-4,80 (4H, м), 7,08 (1H, с), 7,16 (1H, д, J=8,8Гц), 7,38 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,56 (1H, д, J=8,8Гц), 8,88 (1H, д, J=8,3Гц), 10,96 (1H, шир.с), 11,75 (1H, шир.с).
МС (FAB) m/z: 488 (М+Н)+.
Стереоизомер В:
1Н-ЯМР (ДМСО-d6) δ: 1,60-2,10 (4H, м), 2,89 (3H, с), 3,00-3,70 (7H, м), 3,70-3,90 (1H, м), 4,20-4,80 (4H, м), 7,05-7,20 (2H, м), 7,38 (1H, д, J=8,8Гц), 7,68 (1H, с), 8,59 (1H, д, J=8,3Гц), 8,90 (1H, д, J=8,5Гц), 11,26 (1H, шир.с), 11,74 (1H, шир.с).
МС (FAB) m/z: 488 (M+H)+.
[Пример 28]
Гидрохлорид N-[(1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-(гидроксиметил)циклопентил]-5-(1,1-диметил-2-гидроксиэтил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида (стереоизомер А)
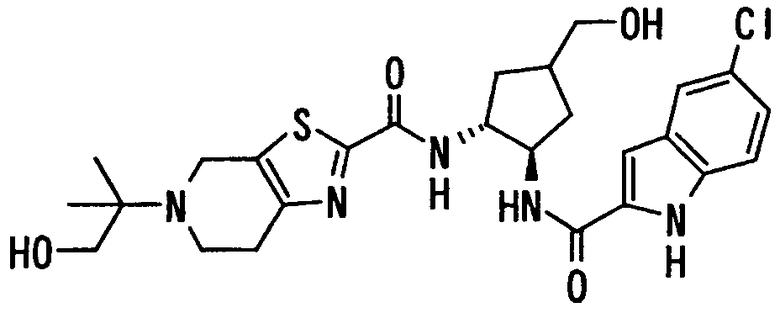
1) Стереоизомеры А и В N-((1R*,2R*)-4-[(бензилокси)метил]-2-{(5-хлориндол-2-ил)карбонил}амино)циклопентил)-5-(2-{[трет-бутил(дифенил)силил]окси}-1,1-диметилэтил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида получали из соединения, полученного в ссылочном примере 85, и соединения, полученного в ссылочном примере 42, подобно способу примера 2.
Стереоизомер А:
1Н-ЯМР (CDCl3) δ: 1,05 (9H, с), 1,168, 1,171 (6H, каждый с), 1,53-1,61 (1H, м), 1,76-1,88 (1H, м), 2,30-2,37 (2H, м), 2,78-2,79 (2H, м), 2,87-2,90 (1H, м), 2,96-3,00 (1H, м), 3,37-3,47 (2H, м), 3,58 (2H, с), 3,96 (1H, кв, J=13,1Гц), 4,41-4,45 (1H, м), 4,51-4,57 (2H, м), 6,88 (1H, д, J=1,5Гц), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,23-7,43 (12H, м), 7,52 (1H, д, J=7,6Гц), 9,37 (1H, шир.с).
Стереоизомер В:
1Н-ЯМР (CDCl3) δ: 1,05 (9H, с), 1,17 (6H, с), 1,43-1,47 (1H, м), 1,85-1,88 (1H, м), 2,09-2,14 (1H, м), 2,58-2,63 (1H, м), 2,78-2,79 (2H, м), 2,86-2,90 (1H, м), 2,96-3,00 (1H, м), 3,38-3,46 (2H, м), 3,59 (2H, с), 3,95 (1H, кв, J=13,3Гц), 4,15-4,20 (1H, м), 4,45-4,56 (3H, м), 6,74 (1H, д, J=2,0Гц), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,27-7,43 (12H, м), 7,57 (1H, д, J=2,0Гц), 9,48 (1H, шир.с).
2) Указанный выше стереоизомер А (288 мг) суспендировали в метиленхлориде (20 мл), добавляли диметилсульфид (1,15 мл) и безводный хлорид алюминия (350 мг) и смесь перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 1N водный раствор (10 мл) гидроксида натрия и смесь экстрагировали метиленхлоридом. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 9:1) с получением 5-(2-{[трет-бутил(дифенил)силил]окси}-1,1-диметилэтил)-N-[(1R*,2R*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-(гидроксиметил)циклопентил]-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида (стереоизомер А) (184 мг).
1Н-ЯМР (CDCl3) δ: 1,04 (9H, с), 1,15 (6H, с), 1,54-1,62 (1H, м), 1,73-1,81 (1H, м), 1,99-2,25 (2H, м), 2,34-2,38 (2H, м), 2,67-2,85 (3H, м), 2,92-2,97 (1H, м), 3,48-3,62 (4H, м), 3,93 (1H, кв, J=15,6Гц), 4,20-4,28 (1H, м), 4,47-4,56 (1H, м), 6,89 (1H, с), 7,11-7,18 (1H, м), 7,24-7,27 (1H, м), 7,32-7,43 (6H, м), 7,54 (1H, д, J=1,7Гц), 7,63 (4H, дд, J=7,8, 1,5Гц), 7,90-7,92 (2H, м), 10,13 (1H, шир.с).
МС (FAB) m/z: 784 (M+H)+.
3) Стереоизомер А (180 мг), полученный на стадии 2), описанной выше, растворяли в 1N тетрагидрофурановом растворе (2 мл) фторида тетрабутиламмония и раствор перемешивали в течение ночи при комнатной температуре. К реакционной смеси добавляли метиленхлорид, 1N водный раствор гидроксида натрия и хлорид натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 19:1). Полученный порошок растворяли в метаноле и добавляли 1N этанольный раствор (229 мкл) хлористоводородной кислоты, затем добавляли этилацетат. Растворитель концентрировали при пониженном давлении с получением указанного в заголовке соединения (63 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,33-1,50 (8H, м), 1,70-1,91 (2H, м), 2,07-2,14 (1H, м), 2,23-2,24 (1H, м), 3,04-3,10 (1H, м), 3,27-3,44 (4H, м), 3,57-3,70 (2H, м), 3,92-3,95 (1H, м), 4,29-4,72 (4H, м), 5,81 (1H, шир.с), 7,11 (1H, с), 7,15 (1H, дд, J=8,6, 2,0Гц), 7,39 (1H, д, J=8,6Гц), 7,68 (1H, д, J=2,0Гц), 8,53-8,56 (1H, м), 8,83 (1H, д, J=8,3Гц), 10,36 (1H, шир.с), 11,75, 11,77 (1H, каждый с).
МС (ESI) m/z: 546 (M+H)+.
[Пример 29]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-4,7,8,10-тетрагидро-6Н-пиразоло[1,2-а]тиазоло[4,5-d]пиридазин-2-карбоксамида
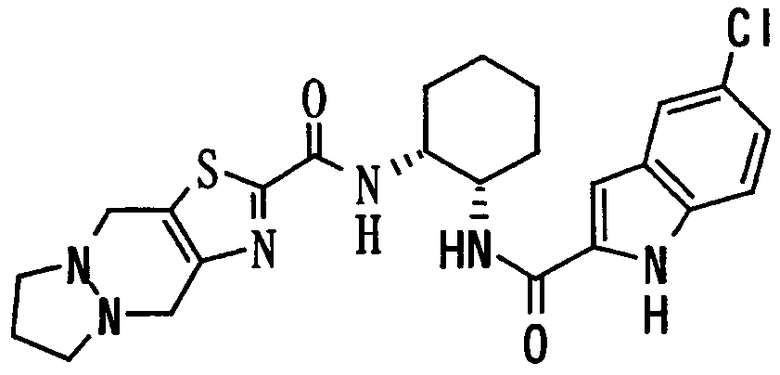
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 71, и соединения, полученного в ссылочном примере 44, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,50 (2H, м), 1,61 (4H, шир.с), 1,80-2,00 (2H, м), 2,27 (2H, шир.с), 2,80-4,80 (10H, м), 7,14 (1H, д, J=1,5Гц), 7,17 (1H, дд, J=8,5, 2,0Гц), 7,41 (1H, д, J=8,5Гц), 7,70 (1H, д, J=2,0Гц), 8,09 (1H, д, J=7,3Гц), 8,44 (1H, шир.с), 11,81 (1H, шир.с).
МС (FAB) m/z: 499 (М+Н)+.
[Пример 30]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-4,6,7,8,9,11-гексагидропиридазино[1,2-а]тиазоло[4,5-d]пиридазин-2-карбоксамида
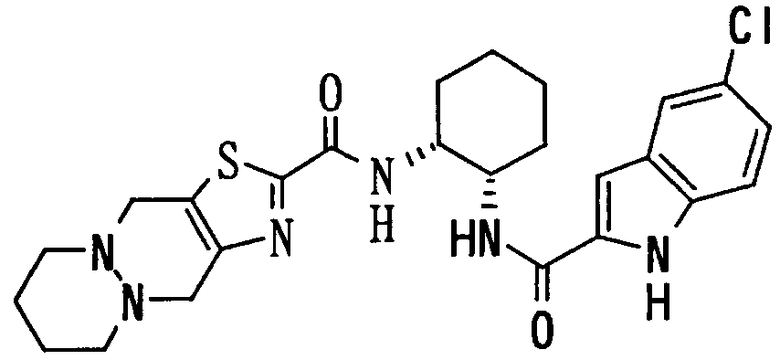
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 46, и соединения, полученного в ссылочном примере 71, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,55 (2H, м), 1,55-2,10 (10H, м), 2,80-4,80 (10H, м), 7,10-7,25 (2H, м), 7,42 (1H, д, J=8,8Гц), 7,72 (1H, д, J=1,7Гц), 8,12 (1H, шир.с), 8,41 (1H, шир.с), 11,83 (1H, шир.с).
МС (FAB) m/z: 513 (М+Н)+.
[Пример 31]
Гидрохлорид 5-хлор-N-{(1R*,2S*)-2-[(5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-илкарбонил)амино]циклогексил}индол-2-карбоксамида
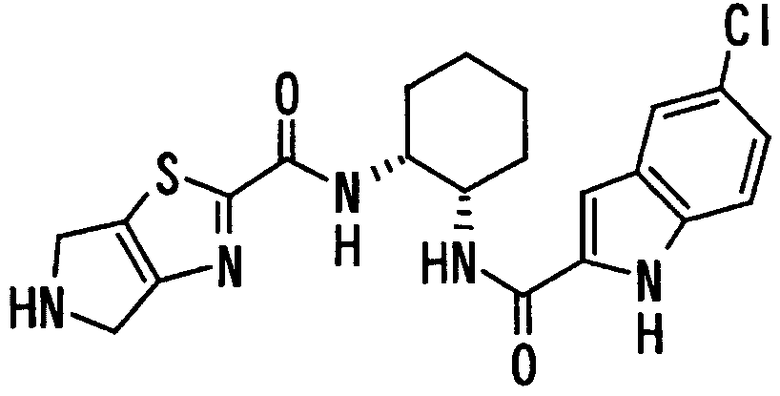
Соединение (171 мг), полученное в ссылочном примере 33, растворяли в диэтиловом эфире (5 мл) в атмосфере аргона, раствор охлаждали до -78°C и добавляли к нему по каплям н-бутиллитий (1,60N гексановый раствор, 385 мкл). Реакционную смесь перемешивали 10 минут при -78°C, барботировали через нее в течение 20 минут диоксид углерода и затем нагревали до комнатной температуры. Реакционную смесь концентрировали при пониженном давлении и остаток растворяли в N,N-диметилформамиде (10 мл). К раствору добавляли соединение (184 мг), полученное в ссылочном примере 71, моногидрат 1-гидроксибензотриазола (76 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (215 мг). Полученную смесь перемешивали в течение 3 суток. Реакционную смесь концентрировали, к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия и отделяли органический слой. Органический слой сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 3:97). К полученному таким образом продукту добавляли этанольный раствор (5 мл) хлористоводородной кислоты, смесь перемешивали при комнатной температуре 1 час и затем реакционную смесь концентрировали. К остатку для его отверждения добавляли этилацетат. Полученный порошок отфильтровывали с получением указанного в заголовке соединения (31 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,52 (2H, м), 1,55-1,80 (4H, м), 1,82-2,05 (2H, м), 4,22 (1H, шир.с), 4,28 (1H, шир.с), 4,38 (2H, с), 4,56 (2H, с), 7,14-7,20 (2H, м), 7,42 (1H, д, J=8,6Гц), 7,71 (1H, д, J=1,7Гц), 8,10 (1H, д, J=7,1Гц), 8,45 (1H, д, J=7,8Гц), 10,10-10,50 (2H, шир.), 11,83 (1H, шир.с).
МС (FAB) m/z: 444 (М+Н)+.
[Пример 32]
трет-Бутил 2-{[((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)амино]карбонил}-5,7-дигидро-6Н-пирроло[3,4-d]пиримидин-6-карбоксилат
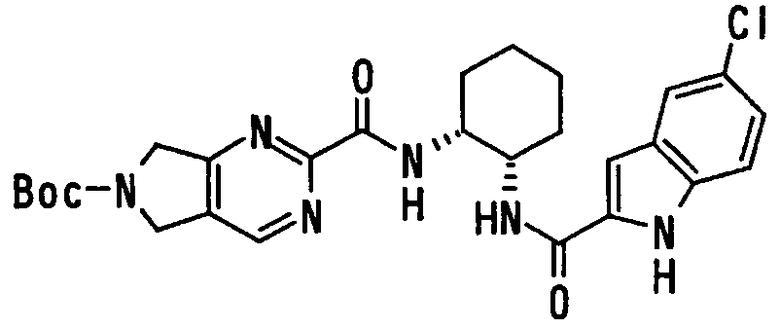
После гидролиза с гидроксидом лития соединения, полученного в ссылочном примере 50, его подвергали взаимодействию с соединением, полученным в ссылочном примере 71, подобно способу примера 2 с получением указанного в заголовке соединения.
1Н-ЯМР (CDCl3) δ: 1,54 (9H, с), 1,55-2,30 (8H, м), 4,23 (1H, шир.с), 4,53 (1H, шир.с), 4,74-4,83 (4H, м), 6,99 (1H, д, J=1,5Гц), 7,19 (1H, дд, J=8,8, 2,1Гц), 7,34 (1H, д, J=8,8Гц), 7,62 (1H, д, J=2,1Гц), 8,11 (1H, шир.с), 8,48-8,53 (1H, шир.), 8,70-8,76 (1H, шир.), 9,60-9,70 (1H, шир.).
МС (ESI) m/z: 539 (M+H)+.
[Пример 33]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-6-метил-6,7-дигидро-5Н-пирроло[3,4-d]пиримидин-2-карбоксамида
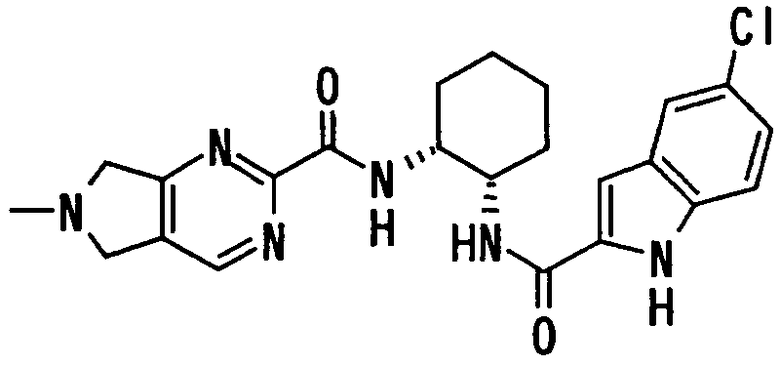
Трифторуксусную кислоту (1 мл) добавляли к раствору соединения (34,0 мг), полученного в примере 32, в метиленхлориде (1 мл) при комнатной температуре и смесь перемешивали в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении, остаток растворяли в метиленхлориде (1 мл) и к раствору добавляли при комнатной температуре триэтиламин (17,6 мкл), уксусную кислоту (7,21 мкл), 35% формалин (8,13 мкл) и триацетоксиборгидрид натрия (20,1 мг). Полученную смесь перемешивали в течение 1 часа. К реакционной смеси добавляли метиленхлорид (10 мл) и насыщенный водный раствор (10 мл) гидрокарбоната натрия для отделения органического слоя. Органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 7:93). К полученному продукту для его отверждения добавляли 1N этанольный раствор хлористоводородной кислоты и этилацетат и полученные твердые частицы отфильтровывали с получением указанного в заголовке соединения (8,0 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,55 (2H, м), 1,55-1,75 (4H, м), 1,80-2,05 (2H, м), 2,98 (3H, шир.с), 4,28 (2H, шир.с), 4,65 (4H, шир.с), 7,14-7,20 (2H, м), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, д, J=2,0Гц), 8,17 (1H, д, J=6,9Гц), 8,65 (1H, д, J=8,3Гц), 8,93 (1H, с), 11,73 (1H, шир.с), 11,82 (1H, шир.с).
МС (FAB) m/z: 453 (М+Н)+.
[Пример 34]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
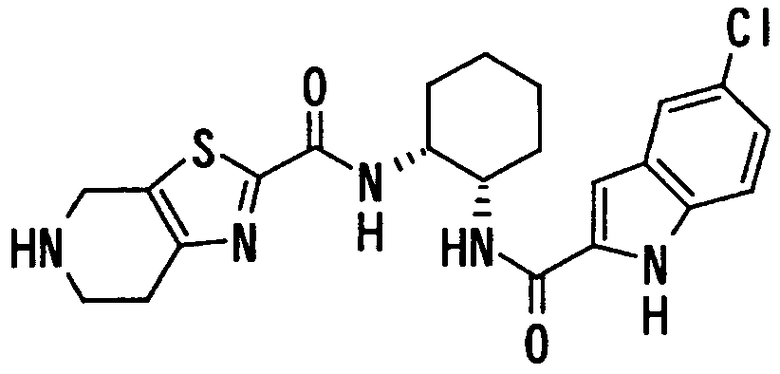
Указанное в заголовке соединение получали обработкой продукта, полученного взаимодействием соединения, полученного в ссылочном примере 71, с соединением, полученным в ссылочном примере 34, хлористоводородной кислотой подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,39-1,52 (2H, м), 1,62 (4H, шир.с), 1,86-2,09 (2H, м), 3,03 (2H, шир.с), 3,40-3,47 (2H, м), 4,17-4,32 (2H, м), 4,44 (2H, с), 7,15 (1H, с), 7,17 (1H, дд, J=8,6, 2,0Гц), 7,41 (1H, д, J=8,6Гц), 7,71 (1H, с), 8,10-8,15 (1H, м), 8,40-8,47 (1H, м), 9,69 (2H, шир.с), 11,85 (1H, с).
МС (FAB) m/z: 458 (M+H)+.
[Пример 35]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-(2-метоксиэтил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
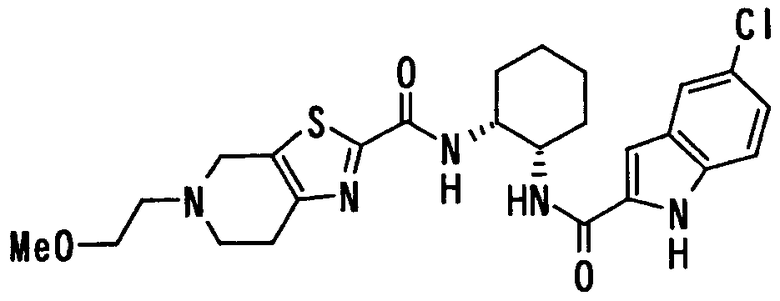
Указанное в заголовке соединение получали из соединения, полученного в примере 34, и 2-метоксиэтилбромида подобно способу примера 25.
1Н-ЯМР (ДМСО-d6) δ: 1,44 (2H, шир.с), 1,62 (4H, шир.с), 1,85-2,10 (2H, м), 2,76-3,21 (6H, м), 3,28 (3H, с), 3,64 (2H, шир.с), 4,00-4,52 (4H, м), 7,14 (1H, с), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,70 (1H, д, J=2,0Гц), 8,08-8,20 (1H, м), 8,36-8,48 (1H, м), 11,84 (1H, с).
МС (FAB) m/z: 516 (M+H)+.
[Пример 36]
Гидрохлорид метил 2-[2-{[((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)амино]карбонил}-6,7-дигидротиазоло[5,4-с]пиридин-5(4Н)-ил]ацетата
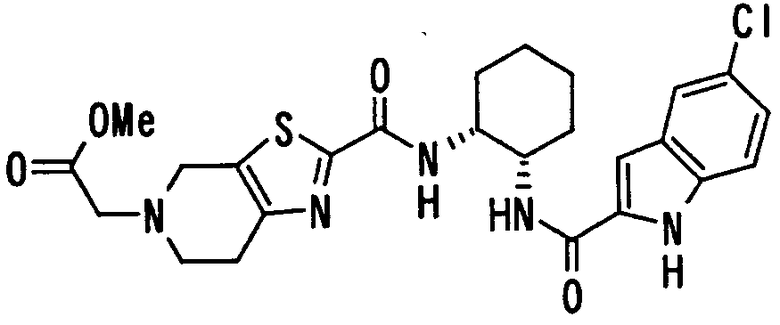
Указанное в заголовке соединение получали из соединения, полученного в примере 34, и метилбромацетата подобно способу примера 25.
1Н-ЯМР (CDCl3) δ: 1,52-1,98 (7H, м), 2,17 (1H, шир.с), 2,87-3,10 (4H, м), 3,49 (2H, с), 3,76 (3H, с), 3,93 (1H, д, J=15,4Гц), 3,99 (1H, д, J=15,4Гц), 4,22 (1H, шир.с), 4,45 (1H, шир.с), 6,86 (1H, д, J=1,2Гц), 7,18 (1H, дд, J=8,8, 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,58-7,63 (2H, м), 7,87 (1H, шир.с), 9,88 (1H, шир.с).
МС (FAB) m/z: 530 (М+Н)+.
[Пример 37]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
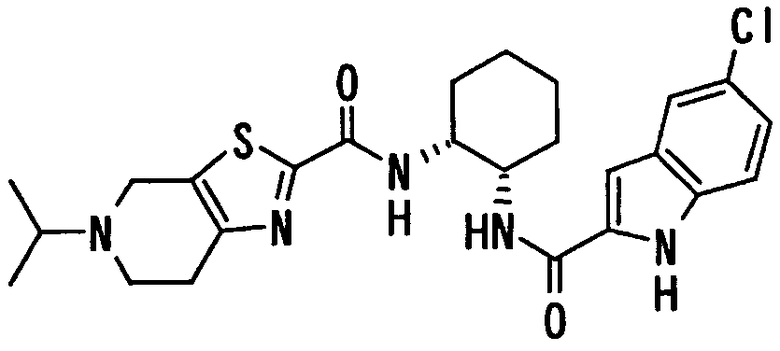
Указанное в заголовке соединение получали из соединения, полученного в примере 34, и ацетона подобно способу примера 24.
1Н-ЯМР (ДМСО-d6) δ: 1,18-1,73 (8H, м), 1,81-2,10 (2H, м), 2,97-3,16 (1H, м), 3,20-3,41 (2H, м), 3,52-3,80 (2H, м), 4,19-4,31 (2H, м), 4,34-4,77 (2H, м), 7,17 (1H, с), 7,18 (1H, дд, J=8,8, 2,0Гц), 7,42 (1H, д, J=8,8Гц), 7,71 (1H, д, J=2,0Гц), 8,15 (1H, шир.с), 8,28-8,51 (1H, м), 11,31 (1H, шир.с), 11,86 (1H, с).
МС (FAB) m/z: 500 (М+Н)+.
[Пример 38]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-(тетрагидро-2Н-пиран-4-ил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
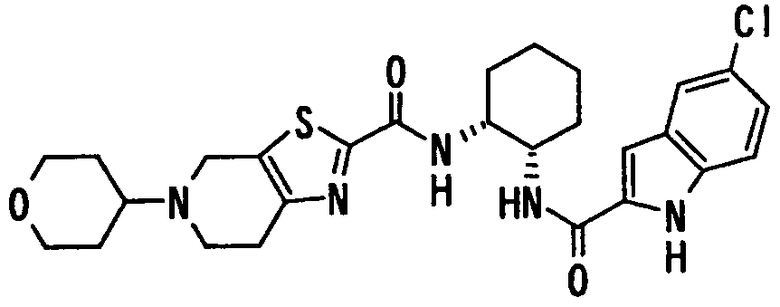
Указанное в заголовке соединение получали из соединения, полученного в примере 34, и тетрагидро-4Н-пиран-4-она подобно способу примера 24.
1Н-ЯМР (ДМСО-d6) δ: 1,30-3,56 (19H, м), 3,70-4,01 (3H, м), 4,17-4,30 (2H, м), 4,32-4,80 (1H, м), 7,15 (1H, с), 7,17 (1H, дд, J=8,6, 2,0Гц), 7,41 (1H, д, J=8,6Гц), 7,71 (1H, д, J=2,0Гц), 8,14 (1H, шир.с), 8,39 (1H, шир.с), 11,84 (1H, с).
МС (FAB) m/z: 542 (M+H)+.
[Пример 39]
трет-Бутил 2-[2-{[((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)амино]карбонил}-6,7-дигидротиазоло[5,4-с]пиридин-5(4Н)-ил]этилкарбамат
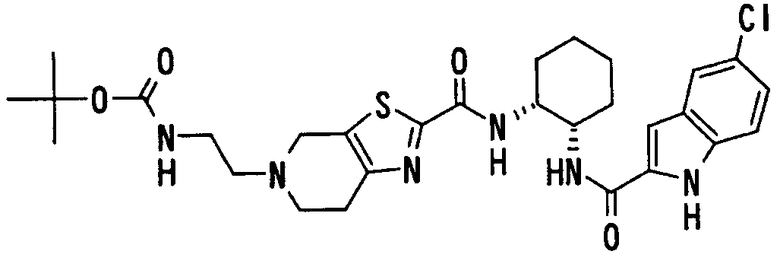
Указанное в заголовке соединение получали из соединения, полученного в примере 34, и N-(трет-бутоксикарбонил)аминоацетальдегида (J. Org. Chem., 1988, Vol. 53, p. 3457) подобно способу примера 24.
1Н-ЯМР (CDCl3) δ: 1,44 (9H, с), 1,54-1,98 (7H, м), 2,10-2,20 (1H, м), 2,74 (2H, шир.с), 2,92 (4H, шир.с), 3,34 (2H, шир.с), 3,84 (2H, шир.с), 4,21 (1H, шир.с), 4,45 (1H, шир.с), 6,86 (1H, с), 7,19 (1H, дд, J=8,8, 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,57-7,63 (2H, м), 7,81 (1H, шир.с), 9,66 (1H, шир.с).
МС (FAB) m/z: 601 (М+Н)+.
[Пример 40]
Гидрохлорид 5-(2-аминоэтил)-N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
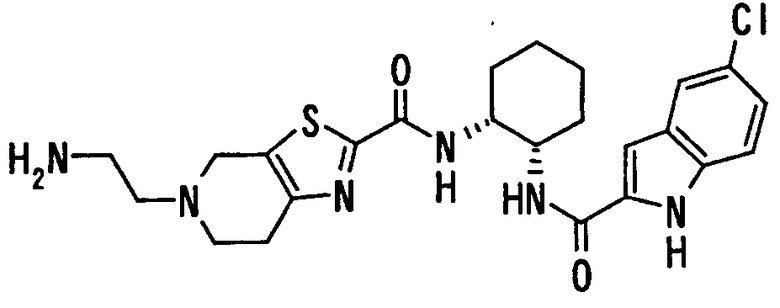
Соединение (450 мг), полученное в примере 39, растворяли в метиленхлориде (5 мл), добавляли насыщенный этанольный раствор (30 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 1 минуты. Реакционную смесь концентрировали при пониженном давлении, к остатку добавляли этилацетат и выпавшие в осадок твердые частицы отфильтровывали с получением указанного в заголовке соединения (367 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,38-1,50 (2H, м), 1,61 (4H, шир.с), 1,85-2,08 (2H, м), 3,00-4,62 (12H, м), 7,14 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, д, J=2,0Гц), 8,12 (1H, д, J=6,6Гц), 8,15-8,68 (4H, м), 11,85 (1H, с).
МС (FAB) m/z: 501 (М+Н)+.
[Пример 41]
Гидрохлорид N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-{2-[(метилсульфонил)амино]этил}-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
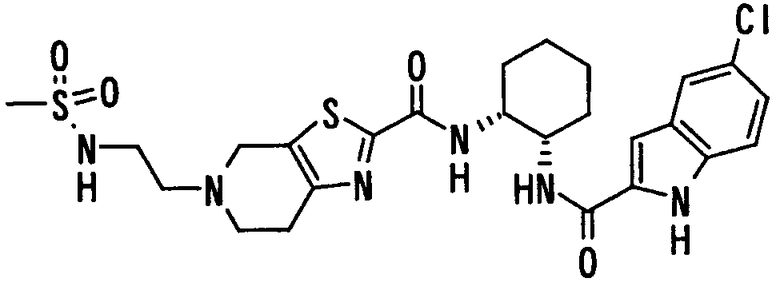
Соединение (110 мг), полученное в примере 40, растворяли в пиридине (3 мл), добавляли метансульфонилхлорид (30 мкл) и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении и добавляли смешанный растворитель метиленхлорид/метанол (85:15) и воду для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3) с получением бледно-желтого пенистого вещества. Полученный продукт суспендировали в 1N хлористоводородной кислоте (0,3 мл) и суспензию концентрировали при пониженном давлении с получением указанного в заголовке соединения (63 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,38-1,50 (2H, м), 1,55-1,70 (4H, м), 1,86-2,05 (2H, м), 2,97 (3H, с), 3,02-3,25 (2H, м), 3,30-3,60 (5H, м), 3,78 (1H, шир.с), 4,18-4,30 (2H, м), 4,45-4,86 (2H, м), 7,14 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,40 (1H, д, J=8,8Гц), 7,41 (1H, шир.с), 7,69 (1H, д, J=2,0Гц), 8,09 (1H, шир.с), 8,43 (1H, шир.с), 11,18 (1H, шир.с), 11,82 (1H, с).
МС (FAB) m/z: 579 (M+H)+.
[Пример 42]
Гидрохлорид метил 2-[2-{[((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)амино]карбонил}-6,7-дигидротиазоло[5,4-с]пиридин-5(4Н)-ил]этилкарбамата
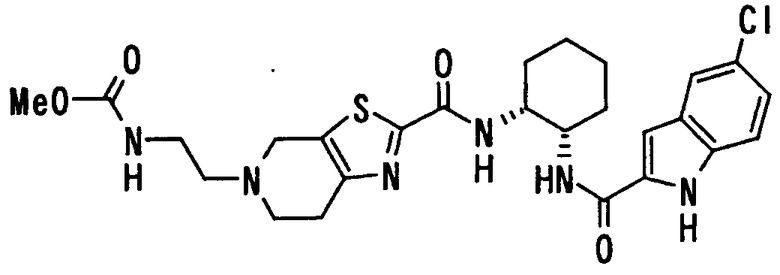
Соединение (144 мг), полученное в примере 40, растворяли в пиридине (3 мл), добавляли триэтиламин (138 мкл) и смесь перемешивали при комнатной температуре в течение 5 минут. К полученному раствору добавляли по каплям раствор, полученный добавлением трифосгена (49 мг) к тетрагидрофурану (1 мл), содержащему метанол (20 мкл). После перемешивания в течение 1 часа реакционную смесь концентрировали при пониженном давлении и остаток растворяли в смешанном растворителе метиленхлорид/метанол (9:1). К раствору добавляли воду для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3) с получением бесцветного пенистого вещества. Полученный продукт суспендировали в 1N хлористоводородной кислоте (0,2 мл) и суспензию концентрировали при пониженном давлении с получением указанного в заголовке соединения (60 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,38-1,50 (2H, м), 1,61 (4H, шир.с), 1,85-2,04 (2H, м), 2,80-3,49 (8H, м), 3,52 (3H, с), 3,62-4,91 (4H, м), 7,14 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,37 (1H, шир.с), 7,40 (1H, д, J=8,8Гц), 7,70 (1H, с), 8,11 (1H, д, J=6,8Гц), 8,40 (1H, шир.с), 11,05 (1H, шир.с), 11,82 (1H, шир.с).
МС (FAB) m/z: 559 (М+Н)+.
[Пример 43]
Гидрохлорид 5-[2-(ацетиламино)этил]-N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
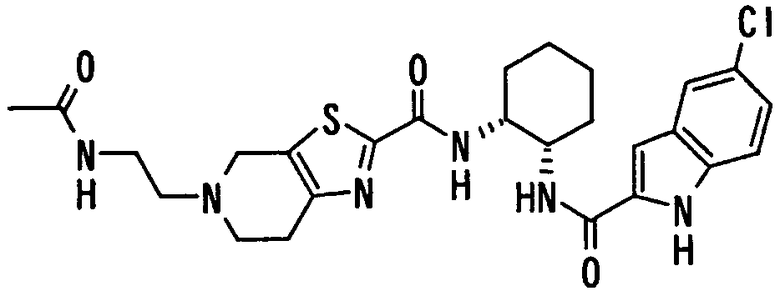
Соединение (90 мг), полученное в примере 40, растворяли в N,N-диметилформамиде (3 мл), добавляли триэтиламин (65 мкл) и уксусный ангидрид (22 мкл) и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид и 0,3N водный раствор гидроксида натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3) с получением бесцветного пенистого вещества. Полученный продукт суспендировали в 1N хлористоводородной кислоте (0,3 мл) и суспензию концентрировали при пониженном давлении с получением указанного в заголовке соединения (73 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,39-1,52 (2H, м), 1,54-1,70 (4H, м), 1,83 (3H, с), 1,84-2,06 (2H, м), 3,02-3,87 (8H, м), 4,16-4,32 (2H, м), 4,40-4,52 (1H, м), 4,78-4,88 (1H, м), 7,14 (1H, с), 7,16 (1H, д, J=8,6Гц), 7,40 (1H, д, J=8,6Гц), 7,70 (1H, с), 8,07-8,17 (1H, м), 8,22-8,30 (1H, м), 8,38-8,52 (1H, м), 11,14 (1H, шир.с), 11,83 (1H, с).
МС (FAB) m/z: 543 (М+Н)+.
[Пример 44]
N-((1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}циклогексил)-5-(2-гидроксиэтил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
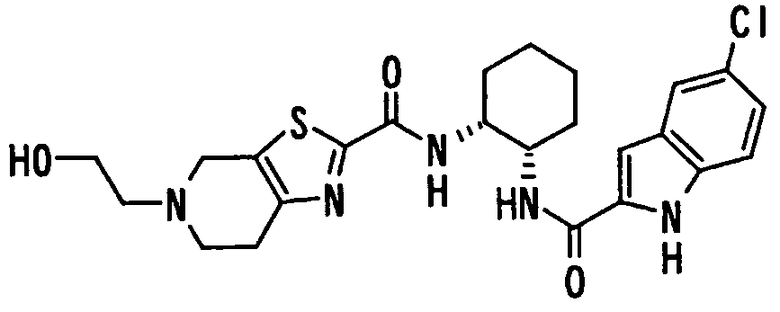
Указанное в заголовке соединение получали из соединения, полученного в примере 34, и 2-бромэтанола подобно способу примера 25.
1Н-ЯМР (ДМСО-d6) δ: 1,37-1,69 (6H, м), 1,86-2,03 (2H, м), 2,54-2,61 (2H, м), 2,75-2,86 (4H, м), 3,52-3,59 (2H, м), 3,75 (2H, с), 4,47 (1H, т, J=5,4Гц), 7,12 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,40 (1H, д, J=8,8Гц), 7,70 (1H, с), 8,05-8,13 (1H, м), 8,28-8,35 (1H, м), 11,78 (1H, с).
МС (FAB) m/z: 502 (M+H)+.
[Пример 45]
Гидрохлорид 5-бутил-N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
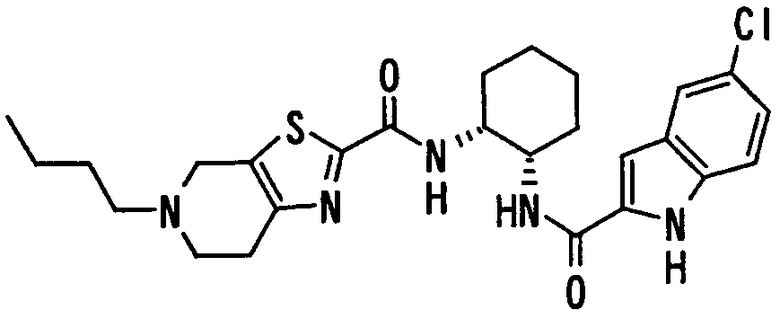
Указанное в заголовке соединение получали из соединения, полученного в примере 34, и н-бромбутана подобно способу примера 25.
1Н-ЯМР (ДМСО-d6) δ: 0,88 (3H, т, J=7,2Гц), 1,20-1,70 (10H, м), 1,87-2,05 (2H, м), 2,55-3,40 (8H, м), 4,16-4,30 (2H, м), 7,13 (1H, с), 7,16 (1H, д, J=8,8Гц), 7,40 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,05-8,14 (1H, м), 8,35 (1H, шир.с), 11,81 (1H, с).
МС (FAB) m/z: 514 (М+Н)+.
[Пример 46]
5-Ацетил-N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
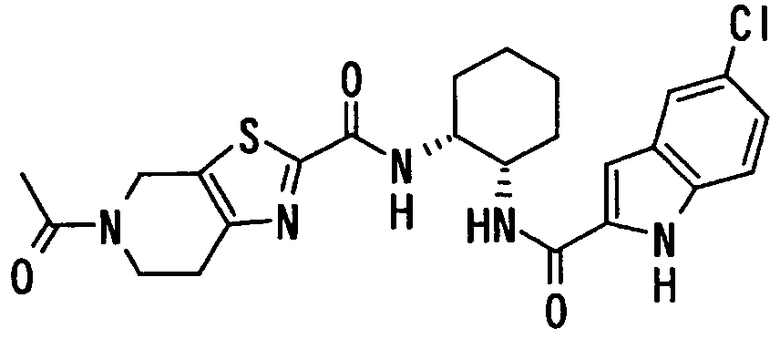
Соединение (100 мг), полученное в примере 34, растворяли в N,N-диметилформамиде (3 мл), добавляли триэтиламин (84 мкл) и уксусный ангидрид (29 мкл) и смесь перемешивали при комнатной температуре в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид и 1N хлористоводородную кислоту для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3) с получением указанного в заголовке соединения (86 мг).
1Н-ЯМР (CDCl3) δ: 1,52-1,85 (5H, м), 1,91 (2H, шир.с), 2,10-2,28 (4H, м), 2,77-3,00 (2H, м), 3,70-4,00 (2H, м), 4,19-4,38 (1H, м), 4,45 (1H, шир.с), 4,68-4,99 (2H, м), 6,85 (1H, с), 7,17-7,22 (1H, м), 7,30-7,39 (1H, м), 7,50-7,84 (3H, м), 9,72-10,05 (1H, м).
МС (FAB) m/z: 500 (М+Н)+.
[Пример 47]
N-((1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}циклогексил)-5-(метилсульфонил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
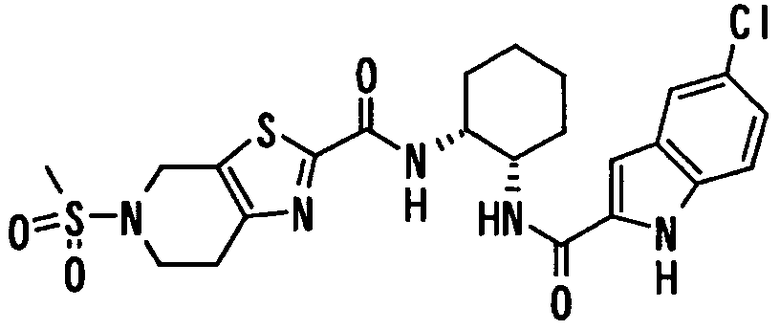
Соединение (100 мг), полученное в примере 34, растворяли в пиридине (3 мл), добавляли триэтиламин (168 мкл) и метансульфонилхлорид (48 мкл) и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид и 1N хлористоводородную кислоту для отделения органического слоя. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:1) с получением указанного в заголовке соединения (79 мг).
1Н-ЯМР (CDCl3) δ: 1,50-1,82 (5H, м), 1,90 (2H, шир.с), 2,13 (1H, шир.с), 2,89 (3H, с), 2,91-2,98 (2H, м), 3,60-3,70 (2H, м), 4,30 (1H, шир.с), 4,44 (1H, шир.с), 4,58 (2H, с), 6,87 (1H, с), 7,19 (1H, д, J=8,8Гц), 7,34 (1H, д, J=8,8Гц), 7,61 (3H, шир.с), 9,91 (1H, шир.с).
МС (FAB) m/z: 536 (М+Н)+.
[Пример 48]
Гидрохлорид 5-метил-N-((1R*,2S*)-2-{[(5-метилиндол-2-ил)карбонил]амино}циклогексил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
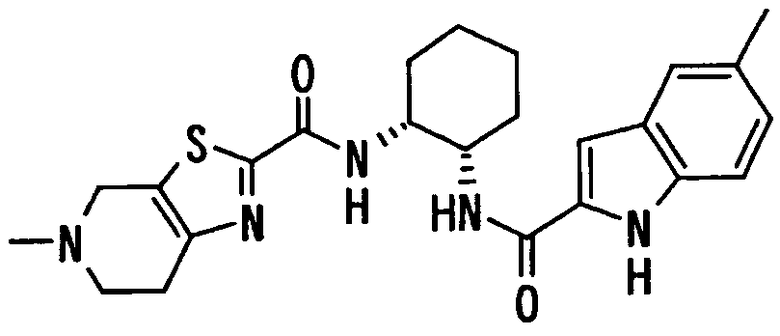
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 67, и 5-метилиндол-2-карбоновой кислоты подобно способу примера 5.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,50 (2H, м), 1,50-1,80 (4H, м), 1,85-2,07 (2H, м), 2,36 (3H, с), 2,88 (3H, с), 3,12 (2H, шир.с), 3,53 (2H, шир.с), 4,15-4,30 (2H, м), 4,30-4,80 (2H, шир.), 7,00 (1H, дд, J=8,4, 1,5Гц), 7,05 (1H, д, J=1,5Гц), 7,30 (1H, д, J=8,4Гц), 7,38 (1H, с), 8,00 (1H, д, J=7,3Гц), 8,43 (1H, шир.с), 11,45 (1H, шир.с), 11,49 (1H, шир.с).
МС (FAB) m/z: 452 (М+Н)+.
[Пример 49]
Этил (1R*,3S*,4R*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
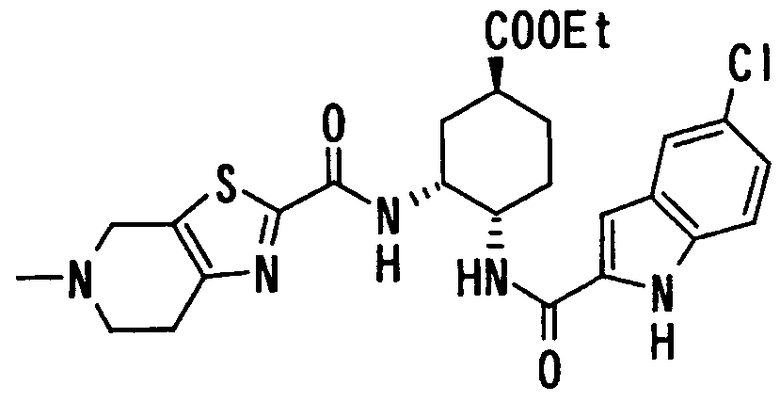
Соединение (1,40 г), полученное в ссылочном примере 91, суспендировали в этаноле (8 мл), добавляли при комнатной температуре насыщенный этанольный раствор (10 мл) хлористоводородной кислоты и смесь перемешивали 12 часов. Растворитель отгоняли при пониженном давлении с получением гидрохлорида этил (1R*,3S*,4R*)-3-амино-4-{[(5-хлориндол-2-ил)карбонил]амино}циклогексанкарбоксилата (1,25 г).
Указанное в заголовке соединение получали из описанного выше продукта и соединения, полученного в ссылочном примере 10, подобно способу примера 2.
1Н-ЯМР (CDCl3) δ: 1,29 (3H, т, J=7,1Гц), 1,52-1,80 (2H, м), 2,03-2,37 (4H, м), 2,53 (3H, с), 2,57-2,71 (1H, м), 3,73 и 3,78 (всего 1H, каждый д, J=14,4Гц), 4,08-4,17 (1H, м), 4,18 (2H, кв, J=7,2Гц), 4,55-4,65 (1H, м), 6,85 (1H, шир.с), 7,21 (1H, дд, J=8,8, 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,48 (1H, д, J=7,6Гц), 7,63 (1H, д, J=2,0Гц), 7,98 (1H, д, J=7,6Гц), 9,30 (1H, с).
МС (ESI) m/z: 544 (М+Н)+.
[Пример 50]
Этил (1S,3R,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
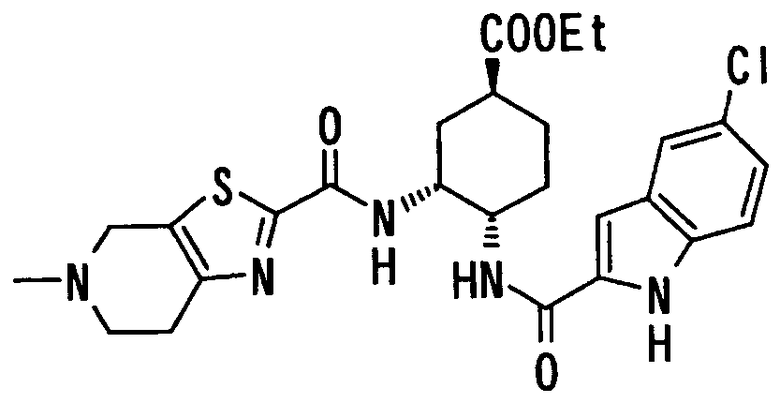
Соединение (4,2 г), полученное в ссылочном примере 97, суспендировали в этаноле (25 мл), добавляли при комнатной температуре насыщенный этанольный раствор (55 мл) хлористоводородной кислоты и смесь перемешивали в течение 11 часов. Растворитель отгоняли при пониженном давлении с получением бесцветных твердых частиц (4,15 г).
Полученный продукт (4,15 г) растворяли в N,N-диметилформамиде (40 мл), к полученному раствору при комнатной температуре добавляли соединение (2,86 г), полученное в ссылочном примере 10, моногидрат 1-гидроксибензотриазола (1,72 г) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (2,15 г) и смесь перемешивали в течение 39 часов. Реакционную смесь концентрировали при пониженном давлении, к остатку добавляли воду и смесь экстрагировали хлороформом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 100:1) с получением указанного в заголовке соединения (1,71 г).
[α]D = -94° (С=1,0, хлороформ).
[Пример 51]
Метил (1R*,3R*,4S*)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
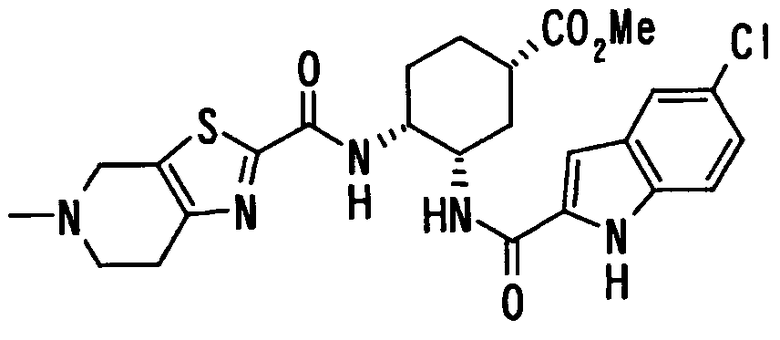
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 107, этанольным раствором хлористоводородной кислоты и затем конденсацией данного соединения с соединением, полученным в ссылочном примере 10, подобно способу примера 49.
1Н-ЯМР (ДМСО-d6) δ: 1,55-1,80 (3H, м), 1,80-2,20 (3H, м), 2,60-2,75 (1H, м), 2,92 (3H, с), 3,15-3,30 (1H, м), 3,30-3,50 (4H, м), 3,57 (3H, с), 3,55-3,70 (1H, м), 4,20-4,30 (1H, м), 4,30-4,40 (1H, м), 7,02 (1H, с), 7,17 (1H, дд, J=8,5, 2,0Гц), 7,41 (1H, д, J=8,5Гц), 7,71 (1H, с), 8,20-8,35 (1H, м), 8,35-8,45 (1H, м), 11,82 (1H, шир.).
МС (FAB) m/z: 530 (М+Н)+.
[Пример 52]
Этил (1R*,3S*,4R*)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
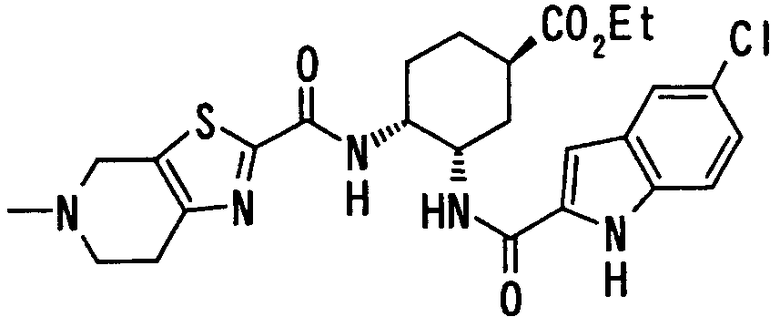
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 98, насыщенным этанольным раствором хлористоводородной кислоты и затем конденсацией его с 5-хлориндол-2-карбоновой кислотой подобно способу примера 49.
1Н-ЯМР (CDCl3) δ: 1,29 (3H, т, J=7,1Гц), 1,82-2,30 (6H, м), 2,49 (3H, с), 2,62-2,73 (1H, м), 3,74-3,85 (2H, м), 3,85-3,93 (2H, м), 3,71 (2H, с), 4,12-4,29 (3H, м), 4,49-4,59 (1H, м), 6,89 (1H, шир.с), 7,21 (1H, дд, J=8,8, 2,0Гц), 7,32 (1H, д, J=8,8Гц), 7,33 (1H, шир.с), 7,41 (1H, шир.с), 7,62 (1H, шир.с), 9,37 (1H, с).
МС (ESI) m/z: 544 (M+H)+.
[Пример 53]
Метил (1R*,3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
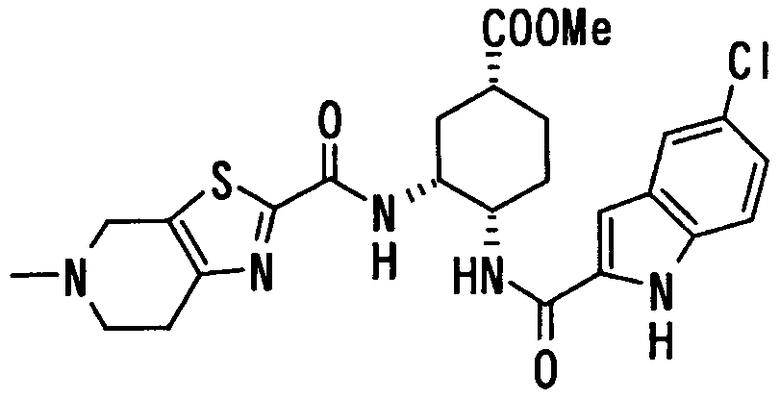
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 106, 4N диоксановым раствором хлористоводородной кислоты и затем конденсацией его с 5-хлориндол-2-карбоновой кислотой подобно способу примера 49.
1Н-ЯМР (ДМСО-d6) δ: 1,65-1,80 (3H, м), 1,80-2,10 (2H, м), 2,15-2,25 (1H, м), 2,55-2,70 (1H, м), 2,89 (3H, с), 3,05-3,20 (1H, м), 3,30-3,50 (4H, м), 3,55-3,65 (1H, м), 3,62 (3H, с), 4,20-4,30 (1H, м), 4,35-4,45 (1H, м), 7,19 (1H, дд, J=8,8, 1,2Гц), 7,23 (1H, с), 7,43 (1H, д, J=8,8Гц), 7,73 (1H, с), 8,03 (1H, д, J=6,8Гц), 8,73 (1H, д, J=8,5Гц), 11,15-11,38 (1H, шир.), 11,85 (1H, с).
МС (FAB) m/z: 530 (M+H)+.
[Пример 54]
Метил (1R,3R,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
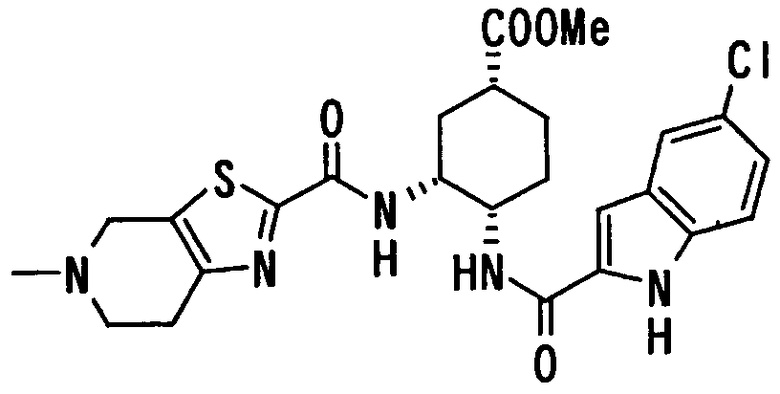
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 112, 4N диоксановым раствором хлористоводородной кислоты и затем конденсацией его с 5-хлориндол-2-карбоновой кислотой подобно способу примера 49.
1Н-ЯМР (ДМСО-d6) δ: 1,67-1,76 (3H, м), 1,88-1,91 (1H, м), 2,01 (1H, шир.с), 2,13-2,22 (1H, м), 2,52-2,67 (4H, м), 2,86 (2H, шир.с), 3,04 (2H, шир.с), 3,33-3,41 (1H, м), 3,61 (3H, с), 4,22-4,36 (3H, м), 7,17-7,22 (2H, м), 7,42 (1H, д, J=8,8Гц), 7,72 (1H, с), 8,00 (1H, д, J=6,9Гц), 8,68 (1H, д, J=8,6Гц), 11,80 (1H, с).
МС (FAB) m/z: 530 (М+Н)+.
[Пример 55]
N-(1R*,2S*,5S*)-5-(Аминокарбонил)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
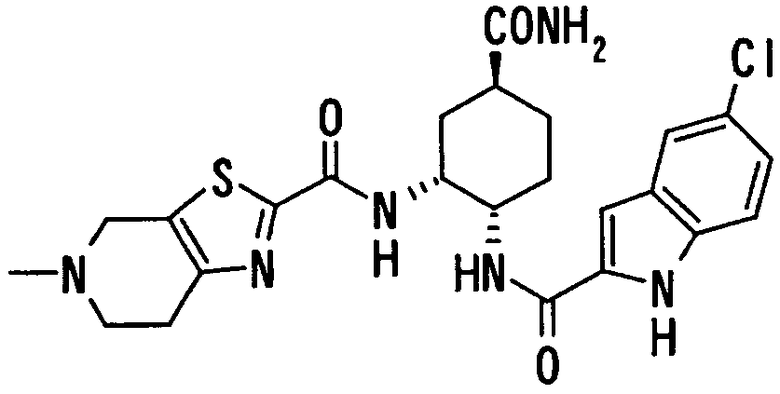
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 113, 4N диоксановым раствором хлористоводородной кислоты и затем конденсацией его с соединением, полученным в ссылочном примере 10.
1Н-ЯМР (CDCl3) δ: 0,78-2,40 (7H, м), 2,53 (3H, с), 2,80-2,89 (1H, м), 2,91-3,00 (1H, м), 3,68-3,76 (2H, м), 4,08-4,19 (1H, м), 4,54-4,65 (1H, м), 6,80 (1H, шир.с), 7,21 (1H, дд, J=8,4, 1,6Гц), 7,33 (1H, д, J=8,4Гц), 7,38-7,43 (1H, м), 7,49-7,55 (1H, м), 7,63 (1H, шир.с), 9,14 (1H, шир.с).
МС (ESI) m/z: 515 (М+Н)+.
[Пример 56]
(1R*,3S*,4R*)-4-{[(5-Хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоновая кислота
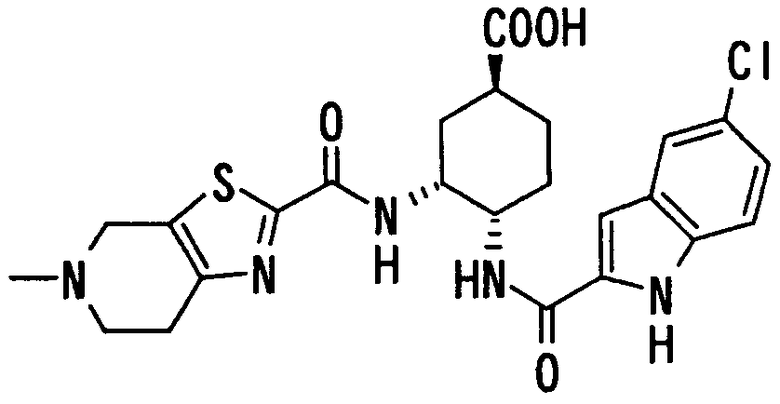
Соединение (916 мг), полученное в примере 49, суспендировали в смешанном растворителе из этанола (10 мл) и тетрагидрофурана (8 мл), добавляли при комнатной температуре 1N водный раствор (3,3 мл) гидроксида натрия и смесь перемешивали в течение 12 часов при той же температуре. После добавления 1N хлористоводородной кислоты (3,3 мл) отгоняли при пониженном давлении растворитель и остаток промывали водой и диэтиловым эфиром с получением указанного в заголовке соединения (712 мг).
[Пример 57]
Гидрохлорид N-{(1R*,2S*,5S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
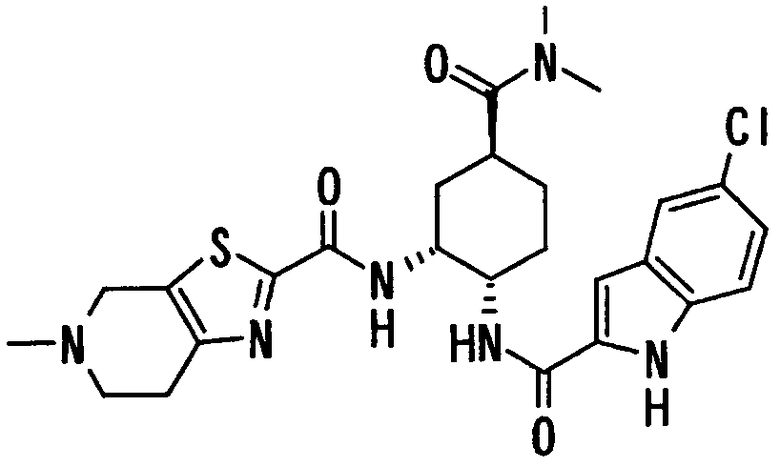
Триэтиламин (0,25 мл), гидрохлорид диметиламина (133 мг), моногидрат 1-гидроксибензотриазола (53 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (75 мг) добавляли к суспензии в хлороформе (10 мл) соединения (168 мг), полученного в ссылочном примере 56, и смесь перемешивали в течение 72 часов. Растворитель отгоняли при пониженном давлении, к остатку добавляли воду и экстрагировали хлороформом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 93:7). Полученные таким образом бесцветные твердые частицы (135 мг) суспендировали в этаноле (5 мл) и к полученной суспензии добавляли 1N этанольный раствор (0,5 мл) хлористоводородной кислоты. Смесь перемешивали 2 часа и отгоняли растворитель с получением указанного в заголовке соединения (112 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,42-2,07 (6H, м), 2,73-3,70 (10H, м), 2,88 (3H, с), 2,97 (3H, с), 4,03-4,20 (1H, м), 4,51-4,67 (1H, м), 7,04 (1H, шир.с), 7,16 (1H, шир., J=8,8Гц), 7,41 (1H, д, J=8,8Гц), 7,68 (1H, шир.с), 8,32-8,47 (2H, м), 10,76 (1H, шир.с).
МС (ESI) m/z: 543 (M+H)+.
[Пример 58]
(1S,3R,4S)-4-{[(5-Хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоновая кислота
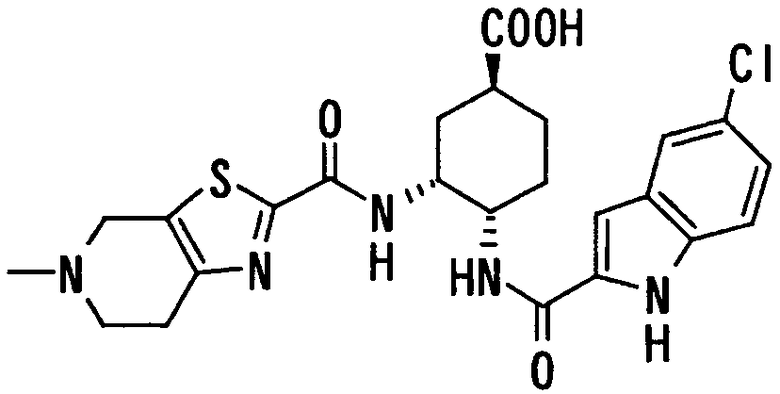
Соединение (1,6 г), полученное в примере 50, суспендировали в смешанном растворителе из этанола (20 мл) и тетрагидрофурана (15 мл), добавляли при комнатной температуре 1N водный раствор (5,9 мл) гидроксида натрия и смесь перемешивали 12 часов при той же температуре. После добавления 1N хлористоводородной кислоты (5,9 мл) отгоняли при пониженном давлении растворитель и остаток промывали водой и диэтиловым эфиром с получением указанного в заголовке соединения (1,19 г).
Т.пл. 234-236оС.
[α]D = -57°C (С=1,0, метанол).
[Пример 59]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(циклопропиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
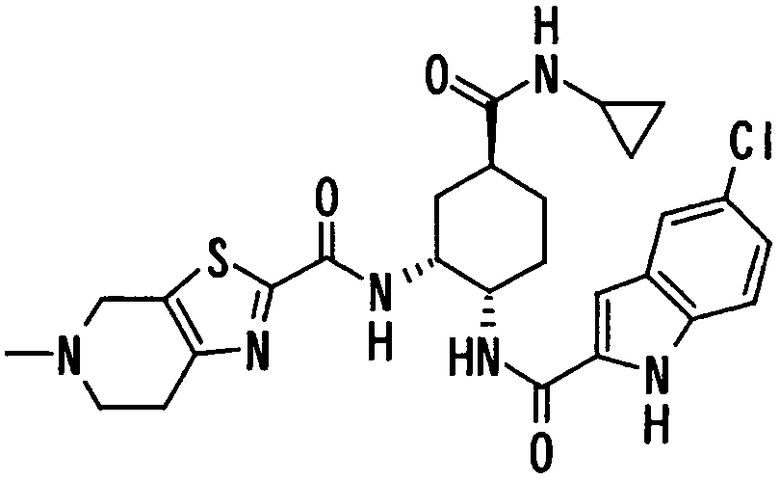
Указанное в заголовке соединение получали из соединения, полученного в примере 58, и циклопропиламина подобно способу примера 57.
1Н-ЯМР (ДМСО-d6) δ: 0,32-0,40 (2H, м), 0,53-0,63 (2H, м), 1,50-2,10 (6H, м), 2,25-2,40 (1H, м), 2,45-2,70 (2H, м), 2,91 (3H, с), 3,05-3,80 (3H, м), 4,05-4,17 (1H, м), 4,30-4,55 (2H, м), 4,55-4,80 (1H, м), 7,03 (1H, д, J=1,5Гц), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,68 (1H, д, J=2,0Гц), 7,86 (1H, шир., J=3,4Гц), 8,06 (1H, шир.с), 8,40 (1H, шир., J=7,6Гц), 11,20-11,60 (1H, шир.), 11,79 (1H, с).
МС (FAB) m/z: 555 (M+H)+.
[Пример 60]
Гидрохлорид N-[(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-(пирролидин-1-илкарбонил)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
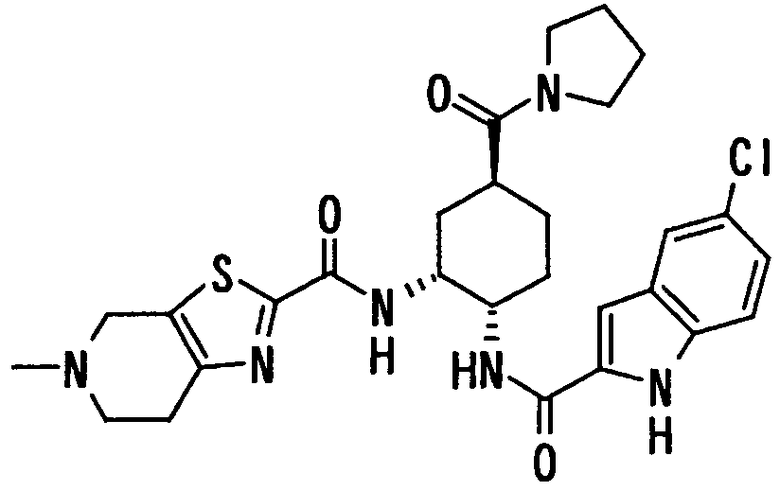
Указанное в заголовке соединение получали из соединения, полученного в примере 58, и пирролидина подобно способу примера 57.
1Н-ЯМР (ДМСО-d6) δ: 1,45-2,10 (10H, м), 2,75-2,90 (2H, м), 2,90 (3H, с), 3,10-3,70 (H, м), 4,05-4,20 (1H, м), 4,25-4,80 (3H, м), 7,05 (1H, с), 7,17 (1H, д, J=8,7Гц), 7,41 (1H, д, J=8,7Гц), 7,69 (1H, с), 8,32 (1H, шир. J=7,6Гц), 8,38 (1H, шир., J=7,1Гц), 11,22 (1H, шир.с), 11,78 (1H, с).
МС (FAB) m/z: 569 (M+H)+.
[Пример 61]
Гидрохлорид N-[(1R*,2S*,5S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-(4-морфолинилкарбонил)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
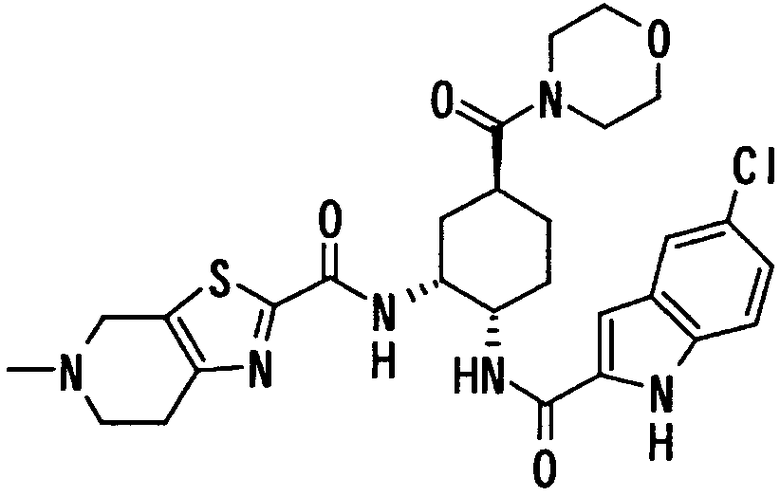
Указанное в заголовке соединение получали из соединения, полученного в примере 56, и морфолина подобно способу примера 57.
1Н-ЯМР (ДМСО-d6) δ: 1,40-2,05 (6H, м), 2,75-3,70 (18H, м), 4,02-4,17 (1H, м), 4,55-4,69 (1H, м), 7,05 (1H, шир.с), 7,17 (1H, шир., J=8,8Гц), 7,41 (1H, д, J=8,8Гц), 7,67 (1H, шир.с), 8,35 (1H, д, J=7,6Гц), 8,40 (1H, д, J=7,6Гц), 10,79 (1H, шир.с).
МС (ESI) m/z: 585 (M+H)+.
[Пример 62]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(этиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
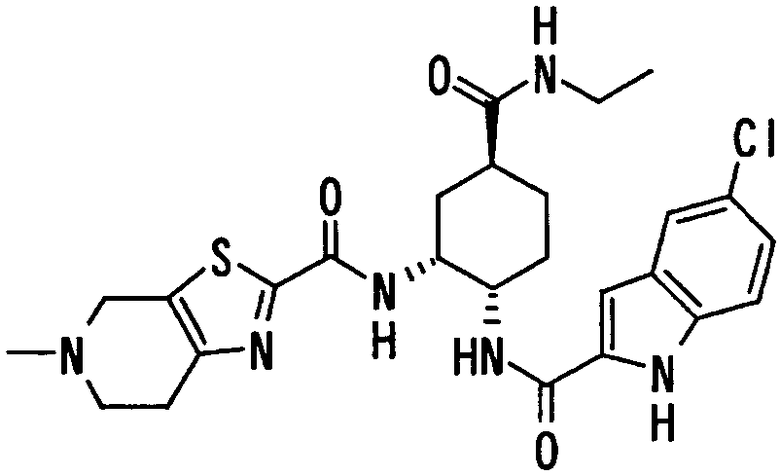
Соединение (150 мг), полученное в примере 58, растворяли в N,N-диметилформамиде (3 мл), к раствору добавляли гидрохлорид N-этиламина (119 мг), моногидрат 1-гидроксибензотриазола (79 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (112 мг) и триэтиламин (326 мкл) и смесь перемешивали при комнатной температуре в течение 4 суток. Растворитель отгоняли при пониженном давлении, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и смесь экстрагировали метиленхлоридом. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 47:3). Полученное таким образом твердое вещество растворяли в метиленхлориде и к раствору добавляли 1N этанольный раствор (171 мкл) хлористоводородной кислоты. Растворитель отгоняли при пониженном давлении, к остатку добавляли метанол и диэтиловый эфир и образовавшийся осадок отфильтровывали, получая указанное в заголовке соединение (74 мг).
1Н-ЯМР (ДМСО-d6) δ: 0,99 (3H, т, J=7,2Гц), 1,57-2,02 (6H, м), 2,33-2,38 (1H, м), 2,92 (3H, с), 3,01-3,08 (2H, м), 3,17-3,20 (2H, с), 3,45-3,70 (2H, м), 4,10-4,17 (1H, м), 4,40-4,69 (3H, м), 7,04 (1H, д, J=2,0Гц), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, д, J=2,0Гц), 7,78-7,81 (1H, м), 8,08-8,12 (1H, м), 8,40 (1H, д, J=8,1Гц), 11,23 (1H, шир.с), 11,79 (1H, шир.с).
МС (FAB) m/z: 543 (М+Н)+.
[Пример 63]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
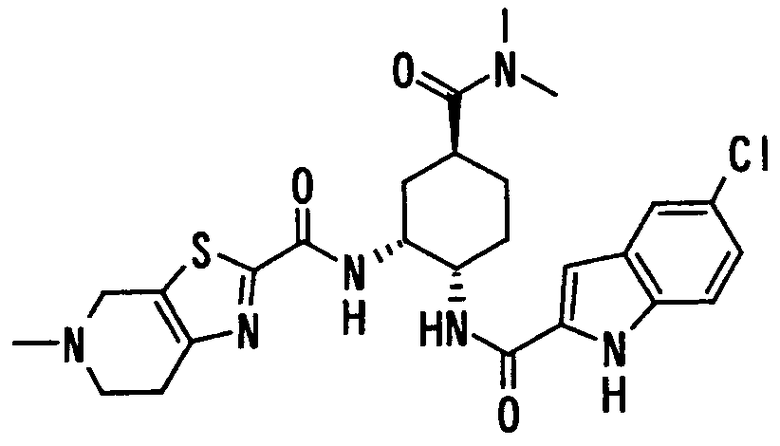
Соединение (900 мг), полученное в примере 58, растворяли в N,N-диметилформамиде (50 мл), к раствору добавляли гидрохлорид диметиламина (304 мг), моногидрат 1-гидроксибензотриазола (262 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (369 мг) и диизопропилэтиламин (1,83 мл) и смесь перемешивали при комнатной температуре в течение 12 часов. Растворитель отгоняли при пониженном давлении, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и смесь экстрагировали метиленхлоридом. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 47:3). Полученные таким образом белые твердые частицы растворяли в метиленхлориде и к раствору добавляли 1N этанольный раствор (1,49 мл) хлористоводородной кислоты. Растворитель отгоняли при пониженном давлении, к остатку добавляли метанол и диэтиловый эфир и образовавшийся осадок отфильтровывали, получая указанное в заголовке соединение (777 мг).
[α]25 D = -53,9° (18°C, c = 0,505 метанол).
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,70-1,85 (3H, м), 1,90-2,05 (2H, м), 2,80 (3H, с), 2,91 (3H, с), 2,95-3,10 (1H, м), 2,97 (3H, с), 3,10-3,75 (4H, м), 4,05-4,15 (1H, м), 4,35-4,75 (3H, м), 7,05 (1H, с), 7,16 (1H, дд, J=8,7, 2,1Гц), 7,41 (1H, д, J=8,6Гц), 7,67 (1H, с), 8,30-8,45 (2H, м), 11,63 (1H, шир.), 11,78 (1H, с).
МС (FAB) m/z: 543 (М+Н)+.
[Пример 64]
Гидрохлорид N-((1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-{[(2-метоксиэтил)(метил)амино]карбонил}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
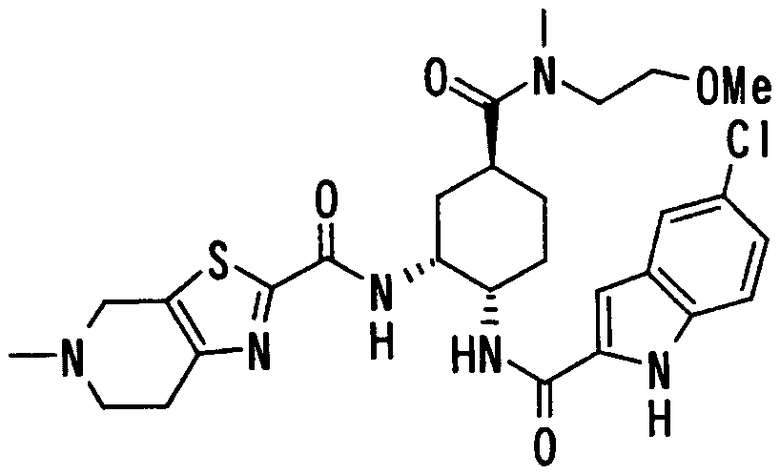
Указанное в заголовке соединение получали из соединения, полученного в примере 58, подобно способу примера 57.
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,99 (6H, м), 2,80, 3,01 (3H, каждый с), 2,91 (3H, с), 3,03 (1H, шир.с), 3,16 (2H, с), 3,23 (3H, с), 3,35-3,67 (6H, м), 4,09-4,16 (1H, м), 4,43-4,67 (3H, м), 7,04-7,06 (1H, м), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,42 (1H, д, J=8,8Гц), 7,69 (1H, шир.с), 8,29-8,41 (2H, м), 11,59 (1H, шир.с), 11,80 (1H, шир.с).
МС (FAB) m/z: 587 (M+H)+.
[Пример 65]
Гидрохлорид N-((1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-{[(2-гидроксиэтил)(метил)амино]карбонил}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
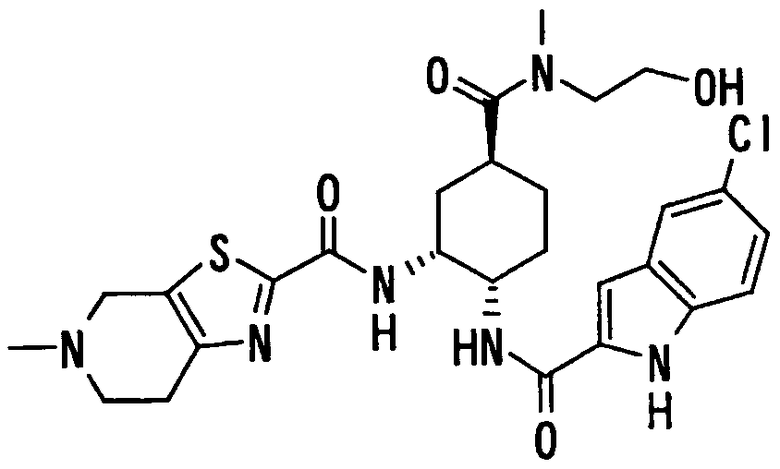
Указанное в заголовке соединение получали из соединения, полученного в примере 58, подобно способу примера 57.
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,55 (1H, м), 1,74-1,84 (3H, м), 1,94-1,97 (2H, м), 2,67, 3,02 (3H, каждый с), 2,91 (3H, с), 3,10-3,68 (9H, м), 4,11-4,13 (1H, м), 4,43-4,66 (4H, м), 7,05 (1H, с), 7,16 (1H, дд, J=8,7, 2,0Гц), 7,41 (1H, д, J=8,7Гц), 7,68 (1H, с), 8,34-8,40 (2H, м), 11,47 (1H, шир.с), 11,79 (1H, с).
МС (FAB) m/z: 573 (M+H)+.
[Пример 66]
Гидрохлорид N-((1R,2S,5S)-5-(1-азетидинилкарбонил)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
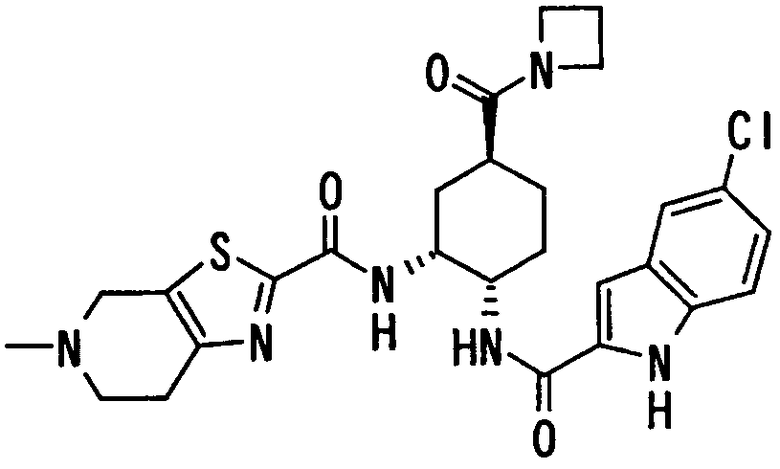
Указанное в заголовке соединение получали из соединения, полученного в примере 58, и гидрохлорида азетидина подобно способу примера 57.
1Н-ЯМР (ДМСО-d6) δ: 1,47-1,55 (1H, м), 1,65-1,82 (3H, м), 1,88-2,01 (2H, м), 2,16 (2H, квинт., J=7,6Гц), 3,17-3,67 (5H, м), 3,82 (2H, т, J=7,6Гц), 4,02-4,14 (3H, м), 4,43-4,67 (3H, м), 7,06 (1H, с), 7,17 (1H, дд, J=8,7, 1,7Гц), 7,41 (1H, д, J=8,7Гц), 7,69 (1H, шир.с), 8,31 (1H, д, J=7,6Гц), 8,38 (1H, д, J=7,6Гц), 11,41 (1H, шир.с), 11,80 (1H, с).
МС (FAB) m/z: 555 (М+Н)+.
[Пример 67]
Гидрохлорид N-((1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-{[(3S)-3-фторпирролидинил]карбонил}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридинкарбоксамида
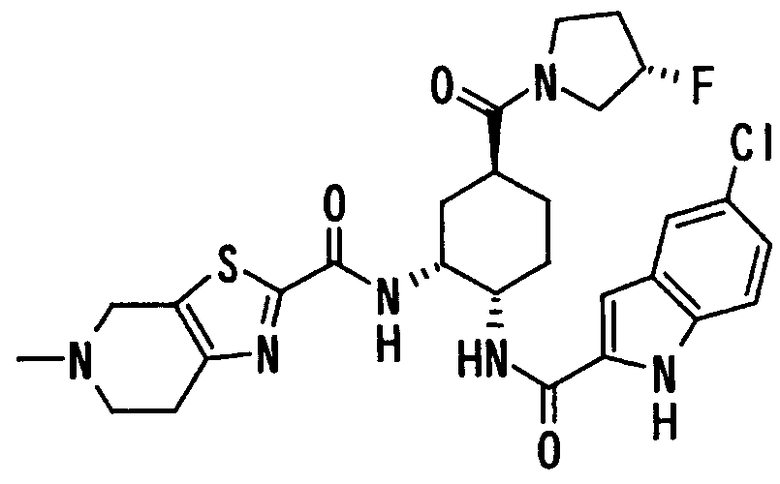
Указанное в заголовке соединение получали из соединения, полученного в примере 58, и (S)-3-фторпирролидина (Synlett., 1995, р. 55) подобно способу примера 57.
1Н-ЯМР (ДМСО-d6) δ: 1,23-3,77 (22H, м), 4,11-4,16 (1H, м), 4,58-4,51 (1H, м), 5,23-5,42 (1H, м), 7,05 (1H, с), 7,16 (1H, д, J=8,3Гц), 7,42 (1H, д, J=8,3Гц), 7,68 (1H, с), 8,34-8,37 (2H, м), 11,78 (1H, с).
МС (FAB) m/z: 587 (M+H)+.
[Пример 68]
(1R*,3R*,4S*)-3-{[(5-Хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат лития
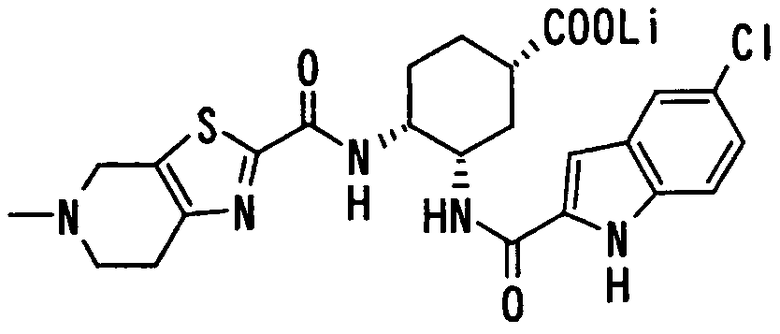
Соединение (1,20 г), полученное в примере 51, растворяли в тетрагидрофуране (32 мл), к раствору добавляли последовательно при охлаждении льдом гидроксид лития (60,8 мг) и воду (4 мл) и смесь перемешивали при комнатной температуре в течение 14 часов. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (1,12 г).
1Н-ЯМР (ДМСО-d6) δ: 1,55-1,70 (2H, м), 1,70-2,05 (4H, м), 2,10-2,20 (1H, м), 2,25-2,40 (4H, м), 2,50-2,80 (4H, м), 3,45-3,65 (3H, м), 4,10-4,30 (2H, м), 7,00-7,20 (2H, м), 7,50-7,65 (2H, м).
[Пример 69]
Гидрохлорид N-{(1R*,2S*,4S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
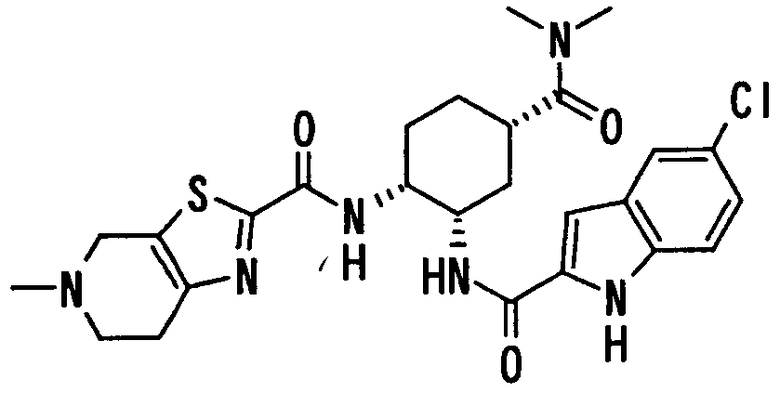
Указанное в заголовке соединение получали из соединения, полученного в примере 68, и диметиламина подобно способу примера 57.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,60 (2H, м), 1,65-1,80 (2H, м), 1,95-2,10 (2H, м), 2,84 (3H, с), 2,90-3,05 (1H, м), 2,92 (3H, с), 3,06 (3H, с), 3,15-3,75 (4H, м), 4,25-4,75 (4H, м), 7,02 (1H, д, J=1,5Гц), 7,15 (1H, дд, J=8,8, 2,1Гц), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, д, J=2,1Гц), 8,05 (1H, д, J=7,7Гц), 8,63 (1H, д, J=7,7Гц), 11,20 (1H, шир.), 11,79 (1H, с).
МС (FAB) m/z: 543 (М+Н)+.
[Пример 70]
Гидрохлорид N-((1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-{[(3R)-3-гидроксипирролидинил]карбонил}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
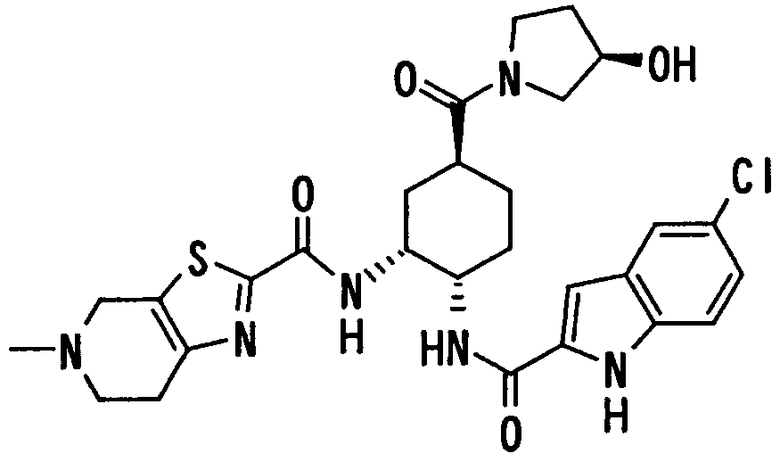
1) Соединение (1,18 г), полученное в ссылочном примере 58, растворяли в метаноле (12 мл), добавляли 1N хлористоводородную кислоту (240 мкл) и гидроксид палладия (221 мг), вводили водород и проводили каталитическое восстановление при нормальном давлении и комнатной температуре в течение 4,5 часов. Катализатор удаляли фильтрованием и фильтрат концентрировали при пониженном давлении до твердого состояния с получением неочищенного гидрохлорида (3R)-3-{[трет-бутил(дифенил)силил]окси}пирролидина (984 мг).
Полученный таким образом продукт (249 мг), продукт (295 мг), полученный в примере 58, гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (126 мг) и моногидрат 1-гидроксибензотриазола (87 мг) растворяли в N,N-диметилформамиде (10 мл). К раствору добавляли по каплям при охлаждении льдом диизопропилэтиламин (450 мкл) и смесь перемешивали при комнатной температуре в течение 12 часов. Растворитель отгоняли при пониженном давлении и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток подвергали колоночной хроматографии на силикагеле (метанол:метиленхлорид = 3:97) с получением N-(1R,2S,5S)-5-[((3R)-3-{[трет-бутил(дифенил)силил]окси}пирролидинил)карбонил]-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида (248 мг).
1Н-ЯМР (CDCl3) δ: 1,06 (9H, с), 1,50-1,60 (1H, м), 1,75-2,10 (5H, м), 2,20-2,50 (2H, м), 2,54 (3H, д, J=2,8Гц), 2,60-3,00 (5H, м), 3,30-3,80 (6H, м), 4,10-4,20 (1H, м), 4,40-4,70 (2H, м), 6,85 (1H, с), 7,15-7,25 (1H, м), 7,30-7,50 (8H, м), 7,60-7,70 (5H, м), 7,90-8,00 (1H, м), 9,38 (1H, с).
МС (FAB) m/z: 823 (M+H)+.
2) Полученный выше продукт (240 мг) растворяли в пиридине (10 мл), добавляли по каплям при охлаждении льдом комплекс (3,0 мл) фтористый водород-пиридин и смесь перемешивали при 0°C в течение 4,5 часов. К реакционной смеси для ее разбавления добавляли при охлаждении льдом этилацетат (80 мл). Разбавленную реакционную смесь выливали на лед. К полученному раствору для его подщелачивания добавляли гидрокарбонат натрия и разделяли жидкости. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:19 → 1:9). Полученный неочищенный продукт растворяли в метиленхлориде и метаноле, к раствору добавляли 1N этанольный раствор (225 мкл) хлористоводородной кислоты и затем сушили его один раз. К остатку для его отверждения добавляли метанол и диэтиловый эфир с получением указанного в заголовке соединения (114 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,60 (1H, м), 1,70-2,10 (6H, м), 2,75-2,85 (1H, м), 2,92 (3H, с), 3,10-3,80 (8H, м), 4,10-5,10 (6H, м), 7,05 (1H, д, J=1,7Гц), 7,16 (1H, дд, J=8,8, 1,7Гц), 7,42 (1H, д, J=8,8Гц), 7,68 (1H, с), 8,30-8,45 (2H, м), 11,10-11,40 (1H, м), 11,78 (1H, с).
МС (FAB) m/z: 585 (М+Н)+.
[Пример 71]
N-((1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5,5-диметоксициклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид или N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4,4-диметоксициклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 118, и соединения, полученного в ссылочном примере 10, подобно способу примера 2.
1Н-ЯМР (CDCl3) δ: 2,11-2,15 (1H, м), 2,21-2,25 (1H, м), 2,41-2,43 (1H, м), 2,46 (3H, с), 2,70-2,75 (1H, м), 2,81-2,88 (1H, м), 3,21 (3H, с), 3,24 (3H, с), 3,49 (1H, с), 3,58 (1H, д, J=15,6Гц), 3,71 (1H, д, J=15,6Гц), 3,87-3,93 (1H, м), 4,26-4,29 (1H, м), 6,85 (1H, д, J=2,0Гц), 7,19 (1H, дд, J=8,5, 2,0Гц), 7,30 (1H, д, J=8,5Гц), 7,62 (1H, с), 9,21 (1H, с).
[Пример 72]
N-((1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-оксоциклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид или N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-оксоциклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
Соединение (100 мг), полученное в примере 71, растворяли в хлороформе (2 мл), добавляли трифторуксусную кислоту (0,5 мл) и воду (0,5 мл) и смесь перемешивали при комнатной температуре в течение 3,5 часов. К реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия и экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и полученный остаток очищали препаративной тонкослойной хроматографией на силикагеле (метиленхлорид:метанол = 19:1). Полученные таким образом белые твердые частицы растворяли в метаноле (4 мл) и к раствору добавляли 1N этанольный раствор (0,38 мл) хлористоводородной кислоты. Растворитель отгоняли при пониженном давлении с получением указанного в заголовке соединения (35 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,83-1,90 (1H, м), 2,08-2,10 (1H, м), 2,28-2,32 (1H, м), 2,5-2,59 (1H, м), 2,87 (3H, с), 2,96 (1H, т, J=13,0Гц), 3,06-3,10 (2H, м), 3,35-3,36 (3H, м), 4,02-4,04 (2H, м), 4,55-4,57 (2H, м), 7,03 (1H, с), 7,15 (1H, д, J=8,8Гц), 7,38 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,43 (1H, д, J=8,8Гц), 8,91 (1H, д, J=8,8Гц), 11,75 (1H, с).
[Пример 73]
N-[(1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-(гидроксиимино)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид или N-[(1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-(гидроксиимино)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
Соединение (133 мг), полученное в примере 72, растворяли в смешанном растворителе из пиридина (8 мл) и метанола (8 мл), добавляли гидрохлорид гидроксиламина (30 мг) и смесь перемешивали при комнатной температуре в течение 3 суток. Реакционную смесь концентрировали, к остатку добавляли воду и смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 97:3 → 17:3) с получением указанного в заголовке соединения (131 мг).
1Н-ЯМР (CDCl3) δ: 1,43-1,86 (3H, м), 1,98-2,03 (1H, м), 2,26-2,30 (1H, м), 2,45 (3H, с), 2,47-2,51 (1H, м), 2,67-2,71 (1H, м), 2,78-2,86 (3H, м), 3,86-3,43 (2H, м), 4,16-4,24 (2H, м), 6,85 (1H, с), 7,16-7,13 (1H, м), 7,20-7,24 (1H, м), 7,46, 7,50 (всего 1H, с), 7,56-7,64 (2H, м), 9,59, 9,62 (общий 1H, с).
[Пример 74]
N-((7R*,8S*)-8-{[(5-Хлориндол-2-ил)карбонил]амино}-1,4-диоксаспиро[4.5]дец-7-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид или N-((7R*,8S*)-7-{[(5-хлориндол-2-ил)карбонил]амино}-1,4-диоксаспиро[4.5]дец-8-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 120, и соединения, полученного в ссылочном примере 10, подобно способу примера 2.
1Н-ЯМР (CDCl3) δ: 1,69-1,87 (6H, м), 2,14-2,17 (1H, м), 2,30-2,32 (1H, м), 2,47 (3H, с), 2,70-2,75 (1H, м), 2,81-2,89 (2H, м), 3,58 (1H, д, J=15,4Гц), 3,72 (1H, д, J=15,4Гц), 3,89-3,91 (1H, м), 3,99 (4H, с), 4,37-4,40 (1H, м), 6,86 (1H, д, J=2,0Гц), 7,19 (1H, дд, J=8,8, 2,0Гц), 7,30 (1H, д, J=8,8Гц), 7,38 (1H, д, J=7,3Гц), 7,62 (1H, д, J=2,0Гц), 9,15 (1H, с).
[Пример 75]
N-[(1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-(метоксиимино)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид или N-[(1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-(метоксиимино)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
1) Соединение (2,21 г), полученное в ссылочном примере 124, растворяли в метиленхлориде (30 мл), добавляли трифторуксусную кислоту (6 мл) и смесь перемешивали при комнатной температуре в течение 1,5 часов. Реакционную смесь концентрировали, сушили с использованием вакуумного насоса, затем растворяли в N,N-диметилформамиде (20 мл) и к раствору добавляли 5-хлориндол-2-карбоновую кислоту (500 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (593 мг), моногидрат 1-гидроксибензотриазола (473 мг) и N-метилморфолин (2,8 мл). Смесь перемешивали при комнатной температуре в течение 10 часов. Добавляли дополнительно 5-хлориндол-2-карбоновую кислоту (242 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (237 мг) и моногидрат 1-гидроксибензотриазола (189 мг) и смесь перемешивали 4 часа. В реакционную смесь добавляли насыщенный водный раствор гидрокарбоната натрия и экстрагировали этилацетатом и смешанным растворителем этилацетат/тетрагидрофуран. Полученные органические слои промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 97:3 → 4:1) с получением N-[(1R*,2S*)-2-амино-5-(метоксиимино)циклогексил]-5-хлориндол-2-карбоксамида (368 мг) и N-[(1R*,2S*)-2-амино-4-(метоксиимино)циклогексил]-5-хлориндол-2-карбоксамида (300 мг).
2) Указанное в заголовке соединение (смесь син- и антиизомеров по метоксииминогруппе) получали из полученного выше N-[(1R*,2S*)-2-амино-5-(метоксиимино)циклогексил]-5-хлориндол-2-карбоксамида или N-[(1R*,2S*)-2-амино-4-(метоксиимино)циклогексил]-5-хлориндол-2-карбоксамида и соединения, полученного в ссылочном примере 10, подобно способу примера 2.
1Н-ЯМР (CDCl3) δ: 1,84-2,00 (3H, м), 2,26-2,56 (3H, м), 2,46 (3H, с), 2,80-2,83 (4H, м), 3,57 (1H, кв, J=15,4Гц), 3,70 (1H, кв, J=15,4Гц), 3,84, 3,85 (всего 3H, с), 4,08-4,14 (1H, м), 4,26-4,30 (1H, м), 6,84 (1H, с), 7,17 (1H, д, J=8,8Гц), 7,27 (1H, д, J=8,8Гц), 7,46-7,48 (2H, м), 7,56 (1H, м), 9,42, 9,55 (общий 1H, с).
[Пример 76]
N-((1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-гидроксициклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (стереоизомер А) или N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-гидроксициклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (стереоизомер А)
1) N-((1R*,2S*)-2-амино-4-{[трет-бутил(дифенил)силил]окси}циклогексил)-5-хлориндол-2-карбоксамид (стереоизомер А) и N-((1R*,2S*)-2-амино-5-{[трет-бутил(дифенил)силил]окси}циклогексил)-5-хлориндол-2-карбоксамид (стереоизомер А) получали, подвергая (1R*,2S*)-форму, полученную в ссылочном примере 125, де(трет-бутоксикарбонилированию) подобно способу стадии 1) примера 75, и взаимодействием образовавшегося продукта с 5-хлориндол-2-карбоновой кислотой.
2) N-((1R*,2S*)-5-{[трет-Бутил(дифенил)силил]окси}-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (стереоизомер А) или N-((1R*,2S*)-4-{[трет-бутил(дифенил)силил]окси}-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (стереоизомер А) получали из продукта, полученного по описанной выше реакции, и соединения, полученного в ссылочном примере 10, подобно способу примера 2.
1Н-ЯМР (CDCl3) δ: 1,06 (9H, с), 1,55-1,61 (1H, м), 1,85-1,90 (1H, м), 2,18-2,25 (1H, м), 2,46 (3H, с), 2,51 (2H, д, J=7,6Гц), 2,72 (1H, м), 3,56 (1H, с), 3,57 (1H, д, J=15,3Гц), 3,72 (1H, д, J=15,3Гц),) 3,71-3,81 (1H, м), 3,88-3,95 (1H, м), 6,78 (1H, с), 7,17 (1H, дд, J=2,0, 8,8Гц), 7,37-7,44 (7H, м), 7,59 (1H, с), 7,65-7,68 (6H, м), 9,30 (1H, с).
3) Указанное в заголовке соединение получали из соединения, полученного по описанной выше реакции, подобно способу стадии 3) примера 28.
1Н-ЯМР (ДМСО-d6) δ: 1,25-1,30 (2H, м), 1,45-1,64 (2H, м) 1,86 (1H, д, J=9,0Гц), 1,98-2,03 (1H, м), 2,33 (3H, с), 2,66-2,73 (2H, м), 2,75-2,79 (2H, м), 3,54 (1H, д, J=15,6Гц), 3,62 (1H, д, J=15,6Гц), 3,96-4,02 (2H, м), 4,78 (1H, д, J=4,2Гц), 7,00 (1H, с), 7,14 (1H, дд, J=2,0, 8,8Гц), 7,38 (1H, д, J=8,8Гц) 7,66 (1H, с), 8,20 (1H, д, J=7,8Гц), 8,54 (1H, д, J=7,8Гц), 11,69 (2H, с).
[Пример 77]
N-((1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-гидрокси-5-метилциклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (стереоизомер А1) или N-((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-гидрокси-4-метициклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (стереоизомер А2)
Указанные в заголовке соединения получали взаимодействием соединения, полученного в ссылочном примере 128, с соединением, полученным в ссылочном примере 10, подобно способу примера 2.
Стереоизомер А1:
1Н-ЯМР (ДМСО-d6) δ: 1,24 (3H, с), 1,33-1,82 (4H, м), 2,34 (3H, с), 2,67-3,64 (8H, м), 4,02-4,10 (2H, м), 4,67 (1H, шир.с), 7,02 (1H, с), 7,13 (1H, д, J=8,6Гц), 7,38 (1H, д, J=8,6Гц), 7,66 (1H, д, J=2,0Гц), 8,21-8,26 (1H, шир.), 8,59 (1H, д, J=8,1Гц), 11,73 (1H, шир.с).
МС (FAB) m/z: 502 (М+Н)+.
Стереоизомер А2:
1Н-ЯМР (ДМСО-d6) δ: 1,25 (3H, с), 1,33-1,79 (4H, м), 2,33 (3H, с), 2,65-3,63 (8H, м), 3,88-3,94 (1H, м), 4,20-4,25 (1H, м), 4,59 (1H, шир.), 7,01 (1H, с), 7,13 (1H, д, J=7,8Гц), 7,38 (1H, д, J=8,6Гц), 7,67 (1H, с), 8,29 (1H, шир.), 8,43 (1H, д, J=9,3Гц), 11,67 (1H, шир.)
МС (FAB) m/z: 502 (М+Н)+.
[Пример 78]
N-[(1R*,2R*,5S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-(гидроксиметил)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
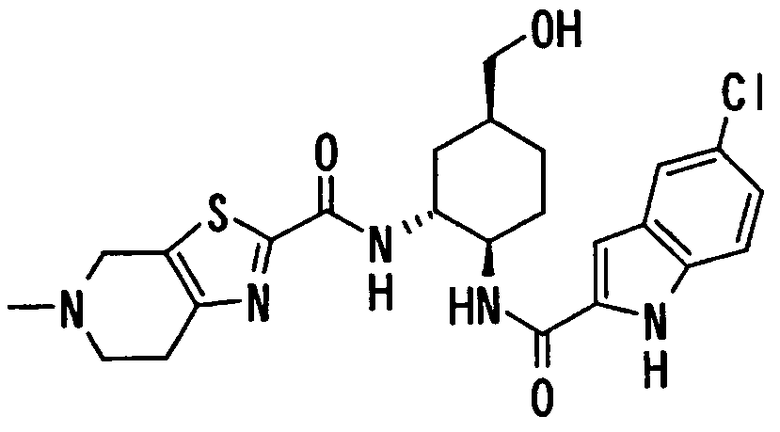
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 129, этанольным раствором хлористоводородной кислоты и затем конденсацией данного соединения с соединением, полученным в ссылочном примере 10, подобно способу примера 49.
1Н-ЯМР (ДМСО-d6) δ: 1,42-1,90 (5H, м), 2,07-2,26 (3H, м), 2,46 (3H, с), 2,67-2,95 (4H, м), 3,55-3,80 (4H, м), 3,80-3,95 (1H, м), 4,13-4,25 (1H, м), 6,84 (1H, шир.с), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,23-7,35 (2H, м), 7,43 (1H, д, J=7,2Гц), 7,58 (1H, шир.с), 9,29 (1H, с).
МС (ESI) m/z: 502 (М+Н)+.
[Пример 79]
N-[(1R*,2S*,5S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-(метоксиметил)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
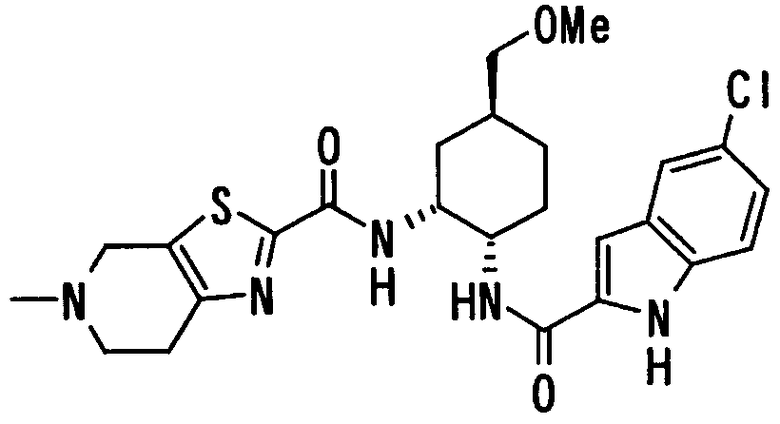
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 135, этанольным раствором хлористоводородной кислоты и затем конденсацией его с соединением, полученным в ссылочном примере 10, подобно способу примера 49.
1Н-ЯМР (CDCl3) δ: 1,20-1,38 (1H, м), 1,50-1,67 (2H, м), 1,88-2,03 (2H, м), 2,03-2,14 (1H, м), 2,21-2,32 (1H, м), 2,53 (3H, с), 2,75-2,95 (2H, м), 3,20-3,35 (2H, м), 3,37 (3H, с), 3,71 (1H, д, J=16,0Гц), 3,76 (1H, J=16,0Гц), 4,04-4,13 (1H, м), 4,53-4,62 (1H, м), 6,85 (1H, д, J=2,0Гц), 7,19 (1H, дд, J=8,8, 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,54 (1H, д, J=7,2Гц), 7,63 (1H, д, J=2,0Гц), 8,07 (1H, д, J=5,6Гц), 9,49 (1H, шир.с).
[Пример 80]
N-((1R*,2S*,5S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-{[(метилсульфонил)амино]метил}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
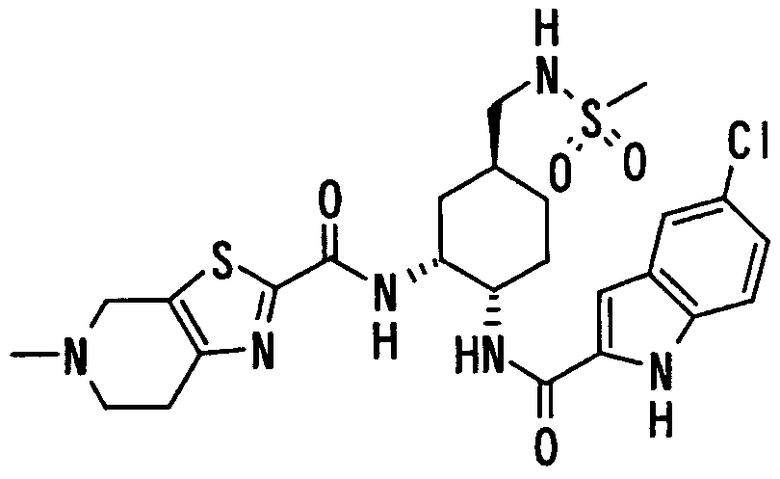
1) Соединение (437 мг), полученное в ссылочном примере 137, растворяли в этаноле (5 мл), добавляли при комнатной температуре 4N диоксановый раствор (5 мл) хлористоводородной кислоты и смесь перемешивали 13 часов. Растворитель отгоняли, остаток растворяли в N,N-диметилформамиде (10 мл) и к раствору добавляли триэтиламин (0,7 мл), соединение (300 мг), полученное в ссылочном примере 10, моногидрат 1-гидроксибензотриазола (162 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (230 мг). Смесь перемешивали 13 часов, добавляли воду и экстрагировали хлороформом. Полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 97:3) с получением N-((1R*,2S*,5S*)-5-(азидометил)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида (330 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,15-2,08 (7H, м), 2,33 (3H, с), 2,34-2,95 (6H, м), 3,64 (2H, с), 4,05-4,17 (1H, м), 4,36-4,47 (1H, м), 7,02 (1H, с), 7,15 (1H, дд, J=8,8, 2,0Гц), 7,40 (1H, д, J=8,8Гц), 7,67 (1H, д, J=2,0Гц), 8,02 (1H, д, J=7,6Гц), 8,44 (1H, д, J=7,6Гц), 11,8 (1H, с).
2) Соединение (300 мг), полученное по описанной выше реакции, растворяли в этаноле (8 мл), добавляли каталитическое количество 10% палладия на углероде и смесь перемешивали при комнатной температуре в течение 168 часов в атмосфере водорода. Нерастворимое вещество отфильтровывали и отгоняли растворитель. Полученный таким образом неочищенный N-((1R*,2S*,5S*)-5-(аминометил)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (150 мг) растворяли в хлороформе (6 мл), добавляли триэтиламин (0,2 мл) и метансульфонилхлорид (0,035 мл) и смесь перемешивали в течение 13 часов. Растворитель отгоняли при пониженном давлении, к остатку добавляли воду и смесь экстрагировали хлороформом. Полученный органический слой промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 24:1) с получением указанного в заголовке соединения (56 мг).
1Н-ЯМР (CDCl3) δ: 1,18-1,34 (2H, м), 1,50-1,75 (4H, м), 1,90-2,30 (4H, м), 2,53 (3H, с), 2,78-2,90 (2H, м), 2,90-3,05 (6H, м), 3,20-3,30 (1H, м), 3,68-3,81 (2H, м), 3,98-4,08 (1H, м), 4,54-4,62 (1H, м), 6,10-6,19 (1H, м), 6,86 (1H, с), 7,19 (1H, дд, J=8,8, 2,0Гц), 7,35 (1H, д, J=8,8Гц), 7,52 (1H, д, J=7,6Гц), 7,62 (1H, д, J=2,0Гц), 8,21 (1H, д, J=5,6Гц), 9,89 (1H, с).
МС (ESI) m/z: 579 (M+H)+.
[Пример 81]
Трифторацетат N-{(1R*,2S*,5S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)метил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
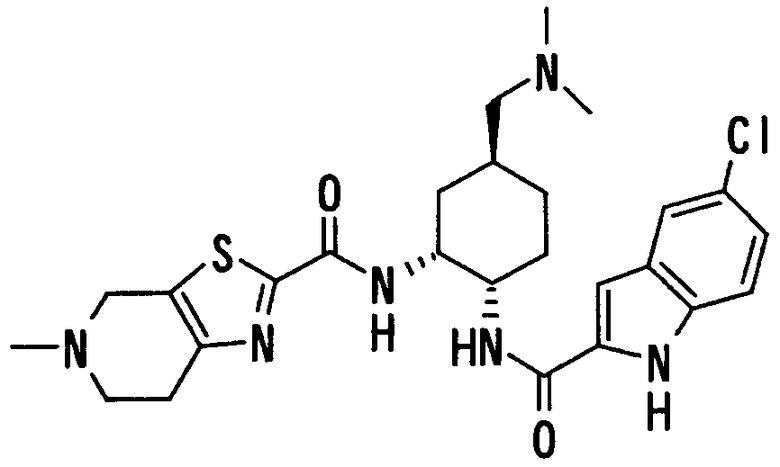
Указанное в заголовке соединение получали из амина, полученного на стадии 2) примера 80, подобно способу примера 24.
1Н-ЯМР (ДМСО-d6) δ: 1,15-2,22 (7H, м), 2,40-2,65 (2H, м), 2,68-2,85 (6H, м), 2,92-3,08 (5H, м), 3,10-3,18 (2H, м), 4,08-4,20 (1H, м), 4,35-4,51 (2H, м), 7,04 (1H, с), 7,14-7,20 (1H, м), 7,41 (1H, д, J=8,8Гц), 7,67 (1H, с), 8,25-8,42 (2H, м), 9,11 (1H, шир.с), 9,89 (1H, с).
МС (ESI) m/z: 529 (M+H)+.
[Пример 82]
трет-Бутил (3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексилкарбамат (изомер В) и трет-бутил (3R*,4S*)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексилкарбамат (изомер В)
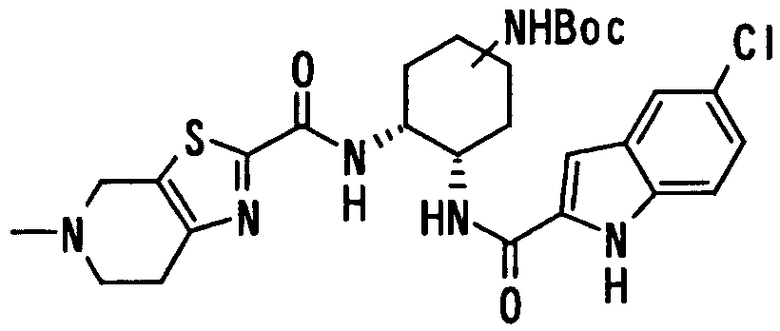
Соединение (стереоизомер В) (1,79 г), полученное в ссылочном примере 140, растворяли в тетрагидрофуране (36 мл), добавляли 10% палладий на углероде (0,40 г) и смесь перемешивали при комнатной температуре в течение 20 часов в атмосфере водорода. После удаления фильтрованием катализатора фильтрат концентрировали при пониженном давлении, остаток растворяли в N,N-диметилформамиде (36 мл), к раствору добавляли п-нитрофенил 5-хлориндол-2-карбоксилат (2,02 г) и смесь перемешивали в течение 16 часов. Реакционную смесь концентрировали при пониженном давлении, к остатку добавляли этилацетат и воду и отфильтровывали нерастворимое вещество. Продукт промывали этилацетатом с получением неочищенного трет-бутил (3R*,4S*)-3-амино-4-{[(5-хлориндол-2-ил)карбонил]амино}циклогексилкарбамата (или (3R*,4S*)-4-амино-3-{[(5-хлориндол-2-ил)карбонил]амино}циклогексилкарбамата) (изомер В1) (1,49 г). Органический слой фильтрата промывали водой и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 30:1 → 10:1) с получением трет-бутил (3R*,4S*)-4-амино-3-{[(5-хлориндол-2-ил)карбонил]амино}циклогексилкарбамата (или трет-бутил (3R*,4S*)-3-амино-4-{[(5-хлориндол-2-ил)карбонил]амино}циклогексилкарбамата) (изомер В2) (0,37 г).
Одно из указанных в заголовке соединений получали из изомера В1 и соединения, полученного в ссылочном примере 10, подобно способу примера 2.
1Н-ЯМР (ДМСО-d6) δ: 1,25-1,50 (1H, м), 1,37 (9H, с), 1,50-1,65 (1H, м), 1,75-2,20 (4H, м), 2,37 (3H, с), 2,70-3,00 (4H, м), 3,60-3,80 (3H, м), 4,13 (1H, шир.с), 4,43 (1H, шир.с),6,92 (1H, д, J=7,1Гц), 7,05 (1H, с), 7,17 (1H, дд, J=8,8, 2,2Гц), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,15 (1H, д, J=7,8Гц), 8,37 (1H, д, J=7,1Гц), 11,78 (1H, с).
МС (FAB) m/z: 587 (М+Н)+.
Другое указанное в заголовке соединение получали из изомера В2 таким же способом.
1Н-ЯМР (ДМСО-d6) δ: 1,15-1,30 (1H, м), 1,35 (9H, с), 1,45-1,60 (1H, м), 1,65-1,75 (1H, м), 1,85-1,95 (1H, м), 2,05-2,20 (2H, м), 2,34 (3H, с), 2,65-2,85 (4H, м), 3,55-3,70 (3H, м), 4,05-4,14 (1H, м}, 4,40 (1H, шир.с), 6,80 (1H, д, J=7,3Гц), 7,15-7,25 (2H, м), 7,43 (1H, д, J=8,8Гц), 7,73 (1H, д, J=2,0Гц), 8,05 (1H, д, J=6,6Гц), 8,51 (1H, д, J=8,8Гц), 11,82 (1H, с).
МС (FAB) m/z: 587 (M+H)+.
[Пример 83]
Гидрохлорид N-((1R*,2S*)-5-амино-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида (или N-((1R*,2S*)-4-амино-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида) (стереоизомер В)
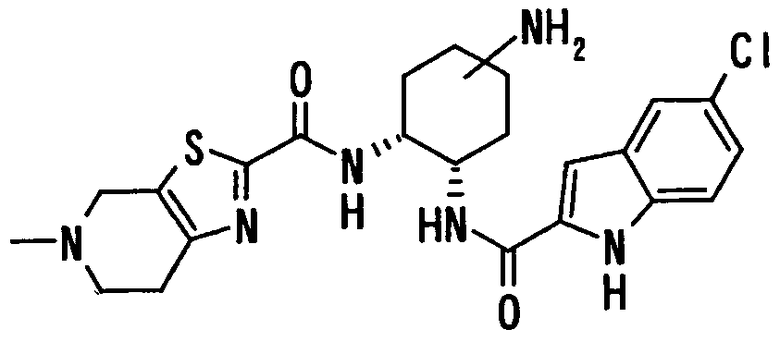
Соединение (стереоизомер В) (1,11 г), синтезированное из изомера В1 в примере 82, суспендировали в метиленхлориде (20 мл), добавляли этанольный раствор (20 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 2 часов. Растворитель отгоняли при пониженном давлении и остаток очищали гель-фильтрованием (Sephadex LH-20, метанол) с получением указанного в заголовке соединения (1,05 г).
1Н-ЯМР (ДМСО-d6) δ: 1,55-1,65 (1H, м), 1,75-1,90 (2H, м), 1,95-2,20 (2H, м), 2,20-2,40 (1H, м), 2,90 (3H, с), 3,10-3,20 (1H, м), 3,20-3,50 (3H, м), 3,65-3,75 (1H, м), 4,10-4,20 (1H, м), 4,35-4,50 (1H, м), 4,55-4,65 (1H, м), 4,65-4,75 (1H, м), 7,07 (1H, с), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,42 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,05-8,30 (3H, шир.), 8,40-8,50 (2H, м), 11,70-11,90 (2H, м).
МС (FAB) m/z: 487 (М+Н)+.
[Пример 84]
N-{(1R*,2S*)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-[(метилсульфонил)амино]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид или N-{(1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-4-[(метилсульфонил)амино]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (стереоизомер В)
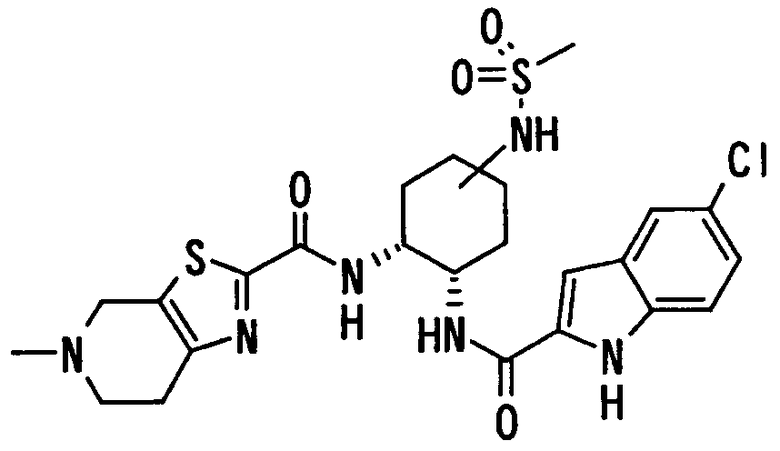
Соединение (0,20 г), полученное в примере 83, суспендировали в метиленхлориде (7 мл), добавляли триэтиламин (0,16 мл) и метансульфонилхлорид (28 мкл) и смесь перемешивали при комнатной температуре в течение 20 часов. После разбавления реакционной смеси метиленхлоридом ее промывали водным раствором гидроксида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 30:1 → 15:1) с получением указанного в заголовке соединения (67,9 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,55 (1H, м), 1,65-1,85 (2H, м), 1,90-2,05 (2H, м), 2,15-2,25 (1H, м), 2,41 (3H, с), 2,75-2,95 (4H, м), 2,92 (3H, с), 3,55-3,80 (3H, м), 4,10-4,20 (1H, м), 4,45-4,55 (1H, м), 7,08 (1H, с), 7,15-7,20 (2H, м), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,27 (1H, д, J=7,3Гц), 8,33 (1H, д, J=8,1Гц), 11,77 (1H, с).
МС (FAB) m/z: 565 (M+H)+.
[Пример 85]
N-((1R*,2S*)-5-(Ацетиламино)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид или N-((1R*,2S*)-4-(ацетиламино)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (стереоизомер В)
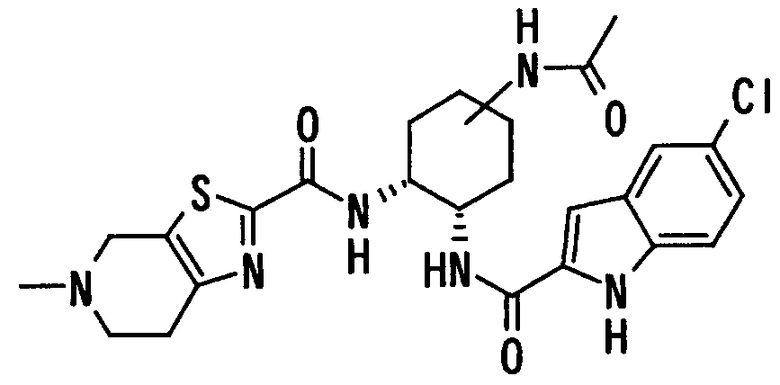
Соединение (стереоизомер В) (0,20 г), полученное в примере 83, суспендировали в метиленхлориде (7 мл), добавляли триэтиламин (0,16 мл) и уксусный ангидрид (34 мкл) и смесь перемешивали при комнатной температуре в течение 20 часов. К реакционной смеси добавляли метиленхлорид и водный раствор гидроксида натрия и отделяли фильтрованием нерастворимое вещество. Органический слой фильтрата отделяли и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 15:1 → 10:1) с получением указанного в заголовке соединения (0,12 г).
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,50 (1H, м), 1,55-1,70 (1H, м), 1,80 (3H, с), 1,80-2,05 (3H, м), 2,05-2,20 (1H, м), 2,47 (3H, с), 2,80-3,00 (4H, м), 3,75-4,00 (3H, м), 4,15-4,30 (1H, м), 4,45-4,55 (1H, м), 7,07 (1H, с), 7,17 (1H, дд, J=8,8, 1,0Гц), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, с), 7,89 (1H, д, J=7,3Гц), 8,24 (1H, д, J=8,1Гц), 8,31 (1H, д, J=7,3Гц), 11,77 (1H, с).
МС (FAB) m/z: 528 (M+H)+.
[Пример 86]
Гидрохлорид N-((1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-{[метокси(метил)амино]карбонил}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
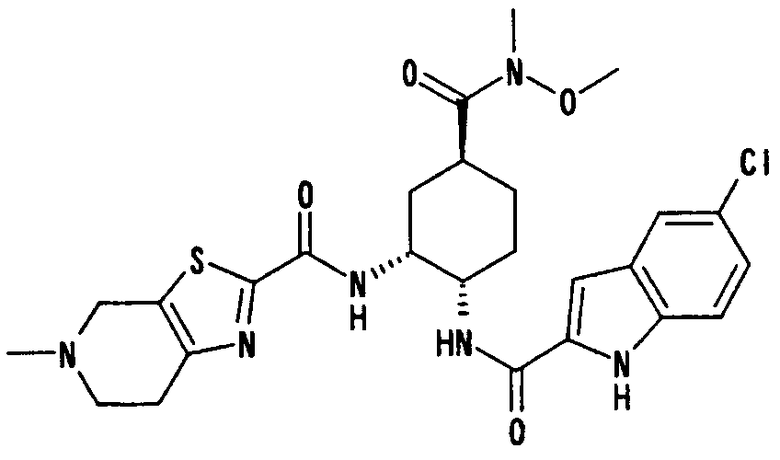
Соединение (250 мг), полученное в примере 58, растворяли в N,N-диметилформамиде (5 мл), добавляли гидрохлорид N,O-диметилгидроксиламина (142 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (111 мг), моногидрат 1-гидроксибензотриазола (89 мг) и N-метилморфолин (213 мл) и смесь перемешивали при комнатной температуре в течение 19 часов. После концентрирования реакционной смеси к остатку добавляли водный раствор гидрокарбоната натрия и смесь экстрагировали этилацетатом. Полученный органический слой промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, затем отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 47:3 → 23:2) с получением бесцветного аморфного твердого вещества (179 мг). Полученный продукт растворяли в смеси метанол-тетрагидрофуран и добавляли 1N этанольный раствор (960 мкл) хлористоводородной кислоты с получением указанного в заголовке соединения.
1Н-ЯМР (ДМСО-d6) δ: 1,57-1,91 (4H, м), 1,96-2,00 (1H, м), 2,10-2,21 (1H, м), 2,92 (3H, с), 2,93-3,03 (2H, м), 3,08 (3H, с), 3,10-3,28 (2H, м), 4,16-4,19 (1H, м), 4,50-4,52 (1H, м), 4,69 (1H, шир.с), 7,06 (1H, с), 7,17 (1H, дд, J=8,8, 1,5Гц), 7,42 (1H, д, J=8,8Гц), 7,70 (1H, с), 8,33 (1H, шир.с), 8,41 (1H, д, J=7,8Гц), 11,81 (1H, шир.с).
МС (ESI) m/z: 559 (M+H)+.
[Пример 87]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(2,2-диметилгидразино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
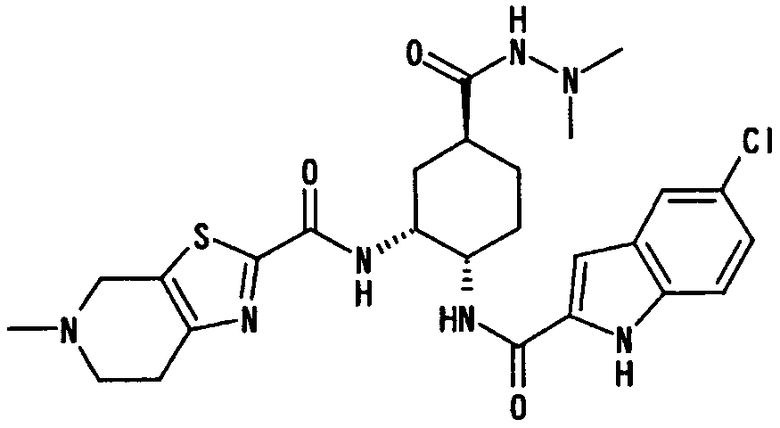
Указанное в заголовке соединение получали из соединения, полученного в примере 58, и N,N-диметилгидразина подобно способу примера 57.
1Н-ЯМР (ДМСО-d6) δ: 1,49-1,54 (1H, м), 1,76-1,81 (2H, м), 1,89-1,93 (2H, м), 2,07-2,17 (1H, м), 2,33-3,60 (14H, м), 4,15-4,19 (1H, м), 4,40-4,47 (2H, м), 4,70-4,72 (1H, м), 7,04 (1H, с), 7,17 (1H, дд, J=8,5, 2,0Гц), 7,42 (1H, д, J=8,5Гц), 7,70 (1H, с), 8,17-8,22 (1H, м), 8,41-8,43 (1H, м), 11,80 (1H, шир.с).
МС (ESI) m/z: 558 (М+Н)+.
[Пример 88]
Гидрохлорид 6-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-2-хинолинкарбоксамида
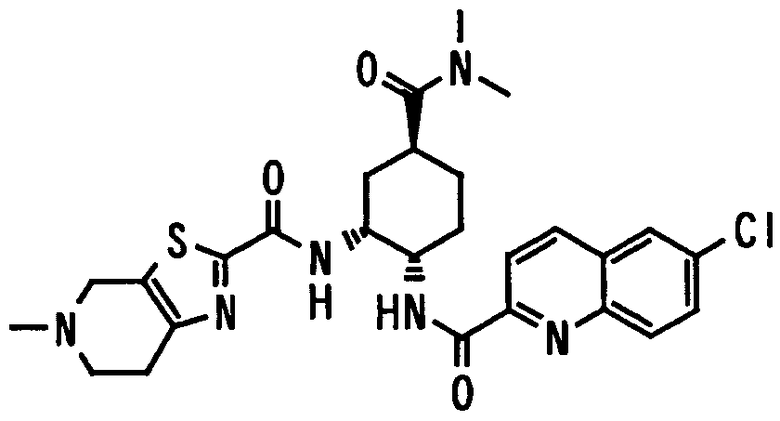
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 145, этанольным раствором хлористоводородной кислоты подобно способу примера 49, и затем конденсацией его с соединением, полученным в ссылочном примере 10.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,75-1,90 (3H, м), 1,90-2,00 (1H, м), 2,00-2,20 (1H, м), 2,80 (3H, с), 2,90 (3H, с), 2,99 (3H, с), 3,10-3,30 (5H, м), 3,56 (1H, шир.), 4,10-4,20 (1H, м), 4,40-4,70 (2H, м), 7,88 (2H, с), 8,15 (1H, д, J=8,6Гц), 8,22 (1H, с), 8,52 (1H, д, J=8,6Гц), 8,72 (1H, д, J=8,3Гц), 8,89 (1H, д, J=8,3Гц).
МС (FAB) m/z: 555 (М+Н)+.
[Пример 89]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлор-4-фториндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
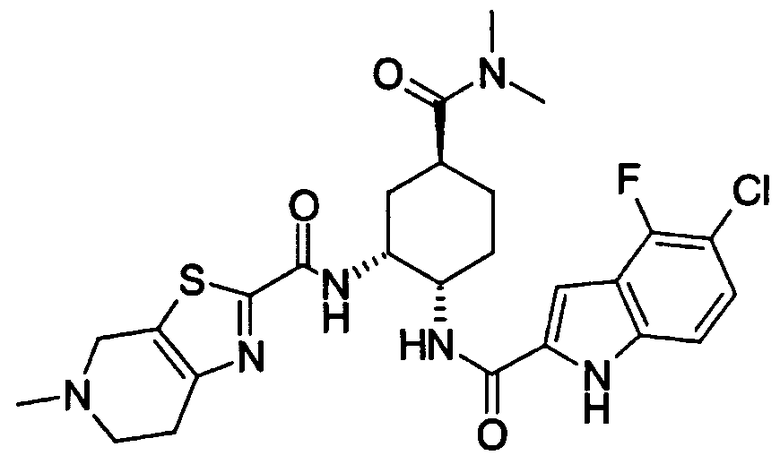
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 144, с соединением, полученным в ссылочном примере 274, подобно способу ссылочного примера 91 и обработкой полученного соединения 4N диоксановым раствором хлористоводородной кислоты и затем соединением, полученным в ссылочном примере 10.
1Н-ЯМР (ДМСО-d6) δ: 1,24-1,98 (6H, м), 2,33-3,33 (6H, м), 2,81 (3H, с), 2,90 (3H, с), 2,99 (3H, с), 4,12 (1H, шир.с), 4,30-4,70 (1H, м), 4,60 (1H, шир.с), 7,21 (1H, с), 7,27 (2H, шир.с), 8,37 (1H, д, J=8,1Гц), 8,43 (1H, д, J=7,6Гц), 12,11 (1H, с).
МС (FAB) m/z: 561 (М+Н)+.
[Пример 90]
Гидрохлорид 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)изохинолин-3-карбоксамида
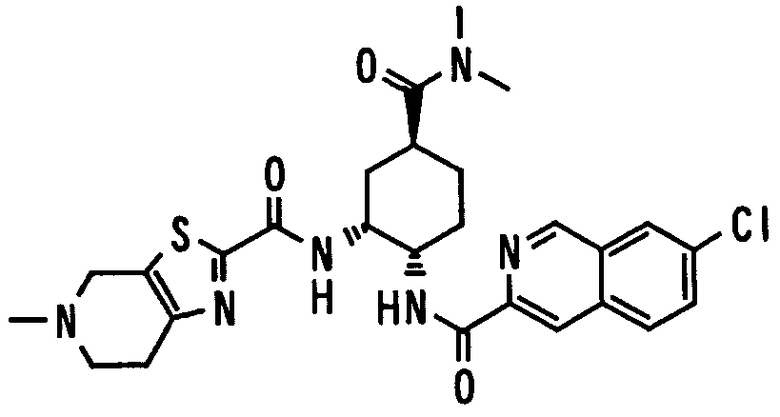
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 146, этанольным раствором хлористоводородной кислоты подобно способу примера 49, и затем конденсацией его с соединением, полученным в ссылочном примере 10.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,65 (1H, м), 1,70-1,85 (3H, м), 1,95-2,10 (1H, м), 2,10-2,20 (1H, м), 2,80 (3H, с), 2,92 (3H, с), 2,96 (3H, с), 2,95-3,10 (1H, м), 3,10-3,40 (3H, м), 3,70-3,80 (1H, м), 4,20-4,30 (1H, м), 4,40-4,60 (2H, м), 4,65-4,80 (1H, м), 7,83-7,93 (1H, м), 8,26 (1H, д, J=8,8Гц), 8,38 (1H, с), 8,60 (1H, с), 8,85-9,00 (2H, м), 9,30-9,40 (1H, м).
МС (FAB) m/z: 555 (M+H)+.
[Пример 91]
Гидрохлорид N-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}тетрагидрофуран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
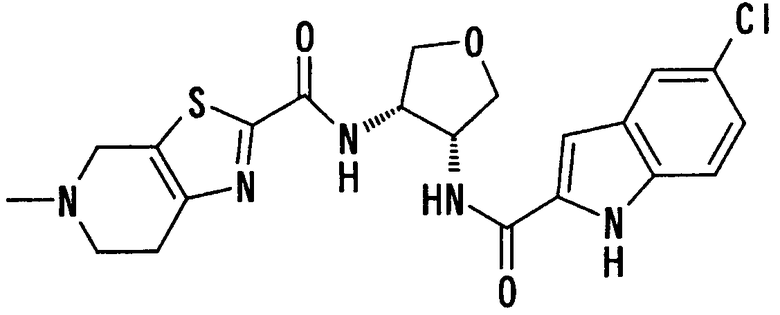
Соединение (0,1 г), полученное в ссылочном примере 10, моногидрат 1-гидроксибензотриазола (78 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (0,2 г) последовательно добавляли к раствору соединения (0,12 г), полученного в ссылочном примере 172, в N,N-диметилформамиде (20 мл) и смесь перемешивали при комнатной температуре в течение 1 суток. Реакционную смесь концентрировали и полученный остаток разбавляли смесью хлороформ-метанол (9:1) и промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия, затем полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 95:5) с получением свободного основания указанного в заголовке соединения. Полученный продукт обрабатывали этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения (0,1 г).
1Н-ЯМР (CDCl3) δ: 2,50 (3H, с), 2,70-2,90 (4H, м), 3,67 (1H, с), 3,70 (1H, с), 3,86 (1H, дд, J=9,2, 6,3Гц), 3,97 (1H, дд, J=9,7, 4,1Гц), 4,15 (1H, дд, J=9,7, 5,8Гц), 4,24 (1H, дд, J=9,2, 7,0Гц), 4,75-4,89 (1H, м), 4,92-5,03 (1H, м), 6,88 (1H, с), 7,20 (1H, дд, J=8,8, 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,35-7,43 (1H, м), 7,58 (1H, д, J=2,0Гц), 7,64 (1H, д, J=7,1Гц), 9,38 (1H, с).
МС (FAB) m/z: 460 (М+Н)+.
[Пример 92]
N-((3S,4S)-4-{[(5-Хлориндол-2-ил)карбонил]амино}тетрагидрофуран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
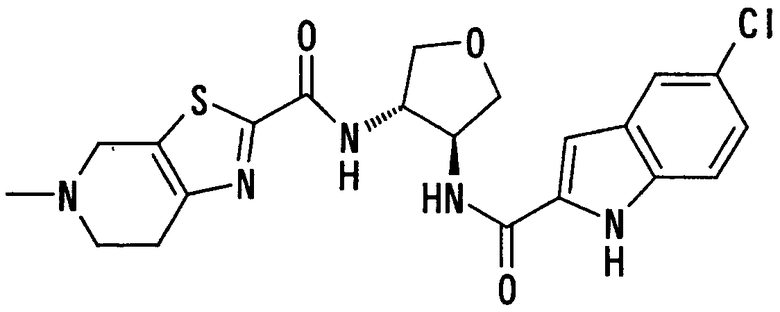
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 183, в соответствии со способами ссылочного примера 172 и примера 91.
1Н-ЯМР (CDCl3) δ: 2,51 (3H, с), 2,83 (2H, т, J=5,3Гц), 2,93 (2H, т, J=5,3Гц), 3,72 (2H, с), 3,78-3,89 (2H, м), 4,31 (1H, дд, J=9,2, 7,3Гц), 4,41-4,56 (2H, м), 4,63-4,75 (1H, м), 6,88 (1H, с), 7,22 (1H, дд, J=8,8, 2,0Гц), 7,32 (1H, д, J=8,8Гц), 7,35-7,46 (1H, м), 7,55 (1H, д, J=7,1Гц), 7,60 (1H, д, J=2,0Гц), 9,38 (1H, с).
МС (FAB) m/z: 460 (M+H+).
[Пример 93]
Гидрохлорид N-((3R,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}тетрагидрофуран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
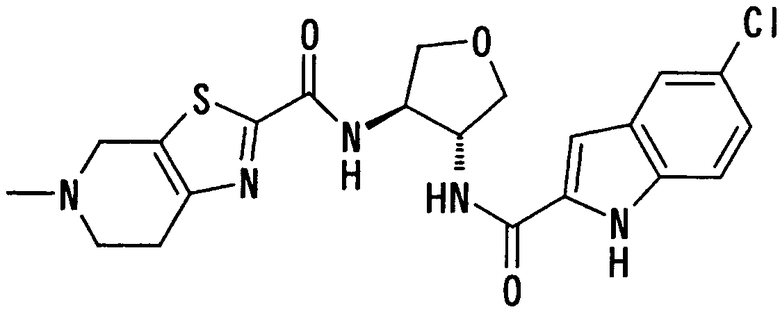
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 187, в соответствии со способами ссылочного примера 172 и примера 91.
Данные 1Н-ЯМР и МС (FAB): такие же, как у энантиомера в примере 92.
[Пример 94]
трет-Бутил (3R,4R)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-карбоксилат

Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 193, и соединения, полученного в ссылочном примере 10, в соответствии со способом примера 91.
Т.пл. 190-192°C.
1Н-ЯМР (CDCl3) δ: 1,45 (9H, с), 2,46 (3H, с), 2,74-2,81 (4H, м), 3,24-3,37 (2H, м), 3,54-3,70 (2H, м), 3,96-4,00 (1H, м), 4,15-4,23 (1H, м), 4,50-4,65 (1H, м), 4,77-4,82 (1H, м), 6,79, 6,87 (всего 1H, каждый с), 7,12-7,95 (5H, м), 9,91, 9,97 (всего 1H, каждый с).
МС (FAB) m/z: 559 (M+H+)
[Пример 95]
Гидрохлорид N-((3R,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}пирролидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
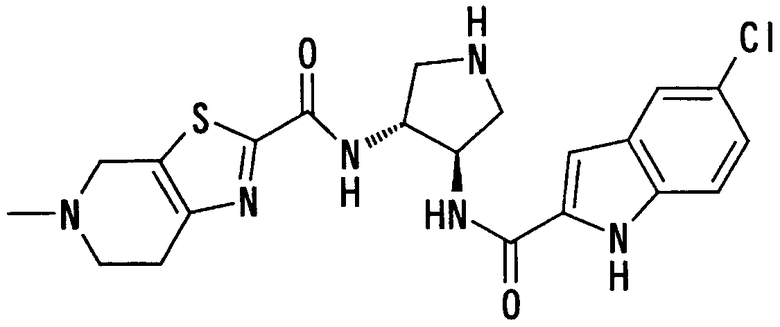
Соединение (170 мг), полученное в примере 94, растворяли в метиленхлориде (3 мл), добавляли при комнатной температуре трифторуксусную кислоту (2 мл) и смесь перемешивали в течение 1 часа. После концентрирования реакционной смеси добавляли хлороформ и насыщенный водный раствор гидрокарбоната натрия. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток очищали препаративной тонкослойной хроматографией на силикагеле (хлороформ:метанол:вода = 7:3:1 нижний слой). К полученному предполагаемому продукту добавляли метанольный раствор хлористоводородной кислоты с получением указанного в заголовке соединения (90 мг) в виде гидрохлорида (Данные ЯМР для свободного основания).
Т.пл. 248-250°C (разложение).
1Н-ЯМР (CDCl3) δ: 2,44 (3H, с), 2,70-2,80 (4H, м), 2,97-3,05 (2H, м), 3,46-3,68 (4H, м), 4,49-4,52 (1H, м), 4,60-4,65 (1H, м), 6,86 (1H, с), 7,05-7,08 (1H, м), 7,20 (1H, д, J=8,5Гц), 7,44 (1H, с), 7,89 (2H, шир.), 10,51 (1H, шир.).
МС (FAB) m/z: 459 (M+H+).
[Пример 96]
Гидрохлорид N-((3S,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-5-оксотетрагидрофуран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
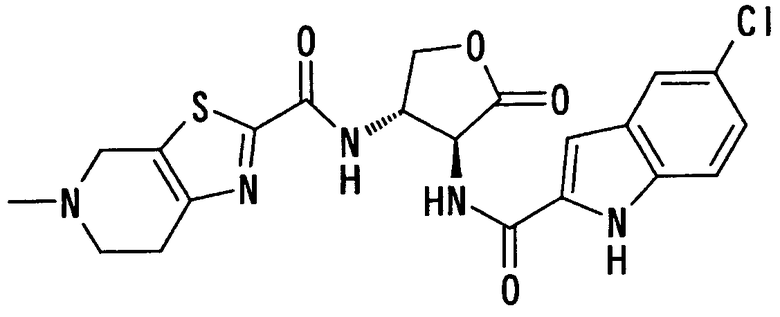
Указанное в заголовке соединение получали удалением трет-бутоксикарбонильной группы соединения, полученного в ссылочном примере 196, подобно способу ссылочного примера 69 и взаимодействием полученного продукта с соединением, полученным в ссылочном примере 10, подобно способу примера 91.
1Н-ЯМР (ДМСО-d6) δ: 2,90 (3H, с), 3,02-3,17 (2H, м), 3,23-3,34 (4H, м), 4,20 (1H, т, J=8,6Гц), 4,61 (1H, т, J=8,6Гц), 4,92-5,01 (1H, м), 5,14-5,26 (1H, м), 7,09 (1H, с), 7,19 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,73 (1H, д, J=2,0Гц), 9,27 (1H, д, J=6,8Гц), 9,35 (1H, д, J=6,8Гц), 11,22-11,33 (1H, м), 11,89 (1H, с).
МС (FAB) m/z: 474 (M+H+).
[Пример 97]
Гидрохлорид N-((3S,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-2-оксотетрагидрофуран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
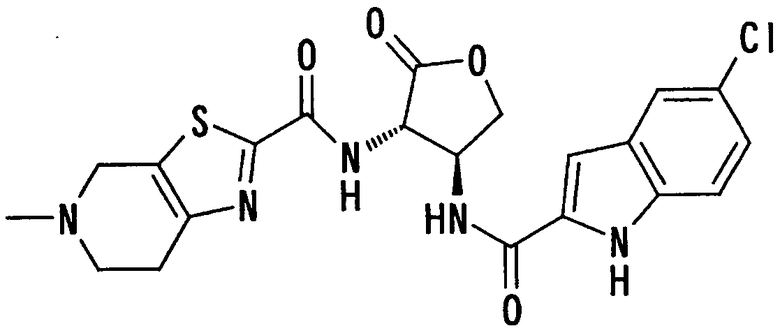
Указанное в заголовке соединение получали удалением трет-бутоксикарбонильной группы соединения, полученного в ссылочном примере 197, подобно способу ссылочного примера 69 и взаимодействием полученного продукта с 5-хлориндол-2-карбоновой кислотой подобно способу примера 91.
1Н-ЯМР (ДМСО-d6) δ: 2,52 (3H, с), 2,83 (2H, т, J=5,9Гц), 2,91-3,00 (2H, м), 3,73 (2H, с), 4,23 (1H, т, J=8,6Гц), 4,40-4,53 (1H, м), 4,96 (1H, дд, J=10,8, 5,2Гц), 5,16 (1H, дд, J=9,2, 7,3Гц), 7,01 (1H, с), 7,25 (1H, дд, J=8,8, 2,0Гц), 7,34 (1H, д, J=8,8Гц), 7,52 (1H, д, J=2,0Гц), 8,01 (1H, д, J=5,4Гц), 8,51-8,63 (1H, м), 9,22 (1H, с).
МС (FAB) m/z: 474 (M+H+).
[Пример 98]
Гидрохлорид этил (3S,4R)-2-(3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}-2-оксопирролидин-1-ил)ацетата
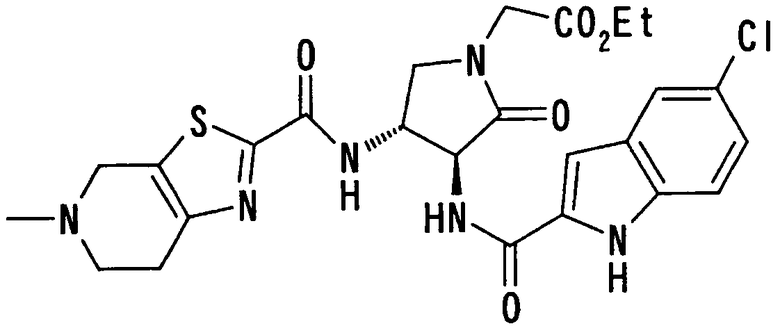
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 199, и соединения, полученного в ссылочном примере 10, подобно способу примера 91. Данные ЯМР для свободного основания.
1Н-ЯМР (ДМСО-d6) δ: 1,19 (3H, т, J=7,1Гц), 2,35 (3H, с), 2,71-2,84 (2H, м), 2,80-2,90 (2H, м), 3,40 (1H, д, J=10,3Гц), 3,61 (2H, д, J=10,8Гц), 3,84 (1H, дд, J=10,3, 5,6Гц), 4,01-4,23 (4H, м), 4,80-4,94 (1H, м), 5,04 (1H, т, J=8,6Гц), 7,01 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,40 (1H, д, J=8,8Гц), 7,69 (1H, д, J=2,0Гц), 8,73 (1H, д, J=8,6Гц), 8,90 (1H, д, J=8,8Гц), 11,86 (1H, с).
МС (FAB) m/z: 559 (M+H+).
[Пример 99]
N-((3R,4S)-4-{[(5-Хлориндол-2-ил)карбонил]амино}-1-метил-5-оксопирролидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
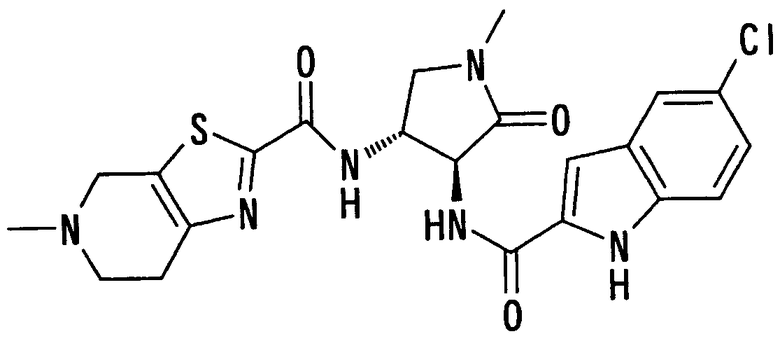
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 201, и соединения, полученного в ссылочном примере 10, подобно способу примера 91.
1Н-ЯМР (CDCl3) δ: 2,49 (3H, с), 2,77-2,82 (2H, м), 2,86-2,91 (5H, м), 3,69 (2H, д, J=1,2Гц), 4,39-4,54 (3H, м), 4,93-4,98 (1H, м), 6,98 (1H, д, J=1,2Гц), 7,05-7,34 (3H, м), 7,63 (1H, д, J=2,0Гц), 8,11 (1H, д, J=7,8Гц), 9,00 (1H, с)
МС (FAB) m/z: 487 (M+H+).
[Пример 100]
Метил 2-[((3R,4R)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)сульфонил]ацетат
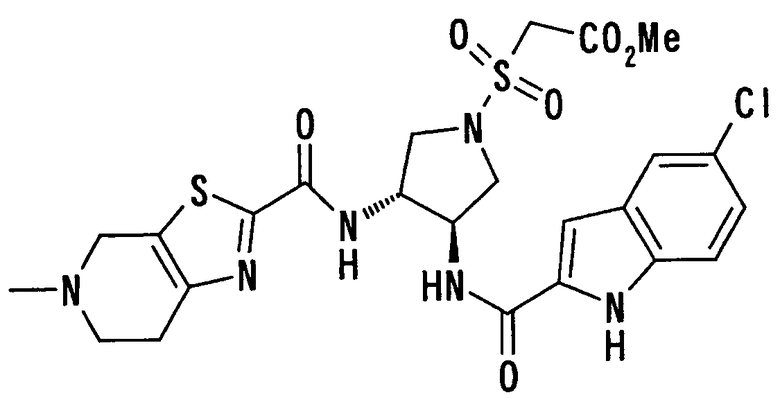
Соединение (230 мг), полученное в примере 95, и триэтиламин (0,10 мл) растворяли в метиленхлориде (6,9 мл) и смесь охлаждали льдом. Добавляли метоксикарбонилметансульфонилхлорид (Synthesis, p. 321, 1975) (105 мг) и полученную смесь нагревали до комнатной температуры и перемешивали в течение ночи. Реакционную смесь разбавляли хлороформом, промывали водой и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток очищали препаративной тонкослойной хроматографией на силикагеле (хлороформ:метанол = 20:1) и превращали в порошок смесью метанол-вода с получением указанного в заголовке соединения (150 мг).
1Н-ЯМР (CDCl3) δ: 2,48 (3H, с), 2,76-2,86 (4H, м), 3,49-3,73 (4H, м), 3,87 (3H, с), 3,94-3,98 (1H, м), 4,08-4,11 (1H, м), 4,13 (2H, с), 4,69-4,72 (1H, м), 4,88-4,91 (1H, м), 6,89 (1H, с), 7,12-7,15 (1H, м), 7,27-7,28 (1H, м), 7,50 (1H, с), 7,81-7,86 (2H, м), 9,92 (1H, с).
МС (FAB) m/z: 595 (M+H+).
[Пример 101]
2-[((3R,4R)-3-{[(5-Хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)сульфонил]уксусная кислота
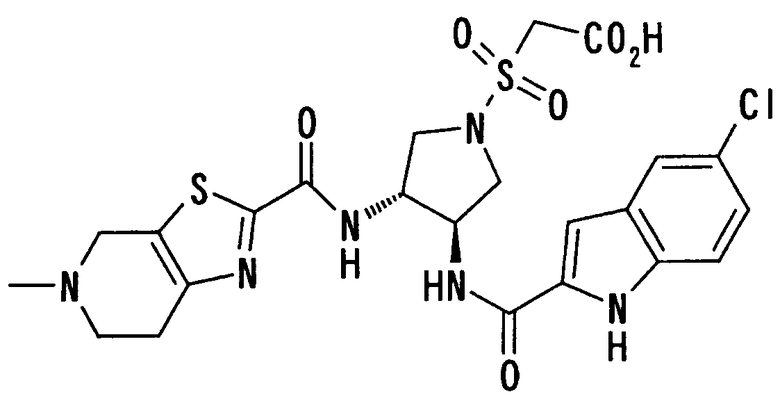
Соединение (100 мг), полученное в примере 100, растворяли в смеси тетрагидрофуран (4 мл)-вода (1 мл) и смесь охлаждали льдом. Добавляли моногидрат гидроксида лития (7,8 мг) и полученную смесь нагревали до комнатной температуры и перемешивали в течение 4 часов. После нейтрализации реакционной смеси 1N хлористоводородной кислотой смесь концентрировали. Осадки отфильтровывали, промывали водой и 50% этанолом и сушили в течение ночи при 50°C при пониженном давлении с получением указанного в заголовке соединения (87 мг).
1Н-ЯМР (ДМСО-d6) δ: 2,50 (3H, с), 2,92 (4H, с), 3,34-3,43 (4H, м), 3,76-3,85 (2H, м), 4,27 (каждый 1H, система AB д, J=14,5Гц), 4,65-4,71 (1H, м), 4,78-4,84 (1H, м), 7,14 (1H, с), 7,18 (1H, д, J=8,8Гц), 7,40 (1H, д, J=8,8Гц), 7,72 (1H, с), 8,87 (1H, д, J=7,8Гц), 9,12 (1H, д, J=8,2Гц), 11,83 (1H, с).
[Пример 102]
Метил 2-((3R,4R)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)ацетат
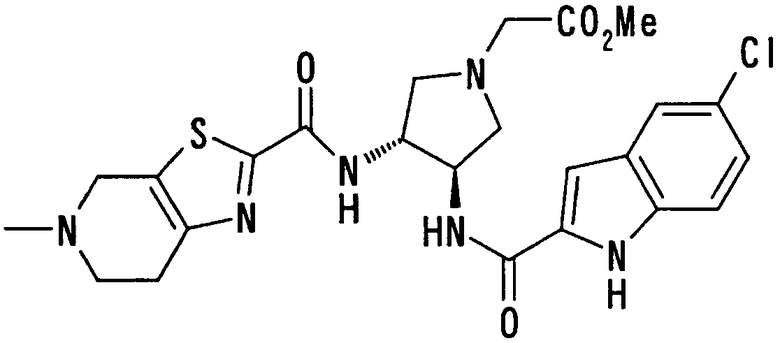
Соединение (230 мг), полученное в примере 95, и карбонат калия (90 мг) растворяли в N,N-диметилформамиде (4,6 мл) и смесь охлаждали льдом. Добавляли метилбромацетат (0,062 мл) и полученную смесь перемешивали 45 минут. Реакционную смесь разбавляли этилацетатом, промывали водой и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток очищали препаративной тонкослойной хроматографией на силикагеле (хлороформ:метанол = 10:1) и отверждали смесью метанол-вода с получением указанного в заголовке соединения (190 мг).
1Н-ЯМР (CDCl3) δ: 2,35 (2H, с), 2,48 (3H, с), 2,73-2,95 (4H, м), 3,34-3,42 (2H, м), 3,46 (2H, кв, J=6,5Гц), 3,67 (2H, кв, J=6,5Гц), 3,75 (3H, с), 4,57-4,71 (2H, м), 6,91 (1H, с), 7,10-7,13 (1H, м), 7,31 (1H, д, J=9,0Гц), 7,53 (1H, с), 7,77 (1H, д, J=8,0Гц), 7,87 (1H, д, J=6,8Гц), 10,22 (1H, с).
МС (FAB) m/z: 531 (M+H+).
[Пример 103]
2-((3R,4R)-3-{[(5-Хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)уксусная кислота
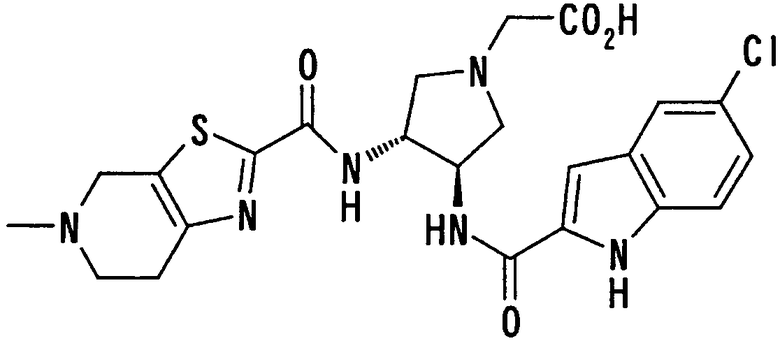
Указанное в заголовке соединение получали из соединения, полученного в примере 102, подобно способу примера 101.
1Н-ЯМР (ДМСО-d6) δ: 2,42 (3H, с), 2,69-2,87 (6H, м), 3,13 (1H, т, J=9,0Гц), 3,22 (1H, т, J=9,0Гц), 3,33 (каждый 1H, система AB д, J=6,8Гц), 3,72 (2H, с), 4,53-4,60 (1H, м), 4,65-4,72 (1H, м), 7,16-7,20 (2H, м), 7,42 (1H, д, J=8,8Гц), 7,70 (1H, с), 8,85 (1H, д, J=7,5Гц), 9,00 (1H, д, J=8,3Гц), 11,79 (1H, с).
[Пример 104]
Метил 3-((3R,4R)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)пропионат
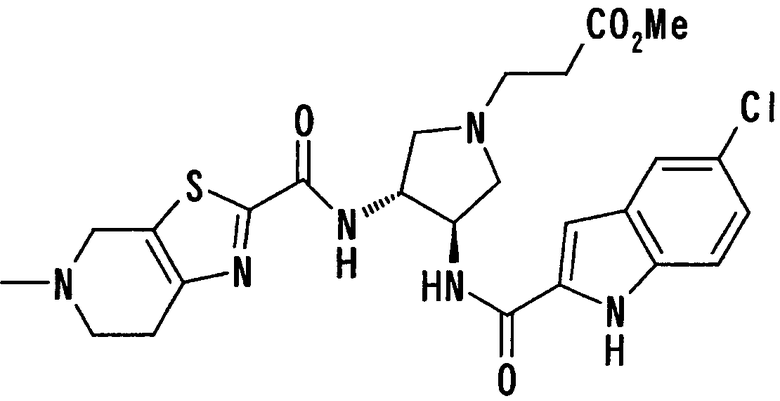
Указанное в заголовке соединение получали из соединения, полученного в примере 95, и метил 3-бромпропионата подобно способу примера 102.
1Н-ЯМР (CDCl3) δ: 1,96-2,20 (2H, м), 2,49 (3H, с), 2,61-2,96 (8H, м), 3,17-3,21 (2H, м), 3,62-3,72 (2H, м), 3,69 (3H, с), 4,46-4,49 (1H, м), 4,56-4,61 (1H, м), 6,87 (1H, с), 7,05-7,14 (1H, м), 7,32 (1H, д, J=9,2Гц), 7,53 (1H, с), 7,65-7,71 (2H, м), 10,02 (1H, с).
МС (FAB) m/z: 545 (M+H+).
[Пример 105]
3-((3R,4R)-3-{[(5-Хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)пропионовая кислота
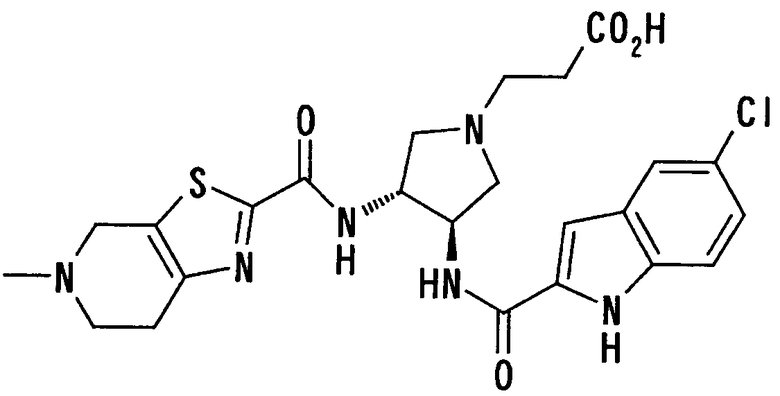
Указанное в заголовке соединение получали из соединения, полученного в примере 104, подобно способу примера 101.
1Н-ЯМР (ДМСО-d6) δ: 2,38 (3H, с), 2,39-2,84 (10H, м), 2,93 (1H, т, J=8,8Гц), 3,05 (1H, т, J=8,8Гц), 3,65 (2H, с), 4,51-4,56 (1H, м), 4,63-4,68 (1H, м), 7,16-7,19 (2H, м), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,81 (1H, д, J=7,8Гц), 8,97 (1H, д, J=8,3Гц), 11,75 (1H, с).
[Пример 106]
Этил 3-((3R,4R)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)-3-оксопропионат
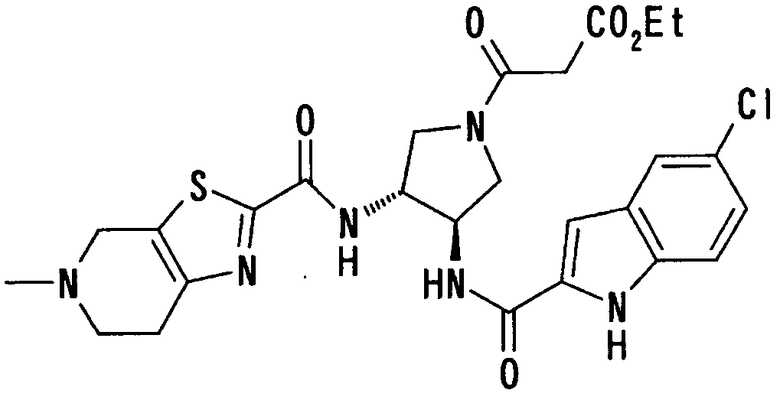
Указанное в заголовке соединение получали из соединения, полученного в примере 95, и этилмалонилхлорида подобно способу примера 100.
1Н-ЯМР (ДМСО-d6) δ: 1,20 (3H, т, J=7,0Гц), 2,37 (3H, с), 2,73-2,75 (2H, м), 2,82-2,84 (2H, м), 3,35-3,38 (2H, м), 3,64 (2H, с), 3,68-3,83 (2H, м), 3,91-4,00 (2H, м), 4,10 (2H, кв, J=7,0Гц), 4,61-4,84 (2H, м), 7,13 (1H, с), 7,18 (1H, дд, J=8,5, 2,0Гц), 7,41 (1H, д, J=8,5Гц), 7,72 (1H, с), 8,73 (1H, т, J=9,0Гц), 9,10 (1H, д, J=9,0Гц), 11,79 (1H, с).
[Пример 107]
3-((3R,4R)-3-{[(5-Хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)-3-оксопропионовая кислота
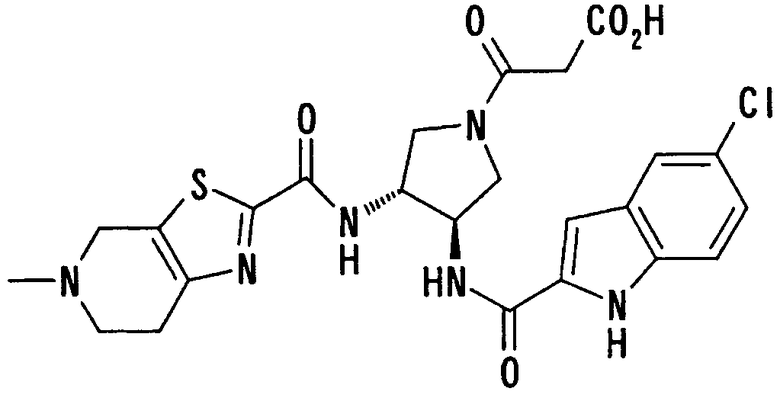
Указанное в заголовке соединение получали из соединения, полученного в примере 106, подобно способу примера 101.
1Н-ЯМР (ДМСО-d6) δ: 2,39 (3H, с), 2,77 (2H, с), 2,85 (2H, с), 3,29-3,55 (4H, м), 3,68 (2H, с), 3,82-4,01 (2H, м), 4,62-4,68 (1H, м), 4,77-4,86 (1H, м), 7,14 (1H, с), 7,18 (1H, д, J=8,8Гц), 7,41 (1H, д, J=8,8Гц), 7,72 (1H, с), 8,75 (1H, т, J=8,8Гц), 9,12 (1H, д, J=7,8Гц), 11,81 (1H, с).
[Пример 108]
Метил 1-[((3R,4R)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)метил]циклопропанкарбоксилат
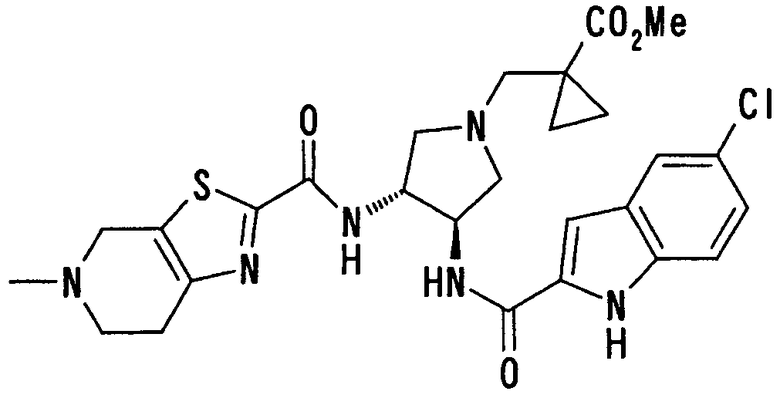
Указанное в заголовке соединение получали из соединения, полученного в примере 95, и метил 1-(бромметил)циклопропанкарбоксилата подобно способу примера 102.
1Н-ЯМР (CDCl3) δ: 0,78-0,79 (2H, м), 1,24-1,26 (2H, м), 2,49 (3H, с), 2,62-2,88 (6H, м), 3,20-3,28 (2H, м), 3,66 (3H, с), 3,61-3,75 (4H, м), 4,45-4,62 (2H, м), 6,86 (1H, с), 7,12-7,15 (1H, м), 7,24-7,28 (1H, м), 7,52 (1H, д, J=8,5Гц), 7,54 (1H, с), 7,69 (1H, д, J=8,0Гц), 10,00 (1H, с).
МС (ESI) m/z: 571 (M+H+).
[Пример 109]
1-[((3R,4R)-3-{[(5-Хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)метил]циклопропанкарбоновая кислота
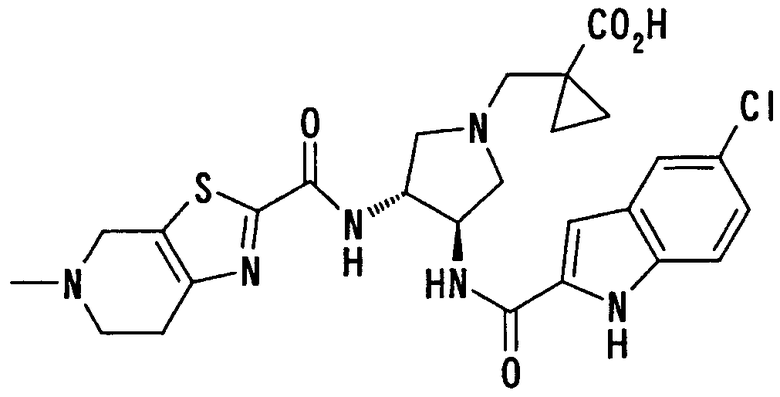
Указанное в заголовке соединение получали из соединения, полученного в примере 108, подобно способу примера 101.
1Н-ЯМР (ДМСО-d6) δ: 0,73-0,78 (2H, м), 1,04-1,07 (2H, м), 2,37 (3H, с), 2,65-2,84 (6H, м), 3,11-3,20 (4H, м), 3,64 (2H, с), 4,59-4,74 (2H, м), 7,16 (1H, с), 7,17 (1H, д, J=8,5Гц), 7,40 (1H, д, J=8,5Гц), 7,70 (1H, с), 8,84 (1H, д, J=7,5Гц), 9,12 (1H, д, J=7,5Гц), 11,77 (1H, с).
[Пример 110]
трет-Бутил (3R,4R)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-карбоксилат
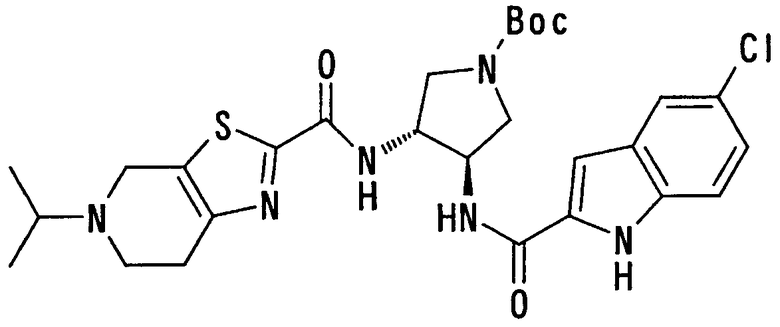
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 193 и ссылочном примере 148, подобно способу примера 91.
1Н-ЯМР (CDCl3) δ: 1,12 (6H, д, J=6,6Гц), 1,47 (9H, с), 2,83-2,88 (4H, м), 2,94-2,99 (1H, м), 3,20-3,29 (1H, м), 3,31-3,42 (1H, м), 3,75-3,81 (2H, м), 3,98 (1H, т, J=8,5Гц), 4,15-4,35 (2H, м), 4,50-4,65 (1H, м), 6,85, 6,91 (всего 1H, каждый с), 7,15-7,90 (5H, м), 9,41, 9,50 (всего 1H, каждый с).
[Пример 111]
N-((3R,4R)-4-{[(5-Хлориндол-2-ил)карбонил]амино}пирролидин-3-ил)-5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
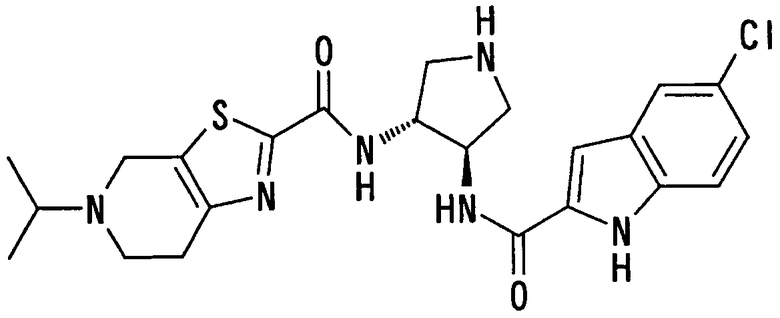
Указанное в заголовке соединение получали из соединения, полученного в примере 110, подобно способу примера 95.
1Н-ЯМР (CDCl3) δ: 1,13 (6H, д, J=6,3Гц), 2,85 (4H, шир.с), 2,96-3,05 (3H, м), 4,51-4,52 (1H, м), 4,76-4,80 (2H, м), 5,36-5,39 (2H, м), 5,53-5,58 (1H, м), 7,17-7,19 (1H, м), 7,27-7,31 (2H, м), 7,57 (1H, с), 7,64 (2H, шир.), 9,82 (1H, шир.).
[Пример 112]
Этил 3-((3R,4R)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)пропионат
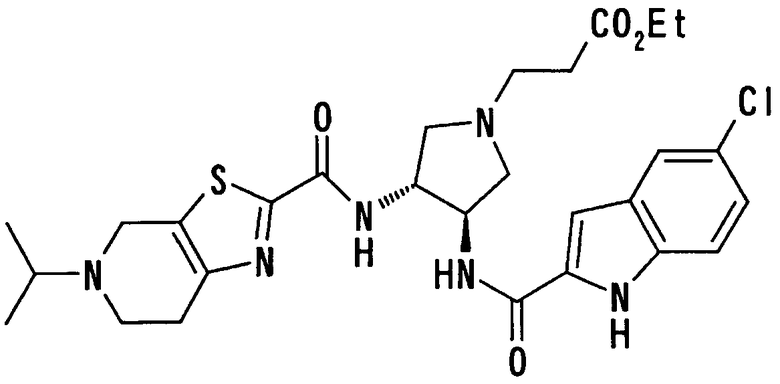
Указанное в заголовке соединение получали из соединения, полученного в примере 111, и этил 3-бромпропионата подобно способу примера 102.
1Н-ЯМР (CDCl3) δ: 1,14 (6H, д, J=6,5Гц), 1,26 (3H, т, J=7,0Гц), 2,51 (3H, т, J=7,0Гц), 2,63 (1H, дд, J=9,5, 6,5Гц), 2,73-2,91 (6H, м), 2,95-3,02 (1H, м), 3,22 (2H, кв, J=7,0Гц), 3,81 (каждый 1H, система AB д, J=14,5Гц), 4,16 (2H, кв, J=7,0Гц), 4,40-4,45 (1H, м), 4,52-4,59 (1H, м), 6,88 (1H, д, J=2,0Гц), 7,17-7,19 (1H, м), 7,30-7,32 (2H, м), 7,59 (1H, с), 7,62 (1H, с), 9,56 (1H, с).
МС (FAB) m/z: 587 (M+H+).
[Пример 113]
3-((3R,4R)-3-{[(5-Хлориндол-2-ил)карбонил]амино}-4-{[(5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-ил)пропионовая кислота
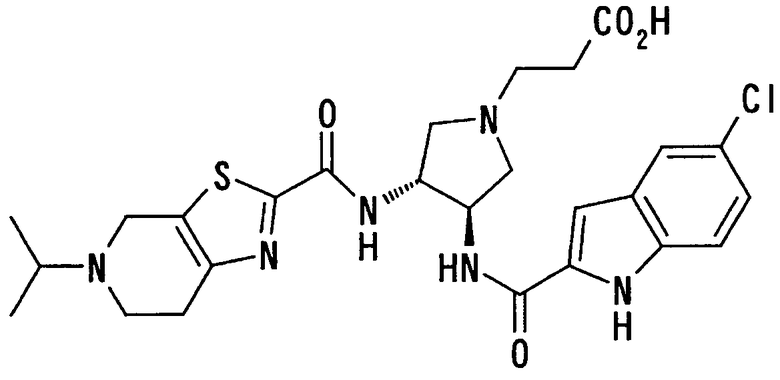
Указанное в заголовке соединение получали из соединения, полученного в примере 112, подобно способу примера 101.
1Н-ЯМР (ДМСО-d6) δ: 1,04 (6H, д, J=6,6Гц), 2,40 (2H, кв, J=7,0Гц), 2,50 (4H, с), 2,60-2,74 (4H, м), 2,90-2,94 (2H, м), 3,02-3,06 (1H, м), 3,20-3,35 (2H, м), 4,50-4,53 (1H, м), 4,61-4,65 (1H, м), 7,15-7,18 (2H, м), 7,41 (1H, д, J=8,8Гц), 7,68 (1H, с), 8,78 (1H, д, J=7,5Гц), 8,90 (1H, д, J=8,0Гц), 11,73 (1H, с).
[Пример 114]
Гидрохлорид N-((3R,4R)-1-ацетил-4-{[(5-хлориндол-2-ил)карбонил]амино}пирролидин-3-ил)-5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
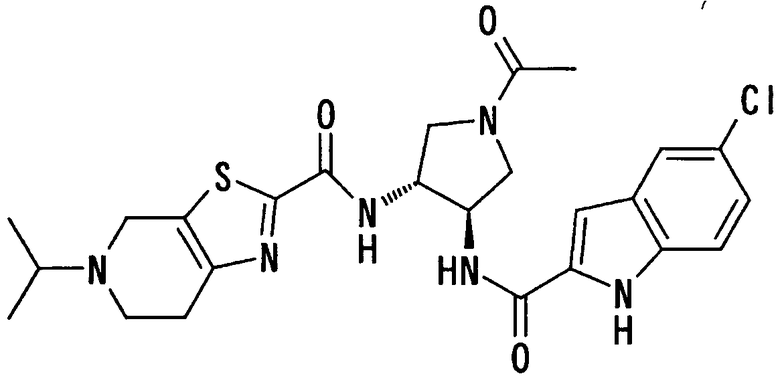
Указанное в заголовке соединение получали из соединения, полученного в примере 111, и уксусного ангидрида подобно способу примера 100.
Т.пл. 254-258°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,34-1,37 (6H, м), 1,96 (3H, с), 3,30-3,55 (5H, м), 3,66-3,82 (3H, м), 3,95 (1H, кв, J=8,3Гц), 4,45-4,82 (4H, м), 7,15 (1H, с), 7,18 (1H, д, J=9,0Гц), 7,41 (1H, д, J=9,0Гц), 7,71 (1H, с), 8,75-8,81 (1H, м), 9,21 (1H, д, J=8,0Гц), 11,32 (1H, шир.), 11,83 (1H, д, J=7,3Гц).
МС (FAB) m/z: 529 (M+H+).
[Пример 115]
Гидрохлорид N-[(3R,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(метилсульфонил)пирролидин-3-ил]-5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
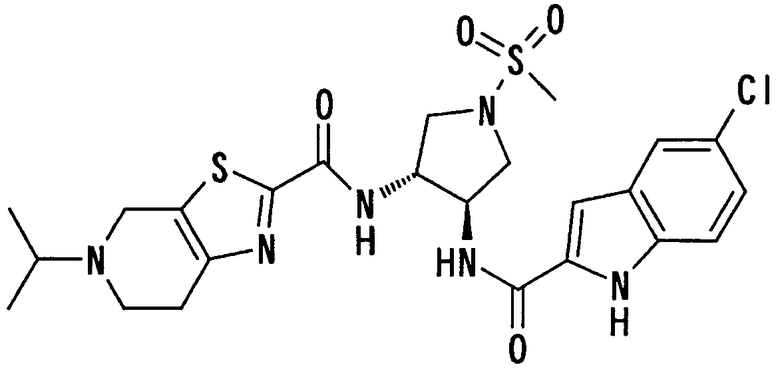
Указанное в заголовке соединение получали из соединения, полученного в примере 111, и метансульфонилхлорида подобно способу примера 100.
Т.пл. 230-235°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,32-1,36 (6H, м), 3,32 (3H, с), 3,43-3,46 (5H, м), 3,68-3,75 (4H, м), 4,48 (1H, м), 4,62-4,72 (2H, м), 4,83 (1H, т, J=5,5Гц), 7,14 (1H, с), 7,18 (1H, д, J=8,6Гц), 7,40 (1H, д, J=8,6Гц), 7,72 (1H, с), 8,82 (1H, шир.), 9,20 (1H, д, J=8,3Гц), 11,30 (1H, шир.), 11,86 (1H, д, J=7,5Гц).
МС (FAB) m/z: 565 (M+H+).
[Пример 116]
Гидрохлорид этил (3R,4R)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пирролидин-1-карбоксилата
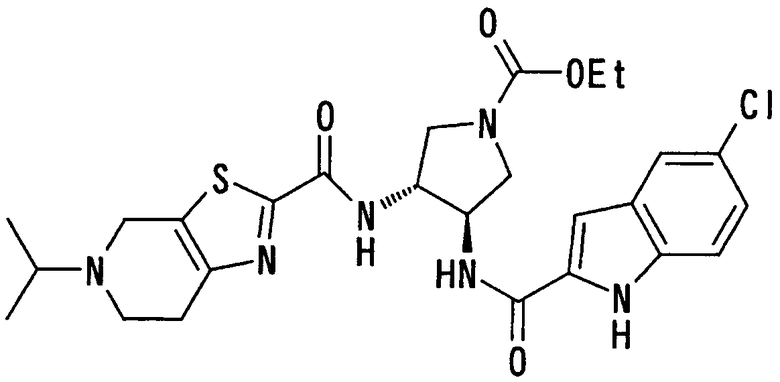
Указанное в заголовке соединение получали из соединения, полученного в примере 111, и этилхлорформиата подобно способу примера 100.
Т.пл. 225-228°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,20 (3H, т, J=7,0Гц), 1,31-1,37 (6H, м), 3,33-3,45 (5H, м), 3,66-3,75 (4H, м), 4,05 (2H, кв, J=7,0Гц), 4,45-4,77 (4H, м), 7,15 (1H, с), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,71 (1H, д, J=2,0Гц), 8,77 (1H, д, J=7,0Гц), 9,20 (1H, д, J=8,0Гц), 11,30 (1H, шир.), 11,83 (1H, д, J=7,5Гц).
МС (FAB) m/z: 559 (M+H+).
[Пример 117]
трет-Бутил (3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-карбоксилат
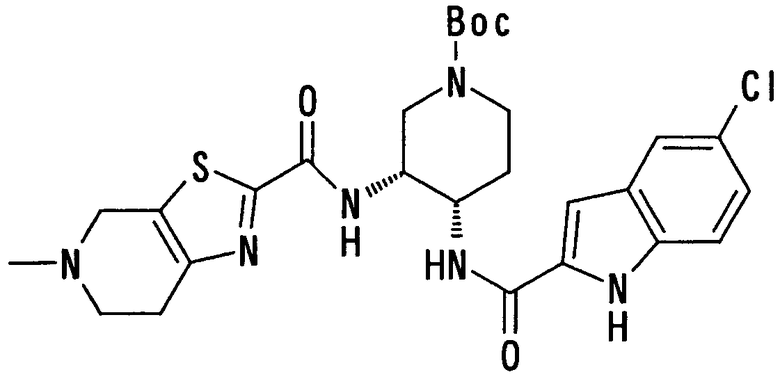
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 207 и ссылочном примере 10, подобно способу примера 91.
Т.пл. 152-154°C (разложение).
1Н-ЯМР (CDCl3) δ: 1,53 (9H, с), 1,62-1,80 (1H, м), 2,23-2,30 (1H, м), 2,52 (3H, с), 2,75-3,05 (5H, м), 3,10-3,25 (1H, м), 3,68-3,82 (2H, м), 4,15-4,45 (4H, м), 6,89 (1H, с), 7,19 (1H, дд, J=8,8, 1,8Гц), 7,32 (1H, д, J=8,8Гц), 7,92 (1H, д, J=1,8Гц), 7,75 (1H, шир.с), 8,21 (1H, шир.с), 9,39 (1H, с).
МС (ESI) m/z: 573 (М+Н)+.
[Пример 118]
Дигидрохлорид N-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
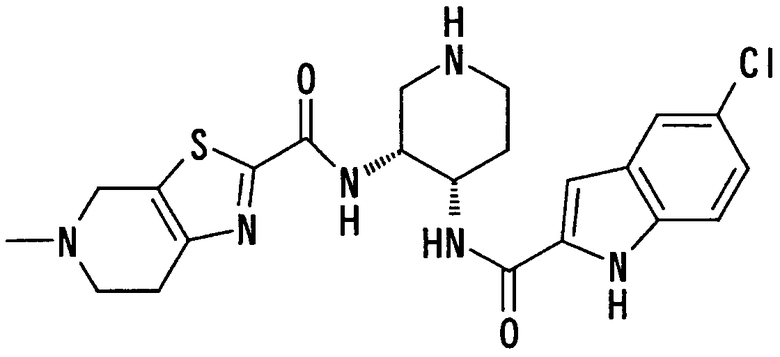
Указанное в заголовке соединение получали из соединения, полученного в примере 117, подобно способу примера 95.
Т.пл. 240-258°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,85-2,00 (1H, м), 2,05-2,20 (2H, м), 2,93 (3H, с), 3,05-3,60 (7H, м), 3,65-3,75 (1H, м), 4,10-4,52 (2H, м), 4,60-4,75 (2H, м), 7,10-7,21 (2H, м), 7,43 (1H, д, J=8,6Гц), 7,70 (1H, с), 8,50 (1H, шир.д, J=7,8Гц), 8,90-9,05 (2H, м), 9,27 (1H, шир.с), 11,9 (1H, шир.д, J=13,4Гц).
МС (ESI) m/z: 473 (M+H)+.
[Пример 119]
трет-Бутил (3R*,4S*)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-карбоксилат
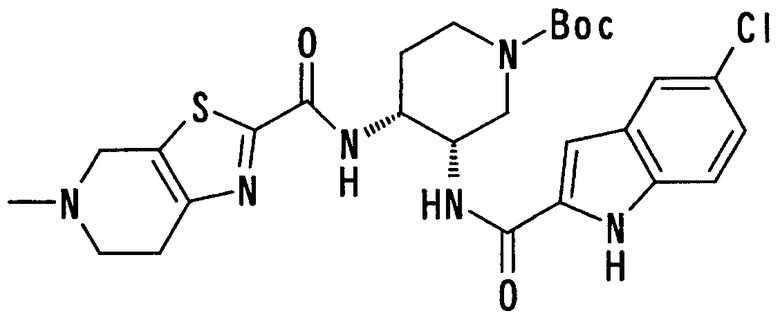
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 208, и 5-хлориндол-2-карбоновой кислоты подобно способу примера 91.
Т.пл. 187-189°C (разложение).
1Н-ЯМР (CDCl3) δ: 1,48 (9H, с), 1,72-1,90 (1H, м), 2,00 (1H, шир.с), 2,00-2,10 (1H, м), 2,45 (3H, с), 2,60-2,70 (2H, м), 2,70-2,80 (2H, м), 3,23 (1H, т, J=10,8Гц), 3,35-3,50 (1H, м), 3,50-3,72 (2H, м), 3,90-4,20 (2H, м), 4,30-4,40 (1H, м), 4,45-4,55 (1H, м), 6,85 (1H, д, J=1,5Гц), 7,17 (1H, дд, J=8,8, 1,9Гц), 7,20-7,30 (1H, м), 7,33 (1H, д, J=8,8Гц), 7,58 (1H, д, J=1,9Гц), 10,17 (1H, с).
МС (ESI) m/z: 573 (M+H+).
[Пример 120]
Дигидрохлорид N-((3R*,4S*)-3-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-4-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
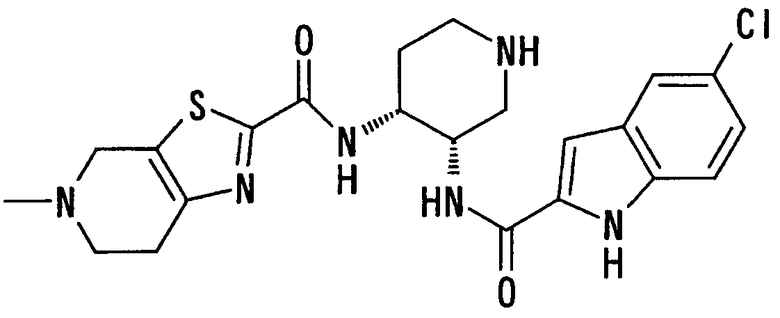
Указанное в заголовке соединение получали из соединения, полученного в примере 119, подобно способу примера 95.
Т.пл. 276-278°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,77-1,88 (1H, м), 2,40-2,50 (2H, м), 2,89 (3H, с), 2,90-3,20 (4H, м), 3,30-3,50 (2H, м), 3,63 (1H, шир.с), 4,33-4,47 (2H, м), 4,62-4,75 (2H, м), 7,18 (1H, дд, J=8,8, 1,9Гц), 7,42 (1H, д, J=8,8Гц), 7,48 (1H, шир.с), 7,71 (1H, д, J=1,9Гц), 8,66 (1H, шир.с), 8,95 (1H, д, J=8,1Гц), 9,20-9,30 (1H, м), 9,45-9,70 (1H, м), 11,61 (1H, с), 11,90 (1H, с).
МС (ESI) m/z: 473 (M+H)+.
[Пример 121]
трет-Бутил (3R*,4S*)-4-{[(5-фториндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-карбоксилат
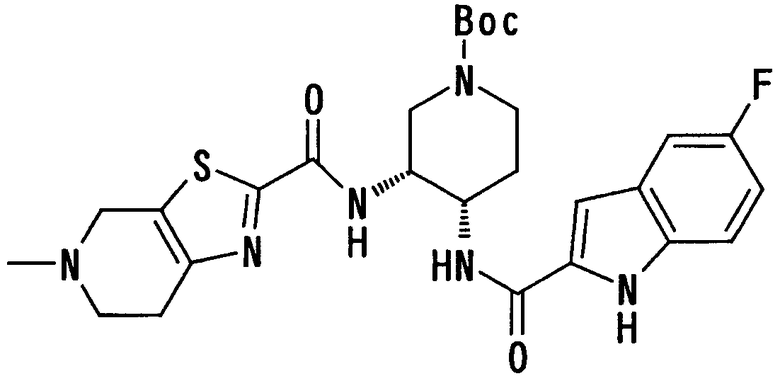
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 209 и ссылочном примере 10, подобно способу примера 91.
1Н-ЯМР (CDCl3) δ: 1,53 (9H, с), 1,65-1,78 (1H, м), 2,23-2,32 (1H, шир.), 2,52 (3H, с), 2,78-3,03 (5H, м), 3,15-3,24 (1H, шир.), 3,68-3,82 (2H, шир.), 4,16-4,45 (4H, шир.), 6,91 (1H, с), 7,02 (1H, тд, J=9,0, 2,7Гц), 7,30 (1H, дд, J=9,0, 2,7Гц), 7,34 (1H, дд, J=9,0, 4,4Гц), 7,65-7,90 (1H, шир.), 8,10-8,40 (1H, шир.), 9,31-9,41 (1H, шир.).
МС (ESI) m/z: 557 (M+H+).
[Пример 122]
Дигидрохлорид N-((3R*,4S*)-4-{[(5-фториндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
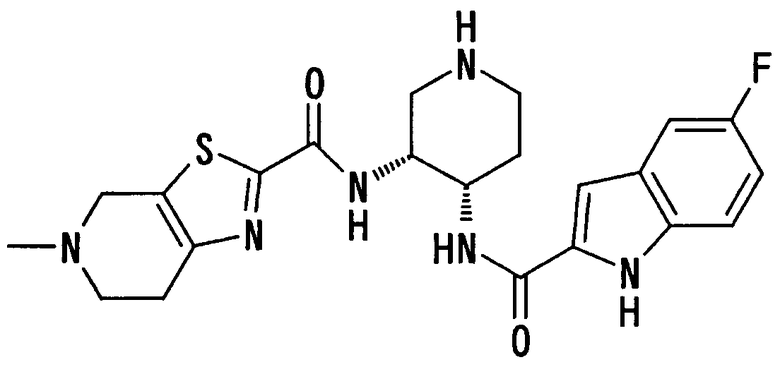
Указанное в заголовке соединение получали из соединения, полученного в примере 121, подобно способу примера 95.
Т.пл. 236-245°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,85-1,98 (1H, шир.), 2,06-2,18 (1H, шир.), 2,89 (3H, с), 3,05-3,75 (8H, с), 4,34-4,54 (2H, шир.), 4,60-4,75 (2H, шир.), 7,04 (1H, тд, J-9,3, 2,4Гц), 7,15 (1H, шир.с), 7,37-7,44 (2H, м), 8,46 (1H, д, J=7,8Гц), 8,88-9,00 (1H, шир.), 9,09-9,27 (2H, шир.), 11,55-11,75 (1H, шир.), 11,76-11,84 (1H, шир.).
МС (FAB) m/z: 457 (M+H+).
[Пример 123]
Гидрохлорид N-((3R*,4S*)-1-ацетил-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
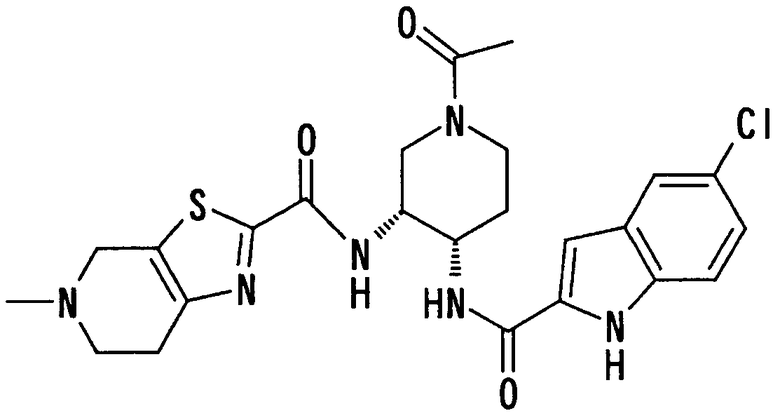
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и уксусного ангидрида подобно способу примера 100.
Т.пл. 215-225°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,65-1,85 (1H, м), 1,88, 2,06 (всего 3H, каждый с), 1,90-2,10 (1H, м), 2,91 (3H, с), 3,00-3,30 (2H, м), 3,30-3,55 (2H, м), 3,60-3,90 (3H, м), 3,98-4,50 (4H, м), 4,65-4,75 (1H, м), 7,09 (1H, д, J=15,6Гц), 7,17 (1H, д, J=8,8Гц), 7,41 (1H, д, J=8,8Гц), 7,71 (1H, с), 8,23-8,53 (2H, м), 11,20-11,55 (1H, м), 11,85 (1H, шир.д, J=5,4Гц).
МС (ESI) m/z: 515 (M+H+).
[Пример 124]
Гидрохлорид N-((3R*,4S*)-1-ацетил-3-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-4-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
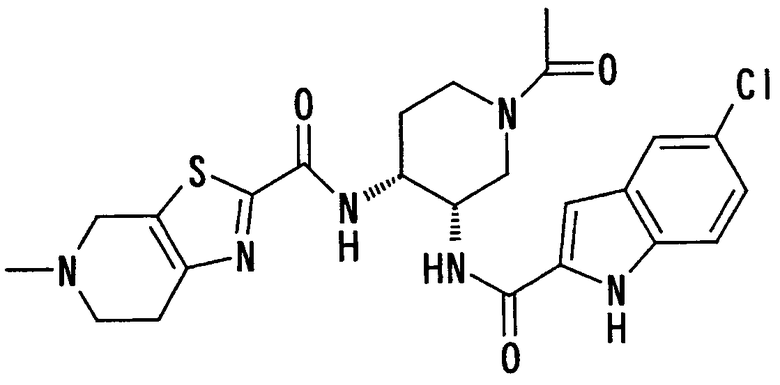
Указанное в заголовке соединение получали из соединения, полученного в примере 120, и уксусного ангидрида подобно способу примера 100.
Т.пл. 225-250°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,65-1,80 (1H, м), 1,81, 2,05 (всего 3H, каждый с), 2,00-2,20 (1H, м), 2,70-2,85 (1H, м), 2,89 (3H, с), 3,00-3,20 (2H, м), 3,20-3,50 (2H, м), 3,64 (1H, шир.с), 3,78-4,30 (2H, м), 4,30-4,50 (3H, м), 4,55-10 4,75 (1H, м), 7,05-7,23 (2H, м), 7,38-7,48 (1H, м), 7,70-7,80 (1H, м), 7,79, 8,12 (всего 1H, каждый д, J=6,8Гц), 8,73, 8,83 (всего 1H, каждый д, J=8,3Гц), 11,20-11,50 (1H, м), 11,89, 11,92 (всего 1H, каждый с).
МС (FAB) m/z: 515 (M+H+).
[Пример 125]
Гидрохлорид N-((3R*,4S*)-1-ацетил-4-{[(5-фториндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
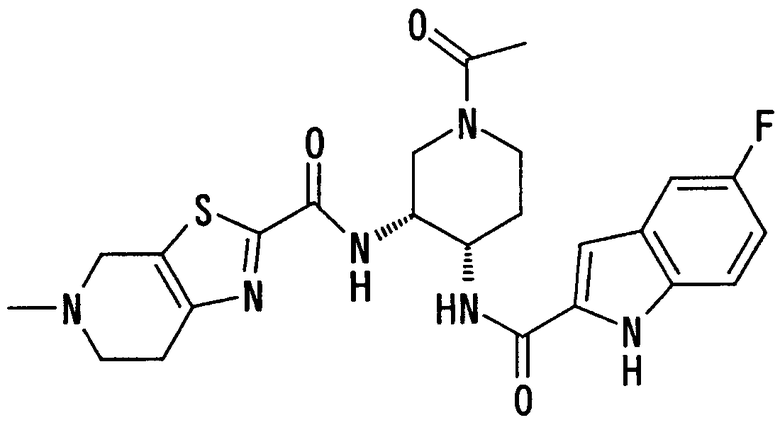
Указанное в заголовке соединение получали из соединения, полученного в примере 122, и уксусного ангидрида подобно способу примера 100.
Т.пл. 202°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,67-1,85 (1H, м), 1,87 (1,5H, с), 1,87-2,10 (1H, м), 2,06 (1,5H, с), 2,88-2,96 (3H, шир.с), 3,05-3,30 (2H, м), 3,32-3,83 (5H, шир.), 3,97-4,33 (2H, м), 4,35-4,50 (2H, шир.), 4,67-4,78 (1H, шир.), 7,01-7,14 (2H, м), 7,38-7,44 (2H, м), 8,25-8,50 (2H, м), 10,85-11,15 (1H, шир.), 11,72-11,80 (1H, шир.).
МС (FAB) m/z: 499 (M+H+).
[Пример 126]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(метилсульфонил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
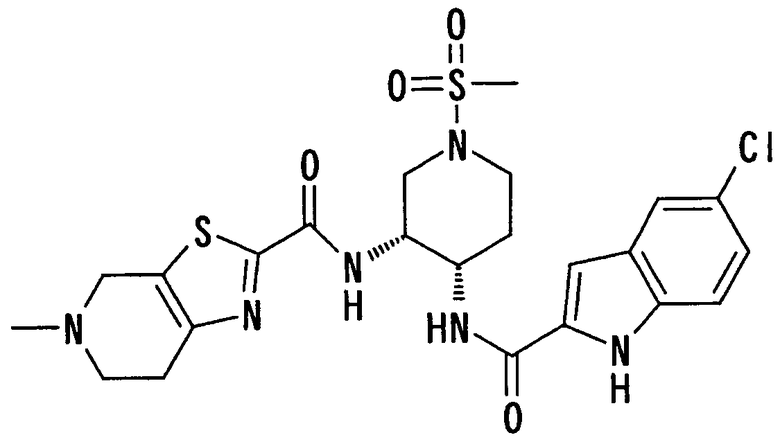
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и метансульфонилхлорида подобно способу примера 100.
Т.пл. 225-230°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,80-1,90 (1H, м), 2,05-2,15 (1H, м), 2,30-2,80 (5H, м), 2,85-3,80 (9H, м), 4,20-4,90 (4H, м), 7,08 (1H, д, J=1,7Гц), 7,18 (1H, дд, J=8,7, 1,7Гц), 7,42 (1H, д, J=8,7Гц), 7,77 (1H, с), 8,02-8,20 (1H, м), 8,40-8,50 (1H, м), 11,00-11,60 (1H, м), 11,87 (1H, с).
МС (ESI) m/z: 551 (M+H+).
[Пример 127]
Гидрохлорид N-[(3R*,4S*)-3-{[(5-хлориндол-2-ил)карбонил]амино}-1-(метилсульфонил)пиперидин-4-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
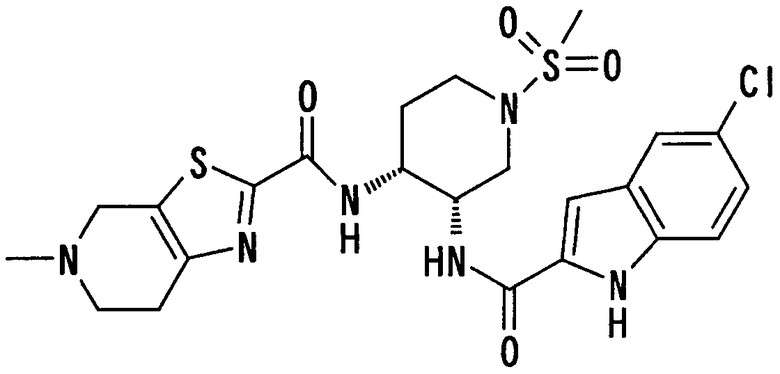
Указанное в заголовке соединение получали из соединения, полученного в примере 120, и метансульфонилхлорида подобно способу примера 100.
Т.пл. 228-245°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,75-1,85 (1H, м), 2,25-2,40 (1H, м), 2,40-2,60 (2H, м), 2,76 (3H, шир.с), 2,90 (3H, с), 2,93-3,05 (3H, м), 3,12 (1H, д, J=10,6Гц), 3,55-3,80 (2H, м), 4,25-4,40 (4H, м), 7,17 (1H, д, J=1,7Гц), 7,19 (1H, дд, J=8,7, 2,0Гц), 7,43 (1H, д, J=8,7Гц), 7,74 (1H, д, J=2,0Гц), 8,03 (1H, д, J=6,6Гц), 8,78 (1H, д, J=7,4Гц), 10,90-11,20 (1H, шир.с), 11,89 (1H, с).
МС (ESI) m/z: 551 (M+H+).
[Пример 128]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-фториндол-2-ил)карбонил]амино}-1-(метилсульфонил)пиперазин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
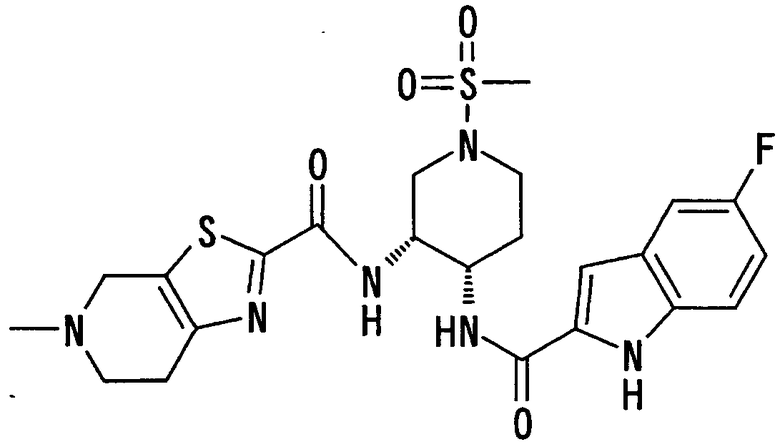
Указанное в заголовке соединение получали из соединения, полученного в примере 122, и метансульфонилхлорида подобно способу примера 100.
Т.пл. 216-250°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,80-1,90 (1H, м), 2,01-2,12 (1H, м), 2,92 (3H, с), 2,94 (3H, с), 3,00-3,80 (8H, м), 4,28-4,53 (3H, м), 4,60-4,80 (1H, шир.), 7,01-7,12 (2H, м), 7,37-7,44 (2H, м), 8,00-8,18 (1H, шир.), 8,39-8,50 (1H, шир.), 11,00-11,60 (1H, шир.), 11,72-11,80 (1H, шир.).
МС (FAB) m/z: 535 (M+H+).
[Пример 129]
Гидрохлорид метил (3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-карбоксилата
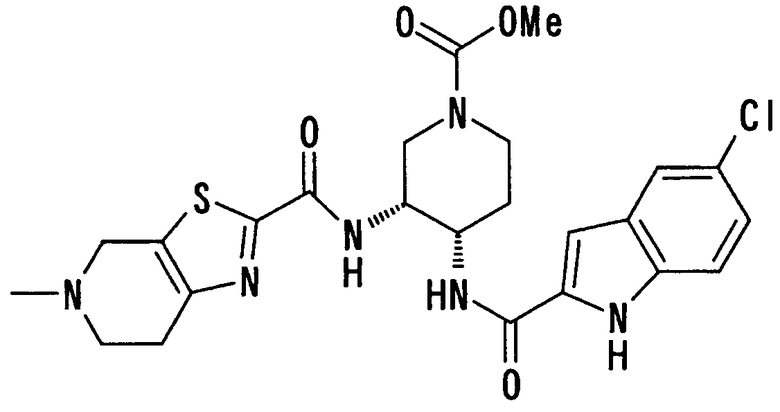
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и метилхлорформиата подобно способу примера 100.
Т.пл. 248-253°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,65-1,78 (1H, м), 1,88-2,03 (1H, м), 2,90 (3H, с), 3,00-3,80 (9H, м), 3,80-3,90 (1H, м), 3,95-4,08 (1H, м), 4,20-4,70 (4H, м), 7,10 (1H, с), 7,17 (1H, дд, J=8,8, 1,8Гц), 7,42 (1H, д, J=8,8Гц), 7,71 (1H, д, J=1,8Гц), 8,29 (1H, шир.с), 8,41 (1H, д, J=8,1Гц), 11,29 (1H, шир.с), 11,85 (1H, с).
МС (ESI) m/z: 531 (M+H+).
[Пример 130]
Гидрохлорид этил (3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-карбоксилата
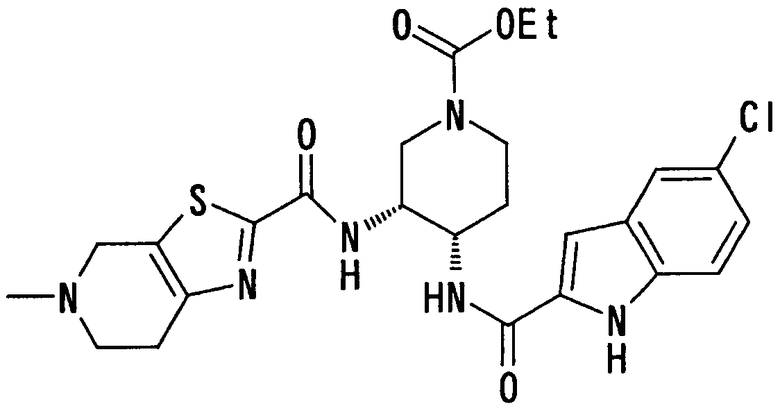
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и этилхлорформиата подобно способу примера 100.
Т.пл. 215-225°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 0,85-1,30 (3H, м), 1,65-1,78 (1H, м), 1,90-2,03 (1H, м), 2,90 (3H, с), 3,10-3,40 (4H, м), 3,48 (1H, шир.с), 3,65 (1H, шир.с), 3,75-4,15 (4H, м), 4,25 (1H, шир.с), 4,32-4,50 (2H, м), 4,66 (1H, шир.с), 7,09 (1H, с), 7,18 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,71 (1H, д, J=2,0Гц), 8,23 (1H, шир.с), 8,45 (1H, шир.д, J=8,1Гц), 11,50 (1H, шир.с), 11,86 (1H, с).
МС (ESI) m/z: 545 (M+H+).
[Пример 131]
Гидрохлорид 2-метоксиэтил (3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-карбоксилата
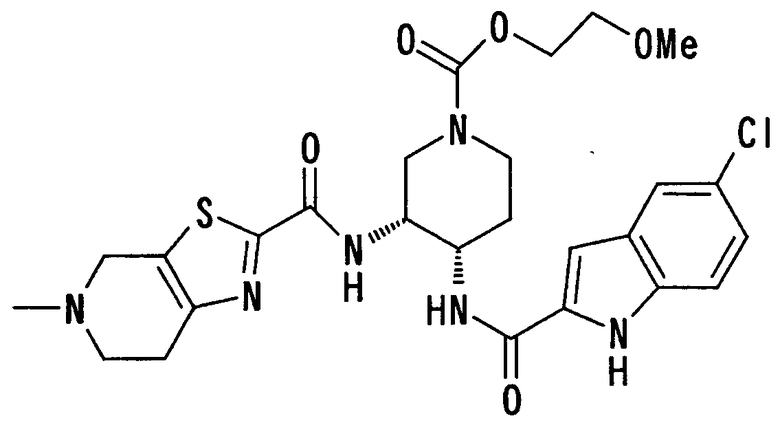
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и 2-метоксиэтилхлорформиата подобно способу примера 100.
Т.пл. 224-226°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,68-1,78 (1H, м), 1,90-2,03 (1H, м), 2,89 (3H, с), 3,00-3,75 (11H, м), 3,80-3,90 (1H, м), 3,95-4,18 (3H, м), 4,20-4,70 (4H, м), 7,10 (1H, с), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,71 (1H, д, J=2,0Гц), 8,26 (1H, шир.с), 8,42 (1H, д, J=7,8Гц), 11,30 (1H, шир.с), 11,86 (1H, с).
МС (ESI) m/z: 575 (M+H+).
[Пример 132]
Гидрохлорид этил (3R*,4S*)-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-карбоксилата
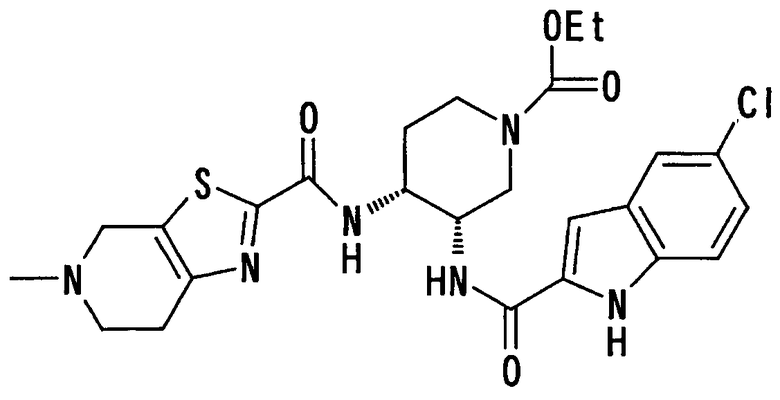
Указанное в заголовке соединение получали из соединения, полученного в примере 120, и этилхлорформиата подобно способу примера 100.
Т.пл. 213-225°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 0,75-1,30 (3H, м), 1,60-1,72 (1H, м), 2,12-2,25 (1H, м), 2,89 (3H, с), 2,95-3,20 (4H, м), 3,40-3,88 (4H, м), 3,90-4,10 (2H, м), 4,10-4,30 (2H, м), 4,30-4,40 (1H, м), 4,40-4,80 (1H, м), 7,10 (1H, с), 7,18 (1H, дд, J=8,8, 2,0Гц), 7,43 (1H, д, J=8,8Гц), 7,74 (1H, с), 8,03 (1H, д, J=5,6Гц), 8,79 (1H, с), 11,37 (1H, с), 11,88 (1H, с).
МС (ESI) m/z: 545 (M+H+).
[Пример 133]
Гидрохлорид N-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-пропионилпиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
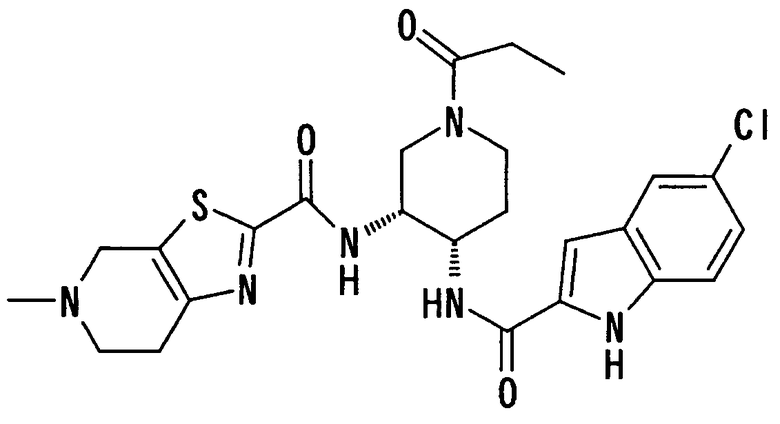
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и пропионилхлорида подобно способу примера 100.
Т.пл. 214-228°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 0,88-1,10 (3H, м), 1,70-2,05 (2H, м), 2,06-2,60 (2H, м), 2,91 (3H, с), 3,14 (2H, шир.с), 3,20-3,90 (5H, м), 3,95-4,80 (5H, м), 7,09 (1H, д, J=11,0Гц), 7,17 (1H, дд, J=8,8, 1,2Гц), 7,41 (1H, д, J=8,8Гц), 7,71 (1H, с), 8,20-8,50 (2H, м), 11,00-11,40 (1H, м), 11,86 (1H, с).
МС (ESI) m/z: 529 (M+H+).
[Пример 134]
Гидрохлорид N-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-изобутирилпиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
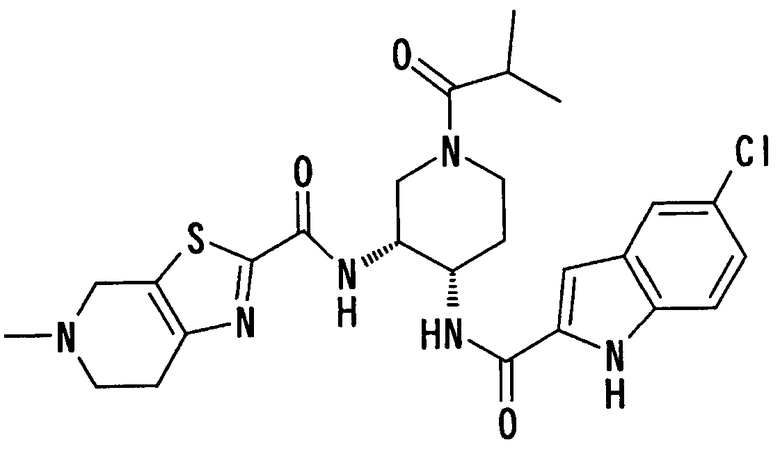
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и изобутирилхлорида подобно способу примера 100.
Т.пл. 266-272°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 0,80-1,15 (6H, м), 1,70-2,05 (2H, м), 2,65-2,80 (1H, м), 2,90 (3H, с), 2,90-4,80 (12H, м), 7,09 (1H, д, J=11,0Гц), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,71 (1H, с), 8,00-8,30 (1H, м), 8,30-10 8,50 (1H, м), 10,95-11,50 (1H, м), 11,86 (1H, с).
МС (ESI) m/z: 543 (M+H+).
[Пример 135]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2,2-диметилпропаноил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
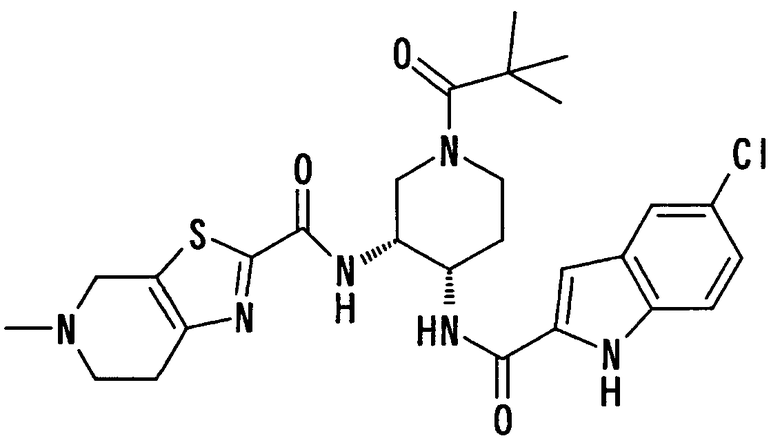
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и пивалоилхлорида подобно способу примера 100.
Т.пл. 250-255°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,20 (9H, с), 1,70-1,81 (1H, м), 1,90-2,00 (1H, м), 2,88 (3H, с), 3,10 (2H, шир.с), 3,20-3,70 (4H, м), 3,95-4,08 (1H, м), 4,10-4,20 (1H, м), 4,25-4,35 (1H, м), 4,35-4,80 (3H, м), 7,10 (1H, с), 7,16 (1H, дд, J=8,8, 1,9Гц), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, д, J=1,9Гц), 8,06 (1H, шир.с), 8,38 (1H, д, J=7,8Гц), 11,31 (1H, шир.с), 11,84 (1H, с).
МС (ESI) m/z: 557 (M+H+).
[Пример 136]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(3,3-диметилбутаноил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
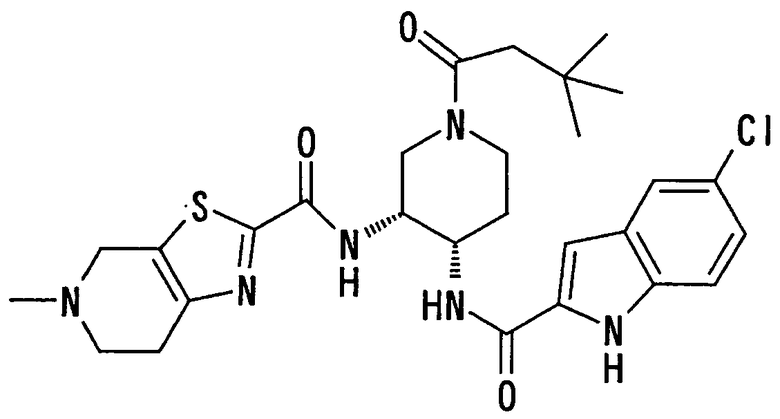
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и трет-бутилацетилхлорида подобно способу примера 100.
Т.пл. 260-265°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 0,91, 1,04 (всего 9H, каждый с), 1,68-1,82 (1H, м), 1,93-2,40 (3H, м), 2,91 (3H, с), 3,00-3,20 (2H, м), 3,20-4,80 (10H, м), 7,08 (1H, с), 7,17 (1H, дд, J=8,7, 1,2Гц), 7,41 (1H, д, J=8,7Гц), 7,69 (1H, д, J=7,6Гц), 7,93-8,18 (1H, м), 8,38-8,45 (1H, м), 10,95-11,30 (1H, м), 11,80-11,90 (1H, м).
МС (ESI) m/z: 571 (M+H+).
[Пример 137]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2,2,2-трифторацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида

Указанное в заголовке соединение получали из соединения, полученного в примере 118, и трифторуксусного ангидрида подобно способу примера 100.
Т.пл. 262-267°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,82-1,98 (1H, м), 2,05-2,21 (1H, м), 2,89 (3H, с), 3,05-3,20 (2H, м), 3,40-3,75 (4H, м), 3,85-3,95 (1H, м), 4,00-4,07 (1H, м), 4,20-4,70 (4H, м), 7,10 (1H, с), 7,18 (1H, дд, J=8,6, 1,9Гц), 7,41 (1H, д, J=8,6Гц), 7,72 (1H, с), 8,47 (1H, дд, J=22,4, 7,9Гц), 8,60 (1H, шир.), 11,08 (1H, шир.с), 11,87 (1H, с).
МС (ESI) m/z: 569 (M+H+).
[Пример 138]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(циклопропилкарбонил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
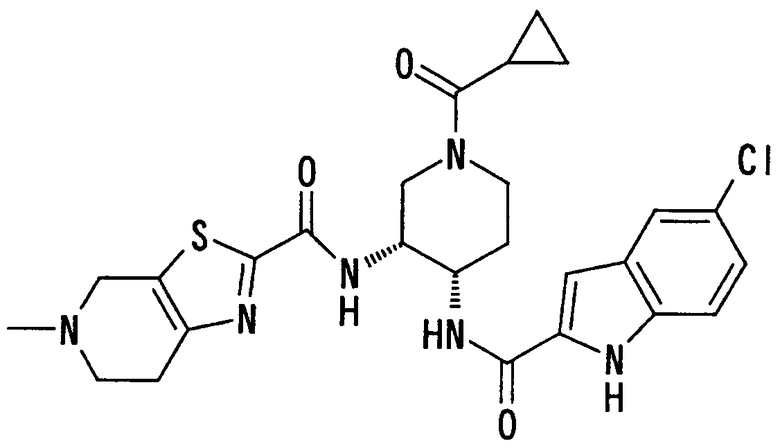
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и циклопропанкарбонилхлорида подобно способу примера 100.
Т.пл. 280-286°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 0,25-0,80 (4H, м), 1,65-2,15 (4H, м), 2,91 (3H, с), 2,90-3,20 (3H, м), 3,35-3,70 (2H, м), 4,00-4,80 (6H, м), 7,06 (1H, с), 7,18 (1H, д, J=8,8Гц), 7,42 (1H, д, J=8,7Гц), 7,71 (1H, с), 8,18 (1H, шир.с), 8,40, 8,48 (всего 1H, каждый шир.с), 11,11 (1H, шир.с), 11,85 (1H, с).
МС (ESI) m/z: 542 (M+H+).
[Пример 139]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(циклобутилкарбонил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
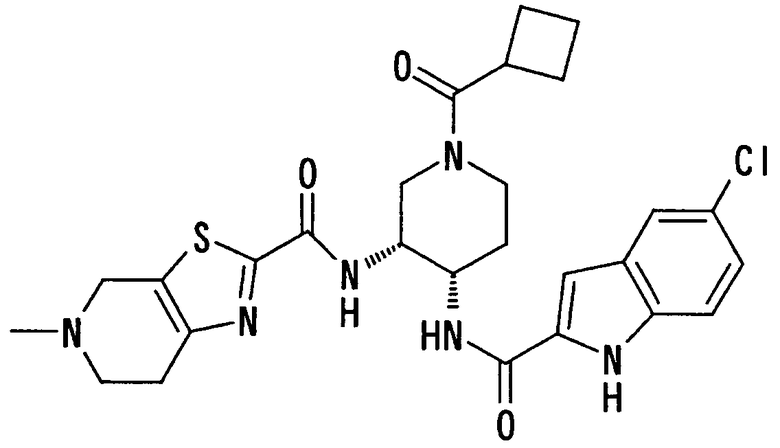
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и циклобутанкарбонилхлорида подобно способу примера 100.
Т.пл. 271-275°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,60-2,30 (8H, м), 2,89 (3H, с), 3,12 (2H, шир.с), 3,20-3,75 (6H, м), 3,75-3,90 (1H, м), 4,05-4,80 (4H, м), 7,08 (1H, с), 7,15 (1H, дд, J=9,0, 2,0Гц), 7,39 (1H, д, J=9,0Гц), 7,68 (1H, д, J=2,0Гц), 8,15 (1H, шир.с), 8,39 (1H, шир.), 11,19 (1H, шир.с), 11,84 (1H, с).
МС (ESI) m/z: 555 (M+H+).
[Пример 140]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(циклопентилкарбонил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
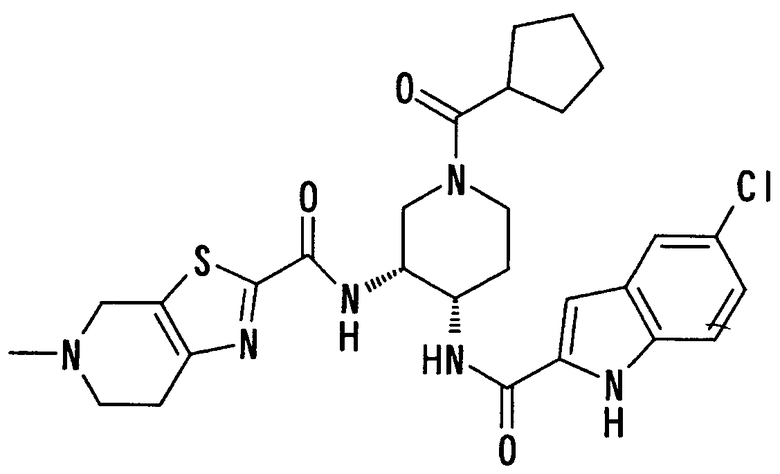
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и циклопентанкарбонилхлорида подобно способу примера 100.
Т.пл. 254-260°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,30-2,10 (10H, м), 2,90 (3H, с), 3,00-3,20 (2H, м), 3,20-3,75 (5H, м), 3,80-4,80 (6H, м), 7,09 (1H, с), 7,17 (1H, дд, J=8,7, 2,0Гц), 7,42 (1H, д, J=8,7Гц), 7,71 (1H, с), 7,95-8,30 (1H, м), 8,35-8,50 (1H, м), 11,23 (1H, шир.с), 11,85 (1H, с).
МС (ESI) m/z: 569 (M+H+).
[Пример 141]
2-((3R*,4S*)-4-{[(5-Хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-ил)-2-оксоэтилацетат
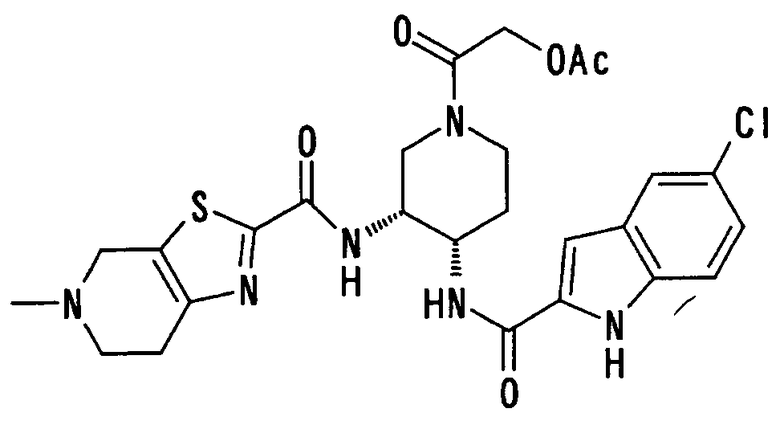
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и ацетоксиацетилхлорида подобно способу примера 100.
1Н-ЯМР (CDCl3) δ: 1,70-2,00 (1H, м), 2,05-2,48 (3H, м), 2,51 (3H, с), 2,70-3,05 (4H, м), 3,05-4,10 (5H, м), 4,20-4,48 (1H, м), 4,50-5,10 (4H, м), 6,87 (1H, шир.с), 7,10-7,82 (4H, м), 7,32 (1H, д, J=8,8Гц), 8,35 (1H, шир.с), 9,34, 9,45 (всего 1H, каждый шир.с).
МС (ESI) m/z: 573 (M+H+).
[Пример 142]
Гидрохлорид N-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-гликолоилпиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
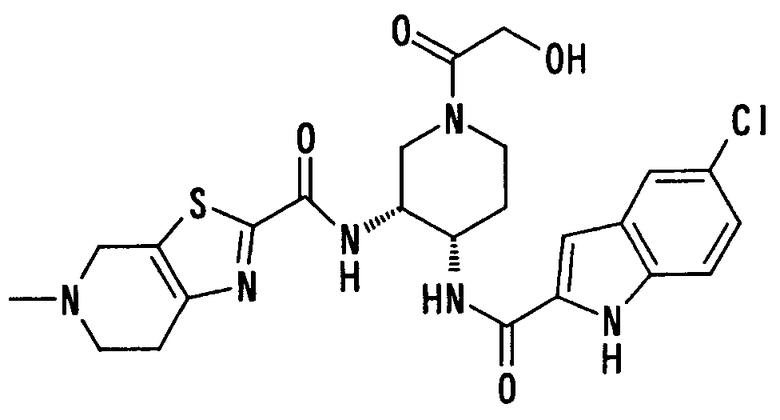
Соединение (301,8 мг), полученное в примере 141, растворяли в тетрагидрофуране (10 мл), добавляли 1N водный раствор (0,53 мл) гидроксида натрия и смесь перемешивали при комнатной температуре в течение 18 часов. Добавляли к реакционной смеси воду и экстрагировали метиленхлоридом. Полученный органический слой последовательно промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении, остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1-10:1) и отгоняли при пониженном давлении растворитель. Полученный таким образом очищенный продукт растворяли в этаноле (3 мл) и метиленхлориде (2 мл), добавляли 1N этанольный раствор хлористоводородной кислоты и смесь перемешивали в течение 30 минут. Отгоняли при пониженном давлении растворитель и остаток отверждали диэтиловым эфиром с получением указанного в заголовке соединения (195 мг).
Т.пл. 216-230°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,70-1,80 (1H, м), 1,88-2,10 (2H, м), 2,68 (3H, с), 3,18 (2H, с), 3,08-3,70 (5H, м), 3,80-3,95 (1H, м), 4,00-4,25 (3H, м), 4,25-4,50 (2H, м), 4,50-4,65 (1H, м), 7,09 (1H, д, J=11,0Гц), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,42 (1H, д, J=8,8Гц), 7,71 (1H, с), 8,33 (1H, шир.с), 8,35-8,50 (1H, м), 10,80-11,30 (1H, шир.с), 11,84 (1H, шир.с).
[Пример 143]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
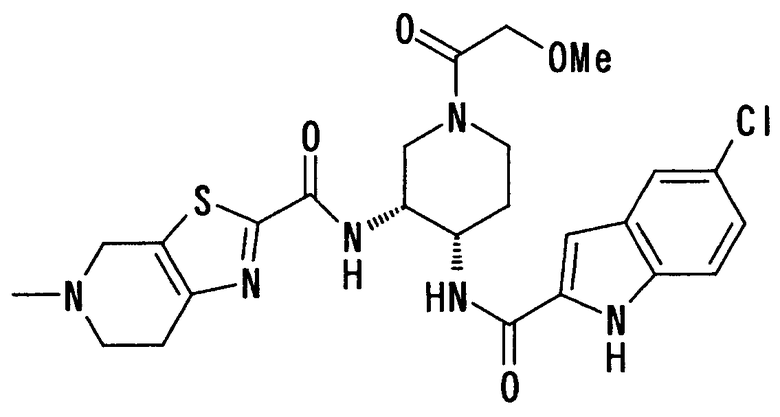
Указанное в заголовке соединение получали из соединения, полученного в примере 118, подобно способу примера 100.
Т.пл. 214-228°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,70-1,80 (1H, м), 1,85-2,05 (1H, м), 2,90 (3H, с), 3,00-3,20 (2H, м), 3,16 (3H, с), 3,22-3,82 (7H, м), 3,88-4,80 (5H, м), 7,09 (1H, д, J=9,0Гц), 7,17 (1H, дд, J=8,8, 1,9Гц), 7,42 (1H, д, J=8,8Гц), 7,70 (1H, д, J=1,9Гц), 8,29 (1H, шир.с), 8,40-8,50 (1H, м), 11,34 (1H, шир.с), 11,86 (1H, с).
МС (ESI) m/z: 545 (M+H)+.
[Пример 144]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-фториндол-2-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
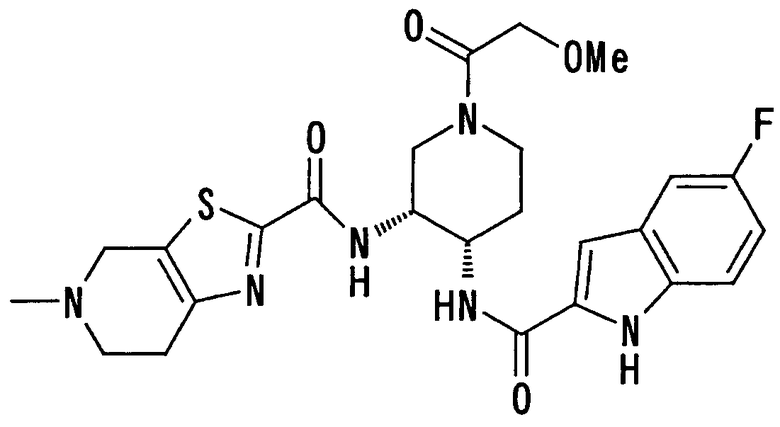
Указанное в заголовке соединение получали из соединения, полученного в примере 122, и метоксиацетилхлорида подобно способу примера 100.
Т.пл. 190-208°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,70-1,83 (1H, шир.), 1,85-2,10 (1H, м), 2,91 (3H, с), 3,00-3,55 (10H, м), 3,62-3,85 (1H, м), 3,90-4,50 (6H, м), 4,63-4,78 (1H, шир.), 7,04 (1H, тд, J=9,4, 2,4Гц), 7,07-7,13 (1H, шир.), 7,37-7,44 (1H, м), 8,16-8,49 (2H, м), 11,30-11,70 (1H, шир.), 11,72-11,80 (1H, шир.).
МС (FAB) m/z: 529 (M+H+).
[Пример 145]
N-((3R*,4S*)-1-(3-{трет-бутил(дифенил)силил}окси)-2,2-диметилпропаноил)-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
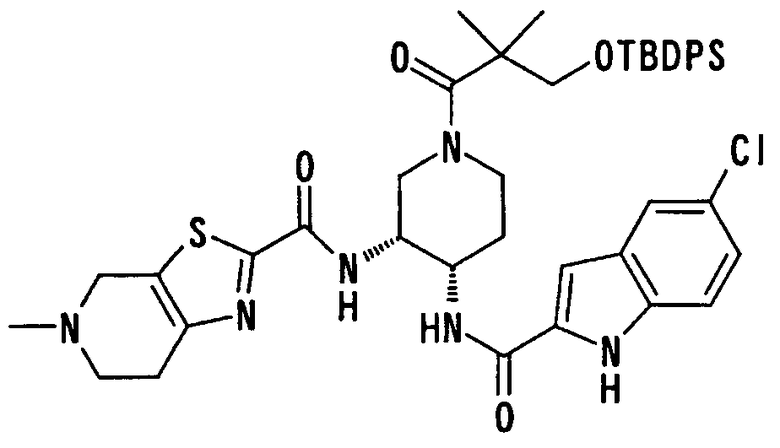
Тионилхлорид (3,0 мл) и каталитическое количество диметилформамида добавляли к раствору соединения (261 мг), полученного в ссылочном примере 158, в хлороформе (10 мл) и смесь перемешивали в течение ночи при 60°C. Реакционную смесь концентрировали при пониженном давлении с получением бледно-желтого масла. Указанное в заголовке соединение получали из данного продукта и соединения (200 мг), полученного в примере 118, подобно способу примера 100.
Т.пл. 153°C.
1Н-ЯМР (CDCl3) δ: 1,07 (9H, с), 1,39 (6H, д, J=3,9Гц), 1,57 (1H, шир.с), 2,26 (1H, д, J=10,7Гц), 2,57 (3H, с), 2,86 (4H, с), 2,97-3,01 (2H, м), 3,78 (4H, с), 4,20 (1H, шир.с), 4,33 (1H, д, J=13Гц), 4,42 (1H, шир.с), 4,67 (1H, д, J=13Гц), 6,88 (1H, с), 7,20-7,23 (1H, м), 7,32-7,46 (7H, м), 7,64-7,65 (6H, м), 7,86 (1H, д, J=6,8Гц), 8,23 (1H, с), 9,10 (1H, с).
[Пример 146]
N-[(3R*,4S*)-4-{[(5-Хлориндол-2-ил)карбонил]амино}-1-(3-гидрокси-2,2-диметилпропаноил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
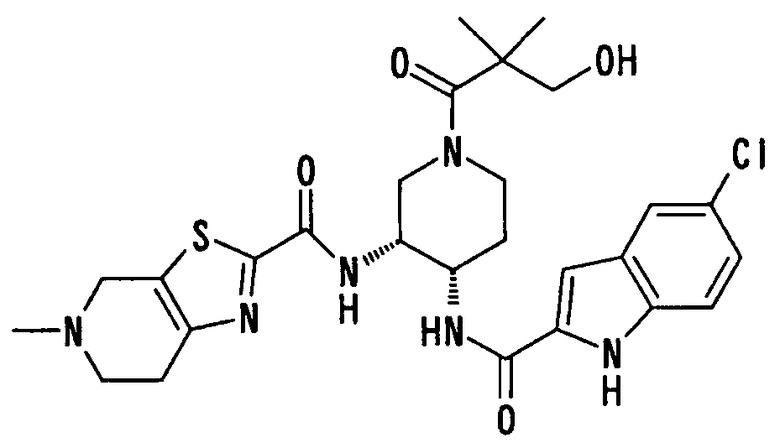
Фторид тетрабутиламмония (1М тетрагидрофурановый раствор, 0,594 мл) добавляли к раствору соединения (241 мг), полученного в примере 145, в тетрагидрофуране (30 мл) при охлаждении льдом и смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении и полученный остаток растворяли в метиленхлориде. Раствор промывали водой и насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель. Полученный остаток очищали препаративной тонкослойной хроматографией на силикагеле (метиленхлорид:метанол = 9:1) с получением указанного в заголовке соединения (116 мг).
Т.пл. 220°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,17 (6H, д, J=8,3Гц), 1,79 (1H, шир.с), 1,91-1,97 (1H, м), 2,49 (3H, с), 2,87 (4H, с), 3,35-3,50 (4H, м), 3,81 (1H, шир.с), 3,97 (1H, м), 4,10-4,15 (1H, м), 4,32 (1H, шир.с), 4,42 (1H, шир.с), 4,52 (1H, т, J=5,7Гц), 7,10 (1H, с), 7,16-7,19 (1H, м), 7,42 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,11 (1H, д, J=8,8Гц), 8,37 (1H, д, J=7,3Гц), 11,8 (1H, с).
МС (FAB) m/z: 573 (M+H+).
[Пример 147]
N-[(3R*,4S*)-4-{[(5-Хлориндол-2-ил)карбонил]амино}-1-(3-метокси-2,2-диметилпропаноил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
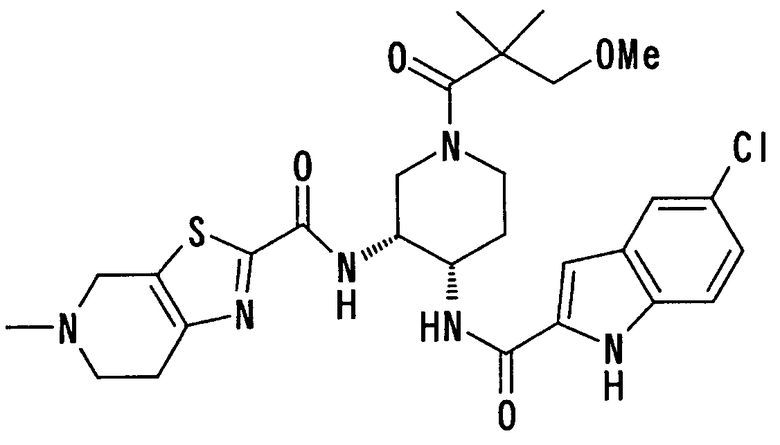
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и соединения, полученного в ссылочном примере 160, подобно способу примера 145.
Т.пл. 240°C (разложение).
1Н-ЯМР (CDCl3) δ: 1,34 (3H, с), 1,37 (3H, с), 1,65-1,77 (1H, м), 2,33-2,37 (1H, м), 2,53 (3H, с), 2,82-3,29 (6H, м), 3,34 (3H, с), 3,41 (1H, д, J=9,3Гц), 3,56 (1H, д, J=9,3Гц), 3,76 (2H, д, J=5,9Гц), 4,26 (1H, м), 4,44-4,53 (2H, м), 4,82 (1H, д, J=13,7Гц), 6,88 (1H, д, J=1,5Гц), 7,20-7,23 (1H, м), 7,33 (1H, д, J=8,8Гц), 7,64 (1H, д, J=1,5Гц), 7,90 (1H, д, J=7,1Гц), 8,22 (1H, д, J=5,1Гц), 9,18 (1H, с).
МС (FAB) m/z: 587 (M+H+).
[Пример 148]
2-((3R*,4S*)-4-{[(5-Хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-ил)-1,1-диметил-2-оксоэтилацетат
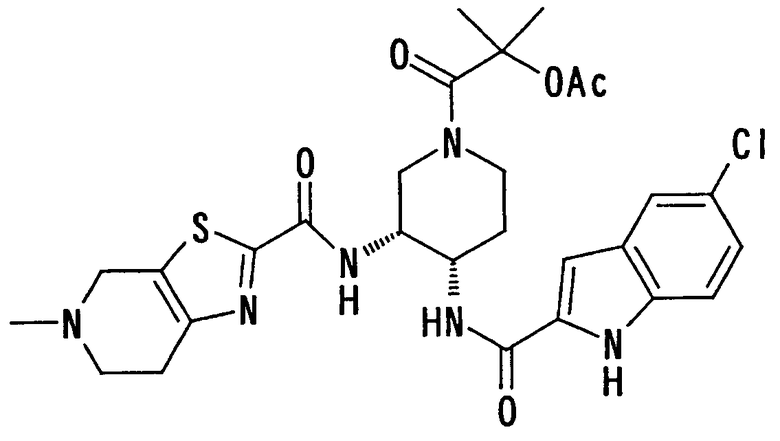
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и 2-ацетоксиизобутирилхлорида подобно способу примера 100.
Т.пл. 190°C (разложение).
1Н-ЯМР (CDCl3) δ: 1,56-1,67 (8H, м), 2,08 (3H, с), 2,35 (1H, д, J=10,5Гц), 2,52 (3H, с), 2,82-2,84 (2H, м), 2,90-2,96 (2H, м), 3,14 (1H, шир.с), 3,75 (2H, с), 4,25 (1H, шир.с), 4,40-4,47 (1H, м), 4,54 (1H, шир.с), 4,80 (1H, шир.с), 6,86 (1H, с), 7,20-7,33 (3H, м), 7,64 (1H, д, J=1,7Гц), 7,76 (1H, д, J=7,3Гц), 9,11 (1H, с).
МС (FAB) m/z: 601 (M+H+).
[Пример 149]
N-[(3R*,4S*)-4-{[(5-Хлориндол-2-ил)карбонил]амино}-1-(2-гидрокси-2-метилпропаноил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
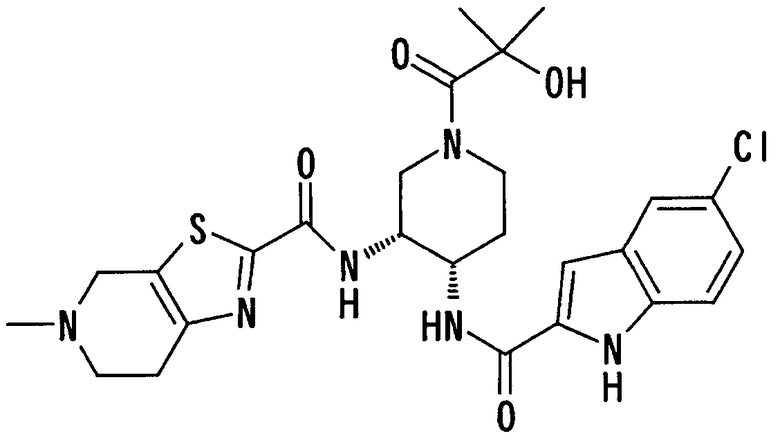
Метоксид натрия (76,8 мг) добавляли к раствору соединения (190 мг), полученного в примере 148, в метаноле (50 мл) и смесь перемешивали в течение ночи при комнатной температуре. После концентрирования реакционной смеси при пониженном давлении полученный остаток очищали препаративной тонкослойной хроматографией на силикагеле (метиленхлорид:метанол = 9:1) с получением указанного в заголовке соединения (130 мг).
Т.пл. 190°C (разложение).
1Н-ЯМР (CDCl3) δ: 1,53 (3H, с), 1,56-1,78 (5H, м), 2,34 (1H, д, J=10,5Гц), 2,53 (3H, с), 2,83-2,86 (2H, м), 2,91-2,93 (2H, м), 3,30 (1H, д, J=12,5Гц), 3,75 (2H, с), 4,28 (1H, д, J=5,6Гц), 4,43 (1H, с), 4,65 (1H, д, J=13,5Гц), 4,95 (1H, д, J=13,5Гц), 6,92 (1H, д, J=1,5Гц), 7,20-7,23 (1H, м), 7,33 (1H, д, J=8,6Гц), 7,65 (1H, д, J=2,0Гц), 8,43 (1H, д, J=5,6Гц), 9,14 (1H, с).
МС (FAB) m/z: 559 (M+H+).
[Пример 150]
Гидрохлорид N-{(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-[(3-гидроксициклобутил)карбонил]пиперидин-3-ил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
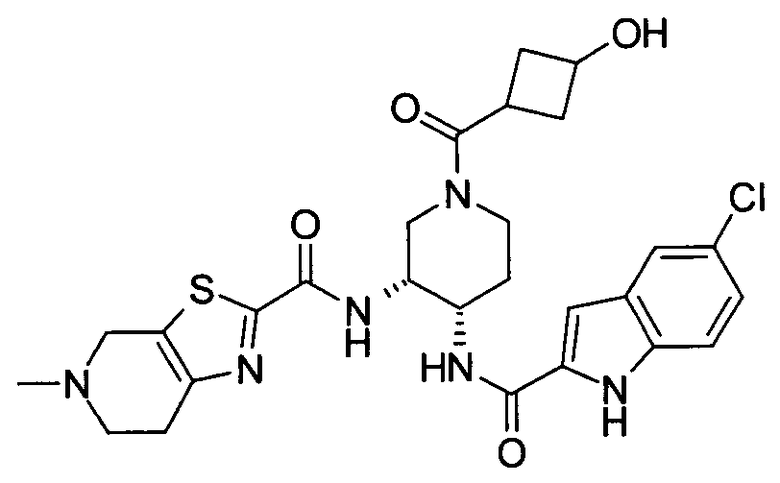
Соединение (306 мг), полученное в примере 118, н-метилморфолин (200 мкл), моногидрат 1-гидроксибензотриазола (87 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (197 мг) добавляли к раствору соединения (117 мг), полученного в ссылочном примере 152, в смешанном растворителе из тетрагидрофурана (20 мл), метиленхлорида (3,0 мл) и N,N-диметилформамида (2,0 мл) и смесь перемешивали при комнатной температуре в течение 3 суток. Реакционную смесь разбавляли метиленхлоридом и добавляли насыщенный водный раствор гидрокарбоната натрия для разделения смеси на два слоя. Полученный органический слой промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия и затем концентрировали при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 10:1) с получением свободного основания (207 мг) указанного в заголовке соединения. Свободное основание обрабатывали 1N этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения.
Т.пл. 200°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,78-2,10 (4H, м), 2,24-2,68 (3H, м), 2,75-5,20 (14H, м), 2,91 (3H, с), 7,08 (0,5H, с), 7,09 (0,5H, с), 7,18 (1H, дд, J=8,8, 2,0Гц), 7,42 (1H, д, J=8,8Гц), 7,70 (1H, д, J=2,0Гц), 8,05-8,28 (1H, шир.), 8,38 (0,5H, шир.д, J=7,3Гц), 8,43 (0,5H, шир.д, J=8,3Гц), 10,80-11,25 (1H, шир.), 11,84 (1H, шир.с).
МС (ESI) m/z: 571 (M+H+).
[Пример 151]
Гидрохлорид N-{(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-[(метоксициклобутил)карбонил]пиперидин-3-ил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
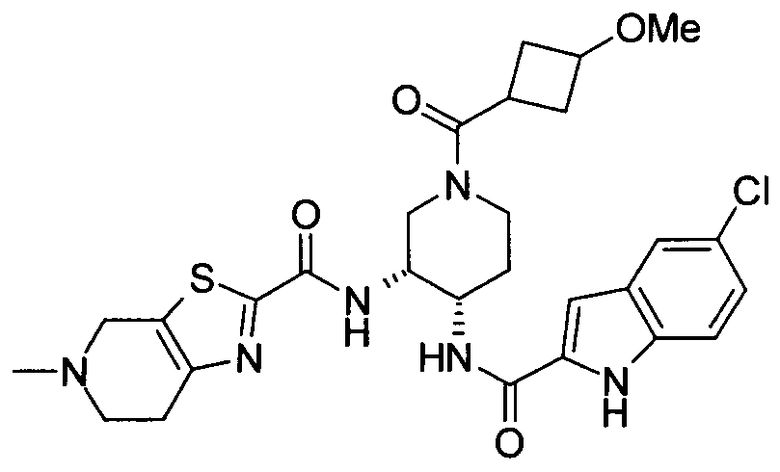
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и соединения, полученного в ссылочном примере 154, подобно способу примера 150.
Т.пл. 191°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,69-2,23 (4H, м), 2,25-2,40 (1H, м), 2,71-2,84 (0,5H, м), 2,89-3,93 (9,5H, м), 2,91 (3H, с), 3,01 (1H, с), 3,14 (2H, с), 4,05-4,80 (5H, м), 7,09 (1H, с), 7,18 (1H, д, J=8,4Гц), 7,42 (1H, д, J=8,4Гц), 7,70 (1H, с), 8,00-8,30 (1H, шир.), 8,36-8,53 (1H, м), 11,25-11,75 (1H, шир.), 11,85 (1H, шир.с).
МС (ESI) m/z: 585 (M+H+).
[Пример 152]
Гидрохлорид N-{(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-[3-метокси-2-(метоксиметил)пропаноил]пиперидин-3-ил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
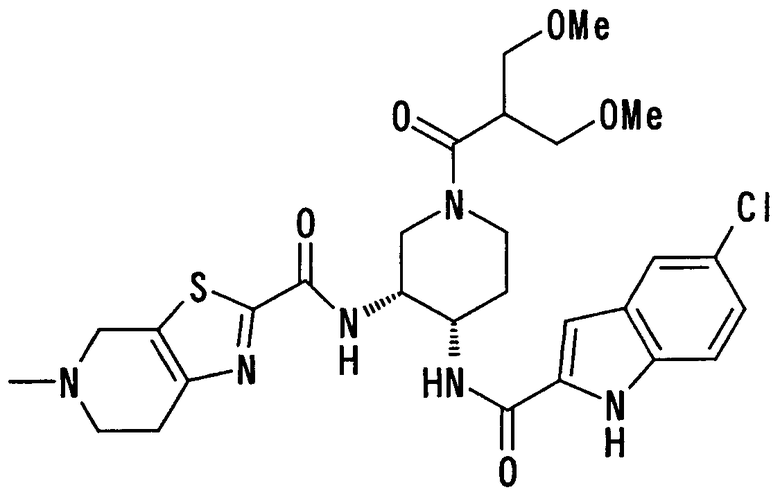
Указанное в заголовке соединение получали конденсацией карбоновой кислоты, полученной гидролизом соединения, полученного в ссылочном примере 155, с соединением, полученным в примере 118, подобно способу примера 150.
Т.пл. 178-184°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,69-1,82 (1H, м), 1,84-2,04 (1H, м), 2,91 (3H, с), 3,00-3,75 (17H, м), 3,95-4,55 (5H, м), 4,60-4,80 (1H, м), 7,10 (1H, шир.с), 7,18 (1H, дд, J=8,8, 2,0Гц), 7,42 (1H, д, J=8,8Гц), 7,69 (0,5H, шир.с), 7,71 (1H, шир.с), 8,18-8,28 (1H, шир.), 8,35-8,50 (1H, шир.), 11,83 (1H, шир.с).
МС (ESI) m/z: 603 (M+H+).
[Пример 153]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}(тетрагидро-2Н-пиран-4-илкарбонил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
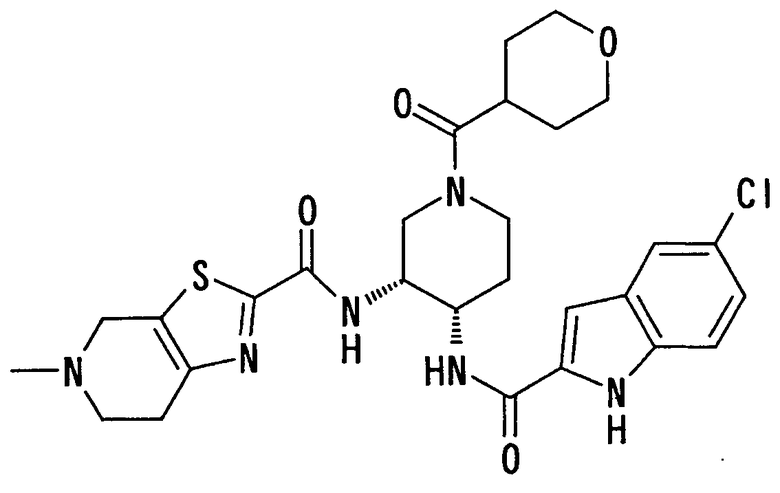
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и соединения, полученного в ссылочном примере 156, подобно способу примера 150.
Т.пл. 225-248°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,55-1,68 (4H, м), 1,70-1,85 (1H, м), 1,85-2,05 (1H, м), 2,60-2,95 (1H, м), 2,89 (3H, с), 2,95-3,20 (3H, м), 3,20-4,00 (9H, м), 4,00-4,80 (4H, м), 7,08 (1H, с), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,42 (1H, д, J=8,8Гц), 7,71 (1H, с), 8,00-8,30 (1H, м), 8,35-8,50 (1H, м), 11,16 (1H, шир.с), 11,85 (1H, с).
МС (ESI) m/z: 585 (M+H+).
[Пример 154]
Гидрохлорид N-((3R*,4S*)-1-бензоил-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
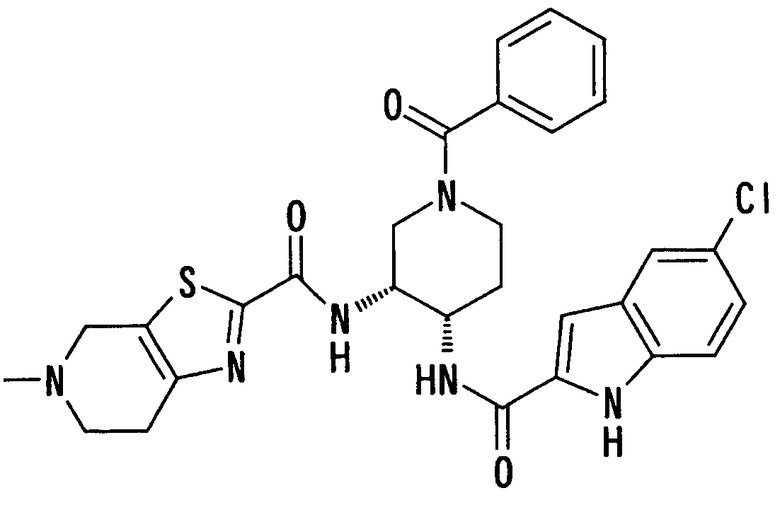
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и бензоилхлорида подобно способу примера 100.
Т.пл. 215-225°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,75-1,90 (1H, м), 1,90-2,20 (1H, м), 2,93 (3H, с), 3,10-4,00 (8H, м), 4,05-4,80 (4H, м), 7,00-7,60 (5H, м), 7,08 (1H, с), 7,16 (1H, дд, J=8,8, 1,6Гц), 7,40 (1H, д, J=8,8Гц), 7,71 (1H, д, J=1,6Гц), 8,31 (1H, шир.с), 8,46 (1H, шир.с), 11,39 (1H, шир.с), 11,86 (1H, с).
МС (FAB) m/z: 577 (M+H+).
[Пример 155]
трет-Бутил (3R*,4S*)-3-({[5-(2-{[трет-бутил(дифенил)силил]окси}-1,1-диметилэтил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил]карбонил}амино)-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-1-карбоксилат
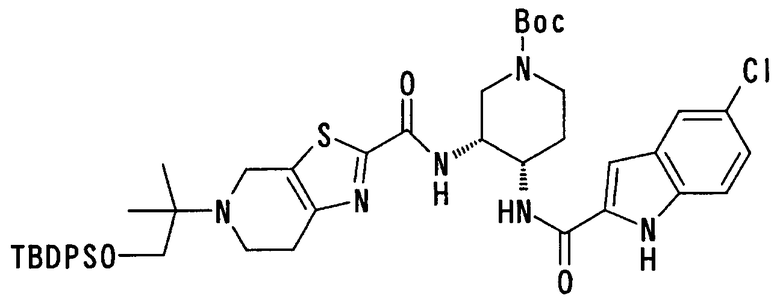
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 207, и соединения, полученного в ссылочном примере 42, подобно способу примера 91.
1Н-ЯМР (ДМСО-d6) δ: 1,00 (9H, с), 1,12 (6H, с), 1,15-1,50 (9H, м), 1,63-1,75 (1H, м), 1,82-2,00 (1H, м), 2,60-2,80 (3H, м), 2,83-2,95 (2H, м), 3,12-3,30 (1H, м), 3,30 (2H, с), 3,58 (2H, с), 3,85-4,10 (2H, м), 4,19 (1H, шир.с), 4,37 (1H, шир.с), 7,04 (1H, с), 7,16 (1H, д, J=9,0Гц), 7,30-7,50 (7H, м), 7,50-7,65 (4H, м), 7,70 (1H, с), 7,99 (1H, д, J=6,8Гц), 8,45 (1H, шир.с), 11,82 (1H, с).
МС (ESI) m/z: 869 (M+H)+.
[Пример 156]
Дигидрохлорид 5-(2-{[трет-бутил(дифенил)силил]окси}-1,1-диметилэтил)-N-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-ил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
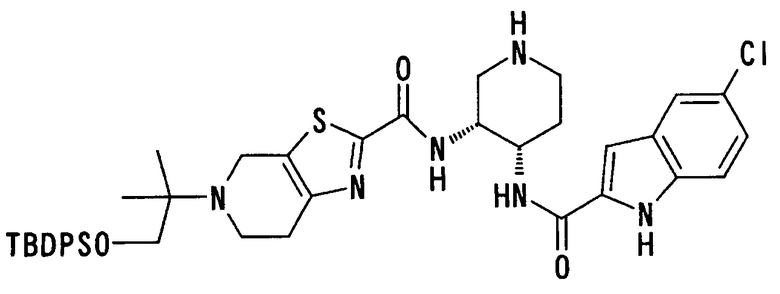
Указанное в заголовке соединение получали обработкой соединения, полученного в примере 155, подобно способу примера 95.
1Н-ЯМР (ДМСО-d6) δ: 1,04 (9H, с), 1,43, 1,48 (всего 6H, каждый с), 1,85-2,00 (1H, м), 2,05-2,20 (1H, м), 2,95-3,20 (2H, м), 3,25-3,60 (6H, м), 3,80-3,90 (1H, м), 3,95-4,05 (1H, м), 4,45-4,55 (1H, м), 4,60-4,85 (3H, м), 7,10-7,20 (2H, м), 7,35-7,55 (7H, м), 7,55-7,75 (5H, м), 8,52 (1H, дд, J=14,4, 7,8Гц), 8,93 (1H, шир.), 9,20-9,40 (2H, м), 11,30-11,50 (1H, м), 11,87, 11,92 (всего 1H, каждый с).
МС (ESI) m/z: 769 (M+H+).
[Пример 157]
5-(2-{[трет-Бутил(дифенил)силил]окси}-1,1-диметилэтил)-N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-ил]-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
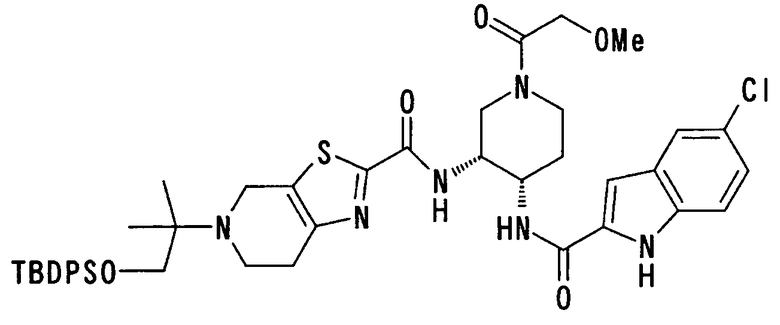
Указанное в заголовке соединение получали из соединения, полученного в примере 156, и метоксиацетилхлорида подобно способу примера 100.
1Н-ЯМР (CDCl3) δ: 1,07 (9H, с), 1,20 (6H, с), 1,60-1,85 (1H, м), 2,25-2,40 (1H, м), 2,36 (2H, с), 2,70-3,20 (4H, м), 3,20-3,55 (4H, м), 3,55-3,70 (2H, м), 3,95-4,10 (3H, м), 4,10-4,90 (4H, м), 6,90 (1H, д, J=1,5Гц), 7,15-7,30 (2H, м), 7,30-7,50 (6H, м), 7,60-7,70 (5H, м), 8,15-8,22 (1H, м), 8,46 (1H, д, J=5,1Гц), 9,28 (1H, с).
МС (ESI) m/z: 842 (M+H+).
[Пример 158]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-ил]-5-(2-гидрокси-1,1-диметилэтил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
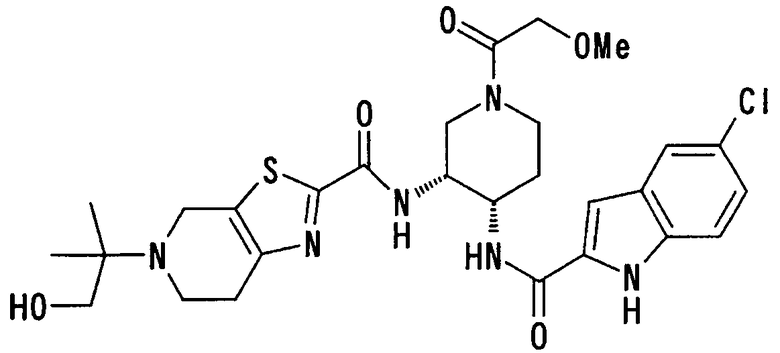
Указанное в заголовке соединение получали из соединения, полученного в примере 157, подобно способу примера 146.
Т.пл. 221-232°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,32 (3H, с), 1,40 (3H, с), 1,70-1,85 (1H, м), 1,85-2,10 (1H, м), 2,60-3,35 (8H, м), 3,40-3,82 (3H, м), 3,85-4,05 (3H, м), 4,05-4,35 (2H, м), 4,50-4,60 (1H, м), 4,55-4,80 (2H, м), 5,75-5,85 (1H, м), 7,08 (1H, шир.с), 7,17 (1H, д, J=8,8Гц), 7,41 (1H, д, J=8,8Гц), 7,71 (1H, с), 8,20-8,35 (1H, м), 8,40-8,55 (1H, м), 10,00-10,35 (1H, м), 11,87 (1H, с).
МС (ESI) m/z: 603 (M+H+).
[Пример 159]
трет-Бутил (3R*,4S*)-4-{[(5-фториндол-2-ил)карбонил]амино}-3-{[(5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-1-карбоксилат
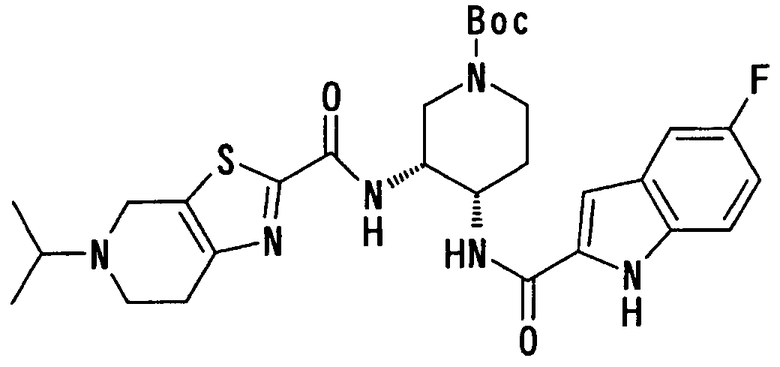
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 209 и соединения, полученного в ссылочном примере 148, подобно способу примера 91.
1Н-ЯМР (CDCl3) δ: 1,16 (6H, д, J=6,6Гц), 1,53 (9H, с), 1,65-1,80 (1H, м), 2,23-2,32 (1H, м), 2,80-3,10 (6H, м), 3,10-3,25 (1H, м), 3,80-3,90 (2H, м), 4,00-4,50 (4H, м), 6,91 (1H, с), 6,95-7,05 (1H, м), 7,25-7,40 (2H, м), 7,74 (1H, шир.с), 8,21 (1H, шир.с), 9,30 (1H, с).
МС (ESI) m/z: 585 (M+H+).
[Пример 160]
Дигидрохлорид N-((3R*,4S*)-4-{[(5-фториндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
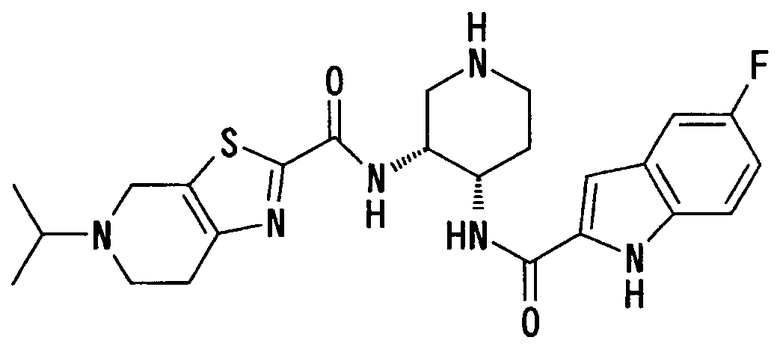
Указанное в заголовке соединение получали обработкой соединения, полученного в примере 159, подобно способу примера 95.
1Н-ЯМР (ДМСО-d6) δ: 1,28-1,40 (6H, м), 1,85-2,00 (1H, м), 2,05-2,20 (1H, м), 2,40-2,60 (1H, м), 2,95-3,90 (8H, м), 4,40-4,55 (2H, м), 4,60-4,75 (2H, м), 7,00-7,20 (2H, м), 7,30-7,50 (2H, м), 8,45-8,60 (1H, м), 8,85-9,05 (1H, м), 9,05-9,50 (2H, м), 11,60-11,90 (2H, м).
МС (ESI) m/z: 485 (M+H+).
[Пример 161]
Гидрохлорид N-[(3R*,4S*)-4-{[(5-фториндол-2-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-ил]-5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
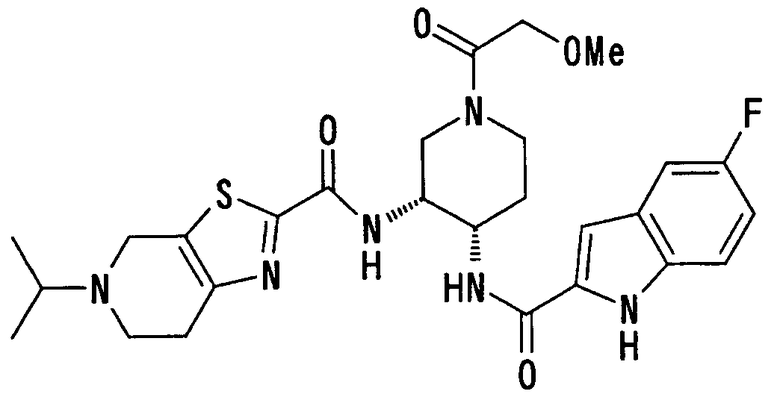
Указанное в заголовке соединение получали из соединения, полученного в примере 160, и метоксиацетилхлорида подобно способу примера 100.
Т.пл. 214-228°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,25-1,40 (6H, м), 1,68-1,82 (1H, м), 1,85-2,10 (1H, м), 2,90-3,60 (8H, м), 3,60-3,85 (2H, м), 3,85-4,40 (5H, м), 4,40-4,55 (2H, м), 4,60-4,75 (1H, м), 7,00-7,15 (2H, м), 7,35-7,50 (2H, м), 8,15-8,50 (2H, м), 10,80-11,30 (1H, м), 11,73 (1H, д, J=6,6Гц).
МС (ESI) m/z: 557 (M+H+).
[Пример 162]
Гидрохлорид N-{(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-[(диметиламино)карбонил]пиперидин-3-ил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
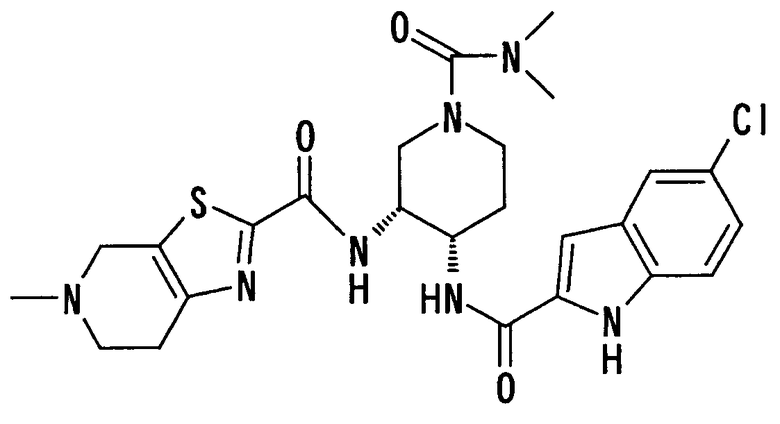
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и N,N-диметилкарбамоилхлорида подобно способу примера 100.
Т.пл. 267-270°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,65-1,78 (1H, м), 1,97-2,10 (1H, м), 2,70 (6H, с), 2,90 (3H, с), 2,95-3,80 (8H, м), 4,25-4,80 (4H, м), 7,08 (1H, с), 7,16 (1H, дд, J=8,8, 1,8Гц), 7,41 (1H, д, J=8,8Гц), 7,70 (1H, с), 8,31 (1H, шир.с), 8,40 (1H, д, J=7,3Гц), 11,15-11,60 (1H, м), 11,82 (1H, с).
МС (ESI) m/z: 544 (M+H+).
[Пример 163]
Гидрохлорид N-{(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-[(этиламино)карбонил]пиперидин-3-ил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
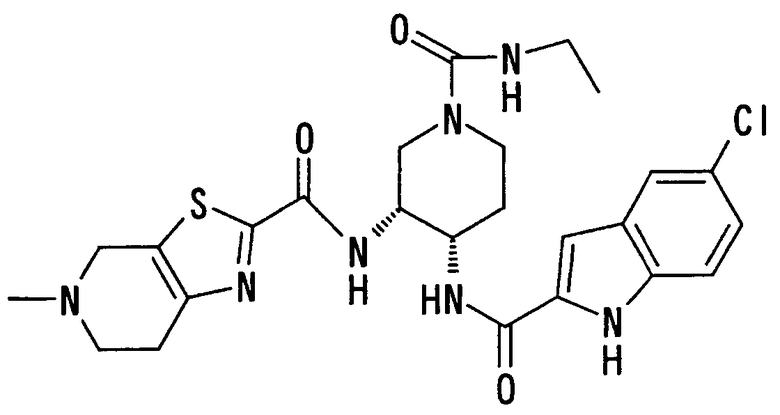
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и этилизоцианата подобно способу примера 100.
Т.пл. 221-235°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 0,98 (3H, т, J=7,1Гц), 1,60-1,70 (1H, м), 1,80-1,95 (1H, м), 2,90 (3H, с), 2,95-3,40 (6H, м), 3,40-4,00 (4H, м), 4,25-4,80 (4H, м), 6,60-6,80 (1H, м), 7,09 (1H, с), 7,16 (1H, дд, J=8,8, 1,9Гц), 7,41 (1H, д, J=8,8Гц), 7,68 (1H, д, J=1,9Гц), 8,02 (1H, шир.с), 8,35 (1H, д, J=7,1Гц), 11,20-11,70 (1H, м), 11,82 (1H, с).
МС (FAB)m/z: 544 (M+H+).
[Пример 164]
Гидрохлорид N-((3R*,4S*)-1-[(трет-бутиламино)карбонил]-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
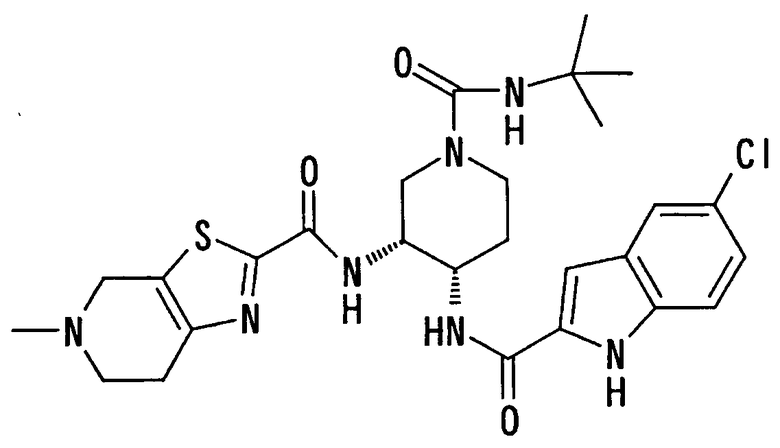
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и трет-бутилизоцианата подобно способу примера 100.
Т.пл. 236-238°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,21 (9H, с), 1,60-1,70 (1H, м), 1,80-1,90 (1H, м), 2,87 (3H, с), 3,00-3,40 (6H, м), 3,49 (1H, шир.с), 3,80-3,90 (1H, м), 3,90-4,00 (1H, м), 4,20-4,35 (2H, м), 4,47 (1H, шир.с), 5,90 (1H, с), 7,06 (1H, с), 7,16 (1H, дд, J=8,8, 1,9Гц), 7,41 (1H, д, J=8,8Гц), 7,67 (1H, д,
J=1,9Гц), 8,04 (1H, д, J=6,8Гц), 8,34 (1H, д, J=7,3Гц), 11,22 (1H, шир.с), 11,79 (1H, с).
МС (FAB) m/z: 572 (M+H+).
[Пример 165]
Дигидрохлорид метил 2-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-3-ил)ацетата
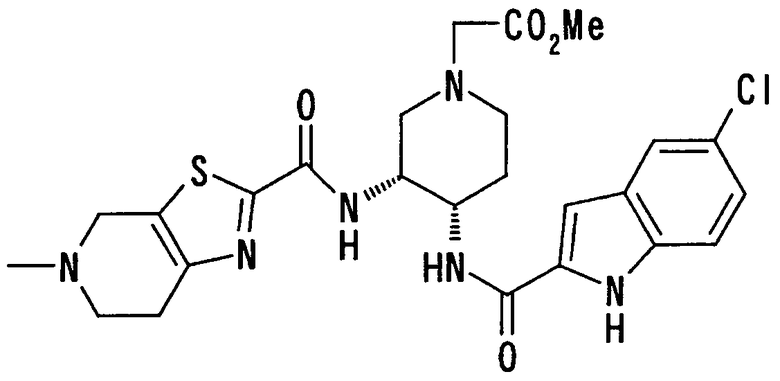
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и метилбромацетата подобно способу примера 102.
Т.пл. 253-255°C (разложение).
1Н-ЯМР (ДМСО-d6, 80°C) δ: 1,95-2,10 (1H, м), 2,10-2,25 (1H, м), 2,88 (3H, с), 3,00-3,73 (8H, м), 3,75 (3H, с), 3,97-4,15 (2H, м), 4,30-4,80 (4H, м), 7,08-7,20 (2H, м), 7,44 (1H, д, J=8,6Гц), 7,63 (1H, д, J=2,0Гц), 8,42 (1H, д, J=7,3Гц), 8,62 (1H, шир.с), 11,82 (1H, шир.с).
МС (ESI) m/z: 545 (M+H+).
[Пример 166]
Гидрохлорид 2-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-3-ил)уксусной кислоты
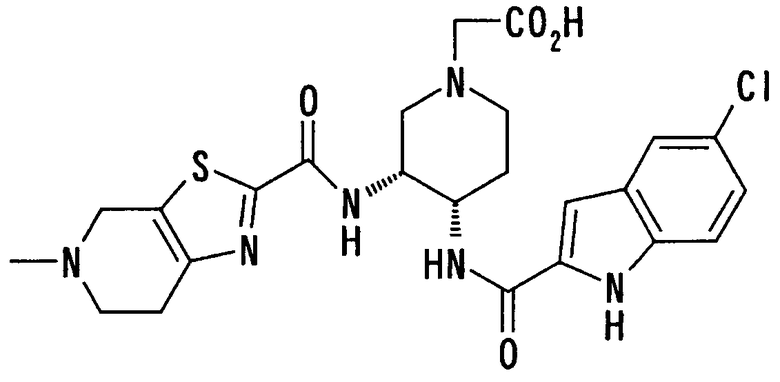
Указанное в заголовке соединение получали обработкой соединения, полученного в примере 165, подобно способу примера 101.
Т.пл. 234-240°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,75-1,95 (1H, м), 2,05-2,20 (1H, м), 2,88 (3H, с), 2,95-3,90 (10H, м), 4,20-4,70 (4H, м), 7,11 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,66 (1H, д, J=2,0Гц), 8,46 (1H, шир.д, J=7,8Гц), 8,65 (1H, шир.с), 11,60-12,70 (2H, шир.с), 11,91 (1H, шир.с).
[Пример 167]
Дигидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2-метоксиэтил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
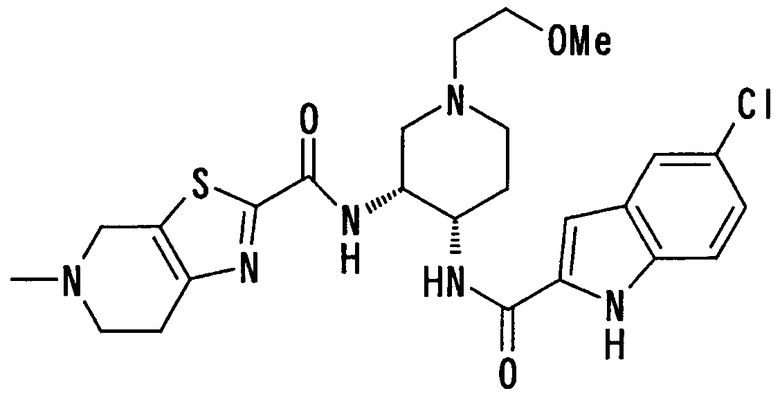
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и 2-бромэтилметилового эфира подобно способу примера 102 (Данные ЯМР для свободного основания).
Т.пл. 238-242°C (разложение).
1Н-ЯМР (CDCl3) δ: 1,75-1,83 (2H, м), 2,27-2,39 (2H, м), 2,52 (3H, с), 2,60-2,66 (1H, м), 2,69-2,75 (1H, м), 2,81-2,90 (2H, м), 2,96-3,07 (2H, м), 3,41 (3H, с), 3,53-3,60 (2H, м), 3,75 (каждый 1H, система AB д, J=15,5Гц), 4,02-4,05 (1H, м), 4,40 (1H, шир.), 6,88 (1H, д, J=1,5Гц), 7,18-7,21 (1H, м), 7,31-7,33 (1H, м), 7,63 (1H, д, J=1,5Гц), 8,17 (1H, д, J=5,0Гц), 8,26 (1H, д, J=7,0Гц), 9,30 (1H, шир.с).
МС (FAB) m/z: 531 (M+H+).
[Пример 168]
Дигидрохлорид N-[(3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2-фторэтил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
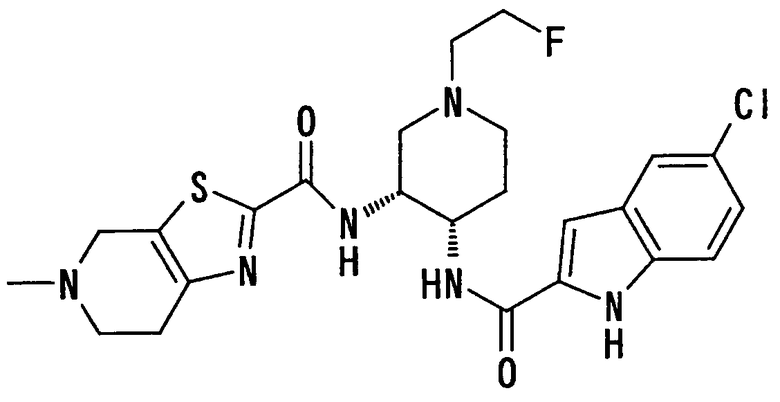
Указанное в заголовке соединение получали из соединения, полученного в примере 118, и 2-фторэтилбромида подобно способу примера 102 (Данные ЯМР для свободного основания).
Т.пл. 228-233°C (разложение).
1Н-ЯМР (CDCl3) δ: 1,77 (2H, дкв, J=12,5, 4,0Гц), 2,28-2,32 (1H, м), 2,41 (1H, т, J=12,5Гц), 2,52 (3H, с), 2,65 (1H, д, J=10,5Гц), 2,76-2,81 (1H, м), 2,83-2,86 (3H, м), 2,98-3,05 (3H, м), 3,75 (каждый 1H, система AB д, J=15,5Гц), 4,02-4,08 (1H, м), 4,45 (1H, шир.), 4,54-4,59 (1H, м), 4,64-4,70 (1H, м), 6,87 (1H, д, J=1,5Гц), 7,19-7,22 (1H, м), 7,32 (1H, д, J=8,5Гц), 7,64 (1H, д, J=2,0Гц), 8,11 (1H, д, J=5,5Гц), 8,20 (1H, д, J=7,3Гц), 9,30 (1H, шир.).
МС (FAB) m/z: 519 (M+H+).
[Пример 169]
Гидрохлорид N-((3R,4S)-1-ацетил-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
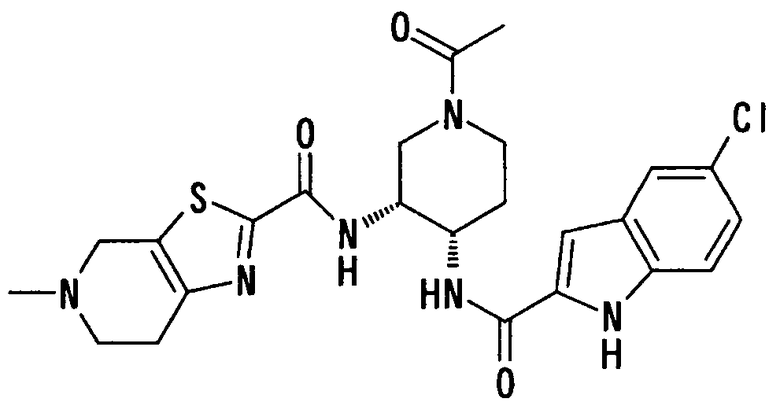
4N Диоксановый раствор (7,0 мл) хлористоводородной кислоты добавляли к диоксановому раствору (15 мл) соединения (630 мг), полученного в ссылочном примере 214, и смесь перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь концентрировали при пониженном давлении. Полученные таким образом желтые твердые частицы (590 мг) и соединение (379 мг), полученное в ссылочном примере 10, использовали для получения свободного основания (330 мг) указанного в заголовке соединения подобно способу примера 91. Полученное свободное основание обрабатывали этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения (Данные ЯМР для свободного основания).
Т.пл. 202-222°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,65-1,85 (1H, м), 1,87, 2,06 (всего 3H, каждый с), 1,88-2,10 (1H, м), 2,37 (3H, с), 2,65-2,77 (2H, м), 2,79-2,89 (2H, м), 2,99-3,09 (0,5H, м), 3,30-3,52 (2H, м), 3,64 (2H, с), 3,70-3,80 (0,5H, м), 3,96-4,21 (2H, м), 4,27 (1H, шир.с), 4,35-4,48 (1H, м), 7,07, 7,11 (всего 1H, каждый с), 7,18 (1H, д, J=8,8Гц), 7,42 (1H, д, J=8,8Гц), 7,71 (1H, с), 8,16-8,22 (1H, м), 8,37, 8,46 (всего 1H, каждый д, J=7,8Гц), 11,81, 11,83 (всего 1H, каждый с).
МС (ESI) m/z: 515 (M+H+).
[α]25 D = -56,4° (c = 0,50, метанол).
[Пример 170]
Гидрохлорид N-((3R,4R)-1-ацетил-4-{[(5-хлориндол-2-ил)карбонил]амино}пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
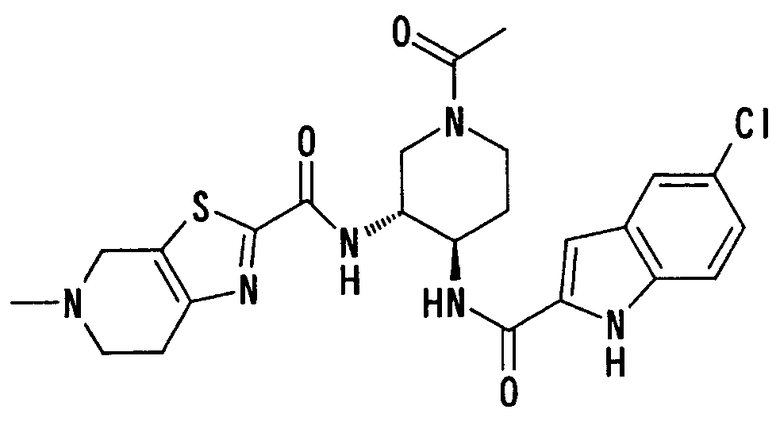
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 219 и ссылочном примере 10, подобно способу примера 169.
Т.пл. 221-238°C.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,56 (0,5H, м), 1,60-1,70 (0,5H, м), 1,89-2,01 (1H, м), 2,05 (3H, с), 2,51-2,67 (1H, м), 2,88 (3H, с), 3,00-3,22 (3H, м), 3,31-3,40 (3H, м), 3,56-3,67 (0,5H, м), 3,78-4,02 (1,5H, м), 4,22-4,44 (2H, м), 4,56-4,72 (1H, м), 7,02 (1H, с), 7,15 (1H, дд, J=8,8, 2,0Гц), 7,37 (1H, д, J=8,8Гц), 7,67 (1H, д, J=2,0Гц), 8,42 (1H, д, J=9,8Гц), 8,67-8,78 (1H, м), 11,02-11,14 (1H, м), 11,72 (0,5H, с), 11,74 (0,5H, с).
МС (FAB) m/z: 515 (M+H+).
[α]25 D = -105,4° (c = 0,58, метанол).
[Пример 171]
Гидрохлорид N-[(3R,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
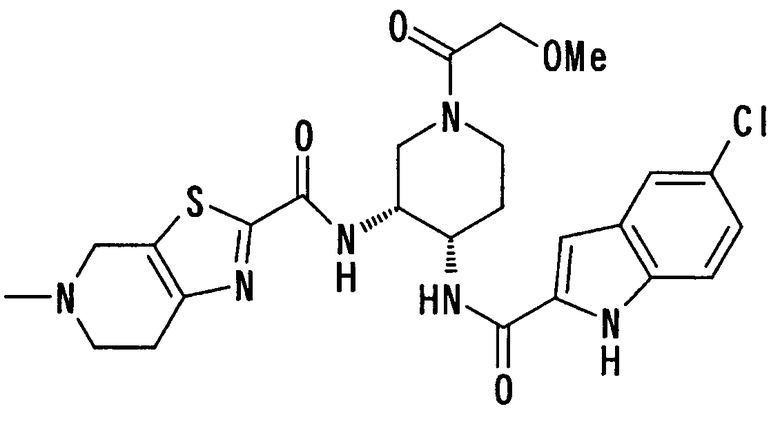
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 221, подобно способу примера 169.
Т.пл. 207-220°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 1,70-1,80 (1H, м), 1,85-2,05 (1H, м), 2,90 (3H, с), 3,00-3,20 (2H, м), 3,16 (3H, с), 3,22-3,82 (7H, м), 3,88-4,80 (5H, м), 7,09 (1H, д, J=9,0Гц), 7,17 (1H, дд, J=8,8, 1,9Гц), 7,42 (1H, д, J=8,8Гц), 7,70 (1H, д, J=1,9Гц), 8,29 (1H, шир.с), 8,40-8,50 (1H, м), 11,20-11,50 (1H, м), 11,85 (1H, с).
МС (ESI) m/z: 545 (M+H+).
[α]25 D = -53,4° (c = 0,52, метанол).
[Пример 172]
Гидрохлорид N-[(3R,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-(2-метоксиацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
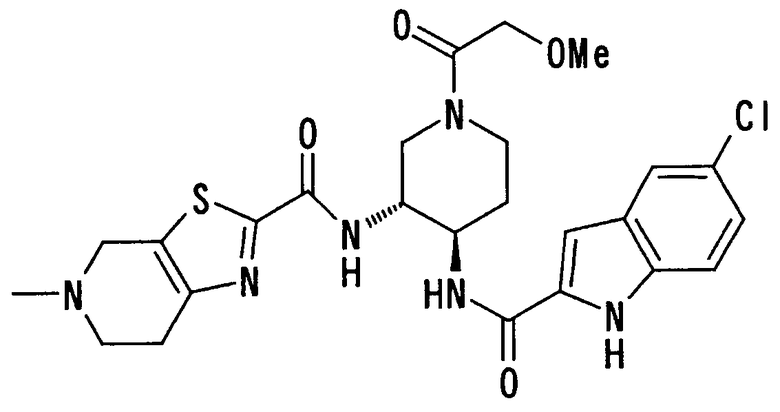
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 223, подобно способу примера 169.
Т.пл. 213-230°C.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,56 (0,5H, м), 1,61-1,70 (0,5H, м), 1,89-2,00 (1H, м), 2,05 (3H, с), 2,45-2,67 (1H, м), 2,88 (3H, с), 3,00-3,21 (4H, м), 3,32-3,56 (7H, м), 3,78-3,89 (2H, м), 4,00-4,24 (2H, м), 4,26-4,43 (2H, м), 7,02 (1H, с), 7,13 (1H, дд, J=8,8, 2,0Гц), 7,37 (1H, д, J=8,8Гц), 7,67 (1H, д, J=2,0Гц), 8,41 (1H, д, J=9,8Гц), 8,74 (1H, д, J=9,8Гц), 10,80-10,90 (1H, м), 11,72 (1H, с).
МС (FAB) m/z: 545 (M+H+).
[α]25 D = -100,3° (c = 0,51, метанол).
[Пример 173]
Гидрохлорид N-((3R,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}-6-оксотетрагидро-2Н-пиран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
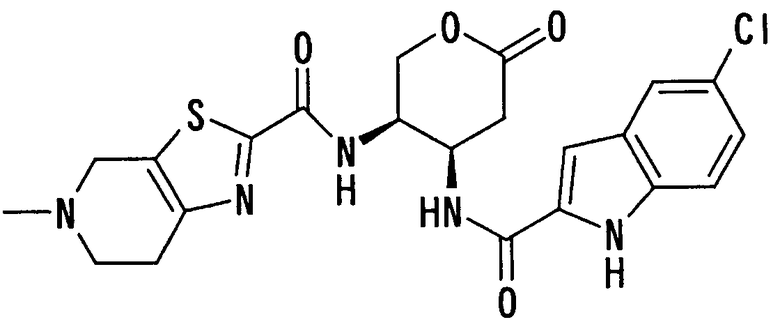
Указанное в заголовке соединение получали из низкополярного соединения, полученного в ссылочном примере 176, и соединения, полученного в ссылочном примере 10, подобно способу примера 169.
1Н-ЯМР (ДМСО-d6) δ: 2,41-2,56 (2H, м), 2,91 (3H, с), 3,01-3,23 (1H, м), 3,24-3,56 (5H, м), 3,62-3,67 (1H, м), 4,21-4,44 (1H, м), 4,56-4,78 (2H, м), 7,11 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,22 (1H, д, J=8,5Гц), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, д, J=2,0Гц), 8,40-8,50 (1H, м), 11,34-11,56 (1H, м), 11,82 (1H, с).
МС (FAB) m/z: 488 (M+H+).
[Пример 174]
Гидрохлорид N-((3R,4S)-4-{[(5-хлориндол-2-ил)карбонил]амино}-6-оксотетрагидро-2Н-пиран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
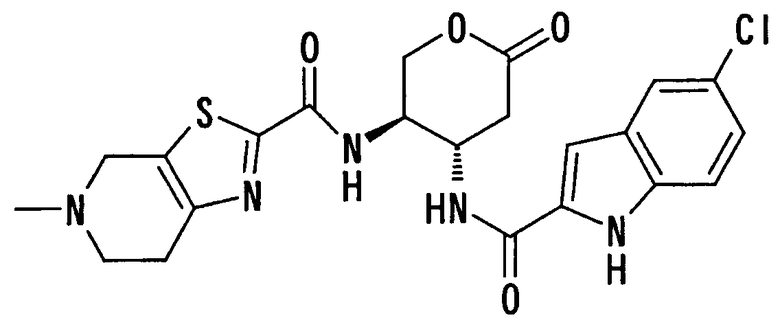
Указанное в заголовке соединение получали из высокополярного соединения, полученного в ссылочном примере 176, и соединения, полученного в ссылочном примере 10, подобно способу примера 169.
1Н-ЯМР (ДМСО-d6) δ: 2,41-2,56 (2H, м), 2,91 (3H, с), 3,23-3,41 (2H, м), 3,43-3,50 (2H, м), 3,56-3,67 (2H, м), 4,37 (1H, дд, J=13,9, 7,1Гц), 4,40-4,50 (1H, м), 4,56-4,78 (2H, м), 7,12 (1H, с), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,41 (1H, д, J=8,8Гц), 7,71 (1H, д, J=2,0Гц), 8,44 (1H, д, J=8,5Гц), 8,15 (1H, д, J=8,5Гц), 11,42-11,53 (1H, м), 11,79 (1H, с).
МС (FAB) m/z: 488 (M+H+).
[Пример 175]
Этил (3R,4S)-5-{[трет-бутил(дифенил)силил]окси}-3-{[(5-хлориндол-2-ил)карбонил]амино}-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}валерат
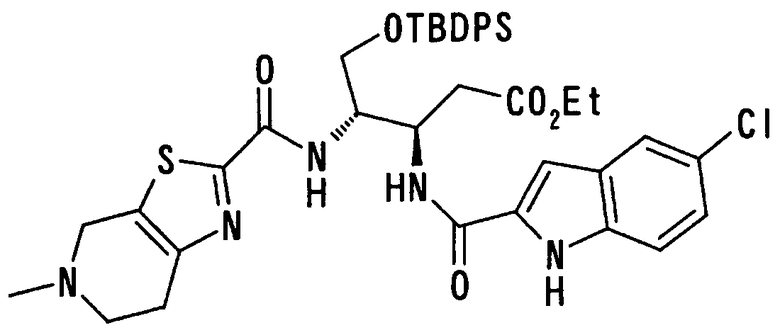
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 225, подобно способу примера 169.
1Н-ЯМР (CDCl3) δ: 1,09 (9H, с), 1,21 (3H, т, J=7,4Гц), 2,49 (3H, с), 2,65 (1H, дд, J=15,9, 5,4Гц), 2,67-2,90 (5H, м), 3,60 (1H, д, J=14,9Гц), 3,72 (1H, д, J=14,9Гц), 3,78-3,91 (2H, м), 4,00-4,21 (2H, м), 4,43-4,50 (1H, м), 4,78-4,89 (1H, м), 6,81 (1H, с), 7,20 (1H, дд, J=8,8, 2,0Гц), 7,32-7,52 (м, 7H), 7,63-7,74 (6H, м), 7,89-8,01 (1H, м), 9,18 (1H, с).
[Пример 176]
Этил (3R,4S)-3-{[(5-хлориндол-2-ил)карбонил]амино}-5-гидрокси-4-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}валерат
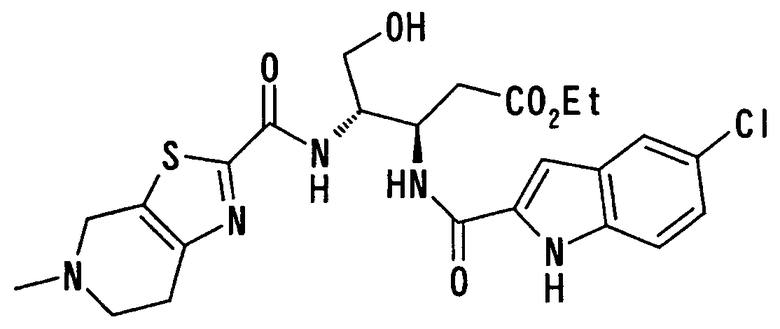
После добавления по каплям фтористого водорода·пиридина (0,4 мл) к смешанному раствору, состоящему из соединения (0,54 г), полученного в примере 175, пиридина (4,0 мл) и тетрагидрофурана (10 мл), при охлаждении льдом реакционную смесь перемешивали 18 часов при постепенном повышении ее температуры до комнатной температуры. Реакционную смесь концентрировали и полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 9:1) с получением указанного в заголовке соединения (0,31 г).
1Н-ЯМР (CDCl3) δ: 1,20 (3H, т, J=7,4Гц), 2,49 (3H, с), 2,67-2,90 (6H, м), 3,62-3,74 (3H, м), 3,78-3,94 (1H, м), 4,00-4,20 (2H, м), 4,30-4,40 (1H, м), 4,80-4,89 (1H, м), 6,93 (1H, с), 7,23 (1H, дд, J=8,8, 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,56 (1H, д, J=8,5Гц), 7,61 (1H, д, J=2,0Гц), 7,88 (1H, д, J=8,5Гц), 9,29 (1H, с).
[Пример 177]
Гидрохлорид N-((3S,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}-6-оксотетрагидро-2Н-пиран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
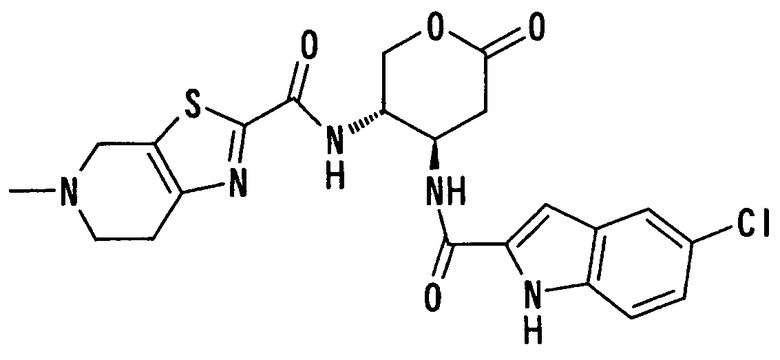
4N Диоксановый раствор (20 мл) хлористоводородной кислоты добавляли к соединению (0,31 г), полученному в примере 176, и смесь кипятили с обратным холодильником в течение 4 часов. Реакционную смесь концентрировали и полученный остаток перекристаллизовывали из диэтилового эфира с получением указанного в заголовке соединения (0,23 г).
Т.пл. 221-238°C (разложение).
1Н-ЯМР и МС (FAB): такие же, как у энантиомера в примере 174.
[Пример 178]
Гидрохлорид N-((3R*,4R*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
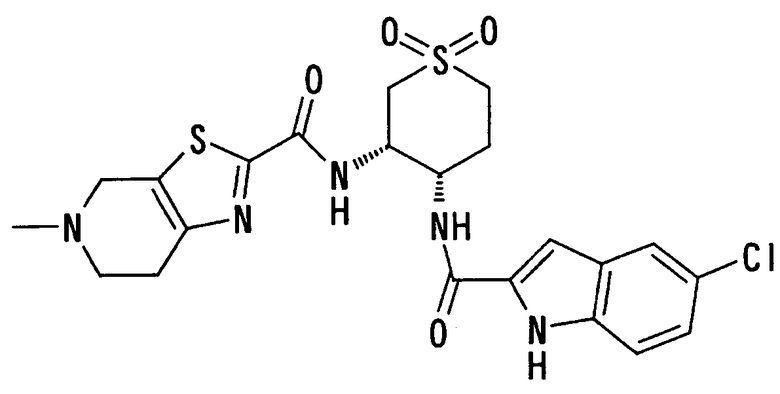
Свободное основание указанного в заголовке соединения получали из соединения, полученного в ссылочном примере 227, и 5-хлориндол-2-карбоновой кислоты подобно способу примера 91. Полученное свободное основание обрабатывали этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения.
Т.пл. 241-244°C.
1Н-ЯМР (ДМСО-d6) δ: 2,14 (1H, шир.), 2,30-2,34 (1H, м), 2,92 (3H, с), 3,10-3,18 (2H, м), 3,41 (4H, шир.), 3,68 (2H, шир.), 4,44 (1H, шир.), 4,63-4,78 (3H, м), 7,16-7,18 (1H, м), 7,21 (1H, с), 7,43 (1H, д, J=8,5Гц), 7,67 (1H, д, J=4,6Гц), 8,39 (1H, шир.), 8,94 (1H, шир.), 11,82 (1H, шир.).
МС (ESI) m/z: 522 (M+H+).
[Пример 179]
Гидрохлорид N-((3R*,4R*)-4-{[(5-фториндол-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
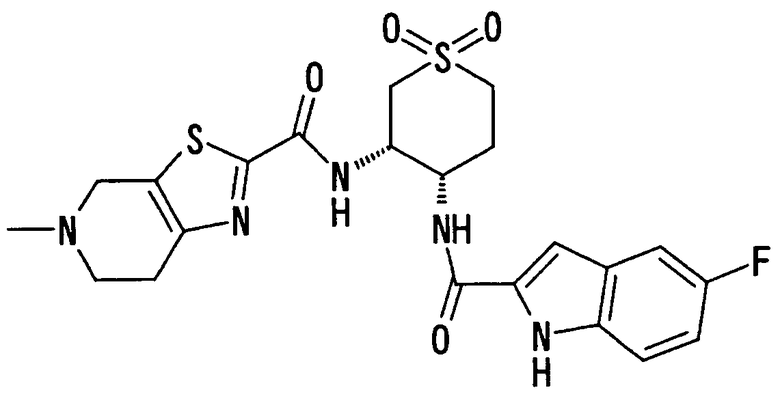
Свободное основание указанного в заголовке соединения получали из соединения, полученного в ссылочном примере 227, и 5-фториндол-2-карбоновой кислоты подобно способу примера 91. Полученное свободное основание обрабатывали этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения.
Т.пл. 243-245°C.
1Н-ЯМР (ДМСО-d6) δ: 2,14 (1H, шир.), 2,30-2,33 (1H, м), 2,92 (3H, с), 3,13 (2H, шир.), 3,51 (4H, шир.), 3,63 (2H, шир.), 4,63 (3H, шир.), 4,78 (1H, шир.), 7,01-7,05 (1H, м), 7,21 (1H, с), 7,37-7,44 (2H, м), 8,36 (1H, шир.), 8,93 (1H, д, J=6,8Гц), 11,72 (1H, шир.).
МС (ESI) m/z: 506 (M+H+).
[Пример 180]
Гидрохлорид N-((3R*,4R*)-3-{[(5-хлориндол-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-4-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
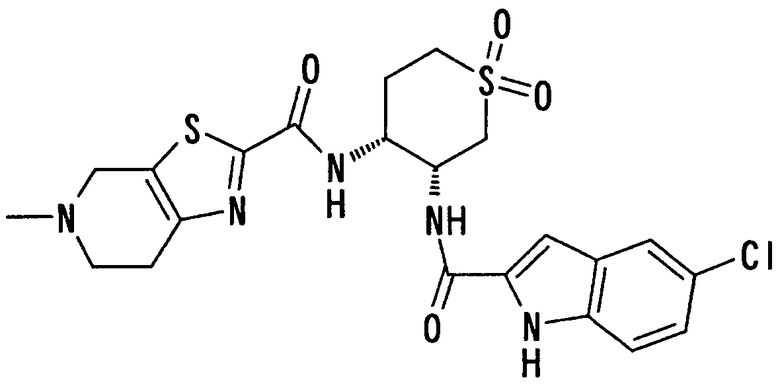
Свободное основание указанного в заголовке соединения получали из соединения, полученного в ссылочном примере 229, и соединения, полученного в ссылочном примере 10, подобно способу примера 91. Полученное свободное основание обрабатывали этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения.
Т.пл. 242-247°C.
1Н-ЯМР (ДМСО-d6) δ: 2,16 (1H, шир.), 2,45 (1H, шир.), 2,93 (3H, с), 3,13 (2H, шир.), 3,26 (4H, шир.), 3,69 (2H, шир.), 4,45 (1H, шир.), 4,65-4,77 (3H, м), 7,01 (1H, с), 7,17 (1H, дд, J=8,7, 1,4Гц), 7,43 (1H, д, J=8,5Гц), 7,69 (1H, с), 8,35-8,40 (1H, м), 9,04 (1H, шир.), 11,86 (1H, с).
МС (ESI) m/z: 522 (M+H+).
[Пример 181]
Гидрохлорид N-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
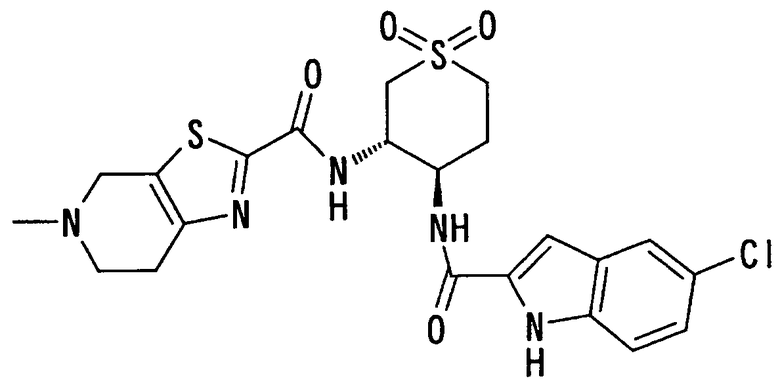
Свободное основание указанного в заголовке соединения получали из соединения, полученного в ссылочном примере 231, и 5-хлориндол-2-карбоновой кислоты подобно способу примера 91. Полученное свободное основание обрабатывали этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения.
Т.пл. 244-249°C.
1Н-ЯМР (ДМСО-d6) δ: 2,17-2,27 (2H, м), 2,90 (3H, с), 3,09 (1H, шир.), 3,18-3,21 (2H, м), 3,31-3,34 (2H, м), 3,60-3,67 (3H, м), 4,41-4,49 (2H, м), 4,54-4,59 (2H, м), 7,04 (1H, с), 7,09-7,13 (1H, м), 7,39 (1H, д, J=8,5Гц), 7,61 (1H, д, J=9,9Гц), 8,52-8,56 (1H, м), 8,83-8,85 (1H, м), 11,65 (1H, д, J=11,9Гц).
МС (ESI) m/z: 522 (M+H+).
[Пример 182]
Гидрохлорид N-((3R*,4S*)-4-{[(5-фториндол-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
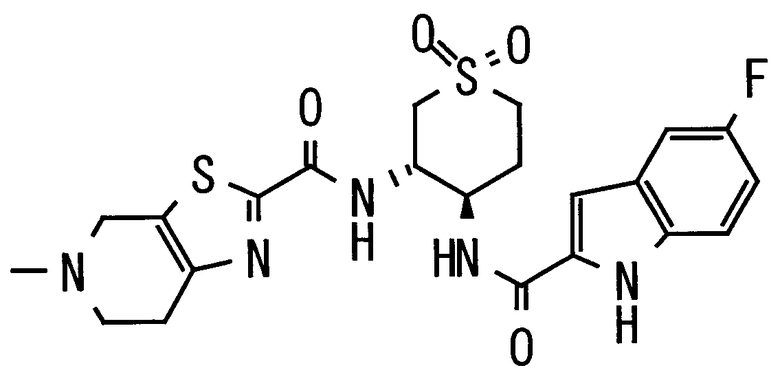
Свободное основание указанного в заголовке соединения получали из соединения, полученного в ссылочном примере 231, и 5-фториндол-2-карбоновой кислоты подобно способу примера 91. Полученное свободное основание обрабатывали этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения.
Т.пл. 236-241°C.
1Н-ЯМР (ДМСО-d6) δ: 2,20-2,24 (2H, м), 2,89 (3H, с), 3,07 (1H, шир.), 3,19-3,22 (2H, м), 3,60-3,66 (4H, м), 4,43-4,58 (5H, м), 6,95-7,00 (1H, м), 7,04 (1H, с), 7,32-7,38 (2H, м), 8,50 (1H, д, J=8,5Гц), 8,83 (1H, д, J=8,5Гц), 11,59 (1H, с).
МС (ESI) m/z: 506 (M+H+).
[Пример 183]
Гидрохлорид N-((3R*,4R*)-3-{[(5-фториндол-2-ил)карбонил]амино}-1,1-диоксогексагидро-1-тиопиран-4-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
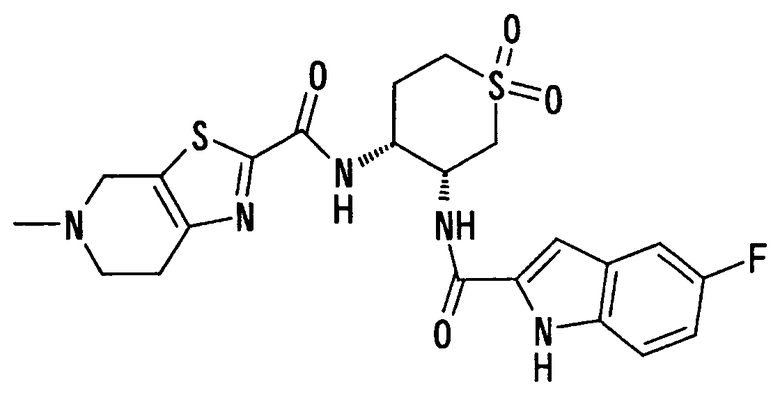
Свободное основание указанного в заголовке соединения получали из соединения, полученного в ссылочном примере 233, и соединения, полученного в ссылочном примере 10, подобно способу примера 91. Полученное свободное основание обрабатывали этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения.
Т.пл. 244-249°C.
1Н-ЯМР (ДМСО-d6) δ: 2,12-2,18 (1H, м), 2,50 (1H, шир.), 2,92 (3H, с), 3,17 (3H, шир.), 3,50-3,61 (5H, м), 4,45 (1H, шир.), 4,62-4,78 (3H, м), 6,98-7,03 (2H, м), 7,36-7,42 (2H, м), 8,30 (1H, шир.), 9,00 (1H, д, J=8,0Гц), 11,74 (1H, с).
МС (ESI) m/z: 506 (M+H+).
[Пример 184]
N-((3S,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-метил-6-оксопиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (низкополярное соединение) и N-((3R,4R)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-метил-6-оксопиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид (высокополярное соединение)
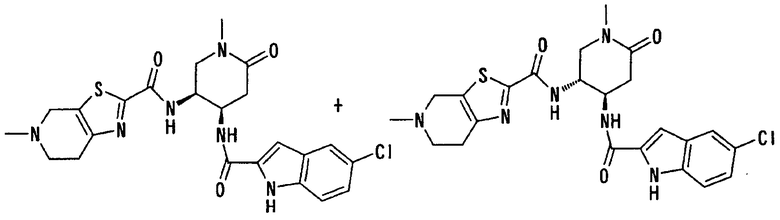
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 236, и соединения, полученного в ссылочном примере 10, подобно способу примера 169.
Низкополярное соединение:
Т.пл. 189-203°C (разложение).
1Н-ЯМР (CDCl3) δ: 2,52 (3H, с), 2,59 (1H, кв, J=8,8Гц), 2,71-2,78 (2H, м), 2,89-3,00 (2H, м), 3,03 (3H, с), 3,12 (1H, дд, J=17,6, 5,4Гц), 3,43 (1H, дд, J=12,7, 5,1Гц), 3,70 (1H, д, J=15,2Гц), 3,77 (1H, д, J=15,2Гц), 3,83 (1H, дд, J=12,7, 3,9Гц), 4,55-4,67 (2H, м), 6,99 (1H, с), 7,23 (1H, дд, J=8,8, 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,65 (1H, д, J=2,0Гц), 8,07 (1H, д, J=5,1Гц), 8,16 (1H, д, J=5,4Гц), 9,43 (1H, с).
МС (FAB) m/z: 501 (M+H+).
Высокополярное соединение:
Т.пл. 183-195°C (разложение).
1Н-ЯМР (ДМСО-d6) δ: 2,33 (3H, с), 2,41-2,50 (1H, м), 2,62-2,73 (3H, м), 2,75-2,81 (1H, м), 2,82 (3H, с), 3,21-3,32 (2H, м), 3,34-3,50 (2H, м), 3,55 (1H, д, J=15,4Гц), 3,63 (1H, д, J=15,4Гц), 4,30-4,40 (0,5H, м), 4,50-4,60 (0,5H, м), 7,04 (1H, с), 7,15 (1H, дд, J=8,8, 2,0Гц), 7,38 (1H, д, J=8,8Гц), 7,67 (1H, д, J=2,0Гц), 8,49 (1H, д, J=8,5Гц), 8,71 (1H, д, J=8,5Гц), 11,74 (1H, с).
МС (FAB) m/z: 501 (M+H+).
[Пример 185]
Гидрохлорид 5-хлор-N-((1R*,2S*)-2-{[4-(пиридин-4-ил)бензоил]амино}циклогексил)индол-2-карбоксамида
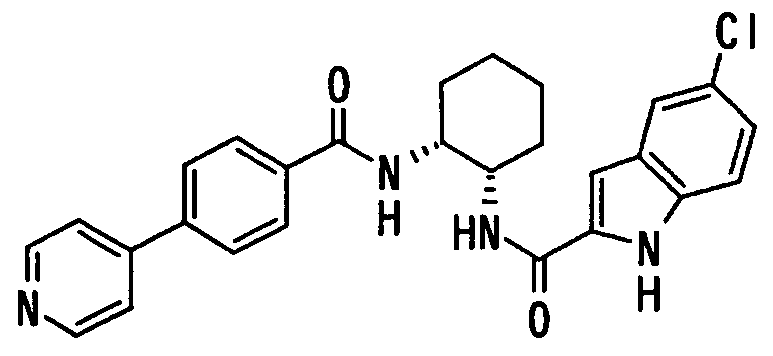
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 71, и соединения, полученного в ссылочном примере 237, подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,52 (2H, м), 1,60-1,80 (4H, м), 1,96-2,10 (2H, м), 4,24-4,39 (2H, м), 7,15 (1H, дд, J=8,8, 2,0Гц), 7,21 (1H, с), 7,40 (1H, д, J=8,8Гц), 7,64 (1H, д, J=2,0Гц), 8,06 (4H, с), 8,18 (1H, J=7,3Гц), 8,34-8,42 (3H, м), 8,94 (2H, д, J=6,9Гц), 11,91 (1H, с).
МС (FAB)m/z: 473 (М+Н)+.
[Пример 186]
N-оксид 4-(4-{[((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)амино]карбонил}фенил)пиридина
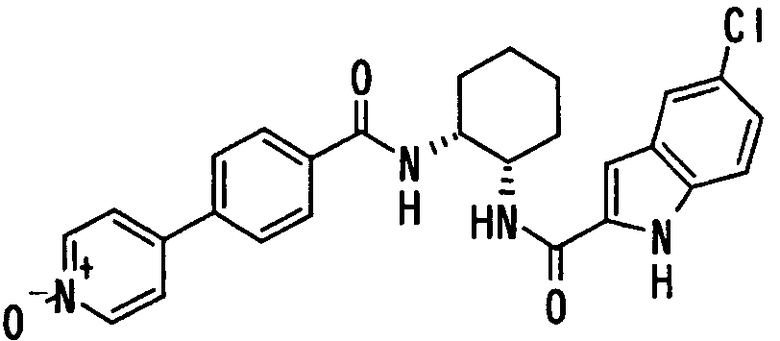
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 71, и соединения, полученного в ссылочном примере 240, подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,52 (2H, м), 1,60-1,80 (4H, м), 1,88-2,00 (2H, м), 4,21-4,36 (2H, м), 7,12-7,18 (2H, м), 7,41 (1H, д, J=8,6Гц), 7,66 (1H, с), 7,80-7,87 (4H, м), 7,91 (2H, д, J=8,3Гц), 8,01 (1H, д, J=7,6Гц), 8,09 (1H, д, J=7,3Гц), 8,27 (2H, д, J=6,6Гц), 11,79 (1H, с).
МС (FAB) m/z: 489 (M+H)+.
[Пример 187]
Гидрохлорид 5-хлор-N-((1R*,2S*)-2-{[4-(пиридин-2-ил)бензоил]амино}циклогексил)индол-2-карбоксамида
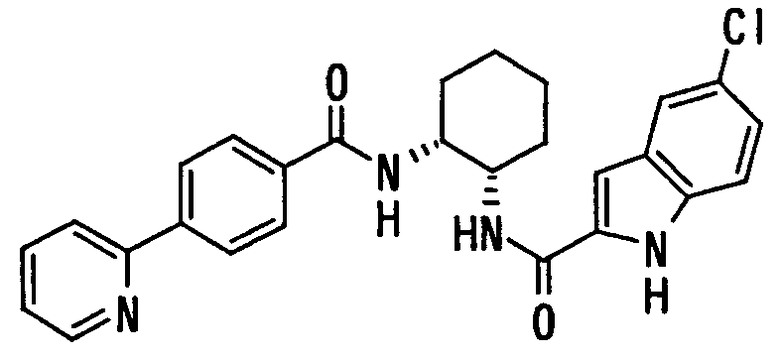
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 71, и 4-(2-пиридил)бензойной кислоты (выложенная заявка № 2000-119253 на патент Японии) подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,39-1,51 (2H, м), 1,60-1,80 (4H, м), 1,89-2,00 (2H, м), 4,24-4,38 (2H, м), 7,12-7,16 (2H, м), 7,36-7,39 (1H, м), 7,42 (1H, д, J=8,8Гц), 7,66 (1H, д, J=2,0Гц), 7,87-7,90 (1H, м), 7,92 (2H, д, J=8,3Гц), 7,98-8,11 (3H, м), 8,15 (2H, д, J=8,3Гц), 8,69 (1H, д, J=4,6Гц), 11,80 (1H, с).
МС (FAB) m/z: 473 (М+Н)+.
[Пример 188]
N-оксид 2-(4-{[((1R*,2S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}циклогексил)амино]карбонил}фенил)пиридина
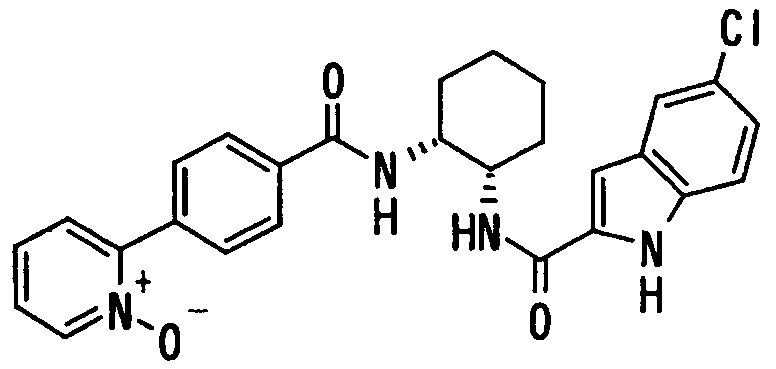
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 71, и соединения, полученного в ссылочном примере 241, подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,39-1,51 (2H, м), 1,60-1,79 (4H, м), 1,89-2,00 (2H, м), 4,23-4,37 (2H, м), 7,12-7,17 (2H, м), 7,39-7,43 (3H, м), 7,61-7,64 (1H, м), 7,67 (1H, д, J=2,0Гц), 7,89 (4H, с), 8,00-8,06 (1H, м), 8,08-8,02 (1H, м), 8,32-8,35 (1H, м), 11,79 (1H, с).
МС (FAB) m/z: 489 (M+H)+.
[Пример 189]
Гидрохлорид 5-хлор-N-[(1R*,2R*)-2-({[5-(4-пиридин-2-ил)тиазол-2-ил]карбонил}амино)циклогексил]индол-2-карбоксамида
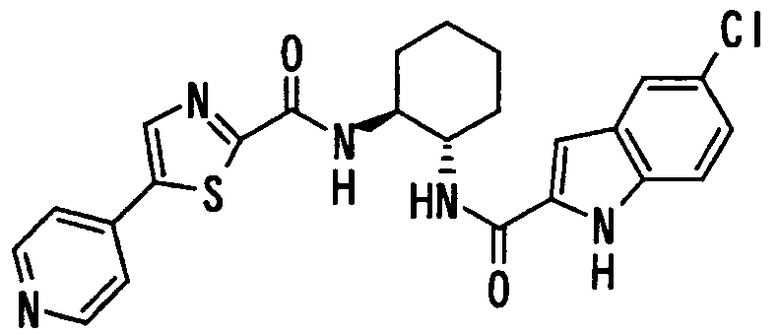
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 69, и 5-(4-пиридил)тиазол-2-карбоксилата лития (выложенная заявка № 2000-143623 на патент Японии) подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,44 (2H, шир.с), 1,65 (4H, шир.с), 1,85-2,06 (2H, м), 4,23 (1H, шир.с), 4,30 (1H, шир.с), 7,14-7,23 (2H, м), 7,41 (1H, д, J=8,8Гц), 7,69 (1H, с), 8,04-8,13 (2H, м), 8,13 (1H, д, J=8,8Гц), 8,59 (1H, д, J=8,0Гц), 8,75-8,87 (3H, м), 11,83 (1H, с).
МС (ESI)m/z: 480 (M+H)+.
[Пример 190]
Гидрохлорид 5-хлор-N-[(1R*,2S*)-2-({[1-(пиридин-4-ил)пиперидин-4-ил]карбонил}амино)циклогексил]индол-2-карбоксамида
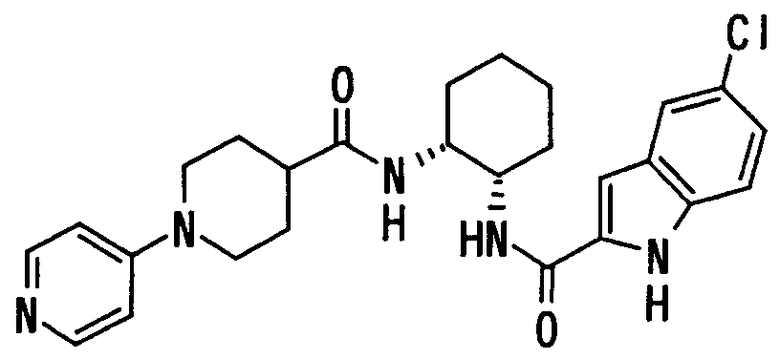
1-(4-Пиридил)пиперидин-4-карбоновую кислоту (Tetrahedron, 1998, Vol. 44, p. 7095) (206 мг) суспендировали в метиленхлориде (50 мл), добавляли при охлаждении льдом тионилхлорид (144 мкл) и смесь перемешивали в течение 30 минут. После добавления к реакционной смеси триэтиламина (969 мкл), добавляли соединение (328 мг), полученное в ссылочном примере 71, и смесь перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь концентрировали при пониженном давлении, к остатку добавляли воду, смесь концентрировали при пониженном давлении и выпавший осадок отфильтровывали с получением указанного в заголовке соединения (310 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,30-2,00 (10H, м), 2,74 (1H, шир.с), 3,18 (2H, кв, J=12,3Гц), 4,03 (1H, шир.с), 4,10-4,25 (3H, м), 7,15-7,55 (4H, м), 7,42 (1H, д, J=8,8Гц), 7,65 (1H, с), 7,91 (1H, д, J=8,8Гц), 8,20-8,35 (3H, м), 11,91 (1H, с), 13,47 (1H, шир.с).
МС (FAB) m/z: 480 (М+Н)+.
[Пример 191]
Гидрохлорид N1-(4-хлорфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
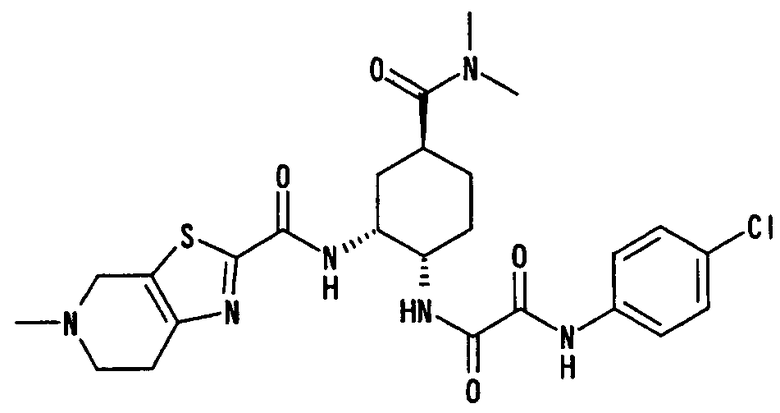
Соединение (288 мг), полученное в ссылочном примере 242, растворяли в тетрагидрофуране (8,0 мл), добавляли последовательно гидроксид лития (46 мг) и воду (1,0 мл) и смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь концентрировали при пониженном давлении с получением неочищенного продукта (292 мг) 2-(4-хлоранилино)-2-оксоацетата лития в виде бесцветного твердого вещества. Полученный неочищенный продукт и соединение, полученное в ссылочном примере 253, растворяли в N,N-диметилформамиде (15 мл), добавляли моногидрат 1-гидроксибензотриазола (164 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (251 мг) и смесь перемешивали при комнатной температуре в течение 64,5 часов. Отгоняли при пониженном давлении растворитель, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей и полученный органический слой сушили над безводным сульфатом натрия. Затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 47:3). Полученные таким образом бледно-желтые твердые частицы растворяли в метиленхлориде, добавляли 1N этанольный раствор (0,52 мл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли метанол и диэтиловый эфир и выпавший осадок отфильтровывали с получением указанного в заголовке соединения (245 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,55 (1H, м), 1,60-1,80 (3H, м), 1,95-2,10 (2H, м), 2,79 (3H, с), 2,80-3,00 (1H, м), 2,92 (3H, с), 2,94 (3H, с), 3,10-3,40 (2H, м), 3,40-3,80 (2H, м), 3,95-4,05 (1H, м), 4,40-4,80 (3H, м), 7,40 (2H, д, J=8,8Гц), 7,83 (2H, д, J=8,8Гц), 8,75 (1H, д, J=7,1Гц), 9,00-9,10 (1H, шир.), 10,81 (1H, с), 11,45-11,75 (1H, м).
МС (FAB) m/z: 547 (M+H)+.
[Пример 192]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
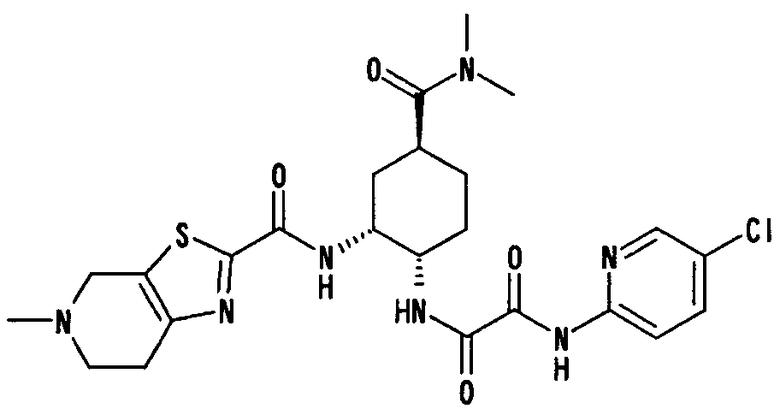
Соединение (240 мг), полученное в ссылочном примере 243, растворяли в тетрагидрофуране (8,0 мл), к раствору добавляли последовательно гидроксид лития (41 мг) и воду (1,0 мл) и смесь перемешивали при комнатной температуре в течение 2,5 часов. Реакционную смесь концентрировали при пониженном давлении с получением 2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетата лития (249 мг).
С другой стороны, 10% палладий на углероде (200 мг) добавляли к раствору соединения (293 мг), полученного в ссылочном примере 252, в метаноле (10 мл) и смесь перемешивали при комнатной температуре в течение 18 часов в атмосфере водорода. После удаления фильтрованием палладия на углероде фильтрат концентрировали при пониженном давлении с получением неочищенного продукта (259 мг) N-{(1R,2S,5S)-2-амино-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида.
Полученный неочищенный продукт (259 мг) и приготовленную выше литиевую соль (249 мг) добавляли к N,N-диметилформамиду (15 мл), добавляли моногидрат 1-гидроксибензотриазола (166 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (235 мг) и смесь перемешивали при комнатной температуре в течение 63,5 часов. Отгоняли при пониженном давлении растворитель, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей и полученный органический слой сушили над безводным сульфатом натрия. Затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 93:7). Полученные таким образом бледно-желтые твердые частицы растворяли в метиленхлориде, к раствору добавляли 1N этанольный раствор (0,855 мл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли метанол и диэтиловый эфир и образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (209 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,57 (1H, м), 1,60-1,80 (3H, м), 1,95-2,13 (2H, м), 2,79 (3H, с), 2,80-3,00 (1H, м), 2,92 (3H, с), 2,94 (3H, с), 3,10-3,40 (2H, м), 3,40-3,80 (2H, м), 3,95-4,05 (1H, м), 4,37-4,80 (3H, м), 7,90-8,10 (2H, м), 8,45 (1H, д, J=2,2Гц), 8,71 (1H, д, J=7,6Гц), 9,10-9,30 (1H, шир.), 10,26 (1H, с), 11,30-11,60 (1H, шир.).
МС (FAB) m/z: 548 (М+Н)+.
[Пример 193]
Гидрохлорид N1-(3-хлорфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
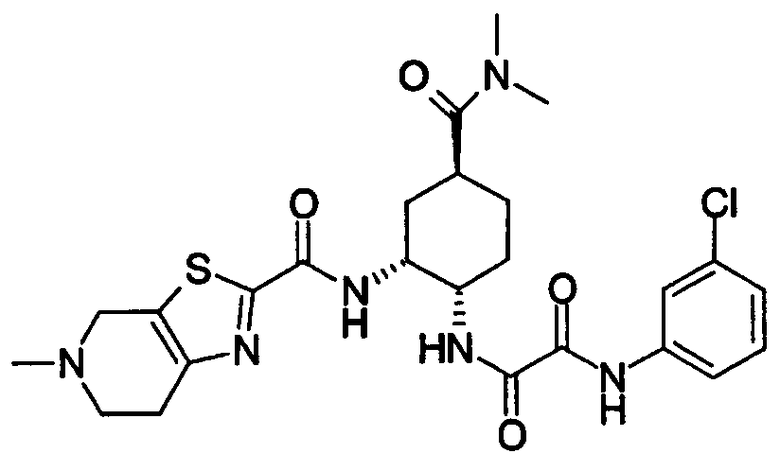
Соединение (222 мг), полученное в ссылочном примере 270, и 3-хлоранилин (63 мкл) растворяли в N,N-диметилформамиде (10 мл), добавляли моногидрат 1-гидроксибензотриазола (68 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (144 мг) и смесь перемешивали при комнатной температуре в течение 40 часов. Отгоняли при пониженном давлении растворитель, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей и полученный органический слой сушили над безводным сульфатом натрия. Затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 30:1). Полученные таким образом бледно-желтые твердые частицы растворяли в метиленхлориде, добавляли 1N этанольный раствор (0,50 мл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли диэтиловый эфир и образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (174 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,62 (1H, м), 1,65-1,90 (3H, м), 1,98-2,20 (2H, м), 2,79 (3H, с), 2,88-3,10 (1H, м), 2,93 (3H, с), 2,94 (3H, с), 3,15-3,40 (2H, м), 3,40-3,90 (2H, м), 3,95-4,10 (1H, м), 4,40-4,80 (3H, м), 7,19 (1H, дд, J=9,3, 2,0Гц), 7,37 (1H, д, J=8,2Гц), 7,77 (1H, д, J=8,3Гц), 7,92-8,05 (1H, м), 8,75 (1H, д, J=7,3Гц), 8,95-9,20 (1H, шир.), 10,87 (1H, с), 11,25-11,45 (1H, шир.).
[Пример 194]
Гидрохлорид N1-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-N2-(4-фторфенил)этандиамида
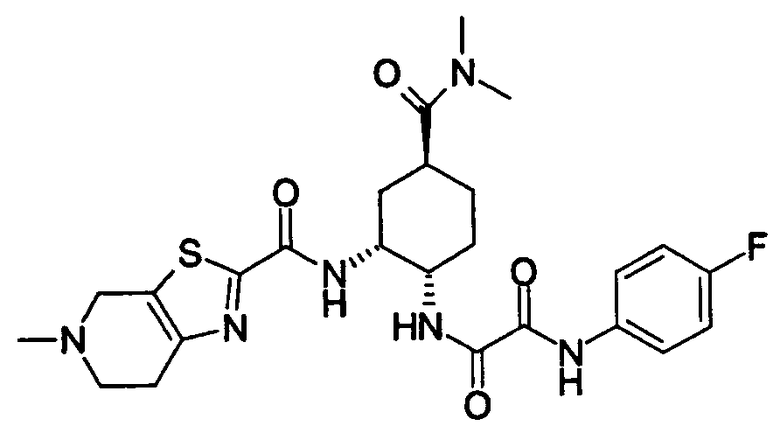
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 254, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,40-2,13 (6H, м), 2,77 (3H, с), 2,93 (3H, с), 2,97 (3H, с), 3,12-3,82 (7H, м), 3,93-4,04 (1H, м), 4,38-4,46 (1H, м), 4,35-4,75 (1H, м), 7,11-7,21 (2H, м), 7,72-7,84 (2H, м), 8,73 (1H, д, J=7,6Гц), 8,93-9,02 (1H, м), 10,70 (1H, с).
МС (FAB) m/z: 531 (М+Н)+.
[Пример 195]
Гидрохлорид N1-(4-бромфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
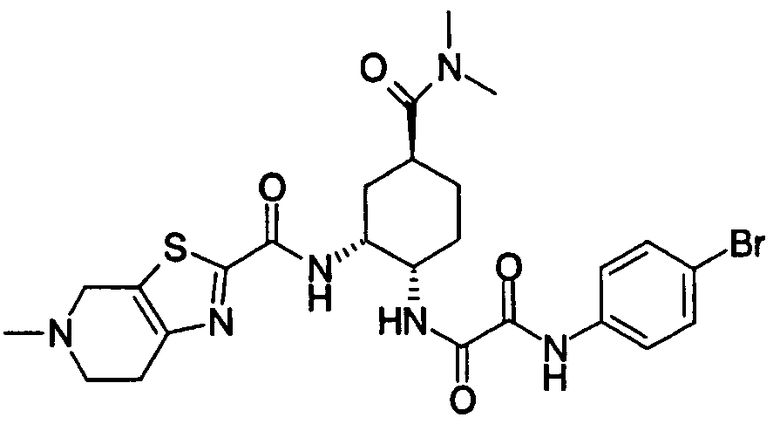
Соединение (152 мг), полученное в ссылочном примере 255, растворяли в тетрагидрофуране (5,0 мл), добавляли последовательно 1N водный раствор (1,20 мл) гидроксида натрия и метанол (5,0 мл) и смесь перемешивали при комнатной температуре в течение 2,5 часов. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид (10 мл) и 1N хлористоводородную кислоту (2,0 мл) для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель с получением неочищенного продукта (280 мг) 2-(4-броманилино)-2-оксоуксусной кислоты в виде бесцветного твердого вещества. Полученный неочищенный продукт и соединение (280 мг), полученное в ссылочном примере 253, растворяли в N,N-диметилформамиде (30 мл), добавляли моногидрат 1-гидроксибензотриазола (90 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (226 мг) и смесь перемешивали при комнатной температуре в течение ночи. Отгоняли при пониженном давлении растворитель, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей и полученный органический слой сушили над безводным сульфатом натрия. Затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 97:3). Полученные таким образом бледно-желтые твердые частицы растворяли в метиленхлориде, добавляли 1N этанольный раствор (191 мкл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли метанол и диэтиловый эфир и образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (103 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,43-1,57 (1H, м), 1,59-1,80 (3H, м), 1,97-2,10 (2H, м), 2,79 (3H, с), 2,84-2,98 (7H, м), 3,18 (2H, шир.с), 3,39-3,72 (2H, м), 3,95-4,05 (1H, м), 4,20-4,80 (3H, м), 7,53 (2H, д, J=8,8Гц), 7,77 (2H, д, J=8,8Гц), 8,75 (1H, д, J=7,3Гц), 8,97-9,09 (1H, м), 10,82 (1H, с), 11,11 (1H, шир.с).
МС (FAB) m/z: 591 (M+H)+.
[Пример 196]
Гидрохлорид N1-(4-хлор-2-метилфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
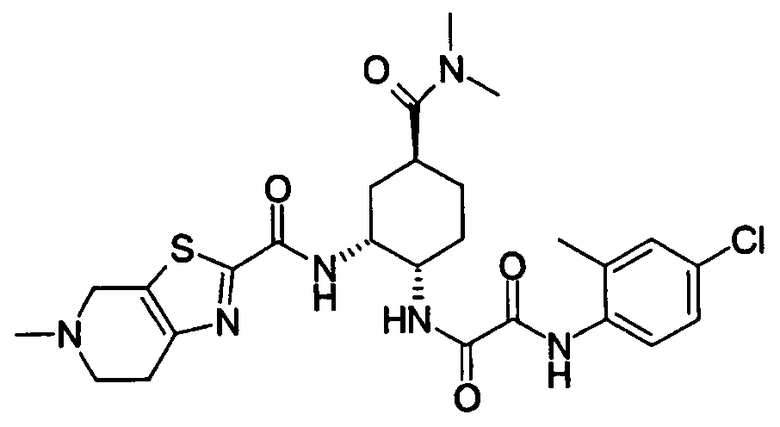
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 256, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,55 (1H, м), 1,60-1,80 (3H, м), 2,00-2,10 (2H, м), 2,19 (3H, с), 2,79 (3H, с), 2,80-3,00 (7H, м), 3,31 (2H, шир.с), 3,40-3,70 (2H, шир.), 3,95-4,05 (1H, м), 4,35-4,70 (3H, м), 7,20-7,30 (1H, м), 7,35 (1H, д, J=2,5Гц), 7,43 (1H, д, J=8,6Гц), 8,76 (1H, д, J=6,6Гц), 9,00-9,15 (1H, шир.), 10,19 (1H, с).
МС (FAB) m/z: 561 (М+Н)+.
[Пример 197]
Гидрохлорид N1-(4-хлор-3-метилфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
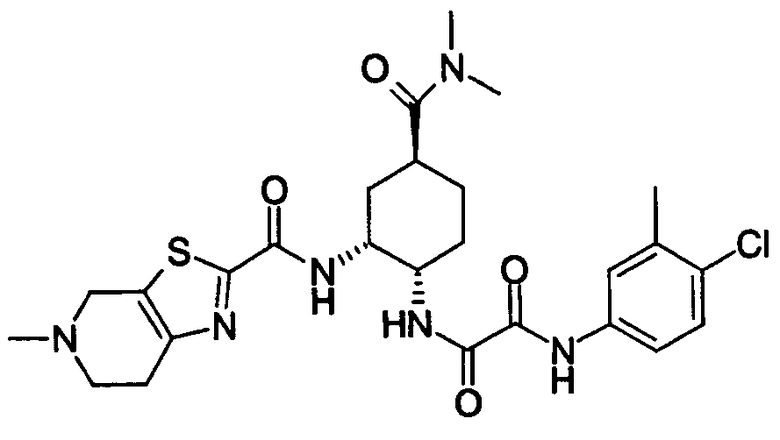
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 257, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,47-1,53 (1H, м), 1,68-1,80 (3H, м), 1,98-2,09 (2H, м), 2,29 (3H, с), 2,79 (3H, с), 2,80-3,00 (1H, м), 2,95 (6H, с), 3,17-3,19 (3H, м), 3,40-3,80 (1H, м), 3,93-4,02 (1H, м), 4,44-4,56 (3H, м), 7,38 (1H, д, J=8,8Гц), 7,65 (1H, д, J=8,8Гц), 7,74 (1H, с), 8,75 (1H, д, J=7,8Гц), 8,96 (1H, д, J=8,0Гц), 10,69 (1H, с).
МС (FAB) m/z: 561 (M+H)+.
[Пример 198]
Гидрохлорид N1-(4-хлор-2-фторфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
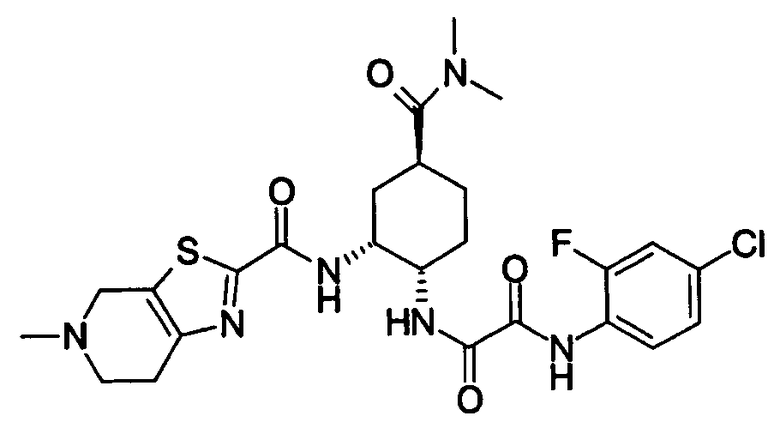
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 258, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,55 (1H, м), 1,58-1,80 (3H, м), 1,95-2,12 (2H, м), 2,77 (3H, с), 2,80-3,00 (1H, м), 2,91 (3H, с), 2,92 (3H, с), 3,10-3,40 (2H, м), 3,40-3,80 (2H, м), 3,95-4,05 (1H, м), 4,30-4,80 (3H, м), 7,29 (1H, д, J=8,5Гц), 7,52 (1H, дд, J=10,3, 2,0Гц), 7,61 (1H, т, J=8,4Гц), 8,72 (1H, д, J=6,8Гц), 9,00-9,20 (1H, шир.), 10,38 (1H, с), 11,20-11,45 (1H, шир.).
МС (FAB) m/z: 565 (М+Н)+.
[Пример 199]
Гидрохлорид N1-(2,4-дихлорфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
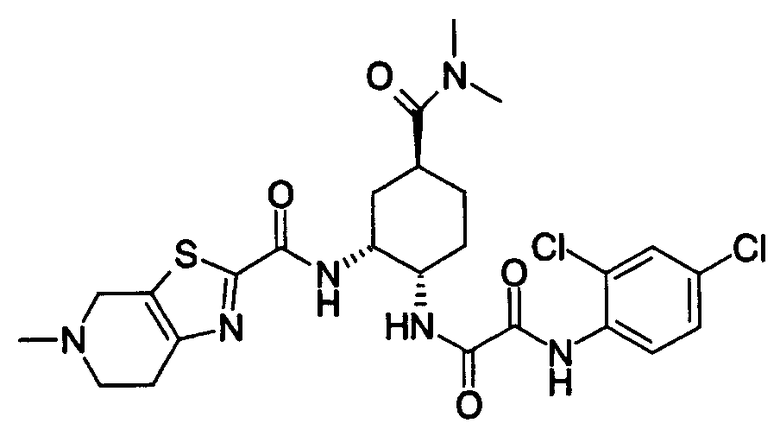
Соединение (300 мг), полученное в ссылочном примере 270, растворяли в N,N-диметилформамиде (5 мл), добавляли 2,4-дихлоранилин (165 мг), гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (260 мг) и моногидрат 1-гидроксибензотриазола (91 мг) и смесь перемешивали при комнатной температуре в течение 2 суток. Отгоняли при пониженном давлении растворитель, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей и полученный органический слой сушили над безводным сульфатом натрия. Затем отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 47:3) с получением свободного основания указанного в заголовке соединения. Полученный продукт растворяли в метиленхлориде, добавляли 1N этанольный раствор (108 мкл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли небольшое количество метанола, добавляли по каплям диэтиловый эфир при облучении ультразвуковыми волнами и отфильтровывали образовавший осадок. Полученный продукт промывали диэтиловым эфиром с получением указанного в заголовке соединения (60 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,77 (4H, м), 2,03-2,12 (2H, м), 2,79 (3H, с), 2,92-2,96 (7H, м), 3,25 (2H, шир.с), 3,49 (1H, шир.с), 3,69 (1H, шир.с), 3,98-4,04 (1H, м), 4,40-4,43 (1H, м), 4,45 (1H, шир.с), 4,69 (1H, шир.с), 7,48 (1H, дд, J=8,5, 2,4Гц), 7,75 (1H, д, J=2,4Гц), 7,89 (1H, д, J=8,5Гц), 8,75 (1H, д, J=6,8Гц), 9,21 (1H, шир.с), 10,25 (1H, с), 11,55 (1H, шир.с).
МС (FAB) m/z: 581 (M+H)+.
[Пример 200]
N1-(3,4-Дихлорфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид
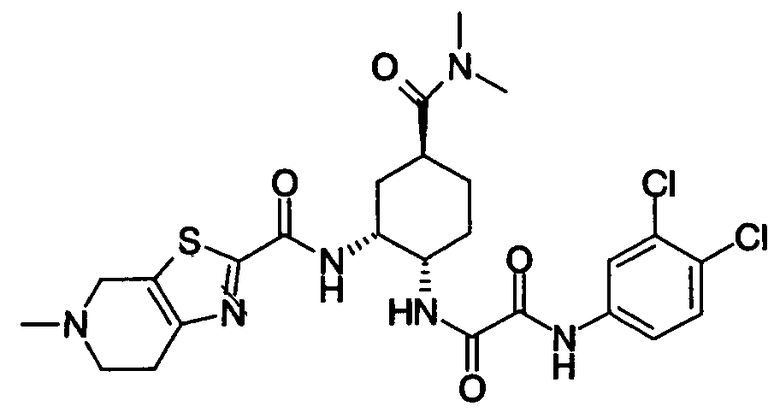
3,4-Дихлоранилин (1,62 г) растворяли в метиленхлориде (20 мл), добавляли последовательно при охлаждении льдом триэтиламин (1,67 мл) и метилхлороксоацетат (1,01 мл) и смесь перемешивали при комнатной температуре в течение 21 часа. Добавляли к реакционной смеси воду и метиленхлорид для разделения жидкостей. Полученный органический слой экстрагировали метиленхлоридом. Органические слои объединяли и сушили над безводным сульфатом магния и отгоняли при пониженном давлении растворитель. Полученный остаток растворяли в этаноле (50 мл), добавляли последовательно воду (25 мл) и моногидрат гидроксида лития (629 мг) и смесь перемешивали при комнатной температуре в течение 12,5 часов. Добавляли дополнительно моногидрат гидроксида лития (629 мг) и смесь перемешивали при комнатной температуре в течение 5,5 часов. Реакционную смесь концентрировали при пониженном давлении до затвердевания. К остатку добавляли воду и диэтиловый эфир для разделения жидкостей. К полученному водному слою для его подкисления добавляли хлористоводородную кислоту. Образовавшееся твердое вещество отфильтровывали с получением неочищенного продукта (1,62 г) 2-(3,4-дихлоранилино)-2-оксоуксусной кислоты в виде бесцветного твердого вещества. Полученный неочищенный продукт (191 мг) и соединение, полученное в ссылочном примере 253, растворяли в N,N-диметилформамиде (10 мл), добавляли моногидрат 1-гидроксибензотриазола (110 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (157 мг) и смесь перемешивали при комнатной температуре в течение 67 часов. Отгоняли при пониженном давлении растворитель, к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и этилацетата для разделения жидкостей и полученный водный слой экстрагировали 3 раза метиленхлоридом. Органические слои объединяли и сушили над безводным сульфатом натрия. Отгоняли при пониженном давлении растворитель, затем остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 95:5) с получением указанного в заголовке соединения (154 мг).
1Н-ЯМР (CDCl3) δ: 1,77-1,88 (1H, м), 1,91-1,95 (1H, м), 2,05-2,10 (3H, м), 2,51 (3H, с), 2,77-2,99 (6H, м), 2,95 (3H, с), 3,05 (3H, с), 3,68 (1H, д, J=15,5Гц), 3,74 (1H, д, J=15,5Гц), 4,08-4,13 (1H, м), 4,69-4,72 (1H, м), 7,40 (2H, с), 7,41 (1H, д, J=7,7Гц), 7,90 (1H, с), 8,01 (1H, д, J=7,7Гц), 9,27 (1H, с).
МС (ESI) m/z: 581 (М+Н)+.
[Пример 201]
N1-(2,4-Дифторфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид
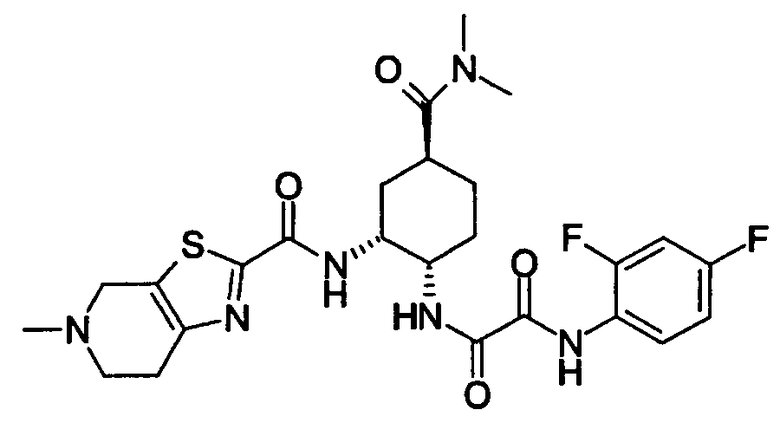
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 259, и конденсацией гидролизата с соединением, полученным в ссылочном примере 253, подобно способу, описанному в примере 191.
1Н-ЯМР (CDCl3) δ: 1,55-1,62 (1H, м), 1,67-1,98 (2H, м), 2,01-2,18 (4H, м), 2,52 (3H, с), 2,77-3,00 (4H, м), 2,95 (3H, с), 2,99 (3H, с), 3,65-3,78 (2H, м), 4,06-4,15 (1H, м), 4,66-4,73 (1H, м), 6,85-6,94 (2H, м), 7,38 (1H, д, J=8,5Гц), 7,96 (1H, д, J=7,3Гц), 8,22-8,29 (1H, м), 9,36 (1H, шир.).
[Пример 202]
N1-(3,4-Дифторфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид
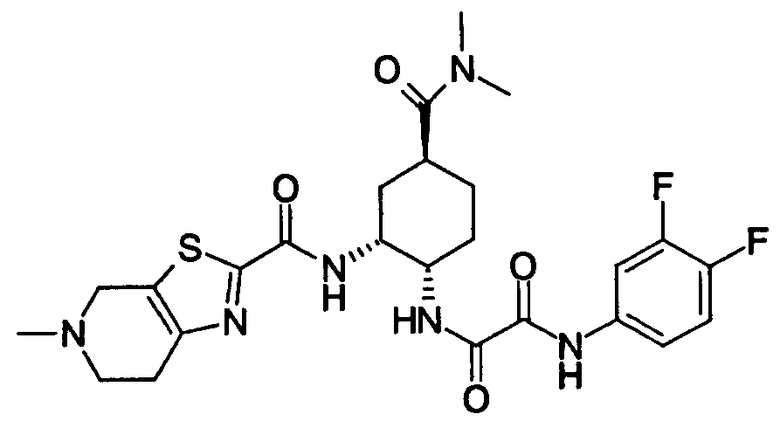
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 260, и конденсацией гидролизата с соединением, полученным в ссылочном примере 253, подобно способу, описанному в примере 191.
1Н-ЯМР (CDCl3) δ: 1,56-1,73 (1H, м), 1,77-1,99 (2H, м), 2,00-2,18 (4H, м), 2,52 (3H, с), 2,75-3,00 (4H, м), 2,95 (3H, с), 3,06 (3H, с), 3,64-3,79 (2H, м), 4,05-4,14 (1H, м), 4,68-4,75 (1H, м), 7,09-7,21 (2H, м), 7,38 (1H, д, J=8,8Гц), 7,72 (1H, ддд, J=12,0, 7,1, 2,6Гц), 7,95 (1H, д, J=7,8Гц), 9,22 (1H, шир.).
[Пример 203]
Гидрохлорид N1-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-N2-(пиридин-4-ил)этандиамида
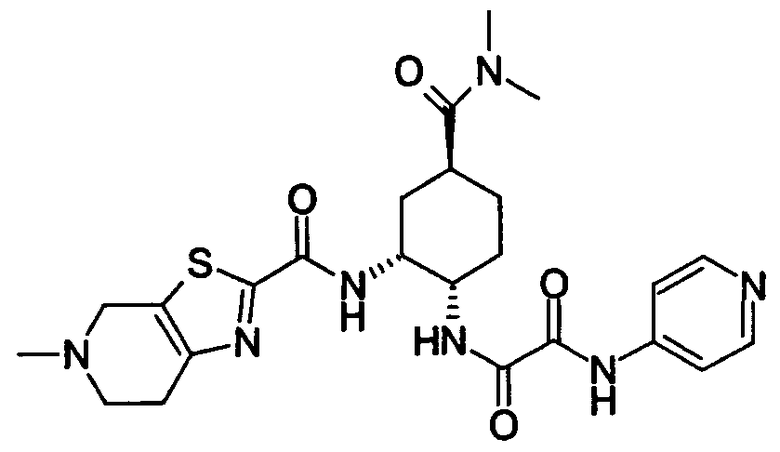
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 261, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,40-2,10 (6H, м), 2,77 (3H, с), 2,927 (3H, с), 2,933 (3H, с), 3,05-4,20 (8H, м), 4,40-4,55 (1H, м), 8,27 (2H, д, J=6,8Гц), 8,67 (1H, д, J=8,0Гц), 8,71 (2H, д, J=6,8Гц), 9,10-9,30 (1H, шир.), 11,81 (1H, с).
МС (FAB) m/z: 514 (М+Н)+.
[Пример 204]
Гидрохлорид N1-(5-бромпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
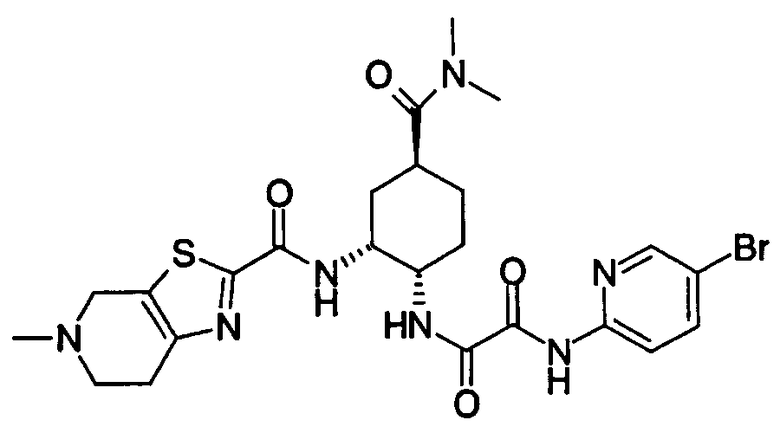
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 262, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 195.
1Н-ЯМР (ДМСО-d6) δ: 1,43-1,57 (1H, м), 1,61-1,81 (3H, м), 1,98-2,15 (2H, м), 2,79 (3H, с), 2,86 (3H, с), 2,89-3,01 (4H, м), 3,18 (2H, шир.с), 3,50 (2H, шир.с), 3,95-4,05 (1H, м), 4,35-4,62 (3H, м), 7,97 (1H, д, J=9,0Гц), 8,12 (1H, дд, J=9,0, 2,4Гц), 8,52 (1H, д, J=2,4Гц), 8,70 (1H, д, J=7,5Гц), 9,18 (1H, д, J=7,5Гц), 10,25 (1H, шир.с).
МС (FAB) m/z: 592 (М+Н)+.
[Пример 205]
Гидрохлорид N1-(6-хлорпиридин-3-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
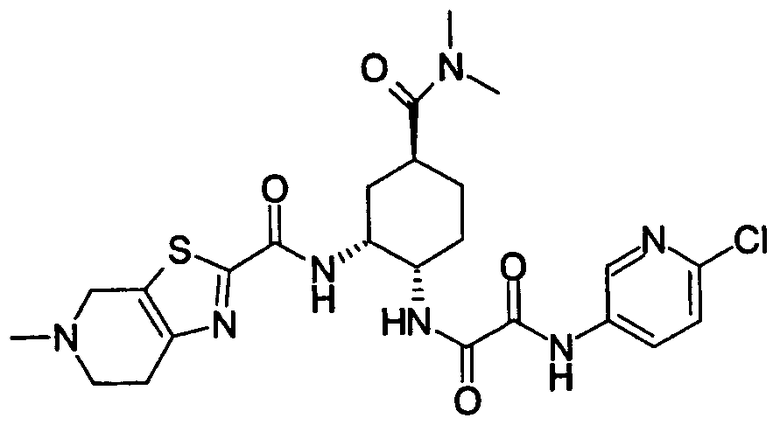
Соединение (200 мг), полученное в ссылочном примере 263, представляющее собой неочищенный продукт, растворяли в метаноле (10 мл), раствор нагревали до 50°C, добавляли 1N водный раствор (3 мл) гидроксида натрия и смесь перемешивали 5 минут. К полученной смеси добавляли 1N хлористоводородную кислоту, доводя рН до слабокислого. Растворитель отгоняли при пониженном давлении с получением остатка, содержащего 2-[(2-хлорпиридин-5-ил)амино]-2-оксоуксусную кислоту. Полученный остаток и соединение (250 мг), полученное в ссылочном примере 253, растворяли в N,N-диметилформамиде (5 мл), добавляли гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (328 мг) и моногидрат 1-гидроксибензотриазола (46 мг) и смесь перемешивали при комнатной температуре в течение 3 суток. Растворитель отгоняли при пониженном давлении и к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 47:3) с получением свободного основания указанного в заголовке соединения в виде бледно-желтого твердого вещества. Полученный продукт растворяли в метиленхлориде, добавляли 1N этанольный раствор (862 мкл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли небольшое количество метанола, добавляли по каплям этилацетат и диэтиловый эфир при облучении ультразвуковыми волнами и отфильтровывали образовавший осадок. Полученный продукт промывали диэтиловым эфиром с получением указанного в заголовке соединения (229 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,46-1,75 (4H, м), 1,99-2,09 (2H, м), 2,79 (3H, с), 2,92-2,95 (7H, м), 3,12-3,53 (3H, м), 3,70 (1H, шир.с), 3,99-4,06 (1H, м), 4,44 (2H, шир.с), 4,69, 4,73 (1H, каждый с), 7,53 (1H, д, J=8,5Гц), 8,23-8,25 (1H, м), 8,72-8,77 (1H, м), 8,85 (1H, с), 9,07, 9,16 (1H, каждый д, J=8,1Гц), 11,09 (1H, д, J=8,1Гц), 11,78 (1H, шир.с).
МС (FAB) m/z: 548 (М+Н)+.
[Пример 206]
Гидрохлорид N1-(6-хлорпиридазин-3-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
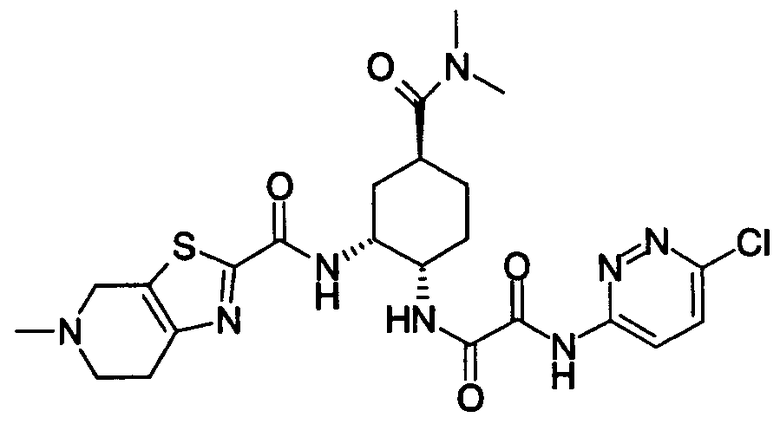
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 264, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,44-1,57 (1H, м), 1,62-1,80 (3H, м), 2,00-2,10 (2H, м), 2,79 (3H, с), 2,86 (3H, шир.с), 2,94 (3H, с), 2,95-3,01 (1H, м), 3,14-3,23 (2H, м), 3,45-3,63 (2H, м), 3,96-4,08 (1H, м), 4,40-4,60 (3H, м), 7,97 (1H, д, J=9,3Гц), 8,26 (1H, д, J=9,3Гц), 8,69 (1H, д, J=7,6Гц), 9,20 (1H, д, J=7,6Гц), 11,06 (1H, с).
МС (FAB) m/z: 549 (M+H)+.
[Пример 207]
Гидрохлорид N1-(5-хлортиазол-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
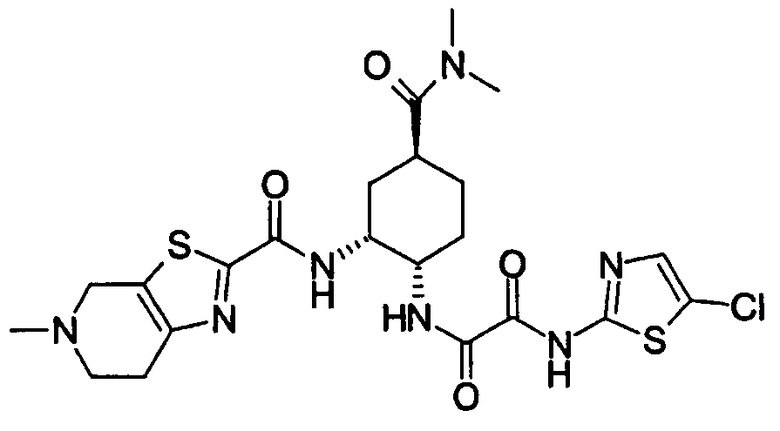
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 265, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,35-2,10 (6H, м), 2,77 (3H, с), 2,92 (3H, с), 2,93 (3H, с), 3,05-4,23 (8H, м), 4,32-4,80 (2H, м), 7,59 (1H, с), 8,63 (1H, д, J=7,6Гц), 9,14 (1H, д, J=7,6Гц).
МС (FAB) m/z: 554 (М+Н)+.
[Пример 208]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамида
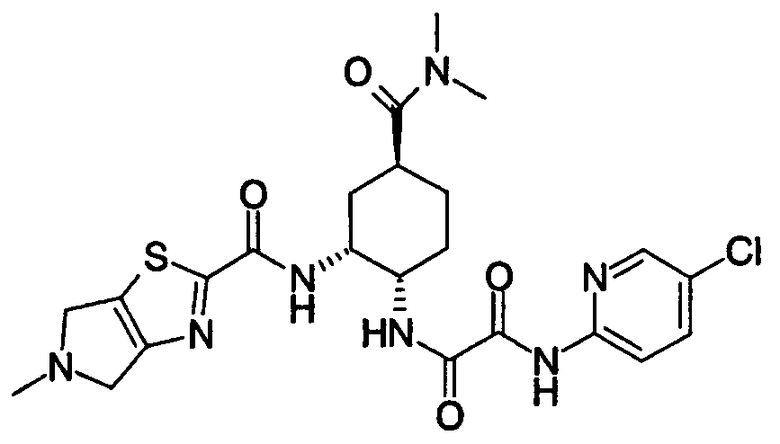
Соединение (210 мг), полученное в ссылочном примере 266, и соединение (350 мг), полученное в ссылочном примере 272, растворяли в N,N-диметилформамиде (15 мл), добавляли моногидрат 1-гидроксибензотриазола (205 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (290 мг) и смесь перемешивали при комнатной температуре в течение 20 часов. Растворитель отгоняли при пониженном давлении и к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия, отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1). Полученные таким образом бледно-желтые твердые частицы растворяли в метиленхлориде, добавляли 1N этанольный раствор (0,46 мл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли метанол и диэтиловый эфир и образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (248 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,47-1,50 (1H, м), 1,69-1,76 (3H, м), 1,98-2,06 (2H, м), 2,79 (3H, с), 2,95 (3H, с), 2,98-3,05 (1H, м), 3,10 (3H, с), 3,49-4,62 (6H, м), 7,98-8,03 (2H, м), 8,45 (1H, с), 8,73 (1H, д, J=7,6Гц), 9,10 (1H, д, J=8,0Гц), 10,30 (1H, с).
МС (FAB) m/z: 534 (М+Н)+.
[Пример 209]
Гидрохлорид N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)ацетил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
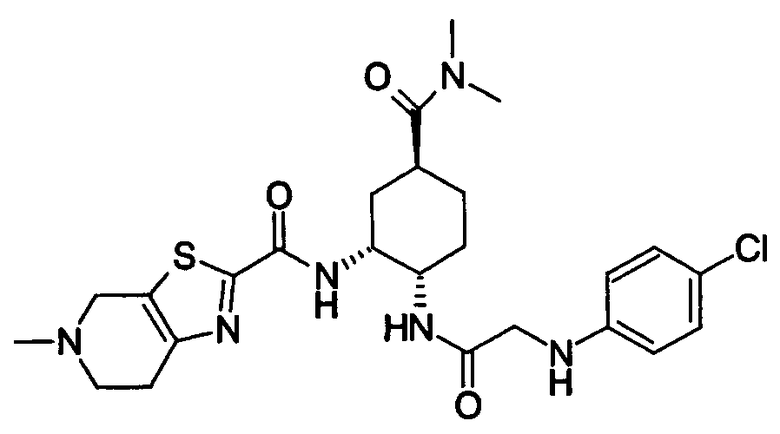
Соединение (2,3 г), полученное в ссылочном примере 267, растворяли в этаноле (10 мл), добавляли 1N водный раствор (20 мл) гидроксида натрия и смесь перемешивали при комнатной температуре в течение 2 часов. После добавления к реакционной смеси 1N хлористоводородной кислоты (20 мл) смесь разбавляли водой и перемешивали в течение 30 минут. Выпавшее в осадок нерастворимое вещество отфильтровывали с получением 2-(4-хлоранилино)уксусной кислоты (1,05 г) в виде бесцветного твердого вещества. Полученное твердое вещество и соединение (0,25 г), полученное в ссылочном примере 253, растворяли в N,N-диметилформамиде (10 мл), добавляли моногидрат 1-гидроксибензотриазола (0,11 г) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (0,23 г) и смесь перемешивали при комнатной температуре в течение 4 суток. Затем реакционную смесь разбавляли хлороформом и промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия, полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 97:3). Полученные таким образом бледно-желтые твердые частицы растворяли в этаноле, добавляли 1N этанольный раствор хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли метанол и диэтиловый эфир и образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (0,15 г).
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,41 (1H, м), 1,59-1,80 (3H, м), 1,82-1,95 (2H, м), 2,76 (3H, с), 2,93 (3H, с), 2,94 (3H, с), 2,99-3,10 (1H, м), 3,10-3,22 (2H, м), 3,42-3,60 (2H, м), 3,60-3,77 (2H, м), 3,80-3,90 (1H, м), 4,35-4,48 (2H, м), 4,68-4,80 (1H, м), 6,40 (1H, д, J=6,7Гц), 6,44 (1H, д, J=6,7Гц), 6,90 (1H, д, J=6,7Гц), 7,00 (1H, д, J=6,7Гц), 7,70-7,89 (1H, м), 8,35-8,42 (1H, м), 11,05-11,38 (1H, м).
[Пример 210]
Гидрохлорид N-{(1R,2S,5S)-2-{[2-(4-хлор-2-фторанилино)ацетил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
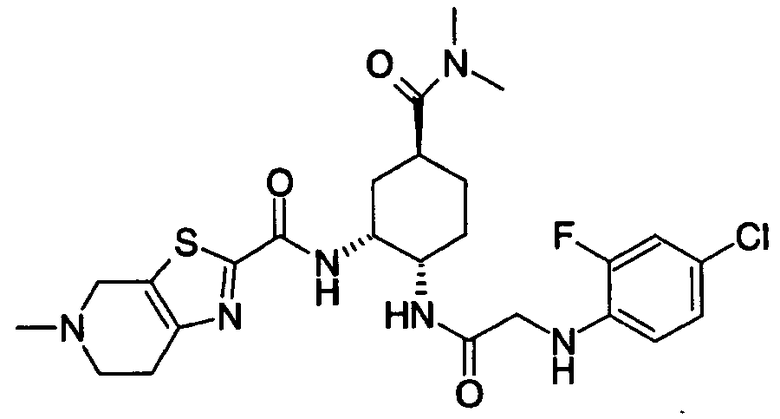
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 268, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 209.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,42 (1H, м), 1,55-1,78 (3H, м), 1,80-2,00 (2H, м), 2,76 (3H, с), 2,92 (3H, с), 2,94 (3H, с), 2,99-3,10 (1H, м), 3,10-3,22 (2H, м), 3,42-3,60 (2H, м), 3,60-3,77 (2H, м), 3,85-4,00 (1H, м), 4,33-4,48 (2H, м), 4,65-4,80 (1H, м), 6,41 (1H, т, J=8,8Гц), 6,73 (1H, дт, J=8,8, 1,2Гц), 7,08 (1H, дд, J=11,7, 1,2Гц), 7,78-7,92 (1H, м), 8,35-8,42 (1H, м), 11,18-11,50 (1H, м).
[Пример 211]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
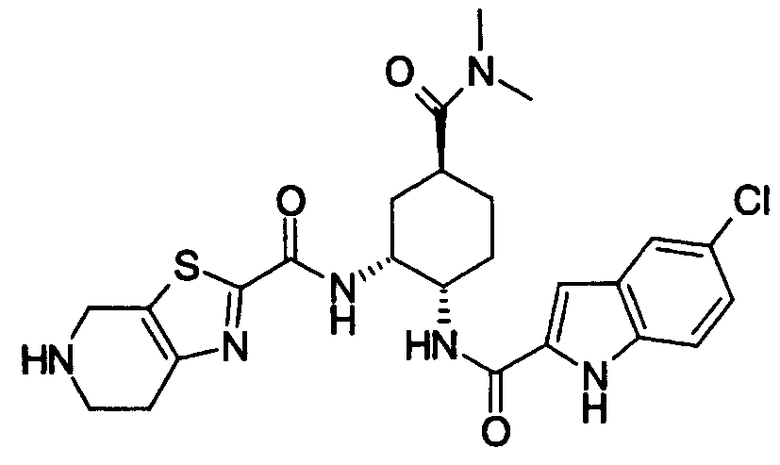
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 432, с соединением, полученным в ссылочном примере 34, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,70-2,15 (6H, м), 2,80 (3H, с), 2,97 (3H, с), 2,95-3,15 (2H, м), 3,35-3,55 (2H, м), 4,05-4,20 (1H, м), 4,46 (2H, с), 4,50-4,65 (1H, м), 7,05 (1H, с), 7,16 (1H, дд, J=8,8, 2,2Гц), 7,41 (1H, д, J=8,8Гц), 7,68 (1H, с), 8,30-8,45 (1H, шир.), 9,30-9,50 (1H, шир.), 11,78 (1H, с).
МС (ESI) m/z: 529 (M+H)+.
[Пример 212]
N-{(1R,2S,5S)-2-{[(5-Хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-(4,5-дигидрооксазол-2-ил)-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
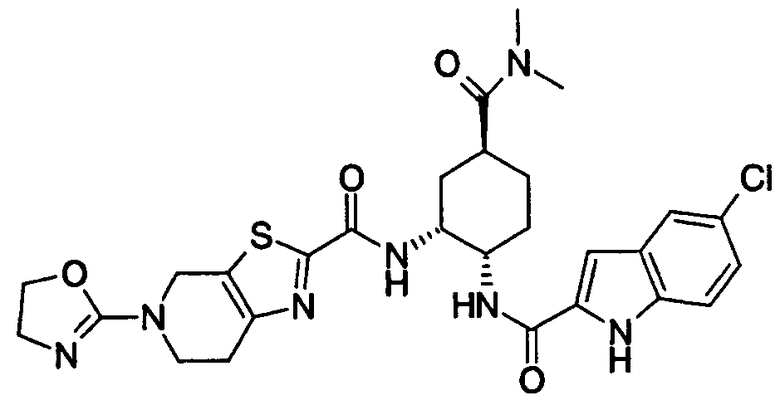
Соединение (250 мг), полученное в примере 211, суспендировали в метиленхлориде, добавляли насыщенный водный раствор гидрокарбоната натрия и смесь интенсивно перемешивали. Полученный органический слой отделяли и сушили над безводным сульфатом магния. Затем добавляли триэтиламин (0,5 мл) и бромэтилизоцианат (43 мкл) и смесь перемешивали при комнатной температуре в течение 20 часов. К реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия и отделяли органический слой. Органический слой сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 22:3) с получением указанного в заголовке соединения (227 мг).
1Н-ЯМР (CDCl3) δ: 1,50-2,15 (4H, м), 2,15-2,40 (2H, м), 2,80-3,00 (1H, м), 2,97 (3H, с), 3,11 (3H, с), 3,70-3,95 (4H, м), 4,10-4,30 (1H, м), 4,30-4,50 (2H, м), 4,60-4,70 (1H, м), 4,74 (2H, с), 6,85 (1H, с), 7,21 (1H, дд, J =8,8, 2,2Гц), 7,34 (1H, д, J=8,8Гц), 7,50 (1H, шир.с), 7,62 (1H, с), 7,87 (1H, шир.с), 9,48 (1H, шир.с).
МС (ESI) m/z: 598 (М+Н)+.
[Пример 213]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлор-4-фториндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
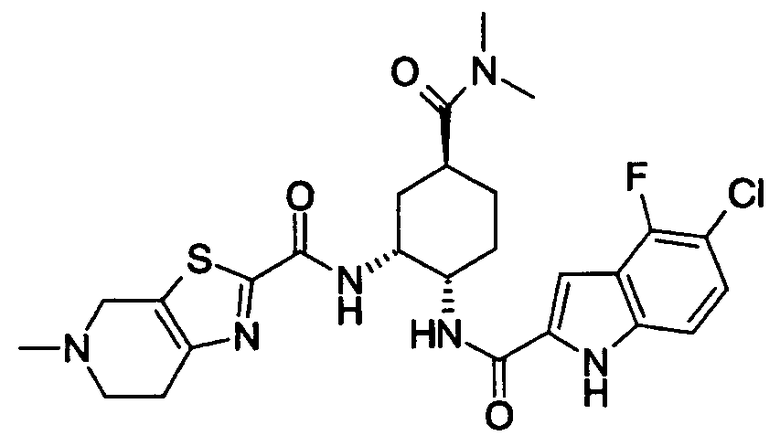
Соединение (140 мг), полученное в ссылочном примере 144, растворяли в N,N-диметилформамиде (10 мл), добавляли соединение (100 мг), полученное в ссылочном примере 274, гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (140 мг) и моногидрат 1-гидроксибензотриазола (110 мг) и смесь перемешивали при комнатной температуре в течение 18 часов. Растворитель отгоняли при пониженном давлении, остаток распределяли между водой и этилацетатом и водный слой экстрагировали этилацетатом. Полученные органические слои объединяли, промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:19) с получением трет-бутил (1R,2S,5S)-2-{[(5-хлор-4-фториндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексилкарбамата (260 мг).
Полученный таким образом порошок растворяли в метиленхлориде (5 мл) и добавляли 4N диоксановый раствор (1,2 мл) хлористоводородной кислоты. После перемешивания реакционной смеси при комнатной температуре в течение 3,5 часов отгоняли при пониженном давлении растворитель. К остатку добавляли метиленхлорид (10 мл) и смесь концентрировали. Повторив данный процесс 3 раза, остаток сушили при пониженном давлении с получением неочищенного N-{(1S,2R,4S)-2-амино-4-[(диметиламино)карбонил]циклогексил}-5-хлор-4-фториндол-2-карбоксамида. Полученный продукт растворяли в N,N-диметилформамиде (50 мл), добавляли соединение (150 мг), полученное в ссылочном примере 10, гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (140 мг) и моногидрат 1-гидроксибензотриазола (110 мг) и смесь перемешивали при комнатной температуре в течение 18 часов. Растворитель отгоняли при пониженном давлении, остаток распределяли в смешанном растворителе вода-этилацетат-тетрагидрофуран и водный слой экстрагировали этилацетатом. Полученные органические слои объединяли, промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:19) с получением свободного основания указанного в заголовке соединения (270 мг). Полученный продукт растворяли в метиленхлориде (10 мл), добавляли 1N этанольный раствор (0,72 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 30 минут. Выпавшие в осадок кристаллы отфильтровывали с получением указанного в заголовке соединения (200 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,24-1,98 (6H, м), 2,33-3,33 (6H, м), 2,81 (3H, с), 2,90 (3H, с), 2,99 (3H, с), 4,12 (1H, шир.с), 4,30-4,70 (1H, м), 4,60 (1H, шир.с), 7,21 (1H, с), 7,27 (2H, шир.с), 8,37 (1H, д, J=8,1Гц), 8,43 (1H, д, J=7,6Гц), 12,11 (1H, с).
МС (FAB) m/z: 561 (М+Н)+.
[Пример 214]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлор-3-фториндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
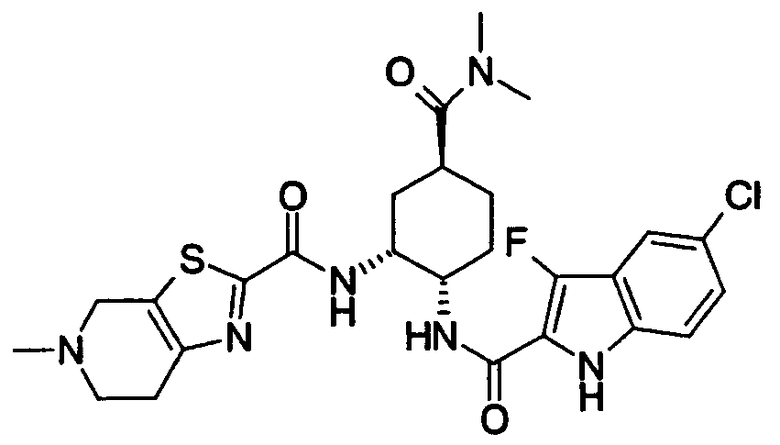
Соединение (250 мг), полученное в ссылочном примере 279, растворяли в метиленхлориде (60 мл) и добавляли 4N диоксановый раствор (1,3 мл) хлористоводородной кислоты. После перемешивания реакционной смеси при комнатной температуре в течение 5,5 часов снова добавляли 4N диоксановый раствор (0,65 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 1 часа. Растворитель отгоняли при пониженном давлении, к остатку добавляли метиленхлорид (10 мл) и смесь концентрировали. Повторяли данный процесс 3 раза. Остаток сушили при пониженном давлении и полученный таким образом неочищенный продукт растворяли в N,N-диметилформамиде (50 мл), добавляли соединение (160 мг), полученное в ссылочном примере 10, гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (150 мг) и моногидрат 1-гидроксибензотриазола (120 мг) и смесь перемешивали при комнатной температуре в течение 18 часов. Растворитель отгоняли при пониженном давлении, остаток распределяли в смешанном растворителе вода-этилацетат и водный слой экстрагировали этилацетатом. Полученные органические слои объединяли, промывали насыщенным водным раствором хлорида натрия и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали дважды колоночной хроматографией на силикагеле (метанол:метиленхлорид = 2:23 → 1:9) с получением свободного основания (260 мг) указанного в заголовке соединения. Полученный продукт растворяли в метиленхлориде, добавляли 1N этанольный раствор (0,69 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 30 минут. Растворитель отгоняли. Остаток растворяли в метаноле и добавляли диэтиловый эфир и гексан. Полученные таким образом кристаллы отфильтровывали с получением указанного в заголовке соединения (230 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,56 (1H, м), 1,73-1,78 (3H, м), 1,94-2,02 (2H, м), 2,33-3,55 (6H, м), 2,80 (3H, с), 2,92 (3H, с), 2,98 (3H, с), 4,17 (1H, шир.с), 4,30-4,80 (1H, шир.), 4,62 (1H, шир.с), 7,25 (1H, д, J=8,8, 1,7Гц), 7,40 (1H, д, J=8,8, 1,7Гц), 7,65 (1H, д, J=1,7Гц), 7,72 (1H, д, J=5,9Гц), 8,74 (1H, д, J=8,0Гц), 10,85-11,35 (1H, шир.), 11,71 (1H, с).
МС (FAB) m/z: 561 (М+Н)+.
[Пример 215]
Гидрохлорид N-{(1R,2S,5S)-2-{[(3-бром-5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
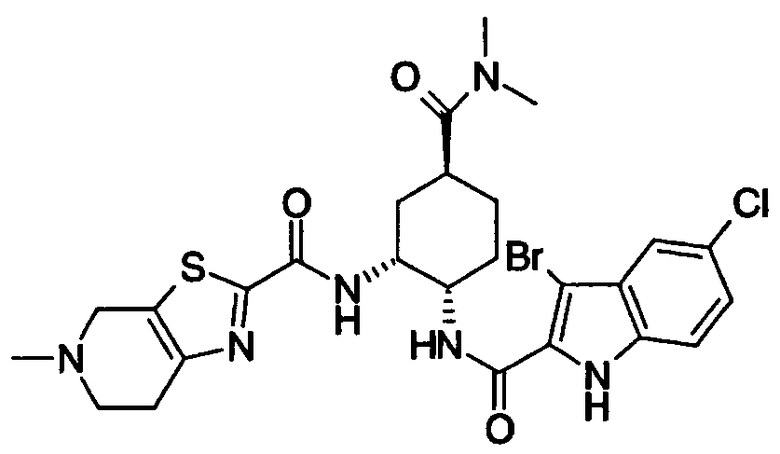
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 282, 4N диоксановым раствором хлористоводородной кислоты и конденсацией полученного таким образом соединения, с соединением, полученным в ссылочном примере 10, подобно способу, описанному в примере 214.
1Н-ЯМР (ДМСО-d6) δ: 1,51-2,01 (6H, м), 2,33-3,29 (7H, м), 2,81 (3H, с), 2,88 (3H, с), 3,01 (3H, с), 4,20 (1H, шир.с), 4,48 (1H, шир.), 4,70-4,73 (1H, м), 7,29 (1H, дд, J=8,9, 1,8Гц), 7,45-7,49 (2H, м), 7,80 (1H, д, J=7,6Гц), 8,76 (1H, д, J=8,8Гц), 12,31 (1H, с).
МС (FAB) m/z: 622 (М+Н)+.
[Пример 216]
Гидрохлорид N-{(1R,2S,5S)-2-{[(3-хлор-5-фториндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
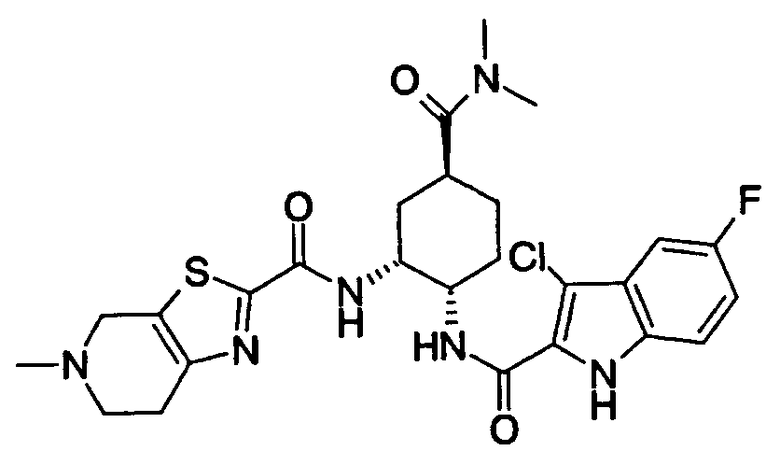
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 253, и соединения, полученного в ссылочном примере 284, подобно способу, описанному в примере 5.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,51 (1H, м), 1,75-2,00 (5H, м), 2,79 (3H, с), 2,92 (3H, с), 2,99 (3H, с), 3,10-3,21 (3H, м), 3,29-3,41 (4H, м), 4,11-4,21 (1H, м), 4,62-4,75 (1H, м), 7,14 (1H, дт, J=8,8, 2,4Гц), 7,24 (1H, дд, J=8,8, 2,4Гц), 7,45 (1H, дд, J=8,8, 4,4Гц), 7,69 (1H, д, J=2,5Гц), 8,79 (1H, д, J=2,5Гц), 12,10 (1H, с).
МС (FAB) m/z: 561 (М+Н)+.
[Пример 217]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлор-3-формилиндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
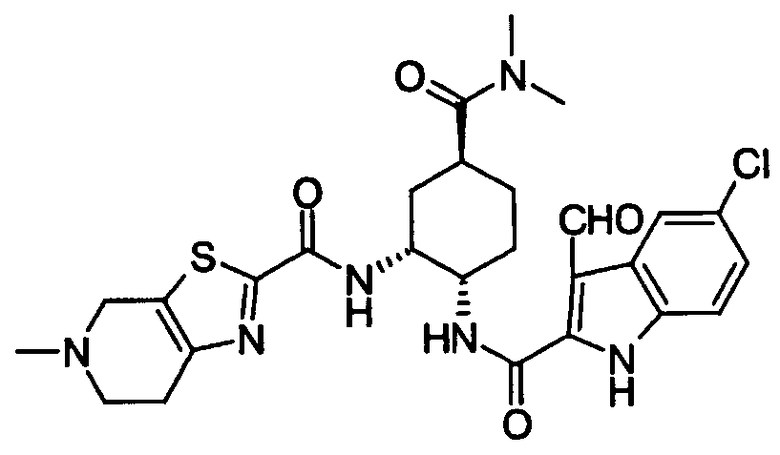
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 253, и соединения, полученного в ссылочном примере 286, подобно способу, описанному в примере 5.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,51 (1H, м), 1,75-1,89 (4H, м), 1,90-2,01 (1H, м), 2,80 (3H, с), 2,91 (3H, с), 3,03 (3H, с), 3,05-3,33 (3H, м), 3,60-3,71 (1H, м), 4,11-4,21 (1H, м), 4,32-4,44 (1H, м), 4,62-4,75 (2H, м), 7,35 (1H, дд, J=8,0, 1,4Гц), 7,56 (1H, д, J=8,0Гц), 8,21 (1H, д, J=1,4Гц), 8,65 (1H, т, J=7,4Гц), 9,92 (1H, д, J=6,8Гц), 10,15 (1H, т, J=9,1Гц), 13,00 (1H, дт, J=6,4Гц).
МС (FAB) m/z: 571 (M+H)+.
[Пример 218]
Гидрохлорид 5-хлор-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил-N3,N3-диметилиндол-2,3-дикарбоксамида
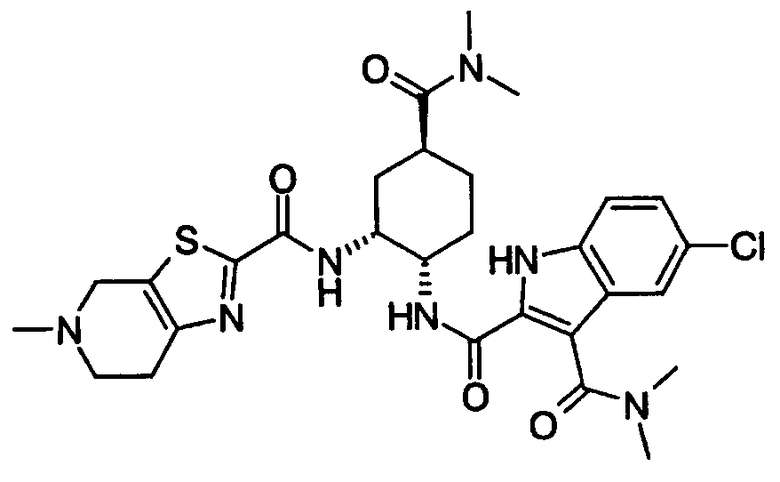
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 253, и соединения, полученного в ссылочном примере 289, подобно способу, описанному в примере 5.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,51 (1H, м), 1,75-2,01 (5H, м), 2,78 (9H, с), 2,93 (3H, с), 3,01 (3H, с), 3,10-3,33 (3H, м), 3,40-3,50 (1H, м), 3,65-3,75 (1H, м), 4,01-4,09 (1H, м), 4,32-4,44 (1H, м), 4,62-4,75 (2H, м), 7,25 (1H, д, J=8,0Гц), 7,40-7,50 (2H, м), 8,62 (1H, шир.), 9,08 (1H, шир.), 12,28 (1H, шир.).
МС (FAB) m/z: 614 (М+Н)+.
[Пример 219]
Гидрохлорид N-{(1R,2S,5S)-2-[(6-хлор-2-нафтоил)амино]-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
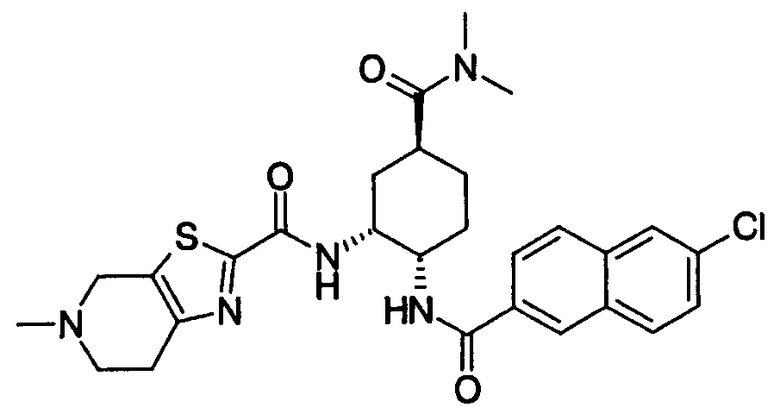
Соединение (270 мг), полученное в ссылочном примере 294, растворяли в метиленхлориде (10 мл), добавляли 1N этанольный раствор (10 мл) хлористоводородной кислоты и смесь перемешивали в течение 90 минут. Растворитель отгоняли при пониженном давлении и полученный остаток растворяли в N,N-диметилформамиде (7 мл). Добавляли соединение (110 мг), полученное в ссылочном примере 10, гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (100 мг) и моногидрат 1-гидроксибензотриазола (70 мг) и смесь перемешивали при комнатной температуре в течение 23 часов. Реакционную смесь концентрировали при пониженном давлении, добавляли воду и экстрагировали этилацетатом. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали дважды колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1 → 10:1). Полученное таким образом свободное основание растворяли в метаноле и добавляли 1N этанольный раствор (0,30 мл) хлористоводородной кислоты. Остаток промывали этилацетатом с получением указанного в заголовке соединения (130 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,70-1,90 (3H, м), 1,90-2,10 (2H, м), 2,81 (3H, с), 2,91 (3H, с), 3,00 (3H, с), 3,00-3,22 (3H, м), 3,53 (2H, шир.), 4,10-4,20 (1H, м), 4,30-4,70 (3H, м), 7,59 (1H, дд, J=8,8, 2,2Гц), 7,87 (1H, д, J=8,5Гц), 7,96 (1H, д, J=8,5Гц), 8,02 (1H, д, J=8,8Гц), 8,10 (1H, д, J=2,2Гц), 8,33 (1H, с), 8,43 (1H, д, J=8,1Гц), 8,52 (1H, д, J=7,3Гц).
МС (FAB) m/z: 554 (М+Н)+.
[Пример 220]
Гидрохлорид 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)циннолин-3-карбоксамида
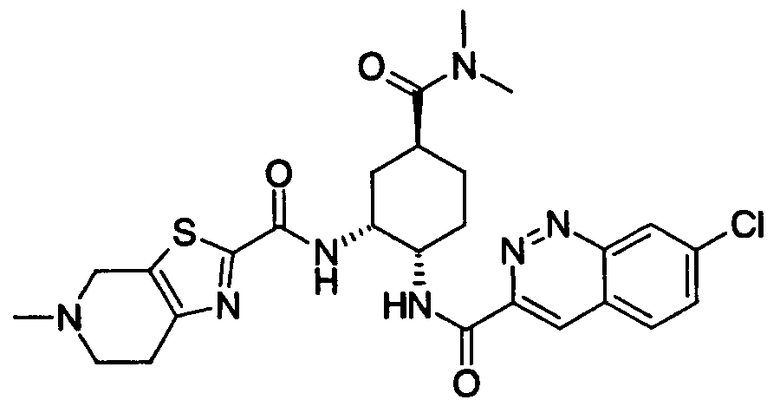
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 299, этанольным раствором хлористоводородной кислоты и затем конденсацией его с соединением, полученным в ссылочном примере 10, подобно способу, описанному в примере 219.
1Н-ЯМР (CDCl3) δ: 1,50-1,65 (1H, м), 1,70-1,90 (3H, м), 2,05-2,15 (1H, м), 2,15-2,30 (1H, м), 2,81 (3H, с), 2,85-3,05 (8H, м), 3,15-3,25 (2H, м), 3,40-3,80 (1H, м), 4,25-4,80 (4H, м), 8,02 (1H, дд, J=8,8, 2,0Гц), 8,38 (1H, д, J=8,8Гц), 8,66 (1H, с), 8,91 (1H, с), 8,96 (1H, д, J=7,3Гц), 9,53 (1H, шир.).
МС (FAB) m/z: 556 (М+Н)+.
[Пример 221]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлорбензимидазол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
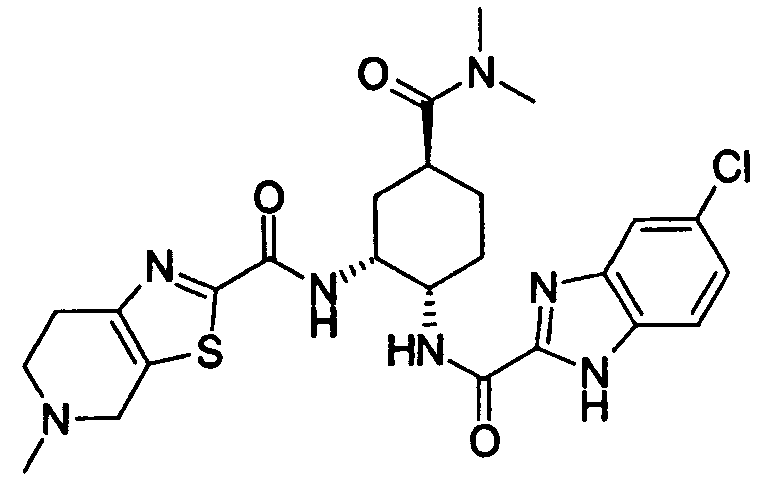
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 300, этанольным раствором хлористоводородной кислоты и затем конденсацией его с соединением, полученным в ссылочном примере 10, подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,60-1,83 (3H, м), 2,00-2,20 (2H, м), 2,78 (3H, с), 2,92 (6H, с), 3,00-3,30 (3H, м), 3,47 (2H, шир.с), 4,10-4,75 (4H, м), 7,30 (1H, д, J=8,8Гц), 7,62 (1H, д, J=12,5Гц), 7,63 (1H, с), 8,75-8,87 (1H, м), 9,09 (1H, дд, J=12,5, 8,8Гц), 11,20-11,40 (1H, м).
МС (FAB) m/z: 546 (M+H)+.
[Пример 222]
Гидрохлорид N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)7-фторизохинолин-3-карбоксамида
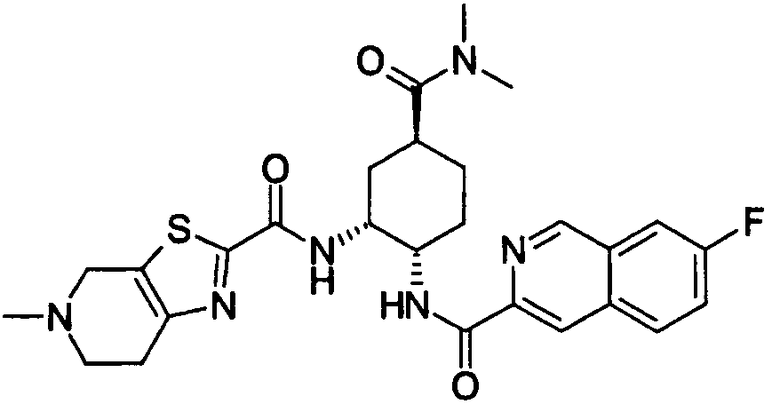
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 253, и соединения, полученного в ссылочном примере 304, подобно способу, описанному в примере 5.
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,60 (1H, м), 1,70-1,85 (3H, м), 1,95-2,05 (1H, м), 2,10-2,20 (1H, м), 2,80 (3H, с), 2,90-3,90 (5H, м), 2,93 (3H, с), 2,96 (3H, с), 4,10-4,75 (4H, м), 7,75-7,85 (1H, м), 8,00-8,05 (1H, м), 8,30-8,35 (1H, м), 8,61 (1H, с), 8,93 (2H, д, J=7,3Гц), 9,31 (1H, с).
МС (FAB) m/z: 539 (М+Н)+.
[Пример 223]
Гидрохлорид N-{(1R,2S,5S)-2-{[(7-хлор-2Н-хромен-3-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
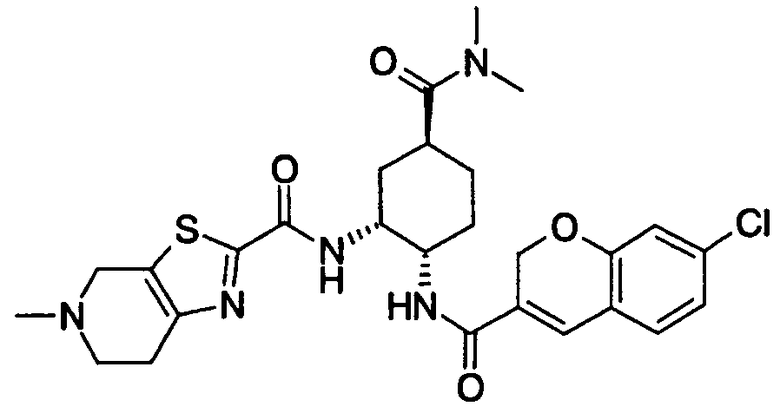
Соединение (220 мг), полученное в ссылочном примере 252, растворяли в метаноле (10 мл), добавляли 10% палладий на углероде (180 мг) и смесь перемешивали при комнатной температуре в течение 4 часов в атмосфере водорода. После фильтрования реакционной смеси фильтрат концентрировали при пониженном давлении и остаток растворяли в N,N-диметилформамиде (30 мл). Добавляли соединение (108 мг), полученное в ссылочном примере 306, моногидрат 1-гидроксибензотриазола (78 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (196 мг) и смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь концентрировали при пониженном давлении и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 100:3) с получением бледно-желтого пенистого вещества. Полученное пенистое вещество растворяли в метиленхлориде (2 мл), добавляли 1N этанольный раствор (363 мкл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли диэтиловый эфир. Образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (175 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,52 (1H, м), 1,55-1,96 (5H, м), 2,78 (3H, с), 2,90 (3H, с), 2,98 (3H, с), 3,01-3,12 (1H, м), 3,13-3,28 (2H, м), 3,40-3,85 (2H, м), 3,92-4,00 (1H, м), 4,35-4,80 (3H, м), 4,84 (1H, д, J=14,5Гц), 4,89 (1H, д, J=14,5Гц), 6,92 (1H, с), 6,98 (1H, дд, J=8,1, 1,7Гц), 7,08 (1H, с), 7,17 (1H, д, J=8,3Гц), 8,12 (1H, д, J=8,1Гц), 8,34 (1H, д, J=8,1Гц).
МС (FAB) m/z: 558 (М+Н)+.
[Пример 224]
Гидрохлорид N-{(1R,2S,5S)-2-{[(Е)-3-(4-хлорфенил)-2-пропеноил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
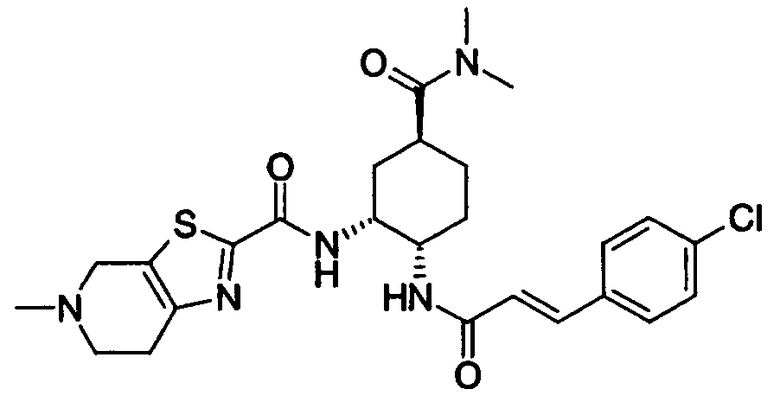
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 307, этанольным раствором хлористоводородной кислоты и затем конденсацией его с соединением, полученным в ссылочном примере 10, подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,55 (1H, м), 1,55-1,90 (4H, м), 2,79 (3H, с), 2,92 (3H, с), 2,99 (3H, с), 3,05-3,30 (3H, м), 3,40-3,55 (1H, м), 3,60-3,75 (1H, м), 3,93-4,03 (2H, м), 4,35-4,50 (1H, м), 4,50-4,60 (1H, м), 4,60-4,75 (1H, м), 6,65 (1H, д, J=15,7 Гц), 7,35 (1H, д, J=15,7 Гц), 7,44 (1H, д, J=8,6 Гц), 7,55 (1H, д, J=8,6 Гц), 8,03 (1H, д, J=8,1Гц), 8,34 (1H, шир.с), 11,25-11,70 (1H, шир.).
МС (ESI) m/z: 530 (M+H)+.
[Пример 225]
Гидрохлорид 6-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-4-оксо-1,4-дигидрохинолин-2-карбоксамида
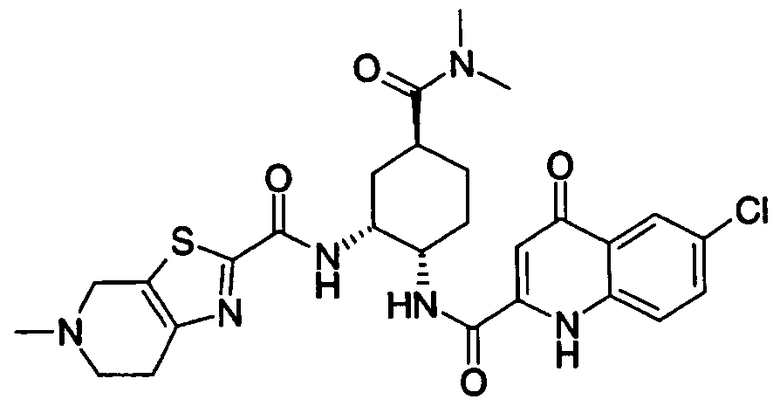
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 253, и соединения, полученного в ссылочном примере 309, подобно способу, описанному в примере 5.
1Н-ЯМР (ДМСО-d6) δ: 1,43-1,60 (1H, м), 1,65-2,10 (3H, м), 2,79 (3H, с), 2,92 (3H, с), 2,99 (3H, с), 3,05-3,20 (2H, м), 3,20-3,80 (5H, м), 4,08-4,20 (1H, м), 4,35-4,50 (1H, м), 4,60-4,70 (1H, м), 4,70 (1H, д, J=15,6Гц), 6,77 (1H, шир.с), 7,73 (1H, д, J=8,9Гц), 7,94 (1H, д, J=8,9Гц), 7,97 (1H, д, J=2,2Гц), 8,54 (1H, шир.с), 8,80-9,00 (1H, м), 11,18-11,42 (1H, шир.д), 11,70-12,50 (1H, шир.).
МС (ESI) m/z: 571 (М+Н)+.
[Пример 226]
трет-Бутил 2-[({(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}амино)карбонил]-4,6-дигидро-5Н-пирроло[3,4-d]тиазол-5-карбоксилат
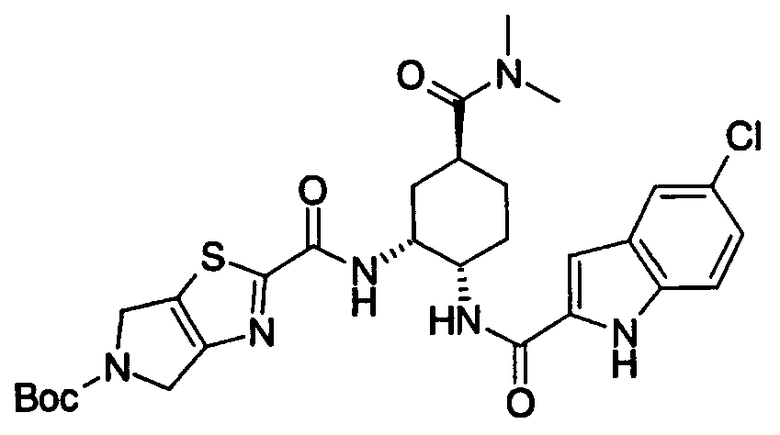
1) Соединение (1,46 г), полученное в ссылочном примере 310, растворяли в метиленхлориде (10 мл), добавляли при комнатной температуре этанольный раствор (10 мл) хлористоводородной кислоты и смесь перемешивали в течение 1 часа. По окончании реакции отгоняли растворитель, смесь концентрировали и к остатку для его отверждения добавляли диизопропиловый эфир. Полученные твердые частицы отфильтровывали с получением гидрохлорида N-{(1S,2R,4S)-2-амино-4-[(диметиламино)карбонил]циклогексил}-5-хлориндол-2-карбоксамида.
2) Полученный продукт растворяли в N,N-диметилформамиде (5 мл), добавляли соединение (1,31 г), полученное в ссылочном примере 406, моногидрат 1-гидроксибензотриазола (640 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (1,36 г) и смесь перемешивали при комнатной температуре в течение 3 суток. Реакционную смесь концентрировали и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия. Затем растворитель отгоняли при пониженном давлении, остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:19) с получением указанного в заголовке соединения (1,22 г).
1Н-ЯМР (CDCl3) δ: 1,53 (9H, с), 1,70-2,40 (6H, м), 2,80-3,20 (7H, м), 4,15-4,25 (1H, м), 4,55-4,80 (5H, м), 6,83 (1H, д, J=1,5Гц), 7,20 (1H, дд, J=8,8, 2,0Гц), 7,33 (1H, д, J=8,8Гц), 7,40-7,50 (1H, м), 7,61 (1H, шир.с), 7,72-7,80 (1H, м), 9,41 (1H, шир.с).
МС (ESI) m/z: 615 (M+H)+.
[Пример 227]
Гидрохлорид 5-хлор-N-{(1S,2R,4S)-2-[[(5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино]-4-[(диметиламино)карбонил]циклогексил}индол-2-карбоксамида
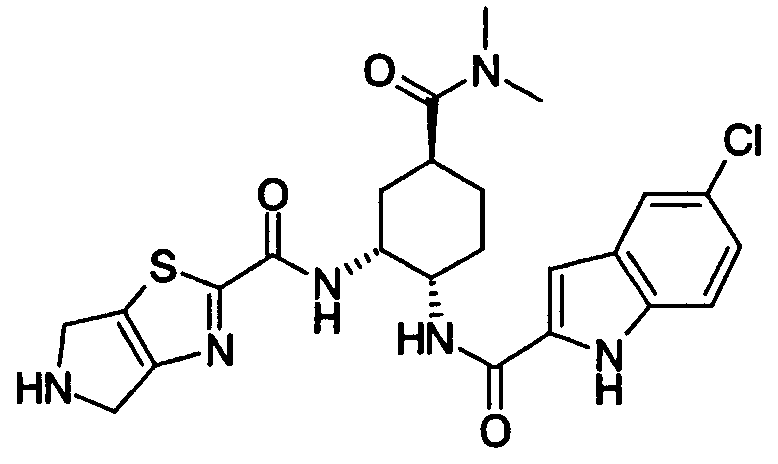
Соединение (1,22 г), полученное в ссылочном примере 226, растворяли в метиленхлориде (5 мл), добавляли этанольный раствор (10 мл) хлористоводородной кислоты и смесь перемешивали в течение 1 часа. После концентрирования реакционной смеси добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей и полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли и остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:9) с получением свободного основания (636 мг) указанного в заголовке соединения в виде бесцветного стекловидного твердого вещества. Свободное основание (200 мг) растворяли в 1N этанольном растворе (1 мл) хлористоводородной кислоты. После концентрирования раствора добавляли этилацетат для отверждения остатка. Полученный таким образом бесцветный порошок отфильтровывали и сушили с получением указанного в заголовке соединения (195 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,70-1,90 (3H, м), 1,90-2,05 (2H, м), 2,80 (3H, с), 2,98 (3H, с), 2,98-3,15 (1H, м), 4,05-4,20 (1H, м), 4,44 (2H, шир.с), 4,58 (3H, шир.с), 7,05 (1H, д, J=1,5Гц), 7,16 (1H, дд, J=8,7, 1,8Гц), 7,42 (1H, д, J=8,7Гц), 7,68 (1H, д, J=1,8Гц), 8,38 (1H, д, J=7,8Гц), 8,42 (1H, д, J=7,8Гц), 10,45-10,65 (2H, шир.), 11,78 (1H, шир.с).
МС (FAB) m/z: 515 (M+H)+.
[Пример 228]
Гидрохлорид 5-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)индол-2-карбоксамида
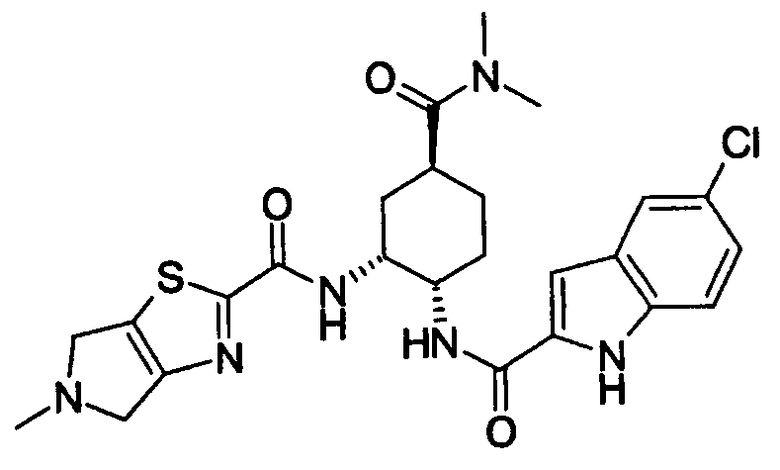
Указанное в заголовке соединение получали из соединения, полученного в примере 227, и формалина подобно способу, описанному в примере 18.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,65-1,90 (3H, м), 1,90-2,05 (2H, м), 2,80 (3H, с), 2,98 (3H, с), 2,98-3,06 (1H, м), 3,06 (3H, с), 4,05-4,20 (1H, м), 4,30-5,00 (5H, шир.с), 7,04 (1H, д, J=1,7Гц), 7,17 (1H, дд, J=8,8, 2,1Гц), 7,41 (1H, д, J=8,8Гц) 7,68 (1H, д, J=2,1Гц), 8,36 (1H, д, J=7,8Гц), 8,42 (1H, д, J=8,1Гц), 11,78 (1H, шир.с), 12,14 (1H, шир.с).
МС (FAB) m/z: 529 (M+H)+.
[Пример 229]
трет-Бутил 2-{[((1R,2S,5S)-5-[(диметиламино)карбонил]-2-{[(5-фториндол-2-ил)карбонил]амино}циклогексил)амино]карбонил}-4,6-дигидро-5Н-пирроло[3,4-d]тиазол-5-карбоксилат
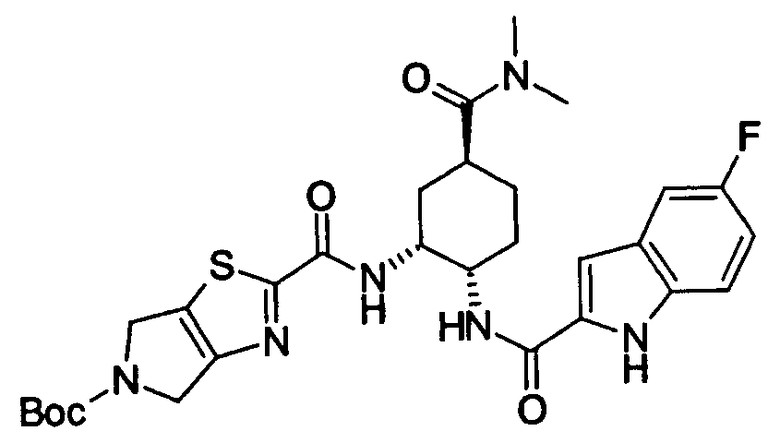
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 311, и соединения, полученного в ссылочном примере 406, подобно способу, описанному в примере 226.
1Н-ЯМР (CDCl3) δ: 1,53 (9H, с), 1,60-2,40 (6H, м), 2,80-3,20 (7H, м), 4,15-4,25 (1H, м), 4,55-4,80 (5H, м), 6,84-6,87 (1H, м), 7,01 (1H, дт, J=2,4, 9,1Гц), 7,25-7,30 (1H, м), 7,34 (1H, дд, J=9,1, 4,3Гц), 7,42-7,49 (1H, м), 7,70-7,80 (1H, м), 9,37-9,45 (1H, м).
МС (ESI) m/z: 599 (M+H)+.
[Пример 230]
Гидрохлорид N-{(1S,2R,4S)-2-[[(5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино]-4-[(диметиламино)карбонил]-5-фториндол-2-карбоксамида
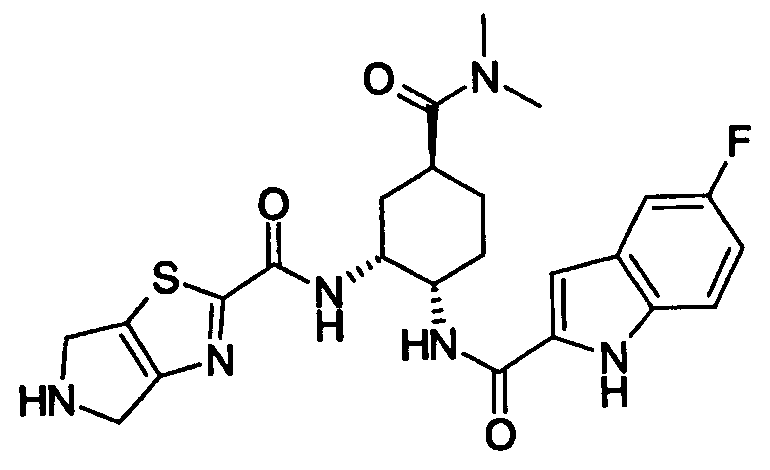
Указанное в заголовке соединение получали из соединения, полученного в примере 229, подобно способу, описанному в примере 227.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,65-1,90 (3H, м), 1,90-2,10 (2H, м), 2,80 (3H, с), 2,97 (3H, с), 2,98-3,15 (1H, м), 4,05-4,20 (1H, м), 4,35-4,50 (2H, м), 4,58 (3H, шир.с), 6,97-7,10 (2H, м), 7,35-7,47 (2H, м), 8,34 (1H, д, J=7,8Гц), 8,41 (1H, д, J=8,1Гц), 10,53 (2H, шир.с), 11,68 (1H, шир.с).
МС (FAB) m/z: 499 (М+Н)+.
[Пример 231]
Гидрохлорид N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил}-5-фториндол-2-карбоксамида
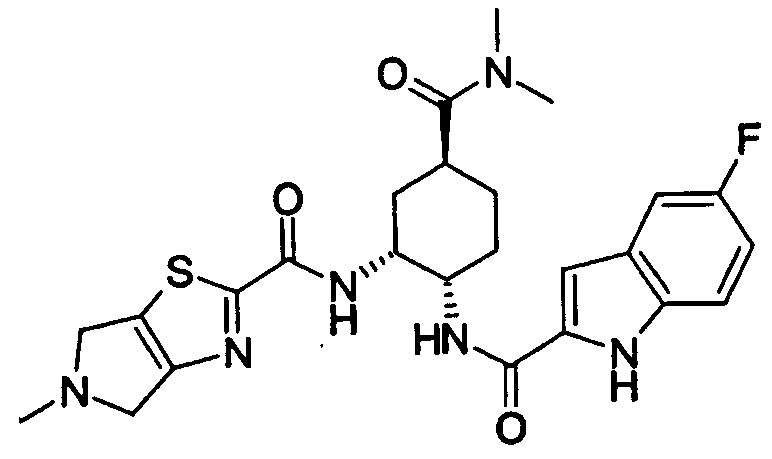
Указанное в заголовке соединение получали из соединения, полученного в примере 230, и формалина подобно способу, описанному в примере 18.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,65-1,90 (3H, м), 1,90-2,10 (2H, м), 2,80 (3H, с), 2,90-3,20 (7H, м), 4,05-4,20 (1H, м), 4,30-5,00 (5H, шир.с), 6,95-7,10 (2H, м), 7,35-7,50 (2H, м), 8,33 (1H, д, J=7,6Гц), 8,41 (1H, д, J=8,1Гц), 11,67 (1H, шир.с), 12,37 (1H, шир.с).
МС (FAB) m/z: 513 (М+Н)+.
[Пример 232]
Гидрохлорид N-{(1R,2S,5S)-2-[(6-хлор-2-нафтоил)амино]-5-[(диметиламино)карбонил]циклогексил}-5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-карбоксамида
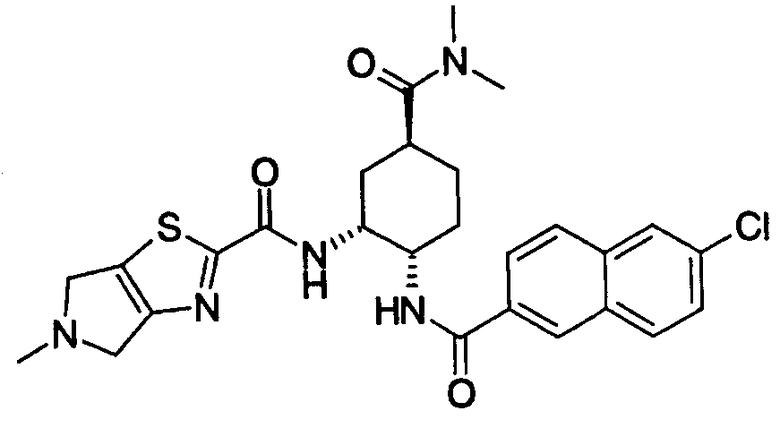
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 294, и соединения, полученного в ссылочном примере 293, подобно способу, описанному в примере 226.
1Н-ЯМР (ДМСО-d6) δ: 1,48-1,56 (1H, м), 1,71-1,84 (3H, м), 1,95-2,04 (2H, м), 2,81 (3H, с), 3,00 (3H, с), 3,02 (3H, с), 3,06-3,15 (2H, м), 4,13-4,14 (1H, м), 4,52-4,63 (4H, м), 7,60 (1H, д, J=8,5Гц), 7,87 (1H, д, J=8,8Гц), 7,96 (1H, д, J=8,5Гц), 8,01 (1H, д, J=8,8Гц), 8,10 (1H, с), 8,32 (1H, с), 8,45 (1H, д, J=8,1Гц), 8,51 (1H, д, J=7,3Гц).
МС (FAB) m/z: 540 (M+H)+.
[Пример 233]
Гидрохлорид 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)циннолин-3-карбоксамида и 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)циннолин-3-карбоксамид
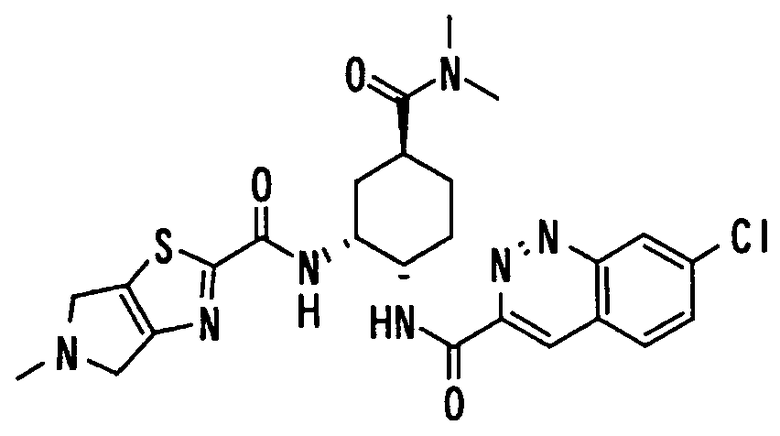
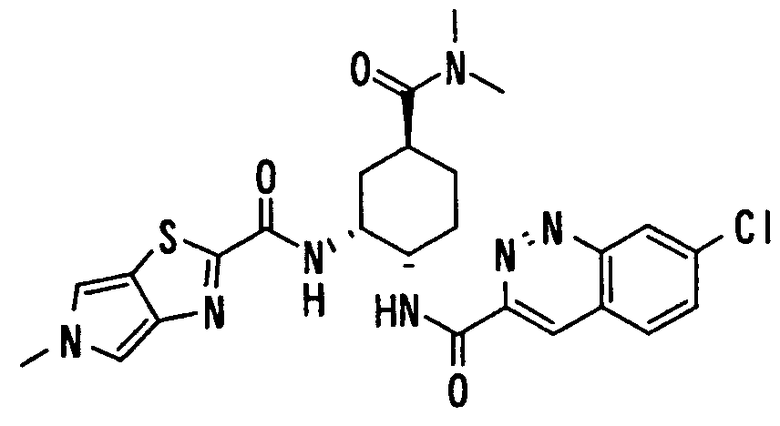
4N Диоксановый раствор (3,0 мл) хлористоводородной кислоты добавляли к суспензии соединения (330 мг), полученного в ссылочном примере 299, в смешанном растворителе из диоксана (3,0 мл) и метиленхлорида (3,0 мл) и смесь перемешивали при комнатной температуре в течение 30 минут. Растворитель отгоняли при пониженном давлении и полученный таким образом белый порошок растворяли в N,N-диметилформамиде (5,0 мл), к раствору добавляли соединение (172 мг), полученное в ссылочном примере 293, моногидрат 1-гидроксибензотриазола (130 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (192 мг) и смесь перемешивали при комнатной температуре в течение 15 часов. Растворитель отгоняли при пониженном давлении и к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия. Полученный органический слой промывали насыщенным раствором соли и затем сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1). К раствору полученного таким образом, в основном высокополярного, соединения в этаноле (4,0 мл) добавляли 1N этанольный раствор (0,35 мл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли этанол и диэтиловый эфир и образовавшийся осадок отфильтровывали, получая гидрохлорид 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)циннолин-3-карбоксамида (184 мг) в качестве основного продукта.
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,65 (1H, м), 1,70-1,90 (3H, м), 2,03-2,12 (1H, м), 2,15-2,30 (1H, м), 2,81 (3H, с), 2,90-3,05 (1H, м), 2,96 (3H, с), 3,07 (3H, с), 4,28-4,37 (1H, м), 4,40-4,95 (5H, шир.), 8,02 (1H, д, J=8,8Гц), 8,38 (1H, д, J=8,8Гц), 8,66 (1H, с), 8,91 (1H, с), 8,97 (1H, д, J=7,1ц), 9,43-9,57 (1H, шир.), 11,75-11,95 (0,5H, шир.), 12,35-11,55 (0,5H, шир.).
МС (FAB) m/z: 542 (М+Н)+.
При очистке колоночной хроматографией на силикагеле был также получен в качестве побочного продукта 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)циннолин-3-карбоксамид (98 г).
1Н-ЯМР (CDCl3) δ: 1,90-2,25 (6H, м), 2,85-3,00 (1H, м), 2,95 (3H, с), 3,05 (3H, с), 3,91 (3H, с), 4,43-4,54 (1H, м), 4,86-4,95 (1H, м), 6,70 (1H, д, J=1,5Гц), 7,19 (1H, д, J=1,5Гц), 7,59 (1H, д, J=8,8Гц), 7,76 (1H, д, J=8,8Гц), 7,95 (1H, д, J=8,8Гц), 8,53 (1H, с), 8,64 (1H, д, J=8,0Гц), 8,73 (1H, с).
МС (FAB) m/z: 540 (М+Н)+.
[Пример 234]
Гидрохлорид 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)изохинолин-3-карбоксамида
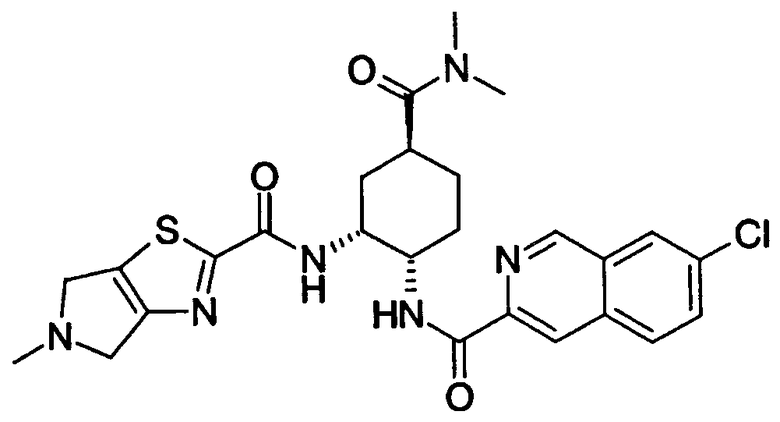
Соединение (500 мг), полученное в ссылочном примере 146, растворяли в этанольном растворе (5 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 30 минут. Растворитель отгоняли при пониженном давлении и остаток растворяли в N,N-диметилформамиде (7 мл), к раствору добавляли соединение (299 мг), полученное в ссылочном примере 293, моногидрат 1-гидроксибензотриазола (71 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (403 мг) и смесь перемешивали при комнатной температуре в течение ночи. Растворитель отгоняли при пониженном давлении и к остатку добавляли насыщенный водный раствор гидрокарбоната натрия и метиленхлорид для разделения жидкостей. Полученный водный слой экстрагировали метиленхлоридом. Органические слои объединяли и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 93:7) с получением свободного основания (260 мг) указанного в заголовке соединения в виде бледно-желтого твердого вещества. Полученный продукт растворяли в метиленхлориде, добавляли 1N этанольный раствор (961 мкл) хлористоводородной кислоты и отгоняли при пониженном давлении растворитель. К остатку добавляли небольшое количество метанола, добавляли по каплям диэтиловый эфир и образовавшийся осадок отфильтровывали. Полученный продукт промывали диэтиловым эфиром с получением указанного в заголовке соединения (260 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,47-1,56 (1H, м), 1,71-1,75 (3H, м), 1,95-1,99 (1H, м), 2,12-2,15 (1H, м), 2,78 (3H, с), 2,95 (3H, с), 2,98 (1H, шир.с), 3,05 (3H, с), 4,19-4,22 (1H, м), 4,44-4,52 (3H, м), 4,74-4,88 (2H, м), 7,87 (1H, дд, J=8,8, 1,7Гц), 8,24 (1H, д, J=8,8Гц), 8,36 (1H, д, J=1,7Гц), 8,58 (1H, с), 8,90-8,92 (2H, м), 9,30 (1H, с), 12,65-12,75 (1H, м).
МС (FAB) m/z: 541 (М+Н)+.
[Пример 235]
трет-Бутил 2-[({(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}амино)карбонил]-6,6-диметил-6,7-дигидротиазоло[4,5-c]пиридин-5(4Н)-карбоксилат
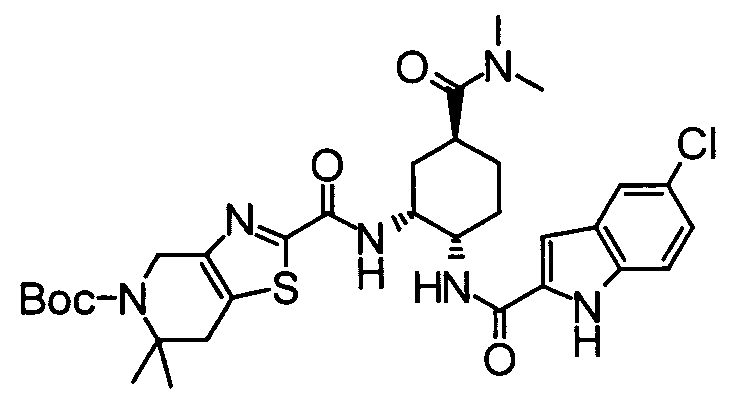
Соединение (95,4 мг), полученное в ссылочном примере 316, растворяли в диэтиловом эфире (1 мл) в атмосфере аргона и добавляли по каплям при -78°C трет-бутиллитий (1,60N пентановый раствор, 244 мкл). После перемешивания смеси в течение 1 часа при -78°C через реакционную смесь барботировали в течение 10 минут диоксид углерода. Реакционную смесь нагревали до комнатной температуры. После концентрирования реакционной смеси при пониженном давлении остаток растворяли в N,N-диметилформамиде (5 мл). К раствору последовательно добавляли соединение (178 мг), полученное в ссылочном примере 432, моногидрат 1-гидроксибензотриазола (48,0 мг) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (136 мг). Полученную смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь концентрировали, к остатку добавляли метиленхлорид и насыщенный водный раствор гидрокарбоната натрия и отделяли органический слой. Органический слой сушили над безводным сульфатом натрия и затем отгоняли при пониженном давлении растворитель. Полученный остаток очищали колоночной хроматографией на силикагеле (метанол:метиленхлорид = 1:19) с получением указанного в заголовке соединения (140 мг).
1Н-ЯМР (CDCl3) δ: 1,50 (9H, с), 1,52 (3H, с), 1,54 (3H, с), 1,70-2,10 (4H, м), 2,15-2,45 (2H, м), 2,80-3,20 (9H, м), 4,10-4,25 (1H, шир.), 4,60-4,75 (3H, м), 6,85 (1H, шир.с), 7,21 (1H, дд, J=8,8, 1,8Гц), 7,34 (1H, д, J=8,8Гц), 7,48 (1H, д, J=7,3Гц), 7,61-7,63 (1H, м), 7,89 (1H, шир.с), 9,27 (1H, шир.с).
МС (ESI) m/z: 657 (М+Н)+.
[Пример 236]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-6,6-диметил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
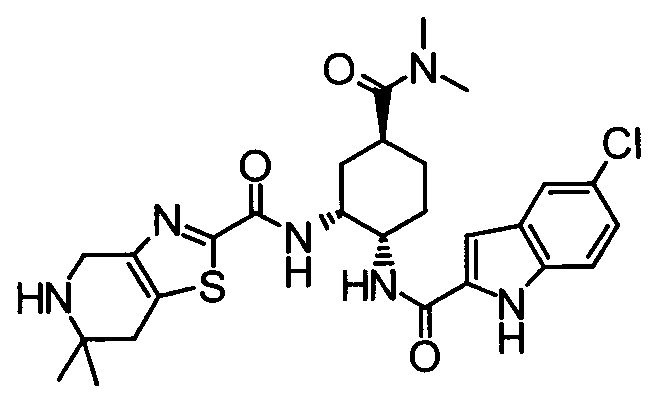
Указанное в заголовке соединение получали из соединения, полученного в примере 235, подобно способу, описанному в примере 227.
1Н-ЯМР (ДМСО-d6) δ: 1,40 (6H, с), 1,45-1,60 (1H, м), 1,70-2,05 (5H, м), 2,81 (3H, с), 2,95-3,15 (6H, м), 4,05-4,20 (1H, шир.), 4,25-4,45 (2H, м), 4,55-4,65 (1H, м), 7,06 (1H, д, J=1,7Гц), 7,17 (1H, дд, J=8,8, 2,0Гц), 7,42 (1H, д, J=8,8Гц), 7,68 (1H, д, J=2,0Гц), 8,34-8,39 (2H, м), 9,77 (1H, шир.с), 9,84 (1H, шир.с), 11,79 (1H, шир.с).
МС (ESI) m/z: 557 (М+Н)+.
[Пример 237]
трет-Бутил 2-[({(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}амино)карбонил]-5,7-дигидро-6Н-пирроло[3,4-d]пиримидин-6-карбоксилат
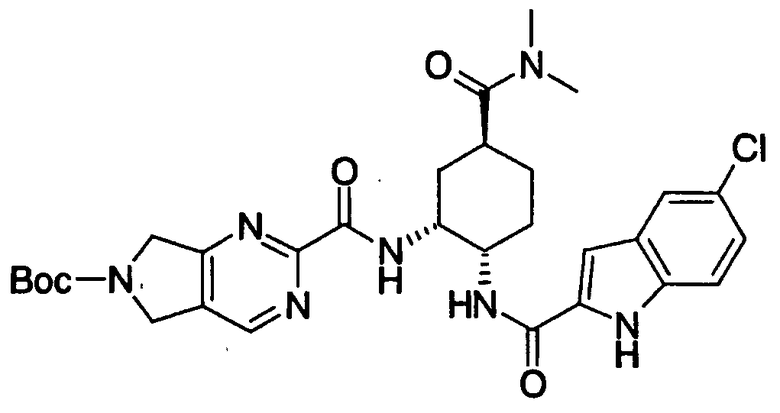
Соединение (1,27 г), полученное в ссылочном примере 50, растворяли в тетрагидрофуране (48 мл), добавляли гидроксид лития (117 мг) и воду (6,0 мл) и смесь перемешивали при комнатной температуре в течение 4,5 часов. Реакционную смесь сушили до твердого вещества при пониженном давлении с получением неочищенной литиевой соли карбоновой кислоты (1,24 г). Полученный продукт конденсировали с соединением, полученным в ссылочном примере 432, подобно способу, описанному на стадии 2) примера 226, с получением указанного в заголовке соединения.
1Н-ЯМР (CDCl3) δ: 1,50-1,70 (1H, м), 1,54 (9H, с), 1,80-2,10 (3H, м), 2,25-2,50 (2H, м), 2,85-2,95 (1H, м), 2,99 (3H, с), 3,14 (3H, с), 4,15-4,25 (1H, м), 4,65-4,75 (1H, м), 4,80-4,90 (4H, м), 6,97 (1H, с), 7,15-7,25 (1H, м), 7,30-7,40 (1H, м), 7,60-7,65 (1H, м), 8,15-8,25 (1H, м), 8,40-8,45 (1H, м), 8,75-8,85 (1H, м), 9,40-9,45 (1H, м).
МС (ESI) m/z: 611 (M+H)+.
[Пример 238]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-6-метил-6,7-дигидро-5Н-пирроло[3,4-d]пиримидин-2-карбоксамида
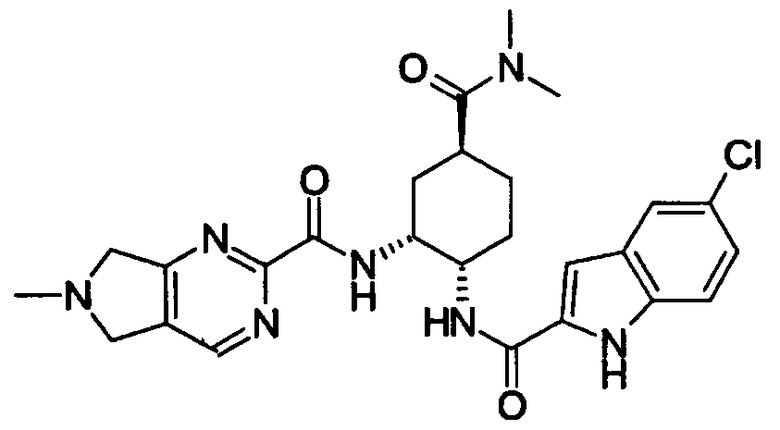
Соединение (367 мг), полученное в примере 237, растворяли в метиленхлориде (10 мл), добавляли трифторуксусную кислоту (10 мл) и смесь перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь сушили до твердого вещества при пониженном давлении. Из полученного таким образом неочищенного продукта и формалина получали указанное в заголовке соединение подобно способу, описанному в примере 18.
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,60 (1H, м), 1,65-2,10 (5H, м), 2,81 (3H, с), 2,90-3,00 (1H, м), 2,96 (3H, с), 3,05 (3H, с), 4,10-4,20 (1H, м), 4,55-4,65 (1H, м), 4,65-4,90 (4H, шир.), 7,06 (1H, с), 7,15 (1H, дд, J=8,7, 2,1Гц), 7,41 (1H, д, J=8,8Гц), 7,66 (1H, д, J=1,7Гц), 8,35-8,45 (1H, м), 8,57 (1H, д, J=8,1Гц), 9,00 (1H, с), 11,80 (1H, с), 11,90-12,20 (1H, м).
МС (FAB) m/z: 524 (М+Н)+.
[Пример 239]
Гидрохлорид 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(6-метил-6,7-дигидротиазоло[4,5-d]пиримидин-2-ил)карбонил]амино}циклогексил)изохинолин-3-карбоксамида
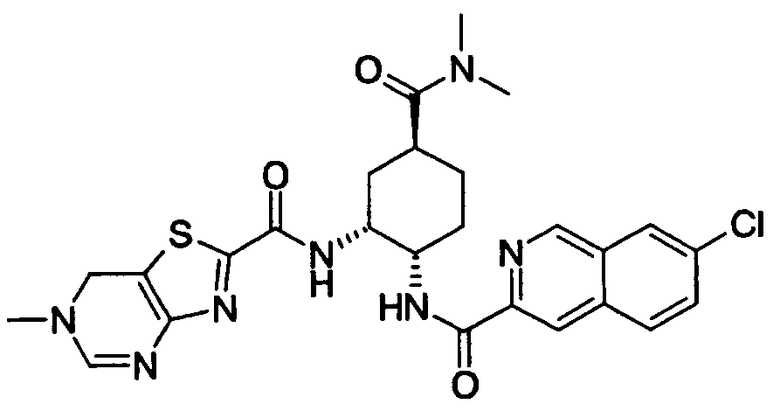
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 146, этанольным раствором хлористоводородной кислоты и затем конденсацией его с соединением, полученным в ссылочном примере 322, подобно способу, описанному в примере 49.
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,60 (1H, м), 1,70-1,90 (3H, м), 1,90-2,15 (2H, м), 2,81 (3H, с), 2,95 (3H, с), 2,90-3,05 (1H, м), 3,26 (3H, с), 4,20-4,55 (2H, м), 5,00 (2H, с), 7,91 (1H, д, J=8,8Гц), 8,27 (1H, д, J=8,8Гц), 8,37 (1H, с), 8,54 (1H, с), 8,62 (1H, с), 8,79 (1H, д, J=8,3Гц), 8,94 (1H, д, J=8,1Гц), 9,32 (1H, с).
МС (ESI) m/z: 554 (М+Н)+.
[Пример 240]
Гидрохлорид 7-хлор-N-((1S,2R,4S)-4-{[этил(метил)амино)]карбонил}-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)изохинолин-3-карбоксамида
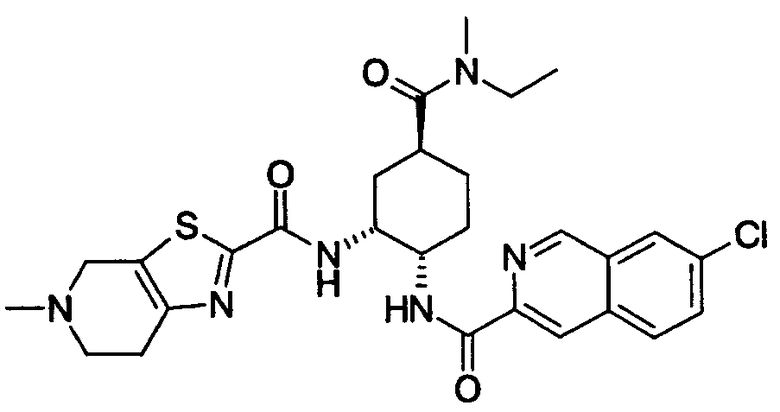
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 325, и соединения, полученного в ссылочном примере 10, подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 0,98, 1,04 (3H, каждый т, J=7,1Гц), 1,52-1,60 (1H, м), 1,74-1,77 (3H, м), 1,96-2,05 (1H, м), 2,15-2,18 (1H, м), 2,77-2,93 (8H, м), 3,17-3,32 (3H, м), 3,49 (1H, шир.с), 4,22 (1H, шир.с), 4,41-4,45 (1H, м), 4,51 (1H, шир.с), 4,69-4,72 (1H, м), 7,89 (1H, д, J=8,7Гц), 8,26 (1H, д, J=8,7Гц), 8,37 (1H, с), 8,60 (1H, с), 8,91-8,98 (2H, м), 9,32 (1H, д, J=6,6Гц), 11,39, 11,53 (1H, каждый м).
МС (FAB) m/z: 569 (М+Н)+.
[Пример 241]
Гидрохлорид N-{((1R*,2S*,5S*)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[2-(диметиламино)-2-оксоэтил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
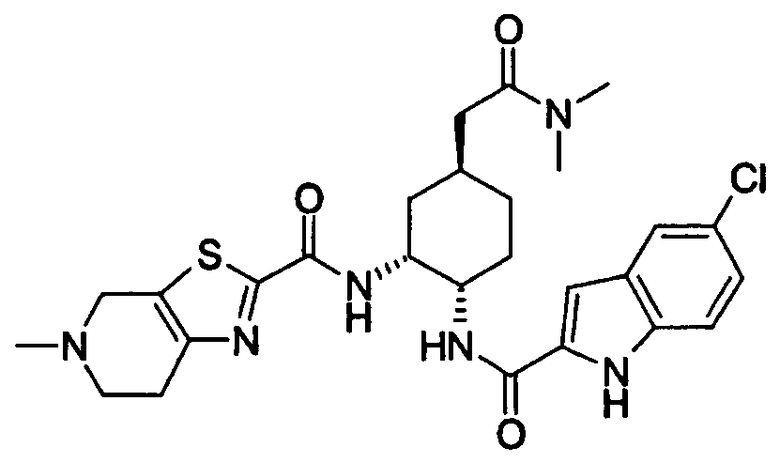
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 336, и соединения, полученного в ссылочном примере 10, подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,13-1,22 (1H, м), 1,40-1,46 (1H, м), 1,68-1,99 (5H, м), 2,18-2,29 (2H, м), 2,80 (3H, с), 2,92 (3H, с), 2,96 (3H, с), 3,22 (2H, шир.с), 3,49 (1H, шир.с), 3,70 (1H, шир.с), 4,09-4,16 (1H, м), 4,42-4,46 (2H, м), 4,67 (1H, шир.с), 7,03 (1H, с), 7,16 (1H, дд, J=8,5, 1,5Гц), 7,42 (1H, д, J=8,5Гц), 7,67 (1H, с), 8,01 (1H, д, J=8,5Гц), 8,40 (1H, д, J=7,8Гц), 11,35-11,58 (1H, м), 11,76 (1H, шир.с).
МС (FAB) m/z: 557 (М+Н)+.
[Пример 242]
Гидрохлорид N-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(метилсульфонил)метил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
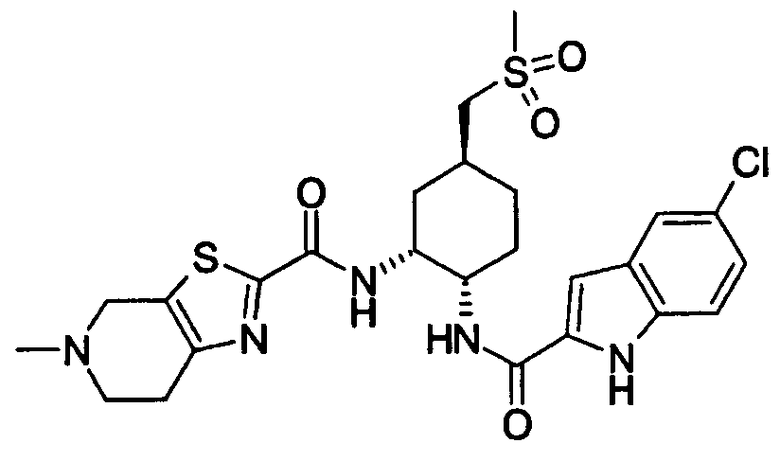
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 340, этанольным раствором хлористоводородной кислоты и затем конденсацией его с соединением, полученным в ссылочном примере 10, подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,40 (1H, м), 1,55-1,62 (1H, м), 1,70-1,76 (1H, м), 1,88-1,94 (1H, м), 2,03-2,07 (1H, м), 2,13-2,17 (1H, м), 2,30-2,33 (1H, м), 2,43-3,48 (10H, м), 3,60-3,73 (2H, м), 4,11-4,16 (1H, м), 4,40-4,42 (2H, м), 4,68-4,73 (1H, м), 7,05 (1H, с), 7,16 (1H, дд, J=2,0, 8,8Гц), 7,41 (1H, д, J=8,8Гц), 7,68 (1H, с), 8,26 (1H, д, J=7,8Гц), 8,39 (1H, д, J=7,8Гц), 11,78 (1H, шир.с).
МС (ESI) m/z: 564 (М+Н)+.
[Пример 243]
N-{(1R,2S,5S)-2-{[(2-Хлор-6Н-тиено[2,3-b]пиррол-5-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
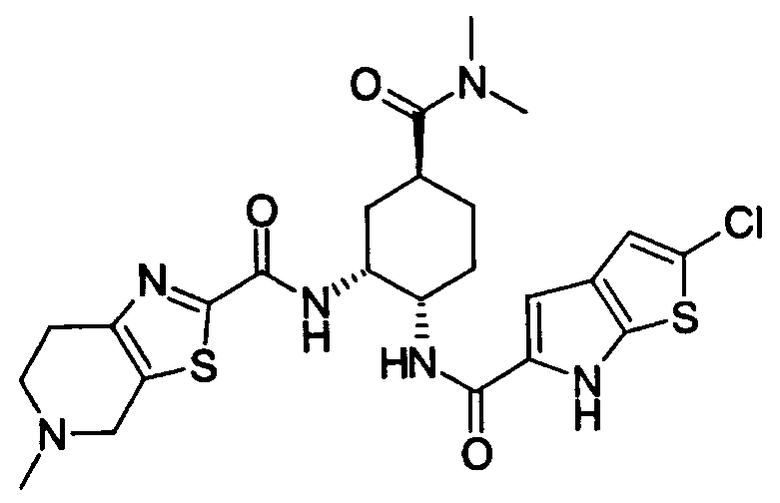
Указанное в заголовке соединение получали гидрированием соединения, полученного в ссылочном примере 252, и затем конденсацией его с соединением, полученным в ссылочном примере 345, подобно способу, описанному в примере 223.
1Н-ЯМР (CDCl3) δ: 1,56-1,66 (1H, м), 1,76-1,93 (2H, м), 2,02-2,06 (1H, м), 2,19-2,26 (1H, м), 2,30-2,34 (1H, м), 2,52 (3H, с), 2,79-2,88 (3H, м), 2,91-2,94 (2H, м), 2,96 (3H, с), 3,09 (3H, с), 3,69-3,77 (2H, м), 4,13-4,19 (1H, м), 4,58-4,61 (1H, м), 6,72 (1H, с), 6,84 (1H, с), 7,50 (1H, д, J=7,3Гц), 7,60 (1H, д, J=5,8Гц), 10,54 (1H, шир.).
МС (ESI) m/z: 549 (M+H)+.
[Пример 244]
Гидрохлорид N-{(1R,2S,5S)-2-{[3-(4-хлорфенил)2-пропиноил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
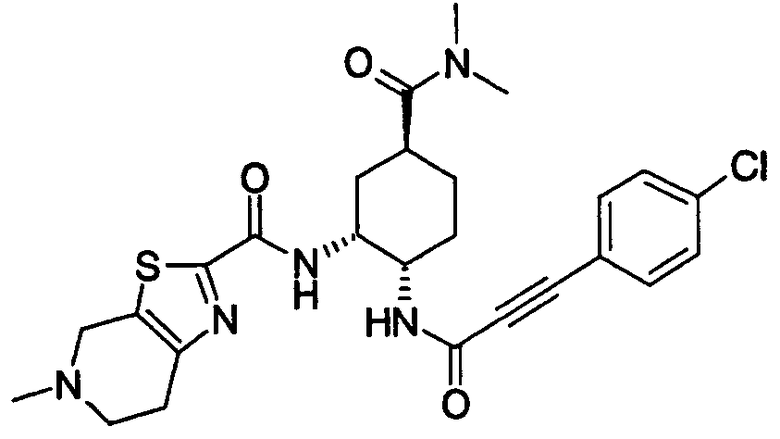
Указанное в заголовке соединение получали гидрированием соединения, полученного в ссылочном примере 252, и затем конденсацией его с соединением, полученным в ссылочном примере 347, подобно способу, описанному в примере 223.
1Н-ЯМР (ДМСО-d6) δ: 1,38-1,50 (1H, м), 1,58-1,92 (4H, м), 2,78 (3H, с), 2,90 (3H, с), 2,97 (3H, с), 3,01-3,24 (3H, м), 3,26-3,80 (2H, м), 3,90-3,98 (1H, м), 4,30-4,78 (3H, м), 7,51 (1H, д, J=8,8Гц), 7,57 (1H, д, J=8,8Гц), 8,34 (1H, д, J=8,8Гц), 8,83 (1H, д, J=7,8Гц).
МС (FAB) m/z: 528 (М+Н)+.
[Пример 245]
Гидрохлорид 6-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-с]пиридин-2-ил)карбонил]амино}циклогексил)-4-оксо-1,4-дигидрохиназолин-2-карбоксамида
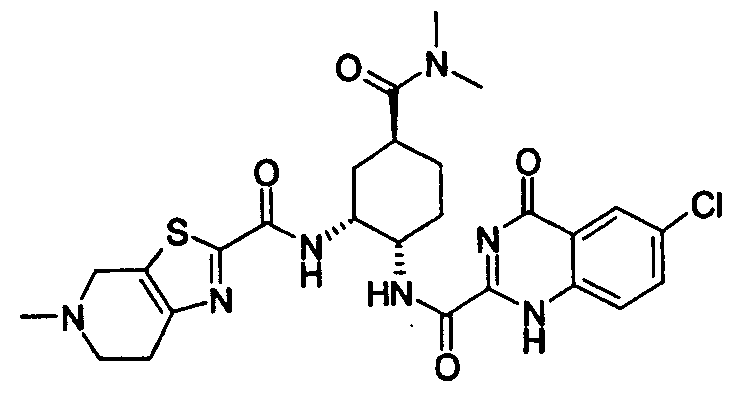
Указанное в заголовке соединение получали гидрированием соединения, полученного в ссылочном примере 252, и затем конденсацией его с соединением, полученным в ссылочном примере 349, подобно способу, описанному в примере 223.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,70-1,90 (3H, м), 1,90-2,20 (3H, м), 2,80 (3H, с), 2,93 (3H, с), 2,97 (3H, с), 2,98-3,80 (4H, м), 4,05-4,20 (2H, м), 4,35-4,80 (3H, м), 7,63 (1H, д, J=8,3Гц), 7,90 (1H, д, J=7,3Гц), 8,75-9,00 (2H, м), 11,00-11,50 (1H, шир.), 12,53 (1H, шир.с).
МС (ESI) m/z: 573 (M+H)+.
[Пример 246]
N-{(1R,2S,5S)-2-{[2-(4-Хлоранилино)-2-оксоэтантиоил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
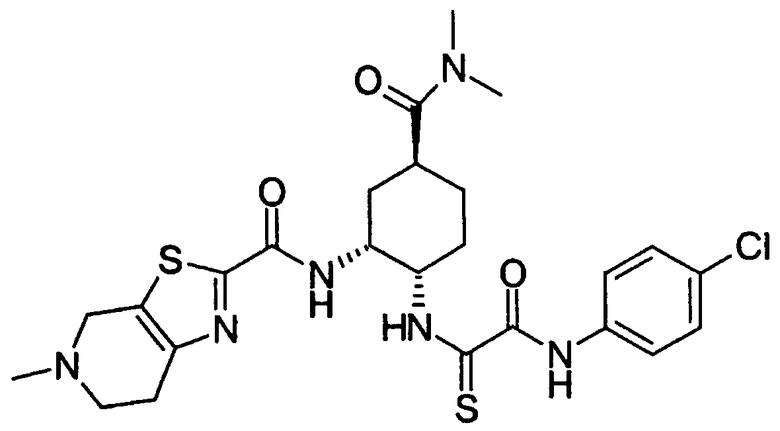
Соединение (184 мг), полученное в ссылочном примере 253, и соединение (150 мг), полученное в ссылочном примере 351, растворяли в смешанном растворителе метанол (1 мл)-метиленхлорид (4 мл), раствор нагревали и перемешивали при 150°C и после отгонки растворителя нагревание продолжали в течение 5 минут. Дав реакционной смеси остыть, образовавшийся продукт очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 24:1) с получением указанного в заголовке соединения (59 мг).
1Н-ЯМР (CDCl3) δ: 1,65-1,90 (2H, м), 1,90-2,00 (1H, м), 2,00-2,15 (2H, м), 2,20-2,30 (1H, м), 2,52 (3H, с), 2,75-2,95 (5H, м), 2,96 (3H, с), 3,07 (3H, с), 3,68 (1H, д, J=15,2Гц), 3,75 (1H, д, J=15,7Гц), 4,45-4,60 (1H, м), 4,80-4,85 (1H, м), 7,31 (2H, д, J=8,8Гц), 7,44 (1H, д, J=8,6Гц), 7,60 (2H, д, J=8,8Гц), 9,99 (1H, д, J=7,6Гц), 10,15 (1H, с).
МС (ESI) m/z: 563 (M+H)+.
[Пример 247]
N-{(1R,2S,5S)-2-({2-[(5-Хлорпиридин-2-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
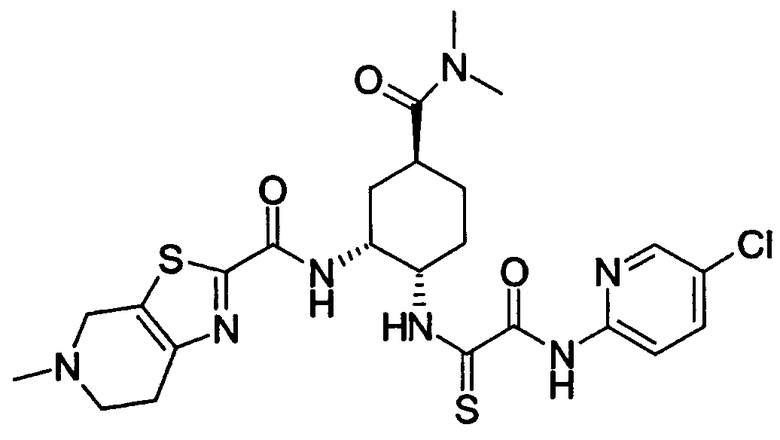
Соединение (184 мг), полученное в ссылочном примере 253, и соединение (150 мг), полученное в ссылочном примере 353, растворяли в смешанном растворителе метанол (0,3 мл)-метиленхлорид (0,3 мл), раствор нагревали и перемешивали при 150°C и после отгонки растворителя нагревание продолжали в течение 5 минут. Дав реакционной смеси остыть, образовавшийся продукт очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 24:1) с получением указанного в заголовке соединения (52 мг).
1Н-ЯМР (CDCl3) δ: 1,60-2,00 (3H, м), 2,00-2,20 (2H, м), 2,25-2,40 (1H, м), 2,53 (3H, с), 2,80-2,95 (5H, м), 2,96 (3H, с), 3,08 (3H, с), 3,70 (1H, д, J=15,4Гц), 3,75 (1H, д, J=15,4Гц), 4,45-4,60 (1H, м), 4,75-4,85 (1H, м), 7,45 (1H, д, J=8,3Гц), 7,67 (1H, дд, J=8,8, 2,5Гц), 8,18 (1H, д, J=8,8Гц), 8,31 (1H, д, J=2,0Гц), 10,06 (1H, д, J=6,3Гц), 10,56 (1H, с).
МС (ESI) m/z: 564 (М+Н)+.
[Пример 248]
N-{(1R,2S,5S)-2-({2-[(5-Хлорпиридин-2-ил)амино]-2-тиоксоацетил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
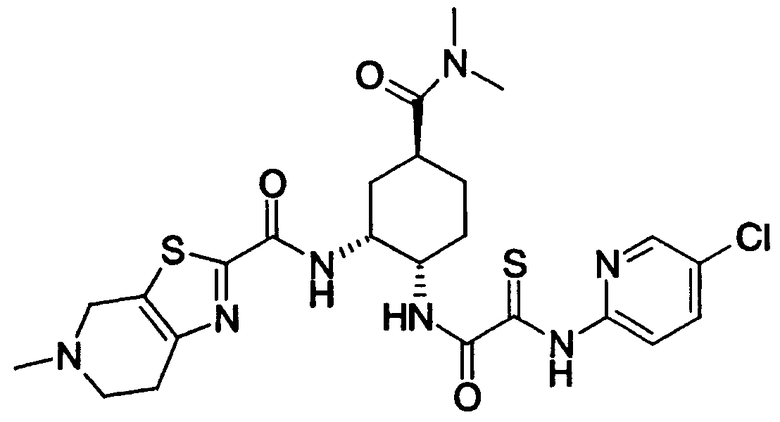
Соединение (72 мг), полученное в ссылочном примере 355, и 2-амино-5-хлорпиридин (100 мг) растворяли в смешанном растворителе метанол (0,2 мл)-метиленхлорид (0,2 мл), раствор нагревали и перемешивали при 150°C и после отгонки растворителя нагревание продолжали в течение 8 минут. Дав реакционной смеси остыть, образовавшийся продукт очищали препаративной тонкослойной хроматографией на силикагеле (метиленхлорид:метанол = 23:2) с получением указанного в заголовке соединения (4 мг).
1Н-ЯМР (CDCl3) δ: 1,60-2,00 (3H, м), 2,00-2,20 (3H, м), 2,53 (3H, с), 2,75-3,00 (5H, м), 2,95 (3H, с), 3,05 (3H, с), 3,65-3,80 (2H, м), 4,05-4,15 (1H, м), 4,70-4,80 (1H, м), 7,28 (1H, д), 7,43 (1H, д, J=9,3Гц), 7,75 (1H, дд, J=8,8, 2,7Гц), 8,41 (1H, д, J=2,7Гц), 9,05 (1H, д, J=8,8Гц), 11,56 (1H, с).
МС (ESI) m/z: 564 (М+Н)+.
[Пример 249]
Гидрохлорид N1-(5-хлор-2-тиенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
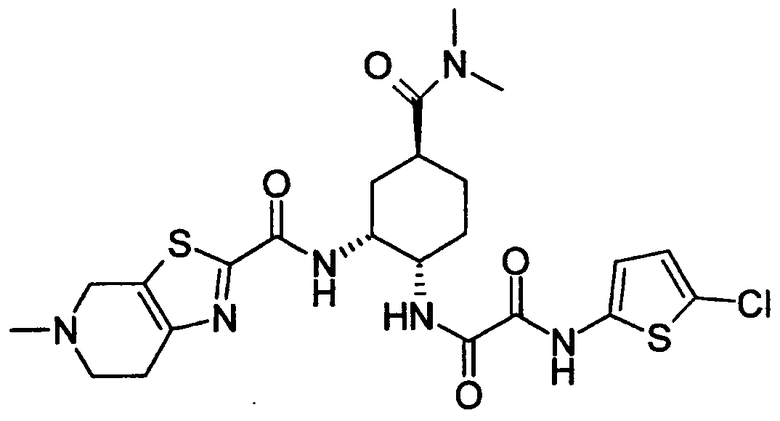
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 356, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,55 (1H, м), 1,60-1,85 (3H, м), 1,90-2,15 (2H, м), 2,79 (3H, с), 2,90-3,15 (1H, м), 2,92 (3H, с), 2,94 (3H, с), 3,15-3,30 (2H, м), 3,50-3,80 (2H, м), 3,95-4,05 (1H, м), 4,35-4,90 (3H, м), 6,90 (1H, д, J=4,2Гц), 6,94 (1H, д, J=4,2Гц), 8,72 (1H, д, J=7,3Гц), 9,13 (1H, шир.с), 11,21 (1H, шир.с), 12,32 (1H, шир.с).
МС (ESI) m/z: 553 (M+H)+.
[Пример 250]
Гидрохлорид N-{(1R,2S,5S)-2-{[(4-хлоранилино)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
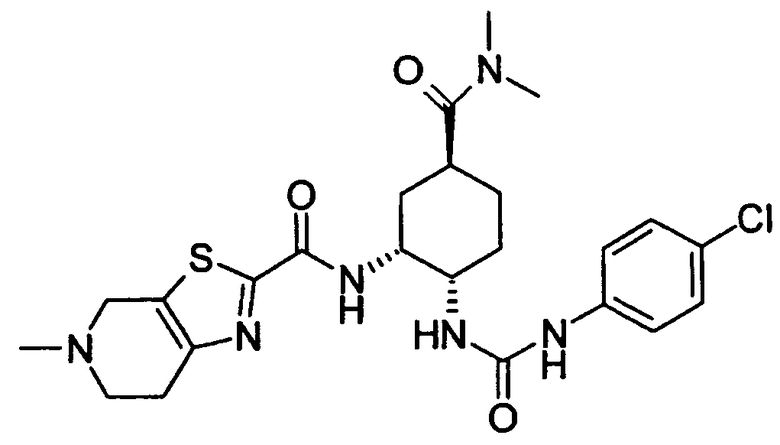
4-Хлорфенилизоцианат (76,8 мг) добавляли к раствору соединения (183 мг), полученного в ссылочном примере 253, в метиленхлориде (20 мл) и смесь перемешивали при комнатной температуре в течение 24 часов. Растворитель отгоняли при пониженном давлении и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 20:1 → 10:1) с отгонкой растворителя. Остаток растворяли в этаноле (2 мл) и метиленхлориде (2 мл), добавляли 1N этанольный раствор (0,4 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь концентрировали при пониженном давлении и остаток отверждали диэтиловым эфиром с получением указанного в заголовке соединения (160 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,50 (1H, м), 1,60-1,90 (5H, м), 2,79 (3H, с), 2,92 (3H, с), 3,00 (3H, с), 3,10-3,60 (4H, м), 3,60-3,90 (2H, м), 4,35-4,80 (3H, м), 6,26 (1H, шир.с), 7,23 (2H, д, J=9,0Гц), 7,37 (2H, д, J=9,0Гц), 8,53 (1H, шир.с), 8,72 (1H, шир.с), 11,35, 11,67 (всего 1H, каждый с).
МС (ESI) m/z: 519 (M+H)+.
[Пример 251]
Гидрохлорид N1-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-N2-(5-фторпиридин-2-ил)этандиамида
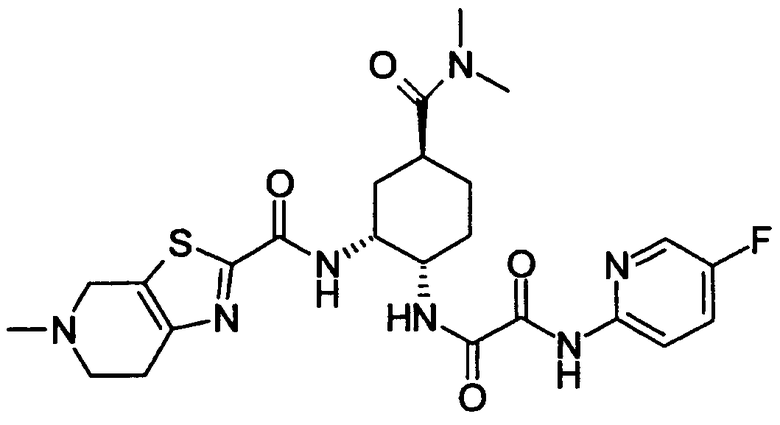
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 357, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,47-1,53 (1H, м), 1,68-1,75 (3H, м), 1,99-2,10 (2H, м), 2,80 (3H, с), 2,80-3,00 (1H, м), 2,95 (6H, с), 3,18-3,21 (2H, м), 3,40-3,80 (2H, м), 3,87-4,82 (4H, м), 7,82-7,85 (1H, м), 8,01-8,05 (1H, м), 8,40 (1H, д, J=2,9Гц), 8,71 (1H, д, J=7,7Гц), 9,13 (1H, д, J=7,3Гц), 10,27 (1H, с).
МС (FAB) m/z: 532 (М+Н)+.
[Пример 252]
Гидрохлорид N1-(4-хлорфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамида
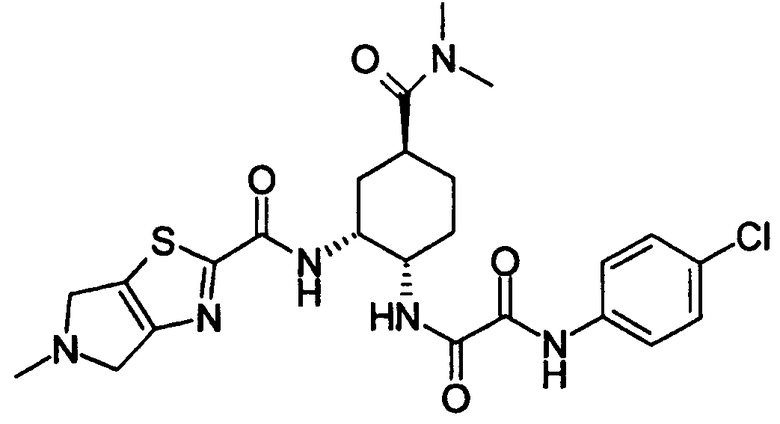
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 242, и соединения, полученного в ссылочном примере 272, подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,47-1,51 (1H, м), 1,69-1,75 (3H, м), 1,98-2,05 (2H, м), 2,80 (3H, с), 2,95 (3H, с), 2,98-3,04 (1H, м), 3,10 (3H, с), 3,40-4,61 (6H, м), 7,41 (2H, д, J=8,8Гц), 7,81 (2H, д, J=8,8Гц), 8,76 (1H, д, J=7,6Гц), 8,95 (1H, д, J=8,3Гц), 10,79 (1H, с).
МС (FAB) m/z: 533 (М+Н)+.
[Пример 253]
Гидрохлорид N1-[4-хлор-2-(трифторметил)фенил]-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
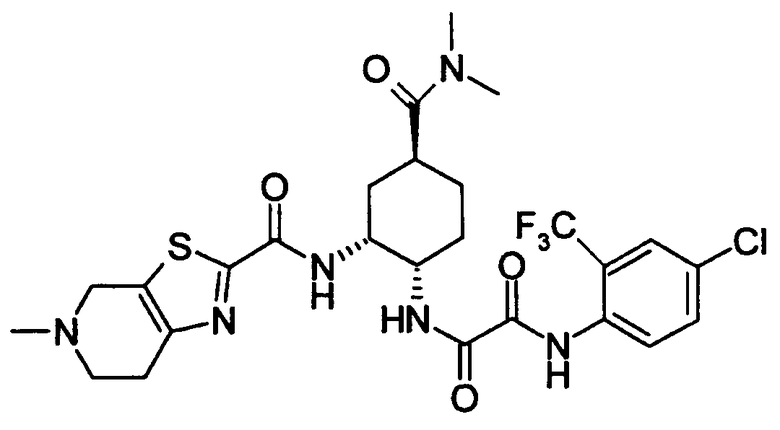
Тионилхлорид (1 мл) добавляли к хлороформному раствору (10 мл) соединения (269 мг), полученного в ссылочном примере 359, и смесь перемешивали при комнатной температуре в течение 30 минут. Растворитель отгоняли при пониженном давлении и остаток сушили. К остатку добавляли метиленхлоридный раствор (7 мл) соединения (286 мг), полученного в ссылочном примере 253, и пиридин (3 мл) при охлаждении льдом. Смесь перемешивали 2 часа при постепенном повышении температуры системы до комнатной температуры. К реакционной смеси добавляли насыщенный водный раствор (10 мл) гидрокарбоната натрия для разделения жидкостей. Полученный органический слой сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении и полученный остаток подвергали колоночной хроматографии на силикагеле (метиленхлорид:метанол = 20:1) и колоночной хроматографии на LH-20 (молекулярное сито, метанол) с получением свободного основания (90 мг) указанного в заголовке соединения в виде бледно-желтого аморфного твердого вещества. К полученному продукту добавляли метиленхлорид (5 мл), этанол (5 мл) и 1N этанольный раствор (1 мл) хлористоводородной кислоты и проводили отгонку и сушку при пониженном давлении с получением указанного в заголовке соединения.
1Н-ЯМР (ДМСО-d6) δ: 1,41-1,55 (1H, м), 1,59-1,80 (3H, м), 1,98-2,13 (2H, м), 2,77 (3H, с), 2,91 (6H, с), 3,12-3,26 (2H, м), 3,30-3,58 (2H, м), 3,60-3,78 (1H, м), 3,94-4,04 (1H, м), 4,35-4,63 (2H, м), 4,64-4,80 (1H, м), 7,73-7,82 (2H, м), 7,85 (1H, с), 8,68-8,73 (1H, м), 9,18 (1H, шир.с), 10,31 (1H, с).
МС (ESI)m/z: 615 (M+H).
[Пример 254]
Гидрохлорид N1-{4-хлор-2-[(диметиламино)карбонил]фенил}-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
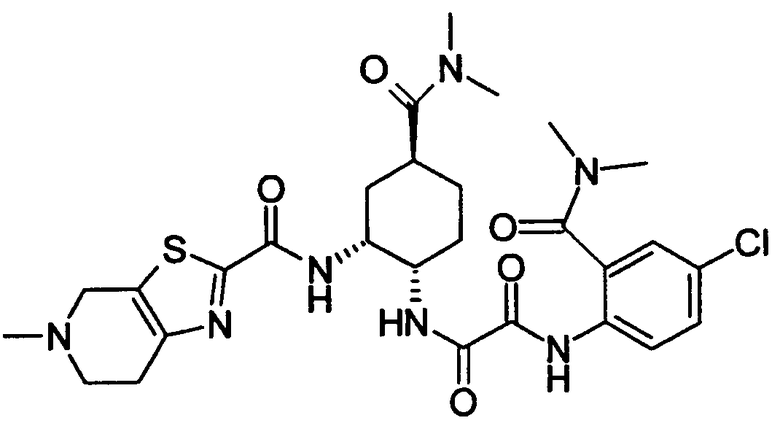
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 362, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,42-1,56 (1H, м), 1,59-1,82 (3H, м), 1,98-2,14 (2H, м), 2,79 (3H, с), 2,91 (3H, с), 2,93 (3H, с), 2,95 (3H, с), 2,98 (3H, с), 3,10-3,30 (4H, м), 3,62-3,79 (1H, м), 3,92-4,01 (1H, м), 4,34-4,50 (2H, м), 4,66-4,79 (1H, м), 7,52 (1H, д, J=2,4Гц), 7,55 (1H, дд, J=2,4, 8,5Гц), 8,05 (1H, д, J=8,5Гц), 8,75 (1H, шир.), 9,10-9,24 (1H, м), 10,52 (1H, с).
МС (ESI) m/z: 618 (М+Н)+.
[Пример 255]
Гидрохлорид N1-[4-хлор-2-(гидроксиметил)фенил]-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
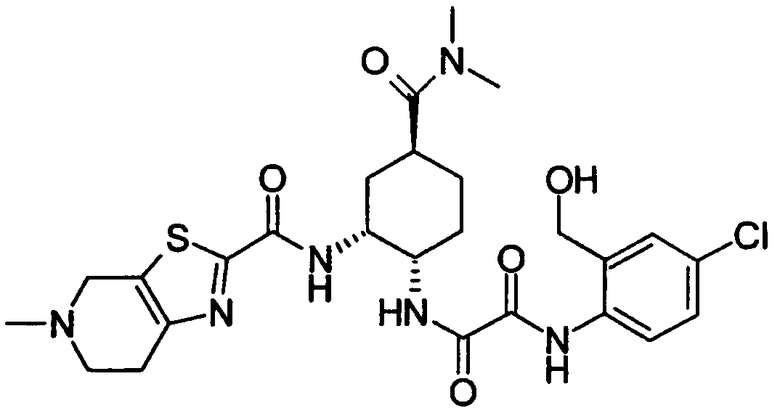
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 270, с 4-хлор-2-гидроксиметиланилином и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 199.
1Н-ЯМР (ДМСО-d6) δ: 1,42-1,57 (1H, м), 1,58-1,81 (3H, м), 1,98-2,14 (2H, м), 2,79 (3H, с), 2,93 (6H, с), 3,12-3,58 (4H, м), 3,67-3,80 (1H, м), 3,94-4,04 (1H, м), 4,37-4,50 (1,5H, м), 4,55 (2H, с), 4,67-4,80 (1H, м), 5,77-5,92 (0,5H, м), 7,37 (1H, дд, J=2,4, 8,6Гц), 7,42 (1H, д, J=2,4Гц), 7,91 (1H, д, J=8,6Гц), 8,74-8,81 (1H, м), 9,03-9,19 (1H, м), 10,79 (1H, с).
МС (ESI) m/z: 577 (М+Н)+.
[Пример 256]
Гидрохлорид N1-(4-хлор-2-метоксифенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
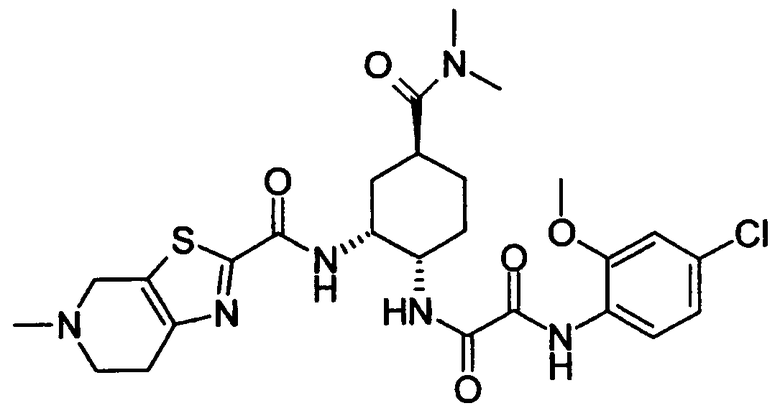
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 364, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,55 (1H, м), 1,58-1,79 (3H, м), 1,94-2,11 (2H, м), 2,77 (3H, с), 2,92 (6H, с), 3,05-3,55 (4H, м), 3,65-3,75 (1H, шир.), 3,90 (3H, с), 3,91-4,00 (1H, м), 4,36-4,47 (2H, шир.), 4,65-4,77 (1H, шир.), 7,04 (1H, дд, J=8,5, 2,0Гц), 7,20 (1H, д, J=2,0Гц), 8,06 (1H, д, J=8,5Гц), 8,65-8,80 (1H, шир.), 9,10-9,25 (1H, шир.), 9,74 (1H, с), 11,10-11,35 (1H, шир.).
МС (ESI) m/z: 577 (М+Н)+.
[Пример 257]
Гидрохлорид N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-2-(гидроксиимино)ацетил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
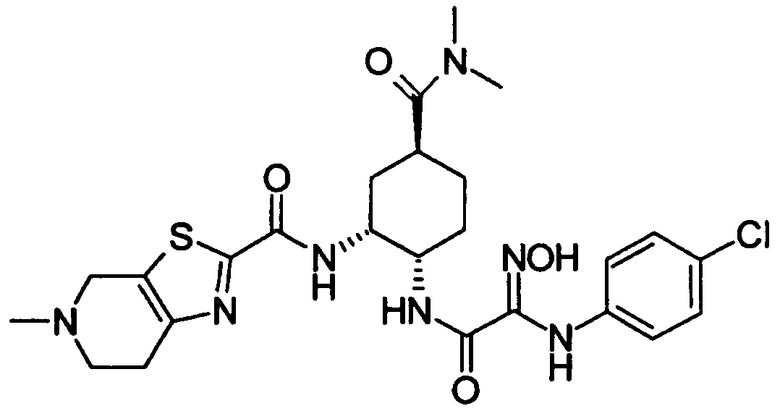
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 366, обработкой хлористоводородной кислотой, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 214.
1Н-ЯМР (ДМСО-d6) δ: 1,41-1,53 (1H, м), 1,57-1,77 (3H, м), 1,88-2,04 (2H, м), 2,77 (3H, с), 2,91 (6H, с), 3,00-3,60 (4H, м), 3,65-3,74 (1H, шир.), 3,87-3,96 (1H, м), 4,37-4,48 (2H, м), 4,66-4,76 (1H, м), 6,70 (2H, д, J=8,8Гц), 7,04 (1H, д, J=8,8Гц), 7,10 (1H, д, J=8,8Гц), 8,40-8,53 (2H, м), 8,57-8,66 (1H, м), 10,30-10,47 (1H, шир.), 10,66-10,76 (1H, шир.).
МС (ESI) m/z: 562 (М+Н)+.
[Пример 258]
Гидрохлорид N1-(4-хлорфенил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамида
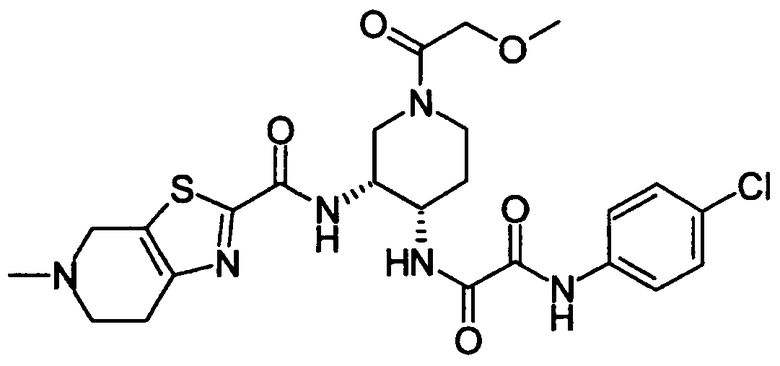
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 367, обработкой хлористоводородной кислотой, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 214.
1Н-ЯМР (ДМСО-d6) δ: 1,60-1,72 (1H, м), 1,99-2,22 (1H, м), 2,90 (3H, с), 3,03-4,80 (17H, м), 7,40 (2H, д, J=8,8Гц), 7,83 (2H, д, J=8,8Гц), 8,56-8,73 (1H, шир.), 9,14-9,33 (1H, шир.), 10,83 (1H, с), 11,20-11,55 (1H, шир.).
МС (ESI) m/z: 549 (M+H)+.
[Пример 259]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамида
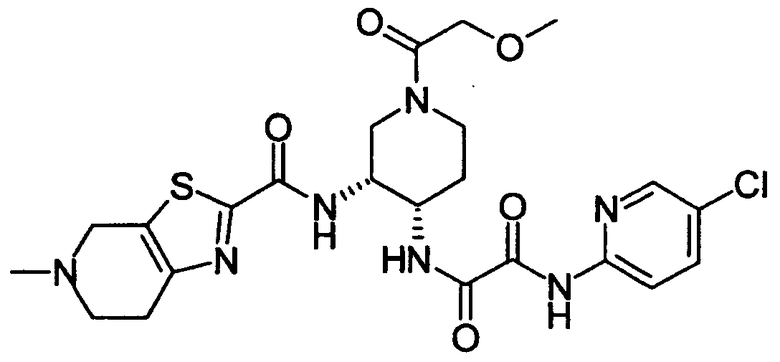
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 368, обработкой хлористоводородной кислотой, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 214.
1Н-ЯМР (ДМСО-d6) δ: 1,60-1,72 (1H, м), 1,98-2,20 (1H, м), 2,90 (3H, с), 3,00-4,77 (17H, м), 7,20-7,35 (0,8H, шир.), 7,48-7,56 (0,2H, шир.), 7,94-8,07 (1H, шир.), 8,40-8,70 (1H, шир.), 8,48-8,70 (1H, шир.), 9,23-9,45 (1H, шир.), 10,21-10,35 (1H, шир.), 11,30-11,70 (1H, шир.).
МС (ESI): m/z: 550 (М+Н)+.
[Пример 260]
Гидрохлорид N1-(5-бромпиридин-2-ил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамида
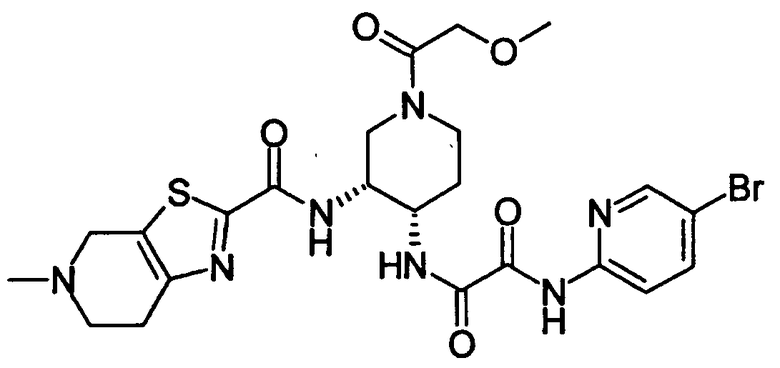
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 369, обработкой хлористоводородной кислотой, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 214.
1Н-ЯМР (ДМСО-d6) δ: 1,60-1,73 (1H, м), 1,97-2,20 (1H, м), 2,90 (3H, с), 3,03-3,52 (7H, м), 3,64-4,07 (5H, м), 4,10-4,50 (4H, м), 4,65-4,78 (1H, м), 7,28-7,35 (0,2H, м), 7,97 (1H, д, J=8,8Гц), 8,11 (1H, дд, J=8,8, 2,2Гц), 8,51 (1H, д, J=2,2Гц), 8,55-8,67 (1H, м), 9,22-9,41 (1H, м), 10,20-10,31 (0,8H, м), 11,25-11,70 (1H, шир.).
МС (ESI) m/z: 594 (М+Н)+.
[Пример 261]
Гидрохлорид N1-(4-хлорфенил)-N3-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)малонамида
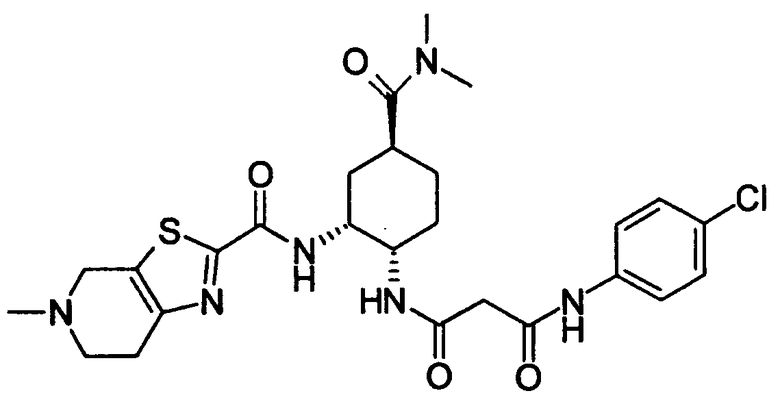
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 371, с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 5.
1Н-ЯМР (ДМСО-d6) δ:1,32-1,50 (1H, м), 1,55-1,87 (5H, м), 2,78 (3H, м), 2,92 (3H, с), 2,98 (3H, с), 2,99-3,00 (1H, м), 3,05-3,50 (5H, м), 3,65-3,75 (1H, м), 3,80-3,92 (1H, м), 4,35-4,45 (1H, м), 4,45-4,55 (1H, м), 4,65-4,80 (1H, м), 7,34 (2H, д, J=8,8Гц), 7,58 (2H, д, J=8,8Гц), 8,00-8,10 (1H, м), 8,30-8,40 (1H, м), 10,29 (1H, д, J=12,5Гц), 12,40 (1H, шир.с).
МС (FAB) m/z: 561 (М+Н)+.
[Пример 262]
Гидрохлорид N1-(3-хлорфенил)-N3-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)малонамида
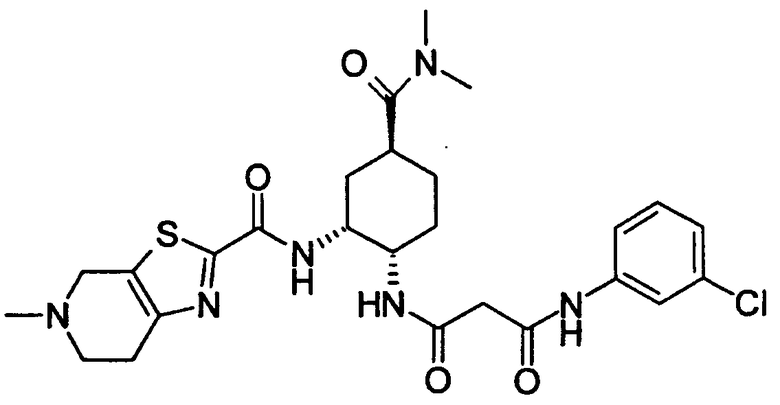
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 373, с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 5.
1Н-ЯМР (ДМСО-d6) δ: 1,32-1,50 (1H, м), 1,55-1,90 (5H, м), 2,77 (3H, с), 2,91 (3H, с), 2,98 (3H, с), 2,99-3,00 (1H, м), 3,05-3,50 (5H, м), 3,65-3,80 (1H, м), 3,80-3,90 (1H, м), 4,35-4,50 (1H, м), 4,50-4,60 (1H, м), 4,65-4,80 (1H, м), 7,09 (1H, д, J=8,8Гц), 7,31 (1H, д, J=8,8Гц), 7,38 (1H, т, J=8,8Гц), 7,79 (1H, с), 8,00-8,10 (1H, м), 8,30-8,40 (1H, м), 10,28 (1H, д, J=12,5Гц), 11,67 (1H, шир.с).
МС (FAB) m/z: 561 (M+H)+.
[Пример 263]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-{[этил(метил)амино]карбонил}-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
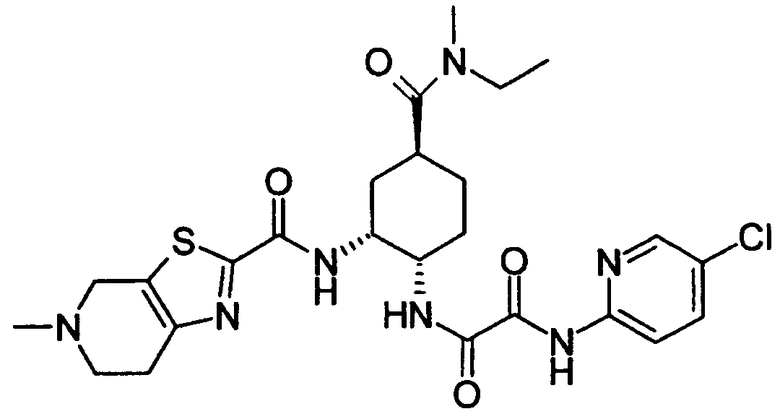
10% Палладий на углероде (0,3 г) добавляли к раствору соединения (0,33 г), полученного в ссылочном примере 404, в этаноле (20 мл) и смесь перемешивали при комнатной температуре в течение 24 часов в атмосфере водорода. После удаления нерастворимого вещества фильтрованием через слой целита фильтрат концентрировали при пониженном давлении. Полученный остаток (0,37 г) растворяли в N,N-диметилформамиде (20 мл), к раствору последовательно добавляли соединение (0,3 г), полученное в ссылочном примере 266, моногидрат 1-гидроксибензотриазола (0,2 г) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (0,37 г) и смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь концентрировали при пониженном давлении и полученный остаток разбавляли смешанным растворителем хлороформ-метанол (9:1) и промывали насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия. Полученный органический слой сушили над безводным сульфатом натрия и отгоняли при пониженном давлении растворитель, затем полученный остаток очищали колоночной хроматографией на силикагеле (хлороформ:метанол = 95:5) и концентрировали требуемую фракцию. Добавляли 1N этанольный раствор хлористоводородной кислоты для образования гидрохлорида. Полученную соль перекристаллизовывали из смешанного растворителя метанол/диэтиловый эфир с получением указанного в заголовке соединения (0,28 г).
1Н-ЯМР (ДМСО-d6) δ: 0,95 (1,5H, т, J=6,9Гц), 1,42 (1,5H, т, J=6,9Гц), 1,40-1,52 (1H, м), 1,60-1,78 (3H, м), 1,92-2,11 (2H, м), 2,74 (3H, с), 2,90 (3H, с), 3,10-3,38 (5H, м), 3,40-3,52 (1H, м), 3,68-3,70 (1H, м), 3,96-4,05 (1H, м), 4,41 (2H, с), 4,70 (1H, д, J=15,9Гц), 8,00-8,01 (2H, м), 8,44 (1H, с), 8,71 (1H, дд, J=10,1, 2,2Гц), 9,14 (0,5H, д, J=7,8Гц), 9,22 (0,5H, д, J=8,3Гц), 10,24 (0,5H, с), 10,28 (0,5H, с), 11,48 (1H, шир.с), 11,61 (1H, шир.с).
МС (FAB) m/z: 562 (М+Н)+.
[Пример 264]
Гидрохлорид N1-(4-хлорфенил)-N2-((1S,2R,4S)-4-{[этил(метил)амино]карбонил}-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
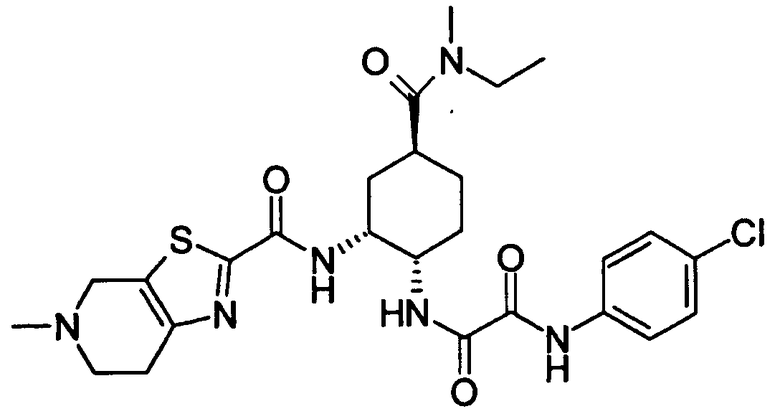
Указанное в заголовке соединение получали преобразованием соединения, полученного в ссылочном примере 404, в амин, конденсацией амина с соединением, полученным в ссылочном примере 374, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 263.
1Н-ЯМР (ДМСО-d6) δ: 0,97 (1,5H, т, J=6,9Гц), 1,04 (1,5H, т, J=6,9Гц), 1,40-1,60 (1H, м), 1,60-1,80 (3H, м), 1,92-2,11 (2H, м), 2,74 (3H, с), 2,89 (3H, с), 3,10-3,32 (5H, м), 3,40-3,52 (1H, м), 3,65-3,80 (1H, м), 3,90-4,05 (1H, м), 4,40 (2H, с), 4,70 (1H, д, J=15,9Гц), 7,39 (2H, д, J=8,8Гц), 7,82 (2H, д, J=8,8Гц), 8,75 (1H, дд, J=10,1, 2,2Гц), 9,00 (0,5H, д, J=7,8Гц), 9,08 (0,5H, д, J=8,3Гц), 10,81 (1H, д, J=4,9Гц), 11,45 (1H, шир.с).
МС (FAB) m/z: 561 (М+Н)+.
[Пример 265]
Гидрохлорид N1-(5-бромпиридин-2-ил)-N2-((1S,2R,4S)-4-{[этил(метил)амино]карбонил}-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
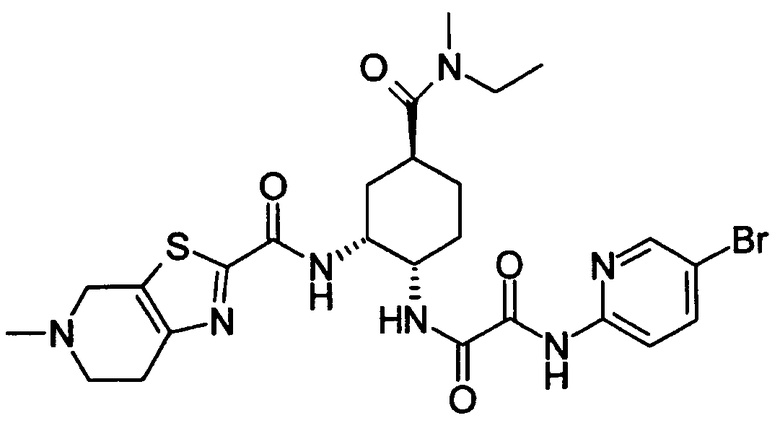
Указанное в заголовке соединение получали преобразованием соединения, полученного в ссылочном примере 404, в амин, конденсацией амина с соединением, полученным в ссылочном примере 375, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 263.
1Н-ЯМР (ДМСО-d6) δ: 1,02 (1,5H, т, J=6,9Гц), 1,08 (1,5H, т, J=6,9Гц), 1,49-1,60 (1H, м), 1,60-1,86 (3H, м), 2,00-2,20 (2H, м), 2,81 (3H, с), 2,97 (3H, с), 3,15-3,42 (6H, м), 3,50-3,60 (1H, м), 3,70-3,82 (1H, м), 4,48 (2H, с), 4,77 (1H, д, J=15,9Гц), 8,04 (1H, д, J=8,8Гц), 8,17 (1H, д, J=8,8Гц), 8,58 (1H, с), 8,78 (1H, дд, J=10,1, 2,2Гц), 9,21 (0,5H, д, J=7,8Гц), 9,29 (0,5H, д, J=8,3Гц), 10,29 (0,5H, с), 10,33 (0,5H, с), 11,53 (0,5H, шир.с), 11,65 (0,5H, шир.с).
МС (FAB) m/z: 607 (М+Н)+.
[Пример 266]
Гидрохлорид N1-(4-хлор-3-фторфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
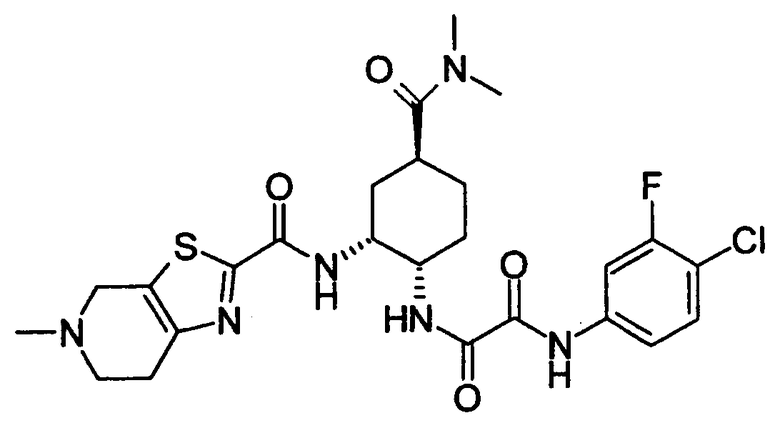
Указанное в заголовке соединение получали преобразованием соединения, полученного в ссылочном примере 252, в амин, конденсацией амина с соединением, полученным в ссылочном примере 378, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 263.
1Н-ЯМР (ДМСО-d6) δ: 1,44-1,52 (1H, м), 1,65-1,76 (3H, м), 2,01-2,07 (2H, м), 2,77 (3H, с), 2,93 (6H, с), 2,94-3,00 (1H, м), 3,10-3,38 (3H, м), 3,68-3,70 (1H, м), 3,96-4,05 (1H, м), 4,42 (2H, с), 4,70 (1H, д, J=15,9Гц), 7,56 (1H, т, J=8,8Гц), 7,68 (1H, д, J=8,8Гц), 7,90 (1H, дд, J=11,7, 1,5Гц), 8,73 (1H, дд, J=12,5, 7,3Гц), 9,06 (1H, дд, J=12,5, 8,1Гц), 11,01 (1H, д, J=5,8Гц), 11,30-11,42 (1H, м).
МС (FAB) m/z: 565 (M+H)+.
[Пример 267]
N-{(1R,2S,5S)-2-{[3-(4-Хлорфенил)-3-оксопропаноил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамид
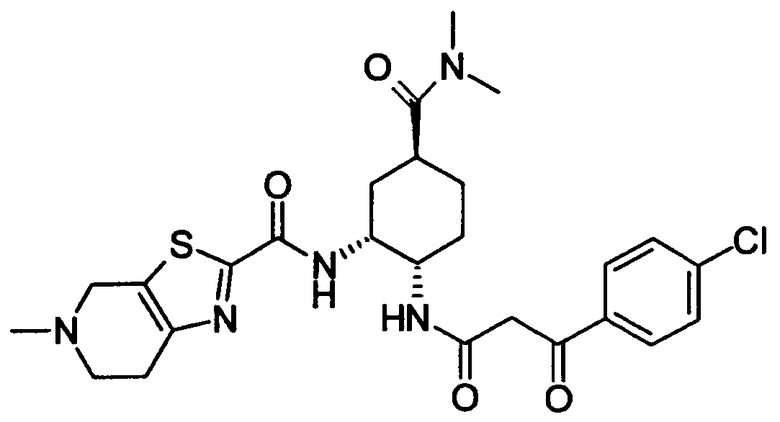
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 383, обработкой хлористоводородной кислотой, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 214.
1Н-ЯМР (CDCl3) (свободное основание) δ: 1,22-1,32 (1H, м), 1,49-1,92 (3H, м), 1,95-2,10 (2H, м), 2,53 (3H, с), 2,70-2,79 (1H, м), 2,80-2,90 (2H, м), 2,93 (6H, с), 2,95-3,09 (2H, м), 3,72 (2H, с), 3,87 (2H, с), 4,05-4,19 (1H, м), 4,60-4,70 (1H, м), 7,20-7,40 (2H, м), 7,42 (2H, д, J=8,3Гц), 7,87 (2H, д, J=8,3Гц).
МС (FAB) m/z: 546 (М+Н)+.
[Пример 268]
N1-(5-Хлорпиридин-2-ил)-N2-((1R,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамид
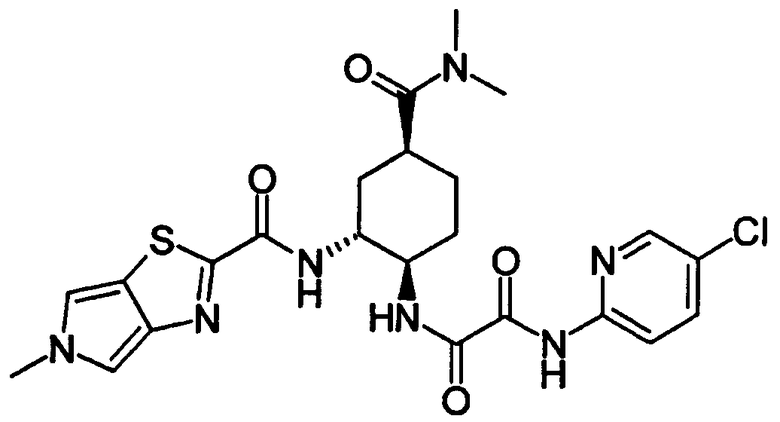
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 386, обработкой хлористоводородной кислотой и конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 293, подобно способу, описанному в примере 214.
1Н-ЯМР (ДМСО-d6) δ: 1,00-2,35 (7H, м), 2,96 (3H, с), 3,04 (3H, с), 3,85-3,95 (1H, м), 3,88 (3H, с), 4,60-4,75 (1H, м), 6,68 (1H, д, J=2,0Гц), 7,17 (1H, д, J=2,0Гц), 7,20-7,32 (1H, м), 7,67 (1H, дд, J=8,8, 2,8Гц), 7,99 (1H, д, J=8,4Гц), 8,21 (1H, д, J=8,8Гц), 8,25 (1H, д, J=2,8Гц), 9,64 (1H, с).
HRMS (FAB) m/z: 532,1520 (M+H)+.
(Вычислено; C23H27ClN7O4S: 532,1534).
[Пример 269]
Гидрохлорид N1-[(5-хлорпиридин-2-ил)амино]-N2-((1R,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
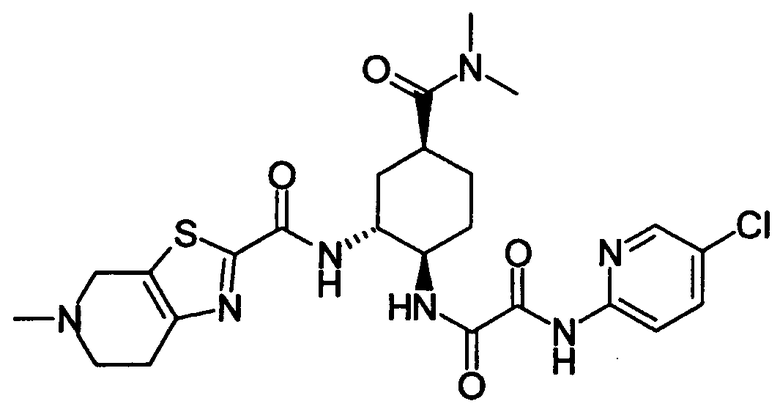
Указанное в заголовке соединение получали восстановлением соединения, полученного в ссылочном примере 387, подобно способу, описанному в примере 253, конденсацией восстановленного продукта с соединением, полученным в ссылочном примере 266, и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 208.
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,98 (6H, м), 2,82 (3H, с), 2,91 (3H, с), 2,95 (3H, с), 2,86-3,92 (7H, м), 4,30-4,81 (2H, м), 7,92-8,09 (2H, м), 8,39-8,47 (1H, м), 8,56-8,72 (2H, м), 10,17 (1H, с).
МС (ESI) m/z: 548 (М+Н)+.
[Пример 270]
N1-(4-Хлорфенил)-N2-((1R,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид
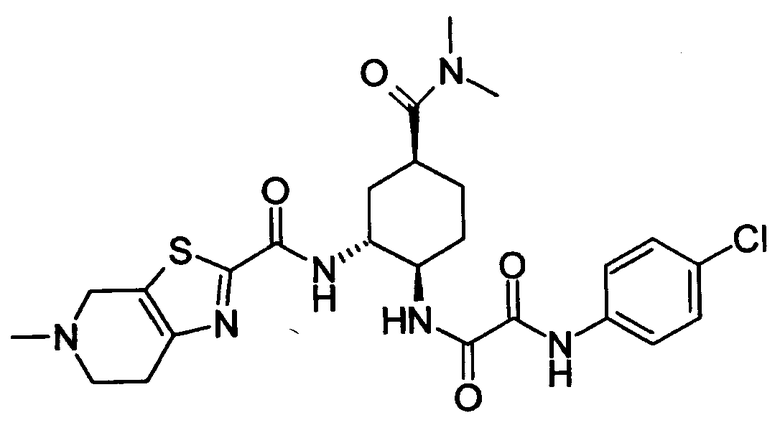
Указанное в заголовке соединение получали восстановлением соединения, полученного в ссылочном примере 387, подобно способу, описанному в примере 253, и конденсацией восстановленного продукта с литиевой солью, полученной гидролизом соединения, полученного в ссылочном примере 242, и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,97 (6H, м), 2,82 (3H, с), 2,91 (3H, с), 2,98 (3H, с), 2,83-3,88 (7H, м), 4,30-4,79 (2H, м), 7,37 (2H, д, J=8,8Гц), 7,89 (2H, д, J=8,8Гц), 8,34 (1H, д, J=8,4Гц), 8,63 (1H, д, J=8,8Гц), 10,72 (1H, с).
МС (ESI) m/z: 547 (M+H)+.
[Пример 271]
Гидрохлорид N1-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-N2-(пиридин-4-ил)этандиамида
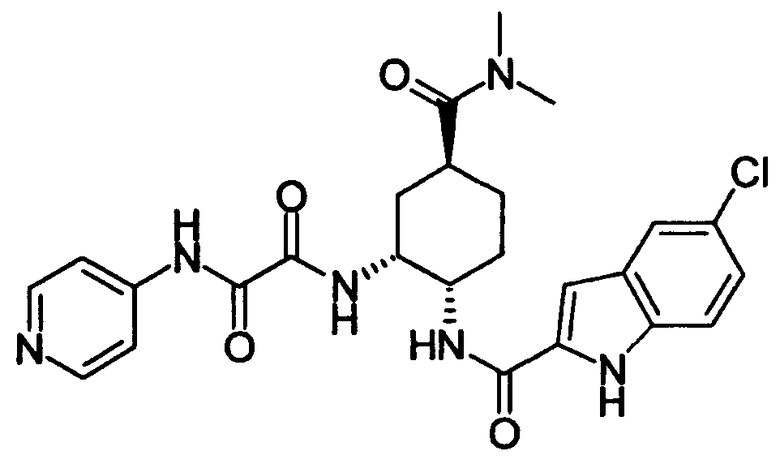
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 310, обработкой хлористоводородной кислотой и конденсацией соединения со снятой защитой с 2-[(пиридин-4-ил)амино]-2-оксоацетатом лития, полученным гидролизом соединения, полученного в ссылочном примере 261, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,40-2,01 (6H, м), 2,79 (3H, с), 3,01 (3H, с), 3,00-3,18 (1H, м), 4,02-4,19 (1H, м), 4,45-4,55 (1H, м), 7,09 (1H, с), 7,13-7,22 (1H, м), 7,41 (1H, д, J=8,4Гц), 7,64 (1H, шир.с), 8,28 (2H, д, J=6,8Гц), 8,36 (1H, д, J=8,0Гц), 8,62 (1H, д, J=8,8Гц), 8,72 (2H, д, J=6,8Гц), 11,74 (1H, с), 11,83 (1H, с).
МС (FAB) m/z: 511 (М+Н)+.
[Пример 272]
Гидрохлорид N1-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-N2-(пиридин-3-ил)этандиамида
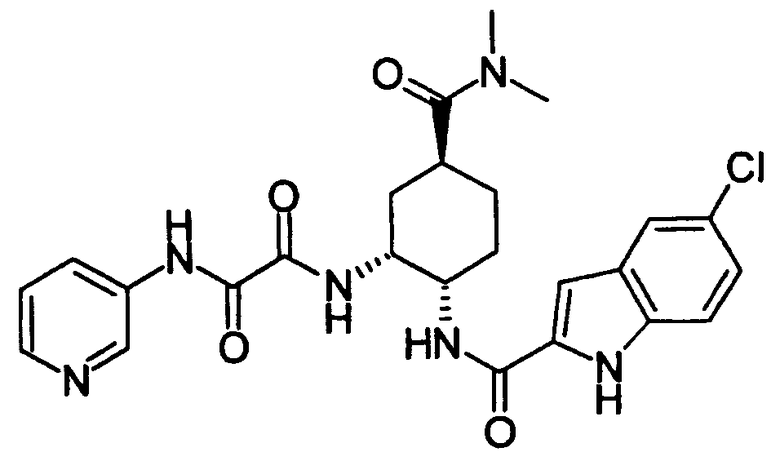
Указанное в заголовке соединение получали, используя в качестве исходных веществ метил 2-[(пиридин-3-ил)амино]-2-оксоацетат, полученный конденсацией 3-аминопиридина с метил 2-хлор-2-оксоацетатом подобно способу, описанному в ссылочном примере 242, и соединение, полученное в ссылочном примере 310, подобно способу, описанному в ссылочном примере 271.
1Н-ЯМР (ДМСО-d6) δ: 1,40-2,05 (6H, м), 2,80 (3H, с), 3,02 (3H, с), 2,92-3,15 (1H, м), 4,02-4,17 (1H, м), 4,42-4,58 (1H, м), 7,10 (1H, с), 7,12-7,19 (1H, м), 7,40 (1H, д, J=8,4Гц), 7,62-7,87 (2H, м), 8,36-8,64 (4H, м), 9,18 (1H, с), 11,39 (1H, с), 11,79 (1H, с).
МС (FAB) m/z: 511 (М+Н)+.
[Пример 273]
Гидрохлорид N1-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-N2-(пиперидин-4-ил)этандиамида
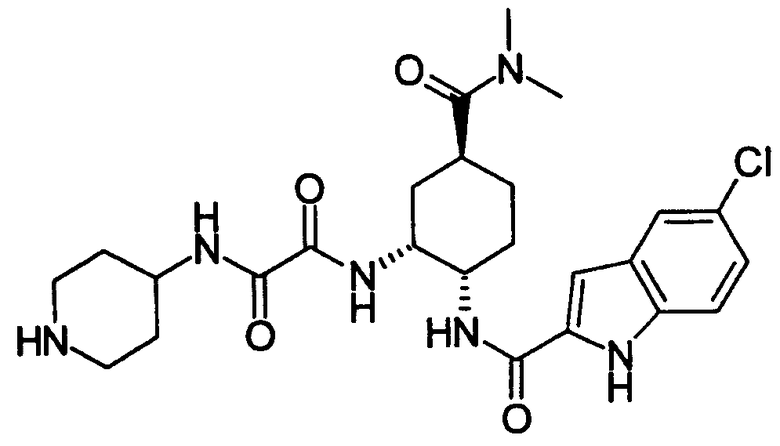
4N Диоксановый раствор (8,0 мл) хлористоводородной кислоты добавляли к раствору соединения (400 мг), полученного в ссылочном примере 389, в этаноле (5,0 мл) при комнатной температуре и смесь перемешивали при той же температуре в течение 5 часов. Растворитель отгоняли при пониженном давлении, остаток промывали метиленхлоридом и нерастворимое вещество отфильтровывали и промывали с получением указанного в заголовке соединения (320 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,38-1,92 (10H, м), 2,77 (3H, с), 2,96 (3H, с), 2,82-3,35 (6H, м), 3,88-4,10 (2H, м), 4,34-4,43 (1H, м), 7,05 (1H, с), 7,11-7,17 (1H, м), 7,38 (1H, д, J=8,8Гц), 7,65 (1H, с), 8,25 (1H, д, J=8,0Гц), 8,34 (1H, д, J=7,6Гц), 8,89 (1H, д, J=8,4Гц), 11,75 (1H, с).
МС (ESI) m/z: 517 (М+Н)+.
[Пример 274]
Гидрохлорид N1-{(1R,2S,5S)-2-{[(5-хлориндол-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-N2-(1-метилпиперидин-4-ил)этандиамида
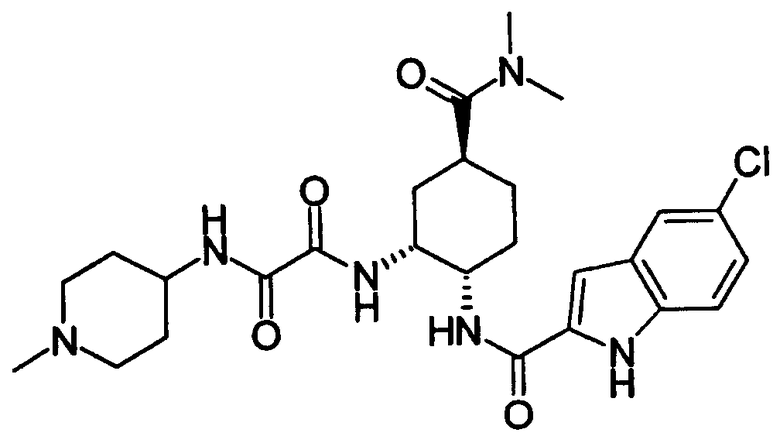
Указанное в заголовке соединение получали метилированием соединения, полученного в ссылочном примере 273, подобно способу, описанному в ссылочном примере 9, и обработкой его хлористоводородной кислотой.
1Н-ЯМР (ДМСО-d6) δ: 1,40-2,01 (11H, м), 2,67 (3H, с), 2,79 (3H, с), 2,98 (3H, с), 2,85-4,48 (7H, м), 7,07 (1H, с), 7,16 (1H, дд, J=8,8, 2,0Гц), 7,40 (1H, д, J=8,8Гц), 7,68 (1H, д, J=2,0Гц), 8,25-8,35 (1H, м), 8,37 (1H, д, J=7,6Гц), 8,90-9,02 (1H, м), 9,82 (1H, шир.с), 11,78 (1H, с).
МС (ESI) m/z: 531 (М+Н)+.
[Пример 275]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-N1-метилэтандиамида
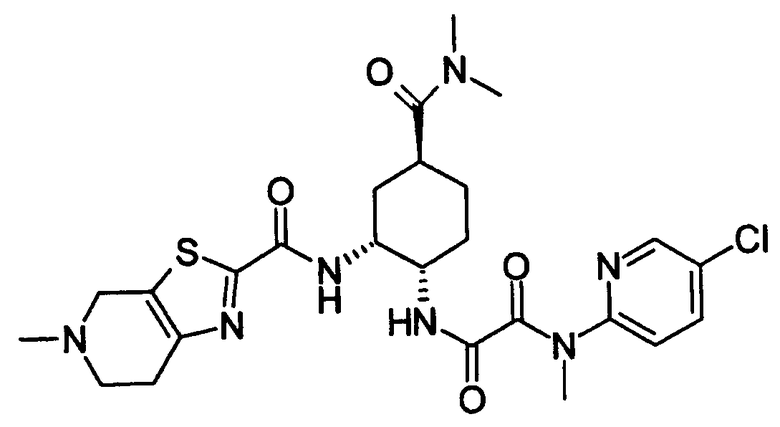
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 390, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,32-1,97 (6H, м), 2,42-2,51 (1H, м), 2,76 (3H, с), 2,91 (3H, с), 2,93 (3H, с), 3,27 (3H, с), 3,00-4,80 (8H, м), 7,45 (1H, шир.с), 7,88-7,97 (1H, м), 8,25-8,41 (2H, м), 8,78-8,91 (1H, м).
МС (FAB) m/z: 562 (М+Н)+.
[Пример 276]
Гидрохлорид N1-(5-хлорпиримидин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
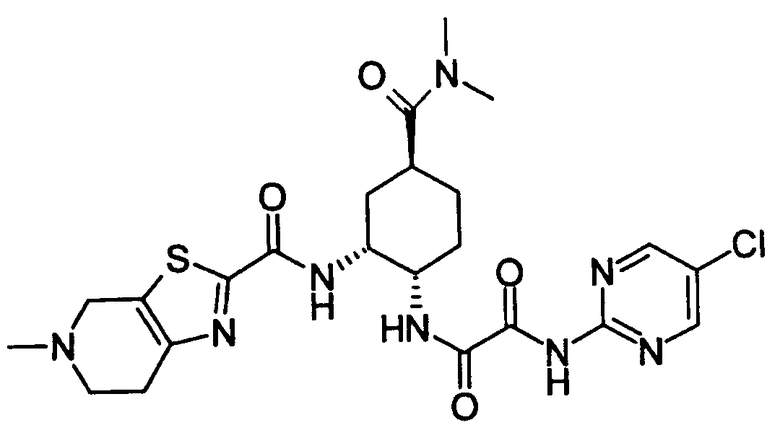
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 391, конденсацией гидролизата с соединением, полученным в ссылочном примере 253, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 191.
1Н-ЯМР (ДМСО-d6) δ: 1,38-2,10 (7H, м), 2,77 (3H, с), 2,90 (3H, с), 2,93 (3H, с), 3,04-4,80 (8H, м), 8,60-8,70 (2H, м), 8,82 (2H, с), 9,08 (1H, шир.с), 10,64 (1H, с), 11,57 (1H, шир.с).
МС (FAB) m/z: 549 (M+H)+.
[Пример 277]
Гидрохлорид N1-(4-хлорфенил)-N2-((1S,2R,4S)-4-{[этил(метил)амино]карбонил}-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамида
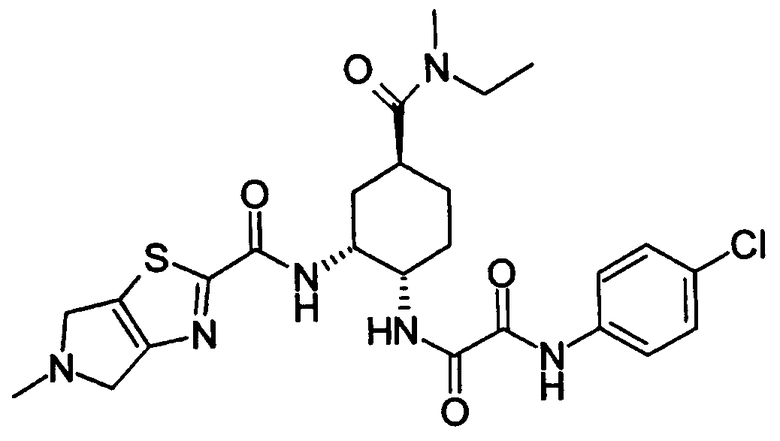
Указанное в заголовке соединение получали восстановлением соединения, полученного в ссылочном примере 392, подобно способу, описанному в примере 253, конденсацией продукта восстановления с карбоновой кислотой, полученной гидролизом соединения, полученного в ссылочном примере 242, и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 195.
1Н-ЯМР (ДМСО-d6) δ: 0,96, 1,02 (3H, каждый т, J=7,0Гц), 1,47-1,58 (1H, м), 1,65-1,77 (3H, м), 1,98-2,08 (2H, м), 2,76-2,91 (4H, м), 3,07 (3H, с), 3,19-3,41 (2H, м), 3,98-4,04 (1H, м), 4,42 (1H, шир.с), 4,46-4,94 (4H, м), 7,41 (2H, д, J=8,8Гц), 7,83 (2H, д, J=8,8Гц), 8,74-8,80 (1H, м), 9,02 (1H, д, J=7,3Гц), 10,82 (1H, с), 12,41 (1H, шир.с).
МС (FAB) m/z: 547 (М+Н)+.
[Пример 278]
Гидрохлорид N1-(5-бромпиридин-2-ил)-N2-((1S,2R,4S)-4-{[этил(метил)амино]карбонил}-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамида
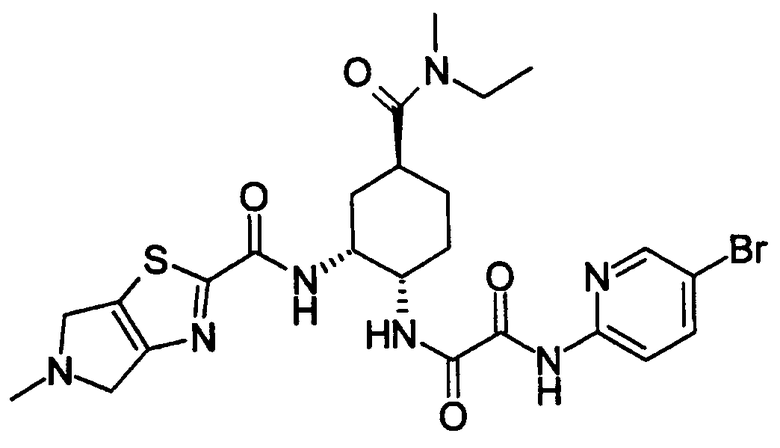
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 392, и соединения, полученного в ссылочном примере 262, подобно способу, описанному в примере 277.
1Н-ЯМР (ДМСО-d6) δ: 0,90-1,08 (3H, м), 1,40-2,13 (6H, м), 2,70-3,53 (13H, м), 3,92-4,08 (1H, м), 4,35-4,47 (1H, м), 7,95 (1H, д, J=8,8Гц), 8,10 (1H, дд, J=8,8, 2,4Гц), 8,50-8,55 (1H, м), 8,68-8,78 (1H, м), 9,12-9,18 (1H, м), 10,26 (1H, с).
МС (FAB) m/z: 592 (М+Н)+.
[Пример 279]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-{[этил(метил)амино]карбонил}-2-{[(5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)этандиамида
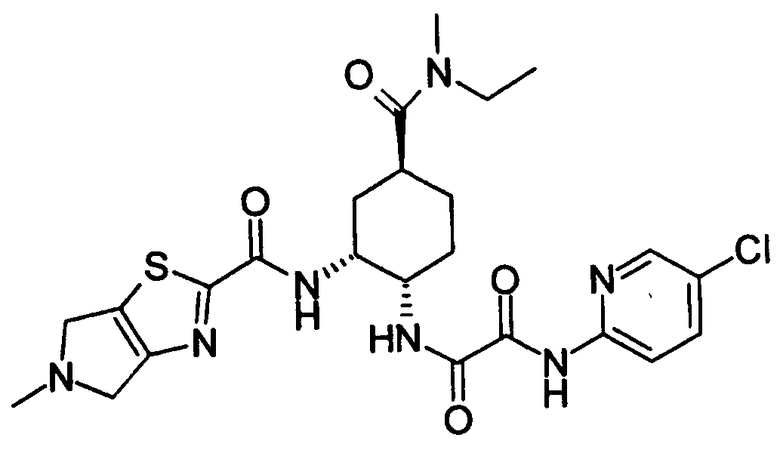
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 392, и соединения, полученного в ссылочном примере 243, подобно способу, описанному в примере 277.
1Н-ЯМР (ДМСО-d6) δ: [0,95 (т, J=7,0Гц), 1,01 (т, J=6,8Гц), 3H], 1,45-1,72 (4H, м), 1,96-2,07 (2H, м), 2,74-2,90 (4H, м), 3,06 (3H, с), 3,18-3,40 (2H, м), 3,95-4,02 (1H, м), 4,41 (1H, шир.с), 4,54-4,90 (4H, м), 8,00 (2H, шир.с), 8,45 (1H, с), 8,70-8,75 (1H, м), 9,15 (1H, шир.с), 10,27 (1H, шир.с), 12,29 (1H, шир.с).
МС (ESI) m/z: 548 (М+Н)+.
[Пример 280]
Гидрохлорид N1-(4-хлор-3-метоксифенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
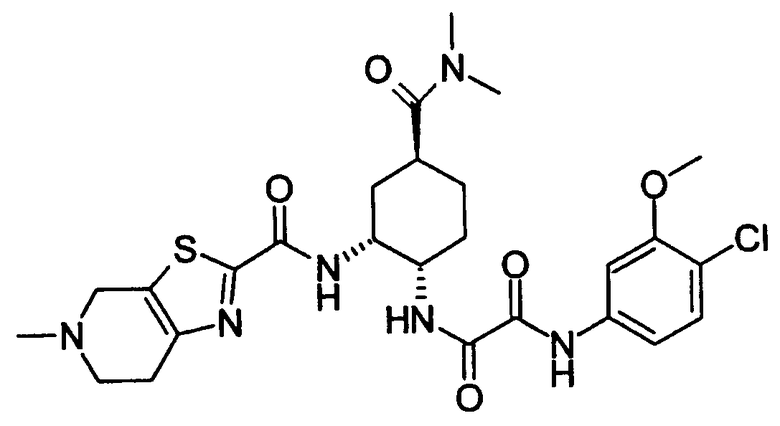
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 395, с соединением, полученным в ссылочном примере 10, и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,46-1,54 (1H, м), 1,67-1,77 (3H, м), 2,01-2,10 (2H, м), 2,79 (3H, с), 2,92-2,98 (7H, м), 3,21 (2H, шир.с), 3,49 (1H, шир.с), 3,69 (1H, шир.с), 3,80 (3H, с), 3,98-4,03 (1H, м), 4,42-4,50 (2H, м), 4,69 (1H, шир.с), 7,37 (1H, д, J=8,7Гц), 7,48 (1H, дд, J=8,7, 2,2Гц), 7,72 (1H, д, J=2,2Гц), 8,75 (1H, д, J=7,3Гц), 9,06 (1H, шир.с), 10,77 (1H, с), 11,44 (1H, шир.с).
МС (FAB) m/z: 577 (М+Н)+.
[Пример 281]
Гидрохлорид N1-(4-хлорфенил)-N2-((1R*,2R*)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклопентил)этандиамида
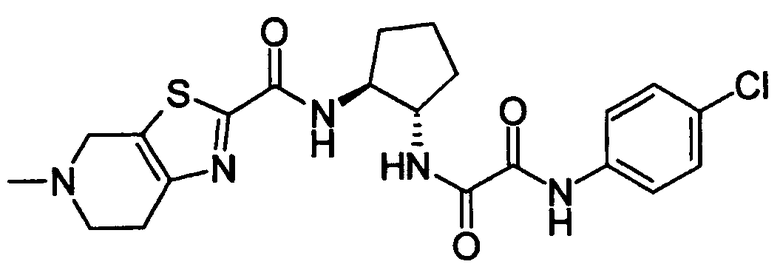
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 242, конденсацией гидролизата с соединением, полученным в ссылочном примере 62, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 195.
1Н-ЯМР (ДМСО-d6) δ: 1,65-1,73 (4H, м), 1,91-1,96 (2H, м), 2,91 (3H, с), 3,15 (2H, шир.с), 3,49 (1H, шир.с), 3,66 (1H, шир.с), 4,32-4,42 (3H, м), 4,66 (1H, шир.с), 7,40 (2H, д, J=8,9Гц), 7,84 (2H, д, J=8,9Гц), 8,92 (1H, д, J=8,5Гц), 9,03 (1H, д, J=8,3Гц), 10,76 (1H, с), 11,32 (1H, шир.с).
МС (FAB) m/z: 462 (М+Н)+.
[Пример 282]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1R*,2R*)-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклопентил)этандиамида
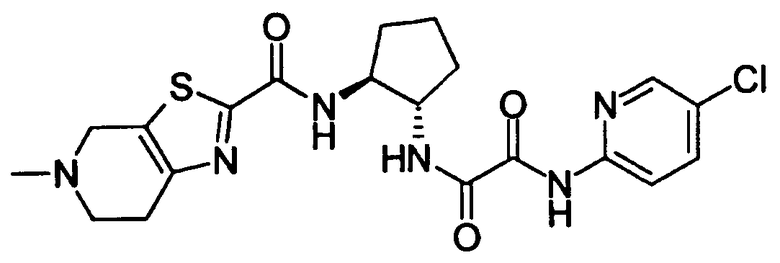
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 62, с соединением, полученным в ссылочном примере 266, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 208.
1Н-ЯМР (ДМСО-d6) δ: 1,71 (4H, шир.с), 1,96 (2H, шир.с), 2,90 (3H, с), 3,14 (1H, шир.с), 3,21 (1H, шир.с), 3,47 (1H, шир.с), 3,68 (1H, шир.с), 4,34-4,45 (3H, м), 4,66 (1H, шир.с), 7,99-8,06 (2H, м), 8,43-8,44 (1H, м), 8,94 (1H, д, J=8,3Гц), 9,20 (1H, д, J=8,5Гц), 10,20 (1H, шир.с), 11,78 (1,1H, шир.с).
МС (FAB) m/z: 463 (M+H)+.
[Пример 283]
N1-((1S,2R,4S)-4-[(Диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)-N2-(4-этинилфенил)этандиамид
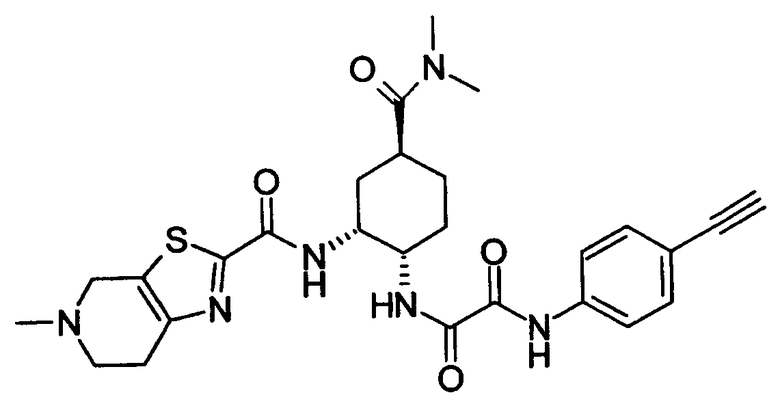
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 252, с соединением, полученным в ссылочном примере 397, подобно способу, описанному в примере 263.
1Н-ЯМР (CDCl3) δ: 1,67-2,16 (6H, м), 2,51 (3H, с), 2,76-2,91 (5H, м), 2,94 (3H, с), 3,04 (3H, с), 3,07 (1H, с), [3,65 (1H, д, J=15,5Гц), 3,73 (1H, д, J=15,5Гц) система AB], 4,09-4,16 (1H, м), 4,72-4,75 (1H, м), 7,42-7,46 (3H, м), 7,58 (2H, д, J=8,5Гц), 8,02 (1H, д, J=8,1Гц), 9,36 (1H, с).
МС (FAB) m/z: 537 (М+Н)+.
[Пример 284]
Гидрохлорид N1-(5-хлорпиразин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
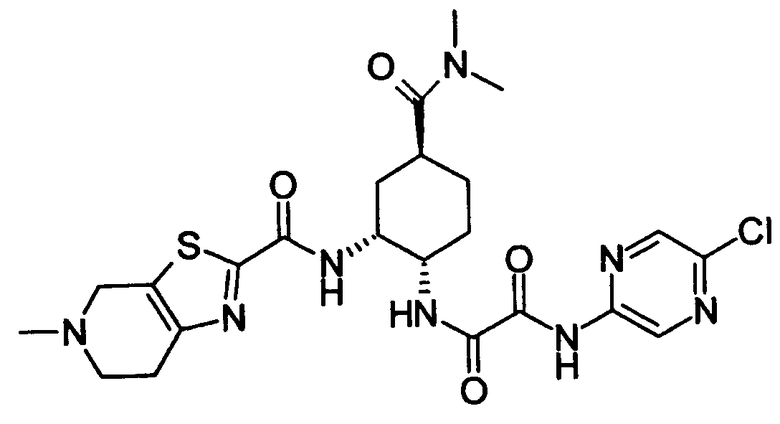
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 253, с соединением, полученным в ссылочном примере 399, подобно способу, описанному в ссылочном примере 97, и затем обработкой продукта конденсации хлористоводородной кислотой.
1Н-ЯМР (ДМСО-d6) δ: 1,44-1,52 (1H, м), 1,65-1,77 (3H, м), 2,00-2,10 (2H, м), 2,77 (3H, с), 2,91-2,97 (7H, м), 3,20 (2H, шир.с), 3,48 (1H, шир.с), 3,68 (1H, шир.с), 3,97-4,02 (1H, м), 4,40-4,46 (2H, м), 4,68 (1H, шир.с), 8,64 (1H, д, J=1,2Гц), 8,70 (1H, д, J=7,3Гц), 9,02 (1H, с), 9,21 (1H, шир.с), 10,91 (1H, шир.с), 11,50 (1H, шир.с).
МС (FAB) m/z: 549 (M+H)+.
[Пример 285]
Гидрохлорид N1-(4-хлор-3-нитрофенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
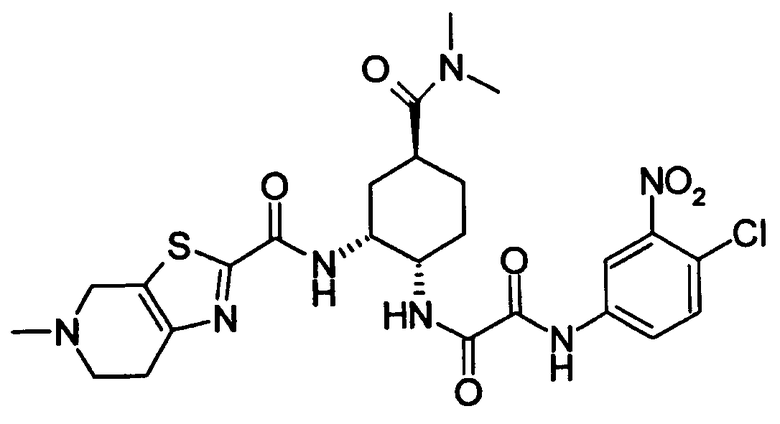
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 253, с соединением, полученным в ссылочном примере 400, подобно способу, описанному в ссылочном примере 97, и затем обработкой продукта конденсации хлористоводородной кислотой.
1Н-ЯМР (ДМСО-d6) δ: 1,44-1,53 (1H, м), 1,66-1,73 (3H, м), 1,97-2,07 (2H, м), 2,77 (3H, с), 2,89-3,05 (7H, м), 3,20 (2H, шир.с), 3,55 (2H, шир.с), 4,00 (1H, шир.с), 4,44 (1H, шир.с), 4,52 (2H, шир.с), 7,75 (1H, д, J=8,8Гц), 8,08 (1H, д, J=8,8Гц), 8,59 (1H, с), 8,71 (1H, д, J=7,3Гц), 9,07 (1H, д, J=8,0Гц), 11,24 (1H, с), 11,58 (1H, шир.с).
МС (FAB) m/z: 592 (М+Н)+.
[Пример 286]
Гидрохлорид N1-(4-хлор-2-нитрофенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
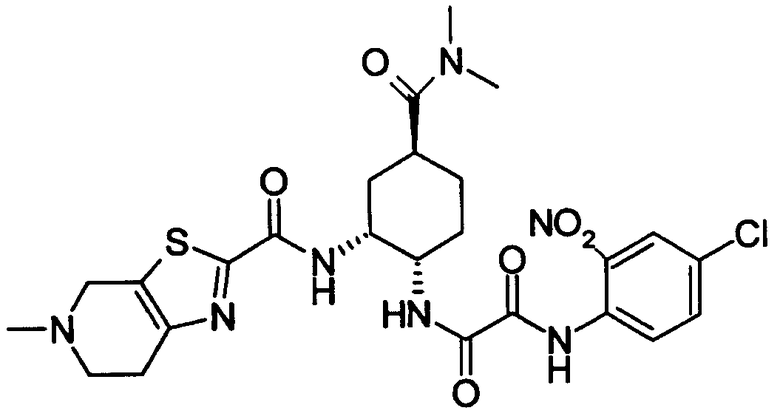
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 253, с соединением, полученным в ссылочном примере 401, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 208.
1Н-ЯМР (ДМСО-d6) δ: 1,46-1,54 (1H, м), 1,66-1,77 (3H, м), 2,03-2,10 (2H, м), 2,79 (3H, с), 2,90-2,93 (7H, м), 3,17-3,28 (2H, м), 3,49 (1H, шир.с), 3,68 (1H, шир.с), 3,99-4,04 (1H, м), 4,41 (1H, шир.с), 4,46 (1H, шир.с), 4,68 (1H, шир.с), 7,89 (1H, д, J=9,0Гц), 8,20-8,21 (2H, м), 8,73 (1H, д, J=6,4Гц), 9,28 (1H, шир.с), 11,49 (1H, шир.с), 11,56 (1H, с).
МС (FAB) m/z: 592 (М+Н)+.
[Пример 287]
Гидрохлорид N1-(3-амино-4-хлорфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
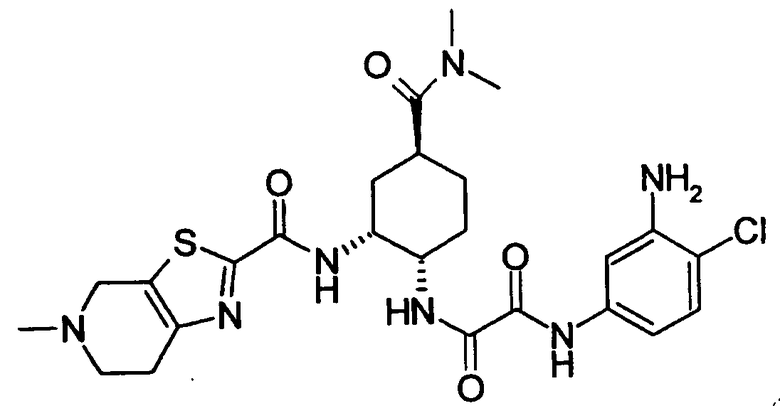
Соединение (236 мг), полученное в примере 285, растворяли в этаноле (25 мл), добавляли каталитическое количество никеля Ренея и смесь перемешивали при комнатной температуре в течение 17 часов в атмосфере водорода. Затем снова добавляли каталитическое количество никеля Ренея и смесь перемешивали еще 7 часов. Катализатор удаляли фильтрованием и растворитель отгоняли при пониженном давлении. Остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 23:2) с получением бледно-желтого твердого вещества (101 мг). Полученный продукт растворяли в метиленхлориде и 1N этанольном растворе (360 мкл) хлористоводородной кислоты. Растворитель отгоняли при пониженном давлении, к остатку добавляли небольшое количество метанола, добавляли по каплям диэтиловый эфир при облучении ультразвуковыми волнами и собирали образовавшийся осадок. Полученный продукт промывали диэтиловым эфиром с получением указанного в заголовке соединения (95 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,53 (1H, м), 1,66-1,73 (3H, м), 1,97-2,10 (2H, м), 2,78 (3H, с), 2,91-2,94 (7H, шир.с), 3,11-3,19 (1H, м), 3,29 (1H, шир.с), 3,48 (1H, шир.с), 3,69 (1H, шир.с), 3,95-4,02 (1H, м), 4,44 (2H, шир.с), 4,68, 4,72 (1H, каждый шир.с), 4,86 (2,5H, шир.с), 6,98 (1H, дд, J=8,5, 1,9Гц), 7,14 (1H, д, J=8,5Гц), 7,35, 7,38 (1H, каждый шир.с), 8,72-8,77 (1H, м), [8,91 (д, J=7,8Гц), 8,99 (д, J=8,5Гц), 1H], 10,45, 10,47 (1H, каждый шир.с), 11,74 (1H, шир.с).
МС (FAB) m/z: 562 (М+Н)+.
[Пример 288]
Гидрохлорид N1-(2-амино-4-хлорфенил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
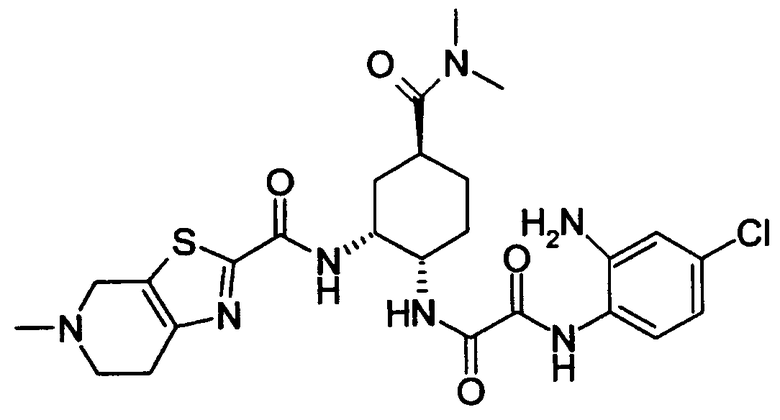
Указанное в заголовке соединение получали из соединения, полученного в примере 286, подобно способу, описанному в примере 287.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,77 (4H, м), 2,06-2,09 (2H, м), 2,78 (3H, с), 2,92 (7H, шир.с), 3,12-3,19 (1H, м), 3,26-3,28 (1H, м), 3,48 (1H, шир.с), 3,70 (1H, шир.с), 4,00-4,44 (5,7H, м), 4,70, 4,74 (1H, каждый шир.с), 6,63-6,66 (1H, м), 6,85 (1H, шир.с), 7,18-7,21 (1H, м), 8,77-8,81 (1H, м), [8,97 (д, J=7,8Гц), 9,06 (д, J=8,1Гц), 1H], 9,98 (1H, с), 11,60 (1H, шир.с).
МС (FAB) m/z: 562 (М+Н)+.
[Пример 289]
Гидрохлорид N1-(6-хлор-4-метилпиридин-3-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
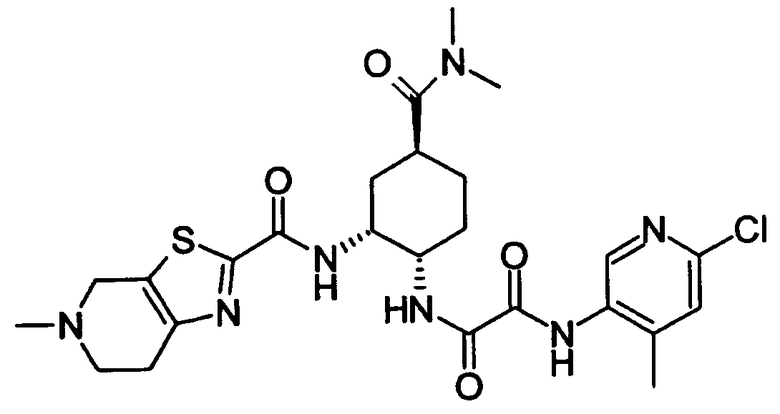
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 270, с соединением, полученным в ссылочном примере 402, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 199.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,54 (1H, м), 1,65-1,77 (3H, м), 2,02-2,08 (2H, м), 2,22 (3H, с), 2,79 (3H, с), 2,89-2,93 (7H, м), 3,19 (2H, шир.с), 3,54 (2H, шир.с), 3,99-4,04 (1H, м), 4,40-4,42 (1H, м), 4,50 (2H, шир.с), 7,49 (1H, с), 8,32 (1H, с), 8,75 (1H, д, J=7,1Гц), 9,09 (1H, д, J=7,3Гц), 10,48 (1H, с), 11,40 (0,9H, шир.с).
МС (FAB) m/z: 562 (M+H)+.
[Пример 290]
Гидрохлорид N-{(1R,2S,5S)-2-({[(Е)-2-(4-хлорфенил)диазенил]карбонил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
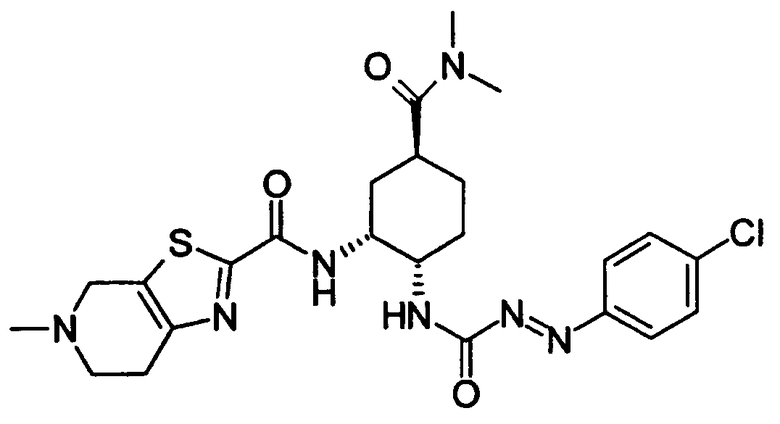
10% Палладий на углероде (200 мг) добавляли к раствору соединения (700 мг), полученного в ссылочном примере 252, в тетрагидрофуране (10 мл) и смесь перемешивали при комнатной температуре в течение 2 суток в атмосфере водорода, затем реакционную смесь фильтровали, соединение, полученное в ссылочном примере 405 (470 мг), добавляли к раствору амина, полученного концентрированием фильтрата, в формамиде (5,0 мл) и смесь перемешивали при 95°C в течение 18 часов. Реакционную смесь концентрировали и добавляли насыщенный водный раствор (50 мл) гидрокарбоната натрия, воду (50 мл) и метиленхлорид (30 мл) для разделения жидкостей, затем полученный водный слой экстрагировали метиленхлоридом (2 х 20 мл). Органические слои объединяли, сушили над безводным сульфатом натрия, концентрировали и очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 12:1). Полученный очищенный продукт обрабатывали 1N этанольным раствором хлористоводородной кислоты с получением указанного в заголовке соединения (100 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,60 (1H, м), 1,65-2,05 (5H, м), 2,80 (3H, с), 2,91 (3H, с), 2,99 (3H, с), 3,00-3,20 (2H, м), 3,20-3,32 (1H, м), 3,43 (1H, шир.с), 3,69 (1H, шир.с), 3,95 (1H, шир.с), 4,45 (1H, шир.с), 4,60-4,80 (2H, м), 7,68 (2H, д, J=8,7Гц), 7,83 (2H, д, J=8,7Гц), 8,41 (1H, шир.с), 8,68 (1H, д, J=7,6Гц), 11,40-11,80 (1H, шир.).
МС (ESI) m/z: 532 (М+Н)+.
[Пример 291]
Гидрохлорид N-{(1R,2S,5S)-2-({[2-(4-хлорфенил)гидразино]карбонил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
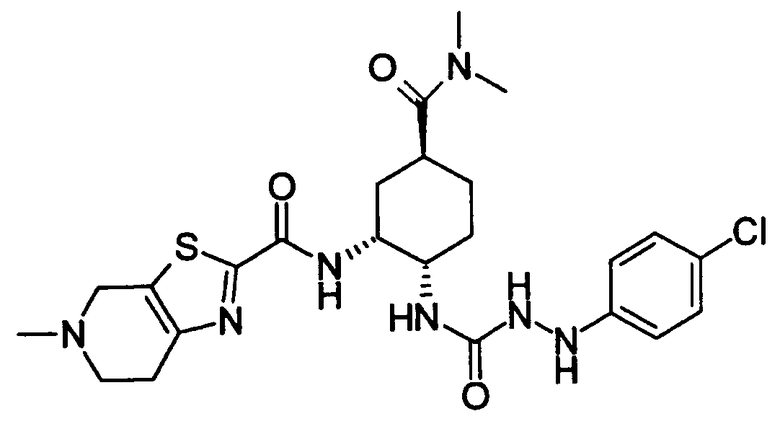
Указанное в заголовке соединение получали, заменяя условия реакции, описанной в примере 290, условиями, при которых перемешивание проводили при 40°C в течение 3 суток.
1Н-ЯМР (ДМСО-d6) δ: 1,30-1,50 (1H, м), 1,50-1,80 (3H, м), 1,80-1,97 (2H, м), 2,76 (3H, с), 2,80-3,05 (2H, м), 2,91 (6H, с), 3,05-3,30 (2H, м), 3,47 (2H, шир.с), 4,30-4,50 (2H, м), 4,72 (1H, т, J=12,8Гц), 6,40-6,60 (2H, м), 6,55-6,70 (2H, м), 6,95-7,20 (2H, м), 7,88 (1H, д, J=11,3Гц), 8,48-8,65 (1H, м), 11,48-11,80 (1H, шир.).
МС (ESI) m/z: 534 (М+Н)+.
[Пример 292]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
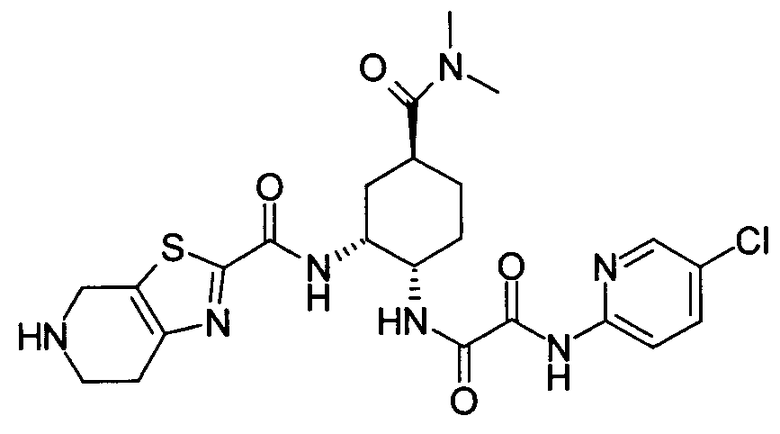
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 34, с соединением, полученным в ссылочном примере 420, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 17.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,55 (1H, м), 1,60-1,80 (3H, м), 1,95-2,10 (2H, м), 2,78 (3H, с), 2,85-3,00 (4H, м), 3,11 (2H, шир.с), 3,40-3,55 (2H, м), 3,95-4,07 (1H, м), 4,37-4,45 (1H, м), 4,48 (2H, шир.с), 8,00-8,01 (2H, м), 8,10 (1H, д, J=7,1Гц), 8,43-8,47 (1H, м), 9,16 (1H, д, J=7,8Гц), 9,43 (2H, шир.с), 10,27 (1H, с).
МС (FAB) m/z: 534 (М+Н)+.
[Пример 293]
Гидрохлорид N-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-[(1-гидроксициклопропил)карбонил]пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
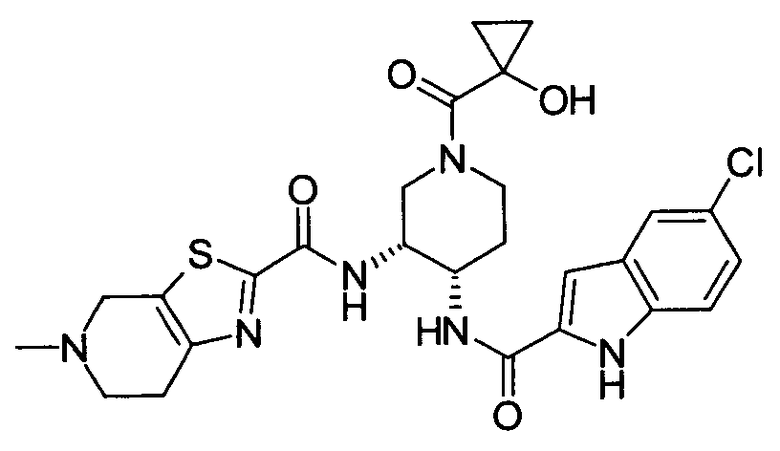
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 118, с 1-гидрокси-1-циклопропанкарбоновой кислотой и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 150.
1Н-ЯМР (ДМСО-d6) δ: 0,60-0,90 (3H, шир.), 0,92-1,03 (1H, м), 1,71-1,84 (1H, м), 1,85-2,03 (1H, м), 2,91 (3H, с), 3,00-3,80 (7H, м), 4,05-4,80 (5H, м), 6,28-6,42 (1H, шир.), 7,09 (1H, с), 7,18 (1H, дд, J=8,8, 1,5Гц), 7,42 (1H, д, J=8,8Гц), 7,70 (1H, д, J=1,5Гц), 8,14-8,29 (1H, шир.), 8,41 (1H, шир.д, J=7,6Гц), 11,83 (1H, с).
МС (ESI) m/z: 557 (М+Н)+.
[Пример 294]
Гидрохлорид N-((3R*,4S*)-4-{[(5-хлориндол-2-ил)карбонил]амино}-1-[(1-метоксициклопропил)карбонил]пиперидин-3-ил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
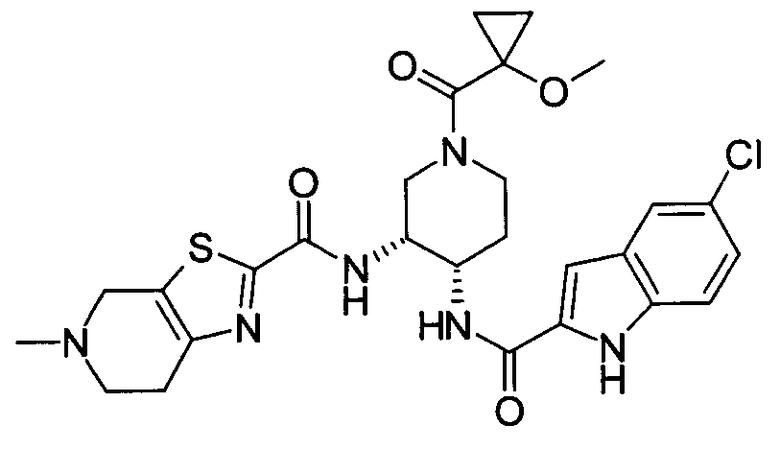
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 118, с соединением, полученным в ссылочном примере 409, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 150.
1Н-ЯМР (ДМСО-d6) δ: 0,65-1,05 (4H, м), 1,74-1,88 (1H, м), 1,92-2,10 (1H, м), 2,91 (3H, с), 3,00-3,80 (10H, м), 4,05-4,83 (6H, м), 7,08 (1H, с), 7,18 (1H, дд, J=8,6, 2,0Гц), 7,42 (1H, д, J=8,6Гц), 7,71 (1H, д, J=2,0Гц), 8,08-8,30 (1H, шир.), 8,41 (1H, шир.д, J=7,8Гц), 10,60-10,80 (0,5H, шир.), 10,85-11,05 (0,5H, шир.), 11,84 (1H, с).
[Пример 295]
Гидрохлорид 7-хлор-N-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)-3-изохинолинкарбоксамида
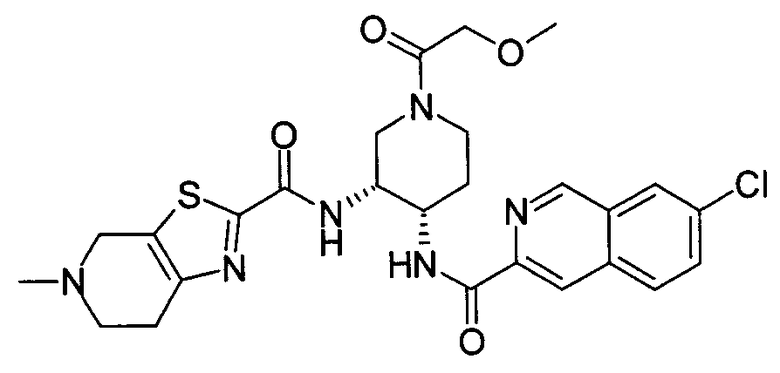
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 410, 4N диоксановым раствором хлористоводородной кислоты для снятия у него защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,60-1,80 (1H, м), 2,13-2,38 (1H, м), 2,90 (3H, с), 3,00-3,87 (10H, м), 3,89-4,10 (2H, м), 4,15-4,58 (4H, м), 4,60-4,78 (1H, м), 7,89 (1H, д, J=8,8Гц), 8,25 (1H, д, J=8,8Гц), 8,37 (1H, с), 8,61 (1H, с), 8,70-8,95 (1H, м), 9,05-9,29 (1H, м), 9,36 (1H, с), 11,20-11,40 (0,5H, шир.), 11,45-11,65 (0,5H, шир.).
МС (ESI) m/z: 557 (М+Н)+.
[Пример 296]
Гидрохлорид N1-(4-хлор-3-фторфенил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамида
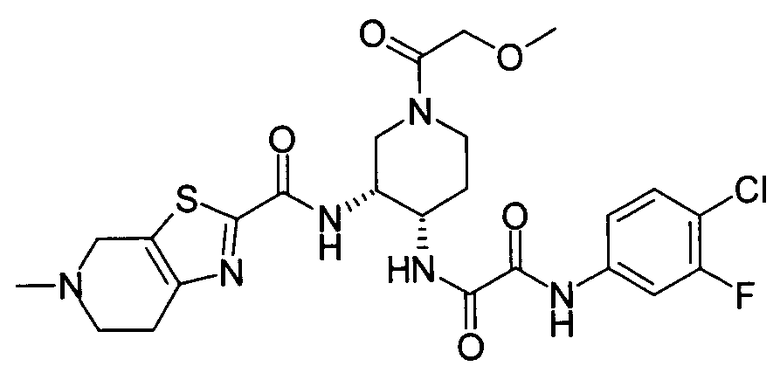
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 411, 4N диоксановым раствором хлористоводородной кислоты для снятия у него защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,60-1,72 (1H, м), 1,98-2,21 (1H, м), 2,91 (3H, с), 3,00-3,52 (9H, м), 3,56-4,05 (3H, м), 4,08-4,50 (4H, м), 4,60-4,78 (1H, шир.), 7,56 (1H, т, J=8,8Гц), 7,70 (1H, д, J=9,0Гц), 7,91 (1H, дд, J=8,8, 2,3Гц), 8,50-8,72 (1H, м), 9,15-9,35 (1H, м), 11,02 (1H, с), 11,15-11,33 (0,5H, шир.), 11,35-11,50 (0,5H, шир.).
МС (FAB) m/z: 567 (M+H)+.
[Пример 297]
Гидрохлорид N1-(5-хлор-2-тиенил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамида
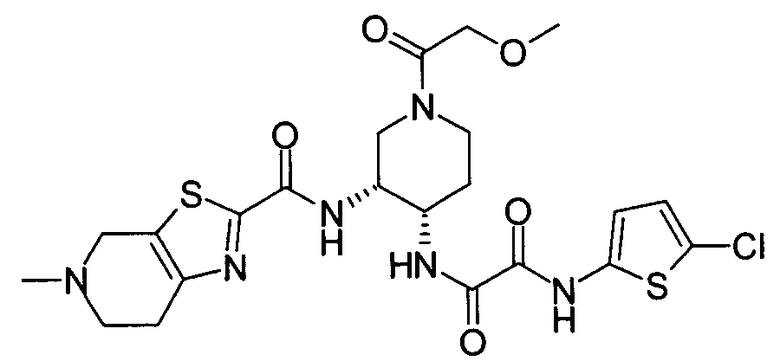
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 412, 4N диоксановым раствором хлористоводородной кислоты для снятия у него защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,60-1,73 (1H, м), 1,96-2,19 (1H, м), 2,91 (3H, с), 3,04-3,54 (9H, м), 3,60-4,05 (3H, м), 4,07-4,34 (3H, м), 4,35-4,54 (1H, шир.), 4,60-4,80 (1H, шир.), 6,89 (1H, д, J=4,2Гц), 6,93 (1H, д, J=4,2Гц), 8,48-8,70 (1H, м), 9,18-9,40 (1H, м), 12,31 (1H, с).
МС (ESI) m/z: 555 (M+H)+.
[Пример 298]
Гидрохлорид N-{(1R,2S,5S)-2-{[2-(4-хлорфенокси)ацетил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
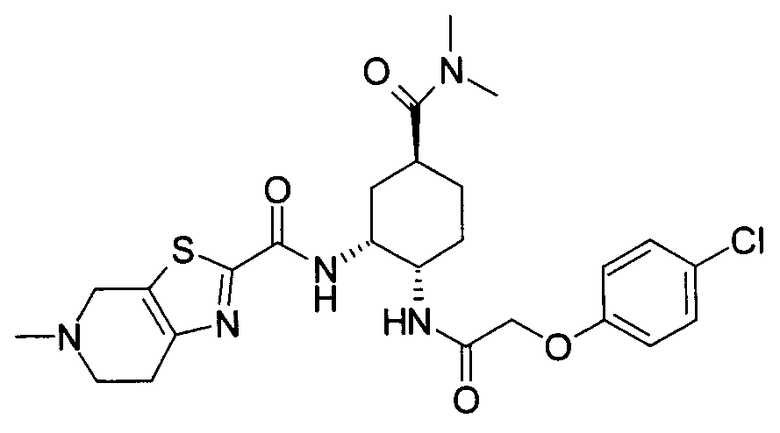
Указанное в заголовке соединение получали восстановлением соединения, полученного в ссылочном примере 252, конденсацией продукта восстановления с п-хлорфеноксиуксусной кислотой и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 223.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,47 (1H, м), 1,55-1,90 (5H, м), 2,77 (3H, с), 2,92 (3H, с), 2,96 (3H, с), 2,98-3,10 (1H, м), 3,10-3,80 (3H, м), 3,85-3,95 (1H, м), 4,35-4,50 (4H, м), 4,50-4,80 (1H, шир.), 6,85 (2H, д, J=8,5Гц), 7,15-7,35 (1H, шир.), 7,88-8,03 (1H, шир.), 8,46 (1H, д, J=8,8Гц), 11,30-11,65 (1H, шир.).
МС (FAB) m/z: 534 (М+Н)+.
[Пример 299]
Гидрохлорид 7-хлор-N-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5Н-пирроло[3,4-d]тиазол-2-ил)карбонил]амино}циклогексил)-3-изохинолинкарбоксамида
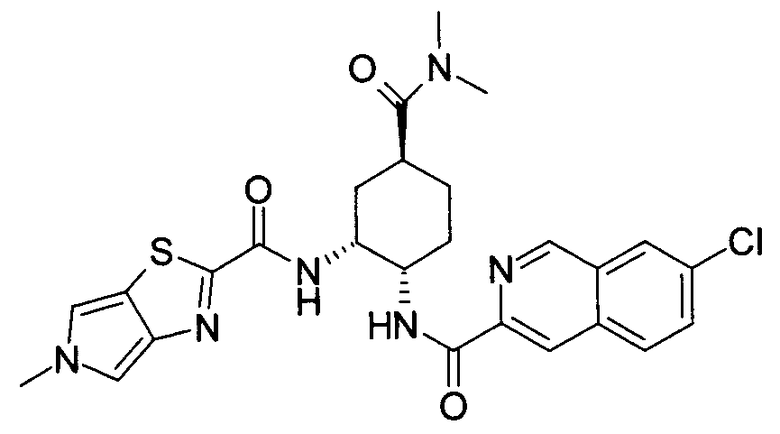
Указанное в заголовке соединение получали конденсацией литиевой соли карбоновой кислоты, полученной гидролизом соединения, полученного в ссылочном примере 413, с соединением, полученным снятием защиты у соединения, полученного в ссылочном примере 146, обработкой кислотой и обработкой продукта конденсации хлористоводородной кислотой.
1Н-ЯМР (ДМСО-d6) δ: 1,00-1,11 (2H, м), 1,45-1,60 (1H, м), 1,65-1,85 (1H, м), 1,95-2,06 (1H, м), 2,10-2,24 (1H, м), 2,78 (3H, с), 2,87-3,02 (1H, м), 2,94 (3H, с), 3,88 (3H, с), 4,16-4,27 (1H, м), 4,45-4,56 (1H, м), 7,03 (1H, с), 7,55 (1H, с), 7,87 (1H, шир.д, J=8,3Гц), 8,24 (1H, шир.д, J=8,8Гц), 8,33 (1H, с), 8,59 (1H, с), 8,85 (1H, шир.д, J=7,6Гц), 9,01 (1H, шир.д, J=7,8Гц), 9,28 (1H, с).
МС (ESI) m/z: 539 (M+H)+.
[Пример 300]
Гидрохлорид N-{(1R,2S,5S)-2-{[(6-хлор-4-оксо-4Н-хромен-2-ил)карбонил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
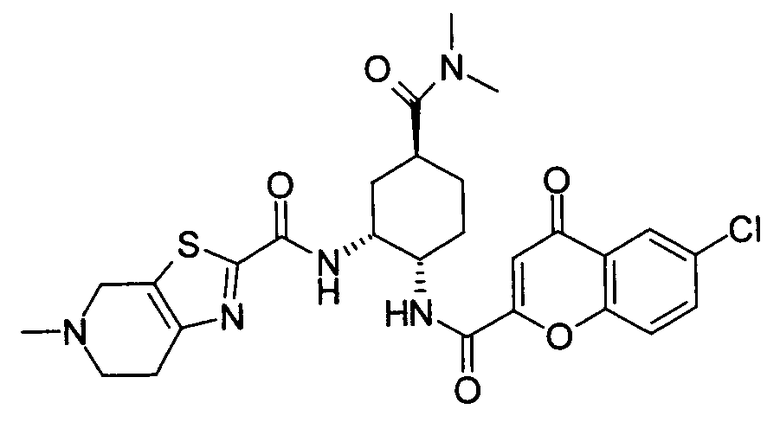
Указанное в заголовке соединение получали конденсацией соединения, полученного обработкой соединения, полученного в ссылочном примере 417, 4N диоксановым раствором хлористоводородной кислоты, с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,40-1,53 (1H, м), 1,67-2,04 (5H, м), 2,40-2,53 (1H, м), 2,80 (3H, с), 2,92 (3H, с), 3,01 (3H, с), 3,09-3,22 (3H, м), 3,66-3,77 (1H, м), 4,01-4,10 (1H, м), 4,34-4,49 (1H, м), 4,58-4,76 (2H, м), 6,80 (1H, д, J=4,9Гц), 7,59-7,70 (1H, м), 7,90-8,00 (1H, м), 7,96 (1H, с), 8,52-8,60 (1H, м), 8,80-8,90 (1H, м), 11,10-11,25 (0,5H, шир.), 11,40-11,55 (0,5H, шир.).
МС (ESI) m/z: 572 (M+H)+.
[Пример 301]
Гидрохлорид 7-хлор-N-((3R,4S)-1-(2-метоксиацетил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)-3-циннолинкарбоксамида
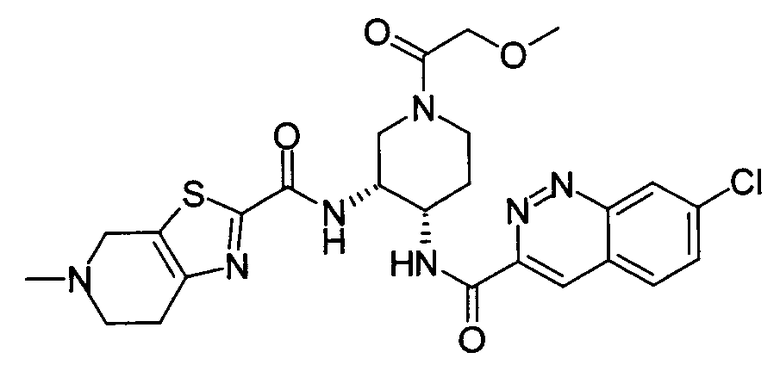
Указанное в заголовке соединение получали конденсацией соединения, полученного обработкой соединения, полученного в ссылочном примере 418, 4N диоксановым раствором хлористоводородной кислоты, с соединением, полученным в ссылочном примере 10, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,70-1,80 (1H, м), 1,85-2,05 (1H, м), 2,90 (3H, с), 3,00-3,20 (2H, м), 3,16 (3H, с), 3,22-3,82 (7H, м), 3,88-4,80 (5H, м), 7,09 (1H, д, J=9,0Гц), 7,17 (1H, дд, J=8,8, 1,9Гц), 7,42 (1H, д, J=8,8Гц), 7,70 (1H, д, J=1,9Гц), 8,29 (1H, шир.с), 8,40-8,50 (1H, м), 11,20-11,50 (1H, шир.м), 11,85 (1H, с).
МС (ESI) m/z: 558 (М+Н)+.
[Пример 302]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиено[3,2-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
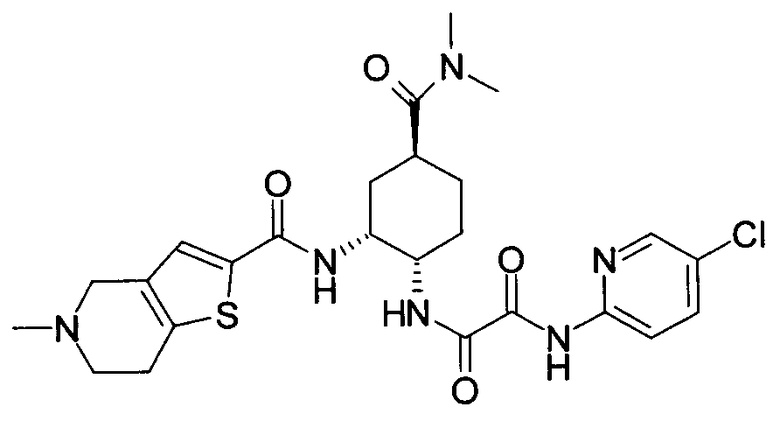
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 421, обработкой хлористоводородной кислотой, метилированием соединения со снятой защитой подобно способу, описанному в примере 18, и обработкой его хлористоводородной кислотой.
1Н-ЯМР (ДМСО-d6) δ: 1,42-1,58 (1H, м), 1,59-1,80 (3H, м), 1,83-1,95 (1H, м), 1,97-2,10 (1H, м), 2,78 (3H, с), 2,89 (3H, с), 2,96 (3H, с), 3,00-3,10 (1H, м), 3,10-3,20 (2H, м), 3,45-3,80 (1H, м), 3,90-4,00 (2H, м), 4,00-4,50 (3H, м), 7,77 (1H, с), 7,95-8,05 (3H, м), 8,44 (1H, т, J=1,6Гц), 8,90 (1H, д, J=8,6Гц), 10,25 (1H, с), 11,12 (1H, шир.с).
МС (ESI) m/z: 547 (М+Н)+.
[Пример 303]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-изопропил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
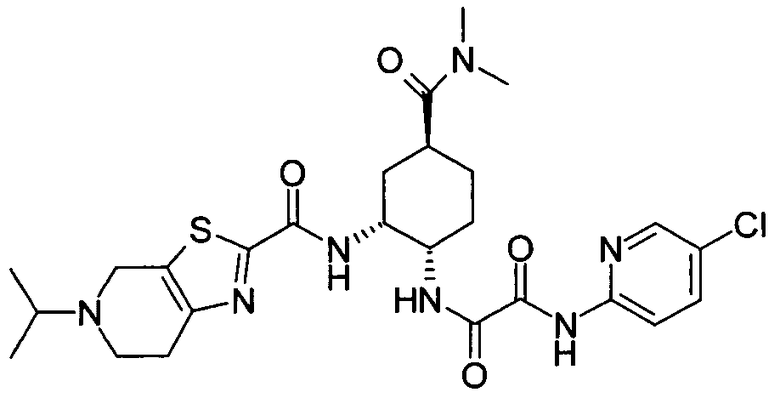
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 418, с соединением, полученным в ссылочном примере 420, и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,30-1,40 (6H, м), 1,38-1,58 (1H, м), 1,59-1,82 (3H, м), 1,95-2,13 (2H, м), 2,40-2,65 (1H, м), 2,49 (3H, с), 2,87-3,55 (4H, м), 2,49 (3H, с), 3,60-3,82 (2H, м), 3,93-4,04 (1H, м), 4,37-4,55 (2H, м), 4,55-4,72 (1H, м), 7,94-8,10 (2H, м), 8,43 (1H, с), 8,64-8,77 (1H, м), 9,12 (1/2H, д, J=7,8Гц), 9,24 (1/2H, д, J=7,8Гц), 10,22 (1/2H, с), 10,26 (1/2H, с), 11,25 (1/2H, шир.с), 11,44 (1/2H, шир.с).
МС (FAB) m/z: 578 (М+Н)+.
[Пример 304]
Гидрохлорид N-((1R,2S,5S)-5-[(диметиламино)карбонил]-2-{[2-(4-фторанилино)-2-оксоэтантиоил]амино}циклогексил)-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
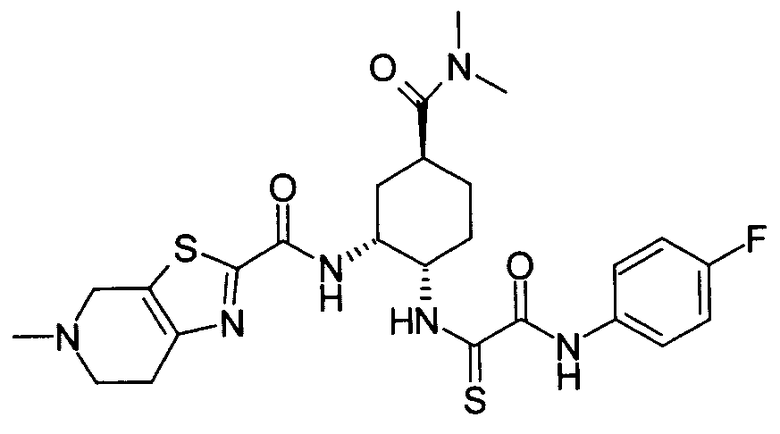
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 424, хлористоводородной кислотой для снятия защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем повторной обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,60-1,80 (3H, м), 2,00-2,10 (1H, м), 2,20-2,35 (1H, м), 2,79 (3H, с), 2,93 (3H, с), 2,95 (3H, с), 2,95-3,10 (1H, м), 3,10-3,30 (2H, м), 3,40-3,60 (1H, м), 3,60-3,80 (1H, м), 4,35-4,50 (1H, м), 4,50-4,60 (1H, м), 4,60-4,80 (2H, м), 7,20 (2H, т, J=8,8Гц), 7,77 (2H, дд, J=9,0, 5,1Гц), 8,80 (1H, шир.), 10,42 (1H, с), 10,93 (1H, шир.), 11,28 (1H, шир.).
МС (ESI) m/z: 547 (М+Н)+.
[Пример 305]
Гидрохлорид N-[(1R,2S,5S)-5-[(диметиламино)карбонил]-2-{[2-[(5-фторпиридин-2-ил)амино]-2-оксоэтантиоил}амино)циклогексил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
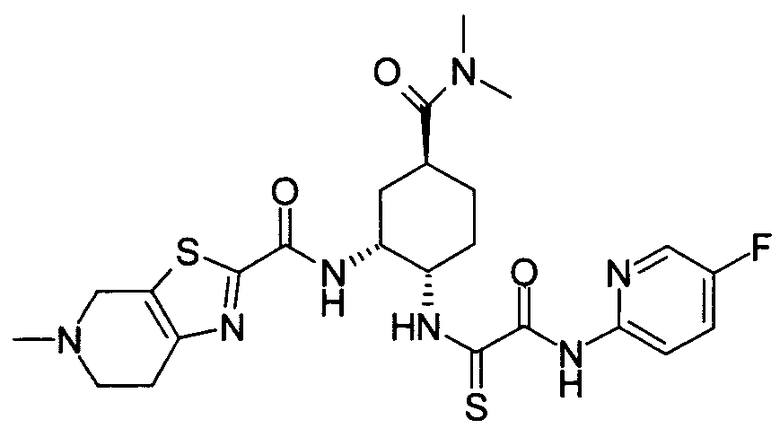
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 427, хлористоводородной кислотой для снятия защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем повторной обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,43-1,57 (1H, м), 1,64-1,87 (3H, м), 2,00 (1H, шир.с), 2,17-2,34 (1H, м), 2,78 (3H, с), 2,90 (3H, с), 2,95 (3H, с), 2,95-3,10 (1H, м), 3,10-3,30 (2H, м), 3,40-3,60 (1H, м), 3,68 (1H, шир.с), 4,44 (1H, шир.с), 4,45-4,56 (1H, м), 4,60-4,73 (2H, м), 7,80-7,90 (1H, м), 8,08 (1H, дд, J=9,1, 3,9Гц), 8,41 (1H, д, J=2,9Гц), 8,79 (1H, д, J=6,6Гц), 10,49 (1H, с), 11,07 (1H, шир.с), 11,69 (1H, шир.).
МС (ESI) m/z: 548 (М+Н)+.
[Пример 306]
N-{(1R,2S,5S)-2-({2-[(5-Хлорпиридин-2-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-5Н-пирроло[3,4-d]тиазол-2-карбоксамид
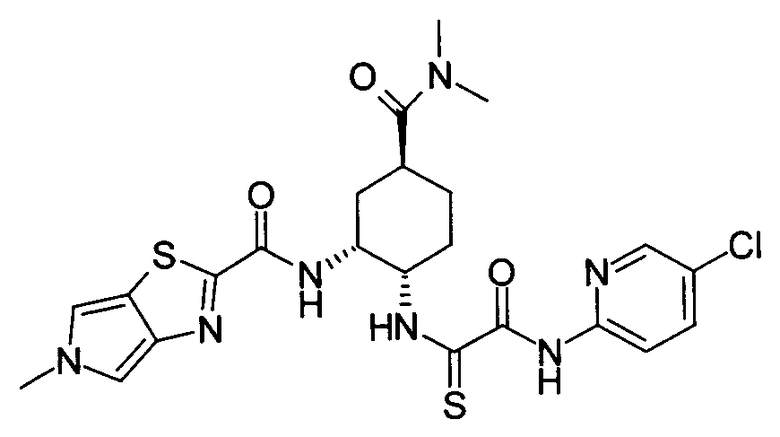
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 428, хлористоводородной кислотой для снятия у него защиты и затем конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 293, подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,58 (1H, м), 1,63-1,73 (2H, м), 1,73-1,87 (2H, м), 2,00-2,10 (1H, м), 2,20-2,35 (1H, м), 2,79 (3H, с), 2,95 (3H, с), 2,96-3,10 (1H, м), 3,89 (3H, с), 4,48-4,58 (1H, м), 4,60-4,70 (1H, м), 7,05 (1H, д, J=1,7Гц), 7,55 (1H, д, J=1,7Гц), 8,00 (1H, дд, J=8,9, 2,4Гц), 8,05 (1H, д, J=8,9Гц), 8,44 (1H, д, J=2,4Гц), 8,71 (1H, д, J=7,3Гц), 10,57 (1H, с), 11,13 (1H, д, J=7,8Гц).
МС (FAB) m/z: 548 (М+Н)+.
[Пример 307]
Гидрохлорид N-{(1R,2S,5S)-2-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-5,6-дигидро-4Н-пирроло[3,4-d]тиазол-2-карбоксамида
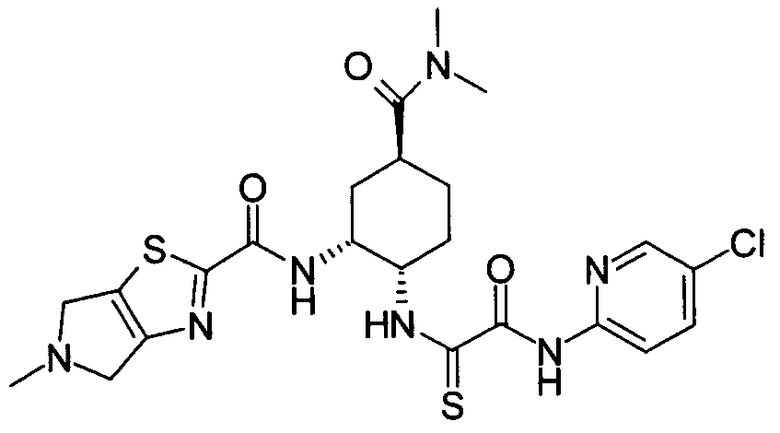
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 428, хлористоводородной кислотой для снятия у него защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 293, в атмосфере аргона и затем обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,42-1,58 (1H, м), 1,65-1,87 (3H, м), 1,97-2,10 (1H, м), 2,17-2,30 (1H, м), 2,80 (3H, с), 2,96 (3H, с), 2,98-3,10 (1H, м), 3,07 (3H, с), 4,30-5,00 (6H, м), 8,00-8,10 (1H, м), 8,46 (1H, д, J=2,4Гц), 8,79 (1H, т, J=7,3Гц), 10,54 (1H, с), 11,04 (1H, д, J=7,8Гц), 12,24 (1H, шир.с).
МС (ESI) m/z: 550 (М+Н)+.
[Пример 308]
N1-(5-Хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-({[6-(диметиламино)-4,5,6,7-тетрагидробензотиазол-2-ил]карбонил}амино)циклогексил]этандиамид
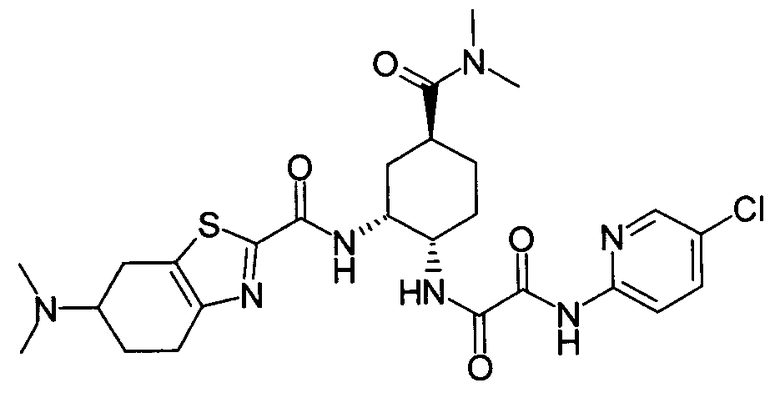
Указанное в заголовке соединение получали снятием защиты у соединения, полученного в ссылочном примере 431, хлористоводородной кислотой, метилированием соединения со снятой защитой подобно способу, описанному в примере 18, и обработкой его хлористоводородной кислотой.
1Н-ЯМР (ДМСО-d6) δ: 1,42-1,58 (1H, м), 1,59-1,80 (3H, м), 1,90-2,12 (3H, м), 2,30-2,45 (1H, м), 2,70-3,00 (11H, м), 2,92 (3H, с), 3,00-3,20 (2H, м), 3,25-3,45 (1H, м), 3,63-3,80 (1H, м), 3,88-4,02 (1H, м), 4,35-4,47 (1H, м), 8,02 (1H, с), 8,42-8,55 (1H, м), 8,60-8,68 (1H, м), 8,93 (1H, дд, J=14,5, 8,2Гц), 9,19 (1H, дд, J=17,7, 8,2Гц), 10,28 (1H, с), 10,91 (1H, шир.с).
МС (ESI) m/z: 576 (М+Н)+.
[Пример 309]
Гидрохлорид N-{(1R,2S,5S)-2-[({[(4-хлорфенил)сульфонил]амино}карбонил)амино]-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
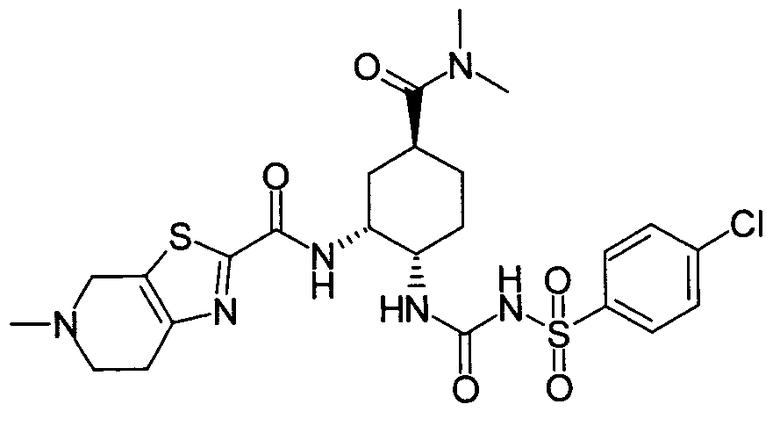
4-Хлорфенилсульфонилизоцианат (148 мкл) добавляли к раствору соединения (328,0 мг), полученного в ссылочном примере 253, в метиленхлориде (10 мл) и смесь перемешивали при комнатной температуре в течение 24 часов. Растворитель отгоняли при пониженном давлении и остаток очищали препаративной тонкослойной колоночной хроматографией на силикагеле (метиленхлорид:метанол = 9:1). Полученный таким образом продукт растворяли в этаноле (2 мл) и метиленхлориде (2 мл), добавляли 1N этанольный раствор (0,25 мл) хлористоводородной кислоты и смесь перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь концентрировали при пониженном давлении и остаток отверждали диэтиловым эфиром с получением указанного в заголовке соединения (104,3 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,25-1,45 (1H, м), 1,45-1,80 (5H, м), 2,76 (3H, с), 2,94 (3H, с), 2,97 (3H, с), 3,00-3,80 (6H, м), 4,35-4,85 (3H, м), 6,53 (1H, шир.с), 7,66 (2H, д, J=8,5Гц), 7,86 (2H, д, J=8,5Гц), 8,50-8,82 (1H, м), 10,64 (1H, шир.с), 11,10-11,80 (1H, шир.).
МС (ESI) m/z: 583 (М+Н)+.
[Пример 310]
N1-(5-Хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамид
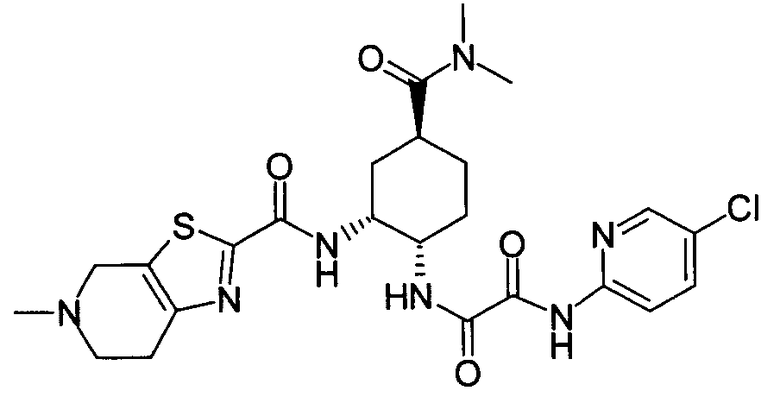
Указанное в заголовке соединение получали из соединения, полученного в ссылочном примере 435, и соединения, полученного в ссылочном примере 10, подобно способу примера 2.
1Н-ЯМР (CDCl3) δ: 1,60-1,98 (3H, м), 2,00-2,16 (3H, м), 2,52 (3H, с), 2,78-2,90 (3H, м), 2,92-2,98 (2H, м), 2,95 (3H, с), 3,06 (3H, с), 3,69 (1H, д, J=15,4Гц), 3,75 (1H, д, J=15,4Гц), 4,07-4,15 (1H, м), 4,66-4,72 (1H, м), 7,40 (1H, д, J=8,8, 0,6Гц), 7,68 (1H, дд, J=8,8, 2,4Гц), 8,03 (1H, д, J=7,8Гц), 8,16 (1H, дд, J=8,8, 0,6Гц), 8,30 (1H, дд, J=2,4, 0,6Гц), 9,72 (1H, с).
МС (ESI) m/z: 548 (М+Н)+.
[Пример 311]
Моногидрат п-толуолсульфоната N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
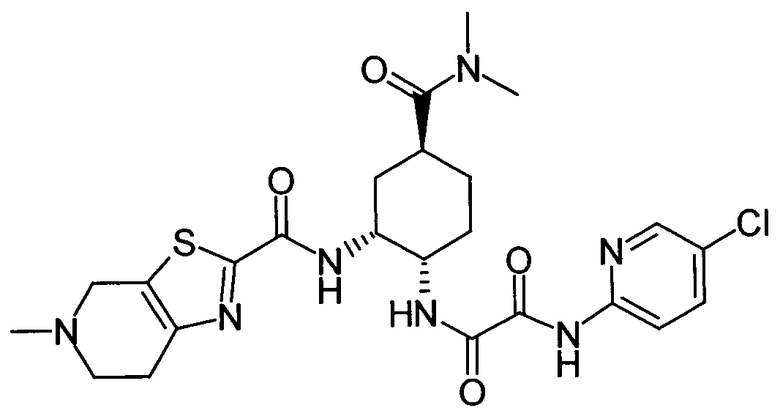
Соединение (6,2 г), полученное в примере 310, растворяли в метиленхлориде (120 мл), к раствору добавляли 1 моль/л этанольный раствор (11,28 мл) п-толуолсульфоновой кислоты и отгоняли растворитель. К остатку добавляли этанол (95 мл), содержащий 15% воды, и смесь перемешивали при 60°C до растворения. Затем раствор охлаждали до комнатной температуры и перемешивали в течение суток. Выпавшие в осадок кристаллы отфильтровывали, промывали этанолом и сушили при комнатной температуре в течение 2 часов при пониженном давлении с получением указанного в заголовке соединения (7,4 г).
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,54 (1H, м), 1,66-1,78 (3H, м), 2,03-2,10 (2H, м), 2,28 (3H, с), 2,79 (3H, с), 2,91-3,02 (1H, м), 2,93 (3H, с), 2,99 (3H, с), 3,13-3,24 (2H, м), 3,46-3,82 (2H, м), 3,98-4,04 (1H, м), 4,43-4,80 (3H, м), 7,11 (2H, д, J=7,8Гц), 7,46 (2H, д, J=8,2Гц), 8,01 (2H, д, J=1,8Гц), 8,46 (1H, т, J=1,8Гц), 8,75 (1H, д, J=6,9Гц), 9,10-9,28 (1H, шир.), 10,18 (1H, шир.), 10,29 (1H, с).
МС (ESI) m/z: 548 (M+H)+.
Элементный анализ: C24H30ClN7O4S·C7H8O3S·H2O.
Вычислено: С 50,43; Н 5,46; N 13,28; Cl 4,80; S 8,69.
Найдено: С 50,25; Н 5,36; N 13,32; Cl 4,93; S 8,79.
Т.пл. (разложение) 245˜248°C.
[Пример 312]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(метиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
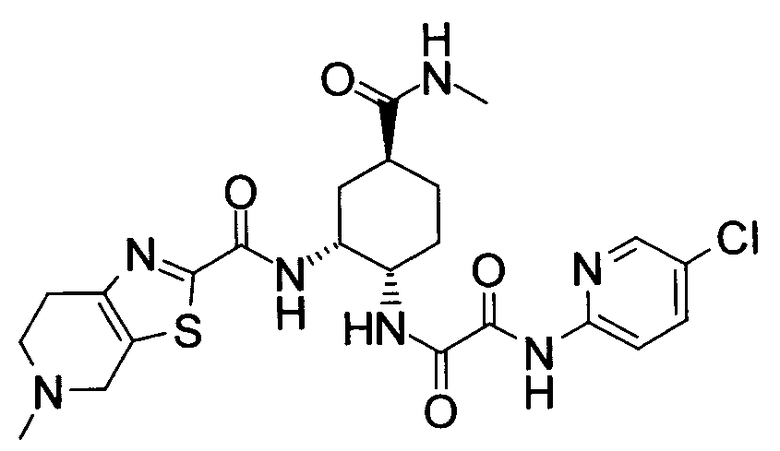
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 437, хлористоводородной кислотой для снятия у него защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем повторной обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,48-1,61 (1H, м), 1,61-1,74 (2H, м), 1,74-1,82 (1H, м), 1,98-2,12 (2H, м), 2,29-2,38 (1H, м), 2,53 (3H, д, J=4,2Гц), 2,92 (3H, с), 3,10-3,40 (4H, шир.), 3,40-3,80 (1H, шир.), 3,97-4,05 (1H, м), 4,28-4,34 (1H, м), 4,34-4,80 (1H, шир.), 7,70-7,78 (1H, м), 7,97-8,07 (2H, м), 8,43-8,50 (1H, м), 8,49 (1H, шир.с), 9,27 (1H, д, J=7,8Гц), 10,26 (1H, шир.с), 11,48 (1H, шир.с).
МС (ESI) m/z: 534 [(M+H)+, Cl35], 535 [(M+H)+, Cl37].
[Пример 313]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((3R,4S)-1-(2-метоксиацетил)-3-{[4-(пиридин-4-ил)бензоил]амино}пиперидин-4-ил)этандиамида
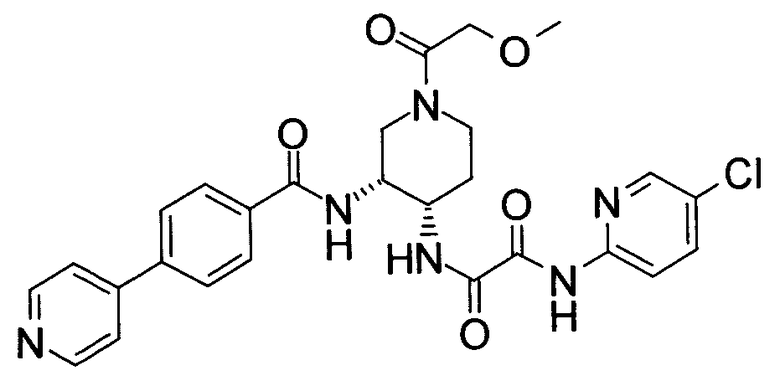
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 368, 4N диоксановым раствором хлористоводородной кислоты для снятия у него защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 237, и затем повторной обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,62-1,75 (1H, м), 2,00-2,20 (1H, м), 2,80-4,40 (11H, м), 7,90-8,00 (4H, м), 8,05-8,13 (2H, м), 8,14-8,43 (3H, м), 8,40-8,45 (1H, м), 8,87-9,04 (3H, м), 10,20-10,50 (2H, шир.).
МС (FAB) m/z: 551 [(M+H)+, Cl35], 553 [(M+H)+, Cl37].
[Пример 314]
Гидрохлорид N-{(1R,2S,5S)-5-[(диметиламино)карбонил]-2-({2-[(5-метилпиридин-2-ил)амино]-2-оксоэтантиоил}амино)циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
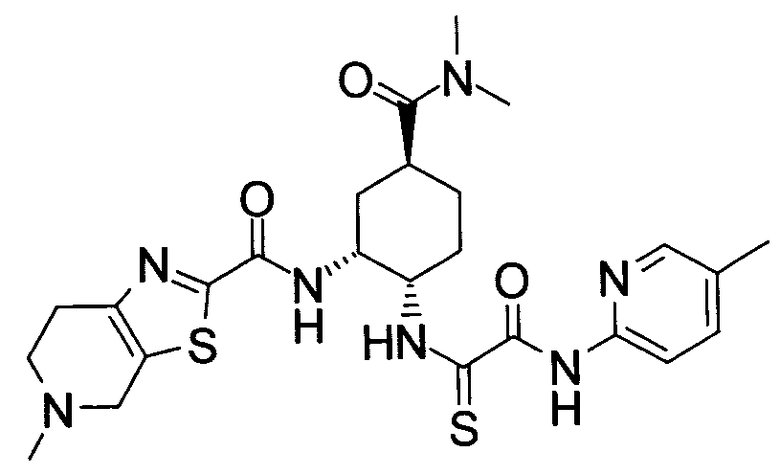
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 440, хлористоводородной кислотой для снятия защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем повторной обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,45-1,60 (1H, м), 1,65-1,90 (3H, м), 2,00-2,10 (1H, м), 2,20-2,40 (1H, м), 2,28 (3H, с), 2,80 (3H, с), 2,91 (3H, с), 2,95-3,10 (1H, м), 2,96 (3H, с), 3,15-3,30 (1H, м), 3,32 (2H, с), 3,50-3,80 (1H, м), 4,45-4,60 (2H, м), 4,60-4,80 (2H, м), 7,72 (1H, д, J=8,5Гц), 7,97 (1H, д, J=8,5Гц), 8,23 (1H, с), 8,83 (1H, д, J=7,3Гц), 10,38 (1H, с), 11,06 (1H, д, J=7,6Гц), 11,49 (1H, шир.с).
МС (ESI) m/z: 544 (M+H)+.
[Пример 315]
Гидрохлорид N-[(3R,4S)-4-{[2-(4-хлоранилино)-2-оксоэтантиоил]амино}-1-(2-метоксиацетил)пиперидин-3-ил]-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
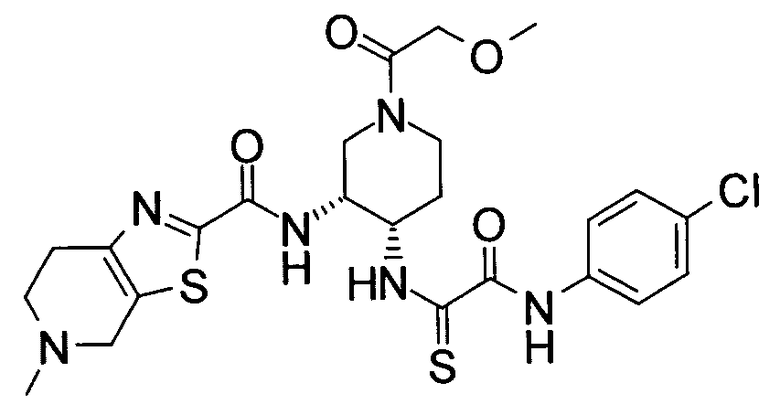
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 441, хлористоводородной кислотой для снятия защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем повторной обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,71-1,82 (1H, м), 2,18-2,44 (1H, м), 2,89 (3H, с), 3,00-4,85 (17H, м), 7,41 (2H, д, J=8,8Гц), 7,77 (2H, д, J=8,8Гц), 8,48-8,73 (1H, м), 10,48 (1H, шир.с), 10,90-11,06 (1H, м), 11,45-11,90 (1H, шир.).
МС (ESI) m/z: 565 [(M+H)+, Cl35], 567 [(M+H)+, Cl37].
[Пример 316]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карботиоил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексил)этандиамида
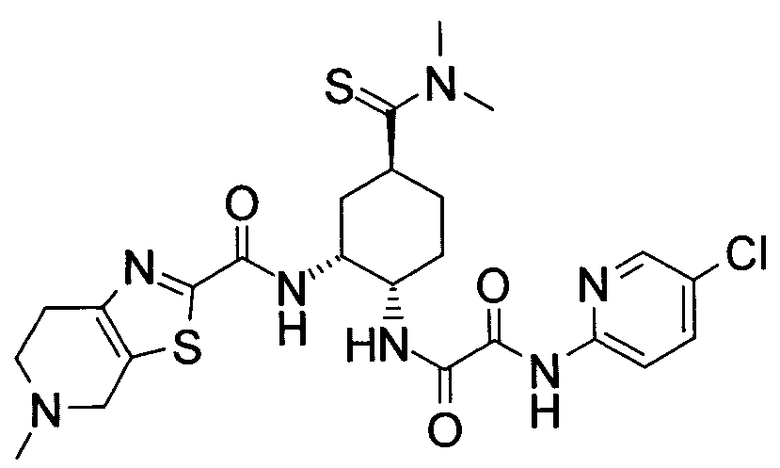
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 445, с соединением, полученным в ссылочном примере 10, и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 3.
1Н-ЯМР (ДМСО-d6) δ: 1,66-2,15 (6H, м), 2,93 (3H, с), 3,15-3,40 (9H, м), 3,49 (1H, шир.с), 3,71 (1H, шир.с), 3,97-4,01 (1H, м), 4,42 (2H, шир.с), 4,70 (1H, шир.с), 8,01 (2H, шир.с), 8,46 (1H, шир.с), 8,78 (1H, д, J=6,8Гц), 9,24 (1H, шир.с), 10,28 (1H, с), 11,29 (1H, шир.с).
МС (FAB) m/z: 564 [(M+H)+, Cl35], 566 [(M+H)+, Cl37].
[Пример 317]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-((3R,4S)-1-(2-метоксиэтантиоил)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}пиперидин-4-ил)этандиамида
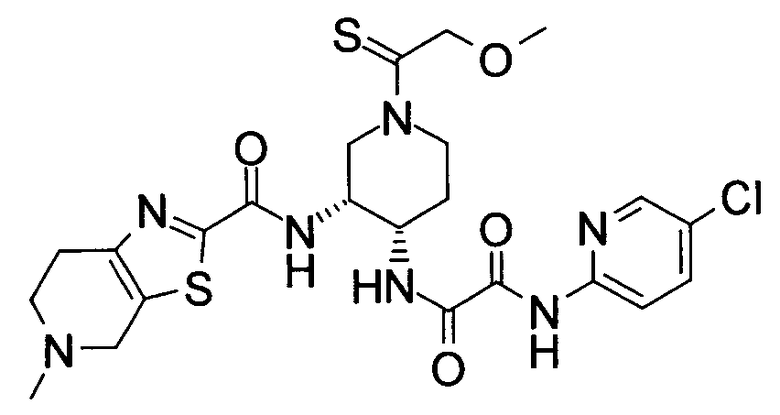
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 448, хлористоводородной кислотой для снятия защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем повторной обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (ДМСО-d6) δ: 1,74-1,85 (1H, м), 2,13-2,35 (1H, м), 2,89 (3H, с), 2,95-3,98 (9H, м), 4,05-5,33 (8H, м), 7,95-8,06 (2H, м), 8,43 (1H, с), 8,48-8,73 (1H, шир.), 9,29-9,45 (1H, шир.), 10,21-10,34 (1H, шир.), 11,45-11,90 (1H, шир.).
МС (ESI) m/z: 566 [(M+H)+, Cl35], 568 [(M+H)+, Cl37].
[Пример 318]
2,2,2-Трихлорэтил (1S,3R,4S)-4-({2-[(5-хлорпиридин-2-ил)амино]-2-оксоацетил}амино)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоксилат
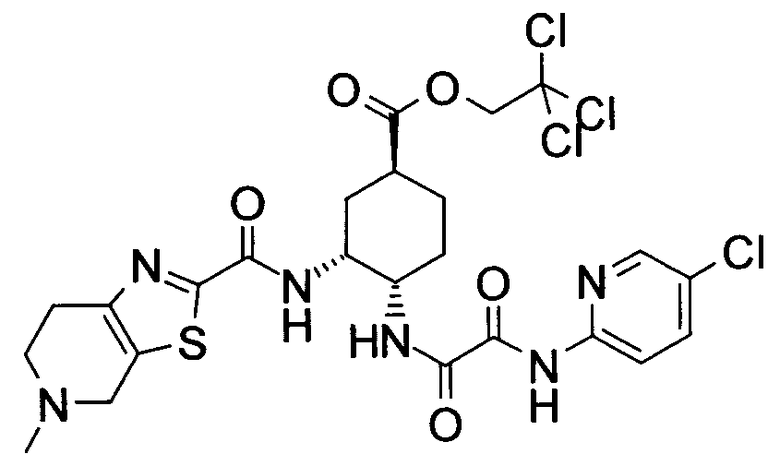
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 453, хлористоводородной кислотой для снятия защиты, конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 10, и затем повторной обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 219.
1Н-ЯМР (CDCl3) δ: 1,60-1,87 (2H, м), 2,04-2,15 (2H, м), 2,21-2,32 (2H, м), 2,52 (3H, с), 2,73-2,89 (3H, м), 2,92-2,98 (2H, м), 3,71 (1H, д, J=15,4Гц), 3,73 (1H, д, J=15,4Гц), 4,08-4,16 (1H, м), 4,66-4,71 (1H, м), 4,72 (1H, д, J=12,0Гц), 4,82 (1H, д, J=12,0Гц), 7,37 (1H, д, J=8,8Гц), 7,69 (1H, дд, J=8,8, 2,4Гц), 8,05 (1H, д, J=8,1Гц), 8,16 (1H, д, J=8,8Гц), 8,30 (1H, д, J=2,4Гц), 9,69 (1H, с).
МС (ESI) m/z: 651 [(M+H)+, 3xCl35], 653 [(M+H)+, 2xCl35, Cl37], 655 [(M+H)+, Cl35, 2xCl37].
[Пример 319]
(1S,3R,4S)-4-({2-[5-Хлорпиридин-2-ил]амино}-2-оксоацетил)амино)-3-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}циклогексанкарбоновая кислота
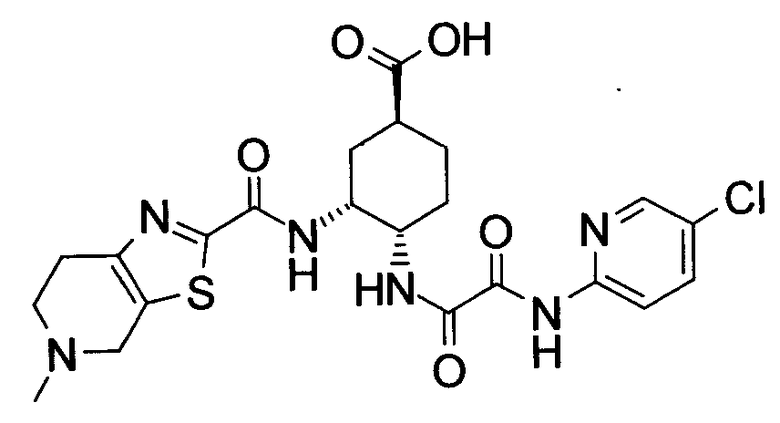
Соединение (475 мг), полученное в примере 318, растворяли в тетрагидрофуране (50 мл), к раствору последовательно добавляли цинк (2,85 г) и уксусную кислоту (5,7 мл) и смесь перемешивали при комнатной температуре в течение 3 часов. К реакционной смеси добавляли целит 545 (2,85 г) и удаляли фильтрованием нерастворимое вещество. Затем фильтрат концентрировали при пониженном давлении, к полученному остатку добавляли метиленхлорид и добавляли при перемешивании 1N водный раствор гидроксида натрия, доводя рН реакционной смеси до 7. После отделения органического слоя к водному слою добавляли насыщенный раствор соли (50 мл) и экстрагировали метиленхлоридом. Полученные органические слои объединяли и сушили над безводным сульфатом магния. Растворитель отгоняли при пониженном давлении и полученный остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 95:5 → 9:1 → 4:1) с получением указанного в заголовке соединения (140 мг).
1Н-ЯМР (ДМСО-d6) δ: 1,50-1,80 (3H, м), 1,84-1,95 (1H, м), 1,95-2,10 (1H, м), 2,15-2,30 (1H, м), 2,38 (3H, с), 2,40-2,50 (1H, м), 2,67-2,80 (2H, м), 2,80-2,95 (2H, м), 3,66 (2H, м), 4,03 (1H, шир.с), 4,33 (1H, шир.с), 7,97-8,10 (2H, м), 8,45 (1H, с), 8,53 (1H, д, J=6,8Гц), 9,19 (1H, д, J=8,3Гц), 10,27 (1H, шир.с).
МС (FAB) m/z: 521 [(M+H)+, 35Cl], 523 [(M+H)+, 37Cl].
[Пример 320]
Гидрохлорид N-{(1R,2S,5S)-2-{[2-(4-хлоранилино)-1-метоксиимино-2-оксоэтил]амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
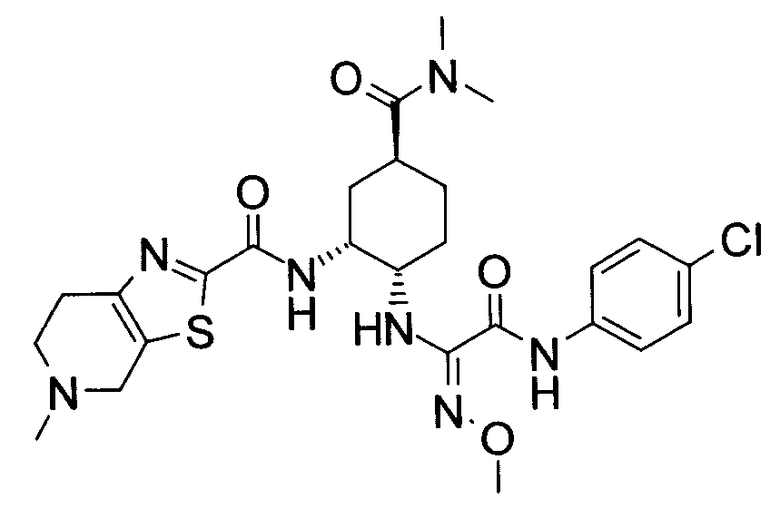
Указанное в заголовке соединение получали гидролизом сложного эфира соединения, полученного в ссылочном примере 454, подобно способу, описанному в примере 142, конденсацией гидролизата с 4-хлоранилином подобно способу, описанному в ссылочном примере 143, и затем обработкой продукта конденсации хлористоводородной кислотой.
1Н-ЯМР (ДМСО-d6) δ: 1,30-1,17 (1H, м), 1,50-1,62 (1H, м), 1,62-1,75 (2H, м), 1,85-2,00 (2H, м), 2,76 (3H, с), 2,93 (6H, шир.с), 3,00-3,10 (1H, м), 3,18 (1H, шир.с), 3,27 (1H, шир.с), 3,49 (1H, шир.с), 3,71 (1H, шир.с), 3,76 (3H, с), 3,93 (1H, шир.с), 4,35-4,50 (2H, м), 4,66-4,77 (1H, м), 6,09 (0,5H, д, J=7,8Гц), 6,19 (0,5H, д, J=7,8Гц), 7,38 (2H, д, J=8,8Гц), 7,71 (2H, д, J=8,8Гц), 8,70-8,79 (1H, м), 10,28 (1H, д, J=11,0Гц), 11,53 (0,5H, шир.с), 11,45 (0,5H, шир.с).
МС (FAB) m/z: 576 [(M+H)+, 35Cl], 578 [(M+H)+, 37Cl].
[Пример 321]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-[(1S,2R,4S)-4-[(диметиламино)карбонил]-2-({[1-(пиридин-4-ил)пиперидин-4-ил]карбонил}амино)циклогексил]этандиамида
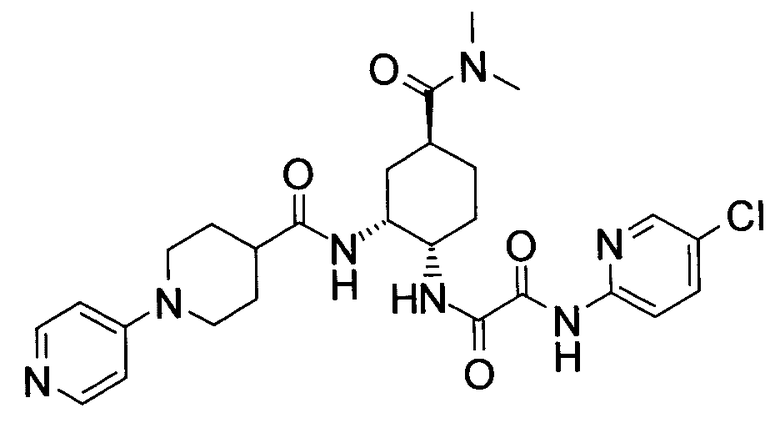
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 420, с 1-(пиридин-4-ил)пиперидин-4-карбоновой кислотой (WO96/10022) и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,35-1,49 (1H, м), 1,49-1,78 (6H, м), 1,78-1,98 (3H, м), 2,75-2,90 (1H, м), 2,78 (3H, с), 3,02 (3H, с), 3,03-3,14 (1H, м), 3,14-3,28 (2H, м), 3,74-3,85 (1H, м), 4,13-4,30 (3H, м), 7,18 (2H, д, J=7,3Гц), 7,99 (2H, с), 8,10-8,23 (3H, м), 8,41 (1H, с), 8,50 (1H, д, J=8,1Гц), 10,19 (1H, с), 13,73 (1H, шир.с).
МС (FAB) m/z: 556 [(M+H)+, 35Cl], 558 [(M+H)+, 37Cl].
[Пример 322]
N1-((1S,2R,4S)-4-[(Диметиламино)карбонил]-2-{[(5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-ил)карбонил]амино}-циклогексил)-N2-(5-этинилпиридин-2-ил)этандиамид
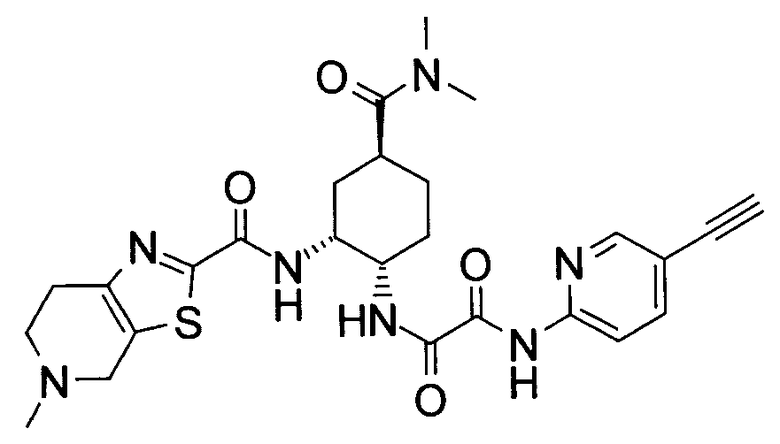
Соединение (348 мг), полученное в ссылочном примере 455, растворяли в тетрагидрофуране (14 мл), к раствору добавляли фторид тетрабутиламмония (1N тетрагидрофурановый раствор, 628 мкл) и смесь перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь обесцвечивали активированным углем (около 1 г) и сушили над безводным сульфатом натрия. После фильтрования отгоняли при пониженном давлении растворитель и остаток очищали колоночной хроматографией на силикагеле (метиленхлорид:метанол = 93:7) и затем растворяли в метиленхлориде (около 1 мл). К раствору добавляли гексан (около 10 мл) и образовавшийся осадок отфильтровывали с получением указанного в заголовке соединения (116 мг).
1Н-ЯМР (CDCl3) δ: 1,62-2,14 (8H, м), 2,52 (3H, с), 2,79-2,95 (6H, м), 3,05 (3H, с), 3,19 (1H, с), [модель AB 3,71 (1H, д, J=15,5Гц), 3,74 (1H, д, J=15,5Гц)], 4,08-4,14 (1H, м), 4,66-4,69 (1H, м), 7,41 (1H, д, J=8,6Гц), 7,80 (1H, дд, J=8,6, 2,2Гц), 8,03 (1H, д, J=7,6Гц), 8,15 (1H, д, J=8,6Гц), 8,46 (1H, д, J=2,2Гц), 9,75 (1H, с).
МС (ESI) m/z: 538 (M+H)+.
[Пример 323]
N1-(5-Хлорпиридин-2-ил)-N2-((1S,2R,4S)-4-[(диметиламино)карбонил]-2-{[(5-метил-5,6-дигидро-4Н-тиено[2,3-c]пиррол-2-ил)карбонил]амино}циклогексил)этандиамид
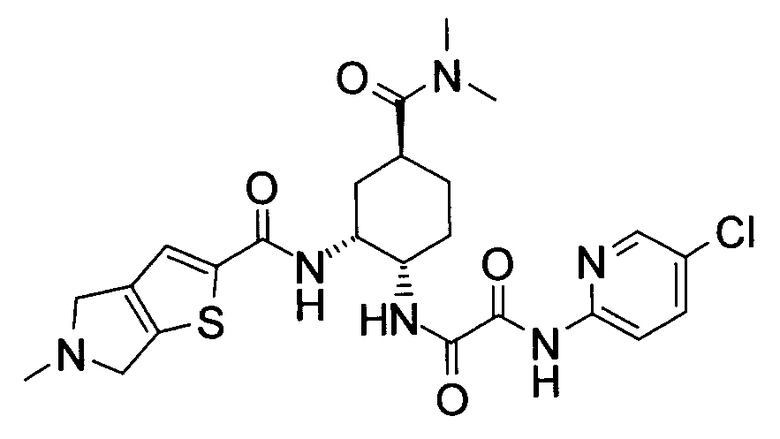
Указанное в заголовке соединение получали гидролизом соединения, полученного в ссылочном примере 456, и конденсацией гидролизата с соединением, полученным в ссылочном примере 420, подобно способу, описанному в примере 191.
1Н-ЯМР (CDCl3) δ: 1,80-2,15 (6H, м), 2,64 (3H, с), 2,76-2,79 (1H, м), 2,94 (3H, с), 3,03 (3H, с), 3,84-3,86 (2H, м), 3,94-3,99 (3H, м), 4,58-4,59 (1H, м), 6,70 (1H, д, J=6,3Гц), 7,31 (1H,S), 7,70 (1H, дд, J=8,8, 2,3Гц), 8,15-8,18 (2H, м), 8,30 (1H, д, J=2,3Гц), 9,72 (1H, шир.с).
МС (FAB) m/z: 533 [(M+H)+, Cl35], 535 [(M+H)+, Cl37].
[Пример 324]
Гидрохлорид N-{(1R,2S,5S)-2-({2-[6-хлорпиридазин-3-ил]амино}-2-оксоэтантиоил)амино}-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
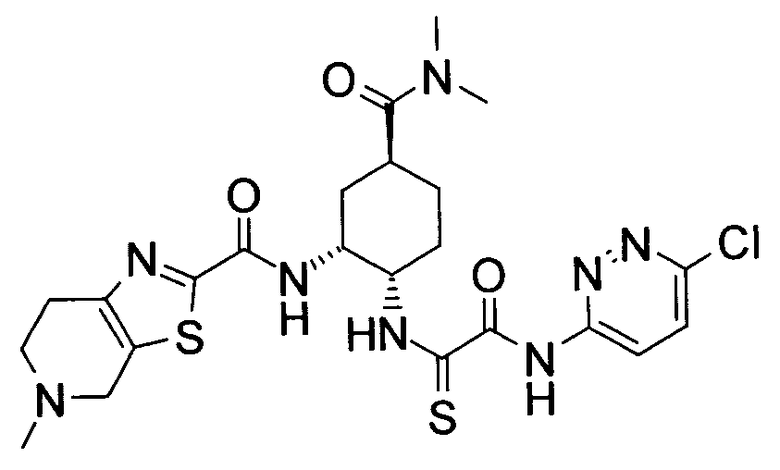
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 460, с соединением, полученным в ссылочном примере 10, и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 3.
1Н-ЯМР (ДМСО-d6) δ: 1,48-1,51 (1H, м), 1,71-1,79 (3H, м), 2,00 (1H, шир.с), 2,20-2,23 (1H, м), 2,78 (3H, с), 2,90 (3H, с), 2,96 (3H, с), 3,05 (1H, шир.с), 3,16-3,47 (3H, м), 3,69 (1H, шир.с), 4,43 (1H, шир.с), 4,53 (1H, шир.с), 4,69 (2H, шир.с), 7,97 (1H, д, J=9,6Гц), 8,32 (1H, д, J=9,6Гц), 8,73 (1H, д, J=7,3Гц), 11,08 (2H, шир.с), 11,61-11,75 (1H, м).
МС (FAB) m/z: 565 [(M+H)+, Cl35], 567 [(M+H)+, Cl37].
[Пример 325]
Гидрохлорид N-{(1R,2S,5S)-2-({2-[(6-хлорпиридин-3-ил)амино]-2-оксоэтантиоил}амино)-5-[(диметиламино)карбонил]циклогексил}-5-метил-4,5,6,7-тетрагидротиазоло[5,4-c]пиридин-2-карбоксамида
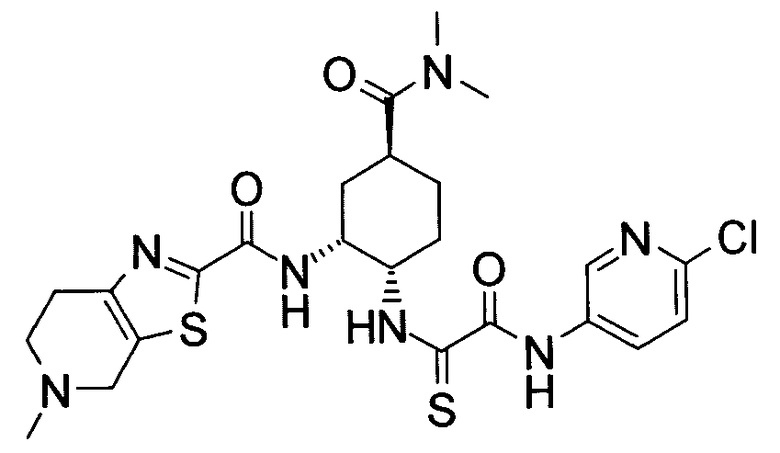
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 464, с соединением, полученным в ссылочном примере 10, и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 3.
1Н-ЯМР (ДМСО-d6) δ: 1,47-1,55 (1H, м), 1,66-1,78 (3H, м), 2,02-2,05 (1H, м), 2,21-2,33 (1H, м), 2,79 (3H, с), 2,91 (3H, с), 2,95 (3H, с), 2,99-3,04 (1H, м), 3,21 (2H, шир.с), 3,45-3,75 (2H, шир.), 4,40-4,75 (4H, м), 7,53 (1H, д, J=8,6Гц), 8,20 (1H, дд, J=8,6, 2,6Гц), 8,77 (1H, д, J=7,3Гц), 8,80 (1H, д, J=2,6Гц), 10,73 (1H, с), 10,94 (1H, шир.д, J=7,6Гц), 11,37 (1H, шир.с).
МС (FAB) m/z: 564 [(M+H)+, Cl35], 566 [(M+H)+, Cl37].
[Пример 326]
N1-[(3R,4S)-3-({[2'-(Аминосульфонил)[1,1'-бифенил]-4-ил]карбонил}амино)-1-(2-метоксиацетил)пиперидин-4-ил]-N2-(5-хлорпиридин-2-ил)этандиамид
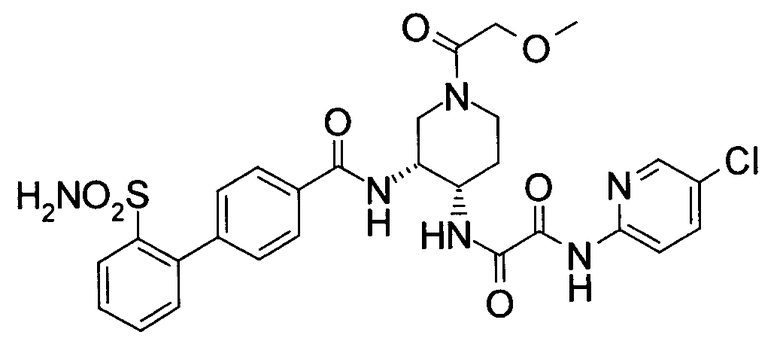
Указанное в заголовке соединение получали обработкой соединения, полученного в ссылочном примере 368, хлористоводородной кислотой для снятия защиты и затем конденсацией соединения со снятой защитой с соединением, полученным в ссылочном примере 465, подобно способу, описанному в примере 219.
1Н-ЯМР (CDCl3) δ: 1,59-1,85 (1H, м), 2,09-2,23 (1H, м), 2,88-3,13 (1H, м), 3,29-3,51 (4H, м), 4,06-4,20 (4H, м), 4,51-4,78 (4H, м), 7,09 (0,25H, шир.с), 7,30 (1H, д, J=7,1Гц), 7,51-7,54 (3,75H, м), 7,60 (1H, т, J=7,0Гц), 7,69 (1H, дд, J=8,9, 2,2Гц), 7,94-7,96 (2H, м), 8,13-8,22 (2H, м), 8,30 (1H, д, J=2,2Гц), 8,91 (0,75H, шир.д, J=5,9Гц), 9,18 (0,25H, шир.с), 9,70 (1H, с).
МС (FAB) m/z: 629 [(M+H)+, Cl35], 631 [(M+H)+, Cl37].
[Пример 327]
Гидрохлорид N1-(5-хлорпиридин-2-ил)-N2-{(1S,2R,4S)-4-[(диметиламино)карбонил]-2-[(тиено[3,2-b]пиридин-2-илкарбонил)амино]циклогексил}этандиамида
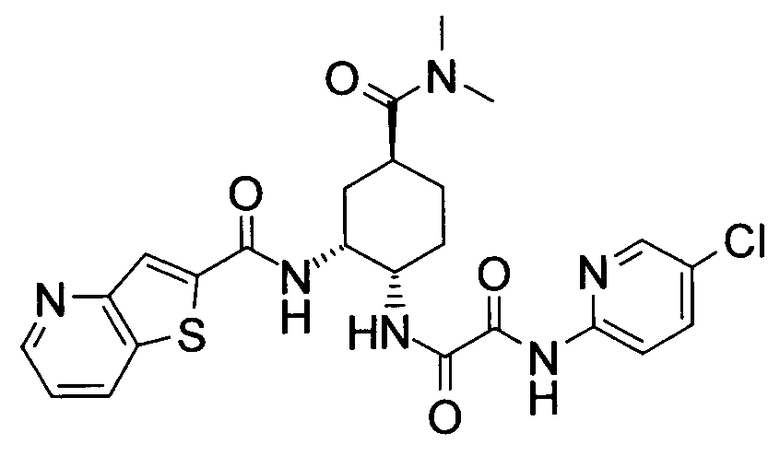
Указанное в заголовке соединение получали конденсацией соединения, полученного в ссылочном примере 420, с тиено[3,2-b]пиридин-2-илкарбоксилатом лития (выложенная заявка № 2001-294572 на патент Японии) и обработкой продукта конденсации хлористоводородной кислотой подобно способу, описанному в примере 2.
1Н-ЯМР (ДМСО-d6) δ: 1,44-1,57 (1H, м), 1,62-1,84 (3H, м), 1,86-1,98 (1H, м), 2,04-2,19 (1H, м), 2,78 (3H, с), 2,99 (3H, с), 3,11-3,25 (1H, м), 3,85-4,10 (1H, шир.), 4,44-4,55 (1H, шир.), 7,51-7,62 (1H, м), 7,98 (2H, шир.с), 8,43 (2H, шир.с), 8,60 (1H, с), 8,66 (1H, шир.д, J=8,1Гц), 8,81 (1H, шир.д, J=4,2Гц), 9,05 (1H, шир.д, J=7,8Гц), 10,24 (1H, с).
МС (ESI) m/z: 529 [(M+H)+, Cl35], 531 [(M+H)+, Cl37].
[Пример 1 испытания]
Определение FXa-ингибирующего эффекта (значение IC50):
5% Растворы (10 мкл) в ДМСО каждого испытуемого соединения с установленными подходящим образом ступенчатыми концентрациями, трис буфер (100 мМ трис, 200 мМ хлорид натрия, 0,2% BSA, рН 7,4) (40 мкл) и 0,0625 Е/мл FXa человека (Enzyme Research Laboratories, Inc., растворенный и разбавленный буфером трис) (10 мкл), помещали соответственно в лунки 96-луночного микропланшета и добавляли 750 мкМ водный раствор (40 мкл) S-2222 (Chromogenix Co.). Измеряли в течение 10 минут при комнатной температуре оптическую плотность при 405 нм и определяли увеличение оптической плотности (ΔOD/мин). В качестве контроля использовали буфер трис вместо испытуемого соединения.
Процент (%) ингибирования, вычисленный с использованием приведенного ниже уравнения, при конечной концентрации испытуемого соединения и конечную концентрацию испытуемого соединения откладывали на графике соответственно по оси ординат и оси абсцисс логарифмической нормальной вероятностной бумаги для определения дозы 50% ингибирования (значение IC50).
Процент ингибирования (%)=[1-(ΔOD/мин испытуемого соединения):(▵/мин контроля)]×100
(Результат)
В таблице показано, что соединения по настоящему изобретению обладают сильным FXa-ингибирующим эффектом.
(IC50): нМ
(IC50): нМ
[Пример 2 испытания]
Определение активности против FXa в плазме крыс после перорального введения:
(А) Введение и взятие крови:
Лекарственный раствор (1 мг/мл), полученный растворением или суспендированием испытуемого соединения (10 мг) в 0,5% метилцеллюлозе (МЦ), вводили перорально крысам (10 мл/кг). Через 0,5, 1, 2 и 4 часа после введения лекарства брали кровь (0,5 мл) из яремной вены, пользуясь шприцем, который содержал 3,13% (мас./об.) водный раствор (50 мкл) дигидрата цитрата тринатрия (количество взятой крови: 0,45 мл). У крыс контрольной группы такое же взятие крови проводили после введения 0,5% раствора МЦ. Каждый образец крови центрифугировали при 1500 х g в течение 10 минут при 4°C для отделения плазмы и плазму хранили при -40°C до использования в следующем определении активности против FXa в плазме.
(В) Определение FXa-ингибирующей активности в плазме:
Для определения активности против FXa в плазме в качестве субстрата использовали S-2222. Смешивали трис буфер (100 мМ трис, 200 мМ хлорид калия, 0,2% BSA, рН 7,4) (5456 мкл), FXa человека (2,5 Е/мл, 44 мкл) и воду (550 мкл). Полученный раствор FXa человека использовали в следующем испытании.
Крысиную плазму (5 мкл), полученную в соответствии с описанной выше методикой (А), помещали в лунки 96-луночного микропланшета и добавляли последовательно описанный выше раствор FXa человека (55 мкл) и 750 мкМ водный раствор (40 мкл) S-2222. Сразу же после этого измеряли при комнатной температуре оптическую плотность при 405 нм спектрофотометром SPECTRAmax 340 или 190 (Molecular Devices Co., U.S.A.), определяя тем самым скорость реакции (ΔOD/мин).
Активность против FXa, т.е. процент (%) ингибирования, вычисляли в соответствии со следующим уравнением:
Процент ингибирования(%)=[1-(ΔOD/мин образца):(среднее значение ΔOD/мин контрольная группа)]×100
(Результат)
Соединения, описанные в примерах 63, 191, 192, 194 и 204, проявили высокую FXa-ингибирующую активность от 62 до 96% при пероральной дозе 10 мг/кг.
Промышленная применимость
Производные циклического диамина по настоящему изобретению оказывают высокий ингибирующий эффект на активированный фактор Х свертывания крови и полезны как лекарственные средства, ингибиторы активированного фактора Х свертывания крови, антикоагулянты, средства для профилактики и/или лечения тромбоза или эмболии, средства для профилактики и/или лечения тромботического заболевания и средства для профилактики и/или лечения инфаркта головного мозга, эмболии головного мозга, инфаркта миокарда, стенокардии, инфаркта легких, эмболии легких, болезни Бюргера, тромбоза глубоких вен, синдрома диссеминированного внутрисосудистого коагулирования, тромбообразования после замены клапана или сустава, тромбообразования и реокклюзии после ангиопластики, синдрома системной воспалительной реакции (SIRS), синдрома заболевания многих органов (MODS), образования тромбов при экстракорпоральном кровообращении или свертывания крови при ее сборе.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ДИАМИНОВ | 2002 |
|
RU2319699C2 |
| ПРОИЗВОДНЫЕ ЭТИЛЕНДИАМИНА И СОДЕРЖАЩИЕ ИХ ИНГИБИТОР FXa И АНТИКОАГУЛЯНТ | 2001 |
|
RU2268259C2 |
| ДИАМИНОВЫЕ ПРОИЗВОДНЫЕ | 2003 |
|
RU2333203C2 |
| ФЕНИЛПИРАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ | 2008 |
|
RU2480456C2 |
| ЦИКЛОАЛКАН-1,3-ДИАМИНОВОЕ ПРОИЗВОДНОЕ | 2019 |
|
RU2793247C2 |
| ИСПОЛЬЗОВАНИЕ ЛИГАНДОВ РЕЦЕПТОРА ЕР4 ДЛЯ ЛЕЧЕНИЯ ОПОСРЕДОВАННЫХ IL-6 ЗАБОЛЕВАНИЙ | 2003 |
|
RU2285527C2 |
| НОВЫЙ ИНГИБИТОР β-ЛАКТАМАЗЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2800050C2 |
| НОВЫЙ ИНГИБИТОР бета-ЛАКТАМАЗЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2693898C2 |
| ПРОИЗВОДНЫЕ 2-ИМИНОПИРРОЛИДИНА | 2002 |
|
RU2270192C2 |
| ЦИКЛОАЛКИЛ-ЗАМЕЩЕННОЕ ПРОИЗВОДНОЕ ИМИДАЗОЛА, ОБЛАДАЮЩЕЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ TAFIa | 2011 |
|
RU2572814C2 |
Изобретение относится к новым соединениям или их солям, которые ингибируют активированный фактор Х свертывания крови, проявляя сильный противосвертывающий эффект. Соединения имеют одну из формул:
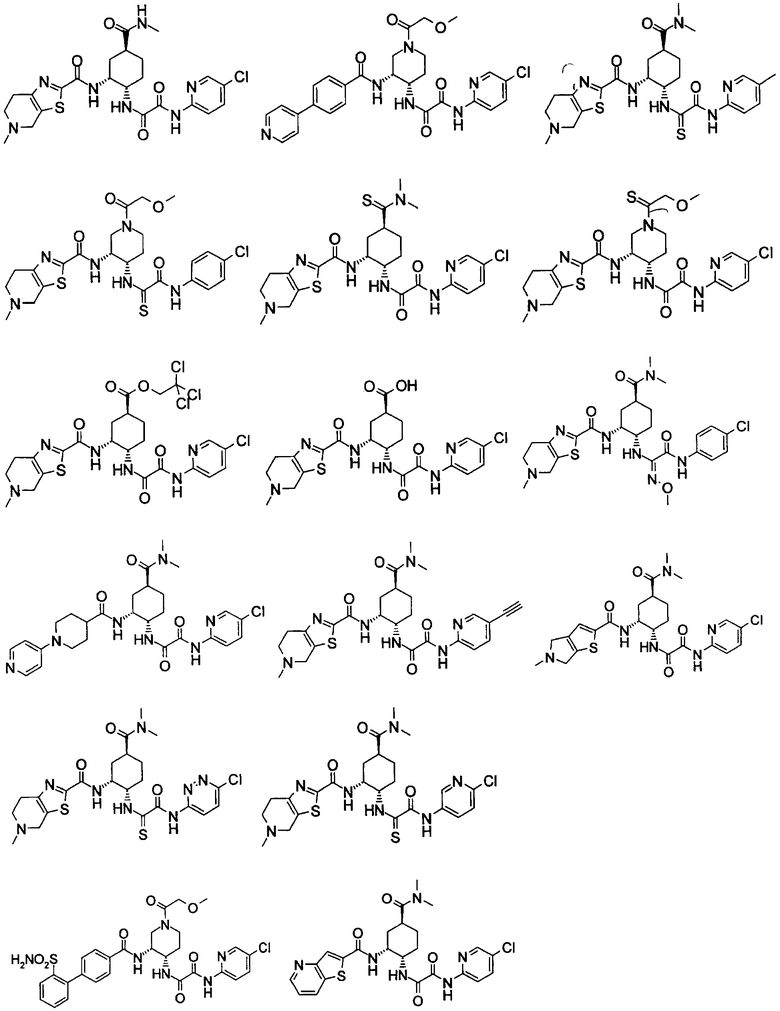
Изобретение также относится к лекарственному средству, ингибитору активированного фактора Х свертывания крови, антикоагулянту, медицинской композиции, содержащих указанные соединения, а также относится к применению их для изготовления лекарственного средства, ингибитора и антикоагулянта. 8 н.п. ф-лы, 1 табл.
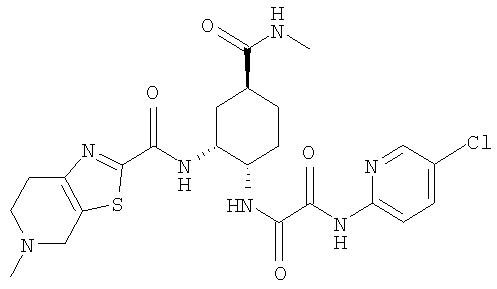
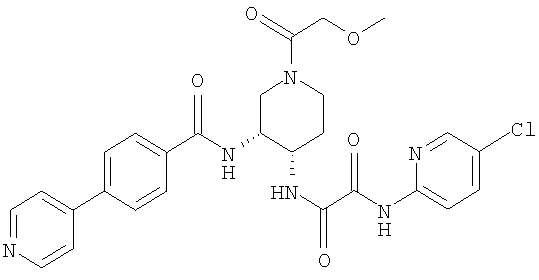
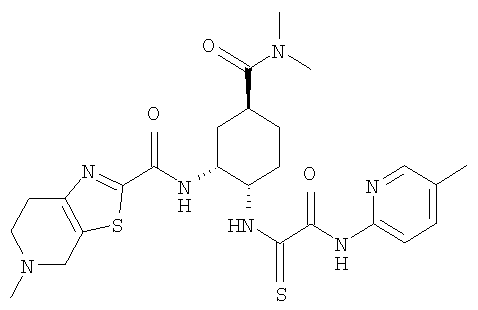
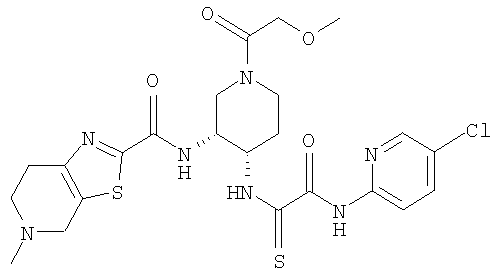
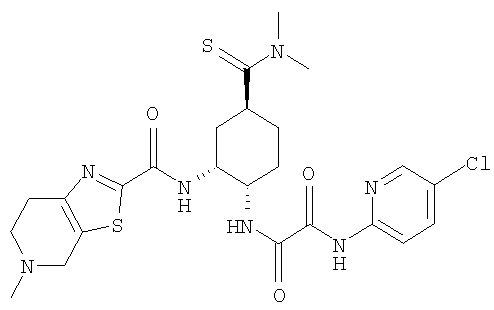
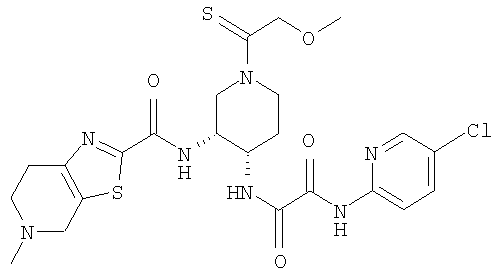

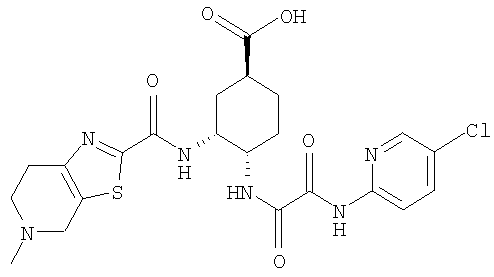
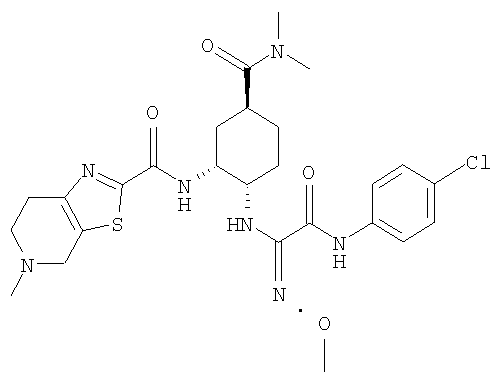
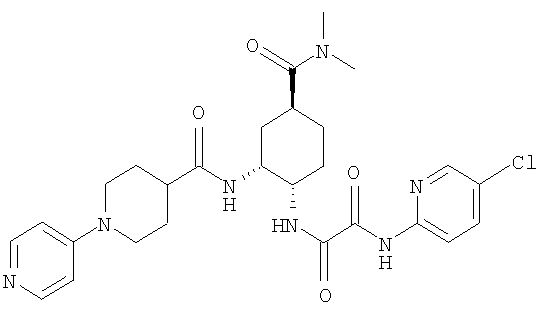
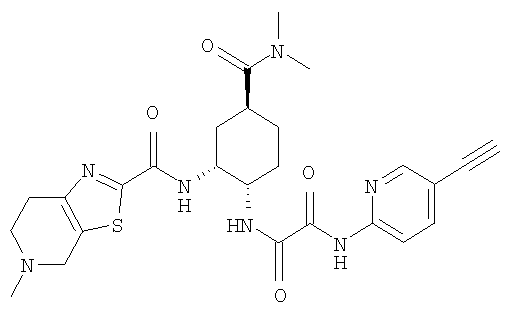
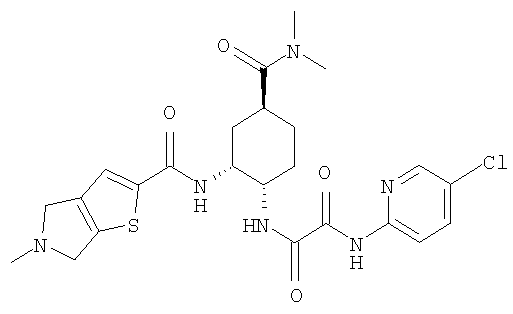
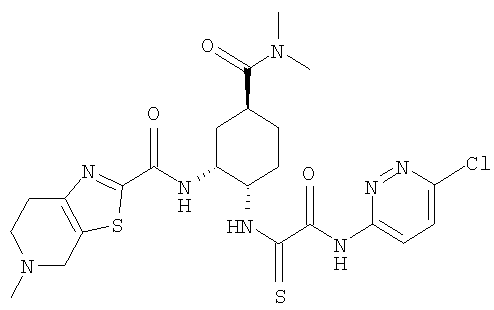
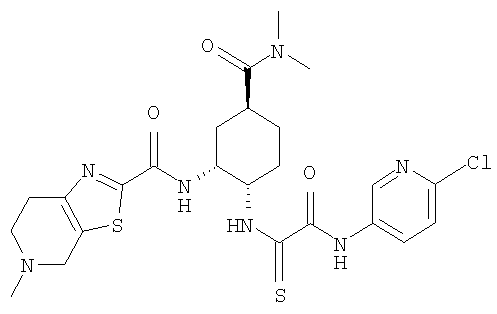
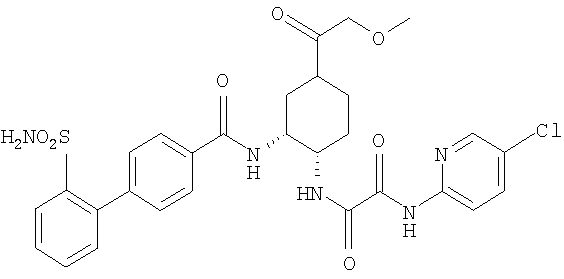 или
или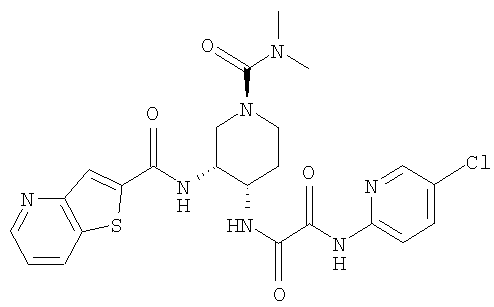
или его соль.
Приоритет по пунктам:
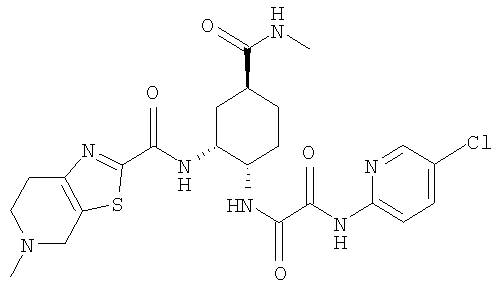
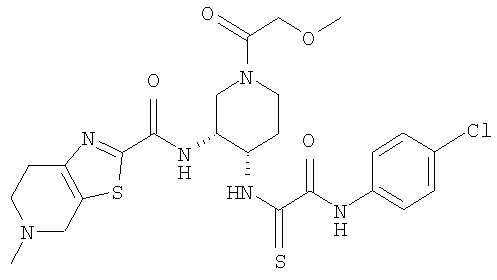


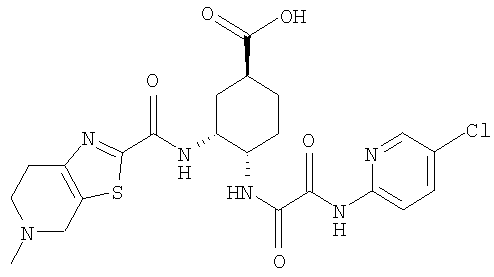
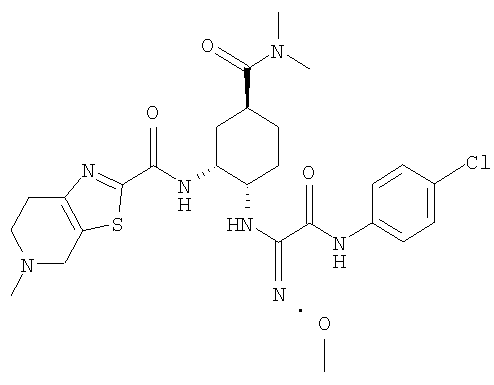
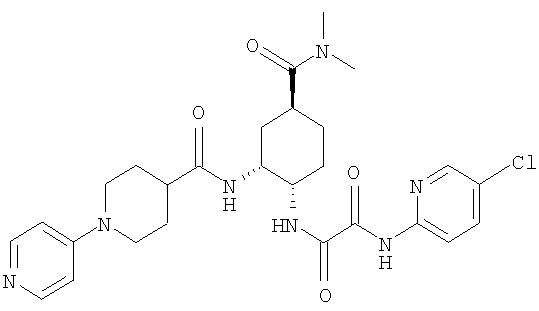
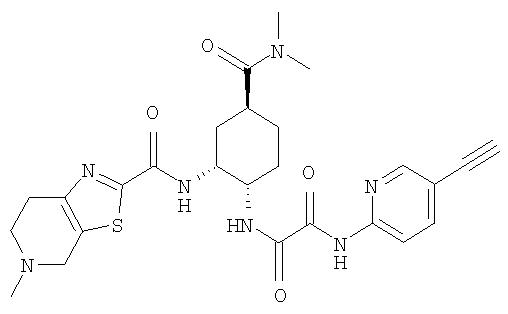
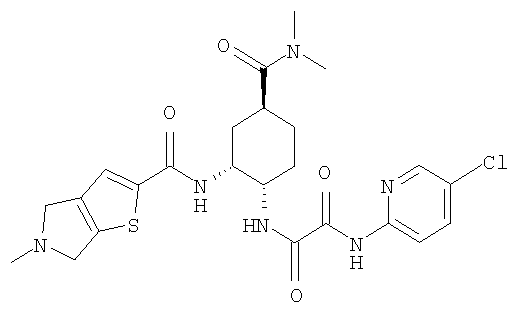
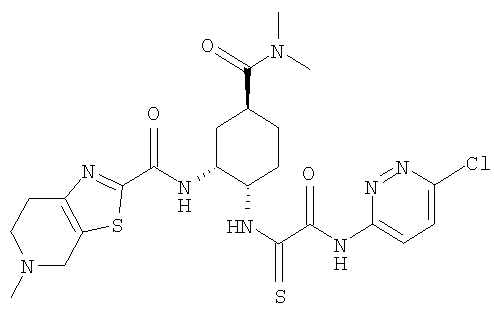
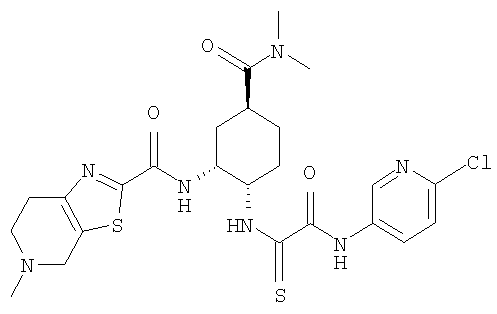
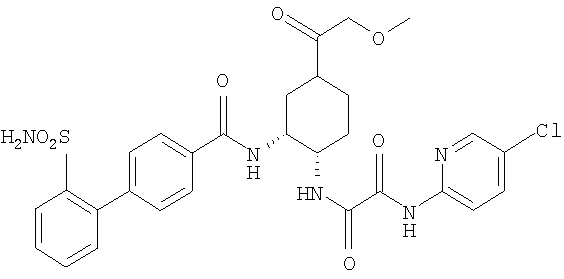 и
и 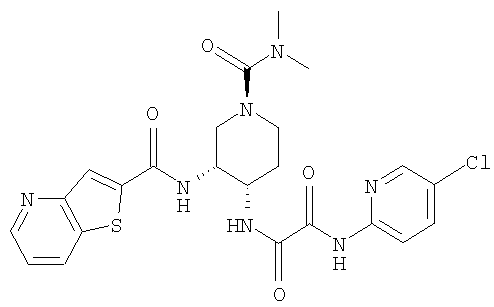



| WO 9845262 A1, 15.10.1998 | |||
| WO 9204017 A1, 19.03.1992 | |||
| WO 8607257 A2,18.12.1986 | |||
| Приспособление для уменьшения теплопередачи от горелки к резервуару с горючим | 1927 |
|
SU9480A1 |
| ВЫСОКОЧАСТОТНЫЙ НАГРЕВАТЕЛЬ | 1943 |
|
SU64902A1 |
| Гидротормоз | 1980 |
|
SU947510A1 |
| WO 9932225 A2, 01.07.1999 | |||
| WO 9710853 A2, 27.03.1997 | |||
| FRANCESCO GASPARRINI et al | |||
| Enantioselective chromatography on brush-type chiral stationary phases containing totally synthetic | |||
Авторы
Даты
2008-01-10—Публикация
2002-08-08—Подача