Изобретение относится к области биологии и медицины, а именно к области регенеративной медицины и тканевой инженерии, и может быть использовано для получения экстрацеллюлярных матриксов органов и тканей, применяемых в реконструктивной хирургии для замены или протезирования функций пораженных органов и тканей.
Экстрацеллюлярный матрикс (ЭЦМ), который используется в тканевой инженерии органов и тканей, может быть получен способом децеллюляризации. Известные способы децеллюляризации предполагают последовательную многоэтапную обработку растворами детергентов и/или ферментов (Amiel GE, Komura М, Shpira О, Yoo JJ, Yazdani S. Berry J, et al. Engineering of blood vessels from acellular collagen matrices coated with human endothelial cells. Tissue Eng 2006, 12:2355; C.Williams, J.Liao, E.M.Joyce, B. Wang, J.B. Leach, M.S. Sacks and J.Y.Wong. Altered structural and mechanical properties in decellularized rabbit carotid arteries, Acta Biomater.5, 993-1005 (2009); патент US 8221777 «Structurally modified acellular tissue engineering scaffolds and methods of production same»; патент RU №2407459, 2009) и различаются по длительности воздействия и концентрации реагентов, в качестве которых используют такие растворы, как Тритон Х-100, трипсин с этилендиаминтетрауксусной кислотой (ЭДТА), фосфатно-солевой буферный раствор, нуклеазы. Как правило, обрабатываемую ткань в процессе децеллюляризации помещают в емкость с реагентом, при этом реагент постоянно перемешивают в течение достаточно длительного времени.
Однако известные способы децеллюляризации обладают недостатками, которые заключаются в том, что из обрабатываемой ткани не удаляются полностью клетки и их остатки (клеточный дебрис), и не исключены серьезные повреждения ЭЦМ.
Из известных аналогов в качестве прототипа к заявляемому способу децеллюляризации выбран способ Amiel GE, Komura М, Shpira О, Yoo JJ, Yazdani S. Berry J, et al. Engineering of blood vessels from acellular collagen matrices coated with human endothelial cells. Tissue Eng 2006, 12:2355, заключающийся в том, что фрагмент кровеносного сосуда последовательно поэтапно погружают в емкость с:
- дистиллированной водой на 24 часа при температуре +4°С,
- 0,05%-ным раствором трипсин-ЭДТА на 1 час,
- питательной средой ДМЕМ с 5%-ным содержанием сыворотки на 24 часа,
- 1%-ным раствором Тритон Х-100 с 0,1% гидрохлоридом аммония (аммиака, нашатырного спирта) на 3 дня при температуре +4°С, при этом на данном этапе процесс обработки осуществляют при постоянном перемешивании раствора с помощью шейкера,
- дистиллированной водой на 24 часа при температуре +4°С,
- фосфатно-солевым буферным раствором на 24 часа при температуре +4°С.
Известный способ обладает теми же недостатками, что и аналоги, а именно не позволяет полностью удалить клетки и остатки их из обрабатываемого материала, и не исключает повреждения клеточного матрикса, так как не рассчитан на обработку кровеносных сосудов малого калибра.
Задачей настоящего изобретения является повышение качества децеллюляризации кровеносных сосудов малого калибра, сохранение их целостности и ультраструктуры для последующей иммобилизации клеток реципиента.
Выполнение поставленной задачи достигается тем, что в способе децеллюляризации кровеносных сосудов малого калибра, заключающемся в том, что для удаления клеточных элементов из обрабатываемого фрагмента кровеносного сосуда используют дистиллированную воду, 0,05%-ный раствор трипсин-ЭДТА, раствор Тритон Х-100 и фосфатно-солевой буферный раствор, фрагмент кровеносного сосуда последовательно поэтапно помещают в емкость с:
дистиллированной водой на 1 час при температуре +4°С,
0,05%-ным раствором трипсина и 0,02%-ной ЭДТА на 1 час при температуре +37°С,
0,075%-ным раствором додецилсульфата натрия на 24 часа при температуре 26°С,
0,25%-ным раствором Тритон Х-100 на 24 часа при температуре 26°С,
раствором, содержащим нуклеазы РНКаза А 20 мкг/мл и ДНКаза I 200 мкг/мл,
при этом после каждого этапа обработки фрагмент кровеносного сосуда трижды промывают в фосфатно-солевом буферном растворе по 10 минут, а весь процесс обработки осуществляют при постоянном перемешивании растворов и одновременной вибрации, создаваемой вибромотором, расположенным на наружной стенке емкости.
Заявляемый способ децеллюляризации кровеносных сосудов малого калибра отличается от аналогов и прототипа комбинацией, последовательностью и длительностью применения децеллюляризующих агентов, их более низкой концентрацией и наличием дополнительного физического воздействия - вибрации, создаваемой вибромотором, закрепленным на наружной стенке емкости, что позволяет эффективнее удалять клетки из обрабатываемого фрагмента кровеносного сосуда с меньшим повреждением ЭЦМ.
Предлагаемый способ децеллюляризации кровеносных сосудов малого калибра (3-4 мм), в качестве которых в эксперименте использовали артерии пуповины человека, включает несколько этапов со сменой децеллюляризующих растворов (ДР), в составе которых используют детергенты и ферменты. Все этапы проводят при постоянном вращательном движении ДР в рабочей емкости, для чего емкость с ДР устанавливают на орбитальном шейкере со скоростью 30 оборотов в минуту и амплитудой движения 10 мм. Кроме того, для наиболее глубокого проникновения ДР в толщу сосудистой стенки и более полного удаления клеточных элементов одновременно используют вибрацию. Для создания вибрации на внешней стороне рабочей емкости с ДР устанавливают небольшой мотор с эксцентриком (вибромотор).
В результате проведенных исследований децеллюляризированных описанным способом кровеносных сосудов малого калибра можно сделать вывод о том, что предлагаемое изобретение обеспечивает достижение поставленной задачи, выражающейся в повышении качества децеллюляризации кровеносных сосудов малого калибра, сохранении их целостности и ультраструктуры для последующей иммобилизации клеток реципиента.
Изобретение является новым и промышленно применимым, так как может быть использовано для получения экстрацеллюлярных матриксов органов и тканей с целью последующего использования в реконструктивной хирургии для замены или протезирования функций пораженных органов и тканей.
Предлагаемое изобретение поясняется чертежами, где:
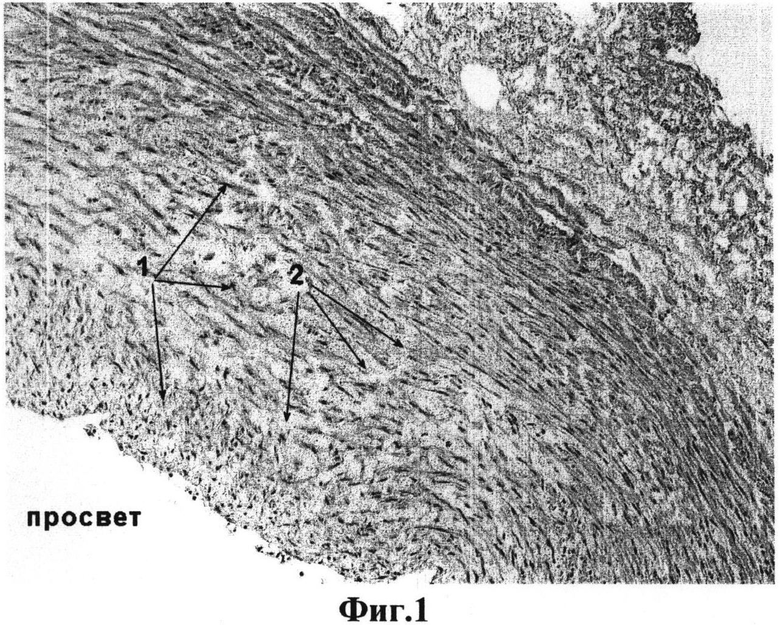
на фиг.1 представлен поперечный срез нативной артерии пуповины человека, окраска гематоксилин-эозин, увеличение ×100, где 1 - клеточные элементы, 2 - соединительная ткань;
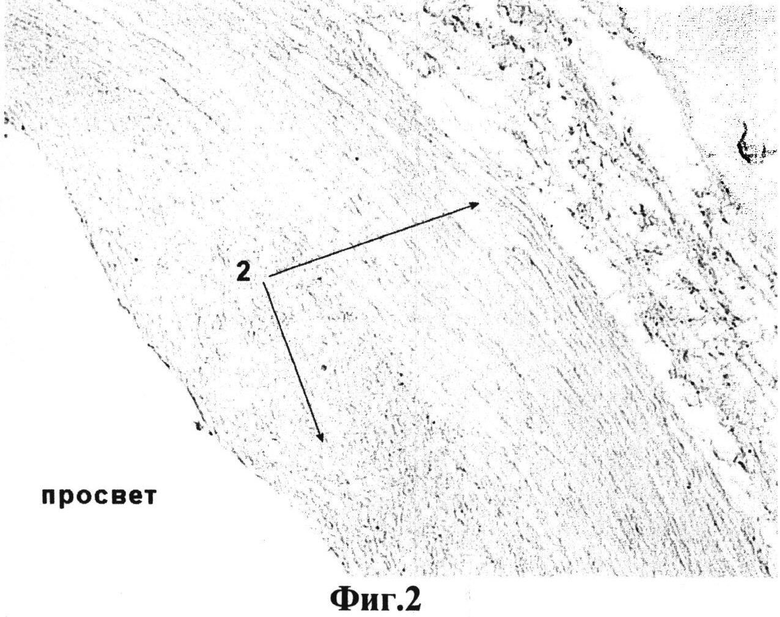
на фиг.2 - поперечный срез децеллюляризированной артерии пуповины человека, окраска гематоксилин-эозин, увеличение ×100, где: 2 - соединительная ткань (экстрацеллюлярный матрикс). Клеточные элементы не визуализируются;
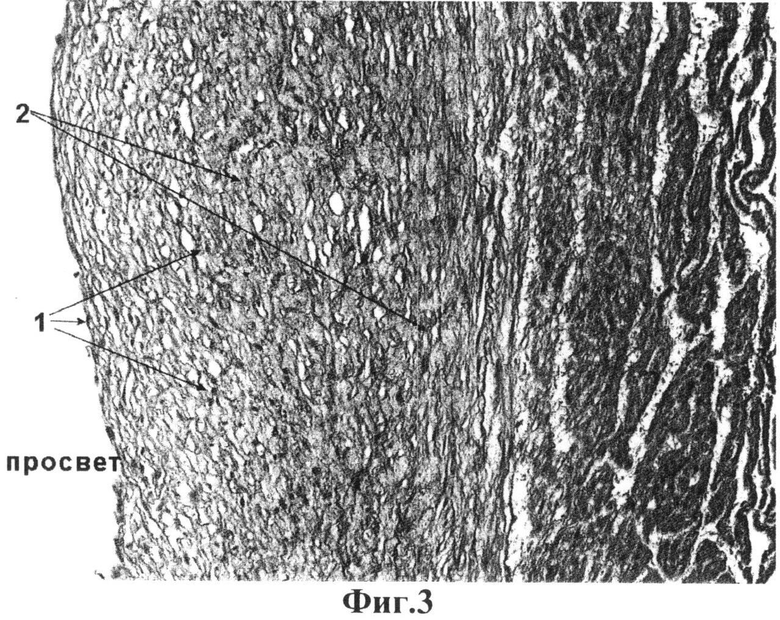
на фиг.3 - поперечный срез нативной артерии пуповины человека, окраска по Ван-Гизону, увеличение ×200, где 1 - клеточные элементы; 2 - соединительная ткань;
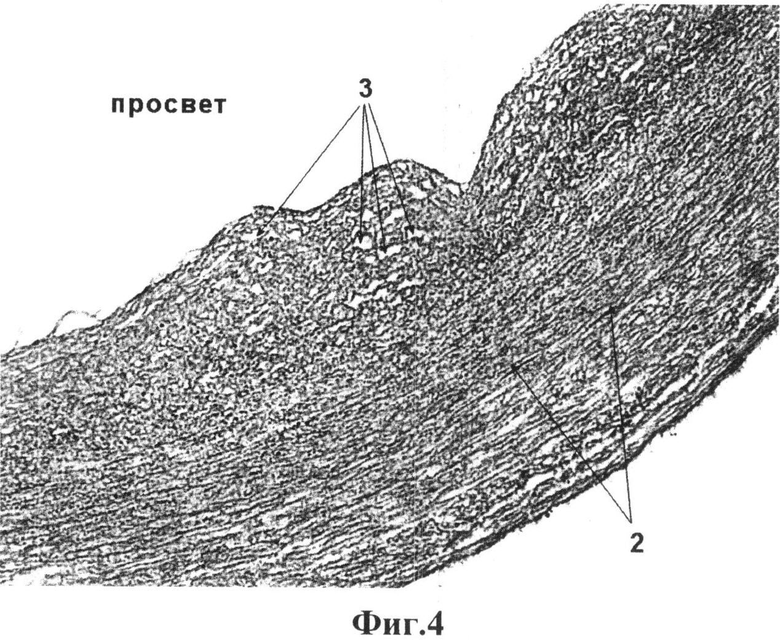
на фиг.4 - поперечный срез децеллюляризированной артерии пуповины человека, окраска по Ван-Гизону, увеличение ×200, где 2 - волокна коллагена (соединительная ткань), 3 - лакуны;
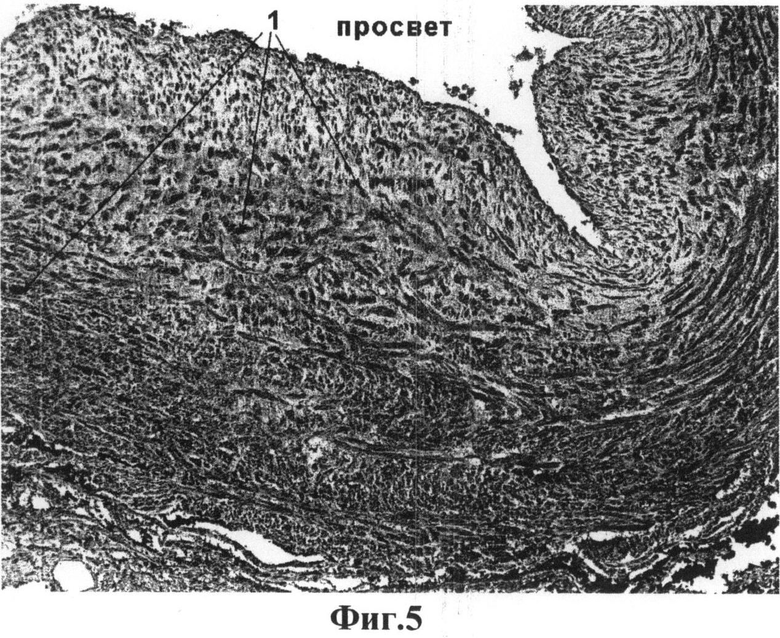
на фиг.5 - поперечный срез нативной артерии пуповины человека, иммуногистохимическая окраска на антиген гладкомышечного актина (а-SMA), увеличение ×100; где: 1 - гладкомышечные клетки;
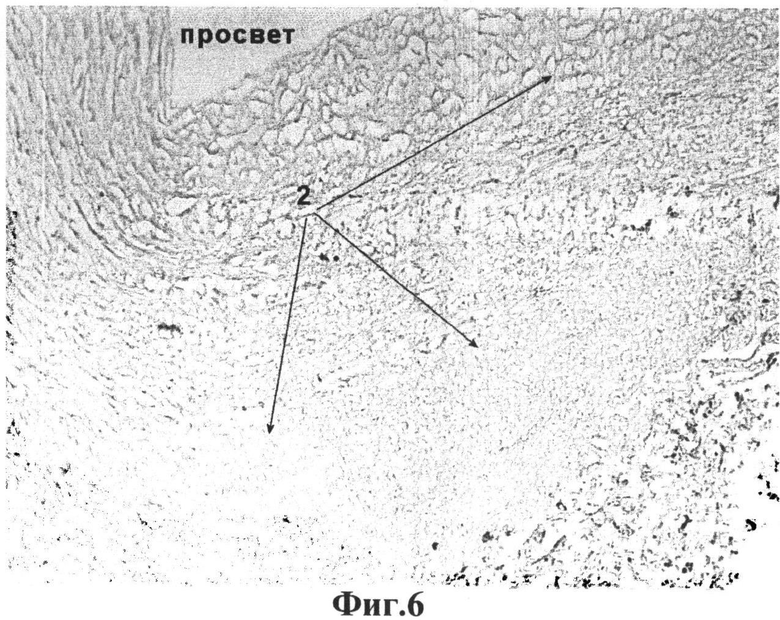
на фиг.6 - поперечный срез децеллюляризированной артерии пуповины человека, иммуногистохимическая окраска на антиген α-гладкомышечного актина, увеличение ×200, где 2- соединительная ткань (экстрацеллюлярный матрикс). Гладкомышечные клетки и их остатки не визуализируются.
Способ осуществляется следующим образом.
На первом этапе производят отмывание фрагмента кровеносного сосуда, в качестве которого использована артерия пуповины человека, от крови в дисциллированной воде в течение 1 часа при температуре +4°С. Так как вода является гипотоническим раствором, происходит осмотический шок и лизис клеток. Затем фрагмент обрабатываемой артерии трижды промывают в буферном растворе по 10 минут. В качестве раствора для промывания после каждого этапа использовали 0,1 М фосфатно-солевой буферный раствор с добавлением 0,02% ЭДТА.
На втором этапе используют раствор трипсина и ЭДТА в течение 1 часа, при температуре +37°С. Раствор содержит 0,05%-й трипсин, 0,02% ЭДТА в 0,1 М фосфатно-солевом буфере без ионов Ca2+ и Mg2+. В клеточной биологии для отделения клеток от поверхности субстрата широко используется смесь трипсина и ЭДТА как в концентрации 0,05%, так и 0,25%. В заявляемом способе используется более низкая концентрация трипсина для предотвращения протеолиза белков матрикса. Трипсин приводит к отделению клеток от ЭЦМ и «разрыхлению» микроструктуры матрикса для более глубокого проникновения детергентов и улучшения удаления клеток из толщи сосудистой стенки в дальнейших этапах децеллюляризации. Функции ЭДТА опосредованы связыванием ионов Ca2+ и Mg2+, которые, во-первых, могут ингибировать действие трипсина, во-вторых, необходимы для адгезии клеток на экстрацеллюлярный матрикс, и, в-третьих, ЭДТА неселективно ингибирует металлопротеиназы матрикса, что предотвращает саморазрушение ЭЦМ.
На третьем этапе, после трехкратного промывания фрагмента сосуда в фосфатно-солевом буферном растворе в течение 10 минут, проводят обработку в растворе додецилсульфата натрия в течение 24 часов при температуре +26°С. ДР на данном этапе содержит 0,075% SDS и 0,02% ЭДТА в ОДМ фосфатно-солевом буфере. Лаурилсульфат натрия (англ. sodium lauryl sulfate, SLS) или додецилсульфат натрия (англ. sodium dodecyl sulfate, SDS) - натриевая соль лаурилсульфокислоты, анионоактивное поверхностно-активное вещество. Применяется для солюбилизации белков клеточных мембран и лизиса клеток с последующим вымыванием клеточного дебриса из матрикса. Для лучшего эффекта децеллюляризации возможно сменить раствор через 1-2 часа.
На четвертом этапе, после трехкратного промывания в фосфатно-солевом буферном растворе в течение 10 минут, обработку проводят раствором Тритон Х-100 в течение 24 часов при температуре +26°С. ДР на данном этапе содержит 0,25% тритон Х-100 и 0,02% ЭДТА в 0,1 М фосфатно-солевом буфере. Тритон Х-100 - неионное поверхностно- активное вещество. Имеет в составе молекулы гидрофобный (4-третоктилфенол) и гидрофильный фрагменты (из остатков оксида этилена, в количестве 9-10). Тритон Х-100 более слабый детергент, чем SDS. Применяется также для солюбилизации белков клеточных мембран и лизиса клеток с последующим вымыванием клеточного дебриса из матрикса. Также для удаления остатков SDS, который достаточно цитотоксичен для последующей рецеллюляризации.
Пятый этап, после очередного трехкратного промывания в фосфатно-солевом буферном растворе в течение 10 минут, заключается в разрушении нуклеиновых кислот, которые ответственны за иммунный ответ у реципиента. Для этого используют нуклеазы, а именно ДНКазу I (200 мкг/мл) и РНКазу А (20 мкг/мл) в течение 6 часов при температуре +37°С.
Окончательный этап заключается в трехкратном промывании участка обрабатываемой артерии в фосфатно-солевом буферном растворе, для окончательного удаления детергентов и инактивации ферментов.
Пример 1
Для получения внеклеточного матрикса кровеносного сосуда малого калибра использовалась артерия пуповины человека. Материал получали непосредственно в родильном зале Федерального специализированного перинатального центра ФГБУ «ФЦСКЭ им. В. А. Алмазова» и при температуре +4°С транспортировали в лабораторию. Время доставки составило не более 2 часов. В стерильных условиях с помощью пинцета и ножниц из пуповины выделялся фрагмент артерии длиной около 5 см. Децеллюляризацию осуществляли в несколько этапов при постоянном перемешивании децеллюляризирующего раствора (ДР), для чего емкость с ДР устанавливали на орбитальном шейкере со скоростью 30 оборотов в минуту и амплитудой движений 10 мм (орбитальный шейкер GFL 3005, GFL, Германия), и дополнительно созданной вибрации, с помощью небольшого мотора с эксцентриком, установленного на внешней стороне рабочей емкости с ДР (вибромотор QX-6A-1, QX Motor, Китай). Первым этапом производили отмывание участка кровеносного сосуда от крови в дистиллированной воде в течение 1 часа при температуре +4°С. Затем участок кровеносного сосуда последовательно помещали в емкость с 0,05% раствором трипсина (Самсон-Мед, Россия) в фосфатно-солевом буфере с этилендиаминтетрауксусной кислотой (ФСБ-ДТА) на 1 час при температуре +37°С, 0,075% раствором додецилсульфата натрия (Amresco, США) на 24 часа при температуре +26°С; 0,25% раствором Тритон Х-100 (Amresco, США.) на 24 часа при температуре +26°С; с нуклеазами (РНКаза А 20 мкг/мл. и ДНКаза I 200 мкг/мл, Росмедбио, Россия). После каждого этапа участок артерии трижды промывали в ФСБ-ЭДТА по 10 минут. После окончательного трехкратного промывания участки артерий исследовали.
Пример 2
Для получения внеклеточного матрикса кровеносного сосуда малого калибра использовалась замороженная артерия пуповины человека. Материал получали непосредственно в родильном зале Федерального специализированного перинатального центра ФГБУ «ФЦСКЭ им. В.А. Алмазова» и при температуре +4°С транспортировали в лабораторию. Время доставки составило не более 2 часов. В стерильных условиях с помощью пинцета и ножниц из пуповины выделялись обе артерии, которые разделялись на участки длиной около 5-6 см. Участки артерий после этого замораживали и хранили при температуре -80°С до их последующего применения. Длительность хранения в замороженном состоянии может составлять до 6 месяцев. Для проведения децеллюляризации фрагмент артерии пуповины размораживали на водяной бане при температуре +37°С, проводили обработку предлагаемым способом и использовали в дальнейших исследованиях.
Проверку качества децеллюляризации по заявляемому способу проводили, используя гистологический и иммуногистохимический анализ, измерение остаточного ДНК и РНК.
На фиг.1 представлена морфологическая картина стенки интактной артерии пуповины человека, окрашенной гемтоксилин-эозин, где видно характерное строение сосудистой стенки, богатой клеточными элементами. На фиг.2 представлена артерия пуповины человека после децеллюляризации по заявляемому способу. Как видно, клеточные элементы полностью отсутствуют, а внеклеточный матрикс имеет неповрежденную структуру. Более подробно внеклеточный матрикс виден на фиг.3 и 4, где гистологические препараты окрашены по Ван-Гизону, используемый для окраски соединительной ткани, особенно коллагеновых волокон, из которых преимущественно и состоит внеклеточный матрикс артерии. Для оценки полноты удаления клеточного дебриса из толщи сосудистой стенки препараты окрашивали на антиген гладкомышечного актина - фиг.5 и 6. На фиг.5 видно толстый массив гладкомышечных клеток в среднем слое артерии (артерия мышечного типа), после децеллюляризации по заявляемому способу антиген гладкомышечного актина визуально не обнаруживается, что косвенно подтверждает не только лизис гладкомышечных клеток, но и удаление клеточного дебриса из всей толщи сосудистой стенки.
Для сравнения количества нуклеиновых кислот в нативных и децеллюляризированных артериях экстрагировали ДНК и РНК из фрагментов сосудов. Количественный анализ производился на спектрофотометре NanoDrop 1000 (Thermo Fisher Scientific, США). В нативной артерии уровень ДНК составил 81,9ng/U1, РНК - 98,4 ng/U1, в децеллюляризированной артерии ни ДНК, ни РНК не определялись.
Эффективность заявляемого способа проверена в серии из 20 последовательных экспериментов, достигнув при этом воспроизводимые результаты. Полученные таким образом децеллюляризированные кровеносные сосуды могут использоваться в дальнейших этапах тканевой инженерии для создания аутологичных сосудистых заменителей в реконструктивной сердечно-сосудистой хирургии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДЕЦЕЛЛЮЛЯРИЗИРОВАННЫХ МАТРИКСОВ ПАРЕНХИМАТОЗНЫХ ОРГАНОВ ЛАБОРАТОРНЫХ ЖИВОТНЫХ | 2016 |
|
RU2653489C2 |
| СПОСОБ УСКОРЕННОЙ ДЕЦЕЛЛЮЛЯРИЗАЦИИ БИОЛОГИЧЕСКОЙ ТКАНИ ИЛИ ОРГАНА | 2019 |
|
RU2714327C1 |
| СПОСОБ ДЕЦЕЛЛЮЛЯРИЗАЦИИ ДЕРМЫ СВИНЬИ ДЛЯ РЕКОНСТРУКТИВНОЙ ПЛАСТИЧЕСКОЙ ХИРУРГИИ | 2022 |
|
RU2791987C1 |
| Способ прогнозирования возможного рецидива аденокарциномы поджелудочной железы после ее резекции или воздействия методами локальной деструкции на примере радиочастотной абляции | 2022 |
|
RU2790982C1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕСКЛЕТОЧНОГО МАТРИКСА ДЕРМЫ ДЛЯ ПОСЛЕДУЮЩЕЙ РЕКОНСТРУКЦИИ ОБШИРНЫХ ДЕФЕКТОВ МЯГКИХ ТКАНЕЙ | 2018 |
|
RU2704489C1 |
| БИОРЕЗОРБИРУЕМЫЙ БИОЛОГИЧЕСКИЙ МАТРИКС ДЛЯ ЗАМЕЩЕНИЯ ДЕФЕКТОВ КОСТНОЙ ТКАНИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2017 |
|
RU2665962C1 |
| Способ получения тканеспецифического матрикса для тканевой инженерии хряща | 2019 |
|
RU2716577C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ БИОИНЖЕНЕРНОГО КАРКАСА СЕРДЦА В ЭКСПЕРИМЕНТЕ НА КРЫСЕ | 2014 |
|
RU2550286C1 |
| Способ восстановления резорбированной альвеолярной костной ткани биоинженерной конструкцией из децеллюляризированных тканей зуба человека | 2019 |
|
RU2716594C1 |
| Способ индукции спонтанной дифференцировки клеток периодонтальной связки и надкостницы в одонтогенном и остеогенном направлениях путем использования децеллюляризированного матрикса зуба и периодонтальной связки человека | 2022 |
|
RU2813729C1 |
Изобретение относится к медицине, а именно к регенеративной медицине и тканевой инженерии, и может быть использовано для получения экстрацеллюлярных матриксов кровеносных сосудов малого калибра. Для этого на первом этапе тканей фрагмент кровеносного сосуда отмывают дистиллированной водой в течение 1 часа при температуре +4°С. Затем фрагмент помещают в 0,05% раствор трипсина и 0,02%-ной ЭДТА на 1 час при температуре +37°С. На третьем этапе проводят обработку в 0,075% растворе додецилсульфата натрия в течение 24 часов при температуре 26°С. Далее фрагмент помещают в 0,25%-ный раствор Тритон Х-100 на 24 часа при температуре 26°С. На четвертом этапе данный фрагмент обрабатывают раствором, содержащим РНКазу А 20 мкг/мл и ДНКазу I 200 мкг/мл, в течение 6 часов при температуре +37°С. При этом после каждого этапа обработки фрагмент кровеносного сосуда трижды промывают в фосфатно-солевом буферном растворе по 10 минут. Весь процесс обработки осуществляют при постоянном перемешивании растворов и одновременной вибрации, создаваемой вибромотором, который расположен на наружной стенке емкости. Способ позволяет повысить качество децеллюляризации кровеносных сосудов малого калибра, сохранить их целостность и ультраструктуру для последующей иммобилизации клеток реципиента. 2 пр., 6 ил.
Способ децеллюляризации кровеносных сосудов малого калибра, заключающийся в том, что для удаления клеточных элементов из кровеносного сосуда используют дистиллированную воду, 0,05%-ный раствор трипсин-ЭДТА, раствор Тритон Х-100 и фосфатно-солевой буферный раствор, отличающийся тем, что фрагмент кровеносного сосуда последовательно поэтапно помещают в емкость с:
дистиллированной водой на 1 час при температуре +4°С,
0,05%-ным раствором трипсина и 0,02%-ой ЭДТА на 1 час при температуре +37°С,
0,075%-ным раствором додецилсульфата натрия на 24 часа при температуре 26°С,
0,25%-ным раствором Тритон Х-100 на 24 часа при температуре 26°С,
раствором, содержащим нуклеазы РНКаза А 20 мкг/мл и ДНКаза I 200 мкг/мл, в течение 6 часов при температуре +37°С,
при этом после каждого этапа обработки фрагмент кровеносного сосуда трижды промывают в фосфатно-солевом буферном растворе по 10 минут, а весь процесс обработки осуществляют при постоянном перемешивании растворов и одновременной вибрации, создаваемой вибромотором, расположенным на наружной стенке емкости.
| AMIEL G.E | |||
| et al., Engineering of blood vessels from acellular collagen matrices coated with human endothelial cells, Tissue Eng | |||
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЕДИНИТЕЛЬНО-ТКАННОГО КАРКАСА МАГИСТРАЛЬНОГО СОСУДА МЛЕКОПИТАЮЩИХ ЖИВОТНЫХ И ЧЕЛОВЕКА | 2009 |
|
RU2407459C1 |
| US 0008221777 B2, 17.07.2012 | |||
| ИВАНОВ А.В | |||
| Экспериментальная тканевая инженерия в создании | |||
Авторы
Даты
2014-01-20—Публикация
2012-11-28—Подача