ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится, главным образом, к антителам, сконструированным с реакционноспособными цистеиновыми остатками, и конкретнее к антителам, имеющим терапевтическое или диагностическое применение. Антитела, сконструированные с цистеином, могут быть конъюгированы с химиотерапевтическими лекарственными средствами, токсинами, аффинными лигандами, такими как биотин, и метками детекции, такими как флюорофоры. Изобретение также относится к способам использования антител и соединений конъюгата антитело-лекарственное средство для in vitro, in situ, и in vivo диагностики или обработки клеток млекопитающих, или связанных патологических состояний.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Терапия антителами была разработана для направленного лечения пациентов, страдающих злокачественными новообразованиями, иммунологическими или ангиогенными нарушениями. Трансмембранные, или имеющие другое расположение, опухолеассоциированные полипептиды специфически экспрессируемые на поверхности раковых клеток по сравнению с нормальной, нераковой клеткой (клетками), были определены в качестве клеточных мишеней для диагностики или лечения рака с помощью антител. Определение таких опухолеассоциированных полипептидов поверхностных антигенов, то есть опухолеассоциированных антигенов (ТАА), делает возможным специфическое нацеливание на раковые клетки для разрушения посредством терапии, основанной на антителах.
Применение конъюгатов антитело-лекарственное средство (ADC), то есть иммуноконъюгатов, для местной доставки цитотоксических или цитостатических средств, т.е. лекарственных средств для уничтожения или ингибирования опухолевых клеток при лечении злокачественного новообразования (Lambert, J. (2005) Curr. Opinion in Pharmacology 5: 543-549; Wu et al (2005) Nature Biotechnology 23(9): 1137-1146; Payne, G. (2003) Cancer Cell 3: 207-212; Syrigos and Epenetos (1999) Anticancer Research 19: 605-614; Niculescu-Duvaz and Springer (1997) Adv. Drug Del. Rev. 26: 151-172; US 4975278) делает возможной направленную доставку лекарственной молекулы к опухоли, и внутриклеточное накопление там, где системное введение этих неконъюгированных лекарственных средств для уничтожения опухолевых клеток также может привести к недопустимым уровням токсичности как для нормальных клеток, так и для опухолевых клеток, подлежащих уничтожению (Baldwin et al (1986) Lancet pp. (Mar. 15, 1986): 603-05; Thorpe, (1985) «Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review» in Monoclonal Antibodies '84: Biological And Clinical Applications, A. Pinchera et al (ed.s), pp. 475-506). Меры по улучшению терапевтического индекса, а именно максимальной эффективности и минимальной токсичности ADC, сфокусированы на селективности поликлональных (Rowland et al (1986) Cancer Immunol. Immunother., 21: 183-87) и моноклональных антител (mAb), а также лекарство-связывающих и лекарство-высвобождающих свойствах (Lambert, J. (2005) Curr. Opinion in Pharmacology 5: 543-549). Лекарственные молекулы, используемые в конъюгатах антитело-лекарственное средство, включают бактериальные токсины белковой природы, такие как дифтерийный токсин, белковые токсины растений, такие как рицин, малые молекулы, такие как ауристатины, гелданамицин (Mandler et al (2000) J. of the Nat. Cancer Inst. 92(19): 1573-1581; Mandler et al (2000) Bioorganic & Med. Chem. Letters 10: 1025-1028; Mandler et al (2002) Bioconjugate Chem. 13: 786-791), майтанзиноиды (EP 1391213; Liu et al (1996) Proc. Natl. Acad. Sci. USA 93: 8618-8623), калихемицин (Lode et al (1998) Cancer Res. 58: 2928; Hinman et al (1993) Cancer Res. 53: 3336-3342), дауномицин, доксорубицин, метотрексат и виндезин (Rowland et al. (1986), выше). Лекарственные молекулы могут действовать на цитотоксические и цитостатические механизмы, включая связывание тубулина, связывание ДНК, или ингибирование топоизомеразы. Некоторые цитотоксические лекарственные средства имеют тенденцию быть неактивными или менее активными при конъюгировании с большими антителами или лигандами белковых рецепторов.
Пептиды ауристатина, ауристатин E (AE) и монометилауристатин (MMAE), синтетические аналоги доластатина (WO 02/088172), в качестве лекарственных молекул были конъюгированы с: (i) химерными моноклональными антителами cBR96 (специфичны к Льюис Y на карциномах); (ii) cAC10, которое специфично к CD30 на гематологических злокачественных новообразованиях (Klussman, et al (2004), Bioconjugate Chemistry 15(4): 765-773; Doronina et al (2003) Nature Biotechnology 21(7): 778-784; Francisco et al (2003) Blood 102(4): 1458-1465; US 2004/0018194); (iii) антителами против CD20, такими как ритуксан (WO 04/032828), для лечения CD-20-экспрессирующих злокачественных новообразований и иммунных нарушений; (iv) антителом 2Н9 против EphB2R для лечения рака ободочной и прямой кишки (Mao et al (2004) Cancer Research 64(3): 781-788); (v) антителом к Е-селектину (Bhaskar et al (2003) Cancer Res. 63: 6387-6394); (vi) трастузумабом (HERCEPTIN®, US 2005/0238649), и (vi) антителами против CD30 (WO 03/043583). Варианты ауристатина Е раскрыты в US 5767237 и US 6124431. Монометилауристатин Е, конъюгированный с моноклональными антителами, раскрыт у Senter et al, Proceedings of the American Association for Cancer Research, том 45, номер реферата 623, представлен 28 марта 2004. Ауристатиновые аналоги MMAE и MMAF были конъюгированы с различными антителами (US 2005/0238649).
Обычные способы присоединения лекарственной молекулы к антителу, т.е. связывание посредством ковалентных связей, как правило, приводят к образованию гетерогенной смеси молекул, в которой молекулы лекарственного средства присоединены к целому ряду участков на антителе. Например, цитотоксические лекарственные средства, обычно, конъюгируют с антителами посредством многочисленных остатков лизина антитела, образуя гетерогенную смесь конъюгата антитело-лекарственное средство. В зависимости от условий реакции, гетерогенная смесь обычно содержит распределение антител с прикрепленными лекарственными молекулами от 0 до 8, или более. Кроме того, в пределах каждой подгруппы конъюгатов с конкретным целочисленным соотношением молекул лекарственного средства к антителу, существует потенциально гетерогенная смесь, в которой молекула лекарственного средства присоединена к различным участкам на антителе. Аналитические и препаративные методы могут быть недостаточными для разделения и характеристики видов молекул конъюгатов антитело-лекарственное средство в составе гетерогенной смеси, полученной в результате реакции конъюгирования. Антитела представляют собой крупные, сложные и структурно разнообразные биомолекулы, часто со множеством реакционноспособных функциональных групп. Их способность реагировать с линкерными реагентами и промежуточными соединениями лекарственное средство-линкер зависит от таких факторов, как рН, концентрация, концентрация соли, и вспомогательных растворителей. Более того, многостадийный процесс конъюгирования может быть невоспроизводимым в результате сложности контролирования условий реакции и характеристик взаимодействующих веществ и промежуточных соединений.
Тиолы цистеина являются реакционноспособными при нейтральном значении рН, в отличие от большинства аминов, которые присоединяют протон, и менее нуклеофильны при значении рН, близком к 7. Поскольку свободные тиоловые (меркаптаны, сульфгидрил) группы являются относительно реакционноспособными, белки с цистеиновыми остатками часто находятся в их окисленной форме в качестве дисульфид-связанных олигомеров, или имеют внутренние мостиковые дисульфидные группы. Внеклеточные белки, как правило, не имеют свободных тиолов (Garman, 1997, Non-Radioactive Labelling: A Practical Approach, Academic Press, London, page 55). Тиоловые группы цистеина антитела, как правило, более реакционноспособны, т.е. более нуклеофильны, по отношению к электрофильным реагентам конъюгирования, чем аминные или карбоксильные группы антитела. Остатки цистеина были введены в белки с использованием методов генной инженерии для образования ковалентных присоединений к лигандам или для образования новых внутримолекулярных дисульфидных связей (Better et al (1994) J. Biol. Chem. 13: 9644-9650; Bernhard et al (1994) Bioconjugate Chem. 5: 126-132; Greenwood et al (1994) Therapeutic Immunology 1: 247-255; Tu et al (1999) Proc. Natl. Acad. Sci USA 96: 4862-4867; Kanno et al (2000) J. of Biotechnology, 76: 207-214; Chmura et al (2001) Proc. Nat. Acad. Sci. USA 98(15): 8480-8484; US 6248564). Тем не менее, конструирование тиоловых групп цистеина посредством мутаций различных аминокислотных остатков белка в аминокислоты цистеина, является потенциально проблематичным, в частности, в случае непарных (свободный Cys) остатков, или тех, которые являются относительно доступными для взаимодействия или окисления. В концентрированных растворах белка, либо в периплазме E.coli, культуральных супернатантах, или частично, или полностью очищенном белке, непарные остатки Cys на поверхности белка могут образовывать пары и окисляться с образованием внутримолекулярных дисульфидов, и, следовательно, белковых димеров или мультимеров. Образование дисульфидных димеров делает новый Cys нереакционноспособным для конъюгирования с лекарственным средством, лигандом или другой меткой. Более того, если белок посредством окисления образует межмолекулярную дисульфидную связь между вновь сконструированным Cys и существующим остатком Cys, тиоловые группы обоих Cys становятся недоступны для участия и взаимодействия активных центров. Кроме того, белок может стать неактивным или неспецифическим в результате неправильного сворачивания или потери третичной структуры (Zhang et al (2002) Anal. Biochem. 311:1-9).
Антитела конструировали с цистеином в виде FAB-фрагментов антител (тиоFab) и экспрессировали в виде полноразмерных, моноклональных IgG (тиоMab) антител (US 2007/0092940, содержание которого включено в настоящий документ посредством ссылки). Антитела ТиоFab и ТиоMab конъюгировали посредством линкеров с вновь введенными тиолами цистеина с использованием тиол-реактивных линкерных реагентов и лекарство-связывающих реагентов, для получения конъюгатов антитело-лекарственное средство (Тио ADC).
TENB2 представляет собой опухолеассоциированный полипептидный антиген (также известный как PR1), и белок TENB2 содержит 2 фоллистатин-подобных домена и консервативный EGF-подобный домен. Ген, кодирующий данный белок, впервые был охарактеризован из библиотеки кДНК человеческого мозга (см. Uchida, et al. (1999) Biochem. Biophys. Res. Commun. 266:593-602), и позднее был выделен из библиотеки кДНК мозга эмбриона человека (см. Horie, et al. (2000) Genomics 67: 146-152). См. также, например, Online Mendelian Inheritance in Man, номер 605734; Unigene Cluster Hs.22791; LocusLink 23671; и другие соответствующие сайты. TENB2 называли PR1, томорегулин, TR, ген гиперпластического полипоза 1, HPP1 и TMEFF2. Последовательность его нуклеиновой кислоты может быть идентифицирована по номерам ATCC AF264150, AB004064, AB017269 и AF179274; и его аминокислотная последовательность может быть идентифицирована по номерам ATCC AAF91397, BAA90820, BAA87897 и AAD55776. Ген TENB2 в базе данных UniGene Cluster имеет идентификационный номер hs.22791, в базе данных Locuslink имеет идентификационный номер 23671, и в базе данных OMIM имеет идентификационный номер 605734.
Ген также связан с некоторыми злокачественными состояниями. Young et al (2001) Proc. Nat'l Acad. Sci. USA 98: 265-270 описали экспрессию в колоректальных полипах. Glynne-Jones et al (2001) Int. J. Cancer 94:178-184 описали его в качестве маркера рака простаты.
В результате его сверхэкспрессии в некоторых опухолях человека, полипептид TENB2 и нуклеиновая кислота, кодирующая этот полипептид, являются объектами для количественного и качественного сравнения между образцами различных тканей млекопитающих. Уникальные профили экспрессии полипептида TENB2, и нуклеиновой кислоты, кодирующей этот полипептид, можно использовать для диагностики и терапевтического лечения некоторых типов злокачественных опухолей млекопитающих.
Недавно были раскрыты некоторые антитела против TENB2, включая антитело # 19 против TMEFF2, и показано, что они могут быть интернализированными и пригодными для лечения пролиферативных состояний предстательной железы, включая например, доброкачественную гиперплазию предстательной железы и рак предстательной железы (PCT/US03/07209; US Ser. № 10/383447, поданной 7 Марта 2003; Vinay et al., «Antibodies Against Cancer Antigen TMEFF2 and Uses Thereof», содержания которых включены путем ссылки).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте, изобретение включает антитело против TENB2, сконструированное с цистеином, содержащее одну или несколько свободных аминокислот цистеина и последовательность, выбранную из последовательностей SEQ ID NO:8-23. Антитело против TENB2, сконструированное с цистеином, может связывать полипептид TENB2. Опухолеассоциированные антигены (TAA), такие как полипептиды TENB2, могут быть получены для использования при создании антител, сконструированных с цистеином, используя методы и информацию, которые хорошо известны и описаны в уровне техники, например, в PCT/US03/07209. Антитело против TENB2, сконструированное с цистеином, может быть получено способом, включающим замену одного или нескольких аминокислотных остатков в родительском антителе против TENB2 на цистеин.
Один или несколько свободных аминокислотных остатков цистеина в антителе против TENB2, сконструированном с цистеином, расположены в легкой цепи или в тяжелой цепи.
В одном аспекте, изобретение включает способ определения наличия белка TENB2 в образце, в котором подозревают наличие указанного белка, включающий воздействие на указанный образец антителом против TENB2, сконструированным с цистеином, и определение связывания указанного антитела с указанным белком TENB2 в указанном образце, где связывание антитела с указанным белком указывает на наличие указанного белка в указанном образце.
Антитела против TENB2, сконструированные с цистеином, можно использовать в качестве "голых" антител (неконъюгированных с лекарственным средством или молекулой-меткой), или в качестве конъюгатов антитело-лекарственное средство (ADC). Антитело против TENB2, сконструированное с цистеином, может быть ковалентно связано с молекулой лекарственного средства ауристатин, в результате чего образуется конъюгат антитело-лекарственное средство. Конъюгат антитело-лекарственное средство может содержать антитело (Ab) против TENB2, сконструированное с цистеином, и молекулу (D) лекарственного средства ауристатин, где антитело против TENB2, сконструированное с цистеином, связано с (D) посредством одной или нескольких аминокислот цистеина с помощью линкерной молекулы (L); соединение имеет формулу I:

где p равно 1, 2, 3 или 4. Молекулы лекарственного средства ауристатин включают MMAE и MMAF.
Аспектом изобретения является способ обнаружения раковых клеток, включающий: (a) воздействие на клетки соединением конъюгата антитело-лекарственное средство; и (b) определение степени связывания соединения конъюгата антитело-лекарственное средство с клетками.
Аспектом изобретения является фармацевтическая композиция, содержащая конъюгат антитело-лекарственное средство, и фармацевтически приемлемый разбавитель, носитель или наполнитель.
Аспектом изобретения является способ ингибирования клеточной пролиферации, включающий обработку опухолевых клеток млекопитающего в среде клеточной культуры соединением конъюгата антитело-лекарственное средство, в результате чего ингибируется пролиферация опухолевых клеток.
Аспектом изобретения является способ лечения рака, включающий введение пациенту фармацевтической композиции. Пациент может применять химиотерапевтическое средство в комбинации с соединением конъюгата антитело-лекарственное средство.
Аспектом изобретения является изделие, содержащее фармацевтическую композицию, контейнер; и листовку-вкладыш в упаковке, или этикетку, в которой указано, что соединение можно использовать для лечения злокачественного новообразования, характеризующегося сверхэкспрессией полипептида TENB2.
Аспектом изобретения является способ получения соединения конъюгата антитело-лекарственное средство формулы I, включающий стадии: (a) взаимодействия сконструированных цистеиновых групп антитела, сконструированного с цистеином, с линкерным реагентом с образованием промежуточного соединения антитело-линкер Ab-L; и (b) взаимодействия Ab-L с активированной молекулой D лекарственного средства; в результате чего образуется конъюгат антитело-лекарственное средство; или включающий стадии: (c) взаимодействия нуклеофильной группы молекулы лекарственного средства с линкерным агентом с образованием промежуточного соединения лекарственное средство-линкер D-L; и (d) взаимодействия D-L с сконструированной цистеиновой группой антитела, сконструированного с цистеином; в результате чего образуется конъюгат антитело-лекарственное средство.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1 представлена последовательность тяжелой цепи: SEQ ID NO:1, и последовательность легкой цепи: SEQ ID NO:2 гуманизированного антитела против TENB2, hu TMEFF2#19.
На фиг.2 представлена последовательность тяжелой цепи: SEQ ID NO:3, и последовательность легкой цепи: SEQ ID NO:2 гуманизированного антитела против TENB2, сконструированного с цистеином, A121C thio hu TMEFF2#19. Сигнальная последовательность не включена в последовательную нумерацию антитела против TENB2.
На фиг.3 представлено выравнивание последовательностей легкой цепи гуманизированного трастузумаба (HuTMAb-LC, SEQ ID NO:4) и легкой цепи hu TMEFF2#19 (SEQ ID NO:5). Нумерация придерживается последовательной нумерации.
На фиг.4 представлено выравнивание последовательностей тяжелой цепи гуманизированного трастузумаба (HuTMAb-HC, SEQ ID NO:6) и тяжелой цепи hu TMEFF2#19 (SEQ ID NO:7). Нумерация придерживается последовательной нумерации.
На фиг.5 изображены конъюгаты антитела против TENB2, сконструированного с цистеином, и лекарственного средства (ADC), где молекула лекарственного средства прикреплена к сконструированной цистеиновой группе в: легкой цепи (LC-ADC); тяжелой цепи (HC-ADC); и в Fc-области (Fc-ADC).
На фиг.6 изображены стадии: (i) восстановления дисульфидных аддуктов цистеина и внутрицепочечных и межцепочечных дисульфидов в антителе против TENB2, сконструированном с цистеином (ТиоMab); (ii) частичного окисления, т.е. переокисления, для повторного формирования межцепочечных и внутрицепочечных дисульфидов; и (iii) конъюгирования переокисленного антитела с промежуточным соединением лекарственное средство-линкер, с образованием конъюгата антитела против TENB2, сконструированного с цистеином, и лекарственного средства (ADC).
На фиг.7 представлена экспрессия TENB2 в раковой и нормальной тканях человека: анализ с олигонуклеотидным микрочипом проводили на РНК, выделенной из 4841 образца тканей человека. Каждый квадратик на графике определяет интенсивность сигнала (среднее отклонение имеет шкалу до 100) TENB2 для образца обозначенной ткани. Зеленые квадратики означают нормальную ткань, красные квадратики означают опухоль, и голубые квадратики отображают ткани других поврежденных тканей.
На фиг.8 представлена экспрессия TENB2 в опухолях предстательной железы человека: верхняя и нижняя панели представляют собой модели эксплантов предстательной железы человека, стабильную клеточную линию среды PC3TENB2 с контрольным вектором и опухолью предстательной железы, соответственно.
На фиг.9 изображена интернализация моноклонального антитела TENB2 (Mab) в клеточной линии среды PC3TENB2 и опухоли LuCaP 70.
На фиг.10 представлены результаты анализа FACS клеток среды PC3 TENB2, после обработки с помощью тио- или стандартного ADC против TENB2.
На фиг.11 представлен анализ клеточного уничтожения на клетках среды PC3 TENB2 с использованием стандартного анти-TENB2 и тио-анти-TENB2 ADC.
На фиг.12 представлен анализ эффективности на клетках среды PC3 TKNB2 с использованием анти-TENB2 и тио-анти-TENB2 ADC (конъюгированный с vc-MMAE или MC-MMAF).
На фиг.13 изображен вестерн-блоттинг с различными эксплантами опухолевой ткани LuCaP, с использованием гуманизированного Ab против TENB2 (hu TMEFF2#19).
На фиг.14 представлены экспериментальные исследования ксенотрансплантов с использованием моделей рака предстательной железы человека LuCaP 70, 77 и 96.1.
На фиг.15 представлена оценка фармакокинетики у крыс, с использованием тио-анти-TENB2 и стандартного ADC.
На фиг.16 представлена оценка безопасности анти-TENB2-vc-MMAE в сравнении с MC-MMAF у крыс.
На фиг.17 представлена оценка безопасности анти-TENB2-vc-MMAE в сравнении с анти-TENB2-MC-MMAF у человекообразных обезьян.
На фиг.18 представлена оценка безопасности тио-анти-TENB2-vc-MMAE в сравнении с анти-TENB2-vc-MMAE у крыс.
ПОДРОБНОЕ ОПИСАНИЕ ИЛЛЮСТРАТИВНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Будет предоставлена подробная информация для некоторых вариантов осуществления данного изобретения, примеры которых проиллюстрированы сопутствующими структурами и формулами. Несмотря на то, что изобретение будет описано в отношении перечисленных вариантов осуществления, будет понятно, что они не предназначены для ограничения изобретения. С другой стороны, изобретение имеет целью охватить все альтернативы, модификации и эквиваленты, которые могут быть включены в объем изобретения, как определено формулой изобретения.
Специалисту в данной области техники известны многие способы и материалы, схожие или эквивалентные описанным в настоящем документе, которые можно использовать при практическом применении настоящего изобретения. Настоящее изобретение никоим образом не ограничено описанными методами и материалами.
ОПРЕДЕЛЕНИЯ
Если не определено иначе, технические и научные термины, используемые в настоящем документе, имеют то же значение, как обычно используемые специалистом в данной области, к которой относится изобретение, и находятся в соответствии с: Singleton et al (1994) Dictionary of Microbiology and Molecular Biology, 2nd Ed., J. Wiley & Sons, New York, NY; and Janeway, C, Travers, P., Walport, M., Shlomchik (2001) Immunobiology, 5th Ed., Garland Publishing, New York.
Термин «антитело» в настоящем документе используется в самом широком смысле и, в частности, охватывает моноклональные антитела, поликлональные антитела, димеры, мультимеры, мультиспецифические антитела (например, биспецифические антитела), и фрагменты антител, при условии, что они проявляют желаемую биологическую активность (Miller et al (2003) Jour. of Immunology 170:4854-4861). Антитела могут быть мышиными или крысиными, человеческими, гуманизированными, химерными или полученными от других биологических видов. Антитело представляет собой белок, который способен распознавать и связывать специфический антиген (Janeway, C., Travers, P., Walport, M., Shlomchik (2001) Immuno Biology, 5th Ed., Garland Publishing, New York). Антиген-мишень, обычно, имеет множество участков связывания, также называемых эпитопами, распознаваемых CDR многочисленных антител. Каждое антитело, которое специфически связывает различные эпитопы, имеет различное строение. Таким образом, один антиген может иметь более чем одно соответствующее антитело. Антитело включает полноразмерную молекулу иммуноглобулина или иммунологически активную часть молекулы полноразмерного иммуноглобулина, а именно, молекулу, которая содержит антигенсвязывающий сайт, который иммуноспецифически связывает антиген-мишень, представляющий интерес, или его часть, такие мишени включают, но не ограничиваются ими, раковые клетки или клетки, которые продуцируют аутоиммунные антитела, ассоциированные с аутоиммунным заболеванием. Иммуноглобулин, раскрытый в настоящем документе, может быть молекулой иммуноглобулина любого типа (например, IgG, IgE, IgM, IgD, и IgA), класса (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2), или подкласса. Иммуноглобулины могут быть получены от любых биологических видов, таких как человек, мышь или крыса, или кролик. Структуру и свойства различных классов антител см., например, в Basic and Clinical Immunology, издание 8, Daniel P. Stites, Abba I. Terr and Tristram G. Parslow (eds.), Appleton & Lange, Norwalk, CT, 1994, страница 71 и Глава 6.
«Фрагменты антител» содержат часть полноразмерного антитела, как правило, его антигенсвязывающую или вариабельную область. Примеры фрагментов антител включают фрагменты Fab, Fab', F(ab')2 и Fv; димерные антитела; линейные антитела; миниантитела (US 5641870, Example 2; Zapata et al (1995) Protein Eng. 8(10): 1057-1062); Olafsen et al (2004) Protein Eng. Design & Sel. 17(4): 315-323), фрагменты, продуцируемые библиотекой экспрессируемых Fab, антиидиотипические антитела (анти-Id), CDR (определяющие комплементарнось области), и эпитопсвязывающие фрагменты любого из вышеперечисленного, которые иммуноспецифически связывают антигены раковых клеток, антигены вирусов или микробные антигены, молекулы одноцепочечных антител; и мультиспецифические антитела, образованные фрагментами антител.
Используемый в настоящем документе термин «моноклональное антитело» относится к антителу, полученному из популяции антител, по существу, гомогенных, т.е., конкретные антитела, образующие популяцию, являются идентичными, за исключением возможных природных мутаций, которые могут присутствовать в незначительном количестве. Моноклональные антитела являются высокоспецифичными, будучи направленными против одного единственного антигенного сайта. Более того, в отличие от препаратов поликлональных антител, которые включают различные антитела, направленные против различных детерминант (эпитопов), каждое моноклональное антитело направлено против одной детерминанты на антигене. В дополнение к их специфичности, моноклональные антитела являются предпочтительными в силу того, что они могут быть синтезированы без контаминации другими антителами. Определение «моноклональное» обозначает характер антитела, как полученного из по существу гомогенной популяции антител, и не должно рассматриваться, как требующее получение антитела каким-либо конкретным способом. Например, моноклональные антитела, используемые в соответствии с настоящим изобретением, могут быть получены посредством гибридомной технологии, впервые описанной Kohler и соавторами (1975) Nature 256:495, или могут быто получены с помощью методов рекомбинантных ДНК (см., например: US 4816567; US 5807715). При использовании гибридомного метода мышь или другое подходящее животное-хозяин, такое как хомячок, иммунизируют, как описано выше, для выявления лимфоцитов, которые продуцируют или способны к продукции антител, которые будут специфически связывать белок, используемый для иммунизации. Альтернативно, лимфоциты могут быть иммунизированы in vitro. После иммунизации лимфоциты выделяют и затем объединяют с клеточной линией миеломы, используя подходящее средство, вызывающее слияние клеток, например, полиэтиленгликоль, для образования клетки гибридомы (Goding, (1986) Monoclonal Antibodies: Principles and Practice, pp.59-103 Academic Press). Моноклональные антитела также могут быть выделены из фаговых библиотек антител с использованием технологий, описанных у Clackson и соавторов (1991) Nature, 352: 624-628; Marks et al (1991) J. Mol. Biol., 222: 581-597.
ДНК, которая кодирует антитело, может быть модифицирована с целью продукции полипептидов химерных или слитых антител, например, путем использования последовательностей константных доменов (CH и CL) тяжелой цепи и легкой цепи человека вместо гомологичных последовательностей мыши (US 4816567; и Morrison, et al., Proc. Natl Acad. Sci. USA, 81: 6851 (1984)), или посредством слияния кодирующей последовательности иммуноглобулина с полной или частичной, кодирующей последовательностью полипептида неиммуноглобулинового происхождения (гетерологичный полипептид). Последовательности полипептида неиммуноглобулинового происхождения можно использовать вместо константных доменов антитела, или их можно использовать вместо вариабельных доменов одного антигенсвязывающего сайта антитела, для создания химерного двухвалентного антитела, содержащего один антигенсвязывающий сайт, имеющий специфичность к одному антигену, и другой антигенсвязывающий сайт, имеющий специфичность к другому антигену.
«Нативные антитела» представляют собой обычно гетеротетрамерные гликопротеины, размером около 150000 дальтон, состоящие из двух идентичных дегких (L) цепей и двух идентичных тяжелых (Н) цепей. Каждая легкая цепь связана с тяжелой цепью одной ковалентной дисульфидной связью, тогда как количество дисульфидных связей различается между тяжелыми цепями различных изотипов иммуноглобулина. Каждая тяжелая и легкая цепь также имеет расположенные на равном расстоянии друг от друга межцепочечные дисульфидные мостики. Каждая тяжелая цепь имеет на одном конце вариабельный домен (VH), за которым следует ряд константных доменов. Каждая легкая цепь имеет вариабельный домен на одном конце (VL) и константный домен на другом конце. Константный домен легкой цепи связан с первым константным доменом тяжелой цепи, и вариабельный домен легкой цепи связан с вариабельным доменом тяжелой цепи. Полагают, что специфические аминокислотные остатки образуют сопряжение между вариабельными доменами легкой цепи и тяжелой цепи.
Моноклональные антитела в этом документе в частности включают «химерные» антитела, в которых часть тяжелой и/или легкой цепи является идентичной с или гомологичной к соответствующим последовательностям антител, полученным от определенных биологических видов или принадлежащих к определенному классу или подклассу антител, в то время как оставшаяся часть цепи (цепей) является идентичной или гомологичной соответствующим последовательностям в антителах, полученных от других биологических видов или принадлежащих другому классу или подклассу антител, а также фрагментов таких антител, при условии, что они проявляют необходимую биологическую активность (US 4816567; и Morrison et al (1984) Proc. Natl. Acad. Sci. USA, 81: 6851-6855). В настоящем документе представляющие интерес химерные антитела включают «приматизированные» антитела, содержащие антигенсвязывающие последовательности вариабельных доменов, полученные от приматов, не принадлежащих к человеческому роду (например, старосветская мартышка, человекообразная обезьяна, и др.), и последовательности константной области человека.
«Гуманизированные» формы отличных от человеческих (например, грызунов) антител представляют собой химерные антитела, которые содержат минимальную последовательность, полученную из нечеловеческого антитела. Преимущественно, гуманизированные антитела представляют собой иммуноглобулины человека (реципиентное антитело), в котором остатки из гипервариабельной области реципиента заменены на остатки из гипервариабельной области биологического вида, отличного от человека, (донорное антитело), например, мыши, крысы, кролика или примата, не относящегося к человеческому роду, имеющего требуемую антительную специфичность, аффинность и потенциал. В ряде случаев, остатки каркасной области (FR) иммуноглобулина человека заменены соответствующими, отличными от человеческих, остатками. Кроме того, гуманизированные антитела могут содержать остатки, которые не обнаружены в реципиентном антителе или в донорном антителе. Эти модификации осуществлены для дополнительного совершенствования функциональной активности антител. В общем, гуманизированные антитела будут содержать по существу все, по меньшей мере, из одного, а обычно, двух вариабельных доменов, в которых все, или в основном все, из гипервариабельных петель соответствуют таковым нечеловеческого иммуноглобулина, и все, или в основном все, FR являются таковыми из последовательности человеческого иммуноглобулина. Гуманизированное антитело также необязательно будет содержать, по меньшей мере, часть константной области иммуноглобулина (Fc), обычно, иммуноглобулина человека. Фрагмент Fc содержит карбоксиконцевые части обеих Н-цепей, удерживаемых вместе дисульфидами. Эффекторные функции антител определены последовательностями в области Fc, которая также частично распознается рецепторами Fc (FcR), обнаруженными в некоторых типах клеток (Jones et al (1986) Nature 321: 522-525; Riechmann et al (1988) Nature 332: 323-329; Presta, (1992) Curr. Op. Struct. Biol. 2: 593-596; Verhoeyen et al (1988) Science, 239: 1534-1536; Sims et al (1993) J. Immunol. 151: 2296; Chothia et al (1987) J. Mol. Biol., 196: 901). В других способах используют определенную каркасную область, полученную из консенсусной последовательности всех легких или тяжелых цепей антител человека определенной подгруппы (Carter et al (1992) Proc. Natl. Acad. Sci. USA, 89: 4285; Presta et al (1993) J. Immunol. 151: 2623).
«Антитело человека» представляет собой такое антитело, которое имеет аминокислотную последовательность, соответствующую той, что принадлежит антителу, продуцируемому у человека, и/или было создано с использованием любой технологии для получения антител человека, как раскрыто в настоящем документе. Это определение антитела человека в частности включает гуманизированные антитела, содержащие антигенсвязывающего остатки нечеловеческого происхождения. Существуют трансгенные животные (например, мыши), которые способны в условиях иммунизации продуцировать полный набор антител человека при отсутствии продуцирования эндогенного иммуноглобулина. Например, было описано, что гомозиготная делеция гена области присоединения тяжелой цепи антитела (JH) В химерной и зародышевой линии мутантых мышей приводит к полному ингибированию продукции эндогенных антител. Перенос элемента гена иммуноглобулина зародышевой линии человека в такую зародышевую линию мутантной мыши приведет к продуцированию антител человека после антигенной стимуляции (Jakobovits et al (1993) Proc. Natl. Acad. Sci. USA, 90: 2551; Jakobovits et al (1993) Nature, 362: 255-258; Bruggemann et al (1993) Year in Immuno. 7: 33; US 5545806; US 5569825; US 5591669; US 5545807; и WO 97/17852).
Антитело со «зрелой аффинностью» имеет одно или несколько изменений в одной или нескольких своих CDR, что приводит к повышению аффинности антитела к антигену по сравнению с антителом, которое не обладает таким изменением (изменениями). Предпочтительные антитела со зрелой аффинностью будут иметь наномолярные или даже пикомолярные аффинности с антигеном-мишенью. Антитела со зрелой аффинностью продуцируют высокую аффинность посредством перестановки VH и VL доменов (Marks et al (1992) Bio/Technology 10: 779-783), или неспецифического мутагенеза остатков CDR и/или каркасной области (Barbas et al (1994) Proc Nat. Acad. Sci, USA 91: 3809-3813; Schicr et al (1995) Gene 169: 147-155; Yelton et al (1995) J. Immunol. 155: 1994-2004; Jackson et al (1995) J. Immunol. 154(7): 3310-9; и Hawkins et al (1992) J. Mol. Biol. 226: 889-896).
«Интактное антитело» в настоящем документе означает такое антитело, которое содержит домены VL и VH, а также константный домен легкой цепи (CL) и константные домены тяжелой цепи CH1, CH2 и CH3. Константные домены могут быть константными доменами с нативными последовательностями (например, константные домены с нативными последовательностями человека), или аминокислотные последовательности их вариантов. Интактное антитело может иметь одну или несколько «эффекторных функций», которые относятся к тем биологическим активностям, связанным с константной областью Fc антитела (нативная последовательность области Fc или аминокислотная последовательность варианта области Fc). Примеры эффекторных функций антитела включают связывание C1q; комплементзависимую цитотоксичность; связывание рецептора Fc; антителозависимую клеточноопосредованную цитотоксичность (ADCC); фагоцитоз; и даун-регуляцию рецепторов клеточной поверхности, таких как рецептор В-клетки и BCR.
Термин «вариант аминокислотной последовательности» относится к полипептидам, имеющим аминокислотные последовательности, которые до некоторой степени отличаются от нативной последовательности полипептида. Обычно, варианты аминокислотных последовательностей будут обладать, по меньшей мере, приблизительно 70% идентичной последовательностью с, по меньшей мере, одним рецепторсвязывающим доменом нативной последовательности полипептида или с, по меньшей мере, одним лигандсвязывающим доменом нативного рецептора, предпочтительно, они будут, по меньшей мере, на приблизительно 80%, более предпочтительно, по меньшей мере, на приблизительно 90% гомологичны с последовательностями рецептор- или лигандсвязывающих доменов. Варианты аминокислотных последовательностей имеют замены, делеции и/или вставки в некоторых положениях внутри аминокислотной последовательности нативной аминокислотной последовательности. Аминокислоты обозначаются посредством общепринятых обозначений, с ипользованием однобуквенного и трехбуквенного кодов.
«Идентичность последовательности» определяется как процентное содержание остатков в варианте аминокислотной последовательности, которые являются идентичными после выравнивания последовательностей и введения пропусков, при необходимости, для достижения максимального процента идентичности последовательности. В уровне техники хорошо известны методы и компьютерные программы для выравнивания последовательностей. Одной такой программой является «Align 2», разработанная компанией Genentech, Inc., которая была зарегистрирована ведомством по охране авторских прав Соединенных Штатов, Вашингтон (округ Колумбия) 20559, 10 Декабря 1991, и чей код встречается в PCT/US03/07209.
«Антителозависимая клеточноопосредованная цитотоксичность» и «ADCC» относятся к клеточноопосредованной реакции, при которой неспецифические цитотоксические клетки, экспрессирующие рецепторы Fc (FcR) (например, натуральные клетки-киллеры (NK), нейтрофилы и макрофаги) распознают связанное антитело с клеткой-мишенью и впоследствии вызывают лизис клетки-мишени. Первичные клетки, опосредующие ADCC, NK-клетки, экспрессируют только FcγRIII, тогда как моноциты экспрессируют FcγRI, FcγRII и FcγRIII. Экспрессия FcR гематопоэтическими клетками, в целом, приведена в Таблице 3 на странице 464 у Ravetch and Kinet, (1991) «Annu. Rev. Immunol.» 9: 457-92. Для оценки ADCC действия представляющей интерес молекулы можно провести in vitro ADCC анализ, например такой, как описан в US 5500362 и US 5821337. Пригодные эффекторные клетки для такого анализа включают мононуклеарные клетки периферической крови (PBMC) и натуральные клетки-киллеры (NK). Альтернативно или дополнительно, ADCC активность представляющей интерес молекулы может быть оценена in vivo, например, на модели животного, такой как описана у Clynes et al (1998) Proc. Nat. Acad. Sci. (USA) 95: 652-656.
«Эффекторными клетками человека» являются лейкоциты, которые экспрессируют рецепторы одной или нескольких константных областей (FcR) и выполняют эффекторные функции. Предпочтительно, данные клетки экспрессируют, по меньшей мере, FcγRIII и выполняют эффекторную функцию ADCC. Примеры лейкоцитов человека, которые опосредуют ADCC, включают мононуклеарные клетки периферической крови (PBMC), натуральные клетки-киллеры (NK), моноциты, цитотоксические Т-клетки и нейтрофилы; с предпочтением клеткам PBMC и NK. Эффекторные клетки могут быть выделены из их нативного источника, например, из крови или PBMC, как описано в настоящем документе.
Термины «рецептор Fc» или «FcR» означают рецептор, который связывается с константной областью Fc антитела. Предпочтительным FcR является нативная последовательность FcR человека. Более того, предпочтительным FcR является тот, который связывает антитело IgG (гамма-рецептор), и включает рецепторы подклассов FcγRI, FcγRII и FcγRIII, включая аллельные варианты этих рецепторов и альтернативно сплайсированные формы рецепторов. Рецепторы FcγRII включают FcγRIIА («активирующий рецептор») и FcγRIIВ («ингибирующий рецептор»), имеющие схожие аминокислотные последовательности, которые различаются в основном их цитоплазматическими доменами. Активирующий рецептор FcγRIIA включает мотив активации иммунорецептора на основе тирозина (ITAM) в своем цитоплазматическом домене. Ингибирующий рецептор FcγRIIB содержит мотив ингибирования иммунорецептора на основе тирозина (ITIM) в своем цитоплазматическом домене. (См. обзор M. in Daeron, (1997) «Annu. Rev. Immunol.» 15: 203-234). FcR рассматриваются у Ravctch and Kinet, (1991) «Annu. Rev. Immunol», 9: 457-92; Capel et al (1994) Immunomethods 4: 25-34; и de Haas et al (1995) J. Lab. Clin. Med. 126: 330-41. Другие FcR, в том числе те, которые будут определены в будущем, охвачены в настоящем документе термином «FcR». Данный термин также включает неонатальный рецептор, FcRn, который ответственен за перенос материнских IgG к зародышу (Guyer et al (1976) J. Immunol, 117: 587 и Kim et al (1994) J. Immunol. 24: 249).
«Комплементзависимая цитотоксичность» или «CDC» относится к лизису клетки-мишени в присутствии комплемента. Активация классического каскада реакций комплемента стимулируется связыванием первого компонента системы комплемента (C1 q) с антителами (соответствующего подкласса), которые связаны с их узнаваемым антигеном (Gazzano-Santoro et al (1996) J. Immunol. Methods 202: 163).
Термин «вариабельный» относится к тому факту, что некоторые части вариабельных доменов различаются экстенсивно в последовательностях между антителами, и используются для связывания и специфичности каждого конкретного антитела для его конкретного антигена. Тем не менее, вариабельность распределена неравномерно на всем протяжении вариабельных доменов антител. Она сконцентрирована в трех сегментах, называемых гипервариабельными областями и в вариабельных доменах легкой цепи, и в вариабельных доменах тяжелой цепи. Более высококонсервативные части вариабельных доменов называются каркасными областями (FR). Каждый из вариабельных доменов нативной тяжелой и легкой цепей включает четыре FR, в основном имеющих β-складчатую конфигурацию, соединенных с тремя гипервариабельными областями, которые образуют петли, соединяющиеся, и в некоторых случаях, образующие часть β-складчатой структуры. Гипервариабельные области в каждой цепи удерживаются вместе в тесной пространственной близости с помощью FR и с гипервариабельными областями другой цепи, участвуя в образовании антигенсвязывающего сайта антител (см. Kabat et al (1991) Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD). Константные домены не вовлечены напрямую в связывание антитела с антигеном, но выполняют различные эффекторные функции, такие как участие антитела в антителозависимой клеточноопосредованной цитотоксичности (ADCC).
Термин «гипервариабельная область», «HVR», или «HV», в данном документе, относится к областям вариабельных доменов антитела, которые гипервариабельны по последовательности и/или формируют структурно определенные петли. Как правило, антитела содержат шесть гипервариабельных областей; три в VH (H1, H2, H3), и три в VL (L1, L2, L3). Ряд описания гипервариабельных областей используется и охвачен настоящим изобретением. Чаще всего используют определяющие комплементарность области Кабата (CDR), основанные на вариабельности последовательностей (Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991)). Chothia вместо этого рассматривает положение структурных петель (Chothia and Lesk J. Mol. Biol. 196: 901-917 (1987)). «Контактные» гипервариабельные области основаны на анализе доступных комплексов кристаллических структур. Остатки каждой из этих гипервариабельных областей указаны ниже. Если не обозначено иначе, будет использоваться нумерация Кабата в соответствии с базой данных Кабата по выровненным последовательностям белков (Wu and Kabat (1970) J. Exp. Med. 132: 211-250; Johnson and Wu (2000) Nuc. Acids Res. 28(1): 214-218). Расположения гипервариабельной области в основном следующие: аминокислоты 24-34 (HVR-L1), аминокислоты 49-56 (HVR-L2), аминокислоты 89-97 (HVR-L3), аминокислоты 26-35A (HVR-H1), аминокислоты 49-65 (HVR-H2) и аминокислоты 93-102 (HVR-H3). Гипервариабельные области также могут содержать «протяженные гипервариабельные области», например: аминокислоты 24-36 (L1) и аминокислоты 46-56 (L2) на VL. Остатки вариабельных доменов пронумерованы по Кабату, выше, для каждого из этих определений. «Измененная гипервариабельная область» в данном документе, представляет собой гипервариабельную область, имеющую одну или несколько (например, от одной до приблизительно 16) аминокислотных замен. «Немодифицированная гипервариабельная область» в данном документе, представляет собой гипервариабельную область, имеющую ту же самую аминокислотную последовательность, что и антитело нечеловеческого происхождения, из которого его выделили, т.е. такую, в которой не содержится одна или несколько аминокислотных замен.
Термины «остатки вариабельных доменов, пронумерованные по Кабату», «аминокислотные положения, пронумерованные по Кабату» и их варианты, относятся к системы нумерации, используемой для вариабельных областей тяжелой цепи или вариабельных областей легкой цепи собрания антител, представленной у Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991). При использовании этой системы нумерации, фактическая линейная аминокислотная последовательность может содержать меньшее число или дополнительные аминокислоты, соответствующие укорочению, или вставке в FR или CDR вариабельного домена. Например, вариабельный домен тяжелой цепи может включать вставку одной аминокислоты (остаток 52А по Кабату) после остатка 52 в Н2 и вставленные остатки (например, 82a, 82b, и 82c, и тому подобное, по Кабату) после остатка 82 в FR тяжелой цепи. Нумерация остатков по Кабату может быть определена для антитела посредством выравнивания областей гомологии последовательности антитела со «стандартной» последовательностью, пронумерованной по Кабату.
«Аффинность связывания», в целом, относится к силе совокупных нековалентных взаимодействий между единственным участком связывания на молекуле (например, антитело) и его партнером по связыванию (например, антиген). Если не обозначено иначе, при использовании в настоящем документе, «аффинность связывания» относится к внутренней связывающей аффинности, что отражает 1:1 взаимодействие между членами связывающейся пары (например, антитело и антиген). Аффинность молекулы Х к ее партнеру Y, в основном можно выразить посредством константы диссоциации (Kd). Аффинность может быть измерена, используя общеупотребительные способы, известные в уровне техники, включая те, которые описаны в настоящем документе. Антитела с низкой аффинностью обычно связывают антиген медленно и имеют тенденцию к быстрой диссоциации, в то время как антитела с высокой аффинностью, обычно, связывают антиген быстрее и имеют тенденцию сохранять связь дольше. В уровне техники известно множество способов измерения аффинности связывания, любой из которых может быть использован в целях настоящего изобретения. Конкретные иллюстративные варианты осуществления описаны далее.
«Антиген» представляет собой предетерминированный полипептид, углевод, нуклеиновую кислоту, липид, гаптен или другое, природное или искусственное соединение, с которым антитело избирательно связывается.
Остатками «каркасной области» или «FR» являются те остатки вариабельного домена, которые отличаются от остатков гипервариабельных областей, как определено в настоящем документе. «Консенсусная каркасная область человека» представляет собой каркасную область, в которой представлены наиболее часто встречающиеся аминокислотные остатки в выборке последовательностей каркасной области VL или VH иммуноглобулина человека. В основном, выбор последовательностей VL или VH иммуноглобулина человека осуществляют из подгруппы последовательностей вариабельных доменов. Как правило, подгруппа последовательностей представляет собой подгруппу, описанную у Kabat et al, Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD. (1991). В одном варианте осуществления, для VL, подгруппа представляет собой подгруппу каппа I по Kabat et al. В одном варианте осуществления, для VH, подгруппа представляет собой подгруппу III по Kabat et al. «Консенсусная каркасная область VH подгруппы III» включает консенсусную последовательность, полученную из аминокислотных последовательностей вариабельной тяжелой подгруппы III по Kabat et al. «Консенсусная каркасная область VL подгруппы I» включает консенсусную последовательность, полученную из аминокислотных последовательностей вариабельной легкой каппа подгруппы I по Kabat et al.
«Fv» является минимальным фрагментом антитела, который содержит полный антигенраспознающий и антигенсвязывающий сайт. Эта область состоит из димера вариабельного домена одной тяжелой и одной легкой цепи в тесной нековалентной связи. Именно в этой конфигурации три гипервариабельных области каждого вариабельного домена взаимодействуют для определения антиген-связывающего сайта на поверхности димера VH-VL. Сообща, данные шесть гепервариабельных области придают антигенсвязывающую специфичность антителу. Однако, даже единственный вариабельный домен (или половина Fv, включающая только три гипервариабельных области, специфичных для антигена), обладает способностью распознавать и связывать антиген, хотя и с более низкой аффинностью, чем целый участок связывания.
Фрагмент Fab также содержит константный домен легкой цепи и первый константный домен (CH1) тяжелой цепи. Фрагменты Fab' отличаются от фрагментов Fab добавлением нескольких остатков на карбоксильном конце домена СР1 тяжелой цепи, включая один или несколько цистеинов шарнирной области антитела. Fab'-SH в настоящем документе является обозначением для Fab', в котором цистеиновый остаток (остатки) в константном домене, несет, по меньшей мере, одну свободную тиоловую группу. Фрагменты антитела F(ab')2, обычно вырабатываются в виде пар фрагментов Fab', которые имеют цистеиновые шарниры между собой. Также известны другие химические соединения фрагментов антител.
«Легкие цепи» антитела из любого вида позвоночных могут быть отнесены к одному из двух совершенно разных типов, называемых каппа (κ) и лямбда (λ), на основании аминокислотных последовательностей их константных доменов.
«Одноцепочные Fv» или «scFv» фрагменты антител включают домены VH и VL антитела, где эти домены представлены одной полипептидной цепью. Предпочтительно, полипептид Fv дополнительно содержит полипептидный линкер между доменами VH и VL, что обеспечивает возможность scFv образовывать необходимую структуру для связывания антигена (Plückthun in The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds., Springer-Verlag, New York, pp. 269-315 (1994)).
Термин «димерное антитело» относится к малым фрагментам антитела с двумя антигенсвязывающими сайтами, эти фрагменты содержат вариабельный домен тяжелой цепи (VH), соединенный с вариабельным доменом легкой цепи (VL) в той же полипептидной цепи (VH - VL). Используя линкер, слишком короткий для обеспечения соединения между двумя доменами на одной и той же цепи, домены вынуждены соединяться с комплементарными доменами другой цепи и образовывать два антигенсвязывающих сайта (EP 404097; WO 93/11161; Hollinger et al (1993) Proc. Natl. Acad. Sci. USA 90: 6444-6448).
«Свободная аминокислота цистеина» относится к остатку аминокислоты цистеина, который был встроен в родительское антитело, имеет тиоловую функциональную группу (-SH) и не соединен или как-то иначе не является частью внутримолекулярного или межмолекулярного дисульфидной мостика.
Термин «значение тиоловой реактивности» представляет собой количественную характеристику реактивности свободных аминокислот цистеина. Значение тиоловой реактивности представляет собой процентное содержание свободной аминокислоты цистеина в антителе, сконструированном с цистеином, которая реагирует с тиол-реактивным реагентом, и преобразовано в максимальное значение 1. Например, свободная аминокислота цистеина в сконструированном с помощью цистеина антителе, которая реагирует в 100%-м объеме с тиол-реактивным реагентом, таким как биотинмалеимидный реагент, с образованием антитела, меченного биотином, имеет значение тиоловой реактивности, равное 1,0. Другая аминокислота цистеина, встроенная в то же самое или другое родительское антитело, которая реагирует с тиол-реактивным реагентом в 80%-ном объеме, имеет значение тиоловой реактивности, равное 0,8. Другая аминокислота цистеина, встроенная в то же самое или другое родительское антитело, которая абсолютно не вступает в реакцию с тиол-реактивным реагентом, имеет значение тиоловой реактивности, равное 0. Определение значения тиоловой реактивности конкретного цистеина может быть проведено посредством анализа ELISA, масс-спектроскопии, жидкостной хроматографии, ауторадиографии, или других количественных аналитических тестов. Тиол-реактивные реагенты, которые обеспечивают захват антитела, сконструированного с цистеином, и сравнение и количественное определение реактивности цистеина, включают биотин-РЕО-малеимид ((+)-биотинил-3-малеимидопропионамидил-3,6-диоксаоктаиндиамин, Oda et al (2001) Nature Biotechnology 19: 379-382, Pierce Biotechnology, Inc.) биотин-BMCC, PEO-йодоацетил биотин, йодоацетил-LC-биотин, и биотин-HPDP (Pierce Biotechnology. Inc.), и Nα-(3-малеимидилпропионил)биоцитин (MPB, Molecular Probes, Eugene, OR). Другие коммерческие источники для биотинилированных, бифункциональных и мультифункциональных линкерных реагентов включают компании Molecular Probes, Eugene, OR, и Sigma, St. Louis, MO
«Родительское антитело» представляет собой антитело, содержащее аминокислотную последовательность, в которой один или несколько аминокислотных остатков заменены на один или несколько остатков цистеина. Родительское антитело может содержать последовательность, нативную или дикого типа. Родительское антитело может иметь предсуществующие аминокислотные модификации (например, вставки, делеции и/или замены) по сравнению с другими нативными, дикого типа или модифицированными формами антитела. Родительское антитело может быть направлено против представляющего интерес антигена-мишени, например, биологически важного полипептида. Также рассмотрены антитела, направленные против неполипептидных антигенов (таких как опухолеассоциированные гликолипидные антигены, см. US 5091178).
«Изолированным» антителом считают то, которое было идентифицировано и выделено и/или восстановлено из компонента его природного окружения. Компоненты загрязняющей примеси его природного окружения представляют собой вещества, которые будут препятствовать диагностическому или терапевтическому использованию данного антитела, и могут включать ферменты, гормоны и другие белковые или небелковые растворимые вещества. В предпочтительных вариантах осуществления антитело будет очищено (1) до более чем 95% по массе антитела, что определяют по методу Лоури, и наиболее предпочтительно до более чем 99% по массе, (2) до степени, достаточной для получения, по меньшей мере, 15 остатков с N-конца или из внутренней аминокислотной последовательности при использовании вращательного секвенатора, или (3) гомогенности по SDS-PAGE в восстанавливающих или невосстанавливающих условиях с использованием окрашивания кумасси синим или предпочтительно серебром. Изолированное антитело включает антитело in situ в рекомбинантных клетках, если не будет присутствовать, по меньшей мере, один компонент природного окружения антитела. Тем не менее, обычно, изолированное антитело получают с использованием, по меньшей мере, одного этапа очистки.
Антитело, «которое связывает» молекулярную мишень или представляющий интерес антиген, например, антигены TENB2 или CA125, представляет собой такое антитело, которое способно связывать этот антиген с достаточной аффинностью, таким образом, чтобы антитело было пригодным для нацеливания на клетку, экспрессирующую антиген. Когда антитело является таким, которое связывает TENB2, оно обычно будет предпочтительно связывать TENB2, и может быть не будет давать значительную перекресную реакцию с другими белками. В таких вариантах осуществления степень связывания антитела с такими не-TENB2 белками (например, белки клеточной поверхности, связывающиеся с эндогенным рецептором) будет менее 10%, как определено с помощью анализа клеточного сортера с возбуждением флуоресценции (FACS) или радиоиммунопреципитации (RIA).
«Обработка», или «лечение», или «облегчение» относятся и к терапевтическому лечению, и к профилактическим или предупредительным мерам, где целью является предотвращение или замедление (уменьшение) целевого патологического состояния или нарушения. Те, кто нуждается в таком лечении, включают уже имеющих данное нарушение, а также и тех, у кого данное нарушение должно быть предотвращено. Человек или млекопитающее успешно «пролечен» относительно рака, экспрессирующего СА125/О772Р полипептид, если после приема терапевтического количества антитела против СА125/О772Р, такого как антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, в соответствие с методами по настоящему изобретению, у пациента наблюдают видимое и/или измеряемое уменьшение в или отсутствии одного или нескольких признаков из перечисленного: уменьшение количества раковых клеток или отсутствие раковых клеток; уменьшение размера опухоли; ингибирование (то есть, замедление до некоторой степени или предпочтительно остановка) инфильтрации раковых клеток в перефирические органы, включая распространение рака в мягкие ткани и кость; ингибирование (то есть, замедление до некоторой степени или предпочтительно остановка) опухолевого метастазирования; ингибирование, до некоторой степени, роста опухоли; и/или ослабление, до некоторой степени, одного или нескольких симптомов, ассоциированных с определенным раком; снижение заболеваемости и смертности, и улучшение качества жизни. В зависимости от степени, в которой антитело против TENB2, сконструированное с цистеином, или его конъюгат антитело-лекарственное средство, может предотвращать рост и/или уничтожать существующие раковые клетки, оно может быть цитостатическим и/или цитотоксическим. Пациент также может ощущать уменьшение этих признаков или симптомов. Рассмотренные выше показатели для оценки успешности лечения и улучшения течения заболевания являются быстро определяемыми посредством рутинных процедур, хорошо известных врачу. Для терапии рака, эффективность может быть измерена, например, оценивая время прогрессирования заболевания (ТТР) и/или определяя скорость реагирования (RR). Метастазирование может быть установлено при определении стадии заболевания и посредством сканирования костей, и по тестам на уровень кальция и других ферментов для выявления распространения процесса в кости. Срезы CT также могут быть выполнены для обзора распространения процесса в область таза и лимфатических сосудов этой области. Рентген грудной клетки и определение уровней печеночных ферментов известными способами используют для выявления метастазов в легкие и печень, соответственно. Другие рутинные способы контролирования заболевания включают трансректальное ультразвуковое исследование (TRUS) и трансректальную пункционную биопсию (TRNB).
Термины «рак» и «раковый» относятся к описанию физиологического состояния у млекопитающих, которое обычно характеризуется нерегулируемым клеточным ростом. «Опухоль» содержит одну или несколько раковых клеток и относится ко всякому опухолевому клеточному росту и пролиферации, либо злокачественному, либо доброкачественному, и ко всем предраковым и раковым клеткам и тканям. Примеры рака включают, но не ограничиваются ими, карциному, лимфому, бластому, саркому, и лейкемию или лимфолейкоз. Более конкретные примеры таких раков включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легких, включая мелкоклеточный рак легких, немелкоклеточный рак легких («NSCLC»), аденокарциному легких и плоскоклеточную карциному легких, рак брюшины, гепатоцеллюлярный рак, гастральный или рак желудка, включая рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, карциному эндометрия или рак матки, рак слюнной железы, рак почки или почечный рак, рак предстательной железы, рак вульвы, рак щитовидной железы, печеночную карциному, рак заднего прохода, карциному полового члена, а также рак головы и шеи.
Раком, который «сверхэкспрессирует» антигенный рецептор, является такой, при котором имеются значительно более высокие уровни рецептора, например, TENB2, на клеточной поверхности, по сравнению с нераковыми клетками ткани того же типа. Такая сверхэкспрессия может быть результатом амплификации гена, или увеличенной транскрипции или трансляции. Сверхэкспрессия рецептора может быть определена при диагностическом или прогностическом исследовании посредством оценки увеличенных уровней рецепторного белка, представленного на поверхности клетки (например, посредством иммуногистохимического анализа; IHC). Альтернативно или дополнительно, можно измерить уровни нуклеиновой кислоты, кодирующей рецептор, в клетке, например, посредством флуоресцентной гибридизациии in situ (FISH; см. WO 98/45479), саузерн-блоттинга или технологий полимеразной цепной реакции (ПЦР), такой как количественная ПЦР с обратной транскриптазой в режиме реального времени (qRT-PCR).
«Эффекторными клетками человека» являются лейкоциты, которые экспрессируют один или несколько FcR и выполняют эффекторные функции. Предпочтительно, данные клетки экспрессируют, по меньшей мере, FcγRIII и выполняют эффекторную функцию ADCC. Примеры лейкоцитов человека, которые опосредуют ADCC, включают мононуклеарные клетки периферической крови (PBMC), натуральные клетки-киллеры (NK), моноциты, цитотоксические Т-клетки и нейтрофилы; с предпочтением PBMC и NK-клеткам. Эффекторные клетки могут быть изолированы из нативного источника, например, из крови.
Термины «клеточно-пролиферативное нарушение» и «пролиферативное нарушение» относятся к нарушениям, которые связаны с атипичной клеточной пролиферацией некоторой степени. В одном варианте осуществления клеточно-пролиферативным заболеванием является рак.
Термин «терапевтически эффективное количество» относится к количеству лекарственного средства, например, конъюгата лекарственное средство-антитело против TENB2, сконструированное с цистеином, или химиотерапевтического средства, эффективного для лечения заболевания или нарушения у млекопитающего. В отношении рака терапевтически эффективное количество лекарственного средства может уменьшать число раковых клеток; уменьшать размер опухоли; ингибировать (т.е., замедлять до некоторой степени или предпочтительно останавливать) инфильтрацию раковых клеток в периферические органы; ингибировать (то есть, замедлять до некоторой степени или предпочтительно останавливать) опухолевое метастазирование; ингибировать, до некоторой степени, рост опухоли; и/или ослаблять, до некоторой степени, один или нескольких симптомов, ассоциированных с раком. В зависимости от степени, в которой лекарственное средство может предотвращать рост и/или уничтожать существующие раковые клетки, оно может быть цитостатическим и/или цитотоксическим. Термин «цитостатический» относится к эффекту ограничения функционирования клеток, например, ограничение клеточного роста или пролиферации клеток. Для терапии рака, эффективность может быть измерена, например, оценивая время прогрессирования заболевания (ТТР) и/или определяя скорость реагирования (RR).
«Химиотерапевтическое средство» представляет собой химическое соединение, используемое для лечения рака. Примеры химиотерапевтических средств включают эрлотиниб (TARCEVA®, Genentech/OSI Pharm.), бортезомиб (VELCADE®, Millenium Pharm.), фулвестрант (FASLODEX®, AstraZeneca), сутент (SU11248, Pfizer), летрозол (FEMARA®, Novartis), иматиниб мезилат (GLEEVEC®, Novartis), PTK787/ZK 222584 (Novartis), оксалиплатин (Eloxatin®, Sanofi), 5-FU (5-фторурацил), лейковорин, Рапамицин (сиролимус, RAPAMUNE®, Wyeth), лапатиниб (TYKERB®, GSK572016, GlaxoSmithKline), лонафарниб (SCH 66336), сорафениб (BAY43-9006, Bayer Labs.), и гефитиниб (IRESSA®, Astrazeneca), AG1478, AG1571 (SU 5271; Суген), алкилирующие агенты, такие как тиотепа и CYTOXAN® циклосфосфамид; алкилсульфонаты, такие как бусульфан, импросульфан и пипосульфан; азиридины, такие как бензодопа, карбоквон, метуредопа и уредопа; этиленимины и метиламеламины, включая алтретамин, триэтиленмеламин, триэтиленфосфорамид, триэтилентиофосфорамид и триметиломеламин; ацетогенины (в особенности, буллатацин и буллатацинон); камптотецин (включая синтетический аналог топотекана); бриостатин; каллистатин; CC-1065 (включая его синтетические аналоги адозелезин, карзелезин и бизелезин); криптофицины (в частности, криптофицин 1 и криптофицин 8); доластатин; дуокармицин (включая синтетические аналоги KW-2189 и CB1-TM1); элеутеробин; панкратистатин; саркодиктиин; спонгистатин; азотистые иприты, такие как хлорамбуцил, хлорнафазин, хлорфосфамид, эстрамустин, ифосфамид, мехлорэтамин, мехлорэтамин оксид гидрохлорид, мелфалан, новембихин, фенестерин, преднимустин, трофосфамид, урамустин; нитрозомочевины, такие как кармустин, хлорозотоцин, фотемустин, ломустин, нимустин и ранимнустин; антибиотики, такие как енедииновые антибиотики (например, калихеамицин, в особенности, калихеамицин гамма 1I и калихемицин омега I1 (Angew Chem Intl. Ed. Engl. (1994) 33: 183-186)); динемицин, включая динемицин А; бисфосфонаты, такие как клодронат; эсперамицин; а также и неокарциностатин хромофор и родственные ему хромофоры хромопротеинового енедиинового антибиотика), аклациномицины, актиномицин, антрамицин, азасерин, блеомицины, кактиномицин, карабицин, карминомицин, карцинофилин, хромомицины, дактиномицин, даунорубицин, деторубицин, 6-диазо-5-оксо-L-норлейцин, ADRIAMYCIN® доксорубицин (включая морфолино-доксорубицин, цианоморфолино-доксорубицин, 2-пирролино-доксорубицин и деоксидоксорубицин), эпирубицин, эзорубицин, идарубицин, марцеллломицин, митомицины, такие как митомицин С, микофенольная кислота, ногаламицин, оливомицины, пепломицин, потфиромицин, пуромицин, квеламицин, родорубицин, стрептонигрин, стрептозоцин, туберцидин, убенимекс, зиностатин, зорубицин; антиметаболиты, такие как метотрексат и 5-фторурацил (5-FU); аналоги фолиевой кислоты, такие как деноптерин, метотрексат, птероптерин, триметрексат; пуриновые аналоги, такие как флударабин, 6-меркаптопурин, тиамиприн, тиогуанин; пиримидиновые аналоги, такие как анцитабин, азацитидин, 6-азауридин, кармофур, цитарабин, дидеоксиуридин, доксифлуридин, эноцитабин, флоксуридин; андрогены, такие как калустерон, дромостанолон пропионат, эпитиостанол, мепитиостан, тестолактон; ингибиторы синтеза и действия кортикостероидов, такие как аминоглутетимид, митотан, трилостан; пополнитель фолиевой кислоты, такой как фолиновая кислота; ацеглатон; альдофосфамид гликозид; аминолевулиновая кислота; энилурацил; амсакрин; бестрабуцил; бисантрен; эдатраксат; дефофамин; демеколцин; диазиквон; элфорнитин; эллиптиния ацетат; эпотилон; этоглюцид; нитрат галлия; гидроксимочевина; лентинан; лонидамин; майтанзиноиды, такие как майтанзин и анзамитоцины; митогуазон; митоксантрон; мопиданмол; нитраэрин; пентостатин; фенамет; пирарубицин; лозоксантрон; подофиллиновая кислота; 2-этилгидразид; прокарбазин; PSK® полисахаридный комплекс (JHS Natural Products, Eugene, OR); разоксан; ризоксин; сизофиран; спирогерманий; тенуазоновая кислота; триазиквон; 2,2'2"-трихлоротриэтиламин; трихотецены (в особенности T-2 токсин, верракурин A, роридин A и ангуидин); уретан; виндезин; дакарбазин; манномустин; митобронитол; митолактол; пипоброман; гацитозин; арабинозид («Ara-C»); циклофосфамид; тиотепа; таксоиды, например, паклитаксел (TAXOL®, Bristol-Myers Squibb Oncology, Princeton, N.J.), ABRAXANE™, не содержащий кремофор, сконструированный с альбумином препарат наночастиц паклитаксела (American Pharmaceutical Partners, Schaumberg, Illinois), и TAXOTERE® доксетаксел (Rhône-Poulenc Rorer, Antony, France); хлоранбуцил; GEMZAR® гемцитабин; 6-тиогуанин; меркаптоптурин; метотрексат; платиновые аналоги, такие как цисплатин и карбоплатин; винбластин; платина; этопозид (VP-16); ифосфамид; митоксантрон; винкристин; NAVELBINE® винорелбин; новантрон; тенипозид; эдатрексат; дауномицин; аминоптерин; кселода; ибандронат; CPT-11; ингибитор топоизомеразы RFS 2000; дифторметилорнитин (DMFO); ретиноиды, такие как ретиноевая кислота; капецитабин; и фармацевтически приемлемые соли, кислоты и производные любого из вышеперечисленного.
Также в определение «химиотерапевтического средства» включены: (i) анти-гормональные средства, которые действуют регулируя или ингибируя действие гормона на опухоль, такие как антиэстрогены и селективные модуляторы рецептора эстрогена (SERM), включая, например, тамоксифен (включая NOLVADEX® тамоксифен), ралоксифен, дролоксифен, 4-гидрокситамоксифен, триоксифен, кеоксифен, LY117018, онапристон и ФАРЕСТОН торемифен; (ii) ингибиторы ароматазы, которые ингибируют фермент ароматазу, регулирующую продукцию эстрогена надпочечниками, такие как, например, 4(5)-имидазолы, аминоглютетимид, MEGASE® мегестрол ацетат, AROMASIN® экземестан, форместан, фадрозол, RIVISOR® ворозол, FEMARA® летрозол и ARIMIDEX® анастрозол; (iii) антиандрогены, такие как флутамид, нилутамид, бикалутамид, лейпролид и гозерилин; а также троксацитабин (аналог 1,3-диоксалана нуклеозида цитозина); (iv) ингибиторы ароматазы; (v) ингибиторы протеинкиназы; (vi) ингибиторы липидкиназы; (vii) антисмысловые олигонуклеотиды, в частности, ингибирующие экспрессию генов в путях передачи сигнала, которые вовлечены в патологическую пролиферацию клеток, такие как, например, PKC-альфа, Ralf и H-Ras; (viii) рибозимы, такие как ингибитор экспрессии VEGF (например, ANGIOZYME® рибозим) и ингибитор экспрессии HER2; (ix) вакцины, такие как вакцины для генотерапии, например, вакцина ALLOVECTIN©, вакцина LEUVECTIN® и вакцина VAXID®; PROLEUKIN® rIL-2; ингибитор топоизомеразы 1 LURTOTECAN®; ABARELIX® rmRH; (x) антиангиогенные средства, например, бевацизумаб (AVASTIN®, Genentech); и (xi) фармацевтически приемлемые соли, кислоты или производные любого из вышеперечисленного.
Термин «цитокин» является родовым термином для белков, выделяемых одной клеточной популяцией, которые действуют на другую клетку как межклеточные медиаторы. Примерами таких цитокинов являются лимфокины, монокины, и традиционные полипептидные гормоны. В число цитокинов включены гормон роста, такие как гормон роста человека, N-метионил-гормон роста человека и гормон роста крупного рогатого скота; паратиреоидный гормон; тироксин; инсулин; проинсулин; релаксин; прорелаксин; гликопротеиновые гормоны, такие как фолликулостимулирующий гормон (FSH), тиреотропный гормон (TSH) и лютеинизирующий гомон (LH); печеночный фактор роста; фактор роста фибробластов; пролактин; плацентарный лактоген; фактор некроза опухоли-α и -β; мюллерова ингибирующая субстанция; мышиный гонадотропин-ассоциированный пептид; ингибин; активин; васкулярный эндотелиальный фактор роста; интегрин; тромбопоэтин (TPO); факторы роста нервов, такие как NGF-β; фактор роста тромбоцитов; трансформирующие факторы роста (TGF), такие как TGF-α и TGF-β; инсулиноподобный фактор роста-I и -II; эритропоэтин (EPO); остеоиндуктивные факторы; интерфероны, такие как интерферон-α, -β, и -γ; колониестимулирующие факторы (CSF), такие как макрофагальный-CSF (M-CSF); гранулоцитомакрофагальный-CSF (GM-CSF); и гранулоцитарный-CSF (G-CSF); интерлейкины (IL), такие как IL-1, IL-1α, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12; фактор некроза опухоли, например, TNF-α или TNF-β; и другие полипептидные факторы, в том числе LIF и кит-лиганд (kit ligand) (KL). Используемый в настоящем документе термин цитокин включает белки природного происхождения или происходящие из культуры рекомбинантных клеток, и биологически активные эквиваленты нативных последовательностей цитокинов.
Термин «метка» означает любую молекулу, которая может быть ковалентно присоединена к антителу, и чья функция заключается в: (i) обеспечении определяемого сигнала; (ii) взаимодействии со второй меткой для модификации определяемого сигнала, обеспеченного первой и второй меткой, например, FRET (флуоресцентный резонансный перенос энергии); (iii) стабилизации взаимодействий или повышение аффинности связывания с антигеном или лигандом; (iv) действии на подвижность, например, электрофоретическую подвижность, или клеточную проницаемость, посредством заряда, гидрофобности, формы или другого физического параметра, или (v) обеспечении улавливающей молекулы, для модулирования лигандной аффинности, антитело/антиген связывания, или ионного комплексообразования.
Используемая в настоящем документе фраза «фармацевтически приемлемая соль» относится к фармацевтически приемлемым органическим или неорганическим солям ADC. Типичные соли включают, но не ограничиваются ими, сульфат, цитрат, ацетат, оксалат, хлорид, бромид, иодид, нитрат, бисульфат, фосфат, кислый фосфат, изоникотинат, лактат, салицилат, кислый цитрат, тартрат, олеат, таннат, пантотенат, битартрат, аскорбат, сукцинат, малеат, гентизинат, фумарат, глюконат, глюкуронат, сахарат, формиат, бензоат, глютамат, метансульфонат, этансульфонат, бензолсульфонат, п-толуолсульфонат, и памоат (например, 1,1'-метилен-бис-(2-гидрокси-3-нафтоат)). Фармацевтически приемлемая соль может иметь включение другой молекулы, такой как ацетат-ион, сукцинат-ион или другой противоион. Противоион может быть любой органической или неорганической молекулой, которая стабилизирует заряд соединения. Кроме того, фармацевтически приемлемая соль может иметь более одного заряженного атома в своей структуре. Варианты, где множественные заряженные атомы входят в состав фармацевтически приемлемой соли, могут иметь множество противоионов. Следовательно, фармацевтически приемлемая соль может иметь один или несколько заряженных атомов и/или один или несколько противононов.
«Фармацевтически приемлемый сольват» относится к ассоциации одной или нескольких молекул растворителя и ADC. Примерами растворителей, которые образуют фармацевтически приемлемые сольваты, включают, но не ограничиваются ими, воду, изопропанол, этанол, метанол, ДМСО, этилацетат, уксусную кислоту и этаноламин.
«Носители», как используется в настоящем документе, включают фармацевтически приемлемые носители, наполнители или стабилизаторы, которые нетоксичны для клетки или млекопитающего, подвергающегося их воздействию в используемых дозах и концентрациях. Часто физиологически приемлемый носитель представляет собой водный рН забуференный раствор. Примеры физиологически приемлемых носителей включают буферы, такие как фосфатный, цитратный и других органических кислот; антиоксиданты, включая аскорбиновую кислоту; низкомолекулярные полипептиды (менее чем приблизительно 10 остатков); белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины; хелатирующие агенты, такие как ЭДТА; спирты сахаров, такие как маннитол и сорбитол; солеобразующие противоионы, такие как натрий; и/или неионные поверхностно-активные вещества, такие как TWEEN®, полиэтиленгликоль (ПЭГ) и PLURONICS®.
Стереохимические определения и условные обозначения используются в настоящем документе, как правило, в соответствии с S. P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms (1984) McGraw-Hill Book Company, New York; and Eliel, E. and Wilen, S., Stereochemistry of Organic Compounds (1994) John Wiley & Sons, Inc., New York. Многие органические соединения существуют в оптически активных формах, т.е., обладают способностью вращать плоскость плоско-поляризованного света. При описании оптически активного соединения префиксы D и L, или R и S, используют для обозначения абсолютной конфигурации молекулы относительно ее хирального центра(ов). Префиксы d и l, или (+) и (-), используют для обозначения знака вращения плоско-поляризованного света данным соединением, где (-) или l означает, что соединение является левовращающим. Соединение с префиксом (+) или d является правовращающим. Для данной химической структуры эти стереоизомеры являются идентичными, если не считать того, что они являются зеркальным отражением друг друга. Определенный стереоизомер также может обозначаться как энантиомер, и смесь таких изомеров часто называется энантиомерной смесью. Смесью энантиомеров 50:50 называется рацемическая смесь или рацемат, которая может возникнут в случае, когда в химической реакции или процессе не происходило стереоселекции или стереоспецифичности. Термины «рацемическая смесь» и «рацемат» относятся к эквимолярной смеси двух энантиомеров, не обладающей оптической активностью.
Следующие сокращения используются в настоящем документе и имеют указанные определения: BME представляет собой бета-меркаптоэтанол, Boc представляет собой N-(трет-бутоксикарбонил), cit представляет собой цитруллин (2-амино-5-уреидопентановая кислота), dap представляет собой долапроин, DCC представляет собой 1,3-дициклогексилкарбодиимид, DCM представляет собой дихлорметан, DEA представляет собой диэтиламин, DEAD представляет собой диэтилазодикарбоксилат, DEPC представляет собой диэтилфосфорилцианидат, DIAD представляет собой диизопропилазодикарбоксилат, DIEA представляет собой N,N-диизопропилэтиламин, dil представляет собой долаизолейцин, DMA представляет собой диметилацетамид, DMAP представляет собой 4-диметиламинопиридин, DME представляет собой диметиловый эфир этиленгликоля (или 1,2-диметоксиэтан), DMF представляет собой N,N-диметилформамид, ДМСО представляет собой диметилсульфоксид, doe представляет собой долафенин, dov представляет собой N,N-диметилвалин, DTNB - это 5,5'-дитиобис(2-нитробензойная кислота), DTPA представляет собой диэтилентриаминпентауксусную кислоту, DTT представляет собой дитиотреитол, EDCI представляет собой 1-(3-диметиламинопропил)-3-этилкарбодиимид гидрохлорид, EEDQ представляет собой 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин, ES-MS представляет собой масс-спектрометрию с электрораспылением, EtOAc представляет собой этилацетат, Fmoc представляет собой N-(9-фторэнилметоксикарбонил), gly представляет собой глицин, HATU представляет собой О-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония гексафторфосфат, HOBt представляет собой 1-гидроксибензотриазол, ВЭЖХ представляет собой высокоэффективную жидкостную хроматографию, ile представляет собой изолейцин, lys представляет собой лизин, MeCN (CH3CN) представляет собой ацетонитрил, MeOH представляет собой метанол, Mtr представляет собой 4-анизилдифенилметил (или 4-метокситритил), nor представляет собой (1S, 2R)-(+)-норэфедрин, PAB представляет собой п-аминобензилкарбамоил, PBS представляет собой забуференный фосфатом физиологический раствор (pH 7), PEG представляет собой полиэтиленгликоль, Ph представляет собой фенил, Pnp представляет собой п-нитрофенил, MC представляет собой 6-малеимидокапроил, phe представляет собой L-фенилаланин, PyBrop представляет собой бромо-трис-пирролидинфосфония гексафторфосфат, SEC представляет собой гель-проникающую хроматографию, Su представляет собой сукцинимид, TFA представляет собой трифторуксусную кислоту, TLC представляет собой тонкослойную хроматографию, UV представляет собой ультрафиолет, и val представляет собой валин.
АНТИТЕЛА ПРОТИВ TENB2, СКОНСТРУИРОВАННЫЕ С ЦИСТЕИНОМ
Соединения по изобретению включают антитела против TENB2, сконструированные с цистеином, где одна или несколько аминокислот любой формы дикого типа или родительского антитела против TENB2, заменена на аминокислоту цистеина. Сконструированная аминокислота цистеина является свободной кислотой цистеина и не является частью внутрицепочечной или межцепочечной дисульфидной единицы. Любая форма антитела против TENB2 может быть сконструирована подобным образом, то есть видоизменена. Например, фрагмент Fab родительского антитела может быть сконструирован для образования сконструированного с цистеином Fab, обозначенного в настоящем документе как «ТиоFab». Подобным образом, родительское моноклональное антитело может быть сконструировано для образования «ТиоMab». Следует отметить, что моносайтовая мутация дает единственный остаток сконструированного цистеина в ТиоFab, в то время как моносайтовая мутация образует два остатка сконструированного цистеина в ТиоMab, вследствие димерной природы антитела IgG. Антитела против TENB2, сконструированные с цистеином, по изобретению, включают моноклональные антитела, гуманизированные или химерные моноклональные антитела, антигенсвязывающие фрагменты антител, слитые полипептиды и аналоги, которые предпочтительно связывают клеточноассоциированные полипептиды TENB2.
Антитела против TENB2, сконструированные с цистеином, сохраняют антигенсвязывающую способность их дикого типа, вариантов родительского антитела против TENB2. Таким образом, антитела против TENB2, сконструированные с цистеином, способны связывать антигены TENB2.
Антитело против TENB2, сконструированное с цистеином, содержит одну или несколько свободных аминокислот цистеина с восстановленными сульфгидрильными (тиол) группами, где антитело против TENB2, сконструированное с цистеином, связывает полипептид TENB2.
В одном варианте осуществления антитело против TENB2, сконструированное с цистеином, получено в результате процесса, включающего замену на цистеин одного или нескольких аминокислотных остатков родительского антитела против TENB2.
Мутанты с замещенными («сконструированными») остатками цистеина (Cys) могут быть оценены на реактивность вновь встроенных, сконструированных тиоловых групп цистеина. Значение тиольной реактивности является относительным, цифровое значение находится в пределах от 0 до 1,0, и может быть измерено для любого антитела, сконструированного с цистеином. Значения тиольной реактивности антител, сконструированных с цистеином, по изобретению могут быть в пределах от 0,6 до 1,0; 0,7 до 1,0; или 0,8 до 1,0.
В одном аспекте изобретение касается изолированного антитела против TENB2, сконструированного с цистеином, содержащего аминокислотную последовательность, кодируемую нуклеотидной последовательностью, которая гибридизуется с комплементом молекулы ДНК, кодирующей (а) антитело, сконструированное с цистеином, имеющее полноразмерную аминокислотную последовательность, как раскрыто в настоящем документе, (b) аминокислотную последовательность антитела, сконструированного с цистеином, в которой отсутствует сигнальный пептид, как раскрыто в настоящем документе, (с) внеклеточный домен трансмембранного белка антитела, сконструированного с цистеином, с или без сигнального пептида, как раскрыто в настоящем документе, (d) аминокислотную последовательность, кодируемую любой из последовательностей нуклеиновой кислоты, раскрытых в настоящем документе, или (е) любой другой специфически определенный фрагмент полноразмерной аминокислотной последовательности антитела, сконструированного с цистеином, как раскрыто в настоящем документе.
В одном аспекте изобретение обеспечивает изолированное антитело против TENB2, сконструированное с цистеином, без сигнальной последовательности N-конца и/или без инициирующего метионина, и кодируемое нуклеотидной последовательностью, которая кодирует такую аминокислотную последовательность, как описано в настоящем документе. Также в настоящем документе описаны процессы получения этого же, где эти процессы включают культивирование клетки-хозяина, содержащей вектор, который содержит молекулу подходящей кодирующей нуклеиновой кислоты, в условиях, подходящих для экспрессии антитела, сконструированного с цистеином, и восстановление антитела, сконструированного с цистеином, из клеточной культуры.
В другом аспекте изобретение обеспечивает изолированное антитело против TENB2, сконструированное с цистеином, в котором либо делетирован трансмембранный домен, либо инактивирован трансмембранный домен. Также в настоящем документе описаны процессы получения этого же, где эти процессы включают культивирование клетки-хозяина, содержащей вектор, который содержит молекулу подходящей кодирующей нуклеиновой кислоты, в условиях, подходящих для экспрессии антитела, сконструированного с цистеином, и восстановление антитела, сконструированного с цистеином, из клеточной культуры.
В других вариантах осуществления изобретение обеспечивает изолированные химерные антитела против TENB2, сконструированные с цистеином, содержащие любое из описанных в настоящем документе антител, сконструированных с цистеином, слитых с гетерогенным (не-TENB2) полипептидом. Примеры таких химерных молекул включают любое из описанных в настоящем документе антител, сконструированных с цистеином, слитое с гетерогенным полипептидом, например, последовательность метки эпитопа или Fc-область иммуноглобулина.
Антитело против TENB2, сконструированное с цистеином, может быть моноклональным антителом, фрагментом антитела, химерным антителом, гуманизированным антителом, одноцепным антителом или антителом, которое конкурентно ингибирует связывание антитела против полипептида TENB2 с его соответствующим эпитопом. Антитела по настоящему изобретению необязательно могут быть конъюгированы с ингибитором роста или цитотоксическим средством, таким как, например, токсин, включая, например, ауристатин, антибиотик, радиоактивный изотоп, нуклеолитический фермент или тому подобное. Антитела по настоящему изобретению необязательно могут быть продуцированы клетками СНО или бактериальными клетками, и предпочтительно ингибировать рост или пролиферацию или индуцировать гибель клетки, с которой они связываются. Для диагностических целей, антитела по настоящему изобретению могут быть помечены меткой детекции, прикреплены к твердофазному носителю, или т.п.
В других вариантах осуществления настоящее изобретение обеспечивает векторы, содержащие ДНК, кодирующую любое из описанных в настоящем документе антител против TENB2, сконструированных с цистеином. Также обеспечены клетки-хозяева, содержащие любой такой вектор. В качестве примера, клетками-хозяевами могут быть клетки СНО, клетки E.coli или дрожжевые клетки. Далее обеспечен процесс получения любого из описанных в настоящем документе полипептидов, включающий культивирование клеток-хозяев в условиях, подходящих для экспрессии требуемого полипептида, и восстановление требуемого полипептида из клеточной культуры.
Родительское антитело и антитело против TENB2, сконструированное с цистеином, связывают полипептид TENB2 или вариант полипептида TENB2, описанный в PCT/US03/07209.
Вариант полипептида TENB2 представляет собой полипептид TENB2, имеющий, по меньшей мере, приблизительно 80% аминокислотной последовательности, идентичной TENB2, которой является: (i) полноразмерная нативная последовательность; (ii) полипептидная последовательность без сигнального пептида; (iii) внеклеточный домен с или без сигнального пептида; (iv) или любой другой фрагмент полноразмерной последовательности полипептида TENB2. Такие варианты полипептида TENB2 включают, например, полипептиды, в которых один или несколько аминокислотных остатков добавлен, или удален, на N- или C-конце полноразмерной нативной аминокислотной последовательности. Как правило, вариант полипептида TENB2 будет иметь аминокислотную последовательность, по меньшей мере, на приблизительно 80% идентичную, альтернативно, по меньшей мере, на приблизительно 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% аминокислотной последовательности идентичной полноразмерной нативной последовательности полипептида TENB2, последовательности полипептида TENB2 без сигнального пептида, внеклеточного домена полипептида TENB2 с или без сигнального пептида, или любого другого специфически определенного фрагмента полноразмерной последовательности полипептида TENB2. Как правило, варианты полипептида TENB2 имеют, по меньшей мере, в длину около 10 аминокислот, альтернативно, по меньшей мере около 20, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 210, 220, 230, 240, 250, 260, 270, 280, 290, 300, 310, 320, 330, 340, 350, 360, 370, 380, 390, 400, 410, 420, 430, 440, 450, 460, 470, 480, 490, 500, 510, 520, 530, 540, 550, 560, 570, 580, 590, 600 аминокислот в длину, или более. Необязательно, варианты полипептида TENB2 будут иметь не более одной консервативной аминокислотной замены, по сравнению с нативной последовательностью полипептида TENB2, альтернативно, не более 2, 3, 4, 5, 6, 7, 8, 9, или 10 замен консервативной аминокислоты, по сравнению с нативной последовательностью полипептида TENB2.
Полипептиды TENB2 могут быть получены посредством рекомбинантной экспрессии в: (i) E.coli с вектором pBR322; (ii) клетках млекопитающих, таких как клетки HEK293 человека (ATCC CCL 1573), клетках COS (фибробласты обезьян, SV-40), клетках ячников китайского хомячка (CHO) с векторм pRK5; (iii) дрожжах, таких как штамм дрожжей AB110; или (iv) клетках насекомых, зараженных бакуловирусом (PCT/US03/07209). Нативные или рекомбинантные полипептиды TENB2 могут быть очищены, используя ряд стандартных технологий, известных в области очистки белка. Например, про-TENB2 полипептид, зрелый TENB2 полипептид, или пре-TENB2 полипептид очищают путем иммуноаффинной хроматографии, используя антитела, специфические к представляющему интерес полипептиду TENB2. В общем случае, иммуноаффинную колонку конструируют посредством ковалентного присоединения антитела против полипептида TENB2 к активированной хроматографической смоле. Полипетиды TENB2 могут быть получены рекомбинантно, как слитый полипептид с гетерогенным полипептидом, который может быть сигнальной последовательностью или другим полипептидом, имеющим специфический сайт расщепления на N-конце зрелого белка или полипептида. Альтернативно, полипептиды TENB2 могут быть получены как слитые полипептиды с сигнальной последовательностью и последовательностью гетерогенного полипептида, что делает возможным очистку слитого полипептида TENB2; примерами таких полипептидов являются полигистидин (HiS6, (SEQ ID NO:24) или His8 (SEQ ID NO:25)), IgG Fc человека, эпитоп FLAG (KDYKDDDDK (SEQ ID NO:26)), и эпитоп gD (KYALADASLKMADPNRFRGKDLPVL (SEQ ID NO:27)). Сигнальная последовательность может быть компонентом вектора, или она может быть частью ДНК, кодирующей антитело против TENB2 или полипептид TENB2, которая встроена в вектор. Сигнальная последовательность может быть сигнальной последовательностью прокариот, выбранной, например, из группы, содержащей лидерные последовательности щелочной фосфатазы, пенециллиназы, lpp, или термостойкого энтеротоксина II. Для дрожжевой секреции, сигнальная последовательность может быть, например, лидерной последовательностью дрожжевой инвертазы, лидерной последовательностью фактора альфа (включая лидерные последовательности α-фактора Saccharomyces и Kluyveromyces (US 5010182)), или лидерной последовательностью кислой фосфатазы, лидерной последовательностью глюкоамилазы C.albicans (EP 0362179), или сигнальной последовательностью, описанной в WO 90/13646. При экспрессии клетками млекопитающих, сигнальные последовательности млекопитающих можно использовать для прямой секреции белка, например, сигнальные последовательности секретируемых полипептидов одного и того же, или родственных видов, а также вирусные секреторные лидерные последовательности.
TENB2-экспрессирующие клетки экспрессируют эндогенный или трансфицированный антиген полипептида TENB2 либо на клеточной поверхности, либо в виде секретируемой формы. Рак, экспрессирующий TENB2, содержит клетки, которые имеют полипептид TENB2, представленный на клеточной поверхности, или те, которые вырабатывают и секретируют полипептид TENB2 с антигенными свойствами. Рак, экспрессирующий TENB2, необязательно продуцирует достаточные уровни полипептида TENB2 на поверхности своих клеток, так что, антитело против TENB2, или его конъюгат антитело-лекарственное средство, может связываться с ним и может оказывать терапевтическое действие в отношении рака. Рак, который сверхэкспрессирует полипептид TENB2, представляет собой такой, который, по сравнению с нераковыми клетками той же самой ткани, имеет значительно более высокие уровни полипептида TENB2 на поверхности раковых клеток, или более высокую продукцию и секрецию. Такая сверхэкспрессия может быть результатом амплификации гена или увеличенной транскрипции или трансляции. Сверхэкспрессия полипептида TENB2 может быть определена в клинических условиях, оценивая повышенные уровни белка TENB2, представленного на поверхности клетки, или секретируемые клеткой (например, путем иммуногистохимического анализа, используя антитела против TENB2, полученные против изолированного полипептида TENB2, который может быть получен, используя технологию рекомбинантных ДНК, из изолированной нуклеиновой кислоты, кодирующей полипептид TENB2; анализа FACS, и тому подобного). Альтернативно или дополнительно, можно измерять уровни нуклеиновой кислоты, кодирующей полипептид TENB2, или мРНК в клетке, например, посредством флуоресцентной гибридизации in situ (FISH), используя зонд на основе нуклеиновой кислоты, соответствующей нуклеиновой кислоте, кодирующей TENB2, или комплементарной ей; (WO 98/45479), саузерн-блоттинга, нозерн-блоттинга, или технологий полимеразной цепной реакции (ПЦР), таких как количественная ПЦР с обратной транскриптазой в режиме реального времени (qRT-PCR). Также можно определить сверхэкспрессию TENB2, измеряя слущивающийся антиген в биологической жидкости, такой как сыворотка, например, используя анализ на основе антитела (US 4933294; WO 91/05264; US 5401638; Sias et al (1990) J. Immunol. Methods 132: 73-80). Могут быть предусмотрены различные другие анализы in vivo. Альтернативно, клетки в организме пациента могут быть подвержены воздействию антитела, которое, необязательно помечено меткой детекции, например, радиоактивным изотопом, и связывание антитела с клеткой в организме пациента можно оценить, например, используя поверхностное сканирование радиоактивности, или по анализу биоптата, взятого у пациента, предварительно подвергнутого воздействию антитела.
Родительское антитело и антитело против TENB2, сконструированное с цистеином, способны связывать, предпочтительно специфически, полипептид TENB2, как описано в настоящем документе. Олигопептиды, связывающие TENB2, могут быть выявлены без проведения чрезмерных экспериментов, используя хорошо известные технологии. В этом отношении, следует отметить, что технологии для скрининга библиотек олигопептидов для поиска олигопептидов, которые способны специфически связываться с полипептидом-мишенью, хорошо известны в данной области (US 5556762; US 5750373; US 4708871; US 4833092; US 5223409; US 5403484; US 5571689; US 5663143; WO 84/03506; WO84/03564; Geysen et al (1984) Proc. Natl. Acad. Sci. USA, 81: 3998-4002; Geysen et al (1985) Proc. Natl. Acad. Sci. USA, 82: 178-182; Geysen et al., in Synthetic Peptides as Antigens, 130-149 (1986); Geysen et al., J. Immunol. Meth., 102: 259-274 (1987); Schoofs et al., J. Immunol., 140: 611-616 (1988), Cwirla, S. E. et al. (1990) Proc. Natl. Acad. Sci. USA, 87: 6378; Lowman, H.B. et al. (1991) Biochemistry, 30: 10832; Clackson, T. et al. (1991) Nature, 352: 624; Marks, J.D. et al. (1991), J. Mol. Biol., 222: 581; Kang, A.S. et al. (1991) Proc. Natl. Acad. Sci. USA, 88: 8363, и Smith, G.P. (1991) Current Opin. Biotechnol., 2: 668).
Родительское антитело и антитело против TENB2, сконструированное с цистеином, по изобретению, включают поликлональные, моноклональные, гуманизированные, человеческие, биспецифические и гетероконъюгатные антитела. Рассматриваются различные формы гуманизированных антител против TENB2. Например, гуманизированное антитело может представлять собой фрагмент антитела, такой как Fab. Альтернативно, гуманизированное антитело может представлять собой интактное антитело, например, интактное IgG1 антитело.
Биспецифические антитела против TENB2 представляют собой антитела, которые имеют связывающую специфичность, по меньшей мере, к двум разным эпитопам. Типичные биспецифические антитела против TENB2 могут связывать два различных эпитопа белка TENB2, как описано в настоящем документе. Другие такие антитела могут совмещать участок связывания TENB2 с участком связывания для другого белка. Альтернативно, область против TENB2 может быть объединена с областью, которая связывает инициирующую молекулу на лейкоците, такую как молекула рецептора Т-клетки (например, CD3), или рецепторы Fc для IgG (FcγR), такие как FcγRI (CD64), FcγRII (CD32) и FcγRIII (CD 16), с тем, чтобы сконцентрировать и локализовать защитные клеточные механизмы клетки, экспрессирующей TENB2. Биспецифические антитела также могут быть использованы для локализации цитотоксических средств в клетках, которые экспрессируют TENB2. Эти антитела имеют область связывания с TENB2 и область, которая связывается с цитотоксическим средством (например, сапорин, анти-интерферон-α, алкалоид барвинка, А-цепь рицина, метотрексат или радиоактивный изотоп гаптена). Биспецифические антитела могут быть получены как полноразмерные антитела, или фрагменты антитела (например, F(ab')2 биспецифические антитела). Традиционное получение полноразмерных биспецифических антител основано на совместной экспрессии двух пар тяжелая цепь-легкая цепь иммуноглобулина, где две цепи имеют различные специфичности (Millstein et al (1983) Nature 305: 537-539).
Гетероконъюгатные антитела против TENB2 также входят в объем настоящего изобретения. Гетероконъюгатные антитела состоят из двух ковалентно связанных антител. Такие антитела, например, были предложены для нацеливания клеток иммунной системы на нежелательные клетки (US 4676980), и для лечения ВИЧ инфекции (WO 91/00360; WO 92/200373; EP 03089). Предусмотрено, что эти антитела могут быть получены in vitro, используя методы, известные в области химии синтетических белков, включая те, в которые вовлечены сшивающие агенты.
Антитела против TENB2 по настоящему изобретению могут быть мультивалентными антителами с тремя или более антигенсвязывающими сайтами (например, четырехвалентные антитела), которые могут быть быстро получены в результате рекомбинантной экспрессии нуклеиновой кислоты, кодирующей полипептидные цепи антитела. Мультивалентное антитело может содержать димеризационный домен и три или более антигенсвязывающих сайта. Предпочтительный димеризационный домен содержит (или состоит из) область Fc или шарнирную область. В этом случае, антитело будет включать Fc-область и три или более аминоконцевых антигенсвязываюших сайта с областью Fc. Здесь предпочтительное мультивалентное антитело содержит (или состоит из) от трех до приблизительно восьми, но предпочтительно четыре, антигенсвязывающих сайта. Мультивалентное антитело содержит, по меньшей мере, одну полипептидную цепь (и предпочтительно две полипептидные цепи), где полипептидная цепь (цепи) содержит два или более вариабельных домена. Например, полипептидная цепь (цепи) может содержать VD1-(X1)n-VD2-(X2)n-Fc, где VD1 является первым вариабельным доменом, VD2 является вторым вариабельным доменом, Fc является одной полипептидной цепью области Fc, X1 и X2 означают аминокислоту или полипептид, и n равно 0 или 1. Например, полипептидная цепь (цепи) может содержать: цепь VH-CH1-гибкий линкер-VH-CH1-область Fc; или цепь VH-CH1-VH-CH1-область Fc. Мультивалентное антитело в настоящем документе предпочтительно дополнительно содержит, по меньшей мере, два (и предпочтительно четыре) полипептида вариабельного домена легкой цепи. Здесь мультивалентное антитело может, например, содержать от приблизительно двух до приблизительно восьми полипептидов вариабельного домена легкой цепи. Предусмотренные в настоящем документе полипептиды вариабельного домена легкой цепи содержат вариабельный домен легкой цепи и необязательно дополнительно содержат домен CL.
Эффекторная функция антитела против TENB2 может быть модифицирована посредством введения одной или нескольких аминокислотных замен в области Fc. Такая модификация может усилить антигензависимую клеточноопосредованную цитотоксичность (ADCC) и/или комплементзависимую цитотоксичность (CDC) антитела против TENB2. Полученное таким образом гомодимерное антитело может обладать улучшенной способностью к интернализации и/или повышенной опосредуемой комплементом киллерной для клеток функцией и антителозависимой цитотоксичностью (ADCC). См. Caron et al., (1992) J. Exp. Med. 176: 1191-1195 и Shopes B., J. (1992) Immunol. 148: 2918-2922. Можно также получить гомодимерные антитела против TENB2 с повышенной противоопухолевой активностью с использованием гетеробифункциональных кросс-линкеров, как описано у Wolff et al., (1993) Cancer Research 53: 2560-2565. Альтернативно можно сконструировать антитело, которое обладает двойными Fc-областями, и тем самым можно повысить способность к комплементарному лизису и ADCC (Stevenson et al., Anti-Cancer Drug Design 3:219-230 (1989).
Время полувыведения антитела против TENB2 в сыворотке крови может быть изменено посредством встраивания реутилизирующего рецепторсвязывающего эпитопа, например, фрагмента антитела (US 573977). В том смысле, в котором он здесь используется, термин «реутилизирующий рецепторсвязывающий эпитоп» относится к эпитопу Fc-области молекулы IgG (например, IgG1, IgG2, IgG3 или IgG4), которая ответственна за увеличение периода полувыведения молекулы IgG из сыворотки крови in vivo.
Моноклональные антитела, связывающиеся с эпитопами TENB2, включая TMEFF2#19, определяют посредством стандартного анализа конкурентного связывания и картирования эпитопов (PCT/US03/07209).
Иммуногистохимический анализ был осуществлен с использованием моноклональных антител TMEFF2#19 (PCT/US03/07209; Sambrook et al Molecular Cloning: A Laboratory Manual, New York: Cold Spring Harbor Press, 1989; Ausubel et al, Current Protocols of Molecular Biology, Unit 3.16, John Wiley and Sons, 1997). Моноклональное антитело TMEFF2#19 проявляет от слабой до сильной степени связывания с 176 из 241 образца рака предстательной железы человека.
Моноклональное антитело TMEFF2#19 интернализируется в клетки, с которыми оно связывает полипептид TENB2 на клеточной поверхности, с высокой скоростью.
Модификации антител против TENB2
Модификации и вариации в антителах против TENB2, описанные в настоящем документе, можно осуществить, например, используя любые известные в уровне техники технические приемы и методические рекомендации для консервативных и неконсервативных мутаций, например, такие, как описаны в US 5364934. Изменения могут представлять собой замену, делецию или инсерцию одного или нескольких кодонов, кодирующих антитело или полипептид, что приводит к изменению аминокислотной последовательности по сравнению с нативной последовательностью антитела против TENB2. Необязательно, вариация может быть осуществлена заменой, по меньшей мере, одной аминокислоты на любую другую аминокислоту в одном или нескольких доменах данного антитела против TENB2. Изменения могут быть осуществлены, используя методы, известные в уровне техники, такие как опосредованный олигонуклеотидами (сайт-направленный) мутагенез, аланин-сканирующий мутагенез и ПЦР мутагенез. Сайт-направленный мутагенез (Carter et al (1986) Nucl. Acids Res., 13: 4331; Zoller et al (1987) Nucl. Acids Res., 10: 6487), кассетный мутагенез (Wells et al (1985) Gene, 34: 315), мутагенез с селекцией рестрикционных фрагментов (Wells et al (1986) Philos. Trans. R. Soc. London SerA, 317: 415) или другие известные технологии можно применить на клонированной ДНК, для продуцирования варианта ДНК антитела против TENB2. Аминокислотные замены могут изменять посттрансляционные процессы антитела против TENB2, такие как изменение числа и положения сайтов гликозилирования или изменение фиксирующих характеристик мембраны. Другие модификации включают дезаминирование глютаминиловых и аспарагиниловых остатков до соответствующих глютамиловых и аспартиловых остатков, соответственно, гидроксилирование пролина и лизина, фосфорилирование гидроксильных групп серильных или треонильных остатков, метилирование α-аминогрупп боковых цепей лизина, аргинина и гистидина (T.E. Creighton, Proteins: Structure and Molecular Properties, (1983) W.H. Freeman & Co., San Francisco, pp. 79-86), ацетилирование N-концевого амина, и амидирование любой С-концевой карбоксильной группы. Антитела против TENB2 могут быть получены путем введения подходящих нуклеотидных замен в кодирующую ДНК, и/или посредством химического синтеза.
Фрагменты антител против TENB2 могут быть укороченными на N-конце или C-конце, или могут быть лишены внутренних остатков, например, при сравнение с полноразмерным антителом против TENB2. Некоторые фрагменты лишены таких аминокислотных остатков, которые не являются необходимыми для требуемой биологической активности антитела против TENB2. Фрагменты антитела против TENB2 могут быть получены посредством любого из целого ряда технологических приемов. Требуемые пептидные фрагменты могут быть синтезированы химически. Альтернативный подход включает создание фрагментов антител посредством ферментативного расщепления, например, посредством обработки белка ферментом, который расщепляет белки в участках, определенных конкретными аминокислотными остатками, или посредством расщепления ДНК подходящими ферментами рестрикции и выделения требуемого фрагмента. Еще один подходящий технологический прием включает изолирование и амплификацию фрагмента ДНК, кодирующей требуемое антитело или фрагмент, посредством полимеразной цепной реакции (ПЦР). Олигонуклеотиды, которые определяют требуемые границы фрагмента ДНК, используются в 5' и 3' праймерах в ПЦР. Предпочтительно, фрагменты антитела против TENB2 имеют, по меньшей мере, одно биологическое и/или иммунологическое действие, общее с нативным антителом против TENB2, раскрытым в настоящем документе.
Чрезвычайно предпочтительный тип замещающего варианта включает замену одного или нескольких остатков гипервариабельной области гуманизированного или человеческого антитела. Обычно, полученный вариант(ы), выбранный для дальнейшей разработки, будет иметь улучшенные биологические характеристики по сравнению с антителом, из которого он образован. Удобный способ получения таких замещающих вариантов включает созревание аффинности с использованием фагового дисплея. Кратко, несколько участков гипервариабельной области (например, 6-7 участков) подвергают мутации для получения всех возможных замен аминокислот в каждом участке. Полученные таким образом варианты антител проявляются моновалентным образом на частицах нитевидного фага в виде слитых конструкций с продуктом гена III М13, упакованного внутри каждой частицы. Воспроизведенные в фаге варианты затем подвергают скринингу на их биологическую активность (например, аффинность связывания), как раскрыто в настоящем документе. Для того чтобы идентифицировать участки-кандидаты гипервариабельной области для модификации, можно провести аланин-сканирующий мутагенез идентифицированных остатков гипервариабельной области, вносящей значительный вклад в связывание антигена. Альтернативно или дополнительно, может быть полезным проведение анализа кристаллической структуры комплекса антиген-антитело для идентификации точек контакта между антителом и полипептидом TENB2 человека. Такие контактные остатки и смежные остатки являются кандидатами для замещения по методам, детально разработанным в настоящем документе. Однажды получив такие варианты, панель вариантов подвергается скринингу, как описано в настоящем документе, и можно отобрать антитела с наилучшими свойствами для дальнейшей разработки в одном или нескольких соответствующих анализах.
Другой тип ковалентной модификации антитела против TENB2, входящий в объем изобретения, содержит изменение нативного характера гликозилирования антитела или полипептида, посредством делеции одной или нескольких углеводных молекул, обнаруженных в нативной последовательности антитела против TENB2 (либо удаляя основной сайт гликозилирования, либо ликвидируя гликозилирование химическим или ферментативным способом), и/или добавляя один или несколько сайтов гликозилирования, которые не присутствуют в нативной последовательности антитела против TENB2. Дополнительно, модификация включает качественные изменения гликозилирования нативных белков, включающие изменение природы и пропорций различных существующих углеводных молекул. Гликозилирование антител и других полипептидов является обычно N-связанным или О-связанным. N-связанное относится к присоединению углеводной группы к боковой цепи остатка аспарагина. Трипептидные последовательности аспарагин-Х-серин и аспарагин-Х-треонин, где Х представляет собой любую аминокислоту, за исключением пролина, являются последовательностями распознавания для ферментативного присоединения углеводной молекулы к аспарагиновой боковой цепи. Таким образом, наличие любой из трипептидных последовательностей в полипептиде создает потенциальный сайт гликозилирования. О-связанное гликозилирование относится к присоединению одного из сахаров N-ацетилгалактозамина, галактозы или ксилозы к гидроксиаминокислоте, чаще всего серину или треонину, хотя также можно использовать 5-гидроксипролин или 5-гидроксилизин. Добавление сайтов гликозилирования к антителу против TENB2 обычно проводят посредством изменения аминокислотной последовательности таким образом, чтобы она содержала одну или несколько из вышеуказанных трипептидных последовательностей (для сайтов N-связанного гликозилирования). Изменение также можно осуществить добавлением, или заменой, одного или более остатков серина или треонина в последовательности антитела против TENB2 (для сайтов О-связанного гликозилирования). Аминокислотная последовательность антитела против TENB2 может быть необязательно изменена посредством замен на уровне ДНК, в частности, посредством мутирования ДНК, кодирующей антитело против TENB2, в предварительно выбранных основаниях, таким образом образуются кодоны, которые будут транслировать требуемые аминокислоты.
Другим способом увеличения числа углеводных молекул в антителе против TENB2 является химическое или ферментативное связывание гликозидов с полипептидом. Такие способы описаны в уровне техники, например, в WO 87/05330, опубликованной 11 сентября 1987, и у Aplin and Wriston, CRC Crit. Rev. Biochem., pp. 259-306 (1981).
Удаление углеводных молекул, присутствующих в антителе против TENB2, может быть совершено химически или ферментативно, или посредством мутационной замены кодонов, кодирующих аминокислотные остатки, которые выполняют роль мишеней для гликозилирования. Способы химического дегликозилирования известны в уровне техники, и описаны, например, у Hakimuddin, et al., Arch. Biochem. Biophys., 259: 52 (1987) и у Edge et al., Anal. Biochem., 118: 131 (1981). Ферментативное расщепление углеводных молекул может быть достигнуто посредством использования множества эндо- и экзо-гликозидаз, как описано у Thotakura et al (1987) Meth. Enzymol. 138: 350.
Другой тип ковалентной модификации антитела против TENB2 включает соединение антитела или полипептида с одним из множества небелковых полимеров, например, полиэтиленгликолем (ПЭГ), полипропиленгликолем, или полиоксиалкиленами, способом, изложенным в US 4640835; US 4496689; US 4301144; US 4670417; US 4791192 или US 4179337. Антитело или полипептид также может быть инкапсулировано в микрокапсулы, полученные, например, посредством технологий коацервации или полимеризации на границе раздела фаз (например, гидроксиметилцеллюлозные или желатиновые микрокапсулы и поли(метилметацилатные) микрокапсулы, соответственно), в коллоидной системе доставки лекарственного средства (например, липосомы, альбуминовые микросферы, микроэмульсии, наночастицы и нанокапсулы), или в макроэмульсиях. Такие технологические методы раскрыты в Remington's Pharmaceutical Sciences, 16th edition, Oslo, A., Ed., (1980).
Антитело против TENB2 по настоящему изобретению может быть модифицировано с тем, чтобы образовать химерные молекулы, содержащие антитело против TENB2, слитое с другим гетерогенным полипептидом или аминокислотной последовательностью. В одном варианте осуществления такая химерная молекула включает слияние антитела против TENB2 с полипептидом-меткой, который обеспечивает эпитоп, с которым антитело против метки может селективно связаться. Эпитоп-метка обычно расположен на амино- или карбокси-конце антитела против TENB2. Присутствие таких эпитоп-меченных форм антитела против TENB2 может быть выявлено, используя антитело против полипептида-метки. Также, обеспечение эпитопа-метки делает возможным быструю очистку антитела против TENB2, посредством аффинной очистки с использованием антитела против метки или другого типа аффинной матрицы, которое связывается с эпитопом-меткой. Различные полипептиды-метки и их соответствующие антитела хорошо известны в уровне техники. Примеры включают метки поли-гистидин (poly-his) или поли-гистидин-глицин (poly-his-gly); полипептид-метку flu HA и его антитело 12CA5 (Field et al (1988) Mol. Cell. Biol., 8: 2159-2165); метку c-myc и его антитела 8F9, 3C7, 6Е10, G4, B7 и 9E10 (Evan et al (1985) Molecular and Cellular Biology, 5: 3610-3616); и метку гликопротеина D (gD) вируса простого герпеса и его антитело (Paborsky et al (1990) Protein Engineering, 3(6): 547-553). Другие полипептиды-метки включают Flag-пептид (Hopp et al (1988) BioTechnology 6: 1204-1210); эпитопный пептид KT3 (Martin et al (1992) Science, 255: 192-194); пептид эпитопа α-тубулина (Skinner et al (1991) J. Biol. Chem., 266:15163-15166); и пептидную метку белка гена 10 Т7 (Lutz-Freyermuth et al (1990) Proc. Natl. Acad. Sci. USA, 87: 6393-6397).
В альтернативном варианте осуществления химерная молекула может содержать слияние антитела против TENB2 с иммуноглобулином или определенной областью иммуноглобулина. Для двухвалентной формы химерной молекулы (также называемая «иммуноадгезин»), такое слияние может быть с областью Fc молекулы IgG. Слияния Ig предпочтительно включают замену растворимой (с делетированным или инактивированным трансмембранным доменом) формы антитела против TENB2 вместо, по меньшей мере, одного вариабельного домена в составе молекулы Ig. В чрезвычайно предпочтительном варианте осуществления, иммуноглобулиновое слияние включает шарнирную, СН2 и СН3, или шарнирную, СН1, СН2 и СН3 области молекулы IgG1 (US 5428130).
Получение антител против TENB2
ДНК, кодирующую вариант аминокислотной последовательности антител против TENB2, сконструированных с цистеином, и родительских антител против TENB2 по изоберетению, получают множеством способов, которые включают, но не ограничены ими, выделение из природного источника (в случае природных вариантов аминокислотной последовательности), получение в результате сайт-направленного (или опосредованного олигонуклеотидами) мутагенеза (Carter (1985) et al Nucleic Acids Res. 13: 4431-4443; Ho et al (1989) Gene (Amst.) 77: 51-59; Kunkel et al (1987) Proc. Natl. Acad. Sci. USA 82: 488; Liu et al (1998) J. Biol. Chem. 273: 20252-20260), ПЦР-мутагенеза (Higuchi, (1990) in PCR Protocols, pp. 177-183, Academic Press; Ito et al (1991) Gene 102: 67-70; Bernhard et al (1994) Bioconjugate Chem. 5: 126-132; и Vallette et al (1989) Nuc. Acids Res. 17: 723-733), и кассетного мутагенеза (Wells et al (1985) Gene 34: 315-323) ранее подготовленной ДНК, кодирующей полипептид. Протоколы мутагенеза, наборы и реагенты коммерчески доступны, например набор для мультисайт-направленного мутагенеза QuikChange® Multi Site-Direct Mutagenesis Kit (Stratagene, La Jolla, CA). Единичные мутации также порождаются в результате олигонуклеотид-направленного мутагенеза с использованием в качестве матрицы двухцепочечной плазмидной ДНК посредством мутагенеза на основе ПЦР (Sambrook and Russel, (2001) Molecular Cloning: A Laboratory Manual, 3rd edition; Zoller et al (1983) Methods Enzymol. 100: 468-500; Zoller, M.J. and Smith, M. (1982) Nucl. Acids Res. 10: 6487-6500). Варианты рекомбинантных антител могут быть сконструированы также посредством манипуляций рестрикционными фрагментами или посредством ПЦР с перекрывающимися участками с синтетическими олигонуклеотидами. Мутагенные праймеры кодируют замену(ы) цистеинового кодона. Стандартные способы мутагенеза могут быть использованы для создания ДНК, кодирующей такие мутантные, сконструированные с цистеином, антитела (Sambrook et al Molecular Cloning, A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., 1989; и Ausubel et al Current Protocols in Molecular Biology, Greene Publishing and Wiley-Interscience, New York, N.Y., 1993).
Технологию фагового дисплея (McCafferty et al (1990) Nature 348: 552-553) можно использовать для получения человеческих антител против TENB2 и фрагментов антител in vitro, из генных наборов вариабельного домена (V) иммуноглобулина от иммунизированных доноров. В соответствии с этой технологией, гены домена V антитела клонированы в пределах рамки считывания, либо в главный, либо в минорный ген оболочечного белка нитевидного бактериофага, такого как М13 или fd, и воспроизводят в виде функциональных фрагментов антитела на поверхности фаговой частицы. Вследствие того, что нитевидная частица содержит копию одноцепочечной ДНК генома фага, отбор на основе функциональных характеристик антитела также приведет к селекции гена, кодирующего антитело, проявляющее такие свойства. Таким образом, фаг воспроизводит некоторые свойства В-клетки (Johnson et al (1993) Current Opinion in Structural Biology 3: 564-571; Clackson et al (1991) Nature, 352: 624-628; Marks et al (1991) J. Mol. Biol. 222: 581-597; Griffith et al (1993) EMBO J. 12: 725-734; US 5565332; US 5573905; US 5567610; US 5229275).
Антитела против TENB2 могут быть синтезированы химически, используя известные методики олигопептидного синтеза, или могут быть получены и очищены с использованием рекомбинантной технологии. Подходящая аминокислотная последовательность, или часть ее, может быть получена посредством прямого пептидного синтеза, используя твердофазные технологии (Stewart et al., Solid-Phase Peptide Synthesis, (1969) W.H. Freeman Co., San Francisco, CA; Merrifield, (1963) J. Am. Chem. Soc, 85: 2149-2154). Синтез белка in vitro может быть осуществлен, используя ручные или автоматизированные способы. Автоматизированный синтез на твердой фазе может быть выполнен, например, задействуя t-BOC или Fmoc защищенные аминокислоты и используя синтезатор пептидов Applied Biosystems Peptide Synthesizer (Foster City, CA) в соответствии с инструкциями фирмы-производителя. Различные участки антитела против TENB2 или полипептида TENB2 могут быть синтезированы химически раздельно и объединены, используя химические или ферментативные способы, для получения желаемого антитела против TENB2 или пептида TENB 2.
Разработаны различные методы получения фрагментов антител. Обычно фрагменты получают протеолитическим расщеплением интактных антител (Morimoto et al., (1992) Journal of Biochemical and Biophysical Methods 24:107-117; и Brennan et al., (1985) Science, 229:81), или получают непосредственно с помощью рекомбинантных клеток-хозяев. Фрагменты Fab, Fv и ScFv антитела против TENB2 все могут быть экспрессированы в, и секретированы из E.coli, таким образом делая возможным простое получение больших количеств этих фрагментов. Фрагменты антитела могут быть выделены из фаговых библиотек антител, обсуждаемых здесь. Альтернативно, Fab'-SH-фрагменты можно непосредственно выделить из E. coli и химически соединить для образования F(ab')2-фрагментов (Carter et al., (1992) Bio/Technology 10:163-167), или выделить непосредственно из культуры рекомбинантных клеток-хозяев. Антитело против TENB2 может быть одноцепочным Fc-фрагментом (scFv) (WO 93/16185; US 5571894; US. 5587458). Фрагмент антитела против TENB2 также может быть «линейным антителом» (US 5641870). Такие фрагменты линейного антитела могут быть моноспецифическими или биспецифическими.
Описание, представленное ниже, относится, главным образом, к получению антител против TENB2, посредством культивирования клеток, трансформированных или трансфицированных вектором, содержащим нуклеиновую кислоту, кодирующую антитело против TENB2. ДНК, кодирующая антитела против TENB2, может быть получена из библиотеки кДНК, созданной из тканей, которые, как считают, обладают мРНК антитела против TENB2, и экспрессируют ее на уровне детекции. Соответственно, ДНК человеческого антитела против TENB2 или полипептида TENB2, может быть обычным образом получена из библиотеки кДНК, созданной из тканей человека. Ген, кодирующий антитело против TENB2, также может быть получен из геномной библиотеки или посредством известных методов синтеза (например, автоматизированный синтез нуклеиновых кислот).
Библиотеки можно подвергнуть скринингу с использованием зондов (например, олигонуклеотиды, состоящие из, по меньшей мере, примерно 20-80 оснований), сконструированных для идентификации представляющего интерес гена или белка, кодируемого этим геном. Скрининг кДНК или геномной библиотеки с выбранным зондом можно провести, используя стандартные методики, например, как описано Sambrook et al., Molecular Cloning: A Laboratory Manual (New York: Cold Spring Harbor Laboratory Press, 1989). Альтернативным способом выделения гена, кодирующего антитело против TENB2 или полипептид TENB2, является способ ПЦР (Sambrook et al., выше; Dieffenbach et al., PCR Primer: A Laboratory Manual, Cold Spring Harbor Laboratory Press, 1995).
Клетки-хозяева трансфицируют или трансформируют экспрессирующим или клонирующим вектором, описанным в настоящем документе для получения антитела против TENB2 или полипептида TENB2, и культивирования в соответствующей питательной среде, модифицированной надлежащим образом для индуцирования промоторов, отбора трансформантов, или амплификации генов, кодирующих требуемые последовательности. Условия культивирования, такие как среда, температура, рН и тому подобное, могут быть выбраны специалистом, без проведения излишних экспериментов. В большинстве случаев, принципы, протоколы и практические технологические приемы для обеспечения максимальной продуктивности клеточных культур, могут быть найдены в Mammalian Cell Biotechnology: a Practical Approach. M. Butler, ed. (IRL Press, 1991) и Sambrook et al., выше.
Подходящие клетки-хозяева для клонирования или экспрессирования ДНК в векторах здесь включают клетки прокариот, дрожжей или высших эукариот. Подходящие прокариоты включают, но не ограничены ими, эубактерии, такие как грам-отрицательные и грам-положительные организмы, например, Enterobacteriaceae, такие как E. coli. Различные штаммы E. coli публично доступны, например, E.coli Kl2 штамм MM294 (ATCC 31446); E. Coli X1776 (ATCC 31537); E. coli штамм W3110 (ATCC 27325) и K5 772 (ATCC 53635). Другие подходящие прокариотические клетки-хозяева включают Enterobacteriaceae, такие как Escherichia, например, E. coli, Enterobacter, Erwinia, Klebsiella, Proteus, Salmonella, например, Salmonella typhimurium, Serratia, например, Serratia marcescans и Shigella, а также Bacilli, такие как B. subtilis и B. licheniformis (например, B.licheniformis 41P, раскрытая в DD 266710, опубликовано 12 апреля 1989), Pseudomonas, такие как P. aeruginosa и Streptomyces. Эти примеры являются иллюстративными, а не ограничивающими. Штамм W3110 является иллюстративным штаммом-хозяином для ферментации продукта рекомбинантной ДНК. Предпочтительно, клетка-хозяин секретируют минимальное количество протеолитических ферментов. Например, штамм W3110 может быть модифицирован таким образом, чтобы обеспечить генетическую мутацию в генах, кодирующих белки, являющиеся эндогенными для хозяина, с примерами таких хозяев, включая E.coli W3110 штамм 1A2, который имеет полный генотип tonA; E.coli W3110 штамм 9E4, который имеет полный генотип tonA ptr3; E.coli W3110 штамм 27C7 (ATCC 55244), который имеет полный генотип tonA ptr3 phoA E15 (argF-lac) 169 degP ompT kanr; E. coli W3110 штамм 37D6, который имеет полный генотип tonA ptr3 phoA E15 (argF-lac) 169 degP ompT rbs7 ilvG kanr; E. coli W3110 штамм 40B4, который представляет собой штамм 37D6 с делецией неканамицин-устойчивого degP; и штамм E.coli, имеющий мутантную периплазматическую протеазу (US 4946783). Альтернативно, являются пригодными методы клонирования in vitro, например, ПЦР или другие полимеразные реакции нуклеиновых кислот.
Полноразмерное антитело, фрагменты антитела и слитые белки из антитела могут продуцироваться бактериями, в частности, когда нет потребности в гликозилировании и эффекторных функциях Fc, например, когда терапевтическое антитело конъюгировано с цитотоксическим агентом (например, токсином), и иммуноконъюгат сам по себе проявляет эффективность в отношении разрушения опухолевых клеток. Полноразмерные антитела имеют более продолжительное время полужизни в циркуляции. Продукция в E. coli может быть более быстрой и более экономичной при использовании, например, экспрессии фрагментов антител и полипептидов в бактериях с областью инициации трансляции (TIR) и сигнальной последовательностью для оптимизации экспрессии и секреции (US 5648237; US 5789199; US 5840523). После экспрессии антитело выделено из клеточной массы E. coli в растворимой фракции и может быть очищено с помощью, например, колонки протеин А или G, в зависимости от изотипа. Окончательную очистку можно провести аналогично процессу очистки антитела, экспрессированного, например, в клетках СНО.
В дополнение к прокариотам, эукариотические микробы, такие как мицелиальные грибы или дрожжи, являются подходящими хозяевами для клонирования или экспрессии векторов, кодирующих антитело против TENB2 или полипептид TENB2. Saccharomyces cerevisiae является общеупотребимым микроорганизмом-хозяином из низших эукариотов. Другие включают http://Schizosaccharomycespom.be (Beach and Nurse, (1981) Nature, 290: 140; EP 139383); организмы-хозява Kluyveromyces (US 4943529; Fleer et al (1991) Bio/Technology, 9: 968-975) такие как, например, K.lactis (MW98-8C, CBS683, CBS4574; Louvencourt et al (1983) J. Bacteriol., 154(2): 737-742), K. fragilis (ATCC 12424), K. bulgaricus (ATCC 16045), K. wickeramii (ATCC 24178), K. waltii (ATCC 56500), K. drosophilarum (ATCC 36906; Van den Berg et al (1990) Bio/Technology, 8: 135), K. thermotolerans и K.marxianus; yarrowia (EP 402226); Pichia pastoris (EP 183070; Sreekrishna et al (1988) J. Basic Microbiol., 28: 265-278); Candida; Trichoderma reesia (EP 244234); Neurospora crassa (Case et al (1979) Proc. Natl. Acad. Sci. USA, 76: 5259-5263); Schwanniomyces, такие как Schwanniomyces occidentalis (EP 394538); и мицелиальные грибы, такие как, например, Neurospora, Penicillium, Tolypocladium (WO 91/00357) и Aspergillus, такие как A. nidulans (Ballance et al (1983) Biochem. Biophys. Res. Commun., 112: 284-289; Tilburn et al (1983) Gene, 26: 205-221; Yelton et al (1984) Proc. Natl. Acad. Sci. USA, 81: 1470-1474) и A. niger (Kelly and Hynes, (1985) EMBO J., 4: 475-479). Метилотрофные дрожжи являются здесь пригодными и включают, но не ограничиваются ими, дрожжи, способные к росту на метаноле, выбранные из рода, включающего Hansenula, Candida, Kloeckera, Pichia, Saccharomyces, Torulopsis и Rhodotorula.
Подходящие клетки-хозяева для экспрессии гликозилированного антитела против TENB2 или полипептида TENB2 также могут быть получены из многоклеточных организмов. Примеры клеток беспозвоночных включают клетки насекомых, например, Drosophila S2 и Spodoptera Sf9, а также клетки растений, такие как культуры клеток хлопка, кукурузы, картофеля, соевых бобов, петунии, таматов и табака. Были идентифицированы клетки-хозяева из многочисленных штаммов и вариантов бакуловируса и соответствующих насекомых-переносчиков, таких как Spodoptera frugiperda (гусеница), Aedes aegypti (москит), Aedes albopictus (москит), Drosophila melanogaster (плодовая мушка) и Bombyx mori. Многообразные вирусные штаммы для трансфицирования доступны публично, например, вариант L-1 Autographa californica NPV и штамм Bm-5 Bombyx mori NPV, и такие вирусы могут быть использованы здесь в соответствии с настоящим изобретением, в частности для трансфицирования клеток Spodoptera frugiperda.
Примерами пригодных клеточных линий млекопитающих являются линия почечных клеток обезьян CV1, трансформированная посредством SV40 (COS-7, ATCC CRL 1651); линия клеток мезонефроса человека (293 или клетки 293, субклонированные для роста в суспензионной культуре, Graham et al (1977) J. Gen Virol. 36: 59); клетки почки детеныша хомячка (BHK, ATCC CCL 10); клетки яичника китайского хомячка/-DHFR (CHO, Urlaub et al (1980) Proc. Natl. Acad. Sci. USA 77: 4216); мышиные клетки Сертоли (TM4, Mather (1980) Biol. Reprod. 23: 243-251); почечные клетки обезьяны (CV1 ATCC CCL 70); почечные клетки африканской зеленой мартышки (VERO-76, ATCC CRL-1587); клетки карциномы шейки матки человека (HELA, ATCC CCL 2); почечные клетки собаки (MDCK, ATCC CCL 34); клетки печени крыс линии Buffalo (BRL 3A, ATCC CRL 1442); легочные клетки человека (W138, ATCC CCL 75); клетки печени человека (Hep G2, HB 8065); мышиные клетки опухоли молочной железы (MMT 060562, ATCC CCL51); клетки TRI (Mather et al (1982) Annals N.Y. Acad. Sci. 383: 44-68); клетки MRC 5; клетки FS4; и клеточная линия гепатомы человека (Hep G2).
Клетки-хозяева трансформируют вышеописанными экспрессирующими или клонирующими векторами для продукции антитела против TENB2, и культивируют в традиционной питательной среде, модифицированной соответствующим образом для индукции промотора, селекции трансформантов и амплификации генов, кодирующих желаемые последовательности. Нуклеиновая кислота (например, кДНК или геномная ДНК), кодирующая антитело против TENB2 или полипептид TENB2, может быть встроена в воспроизводимый вектор для клонирования (амплификация ДНК) или экспрессии. Вектор может быть, например, в виде плазмиды, космиды, вирусной частицы или фага. Соответствующая последовательность нуклеиновой кислоты может быть встроена в вектор посредством разнообразных процедур.
Ингибирование роста опухолевых клеток in vitro или in vivo можно определить различными способами, известными в уровне техники, например, ингибирование пролиферации клеток опухоли, экспрессирующей TENB2, in vitro или in vivo на приблизительно 25-100% по сравнению с необработанной опухолевой клеткой, или на приблизительно 30-100%, или приблизительно 50-100% или 70-100%, в одном варианте осуществления при концентрации антитела от приблизительно 0,5 до 30 мкг/мл. Ингибирующие эффекты антитела против TENB2 на рост опухоли in vitro могут быть оценены способами, известными в уровне техники, например, используя клетки, которые экспрессируют полипептид TENB2, либо эндогенно, либо после трансфекции геном TENB2. Например, подходящая опухолевая клеточная линия и клетки, трансфицированные TENB2, можно обработать моноклональным антителом против TENB2 в различных концентрациях в течение нескольких дней (например, 2-7), и окрасить кристаллическим фиолетовым или МТТ, или провести анализ посредством какого-либо другого колориметрического способа. Ослабленный сигнал означает ингибирование роста. Другим способом оценки пролиферации является сравнение поглощения Н3-тимидина обработанными клетками в присутствии или отсутствии антитела против TENB2. После обработки клетки собирают, и активность, инкорпарированную в ДНК, количественно определяют с помощью сцинтилляционного счетчика. Снижение радиоактивности будет свидетельствовать об ингибировании пролиферации. Для отбора антитела против TENB2, которое индуцирует клеточную гибель, потерю целостности мембраны, что выявляется, например, по поглощению йодида пропидия (PI), трипанового синего или 7AAD, можно провести оценку относительно контроля. Подходящие положительные контроли включают обработку выбранной клеточной линии антителом, ингибирующим рост, для которого известна ингибирующая рост активность клеточной линии. Ингибирование роста может быть измерено при концентрации антитела в клеточной культуре от приблизительно 0,5 до 30 мкг/мл или от приблизительно 0,5 нМ до 200 нМ, когда ингибирование роста определяют через 1-10 дней после воздействия антителом на опухолевые клетки. Антитело является ингибирующим рост in vivo, если введение антитела против TENB2 в дозе от приблизительно 1 мкг/кг до приблизительно 100 мг/кг массы тела, приведет к уменьшению размера опухоли или уменьшению клеточной пролиферации в период времени от приблизительно 5 дней до приблизительно 3 месяцев с момента первого введения антитела, предпочтительно в течение от приблизительно 5 до 30 дней.
Получение антител против TENB2, сконструированных с цистеином
Методы конструирования, отбора и получения по изобретению делают возможным получение антител против TENB2, сконструированных с цистеином, являющихся реационноспособными с электрофильной функциональностью. Эти методы дополнительно обеспечивают соединения конъюгатов антитела, такие как соединения конъюгата антитело-лекарственное средство (ADC), с молекулами лекарственного средства в обозначенных, сконструированных, селективных сайтах. Реактивные остатки цистеина на поверхности антитела обеспечивают специфическое конъюгирование молекулы лекарственного средства посредством тиоловых реактивных групп, таких как малеимид или галоацетил. Нуклеофильная реакционная способность тиоловой функциональности остатка Cys для малеимидной группы в приблизительно 1000 раз выше по сравнению с функциональностью любой другой аминокислоты в белке, например, аминогруппы остатков лизина или N-концевой аминогруппы. Тиолы со специфической функциональностью в иодоацетильных и малеимидных реагентах могут вступать в реакцию с аминогруппами, но требуется более высокое значение рН (>9,0) и более продолжительное время реакции (Garman, 1997, Non-Radioactive Labelling: A Practical Approach, Academic Press, London). Количество свободных тиолов в белке может быть определено, используя стандартный способ Элмана. Иммуноглобулин М представляет собой пример дисульфид-связанного пентамера, в то время как иммуноглобулин G представляет собой пример белка с внутренними дисульфидными мостиками, связывающими субъединицы вместе. В белках такого типа уменьшение дисульфидных связей с помощью реагента, такого как дитиотреитол (DTT) или селенол (Singh et al (2002) Anal. Biochem. 304: 147-156) необходимо для образования реактивного свободного тиола. Этот подход может привести к потере третичной структуры антитела и антигенсвязывающей специфичности.
Анализ PHESELECTOR (ELISA фага для отбора реактивных тиолов) делает возможным определение реактивных групп цистеина в антителе-Fab в фаговом формате ELISA, тем самым облегчая конструирование антител с цистеином (US 2007/0092940). Антиген, который связывается с антителом, сконструированным с цистеином, наносят на поверхность лунки, затем инкубируют с фаговыми частицами, проявляющими Fab, сконструированным с цистеином, добавляют вторичное антитело, меченное HRP, и определяют коэффициент поглощения. Можно провести скрининг мутантных белков, экспрессируемых фагом, быстрым, надежным, высокопроизводительным методом. Библиотеки антител, сконструированных с цистеином, могут быть созданы и подвергнуты отбору по связывающей активности, используя тот же подход, что и для идентификации соответствующей инкорпорации реактивных сайтов свободного цистеина, из случайных белково-фаговых библиотек антител или других белков. Эта технология включает реагирование цистеина мутантных белков, экспрессируемых фагом, с аффинным реагентом или репортерной группой, которая также является тиол-реактивной.
Анализ PLIESELECTOR позволяет проводить скрининг реактивных тиоловых групп в антителах. Примером является идентификация этим способом варианта А121С. Целая молекула Fab может быть эффективно исследована для обнаружения большего числа вариантов ТиоFab с реактивными тиоловыми группами. Параметр, фракционную доступность поверхности, использовали для идентификации и количественного анализа доступности растворителя к аминокислотным остатками в полипептиде. Доступность поверхности может быть выражена как площадь поверхности (Å2), которая может контактировать с молекулой растворителя, например, водой. Занятое водой пространство приблизительно выражено как сфера с радиусом 1,4 Å. Програмное обеспечение находится в свободном доступе или лицензируемое (Secretary to CCP4, Daresbury Laboratory, Warrington, WA4 4AD, United Kingdom, Fax: (+44) 1925 603825, or by internet: http://www.ccp4.ac.uk/dist/html/INDEX.html) как пакет CCP4 кристаллографических программ, в которых используются алгоритмы для расчета доступности поверхности каждой аминокислоты белка с известными координатами, полученными с помощью рентгеноструктурной кристаллографии («The CCP4 Suite: Programs for Protein Crystallography» (1994) Acta. Cryst. D50: 760-763). Двумя иллюстративными модулями программного обеспечения, которые осуществляют расчет доступности поверхности, являются «AREAIMOL» и «SURFACE», основанные на алгоритмах B.Lee и F.M.Richards (1971) J.Mol.Biol. 55: 379-400. AREAIMOL определяет доступную поверхность белка для растворителя как местоположение центра сферы зонда (представляет собой молекулу растворителя), поскольку переворачивает ван-дер-ваальсовы поверхности белка. AREAIMOL рассчитывает площадь доступной поверхности для растворителя, генерируя поверхностные точки на расширенной окружности около каждого атома (на расстоянии от центра атома, равном сумме радиусов атома и зонда), и удаляя те, которые находятся в пределах эквивалентных сфер, ассоциированных с соседними атомами. AREAIMOL вычисляет площадь атомов, доступную для растворителя, в координатном файле PDB и суммирует доступную площадь для остатков, для цепи или для целой молекулы. Доступные площади (или различия площадей) для конкретных атомов могут быть записаны в файле выходных данных псевдо-PDB. AREAIMOL допускает единственный радиус для каждого элемента и распознает только ограниченное количество различных элементов.
AREAIMOL и SURFACE выдают абсолютную доступность, то есть число квадрантных Ангстремов (Å). Фракционную доступность поверхности вычисляют относительно стандартного состояния свойственного аминокислоте в полипептиде. Эталонным состоянием является трипептид Gly-X-Gly, где Х представляет собой представляющую интерес аминокислоту, и стандартное состояние должно быть «растянутой» конформацией, то есть как в бета-цепях. Растянутая конформация увеличивает до максимума доступность Х. Расчитанную площадь доступности делят на площадь доступности эталонного состояния трипептида Gly-X-Gly и получают частное, которое представляет собой фракционную доступность. Процент доступности представляет собой фракционную доступность, умноженную на 100. Другой иллюстративный алгоритм для подсчета доступной поверхности основан на модуле SOLV программы xsae (Broger, C, F. Hoffman-LaRoche, Basel), который подсчитывает фракционную доступность аминокислотного остатка для водной сферы на основе рентгенографических координат полипептида. Фракционная поверхностная доступность для каждой аминокислоты в антителе может быть вычислена с использованием доступной информации о кристаллической структуре (Eigenbrot et al. (1993) J Mol Biol. 229: 969-995).
ДНК, кодирующую антитела, сконструированные с цистеином, можно быстро выделить и определить ее последовательность, используя общепринятые способы (например, используя олигонуклеотидные зонды, которые способны специфически связываться с генами, кодирующими тяжелые и легкие цепи мышиных антител). Клетки гибридомы выступают в качестве источника такой ДНК. После выделения ДНК может быть помещена в экспрессирующие векторы, которые затем трансфицируют в клетки-хозяева, такие как клетки E.coli, клетки COS обезьяны, клетки яичника китайского хомячка (CHO), или другие клетки-хозяева млекопитающих, например, клетки миеломы (US 5807715; US 2005/0048572; US 2004/0229310), которые иным способом не продуцируют белок антитела, для достижения синтеза моноклональных антител в рекомбинантных клетках-хозяевах.
После конструирования и отбора, антитела, сконструированные с цистеином, например, ТиоFab со сконструированными, чрезвычайно реактивными непарными остатками Cys, могут быть получены посредством: (i) экспрессии в бактериальной, например E. coli, системе (Skerra et al (1993) Curr. Opinion in Immunol. 5: 256-262; Plückthun (1992) Immunol. Revs. 130: 151-188) или системе клеточной культуры млекопитающего (WO 01/00245), например, клетках яичника китайского хомячка (CHO); и (ii) очистки с использованием общих технологий очистки белков (Lowman et al (1991) J. Biol. Chem. 266(17): 10982-10988).
Тиоловые группы сконструированного Cys реагируют с электрофильными линкерными реагентами и промежуточными соединениями лекарственное средство-линкер, для образования конъюгатов антитела, сконструированного с цистеином, и лекарственного средства, и других меченых антител, сконструированных с цистеином. Остатки Cys в антителах, сконструированных с цистенином, и присутствующие в родительских антителах, которые являются спаренными и формируют межцепочечные и внутрицепочечные дисульфидные связи, не имеют ни одной реактивной тиоловой группы (если только не обработаны восстанавливающим веществом) и не реагируют с нуклеофильными линкерными реагентами или промежуточными соединениями лекарственное средство-линкер. Свежесконструированный остаток Cys может оставаться неспаренным и способен реагировать, например конъюгироваться, с электрофильным линкерным реагентом или промежуточным соединением лекарственное средство-линкер, как, например, лекарственное средство-малеимид. Примеры промежуточных соединений лекарственное средство-линкер включают: MC-MMAE, MC-MMAF, MC-vc-PAB-MMAE, и MC-vc-PAB-MMAF. Структурные положения сконструированных остатков Cys тяжелой и легкой цепей пронумерованы в соответствии с системой последовательной нумерации. Эта система последовательной нумерации согласована с системой нумерации по Кабату (Kabat et al., (1991) Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD), начинаясь с N-конца, отличается от схемы нумерации по Кабату (нижний ряд) вставками, обозначенными a,b,c. Используя систему нумерации по Кабату, фактическая линейная аминокислотная последовательность может содержать меньшее или дополнительное количество аминокислот, что связано с укорочением или вставками в FR или CDR вариабельного домена. Вариантные участки тяжелой цепи, сконструированной с цистеином, определяют по схемам последовательной нумерации и нумерации по Кабату.
В одном варианте осуществления антитело против TENB2, сконструированное с цистеином, получают способом, включающим:
(a) замену одного или нескольких аминокислотных остатков родительского антитела против TENB2 на цистеин; и
(b) определение тиоловой реактивности антитела против TENB2, сконструированного с цистеином, по реагированию антитела, сконструированного с цистеином, с тиол-реактивным реагентом.
Антитело, сконструированное с цистеином, может быть более реакционноспособным, чем родительское антитело, с тиол-реактивным реагентом.
Свободные аминокислотные остатки цистеина могут быть расположены в тяжелой или легкой цепях, или в константных или в вариабельных доменах. Фрагменты антител, например, Fab, также могут быть сконструированы с одной или несколькими аминокислотами цистеина, замещающими аминокислоты фрагмента антитела, с образованием фрагментов антитела, сконструированных с цистеином.
Другой вариант осуществления данного изобретения обеспечивает способ получения (изготовления) антитела против TENB2, сконструированного с цистеином, включающий:
(a) встраивание одной или нескольких аминокислот цистеина в родительское антитело против TENB2, для создания антитела против TENB2, сконструированного с цистеином; и
(b) определение тиоловой реактивности антитела, сконструированного с цистеином, с тиол-реактивным реагентом;
где антитело, сконструированное с цистеином, может быть более реактивным, чем родительское антитело, с тиол-реактивным реагентом.
Стадия (a) способа получения антитела, сконструированного с цистеином, может включать:
(i) мутагенез последовательности нуклеиновой кислоты, кодирующей антитело, сконструированное с цистеином;
(ii) экспрессирование антитела, сконструированного с цистеином; и
(iii) выделение и очистку антитела, сконструированного с цистеином.
Стадия (b) способа получения антитела, сконструированного с цистеином, может включать экспрессирование антитела, сконструированного с цистеином, вирусной частицей, выбранной из фага или фагемидной частицы.
Стадия (b) способа получения антитела, сконструированного с цистеином, также может содержать:
(i) реагирование антитела, сконструированного с цистеином, с тиол-реактивным аффинным реагентом, для создания аффинного меченого антитела, сконструированного с цистеином; и
(ii) измерение связывания аффинного меченого антитела, сконструированного с цистеином, с поглощающей средой.
Другим вариантом осуществления изобретения является способ скрининга на тиоловую реактивность антител, сконструированных с цистеином, с чрезвычайно реактивными неспаренными аминокислотами цистеина, включающий:
(a) встраивание одной или нескольких аминокислот цистеина в родительское антитело, для создания антитела, сконструированного с цистеином;
(b) взаимодействие антитела, сконструированного с цистеином, с тиол-реактивным аффинным реагентом, для создания аффинного меченого антитела, сконструированного с цистеином; и
(c) измерение связывания аффинного меченого антитела, сконструированного с цистеином, с поглощающей средой; и
(d) определение тиоловой реактивности антитела, сконструированного с цистеином, с тиол-реактивным реагентом.
Стадия (a) метода скрининга антител, сконструированных с цистеином, может включать:
(i) мутагенез последовательности нуклеиновой кислоты, кодирующей антитело, сконструированное с цистеином;
(ii) экспрессирование антитела, сконструированного с цистеином; и
(iii) выделение и очистку антитела, сконструированного с цистеином.
Стадия (b) метода скрининга антител, сконструированных с цистеином, может включать экспрессирование антитела, сконструированного с цистеином, вирусной частицей, выбранной из фага или фагемидной частицы.
Стадия (b) способа получения антитела, сконструированного с цистеином, дополнительно может включать:
(i) взаимодействие антитела, сконструированного с цистеином, с тиол-реактивным аффинным реагентом, для создания аффинного меченого антитела, сконструированного с цистеином; и
(ii) измерение связывания аффинного меченого антитела, сконструированного с цистеином, с поглощающей средой.
Варианты IgG TMEFF2#19, сконструированные с цистеином
Цистеин был встроен в положение 121 тяжелой цепи (последовательная нумерация без сигнальной последовательности) в полноразмерные, гуманизированные родительские моноклональные антитела TMEFF2#19 против TENB2 посредством методов конструирования цистеина, описанных в настоящем документе, для получения гуманизированного варианта A121C thio hu против TENB2 TMEFF2#19, с последовательностью тяжелой цепи: SEQ ID NO:1, и последовательностью легкой цепи: SEQ ID NO:2, фиг.1. Эти моноклональные антитела, сконструированные с цистеином, были экспрессированы в клетках CHO (клетки яичника китайского хомячка) в результате кратковременной ферментации в среде, содержащей 1 мМ цистеин.
Согласно одному варианту осуществления гуманизированные антитела TMEFF2#19 против TENB2, сконструированные с цистеином, содержат одну или несколько из следующих последовательностей вариабельной области тяжелой цепи со свободной аминокислотой цистеина (Таблица 1).
Сравнение нумерации тяжелой цепи между последовательной нумерацией, нумерацией по Кабату и нумерацией Eu для вариантов антитела hu TMEFF2#19 против TENB2, сконструированных с цистеином
В соответствии с одним вариантом осуществления гуманизированное антитело TMEFF2#19 против TENB2, сконструированное с цистеином, содержит одну или несколько из следующих последовательностей вариабельной области легкой цепи со свободной аминокислотой цистеина (Таблица 2).
Сравнение нумерации легкой цепи между последовательной нумерацией и нумерацией по Кабату для вариантов антитела hu TMEFF2#19 против TENB2, сконструированных с цистеином
Меченые антитела против TENB2, сконструированные с цистеином
Антитела против TENB2, сконструированные с цистеином, могут быть сайтспецифически и эффективно соединены с тиол-реактивным реагентом. Тиол-реактивный реагент может быть многофункциональным линкерным реагентом, меченым реагентом захвата, т.е. аффинности (например биотин-линкерный реагент), меткой детекции (например, флуорофорный реагент), твердофазным иммобилизирующим реагентом (например, SEPHAROSE™, полистирол или стекло) или промежуточным соединением лекарственное средство-линкер. Одним примером тиол-реактивного реагента является N-этил-малеимид (NEM). В иллюстративном варианте осуществления реакция ТиоFab с биотин-линкерным реагентом обеспечивает биотилинированное ТиоFab, посредством чего наличие и реактивность сконструированного остатка цистеина могут быть выявлены и измерены. Реакция ТиоFab с многофункциональным линкерным реагентом обеспечивает ТиоFab с функционализированным линкером, который далее может реагировать с молекулой лекарственного средства или другой меткой. Реакция ТиоFab с промежуточным соединением лекарственное средство-линкер обеспечивает конъюгат лекарственного средства с ТиоFab.
Иллюстративные методы, описанные в настоящем документе, могут быть применены, в целом, для идентификации и получения антител, и в более общем смысле, для других белков, используя конструкцию и стадии скрининга, описанные в настоящем документе.
Такой подход может быть применен для конъюгирования других тиол-реактивных реагентов, в которых реактивной группой является, например, малеимид, иодацетамид, пиридилдисульфид или другой тиол-реактивный партнер по конъюгированию (Haugland, 2003, Molecular Probes Handbook of Fluorescent Probes and Research Chemicals, Molecular Probes, Inc.; Brinkley, 1992, Bioconjugate Chem. 3: 2; Garman, 1997, Non-Radioactive Labelling: A Practical Approach, Academic Press, London; Means (1990) Bioconjugate Chem. 1: 2; Hermanson, G. in Bioconjugate Techniques (1996) Academic Press, San Diego, pp. 40-55, 643-671). Тиол-реактивным реагентом может быть молекула лекарственного средства, флуорофор, такой как флуоресцентный краситель, подобный флуоресцеину или родамину, хелатирующий агент для металлов, использующихся в диагностической визуализации или радиотерапии, пептидиловая или непептидиловая метка или метка детекции, или агенты, модифицирующие клиренс, такие как различные изомеры полиэтиленгликоля, пептид, который связывается с третьим компонентом, или другой углеводный или липофильный агент.
Применение антител против TENB2, сконструированных с цистеином
Антитела против TENB2, сконструированные с цистеином, и их конъюгаты можно использовать в качестве терапевтических и/или диагностических средств. Настоящее изобретение дополнительно обеспечивает способы профилактики, контролирования, лечения или облегчения одного или нескольких симптомов, ассоциированных с нарушением, связанным с TENB2. В частности, настоящее изобретение обеспечивает способы профилактики, контролирования, лечения или облегчения одного или нескольких симптомов, ассоциированных с нарушением, сопровождающимся пролиферацией клеток, таким как рак, например, рак яичников, рак шейки матки, рак матки, рак поджелудочной железы, рак легких или рак молочной железы. Настоящее изобретение также дополнительно обеспечивает способы диагностики нарушения, связанного с TENB2, или предрасположенности к такому нарушению, а так же способы для выявления антител, и антигенсвязывающих фрагментов антител, которые предпочтительно связывают клеточноассоциированные полипептиды TENB2.
Другой вариант осуществления настоящего изобретения относится к использованию антитела против TENB2, сконструированного с цистеином, для получения лекарственного средства, пригодного для лечения состояния, обусловленного нарушением, связанным с TENB2.
КОНЪЮГАТЫ ЛЕКАРСТВЕННОГО СРЕДСТВА И АНТИТЕЛА ПРОТИВ TENB2, СКОНСТРУИРОВАННОГО С ЦИСТЕИНОМ
Другим аспектом изобретения является соединение конъюгата лекарственного средства и антитела, включающее антитело (Ab) против TENB2, сконструированное с цистеином, и молекулу (D) лекарственного средства ауристаин, в котором антитело, сконструированное с цистеином, присоединено к D посредством одной или нескольких свободных аминокислот цистеина с помощью линкерной молекулы (L); соединение имеет формулу I:

где p равно 1, 2, 3, или 4; и где антитело, сконструированное с цистеином, получено способом, включающим замену одного или нескольких аминокислотных остатков в родительском антителе против TENB2 на одну или несколько свободных аминокислот цистеина.
На фиг.5 представлены варианты осуществления конъюгатов (ADC) антител против TENB2, сконструированных с цистеином, с лекарственным средством, где молекула лекарственного средства ауристатин присоединена к сконструированной цистеиновой группе в: легкой цепи (LC-ADC); тяжелой цепи (HC-ADC); и в Fc-области (Fc-ADC).
Потенциальные преимущества конъюгатов лекарственного средства и антитела против TENB2, сконструированного с цистеином, включают увеличенную безопасность (более высокий терапевтический индекс), улучшенные параметры фармакокинетики, сохраняются межцепочечные дисульфидные связи в антителе, что может стабилизировать конъюгат и сохранить его активную связывающую конформацию, определены сайты конъюгирования лекарственного средства, и получение конъюгатов лекарственного средства с антителом, сконструированным с цистеином, путем конъюгирования антител, сконструированных с цистеином, с реагентами лекарственное средство-линкер в результате приведет к образованию более гомогенного продукта.
Лекарственные молекулы
Молекула лекарственного средства ауристатин в конъюгатах антитело-лекарственное средство (ADC) по Формуле I, включает доластатины, ауристатины (US 5635483; US 5780588; US 5767237; US 6124431), и их аналоги или производные. Было показано, что доластатины и ауристатины препятствуют динамическим свойствам микротрубочек, гидролизу GTP и ядерному и клеточному делению (Woyke et al (2001) Antimicrob. Agents and Chemother. 45(12): 3580-3584) и обладают противораковой (US 5663149) и противогрибковой активностью (Pettit et al (1998) Antimicrob. Agents Chemother. 42: 2961-2965). Различные формы лекарственной молекулы доластатина или ауристатина могут быть ковалентно связаны с антителом через N (амино)-конец или C (карбоксильный) конец пептидной лекарственной молекулы (WO 02/088172; Doronina et al (2003) Nature Biotechnology 21(7): 778-784; Francisco et al (2003) Blood 102(4): 1458-1465).
Иллюстративные варианты воплощения ауристина включают N-концевые связанные лекарственные молекулы монометилауристина DE и DF, раскрытых в: WO 2005/081711; Senter et al, Proceedings of the American Association for Cancer Research, Volume 45, Abstract Number 623, presented March 28, 2004, описания каждого из которых включено в настоящий документ в качестве ссылки в их полном объеме. Иллюстративные молекулы лекарственного средства ауристатин включают MMAE и MMAF.
Молекула лекарственного средства ауристатин (D) в конъюгатах антитело-лекарственное средство (ADC) по Формуле I, включает молекулы лекарственного средства монометиауристатин MMAE и MMAF. N-конец молекулы лекарственного средства MMAE или MMAF ковалентно связан через линкер со сконструированным цистеином антитела.
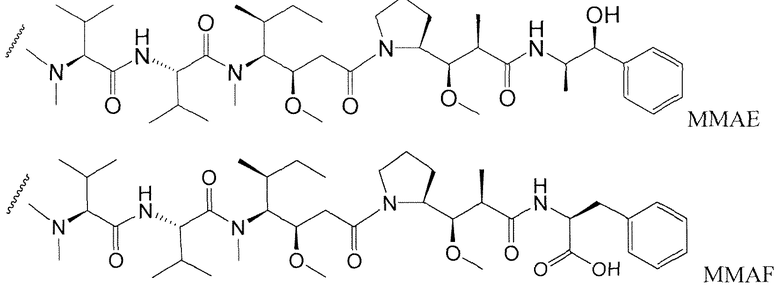
Другие примеры молекул лекарственного средства ауристатин включают соединения монометилвалина, имеющие карбокси-модификации фениаланина на С-конце пентапептидной лекарственной молекулы ауристатина (WO 2007/008848) и соединения монометилвалина, имеющие модификации боковой цепи фенилаланина на С-конце пентапептидной лекарственной молекулы ауристатина (WO 2007/008603).
Обычно, лекарственные молекулы на основе пептида, могут быть получены посредством формирования пептидной связи между двумя или более аминокислотами и/или пептидными фрагментами. Такие пептидные связи могут быть получены, например, по методу синтеза в жидкой фазе (см. E. Schroder and K. Lubke, "The Peptides", volume 1, pp 76-136, 1965, Academic Press), который хорошо известен в области химии пептидов.
Линкеры
«Линкер», «линкерная единица», или «связь» означает химический фрагмент, включающий ковалентную связь или цепочку атомов, которая ковалентно соединяет антитело с лекарственной молекулой. В различных вариантах осуществления линкер обозначен как L. «Линкер» (L) представляет собой бифункциональную или многофонкциональную молекулу, которую можно использовать для связи одной или нескольких лекарственных молекул (D) с антительной единицей (Ab) для образования конъюгатов антитело-лекарственное средство (ADC) Формулы I. Конъюгаты антитело-лекарственное средство (ADC) удобно получать, используя линкер, имеющий реактивную функциональность для связывания лекарственного средства с антителом. Тиол цистеина антитела (Ab), сконструированного с цистеином, может образовывать связь с электрофильной функциональной группой линкерного реагента, лекарственной молекулой или промежуточным соединением лекарственное средство-линкер.
В одном аспекте, линкер имеет реакционноспособный участок, в котором находится электрофильная группа, являющаяся реакционноспособной с нуклеофильным цистеином, присутствующим на антителе. Тиол цистеина антитела является реакционноспособным с электрофильной группой линкера и образует ковалентную связь с линкером. Пригодные электрофильные группы включают, но не ограничены ими, малеимидные и галогенацетамидные группы.
Линкеры включают двухвалентные радикалы, такие как алкилдиил, арилен, гетероарилен, такие молекулы, как: -(CR2)nO(CR2)n-, повторяющиеся единицы алкилокси (например, полиэтиленокси, PEG, полиметиленокси) и алкиламино (например, полиэтиленамино, Jeffamine™); и эфиры двухосновных кислот и амиды, включая сукцинат, сукцинамид, эфир дигликолевой кислоты, малонат и капроамид.
Антитела, сконструированные с цистеином, вступают в реакцию с линкерными реагентами или промежуточными соединениями лекарственное средство-линкер, с электрофильными функциональными группами, такими как малеимид или α-галогенкарбонил, в соответствии с методом конъюгирования, представленным на странице 766 у Klussman, et al (2004), Bioconjugate Chemistry 15(4): 765-773, и в соответствии с протоколом из Примера 3.
Линкер может состоять из одного или нескольких линкерных компонентов. Иллюстративные линкерные компоненты включают 6-малеимидокапроил («MC»), малеимидопропаноил («MP»), валин-цитрулин («val-cit» или «vc»), аланин-фенилаланин («ala-phe» или «af»), п-аминобензилоксикарбонил («PAB»), N-сукцинимидил-4-(2-пиридилтио)пентоат («SPP»), N-сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат («SMCC»), N-сукцинимидил(4-йодо-ацетил)амонобензоат («SIAB»), этилэтиленокси-CH2CH2O- в виде одной или нескольких повторяющихся единиц («EO» или «PEO»). Дополнительные линкерные компоненты известны в уровне техники и некоторые описаны в настоящем документе.
В одном варианте осуществления линкер L ADC имеет формулу:
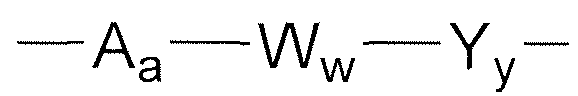
где:
-A- представляет собой элемент поперечной связи, ковалентно связанный с тиолом цистеина антитела (Ab);
a равно 0 или 1;
каждый -W- независимо представляет собой аминокислотную единицу;
w независимо представляет собой целое число от 0 до 12;
-Y- представляет собой спейсерную единицу, ковалентно связанную с молекулой лекарственного средства; и
y равно 0, 1 или 2.
Элемент поперечной связи
Элемент поперечной связи (-A-), когда присутствует, способен связывать антительную единицу с аминокислотной единицей (-W-). При этом антитело (Ab) имеет тиольную группу свободного цистеина, которая может образовывать связь с электрофильной функциональной группой элемента поперечной связи. Примеры элементов поперечной связи конъюгатов по формуле I, отображены формулами II и III, где Ab-, -W-, -Y-, -D, w и y определены выше, и R17 представляет собой двухвалентный радикал, выбранный из (CH2)r, C3-C8 карбоциклила, О-(CH2)r, арилена, (CH2)r-арилена, -арилен-(CH2)r-, (CH2)r-(C3-C8 карбоциклил), (C3-C8 карбоциклил)-(CH2)r, C3-C8 гетероциклила, (CH2)r-(C3-C8 гетероциклил), -(C3-C8 гетероциклил)-(CH2)r-, -(CH2)rC(О)NRb(CH2)r-, -(CH2CH2O)r- -(CH2CH2O)r-CH2-, -(CH2)rC(О)NRb(CH2CH2O)r-, -(CH2)rC(О)NRb(CH2CH2O)r-CH2-, -(CH2CH2O)rC(О)NRb(CH2CH2O)r-, -(CH2CH2O)rC(О)NRb(CH2CH2O)-CH2-, и -(CH2CH2O)rC(О)NRb(CH2)r-; где Rb представляет собой H, C1-C6 алкил, фенил или бензил; и r независимо является целым числом от 1 до 10.
Арилен включает двухвалентные радикалы ароматических улеводородов из 6-20 атомов улерода, полученные в результате удаления двух атомов водорода из системы ароматического кольца. Типичные ариленовые группы включают, но не ограничены ими, радикалы, полученные из бензола, замещенного бензола, нафталина, антрацена, бифенила и тому подобного.
Гетероциклические группы включают кольцевую систему, в которой один или несколько кольцевых атомов представляет собой гетероатом, например, азота, кислорода или серы. Гетероциклический радикал включает от 1 до 20 атомов углерода, и от 1 до 3 гетероатомов, выбранных из N, O, P или S. Гетероцикл может быть моноциклом, имеющим от 3 до 7 членов кольца (от 2 до 6 атомов углерода и от 1 до 3 гетороатомов, выбранных из N, O, P и S), или бициклом, имеющим от 7 до 10 членов кольца (от 4 до 9 атомов углерода и от 1 до 3 гетороатомов, выбранных из N, O, P и S), например: бициклосистема [4,5], [5,5], [5,6] или [6,6]. Гетероциклы описаны у Paquette, Leo A.; «Principles of Modern Heterocyclic Chemistry» (W.A. Benjamin, New York, 1968), в частности Главы 1, 3, 4, 6, 7 и 9; «The Chemistry of Heterocyclic Compounds, A series of Monographs» (John Wiley & Sons, New York, 1950 to present), в частности тома 13, 14, 16, 19 и 28; и J. Am. Chem. Soc. (1960) 82: 5566.
Примеры гетероциклов включают в порядке иллюстрации, но не ограничиваясь ими, включают пиридил, дигидропиридил, тетрагидропиридил (пиперидил), тиазолил, тетрагидротиофенил, тетрагидротиофенил с окисленной серой, пиримидинил, фуранил, тиенил, пирролил, пиразолил, имидазолил, тетразолил, бензофуранил, тианафталенил, индолил, индоленил, хинолинил, изохинолинил, бензимидазолил, пиперидинил, 4-пиперидонил, пирролидинил, 2-пирролидонил, пирролинил, тетрагидрофуранил, бис-тетрагидрофуранил, тетрагидропиранил, бис-тетрагидропиранил, тетрагидрохинолинил, тетрагидроизохинолинил, декагидрохинолинил, октагидроизохинолинил, азоцинил, триазинил, 6Н-1,2,5-тиадиазинил, 2Н,6Н-1,5,2-дитиазинил, тиенил, тиантренил, пиранил, изобензофуранил, хроменил, ксантенил, феноксантинил, 2Н-пирролил, изотиазолил, изоксазолил, пиразинил, пиридазинил, индолизинил, изоиндолил, 3Н-индолил, 1H-индазолил, пуринил, 4Н-хинолизинил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинил, птеридинил, 4Ah-карбазолил, карбазолил, β-карболинил, фенантридинил, акридинил, пиримидинил, фенантролинил, феназинил, фенотиазинил, фуразанил, феноксазинил, изохроманил, хроманил, имидазолидинил, имидазолинил, пиразолидинил, пиразолинил, пиперазинил, индолинил, изоиндолинил, хинуклидинил, морфолинил, оксазолидинил, бензотриазолил, бензизоксазолил, оксиндолил, бензоксазолинил и изатиноил.
Карбоциклильные группы включают насыщенное или ненасыщенное кольцо, имеющее от 3 до 7 атомов углерода, в виде моноцикла, или от 7 до 12 атомов углерода в виде бицикла. Моноциклические карбоциклы имеют в кольце от 3 до 6 атомов, еще более типично, от 5 до 6 атомов. Бициклические карбоциклы имеют от 7 до 12 атомов в кольце, например, упорядоченные как бициклосистема [4,5], [5,5], [5,6] или [6,6], или 9 или 10 атомов в кольце, упорядоченные как бициклосистема [5,6] или [6,6]. Примеры моноциклических карбоциклов включают циклопропил, циклобутил, циклопентил, 1-циклопент-1-енил, 1-циклопент-2-енил, 1-циклопент-3-енил, циклогексил, 1-циклогекс-1-енил, 1-циклогекс-2-енил, 1-циклогекс-3-енил, циклогептил и циклооктил.
Исходя из иллюстративных вариантов осуществления ADC по формуле I, таких как II-V, следует понимать, что даже там, где не обозначено явно, от 1 до 4 молекул лекарственного средства присоединены к антителу (p=1-4), в зависимости от числа сконструированных остатков цистеина.
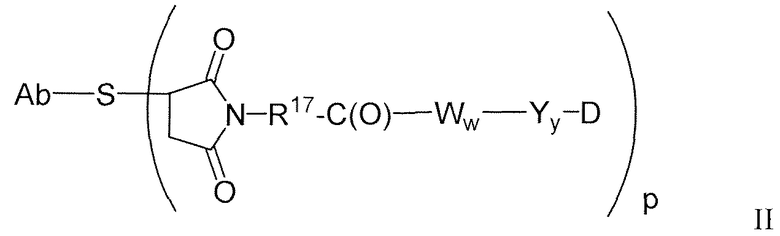
Иллюстративный элемент поперечной связи Формулы II получен из малеимидокапроила (МС), где R17 представляет собой-(CH2)5-:
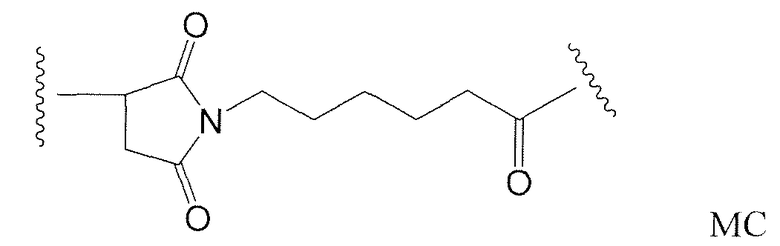
Иллюстративный элемент поперечной связи Формулы II получен из малеимидопропаноила (МР), где R17 представляет собой -(CH2)2-:
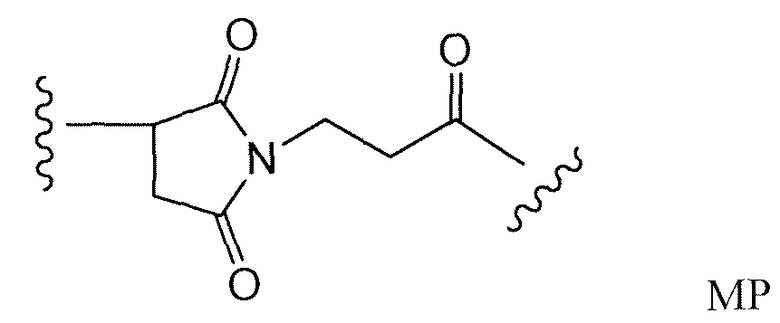
Другой иллюстративный элемент поперечной связи Формулы II, где R17 представляет собой -(CH2CH2O)r-CH2-, и r равен 2:
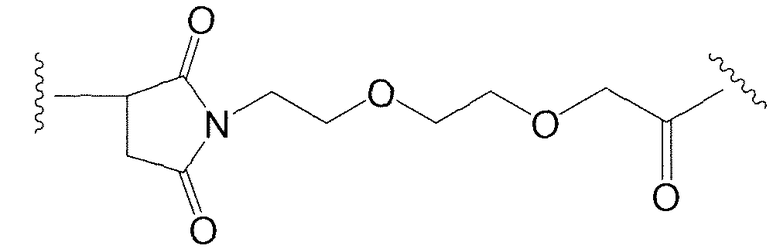
Другой иллюстративный элемент поперечной связи Формулы II, где R17 представляет собой (CH2)rC(O)NRb(CH2CH2O)r-CH2-, где Rb представляет собой H, и каждый r равен 2:
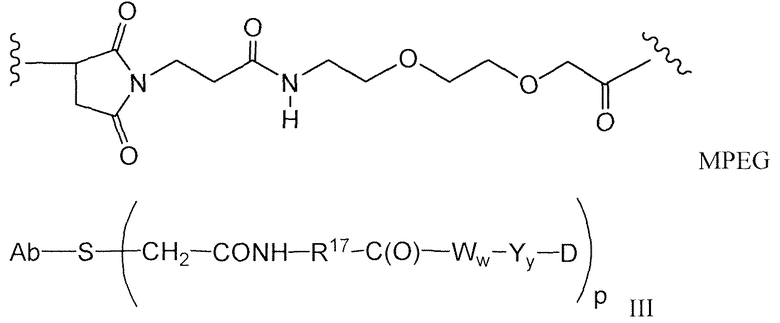
Пример элемента поперечной связи Формулы III, где R17 представляет собой -(CH2)5-:
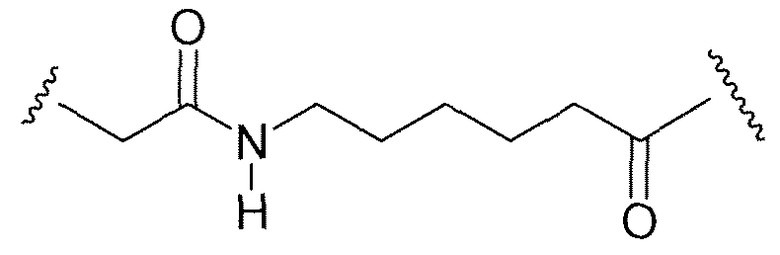
В другом варианте осуществления элемент поперечной связи присоединен к антителу против TENB2, сконструированного с цистеином, посредством дисульфидной связи между атомом серы сконструированного цистеина в антителе, и атомом серы элемента поперечной связи. Характерный элемент поперечной связи по этому варианту осуществления описан Формулой IV, где R17, Ab-, -W-, -Y-, -D, w и y определены выше.
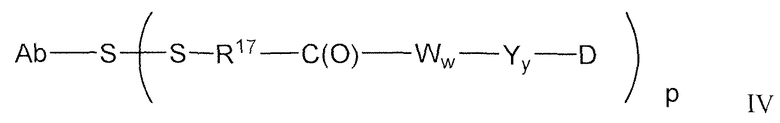
В еще одном варианте осуществления реактивная группа элемента поперечной связи содержит тиол-реактивную функциональную группу, которая может образовывать связь с тиолом свободного цистеина антитела. Примеры тиол-реактивных функциональных групп включают, но не ограничиваются ими, малеимид, α-галогенацетил, активированные эфиры, такие как эфиры сукциниммида, эфиры 4-нитрофенила, эфиры пентафторфенила, эфиры тетрафторфенила, ангидриды, хлорангидриды, сульфонилхлориды, изоцианаты и изотиоцианаты. Характерные элементы поперечной связи по этому варианту осуществления описаны Формулами Va и Vb, где R17, Ab-, -W-, -Y-, -D, w и y определены выше;
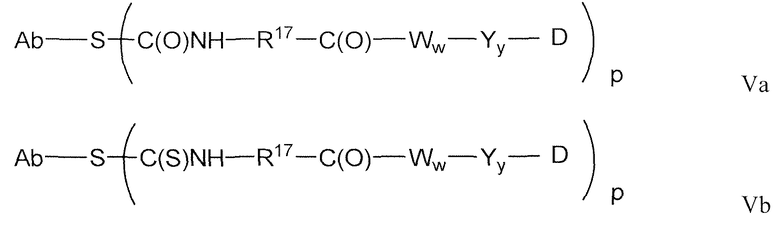
В другом варианте осуществления линкер может быть линкером разветвленного типа для ковалентного связывания более чем одной молекулы лекарственного средства с антителом посредством разветвленной многофункциональной линкерной молекулы (Sun et al (2002) Bioorganic & Medicinal Chemistry Letters 12: 2213-2215; Sun et al (2003) Bioorganic & Medicinal Chemistry 11: 1761-1768; King (2002) Tetrahedron Letters 43: 1987-1990). Разветвленные линкеры могут повысить молярное отношение лекарственного средства к антителу, а именно, нагрузку, что относится к эффективности ADC. Таким образом, в случае, когда антитело, сконструированное с цистеином, несет только одну реактивную тиоловую группу цистеина, большое число молекул лекарственного средства могут быть присоединены посредством разветвленного линкера.
Аминокислотная единица
Линкер может содержать аминокислотные остатки. Аминокислотная единица (-Ww-), когда присутствует, связывает антитело (Ab) с молекулой (D) лекарственного средства конъюгата (ADC) лекарственного средства и антитела, сконструированного с цистеином по изобретению.
-Ww- представляет собой дипептидную, трипептидную, тетрапептидную, пентапептидную, гексапептидную, гептапептидную, октапептидную, нонапептидную, декапептидную, ундекапептидную или додекапептидную единицу. Аминокислотные остатки, которые содержат аминокислотную единицу, включают те, которые встречаются в природе, а также неосновные аминокислоты и не встречающиеся в природе аналоги аминокислот, например, цитруллин. Каждая единица -W- независимо имеет формулу, указанную ниже в квадратных скобках, и w является целым числом от 0 до 12:
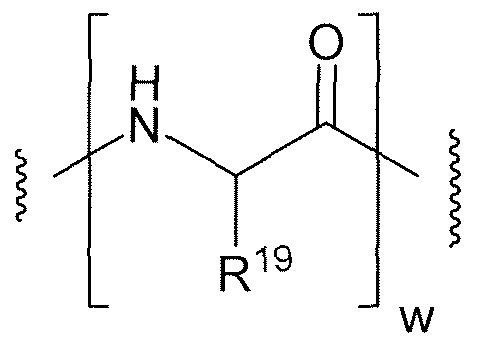
где R19 представляет собой водород, метил, изопропил, изобутил, втор-бутил, бензил, п-гидроксибензил, -CH2OH, -CH(OH)CH3, -CH2CH2SCH3, -CH2CONH2, -CH2COOH, -CH2CH2CONH2, -CH2CH2COOH, -(CH2)3NHC(=NH)NH2, -(CH2)3NH2, -(CH2)3NHCOCH3, -(CH2)3NHCHO, -(CH2)4NHC(=NH)NH2, -(CH2)4NH2, -(CH2)4NHCOCH3, -(CH2)4NHCHO, -(CH2)3NHCONH2, -(CH2)4NHCONH2, -CH2CH2CH(ОН)CH2NH2, 2-пиридилметил, 3-пиридилметил-, 4-пиридилметил-, фенил, циклогексил,
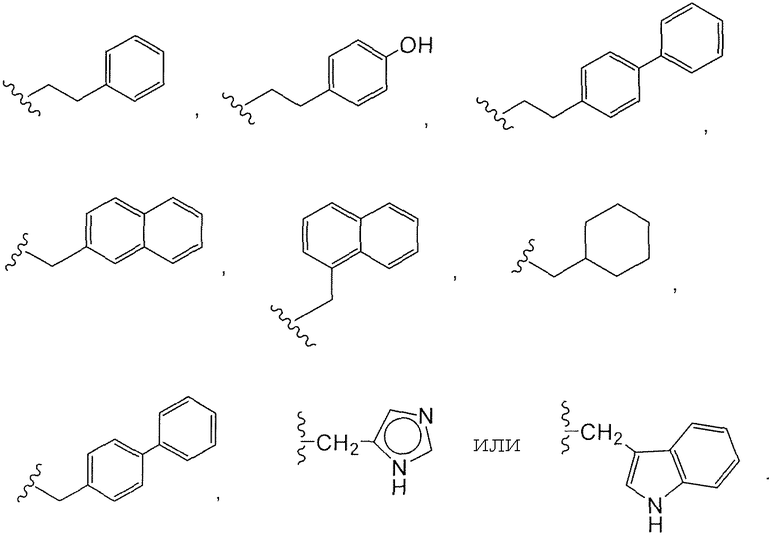
В случае, когда R19 не является водородом, атом углерода, к которому присоединен R19, является хиральным. Каждый атом углерода, к которому присоединен R19, независимо находится в (S) или (R) конфигурации, или является рацемической смесью. Аминокислотные единицы могут, таким образом, быть энантиомерно чистыми, рацемическими или диастереомерными.
Иллюстративные -Ww- аминокислотные единицы включают дипептиды, трипептиды, тетрапептиды или пентапептиды. Иллюстративные дипептиды включают: валин-цитруллин (vc или val-cit), аланин-фенилаланин (af или ala-phe). Иллюстративные трипептиды включают: глицин-валин-цитруллин (gly-val-cit) и глицин-глицин-глицин (gly-gly-gly). Аминокислотные остатки, которые содержат аминокислотный линкерный компонент, включают те, которые встречаются в природе, а также минорные аминокислоты и не встречающиеся в природе аналоги аминокислот, такие как цитруллин.
Аминокислотная единица может быть ферментативно расщеплена одним или несколькими ферментами, включая опухолеассоциированную протеазу, для высвобождения молекулы лекарственного средства (-D), которая в одном варианте осуществления является протонированной in vivo при высвобождении для обеспечения лекарственного средства (D). Компоненты аминокислотного линкера могут быть сконструированы и оптимизированы по их селективности к ферментативному расщеплению определенными ферментами, например, опухолеассоциированной протеазой, катепсином В, С и D или протеазой плазмина.
Спейсерная единица
Спейсерная единица (-Yy-), когда присутствует (y=1 или 2), связывает аминокислотную единицу (-Ww-) с молекулой лекарственного средства (D), в случае, когда аминокислотная единица присутствует (w=1-12). Альтернативно, спейсерная единица связывает элемент поперечной связи с молекулой лекарственного средства, когда аминокислотная единица отсутствует. Спейсерная единица также связывает молекулу лекарственного средства с антительной единицей, в случае, когда отсутствует и аминокислотная единица, и элемент поперечной связи (w, y = 0). Спейсерные единицы бывают двух типов: самоотщепляющиеся и не-самоотщепляющиеся. Не-самоотщепляющаяся спейсерная единица является такой, в которой часть или вся спейсерная единица остается связанной с молекулой лекарственного средства после расщепления, в частности ферментативного, аминокислотной единицы от конъюгата антитело-лекарственное средство или лекарственное средство-линкер. Когда ADC, содержащий глицин-глициновую спейсерную единицу или глициновую спейсерную единицу, подвергается ферментативному расщеплению протеазой, ассоциированной с опухолевыми клетками, протеазой, ассоциированной с раковыми клетками, или лимфоцитассоциированной протеазой, фрагмент глицин-глицин-лекарственная молекула или глицин-лекарственная молекула отщепляется от Ab-Aa-Ww-. В одном варианте осуществления имеет место реакция независимого гидролиза в пределах клетки-мишени, приводящая к расщеплению связи глицин-лекарственная молекула и высвобождению лекарственного средства.
В другом варианте осуществления, -Yy- представляет собой п-аминобезилкарбамоиловую (PAB) единицу, чья фениленовая часть заменена на Qm, где Q представляет собой -C1-C8 алкил, -О-(C1-C8 алкил), -галоген,- нитро или -циано; и m является целым числом от 0 до 4.
Иллюстративными вариантами осуществления не-самоотщепляющейся спейсерной единицы (-Y-) являются: -Gly-Gly-; -Gly-: -Ala-Phe-; -Val-Cit-.
В одном варианте осуществления обеспечена лекарственная молекула-линкер или ADC, где отсутствует спейсерная единица (y=0), или ее фармацевтически приемлемая соль или сольват.
Альтернативно, ADC, содержащий самоотщепляющуюся спейсерную единицу, может высвобождать -D. В одном варианте осуществления, -Y- представляет собой группу PAB, которая связана с -Ww- через атом аминного азота группы PAB, и непосредственно соединена с -D через карбонатную, карбаматную или эфирную группу, где ADC имеет типичную структуру:
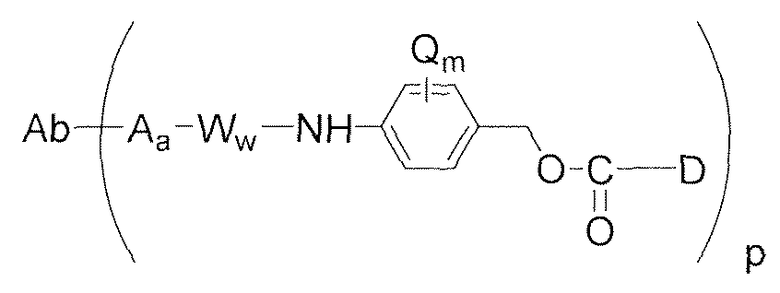
где Q представляет собой -C1-C8 алкил, -О-(C1-C8 алкил), -галоген, -нитро или -циано; m является целым числом от 0 до 4; и p имеет значение от 1 до 4.
Другие примеры самоотщепляющихся спейсерных единиц включают, но не ограничиваются ими, ароматические соединения, которые являются электронно сходными с группой PAB, такие как производные 2-аминоимидазол-5-метанола (Hay et al. (1999) Bioorg. Med. Chem. Lett. 9: 2237), гетероциклические аналоги PAB (US 2005/0256030), бета-глюкуронид (WO 2007/011968), и орто- или пара-аминобензилацетали. Можно использовать спейсеры, которые подвергаются реакции циклизации при гидролизе амидной связи, такие, например, как замещенные и незамещенные амиды 4-аминомасляной кислоты (Rodrigues et al (1995) Chemistry Biology 2: 223), соответственно замещенные бицикло[2.2.1] и бицикло[2.2.2] кольцевые системы (Storm et al (1972) J. Amer. Chem. Soc. 94: 5815) и амиды 2-аминофенилпропионовой кислоты (Amsberry, et al (1990) J. Org. Chem. 55: 5867). Удаление аминсодержащих лекарственных средств, в которых замещен глицин (Kingsbury et al (1984) J. Med. Chem. 27:1447), также является примером самоотщепляющейся спейсерной единицы, пригодной в ADC.
Типичные спейсерные единицы (-Yy-) представлены Формулами X-XII:
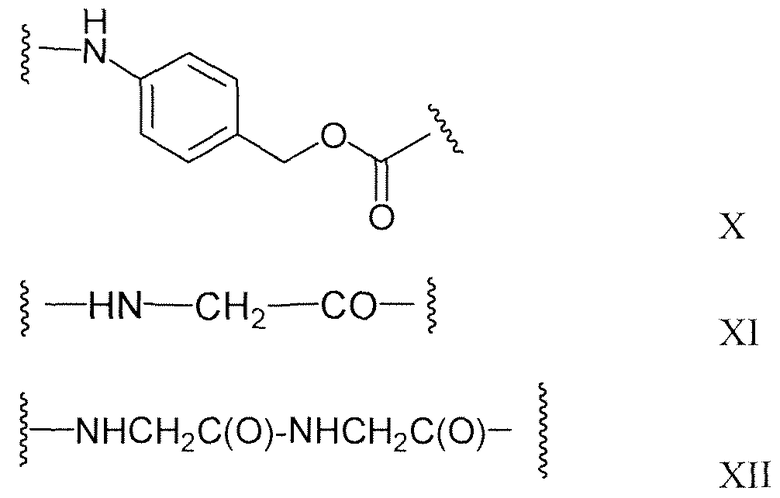
Разветвленные линкеры
В другом варианте осуществления, линкер L может быть линкером разветвленного типа для ковалентного соединения более одной молекулы лекарственного средства с антителом посредством разветвленной, многофункциональной линкерной молекулы (Sun et al (2002) Bioorganic & Medicinal Chemistry Letters 12: 2213-2215; Sun et al (2003) Bioorganic & Medicinal Chemistry 11: 1761-1768). Разветвленные линкеры могут повысить молярное отношение лекарственного средства к антителу, т.е. нагрузку, что относится к эффективности ADC. Таким образом, в случае, когда антитело, сконструированное с цистеином, несет только одну реактивную тиоловую группу цистеина, большое число молекул лекарственного средства могут быть присоединены посредством разветвленного линкера. Примерные варианты осуществления разветвленных, дендритных линкеров включают 2,6-бис(гидроксиметил)-п-крезольные и 2,4,6-трис(гидроксиметил)фенольные дендримерные единицы (WO 2004/01993; Szalai et al (2003) J. Amer. Chem. Soc. 125: 15688-15689; Shamis et al (2004) J. Amer. Chem. Soc. 126: 1726-1731; Amir et al (2003) Angew. Chem. Int. Ed. 42: 4494-4499).
В одном варианте осуществления спейсерная единица представляет собой разветвленный бис(гидроксиметил)стирол (BHMS), который можно использовать для инкорпорирования и высвобождения множества лекарственных средств, имеющий структуру:
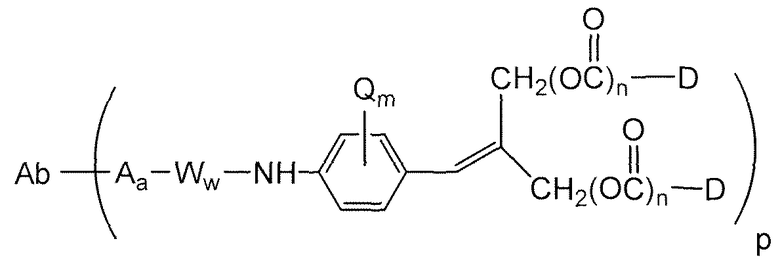
содержащую дендримерную единицу 2-(4-амминобензилиден)пропан-1,3-диол (WO 2004/043493; de Groot et al (2003) Angew. Chem. Int. Ed. 42: 4490-4494), где Q представляет собой -C1-C8 алкил, -О-(C1-C8 алкил), -галоген, -нитро или -циано; m является целым числом от 0 до 4; и p имеет значение от 1 до 4.
Иллюстративные варианты осуществления соединений конъюгата антитело-лекарственное средство Формулы I, включают XIIIa (MC), XIIIb (val-cit), XIIIc (MC-val-cit), и XIIId (MC-val-cit-PAB):
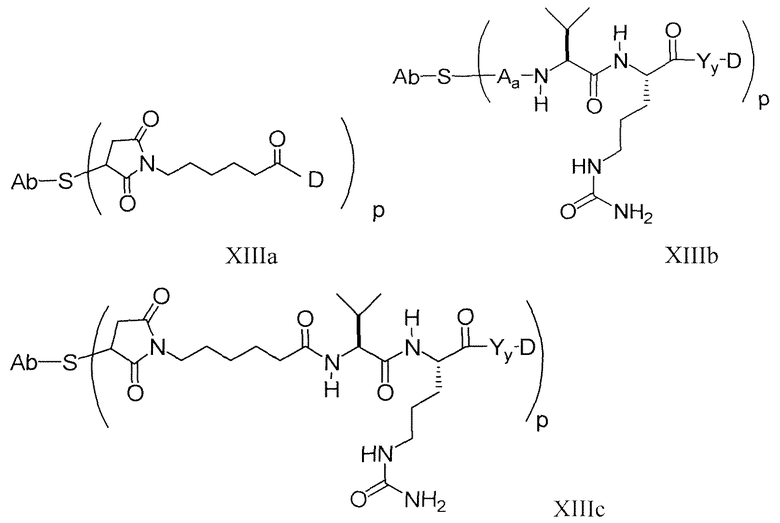
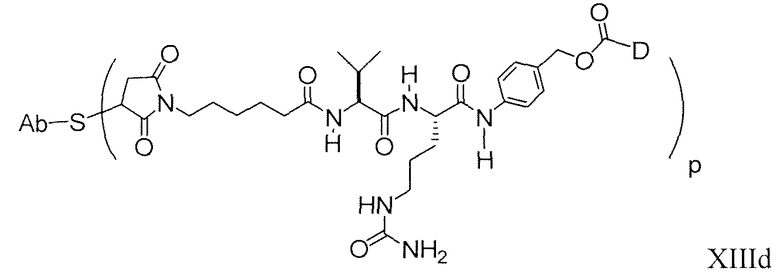
Другие иллюстративные варианты осуществления соединений конъюгата антитело-лекарственное средство Формулы Ia, включают XIVa-e:
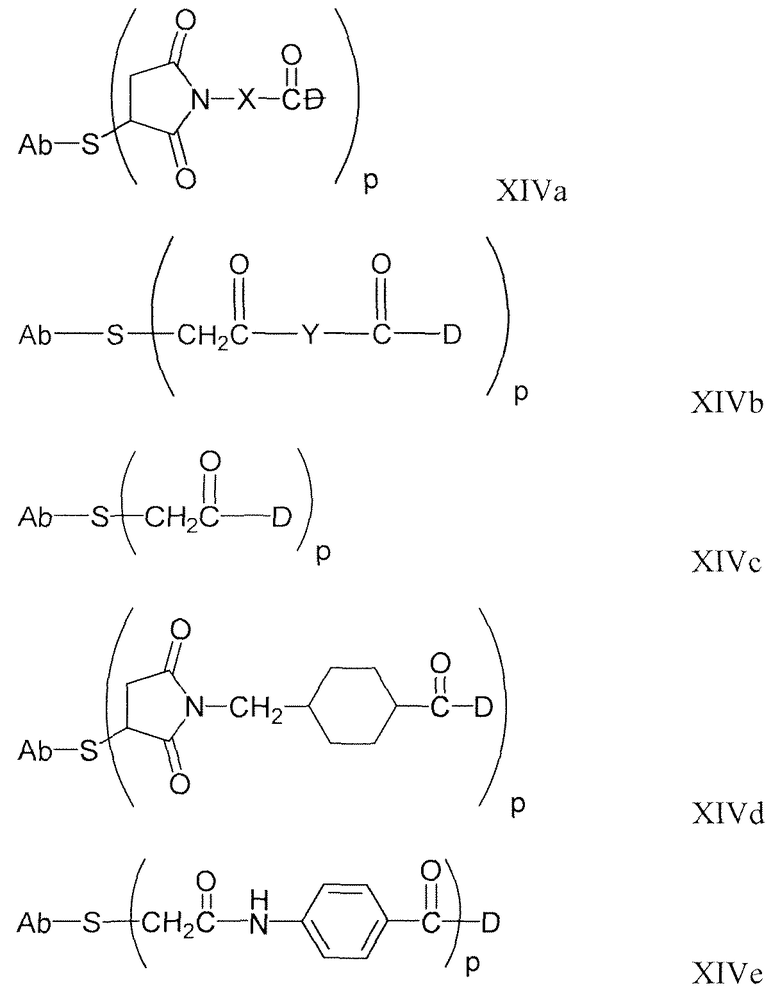
где X представляет собой:
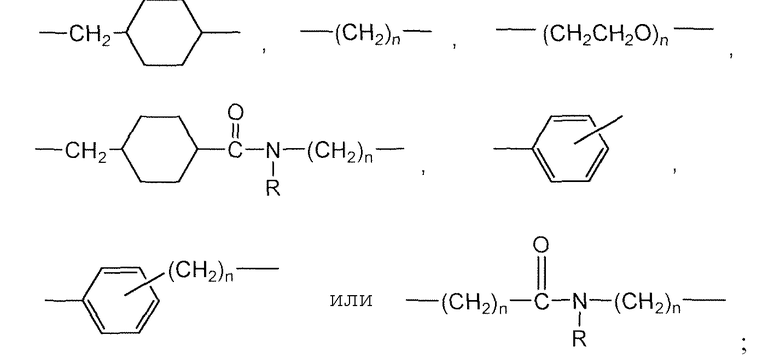
Y представляет собой:
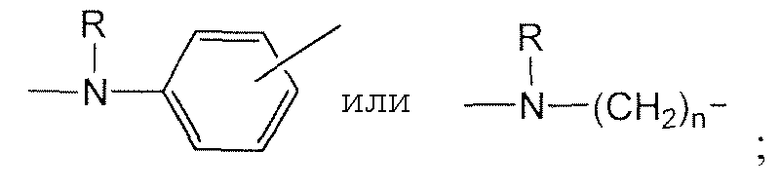
где R независимо представляет собой H или C1-C6 алкил; и n равно от 1 до 12.
В другом варианте осуществления линкер имеет реактивную функциональную группу, которая имеет нуклеофильную группу, являющуюся реакционноспособной с электрофильной группой, представленной в антителе. Пригодные электрофильные группы в антителе включают, но не ограничены ими, альдегидные и кетоновые карбонильные группы. Гетероатом нуклеофильной группы линкера может вступать в реакцию с электрофильной группой на антителе и формировать ковалентную связь с антительной единицей. Пригодные нуклеофильные группы линкера включают, но не ограничены ими, гидразид, оксим, амино, гидразин, тиосемикарбазон, гидразинкарбоксилат и арилгидразид. Электрофильная группа на антителе обеспечивает ковалентный сайт для прикрепления к линкеру.
Обычно, линкеры пептидного типа могут быть получены посредством образования пептидной связи между двумя или более аминокислотными и/или пептидными фрагментами. Такие пептидные связи можно получить, например, используя метод синтеза в жидкой фазе (E. Schröder and K. Lübke (1965) «The Peptides», volume 1, pp 76-136, Academic Press), который хорошо известен в области химии белков. Линкерные промежуточные вещества могут быть собраны с помощью любой комбинации или последовательности реакций, включающих спейсерную единицу, элемент поперечной связи и аминокислотную единицу. Спейсерная единица, элемент поперечной связи и аминокислотная единица могут задействовать реактивные функциональные группы, которые по своей природе являются электрофильными, нуклеофильными или свободнорадикальными. Реактивные функциональные группы включают, но не ограничиваются ими, карбоксилы, гидроксилы, пара-нитрофенилкарбонат, изотиоцианат и уходящие группы, такие как О-мезил, О-тозил, -Cl, -Br, -I; или малеимид.
В другом варианте осуществления линкер может быть замещен группами, которые модулируют растворимость и реактивность. Например, заряженная замещающая группа, такая как сульфонат (-SO3 -) или аммиак, может повысить растворимость в воде реагента и облегчить реакцию связывания линкерного реагента с антителом или молекулой лекарственного средства, или облегчить реакцию связывания Ab-L (промежуточное соединение антитело-линкер) с D или D-L (промежуточное соединение лекарственное средство-линкер) с Ab, в зависимости от синтетического подхода, используемого для получения ADC.
Линкерные реагенты
Конъюгаты антитела и ауристатина могут быть получены с использованием разнообразных бифункциональных линкерных реагентов, таких как N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP), сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (SMCC), иминотиолан (IT), бифункциональные производные имидоэфиров (например, диметиладипимидат HCl), активные эфиры (например, дисукцинимидилсуберат), альдегиды (например, глютаральдегид), бис-азидосоединения (такие как бис(п-азидобензоил)гександиамин), производные бис-диазония (такие как бис-(п-диазонийбензоил)этилендиамин), диизоцианаты (такие как толуол-2,6-диизоцианат) и бис-активные фтористые соединения (такие как 1,5-дифтор-2,4-динитробензол).
Конъюгаты антитело-лекарственное средство также можно получить, используя линкерные реагенты: BMPEO, BMPS, EMCS, GMBS, HBVS, LC-SMCC, MBS, MPBH, SBAP, SIA, SIAB, SMPB, SMPH, сульфо-EMCS, сульфо-GMBS, сульфо-KMUS, сульфо-MBS, сульфо-SIAB, сульфо-SMCC и сульфо-SMPB, и SVSB (сукцинимидил-(4-винилсульфон)бензоат), и включая бис-малеимидные реагенты: DTME, BMB, BMDB, BMH, BMOE, BM(PEO)3 и BM(PEO)4, которые являются коммерчески доступными от Pierce Biotechnology, Inc., P.O. Box 117, Rockford, IL. 61105, USA. Бис-малеимидные реагенты делают возможным соединение тиоловой группы антитела, сконструированного с цистеином, с тиол-содержащей лекарственной молекулой, меткой или линкерным промежуточным соединением, в последовательном или параллельном режиме. Другие функциональные группы, кроме малеимида, которые являются реакционноспособными с тиоловой группой антитела, сконструированного с цистеином, молекулой лекарственного вещества, меткой или линкерным промежуточным соединением, включают йодацетамид, бромацетамид, винилпиридин, дисульфид, пиридилдисульфид, изоцианат и изотиоцианат.
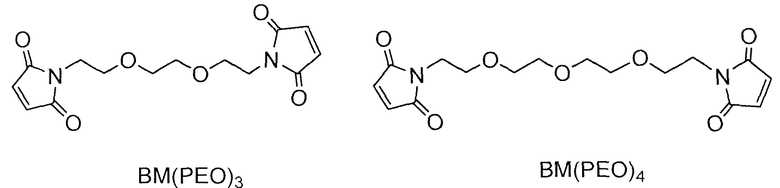
Пригодные линкерные реагенты также могут быть получены из различных коммерческих источников, таких как Molecular Biosciences Inc.(Boulder, CO), или синтезированы в соответствии с процедурами, описанными у Toki et al (2002) J. Org. Chem. 67: 1866-1872; Walker, M.A. (1995) J. Org. Chem. 60: 5352-5355; Frisch et al (1996) Bioconjugate Chem. 7: 180-186; US 6214345; WO 02/088172; US 2003130189; US 2003096743; WO 03/026577; WO 03/043583; и WO 04/032828.
Элементы поперечной связи формулы (IIIa) могут быть встроены в линкер посредством взаимодействия следующих линкерных реагентов с N-концом аминокислотной единицы:
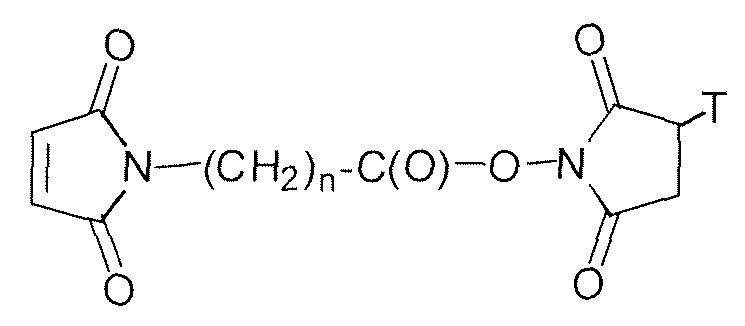
где n представляет собой целое число от 1 до 10, и T представляет собой -H или -SO3Na;

где n представляет собой целое число от 0 до 3;
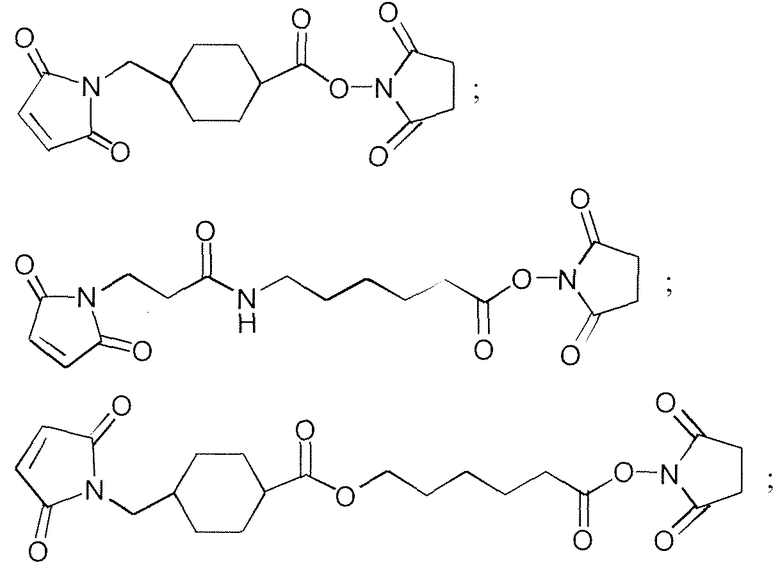
и
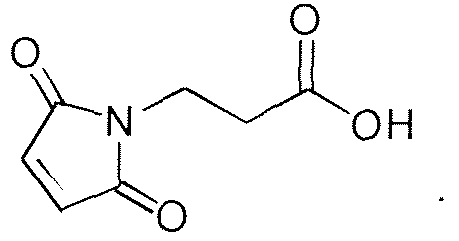
Элементы поперечной связи могут быть встроены в линкер посредством взаимодействия следующих бифункциональных реагентов с N-концом аминокислотной единицы:
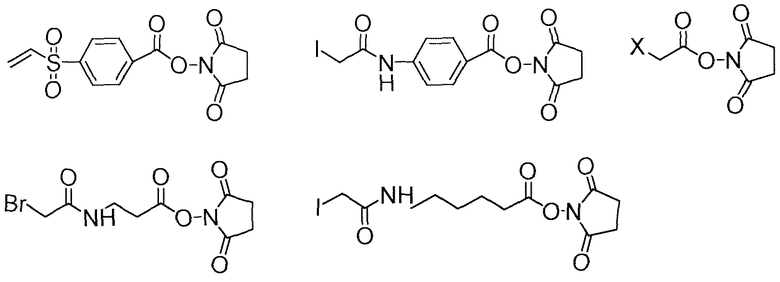
где X представляет собой Br или I.
Элементы поперечной связи формулы также могут быть встроены в линкер посредством взаимодействия следующих бифункциональных реагентов с N-концом аминокислотной единицы:
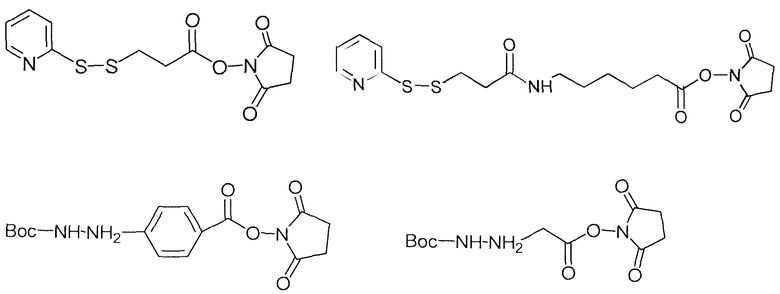
Иллюстративный валин-цитруллин (val-cit или vc) дипептидный линкерный реагент, имеющий малеимидный элемент поперечной связи и пара-аминобензилкарбамоиловый (PAB) самоотщепляющийся спейсер, имеет структуру:
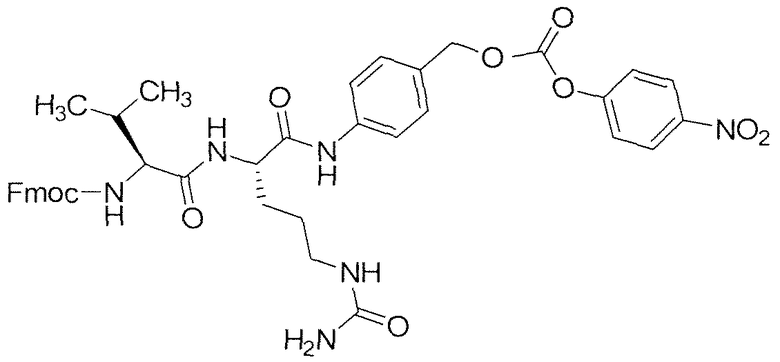
Иллюстративный phe-lys (Mtr, моно-4-метокситритил) дипептидный линкерный реагент, имеющий малеимидный элемент поперечной связи и PAB самоотщепляющуюся спейсерную единицу, может быть получен в соответствии с Dubowchik, et al. (1997) Tetrahedron Letters, 38:5257-60, и имеет структуру:
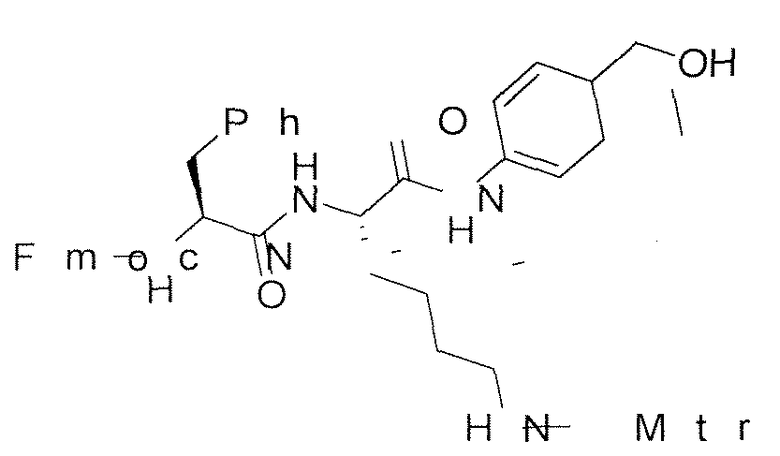
Примеры промежуточных соединений лекарственное средство-линкер:
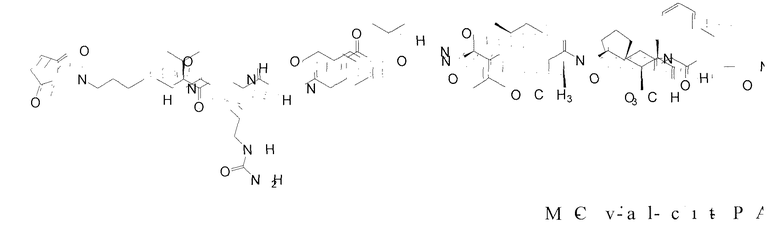
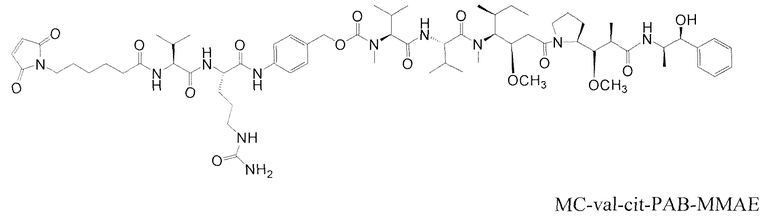
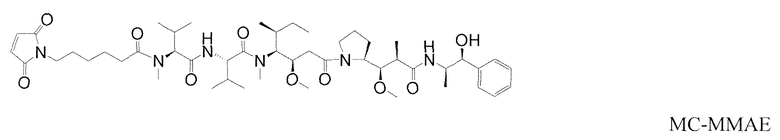
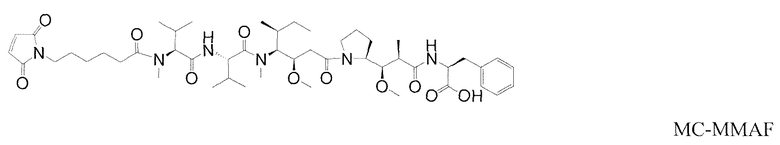
Иллюстративные соединения конъюгатов антитело-лекарственное средство по изобретению включают:
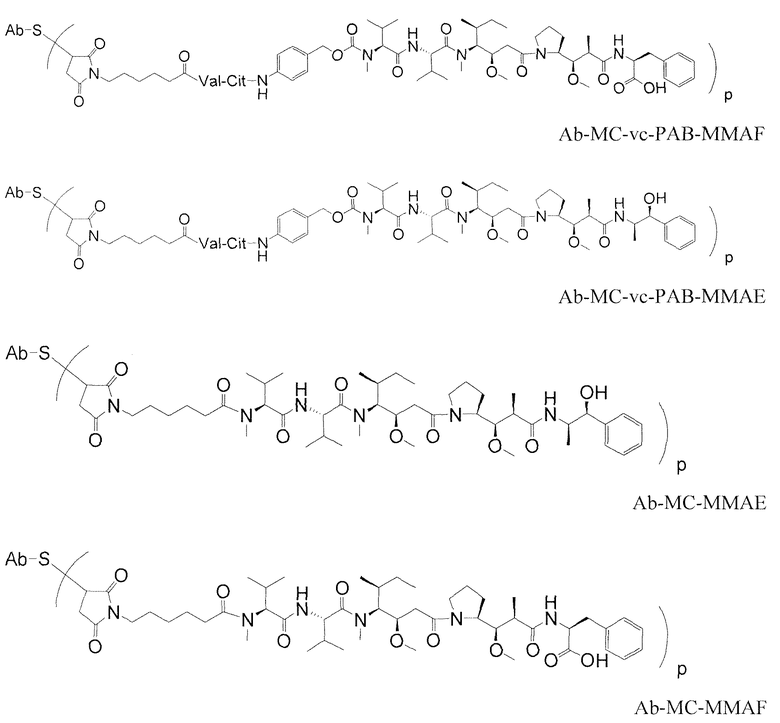
где Val представляет собой валин; Cit представляет собой цитруллин; p равно 1, 2, 3, или 4; и Ab представляет собой антитело против TENB2, сконструированное с цистеином.
Получение конъюгатов антитела против TENB2, сконструированного с цистеином, и лекарственного средства
ADC Формулы I может быть получен несколькими способами, в которых используются реакции органической химии, условия и реагенты, известные специалисту в уровне техники, включая: (1) реакцию цистеиновой группы антитела, сконструированного с цистеином, с линкерным реагентом, с образованием промежуточного соединения антитело-линкер Ab-L, посредством ковалентной связи, с последующей реакцией с активированной молекулой D лекарственного средства; и (2) реакцию нуклеофильной группы молекулы лекарственного средства с линкерным реагентом, с образованием промежуточного соединения лекарственное средство-линкер D-L, посредством ковалентной связи, с последующей реакцией с цистеиновой группой антитела, сконструированного с цистеином. Способы конъюгирования (1) и (2) могут быть использованы с разнообразными антителами, сконструированными с цистеином, молекулами лекарственных средств, и линкерами, для получения конъюгатов антитело-лекарственное средство формулы I.
Тиоловые группы цистеина антител являются нуклеофильными и способны вступать в реакцию с образованием ковалентных связей с электрофильными группами линкерных реагентов и промежуточных соединений лекарственное средство-линкер, включающих: (i) активные эфиры, такие как эфиры NHS, эфиры HOBt, галогенформиаты и галогенангидриды; (ii) алкилгалогениды и бензилгалогениды, такие как галогенацетамиды; (iii) альдегидные, кетоновые, карбоксильные и малеимидные группы; и (iv) дисульфиды, в том числе пиридилдисульфиды, посредством сульфидных замен. Нуклеофильные группы молекулы лекарственного средства включают, но не ограничиваются ими: амино, тиоловые, гидроксильные, гидразидные, оксим, гидразиновые, тиосемикарбозоновые, гидразинкарбоксилатные и арилгидразидные группы, способные вступать в реакцию с образованием ковалентных связей с электрофильными группами линкерных молекул и линкерных реагентов.
Антитела, сконструированные с цистеином, можно сделать рекционноспособными для конъюгирования с линкерными реагентами, посредством обработки восстановителем, таким как DTT (реагент Клеланда, дитиотреитол) или TCEP (трис(2-карбоксиэтил)фосфингидрохлорид; Getz et al (1999) Anal. Biochem. Vol 273: 73-80; Soltec Ventures, Beverly, MA), с последующим переокислением для восстановления межцепочечных и внутрицепочечных дисульфидных связей (Пример 2). Например, полноразмерные моноклональные антитела, сконструированные с цистеином (ТиоMab), экспрессируемые в клетках CHO, восстанавливают с приблизительно 50-кратным избытком TCEP в течение 3 часов при 37°C, для восстановления дисульфидных связей в цистеиновых аддуктах, которые могут формироваться между вновь встроенными остатками цистеина и цистеином, присутствующим в культуральной среде. Восстановленное ТиоMab разбавляют и нагружают на колонку HiTrap S в 10 мМ ацетата натрия, pH 5, и элюируют с помощью PBS, содержащего 0,3 M хлорида натрия. Дисульфидные связи были заново сформированы между остатками цистеина, присутствующими в родительском Mab, используя разбавленный (200 нМ) водный сульфат меди (CuSO4) при комнатной температуре в течение ночи. Альтернативно, дегидроаскорбиновая кислота (DHAA) является эффективным окислителем для повторного формирования внутрицепочечных дисульфидных групп антитела, сконструированного с цистеином, после восстановительного расщепления цистеиновых аддуктов. Могут быть использованы другие окислители, т.е. окисляющие агенты, и окислительные условия, известные в уровне техники. Также эффективно окисление атмосферным воздухом. На этом этапе мягкого, частичного переокисления эффективно и с высокой точностью воспроизведения образуются внутрицепочечные дисульфиды, и защищены тиоловые группы вновь встроенных остатков цистеина. Добавляли приблизительно 3-кратный избыток промежуточного соединения лекарственное средство-линкер, например MC-vc-PAB-MMAE, по отношению к антителу (приблизительно 1,5-кратный избыток относительно вновь встроенных остатков цистеина), смешивали и оставляли при комнатной температуре приблизительно на час для обеспечения конъюгирования и образования конъюгата антитело TMEFF2#19 против TENB2 - лекарственное средство. Конъюгированную смесь подвергали фильтрации в геле, и нагружали и элюировали через колонку HiTrap S для удаления избытка промежуточного соединения лекарственное средство-линкер и других примесей.
На фиг.6 представлен общий процесс получения антитела, сконструированного с цистеином, экспрессированного клеточной культурой, для конъюгирования. В случае, когда клеточная культуральная среда содержит цистеин, дисульфидные аддукты могут формироваться между вновь введенной аминокислотой цистеина и цистеином культуральной среды. Эти цистеиновые аддукты, изображенные в виде кольца в иллюстративном ТиоMab (слева) на Фиг.6, должны быть восстановлены для создания антител, сконструированных с цистеином, реакционноспособных для конъюгирования. Цистеиновые аддукты, предположительно наряду с различными межцепочечными дисульфидными связями, восстановительно расщепляют для образования восстановленной формы антитела с помощью восстановителей, таких как TCEP. Межцепочечные дисульфидные связи между парными остатками цистеина восстанавливают в условиях частичного окисления сульфатом меди, DHAA, или воздействуя кислородом окружающей среды. Вновь встроенные, сконструированные и непарные остатки цистеина, остаются доступными для реакции с линкерными реагентами или промежуточными соединениями лекарственное средство-линкер с образованием конъюгатов антител по изобретению. Антитела ТиоMab, экспрессированные в клеточных линиях млекопитающих, приводят к образованию внешне конъюгированного аддукта Cys с сконструированным Cys через формирование связи -S-S-. Таким образом, очищенные ТиоMab обрабатывают с помощью восстановительных и переокислительных процедур, описанных в Примере 2, для получения реакционноспосбоных ТиоMab. Эти ТиоMab используют для конъюгирования с цитотоксическими лекарственными средствами, содержащими малеимид, флуорофорами и другими метками.
Анализ реакций конъюгата антитела, сконструированного с цистеином, и лекарственного средства, показывает уменьшенную гетерогенность по сравнению с конъюгатами антитела и лекарственного средства, полученными в результате обеднения внутрицепочечных или межцепочечных дисульфидных связей с последующим конъюгированием (стандартный ADC) с тиол-реактивным промежуточным соединением лекарственное средство-линкер.
Методы скрининга
Еще один вариант осуществления настоящего изобретения относится к способу определения присутствия полипептида TENB2 в образце, в котором предполагается наличие полипептида TENB2, где способ включает воздействие на образец антителом против TENB2, сконструированным с цистеином, или его конъюгатом антитело-лекарственное средство, который связывает полипептид TENB2, и определение связывания антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, с полипептидом TENB2 в образце, где наличие такого связывания указывает на присутствие полипептида TENB2 в образце. Необязательно, образец может содержать клетки (которые могут быть раковыми клетками), в которых подозревают экспрессию полипептида TENB2. Антитело против TENB2, или его конъюгат антитело-лекарственное средство, используемое в данном методе, может необязательно быть помечено меткой детекции, прикреплено к твердому носителю, или тому подобное.
Другой вариант осуществления настоящего изобретения относится к способу диагностики наличия опухоли у млекопитающего, где способ включает (a) взаимодействие пробного образца, содержащего клетки ткани, полученные от млекопитающего, с антителом против TENB2, сконструированного с цистеином, или его конъюгатом антитело-лекарственное средство, которое связывает полипептид TENB2, и (b) определение формирования комплекса между антителом против TENB2, сконструированного с цистеином, или его конъюгатом конъюгатом антитело-лекарственное средство, и полипептидом TENB2 в пробном образце, где формирование комплекса является признаком наличия опухоли у млекопитающего. Необязательно, антитело против TENB2, сконструированное с цистеином, или его конъюгат антитело-лекарственное средство, может быть помечено меткой детекции, прикреплено к твердому носителю, или тому подобное, и/или пробный образец клеток ткани получен от индивидуума, у которого подозревают наличие раковой опухоли.
Анализ клеточной пролиферации in vitro
В одном варианте осуществления настоящее изобретение относится к способу ингибирования роста клетки, которая экспрессирует полипептид TENB2, где способ включает взаимодействие клетки с антителом против TENB2, сконструированного с цистеином, или его конъюгатом антитело-лекарственное средство, с полипептидом TENB2, вызывая ингибирование роста клетки, экспрессирующей TENB2. Клетка может быть раковой клеткой и связывать антитело, сконструированное с цистеином, или его конъюгат антитело-лекарственное средство, с полипептидом TENB2, вызывая гибель клетки, экспрессирующей полипептид TENB2.
Как правило, цитотоксическая или цитостатическая активность конъюгата антитело-лекарственное средство (ADC) оценивают посредством: воздействия на клетки млекопитающих, экспрессирующие полипептид TENB2, ADC в клеточной культуральной среде; культивирования клеток в течение промежутка времени от приблизительно 6 часов до приблизительно 5 дней; и оценки клеточной жизнеспособности. Клетки млекопитающих, пригодные для анализа пролиферации, включают: (1) опухолевый ксенотрансплантат LuCaP77, экспрессирующий полипептид TENB2; (2) клеточную линию, происходящую из PC3, сконструированную для стабильной экспрессии части полипептида TENB2 на своей клеточной поверхности (PC3/TENB2); и (3) клеточную линию PC3, которая не экспрессирует полипептид TENB2 (PC3/neo). Основанные на клетках анализы in vitro используют для оценки жизнеспособности (пролиферация), цитотоксичности и индукции апоптоза (активация каспаз) ADC по изобретению.
Фармакокинетика - сывороточный клиренс и стабильность
Распределение конъюгатов антитело против TENB2-лекарственное средство in vivo было проанализировано посредством измерения концентраций конъюгата антитела и лекарственного средства в сыворотке крови после однократного внутривенного болюсного введения крысам линии Sprague-Dawley. Концентрации конъюгатов антитело-лекарственное средство, несущих, по меньшей мере, одно цитотоксическое лекарственное средство, измеряли с помощью ELISA, в которой использовали анти-ММАЕ для захвата, и внеклеточный домен биотинилированного TENB2 (ECD) и конъюгат стрептавидина с пероксидазой хрена (HRP) для детекции. Общие концентрации TMEFF2#19 и ThioTMEFF2#19 в сыворотке крови измеряли с помощью ELISA, в которой использовали TENB2 ECD для захвата и HRP против Fc-фрагмента человека в качестве вторичного антитела. Этот анализ определяет любое антитело против TENB2, как с, так и без конъюгированного MMAE. Эти анализы имеют нижние пределы количественного определения 16,4 нг/мл с минимальным разведением 1:100. Зависимость сывороточная концентрация-время для каждого животного анализировали с использованием двухкамерной модели с в/в вводом болюса, элиминации первого порядка, макро-констант скорости (Model 8, WinNonlin Fro v.5.0.1, Pharsight Corporation, Mountain View, CA). Предельное соответствие было основано на предварительной оценке, среднеквадратической погрешности для расчета и проценте коэффициента вариаций для первичных и вторичных параметров, а также на проверке графиков остатков между наблюдаемыми и расчетными данными зависимости концентрация-время. Индивидуальные первичные параметры фармакокинетики ФК включают отрезки начального момента времени (А и В), ассоциированные с фазами альфа и бета, соответственно, и микро-константы скорости (альфа и бета). Использовали следующие параметры моделирования: первоначальные расчеты осуществляли с помощью WinNonlin; концентрации оценивали по обратной величине квадрата расчетной концентрации (1/ŷ2); использовали алгоритм нахождения наименьшего значения Нелдера-Мида. Были описаны следующие параметры ФК: AUC0INF, CL, Cmax, MRT, t1/2,а, t1/2,b, V1 и Vss.
Результаты 28-дневных фармакокинетических испытаний у крыс представлены на фиг.15. Крысам вводили 5 мг/кг массы тела тиоTMEFF2#19-VC-MMAE или 5 мг/кг TMEFF2#19-VC-MMAE. Сыворотку крови мышей собирали через 5 минут, 1 час, 6 часов, 24 часа и 2, 3, 4, 8, 11, 15, 21 и 28 дней после введения доз. Линейную кинетику дозы наблюдали для ch TMEFF2#19-VC-MMAE между дозами 0,5 и 5 мг/кг, поэтому данные для дозы 5 мг/кг были арифметически преобразованы для отражения расчетных данных при 5 мг/кг для сравнения с тиоTMEFF2# 19-VC-MMAE.
Токсичность у грызунов
Токсичность конъюгатов антитела против TENB2, сконструированного с цистеином, и лекарственного средства определяли на моделях острой токсичности у крыс и человекообразных обезьян. Токсичность ADC исследовали посредством введения ADC самкам крыс линии Sprague-Dawley и человекообразных обезьян, и последующего изучения и анализа действия на разные органы. На основании общих наблюдений (масса тела), параметров клинической патологии (биохимические и гематологические показатели сыворотки крови) и гистопатологии, токсичность ADC может быть зарегистрирована, охарактеризована и оценена. Было обнаружено, что при эквивалентных уровнях доз мишень-зависимые эффекты не проявлялись. Мишень-независимую токсичность наблюдали при дозе, превышающей эффективные дозы в моделях опухоли животных.
МЕТОДЫ ЛЕЧЕНИЯ
Другой вариант осуществления настоящего изобретения относится к способу терапевтического лечения млекопитающего, имеющего злокачественную опухоль, содержащую клетки, которые экспрессируют полипептид TENB2, где способ включает введение млекопитающему терапевтически эффективного количества антитела, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, которое связывается с полипептидом TENB2, таким образом приводя к эффективному терапевтическому лечению опухоли.
Другой вариант осуществления настоящего изобретения относится к способу лечения или предотвращения клеточно-пролиферативного нарушения, связанного с измененной, предпочтительно повышенной, экспрессией или активностью полипептида TENB2, где способ включает введение нуждающемуся в таком лечении субъекту эффективного количества антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство. Примером клеточно-пролиферативного нарушения является рак. Эффективное лечение или предотвращение клеточно-пролиферативного нарушения может быть результатом направленного уничтожения или ингибирования роста клеток, которые экспрессируют полипептид TENB2, или противодействия потенциальной активности полипептида TENB2 в отношении клеточного роста с помощью антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство.
Еще один вариант осуществления настоящего изобретения относится к способу связывания антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, с клеткой, которая экспрессирует полипептид TENB2, где способ включает взаимодействие указанного антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, в условиях, которые являются подходящими для связывания антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, с указанным полипептидом TENB2, и обеспечивающими возможность связывания между ними. В предпочтительных вариантах осуществления антитело против TENB2, сконструированное с цистеином, или его конъюгат антитело-лекарственное средство, является меченным с помощью молекулы или соединения, которое является пригодным для количественного и/или качественного определения местоположения и/или степени связывания антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, с клеткой.
Другие варианты осуществления настоящего изобретения относятся к использованию антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, при получении лекарственного средства, пригодного для (i) терапевтического лечения или диагностического выявления злокачественного новообразования или опухоли, или (ii) терапевтического лечения или профилактики клеточно-пролиферативного нарушения.
Другой вариант осуществления настоящего изобретения относится к способу ингибирования роста раковой клетки, где рост указанной раковой клетки, по меньшей мере, частично зависит от потенциирующего рост эффекта(ов) полипептида TENB2, где способ включает контактирование полипептида TENB2 с антителом против TENB2, сконструированного с цистеином, или его конъюгатом антитело-лекарственное средство, тем самым противодействуя потенциирующему рост действию полипептида TENB2, что в свою очередь задерживает рост раковой клетки, тем самым подавляется рост раковой клетки.
Другой вариант осуществления настоящего изобретения относится к способу терапевтического лечения опухоли у млекопитающего, где рост указанной опухоли, по меньшей мере, частично зависит от потенциирующего рост эффекта(ов) полипептида TENB2, где способ включает введение млекопитающему терапевтически эффективного количества антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, которое связывает полипептид TENB2, тем самым противодействуя потенциирующему рост действию указанного полипептида TENB2, что приводит к эффективному терапевтическому лечению опухоли.
Антитела, фрагменты антител и их конъюгаты, распознают внеклеточные эпитопы белков клеточной мембраны TENB2, которые высвобождаются в межклеточную жидкость. Изобретение дополнительно обеспечивает способ определения, мониторинга и лечения злокачественных новообразований, таких как рак молочной железы и рак яичников, используя антитела, фрагменты антител и конъюгаты.
Конъюгаты антитело-лекарственное средство (ADC) по настоящему изобретению можно использовать для лечения различных заболеваний или нарушений, например, характеризующихся сверхэкспрессией опухолевого антигена TENB2. Примеры состояний или гиперпролиферативных нарушений включают доброкачественные или злокачественные опухоли, включая рак предстательной железы.
Соединения ADC, идентифицированные в экспериментальных моделях на животных и анализах, на основе клеток, могут быть дополнительно протестированы в клинических испытаниях на высших приматах и людях, имеющих опухоль. Клиническое испытание может иметь целью оценку эффективности ADC в комбинации с известными лечебными схемами, такими как радиационная и/или химиотерапия, с использованием известных химиотерапевтических и/или цитотоксических средств.
Как правило, заболевание или нарушение, подвергающееся лечению, является гиперпролиферативным нарушением, таким как рак. Примеры рака, подвергающегося лечению, в настоящем документе включают, но не ограничены ими, карциному, лимфому, бластому, саркому и лейкемию или лимфолейкоз. Более конкретные примеры таких злокачественных новообразований включают плоскоклеточный рак (например, плоскоклеточный рак эпителия), рак легких, включая мелкоклеточный рак легких, немелкоклеточный рак легких, аденокарциному легких и плоскоклеточную карциному легких, рак брюшины, гепатоцеллюлярный рак, рак ЖКТ или рак желудка, включая рак желудочно-кишечной локализации, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, карциному эндометрия или матки, карциному слюнных желез, рак почки или почечный рак, рак предстательной железы, рак вульвы, рак щитовидной железы, печеночную карциному, карциному анального канала, карциному полового члена, а также рак головы и шеи.
Для профилактики или лечения заболевания, подходящая дозировка ADC будет зависеть от типа подвергающегося лечению заболевания, как определено выше, тяжести и течения заболевания, того, вводится ли молекула в целях профилактики или лечения, предыдущей терапии, истории болезни пациента и реакции на антитело, и индивидуального суждения лечащего врача. Молекула соответственно вводится пациенту однократно или в рамках серийной обработки. В зависимости от типа и тяжести заболевания, от приблизительно 1 мкг/кг до 15 мг/кг (например, 0,1-20 мг/кг) молекулы является начальной возможной дозой для введения пациенту, например, либо посредством одного или нескольких отдельных введений, либо посредством продолжительной инфузии. Типичная дневная доза может находиться в диапазоне от приблизительно 1 мкг/кг до 100 мг/кг или более, в зависимости от факторов, упомянутых выше. Типичная доза ADC для введения пациенту находится в диапазоне от приблизительно 0,1 до приблизительно 10 мг/кг массы тела пациента.
Для повторных введений в течение нескольких дней или дольше, в зависимости от состояния, лечение поддерживается до тех пор, пока не наступит желаемое подавление симптомов заболевания. Иллюстративный режим дозировки включает введение антитела против TENB2 в начальной ударной дозе приблизительно 4 мг/кг, с последующим введением поддерживающей еженедельной дозы приблизительно 2 мг/кг. Могут быть пригодны другие режимы дозировки. Прогресс лечения можно легко контролировать, используя обычные технологические приемы и анализы, в том числе ультразвуковую визуализацию.
Введение конъюгатов антитело-лекарственное средство
Конъюгаты антитело-лекарственное средство (ADC) по изобретению могут быть введены любым путем, подходящим для подвергающегося лечению состояния. Обычно ADC будет вводиться парентерально, т.е., посредством инфузии, подкожно, внутрибрюшинно, внутримышечно, внутривенно, внутрикожно, интратекально и эпидурально.
Фармацевтические композиции
Фармацевтические композиции терапевтических конъюгатов антитело-лекарственное средство (ADC) по изобретению, обычно готовят для парентерального введения, т.е. болюсных, внутривенных, внутриопухолевых инъекций, с фармацевтически приемлемым парентеральным носителем, и в виде однократной, стерильной инъецируемой дозы. Конъюгат антитело-лекарственное средство (ADC), имеющий требуемую степень чистоты, необязательно смешивают с фармацевтически приемлемыми разбавителями, носителями, наполнителями или стабилизаторами (Remington's Pharmaceutical Sciences (1980) 16th edition, Osol, A. Ed.) в виде лиофилизированной композиции, либо в виде водного раствора.
Приемлемые разбавители, носители, наполнители и стабилизаторы являются нетоксичными для реципиентов в используемых дозах и концентрациях, и включают буферы, такие как фосфат, цитрат и другие органические кислоты; антиоксиданты, включая аскорбиновую кислоту и метионин; консерванты (такие как октадецилдиметилбензиламмония хлорид; гексаметония хлорид; бензалкония хлорид; бензетония хлорид; фенол, бутиловый или бензиловый спирт; алкилпарабены, такие как метил- или пропилпарабен; катехол; резорцин; циклогексанол; 3-пентанол и м-крезол); низкомолекулярные (менее чем примерно 10 остатков) полипептиды; белки, такие как сывороточный альбумин, желатин или иммуноглобулины; гидрофильные полимеры, такие как поливинилпирролидон; аминокислоты, такие как глицин, глутамин, аспарагин, гистидин, аргинин или лизин; моносахариды, дисахариды и другие углеводы, включая глюкозу, маннозу или декстрины, хелатообразующие агенты, такие как ЭДТА; сахара, такие как сахароза, маннит, трегалоза или сорбит; солеобразующие противоионы, такие как натрий; комплексы с металлами (например, комплексы Zn-белок); и/или неионогенные поверхностно-активные вещества, такие как TWEENTM, PLURONICSTM или полиэтиленгликоль (ПЭГ).
Активные фармацевтические ингредиенты могут быть также включены в приготовленные микрокапсулы, например, с помощью методов коацервации или межфазной полимеризацией, например, в микрокапсулы из гидроксиметилцеллюлозы или желатина или микрокапсулы из поли(метилметацилата), соответственно, в коллоидные системы для доставки лекарственных средств (например, липосомы, альбуминовые микросферы, микроэмульсии, наночастицы и нанокапсулы) или в макроэмульсии. Такие технологии раскрыты в Remington's Pharmaceutical Sciences 16th edition, Osol, A. Ed. (1980).
Можно приготовить препараты с непрерывным высвобождением. Подходящие примеры препаратов с непрерывным высвобождением включают полупроницаемые матрицы из твердых гидрофобных полимеров, содержащие ADC, матрицы находятся в виде имеющих определенную форму препаратов, например, пленок или микрокапсул. Примеры матриц с непрерывным высвобождением включают полиэфиры, гидрогели (например, поли(2-гидроксиэтилметакрилат) или поли(виниловый спирт)), полилактиды (US №3773919), сополимеры L-глутаминовой кислоты и гамма-этил-L-глутамата, недеградируемый этиленвинилацетат, деградируемые сополимеры молочной кислоты-гликолевой кислоты, такие как LUPRON DEPOTTM (инъекцируемые микросферы, состоящие из сополимера молочной кислоты-гликолевой кислоты и леупролидацетата), и поли-D-(-)-3-гидроксимасляную кислоту.
Композиции включают те, которые пригодны для вышеуказанных путей введения. Композиции могут быть удобно представлены в форме одноразовой дозы и могут быть приготовлены посредством любого способа, известного в области фармацевтики. Технологические приемы и прописи составов, как правило, находят в Remington's Pharmaceutical Sciences (Mack Publishing Co., Easton, PA). Такие способы включают этап обеспечения связи действующего ингредиента с носителем, который состоит из одного или нескольких вспомогательных ингредиентов. Как правило, композиции получают посредством обеспечения равномерной и тесной связи действующего ингредиента и жидких носителей, или тонкоизмельченных твердых носителей, или и того, и другого, а затем, при необходимости, формируя продукт.
Водные суспензии по изобретению содержат действующие вещества в смеси с наполнителями, подходящими для производства водных суспензий. Такие наполнители включают суспендирующее вещество, такое как натрийкарбоксиметилцеллюлоза, кроскармеллоза, повидон, метилцеллюлоза, гидроксипропилметилцеллюлоза, алгинат натрия, поливинилпирролидон, трагакантовая камедь и аравийская камедь, и диспергирующие или увлажняющие вещества, такие как природный фосфатид (например, лецитин), продукт конденсации алкиленоксида и жирной кислоты (например, полиоксиэтиленстеарат), продукт конденсации этиленоксида и длинноцепочечного алифатического спирта (например, гептадекаэтиленоксицетанол), продукт конденсации этиленоксида с неполными сложными эфирами, происходящими от жирных кислот и гексита, (например полиэтиленсорбитанмоноолеат). Водные суспензии могут также содержать один или несколько консервантов, например, этил- или н-пропил-п-гидроксибензоат, один или несколько окрашивающих агентов, один или несколько ароматизирующих агентов и один или несколько подслащивающих агентов, например сахарозу или сахарин.
Фармацевтические композиции ADC могут быть в форме стерильного инъецируемого препарата, такого как стерильная инъецируемая водная или маслянистая суспензия. Суспензия может быть создана в соответствии с известными в уровне техники процессами, используя те подходящие диспергирующие или увлажняющие вещества, которые были упомянуты выше. Стерильный препарат для инъекций может также представлять собой стерильный раствор или суспензию в нетоксичном разбавителе или растворителе, пригодном для парентерального введения, такой как раствор в 1,3-бутандиоле, или получен в виде лиофилизированного порошка. К приемлемым носителям и растворителям, которые можно использовать, относятся вода, раствор Рингера и изотонический физиологический раствор. В дополнение, в качестве растворителя или суспендирующей среды удобно использовать стерильные нелетучие масла. Для этой цели можно использовать любое мягкое нелетучее масло, в том числе синтетические моно- и диглицериды. Дополнительно, для получения инъекционных препаратов могут быть использованы также жирные кислоты, такие как олеиновая кислота.
Количество активного ингредиента, смешиваемого с носителями для изготовления одноразовых лекарственных форм, зависит от состояния пациента и конкретного способа введения лекарственного средства. Например, водный раствор, предназначенный для внутривенной инфузии, может содержать от приблизительно 3 до 500 мкг действующего вещеста в милилитре раствора, для того чтобы можно было осуществить инфузию подходящего объема при скорости приблизительно 30 мл/час.
Композиции, пригодные для парентерального введения, включают водные и неводные стерильные растворы для инъекций, которые могут содержать антиоксиданты, буферы, бактериостаты и растворенные вещества, которые делают композицию изотонической с кровью предполагаемого реципиента; и водные и неводные стерильные суспензии, которые могут включать суспендирующие вещества и загустители.
Несмотря на то, что пероральное применение белковых лекарственных средств является нежелательным по причине гидролиза или денатурации в желудочно-кишечном тракте, композиции ADC, пригодные для перорального введения, могут быть приготовлены в виде дискретных единиц, таких как капсулы, облатки или таблетки, каждая из которых содержит предусмотренное количество ADC.
Композиции могут быть упакованы в однодозовые или многодозовые контейнеры, например, запаянные ампулы и флаконы, и могут храниться в высушенном замораживанием (лиофилизированном) состоянии, требуя только добавления стерильного жидкого носителя, например, воды для инъекций, непосредственно перед применением. Приготовленные для немедленного введения растворы или суспензии для инъекций получены из стерильных порошков, гранул и таблеток ранее описанных типов. Предпочтительными составами единичной дозы являются те, которые содержат суточную дозу или единую суточную субдозу, как ранее изложено в настоящем документе, или их соответствующую долю активного ингредиента.
Композиции по изобретению также могут быть составлены в виде иммунолипосом. «Липосома» представляет собой малый носитель, содержащий различные типы липидов, фосфолипидов и/или поверхностно-активного вещества, который является пригодным для доставки лекарственного вещества в организм млекопитающего. Компоненты липосомы обычно упорядочены в виде двухслойного образования, схожего с расположением липидов в биологических мембранах. Липосомы, содержащие антитела, получены в соответствии с методами, известными в уровне техники, такими, как описанные у Epstein et al (1985) Proc. Natl. Acad. Sci. USA 82: 3688; Hwang et al (1980) Proc. Natl Acad. Sci. USA 77: 4030; US 4485045; US 4544545; US 5013556; WO 97/38731. Липосомы могут быть созданы методом обращенно-фазового выпаривания, используя липидную композицию, содержащую фосфатидилхолин, холестерин и ПЭГ-производное фосфатидилхолина (PEG-PE). Липосомы могут быть экструдированы через фильтры с определенным размером пор для сбора липосом с требуемым диаметром. Фрагменты Fab' композиций по настоящему изобретению могут быть конъюгированы с липосомами (Martin et al (1982) J. Biol. Chem. 257: 286-288), посредством дисульфидной реакции обмена. Химиотерапевтическое средство необязательно содержится в липосоме (Gabizon et al (1989) J. National Cancer Inst. 81(19): 1484).
Комбинированная терапия
Конъюгат антитело-лекарственное средство (ADC) по изобретению может комбинироваться в фармацевтической комбинированной композиции или схеме приема лекарственного средства в виде комбинированной терапии, со вторым соединением, имеющим противораковые свойства. Второе соединение в фармацевтической комбинированной композиции или схеме приема лекарственного средства предпочтительно имеет взаимодополняющие действия с ADC в комбинации, с тем, чтобы они не оказывали неблагоприятного действия друг на друга.
Второе соединение может быть химиотерапевтическим средством, цитотоксическим средством, цитокином, ингибитором роста, противогормональным средством и/или кардиозащитным средством. Такие молекулы соответственно присутствуют в комбинации в количествах, эффективных для достижения поставленной цели. Фармацевтическая композиция, содержащая ADC по изобретению, также может иметь терапевтически эффективное количество химиотерапевтического средства, такого как ингибитор формирования тубулина, ингибитор топоизомеразы, интеркалятор ДНК или связывающее ДНК вещество.
Другие схемы лечения могут комбинироваться при введении противоракового средства, установленного в соответствии с изобретением. Комбинированную терапию можно применять в одновременном или последовательном режиме. При последовательном введении комбинацию можно вводить посредством одного или нескольких введений. Комбинированное введение включает совместное введение, с использованием отдельных составов или единичной фармацевтической композиции, и последовательное введение в любом порядке, где предпочтительно существует промежуток времени, в течение которого оба (или все) действующие ингредиенты одновременно проявляют свои биологические действия.
В одном варианте осуществления лечение с использованием ADC предусматривает комбинированное введение антитела против TENB2, сконструированное с цистеином, или его конъюгата антитело-лекарственное средство, и одного или нескольких химиотерапевтических средств, терапевтических биологических или ингибирующих рост веществ, включая совместное введение коктейлей из различных химиотерапевтических средств. Химиотерапевтические средства включают, но не ограничены ими: таксаны (такие как паклитаксел и доцетаксел); соединения, содержащие платину, такие как карбоплатин; ингибиторы EGFR, такие как эрлотиниб и гефитиниб; ингибиторы тирозинкиназы, такие как иматиниб; и антибиотики антрациклинового ряда (такие как доксорубицин или доксил). Терапевтические биологические вещества для применения в комбинации с антителом против TENB2, сконструированным с цистеином, или его конъюгатом антитело-лекарственное средство, включают бевацизумаб (Avastin®) или пертузумаб (Omnitarg™, Genentech Inc). Получение и режим дозировки таких химиотерапевтических средств можно осуществлять в соответствии с рекомендациями производителя или на основе опыта квалифицированного практикующего врача. Получение и режим дозировки для такой химиотерапии описаны в «Chemotherapy Service», (1992) Ed., M.C. Perry, Williams & Wilkins, Baltimore, Md.
ADC может быть комбинирован с антигормональным соединением; например, антиэстрогенным соединением, таким как тамоксифен; антипрогестеронами, такими как онапристон (EP 616812); или антиандрогеном, таким как флутамид, в дозах, известных для таких молекул. В случае, когда лечение проводится в отношении гормоннезависимого рака, пациент изначально мог быть подвергнут антигормональной терапии, а после того, как рак станет гормоннезависимым, пациенту может вводиться ADC (и необязательно другие вещества, описанные в настоящем документе). Также может быть благоприятно совместное введение пациенту кардиозащитного средства (для предотвращения или уменьшения миокардиальной дисфункции, связанной с данным видом терапии) или одного или нескольких цитокинов. В дополнение к вышеуказанным лечебным схемам, пациент может быть подвергнут удалению раковых клеток хирургическим путем и/или лучевой терапии.
Подходящими дозами для любого из вышеупомянутых веществ для совместного введения являются используемые в настоящее время, и они могут быть снижены вследствие комбинированного действия (синергизм) недавно идентифицированного вещества и других химиотерапевтических средств или видов лечения.
Комбинированная терапия может обеспечивать «синергизм» и доказывать «синергитическое действие», т.е. достигнутый эффект, когда действие ингредиентов, использующихся вместе, превышает сумму эффектов, являющихся результатом применения каждого соединения по отдельности. Синергитический эффект может быть достигнут, когда действующие ингредиенты: (1) входят в один состав и вводятся или доставляются одновременно в составе комбинированной однодозовой композиции; (2) доставляются поочередно или параллельно в виде отдельных композиций; или (3) посредством некого другого режима. В случае, когда доставка осуществляется в рамках поочередной терапии, синергитический эффект может быть достигнут, когда соединения вводятся или доставляются последовательно, например, посредством раздельных инъекций в разных шприцах. В большинстве случаев, во время поочередной терапии, эффективная доза каждого действующего ингредиента вводится последовательно, т.е. сериями, в то время как в рамках комбинированной терапии эффективные дозы двух или более действующих ингредиентов вводятся вместе.
Метаболиты конъюгатов антитело-лекарственное средство
Также в объем изобретения попадают in vivo метаболические продукты описанных в настоящем документе соединений ADC, в той степени, что такие продукты являются новыми и неочевидными в рамках предшествующего уровня техники. Такие продукты могут быть результатом, например, окисления, восстановления, гидролиза, амидирования, этерификации, ферментативного расщепления, и тому подобного, вводимого соединения. Соответственно, изобретение включает новые и неочевидные соединения, получаемые в результате процесса, включающего контактирование соединения по изобретению с млекопитающим, в течение промежутка времени, достаточного для образования его метаболического продукта.
Метаболические продукты обычно выявляют посредством получения ADC, меченного радиоактивным изотопом (например, 14С или 3Н), введения его парентерально в определяемой дозе (например, больше чем приблизительно 0,5 мг/кг) животному, такому как крыса, мышь, морская свинка, обезьяна, или человеку, обеспечивая достаточное время для того, чтобы начался обмен веществ (обычно от приблизительно 30 секунд до 30 часов), и выделения его конверсионных продуктов из мочи, крови или других биологических образцов. Такие продукты легко выделить, поскольку они меченые (другие выделяют посредством использования антител, способных связывать эпитопы, сохранившиеся в метаболите). Состав метаболитов определяют удобным способом, например посредством МС, ЖХ/МС или ЯМР анализа. В большинстве случаев, анализ метаболитов осуществляют тем же способом, как и при общепринятых исследованиях метаболизма лекарственных веществ, хорошо известных специалисту в данной области. Продукты переработки, пока они не обнаружены другим путем in vivo, являются пригодными для диагностического анализа терапевтических доз соединений ADC по изобретению.
ИЗДЕЛИЯ
В другом варианте осуществления изобретения обеспечивается изделие, или «набор», содержащий вещества, пригодные для лечения нарушений, описанных выше. Изделие включает контейнер и этикетку или листовку-вкладыш на, или входящую в состав контейнера. Листовка-вкладыш может относиться к инструкции, стандартно включаемой в коммерческие упаковки терапевтических средств, и содержит информацию о показаниях, дозах, способе введения, противопоказаниях и/или предупреждениях, касающихся применения таких терапевтических средств. Подходящие контейнеры включают, например, бутыли, флаконы, шприцы, блистерную упаковку и т.д. Контейнеры могут быть изготовлены из различных материалов, таких как стекло или пластик.
В одном варианте осуществления изделие содержит контейнер и композицию антитела против TENB2, сконструированного с цистеином, или его конъюгата антитело-лекарственное средство, находящуюся внутри контейнера. Изделие может дополнительно содержать этикетку, прикрепленную к контейнеру, или листовку-вкладыш, входящую в состав контейнера, в которой указано, что композиция предназначена для терапевтического лечения или диагностического обнаружения опухоли. Контейнер, в котором содержится композиция, оптимален для хранения и доставки лекарства и может иметь стерильное входное отверстие (например, контейнер может быть мешком для раствора для внутривенного введения, или флаконом, имеющим пробку, прокалываемую иглой для подкожных инъекций). На этикетке или упаковочном вкладыше указывается, что композиция используется для лечения выбранного состояния, например, рака. Альтернативно или дополнительно, изделие может дополнительно содержать второй (или третий) контейнер, содержащий фармацевтически приемлемый буфер, такой как бактериостатическая вода для инъекций (BWFI), забуференный фосфатом физиологический раствор, раствор Рингера и раствор декстрозы. Оно может дополнительно включать другие вещества, выгодные с промышленной точки зрения и с точки зрения использования, включая другие буферы, разбавители, фильтры, иглы и шприцы.
Следующие примеры предложены только для иллюстративных целей, и не предназначены для ограничения объема настоящего изобретения никаким образом.
Все цитируемые в настоящем описании изобретения патенты и справочная литература включены в настоящий документ путем ссылки во всей своей полноте.
ПРИМЕРЫ
Коммерчески доступные реагенты, упомянутые в примерах, использовали в соответствии с рекомендациями фирмы-производителя, если не указано иначе. Источником клеток, обозначенных в следующих примерах и по всему описанию посредством входящих номеров АТСС, является Американская Коллекция Типовых Культур, Manassas, VA.
Пример 1 Получение антител против TMEFF2#19
Гуманизированные антитела TMEFF2#19 были получены в соответствии с PCT/US03/07209. На фиг.1 представлена аминокислотная последовательность тяжелой цепи (SEQ ID NO:1) и аминокислотная последовательность легкой цепи (SEQ ID NO:2).
Пример 2 Получение антител против TENB2, сконструированных с цистеином, для конъюгирования посредством восстановления и переокисления
Полноразмерные моноклональные антитела против TENB2, сконструированные с цистеином (ТиоMab), экспрессированные в клетках СНО, производят аддукты цистеина (цистины) в сконструированных цистеинах в условиях клеточной культуры. Для высвобождения реактивных тиоловых групп сконструированных с цистеином, ТиоMab растворяли в 500 мМ борате натрия и 500 мМ хлориде натрия при значении рН около 8,0 и восстанавливали с помощью приблизительно 50-100 кратного избытка 1 мМ ТСЕР (трис(2-карбоксиэтил)фосфингидрохлорид; Getz et al (1999) Anal. Biochem. Vol 273: 73-80; Soltec Ventures, Beverly, MA) в течение приблизительно 1-2 часов при 37°C. Восстановленное ТиоMab (фиг.6) разбавляли и нагружали на колонку HiTrap S в 10 мМ ацетате натрия, pH 5, и элюировали PBS, содержащего 0,3 M хлорид натрия. Элюированное восстановленное ТиоMab обрабатывали 2 мМ дегидроаскорбиновой кислотой (dhAA) при значении рН 7 в течение 3 часов, или 2 мМ водным сульфатом меди (CuSO4) при комнатной температуре в течение ночи. Также может быть эффективно окисление атмосферным воздухом. Буфер обменивали посредством элюции через смолу Sephadex G25 и проводили элюцию PBS с 1 мМ DTPA. Значение отношения тиол/Ab проверяли посредством определения концентрации восстановленного антитела по абсорбции раствора при 280 нм, и концентрации тиола посредством реакции с DTNB (Aldrich, Milwaukee, WI) и определения абсорбции при 412 нм.
Пример 3 Конъюгирование антител против TENB2, сконструированных с цистеином, и промежуточных соединений лекарственное средство-линкер
После процедур восстановления и переокисления по примеру 2, антитело против TENB2, сконструированное с цистеином, растворяли в буфере PBS (забуференный фосфатом физиологический раствор) и охлаждали на льду. Приблизительно 1,5 молярных эквивалента, относительно сконструированного цистеина, на антитело, промежуточного соединения лекарственное средство ауристатин-линкер, такого как MC-MMAE (малеимидокапроил-монометилауристатин Е), MC-MMAF, MC-val-cit-PAB-MMAE или MC-val-cit-PAB-MMAF, с тиол-реактивной функциональной группой, такой как малеимидо, растворяли в ДМСО, разводили в ацетонитриле или воде, и добавляли к охлажденному восстановленному, переокисленному антителу в PBS. Приблизительно через один час добавляли избыток малеимида для ингибирования реакции и кэпирования любых не вступивших в реакцию тиоловых групп антитела. Реакционную смесь концентрировали посредством ультрафильтрации в процессе центрифугирования, и конъюгат лекарственное средство-антитело против TENB2, сконструированное с цистеином, очищали и обессоливали с помощью элюции через смолу G25 в PBS, фильтровали через 0,2 мкм фильтры в стерильных условиях и замораживали для хранения.
Посредством вышеописанных процедур были приготовлены следующие конъюгаты антитело против TENB2, сконструированное с цистеином, - лекарственное средство:
тио hu TMEFF2#19-MC-MMAF посредством конъюгирования A114C (Кабат) тио huTMEFF2#19 и MC-MMAF; и
тио hu TMEFF2#19-MC-val-cit-PAB-MMAE посредством конъюгирования A114C (Кабат) тио huTMEFF2#19 и MC-val-cit-PAB-MMAE.
Пример 4 Материалы и методы для иммуногистохимии, анализа интернализации, FACS, анализа клеточного киллинга, вестерн-блоттинга, анализа ксенотрансплантатов, анализа фармакокинетики и оценки безопасности.
Антитела и рекомбинантные белки: гуманизированное Mab PR1 против tenb2 было получено от PDL. ТиоMab PR1 против tenB2 (HC-A121C; последовательная нумерация) и белок tenB2ECD Flag были получены способом, обсуждаемым выше.
Клеточные линии и ксенотрансплантаты опухолей человека: PC3 представляет собой клеточную линию карциномы предстательной железы человека (ATCC). Клеточная линия, стабильная в среде PC3TenB2, была разработана компанией Genentech. Модели экспланта предстательной железы человека, LuCap70, 77 и 96.1, были получены в Университете г. Вашингтон.
Экспрессия РНК и белка: анализ экспрессии РНК, иммунологические процедуры (ИГХ, вестерн), связывание антитела (FACS) и интернализация, придерживаются ранее опубликованных методов (Cancer research 64,781-788 (2004)).
Получение стандартных или ТиоMab анти-TenB2-Валин-Цитруллин(vc)-монометилауристатин E (MMAE) и лекарственных конъюгатов (ADC), содержащих MC-MMAF: конъюгирование стандартных, тио-mab и контрольных mab с vc-MMAE, MC-MMAF ADC осуществляли, как описано выше.
In vitro клеточный киллинг и in vivo исследования: анализ клеточного киллинга проводили схожим образом, как описано в Cancer research 64,781-788 (2004). Каждую опухолевую линию модели экспланта предстательной железы поддерживали посредством серийной трансплантации кастрированным (андроген-независимая модель, LuCap70) или некастрированным (андроген-зависимая модель, LuCAP77 и LuCAP96.1) самцам мышей SCID с врожденным отсутствием клеток-киллеров, выведенным в лаборатории Чарльза Ривера. Опухоли измеряли один или два раза в неделю на протяжении исследования.
Модели на крысах и человекообразных обезьянах для оценки безопасности: Mab против tenb2 специфически распознает мишень tenb2 человека, обезьяны и крыс (FS I домен).
Исследование фармакокинетики: использовали стандартные протоколы и методы анализа.
Результаты показывают, что TenB2 человека (TMEFF2), обычно, ограничен для экспрессии в предстательной железе и ЦНС, и имеет значительно повышенные уровни в пораженной раком предстательной железе. Также показано, что антитела против TenB2 быстро интернализуются. В различных анализах клеточного киллинга показано, что эти антитела, когда конъюгированы с MMAE и MMAF, уничтожают клетки опухоли предстательной железы in vitro и in vivo. Кроме того, эффективные дозы TENB2-ADC были значительно ниже, чем те, которые требуются для установления токсических эффектов у грызунов и приматов.
Приведенное выше письменное описание предполагается достаточным для предоставления возможности специалисту в данной области осуществлять изобретение на практике. Объем настоящего изобретения не ограничен представленной концепцией, поскольку представленный вариант осуществления предназначен только в качестве примера некоторых аспектов изобретения, и любые компоненты, которые являются функционально эквивалентными, находятся в объеме данного изобретения. Представленные в настоящем документе факты не создают допущения, что письменное описание, содержащееся в настоящем документе, является недостаточным для обеспечения практического применения любого аспекта данного изобретения, в том числе его наилушего способа, и не должны рассматриваться как ограничивающие объем пунктов формулы изобретения представленными конкретными иллюстрациями. Действительно, различные модификации изобретения в дополнение к представленным и описанным в рамках настоящей заявки вариантам, из указанного выше описания будут очевидны специалистам в данной области и входят в объем прилагаемой формулы изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2436796C9 |
| АНТИ-CD79b АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2009 |
|
RU2553566C2 |
| АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2639543C9 |
| АНТИ-CD79b АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2008 |
|
RU2511410C2 |
| АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ, ВИЗУАЛИЗИРУЕМЫЕ ПРИ ПОМОЩИ ИММУНО-ПОЗИТРОН-ЭМИССИОННОЙ ТОМОГРАФИИ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2613886C2 |
| ПЕПТИДОМИМЕТИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ КОНЪЮГАТЫ АНТИТЕЛ С ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ | 2014 |
|
RU2689388C1 |
| ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА ПРОТИВ CD79b И ИММУНОКОНЪЮГАТЫ И СПОСОБЫ ПРИМЕНЕНИЯ | 2008 |
|
RU2557319C2 |
| МУЛЬТИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА, АНАЛОГИ АНТИТЕЛ, КОМПОЗИЦИИ И СПОСОБЫ | 2010 |
|
RU2580038C2 |
| АНТИ-CD79b АНТИТЕЛА И ИММУНОКОНЪЮГАТЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2791984C2 |
| ПОЛУЧЕННЫЕ С ПОМОЩЬЮ ГЕННОЙ ИНЖЕНЕРИИ АНТИТЕЛА С ЦИСТЕИНОВЫМИ ЗАМЕНАМИ И ИХ КОНЪЮГАТЫ | 2011 |
|
RU2626537C2 |









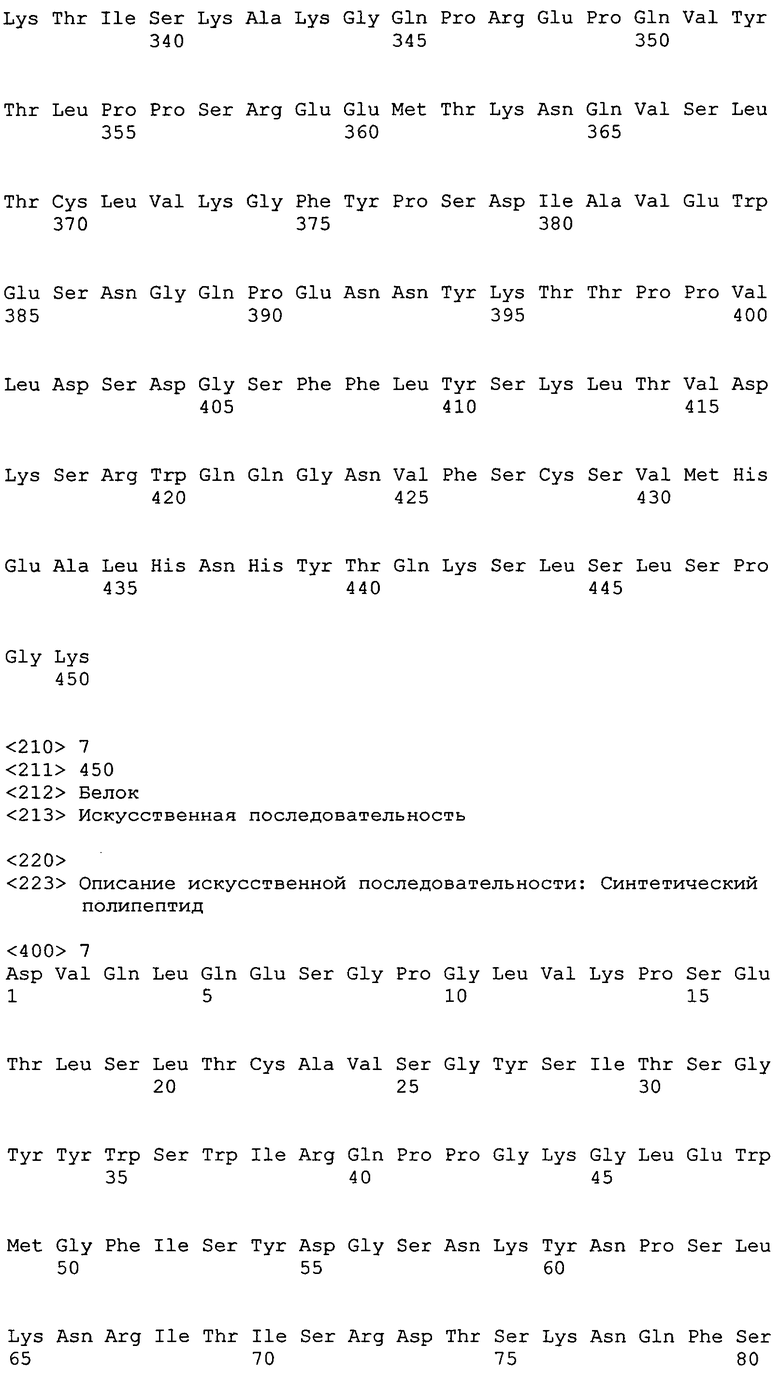








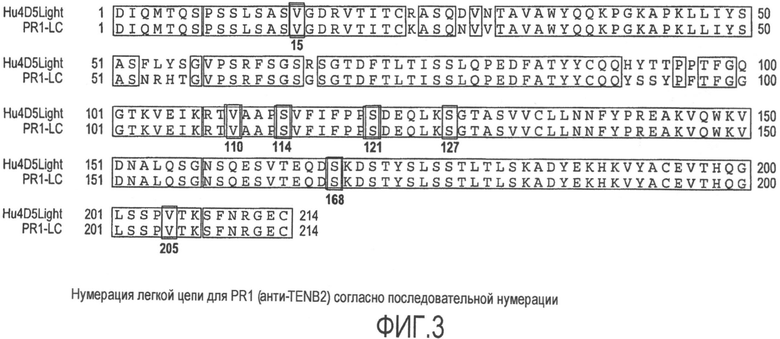

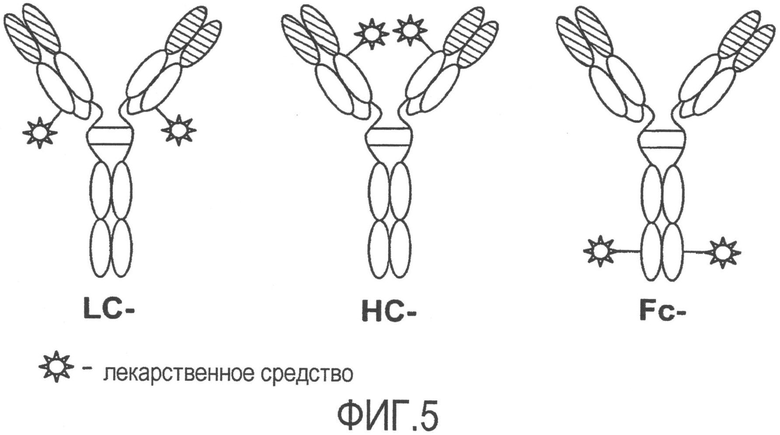
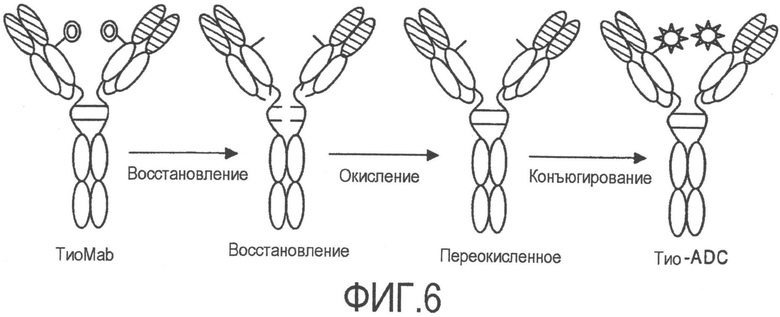
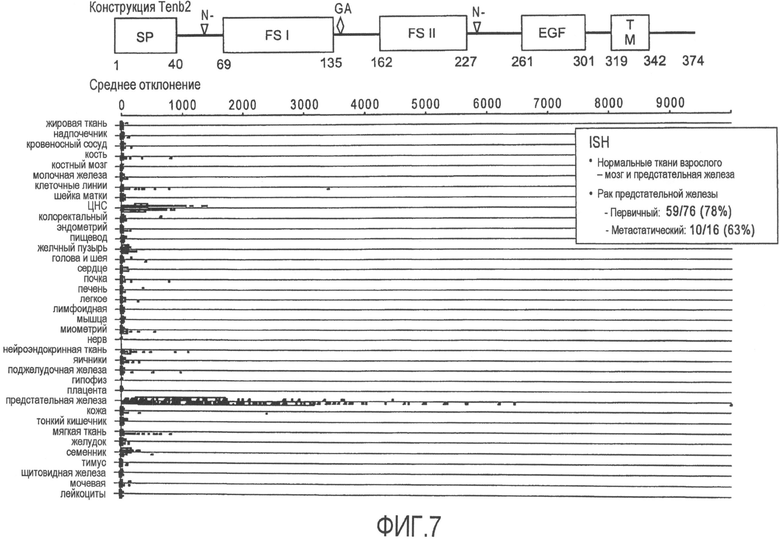
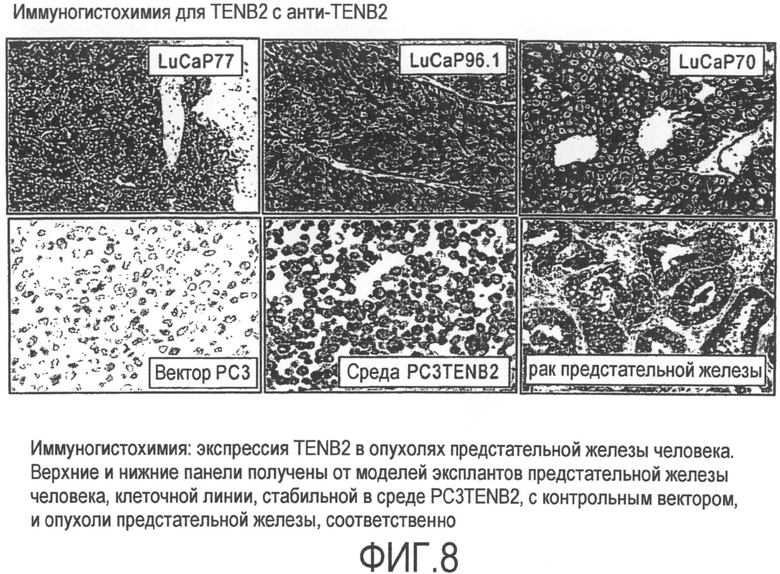
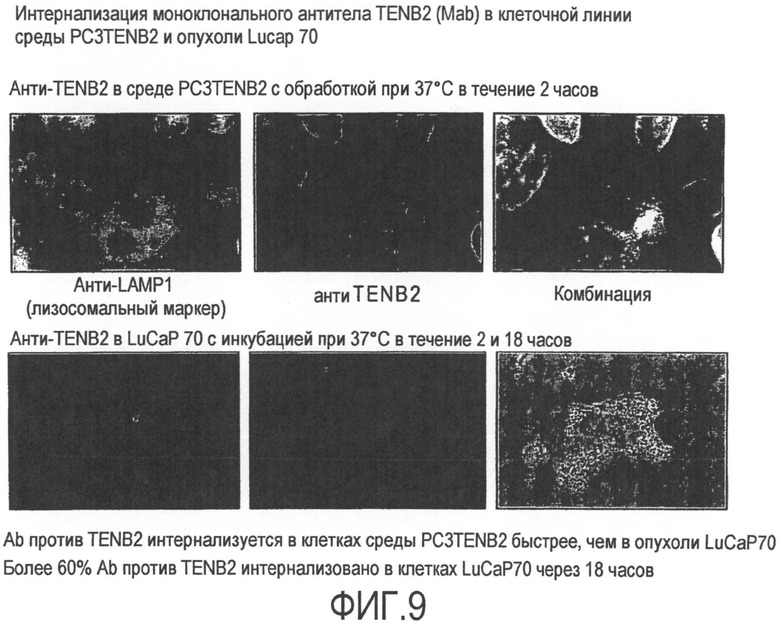
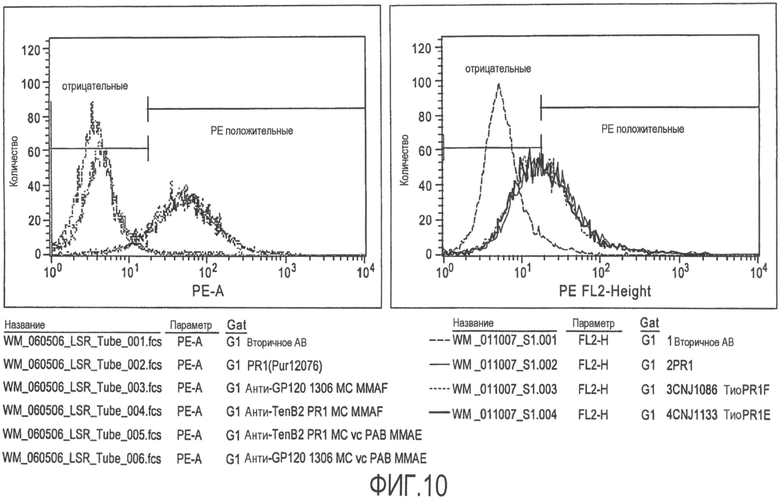
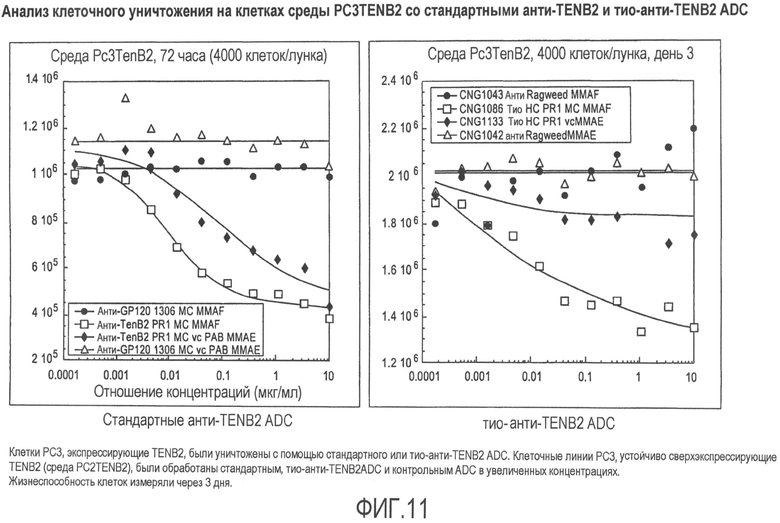
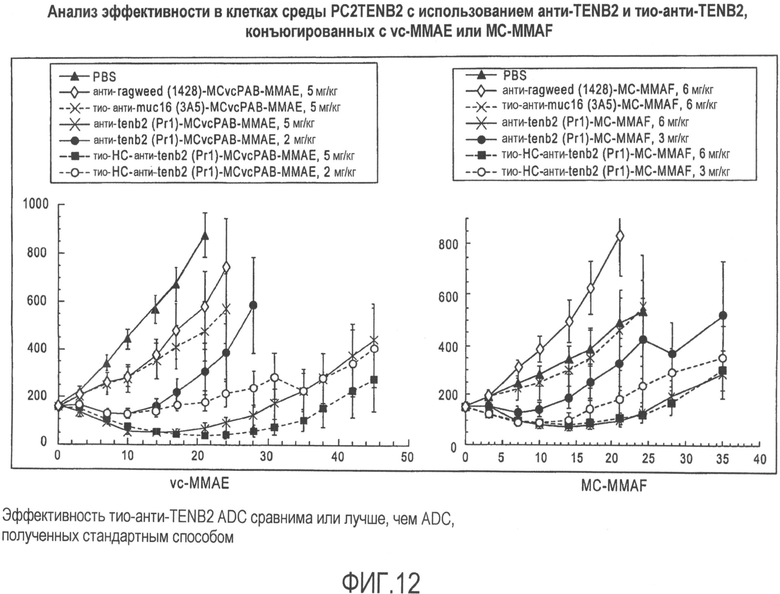

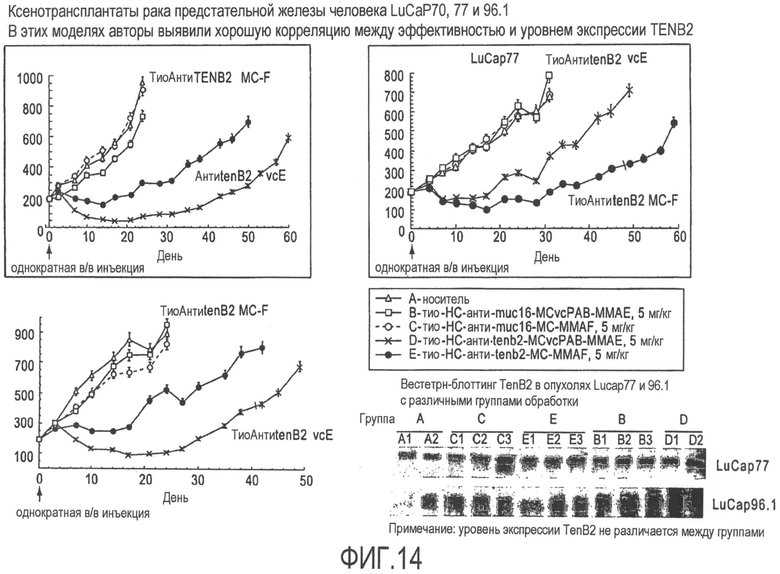
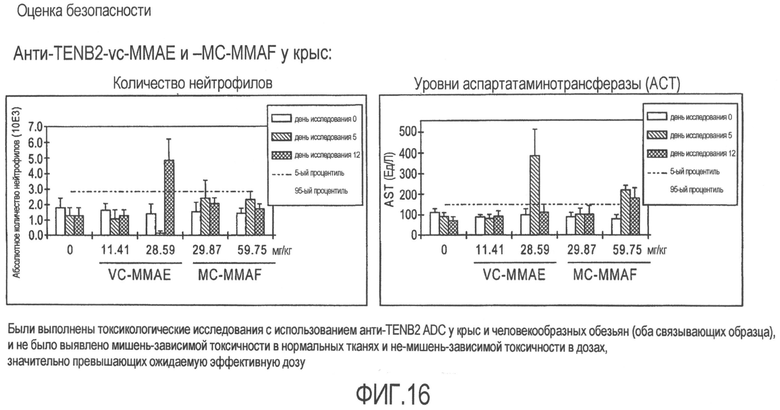
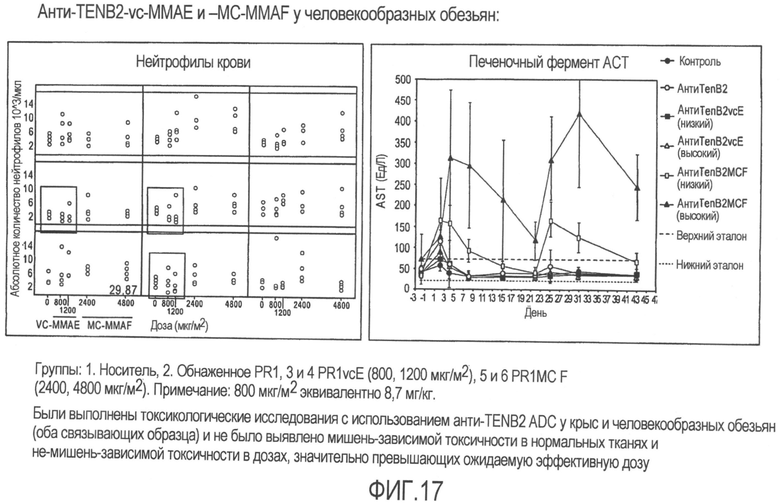
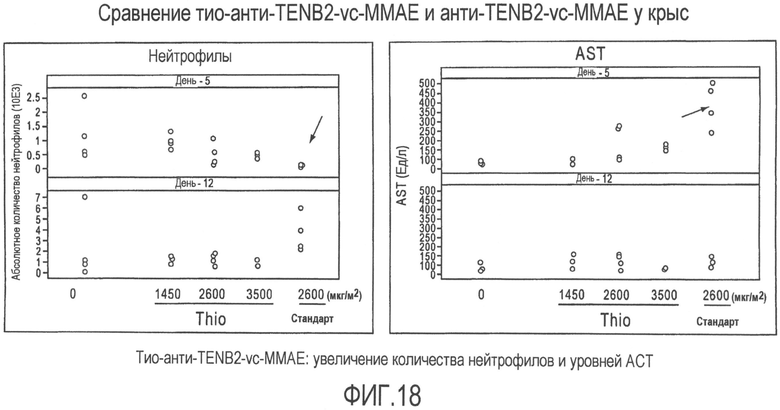
Изобретение относится к биотехнологии. Предложено антитело, специфичное к TENB2, содержащее легкую и тяжелую цепи. Тяжелая цепь содержит замену на свободный (реакционноспособный) цистеин А121С, что соответствует А114С (нумерация по Кабату) или А118С (нумерация по Eu). Предложены варианты конъюгата для лечения рака предстательной железы, содержащего антитело, ковалентно связанное с ауристатином, в том числе посредством линкера. Описаны: фармацевтическая композиция для лечения рака предстательной железы, использующая в качестве активного начала антитело или его конъюгат; изделие для лечения рака предстательной железы на основе такой композиции. Предложены: способ определения белка TENB2 в образце - на основе антитела, а также анализ для выявления клеток рака предстательной железы у млекопитающего и способ ингибирования клеточной пролиферации - на основе конъюгата антитела и ауристатина. Описан способ получения конъюгата антитела (Аb) и ауристатина (D) с формулой Ab-(L-D)p, где р равно от 1 до 4, а L - линкер. Использование изобретения обеспечивает конъюгаты с повышенной стабильностью в сыворотке по сравнению с такими же конъюгатами без замены А121С в антителе, что может найти применение в медицине. 9 н. и 24 з.п. ф-лы, 18 ил., 2 табл., 4 пр.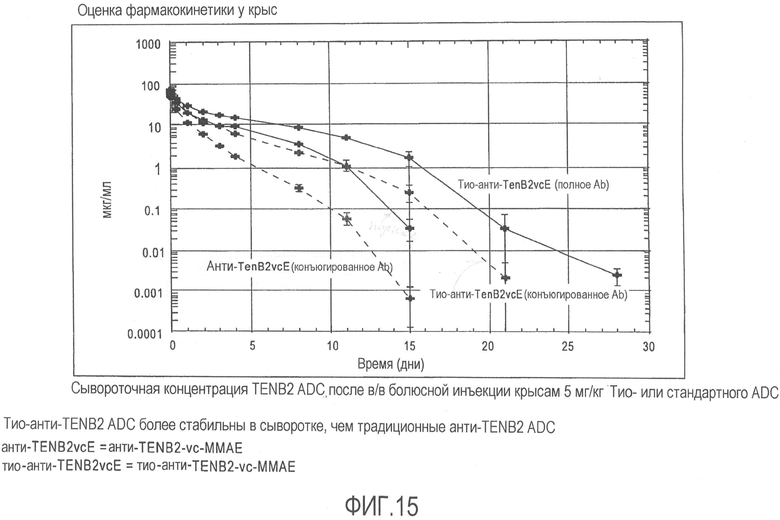
1. Антитело, специфичное к TENB2, содержащее легкую и тяжелую цепи, где тяжелая цепь содержит замену на свободный цистеин: Д121С, что соответствует А114С (нумерация по Кабату) или А118С (нумерация по Eu).
2. Антитело, специфичное к TENB2, по п.1, где антитело, специфичное к TENB2, связывается с TENB2 полипептидом.
3. Антитело, специфичное к TENB2, по п.1, содержащее последовательность тяжелой цепи, содержащую:

и последовательность легкой цепи, содержащую:

4. Антитело, специфичное к TENB2, по любому из пп.1-3, которое продуцируется в бактериях или в клетках СНО.
5. Антитело, специфичное к TENB2, по любому из пп.1-4, где родительское антитело, специфичное к TENB2, выбрано из моноклонального антитела, биспецифического антитела, химерного антитела, антитела человека и гуманизированного антитела.
6. Антитело, специфичное к TENB2, по любому из пп.1-4, где родительское антитело, специфичное к TENB2, представляет собой фрагмент антитела, предпочтительно Fab-фрагмент.
7. Конъюгат антитело - лекарственное средство, содержащий антитело, специфичное к TENB2, по любому из пп.1-3, ковалентно связанное с молекулой лекарственного средства ауристатин, посредством чего образуется конъюгат антитело - лекарственное средство, для лечения рака предстательной железы.
8. Конъюгат антитело - лекарственное средство по п.7, содержащий антитело (Аb), специфичное к TENB2, и молекулу (D) лекарственного средства ауристатин, где антитело, специфичное к TENB2, связано с D посредством одной или нескольких свободных аминокислот цистеина с помощью линкерной молекулы (L); где конъюгат имеет формулу I:

где р равно 1, 3, 4 или предпочтительно 2.
9. Конъюгат антитело - лекарственное средство по п.8, где L имеет формулу:
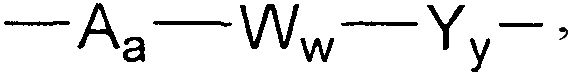
где:
А представляет собой элемент поперечной связи, ковалентно соединенный с тиолом цистеина антитела (Аb);
а равно 0 или 1;
каждый W независимо представляет собой аминокислотную единицу;
w является целым числом от 0 до 12;
Y представляет собой спейсерную единицу, ковалентно связанную с молекулой лекарственного средства; и
y равно 0, 1 или 2.
10. Конъюгат антитело - лекарственное средство по п.9, имеющий формулу:
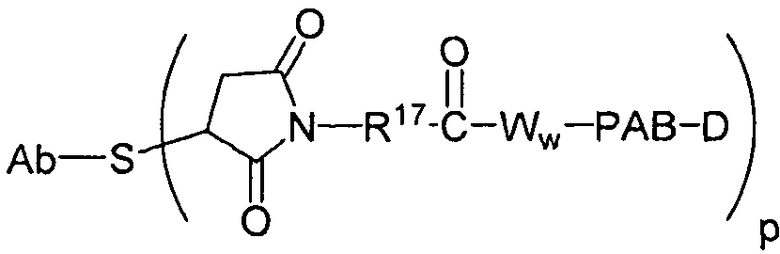
где PAB представляет собой пара-аминобензилкарбамоил, и R17 является двухвалентным радикалом, выбранным из (CH2)r, C3-C8 карбоциклила, О-(CH2)r, арилена, (CH2)r-арилена, -арилен-(CH2)r-, (CH2)r-(C3-C8 карбоциклил), (C3-C8 карбоциклил)-(CH2)r, C3-C8 гетероциклила, (CH2)r-(C3-C8 гетероциклил), -(C3-C8 гетероциклил)-(CH2)r-, -(CH2)rC(О)NRb(CH2)r-, -(CH2CH2O)r-, -(CH2CH2O)r-CH2-, -(CH2)rC(О)NRb(CH2CH2O)r-, -(CH2)rC(О)NRb(CH2CH2O)r-CH2-, -(CH2CH2O)rC(О)NRb(CH2CH2O)r-, -(CH2CH2O)rC(О)NRb(CH2CH2O)r-CH2- и -(CH2CH2O)rC(О)NRb(CH2)r-; где Rb представляет собой H, C1-C6 алкил, фенил или бензил; и r независимо представляет собой целое число от 1 до 10.
11. Конъюгат антитело - лекарственное средство по п.9, где Ww представляет собой валин-цитруллин.
12. Конъюгат антитело - лекарственное средство по п.9, имеющий формулу:
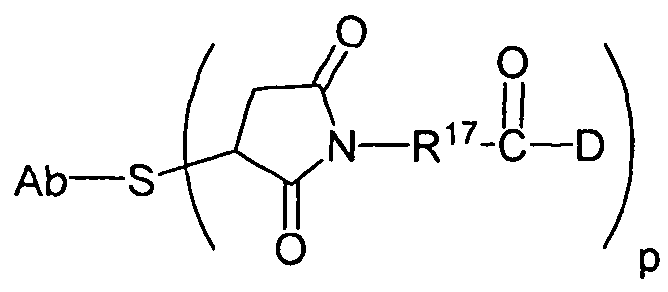
13. Конъюгат антитело - лекарственное средство по п.10 или 12, где R17 представляет собой (CH2)5 или (CH2)2.
14. Конъюгат антитело - лекарственное средство по п.9, имеющий формулу:
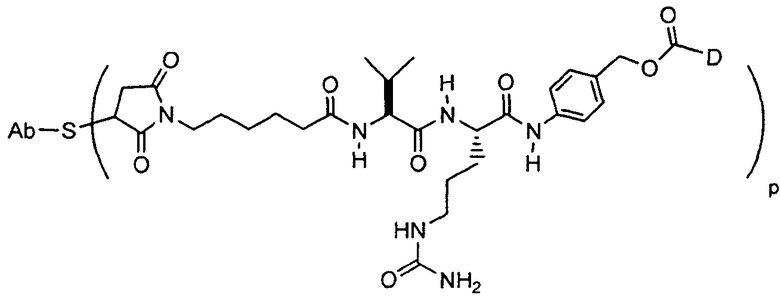
15. Конъюгат антитело - лекарственное средство по п.8, где L представляет собой SMCC или ВМРЕО.
16. Конъюгат антитело - лекарственное средство по п.8, где D представляет собой либо ММАЕ, предпочтительно имеющее структуру:
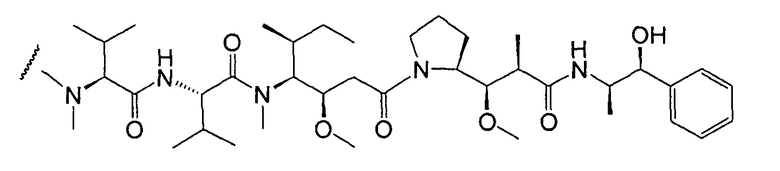
где волнистая линия обозначает сайт соединения с линкером L;
либо MMAF, предпочтительно имеющее структуру:
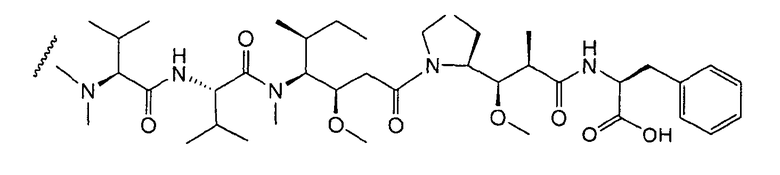
где волнистая линия обозначает сайт соединения с линкером L.
17. Конъюгат антитело - лекарственное средство по любому из пп.8-16, где родительское антитело, специфичное к TENB2, выбрано из моноклонального антитела, биспецифического антитела, химерного антитела, антитела человека и гуманизированного антитела.
18. Конъюгат антитело - лекарственное средство по любому из пп.8-16, где родительское антитело, специфичное к TENB2, представляет собой фрагмент антитела, предпочтительно Fab-фрагмент.
19. Конъюгат антитело - лекарственное средство по п.7, где L представляет собой MC-val-cit-PAB или МС, SMCC, SPP или ВМРЕО.
20. Конъюгат антитело - лекарственное средство для лечения рака предстательной железы, выбранный из структур:
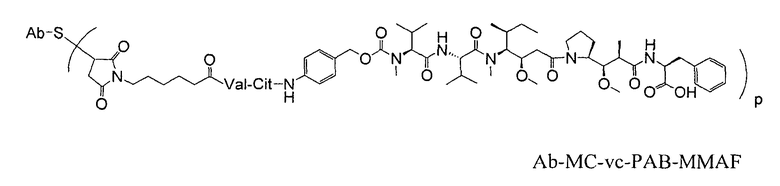
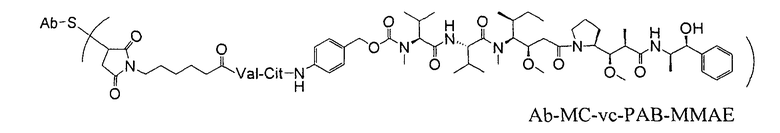
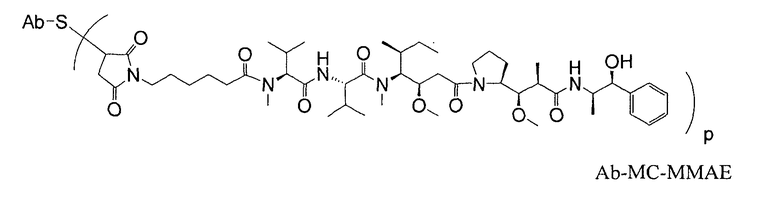
и
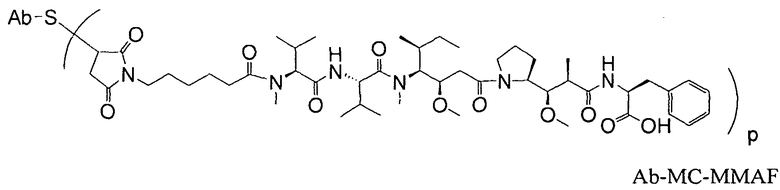
где Val представляет собой валин; Cit представляет собой цитруллин; р равно 1, 2, 3 или 4; и Ab является антителом, специфичным к TENB2, по п.1.
21. Конъюгат антитело - лекарственное средство по п.18, где Ab содержит SEQ ID NO:2.
22. Фармацевтическая композиция для лечения рака предстательной железы, содержащая терапевтически эффективное количество антитела, специфичного к TENB2, по п.1 или конъюгата антитело - лекарственное средство по п.7, и фармацевтически приемлемый разбавитель, носитель или наполнитель.
23. Фармацевтическая композиция, содержащая конъюгат антитело - лекарственное средство, по п.22, дополнительно содержащая терапевтически эффективное количество химиотерапевтического средства, выбранного из летрозола, оксалиплатина, доксетаксела, 5-фторурацила, лапатиниба, капецитабина, лейковорина, эрлотиниба, пертузумаба, бевацизумаба и гемцитабина.
24. Изделие для лечения рака предстательной железы, содержащее:
фармацевтическую композицию, содержащую конъюгат антитело - лекарственное средство, по п.22;
контейнер; и
листовку-вкладыш или этикетку, на которой указано, что соединение можно использовать для лечения рака предстательной железы.
25. Способ определения присутствия белка TENB2 в образце, в котором подозревают наличие указанного белка, включающий воздействие на указанный образец антителом, специфичным к TENB2, по п.1, и определение связывания указанного антитела с указанным белком TENB2 в указанном образце, где связывание антитела с указанным белком указывает на наличие указанного белка в указанном образце.
26. Способ по п.25, где указанное антитело ковалентно связано с меткой, выбранной из флуоресцентного красителя, радиоизотопа, биотина или металл-комплексообразующего лиганда, или где указанный образец содержит клетку, в которой подозревают экспрессию указанного белка TENB2, где указанная клетка предпочтительно является раковой клеткой предстательной железы, яичника, молочной железы, легкого или поджелудочной железы.
27. Анализ для выявления клеток рака предстательной железы у млекопитающего, включающий:
(a) воздействие на клетки, полученные от млекопитающего, конъюгатом антитело - лекарственное средство по п.7; и
(b) определение формирования комплекса между конъюгатом антитело - лекарственное средство и полипептидом TENB2 в указанных клетках, где формирование комплекса является признаком наличия клеток рака предстательной железы у млекопитающего.
28. Способ ингибирования клеточной пролиферации, включающий обработку клеток опухоли млекопитающего в среде клеточной культуры конъюгатом антитело - лекарственное средство по п.7, посредством чего ингибируется пролиферация опухолевых клеток, где клетки опухоли млекопитающего представляют собой клетки опухоли предстательной железы.
29. Фармацевтическая композиция по п.22 для применения в способе лечения рака предстательной железы, где способ включает введение пациенту указанной фармацевтической композиции.
30. Фармацевтическая композиция по п.29, где способ включает введение пациенту химиотерапевтического средства, где химиотерапевтическое средство выбрано из летрозола, цисплатина, карбоплатина, таксола, паклитаксела, оксалиплатина, доксетаксела, 5-фторурацила, лейковорина, эрлотиниба, пертузумаба, бевацизумаба, лапатиниба и гемцитабина.
31. Способ получения конъюгата антитело - лекарственное средство, содержащего антитело (Аb), специфичное к TENB2, по п.1 и молекулу (D) лекарственного средства ауристатин, где указанное антитело соединено с D посредством одной или нескольких сконструированных аминокислот цистеина с помощью линкерной молекулы (L); где конъюгат имеет формулу I:

где р равно 1, 2, 3, или 4; где способ включает стадии:
(a) взаимодействия сконструированной цистеиновой группы в указанном антителе с линкерным реагентом с образованием промежуточного соединения антитело-линкер Ab-L; и
(b) взаимодействия Ab-L с активированной молекулой D лекарственного средства; в результате чего образуется конъюгат антитело - лекарственное средство;
или включает стадии:
(c) взаимодействия нуклеофильной группы молекулы лекарственного средства с линкерным реагентом с образованием промежуточного соединения лекарственное средство - линкер D-L; и
(d) взаимодействия D-L со сконструированной цистеиновой группой в указанном антителе; в результате чего образуется конъюгат антитело - лекарственное средство,
где способ необязательно включает стадию экспрессии указанного антитела в клетках яичников китайского хомячка (СНО).
32. Способ по п.31, дополнительно включающий стадию обработки экспрессированного антитела восстановителем, где восстановитель предпочтительно выбран из ТСЕР и DTT.
33. Способ по п.32, дополнительно включающий стадию обработки экспрессированного антитела окислителем, после обработки восстановителем, где окислитель предпочтительно выбран из сульфата меди, дегидроаскорбиновой кислоты и воздуха.
| WO 2006034488 А2, 30.03.2006 | |||
| WO 2005117986 А2, 15.12.2005 | |||
| WO 200375855 А2, 18.09.2003 | |||
| СПОСОБ ПОЛУЧЕНИЯ ПРИРОДНОГО ГУМАНИЗИРОВАННОГО АНТИТЕЛА | 1998 |
|
RU2221809C2 |
Авторы
Даты
2014-01-27—Публикация
2008-10-16—Подача