Перекрестная ссылка на приоритетные заявки
[0001] Настоящей патентной заявкой заявлен приоритет согласно патентной заявке США №12/395,455, поданной 27 февраля 2009 г., озаглавленной "Устройство для эндолюминальной лазерной абляции и способ лечения вен", предварительной патентной заявке США №61/104,956, поданной 13 октября 2008 г., озаглавленной "Устройство для эндолюминальной лазерной абляции и способ лечения вен", предварительной патентной заявке США №61/079,024, поданной 8 июля 2008 г., озаглавленной "Радиально излучающее устройство и способ лечения вен", и предварительной патентной заявке США №61/067,537, поданной 28 февраля 2008, озаглавленной "Устройство для быстрой вставки и усовершенствованный способ лазерного лечения сосудов", каждая из которых полностью включена в настоящую заявку путем ссылки и является частью настоящего раскрытия.
Предпосылки к созданию изобретения
Область изобретения
[0002] Настоящее изобретение относится к лазерному эндоваскулярному лечению, в частности, к лечению заболеваний сосудов, таких как венозная недостаточность, при помощи лазерной энергии с использованием оптоволокна.
Заявление о раскрытии информации
[0003] Венозная система нижних конечностей человека по существу состоит из системы поверхностных вен и системы глубоких вен, соединенных перфорантными венами. Система поверхностных вен содержит большие и малые подкожные вены, а система глубоких вен содержит передние и задние большеберцовые вены, которые сходятся, формируя подколенную вену около колена. Подколенная вена, в свою очередь, переходит в бедренную вену, когда к ней присоединяется малая подкожная вена.
[0004] Венозная система содержит клапаны, помогающие обеспечить односторонний кровоток обратно к сердцу. Венозные клапаны представляют собой двустворчатые клапаны, где каждая створка формирует резервуар с кровью. Двустворчатые венозные клапаны сводят свои свободные поверхности по направлению друг к другу под воздействием давления обратного кровотока. При нормальной работе обратный кровоток предотвращается, и осуществляется только прямой кровоток к сердцу. Двустворчатый клапан становится ослабленным, когда его створки неспособны правильно закрываться под давлением обратного кровотока и допускают обратный кровоток. Когда происходит обратный кровоток, на нижних венозных участках повышается давление, что, в свою очередь, приводит к расширению вен и недостаточности других клапанов.
[0005] Недостаточность клапанов, называемая венозной недостаточностью, представляет собой хроническое заболевание, которое может привести к нарушению окраски кожи, варикозному расширению вен, боли, опухание и изъязвлениям. Варикозные вены представляют собой кровеносные сосуды, которые расширились, изогнулись, и стенки которых перестали быть эластичными. Вследствие расширения кровеносных сосудов клапаны не могут полностью закрыться, и вены теряют способность переносить кровь обратно к сердцу. Это приводит к накоплению крови внутри сосудов, что, в свою очередь, приводит к дальнейшему увеличению и искривлению вен. Варикозные вены обычно имеют синий или фиолетовый цвет и могут выпирать в искривленном виде через поверхность кожи, что приводит к характерному неприятному внешнему виду. Варикозные вены обычно формируются в подкожных венах ног, подвергающихся высокому давлению у стоящего человека. Другие виды варикозных вен включают венозные озерца, сетчатые вены и телеангиэктазии.
[0006] Существует несколько способов лечения указанных типов заболеваний сосудов. Некоторые из этих способов направлены лишь на облегчение определенных симптомов, и не устраняют варикозные вены, а также не предотвращают их повторное появление. Указанные способы включают поднятие ног в лежачем положении или при использовании подставки для ног в сидячем положении, эластичные чулки и специальные упражнения.
[0007] Варикозные вены часто лечат способом удаления больных вен. При лечении указанными способами кровь, которая могла бы протекать через удаленные вены, заставляют течь по оставшимся здоровым венам. Для удаления проблемных вен могут быть использованы различные способы, включая хирургическое вмешательство, склеротерапию, электрокаустику и лечение при помощи лазера.
[0008] В склеротерапии используется тонкая игла, с помощью которой производится инъекция раствора напрямую в вену. Указанный раствор раздражает выстилку вены, заставляя ее отекать, а кровь сворачиваться. Вена превращается в рубцовую ткань, которая в итоге может стать незаметной. Некоторые врачи используют склеротерапию для лечения как варикозных, так и паукообразных вен. На сегодняшний день обычно используемые склерозирующие средства включают гипертонический физиологический раствор или Сотрадекол (Sotradecol™) (тетрадецилсульфат натрия). Склерозирующее средство действует на внутренню выстилку стенок вены, заставляя их смыкаться и блокировать кровоток. Склеротерапия может привести к различным осложнениям. Люди, страдающие аллергией, могут обнаружить аллергическую реакцию, зачастую весьма сильную. Если игла введена неправильно, склеротирующее средство может обжечь кожу или оставить на ней непроходящую отметину или пятно. Кроме того, склеротерапия может иногда приводить к образованию тромбов или движущихся тромбов. Согласно некоторым исследованиям крупные варикозные вены при использовании склеротерапии могут быть более склонны к повторному открытию, и поэтому лечение склеротерапией обычно ограничивается венами меньше определенного размера.
[0009] Экстирпация вен представляет собой хирургическую процедуру, используемую для лечения варикозных вен под общим или местным наркозом. Проблемные вены удаляются из тела путем пропуска гибкого устройства через вену и его удаления через надрез в районе паха. Более мелкие ветви указанных вен также удаляются подобным устройством либо удаляются через несколько мелких надрезов (т.е. амбулаторной флебэктомией). Затем вены, соединенные с глубокими венами, перерезаются.
[00010] Одним из недостатков экстирпации вен является тот факт, что она может привести к образованию шрамов на месте надрезов и иногда может вызывать образование тромбов. Еще один недостаток заключается в том, что экстирпация вен может быть болезненной, занимать много времени и может иметь длительный период восстановления. Еще одним недостатком экстирпации вен является то, что при их осуществлении могут быть повреждены коллатеральные ветви удаленной вены, которые могут кровоточить и, в свою очередь, приводить к гематомам или иным осложнениям, таким как потеря крови, боль, заражение, повреждения нервов и опухание. Еще одним недостатком экстирпации вен является то, что вследствие повреждений, нанесенных обрабатываемому участку пациенты могут испытывать боль и дискомфорт в течение нескольких часов или даже нескольких дней после операции. Еще одним недостатком экстирпации вен является то, что они могут иметь и другие отрицательные побочные эффекты, связанные с тем, что подобные хирургические процедуры проводятся под наркозом, включая тошноту, рвоту и риск заражения раны.
[00011] Еще одним хорошо известным способом лечения венозной недостаточности является использование высоких частот (радиочастот RF). Пример высокочастотного способа описан в патентной заявке США №2006/0069471, Parley и др. Через катетер в вену вводятся электроды, которые соприкасаются со стенкой вены и через которые подается высокочастотная энергия с целью избирательного нагревания стенки вены. Высокочастотная энергия подается направленно через электроды на участки стенки вены, соприкасающиеся с электродами, с целью вызвать местное нагревание и фиброз венозной ткани. Одним из недостатков высокочастотных способов является то, что они требуют постоянного контакта между высокочастотными электродами и стенкой вены и по существу подают энергию только через такие места соприкосновения. Другой недостаток высокочастотных способов заключается в том, что они могут занимать значительно больше времени и вызывают больший стресс у пациента, чем желательно. Еще одним недостатком высокочастотных способов является то, что высокочастотные катетеры и электроды могут быть относительно сложными и более дорогими в производстве, чем желательно.
[00012] Еще одним известным науке минимально инвазивным способом лечения варикозных вен является эндолюминальная лазерная абляция. В ходе обычной известной процедуры эндолюминальной лазерной абляции в вену, подлежащую лечению, с помощью стилет-катетера вводят оптоволокно. Оптоволоконная нить снабжена плоской излучающей поверхностью на дистальном конце. Примерная известная процедура эндолюминальной лазерной абляции содержит следующие этапы. Сначала в вену, подлежащую лечению, вводится проволочный проводник, предпочтительно с помощью инъекционной иглы. Затем по проволочному проводнику пускают стилет-катетер, и проводят его к месту лечения. После чего проволочный проводник удаляют, оставляя стилет-катетер на месте. Затем через стилет-катетер проводится оптоволокно (соединенное с лазерным источником), которое располагается таким образом, что плоская излучающая поверхность на дистальном конце волокна и стилет-катетер находятся в одном месте. После этого ткань, окружающая вену, подлежащую лечению, подвергается тумесцентной анестезии. Перед обработкой лазером, стилет-катетер оттягивают назад от плоской излучающей поверхности на расстояние, достаточное для того, чтобы не дать излучаемой лазерной энергии повредить катетер. Затем запускается лазер, излучающий лазерную энергию через плоскую излучающую поверхность в кровь и/или стенку вены прямо напротив излучающей поверхности. Пока излучается лазерная энергия, лазерное волокно и стилет-катетер отводят с целью осуществить лечение и закрытие вены на участке желаемой длины. Лазерная энергия впитывается кровью и/или тканью стенки вены, и, в свою очередь, наносит температурные повреждения и вызывает фиброз вены.
[00013] Патент США №6,200,332, Del Giglio, описывает пример известного устройства и способа подкожного лечения лазером с использованием минимума инсерций на участке лечения. Распространенные анормальности сосудов, такие как расстройства капилляров, звездчатая гемангиома, гемангиома и варикозные вены могут быть устранены избирательно. В структуру сосудов вводится игла, и целевые анормальности подвергаются лазерному излучению. Устройство позволяет ориентировать и располагать доставляющее лазер оптоволокно в ходе лечения. Удлинитель позволяет поддерживать оптоволокно в фиксированном положении по отношению к ручному блоку и на фиксированном расстоянии от него, что позволяет пользователю понимать, насколько глубоко волокно введено в вену.
[00014] Патент США №6,398,777, Navarro и др., описывает другую процедуру эндолюминальной лазерной абляции, в ходе которой подкожный доступ к полости вены достигается при помощи ангиокатетера, через который вводится нить оптоволокна. Нить фиброволокна имеет наконечник без покрытия, имеющий плоскую излучающую поверхность. Согласно патенту '777 вену сжимают вручную, например рукой или при помощи компресса, с целью привести ее в соприкосновение с плоской излучающей поверхностью наконечника оптоволокна. Лазерную энергию подают в виде высокоэнергетичных импульсов на участок стенки вены, соприкасающийся с непокрытым наконечником оптоволокна. Длина волны лазерной энергии находится в пределах от примерно 532 нм до примерно 1064 нм, а продолжительность каждого импульса составляет от примерно 0,2 сек. до примерно 10 сек. Каждый импульс доставляет от примерно 5 Вт до примерно 20 Вт энергии стенке вены. Согласно патенту '777 и другим известным процедурам эндолюминальной лазерной абляции подводится энергия, достаточная для того, чтобы обеспечить повреждение всей толщины стенки вены, что в итоге приводит к фиброзу стенки вены и смыканию большой подкожной вены.
[00015] В соответствии с патентом '777 известна подача энергии сравнительно высоких уровней (т.е., не менее 80 Дж/см) для повышения успешности лечения венозной недостаточности подкожных вен эндолюминальной лазерной абляцией Timperman и др. указывают, что внутривенное лечение подкожных вен лазером особенно успешно при подаче доз свыше 80 Дж/см. Timperman и др. собрали данные, касающиеся длины подвергаемой лечению вены и общего объема использованной энергии на основе 111 обработанных вен. Длина волны использованной лазерной энергии составляла 810 нм или 940 нм. Из 111 обработанных вен, 85 остались закрытыми (77,5%) в последующий период. В указанной группе успешно обработанных вен средний уровень подведенной энергии составил 63,4 Дж/см. В группе из 26 неудачно обработанных вен средний уровень использованной энергии составил 46,6 Дж/см. У пациентов, получивших дозы в 80 Дж/см и выше, неудачной обработки выявлено не было. Р. Timperman, M. Sichlau, R. Ryu, "Использование повышенного уровня энергии повышает успешность лечения способом внутривенной лазерной обработки венозной недостаточности подкожных вен", Журнал сосудистой и инвазивной радиологии, том 15, издание 10, стр.1061-1063(2004).
[00016] Одним из недостатков, связанных с этим и другими известными способами лечения эндолюминальной лазерной абляцией, является то, что лазерное излучение выводится лишь через очень маленькую плоскую излучающую поверхность на непокрытом наконечнике волокна. В результате, по существу лишь очень маленький локализованный участок крови и/или стенки вены напротив плоской излучающей поверхности напрямую получает излучаемую лазерную энергию в определенный момент времени. Еще одним недостатком подобных известных устройств и способов эндолюминальной лазерной абляции является то, что лазерное излучение из плоской излучающей поверхности волокна направлено исключительно вперед. Соответственно, по существу излучение не направлено радиально или латерально из наконечника волокна, вследствие чего лазерное излучение относительно локализовано. Дополнительный недостаток заключается в том, что сравнительно высокий уровень энергии, подаваемой в вену, создает зону значительно повышенной температуры, что может, в свою очередь, повысить соответствующие болевые ощущения в окружающих тканях. Сравнительно высокие уровни подаваемой энергии также могут привести к повышению температурных повреждений окружающих тканей. Чем сильнее температурные повреждения, тем выше шанс болевых ощущений после процедуры, появления гематом и возникновения парестезии. Парестезия представляет собой аномальное и/или неприятное ощущение, возникающее вследствие повреждения нервов. Еще одним недостатком является то, что такой сравнительно высокий уровень доставки энергии и/или локализованная концентрация лазерного излучения могут приводить к перфорации вен. Как следствие, подобные известные процедуры эндолюминальной лазерной абляции могут требовать использования большого количества анестетика, например, местной тумесцентной анестезии, большего времени, и могут приводить к повышенному стрессу как у пациента, так и у лечащего врача.
[00017] Еще одним недостатком эндолюминальной лазерной абляции является то, что используется тумесцентный способ, требующий значительного объема тумесцентной анестезии. Например, типичный известный способ лечения эндолюминальной лазерной абляцией требует по меньшей мере от примерно 100 мл до примерно 300 мл или больше тумесцентного анестезирующего агента в зависимости от длины обрабатываемой вены. Тумесцентный анестезирующий агент вводится в ткань по всей длине вены. В некоторых случаях тумесцентный анестезирующий агент вводится в перивенозную полость, ограниченную одной или несколькими фасциальными оболочками, окружающими вену. В других случаях тумесцентный анестезирующий агент вводится в ткань ноги, окружающую вену. Тумесцентный анестезирующий агент обычно по существу состоит из разбавленных концентраций лидокаина и эфинефрина в физрастворе. Одним из недостатков таких тумесцентных способов является то, что анестетик является токсичным, и в некоторых случаях, когда, например, используется значительный его объем, анестетик может вызвать у пациентов побочные эффекты, такие как конвульсии. Еще одним недостатком тумесцентного способа является то, что у пациентов может возникнуть нежелательный рост кровяного давления вследствие использования эфинефрина. Еще один недостаток тумесцентного способа заключается в том, что он требует введения значительного объема жидкого анестетика по всей длине вены, что делает процедуру эндолюминальной лазерной абляции значительно более длительной, а также может приводить к неприятным побочным эффектам, таким как черные и синие отметины, и прочие побочные эффекты, связанные с использованием столь больших объемов анестетика.
[00018] Хотя тумесцентная анестезия или тумесцентная инфузия холодного физраствора, используемые в известном тумесцентном способе эндолюминальной лазерной абляции, создают отвод тепла вокруг вены, может возникать значительно более высокий уровень температурных повреждений, чем было бы желаемо. Чем сильнее температурные повреждения, тем выше шанс болевых ощущений после процедуры, появления гематом и возникновения парестезии. Например, значительное количество тумесцентного анестетика, используемое в известных процедурах эндолюминальной лазерной абляции, не позволяет пациенту ощущать тепловую стимуляцию нервов и тем самым не дает пациенту возможности попросить врача остановить процедуру или изменить ее с целью предотвращения нежелательных температурных повреждений. Ветви большеберцового нерва и общего малоберцового нерва могут подвергаться подобным повреждениям. Общий малоберцовый нерв расположен близко к поверхности кожи на латеральной части ноги ниже колена, и температурные повреждения этого нерва могут привести к отвислой стопе. Сходным образом, большеберцовый нерв может быть поврежден при работе на верхнем участке подколенной ямки. В зависимости от их степени температурные повреждения большеберцового нерва могут привести к дисфункции мышц голени и стопы. Икроножный нерв и подкожный нерв сходным образом подвержены возможности температурных повреждений при проведении эндолюминальной лазерной абляции малой подкожной вены или большой подкожной вены ниже колена. Икроножный нерв проходит очень близко от малой подкожной вены, в особенности дистально ближе к лодыжке. Подкожный нерв проходит очень близко от большой подкожной вены под коленом, в особенности, опять же, дистально ближе к лодыжке. Использование значительного количества анестетика, такого как тумесцентный анестетик, может невольно привести к температурным повреждениям этих нервов.
[00019] Патент США №6,986,766 относится к нанесению отметок на оптоволокно для определения положения волокна относительно стилет-катетера. Однако указанное изобретение и изобретения, связанные с ним, не содержат информацию для определения скорости обратного отвода лазерного волокна в ходе лазерной обработки. Медленный неконтролируемый обратный отвод лазерного волокна или катетера может послужить причиной перегрева и перфорации стенки сосуда, так как даже у самого лучшего хирурга могут возникнуть проблемы при отводе волокна с определенной скоростью с целью поддержания подходящей температуры нагревания стенки сосуда. С другой стороны, излишне высокая скорость обратного отвода может привести к недостаточному для закрытия сосуда количеству излучаемой энергии.
[00020] Патентная заявка США №2004/0199151, Neuberger, права на которую переданы правообладателю по настоящему изобретению, и которая полностью включена в настоящую заявку путем ссылки и является частью настоящего раскрытия, описывает систему и способ контролируемого выпуска излучения при подкожных способах лечения облучением. Лазер соединен с оптоволокном, которое вводится под кожу или в сосудистую полость до определенного места. Затем на обрабатываемый участок подается излучение и при этом волокно одновременно отводится к месту входа. Волокно выводится вручную с заранее определенной скоростью, а излучение оказывает свое воздействие при постоянном уровне мощности или энергии. Для поддержания постоянной необходимой плотности энергии скорость отвода измеряется и поступает на управляющий механизм. Управляющий механизм регулирует испускаемую энергию, длительность импульсов или скорость импульсов с целью удостовериться, что вена или ткань получает стабильную дозу энергии. Хотя это решение является значительно более совершенным, чем известные аналоги, излучение выводится с плоской излучающей поверхности, расположенной на наконечнике волокна и направлено в первую очередь в продольном направлении.
[00021] Соответственно, задачей настоящего изобретения является исправление одного или нескольких описанных выше недостатков, известных из уровня техники.
Раскрытие изобретения
[00022] Настоящее изобретение раскрывает усовершенствованный способ и устройство для безопасной и эффективной эндолюминальной лазерной абляции, которая может быть проведена при сравнительно низкой плотности энергии.
[00023] В некоторых вариантах выполнения устройство для эндолюминального лечения кровеносного сосуда содержит гибкий волновод, имеющий удлиненную ось, проксимальный конец оптически соединимый с источником излучения, и дистальный конец, выполненный с возможность размещения в кровеносном сосуде. Дистальный конец содержит излучающую поверхность, излучающую волны от источника излучения латерально по отношению к удлиненной оси волновода на отходящий под углом участок окружающей стенки сосуда.
[00024] В некоторых вариантах выполнения устройство содержит излучающую поверхность (или поверхности), излучающую лазерную энергию радиально и по существу по окружности в окружающую стенку кровеносного сосуда и любую кровь, физраствор и/или иную текучую среду, расположенную между стенкой и поверхностью. В некоторых вариантах выполнения устройство вырабатывает лазерную энергию постоянно или в виде импульсов радиально через оптоволокно по существу с конической излучающей поверхности для достижения радиального излучения на 360°. Некоторые варианты выполнения устройства дополнительно включают по существу коническую отражающую поверхность, расположенную аксиально на некотором расстоянии относительно конической излучающей поверхности и необращенную к ней, для увеличения эффективности радиального излучения путем отражения радиальной или остаточной окружной, либо подаваемой в прямом направлении энергии.
[00025] В некоторых вариантах выполнения несколько пазов, выемок или иных средств аксиально расположены на некотором расстоянии друг от друга по длине волокна, заставляя излучение частично подаваться радиально наружу от волокна, и частично передаваться последующим пазам или пазу. В некоторых вариантах выполнения плотность энергии поддерживается на сравнительно низком уровне, предпочтительно около 10 Вт/см2 или ниже. В других на данный момент предпочтительных вариантах выполнения излучающий участок волокна имеет длину от примерно 1 см до примерно 100 см в соответствии с длиной обрабатываемой вены.
[00026] В некоторых вариантах выполнения способ эндолюминального лечения кровеносного сосуда содержит следующие этапы:
(i) введение волновода, имеющего удлиненную ось, в кровеносный сосуд;
(ii) передача излучения по волноводу и
(iii) выход излучения латерально по отношению к удлиненной оси волновода на отходящий под углом участок окружающей стенки сосуда.
[00027] В некоторых подобных вариантах выполнения этап выхода излучения содержит выход излучения латерально на участок окружающей стенки сосуда, отходящей под углом по меньшей мере 90°. В некоторых подобных вариантах выполнения этап выхода излучения содержит выход излучения латерально на участок окружающей стенки сосуда, отходящей под углом по меньшей мере от 90° до примерно 360°. Некоторые варианты выполнения дополнительно включают этап выхода излучения по существу радиально по отношению к удлиненной оси волновода по существу кольцеобразно на окружающую стенку сосуда. Некоторые варианты выполнения дополнительно включают этап отражения направленного вперед излучения по существу латерально по отношению к удлиненной оси по существу кольцеобразно на окружающую стенку сосуда. Некоторые варианты выполнения дополнительно включают этап передачи излучения мощностью менее примерно 10 Вт при длине волны в пределах от примерно 980 нм до примерно 1900 нм.
[00028] В некоторых вариантах выполнения способ эндолюминального лечения кровеносного сосуда содержит следующие этапы:
(i) введение устройства для подачи энергии, имеющего удлиненную ось, в кровеносный сосуд;
(ii) поддержание примерно постоянного размера кровеносного сосуда до и после введения устройства для подачи энергии в кровеносный сосуд;
(iii) подачу энергии из устройства для подачи энергии латерально по отношению к удлиненной оси устройства к окружающей стенке кровеносного сосуда по существу без изменения формы, уплощения, сжатия или перемещения стенки кровеносного сосуда по направлению к устройству для подачи энергии и
(iv) температурное повреждение кровеносного сосуда.
[00029] В некоторых вариантах выполнения способ эндолюминального лечения кровеносного сосуда содержит следующие этапы:
(i) введение устройства для подачи энергии, имеющего удлиненную ось, в кровеносный сосуд;
(ii) подачу энергии из устройства для подачи энергии к окружающей стенке кровеносного сосуда по существу без изменения формы, уплощения, сжатия или перемещения стенки кровеносного сосуда по направлению к устройству для подачи энергии;
(iii) по существу поглощение поданной энергии внутри стенки кровеносного сосуда и нанесение достаточных для смыкания кровеносного сосуда повреждений внутрисосудистому эндотелию и
(iv) по существу предотвращение переноса поданной энергии уровня, способного нанести температурные повреждения ткани, окружающей кровеносный сосуд, через стенку кровеносного сосуда в такую ткань.
[00030] В некоторых вариантах выполнения способ дополнительно содержит этап подачи энергии в виде лазерного излучения по меньшей мере одной по существу заранее определенной длины волны и по меньшей мере при одной скорости подачи энергии, что приводит по существу к поглощению поданного излучения внутри стенки кровеносного сосуда с целью нанести достаточные повреждения внутрисосудистому эндотелию и заставить кровеносный сосуд сомкнуться, и по существу предотвращает перенос поданной энергии уровня, способного нанести температурные повреждения окружающей ткани, через стенку кровеносного сосуда в указанную ткань.
[00031] В некоторых вариантах выполнения способ эндолюминального лечения кровеносного сосуда содержит следующие этапы:
(i) введение устройства для подачи энергии в кровеносный сосуд;
(ii) подачу заранее определенного количества энергии на единицу длины кровеносного сосуда из устройства для подачи энергии к обрабатываемому участку кровеносного сосуда, где указанное количество энергии достаточно велико для закрытия кровеносного сосуда, но достаточно низко по существу для недопущения необходимости введения анестетика вдоль обрабатываемого участка; и
(iii) температурное повреждение и закрытие кровеносного сосуда.
[00032] В некоторых вариантах выполнения способ эндолюминального лечения варикозных вен содержит следующие этапы:
(i) введение устройства для подачи энергии в варикозную вену;
(ii) подачу заранее определенного количества энергии на единицу длины вены из устройства для подачи энергии в обрабатываемый участок вены, где указанное количество энергии в среднем составляет 30 Дж/см или ниже; и
(iii) температурное повреждение и закрытие вены.
[00033] В некоторых вариантах выполнения устройство содержит крышку, плотно закрепленную на дистальном конце волокна. В некоторых подобных вариантах выполнения дистальный конец волокна содержит плоскую излучающую поверхность, а крышка закрывает излучающую поверхность. В других вариантах выполнения дистальный конец волокна содержит радиально излучающую поверхность, такую как коническая поверхность, и отражающую поверхность, а крышка закрывает как излучающую, так и отражающую поверхности. В некоторых вариантах выполнения крышка выполнена из кварца или другого пропускающего излучение материала, который сплавлен, скреплен посредством связующего или иным способом прочно прикреплен к сердечнику волокна с целью защиты сердечника волокна и его излучающих поверхностей, а также переноса сквозь указанную крышку излучаемого и отражаемого излучения. В других вариантах изобретения крышка выполнена из относительно гибкого прозрачного материала, такого как полимерный тефлон ПФА или тефлон АФ, для получения относительно длинного, гибкого участка излучения. В случае использования относительно низких, поглощаемых длин волны крышка может быть выполнена из непрозрачного материала для того, чтобы преобразовать всю излучаемую энергию или ее часть в тепло. В некоторых вариантах изобретения крышка и/или волокно содержит средства контроля за температурой внутри вены и/или регуляции входной энергии и/или скорости обратного отвода волокна.
[00034] Одним преимуществом настоящих устройств и способов является то, что они могут обеспечить сравнительно быстрое, безопасное, эффективное и/или надежное лечение по сравнению с описанными выше известными способами лечения.
[00035] Еще одно преимущество предпочтительных на данный момент вариантов выполнения изобретения заключается в том, что с их помощью можно добиться по существу равномерной и по существу одинаковой для подачи излучения при сравнительно низких плотностях энергии к стенке вены, тем самым минимизируя риск перфорации вены и, в свою очередь, снижая болевые ощущения после процедуры по сравнению с известными способами лечения.
[00036] Еще одним преимуществом некоторых предпочтительных вариантов выполнения изобретения является то, что они могут обеспечить безопасное и эффективное лечение венозной недостаточности, избегая необходимости применения общей или местной тумесцентной анестезии. В некоторых подобных вариантах выполнения по существу нет необходимости в анестезии вдоль обрабатываемого участка кровеносного сосуда. В других вариантах нет необходимости в общей или местной анестезии и тем более в тумесцентной анестезии.
[00037] Дополнительное преимущество некоторых вариантов выполнения изобретения заключается в том, что они обеспечивают создание устройства и способа для внутрисосудистого лечения путем облучения в множественных, расположенных на равном расстоянии друг от друга местах, а также обширного диффузного излучения.
[00038] Описанные выше, а также иные задачи, свойства и преимущества раскрытых здесь изобретений и/или предпочтительных на данный момент вариантов их выполнения будут разъяснены в нижеследующем подробном описании, изложенном вкупе с приложенными чертежами.
Краткое описание чертежей
[00039] Фиг.1а представляет собой вид в перспективе первого варианта выполнения оптоволокна, содержащего по существу коническую излучающую поверхность на наконечнике оптоволокна, по существу коническую отражающую поверхность, расположенную аксиально на определенном расстоянии от излучающей поверхности и обращенную к ней, и крышку, закрывающую излучающую и отражающую поверхности для достижения эффективного радиального излучения лазерной энергии на 360°.
[00040] Фиг.1b представляет собой частичный боковой вид в вертикальном разрезе оптоволокна, изображенного на фиг.1а, и увеличенный вид его дистального участка.
[00041] Фиг.2а представляет собой частичный вид в перспективе другого варианта выполнения оптоволокна, находящегося внутри кровеносного сосуда.
[00042] Фиг.2b представляет собой частичный боковой вид в вертикальном разрезе оптоволокна, изображенного на фиг.2а.
[00043] Фиг.2b представляет собой вид сзади в вертикальном разрезе оптоволокна, изображенного на фиг.2а, где для простоты удалена часть кровеносного сосуда.
[00044] Фиг.3 представляет собой достаточно схематичную иллюстрацию оптоволокна, изображенного на фиг.1 или 2, помещенного в обрабатываемую вену.
[00045] Фиг.4 представляет собой схематичную диаграмму предпочтительного варианта выполнения устройства, содержащего источник лазерного излучения, оптоволокно, температурный датчик, модуль регулирования мощности и привод обратного отвода, управляемый контроллером скорости обратного отвода.
[00046] Фиг.5 представляет собой частичный вид в перспективе другого варианта выполнения оптоволокна, содержащего защитную кварцевую крышку, сердечник дистального конца оптоволокна с поверхностными пазами, отражающую поверхность и проволочный проводник, прикрепленный к дистальному концу волокна и дистально отходящий от него, а также увеличенный вид прикрепления проволочного проводника к крышке.
[00047] Фиг.6 представляет собой частичный вид в перспективе другого варианта выполнения оптоволокна, содержащего оптоволоконный комплект с прикрепленным к дистальному концу кварцевой защитной крышки проволочным проводником.
[00048] Фиг.7а представляет собой частичный вид в перспективе другого варианта выполнения оптоволокна, где наконечник оптоволокна задает отражающий конус.
[00049] Фиг.7b представляет собой частичный вид в поперечном разрезе наконечника оптоволокна, изображенного на фиг.7а.
[00050] Фиг.8а представляет собой частичный вид в перспективе и поперечном разрезе другого варианта выполнения оптоволокна, включая наконечник оптоволокна с отражающим зазором.
[00051] Фиг.8b представляет собой вид в поперечном разрезе наконечника оптоволокна, изображенного на фиг.8а, и увеличенный вид его части.
[00052] Фиг.9 представляет собой частичный вид в поперечном разрезе другого варианта выполнения оптоволокна, включая внешний рукав, закрепленный с возможностью скольжения на волокне и/или крышке, которая задает внутреннюю отражающую поверхность для предотвращения переноса через него лазерного излучения и управления излучающим участком волокна.
[00053] Фиг.10 представляет собой частичный вид в поперечном разрезе другого варианта выполнения оптоволокна, включая по существу плоскую излучающую поверхность, герметично закрытую защитной, пропускающей излучение крышкой.
[00054] Фиг.11 представляет собой частичный вид в поперечном разрезе другого варианта выполнения оптоволокна, включая по существу плоскую излучающую поверхность, герметично закрытую защитным, пропускающим излучение рукавом.
Подробное описание предпочтительных вариантов выполнения
[00055] Предпочтительные на данный момент варианты выполнения изложены ниже со ссылкой на приложенные чертежи, где сходные числовые обозначения используются для обозначения сходных элементов на различных чертежах. Как описано ниже, предпочтительные на данный момент варианты выполнения обеспечивают создание усовершенствованного способа и устройства для безопасного и эффективного эндолюминального лечения венозной недостаточности при низком уровне плотности энергии. Некоторые предпочтительные на данный момент варианты выполнения также используют радиально направленную, пульсирующую или постоянную энергию из оптоволокна. Для кругового облучения используется конический или почти конический дистальный конец волокна с расположенной напротив конической отражающей поверхностью, закрепленной на дистальном участке крышки. Для обширного радиального облучения могут быть использованы множественные, расположенные на равном или неравном расстоянии друг от друга излучающие пазы, размещенные продольно на конце волокна.
[00056] Еще одним свойством некоторых на данный момент предпочтительных вариантов выполнения является возможность получения обширного участка излучения. Это может быть достигнуто путем соответственного размещения групп противолежащих конусов, через комбинацию различных переменных, т.е. рез под углом конических поверхностей, расстояние между конусами, показатель преломления материала крышки и состав газа, остающегося в промежутке. Дополнительно может быть использован набор различных линз, такой как множество различных линз, расположенных аксиально на определенном расстоянии друг от друга. Кроме того, могут быть использованы слегка усеченные конические наконечники с соответствующими поправками для лучевых рисунков, сформированных на промежуточном участке. Указанные переменные могут быть подогнаны при изменении ширины круглого поперечного сечения обрабатываемого сосуда, а также распределения плотности энергии по длине промежутка. Например, при необходимости можно достичь по существу равномерной плотности энергии на всем поперечном сечении, подвергаемом излучению.
[00057] На фиг.1а и 1b показан первый вариант выполнения оптоволоконного комплекта 100. Оптоволокно 100 содержит покрытие 146, сердечник 140 и кварцевую крышку 106. Наконечник оптоволокна предпочтительно задает по существу коническую излучающую поверхность 110 для достижения радиального излучения на 360°. Предпочтительно по существу коническая отражающая поверхность 112 расположена аксиально по отношению к излучающей поверхности 110 и обращена к ней, для повышения эффективности и спланированного распределения на участке радиального излучения. Из чертежа видно, что излучающая и отражающая поверхности герметично закрыты кварцевой крышкой 106, которая неподвижно закреплена на конце волокна и ограничивает воздушный или газовый промежуток на излучающей поверхности для достижения радиального/кольцевого излучения. Соответствующим образом вследствие углового расположения излучающей поверхности 110 и разницы в показателях преломления между излучающей поверхностью 110 и воздухом или иным газом, расположенным в герметичной крышке 106, лазерное излучение испускается радиально (т.е. поперечно или латерально по отношению к удлиненной оси волокна) и кольцеобразно из волокна напрямую на окружающую стенку сосуда. Предпочтительно излучающая поверхность 110 расположена под острым углом к удлиненной оси волокна, что позволяет осуществлять по существу полное отражение испускаемого излучения латерально по отношению к удлиненной оси волокна. В некоторых вариантах выполнения излучение выпускается латерально и кольцеобразно на окружающую стенку сосуда, а кольцевидный луч излучения проходит через арку (т.е. распространение луча), определенную числовой апертурой волокна. В некоторых вариантах выполнения распространение кольцевидного луча определено углом в пределах от примерно 30° до примерно 40°. В дополнение, примерный центр луча предпочтительно ориентирован на угол в пределах от примерно 70° до примерно 90° относительно удлиненной оси волокна.
[00058] Одним из преимуществ указанной новой конфигурации является то, что по существу все излучение осуществляется радиально, и тем самым значительно повышается эффективность радиального излучения по сравнению с описанными выше известными вариантами. Латерально или радиально излучаемый кольцеобразный луч может иметь значительно меньший объем, чем аксиально или фронтально направленный конический луч, излучаемый, например, плоским волокном с непокрытым наконечником, и таким образом латерально излучаемый луч может более прямо и эффективно облучать стенку сосуда. В дополнение, характеристики излучения могут быть пригнаны к изменяющейся длине кольцеобразного участка кровеносного сосуда или иной обрабатываемой полой анатомической конструкции, а также распределению плотности энергии по длине подобного кольцеобразного участка. Например, в другом варианте выполнения многопазный дистальный конец волокна, имеющий линейное распределение пазов, расположенных аксиально на расстоянии друг от друга, может быть использован для облучения обширного участка линейной арки стенки вены, что, в свою очередь, обеспечивает эффективное лечение при относительно низкой плотности энергии. В предпочтительном варианте выполнения волокно с линейно распределенным многопазным дистальным концом раскачивается вперед-назад или вращается (т.е. примерно в один оборот) во время облучения с целью достижения радиальной стимуляции стенки вены на 360°. В альтернативном варианте пазы могут быть смещены по отношению к волокну, обеспечивая по существу круглый рисунок при обратном отводе или вращениях.
[00059] На фиг.2а, 2b и 2с приведен еще один вариант выполнения оптоволокна 200. Оптоволокно 200 содержит обычный участок 202, проходящий вдоль большей части длины волокна от проксимального конца, который оптически соединен с источником лазера, к испускающему лазерное излучение участку дистального конца 204. Излучающий участок 204 содержит несколько равномерно расположенных пазов, предпочтительно расположенных на расстоянии примерно 1 мм друг от друга, для достижения радиального лазерного излучения 218 вдоль излучающего участка. Каждый паз 208 заставляет часть излучения выходить частично радиально наружу от волокна 218, а оставшееся излучение 216 частично переносится к последующему пазу 208.
[00060] Наконечник оптического волокна 210 может иметь по существу коническую форму для достижения радиального излучения на 360°, а напротив него расположена предпочтительно коническая отражающая поверхность 212, которая, как объяснено выше, повышает эффективность и распределение радиального излучения на 360° путем отражения любой остаточной или направленной вперед передаваемой энергии в радиальном направлении на 360°.
[00061] Излучающий участок 204 волокна 200 закрыт защитной крышкой 206. В одном предпочтительном варианте выполнения, если используемая длина волны хорошо поглощается в целевой ткани 214, защитная крышка 206 выполнена из кварца или иного пропускающего излучение или по существу пропускающего излучение материала (т.е. материала, способного пропускать сквозь себя излучение или значительную его часть), такого как полимерный тефлон АФ или тефлон ПФА, для получения относительно длинного гибкого излучающего участка. В другом предпочтительном варианте выполнения, если используемая длина волны слабо поглощается в целевой ткани 214, защитная крышка 206 выполнена из не пропускающего излучение материала (т.е. материала, поглощающего испускаемое излучение) с целью превратить по существу все или часть радиального излучения в тепло, чтобы нанести температурные повреждения стенке вены. Благодаря этому достигается смыкание вен термическим способом вместо прямого лазерного излучения.
[00062] На фиг.3 приведен еще один вариант выполнения оптоволокна 320, размещенного на заранее определенном месте в вене 314. Из данного чертежа ясно, что благодаря относительно длинному излучающему участку оптоволокна 320 большой участок вены может быть обработан при каждом положении (т.е. вена может быть подвергнута сегментарной абляции). Длина излучающего участка волокна может представлять собой любую желаемую длину, включая помимо прочего длину в пределах от примерно 1 см до примерно 100 см, в пределах от примерно 1 см до примерно 75 см или в пределах от примерно 1 см до примерно 50 см. В конкретном случае, где длина излучающего участка совпадает с длиной обрабатываемого участка вены, можно провести более быструю и более простую обработку, так как может не быть необходимости в контролируемом обратном отводе. В одном подобном варианте выполнения больной участок может быть обработан одновременно по всей длине, а волокно может быть отведено при смыкании стенки вены. В других вариантах выполнения пазы достаточно разнесены (т.е. разнесены в пределах от 1/2 см до 2 см, а в одном варианте выполнения, примерно на 1 см) и проходят вдоль участка волокна достаточной длины с целью обработки всего кровеносного сосуда или его желаемого участка, при которой волокно по существу остается на месте без обратного отвода. В других вариантах выполнения кровеносный сосуд подвергается сегментарной абляции путем обработки выступающих участков последовательно. В одном подобном варианте выполнения волокно удерживается на месте внутри первого участка кровеносного сосуда, а лазер включается для обработки первого участка, затем лазер выключается, а волокно вытягивается назад и помещается внутрь второго участка сосуда, после чего волокно удерживается на месте внутри второго участка кровеносного сосуда, а лазер включается для обработки второго участка; указанные этапы повторяются для обработки любых дополнительных участков кровеносного сосуда, как того требует процедура. В других вариантах выполнения лазер не отключается во время обратного отвода или перемещения от одного участка вены к другому. В других вариантах выполнения волокно удерживается на месте при обработке лазером некоторых участков кровеносного сосуда, и отводится обратно, обрабатывая при этом другие участки кровеносного сосуда.
[00063] Как показано на фиг.4, другой вариант выполнения системы эндолюминальной лазерной абляции содержит источник 424 лазерного излучения, оптоволокно 420, температурный датчик 426, модуль 428 для регулирования мощности и привод 430 для обратного отвода, управляемый контроллером 432 скорости обратного отвода. В ходе обработки, модуль 428 получает значения температуры от температурного датчика 426, предпочтительно термопары, расположенного рядом с целевой тканью. В одном варианте выполнения температурный датчик закреплен на волокне или крышке в непосредственной близости от их излучающей/отражающей поверхностей. Модуль 428 обрабатывает данные, полученные от температурного датчика 426, и посылает ответ как источнику 424, так и контроллеру 432. В одном варианте выполнения модуль 428 высчитывает идеальную или желаемую плотность энергии и скорость обратного отвода, и отсылает эту информацию соответственно контроллеру 428 лазерного излучения и контроллеру 432. Контроллер 432 управляет приводом 430 для отвода волокна по кровеносному сосуду, а источник 424 устанавливает мощность лазера в соответствие с контрольными сигналами, полученными от модуля 428. Одним преимуществом указанных вариантов выполнения является то, что плотность энергии и/или скорость обратного отвода оптоволокна может быть подогнана в ходе процедуры эндолюминального лечения, например, чтобы точно обеспечить закрытие вен, при этом по существу предотвращая возникновение локализованных горячих участков, которые в ином случае могли бы привести к перфорации стенки вены, или по существу предотвращая перегрев вены и/или окружающих тканей, который в ином случае причинял бы пациенту излишнюю боль или дискомфорт. В другом варианте выполнения, с ручным обратным отводом, модуль 428 предлагает лечащему врачу идеальные или необходимые значения плотности энергии и скорости обратного отвода, отображая их на дисплее, что позволяет обеспечить более эффективный ручной обратный отвод. Система и/или компоненты системы мониторинга температуры и контроля за скоростью обратного отвода, а также иные системные переменные могут быть подготовлены и использованы в соответствии с принадлежащей тому же правообладателю патентной заявкой США, №. 11/900,248, поданной 11 сентября 2007 г., озаглавленной "Устройство и способ лечения вен", и патентной заявки США, №11/443,143, поданной 30 мая 2006, озаглавленной "Энергорегулируемое медицинское подкожное облучение", каждая из которых в прямой форме полностью включена в настоящую заявку путем ссылки и является частью настоящего раскрытия.
[00064] В некоторых на данный момент предпочтительных вариантах выполнения используется низкая плотность энергии, например около 10 Вт/см2 или ниже, но и достаточно высокие плотности энергии могут быть поданы к вене на достаточно короткое время, чтобы обеспечить денатурацию коллагенов, сокращение и удаление вены. Это может быть усилено при помощи расширенной излучающей зоны (или участка), а также радиального облучения на 360°, благодаря чему при обратном отводе участки, первично облученные проксимальной стороной излучающего участка, продолжают получать облучение от центральной и дистальной сторон излучающего участка.
[00065] На фиг.5 приведен еще один вариант выполнения оптоволокна 500. Оптоволокно 500 содержит обычный участок 502, проходящий вдоль большей части длины волокна от проксимального конца, который оптически соединен с источником лазера, к испускающему лазерное излучение участку 504 дистального конца. Излучающий участок 504 содержит несколько пазов, расположенных на одинаковом или неодинаковом расстоянии друг от друга с целью достижения радиального лазерного излучения вдоль излучающего участка. Наконечник 510 оптического волокна имеет стандартный дистальный конец под предельным углом, но предпочтительно имеет показанную по существу коническую форму для достижения радиального излучения на 360°, и содержит коническую отражающую поверхность 512, расположенную на расстоянии от излучающей поверхности и обращенную к ней для повышения эффективности радиального излучения путем отражения любой остаточной или направленной вперед передаваемой энергии в радиальном направлении.
[00066] Проволочный проводник 534 прикреплен к кварцевой крышке 506 при помощи механической системы прикрепления/удаления проволочного проводника 536. При введении лечебного комплекта в кровеносный сосуд 514 проволочный проводник 534 остается прикрепленным к оптическому волокну благодаря его проиллюстрированной конфигурации. В месте прикрепления проволочный проводник 534 имеет соответствующую форму в месте 538, благодаря чему система 536 прикрепления предотвращает отделение при проталкивании внутрь, но позволяет отделение при отводе назад, тем самым обеспечивая его извлечение до процедуры или в ее начале. В другом варианте выполнения, проволочный проводник прикреплен при помощи приемлемого в медицине адгезива, например воска орцианоакрилата. Специалисту понятно, что согласно настоящему описанию проволочный проводник может быть прикреплен с использованием различных способов, включая любой из различных адгезивов или прочих механизмов прикрепления, известных сейчас или в будущем. Проволочный проводник может быть отделен после правильного размещения лечебного комплекта внутри кровеносного сосуда путем лазерного излучения, которое смягчает адгезив или снижает степень его связывания. После отделения проволочный проводник 534 удаляется, оставляя закрытое крышкой оптоволокно 500 в правильном положении и готовым к лазерной обработке. В ходе обработки оптоволокно отводится по направлению к месту ввода, сжимая кровеносный сосуд 514 и предпочтительно закрывая его.
[00067] В другом предпочтительном варианте выполнения показанном на фиг.6, оптоволоконный комплект 600 содержит оптоволокно, кварцевую крышку 606 и проволочный проводник 634. Радиальное лазерное излучение осуществляется при помощи множества поверхностных пазов 608 с отражающими поверхностями 610, выполненных на дистальном участке оптического сердечника волокна. В этом случае, проволочный проводник 634 предпочтительно прикреплен к дистальному концу крышки 606. Таким образом оптоволоконный комплект 600 может быть легко введен и проведен через кровеносный сосуд 614 к желаемому месту расположения в один этап без необходимости удаления проволочного проводника 634. После достижения желаемого местоположения, лечащий врач приступает к лазерной обработке, отводя оптоволоконный комплект 600 по направлению к месту ввода, сжимая кровеносный сосуд 614 и предпочтительно закрывая его.
[00068] На фиг.7а и 7b показан еще один вариант выполнения оптоволокна 700. Оптоволокно 700 добивается радиального излучения при помощи отражающего конуса 742, размещенного на наконечнике оптоволокна 700. В данном варианте выполнения отражающий конус 742 определен вогнутой, по существу конической поверхностью. Соответственно, излучение, передаваемое через сердечник волокна 740 радиально испускается на 360° по достижении наконечника волокна. Предпочтительно вогнутая, по существу коническая поверхность конуса 742 имеет острый угол по отношению к удлиненной оси в пределах от примерно 30° до примерно 50°. Как и в случае с другими вариантами выполнения, описанными выше, одним преимуществом указанной новой вогнутой конической формы является то, что с ее помощью достигается эффективное радиальное излучение на 360° на окружающую стенку сосуда.
[00069] На фиг.8а и 8b показан еще один вариант выполнения оптоволокна 800. Оптоволокно 800 обеспечивает радиальное излучение при помощи имеющего коническую форму отражающего зазора, выполненного на наконечнике оптоволокна. Как видно из чертежа, зазор 844 задан выпуклой, по существу конической излучающей поверхностью, выполненной на дистальном конце сердечника волокна 840, и вогнутой, по существу конической поверхностью, которая является достаточно прозрачной для пропуска излучения и расположена аксиально по отношению к излучающей поверхности на некотором расстоянии от нее, формируя посередине зазор 844. В данном варианте выполнения излучение, передаваемое через сердечник волокна 840, радиально испускается по достижении наконечника волокна благодаря различиям в свойствах преломления между воздухом или иным газом внутри зазора 844 и сердечником волокна 840. Соответственно, излучение испускается радиально (т.е. в латеральном направлении по отношению к удлиненной оси волокна) кольцеобразно или окружно на прилегающую окружающую стенку сосуда. Указанная конфигурация с наконечником-диффузером обеспечивает эффективное радиальное излучение на 360°. Как видно из чертежа, между внешней периферией зазора 844 и внешней частью волокна 800 формируется относительно тонкая стенка, используемая для закрытия зазора внутри наконечника волокна и поэтому для поддержания требуемого перехода сердечник-газ в зазоре для обеспечения кольцеобразного радиального лазерного излучения. Как и в случае с другими вариантами выполнения, описанными здесь, указанная новая конфигурация обеспечивает эффективное радиальное излучение на окружающую стенку сосуда. Как видно из чертежа, дистальный наконечник волокна 800 имеет расширенный диаметр, или луковицеобразный участок, который в проиллюстрированном варианте выполнения по существу имеет форму полушария для облегчения передвижения наконечника по кровеносному сосуду. Специалисту понятно, что согласно настоящему описанию, хотя луковицеобразный участок имеет форму полушария, он также может принимать множество различных луковицеобразных и сходных форм и конфигураций, известных сейчас или в будущем.
[00070] В другом варианте выполнения, показанном на фиг.9, крышка 906 волокна 900 частично покрыта рукавом 946, выполненным из отражающего излучение материала. Как показано стрелками на фиг.9, рукав 946 может сдвигаться аксиально по отношению к крышке 906 и волокну 900 с целью управления аксиальной длиной излучающего участка волокна. Как видно из чертежа, рукав 946 может полностью покрывать желаемое количество радиально излучающих пазов 908 или определенную часть дистального излучающего участка. Соответственно одно преимущество варианта выполнения, изображенного на фиг.9, заключается в том, что он позволяет врачу регулировать длину излучающего участка или части волокна. В одном варианте выполнения длина излучающего участка установлена в соответствии с длиной сосуда 914 или его участка, подвергаемого лечению, для выполнения сегментарной абляции подобного участка или участков. В другом варианте выполнения удлиненный излучающий участок отводится назад по вене при обработке, позволяя постепенно обработать один или несколько обрабатываемых участков при помощи по существу всего удлиненного излучающего участка. Если участок вены короче, чем длина излучающего волокна, рукав может быть использован для скрытия излучающего участка, который находится вне вены в ходе облучения. Рукав предпочтительно выполнен из отражающего материала известного специалистам типа, способного выполнять указанную функцию. Даже при использовании идеальных зеркальных поверхностей, отраженный свет будет проходить обратно через волокно таким образом, что некоторая часть излучения будет собрана, часть - рассеяна, и еще часть будет поглощена. Соответственно определенное количество энергии, излученной на пазах, покрытых рукавом, теряется в виде тепла. Тем не менее, так как плотность вовлеченной энергии низка, любое подобное накопление тепла может поддерживаться в ходе лечения эндолюминальной лазерной абляцией в рамках минимально приемлемого значения.
[00071] На фиг.10 приведен еще один вариант выполнения оптоволокна 1100. Оптоволокно 1100 по существу сходно с оптоволокном 100, описанным выше со ссылкой на фиг.1а и 1b, и соответственно, сходные числовые обозначения, которым предшествует обозначение ”11” вместо обозначения ”1”, используются для указания сходных элементов. Главным отличием оптоволокна 1100 от оптоволокна 100 является то, что наконечник оптоволокна задает по существу плоскую излучающую поверхность 1110, герметично закрытую защитной крышкой 1106. Крышка 1106 выполнена из достаточно прозрачного для испускаемого излучения материала, позволяя излучению проходить сквозь крышку и внутрь стенки сосуда. В одном варианте выполнения крышка 1106 выполнена из кварца и прикреплена к сердечнику волокна при помощи адгезива, как описано выше; однако, при необходимости крышка может быть выполнена из любого материала из множества различных материалов и может быть неподвижно закреплена на дистальном конце волокна любым из множества различных способов, известных сейчас или в будущем. Как видно из чертежа, защитная крышка 1106 проходит дистально по отношению к плоской излучающей поверхности 1110 волокна и имеет дистальный конец 1107, который закруглен для облегчения передвижения закрытого крышкой волокна по извилистому кровеносному сосуду. Дистальный конец 1107 крышки 1106 проходит дистально по отношению к плоской излучающей поверхности 1110 волокна на аксиальном расстоянии, которое предпочтительно находится в пределах от примерно 2 до примерно 6 диаметров сердечника волокна, более предпочтительно в пределах от примерно 3 до примерно 5 диаметров сердечника волокна. В проиллюстрированном варианте выполнения дистальный конец 1107 крышки 1106 проходит дистально по отношению к плоской излучающей поверхности 1110 волокна на аксиальном расстоянии, примерно составляющем 4 диаметра сердечника волокна. Как видно из чертежа, защитная крышка 1106 задает внутреннее пространство 1109, проходящее между плоской излучающей поверхностью 1110 и дистальным концом 1107 крышки, что позволяет передаваемому излучению проходить через пространство и стенку крышки, но предотвращает любое соприкосновение между плоской излучающей поверхностью и стенкой кровеносного сосуда и в целом защищает излучающую поверхность волокна. В отличие от оптоволокна 100, описанного выше, оптоволокно 1100 не задает по существу коническую излучающую поверхность или по существу коническую отражающую поверхность. Таким образом, оптоволокно 1100 излучает по существу конический луч вперед или в аксиальном направлении от волокна.
[00072] На фиг.11 приведен еще один вариант выполнения оптоволокна 1200. Оптоволокно 1200 по существу сходно с оптоволокном 1100, описанным выше в связи с фиг.10, и соответственно, сходные числовые обозначения, которым предшествует обозначение ”12” вместо обозначения ”11”, используются для указания сходных элементов. Главным отличием оптоволокна 1200 от оптоволокна 1100 является то, что волокно 1200 содержит открытый защитный рукав 1206 вместо закрытой защитной крышки. Защитный рукав 1206 выполнен из достаточно прозрачного для испускаемого излучения материала, позволяя излучению проходить сквозь рукав и внутрь стенки сосуда. В одном варианте выполнения защитный рукав 1206 выполнен из кварца и прикреплен к сердечнику волокна при помощи адгезива по существу тем же способом, что и защитная крышка, описанная выше; однако при необходимости защитный рукав может быть выполнен из любого материала из множества различных материалов и может быть неподвижно закреплен на дистальном конце волокна любым из множества различных способов, известных сейчас или в будущем. Как видно из чертежа, защитный рукав 1206 проходит дистально по отношению к плоской излучающей поверхности 1210 волокна и задает дистальный конец 1207, который закруглен или изогнут внутрь по направлению к центральной апертуре 1209. Дистальный конец 1207 изогнут внутрь для облегчения передвижения наконечника волокна по кровеносному сосуду. Защитный рукав 1207 проходит дистально по отношению к плоской излучающей поверхности 1210 волокна на аксиальном расстоянии, которое предпочтительно находится в пределах от примерно 2 до примерно 6 диаметров сердечника волокна, более предпочтительно в пределах от примерно 3 до примерно 5 диаметров сердечника волокна. В проиллюстрированном варианте выполнения защитный рукав 1207 проходит дистально по отношению к плоской излучающей поверхности 1210 волокна на аксиальном расстоянии, примерно составляющем 4 диаметра сердечника волокна. В отличие от оптоволокна 100, описанного выше, оптоволокно 1200 не задает по существу коническую излучающую поверхность или по существу коническую отражающую поверхность. Таким образом, оптоволокно 1200 излучает по существу конический луч вперед или в аксиальном направлении от волокна.
[00073] При работе некоторых на данный момент предпочтительных вариантов выполнения оптоволокно или иной волновод сначала вводится в обрабатываемую вену. При необходимости в месте доступа можно ввести местный послойный анестетик, такой как 0,5% раствор лидокаина (предпочтительно без эпинефрина). В одном варианте выполнения в месте доступа вводится примерно 1/2 мл подобного местного анестетика. В месте доступа вводится проводниковая игла, проводимая в вену для получения доступа к вене. Затем, через проводниковую иглу в вену может быть введен проволочный проводник. Затем, стилет-катетер может быть введен по проволочному проводнику в вену. Стилет-катетер может иметь форму любого из множества различных стилет-катетеров, известных сейчас или в будущем, включая короткий стилет-катетер, обеспечивающий доступ к относительно короткому участку вены, прилегающей к месте доступа (например, имеющий длину в менее чем примерно 11 см, или в пределах от примерно 6 см до примерно 11 см), либо более длинный стилет-катетер, который может занимать всю длину обрабатываемой вены. Затем проволочный проводник удаляют через катетер. Затем, через стилет-катетер вводится оптическое волокно, до тех пор, пока излучающий наконечник волокна не будет расположен примерно в 1-1/2 см или на ином желаемом расстоянии ниже сафено-феморального соединения. Наконечник волокна располагается в подходящем начальном месте ниже сафено-феморального соединения при помощи ультразвукового слежения и/или путем передачи красного или иного заметного луча через волокно для того, чтобы визуально отслеживать начальное положение наконечника волокна сквозь кожу.
[00074] Одним преимуществом на данный момент предпочтительных вариантов выполнения является то, что крышка или иной дистальный участок наконечника волокна закруглен, тем самым облегчая введение его через извилистую вену, и устраняя необходимость использования стилет-катетера и проволочного проводника во многих, если не всех, случаях. В предпочтительных вариантах выполнения волокна имеют внешний диаметр в пределах от примерно 1235 мкм до примерно 1365 мкм, крышки имеют внешний диаметр в пределах от примерно 1800 мкм до примерно 2000 мкм, а закругленный дистальный участок крышки определен радиусом в пределах от примерно 900 мкм до примерно 1000 мкм. Соответственно, хотя использование стилет-катетера и проволочного проводника описано выше, указанные этапы могут быть пропущены. В другом варианте, если используется стилет-катетер, он может быть удален из вены до обработки лазером и обратного отвода волокна. Например, если используется длинный стилет-катетер, стилет-катетер может быть отведен назад и выведен из вены до обработки лазером и обратного отвода волокна. Сходным образом, если используется отрывной стилет-катетер, катетер может быть оторван и удален из вены до обработки лазером и обратного отвода волокна. Если используется относительно короткий стилет-катетер, катетер может быть удален из вены, или оставлен в месте доступа во время обработки лазером и обратного отвода.
[00075] Когда наконечник волокна установлен на начальном участке непосредственно ниже сафено-феморального соединения или на другом необходимом начальном участке, включается лазер, излучающий лазерную энергию в кровеносный сосуд. При использовании радиально излучающих волокон, лазерная энергия направлена предпочтительно радиально и кольцеобразно на окружающую стенку кровеносного сосуда. С другой стороны, при использовании плоскоконечных волокон лазерная энергия излучается в виде по существу конического, аксиально направленного луча. При излучении волокно отводится назад по существу с заданной скоростью, основанной на длине волн и мощности, используемой для повреждения или уничтожения достаточного участка внутрисосудистого эндотелия, с целью достижения закрытия сосуда. Предпочтительно энергия на единицу длины, поданная кровеносному сосуду, достаточно высока для того, чтобы закрыть вену, но достаточно низка, чтобы по существу избежать необходимости анестезии по длине обрабатываемого сосуда. В предпочтительных на данный момент вариантах выполнения энергия на единицу длины, доставляемая обрабатываемому участку кровеносного сосуда, в среднем ниже 80 Дж/см, предпочтительно ниже 50 Дж/см, более предпочтительно ниже 40 Дж/см, более предпочтительно ниже 30 Дж/см, более предпочтительно ниже 20 Дж/см и наиболее предпочтительно ниже 10 Дж/см. В некоторых вариантах выполнения энергия на единицу длины, подаваемая обрабатываемому участку кровеносного сосуда, в среднем находится в пределах от примерно 3 Дж/см до примерно 15 Дж/см и предпочтительно находится в пределах от примерно 5 Дж/см до примерно 10 Дж/см. В этих вариантах выполнения и как описано ниже длина волны излучения предпочтительно относительно сильно поглощается водой и относительно слабо поглощается гемоглобином или оксигемоглобином (например, не менее примерно 1064 нм). Одно преимущество подобных заданных уровней энергии и/или длины волны заключается в том, что (i) энергия может быть по существу полностью поглощена стенкой кровеносного сосуда, (ii) внутрисосудистый эндотелий в достаточной степени повреждается для достижения закрытия сосуда и (iii) перенос любого значительного излучения в ткани, окружающие кровеносный сосуд, по существу предотвращается, благодаря чему удается избежать необходимости анестезии вдоль обрабатываемого участка сосуда.
[00076] Также, в предпочтительных на данный момент вариантах изобретения энергия, такая как лазерное излучение, может подаваться на постоянной основе или в виде отдельных импульсов. Было обнаружено, что подача энергии в виде отдельных импульсов может обеспечить подачу на обрабатываемый участок в среднем более высокого количества энергии на единицу длины без использования анестетика на указанном обрабатываемом участке по сравнению с подачей лазерной энергии на постоянной основе (т.е. большее количество пульсирующей энергии может быть поглощено сосудом по сравнению с постоянной энергией, при этом по существу предотвращая перенос значительного количества энергии через стенку сосуда, что могло бы в ином случае повредить окружающие ткани). Кроме того, при в целом равных прочих факторах, чем выше процент времени, когда при подаче пульсирующей энергии цикл работы находится в "выключенном" состоянии, по отношению к "включенному", тем выше может быть энергия на единицу длины, в среднем подаваемая на обрабатываемый участок кровеносного сосуда, по существу не требуя введения анестетика вдоль обрабатываемого участка. В некоторых подобных вариантах выполнения более примерно 1/2 рабочего цикла приходится на "выключенное" состояние и предпочтительно от примерно 1/2 до примерно 2/3 рабочего цикла приходится на "выключенное" состояние. Пульсирование может значительно повысить скорость ослабления излучения в ткани стенки сосуда по сравнению с постоянным излучением, тем самым приводя к меньшей глубине проникновения при определенной скорости подачи энергии (например, Дж/см, в среднем доставляемые внутрисосудистым устройством подачи энергии), чем при отсутствии пульсирования (например, при постоянном излучении). Соответственно, одним преимуществом подачи энергии в виде импульсов является то, что она позволяет обеспечить более высокую скорость подачи энергии и поэтому может обеспечить подачу большего количества энергии на внутрисосудистый эндотелий без использования анестетика вдоль обрабатываемого участка сосуда. Термин "импульсный режим" использован здесь для обозначения любого из возможных способов, известных сейчас или в будущем, для формирования цикла работы энергии, подаваемой кровеносному сосуду (т.е. повторяющегося периода, на протяжении части которого подача энергии активна, и другой части, на протяжении которой подача энергии неактивна), такого как цикл работы лазерного излучения, включая помимо прочего пульсирование, многократно повторяющееся включение и выключение источника энергии, и прерывание луча энергии, например при помощи затвора.
[00077] В некоторых предпочтительных на данный момент вариантах выполнения, длина волны излучения составляет примерно 1470 нм ± примерно 30 нм. В других предпочтительных вариантах выполнения, длина волны излучения составляет примерно 1950 нм ± примерно 30 нм. Другие варианты изобретения используют длину волны излучения в примерно 810 нм, примерно 940 нм, примерно 1064 нм, примерно 1320 нм, примерно 2100 нм, примерно 3000 нм, и примерно 10,000 нм, каждая ± примерно 30 нм. Одним преимуществом длин волны, значительно лучше поглощаемых водой, чем гемоглобином и оксигемоглобином, является то, что подобные длины волны не сильно поглощаются водой, но сильно поглощаются тканью кровеносного сосуда. Соответственно, волны указанных длин обычно по существу проходят сквозь кровь, проходящую между излучающей поверхностью или поверхностями волокна и стенкой сосуда, и, в свою очередь, хорошо поглощаются стенкой сосуда. Волны указанных длин, подаваемые со скоростью ниже заданной скорости подачи энергии, по существу полностью поглощаются тканью стенки кровеносного сосуда для того, чтобы, в свою очередь, повредить или уничтожить внутрисосудистый эндотелий на достаточной для облегчения закрытия кровеносного сосуда глубине. Предпочтительно подобные повреждения внутрисосудистого эндотелия совершаются на глубине в среднем по меньшей мере в примерно 1/3 толщины внутрисосудистого эндотелия, или в среднем в пределах от примерно 1/3 до примерно 2/3 толщины внутрисосудистого эндотелия. В результате волны указанных длин могут легче поглощаться при заданных низких скоростях подачи энергии (т.е. на обрабатываемый участок кровеносного сосуда энергия в среднем подается со скоростью ниже 50 Дж/см, предпочтительно ниже 40 Дж/см, более предпочтительно ниже 30 Дж/см, более предпочтительно ниже 20 Дж/см и наиболее предпочтительно ниже 10 Дж/см), которых не смотря на это оказывается достаточно для повреждения или уничтожения внутрисосудистого эндотелия на достаточной для облегчения закрытия кровеносного сосуда глубине. В дополнение, так как подобное излучение по существу полностью поглощается стенкой кровеносного сосуда, по существу предотвращается нагревание тканей, расположенных рядом или прилегающих к стенке сосуда, благодаря чему процедура может быть проведена по существу без применения анестетика рядом с обрабатываемым участком кровеносного сосуда (например, местный нетумесцентный анестетик может быть введен только в месте доступа, либо лишь в одной или немногих точках на усмотрение врача или по просьбе конкретного пациента). Подобные длины волны предпочтительно выше или равны примерно 1064 нм, и включая помимо прочего примерно 1320 нм, примерно 1470 нм, примерно 1950 нм, примерно 2100 нм, примерно 3000 нм и примерно 10,000 нм, каждая ± примерно 50 нм.
[00078] В некоторых вариантах выполнения длина волны излучения составляет примерно 1470 нм, ± примерно 30 нм, мощность составляет менее примерно 10 Вт, предпочтительно менее примерно 8 Вт, более предпочтительно менее примерно 5 Вт и наиболее предпочтительно в пределах от примерно 1 Вт до примерно 3 Вт. В одном варианте выполнения лазер работает на постоянной основе (хотя импульсный режим может быть использован при необходимости), и лазер отводится назад со скоростью в пределах от примерно 1 сек/см до примерно 20 сек/см, более предпочтительно в пределах от примерно 3 сек/см до примерно 15 сек/см, и наиболее предпочтительно в пределах от примерно 5 сек/см до примерно 10 сек/см. В одном примерном варианте выполнения большая подкожная вена длиной примерно 10 см была закрыта при использовании по существу радиального излучения с длиной волны в примерно 1470 нм, при уровне мощности в примерно 2 Вт, со скоростью обратного отвода примерно 5 сек/см. В этом конкретном примере местный послойный анестетик был введен лишь в месте доступа и не вводился или иначе требовался на протяжении всей остальной процедуры.
[00079] В других примерных вариантах выполнения, несколько других вен (больших подкожных) было закрыто с использованием плоскоконечного волокна, закрытого кварцевой крышкой (см. фиг.10). Излучение имело длину волны в примерно 1470 нм, а энергия, поданная на единицу длины кровеносного сосуда в среднем составляла около 10 Дж/см (т.е. около 1 Вт при скорости обратного отвода в примерно 10 сек/см). В каждом из указанных случаев не использовался местный тумесцентный или общий анестетик. Вместо этого был использован местный послойный анестетик (1/2% лидокаина без эпинефрина) лишь по желанию пациента или по решению врача. В некоторых случаях пациентам не вводили анестетик. В других случаях небольшое количество анестетика было введено в месте доступа. В других случаях, небольшое количество анестетика было введено в месте доступа и рядом с сафено-феморальным соединением. Одной из причин введения небольшого количества подобного местного анестетика на участках, прилегающих к сафено-феморальному соединению, явился тот факт, что диаметр вен на этом участке обычно наибольший, и соответственно, скорость обратного отвода, а также средняя энергия на единицу длины, в среднем подаваемая на кровеносный сосуд, на этом участке могут быть выше, чем на расположенных дистально зонах лечения.
[00080] В других примерных вариантах выполнения несколько различных варикозных вен (больших подкожных) было закрыто с использованием плоскоконечного волокна, закрытого кварцевой крышкой (см. фиг.10). Длина волны поданного излучения составляла около 1470 нм. Первостепенная процедура включала подачу излучения со скоростью в пределах от примерно 20 Дж/см до примерно 30 Дж/см; однако некоторые пациенты получили энергию при меньшей скорости подачи (в пределах от примерно 10 Дж/см до примерно 20 Дж/см), и тем самым поданная энергия на единицу длины была в среднем в пределах в пределах от примерно 10 Дж/см до примерно 30 Дж/см (среднее значение составило около 22 Дж/см). Первостепенная процедура также включала подачу излучения на уровне мощности в примерно 3 Вт в постоянном режиме; однако некоторые пациенты получили излучение мощностью около 3 Вт в импульсном режиме при 50% цикле работы (около 1/2 секунды во включенном виде и около 1/2 секунды в выключенном виде). Диаметр вен составлял от примерно 3 мм до примерно 22 мм (средний диаметр вены составил около 8,2 мм). Все процедуры были выполнены без какой-либо тумесцентной анестезии или общей анестезии и без какого-либо предварительного изменения формы вен или иного их сжатия. Несколько пациентов не получили никакого анестетика, а другие получили сравнительно небольшой объем местного послойного анестетика (1/2% лидокаина без эпинефрина). Из 31 пациента средний объем использованного в ходе всей процедуры местного анестетика составил около 28 мл, а 7 пациентов получили менее 10 мл. В целом считается, что чем меньше скорость подачи энергии, тем меньший объем анестетика требуется или вообще желателен. Кроме того, в целом подача лазерной энергии в импульсном режиме потребовала меньшего объема анестетика, чем подача энергии в постоянном режиме. Во всех случаях анестетик вводился местно по указанию врача или желанию пациента. Послеоперационные результаты через 24 часа показали, что свыше 90% обработанных вен сомкнулись, демонстрируя отличные показатели утолщения стенок вен. Кроме того, послеоперационные гематомы и жалобы на боль практически отсутствовали; отдельные гематомы появились лишь у примерно 5-10% пациентов, в основном в месте доступа в вену; жалобы на послеоперационный дискомфорт были минимальны, лишь небольшое число пациентов использовали обезболивающие (например, аспирин, ацетаминофен и т.п.).
[00081] Соответственно, важным преимуществом предпочтительных на данный момент вариантов выполнения является то, что не требуется ни местная тумесцентная, ни общая анестезия. Как указано выше, во многих случаях может быть использовано лишь небольшое количество местной послойной анестезии на месте доступа в вену, и то если это необходимо. Если во время процедуры пациент испытывает дискомфорт, врач может ввести небольшое количество местного послойного анестетика (например, лидокаина предпочтительно без эпинефрина) в месте или на участке, на котором ощущается дискомфорт. В любом случае требуется не более 1 ампулы (около 50 мл) местного послойного анестетика (например, лидокаина предпочтительно без эпинефрина) в ходе процедуры, и лишь небольшая часть указанной ампулы может понадобиться в зависимости от длины обрабатываемой вены и/или чувствительности пациента к любому дискомфорту, кажущемуся или иначе проявившемуся.
[00082] Некоторые варианты выполнения настоящего изобретения включают введение достаточного количества анестетика рядом с бедренным нервом для достижения сенсорной блокады, но не моторной блокады бедра для анестезии обрабатываемого участка. Одна подобная процедура содержит следующие этапы. Нахождение при помощи ультразвука ветви бедренного нерва между сафено-феморальным соединением и бедренной артерией. Введение при помощи ультразвука определенного количества местного анестетика (например, около 1/2% лидокаина) над нервом в месте, рядом с нервом, но не касаясь его (снаружи от кровеносного сосуда или любой оболочки, окружающей обрабатываемый кровеносный сосуд). Определенное количество местного анестетика достаточно для возникновения сенсорной блокады, но недостаточно для возникновения моторной блокады. В предпочтительных на данный момент вариантах выполнения определенное количество находится в пределах от примерно 10 до примерно 30 см3 примерно 1/2% лидокаина и наиболее предпочтительно в пределах от примерно 15 до примерно 25 см3 примерно 1/2% лидокаина. Объем анестетика может варьироваться в зависимости от степени разбавления (например, концентрации лидокаина в физрастворе или ином растворе). Обычно, если концентрация лидокаина выше, то вводимый объем ниже, и наоборот. Обычно не нужно вводить какой-либо дополнительный анестетик в ходе процедуры; однако при необходимости может быть нанесено небольшое количество местного анестетика в месте доступа, такого как местный анестетик или несколько кубических сантиметров раствора лидокаина. Затем процедура проводится как описано выше, например, игла вводится в вену; короткий стилет-катетер вводится через иглу в вену; волокно с крышкой вводится через стилет-катетер до сафено-феморального соединения; включается лазер и волокно отводится обратно со скоростью в пределах от примерно 20 Дж/см до примерно 30 Дж/см или иначе, как описано здесь.
[00083] Другие варианты выполнения настоящего изобретения включают использование внутривенного способа или "капельницы" для введения в обрабатываемый кровеносный сосуд с целью проведения местной анестезии обрабатываемого участка. Одна подобная процедура содержит этапы, на которых вводится небольшое количество лидокаина на месте доступа с целью анестезии кожи в месте доступа при необходимости (например, несколько кубических сантиметров раствора лидокаина); в месте доступа в обрабатываемый кровеносный сосуд вводится игла; короткий стилет-катетер вводится через иглу в кровеносный сосуд; покрытое рукавом волокно вводится через короткий стилет-катетер, а наконечник покрытого рукавом волокна размещается на начальной месте ниже сафено-феморального соединения; покрытое рукавом волокно может быть обычным "охлаждаемым жидкостью" волокном, позволяющим введение жидкости между рукавом и волокном, и содержащим один или несколько выходных каналов, расположенных проксимально к наконечнику волокна, что обеспечивает капание или иную дозированную подачи жидкости (в данном случае, разбавленного анестетического раствора) в кровеносный сосуд, расположенный проксимально к наконечнику волокна; закапывание разбавленного анестетитческого раствора (например, раствора лидокаина) в кровеносный сосуд, начиная от сафено-феморального соединения или начальной точки ниже сафено-феморального соединения; после начала действия лидокаина, включается лазер, а волокно отводится назад с необходимой скоростью (например, примерно от 20 Дж/см до примерно 30 Дж/см или иной, как описано здесь); выходные каналы для разбавленного анестетика находятся проксимально по отношению к наконечнику волокна, и таким образом анестетик подается на участки кровеносного сосуда непосредственно перед обработкой лазером, благодаря чему обрабатываемый лазером участок сосуда анестезируется перед обработкой.
[00084] Другие варианты выполнения настоящего изобретения включают местную анестезию обрабатываемого участка путем введения местного нетумесцентного анестетика перед введением волокна в кровеносный сосуд. В некоторых подобных вариантах выполнения, небольшое количество разбавленного анестетика (например, 1% раствор лидокаина) вводится на месте доступа, на средней точке кровеносного сосуда (например, на «Hunters Crossing» или рядом с ним) и на сафено-феморальном соединении или рядом с ним, а количество введенного в каждой точке местного анестетика составляет не более, чем примерно 3-5 мл, а общее введенное количество не превышает примерно 9-15 мл.
[00085] В других вариантах выполнения любые из множества других способов лечения, известных сейчас или в будущем, могут быть использованы для расслабления пациента и/или обезболивания, анестезии и/или снижения чувствительности к болевым раздражителям. Подобные способы включают помимо прочего электроанальгезию, электроанестезию, нейростимуляцию, нейромодуляцию и иные физические или вербальные способы обезболивания, анестезии и/или снижения чувствительности к болевым раздражителям. Другие подобные способы включают обезболивание электрическим током на основе, например, чрескожной или подкожной стимуляции нервов, глубокой стимуляции, стимуляции задней части спинного мозга, и электрическую чрескожную стимуляцию головного мозга. Настоящее описание анестетиков и анальгетиков не подразумевает, что какие-либо анестетики или анальгетики необходимы в связи с раскрытыми устройствами и способами для эндолюминального лечения. Многие предпочтительные варианты выполнения вообще не подразумевают использование какого-либо анестетика или анальгетика или в лучшем случае используют небольшое количество местного анестетика или анальгетика в месте доступа или ином месте, в котором необходимо остановить любую локализованную боль, кажущуюся или иначе проявившуюся у пациента.
[00086] Соответственно, важным преимуществом устройств и процедур, раскрытых здесь, является то, что с их помощью можно избежать описанных выше недостатков, связанных с тумесцентным способом, включая потенциальную токсичность и/или побочные реакции у пациентов, связанные с подобными анестетиками, более частые случаи температурного повреждения окружающих тканей, и послеоперационная боль и гематомы, случающиеся при использовании высоких уровней энергии, применяемых в процедурах по тумесцентному способу. Еще одно преимущество предпочтительных на данный момент вариантов выполнения над известными процедурами по тумесцентному способу заключается в том, что кровеносный сосуд сохраняет примерно прежние размеры до и после введения в него устройства для подачи энергии, а энергия подается на окружающую стенку кровеносного сосуда без предварительного изменения формы, уплощения, сжатия или перемещения стенки кровеносного сосуда по направлению к устройству для подачи энергии.
[00087] Как описано выше, крышка или иная структура на излучающем конце волокна создает закругленный, имеющий по существу относительно большой диаметр, дистальный участок наконечника волокна, тем самым облегчая введение и обратный отвод по вене. Еще одним преимуществом подобной расширенной структуры наконечника волокна по сравнению с известными из уровня техники волокнами с непокрытым наконечником является то, что наконечник замещает больший объем или участок полости вены. Еще одним преимуществом некоторых предпочтительных на данный момент вариантов выполнения является то, что лазерное излучение подается радиально и кольцеобразно от волокна к окружающему кольцеобразному участку стенки вены, тем самым более прямо и эффективно перенося излучение в стенку вены, по сравнению с известными способами и устройствами для эндолюминальной лазерной абляции. Еще одним преимуществом некоторых предпочтительных на данный момент вариантов выполнения является то, что наконечник оптоволокна может иметь значительно большую площадь излучающей поверхности по сравнению с известными непокрытыми наконечниками или иными волокнами с плоской излучающей поверхностью, и кроме того, излучение подается латерально/радиально. В результате, лазерное излучение переносится напрямую на значительно больший участок окружающей ткани стенки вены и благодаря этому может подаваться при значительно более низких значениях плотности энергии по сравнению с известными процедурами эндолюминальной лазерной абляции с целью тем самым значительно облегчить лечение без образования горячих участков, которые могли бы стать причиной перфорации стенок вены, перегрева окружающих тканей и связанных с этим боли и дискомфорта, испытываемых пациентом. Соответственно, еще одним преимуществом предпочтительных на данный момент вариантов выполнения является то, что они могут использовать значительно более низкий уровень мощности по сравнению с известными процедурами эндолюминальной лазерной абляции.
[00088] Еще одно преимущество некоторых предпочтительных на данный момент вариантов выполнения заключается в том, что используемые длины волн лазера хорошо поглощаются водой и поэтому хорошо поглощаются тканью стенок кровеносного сосуда. В результате, лазерное излучение напрямую поступает на окружающий кольцеобразный участок стенки сосуда и поглощается им на достаточную глубину внутрисосудистого эндотелия для уничтожения или повреждения поглощающего эндотелия и, в свою очередь, обеспечивает закрытие кровеносного сосуда. Термины "закрытие кровеносного сосуда", "закрыть кровеносный сосуд", "смыкать кровеносный сосуд" и сходные им термины используются здесь для обозначения закрытия или сжатия кровеносного сосуда, достаточного по существу для предотвращения кровотока по указанному кровеносному сосуду после его обработки. Еще одним преимуществом некоторых предпочтительных на данный момент вариантов выполнения является то, что вследствие того, что лазерное излучение напрямую и эффективно подается на стенку сосуда и поглощается, ей по существу удается избежать значительного поглощения излучения окружающими тканями и последующих температурных повреждений. В результате, предпочтительные на данный момент варианты выполнения не только требуют меньшего количества энергии, чем известные процедуры эндолюминальной лазерной абляции, но также требуют меньшего количества анестетика, или вовсе его не требуют, и позволяют не использовать местную тумесцентную анестезию, с которой связано множество недостатков и проблем.
[00089] При необходимости для охлаждения и/или онемения вены перед обработкой и обратным отводом волокна можно использовать промывание физраствором, например, промывание холодным физраствором. В некоторых подобных вариантах выполнения применяется очень холодный физраствор (например, от примерно 30°F (-1°C) до примерно 40°F (4°C), более предпочтительно от примерно 32°F (0°С) до примерно 35°F (2°C)) для ускорения онемения вены перед лечением. В одном варианте выполнения холодный физраствор подается в вену с помощью стилет-катетера до введения волокна. В другом варианте выполнения холодный физраствор подается в вену с помощью стилет-катетера после введения волокна и/или во время отвода стилет-катетера перед обработкой лазером. В еще одном варианте выполнения холодный физраствор подается в вену с помощью рукава, окружающего волокно во время обработки лазером и обратного отвода волокна. В последнем варианте выполнения холодный физраствор подается через один или несколько выходных каналов, расположенных рядом с излучающим наконечником волокна (например, у основания кварцевой крышки). Один подобный вариант выполнения использует обычный охлажденный жидкостью рукав волокна.
[00090] В некоторых вариантах выполнения к волокну или иному волноводу подается ультразвуковая энергия для обеспечения гладкого обратного отвода по вене либо обратного отвода по существу с постоянной или иной необходимой скоростью. В одном варианте выполнения ультразвуковой преобразователь соединен с проксимальным концом волокна, сообщая ультразвуковые вибрации излучающему наконечнику или участку волокна в ходе обработки лазером и обратного отвода. В другом варианте выполнения ультразвуковой преобразователь или вибратор прикреплен к крышке или иным образом прилегает к излучающему наконечнику или участку волокна, сообщая ему ультразвуковые вибрации в ходе обработки лазером и обратного отвода по вене.
[00091] В некоторых вариантах выполнения настоящего изобретения волокно является медицинским волокном с фторополимерной крышкой или иным устройством для подачи лазерной или световой энергии на волоконной основе с фторополимерной излучающей поверхностью. Одно преимущество фторополимерной излучающей поверхности заключается в том, что она не прилипает к стенке кровеносного сосуда или свернувшейся крови в сосуде, и тем самым ее может быть проще отвести обратно по кровеносному сосуду, чем иные устройства.
[00092] Еще в одном предпочтительном варианте выполнения оптоволоконный комплект снабжен тремя или более раздвижными ручками с эффектом запоминания формы. При введении лечебного комплекта раздвижные ручки постоянно соприкасаются с защитным покрытием. По достижении подходящего положения раздвижные ручки активируются при помощи внутреннего/внешнего источника энергии, раздвигая свои дистальные концы до тех пор, пока не соприкоснутся с внутренней поверхностью кровеносного сосуда. Как следствие, оптоволоконный комплект по существу располагается по центру целевой ткани, дополнительно облегчая по существу равномерное нагревание внутренней поверхности и дополнительно предотвращая соприкосновение со стенкой вены или ее перфорацию. По существу равномерно нагреваемая поверхность должна, в свою очередь, сжиматься более равномерно и эффективно сжимать кровеносный сосуд до достижения полного закрытия, где это необходимо.
[00093] В предпочтительных на данный момент вариантах выполнения длины волн выбраны с целью обеспечить достаточно высокий уровень поглощения целевой тканью, например, около 1470 нм ± около 30 нм и/или около 1950 нм ± около 30 нм. Как будет ясно специалисту, указанные длины волн являются лишь примером, и любые из множества иных длин волн, известных сейчас или в будущем, могут быть использованы в равной мере, включая помимо прочего длины около 810 нм, 940 нм, 980 нм, 1064 нм, 1320 нм, 2100 нм, 3000 нм, и 10,000 нм, каждая ± около 30 нм. Одно преимущество длин волн в 1470 нм и 1950 нм заключается в том, что они хорошо поглощаются водой и поэтому хорошо поглощаются целевой тканью стенок кровеносного сосуда. Поглощение волн длиной в 1470 нм и 1950 нм тканью стенки кровеносного сосуда примерно на 1-3 порядка выше, чем для волн длиной 980 нм, и еще значительно выше для большинства других используемых длин волн.
[00094] Защитные пропускающие излучение крышки согласно предпочтительным на данный момент вариантам выполнения изобретения могут быть изготовлены и прикреплены к волокну в соответствии с принадлежащей тому же правообладателю патентной заявкой США, №11/592,598, поданной 3 ноября 2006, озаглавленной "Оптическое волокно, выполненное с возможностью бокового излучения, для применения в устройствах большой мощности", которая полностью включена в настоящую заявку путем ссылки и является частью настоящего раскрытия. Волокна и прочие компоненты устройств могут быть идентичны или сходны с устройствами, компонентами и различными их аспектами, описанными в принадлежащей тому же правообладателю предварительной патентной заявке США, №61/067,537, поданной 28 февраля 2008 под номером экспресс-почты EB429577158US, озаглавленной "Устройство для быстрой вставки и усовершенствованный способ лазерного лечения сосудов", которая полностью включена в настоящую заявку путем ссылки и является частью настоящего раскрытия.
[00095] Как указано выше, в некоторых предпочтительных вариантах выполнения закрытие стенки кровеносного сосуда достигается путем температурного повреждения или уничтожения в среднем по меньшей мере 1/3 толщины внутрисосудистого эндотелия, или путем температурного повреждения или уничтожения толщины внутрисосудистого эндотелия в среднем в пределах от примерно 1/3 до примерно 2/3 его толщины. Как также указано выше, длины волн, хорошо поглощаемые водой и поданные с заданной скоростью доставки энергии, по существу полностью поглощаются на глубине по меньшей мере около 1/3 либо в пределах от около 1/3 до около 2/3 толщины внутрисосудистого эндотелия с целью, в свою очередь, предотвратить перенос значительного уровня излучения на окружающие ткани и тем самым избежать необходимости применения анестетика вдоль обрабатываемого сосуда. Внутрисосудистый эндотелий может быть поврежден с целью облегчения закрытия кровеносного сосуда при помощи иных механизмов, нежели радиация. Например, патент США №6,402,745, ("патент 745") раскрывает внутривенный электрод-хлыст для абляции вен, полностью включен в настоящую заявку путем ссылки и является частью настоящего раскрытия. Некоторые варианты выполнения патента 745 не доставляют электрическую энергию к внутрисосудистому эндотелию, а другие варианты выполнения доставляют. В соответствии с одним вариантом выполнения настоящего изобретения внутривенное устройство содержит вращающийся хлыст или иное устройство для обдирания или истирания внутрисосудистого эндотелия, как раскрыто, например, в патенте 745, а также основное внутрисосудистое устройство для подачи энергии, которое подает достаточное количество энергии внутрисосудистому эндотелию, что вкупе с обдиранием или истиранием при помощи хлыста или иного устройства в достаточной степени повреждает по меньшей мере около 1/3, до примерно 2/3 глубины эндотелия с целью закрытия кровеносного сосуда. В некоторых подобных вариантах выполнения устройство для подачи энергии является оптическим волноводом, который доставляет излучение с длиной волны, хорошо поглощающейся в воде (т.е. около 1064 нм или выше). В некоторых подобных вариантах выполнения излучение подается импульсным способом, что позволяет обеспечивать относительно высокую скорость подачи энергии по существу без использования какого-либо анестетика вдоль обрабатываемого участка или участков кровеносного сосуда. Обдирание или истирание при помощи хлыста или подобного ему устройства может обеспечить еще более низкую скорость подачи энергии на стенку кровеносного сосуда, позволяя в достаточной степени повредить сосуд, чтобы он закрылся, и не использовать какой-либо анестетик вдоль обрабатываемого участка или участков сосуда.
[00096] Выше описаны различные предпочтительные варианты выполнения настоящего изобретения со ссылкой на приложенные чертежи, однако необходимо понимать, что изобретение не ограничено этими конкретными вариантами выполнения и что различные изменения и модификации могут быть осуществлены специалистами, если указанные изменения не выходят за рамки объема настоящего изобретения, определенного в приложенной формуле изобретения. Например, излучение может подаваться в импульсном или постоянном режиме и может содержать волны одной или нескольких длин. Дополнительно, излучение может подаваться устройствами, отличными от лазеров, включая помимо прочего светодиоды и сверхлюминесцентные светодиоды. Дополнительно, оптоволокна могут иметь форму любого из множества различных типов оптоволокна или волноводов, известных сейчас или в будущем, которые могут иметь любой из множества различных сердечников, покрытий, кожухов, конечных крышек, защитных рукавов, отражающих поверхностей и/или различных линз, известных сейчас или в будущем. Например, хотя многие волокна, описанные здесь, являются покрытыми, могут использоваться и волокна без крышек, включая волокна с непокрытыми наконечниками. Далее, излучающие поверхности могут принимать любые из множества различных форм и конфигураций, известных сейчас или в будущем. Например, хотя определенные варианты выполнения используют излучающие поверхности по существу конической формы, с равным успехом могут быть использованы и излучающие поверхности, имеющие иные дугообразные поверхностные контуры (т.е. изогнутые поверхностные контуры), или имеющие недугообразные поверхностные контуры, такие как плоские и/или угловые излучающие поверхности. Дополнительно, способы лечения вен могут использовать любые из множества различных устройств с использованием анестезии или без нее, включая помимо прочего устройства без рукавов или катетеров, или с любыми из множества различных типов рукавов или катетеров, включая помимо прочего короткие, длинные и/или отрывные стилет-катетеры без проволочных проводников или с ними, включая помимо прочего проволочные проводники прикрепленные, отделимые или вообще не прикрепленные к волокну или волноводу. Кроме того, могут быть в равной степени использованы любые формы из множества различных форм энергии и устройств для подачи энергии, известных сейчас или в будущем, для лечения кровеносных сосудов с различными аспектами изобретений, раскрытых здесь. Например, устройство для подачи энергии может иметь форму (i) волновода или оптического волокна, излучающего лазерную энергию, как описано выше; (ii) микроволнового катетера или устройства, излучающего микроволновую энергию; (iii) высокочастотного катетера или устройства, излучающего высокочастотную энергию; (iv) электрического катетера или устройства, излучающего электроэнергию; и (v) ультразвукового катетера или устройства, излучающего ультразвуковую энергию. Соответственно, настоящее подробное описание предпочтительных на данный момент вариантов выполнения изобретения должно восприниматься как иллюстративный пример, не ограниченный изложенными вариантами.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ И УСТРОЙСТВО ЭНДОЛЮМИНАЛЬНОГО ЛЕЧЕНИЯ КРОВЕНОСНОГО СОСУДА | 2012 |
|
RU2526414C2 |
| Устройство для эндолюминального лечения варикозной болезни | 2022 |
|
RU2790759C1 |
| УСТРОЙСТВО ДЛЯ ЭНДОЛЮМИНАЛЬНОГО ЛЕЧЕНИЯ КРОВЕНОСНОГО СОСУДА | 2014 |
|
RU2557888C1 |
| Устройство для эндовенозной лазерной облитерации извитых притоков большой и малой подкожных вен нижних конечностей | 2023 |
|
RU2817685C1 |
| КОМБИНИРОВАННЫЙ ИНСТРУМЕНТ ДЛЯ ЭНДОВАЗАЛЬНОЙ ЛАЗЕРНОЙ ОБЛИТЕРАЦИИ ВЕН | 2017 |
|
RU2648821C1 |
| СПОСОБ ЛАЗЕРНОЙ ОБЛИТЕРАЦИИ ПОВЕРХНОСТНЫХ ИЗВИТЫХ ВЕН | 2021 |
|
RU2806873C2 |
| МЕДИЦИНСКОЕ УСТРОЙСТВО, НАБОР ДЛЯ ЛЕЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ НАРУШЕННЫХ КРОВЕНОСНЫХ СОСУДОВ, ПОЛОСТЕЙ ОРГАНИЗМА И ПРОТОКОВ ОРГАНИЗМА, А ТАКЖЕ СПОСОБ РАЗМЕЩЕНИЯ МЕДИЦИНСКОГО ТЕКУЧЕГО ВЕЩЕСТВА В ОКРУЖАЮЩЕЙ ИХ ТКАНИ | 2015 |
|
RU2712089C2 |
| СПОСОБ ЛЕЧЕНИЯ ВАРИКОЗНОЙ БОЛЕЗНИ НИЖНИХ КОНЕЧНОСТЕЙ С ИСПОЛЬЗОВАНИЕМ ЭНДОВАЗАЛЬНОЙ ЛАЗЕРНОЙ КОАГУЛЯЦИИ ВЕН | 2012 |
|
RU2514337C2 |
| СПОСОБ ЭНДОВАЗАЛЬНОЙ ЛАЗЕРНОЙ ОБЛИТЕРАЦИИ НЕСОСТОЯТЕЛЬНОЙ БОЛЬШОЙ ПОДКОЖНОЙ ВЕНЫ ПРИ ПОСТТРОМБОФЛЕБИТИЧЕСКИХ ИЗМЕНЕНИЯХ И АНАТОМИЧЕСКИ СЛОЖНОМ СТРОЕНИИ ЕЕ УСТЬЯ | 2017 |
|
RU2653639C1 |
| УСТРОЙСТВО ДЛЯ ЛЕЧЕНИЯ ТКАНИ ОРГАНИЗМА | 2019 |
|
RU2759891C1 |
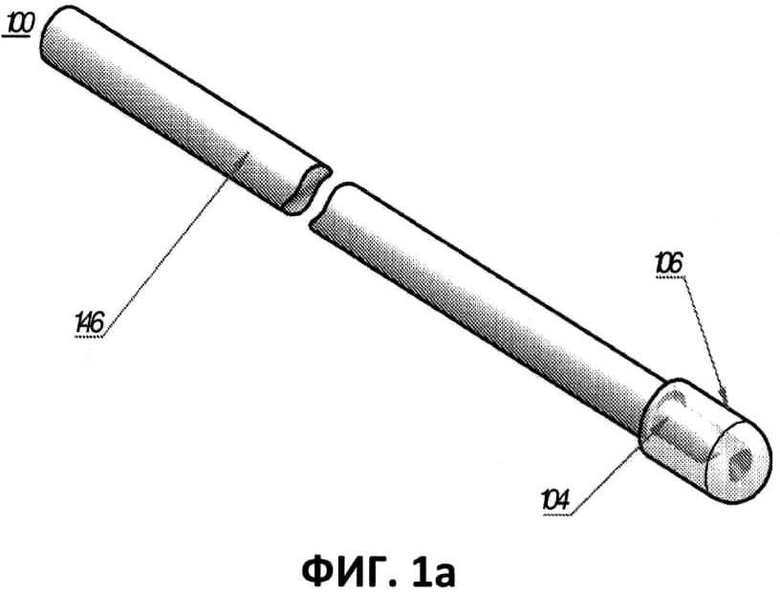
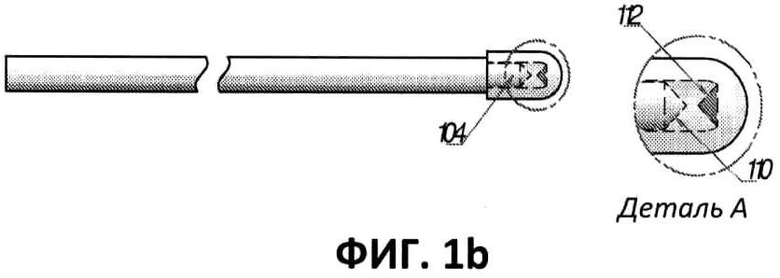
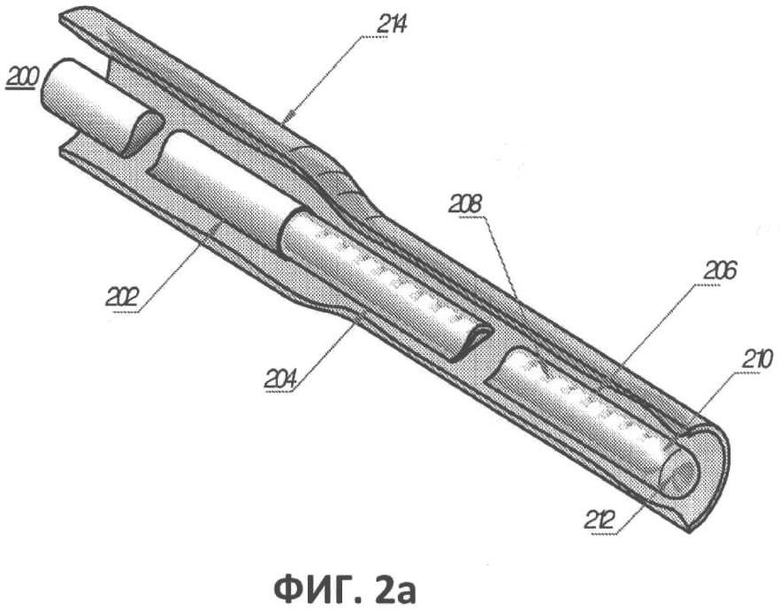
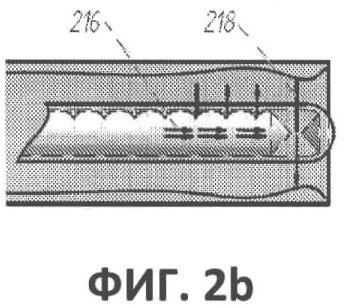
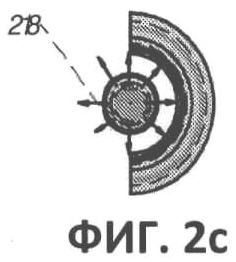
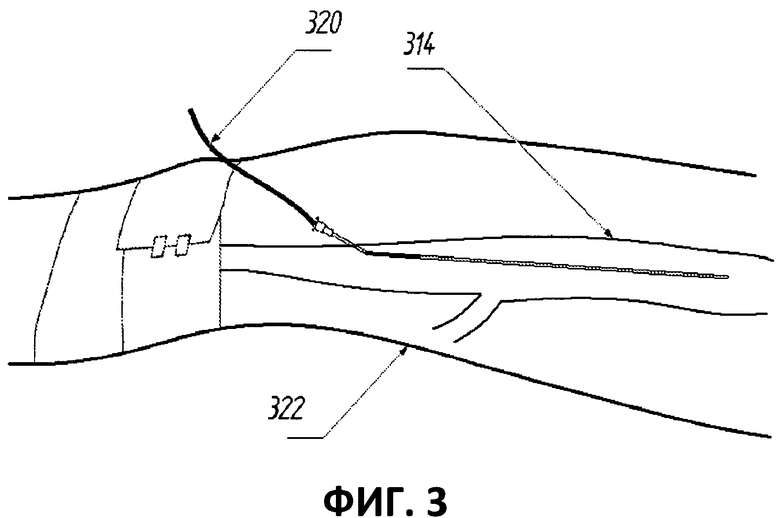
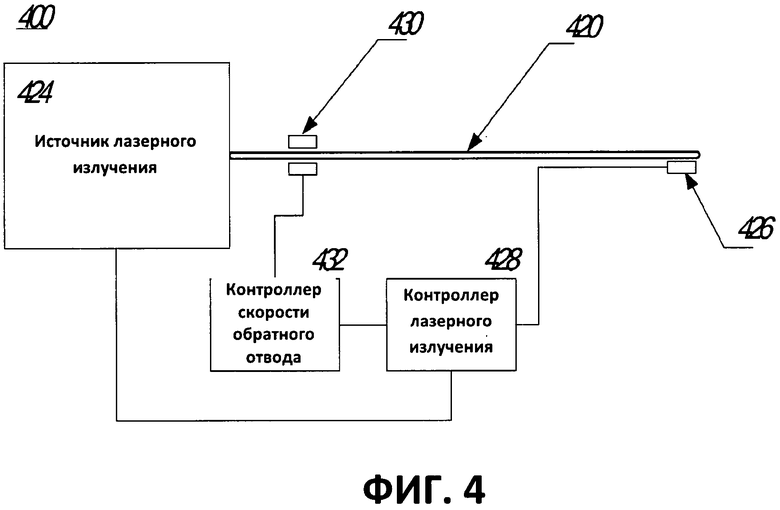
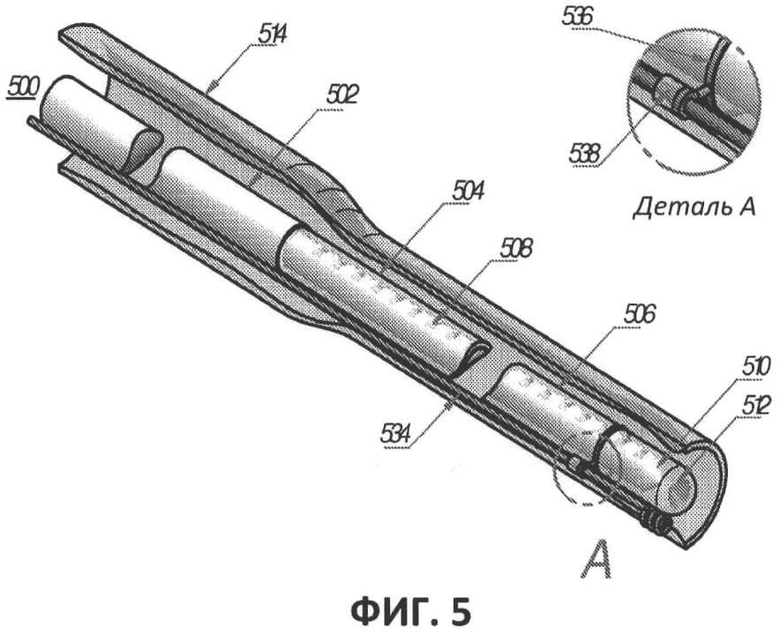
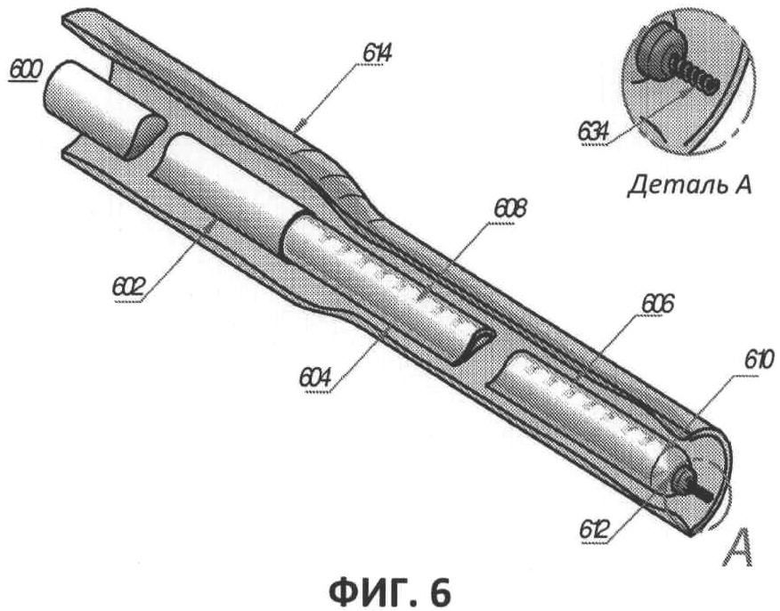
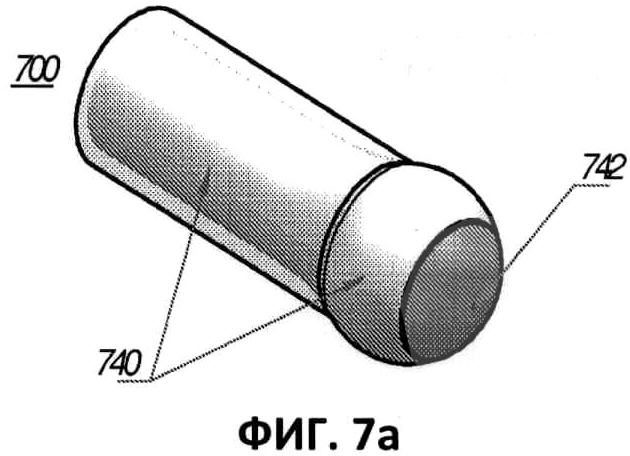
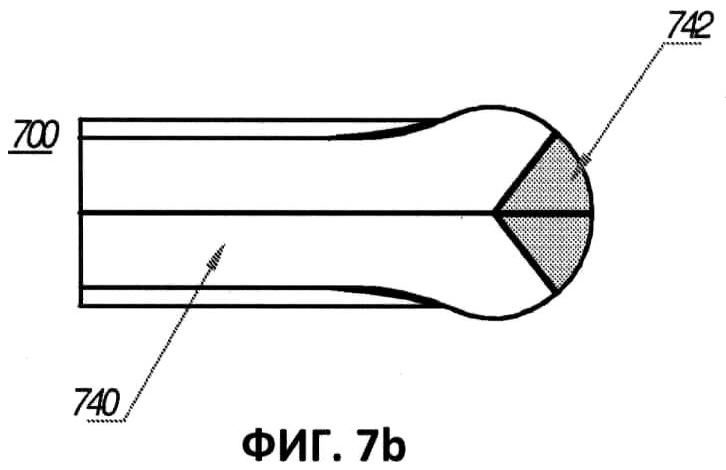
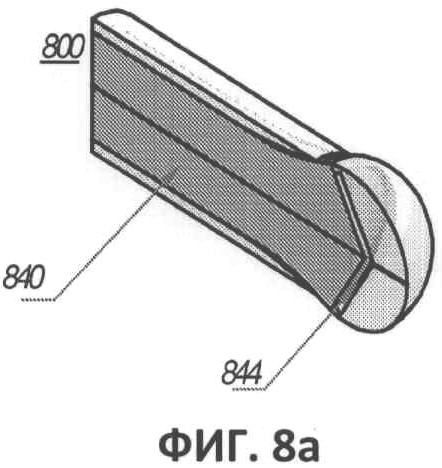
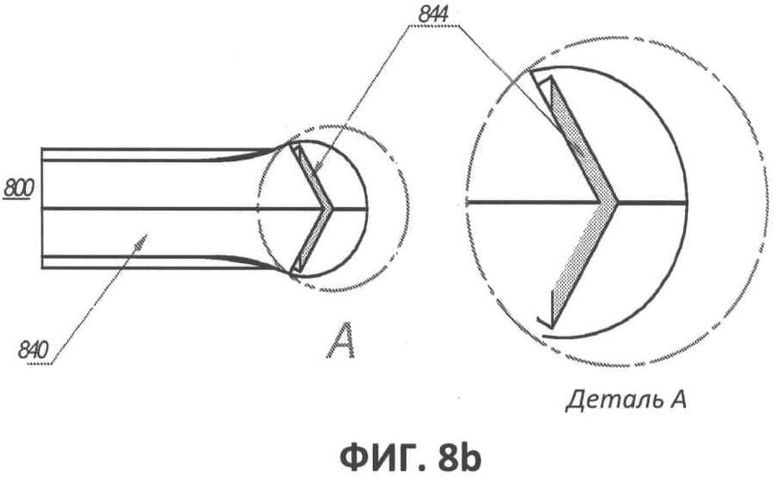
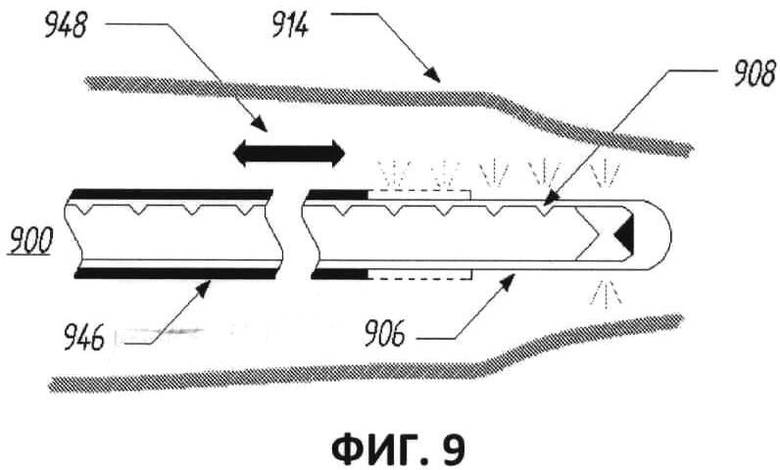
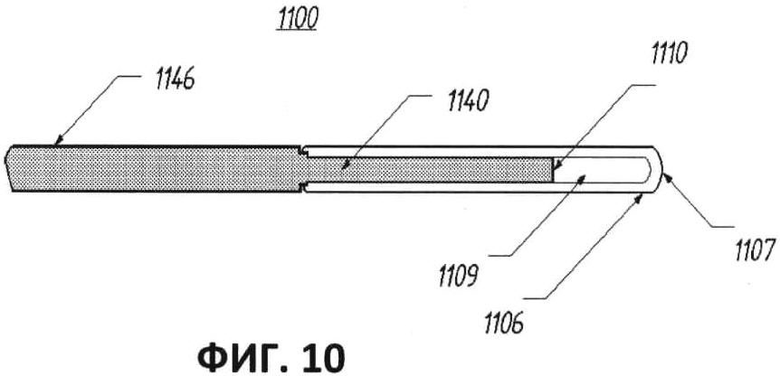
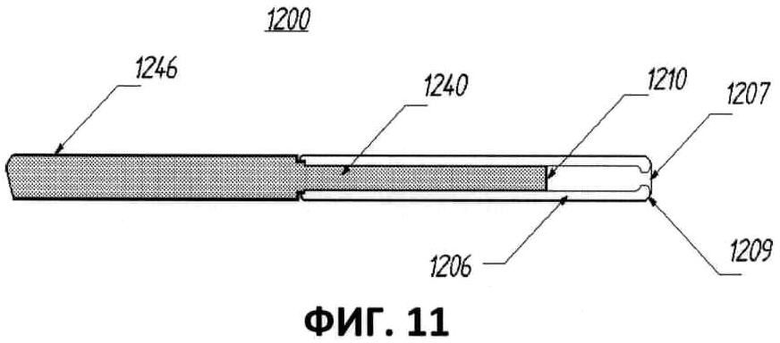
Группа изобретений относится к области медицины. Устройство содержит: гибкий волновод с удлиненной осью, проксимальный конец оптически соединен с источником излучения, дистальный конец выполнен для размещения в кровеносном сосуде и содержит испускающую поверхность, испускающую излучение от источника излучения в сторону по отношению к удлиненной оси волновода на проходящий в угловом диапазоне участок окружающей стенки сосуда, охватывающие средства для охвата испускающих средств и формирования газовой границы раздела для преломления испускаемого излучения в сторону по отношению к удлиненной оси волновода. Вариантом выполнения охватывающего средства является крышка, жестко прикрепленная к волноводу, герметичная по отношению к нему и прозрачная для испускаемого излучения. Способ эндолюминального лечения кровеносного сосуда включает: введение волновода; передачу излучения по волноводу; испускание излучения одновременно в сторону на участок окружающей стенки сосуда, проходящей в угловом диапазоне примерно 360°. Применение данной группы изобретений позволяет расширить арсенал технических средств и повысить безопасность и эффективность эндолюминальной лазерной абляции. 3 н. и 20 з.п. ф-лы, 11 ил.
1. Устройство для эндолюминального лечения кровеносного сосуда, содержащее:
гибкий волновод, имеющий удлиненную ось, проксимальный конец, оптически соединимый с источником излучения, дистальный конец, выполненный с возможностью размещения в кровеносном сосуде и содержащий по меньшей мере одну испускающую поверхность, испускающую излучение от источника излучения в сторону по отношению к удлиненной оси волновода на проходящий в угловом диапазоне участок окружающей стенки сосуда, и крышку, которая жестко прикреплена к волноводу, герметична по отношению к нему, по существу прозрачна для испускаемого излучения, охватывает указанную по меньшей мере одну испускающую поверхность и образует границу раздела газа и волновода, которая преломляет испускаемое излучение в сторону по отношению к удлиненной оси волновода на окружающую стенку сосуда.
2. Устройство по п.1, в котором указанная по меньшей мере одна испускающая поверхность расположена в угловом диапозоне по отношению к удлиненной оси волновода.
3. Устройство по п.2, в котором указанная по меньшей мере одна испускающая поверхность образует изогнутый поверхностный контур и проходит в угловом диапазоне по меньшей мере от примерно 90° до примерно 360°.
4. Устройство по п.2, в котором указанная по меньшей мере одна испускающая поверхность имеет по существу коническую форму и является по существу выпуклой или вогнутой.
5. Устройство по п.1, дополнительно содержащее отражающую поверхность, отстоящую от указанной по меньшей мере одной испускающей поверхности в дистальном направлении и обращенную к ней для отражения направленного вперед излучения в сторону по отношению к удлиненной оси волновода.
6. Устройство по п.5, в котором отражающая поверхность образует изогнутый поверхностный контур, ориентированный под острым углом по отношению к удлиненной оси волновода.
7. Устройство по п.6, в котором отражающая поверхность имеет по существу коническую форму и является по существу выпуклой или вогнутой.
8. Устройство по любому из пп.1-7, дополнительно содержащее отражающую поверхность для отражения излучения, расположенную в крышке, отстоящую от указанной по меньшей мере одной испускающей поверхности и обращенную к ней для отражения направленного вперед излучения в сторону по отношению к удлиненной оси волновода.
9. Устройство по п.1, в котором указанная по меньшей мере одна испускающая поверхность включает первую испускающую поверхность, выполненную на дистальном конце волновода, и вторые испускающие поверхности, расположенные в проксимальном направлении по отношению к первой испускающей поверхности и отстоящие друг от друга в осевом направлении, причем первая и вторые испускающие поверхности образуют испускающий дистальный участок, испускающий излучение в сторону.
10. Устройство по п.9, в котором первая испускающая поверхность имеет по существу коническую форму, каждая из вторых испускающих поверхностей образует изогнутый поверхностный контур, проходящий в угловом диапазоне по отношению к удлиненной оси волновода, и испускает часть излучения, прошедшего по волноводу, в сторону по отношению к удлиненной оси на окружающий изогнутый участок сосуда, и позволяет остальному прошедшему излучению проходить по волноводу и испускания в сторону любой второй испускающей поверхности, расположенной далее в дистальном направлении, и первой испускающей поверхности.
11. Устройство по п.9, дополнительно содержащее крышку, которая проходит в осевом направлении, охватывает указанный испускающий дистальный участок, образует газовую границу раздела на каждой из первой и вторых испускающих поверхностей, герметична по отношению к внешней части волновода, по существу прозрачна для испускаемого излучения, является достаточно гибкой для обеспечения изгиба волновода при его прохождении по извилистому кровеносному сосуду, и взаимодействует с указанным изогнутым поверхностным контуром, проходящим в угловом диапазоне, по меньшей мере первой и вторых испускательных поверхностей для преломления излучения в сторону по отношению к удлиненной оси волновода.
12. Устройство по п.9, дополнительно содержащее рукав, установленный на волноводе с возможностью перемещения и образующий внутреннюю отражающую поверхность для отражения излучения, испускаемого в сторону, внутрь и управления осевой длиной указанного испускающего дистального участка.
13. Устройство по п.1, дополнительно содержащее источник излучения, температурный датчик, термически соединенный с дистальным участком волновода для мониторинга температуры в кровеносном сосуде и передачи сигналов, соответствующих температуре, и управляющий модуль, электрически соединенный с температурным датчиком для регулирования выходной мощности источника излучения, на основании указанного модуля.
14. Устройство по п.13, дополнительно содержащее отводящий привод, соединенный с волноводом с возможностью передачи приводного усилия для управления скоростью отвода волновода, причем управляющий модуль электрически соединен с отводящим приводом для регулирования скорости отвода волновода в зависимости от температуры дистального участка волновода.
15. Устройство по п.1, дополнительно содержащее проволочный проводник, соединенный с волноводом с возможностью отсоединения или жестко закрепленный на нем и включающий дистальный участок, отходящий в дистальном направлении от дистального конца волновода для проведения волновода по кровеносному сосуду.
16. Устройство по п.1, в котором волновод представляет собой оптоволокно.
17. Устройство по п.1, дополнительно содержащее по меньшей мере один лазерный источник, вырабатывающий лазерное излучение по меньшей мере на длине волны примерно 1470 нм или примерно 1950 нм ± примерно 30 нм, мощностью не более 10 Вт, причем проксимальный конец волновода оптически соединен с указанным по меньшей мере одним лазерным источником, а указанная по меньшей мере одна испускающая поверхность волновода испускает излучение в сторону по отношению к удлиненной оси волновода на окружающую стенку сосуда в виде кольцеобразного пятна, проходящего вдоль оси.
18. Устройство по п.17, дополнительно содержащее электрическое отводящее устройство, соединенное с волноводом с возможностью передачи приводного усилия и выполненное с возможностью отвода волновода по кровеносному сосуду с подачей лазерного излучения со средней скоростью подачи энергии на стенку сосуда менее примерно 30 Дж/см.
19. Устройство для эндолюминального лечения кровеносного сосуда, содержащее: гибкий волновод, имеющий удлиненную ось, проксимальный конец, оптически соединимый с источником излучения, дистальный конец, выполненный с возможностью размещения в кровеносном сосуде, и включающий испускающие средства для испускания излучения от источника излучения в сторону по отношению к удлиненной оси волновода на проходящий в угловом диапазоне участок окружающей стенки сосуда, и охватывающие средства для охвата испускающих средств и формирования газовой границы раздела для преломления испускаемого излучения в сторону по отношению к удлиненной оси волновода.
20. Устройство по п.19, дополнительно содержащее отражающие средства для отражения направленного вперед излучения в сторону по отношению к удлиненной оси волновода.
21. Устройство по п.19, дополнительно содержащее диффузные испускающие средства для испускания диффузного излучения в сторону по отношению к удлиненной оси волновода на участок волновода, проходящий вдоль оси.
22. Устройство по п.21, дополнительно содержащее регулирующие средства для регулирования длины диффузных испускающих средств.
23. Способ эндолюминального лечения кровеносного сосуда, включающий:
(i) введение волновода, имеющего удлиненную ось, в кровеносный сосуд;
(ii) передачу излучения по волноводу;
(iii) испускание излучения в сторону по отношению к удлиненной оси волновода на проходящий в угловом диапазоне участок окружающей стенки сосуда, причем испускание излучения включает испускание излучения одновременно в сторону на участок окружающей стенки сосуда, проходящей в угловом диапазоне примерно 360°.
| US 5242438 A, 07.09.1993 | |||
| US 20050015123 A1, 20.01.2005 | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| US 5292320 A1, 08.03.1994 | |||
| US 20030199860 A1, 23.10.2003 | |||
| RU 92008497 A, 20.04.1996. | |||
Авторы
Даты
2014-02-20—Публикация
2009-03-02—Подача