Область техники, к которой относится изобретение
Изобретение относится к области кардиологии и может быть использовано при окислительном стрессе, возникающем при гипоксии и реоксигенации, а также при ишемии и реперфузии сердца.
Уровень техники
Известно использование различных веществ в качестве антигипоксических препаратов.
Так, из литературы известны попытки поддержать синтез АТФ в митохондриях благодаря стимуляции субстратного фосфорилирования посредством добавления к гипоксическому перфузату глутамата и/или аспартата - субстратов цикла Кребса. В серии работ на изолированном сердце было показано, что ферменты цикла Кребса могут продуцировать некоторое количество АТФ даже в полностью аноксических условиях [Penney DG, Cascarano J. Anaerobic rat heart. Effects of glucose and tricarboxylic acid-cycle metabolites on metabolism and physiological performance. Biochem J. 1970; 118(2):221-7]. Добавление глутамата и/или аспартата позволяло поддерживать синтез АТФ, хотя и на значительно сниженном уровне - порядка 7% от нормального, что улучшало восстановление сократительной функции сердца при реоксигенации [Писаренко О.И, Соломатина Е.С, Студнева И.М, Иванов В.Э, Капелько В.И. Эффект экзогенных аминокислот на сократительную функцию и обмен азотистых соединений в аноксическом сердце. Кардиология 1982, 11, 63-67; Писаренко О.И., Соломатина Е.С., Студнева И.М., Иванов В.Э., Капелько В.И. Влияние экзогенной глутаминовой кислоты на анаэробное образование АТФ в мышце сердца. Биохимия 1984, 49, 2019-2025; Pisarenko O.I., Solomatina E.S., Studneva I.M., Ivanov V.E., Kapelko V.I., Smirmov V.N. On the mechanism of the enhanced ATP formation in hypoxic myocardium caused by glutamic acid. Basic Res. Cardiol. 1985, 80, 126-134].
Из литературы известно положительное действие различных антиоксидантов. Возникновение окислительного стресса при реоксигенации обусловлено взрывоподобным образованием активных форм кислорода в митохондриях. Образование активных форм кислорода уменьшалось под влиянием ловушки радикалов - тайрона или ингибиторов ксантиноксидазы или NADPH, что указывает на множественность путей образования свободных радикалов. Также и другой перехватчик свободных радикалов, N-ацилцистеин, существенно уменьшал нарушения сократительной функции после ишемии-реперфузии [Saini-Chohan HK, Dhalla NS. Attenuation of ischemia-reperfusion-induced alterations in intracellular Ca2+in cardiomyocytes from hearts treated with N-acetylcysteine and N-mercaptopropionyl-glycine. Can J Physiol Pharmacol. 2009; 87(12):1110-9.]. Однако тайрон является синтетическим токсичным продуктом и по этой причине не может быть использован в качестве лекарственного препарата, а N-ацилцистеин применяется в высоких дозировках (10-15 мМ), что нерентабельно. Другими, более естественными антиоксидантами являются витамины Е и С, бета-каротин, полифенолы, но попытки их применения в клинической практике не принесли ожидаемых результатов.
Из литературы известен антигипоксический эффект предшественника образования NO-L-аргинина. Добавление его к перфузату изолированного сердца в концентрации 3 мМ улучшало восстановление сократительной функции сердца после реоксигенации с 2 до 12% от исходного уровня (Angelos M.G., Kutala V.K., Torres C.A., He G., Stoner J.D., Mohammad M., Kuppusamy P. Hypoxic reperfusion of the ischemic heart and oxygen radical generation. Am J Physiol Heart Circ Physiol 290: H341-H347, 2006). При этом выяснилось, что эффект достигается только при добавлении аргинина к исходному перфузату, т.е. до гипоксии. Добавление же его в период гипоксии или реоксигенации оказалось неэффективным. В другой работе [Вассаrо С., Bennardini F., Dini G., Franconi F., Giotti A. Cardiac hypoxia and subsequent reoxygenation: sensitivity to L-arginine methylester. Br. J. Pharmac. 1986, 87, 649-656] было показано антиаритмическое действие L-метиларгинина (7,5 мМ), лучше проникающего через мембраны, во время гипоксии и реоксигенации. Эти работы показали определенную значимость оксида азота для уменьшения гипоксического повреждения миокарда, но применение их в миллимолярной концентрации ограничивает их возможное использование в качестве лекарственного препарата.
По результатам анализа патентных документов, к основным тенденциям защиты миокарда от повреждения при гипоксии относятся: применение антиоксидантов общего действия для снижения последствий окислительного стресса; применение блокаторов адренорецепторов для снижения потребности миокарда в кислороде; применение доноров оксида азота, который в умеренных количествах выступает как конкурент супероксида, препятствуя избыточному окислению внутриклеточных и мембранных белков; применение глутатиона и этилглутатиона для повышения уровня глутатионилирования внутриклеточных белков.
В патенте RU 2325915 описан способ предупреждения ишемических и реперфузионных повреждений изолированного сердца с помощью липосом, вводимых в перфузат. Липосомы включают токоферол и содержат антиоксидантные ферменты (супероксиддисмутазу, каталазу) и восстановленный глутатион во внутренней фазе липосом. При этом перфузию проводят ретроградно через аортальную канюлю сначала оксигенированным раствором в течение 15 мин, а затем в течение 1-5 мин перфузируют неоксигенированным раствором с добавкой липосом, причем указанные процедуры проводят 2-5 раз с продолжительностью последующих периодов перфузии оксигенированным раствором 2-10 мин. Применение способа позволяет значительно улучшить восстановление сократительной функции и ритма сердца после длительной тотальной ишемии и реперфузии. Однако действие глутатиона не доказано, так как эффект антиоксидантных ферментов должен заведомо быть сильнее. Кроме того, модель постишемической реперфузии более сложна по сравнению с постгипоксической реоксигенацией (конечные продукты клеточного метаболизма остаются в клетках и еще более нарушают метаболизм).
Патент RU 2096034 раскрывает новый лекарственный препарат - фармацевтическую композицию, индуцирующую биосинтез глутатиона, активность глутатионтрансферазы и оказывающую антитоксическое, радиопротекторное и антигипоксическое действие, а также способы лечения и профилактики гипоксических состояний с ее использованием. Данный препарат предлагается использовать в медицине для повышения резистентности организма посредством избирательной индукции биосинтеза глутатиона и активности глутатионтрансфезы. В качестве действующего вещества композиция содержит эффективное количество смеси L-глутаминовой кислоты, глицина и серосодержащей аминокислоты, выбранной из группы, включающей цистеин, цистин и метионин, при массовом соотношении компонентов 1:1:1. В данном патенте используются три аминокислоты, из которых в клетках синтезируется глутатион. При этом сам глутатион был использован в качестве препарата сравнения, который по результатам исследований не оказывал должного эффекта. В числе примеров в патенте фигурирует и модель создания гипоксии изолированного сердца. Однако при этом авторами представлена информация о повышении содержания глутатиона в печени, но не в миокарде. Кроме того, по мнению авторов, повышенный уровень функции сердца в период гипоксии является положительным аргументом, но это весьма сомнительно, так как при этом расходуются запасы АТФ, что ухудшает восстановление деятельности сердца при реоксигенации. Кроме того, работа проведена на сердцах беременных самок с измененным метаболизмом; такой объект не может считаться адекватным для использования в качестве эталона миокарда.
Патент RU 2255756 раскрывает тетрапептид аланил-глутамил-аспартил-аргинин общей формулы Ala-Glu-Asp-Arg, обладающий биологической активностью, проявляющейся в восстановлении функции миокарда после ишемии (опубликован также как US 2008269141 (A1), WO 2006001728 (A1), ES 2302067 (Т3), ЕР 1758923 (A1), EP 1758923 (В1), EP 1758923 (В8), DE 602004011843 (Т2), АТ 386047 (Т), что свидетельствует о значимости данного технического решения). Изобретение относится к лекарственным средствам для лечения заболеваний сердечно-сосудистой системы и может быть использовано как средство, восстанавливающее функцию миокарда, при лечении различных форм данной патологии. Однако эффективность глутамата и аспартата была показана уже давно в лаборатории РКНПК (1983-1985 гг.), аргинин полезен как предшественник оксида азота.
В патентах RU 2011142254 и RU 2441873 использованы биядерные катионные нитрозильные комплексы железа, к которым в качестве действующего вещества присоединены антиметаболиты пуриновых оснований ДНК для подавления синтеза ДНК, или природные алифатические тиолилы, действие которых реализуется через апоптоз и цитотоксичность. В связи с чем, данные комплексы предлагается использовать в качестве противоопухолевых средств. Однако такое применение стоит далеко от задачи данного изобретения.
Наиболее близким по сути аналогом (прототипом) является патент RU 2438698 (МПК: А61К 38/28, А61К 33/14, А61К 31/7004, А61К 31/194, А61К 31/295, А61Р 9/00, Статус: по данным на 06.07.2012 - действует, приоритет 12.05.2010, Заявитель - Федеральное государственное учреждение "Российский кардиологический научно-производственный комплекс" Министерства здравоохранения и социального развития Российской Федерации (ФГУ "РКНПК" Минздравсоцразвития России) (RU), Российская Федерация в лице Министерства образования и науки Российской Федерации (Минобрнауки России). В патенте раскрыта ВОДОРАСТВОРИМАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СВОЙСТВАМИ КАРДИОПРОТЕКТОРА, которая может быть использована в качестве лекарственного средства при инфаркте миокарда и операциях на сердце в условиях искусственного кровообращения. Водорастворимая композиция для внутривенного введения содержит ингредиенты при следующем соотношении, мас.%: D-глюкоза 23,40-28,60, калия хлорид 0,14-0,16, калиевая соль L-аспарагиновой кислоты 0,81-0,99, полумагниевая соль L-аспарагиновой кислоты (магния L-аспарагинат) 0,72-0,88, инсулин человеческий генно-инженерный (в МЕ/л) 54,00-66,00, динитрозильный комплекс железа (II) (ДНЖК) с глутатионом 0,19-0,23, вода для инъекций остальное, при этом pH раствора 7,4±0,1 при 22°С. Применение композиции обеспечивает ограничение размеров инфаркта миокарда, восстановление метаболического состояния сердца при реперфузии, снижает повреждения мембран постишемических кардиомиоцитов при меньших нарушениях гемодинамики по сравнению с традиционно использующимися препаратами.
Однако известная из RU 2438698 композиция представляет собой сложную смесь, в которой помимо ДНКЖ присутствуют калиевые и магниевые соли аспарагиновой кислоты, а также инсулин; эти компоненты, как показано ранее (например, смесь ГИК - глюкоза, инсулин, калий, а также соли аспарагиновой кислоты), обладают самостоятельным защитным действием на ишемический миокард, поэтому вклад собственно ДНКЖ трудно идентифицировать. В данной работе показано, что под действием этой композиции происходит ограничение размера инфаркта, но совершенно не исследовано функциональное состояние миокарда в данной зоне. Поэтому остается неизвестным, изменяется ли состояние кальций-транспортирующих белков. При этом авторы использовали модель ишемии-реперфузии in vivo, которая помимо гипоксии включает в себя и собственно ишемические последствия - прекращение оттока продуктов метаболизма клеток, что ведет к сильному закислению цитоплазмы, которое само по себе прекращает сократительную активность.
Раскрытие изобретения
Задачей изобретения является создание средства для предупреждения и лечения гипоксического повреждения миокарда, которое было бы более эффективно, чем известные средства для этих целей.
Техническим результатом, на достижение которого направлено заявленное изобретение, является уменьшение гипоксической контрактуры, интенсивности аритмий и улучшение восстановления сократительной функции сердца после реоксигенации.
Данный технический результат обеспечивается созданием биядерной формы динитрозильного комплекса железа с этиловым эфиром глутатиона (ДНКЖ-ЭЭГ) [(EEGS)2Fe2(NO)4] и композиции для уменьшения функциональных нарушений миокарда, подвергнутого гипоксии-реоксигенации, на его основе.
Биядерная форма динитрозильного комплекса железа с этиловым эфиром глутатиона (ДНКЖ-ЭЭГ) формулы [(EEGS)2Fe2(NO)4] имеет структурную формулу:
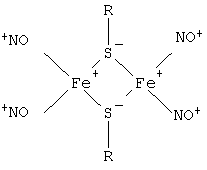
где R-S обозначает этиловый эфир глутатиона, содержащий тиоловую группу.
Анализ научно-технической литературы и патентных документов показывает, что заявляемое нами соединение - динитрозильные комплексы железа с этилглутатионом в качестве лиганда - является оригинальным.
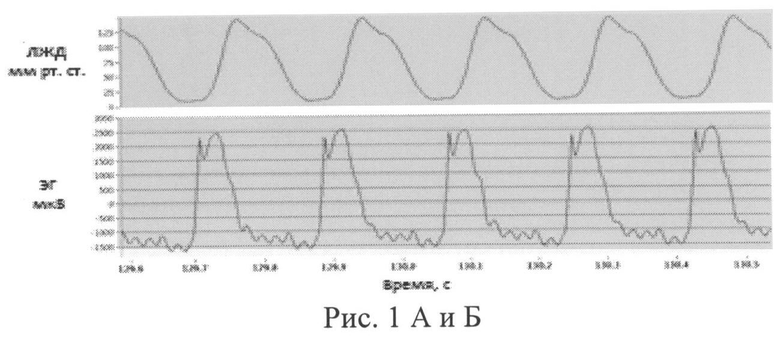
Для исследования свойств композиции и осуществления способа уменьшения функциональных нарушений миокарда, подвергнутого гипоксии-реоксигенации, композиция вносится в гипоксический раствор, который перфузирует изолированное сердце крысы и находится в нем в постоянной концентрации в течение всего периода гипоксии, длящегося 30 минут. В этом периоде наблюдают за ростом диастолического давления в изоволюмическом баллончике, находящемся в полости левого желудочка. Рост давления в нем сигнализирует о развитии гипоксической контрактуры миокарда. Одновременно определяют интенсивность аритмий по ЭКГ - подсчитывают количество экстрасистол, в том числе - приступов желудочковой тахикардии или фибрилляции. Такая же работа проводится и в периоде реоксигенации. В конце реоксигенации измеряют все регистрируемые показатели и определяют степень восстановления сократительной функции по индексу работы сердца, представляющему произведение развиваемого давления и частоты сокращений, по отношению к исходному периоду перед гипоксией. Все полученные данные в группе опытов подвергают статистической обработке и сравнивают с аналогичными результатами, полученными в контрольной группе, т.е. без добавления заявляемой композиции.
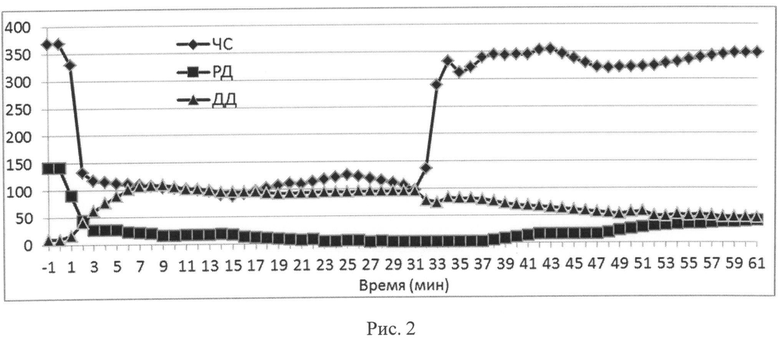
Изобретение поясняется рисунками, где на рис.1 представлена запись сигналов развиваемого давления (А) и ЭКГ (Б), а на рис.2 - общая картина изменения частоты сокращений (ЧС), развиваемого давления (РД) и диастолического давления (ДД) в левом желудочке во время гипоксии и реоксигенации сердца. Величина диастолического давления во время гипоксии характеризует степень гипоксической контрактуры.
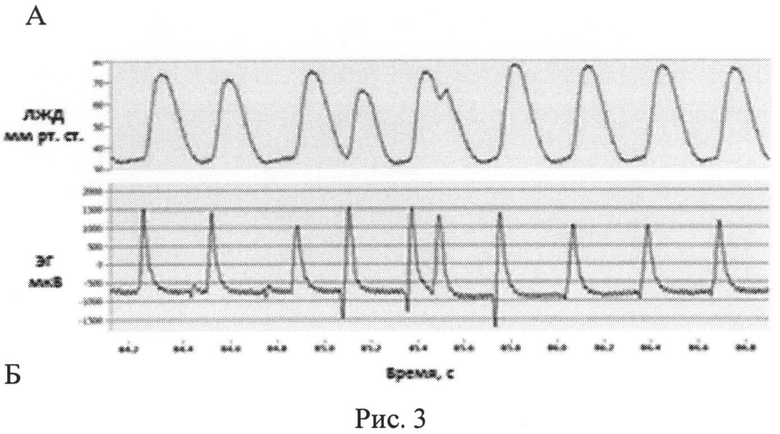
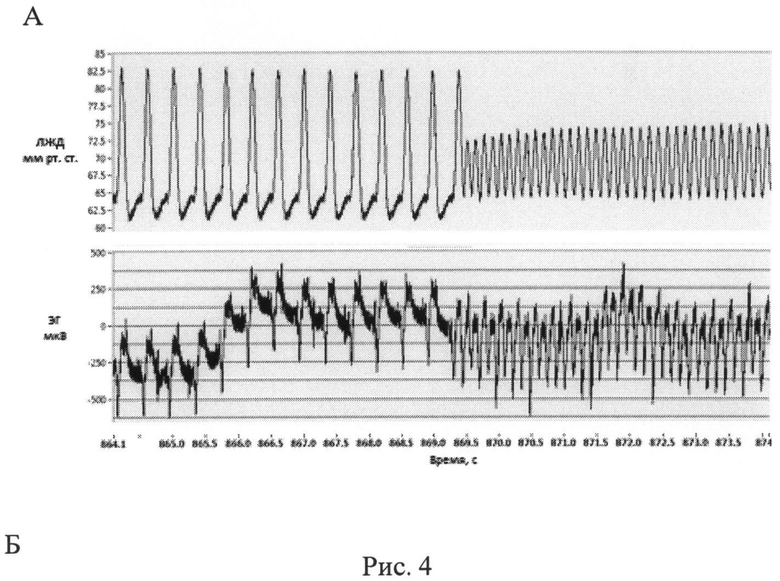
На рис.3 и 4 показаны иллюстрации одиночных экстрасистол (А) и возникновение приступа желудочковой тахикардии (Б).
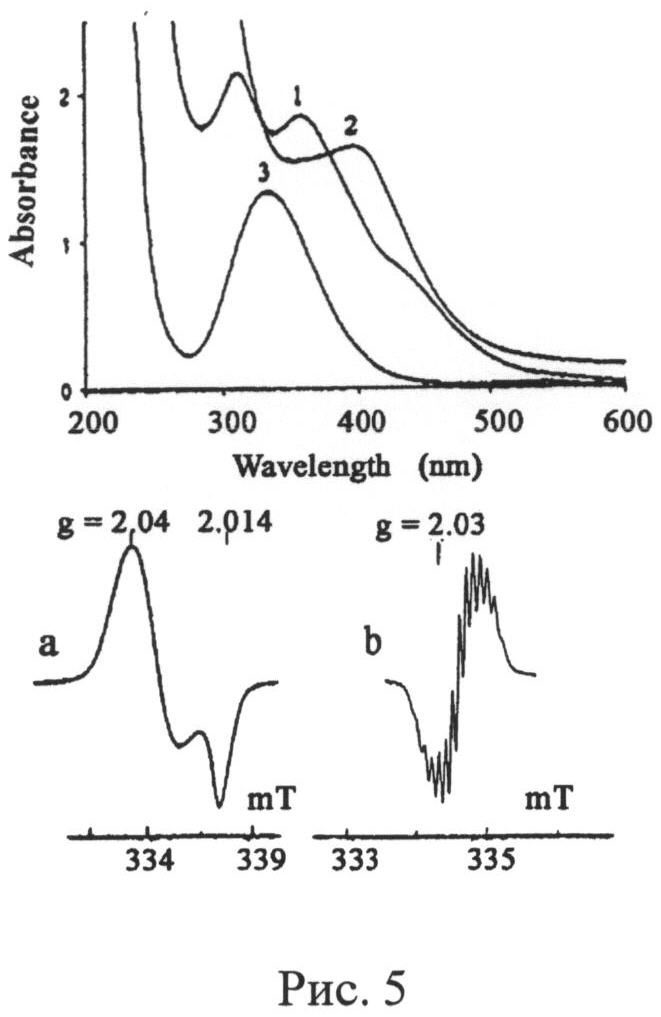
На рис.5: Верхняя панель - спектры поглощения 0,25 мМ раствора Б-ДНКЖ с EEGS при pH 7.2 (спектр 1), 0.4 мМ раствора М-ДНКЖ с EEGS при pH 11,0 (спектр 2) и 1.5 мM раствора EEGS-NO (спектр 3). Нижняя панель - Сигналы ЭПР растворов М-ДНКЖ с EEGS, зарегистрированные при 77К (а) или комнатной температуре (b). Б-ДНКЖ с EEGS синтезирован в соответствии с указанным протоколом B-DNIC и разбавлен в 10 раз дистиллированной водой.
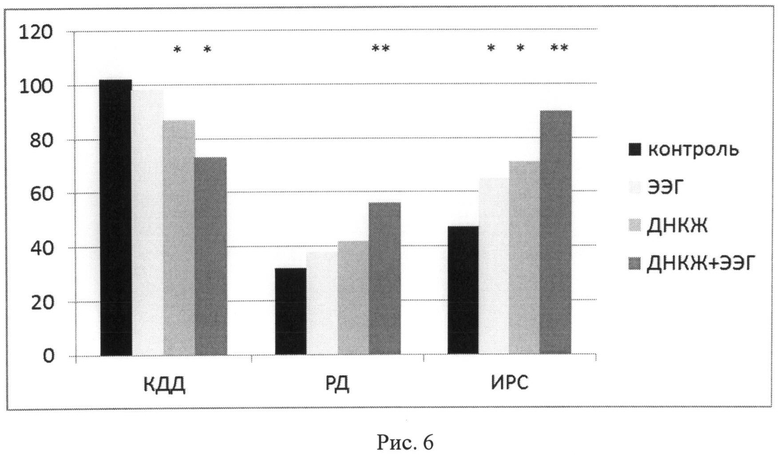
Рис.6: Показатели сократительной функции изолированного сердца после реоксигенации (КДД - максимальная величина диастолического давления при гипоксии, РД - развиваемое давление, ИРС - индекс работы сердца, произведение частоты сокращений на развиваемое давление, оба - в процентах к исходным величинам перед гипоксией). Серии опытов: контроль, ЭЭГ - этиловый эфир глутатиона, ДНКЖ самостоятельно и с этиловым эфиром глутатиона. Звездочками обозначены статистически достоверные различия по сравнению с соответствующим контролем (p<0.05 и p<0.01).
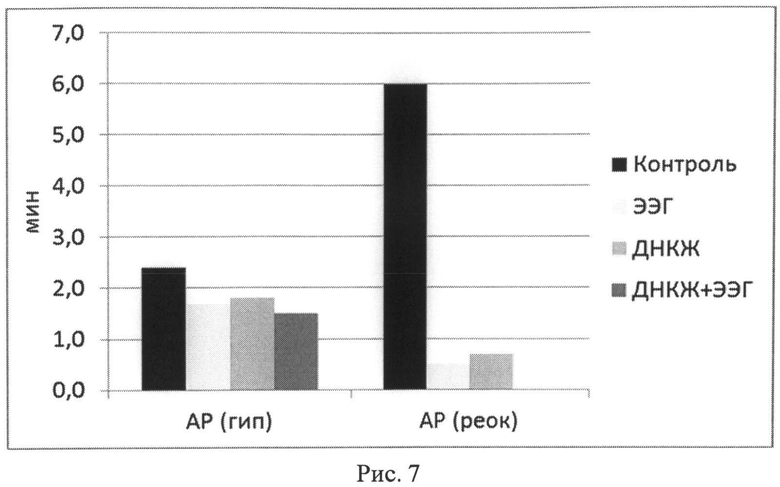
Рис.7: Средняя длительность аритмий изолированного сердца (мин) во время гипоксии (АР, гип) и реоксигенации (АР, реок). Серии опытов: Контроль общий, ЭЭГ - этиловый эфир глутатиона, ДНКЖ самостоятельно и с этиловым эфиром глутатиона. В последней серии аритмий не было вообще.
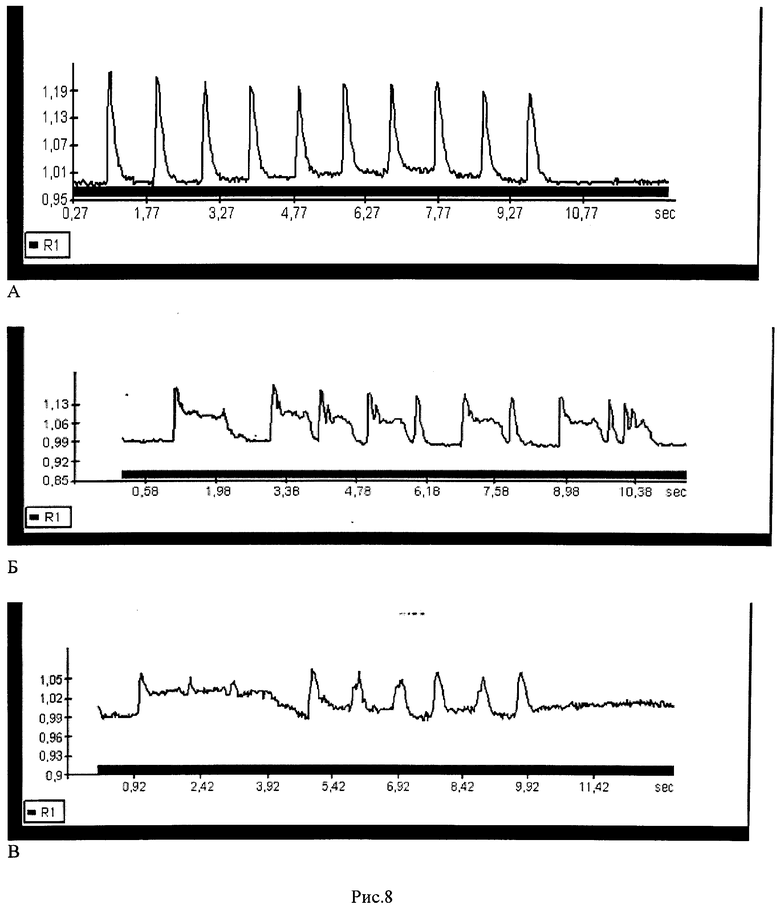
Рис.8: Сравнение динамики содержания свободного внутриклеточного Са2+ в кардиомиоцитах при нормоксии (А), гипоксии (Б) и реоксигенации (В). Показана запись типичного кардиомиоцита. По ординате - изменение интенсивности флуоресценции Са2+ - индикатора Fluo-4 в саркоплазме кардиомиоцита (отн. ед). По абсциссе - время (с). Клетки стимулировали прямоугольными электрическими импульсами с частотой 1 Гц.
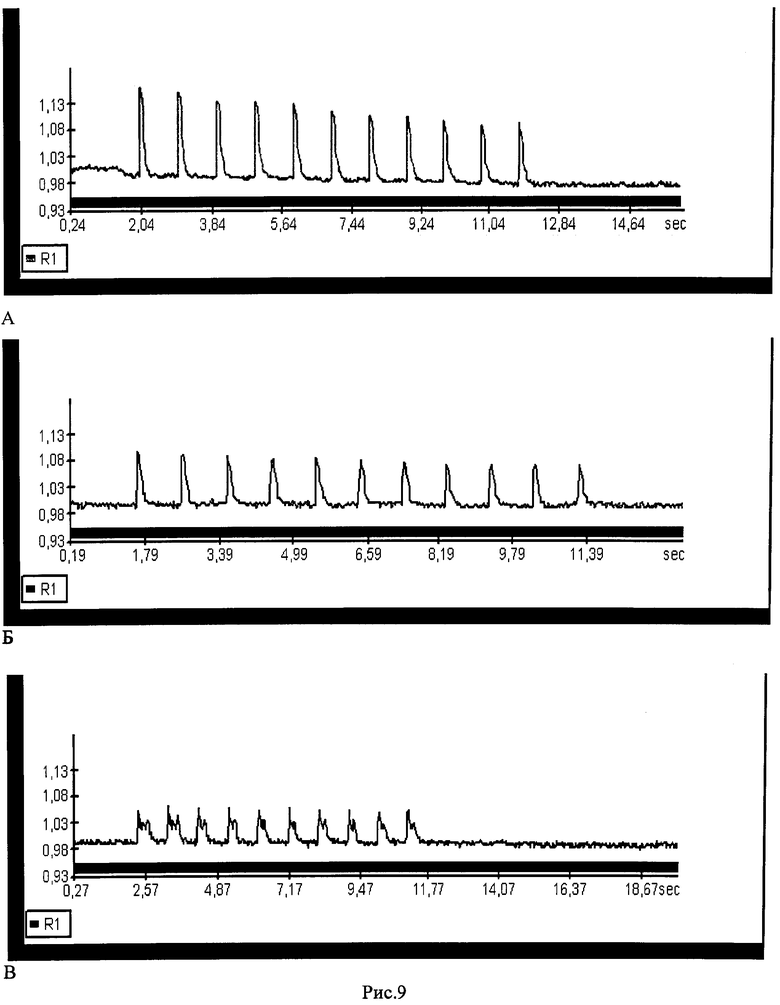
Рис.9: Сравнение динамики содержания свободного внутриклеточного Са2+ в кардиомиоцитах при нормоксии (А), гипоксии 2 мин (Б) и реоксигенации (В) в присутствии этилглутатиона. По ординате - изменение интенсивности флуоресценции Са2+ - индикатора Fluo-4 в саркоплазме кардиомиоцита (отн. ед). По абсциссе - время (сек). Клетки стимулировали прямоугольными электрическими импульсами с частотой 1 Гц. Показана запись типичного кардиомиоцита.
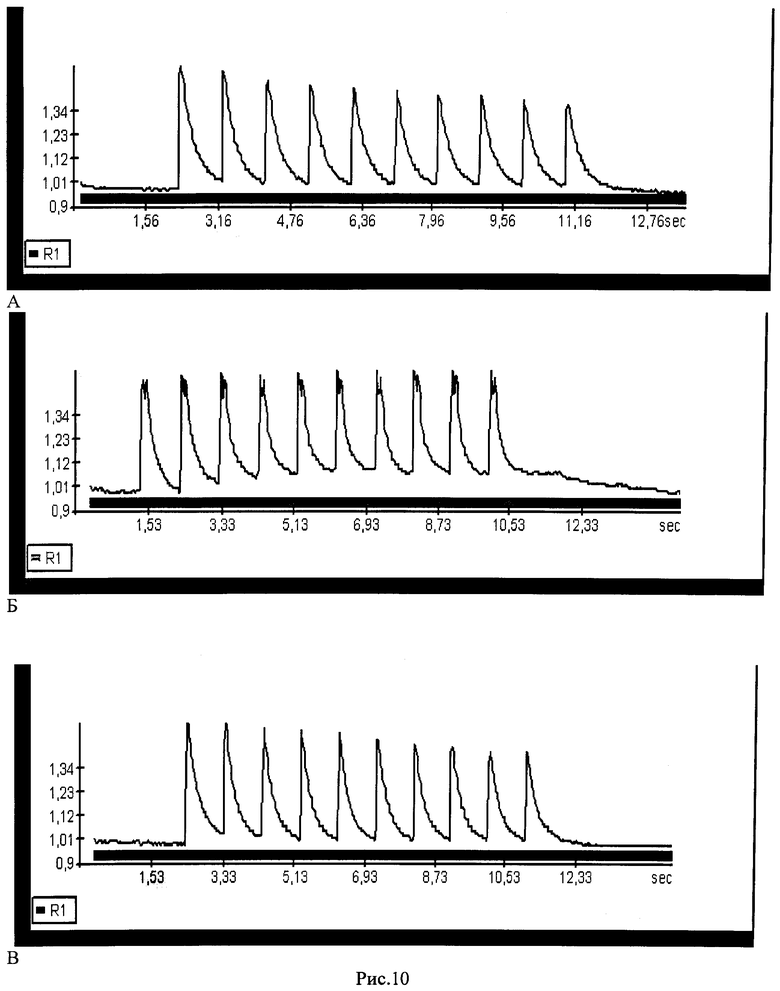
Рис.10: Сравнение динамики колебаний свободного внутриклеточного Са2+ в типичном кардиомиоците при нормоксии (А), гипоксии 2 мин (Б) и реоксигенации 10 мин (В) в присутствии 30 нМ ДНКЖ. По ординате - изменение интенсивности флуоресценции Са2+-индикатора Fluo-4 в саркоплазме кардиомиоцита (отн. ед). По абсциссе - время (сек). Клетки стимулировали прямоугольными электрическими импульсами с частотой 1 Гц.
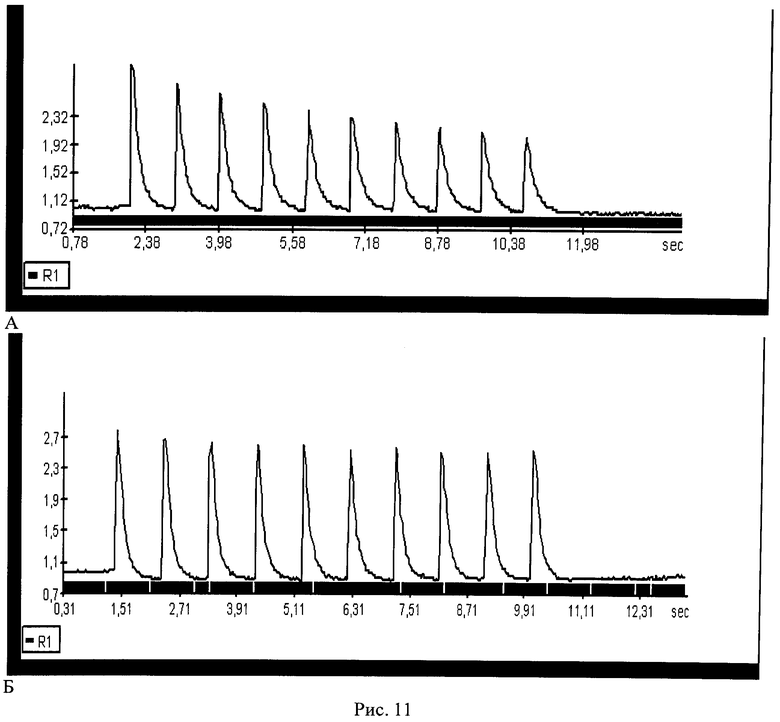
Рис.11. Динамика колебаний свободного внутриклеточного Са2+ в типичном кардиомиоците при нормоксии (А), гипоксии 2 мин (Б) в присутствии 30 нМ ДНКЖ с ЭЭГ.
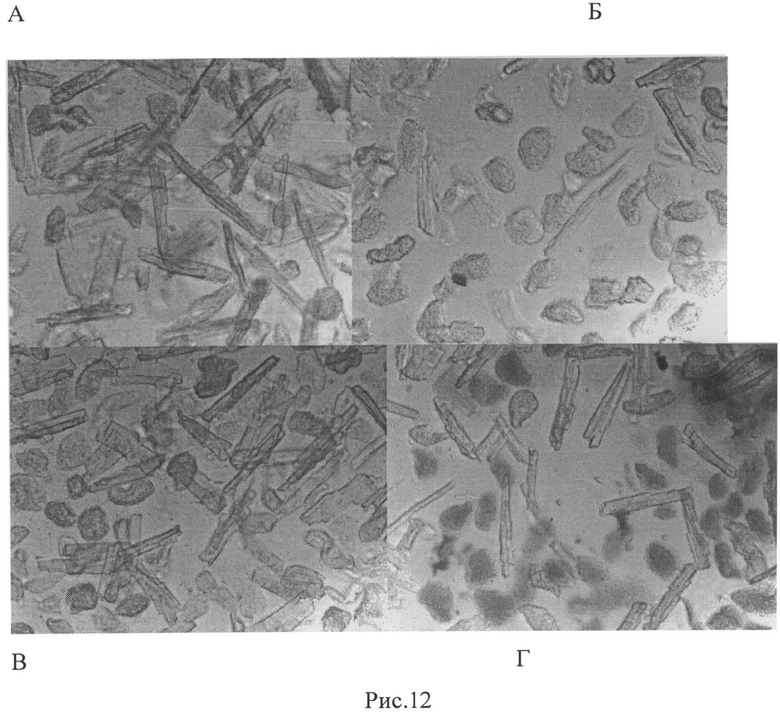
Рис.12. Фазово-контрастная микроскопия свежевыделенных кардиомиоцитов взрослой крысы, подвергнутых гипоксии-реоксигенации в присутствии 1 мМ этиловым эфиром глутатиона (ЭЭГ). А - нормоксия; Б - гипоксия, 2 мин; В - гипоксия 10 мин, в присутствии 1 мМ ЭЭГ; Г - реоксигенация 10 мин в присутствии 1 мМ ЭЭГ. Увеличение ×20.
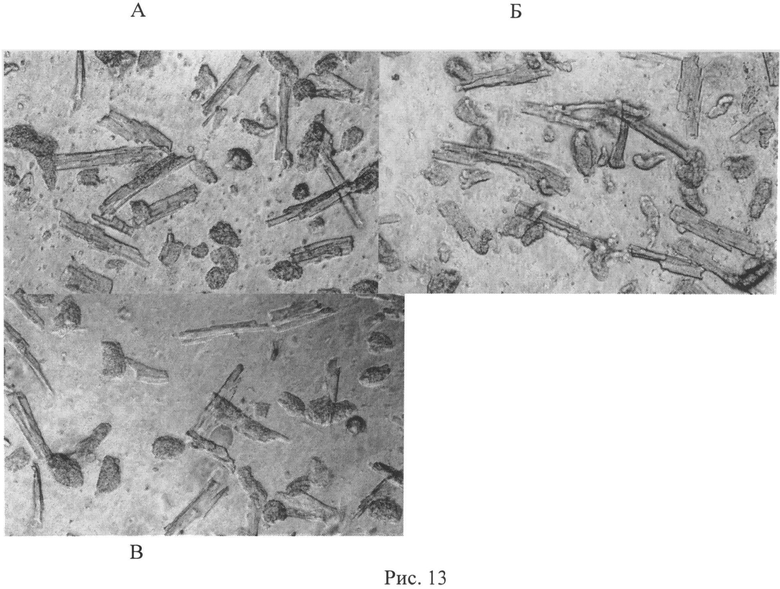
Рис.13. Фазово-контрастная микроскопия свежевыделенных кардиомиоцитов взрослой крысы, подвергнутых гипоксии-реоксигенации в присутствии 30 нМ ДНКЖ. А - нормоксия; Б - гипоксия, 2 мин; В - реоксигенация 10 мин в присутствии 30 нМ ДНКЖ. Увеличение ×20.
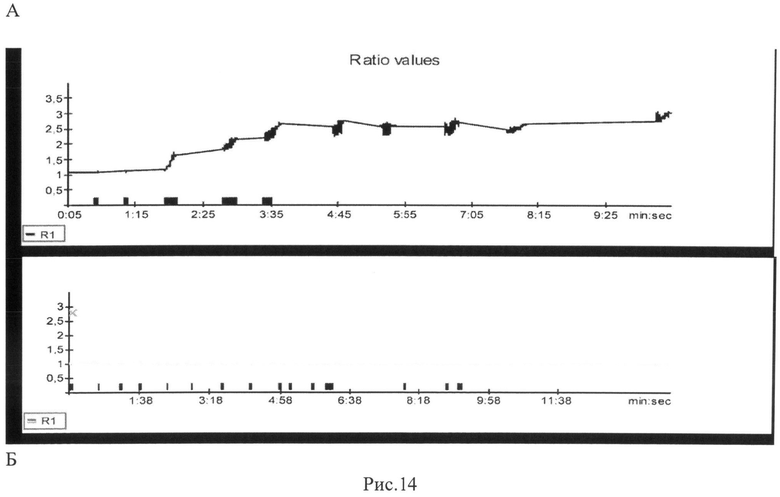
Рис.14. Динамика накопления свободных радикалов в кардиомиоцитах при гипоксии и реоксигенации (А) и электростимуляции оксигенируемых клеток (Б). По ординате - изменение интенсивности флуоресценции DHR в кардиомиоците (отн. ед), по абсциссе - время (сек). Синие маркеры по абсциссе указывают на периоды записи флуоресцентного сигнала, которые также совпадали с периодами электростимуляции, в остальные периоды времени клетки не освещали для избегания чрезмерного выгорания индикатора.
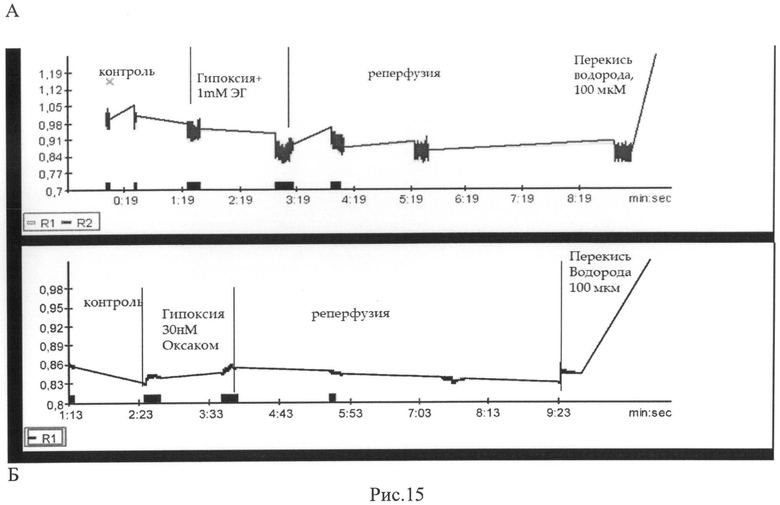
Рис.15. Влияние этилового эфира глутатиона (ЭЭГ, А) и ДНКЖ (Оксаком, Б) на генерацию свободных радикалов в кардиомиоцитах при гипоксии-реоксигенации. По ординате - изменение интенсивности флуоресценции DHR в кардиомиоците (отн. ед), по абсциссе -время (сек). Синие маркеры по абсциссе указывают на периоды записи флуоресцентного сигнала, которые также совпадали с периодами 10-секундной электростимуляции клеток.
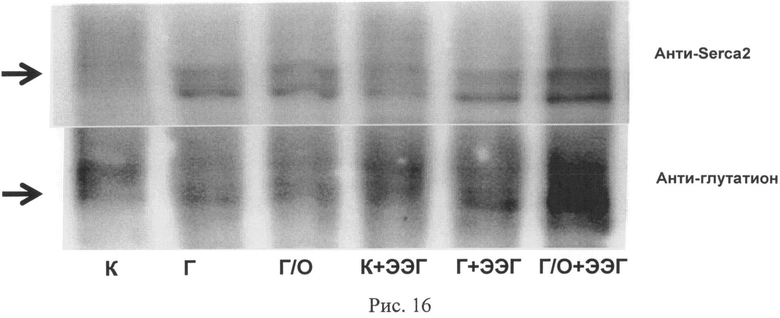
Рис.16. Иммунодетекция степени глутатионилирования Са2+-АТФазы саркоплазматического ретикулума (SERCA2) кардиомиоцитов в контрольных нормоксических условиях (К), при гипоксии (Г), при гипоксии-реоксигенации (Г/О) и при тех же условиях в присутствии 1 мМ этилового эфира глутатиона (ЭЭГ).
Осуществление изобретения
Синтез биядерной формы динитрозильного комплекса железа с этиловым эфиром глутатиона (Б-ДНКЖ-ЭЭГ) (формула [(EEGS)2Fe2(NO)4]) сводился к последовательному добавлению в определенный объем дистиллированной воды этилглутатиона (EEGS), соли сернокислого железа, а затем нитрита натрия при молярном соотношении этих соединений соответственно 2:1:1 с последующим (через определенное время) повышением pH раствора до нейтральных значений. Синтез проводился на воздухе при комнатной температуре.
Синтез использовавшегося в наших опытах 2,5 мМ раствора Б-ДНКЖ-ЭЭГ в 10 мл дистиллированной воды осуществлялся согласно следующему протоколу, включающему три стадии.
Стадия 1 сводилась к получению в растворе S-нитрозотиола EEGS (EEGS-NO). Для достижения этого 66 мг этилового эфира глутатиона EEGS (20 мМ EEGS) добавляли на воздухе к 10 мл дистиллированной воды, помещенной в стеклянную пробирку высотой 15 см с диаметром 1,5 см, в результате чего pH раствора снижался до 4,0. Последующее введение 28 мг FeSO4×7H2O (10 мM) приводило к дальнейшему снижению pH до 3,8. Далее в раствор добавляли при 1 минутном встряхивании пробирки 6,9 мг NaNO2 (10 мМ). При пониженном pH раствора (pH=3,8) добавленный нитрит протонировался с образованием азотистой кислоты, способной S-нитрозировать тиолы, что и приводило к образованию EEGS-NO (10 мМ) по реакции [D.L.H. Williams, Nitrosation Reactions and the Chemistry of Nitric Oxide, (Elsevier, Amsterdam 2004).]:
HNO2+EEGSH=EEGS-NO+H2O.
Образование EEGS-NO сопровождалось появлением розовой окраски раствора. Синтез заканчивался через 1,5-2 часа, о чем можно было судить по увеличению интенсивности полосы оптического поглощения EEGS-NO на 334 нм с коэффициентом экстинкции ε=908 М-1см-1 (Рис.5, верхняя панель, спектр 3). За это время весь нитрит (10 мМ) и 10 мМ EEGS уходили на синтез EEGS-NO. В растворе оставалось 10 мМ свободного EEGS, часть которого (5 мМ) включалась далее в синтез Б-ДНКЖ-ЭЭГ.
На Стадии 2 осуществлялся синтез Б-ДНКЖ-ЭЭГ. Для этого pH раствора повышали до 7,2 добавлением капель 10 мМ раствора NaOH. Повышение pH раствора контролировали, используя стандартный pH-метр (например, UP-5 pH meter (Denver Instrument, Denver, USA). Раствор приобретал оранжево-коричневую окраску, характерную для Б-ДНКЖ-ЭЭГ. Полный синтез этого комплекса заканчивался за 10 и более часов (в течение, например, ночи). Медленное повышение pH при титровании раствора щелочью обеспечивалось буферной емкостью имеющегося в растворе.
На первом этапе синтеза Б-ДНКЖ-ЭЭГ возникала по механизму, показанному на Схеме 1, моноядерная форма ДНКЖ-ЭЭГ (М-ДНКЖ-ЭЭГ - формула [(EEGS)2Fe(NO)2])
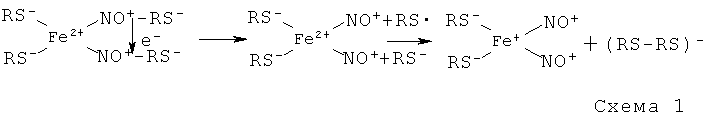
На схемах 1 и 2 литерой RS обозначен этиловый эфир глутатиона, содержащий тиоловую группу.
Далее образующиеся М-ДНКЖ-ЭЭГ превращались в соответствии со схемой 2 в Б-ДНКЖ-ЭЭГ
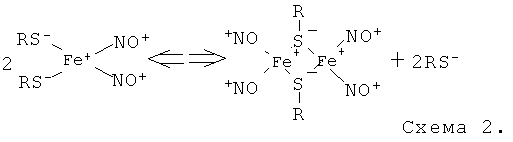
Стадия 3 сводилась к удалению из раствора образовавшегося Б-ДНКЖ ЭЭГ появившихся гидроокисных водонерастворимых комплексов железа (5 мМ), не включившегося в Б-ДНКЖ-ЭЭГ. Для удаления этих комплексов раствор пропускали на воронке через бумажный фильтр.
Концентрацию образующихся Б-ДНКЖ-ЭЭГ определяли оптическим методом по интенсивности полос на 310 или 360 нм с коэффициентами экстинкции соответственно равными ε=9200 и 7400 M-1см-1 [A.F.Vanin, A.P.Poltorakov, V.D.Mikoyan, L.N.Kubrina, D.Sh.Burbaev, Nitric Oxide, Biol. & Chem. 23, 1236-1249 (2010)] в спектре поглощения этих комплексов, приведенных на Рис.5, верхняя панель, спектр 1). В соответствии с этими расчетами, концентрация Б-ДНКЖ-ЭЭГ, полученного в соответствии с описанным протоколом, составляла 2,5 мМ в перечете на Б-ДНКЖ или 5 мМ в пересчете на один атом железа в комплексе. Таким образом, после завершения синтеза этого комплекса из 20 мМ добавленного EEGS в растворе оставалось 5 мМ последнего в свободном состоянии. Из 10 мМ железа 5 мМ включалось в Б-ДНКЖ, остальные 5 мМ удалялись из раствора в виде гидроокисных комплексов.
Полученный Б-ДНКЖ-ЭЭГ представляет собой диамагнитный тиоэфир EEGS и красной соли Руссена. Диамагнетизм этого комплекса определяется спариванием спинов двух Fe(NO)2 групп в Б-ДНКЖ («антиферромагнитным взаимодействием») по двум серным мостикам (по сохранившимся в EEGS тиоловым группам). В полученном препарате Б-ДНКЖ-ЭЭГ имеется небольшая примесь (~5%) М-ДНКЖ-ЭЭГ. Она становится доминирующей при повышении pH раствора до 10-11. При этом исчезает спектр поглощения Б-ДНКЖ и вместо него регистрируется спектр поглощения М-ДНКЖ с полосой на 390 нм (Рис.5, верхняя панель, спектр 2). Этот парамагнитный комплекс характеризуется также сигналом электронного парамагнитного резонанса, имеющим анизотропную форму при его регистрации при 77 К с g⊥=2.04, g||=2.014, gaver.=2.03. При комнатной температуре регистрации он имеет форму симметричного синглета с центром при g=2.03 (Рис.5, нижняя панель, сигналы а, b).
Пример 1. Результаты применения композиции ДНКЖ с этилглутатионом при гипоксии-реоксигенации сердца
Создание пробной партии нового вещества ДНКЖ+ЭЭГ, изложенное в предыдущем разделе, позволило нам выполнить тестовую серию опытов на изолированном сердце и на кардиомиоцитах. При этом новый комплекс применяли в той же концентрации, что и ДНКЖ - 30 нМ. На рис.6 представлены результаты всех трех серий опытов в сравнении с общим контролем.
Результаты свидетельствуют, что как ДНКЖ, так и его комплекс с этилглутатионом достоверно снижали уровень диастолического давления во время гипоксии (гипоксическую контрактуру) на 14-24%, в то время как этилглутатион был неэффективен. Восстановление индекса работы сердца улучшалось в группах этилглутатиона и ДНКЖ по сравнению с контролем только при парном сравнении, в то время как ДНКЖ в комплексе с этилглутатионом достоверно повышал степень восстановления по сравнению с контролем при сравнении всего массива данных более чем в 1,5 раза - с 32±6 в контроле до 56±5%.
На рис.7 приведены результаты аналогичных опытов, в которых анализировали возникновение аритмий в гипоксическом и реоксигенационном периодах. Во время гипоксии средняя длительность аритмий во всех сериях была примерно одинаковой - от 1,5 до 2,5 мин. Но ситуация коренным образом изменилась во время реоксигенации. В контрольных опытах средняя длительность аритмий в опыте составила около 6 мин. Все примененные вещества снижали этот индекс в 6-10 раз, а в опытах с применением ДНКЖ с этилглутатионом аритмии не было ни в одном опыте из 8. Этот результат хорошо согласуется с нашими данными, показавшими, что оба компонента нового комплекса успешно предупреждают рост свободных радикалов кислорода во время реоксигенации.
Таким образом, результаты выполненных опытов на изолированном сердце позволяют считать, что комплекс ДНКЖ с этилглутатионом является более эффективным, чем любой из его компонентов в отдельности. Данный комплекс оказывает защитное действие также в диапазоне 10-100 нМ.
Пример 2. Действие этилглутатиона и ДНКЖ на кальциевый транспорт кардиомиоцитов при гипоксии
Полученные результаты дополнены изучением действия этилглутатиона и ДНКЖ, а также ДНКЖ с ЭЭГ на изолированных кардиомиоцитах. При этом с помощью флуоресцентного индикатора Fluo-4 регистрировали колебания миоплазматического Са++ при электростимуляции. При гипоксии изменяется вид кривой, характеризующей изменение содержания свободного Са2+ в цитоплазме кардиомиоцитов во времени. В нормоксических условиях на каждый электрический стимул приходится один пик подъема концентрации Са2+ (рис.8А). Все пики имеют одинаковую амплитуду и практически симметричную форму. Пики хорошо разрешены, т.е. между стимуляциями клеток уровень Са2+ в них опускается до базального. После 2-минутной гипоксии кардиомиоцитов (Б) наблюдается возникновение «купола» на половине высоты нисходящего плеча, отражающего замедление выведения Са2+ из саркоплазмы в саркоплазматический ретикулум. При этом восходящее плечо (возрастание Са2+ в саркоплазме, отражающее работу Са2+ каналов) изменяется меньше, но амлитуда пиков падает примерно в 1.4 раза.
Также обращает на себя внимание то, что ритм высвобождения Са2+ не воспроизводит ритм электрической стимуляции клеток. Так, на 10 электрических импульсов, стандартно подаваемых в камеру с клетками, происходит только 7 кальциевых ответов. Промежутки между Са2+ пиками также неравномерные, но практически всегда между пиками достигается базальный уровень Са2+. При этом отмечаются флуктуации базального уровня Са2+, достигающие в отдельных случаях половины амплитуды Са2+ пика. Таким образом, в состоянии гипоксии при функциональной нагрузке в кардиомиоцитах нарушается транспорт Са2+,обеспечивающий сократительную активность. Судя по характеру кривых изменения концентрации Са2+, главным образом страдает процесс удаления Са2+ из цитоплазмы, в то время как процесс его поступления в цитоплазму нарушен меньше. Это хорошо согласуется с тем фактом, что удаление Са2+ из цитоплазмы, осуществляемое Са2+-АТФазами сарколеммы и саркоплазматического ретикулума (SERCA), - энергозависимый процесс, который замедляется по причине падения содержания маркоэргов (АТФ и креатинфосфат) в клетке при недостатке кислорода. Реоксигенация (В) не восстанавливает нормальный ритм, несколько пиков остаются затянутыми, удаление Са++ из миоплазмы неполное.
Преинкубация кардиомиоцитов с этилглутатионом в концентрации 1 мМ в условиях нормоксии не сказывается на характере Са2+ пиков при электрической стимуляции (рис.9А). Они возникают в ответ на каждый электрический импульс и остаются симметричными. Длительность пиков составляет около 200 мс. При переводе кардиомиоцитов в гипоксический буфер и инкубации в нем в течение 2 мин в присутствии ЭГ амплитуда, частота и продолжительность Са2+ пиков не изменяются (рис.9Б). Реоксигенация сопровождается восстановлением нормального ритма, хотя амплитуда кальциевых спайков снижена (рис.9В).
Таким образом, присутствие 1 мМ ЭГ не сказывается на динамике свободного внутриклеточного Са2+ в кардиомиоцитах, стимулированных импульсами электрического тока в условиях нормоксии. При этом в гипоксических условиях ЭГ предотвращает/обращает нарушения Са2+ транспорта, воздействуя, вероятно, и на процесс поступления Са2+ в саркоплазму, и на процесс его удаления из нее. Поскольку второй процесс является энергозависимым, его коррекция ЭГ в условиях энергодефицита при гипоксии может определяться повышением эффективности работы Са2+-насосов кардиомиоцитов, в частности, путем поддержания восстановленного состояния их тиоловых групп и/или обратимой их защиты S-глутатионилированием.
Сократительная активность кардиомиоцитов полностью соответствовала параметрам Са2+-транспорта. За каждым пиком подъема Са2+ следовало одиночное сокращение тела клетки. Амплитуда Са2+ пиков была прямо пропорциональна степени укорочения кардиомиоцитов. Растянутые Са2+ - пики в условиях гипоксии сопровождались таким же длительным сокращением клеток. Таким образом, влияние ЭГ на сократительную активность кардиомиоцитов в нашей модели в основном определялось влиянием этого вещества на Са2+-транспорт.
Полученные данные свидетельствуют о том, что этиловый эфир глутатиона оказывает выраженное корректирующее действие на динамику выведения Са++ из саркоплазмы кардиомиоцитов, которая значительно замедляется при гипоксии. В условиях преинкубации кардиомиоцитов с 1 мМ ЭЭГ нарушений в работе Са++-насосов кардиомиоцитов через 2 мин гипоксии не наблюдалось. Введение ЭЭГ в раствор после начала гипоксического воздействия также обращало нарушения Са++-транспорта в кардиомиоцитах. Важно отметить, что после реоксигенации в присутствии ЭЭГ нормальный ритм ответов на электростимулы полностью сохранялся.
В опытах с применением ДНКЖ гипоксические изменения кальциевых спайков были такими же, как и в предыдущей серии. Присутствие 30 нМ ДНКЖ не сказалось на динамике свободного внутриклеточного Са2+ в кардиомиоцитах, стимулированных импульсами электрического тока в условиях нормоксии (рис.10А). При этом в гипоксических условиях ДНКЖ предотвращает нарушения Са2+-транспорта, хотя базальный уровень Са++ несколько повышается (рис.10Б). Однако после реоксигенации в присутствии ДНКЖ восстанавливался не только нормальный ритм ответов, но и амплитуда кальциевых спайков, что свидетельствует о практически полном восстановлении кальциевого транспорта в миоцитах (рис.10В). Как видно из записей, при гипоксии больше страдает процесс обратного поглощения Са2+ в саркоплазматический ретикулум, за который ответственна SERCA2. Поскольку этот процесс является энергозависимым, его коррекция ДНКЖ в условиях энергодефицита при гипоксии может определяться повышением эффективности работы Са2+-насосов кардиомиоцитов, в частности, путем поддержания восстановленного состояния их тиоловых групп и/или обратимой их защиты S-нитрозилированием. Таким образом, влияние ДНКЖ на сократительную активность кардиомиоцитов в нашей модели в основном определялось его воздействием на процесс поглощения Са2+ в саркоплазматический ретикулум.
Динамика кальциевых ответов в присутствии ДНКЖ с этилглутатионом близко соответствовала аналогичной динамике при применении одного ДНКЖ (рис.11А). Более того, примененная композиция полностью нормализовала несколько затухающие ответы кальциевых спайков в исходном состоянии (рис.11Б). Обращает на себя внимание высокая амплитуда спайков, свидетельствующая об отсутствии нарушений в системе кальциевого транспорта.
Пример 3. Действие этилглутатиона и ДНКЖ на структурные изменения кардиомиоцитов при гипоксии
Защитное действие этилглутатиона или ДНКЖ на функциональную активность кардиомиоцитов сочеталось с лучшей сохранностью их структуры в гипоксических условиях. В норме свежевыделенные кардиомиоциты из сердца взрослой крысы представляют собой хорошо преломляющие свет длинные крупные палочковидные клетки с четкими краями (рис.12А). При фазово-контрастной микроскопии видна поперечная исчерченность клеток, отражающая распределение в клетке сократительного аппарата саркомерного типа. Среди вытянутых кардиомиоцитов встречаются округлые суперсокращенные клетки, но их количество невелико (10-15%). По всей видимости, эти клетки представляют собой кардиомиоциты, погибшие при выделении. У них была нарушена целостность сарколеммы и/или не были закрыты щелевые контакты при диссоциации клеток друг от друга. В результате произошло неконтролируемое повышение концентрации Са2+ внутри клеток и их необратимое сокращение и апоптоз. После содержания кардиомиоцитов в условиях гипоксии в течение 2 мин распределение длинных и круглых клеток существенно изменяется (рис.12Б). Начинают преобладать суперсокращенные клетки, в то время как нативные кардиомиоциты составляют не более 10% от общего числа клеток. Пролонгированная гипоксия до 10 мин приводит к полному исчезновению вытянутых кардиомиоцитов.
Преинкубация кардиомиоцитов с 1 мМ этилглутатиона в условиях нормоксии не приводит к видимым структурным изменениям клеток. В клеточной популяции продолжают преобладать длинные клетки. Присутствие этилглутатиона защищает кардиомиоциты от гипоксии. Через 10 мин после начала гипоксической инкубации в присутствии 1 мМ этилглутатиона в изоляте остается около 30-40% вытянутых кардиомиоцитов (рис.12В). При последующей реоксигенации в течение 10 мин не менее 30% кардиомиоцитов продолжает оставаться вытянутыми с четкими краями, в то время как реоксигенация контрольных кардиомиоцитов, подвергнутых гипоксии в течение 10 мин, не приводит к смене их округлой формы на вытянутую, т.е. эти клетки при гипоксии перешли в стадию необратимых изменений (рис.12Г).
Преинкубация кардиомиоцитов с 30 нМ ДНКЖ в условиях нормоксии не приводит к видимым структурным изменениям клеток (рис.13А). В клеточной популяции продолжают преобладать длинные клетки (53%). Присутствие ДНКЖ защищает кардиомиоциты от гипоксии. Через 2 мин после начала гипоксической инкубации в присутствии 30 нМ ДНКЖ в изоляте остается около 52% вытянутых кардиомиоцитов, т.е. столько же, сколько их было в первичном изоляте (рис.13Б). При последующей реоксигенации в течение 10 мин более 40% кардиомиоцитов продолжает оставаться вытянутыми с четкими краями (рис.13В). Таким образом, ДНКЖ в низких дозах эффективно защищает кардиомиоциты от повреждения и гибели, что выражается в очень небольшом накоплении структурно измененных округлых клеток.
Пример 4. Действие этилглутатиона и ДНКЖ на метаболизм кардиомиоцитов при гипоксии
Определение содержания глутатиона в кардиомиоцитах проводили на основе специально разработанной методики. Результаты показали, что содержание глутатиона в кардиомиоцитах снижается при гипоксии-реоксигенации как в контрольных условиях, так и при добавлении этилглутатиона (табл.1).
Как видно из представленной таблицы, при гипоксии, а также при последующей реоксигенации уровень глутатиона в контрольных опытах снижался в 1,7 раза. Это снижение может быть следствием как трансформации глутатиона в измененных клетках, так отражать гибель клеток при гипоксии, сопровождающуюся разрушением плазматической мембраны и выходом содержащегося в клетках глутатиона в раствор. В то же время следует отметить, что при инкубации кардиомиоцитов в присутствии 1 мМ этилглутатиона снижение уровня глутатиона на фоне гипоксии-реоксигенации выражено значительно слабее и составляет только порядка 10%, в то время как в контрольных опытах оно составляло 41%. Этот результат свидетельствует о защитном действии глутатиона при гипоксии-реоксигенации.
Измерение уровня свободных радикалов кислорода в кардиомиоцитах было выполнено с использованием флуоресцентного индикатора дигидрородамина (DHR) фирмы In-vitrogen. Эта незаряженная молекула проникает в клетки и далее в митохондрии, которые являются основным источником свободных радикалов в кардиомиоцитах. В клетках DHR превращается в т.н. дигидрородамин 123 и является сенсором свободных радикалов как в митохондриях, так и в саркоплазме.
Как видно на рис.14А, при гипоксии накопление свободных радикалов возрастает, При реоксигенации концентрация свободных радикалов также возрастает, однако при последующих стимуляциях клеток значительного увеличения концентрации свободных радикалов не наблюдалось. По-видимому, это объясняется с тем, что системы антиоксидантной защиты вернулись в исходное состояние после эпизода гипоксии и ранней реоксигенации. В то же время сократительная активность кардиомиоцитов в условиях оксигенации в течение того же периода не сопряжена с увеличенной генерацией свободных радикалов (рис.14Б).
В присутствии 1 мМ этилглутатиона (Рис.15, А) заметных колебаний содержания свободных радикалов в кардиомиоцитах во время гипоксии и реоксигенации не происходило, но при этом добавление 100 мкМ перекиси водорода резко изменяло ход кривой. Аналогично, в присутствии 30 нМ ДНКЖ не наблюдалось существенных изменений уровня свободных радикалов (Рис.15, Б), но контрольное добавление перекиси вызывало драматический эффект, показывая, что метод адекватно регистрирует свободные радикалы в том случае, если их количество превышает нейтрализующую емкость этилглутатиона и ДНКЖ.
Таким образом, гипоксия и последующая реоксигенация, в особенности ранняя ее фаза после гипоксии, сопровождаются генерацией свободных радикалов в изолированных кардиомиоцитах крыс. Сократительная активность клеток также сочеталась с повышением содержания свободных радикалов. В то же время в присутствии 1 мМ этилглутатиона или 30 нМ ДНКЖ происходит подавление генерации свободных радикалов. Если механизм антиоксидантного эффекта этилглутатиона понятен и, по-видимому, связан с нейтрализацией самих свободных радикалов, то механизм антирадикального действия ДНКЖ требует дальнейшего изучения.
Окисление тиоловых групп SERCA2 и других белков кальциевого транспорта, происходящее при окислительном стрессе, снижает скорость транслокации ионов Са2+ и препятствует расслаблению сократительного аппарата кардиомиоцита. Одним из физиологических механизмов повышения активности SERCA2 служит глутатионилирование этого белка по остатку Cys674. Глутатионилирование выполняет также защитную функцию, поскольку глутатион связывается с окисленными тиоловыми группами в составе белка, а последующее действие глутатионредуктазы приводит к восстановлению SH-групп и повышению активности транслокации Са2+ в саркоплазматический ретикулум.
Для изучения механизма защитного действия этилглутатиона была разработана методика измерения уровня глутатионилирования кальций-транспортирующих белков кардиомиоцитов при помощи антител к SERCA2 и глутатиону. Оптимизация условий детекции глутатионилирования SERCA2 показала, что в присутствии 1 мМ этилглутатиона при 2-минутной гипоксии достигалось повышение уровня глутатионилирования SERCA2 по сравнению с условиями нормоксии или гипоксии в отсутствие этилглутатиона в среде инкубации кардиомиоцитов (рис.16).
В присутствии 1 мМ глутатиона гипоксия-реоксигенация кардиомиоцитов приводила к значительному повышению количества глутатиона, обнаруживаемого в составе SERCA2. Результаты этих исследований показывают, что присутствие этилглутатиона приводит к повышению уровня глутатионилирования SERCA2 в условиях гипоксии и гипоксии-реоксигенации и коррелирует с наблюдаемым защитным эффектом этилглутатиона, препятствуя нарушению сократительной активности кардиомиоцитов при гипоксии.
Таким образом, разработанный метод защиты кардиомиоцитов от повреждения в условиях гипоксии посредством введения в среду инкубации 1 мМ этилглутатиона позволяет эффективно предотвратить снижение и/или восстановить сократительную активность изолированных кардиомиоцитов в ответ на электрическую стимуляцию. В присутствии 1 мМ ЭГ при гипоксии происходит глутатионилирование Са2+-АТФазы саркоплазматического ретикулума кардиомиоцитов, коррелирующее с восстановлением активности сократительного аппарата кардиомиоцитов и динамики флуоресценции Fluo-4 - индикатора концентрации свободного Са2+ в цитоплазме кардиомиоцитов.
Таким образом, создание биядерной формы динитрозильного комплекса железа с этиловым эфиром глутатиона (ДНКЖ-ЭЭГ) [(EEGS)2Fe2(NO)4] осуществлено на базе полученных сведений о наличии защитного действия каждого соединения с учетом того, что этилглутатион обладал более сильным антиаритмическим действием, чем ДНКЖ. Кроме того, перспективность нового соединения определяется вероятным ускорением прохождения ДНКЖ через клеточные мембраны благодаря наличию этилового радикала.
Новая композиция, включающая динитрозильные комплексы железа (ДНКЖ) с этиловым эфиром глутатиона (ДНКЖ-ЭЭГ) [(EEGS)2Fe2(NO)4], создана для применения в кардиологии, а именно - для уменьшения гипоксических и реоксигенационных нарушений функции миокарда посредством воздействия на белки кальциевого транспорта кардиомиоцитов. Раскрытие механизма защитного действия этилглутатиона и ДНКЖ при гипоксии-реоксигенации миокарда и усиление защитного действия при совместном использовании компонентов заявляемой композиции позволяет рекомендовать ее как перспективную основу для создания кардиотропного препарата в ситуациях гипоксического или ишемического повреждения миокарда.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЗАЩИТЫ КЛЕТОК ОТ ПОВРЕЖДЕНИЯ ПРИ ГИПОКСИИ ПУТЕМ ГЛУТАТИОНИЛИРОВАНИЯ КАТАЛИТИЧЕСКОЙ СУБЪЕДИНИЦЫ Na, К-АТФазы | 2013 |
|
RU2544958C2 |
| ПРИМЕНЕНИЕ БИЯДЕРНОГО СЕРА-НИТРОЗИЛЬНОГО КОМПЛЕКСА ЖЕЛЕЗА АНИОННОГО ТИПА В КАЧЕСТВЕ ВАЗОДИЛАТАТОРНОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2010 |
|
RU2437667C1 |
| ВОДОРАСТВОРИМАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СВОЙСТВАМИ КАРДИОПРОТЕКТОРА | 2010 |
|
RU2438698C1 |
| Средство, обладающее противовирусной активностью в отношении SARS-CoV-2, и способ его применения | 2022 |
|
RU2797619C1 |
| ПРИМЕНЕНИЕ БИЯДЕРНОГО СЕРА-НИТРОЗИЛЬНОГО КОМПЛЕКСА ЖЕЛЕЗА КАТИОННОГО ТИПА В КАЧЕСТВЕ ВАЗОДИЛАТАТОРНОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2010 |
|
RU2460531C2 |
| СРЕДСТВО ДЛЯ СТИМУЛЯЦИИ СИНТЕЗА ГЛИКОГЕНА В СЕРДЕЧНОЙ МЫШЦЕ И СПОСОБ СТИМУЛЯЦИИ СИНТЕЗА ГЛИКОГЕНА В СЕРДЕЧНОЙ МЫШЦЕ | 2010 |
|
RU2438679C1 |
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ ИШЕМИЧЕСКИХ И РЕПЕРФУЗИОННЫХ ПОВРЕЖДЕНИЙ ИЗОЛИРОВАННОГО СЕРДЦА | 2002 |
|
RU2325915C2 |
| СПОСОБ ЗАЩИТЫ ЭРИТРОЦИТОВ У КАРДИОХИРУРГИЧЕСКИХ БОЛЬНЫХ, ОПЕРИРОВАННЫХ В УСЛОВИЯХ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ | 2019 |
|
RU2729026C1 |
| КОМПЛЕКС ГАРЦИНОЛА И ЦИКЛОДЕКСТРИНА И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 2011 |
|
RU2566065C2 |
| Противогипоксическое вещество для экспериментальных исследований | 1987 |
|
SU1461461A1 |
Изобретение относится к биядерной форме динитрозильного комплекса железа с этиловым эфиром глутатиона (ДНКЖ-ЭЭГ) формулы [(EEGS)2Fe2(NO)4] со структурной формулой:

где R-S обозначает этиловый эфир глутатиона, содержащий тиоловую группу. Изобретение также относится к композиции для уменьшения функциональных нарушений миокарда, подвергнутого гипоксии-реоксигенации, которая содержит биядерную форму динитрозильного комплекса железа с этиловым эфиром глутатиона (ДНКЖ-ЭЭГ), как указано выше, и фармацевтически приемлемый носитель. Также раскрывается применение ДНКЖ-ЭЭГ в качестве противогипоксического средства. Технический результат заключается в уменьшении гипоксической контрактуры, интенсивности аритмий и улучшении восстановления сократительной функции сердца после реоксигенации. 3 н.п. ф-лы, 1 табл., 16 ил., 4 пр.
1. Биядерная форма динитрозильного комплекса железа с этиловым эфиром глутатиона (ДНКЖ-ЭЭГ) формулы [(EEGS)2Fe2(NO)4] со структурной формулой:

где R-S обозначает этиловый эфир глутатиона, содержащий тиоловую группу.
2. Композиция для уменьшения функциональных нарушений миокарда, подвергнутого гипоксии-реоксигенации, содержащая биядерную форму динитрозильного комплекса железа с этиловым эфиром глутатиона (ДНКЖ-ЭЭГ) по п.1 и фармацевтически приемлемый носитель.
3. Применение биядерной формы динитрозильного комплекса железа с этиловым эфиром глутатиона (ДНКЖ-ЭЭГ) по п.1 в качестве противогипоксического средства.
| ВОДОРАСТВОРИМАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СВОЙСТВАМИ КАРДИОПРОТЕКТОРА | 2010 |
|
RU2438698C1 |
| RU 2291880 C1 20.01.2007 | |||
| WO 2009148346 A1 10.12.2009 | |||
| ПРИМЕНЕНИЕ БИЯДЕРНОГО СЕРА-НИТРОЗИЛЬНОГО КОМПЛЕКСА ЖЕЛЕЗА КАТИОННОГО ТИПА В КАЧЕСТВЕ ВАЗОДИЛАТАТОРНОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2010 |
|
RU2460531C2 |
| ПРИМЕНЕНИЕ БИЯДЕРНОГО СЕРА-НИТРОЗИЛЬНОГО КОМПЛЕКСА ЖЕЛЕЗА АНИОННОГО ТИПА В КАЧЕСТВЕ ВАЗОДИЛАТАТОРНОГО ЛЕКАРСТВЕННОГО СРЕДСТВА | 2010 |
|
RU2437667C1 |
Авторы
Даты
2014-07-20—Публикация
2013-06-14—Подача