Изобретение относится к области медицины и предназначено для использования в качестве лекарственного средства при инфаркте миокарда и операциях на сердце в условиях искусственного кровообращения.
Основными повреждающими факторами ишемии и реперфузии сердца являются изменения в энергетическом обеспечении миокардиальных клеток и генерация активных форм кислорода (АФК), сопряженные с нарушениями внутриклеточного ионного гомеостаза. Их воздействие на ишемизированный миокард способно полностью блокировать окислительное фосфорилирование, повреждать структуру митохондриальных и плазматических мембран, вызывать контрактуру миофибрилл, быть причиной отсутствия восстановления кровотока и гибели кардиомиоцитов. Эти нарушения диктуют необходимость использования во время восстановления коронарного кровотока корректоров метаболизма и антиоксидантов для восстановления энергетического обеспечения кардиомиоцитов и инактивации образующихся АФК [1]. Как правило, такой подход снижает необратимые повреждения миокарда, возникновение аритмий и уменьшает постишемическую дисфункцию сердца [2]. Несмотря на достижения современной фармакологии, летальность исходов, вызванная необратимым ишемическим и реперфузионным повреждением миокарда, в России и развитых странах мира остается высокой. Это связано в первую очередь с отсутствием эффективных препаратов, одновременно обладающих свойствами метаболических протекторов, стабилизаторов мембран и вазодилататоров. В настоящее время предпринимаются попытки решения этой задачи путем использования корректоров метаболизма или доноров оксида азота (NO).
Применение оксида азота (NO) и его доноров в кардиологии обусловлено тем, что NO является эндогенным продуктом миокарда, вовлеченным в регуляцию сосудистого тонуса, сердечной сократимости, агрегации тромбоцитов, защиты клеток от некроза и апоптоза [3]. Большинство экзогенных доноров NO, рекомендованных для лечения ишемии миокарда и острой сердечной недостаточности, нашли применение в качестве вазодилататоров или ингибиторов агрегации тромбоцитов [4]. К ним относятся органические нитраты (нитроглицерин, эринит, нитросорбид), гетероциклические амиды (никорандил) и комплексные соединения железа с NO (нитропруссид). Полагают, что важнейшим механизмом действия наиболее изученного донора NO - нитроглицерина - является уменьшение пред- и постнагрузки на сердце, снижение потребности миокарда в энергии в результате расширения периферических сосудов и депонирования крови в венах [5]. Имеются данные о том, что нитроглицерин ограничивает агрегацию тромбоцитов [6]. Его способность уменьшать размеры острого инфаркта миокарда (ИМ) и повреждения мембран ишемизированных кардиомиоцитов была подтверждена экспериментально [7]. Эти факты послужили основой для выбора нитроглицерина в качестве аналога разрабатываемого кардиопротектора. Несмотря на длительное применение в кардиологии, в доступной литературе нет сведений о его влиянии на метаболические показатели ишемизированного сердца. Хорошо документированы негативные эффекты этого препарата - быстрое развитие толерантности (феномен, не имеющий четкого объяснения и способа коррекции), побочные эффекты (головная боль и более опасный - коллапс), неудобства его применения и хранения [8-10]. Положительного влияния нитроглицерина (и пролонгированных нитратов) на прогноз жизни больных острым ИМ или недавно перенесших ИМ, продемонстрировать не удалось. Так, в исследованиях ISIS-4 (Fourth International Study of Infarct Survival) и GISSI-3 (Gruppo Italiano per lo Studio della Sopravvivenza nell'Infarto Miocardico) не было выявлено значимого положительного влияния нитроглицерина на смертность и частоту развития осложнений у больных после острого ИМ [11]. В последнем варианте рекомендаций Европейского общества кардиологов его внутривенное введение не рекомендуется для использования у всех больных острым ИМ.
Для снижения нарушений обмена в миокарде при ишемии и реперфузии применяются протекторы, в состав которых входят естественные метаболиты сердца - "метаболический коктейль" глюкоза-инсулин-калий (ГИК), аспартат калия и магния (аспаркам, панангин), производные сукцината (мексикор), а также синтетические ингибиторы окисления свободных жирных кислот (триметазидин, милдронат). Их кардиозащитное действие основано на улучшении энергетического состояния ишемизированных кардиомиоцитов - поддержке более высоких уровней АТФ и фосфокреатина (ФКр) в условиях ишемии, что обеспечивает лучшее восстановление функции сердца при возобновлении кровообращения [2, 12-15]. Большинство из этих препаратов снижает уровень циркулирующих в крови свободных жирных кислот (СЖК) или уменьшает их потребление миокардом [12, 13]. Это ограничивает токсическое действие СЖК на ишемизированный миокард, связанное с повреждением мембран, которое приводит к возникновению аритмий и подавлению функции сердца [14-16]. Помимо этого, метаболические протекторы увеличивают захват K+ и предотвращают перегрузку кардиомиоцитов ионами Ca2+ и Na+, способствуют транспорту глюкозы в клетки [15]. Следствием этого является снижение возбудимости и проводимости миокарда при реперфузии, меньшее развитие реперфузионной контрактуры, уменьшение возникновения аритмий и развития ИМ [17]. На основании этих данных в качестве одного из прототипов разрабатываемого кардиопротектора был выбран широко использующийся препарат - смесь ГИК. Целесообразность использования ГИК была подтверждена нами ранее по восстановлению метаболических, морфологических и функциональных показателей сердца на моделях ишемии и реперфузии миокарда in vitro и in vivo [18-20]. В клинических испытаниях различных составов ГИК у больных с острым ИМ были также отмечены улучшения биохимических показателей крови и функции сердца [12]. В то же время была выявлена недостаточная эффективность в клиническом исходе заболевания - низкое ограничение размеров ИМ и уменьшения смертности больных [21, 22]. Эти особенности ГИК, так же как и других метаболических протекторов, обусловлены отсутствием вазодилатационной способности и антиоксидантной активности. В дополнение у ряда пациентов были отмечены дискомфорт в эпигастральной области, тошнота, аллергические реакции и головная боль [21]. Указанные недостатки существенно ограничивают использование ГИК в клинической практике.
Приведенные результаты экспериментальных и клинических исследований предполагают необходимость внедрения более безопасных и эффективных доноров NO и метаболических протекторов в практику терапии острого коронарного синдрома. В связи с этим задачей настоящего изобретения является создание водорастворимого кардиопротектора, обладающего свойствами регулятора метаболизма, стабилизатора мембран и вазодилататора. Задача решается комбинированием железо (II)-органического комплекса с оксидом азота, а именно, динитрозильного комплекса железа с глутатионом (ДНКЖ-Глн), с полиионной биологически активной средой, содержащей энергетические субстраты и инсулин.
Принципиально важно, что стабилизированные полимерной матрицей железоорганические комплексы с оксидом азота являются твердофазными соединениями, поэтому их использование в составе потенциальных лекарственных средств требует разработки водорастворимой формы. Подход, использованный при создании препарата, заключался в применении биологически активной среды для растворения стабилизированного декстраном ДНКЖ-Глн, обладающей кардиопротекторными свойствами. В ее состав включены: d-глюкоза, калиевая и магниевая соли l-аспарагиновой кислоты и инсулин. Использование такой среды снижает потенциальную цитотоксичность комплекса. Известно, что результатом избыточной биодоступности оксида азота является блокирование дыхания митохондрий и ингибирование цикла трикарбоновых кислот и ключевых ферментов гликолитического потока (фосфофруктокиназы и глицеральдегид-3-фосфатдегидрогеназы) [23]. В условиях энергетического дефицита это может приводить к необратимым летальным повреждениям миокардиальных клеток, что исключается при совместном применении ДНКЖ-Глт и биологически активной среды.
Созданный кардиопротектор представляет собой водорастворимую композицию (рН 7,4), содержащую d-глюкозу, калия хлорид, калиевую соль 1-аспарагиновой кислоты, полумагниевую соль l-аспарагиновой кислоты, инсулин человеческий генно-инженерный, ДНКЖ-Глн и воду при следующем соотношении ингредиентов (мас.%):
Состав заявляемого кардиопротектора оригинален и не описан в доступной литературе. Сочетание его компонентов также не является очевидным и не может быть подобрано эмпирическим путем. Библиография патентов по динитрозильным комплексам железа (II) с низкомолекулярными тиол-содержащими лигандами не содержит сведений по предмету изобретения - разработке на основе доноров NO такой химической структуры кардиопротектора для уменьшения повреждений сердца при ишемии и реперфузии.
Способ приготовления кардиопротектора для экспериментов на животных.
Состоит из трех этапов: 1) приготовления среды с энергетическими субстратами, 2) приготовления динитрозильного комплекса железа с глутатионом, 3) получения водорастворимой формы кардиопротектора с заданной концентрацией ДНКЖ-Глт.
Приготовление среды с d-глюкозой, K-Mg солями l-аспарагиновой кислоты и инсулином. К 100 мл дистиллированной воды добавляют 26,0 г d-глюкозы, 150,6 мг калия хлорида и перемешивают при слабом нагревании (37-40°C) до полного растворения. В полученный раствор добавляют 904,0 мг калиевой соли l-аспарагиновой кислоты и 800,5 мг полумагниевой соли l-аспарагиновой кислоты и растворяют, перемешивая при комнатной температуре. pH полученной прозрачной смеси доводят 2N HCl до pH 7,4±0,1 при 25°C. Конечная концентрация компонентов составляет в мМ: d-глюкоза - 1200,0; калий хлорид - 20,2; калиевая соль l-аспарагиновой кислоты - 44,0 и полумагниевая соль l-аспарагиновой кислоты 23,0. В раствор вводят суспензию человеческого инсулина до концентрации 60 Ед/л и тщательно перемешивают.
Приготовление динитрозильного комплекса железа с восстановленным глутатионом. В 57 мл дистиллированной воды растворяют 5 г глутатиона, в 3 мл дистиллированной воды растворяют 305 мг нитрита натрия. Растворы смешивают и выдерживают при 4°C 10 мин до появления розовой окраски в результате образования S-нитрозоглутатиона. 5% раствор декстрана в цитрат-фосфатном буфере готовят, растворяя 50 г декстрана (30-40 кДа) и 9 г NaCl в 400 мл дистиллированной воды. Далее к 60 мл этого раствора добавляют 30 мл 100 мМ фосфат-цитратного буфера (pH 7,4), а затем 130 мл дистиллированной воды. Конечный объем 5% раствора декстрана в буфере составляет 220 мл. В него добавляют раствор S-нитрозоглутатиона и после перемешивания доводят рН до 7,4±0,1 30% раствором NaOH. К полученной смеси добавляют 20 мл дистиллированной воды с растворенными 450 мг FeSO4×7H2O и 2,5 мг цитрата натрия. Смесь приобретает оранжевую окраску, вызванную образованием ДНКЖ-Глт. Раствор отфильтровывают через 5 мкм фильтр Millipore и разливают в ампулы по 0,5 мл для высушивания в вакууме. Химические реакции, приводящие к образованию ДНКЖ:
нитрит натрия+глутатион→нитрозоглутатион;
нитрозоглутатион+FeSO4+глутатион→ДНКЖ-Глт+дисульфида глутатиона.
Одна ампула содержит 22 мг сухого вещества или 1,8 мкмоль ДНКЖ-Глт в пересчете на железо (II) в комплексе.
Получение водорастворимых форм препарата. Препарат готовят, растворяя ДНКЖ-Глт в среде с d-глюкозой, K-Mg солями l-аспарагиновой кислоты и инсулином, для создания дозы 1 мкмоль ДНКЖ/кг веса.
Методы оценки биологической активности кардиопротектора.
Для исследования свойств препарата использована модель региональной ишемии и реперфузии миокарда у крыс in vivo, обеспечивающая анализ его влияния на показатели гемодинамики, ограничение размеров инфаркта миокарда, восстановление метаболического состояния ишемизированного сердца и снижение повреждения мембран кардиомиоцитов.
Модель региональной ишемии и реперфузии миокарда у крыс in vivo. У наркотизированных 20% уретаном крыс Wistar (120 мг/кг внутрибрюшинно) в условиях трахеотомии осуществляют искусственную вентиляцию легких комнатным воздухом с помощью аппарата KTR-5 (Hugo Sacks Electronik). Яремную вену катетеризируют для окрашивания интактной зоны сердца раствором Эванса в конце опыта. Сонную артерию катетеризируют для регистрации артериального давления (АД) с помощью Мингографа-804 (Siemens Elema). Грудную клетку вскрывают продольным рассечением грудины и освобождают сердце от перикарда. Для создания региональной ишемии миокарда левый желудочек (ЛЖ) прошивают атравматической иглой 5-0 под левым ушком в направлении, перпендикулярном большой оси сердца. При этом затягивание лигатуры на передней нисходящей коронарной артерии (ПНА), находящейся в толще прошитого миокарда, прекращает кровоснабжение участка миокарда; ослабление лигатуры приводит к восстановлению коронарного притока. Показатели кислотно-основного баланса артериальной крови (pH, pO2 и pCO2) в течение всего опыта контролируют на кислотно-основном газоанализаторе ABL-30 (Radiometer) и поддерживают на физиологическом уровне. После окончания препарирования следует 30-минутный период стабилизации гемодинамических показателей (исходное состояние). Затем выполняют окклюзию ПНА на 40 мин, продолжительность последующей реперфузии составляет 60 мин [20].
Определение размеров инфаркта миокарда. В конце опыта для идентификации зоны риска (ЗР) и интактной области миокарда окклюдируют ПНА и в яремную вену вводят болюсно 2% раствор Эванса (2 мл). Затем вырезают сердце и отделяют ЛЖ, который замораживают при температуре -20°C до гистохимического определения размеров ИМ прокрашиванием ткани 2,3,5-трифенилтетразолий хлоридом. Для этого из ЛЖ готовят поперечные срезы толщиной около 1,5-2 мм, которые инкубируют 10 мин в 1% растворе 2,3,5-трифенилтетразолий хлорида в 0,1 М фосфатном буфере (pH 7,4 при температуре 37°C). Полученные образцы сканируют, площади ИМ и ЗР определяют методом компьютерной планиметрии, используя программу Imagecal. После этого срезы взвешивают для определения массы ЛЖ. В каждой группе рассчитывают отношения ЗР/масса ЛЖ и ИМ/ЗР в процентах.
Метаболическое состояние сердца. По окончании периодов стабилизации гемодинамики (исходное состояние), ишемии и реперфузии ткань ЗР замораживают щипцами Волленбергера, охлажденными в жидком азоте, для последующего определения метаболитов. Замороженные образцы ткани миокарда гомогенизируют в холодной 6% HClO4 (10 мл/г ткани) с помощью гомогенизатора Ultra-Turrax Т-25 (IKA-Labortechnik, Германия). Белки осаждают центрифугированием при 3000 g и температуре 4°C в течение 10 мин. Супернатанты нейтрализуют 5 М K2CO3 до pH 7,4. Осадок KClO4 отделяют центрифугированием в тех же условиях. Безбелковые экстракты хранят при температуре -20°C до определения метаболитов. Сухие веса образцов определяют взвешиванием части ткани после экстракции HClO4 и высушивания при температуре 110°C в течение ночи. Метаболиты в тканевых экстрактах определяют спектрофотометрически, их содержание выражают в мкмоль/г сухого веса.
Повреждения клеточных мембран. Оценивают по увеличению активности лактатдегидрогеназы (ЛДГ) и МВ-фракции креатинфосфокиназы (МВ-КФК) в плазме в конце реперфузии. Кровь собирают в гепаринизированные пробирки из венозного катетера в исходном состоянии (перед окклюзией ПНА) и после часа реперфузии. Плазму отделяют центрифугированием (2000 об/мин в течение 10 мин при 10°C). Активность ферментов в свежевыделенной плазме определяют спектрофотометрически при λ=340 нм, используя наборы фирмы BioSystems и реактивы фирмы Sigma-Aldrich.
Показатели функциональной гемодинамики. Изменения среднего артериального давления (АД ср.) и частоты сокращений сердца (ЧСС) регистрируют в режиме on line с помощью Мингографа-804 (Siemens Elema) в ходе всего опыта. Полученные результаты статистически анализируют, сравнивая с исходным состоянием и изменениями в контроле (в отсутствие препарата) или под действием препаратов сравнения. Различия между группами оценивают с помощью анализа варианс (ANOVA) и считают статистически достоверными при p<0,05.
Препараты сравнения. Использовали нитроглицерин (Перлинганит) и смесь глюкоза-инсулин-калий (ГИК) следующего состава: глюкоза 2,8 М, инсулин человеческий генно-инженерный 100 МЕ/л, KCl 0,1 М. Нитроглицерин, являясь донором NO, обеспечивает периферическую вазодилатацию и обладает коронарорасширяющим действием, способен снижать необратимые повреждения постишемических кардиомиоцитов. ГИК - метаболический протектор, воздействует на процессы внутриклеточного обмена, ограничивает размеры ИМ [12, 20, 5, 7]. В настоящее время оба препарата используются в клинической практике при терапии повреждений сердца при остром коронарном синдроме.
Пример 1. Ограничение размеров инфаркта миокарда.
Тестирование кардиопротектора и сопоставление его эффектов с действием нитроглицерина и ГИК проведено на модели региональной ишемии и реперфузии миокарда у крыс in vivo. Выполнено две серии опытов с внутривенным введением препаратов: 1 - до окклюзии ПНА и 2 - после региональной ишемии на первой минуте реперфузии. ГИК, нитроглицерин и кардиопротектор вводили внутривенно из расчета 1 мл/кг веса животного. Доза нитроглицерина (1 мкмоль/кг массы крысы) была эквимолярна содержанию ДНКЖ-Глт в кардиопротекторе. В контроле внутривенно вводили равный объем физиологического раствора.
Гистохимический анализ срезов ЛЖ после реперфузии не выявил достоверных различий в размере ЗР между группами. Среднее отношение ЗР/вес ЛЖ (в %) для всех групп составляло 35,9±4,0%. Это указывало на правомочность сравнения данных по ограничению ИМ в исследуемых группах.
При введении препаратов перед окклюзией коронарной артерии наблюдали достоверное снижение ИМ по сравнению с контролем. При этом способность ограничивать ИМ снижалась в ряду кардиопротектор>нитроглицерин>ГИК. Видно, что размер ИМ при использовании кардиопротектора был достоверно ниже, чем при введении ГИК (p<0,05). Хотя при введении кардиопротектора ИМ был меньше, чем при использовании нитроглицерина, различия между группами не достигали уровня статистической значимости (р=0,53).
При введении препаратов после окончания периода региональной ишемии (на первой минуте реперфузии) достоверное ограничение ИМ по сравнению с контролем происходило под действием кардиопротектора и ГИК. Значимых различий в ограничении ИМ при введении нитроглицерина по сравнению с контролем не наблюдали (p=0,066). Средние значения размера ИМ были минимальны при введении кардиопротектора: на 20±1% ниже этого показателя в группе ГИК (p<0,05).
Полученные результаты демонстрируют преимущества применения кардиопротектора, в особенности на стадии ранней реперфузии, для ограничения ИМ по сравнению с традиционно использующимися для этой цели лекарственными средствами.
Пример 2. Метаболическое состояние сердца при реперфузии.
По окончании реперфузии в сердцах исследованных групп были определены уровни макроэргических фосфатов (АТФ, АДФ, АМФ и ФКр), креатина (Кр) и конечных продуктов гликолиза (лактата и пирувата) для оценки влияния препаратов на метаболизм миокарда. На основании этих данных были рассчитаны показатели энергетического состояния постишемического сердца:
энергетический заряд кардиомиоцитов - ЭЗ=(АТФ+0,5АДФ)/ΣАН;
степени фосфорилирования АТФ и фосфокреатина - АТФ/АДФ,
фосфокреатин/креатин (ФКр/Кр);
отношение лактат/пируват, характеризующее степень восстановления цитоплазматических пиридиндинуклеотидов [NAD+]/[NADH] [24].
Сопоставление полученных данных с метаболическим состоянием сердца в исходном состоянии (до моделирования ишемии и реперфузии) приведено в табл.2.
Из данных, представленных в табл.2, видно, что в контроле энергетическое состояние ЗР к концу реперфузии было существенно снижено по сравнению с исходным состоянием сердца. На это указывают более низкие значения ЭЗ и отношений АТФ/АДФ и ФКр/Кр и более чем на порядок увеличенное отношение лактат/пируват. Введение кардиопротектора или обоих препаратов сравнения достоверно улучшало большинство показателей метаболического состояния ЗР, приближая их к значениям в исходном состоянии. Исключение составляло отношение лактат/пируват в группе ГИК, которое статистически достоверно не отличалось от значения в контроле. Из анализа показателей следует, что восстановление метаболического статуса ЗР после введения препаратов улучшалось в ряду ГИК<нитроглицерин<кардиопротектор и соответствовало их способности ограничивать размеры ИМ (табл.1). Причем, под действием введения кардиопротектора восстановление ЭЗ кардиомиоцитов было достоверно лучше, чем в группе ГИК, а отношения АТФ/АДФ и ФКр/Кр достоверно выше, чем после использования любого из препаратов сравнения. Полученные результаты указывают, что применение кардиопротектора обеспечивало более эффективное восстановление аэробного обмена в ЗР при реперфузии.
Пример 3. Повреждения мембран кардиомиоцитов.
Маркерами повреждения сарколеммы постишемических кардиомиоцитов служили активности лактатдегидрогеназы (ЛДГ) и МВ-фракции креатинфосфокиназы (МВ-КФК) в плазме. Сравнение увеличения активностей обоих ферментов в исследуемых группах в конце реперфузии в сопоставлении со значениями в исходном состоянии представлено в табл.3.
В исходном состоянии активность ЛДГ в плазме была практически одинаковой во всех исследуемых группах (табл.3). Развитие ИМ сопровождалось значительным (в 12 раз) увеличением активности ЛДГ в плазме к концу реперфузии в контроле по сравнению с исходным значением. Введение кардиопротектора, так же как и препаратов сравнения, перед региональной ишемией достоверно снижало выход фермента в кровоток. При этом минимальное повышение активности ЛДГ было обнаружено при использовании кардиопротектора. Оно было достоверно ниже, чем после введения ГИК и нитроглицерина, и составляло около 70% от значения в контроле.
В исходном состоянии не было обнаружено достоверных различий между группами в активности МВ-КФК. К окончанию реперфузии активность МВ-КФК в контроле возрастала более чем в 4 раза по сравнению с исходным значением. Достоверное снижение активности МВ-КФК в плазме в конце реперфузии по сравнению с этим показателем в контроле происходило под действием всех препаратов. Однако в случае введения кардиопротектора активность фермента была ниже на 15 и 28%, чем в группе нитроглицерина и ГИК, соответственно (p<0,05).
Таким образом, применение обоих маркеров повреждения клеточных мембран (ЛДГ и более специфичного - МВ-КФК) однозначно свидетельствует о большей стабильности сарколеммы постишемических кардиомиоцитов ЗР в случае использования кардиопротектора предлагаемого состава.
Пример 4. Изменения гемодинамики у крыс в условиях региональной ишемии и реперфузии сердца.
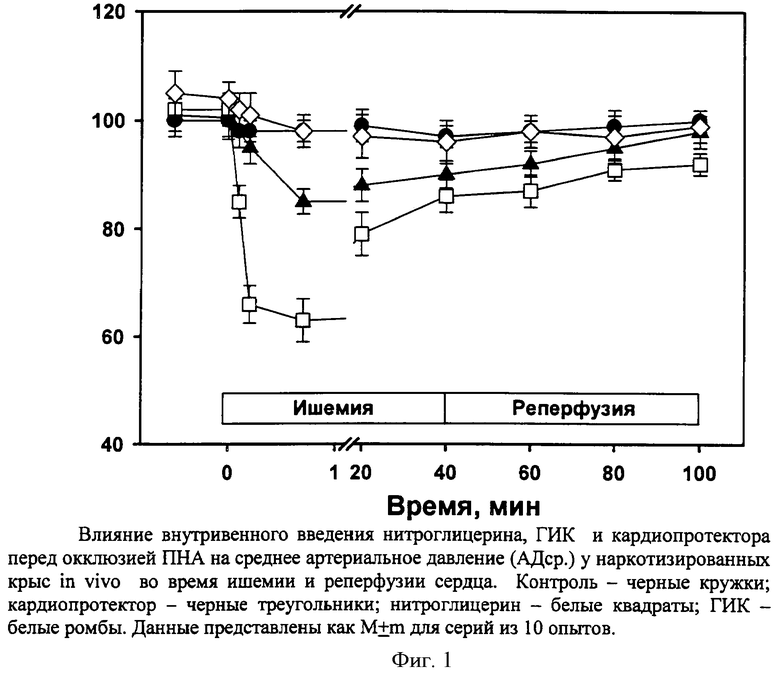
Действие препаратов на показатели функциональной гемодинамики у крыс in vivo изучено при их введении перед окклюзией коронарной артерии. Препараты и физиологический раствор вводили, как указано в разделе "Ограничение размеров инфаркта миокарда". Результаты представлены на фиг.1 и в табл.4.
При анализе динамики артериального давления было выявлено: 1) отсутствие вазадилататорного ответа после введения ГИК в противоположность кардиопротектору и нитроглицерину, 2) менее резкое падение АДср. в первой фазе действия по сравнению с нитроглицерином, 3) способность кардиопротектора к пролонгированному гипотензивному эффекту в сочетании с полным восстановлением АДср. к окончанию реперфузии (фиг.1).
При анализе изменений ЧСС было обнаружено: 1) достоверно меньшее снижение этого показателя при введении кардиопротектора во время окклюзии коронарной артерии, чем в случае нитроглицерина, 2) значительное уменьшение продолжительности аритмий (в среднем в 3 раза) во время региональной ишемии по сравнению с обоими препаратами сравнения (табл.4).
Таким образом, сопоставление действия препаратов сравнения с влиянием кардиопротектора на показатели гемодинамики у крыс in vivo свидетельствует о преимуществах применения последнего при региональной ишемии миокарда и последующей реперфузии ЗР. Они заключаются в меньших нарушениях гемодинамики при сохранении пролонгированного вазодилатационного эффекта и снижении длительности аритмий. Взятые вместе, полученные результаты указывают на перспективность использования кардиопротектора указанного состава для уменьшения ишемического и реперфузионного повреждения миокарда.
Варьирование концентраций компонентов кардиопротектора.
Были тестированы два модифицированных состава кардиопротектора, содержащие более низкие и более высокие концентрации основных действующих веществ - d-глюкозы, калиевой и полумагниевой соли l-аспарагиновой кислоты, ДНКЖ-Глн. Конечный рН кардиопротекторов был неименным и составлял 7,4±0,1 при 22°C (табл.5). Эффективность этих препаратов оценивали на модели региональной ИМ и реперфузии у крыс in vivo по ограничению размеров инфаркта миокарда при одновременном измерении гемодинамических показателей и активности фракции МВ-КФК в плазме.
Данные табл.6 показывают, что в сериях опытов с кардиопротектором-1 и кардиопротектором-2 величины отношения ЗР/вес ЛЖ (в %) не различались от таковых в контроле и в опытах с кардиопротектором оптимального состава. Снижение, так же как и увеличение содержания основных действующих компонентов, увеличивало отношение ИМ/ЗР (в %) в 1,2 и 1,3 раза, соответственно, по сравнению с этим показателем при использовании кардиопротектора оптимального состава. В обоих случаях это приводило к отсутствию достоверного уменьшения размеров инфаркта по сравнению с контролем, то есть к потере защитного действия.
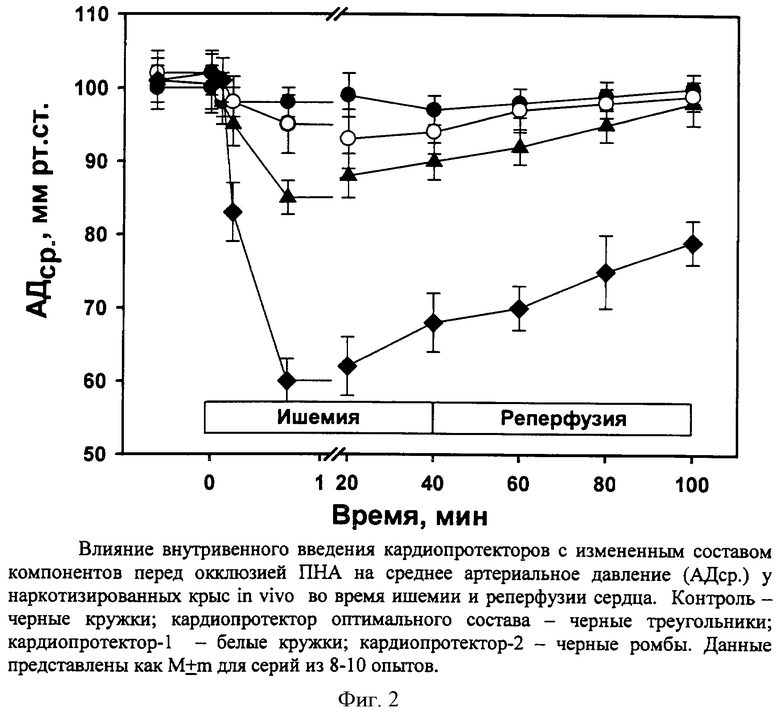
На фиг.2 показаны изменения в АДср. у крыс во время ишемии и реперфузии сердца при введении кардиопротектора-1 и кардиопротектора-2. Видно, что уменьшение содержания ДНКЖ-Глт в кардиопротекторе-1 в 2,5 раза по сравнению с кардиопротектором оптимального состава значительно снижало вазодилатационное действие препарата на первой фазе после введения и отменяло его пролонгированный гипотензивный эффект. В этом случае АДср. восстанавливалось до исходного значения на ранней стадии реперфузии и достоверно не отличалось от значений в контроле, то есть при введении физиологического раствора. Такая динамика АДср. указывала на недостаточное выделение NO из ДНКЖ и отсутствие связывания комплекса с белками плазмы и эритроцитами [25]. Напротив, при введении кардиопротектора-2 с 2,5 раза увеличенным содержанием ДНКЖ-Глт в течение первых минут происходило резкое снижение АДср. до 59±3% от исходного уровня. К окончанию региональной ишемии АДср. оставалось сниженным до 68±4% и практически не восстанавливалось в дальнейшем, составляя 79±4% от исходного уровня в конце реперфузии. Очевидно, что выделение избытка NO из ДНКЖ-Глт могло быть причиной летального повреждения кардиомиоцитов зоны риска [23] и, как следствие, увеличения размеров инфаркта (табл.6).
В сериях опытов с введением кардиопротектора-1 и кардиопротектора-2 не было обнаружено уменьшения продолжительности аритмий во время региональной ишемии. Длительность нарушений ритма достоверно не отличалась от значения в контроле и составляла 498±40 и 668±62 сек для кардиопротектора-1 и кардиопротектора-2, соответственно, таким образом, превышая этот показатель в 2,5 и 3,3 раза для препарата оптимального состава (205±13 сек, табл.4).
Результаты определения активности МВ-КФК в плазме крыс in vivo при введении кардиопротекторов с измененным составом компонентов приведены в табл.7. Видно, что использование кардиопротектора-1 и кардиопротектора-2 не снижало активность фермента в конце реперфузии по сравнению с контролем. В этих случаях активность этого маркера повреждения клеточных мембран была в среднем в 1,6 раза выше, чем в опытах с введением кардиопротектора оптимального состава. Эти данные указывали на отсутствие уменьшения разрывов сарколеммы постишемических кардиомиоцитов, что хорошо согласовывалось с увеличением размеров ИМ под влиянием кардиопротекторов с измененным составом компонентов (табл.6).
Полученные результаты свидетельствуют о том, что варьирование содержания компонентов не приводит к увеличению защиты миокарда от ишемического и реперфузионного повреждения. Напротив, эти изменения вызывают отмену защитного действия препарата по всем исследованным показателям. Таким образом, оптимальным является состав кардиопротектора, указанный на странице 4. Его применение обеспечивает большее ограничение размеров инфаркта миокарда, лучшее восстановление метаболического состояния сердца при реперфузии, наибольшую стабильность мембран постишемических кардиомиоцитов и меньшие нарушения гемодинамики по сравнению с традиционно использующимися препаратами.
Источники информации


| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ПРОТИВ ГИПОКСИИ МИОКАРДА | 2013 |
|
RU2522953C1 |
| ТЕТРАДЕКАПЕПТИДЫ, УЛУЧШАЮЩИЕ ВОССТАНОВИТЕЛЬНУЮ ФУНКЦИЮ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ ПРИ ИШЕМИИ | 2017 |
|
RU2648846C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ИШЕМИИ МИОКАРДА ПРИ КОРОНАРОИНВАЗИВНЫХ ВМЕШАТЕЛЬСТВАХ | 1999 |
|
RU2146933C1 |
| СПОСОБ ПОВЫШЕНИЯ ДВИГАТЕЛЬНОЙ АКТИВНОСТИ НА СТАЦИОНАРНОМ ЭТАПЕ РЕАБИЛИТАЦИИ ГЕРИАТРИЧЕСКИХ БОЛЬНЫХ С ИНФАРКТОМ МИОКАРДА, НЕ ПОДВЕРГАВШИХСЯ КОРОНАРНОЙ РЕПЕРФУЗИИ И РЕВАСКУЛЯРИЗАЦИИ | 2014 |
|
RU2546410C1 |
| СПОСОБ КОРРЕКЦИИ ПРОЦЕССОВ ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ У БОЛЬНЫХ ОСТРЫМ ИНФАРКТОМ МИОКАРДА | 2016 |
|
RU2627458C1 |
| Способ уменьшения размера ишемически-реперфузионного повреждения миокарда с применением квинакрина | 2019 |
|
RU2716596C1 |
| БРОМИД 1-(β-ФЕНИЛЭТИЛ)-4-АМИНО-1,2,4-ТРИАЗОЛИЯ (МТ), ОБЛАДАЮЩИЙ КАРДИОПРОТЕКТИВНЫМ, ПРОТИВОИШЕМИЧЕСКИМ, АНТИГИПЕРТЕНЗИВНЫМ, АНТИОКСИДАНТНЫМ, ПРОТЕИНСИНТЕТИЧЕСКИМ И ЭНЕРГОТРОПНЫМ ДЕЙСТВИЕМ | 2008 |
|
RU2404974C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ КАРДИОПРОТЕКТОРНЫМ ДЕЙСТВИЕМ, И ГАЛОГЕНИДЫ 1,3-ДИЗАМЕЩЕННЫХ 2-АМИНОБЕНЗИМИДАЗОЛИЯ | 2013 |
|
RU2526902C1 |
| ПЕПТИДНОЕ СОЕДИНЕНИЕ, ВОССТАНАВЛИВАЮЩЕЕ ФУНКЦИЮ МИОКАРДА | 2004 |
|
RU2255756C1 |
| Способ кардиопротекции ишемических и реперфузионных повреждений в остром периоде инфаркта миокарда | 2019 |
|
RU2712448C1 |
Изобретение относится к области медицины и химико-фармацевтической промышленности, в частности к лекарственному средству, используемому при инфаркте миокарда и операциях на сердце в условиях искусственного кровообращения. Водорастворимая композиция для внутривенного введения содержит ингредиенты при следующем соотношении, мас.%: D-глюкоза 23,40-28,60, калия хлорид 0,14-0,16, калиевая соль L-аспарагиновой кислоты 0,81-0,99, полумагниевая соль L-аспарагиновой кислоты (магния L-аспарагинат) 0,72-0,88, инсулин человеческий генно-инженерный (в МЕ/л) 54,00-66,00, динитрозильный комплекс железа (II) с глутатионом 0,19-0,23, вода для инъекций остальное, при этом рН раствора 7,4±0,1 при 22°С. Применение композиции обеспечивает ограничение размеров инфаркта миокарда, восстановление метаболического состояния сердца при реперфузии, снижает повреждения мембран постишемических кардиомиоцитов при меньших нарушениях гемодинамики по сравнению с традиционно использующимися препаратами. 2 ил., 7 табл.
Водорастворимая композиция, обладающая свойствами кардиопротектора, для внутривенного введения, включающая d-глюкозу, калия хлорид, инсулин человеческий генно-инженерный и воду, отличающаяся тем, что она дополнительно содержит калиевую соль 1-аспарагиновой кислоты, полумагниевую соль 1-аспарагиновой кислоты и динитрозильный комплекс железа(II) с глутатионом при следующем соотношении ингредиентов, мас.%:
при этом рН раствора 7,4±0,1 при 22°С.
| Досон Р | |||
| Справочник биохимика, 1991, с.374 | |||
| Видоизменение прибора с двумя приемами для рассматривания проекционные увеличенных и удаленных от зрителя стереограмм | 1919 |
|
SU28A1 |
| Найдено в Интернете: [http://reslib.com/book/Spravochnik_biohimika_Doson_R_] | |||
| КАРДИОПЛЕГИЧЕСКИЙ РАСТВОР "ИНФУЗОЛ" | 2002 |
|
RU2226093C1 |
Авторы
Даты
2012-01-10—Публикация
2010-05-12—Подача