Объектом настоящего изобретения является новый способ получения [4-(2-хлор-4-метокси-5-метилфенил)-5-метилтиазоло-2-ил]-[2-циклопропил-1-(3-фтор-4-метилфенил)-этил]-амина формулы (I)
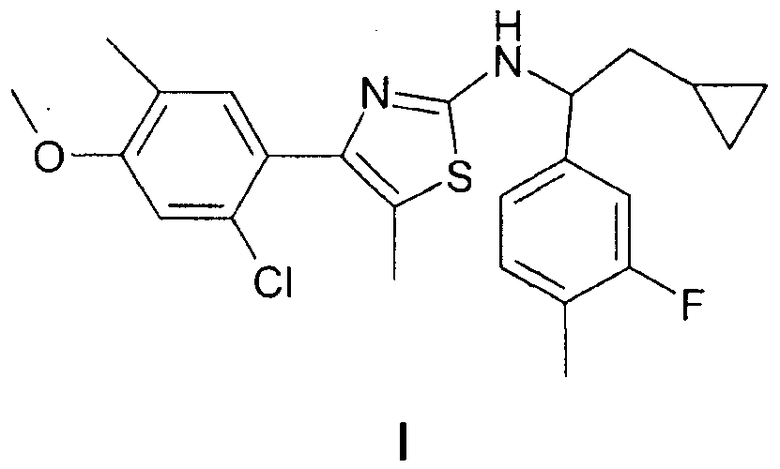
и новые промежуточные соединения (интермедиаты) способа получения.
Соединение формулы (I) является ключевым интермедиатом для получения [4-(2-хлор-4-метокси-5-метилфенил)-N-пропинил-5-метил-тиазоло-2-ил]-[2-циклопропил-1-(3-фтор-4-метилфенил)-этил]-амина формулы (VI),
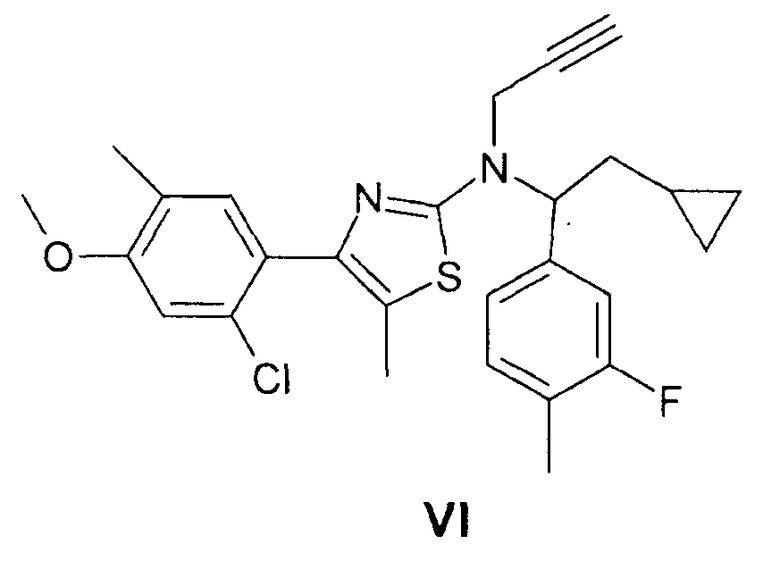
который является известным антагонистом рецептора CRF1 (кортикотропинвысвобождающий фактор 1) с сильным антидепрессивным и/или (анксиолитическим) седативным действием.
В настоящее время тиазоламин формулы (I) получают в несколько стадий, применяя синтез Hantzsch (WO2001005776 Sanofi-Aventis).
Применяющийся до настоящего времени способ получения (WO2001005776 Sanofi-Aventis) исходит из соединения общей формулы (II)
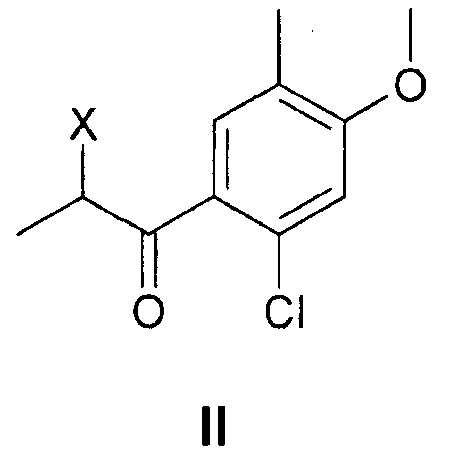
где X обозначает атом галогена. Однако это соединение легко разлагается, вызывает раздражение, его качество сложно воспроизвести, его выделение и обработка затруднительны.
Целью авторов было найти исходный материал для получения соединения формулы (I), который легко определяется, легок в обработке, который хорошо кристаллизуется и может быть без труда получен с высоким выходом. К удивлению авторов, они обнаружили, что 2-тиоцианат-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-он формулы (III)
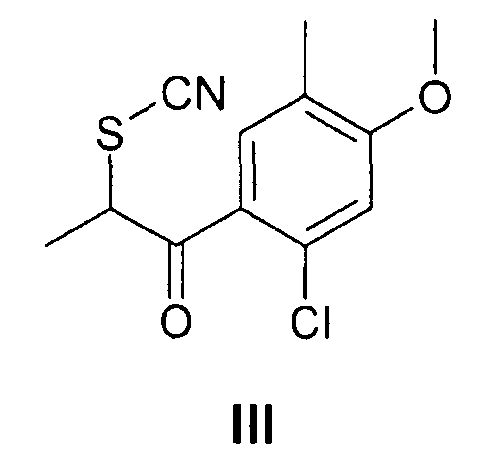
является исходным материалом, который удовлетворяет всем указанным условиям. Следующим преимуществом применения соединения формулы (III) является то, что в определенных условиях, т.е. в присутствии катализатора фазового переноса он может быть легко получен в водной среде из ранее использовавшегося соединения общей формулы (II). Этот предлагаемый настоящим изобретением новый способ является экологически чистым, так как образуются только водные отходы, количество использованных органических растворителей мало, и растворители можно использовать повторно, способ может быть осуществлен в промышленном масштабе и дает высокочистый продукт с высоким выходом.
Получение кетонового производного (III) в водных условиях удивительно, так как тиоцианатная группа чувствительна к воде, она может легко превратиться в изотиоцианат или подвергаться гидролизу. Поэтому, согласно уровню техники, его получают либо в ионной жидкости (Tetrahedron Letters 46 (2005) 1489-1491), либо в спиртовой среде (J. Indian Chem. Soc., 81 (2004) 786-788), но в любом случае в отсутствие воды.
Объектом изобретения является новый способ получения [4-(2-хлор-4-метокси-5-метилфенил)-5-метил-тиазоло-2-ил]-[2-циклопропил-1-(3-фтор-4-метилфенил)-этил]-амина формулы (I)

в котором
a) 2-галоген-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-он общей формулы (II)

где X обозначает галоген, приводят во взаимодействие с тиоцианатом щелочного металла в присутствии катализатора фазового переноса, и
b) полученный таким образом 2-тиоцианат-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-он формулы (III)

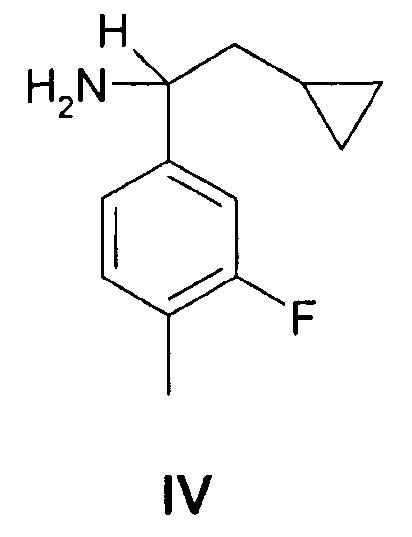
или его таутомерную форму подвергают взаимодействию с 2-циклопропил-1-(3-фтор-4-метилфенил)-этиламином формулы (IV)

Чтобы получить подходящий оптически активный изомер соединения формулы (I), авторы исходили из соответствующего оптически активного амина формулы (IV).
В одном варианте осуществления способа, согласно изобретению, на этапе a) реакцию проводят в бинарной системе, состоящей из апротонного растворителя и воды.
В одном альтернативном варианте способа, согласно изобретению, соединение общей формулы (II), где X благоприятно обозначает группу хлор или бром, предпочтительно бром, растворяют в апротонном органическом растворителе и приводят в реакцию с водным раствором тиоцианата щелочного металла, предпочтительно тиоцианата калия, в присутствии катализатора фазового переноса, предпочтительно TBAB (тетрабутиламмонийбромид). Из реакционной смеси после разбавления ее водой отделяют органическую фазу. В данном случае после замены растворителя соединение формулы (III) может быть легко кристаллизовано с высоким выходом.
В одном варианте стадии b) соединение формулы (III) добавляют в соединение формулы (IV), чтобы получить желаемый продукт с высоким выходом и с благоприятным профилем примесей.
Чтобы достичь наилучшего выхода, период добавления длится по меньшей мере один час.
На стадии b) благоприятно использовать неполярный апротонный растворитель, предпочтительно метилциклогексан или толуол. Стадия b) предпочтительно проводится в температурном диапазоне от 25°C и до температуры флегмы, наиболее предпочтительно - при температуре флегмы.
Соединения общей формулы (II) и амин формулы (IV), а также их получение известны из патентной заявки, опубликованной под № WO2001005776.
Следующим объектом изобретения является новое соединение формулы (III) и его таутомеры, а также их получение.
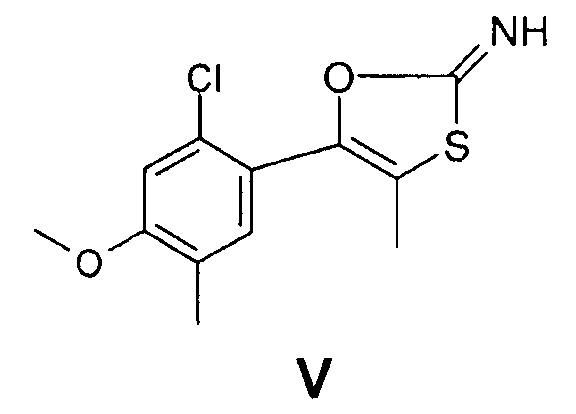
Из этих таутомеров соединения (III) объектом изобретения является также 5-(2-хлор-4-метокси-5-метилфенил)-4-метил-[1.3]-оксатиол-2-илиденамин формулы (V)
Дальнейшие детали предлагаемого способа демонстрируются в следующих примерах, не ограничивающих объем притязаний.
ПРИМЕРЫ
Пример 1. Получение соединения (III) из соединения (II) в дихлорметане (DCM)
291,5 г 2-бром-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-она (II) растворяют в 291 г DCM, добавляют туда 5,3 г катализатора TBAB (тетрабутиламмонийбромид).
167 г KSCN растворяют в 83,6 г воды. Водный раствор добавляют в раствор DCM. Полученную бинарную систему нагревают до 40°C (температура флегмы - паров обратного холодильника) и перемешивают 3-4 часа.
Реакция сопровождается выпадением в осадок соли. В смесь добавляют воду до растворения соли. Нижнюю, водную фазу отделяют, а верхнюю, органическую фазу выпаривают, одновременно добавляя в нее 870 мл метанола (MeOH). Из метанольного раствора при охлаждении кристаллизуется соединение (III). Кристаллы отфильтровывают и промывают несколько раз MeOH.
Выход: 90-95%
Температура плавления: 75°C (MeOH)
ИК-спектр: 2158 см-1 (CN), 1664 см-1 (C=O)
1Η-ЯМР спектр (ДМСО-d6, TMS): 7,73 (1H, с), 7,14 (1H, с), 5,28 (1H, квинтет, J=7,2 Гц), 3,89 (3H, с), 2,16 (3H, с), 1,60 (3H, д, J=7,2 Гц)
13C-ЯМР спектр: 194,7, 160,9, 132,6, 131,5, 126,3, 125,5, 113,5, 111,4, 56,7, 49,4, 18,8, 15,8
Пример 2. Получение соединения (III) из соединения (II) в метилциклогексане (MCH)
Методика получения такая же, как описано в примере 1, но в качестве растворителя вместо DCM используется MCH. Продукт кристаллизуется из MCH при охлаждении.
Выход: 60%
Пример 3. Получение соединения (V) из соединения (III) в неполярном растворителе в присутствии амина
26,4 г соединения (III) (полученного, как описано в примере 1 или 2) суспендируют в 52 мл MCH. В смесь в стехиометрическом количестве добавляют амин (предпочтительно бензиламин).
Смесь перемешивают в течение 0,5-1 часа (на время реакции влияет структура амина). Получают густой осадок, его отфильтровывают и промывают несколько раз метилциклогексаном.
Выход: 85%
Пример 4. Получение соединения (V) из соединения (III) в третичном амине как растворителе
Методика получения такая же, как описано в примере 3, с тем отличием, что соединение (III) суспендируют в триэтиламине в качестве растворителя, а не в MCH, и в смесь не добавляют никакого другого амина.
Выход: 85%
Температура плавления: 106°C (EtOH)
ИК-спектр: 3253 см-1 (NH), 1679 см-1 (C=N)
1Η-ЯМР спектр (ДМСО-d6, TMS): 7,30 (1H, с), 7,14 (1H, с), 3,86 (3H, с), 2,14 (3H, с), 1,88 (3H, с)
13C-ЯМР спектр: 163,1 (с), 158,9 (с), 138,9 (д), 133,0 (с), 131,4 (с), 125,3 (с), 118,3 (с), 111,8 (д), 111,5 (с), 56,0 (т), 15,3 (т), 11,6 (т)
Пример 5. Получение соединения (I) из соединения (III) в метилциклогексане (MCH)
26,3 г выделенного продукта (III) растворяют в 52 мл MCH. Реакционную смесь нагревают до 85-90°C и добавляют в раствор 19,2 г амина (IV) в MCH (20%) при температуре 85-90°C. Продолжительность добавления 2-4 часа. После добавления реакционную смесь перемешивают при 85-90°C в течение одного часа. Раствор неочищенного продукта (I) в MCH охлаждают и осажденные кристаллы отфильтровывают. Кристаллический продукт покрывают небольшим количеством MCH.
Выход: 80%
Пример 6. Получение соединения (I) из соединения (III) в MCH и MeOH
Методика получения такая же, как описано в примере 5, но продукт (I) кристаллизуется из MeOH, а не из MCH, после замены растворителя.
Выход: 90%
Пример 7. Получение соединения (I) из соединения (V)
Методика получения такая же, как описано в примерах 5 и 6, но вместо соединения (III) используется соединение (V) в таком же количестве.
Выход: 85%
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-АМИНО-4-ХЛОР-1,3,5-ТРИАЗИНОВ | 1999 |
|
RU2271353C2 |
| СПОСОБ ПОЛУЧЕНИЯ 3-(2-ХЛОРО-5-ТИАЗОЛИЛМЕТИЛ)-5-МЕТИЛ-4-НИТРОИМИНОТЕТРАГИДРО-1,3,5-ОКСАДИАЗИНА | 2000 |
|
RU2258704C2 |
| НОВЫЙ ХИМИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ 6-ХЛОР-4-(4-ФТОР-2-МЕТИЛФЕНИЛ)ПИРИДИН-3-АМИНА, КЛЮЧЕВОГО ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ ДЛЯ ПРОИЗВОДСТВА NT-814 | 2024 |
|
RU2840774C2 |
| ПОЛУГИДРОХЛОРИД 8-ЦИАН-1-ЦИКЛОПРОПИЛ-7-(1S,6S-2,8-ДИАЗАБИЦИКЛО[4.3.0]НОНАН-8-ИЛ)-6-ФТОР-1, 4-ДИГИДРО-4-ОКСО-3-ХИНОЛИНКАРБОНОВОЙ КИСЛОТЫ | 1999 |
|
RU2242475C2 |
| ПРОИЗВОДНЫЕ 2-АНИЛИНО-ПИРИМИДИНА ИЛИ ИХ СОЛИ, ПРОЯВЛЯЮЩИЕ ФУНГИЦИДНУЮ АКТИВНОСТЬ | 1992 |
|
RU2045520C1 |
| НОВЫЕ 2-ЦИАНО-1,3-ДИОНОВЫЕ ПРОИЗВОДНЫЕ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ГЕРБИЦИДНАЯ КОМПОЗИЦИЯ, СПОСОБ ПОДАВЛЕНИЯ СОРНЯКОВ | 1994 |
|
RU2149869C1 |
| НОВОЕ ПРОИЗВОДНОЕ 3-ГИДРОКСИ-5-АРИЛИЗОТИАЗОЛА | 2010 |
|
RU2567755C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-АМИНО-5-ФТОР-3-ГАЛОГЕН-6-(ЗАМЕЩЕННЫХ)ПИКОЛИНАТОВ | 2012 |
|
RU2545074C1 |
| 4-ФЕНОКСИ-НИКОТИНАМИДЫ ИЛИ 4-ФЕНОКСИ-ПИРИМИДИН-5-КАРБОКСАМИДЫ | 2011 |
|
RU2565077C2 |
| ФЕНОКСИМЕТИЛЬНЫЕ ПРОИЗВОДНЫЕ | 2016 |
|
RU2746481C1 |
Изобретение относится к способу получения [4-(2-хлор-4-метокси-5-метилфенил)-5-метилтиазоло-2-ил]-[2-циклопропил-1-(3-фтор-4-метилфенил)-этил]-амина формулы (I) (вариантам) и новым промежуточным соединениям способа получения. Способ получения соединения формулы (I) осуществляют путем взаимодействия a) соединения общей формулы (II), где X обозначает галоген, подвергают взаимодействию с тиоцианатом щелочного металла в присутствии катализатора фазового переноса, и b) полученный таким образом 2-тиоцианат-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-он формулы (III) или его таутомерную форму подвергают взаимодействию с 2-циклопропил-1-(3-фтор-4-метилфенил)-этиламином формулы (IV). Изобретение относится к 2-тиоцианат-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-ону формулы (III) и его таутомеру. Изобретение также относится к способу получения получения 2-тиоцианат-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-она формулы (III) за счет взаимодействия его производного общей формулы (II), где X обозначает галоген, с тиоцианатом щелочного металла в присутствии катализатора фазового переноса. Технический результат - экологически чистый способ получения целевого соединения формулы (I) за счет образования только водных отходов, низкого количества используемых органических растворителей с получением высокочистого продукта с высоким выходом. 4 н. и 9 з.п. ф-лы, 7 пр.



1. Способ получения [4-(2-хлор-4-метокси-5-метилфенил)-5-метилтиазоло-2-ил]-[2-циклопропил-1-(3-фтор-4-метилфенил)-этил]-амина формулы (I)

отличающийся тем, что
a) соединение общей формулы (II)

где X обозначает галоген, подвергают взаимодействию с тиоцианатом щелочного металла в присутствии катализатора фазового переноса, и
b) полученный таким образом 2-тиоцианат-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-он формулы (III)

или его таутомерную форму подвергают взаимодействию с 2-циклопропил-1-(3-фтор-4-метилфенил)-этиламином формулы (IV)

2. Способ по п. 1, отличающийся тем, что на стадии b) к амину формулы (IV) добавляют кетон формулы (III).
3. Способ по п. 2, отличающийся тем, что добавление кетона формулы (III) к амину формулы (IV) осуществляют в течение по меньшей мере 1 часа.
4. Способ по любому из пп.1-3, отличающийся тем, что на стадии a) реакция проводится в бинарной системе, состоящей из апротонного растворителя и воды.
5. Способ по п.1, отличающийся тем, что стадия b) проводится в неполярном апротонном растворителе.
6. Способ по п.5, отличающийся тем, что неполярный апротонный растворитель, который используют на стадии b), является метилциклогексаном или толуолом.
7. Способ по п.1, отличающийся тем, что стадия b) проводится при температуре от 25°C и до температуры флегмы.
8. Способ по п.7, отличающийся тем, что стадия b) проводится при температуре флегмы.
9. Способ по п.1, отличающийся тем, что в общей формуле (II) X означает бром.
10. 2-тиоцианат-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-он

формулы (III) и его таутомеры.
11. Таутомер соединения формулы (III) по п.10, представляющий собой 5-(2-хлор-4-метокси-5-метилфенил)-4-метил-[1.3]-оксатиол-2-илиденамин формулы (V)

12. Способ получения 2-тиоцианат-1-(2-хлор-4-метокси-5-метилфенил)-пропан-1-она формулы (III)

отличающийся тем, что его производное общей формулы (II)
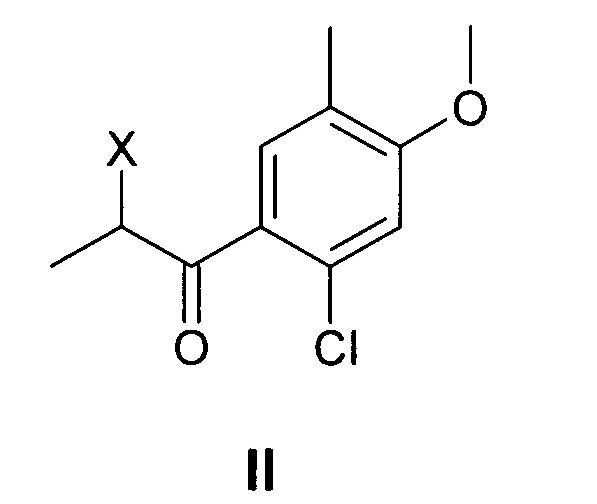
где X обозначает галоген, приводят во взаимодействие с тиоцианатом щелочного металла в присутствии катализатора фазового переноса.
13. Способ получения [4-(2-хлор-4-метокси-5-метилфенил)-5-метилтиазол-2-ил]-[2-циклопропил-1-(3-фтор-4-метилфенил)-этил]-амина формулы (I)

отличающийся тем, что 2-тиоцианат-1-(2-хлор-4-метокси-5-метил-фенил)-пропан-1-он формулы (III)

подвергают взаимодействию с 2-циклопропил-1-(3-фтор-4-метилфенил)-этиламином формулы (IV)

путем добавления к амину формулы (IV) кетона формулы (III).
| Судовой реактивный движитель | 1926 |
|
SU5159A1 |
| KIASAT A.R | |||
| et al.: "A facile and convenient method for synthesis of alkyl thiocyanates under homogeneous phase transfer catalyst conditions", CHINESE CHEMICAL LETTERS, 2008, vol.19, no.11, p.1301-1304 | |||
| MERIJANIAN A et al.:"Steric effect of ortho substituents on acid-catalyzed cyclization of thiocyanatoacetophenones", | |||
Авторы
Даты
2014-07-27—Публикация
2010-04-26—Подача