Перекрестная ссылка на родственные заявки
Данная заявка притязает на приоритет предварительной заявки на патент США № 61/014716, поданной 18 декабря 2007 г., которая полностью включена в настоящее описание изобретения ссылкой.
Область техники, к которой относится изобретение
Настоящее изобретение относится к антителам (таким как химерные и гуманизированные антитела), которые узнают углеводсодержащий эпитоп на CD43 и карциноэмбриональном антигене (СЕА), экспрессируемых на негемопоэтических опухолевых или раковых клетках. Указанные антитела способны индуцировать гибель (например, апоптоз) негемопоэтических опухолевых или раковых клеток при отсутствии конъюгации с цитотоксином и иммунной эффекторной функции. Указанные антитела могут быть использованы в качестве диагностических и терапевтических средств.
Уровень техники
CD43 (именуемый также сиалофорином или лейкосиалином) представляет собой сильно сиалилированную молекулу, экспрессированную в большом количестве на большинстве лейкоцитов человека, включая все Т-клетки и тромбоциты с молекулярной массой в пределах от 115000 до 135000. Экспрессия CD43 нарушена на Т-клетках мужчин, страдающих синдромом Вискота-Олдрича, который является сцепленным с Х-хромосомой рецессивным иммунодефицитом (Remold-O'Donnell et al. (1987) Blood 70(1):104-9; Remold-O'Donnel et al. (1984) J. Exp. Med. 159:1705-23).
Функциональные исследования показали, что моноклональное антитело против CD43 стимулирует пролиферацию Т-лимфоцитов в периферической крови (Mentzer et al. (1987) J. Exp. Med. 1; 165 (5):1383-92; Park et al. (1991) Nature, 350:706-9) и активацию моноцитов (Nong et al. (1989) J. Exp. Med. 1:170(1):259-67). Моноклональное антитело L11 против CD43 блокирует связывание Т-клеток с лимфатическим узлом и образование пейеровых бляшек. Антитело L11 ингибирует проникновение Т-клеток из крови в организованные вторичные лимфоидные ткани (McEvoy et al. (1997) J. Exp. Med. 185:1493-8). Моноклональное антитело, узнающее молекулу CD43, вызывает апоптоз гемопоэтических клеток-предшественников (НРС) костного мозга с отрицательной реакцией на маркер линии дифференцировки, которые экспрессируют CD34 с высокой степенью плотности (Bazil et al. (1996) Blood, 87(4):1271-81), и Т-лимфобластоидных клеток человека (Brown et al. (1996) J. Biol. Chem. 271:27686-95). Недавно выполненные исследования показали, что CD43 действует в качестве лиганда для Е-селектина на Т-клетках человека (Matsumoto et al. (2005) J. Immunol. 175:8042-50; Fuhlbrigge et al. (2006) Blood, 107:1421-6).
Кроме того, было установлено, что определенные негемопоэтические опухолевые клетки, в частности клетки колоректальной аденокарциномы, также экспрессируют молекулы CD43 на поверхности клеток. Santamaria et al. (1996) Cancer Research, 56:3526-9; Baeckstrom et al. (1995) J. Biol. Chem. 270:13688-92; Baeckstrom et al. (1997) J. Biol. Chem. 272:11503-9; Sikut et al. (1997) Biochem. Biophy. Res. Commun. 238:612-6. Было установлено, что гликаны на CD43, экспрессированном в линии клеток рака ободочной кишки (COLO205), отличаются от гликанов CD43 лейкоцитов (Baeckstrom et al. (1997) J. Biol. Chem. 272:11503-9). Хотя было высказано предположение, что сверхэкспрессия CD43 активирует белок-супрессор опухоли р53 (Kadaja et al. (2004) Oncogene 23:2523-30) и, таким образом, подавляет субпопуляцию генов-мишеней NF-каппа-В, частично путем ингибирования транскрипционной активности р65 (Laos et al. (2006) Int. J. Oncol. 28:695-704), по-прежнему отсутствуют прямые свидетельства участия CD43 в онкогенезе рака ободочной кишки. Стандартное антитело против CD43 не нашло практического применения в качестве терапевтического средства против негемопоэтических опухолевых клеток из-за сильного связывания данного антитела как с опухолевыми клетками, так и с иммунокомпетентными Т-клетками. Поэтому существует потребность в создании антител, которые специфически связываются с CD43, экспрессированным на негемопоэтических опухолевых или раковых клетках, но не связываются с CD43, экспрессированным на лейкоцитах или других гемопоэтических клетках. Такие антитела могут быть полезны в качестве терапевтических средств для лечения CD43-экспрессирующего рака негемопоэтического происхождения.
СЕА обычно экспрессирован в разных тканях железистого эпителия (таких как желудочно-кишечный тракт, дыхательные пути и мочеполовые пути), где указанный антиген локализован на апикальной поверхности клеток (Hammarstrom, S. (1999) Semin. Cancer Biol. 9, 67-81). В опухолях, образующихся из указанных тканей, имеет место повышенный уровень экспрессии СЕА, распространяющегося от апикальной мембранной области по всей поверхности клетки при одновременной секреции белка в кровь (Hammarstrom, S. (1999) Semin. Cancer. Biol. 9, 67-81). Чрезмерная экспрессия СЕА была отмечена во многих типах рака, включая колоректальный рак, рак поджелудочной железы, рак легкого, рак желудка, гепатоцеллюлярный рак, рак молочной железы и рак щитовидной железы. Поэтому СЕА служит в качестве маркера опухоли, и иммунологические анализы, позволяющие измерить повышенное содержание СЕА в крови субъектов, больных раком, уже давно используются в клинической практике для прогнозирования и лечения рака (Gold P., et al. (1965) J. Expl. Med. 122:467-81; Chevinsky, A.H. (1991) Semin. Surg. Oncol. 7, 162-166; Shively, J.E. et al. (1985) Crit. Rev. Oncol. Hematol. 2, 355-399).
Гораздо важнее то, что СЕА стал потенциально полезным опухолеассоциированным антигеном для целенаправленной терапии (Kuroki M., et al. (2002) Anticancer Res. 22:4255-64). Были разработаны две основные стратегии использования СЕА в качестве мишени для иммунотерапии рака. Один метод состоит в направленном воздействии на гены-самоубийцы (ген синтазы оксида азота (iNOS)) (Kuroki M. et al., (2000) Anticancer Res. 20(6A):4067-71) или изотопы (Wilkinson R.W. et al., (2001) PNAS USA 98, 10256-60, Goldenberg, D.M. (1991) Am. J. Gastroenterol., 86:1392-1403, Olafsen T. et al., Protein Engineering, Design & Selection, 17, 21-27, 2004) к СЕА-экспрессирующим опухолевым клеткам при помощи антител против СЕА. Указанный метод был также расширен до использования антитела или фрагмента антитела, конъюгированного с терапевтическими агентами, такими как лекарственные средства, токсины, радиоактивные изотопы, иммуномодуляторы или цитокины. Другой метод состоит в использовании иммунологической цитолитической активности, в частности, антителозависимой клеточноопосредованной цитотоксичности (ADCC) или комплементзависимой цитотоксичности (CDC), для устранения СЕА-экспрессирующих опухолевых клеток (Imakiire T. et al., (2004) Int. J. Cancer. 108, 564-570). При осуществлении указанных методов часто происходит высвобождение цитокинов, что вызывает системные побочные эффекты.
Антитела, узнающие углеводсодержащий эпитоп на CD43 и СЕА, экспрессируемых на негемопоэтических раковых клетках, описаны в публикации заявки на патент США № 2008/0171043 и РСТ WO 07/146172. Указанные антитела могут индуцировать апоптоз негемопоэтических раковых клеток при отсутствии конъюгации с цитотоксином и иммунной эффекторной функции.
Все ссылки, публикации и заявки на патенты, приведенные в настоящем изобретении, полностью включены в настоящее описание изобретения в виде ссылки.
Сущность изобретения
Настоящее изобретение относится к антителам (таким как химерные и гуманизированные антитела), которые специфически связываются с эпитопом на CD43 и/или СЕА, экспрессируемых негемопоэтической раковой клеткой, но специфически не связываются с CD43, экспрессируемым лейкоцитом или клеткой Джурката, и могут индуцировать апоптоз негемопоэтической раковой клетки после связывания с эпитопом, экспрессированным на поверхности негемопоэтической раковой клетки при отсутствии конъюгации с цитотоксином и иммунной эффекторной функции, при этом указанный эпитоп содержит углевод и связывание антитела с данным эпитопом ингибируется углеводом, имеющим структуру Lea, структуру Lea-лактозы, структуру LNDFH II или структуру LNT. В некоторых вариантах осуществления изобретения эпитоп, с которым связываются указанные антитела, чувствителен к фукозе.
В некоторых вариантах осуществления изобретения указанные антитела являются химерными или гуманизированными антителами, полученными из мышиного антитела m5F1, имеющего инсерцию, делецию или замену по меньшей мере одной аминокислоты в шарнирной области константной области тяжелой цепи.
Некоторые варианты осуществления изобретения относятся к выделенным антителам, включающим тяжелую цепь и легкую цепь, где (а) тяжелая цепь содержит вариабельную область тяжелой цепи, включающую три области, определяющие комплементарность, из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи IgG1 человека, при этом шарнирная область константной области тяжелой цепи содержит инсерцию, делецию или замену по меньшей мере одной аминокислоты; и (b) легкая цепь содержит вариабельную область легкой цепи, включающую три области, определяющие комплементарность, из аминокислотной последовательности SEQ ID NO:2, и константную область легкой цепи из легкой каппа-цепи человека или константную область легкой цепи из легкой каппа-цепи человека, включающую инсерцию, делецию или замену по меньшей мере одной аминокислоты. В некоторых вариантах осуществления изобретения константная область тяжелой цепи содержит аминокислотную последовательность SEQ ID NO:27 или SEQ ID NO:29.
В некоторых вариантах осуществления изобретения со стороны N-конца аминокислоты К218 в шарнирной области IgG1 человека вставлены одна, две, три, четыре, пять, шесть, семь, восемь, девять или десять аминокислот, при этом нумерация остатков соответствует системе нумерации EU. См. публикацию Burton, Mol. Immunol. 22:161-206, 1985. В некоторых вариантах осуществления изобретения со стороны N-конца аминокислоты К218 вставлены аминокислотные остатки KSD.
В некоторых вариантах осуществления изобретения антитела включают: (а) вариабельную область тяжелой цепи, содержащую три CDR-области из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, содержащую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:11-30; и (b) вариабельную область легкой цепи, содержащую три CDR-области из аминокислотной последовательности SEQ ID NO:2, и константную область легкой цепи, содержащую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:10 и 31-37. В некоторых вариантах осуществления изобретения указанное антитело является гуманизированным антителом. В некоторых вариантах осуществления изобретения указанное антитело является химерным антителом. В некоторых вариантах осуществления изобретения вариабельная область тяжелой цепи включает аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:1, 3 и 87-91. В некоторых вариантах осуществления изобретения вариабельная область легкой цепи включает аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:2, 4 и 92-96. В некоторых вариантах осуществления изобретения вариабельная область тяжелой цепи антитела включает аминокислотную последовательность остатков 20-137 SEQ ID NO:1 или SEQ ID NO:3 или аминокислотную последовательность вариабельной области из SEQ ID NO:1 или SEQ ID NO:3. В некоторых вариантах осуществления изобретения вариабельная область легкой цепи антитела включает аминокислотную последовательность остатков 20-131 SEQ ID NO:2, аминокислотную последовательность вариабельной области из SEQ ID NO:2, аминокислотную последовательность остатков 21-132 SEQ ID NO:4 или аминокислотную последовательность вариабельной области из SEQ ID NO:4.
В некоторых вариантах осуществления изобретения антитело по настоящему изобретению включает тяжелую цепь и легкую цепь, при этом тяжелая цепь содержит вариабельную область тяжелой цепи, включающую аминокислотную последовательность остатков 20-137 SEQ ID NO:1 или аминокислотную последовательность вариабельной области из SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность SEQ ID NO:27, и легкая цепь содержит вариабельную область легкой цепи, включающую аминокислотную последовательность остатков 20-131 SEQ ID NO:2 или аминокислотную последовательность вариабельной области из SEQ ID NO:2, и константную область легкой цепи, включающую аминокислотную последовательность SEQ ID NO:10.
В некоторых вариантах осуществления изобретения антитело по настоящему изобретению включает тяжелую цепь и легкую цепь, при этом тяжелая цепь содержит вариабельную область тяжелой цепи, включающую аминокислотную последовательность остатков 20-137 SEQ ID NO:1 или аминокислотную последовательность вариабельной области из SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность SEQ ID NO:29, и легкая цепь содержит вариабельную область легкой цепи, включающую аминокислотную последовательность остатков 20-131 SEQ ID NO:2 или аминокислотную последовательность вариабельной области из SEQ ID NO:2, и константную область легкой цепи, включающую аминокислотную последовательность SEQ ID NO:34.
В некоторых вариантах осуществления изобретения антитело по настоящему изобретению включает тяжелую цепь и легкую цепь, при этом тяжелая цепь содержит вариабельную область тяжелой цепи, включающую аминокислотную последовательность остатков 20-137 SEQ ID NO:1 или аминокислотную последовательность вариабельной области из SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность SEQ ID NO:29, и легкая цепь содержит вариабельную область легкой цепи, включающую аминокислотную последовательность остатков 20-131 SEQ ID NO:2 или аминокислотную последовательность вариабельной области из SEQ ID NO:2, и константную область легкой цепи, включающую аминокислотную последовательность SEQ ID NO:35.
Настоящее изобретение относится также к антигенсвязывающим фрагментам антител, раскрытых в настоящем описании изобретения.
Настоящее изобретение относится также к фармацевтическим композициям, включающим одно или несколько антител по настоящему изобретению или их антигенсвязывающие фрагменты и фармацевтически приемлемый носитель.
Настоящее изобретение относится к полинуклеотидам и векторам, включающим последовательность нуклеиновой кислоты, кодирующую тяжелую цепь антитела по настоящему изобретению и/или легкую цепь антитела по настоящему изобретению или его фрагмента. В некоторых вариантах осуществления изобретения полинуклеотиды и векторы включают последовательность нуклеиновой кислоты, кодирующую тяжелую цепь, содержащую вариабельную область тяжелой цепи, включающую три CDR-области из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:11-30. В некоторых вариантах осуществления изобретения полинуклеотиды и векторы включают последовательность нуклеиновой кислоты, кодирующую легкую цепь, содержащую вариабельную область легкой цепи, включающую три CDR-области из аминокислотной последовательности SEQ ID NO:2, и константную область легкой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:10 и 31-37.
Настоящее изобретение относится также к клеткам-хозяевам, содержащим полинуклеотиды и векторы, раскрытые в настоящем описании изобретения.
Настоящее изобретение далее относится к способам получения любых антител или их антигенсвязывающих фрагментов, рассмотренных в настоящем описании изобретения. Указанные способы могут включать стадию экспрессии одного или нескольких полинуклеотидов, кодирующих антитела (которые могут быть экспрессированы отдельно в виде единичной тяжелой или легкой цепи, либо в одном векторе могут быть экспрессированы как тяжелая цепь, так и легкая цепь) или их антигенсвязывающие фрагменты в приемлемой клетке-хозяине. В некоторых вариантах осуществления изобретения экспрессированные антитела или их антигенсвязывающие фрагменты отделяют и/или выделяют. Настоящее изобретение относится также к антителам или антигенсвязывающим фрагментам, полученным указанными способами.
Настоящее изобретение относится к способу лечения рака негемопоэтического происхождения у субъекта, который включает введение указанному субъекту эффективного количества композиции, содержащей одно или несколько антител по настоящему изобретению, которые связываются с раковыми клетками в организме субъекта. В некоторых вариантах осуществления изобретения рак негемопоэтического происхождения является колоректальным раком, раком поджелудочной железы или раком желудка. В некоторых вариантах осуществления изобретения антитело конъюгировано с цитотоксином.
Настоящее изобретение относится к способу замедления развития рака негемопоэтического происхождения (в частности, к замедлению и/или торможению развития рака) у субъекта, который включает введение указанному субъекту эффективного количества композиции, содержащей одно или несколько антител по настоящему изобретению, которые связываются с раковыми клетками в организме субъекта. В некоторых вариантах осуществления изобретения рак негемопоэтического происхождения является колоректальным раком, раком поджелудочной железы или раком желудка. В некоторых вариантах осуществления изобретения антитело конъюгировано с цитотоксином.
Настоящее изобретение относится также к способу лечения рака негемопоэтического происхождения у субъекта, который включает введение указанному субъекту определенного количества одного или нескольких антител по настоящему изобретению и определенного количества другого противоракового средства, при этом одно или несколько антител связываются с раковыми клетками в организме субъекта, благодаря чему одно или несколько антител совместно с противораковым средством обеспечивают эффективное лечение рака у указанного субъекта. В некоторых вариантах осуществления изобретения рак негемопоэтического происхождения является колоректальным раком, раком поджелудочной железы или раком желудка. В некоторых вариантах осуществления изобретения противораковое средство является химиотерапевтическим средством.
Настоящее изобретение далее относится к наборам, включающим фармацевтическую композицию, содержащую одно или несколько антител по настоящему изобретению. В некоторых вариантах осуществления изобретения наборы дополнительно включают инструкции по введению субъекту эффективного количества фармацевтической композиции для лечения рака негемопоэтического происхождения. В некоторых вариантах осуществления изобретения наборы включают инструкции по введению фармацевтической композиции совместно с другим противораковым средством. В некоторых вариантах осуществления изобретения антитело включает (а) вариабельную область тяжелой цепи, включающую три CDR-области из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:11-30; и (b) вариабельную область легкой цепи, включающую три CDR-области из аминокислотной последовательности SEQ ID NO:2, и константную область, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:10 и 31-37.
Настоящее изобретение относится также к наборам, включающим первую фармацевтическую композицию, содержащую антитело или антигенсвязывающий фрагмент по настоящему изобретению, вторую фармацевтическую композицию, содержащую другое противораковое средство, и инструкции по совместному введению субъекту первой фармацевтической композиции и второй фармацевтической композиции для лечения рака негемопоэтического происхождения.
Следует отметить, что некоторые или все признаки разных вариантов осуществления изобретения могут быть объединены с образованием других вариантов осуществления настоящего изобретения. Специалисту в данной области должны быть очевидны вышеуказанные и другие цели настоящего изобретения.
Краткое описание фигур
На фиг.1 показан сравнительный анализ аминокислотных последовательностей константной области тяжелой цепи IgG3 мыши (SEQ ID NO:138) и константной области тяжелой цепи IgG1 человека (SEQ ID NO:139). Шарнирная область подчеркнута. Как показано на данной фигуре, идентичность аминокислот составляет 214/333 (64,3%), сходство составляет 261/333 (78,4%) и разрывы составляют 6/333 (1,8%).
На фиг.2(А-Е) показан сравнительный анализ аминокислотных последовательностей немодифицированных и модифицированных константных областей тяжелой цепи IgG1 человека, и на фигуре 2F показан сравнительный анализ аминокислотных последовательностей немодифицированных и модифицированных константных областей легкой каппа-цепи IgG1 человека.
На фиг.3 показано связывание антител m5F1, c5F1v0, c5F1v15 и c5F1v16 с клетками Colo205 по результатам проточного цитометрического анализа при использовании антител в разных концентрациях от 0,125 мкг/мл до 4 мкг/мл. Фоновыми сигналами (MFI) для контрольных антител являются: вторичное антитело против мыши: 3; вторичное антитело против человека: 3; IgG мыши: 4; IgG человека: 5. Все антитела, m5F1, c5F1v0, c5F1v15 и c5F1v16, характеризуются значительным связыванием с клетками Colo205 по сравнению с фоновыми сигналами.
На фиг.4(А и В) показан сравнительный анализ аминокислотных последовательности VH(a) и VL(b) антител h5F1M, h5F1A Va, h5F1A Vs, h5F1M Va и h5F1M Vs.
Подробное описание изобретения
Определения терминов
Термин “антитело” означает молекулу иммуноглобулина, способную специфически связываться с мишенью, такой как углевод, полинуклеотид, липид, полипептид и т.д., при помощи по меньшей мере одного сайта узнавания антигена, расположенного в вариабельной области молекулы иммуноглобулина. В использованном здесь значении указанный термин означает не только интактные поликлональные или моноклональные антитела, но также их фрагменты (такие как Fab, Fab', F(ab')2, Fv), одноцепочечный фрагмент (ScFv), их мутанты, слитые белки, включающие антитело, и любую другую модифицированную конфигурацию молекулы иммуноглобулина, которая включает сайт узнавания антигена. Антитело является антителом любого класса, таким как IgG, IgA или IgM (или их подкласса), при этом указанное антитело не обязательно должно относиться к любому определенному классу. В зависимости от аминокислотной последовательности константной области тяжелых цепей антитела иммуноглобулины могут быть отнесены к разным классам. Существует пять основных классов иммуноглобулинов: IgA, IgD, IgE, IgG и IgM, и некоторые из указанных классов могут быть далее разделены на подклассы (изотипы), например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2. Константные области тяжелой цепи, которые соответствуют другим классам иммуноглобулинов, именуются соответственно альфа, дельта, эпсилон, гамма и мю. Хорошо известны субъединичные структуры и трехмерные конфигурации разных классов иммуноглобулинов.
Антитело по настоящему изобретению дополнительно включает биспецифические, полиспецифические, одноцепочечные, химерные и гуманизированные молекулы, обладающие сродством к полипептиду, сообщаемым по меньшей мере одной областью, определяющей комплементарность, (CDR) антитела. Антитела по настоящему изобретению включают также антитела с одной областью, которая является или вариабельной областью тяжелой цепи антитела, или вариабельной областью легкой цепи антитела. Holt et al., (2003), Trends Biotechnol. 21:484-490. В данной области хорошо известны способы получения антител с одной областью, содержащих или вариабельную область тяжелой цепи антитела, или вариабельную область легкой цепи антитела, включающую три из шести естественных областей, определяющих комплементарность, антитела. См., например, публикацию Muyldermans, Rev. Mol. Biotechnol. 74:277-302, 2001.
В использованном здесь значении термин “моноклональное антитело” означает антитело из популяции по существу гомогенных антител, то есть отдельные антитела, образующие популяцию, являются идентичными, за исключением возможных естественных мутаций, которые могут присутствовать в незначительных количествах. Моноклональные антитела обычно являются высоко специфичными, направленно воздействующими на одну область детерминанты в молекуле антигена. Кроме того, в отличие от препаратов на основе поликлональных антител, которые обычно включают разные антитела, направленно воздействующие на разные детерминанты (эпитопы), каждое моноклональное антитело направленно воздействует на одну детерминанту антигена. Определение “моноклональное” служит для обозначения характера антитела, получаемого из по существу гомологичной популяции антител, и не ограничивает получение данного антитела любым конкретным способом. Например, моноклональные антитела, предназначенные для использования в соответствии с настоящим изобретением, могут быть получены способом гибридом, впервые описанным в публикации Kohler and Milstein, (1975), Nature, 256:495, или способами рекомбинантных ДНК, описанными в патенте США № 4816567. Моноклональные антитела могут быть также выделены из библиотек фагов, созданных методами, описанными, например, в публикации McCafferty et al., (1990), Nature, 348:552-554.
В использованном здесь значении термин “химерное антитело” означает антитело, содержащее вариабельную область или часть вариабельной области первого вида и константную область второго вида. Интактное химерное антитело включает две копии химерной легкой цепи и две копии химерной тяжелой цепи. В данной области известно получение химерных антител (Cabilly et al. (1984), Proc. Natl. Acad. Sci. USA, 81:3273-3277; Harlow and Lane (1988), Antibodies: a Laboratory Manual, Cold Spring Harbor Laboratory). В указанных химерных антителах вариабельная область как легкой, так и тяжелой цепей обычно имитирует вариабельные области антител, полученных у одного вида млекопитающих, в то время как константные области гомологичны последовательностям в антителах, выделенных у другого вида. В некоторых вариантах осуществления изобретения в вариабельной области и/или константной области могут быть модифицированы аминокислоты.
“Выделенное” антитело является антителом, которое было идентифицировано и выделено из естественного окружения.
В использованном здесь значении термин “по существу чистый” означает вещество, которое является чистым (то есть свободным от загрязняющих примесей) по меньшей мере на 50%, более предпочтительно по меньшей мере на 90%, более предпочтительно по меньшей мере на 95%, более предпочтительно по меньшей мере на 98%, еще предпочтительнее по меньшей мере на 99%.
В использованном здесь значении “гуманизированные” антитела означают формы антител, отличных от человеческих (например, мышиных), которые являются специфичными химерными иммуноглобулинами, цепями иммуноглобулинов или их фрагментами (такими как Fv, Fab, Fab', F(ab')2 или другие антигенсвязывающие последовательности антител) и содержат минимальную последовательность, выделенную из иммуноглобулина, отличного от человеческого. В большинстве случаев гуманизированные антитела являются иммуноглобулинами человека (реципиентное антитело), в которых остатки из области, определяющей комплементарность, (CDR) реципиента заменены остатками из CDR вида, отличного от человека (донорное антитело), такого как мышь, крыса или кролик, обладающего требуемой специфичностью, сродством и антигенсвязывающей способностью. В некоторых случаях остатки каркасной области (FR) Fv-фрагмента иммуноглобулина человека заменены соответствующими остатками, отличными от человеческих. Кроме того, гуманизированное антитело может включать остатки, отсутствующие как в реципиентном антителе, так и во введенных последовательностях CDR или каркасной области, но включенные для дальнейшего улучшения и оптимизации характеристик антитела. Как правило, гуманизированное антитело включает по существу все вариабельные области, по меньшей мере одну и обычно две, в которых все или по существу все CDR-области соответствуют указанным областям иммуноглобулина, отличного от человеческого, и все или по существу все каркасные области являются каркасными областями консенсусной последовательности иммуноглобулина человека. Гуманизированное антитело оптимально также включает по меньшей мере часть константной области или домена (Fc) иммуноглобулина, обычно иммуноглобулина человека. Антитела могут иметь Fc-области, модифицированные в соответствии с описанием, приведенным в публикации WO 99/58572. Другие формы гуманизированных антител содержат одну или несколько CDR-областей (одну, две, три, четыре, пять, шесть), измененных по сравнению с первоначальным антителом, которые также именуются одной или несколькими CDR-областями, “выделенными из” одной или нескольких CDR-областей первоначального антитела.
В использованном здесь значении термин “человеческое антитело” означает антитело, содержащее аминокислотную последовательность, соответствующую аминокислотной последовательности антитела, продуцированного человеком и/или полученного любыми методами получения человеческих антител, известными в данной области или рассмотренными в настоящем описании изобретения. В данное определение человеческого антитела входят антитела, включающие по меньшей мере один полипептид тяжелой цепи человека или по меньшей мере один полипептид легкой цепи человека. В качестве одного такого примера можно привести антитело, включающее полипептиды легкой цепи мыши и тяжелой цепи человека. Человеческие антитела могут быть получены разными методами, известными в данной области. В одном варианте осуществления изобретения человеческое антитело выбирают из библиотеки фагов, экспрессирующей человеческие антитела (Vaughan et al., 1996, Nature Biotechnology, 14:309-314; Sheets et al., (1998), PNAS, (USA) 95:6157-6162; Hoogenboom and Winter, 1991, J. Mol. Biol., 227:381; Marks et al., (1991), J. Mol. Biol., 222:581). Человеческие антитела могут быть также получены путем введения локусов иммуноглобулина человека трансгенным животным, например, мышам, у которых были частично или полностью инактивированы гены эндогенного иммуноглобулина. Данный метод описан в патентах США №№ 5545807, 5545806, 5569825, 5625126, 5633425 и 5661016. Альтернативно человеческое антитело может быть получено путем иммортализации В-лимфоцитов человека, продуцирующих антитело против антигена-мишени (такие В-лимфоциты могут быть выделены у субъекта или могут быть иммунизированы in vitro). См., например, публикации Cole et al., Monoclonal Antibodies and Cancer Therapy, Alan R. Liss, p.77 (1985); Boerner et al., (1991), J. Immunol., 147(1):86-95; и патент США № 5750373.
Термин “вариабельная область” антитела означает вариабельную область легкой цепи антитела или вариабельную область тяжелой цепи антитела, рассматриваемые отдельно или в комбинации. Вариабельные области тяжелой и легкой цепей состоят из четырех каркасных областей (FR), соединенных тремя областями, определяющими комплементарность (CDR), известными также как гипервариабельные участки. CDR-области в каждой цепи удерживаются в непосредственной близости друг от друга каркасными областями (FR) и вместе с CDR-областями из другой цепи способствуют образованию антигенсвязывающего центра антител. Существуют по меньшей мере два метода определения CDR-областей: (1) метод на основе вариабельности последовательностей в разных видах (Kabat et al., Sequences of Proteins of Immunological Interest, (5th ed., 1991, National Institutes of Health, Bethesda, MD)); и (2) метод на основе кристаллографического исследования комплексов антиген-антитело (Al-lazikani et al., (1997) J. Molec. Biol. 273:927-948)). В использованном здесь значении CDR может означать CDR-области, выявленные любым методом или комбинацией обоих методов.
Термин “константная область” антитела означает константную область легкой цепи антитела или константную область тяжелой цепи антитела, рассматриваемые отдельно или в комбинации. Константная область антитела обычно обеспечивает устойчивость структуры и выполняет другие биологические функции, такие как сборка цепи антитела, секреция, трансплацентарная подвижность и связывание комплемента, но не участвует в связывании с антигеном. Аминокислотная последовательность и последовательности соответствующих экзонов в генах константной области зависят от вида, из которого они выделены; однако изменения аминокислотной последовательности, ведущие к образованию аллотипов, весьма ограничены для конкретных константных областей определенного вида. Вариабельная область каждой цепи присоединена к константной области при помощи линкерной полипептидной последовательности. Линкерная последовательность обозначена как последовательность “J” в гене легкой цепи и как комбинация последовательности “D” и последовательности “J” в гене тяжелой цепи.
В использованном здесь значении термины “антителозависимая клеточноопосредованная цитотоксичность” и “ADCC” означают клеточноопосредованную реакцию, в соответствии с которой неспецифические цитотоксические клетки, экспрессирующие Fc-рецепторы (FcR) (например, естественные клетки-киллеры (NK-клетки), нейтрофилы и макрофаги) узнают связанное антитело на клетке-мишени и вызывают лизис такой клетки-мишени. Активность ADCC представляющей интерес молекулы можно оценить при помощи анализа ADCC in vitro, аналогичного описанному в патенте США № 5500362 или 5821337. Эффекторные клетки, пригодные для выполнения таких анализов, включают мононуклеарные клетки (РВМС) и NK-клетки периферической крови. Альтернативно или дополнительно активность ADCC представляющей интерес молекулы можно определить in vivo, например, в животной модели, аналогичной описанной в публикации Clynes et al., 1998, PNAS (USA), 95:652-656.
Термины “комплементзависимая цитотоксичность” и “CDC” означают лизис мишени в присутствии комплемента. Путь активации комплемента инициируется связыванием первого компонента системы комплементов (C1q) с молекулой (например, антителом), образующей комплекс с родственным антигеном. Для оценки активации комплемента может быть выполнен анализ CDC, например, аналогичный описанному в публикации Gazzano-Santoro et al., J. Immunol. Methods, 202:163 (1996).
Термины “полипептид”, “олигопептид”, “пептид” и “белок” имеют взаимозаменяемые значения в настоящем описании изобретения и означают полимеры аминокислот любой длины. Полимер может быть линейным или разветвленным, он может включать модифицированные аминокислоты и может прерываться кислотами, отличными от аминокислот. В определение указанных терминов входит также полимер аминокислоты, модифицированный естественным или искусственным путем, например, в результате образования дисульфидной связи, гликозилирования, липидирования, ацетилирования, фосфорилирования или любых других манипуляций или модификаций, таких как конъюгация с компонентом, используемым в качестве метки. В определение указанных терминов также входят, например, полипептиды, содержащие один или несколько аналогов аминокислоты (включающие, например, неприродные аминокислоты и т.д.), а также другие модификации, известные в данной области. Следует отметить, что поскольку полипептиды по настоящему изобретению созданы на основе антитела, то указанные полипептиды могут существовать в виде отдельных цепей или связанных цепей.
Термины “полинуклеотид” или “нуклеиновая кислоты” имеют взаимозаменяемые значения в настоящем описании изобретения, означают полимеры нуклеотидов любой длины и включают ДНК и РНК. Указанные нуклеотиды могут быть дезоксирибонуклеотидами, рибонуклеотидами, модифицированными нуклеотидами или основаниями и/или их аналогами либо любым субстратом, который может быть введен в полимер ДНК- или РНК-полимеразой. Полинуклеотид может включать модифицированные нуклеотиды, такие как метилированные нуклеотиды и их аналоги. При наличии модификации структура нуклеотида может быть изменена до или после сборки полимера. Последовательность нуклеотидов может прерываться компонентами, не являющимися нуклеотидами. Полинуклеотид может быть дополнительно модифицирован после полимеризации, например, путем конъюгации с компонентом, используемым в качестве метки. Другие типы модификаций включают, например, “кэпы”, замены одного или нескольких естественных нуклеотидов аналогом, межнуклеотидные модификации, например, замены с неполяризованными связями (такие как, например, метилфосфонаты, сложные фосфотриэфиры, фосфоамидаты, карбаматы и т.д.) и замены с поляризованными связями (такие как, например, фосфортиоаты, фосфордитиоаты и т.д.), замены, содержащие боковые цепи, такие как, например, белки (например, нуклеазы, токсины, антитела, сигнальные пептиды, ply-L-лизин и т.д.), замены с интеркаляторами (такие как, например, акридин, псорален и т.д.), замены, содержащие хелаторы (такие как, например, металлы, радиоактивные металлы, бор, окислительные металлы и т.д.), замены, содержащие алкилаторы, замены с модифицированными связями (такие как, например, альфа-аномерные нуклеиновые кислоты и т.д.), а также немодифицированные формы полинуклеотидов. Кроме того, любые гидроксильные группы, обычно присутствующие в сахарах, могут быть заменены, например, фосфонатными группами, фосфатными группами, защищенными стандартными защитными группами, активированы с целью получения дополнительных связей с дополнительными нуклеотидами или конъюгированы с твердыми носителями. 5'- и 3'-концевая группа ОН может быть фосфорилирована или замещена аминами или органическими кэппирующими группами, содержащими 1-20 атомов углерода. Другие гидроксилы также могут быть заменены с использованием стандартных защитных групп. Полинуклеотиды могут также содержать аналоги сахаров рибозы или дезоксирибозы, известные в данной области, которые включают, например, 2'-О-метил-, 2'-О-аллил-, 2'-фтор- или 2'-азидорибозу, карбоциклические аналоги сахаров, α-аномерные сахара, эпимерные сахара, такие как арабиноза, ксилозы или ликсозы, пиранозы, фуранозы, седогептулозы, ациклические аналоги и основные аналоги нуклеозидов, такие как метилрибозид. Одна или несколько сложных фосфодиэфирных связей могут быть заменены альтернативными связующими группами. Такие альтернативные связующие группы включают, не ограничиваясь ими, варианты, в которых фосфат заменен Р(О)S (”тиоат”), Р(S)S (”дитиоат”), (О)NR2 (”амидат”), Р(О)R, P(O)OR', CO или СН2 (”формацеталь”), где R или R' независимо означают Н, замещенный или незамещенный алкил (1-20 атомов углерода), необязательно содержащий простую эфирную (-О-) связь, арил, алкенил, циклоалкил, циклоалкенил или аралдил. Не все связи в полинуклеотиде должны быть идентичными. Приведенное выше описание относится ко всем полинуклеотидам, приведенным в настоящем описании изобретения, включая РНК и ДНК.
В использованном здесь значении термин “вектор” означает конструкцию, способную доставлять и предпочтительно экспрессировать один или несколько представляющих интерес генов или последовательностей в клетке-хозяине. Примеры векторов включают, не ограничиваясь ими, вирусные векторы, экспрессирующие векторы на основе депротеинизированной ДНК или РНК, плазмиду, космиду или фаговые векторы, экспрессирующие векторы на основе ДНК или РНК, ассоциированные с катионными конденсирующими агентами, экспрессирующие векторы на основе ДНК или РНК, инкапсулированные в липосомы, и определенные эукариотические клетки, такие как клетки-продуценты.
В использованном здесь значении термин “последовательность, регулирующая экспрессию” означает последовательность нуклеиновой кислоты, которая направляет транскрипцию нуклеиновой кислоты. Последовательность, регулирующая экспрессию, может быть промотором, таким как конститутивный или индуцибельный промотор, или энхансером. Последовательность, регулирующая экспрессию, функционально связана с транскрибируемой последовательностью нуклеиновой кислоты.
В использованном здесь значении термин “эффективная доза” или “эффективное количество” лекарственного средства, соединения или фармацевтической композиции означает количество, достаточное для достижения благоприятных или требуемых результатов. При профилактическом применении благоприятные или требуемые результаты означают устранение или уменьшение риска, ослабление тяжести или задержку возникновения заболевания, включая биохимические, гистологические и/или поведенческие симптомы заболевания, его осложнения, промежуточные патологические фенотипы, возникающие в процессе развития заболевания. При терапевтическом применении благоприятные или требуемые результаты означают ослабление одного или нескольких симптомов заболевания, улучшение качества жизни субъектов, страдающих данным заболеванием, уменьшение дозы других лекарственных средств, необходимых для лечения данного заболевания, усиление эффекта, достигаемого другим лекарственным средством, такого как направленное воздействие, замедление развития заболевания и/или увеличение продолжительности жизни. В случае рака или опухоли эффективное количество лекарственного средства может обеспечить сокращение числа раковых клеток; уменьшение объема опухоли; ингибирование (то есть замедление в некоторой степени и предпочтительно прекращение) инфильтрации раковых клеток в периферические органы; ингибирование (то есть замедление в некоторой степени и предпочтительно прекращение) образования метастазов опухоли; ингибирование в некоторой степени роста опухоли и/или ослабление в некоторой степени одного или нескольких симптомов, ассоциированных с данным нарушением. Эффективную дозу можно вводить в один или несколько приемов. В соответствии с целями настоящего изобретения эффективная доза лекарственного средства, соединения или фармацевтической композиции представляет собой количество, достаточное для профилактического или терапевтического лечения прямыми или непрямыми методами. Как должно быть понятно в контексте клинической практики, эффективная доза лекарственного средства, соединения или фармацевтической композиции может быть получена или не получена при использовании совместно с другим лекарственным средством, соединением или фармацевтической композицией. Таким образом, “эффективная доза” может быть рассмотрена с точки зрения введения одного или нескольких лекарственных средств, при этом считается, что одно средство введено в эффективном количестве, если при совместном введении с одним или несколькими другими средствами может быть достигнут или имеет место требуемый результат.
В использованном здесь значении термин “в сочетании с” означает применение одного способа терапевтического воздействия в дополнение к другому способу терапевтического воздействия. Таким образом, термин “в сочетании с” означает применение одного способа терапевтического воздействия до, во время или после применения другого способа терапевтического воздействия к нуждающемуся субъекту.
В использованном здесь значении термин “лечение” означает метод достижения благоприятных или требуемых результатов, включая предпочтительно клинические результаты. В соответствии с целями настоящего изобретения благоприятные или требуемые клинические результаты включают, не ограничиваясь ими, один или несколько следующих результатов: уменьшение пролиферации (или разрушение) раковых клеток, ослабление симптомов, обусловленных данным заболеванием, улучшение качества жизни субъектов, страдающих данным заболеванием, сокращение дозы других лекарственных средств, необходимых для лечения заболевания, замедление развития заболевания и/или увеличение продолжительности жизни субъектов.
В использованном здесь значении термин “замедление развития заболевания” означает задержку, воспрепятствование, замедление, торможение, стабилизацию и/или отсрочку развития заболевания (такого как рак). Задержка может иметь разную продолжительность в зависимости от истории болезни и/или состояния субъекта, подлежащего лечению. Как должно быть известно специалисту в данной области, достаточная или значительная задержка фактически может быть равнозначна предотвращению развитию заболевания у субъекта. Например, можно замедлить развитие рака на поздней стадии, в частности, предотвратить образование метастазов.
Термин “субъект” означает млекопитающее, более предпочтительно человека. Млекопитающие также включают, не ограничиваясь ими, сельскохозяйственных животных, спортивных животных, домашних животных (таких как кошки, собаки, лошади), приматов, мышей и крыс.
В использованном здесь значении термин “специфически узнает” или “специфически связывается” означает измеряемые или воспроизводимые взаимодействия, такие как притяжение или связывание мишени с антителом, которое является показателем наличия мишени в присутствии гетерогенной популяции молекул, включающей биологические молекулы. Например, антитело, которое специфически или предпочтительно связывается с эпитопом, является антителом, которое связывается с указанным эпитопом с большим сродством, авидностью, гораздо легче и/или в течение более длительного периода, чем с другими эпитопами мишени или эпитопами молекул, не являющихся мишенями. Из данного определения следует, что, например, антитело (часть или эпитоп), которое специфически или предпочтительно связывается с первой мишенью, может или не может специфически или предпочтительно связываться со второй мишенью. Таким образом, термин “специфическое связывание” или “предпочтительное связывание” не обязательно предполагает (хотя и может включать) исключительное связывание. Антитело, специфически связывающееся с мишенью, может иметь константу ассоциации, равную по меньшей мере примерно 103 М-1 или 104 М-1, иногда примерно 105 М-1 или 106 М-1, в других случаях примерно 106 М-1 или 107 М-1, примерно 108 М-1 - 109 М-1, примерно 1010 М-1 - 1011 М-1 или выше. Для отбора антител, обладающих специфической иммунореактивностью в отношении определенного белка, могут быть использованы разные иммуноанализы. Например, для отбора моноклональных антител, обладающих специфической иммунореактивностью в отношении определенного белка, обычно используют твердофазные иммуноферментные анализы (ELISA). См., например, публикацию Harlow and Lane (1988), Antibodies, A Laboratory Manual, Cold Spring Harbor Publications, New York, для ознакомления с описанием иммуноанализов и условий, которые могут быть использованы для определения специфической иммунореактивности.
В использованном здесь значении термины “рак”, “опухоль”, “раковый” и “злокачественный” определяют или описывают физиологическое состояние у млекопитающих, которое обычно характеризуется нерегулируемым ростом клеток. Примеры рака включают, не ограничиваясь ими, карциному, в том числе аденокарциному, лимфому, бластому, меланому и саркому. Более конкретные примеры таких типов рака включают плоскоклеточный рак, мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого, плоскоклеточную карциному легкого, рак желудочно-кишечного тракта, лимфому Ходжкина и неходжкинскую лимфому, рак поджелудочной железы, глиобластому, рак шейки матки, глиому, рак яичника, рак печени, такой как карцинома печени и гепатома, рак мочевого пузыря, рак молочной железы, рак ободочной кишки, колоректальный рак, карциному эндометрия или матки, карциному слюнной железы, рак почки, такой как почечно-клеточный рак и опухоли Вильмса, базальноклеточный рак, меланому, рак предстательной железы, рак щитовидной железы, рак яичка, рак пищевода и разные типы рака головы и шеи.
В значении, использованном в настоящем описании изобретения и прилагаемой формуле изобретения, формы единственного числа включают также формы множественного числа, за исключением тех случаев, когда из контекста ясно следует обратное. Например, термин “антитело” в единственном числе означает как одно, так и множество антител, в частности, молярные количества, и включает его эквиваленты, известные специалистам в данной области, и так далее.
Следует отметить, что объекты и варианты осуществления изобретения, рассмотренные в настоящем описании изобретения, включают объекты и варианты, определяемые терминами “состоящие из” и/или “состоящие по существу из”.
Антитела и полипептиды, которые специфически связываются с углеводным эпитопом на CD43 и СЕА, экспрессируемых на негемопоэтических раковых клетках
Настоящее изобретение относится к выделенным антителам и полипептидам, полученным из антител, которые специфически связываются с эпитопом на CD43 и/или СЕА, экспрессируемых на негемопоэтических раковых клетках, но специфически не связываются с CD43, экспрессируемым лейкоцитом (таким как периферическая Т-клетка) или клеткой Джурката.
Некоторые варианты осуществления изобретения относятся к антителу, включающему вариабельную область тяжелой цепи, содержащую одну или несколько CDR-областей SEQ ID NO:1, и константную область тяжелой цепи IgG1 человека. В некоторых вариантах осуществления изобретения указанное антитело включает вариабельную область легкой цепи, содержащую одну или несколько CDR-областей SEQ ID NO:2, и константную область легкой каппа-цепи.
В некоторых вариантах осуществления изобретения один или несколько аминокислотных остатков в константной области тяжелой цепи и/или константной области легкой цепи антитела модифицированы (включая инсерцию, делецию и замену аминокислоты). Например, аминокислотные остатки могут быть модифицированы так, как показано в разделе “Примеры”.
Некоторые варианты осуществления изобретения относятся к антителу, включающему: (а) вариабельную область тяжелой цепи, содержащую одну или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, содержащую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:11-30; и (b) вариабельную область легкой цепи, содержащую одну или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:2, и константную область легкой цепи, содержащую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:10 и 31-37. В некоторых вариантах осуществления изобретения одна или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:1 являются тремя CDR-областями из аминокислотной последовательности SEQ ID NO:1. В некоторых вариантах осуществления изобретения одна или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:2 являются тремя CDR-областями из аминокислотной последовательности SEQ ID NO:2. В некоторых вариантах осуществления изобретения CDR1, CDR2 и CDR3 в тяжелой цепи включают соответственно аминокислотные последовательности SYVMH (SEQ ID NO:168), YINPYNGGTQYNEKFKG (SEQ ID NO:169) и RTFPYYFDY (SEQ ID NO:170). В некоторых вариантах осуществления изобретения CDR1, CDR2 и CDR3 в легкой цепи включают соответственно аминокислотные последовательности RSSQSILHSNGNTYLE (SEQ ID NO:171), KVSNRFS (SEQ ID NO:172) и FQGSHAPLT (SEQ ID NO:173). В некоторых вариантах осуществления изобретения вариабельная область тяжелой цепи включает аминокислотную последовательность вариабельной области из SEQ ID NO:1 или 3. В некоторых вариантах осуществления изобретения вариабельная область легкой цепи включает аминокислотную последовательность вариабельной области из SEQ ID NO:2 или 4.
В некоторых вариантах осуществления изобретения одна или несколько CDR-областей, выделенных из аминокислотной последовательности SEQ ID NO:1 и/или SEQ ID NO:2, по меньшей мере примерно на 85%, по меньшей мере примерно на 86%, по меньшей мере примерно на 87%, по меньшей мере примерно на 88%, по меньшей мере примерно на 89%, по меньшей мере примерно на 90%, по меньшей мере примерно на 91%, по меньшей мере примерно на 92%, по меньшей мере примерно на 93%, по меньшей мере примерно на 94%, по меньшей мере примерно на 95%, по меньшей мере примерно на 96%, по меньшей мере примерно на 97%, по меньшей мере примерно на 98% или по меньшей мере примерно на 99% идентичны по меньшей мере одной, по меньшей мере двум, по меньшей мере трем, по меньшей мере четырем, по меньшей мере пяти или по меньшей мере шести CDR-областям SEQ ID NO:1 и/или SEQ ID NO:2.
Антитела и полипептиды по настоящему изобретению могут далее характеризоваться одним или несколькими следующими признаками: (а) связывание антитела или полипептида с эпитопом уменьшается при обработке молекулы, включающей указанный эпитоп, α-1→(2,3,4)-фукозидазой; (b) связывание антитела или полипептида с эпитопом ингибируется углеводом, имеющим структуру Lea, структуру Lea-лактозы, структуру LNDFH II и/или структуру LNT; (с) антитело или полипептид индуцирует гибель негемопоэтической раковой клетки (в результате апоптоза) после связывания с эпитопом, экспрессированным на поверхности раковой клетки, при отсутствии конъюгации с цитотоксином и иммунной эффекторной функции; (d) антитело или полипептид ингибирует рост или пролиферацию негемопоэтической раковой клетки после связывания с эпитопом, экспрессированным на поверхности раковой клетки; и (е) антитело или полипептид устраняет или предотвращает у субъекта рак негемопоэтического происхождения, экспрессирующий эпитоп на поверхности клетки, такой как колоректальный рак и рак желудка.
В использованном здесь значении термин “ингибирование” означает частичное и полное ингибирование. Например, углевод, имеющий структуру Lea, структуру Lea-лактозы, структуру LNDFH II и/или структуру LNT, ингибирует связывание антитела или полипептида с эпитопом на CD43 или СЕА по меньшей мере примерно на 20%, по меньшей мере примерно на 30%, по меньшей мере примерно на 40%, по меньшей мере примерно на 50%, по меньшей мере примерно на 60%, по меньшей мере примерно на 70%, по меньшей мере примерно на 80% или по меньшей мере примерно на 90%. Связывание антитела с эпитопом может быть ингибировано прямой конкуренцией или другими механизмами.
Примеры негемопоэтических раковых клеток, экспрессирующих указанный эпитоп, включают, не ограничиваясь ими, клетки колоректального рака (такие как COLO205 и DLD-1), клетки рака желудка (такие как NCI-N87) и клетки рака поджелудочной железы (такие как SU.86.86, № АТСС CRL-1837).
Антитела и полипептиды по настоящему изобретению могут узнавать внеклеточный домен CD43, присутствующего на негемопоэтической раковой клетке, но не связываются с внеклеточным доменом CD43 лейкоцита (например, периферической Т-клетки) или внеклеточным доменом CD43, экспрессируемым на клетке Джурката (клетка лимфобластоидного лейкоза). В некоторых вариантах осуществления изобретения новые антитела или полипептиды по настоящему изобретению специфически не связываются с CD43, экспрессируемым клеткой гемопоэтического происхождения.
В объем настоящего изобретения входят модификации антител или полипептидов по настоящему изобретению, включающие функционально эквивалентные антитела без существенного изменения свойств, и варианты с повышенной или пониженной активностью и/или сродством. Например, аминокислотная последовательность антитела может быть мутирована с целью получения антитела с требуемым сродством связывания с CD43 или СЕА, экспрессируемых раковой клеткой. Модификация полипептидов является обычной практикой в данной области и не требует подробного описания. Примеры модифицированных полипептидов включают полипептиды с консервативными заменами аминокислотных остатков, одной или несколькими делециями или добавлениями аминокислот, которые не вызывают значительного вредного изменения функциональной активности, или использование химических аналогов.
Инсерции аминокислотной последовательности включают слияния у амино- и/или карбоксильного конца длиной от одного остатка до полипептидов, содержащих сто или более остатков, а также инсерции одного или нескольких аминокислотных остатков внутри последовательности. Примеры концевых инсерций включают антитело с N-концевым метионильным остатком или антитело, слитое с меткой эпитопа. Другие варианты инсерций молекулы антитела включают слияние с N- или С-концом антитела фермента или полипептида, который увеличивает время полужизни антитела в кровяном русле.
Варианты замен включают удаление по меньшей мере одного аминокислотного остатка в молекуле антитела и введение на его место другого остатка. Сайты, представляющие наибольший интерес для мутагенеза методом замен, включают гипервариабельные участки, но возможны также замены в каркасной области (FR). Консервативные замены показаны в приведенной ниже таблице под заголовком “консервативные замены”. В тех случаях, когда такие замены вызывают изменение биологической активности, могут быть произведены более значительные замены, приведенные в нижеследующей таблице под заголовком “иллюстративные замены” или описанные ниже при рассмотрении классов аминокислот, и выполнен скрининг продуктов.
Замены аминокислот
Значительные изменения биологических свойств антитела достигаются в результате выбора замен, которые оказывают существенно отличающееся воздействие на (а) структуру остова полипептида в месте замены, например, образуя пластинчатую или спиральную структуру, (b) заряд или гидрофобность молекулы на сайте-мишени или (с) структуру боковой цепи. Природные остатки разделены на группы на основании общих свойств боковых цепей:
(1) Неполярные: норлейцин, Met, Ala, Val, Leu, Ile;
(2) Полярные без заряда: Cys, Ser, Thr, Asn, Gln;
(3) Кислотные (отрицательно заряженные): Asp, Glu;
(4) Основные (положительно заряженные): Lys, Arg;
(5) Остатки, влияющие на ориентацию цепи: Gly, Pro; и
(6) Ароматические: Trp, Tyr, Phe, His.
Неконсервативные замены производят, заменяя член одного из указанных классов членом другого класса.
Любой остаток цистеина, не участвующий в сохранении соответствующей структуры антитела, может быть также заменен, обычно серином, для улучшения устойчивости молекулы к окислению и предотвращения аберрантного перекрестного сшивания. И наоборот, в антитело может быть введена одна или несколько цистеиновых связей для повышения его устойчивости, в частности, тогда, когда антитело является фрагментом антитела, таким как Fv-фрагмент.
Аминокислотные модификации могут иметь широкий диапазон от замены одной или нескольких аминокислот от полного изменения области, такой как вариабельная область. Изменения вариабельной области могут изменить сродство связывания и/или специфичность. В некоторых вариантах осуществления изобретения в CDR-области может быть произведено не более одной-пяти консервативных замен аминокислот. В других вариантах осуществления изобретения в CDR-области может быть произведено не более одной-трех консервативных замен аминокислот. В других вариантах осуществления изобретения CDR-область представляет собой CDR H3 и/или CDR L3.
Кроме того, модификации включают гликозилированные и негликозилированные полипептиды, а также полипептиды с другими посттрансляционными модификациями, такими как, например, гликозилирование разными сахарами, ацетилирование и фосфорилирование. Антитела гликозилируют в консервативных положениях константных областей (Hefferis and Lund, (1997), Chem. Immunol. 65:111-128; Wright and Morrison, (1997), TibTECH 15:26-32). Олигосахаридные боковые цепи иммуноглобулинов влияют на функцию белка (Boyd et al., (1996), Mol. Immunol. 32:1311-1318; Wittwe and Howard, (1990), Biochem. 29:4175-4180) и внутримолекулярное взаимодействие между частями гликопротеина, в результате чего может быть изменена конформация и трехмерная поверхность гликопротеина (Hefferis and Lund, см. выше; Wyss and Wagner, (1996), Current Opin. Biotech. 7:409-416). Олигосахариды могут также служить для направленной доставки данного гликопротеина к определенным молекулам на основании специфических структур узнавания. Как было установлено, гликозилирование антител влияет на антителозависимую клеточноопосредованную цитотоксичность (ADCC). В научной литературе, в частности, отмечалось, что клетки СНО с регулируемой тетрациклином экспрессией β(1,4)-N-ацетилглюкозаминилтрансферазы III (GnTIII), гликозилтрансферазы, катализирующей образование рассекающей GlcNAc, характеризуются лучшей активностью ADCC (Umana et al., (1999), Mature Biotech. 17:176-180).
Гликозилирование антител обычно является N-связанным или О-связанным. N-связанное гликозилирование предполагает присоединение углеводной части к боковой цепи остатка аспарагина. Трипептидные последовательности аспарагин-Х-серин, аспарагин-Х-треонин и аспарагин-Х-цистеин, где Х является любой аминокислотой, за исключением пролина, представляют собой последовательности узнавания для ферментативного присоединения углеводной части к боковой цепи аспарагина. Таким образом, присутствие указанных трипептидных последовательностей в полипептиде создает потенциальный сайт гликолизирования. О-связанное гликозилирование предполагает присоединение одного из сахаров N-ацетилгалактозамина, галактозы или ксилозы к гидроксиаминокислоте, обычно к серину или треонину, хотя может быть также использован 5-гидроксипролин или 5-гидроксилизин.
Сайты гликозилирования обычно вводят в антитело путем изменения аминокислотной последовательности таким образом, чтобы она содержала одну или несколько вышеуказанных трипептидных последовательностей (для сайтов N-связанного гликозилирования). Изменение можно также произвести путем добавления или замены одного или нескольких остатков серина или треонина в последовательности исходного антитела (сайты для О-связанного гликозилирования).
Паттерн гликозилирования антител можно также изменить без изменения нуклеотидной последовательности. Гликозилирование в значительной степени зависит от клетки-хозяина, используемой для экспрессии антитела. Так как клетка, используемая для экспрессии рекомбинантных гликопротеинов, например, антител, в качестве потенциальных лекарственных средств, редко бывает нативной клеткой, можно ожидать изменений в паттерне гликозилирования антител (см., например, публикацию Hse et al., (1997), J. Biol. Chem. 272:9062-9070).
Антитела по настоящему изобретению могут включать фрагменты антител (например, Fab, Fab', F(ab')2, Fv, Fc и т.д.), химерные антитела, одноцепочечные (ScFv), их мутанты, слитые белки, включающие антитело, и любую другую модифицированную конфигурацию молекулы иммуноглобулина, которая включает сайт узнавания антигена требуемой специфичности. Антитела могут быть мышиными, крысиными, верблюжьими, человеческими или могут иметь любое другое происхождение (включая гуманизированные антитела).
Сродство связывания полипептида (включая антитело) к CD43 или СЕА может быть менее примерно 500 нМ, примерно 400 нМ, примерно 300 нМ, примерно 200 нМ, примерно 100 нМ, примерно 50 нМ, примерно 10 нМ, примерно 1 нМ, примерно 500 пМ, примерно 100 пМ или примерно 50 пМ. Как хорошо известно в данной области, сродство связывания может быть выражено в виде KD или константы диссоциации, и повышенное сродство связывания соответствует более низкому значению KD. Одним методом определения сродства связывания антитела к CD43 или СЕА является измерение сродства связывания монофункциональных Fab-фрагментов антитела. Для получения монофункциональных Fab-фрагментов антитело (например, IgG) можно расщепить папаином или экспрессировать рекомбинантным методом. Сродство Fab-фрагмента антитела можно определить методом резонанса поверхностных плазмонов (система измерения резонанса поверхностных плазмонов (SPR) BIAcore3000™, BIAcore, INC, Piscaway, NJ) и ELISA. Определяют скорости кинетической ассоциации (kon) и скорости диссоциации (koff) (измерение обычно производят при 25°С) и вычисляют значения константы равновесной диссоциации (KD) из отношения koff/kon.
В некоторых вариантах осуществления изобретения антитела и полипептиды по настоящему изобретению уменьшают число раковых клеток и/или ингибируют рост или пролиферацию опухолевых или раковых клеток, содержащих указанный эпитоп. Уменьшение числа клеток или ингибирование роста или пролиферации клеток предпочтительно составляет по меньшей мере примерно 10%, примерно 20%, примерно 30%, примерно 40%, примерно 50%, примерно 65%, примерно 75% или больше по сравнению с клетками, не подвергнутыми воздействию антитела или полипептидов. Раковые клетки включают, не ограничиваясь ими, колоректальный рак, рак поджелудочной железы, рак легкого и рак желудка.
В некоторых вариантах осуществления изобретения антитела и полипептиды по настоящему изобретению могут самостоятельно индуцировать гибель клеток, например, в результате апоптоза, после связывания с указанным эпитопом, экспрессированным на поверхности негемопоэтической раковой клетки. Термин “индуцировать гибель клеток” в использованном здесь значении означает, что антитела или полипептиды по настоящему изобретению могут непосредственно взаимодействовать с молекулой, экспрессированной по поверхности клетки, при этом одного связывания/взаимодействия является достаточно для индуцирования гибели клеток без помощи других факторов, таких как конъюгация с цитотоксином или другие иммунные эффекторные функции, то есть комплементзависимая цитотоксичность (CDC), антителозависимая клеточноопосредованная цитотоксичность (ADCC) или фагоцитоз.
В использованном здесь значении термин “апоптоз” означает направленный на гены процесс внутриклеточного разрушения клетки. Апоптоз следует отличать от некроза; апоптоз включает разрушение цитоскелета, сжатие и конденсацию цитоплазмы, экспрессию фосфатидилсерина на наружной поверхности клеточной мембраны и выделение пузырьков, в результате чего происходит образование пузырьков, связанных с клеточной мембраной, или апоптических телец. Указанный процесс определяется также как “запрограммированная гибель клетки”. В процессе апоптоза наблюдаются такие типичные явления, как искривление клеточных поверхностей, конденсация ядерного хроматина, фрагментация хромосомной ДНК и утрата митохондриальной функции. Для обнаружения апоптоза могут быть использованы разные известные методы, такие как окрашивание клеток аннексином V, иодидом пропидия, анализ фрагментации ДНК и YO-PRO-1 (Invitrogen).
Методы обнаружения гибели клетки (такой как апоптоз) включают, не ограничиваясь ими, выявление морфологии, фрагментации ДНК, ферментативной активности, расщепления полипептидов и т.д. См. публикации Siman et al., U.S. Pat. No. 6048703; Martin and Green (1995), Cell, 82:349-52; Thomberry and Lazebnik (1998), Science, 281:1312-6; Zou et al., U.S. Pat. No. 6291643; Scovassi and Poirier (1999), Mol. Cell Biochem., 199:125-37; Wyllie et al. (1980), Int. Rev. Cytol., 68:251-306; Belhocine et al. (2004), Technol. Cancer Res. Treat., 3(l):23-32, которые включены в настоящее описание изобретения в виде ссылки.
В некоторых вариантах осуществления изобретения антитела и полипептиды по настоящему изобретению узнают структурный эпитоп, экспрессируемый на негемопоэтической раковой клетке, который имеет структуру, физические и химические характеристики которой эквиваленты структуре, образованной трипептидом, N'-Trp-Pro-Ile-C'. В использованном здесь значении выражение “эпитоп, имеющий структуру, физические и химические характеристики которой эквиваленты структуре, образованной пептидом” означает, что обе структуры обладают одинаковым физическим и химическим свойством, имеющим отношение к связыванию с антителом, благодаря чему антитело, которое специфически связывается с одной структурой, будет связываться с обеими структурами. В некоторых вариантах осуществления изобретения антитела и полипептиды связываются с полипептидом, включающим аминокислотную последовательность N'-Trp-Pro-Ile-C' у N-конца полипептида.
В некоторых вариантах осуществления изобретения антитела и полипептиды по настоящему изобретению конкурируют с антителом m5F1 или h5F1 за связывание с эпитопом, экспрессированным на поверхности раковой клетки. В некоторых вариантах осуществления изобретения антитела или полипептиды по настоящему изобретению связываются с эпитопом на CD43 или СЕА, с которым связывается по меньшей мере одно из антител m5F1 или h5F1.
Чтобы определить, связываются ли два антитела с одним и тем же эпитопом в результате узнавания идентичных или стерически перекрывающихся эпитопов, или одно антитело конкурентно ингибирует связывание другого антитела с данным антигеном, можно использовать конкурентно-связывающие анализы. Такие анализы известны в данной области. Как правило, антиген или антигенэкспрессирующие клетки иммобилизуют на многолуночном планшете и измеряют способность немеченых антител блокировать связывание меченых антител. При выполнении таких конкурентно-связывающих анализов используют обычные метки, такие как радиоактивные метки или ферментные метки.
В некоторых вариантах осуществления изобретения область, определяющая комплементарность, является CDR-областью Кабата. В других вариантах осуществления изобретения область, определяющая комплементарность, является CDR-областью Хотиа. В других вариантах осуществления изобретения область, определяющая комплементарность, представляет собой комбинацию CDR-областей Кабата и Хотиа (именуемую также “объединенная CDR-область” или “расширенная CDR-область”). Другими словами, в любом варианте осуществления изобретения, в котором использовано несколько CDR-областей, такие области могут быть CDR-областями Кабата, Хотиа и/или объединенными CDR-областями.
Методы создания антител и полипептидов, получаемых из антител, хорошо известны в данной области и рассмотрены в настоящем описании изобретения. Полученные антитела могут быть испытаны на наличие специфического связывания с эпитопом на CD43 или СЕА, экспрессируемых негемопоэтическими раковыми или опухолевыми клетками, и отсутствие специфического связывания с CD43-экспрессирующим лейкоцитом, клетками Джурката и/или другими CD43-экспрессирующими клетками гемопоэтического происхождения. Для испытания могут быть использованы раковые клетки или внеклеточный домен (в том числе его фрагменты), содержащие указанный эпитоп.
Линия клеток Джурката представляет собой клетки лимфобластоидного лейкоза и была выделена из периферической крови 14-летнего мальчика Шнейдером и др. (Schneider et al., Int. J. Cancer 19:621-626, 1977). Разные линии клеток Джурката можно приобрести коммерческим путем, например, из Американской коллекции типовых культур (например, АТСС TIB-152, ATCC TIB-153, ATCC CRL-2678).
Специфичность связывания полученных антител можно определить путем иммунопреципитации или выполнения анализа связывания in vitro, такого как радиоиммуноанализ (RIA) или твердофазный иммуноферментный анализ (ELISA). Такие методы и анализы хорошо известны в данной области. Сродство связывания моноклонального антитела можно, например, определить при помощи анализа Скатчарда, описанного в публикации Munson and Pollard (1980), Anal. Biochem., 107-220.
Идентифицированные антитела могут быть далее испытаны в отношении их способности индуцировать гибель клетки (например, апоптоз) и/или ингибировать рост или пролиферацию клеток при помощи методов, известных в данной области и рассмотренных в настоящем описании изобретения.
Антитела по настоящему изобретению могут быть также получены методами рекомбинантных ДНК, описанными в патентах США № 4816567 и 6331415, которые включены в настоящее описание изобретения в виде ссылки. Например, ДНК, кодирующую моноклональные антитела по настоящему изобретению, можно легко выделить и секвенировать стандартными методами (например, используя олигонуклеотидные зонды, способные специфически связываться с генами, кодирующими тяжелую и легкую цепи мышиных антител). Клетки гибридомы по настоящему изобретению служат в качестве предпочтительного источника такой ДНК. Выделенную ДНК можно ввести в экспрессирующие векторы, которые затем трансфицируют в клетки-хозяева, такие как клетки COS обезьян, клетки яичника китайского хомячка (СНО) или миеломные клетки, которые в противном случае не продуцируют белок иммуноглобулина, для синтеза моноклональных антител в рекомбинантных клетках-хозяевах. ДНК можно также модифицировать, например, путем введения кодирующей последовательности для константных областей тяжелой и легкой цепей человека вместо гомологичных мышиных последовательностей (патент США № 4816567) или путем ковалентного присоединения к кодирующей последовательности иммуноглобулина всей или части кодирующей последовательности для полипептида, не являющегося иммуноглобулином. Такой полипептид, не являющийся иммуноглобулином, может быть введен вместо константных областей антитела по настоящему изобретению или вместо вариабельных областей одного антигенсвязывающего центра антитела по настоящему изобретению для создания химерного бивалентного антитела.
В некоторых вариантах осуществления изобретения антитела по настоящему изобретению экспрессируют из двух экспрессирующих векторов. Первый экспрессирующий вектор кодирует тяжелую цепь антитела (например, гуманизированного антитела) и включает первую часть, кодирующую вариабельную область тяжелой цепи антитела, и вторую часть, кодирующую константную область тяжелой цепи антитела. В некоторых вариантах осуществления изобретения первая часть кодирует тяжелую цепь, содержащую вариабельную область тяжелой цепи, включающую одну или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:11-30. В некоторых вариантах осуществления изобретения одна или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:1 являются тремя CDR-областями из аминокислотной последовательности SEQ ID NO:1. Второй экспрессирующий вектор кодирует легкую цепь антитела и включает первую часть, кодирующую вариабельную область легкой цепи антитела, и вторую часть, кодирующую константную область легкой цепи антитела. В некоторых вариантах осуществления изобретения первая часть кодирует легкую цепь, содержащую вариабельную область легкой цепи, включающую одну или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:2, и константную область легкой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:10 и 31-37. В некоторых вариантах осуществления изобретения одна или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:2 являются тремя CDR-областями из аминокислотной последовательности SEQ ID NO:2.
Альтернативно антитела (например, гуманизированное антитело) по настоящему изобретению экспрессируют из единичного экспрессирующего вектора. Единичный экспрессирующий вектор кодирует как тяжелую цепь, так и легкую цепь антител по настоящему изобретению. В некоторых вариантах осуществления изобретения экспрессирующий вектор включает полинуклеотидную последовательность, кодирующую тяжелую цепь, содержащую вариабельную область тяжелой цепи, включающую одну или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:11-30, и вариабельную область легкой цепи, включающую одну или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:2, и константную область легкой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:10 и 31-37. В некоторых вариантах осуществления изобретения одна или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:1 являются тремя CDR-областями из аминокислотной последовательности SEQ ID NO:1. В некоторых вариантах осуществления изобретения одна или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:2 являются тремя CDR-областями из аминокислотной последовательности SEQ ID NO:2.
Экспрессирующий вектор обычно содержит последовательности, регулирующие транскрипцию и трансляцию, которые выделяют из вида, совместимого с клеткой-хозяином. Кроме того, вектор обычно несет специфические гены, способные производить отбор по фенотипу в трансформированных клетках.
Известен целый ряд рекомбинантных экспрессирующих систем хозяин-вектор для эукариотических клеток, которые могут быть использованы в настоящем изобретении. Например, наиболее часто для эукариотических микроорганизмов используют Saccharomyces cerevisiae или обычные хлебопекарные дрожжи, хотя существует ряд других штаммов, таких как Pichia pastoris. В качестве хозяев могут быть также использованы линии клеток, выделенные из многоклеточных организмов, такие как Sp2/0 или клетки яичника китайского хомячка (СНО), которые могут быть приобретены из АТСС. Типичными плазмидными векторами, пригодными для трансформации эукариотических клеток, являются, например, pSV2neo и pSV2gpt (ATCC), pSVL и pSVK3 (Pharmacia) и pBPV-1/pML2d (International Biotechnology, Inc.).
Эукариотические клетки-хозяева, пригодные для использования в настоящем изобретении, предпочтительно являются клетками гибридомы, миеломными клетками, клетками плазмацитомы или лимфомы. Однако могут быть использованы другие эукариотические клетки-хозяева при условии, что такие клетки-хозяева млекопитающих способны узнавать транскрипционные и трансляционные последовательности ДНК для экспрессии белков, процессировать лидерный пептид путем расщепления лидерной последовательности и секреции белков и производить посттрансляционные модификации белков, например, гликозилирование.
Таким образом, настоящее изобретение относится к эукариотическим клеткам-хозяевам, которые трансформированы рекомбинантными экспрессирующими векторами, включающими конструкции на основе ДНК, рассмотренные в настоящем описании изобретения, и способны экспрессировать антитела или полипептиды по настоящему изобретению. В некоторых вариантах осуществления изобретения трансформированные клетки-хозяева по настоящему изобретению включают по меньшей мере одну конструкцию на основе ДНК, содержащую последовательности ДНК легкой и тяжелой цепей и последовательности, регулирующие транскрипцию и трансляцию, которые расположены относительно последовательностей ДНК, кодирующих легкую и тяжелую цепи, с возможностью управления экспрессией антител или полипептидов.
Клетки-хозяева, использованные в настоящем изобретении, могут быть трансформированы разными стандартными методами трансфекции, хорошо известными в данной области. Стандартные методы трансфекции, которые могут быть использованы, включают методы электропорации, слияния протопластов и преципитации фосфатом кальция. Такие методы описаны в публикациях F. Toneguzzo et al. (1986), Mol. Cell. Biol., 6:703-706; G. Chu et al., Nucleic Acid Res. (1987), 15:1311-1325; D. Rice et al., Proc. Natl. Acad. Sci. USA (1979), 79:7862-7865; и V. Oi et al., Proc. Natl. Acad. Sci. USA (1983), 80:825-829.
В случае использования двух экспрессирующих векторов оба экспрессирующих вектора могут быть трансфицированы в клетку-хозяина друг за другом отдельно или вместе (коперенос или котрансфекция).
Настоящее изобретение относится также к способу получения антител или полипептидов, который включает культивирование клетки-хозяина, содержащей экспрессирующие векторы, кодирующие антитела или полипептиды, и выделение антител или полипептидов из культуры методами, хорошо известными специалисту в данной области. В некоторых вариантах осуществления изобретения антитела могут быть выделены или очищены стандартными методами очистки иммуноглобулинов, такими как, например, очистка белком А-сефарозой, хроматография на гидроксилапатите, гель-электрофорез, диализ или аффинная хроматография.
Кроме того, требуемые антитела могут быть продуцированы в организме трансгенного животного. Приемлемое трансгенное животное может быть получено стандартными методами, которые включают микроинъецирование в яйцеклетки соответствующих экспрессирующих векторов, введение яйцеклеток псевдобеременным самкам и отбор потомства, экспрессирующего требуемое антитело.
Настоящее изобретение относится также к химерным антителам, которые специфически узнают указанный эпитоп на CD43 и СЕА, экспрессируемых раковой клеткой. Например, вариабельные и константные области химерного тела принадлежат разным видам. В некоторых вариантах осуществления изобретения вариабельные области, как тяжелой цепи, так и легкой цепи, получают из мышиных антител, рассмотренных в настоящем описании изобретения. В некоторых вариантах осуществления изобретения вариабельные области включают аминокислотные последовательности из вариабельных областей SEQ ID NO:1 и SEQ ID NO:2 или остатков 20-137 SEQ ID NO:1 и остатков 20-131 SEQ ID NO:2. В некоторых вариантах осуществления изобретения константные области, как тяжелой цепи, так и легкой цепи, получены из человеческих антител.
Химерное антитело по настоящему изобретению может быть получено методами, хорошо известными в данной области. См., например, патент США № 6808901, патент США № 6652852, патент США № 6329508, патент США № 6120767 и патент США № 5677423, которые включены в настоящее описание изобретения в виде ссылки. Как правило, химерное антитело может быть создано путем получения кДНК, кодирующих вариабельные области тяжелой и легкой цепей антитела, введения кДНК в экспрессирующий вектор, который после переноса в эукариотические клетки-хозяева экспрессирует химерное антитело по настоящему изобретению. Экспрессирующий вектор предпочтительно несет функционально полную последовательность константной области тяжелой или легкой цепи, что позволяет легко ввести в экспрессирующий вектор любую последовательность вариабельной области тяжелой или легкой цепи.
Настоящее изобретение относится к гуманизированному антителу, которое специфически узнает указанный эпитоп на CD43 и СЕА, экспрессируемых негемопоэтической раковой клеткой. Гуманизированное антитело обычно является человеческим антителом, в котором остатки из CDR-областей заменены остатками из CDR-областей вида, отличного от человека, такого как мышь, крыса или кролик, обладающего требуемой специфичностью, сродством и потенциалом. В некоторых случаях остатки Fv-фрагмента каркасной области человеческого антитела заменены соответствующими остатками, отличными от человеческих.
Моноклональное антитело гуманизируют, выполняя четыре общих стадий. Указанные стадии включают: (1) определение нуклеотидной и предполагаемой аминокислотной последовательности исходных вариабельных областей легкой и тяжелой цепей; (2) конструирование гуманизированного антитела, то есть принятие решения о том, какая каркасная область антитела будет использована в процессе гуманизации; (3) выполнение фактических методов гуманизации и (4) трансфекцию и экспрессию гуманизированного антитела. См., например, патенты США № 4816567, 5807715, 5866692, 6331415, 5530101, 5693761, 5693762, 5585089, 6180370 и 6548640. Например, созданная константная область может в большей степени напоминать константные области человека во избежание иммунной реакции, если данное антитело используется в клинических исследованиях и для лечения людей. См., например, патенты США № 5997867 и 5866692.
Важно, чтобы антитела были гуманизированы с сохранением высокого сродства к антигену и других благоприятных биологических свойств. Для достижения указанной цепи гуманизированные антитела могут быть получены в результате выполнения анализа исходных последовательностей и разных концептуальных гуманизированных продуктов с использованием трехмерных моделей исходных и гуманизированных последовательностей. Специалистам в данной области знакомы общедоступные трехмерные модели иммуноглобулина. Существуют компьютерные программы, которые иллюстрируют и воспроизводят вероятные трехмерные конформационные структуры выбранных последовательностей кандидатов иммуноглобулина. Исследование полученных изображений позволяет произвести анализ возможной роли остатков в функционировании последовательности кандидата иммуноглобулина, то есть анализ остатков, которые влияют на способность кандидата иммуноглобулина связываться с его антигеном. Таким образом могут быть выбраны остатки каркасной области и объединены из консенсусной и вводимой последовательности для достижения требуемой характеристики антитела, такой как повышенное сродство к антигену-мишени. Как правило, остатки CDR непосредственно и в значительной степени влияют на связывание с антигеном. Гуманизированные антитела могут также содержать модификации в шарнирной области, улучшающие одну или несколько характеристик данного антитела.
В соответствии с другой альтернативой антитела могут быть исследованы и созданы рекомбинантным методом отображения на фаге. См., например, патенты США № 5565332, 5580717, 5733743 и 6265150 и публикацию Winter et al., Annu. Rev. Immunol. 12:433-455 (1994). Альтернативно метод отображения на фаге (McCafferty et al., Nature 348:552-553 (1990)) может быть использован для получения человеческих антител и фрагментов антител in vitro из набора генов вариабельной (V) области иммуноглобулина, полученных у неиммунизированных доноров. В соответствии с указанным методом гены V-области антитела клонируют в рамке считывания в ген мажорного или минорного белка оболочки нитевидного бактериофага, такого как М13 или fd, и отображают в виде функциональных фрагментов антитела на поверхности фаговой частицы. Так как нитевидная частица содержит копию одноцепочечной ДНК генома фага, отбор на основании функциональных свойств антитела также приводит к отбору гена, кодирующего антитело, обладающее указанными свойствами. Таким образом, фаг имитирует некоторые свойства В-клетки. Отображение на фаге может быть выполнено в разных форматах; см., например, публикацию Johnson, Kevin S. and Chiswell, David J., Current Opinion in Structural Biology 3, 564-571 (1993). Для отображения на фаге может быть использовано несколько источников сегментов гена V-области. Клаксон и др. (Clackson et al., Nature 352:624-628 (1991)) выделили разнообразные антитела против оксазолона из небольшой произвольной комбинаторной библиотеки генов V-области, полученных из селезенок иммунизированных мышей. Может быть создан целый спектр генов V-области, полученных у неиммунизированных людей-доноров, и антитела к разнообразному набору антигенов (включая аутоантигены) могут быть выделены методами, описанными в публикации Mark et al., J. Mol. Biol. 222:581-597 (1991) или Griffith et al., EMBO J. 12:725-734 (1993). В случае естественной иммунной реакции гены антител накапливают мутации с высокой частотой (соматическая сверхмутация). Некоторые введенные изменения сообщают более высокое сродство, и В-клетки, отображающие поверхностный иммуноглобулин, обладающий высоким сродством, предпочтительно реплицируют и дифференцируют во время последующей антигенной стимуляции. Вышеуказанный естественный процесс может быть имитирован при помощи метода, известного как “перестановка цепи”. Marks et al., Bio/Technol. 10:779-783 (1992). При выполнении данного метода сродство “первичных” человеческих антител, полученных методом отображения на фаге, может быть улучшено в результате последовательной замены генов V-области тяжелой и легкой цепей естественными вариантами (наборами) генов V-области, полученных у неиммунизированных доноров. Указанный метод позволяет получать антитела и фрагменты антител со сродством в диапазоне пМ-нМ. Стратегия получения очень большого спектра антител на фаге (известного также как “материнские библиотеки”) описана в публикации Waterhouse et al., Nucl. Acids Res. 21:2265-2266 (1993). Метод перестановки генов может быть также использован для получения человеческих антител из антител грызунов, при этом человеческое антитело обладает сродством и специфичностью, подобными исходному антителу грызуна. В соответствии с указанным методом, который известен также как “импринтинг эпитопа”, ген V-области тяжелой или легкой цепи антител грызунов, полученных методом отображения на фаге, заменяется генами V-области человека, в результате чего образуется грызун-человеческая химера. Отбор по антигену позволяет выделить вариабельные области человека, способные восстанавливать функциональный антигенсвязывающий центр, то есть эпитоп управляет (запечатлевает) выбором партнера. При повторении указанного процесса с целью замены оставшейся V-области грызуна получают человеческое антитело (см. публикацию РСТ № WO 93/06213, опубликованную 1 апреля 1993 г.). В отличие от традиционной гуманизации антител грызунов путем пересадки CDR указанный метод позволяет получить полностью человеческие антитела, которые не содержат остатков каркасной области или CDR грызунов. Очевидно, что, хотя приведенное выше описание относится к гуманизированным антителам, общие рассмотренные принципы применимы к созданию антител, например, для собак, кошек, приматов, лошадей и коров.
В некоторых вариантах осуществления изобретения указанное антитело является полностью человеческим антителом. Антитела, отличные от человеческих, которые специфически связываются с антигеном, могут быть использованы для получения полностью человеческого антитела, связывающегося с данным антигеном. Например, квалифицированный специалист может использовать метод замены цепи, в соответствии с которым тяжелая цепь антитела, отличного от человеческого, коэкспрессирована с библиотекой, экспрессирующей разные легкие цепи человека. Полученные гибридные антитела, содержащие одну легкую цепь человека и одну тяжелую цепь, отличную от человеческой, затем исследуют в отношении связывания с антигеном. Легкие цепи, которые участвуют в связывании антигена, затем коэкспрессируют с библиотекой тяжелых цепей человеческого антитела. Полученные человеческие антитела еще раз исследуют на связывание с антигеном. Такие методы описаны в патенте США № 5565332. Кроме того, антиген может быть использован для вакцинации животного, которое является трансгенным для генов иммуноглобулина человека. См., например, патент США № 5661016.
Указанное антитело может быть биспецифическим антителом, а именно моноклональным антителом, которое обладает специфичностью связывания в отношении по меньшей мере двух разных антигенов и может быть получено с использованием антител по настоящему изобретению. Методы получения биспецифических антител известны в данной области (см., например, публикацию Suresh et al., (1986), Methods in Enzymology 121:210). Рекомбинантные методы получения биспецифических антител традиционно основаны на коэкспрессии двух пар тяжелой цепи-легкой цепи иммуноглобулина с двумя тяжелыми цепями, обладающими другой специфичностью (Millstein and Cuello, (1983), Nature 305, 537-539).
В соответствии с одним методом получения биспецифических антител вариабельные области антитела с требуемой специфичностью связывания (сайты объединения антиген-антитело) сливают с последовательностями константной области иммуноглобулина. Слияние предпочтительно производят с константной областью тяжелой цепи иммуноглобулина, включающей по меньшей мере часть шарнирной области, СН2- и СН3-областей. Желательно, чтобы первая константная область тяжелой цепи (СН1), содержащая сайт, необходимый для связывания с легкой цепью, присутствовала по меньшей мере в одном из слияний. ДНК, кодирующие слияния тяжелых цепей иммуноглобулина и, при желании, легкую цепь иммуноглобулина, вводят в разные экспрессирующие векторы и котрансфицируют в приемлемый организм-хозяин. Такой метод обеспечивает большую гибкость в регулировании взаимных пропорций трех полипептидных фрагментов в тех вариантах осуществления изобретения, когда разные соотношения трех полипептидных цепей, используемых в конструкции, позволяют получить оптимальный выход. Однако можно ввести кодирующие последовательности для двух или всех трех полипептидных цепей в одном экспрессирующем векторе, когда экспрессия по меньшей мере двух полипептидных цепей в одинаковом соотношении позволяет получить высокий выход или когда соотношение не имеет особого значения.
В соответствии с одним методом биспецифические антитела состоят из гибридной тяжелой цепи иммуноглобулина, в которой первая специфичность связывания находится в одном домене, и гибридная пара тяжелой цепи-легкой цепи иммуноглобулина (обеспечивающая вторую специфичность связывания) находится в другом домене. Такая асимметричная структура при наличии легкой цепи иммуноглобулина только в одной половине биспецифической молекулы облегчает отделение требуемого биспецифического соединения от нежелательных комбинаций цепей иммуноглобулина. Указанный метод описан в публикации РСТ № WO 94/04690, опубликованной 3 марта 1994 г.
Гетероконъюгированные антитела, содержащие два ковалентно связанных антитела, также входят в объем настоящего изобретения. Такие антитела используются для направленной доставки клеток иммунной системы к нежелательным клеткам (патент США № 4676980) и для лечения ВИЧ-инфекции (публикации РСТ № WO 91/00360 и WO 92/200373; и европейский патент № 03089). Гетероконъюгированные антитела могут быть получены стандартными методами перекрестного сшивания. Приемлемые перекрестно-сшивающие агенты и методы хорошо известны в данной области и описаны в патенте США № 4676980.
Одноцепочечные Fv-фрагменты также могут быть получены методом, описанным в публикации Iliades et al., 1997, FEBS Letters, 409:437-441. Связывание таких одноцепочечных фрагментов при помощи разных линкеров описано в публикации Kortt et al., 1997, Protein Engineering, 10:423-433. В данной области хорошо известны разные методы рекомбинантного получения и манипуляции антителами.
Следует отметить, что в объем настоящего изобретения входят не только вышеописанные моноклональные антитела, но также любые фрагменты указанных антител, содержащие активную область связывания таких антител, в частности Fab, F(ab')2, scFv, Fv фрагменты и тому подобные. Такие фрагменты могут быть получены из моноклональных антител по настоящему изобретению при помощи методов, хорошо известных в данной области (Rousseaux et al. (1986), in Methods Enzynol., 121:663-69, Academic Press).
Методы получения фрагмента антитела хорошо известны в данной области. Например, фрагмент антитела может быть получен путем ферментативного расщепления антител пепсином с образованием фрагмента длиной 100 кДа, обозначаемого F(ab')2. Указанный фрагмент может быть дополнительно расщеплен тиоловым восстановителем необязательно с использованием блокирующей группы для сульфгидрильных групп, образующихся в результате расщепления дисульфидных связей, с образованием одновалентных Fab'-фрагментов длиной 50 кДа. Альтернативно в результате ферментативного расщепления папаином сразу образуются два одновалентных Fab-фрагмента и Fc-фрагмент. Указанные методы описаны, например, в патентах США № 4036945 и 4331647 и содержащихся в них ссылках, которые включены в настоящее описание изобретения в виде ссылки. См. также публикации Nisonoff et al. (1960), Arch. Biochem. Biophys. 89:230; Porter (1959), Biochem. J. 73:119, Edelman et al., in Methods in Enzymology, vol.1, page 422 (Academic Press, 1967).
Альтернативно Fab-фрагмент может быть получен путем введения ДНК, кодирующей Fab-фрагмент антитела, в экспрессирующий вектор для прокариотических клеток или в экспрессирующий вектор для эукариотических клеток и введения указанного вектора в прокариотическую или эукариотическую клетку для экспрессии Fab-фрагмента.
Помимо выбора клеток-хозяев, факторы, влияющие на гликолизирование в процессе рекомбинантного получения антител, включают режим выращивания, состав среды, плотность культуры, насыщение кислородом, рН, методы очистки и тому подобные. Были предложены разные методы изменения паттерна гликозилирования, достигаемого в конкретном организме-хозяине, включая введение и сверхэкспрессию определенных ферментов, участвующих в продуцировании олигосахаридов (патенты США № 5047335, 5510261 и 5278299). Гликозилирование или определенные типы гликозилирования могут быть ферментативно удалены из гликопротеина, например, при помощи эндогликозидазы Н (Endo H), N-гликозидазы F, эндогликозидазы F1, эндогликозидазы F2, эндогликозидазы F3. Кроме того, рекомбинантная клетка-хозяин может быть генетически создана дефектной при процессировании полисахаридов определенных типов. Вышеуказанные и подобные методы хорошо известны в данной области.
В некоторых вариантах осуществления изобретения антитела по настоящему изобретению могут быть модифицированы при помощи методов связывания, известных в данной области, которые включают, не ограничиваясь ими, ферментативные способы, окислительное замещение и хелатообразование. Модификации могут быть использованы, например, для присоединения меток для иммуноанализа. Модифицированные полипептиды, полученные методами, применяемыми в данной области, могут быть исследованы при помощи стандартных анализов, известных в данной области, некоторые из которых описаны ниже и в разделе “Примеры”.
Антитело или полипептид по настоящему изобретению может быть конъюгирован (например, связан) с таким агентом, как терапевтический агент и метка. Примеры терапевтических агентов включают радиоактивные части, цитотоксины или химиотерапевтические молекулы.
Антитело (или полипептид) по настоящему изобретению может быть связано с меткой, такой как флуоресцентная молекула, радиоактивная молекула, фермент или любые другие метки, известные в данной области. В использованном здесь значении термин “метка” означает любую молекулу, которая может быть обнаружена. В определенном варианте осуществления изобретения антитело может быть мечено путем введения аминокислоты, меченной радиоактивным изотопом. В определенном варианте осуществления изобретения к антителу может быть присоединен биотин, который может быть обнаружен меченым авидином (например, стрептавидином, содержащим флуоресцентный маркер или обладающим ферментативной активностью, который может быть обнаружен оптическими или колориметрическими методами). В определенных вариантах осуществления изобретения метка может быть введена или присоединена к другому реагенту, который в свою очередь связывается с представляющим интерес антителом. Например, метка может быть введена или присоединена к антителу, которое в свою очередь специфически связывается с представляющим интерес антителом. В определенных вариантах осуществления изобретения метка или маркер также могут быть терапевтическими агентами. В данной области известны разные методы мечения полипептидов и гликопротеинов, которые могут быть использованы в настоящем изобретении. Определенные общие классы меток включают, не ограничиваясь ими, ферментные, флуоресцентные, хемилюминесцентные и радиоактивные метки. Примеры меток для полипептидов включают, не ограничиваясь ими, радиоактивные изотопы или радионуклиды (например, 3Н, 14С, 15N, 35S, 90Y, 99Tc, 111In, 125I, 131I), флуоресцентные метки (например, изотиоцианат флуоресцеина (FITC), родамин, лантанид фосфора, фикоэритрин (РЕ)), ферментные метки (например, пероксидаза хрена, β-галактозидаза, люцифераза, щелочная фосфатаза, глюкозооксидаза, глюкоза-6-фосфат-дегидрогеназа, алкогольдегидрогеназа, малатдегидрогеназа, пенициллиназа, люцифераза), хемилюминесцентные вещества, биотинильные группы, заранее определенные полипептидные эпитопы, узнаваемые вторичным репортером (например, парные последовательности лейциновых зипперов, сайты связывания для вторичных антител, металлсвязывающие домены, метки эпитопов). В определенных вариантах осуществления изобретения метки присоединяют при помощи спейсеров разной длины для уменьшения возможного стерического несоответствия.
Настоящее изобретение относится также к фармацевтическим композициям, включающим антитела или полипептиды по настоящему изобретению и фармацевтически приемлемый носитель или эксципиенты. В данной области известны фармацевтически приемлемые эксципиенты, которые являются относительно инертными веществами, облегчающими введение фармакологически эффективного вещества. Например, эксципиент может сообщать форму или консистенцию или действовать в качестве разбавителя. Приемлемые эксципиенты включают, не ограничиваясь ими, стабилизаторы, смачивающие и эмульгирующие вещества, соли для изменения осмотической концентрации раствора, инкапсулирующие агенты, буферы и вещества, усиливающие проникновение через кожу. Эксципиенты, а также препараты для парентерального и непарентерального введения лекарственных средств представлены в публикации Remington, The Science and Practice of Pharmacy, 20th Ed. Mack Publishing (2000).
Некоторые варианты осуществления изобретения относятся к композициям (рассмотренным в настоящем описании изобретения), которые предназначены для использования в любых способах по настоящему изобретению, как в качестве лекарственного средства, так и для получения лекарственного средства.
Полинуклеотиды, векторы и клетки-хозяева
Настоящее изобретение относится также к полинуклеотидам, включающим нуклеотидную последовательность, кодирующую любые моноклональные антитела и полипептиды по настоящему изобретению. В некоторых вариантах осуществления изобретения полипептиды включают последовательности вариабельных областей легкой цепи и/или тяжелой цепи.
В некоторых вариантах осуществления изобретения полинуклеотиды включают последовательность нуклеиновой кислоты, кодирующую тяжелую цепь, содержащую вариабельную область тяжелой цепи, включающую одну или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:11-30, и/или последовательность нуклеиновой кислоты, кодирующую легкую цепь, содержащую вариабельную область легкой цепи, включающую одну или несколько CDR-областей из аминокислотной последовательности SEQ ID NO:2, и константную область легкой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:10 и 31-37. В некоторых вариантах осуществления изобретения полинуклеотиды содержат последовательность нуклеиновой кислоты, кодирующую тяжелую цепь, содержащую вариабельную область тяжелой цепи, включающую три CDR-области из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:11-30, и/или последовательность нуклеиновой кислоты, кодирующую легкую цепь, содержащую вариабельную область легкой цепи, включающую три CDR-области из аминокислотной последовательности SEQ ID NO:2, и константную область, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:10 и 31-37.
Специалистам в данной области должно быть известно, что вследствие вырожденности генетического кода существует много нуклеотидных последовательностей, кодирующих полипептид по настоящему изобретению. Некоторые из указанных полинуклеотидов обладают минимальной гомологией с нуклеотидной последовательностью любого нативного гена. Таким образом, полинуклеотиды, которые отличаются вследствие различий в использовании кодона, входят в объем настоящего изобретения. Кроме того, аллели генов, содержащие полинуклеотидные последовательности по настоящему изобретению, также входят в объем настоящего изобретения. Аллели представляют собой эндогенные гены, измененные в результате одной или нескольких мутаций, таких как делеции, добавления и/или замены нуклеотидов. Полученная мРНК и белок могут, хотя и не обязательно, иметь измененную структуру или функцию. Аллели могут быть идентифицированы стандартными методами (такими как гибридизация, амплификация и/или сравнение последовательностей в базе данных).
Полинуклеотиды по настоящему изобретению могут быть получены при помощи химического синтеза, методов рекомбинантных ДНК или полимеразной цепной реакции (ПЦР). Методы химического синтеза полинуклеотидов хорошо известны в данной области и не нуждаются в подробном рассмотрении в настоящем описании изобретения. Специалист в данной области может использовать последовательности по настоящему изобретению и промышленный синтезатор ДНК для получения требуемой последовательности ДНК.
Для получения полинуклеотидов методами рекомбинантных ДНК, полинуклеотид, включающий требуемую последовательность, может быть введен в приемлемый вектор, который в свою очередь может быть введен в приемлемую клетку-хозяина для репликации и амплификации, как будет далее рассмотрено в настоящем описании изобретения. Полинуклеотиды могут быть введены в клетки-хозяина любыми способами, известными в данной области. Клетки трансформируют в результате введения экзогенного полинуклеотида путем прямого поглощения, эндоцитоза, трансфекции, F-спаривания или электропорации. После введения экзогенный полинуклеотид может находиться в клетке в виде невстроенного вектора (такого как плазмида) или встроенного в геном клетки-хозяина. Амплифицированный таким образом полинуклеотид может быть выделен из клетки-хозяина методами, хорошо известными в данной области. См., например, публикацию Sambrook et al. (1989).
Альтернативно последовательности ДНК могут быть репродуцированы при помощи полимеразной цепной реакции (ПЦР). Методы выполнения ПЦР хорошо известны в данной области и описаны в патентах США № 4683195, 4800159, 4754065 и 4683202, а также в публикации PCR: The Polymerase Chain Reaction, Mullis et al., eds., Birkauswer Press, Boston (1994).
Настоящее изобретение относится также к векторам (таким как клонирующие векторы, экспрессирующие векторы), включающим последовательность нуклеиновой кислоты, кодирующую любые полипептиды (в том числе антитела) по настоящему изобретению. Приемлемые клонирующие векторы могут быть созданы стандартными методами или могут быть выбраны из большого числа клонирующих векторов, имеющихся в данной области. Несмотря на то, что выбранный клонирующий вектор может изменяться в зависимости от предположительно используемой клетки-хозяина, пригодные клонирующие векторы обычно способны аутореплицировать, могут иметь одну мишень для конкретной рестрикционной эндонуклеазы и/или могут нести гены для маркера, который может быть использован при отборе клонов, содержащих указанный вектор. Приемлемые примеры включают плазмиды и бактериальные вирусы, например, pUC18, pUC19, Bluescript (например, pBS SK+) и его производные, mp18, mp19, pBR322, pMB9, ColE1, pCR1, RP4, фаговые ДНК, и шаттл-векторы, такие как pSA3 и рАТ28. Указанные и многие другие клонирующие векторы могут быть приобретены у коммерческих поставщиков, таких как BioRad, Stratagene и Invitrogen.
Экспрессирующие векторы обычно представляют собой реплицируемые полинуклеотидные конструкции, содержащие полинуклеотид по настоящему изобретению. Экспрессирующий вектор может реплицировать в клетках-хозяевах в виде эпитом или неотъемлемой части хромосомной ДНК. Приемлемые экспрессирующие векторы включают, не ограничиваясь ими, плазмиды, вирусные векторы, включающие аденовирусы, аденоассоциированные вирусы, ретровирусы, космиды и экспрессирующие векторы, описанные в публикации РСТ № WO 87/04462. Векторы могут включать, не ограничиваясь ими, один или несколько следующих элементов: сигнальную последовательность, ориджин репликации, один или несколько генов-маркеров, приемлемые элементы, управляющие транскрипцией (такие как промоторы, энхансеры и терминатор). Для экспрессии (то есть трансляции) обычно также необходим один или несколько элементов, управляющих трансляцией, таких как сайты связывания рибосом, сайты инициации трансляции и терминирующие кодоны.
Векторы, содержащие представляющие интерес полинуклеотиды, могут быть введены в клетку-хозяина любыми приемлемыми способами, включающими электропорацию, трансфекцию с использованием хлорида кальция, хлорида рубидия, фосфата кальция, DEAE-декстрана или других веществ, микропроекционную бомбардировку, липофекцию и инфицирование (например, в тех случаях, когда вектор является инфекционным агентом, таким как вирус коровьей оспы). Выбор способа введения векторов или полинуклеотидов часто зависит от особенностей клетки-хозяина.
Настоящее изобретение относится также к клеткам-хозяевам, включающим любые полинуклеотиды или векторы по настоящему изобретению. Любые клетки-хозяева, способные сверхэкспрессировать гетерологичные ДНК, могут быть использованы для выделения генов, кодирующих представляющее интерес антитело, полипептид или белок. Неограничивающие примеры клеток-хозяев млекопитающих включают, не ограничиваясь ими, клетки COS, HeLa и СНО. См. также публикацию РСТ № WO 87/04462. Приемлемые клетки-хозяева, отличные от клеток млекопитающих, включают прокариотические клетки (такие как E. coli или B. subtillis) и дрожжи (такие как S. cerevisae, S. pombe или K. lactis).
Диагностические применения
Настоящее изобретение относится к способу применения антител, полипептидов и полинуклеотидов по настоящему изобретению для обнаружения, диагностики и контроля за развитием заболевания, нарушения или состояния, ассоциированного с экспрессией указанного эпитопа (повышенный или пониженный уровень по сравнению с нормальным образцом и/или патологическая экспрессия, например, наличие экспрессии в тканях и/или клетках, в которых обычно отсутствует экспрессия данного эпитопа).
В некоторых вариантах осуществления изобретения указанный способ включает обнаружение экспрессии эпитопа в образце, полученном у субъекта с подозрением на рак, такой как колоректальный рак, рак поджелудочной железы, рак желудка и рак легкого. Указанный способ обнаружения предпочтительно включает контактирование образца с антителом, полипептидом или полинуклеотидом по настоящему изобретению и выявление отличия уровня связывания от аналогичного уровня в контрольном или сравнительном образце. Указанный способ может быть также использован для определения пригодности антител или полипептидов по настоящему изобретения для соответствующего лечения субъекта.
В использованном здесь значении термин “образец” или “биологический образец” означает весь организм или отдельные ткани, клетки или компоненты (например, биологические жидкости, которые включают, не ограничиваясь ими, кровь, слизь, лимфатическую жидкость, синовиальную жидкость, цереброспинальную жидкость, слюну, амниотическую жидкость, амниотическую пуповинную кровь, мочу, влагалищное отделяемое и семенную жидкость). Термин “образец” или “биологический образец” дополнительно означает гомогенат, лизат или экстракт, полученный из всего организма или отдельных тканей, клеток или компонентов, его фракции или части, которые включают, не ограничиваясь ими, плазму, сыворотку, цереброспинальную жидкость, лимфатическую жидкость, наружные срезы кожи, дыхательных путей, кишечника и мочеполовых путей, слезы, слюну, молоко, клетки крови, опухоли, органы. Чаще всего образец получают у животного, но термин “образец” или “биологический образец” может также относиться к клеткам или тканям, анализируемым in vivo, то есть без удаления у животного. Обычно, если “образец” или “биологический образец” содержит клетки животного, то данный термин может также относиться к неклеточному биологическому материалу, такому как неклеточные фракции крови, слюны или мочи, которые могут быть использованы для измерения ассоциированных с раком уровней полинуклеотидов или полипептидов. Термин “образец” или “биологический образец” дополнительно означает среду, такую как питательный бульон или гель, в которой происходило размножение организма, содержащего клеточные компоненты, такого как белки или молекулы нуклеиновой кислоты.
В одном варианте осуществления изобретения клетки или клеточный/тканевый лизат контактируют с антителом и определяют связывание антитела с клеткой. Если анализируемые клетки демонстрируют активность связывания, сравнимую с контрольной клеткой ткани такого же типа, можно сделать вывод о том, что анализируемая клетка является раковой. В некоторых вариантах осуществления изобретения анализируемые клетки получают из тканей человека.
Для обнаружения специфического связывания антитело-антиген могут быть использованы разные методы, известные в данной области. Типичные иммуноанализы, которые могут быть выполнены в соответствии с настоящим изобретением, включают флуоресцентный поляризационный иммуноанализ (FPIA), флуоресцентный иммуноанализ (FIA), иммуноферментный анализ (EIA), иммунонефелометрический анализ ингибирования (NIA), твердофазный иммуноферментный анализ (ELISA) и радиоиммуноанализ (RIA). Индикаторная часть или меченая группа может быть присоединена к антителам и выбрана в соответствии с потребностями разных применений данного метода, которые часто определяются доступностью оборудования для анализа и процедурами, совместимыми с иммуноанализом. Приемлемые метки включают, не ограничиваясь ими, радиоактивные изотопы (например, 125I, 131I, 35S, 3H или 32Р), ферменты (например, щелочную фосфатазу, пероксидазу хрена, люциферазу или β-галактозидазу), флуоресцентные части или белки (например, флуоресцеин, родамин, фикоэритрин, GFP или BFP) или люминесцентные части (например, наночастицы Qdot™, поставляемые корпорацией Quantum Dot Corporation, Palo Alto, CA). Специалистам в данной области известны общие методы выполнения разных вышеуказанных иммуноанализов.
В соответствии с целями диагностики полипептид, включающий антитела, может быть мечен детектируемой частью, которая включает, не ограничиваясь ими, радиоактивные изотопы, флуоресцентные метки и разные метки ферментного субстрата, известные в данной области. В данной области известны методы конъюгации меток с антителом.
В некоторых вариантах осуществления изобретения полипептиды, включающие антитела по настоящему изобретению, не требуют мечения, и их присутствие может быть обнаружено при помощи меченого антитела, которое связывается с антителами по настоящему изобретению.
Антитела по настоящему изобретению могут быть использованы при выполнении любых известных анализов, таких как конкурентно-связывающие анализы, сэндвич-анализы прямого и непрямого связывания и иммунопреципитационные анализы. Zola, Monoclonal Antibodies: A Manual of Techniques, pp.147-158 (CRC Press, Inc. 1987).
Антитела и полипептиды могут быть также использованы при выполнении диагностических анализов in vivo, таких как визуализация in vivo. Антитело или полипептид обычно метят радиоактивным изотопом (таким как 111In, 99Tc, 14C, 131I, 125I или 3Н), чтобы представляющие интерес клетки или ткань можно было локализовать при помощи иммуносцинтиографии.
Антитело может быть также использовано в качестве окрашивающего реагента в случае патологии при помощи методов, хорошо известных в данной области.
Терапевтические применения
Антитела по настоящему изобретению способны индуцировать гибель негемопоэтических раковых клеток. Таким образом, настоящее изобретение относится к терапевтическим применениям антител и полипептидов по настоящему изобретению для лечения и/или замедления развития рака, такого как колоректальный рак, рак легкого, рак поджелудочной железы, рак желудка, рак молочной железы, гепатоцеллюларный рак и рак щитовидной железы. Антителами по настоящему изобретению можно лечить любой рак, такой как рак ободочной кишки, колоректальный рак, рак легкого, рак молочной железы, опухоль головного мозга, злокачественная меланома, рак почки, рак мочевого пузыря, лимфомы, Т-клеточная лимфома, множественная миелома, рак желудка, рак поджелудочной железы, рак шейки матки, эндометриальная карцинома, рак яичника, рак пищевода, рак печени, плоскоклеточный рак головы и шеи, рак кожи, рак мочевых путей, рак предстательной железы, хориокарцинома, рак горла, рак гортани, гиперплазия стромы яичника, андробластома, гиперплазия эндометрия, эндометриоз, эмбриома, фибросаркома, саркома Капоши, гемангиома, кавернозная гемангиома, ангиобластома, ретинобластома, астроцитома, нейрофиброма, олигодендроглиома, медуллобластома, ганглионейробластома, глиома, рабдомиосаркома, гамартобластома, остеогенная саркома, лейомиосаркома, саркома щитовидной железы и опухоль Вильмса, если раковая клетка экспрессирует эпитоп, узнаваемый антителами по настоящему изобретению. Указанный способ может дополнительно включать стадию обнаружения связывания антитела или полипептида по настоящему изобретения с опухолевой или раковой клеткой у субъекта, нуждающегося в лечении.
Субъекту, нуждающемуся в лечении, обычно вводят эффективное количество композиции, содержащей антитело или полипептид, что позволяет ингибировать рост раковой клетки и/или индуцировать гибель раковой клетки. Композицию предпочтительно получают с использованием фармацевтически приемлемого носителя.
В одном варианте осуществления изобретения получаемая композиция предназначена для введения в виде внутрибрюшинных, внутривенных, подкожных и внутримышечных инъекций, а также другими способами введения, такими как пероральное введение, введение через слизистую оболочку, введение ингаляцией, сублингвальное введение и т.д.
Другой вариант осуществления настоящего изобретения также включает введение композиции, содержащей антитела или полипептиды по настоящему изобретению, конъюгированные с другими молекулами, такими как детектируемые метки, терапевтические или цитотоксические агенты. Указанные агенты могут включать, не ограничиваясь ими, радиоактивные изотопы, токсины, токсоиды, воспалительные агенты, ферменты, антисмысловые молекулы, пептиды, цитокины или химиотерапевтические средства. Специалистам в данной области известны методы конъюгации антител с такими молекулами. См., например, публикации РСТ WO 92/08495, WO 91/14438, WO 89/12624, патент США № 5314995 и европейский патент № 396387, которые полностью включены в настоящее описание изобретения в виде ссылки.
В одном варианте осуществления изобретения композиция содержит антитело или полипептид, конъюгированный с цитотоксическим агентом. Цитотоксические агенты могут включать любые агенты, которые являются губительными для клеток. Предпочтительный класс цитотоксических агентов, которые могут быть конъюгированы с антителами или их фрагментами, может включать, не ограничиваясь ими, паклитаксол, цитохалазин В, грамицидин D, бромид этидия, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол, пуромицин и их аналоги или гомологи.
Доза, необходимая для лечения, зависит от выбора способа введения, характера препарата, природы заболевания субъекта, роста, массы тела, площади поверхности, возраста и пола субъекта; других вводимых лекарственных средств и решения лечащего врача. Приемлемые дозы находятся в пределах 0,01-1000,0 мг/кг.
Могут быть использованы любые нижеследующие дозы: доза, равная по меньшей мере примерно 50 мг/кг массы тела; по меньшей мере примерно 10 мг/кг массы тела; по меньшей мере примерно 3 мг/кг массы тела; по меньшей мере примерно 1 мг/кг массы тела; по меньшей мере примерно 750 мкг/кг массы тела; по меньшей мере примерно 500 мкг/кг массы тела; по меньшей мере примерно 250 мкг/кг массы тела; по меньшей мере примерно 100 мкг/кг массы тела; по меньшей мере примерно 50 мкг/кг массы тела; по меньшей мере примерно 10 мкг/кг массы тела; по меньшей мере примерно 1 мкг/кг массы тела или меньше. Может быть произведено повторное введение в течение нескольких дней или более продолжительного периода времени в зависимости от состояния субъекта до достижения желаемого подавления симптомов заболевания. Иллюстративная схема введения включает введение еженедельной дозы, равной примерно 6 мг/кг антитела. Однако могут быть использованы другие схемы введения в зависимости от фармакокинетического воздействия, которого желает достичь лечащий врач. Эмпирические данные, такие как время полужизни, обычно помогают определить дозу. Результат такого лечения можно легко контролировать при помощи стандартных методов и анализов.
Некоторым субъектам может потребоваться введение нескольких доз. Частота введения может быть определена и отрегулирована в процессе лечения. Например, частоту введения можно определить или отрегулировать в зависимости от типа и стадии рака, подлежащего лечению, профилактического или терапевтического введения, предшествующего лечения, клинической истории болезни субъекта, реакции на данное средство и решения лечащего врача. Лечащий врач обычно продолжает введение терапевтического антитела (такого как химерное антитело 5F1) до тех пор, пока соответствующая доза не обеспечит достижения требуемого результата. В некоторых случаях могут быть использованы препараты антител с пролонгированным действием. В данной области известны разные препараты и устройства для достижения пролонгированного действия.
В одном варианте осуществления изобретения дозы для антител или полипептидов могут быть определены эмпирически для субъектов, которым было произведено одно или несколько введений. Субъектам вводят возрастающие дозы антител или полипептидов. Для оценки эффективности антител или полипептидов можно контролировать маркеры симптомов заболевания, таких как CD43 или СЕА. Эффективность in vivo можно также определить, измеряя опухолевую массу или объем, время развития заболевания (TDP) и/или скорости реакции (RR).
Введение антитела или полипептида способом по настоящему изобретению может быть непрерывным или прерывистым, например, в зависимости от физиологического состояния реципиента, терапевтического или профилактического введения и других факторов, известных квалифицированным лечащим врачам. Введение антитела или полипептида может быть по существу непрерывным в течение заранее выбранного периода времени или может быть периодическим с промежутками между дозами.
Другие препараты имеют приемлемые формы доставки, известные в данной области, которые включают, не ограничиваясь ими, такие носители, как липосомы. См., например, публикацию Mahato et al. (1997) Pharm. Res. 14:853-859. Липосомные препараты включают, не ограничиваясь ими, цитофектины, многослойные везикулы и однослойные везикулы.
В другом варианте осуществления изобретения композиция может включать одно или несколько противораковых средств, одно или несколько антител по настоящему изобретению либо антитело или полипептид, который связывается с другим антигеном. Такая композиция может содержать по меньшей мере одно, по меньшей мере два, по меньшей мере три, по меньшей мере четыре, по меньшей мере пять разных антител. Антитела и другие противораковые средства могут находиться в одном препарате (например, в смеси, как такие препараты часто определяются в данной области) или в отдельных препаратах, вводимых одновременно или последовательно, являясь при этом особенно полезными при лечении более широкого круга субъектов.
Полинуклеотид, кодирующий любые антитела или полипептиды по настоящему изобретению, может быть также использован для доставки и экспрессии любых антител или полипептидов по настоящему изобретению в требуемой клетке. Очевидно, что экспрессирующий вектор может быть использован для прямой экспрессии антитела или полипептида. Экспрессирующий вектор может быть введен любым способом, известным в данной области, например, внутрибрюшинно, внутривенно, внутримышечно, подкожно, интратекально, интравентрикулярно, перорально, энтерально, парентерально, назально, дермально, сублингвально или путем ингаляции. Например, введение экспрессирующих векторов включает местное или системное введение, в том числе инъекцию, пероральное введение, введение с помощью аппарата для выстреливания частиц или катетера и местное введение. Специалисту в данной области должны быть известны способы введения экспрессирующих векторов для экспрессии экзогенного белка in vivo. См., например, патенты США № 6436908, 6413942 и 6376471.
Может быть также произведена направленная доставка терапевтических композиций, включающих полинуклеотид, кодирующий любые антитела или полипептиды по настоящему изобретению. Опосредованные рецептором методы доставки ДНК описаны, например, в следующих публикациях Findeis et al., Trends Biotechnol. (1993) 11:202; Chiou et al., Gene Therapeutics: Methods And Applications Of Direct Gene Transfer (J. A. Wolff, ed.) (1994); Wu et al., J. Biol. Chem. (1988) 263:621; Wu et al., J. Biol. Chem. (1994) 269:542; Zenke et al. (1990), Proc. Natl. Acad. Sci. USA, 87:3655; Wu et al. (1991), J. Biol. Chem. 266:338. Терапевтические композиции, содержащие полинуклеотид, вводят в количестве от около 100 нг до около 200 мг ДНК для местного применения в соответствии с методами генотерапии. В процессе генотерапии могут быть также использованы концентрации в пределах от около 500 нг до около 50 мг, от около 1 мкг до около 2 мг, от около 5 мкг до около 500 мкг и от около 20 мкг до около 100 мкг ДНК.
Терапевтические полинуклеотиды и полипептиды по настоящему изобретению могут быть доставлены с помощью векторов для доставки генов. Вектор для доставки генов может иметь вирусное или невирусное происхождение (см. публикации Jolly (1994), Cancer Gene Therapy 1:51; Kimura (1994), Human Gene Therapy 5:845; Connelly (1985), Human Gene Therapy 1:185; и Kaplitt (1994), Nature Genetics 6:148). Экспрессия таких кодирующих последовательностей может быть индуцирована при помощи эндогенных или гетерологичных промоторов млекопитающих. Экспрессия кодирующей последовательности может быть конститутивной или регулируемой.
В данной области хорошо известны векторы на основе вирусов, предназначенные для доставки и экспрессии необходимого полинуклеотида в требуемой клетке. Типичные векторы на основе вирусов включают, не ограничиваясь ими, векторы на основе рекомбинантных ретровирусов, описанные, например, в публикациях РСТ № WO 90/07936; WO 94/03622; WO 93/25698; WO 93/25234; WO 93/11230; WO 93/10218; WO 91/02805; патентах США №№ 5219740, 4777127; патенте Великобритании № 2200651 и европейском патенте № 0345242; векторы на основе альфавируса, например, векторы на основе вируса Синдбис, вируса лихорадки леса Семлики (АТСС VR-67; ATCC VR-1247), вируса Росс Ривер (ATCC VR-373; ATCC VR-1246) и вируса венесуэльского энцефалита лошадей (АТСС VR-923; ATCC VR-1250; ATCC VR 1249; ATCC VR-532)) и векторы на основе аденоассоциированного вируса (AAV), описанные, например, в публикациях РСТ № WO 94/12649, WO 93/03769, WO 93/19191, WO 94/28938, WO 95/11984 и WO 95/00655. Можно также ввести ДНК, связанную с убитым аденовирусом, в соответствии с описанием, приведенным в публикации Curiel (1992), Hum. Gene Ther. 3:147.
Могут быть также использованы векторы для невирусной доставки и способы их применения, которые включают, не ограничиваясь ими, поликатионную конденсированную ДНК, связанную или не связанную с убитым аденовирусом (см., например, публикацию Curiel (1992), Hum. Gene. Ther. 3:147); ДНК, связанную с лигандом (см., например, публикацию Wu (1989), J. Biol. Chem. 264:16985); векторы для доставки в эукариотические клетки (см., например, патент США № 5814482, публикации РСТ № WO 95/07994, WO 96/17072, WO 95/30763 и WO 97/42338) и нейтрализацию заряда нуклеиновой кислоты или слияние с клеточными мембранами.
Может быть также использована депротеинизированная ДНК. Типичные методы введения депротеинизированной ДНК описаны в публикации РСТ № WO 90/11092 и патенте США № 5580859. Липосомы, которые могут служить в качестве носителей для доставки генов, описаны в патенте США № 5422120, публикациях РСТ №№ WO 95/13796, WO 94/23697, WO 91/14445 и европейском патенте № 0524968. Дополнительные методы описаны в публикациях Philip (1994), Mol. Cell Biol. 14:2411 и Woffendin (1994), PNAS 91:1581.
Кроме того, настоящее изобретение относится к способу лечения рака у субъекта, который включает: а) введение указанному субъекту эффективного количества композиции, включающей антитело по настоящему изобретению; и b) проведение дополнительной противораковой терапии. В некоторых вариантах осуществления изобретения дополнительная терапия включает хирургическую операцию, лучевую терапию, гормональную терапию, генотерапию, терапию другими антителами и химиотерапию. Композицию, содержащую антитело, можно вводить одновременно с проведением дополнительной терапии (например, одновременное введение) и/или последовательно (например, последовательное введение). Например, композицию, содержащую антитело, можно вводить отдельно от дополнительной терапии с интервалом времени не более чем примерно 15 минут, например, примерно 10, 5 или 1 минута. Альтернативно композицию, содержащую антитело, можно вводить отдельно от дополнительной терапии с интервалом времени более чем примерно 15 минут, например, примерно 20, 30, 40, 50 или 60 минут, 1 день, 2 дня, 3 дня, 1 неделя, 2 недели, 1 месяц или больше.
Композицию, содержащую антитело по настоящему изобретению, можно вводить последовательно или одновременно с одним или несколькими другими лекарственными средствами, такими как химиотерапевтические средства (такие как 5-FU, 5-FU/MTX, 5-FU/лейковорин, левамизол, иринотекан, оксалиплатин, капецитабин или урацил/тегафур), иммуноадъюванты, ингибиторы роста, цитотоксические агенты, цитокины и т.д. Количество вводимого антитела и лекарственного средства зависит от типа применяемых лекарственных средств, патологического состояния, подлежащего лечению, схемы и способов введения, но обычно меньше количества, вводимого при отдельном использовании каждого лекарственного средства.
После введения композиции, содержащей антитело по настоящему изобретению, можно разными методами, хорошо известными специалисту в данной области, определить эффективность композиции как in vitro, так и in vivo. Хорошо известны разные животные модели, используемые для исследования противораковой активности композиции-кандидата. Такие методы включают трансплантацию человеческой опухоли бестимусным голым мышам или мышам scid/scid, или генетические модели опухоли мышей, такие как мыши с отсутствием гена р53. Природа указанных животных моделей позволяет с их помощью прогнозировать in vivo реакции людей. Такие модели могут быть созданы путем введения клеток сингенетическим мышам стандартными методами, такими как подкожная инъекция, инъекция в хвостовую вену, имплантация в селезенку, внутрибрюшинная имплантация, имплантация под капсулу почки и т.д.
Наборы
Настоящее изобретение относится также к наборам, предназначенным для использования при осуществлении способов по настоящему изобретению. Наборы по настоящему изобретению включают один или несколько контейнеров, содержащих очищенное антитело или полипептид по настоящему изобретению и инструкции по применению в соответствии со способами по настоящему изобретению, рассмотренными в настоящем описании изобретения. В некоторых вариантах осуществления изобретения указанные инструкции включают описание введения антитела для лечения и/или замедления развития рака негемопоэтического происхождения, такого как колоректальный рак, в соответствии со способами по настоящему изобретению. Указанный набор может дополнительно включать описание выбора субъекта, подходящего для лечения, с учетом наличия и стадии заболевания или экспрессии эпитопа на раковых клетках данного субъекта.
В некоторых вариантах осуществления изобретения наборы для обнаружения раковой клетки в образце включают антитело или полипептид по настоящему изобретению и реагенты, необходимые для обнаружения связывания указанного антитела или полипептида с клеткой в образце.
Инструкции, относящиеся к применению антител или полипептидов для лечения или замедления развития рака, обычно включают информацию о дозе, схеме введения и способе введения для предполагаемого лечения. Контейнеры могут содержать одноразовые дозы, нерасфасованное лекарственное средство (например, упаковки лекарственных средств для многократного приема) или дозы меньше стандартных доз. Инструкции, прилагаемые к наборам по настоящему изобретению, обычно напечатаны на наклейке или вкладыше в упаковку (например, в набор вложен лист бумаги), но допустимы также машиночитаемые инструкции (например, инструкции на магнитном или оптическом диске).
Наклейка или вкладыш в упаковку содержит информацию о том, что данная композиция предназначена для лечения рака, рассмотренного в настоящем описании изобретения. Могут быть предусмотрены инструкции по выполнению любых способов по настоящему изобретению.
Наборы по настоящему изобретению находятся в приемлемой упаковке. Приемлемая упаковка включает, не ограничиваясь ими, ампулы, флаконы, банки, гибкие упаковки (например, герметичные миларовые или пластиковые пакеты) и тому подобные. В объем настоящего изобретения также входят упаковки, предназначенные для использования вместе со специальным устройством, таким как ингалятор, устройство для введения в нос (например, распылитель) или устройство для вливания, такое как мини-насос. Набор может обеспечивать возможность стерильного доступа (например, контейнер может представлять собой мешок для внутривенного раствора или флакон с пробкой, проницаемой для иглы для подкожных инъекций). Контейнер также может обеспечивать возможность стерильного доступа (например, контейнер может представлять собой мешок для внутривенного раствора или флакон с пробкой, проницаемой для иглы для подкожных инъекций). По меньшей мере один активный агент в композиции является антителом по настоящему изобретению. Указанный контейнер может дополнительно включать второй фармацевтически активный агент.
Наборы могут необязательно включать дополнительные компоненты, такие как буферы и необходимая информация. Указанный набор обычно включает контейнер и наклейку или вкладыш в упаковку, которые или находятся на контейнере, или прилагаются к контейнеру.
ПРИМЕРЫ
Приведенные ниже примеры служат для иллюстрации изобретения и не ограничивают его объем.
Пример 1. Клонирование вариабельных областей легкой и тяжелой цепей антитела 5F1
Как указано в заявке на патент США № 11/811303, поданной 06/07/07 (публикация США № 2008/0171043), кДНК вариабельных областей легкой и тяжелой цепей антитела 5F1 амплифицировали при помощи ПЦР и синтезированные кДНК субклонировали в pCRII (Invitrogen) для определения последовательности. Нуклеотидные последовательности были получены из нескольких независимых клонов и подвергнуты анализу. Идентичные последовательности кДНК из независимых клонов были выбраны для представления V-области легкой или тяжелой цепи каждого антитела. В приведенной ниже таблице 2 показаны транслированные аминокислотные последовательности и нуклеотидные последовательности, кодирующие V-области легкой и тяжелой цепей мышиного антитела 5F1 (m5F1) и гуманизированного антитела 5F1Vc (h5F1Vc).
Таблица 2. Аминокислотные последовательности вариабельных областей антител и последовательности нуклеиновой кислоты, кодирующие вариабельные области антител (CDR-области подчеркнуты; сигнальные пептидные последовательности выделены курсивом)
Аминокислотная последовательность тяжелой цепи антитела m5F1 (SEQ ID NO:1) и нуклеотидная последовательность (SEQ ID NO:5)
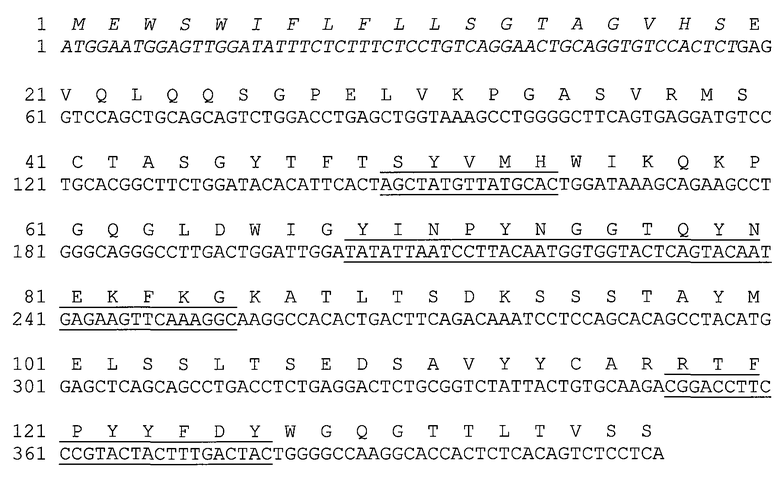
Аминокислотная последовательность легкой цепи антитела m5F1 (SEQ ID NO:2) и нуклеотидная последовательность (SEQ ID NO:6)


Аминокислотная последовательность тяжелой цепи антитела h5F1Vc (SEQ ID NO:3) и нуклеотидная последовательность (SEQ ID NO:7)
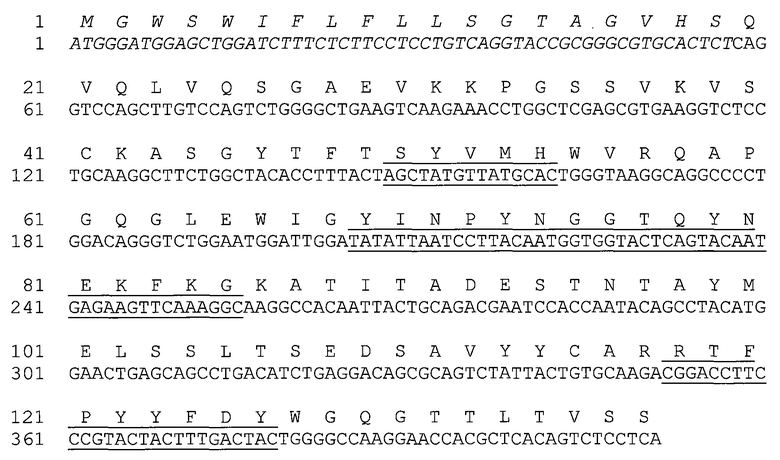
Аминокислотная последовательность легкой цепи h5F1Vc (SEQ ID NO:4) и нуклеотидная последовательность (SEQ ID NO:8)
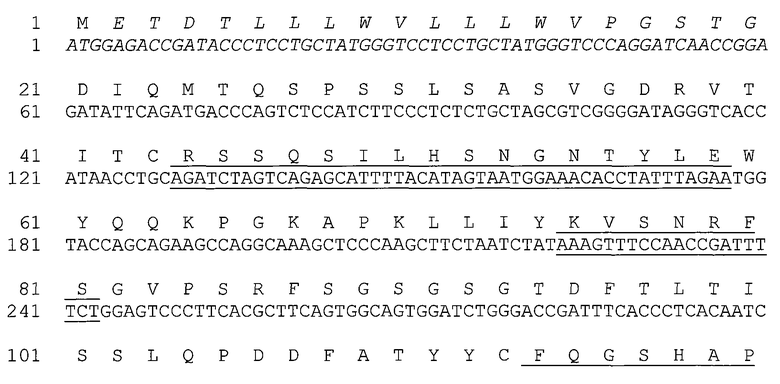

Пример 2. Модифицированная версия вариантов химерного антитела 5F1
Изотипом мышиного антитела 5F1 является IgG3 мыши. Для устранения проблемы, связанной с реакцией на антитела человека против мыши (НАМА), и обеспечения более эффективных Fc-зависимых функций в организме человека была создана химерная форма антитела 5F1 (c5F1) (c5F1-v0; для тяжелой цепи: SEQ ID NO:1 (VH), NO:9 (CH); для легкой цепи: SEQ ID NO:2 (VL), NO:10 (CL), см. таблицу 2 и фиг.2) путем объединения вариабельной (V) области мышиного антитела 5F1 с константной областью IgG1 человека. Сравнивали также аминокислотные последовательности константной области тяжелой цепи, которая включает СН1-область, шарнирную область, СН2- и СН3-области IgG1 человека и IgG3 мыши. В результате сравнения последовательностей было установлено, что СН1-область и шарнирная область характеризуются наибольшим различием между IgG3 мыши и IgG1 человека (фиг.1). В значении, использованном в настоящем описании изобретения при сравнении последовательностей, “*” означает, что остатки в данном столбце идентичны во всех последовательностях, подвергнутых сравнению, “:” означает, что имели место консервативные замены, и “.” означает, что имели место полуконсервативные замены. Для получения антитела c5F1 с индуцирующей апоптоз активностью, эквивалентной аналогичному показателю мышиного антитела 5F1, было произведено несколько модификаций в СН1-области и/или шарнирной области тяжелой цепи антитела c5F1 (таблица 3; нумерация остатков в таблице 3 произведена в соответствии с системой нумерации EU, описанной в публикации Burton, Mol. Immunol. 22:161-206, 1985), и несколько модификаций в легкой цепи антитела c5F1 (таблица 4). В некоторых случаях модифицированная тяжелая цепь была экспрессирована вместе с модифицированной у С-конца легкой цепью (таблица 5). См. также фиг. 2 для ознакомления с аминокислотными последовательностями тяжелой цепи и легкой цепи.
Модификация тяжелой цепи v0[H] на основании константной области IgG1 человека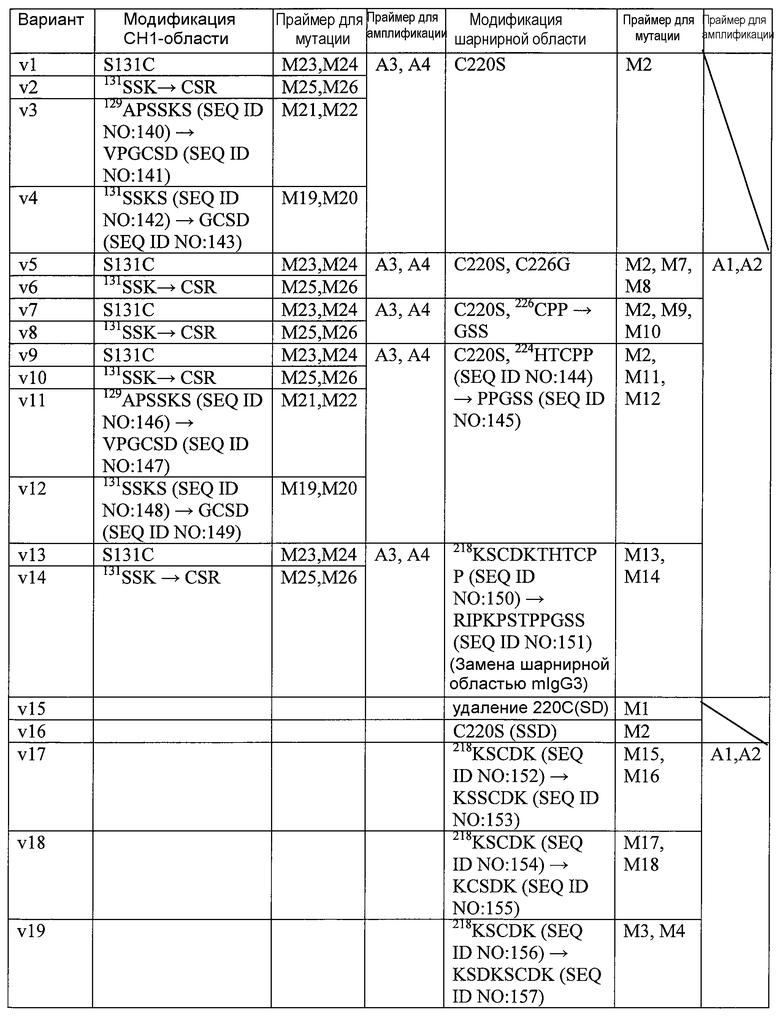
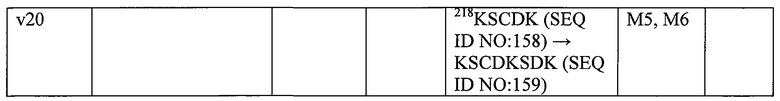
Модификации константной области легкой цепи v0[L] на основании каппа-цепи IgG1 человека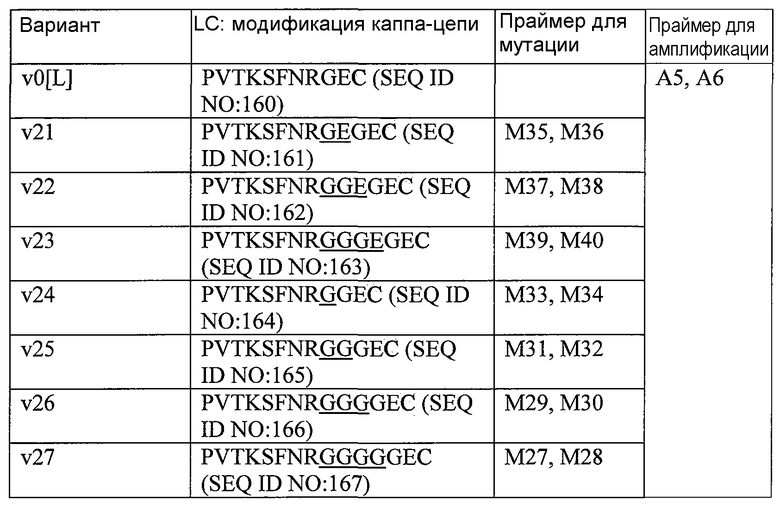
Химерные антитела, включающие комбинацию модифицированных константных областей тяжелой и/или легкой цепи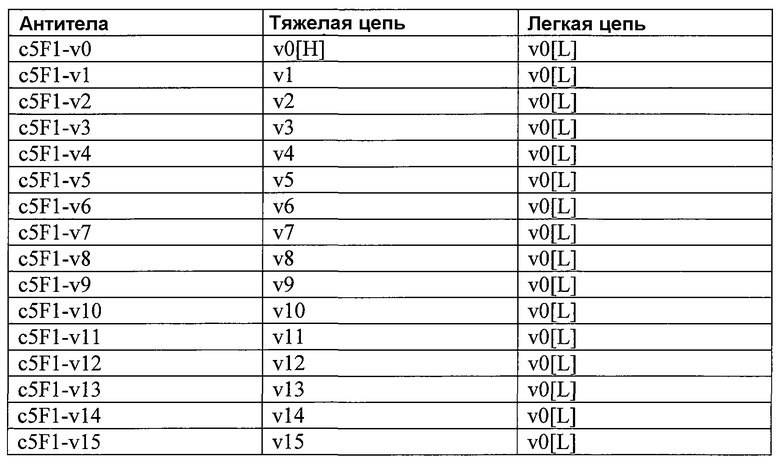
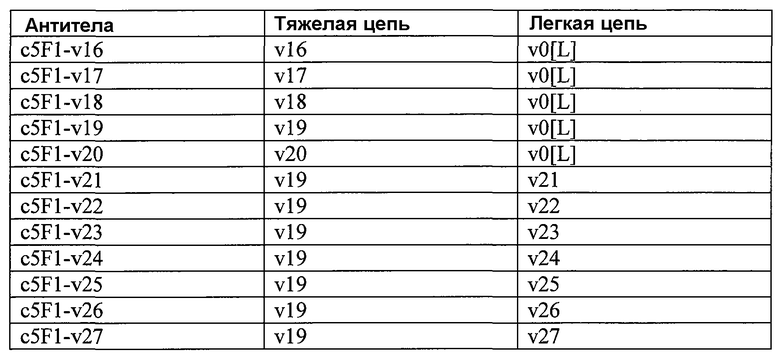
Пример 3. Введение изменений в константные области тяжелой и легкой цепей химерного антитела 5F1
Чтобы облегчить продуцирование и очистку антитела, для экспрессии химерного антитела 5F1 (c5F1) использовали вектор pcDNA5-FRT-hIgG1 (созданный в компании AbGenomics), содержащий константные области тяжелой цепи и легкой каппа-цепи IgG1 человека. Вариабельные области генов тяжелой цепи и легкой цепи антитела m5F1 амплифицировали отдельно при помощи ПЦР с использованием соответственно пар праймеров m5F1HC-XbaI f/m5F1HC-XbaI r и m5F1LC-XbaI f/m5F1LC-XbaI r (таблица 6, праймеры А3/А7 и А8/А9). Продукты ПЦР расщепляли XbaI и последовательно вставляли в вектор pcDNA5-FRT-hIgG1. Полностью собранную c5F1-экспрессирующую плазмиду c5F1/pcDNA5-FRT-hIgG1, содержащую ген тяжелой цепи и ген легкой цепи c5F1, использовали для экспрессии немодифицированного антитела c5F1. Такую же плазмиду использовали в качестве матрицы для введения модификаций в антитело c5F1.
Конструкции с делецией (v15) и заменой S (v16) в положении остатка 220 (нумерация EU) были созданы в результате выполнения сайтнаправленного мутагенеза при помощи ПЦР с использованием праймеров (таблица 6), вводящих мутации в гены c5F1/pcDNA5-FRT-hIgG1, из набора для сайтнаправленного мутагенеза QuickChange Multi (Stratagene, № по каталогу 200531-5) в соответствии с инструкциями производителя. Олигонуклеотид М1 (5'-CAGAGCCCAAATCTGACAAAACTCACAC-3' (SEQ ID NO:47)) использовали для делеции Cys в положении остатка 220 (v15), и олигонуклеотид М2 (5'-CAGAGCCCAAATCTTCTGACAAAACTCACAC-3' (SEQ ID NO:48)) использовали для замены Ser в положении остатка 220 (v16). Во избежание возможных случайных мутаций, вводимых при выполнении ПЦР в процессе сайтнаправленного мутагенеза, фрагменты ДНК, содержащие модификацию, вырезали при помощи AgeI (в СН1-области) и XmaI (в СН3-области) и повторно клонировали в первоначальный вектор c5F1/pcDNA5-FRT-hIgG1 для замены исходных немодифицированных областей.
Альтернативно для создания всех остальных модификаций выполняли ПЦР с перекрыванием (таблицы 3-6). Две полимеразные цепные реакции выполняли для создания двух фрагментов продуктов ДНК, содержащих требуемые мутации и перекрывающую последовательность, состоящую по меньшей мере из 20 нуклеотидов. Два продукта ПЦР затем смешивали, денатурировали и подвергали повторной гибридизации. Другую ПЦР с двумя внешними праймерами (из предыдущих двух ПЦР) использовали для амплификации собранного, непроцессированного фрагмента ДНК. Например, для v1 использовали пары праймеров А4/М23 и М24/А3 (таблица 6) с целью создания первых двух фрагментов при помощи ПЦР. Два фрагмента, полученных в результате выполнения ПЦР, затем смешивали, повторно гибридизировали и использовали внешний праймер (А3 и А4) для создания полноразмерного продукта ПЦР. И наконец, фрагменты ДНК, содержащие модификацию, повторно клонировали в первоначальный вектор c5F1/pcDNA5-FRT-hIgG1. Фрагмент, содержащий модификацию СН1-области, повторно клонировали на сайтах XbaI (в начале V-области тяжелой цепи) и AgeI (в СН1-области). Фрагмент, содержащий модификацию шарнирной области, повторно клонировали на сайтах AgeI (в СН1-области) и XmaI (в СН3-области). Для получения С-концевой модификации легкой цепи продукты ПЦР клонировали на сайтах AvrII (в конце V-области легкой цепи) и BamHI (внизу от кодирующей последовательности легкой цепи) для замены первоначальных немодифицированных последовательностей.
Плазмиды, содержащие или не содержащие модификацию, затем трансфицировали в клетки Flp-In-CHO (Invitrogen, № по каталогу R758-07), используя липофетамин 2000 (Invitrogen, № по каталогу 11668-019). Культуральную среду, содержащую немодифицированные или модифицированные антитела c5F1, собирали и антитело очищали белком А. Очищенное антитело исследовали в отношении связывания и индуцирующей апоптоз активности в клетках COLO205.
Анализ связывания
Очищенные антитела m5F1, c5F1-v0, c5F1-v15 и c5F1-v16 в концентрации 0,125-4 мкг/мл добавляли к клеткам COLO205 в количестве 1,5×105 и инкубировали в течение 30 минут при 4°С, дважды промывали физиологическим раствором с фосфатным буфером (PBS), содержащим 2% FBS и 0,05% NaN3, и инкубировали с 1 мкг/мл соответствующих вторичных антител (R-PE-конъюгированный F(ab')2-фрагмент антитела козы против IgG(H+L) мыши, Southern Biotech, № по каталогу 1032-09; или R-PE-конъюгированное антитело козы против IgG человека, Southern Biotech, № по каталогу 2040-09) при 4°С в течение 30 минут. В конце окрашивания образцы дважды промывали PBS, содержащим 2% FBS и 0,05% NaN3, и анализировали при помощи проточного цитометра. Все проточные цитометрические анализы выполняли в проточном цитометре BD-LSR (Becton Dickinson), используя программное обеспечение Cell Quest.
Анализ апоптоза
Клетки COLO205 в количестве 1,5×105 высевали в лунки 96-луночных планшетов. Аликвоты очищенных антител m5F1, c5F1-v0, c5F1-v15, c5F1-v16 и контрольных антител в концентрации 2-32 мкг/мл получали в культуральной среде непосредственно перед использованием и добавляли в каждую лунку. Образец, обработанный m9E10 и h16C11A, использовали в качестве контрольного изотипа. Обработанные клетки выдерживали в термостате при 37°С в течение 6 часов до выполнения анализа апоптоза методом клеточного сортинга с возбуждением флуоресценции (FACS). При выполнении анализа апоптоза клеток измеряли окрашивание аннексином V, используя набор для обнаружения апоптоза, включающий аннексин-V-FITC, (Strong Biotech, № по каталогу AVK250), в соответствии с инструкциями производителя. Обработанные клетки собирали и ресуспендировали в связывающем буфере для аннексина V, содержащем аннексин V-FITC, при комнатной температуре. Клетки инкубировали в темноте в течение 15 минут и затем дважды промывали 200 мкл связывающего буфера для аннексина V. Перед выполнением анализа FACS добавляли 0,25 мкг/мл йодида пропидия (PI). Все проточные цитометрические анализы выполняли в проточном цитометре BD-LSR (Becton Dickinson), используя программное обеспечение Cell Quest. Клетки с положительной реакцией на аннексин V и/или клетки с положительной реакцией на PI считаются апоптическими клетками.
Праймеры, использованные для введения мутаций в ген антитела c5F1
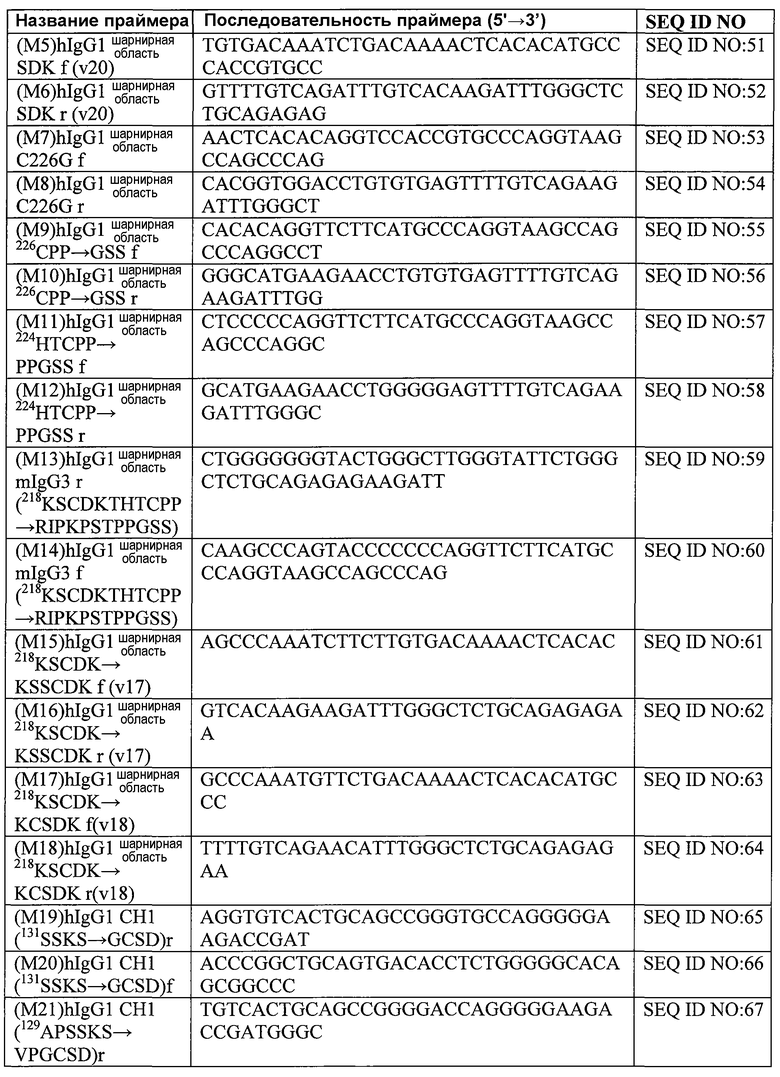
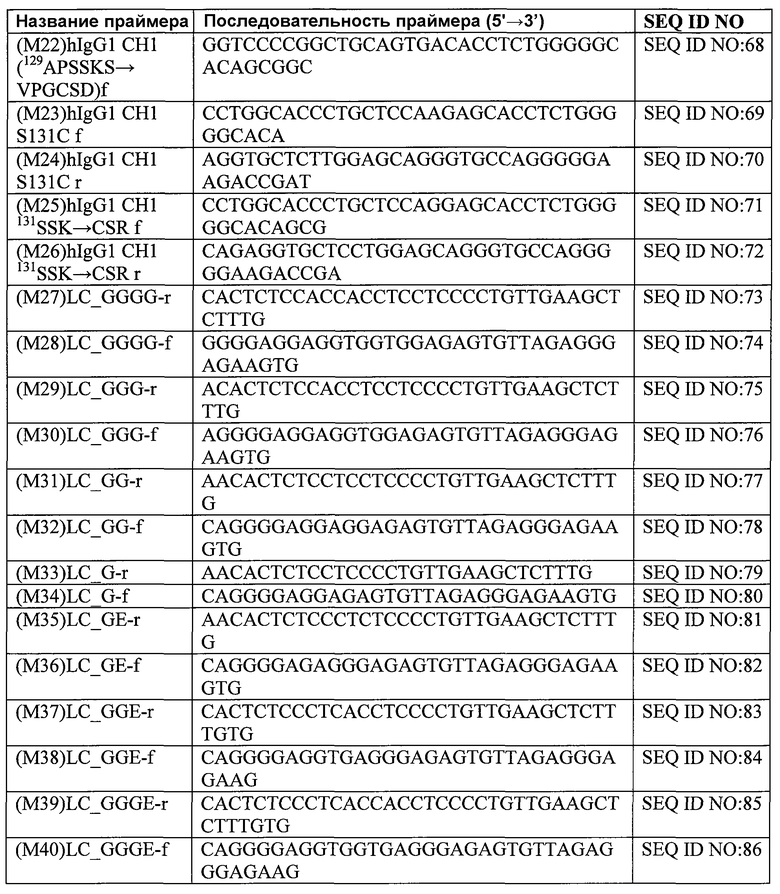
Результат
Данные связывания и индукции апоптоза для вариантов антител 5F1, полученные в результате выполнения проточного цитометрического анализа, показаны на фиг.3 и в приведенной ниже таблице 7. Антитела c5F1-v0, c5F1-v15 и c5F1-v16 связываются с клетками COLO205 и индуцируют апоптоз клеток COLO205 так же, как мышиное антитело m5F1. Антитела c5F1-v15 и c5F1-v16 связываются с клетками COLO205 в меньшей степени по сравнению с антителом c5F1. Что касается индукции апоптоза, то воздействие, наблюдаемое в клетках, обработанных антителом c5F1-v0, не было таким же эффективным, как при использовании антитела m5F1. Однако при использовании форм с модифицированной шарнирной областью (c5F1-v15 и c5F1-v16) индуцирующая апоптоз активность была восстановлена. Антитела c5F1-v15 и c5F1-v16 индуцировали апоптоз клеток COLO205 почти так же эффективно, как антитело m5F1, несмотря на то, что активность связывания антител c5F1-v15 и c5F1-v16 с клетками COLO205, по-видимому, была ниже, чем у антитела c5F1-v0. Антитела контрольного изотипа 9Е10 (контрольный изотип Ig мыши) и h16C11A (контрольный изотип IgG человека) в концентрации 32 мкг/мл не индуцировали апоптоз клеток COLO205.
Анализ апоптоза, индуцируемого антителами 5F1 в клетках COLO205 через шесть часов
Пример 4. Гуманизация антител 5F1
Был также создан гуманизированный вариант антитела 5F1 (фиг.4) и введен в экспрессирующие плазмиды с модификациями константных областей (см. примеры 2 и 3).
Область, определяющая комплементарность, (CDR) была использована для создания вариабельной области гуманизированного антитела 5F1 (h5F1M), в котором CDR-области вариабельной области мышиного антитела 5F1 введены в каркасную область вариабельной области IgG1 человека (акцепторное антитело) методом рекомбинантных ДНК. Чтобы определить наиболее подходящее акцепторное антитело для мышиного антитела 5F1, последовательности вариабельной области мышиного антитела 5F1 анализировали вместе с базой данных иммуноглобулинов, созданной в компании AbGenomics. Мышиное антитело М195 (Man Sung Со et al., J. Immunol. 148(4):1149-1154 (15 февраля 1992 г.) лучше всего соответствовало мышиному антителу 5F1. Человеческое антитело Eu (Man Sung Со et al., J. Immunol. 148(4):1149-1154 (15 февраля 1992 г.) было выбрано в качестве акцепторного антитела. Нуклеотидные последовательности были сконструированы и синтезированы с возможностью создания гуманизированного варианта антитела 5F1 с тремя CDR-областями мышиного антитела 5F1, введенными в каркасную область вариабельных областей антитела Eu.
Для создания каждого гена V-области антитела h5F1M были синтезированы четыре пары олигонуклеотидов длиной 55-70 оснований, которые затем образовали перекрывающиеся области, состоящие по меньшей мере из 18 нуклеотидов (таблица 8, для тяжелой цепи: Н1-Н8, для легкой цепи: L1-L8). Сборку и амплификацию всех генов V-области выполняли в четыре этапа: 1) четыре пары комплементарных олигонуклеотидов (для тяжелой цепи: Н1/Н2, H3/H4, H5/H6 и Н7/Н8; для легкой цепи: L1/L2, L3/L4, L5/L6 и L7/L8) гибридизировали и области с 3'-концевыми разрывами заполняли фрагментом Кленова при выполнении отдельных реакций с образованием четырех фрагментов двухцепочечной ДНК (дцДНК); 2) полученные четыре фрагмента дцДНК смешивали попарно, денатурировали, повторно гибридизировали и 3'-концевой разрыв заполняли в результате выполнения двух отдельных реакций с образованием двух фрагментов дцДНК; 3) два полученных фрагмента дцДНК смешивали, денатурировали, повторно гибридизировали и 3'-концевой разрыв заполняли с образованием полноразмерной дцДНК; и 4) затем выполняли ПЦР с двумя внешними праймерами (для тяжелой цепи: А10 и А11, для легкой цепи: А12 и А13 (таблица 8), содержащими сайт XbaI, для амплификации собранных фрагментов VL и VH.
XbaI-содержащие фрагменты VH и VL затем вводили в вектор pcDNA5-FRT-hIgG1 на сайтах NheI и AvrII соответственно для тяжелой цепи и легкой цепи. Плазмиду h5F1M/pcDNA5-FRT-hIgG1, экспрессирующую полностью собранное антитело h5F1M и содержащую ген тяжелой цепи и легкой цепи антитела h5F1M, использовали для экспрессии немодифицированного антитела h5F1M. Такая же плазмида была использована в качестве матрицы для введения модификаций в антитело h5F1M (фиг.4).
Модификация антитела h5F1M
Полимеразную цепную реакцию с перекрыванием и сайтнаправленный мутагенез на основе ПЦР использовали для модификации вариабельной области антитела h5F1M (фиг.4) с помощью праймеров, указанных в таблицах 8 и 9. Немодифицированные или модифицированные вариабельные области антитела h5F1 были введены в константную область (немодифицированную или модифицированную) IgG человека, как показано в примерах 2 и 3. Экспрессирующие плазмиды затем трансфицировали клетки СНО. Супернатанты собирали и антитела очищали белком А. Очищенные антитела испытывали в отношении характеристик связывания и индукции апоптоза клеток COLO205.
Список праймеров, использованных при создании вариантов гуманизированных антител 5F1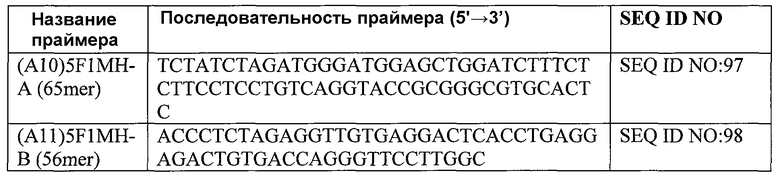
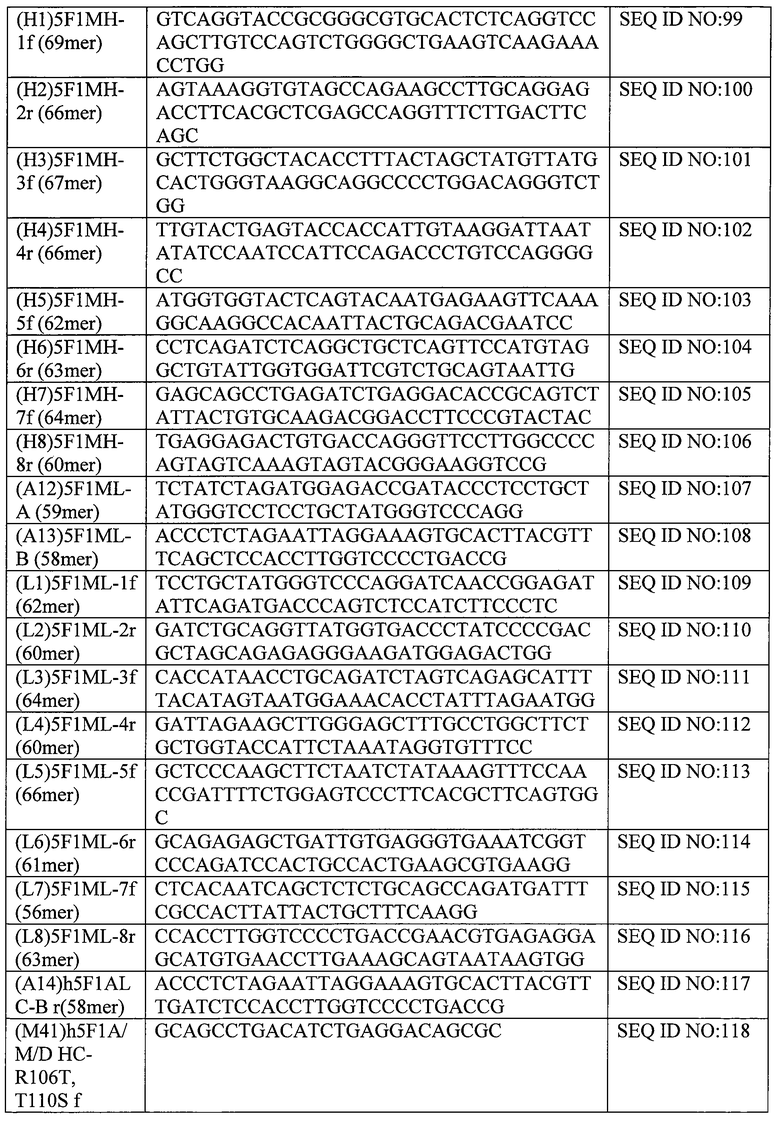
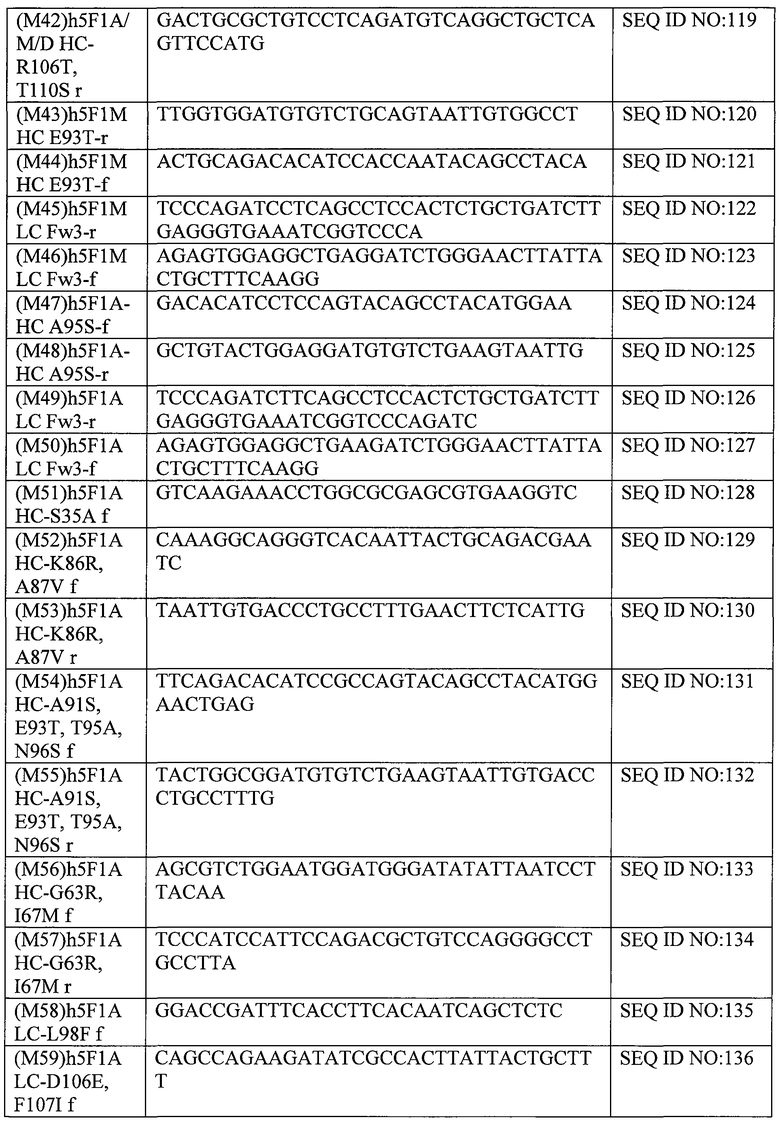
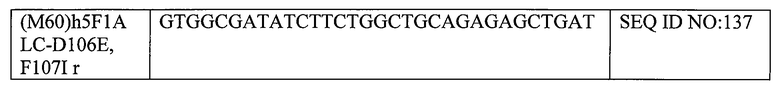
Праймеры для модификации антитела h5F1M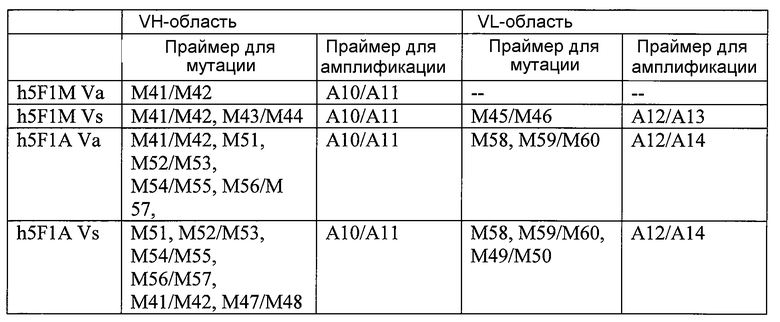
Пример 5. Исследование вариантов химерного антитела 5F1
Связывание антител с клетками Colo205
Очищенные антитела m5F1, c5F1-v0, c5F1-v17, c5F1-v24 и c5F1-v25 в концентрации 1 мкг/мл добавляли к клеткам Colo205 в количестве 2×105, инкубировали в течение 30 минут при 4°С, дважды промывали PBS, содержащим 1% FBS, и инкубировали с 1 мкг/мл соответствующих вторичных антител (R-PE-конъюгированный F(ab')2-фрагмент антитела козы против IgG(H+L) мыши, Southern Biotech, № по каталогу 1032-09; или R-PE-конъюгированное антитело козы против IgG человека, Sothern Biotech, № по каталогу 2040-09) при 4°С в течение 30 минут. В конце окрашивания образцы дважды промывали PBS, содержащим 1% FBS и 0,05% NaN3, и анализировали при помощи проточного цитометра. Все проточные цитометрические анализы выполняли в проточном цитометре BD-LSR (Becton Dickinson), используя программное обеспечение Cell Quest. Данные, приведенные в таблице 10, показывают, что все испытанные варианты антител 5F1 могут связываться с клетками Colo205.
Связывание с клетками Colo205
Анализ апоптоза
Клетки Colo205 в количестве 1,5×105 высевали в лунки 96-луночных планшетов. Аликвоты очищенных антител m5F1, c5F1, c5F1-v17, c5F1-v24, c5F1-v25 и контрольных антител в концентрации 8-32 мкг/мл получали в культуральной среде непосредственно перед использованием и добавляли в каждую лунку. Обработанные клетки выдерживали в термостате при 37°С в течение 6 часов до выполнения анализа апоптоза методом клеточного сортинга с возбуждением флуоресценции (FACS). При выполнении анализа апоптоза клеток измеряли окрашивание аннексином V, используя набор для обнаружения апоптоза, включающий аннексин-V-FITC (Strong Biotech, № по каталогу AVK250) в соответствии с инструкциями производителя. Обработанные клетки собирали и ресуспендировали в связывающем буфере для аннексина V, содержащем аннексин V-FITC, при комнатной температуре. Клетки инкубировали в темноте в течение 15 минут и затем дважды промывали 200 мкл связывающего буфера для аннексина V. Перед выполнением анализа FACS добавляли 0,25 мкг/мл йодида пропидия (PI). Все проточные цитометрические анализы выполняли в проточном цитометре BD-LSR (Becton Dickinson), используя программное обеспечение Cell Quest. Клетки с положительной реакцией на аннексин V и/или клетки с положительной реакцией на PI считаются апоптическими клетками. Данные, приведенные в таблице 11, показывают, что все испытанные варианты антител 5F1 могут индуцировать апоптоз клеток Colo205.
Индукция апоптоза клеток Colo205
Исследование ксенотрансплантатов
Клетки Colo205 в количестве 5×105 имплантировали подкожно в боковую область задней конечности 6-7-недельным мышам SCID в 0-й день. Мышам внутрибрюшинно инъекцировали антитела в количестве 30 мг/кг в 0-й день после инокуляции опухолевых клеток и производили повторное введение на 4-й, 7-й, 11-й, 14-й и 18-й день. В каждой экспериментальной группе было шесть мышей. Рост опухоли определяли, измеряя объем опухоли (мм3) штангенциркулем два раза в неделю, и величину опухоли вычисляли по формуле: π/6 × больший диаметр х (меньший диаметр)2 (Kievit E., Cancer Research, 60:6649-55). Мышей умерщвляли на 21-й день, опухоли удаляли и измеряли массу опухоли. Результаты, приведенные в таблице 12, свидетельствуют о противоопухолевом действии всех испытанных антител по сравнению с введением PBS.
Исследование ксенотрансплантатов
Синергическое действие антител 5F1 совместно с оксалиплатином в отношении индукции апоптоза клеток Colo205
Клетки Colo205 в количестве 1,4×105 высевали в лунки 96-луночных планшетов. Аликвоты оксалиплатина, восстановленного в 5% растворе глюкозы, получали непосредственно перед использованием и добавляли в каждую лунку в конечной концентрации, равной 1 и 10 мкг/мл, отдельно или совместно с аликвотами очищенных антител c5F1-v17, c5F1-v24, c5F1-v25 и контрольных антител в конечных концентрациях, равных 10 и 30 мкг/мл. Обработанные клетки выдерживали в термостате при 37°С в течение 24 часов до выполнения анализа апоптоза методом FACS. При выполнении анализа апоптоза клеток измеряли окрашивание аннексином V, используя набор для обнаружения апоптоза, включающий аннексин-V-FITC (Strong Biotech, № по каталогу AVK250) в соответствии с инструкциями производителя. Обработанные клетки собирали и ресуспендировали в связывающем буфере для аннексина V, содержащем аннексин V-FITC, при комнатной температуре. Клетки инкубировали в темноте в течение 15 минут и дважды промывали 200 мкл связывающего буфера для аннексина V. Перед выполнением анализа FACS добавляли 0,5 мкг йодида пропидия (PI). Все проточные цитометрические анализы выполняли в проточном цитометре BD-LSR (Becton Dickinson), используя программное обеспечение Cell Quest. Клетки с положительной реакцией на аннексин V и/или клетки с положительной реакцией на PI считаются апоптическими клетками. Данные, приведенные в таблице 13, свидетельствуют о синергическом действии всех испытанных антител 5F1 совместно с оксалиплатином в отношении индукции апоптоза раковых клеток Colo205.
Действие антител 5F1 совместно с оксалиплатином
Связывание антитела m5F1 с клетками SU.86.86 рака поджелудочной железы и индукция апоптоза указанных клеток
Очищенное антитело m5F1 и контрольные антитела в концентрации 1 мкг/мл добавляли к клеткам SU.86.86 в количестве 2×105 и инкубировали в течение 1 часа при 4°С, дважды промывали PBS, содержащим 1% FBS, и затем инкубировали с 1 мкг/мл соответствующих вторичных антител (R-PE-конъюгированный F(ab')2-фрагмент антитела козы против IgG(H+L) мыши, Southern Biotech, № по каталогу 1032-09) при 4°С в течение 1 часа. В конце окрашивания образцы дважды промывали PBS, содержащим 1% FBS, и анализировали при помощи проточного цитометра. Все проточные цитометрические анализы выполняли в проточном цитометре BD-LSR (Becton Dickinson), используя программное обеспечение Cell Quest.
Связывание антитела 5F1 с клетками SU.86.86
Клетки SU.86.86 в количестве 2×105 высевали в лунки 12-луночных планшетов. Аликвоты очищенного антитела m5F1 в концентрации 2-32 мкг/мл получали в культуральной среде непосредственно перед использованием и добавляли в каждую лунку. Контрольное антитело в концентрации 32 мкг/мл использовали для измерения фонового сигнала. Обработанные клетки выдерживали в термостате при 37°С в течение 6 часов до выполнения анализа методом FACS. При выполнении анализа апоптоза клеток измеряли окрашивание аннексином V, используя набор для обнаружения апоптоза, включающий аннексин-V-FITC (Strong Biotech, № по каталогу AVK250) в соответствии с инструкциями производителя. Обработанные клетки собирали и ресуспендировали в связывающем буфере для аннексина V, содержащем аннексин V-FITC, при комнатной температуре. Клетки инкубировали в темноте в течение 15 минут и дважды промывали 200 мкл связывающего буфера для аннексина V. Перед выполнением анализа FACS добавляли 0,25 мкг/мл йодида пропидия (PI). Все проточные цитометрические анализы выполняли в проточном цитометре BD-LSR (Becton Dickinson), используя программное обеспечение Cell Quest. Клетки с положительной реакцией на аннексин V и/или клетки с положительной реакцией на PI считаются апоптическими клетками.
Индукция апоптоза клеток SU.86.86 антителом m5F1
Данные, приведенные в таблицах 14 и 15, показывают, что антитело m5F1 может связываться линией клеток SU.86.86 рака поджелудочной железы, при этом связывание с антителом m5F1 вызывает апоптоз клеток SU.86.86.
Эксперименты по связыванию были выполнены с использованием антител c5F1.v15, c5F1.v16 и c5F1.v24. Указанные антитела характеризовались значительным связыванием с клетками SU.86.86. Анализ апоптоза выполняли в отношении антитела c5F1.v15. Данные показывают, что указанное антитело в концентрации 8 мкг/мл и 32 мкг/мл индуцирует апоптоз клеток SU.86.86 только в присутствии кросс-линкера мыши против IgG человека, который является специфическим Fcγ-фрагментом (Jackson ImmunoResearch 209-005-098).
Ссылки
Pimenidou, A., Madden, L.A., Topping, K.P., Smith, K.A., Monson, J.R., and Greenman, J. (2004) Novel CD43 specific phage antibodies react with early stage colorectal tumours. Oncol. Rep. 11(2):327-31.
Fernandez-Rodriguez, J., Andersson, C.X., Laos, S., Baeckstrom, D., Sikut, A., Sikut, R., and Hansson, G.C. (2002) The leukocyte antigen CD43 is expressed in different cell lines of nonhematopoietic origin. Tumour Biol. 23(4):193-201.
Cermak, L., Simova, S., Pintzas, A., Horejsi, V., and Andera, L. (2002) Molecular mechanisms involved in CD43-mediated apoptosis of TF-1 cells. Roles of transcription Daxx expression, and adhesion molecules. J Biol Chem. 8; 277(10):7955-61.
Carlow, D.A., Corbel, S.Y., and Ziltener, H.J. (2001) Absence of CD43 fails to alter T cell development and responsiveness. J Immunol. 166(1):256-61.
Nieto, M., Rodriguez-Fernandez, J.L., Navarro, F., Sancho, D., Frade, J.M., Mellado, M., Martinez-A.C., Cabanas, C., and Sanchez-Madrid, F. (1999) Signaling through CD43 induces natural killer cell activation, chemokine release, and PYK-2 activation. Blood. 94(8):2767-77.
Sikut, R., Andersson, C.X., Sikut, A., Fernandez-Rodriguez, J., Karlsson, N.G., and Hansson, G.C. (1999) Detection of CD43 (leukosialin) in colon adenoma and adenocarcinoma by novel monoclonal antibodies against its intracellular domain. Int. J. Cancer. 82(l):52-8.
Lopez, S., Seveau, S., Lesavre, P., Robinson, M.K., and Halbwachs-Mecarelli, L. (1998) CD43 (sialophorin, leukosialin) shedding is an initial event during neutrophil migration, which could be closely related to the spreading of adherent cells. Cell Adhes. Commun. 5(2):151-60.
Stockton, B.M., Cheng, G., Manjunath, N., Ardman, B., and von Andrian, U.H. (1998) Negative regulation of T cell homing by CD43. Immunity. 8(3):373-81.
McEvoy, L.M., Jutila, M.A., Tsao, P.S., Cooke, J.P., and Butcher, E.C. (1997) Anti-CD43 inhibits monocyte-endothelial adhesion in inflammation and atherogenesis. Blood. 90(9):3587-94.
Manjunath, N., Correa, M., Ardman, M., and Ardman, B. (1995) Negative regulation of T-cell adhesion and activation by CD43. Nature. 377(6549):535-8.
Pallant, A., Eskenazi, A., Mattei, M.G., Fournier, R.E.K., Carlsson, S.R., Fukuda, M., and Frelinger, J.G. (1989) Characterization of cDNA encoding human leukosialin and localization of the leukosialin gene to chromosome 16. Proc. Natl. Acad. Sci. USA 86:1328-32.
Shelley, C.S., Remold-O'Donnell, E., Davis III, A.E., Bruns, G.A.P., Rosen, F.S., Carroll, M.C., and Whitehead, A.S. (1989) Molecular characterization of sialophorin (CD43), the lymphocyte surface sialoglycoprotein defective in Wiskott-Aldrich syndrome. Proc. Natl. Acad. Sci. USA 86:2819-23.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА, РАСПОЗНАЮЩИЕ СОДЕРЖАЩИЙ УГЛЕВОДЫ ЭПИТОП НА CD-43 И СЕА, ЭКСПРЕССИРУЕМЫХ НА ЗЛОКАЧЕСТВЕННЫХ КЛЕТКАХ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2007 |
|
RU2461572C2 |
| АНТИТЕЛА, РАСПОЗНАЮЩИЕ СОДЕРЖАЩИЙ УГЛЕВОДЫ ЭПИТОП НА CD-43 И СЕА, ЭКСПРЕССИРУЕМЫХ НА ЗЛОКАЧЕСТВЕННЫХ КЛЕТКАХ, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2012 |
|
RU2616868C2 |
| Антитела к CD43 и их применение для лечения рака | 2016 |
|
RU2694903C1 |
| ЧЕТЫРЕХВАЛЕНТНЫЕ АНТИТЕЛА К PSGL-1 И ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2766000C2 |
| АНТИ-PD-1 АНТИТЕЛА | 2017 |
|
RU2752832C2 |
| КОВАЛЕНТНЫЕ ДИАНТИТЕЛА И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2593720C2 |
| СПОСОБЫ ЛЕЧЕНИЯ ГЛАЗНЫХ БОЛЕЗНЕЙ | 2008 |
|
RU2434639C2 |
| ИНТЕРЛЕЙКИН-13-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2016 |
|
RU2650767C2 |
| ИНТЕРЛЕЙКИН-13-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2012 |
|
RU2605327C2 |
| ИНТЕРЛЕЙКИН-13-СВЯЗЫВАЮЩИЕ БЕЛКИ | 2007 |
|
RU2472807C2 |

















































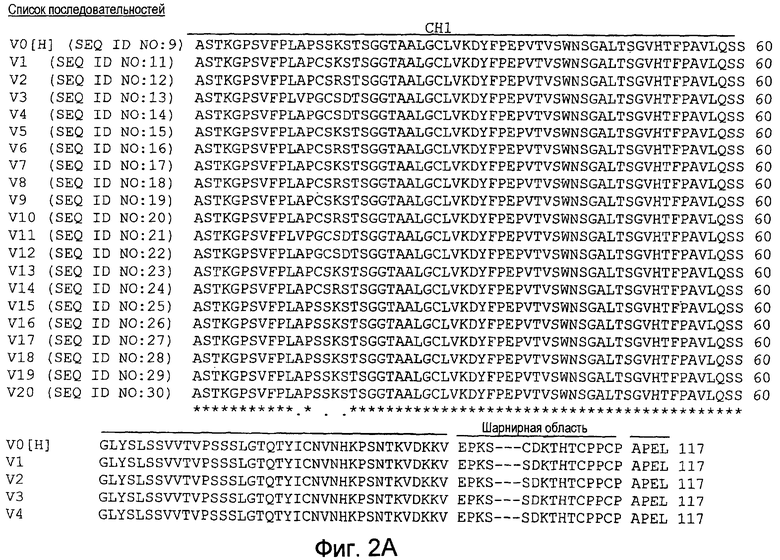



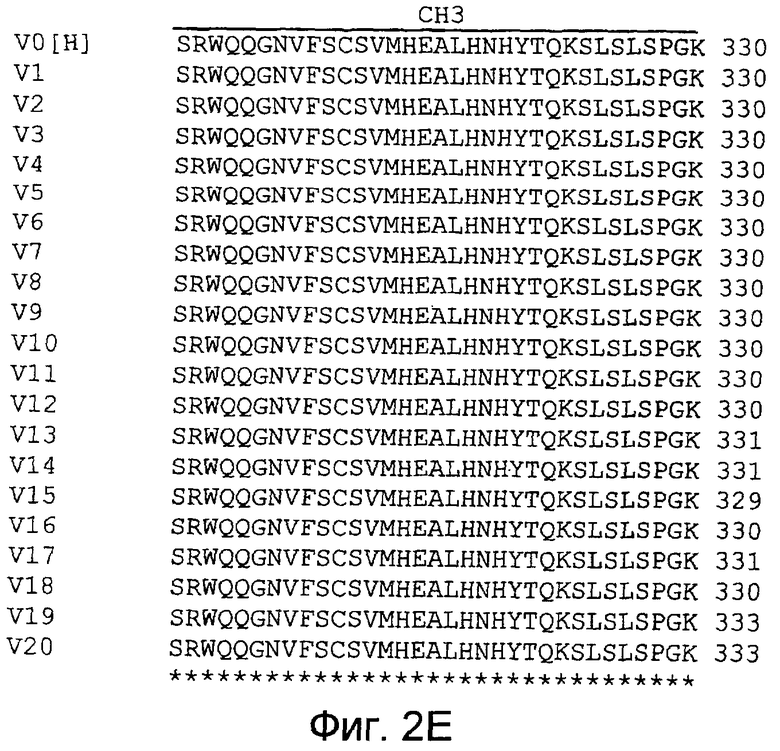
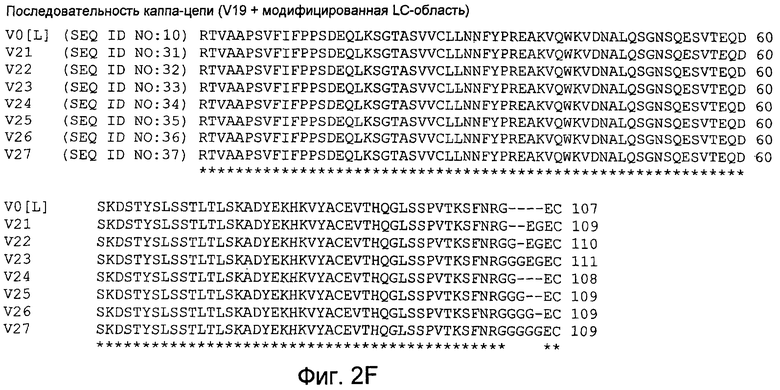
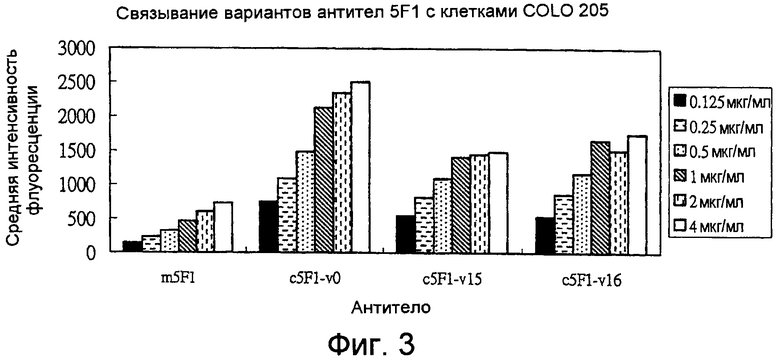
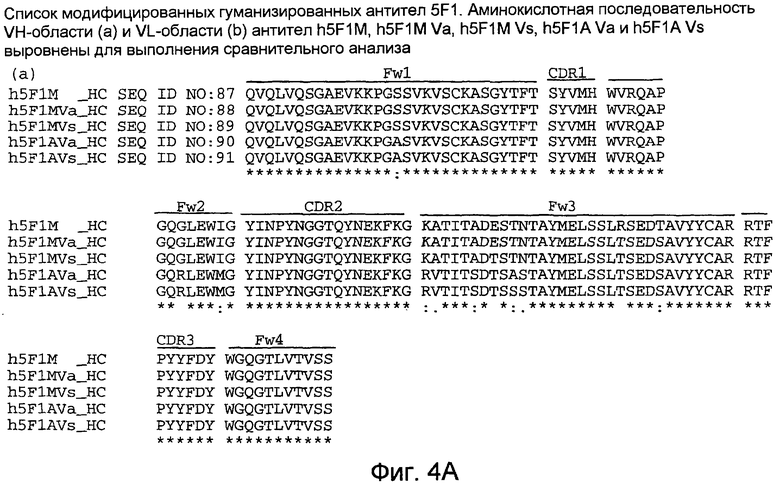
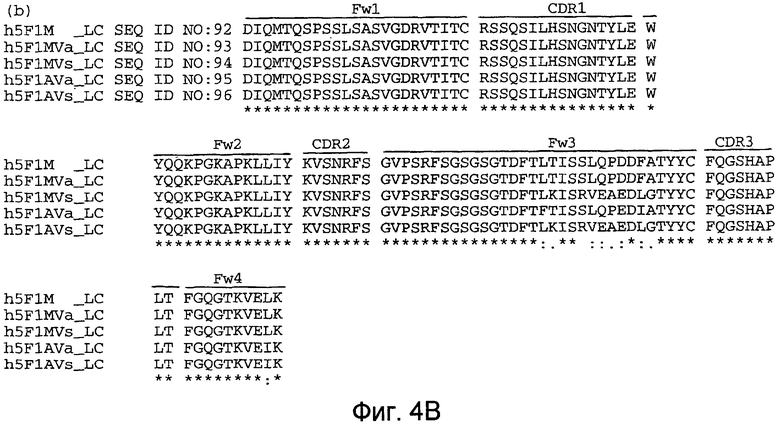
Настоящее изобретение относится к области иммунологии. Предложено антитело, специфически связывающееся с эпитопом на CD43 и CEA и имеющее модификации в константной области тяжелой и/или легкой цепи. Рассмотрены полинуклеотиды, вектор, клетка-хозяин и способы получения антитела по изобретению, а также фармацевтическая композиция, набор и способ лечения рака негемопоэтического происхождения. Данное изобретение может найти дальнейшее применение в терапии и диагностике заболеваний, опосредованных CD43 или CEA. 13 н. и 22 з.п. ф-лы , 15 табл., 5 пр., 4 ил.
1. Выделенное антитело, которое специфически связывается с эпитопом на CD43 и/или карциноэмбриональном антигене (СЕА), экспрессируемых негемопоэтической раковой клеткой, включающее тяжелую цепь и легкую цепь, в котором:
(а) тяжелая цепь содержит вариабельную область тяжелой цепи, включающую три области, определяющие комплементарность, (CDR) из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO:11-30; и
(b) легкая цепь содержит вариабельную область легкой цепи, включающую три области, определяющие комплементарность, (CDR) из аминокислотной последовательности SEQ ID NO:2, и константную область легкой цепи, включающую аминокислотную последовательность, выбранную из SEQ ID NO:10 и 31-37.
2. Антитело по п.1, которое является гуманизированным антителом.
3. Антитело по п.1, которое является химерным антителом.
4. Антитело по п.1, в котором константная область тяжелой цепи включает аминокислотную последовательность SEQ ID NO:27.
5. Антитело по п.4, в котором константная область легкой цепи включает аминокислотную последовательность SEQ ID NO:10.
6. Антитело по п.5, в котором вариабельная область тяжелой цепи включает аминокислотную последовательность остатков 20-137 последовательности SEQ ID NO:1 и константная область тяжелой цепи включает аминокислотную последовательность SEQ ID NO:27, вариабельная область легкой цепи включает аминокислотную последовательность остатков 20-131 последовательности SEQ ID NO:2 и константная область легкой цепи включает аминокислотную последовательность SEQ ID NO:10.
7. Антитело по п.1, в котором константная область тяжелой цепи включает аминокислотную последовательность SEQ ID NO:29.
8. Антитело по п.7, в котором константная область легкой цепи включает аминокислотную последовательность SEQ ID NO:34.
9. Антитело по п.8, в котором вариабельная область тяжелой цепи включает аминокислотную последовательность остатков 20-137 последовательности SEQ ID NO:1 и константная область тяжелой цепи включает аминокислотную последовательность SEQ ID NO:29, вариабельная область легкой цепи включает аминокислотную последовательность остатков 20-131 последовательности SEQ ID NO:2 и константная область легкой цепи включает аминокислотную последовательность SEQ ID NO:34.
10. Антитело по п.7, в котором константная область легкой цепи включает аминокислотную последовательность SEQ ID NO:35.
11. Антитело по п.10, в котором вариабельная область тяжелой цепи включает аминокислотную последовательность остатков 20-137 последовательности SEQ ID NO:1 и константная область тяжелой цепи включает аминокислотную последовательность SEQ ID NO:29, вариабельная область легкой цепи включает аминокислотную последовательность остатков 20-131 последовательности SEQ ID NO:2 и константная область легкой цепи включает аминокислотную последовательность SEQ ID NO:35.
12. Антитело по любому из пп.1-11, которое специфически связывается с эпитопом на CD43 и карциноэмбриональным антигеном (СЕА), экспрессируемых негемопоэтической раковой клеткой, выбранной из группы, состоящей из клетки колоректального рака, клетки рака поджелудочной железы или клетки рака желудка.
13. Антитело по любому из пп.1-11, которое конъюгировано с цитотоксическим агентом.
14. Антитело по п.13, где цитотоксический агент представляет собой радиоактивный изотоп или токсин.
15. Полинуклеотид для экспрессии тяжелой цепи антитела, кодирующий тяжелую цепь антитела по любому из пп.1-14.
16. Полинуклеотид для экспрессии легкой цепи антитела, кодирующий легкую цепь антитела по любому из пп.1-14.
17. Полинуклеотид для экспрессии тяжелой и легкой цепей антитела, кодирующий тяжелую и легкую цепи антитела по любому из пп.1-14.
18. Вектор для экспрессии тяжелой и/или легкой цепей антитела, включающий последовательность нуклеиновой кислоты, кодирующую тяжелую и/или легкую цепь антитела по любому из пп.1-14.
19. Клетка-хозяин для экспрессии антитела, включающая (а) один вектор по п.18, где вектор кодирует легкую и тяжелую цепи антитела, или (b) два вектора по п.18, где первый вектор кодирует тяжелую цепь антитела и второй вектор кодирует легкую цепь антитела.
20. Способ получения антитела, который включает культивирование клетки-хозяина по п.19, продуцирующей антитело, кодированное нуклеиновой кислотой, и выделение антитела, продуцированного клеткой-хозяином.
21. Способ получения антитела, который включает экспрессию в клетке-хозяине:
(а) полинуклеотида, включающего последовательность нуклеиновой кислоты, кодирующую тяжелую цепь, содержащую вариабельную область тяжелой цепи, включающую три CDR-области из аминокислотной последовательности SEQ ID NO:1, и константную область тяжелой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:11-30; и
(b) полинуклеотида, включающего последовательность нуклеиновой кислоты, кодирующую легкую цепь, содержащую вариабельную область легкой цепи, включающую три CDR-области из аминокислотной последовательности SEQ ID NO:2, и константную область легкой цепи, включающую аминокислотную последовательность, выбираемую из группы, состоящей из SEQ ID NO:10 и 31-37;
при этом полинуклеотиды, кодирующие тяжелую цепь и легкую цепь, коэкспрессированы в указанной клетке-хозяине.
22. Способ по п.20 или 21, в котором антитело является антителом, выделенным из культуры клеток.
23. Фармацевтическая композиция для лечения рака негемопоэтического происхождения, включающая антитело по любому из пп.1-14 в эффективном количестве и фармацевтически приемлемый носитель.
24. Набор для лечения рака негемопоэтического происхождения, включающий фармацевтическую композицию, содержащую антитело по любому из пп.1-14 и фармацевтически приемлемый носитель.
25. Набор по п.24, который дополнительно включает инструкции по введению субъекту эффективного количества фармацевтической композиции для лечения рака негемопоэтического происхождения.
26. Набор по п.24, который дополнительно включает инструкции по введению субъекту фармацевтической композиции совместно с другим противораковым средством для лечения рака негемопоэтического происхождения.
27. Набор по п.24, где рак негемопоэтического происхождения является колоректальным раком, раком поджелудочной железы или раком желудка.
28. Набор для лечения рака негемопоэтического происхождения, включающий первую фармацевтическую композицию, содержащую антитело по любому из пп. 1-14 и фармацевтически приемлемый носитель, и вторую фармацевтическую композицию, содержащую другое противораковое средство.
29. Набор по п.28, дополнительно включающий инструкции по введению субъекту первой фармацевтической композиции и второй фармацевтической композиции для совместного лечения рака негемопоэтического происхождения.
30. Набор по п.28, где рак негемопоэтического происхождения является колоректальным раком, раком поджелудочной железы или раком желудка.
31. Способ лечения рака негемопоэтического происхождения у субъекта, больного раком, который включает введение указанному субъекту эффективного количества композиции, включающей антитело по любому из пп.1-14.
32. Способ по п.31, в котором рак негемопоэтического происхождения является колоректальным раком, раком поджелудочной железы или раком желудка.
33. Способ лечения рака негемопоэтического происхождения у субъекта, который включает введение указанному субъекту определенного количества антитела по любому из пп.1-14 и определенного количества другого противоракового средства, при этом указанное антитело совместно с указанным противораковым средством обеспечивают эффективное лечение рака у субъекта.
34. Способ по п. 33, в котором противораковое средство является химиотерапевтическим средством.
35. Способ по п.33, в котором рак негемопоэтического происхождения является колоректальным раком, раком поджелудочной железы или раком желудка.
| DORAI H | |||
| et al., "Role of inter-heavy and light chain disulfide bonds in the effector functions of human immunoglobulin IgG1", Molecular Immunology (1992), 29(12): 1487-1491 | |||
| ROUX K.H | |||
| et al., "Comparisons of the Ability of Human IgG3 Hinge Mutants, IgM, IgE, and IgA2, to Form Small Immune Complexes: A Role for Flexibility and Geometry", J Immunol |
Авторы
Даты
2014-09-20—Публикация
2008-12-18—Подача