Область техники, к которой относится изобретение
Настоящее изобретение относится к определенным сульфонамидам, их N-оксидам, солям и композициям, подходящим для агрономических и неагрономических применений, и способам их применения для борьбы с паразитическими нематодами как в агрономической, так и в неагрономической окружающей среде.
Предшествующий уровень техники
Борьба с паразитическими нематодами растений является чрезвычайно важной для достижения высокой эффективности урожая. Повреждение корня, вызванное нематодой, может вызывать значительное уменьшение урожайности и качества, и, таким образом, приводит к повышенной стоимости для потребителя. Из-за распространенного развития устойчивости к антигельминтным средствам у нематодных паразитов, нематоды продолжают вызывать проблемы у домашнего скота, несмотря на доступные химические терапевтические средства. Продолжает существовать потребность в новых соединениях, которые более эффективны, менее дорогостоящие, менее токсичны, безопасны для окружающей среды или обладают различными способами действия.
В публикации европейской патентной заявки № 0244166 A2 раскрыты соединения формулы i в качестве гербицидов:
 ,
,
где, в том числе, R представляет собой H или органический заместитель, W представляет собой O или S, L представляет собой арильную или гетероарильную часть, и A выбран из перечня би-, три- и квадрициклических гетероциклических групп.
Соединения настоящего изобретения не раскрыты в указанной публикации.
Сущность изобретения
Настоящее изобретение относится к соединениям формулы 1 (включая все стереоизомеры), их N-оксидам и солям и содержащим их композициям, и их применению для борьбы с паразитической нематодой:
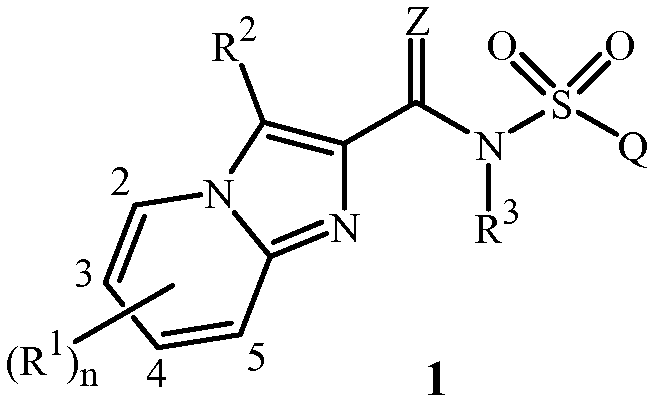 ,
,
где
Z представляет собой O или S;
каждый R1 независимо представляет собой галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, OC(O)OR8, OC(O)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)C(O)R7, N(R10)C(O)NR11R12, N(R10)S(O)2R9 или N(R10)S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей циано, нитро, OR4, NR5R6, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
R2 представляет собой H, галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, OC(O)OR8, OC(O)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)C(O)R7, N(R10)C(O)NR11R12, N(R10)S(O)2R9 или N(R10)S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей циано, нитро, OR4, NR5R6, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
R3 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей циано, нитро, OR4, NR5R6, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или C1-C6алкил, замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей фенил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
Q представляет собой фенил, нафталинил, 5- или 6-членное гетероароматическое кольцо или 8-10-членную гетероароматическую бициклическую кольцевую систему, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, OC(O)OR8, OC(O)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)C(O)R7, N(R10)C(O)NR11R12, N(R10)S(O)2R9, N(R10)S(O)2NR11R12 и R14;
каждый X независимо представляет собой O или S;
каждый R4 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C1-C6алкил, C2-C6алкенил или C2-C6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, включающей циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R4a независимо представляет собой H, C1-C6алкил или C1-C6галогеналкил;
каждый R5 независимо представляет собой H, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R5a независимо представляет собой H или C1-C6алкил;
каждый R6 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a;
каждый R6a независимо представляет собой H, C1-C6алкил, C(O)R13 или C(O)OR13;
каждый R7 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R7a независимо представляет собой C1-C6алкил или C1-C6галогеналкил;
каждый R8 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, C2-C6алкенил или C2-C6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, включающей циано, нитро, OR4, NR5R6, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R8a независимо представляет собой C1-C6алкил или C1-C6галогеналкил;
каждый R9 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, C2-C6алкенил или C2-C6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, включающей циано, нитро, OR4, NR5R6, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R9a независимо представляет собой C1-C6алкил или C1-C6галогеналкил;
каждый R10 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12;
каждый R10a независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил;
каждый R11 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, C2-C6алкенил или C2-C6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, включающей циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, C(O)NR11aR12, S(O)mR9a или S(O)2NR11aR12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11aR12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11aR12, NR5aR6a, OC(O)R7a и N(R10a)C(O)R7a;
каждый R11a независимо представляет собой H, C1-C6алкил, C2-C6алкенил или C2-C6алкинил;
каждый R12 независимо представляет собой H, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R13 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a;
каждый R14 независимо представляет собой C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, C2-C6алкенил или C2-C6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, включающей циано, нитро, OR4, NR5R6, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
каждый R15 независимо представляет собой C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
каждый m независимо равен 0, 1 или 2; и
n равно 0, 1, 2, 3 или 4.
Настоящее изобретение также относится к таким соединениям формулы 1 (включая все стереоизомеры), их N-оксидам и солям и содержащим их композициям, и их применению для борьбы с паразитической нематодой, как описано выше и ниже в данном описании, при условии, когда n равно 2, и один R1 представляет собой CF3 в положении 3 формулы 1, а другой R1 представляет собой Cl в положении 5 формулы 1, и R2 и R3 представляют собой H, тогда Q является другим, чем 2-хлорфенил, 2-хлор-6-метилфенил, 2,6-дихлорфенил, 2-хлор-4-фторфенил, 2,5-бис(2,2,2-трифторэтокси)фенил, 2,4,6-трихлорфенил, 2-хлор-5-(трифторметил)фенил или 3,5-диметил-4-изоксазолил.
Настоящее изобретение также обеспечивает композицию, содержащую соединение формулы 1, его N-оксид или соль и по меньшей мере один дополнительный компонент, выбранный из группы, включающей поверхностно-активные вещества, твердые разбавители и жидкие разбавители. Согласно одному варианту осуществления, настоящее изобретение также обеспечивает композицию для борьбы с паразитической нематодой, содержащей соединение формулы 1, его N-оксид или соль и по меньшей мере один дополнительный компонент, выбранный из группы, включающей поверхностно-активные вещества, твердые разбавители и жидкие разбавители, причем, указанная композиция необязательно дополнительно содержит по меньшей мере одно дополнительное биологически активное соединение или средство.
Настоящее изобретение обеспечивает способ борьбы с паразитической нематодой, включающий контакт паразитической нематоды или окружающей ее среды с биологически эффективным количеством соединения формулы 1, его N-оксида или соли (например, таким как композиция, описанная в данном описании). Настоящее изобретение также относится к такому способу, где паразитическую нематоду или окружающую ее среду приводят в контакт с композицией, содержащей биологически эффективное количество соединения формулы 1, его N-оксида или соли и по меньшей мере одного дополнительного компонента, выбранного из группы, включающей поверхностно-активные вещества, твердые разбавители и жидкие разбавители, причем указанная композиция необязательно дополнительно содержит биологически эффективное количество по меньшей мере одного дополнительного биологически активного соединения или средства.
Настоящее изобретение также обеспечивает способ защиты семян от паразитической нематоды, включающий контакт семян с биологически эффективным количеством соединения формулы 1, его N-оксидом или солью (например, таким как композиция, описанная в данном описании). Настоящее изобретение также относится к обработанным семенам.
Подробное описание настоящего изобретения
Как используется в данном описании, выражения “содержит”, “содержащий”, “включает”, “включающий”, “имеет”, “имеющий”, “вмещать”, “вмещающий”, “характеризующийся” или любой другой их вариант предназначены покрывать неисключительное включение, за исключением какого-либо ограничения, явно указанного. Например, композиция, смесь, процесс или способ, которые включают перечень элементов, необязательно ограничены только этими элементами, а могут включать другие элементы, явно не перечисленные или не присущие такой композиции, смеси, процессу или способу.
Переходная фраза “состоящий из” исключает любой конкретно не обозначенный элемент, стадию или ингредиент. В пункте формулы изобретения эта фраза будет закрывать пункт для включения материалов, отличных от тех, что перечислены, кроме примесей, обычно связанных с ними. Когда фраза “состоящий из” появляется в части основы пункта формулы, а не сразу после преамбулы, она ограничивает только элемент, изложенный в этой части; другие элементы не исключаются из пункта формулы в целом.
Переходная фраза “состоящий, главным образом, из” используется для определения композиции или способа, которое включает материалы, стадии, признаки, компоненты или элементы, в дополнение к раскрытым буквально, при условии, что эти дополнительные материалы, стадии, признаки, компоненты или элементы действительно существенно не влияют на основную и новую характеристику(и) заявленного изобретения. Выражение “состоящий, главным образом, из” занимает среднее положение между “содержащий” и “состоящий из”.
Где авторы определили изобретение или его часть открытым выражением, таким как “содержащий”, будет легко понять, что (если не указано иное), описание следует также понимать как описание такого изобретения с использованием выражения “состоящий, главным образом, из” или “состоящий из”.
Кроме того, если явно не указано иное, “или” относится к включающему или, но не исключающему или. Например, условие A или B удовлетворяется любым одним из следующего: A является верным (или присутствует), и B является неверным (или отсутствует), A является неверным (или отсутствует), и B является верным (или присутствует), и оба A и B являются верными (или присутствуют).
Также, единственное число элемента или компонента данного изобретения предназначены для неограничивающего рассмотрения числа случаев (т.е. событий) элемента или компонента. Следовательно, единственное число следует читать как включение одного или по меньшей мере одного, и форма единственного числа элемента или компонента также включает множественную, если число очевидно не означает единственное число.
Как используют в данном описании и формуле изобретения, термин “нематода” относится к живому организму Phylum Nematoda. Как определено в общем, “паразит” живет или растет внутри или питается другим живущим организмом (таким как растение, животное или человек), описанным как “хозяин”. Как приведено в настоящем описании и формуле изобретения, “паразитическая нематода” является, в частности, нематодой, которая портит или повреждает ткань или вызывает другие формы заболеваний у растений, животных (в частности, позвоночных) или людей.
Паразитная “инвазия” относится к присутствию паразитов в большом количестве, что представляет угрозу растениям, людям или животным. Присутствие может быть в окружающей среде, например, в жилище человека или животного, или окружающем имуществе или структурах, в сельскохозяйственной культуре или другом типе растения, в подстилке животного, на коже или шерсти животного, и т.д. Когда указанная инвазия находится в животном, например в крови или других внутренних тканях, термин инвазия также является синонимом термину “инфекция”, поскольку этот термин обычно понятен в данной области, если не указано иное.
Как определено в настоящем описании и формуле изобретения, выражения “паразитицидный” и “паразитицидно” относится к видимым воздействиям на паразитическую нематоду для обеспечения защиты растения, животного или человека от нематоды. Паразитицидное воздействие обычно относятся к снижению возникновения или активности целевой паразитической нематоды. Такое воздействие на нематоду включают некроз, гибель, замедленный рост, ослабленную подвижность или уменьшенную способность удерживаться на или в растении-хозяине, животном или человеке, сокращенное питание и ингибирование размножения. Указанные воздействия на паразитические нематоды обеспечивают борьбу (включая предотвращение, уменьшение или устранение) с паразитической инвазией или инфекцией растения, животного или человека. Следовательно “борьба” с паразитической нематодой означает достижение паразитицидного эффекта на нематоду. Выражения “паразитицидно эффективное количество” и “биологически эффективное количество” в контексте применения химического соединения для борьбы с паразитической нематодой относится к количеству соединения, которое достаточно для борьбы с паразитической нематодой.
Термин “агрономический” относится к производству полевых сельскохозяйственных культур, таких как пищевые и волокнистые, и включает выращивание соевых бобов и других бобовых растений, хлебных злаков (таких как пшеница, овес, ячмень, рожь, рис, маис/кукурузу), лиственных овощей (таких как латук, капуста и другие капустные урожаи), плодоносных овощей (таких как помидоры, перец, баклажан, крестоцветные и тыква), картофеля, батата, винограда, хлопка, плодов дерева (таких как семечковые, косточковые и цитрус), небольших фруктов (ягоды, вишни) и других специальных культур (таких как, канола, подсолнечник, оливки).
Термин “неагрономический” относится к отличному от полевых сельскохозяйственных культур, такому как применение в садовых культурах (таких как теплица, рассадник или декоративные растения, не растущие в поле), жилищных, сельскохозяйственных, коммерческих и промышленных структурах, травяных пластах (таких как тепличное хозяйство, питомник, площадка для игры в гольф, газон, спортивные площадки и т.д.), древесных продуктах, хранящихся продуктах, лесоводстве, относящемся к сельскому хозяйству, и контроле за растительностью, общественном здравоохранении (т.е. человек) и ветеринарии (например, прирученные животные, такие как питомцы, домашний скот и домашняя птица, неприрученные животные, такие как в живой природе).
Неагрономическое применение включают защиту животного от паразитической нематоды введением паразитицидно эффективного (т.е. биологически эффективного) количества соединения настоящего изобретения, обычно в форме композиции, составленной для ветеринарного применения, защищаемому животному.
В приведенных выше перечислениях термин “алкил”, используемый или отдельно, или в сочетании слов, таком как “галогеналкил”, включает алкил с прямой или разветвленной цепью, такой как, метил, этил, н-пропил, изопропил или различные изомеры бутила, пентила или гексила. “Алкенил” включает алкены с прямой или разветвленной цепью, такие как этенил, 1-пропенил, 2-пропенил и различные изомеры бутенила, пентенила и гексенила. “Алкенил” также включает полиены, такие как 1,2-пропадиенил и 2,4-гексадиенил. “Алкинил” включает алкины с прямой или разветвленной цепью, такие как этинил, 1-пропинил, 2-пропинил и различные изомеры бутинила, пентинила и гексинила. “Алкинил” может также включать части, включающие множество тройных связей, такой как 2,5-гексадиинил.
“Алкокси” включает, например, метокси, этокси, н-пропилокси, изопропилокси и различные изомеры бутокси, пентокси и гексилокси. “Алкоксиалкил” означает алкокси замещение на алкиле. Примеры “алкоксиалкила” включают CH3OCH2, CH3OCH2CH2, CH3CH2OCH2, CH3CH2CH2CH2OCH2 и CH3CH2OCH2CH2.
“Циклоалкил” включает, например, циклопропил, циклобутил, циклопентил и циклогексил. Термин “циклоалкилалкил” означает циклоалкильное замещение на алкильной части. Примеры “циклоалкилалкила” включают циклопропилметил, циклопентилэтил и другие циклоалкильные части, связанные с алкильными группами с прямой или разветвленной цепью. “Циклоалкенил” включает группы, такие как циклопентенил и циклогексенил, а также группы с более чем одной двойной связью, такие как 1,3- и 1,4-циклогексадиенил. Термин “циклоалкилциклоалкил” означает циклоалкильное замещение на другом циклоалкильном кольце, где каждое циклоалкильное кольцо независимо содержит от 3 до 7 атомов углерода в качестве членов кольца. Примеры циклоалкилциклоалкила включают циклопропилциклопропил (такой как 1,1'-бициклопропил-1-ил, 1,1'-бициклопропил-2-ил), циклогексилциклопентил (такой как 4-циклопентилциклогексил) и циклогексилциклогексил (такой как 1,1'-бициклогексил-1-ил), и различные цис- и транс-циклоалкилциклоалкильные изомеры (такие как (1R,2S)-1,1'-бициклопропил-2-ил и (1R,2R)-1,1'-бициклопропил-2-ил).
Термин “галоген”, или отдельно, или в сочетании слов, таком как “галогеналкил”, или когда используется в описании, таком как “алкил, замещенный галогеном”, включает фтор, хлор, бром или йод. Кроме того, когда используется в сочетании слов, таком как “галогеналкил”, или когда используется в описании, таком как “алкил, замещенный галогеном”, указанный алкил может быть частично или полностью замещен атомами галогена, которые могут быть одинаковыми или различными. Примеры “галогеналкила” или “алкила, замещенного галогеном” включают F3C, ClCH2, CF3CH2 и CF3CCl2. Термины “галогеналкокси”, “галогеналкенил”, “галогеналкинил” и подобные определены аналогично выражению “галогеналкил”. Примеры “галогеналкокси” включают CF3O, CCl3CH2O, HCF2CH2CH2O и CF3CH2O. Примеры “галогеналкенила” включают (Cl)2C=CHCH2 и CF3CH2CH=CHCH2. Примеры “галогеналкинила” включают HC≡CCHCl, CF3C≡C, CCl3C≡C и FCH2C≡CCH2.
Химическая аббревиатура C(O), как используется в данном описании, представляет собой карбонильную часть. Например, C(O)CH3 представляет собой ацетильную группу. Химическая аббревиатуры CO2 и C(O)O, как используется в данном описании, представляет собой часть сложного эфира. Например, CO2Me и C(O)OMe представляют собой сложный метиловый эфир.
“OCN” означает -O-C≡N, и “SCN” означает -S-C≡N.
Общее число атомов углерода в замещающей группе отмечено индексом “Ci-Cj”, где i и j являются числами от 1 до 14. C2алкоксиалкил означает CH3OCH2; C3алкоксиалкил означает, например, CH3CH(OCH3), CH3OCH2CH2 или CH3CH2OCH2; и C4алкоксиалкил означает различные изомеры алкильной группы, замещенной алкоксигруппой, содержащей всего четыре атома углерода, примеры включают CH3CH2CH2OCH2 и CH3CH2OCH2CH2.
Когда соединение замещено заместителем, имеющим подстрочный индекс, он показывает число указанных заместителей, которое может превышать 1, причем указанные заместители (когда они превышают 1) независимо выбраны из группы определенных заместителей, например, R1, n равно 0, 1, 2, 3 или 4. Когда группа содержит заместитель, которым может быть водород, например, R2 или R3, тогда, если этот заместитель взят как водород, следует помнить, что он является эквивалентом указанной группе, являющейся незамещенной. Когда переменная группа, как показано, необязательно присоединена к положению, например (Rv)r в U-29 приложения 1, где r может быть 0, то водород может находиться в данном положении, даже если не указан в определении переменной группы. Когда для одного или более положений в группе указано что "нет замещений” или являются “незамещенными”, то присоединяются атомы водорода, чтобы занять любую свободную валентность.
Если не указано иное, “кольцо” или “кольцевая система” как компонент формулы 1 (например, заместитель Q) является карбоциклическим или гетероциклическим. Термин “кольцевая система” означает два или несколько слитых колец. Термин “гетероциклическое кольцо” означает кольцо, в котором по меньшей мере один атом, формирующий скелет кольца, не является углеродом, а является, например, азотом, кислородом или серой. Обычно гетероциклическое кольцо содержит не более 4 атомов азота, не более 2 атомов кислорода и не более 2 атомов серы. Если не указано иное, гетероциклическое кольцо может быть насыщенным, частично ненасыщенным или полностью ненасыщенным кольцом. Термин “гетероциклическая кольцевая система” означает кольцевую систему, в которой по меньшей мере одно кольцо кольцевой системы является гетероциклическим кольцом. Если не указано иное, гетероциклические кольца и кольцевые системы могут быть присоединены через любой доступный углерод или азот заменой водорода на указанном углероде или азоте.
“Ароматический” указывает, что каждый из атомов кольца, по существу, находится в одной и той же плоскости и имеет p-орбиталь, перпендикулярную плоскости кольца, и в которой (4n+2) π электроны, где n является положительным целым числом, связаны с кольцом согласно правилу Хюккеля. Когда полностью ненасыщенное гетероциклическое кольцо отвечает правилу Хюккеля, тогда указанное кольцо также называют “гетероароматическим кольцом”. Термин “гетероароматическая кольцевая система” означает гетероциклическую кольцевую систему, в которой по меньшей мере одно кольцо кольцевой системы является ароматическим.
Как используется в данном описании, будут применяться следующие обозначения, если не указано иное. Термин “необязательно замещенный” используется взаимозаменяемо с термином “замещенный или незамещенный” или с термином “(не)замещенный”. Термин “необязательно замещенный 1-4 заместителями” означает, что заместители отсутствуют (т.е. незамещенный) или, что присутствуют 1, 2, 3 или 4 заместителя (ограничено числом доступных положений соединения). Если не указано иное, необязательно замещенная группа может иметь заместитель в каждом замещаемом положении группы, и каждое замещение не зависит от другого.
Когда заместителем является 5- или 6-членное, содержащее азот гетероароматическое кольцо, оно может быть присоединено к остатку формулы 1 через любой доступный кольцевой атом углерода или азота, если не описано иное.
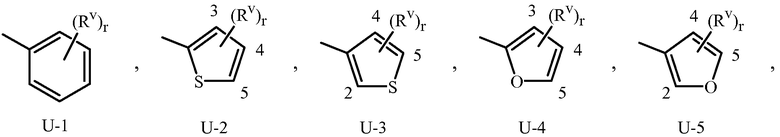
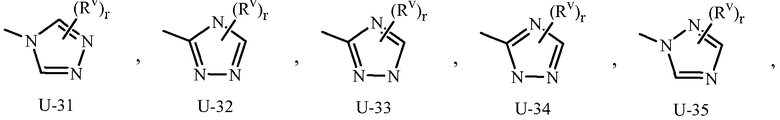
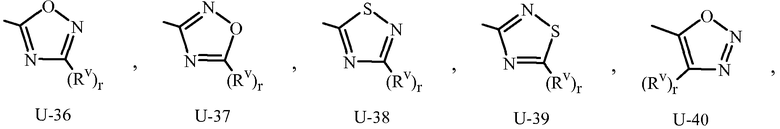
Примером фенила, необязательно замещенного одним-пятью заместителями, является кольцо, проиллюстрированное как U-1 в приложении 1, где Rv является таким, как определено в описании сущности настоящего изобретения для R1, R2, R3 или Q, и r является целым числом от 0 до 5.
Примеры необязательно замещенного 5- или 6-членного гетероароматического кольца включают кольца U-2-U-61, проиллюстрированные в приложении 1, где Rv является любым заместителем, как определено в описании сущности настоящего изобретения для R1, R2, R3 или Q, и r является целым числом от 0 до 4, ограниченным количеством доступных положений в каждой U группе. Поскольку U-29, U-30, U-36, U-37, U-38, U-39, U-40, U-41, U-42 и U-43 имеют только одно доступное положение для таких U групп, r ограничено целым числом 0 или 1, и r, являясь 0, означает, что U группа является незамещенной, и в положении, отмеченном (Rv)r, присутствует водород.
Приложение 1








 и
и 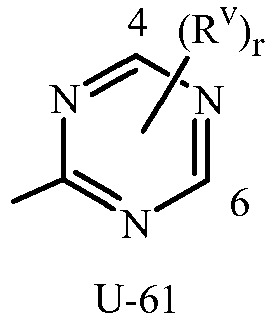 .
.
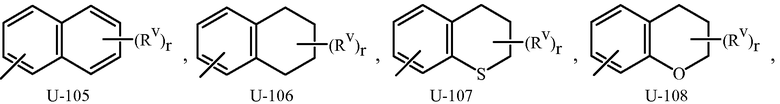
Как отмечено выше, Q может быть (среди прочих) 8-10-членной гетероароматической бициклической кольцевой системой, необязательно замещенной заместителями, выбранными из группы заместителей, как определено в описании сущности изобретения. Примеры необязательно замещенных 8-, 9- или 10-членных гетероароматических бициклических кольцевых систем включают кольца U-81-U-123, проиллюстрированные в приложении 3, где Rv является любым заместителем, как определено в описании сущности настоящего изобретения для Q, и r обычно является целым числом от 0 до 4.
Приложение 3









 и
и  .
.
Хотя Rv группы показаны в структурах U-1-U-123, следует отметить, что они не являются необходимыми для присутствия, поскольку они являются необязательными заместителями. Атомы азота, которые требуют замещения для заполнения их валентности, замещены H или Rv. Следует отметить, что когда точка присоединения между (Rv)r и U группой показана как плавающая, (Rv)r может быть присоединена к любому доступному атому углерода или атому азота U группы. Следует отметить, что когда точка присоединения в U группе показана как плавающая, U группа может быть присоединена к остатку формулы 1 через любой доступный углерод или азот U группы заменой атома водорода. Следует отметить, что некоторые U группы могут быть замещены только менее чем 4 группами Rv (например, U-2-U-5, U-7-U-48 и U-52-U-61).
Широкий ряд способов синтеза известны в данной области делает возможным получение ароматических и неароматических гетероциклических колец и кольцевых систем; для расширенных обзоров см. восьмой том Comprehensive Heterocyclic Chemistry, главные редакторы A.R. Katritzky and C.W. Rees, Pergamon Press, Oxford, 1984 и двенадцатый том Comprehensive Heterocyclic Chemistry II, главные редакторы A.R. Katritzky, C.W. Rees and E. F. V. Scriven, Pergamon Press, Oxford, 1996.
Соединения настоящего изобретения могут существовать в виде одного или более стереоизомеров. Различные стереоизомеры включают энантиомеры, диастереомеры, атропизомеры и геометрические изомеры. Специалисту в данной области будет понятно, что один стереоизомер может быть более активным и/или может проявлять положительные эффекты, когда обогащен относительно другого стереоизомера(ов) или когда отделен от другого стереоизомера(ов). Дополнительно, специалисту в данной области известно, как отделить, обогатить и/или селективно получить указанные стереоизомеры. Соединения настоящего изобретения могут присутствовать в виде смеси стереоизомеров, отдельных стереоизомеров или в виде оптически активной формы.
Соединения, выбранные из формулы 1, (включая все стереоизомеры, его N-оксиды и соли), обычно существуют в более чем одной форме, и формула 1, таким образом, включает все кристаллические и не кристаллические формы соединений, которые представлены формулой 1. Некристаллические формы включают варианты осуществления, которые являются твердыми веществами, такими как воски и смолы, а также варианты осуществления, которые являются жидкостями, такими как растворы и расплавы. Кристаллические формы включают варианты осуществления, которые в основном представляют собой монокристаллический тип, и варианты осуществления, которые представляют собой смесь полиморфов (т.е. различные кристаллические типы). Термин “полиморф” относится к конкретной кристаллической форме химического соединения, которое может кристаллизоваться в различные кристаллические формы, причем такие формы имеют различные упаковки и/или конформации молекул в кристаллической решетке. Хотя полиморфы могут иметь один и тот же химический состав, они также могут отличаться по составу из-за присутствия или отсутствия совместно кристаллизованной воды или других молекул, которые могут быть слабо или сильно связаны в решетке. Полиморфы могут отличаться по таким химическим, физическим и биологическим свойствам как форма кристалла, плотность, твердость, цвет, химическая стабильность, точка плавления, гигроскопичность, способность суспендироваться, скорость растворения и биодоступность. Специалисту в данной области будет понятно, что полиморф соединения, представленного формулой 1, может проявлять благоприятные эффекты (например, возможность использования при получении требуемых составов, улучшенная биологическая характеристика) по сравнению с другим полиморфом или смесью полиморфов такого же соединения, представленного формулой 1. Получение и выделение определенного полиморфа соединения, представленного формулой 1, может быть достигнуто способами, известными специалистам в данной области техники, включая, например, кристаллизацию с использованием выбранных растворителей и температур.
Специалисту в данной области будет понятно, что не все содержащие азот гетероциклы могут образовывать N-оксиды, поскольку азот требует доступную неподеленную пару для окисления до оксида; специалисту в данной области известны такие содержащие азот гетероциклы, которые могут образовывать N-оксиды. Специалисту в данной области также очевидно, что третичные амины могут образовывать N-оксиды. Способы синтеза для получения N-оксидов гетероциклов и третичных аминов очень хорошо известны специалисту в данной области, включая окисление гетероциклов и третичных аминов перкислотами, такими как перуксусная и 3-хлорпербензойная кислота (MCPBA), пероксид водорода, алкилгидропероксиды, такие как трет-бутилгидропероксид, перборат натрия и диоксираны, такие как диметилдиоксиран. Такие способы получения N-оксидов подробно описаны и рассмотрены в литературе, см., например: T.L. Gilchrist в Comprehensive Organic Synthesis, том 7, стр. 748-750, S.V. Ley, Изд., Pergamon Press; M. Tisler и B. Stanovnik в Comprehensive Heterocyclic Chemistry, том 3, стр. 18-20, A.J. Boulton and A. McKillop, Изд., Pergamon Press; M.R. Grimmett and B.R.T. Keene в Advances in Heterocyclic Chemistry, том 43, стр. 149-161, A.R. Katritzky, Изд., Academic Press; M. Tisler and B. Stanovnik в Advances in Heterocyclic Chemistry, том 9, стр. 285-291, A.R. Katritzky and A.J. Boulton, Изд., Academic Press; и G.W.H. Cheeseman and E.S.G. Werstiuk в Advances in Heterocyclic Chemistry, том 22, стр. 390-392, A.R. Katritzky and A.J. Boulton, Изд., Academic Press.
Специалисту в данной области будет очевидно, что, поскольку в окружающей среде и в физиологических условиях соли химических соединений находятся в равновесии с их соответствующими несолевыми формами, соли разделяют биологическую полезность несолевых форм. Таким образом, широкий ряд солей соединений формулы 1 могут быть использованы для борьбы с паразитическими нематодами. Соли соединений формулы 1 включают кислотно-аддитивные соли с неорганическими или органическими кислотами, такими как бромистоводородная, хлористоводородная, азотная, фосфорная, серная, уксусная, масляная, фумаровая, молочная, малеиновая, малоновая, щавелевая, пропионовая, салициловая, виннокаменная, 4-толуолсульфоновая или валериановая кислоты. Когда соединение формулы 1 содержит кислотную часть, такую как карбоновая кислота, фенол или сульфониламид (т.е. когда R3 представляет собой H), соли также включают соли, образованные с органическими или неорганическими основаниями, такими как пиридин, триэтиламин или аммиак, или амиды, гидриды, гидроксиды или карбонаты натрия, калия, лития, кальция, магния или бария. Соответственно, настоящее изобретение включает соединения, выбранные из формулы 1, их N-оксиды и соли.
Варианты осуществления настоящего изобретения, как описано при описании существа настоящего изобретения, включают описанное ниже. В следующих вариантах осуществления соединение формулы 1 включает его стереоизомеры, N-оксиды и соли, и ссылка на “соединение формулы 1” включает определения заместителей, определенных при описании существа настоящего изобретения, если они дополнительно не определены в вариантах осуществления.
Вариант осуществления 1. Соединение формулы 1, где Z представляет собой O.
Вариант осуществления 2. Соединение формулы 1, где Z представляет собой S.
Вариант осуществления 3. Соединение формулы 1 или вариант осуществления 1 или 2, где каждый R1 независимо представляет собой галоген, циано, нитро, OR4, C1-C6алкил или C1-C6галогеналкил.
Вариант осуществления 3a. Соединение согласно варианту осуществления 3, где каждый R1 независимо представляет собой галоген, C1-C6галогеналкил или C1-C6галогеналкокси (т.е. OR4, и R4 представляет собой C1-C6галогеналкил).
Вариант осуществления 3b. Соединение согласно варианту осуществления 3a, где n равно 2, и один R1 находится в положении 3 формулы 1, а второй R1 находится в положении 5 формулы 1.
Вариант осуществления 3c. Соединение согласно варианту осуществления 3a или 3b, где каждый R1 независимо представляет собой галоген или C1-C2галогеналкил.
Вариант осуществления 3d. Соединение согласно варианту осуществления 3c, где каждый R1 независимо представляет собой F, Cl, Br или CF3.
Вариант осуществления 3e. Соединение согласно варианту осуществления 3c, где n равно 2, и каждый R1 независимо представляет собой F, Cl, Br или CF3.
Вариант осуществления 3f. Соединение формулы 1, где n равно 1, и R1 представляет собой CF3 и находится в положении 3 формулы 1.
Вариант осуществления 3g. Соединение формулы 1, где n равно 2, и один R1 представляет собой CF3 и находится в положении 3 формулы 1, а второй R1 представляет собой Cl и находится в положении 5 формулы 1.
Вариант осуществления 3h. Соединение формулы 1, где n равно 2, и один R1 представляет собой CF3 и находится в положении 3 формулы 1, а второй R1 представляет собой Br и находится в положении 5 формулы 1.
Вариант осуществления 3i. Соединение формулы 1, где n равно 2, и один R1 представляет собой CF3 и находится в положении 3 формулы 1, а второй R1 представляет собой F и находится в положении 5 формулы 1.
Вариант осуществления 4. Соединение формулы 1 или согласно любому из вариантов осуществления 1-3i, где Q представляет собой фенил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4a. Соединение согласно варианту осуществления 4, где Q представляет собой фенил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил, C1-C3галогеналкил и C(O)R7b;
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил; и
каждый R7b независимо представляет собой C1-C3алкил.
Вариант осуществления 4b. Соединение согласно варианту осуществления 4, где Q представляет собой фенил, пиридинил, пиразолил, оксазолил, тиазолил, изоксазолил, изотиазолил, фуранил или тиенил, каждый необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4c. Соединение согласно варианту осуществления 4b, где Q представляет собой фенил, пиридинил, пиразолил, оксазолил, тиазолил, изоксазолил, изотиазолил, фуранил или тиенил, каждый необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил и C1-C3галогеналкил; и
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил.
Вариант осуществления 4d. Соединение согласно варианту осуществления 4b, где Q представляет собой фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4e. Соединение согласно варианту осуществления 4d, где Q представляет собой фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил, C1-C3галогеналкил и C(O)R7b;
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил; и
каждый R7b независимо представляет собой C1-C3алкил.
Вариант осуществления 4f. Соединение согласно варианту осуществления 4b, где Q представляет собой пиридинил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4g. Соединение согласно варианту осуществления 4f, где Q представляет собой пиридинил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил и C1-C3галогеналкил; и
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил.
Вариант осуществления 4h. Соединение согласно варианту осуществления 4b, где Q представляет собой пиразолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4i. Соединение согласно варианту осуществления 4h, где Q представляет собой пиразолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил и C1-C3галогеналкил; и
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил.
Вариант осуществления 4j. Соединение согласно варианту осуществления 4b, где Q представляет собой оксазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4k. Соединение согласно варианту осуществления 4j, где Q представляет собой оксазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил и C1-C3галогеналкил; и
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил.
Вариант осуществления 4l. Соединение согласно варианту осуществления 4b, где Q представляет собой тиазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4m. Соединение согласно варианту осуществления 4l, где Q представляет собой тиазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил и C1-C3галогеналкил; и
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил.
Вариант осуществления 4n. Соединение согласно варианту осуществления 4b, где Q представляет собой изоксазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4o. Соединение согласно варианту осуществления 4n, где Q представляет собой изоксазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил и C1-C3галогеналкил; и
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил.
Вариант осуществления 4p. Соединение согласно варианту осуществления 4b, где Q представляет собой изотиазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4q. Соединение согласно варианту осуществления 4p, где Q представляет собой изотиазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил и C1-C3галогеналкил; и
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил.
Вариант осуществления 4r. Соединение согласно варианту осуществления 4b, где Q представляет собой фуранил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4s. Соединение согласно варианту осуществления 4r, где Q представляет собой фуранил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил и C1-C3галогеналкил; и
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил.
Вариант осуществления 4t. Соединение согласно варианту осуществления 4b, где Q представляет собой тиенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 4u. Соединение согласно варианту осуществления 4t, где Q представляет собой тиенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4a, C1-C3алкил и C1-C3галогеналкил; и
каждый R4a независимо представляет собой C1-C3алкил или C1-C3галогеналкил.
Вариант осуществления 4v. Соединение согласно варианту осуществления 4b, где Q представляет собой фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4, NR5R6, C1-C4алкил, C1-C4галогеналкил, C(X)R7 и C(O)OR8.
Вариант осуществления 4w. Соединение согласно варианту осуществления 4b, где Q представляет собой пиридинил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4, NR5R6, C1-C4алкил, C1-C4галогеналкил, C(X)R7 и C(O)OR8.
Вариант осуществления 4x. Соединение согласно варианту осуществления 4b, где Q представляет собой фуранил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4, NR5R6, C1-C4алкил, C1-C4галогеналкил, C(X)R7 и C(O)OR8.
Вариант осуществления 5. Соединение формулы 1 или согласно любому из вариантов осуществления 1-4x, где R2 представляет собой H, галоген или C1-C6алкил.
Вариант осуществления 5a. Соединение согласно варианту осуществления 5, где R2 представляет собой H, F, Cl, Br или C1-C2алкил.
Вариант осуществления 5b. Соединение согласно варианту осуществления 5a, где R2 представляет собой H, Cl, Br или CH3.
Вариант осуществления 5c. Соединение согласно варианту осуществления 5a, где R2 представляет собой H.
Вариант осуществления 6. Соединение формулы 1 или согласно любому из вариантов осуществления 1-5c, где R3 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C(X)R7, C(O)OR8 или S(O)mR9; или C1-C6алкил, замещенный 1 или 2 OR4.
Вариант осуществления 6a. Соединение согласно варианту осуществления 6, где R3 представляет собой H или C1-C6алкил.
Вариант осуществления 6b. Соединение согласно варианту осуществления 6a, где R3 представляет собой H.
Вариант осуществления 7. Соединение формулы 1 или согласно любому из вариантов осуществления 1-6b, где R4 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C1-C6алкил, C2-C6алкенил или C2-C6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4a, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12.
Вариант осуществления 8. Соединение формулы 1 или согласно любому из вариантов осуществления 1-7, где R5 представляет собой H, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a.
Вариант осуществления 9. Соединение формулы 1 или согласно любому из вариантов осуществления 1-8, где R6 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил или C2-C6алкинил; или C3-C7циклоалкил или C4-C8циклоалкилалкил, каждый необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, C1-C4алкил, C1-C4галогеналкил и OR4a;
Вариант осуществления 10. Соединение формулы 1 или согласно любому из вариантов осуществления 1-9, где R7 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a.
Вариант осуществления 11. Соединение формулы 1 или согласно любому из вариантов осуществления 1-10, где R8 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил, C6-C14циклоалкилциклоалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4a, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12.
Вариант осуществления 12. Соединение формулы 1 или согласно любому из вариантов осуществления 1-11, где R9 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4a, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12.
Вариант осуществления 13. Соединение формулы 1 или согласно любому из вариантов осуществления 1-12, где R10 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил или C2-C6алкинил.
Вариант осуществления 14. Соединение формулы 1 или согласно любому из вариантов осуществления 1-13, где R14 представляет собой C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12.
Варианты осуществления настоящего изобретения, включая варианты осуществления 1-14 выше, а также любые другие варианты осуществления, описанные в данном описании, могут быть комбинированы любым способом, и описания переменных в вариантах осуществления относятся не только к соединениям формулы 1, но также к исходным соединениям и промежуточным соединениям, используемым для получения соединения формулы 1. Кроме того, варианты осуществления настоящего изобретения, включая варианты осуществления 1-14 выше, а также любые другие варианты осуществления, описанные в данном описании, и любая их комбинация, относятся к композициям и способам настоящего изобретения.
Проиллюстрированы комбинации вариантов осуществления 1-14:
Вариант осуществления A. Соединение формулы 1, где
Z представляет собой O; и
Q представляет собой фенил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления B. Соединение согласно варианту осуществления A, где
Q представляет собой фенил, пиридинил, пиразолил, оксазолил, тиазолил, изоксазолил, изотиазолил, фуранил или тиенил, каждый необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления C. Соединение согласно варианту осуществления B, где
каждый R1 независимо представляет собой галоген, циано, нитро, OR4, C1-C6алкил или C1-C6галогеналкил;
R2 представляет собой H, галоген или C1-C6алкил;
R3 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C(X)R7, C(O)OR8 или S(O)mR9; или C1-C6алкил, замещенный 1 или 2 OR4; и
n равно 1 или 2.
Специфические варианты осуществления включают соединения формулы 1, выбранные из группы, включающей:
Дополнительные варианты осуществления настоящего изобретения, как описано при описании существа настоящего изобретения, включают описанные ниже. В следующих вариантах осуществления, соединение формулы 1p включает его стереоизомеры, N-оксиды и соли, и ссылка на “соединение формулы 1p” включает определения заместителей, определенных при описании существа настоящего изобретения, если дополнительно не определено в вариантах осуществления.
Вариант осуществления 15. Соединение формулы 1p
 ,
,
где
Z представляет собой O или S;
каждый R1 независимо представляет собой галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a или N(R10)C(O)R7a; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный галогеном, циано, нитро, OR4, NR5R6, C1-C6алкилом, C1-C6галогеналкилом, C2-C6алкенилом, C2-C6галогеналкенилом, C2-C6алкинилом, C2-C6галогеналкинилом, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
R2 представляет собой H, галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12;
R3 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
Q представляет собой фенил, нафталинил, 5- или 6-членное гетероароматическое кольцо или 8-10-членную гетероароматическую бициклическую кольцевую систему, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a, N(R10)C(O)R7a и R14;
каждый X независимо представляет собой O или S;
каждый R4 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4a, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R4a независимо представляет собой H, C1-C6алкил или C1-C6галогеналкил;
каждый R5 независимо представляет собой H, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R5a независимо представляет собой H или C1-C6алкил;
каждый R6 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a;
каждый R6a независимо представляет собой H, C1-C6алкил, C(O)R13 или C(O)OR13;
каждый R7 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R7a независимо представляет собой C1-C6алкил или C1-C6галогеналкил;
каждый R8 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R8a независимо представляет собой C1-C6алкил или C1-C6галогеналкил;
каждый R9 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R9a независимо представляет собой C1-C6алкил или C1-C6галогеналкил;
каждый R10 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12;
каждый R10a независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил;
каждый R11 независимо представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a)mR9a; или C1-C6алкил, замещенный галогеном, циано, нитро, OR4a, NR5aR6a, C1-C6алкилом, C1-C6галогеналкилом, C2-C6алкенилом, C2-C6галогеналкенилом, C2-C6алкинилом, C2-C6галогеналкинилом, C(X)R7a, C(O)OR8a, C(O)NR11aR12, S(O)mR9a или S(O)2NR11aR12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C(X)R7a, C(O)OR8a, C(O)NR11aR12, OR4a, C2-C6алкоксиалкил, S(O)mR9a, S(O)2NR11aR12, NR5aR6a, OC(O)R7a и N(R10a)C(O)R7a;
каждый R11a независимо представляет собой H, C1-C6алкил, C2-C6алкенил или C2-C6алкинил;
каждый R12 независимо представляет собой H, C1-C6алкил, C2-C6алкенил или C2-C6алкинил;
каждый R13 независимо представляет собой H или C1-C4алкил;
каждый R14 независимо представляет собой C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
каждый m независимо равен 0, 1 или 2; и
n равно 0, 1, 2, 3 или 4.
Вариант осуществления 16. Соединение формулы 1p, где Z представляет собой O.
Вариант осуществления 17. Соединение формулы 1p, где Z представляет собой S.
Вариант осуществления 18. Соединение формулы 1p или вариант осуществления 1 или 2, где каждый R1 независимо представляет собой галоген, циано, нитро, OR4, C1-C6алкил или C1-C6галогеналкил.
Вариант осуществления 18a. Соединение согласно варианту осуществления 18, где каждый R1 независимо представляет собой галоген, C1-C6галогеналкил или C1-C6галогеналкокси (т.е. OR4, и R4 представляет собой C1-C6галогеналкил).
Вариант осуществления 18b. Соединение согласно варианту осуществления 18a, где n равно 2, и один R1 находится в положении 3, и второй R1 находится в положении 5.
Вариант осуществления 18c. Соединение согласно варианту осуществления 18a или 18b, где каждый R1 независимо представляет собой галоген или C1-C2галогеналкил.
Вариант осуществления 18d. Соединение согласно варианту осуществления 18c, где каждый R1 независимо представляет собой Cl, Br или CF3.
Вариант осуществления 18e. Соединение согласно варианту осуществления 18c, где n равно 2, и каждый R1 независимо представляет собой Cl, Br или CF3.
Вариант осуществления 18f. Соединение формулы 1p, где n равно 1, и R1 представляет собой CF3 и находится в положении 3.
Вариант осуществления 18g. Соединение формулы 1p, где n равно 2, и один R1 представляет собой CF3 и находится в положении 3, и второй R1 представляет собой Cl и находится в положении 5.
Вариант осуществления 18h. Соединение формулы 1p, где n равно 2, и один R1 представляет собой CF3 и находится в положении 3, и второй R1 представляет собой Br и находится в положении 5.
Вариант осуществления 19. Соединение формулы 1p или согласно любому из вариантов осуществления 15-18h, где Q представляет собой фенил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19a. Соединение согласно варианту осуществления 19, где Q представляет собой фенил, пиридинил, пиразолил, оксазолил, тиазолил, изоксазолил, изотиазолил или тиенил, каждый необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19b. Соединение согласно варианту осуществления 19a, где Q представляет собой фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19c. Соединение согласно варианту осуществления 19a, где Q представляет собой пиридинил необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19d. Соединение согласно варианту осуществления 19a, где Q представляет собой пиразолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19e. Соединение согласно варианту осуществления 19a, где Q представляет собой оксазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19f. Соединение согласно варианту осуществления 19a, где Q представляет собой тиазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19g. Соединение согласно варианту осуществления 19a, где Q представляет собой изоксазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19h. Соединение согласно варианту осуществления 19a, где Q представляет собой изотиазолил, необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19i. Соединение согласно варианту осуществления 19a, где Q представляет собой тиенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления 19j. Соединение согласно варианту осуществления 19b, где Q представляет собой фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4, C1-C4алкил, C1-C4галогеналкил, C(X)R7 и C(O)OR8.
Вариант осуществления 19k. Соединение согласно варианту осуществления 19c, где Q представляет собой пиридинил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, OR4, C1-C4алкил, C1-C4галогеналкил, C(X)R7 и C(O)OR8.
Вариант осуществления 20. Соединение формулы 1p или согласно любому из вариантов осуществления 15-19k, где R2 представляет собой H, галоген или C1-C6алкил.
Вариант осуществления 20a. Соединение согласно варианту осуществления 20, где R2 представляет собой H, F, Cl, Br или C1-C2алкил.
Вариант осуществления 20b. Соединение согласно варианту осуществления 20a, где R2 представляет собой H, Cl, Br или CH3.
Вариант осуществления 21. Соединение формулы 1p или согласно любому из вариантов осуществления 15-20b, где R3 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C(X)R7, C(O)OR8 или S(O)mR9; или C1-C6алкил, замещенный 1 или 2 OR4.
Вариант осуществления 21a. Соединение согласно варианту осуществления 21, где R3 представляет собой H или C1-C6алкил.
Вариант осуществления 21b. Соединение согласно варианту осуществления 21a, где R3 представляет собой H.
Вариант осуществления 22. Соединение формулы 1p или согласно любому из вариантов осуществления 15-21b, где R4 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4a, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12.
Вариант осуществления 23. Соединение формулы 1p или согласно любому из вариантов осуществления 15-22, где R5 представляет собой H, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a.
Вариант осуществления 24. Соединение формулы 1p или согласно любому из вариантов осуществления 15-23, где R6 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил или C2-C6алкинил; или C3-C7циклоалкил или C4-C8циклоалкилалкил, каждый необязательно замещенный 1 или 2 заместителями, независимо выбранными из группы, включающей галоген, циано, C1-C4алкил, C1-C4галогеналкил и OR4a.
Вариант осуществления 25. Соединение формулы 1p или согласно любому из вариантов осуществления 15-24, где R7 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a.
Вариант осуществления 26. Соединение формулы 1p или согласно любому из вариантов осуществления 15-25, где R8 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4a, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12.
Вариант осуществления 27. Соединение формулы 1p или согласно любому из вариантов осуществления 15-26, где R9 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил или C2-C6галогеналкинил; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4a, NR5aR6a, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12.
Вариант осуществления 28. Соединение формулы 1p или согласно любому из вариантов осуществления 15-27, где R10 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил или C2-C6алкинил.
Вариант осуществления 29. Соединение формулы 1p или согласно любому из вариантов осуществления 15-28, где R14 представляет собой C3-C7циклоалкил, C4-C8циклоалкилалкил или C5-C7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, C1-C4алкил, C1-C4галогеналкил, OR4a и S(O)mR9a; или C1-C6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C6алкил, C1-C6галогеналкил, C2-C6алкенил, C2-C6галогеналкенил, C2-C6алкинил, C2-C6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12.
Варианты осуществления настоящего изобретения, включая вышеизложенные варианты осуществления 15-29, а также любые другие варианты осуществления, описанные в данном описании, могут быть комбинированы любым способом, и описания переменных в вариантах осуществления относятся не только к соединениям формулы 1p, но также исходным соединениям и промежуточным соединениям, используемым для получения соединений формулы 1p. Кроме того, варианты осуществления настоящего изобретения, включая приведенные выше варианты осуществления 15-29, а также любые другие варианты осуществления, описанные в данном описании, и любая их комбинация, относятся к композициям и способам настоящего изобретения.
Проиллюстрированы комбинации вариантов осуществления 15-29:
Вариант осуществления A1. Соединение формулы 1p, где
Z представляет собой O; и
Q представляет собой фенил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления B1. Соединение согласно варианту осуществления A1, где
Q представляет собой фенил, пиридинил, пиразолил, оксазолил, тиазолил, изоксазолил, изотиазолил или тиенил, каждый необязательно замещенный 1-3 заместителями, независимо выбранными из группы, включающей галоген, циано, нитро, OR4, NR5R6, C1-C4алкил, C2-C4алкенил, C2-C4алкинил, C1-C4галогеналкил, C2-C4галогеналкенил, C2-C6алкоксиалкил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
Вариант осуществления C1. Соединение согласно варианту осуществления B1, где
каждый R1 независимо представляет собой H, галоген, циано, нитро, OR4, C1-C6алкил или C1-C6галогеналкил;
R2 представляет собой H, галоген или C1-C6алкил;
R3 представляет собой H, C1-C6алкил, C1-C6галогеналкил, C(X)R7, C(O)OR8 или S(O)mR9; или C1-C6алкил, замещенный 1 или 2 OR4; и
n равно 1 или 2.
Следует отметить, что соединения настоящего изобретения характеризуются благоприятными метаболическими и/или почвенными остаточными особенностями и проявляют активность в борьбе со спектром агрономических и неагрономических паразитических нематод.
Особенно следует отметить, что ввиду борьбы со спектром паразитических нематод и экономической важности, защита агрономических сельскохозяйственных культур от порчи или повреждения, вызванных паразитическими нематодами, посредством контроля паразитических нематод является вариантами осуществления настоящего изобретения. Соединения настоящего изобретения благодаря своим благоприятным свойствам транслокации или систематичности в растениях также защищают лиственную или другие части растения, которые прямо не находятся в непосредственном контакте с соединением формулы 1 или композицией, содержащей данное соединение.
Также представляющими интерес в качестве вариантов осуществления настоящего изобретения являются композиции, содержащие соединение по любому из предшествующих вариантов осуществления, а также любые другие варианты осуществления, описанные в данном описании, и любые их комбинации, и по меньшей мере один дополнительный компонент, выбранный из группы, включающей поверхностно-активное вещество, твердый разбавитель и жидкий разбавитель, причем указанные композиции необязательно дополнительно содержат по меньшей мере одно дополнительное биологически активное соединение или средство.
Кроме того, примечательными в качестве вариантов осуществления настоящего изобретения являются композиции для борьбы с паразитической нематодой, содержащие соединение по любому из предшествующих вариантов осуществления, а также любые другие варианты осуществления, описанные в данном описании, и любые их комбинации, и по меньшей мере один дополнительный компонент, выбранный из группы, включающей поверхностно-активное вещество, твердый разбавитель и жидкий разбавитель, причем указанные композиции необязательно дополнительно содержат по меньшей мере одно дополнительное биологически активное соединение или средство. Варианты осуществления настоящего изобретения, кроме того, включают способы борьбы с паразитической нематодой, включающие контакт паразитической нематоды или окружающей ее среды с биологически эффективным количеством соединения по любому из предшествующих вариантов осуществления (например, таким как композиция, описанная в данном описании).
Варианты осуществления настоящего изобретения также включают композицию, содержащую соединение по любому из предшествующих вариантов осуществления, в форме жидкого состава для пропитки почвы. Варианты осуществления настоящего изобретения, кроме того, включают способы борьбы с паразитической нематодой, включающие контакт почвы с жидкой композицией, такой как пропитка почвы, содержащей биологически эффективное количество соединения по любому из предшествующих вариантов осуществления.
Варианты осуществления настоящего изобретения также включают композицию в виде спрея для борьбы с паразитической нематодой, содержащую биологически эффективное количество соединения по любому из предшествующих вариантов осуществления и пропеллент. Варианты осуществления настоящего изобретения, кроме того, включают композицию-приманку для борьбы с паразитической нематодой, содержащую биологически эффективное количество соединения по любому из предшествующих вариантов осуществления, один или более пищевых материалов, необязательно аттрактант и необязательно увлажнитель.
Варианты осуществления настоящего изобретения также включают способы защиты семян от паразитической нематоды, включающие контакт семян с биологически эффективным количеством соединения по любому из предшествующих вариантов осуществления.
Варианты осуществления настоящего изобретения также включают способы борьбы с паразитической нематодой, включающие контакт паразитической нематоды или ее окружающей среды с биологически эффективным количеством соединения формулы 1, его N-оксидом или солью (например, таким как композиция, описанная в данном описании), при условии, что способы не являются способами медицинского лечения организма человека или животного терапией.
Настоящее изобретение также относится к таким способам, где паразитическую нематоду или ее окружающую среду приводят в контакт с композицией, содержащей биологически эффективное количество соединения формулы 1, его N-оксида или соли и по меньшей мере один дополнительный компонент, выбранный из группы, включающей поверхностно-активные вещества, твердые разбавители и жидкие разбавители, причем указанная композиция необязательно дополнительно содержит биологически эффективное количество по меньшей мере одного дополнительного биологически активного соединения или средства, при условии, что способы не являются способами медицинского лечения организма человека или животного терапией.
Один или несколько из следующих способов и вариаций, как описано на схемах 1-8, могут быть использованы для получения соединений формулы 1. Определения X, Q, R1, R2 и R3 в соединениях формул 1a-1c и 2-10 ниже являются такими, как определено выше при описании существа настоящего изобретения, если не указано иное. Формулы 1a-1c представляют собой различные подвиды формулы 1, и все заместители для Формул 1a-1c являются такими, как определено выше для формулы 1, если не указано иное. Комнатная температура составляет приблизительно от 20 до 25°C.
Соединения формулы 1a (т.е. формулы 1, где Z представляет собой кислород, и R3 представляет собой H) можно получить взаимодействием карбоновых кислот формулы 2 с арильными или гетероарильными сульфонамидами формулы 3, как показано на схеме 1. Обычно, реагент сочетания амидов и катализатор, такой как N,N-диметиламинопиридин (DMAP), используют в способе схемы 1. Реагенты сочетания амидов включают гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимид (EDC), N,N'-бициклогексилкарбодиимид (DCC) и 1,1'-карбонилдиимидазол (CDI). Реакцию можно проводить при температуре в диапазоне от комнатной температуры до температуры кипения растворителя с обратным холодильником. Конкретные растворители включают спирты, эфиры, сложные эфиры, амиды и галогенированные углеводороды. Для стадии D примера синтеза 1 отдельно описана система условий, использующая EDC/DMAP в смешанном растворителе из 1:1 трет-бутанола и дихлорметана.
Схема 1

Соединения формулы 1a также могут быть получены взаимодействием хлорангидридов карбоновой кислоты формулы 4 с арильными или гетероарильными сульфонамидами формулы 3, как показано на схеме 2. Реакция обычно включает использование основания, такого как триэтиламин или пиридин, и необязательно катализатора, такого как DMAP, в присутствии растворителя. Реакцию можно проводить при температурах в диапазоне от комнатной температуры до температуры кипения растворителя с обратным холодильником. Конкретные растворители включают эфиры, сложные эфиры и галогенированные углеводороды.
Схема 2
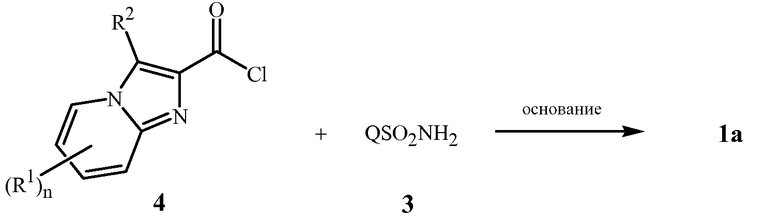
Соединения формулы 1b, где R3 представляет собой необязательно замещенный алкил, алкенил, алкинил или циклоалкил, могут быть получены взаимодействием соединений формулы 1a с соответственно замещенными алкил-, алкенил-, алкинил- или циклоалкилгалогенидами и основанием, как показано на схеме 3. Конкретные условия реакции включают карбонат калия в качестве основание и ДМФА в качестве растворителя.
Схема 3
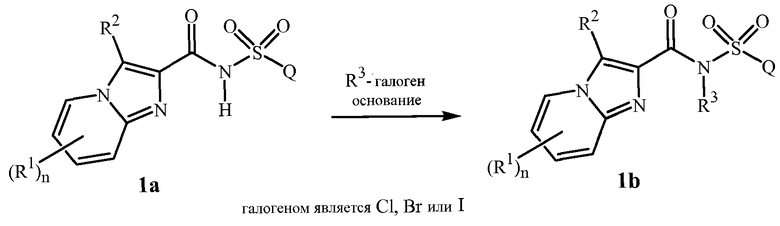
Соединения формулы 1b, где R3 представляет собой C(X)R7, C(O)OR8, C(O)NR11R12, S(O)2R9 или S(O)2NR11R12, могут быть получены взаимодействием соединений формулы 1a с ацил- или сульфонилгалогенидами (например, ClC(X)R7, ClC(O)OR8, ClC(O)NR11R12, ClS(O)2R9 или ClS(O)2NR11R12) способами ацилирования или сульфонилирования, хорошо известными в данной области.
Соединения формулы 1b, где R3 представляет собой необязательно замещенный алкил, алкенил, алкинил, циклоалкил или фенил, могут быть получены взаимодействием хлорангидридов формулы 4 с сульфонамидами формулы 9, как показано на схеме 4. Альтернативно, соединения формулы 1b, где R3 представляет собой необязательно замещенный алкил, алкенил, алкинил, циклоалкил или фенил, могут быть получены взаимодействием карбоновых кислот формулы 2 с сульфонамидами формулы 9 способом по схеме 1.
Схема 4

Тиоамиды формулы 1c (т.е. формулы 1, где X представляет собой серу) могут быть получены взаимодействием соединений формулы 1b (т.е. формула 1, где X представляет собой O) с тионирующими реагентами, такими как пентасульфид фосфора или реагент Лауссона, как показано на схеме 5.
Схема 5

Соединения формулы 2b (т.е. формулы 2, где R2 представляет собой бром) могут быть получены взаимодействием соединений формулы 2a (т.е. формула 2, где R2 представляет собой H) с бромом в уксусной кислоте в присутствии ацетата натрия, как описано в Heterocycles 2002, 57(1), 21-38.
Схема 6
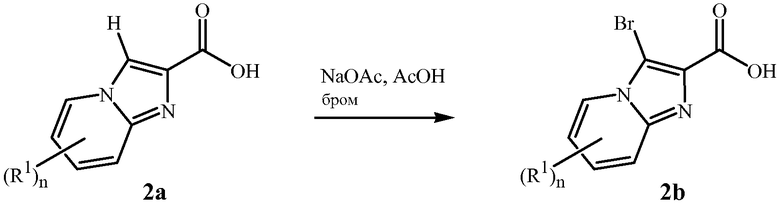
Соединения формулы 2, где R2 представляет собой циано, могут быть получены взаимодействием соединений формулы 2b с CuCN способами, известными в данной области. Соединения формулы 2, где R2 представляет собой нитро, могут быть получены взаимодействием соединений формулы 2a с азотной кислотой/серной кислотой, как описано в Bioorganic Med. Chem. Lett. 2005, 15(11), 2790-2794. Соединения формулы 2, где R2 представляет собой OR4, NR5R6 или SR9, можно получить из соединений формулы 2, где R2 представляет собой F, стандартными реакциями замещения, хорошо известными в данной области. Соединения формулы 2, где R2 представляет собой F, можно получить, как описано в Russian Chem. Bull. 2005, 54(2), 470-471.
Карбоновые кислоты формулы 2 и хлорангидриды формулы 4 можно получить путем взаимодействий, как показано на схеме 7. Взаимодействие подходящим образом замещенного 2-аминопиридина формулы 5 с 2-бромпируватом формулы 6, где R2 представляет собой H, необязательно замещенный алкил, алкенил, алкинил, C(O)R7, C(O)OR8 или C(O)NR11R12, или необязательно замещенный фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, при температурах в диапазоне от комнатной температуры до температуры кипения растворителя дает сложный эфир карбоновой кислоты формулы 7 вместе с подходящими количествами спирта формулы 8. Нагревание реакционной смеси до кипения в растворителе, таком как 1,2-диметоксиэтан, приводит к полному преобразованию спирта 8 в сложный эфир 7. Обработка смеси сложных эфиров 7 и 8 водным гидроксидным основанием, таким как гидроксид натрия, в смешивающемся с водой растворителе, таком как этанол, приводит в результате к гидролизу сложного эфира с образованием карбоновой кислоты формулы 2 после подкисления сильной кислотой, такой как хлористоводородная кислота. Данный способ описан подробно на стадии C примера синтеза 1. Карбоновую кислоту формулы 2 можно преобразовать в хлорангидрид формулы 4 хорошо известными способами преобразования, такими как обработка тионилхлоридом или оксалилхлоридом с каталитическим количеством N,N-диметилформамида (ДМФА) в умеренно полярных, апротонных растворителях, включающих дихлорметан, дихлорэтан, толуол и этилацетат. Промежуточные химические соединения формулы 6 можно получить разнообразными хорошо известными способами синтеза, включая бромирование необязательно замещенных пируватов или лактатов (альфа-гидрокси сложные эфиры). Конкретные условия реакции включают прямое бромирование бромом (см., например, JACS 1944, 66, 1656-1659) или CuBr2 в смеси этилацетат/хлороформ (см., например, JOC 2002, 67(4), 1102-1108), или взаимодействие лактата с N-бромсукцинимидом в CCl4 (см., например, JACS 1954, 76, 5796-5797).
Схема 7


Сульфонамиды формул 3 и 9 известны в химической литературе или коммерчески доступны. Как показано на схеме 8, сульфонамиды формулы 3 быстро получают из соответствующих сульфонилхлоридов формулы 10 взаимодействием с аммиаком, тогда как сульфонамиды формулы 9 быстро получают из соответствующих сульфонилхлоридов формулы 10 взаимодействием с R3NH2. Промежуточные соединения сульфонилхлорида коммерчески доступны или могут быть получены большим разнообразием способов, известных в литературе. Три из самых общепринятых способов получения сульфонилхлорида показаны на схеме 8, включая (a) прямое хлорсульфонилирование ароматических и гетероароматических систем хлорсульфоновой кислотой, (b) окисление сульфидов (например, гипохлоритом натрия) в присутствии хлористоводородной кислоты и (c) диазотирование и хлорсульфонилирование ароматических и гетероароматических аминов. Указанные три способа являются только иллюстративными; большое разнообразие других способов синтеза доступны для получения сульфонилхлоридов и сульфонамидов.
Схема 8

Примеры промежуточных соединений, используемых при получении соединений по настоящему изобретению, показаны в таблицах I-1-I-12. В таблицах используются следующие аббревиатуры: Me означает метил, Et означает этил, и-Pr означает изопропил, н-Pr означает нормальный пропил, OMe означает метокси и SMe означает тиометокси.







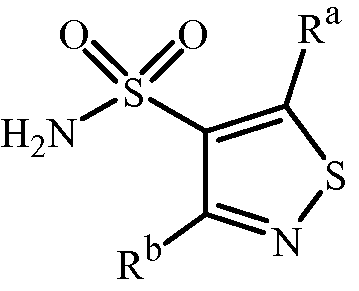


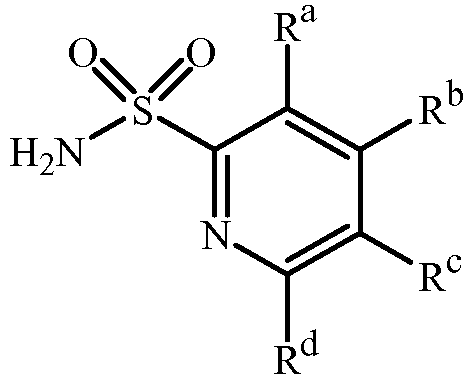



Следует понимать, что некоторые реагенты и реакционные условия, описанные выше для получения соединений формулы 1, могут быть несовместимыми с определенными функциональными группами, присутствующими в промежуточных соединениях. В таких случаях включение последовательностей защиты/снятия защиты или взаимопревращений функциональных групп в синтезе поможет в получении желаемых продуктов. Применение и выбор защитных групп будут очевидны для специалиста в химическом синтезе (см., например, Greene, T.W.; Wuts, P. G. M. Protective Groups in Organic Synthesis, 2-е изд.; Wiley: New York, 1991). Специалисту в данной области будет очевидно, что в некоторых случаях после введения данного реагента, как это показано на какой-либо отдельной схеме, может быть необходимо выполнить дополнительные стандартные стадии синтеза, не описанные подробно, для завершения синтеза соединений формулы 1. Специалисту в данной области также будет очевидно, что может быть необходимо выполнить комбинацию стадий, показанных на вышеприведенных схемах, в другом порядке, чем предполагается конкретной последовательностью, представленной для получения соединений формулы 1.
Специалисту в данной области также будет очевидно, что соединения формулы 1 и промежуточные соединения, описанные в данном описании, могут быть подвергнуты различным электрофильным, нуклеофильным, радикальным, металлорганическим, окислительным и восстановительным реакциям для добавления заместителей или модификации существующих заместителей.
Без дополнительного уточнения, считается, что специалист в данной области с использованием предыдущего описания, может применить данное изобретение в полной мере. Последующие примеры синтеза, следовательно, должны рассматриваться только как иллюстративные, а не ограничивающие изобретение каким-либо образом в любой форме. Стадии в следующих примерах синтеза иллюстрируют методику для каждой стадии в общей синтетической трансформации, и исходный материал для каждой стадии необязательно должен быть получен конкретным циклом получения, методика которого описана в других примерах или стадиях. Спектры 1H ЯМР представлены в миллионных долях слабого поля от тетраметилсилана; “с” означает синглет, “д” означает дуплет, “дд” означает дуплет дуплетов, “шир.с.” означает широкий синглет. Комнатная температура составляет приблизительно от 20 до 25°C.
Пример синтеза 1
Получение 8-хлор-N-[(2-хлор-5-метоксифенил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
Стадия A: Получение 2-хлор-5-метоксибензолсульфонилхлорида
В 3-горлую колбу, оборудованную конденсатором с сухим льдом, добавляли уксусную кислоту (80 мл) и хлорид меди (0,8 г). Смесь охлаждали до 0°C, конденсировали диоксид серы (5 мл) в реакционную колбу и затем реакционную смесь перемешивали 30 минут. В отдельную 200 мл круглодонную колбу добавляли концентрированную хлористоводородную кислоту (32 мл), уксусную кислоту (8 мл) и гидрохлорид 2-хлор-5-метиланилина (3,2 г, 16 ммоль). Полученную смесь охлаждали до 0°C и добавляли по каплям нитрит натрия (1,25 г, 18,1 ммоль) в воде (8 мл), при этом поддерживая температуру ниже 10°C. Реакционную смесь перемешивали 30 минут и затем добавляли по каплям к раствору диоксида серы. Полученную в результате реакционную смесь перемешивали при комнатной температуре 1 час. По каплям добавляли воду, и осаждалось желтовато-коричневое твердое вещество. Твердое вещество отделяли фильтрованием и промывали водой, с получением 2,5 г указанного в заголовке соединения.
1H ЯМР (CDCl3) δ 7,64 (д, 1H), 7,52 (д, 1H), 7,17 (д, 1H), 3,89 (с, 3H).
Стадия B: Получение 2-хлор-5-метоксибензолсульфонамида
К раствору 2-хлор-5-метоксибензолсульфонилхлорида (2,5 г, 10,4 ммоль) (т.е. продукт стадии A) в тетрагидрофуране (30 мл) добавляли по каплям 30% гидроксид аммония (3,0 мл, 25,7 ммоль). Реакционную смесь перемешивали 15 минут, в течение которых образовывалась суспензия. К полученной смеси добавляли воду (10 мл) и тетрагидрофуран выпаривали при пониженном давлении, оставляя водную суспензию желтовато-коричневого твердого вещества. Твердое вещество отделяли фильтрованием и промывали водой, с получением 2,2 г указанного в заголовке соединения.
1H ЯМР (CDCl3) δ 7,63 (д, 1H), 7,43 (д, 1H), 7,03 (д, 1H), 5,13 (шир.с., 2H), 3,85 (с, 3H).
Стадия C: Получение 8-хлор-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоновой кислоты
К раствору 2-амино-3-хлор-5-(трифторметил)пиридина (24,7 г, 126 ммоль) в 1,2-диметоксиэтане (260 мл) при 0°C добавляли по каплям этилбромпируват (17,43 мл, 138 ммоль). Реакционную смесь нагревали до комнатной температуры и перемешивали три дня до образования суспензии. Реакционную смесь затем экстрагировали дихлорметаном (2×200 мл) и промывали водой (2×200 мл). Комбинированные экстракты дихлорметана сушили над сульфатом магния и концентрировали при пониженном давлении, с получением твердого остатка. Комбинированные водные промывки насыщали карбонатом натрия, экстрагировали этилацетатом (2×200 мл) и сушили над сульфатом магния. Комбинированные экстракты этилацетата и остаток, полученный при концентрации дихлорметана, объединяли и смесь концентрировали при пониженном давлении, с получением твердого вещества.
Твердое вещество растворяли в этаноле (800 мл) и добавляли по каплям водный 50% гидроксид натрия (40 г, 500 ммоль), комбинированный с дополнительной водой (150 мл). Реакционную смесь перемешивали при комнатной температуре в течение всей ночи с образованием суспензии. Реакционную смесь подкисляли до pH 2 концентрированной хлористоводородной кислотой, затем охлаждали и перемешивали несколько часов с осаждением твердого вещества. Твердый продукт отделяли фильтрованием, используя фильтровальную воронку со стеклообразной фриттой, промывали водой и сушили на воздухе в токе воздуха в течение ночи, с получением 13 г указанного в заголовке соединения в виде твердого вещества.
1H ЯМР (CDCl3) δ 8,51 (с, 1H), 8,40 (с, 1H), 7,55 (с, 1H).
Стадия D: Получение 8-хлор-N-[(2-хлор-5-метоксифенил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
К карбоновой кислоте со стадии C (243 мг, 0,92 ммоль) добавляли раствор 4-(диметиламино)пиридина (340 мг, 2,76 ммоль) и гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида (232 мг, 2,3 ммоль) в трет-бутаноле (5 мл) и дихлорметане (5 мл). Реакционную смесь перемешивали в течение 15 минут, добавляли 2-хлор-5-метоксибензолсульфонамид (190 мг, 0,86 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем добавляли дихлорметан (200 мл), смесь экстрагировали 1н хлористоводородной кислотой (3×100 мл), отделенную органическую фазу сушили над сульфатом магния и концентрировали при пониженном давлении, с получением твердого вещества. Твердое вещество промывали диэтиловым эфиром, с получением 240 мг указанного в заголовке соединения, соединения настоящего изобретения, в виде белого твердого вещества, т.пл. 211-212°C.
1H ЯМР (CDCl3) δ 10,10 (шир.с., 1H), 8,46 (с, 1H), 8,27 (с, 1H), 7,86 (д, 1H), 7,54 (с, 1H), 7,38 (д, 1H), 7,09 (дд, 1H) 3,91 (с, 3H).
Пример синтеза 2
Получение 8-хлор-N-[(4-циано-2,5-диметилфенил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
Стадия A: Получение 4-бром-2,5-диметилбензолсульфонамида
К хлорсульфоновой кислоте (4,2 мл, 63 ммоль), охлажденной до 10°C, добавляли по каплям 2-бром-п-ксилол (5,0 г, 27 ммоль) в течение 15 минут. Реакционную смесь перемешивали дополнительно 10 минут и затем выливали при перемешивании в 125 мл раздробленного льда с осаждением белого твердого вещества. Твердое вещество отделяли фильтрованием и промывали водой. Твердое вещество растворяли в тетрагидрофуране (40 мл) и добавляли 30% водный раствор гидроксида аммония (8,0 мл). Реакционную смесь перемешивали в течение 10 минут и концентрировали при пониженном давлении с осаждением белого твердого вещества. Твердое вещество отделяли фильтрованием и промывали водой, с получением 4,6 г указанного в заголовке соединения в виде твердого вещества.
1H ЯМР (CDCl3) δ 7,87 (с, 1H), 7,52 (с, 1H), 4,75 (шир.с., 2H), 2,61 (с, 3H), 2,41 (с, 3H).
Стадия B: Получение 4-циано-2,5-диметилбензолсульфонамида
К раствору 4-бром-2,5-диметилбензолсульфонамида (4,6 г, 22 ммоль, продукт стадии A) в N-метилпирролидиноне (30 мл) добавляли цианид меди (2,5 г, 28 ммоль), и реакционную смесь нагревали при 200°C в течение 30 минут. Реакции затем давали возможность охладиться и выливали в 200 мл раздробленного льда с осаждением твердого вещества. К полученной смеси добавляли дихлорметан (500 мл) и смесь нагревали с растворением белого твердого вещества. Смесь затем фильтровали для удаления любых нерастворенных твердых веществ, фазы разделяли и дихлорметан промывали водой (2×100 мл), сушили над сульфатом магния и выпаривали при пониженном давлении, с получением масла. Масло растворяли в тетрагидрофуране (30 мл) и воде (30 мл), раствор концентрировали при пониженном давлении с осаждением твердого вещества. Полученное твердое вещество отделяли фильтрованием и промывали водой, с получением 2,5 г указанного в заголовке соединения.
1H ЯМР (CDCl3) δ 7,98 (с, 1H), 7,56 (с, 1H), 4,89 (шир.с., 2H), 2,66 (с, 3H), 2,58 (с, 3H).
Стадия C: Получение 8-хлор-N-[(4-циано-2,5-диметилфенил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
К раствору 8-хлор-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоновой кислоты (2,5 г, 9,5 ммоль, полученной, как описано в примере 1, стадия C) в трет-бутаноле (70 мл) и дихлорметане (70 мл) добавляли 4-(диметиламино)пиридин (3,47 г, 28,4 ммоль) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (4,54 г, 23,7 ммоль). Реакционную смесь перемешивали в течение 15 минут, затем добавляли 4-циано-2,5-диметилбензолсульфонамид (1,85 г, 8,85 ммоль) и перемешивали в течение ночи при комнатной температуре. Затем добавляли дихлорметан (200 мл), смесь промывали 1н хлористоводородной кислотой (3×100 мл), органическую фазу собирали и сушили над сульфатом магния, затем концентрировали при пониженном давлении, с получением твердого соединения. Твердое вещество отделяли фильтрованием, промывали диэтиловым эфиром и перекристаллизовывали из смеси гексан/этилацетат, с получением 1,5 г указанного в заголовке соединения, соединения настоящего изобретения, в виде твердого вещества, т.пл. 228-229°C.
1H ЯМР (CDCl3) δ 9,97 (шир.с., 1H), 8,47 (с, 1H), 8,26 (с, 1H), 8,24 (с, 1H), 7,56 (с, 1H), 7,54 (с, 1H), 2,71 (с, 3H), 2,63 (с, 3H).
Пример синтеза 3
Получение 8-хлор-N-[(2-хлор-5-этилфенил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
Стадия A: Получение 2-хлор-5-этилбензолсульфонилхлорида
Хлорсульфоновую кислоту (4,0 мл, 59 ммоль) охлаждали до 0°C и добавляли по каплям 1-хлор-4-этилбензол (1,0 мл, 7,5 ммоль) в течение 30 минут. Реакционную смесь перемешивали в течение 45 минут при 0°C, выливали при перемешивании в 125 мл раздробленного льда и затем экстрагировали этилацетатом (2×100 мл). Слои этилацетата объединяли, промывали водой (100 мл) и сушили над сульфатом магния. Этилацетат концентрировали при пониженном давлении, с получением масла, определенного как смесь изомеров приблизительно 1:1. Полученную смесь хроматографировали на силикагеле, элюируя с градиентом смеси гексан/этилацетат, с получением 0,41 г указанного в заголовке соединения.
1H ЯМР (CDCl3) δ 7,97 (с, 1H), 7,53 (д, 1H), 7,49 (д, 1H), 2,75 (кв, 2H), 1,29 (т, 3H).
Стадия B: Получение 2-хлор-5-этилбензолсульфонамида
К раствору 2-хлор-5-этилбензолсульфонилхлорида (0,41 г, 1,7 ммоль, продукт стадии A) в тетрагидрофуране (30 мл) добавляли по каплям 30% гидроксид аммония (0,41 мл, 3,5 ммоль). Реакционную смесь перемешивали 15 минут, во время чего образовывалась суспензия. К полученной смеси добавляли воду (10 мл) и тетрагидрофуран выпаривали при пониженном давлении с осаждением твердого вещества. Твердое вещество растворяли в диэтиловом эфире, сушили над сульфатом магния и концентрировали при пониженном давлении. Диэтиловый эфир и гексан добавляли к осажденному твердому веществу. Твердое вещество отделяли фильтрованием, с получением 190 мг указанного в заголовке соединения.
1H ЯМР (CDCl3) δ 7,95 (с, 1H), 7,43 (д, 1H), 7,35 (д, 1H), 5,08 (шир.с., 2H), 2,71 (кв, 2H), 1,25 (т, 3H).
Стадия C: Получение 8-хлор-N-[(2-хлор-5-этилфенил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
К раствору 8-хлор-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоновой кислоты (100 мг, 0,38 ммоль, полученной, как описано в примере 1 стадия C), в смеси 1:1 трет-бутанола (5 мл) и дихлорметана (5 мл) добавляли 4-(диметиламино)пиридин (138 мг, 1,1 ммоль) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (182 мг, 0,95 ммоль). Реакционную смесь перемешивали в течение 15 минут, добавляли 2-хлор-5-этилбензолсульфонамид (74 мг, 0,34 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем добавляли дихлорметан (100 мл), смесь промывали 1н хлористоводородной кислотой (3×50 мл), органическую фазу сушили над сульфатом магния и концентрировали при пониженном давлении, с получением твердого вещества. Твердое вещество промывали диэтиловым эфиром, с получением 84 мг указанного в заголовке соединения, соединения настоящего изобретения, в виде твердого вещества, т.пл. 214-215°C.
1H ЯМР (CDCl3) δ 10,12 (шир.с., 1H), 8,45 (с, 1H), 8,26 (с, 1H), 8,20 (с, 1H), 7,53 (с, 1H), 7,40 (с, 2H), 2,77 (кв, 2H), 1,30 (т, 3H).
Пример синтеза 4
Получение 8-хлор-N-[(1-этил-3-метил-1H-пиразол-4-ил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
Стадия A: Получение 1-этил-3-метил-1H-пиразол-4-сульфонамида
К раствору 1-этил-3-метил-1H-пиразол-4-сульфонилхлорида (0,154 г, 0,73 ммоль, Matrix Scientific) в тетрагидрофуране (10 мл) добавляли по каплям водный раствор 30% гидроксида аммония (0,20 мл, 1,7 ммоль). Реакционную смесь перемешивали в течение 1 часа, добавляли воду (2 мл) и растворитель концентрировали при пониженном давлении с осаждением твердого вещества. Твердое вещество отделяли фильтрованием, промывали водой и сушили, с получением 41 мг указанного в заголовке соединения.
1H ЯМР (CDCl3) δ 7,80 (с, 1H), 4,75 (шир.с., 1H), 4,11 (кв, 2H), 2,44 (с, 3H), 1,49 (т, 3H).
Стадия B: Получение 8-хлор-N-[(1-этил-3-метил-1H-пиразол-4-ил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
К раствору 8-хлор-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоновой кислоты (63 мг, 0,24 ммоль, полученной, как описано в примере 1, стадия C) в смеси 1:1 трет-бутанола (5 мл) и дихлорметана (5 мл) добавляли 4-(диметиламино)пиридин (88 мг, 0,71 ммоль) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (117 мг, 0,60 ммоль). Реакционную смесь перемешивали 15 минут, затем добавляли 1-этил-3-метил-1H-пиразол-4-сульфонамид (41 мг, 0,22 ммоль, продукт стадии A), и реакционную смесь перемешивали при комнатной температуре в течение ночи. Добавляли дихлорметан (100 мл) и смесь промывали 1н хлористоводородной кислотой (3×50 мл). Органическую фазу отделяли, сушили над сульфатом магния и концентрировали при пониженном давлении, с получением твердого вещества. Твердое вещество суспендировали в смеси диэтилового эфира и гексана, фильтровали и сушили, с получением 25 мг указанного в заголовке соединения, соединения настоящего изобретения, в виде твердого вещества, т.пл. 189-190°C.
1H ЯМР (CDCl3) δ 9,85 (шир.с., 1H), 8,47 (с, 1H), 8,29 (с, 1H), 8,10 (с, 1H), 7,53 (с, 1H), 4,14 (кв, 2H), 2,51 (с, 3H), 1,51 (т, 3H).
Пример синтеза 5
Получение 8-хлор-N-[(3-хлор-1-этил-1H-пиразол-4-ил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
Стадия A: Получение 1-этил-1H-пиразол-3-иламина
К раствору карбоната калия (2,76 г, 20,0 ммоль) в воде (10 мл) добавляли этилгидразиноксалат (3,0 г, 20 ммоль), с последующим добавлением по каплям 2-хлоракрилонитрила (1,6 мл, 20 ммоль) в течение 30 минут. Смесь перемешивали при комнатной температуре 2 часа и затем нагревали при 50°C 2 часа. Реакционную смесь охлаждали и экстрагировали этилацетатом (2×100 мл). Этилацетат сушили над сульфатом магния и выпаривали при пониженном давлении, с получением масла. Масло хроматографировали на силикагеле, элюируя гексаном и этилацетатом, в качестве элюента, с получением 540 мг указанного в заголовке соединения.
1H ЯМР (CDCl3) δ 7,12 (д, 1H) 5,57 (д, 1H), 3,96 (кв, 2H), 3,59 (шир.с., 1H), 1,42 (т, 3H).
Стадия B: Получение 3-хлор-1-этил-1H-пиразола
К раствору 1-этил-1H-пиразол-3-иламина (0,54 г, 4,86 ммоль, продукт стадии A) в концентрированной хлористоводородной кислоте (5 мл) при 0°C добавляли по каплям раствор нитрита натрия (369 мг, 5,35 ммоль) в воде (1 мл), при этом поддерживая температуру ниже 10°C. Реакционную смесь перемешивали 30 минут, добавляли по каплям раствор хлорида меди (I) в концентрированной хлористоводородной кислоте (2 мл), и полученную в результате реакционную смесь затем нагревали до 60°C. Каталитическое количество хлорида меди добавляли при 60°C (инициируя выделение газа). Реакционную смесь перемешивали в течение 5 минут и затем выливали на 100 мл раздробленного льда, содержащего 50% гидроксид натрия (5 мл) и тщательно перемешивали. Водную смесь экстрагировали дихлорметаном (2×150 мл), органический слой отделяли, промывали водой, сушили над сульфатом магния и концентрировали при пониженном давлении, с получением 0,42 г указанного в заголовке соединения.
1H ЯМР (CDCl3) δ 7,31 (д, 1H), 6,15 (д, 1H), 4,11 (кв, 2H), 1,47 (т, 3H).
Стадия C: Получение 3-хлор-1-этил-1H-пиразол-4-сульфонилхлорида
3-хлор-1-этил-1H-пиразол (0,42 г, 3,2 ммоль, продукт стадии B) добавляли к хлорсульфоновой кислоте (2,0 мл, 30 ммоль) при комнатной температуре, смесь медленно нагревали до 100°C и затем нагревали при 100-110°C в течение 2 часов. Реакционную смесь охлаждали, выливали при перемешивании на 150 мл раздробленного льда и экстрагировали диэтиловым эфиром (2×100 мл). Экстракты эфира объединяли, промывали водой (100 мл), сушили над сульфатом магния и концентрировали при пониженном давлении, с получением 0,5 г указанного в заголовке соединения в виде масла.
1H ЯМР (CDCl3) δ 8,00 (с, 1H), 4,20 (кв, 2H), 1,56 (т, 3H).
Стадия D: Получение 3-хлор-1-этил-1H-пиразол-4-сульфонамида
К раствору 3-хлор-1-этил-1H-пиразол-4-сульфонилхлорида (0,5 г, 2,2 ммоль, продукт стадии D) в тетрагидрофуране (20 мл) добавляли по каплям 30% гидроксид аммония (3,0 мл, 24 ммоль). Реакционную смесь нагревали до кипения струйной воздушной сушилкой и затем перемешивали в течение 30 минут. Тетрагидрофуран удаляли при пониженном давлении, добавляли воду (50 мл), и реакционную смесь экстрагировали этилацетатом (2×100 мл). Этилацетат сушили над сульфатом магния и концентрировали при пониженном давлении, с получением твердого вещества. Твердое вещество промывали гексаном и сушили, с получением 282 мг указанного в заголовке соединения.
1H ЯМР (CDCl3) δ 7,84 (с, 1H), 4,94 (шир.с., 1H), 4,15 (кв, 2H), 1,51 (т, 3H).
Стадия E: Получение 8-хлор-N-[(3-хлор-1-этил-1H-пиразол-4-ил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
К раствору 8-хлор-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоновой кислоты (110 мг, 0,42 ммоль, полученной, как описано в примере 1, стадия C) в смеси 1:1 трет-бутанола (5 мл) и дихлорметана (5 мл) добавляли 4-(диметиламино)пиридин (152 мг, 1,25 ммоль) и гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида (96 мг, 0,5 ммоль). Реакционную смесь перемешивали в течение 15 минут, затем добавляли 3-хлор-1-этил-1H-пиразол-4-сульфонамид (81 мг, 0,38 ммоль, продукт стадии D) и перемешивание продолжали при комнатной температуре в течение ночи. Затем добавляли дихлорметан (100 мл) и смесь экстрагировали 1н хлористоводородной кислотой (3×50 мл). Отделенные органические фазы объединяли, сушили над сульфатом магния и концентрировали при пониженном давлении, с получением твердого вещества. Твердое вещество суспендировали в смеси диэтилового эфира и гексана и фильтровали, с получением 85 мг указанного в заголовке соединения, соединение настоящего изобретения, в виде твердого вещества, т.пл. 184-185°C.
1H ЯМР (CDCl3) δ 9,96 (шир.с., 1H), 8,47 (с, 1H), 8,29 (с, 1H), 8,16 (с, 1H), 7,54 (с, 1H), 4,17 (кв, 2H), 1,54 (т, 3H).
Пример синтеза 6
Получение 8-бром-N-[(2-хлор-5-метоксифенил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
Стадия A: Получение 8-бром-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоновой кислоты
К раствору 2-амино-3-бром-5-(трифторметил)пиридина (10,0 г, 41,5 ммоль) в 1,2-диметоксиэтане (300 мл) при комнатной температуре добавляли по каплям этилбромпируват (9,889 г, 45,64 ммоль). Реакционную смесь нагревали при кипячении с обратным холодильником в течение 18 часов. 1,2-диметоксиэтан удаляли при пониженном давлении и остаточное твердое вещество перекристаллизовывали из 1-хлорбутана. Твердое вещество отделяли фильтрованием и сушили, с получением не совсем белого твердого вещества, этилового эфира 8-бром-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоновой кислоты (11,044 г).
Твердое вещество, полученное выше, растворяли в тетрагидрофуране (150 мл) и добавляли раствор LiOH (2,353 г, 98,29 ммоль) в воде (100 мл). Реакционную смесь перемешивали при комнатной температуре 4 часа. Тетрагидрофуран удаляли при пониженном давлении, с получением водного раствора, который охлаждали до 5°C. По каплям добавляли разбавленный HCl до достижения pH <5,0. Через несколько минут твердое вещество начало осаждаться из раствора. Твердое вещество отделяли фильтрованием, один раз промывали водой (50 мл) и сушили в вакуумной печи в течение 18 часов при 80°C, с получением 8,632 г указанного в заголовке соединения в виде твердого вещества.
1H ЯМР (ДМСО-d6) δ 13,17 (шир.с., 1H), 9,31 (с, 1H), 8,69 (с, 1H), 8,03 (с, 1H).
Стадия B: Получение 8-бром-N-[(2-хлор-5-метоксифенил)сульфонил]-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
К продукту стадии A (200 мг, 0,647 ммоль) добавляли раствор 4-(диметиламино)пиридина (237 мг, 1,94 ммоль) и гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида (309 мг, 1,62 ммоль) в смеси 1:1 трет-бутанола (5 мл) и дихлорметана (5 мл). Реакционную смесь перемешивали в течение 15 минут, добавляли 2-хлор-5-метоксибензолсульфонамид (129 мг, 0,582 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем добавляли дихлорметан (200 мл), смесь экстрагировали 1н хлористоводородной кислотой (3×100 мл), отделенные органические фазы объединяли, сушили над сульфатом магния и концентрировали при пониженном давлении, с получением твердого вещества. Твердое вещество промывали диэтиловым эфиром, с получением 234 мг указанного в заголовке соединения, соединение настоящего изобретения, в виде белого твердого вещества, т.пл. 191-192°C.
1H ЯМР (CDCl3) δ 10,1 (шир.с., 1H), 8,51 (с, 1H), 8,30 (с, 1H), 7,87 (д, 1H), 7,72 (с, 1H), 7,38 (д, 1H), 7,08 (дд, 1H) 3,91 (с, 3H).
Пример синтеза 7
Получение 8-хлор-N-[(2-хлор-5-метоксифенил)сульфонил]-3-метил-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
Стадия A: Получение этилового эфира 3-бром-2-оксомасляной кислоты
2-оксомасляную кислоту (10,0 г, 97,2 ммоль) растворяли в этаноле (100 мл) и добавляли моногидрат п-толуолсульфоновой кислоты (0,1 г). Реакционную смесь нагревали при кипячении с обратным холодильником в течение 48 часов. После охлаждения реакционной смеси до комнатной температуры, этанол удаляли при пониженном давлении, с получением 11,4 г этилового эфира 2-оксомасляной кислоты.
Этиловый эфир 2-оксомасляной кислоты, полученный выше, растворяли в хлороформе (100 мл) и по каплям добавляли бром (20,964 г, 131,19 ммоль) при комнатной температуре. Реакционную смесь перемешивали 18 часов. Концентрация реакционной смеси при пониженном давлении давала 12,0 г указанного в заголовке соединения в виде оранжевого масла.
1H ЯМР (CDCl3) δ 4,39 (кв, 2H), 4,32 (кв, 1H), 1,88 (д, 3H), 1,39 (т, 3H).
Стадия B: Получение 8-хлор-3-метил-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоновой кислоты
К раствору 2-амино-3-хлор-5-(трифторметил)пиридина (11,3 г, 57,5 ммоль) в диоксане (200 мл) при комнатной температуре добавляли по каплям этиловый эфир 3-бром-2-оксомасляной кислоты (12,017 г, 57,49 ммоль, продукт стадии A). Реакционную смесь нагревали при кипячении с обратным холодильником в течение 24 часов, охлаждали и удаляли диоксан при пониженном давлении. Хроматография на силикагеле при элюировании градиентом смеси гексан/этилацетат, давала 17,3 г этилового эфира 8-хлор-3-метил-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоновой кислоты в виде твердого вещества.
Твердое вещество, полученное выше, растворяли в тетрагидрофуране (100 мл) и добавляли раствор LiOH (3,365 г, 140,8 ммоль) в воде (50 мл). Реакционную смесь перемешивали при комнатной температуре 18 часов. Тетрагидрофуран удаляли при пониженном давлении, с получением водного раствора, который охлаждали до 5°C. Добавляли по каплям разбавленный HCl до достижения pH <5,0. Через несколько минут твердое вещество начинало осаждаться. Твердое вещество отделяли фильтрованием, промывали водой (50 мл) и сушили при 80°C в вакуумной печи в течение 18 часов, с получением 15,7 г твердого вещества.
1H ЯМР (ДМСО-d6) δ 13,1 (шир.с., 1H), 8,84 (с, 1H), 7,80 (с, 1H), 2,82 (с, 3H).
Стадия C: Получение 8-хлор-N-[(2-хлор-5-метоксифенил)сульфонил]-3-метил-6-(трифторметил)имидазо[1,2-a]пиридин-2-карбоксамида
К карбоновой кислоте, полученной на стадии B (200 мг, 0,72 ммоль), добавляли раствор 4-(диметиламино)пиридина (262 мг, 2,15 ммоль) и гидрохлорида 1-(3-диметиламинопропил)-3-этилкарбодиимида (344 мг, 1,79 ммоль) в смешанном растворителе из 1:1 трет-бутанола (5 мл) и дихлорметана (5 мл). Реакционную смесь перемешивали в течение 15 минут, добавляли 2-хлор-5-метоксибензолсульфонамид (143 мг, 0,65 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение ночи. Затем добавляли дихлорметан (200 мл), смесь экстрагировали 1н хлористоводородной кислотой (3×100 мл) и разделенные органические слои объединяли, сушили над сульфатом магния и концентрировали при пониженном давлении, с получением твердого вещества. Твердое вещество промывали диэтиловым эфиром, с получением 118 мг указанного в заголовке соединения, соединение настоящего изобретения, в виде белого твердого вещества, т.пл. 222-223°C.
1H ЯМР (ДМСО-d6) δ 10,0 (шир.с., 1H), 8,94 (с, 1H), 7,96 (с, 1H), 7,65 (д, 1H), 7,59 (д, 1H), 7,30 (дд, 1H), 3,87 (с, 3H) 2,71 (с, 3H).
Методиками, описанными выше в данном описании, вместе со способами, известными в данной области, могут быть получены следующие соединения таблиц 1-22. В таблицах использовали следующие аббревиатуры: Me означает метил, Et означает этил, OMe означает метокси, SMe означает метилтио, и NMe2 означает диметиламино.

R
1a
представляет собой CF
3
, R
1b
представляет собой Cl, R
2
и R
3
представляют собой H
Таблица 2
Таблица 2 составлена так же, как и таблица 1, за исключением того, что R2 представляет собой Cl. Например, первое соединение в таблице 2, где R1a представляет собой CF3, R1b представляет собой Cl, R2 представляет собой Cl, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:

Таблица 3
Таблица 3 составлена так же, как и таблица 1, за исключением того, что R2 представляет собой Br. Например, первое соединение в таблице 3, где R1a представляет собой CF3, R1b представляет собой Cl, R2 представляет собой Br, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:

Таблица 4
Таблица 4 составлена так же, как и таблица 1, за исключением того, что R2 представляет собой Me. Например, первое соединение в таблице 4, где R1a представляет собой CF3, R1b представляет собой Cl, R2 представляет собой Me, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:
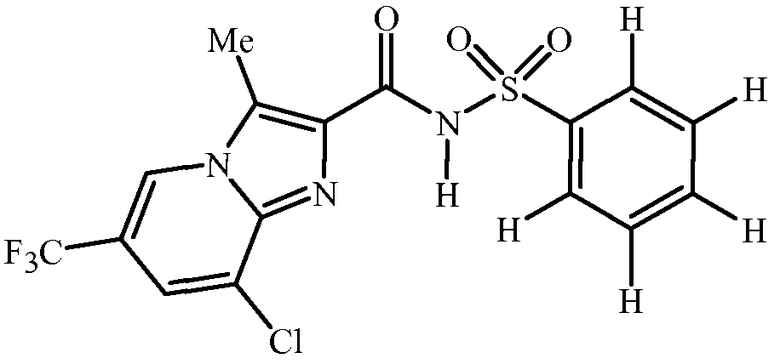
Таблица 5
Таблица 5 составлена так же, как и таблица 1, за исключением того, что R1a и R1b представляют собой H. Например, первое соединение в таблице 5, где R1a представляет собой H, R1b представляет собой H, и R2, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:
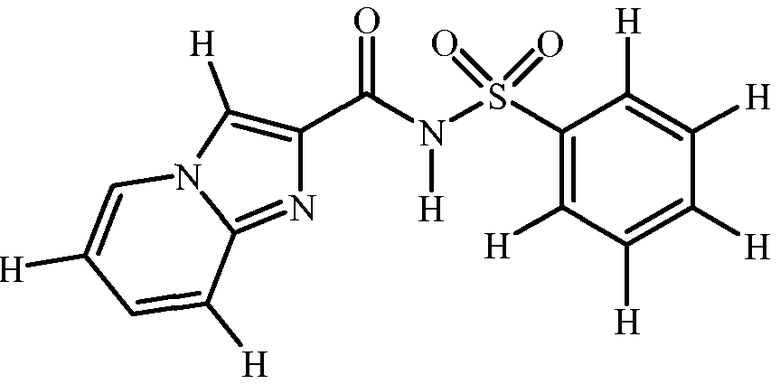
Таблица 5a
Таблица 5a составлена так же, как и таблица 1, за исключением того, что R1a представляет собой Cl, и R1b представляет собой H. Например, первое соединение в таблице 5a, где R1a представляет собой Cl, R1b представляет собой H, и R2, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:

Таблица 5b
Таблица 5b составлена так же, как и таблица 1, за исключением того, что R1a представляет собой Br, и R1b представляет собой H. Например, первое соединение в таблице 5b, где R1a представляет собой Br, R1b представляет собой H, и R2, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже.

Таблица 5c
Таблица 5c составлена так же, как и таблица 1, за исключением того, что R1b представляет собой H. Например, первое соединение в таблице 5c, где R1a представляет собой CF3, R1b представляет собой H, и R2, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:

Таблица 6
Таблица 6 составлена так же, как и таблица 1, за исключением того, что R1b представляет собой Br. Например, первое соединение в таблице 6, где R1a представляет собой CF3, R1b представляет собой Br, и R2, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:

Таблица 6a
Таблица 6 составлена так же, как и таблица 1, за исключением того, что R1b представляет собой F. Например, первое соединение в таблице 6, где R1a представляет собой CF3, R1b представляет собой F, и R2, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:

Таблица 7
Таблица 7 составлена так же, как и таблица 1, за исключением того, что R1a и R1b представляют собой Cl. Например, первое соединение в таблице 7, где R1a и R1b представляют собой Cl, и R2, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:

Таблица 8
Таблица 8 составлена так же, как и таблица 1, за исключением того, что R1a и R1b представляют собой Br. Например, первое соединение в таблице 8, где R1a и R1b представляют собой Br, и R2, R3 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:

Таблица 9
Таблица 9 составлена так же, как и таблица 1, за исключением того, что R3 представляет собой Me. Например, первое соединение в таблице 9, где R1a представляет собой CF3, R1b представляет собой Cl, R3 представляет собой Me, и R2 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:
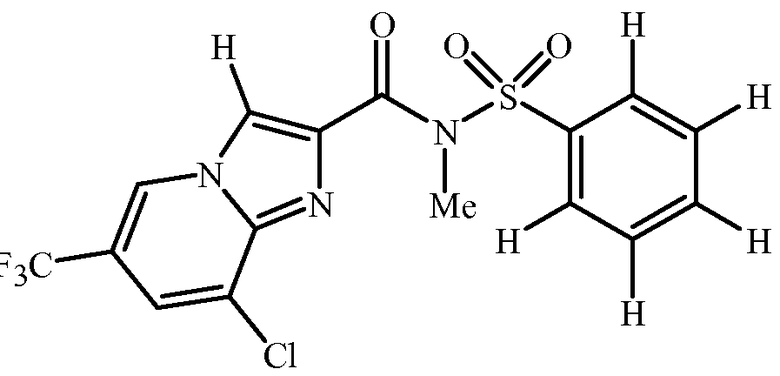
Таблица 10
Таблица 10 составлена так же, как и таблица 1, за исключением того, что R3 представляет собой Et. Например, первое соединение в таблице 10, где R1a представляет собой CF3, R1b представляет собой Cl, R3 представляет собой Et, и R2 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:
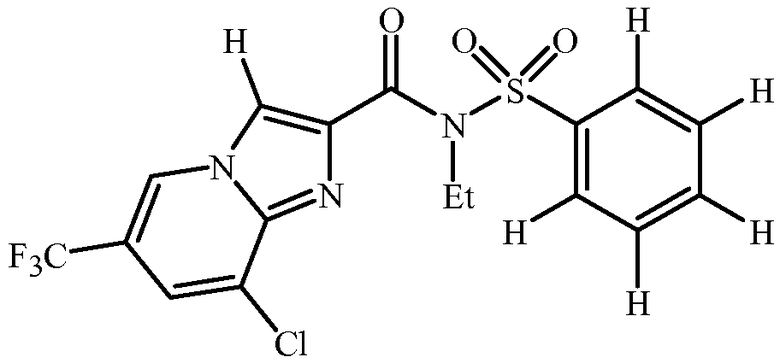
Таблица 11
Таблица 11 составлена так же, как и таблица 1, за исключением того, что R3 представляет собой пропаргил (т.е. CH2C≡CH). Например, первое соединение в таблице 11, где R1a представляет собой CF3, R1b представляет собой Cl, R3 представляет собой пропаргил, и R2 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:

Таблица 12
Таблица 12 составлена так же, как и таблица 1, за исключением того, что R3 представляет собой бензил (т.е. CH2C6H5). Например, первое соединение в таблице 12, где R1a представляет собой CF3, R1b представляет собой Cl, R3 представляет собой бензил, и R2 и Ra-Re представляют собой H, является структурой, показанной непосредственно ниже:


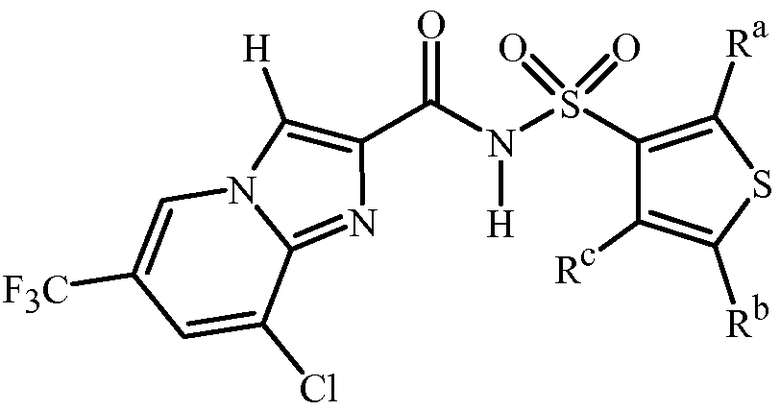


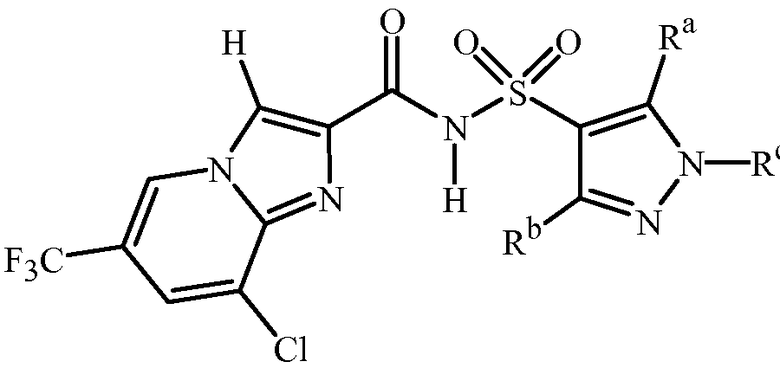

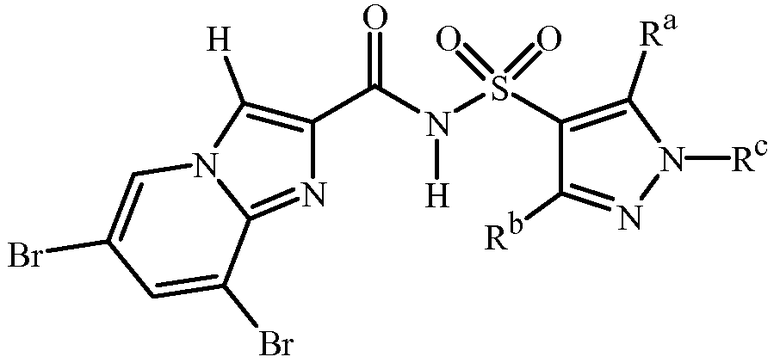

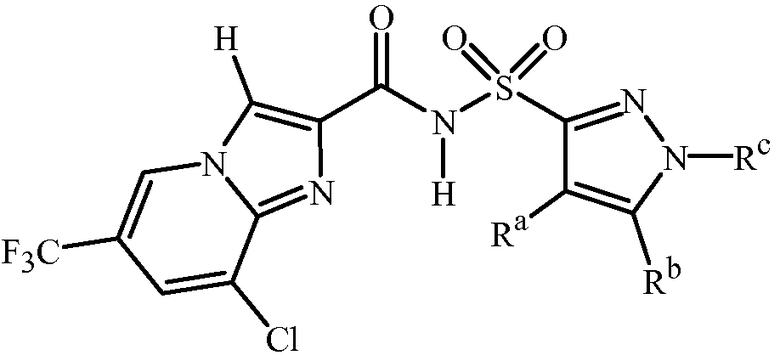
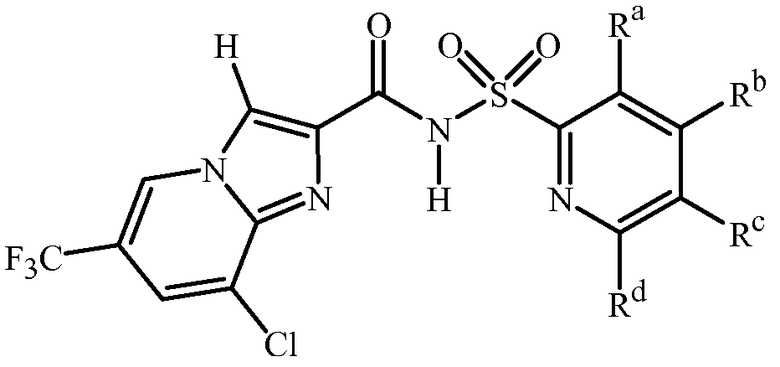


Соединение настоящего изобретения обычно будет применяться в качестве активного ингредиента для борьбы с паразитической нематодой в композиции, т.е. составе, по меньшей мере с одним дополнительным компонентом, выбранным из группы, состоящей из поверхностно-активного вещества, твердых разбавителей и жидких разбавителей, которые служат в качестве носителя. Ингредиенты состава или композиции выбирают таким образом, чтобы они соответствовали физическим свойствам активного ингредиента, способу внесения и факторам окружающей среды, таким как тип почвы, влага и температура.
Подходящие для применения составы включают как жидкие, так и твердые композиции. Жидкие композиции включают растворы (включая, эмульгируемые концентраты), суспензии, эмульсии (включая микроэмульсии и/или суспоэмульсии) и подобные, которые необязательно могут быть сгущены в гели. Общими типами водных жидких композиций являются растворимый концентрат, суспендируемый концентрат, капсульная суспензия, концентрированная эмульсия, микроэмульсия и суспоэмульсия. Общими типами безводных жидких композиций являются эмульгируемый концентрат, микроэмульгируемый концентрат, диспергируемый концентрат и масляная дисперсия.
Общими типами твердых композиций являются дусты, порошки, гранулы, пеллеты, периллы, пастилки, таблетки, наполненные пленки (включая покрытия для семян) и подобное, которые могут быть диспергируемыми в воде (“смачиваемыми”) или растворимыми в воде. Пленки и покрытия, образованные из образующих пленку растворов или текучих суспензий, особенно полезны для обработки семян. Активный ингредиент может быть (микро)капсулирован и затем сформирован в суспензию или твердый состав; альтернативно, полный состав активного ингредиента может быть инкапсулирован (или “покрыт”). Инкапсулирование может контролировать или замедлять высвобождение активного ингредиента. Эмульгируемая гранула объединяет преимущества состава эмульгируемого концентрата и сухого гранулярного состава. Высокопрочные композиции, прежде всего, используются в качестве промежуточных соединений для дальнейшего составления в композицию.
Распыляемые составы обычно распространяют в подходящей среде перед распылением. Такие жидкие и твердые составы сформулированы таким образом, чтобы легко растворяться в среде распыления, обычно воде. Распыляемые объемы могут варьировать приблизительно от одного до нескольких тысяч литров на гектар, но более конкретно находятся в диапазоне приблизительно от десяти до нескольких сотен литров на гектар. Распыляемые составы могут быть смешаны в емкости с водой или другой подходящей средой для обработки листьев воздушным или почвенным внесением или для внесения в среду произрастания растения. Жидкие и сухие составы могут быть отмерены непосредственно в системы капельного орошения или отмерены в борозду во время посева. Жидкие и твердые составы могут быть нанесены на семена сельскохозяйственных культур и другую желаемую растительность в качестве обработки семян перед посевом для защиты развивающихся корней и других подземных частей растений и/или листвы путем системного поглощения.
Составы обычно будут содержать эффективное количество активного ингредиента, разбавителя и поверхностно-активного вещества в следующих приблизительных диапазонах, которое добавляется до 100 массовых процентов.
Твердые разбавители включают, например, глины, такие как бентонит, монтмориллонит, аттапульгит и каолин, гипс, целлюлозу, диоксид титана, оксид цинка, крахмал, декстрин, сахара (например, лактоза, сахароза), кремнезем, тальк, слюду, диатомовую землю, мочевину, карбонат кальция, карбонат и бикарбонат натрия и сульфат натрия. Конкретные твердые разбавители описаны у Watkins et al., в Handbook of Insecticide Dust Diluents and Carriers, 2-е изд., Dorland Books, Caldwell, New Jersey.
Жидкие разбавители включают, например, воду, N,N-диметилалканамиды (например, N,N-диметилформамид), лимонен, диметилсульфоксид, N-алкилпирролидоны (например, N-метилпирролидинон), этиленгликоль, триэтиленгликоль, пропиленгликоль, дипропиленгликоль, полипропиленгликоль, пропиленкарбонат, бутиленкарбонат, парафины (например, белые минеральные масла, нормальные парафины, изопарафины), алкилбензолы, алкилнафталины, глицерин, глицеринтриацетат, сорбит, триацетин, ароматические углеводороды, деароматизированные алифатические углеводороды, алкилбензолы, алкилнафталины, кетоны, такие как циклогексанон, 2-гептанон, изофорон и 4-гидрокси-4-метил-2-пентанон, ацетаты, такие как изоамилацетат, гексилацетат, гептилацетат, октилацетат, нонилацетат, тридецилацетат и изоборнилацетат, другие сложные эфиры, такие как алкилированные сложные эфиры лактата, двухосновные сложные эфиры и γ-бутиролактон, и спирты, которые могут быть линейными, разветвленными, насыщенными или ненасыщенными, такие как метанол, этанол, н-пропанол, изопропиловый спирт, н-бутанол, изобутиловый спирт, н-гексанол, 2-этилгексанол, н-октанол, деканол, изодециловый спирт, изооктадеканол, цетиловый спирт, лауриловый спирт, тридециловый спирт, олеиловый спирт, циклогексанол, тетрагидрофурфуриловый спирт, диацетоновый спирт и бензиловый спирт. Жидкие разбавители также включают глицериновые сложные эфиры насыщенных и ненасыщенных жирных кислот (обычно C6-C22), такие как растительные масла семян и плодов (например, масла из оливы, клещевины, семян льна, кунжута, кукурузы (маиса), арахиса, подсолнечника, семян винограда, сафлора, семян хлопка, сои, семян рапса, кокоса и ядра кокосового ореха), животные жиры (например, говяжий жир, свиной жир, топленый свиной жир, жир печени трески, рыбий жир) и их смеси. Жидкие разбавители также включают алкилированные жирные кислоты (например, метилированные, этилированные, бутилированные), где жирные кислоты могут быть получены гидролизом глицериновых сложных эфиров из растительных и животных источников, и могут быть очищены дистилляцией. Конкретные жидкие разбавители описаны у Marsden, в Solvents Guide, 2-е изд., Interscience, New York, 1950.
Твердые и жидкие композиции настоящего изобретения часто содержат один или более поверхностно-активных веществ. При добавлении в жидкость, поверхностно-активные вещества (также известные как “поверхностно-активные средства”) обычно модифицируют, чаще всего снижают, поверхностное натяжение жидкости. В зависимости от природы гидрофильных и липофильных групп в молекуле поверхностно-активного вещества, поверхностно-активные вещества могут быть использованы в качестве смачивающих средств, дисперсантов, эмульгаторов или противовспенивающих средств.
Поверхностно-активные вещества могут быть классифицированы как неионные, анионные или катионные. Неионные поверхностно-активные вещества, используемые для настоящих композиций, включают, но не ограничиваются ими: спиртовые алкоксилаты, такие как спиртовые алкоксилаты на основе природных и синтетических спиртов (которые могут быть разветвленными или линейными) и полученные из спиртов и этиленоксида, пропиленоксида, бутиленоксида или их смесей; аминэтоксилаты, алканoламиды и этоксилированные алканоламиды; алкоксилированные триглицериды, такие как этоксилированные соевое, касторовое и рапсовое масла; алкилфенолалкоксилаты, такие как октилфенолэтоксилаты, нонилфенолэтоксилаты, динонилфенолэтоксилаты и додецилфенолэтоксилаты (полученные из фенолов и этиленоксида, пропиленоксида, бутиленоксида или их смесей); блок-полимеры, полученные из этиленоксида или пропиленоксида, и обратимые блок-полимеры, где концевые блоки получены из пропиленоксида; этоксилированные жирные кислоты; этоксилированные жирные сложные эфиры и масла; этоксилированные метиловые сложные эфиры; этоксилированный тристирилфенол (включая полученные из этиленоксида, пропиленоксида, бутиленоксида или их смесей); сложные эфиры жирных кислот, глицериновые сложные эфиры, производные на основе ланолина, полиэтоксилированные сложные эфиры, такие как полиэтоксилированные сложные эфиры сорбита и жирных кислот, полиэтоксилированные сложные эфиры сорбита и жирных кислот и полиэтоксилированные сложные эфиры глицерина и жирных кислот; другие производные сорбита, такие как сложные эфиры сорбита; полимерные поверхностно-активные вещества, такие как статистические coполимеры, блок-coполимеры, алкидные пэг (полиэтиленгликоль) смолы, привитые или комбинированные полимеры и звездообразные полимеры; полиэтиленгликоли (пэги); полиэтиленгликолевые сложные эфиры жирных кислот; поверхностно-активные вещества на основе силикона; и производные сахаров, такие как сложные эфиры сахарозы, алкилполигликозиды и алкилполисахариды.
Используемые анионные поверхностно-активные вещества включают, но не ограничиваются ими: алкиларилсульфоновые кислоты и их соли; карбоксилированный спирт или алкилфенольные этоксилаты; дифенилсульфонатные производные; лигнин и производные лигнина, такие как лигносульфонаты; малеиновую или янтарную кислоту или их ангидриды; олефинсульфонаты; фосфатные сложные эфиры, такие как фосфатные сложные эфиры спиртовых алкоксилатов, фосфатные сложные эфиры алкилфенольных алкоксилатов и фосфатные сложные эфиры стирилфенольных этоксилатов; поверхностно-активные вещества на основе белка; производные саркозина; сульфат стирилфенолового эфира; сульфаты и сульфонаты масла и жирных кислот; сульфаты и сульфонаты этоксилированных алкилфенолов; сульфаты спиртов; сульфаты этоксилированных спиртов; сульфонаты аминов и амидов, такие как N,N-алкилтаураты; сульфонаты бензола, кумола, толуола, ксилола и додецила, и тридецилбензолов; сульфонаты конденсированных нафталинов; сульфонаты нафталина и алкилнафталина; сульфонаты фракционированной нефти; сульфосукцинаматы и сульфосукцинаты и их производные, такие как диалкилсульфосукцинатные соли.
Используемые катионные поверхностно-активные вещества включают, но, не ограничиваясь ими: амиды и этоксилированные амиды; амины, такие как N-алкилпропандиамины, трипропилентриамины и дипропилентетрамины, и этоксилированные амины, этоксилированные диамины и пропоксилированные амины (полученные из аминов и этиленоксида, пропиленоксида, бутиленоксида или их смесей); аминные соли, такие как аминацетаты и диаминные соли; соли четвертичного аммония, такие как четвертичные соли, этоксилированные четвертичные соли и дичетвертичные соли; и аминоксиды, такие как алкилдиметиламиноксиды и бис-(2-гидроксиэтил)алкиламиноксиды.
Также используемыми для данных композиций являются смеси неионных и анионных поверхностно-активных веществ или смеси неионных и катионных поверхностно-активных веществ. Неионные, анионные и катионные поверхностно-активные вещества и их рекомендованные применения раскрыты в ряде опубликованных ссылочных материалов, включая McCutcheon's Emulsifiers and Detergents, ежегодный American and International Editions published by McCutcheon's Division, The Manufacturing Confectioner Publishing Co.; Sisely and Wood, Encyclopedia of Surface Active Agents, Chemical Publ. Co., Inc., New York, 1964; and A. S. Davidson and B. Milwidsky, Synthetic Detergents, Seventh Edition, John Wiley and Sons, New York, 1987.
Композиции настоящего изобретения также могут содержать вспомогательные вещества и добавки, известные специалистам данной области техники как вспомогательные средства состава (некоторые их которых можно считать функционирующими также в качестве твердых разбавителей, жидких разбавителей или поверхностно-активных веществ). Такие вспомогательные вещества и добавки могут контролировать: pH (буферы), вспенивание во время обработки (противовспениватели, такие как полиорганосилоксаны), осаждение активных ингредиентов (суспендирующие средства), вязкость (тиксотропные загустители), рост микробов в контейнере (противомикробные средства), замерзание продуктов (антифризы), цвет (красители/пигментные дисперсии), вымывание (пленкообразователи или связующие), выпаривание (замедлители выпаривания) и другие свойства состава. Пленкообразователи включают, например, поливинилацетаты, поливинилацетатные coполимеры, поливинилпирролидон-винилацетатный сополимер, поливиниловые спирты, coполимеры поливинилового спирта и воск. Примеры вспомогательных веществ и добавок включают перечисленные в McCutcheon's Volume 2: Functional Materials, ежегодный International and North American Editions published by McCutcheon's Division, The Manufacturing Confectioner Publishing Co.; и PCT публикации WO 03/024222.
Соединение формулы 1 и любые другие активные ингредиенты обычно включают в настоящие композиции путем растворения активного ингредиента в растворителе или путем диспергирования в жидком или сухом разбавителе. Растворы, включая эмульгируемые концентраты, могут быть получены простым смешиванием ингредиентов. Если растворитель жидкой композиции, предназначенной для применения в качестве эмульгируемого концентрата, не смешивается с водой, обычно добавляют эмульгатор для эмульгирования содержащего активный ингредиент растворителя при разбавлении водой. Суспензии активного ингредиента с диаметром частиц до 2000 мкм могут быть влажно измельчены с использованием мельницы для размола в среде, с получением частиц со средним диаметром менее 3 мкм. Водные суспензии могут быть превращены в готовые суспендированные концентраты (см., например, патент США 3060084) или затем обработаны сушкой распылением для образования диспергируемых в воде гранул. Для сухих составов обычно требуются процессы сухого размола, которые дают средний диаметр частиц в диапазоне от 2 до 10 мкм. Дусты и порошки могут быть получены путем смешивания и обычно измельчения (такого как молотковой мельницей или струйной мельницей). Гранулы и пеллеты могут быть получены распылением активного материала на предварительно гранулированные носители или техниками агломерации. См. Browning, “Agglomeration”, Chemical Engineering, December 4, 1967, стр. 147-48, Perry's Chemical Engineer's Handbook, 4-е изд., McGraw-Hill, New York, 1963, стр. 8-57 и следующие, и WO 91/13546. Пеллеты могут быть получены, как описано в патенте США 4172714. Диспергируемые в воде и растворимые в воде гранулы могут быть получены, как обсуждается в патенте США 4144050, патенте США 3920442 и патенте Германии 3246493. Таблетки могут быть получены, как обсуждается в патенте США 5180587, патенте США 5232701 и патенте США 5208030. Пленки могут быть получены, как обсуждается в патенте Великобритании 2095558 и патенте США 3299566.
Для дальнейшей информации об области составления композиций, см. T.S. Woods, “The Formulator's Toolbox-Product Forms for Modern Agriculture” в Pesticide Chemistry and Bioscience, The Food-Environment Challenge, T. Brooks and T. R. Roberts, Изд., Proceedings of the 9th International Congress on Pesticide Chemistry, The Royal Society of Chemistry, Cambridge, 1999, стр. 120-133. См. также патент США 3235361, кол. 6, строка 16-кол. 7, строка 19 и примеры 10-41; патент США 3309192, кол. 5, строка 43-кол. 7, строка 62 и примеры 8, 12, 15, 39, 41, 52, 53, 58, 132, 138-140, 162-164, 166, 167 и 169-182; патент США 2891855, кол. 3, строка 66-кол. 5, строка 17 и примеры 1-4; Klingman, Weed Control as a Science, John Wiley and Sons, Inc., New York, 1961, стр. 81-96; Hance et al., Weed Control Handbook, 8-е изд., Blackwell Scientific Publications, Oxford, 1989; и Developments in formulation technology, PJB Publications, Richmond, UK, 2000.
В следующих примерах все составы приготовлены традиционными путями. Номера соединений относятся к соединениям в таблицах индексов A-D. Без дальнейшего уточнения полагают, что специалист в данной области с использованием предыдущего описания может использовать настоящее изобретение в полной мере. Следующие примеры, следовательно, должны рассматриваться только как иллюстративные, а не ограничивающие настоящее изобретение каким-либо образом. Проценты являются массовыми, если не указано иное.
Пример A
Пример B
Пример C
Пример D
Пример E
Пример F
Пример G
Пример H
Соединения настоящего изобретения проявляют активность против широкого спектра паразитических вредителей. Такие вредители включают беспозвоночных, заселяющих разнообразную окружающую среду, такую как, например, листва растения, корни, почву, собранные сельскохозяйственные культуры или другие продукты питания, строительные конструкции или наружные покровы животного. Указанные вредители включают, например, беспозвоночных, питающихся листвой (включая листья, стебли, цветки и плоды), семенами, древесиной, текстильными волокнами или кровью или тканями животного, и, таким образом, вызывающих порчу или повреждение, например, выращиваемых или хранящихся агрономических сельскохозяйственных культур, лесов, тепличных сельскохозяйственных культур, декоративных растений, сельскохозяйственных культур в рассадниках, хранящихся продуктов питания или волоконных продуктов, или домов или других структур или их содержимого, или являющихся вредными для здоровья животного или общественного здравоохранения. Специалистам в данной области техники будет понятно, что все соединения равно эффективны против всех этапов роста всех вредителей.
Настоящие соединения и композиции, таким образом, могут быть полезны агрономически для защиты полевых сельскохозяйственных культур от паразитических нематод, а также неагрономически для защиты других садовых культур и растений от травоядных паразитических нематод. Такая полезность включает защиту сельскохозяйственных культур и других растений (т.е. как агрономическую, так и неагрономическую), которые содержат генетический материал, введенный генной инженерией (т.е. трансгенный) или модифицированный мутагенезом для обеспечения преимущественных признаков. Примеры таких признаков включают устойчивость к гербицидам, устойчивость к растительноядным вредителям (таким как насекомые, клещи, тля растительная, пауки, нематоды, улитки, фитопатогенные грибы, бактерии и вирусы), улучшенный рост растений, повышенную устойчивость к побочным условиям выращивания, таким как высокая или низкая температуры, высокая или низкая влажность почвы и высокая соленость, увеличенное цветение или плодоношение, большие выходы урожая, более быстрое созревание, более высокое качество и/или питательная ценность продукта собранного урожая, или улучшенное хранение или свойства обработки собранных продуктов. Трансгенные растения можно модифицировать для экспрессии многих признаков. Примеры растений, обладающих признаками, обеспеченными генной инженерией или мутагенезом, включают разновидности кукурузы, хлопка, сои и картофеля, экспрессирующие инсектицидный токсин Bacillus thuringiensis, такой как YIELD GARD®, KnockOut®, StarLink®, Bollgard®, NuCOTN® и NewLeaf®, и разновидности устойчивых к гербициду кукурузы, хлопка, сои и рапсовых семян, таких как Roundup Ready®, Liberty Link®, IMI®, STS® и Clearfield®, а также зерновые, экспрессирующие N-ацетилтрансферазу (GAT), для обеспечения устойчивости к гербициду глифосату, или зерновые, содержащие ген HRA, обеспечивающий устойчивость к гербицидам, ингибирующим ацетолактатсинтазу (ALS). Настоящие соединения и композиции могут взаимодействовать синергически с признаками, введенными генной инженерией или модифицированными мутагенезом, таким образом, усиливая фенотипическую экспрессию или эффективность признаков или увеличивая эффективность борьбы с паразитической нематодой настоящих соединений и композиций. В частности, настоящие соединения и композиции могут синергически взаимодействовать с фенотипической экспрессией белков или другими натуральными продуктами, токсическими для паразитических нематод, для обеспечения более чем дополнительного контроля над такими вредителями.
Композиции настоящего изобретения могут также необязательно содержать растительные питательные вещества, например, композицию удобрения, содержащую по меньшей мере одно растительное питательное вещество, выбранное из азота, фосфора, калия, серы, кальция, магния, железа, меди, бора, марганца, цинка и молибдена. Следует отметить композиции, содержащие по меньшей мере одну композицию удобрения, содержащую по меньшей мере одно растительное питательное вещество, выбранное из азота, фосфора, калия, серы, кальция и магния. Композиции настоящего изобретения, которые дополнительно содержат по меньшей мере одно растительное питательное вещество, могут быть в форме жидкостей или твердых веществ. Следует отметить твердые составы в форме гранул, небольших палочек или таблеток. Твердые составы, содержащие композицию удобрения, можно получить смешиванием соединения или композиции настоящего изобретения с композицией удобрения вместе с формулирующими ингредиентами и последующим получением состава способами, такими как грануляция или экструзия. Альтернативно, твердые составы можно получить распылением раствора или суспензии соединения или композиции настоящего изобретения в летучем растворителе на ранее полученную композицию удобрения в форме упорядоченно стабильных смесей, например, гранул, небольших палочек или таблеток, и последующим выпариванием растворителя.
Соединения настоящего изобретения могут проявлять активность против широкого спектра паразитических нематод, которые живут или растут внутри или питаются на растениях (например, листва, плод, стебли, корни или семена) или животных и людях (например, в сосудистых или дигестивных системах или других тканях), и, следовательно, причиняют вред выращиванию и сохраненным агрономическим зерновым культурам, лесничеству, зерновым в теплицах, декоративным растением и зерновым в рассадниках, или поражают состояние здоровья животного и человека. Сельскохозяйственными культурами, представляющими интерес, являются плодоносные овощи, такие как пасленовые и тыквенные сельскохозяйственные культуры, сельскохозяйственные культуры на плантациях, такие как банан и кофе, корнеплоды, такие как картофель, лук и морковь, и полевые культуры, такие как табак, земляной орех, хлопок, сахарный тростник и соя.
Соединения настоящего изобретения могут обладать активностью в отношении членов обоих классов Adenophorea и Secernentea из типа Nematoda, включая экономически важные члены подклассов Enoplida, Dorylaimida, Rhabditida, Strongylida, Ascarida, Oxyurida, Spirurida, Tylenchida и Aphelenchida, например, но, не ограничиваясь ими, экономически важные сельскохозяйственные вредители, такие как яванские галловые нематоды рода Meloidogyne, цистообразующие нематоды рода Heterodera и Globodera, приносящие вред нематоды рода Pratylenchus, почковидные нематоды рода Rotylenchulus, земляные нематоды рода Radopholus, жалящие нематоды рода Belonolaimus, спиральные нематоды рода Helicotylenchus и Scutellonema, цитрусовые нематоды рода Tylenchulus, нематоды, вызывающие тупоконечность корней рода Trichodorus и Paratrichodorus, кинжал-нематоды рода Xiphinema, нематоды, останавливающие рост рода Tylenchorhynchus, игольчатые нематоды рода Longidorus и Paralongidorus, копьеобразные нематоды рода Hoplolaimus, кольцевые нематоды семейства Criconematidae, стеблевые нематоды рода Ditylenchus и Anguina, и лиственные/стеблевые нематоды рода Aphelenchoides и Rhadinaphelenchus; и паразиты здоровья животного и человека (т.е. экономически важные круглые черви, такие как Strongylus vulgaris у лошадей, Toxocara canis у собак, Haemonchus contortus у овец, Dirofilaria immitis у собак и т.д.).
Следует отметить применение соединений настоящего изобретения для борьбы с южными нематодами, вызывающими тупоконечность корней (Meloidogyne incognita). Специалистам в данной области будет очевидно, что не все соединения равно эффективны относительно всех этапов роста всех нематод.
Соединения настоящего изобретения могут также обладать активностью в отношении членов Phylum Platyhelminthes, классов Cestoda (ленточные черви) и Trematoda (плоские черви), включая паразитов (т.е. экономически важные плоские черви и ленточные черви), причиняющих вред здоровью животного и человека (например, Anoplocephala perfoliata у лошадей, Fasciola hepatica у жвачных животных и т.д.).
Соединения настоящего изобретения могут быть также смешаны с одним или несколькими другими биологически активными соединениями или средствами, включая инсектициды, фунгициды, нематоциды, бактерициды, акарициды, гербициды, гербицидные сафенеры, регуляторы роста, такие как ингибиторы линьки насекомого и стимуляторы укоренения, химические стерилизаторы, химические сигнальные вещества, репелленты, аттрактанты, феромоны, стимуляторы подпитки, другие биологически активные соединения или энтомопатогенные бактерии, вирус или грибы для образования многокомпонентного пестицида, дающего даже более широкий спектр агрономической и неагрономической полезности. Таким образом, настоящее изобретение также относится к композиции, содержащей соединение формулы 1, его N-оксид или соль и эффективное количество по меньшей мере одного дополнительного биологически активного соединения или средства, и которая может дополнительно содержать по меньшей мере одно из поверхностно-активных веществ, твердых разбавителей или жидких разбавителей. Для смесей настоящего изобретения другие биологически активные соединения или средства могут быть сформулированы вместе с настоящими соединениями, включая соединения формулы 1, для образования заранее приготовленной смеси, или другие биологически активные соединения или средства могут быть сформулированы отдельно от настоящих соединений, включая соединения формулы 1, и два состава объединяют вместе перед нанесением (например, в распылительном баке) или, альтернативно, наносят последовательно.
Примерами таких биологически активных соединений или средств, с которыми сформулированы соединения настоящего изобретение, являются инсектициды, такие как абамектин, ацефат, ацеквиноцил, ацетамиприд, акринатрин, амидофлумет, амитраз, авермектин, азадирактин, азинфос-метил, бифентрин, бифеназат, бистрифлурон, борат, бупрофезин, кадусафос, карбарил, карбофуран, картап, карзол, хлорантранилипрол, хлорфенапир, хлорфлуазурон, хлорпирифос, хлорпирифос-метил, хромафенозид, клофентезин, клотианидин, циантранилипрол, цифлуметофен, цифлутрин, бета-цифлутрин, цигалотрин, гамма-цигалотрин, лямбда-цигалотрин, циперметрин, альфа-циперметрин, зета-циперметрин, циромазин, дельтаметрин, диафентиурон, диазинон, диелдрин, дифлубензурон, димефлутрин, димегипо, диметоат, динотефуран, диофенолан, эмамектин, эндосульфан, эсфенвалерат, этипрол, этофенпрокс, этоксазол, фенбутатин оксид, фенотиокарб, феноксикарб, фенпропатрин, фенвалерат, фипронил, флоникамид, флубендиамид, флуцитринат, флуфенерим, флуфеноксурон, флувалинат, тау-флувалинат, фонофос, форметанат, фостиазат, галофенозид, гексафлумурон, гекситиазокс, гидраметилнон, имидаклоприд, индоксакарб, инсектицидное мыло, изофенфос, луфенурон, малатион, метафлумизон, метальдегид, метамидофос, метидатион, метиодикарб, метомил, метопрен, метоксихлор, метофлутрин, монокротофос, метоксифенозид, нитенпирам, нитиазин, новалурон, новифлумурон, оксамил, паратион, паратион-метил, перметрин, форат, фозалон, фосмет, фосфамидон, пиримикарб, профенофос, профлутрин, пропаргит, протрифенбут, пиметрозин, пирафлупрол, пиретрин, пиридабен, пиридалил, пирифлуквиназон, пирипрол, пирипроксифен, ротенон, рианодин, спинеторам, спиносад, спиродиклофен, спиромезифен, спиротетрамат, сульпрофос, тебуфенозид, тебуфенпирад, тефлубензурон, тефлутрин, тербуфос, тетрахлорвинфос, тетраметрин, тиаклоприд, тиаметоксам, тиодикарб, тиосултапнатрий, толфенпирад, тралометрин, триазамат, трихлорфон, трифлумурон, дельта-эндотоксины Bacillus thuringiensis, энтомопатогенные бактерии, энтомопатогенные вирусы и энтомопатогенные грибы.
Следует отметить инсектициды, такие как абамектин, ацетамиприд, акринатрин, амитраз, авермектин, азадирактин, бифентрин, бупрофезин, кадусафос, карбарил, картап, хлорантранилипрол, хлорфенапир, хлорпирифос, клотианидин, циантранилипрол, цифлутрин, бета-цифлутрин, цигалотрин, гамма-цигалотрин, лямбда-цигалотрин, циперметрин, альфа-циперметрин, зета-циперметрин, циромазин, дельтаметрин, диелдрин, динотефуран, диофенолан, эмамектин, эндосульфан, эсфенвалерат, этипрол, этофенпрокс, этоксазол, фенотиокарб, феноксикарб, фенвалерат, фипронил, флоникамид, флубендиамид, флуфеноксурон, флувалинат, форметанат, фостиазат, гексафлумурон, гидраметилнон, имидаклоприд, индоксакарб, луфенурон, метафлумизон, метиодикарб, метомил, метопрен, метоксифенозид, нитенпирам, нитиазин, новалурон, оксамил, пиметрозин, пиретрин, пиридабен, пиридалил, пирипроксифен, рианодин, спинеторам, спиносад, спиродиклофен, спиромесифен, спиротетрамат, тебуфенозид, тетраметрин, тиаклоприд, тиаметоксам, тиодикарб, тиосултапнатрий, тралометрин, триазамат, трифлумурон, дельта-эндотоксины Bacillus thuringiensis, все штаммы вирусов Bacillus thuringiensis и все штаммы Nucleo polyhydrosis.
Один вариант осуществления биологических средств для смешивания с соединениями настоящего изобретения включают энтомопатогенные бактерии, такие как Bacillus thuringiensis, и инкапсулированные дельта-эндотоксины Bacillus thuringiensis, такие как MVP® и MVPII® биоинсектициды, полученные способом CellCap® (CellCap®, MVP® и MVPII® являются торговыми марками Mycogen Corporation, Indianapolis, Indiana, USA); энтомопатогенные грибы, такие как зеленые мускардиновые грибы; и энтомопатогенные (как встречающиеся в природе, так и генетически модифицированные) вирусы, включая бакуловирус, вирус ядерного полиэдроза (NPV), такой как Helicoverpa zea вирус ядерного полиэдроза (HzNPV), Anagrapha falcifera вирус ядерного полиэдроза (AfNPV); и вирус гранулеза (GV), такой как вирус гранулеза Cydia pomonella (CpGV).
Следует отметить такую комбинацию, где другой активный ингредиент для борьбы с беспозвоночными вредителями принадлежит к другому химическому классу или имеет другое место действия, в отличие от соединения формулы 1. В определенных случаях комбинация с по меньшей мере одним другим активным ингредиентом для борьбы с беспозвоночными вредителями, имеющим подобный спектр борьбы, но другое место действия, будет особенно предпочтительным для управления сопротивлением. Таким образом, композиция настоящего изобретения может дополнительно содержать по меньшей мере один дополнительный активный ингредиент для борьбы с беспозвоночными вредителями, имеющий подобный спектр борьбы, но принадлежащий другому химическому классу или имеющий другое место действия. Эти дополнительные биологически активные соединения или средства включают, но, не ограничиваясь ими, модуляторы натриевого канала, такие как бифентрин, циперметрин, цигалотрин, лямбда-цигалотрин, цифлутрин, бета-цифлутрин, дельтаметрин, димефлутрин, эсфенвалерат, фенвалерат, индоксакарб, метофлутрин, профлутрин, пиретрин и тралометрин; ингибиторы холинэстеразы, такие как хлорпирифос, метомил, оксамил, тиодикарб и триазамат; неоникотиноиды, такие как ацетамиприд, клотианидин, динотефуран, имидаклоприд, нитенпирам, нитиазин, тиаклоприд и тиаметоксам; инсектицидные макроциклические лактоны, такие как спинеторам, спиносад, абамектин, авермектин и эмамектин; антагонисты GABA (γ-аминомасляная кислота)-зависимого хлоридного канала, такие как авермектин, или блокаторы, такие как этипрол и фипронил; ингибиторы хитинового синтеза, такие как бупрофезин, циромазин, флуфеноксурон, гексафлумурон, луфенурон, новалурон, новифлумурон и трифлумурон; имитаторы ювенильного гормона, такие как диофенолан, феноксикарб, метопрен и пирипроксифен; лиганды октопаминового рецептора, такие как амитраз; ингибиторы линьки и агонисты экдизона, такие как азадирактин, метоксифенозид и тебуфенозид; лиганды рианодинового рецептора, такие как рианодин, антраниловые диамиды, такие как хлорантранилипрол, циантранилипрол и флубендиамид; аналоги нереистоксина, такие как картап; митохондриальные ингибиторы переноса электронов, такие как хлорфенапир, гидраметилнон и пиридабен; жидкие ингибиторы биосинтеза, такие как спиродиклофен и спиромезифен; циклодиеновые инсектициды, такие как диелдрин или эндосульфан; пиретроиды; карбаматы; инсектицидные мочевины; и биологические средства, включая вирусы ядерного полиэдроза (NPV), члены Bacillus thuringiensis, инкапсулированные дельта-эндотоксины Bacillus thuringiensis и другие, встречающиеся в природе или генетически модифицированные инсектицидные вирусы.
Дополнительными примерами биологически активных соединений или средств, с которыми соединения настоящего изобретения могут быть сформулированы, являются: фунгициды, такие как ацибензолар, алдиморф, амисульбром, азаконазол, азоксистробин, беналаксил, беномил, бентиаваликарб, бентиаваликарб-изопропил, биномиал, бифенил, битертанол, бластицидин-S, бордоская жидкость (трехосновный сульфат меди), боскалид/никобифен, бромуконазол, бупиримат, бутиобат, карбоксин, карпропамид, каптафол, каптан, карбендазим, хлорнеб, хлорталонил, хлозолинат, клотримазол, оксихлорид меди, соли меди, такие как сульфат меди и гидроксид меди, циазофамид, цифлунамид, цимоксанил, ципроконазол, ципродинил, дихлофлуанид, диклоцимет, дикломезин, диклоран, диэтофенкарб, дифеноконазол, диметоморф, димоксистробин, диниконазол, диниконазол-M, динокап, дискостробин, дитианон, додеморф, додин, эконазол, этаконазол, эдифенфос, эпоксиконазол, этабоксам, этиримол, этридиазол, фамоксадон, фенамидон, фенаримол, фенбуконазол, фенкарамид, фенфурам, фенгексамид, феноксанил, фенпиклонил, фенпропидин, фенпропиморф, фентинацетат, фентингидроксид, фербам, ферфуразоат, феримзон, флуазинам, флудиоксонил, флуметовер, флуопиколид, флуоксастробин, флуквинконазол, флуквинконазол, флусилазол, флусульфамид, флутоланил, флутриафол, фолпет, фозетил-алюминий, фуберидазол, фуралаксил, фураметапир, гексаконазол, гимексазол, гуазатин, имазалил, имибенконазол, иминоктадин, йодикарб, ипконазол, ипробенфос, ипродион, ипроваликарб, изоконазол, изопротиолан, казугамицин, крезоксим-метил, манкозеб, мандипропамид, манеб, мапанипирин, мефеноксам, мепронил, металаксил, метконазол, метасульфокарб, метирам, метоминостробин/феноминостробин, мепанипирим, метрафенон, миконазол, миклобутанил, нео-асозин (железистый метанарсонат), нуаримол, октилинон, офурас, оризастробин, оксадиксил, оксолиновая кислота, окспоконазол, оксикарбосин, паклобутразол, пенконазол, пенцикурон, пентиопирад, перфуразоат, фосфоновая кислота, фталид, пикобензамид, пикоксистробин, полиоксин, пробеназол, прохлораз, процимидон, пропамокарб, пропамокарб-гидрохлорид, пропиконазол, пропинеб, прохиназид, протиоконазол, пираклостробин, приазофос, пирифенокс, пириметанил, пирифенокс, пиролнитрин, пирохилон, хинконазол, хиноксифен, хинтозен, силтиофам, симеконазол, спироксамин, стрептомицин, сера, тебуконазол, текразин, теклофталам, текназен, тетраконазол, тиабендазол, тифлузамид, тиофанат, тиофанат-метил, тирам, тиадинил, толклофос-метил, толифлуанид, триадимефон, триадименол, триаримол, триазоксид, тридеморф, триморфамид трициклазол, трифлоксистробин, трифорин, тритиконазол, униконазол, валидамицин, винклозолин, зинеб, зирам и зоксамид; нематоциды, такие как алдикарб, имициафос, оксамил и фенамифос; бактерициды, такие как стрептомицин; акарициды, такие как амитраз, хинометионат, хлорбензилат, цигексатин, дикофол, диенохлор, этоксазол, феназахин, фенбутатина оксид, фенпропатрин, фенпироксимат, гекситиазокс, пропаргит, пиридабен и тебуфенпирад.
В определенных случаях комбинации соединения настоящего изобретения с другими биологически активными (в частности, контроль за беспозвоночными вредителями) соединениями или средствами (т.е. активные ингредиенты) могут привести к более чем добавочному (т.е. синергическому) эффекту. Уменьшение количества активных ингредиентов, высвобождаемых в окружающую среду, и при этом, гарантируя эффективный контроль за беспозвоночными вредителями, всегда является желательным. Когда возникает синергизм с активными ингредиентами для борьбы с беспозвоночными вредителями при нормах внесения, дающих агрономически удовлетворительные уровни борьбы с беспозвоночными вредителями, такие комбинации могут быть преимущественными для снижения стоимости растениеводства и уменьшения нагрузки от воздействия факторов окружающей среды.
Соединения настоящего изобретения и их композиции можно наносить на растения, генетически трансформированные для выражения токсичности белков для беспозвоночных вредителей (такие как дельта-эндотоксины Bacillus thuringiensis). Такое нанесение может обеспечить более широкий спектр защиты растений и может быть преимущественным для управления устойчивостью. Эффект экзогенно нанесенных соединений настоящего изобретения может быть синергическим с экспрессируемыми белками токсина.
Общие ссылки на такие сельскохозяйственные средства защиты (т.е. инсектициды, фунгициды, нематоциды, акарициды, гербициды и биологические средства) включают The Pesticide Manual, 13-е издание, C. D. S. Tomlin, Изд., British Crop Protection Council, Farnham, Surrey, U.K., 2003 и The BioPesticide Manual, 2-е издание, L. G. Copping, Изд., British Crop Protection Council, Farnham, Surrey, U.K., 2001.
Для вариантов осуществления, где используют один или несколько таких различных партнеров смешивания, массовое соотношение таких различных партнеров смешивания (всего) к соединению формулы 1 обычно составляет приблизительно от 1:3000 до приблизительно 3000:1. Следует отметить массовые соотношения приблизительно от 1:300 до приблизительно 300:1 (например, соотношения приблизительно от 1:30 до приблизительно 30:1). Специалист в данной области путем несложного эксперимента может легко определить биологически эффективное количество активных ингредиентов, необходимых для желаемого спектра биологической активности. Будет очевидно, что включая эти дополнительные компоненты можно расширить спектр контролируемых паразитических нематод помимо спектра, контролируемого исключительно соединением формулы 1.
В таблице A перечислены конкретные комбинации соединения формулы 1 с другими иллюстративными средствами для борьбы с беспозвоночными вредителями смесей, композиций и способов настоящего изобретения, и она включает дополнительные варианты осуществления диапазонов массового соотношения для нормы внесения удобрений. В первой колонке таблицы A приведены конкретные средства для борьбы с беспозвоночными вредителями (например, “абамектин” в первой линии). Во второй колонке таблицы A представлен способ действия (если известно) или химический класс средств для борьбы с беспозвоночными вредителями. В третьей колонке таблицы A представлен вариант(ы) осуществления диапазонов массовых соотношений для норм, при которых можно наносить средство для борьбы с беспозвоночными вредителями относительно соединения формулы 1 (например, “50:1-1:50” абамектина относительно соединения формулы 1 по массе). Таким образом, например, первая линия таблицы A, в частности, раскрывает комбинацию соединения формулы 1 с абамектином, которую можно наносить в массовом соотношении от 50:1 до 1:50. Остальные линии таблицы A составлены подобным образом.
Следует отметить композицию настоящего изобретения, где по меньшей мере одно дополнительное биологически активное соединение или средство выбрано из средств для борьбы с беспозвоночными вредителями, приведенных в таблице A выше.
Массовые соотношения соединения формулы 1, его N-оксида или соли с дополнительным средством для борьбы с беспозвоночными вредителями обычно составляют от 1000:1 до 1:1000, согласно одному варианту осуществления от 500:1 до 1:500, согласно другому варианту осуществления от 250:1 до 1:200 и согласно другому варианту осуществления от 100:1 до 1:50.
Изложенное ниже в таблицах B1-B14 является вариантами осуществления конкретных композиций, содержащих соединение формулы 1 (номера соединений (№ соед.) относительно соединений в таблицах индексов A-D) и дополнительное средство для борьбы с беспозвоночными вредителями.
Таблица B2
Таблица B2 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 19. Например, первая смесь в таблице B2 названа B2-1 и является смесью соединения 19 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B3
Таблица B3 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 30. Например, первая смесь в таблице B3 названа B3-1 и является смесью соединения 30 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B4
Таблица B4 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 68. Например, первая смесь в таблице B4 названа B4-1 и является смесью соединения 20 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B5
Таблица B5 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 170. Например, первая смесь в таблице B5 названа B5-1 и является смесью соединения 170 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B6
Таблица B6 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 179. Например, первая смесь в таблице B6 названа B6-1 и является смесью соединения 179 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B7
Таблица B7 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 180. Например, первая смесь в таблице B7 названа B7-1 и является смесью соединения 180 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B8
Таблица B8 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 356. Например, первая смесь в таблице B8 названа B8-1 и является смесью соединения 356 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B9
Таблица B9 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.” заменена ссылкой на соединение 357. Например, первая смесь в таблице B9 названа B9-1 и является смесью соединения 357 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B10
Таблица B10 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 382. Например, первая смесь в таблице B10 названа B10-1 и является смесью соединения 382 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B11
Таблица B11 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.” заменена ссылкой на соединение 413. Например, первая смесь в таблице B11 названа B11-1 и является смесью соединения 413 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B12
Таблица B12 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 465. Например, первая смесь в таблице B12 названа B12-1 и является смесью соединения 465 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B13
Таблица B13 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 474. Например, первая смесь в таблице B13 названа B13-1 и является смесью соединения 474 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Таблица B14
Таблица B14 идентична таблице B1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 394. Например, первая смесь в таблице B14 названа B14-1 и является смесью соединения 394 и дополнительного средства абамектин для борьбы с беспозвоночными вредителями.
Конкретные смеси, приведенные в таблице B1-B14, обычно комбинируют соединение формулы 1 с другим средством от беспозвоночных вредителей в соотношениях, уточненных в таблице A.
Изложенное ниже в таблицах C1-C14 является вариантами осуществления конкретных композиций, содержащих соединение формулы 1 (номера соединений (№ соед.) относительно соединений в таблицах индексов A-D) и дополнительный фунгицид.
Таблица C2
Таблица C2 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 19. Например, первая смесь в таблице C2 названа C2-1 и является смесью соединения 19 и дополнительного фунгицида пробеназола.
Таблица C3
Таблица C3 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 30. Например, первая смесь в таблице C3 названа C3-1 и является смесью соединения 30 и дополнительного фунгицида пробеназола.
Таблица C4
Таблица C4 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 68. Например, первая смесь в таблице C4 названа C4-1 и является смесью соединения 68 и дополнительного фунгицида пробеназола.
Таблица C5
Таблица C5 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 170. Например, первая смесь в таблице C5 названа C5-1 и является смесью соединения 170 и дополнительного фунгицида пробеназола.
Таблица C6
Таблица C6 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 179. Например, первая смесь в таблице C6 названа C6-1 и является смесью соединения 179 и дополнительного фунгицида пробеназола.
Таблица C7
Таблица C7 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 180. Например, первая смесь в таблице C7 названа C7-1 и является смесью соединения 180 и дополнительного фунгицида пробеназола.
Таблица C8
Таблица C8 идентична таблицей C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 356. Например, первая смесь в таблице C8 названа C8-1 и является смесью соединения 356 и дополнительного фунгицида пробеназола.
Таблица C9
Таблица C9 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 357. Например, первая смесь в таблице C9 названа C9-1 и является смесью соединения 357 и дополнительного фунгицида пробеназола.
Таблица C10
Таблица C10 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 382. Например, первая смесь в таблице C10 названа C10-1 и является смесью соединения 382 и дополнительного фунгицида пробеназола.
Таблица C11
Таблица C11 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 413. Например, первая смесь в таблице C11 названа C11-1 и является смесью соединения 413 и дополнительного фунгицида пробеназола.
Таблица C12
Таблица C12 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 465. Например, первая смесь в таблице C12 названа C12-1 и является смесью соединения 465 и дополнительного фунгицида пробеназола.
Таблица C13
Таблица C13 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 474. Например, первая смесь в таблице C13 названа C13-1 и является смесью соединения 474 и дополнительного фунгицида пробеназола.
Таблица C14
Таблица C14 идентична таблице C1, за исключением того, что каждая ссылка на соединение 7 в колонке, названной “№ соед.”, заменена ссылкой на соединение 394. Например, первая смесь в таблице C14 названа C14-1 и является смесью соединения 394 и дополнительного фунгицида пробеназола.
Борьбу с паразитическими нематодами при агрономических и неагрономических применениях осуществляют путем нанесения одного или более соединений настоящего изобретения, обычно в форме композиции, в биологически эффективном количестве в окружающую среду животных, включая агрономическое и/или неагоромическое местоположение инвазии, на защищаемую область или непосредственно на контролируемых вредителей.
Таким образом, настоящее изобретение включает способ борьбы с паразитической нематодой при агрономических и/или неагрономических применениях, включающий контакт паразитической нематоды или окружающей ее среды с биологически эффективным количеством одного или нескольких соединений настоящего изобретения или с композицией, содержащей по меньшей мере одно такое соединение или композицию, содержащую по меньшей мере одно такое соединение, и по меньшей мере одно дополнительное биологически активное соединение или средство. Примеры подходящих композиций, содержащих соединение настоящего изобретения и по меньшей мере одно дополнительное биологически активное соединение или средство, включают гранулярные композиции, где дополнительное активное соединение присутствует в той же грануле, что и соединение настоящего изобретения, или на гранулах, отдельных от гранул соединения настоящего изобретения.
Чтобы добиться контакта с соединением или композицией настоящего изобретения для защиты полевых культур от паразитических нематод, соединение или композицию обычно наносят на семена сельскохозяйственной культуры перед посевом, на лиственную часть (например, листья, стебли, цветки, плоды) сельскохозяйственных растений, или на почву или другую среду для выращивания перед или после посева сельскохозяйственной культуры.
Одним вариантом осуществления способа контакта является распыление. Альтернативно, гранулярную композицию, содержащую соединение по настоящему изобретению, можно наносить на лиственную часть растения или почву. Соединения по настоящему изобретению могут быть также эффективно доставлены путем поглощения растением при помощи контакта растения с композицией, содержащей соединение настоящего изобретения, нанесенной в форме жидкого состава для пропитки почвы, гранулярного состава на почву, путем обработки ящика с рассадой или глубины пересадок. Следует отметить композицию настоящего изобретения в форме жидкого состава для пропитки почвы. Также следует отметить способ борьбы с паразитической нематодой, включающий контакт паразитической нематоды или окружающей ее среды с биологически эффективным количеством соединения настоящего изобретения или с композицией, содержащей биологически эффективное количество соединения настоящего изобретения. Кроме того, следует отметить настоящий способ, где окружающей средой является почва, и композицию наносят на почву в форме состава для пропитки почвы. Дополнительно следует отметить, что соединения настоящего изобретения также эффективны при локальном нанесении на расположение инвазии. Другие способы контакта включают нанесение соединения или композиции настоящего изобретения распрыскиваемыми растворами непосредственного действия и с последействием, воздушно распыляемыми растворами, гелями, покрытиями семян, микрокапсуляцией, системным потреблением, протравкой, через ушные бирки, болюсами, увлажнителями, фумигантами, аэрозолями, дустами и многими другими. Один вариант осуществления способа контакта включает упорядоченно стабильную гранулу удобрения, палочку или таблетку, содержащие соединение или композицию настоящего изобретения. Соединениями настоящего изобретение также могут быть пропитаны материалы для изготовления устройства для борьбы с беспозвоночными (например, ловля насекомых).
Соединения настоящего изобретения также полезны при обработке семян для защиты семян от паразитических нематод. В контексте настоящего описания и формулы изобретения обработка семян означает контакт семян с биологически эффективным количеством соединения настоящего изобретения, которое обычно составлено в композицию настоящего изобретения. Такая обработка семян защищают семена от беспозвоночных почвенных вредителей и обычно может также защитить корни и другие растительные части, соприкасающиеся с почвой, рассаду, развивающуюся из прорастающих семян. Обработка семян может также обеспечивать защиту лиственной части транслокацией соединения настоящего изобретения или второго активного ингредиента в течение развития растения. Обработку семян можно применять ко всем типам семян, включая такие, из которых растения, генетически трансформированные с экспрессией специализированных признаков, будут произрастать. Иллюстративные примеры генетически трансформированных растений включают такие, которые экспрессируют белки, токсические для паразитических нематод, такие как токсин Bacillus thuringiensis, или такие, которые экспрессируют устойчивость к гербициду, как глифосатацетилтрансфераза, которые обеспечивают устойчивость к глифосату.
Один способ обработки семян представляет собой распыление или опыливание семян соединением настоящего изобретения (т.е. в виде составленной композиции) перед высеванием семян. Композиции, составленные для обработки семян, обычно содержат пленкообразователь или адгезивное средство. Следовательно, как правило, покрывающая семена композиция настоящего изобретения содержит биологически эффективное количество соединения формулы 1, его N-оксида или соли и пленкообразователь или адгезивное средство. Семена могут быть покрыты распылением жидкого суспендированного концентрата прямо на слой семян во вращающемся барабане и последующей сушкой семян. Альтернативно, на семена могут быть распылены другие типы состава, такие как смачиваемые порошки, растворы, суспоэмульсии, эмульгируемые концентраты и эмульсии в воде. Этот процесс, в частности, может быть использован для нанесения пленочных покрытий на семена. Различные машины для нанесения покрытий и способы доступны специалисту в данной области техники. Подходящие способы включают описанные P. Kosters et al., в Seed Treatment: Progress and Prospects, 1994 BCPC Mongraph No. 57, и приведенных там ссылках.
Обработанные семена обычно содержат соединение настоящего изобретения в количестве приблизительно от 0,1 г до 1 кг на 100 кг семян (т.е. приблизительно от 0,0001 до 1% по массе семян перед обработкой). Жидкая суспензия, сформулированная для обработки семян, обычно содержит приблизительно от 0,5 до приблизительно 70% активного ингредиента, приблизительно от 0,5 до приблизительно 30% пленкообразующего адгезива, приблизительно от 0,5 до приблизительно 20% диспергируемого средства, от 0 до приблизительно 5% загустителя, от 0 до приблизительно 5% пигмента и/или красителя, от 0 до приблизительно 2% противовспенивающего средства, от 0 до приблизительно 1% консерванта и от 0 до приблизительно 75% летучего жидкого разбавителя.
Для агрономических применений, норма нанесения, необходимая для эффективной борьбы (т.е. “биологически эффективное количество”), будет зависеть от таких факторов, как виды контролируемых нематод, цикл жизни нематоды, стадии жизни, ее размер, местоположение, время года, растение-хозяин или животное, пищевое поведение, брачное поведение, окружающая влага, температура и т.п. При нормальных обстоятельствах, нормы нанесения приблизительно от 0,01 до 2 кг активных ингредиентов на гектар являются достаточными для борьбы с нематодами в агрономических экосистемах, но только 0,0001 кг/гектар может быть достаточной или до 8 кг/гектар может требоваться. Для неагрономических применений, эффективные нормы применения будут составлять диапазон приблизительно от 1,0 до 50 мг/квадратный метр, но только 0,1 мг/квадратный метр может быть достаточной или до 150 мг/квадратный метр может требоваться. Специалист в данной области может легко определить биологически эффективное количество, необходимое для желаемого уровня борьбы с паразитической нематодой.
Соединения по настоящему изобретению, полученные способами, описанными в данном описании, показаны в таблицах индексов A-E. Для масс-спектрометрических данных числовое значение, сообщенное в колонке “AP+ (M+1)”, является молекулярной массой наблюдаемого молекулярного иона, образованного добавлением H+ (молекулярная масса 1) к молекуле, имеющей самый большой изотопный избыток (т.е. M); числовое значение, сообщенное в колонке “AP- (M-1)”, является молекулярной массой наблюдаемого молекулярного иона, образованного при потере H+ (молекулярная масса 1) от молекулы, имеющей самый большой изотопный избыток (т.е. M). Присутствие молекулярных ионов, содержащих один или несколько изотопов с более высокой атомной массой более низкого избытка (например, 37Cl, 81Br), не сообщено. Сообщенные пики M+1 и M-1 наблюдали при помощи масс-спектрометрии, применяя химическую ионизацию при атмосферном давлении (AP+).
В таблицах индексов использовали следующие аббревиатуры: "Соед." означает соединение. Переменные “R” и “(R1)n” представляют собой один или комбинацию заместителей, как представлено в таблицах индексов. Аббревиатура “прим.” означает “пример” и сопровождается цифрой, указывающей в каком примере синтеза получено соединение.
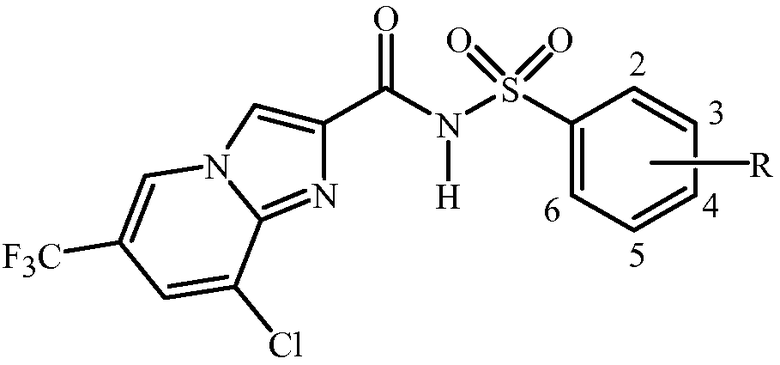
(M+1)
(M-1)
(прим. 1)
(прим. 2)
** “-” означает, что R представляет собой H (т.е. фенильное кольцо незамещено)
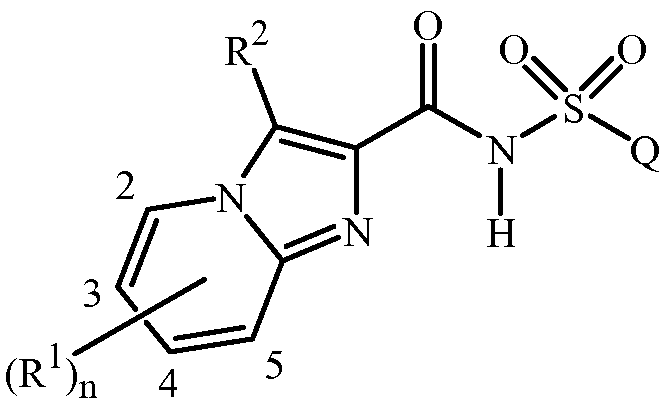
R
2
представляет собой H
(M+1)
(M-1)
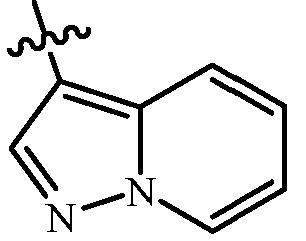
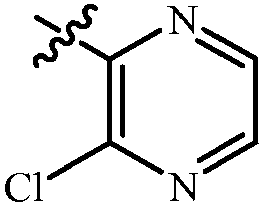






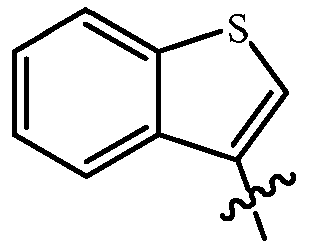



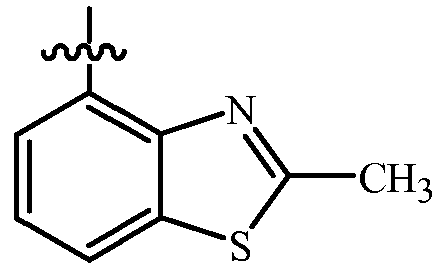

(M+1)
(M-1)




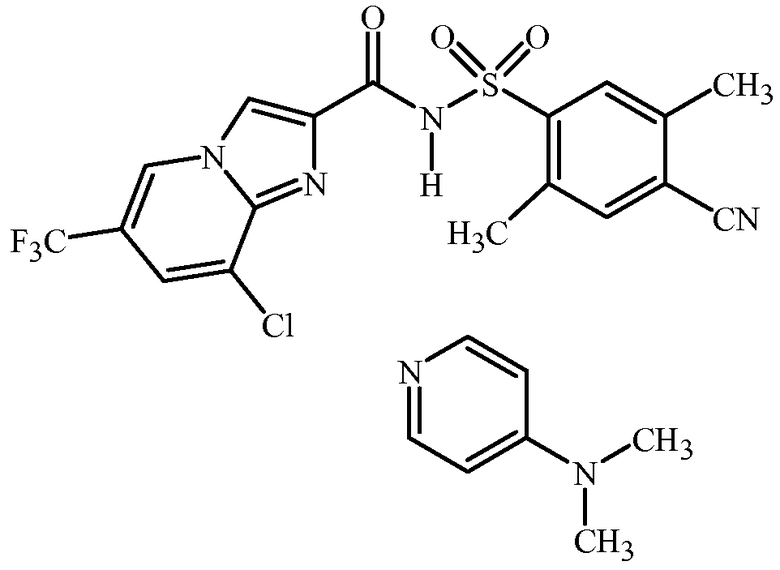
В следующих тестах показана эффективность борьбы соединений настоящего изобретения со специфическими вредителями. “Эффективность борьбы” представляет ингибирование развития паразитической нематоды (включая смертность), что вызывает существенно сниженную подпитку. Однако защита при борьбе с вредителями, предоставляемая соединениями, не ограничена этими образцами.
Биологические примеры настоящего изобретения
Тест A
Борьбу с южной галловой нематодой (Meloidogyne incognita) путем контакта и/или системными средствами оценивали на испытательных стендах, состоящих из небольших открытых контейнеров, заполненных смесью песчаной почвы и сеянцами огурца.
Тестируемые соединения составляли в композицию, используя раствор, содержащий 50% ацетона и 50% воды. Тестируемые соединения наносили непосредственно на почву испытательных стендов при концентрациях активного ингредиента 250 или 50 частей на миллион. Каждый тест повторяли 3 раза. После обработки испытательные стенды сушили в течение 1 часа, затем приблизительно 250 ювенильных (J2) личинок второй стадии капали из пипетки в почву. Испытательные стенды выдерживали при 27°C и смачивали при необходимости 7 дней.
Нематоцидную эффективность определяли по количеству образования корневого галла, наблюдаемому по сравнению с необработанным контролем. Отсутствие образования галла оценивалось как 100% эффективность при борьбе с нематодой. Образование галла эквивалентно найденному в необработанном контроле оценивалось как 0% эффективность при борьбе с нематодой. Не была дана оценка борьбы с нематодой соединениям, проявляющим существенную фитотоксичность.
Из соединений, исследованных при концентрации 250 частей на миллион, следующие обеспечили хороший уровень защиты растения (50% или более уменьшение образования корневого галла по сравнению с контролями, обработанными растворителями) и не проявляли существенной фитотоксичности: 4, 5, 6, 7, 9, 10, 11, 12, 13, 17, 19, 24, 25, 28, 29, 30, 32, 34, 38, 57, 59, 63, 65, 66, 67, 68, 69, 70, 71, 72, 73, 75, 83, 89, 90, 93, 101, 106, 107, 108, 109, 110, 111, 112, 113, 114, 116, 117, 120, 126, 130, 131, 132, 133, 134, 136, 137, 139, 140, 143, 145, 149, 152, 157, 159, 162, 163, 167, 169, 170, 171, 172, 174, 175, 176, 179, 180, 181, 184, 186, 188, 193, 206, 241, 244, 245, 248, 251, 252, 253, 257, 258, 259, 272, 274, 279, 285, 292, 294, 297, 298, 299, 301, 313, 314, 315, 317, 318, 319, 323, 329, 331, 332, 333, 334, 340, 341, 342, 344, 345, 347, 348, 355, 359, 360, 361, 364, 365, 366, 367, 371, 372, 373, 375, 377, 378, 379, 380, 381, 382, 383, 384, 385, 386, 387, 388, 393, 394, 395, 396, 397, 402, 403, 404, 405, 406, 407, 408, 409, 410, 411, 412, 413, 414, 415, 417, 418, 419, 420, 421, 422, 424, 425, 426, 427, 429, 430, 436, 439, 441, 442, 443, 444, 445, 449, 450, 451, 458, 459, 460, 461, 462, 464, 465, 466, 467, 468, 469, 470, 471, 472, 474, 475, 476, 477, 478 и 479.
Из соединений, исследованных при концентрации 50 частей на миллион, следующие обеспечили хороший уровень защиты растения (50% или более уменьшение образования корневого галла по сравнению с контролями, обработанными растворителями) и не проявляли существенной фитотоксичности: 2, 4, 7, 9, 10, 11, 13, 19, 30, 59, 63, 66, 67, 68, 69, 71, 73, 86, 90, 94, 101, 103, 105, 107, 108, 109, 110, 111, 113, 114, 116, 117, 130, 132, 133, 137, 139, 140, 143, 149, 151, 157, 162, 163, 167, 170, 175, 176, 179, 180, 241, 245, 248, 251, 252, 258, 259, 268, 272, 274, 279, 292, 297, 298, 314, 315, 316, 317, 318, 319, 329, 331, 332, 337, 341, 342, 343, 348, 356, 357, 359, 366, 367, 371, 372, 373, 377, 378, 379, 380, 381, 382, 383, 384, 386, 388, 394, 395, 396, 397, 401, 402, 403, 405, 406, 407, 408, 410, 411, 413, 414, 415, 416, 419, 420, 424, 427, 428, 429, 430, 431, 436, 439, 441, 442, 443, 444, 445, 449, 451, 458, 459, 460, 462, 465, 466, 467, 469, 470, 471, 474, 475, 477, 478 и 479.
Изобретение относится к соединениям формулы 1:

где Z представляет собой O или S и R1, R2, R3, Q и n являются такими, как определено в описании, их N-оксидам, солям и содержащим их композициям. Осуществляют борьбу с паразитической нематодой путем контактирования нематоды или окружающей ее среды с биологически эффективным количеством соединения или композиции. Изобретение позволяет повысить эффективность борьбы с паразитическими нематодами. 4 н. и 10 з.п. ф-лы.
1. Соединение формулы 1:
 ,
,
где
Z представляет собой О или S;
каждый R1 независимо представляет собой галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, С1-С6алкил, С1-С6галогеналкил, C2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7, OC(O)OR8, OC(O)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)С(О)R7, N(R10)С(О)NR11R12, N(R10)S(O)2R9 или N(R10)S(O)2NR11R12; или С3-С7циклоалкил, C4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, C1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, C2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
R2 представляет собой H, галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, C2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, ОС(О)OR8, ОС(О)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)С(О)R7, N(R10)С(О)NR11R12, N(R10)S(О)2R9 или N(R10)S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил C6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, ОС(O)R7a и N(R10)С(О)R7a;
R3 представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-С7циклоалкил, С4-С8циклоалкилалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или С1-С6алкил, замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из фенила или 5- или 6-членного гетероароматического кольца, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, С(О)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)С(О)R7a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
Q представляет собой фенил, нафталинил, 5- или 6-членное гетероароматическое кольцо или 8-10-членную гетероароматическую бициклическую кольцевую систему, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, C1-С6алкила, С1-С6галогеналкила, С2-С6алкенила, С2-С6галогеналкенила, С2-С6алкинила, С2-С6галогеналкинила, C(X)R7, С(О)OR8, C(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, OC(O)OR8, ОС(O)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)C(O)R7, N(R10)С(О)NR11R12, N(R10)S(O)2R9, N(R10)S(O)2NR11R12 и R14;
каждый X независимо представляет собой О или S;
каждый R4 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкил, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R4a независимо представляет собой H, С1-С6алкил или C1-С6 галогеналкил;
каждый R5 независимо представляет собой Н, NR5aR6a, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, С(О)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R5a независимо представляет собой H или С1-С6алкил;
каждый R6 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4 галогеналкила, OR4a и S(O)mR9a;
каждый R6a независимо представляет собой Н, С1-С6алкил, C(O)R13 или С(О)OR13;
каждый R7 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R7a независимо представляет собой С1-С6алкил или C1-С6галогеналкил;
каждый R8 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R8a независимо представляет собой С1-С6алкил или С1-С6галогеналкил;
каждый R9 независимо представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(О)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R9a независимо представляет собой С1-С6алкил или C1-С6галогеналкил;
каждый R10 независимо представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12;
каждый R10a независимо представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил;
каждый R11 независимо представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, C(O)NR11aR12, S(O)mR9a или S(О)2NR11aR12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11aR12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(O)2NR11aR12, NR5aR6a, OC(O)R7a и N(R10a)С(О)R7a;
каждый R11a независимо представляет собой Н, С1-С6алкил, С2-С6алкенил или С2-С6алкинил;
каждый R12 независимо представляет собой Н, NR5aR6a, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4 галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенил, С2-С4алкинила, C1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R13 независимо представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, C6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4алогеналкила, OR4a и S(O)mR9a;
каждый R14 независимо представляет собой С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(О)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, C1-С4алкила, С2-С4алкенила, C2-С4алкинила, C1-C4гaлoгeнaлкилa, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)С(О)R7a;
каждый R15 независимо представляет собой C1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, C1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, ОС(О)R7a и N(R10)С(О)R7a;
каждый m независимо равен 0, 1 или 2; и
n равно 0, 1, 2, 3 или 4;
при условии, когда n равно 2, и один R1 представляет собой CF3 в положении 3 формулы 1, а другой R1 представляет собой Сl в положении 5 формулы 1, и R2 и R3 представляют собой Н, тогда Q является другим, чем 2-хлорфенил, 2-хлор-6-метилфенил, 2,6-дихлорфенил, 2-хлор-4-фторфенил, 2,5-бис(2,2,2-трифторэтокси)фенил, 2,4,6-трихлорфенил, 2-хлор-5-(трифторметил)фенил или 3,5-диметил-4-изоксазолил,
его N-оксид или соль.
2. Соединение по п.1, где
Z представляет собой О; и
Q представляет собой фенил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4 галогеналкила, С2-С4 галогеналкенила, C2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)C(O)R7a.
3. Соединение по п.2, где
Q представляет собой фенил, пиридил, пиразолил, оксазолил, тиазолил, изоксазолил, изотиазолил, фуранил или тиенил, каждый необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, C1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(X)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)С(О)R7a.
4. Соединение по п.2 или 3, где
каждый R1 независимо представляет собой галоген, циано, нитро, OR4, С1-С6алкил или C1-С6галогеналкил;
R2 представляет собой Н, галоген или С1-С6алкил;
R3 представляет собой Н, С1-С6алкил, С1-С6галогеналкил, C(X)R7, C(O)OR8 или S(O)mR9; или С1-С6алкил, замещенный 1 или 2 OR4; и
n равно 1 или 2.
5. Соединение по п.1, которое выбирают из группы, состоящей из:
8-хлор-N-[(2-хлор-5-метоксифенил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
8-хлор-N-[(4-циано-2,5-диметилфенил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
N-[(5-ацетил-2-хлорфенил)сульфонил]-8-хлор-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
8-хлор-N-[(3-метил-2-тиенил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
8-хлор-N-[(4-метил-2-тиенил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
8-хлор-N-[(3-хлор-1-метил-1H-пиразол-4-ил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
8-хлор-N-[(5-метокси-2-нитрофенил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида;
8-хлор-N-[(2-хлор-5-этилфенил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
8-хлор-N-[(1-этил-3-метил-1H-пиразол-4-ил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
8-бpoм-N-[(2-хлор-5-метоксифенил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
N-[(2-бром-5-метилфенил)сульфонил]-8-хлор-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
8-хлор-N-[(2-хлор-5-метилфенил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида,
8-хлор-N-[(3-хлор-1-этил-1H-пиразол-4-ил)сульфонил]-6-(трифторметил)имидазо[1,2-а]пиридин-2-карбоксамида и
N-[(5-ацетил-2-метилфенил)сульфонил]-8-хлор-6-(трифторметил)имидазо[1,2-а] пиридин-2-карбоксамида.
6. Композиция для борьбы с паразитическими нематодами, содержащая соединение формулы 1:
 ,
,
где
Z представляет собой О или S;
каждый R1 независимо представляет собой галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, C1-С6алкил, С1-С6галогеналкил; C2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7, ОС(О)OR8, OC(O)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)С(О)R7, N(R10)С(О)NR11R12, N(R10)S(O)2R9 или N(R10)S(О)2NR11R12; или С3-С7циклоалкил, C4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкила, замещенного 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, C2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, С(О)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
R2 представляет собой H, галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, ОС(О)OR8, ОС(О)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)С(О)R7, N(R10)С(О)NR11R12, N(R10)S(О)2R9 или N(R10)S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил C6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, C1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)С(О)R7a;
R3 представляет собой H, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 или S(O)2NR11R12; или C3-С7циклоалкил, С4-С8циклоалкилалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(О)2NR11R12; или C1-С6алкил, замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из фенила или 5- или 6-членного гетероароматического кольца, каждое необязательно замещенное 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, C1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)С(О)R7a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
Q представляет собой фенил, нафталинил, 5- или 6-членное гетероароматическое кольцо или 8-10-членную гетероароматическую бициклическую кольцевую систему, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, C1-С6алкила, С1-С6галогеналкила, С2-С6алкенила, С2-С6галогеналкенила, С2-С6алкинила, С2-С6галогеналкинила, C(X)R7, С(О)OR8, C(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, OC(O)OR8, ОС(О)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)C(O)R7, N(R10)С(О)NR11R12, N(R10)S(О)2R9, N(R10)S(O)2NR11R12 и R14;
каждый X независимо представляет собой О или S;
каждый R4 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, С(O)NR11R12, S(O)mR9a или S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R4a независимо представляет собой H, С1-С6алкил или С1-С6галогеналкил;
каждый R5 независимо представляет собой Н, NR5aR6a, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, С(О)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, C2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R5a независимо представляет собой H или C1-С6алкил;
каждый R6 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a;
каждый R6a независимо представляет собой Н, С1-С6алкил, C(O)R13 или С(О)OR13;
каждый R7 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R7a независимо представляет собой С1-С6алкил или С1-С6галогеналкил;
каждый R8 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(О)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R8a независимо представляет собой С1-С6алкил или C1-С6галогеналкил;
каждый R9 независимо представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, C6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R9a независимо представляет собой С1-С6алкил или С1-С6галогеналкил;
каждый R10 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12;
каждый R10a независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил;
каждый R11 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, C(O)NR11aR12, S(O)mR9a или S(О)2NR11aR12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11aR12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(O)2NR11aR12, NR5aR6a, OC(O)R7a и N(R10a)С(О)R7a;
каждый R11a независимо представляет собой Н, С1-С6алкил, С2-С6алкенил или С2-С6алкинил;
каждый R12 независимо представляет собой Н, NR5aR6a, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R13 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a;
каждый R14 независимо представляет собой С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, C1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенил, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)С(О)R7a;
каждый R15 независимо представляет собой С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, C1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, ОС(О)R7a и N(R10)С(О)R7a;
каждый m независимо равен 0, 1 или 2; и
n равно 0, 1, 2, 3 или 4,
его N-оксид или соль
и по меньшей мере один дополнительный компонент, выбранный из группы, состоящей из поверхностно-активных веществ, твердых разбавителей и жидких разбавителей.
7. Композиция по п.6, где указанная композиция дополнительно содержит по меньшей мере одно дополнительное биологически активное соединение или средство.
8. Композиция по п.7, где по меньшей мере одно дополнительное биологически активное соединение или средство выбирают из группы, состоящей из абамектина, ацефата, ацеквиноцила, ацетамиприда, акринатрина, амидофлумета, амитраза, авермектина, азадирахтина, азинфос-метила, бифентрина, бифеназата, бистрифлурона, бората, бупрофезина, карбарила, карбофурана, картапа, карзола, хлорантранилипрола, хлорфенапира, хлорфлуазурона, хлорпирифоса, хлорпирифос-метила, хромафенозида, клофентезина, клотианидина, циантранилипрола, цифлуметофена, цифлутрина, бета-цифлутрина, цигалотрина, гамма-цигалотрина, лямбда-цигалотрина, циперметрина, альфа-циперметрина, зета-циперметрина, циромазина, дельтаметрина, диафентиурона, диазинона, диелдрина, дифлубензурона, димефлутрина, димегипоа, диметоата, динотефурана, диофенолана, эмамектина, эндосульфана, эсфенвалерата, этипрола, этофенпрокса, этоксазола, фенбутатина оксида, фенотиокарба, феноксикарба, фенпропатрина, фенвалерата, фипронила, флоникамида, флубендиамида, флуцитрината, флуфенерима, флуфеноксурона, флувалината, тау-флувалината, фонофоса, форметаната, фостиазата, галофенозида, гексафлумурона, гекситиазокса, гидраметилнона, имидаклоприда, индоксакарба, инсектицидного мыла, изофенфоса, луфенурона, малатиона, метафлумизона, метальдегида, метамидофоса, метидатиона, метиодикарба, метомила, метопрена, метоксихлора, метофлутрина, монокротофоса, метоксифенозида, нитенпирама, нитиазина, новалурона, новифлумурона, оксамила, паратиона, паратион-метила, перметрина, фората, фозалона, фосмета, фосфамидона, пиримикарба, профенофоса, профлутрина, пропаргита, протрифенбута, пиметрозина, пирафлупрола, пиретрина, пиридабена, пиридалила, пирифлуквиназона, пирипрола, пирипроксифена, ротенона, рианодина, спинеторама, спиносада, спиродиклофена, спиромезифена, спиротетрамата, сульпрофоса, тебуфенозида, тебуфенпирада, тефлубензурона, тефлутрина, тербуфоса, тетрахлорвинфоса, тетраметрина, тиаклоприда, тиаметоксама, тиодикарба, тиосултап-натрия, толфенпирада, тралометрина, триазамата, трихлорфона, трифлумурона, всех штаммов Bacillus thuringiensis, энтомопатогенных бактерий, всех штаммов вирусов Nucleo polyhydrosis, энтомопатогенных вирусов и энтомопатогенных грибов.
9. Композиция по п.8, где по меньшей мере одно дополнительное биологически активное соединение или средство выбирают из группы, состоящей из абамектина, ацетамиприда, акринатрина, амитраза, авермектина, азадирахтина, бифентрина, бупрофезина, карбарила, картапа, хлорантранилипрола, хлорфенапира, хлорпирифоса, клотианидина, циантранилипрола, цифлутрина, бета-цифлутрина, цигалотрина, лямбда-цигалотрина, гамма-цигалотрина, циперметрина, альфа-циперметрина, зета-циперметрина, циромазина, дельтаметрина, диелдрина, динотефурана, диофенолана, эмамектина, эндосульфана, эсфенвалерата, этипрола, этофенпрокса, этоксазола, фенотиокарба, феноксикарба, фенвалерата, фипронила, флоникамида, флубендиамида, флуфеноксурона, флувалината, форметаната, гексафлумурона, гидраметилнона, имидаклоприда, индоксакарба, луфенурона, метафлумизона, метиодикарба, метомила, метопрена, метоксифенозида, нитенпирама, нитиазина, новалурона, оксамила, пиметрозина, пиретрина, пиридабена, пиридалила, пирипроксифена, рианодина, спинеторама, спиносада, спиродиклофена, спиромезифена, спиротетрамата, тебуфенозида, тетраметрина, тиаклоприда, тиаметоксама, тиодикарба, тиосултап-натрия, тралометрина, триазамата, трифлумурона, всех штаммов Bacillus thuringiensis и всех штаммов вирусов Nucleo polyhydrosis.
10. Способ борьбы с паразитической нематодой, включающий контакт паразитической нематоды или окружающей ее среды с биологически эффективным количеством соединения формулы 1:
 ,
,
где
Z представляет собой О или S;
каждый R1 независимо представляет собой галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7, ОС(О)OR8, OC(O)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)С(О)R7, N(R10)С(О)NR11R12, N(R10)S(O)2R9 или N(R10)S(O)2NR11R12; или С3-С7циклоалкил, C4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, С(О)NR11R12, S(O)mR9 и S(О)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
R2 представляет собой H, галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, C1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, C2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, OC(O)OR8, ОС(О)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)С(О)R7, N(R10)С(О)NR11R12, N(R10)S(O)2R9 или N(R10)S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)С(О)R7a;
R3 представляет собой H, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или C1-С6алкил, замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из фенила или 5- или 6-членного гетероароматического кольца, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)С(О)R7a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
Q представляет собой фенил, нафталинил, 5- или 6-членное гетероароматическое кольцо или 8-10-членную гетероароматическую бициклическую кольцевую систему, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, C1-С6алкила, С1-С6галогеналкила, С2-С6алкенила, С2-С6галогеналкенила, С2-С6алкинила, С2-С6галогеналкинила, C(X)R7, С(О)OR8, C(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, OC(O)OR8, ОС(О)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)C(O)R7, N(R10)С(O)NR11R12, N(R10)S(O)2R9, N(R10)S(O)2NR11R12 и R14;
каждый X независимо представляет собой О или S;
каждый R4 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R4a независимо представляет собой H, С1-С6алкил или C1-С6галогеналкил;
каждый R5 независимо представляет собой Н, NR5aR6a, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, С(О)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R5a независимо представляет собой H или С1-С6алкил;
каждый R6 независимо представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a;
каждый R6a независимо представляет собой Н, С1-С6алкил, C(O)R13 или С(О)OR13;
каждый R7 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R7a независимо представляет собой С1-С6алкил или С1-С6галогеналкил;
каждый R8 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R8a независимо представляет собой С1-С6алкил или С1-С6галогеналкил;
каждый R9 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(О)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R9a независимо представляет собой С1-С6алкил или С1-С6галогеналкил;
каждый R10 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12,
каждый R10a независимо представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил;
каждый R11 независимо представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, C(O)NR11aR12, S(O)mR9a или S(О)2NR11aR12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, С(O)NR11aR12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(O)2NR11aR12, NR5aR6a, OC(O)R7a и N(R10a)С(О)R7a;
каждый R11a независимо представляет собой Н, С1-С6алкил, С2-С6алкенил или С2-С6алкинил;
каждый R12 независимо представляет собой Н, NR5aR6a, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R13 независимо представляет собой H, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a;
каждый R14 независимо представляет собой С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, C1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, C1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)С(О)R7a;
каждый R15 независимо представляет собой C1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, C4-С8циклоалкилалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, C1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, ОС(О)R7a и N(R10)С(О)R7a;
каждый m независимо равен 0, 1 или 2; и
n равно 0, 1, 2, 3 или 4,
его N-оксида или соли.
11. Способ по п.10, где окружающей средой является растение.
12. Способ по п.10, где окружающей средой являются семена.
13. Способ по п.12, где семена покрывают соединением формулы 1, его N-оксидом или солью, составленным в композицию, содержащую пленкообразователь или адгезивное средство.
14. Обработанные семена, содержащие соединение формулы 1:
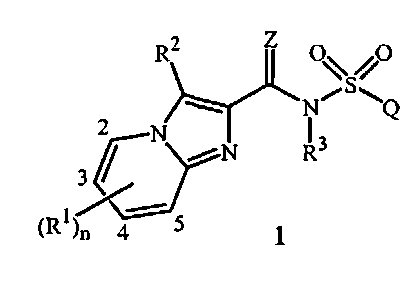 ,
,
где
Z представляет собой О или S;
каждый R1 независимо представляет собой галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7, OC(O)OR8, OC(O)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)С(О)R7, N(R10)С(O)NR11R12, N(R10)S(O)2R9 или N(R10)S(О)2NR11R12; или С3-С7циклоалкил, C4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
R2 представляет собой H, галоген, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, C2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, OC(O)OR8, ОС(О)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)С(О)R7, N(R10)С(О)NR11R12, N(R10)S(О)2R9 или N(R10)S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил C6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(О)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, C1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, ОС(О)R7a и N(R10)С(О)R7a;
R3 представляет собой Н, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, C(O)OR8, С(О)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или С1-С6алкил, замещенный 1 или 2 заместителями, независимо выбранными из группы, состоящей из фенила или 5- или 6-членного гетероароматического кольца, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)С(О)R7a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, C2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)C(O)R7a;
Q представляет собой фенил, нафталинил, 5- или 6-членное гетероароматическое кольцо или 8-10-членную гетероароматическую бициклическую кольцевую систему, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, SF5, OCN, SCN, Si(R15)3, OR4, NR5R6, C1-С6алкила, C1-С6галогеналкила, С2-С6алкенила, С2-С6галогеналкенила, С2-С6алкинила, С2-С6галогеналкинила, C(X)R7, С(О)OR8, С(X)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7, ОС(О)OR8, ОС(О)NR11R12, OS(O)2R9, OS(O)2NR11R12, N(R10)C(O)R7, N(R10)С(O)NR11R12, N(R10)S(O)2R9, N(R10)S(O)2NR11R12 и R14;
каждый X независимо представляет собой О или S;
каждый R4 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкил, S(O)mR9a, S(O)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R4a независимо представляет собой H, С1-С6алкил или С1-С6галогеналкил;
каждый R5 независимо представляет собой Н, NR5aR6a, С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R5a независимо представляет собой H или С1-С6алкил;
каждый R6 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a;
каждый R6a независимо представляет собой Н, С1-С6алкил, C(O)R13 или С(О)OR13;
каждый R7 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R7a независимо представляет собой С1-С6алкил или С1-С6галогеналкил;
каждый R8 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(О)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R8a независимо представляет собой С1-С6алкил или C1-С6галогеналкил;
каждый R9 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или C1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R9a независимо представляет собой С1-С6алкил или С1-С6галогеналкил;
каждый R10 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7a, C(O)OR8a, C(O)NR11R12, S(O)mR9a или S(O)2NR11R12;
каждый R10a независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил;
каждый R11 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4a, NR5aR6a, C(X)R7a, C(O)OR8a, C(O)NR11aR12, S(O)mR9a или S(O)2NR11aR12; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-C4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, C(O)NR11aR12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(O)2NR11aR12, NR5aR6a, OC(O)R7a и N(R10a)С(О)R7a;
каждый R11a независимо представляет собой Н, С1-С6алкил, С2-С6алкенил или С2-С6алкинил;
каждый R12 независимо представляет собой Н, NR5aR6a, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил, С2-С6галогеналкинил, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9 или S(О)2NR11R12; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, C1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-3 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, C(X)R7a, C(O)OR8a, С(О)NR11R12, OR4a, С2-С6алкоксиалкила, S(O)mR9a, S(О)2NR11R12, NR5aR6a, OC(O)R7a и N(R10)C(O)R7a;
каждый R13 независимо представляет собой Н, С1-С6алкил, С1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a;
каждый R14 независимо представляет собой С3-С7циклоалкил, С4-С8циклоалкилалкил, С6-С14циклоалкилциклоалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или С1-С6алкил, С2-С6алкенил или С2-С6алкинил, каждый замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из циано, нитро, OR4, NR5R6, C(X)R7, C(O)OR8, C(O)NR11R12, S(O)mR9 и S(O)2NR11R12; или фенил, нафталинил или 5- или 6-членное гетероароматическое кольцо, каждые необязательно замещенные 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, C1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(O)2NR11R12, OC(O)R7a и N(R10)С(О)R7a;
каждый R15 независимо представляет собой С1-С6алкил, C1-С6галогеналкил, С2-С6алкенил, С2-С6галогеналкенил, С2-С6алкинил или С2-С6галогеналкинил; или С3-С7циклоалкил, С4-С8циклоалкилалкил или С5-С7циклоалкенил, каждый необязательно замещенный 1-4 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, С1-С4алкила, С1-С4галогеналкила, OR4a и S(O)mR9a; или фенил, необязательно замещенный 1-5 заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, OR4, NR5R6, С1-С4алкила, С2-С4алкенила, С2-С4алкинила, С1-С4галогеналкила, С2-С4галогеналкенила, С2-С6алкоксиалкила, C(X)R7, С(О)OR8, C(O)NR11R12, S(O)mR9, S(О)2NR11R12, OC(O)R7a и N(R10)С(O)R7a;
каждый m независимо равен 0, 1 или 2; и
n равно 0, 1, 2, 3 или 4,
его N-оксид или соль в количестве от 0,0001 до 1% по массе семян перед обработкой.
| US 4179277 A 18.12.1979 | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| ФТОРАЛКЕНИЛЬНЫЕ СОЕДИНЕНИЯ ИЛИ ИХ СЕЛЬСКОХОЗЯЙСТВЕННО ПРИЕМЛЕМЫЕ СОЛИ, КОМПОЗИЦИЯ ДЛЯ БОРЬБЫ С ЗАРАЖЕНИЕМ РАСТЕНИЙ НЕМАТОДАМИ, СПОСОБ БОРЬБЫ С ЗАРАЖЕНИЕМ РАСТЕНИЙ НЕМАТОДАМИ И СПОСОБЫ СИСТЕМНОГО ПОДАВЛЕНИЯ ЗАРАЖЕНИЯ РАСТЕНИЙ НЕМАТОДАМИ | 1992 |
|
RU2117658C1 |
Авторы
Даты
2014-10-20—Публикация
2010-05-04—Подача