Область техники, к которой относится изобретение
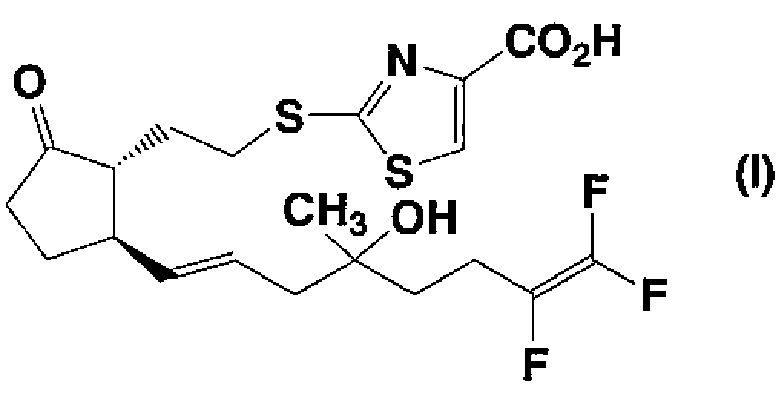
Настоящее изобретение относится к соединению, обладающему сокращающей активностью в отношении детрузора мочевого пузыря и релаксирующей активностью в отношении уретрального сфинктера, где соединение представлено формулой (I):
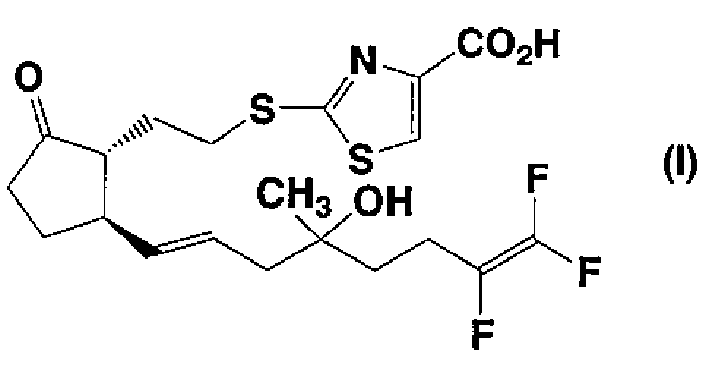
в которой все из символов имеют такие же значения, как описано ниже, его соли, его сольвату, его пролекарству, его смеси с диастереомером в произвольном соотношении или к его циклодекстриновому клатрату (в дальнейшем, соединение, представленное формулой (I), его соль, его сольват, его пролекарство, его смесь с диастереомером в произвольном соотношении или его циклодекстриновый клатрат также просто упоминают как «соединение согласно настоящему изобретению»). Настоящее изобретение также относится к фармацевтической композиции, содержащей соединение согласно настоящему изобретению в качестве активного ингредиента.
Предпосылки создания изобретения
Что касается симптома, когда мочевой пузырь не может быть порожним (неполное опорожнение полости мочевого пузыря), что происходит в результате недостаточного сокращения при мочеиспускании, недавно была предложена новая терминология: «недостаточно активный мочевой пузырь».
Причиной возникновения недостаточно активного мочевого пузыря является дисфункция сокращения мочевого пузыря, т.е. клиническое состояние, когда сокращение детрузора мочевого пузыря снижено (недостаточная активность детрузора), или комбинация с дисфункцией уретральной релаксации (дисфункция в отношении низкой проходимости мочевыводящих путей), т.е. клиническое состояние с недостаточным расслаблением уретрального сфинктера и дисфункцией сокращения мочевого пузыря, которое классифицируется на нейрогенный недостаточно активный мочевой пузырь, миогенный недостаточно активный мочевой пузырь, индуцируемый лекарственным средством недостаточно активный мочевой пузырь, связанный с возрастом недостаточно активный мочевой пузырь и недостаточно активный мочевой пузырь, индуцируемый другими факторами (например, недостаточно активный мочевой пузырь вследствие низкой проходимости мочевыводящих путей, инфекции и стресса, и т.д.), в зависимости от причин.
Примеры каузативных заболеваний в случае нейрогенного недостаточно активного мочевого пузыря включают: нарушения периферической нервной системы, такие как диабет, дисковая грыжа, стеноз позвоночного канала, синдром Гийена-Барре и вызываемый герпесным опоясывающим лишаем периферический неврит; заболевания спинного мозга, например супрануклеарное повреждение спинного мозга, опухоль спинного мозга, шейный спондилез, сосудистые заболевания спинного мозга, расщепление позвоночника, синдром миеломенингоцеле и ограниченной хорды; и заболевания головного мозга, такие как деменция, церебрально-васкулярные заболевания, болезнь Паркинсона, относящаяся к спинному мозгу и мозжечку дегенерация, оливопонтоцеребеллярная атрофия (ОРСА), синдром Шая-Дрейджера, опухоль головного мозга, рассеянный склероз, церебральная травма и энцефалит и т.д. В некоторых случаях причиной возникновения недостаточно активного мочевого пузыря является хирургическое повреждение тазового нерва, подчревного нерва или относящегося к наружным половым органам нерва, контролирующих функции опорожнения, после хирургических операций тазовых внутренних органов (рак матки или ректальный рак).
Причиной возникновения миогенного недостаточно активного мочевого пузыря в значительной степени является криптогенная сниженная активность детрузора мочевого пузыря.
Примеры индуцируемого лекарственным средством недостаточно активного мочевого пузыря включают недостаточно активный мочевой пузырь, возникающий за счет антихолинергических лекарственных средств, т.е. лекарственных средств, которые ингибируют высвобождение ацетилхолина, и других факторов.
Кроме того, у пожилых людей, как правило, проявляется боль при мочеиспускании (дизурия), вызываемая ослабленной активностью мочевого пузыря, и, в результате, связанный с возрастом недостаточно активный мочевой пузырь приводит к значительной проблеме при старении.
Другие примеры факторов, которые вызывают появление недостаточно активного мочевого пузыря, включают низкую проходимость мочевыводящих путей, вызываемую гиперплазией предстательной железы, контрактурой шейки мочевого пузыря или пролапсом матки, инфекциями, как, например, цистит и уретрит, и стрессом (смотрите непатентные документы 1, 2 и 3).
Для лечения недостаточно активного мочевого пузыря используют лекарственные средства, которые усиливают сократительную способность детрузора мочевого пузыря или снижают уретральную резистентность за счет расслабления уретрального сфинктера. Например, холинергические средства, такие как бетанекол, и ингибиторы ацетилхолинэстеразы, такие как дистигмин, используют в качестве лекарственных средств для усиления сократительной способности детрузора мочевого пузыря. Однако бетанекол также способствует сокращению детрузора мочевого пузыря в период накопления мочи, что наносит вред функции накопления мочи в мочевом пузыре и в то же самое время вызывает побочные эффекты, такие как слезотечение, потоотделение, желудочно-кишечные нарушения, абдоминальная боль и т.д. Следовательно, существуют противопоказания для беременных женщин и пациентов, страдающих от язвы желудка и двенадцатиперстной кишки, врожденной непроходимости кишечного тракта, астмы, гипертиреоидизма и т.д. В качестве ингибиторов ацетилхолинэстеразы используют, например, дистигмин и неостигмин. Так как ингибиторы ацетилхолинэстеразы усиливают активность ацетилхолина, высвобождаемого из тазовых нервных окончаний при мочеиспускании, усиливая сокращение детрузора мочевого пузыря при мочеиспускании, их считают превосходными лекарственными средствами, когда принимают во внимание физиологический механизм мочеиспускания. Однако, так как дистигмин сокращает детрузор мочевого пузыря и также вызывает сокращение уретрального сфинктера вследствие своей сильной никотиноподобной активности в отношении усиления уретральной резистентности, эффективность опорожнения является незначительной и действие с точки зрения клинического применения является неудовлетворительным. Дополнительно, также указан риск опорожнения под высоким давлением (смотрите непатентный документ 4).
В качестве лекарственных средств для расслабления уретрального сфинктера и снижения уретральной резистентности были использованы, например, антагонисты α1-рецептора, такие как тамсулозин, празозин, альфузозин, нафтопидил, урапидил и т.д., и сообщалось, что эти лекарственные средства являются эффективными для уменьшения интенсивности субъективных симптомов, таких как ощущение остаточной мочи и никтурия. Однако, так как имеются антигипертензивные эффекты, включая ортостатическую гипотензию и т.д., в качестве побочного эффекта, должна быть проявлена осторожность при их введении. Дополнительно, не было сообщения, показывающего удовлетворительные воздействия на недостаточно активный мочевой пузырь.
А именно, лекарственные средства, в настоящее время используемые для лечения недостаточно активного мочевого пузыря, не являются клинически удовлетворительными с точки зрения терапевтических воздействий и безопасности.
С другой стороны, в патентном документе 1 раскрывается соединение для улучшения кровотока в случае нервных тканей «конского хвоста», представленное формулой (А):
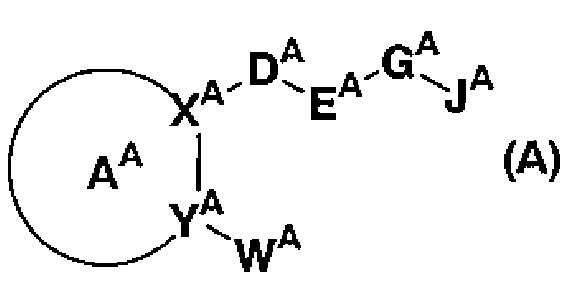
где цикл АА представляет собой 5- или 6-членную циклическую группу, которая может содержать 1-3 гетероатома, выбираемых из атомов азота, кислорода и серы, или, дополнительно, может иметь заместители, ХА и YA, каждый, независимо представляет собой атом азота или атом углерода, DA представляет собой углеводородную группу, которая может иметь заместители, ЕА представляет собой связь, атом кислорода или атом серы, который может быть окислен, GA представляет собой связь, углеводородную группу, которая может иметь заместители, или гетероциклическую группу, которая может иметь заместители, JA представляет собой кислотную группу, которая может быть защищена, и WA представляет собой углеводородную группу, которая может иметь заместители. Дополнительно, раскрывается, что соединение, представленное формулой (А), является эффективным в случае расстройства мочевого пузыря, вызываемого сжатием «конского хвоста» (смотрите патентный документ 1).
Дополнительно, соединение, обладающее активностью в отношении регенерации или защиты нерва, представлено формулой (В):
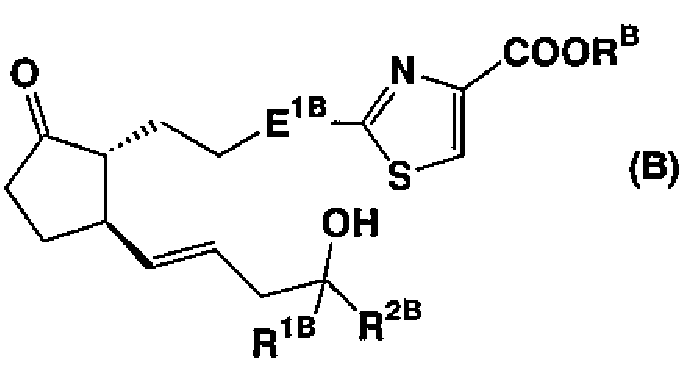
где Е1В представляет собой атом кислорода или атом серы, который может быть окислен, RB представляет собой атом водорода или С1-С8-алифатическую углеводородную группу, R1B представляет собой атом водорода или С1-С4-алифатическую углеводородную группу, и R2B представляет собой углеводородную группу, которая может иметь раскрытые заместители (смотрите патентный документ 2).
Соединение согласно настоящему изобретению не раскрыто в каком-либо литературном источнике.
Дополнительно, нигде не описано и не предполагается, что соединение согласно настоящему изобретению воздействует на детрузор мочевого пузыря и уретральный сфинктер для усиления сократительной способности детрузора мочевого пузыря и, с другой стороны, расслабления уретрального сфинктера; может уменьшать интенсивность дисфункции сокращения мочевого пузыря или дисфункции уретральной релаксации путем обоих воздействий; и проявляет эффективность против недостаточно активного мочевого пузыря, включая миогенный, индуцированный лекарственным средством, связанный с возрастом недостаточно активный мочевой пузырь, и т.д. Дополнительно, нигде не описано и не предполагается, что соединение согласно настоящему изобретению обладает минимальным риском в отношении побочных воздействий на мочевую систему, сердечно-сосудистую систему и пищеварительную систему и обладает превосходной фармакокинетикой, включая пероральную абсорбциионную способность, метаболическую стабильность и эффективную продолжительность действия.
ДОКУМЕНТЫ ИЗВЕСТНОГО УРОВНЯ ТЕХНИКИ
Патентные документы
Патентный документ 1: Международная публикация WO 2005/053707;
Патентный документ 2: Международная публикация WO 2006/129788.
Непатентные документы
Непатентный документ 1: Nursing Standard, май 2005 года, 11-17; 19(35): 57-64; опр. 66-7;
Непатентный документ 2: Practice of Intractable and Chronic Dysuria, Urology View, том 2(5), стр.57-65, 2004;
Непатентный документ 3: The standardization of terminology in functions of lower urinary tract: report from the International Continence Society (ICS) Standardization Steering Committee, Journal of the Japan Neurogenic Bladder Society, том 14(2), стр.104-118, публикация от 20 декабря 2003 года;
Непатентный документ 4: Diagnosis and Therapy of Neurogenic Bladder, 2-е изд., стр.105-106, стр.139, Igaku-Shoin Ltd. (1990).
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Проблемы, решаемые данным изобретением
Так как холинергические средства, ингибиторы ацетилхолинэстеразы и антагонисты α1-рецептора, которые используют для лечения недостаточно активного мочевого пузыря, обладают только или активностью в отношении усиления сократительной способности детрузора мочевого пузыря, или активностью в отношении расслабления уретрального сфинктера, в качестве механизмов их действия, эти средства оказывают недостаточные воздействия с точки зрения клинического применения. Кроме того, так как лекарственные средства воздействуют на автономную нервную систему, показано проявление побочных эффектов в органах, других, чем мочевой пузырь.
При данных обстоятельствах, существует необходимость в лекарственном средстве, которое воздействует на гладкие мышцы, вовлеченные в мочеиспускание, особенно, детрузор мочевого пузыря и уретральный сфинктер, в отношении сокращения мочевого пузыря и расслабления уретры, в случае которого достигаются очень высокие эффекты в отношении мочеиспускания.
Так как хронические заболевания, как, например, недостаточная активность мочевого пузыря, требуют долговременного введения лекарственных средств, существует потребность в терапевтических средствах, которые обладают незначительным риском в отношении побочных эффектов и могут быть введены перорально, причем принимаются во внимание безопасность и удобство для пациентов.
Способ решения проблем
В результате обширных исследований, авторами настоящего изобретения найдено, что соединение согласно настоящему изобретению воздействует на две гладкие мышцы, т.е. детрузор мочевого пузыря и уретральную гладкую мышцу, с проявлением неожиданных двух активностей, в отношении усиления сокращения детрузора мочевого пузыря и, с другой стороны, расслабления уретрального сфинктера, и может быть предусмотрено в качестве очень эффективного терапевтического средства для недостаточно активного мочевого пузыря в целях уменьшения интенсивности как дисфункции сокращения мочевого пузыря, так и дисфункции уретральной релаксации. Авторами настоящего изобретения также найдено, что соединение согласно настоящему изобретению проявляет незначительный риск побочных воздействий на мочевую систему, сердечно-сосудистую систему и пищеварительную систему и обладает превосходной фармакокинетикой, включая пероральную абсорбционную способность, метаболическую стабильность, продолжительность действия и т.д., достигая цели настоящего изобретения.
А именно, настоящее изобретение относится:
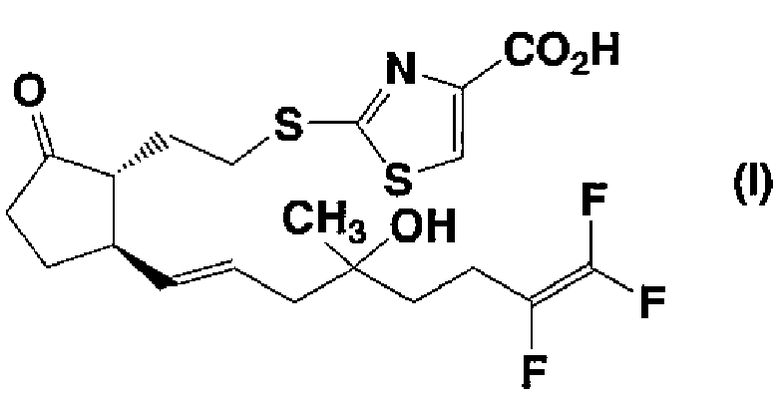
1) к соединению, представленному формулой (I):
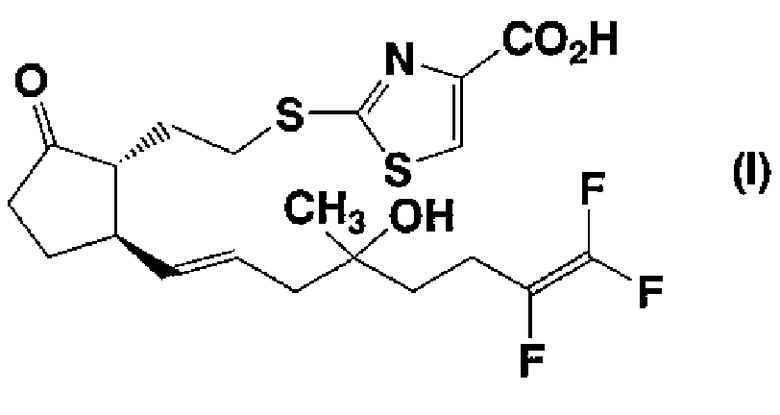
где 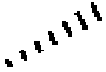 представляет собой α-конфигурацию;
представляет собой α-конфигурацию;
 представляет собой β-конфигурацию; и
представляет собой β-конфигурацию; и
 представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь,
представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь,
его соли, его сольвату, его пролекарству или его смеси с диастереомером в произвольном соотношении или его циклодекстриновому клатрату;
2) к соединению по вышеуказанному п.1, где соединение представляет собой:
(1) 2-[(2-{(1R,5R)-2-оксо-5-[(1E)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту,
(2) 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту, или
(3) 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4R)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту;
3) к смеси в произвольном соотношении по вышеуказанному п.1, где соединение представляет собой 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту и диастереомер представляет собой 2-[(2-{(1S,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту;
4) к фармацевтической композиции, содержащей, в качестве активного ингредиента, соединение, представленное формулой (I):
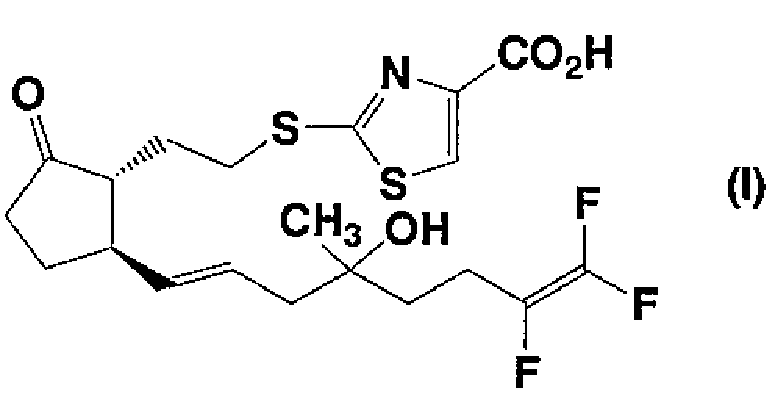
где все из символов имеют такие же значения, как определено в вышеуказанном п.1,
его соль, его сольват, его пролекарство или его смесь с диастереомером в произвольном соотношении или его циклодекстриновый клатрат;
5) к фармацевтической композиции по вышеуказанному п.4, где фармацевтическая композиция представляет собой средство для сокращения детрузора мочевого пузыря и расслабления уретрального сфинктера;
6) к фармацевтической композиции по вышеуказанному п.5, где фармацевтическая композиция представляет собой средство для предупреждения, лечения и/или уменьшения интенсивности дисфункции сокращения мочевого пузыря и/или дисфункции уретральной релаксации;
7) к фармацевтической композиции по вышеуказанному п.6, где дисфункцией сокращения мочевого пузыря и/или дисфункцией уретральной релаксации является недостаточно активный мочевой пузырь;
8) к лекарственному средству, содержащему соединение, представленное формулой (I):
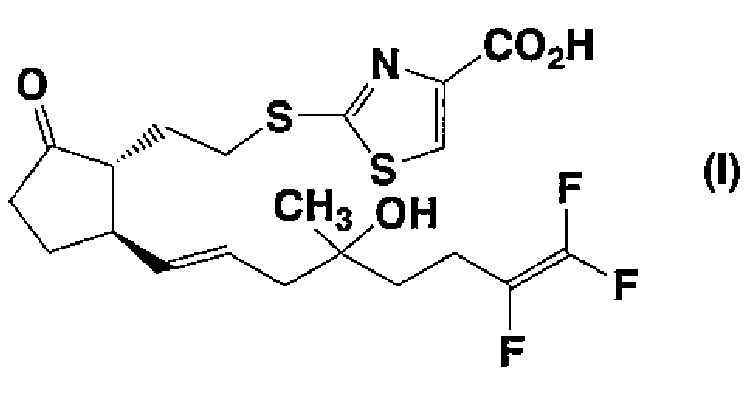
где все из символов имеют такие же значения, как определено в п.1,
его соль, его сольват, его пролекарство, его смесь с диастереомером в произвольном соотношении или его циклодекстриновый клатрат и, по меньшей мере, одно лекарственное средство, выбираемое из антагонистов α1-рецептора и ингибиторов ацетилхолин-эстеразы, в комбинации;
9) к способу сокращения детрузора мочевого пузыря и расслабления уретрального сфинктера, включающему введение млекопитающему эффективного количества соединения, представленного формулой (I):
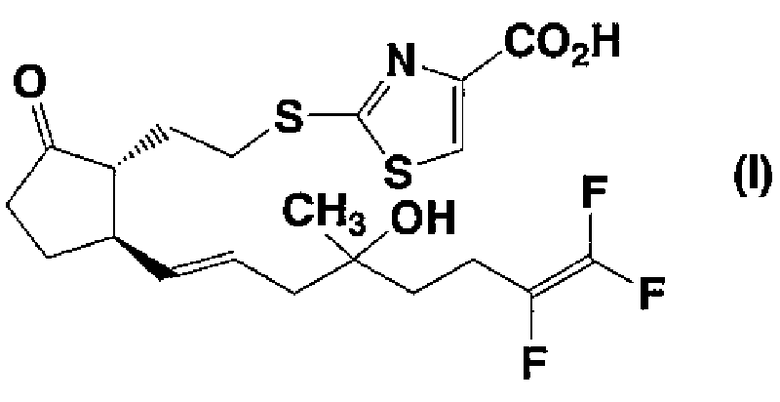
где все из символов имеют такие же значения, как описано в п.1,
его соли, его сольвата, его пролекарства, его смеси с диастереомером в произвольном соотношении или его циклодекстринового клатрата;
10) к способу предупреждения, лечения и/или уменьшения интенсивности дисфункции сокращения мочевого пузыря и/или дисфункции уретральной релаксации, включающему введение млекопитающему эффективного количества соединения, представленного формулой (I):
где все из символов имеют такие же значения, как описано в п.1,
его соли, его сольвата, его пролекарства, его смеси с диастереомером в произвольном соотношении или его циклодекстринового клатрата;
11) к применению соединения, представленного формулой (I):
где все из символов имеют такие же значения, как описано в п.1,
его соли, его сольвата, его пролекарства, его смеси с диастереомером в произвольном соотношении или его циклодекстринового клатрата, для получения средства, вызывающего сокращение детрузора мочевого пузыря, и средства, расслабляющего уретральный сфинктер;
12) к применению соединения, представленного формулой (I):

где все из символов имеют такие же значения, как описано в п.1,
его соли, его сольвата, его пролекарства, его смеси с диастереомером в произвольном соотношении или его циклодекстринового клатрата, для получения средства для предупреждения, лечения и/или уменьшения интенсивности дисфункции сокращения мочевого пузыря и/или дисфункции уретральной релаксации;
13) к соединению, представленному формулой (I):

где все из символов имеют такие же значения, как описано в п.1,
его соли, его сольвату, его пролекарству, его смеси с диастереомером в произвольном соотношении или его циклодекстриновому клатрату, предназначенному для сокращения детрузора мочевого пузыря и расслабления уретрального сфинктера; и
14) к соединению, представленному формулой (I):

где все из символов имеют такие же значения, как описано в п.1,
его соли, его сольвату, его пролекарству, его смесь с диастереомером в произвольном соотношении или его циклодекстриновому клатрату, предназначенному для предупреждения, лечения и/или уменьшения интенсивности дисфункции сокращения мочевого пузыря и/или дисфункции уретральной релаксации.
Эффекты настоящего изобретения
Соединение согласно настоящему изобретению обладает сокращающей активностью в отношении детрузора мочевого пузыря и расслабляющей активностью в отношении уретрального сфинктера. Следовательно, соединение согласно настоящему изобретению может быть использовано для уменьшения интенсивности дисфункции сокращения мочевого пузыря и/или дисфункции уретральной релаксации. Таким образом, соединение согласно настоящему изобретению является эффективным в качестве средства для предупреждения и/или лечения недостаточно активного мочевого пузыря. Дополнительно, соединение согласно настоящему изобретению является эффективным в качестве средства для уменьшения интенсивности различных симптомов, связанных с недостаточно активным мочевым пузырем.
Соединение согласно настоящему изобретению обладает незначительным риском побочных воздействий на мочевую систему. Например, соединение согласно настоящему изобретению не проявляет симптома накопления, такого как уменьшение емкости мочевого пузыря, что представляет собой, при эффективной дозе, высокий риск для пациентов, страдающих от урологических заболеваний.
Так как соединение согласно настоящему изобретению вызывает незначительные изменения в случае кровяного давления или в случае частоты сердечных сокращений, при введении в высокой дозе, а также в эффективной дозе, соединение согласно настоящему изобретению проявляет незначительный риск побочных эффектов у пациентов, страдающих от заболеваний, протекающих с расстройством кровообращения, таких как гипертензия. Следовательно, соединение согласно настоящему изобретению оказывает незначительное воздействие на сердечную функцию.
Соединение согласно настоящему изобретению не оказывает побочных воздействий на пищеварительную систему, например пищеварительные симптомы, такие как диарея, при введении в эффективной дозе.
Соединение согласно настоящему изобретению обладает хорошей мембранной проницаемостью и превосходной пероральной абсорбционной способностью.
Соединение согласно данному изобретению является стабильным против печеночного метаболизма и обладает низким системным клиренсом. Следовательно, соединение согласно настоящему изобретению может долговременно проявлять лекарственную эффективность.
Как описано выше, соединение согласно настоящему изобретению обладает эффектами очень сильного мочеиспускания, высокой безопасностью и превосходной фармакокинетикой.
Краткое описание чертежей
На фиг.1 показано воздействие соединения согласно настоящему изобретению на объем остаточной мочи (верхняя диаграмма) и емкость мочевого пузыря (нижняя диаграмма) в моделях недостаточно активного мочевого пузыря.
На фиг.2 показаны эффекты сравнительного воздействии соединения на объем остаточной мочи (верхняя диаграмма) и емкость мочевого пузыря (нижняя диаграмма) в моделях недостаточно активного мочевого пузыря.
На фиг.3 показаны воздействия соединения согласно настоящему изобретению и сравнительного соединения на кровяное давление в случае нормальных крыс.
На фиг.4 показаны воздействия соединения согласно настоящему изобретению и сравнительного соединения на частоту сердечных сокращений в случае нормальных крыс.
На фиг.5 показаны воздействия соединения согласно настоящему изобретению на кровяное давление в случае крыс-гипертоников.
На фиг.6 показаны воздействия сравнительного соединения на кровяное давление в случае крыс-гипертоников.
На фиг.7 показана сердечная деятельность при воздействии соединения согласно настоящему изобретению (верхний график) и сравнительного соединения (нижний график) в случае обезьян рода Cynomolgus.
На фиг.8 показаны двойные продукты соединения согласно настоящему изобретению (верхний график) и сравнительного соединения (нижний график) в случае обезьян рода Cynomolgus.
Способ осуществления данного изобретения
Настоящее изобретение относится к соединению, представленному формулой (I):

где все из символов имеют такие же значения, как описано выше,
его соли, его сольвату, его пролекарству, его смеси с диастереомером в произвольном соотношении или его циклодекстриновому клатрату, и к фармацевтической композиции, содержащей соединение согласно настоящему изобретению в качестве активного ингредиента.
Если не указано иначе, то в контексте настоящего описания квалифицированному специалисту в данной области очевидно, что символ 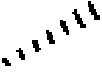 представляет собой связь с «дальней» стороной бумаги (т.е. α-конфигурация);
представляет собой связь с «дальней» стороной бумаги (т.е. α-конфигурация);
символ  представляет собой связь с «передней» стороной бумаги (т.е. β-конфигурация); и
представляет собой связь с «передней» стороной бумаги (т.е. β-конфигурация); и
символ  представляет собой α-конфигурацию, β-конфигурацию или их смесь.
представляет собой α-конфигурацию, β-конфигурацию или их смесь.
В качестве соединения согласно настоящему изобретению предпочтительным является:
(1) 2-[(2-{(1R,5R)-2-оксо-5-[(1E)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота,
(2) 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота, или
(3) 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4R)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота. Конкретно, предпочтительной является 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 17), описанная в примере 17.
В качестве соли предпочтительной является водорастворимая соль. Примеры подходящих солей включают соли щелочных металлов (как, например, кальций, натрий и т.д.), соли щелочноземельных металлов (как, например, калий, магний и т.д.), соли аммония, соли фармацевтически приемлемых органических аминов (например, тетраметиламмоний, триэтиламин, метиламин, диметиламин, циклопентиламин, бензиламин, фенетиламин, моноэтаноламин, диэтаноламин, трис(гидроксиметил)аминометан, лизин, аргинин и N-метил-D-глюкамин и т.д.) и аддитивные соли кислот.
Аддитивными солями кислот предпочтительно являются водорастворимые соли. Примеры подобных аддитивных солей кислот включают соли неорганических кислот, как, например, гидрохлориды, гидробромиды, гидроиодиды, сульфаты, фосфаты и нитраты; и соли органических кислот, как, например, ацетаты, лактаты, тартраты, бензоаты, цитраты, метансульфонаты, этансульфонаты, бензолсульфонаты, толуолсульфонаты, изетионаты, глюкуронаты и глюконаты.
Соединение, представленное формулой (I), и его соли также могут быть превращены в соответствующие сольваты любыми подходящими способами.
Предпочтительно, чтобы сольват являлся низкотоксичным и водорастворимым сольватом. Примеры пригодных сольватов включают сольваты на основе воды и спиртов (например, этанол и т.д.).
Пролекарство соединения, представленного формулой (I), его соли или его сольвата, относится к соединению, которое превращается in vivo в соединение, представленное формулой (I), его соль или его сольват, например, путем ферментативных реакций и реакций с кислотой желудочного сока. Пролекарство соединения, представленного формулой (I), его соли, или его сольвата, может представлять собой, например, соединение, в котором гидроксильная группа соединения, представленного формулой (I), ацилирована, алкилирована, фосфорилирована или борирована (например, соединение, в котором гидроксильная группа соединения, представленного формулой (I), ацетилирована, пальмитоилирована, пропаноилирована, пивалоилирована, сукцинилирована, фумарилирована или аланилирована, диметиламинометилкарбонилирована); или соединение, в котором карбоксильная группа соединения, представленного формулой (I), этерифицирована или амидирована (например, соединение, в котором карбоксильная группа соединения, представленного формулой (I), этерифицирована с образованием сложного метилового эфира, сложного этилового эфира, сложного пропилового эфира, сложного изопропилового эфира, сложного бутилового эфира, сложного изобутилового эфира, сложного трет-бутилового эфира, сложного фенилового эфира, сложного карбоксиметилового эфира, сложного диметиламинометилового эфира, сложного пивалоилоксиметилового эфира, сложного 1-{(этоксикарбонил)окси}этилового эфира, сложного фталидилового эфира, сложного (5-метил-2-оксо-1,3-диоксолен-4-ил)метилового эфира, сложного 1-{[(циклогексилокси)карбонил]окси}этилового эфира или метиламидирована). Эти соединения могут быть получены известными в данной области способами. Пролекарство соединения, представленного формулой (I), может находиться или в сольватированной или в несольватированной форме. Пролекарство соединения, представленного формулой (I), может быть пролекарством, которое превращается в соединение, представленное формулой (I), при физиологических условиях, как описано в сборнике “Development of Medicines”, том 7, “Molecular Design”, сс.163-198, опубликованном HirokawaShoten в 1990 году.
Соединение, представленное формулой (I), может быть меченным с помощью изотопа (например, 2Н, 3Н, 11С, 13С, 14С, 13N, 15N, 15O, 17O, 18O, 35S, 18F, 36Cl, 123I или 125I и т.д.).
Пролекарство соединения, представленного формулой (I), его соли или его сольвата, может представлять собой, например, соединение, представленное формулой (I-a):
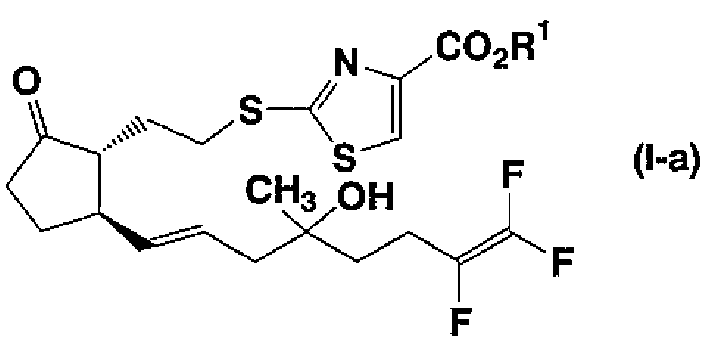
где R1 представляет собой С1-С4-алкильную группу, такую как метил, этил, пропил, изопропил, бутил, изобутил или трет-бутил и т.д., и символы имеют такие же значения, как указано выше.
Соединение, представленное формулой (I), его соль, его сольват, его пролекарство или его смесь с диастереомером в произвольном соотношении может быть превращено в циклодекстриновый клатрат, используя α-, β- или γ-циклодекстрин, или их смесь, любыми способами, указанными в описаниях изобретений согласно патентам Японии JP-B-S50-3362, JP-B-S52-31404 и JP-B-S61-52146. За счет превращения в циклодекстриновый клатрат, так как стабильность увеличивается и растворимость в воде увеличивается, соединение становится пригодным в случае применения в качестве лекарственного средства. Включение соединения, представленного формулой (I), его соли, его сольвата или его пролекарства, в циклодекстрин может быть определено путем анализа с помощью дифференциальной сканирующей калориметрии или порошковой рентгенографии.
Настоящее изобретение включает диастереомерную смесь диастереомера соединения, представленного формулой (I), и соединения, представленного формулой (I), в произвольном соотношении.
Например, в качестве диастереомера представлена 2-[(2-{(1S,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 20):
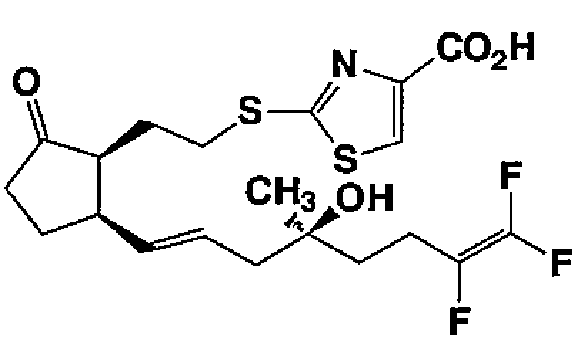
В связи с этим, в качестве смеси в произвольном соотношении, предпочтительной является смесь, где соотношение диастереомера соединения, представленного формулой (I), к соединению, представленному формулой (I), составляет 1-20%, в расчете на соединение, представленное формулой (I). Более предпочтительной является смесь, где соотношение соединения, представленного формулой (I), к диастереомеру = 9:1.
Способы получения соединения согласно настоящему изобретению
Соединения согласно настоящему изобретению можно получать с помощью подходящим образом модифицированных и комбинированных способов, известных в данной области, например способов, описанных в Международной публикации WO 2005/053707, Международной публикации WO 2006/129788 и Synlett 2002, № 1, 239-242, и в Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2-е изд. (Richard C. Larock, John Wiley & Sons Inc, 1999), способов, указанных ниже, или способов, указанных в примерах.
Например, соединение, представленное формулой (I), можно получать путем подвергания соединения формулы (II):
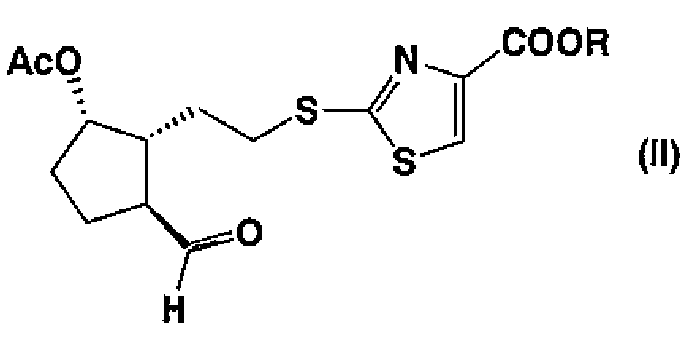
где Ас представляет собой ацетильную группу, R представляет собой защитную группу для карбоксильной группы (например, С1-С4-алкильную группу, например метил, этил, пропил, изопропил, бутил, изобутил или трет-бутил и т.д.), и соединения формулы (III):
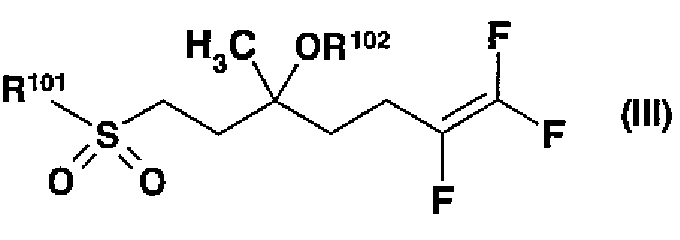
где R101 представляет собой арильную группу (например, 1-фенил-1Н-тетразолил, фенил и т.д.), R102 представляет собой защитную группу (например, триметилсилил, трет-бутилдиметилсилил и т.д.), следующим реакциям и дальнейшему снятию защиты и окислению ацетильной группы, затем удалению защитной группы.
Реакции между соединением, представленным формулой (II), и соединением, представленным формулой (III), известны. Например, реакцию осуществляют в присутствии основания (например, гексаметилдисилазид калия, диизопропиламид лития или бутиллитий и т.д.), в органическом растворителе (например, безводный тетрагидрофуран, диметоксиэтан, толуол или диметилформамид и т.д.), при температуре в диапазоне от примерно -100ºС до -20ºС.
Реакции для удаления защитных групп, таких как ацетильная группа, известны в данной области, и их можно осуществлять согласно следующей методике.
Примеры защитной группы для карбоксильной группы включают С1-С4-алкильную группу, такую как метил, этил, пропил, изопропил, бутил, изобутил или трет-бутил, аллильную группу, трихлорэтильную группу, бензильную (Bn) группу, фенацильную группу и т.д.
Примеры защитной группы для гидроксильной группы включают метил, тритил, метоксиметил (МОМ), 1-этоксиэтил (ЕЕ), метоксиэтоксиметил (МЕМ), 2-тетрагидропиранил (ТНР), триметилсилил (TMS), триэтилсилил (TES), трет-бутилдиметилсилил (TBDMS или TBS), трет-бутилдифенилсилил (TBDPS), ацетил (Ас), пивалоил, бензоил, бензил (Bn), п-метоксибензил, аллилоксикарбонил (Alloc) или 2,2,2-трихлорэтоксикарбонил (Troc) и т.д.
В дополнение к этим защитным группам, любая группа, которая может быть без труда и селективно удалена, может быть использована в качестве защитной группы для карбоксильной или гидроксильной группы. Например, можно использовать защитные группы, описанные в руководстве T.W. Greene, Protective Groups in Organic Synthesis, Wiley, New York, 1999.
Реакции в целях удаления защитных групп для карбоксильной или гидроксильной группы хорошо известны в данной области, например:
(1) снятие защиты путем щелочного гидролиза,
(2) снятие защиты в кислых условиях,
(3) снятие защиты путем гидрогенолиза,
(4) снятие защиты с использованием силильных групп,
(5) снятие защиты с использованием металлов, и
(6) снятие защиты с использованием комплексов металлов.
Эти способы теперь раскрываются подробно.
(1) Снятие защиты путем щелочного гидролиза осуществляют, например, используя гидроксид щелочного металла (например, гидроксид натрия, гидроксид калия, гидроксид лития и т.д.), гидроксид щелочноземельного металла (например, гидроксид бария, гидроксид кальция и т.д.), карбонат (например, карбонат натрия, карбонат калия и т.д.), их водный раствор или их смесь в органическом растворителе (например, метанол, тетрагидрофуран, диоксан и т.д.), при температуре в диапазоне от примерно 0ºС до примерно 40ºС.
(2) Снятие защиты в кислых условиях осуществляют, например, используя органическую кислоту (например, уксусная кислота, трифторуксусная кислота, метансульфоновая кислота, п-толуолсульфокислота и т.д.), неорганическую кислоту (например, соляная кислота, серная кислота и т.д.) или их смесь (например, бромоводородная кислота/уксусная кислота и т.д.), в органическом растворителе (например, дихлорметан, хлороформ, диоксан, этилацетат, анизол и т.д.), при температуре в диапазоне от примерно 0ºС до примерно 100ºС.
(3) Снятие защиты путем гидрогенолиза осуществляют, например, в растворителе (например, растворителе на основе простого эфира (например, тетрагидрофуран, диоксан, диметоксиэтан, диэтиловый эфир и т.д.), растворителе на основе спирта (например, метанол, этанол и т.д.), растворителе на основе бензола (например, бензол, толуол и т.д.), растворителе на основе кетона (например, ацетон, метилэтилкетон и т.д.), растворителе на основе нитрила (например, ацетонитрил и т.д.), растворителе на основе амида (например, диметилформамид и т.д.), в воде, этилацетате, уксусной кислоте или смешанном растворителе из двух или более таких растворителей), в присутствии катализатора (например, палладий-на-угле, палладиевая чернь, гидроксид палладия, оксид платины, никель Ренея и т.д.), в атмосфере водорода, или в присутствии формиата аммония, при давлении окружающей среды или при давлении сжатия, при температуре в диапазоне от примерно 0ºС до примерно 200ºС.
(4) Снятие защиты с использованием силильных групп можно осуществлять, например, используя тетрабутиламмонийфторид, в органическом растворителе (например, тетрагидрофуран или ацетонитрил и т.д.), который смешивается с водой, при температуре в диапазоне от примерно 0ºС до примерно 40ºС.
(5) Снятие защиты с использованием металлов можно осуществлять, например, в кислотном растворителе (например, уксусная кислота, буфер с рН-значением от примерно 4,2 до примерно 7,2, или смешанный раствор его с органическим растворителем, таким как тетрагидрофуран и т.д.), в присутствии порошкообразного цинка, при температуре в диапазоне от примерно 0ºС до примерно 40ºС, если необходимо, при обработке ультразвуком.
(6) Снятие защиты с использованием комплексов металлов осуществляют, например, используя комплекс металла (например, тетракис(трифенилфосфин)палладий(0), бис(трифенилфосфин)-палладий(II)дихлорид, палладий(II)ацетат или трис(трифенилфосфин)родий(I)хлорид и т.д.), в органическом растворителе (например, дихлорметан, диметилформамид, тетрагидрофуран, этилацетат, ацетонитрил, диоксан или этанол и т.д.), воде или получаемом из них смешанном растворителе, в присутствии улавливающего реагента (например, трибутилоловогидрид, триэтилсилан, димедон, морфолин, диэтиламин или пирролидин и т.д.), органической кислоты (например, уксусная кислота, муравьиная кислота или 2-этилгексановая кислота и т.д.) и/или соли органической кислоты (например, 2-этилгексаноат натрия или 2-этилгексаноат калия и т.д.), совместно или без фосфинового реагента (например, трифенилфосфин и т.д.), при температуре в диапазоне от примерно 0ºС до примерно 40ºС.
В дополнение к этому, реакции снятия защиты также можно осуществлять, например, с помощью способов, описанных в руководстве T.W. Greene, Protective Groups in Organic Synthesis, Wiley, New York, 1999.
Хотя это может быть несомненно известно квалифицированному специалисту в данной области, путем выбора реакций снятия защиты может быть легко получен желательный активный ингредиент согласно настоящему изобретению.
Окисление известно в данной области и может быть осуществлено, например, используя реагент ТЕМРО (2,2,6,6-тетраметилпиперидин-1-оксил) и реоксидант (водный раствор пероксида водорода, гипохлорит натрия, 3-хлорнадбензойная кислота, иодбензолдиацетат, пероксимоносульфат калия (Oxone®) и т.д.), в органическом растворителе (хлороформ, дихлорметан, тетрагидрофуран, толуол, ацетонитрил, этилацетат, вода и т.д.) или в получаемом из этих растворителей смешанном растворителе, в присутствии или в отсутствие четвертичной аммониевой соли (тетрабутиламмонийхлорид, тетрабутиламмонийбромид и т.д.), в присутствии или в отсутствие неорганической соли (бромид натрия, бромид калия и т.д.) или в присутствии или в отсутствие неорганического основания (гидрокарбонат натрия, ацетат натрия и т.д.), при температуре в диапазоне от примерно -20ºС до примерно 60ºС.
Соединения, в качестве исходных материалов, в реакциях, указанных в настоящем описании, известны в данной области или могут быть легко получены способами, известными в данной области. Например, соединение, представленное формулой (II), можно получать, например, способом, описанным в Международной публикации WO 2006/129788. Соединение, представленное формулой (III), можно получать, например, способами, описанными в нижеприводимых примерах.
Реакции, указанные в настоящем описании, можно осуществлять, используя водяную баню, масляную баню, песчаную баню или микроволновую печь, в случае реакций с нагреванием, которое очевидно для квалифицированного специалиста в данной области.
В случае реакций, указанных в настоящем описании, может быть подходящим образом использован твердый реагент, содержащийся в полимере (как, например, полистирол, полиакриламид, полипропилен и полиэтиленгликоль и т.д.).
В реакциях, указанных в настоящем описании, продукты реакции можно очищать обычными способами, например путем дистилляции в условиях окружающей среды или при пониженном давлении, с помощью высокоэффективной жидкостной хроматографии, используя силикагель или силикат магния, тонкослойной хроматографии, хроматографии с ионообменной смолой, хроматографии с удаляющей примеси смолой-акцептором, колоночной хроматографии, промывки, перекристаллизации и т.д. Очистку можно осуществлять после каждой реакции или после нескольких реакций.
Токсичность
Соединение согласно настоящему изобретению вызывает меньшие побочные эффекты и, таким образом, является достаточно безопасным для применения в качестве лекарственного средства.
Применения в лекарственных средствах
Соединение согласно настоящему изобретению воздействует на две гладкие мышцы, т.е. детрузор мочевого пузыря и уретральный сфинктер, ассоциированные с недостаточно активным мочевым пузырем. Соединение согласно настоящему изобретению обладает способностью усиливать сокращаемость детрузора мочевого пузыря и, с другой стороны, расслаблять уретральный сфинктер. Как правило, лекарственные средства, воздействующие на гладкие мышцы, индуцируют сокращение гладких мышц в любом месте, если лекарственные средства промотируют сокращение, или индуцируют расслабление гладких мышц в любом месте, если лекарственные средства промотируют релаксацию.
Не существует такого соединения, как соединение согласно настоящему изобретению, которое промотирует сокращение некоторых гладких мышц, тогда как оно в то же самое время промотирует релаксацию других гладких мышц.
Так как соединение согласно настоящему изобретению воздействует на гладкие мышцы, конкретно на детрузор мочевого пузыря и уретральный сфинктер, для промотирования сокращения детрузора мочевого пузыря и расслабления уретрального сфинктера, оно может уменьшать интенсивность дисфункции сокращения мочевого пузыря или дисфункции уретральной релаксации и, таким образом, оно является эффективным в качестве средства для предупреждения и/или лечения недостаточно активного мочевого пузыря. Дополнительно, соединение согласно настоящему изобретению является эффективным в качестве средства для уменьшения интенсивности различных симптомов, связанных с недостаточно активным мочевым пузырем, как, например, медленный поток мочи, разделенный поток мочи, блокированный поток мочи, замедленное мочеиспускание, опорожнение при абдоминальном давлении, ощущение остаточной мочи, недержание мочи вследствие переполнения мочевого пузыря, энурез и/или капание мочи после мочеиспускания. Соединение согласно настоящему изобретению является особенно эффективным в качестве средства для улучшения состояния в случае разделенного потока мочи, блокированного потока мочи, опорожнения при абдоминальном давлении, ощущения остаточной мочи, недержания мочи вследствие переполнения мочевого пузыря, энуреза и/или капания мочи после мочеиспускания.
Соединение согласно настоящему изобретению также является эффективным для предупреждения и/или лечения стеноза позвоночного канала, шейного спондилеза, заболеваний периферической нервной системы, иммунных заболеваний (боковой амиотрофический склероз (ALS), рассеянный склероз, синдром Шегрена, хронический суставный ревматизм, аутоиммунные заболевания, такие как системные эритематоды, ответные реакции отторжения органа после трансплантации и т.д.), аллергических заболеваний (например, бронхиальная астма, аллергическое назальное воспаление, аллергическое воспаление конъюнктивы, атопический дерматит, пищевая аллергия и т.д.), гибели нервных клеток, дисменореи, преждевременных родов, выкидыша, алопеции, нервных ретинальных заболеваний, таких как глаукома, эректильной дисфункции, артрита, повреждения легких, пневмофиброза, эмфиземы, бронхита, хронических обструктивных респираторных дистресс-синдромов, повреждения печени, острого гепатита, цирроза печени, шока, нефрита (как, например, острый нефрит, хронический нефрит и т.д.), дисфункции почек, панкреатита, синдрома системного воспалительного ответа, сепсиса, гемофагоцитарного синдрома, синдрома активации макрофагов, болезни Стилла, болезни Кавасаки, повреждения при ожоге, системных гранулематозных заболеваний, язвенного колита, болезни Крона, гиперцитокинемии после диализа, дисфункции множественных органов, болезней костей (перелом кости, повторный перелом, трудноизлечимый перелом, дисфункция сцепления костей, псевдоартроз, остеомаляция, болезнь Педжета, жесткий спондилит, метастаз при раковом заболевании костей, деформирующий артроз, разрушение хрящевых костей при подобных их заболеваниях и т.д.).
Соединение согласно настоящему изобретению и другие лекарственные средства можно вводить в комбинации с другими лекарственными средствами в целях 1) дополнения и/или усиления профилактических и/или терапевтических эффектов соединения, 2) улучшения фармакокинетики и абсорбции соединения, снижения дозировки соединения и/или 3) уменьшения побочных эффектов соединения.
Что касается комбинированного средства из соединения согласно настоящему изобретению и других лекарственных средств, его можно вводить в комбинации с другими лекарственными средствами в виде смеси, в которой два ингредиента смешаны в одном лекарственном средстве, или в виде раздельных лекарственных средств. Введение двух ингредиентов в виде раздельных лекарственных средств включает одновременное введение и введение с интервалом во времени. При введении с интервалом во времени возможно, что соединение согласно настоящему изобретению вводят вначале, а другие лекарственные средства вводят позднее, или возможно, что другие лекарственные средства вводят вначале и соединение согласно настоящему изобретению вводят позднее, причем способы введения двух ингредиентов могут быть одинаковыми или отличными друг от друга.
Примеры лекарственных средств, подходящих для дополнения и/или усиления эффектов соединения согласно настоящему изобретению, включают ингибиторы ацетилхолинэстеразы (например, дистигмин и неостигмин, и т.д.) и антагонисты α1-рецептора (например, тамсулозин, празозин, альфузозин, нафтопидил, урапидил и т.д.).
Не существует особого ограничения относительно массового соотношения соединения согласно настоящему изобретению по отношению к другим лекарственным средствам.
Другие лекарственные средства могут представлять собой комбинацию лекарственных средств одного и того же рода или двух или более различных родов.
Другие лекарственные средства для дополнения и/или усиления эффектов соединения согласно настоящему изобретению включают не только доступные в настоящее время лекарственные средства, но и лекарственные средства, которые должны быть найдены, базируясь на вышеуказанном механизме.
В случае, когда комбинированное средство из соединения согласно настоящему изобретению с другими лекарственными средствами используют в вышеуказанных целях, его обычно вводят системно или локально или перорально или парентерально.
Хотя доза может изменяться в зависимости от рода лекарственного средства и может зависеть от возраста, массы тела, симптомов, подразумеваемых терапевтических эффектов, способов введения, времени лечения и т.д., соединение согласно настоящему изобретению обычно может быть введено перорально в дозе, находящейся в диапазоне от 1 нг до 100 мг, каждый раз, в случае взрослого человека, один или несколько раз в сутки, или может быть введено парентерально, в дозе, находящейся в диапазоне от 0,1 нг до 10 мг, каждый раз, в случае взрослого человека, один или несколько раз в сутки, или, альтернативно, может быть введено непрерывно внутривенно в течение периода времени от 1 до 24 часов в сутки.
Так как дозу можно изменять в зависимости от различных условий, как описано выше, имеются случаи, где доза является достаточной в меньшем количестве, чем доза, описанная выше, тогда как имеются случаи, где необходимо введение в большем объеме, чем объем, описанный выше.
В случае, где вводят соединение согласно настоящему изобретению или комбинированное средство из соединения согласно настоящему изобретению и другого лекарственного средства, его можно использовать в виде внутренних твердых готовых лекарственных форм или внутренних жидких готовых лекарственных форм для перорального введения и в виде инъецируемых наружных готовых лекарственных форм, суппозиториев и ингаляций и т.д. для парентерального введения.
Примеры внутренних твердых готовых лекарственных форм, подходящих для перорального введения, включают таблетки, пилюли, капсулы, порошки и гранулы. Капсулы включают твердые капсулы и мягкие капсулы.
Внутренние твердые готовые лекарственные формы можно получать, используя только один или более активных ингредиентов, или путем смешения одного или более активных ингредиентов, например, с эксципиентом (лактоза, маннит, глюкоза, микрокристаллическая целлюлоза, крахмал и т.д.), связующим веществом (гидроксипропилцеллюлоза, поливинилпирролидон, метасиликат магния и оксида алюминия и т.д.), дезинтегрирующим агентом (кальцийкарбоксиметилцеллюлоза и т.д.), смазочным веществом (стеарат магния и т.д.), стабилизатором или способствующим растворению агентом (глутаминовая кислота, аспарагиновая кислота и т.д.), с приготовлением готовой лекарственной формы способами, известными в данной области. Если необходимо, на твердые готовые лекарственные формы можно наносить покрытие с помощью агента для нанесения покрытия (например, белый сахар, желатин, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлозофталат и т.д.) и можно покрывать двумя или более слоями. Также сюда включены капсулы из абсорбируемых материалов, как, например, желатин.
Примеры внутренних жидких готовых лекарственных форм, подходящих для перорального введения, включают фармацевтически приемлемые водные растворы, суспендирующие агенты, эмульгирующие агенты, сиропы, эликсиры и т.д. В таких жидких готовых лекарственных формах одно или более активных веществ растворены, суспендированы или эмульгированы в растворителе, который обычно используется в данной области (например, дистиллированная вода, этанол, получаемый из них смешанный раствор и т.д.). Жидкие готовые лекарственные формы могут содержать смачивающий агент, суспендирующий агент, эмульгирующий агент, подсластитель, вкусовой агент, ароматизатор, консервант, забуферивающий агент и т.д.
Наружные готовые лекарственные формы для парентерального введения включают, например, мази, гели, крема, припарки, пластыри, жидкие мази, аэрозоли, лекарственные формы для ингаляции и спреи. Такие готовые лекарственные формы включают одно или более активных веществ, и их получают способами, известными или обычно используемыми в данной области.
Мази получают способами, известными или обычно используемыми в данной области. Например, мазь можно получать путем растирания или расплавления одного или более активных веществ в основе. Основу для мази выбирают из таковых, известных или обычно используемых в данной области. Примеры таких основ для мази включают высшие жирные кислоты и эфиры высших жирных кислот (адипиновая кислота, миристиновая кислота, пальмитиновая кислота, стеариновая кислота, олеиновая кислота, адипат, миристат, пальмитат, стеарат, олеат и т.д.), воски (пчелиный воск, парафин, церезин и т.д.), поверхностно-активные вещества (фосфаты простых полиоксиэтиленалкиловых эфиров и т.д.), высшие спирты (цетиловый спирт, стеариловый спирт, кетостеариловый спирт и т.д.), силиконовое масло (диметилполисилоксан и т.д.), углеводороды (гидрофильный вазелин, белый вазелин, очищенный ланолин, жидкий парафин и т.д.), гликоли (этиленгликоль, диэтиленгликоль, пропиленгликоль, полиэтиленгликоль, макроголы и т.д.), растительные масла (касторовое масло, оливковое масло, кунжутное масло, терпентин и т.д.), животные масла (норковое масло, яичное масло, сквалан, сквален и т.д.), воду, ускорители абсорбции и противочесоточные агенты. Эти основы для мазей можно использовать отдельно или в виде смеси двух или более из них. Мази, дополнительно, могут включать увлажнитель, консервант, стабилизатор, антиоксидант, вкусовой агент и т.д.
Гели получают способами, известными или обычно используемыми в данной области. Например, гель можно получать путем расплавления одного или более активных веществ в основе. Основу для геля выбирают из таковых, известных или обычно используемых в данной области. Примеры таких основ для гелей включают низшие спирты (этанол, изопропиловый спирт и т.д.), желирующие агенты (карбоксиметилцеллюлоза, гидроксиэтилцеллюлоза, гидроксипропилцеллюлоза, этилцеллюлоза и т.д.), нейтрализующие агенты (триэтаноламин, диизопропаноламин и т.д.), поверхностно-активные вещества (полиэтиленгликольмоностеарат и т.д.), камеди, воду, ускорители абсорбции и противочесоточные агенты. Эти основы для гелей можно использовать отдельно или в виде смеси двух или более из них. Гели, дополнительно, могут включать консервант, антиоксидант, вкусовой агент и т.д.
Кремы получают способами, известными или обычно используемыми в данной области. Например, крем можно получать путем расплавления или эмульгирования одного или более активных веществ в основе. Основу для крема выбирают из таковых, известных или обычно используемых в данной области. Примеры таких основ для крема включают эфиры высших жирных кислот, низшие спирты, углеводороды, многоатомные спирты (пропиленгликоль, 1,3-бутиленгликоль и т.д.), высшие спирты (2-гексилдеканол, цетиловый спирт и т.д.), эмульгаторы (простые полиоксиэтиленалкиловые эфиры, эфиры жирных кислот и т.д.), воду, ускорители абсорбции и противочесоточные агенты. Эти основы для кремов можно использовать отдельно или в виде смеси двух или более из них. Кремы, дополнительно, могут включать консервант, антиоксидант, вкусовой агент и т.д.
Припарки получают способами, известными или обычно используемыми в данной области. Например, припарку можно получать путем расплавления одного или более активных веществ в основе, перемешивания, с последующим равномерным нанесением покрытия на носитель. Основу для припарки выбирают из известных или обычно используемых в данной области. Примеры таких основ для припарок включают загустители (например, полиакриловая кислота, поливинилпирролидон, гуммиарабик, крахмал, желатин, метилцеллюлоза и т.д.), смачивающие агенты (например, мочевина, глицерин, пропиленгликоль и т.д.), наполнители (каолин, оксид цинка, тальк, кальций, магний и т.д.), воду, солюбилизатор, вещества для повышения клейкости и противочесоточные агенты. Эти основы для припарок можно использовать отдельно или в виде смеси двух или более из них. Припарки, дополнительно, могут включать консервант, антиоксидант, вкусовой агент и т.д.
Пластыри получают способами, известными или обычно используемыми в данной области. Например, пластырь можно получать путем расплавления одного или более активных веществ в основе и равномерного нанесения покрытия из расплава на носитель. Основу для пластыря выбирают из таковых, известных или обычно используемых в данной области. Примеры таких основ для пластыря включают полимерные основы, масла и жиры, высшие жирные кислоты, загустители и противочесоточные агенты. Эти основы для пластыря можно использовать отдельно или в виде смеси двух или более из них. Пластыри, дополнительно, могут включать консервант, антиоксидант, вкусовой агент и т.д.
Жидкие мази получают способами, известными или обычно используемыми в данной области. Например, жидкую мазь можно получать путем растворения, суспендирования или эмульгирования одного или более активных веществ в одной или более основах, выбираемых из воды, спиртов (этанол, полиэтиленгликоль и т.д.), высших жирных кислот, глицерина, мыл, эмульгирующих и суспендирующих агентов. Эти жидкие мази, дополнительно, могут включать консервант, антиоксидант, вкусовой агент и т.д.
Аэрозоли, лекарственные формы для ингаляции и спреи могут содержать стабилизатор, такой как бисульфит натрия, или забуферивающий агент, например изотонический агент, такой как хлорид натрия, цитрат натрия или лимонная кислота, в дополнение к разбавителю, который обычно используется в данной области.
Готовые инъецируемые лекарственные формы для парентерального введения могут быть, например, в виде растворов, суспензий, эмульсий и инъецируемых твердых готовых лекарственных форм, которые растворяют или суспендируют в растворителях при использовании. Такие инъецируемые готовые лекарственные формы используют при растворении, суспендировании или эмульгировании одного или более активных веществ в растворителе. Примеры подходящих растворителей включают дистиллированную воду для инъекций, физиологический солевой раствор, растительные масла, пропиленгликоль, полиэтиленгликоль, спирты, такие как этанол, и их комбинации. Инъецируемые готовые лекарственные формы могут включать стабилизаторы, способствующие растворению агенты (например, глутаминовая кислота, аспарагиновая кислота, Polysolvate 80® и т.д.), суспендирующие агенты, эмульгирующие агенты, успокаивающие средства, буферы и консерванты. Инъецируемые готовые лекарственные формы получают путем стерилизации или дезинфекции на конечных стадиях. Асептические твердые готовые лекарственные формы, например лиофилизированные твердые готовые лекарственные формы, также можно использовать при дезинфекции или растворении в асептической дистиллированной воде для инъекций или других растворителях перед применением.
Примеры лекарственных форм для ингаляций для парентерального введения включают аэрозоли, порошки для ингаляции или жидкие средства для ингаляции. Жидкие средства для ингаляции можно растворять или суспендировать в воде или другой подходящей среде перед применением.
Лекарственные формы для ингаляций получают способами, известными в данной области.
Например, жидкие средства для ингаляции получают путем выбора соответствующих консервантов (бензальконийхлорид, парабен и т.д.), красителей, буферов (фосфат натрия, ацетат натрия и т.д.), изотонических агентов (хлорид натрия, концентрированный глицерин и т.д.), загустителей (карбоксивиниловый полимер и т.д.) и обладающего свойством абсорбции вещества, в зависимости от необходимости.
Порошки для ингаляции получают путем выбора соответствующих смазочных веществ (стеариновая кислота, ее соли и т.д.), связующих веществ (крахмал, декстрин и т.д.), эксципиентов (лактоза, целлюлоза и т.д.), красителей, консервантов (бензальконийхлорид, парабен и т.д.) и обладающего свойством абсорбции вещества, в зависимости от необходимости.
В случае введения жидкостей для ингаляции, обычно используют разбрызгиватели (пульверизаторы, распылители). Для введения порошков для ингаляции, обычно используют ингаляторы для введения порошкообразных лекарственных средств.
Другие композиции для парентерального введения включают одно или более активных веществ и представляют собой, например, суппозитории для интраректального введения и пессарии для интравагинального введения.
ПРИМЕРЫ
Настоящее изобретение подробно поясняется с помощью примеров. Однако настоящее изобретение не ограничено этими примерами.
Растворители, указанные в круглых скобках в виде разделенной на части порции в случае хроматографии и ТСХ, представляют собой растворители, используемые для элюирования или проявления, и их соотношение означает объемное соотношение.
Данные ЯМР означают данные 1Н-ЯМР при 300 МГц, за исключением указанного иначе. В круглых скобках в случае данных ЯМР указываются растворители, используемые для измерения.
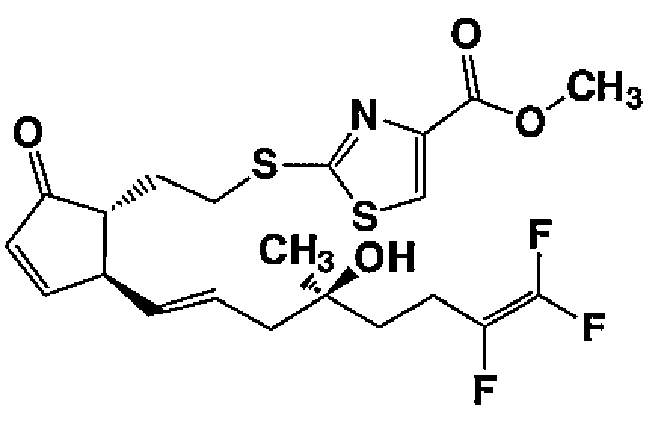
Соединения, используемые согласно данному контексту, называют с помощью компьютерной программы, которая дает химические названия в соответствии с правилами ИЮПАК, ACD/Name Batch (зарегистрированная торговая марка) или в соответствии с номенклатурой ИЮПАК. Например, 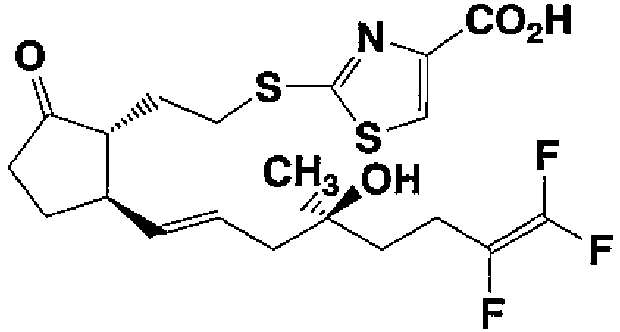 называют как 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота.
называют как 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота.
Примеры получения
Пример 1
4,5,5-трифтор-N-метокси-N-метил-4-пентенамид (соединение 1)
N,O-диметилгидроксиамингидрохлорид (3,5 г), 1-этил-3-(3-диметиламинопропил)карбодиимидгидрохлорид (6,9 г) и триэтиламин (9,2 мл) добавляют к раствору 4,5,5-трифторпент-4-еновой кислоты (номер по CAS 110003-22-0 (5,0 г)), в растворе метиленхлорида (64 мл), при использовании бани с холодной водой, и осуществляют перемешивание при комнатной температуре в течение ночи. Реакционный раствор концентрируют и разбавляют этилацетатом. Разбавленный раствор промывают 1 н. соляной кислотой, водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют, получая указанное в заголовке соединение (6,4 г), имеющее следующие физические свойства:
ТСХ: Rf 0,50 (этилацетат:гексан=1:2);
ЯМР (CDCl3): δ 2,51-2,77 (м, 4Н), 3,10 (с, 3Н), 3,69 (с, 3Н).
Пример 2
Этил-6,7,7-трифтор-3-оксо-6-гептеноат (соединение 2)
Этилацетат (4,8 мл) медленно, по каплям, добавляют к раствору гексаметилдисилазида лития в тетрагидрофуране (1 М раствор, 48 мл), при температуре -78ºС, затем перемешивают в течение 30 минут. Раствор соединения 1 (6,4 г) в безводном тетрагидрофуране (33 мл), медленно, по каплям, добавляют к реакционному раствору при той же температуре, затем перемешивают в течение 30 минут. К реакционному раствору добавляют 2 н. соляную кислоту (30 мл), затем экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют. Полученный остаток очищают путем колоночной хроматографии на силикагеле (гексан:этилацетат=20:1→15:1), получая указанное в заголовке соединение (4,94 г), имеющее следующие физические свойства:
ТСХ: Rf 0,63 (этилацетат:гексан=1:2);
ЯМР (CDCl3): δ 1,29 (т, J=7,1 Гц, 3Н), 2,50-2,71 (м, 2Н), 2,83 (т, J=7,2 Гц, 2Н), 3,47 (с, 2Н), 4,21 (кв., 2Н).
Пример 3
6,7,7-трифтор-6-гептен-1,3-диол (соединение 3)
Раствор соединения 2 (4,71 г), в трет-бутилметиловом эфире (52 мл), медленно, по каплям, добавляют к гидриду лития и бора (1,4 г), при охлаждении льдом, затем перемешивают при комнатной температуре в течение 4 часов. Реакционный раствор выливают в насыщенный водный раствор хлорида аммония, при охлаждении льдом, и промывают этилацетатом. Органический слой промывают насыщенным солевым раствором, сушат над сульфатом натрия и концентрируют, получая указанное в заголовке соединение (3,87 г), имеющее следующие физические свойства:
ТСХ: Rf 0,31 (этилацетат:гексан=2:1);
ЯМР (CDCl3): δ 1,66-1,83 (м, 4Н), 2,17-2,66 (м, 2Н), 3,71-4,06 (м, 3Н).
Пример 4
6,7,7-трифтор-1-[(1-фенил-1Н-тетразол-5-ил)тио]-6-гептен-3-ол (соединение 4)
Соединение 3 (3,87 г) растворяют в толуоле (50 мл) и добавляют туда 2 н. водный раствор гидроксида натрия (50 мл), тетрабутиламмонийбромид (700 мг) и тозилхлорид (4,10 г), при охлаждении льдом, затем перемешивают в течение 30 минут. К реакционному раствору добавляют 1-фенил-1Н-тетразол-5-тиол (4,60 г), затем перемешивают при 60ºС в течение ночи. Реакционный раствор выливают в воду и экстрагируют трет-бутилметиловым эфиром. Органический слой промывают насыщенным солевым раствором, сушат над сульфатом натрия и концентрируют. Полученный остаток очищают путем колоночной хроматографии на силикагеле (гексан:этилацетат=4:1→7:3), получая указанное в заголовке соединение (5,43 г), имеющее следующие физические свойства:
ТСХ: Rf 0,37 (этилацетат:гексан=2:1);
ЯМР (CDCl3): δ 1,64-1,83 (м, 2Н), 1,88-2,02 (м, 2Н), 2,31-2,61 (м, 2Н), 3,34-3,88 (м, 3Н), 7,46-7,69 (м, 5Н).
Пример 5
6,7,7-трифтор-1-[(1-фенил-1Н-тетразол-5-ил)тио]-6-гептен-3-он (соединение 5)
Бромид калия (830 мг), 2,2,6,6-тетраметилпиперидин-1-оксил (199 мг) и водный раствор гипохлорита натрия (10% раствор, 6,1 мл) добавляют к раствору соединения 4 (2,18 г) в ацетонитриле (32 мл), при охлаждении льдом, затем перемешивают в течение 2 часов. К реакционному раствору добавляют насыщенный водный раствор тиосульфата натрия, при той же температуре, затем экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют, получая указанное в заголовке соединение (2,17 г), имеющее следующие физические свойства:
ТСХ: Rf 0,50 (этилацетат:гексан=1:2);
ЯМР (CDCl3): δ 2,48-2,77 (м, 4Н), 3,14 (т, J=6,4 Гц, 2Н), 3,57 (т, J=6,4 Гц, 2Н), 7,54 (с, 5Н).
Пример 6
6,7,7-трифтор-3-метил-1-[(1-фенил-1Н-тетразол-5-ил)тио]-6-гептен-3-ол (соединение 6)
Раствор метилмагнийбромида в диэтиловом эфире (3,0 М раствор, 4,2 мл) добавляют к раствору соединения 5 (2,17 г) в безводном тетрагидрофуране (22 мл), при температуре -78ºС. Смешанный раствор перемешивают в течение 30 минут при той же температуре и в течение 30 минут при охлаждении льдом. К реакционному раствору добавляют насыщенный водный раствор гидрокарбоната натрия, при охлаждении льдом, затем экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют. Полученный остаток очищают путем колоночной хроматографии на силикагеле (гексан:этилацетат=7:3), получая указанное в заголовке соединение (1,88 г), имеющее следующие физические свойства:
ТСХ: Rf 0,39 (этилацетат:гексан=1:2);
ЯМР (CDCl3): δ 1,29 (с, 3Н), 1,69-1,92 (м, 2Н), 1,99-2,19 (м, 2Н), 2,30-2,59 (м, 2Н), 3,33-3,67 (м, 2Н), 7,42-7,70 (м, 5Н).
Пример 7
6,7,7-трифтор-3-метил-1-[(1-фенил-1Н-тетразол-5-ил)сульфонил]-6-гептен-3-ол (соединение 7)
Гексааммонийгептамолибдентетрагидрат (318 мг) и водный раствор пероксида водорода (30% раствор, 1,8 мл) добавляют к раствору соединения 6 (1,84 г) в метаноле (26 мл), при охлаждении льдом, затем перемешивают при комнатной температуре в течение ночи. К реакционному раствору добавляют насыщенный водный раствор тиосульфата натрия, при охлаждении льдом, затем экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют, получая указанное в заголовке соединение (2,0 г), имеющее следующие физические свойства:
ТСХ: Rf 0,41 (этилацетат:гексан=1:2);
ЯМР (CDCl3): δ 1,30 (с, 3Н), 1,69-1,86 (м, 2Н), 2,06-2,24 (м, 2Н), 2,30-2,57 (м, 2Н), 3,80-4,00 (м, 2Н), 7,51-7,78 (м, 5Н).
Пример 8
1-фенил-5-({6,7,7-трифтор-3-метил-3-[(триметилсилил)окси]-6-гептен-1-ил}сульфонил)-1Н-тетразол (соединение 8)
Имидазол (524 мг) и триметилсилилхлорид (0,79 мл) добавляют к раствору соединения 7 (2,0 г) в диметилформамиде (11 мл), при охлаждении льдом, затем перемешивают при комнатной температуре в течение 5 часов. Реакционный раствор выливают в воду и экстрагируют этилацетатом. Органический слой промывают насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют. Полученный остаток очищают с помощью колоночной хроматографии на силикагеле (гексан:этилацетат=9:1), получая указанное в заголовке соединение (2,16 г), имеющее следующие физические свойства:
ТСХ: Rf 0,72 (этилацетат:гексан=1:2);
ЯМР (CDCl3): δ 0,15 (с, 9Н), 1,35 (с, 3Н), 1,66-1,86 (м, 2Н), 1,96-2,19 (м, 2Н), 2,25-2,46 (м, 2Н), 3,74-3,88 (м, 2Н), 7,56-7,67 (м, 3Н), 7,68-7,74 (м, 2Н).
Пример 9
Этил-2-({2-[(1R,2S,5S)-2-(ацетилокси)-5-формилциклопентил]этил}тио)-1,3-тиазол-4-карбоксилат (соединение 9)
Триэтиламин (3,7 мл) и комплекс триоксид серы·пиридин (1,7 г) добавляют к раствору этил-2-({2-[(1R,2S,5S)-2-(ацетилокси)-5-(гидроксиметил)циклопентил]этил}тио)-1,3-тиазол-4-карбоксилата (500 мг) (смотрите соединение 7, описанное в Международной публикации WO 2006/129788) в смеси диметилсульфоксид (4,0 мл)/этилацетат (8,0 мл), при температуре 10ºС, затем перемешивают при комнатной температуре в течение 30 минут. К реакционному раствору добавляют 1 н. соляную кислоту, затем экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют, получая указанное в заголовке соединение (497 мг), имеющее следующие физические свойства:
ТСХ: Rf 0,27 (гексан:этилацетат=2:1);
ЯМР (CDCl3): δ 1,32-1,49 (м, 3Н), 1,78-2,15 (м, 9Н), 2,35-2,51 (м, 1Н), 2,69-2,84 (м, 1Н), 3,10-3,31 (м, 2Н), 4,32-4,48 (м, 2Н), 5,29-5,37 (м, 1Н), 8,02 (с, 1Н), 9,67 (д, J=2,74 Гц, 1Н).
Пример 10
Этил-2-{[2-((1R,2S,5R)-2-(ацетилокси)-5-{(1E)-7,8,8-трифтор-4-метил-4-[(триметилсилил)окси]-1,7-октадиен-1-ил}циклопентил)этил]тио}-1,3-тиазол-4-карбоксилат (соединение 10)
Раствор гексаметилдисилазида калия в толуоле (0,5 М, 4,8 мл) медленно, по каплям, добавляют к раствору соединения 8 (1,13 г) в 1,2-диметоксиэтане (8,0 мл), при температуре -78ºС, затем перемешивают при той же температуре в течение 30 минут. К реакционному раствору медленно, по каплям, добавляют раствор соединения 9 (461 мг) в 1,2-диметоксиэтане (5,0 мл), при той же температуре. После перемешивания при той же температуре в течение 30 минут, температуру повышают до 0ºС. Добавляют насыщенный водный раствор гидрокарбоната натрия, затем экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют. Полученный остаток очищают путем колоночной хроматографии на силикагеле (гексан:этилацетат=8:1), получая указанное в заголовке соединение (703 мг), имеющее следующие физические свойства:
ТСХ: Rf 0,71 (этилацетат:гексан=1:2);
ЯМР (CDCl3): δ 0,10 (с, 9Н), 1,39 (т, J=7,1 Гц, 3Н), 1,49-2,48 (м, 17Н), 3,10-3,40 (м, 2Н), 4,40 (кв., J=7,1 Гц, 2Н), 5,18-5,53 (м, 3Н), 8,02 (с, 1Н).
Пример 11
2-[(2-{(1R,2S,5R)-2-гидрокси-5-[(1E)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 11)
К раствору соединения 10 (703 г) в этаноле (6,0 мл) добавляют 2 н. водный раствор гидроксида натрия (2,4 мл), при охлаждении льдом, затем перемешивают при комнатной температуре в течение ночи. К реакционному раствору добавляют 1 н. соляную кислоту, при той же температуре, затем перемешивают в течение 30 минут. К реакционному раствору добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют, получая указанное в заголовке соединение (538 мг), имеющее следующие физические свойства:
ТСХ: Rf 0,21 (этилацетат:метанол=5:1);
ЯМР (CDCl3): δ 1,19 (с, 3Н), 1,32-1,50 (м, 2Н), 1,61-1,92 (м, 4Н), 1,94-2,56 (м, 8Н), 2,81-2,99 (м, 1Н), 3,49-3,67 (м, 1Н), 4,56 (м, 1Н), 5,27-5,62 (м,2Н), 8,08 (с, 1Н).
Пример 12
2-[(2-{(1R,2S,5R)-2-(ацетилокси)-5-[(1E)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 12)
Безводную уксусную кислоту (0,33 мл) добавляют к раствору соединения 11 (538 мг) в пиридине (6,0 мл), при охлаждении льдом, затем перемешивают при комнатной температуре в течение ночи. Реакционный раствор выливают в 1 н. соляную кислоту и экстрагируют этилацетатом. Органический слой промывают насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют, получая указанное в заголовке соединение (589 мг), имеющее следующие физические свойства:
ТСХ: Rf 0,27 (этилацетат:метанол=5:1);
ЯМР (CDCl3): δ 1,16-1,21 (м, 3Н), 1,34-2,54 (м, 17Н), 3,10-3,53 (м, 2Н), 5,33-5,61 (м, 3Н), 8,11 (с, 1Н).
Пример 13
(10S,12E,13aR,16S,16aR)-10-метил-8-оксо-10-(3,4,4-трифтор-3-бутен-1-ил)-1,10,11,13а,14,15,16,16а-октагидро-2Н,8Н-7,4-(азено)циклопента[j][1,5,7]оксадитиациклопентадецин-16-илацетат (форма низкой полярности: соединение 13А)
(10R,12E,13aR,16S,16aR)-10-метил-8-оксо-10-(3,4,4-трифтор-3-бутен-1-ил)-1,10,11,13а,14,15,16,16а-октагидро-2Н,8Н-7,4-(азено)циклопента[j][1,5,7]оксадитиациклопентадецин-16-илацетат (форма высокой полярности: соединение 13В)
К раствору соединения 12 (589 мг) в толуоле (58 мл) при комнатной температуре добавляют 4,4-диметиламинопиридин (567 мг). Реакционный раствор нагревают до температуры 100ºС и добавляют туда 2,4,6-трихлорбензоилхлорид (0,37 мл). После перемешивания в течение 15 минут охлаждают до комнатной температуры. Реакционный раствор выливают в насыщенный водный раствор гидрокарбоната натрия и экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют. Полученный остаток очищают путем колоночной хроматографии на силикагеле (гексан:этилацетат=15:1), получая указанные в заголовке соединения (соединение 13А: 200 мг, соединение 13В: 120 мг), имеющие следующие физические свойства:
Соединение 13А:
ТСХ: Rf 0,49 (этилацетат:гексан=1;4);
ЯМР (СВDl3): δ 1,32-2,22 (м, 14Н), 2,27-2,50 (м, 3Н), 2,55-2,75 (м, 2Н), 2,78-3,00 (м, 2Н), 3,22-3,40 (м, 1Н), 5,26-5,35 (м, 1Н), 5,37-5,50 (м, 1Н), 5,55-5,71 (м, 1Н), 7,98 (с, 1Н).
Соединение 13 В:
ТСХ: Rf 0,46 (этилацетат:гексан=1:4);
ЯМР (CDCl3): δ 1,32-2,61 (м, 19Н), 2,80-3,01 (м, 2Н), 3,18-3,32 (м, 1Н), 5,26-5,36 (м, 1Н), 5,44-5,69 (м, 2Н), 7,96 (с, 1Н).
Пример 14
2-[(2-{(1R,2S,5R)-2-гидрокси-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 14)
Соединение 13А (200 мг) растворяют в смешанном растворителе из метанола (1,0 мл) и тетрагидрофурана (2,0 мл) и добавляют 2 н. водный раствор гидроксида натрия (0,62 мл), затем перемешивают при комнатной температуре в течение ночи. Реакционный раствор выливают в 1 н. соляную кислоту и экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют, получая указанное в заголовке соединение (190 мг), имеющее следующие физические свойства:
ТСХ: Rf 0,21 (этилацетат:метанол=5:1);
ЯМР (СОСl3): δ 1,19 (с, 3Н), 1,33-1,52 (м, 2Н), 1,59-2,14 (м, 7Н), 2,20 (д, J=6,6 Гц, 2Н), 2,25-2,51 (м, 3Н), 2,81-3,01 (м, 1Н), 3,50-3,67 (м, 1Н), 4,51-4,59 (м, 1Н), 4,31-5,54 (м, 2Н), 8,07 (с, 1Н).
Пример 15
Метил-2-[(2-{(1R,2S,5R)-2-гидрокси-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоксилат (соединение 15)
Карбонат калия (340 мг) и метилйодид (0,09 мл) добавляют к раствору соединения 14 (190 мг) в диметилформамиде (2,1 мл), затем перемешивают при комнатной температуре в течение ночи. Реакционный раствор выливают в воду и экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют, получая указанное в заголовке соединение (196 мг), имеющее следующие физические свойства:
ТСХ: Rf 0,36 (этилацетат:гексан=1:1);
ЯМР (CDCl3): δ 1,18 (с, 3Н), 1,29-1,49 (м, 2Н), 1,53-1,88 (м, 4Н), 1,91-2,11 (м, 3Н), 2,19 (д, J=6,2 Гц, 2Н), 2,27-2,52 (м, 3Н), 2,82-2,97 (м, 1Н), 3,50-3,68 (м, 1Н), 3,92 (с, 3Н), 4,42-4,53 (м, 1Н), 5,30-5,51 (м, 2Н), 7,98 (с, 1Н).
Пример 16
Метил-2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоксилат (соединение 16)
Диизопропилэтиламин (0,43 мл) и комплекс триоксида серы и пиридина (196 мг) добавляют к раствору соединения 15 (196 мг) в смеси диметилсульфоксид (1,4 мл)/этилацетат (2,8 мл), при охлаждении льдом, затем перемешивают в течение 15 минут. К реакционному раствору добавляют воду, затем экстрагируют этилацетатом. Органический слой промывают 1 н. соляной кислотой, водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют. Полученный остаток очищают путем колоночной хроматографии на силикагеле (гексан:этилацетат=3:2), получая указанное в заголовке соединение (152 мг), имеющее следующие физические свойства:
ТСХ: Rf 0,45 (этилацетат:гексан=1:1);
ЯМР (CDCl3): δ 1,16 (с, 3Н), 1,46-2,63 (м, 14Н), 3,37-3,49 (м, 2Н), 3,91 (с, 3Н), 5,45-5,57 (м, 1Н), 5,61-5,76 (м, 1Н), 8,01 (с, 1Н).
Пример 17
2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 17)
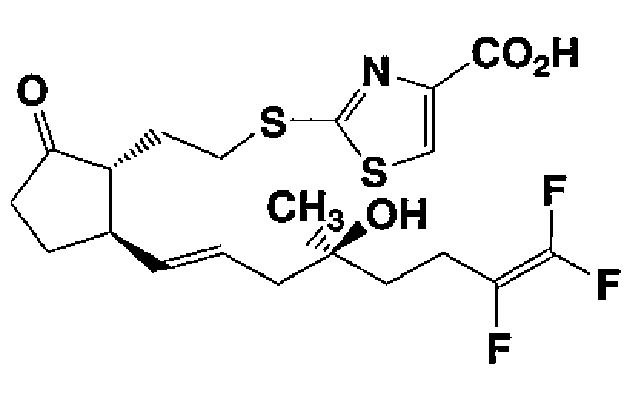
Соединение 16 (152 мг) растворяют в смеси 1,2-диметоксиэтан (2,0 мл)/вода (1,0 мл) и добавляют туда гидроксид лития (16,0 мг), при охлаждении льдом, затем перемешивают при комнатной температуре в течение 2 часов. Реакционный раствор выливают в 5%-ный водный раствор гидросульфата калия и экстрагируют этилацетатом. Органический слой промывают водой и насыщенным солевым раствором, сушат над безводным сульфатом натрия и концентрируют. Полученный остаток очищают путем колоночной хроматографии на силикагеле (гексан:этилацетат=1:1→метанол:этилацетат=1:10), получая указанное в заголовке соединение (127 мг, аморфная структура, вязкое масло), имеющее следующие физические свойства:
ТСХ: Rf 0,20 (этилацетат:метанол=5:1);
ЯМР (CDCl3): δ 1,21 (с, 3Н), 1,55-1,80 (м, 3Н), 1,88-2,60 (м, 11Н), 3,37 (т, J=7,50 Гц, 2Н), 5,54 (дд, J=14,82, 7,68 Гц, 1Н), 5,62-5,76 (м, 1Н), 8,11 (с, 1Н).
Пример 18
2-[(2-{(1R,5R)-2-оксо-5-[(1E,4R)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 18)
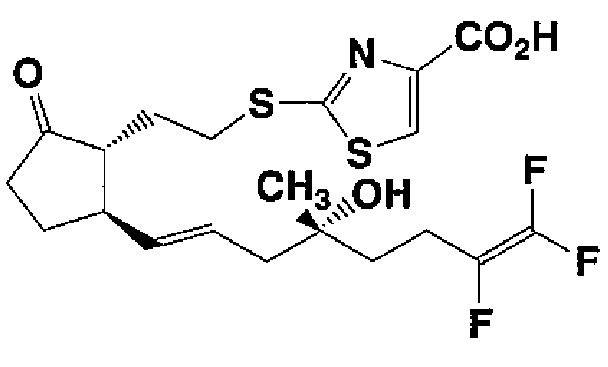
Следуют той же методике примеров 14→15→16→17, за исключением того, что соединение 13В используют вместо соединения 13А, получая указанное в заголовке соединение (57,3 мг, аморфное, вязкое масло).
ТСХ: Rf 0,20 (этилацетат:метанол=5:1);
ЯМР (CDCl3): δ 1,21 (с, 3Н), 1,56-1,79 (м, 3Н), 1,91-2,59 (м, 11Н), 3,31-3,42 (м, 2Н), 5,54 (дд, J=15,57, 8,04 Гц, 1Н), 5,61-5,77 (м, 1Н), 8,11 (с, 1Н).
Пример 19
2-[(2-{(1R,5R)-2-оксо-5-[(1E)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 19)
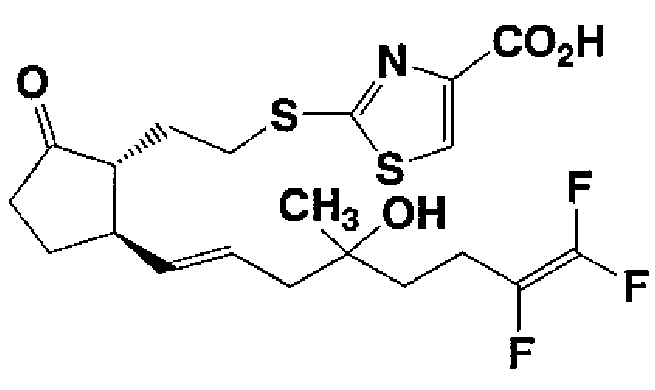
Следуют той же методике примеров 15→16→17, за исключением того, что соединение 11 используют вместо соединения 14, получая указанное в заголовке соединение (7,6 мг, аморфное, вязкое масло).
ТСХ: Rf 0,71 (этилацетат:метанол:уксусная кислота=8:1:1);
ЯМР (CDCl3): δ 1,21 (с, 3Н), 1,56-1,80 (м, 3Н), 1,90-2,60 (м, 11Н), 3,18-3,62 (м, 2Н), 5,54 (дд, J=15,3, 7,8 Гц, 1Н), 5,60-5,75 (м, 1Н), 8,10 (с, 1Н).
Пример 20
2-[(2-{(1S,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 20)
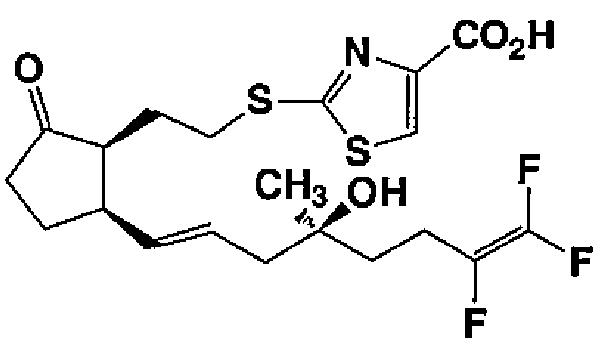
ТСХ: Rf 0,50 (метанол:хлороформ=1:9);
ЯМР (CDCl3): δ 8,13 (с, 1Н), 5,66 (дт, J=15,6 Гц, 1Н), 5,40 (дд, J=15,9 Гц, 1Н), 3,50-3,25 (м, 2Н), 3,15-3,05 (м, 1Н), 3,00-2,50 (м, 1Н), 2,50-2,25 (м, 4Н), 2,23 (д, J=6 ГЦ, 2Н), 2,20-2,00 (м, 3Н), 2,00-1,85 (м, 1Н), 1,85-1,60 (м, 3Н), 1,21 (с, 3Н).
Пример 21
Метил-2-[(2-{(1R,5S)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]-3-циклопентен-1-ил}этил)тио]-1,3-тиазол-4-карбоксилат (соединение 21)
ТСХ: Rf 0,38 (этилацетат:гексан=1:1);
ЯМР (CDCl3): δ 1,19 (с, 3Н), 1,60-1,80 (м, 2Н), 1,95 (м, 1Н), 2,23 (д, J=7,5 Гц, 2Н), 2,20-2,48 (м, 4Н), 3,30 (м, 1Н), 3,44-3,58 (м, 2Н), 3,91 (с, 3Н), 5,48 (дд, J=15,0, 8,4 Гц, 1Н), 5,84 (дт, J=15,0, 7,2 Гц, 1Н), 6,17 (дд, J=5,7, 2,1 Гц, 1Н), 7,49 (дд, J=5,7, 2,4 Гц, 1Н), 8,01 (с, 1Н).
Пример 22
β-циклодекстриновый клатрат 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоксилата натрия (молярное соотношение компонентов смеси=1:3)
Натриевую соль соединения 17 (8,12 мг) и β-циклодекстрин (56,88 мг) взвешивают и растворяют в очищенной воде (5 мл). Этот раствор оставляют стоять в течение 30 минут, лиофилизируют и сушат при пониженном давлении, при комнатной температуре, в течение ночи, получая указанное в заголовке соединение (64,8 мг).
ЯМР (D2O)
Пики от 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоксилата натрия: 7,81 (с, 1Н), 5,57-5,40 (м, 2Н), 3,26-3,19 (м, 2Н), 2,49 (м, 1Н), 2,35-1,98 (м, 9Н), 1,83 (м, 1Н), 1,64 (м, 1Н), 1,55-1,46 (м, 2Н), 1,01 (с, 3Н).
Пики от β-циклодекстрина: 4,91 (д, J=3,6 Гц, 1Н), 3,81-3,63 (м, 4Н), 3,51-3,41 (м, 2Н).
Биологические примеры
Путем следующих экспериментов продемонстрировано, что соединение согласно настоящему изобретению представляет собой соединение, обладающее активностью в отношении сокращения мочевого пузыря и расслабления уретры, не вызывает побочных эффектов и обладает хорошей фармакокинетикой, как, например, пероральная абсорбционная способность.
Дополнительно, также были проведены следующие сравнительные эксперименты для демонстрации того, что соединение согласно настоящему изобретению имеет лучшую фармакокинетику, как например, безопасность и пероральная абсорбционная способность, чем соединения, описанные в документах известного уровня техники.
Сравнительное соединение А: 2-[(2-{(1R,2R)-2-[(1E,4S)-4-гидрокси-4,7-диметил-1,7-октадиен-1-ил]-5-оксоциклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (4S-форма соединения 18-6, описанного в Международной публикации WO 2006/129788);
Сравнительное соединение В: 2-[(2-{(1R,2R)-2-[(1E,4S)-4-гидрокси-4-метил-1-нонен-1-ил]-5-оксоциклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (соединение 17-1, описанное в Международной публикации WO 2006/129788);
Сравнительное соединение С: 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-8,8,8-трифтор-4-гидрокси-4-метил-1-октенил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (4S-форма соединения 18-1, описанного в Международной публикации WO 2006/129788);
Сравнительное соединение D: 2-[(2-{(1R,2R)-2-[(1E,4S)-4-гидрокси-4-метил-1,7-октадиен-1-ил]-5-оксоциклопентил}этил)тио]-1,3-тиазол-4-карбоновая кислота (4S-форма соединения 32, описанного в Международной публикации WO 2006/129788);
Сравнительное соединение Е: 2-[(2-{(4S)-2-оксо-4-[(1E,4S)-8,8,8-трифтор-4-гидрокси-4-метил-1-октенил]-1,3-оксазолидин-3-ил}этил)сульфанил]-1,3-тиазол-4-карбоновая кислота (соединение 65-2, описанное в Международной публикации WO 2005/053707).
(1) Оценка активности в отношении сокращения детрузора мочевого пузыря и расслабления уретрального сфинктера
Конструирование резаных образцов
Крыс анестезировали с помощью пентобарбитала с последующим абдоминальным рассечением для удаления мочевых пузырей и уретр. Мочевые пузыри разрезали в продольном направлении для получения образцов в виде полосок размером примерно 10×3 мм. Дополнительно, каждую из уретр также разрезали в продольном направлении для получения образцов размером примерно 10×3 мм. Полученные образцы суспендировали в буфере Кребса (температура 37ºС, 5 мл), который аэрировали смешанным газом из 95% О2 и 5% СО2. Величины растяжения образцов измеряли, используя систему Magnus, оснащенную изометрическим датчиком и усилителем, и измеренные величины регистрировали на компьютере при использовании системы сбора данных.
Воздействия соединений на мочевые пузыри
Образцы суспендировали при нагрузке примерно 0,5 г. Спустя более чем 1 час добавляли хлорид калия (100 ммоль/л) и наблюдали ответную реакцию в отношении максимального сокращения. После промывки с помощью буфера Кребса образцы суспендировали при нагрузке примерно 0,5 г для стабилизации. Добавляли раствор хлорида калия (7,5 ммоль/л) для индуцирования сокращения образцов. После стабилизации индуцирующей сокращение ответной реакции кумулятивным образом добавляли тестируемое соединение и наблюдали ответную реакцию до и после обработки лекарственным средством.
Воздействие соединений на уретры
Образцы суспендировали при нагрузке примерно 0,5 г. Спустя более чем 1 час к суспензии добавляли хлорид калия (100 ммоль/л) и наблюдали ответную реакцию в отношении максимального сокращения. После промывки с помощью буфера Кребса образцы суспендировали при нагрузке примерно 0,5 г для стабилизации. После этого к суспензии добавляли фенилэфрин (100 ммоль/л) для индуцирования сокращения образцов. После стабилизации индуцирующей сокращение ответной реакции кумулятивным образом добавляли тестируемое соединение и наблюдали ответную реакцию до и после обработки лекарственным средством.
Результаты
Результаты представлены в таблицах 1 и 2.
Из вышеприведенных экспериментальных результатов следует, что соединение 17 вызывает сокращение детрузора мочевого пузыря и релаксацию уретрального сфинктера. Следовательно, соединение согласно настоящему изобретению воздействует на мочевой пузырь и уретру в отношении уменьшения интенсивности дисфункции сокращения мочевого пузыря и дисфункции уретральной релаксации, что является эффективным в случае недостаточно активного мочевого пузыря.
(2) Определение объемов остаточной мочи и емкостей мочевого пузыря в случае моделей недостаточно активного мочевого пузыря
Конструирование животных моделей и постоянного пребывания катетеров
Модели недостаточно активного мочевого пузыря конструировали в соответствии со следующей методикой. Самок крыс Wistar (в возрасте 8-9 недель) анестезировали путем интраперитонеального введения сомнопентила (40 мг/кг), с последующим выбриванием спины, и фиксировали в абдоминальных положениях. Каждую из дорсальных областей дезинфицировали с помощью хлоргексидинглюконата (жидкость с 5% гибитана). Область талии срединно разрезали для раскрытия позвоночника. После процесса эксцизии пятого поясничного остистого отростка в шестую поясничную область вставляли силиконовую прокладку через отверстие, просверленное с помощью мини-сверла. В целях избежания инфекций, после завершения хирургической операции в область разреза по каплям добавляли калийбензилпенициллин (25000 Ед/0,25 мл/организм). Мышцу и кожу области разреза сшивали шелковыми нитями и на область наложения шва наносили йодный раствор. После операции поддерживание опорожнения осуществляли путем мануальных компрессий три раза в сутки. В целях избежания инфекций подкожно вводили калийпенициллин G (1,25 единиц/организм). За более чем 5 суток до цистометрической оценки в мочевой пузырь вводили постоянно устанавливаемый катетер для получения цистометрограммы. Осуществляли анестезию с помощью натрийпентобарбитала (40 мг/кг путем интраперитонеального введения) и рассечение вдоль медианы живота, затем осуществляли разрез верхушки мочевого пузыря. Катетер для получения цистометрограммы, заполненный физиологическим солевым раствором, вставляли в мочевой пузырь через отверстие в апикальной области и фиксировали путем наложения лигарутры, используя шелковые нити для хирургических швов. Другой конец катетера фиксировали на дорсальной гиподерме. Область разреза нижней части спины и живота сшивали с помощью шелковых нитей. В мышцу ягодичной области осуществляли инфузию вициллина S500 (Meiji Co., Ltd., титр 10 мг/0,1 мл дистиллированная вода/крыса).
Подготовка к цистометрии
Крыс анестезировали (диэтиловым) эфиром и помещали в клетку Bollmann спустя 2 недели после конструирования моделей. С фронтальным концом каждого из катетеров мочевого пузыря связывали через трехходовой кран датчик давления и регистрировали внутрипузырное давление, используя регистратор усиления растягивающего давления. Один конец трехходового крана связывали с шприцом для внутрипузырной инстилляции, установленным на инфузионном насосе, а другой конец связывали с удлинительной трубкой, заполненной физиологическим солевым раствором, которую использовали для отвода остаточной мочи. Обработанных крыс оставляли в том же состоянии до тех пор, пока крысы не выходили из состояния анестезии.
Методика эксперимента
Перорально вводили воду для инъекции (группа с наполнителем) и тестируемое соединение (5 мг/кг). Спустя 1 час в мочевой пузырь вводили путем перфузии физиологический солевой раствор с объемной скоростью потока 2 мл/час и определяли параметры опорожнения (емкость мочевого пузыря и объем остаточной мочи). После осуществления перфузии в течение 1 часа и непосредственно после мочеиспускания перфузию прекращали и удаляли остаточную мочу из мочевого пузыря. Параметры опорожнения рассчитывали в случае каждой цистометрии. Что касается объемов остаточной мочи, сравнивали значения в случае группы с наполнителем и группы, где введено тестируемое соединение. Что касается емкостей мочевого пузыря, сравнивали значения в случае нормальной группы и тест-группы, где введено тестируемое соединение.
Результаты
Результаты представлены на фиг.1 и 2. Соединение 17 не воздействует на емкость мочевого пузыря в дозе (0,01 мг/кг), вызывающей значительное уменьшение объема остаточной мочи в случае моделей недостаточно активного мочевого пузыря. В противоположность, сравнительное соединение А при эффективной дозе (0,01 мг/кг) вызывает значительное уменьшение емкости мочевого пузыря.
Полагают, что уменьшение емкости мочевого пузыря, чем нормальный уровень, приводит к симптому накопления, когда моча не может быть накоплена, результатом чего является частое мочеиспускание, которое представляет собой побочное воздействие на мочевую систему.
Из результатов следует, что соединение согласно настоящему изобретению является эффективным в качестве терапевтического агента для недостаточно активного мочевого пузыря и в эффективной дозе не оказывает побочных воздействий на мочевую систему.
(3) Определение кровяного давления и частоты сердечных сокращений в случае нормальных крыс
Методика измерения
Кровяное давление и частоту сердечных сокращений самок крыс Wistar определяли в соответствии со следующей методикой. В день измерения, постоянное установление катетеров для измерения кровяного давления и частоты сердечных сокращений осуществляли под анестезией с помощью (диэтилового) эфира. Заднюю часть шеи каждой крысы разрезали; питательный катетер (Atom Medical Corporation), наполненный гепаринизированным физиологическим солевым раствором, вводили через заднюю часть шеи; катетер вставляли в общую сонную артерию; и хирургический разрез закрывали. Измерения осуществляли в клетке Bollmann в состоянии нахождения крыс в сознании и оценки осуществляли после подтверждения, что индивидуальные параметры стабилизированы. После подтверждения стабилизации кровяного давления и частоты сердечных сокращений перорально вводили в дозе 5 мл/кг тестируемое соединение, которое подготовляли, используя воду для инъекции, содержащую эквимолярное количество NaOH.
Катетер, выводимый из задней части шеи, связывали с датчиком давления (DX-200, NIHON KOHDEN CORP.) и кровяное давление и частоту сердечных сокращений измеряли, используя усилитель для измерения давления (Gould Instrument). Кровяное давление и частому сердечных сокращений рагистрировали, используя регистратор (LINEARCORDER WR3320, GRAPHTEC). В случае каждого индивидуума, степени увеличения и уменьшения, в среднем, кровяного давления и частоты сердечных сокращений до введения и спустя 30, 60, 120 и 180 минут после введения рассчитывали, принимая во внимание значения в случае каждого индивидуума до введения. Изменения кровяного давления и частоты сердечных сокращений оценивали до и после введения тестируемого соединения.
Результаты
На фиг.3 и 4 представлены результаты, полученные после введения соединения согласно настоящему изобретению (0,3 мг/кг) и сравнительного соединения (0,3 мг/кг).
Соединение 17 не оказывает воздействия на кровяное давление в дозе, соответствующей концентрации 0,3 мг/кг. Кроме того, соединение 17 не оказывает воздействия на кровяное давление даже в дозе, соответствующей концентрации 1 мг/кг. В противоположность, соединение А проявляет тенденцию к повышению кровяного давления в дозе, соответствующей концентрации 0,3 мг/кг, и к повышению примерно на 10% кровяного давления в дозе, соответствующей концентрации 1 мг/кг. Кроме того, сравнительное соединение В, сравнительное соединение С и сравнительное соединение D проявляют тенденцию к снижению кровяного давления в дозе, соответствующей концентрации 0,3 мг/кг.
Соединение 17 не оказывает воздействия на частоту сердечных сокращений в дозе, соответствующей концентрации 0,3 мг/кг. В противоположность, сравнительное соединение В, сравнительное соединение С и сравнительное соединение D в дозе, соответствующей концентрации 0,3 мг/кг, вызывают примерно 20%-ное увеличение частоты сердечных сокращений.
Вышеприведенные результаты показывают, что сравнительные соединения обладают риском влияния на кровяное давление и частоту сердечных сокращений, тогда как соединение согласно настоящему изобретению обладает незначительным воздействием на кровяное давление и частоту сердечных сокращений.
Следовательно, соединение согласно настоящему изобретению обладает незначительным риском побочных воздействий на сердечно-сосудистую систему.
(4) Измерение кровяного давления и частоты сердечных сокращений в случае крыс-гипертоников
Определяли кровяное давление и частоту сердечных сокращений в случае самцов крыс со спонтанной гипертонией. В день измерения, постоянное установление катетера для измерения кровяного давления и частоты сердечных сокращений и подлежащего введению вещества осуществляли под анестезией с помощью (диэтилового) эфира. Заднюю часть шеи каждой крысы разрезали; питательный катетер (Atom Medical Corporation), наполненный гепаринизированным физиологическим солевым раствором, вводили через заднюю часть шеи; катетер вставляли в общую сонную артерию и внутреннюю яремную вену и хирургический разрез закрывали. Измерения осуществляли в клетке Bollmann в состоянии нахождения крыс в сознании и оценки осуществляли после подтверждения, что индивидуальные параметры стабилизированы. После подтверждения стабилизации кровяного давления и частоты сердечных сокращений, внутривенно непрерывно вводили тестируемое соединение с объемной скоростью потока 5 мл/кг/час в течение 30 минут.
Катетер, выводимый из задней части шеи, связывали с датчиком давления (DX-200, NIHON KOHDEN CORP.) и кровяное давление и частоту сердечных сокращений измеряли, используя усилитель кровяного давления (Gould Instrument). Кровяное давление и частоту сердечных сокращений регистрировали, используя регистратор (LINEARCORDER WR3320, GRAPHTEC). Кровяное давление и частоту сердечных сокращений конвертировали в значения на бумаге для регистрации до введения и спустя 2,5, 5, 10, 15, 30, 45 и 60 минут после введения. Для каждого индивидуума, оценивали степени увеличения и уменьшения в параметрах относительно значения до введения (оценка во время 0 минут).
Результаты
Результаты представлены на фиг.5 и 6.
Соединение 17 не воздействует на кровяное давление. В противоположность, сравнительное соединение В снижает примерно на 10% кровяное давление при введении в дозе 100 нг/кг/мин. Дополнительно, оно снижает кровяное давление примерно на 25% при введении в дозе 300 нг/кг/мин.
Из результатов следует, что соединение согласно настоящему изобретению обладает незначительным риском побочных воздействий на сердечно-сосудистую систему в случае пациентов, страдающих сердечно-сосудистыми заболеваниями, такими как гипертензия.
(5) Пищеварительные симптомы
Используя самцов крыс в возрасте 6 недель, наблюдали обычные состояния крыс после повторяющегося перорального введения тестируемого соединения в дозе 0,1 мг/кг в течение 4 суток.
Результаты
Отсутствие пищеварительных симптомов, таких как «мягкие» фекалии, наблюдали в группах, которым вводили соединение 17. В противоположность, «мягкие» фекалии наблюдали в группах, которым вводили сравнительное соединение С, с первого дня после введения.
Таким образом, соединение согласно настоящему изобретению является безопасным, не вызывающим побочных воздействий на пищеварительную систему.
(6) Оценка мембранной проницаемости лекарственных средств (пероральная абсорбционная способность)
Проницаемость лекарственных средств через искусственные мембраны определяли путем анализа параллельной проницаемости искусственной мембраны (РАМРА) при следующих условиях. Для измерений использовали РАМРА-систему (pION). Мембранную проницаемость оценивали путем измерения коэффициентов мембранной проницаемости при трех значениях рН и суммирования значений (РАМРА(SUM) (см/с).
Липидная мембрана: GIT-0 (pION)
Длина волны: 190-498 нм
Время инкубации: 4 часа
Температура инкубации: 25ºС
Донор: содержащий 5% ДМСО буфер
Значение рН: 3 точки при 5,0, 6,2 и 7,4
Концентрация соединения: 50 мкмоль/л
Результаты
Коэффициенты мембранной проницаемости соединения 17 составляют 59,3 см/с, которые показывают очень хорошую мембранную проницаемость. С другой стороны, коэффициенты мембранной проницаемости сравнительного соединения Е составляют 0,6 см/с, и это может указывать на то, что мембранная проницаемость является низкой.
Результаты наводят на мысль, что соединение согласно настоящему изобретению обладает хорошей мембранной проницаемостью и является превосходным в отношении пероральной абсорбционной способности.
(7) Оценка системного клиренса
Эквимолярное количество гидроксида натрия и дистиллированную воду для инъекций добавляли к каждому из тестируемых соединений для получения водного раствора с концентрацией 1 мг/мл. Водный раствор разводили физиологическим солевым раствором вплоть до концентрации, достигающей 0,001 мг/мл, и быстро вводили в дозе 0,001 мг/мл/кг обезьянам рода Cynomolgus через головную вену. Спустя 2 минуты, 5 минут, 15 минут, 30 минут, 1 час, 2 часа, 4 часа, 6 часов, 8 часов и 24 часа после введения через гепаринизированные шприцы отбирали кровь из головной вены (участки, не использованные для введения). После центрифугирования отбирали плазму крови и хранили при температуре -80ºС до предварительной обработки. Плазму крови подвергали предварительной обработке путем смешения с ацетонитрилом и центрифугирования для удаления белков с последующим измерением путем LC/MS/MS. Изменения концентрации в плазме крови анализировали, используя WinNonlin 4.0.1, для оценки системного клиренса тестируемого соединения.
Результаты
Системный клиренс соединения 17 составляет 3,6 мл/мин/кг, который показывает медленную потерю из организма и эффективность непрерывного действия лекарственного средства. В противоположность, системный клиренс сравнительного соединения D составляет 23,9 мл/мин/кг, который является отчетливо выше клиренса, чем таковой соединения 17, и показывает очень быструю потерю из организма по сравнению с соединением 17.
(8) Оценка стабильности в лиофилизированных печеночных клетках
Среду КНЕМ 5100, которая включает человеческие лиофилизированные печеночные клетки после растворения (конечная концентрация живых клеток: 1×106 клеток/мл), и тестируемое соединение (ацетонирильный или метанольный раствор, конечная концентрация ≤1%) инкубировали при температуре 37ºС. Немедленно после реакции и вместе с прохождением времени реакции, из среды отбирали несколько порций образцов.
Концентрации тестируемого соединения в образцах определяли путем LC/MS/MS. Остаточную долю тестируемого соединения, относящуюся к таковой немедленно после реакции, рассчитывали по следующему уравнению:
Остаточная доля = концентрация тестируемого соединения в образце после реакции/концентрация тестируемого соединения в образце немедленно после реакции ×100(%)
По единой логарифмической шкале строили график зависимости остаточных долей от времени реакции для расчета констант потерь. Тест повторяли (n=2) и полученные значения усредняли.
Результаты
Результаты представлены ниже.
Остаточная доля сравнительного соединения В составляет 80% или меньше спустя 1 час после реакции и около 60% спустя 2 часа после реакции. В противоположность, остаточная доля соединения 17 составляет 100% спустя 1 час после реакции и 80% или даже более спустя 2 часа после реакции.
Результаты показывают высокую стабильность соединения согласно настоящему изобретению к метаболизму в печени.
(9) Воздействия на сердечную функцию
Обезьян рода Cynomolgus анестезировали с помощью пентобарбитала (в начальной дозе 20-30 мг/кг путем внутривенного введения; в дозе 4-5 мг/кг/час путем непрерывного внутривенного введения). Вставляли трахеальную трубку и осуществляли искусственную вентиляцию легких (свежий воздух плюс чистый кислород, вентиляционный объем: 10-15 мл/кг, частота вентиляции: 10-15 раз в минуту). В правом положении лежа, грудную клетку с левой стороны вскрывали между четвертым и пятым межреберными промежутками. Общую сонную артерию (начало левой передней нисходящей артерии или огибающее ответвление) и начало восходящей главной артерии расслаивали и там устанавливали датчики для измерения кровотока. Скорости кровотока определяли, используя электронный измеритель кровотока или ультразвуковой измеритель кровотока. Кровяное давление измеряли, используя датчик давления в положении, где катетер вставлен в правую бедренную артерию. Левое вентрикулярное внутреннее давление измеряли в положении, где катетер вставлен из левой сонной артерии в левый желудочек. Электрокардиограмму получали, используя игольчатые электроды, установленные в правую подмышку и грудную клетку с левой стороны. После того как катетеры для введения вставлены в правую и левую головные вены и бедренные вены, через них вводили тестируемое соединение, пентобарбитал (под анестезией) или водный раствор (SOLITA T3, содержащий 1,2% NaHCO3). Тестируемое соединение вводили непрерывно внутривенно в течение 30 минут, используя систему непрерывной инфузии. Кровяное давление, левое вентрикулярное внутреннее давление, скорость кровотока через коронарную артерию и данные электрокардиограммы одновременно вводили в систему Powerlab (LabChart 6, AD Instruments) для измерения/расчета среднего кровяного давления, частоты сердечных сокращений, среднего кровотока через коронарную артерию, пульсирующего объема крови, ударного объема крови (пульсирующий объем/частота сердечных сокращений), максимального первого отклонения от нормы левого вентрикулярного внутреннего давления, общей резистентности периферических кровеносных сосудов (средняя величина кровяного давления/пульсирующий объем крови), сердечной работоспособности (средняя величина кровяного давления х пульсирующий объем крови) и двойного продукта (систолическое артериальное давление х частота сердечных сокращений), что свидетельствует о потреблении кислорода миокардом.
Средние значения всех параметров оценки в течение 1 минуты получали до введения, немедленно после введения и спустя 10 минут, 20 минут и 30 минут после введения и рассчитывали изменения средних значений по отношению к значению, измеряемому до введения, которое определяли как 100%.
Результаты
Сердечная работоспособность и двойные продукты представлены на фиг.7 и 8. Соединение 17 и двойной продукт в дозах 30 нг/кг/мин и 10 нг/кг/мин не ухудшают сердечной работоспособности. Дополнительно, соединение 17 не ухудшает других параметров функции сердца, включая скорость кровотока через коронарную артерию. В противоположность, сравнительное соединение В оказывает ингибирующее действие на функции сердца.
Из вышеуказанного следует, что соединение согласно настоящему изобретению представляет собой безопасное соединение, которое не влияет на функции сердца.
(10) Воздействия на модели дисфункции мочевыделения
Конструирование животных моделей
Модели дисфункции мочевыделения конструировали в соответствии со следующей методикой. После анестезии обезьян рода Cynomolgus, участок от надлобковой области до абдоминальной области выбривали с последующей фиксацией в положении лежа на спине. Выбритый участок дезинфицировали и четыре конечности фиксировали. При использовании электрохирургического скальпеля участок кожи от надлобковой области до умбиликальной области и перитонеальной мембраны последовательно рассекали с последующим повреждением тазового нерва и удалением матки. После хирургической операции в разрезанную область по каплям вводили содержащий вициллин физиологический солевой раствор. Перитонеальную мембрану и кожу разрезанной области сшивали с помощью шелковых нитей и дезинфицировали. Вициллин вводили в течение 7 последовательных суток после хирургии. Мелоксикам вводили один раз в сутки в течение 7 последовательных суток для устранения боли в периоперационный период.
Методика эксперимента
Обезьян рода Cynomolgus сажали на «стулья для обезьян» с последующей фиксацией кистей рук и нижних конечностей с помощью завязок. Перорально вводили воду для инъекций, а физиологический солевой раствор и тестируемое соединение (60 нг/кг/час) вводили непрерывно внутривенно для предоставления возможности обильного мочеиспускания. Максимальную скорость потока мочи измеряли, используя датчик для определения массы мочи.
Результаты
В случае модели дисфункции мочевыделения, соединение 17 показало 61% улучшения в случае максимальной скорости потока мочи по отношению к группе с наполнителем. В противоположность, сравнительное соединение В и сравнительное соединение D показали только 27% и 36% улучшения в случае максимальной скорости потока мочи по отношению к группе с наполнителем.
Согласно результатам, показано, что соединение согласно настоящему изобретению является очень эффективным в промотировании мочеиспускания.
Результаты, полученные в биологических примерах (1)-(10), выявили, что соединение согласно настоящему изобретению обладает сокращающей мочевой пузырь активностью и уретральной релаксирующей активностью и в высокой степени промотирующей мочеиспускание активностью. Дополнительно, соединение согласно настоящему изобретению представляет собой соединение, которое является превосходным в отношении безопасности и способно избегать любого риска оказания побочных действий на мочевую систему, сердечно-сосудистую систему и пищеварительную систему, что не может быть достигнуто при использовании любых соединений, описанных в уровне техники. Кроме того, соединение согласно настоящему изобретению обладает превосходной фармакокинетикой, включая пероральную абсорбционную способность и метаболическую стабильность.
Примеры получения готовой лекарственной формы
Пример 1 получения готовой лекарственной формы
Соединение 17 (5,0 г), кальцийкарбоксиметилцеллюлозу (20 г), стеарат магния (10 г) и микрокристаллическую целлюлозу (920 г) смешивают обычным способом, затем подвергают сжатию с получением 10000 таблеток, где в каждой из таблеток находится 0,5 мг активного ингредиента.
Пример 2 получения готовой лекарственной формы
Соединение 17 (2,0 г), маннит (500 г) и дистиллированную воду (10 л) смешивают обычным способом, затем подвергают стерилизации обычным способом. 1 мл раствора вводят в ампулу и подвергают сушке вымораживанием по обычному способу. В целом получают 10000 ампул, где в каждой из ампул содержится 0,2 мг активного ингредиента.
Промышленная применимость
Соединение согласно настоящему изобретению обладает сокращающей активностью в отношении детрузора мочевого пузыря и релаксирующей активностью в отношении уретрального сфинктера. Следовательно, соединение согласно настоящему изобретению может уменьшать интенсивность дисфункции сокращения мочевого пузыря и/или дисфункции уретральной релаксации и является особенно эффективным в качестве агента для предотвращения и/или лечения недостаточно активного мочевого пузыря. Дополнительно, соединение согласно настоящему изобретению является эффективным в качестве агента для уменьшения интенсивности различных симптомов, связанных с недостаточно активным мочевым пузырем. Следовательно, соединение согласно настоящему изобретению является очень безопасным и проявляет превосходную фармакокинетику, включая пероральную абсорбционную способность, и т.д. Следовательно, соединение согласно настоящему изобретению является очень полезным в качестве лекарственного средства.
| название | год | авторы | номер документа |
|---|---|---|---|
| АМИНОВАЯ СОЛЬ И ЕЕ КРИСТАЛЛЫ | 2013 |
|
RU2658823C2 |
| АГЕНТ ДЛЯ РЕГЕНЕРАЦИИ И/ИЛИ ЗАЩИТЫ НЕРВОВ | 2006 |
|
RU2420316C2 |
| ЗАМЕЩЕННЫЕ ЦИКЛОПЕНТАНЫ, ОБЛАДАЮЩИЕ ПРОСТАГЛАНДИНОВОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2505530C2 |
| НОВЫЙ ЭФИР УКСУСНОЙ КИСЛОТЫ ИЛИ ЕГО СОЛЬ | 2013 |
|
RU2585759C2 |
| КОМБИНИРОВАННОЕ ЛЕЧЕНИЕ АГОНИСТОМ ТОЛЛ-ПОДОБНОГО РЕЦЕПТОРА (TLR7) И ИНГИБИТОРОМ СБОРКИ КАПСИДА ВИРУСА ГЕПАТИТА В | 2016 |
|
RU2718917C2 |
| ПИРИМИДИН- И АЗОТСОДЕРЖАЩЕЕ БИЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2020 |
|
RU2827867C1 |
| 3-АМИНОЦИКЛОПЕНТАНКАРБОКСАМИДНЫЕ ПРОИЗВОДНЫЕ | 2013 |
|
RU2641913C2 |
| ИНГИБИТОР ГЕКСОН-ГЛЮКОКИНАЗЫ И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2797185C2 |
| ИНГИБИТОРЫ КАНАЛОВ С ТРАНЗИТОРНЫМ ПОТЕНЦИАЛОМ НА ОСНОВЕ ОКСАДИАЗОЛОВ | 2019 |
|
RU2818244C2 |
| Соединения циклопентана | 2019 |
|
RU2794997C2 |
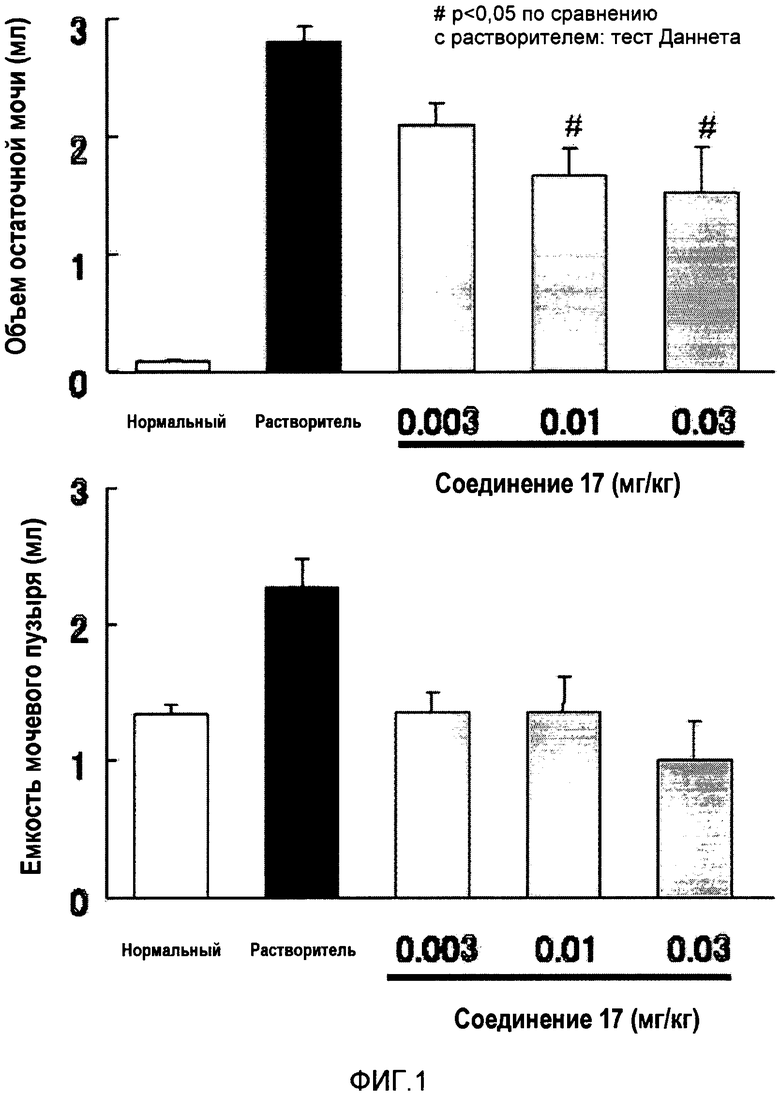
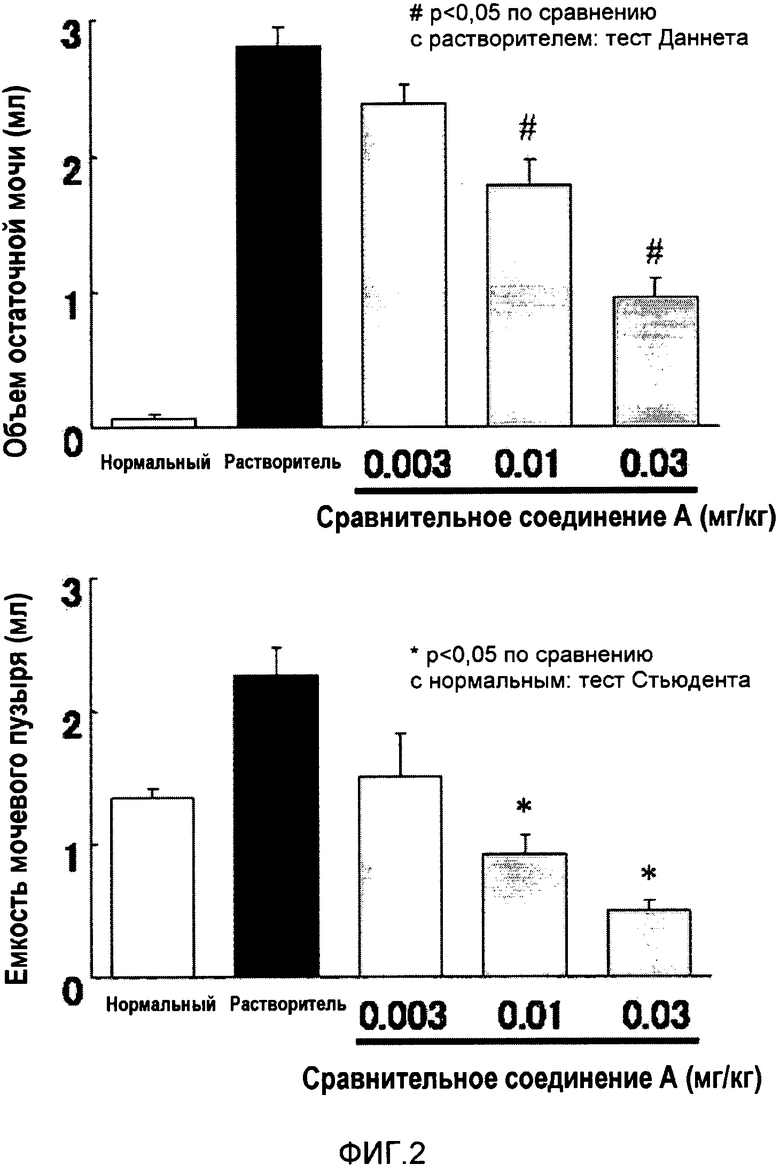
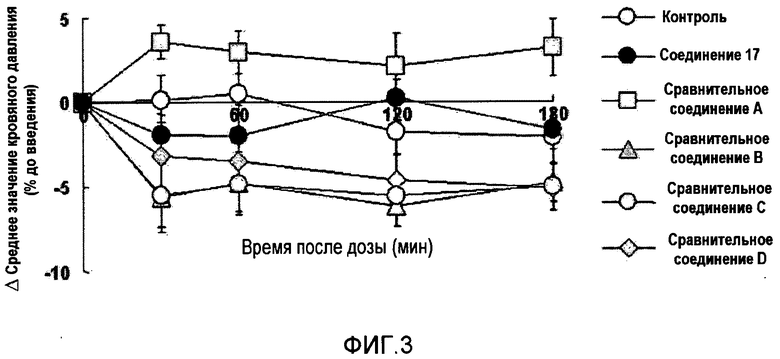
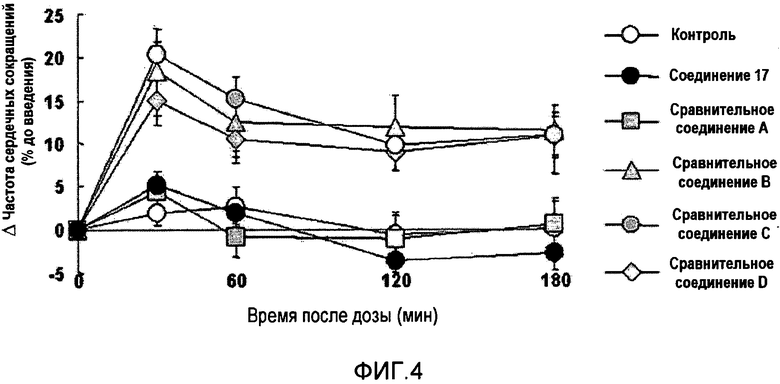
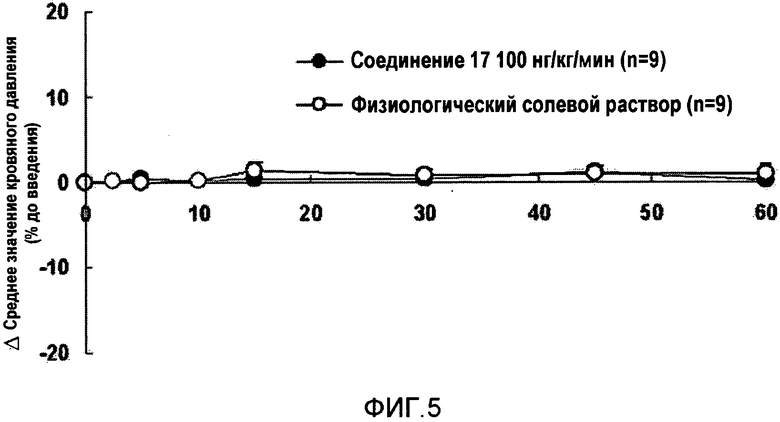
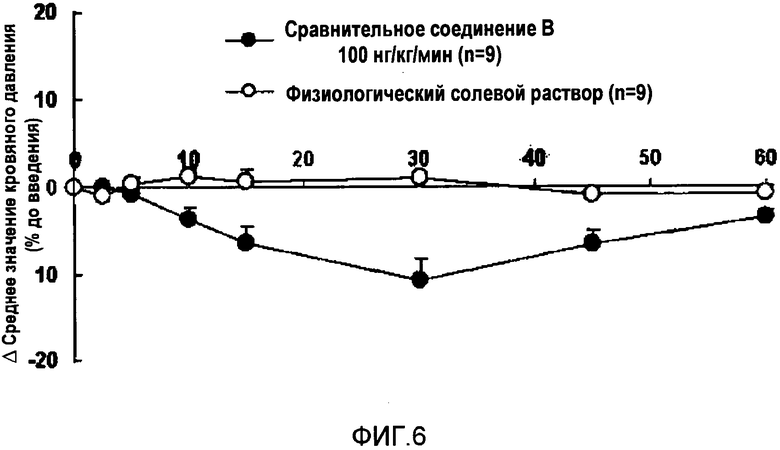
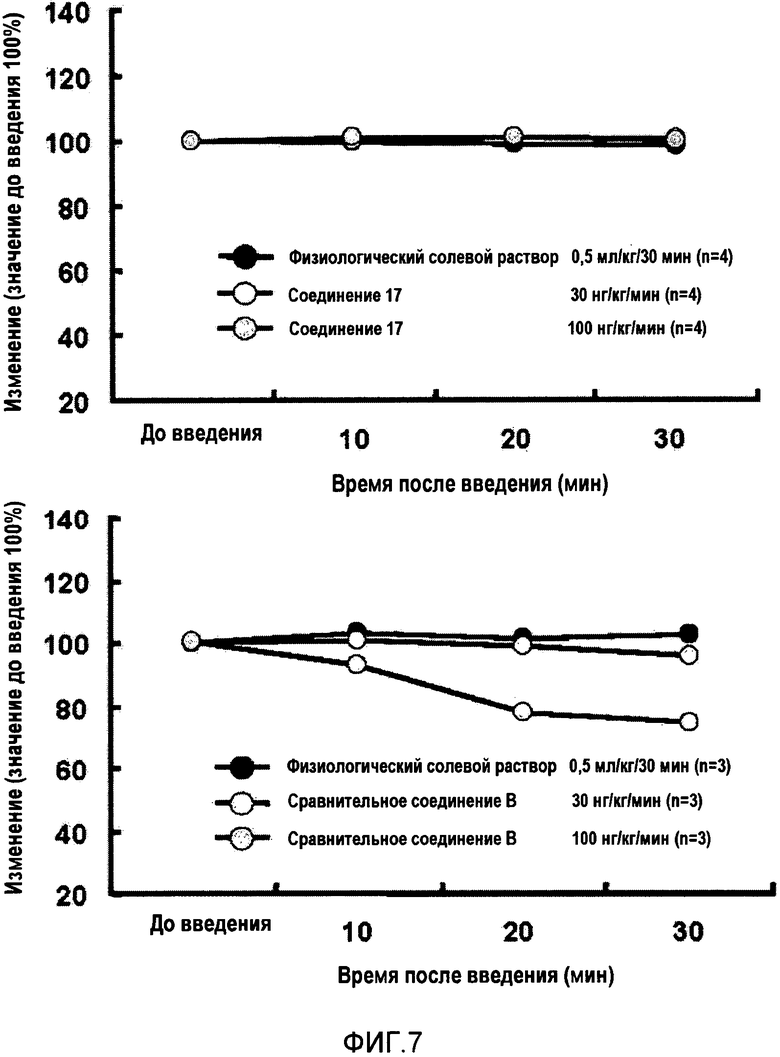
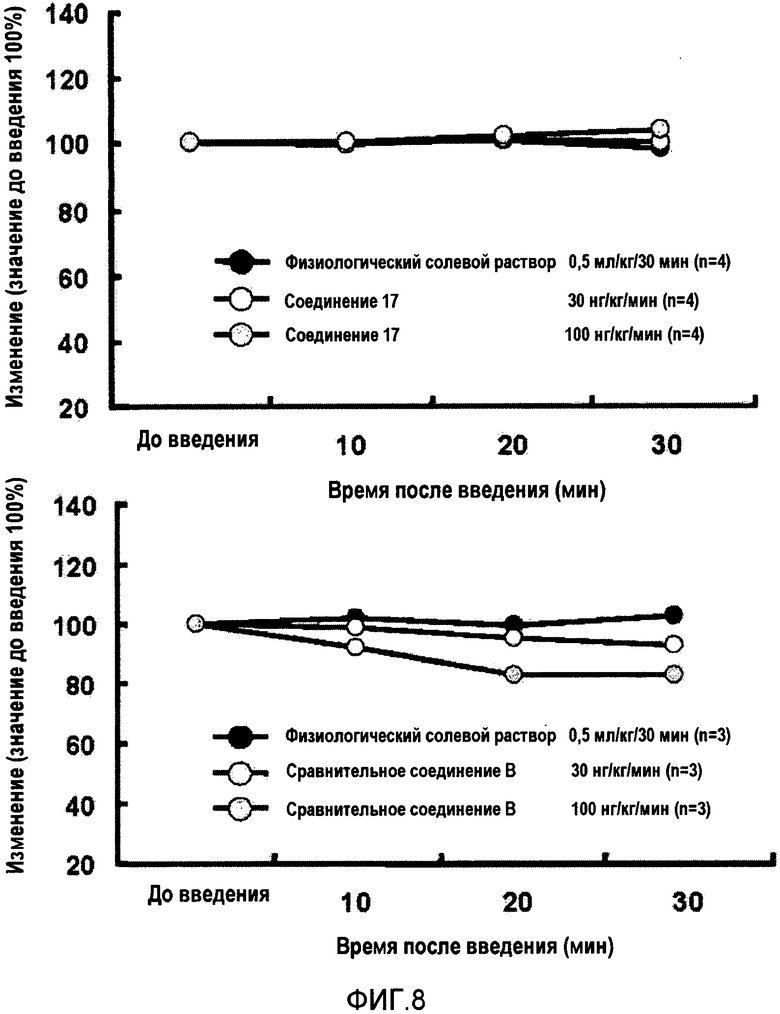
Изобретение относится к соединению, представленному формулой (I), где  представляет собой α-конфигурацию;
представляет собой α-конфигурацию;  представляет собой β-конфигурацию; и
представляет собой β-конфигурацию; и  представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь, его соль, или его смесь с диастереомером в произвольном соотношении, или его циклодекстриновый клатрат. Изобретение относится к фармацевтической композиции для предупреждения, лечения и/или уменьшения интенсивности дисфункции сокращения мочевого пузыря и/или дисфункции уретральной релаксации, содержащей, в качестве активного ингредиента, соединение, представленное формулой (I). Изобретение также относится к соединению, представленному формулой (I-a), где R1 представляет собой C1-C4-алкильную группу, такую как метил, этил, пропил, изопропил, бутил, изобутил или трет-бутил;
представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь, его соль, или его смесь с диастереомером в произвольном соотношении, или его циклодекстриновый клатрат. Изобретение относится к фармацевтической композиции для предупреждения, лечения и/или уменьшения интенсивности дисфункции сокращения мочевого пузыря и/или дисфункции уретральной релаксации, содержащей, в качестве активного ингредиента, соединение, представленное формулой (I). Изобретение также относится к соединению, представленному формулой (I-a), где R1 представляет собой C1-C4-алкильную группу, такую как метил, этил, пропил, изопропил, бутил, изобутил или трет-бутил;  представляет собой α-конфигурацию;
представляет собой α-конфигурацию;  представляет собой β-конфигурацию; и
представляет собой β-конфигурацию; и  представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь, его соль, или его смесь с диастереомером в произвольном соотношении, или его циклодекстриновый клатрат. Технический результат - соединение согласно настоящему изобретению пригодно в качестве превосходного агента для предупреждения, лечения и/или улучшения недостаточно активного мочевого пузыря. 5 н. и 3 з.п. ф-лы, 3 табл., 8 ил., 24 пр.,
представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь, его соль, или его смесь с диастереомером в произвольном соотношении, или его циклодекстриновый клатрат. Технический результат - соединение согласно настоящему изобретению пригодно в качестве превосходного агента для предупреждения, лечения и/или улучшения недостаточно активного мочевого пузыря. 5 н. и 3 з.п. ф-лы, 3 табл., 8 ил., 24 пр.,
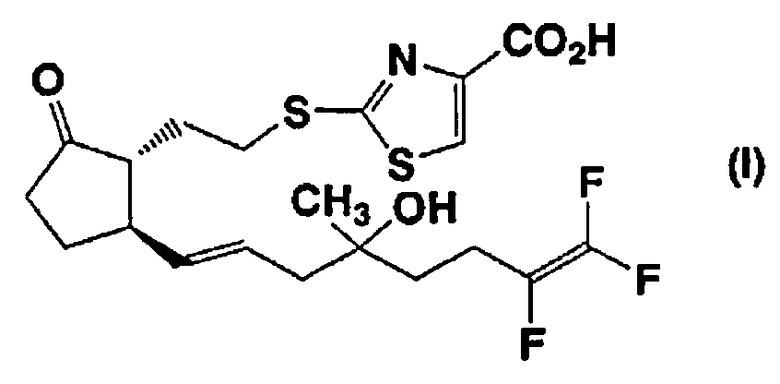
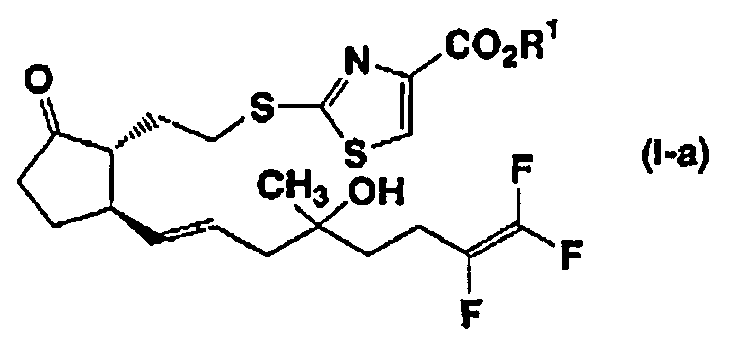
1. Соединение, представленное формулой (I):

где  представляет собой α-конфигурацию;
представляет собой α-конфигурацию;
 представляет собой β-конфигурацию; и
представляет собой β-конфигурацию; и
 представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь,
представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь,
его соль, или его смесь с диастереомером в произвольном соотношении, или его циклодекстриновый клатрат.
2. Соединение по п.1, где соединение представляет собой:
(1) 2-[(2-{(1R,5R)-2-оксо-5-[(1E)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту,
(2) 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту, или
(3) 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4R)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту.
3. Соединение по п.1, представляющее собой смесь в произвольном соотношении соединения, которое представляет собой 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту, и диастереомера, который представляет собой 2-[(2-{(1S,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту.
4. Фармацевтическая композиция для предупреждения, лечения и/или уменьшения интенсивности дисфункции сокращения мочевого пузыря и/или дисфункции уретральной релаксации, содержащая, в качестве активного ингредиента, соединение, представленное формулой (I):
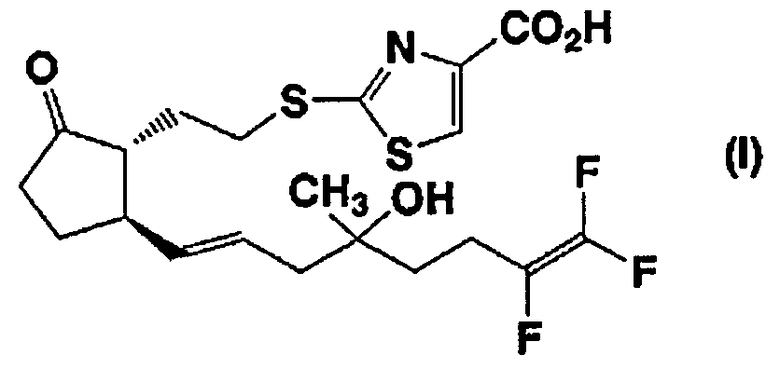
где все из символов имеют такие же значения, как определено в п.1,
его соль, или его смесь с диастереомером в произвольном соотношении, или его циклодекстриновый клатрат.
5. Фармацевтическая композиция по п.4, где дисфункцией сокращения мочевого пузыря и/или дисфункцией уретральной релаксации является недостаточно активный мочевой пузырь.
6. Соединение, представляющее собой 2-[(2-{(1R,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту или ее соль.
7. Соединение, представляющее собой 2-[(2-{(1S,5R)-2-оксо-5-[(1E,4S)-7,8,8-трифтор-4-гидрокси-4-метил-1,7-октадиен-1-ил]циклопентил}этил)тио]-1,3-тиазол-4-карбоновую кислоту или ее соль.
8. Соединение, представленное формулой (I-a):

где R1 представляет собой C1-C4-алкильную группу, такую как метил, этил, пропил, изопропил, бутил, изобутил или трет-бутил;
 представляет собой α-конфигурацию;
представляет собой α-конфигурацию;
 представляет собой β-конфигурацию; и
представляет собой β-конфигурацию; и
 представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь,
представляет собой α-конфигурацию, β-конфигурацию или их произвольную смесь,
его соль, или его смесь с диастереомером в произвольном соотношении, или его циклодекстриновый клатрат.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ проходки вертикальной выработки | 1990 |
|
SU1707208A1 |
| Железнодорожное колесо | 1990 |
|
SU1782830A1 |
| ПРОИЗВОДНОЕ 8-АЗАПРОСТАГЛАНДИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, АГЕНТ ДЛЯ ПРОФИЛАКТИКИ ЗАБОЛЕВАНИЙ | 2003 |
|
RU2306309C2 |
Авторы
Даты
2014-10-20—Публикация
2010-06-09—Подача