Изобретение относится к области фармации и касается способа получения средства, обладающего противоязвенным действием.
Одной из актуальных проблем современной гастроэнтерологии является поиск и изучение новых высокоэффективных средств лечения заболеваний органов желудочно-кишечного тракта. Несмотря на значительные успехи, достигнутые в области синтетических противоязвенных средств, растения продолжают оставаться одним из перспективных источников получения новых биологически активных соединений. Например, широко используются препараты из растительного сырья, такие как «Викаир», «Викалин», «Бефунгин» и др., обладающие противоязвенным действием (Машковский М.Д. Лекарственные средства. 15-е изд., перераб., испр. и доп. М.: ООО «Изд-во Новая Волна», 2005. 1200 с.: ил.).
Среди растительных сырьевых источников, содержащих биологически активные вещества (БАВ) противоязвенного действия, следует выделить кору осины обыкновенной (Populus tremula L.), семейство ивовых (Salicaceae), род тополь (Populus), которая содержит в значительных количествах различные фенольные соединения (фенологликозиды, фенолокислоты, флавоноиды) (Турецкова В.Ф. Теоретическое и экспериментальное обоснование рационального использования коры и побегов облепихи крушиновидной и коры осины обыкновенной: автореф. дис.… д-ра. фарм. наук. Пермь, 2001. 49 с.).
Известен способ получения средства, обладающего противоязвенным действием, из листьев ивы в виде настоя, представляющего собой водную вытяжку из высушенных измельченных листьев ивы, получаемую путем экстрагирования сырья кипящей водой при соотношении компонентов 1:9, времени настаивания 30 мин, охлаждения - 45 мин (Патент №2187322).
Недостатками известного способа являются:
- невозможность использования в промышленных условиях в связи с химической и микробиологической нестабильностью водных извлечений при хранении (срок хранения не более 1 суток);
- использование кипящей воды в процессе изготовления, что сможет привести к разрушению основных БАВ (фенологликозидов) данного вида сырья.
Наиболее близким по достигаемому техническому результату, прототипом, является способ получения средства, обладающего противоязвенным действием, суть которого заключается в том, что экстрагируют 40° этиловым спиртом измельченную до 5-10 мм кору осины с законченным или незаконченным циклом в батарее из 5-6 диффузоров при 18-25°C и при соотношении сырье:экстрагент 1:2,3-3,0 в течение 8-16 часов однократно, отстаивают в течение 3 суток при температуре 6-8°C, сгущают в течение 18 ч при 32°C под вакуумом, а затем высушивают в вакуум-сушильном шкафу при 40°C в течение 3-6 ч или 40-градусное извлечение сушат распылительным методом, предварительно отогнав под вакуумом 1/2 часть экстрагента или разбавив 40-градусное извлечение в 2 раза водой, при температуре на входе 120°C, а на выходе 65°C в течение 2-3 с (Патент №2086251).
Недостатками известного способа являются:
- невозможность обеспечения высокой точности дозирования, так как он не является дозированным лекарственным средством;
- невозможность маскировки горького вкуса;
- возможность снижения стабильности за счет отсыреваемости экстракта при хранении.
Техническим результатом заявляемого изобретения является увеличение точности дозирования и эффективности действия экстракта, а также уменьшение отсыреваемости и повышение удобства его применения за счет введения вспомогательного вещества лудипресса и/или использования капсулированной лекарственной формы.
Технический результат достигается тем, что к экстракту коры осины сухому добавляют лудипресс в массовом соотношении 35:13 соответственно с последующим наполнением твердых желатиновых капсул по 0,48 г полученной массы.
Авторы предлагают способ получения средства, обладающего противоязвенным действием, позволяющий повысить гастрозащитную активность экстракта коры осины сухого, а также устранить его отсыреваемость с одновременным коррегированием органолептических свойств.
Способ осуществляют следующим образом
Способ проиллюстрирован фиг.1-15.
На фиг.1 представлены данные по изучению технологических свойств экстракта коры осины сухого.
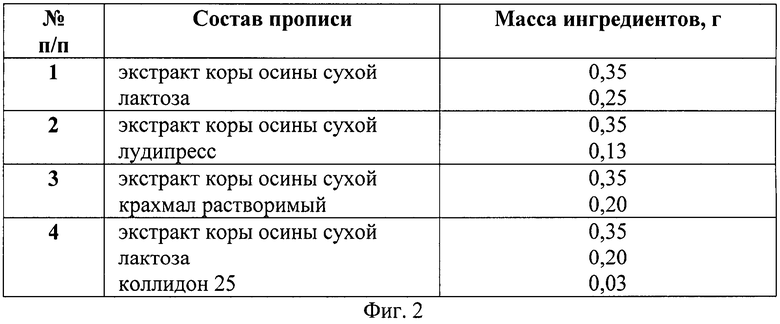
На фиг.2 предложены четыре прописи, в состав которых включили различные количества вспомогательных веществ, позволяющих регулировать технологические свойства экстракта коры осины сухого.
На фиг.3 представлены данные по изучению влажности изучаемых составов, полученных по различным прописям, где 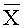
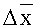
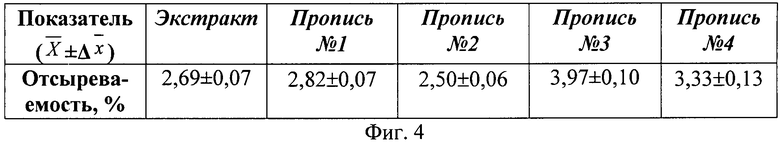
На фиг.4 дана таблица по изучению отсыреваемости изучаемых составов, где 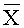
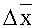
На фиг.5 представлены данные по изучению гигроскопичности исследуемых составов, где 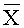
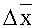
На фиг.6 представлены данные по изучению сыпучести и углу естественного откоса исследуемых составов, где 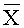
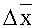
На фиг.7 представлена таблица по изучению показателя насыпного объема изучаемых составов, где 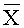
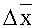
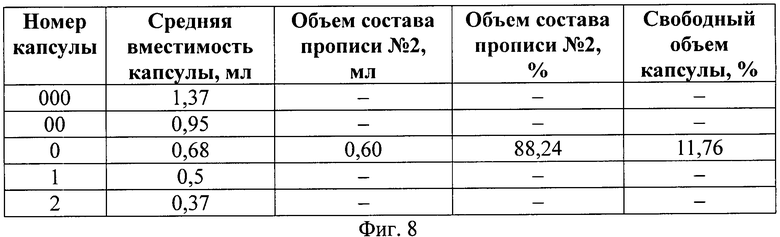
На фиг.8 даны расчетные данные по подбору размера твердых желатиновых капсул.
На фиг.9 дана таблица анализа полученных капсул по показателям «Описание», «Влажность» и «Микробиологическая частота» в течение года хранения, где 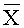
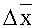
На фиг.10 представлена средняя масса капсул, отклонение массы каждой капсулы и массы содержимого каждой капсулы в течение одного года хранения.
На фиг.11 представлены данные по количественному содержанию основных групп БАВ в течение одного года хранения, где 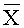
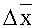
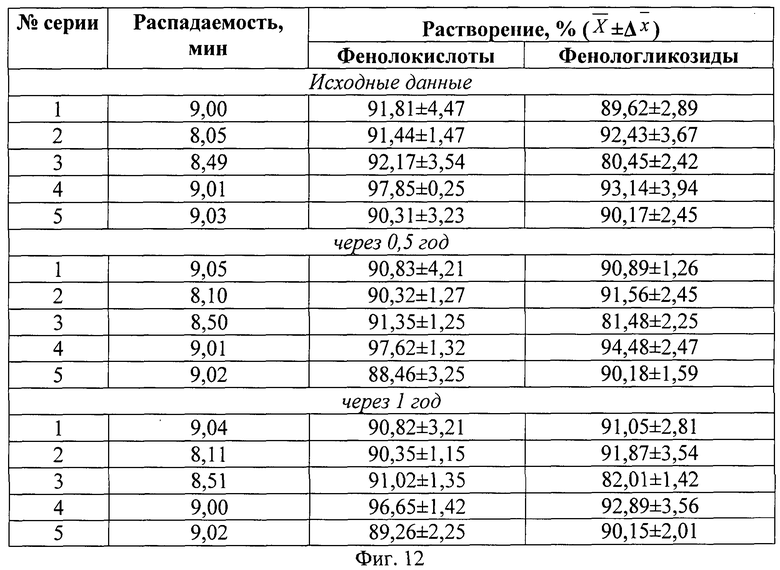
На фиг.12 представлены основные показатели тестов «Распадаемость» и «Растворение» в течение одного года хранения, где 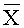
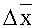
На фиг.13 представлено влияние курсового назначения экстракта коры осины, таблетированной и капсулированной смесей, на развитие нейрогенного язвообразования в слизистой желудка у мышей-самок CD1 (X±m) (в данной таблице и 2, 3 перед уровнем значимости P указаны номера сравнимаемых групп).
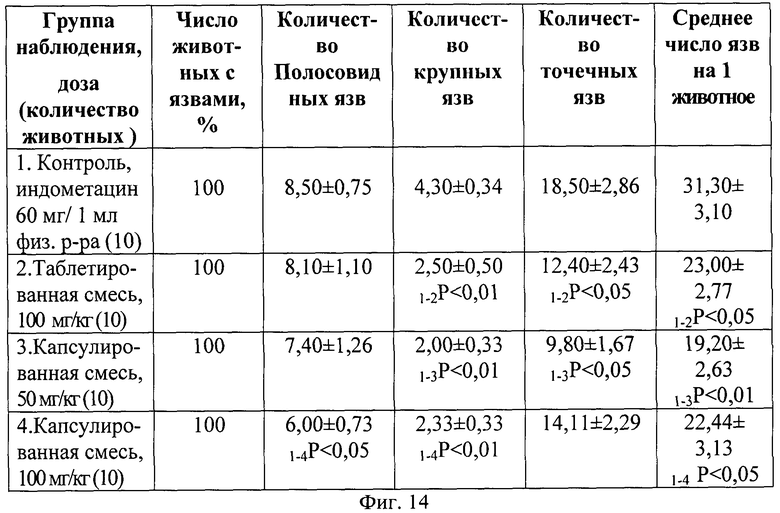
На фиг.14 представлено влияние курсового назначения экстракта коры осины, таблетированной и капсулированной смесей, на развитие индометацинового язвообразования в слизистой желудка у крыс-самок CD1 (X±m).
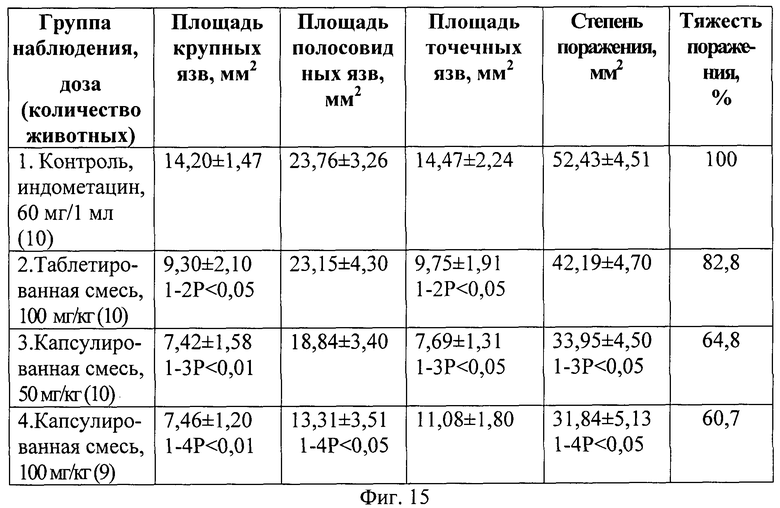
На фиг.15 представлено влияние курсового назначения экстракта коры осины, таблетированной и капсулированной смесей, на развитие индометацинового язвообразования в слизистой желудка у крыс-самок CD1 (X±m).
Пример выполнения способа
350 г измельченного экстракта коры осины сухого, полученного с использованием многоступенчатого противоточного экстрагирования спиртом этиловым 40% с последующей очисткой, сгущением под вакуумом при температуре 40-50°C и сушкой в вакуумном шкафу при температуре 40-50°C, тщательно смешивают с 130 г лудипресса (0-BASF, Германия), полученной смесью наполняют твердые желатиновые капсулы цилиндрической формы с гладкой поверхностью 0 номера по 0,48 г на автомате (или полуавтомате) для наполнения капсул.
Полученные капсулы имеют среднюю массу 0,546 г, отклонение от средней массы 0,05-4,12%, среднее содержимое капсулы 0,484 г, отклонение от среднего содержимого капсулы 0,10-4,96%; содержание фенологликозидов 0,0832±0,0037 г; содержание салицина 0,0202±0,0020 г; содержание фенолокислот 0,0253±0,0010 г; распадаемость составляет 9,01 мин; растворение фенологликозидов 93,14±3,94%, растворение фенолокислот 97,85±0,25%; по микробиологической чистоте соответствуют категории 3Б.
Заявляемый способ получения средства, обладающего противоязвенным действием с экстрактом коры осины сухим, имеет следующие преимущества перед известным: увеличение точности дозирования и эффективности действия экстракта, а также уменьшение отсыреваемости и повышение удобства его применения за счет научно-обоснованного выбора фармацевтических факторов (введения вспомогательного вещества лудипресса и/или использования капсулированной лекарственной формы).
С точки зрения биофармации эффективность действия лекарственного препарата в значительной мере зависит от правильного выбора фармацевтических факторов, используемых при разработке и производстве лекарственных средств, и, в первую очередь, от применяемых вспомогательных веществ. С современных позиций нет индифферентных и универсальных вспомогательных веществ, в связи с чем состав каждого конкретного препарата должен быть научно обоснован [Тенцова А.И., 1971; Демина Н.Б, 2013].
Выбор вспомогательного вещества и лекарственной формы проведен на основании изложенных ниже фармакотехнологических экспериментов.
Результаты проведенных исследований по изучению технологических свойств экстракта показали, что он обладает удовлетворительной сыпучестью, большим насыпным объемом, невысокой влажностью, отсыреваемостью и достаточно высокой гигроскопичностью (фиг.1).
Анализ технологических свойств экстракта коры осины сухого позволил предположить возможность изготовления твердых желатиновых капсул с крышечкой с добавлением вспомогательных веществ, улучшающих сыпучесть и снижающих гигроскопичность. В связи с чем нами было разработано и получено 4 прописи, в состав которых включили различные количества вспомогательных веществ, позволяющих регулировать вышеназванные показатели и изучить их технологические свойства (фиг.2).
Анализ результатов показал, что влажность (фиг.3) и отсыреваемость (фиг.4) сухого экстракта снижал только лудипресс (пропись №2), все остальные вспомогательные вещества, наоборот, увеличивали данные показатели. Гигроскопичность прописи №2 с лудипрессом по сравнению с экстрактом снижалась с 20,43±0,56 до 11,27±0,47% (фиг.5).
Поэтому дальнейшие исследования по определению технологических свойств были проведены со всеми выше указанными смесями.
Результаты исследований свидетельствуют о том, что лучшей сыпучестью обладает капсулированная масса, приготовленная по прописи №2 (фиг.6). Все прописи имеют высокие показатели насыпного объема (от 803,86±0,24 до 909,5 5±0,46 кг/м3) (фиг.7).
Сопоставление полученных данных по технологическим показателям позволило сделать заключение о том, что наиболее рационально изготавливать капсулы по прописи №2, так, данная пропись обеспечивает одновременно хорошую сыпучесть, а также более низкую влажность, отсыреваемость и гигроскопичность капсулируемой массы.
Подбор размера твердых желатиновых капсул для выбранной прописи осуществляют исходя из средней вместимости капсулы согласно требованиям ГФ XI, т.2., с.144, статья «Капсулы».
Вместимость капсулы рассчитывают по формуле:
 ,
,
где V - средняя вместимость капсулы, мл;
m - масса экстракта коры осины сухого;
p - насыпной объем, г/см3.
Расчеты показали, что для капсулирования терапевтической дозы экстракта коры осины сухого по прописям №2 необходимо использовать капсулы 0 номера (фиг.8).
Изучение стабильности полученного капсулированного препарата по показателям, регламентируемым требованиями ГФ XI изд., ОФС «Капсулы» и ОСТу 91500.05.001-00 «Стандарты качества лекарственных средств. Основные положения», а также влажность содержимого капсул в процессе естественного хранения при относительной влажности воздуха 40% и температуре 15-25°C в течение одного года представлены в таблицах (фиг.9-12).
Из данных, представленных на (фиг.9), следует, что показатели описание, влажность содержимого капсул и микробиологическая чистота соответствуют предъявляемым требованиям и не изменяются в течение одного года.
Определение средней массы капсул, отклонения массы каждой капсулы и массы содержимого показало, что все серии соответствуют предъявленным требованиям (фиг.10).
Исследование стабильности капсулированного препарата по содержанию двух групп БАВ (фенолокислоты и фенологликозиды методом СФМ), а также основного фенологликозида салицина методом ВЭЖХ показало, что содержание действующих веществ практически не изменяется в течение одного года хранения (фиг.11).
Высокие показатели тестов «Распадаемость» и «Растворение», соответствующие требованиям ГФ XI изд. и ОФС 42-0003-00 «Растворение» (фиг.12) исследуемого экспериментального препарата, подтверждают рациональность выбора капсул в качестве лекарственной формы.
Учитывая тот факт, что вспомогательные вещества являются одним из наиболее значимых факторов, оказывающим влияние на эффективность действия лекарственных веществ, далее была проведена сравнительная оценка фармакологической активности равных доз экстракта коры осины в присутствии выбранного выше в технологических исследованиях вспомогательного вещества лудипресса для получения капсул и смеси крахмала и талька, применяемой ранее при получении таблеток с экстрактом коры осины сухим (Патент №2124899).
Сравнительная оценка фармакологической активности таблетируемой смеси экстракта коры осины сухого и его капсулируемой смеси проведена на моделях нейрогенного и индометацинового ульцерогенеза на двух видах животных (52 аутбредных мышах-самках CD1 и 39 аутбредных крысах-самках CD). Выбор данных моделей язвообразования обусловлен важностью факторов патогенеза, лежащих в основе этих моделей, в инициации и хронизации язвенного процесса желудка и двенадцатиперстной кишки и других кислотозависимых заболеваний ЖКТ.
Нейрогенная язва. В механизме генеза модели «стресс-язвы» ведущее место занимает нейрогуморальный фактор, поэтому данная модель является наиболее адекватной среди быстровоспроизводимых «острых» экспериментальных язв [Заводская И.С., Морева Е.В., 1981]. Модель нейрогенного повреждения используется в качестве скрининговой для выявления средств, обладающих противоязвенной активностью. Методика исследования заключалась в следующем: мышей подвешивали корнцангами за кожную шейную складку, в результате 24-часовой частичной иммобилизации у животных развивалось язвенное поражение слизистой оболочки желудка. Последнее введение препарата приходилось за 1 ч до начала действия язвообразующего фактора (курс составил 4 введения).
Индометациновая язва. Ульцерогенное действие нестероидных противовоспалительных средств (НПВС), применяемых по жизненным показаниям в рамках кардиальной и противоревматической терапии, определяет актуальность разработки профилактических и лечебных гастроэнтерологических мероприятий. Среди нестероидных противовоспалительных препаратов индометацин обладает наиболее выраженным ульцерогенным действием, что послужило основанием для выбора данного препарата в качестве повреждающего агента.
Модель индометацинового повреждения слизистой желудка крыс воспроизводили путем однократного внутрижелудочного введения индометацина в дозе 60 мг/кг в 1 мл физиологического раствора по окончании курсового назначения (4 сут) исследуемых субстанций.
Последнее введение субстанций приходилось за 1 ч до начала действия язвообразующего фактора.
Критерии эффективности противоязвенной активности
В конце экспериментов мышей умерщвляли методом краниоцервикальной дислокации, крыс - ингаляцией CO2, желудки извлекали, вскрывали по малой кривизне, промывали холодным физиологическим раствором и макроскопически с помощью лупы при ярком освещении определяли число и площадь деструкций, которые дифференцировали на точечные (менее 1 мм) и крупные (более 1 мм). Подсчитывали среднее количество изъязвлений на одно животное в группе, процент животных с язвами [Хаджай Я.И. и др., 1962].
Индекс Паулса (ИП) определяли как интегральный показатель количества деструкций по формуле:

Противоязвенную активность (ПА) препаратов определяли как отношение индекса Паулса в контрольной группе к индексу Паулса в опытной группе. Исследуемое средство считали активным, если ПА составляла 2 и более единиц [Pauls F., Wick A.M., Mac Key E.M. et al., 1947; Добряков Ю.И., 1978]. Степень повреждения (СП) слизистой оболочки желудка и тяжесть повреждения (ТП) характеризовали на основании расчетов суммарной длины всех повреждений слизистой оболочки желудка (в мм) у каждой крысы и процентного уменьшения ТП у опытных животных по отношению к этому показателю у контрольных крыс.
Модель нейрогенного повреждения
На модельной системе нейрогенного повреждения слизистой желудка мышей были сформированы следующие группы.
1. Стресс-контроль (11) - мыши получали растворитель - дистиллированную воду в объеме 0,4 мл внутрижелудочно через зонд ежесуточно профилактическим курсом в течение 4 сут, последнее введение за 1 ч до иммобилизации.
2. Экстракт коры осины, таблетируемая смесь, 100 мг/кг (10) - мыши получали препарат в объеме 0,4 мл дистиллированной воды внутрижелудочно через зонд ежесуточно профилактическим курсом в течение 4 сут, последнее введение за 1 ч до иммобилизации.
3. Экстракт коры осины, таблетируемая смесь, 200 мг/кг (10) - мыши получали препарат в объеме 0,4 мл дистиллированной воды внутрижелудочно через зонд ежесуточно профилактическим курсом течение 4 сут, последнее введение за 1 ч до иммобилизации.
4. Экстракт коры осины, капсулируемая смесь, 100 мг/кг (10) - мыши получали препарат в объеме 0,4 мл дистиллированной воды внутрижелудочно через зонд ежесуточно профилактическим курсом в течение 4 сут, последнее введение за 1 ч до иммобилизации.
5. Экстракт коры осины, капсулируемая смесь, 200 (11) - мыши получали препарат в объеме 0,4 мл внутрижелудочно через зонд ежесуточно профилактическим курсом в течение 4 сут, последнее введение за 1 ч до иммобилизации.
Профилактическое курсовое внутрижелудочное введение капсулируемой смеси в дозах 100 и 200 мг/кг приводило к существенному повышению резистентности слизистой оболочки желудка мышей к повреждающему действию иммобилизационного стресса (фиг.13). Гастрозащитное действие новой лекарственной формы выразилось в значительном снижении числа животных с язвами (P<0,01) в обеих исследуемых группах по сравнению с показателем стресс-контроля. Следует отметить существенное снижение среднего количества язв в группах назначения капсулируемой смеси в дозах 100 (P<0,05) и 200 (Р<0,01) мг/кг за счет уменьшения числа точечных деструкций в 2,6 и 5,1 раза (P<0,05), снижения количества крупных язв в 9,1 (P<0,05) и 5,1 раза соответственно по сравнению с аналогичными показателями группы стресс-контроля. В пользу эффективности новой лекарственной формы, на основе исследуемой капсулируемой смеси, свидетельствует отсутствие полосовидных язв при использовании дозы 100 мг/кг и значительное снижение этого показателя в 1,7 раза в группе назначения 200 мг/кг. Выявленный эффект носил дозозависимый характер: увеличение дозы приводило к повышению противоязвенной активности (капсулируемая смесь в дозе 100 мг/кг - 6,33; в дозе 200 мг/кг - 8,26).
Препарат сравнения - экстракт коры осины (таблетируемая смесь) проявил выраженную противоязвенную активность на модели нейрогенного повреждения. Среднее количество язв на одно животное, число крупных и точечных деструкций значимо не отличались от таковых показателей групп назначения капсулированной смеси. Следует отметить некоторое снижение числа животных с язвами после применения таблетируемой смеси в обеих дозах по сравнению с аналогичным показателем группы стресс-контроля (70% и 80% против 90,9%). Более высокий антиульцерогенный эффект при использовании дозы 100 мг/кг (2,86 балла) обусловлен уменьшением среднего числа язв в 2,2 раза (P<0,05), количества точечных язв в 2,82 раза (P<0,05). Полученные результаты при использовании таблетируемой смеси в обеих дозах (2,86 и 2,07 балла) воспроизвели данные ранее проведенных экспериментов.
Анализ показателей противоязвенной эффективности исследуемых лекарственных форм позволил выявить значительную преимущественную специфическую активность капсулируемой смеси. Так, при использовании таблетируемой смеси число животных с язвами не имело статистически значимого отличия с таковым показателем стресс-контроля, тогда как в результате введения капсулируемой смеси в обеих дозах отмечалось снижение количества животных с язвами 50% и 45,5% против 70% и 80%. Аналогичная тенденция наблюдалась в отношении других результатов изучаемой смеси. Если значения полосовидных изъязвлений группы сравнения практически не отличались от контрольных показателей, то в случае применения капсулируемой смеси отмечалось, либо отсутствие, либо снижение в 1,7 этого показателя. Статистически достоверное снижение числа крупных язв фиксировалось при использовании капсулируемой смеси в дозе 100 мг/кг, значительное уменьшение данного показателя (доза 200 мг/кг) в 2,8 и 3,3 раза относительно эффекта таблетируемой смеси (100 и 200 мг/кг). В результате совокупности выявленных изменений выявлено статистически значимое снижение среднего числа язв на 1 животное в обеих опытных группах, тогда как при использовании таблетируемой смеси - при введении в оптимальной дозе 100 мг/кг. При сравнении противоязвенной активности прототипа и капсулируемой смеси продемонстрировано значительное преимущество новой субстанции, которое выразилось в увеличении эффекта в 2,2 и 4,0 раза.
Таким образом, результаты проведенных экспериментов позволяют утверждать о значительном гастрозащитном эффекте - капсулируемой смеси, используемой для получения новой лекарственной формы экстракта коры осины сухого - на модели нейрогенного язвообразования, превалирующем по сравнению с эффективностью прототипа (таблетируемой смеси).
Модель индометацинового язвообразования
На модельной системе индометацинового повреждения слизистой желудка аутбредных крыс-самок были сформированы следующие группы.
1. Контрольная группа (n=10) - крысы получали дистиллированную воду в объеме 0,5 мл внутрижелудочно через зонд однократно ежесуточно профилактическим курсом в течение 4 сут, последнее введение приходилось за 1 ч до применения индометацина.
2. Экстракт коры осины, таблетируемая смесь, 100 мг/кг (10) - крысы получали препарат в объеме 0,5 мл дистиллированной воды внутрижелудочно ежесуточно профилактическим курсом в течение 4 сут, последнее введение приходилось за 1 ч до применения индометацина.
3. Экстракт коры осины, капсулируемая смесь, 50 мг/кг (10) - крысы получали препарат в объеме 0,5 мл дистиллированной воды внутрижелудочно ежесуточно профилактическим курсом в течение 4 сут, последнее введение приходилось за 1 ч до применения индометацина.
4. Экстракт коры осины, капсулируемая смесь, 100 (9) - крысы получали препарат в объеме 0,5 мл внутрижелудочно ежесуточно профилактическим курсом в течение 4 сут, последнее введение приходилось за 1 ч до применения индометацина.
Новая лекарственная форма экстракта коры осины - капсулируемая смесь, вводимая профилактическим курсом в дозах 50 и 100 мг/кг внутрижелудочно ежедневно в течение 4 сут, ограничивала образование всех видов язвенных деструкций, возникающих после воздействия индометацина. Так, использование субстанции в дозе 50 мг/кг приводило к снижению числа точечных в 1,9 раза, крупных в 2,2 раза (P<0,01) по сравнению с соответствующими показателями группы нелеченых животных (фиг.14). В результате чего среднее количество деструкций статистически значимо уменьшилось в 1,6 раза (P<0,01). При этом отмечается снижение площади всех язвенных деструкций (фиг.15): крупных - 1,9 раза (P<0,01), полосовидных - 1,3 раза, точечных - 1,9 раза (P<0,05). Выявленные позитивные изменения нашли отражение в уменьшении степени поражения в 1,5 раза (P<0,05) и тяжести поражения до 64,8 против 100% контрольной группы.
Однонаправленные изменения наблюдаются при использовании капсулируемой смеси в дозе 100 мг/кг (фиг.14 и 15). Отмечается достоверное снижение количества полосовидных язв в 1,4 раза (P<0,05), крупных язв - 1,8 раза (P<0,05), точечных язв - 1,3 раза, вследствие чего среднее число язв уменьшилось в 1,4 раза (P<0,05). Вышесказанное и выявленные другие существенные позитивные изменения при назначения дозы 100 мг/кг нашли отражение в виде уменьшения площади крупных язв в 1,9 раза (P<0,01), полосовидных - в 1,8 раза (P<0,05), в результате чего степень поражения снизилась в 1,6 раза (P<0,05), а тяжесть поражения до 60,7% против 100% контрольной группы.
При анализе эффективности сравниваемой таблетируемой смеси в дозе 100 мг/кг необходимо отметить, что курсовое применение субстанции приводило к статистически значимому снижению количества крупных дефектов в 1,7 раза, точечных деструкций - в 1,5 раза, среднего числа язв - в 1,4 (P<0,05) раза (фиг.14). Гастрозащитный эффект проявлялся в уменьшении таких показателей язвенного процесса, как площадь крупных язв в 1,5 раза (P<0,05), точечных язв - в 1,5 раза (P<0,05), степени поражения - 1,2 раза, тяжести поражения - до 82,8% против 100% контрольной группы.
Таким образом, на модели индометацинового повреждения слизистой желудка у крыс выявлен выраженный противоязвенный эффект при использовании капсулируемой смеси экстракта коры осины в дозах 50 и 100 мг/кг, который превосходил аналогичную активность прототипа - таблетируемой смеси (64,8 и 60,7% против 82,8% соответственно).
Резюмируя вышесказанное, можно сделать вывод в пользу превалирующей противоязвенной активности - капсулируемой смеси, а следовательно, и новой лекарственной формы экстракта коры осины сухого на двух моделях экспериментального ульцерогенеза у мышей и крыс. Эффект варьировал в зависимости от генеза язвенных деструкций. В случае нейрогенного язвообразования эффективность нового средства возрастала в 2,2-4,0 раза, на модели индометацинового язвообразования на 18,0-22,1% по сравнению с активностью прототипа.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОЯЗВЕННОГО ГАСТРОРЕТЕНТИВНОГО СРЕДСТВА | 2013 |
|
RU2531092C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ "БИОСИНОЛ", ОБЛАДАЮЩАЯ ГАСТРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2397775C1 |
| Средство, обладающее гастропротекторной активностью | 2016 |
|
RU2629090C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ГАСТРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2536225C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОЯЗВЕННОЙ, АНТИСТРЕССОРНОЙ И ГЕМОСТАТИЧЕСКОЙ АКТИВНОСТЯМИ | 2012 |
|
RU2495674C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ГАСТРОПРОТЕКТИВНОЙ (ПРОТИВОЯЗВЕННОЙ) АКТИВНОСТЬЮ | 2016 |
|
RU2637644C1 |
| СПОСОБ ПРОФИЛАКТИКИ ЯЗВООБРАЗОВАНИЯ НА СЛИЗИСТОЙ ОБОЛОЧКЕ ЖЕЛУДКА | 2011 |
|
RU2481111C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОЯЗВЕННОГО СРЕДСТВА | 1997 |
|
RU2124899C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОЯЗВЕННЫМ ДЕЙСТВИЕМ | 1994 |
|
RU2086251C1 |
| Способ получения средства, обладающего гастропротективной, противовоспалительной, антиоксидантной активностью | 2018 |
|
RU2679310C1 |









Изобретение относится к фармацевтической промышленности, в частности к способу получения средства, обладающего противоязвенным действием. Способ получения средства, обладающего противоязвенным действием, путем экстракции коры осины 40% спиртом этиловым с использованием многоступенчатого противоточного экстрагирования с последующей очисткой, сгущением под вакуумом и сушкой в вакуумном шкафу, добавления к полученному сухому экстракту лудипресса, при определенных условиях, с последующим наполнением твердых желатиновых капсул. 15 ил.
Способ получения средства, обладающего противоязвенным действием, путем экстракции коры осины 40% спиртом этиловым с использованием многоступенчатого противоточного экстрагирования с последующей очисткой, сгущением под вакуумом при температуре 40-50°C и сушкой в вакуумном шкафу при температуре 40-50°C, добавления к полученному сухому экстракту лудипресса в массовом соотношении 35:13 соответственно с последующим наполнением твердых желатиновых капсул по 0,48 г полученной массы.
Авторы
Даты
2014-11-20—Публикация
2013-01-09—Подача