Изобретение относится к технологии получения борорганических соединений, в частности моногалогенпроизводных 1,2-, 1,7-, 1,12-дикарба-клозо-додекаборанов(12) (о-, м-, п-карборанов, соответственно), а именно 9-хлор-, 9-бром-, 9-иод-о(м)-карборанов и 2-хлор-, 2-бром-, 2-иод-п-карборанов, которые могут быть использованы в качестве структурных единиц для синтеза супрамолекулярных систем. 9-Галоген-о(м)- и 2-галоген-п-карбораны являются исходными соединениями для дальнейшего синтеза 9(9,2)-фтор-, 9(9,2)-алкил- и 9(9,2)-арил-о(м,п)-карборанов - перспективных структур для молекулярной электроники. Кроме того, иодпроизводные карборанов находят применение как рентгеноконтрастные вещества и субстраты в борнейтронозахватной терапии.
В известных способах получения 9(9,2)-галоген-о(м,п)-карборанов электрофильным галогенированием замену атома водорода на атом галогена осуществляют взаимодействием о-, м- и п-карборанов с элементарным галогеном (в качестве иодирующих агентов также используют межгалогенные соединения ICl и IBr) в среде тетрахлорида углерода (CCl4), трихлорметана (CHCl3), метиленхлорида (CH2Cl2) или дисульфида углерода (CS2) в присутствии кислот Льюиса: AlCl3, AlBr3, FeCl3. Синтез проводят при температуре кипения растворителя. (Schroeder H., Heying T.L., Reiner J.R. Inorg. Chem., 1963, v.2, No.6. P.1092. Захаркин Л.И., Охлобыстин О.Ю., Семин Г.К., Бабушкина Т.А. Изв. АН СССР, сер. хим., 1965, №10. С.1913. Захаркин Л.И., Калинин В.Н. ДАН СССР, 1966, т.169, №3. С.590. Захаркин Л.И., Калинин В.Н. Ж. общ. хим., 1966, т.36. С.2218. Станко В.И., Климова А.И., Климова Т.П. Ж. общ. хим., 1967, т.37. С.2236. Станко В.И., Братцев В.А., Вострикова В.А., Данилова Г.Н. Ж. общ. хим., 1968, т.38. С.1348. Станко В.И., Гольтяпин Ю.В. Ж. общ. хим., 1969, т.39. С.711. Sieckhaus J.F., Semenuk N.S., Knowles T.A., Schroeder H. Inorg. Chem., 1969, v.8, No.11. P.2452. Станко В.И., Гольтяпин Ю.В. Ж. общ. хим., 1970, т.40. С.127. Jiang W., Knobler C.B., Curtis C.E., Mortimer, M.D., Hawthorne M.F. Inorg. Chem., 1995, v.34, No.13. P.3491. Пат. США US 5489673, МПК C07H 23/00, C07H 5/06, A61K 49/04, 1996).
К недостаткам данных способов можно отнести следующее:
- обработка о-, м- и п-карборанов галогенами в условиях электрофильного галогенирования приводит не только к моногалогенпроизводным, но также и к ди-, три-, тетра- и поли-В-галогенкарборанам, что требует тщательного и трудоемкого разделения конечных продуктов реакции;
- сравнительно низкий выход целевых продуктов, а именно 9(9,2)-галоген-о(м,п)-карборанов;
- использование галогенсодержащих кислот Льюиса, не идентичных по внедряемому в карборановое ядро галогену, приводит к образованию смешанных галогенпроизводных о-, м- и п-карборанов, что еще более затрудняет разделение реакционной смеси на индивидуальные компоненты;
- использование элементарных галогенов представляет опасность как для окружающей среды, так и для персонала;
- галогенсодержащие растворители являются озоноразрушающими средствами.
Известны способы получения галогенпроизводных карборанов фотохимическим (радикальным) галогенированием о-, м- и п-карборанов элементарными галогенами в среде галогенсодержащих органических растворителей под воздействием УФ-облучения. (Захаркин Л.И., Калинин В.Н. Ж. общ. хим., 1966, т.36. С.362. Захаркин Л.И., Калинин В.Н. ДАН СССР, 1967, т.173. С.1091. Sieckhaus J.F., Semenuk N.S., Knowles T.A., Schroeder H. Inorg. Chem. 1969, v.8, No.11. P.2452. Станко В.И., Климова Т.В., Белецкая И.П. ДАН СССР, 1977, т.234. С.1347. Захаркин Л.И., Ольшевская В.А. Изв. АН СССР, сер. хим., 1987. С.1608. Авт. свид. СССР №1657506, МПК C07F 5/02, C08K 5/55, 1991).
К недостаткам данных способов относится следующее:
- сравнительно низкий выход целевых продуктов;
- получение смеси моно-, ди- и полигалоген-о(м,п)-карборанов;
- использование элементарных галогенов представляет опасность как для окружающей среды, так и для персонала;
- применение УФ-облучения без надлежащей защиты представляет опасность для персонала;
- галогенсодержащие растворители являются озоноразрушающими средствами.
Также известен способ получения нидо-9,11-Х2-7,8-C2B9H10 --анионов (X=Cl, Br, I) с применением галогенсукцинимидов (Santos B.C., Pinkerton A.B., Kinkead S.A., Hurlburt P.K., Jasper S.A., Sellers C.W., Huffman J.C., Todd L.J. Polyhedron, 2000, v.19, P.1777). Реакцию галогенирования нидо-7,8-C2B9H12 --аниона галогенсукцинимидами осуществляют в таких растворителях, как ацетонитрил, тетрагидрофуран, бензол, хлористый метилен, диметилформамид или диметилсульфоксид как при комнатной температуре, так и при температуре кипения растворителя.
Однако данным способом синтезируют исключительно дигалогенпроизводные аниона додекагидродикарба-нидо-ундекабората (в виде алкиламмониевых солей), а не моногалогенпроизводные о(м,п)-карборанов. Кроме того, указанная реакция сопровождается образованием ряда побочных продуктов.
Наиболее близким по технической сущности и принятым нами в качестве прототипа является способ получения 9-галоген-о-карборанов (Пат. РФ RU 2454422, C07F 5/02, 2011), заключающийся в галогенировании о-карборана N-галогенимидами(амидами), в числе которых: 1,3-дигалоген-5,5-диметилгидантоины, тригалоген-изоциануровые кислоты, N-галоген-арилсульфонамиды и их натриевые соли, N-галогенфталимиды, где галоген=Cl, Br, I; арил=фенил, п-толил, в среде кислотного органического растворителя, в качестве которого применяют одноосновные жидкие органические кислоты алифатического ряда R-COOH, где R=H, CnH2n+1, CnF2n+1, n=1-3. Однако этим способом получают только моногалогенпроизводные о-карборана. Кроме того, поскольку реакцию проводят при температуре кипения кислотного органического растворителя, температура процесса достаточно высокая от 100 до 140°C в зависимости от типа кислоты.
Задача данного изобретения заключается в создании простого региоселективного, эффективного экологически чистого («зеленая химия»), пожаро- и взрывобезопасного способа получения 1,2-, 1,7-, 1,12-дикарба-клозо-додекаборанов(12) - [9(9,2)-галоген-о(м,п)-карборанов] с высоким выходом целевых продуктов при снижении энергозатрат.
Поставленная задача достигается тем, что предложен способ получения 1,2-, 1,7-, 1,12-дикарба-клозо-додекаборанов(12) [9(9,2)-галоген-о(м,п)-карборанов], включающий взаимодействие о(м,п)-карборанов с галогенирующими агентами, в качестве которых используют N-галогенимиды(амиды): N-галоген-сукцинимиды, 1,3-дигалоген-5,5-диметилгидантоины, тригалоген-изоциануровые кислоты, N-галогенарил-сульфонамиды и их натриевые соли, N-галогенфталимиды, где галоген=Cl, Br, I; арил=фенил, п-толил, в среде кислотного органического растворителя, в качестве которого применяют одноосновные жидкие органические кислоты алифатического ряда R-COOH, где R=H, CnH2n+1, CnF2n+1, n=1-3, с последующим выделением конечного продукта, отличающийся тем, что процесс проводят с использованием ультразвуковой активации (35 кГц, 120 Вт) в присутствии катализатора, в качестве которого используют сильные кислоты: серную (H2SO4), метансульфоновую (CH3SO2OH) и трифторометансульфоновую (CF3SO2OH) в количестве 0,1-1,0 мол.%, при этом процесс ведут при температуре 20-50°C в течение 2-4 часов, при этом способ позволяет получать орто-, мета- и пара-изомеры 9(9,2)-галоген-карборанов.
Достигнутый технический результат состоит в создании универсального способа для синтеза орто-, мета- и пара- изомеров 9(9,2)-галоген-карборанов. За счет совместного использования катализатора и ультразвуковой активации уменьшается продолжительность, а следовательно, увеличивается производительность процесса; по сравнению с прототипом выход 9-галогенпроизводных орто-карборанов увеличивается от 1 до 17%, снижаются энергозатраты вследствие более низкой температуры проведения процесса, которая обеспечивается исключительно ультразвуковым воздействием без дополнительного обогрева. При этом предложенный способ сохраняет достоинства способа-прототипа, а именно, реакция не экзотермична, проводится на воздухе (без использования инертной атмосферы), исключается стадия абсолютирования растворителей, экологически безопасна (не используются галогенированные растворители), процесс пожаро- и взрывобезопасен.
Выходы конечных продуктов составляют 70-90% от теории на очищенный (перекристаллизованный из н-гептана) продукт, причем образуются исключительно моногалогенпроизводные о(м,п)-карборанов в соответствии с уравнениями реакций:
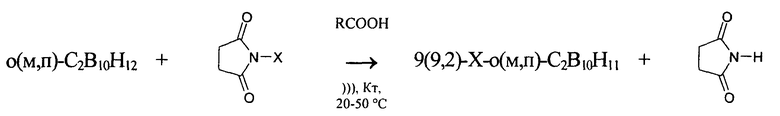
где X=Cl, Br, I.
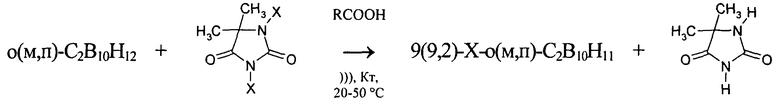
где X=Cl, Br.
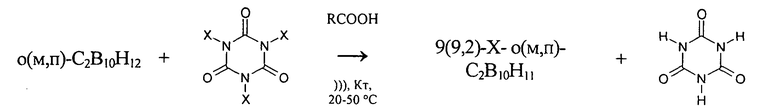
где Х=Cl, Br.
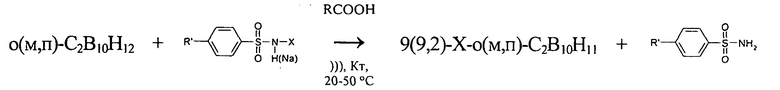
где Х=Cl, Br; R′=Н, СН3.
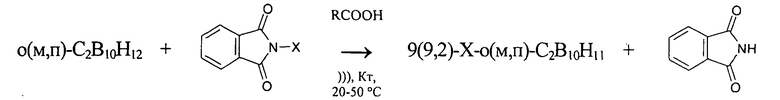
где X - Cl, Br, I.
везде R=H, CnH2n+1, CnF2n+1, n=1-3;
))) - ультразвуковая активация;
Кт - катализатор.
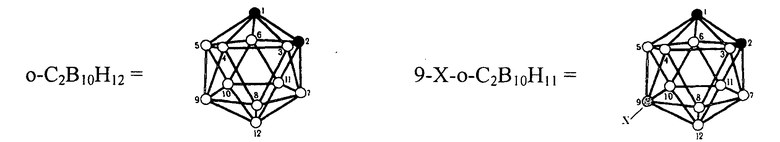
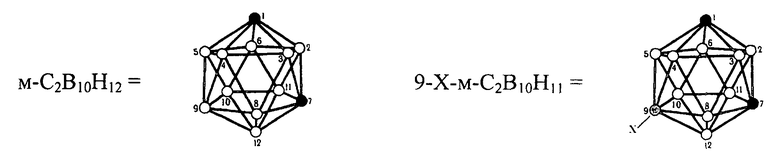
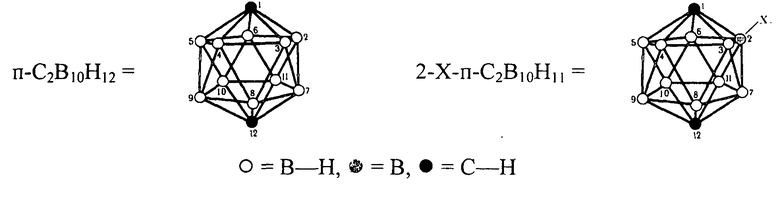
Синтез 9(9,2)-галогенпроизводных о(м,п)-карборанов реакцией галогенирования проводят в воздушной атмосфере в круглодонной колбе, снабженной термометром, обратным холодильником и погруженной в УЗ-ванну, заполненную рабочей жидкостью - дистиллированной водой.
Перемешивание реакционной массы и ее нагревание от 20°C до 50°C осуществляется за счет воздействия ультразвуковых волн (35 кГц, 120 Вт). В колбу загружают расчетное количество о(м,п)-карборана, галогенирующего агента и кислотного органического растворителя. Реакционную массу облучают ультразвуком при комнатной температуре в течение 5-10 минут, затем добавляют катализатор в виде 0,1 молярного раствора в соответствующем кислотном органическом растворителе и продолжают облучение ультразвуком. Нагревание реакционной массы от 20 до 50°C, индуцируемое УЗ-активацией, протекает в течение 2 часов. Общая продолжительность процесса составляет от 2 часов для монобромпроизводного о-карборана и до 4 часов для монохлорпроизводного п-карборана. После охлаждения до температуры окружающей среды реакционную массу обрабатывают дистиллированной водой, в результате чего целевой продукт выпадает в осадок, который фильтруют, дважды промывают дистиллированной водой, отжимают и сушат в вакууме (10-30 мм рт.ст.) при 70-80°C. Затем продукт перекристаллизовывают из кипящего н-гептана (т. кип. 97-99°C). Образующиеся в процессе реакции имиды и амиды остаются в водно-кислотном растворе.
Ниже приведены примеры осуществления предлагаемого способа.
Пример 1. Получение 9-бром-о-карборана
В трехгорлую круглодонную колбу (0,25 л), снабженную термометром и обратным холодильником, загружают 7,3 г (50,0 ммоль) о-карборана (с учетом 99% чистоты), 10,0 г (55,0 ммоль) N-бромсукцинимида и 100 мл 99%-ной уксусной кислоты. Включают УЗ-ванну и реакционную массу облучают при комнатной температуре в течение 10 мин. Затем добавляют 0,5 ммоль серной кислоты в виде 0,1 молярного раствора в уксусной кислоте (5 мл). После чего реакционную массу облучают ультразвуком при температуре 20-50°C в течение 2 часов. По окончании УЗ-активации реакционную массу охлаждают до комнатной температуры, прибавляют 300 мл дистиллированной воды. Образовавшийся осадок фильтруют на фильтре Шотта, промывают 2×200 мл дистиллированной воды, отжимают и сушат в вакууме (30 мм рт.ст.) при 70°C. Затем целевой продукт перекристаллизовывают из кипящего н-гептана (т. кип. 97-99°C). Общий выход 75% от теории. Тпл 205-208°C.
Пример 2. Получение 9-иод-о-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) о-карборана (с учетом 99% чистоты), 13,0 г (55,0 ммоль) N-иодсукцинимида (95%-ной чистоты) и 100 мл 99%-ной уксусной кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 10 мин. Затем добавляют 0,05 ммоль серной кислоты в виде 0,1 молярного раствора в уксусной кислоте (0,5 мл). Продолжительность реакции 2 часа. Общий выход 85% от теории. Тпл 119-121°C.
Пример 3. Получение 9-хлор-о-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) о-карборана (с учетом 99% чистоты), 4,4 г (18,4 ммоль) трихлор-N-изоциануровой кислоты (97%-ной чистоты) и 100 мл 99%-ной уксусной кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 10 мин. Затем добавляют 0,5 ммоль серной кислоты в виде 0,1 молярного раствора в уксусной кислоте (5 мл). Продолжительность реакции 2 часа. Общий выход 89% от теории.
Тпл 228-232°C.
Пример 4. Получение 9-хлор-о-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) о-карборана (с учетом 99% чистоты), 5,53 г (27,5 ммоль) 1,3-дихлор-5,5-диметилгидантоина (98%-ной чистоты) и 100 мл 99%-ной пропионовой кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 5 мин. Затем добавляют 0,5 ммоль метансульфоновой кислоты в виде 0,1 молярного раствора в пропионовой кислоте (5 мл). Продолжительность реакции 3 часа. Общий выход 87% от теории. Тпл 228-232°C.
Пример 5. Получение 9-бром-о-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) о-карборана (с учетом 99% чистоты), 8,02 г (27,5 ммоль) 1,3-дибром-5,5-диметилгидантоина (98%-ной чистоты) и 100 мл 99%-ной пропионовой кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 5 мин. Затем добавляют 0,25 ммоль метансульфоновой кислоты в виде 0,1 молярного раствора в пропионовой кислоте (2,5 мл). Продолжительность реакции 2 часа. Общий выход 85% от теории. Тпл 205-208°C.
Пример 6. Получение 9-хлор-о-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) о-карборана (с учетом 99% чистоты), 15,81 г (55,0 ммоль) хлорамина Т тригидрата 98%-ной чистоты (натриевая соль N-хлор-п-толуолсульфонамида тригидрат) и 100 мл 97%-ной муравьиной кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 5 мин. Затем добавляют 0,5 ммоль метансульфоновой кислоты в виде 0,1 молярного раствора в муравьиной кислоте (5 мл). Продолжительность реакции 3 часа. Общий выход 71% от теории. Тпл 228-232°C.
Пример 7. Получение 9-иод-о-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) о-карборана (с учетом 99% чистоты), 13,0 г (55,0 ммоль) N-иодсукцинимида (95%-ной чистоты) и 100 мл 99%-ной трифторуксусной кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 10 мин. Затем добавляют 0,05 ммоль метансульфоновой кислоты в виде 0,1 молярного раствора в трифторуксусной кислоте (0,5 мл), Продолжительность реакции 2 часа. Общий выход 86% от теории. Тпл 119-121°C.
Пример 8. Получение 9-иод-м-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) м-карборана (с учетом 99% чистоты), 13,0 г (55,0 ммоль) N-иодсукцинимида (95%-ной чистоты) и 100 мл 99%-ной уксусной кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 10 мин. Затем добавляют 0,05 ммоль трифторметансульфоновой кислоты в виде 0,1 молярного раствора в уксусной кислоте (0,5 мл). Продолжительность реакции 3 часа. Общий выход 75% от теории.
Пример 9. Получение 9-хлор-м-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) м-карборана (с учетом 99% чистоты), 4,4 г (18,4 ммоль) трихлор-N-изоциануровой кислоты (97%-ной чистоты) и 100 мл 99%-ной уксусной кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 10 мин. Затем добавляют 0,25 ммоль трифторметансульфоновой кислоты в виде 0,1 молярного раствора в уксусной кислоте (2,5 мл). Продолжительность реакции 3 часа. Общий выход 78% от теории.
Пример 10. Получение 9-бром-м-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) м-карборана (с учетом 99% чистоты), 8,02 г (27,5 ммоль) 1,3-дибром-5,5-диметилгидантоина (98%-ной чистоты) и 100 мл 99%-ной пропионовой кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 5 мин. Затем добавляют 0,25 ммоль метансульфоновой кислоты в виде 0,1 молярного раствора в пропионовой кислоте (2,5 мл). Продолжительность реакции 3 часа. Общий выход 73% от теории.
Пример 11. Получение 2-бром-п-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) п-карборана (с учетом 99% чистоты), 8,02 г (27,5 ммоль) 1,3-дибром-5,5-диметилгидантоина (98%-ной чистоты) и 100 мл 99%-ной пропионовой кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 5 мин. Затем добавляют 0,25 ммоль трифторметансульфоновой кислоты в виде 0,1 молярного раствора в пропионовой кислоте (2,5 мл), Продолжительность реакции 4 часа. Общий выход 72% от теории.
Пример 12. Получение 2-хлор-п-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) п-карборана (с учетом 99% чистоты), 4,4 г (18,4 ммоль) трихлор-N-изоциануровой кислоты (97%-ной чистоты) и 100 мл 99%-ной пропионовой кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 10 мин. Затем добавляют 0,25 ммоль трифторметансульфоновой кислоты в виде 0,1 молярного раствора в пропионовой кислоте (2,5 мл). Продолжительность реакции 4 часа. Общий выход 78% от теории.
Пример 13. Получение 2-хлор-п-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) п-карборана (с учетом 99% чистоты), 7,5 г (55,0 ммоль) N-хлорсукцинимида (98%-ной чистоты) и 100 мл 99%-ной трифторуксусной кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 10 мин. Затем добавляют 0,5 ммоль метансульфоновой кислоты в виде 0,1 молярного раствора в трифторуксусной кислоте (5 мл). Продолжительность реакции 4 часа. Общий выход 77% от теории.
Пример 14. Получение 2-иод-п-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) п-карборана (с учетом 99% чистоты), 13,0 г (55,0 ммоль) N-иодсукцинимида (95%-ной чистоты) и 100 мл 97%-ной муравьиной кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 10 мин. Затем добавляют 0,05 ммоль трифторметансульфоновой кислоты в виде 0,1 молярного раствора в муравьиной кислоте (0,5 мл). Продолжительность реакции 3 часа. Общий выход 76% от теории.
Пример 15. Получение 2-бром-п-карборана
Галогенирование осуществляют аналогично примеру 1.
Загружают 7,3 г (50,0 ммоль) п-карборана (с учетом 99% чистоты), 9,88 г (55,0 ммоль) N-бромсукцинимида (99%-ной чистоты) и 100 мл 99%-ной изомасляной кислоты. Реакционную массу перемешивают ультразвуком при комнатной температуре в течение 10 мин. Затем добавляют 0,5 ммоль серной кислоты в виде 0,1 молярного раствора в изомасляной кислоте (5 мл). Продолжительность реакции 4 часа. Общий выход 73% от теории.
Для подтверждения идентичности полученных 9(9,2)-галоген-о(м,п)-карборанов использовался метод спектроскопии ЯМР на ядрах 1H, 11B, 13C.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ РЕГИОСЕЛЕКТИВНОГО СИНТЕЗА МОНОГАЛОГЕНПРОИЗВОДНЫХ 1,2-,1,7-,1,12-ДИКАРБА-КЛОЗО-ДОДЕКАБОРАНОВ(12) С ИСПОЛЬЗОВАНИЕМ УЛЬТРАЗВУКОВОЙ АКТИВАЦИИ | 2013 |
|
RU2536686C1 |
| СПОСОБ РЕГИОСЕЛЕКТИВНОГО СИНТЕЗА МОНОГАЛОГЕНПРОИЗВОДНЫХ 1,2-, 1,7-, 1,12-ДИКАРБА-КЛОЗО-ДОДЕКАБОРАНОВ(12) | 2013 |
|
RU2521592C1 |
| СПОСОБ РЕГИОСЕЛЕКТИВНОГО СИНТЕЗА 9-ГАЛОГЕНПРОИЗВОДНЫХ О-КАРБОРАНА | 2011 |
|
RU2454422C1 |
| СПОСОБ ПОЛУЧЕНИЯ 7,8(7,9)-ДОДЕКАГИДРОДИКАРБА-НИДО-УНДЕКАБОРАТОВ АЛКИЛАММОНИЯ И АЛКИЛГУАНИДИНИЯ | 2013 |
|
RU2537404C1 |
| СПОСОБ ПОЛУЧЕНИЯ 7,8(7,9)-ДОДЕКАГИДРОДИКАРБА-НИДО-УНДЕКАБОРАТОВ АЛКИЛАММОНИЯ | 2013 |
|
RU2517439C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ И НЕЗАМЕЩЕННЫХ 7,8-ДОДЕКАГИДРОДИКАРБА-НИДО-УНДЕКАБОРАТОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ С ИСПОЛЬЗОВАНИЕМ УЛЬТРАЗВУКОВОЙ АКТИВАЦИИ | 2017 |
|
RU2664328C1 |
| СПОСОБ ПОЛУЧЕНИЯ С, С'-КАРБОРАНДИКАРБОНОВЫХ КИСЛОТ | 2014 |
|
RU2559625C1 |
| СПОСОБ ПОЛУЧЕНИЯ БОРИРОВАННЫХ ПОРФИРИНОВ | 2013 |
|
RU2551539C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-АМИНО-5-ФТОР-3-ГАЛОГЕН-6-(ЗАМЕЩЕННЫХ)ПИКОЛИНАТОВ | 2013 |
|
RU2632203C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-АМИНО-5-ФТОР-3-ГАЛОГЕН-6-(ЗАМЕЩЕННЫХ)ПИКОЛИНАТОВ | 2012 |
|
RU2545074C1 |
Изобретение относится к способу получения моногалогенпроизводных 1,2-,1,7-,1,12-дикарба-клозо-додекаборанов(12). Способ включает взаимодействие о(м,п)-карборанов с галогенирующими агентами, в качестве которых используют N-галогенимиды(амиды): N-галоген-сукцинимиды, 1,3-дигалоген-5,5-диметилгидантоины, тригалоген-изоциануровые кислоты, N-галогенарил-сульфонамиды и их натриевые соли, N-галогенфталимиды, где галоген = Cl, Br, I; арил = фенил, п-толил, в среде кислотного органического растворителя. В качестве растворителя применяют одноосновные жидкие органические кислоты алифатического ряда R-COOH, где R=H, CnH2n+1, CnF2n+1, n=1-3. При этом процесс проводят с использованием ультразвуковой активации в присутствии катализатора, в качестве которого используют сильные кислоты: серную (H2SO4), метансульфоновую (CH3SO2OH) и трифторометансульфоновую (CF3SO2OH) в количестве 0,1-1,0 мол.%. Процесс ведут при температуре 20-50°C в течение 2-4 часов. Изобретение позволяет снизить энергозатраты. 15 пр.
Способ получения моногалогенпроизводных 1,2-,1,7-,1,12-дикарба-клозо-додекаборанов(12), включающий взаимодействие о(м,п)-карборанов с галогенирующими агентами, в качестве которых используют N-галогенимиды(амиды): N-галоген-сукцинимиды, 1,3-дигалоген-5,5-диметилгидантоины, тригалоген-изоциануровые кислоты, N-галогенарил-сульфонамиды и их натриевые соли, N-галогенфталимиды, где галоген = Cl, Br, I; арил = фенил, п-толил, в среде кислотного органического растворителя, в качестве которого применяют одноосновные жидкие органические кислоты алифатического ряда R-COOH, где R=H, CnH2n+1, CnF2n+1, n=1-3, с последующим выделением конечного продукта, отличающийся тем, что процесс проводят с использованием ультразвуковой активации в присутствии катализатора, в качестве которого используют сильные кислоты: серную (H2SO4), метансульфоновую (CH3SO2OH) и трифторометансульфоновую (CF3SO2OH) в количестве 0,1-1,0 мол.%, при этом процесс ведут при температуре 20-50°C в течение 2-4 часов, при этом способ позволяет получать орто-, мета- и пара-изомеры 9(9,2)-галоген-карборанов.
| СПОСОБ РЕГИОСЕЛЕКТИВНОГО СИНТЕЗА 9-ГАЛОГЕНПРОИЗВОДНЫХ О-КАРБОРАНА | 2011 |
|
RU2454422C1 |
| SANTOS Е.С | |||
| ЕТ AL, SYNTHESES OF nido-9,11-Х2-7,8-С2В9Н10- ANIONS (Х=Сl, Br OR I) AND THE SYNTHESIS AND STRUCTURAL CHARACTERIZATION OF N(C2H5)4[commo-3, 3'-Co(4,7-Br2-3,1,2-CoC2B9H9)2], POLYHEDRON, 2000, v.19, p.1777-1781 | |||
| US 3562324 A, 09.02.1971 | |||
| Хлорированные карборанпроизводные с активными функциональными группами как антипиренная добавка к целлюлозе | 1989 |
|
SU1657506A1 |
Авторы
Даты
2014-12-20—Публикация
2013-08-08—Подача