Область техники, к которой относится изобретение
Настоящая заявка относится к области органической химии и фармацевтической химии.
Уровень техники
TNFα представляет собой цитокин, вырабатываемый в основном мононуклеарными фагоцитами в ответ на иммуностимуляторы. TNFα способен участвовать в большинстве процессов, таких как дифференцировка, агрегация и пролиферация клеток, деградация белка и т.п. При низком уровне TNFα обладает защитными эффектами, направленными на предупреждение инфекционных субстанций, опухолей и повреждений тканей. Однако избыточное высвобождение TNFα будет индуцировать заболевания. Например, когда TNFα вводят млекопитающим или человеку, он будет индуцировать или усиливать воспаление, лихорадочное состояние, сердечно-сосудистые эффекты, кровотечение, свертывание крови и острую реакцию, похожую на острую инфекцию и шоковые состояния. Избыток или неконтролируемое количество TNFα, продуцируемое в организмах животных или человека, часто указывает на наличие следующих заболеваний: эндотоксикоза и/или синдромов токсического шока, кахексии, нервных дыхательных синдромов у взрослых, злокачественных опухолей (таких как солидные опухоли и опухоли кровеносных сосудов), болезней сердца (таких как острая сердечная недостаточность), вирусных инфекций, генетических заболеваний, воспалительных заболеваний, аллергических заболеваний или аутоиммунных болезней.
Злокачественная опухоль является особенно деструктивным заболеванием. Повышенный уровень TNFα в крови указывает на риски наличия злокачественных опухолей или распространения злокачественных опухолей. Обычно у здорового субъекта опухолевые клетки не могут выживать в системе циркулирования (крови). Одна из причин заключается в том, что внутренняя стенка сосуда является препятствием для экстравазации онкоцитов. Исследования показывают, что ELAM-1 на эндотелиальных клетках может опосредовать усиление адгезии опухолевых клеток толстой кишки на эндотелии, обработанном цитокинами.
Циклический аденозинмонофосфат (цАМФ) также принимает участие во многих заболеваниях и расстройствах, таких как, но не ограничиваясь перечисленным, астма, воспаление и другие расстройства. Когда возникает воспаление, повышенная концентрация цАМФ в лейкоцитах будет ингибировать активацию лейкоцитов и затем высвобождать факторы, регулирующие воспаление, включая TNFα, NF-ΚB и т.п. Повышенный уровень цАМФ также будет вызывать расслабление гладкой мускулатуры дыхательных путей.
Основной клеточный механизм инактивации цАМФ заключается в том, что семейство изоферментов, известное как фосфодиэстеразы циклических нуклеотидов (PDE), разрушает цАМФ. Известно, что существует одиннадцать членов PDE-семейства. К настоящему времени было показано, что для ингибирования высвобождения медиаторов воспаления и расслабления гладкой мускулатуры дыхательных путей особенно эффективно ингибирование фермента PDE4. Следовательно, фермент PDE4 является одной из мишеней лекарственного лечения, представляющей интерес. Ингибирование фермента PDE4 вызывает повышенный уровень цАМФ и тем самым регулирует уровень TNFα, обеспечивая при этом лечение воспаления, такого как септический шок, септицемия, эндоксиновый бактериально-токсический шок, гемический шок, септический синдром заболевания, ишемически-реперфузионное повреждение, микобактериальная малярийная инфекция, менингит, псориаз, острая сердечная недостаточность, фиброзирующее заболевание, кахексия, отторжение трансплантата, опухоль, заболевание, связанное с аутоиммунными расстройствами, возможная СПИД-инфекция, ревматоидный артрит, ревматоидный спондилит, остеоартрит, другое воспалительное заболевание, болезнь Крона, ульцеративный колит, рассеянный склероз, системная красная волчанка, лепрозная узловатая эритема, радиационное повреждение, гипероксическое повреждение легких и т.п., инфекционное заболевание, иммунное заболевание или другое злокачественное заболевание.
Современные ингибиторы фермента PDE4 проявляют клиническую эффективность в отношении различных воспалительных заболеваний, включая астму, хроническую обструктивную болезнь легких (ХОБЛ), аллергический ринит, аллергический дерматит и т.п. В моделях на животных они также показывают эффективность в отношении других различных заболеваний, включая артрит, септицемию и т.п. Однако у них имеются неблагоприятные реакции, такие как тошнота, рвота и т.п., поскольку они не могут специфически ингибировать фермент PDE4, так что их клиническое применение на практике ограничено. Следовательно, для того чтобы уменьшить неблагоприятные реакции лекарственного средства и сохранить его противовоспалительную активность, возможно получение специфических ингибиторов фермента PDE4.
Сущность изобретения
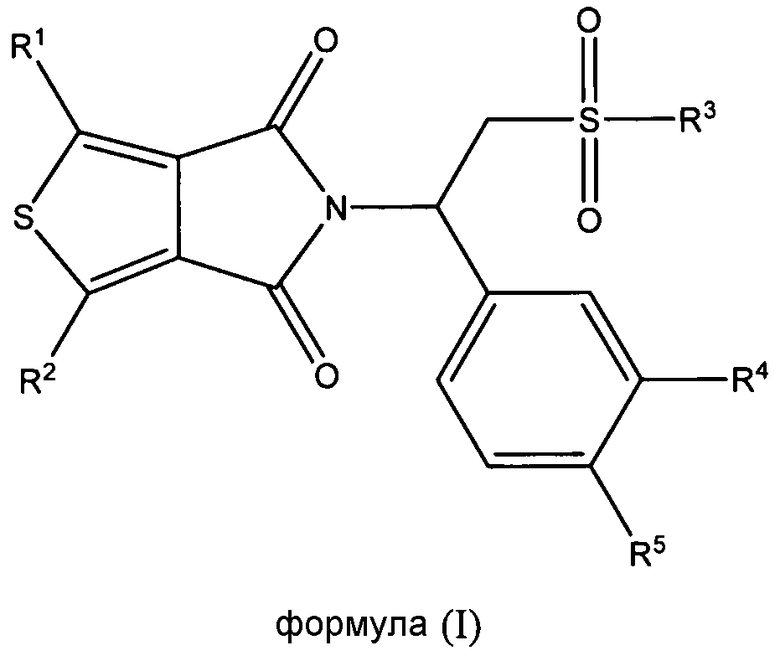
В одном из аспектов настоящая заявка относится к соединению формулы (I), его стереоизомеру, энантиомеру, или таутомеру, или к смеси его стереоизомеров, его фармацевтически приемлемой соли, его полиморфной модификации, его сольвату, его пролекарству или его метаболиту:
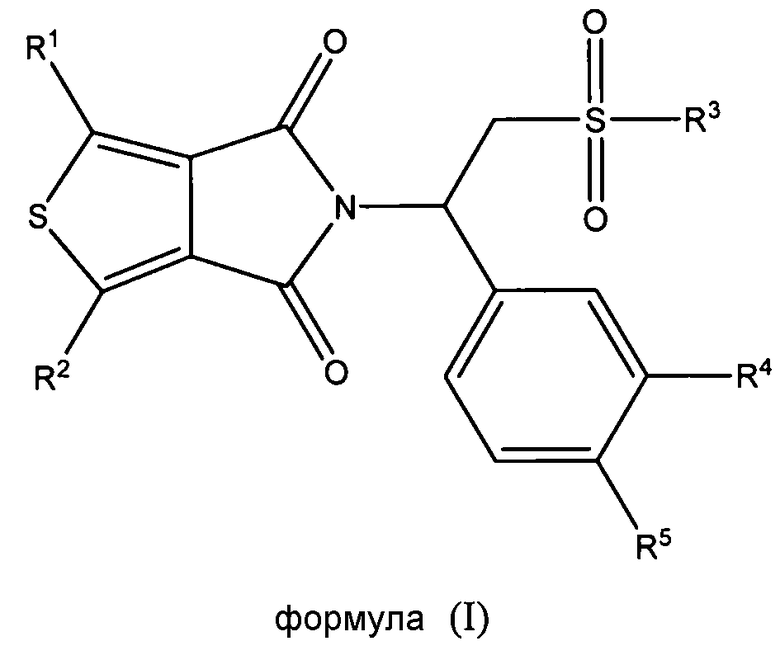
в которой
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из О, S и NR8; и
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
В еще одном аспекте настоящая заявка относится к способу получения соединения формулы (I), включающему в себя взаимодействие соединения формулы (A-IV) с соединением формулы (A-VII) с получением соединения формулы (I):
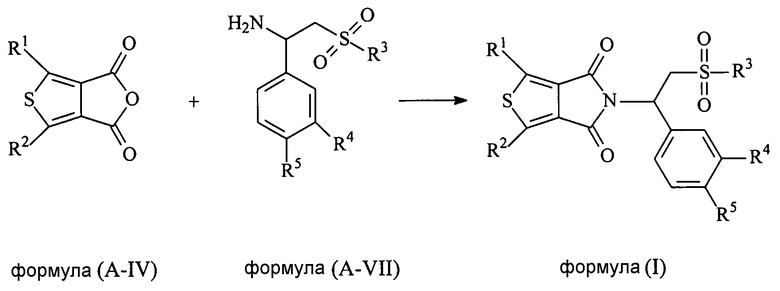
в которых
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из О, S и NR8;
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
В еще одном аспекте настоящая заявка относится к фармацевтической композиции, содержащей фармацевтически приемлемый носитель и терапевтически эффективное количество соединения формулы (I), его стереоизомера, энантиомера или таутомера, или смеси его стереоизомеров, его фармацевтически приемлемой соли, его полиморфной модификации, его сольвата, его пролекарства или его метаболита,
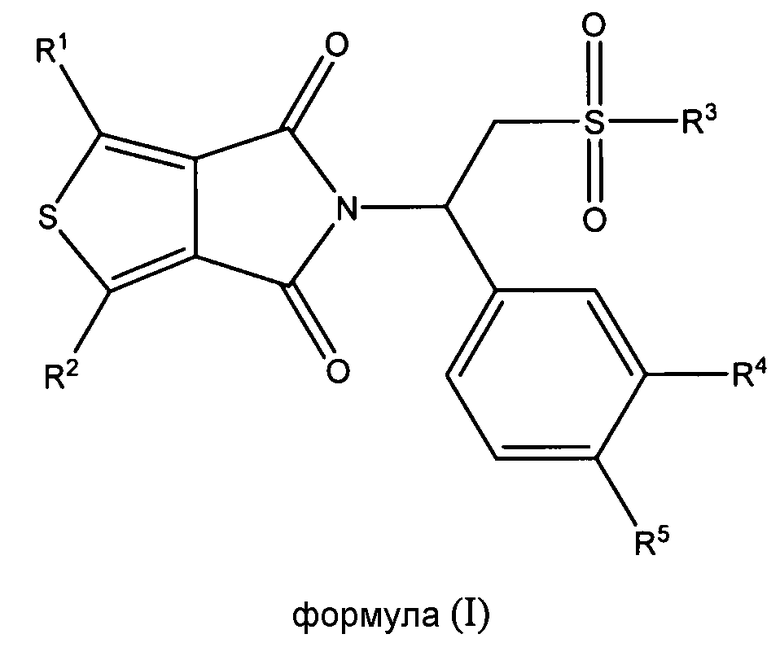
в которой
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
Каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
Каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из О, S и NR8;
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
В еще одном аспекте настоящая заявка относится к способу уменьшения активности фермента PDE4, включающему в себя контактирование фермента PDE4 с терапевтически эффективным количеством соединения формулы (I), его стереоизомера, энантиомера, или таутомера, или смеси его стереоизомеров, его фармацевтически приемлемой соли, его полиморфной модификации, его сольвата, его пролекарства или его метаболита,
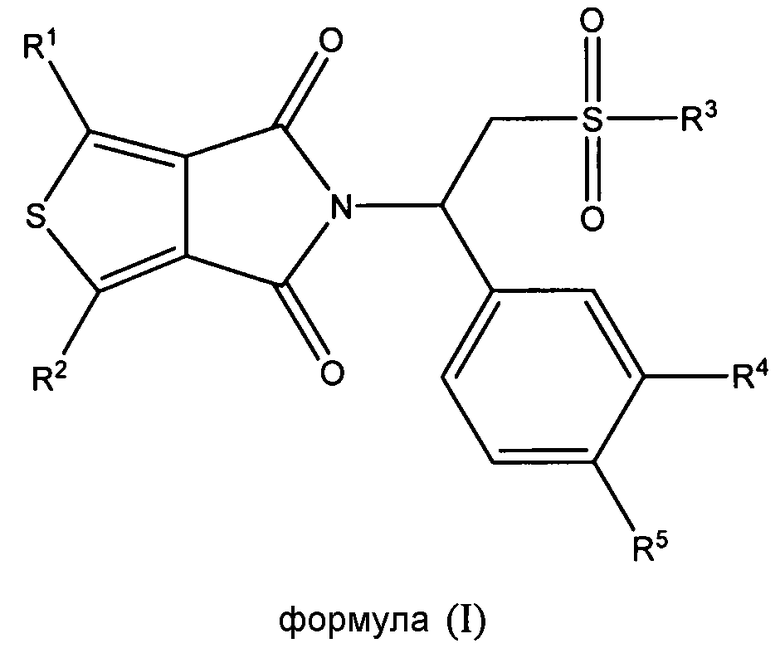
в которой
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
Каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
Каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из O, S и NR8;
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
В еще одном аспекте настоящая заявка относится к способу лечения заболеваний или состояний, опосредованных ферментом PDE4, включающему в себя введение субъекту, нуждающемуся в лечении, терапевтически эффективного количества соединения формулы (I), его стереоизомера, энантиомера или таутомера или смеси его стереоизомеров, его фармацевтически приемлемой соли, его полиморфной модификации, его сольвата, его пролекарства или его метаболита,
в которой
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
Каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
Каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из O, S и NR8;
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
Подробное описание изобретения
Чтобы обеспечить понимание различных описываемых вариантов осуществления изобретения, в следующее описание включены некоторые конкретные детали. Однако специалисту в данной области будет понятно, что варианты осуществления изобретения можно применять на практике без одной или нескольких таких конкретных деталей или с другими способами, компонентами, материалами и т.д.
Если контекст описания не требует иного, на всем протяжении описания и формулы изобретения, которая следует за ним, термин "содержать" и его вариации, такие как "содержит" и "содержащий" должны интерпретироваться в открытом, широком смысле, который понимается как "включают в себя, но не ограничиваются перечисленным".
На всем протяжении данного описания ссылка на "один из вариантов осуществления изобретения" или "вариант осуществления изобретения", или "еще один вариант осуществления изобретения", или "некоторые варианты осуществления изобретения " означает, что отдельный определяемый признак, структура или характерная особенность, описанные в связи с вариантами осуществления изобретения, включены по меньшей мере в один вариант осуществления изобретения. Следовательно, появление фраз "в одном из вариантов осуществления изобретения", или "в варианте осуществления изобретения", или "в еще одном варианте осуществления изобретения", или "в некоторых вариантах осуществления изобретения" в различных местах на протяжении данного описания необязательно относится только к одному и тому же варианту осуществления изобретения. Более того, отдельные признаки, структуры или характерные особенности могут объединяться любым подходящим образом в одном или нескольких вариантах осуществления изобретения.
Следует отметить, что применяемые в данном описании и прилагаемой формуле изобретения формы единственного числа ("a", "an" и "the") включают в себя множество определяемых объектов, если в контексте очевидным образом не указано иначе. Следовательно, например, реакционная смесь, содержащая "катализатор", содержит один катализатор, два или более катализаторов. Также следует отметить, что применение "или" означает "и/или", если не указано иначе.
Определения
Некоторым упомянутым здесь химическим группам предшествует условное обозначение, указывающее суммарное число атомов углерода, которое должно находиться в обозначаемой химической группе. Например, C7-C12-алкил описывает алкил, который указан ниже, содержащий в целом от 7 до 12 атомов углерода, и C4-C12-циклоалкилалкил описывает циклоалкилалкил, который указан ниже, содержащий в целом от 4 до 12 атомов углерода. Суммарное число атомов углерода в условном обозначении не включает в себя атомы углерода, которые могут присутствовать в заместителях описанных групп.
Соответственно, применяемые в описании и прилагаемой формуле изобретения, если не указано нечто противоположное, следующие термины имеют значения, указывающие:
"Гидрокси" относится к группе -OH.
"Циано" относится к группе -CN.
"Нитро" относится к группе -NO2.
Применяемый здесь термин "алкил" относится к алифатической углеводородной группе. Алкильный фрагмент может представлять собой "насыщенную алкильную" группу, что означает, что она не содержит каких-либо алкеновых или алкиновых фрагментов. Алкильный фрагмент также может представлять собой "ненасыщенный алкильный" фрагмент, что означает, что он содержит по меньшей мере один алкеновый или алкиновый фрагмент. "Алкеновый" фрагмент относится к углеводородной группе с прямой или разветвленной цепью, содержащей от двух до восьми атомов углерода и по меньшей мере одну двойную связь углерод-углерод, который присоединен к остатку молекулы простой одинарной связью, например, этенил, проп-1-енил, бут-1-енил, пент-1-енил, пент-1,4-диенил, и т.п. "Алкиновый" фрагмент относится к углеводородной группе с прямой или разветвленной цепью, содержащей от двух до восьми атомов углерода и по меньшей мере одну тройную связь углерод-углерод, который присоединен к остатку молекулы простой одинарной связью. Алкильный фрагмент, как насыщенный, так и ненасыщенный, может иметь разветвленную цепь или прямую цепь.
Алкильная группа может содержать от 1 до 20 атомов углерода (всякий раз, когда такое выражение встречается в настоящем документе, числовой диапазон, такой как "от 1 до 20", относится к каждому целому числу из заданного диапазона чисел; например, "от 1 до 20 атомов углерода" означает, что алкильная группа может состоять из 1 атома углерода, 2 атомов углерода, 3 атомов углерода и т.д. до 20 атомов углерода и, включая 20 атомов углерода, несмотря на то, что настоящее определение также распространяется на случай термина "алкил", когда числовой диапазон не определен). Алкильная группа также может представлять собой алкил среднего размера, содержащий от 1 до 10 атомов углерода. Алкильная группа также может представлять собой низший алкил, содержащий от 1 до 5 атомов углерода. Алкильная группа соединений согласно настоящей заявке может определяться как "C1-C4-алкил" или с помощью похожих определений. В качестве только примера "C1-C4-алкил" обозначает, что в алкильной цепи присутствует от одного до четырех атомов углерода, то есть алкильная цепь выбрана из группы, состоящей из метила, этила, пропила, изопропила, н-бутила, изобутила, втор-бутила и т-бутила.
Алкильная группа необязательно может быть замещенной, то есть может быть замещенной или незамещенной. Когда алкильная группа является замещенной, группу-заместитель (заместители) выбирают в индивидуальном порядке и независимо из циклоалкила, арила, гетероарила, гетероалициклических групп, гидрокси, алкокси, арилокси, меркапто, алкилтио, арилтио, циано, атома галогена, карбонила, тиокарбонила, O-карбамила, N-карбамила, O-тиокарбамила, N-тиокарбамила, C-амидо, N-амидо, S-сульфонамидо, N-сульфонамидо, C-карбоксила, O-карбоксила, изоцианато, тиоцианато, изотиоцианато, нитро, силила, тригалогенметансульфонила, -NR'R" или амино, включая моно- и дизамещенную аминогруппу и ее защищенные производные. Типичные алкильные группы включают в себя, но никоим образом не ограничиваются перечисленным, метил, этил, пропил, изопропил, бутил, изобутил, т-бутил, пентил, гексил, этил, пропенил, бутенил, циклопропил, циклобутил, циклопентил, циклогексил и т.п. Всякий раз, когда заместитель описан как "необязательно замещенный", такой заместитель может быть замещен одним из указанных выше заместителей.
"C1-C4-алкил" относится к алкильной группе, которая определена выше, содержащей от одного до четырех атомов углерода. C1-C4-алкильная группа необязательно может быть замещена таким образом, как указано для алкильной группы.
"C1-C6-алкил" относится к алкильной группе, которая определена выше, содержащей от одного до шести атомов углерода. C1-C6-алкильная группа необязательно может быть замещена таким образом, как указано для алкильной группы.
"C1-C12-алкил" относится к алкильной группе, которая определена выше, содержащей от одного до двенадцати атомов углерода. C1-C12-алкильная группа необязательно может быть замещена таким образом, как указано для алкильной группы.
"C2-C6-алкил" относится к алкильной группе, которая определена выше, содержащей от двух до шести атомов углерода. C2-C6-алкильная группа необязательно может быть замещена таким образом, как указано для алкильной группы.
"C3-C6-алкил" относится к алкильной группе, которая определена выше, содержащей от трех до шести атомов углерода. C3-C6-алкильная группа необязательно может быть замещена так же, как указано для алкильной группы.
"C3-C12-алкил" относится к алкильной группе, которая определена выше, содержащей от трех до двенадцати атомов углерода. C3-C12-алкильная группа необязательно может быть замещена так же, как указано для алкильной группы.
"C6-C12-алкил" относится к алкильной группе, которая определена выше, содержащей от шести до двенадцати атомов углерода. C6-C12-алкильная группа необязательно может быть замещена так же, как указано для алкильной группы.
"C7-C12-алкил" относится к алкильной группе, которая определена выше, содержащей от семи до двенадцати атомов углерода. C7-C12-алкильная группа необязательно может быть замещена так же, как указано для алкильной группы.
Применяемый здесь термин "алкокси" относится к формуле -OR, в которой R представляет собой алкильную группу, которая определена выше, например, метокси, этокси, н-пропокси, 1-метилэтокси (изопропокси), н-бутокси, изобутокси, втор-бутокси, т-бутокси, амокси, т-амокси и т.п.
Применяемый здесь термин "алкилтио" относится к формуле -SR, в которой R представляет собой алкильную группу, которая определена выше, например, метилмеркапто, этилмеркапто, н-пропилмеркапто, 1-метилэтилмеркапто (изопропилмеркапто), н-бутилмеркапто, изобутилмеркапто, втор-бутилмеркапто, т-бутилмеркапто и т.п.
Применяемый здесь термин "алкилен" относится к прямой или разветвленной двухвалентной углеводородной цепи, соединяющей остаток молекулы с радикальной группой, состоящей из атомов углерода и водорода и содержащей от одного до восьми атомов углерода, например, метилен, этилен, пропилен, н-бутилен, этенилен, пропенилиден, н-бутенилиден. Алкиленовая цепь может присоединяться к остатку молекулы и радикальной группе через один атом углерода в пределах цепи или через любые два атома углерода в пределах цепи.
Применяемый здесь термин "арил" относится к карбоциклическому (только атомы углерода) кольцу или двум или более конденсированным кольцам (кольца, в которых совместно участвуют два соседних атома углерода), которые имеют систему полностью делокализованных π-электронов. Примеры арильной группы включают в себя, но не ограничиваются перечисленным, флуоренил, фенил и нафтил. Арильная группа, например, может содержать от пяти до двенадцати атомов углерода. Арильная группа согласно настоящей заявке может быть замещенной или незамещенной. Когда арильная группа является замещенной, атомы водорода замещены группой-заместителем (заместителями), которая представляет собой одну или несколько групп, независимо выбранных из алкила, циклоалкила, арила, гетероарила, гетероалициклила, гидрокси, защищенной гидрокси-группы, алкокси, арилокси, меркапто, алкилтио, арилтио, циано, атома галогена, карбонила, тиокарбонила, O-карбамила, N-карбамила, O-тиокарбамила, N-тиокарбамила, C-амидо, N-амидо, S-сульфонамидо, N-сульфонамидо, C-карбоксила, защищенного C-карбоксила, O-карбоксила, изоцианато, тиоцианато, изотиоцианато, нитро, силила, тригалогенметансульфонила, -NR'R" (R' и R" представляют собой алкильные группы, которые указаны в настоящей заявке) или защищенной аминогруппы.
Применяемый здесь, термин "галоген" относится к атому брома, хлора, фтора или йода.
"Циклоалкил" относится к неароматической моноциклической или бициклической углеводородной группе, состоящей только из атомов углерода и водорода, содержащей от трех до пятнадцати атомов углерода, предпочтительно содержащей от трех до двенадцати атомов углерода, и которая является стабильной, насыщенной или ненасыщенной, и присоединена к остатку молекулы с помощью простой одинарной связи, например, циклопропил, циклобутил, циклопентил, циклогексил, циклодецил и т.п. Если в описании специально не оговаривается иное, подразумевается, что термин "циклоалкил" включает в себя циклоалкильные группы, которые необязательно замещены одним или несколькими заместителями, выбранными из группы, состоящей из циклоалкила, арила, гетероарила, гетероалициклической группы, гидрокси, алкокси, арилокси, меркапто, алкилтио, арилтио, циано, атома галогена, карбонила, тиокарбонила, O-карбамила, N-карбамила, O-тиокарбамила, N-тиокарбамила, C-амидо, N-амидо, S-сульфонамидо, N-сульфонамидо, C-карбоксила, O-карбоксила, изоцианато, тиоцианато, изотиоцианато, нитро, силила, тригалогенметансульфонила, -NR'R" (R' и R" представляют собой алкильные группы, которые указаны в настоящей заявке) или амино, включая монозамещенную и дизамещенную аминогруппу и ее защищенные производные.
"C3-C6-циклоалкил" относится к циклоалкильной группе, которая определена выше, содержащей от трех до шести атомов углерода. C3-C6-циклоалкильная группа необязательно может быть замещена так же, как указано для циклоалкила.
"C3-C10-циклоалкил" относится к циклоалкильной группе, которая определена выше, содержащей от трех до десяти атомов углерода. C3-C10-циклоалкильная группа необязательно может быть замещена так же, как указано для циклоалкила.
"C3-C12-циклоалкил" относится к циклоалкильной группе, которая определена выше, содержащей от трех до двенадцати атомов углерода. C3-C12-циклоалкильная группа необязательно может быть замещена так же, как указано для циклоалкила.
Применяемый здесь термин "гетероциклил" относится к стабильной 3-12-членной неароматической циклической группе, которая состоит из атомов углерода и содержит от одного до пяти гетероатомов, выбранных из группы, состоящей из атомов азота, кислорода и серы. Примеры таких гетероциклильных групп включают в себя, но не ограничиваются перечисленным, диоксоланил, декагидроизохинолил, имидазолинил, имидазолидинил, изотиазолидинил, изоксазолидинил, морфолинил, окстагидроиндолил, октагидроизоиндолил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, оксазолидинил, пиперидинил, пиперазинил, 4-пиперидонил, пирролидинил, пиразолидинил, тиазолидинил, тетрагидрофурил, тритианил, тетрагидропиранил, тиоморфолинил, тиаморфолинил, 1-оксотиоморфолинил и 1,1-диоксотиоморфолинил. Если в описании специально не оговаривается иное, подразумевается, что термин "гетероциклоалкил" включает в себя гетероциклильные группы, которые указаны выше, которые необязательно замещены одним или несколькими заместителями, выбранными из группы, состоящей из циклоалкила, арила, гетероарила, гетероалициклической группы, гидрокси, алкокси, арилокси, меркапто, алкилтио, арилтио, циано, атома галогена, карбонила, тиокарбонила, O-карбамила, N-карбамила, O-тиокарбамила, N-тиокарбамила, C-амидо, N-амидо, S-сульфонамидо, N-сульфонамидо, C-карбоксила, O-карбоксила, изоцианато, тиоцианато, изотиоцианато, нитро, силила, тригалогенметансульфонила, -NR'R" (R' и R" представляют собой алкильные группы, которые указаны в настоящей заявке) или амино, включая монозамещенную и дизамещенную аминогруппу и ее защищенные производные.
Подразумевается, что термин "пролекарства" обозначает соединение, которое в физиологических условиях или путем сольволиза может превращаться в биологически активное соединение согласно настоящей заявке. Следовательно, термин "пролекарство" относится к метаболическому предшественнику соединения согласно настоящей заявке, которое является фармацевтически приемлемым. Пролекарство может являться неактивным, когда его вводят субъекту, нуждающемуся в лечении, но превращается in vivo в активное соединение согласно настоящей заявке. Пролекарства обычно быстро трансформируются in vivo, давая при этом исходное соединение согласно настоящей заявке, например, путем гидролиза в крови. Соединение-пролекарство часто имеет преимущества в растворимости, тканевой совместимости или замедленном высвобождении в организме млекопитающего (см. публикацию Bundgard H., Design of Prodrugs (1985), стр. 7-9, 21-24 (Elsevier, Amsterdam)).
Обсуждение пролекарств приводится в публикации Higuchi T. и др. "Pro-drugs as Novel Delivery Systems" A.C.S. Symposium Series, т. 14 и в публикации Bioreversible Carriers in Drug Design, ed. Edward B. Roche, American Pharmaceutical Association и Pergamon Press, 1987, обе из которых включены в настоящий документ в полном объеме путем ссылки.
Также подразумевается, что термин "пролекарство" включает в себя любые ковалентно связанные носители, которые высвобождают активное соединение согласно настоящей заявке in vivo, когда такое пролекарство вводят млекопитающему. Пролекарства соединения согласно настоящей заявке можно получать путем модификации функциональных групп, присутствующих в соединении согласно настоящей заявке, таким образом, чтобы модификации расщеплялись либо в результате обычного преобразования, либо in vivo до исходного соединения согласно настоящей заявке. Пролекарства включают в себя соединения согласно настоящей заявке, в которых гидроксигруппа, аминогруппа или меркаптогруппа связаны с любыми группами, которые, когда пролекарство соединения согласно настоящей заявке вводят млекопитающему, расщепляется с образованием свободной гидроксигруппы, свободной аминогруппы или свободной меркаптогруппы, соответственно. Примеры пролекарств включают в себя, но не ограничиваются перечисленным, ацетатные, формиатные и бензоатные производные спиртовых или аминофункциональных групп в соединениях согласно настоящей заявке и т.п.
"Необязательный" или "необязательно" означает, что описанное далее событие в силу обстоятельств может произойти или может не произойти, и что описание включает в себя случаи, когда упомянутое событие или обстоятельство происходит, и случаи, при которых оно не происходит. Например, "необязательно замещенный арил" означает, что арильная группа может быть замещена или может быть незамещена, и описание включает в себя как замещенные арильные группы, так и арильные группы без замещения.
"Фармацевтически приемлемый носитель" включает в себя без ограничения любое вспомогательное лекарственное вещество, носитель, инертный наполнитель, вещество, способствующее скольжению, подсластитель, разбавитель, консервант, краситель/окрашивающее средство, усилитель вкуса и запаха, поверхностно-активное вещество, увлажняющее средство, диспергатор, суспендирующее средство, стабилизатор, изоосмотическое средство, растворитель или эмульгатор и т.д., которые утверждены Управлением по контролю за продуктами питания и лекарственными средствами США, как приемлемые для применения для человека и животных и не оказывающие побочных эффектов на получение фармацевтической композиции.
"Фармацевтически приемлемые соли" включают в себя как "фармацевтически приемлемые аддитивные соли кислот", так и "фармацевтически приемлемые аддитивные соли оснований".
"Фармацевтически приемлемая аддитивная соль кислоты" относится к таким солям, которые сохраняют биологическую эффективность и свойства свободных оснований и которые не являются биологически или иным образом неприемлемыми, и которые образуются с неорганическими кислотами, такими как, но, не ограничиваясь перечисленным, хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и т.п.; и с органическими кислотами, такими как, но, не ограничиваясь перечисленным, уксусная кислота, 2,2-дихлоруксусная кислота, адипиновая кислота, альгиновая кислота, аскорбиновая кислота, аспарагиновая кислота, бензолсульфоновая кислота, бензойная кислота, 4-ацетамидобензойная кислота, камфановая кислота, камфор-10-сульфоновая кислота, каприновая кислота, капроновая кислота, каприловая кислота, угольная кислота, коричная кислота, лимонная кислота, цикламовая кислота, додецилсерная кислота, этан-1,2-дисульфоновая кислота, этансульфоновая кислота, 2-гидроксиэтансульфоновая кислота, муравьиная кислота, фумаровая кислота, галактаровая кислота, гентизиновая кислота, глюкогептоновая кислота, глюконовая кислота, глюкуроновая кислота, глутаминовая кислота, глутаровая кислота, 2-оксоглутаровая кислота, глицерофосфорная кислота, гликолевая кислота, гиппуровая кислота, изомасляная кислота, молочная кислота, лактобионовая кислота, лауриновая кислота, малеиновая кислота, яблочная кислота, малоновая кислота, миндальная кислота, метансульфоновая кислота, слизевая кислота, нафталин-1,5-дисульфоновая кислота, нафталин-2-сульфоновая кислота, 1-гидрокси-2-нафтойная кислота, никотиновая кислота, олеиновая кислота, оротовая кислота, щавелевая кислота, пальмитиновая кислота, памовая кислота, пропионовая кислота, пироглутаминовая кислота, пировиноградная кислота, салициловая кислота, 4-аминосалициловая кислота, себациновая кислота, стеариновая кислота, янтарная кислота, винная кислота, тиоциановая кислота, п-толуолсульфоновая кислота, трифторуксусная кислота, ундеценовая кислота и т.п.
"Фармацевтически приемлемая аддитивная соль основания" относится к таким солям, которые сохраняют биологическую эффективность и свойства свободных кислот, которые не являются биологически или иным образом неприемлемыми. Такие соли получают при добавлении неорганического или органического основания к свободной кислоте. Соли, получаемые из неорганических оснований, включают в себя, но не ограничиваются перечисленным, соли натрия, калия, лития, аммония, кальция, магния, железа, цинка, меди, марганца, алюминия и т.п. Предпочтительными неорганическими солями являются соли аммония, натрия, калия, кальция и магния. Соли, получаемые из органических оснований, включают в себя, но не ограничиваются перечисленным, соли первичных, вторичных и третичных аминов, замещенных аминов, включая замещенные амины природного происхождения, соли циклических аминов и основных ионообменных смол, такие как соли аммония, изопропиламина, триметиламина, диэтиламина, триэтиламина, трипропиламина, диэтаноламина, этаноламина, деанола, 2-диметиламиноэтанола, 2-диэтиламиноэтанола, дициклогексиламина, лизина, аргинина, гистидина, кофеина, прокаина, гидрабамина, холина, бетаина, бенетамина, бензатина, этилендиамина, глюкозамина, метилглюкозамина, теобромина, триэтаноламина, трометамола, пурина, пиперазина, пиперидина, N-этилпиперидина, полиаминных смол и т.п. Особенно предпочтительными органическими основаниями являются изопропиламин, диэтиламин, этаноламин, триметиламин, дициклогексиламин, холин и кофеин.
Часто при кристаллизациях образуется сольват соединения согласно настоящей заявке. Применяемый здесь термин "сольват" относится к агрегированному комплексу, который содержит одну или несколько молекул соединения согласно настоящей заявке с одной или несколькими молекулами растворителя. Растворитель может представлять собой воду, в случае которой сольват может являться гидратом. Альтернативно растворителем может быть органический растворитель. Следовательно, соединения согласно настоящей заявке могут существовать в виде гидрата, включая моногидрат, дигидрат, полугидрат, полуторагидрат, тригидрат, тетрагидрат и т.п., а также в виде соответствующих сольватированных форм. Соединение согласно настоящей заявке может представлять собой истинный сольват, хотя в других случаях соединение согласно настоящей заявке может просто сохранять дополнительную воду или содержать смесь воды и какого-нибудь дополнительного растворителя.
Термин "полиморфная модификация" относится к компоненту, имеющему идентичную химическую формулу, но обладающему другими структурами.
Термин "фармацевтическая композиция" относится к препарату соединения согласно настоящей заявке и среде, обычно применяемой в данной области для доставки биологически активного соединения млекопитающим, например человеку. Такая среда включает в себя все фармацевтически приемлемые носители, разбавители или инертные наполнители для фармацевтических композиций.
"Терапевтически эффективное количество" относится к такому количеству соединения согласно настоящей заявке, которое, когда его вводят млекопитающему, предпочтительно человеку, достаточно для эффективного лечения, как указано ниже, опосредованного ферментом PDE4 заболевания или состояния млекопитающего, предпочтительно человека. Количество соединения согласно настоящей заявке, которое составляет "терапевтически эффективное количество", будет меняться в зависимости от соединения, состояния, его тяжести и возраста млекопитающего, подвергаемого лечению, в то же время может определяться обычным специалистом в данной области, исходящим из своих собственных знаний и данного описания.
Применяемый здесь термин "проведение лечения" или "лечение" распространяется на лечение представляющего интерес заболевания или состояния млекопитающего, предпочтительно человека, имеющего заболевание или расстройство, представляющее интерес, и включают в себя:
(i) предупреждение возникновения заболевания или состояния у млекопитающего, в частности, когда такое млекопитающее предрасположено к такому состоянию, но его наличие еще не диагностировано;
(ii) ингибирование заболевания или состояния, то есть прекращение его развития; или
(iii) облегчение тяжести заболевания или состояния, то есть осуществление регрессии заболевания или состояния.
Применяемые здесь термины "заболевание" и "состояние" могут применяться взаимозаменяемо или могут отличаться друг от друга в том случае, когда возбудитель конкретного заболевания или состояния может быть неизвестен (то есть этиология еще не разработана) и, следовательно, болезнь еще не распознается в качестве заболевания, а только в качестве нежелательного состояния или синдрома, для которого клиницистами идентифицирован более или менее специфический набор симптомов.
Соединения согласно настоящей заявке или их фармацевтически приемлемая соль могут содержать один или несколько центров асимметрии и поэтому могут приводить к образованию энантиомеров, диастереоизомеров и других стереоизомерных форм, которые можно определить в терминах абсолютной стереохимии как (R)-, или (S)-, или (D)- или (L)- для аминокислот. Подразумевается, что настоящая заявка включает в себя все такие возможные изомеры, а также их рацемические и оптически чистые формы. Оптически активные (+) и (-), (R)- и (S)- или (D)- и (L)- изомеры можно получать с применением хиральных синтонов или хиральных реагентов, или разделять смеси с применением традиционных методик, таких как ВЭЖХ с хиральной колонкой. Когда описанные здесь соединения содержат олефиновые двойные связи или другие центры геометрической асимметрии, и если не указано иначе, подразумевается, что соединения включают в себя как E, так и Z-геометрические изомеры. Точно так же подразумевается, что в настоящую заявку должны быть включены все таутомерные формы.
Термин "стереоизомер" относится к соединению, образованному теми же атомами, связанными теми же связями, но имеющему другие трехмерные структуры, которые не являются взаимозаменяемыми. В настоящей заявке рассматриваются различные стереоизомеры и их смеси.
Термин "таутомер" относится к сдвигу протона от одного атома молекулы к другому атому той же самой молекулы. Настоящая заявка включает в себя таутомеры любого упомянутого соединения.
Конкретные варианты осуществления изобретения
В одном из аспектов настоящая заявка относится к соединению формулы (I), его стереоизомеру, энантиомеру или таутомеру или к смеси его стереоизомеров, его фармацевтически приемлемой соли, его полиморфной модификации, его сольвату, его пролекарству или его метаболиту:
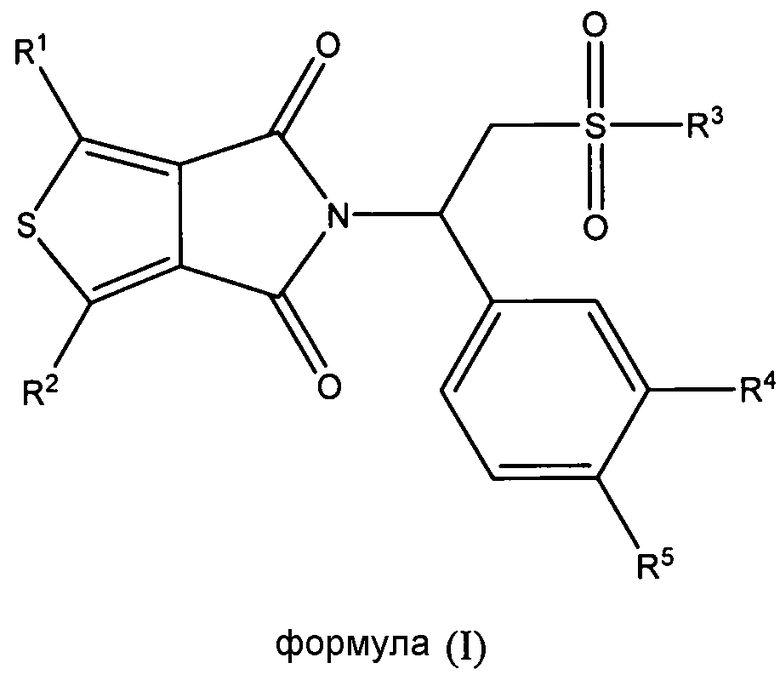
в которой
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из O, S и NR8;
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
В некоторых вариантах осуществления изобретения C1-C8-алкил выбран из группы, состоящей из C1-C4-алкила и C1-C6-алкила.
В некоторых вариантах осуществления изобретения C1-C8-алкокси выбран из группы, состоящей из C1-C4-алкокси и C1-C6-алкокси.
В некоторых вариантах осуществления изобретения C1-C8-алкилтио выбран из группы, состоящей из C1-C4-алкилтио и C1-C6-алкилтио.
В некоторых вариантах осуществления изобретения C3-C10-циклоалкил выбран из C3-C6-циклоалкила.
В некоторых вариантах осуществления изобретения каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, метила, этила, нитро, NH2, NHCH3, CH3C(О)NH, CH3CH2C(О)NH, CH3SO2NH и ClCH2C(О)NH.
В некоторых вариантах осуществления изобретения R3 выбран из группы, состоящей из C1-C8-алкила и C1-C8-алкокси.
В некоторых вариантах осуществления изобретения R3 выбран из группы, состоящей из C1-C8-алкила, C1-C8-алкокси, C1-C8-алкил(C1-C8-алкилен)окси, C5-C12-арила и C5-C12-арил(C1-C8-алкилен)окси.
В некоторых вариантах осуществления изобретения R3 выбран из группы, состоящей из метила, этила и пропила.
В некоторых вариантах осуществления изобретения каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, C1-C8-алкила, галогензамещенного C1-C8-алкила, C1-C8-алкокси, C1-C8-алкилтио, циано, C3-C10-циклоалкила, (C1-C8-алкилен)C3-C10-циклоалкила, C3-C10-циклоалкил(C1-C8-алкилен)окси, C3-C10-циклоалкилокси, C5-C12-арила, C5-C12-арилокси и C5-C12-арил(C1-C8-алкилен)окси.
В некоторых вариантах осуществления изобретения каждый из R4 и R5 независимо выбран из группы, состоящей из C1-C8-алкокси, галогензамещенного C1-C8-алкокси и C5-C12-арилокси.
В некоторых вариантах осуществления изобретения каждый из R4 и R5 независимо выбран из группы, состоящей из метокси, дифторметокси, трифторметокси, этокси, пропокси и бензилокси.
В некоторых вариантах осуществления изобретения R8 выбран из группы, состоящей из атома водорода, C1-C8-алкила, галогензамещенного C1-C8-алкила, C1-C8-алкила, замещенного (C1-C8-алкилзамещенный амино), и C3-C12-гетероциклоалкилзамещенного C1-C8-алкила.
В некоторых вариантах осуществления изобретения R8 выбран из группы, состоящей из атома водорода, метила, этила, диметиламинометила, диэтиламинометила, пиперидилметила и морфолинилметила.
В некоторых вариантах осуществления изобретения соединение формулы (I) выбрано из группы, состоящей из:
N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
1-амино-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
(S)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
(R)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-нитро-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
N-(5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид,
N-(5-(1-(3,4-диметоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
(S)-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
(R)-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
(S)-5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
(S)-5-(1-(3,4-диметоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-нитро-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-амино-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
N-(5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
5-(1-(3,4-диметоксифенил)-2-(метилсульфонил)этил)-1-нитро-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
5-(1-(3,4-диметоксифенил)-2-(метилсульфонил)этил)-1-амино-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-1-нитро-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-1-амино-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-метиламино-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
2-хлор-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)метансульфонамида,
(S)-1-амино-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
(R)-1-амино-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетона,
N-(5-(1-(3-этокси-4-дифторметоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
N-(5-(1-(3-этокси-4-трифторметоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
(S)-N-(5-(1-(3-этокси-4-дифторметоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
(R)-N-(5-(1-(3-этокси-4-дифторметоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
(S)-N-(5-(1-(3-этокси-4-трифторметоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
(R)-N-(5-(1-(3-этокси-4-трифторметоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
N-(5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)пропионамида,
2-(диметиламино)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
2-(диэтиламино)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида,
2-(пиперидил)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-илацетамида и
2-(морфолинил)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамида.
В еще одном аспекте настоящая заявка относится к способу получения соединения формулы (I), включающему в себя взаимодействие соединения формулы (A-IV) с соединением формулы (A-VII) с получением соединения формулы (I):
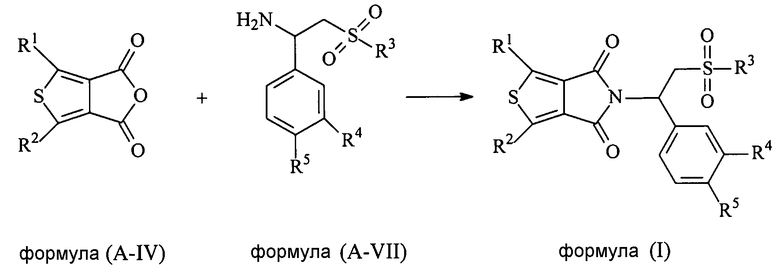
в которых
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из O, S и NR8;
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
В некоторых вариантах осуществления изобретения при взаимодействии соединения формулы (A-IV) с соединением формулы (A-VII) с получением соединения формулы (I) в качестве катализатора добавляют третичный амин.
Подходящие примеры катализатора, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, пиридин, 4-диметиламинопиридин, 4-пирролидинилпиридин и их смесь.
В некоторых вариантах осуществления изобретения при взаимодействии соединения формулы (A-IV) с соединением формулы (A-VII) с получением соединения формулы (I) дополнительно можно добавлять дегидратирующее средство.
Подходящие примеры дегидратирующего средства, которое может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, DCC, EDC•HCl, CDI, DIC, сложный диэтиловый эфир азодикарбоновой кислоты, сложный диизопропиловый эфир азодикарбоновой кислоты, сложный дибензиловый эфир азодикарбоновой кислоты и их смесь.
В некоторых вариантах осуществления изобретения при взаимодействии соединения формулы (A-IV) с соединением формулы (A-VII) с получением соединения формулы (I) дополнительно можно добавлять активирующее средство.
Подходящие примеры активирующего средства, которое может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, N-гидроксисукцинимид, HOBt, HOAt, BOP, Cl-HOBt, DEPBT, HATU, HBTU, HCTU, HOOBt, PyBOP, TATU, TBTU и их смесь.
В некоторых вариантах осуществления изобретения взаимодействие соединения формулы (A-IV) с соединением формулы (A-VII) с получением соединения формулы (I) проводят в органическом растворителе.
Подходящие примеры органического растворителя, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, хлороформ, дихлорметан, дихлорэтан, тетрагидрофуран, простой диэтиловый эфир, простой изопропиловый эфир, этилацетат, простой диметиловый эфир гликоля, простой диэтиловый эфир гликоля, бензол, толуол, н-гексан, циклогексан, ДМФА, ДМСО, простой метилэтиловый эфир, простой метилпропиловый эфир, простой метил-т-бутиловый эфир, ацетон, бутанон, метилформиат, этилформиат, пропилформиат, бутилформиат, метилацетат, пропилацетат, бутилацетат и их смесь.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-IV) с соединением формулы (A-VII) с получением соединения формулы (I) проводят при -10°C-200°C.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-IV) с соединением формулы (A-VII) с получением соединения формулы (I) проводят при -10°C-150°C.
В некоторых вариантах осуществления изобретения дегидратацию соединения формулы (A-III) проводят с получением соединения формулы (A-IV),
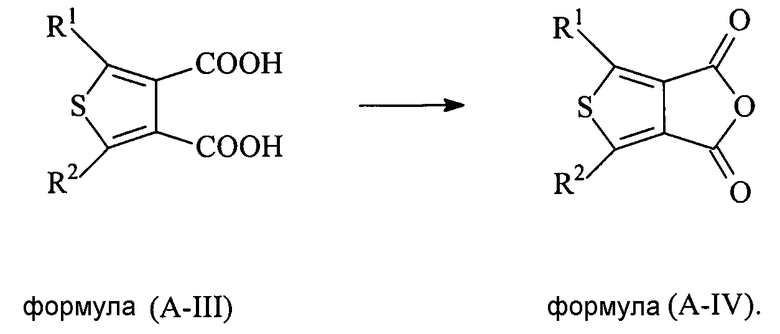
Подходящие примеры дегидратирующего средства, которое может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, уксусный ангидрид, трифторуксусный ангидрид и их смесь.
В некоторых вариантах осуществления изобретения дегидратацию соединения формулы (A-III) с получением соединения формулы (A-IV) проводят в органическом растворителе.
Подходящие примеры органического растворителя, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, хлороформ, дихлорметан, дихлорэтан, тетрагидрофуран, простой диэтиловый эфир, простой изопропиловый эфир, циклогексан, н-гексан, этилацетат, простой диметиловый эфир гликоля, простой диэтиловый эфир гликоля, бензол, толуол, ДМФА, ДМСО, ацетон, бутанон, простой метилэтиловый эфир, простой метил-т-бутиловый эфир, простой метилпропиловый эфир, метилформиат, этилформиат, пропилформиат, бутилформиат, метилацетат, пропилацетат, бутилацетат, уксусную кислоту, трифторуксусную кислоту и их смесь.
В некоторых вариантах осуществления изобретения соединение формулы (A-III) получают из соединения формулы (A-II) в присутствии кислоты или основания,
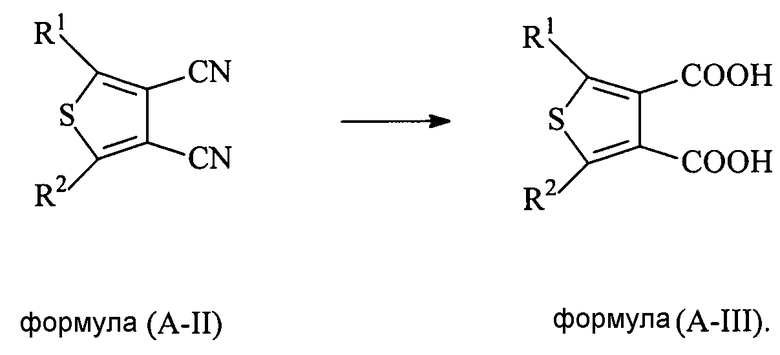
Подходящие примеры основания, которое может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, гидроксид натрия, гидроксид калия, гидроксид лития и их смесь.
Подходящие примеры кислоты, которая можно применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, хлористоводородную кислоту, серную кислоту, фосфорную кислоту, метансульфоновую кислоту, этансульфоновую кислоту и их смесь.
В некоторых вариантах осуществления изобретения соединение формулы (A-III) получают из соединения формулы (A-II) в растворителе в присутствии кислоты или основания.
Подходящие примеры растворителя, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, хлороформ, дихлорметан, дихлорэтан, тетрагидрофуран, простой диэтиловый эфир, простой изопропиловый эфир, циклогексан, н-гексан, этилацетат, простой диметиловый эфир гликоля, простой диэтиловый эфир гликоля, бензол, толуол, ДМФА, ДМСО, ацетон, бутанон, простой метилэтиловый эфир, простой метил-т-бутиловый эфир, простой метилпропиловый эфир, метилформиат, этилформиат, пропилформиат, бутилформиат, метилацетат, пропилацетат, бутилацетат, уксусную кислоту, трифторуксусную кислоту, воду и их смесь.
В некоторых вариантах осуществления изобретения соединение формулы (A-III) получают из соединения формулы (A-II) при 0°C-200°C в присутствии кислоты или основания.
В некоторых вариантах осуществления изобретения соединение формулы (A-III) получают из соединения формулы (A-II) при 50°C-200°C в присутствии кислоты или основания.
В некоторых вариантах осуществления изобретения соединение формулы (A-III) получают из соединения формулы (A-II) при 80°C-180°C в присутствии кислоты или основания.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-I) с цианидом проводят с получением соединения формулы (A-II),
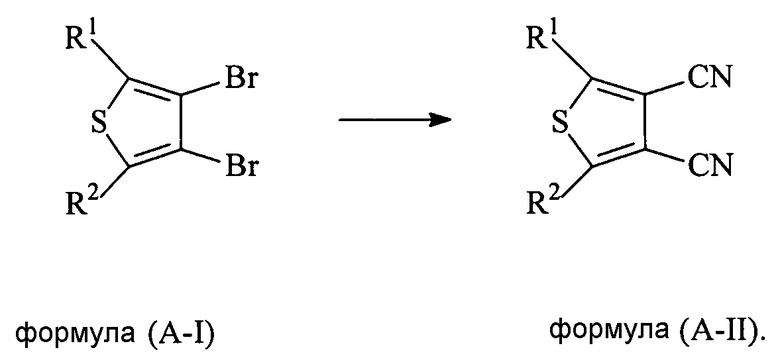
Подходящие примеры цианида, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, цианид меди (I), цианид натрия, цианид калия и цианид ртути.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-I) с цианидом проводят в органическом растворителе с получением соединения формулы (A-II).
Подходящие примеры органического растворителя, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, ДМФА, ДМСО, ацетамид, N-метилпирролидон, простой диметиловый эфир диэтиленгликоля, простой диэтиловый эфир диэтиленгликоля и их смесь.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-I) с цианидом проводят при 50°C-250°C с получением соединения формулы (A-II).
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-I) с цианидом проводят при 100°C-250°C с получением соединения формулы (A-II).
В некоторых вариантах осуществления изобретения соединение формулы (A-VII) получают путем взаимодействия соединения формулы (A-VI) в присутствии средства для снятия защиты,
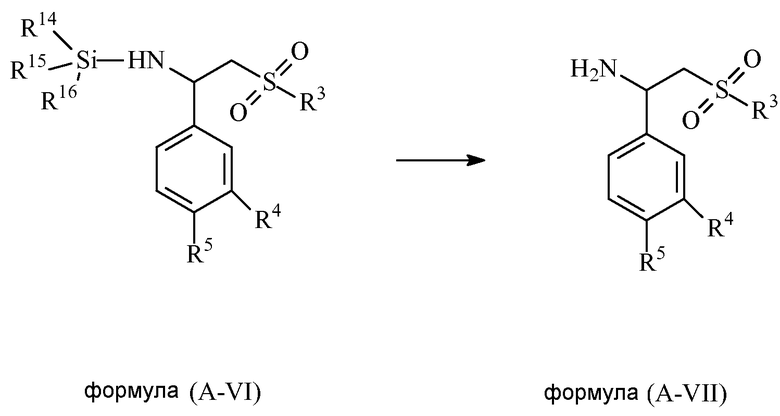
Подходящие примеры средства для снятия защиты, которое может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, фторид тетрабутиламмония, фторид тетраэтиламмония, хлористоводородную кислоту, серную кислоту, фосфорную кислоту, азотную кислоту, уксусную кислоту, трифторуксусную кислоту, муравьиную кислоту, метансульфоновую кислоту, этансульфоновую кислоту, бензолсульфоновую кислоту, п-толуолсульфоновую кислоту и их смесь.
В некоторых вариантах осуществления изобретения соединение формулы (A-VII) получают путем взаимодействия соединения формулы (A-VI) в присутствии средства для снятия защиты в растворителе.
Подходящие примеры растворителя, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, хлороформ, дихлорметан, дихлорэтан, тетрагидрофуран, простой диэтиловый эфир, простой изопропиловый эфир, этилацетат, этанол, метанол, пропиловый спирт, бутиловый спирт, этиленгликоль, простой диметиловый эфир гликоля, простой монометиловый эфир этиленгликоля, простой моноэтиловый эфир этиленгликоля, простой диэтиловый эфир гликоля, бензол, толуол, н-гексан, циклогексан, ДМФА, ДМСО, уксусную кислоту, трифторуксусную кислоту, простой метилэтиловый эфир, простой метилпропиловый эфир, простой метил-т-бутиловый эфир, ацетон, бутанон, метилформиат, этилформиат, пропилформиат, бутилформиат, метилацетат, пропилацетат, бутилацетат, воду и их смесь.
В некоторых вариантах осуществления изобретения соединение формулы (A-VII) получают путем взаимодействия соединения формулы (A-VI) в присутствии средства для снятия защиты при -20°C-200°C.
В некоторых вариантах осуществления изобретения соединение формулы (A-VII) получают путем взаимодействия соединения формулы (A-VI) в присутствии средства для снятия защиты при 0°C-200°C.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-V) с CH3S(О)2R3 и (R14R15R16Si)2NM проводят в присутствии сильного основания с получением соединения формулы (A-VII),
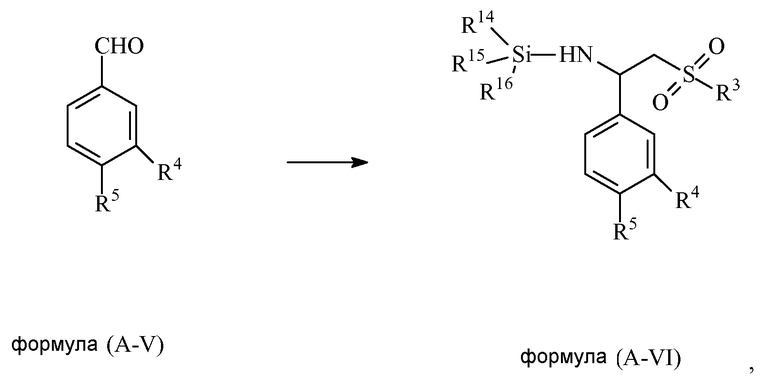
в которых группа, представленная с помощью R3 в CH3S(О)2R3 является идентичной группе, представленной с помощью R3 в соединении формулы (I), и на которой каждый из R14, R15 или R16 в (R14Rl5R16Si)2NM независимо выбран из группы, состоящей из алкила и фенила, и M выбран из группы, состоящей из натрия, калия и лития.
Подходящие примеры сильного основания, которое может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, алкиллитий, алкилнатрий, алкилкалий, алкоголят натрия, алкоголят калия, алкоголят лития, алкиламид натрия, алкиламид лития и алкиламид калия.
В некоторых вариантах осуществления изобретения подходящие примеры сильного основания, которое можно применять в настоящей заявке, включают в себя, но не ограничиваются перечисленным, н-бутиллитий, т-бутиллитий, метиллитий, этиллитий, метилат натрия, метилат калия, метилат лития, диметиламид лития, диэтиламид лития, дипропиламид лития, диизопропиламид лития и их смесь.
Подходящие примеры (R14R15R16Si)2NM, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, бис(триметилсилил)амид лития, бис(триэтилсилил)амид лития, бис(трипропилсилил)амид лития, бис(триизопропилсилил)амид лития, бис(диметилэтилсилил)амид лития, бис(диметилпропилсилил)амид лития, бис(диметилизопропилсилил)амид лития, бис(диметилфенилсилил)амид лития, бис(диметилбензилсилил)амид лития, бис(диэтилметилсилил)амид лития, бис(диэтилпропилсилил)амид лития, бис(диэтилизопропилсилил)амид лития, бис(диэтилфенилсилил)амид лития, бис(диэтилбензилсилил)амид лития, бис(диизопропилметилсилил)амид лития, бис(диизопропилэтилсилил)амид лития, бис(диизопропилфенилсилил)амид лития, бис(диизопропилбензилсилил)амид лития, бис(триметилсилил)амид натрия, бис(триэтилсилил)амид натрия, бис(трипропилсилил)амид натрия, бис(триизопропилсилил)амид натрия, бис(диметилэтилсилил)амид натрия, бис(диметилпропилсилил)амид натрия, бис(диметилизопропилсилил)амид натрия, бис(диметилфенилсилил) амид натрия, бис(диметилбензилсилил)амид натрия, бис(диэтилметилсилил)амид натрия, бис(диэтилпропилсилил)амид натрия, бис(диэтилизопропилсилил)амид натрия, бис(диэтилфенилсилил)амид натрия, бис(диэтилбензилсилил)амид натрия, бис(диизопропилметилсилил)амид натрия, бис(диизопропилэтилсилил)амид натрия, бис(диизопропилфенилсилил)амид натрия, бис(диизопропилбензилсилил)амид натрия, бис(триметилсилил)амид калия, бис(триэтилсилил)амид калия, бис(трипропилсилил)амид калия, бис(триизопропилсилил)амид калия, бис(диметилэтилсилил)амид калия, бис(диметилпропилсилил)амид калия, бис(диметилизопропилсилил)амид калия, бис(диметилфенилсилил)амид калия, бис(диметилбензилсилил)амид калия, бис(диэтилметилсилил)амид калия, бис(диэтилпропилсилил)амид калия, бис(диэтилизопропилсилил)амид калия, бис(диэтилфенилсилил)амид калия, бис(диэтилбензилсилил)амид калия, бис(диизопропилметилсилил)амид калия, бис(диизопропилэтилсилил)амид калия, бис(диизопропилфенилсилил)амид калия и бис(диизопропилбензилсилил)амид калия.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-V) с CH3S(О)2R3 и (R14R15R16Si)2NM с получением соединения формулы (A-VII) проводят с катализатором в присутствии сильного основания.
Подходящие примеры катализатора, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, фторирующее средство.
Подходящие примеры фторирующего средства, которое может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, трифторид бора.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-V) с CH3S(О)2R3 и (Rl4R15R16Si)2NM с получением соединения формулы (A-VII) проводят в присутствии сильного основания при -100°C-100°C.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (A-V) с CH3S(О)2R3 и (R14R15R16Si)2NM с получением соединения формулы (A-VII) проводят в присутствии сильного основания при -100°C-50°C.
В еще одном аспекте настоящая заявка относится к способу получения соединения формулы (B-III), включающему в себя взаимодействие соединения формулы (B-II) с соединением формулы R11-Y, (R12)2Y или Y-R13-Z с получением соединения формулы (B-III),
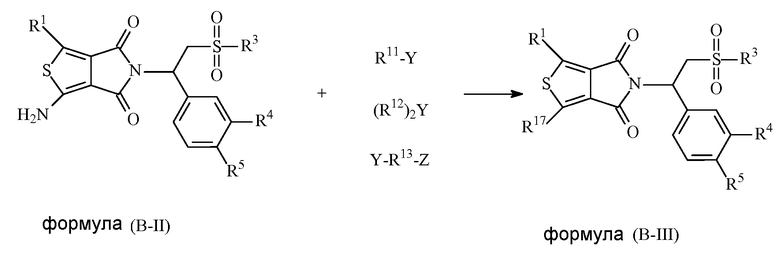
в которых
R1 выбран из группы, состоящей из атома водорода, атома галогена, C1-C8-алкила, C1-C8-алкокси, гидрокси, циано, нитро и NR6R7;
R3 выбран из группы, состоящей из гидрокси, C1-C8-алкила, C1-C8-алкокси, C1-C8-алкил(C1-C8-алкилен)окси, C5-C12-арила, C5-C12-арил(C1-C8-алкилен)окси и NR6R7;
каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, C1-C8-алкила, C1-C8-алкокси, C1-C8-алкилтио, циано, C3-C10-циклоалкила, (C1-C8-алкилен)C3-C10-циклоалкила, C3-C10-циклоалкил(C1-C8-алкилен)окси, C3-C10-циклоалкилокси, C5-C12-арила, C5-C12-арилокси и C5-C12-арил(C1-C8-алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, C1-C8-алкила, арила, C(О)R8 и SO2R8, или R6 и R7 вместе представляют собой 1,4-бутилиден, 1,5-пентилиден, 1,6-гексилиден или CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из O, S и NR8;
R8 выбран из группы, состоящей из атома водорода и галогензамещенного C1-C8-алкила;
R11 в R11-Y выбран из группы, состоящей из C1-C8-алкила, C5-C12-арила, C(О)R8 и S(О)2R8; Y выбран из группы, состоящей из атома галогена, OMs и OTs;
R12 в (R12)2Y выбран из С(О)R8; и Y представляет собой О;
R13 в Y-R13-Z выбран из группы, состоящей из 1,4-бутилидена, 1,5-пентилидена, 1,6-гексилидена и CH2CH2XCH2CH2; каждый Y и Z независимо выбран из группы, состоящей из атома галогена, OMs и OTs, X представляют собой O, S или NR8.
В некоторых вариантах осуществления изобретения к реакционной смеси, применяемой для реакции соединения формулы (B-II) с соединением формулы R11-Y, (R12)2Y или Y-R13-Z с получением соединения формулы (B-II), добавляют щелочной реагент.
Подходящие примеры щелочного реагента, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, триэтиламин, триметиламин, трипропиламин, диизопропилэтиламин, пиридин, N-метилморфолин, N-этилморфолин, N-метилпиперидин, N-этилпиперидин, N-метилпирролидин, N-этилпирролидин, 4-диметиламинопиридин, 4-пирролидинилпиридин, 2-метилпиридин, 3-метилпиридин, 4-метилпиридин, 2,6-диметилпиридин, 2,4,6-триметилпиридин, гидроксид натрия, гидроксид калия, гидроксид лития, карбонат натрия, карбонат калия, карбонат лития, карбонат цезия, гидрид натрия, гидрид калия, гидрид лития, алюмогидрид лития, метилат натрия, метилат калия, метилат лития, этилат натрия, этилат калия, этилат лития, изопропилат натрия, изопропилат калия, изопропилат лития, (R14R15R16Si)2NM, амид натрия, амид лития, амид калия и их смесь, где каждый из R14, R15 и R16 в (R14R15R16Si)2NM независимо выбран из группы, состоящей из C1-C8-алкила и фенила, M выбран из группы, состоящей из натрия, калия и лития.
Подходящие примеры (R14R15R16Si)2NM, которые могут применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, бис(триметилсилил)амид лития, бис(триэтилсилил)амид лития, бис(трипропилсилил)амид лития, бис(триизопропилсилил)амид лития, бис(диметилэтилсилил)амид лития, бис(диметилпропилсилил)амид лития, бис(диметилизопропилсилил)амид лития, бис(диметилфенилсилил)амид лития, бис(диметилбензилсилил)амид лития, бис(диэтилметилсилил)амид лития, бис(диэтилпропилсилил)амид лития, бис(диэтилизопропилсилил)амид лития, бис(диэтилфенилсилил)амид лития, бис(диэтилбензилсилил)амид лития, бис(диизопропилметилсилил)амид лития, бис(диизопропилэтилсилил)амид лития, бис(диизопропилфенилсилил)амид лития, бис(диизопропилбензилсилил)амид лития, бис(триметилсилил)амид натрия, бис(триэтилсилил)амид натрия, бис(трипропилсилил)амид натрия, бис(триизопропилсилил)амид натрия, бис(диметилэтилсилил)амид натрия, бис(диметилпропилсилил)амид натрия, бис(диметилизопропилсилил)амид натрия, бис(диметилфенилсилил)амид натрия, бис(диметилбензилсилил)амид натрия, бис(диэтилметилсилил)амид натрия, бис(диэтилпропилсилил)амид натрия, бис(диэтилизопропилсилил)амид натрия, бис(диэтилфенилсилил)амид натрия, бис(диэтилбензилсилил)амид натрия, бис(диизопропилметилсилил)амид натрия, бис(диизопропилэтилсилил)амид натрия, бис(диизопропилфенилсилил) амид натрия, бис(диизопропилбензилсилил)амид натрия, бис(триметилсилил)амид калия, бис(триэтилсилил)амид калия, бис(трипропилсилил)амид калия, бис(триизопропилсилил)амид калия, бис(диметилэтилсилил)амид калия, бис(диметилпропилсилил)амид калия, бис(диметилизопропилсилил)амид калия, бис(диметилфенилсилил)амид калия, бис(диметилбензилсилил)амид калия, бис(диэтилметилсилил)амид калия, бис(диэтилпропилсилил)амид калия, бис(диэтилизопропилсилил)амид калия, бис(диэтилфенилсилил)амид калия, бис(диэтилбензилсилил)амид калия, бис(диизопропилметилсилил)амид калия, бис(диизопропилэтилсилил)амид калия, бис(диизопропилфенилсилил)амид калия и бис(диизопропилбензилсилил)амид калия.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (B-II) с соединением формулы R11-Y, (R12)2Y или Y-R13-Z проводят в растворителе с получением соединения формулы (B-II).
Подходящие примеры растворителя, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, хлороформ, дихлорметан, дихлорэтан, тетрагидрофуран, ацетон, бутанон, метилацетат, пропилацетат, бутилацетат, изопропилацетат, метилформиат, этилформиат, пропилформиат, бутилформиат, изопропилформиат, метилпропионат, этилпропионат, пропилпропионат, бутилпропионат, изопропилпропионат, простой метиловый эфир, простой диэтиловый эфир, простой метилдиэтиловый эфир, простой метил-т-бутиловый эфир, простой этил-т-бутиловый эфир, простой метилизопропиловый эфир, простой этилизопропиловый эфир, простой изопропиловый эфир, этилацетат, этанол, метанол, пропиловый спирт, бутиловый спирт, этиленгликоль, простой диметиловый эфир гликоля, простой монометиловый эфир этиленгликоля, простой моноэтиловый эфир этиленгликоля, простой диэтиловый эфир гликоля, бензол, толуол, н-гексан, циклогексан, ДМФА, ДМСО, петролейный эфир, вода и их смесь.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (B-II) с соединением формулы R11-Y, (R12)2Y или Y-R13-Z с получением соединения формулы (B-II) проводят при -20°C-200°C.
В некоторых вариантах осуществления изобретения реакцию соединения формулы (B-II) с соединением формулы R11-Y, (R12)2Y или Y-R13-Z с получением соединения формулы (B-II) проводят при -10°C-100°C.
В некоторых вариантах осуществления изобретения соединение формулы (B-II) получают из соединения формулы (B-I),
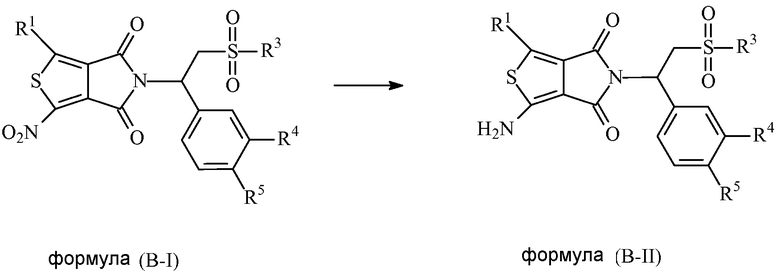
в которых
R1 выбран из группы, состоящей из атома водорода, атома галогена, C1-C8-алкила, C1-C8-алкокси, гидрокси, циано, нитро и NR6R7;
R3 выбран из группы, состоящей из гидрокси, C1-C8-алкила, C1-C8-алкокси, C1-C8-алкил(C1-C8-алкилен)окси, C5-C12-арила, C5-C12-арил(C1-C8-алкилен)окси и NR6R7;
каждый из R4 и R5 по отдельности выбран из группы, состоящей из атома водорода, гидрокси, C1-C8-алкила, C1-C8-алкокси, C1-C8-алкилтио, циано, C3-C10-циклоалкила, (C1-C8-алкилен)C3-C10-циклоалкила, C3-C10-циклоалкил(C1-C8-алкилен)окси, C3-C10-циклоалкилокси, C5-C12-арила, C5-C12-арилокси и C5-C12-арил(C1-C8-алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, C1-C8-алкила, арила, C(О)R8 или SO2R8, или R6 и R7 вместе представляют собой 1,4-бутилиден, 1,5-пентилиден, 1,6-гексилиден и CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из O, S и NR8;
R8 выбран из группы, состоящей из атома водорода и галогензамещенного C1-C8-алкила.
В некоторых вариантах осуществления изобретения реакцию получения соединения формулы (B-II) с соединением формулы (B-I) проводят в присутствии восстановителя.
Подходящие примеры восстановителя, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, порошок железа, порошок гидросульфита натрия, порошок цинка и водород.
В некоторых вариантах осуществления изобретения реакцию получения соединения формулы (B-II) с соединением формулы (B-I) проводят в присутствии катализатора.
Подходящие примеры катализатора, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, тяжелые металлы, такие как палладий, платина, родий, никель, рутений, иридий и т.д. и их оксиды или соли, такие как гидрохлориды; серную кислоту, фосфорную кислоту, муравьиную кислоту, уксусную кислоту, пропионовую кислоту, метансульфоновую кислоту, этансульфоновую кислоту, бензолсульфоновую кислоту и п-толуолсульфоновую кислоту.
В некоторых вариантах осуществления изобретения реакцию получения соединения формулы (B-II) с соединением формулы (B-I) проводят в присутствии следующих катализаторов: гидрохлорид, серная кислота, фосфорная кислота, муравьиная кислота, уксусная кислота, пропионовая кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, палладий на углероде, платина на углероде, диоксид платины, хлорид палладия, хлорид платины, никель Ренея или их смесь.
В некоторых вариантах осуществления изобретения реакцию получения соединения формулы (B-II) с соединением формулы (B-I) проводят в растворителе.
Подходящие примеры растворителя, который может применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, метанол, этанол, пропиловый спирт, бутиловый спирт, изопропиловый спирт, хлороформ, дихлорметан, тетрахлорид углерода, 1,2-дихлорэтан, простой диметиловый эфир гликоля, простой диэтиловый эфир гликоля, простой диэтиловый эфир, простой метилэтиловый эфир, простой метилпропиловый эфир, простой метилбутиловый эфир, простой этилпропиловый эфир, простой метил-т-бутиловый эфир, тетрагидрофуран, этилацетат, метилацетат, пропилацетат, бутилацетат, метилпропионат, этилпропионат, метилформиат, этилформиат, пропилформиат, изопропилацетат, ацетон, бутанон, пиридин, ДМФА, ДМСО, ацетонитрил, пропионитрил, бензол, толуол, вода и их смесь.
В некоторых вариантах осуществления изобретения соединение формулы (B-II) получают из соединения формулы (B-I) при -20°C-250°C.
В некоторых вариантах осуществления изобретения соединение формулы (B-II) получают из соединения формулы (B-I) при 0°C-150°C.
В некоторых вариантах осуществления изобретения соединение формулы (B-II) получают из соединения формулы (B-I) при 1 атм -100 атм.
В некоторых вариантах осуществления изобретения соединение формулы (B-II) получают из соединения формулы (B-I) при 1 атм -20 атм.
В еще одном аспекте настоящая заявка относится к фармацевтической композиции, содержащей фармацевтически приемлемый носитель и терапевтически эффективное количество соединения формулы (I), его стереоизомера, энантиомера или таутомера или смеси его стереоизомеров, его фармацевтически приемлемой соли, его полиморфной модификации, его сольвата, его пролекарства или его метаболита,
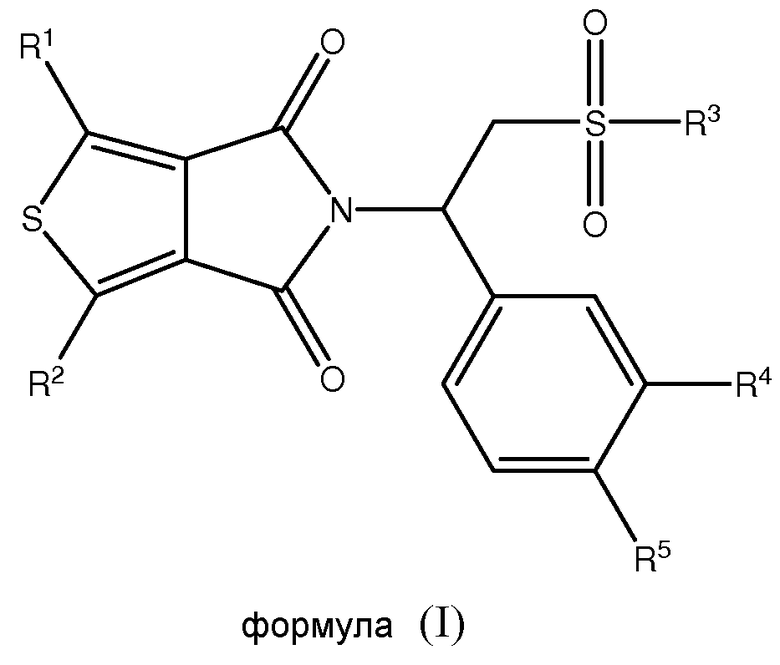
в которой
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из O, S и NR8;
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
Примеры фармацевтически приемлемого носителя, разбавителя или инертного наполнителя, которые могут применяться в фармацевтической композиции согласно настоящей заявке, включают в себя, но не ограничиваются перечисленным, любое вспомогательное лекарственное вещество, носитель, инертный наполнитель, вещество, способствующее скольжению, подсластитель, разбавитель, консервант, краситель/окрашивающее средство, усилитель вкуса и запаха, поверхностно-активное вещество, увлажняющее средство, диспергатор, суспендирующее средство, стабилизатор, изоосмотическое средство, растворитель или эмульгатор, которые утверждены Управлением по контролю за продуктами питания и лекарственными средствами США как приемлемые для применения для человека и животных.
В некоторых вариантах осуществления изобретения фармацевтическая композиция согласно настоящей заявке дополнительно содержит по меньшей мере еще один активный ингредиент.
Подходящие примеры активных ингредиентов, которые можно применять в настоящей заявке, включают в себя, но не ограничиваются перечисленным, хлорметин (азотистый иприт), азиридин, метилмеламин, алкилсульфонат, нитрозомочевину, триазен, фолацин, аналог пиримидина, аналог пурина, алкалоид винка, эпидофиллотоксин, антибиотик, ингибитор топоизомеразы, противоопухолевую вакцину, ацивицин, акларубицин, акодазол гидрохлорид, акронин, адозелесин, алдеслейкин, амбомицин, аметатрон ацетат, аминоглутетимид, амсакрин, анастрозол, антрамицин, аспарагиназу, азитромицин, азацитидин, препарат азетепа, азотомицин, батимастат, препарат бензодепа, бикалутамид, бисантрен гидрохлорид, биснафид мезилат, бизелезин, блеомицин сульфат, бусульфан, актиномицин C, калустерон, карацемид, карбетимер, карбоплатин, кармустин, карубицин гидрохлорид, хлорамбуцил, циролемицин, кладрибин, криснатол мезилат, циклофосфамид, цитарабин, дакарбазин, актиномицин D, даунорубицин гидрохлорид, децитабин, доцетаксел, доксорубицин, дролоксифен гидрохлорид, эпирубицин гидрохлорид, эсорубицин гидрохлорид, эстрамустин, этанидазол, этопозид, флоксуридин, флуороурацил, флуроцитабин, гемцитабин, идарубицин гидрохлорид, ифосфамид, интерлейкин II, интерферон α-2a, интерферон α-2b, иринотекан гидрохлорид, летрозол, меркаптопурин, метотрексат, метропин, митомицин, митоксантрон, паклитаксел, прокарбазин, препарат тиотепа, винбластин, винкристин, ингибитор ангиогенеза, камптотецин, гексадекадрол, аспирин, ацетаминофен, индометацин, ибупрофен, кетопрофен, мелоксикам, кортикостероид и адреналовый кортикостероид.
В некоторых вариантах осуществления изобретения фармацевтическую композицию согласно настоящей заявке получают в виде таблетки, раствора, гранулы, пластыря, мази, капсулы, аэрозоля или суппозитория, вводимых с помощью парентерального, трансдермального, мукозального, назального, буккального, подъязычного или перорального способа введения.
В еще одном аспекте настоящая заявка относится к способу уменьшения активности фермента PDE4, включающему в себя контактирование фермента PDE4 с терапевтически эффективным количеством соединения формулы (I), его энантиомером или таутомером или смесью его стереоизомеров, его фармацевтически приемлемой солью, его полиморфной модификацией, его сольватом, его пролекарством или его метаболитом,
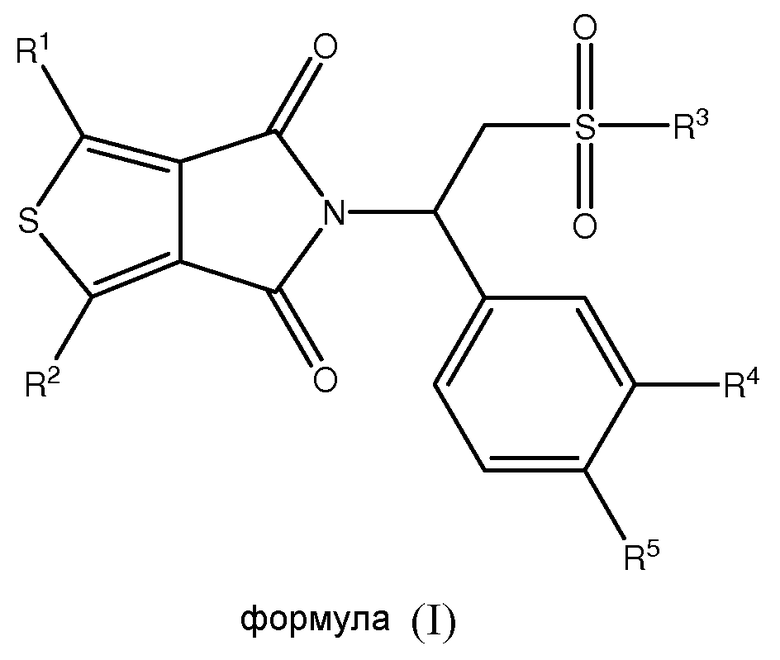
в которой
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из O, S и NR8;
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
В некоторых вариантах осуществления изобретения контактирование фермента PDE4 с терапевтически эффективным количеством соединения формулы (I), его энантиомера или таутомера или смеси его стереоизомеров, его фармацевтически приемлемой соли, его полиморфной модификации, его сольвата, его пролекарства или его метаболита осуществляют in vitro.
В еще одном аспекте настоящая заявка дополнительно относится к способу лечения заболеваний или состояний, опосредованных ферментом PDE4, включающим в себя введение субъекту, нуждающемуся в лечении, терапевтически эффективного количества соединения формулы (I), его стереоизомера, энантиомера или таутомера или смеси его стереоизомеров, его фармацевтически приемлемой соли, его полиморфной модификации, его сольвата, его пролекарства или его метаболита,
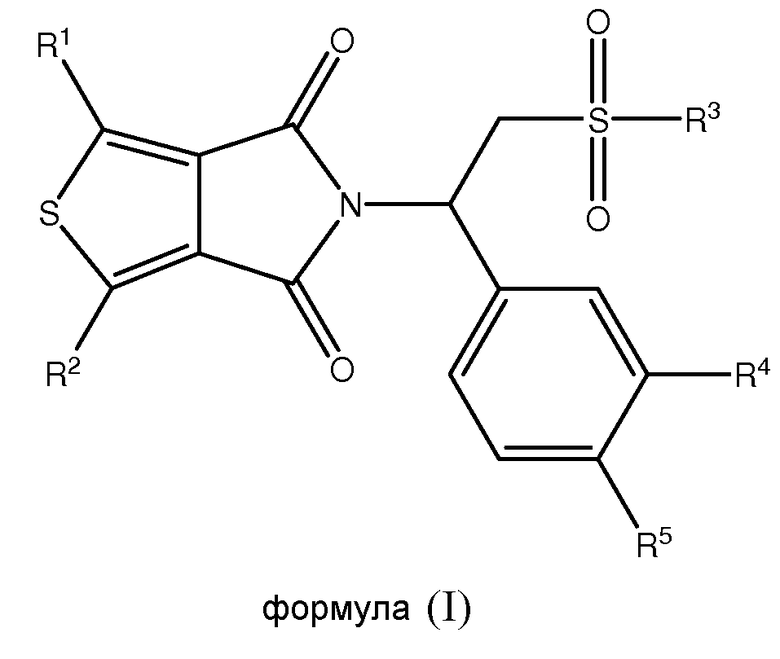
в которой
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, атома галогена, необязательно замещенного алкила, необязательно замещенного алкокси, гидрокси, циано, нитро и необязательно замещенного NR6R7;
R3 выбран из группы, состоящей из гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкил(алкилен)окси, необязательно замещенного арила, необязательно замещенного арил(алкилен)окси и необязательно замещенного NR6R7;
каждый из R4 и R5 независимо выбран из группы, состоящей из атома водорода, гидрокси, необязательно замещенного алкила, необязательно замещенного алкокси, необязательно замещенного алкилтио, циано, необязательно замещенного циклоалкила, необязательно замещенного (алкилен)циклоалкила, необязательно замещенного циклоалкил(алкилен)окси, необязательно замещенного циклоалкилокси, необязательно замещенного арила, необязательно замещенного арилокси и необязательно замещенного арил(алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, необязательно замещенного алкила, необязательно замещенного арила, необязательно замещенного C(О)R8 и необязательно замещенного SO2R8, или R6 и R7 вместе представляют собой необязательно замещенный 1,4-бутилиден, необязательно замещенный 1,5-пентилиден, необязательно замещенный 1,6-гексилиден или необязательно замещенный CH2CH2XCH2CH2, в котором X выбран из группы, состоящей из O, S и NR8;
R8 выбран из группы, состоящей из атома водорода и необязательно замещенного алкила.
В некоторых вариантах осуществления изобретения заболевания или состояния выбраны из группы, состоящей из воспалительных заболеваний или состояний, инфекционных заболеваний или состояний, иммунных заболеваний или состояний и злокачественных заболеваний или состояний.
В некоторых вариантах осуществления изобретения примеры заболеваний или состояний включают в себя, но не ограничиваются перечисленным, карциному головы, карциному щитовидной железы, злокачественную опухоль горла, злокачественную опухоль глаза, злокачественную опухоль кожи, злокачественную опухоль полости рта, злокачественную опухоль гортани, злокачественную опухоль пищевода, злокачественную опухоль молочной железы, злокачественную опухоль кости, лейкемию, миелому, злокачественную опухоль легкого, злокачественную опухоль толстой кишки, карциному сигмовидной ободочной кишки, злокачественную опухоль прямой кишки, злокачественную опухоль желудка, злокачественную опухоль предстательной железы, злокачественную опухоль молочной железы, злокачественную опухоль яичников, злокачественную опухоль почек, злокачественную опухоль печени, злокачественную опухоль поджелудочной железы, злокачественную опухоль головного мозга, злокачественную опухоль кишечника, злокачественную опухоль сердца, адреналовую карциному, злокачественную опухоль подкожных тканей, злокачественную опухоль лимфоузлов, злокачественную меланому, злокачественную глиому, ВИЧ, гепатит, синдром дыхательных расстройств взрослого типа, заболевание, связанное с деминерализацией кости, хроническую обструктивную болезнь легких, хроническое воспаление легких, дерматит, воспалительное заболевание кожи, атопический дерматит, кистозный фиброз, септический шок, пиемию, эндоксиновый бактериально-токсический шок, динамический кровяной шок (резкое падение кровяного давления), септический синдром заболевания, ишемически-реперфузионное повреждение, менингит, псориаз, фиброзное заболевание, кахексию, отторжение трансплантата, связанное с реакцией "трансплантат против хозяина", аутоиммунное заболевание, ревматоидный спондилит, артритный симптом (такой как ревматоидный артрит или остеоартрит), остеопороз, болезнь Крона, ульцеративный колит, энтерит, рассеянный склероз, системную красную волчанку, лепрозную узловатую эритему при лепре (ENL), радиационное повреждение, астму, гипероксическое повреждение легких, инфекции, вызванные микроорганизмами, и инфекционный синдром, вызванный микроорганизмами.
В некоторых вариантах осуществления изобретения примеры инфекций, вызванных микроорганизмами, и инфекционного синдрома, вызванного микроорганизмами, опосредованных ферментом PDE4 и подлежащих лечению согласно настоящей заявке, включают в себя, но не ограничиваются перечисленным, бактериальные инфекции, грибковые инфекции, малярию, микобактериальные инфекции и оппортунистические инфекции, индуцированные ВИЧ.
В некоторых вариантах осуществления изобретения субъекту, нуждающемуся в способе лечения заболеваний или состояний, опосредованных ферментом PDE4, вводят однократную дозу в количестве 0,1 мг-1000 мг соединения формулы (I).
В некоторых вариантах осуществления изобретения субъекту, нуждающемуся в способе лечения заболеваний или состояний, опосредованных ферментом PDE4, вводят однократную дозу в количестве 1 мг-1000 мг соединения формулы (I).
В некоторых вариантах осуществления изобретения способ лечения заболеваний или состояний, опосредованных ферментом PDE4, дополнительно содержит введение субъекту, нуждающемуся в лечении по меньшей мере еще одного активного ингредиента.
Подходящие примеры активных ингредиентов, которые могут применяться в настоящей заявке, включают в себя, но не ограничиваются перечисленным, хлорметин, азиридин, метилмеламин, алкилсульфонат, нитрозомочевину, триазен, фолацин, аналог пиримидина, аналог пурина, алкалоид винка, эпидофиллотоксин, антибиотик, ингибитор топоизомеразы, противоопухолевую вакцину, ацивицин, акларубицин, акодазол гидрохлорид, акронин, адозелесин, алдеслейкин, амбомицин, аметатрон ацетат, аминоглутетимид, амсакрин, анастрозол, антрамицин, аспарагиназу, азитромицин, азацитидин, препарат азетепа, азотомицин, батимастат, препарат бензодепа, бикалутамид, бисантрен гидрохлорид, биснафид мезилат, бизелезин, блеомицин сульфат, бусульфан, актиномицин C, калустерон, карацемид, карбетимер, карбоплатин, кармустин, карубицин гидрохлорид, хлорамбуцил, циролемицин, кладрибин, криснатол мезилат, циклофосфамид, цитарабин, дакарбазин, актиномицин D, даунорубицин гидрохлорид, децитабин, доцетаксел, доксорубицин, доксорубицин гидрохлорид, дролоксифен, эпирубицин гидрохлорид, эсорубицин гидрохлорид, эстрамустин, этанидазол, этопозид, флоксуридин, флуороурацил, флуроцитабин, гемцитабин, идарубицин гидрохлорид, ифосфамид, интерлейкин II, интерферон α-2a, интерферон α-2b, иринотекан гидрохлорид, летрозол, меркаптопурин, метотрексат, метропин, митомицин, митоксантрон, паклитаксел, прокарбазин, препарат тиотепа, винбластин, винкристин, ингибитор ангиогенеза, камптотецин, гексадекадрол, аспирин, ацетаминофен, индометацин, ибупрофен, кетопрофен, мелоксикам, кортикостероид и адреналовый кортикостероид.
В некоторых вариантах осуществления изобретения субъекту, нуждающемуся в данном способе лечения заболеваний или состояний, опосредованных ферментом PDE4, одновременно, параллельно, по отдельности или последовательно вводят соединение формулы (I) и по меньшей мере еще один активный ингредиент.
ПРИМЕРЫ
Несмотря на то, что любой специалист в данной области способен получить соединения согласно настоящей заявке в соответствии с описанными выше общими методиками, для удобства в этом месте данного описания предлагаются более конкретные детали методик синтеза соединения согласно настоящей заявке. И в этом случае все реагенты и условия реакций, используемые при синтезе, известны специалистам в данной области и доступны из общедоступных коммерческих источников.
Сокращения
CDI: 1,1'-карбонилдиимидазол;
DCM: дихлорметан;
ТГФ: тетрагидрофуран;
TFA: трифторуксусная кислота;
DMAP: 4-(N,N-диметиламино)пиридин;
TEA: триэтиламин;
ДМФА: N,N-диметилформамид;
ДМСО: диметилсульфоксид;
HOBt: 1-гидроксибензотриазол;
DCC: N,N-дициклогексилкарбодиимид;
TBFA: фторид тетрабутиламмония;
EDC•HCl: гидрохлорид 1-(3-диметиламинопропил)-3-этилкарбодиимида;
Fmoc: 9-флуоренилметоксикарбонил;
MOM: метоксиметил;
MEM: метоксиэтоксиметил;
MTM: метилтиометил;
SEM: 2-(триметилсилил)этоксиметил;
TMSE: 2-(триметилсилил)этил;
DIC: N,N'-диизопропилкарбодиимид;
HOAt: 1-гидрокси-7-азобензотриазол;
BOP: гексафторфосфат (бензотриазол-1-илокси-три(диметиламино)фосфония;
Cl-HOBt: 6-хлор-1-гидроксибензотриазол;
DEPBT: 3-(диэтоксифосфорилокси)-1,2,3-фентриазин-4-он;
HATU: гексафторфосфат бис(диметиламино)метилентриазол[4,5-B]пиридин-3-оксида;
HBTU: гексафторфосфат бензотриазол-N,N,N',N'-тетраметилмочевины;
HCTU: гексафторфосфат 6-хлорбензотриазол-1,1,3,3-тетраметилмочевины;
HOOBt: 3-гидрокси-1,2,3-фентриазин-4(3H)-он;
PyBOP: гексафторфосфорная кислота.бензотриазол-1-илокситрипирролидинилфосфин;
TATU: тетрафторборат О-(7-азобензотриазол-1-ил)-N,N,N',N'-тетраметилмочевины;
TBTU: тетрафторборат О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилмочевины;
OMS: сложный эфир метансульфоновой кислоты;
OTS: сложный эфир п-толуолсульфоновой кислоты.
Получение соединений согласно настоящей заявке иллюстрируется, но не ограничивается следующими примерами.
Соединение 1a
4-метокси-3-этоксибензальдегид
В 500 мл трехгорлую колбу, оборудованную механической мешалкой и трубкой для подвода инертного газа, добавляли 30,5 г изованилина, 55,2 г карбоната калия, 49,9 г йодэтана и 140 мл ДМФА. Смесь перемешивали в течение ночи при комнатной температуре. Смесь выливали в 1400 мл воды, и затем экстрагировали полученную смесь этилацетатом (600 мл × 2). Этилацетатные слои объединяли. Органической фазу промывали насыщенным раствором Na2CО3 (200 мл × 3), 200 мл воды и 200 мл насыщенного раствора NaCl, сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали, получая при этом бледно-желтый твердый продукт. Твердый продукт перекристаллизовывали из смеси растворителей: этилацетат и петролейный эфир (1:4), получая при этом белые игольчатые кристаллы (32,9 г). МС (m/z): 181 [M+1]+.
Следующие соединения 1b-1d получали тем же способом, который описан выше.
Соединение 1b
4-этокси-3-метоксибензальдегид
Повторяли способ получения соединения 1a с применением ванилина вместо изованилина, получая при этом твердый продукт.
МС (m/z): 181 [M+1]+.
Соединение 1c
3,4-диметоксибензальдегид
Повторяли способ получения соединения по примеру 1a с применением йодметана вместо йодэтана, получая при этом твердый продукт. МС(m/z): 167 [M+1]+.
Соединение 1d
3-фенилметокси-4-метоксибензальдегид
Повторяли способ получения соединения по примеру 1a с применением бензилхлорида вместо йодэтана, получая при этом твердый продукт. МС(m/z): 243 [M+1]+.
Соединение 2a
1-(3-этокси-4-метоксифенил-2-(метилсульфонил)-N-(триметилсилил)этиламин
В 500 мл трехгорлую колбу, оборудованную магнитной мешалкой и трубкой для подвода инертного газа, добавляли 3,7 г диметилсульфона и 160 мл ТГФ. Смесь охлаждали до -78°C и по каплям добавляли в смесь 22 мл н-бутиллития (2,2 M раствор в н-гексане). После добавления смесь поддерживали при температуре -78°C и перемешивали в течение 30 минут, получая при этом соединение A. В 250 мл трехгорлую колбу, оборудованную магнитной мешалкой и трубкой для подвода инертного газа, добавляли 7,1 г соединения 1а. Колбу охлаждали на бане со смесью льда и соли. В колбу по каплям добавляли 43 мл бис(триметилсилил)амида лития (1,06 M раствор в ТГФ). После добавления смесь перемешивали в течение 15 минут, и затем к смеси по каплям добавляли 10 мл раствора трифторида бора в простом диэтиловом эфире. Полученную смесь перемешивали в течение 5 минут, получая при этом соединение B. Соединение B подвергали превращению в A. Смесь медленно нагревали до комнатной температуры (в течение около 1,5 часов). Реакцию гасили с помощью 200 мл 1,6 н. раствора K2CO3. Смесь перемешивали в течение 30 минут и затем разделяли. Водный слой экстрагировали этилацетатом (200 мл × 3). Все органические слои объединяли. Полученную органическую фазу промывали 200 мл насыщенного раствора NaCl, сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали, получая при этом 10 г бледно-желтого твердого продукта в виде пены.
Следующие соединения 2b-2d получали тем же способом, который описан выше.
Соединение 2b:
1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)-N-(триметилсилил)этиламин
Соединение 2c:
1-(3,4-диметоксифенил)-2-(метилсульфонил)-N-(триметилсилил)этиламин
Соединение 2d:
1-(3-фенилметоксиметоксифенил)-2-(метилсульфонил)-N-(триметилсилил)этиламин
Соединение 3a
1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этиламин
В 500 мл одногорлую колбу, оборудованную магнитной мешалкой, добавляли 10 г соединения 2a, 100 мл простого диэтилового эфира и 100 мл 4 н. раствора HCl. Смесь перемешивали в течение 30 минут при комнатной температуре и разделяли. Органической слой экстрагировали 4 н. раствором HCl (100 мл × 3). Водные слои объединяли. pH водной фазы доводили до 12 с помощью 4 н. раствора гидроксида натрия на бане со льдом. Полученную смесь экстрагировали этилацетатом (200 мл × 3). Органические слои объединяли. Органическую фазу промывали 200 мл насыщенного раствора NaCl, сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали. После очистки колоночной хроматографией получали 1,5 г твердого продукта белого цвета.
1H ЯМР (CDCl3): 8 6,93-6,84 (м, ЗН), 4,60 (д, 1H, J=8 Гц), 4,12 (кв., 2H, J=4 Гц), 3,87 (с, 3H), 3,37-3,21 (м, 2H), 2,92 (с, 3H), 1,86 (с, 2H), 1,48 (т, 3H, J=4 Гц); МС(m/z): 274 [M+1]+; Хиральная ВЭЖХ (изопропанол/н-гексан/диэтиламин = 35/65/0,1, колонка chiralcel® OJ-H, 250×4,6 мм, 1,0 мл/мин, @234 нм): 15,2 минут (R-изомер, 49,8%), 17,3 минут (S-изомер, 50,2%).
Следующие соединения 3b-3d получали тем же способом, который описан выше.
Соединение 3b:
1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этиламин
МС (m/z): 274 [M+1]+
Соединение 3c:
1-(3,4-диметоксифенил)-2-(метилсульфонил)этиламин
МС (m/z): 260 [M+1]+
Соединение 3d:
1-(3-фенилметоксиметоксифенил)-2-(метилсульфонил)этиламин
МС(m/z): 336 [M+1]+
Соединение 4a
Соль (S)-1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этиламин•N-ацетил-L-валин
В 100 мл одногорлую колбу, оборудованную магнитной мешалкой, обратным холодильником и трубкой для подвода инертного газа, добавляли 6,920 г соединения 3a, 2,418 г N-ацетил-L-валина и 50 мл безводного метанола. Смесь кипятили с обратным холодильником на масляной бане в течение 1 часа, перемешивали в течение 3 часов при комнатной температуре и фильтровали в вакууме, получая при этом твердый продукт белого цвета. Твердый продукт белого цвета добавляли в 25 мл безводного метанола. Полученную смесь кипятили с обратным холодильником в течение 1 часа, перемешивали при комнатной температуре в течение 3 часов и фильтровали в вакууме, получая при этом 6,752 г твердого продукта белого цвета.
Соединение 4b
(S)-1-(3-этокси-4-метоксифенил-2-(метилсульфонил)этиламин
В 250 мл одногорлую колбу, оборудованную магнитной мешалкой, добавляли 6,752 г соединения 4a, 150 мл дихлорметана и 150 мл воды. К смеси на бане со льдом по каплям добавляли 5% водный раствор гидроксида натрия, доводя при этом pH до 11. Полученную смесь разделяли. Водный слой экстрагировали 150 мл дихлорметана. Дихлорметановые слои объединяли. Органическую фазу промывали 100 мл насыщенного раствора NaCl, сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали, получая при этом 2,855 г твердого продукта белого цвета (99,0% э.и.). МС (m/z): 274 [M+1]+; Хиральная ВЭЖХ (изопропанол/н-гексан/диэтиламин = 35/65/0,1, колонка chiralcel® OJ-H, 250 × 4,6 мм, 1,0 мл/мин, @234 нм): 15,2 минут (R-изомер, 0,5%), 17,3 минут (S-изомер, 15 99,5%).
Соединение 4c
Соль (R)-1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этиламин•N-ацетил-D-лейцина
В 100 мл одногорлую колбу, оборудованную магнитной мешалкой, обратным холодильником и трубкой для подвода инертного газа, добавляли 1,365 г соединения 3a, 0,519 г N-ацетил-D-лейцина, 10 мл безводного метанола. Смесь кипятили с обратным холодильником на масляной бане в течение 1 часа, перемешивали в течение 3 часов при комнатной температуре и фильтровали в вакууме, получая при этом 1,290 г твердого продукта белого цвета. Твердый продукт белого цвета добавляли в 10 мл безводного метанола. Полученную смесь кипятили с обратным холодильником в течение 1 часа, перемешивали в течение 3 часов при комнатной температуре и фильтровали в вакууме, получая при этом 1,042 г твердого продукта белого цвета.
Соединение 4d
(R)-1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этиламин
В 250 мл одногорлую колбу, оборудованную магнитной мешалкой, добавляли соединение 4c, 50 мл дихлорметана и 50 мл воды. К смеси по каплям добавляли 5% водный раствор гидроксида натрия на бане со льдом, доводя при этом значение pH до 11. Полученную смесь разделяли. Водный слой экстрагировали 50 мл дихлорметана. Дихлорметановые слои объединяли. Органическую фазу промывали 50 мл насыщенного раствора NaCl, сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали, получая при этом 0,622 г твердого продукта белого цвета (99,0% э.и.). МС (m/z): 274 [M+1]+; Хиральная ВЭЖХ (изопропиловый спирт/н-гексан/диэтиламин = 35/65/0,1, колонка chiralcel® OJ-H,, 250 × 4,6 мм, 1,0 мл/мин, @234 нм): 15,2 минут (R-изомер, 99,5%), 17,3 минут (S-изомер, 0,5%).
Соединение 5
3,4-дицианотиофен
В 2000 мл трехгорлую колбу, оборудованную магнитной мешалкой, обратным холодильником и трубкой для подвода инертного газа, добавляли 96,8 г 3,4-дибромтиофена, 104 г цианида меди(I) и 100 мл безводного ДМФА. Смесь нагревали при кипячении с обратным холодильником в течение 4 часов и охлаждали до комнатной температуры. К реакционной смеси добавляли раствор 400 г FeCl3•6H2О в 700 мл 1,7 н. раствора хлористоводородной кислоты. В течение 30 минут поддерживали температуру реакционного раствора при 60°C-70°C. После достаточного охлаждения к реакционному раствору добавляли 500 мл DCM. Полученную смесь делили на несколько порций. Каждую порцию, составляющую 300 мл, экстрагировали DCM (300 мл × 2). Все DCM-слои объединяли. Экстракт делили на несколько порций. Каждую порцию, составляющую 600 мл, последовательно промывали 6 н. раствором хлористоводородной кислоты (50 мл × 2), водой, насыщенным водным раствором Na2CО3 и насыщенным солевым раствором, сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали, получая при этом твердый продукт желтого цвета. Твердый продукт желтого цвета промывали смесью растворителей (этилацетат и петролейный эфир (1:1)) и фильтровали, получая при этом 21 г твердого продукта белого цвета. 1H ЯМР (CDCl3): δ 8,07 (s, 2H).
Соединение 6
Тиофен-3,4-дикарбоновая кислота
В 500 мл круглодонную колбу, оборудованную электромагнитной мешалкой и обратным холодильником, добавляли 15,978 г соединения 5, 43,997 г гидроксида калия и 174 мл этиленгликоля. Смесь кипятили с обратным холодильником в течение 4 часов. После охлаждения к реакционной смеси добавляли 350 мл воды. Полученную смесь экстрагировали простым диэтиловым эфиром (100 мл × 2). Слои, полученные с простым диэтиловым эфиром, удаляли. К водному слою на бане со льдом добавляли избыточное количество концентрированной хлористоводородной кислоты, получая при этом белый осадок. Белый осадок отфильтровали, и твердый продукт растворяли в простом диэтиловом эфире (около 2000 мл). Фильтрат экстрагировали простым диэтиловым эфиром (300 мл × 3). Все слои, полученные с простым диэтиловым эфиром, объединяли. Органическую фазу сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали, получая при этом 15 г твердого продукта белого цвета. Твердый продукт белого цвета перекристаллизовывали из воды.
1H ЯМР (ДМСО-d6): δ 10,35 (уш. с, 2H), 8,17 (с, 2H); МС (m/z): 171 [M-1]+.
Соединение 7
Тиофен[3,4-c]фуран-1,3-дикетон
В 250 мл круглодонную колбу, оборудованную электромагнитной мешалкой, обратным холодильником и осушительной трубкой, добавляли 15 г соединения 6 и 120 мл уксусного ангидрида. Смесь кипятили с обратным холодильником в течение 3 часов. Растворитель выпаривали, получая при этом 13 г твердого продукта коричневого цвета.
Соединение 8
2-нитротиофен-3,4-дикарбоновая кислота
В 250 мл круглодонную колбу, оборудованную электромагнитной мешалкой и осушительной трубкой, добавляли 40 мл дымящейся азотной кислоты (содержание 95%). Колбу охлаждали до 0°C-5°C на бане со льдом. Порциями (1 г в каждый порции) добавляли 10 г соединения 7. После добавление смесь подвергали взаимодействию в течение 30 минут при обычной температуре (выделялся твердый продукт желтого цвета). Реакционную смесь выливали в 80 г смеси воды со льдом. Полученную смесь экстрагировали этилацетатом (100 мл × 3). Все этилацетатные слои объединяли. Органической фазу последовательно промывали 50 мл × 2 воды и насыщенным солевым раствором, сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали, получая при этом 10 г твердого продукта желтого цвета. МС(m/z): 216 [M-1]+.
Соединение 9
4-нитротиофен [3,4-c]фуран-1,3-дикетон
В 250 мл круглодонную колбу, оборудованную электромагнитной мешалкой, обратным холодильником и осушительной трубкой, добавляли 10 г соединения 8 и 100 мл уксусного ангидрида. Смесь кипятили с обратным холодильником в течение 3 часов. Растворитель выпаривали, получая при этом 9 г твердый продукта коричневого цвета.
ПРИМЕР 1
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-нитро-5H-тиофен[3,4-c]пиррол-4,6-дикетон
В 250 мл круглодонную колбу, оборудованную электромагнитной мешалкой и осушительной трубкой, добавляли 1,99 г соединения 9, 2,73 г соединения 3a и 100 мл ТГФ. Смесь перемешивали в течение ночи при комнатной температуре. Добавляли 1,944 г CDI. Полученную смесь кипятили с обратным холодильником на масляной бане в течение 2 часов. Смесь охлаждали до комнатной температуры на открытом воздухе. Добавляли 200 мл этилацетата и 150 мл воды. Смесь экстрагировали и разделяли. Органический слой промывали 100 мл 0,5 н. раствора HCl, 100 мл насыщенного раствора NaCl, затем сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали. После очистки колоночной хроматографией получали 3,541 г твердого продукта светло-желтого цвета. МС(m/z): 453 [M-1]+.
ПРИМЕР 2
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-амино-5H-тиофен[3,4-c]пиррол-4,6-дикетон
В 250 мл круглодонную колбу, оборудованную электромагнитной мешалкой, обратным холодильником и осушительной трубкой, добавляли 2,27 г 5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-нитро-5H-тиофен[3,4-c]пиррол-4,6-дикетона и 100 мл ТГФ. Смесь нагревали при кипячении с обратным холодильником. Добавляли 1,4 г восстановленного порошкообразного железа. Полученную смесь кипятили с обратным холодильником в течение 2 часов и фильтровали в вакууме. Фильтрат выпаривали. Добавляли 200 мл этилацетата и 150 мл воды. Смесь экстрагировали и разделяли. Органической слой промывали 100 мл воды, 100 мл насыщенного раствора NaCl, затем сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали. После очистки колоночной хроматографией получали 1,68 г твердого продукта желтовато-коричневого цвета. МС(m/z): 425 [M+1]+.
ПРИМЕР 3
N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид
Способ I: В 50 мл круглодонную колбу, оборудованную электромагнитной мешалкой, обратным холодильником и осушительной трубкой, добавляли 0,1 г 5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-амино-5H-тиофен[3,4-c]пиррол-4,6-дикетона, 0,005 г DMAP и 10 мл уксусного ангидрида. Смесь нагревали до 60°C и перемешивали в течение 6 часов. Растворитель выпаривали. После очистки колоночной хроматографией получали 0,02 г твердого продукта белого цвета.
Способ II: В 50 мл круглодонную колбу, оборудованную электромагнитной мешалкой, обратным холодильником и осушительной трубкой, добавляли 0,1 г 5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-амино-5H-тиофен[3,4-c]пиррол-4,6-дикетона и 5 мл пиридина. На бане со льдом добавляли по каплям 0,2 мл ацетилхлорида и перемешивали в течение 1 часа при комнатной температуре. Растворитель выпаривали. Добавляли 50 мл этилацетата и 20 мл воды. Смесь экстрагировали и разделяли. Органической слой промывали 20 мл 2 н. раствора HCl, 20 мл насыщенного раствора NaCl, затем сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали. После очистки колоночной хроматографией получали 0,08 г белого твердого продукта в виде пены. МС(m/z): 465 [M-1]+. 1H ЯМР (CDCl3): δ 9,12 (с, 1H), 7,33 (с, 1H), 7,08 (с, 1H), 7,07 (с, 1H), 6,83 (д, 1H, J=6 Гц), 5,82 (дд, 1H, J=3 Гц, J=7 Гц), 4,56 (дд, 1H, J=5 Гц, J=11 Гц), 4,12 (кв., 2H, J=3 Гц), 3,86 (с, 3H), 3,76 (дд, 1H, J=5 Гц, J=11 Гц), 2,88 (с, 3H), 2,29 (с, 3H), 1,47 (т, 3H, J=5 Гц).
ПРИМЕР 4
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
В 50 мл круглодонную колбу, оборудованную электромагнитной мешалкой и осушительной трубкой, добавляли 0,077 г соединения 7, 0,137 г соединения 3a и 10 мл ТГФ. Смесь перемешивали в течение ночи при комнатной температуре. Добавляли 0,122 г CDI. Смесь кипятили с обратным холодильником в течение 2 часов на масляной бане и охлаждали до комнатной температуры на открытом воздухе. В смесь добавляли 100 мл этилацетата и 50 мл воды. Полученную смесь экстрагировали и разделяли. Органический слой промывали 20 мл 0,5 н. раствора HCl, 20 мл насыщенного раствора NaCl, затем сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали, получая при этом 0,121 г твердого продукта белого цвета.
МС (m/z): 410 [M+1]+.
ПРИМЕР 5
(S)-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 4 с соединением 4b вместо соединения 3a, получая при этом твердый продукт.
МС(m/z): 410 [M+1]+.
ПРИМЕР 6
(R)-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 4 с соединением 4d вместо соединения 3a, получая при этом твердый продукт.
МС (m/z): 410 [M+1]+.
ПРИМЕР 7
5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 4 с соединением 3b вместо соединения 3a, получая при этом твердый продукт.
МС(m/z): 410 [M+1]+.
ПРИМЕР 8
5-(1-(3,4-диметоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 4 с соединением 3c вместо соединения 3a, получая при этом твердый продукт.
МС(m/z): 396 [M+1]+.
ПРИМЕР 9
5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 4 с соединением 3d вместо соединения 3a, получая при этом твердый продукт.
МС (m/z): 472 [M+1]+.
ПРИМЕР 10
5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-нитро-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 1 с соединением 3d вместо соединения 3a, получая при этом твердый продукт.
МС(m/z): 515[M-1]+.
ПРИМЕР 11
5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-амино-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 2 с соединением, указанным в заголовке примера 10, вместо соединения, указанного в заголовке примера 1, получая при этом твердый продукт.
МС (m/z): 487 [M+1]+.
ПРИМЕР 12
N-(5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид
Повторяли процедуру получения по примеру 3 с соединением, указанным в заголовке примера 11, вместо соединения, указанного в заголовке примера 2, получая при этом твердый продукт.
МС (m/z): 527 [M-1]+.
ПРИМЕР 13
5-(1-(3,4-диметоксифенил)-2-(метилсульфонил)этил)-1-нитро-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 1 с соединением 3c вместо соединения 3a, получая при этом твердый продукт.
МС(m/z): 439 [M-1]+.
ПРИМЕР 14
5-(1-(3,4-диметоксифенил)-2-(метилсульфонил)этил)-1-амино-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 2 с соединением, указанным в заголовке примера 13, вместо соединения, указанного в заголовке примера 1, получая при этом твердый продукт.
МС(m/z): 411 [M+1]+.
ПРИМЕР 15
5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-1-нитро-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 1 с соединением 3b вместо соединения 3a, получая при этом твердый продукт.
МС(m/z): 453 [M-1]+.
ПРИМЕР 16
5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-1-амино-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли процедуру получения по примеру 2 с соединением, указанным в заголовке примера 15, вместо соединения, указанного в заголовке примера 1, получая при этом твердый продукт.
МС(m/z): 425 [M+1]+.
ПРИМЕР 17
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-метиламино-5H-тиофен[3,4-c]пиррол-4,6-дикетон
В 10 мл ацетона растворяли 0,085 г соединения, указанного в заголовке примера 2. К смеси добавляли 0,5 мл йодметана. Полученную смесь нагревали до 80°C и подвергали взаимодействию в течение 6 часов. После охлаждения добавляли 100 мл воды. Смесь экстрагировали этилацетатом (30 мл × 3). Органические слои объединяли. Органическую фазу последовательно промывали 30 мл воды и насыщенным солевым водным раствором, сушили над безводным MgSO4 и фильтровали. Растворитель выпаривали. После выделения колоночной хроматографией на силикагеле получали 0,033 г твердого продукта. МС(m/z): 439 [M+1]+.
ПРИМЕР 18
2-хлор-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен [3,4-c]пиррол-1-ил)ацетамид
Повторяли процедуру получения по способу II примера 3 с применением хлорацетилхлорида вместо ацетилхлорида, получая при этом твердый продукт.
МС (m/z): 499 [M-1]+.
ПРИМЕР 19
N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)метансульфонамид
Повторяли процедуру получения по способу II примера 3 с применением метансульфонилхлорида вместо ацетилхлорида, получая при этом твердый продукт.
МС(m/z): 501 [M-1]+.
ПРИМЕР 20
(S)-1-нитро-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли способ получения по примеру 1 с применением соединения 4b и соединения 9.
ПРИМЕР 21
(S)-1-амино-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли способ получения по примеру 2 с соединением, указанным в заголовке примера 20. МС(m/z): 425 [M+1]+.
ПРИМЕР 22
(R)-1-нитро-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли способ получения по примеру 1 с применением соединения 4d и соединения 9.
ПРИМЕР 23
(R)-1-амино-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5H-тиофен[3,4-c]пиррол-4,6-дикетон
Повторяли способ получения по примеру 2 с применением соединения, указанного в заголовке примера 22. МС(m/z): 425 [M+1]+.
ПРИМЕР 24
(S)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид
Повторяли способ получения по примеру 3 с применением соединения, указанного в заголовке примера 21. МС(m/z): 465 [M-1]+; Хиральная ВЭЖХ (безводный этанол/н-гексан/диэтиламин = 40/60/0,1; колонка chiralcel® OJ-H,, 250×4,6 мм, 1,0 мл/мин, @230 нм): 9,8 минут (R-изомер, 1,2%), 13,8 минут (S-изомер, 98,8%).
1H ЯМР (CDCl3): δ 9,27 (с, 1H), 7,30 (с, 1H), 7,07 (с, 1H), 7,05 (с, 1H), 6,81 (д, 1H, J=6 Гц), 5,81 (дд, 1H, J=3 Гц, J=7 Гц), 4,54 (дд, 1H, J=8 Гц, J=11 Гц), 4,08 (кв., 2H, J=3 Гц), 3,84 (с, 3H), 3,73 (дд, 1H, J=8 Гц, J=11 Гц), 2,86 (с, 3H), 2,27 (с, 3H), 1,45 (т, 3H, J=5 Гц).
ПРИМЕР 25
(R)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид
Повторяли способ получения по примеру 3 с применением соединения, указанного в заголовке примера 23. МС(m/z): 465 [M-1]+; Хиральная ВЭЖХ (безводный этанол/н-гексан/диэтиламин = 40/60/0,1; колонка chiralcel® OJ-H, 250×4,6 мм, 1,0 мл/мин, @230 нм): 9,8 минут (R-изомер, 99,5%), 13,8 минут (S-изомер, 0,5%).
ПРИМЕР 26
N-(5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид
Повторяли способ получения соединения, указанного в заголовке примера 3, с применением соединения, указанного в заголовке примера 16. МС(m/z): 465 [M-1]+.
ПРИМЕР 27
N-(5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)пропионамид
Повторяли процедуру получения по примеру 3 с применением соединения, указанного в заголовке примера 11, и пропионилхлорида, получая при этом твердый продукт. МС(m/z): 541 [M-1]+.
ПРИМЕР 28
2-(диметиламино)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид
В 10 мл тетрагидрофурана растворяли 50 мг соединения, указанного в заголовке примера 18. Добавляли 0,3 мл 2 н. раствора диметиламина в тетрагидрофуране. Смесь перемешивали в течение ночи при комнатной температуре. После завершения реакции добавляли 100 мл воды. Полученную смесь экстрагировали этилацетатом (40 мл × 3). Органические слои объединяли. Органическую фазу последовательно промывали 40 мл воды и насыщенным солевым водным раствором, сушили над безводным сульфатом магния, фильтровали. Растворитель выпаривали. После выделения колоночной хроматографией на силикагеле получали 40 мг твердого продукта. МС(m/z): 510 [M+1]+.
ПРИМЕР 29
2-(диэтиламино)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид
Повторяли способ получения по примеру 28 с применением диэтиламина вместо диметиламина, получая при этом указанное в заголовке соединение по примеру 29. МС(m/z): 538 [M+1]+.
ПРИМЕР 30
2-(пиперидил)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид
Повторяли способ получения по примеру 28 с применением пиперидина вместо диметиламина, получая при этом указанное в заголовке соединение по примеру 30. МС(m/z): 550 [M+1]+.
ПРИМЕР 31
2-(морфолинил)-N-(5-(l-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4H-тиофен[3,4-c]пиррол-1-ил)ацетамид
Повторяли способ получения по примеру 28 с применением морфолина вместо диметиламина, получая при этом указанное в заголовке соединение по примеру 31. МС(m/z): 552 [M+1]+.
ПРИМЕР 32
Фармакологическое исследование
1. Эффекты мононуклеарных клеток (PBMC), стимулированных ЛПС, в отношении TNFα
Исследование в отношении высвобождения цитокина TNFα мононуклеарными клетками периферической крови (PBMC) человека после стимуляции липополисахаридом (ЛПС) можно проводить in vitro. Способ исследования ингибирования высвобождения цитокина TNFα клетками PBMC после стимуляции ЛПС, фармацевтическими активными ингредиентами согласно настоящей заявке описан далее.
Клетки PBMC получали из крови, обработанной гепарином, по меньшей мере от трех доноров-добровольцев. Для получения клеток PBMC кровь, обработанную гепарином, по меньшей мере от трех доноров-добровольцев подвергали градиентному выделению клеток PBMC согласно известному способу. Клетки PBMC собирали и три раза промывали в среде 1640 (10% фетальной бычьей сыворотки, 2 мМ L-глютамина, 100 мМ меркаптоэтанола, 50 мкг/мл стрептомицина и 50 Ед/мл пенициллина). Клетки PBMC добавляли в 24-луночный планшет при концентрации 1×106 клеток/мл среды 1640. Испытуемое соединение растворяли в диметилсульфоксиде и получали в виде раствора испытуемого соединения требуемой концентрации. Раствор добавляли в культуры клеток. После инкубирования в CО2-инкубаторе (5% CO2, влажность 90%) в течение 1 часа добавляли ЛПС (Sigma) до 0,1 нг/мл (за исключением контрольного образца).
После дополнительного инкубирования среды в течение 20 часов измеряли содержание TNFα в супернатанте среды культивирования PBMC с помощью стандартного способа с применением коммерческого набора ELISA (U.S Genzyme Co). Степень ингибирования TNFα рассчитывали с использованием значения, измеренного для контрольной лунки, не обработанной активными ингредиентами, и значения, измеренного для испытуемой лунки, содержащей испытуемое соединение. Концентрацию, вызывающую 50%-ное ингибирование высвобождения TNFα (значение IC50), рассчитывали с помощью метода нелинейного регрессивного анализа. Каждую концентрацию одновременно измеряли дважды и рассчитывали среднее значение. Некоторые результаты испытания приведены в таблице 1.
Активность соединений в отношении ингибирования высвобождения TNFα мононуклеарными клетками, стимулированными ЛПС
(мкм)
(мкм)
(мкм)
2. Ингибиторная активность и селективная ингибиторная активность соединений в отношении ферментов PDE
(1) Ингибирующее действие соединений в отношении гидролиза цАМФ под действием фермента PDE4 исследовали путем ингибирования активности фермента PDE4. Процедуры анализа описаны далее.
Гуманизированные PDE4A1A, PDE4B1 и PDE4D2 приобретали в компании BPS bioscience (каталожные №№: 60040, 60041 и 60043 соответственно). Ферментативные реакции проводили в буфере, содержащем 10 мМ Tris-HCl (pH 7,4) и 1 мМ MgCl2. Концентрация цАМФ составляла 5 мкМ. Температуру реакции поддерживали при 37°C от 15 минут до 30 минут с тем, чтобы контролировать превращение субстрата в пределах 20%. Реакцию гасили равным объемом ацетонитрила. Продуцируемое количество субстрата АМФ измеряли с помощью ВЭЖХ-МС. Ингибиторную активность соединений в отношении фермента PDE4 получали путем сравнения продуцируемых количеств АМФ в экспериментальных группах, содержащих соединения, с количествами АМФ в контрольных группах, не содержащих соединений. Данные приведены в таблице 2.
(2) Ингибиторная активность в отношении PDE2 (селективность в отношении фермента PDE):
Гуманизированный PDE2A приобретали в компании BPS bioscience (каталожный №: 60020). Ферментативную реакцию проводили в буфере, содержащем 10 мМ Tris-HCl (pH 7,4) и 1 мМ MgCl2. Концентрация цАМФ составляла 5 мкМ. Температуру реакции поддерживали при 37°C в течение 30 минут с тем, чтобы контролировать превращение субстрата в пределах 20%. Реакцию гасили равным объемом ацетонитрила. Продуцируемое количество субстрата АМФ измеряли с помощью ВЭЖХ-МС. Ингибиторную активность соединений в отношении фермента PDE2 получали путем сравнения продуцируемых количеств АМФ в экспериментальных группах, содержащих соединения, с количествами АМФ в контрольных группах, не содержащих соединений. Данные приведены в таблице 2.
Ингибиторная активность соединений в отношении фермента PDE4 и селективная ингибиторная активность соединений в отношении ферментов PDE
Из вышеизложенного будет понятно, что хотя конкретные варианты осуществления настоящей заявки, описаны здесь с целью иллюстрации, без отклонения от сущности и объема настоящей заявки можно осуществлять различные модификации. Соответственно, настоящая заявка не ограничивается ничем, кроме прилагаемой формулы изобретения.
Изобретение относится к соединению формулы (I)
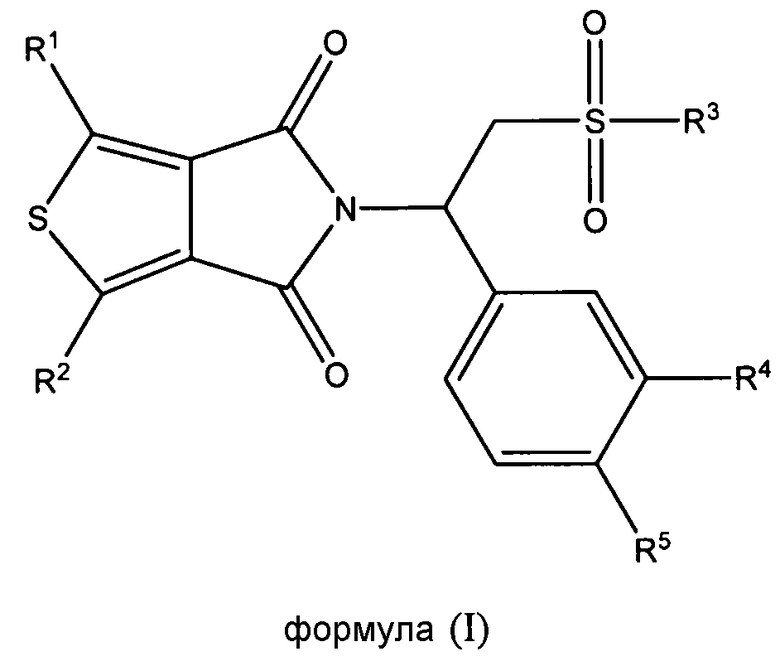
в которой, каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, нитро и NR6R7; R3 представляет собой C1-C8алкил; каждый из R4 и R5 независимо выбран из группы, состоящей из C1-C8алкокси, фенокси и фенил(C1-C8алкилен)окси; каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, C1-C8алкила, C(O)R8 и SO2R8;R8 выбран из группы, состоящей из атома водорода, C1-C8алкила, галогензамещенного C1-C8-алкила, C1-C8-алкила, замещенного (C1-C8-алкилзамещенный амино), C1-C8-алкила, замещенного пиперидином и C1-C8-алкила, замещенного морфолином, которые могут быть использованы для снижения активности фермента PDE4 или для лечения заболеваний или состояний, опосредованных ферментом PDE4.6 н.и 15 з.п. ф-лы., 2 табл., 32 пр.
1. Соединение формулы (I), его стереоизомер или их фармацевтически приемлемая соль:
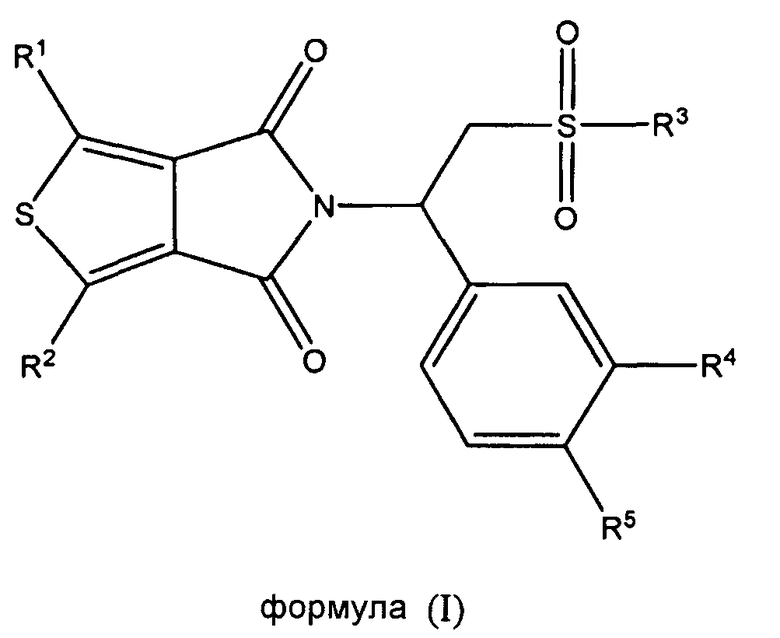
в которой
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, нитро и NR6R7;
R3 представляет собой C1-C8алкил;
каждый из R4 и R5 независимо выбран из группы, состоящей из C1-C8алкокси, фенокси и фенил(C1-C8алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, C1-C8алкила, C(O)R8 и SO2R8;
R8 выбран из группы, состоящей из атома водорода, C1-C8алкила, галогензамещенного C1-C8-алкила, C1-C8-алкила, замещенного (C1-C8-алкилзамещенный амино), C1-C8-алкила, замещенного пиперидином и C1-C8-алкила, замещенного морфолином.
2. Соединение формулы (I) по п.1, в которой каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, нитро, NH2, NHCH3, CH3C(O)NH, СН3СН2С(О)NH, СН3SO2NH и ClCH2C(O)NH.
3. Соединение формулы (I) по п.1, в которой R3 выбран из группы, состоящей из метила, этила и пропила.
4. Соединение формулы (I) по п.1, в которой каждый из R4 и R5 независимо выбран из группы, состоящей из метокси, этокси, пропокси и фенокси.
5. Соединение формулы (I) по п.1, в которой R8 выбран из группы, состоящей из метила, этила, диметиламинометила, диэтиламинометила, пиперидилметила и морфолинилметила.
6. Соединение формулы (I) по п.1, которое выбрано из группы, состоящей из:
N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида,
1-амино-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
(S)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида,
(R)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида,
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-нитро-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида,
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
(S)-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
(R)-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-нитро-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-амино-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
N-(5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида,
5-(1-(3,4-диметоксифенил)-2-(метилсульфонил)этил)-1-нитро-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
5-(1-(3,4-диметоксифенил)-2-(метилсульфонил)этил)-1-амино-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-1-нитро-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
5-(1-(3-метокси-4-этоксифенил)-2-(метилсульфонил)этил)-1-амино-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-1-метиламино-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
2-хлор-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида,
N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)метансульфонамида,
(S)-1-амино-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
(R)-1-амино-5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-5Н-тиофен[3,4-с]пиррол-4,6-дикетона,
(R)-N-(5-(1-(3-этокси-4-трифторметоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида,
N-(5-(1-(3-фенилметокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-диоксо-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)пропионамида,
2-(диметиламино)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида,
2-(диэтиламино)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида,
2-(пиперидил)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида и
2-(морфолинил)-N-(5-(1-(3-этокси-4-метоксифенил)-2-(метилсульфонил)этил)-4,6-дикетон-5,6-дигидро-4Н-тиофен[3,4-с]пиррол-1-ил)ацетамида.
7. Способ получения соединения формулы (I), включающий в себя взаимодействие соединения формулы (А-IV) с соединением формулы (А-VII) с получением соединения формулы (I):
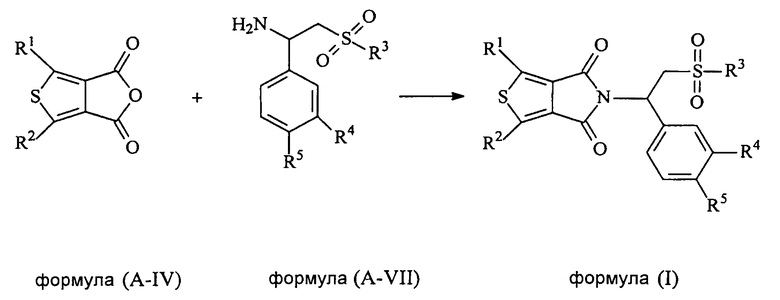
в которых
каждый из R1 и R2 независимо выбран из группы, состоящей из атома водорода, нитро и NR6R7;
R3 представляет собой C1-C8алкил;
каждый из R4 и R5 независимо выбран из группы, состоящей из C1-C8алкокси, фенокси и фенил(C1-C8алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, C1-C8алкила, C(O)R8 и SO2R8;
R8 выбран из группы, состоящей из атома водорода, C1-C8алкила, галогензамещенного C1-C8-алкила, C1-C8-алкила, замещенного (C1-C8-алкилзамещенный амино), C1-C8-алкила, замещенного пиперидином и C1-C8-алкила, замещенного морфолином.
8. Способ по п.7, в котором при взаимодействии соединения формулы (А-IV) с соединением формулы (A-VII) с получением соединения формулы (I) в качестве катализатора добавляют третичный амин, и в котором третичный амин предпочтительно выбран из группы, состоящей из пиридина, 4-диметиламинопиридина, 4-пирролидинилпиридина и их смеси.
9. Способ получения соединения формулы (B-III), включающий в себя взаимодействие соединения формулы (В-II) с соединением формулы R11-Y или (R12)2Y с получением соединения формулы (B-III),
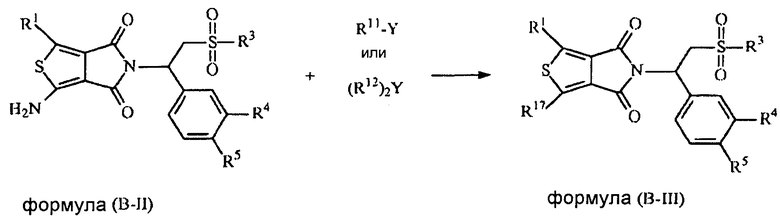 в которых,
в которых,
R1 выбран из группы, состоящей из атома водорода, нитро и NR6R7;
R3 представляет собой C1-C8алкил;
каждый из R4 и R5 независимо выбран из группы, состоящей из C1-C8алкокси, фенокси и фенил(C1-C8алкилен)окси;
каждый из R6 и R7 независимо выбран из группы, состоящей из атома водорода, C1-C8алкила, C(O)R8 и SO2R8;
R8 выбран из группы, состоящей из атома водорода, C1-C8алкила, галогензамещенного C1-C8-алкила, C1-C8-алкила, замещенного (C1-C8-алкилзамещенный амино), C1-C8-алкила, замещенного пиперидином и C1-C8-алкила, замещенного морфолином;
R11 в соединении R11-Y выбран из группы, состоящей из C1-C8алкила, C5-C12арила, С(O)R8 и S(O)2R8, Y выбран из группы, состоящей из галогена, OMs и OTs;
R12 в соединении (R12)2Y выбран из C(O)R8, и Y представляет собой O; R17 выбран из группы, состоящей из NH(C1-C8алкила), NHC(O)R8 и NHS(O)2R8.
10. Фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и терапевтически эффективное количество соединения по п.1, его стереоизомера или его фармацевтически приемлемой соли, для снижения активности фермента PDE4 или для лечения заболеваний или состояний, опосредованных ферментом PDE4.
11. Фармацевтическая композиция по п.10, дополнительно содержащая по меньшей мере еще один активный ингредиент.
12. Фармацевтическая композиция по п.11, в которой активный ингредиент выбран из группы, состоящей из хлорметина, азиридина, метилмеламина, алкилсульфоната, нитрозомочевины, триазена, фолацина, аналога пиримидина, аналога пурина, алкалоида винка, эпидофиллотоксина, антибиотика, ингибитора топоизомеразы, противоопухолевой вакцины, ацивицина, акларубицина, акодазола гидрохлорида, акронина, адозелесина, алдеслейкина, амбомицина, аметатрона ацетата, аминоглутетимида, амсакрина, анастрозола, антрамицина, аспарагиназы, азитромицина, азацитидина, препарата азетепа, азотомицина, батимастата, препарата бензодепа, бикалутамида, бисантрена гидрохлорида, биснафида мезилата, бизелезина, блеомицина сульфата, бусульфана, актиномицина С, калустерона, карацемида, карбетимера, карбоплатина, кармустина, карубицина гидрохлорида, хлорамбуцила, циролемицина, кладрибина, криснатола мезилата, циклофосфамида, цитарабина, дакарбазина, актиномицина D, даунорубицина гидрохлорида, децитабина, доцетаксела, доксорубицина, доксорубицина гидрохлорида, дролоксифена, эпирубицина гидрохлорида, эсорубицина гидрохлорида, эстрамустина, этанидазола, этопозида, флоксуридина, флуороурацила, флуроцитабина, гемцитабина, идарубицина гидрохлорида, ифосфамида, интерлейкина II, интерферона α-2а, интерферона α-2b, иринотекана гидрохлорида, летрозола, меркаптопурина, метотрексата, метропина, митомицина, митоксантрона, паклитаксела, прокарбазина, препарата тиотепа, винбластина, винкристина, ингибитора ангиогенеза, камптотецина, гексадекадрола, аспирина, ацетаминофена, индометацина, ибупрофена, кетопрофена, мелоксикама, кортикостероида и адреналового кортикостероида.
13. Фармацевтическая композиция по п.10, получаемая в виде таблетки, раствора, гранулы, пластыря, мази, капсулы, аэрозоля или суппозитория, вводимого с помощью парентерального, трансдермального, мукозального, назального, буккального, подъязычного или перорального способа введения.
14. Применение соединения по п.1, его стереоизомера или его фармацевтически приемлемой соли для получения лекарственного средства для уменьшения активности фермента PDE4.
15. Применение соединения по п.1, его стереоизомера или его фармацевтически приемлемой соли для получения лекарственного средства для лечения заболеваний или состояний, опосредованных ферментом PDE4.
16. Применение по п.15, в котором заболевания или состояния выбраны из группы, состоящей из воспалительных заболеваний или состояний, инфекционных заболеваний или состояний, иммунных заболеваний или состояний и злокачественных заболеваний или состояний.
17. Применение по п.16, в котором заболевания или состояния выбраны из группы, состоящей из карциномы органов головы, карциномы щитовидной железы, злокачественной опухоли горла, злокачественной опухоли глаза, злокачественной опухоли кожи, злокачественной опухоли полости рта, злокачественной опухоли гортани, злокачественной опухоли пищевода, злокачественной опухоли молочной железы, злокачественной опухоли кости, лейкемии, миеломы, злокачественной опухоли легкого, злокачественной опухоли толстой кишки, карциномы сигмовидной ободочной кишки, злокачественной опухоли прямой кишки, злокачественной опухоли желудка, злокачественной опухоли предстательной железы, злокачественной опухоли молочной железы, злокачественной опухоли яичников, злокачественной опухоли почек, злокачественной опухоли печени, злокачественной опухоли поджелудочной железы, злокачественной опухоли головного мозга, злокачественной опухоли кишечника, злокачественной опухоли сердца, адреналовой карциномы, злокачественной опухоли подкожных тканей, злокачественной опухоли лимфоузлов, злокачественной меланомы, злокачественной глиомы, ВИЧ, гепатита, синдрома дыхательных расстройств взрослого типа, заболевания, связанного с деминерализацией кости, хронической обструктивной болезни легких, хронического воспаления легких, дерматита, воспалительного заболевания кожи, атопического дерматита, кистозного фиброза, септического шока, пиемии, эндоксинового бактериально-токсического шока, динамического кровяного шока (резкого падения кровяного давления), септического синдрома заболевания, ишемически-реперфузионного повреждения, менингита, псориаза, фиброзного заболевания, кахексии, отторжения трансплантата, связанного с реакцией ″трансплантат против хозяина″, аутоиммунного заболевания, ревматоидного спондилита, артритного симптома (такого как ревматоидный артрит или остеоартрит), остеопороза, болезни Крона, ульцеративного колита, энтерита, рассеянного склероза, системной красной волчанки, лепрозной узловатой эритемы при лепре (ENL), радиационного повреждения, астмы, гипероксического повреждения легких, инфекций, вызванных микроорганизмами, и инфекционного синдрома, вызванного микроорганизмами.
18. Применение по п.15, при котором лекарственное средство содержит однократную дозу в количестве 0,1 мг-1000 мг соединения формулы (I).
19. Применение по п.15, при котором лекарственное средство дополнительно содержит по меньшей мере еще один активный ингредиент.
20. Применение по п.19, при котором активный ингредиент выбран из группы, состоящей из хлорметина, азиридина, метилмеламина, алкилсульфоната, нитрозомочевины, триазена, фолацина, аналога пиримидина, аналога пурина, алкалоида винка, эпидофиллотоксина, антибиотика, ингибитора топоизомеразы, противоопухолевой вакцины, ацивицина, акларубицина, акодазола гидрохлорида, акронина, адозелесина, алдеслейкина, амбомицина, аметатрона ацетата, аминоглутетимида, амсакрина, анастрозола, антрамицина, аспарагиназы, азитромицина, азацитидина, препарата азетепа, азотомицина, батимастата, препарата бензодепа, бикалутамида, бисантрена гидрохлорида, биснафида мезилата, бизелезина, блеомицина сульфата, бусульфана, актиномицина С, калустерона, карацемида, карбетимера, карбоплатина, кармустина, карубицина гидрохлорида, хлорамбуцила, циролемицина, кладрибина, криснатола мезилата, циклофосфамида, цитарабина, дакарбазина, актиномицина D, даунорубицина гидрохлорида, децитабина, доцетаксела, доксорубицина, доксорубицина гидрохлорида, дролоксифена, эпирубицина гидрохлорида, эсорубицина гидрохлорида, эстрамустина, этанидазола, этопозида, флоксуридина, флуороурацила, флуроцитабина, гемцитабина, идарубицина гидрохлорида, ифосфамида, интерлейкина II, интерферона α-2а, интерферон α-2b, иринотекана гидрохлорида, летрозола, меркаптопурина, метотрексата, метропина, митомицина, митоксантрона, паклитаксела, прокарбазина, препарата тиотепа, винбластина, винкристина, ингибитора ангиогенеза, камптотецина, гексадекадрола, аспирина, ацетаминофена, индометацина, ибупрофена, кетопрофена, мелоксикама, кортикостероида и адреналового кортикостероида.
21. Применение по п.20, при котором соединение формулы (I) и по меньшей мере еще один активный ингредиент вводят одновременно, параллельно, по отдельности или последовательно.
| CN 101186612 А, 28.05.2008 | |||
| HON-WAH MAN ET AL, J.Med.Chem., vol.52, no.6, 2009, p.p | |||
| Прибор для задней заточки радиальных режущих кромок на конических концах инструментов | 1917 |
|
SU1522A1 |
| WO 00/25777 A1, 11.05.2000 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Предохранительный мембранный клапан | 1973 |
|
SU467206A1 |
Авторы
Даты
2014-12-27—Публикация
2010-05-14—Подача