Область техники, к которой относится изобретение
Настоящее изобретение относится к композиции для уменьшения повреждения, вызванного ультрафиолетовым излучением, включающей одно или более соединений, выбранных из группы, состоящей из метионина и D-серина, а также их производных и/или солей, к способу улучшения состояния при заболевании кожи, вызванном воздействием ультрафиолетового излучения, и косметического состояния кожи, включающему стадию введения одного или более соединений, выбранных из группы, состоящей из метионина и D-серина, а также их производных и/или солей.
Уровень техники
Ультрафиолетовое излучение подразделяют на длинноволновую область ультрафиолетового излучения с длиной волны более чем приблизительно 320 нм (УФ-A), средневолновую область ультрафиолетового излучения от приблизительно 320 до приблизительно 280 нм (УФ-B) и коротковолновую область ультрафиолетового излучения с длиной волны менее чем приблизительно 280 нм (УФ-C). Среди перечисленного, УФ-C не содержится в солнечном свете, достигающем земли, поскольку его поглощает озоновый слой. Хотя УФ-A и УФ-B содержатся в солнечном свете, достигающем земли, УФ-B частично поглощается озоновым слоем. Впрочем, так как УФ-A не поглощается озоновым слоем, оно преобладает в ультрафиолетовом излучении, достигающем земли, и вызывает повреждение кожи.
В Непатентной литературе 1 раскрыты заболевания, в которые вовлечено ультрафиолетовое излучение, включая морщины, эритему, пигментную ксеродерму, хронический актинический дерматит, плоскоклеточную карциному, базально-клеточную карциному, злокачественную меланому, болезнь Боуэна, солнечный кератоз, фотодерматоз, световую оспу и фотодерматит, тогда как в Непатентной литературе 2 в качестве примеров приводятся солнечный дерматит, хроническая актиническая дерматопатия, актинический кератоз, актинический хейлит, синдром Фавра-Ракушо, фотодерматоз, фотодерматит, брелоковый дерматит, фоточувствительная лекарственная сыпь, полиморфная световая сыпь, световая оспа, солнечная крапивница, хронический фоточувствительный дерматит, пигментная ксеродерма, веснушки, порфирия, пеллагра, болезнь Хартнапа, солнечный кератоз, дерматомиозит, плоский лишай, болезнь Дарье, красный волосистый питириаз, розовые угри, атопический дерматит, хлоазма, простой герпес и красная волчанка.
Документы предшествующего уровня техники
Непатентные документы
Непатентный документ 1: "HIFUSHIKKAN SAISHIN NO CHIRYO (Latest methods for treating dermal diseases - Новейшие способы лечения кожных болезней)", 2005-2006 (NankodoCo., Ltd.)
Непатентный документ 2: "HYOJUN HIFUKAGAKU (Standard dermatology - Стандартная дерматология)", 7-е издание (Igaku-Shoin Ltd.)
Задачи, решаемые изобретением
Известные стандартные средства для предупреждения и/или лечения повреждений кожи, вызванных ультрафиолетовым излучением, включают УФ-рассеивающее средство, которое предотвращает поглощение ультрафиолета кожей, такое как оксид титана, поглотитель ультрафиолетового излучения, такой как этилгексил-п-метоксикоричная кислота, или антиоксидант, который улавливает свободные радикалы, образующиеся при воздействии ультрафиолета. УФ-рассеивающее средство или поглотитель ультрафиолетового излучения, впрочем, не используют ежедневно, хотя он эффективно предотвращает солнечные ожоги вне помещения. Антиоксидант предоставляет некоторые проблемы в том, что касается стабильности и безопасности. Кроме того, известные средства для лечения вызванных ультрафиолетовым излучением повреждений кожи ограничиваются лишь симптоматическими средствами для лечения. Таким образом, требуется разработать композицию для уменьшения повреждения, вызванного ультрафиолетовым излучением, препарат для наружного применения на коже, средство против морщин, солнцезащитное средство, фармацевтическую композицию для лечения и/или предупреждения кожных заболеваний, пищевую композицию или фармацевтический продукт для катаракты, который может применяться ежедневно и является стабильным и безопасным.
Способы решения задачи
Настоящее изобретение предоставляет композицию для уменьшения повреждения, вызванного ультрафиолетовым излучением, включающую одно или более соединений, выбранных из группы, состоящей из метионина и его производных и/или солей.
В композиции согласно изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, метионин, описанный выше, может находиться в D-форме.
Настоящее изобретение предоставляет композицию для уменьшения повреждения, вызванного ультрафиолетовым излучением, включающую одно или более соединений, выбранных из группы, состоящей из D-серина и его производных и/или солей.
В композиции согласно изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, производное D-серина, описанное выше, может являться D-циклосерином.
Композиция согласно изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, может быть нанесена в качестве препарата для наружного применения на коже.
В композиции согласно изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, препарат для наружного применения на коже, описанный выше, может являться средством против морщин.
В композиции согласно изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, препарат для наружного применения на коже, описанный выше, может являться солнцезащитным средством.
В композиции согласно изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, препарат для наружного применения на коже, описанный выше, может применяться в качестве фармацевтического продукта для кожного заболевания.
Кожное заболевание, описанное выше, может быть выбрано из группы, состоящей из эритемы, солнечного дерматита, хронической актинической дерматопатии, актинического кератоза, актинического хейлита, болезни Фавра-Ракушо, фотодерматоза, фотодерматита, брелокового дерматита, фоточувствительной лекарственной сыпи, полиморфной световой сыпи, hydroa vacciniforme, световой оспы, солнечной крапивницы, хронического фоточувствительного дерматита, пигментной ксеродермы, веснушек, порфирии, пеллагры, болезни Хартнапа, солнечного кератоза, дерматомиозита, плоского лишая, болезни Дарье, красного волосистого питириаза, розовых угрей, атопического дерматита, хлоазмы, простого герпеса, красной волчанки, плоскоклеточной карциномы, базально-клеточной карциномы и болезни Боуэна.
В композиции согласно изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, фармацевтический продукт для кожного заболевания, описанный выше, может быть средством для лечения кожного заболевания.
В композиции согласно настоящему изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, фармацевтический продукт для кожного заболевания, описанный выше, может быть средством для предупреждения кожного заболевания.
Композиция согласно настоящему изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, может применяться в качестве пищевого продукта.
Композиция согласно настоящему изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, может применяться в качестве фармацевтического продукта для катаракты.
В композиции согласно настоящему изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, фармацевтический продукт для катаракты, описанный выше, может являться средством для лечения или предупреждения катаракты.
Композиция согласно настоящему изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, может применяться в качестве глазных капель.
Катаракта, описанная выше, может являться старческой катарактой.
Настоящее изобретение предоставляет композицию за исключением того, что композиция применяется перорально для уменьшения повреждения, вызванного ультрафиолетовым излучением, включающую одно или более соединений, выбранных из группы, состоящей из метионина и его производных и/или солей. Метионин, описанный выше, может находиться в D-форме.
Настоящее изобретение предоставляет способ лечения и/или предупреждения кожного заболевания, вызванного воздействием ультрафиолетового излучения, включающий стадию введения композиции для уменьшения повреждения, вызванного ультрафиолетовым излучением, где композиция состоит из одного или более соединений, выбранных из группы, состоящей из метионина и D-серина, а также их производных и/или солей. Кожное заболевание, описанное выше, может быть выбрано из группы, состоящей из эритемы, солнечного дерматита, хронической актинической дерматопатии, актинического кератоза, актинического хейлита, болезни Фавра-Ракушо, фотодерматоза, фотодерматита, брелокового дерматита, фоточувствительной лекарственной сыпи, полиморфной световой сыпи, световой оспы, солнечной крапивницы, хронического фоточувствительного дерматита, пигментной ксеродермы, веснушек, порфирии, пеллагры, болезни Хартнапа, солнечного кератоза, дерматомиозита, плоского лишая, болезни Дарье, красного волосистого питириаза, розовых угрей, атопического дерматита, хлоазмы, простого герпеса, красной волчанки, плоскоклеточной карциномы, базально-клеточной карциномы и болезни Боуэна. Метионин, описанный выше, может находиться в D-форме. Производное D-серина, описанное выше, может являться D-циклосерином.
Настоящее изобретение предоставляет способ лечения и/или предупреждения кожного заболевания, вызванного воздействием ультрафиолетового излучения, включающий стадию введения композиции для уменьшения повреждения, вызванного ультрафиолетовым излучением, где композиция состоит из одного или более соединений, выбранных из группы, состоящей из метионина и его производных и/или солей, за исключением пероральных композиций. Кожное заболевание, описанное выше, может быть выбрано из группы, состоящей из эритемы, солнечного дерматита, хронической актинической дерматопатии, актинического кератоза, актинического хейлита, болезни Фавра-Ракушо, фотодерматоза, фотодерматита, брелокового дерматита, фоточувствительной лекарственной сыпи, полиморфной световой сыпи, световой оспы, солнечной крапивницы, хронического фоточувствительного дерматита, пигментной ксеродермы, веснушек, порфирии, пеллагры, болезни Хартнапа, солнечного кератоза, дерматомиозита, плоского лишая, болезни Дарье, красного волосистого питириаза, розовых угрей, атопического дерматита, хлоазмы, простого герпеса, красной волчанки, плоскоклеточной карциномы, базально-клеточной карциномы и болезни Боуэна. Метионин, описанный выше, может находиться в D-форме.
Настоящее изобретение предоставляет способ улучшения косметического состояния кожи, включающий стадию введения композиции для уменьшения повреждения, вызванного ультрафиолетовым излучением, где композиция состоит из одного или более соединений, выбранных из группы, состоящей из метионина и D-серина, а также их производных и/или солей. В способе улучшения косметического состояния кожи, описанном выше, композиция для уменьшения повреждения, вызванного ультрафиолетовым излучением, включающая одно или более соединений, выбранных из группы, состоящей из метионина и D-серина, а также их производных и/или солей, описанных выше, может являться препаратом для наружного применения на коже или пищевой композицией. Метионин, описанный выше, может находиться в D-форме. Производное D-серина, описанное выше, может являться D-циклосерином.
Настоящее изобретение предоставляет способ улучшения косметического состояния кожи, включающий стадию введения композиции за исключением того, что композиция применяется перорально для уменьшения повреждения, вызванного ультрафиолетовым излучением, где композиция состоит из одного или более соединений, выбранных из группы, состоящей из метионина и его производных и/или солей. В способе улучшения косметического состояния кожи, описанном выше, композиция за исключением того, что композиция применяется перорально для уменьшения повреждения, вызванного ультрафиолетовым излучением, включающая одно или более соединений, выбранных из группы, состоящей из метионина и его производных и/или солей, описанных выше, может являться препаратом для наружного применения на коже. Метионин, описанный выше, может находиться в D-форме.
В способе улучшения косметического состояния кожи согласно изобретению улучшение косметического состояния кожи включает, помимо прочего, обработку против морщин и/или солнцезащитную обработку.
Настоящее изобретение может предоставлять способ лечения и/или предупреждения катаракты, включающий стадию введения композиции, включающей одно или более соединений, выбранных из группы, состоящей из метионина и D-серина, а также их производных и/или солей. Метионин, описанный выше, может находиться в D-форме. Производное D-серина, описанное выше, может являться D-циклосерином.
В способе лечения и/или предупреждения катаракты согласно изобретению фармацевтический продукт для катаракты, описанный выше, может являться глазными каплями.
В способе лечения и/или предупреждения катаракты согласно изобретению катаракта, описанная выше, может являться старческой катарактой.
Используемая в настоящей заявке "соль" метионина, D-серина или D-циклосерина относится к любой соли, включающей соли металлов и соли аминов, при условии, что эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, обеспечиваемый метионином, D-серином или D-циклосерином, не снижается. Соль металла, описанная выше, может включать соль щелочного металла, соль щелочноземельного металла и т.п. Соль амина, описанная выше, может включить соль триэтиламина, соль бензиламин и т.п.
Используемое в настоящей заявке "производное" метионина или D-серина относится к молекуле метионина или D-серина, которая ковалентно связана с любой замещающей группой по ее аминогруппе, карбоксильной группе или боковой цепи, при условии, что эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, обеспечиваемый метионином или D-серином, не снижается. Замещающая группа, указанная выше, включает, помимо прочего, защитную группу, такую как N-фенилацетильную группу, 4,4'-диметокситритильную (DMT) группу и т.д.; биологическую макромолекулу, такую как белок, пептид, сахарид, липид, нуклеиновую кислоту и т.д.; синтетический полимер, такой как полистирол, полиэтилен, поливинил, сложный полиэфир и т.д.; и функциональную группу, такую как сложноэфирная группа, и т.д. Сложноэфирная группа, указанная выше, может включать, например, метиловый сложный эфир, этиловый сложный эфир, другой алифатический сложный эфир или ароматический сложный эфир. В производном D-серина, описанном выше, аминогруппа и/или карбоксильная группа, смежная с α (альфа)-атомом углерода аминокислоты, может формировать гетероциклическое кольцо, как в случае D-циклосерина, вместе с любой группой.
Так как аминокислота существует в виде оптического изомера, который находится в L-форме или D-форме, а природный белок состоит из L-аминокислот, связанных пептидными связями, и используются только L-аминокислоты за некоторыми исключениями, например, стенка бактериальных клеток, считали, что в организме млекопитающих, включая человека, присутствуют и используются только L-аминокислоты (Kinouchi, T. et al., TANPAKUSHITSU KAKUSAN KOSO (PROTEINS, NUCLEIC ACIDS AND ENZYMES), 50:453-460(2005), Lehninger Principles of Biochemistry [Том 1] 2-е изд., стр. 132-147 (1993), перевод с японского языка, Hirokawa Publishing Co., Harper's Biochemistry, оригинальная версия, 22-е изд., стр. 21-30 (1991), перевод с японского языка, Maruzen Co., Ltd.). Таким образом, в течение длительного времени в качестве аминокислот в научном и промышленном отношении главным образом использовались только L-аминокислоты.
Исключительные случаи, когда используется D-аминокислота, включают, например, случай использования в качестве сырья для антибиотиков, продуцируемых микроорганизмом и случай пищевой добавки с применением D-аминокислоты в смеси DL-аминокислот только с целью снижения стоимости за счет исключения фракционирования с получением только L-аминокислоты из смеси L-аминокислоты и D-аминокислоты. Впрочем, в промышленности не было ни одного случая применения только D-аминокислоты, не содержащей L-аминокислоты, в качестве биологически активного вещества.
D-серин и D-аспарагиновая кислота были изучены до сравнительно высокого уровня благодаря своим более высоким отношениям D-форм. D-серин локализован в головном мозге и гиппокампе и, как известно, задействован в модуляторе NMDA рецептора в мозге. D-аспарагиновая кислота, как продемонстрировали, локализована в яичке и шишковидном теле, и, как сообщали, участвует в регулировании секреции гормонов (Неакцептованная заявка на патент Японии 2005-3558). Впрочем, физиологические эффекты D-серина и D-аспарагиновой кислоты на коже не были изучены.
Как указано в Примерах, описанных ниже, до настоящего времени не было известно, что метионин, D-серин и D-циклосерин, как имеющие L-форму или D-форму, или их смесь, вызывали эффект уменьшения повреждения, вызванного ультрафиолетовым излучением. Таким образом, композиция согласно настоящему изобретению для уменьшения повреждения, вызванного ультрафиолетовым излучением, включающая метионин, D-серин и/или D-циклосерин, представляет собой новое изобретение.
Недавно сообщали, что мышам ddY давали доступ к 10 мМ водному раствору D-аминокислоты в течение 2 недель, а затем в каждом органе определяли концентрацию D-аминокислоты, которая составила 3-1000 пмоль в каждой железе в шишковидном теле и 2-500 пмоль на грамм влажной ткани мозга (Morikawa, A. et al., Amino Acids, 32:13-20 (2007)). На основе данного сообщения вычисляли нижний предел ежедневной дозы метионина, D-серина и D-циклосерина, содержащихся в композиции настоящего изобретения.
Как указано в Примерах, описанных ниже, метионин, который относится к настоящему изобретению, проявляет эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, при концентрации в пределах от 0,001 до 100 мкМ (микромоль) в культуре фибробластов человека. Соответственно, количество метионина, содержащегося в фармацевтической композиции настоящего изобретения, средстве против морщин, солнцезащитном средстве, препарате для наружного применения на коже и фармацевтическом продукте для катаракты, может изменяться в широких пределах, при условии, что метионин доставляется в фибробласт кожной ткани in vivo в диапазоне концентраций, указанном выше. В том случае, когда композиция настоящего изобретения является препаратом для наружного применения, содержание метионина может составлять от 0,0000015% по массе до 50% по массе в общем количестве композиции изобретения или до максимальной массовой концентрации, которую возможно ввести в композицию. Таким образом, если композиция, описанная выше, является препаратом для наружного применения, содержание метионина предпочтительно составляет от 0,000003% по массе до 30% по массе, наиболее предпочтительно от 0,00003% по массе до 3% по массе. Нижний предел ежедневной дозы D-метионина, содержащегося в композиции настоящего изобретения, может составлять 0,01 нг, предпочтительно 0,1 нг, более предпочтительно 1 нг на кг массы тела. Нижний предел ежедневной дозы L-метионина, содержащегося в композиции настоящего изобретения, меньше, чем доза клинического препарата (2 мг или больше на кг массы тела), и может составлять 0,01 мг, предпочтительно 0,1 мг, более предпочтительно 1 мг на кг массы тела.
Как указано в Примерах, описанных ниже, D-серин изобретения проявляет эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, при концентрации в пределах от 0,01 до 100 мкМ на культуре фибробластов человека. Таким образом, количество D-серина, содержащегося в фармацевтической композиции настоящего изобретения, средстве против морщин, солнцезащитном средстве, препарате для наружного применения на коже и фармацевтическом продукте для катаракты, может изменяться в широких пределах, при условии, что D-серин доставляется в фибробласт кожной ткани in vivo в диапазоне концентраций, указанном выше. В том случае, когда композиция настоящего изобретения является препаратом для наружного применения, содержание D-серина может составлять от 0,000015% по массе до 50% по массе в общем количестве композиции изобретения или до максимальной массовой концентрации, которую возможно ввести в композицию. Таким образом, если композиция, описанная выше, является препаратом для наружного применения, содержание D-серина предпочтительно составляет от 0,00003% по массе до 30% по массе, наиболее предпочтительно от 0,0003% по массе до 3% по массе. Если композиция настоящего изобретения является препаратом для внутреннего применения, содержание D-серина может составлять от 0,00001% по массе до 100% по массе. Если композиция изобретения является препаратом для внутреннего применения, содержание D-серина предпочтительно составляет от 0,00002% по массе до 80% по массе, наиболее предпочтительно от 0,0002% по массе до 60% по массе. Нижний предел ежедневной дозы D-серина, содержащегося в композиции настоящего изобретения, может составлять 0,01 нг, предпочтительно 0,1 нг, более предпочтительно 1 нг на кг массы тела.
Как указано в Примерах, описанных ниже, D-циклосерин изобретения проявляет эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, при концентрации в пределах от 1 до 100 мкМ (микромоль) в культуре фибробластов человека. Таким образом, количество D-циклосерина, содержащегося в фармацевтической композиции настоящего изобретения, средстве против морщин, солнцезащитном средстве, препарате для наружного применения на коже и фармацевтическом продукте для катаракты, может изменяться в широких пределах, при условии, что D-циклосерин доставляется в фибробласт в кожной ткани in vivo в диапазоне концентраций, указанном выше. Если композиция настоящего изобретения является препаратом для наружного применения, содержание D-циклосерина может составлять от 0,0000015% по массе до 50% по массе в общем количестве композиции изобретения или до максимальной массовой концентрации, которую возможно ввести в композицию. Таким образом, если композиция, описанная выше, является препаратом для наружного применения, содержание D-циклосерина предпочтительно составляет от 0,000003% по массе до 30% по массе, наиболее предпочтительно от 0,00003% по массе до 3% по массе. Нижний предел ежедневной дозы D-циклосерина, содержащегося в композиции настоящего изобретения, может составлять 0,01 мкг (микрограмм), предпочтительно 0,1 мкг (микрограмм), более предпочтительно 1 мкг (микрограмм) на кг массы тела.
Фармацевтическая композиция настоящего изобретения может дополнительно включать одну или более фармацевтически приемлемых добавок, в дополнение к метионину и D-серину, солям и/или производным D-серина и метионина, способным высвобождать метионин и D-серин под действием ферментов, метаболизирующих лекарственное средство и т.п. in vivo, при условии, что эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, обеспечиваемый метионином и D-серином, не снижается. Такая добавка включает, помимо прочего, разбавитель, вещество, способствующее набуханию, связующее вещество, клейкое вещество, скользящее вещество, вещество, способствующее текучести, пластификатор, разрыхлитель, растворитель-носитель, буферное вещество, краситель, ароматизатор, подсластитель, консервант, стабилизатор, адсорбент, а также другие фармацевтические добавки, известные квалифицированным специалистам.
Средство против морщин и/или солнцезащитное средство настоящего изобретения могут быть приготовлены с применением только метионина, D-серина и D-циклосерина, солей метионина, D-серина и D-циклосерина, и/или производных, способных высвобождать метионин, D-серин и D-циклосерин под действием ферментов, метаболизирующих лекарственное средство и т.п. in vivo. Впрочем, другие компоненты, используемые в препаратах для наружного применения на коже, таких как косметические и фармацевтические продукты, включая лечебную косметику, могут быть надлежащим образом включены в композицию так, чтобы не был снижен эффект изобретения. Такие другие компоненты (необязательно вводимые в композицию компоненты) включают, например, масла, поверхностно-активные вещества, порошки, красители, воду, спирты, загустители, хелатирующие вещества, силиконы, антиоксиданты, УФ-поглотители, смачивающие вещества, ароматизаторы, различные лекарственные компоненты, консерванты, регуляторы pH, нейтрализующее вещество и т.п.
Препарат для наружного применения на коже согласно настоящему изобретению может быть любым из средств, традиционно применяемых в качестве препарата для наружного применения на коже и косметической композиции, таким как мазь, крем, эмульсия, лосьон, косметическая маска, соль для ванны и т.п., при этом их лекарственные формы конкретно не указаны.
В препараты для наружного применения на коже согласно изобретению могут быть надлежащим образом при необходимости включены другие компоненты, используемые в препаратах для наружного применения на коже, таких как косметические и фармацевтические продукты, включая лекарственную косметику, при условии, что эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, обеспечиваемый метионином, D-серином и D-циклосерином, не снижается. Такие другие компоненты (необязательно вводимые в композицию компоненты) включают, например, масла, поверхностно-активные вещества, порошки, красители, воду, спирты, загустители, хелатирующие вещества, силиконы, антиоксиданты, УФ-поглотители, смачивающие вещества, ароматизаторы, различные лекарственные компоненты, консерванты, регуляторы pH, нейтрализующее вещество.
Пищевая композиция настоящего изобретения может также включать, в дополнение к D-серину и D-циклосерину, соли D-серина и D-циклосерина и/или производные, способные высвобождать D-серин и D-циклосерин под действием ферментов, метаболизирующих лекарственное средство и т.п. in vivo, и дополнительно разрешенный в пищевой промышленности компонент, такой как специя, краситель, консервант, при условии, что эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, обеспечиваемый D-серином и D-циклосерином, не снижается.
Пищевая композиция настоящего изобретения может быть любой из традиционно применяемых в качестве пищевой композиции, такой как напиток, жевательный мармелад, конфета, подсластитель в таблетках, которыми она не ограничивается.
Краткое описание фигур
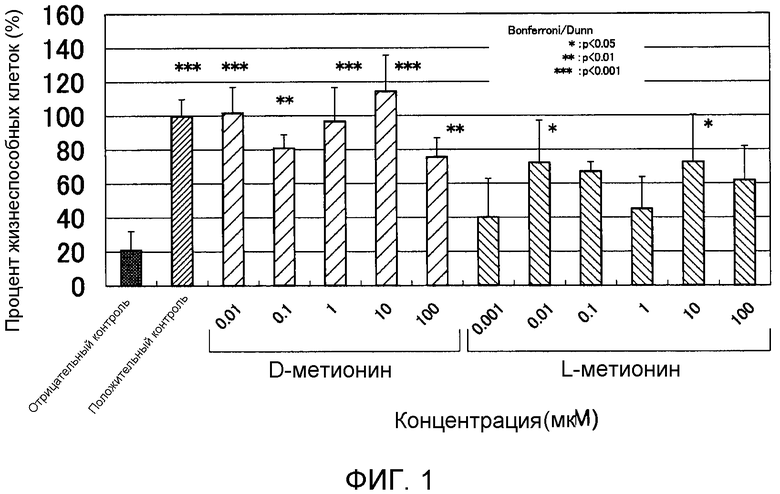
Фигура 1 представляет собой график, на котором показан эффект добавления L- или D-метионина перед обработкой нормальных фибробластов кожи человека ультрафиолетовым излучением.
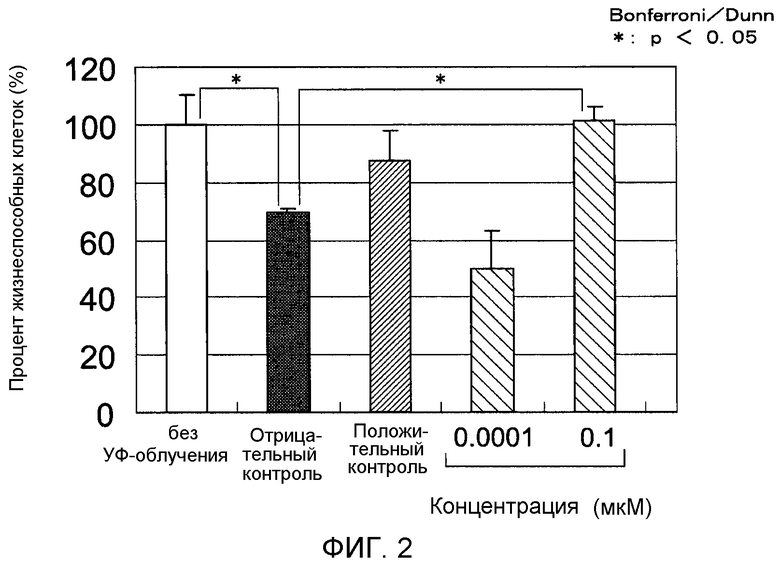
Фигура 2 представляет собой график, на котором показан эффект добавления D-метионина перед обработкой нормальных фибробластов кожи человека ультрафиолетовым излучением.
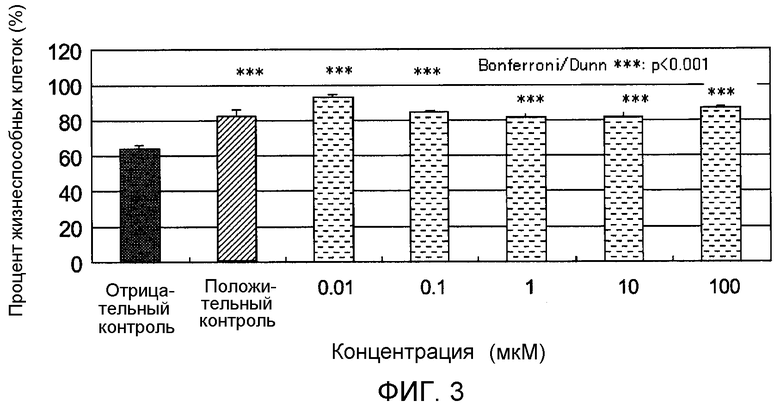
Фигура 3 представляет собой график, на котором показан эффект добавления D-метионина после обработки нормальных фибробластов кожи человека ультрафиолетовым излучением.
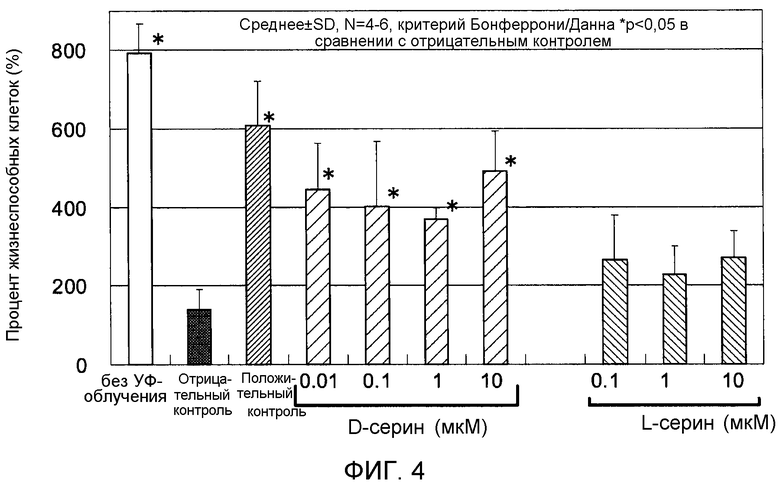
Фигура 4 представляет собой график, на котором показан эффект добавления L- или D-серина перед обработкой нормальных фибробластов кожи человека ультрафиолетовым излучением.
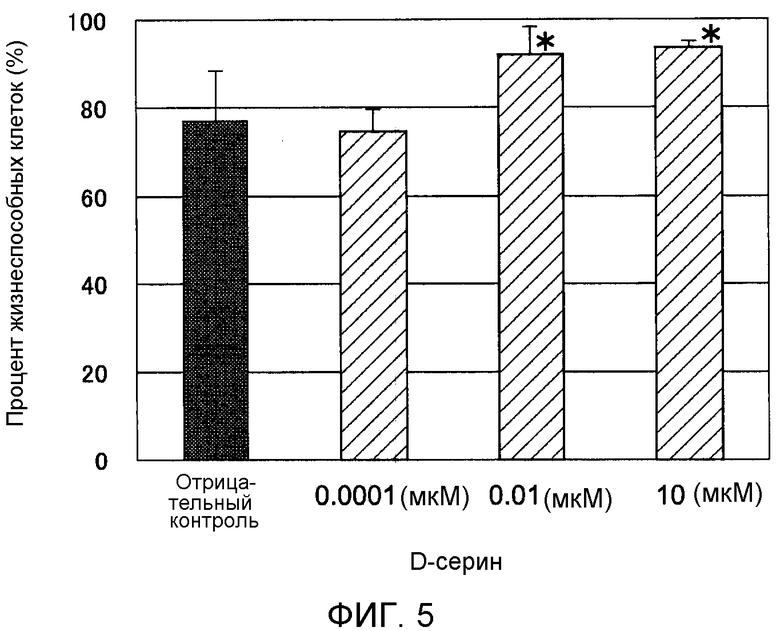
Фигура 5 представляет собой график, на котором показан эффект добавления D-серина перед обработкой нормальных фибробластов кожи человека ультрафиолетовым излучением.
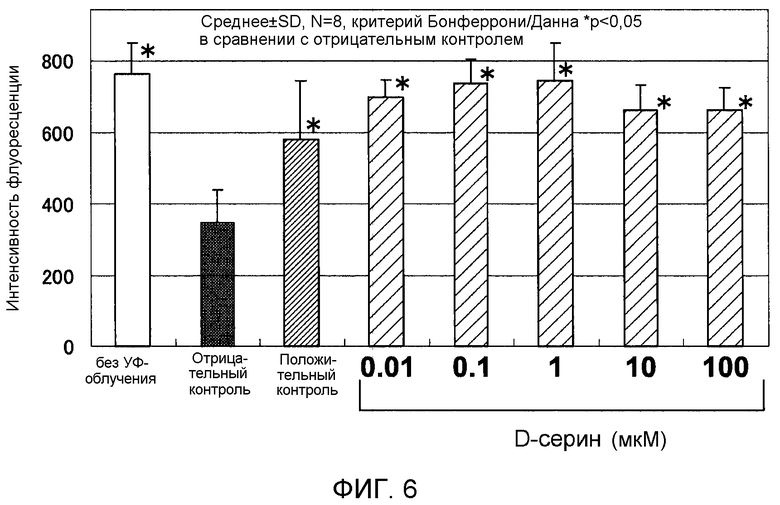
Фигура 6 представляет собой график, на котором показан эффект добавления D-серина после обработки нормальных фибробластов кожи человека ультрафиолетовым излучением.
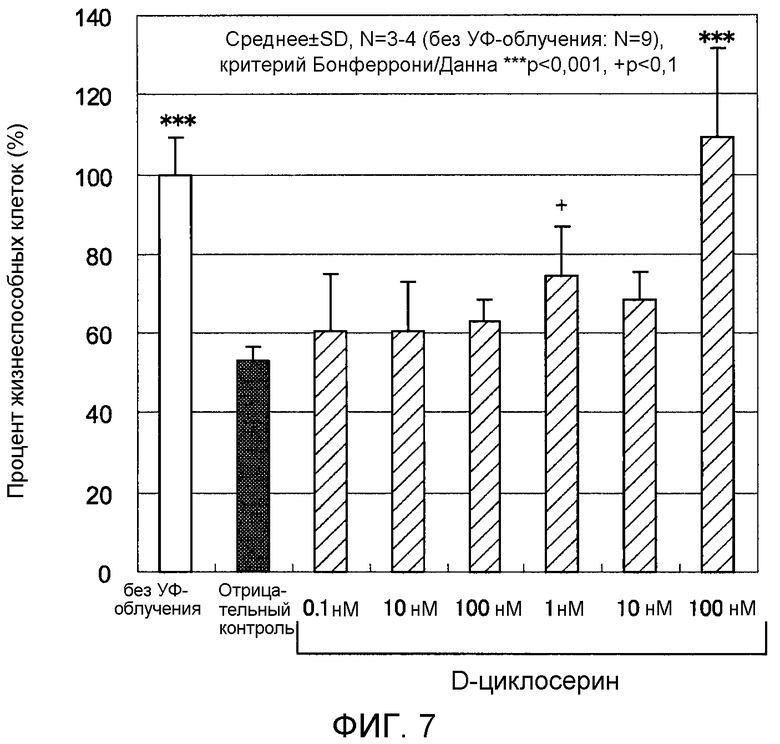
Фигура 7 представляет собой график, на котором показан эффект добавления D-циклосерина после обработки нормальных фибробластов кожи человека ультрафиолетовым излучением.
Описание вариантов осуществления
Примеры настоящего изобретения, описанные ниже, предназначены лишь для пояснения изобретения, а не ограничения его объема. Объем изобретения ограничивается исключительно в соответствии с содержанием формулы.
Все документы, процитированные в настоящем описании, полностью включены путем отсылки.
Пример 1
Эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, под действием метионина
Методы
Культура клеток
Используемой клеткой являлся коммерческий неонатальный фибробласт кожи человека (Cryo NHDF-нео, Sanko-Junyaku Co., Ltd.). Указанный тип клеток инокулировали в 2×105 клеток/мл в коммерческий культуральный планшет диаметром 35 мм (BD FALCON 353001, Becton Dickinson Japan), где их культивировали в коммерческой среде для культуры клеток (D-MEM (1 г/л глюкозы, Wako Pure Chemical Industries, Ltd.) с добавкой 10% эмбриональной бычьей сыворотки (в дальнейшем называемой "нормальной средой"). Клетка, описанная выше, может культивироваться в нормальной среде, описанной выше, с добавкой антибиотика (15240-062, Gibco) в концентрации 1%. Указанную клетку культивировали приблизительно в течение 24 часов при 5% CO2 в насыщенной парами воды атмосфере при 37°C (градусы Цельсия).
Затем культуральную среду для культивирования клетки, описанной выше, меняли на 1 мл среды BSO с добавкой ингибитора биосинтеза глутатиона BSO (L-бутионин-(S,R)-сульфоксимин, Wako Pure Chemical Industries, Ltd.) при 1×10-3%, в которой культуру поддерживали в течение приблизительно 24 часов при 5% CO2 в насыщенной парами воды атмосфере при 37°C (градусы Цельсия). Среду BSO, описанную выше, приготавливали путем 200-кратного разведения стокового раствора, содержащего 0,2% спиртовой раствор BSO, нормальной средой, описанной выше.
Добавление аминокислоты перед обработкой ультрафиолетовым излучением
Для определения эффекта от добавления метионина перед обработкой ультрафиолетовым излучением (в дальнейшем называемого "добавлением метионина до облучения") культуральную среду меняли на среду BSO с добавкой 0,0001 - 100 мкМ (микромоль) L-метионина (131-01603, Wako Pure Chemical Industries Ltd.) или D-метионина (2807, Peptide Institute Inc.) за 24 часа до облучения. Облучение ультрафиолетом после замены на среду с добавкой 0,1 мкМ (микромоль) D-пролина (165-14671, Wako Pure Chemical Industries Ltd.) использовали в качестве положительного контроля, тогда как облучение ультрафиолетом среды без добавки такой аминокислоты использовали в качестве отрицательного контроля.
Среда для УФ облучения
Хлорид железа (II) растворяли в дистиллированной воде при 2×10-3% и полученный раствор подвергали 200-кратному разведению (конечная концентрация: 1×10-5%) фосфатно-солевым буфером PBS (+), содержащим ион кальция и ион магния, получив среду (в дальнейшем называемую "Средой для УФ облучения"), которую предварительно нагревали до 37°C перед использованием.
УФ облучение
Перед УФ-A облучением культуральную среду меняли на 1 мл среды для УФ облучения, описанной выше. УФ-A облучение проводили с использованием устройства равномерного УФ-облучения UVE-502S+EL-160 (SAN-EI ELECTRIC), облучая культуральный планшет с высоты приблизительно 20 см УФ-излучением с длиной волны 320 - 400 нм при 8 Дж/см2 и 9 Дж/см2, в состоянии, когда крышка соответствующего культурального планшета была снята. Дозу УФ-излучения измеряли, используя УФ-радиометр UVR-3036/S (Topcon Corporation).
Добавление аминокислоты после обработки ультрафиолетовым излучением
После УФ-A облучения при 8 Дж/см2 среду заменяли нормальной средой, описанной выше, и поддерживали культуру при 5% CO2 в насыщенной парами воды атмосфере при 37°C (градусы Цельсия) в течение 40 часов. Для определения эффекта от добавления метионина после УФ-облучения (в дальнейшем называемого "добавление метионина после облучения") в указанную среду после 40 ч культивирования добавляли 0,001-100 мкМ (микромоль) L- или D-метионина. Облучение ультрафиолетом после замены на среду с добавкой 0,1 мкМ (микромоль) D-пролина использовали в качестве положительного контроля, тогда как облучение ультрафиолетом среды без добавки такой аминокислоты использовали в качестве отрицательного контроля.
Оценка повреждения клеток при облучении до и после добавления
Следующим шагом в среду культивирования добавляли Alamar Blue (торговое наименование, Biosource, Biosource International Inc. и Invitrogen) до конечной концентрации 10%, после чего определяли интенсивность флуоресценции супернатанта через три часа при длине волны возбуждения 544 нм и длине волны флуоресценции 590 нм, как описано Ahmed S.A. et al. J. Immunol. Method. 170, 211-224 (1994), и в соответствии с инструкцией производителя. Процент жизнеспособных клеток получали как процент от отношения, вычисляемого путем деления интенсивности флуоресценции Alamar Blue при каждом условии эксперимента на интенсивность флуоресценции в группе отрицательного контроля без добавки аминокислоты.
Результаты добавления метионина перед облучением (1)
На Фигуре 1 показаны результаты эксперимента по оценке влияния L- или D-метионина на повреждение фибробластов, вызванное обработкой ультрафиолетовым излучением УФ-A при 9 Дж/см2. Планки погрешностей для релевантных условий эксперимента соответствуют стандартным отклонениям измеренных значений результатов экспериментов, повторенных четыре раза при одинаковых условиях. Звездочка (*) обозначает P<5%, звездочка (**) обозначает P<1% и звездочка (***) обозначает P<0,1% согласно критерию Бонферрони/Данна.
Процент жизнеспособных клеток без добавления аминокислоты перед облучением УФ-A 9 Дж/см2 (отрицательный контроль) составил 24%. Процент жизнеспособных клеток с добавлением D-пролина при 0,1 мкМ (микромоль) перед облучением (положительный контроль) составил 100%, что указывает на супрессию гибели клеток. Добавление перед облучением D-метионина при 0,01 мкМ (микромоль), 0,1 мкМ (микромоль), 1 мкМ (микромоль), 10 мкМ (микромоль) или 100 мкМ (микромоль) приводило к проценту жизнеспособных клеток 102%, 81%, 97%, 114% или 76%, соответственно. Добавление перед облучением L-метионина при 0,001 мкМ (микромоль), 0,01 мкМ (микромоль), 0,1 мкМ (микромоль), 1 мкМ (микромоль), 10 мкМ (микромоль) или 100 мкМ (микромоль) приводило к проценту жизнеспособных клеток 40%, 72%, 67%, 45%, 73% или 62%. На основании представленных результатов можно утверждать, что добавление L- или D-метионина приводило к увеличению процента жизнеспособных клеток и уменьшению гибели клеток.
Результаты добавления метионина перед облучением (2)
На Фигуре 2 показаны результаты эксперимента по оценке влияния D-метионина на повреждение фибробластов, вызванное обработкой ультрафиолетовым излучением УФ-A при 9 Дж/см2. Планки погрешностей для релевантных условий эксперимента соответствуют стандартным отклонениям измеренных значений результатов экспериментов, повторенных три-четыре раза при одинаковых условиях. Звездочка (*) обозначает p<5% согласно критерию Бонферрони/Данна.
Процент жизнеспособных клеток без УФ-облучения и без добавления аминокислоты (в дальнейшем называемый "без УФ-облучения") составил 100%. Процент жизнеспособных клеток без добавления аминокислоты перед облучением УФ-A 9 Дж/см2 (отрицательный контроль) составил 69%. Процент жизнеспособных клеток с добавлением D-пролина при 0,1 мкМ перед облучением (положительный контроль) составил 88%, что указывает на снижение гибели клеток. Добавление перед облучением D-метионина при 0,0001 мкМ (микромоль) и 0,1 мкМ (микромоль) приводило к проценту жизнеспособных клеток 50% и 101%. На основании представленных результатов можно утверждать, что добавление D-метионина при 0,0001 мкМ (микромоль) не приводило к какому-либо увеличению процента жизнеспособных клеток, однако добавление D-метионина при 0,1 мкМ (микромоль) привело к увеличению процента жизнеспособных клеток и снижению гибели клеток.
Результаты добавления метионина после облучения
На Фигуре 3 показаны результаты эксперимента по оценке влияния D-метионина на повреждение фибробластов, вызванное обработкой ультрафиолетовым излучением УФ-A при 8 Дж/см2. Планки погрешностей для релевантных условий эксперимента соответствуют стандартным отклонениям измеренных значений результатов экспериментов, повторенных четыре раза при одинаковых условиях. Звездочка (***) обозначает p <0,1% согласно критерию Бонферрони/Данна.
Процент жизнеспособных клеток без добавления аминокислоты после облучений УФ-A 8 Дж/см2 (отрицательный контроль) составил 64%. Процент жизнеспособных клеток в присутствии D-пролина, добавленного при 0,1 мкМ (микромоль) после облучения, составил 82%, что указывает на снижение гибели клеток. Добавление после облучения D-метионина при 0,01 мкМ (микромоль), 0,1 мкМ (микромоль), 1 мкМ (микромоль), 10 мкМ (микромоль) или 100 мкМ (микромоль) привело к проценту жизнеспособных клеток 93%, 84%, 82%, 81% или приблизительно 87%. На основании представленных результатов можно утверждать, что добавление D-метионина приводило к увеличению процента жизнеспособных клеток и снижению гибели клеток. Было также показано, что эффект снижения гибели клеток наблюдался независимо от времени добавления D-метионина до или после УФ-облучения. Кроме того, L-метионин также уменьшал гибель клеток, вызванную УФ-излучением. Таким образом, предложили, что нет никакой связи со временем добавления L-метионина, добавляемого до или после УФ-облучения.
Пример 2
Эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, под действием серина
Методы
Культивирование клеток, добавление аминокислот перед УФ-облучением, УФ-облучение, добавление аминокислот после УФ-облучения и измерение повреждения клеток проводили аналогично Примеру 1. Обработку ультрафиолетовым излучением (УФ-A) проводили при 7,5 или 9 Дж/см2. Для определения эффекта от добавления серина перед облучением ультрафиолетом (в дальнейшем называемого "добавление серина перед облучением") и эффекта от добавления серина после облучения ультрафиолетом (в дальнейшем называемого "добавление серина после облучения") использовали L-серин (197-00403, Wako Pure Chemical Industries Ltd.) и D-серин (197-08823, Wako Pure Chemical Industries Ltd.) при 0,0001 - 100 мкМ (микромоль). Эффект от добавления серина после облучения оценивали при облучении клеток с плотностью энергии 7,5 Дж/см2 УФ-A, с последующей заменой среды нормальной средой, в которой культуру поддерживали в течение 21 часа, и добавлением D-серина к данной среде, культивируемой в течение 21 часа.
Результаты добавления серина перед облучением (1)
На Фигуре 4 показаны результаты эксперимента по оценке влияния добавления L-серина и D-серина перед облучением на повреждение фибробластов, вызванное облучением УФ-A при 9 Дж/см2. Планки погрешностей для релевантных условий эксперимента соответствуют стандартным отклонениям измеренных значений результатов экспериментов, повторенных четыре-шесть раз при одинаковых условиях. Звездочка (*) обозначает p<5% согласно критерию Бонферрони/Данна.
Интенсивность флуоресценции Alamar Blue (торговое наименование) без облучения ультрафиолетом составляла 794. Интенсивность флуоресценции без добавления аминокислоты перед облучением УФ-A при 9 Дж/см2 (отрицательный контроль) составляла 140. Интенсивность флуоресценции с добавлением D-пролина при 0,1 мкМ (микромоль) перед облучением (положительный контроль) составляла до 610, что указывало на уменьшенное повреждение клеток. Интенсивности флуоресценции с добавлением D-серина при 0,01 мкМ (микромоль), 0,1 мкМ (микромоль), 1 мкМ (микромоль) и 10 мкМ (микромоль) перед облучением составляли 445, 402, 371 и 491, соответственно. Интенсивности флуоресценции с добавлением L-серина при 0,1 мкМ (микромоль), 1 мкМ (микромоль) и 10 мкМ (микромоль) перед облучением составляли 265, 227 и 270, соответственно. На основании представленных результатов можно утверждать, что добавление L-серина перед облучением практически не приводило к какому-либо уменьшению повреждения клеток. Между тем, добавление D-серина перед облучением приводило к статистически значимому увеличению интенсивности флуоресценции, что указывает на уменьшение повреждения клеток.
Результаты добавления серина перед облучением (2)
На Фигуре 5 показаны результаты эксперимента по оценке влияния добавления D-серина перед облучением на повреждение фибробластов, вызванное облучением УФ-A при 8 Дж/см2. Планки погрешностей для релевантных условий эксперимента соответствуют стандартным отклонениям измеренных значений результатов экспериментов, повторенных четыре раза при одинаковых условиях. Звездочка (*) обозначает p<5% согласно критерию Бонферрони/Данна.
Процент жизнеспособных клеток без облучения ультрафиолетом составил 100%. Процент жизнеспособных клеток без добавления аминокислоты перед облучением УФ-A 8 Дж/см2 (отрицательный контроль) составил 77%. Проценты жизнеспособных клеток с добавлением D-серина при 0,0001 мкМ (микромоль), 0,01 мкМ (микромоль) и 10 мкМ (микромоль) перед облучением составили 74%, 92% и 93%, соответственно. На основании представленных результатов можно утверждать, что повреждение клеток, вызванное ультрафиолетовым излучением, характеризовалось тем, что добавление D-серина при 0,0001 мкМ (микромоль) приводило к увеличению процента жизнеспособных клеток, при этом добавление D-серина при 0,1 мкМ (микромоль) и 10 мкМ (микромоль) приводило к увеличению процента жизнеспособных клеток, указывая на снижение гибели клеток.
Результаты добавления серина после облучения
На Фигуре 6 показаны результаты эксперимента по оценке влияния добавления D-серина после облучения на повреждение фибробластов, вызванное облучением УФ-A при 7,5 Дж/см2. Планки погрешностей для релевантных условий эксперимента соответствуют стандартным отклонениям измеренных значений результатов экспериментов, повторенных восемь раз при одинаковых условиях. Звездочка (*) обозначает p<5% согласно критерию Бонферрони/Данна.
Интенсивность флуоресценции Alamar Blue (торговое наименование) без облучения ультрафиолетом составляла 764. Интенсивность флуоресценции без добавления аминокислоты после облучения УФ-A при 7,5 Дж/см2 (отрицательный контроль) составляла 348. Интенсивность флуоресценции с добавлением D-пролина при 0,1 мкМ (микромоль) после облучения (положительный контроль) составляла до 579, что указывало на уменьшение повреждения клеток. Интенсивности флуоресценции с добавлением D-серина при 0,01 мкМ (микромоль), 0,1 мкМ (микромоль), 1 мкМ (микромоль), 10 мкМ (микромоль) и 100 мкМ (микромоль) после облучения составляли 697, 735, 742, 664 и 663, соответственно. На основании представленных результатов можно утверждать, что добавление D-серина после облучения приводило к статистически значимому увеличению интенсивности флуоресценции, что указывает на уменьшение повреждения клеток. Было также показано, что эффект уменьшения повреждения клеток достигался независимо от времени добавления D-серина, производимого до или после УФ-облучения.
Пример 3
Эффект уменьшения повреждения, вызванного ультрафиолетовым излучением, при воздействии D-циклосерина
Методы
Культивирование клеток, добавление аминокислот перед УФ-облучением, УФ-облучение, добавление аминокислот после УФ-облучения и измерение повреждения клеток проводили аналогично Примеру 1. Обработку ультрафиолетовым излучением (УФ-A) проводили при 9 Дж/см2. Для определения эффекта от добавления D-циклосерина перед облучением ультрафиолетом (в дальнейшем называемого "добавление циклосерина перед облучением") использовали D-циклосерин (C6880, Sigma) при 0,0001-100 мкМ.
Результаты добавления D-циклосерина перед облучением
На Фигуре 7 показаны результаты эксперимента по оценке влияния добавления D-циклосерина перед облучением на повреждение фибробластов, вызванное УФ-A облучением при 9 Дж/см2. Планки погрешностей для релевантных условий эксперимента соответствуют стандартным отклонениям измеренных значений результатов экспериментов, повторенных три-четыре раза при одинаковых условиях. Символ (+) и звездочка (***) обозначают p<10% и p<0,1%, соответственно, согласно критерию Бонферрони/Данна.
Процент жизнеспособных клеток без добавления аминокислоты перед УФ-A облучением при 9 Дж/см2 (отрицательный контроль) составлял 53%. Процент жизнеспособных клеток с добавленным D-циклосерина при 0,1 нМ, 10 нМ, 100 нМ, 1 мкМ (микромоль), 10 мкМ (микромоль) и 100 мкМ (микромоль) перед облучением составлял 60%, 60%, 63%, 74%, 69% и 109%. На основании представленных результатов можно утверждать, что добавление D-циклосерина приводило к увеличению процента жизнеспособных клеток, что указывает на снижение гибели клеток.
На основе настоящего изобретения, ниже представлены составы примеров композиций, включающих метионин, серин и/или D-циклосерин, таких как эмульсионная композиция, композиция пластыря, таблетка, мягкая капсула, гранула, напиток, конфета, печенье, паста мисо, французский соус, майонез, французский хлеб, соевый соус, йогурт, сушеная приправа в порошке для риса, заправка/соус для натто (японская сброженная соевая паста), натто, неочищенный черный уксус, крем, крем для тела, гелевая композиция, отшелушевающая маска, влажное обертывание, эмульсия, лосьон для лица и аэрозольная композиция. Метионин в следующих Примерах композиций находился в D-форме и/или L-форме. Данные примеры композиций приведены исключительно с целью примера и не рассматриваются как ограничение объема изобретения.
(% по массе)
(% по массе)
Способ приготовления Примера композиции 10 (Печенье)
Сахарный песок добавляют порциями в масло при перемешивании, затем добавляют яйцо, D-серин и/или D-циклосерин вместе с ароматизатором и перемешивают. После полного перемешивания добавляют однородно просеянную пшеничную муку и медленно перемешивают, после чего ставят тесто в холодильный шкаф для отстойки. Затем тесто формуют и выпекают в течение 15 минут при 170°C (градусы Цельсия), получив печенье.
Способ приготовления Примера композиции 11 (паста Мисо (соевая))
Осоложенный рис тщательно смешивают с солью. Промытую сою вымачивают в трех объемах воды, которую затем сливают и добавляют новую порцию воды при кипении, которую сливают через сито, чтобы собрать бульон (жидкость танемицу), в котором растворяют D-серин и/или D-циклосерин до 10% в/об. Вареные бобы сразу же измельчают, соединяют с осоложенным рисом, смешанным с солью, к которым добавляют жидкость танемицу, описанную выше, содержащую растворенный D-серин и/или D-циклосерин, и равномерно перемешивают с получением массы глиноподобной консистенции. Делают шарики, которые плотно укладывают в контейнер, не оставляя пустот, после чего поверхность содержимого разравнивают и накрывают пластиковой пленкой. Через три месяца содержимое переносят в новый контейнер, разравнивают поверхность и накрывают пластиковой пленкой. Вместо добавления D-серина и/или D-циклосерина к жидкости танемицу можно использовать осоложенный рис, дающий большое количество D-серина и/или D-циклосерина. Такой осоложенный рис может быть отобран при определении количества D-серина и/или D-циклосерина с помощью способа, описанного в неакцептованной заявке на патент Японии 2008-185558. В альтернативе D-серин и/или D-циклосерин, или их соль могут быть добавлены в коммерческую пасту мисо.
Способ приготовления Примера композиции 12 (Французский соус)
Уксус соединяют с поваренной солью и D-серином и/или D-циклосерином, тщательно перемешивают, и затем добавляют перец.
Способ приготовления Примера композиции 13 (Майонез)
Яичный желток (комнатной температуры) соединяют с уксусом, солью, перцем и D-серином и/или D-циклосерином и тщательно перемешивают с использованием взбивающего устройства. Перемешивание продолжают и порциями добавляют растительное масло с получением эмульсии. Наконец добавляют сахар и перемешивают смесь.
Способ приготовления Примера композиции 14 (Французский хлеб)
Теплую воду соединяют с 1 г сахара и сухих дрожжей, которые затем оставляют для предварительного брожения. Муку твердых сортов пшеницы, муку мягких сортов пшеницы, соль и 5 г сахара помещают в дежу вместе с D-серином и/или D-циклосерином, после чего добавляют подошедшие дрожжи. После тщательного перемешивания тесто формируют в шар и проводят первичное брожение при 30°C. Тесто снова перемешивают и оставляют для расстойки, а затем придают нужную форму и подвергают окончательному брожению с использованием электронной ферментационной машины. После формирования булочек проводят выпечку в течение 30 минут в печи при 220°C (градусы Цельсия).
Способ приготовления Примера композиции 15 (Соевый соус)
В коммерческий соевый соус добавляют D-серин и/или D-циклосерин и тщательно перемешивают. Вместо добавления D-серина и/или D-циклосерина, или их соли при ферментировании соевого соуса может использоваться осоложенный рис, дающий большое количество D-серина и/или D-циклосерина. Такой осоложенный рис может быть выбран при помощи количественного анализа D-серина и/или D-циклосерина способом, описанным в неакцептованной заявке на патент Японии 2008-185558.
Способ приготовления Примера композиции 16 (Йогурт)
Брожение проводят при температуре от 40°C (градусы Цельсия) до 45°C (градусы Цельсия). Могут использоваться другие коммерческие культуры микроорганизмов для брожения, а D-серин и/или D-циклосерин могут быть добавлены в коммерческий йогурт. Вместо добавления D-серина и/или D-циклосерина, или их соли, для брожения может использоваться организм, продуцирующий большое количество D-серина и/или D-циклосерина. Такой организм может быть выбран при помощи количественного анализа D-серина и/или D-циклосерина способом, описанным в неакцептованной заявке на патент Японии 2008-185558.
Способ приготовления Примера композиции 19 (Натто)
Вместо добавления D-серина и/или D-циклосерина, или их соли для приготовления натто может использоваться организм, продуцирующий большое количество D-серина и/или D-циклосерина. Такой организм может быть выбран при помощи количественного анализа D-серина и/или D-циклосерина способом, описанным в неакцептованной заявке на патент Японии 2008-185558.
Способ приготовления Примера композиции 20 (Неочищенный черный уксус)
Вместо добавления D-серина и/или D-циклосерина, или их соли для приготовления уксуса, черного уксуса или неочищенного уксуса может использоваться организм, продуцирующий большое количество D-серина и/или D-циклосерина. Такой организм может быть выбран при помощи количественного анализа D-серина и/или D-циклосерина способом, описанным в неакцептованной заявке на патент Японии 2008-185558.
(% по массе)
(% по массе)
(% по массе)
(% по массе)
(% по массе)
(% по массе)
(% по массе)
(% по массе)
(% по массе)
(% по массе)
(% по массе)
(% по массе)
(% по массе)
Способ наполнения для Примера композиции 34 (Аэрозольный спрей с мочевиной)
Стоковым раствором для приготовления аэрозольного препарата с мочевиной для наружного применения и диметиловым эфиром заполняют стойкий к давлению алюминиевый аэрозольный баллон, внутренняя поверхность которого покрыта Тефлоном (торговое наименование) с получением аэрозольного препарата.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМПОЗИЦИИ ДЛЯ СМЯГЧЕНИЯ ПОРАЖЕНИЙ, ВЫЗВАННЫХ УЛЬТРАФИОЛЕТОВЫМ ИЗЛУЧЕНИЕМ | 2010 |
|
RU2519206C2 |
| КОМПОЗИЦИЯ ДЛЯ ЗАЩИТЫ КОЖИ ОТ ВОЗДЕЙСТВИЯ ВРЕДНЫХ ВЕЩЕСТВ, СВЕТА И СТРЕССА | 2021 |
|
RU2792212C1 |
| ПЕПТИДЫ С ЗАЩИТНОЙ АКТИВНОСТЬЮ ОТ ПОВРЕЖДЕНИЯ КЛЕТОК И ЛИПОСОМАЛЬНЫЕ СОСТАВЫ | 2020 |
|
RU2833316C1 |
| КОМПОЗИЦИЯ ДЛЯ СТИМУЛИРОВАНИЯ ПРОДУЦИРОВАНИЯ ЛАМИНИНА-332 | 2010 |
|
RU2581916C2 |
| КОМПОЗИЦИИ, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ КОЖНЫХ ПРИЗНАКОВ СТАРЕНИЯ | 2005 |
|
RU2409290C2 |
| ПЕПТИДНАЯ ЗАЩИТА ПРОТИВ ТОКСИЧЕСКОГО ВОЗДЕЙСТВИЯ УЛЬТРАФИОЛЕТОВОГО ИЗЛУЧЕНИЯ | 2010 |
|
RU2565535C2 |
| ПТЕРОСТИЛЬБЕН (PTER) ДЛЯ ПРИМЕНЕНИЯ В ПРОФИЛАКТИКЕ И/ИЛИ ЛЕЧЕНИИ КОЖНЫХ ЗАБОЛЕВАНИЙ, ПОВРЕЖДЕНИЙ ИЛИ ТРАВМ | 2010 |
|
RU2578031C2 |
| АНТИОКСИДАНТНАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2535099C2 |
| КОМПОЗИЦИИ ДЛЯ ВОССТАНОВЛЕНИЯ КОЖИ, СОДЕРЖАЩИЕ АКТИВАТОРЫ ЦИРКАДНЫХ ГЕНОВ И СИНЕРГИЧЕСКУЮ КОМБИНАЦИЮ АКТИВАТОРОВ ГЕНА sirt1 | 2010 |
|
RU2494756C1 |
| ВЫДЕЛЕННЫЙ ПЕПТИД ДЛЯ УСИЛЕНИЯ РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТИ КЕРАТИНОЦИТОВ, КОМПОЗИЦИЯ ДЛЯ ЗАЖИВЛЕНИЯ РАН У МЛЕКОПИТАЮЩЕГО И ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПРИМЕНЕНИЯ ПРИ ЗАЖИВЛЕНИИ РАН У МЛЕКОПИТАЮЩЕГО | 2007 |
|
RU2458069C2 |
Изобретение относится к области фармацевтики и представляет собой композицию для уменьшения повреждения, вызванного ультрафиолетовым излучением, включающая одно или более соединений, выбранных из группы, состоящей из D-метионина и его солей. Изобретение обеспечивает создание стабильной и безопасной композиции, которая может применяться ежедневно. 9 з.п. ф-лы, 37 пр., 7 ил.
1. Композиция для уменьшения повреждения, вызванного ультрафиолетовым излучением, включающая одно или более соединений, выбранных из группы, состоящей из D-метионина и его солей.
2. Композиция по п.1, где композиция наносится в качестве препарата для наружного применения на коже.
3. Композиция по п.1 или 2, где композиция является средством против морщин.
4. Композиция по п.1 или 2, где композиция является солнцезащитным средством.
5. Композиция по п.1 или 2, где композиция применяется в качестве фармацевтического продукта для кожного заболевания.
6. Композиция по п.5, где кожное заболевание выбрано из группы, состоящей из эритемы, солнечного дерматита, хронической актинической дерматопатии, актинического кератоза, актинического хейлита, болезни Фавра-Ракушо, фотодерматоза, фотодерматита, брелокового дерматита, фоточувствительной лекарственной сыпи, полиморфной световой сыпи, световой оспы, солнечной крапивницы, хронического фоточувствительного дерматита, пигментной ксеродермы, веснушек, порфирии, пеллагры, болезни Хартнапа, солнечного кератоза, дерматомиозита, плоского лишая, болезни Дарье, красного волосистого питириаза, розовых угрей, атопического дерматита, хлоазмы, простого герпеса, красной волчанки, плоскоклеточной карциномы, базально-клеточной карциномы и болезни Боуэна.
7. Композиция по п.5, где фармацевтический продукт для кожного заболевания является средством для лечения кожного заболевания.
8. Композиция по п.6, где фармацевтический продукт для кожного заболевания является средством для лечения кожного заболевания.
9. Композиция по п.5, где фармацевтический продукт для кожного заболевания является средством для предупреждения кожного заболевания.
10. Композиция по п.6, где фармацевтический продукт для кожного заболевания является средством для предупреждения кожного заболевания.
| Karen E | |||
| Burke | |||
| Oral and Topical L-Selenomethionine Protection from Ultraviolet-Induced Sunburn, Tanning and Skin Cancer // Journal of Orthomolecular Medicine | |||
| Vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| Пуговица | 0 |
|
SU83A1 |
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| WO 2006031720 A2, 23.03.2006 | |||
| СПОСОБ ДИСТАНЦИОННОГО РАСПОЗНАВАНИЯ И КОРРЕКЦИИ С ПОМОЩЬЮ ВИРТУАЛЬНОЙ РЕАЛЬНОСТИ ПСИХОЭМОЦИОНАЛЬНОГО СОСТОЯНИЯ ЧЕЛОВЕКА | 2018 |
|
RU2711976C1 |
| WO 2009024350 A2, 26.02.2009 | |||
| Teresa S | |||
| RAFFERTY et al | |||
| Differential | |||
Авторы
Даты
2014-12-27—Публикация
2010-09-14—Подача