Введение
Изобретение относится к фармацевтической промышленности, а именно к новому сокристаллу 2-гидроксибензамида, пригодному для фармацевтических препаратов.
Уровень техники
2-гидроксибензамид, именуемый также салициламидом,
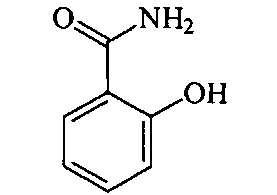
является известным фармацевтическим ингредиентом (API), обладающим противовоспалительным, анальгезирующим, жаропонижающим действием, а также снижает агрегацию тромбоцитов [Hart Е.R. The toxicity and analgetic potency of salicylamide and certain of its derivatives as compared with established analgetic-antipyretic drugs // The Journal of pharmacology and experimental therapeutics - 1947 - 89(3) - P.205-209; Bates T.R., Lambert D.A., and Johns W.H. Correlation Between the Rate of Dissolution and Absorption of Salicylamide from Tablet and Suspension Dosage Forms // J. Pharm. Science - 1969 - 58(12) - P.1468-1470].
2-гидроксибензамид может использоваться для профилактики лихорадочного синдрома (простудные и инфекционные заболевания); болевого синдрома слабой и средней интенсивности: артралгия, миалгия, невралгия, мигрень, зубная и головная боль, альгодисменорея. Кроме того, назначается при болях при травмах, ожогах; воспалительных заболеваниях суставов (ревматоидный артрит, реактивный артрит, остеоартрит, спондилоартропатия, анкилозирующий спондилоартрит, подагра) и мягких тканей (бурсит, тендовагинит); ревмокардита.
Блокирует циклооксигеназу, нарушает метаболизм арахидоновой кислоты, уменьшает количество простагландинов как в очаге воспаления, так и в здоровых тканях, подавляет экссудативную и пролиферативную фазу воспаления. Уменьшает проницаемость капилляров; стабилизирует лизосомальные мембраны; тормозит выработку макроэргов (прежде всего АТФ) в процессах окислительного фосфорилирования; тормозит синтез или инактивирует медиаторы воспаления, в т.ч. гистамин, брадикинин, лимфокины, фактор комплемента и другие неспецифические эндогенные «повреждающие факторы». Блокирует взаимодействие брадикинина с тканевыми рецепторами, восстанавливает нарушенную микроциркуляцию и снижает болевую чувствительность в очаге воспаления, снижает образование тромбоксана. Влияет на таламические центры болевой чувствительности (локальная блокада синтеза ПГУ1, ПГЕ2 и ПГF2α). Анальгетическое действие обусловлено снижением концентрации биогенных аминов, обладающих альгогенными свойствами, и увеличением порога болевой чувствительности рецепторного аппарата. Уменьшает, за счет угнетения синтеза простагландинов, перевозбуждение центра терморегуляции. При лихорадке усиливает теплоотдачу за счет расширения кожных сосудов и угнетает теплопродукцию вследствие снижения мышечного дрожательного термогенеза - озноба (жаропонижающее действие). Терапевтическая активность 2-гидроксибензамида при различных заболеваниях была описана в клинической литературе, например [Borovsky М.P. Antipyretic activity of acetylsalicylic acid and salicylamide suspension in pediatrics. A comparative clinical evaluation in two hundred six cases // American journal of diseases of children. - 1960 - V.100 - P.23-30]. Хотя наиболее значимой характеристикой лекарственного соединения, такого как 2-гидроксибензамид, является терапевтическая эффективность, не менее важным с точки зрения фармакокинетических показателей являются формы предлагаемого лекарственного препарата. Например, аморфная форма, соль, сокристалл, полиморфные модификации, поскольку они имеют различные физические и химические свойства, что сказывается на фармацевтических параметрах API, таких как стабильность при хранении, сжимаемость и другие. Одними из определяющих факторов биодоступности являются растворимость и кинетические показатели растворения, поскольку низкая растворимость лекарственного соединения в биологических жидкостях приводит к низкой эффективности лекарственного препарата. Поэтому увеличение растворимости препарата является актуальной технической задачей.
Известны различные способы повышения скорости и уровня растворимости лекарственного соединения:
- тонкое измельчение для создания большей площади поверхности растворяемого соединения [Chaumeil J.С. Micronisation: a method of improving the Bioavailability of poorly soluble drugs // Methods Find. Exp.Clin. Pharmcol. - 1998 - 20(3) - P.211-215];
- использование солей исследуемых объектов с улучшенной растворимостью [Agharkar S., Lindenbaum S., Higuchi Т. Enhancement of solubility of drug salts by hydrophilic counter-ions: properties of organic salts of an anti-malarial drug // J. Pharm. Sci. - 1976-65(5) - P.747-749];
- растворение в сложных [Amin K., Dannenfelser R.-M., Zielinski J., Wang B. Lyophilization of polyethylene glycol mixtures // J. Pharm. Sci. - 2004 - 93(9) - P.2244-2249] и мицеллярных растворителях [Torchillin V.P. Micellar nanocarriers: pharmaceutical perspectives // Pharm. Res. - 2007 - 24(1) - P.1-16];
- образование супрамолекулярных комплексов с циклодекстринами [Rajewski R.A., Stella V.J. Pharmaceutical applications of cyclodextrins. 2. In vivo drug delivery // J. Pharm. Sci. - 1996 - 85(11) - P.1142-1169];
- использование фосфолипидных везикул, наполненных липофильными соединениями [Humberstone A.J., Charman W.N. Lipid-based vehicles for the oral delivery of poorly soluble drugs // Adv. Drug Deliv. Rev. - 1997 - 25(1) - P.103-128].
Однако известные способы обладают недостатками, ограничивающими возможность их использования. Так, хотя тонкое измельчение увеличивает скорость растворения лекарственного средства, однако оно не увеличивает равновесную растворимость вещества. Часто для лекарственных соединений возрастание ван-дер-ваальсовых взаимодействий между мелкими частицами и их электростатическое притяжение ведут к уменьшению эффективной площади растворения и, таким образом, ограничивается предел их биологической активности. Повышение растворимости лекарственного соединения путем создания его солей неприемлемо, так как в фармацевтике используются в основном слабо ионизируемые и нейтральные молекулы, а соли в данный класс соединений не входят.
Использование сложных и мицеллярных растворителей предполагает приемлемую растворимость и совместимость молекул лекарственного соединения с растворителем, что не всегда достижимо. Повышение растворимости путем образования комплексов с циклодекстринами, а также использование фосфолипидных везикул применимо для лекарственных соединений пролонгированного действия, однако нередко требуются лекарства быстрого действия, например нестероидные противовоспалительные средства.
Известно также, что повысить растворимость можно за счет образования сокристаллической формы API с компонентом, способствующим увеличению растворения. Сокристаллы представляют собой супрамолекулярные системы, где одним из компонентов является плохо растворимый активный фармацевтический ингредиент, т.е. молекула лекарственного соединения, тогда как в качестве второго компонента выступает молекула хорошо растворимого соединения, которая полностью усваивается организмом и участвует в ферментативных процессах [Lara-Ochoa F. and Espinosa-Pérez G. Cocrystals definitions // Supramolecular Chemistry. - 2007 - 19(8) - P.553-557].
Сокристаллы, использующиеся в фармацевтической индустрии, привлекательны тем, что дают возможность получения новых кристаллических форм активного фармацевтического ингредиента со специальными свойствами, такими как улучшенная растворимость, термическая стабильность, улучшенные механические свойства и др. При этом возможность выбора компонентов сокристалла значительно облегчает, так сказать, «точную настройку» физических свойств сокристалла.
В сокристалле 2-гидроксибензамида с ацетазоламидом [Arenas-Garcia J.I., Herrera-Ruiz D., Mondragon-Vasquez K., et al. Modification of the Supramolecular Hydrogen-Bonding Patterns of Acetazolamide in the Presence of Different Cocrystal Formers: 3:1, 2:1, 1:1, and 1:2 Cocrystals from Screening with the Structural Isomers of Hydroxybenzoic Acids, Aminobenzoic Acids, Hydroxybenzamides, Aminobenzamides, Nicotinic Acids, Nicotinamides, and 2,3-Dihydroxybenzoic Acids // Crystal growth & design - 2012 - 12(2) - P.811-824] роль активного фармацевтического ингредиента играет ацетазоламид, тогда как 2-гидроксибензамид лишь повышает растворимость.
Известен также сокристалл 2-гидроксибензамида с 4-ацетамидобензойной кислотой [Манин А.Н. Физико-химические свойства кристаллов и растворов производных бензамида и ацетанилида. Дис. … к-та. химич. наук. 02.00.04 Иваново, 2011. - 172 с.]. Но несмотря на то что растворимость этого сокристалла в воде и повышается на 25%, второй компонент сокристалла не является ни витамином, ни другим полезным для организма препаратом, поэтому использование данного сокристалла в фармацевтической промышленности нецелесообразно.
Салициловая кислота, в свою очередь, обладает выраженным противовоспалительным действием. Салициловая кислота служит основой для производства многих лекарств, обладает слабыми антисептическими, раздражающими и кератолитическими (в больших количествах) свойствами.
Таким образом, она может использоваться в фармацевтических целях, как и сокристалл 2-гидроксибензамида с салициловой кислотой.
Сущность изобретения
Техническая задача изобретения состояла в поиске сокристаллической формы 2-гидроксибензамида, позволяющей повысить его растворимость и пригодной для использования в фармацевтической промышленности.
Сущность изобретения состоит в следующем.
Сокристаллическая форма 2-гидроксибензамида с салициловой кислотой, где молярное соотношение 2-гидроксибензамида с салициловой кислотой составляет 1:1, имеет эндотермический пик от 116 до 124°C по данным измерения при помощи дифференциальной сканирующей калориметрии и имеет пики при 2θ(°)11.5, 14.8, 16.7, 18.8, 22.2, 23.5, 27.0 по данным измерения дифракции рентгеновского излучения на порошке.
Заявленное изобретение позволяет получить следующее преимущество - повышение растворимости в воде в 2.6 раза по сравнению с показателями растворимости 2-гидроксибензамида в чистом виде. Данные по растворимости были получены для водного раствора при комнатной температуре на установке для измерения растворимости твердых соединений методом изотермического насыщения. Пробы отбирали в точках примерно 0.1, 0.25, 0.4, 0.5, 0.75, 1.5, 2.5 часа и анализировали при помощи спектрофотометра VARIAN CARY 50 в ультрафиолетовой области спектра, рабочий диапазон длин волн λ=190÷400 нм.
Заявленный новый сокристалл - твердое кристаллическое стабильное вещество, не распадается, не подвержено воздействию влаги и удобен для приготовления стабильных фармацевтических препаратов.
Структура заявленного сокристалла доказана двумя методами, в совокупности достаточными для утверждения об образовании нового соединения:
- дифракция в рентгеновских лучах (XPRD),
- дифференциальная сканирующая калориметрия (DSC).
На фиг.1 представлен типичный профиль XPRD сокристалла - 2-гидроксибензамидхалициловая кислота (1:1).
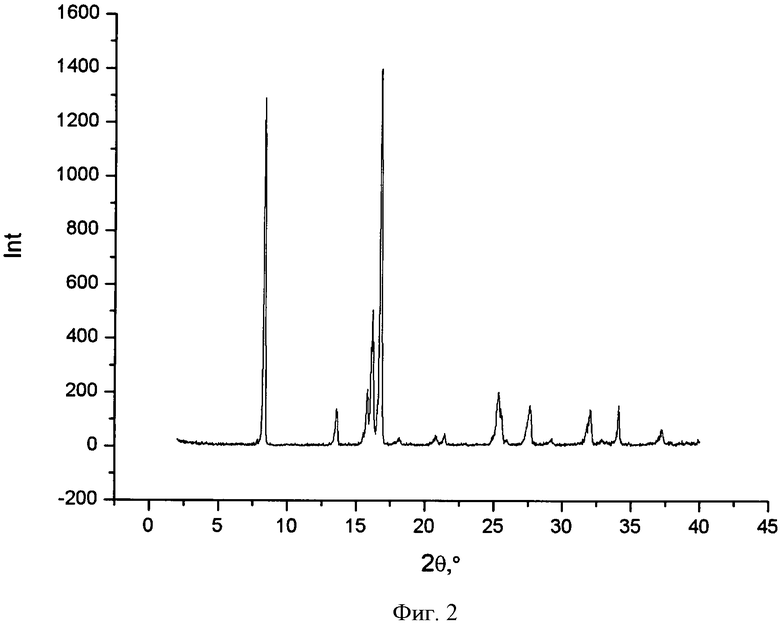
На фиг.2 представлен типичный профиль XPRD 2-гидроксибензамида в чистом виде.
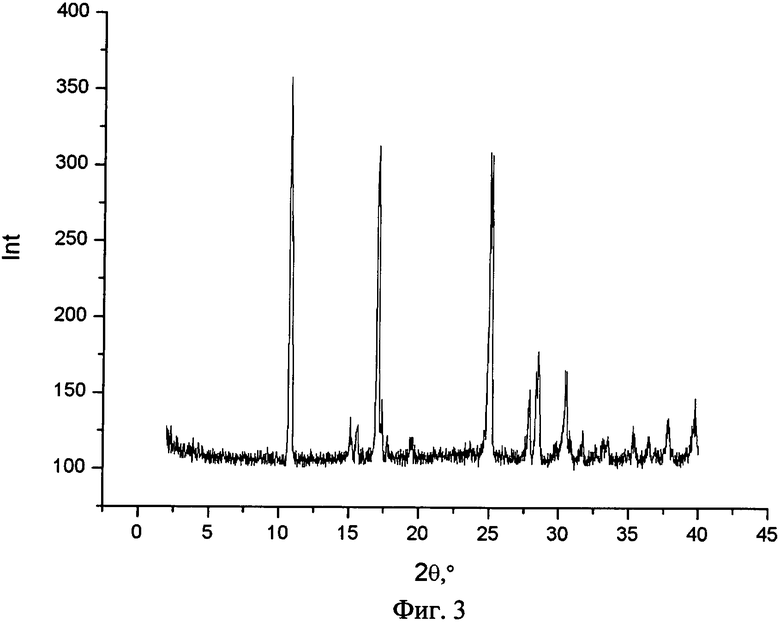
На фиг.3 представлен типичный профиль XPRD салициловой кислоты в чистом виде.
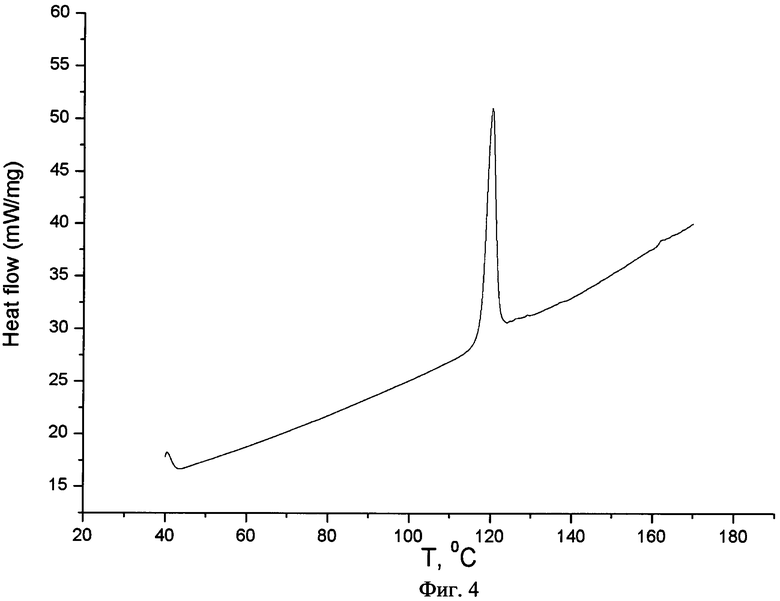
На фиг.4 представлена типичная термограмма DSC сокристалла - 2-гидроксибензамидхалициловая кислота (1:1).
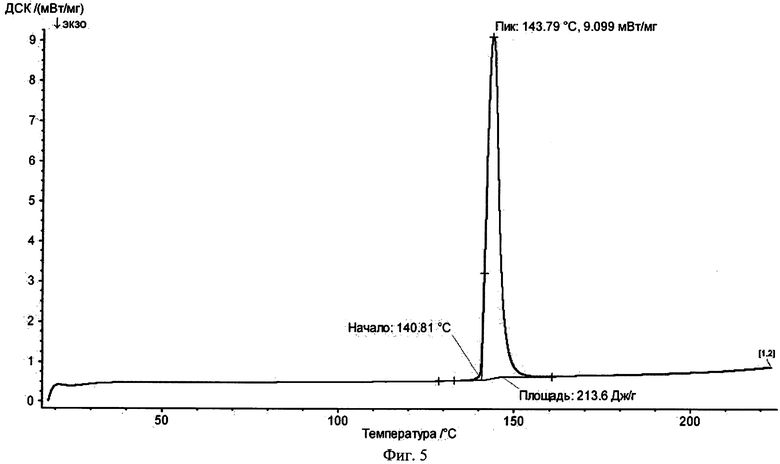
На фиг.5 представлена типичная термограмма DSC 2-гидроксибензамида в чистом виде.
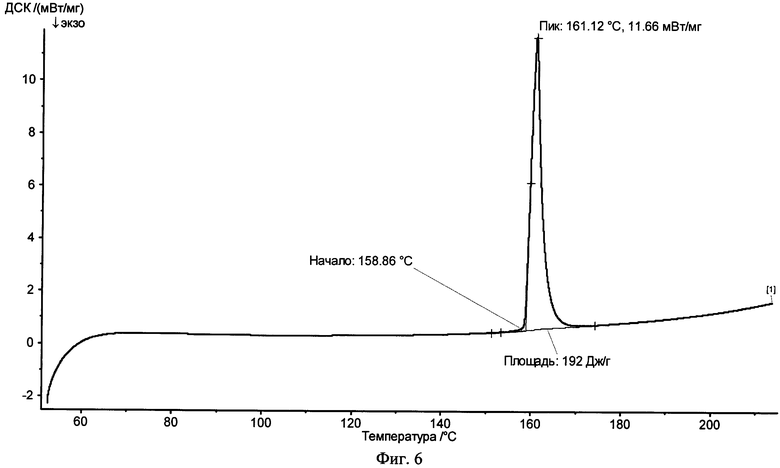
На фиг.6 представлена типичная термограмма DSC салициловой кислоты в чистом виде.
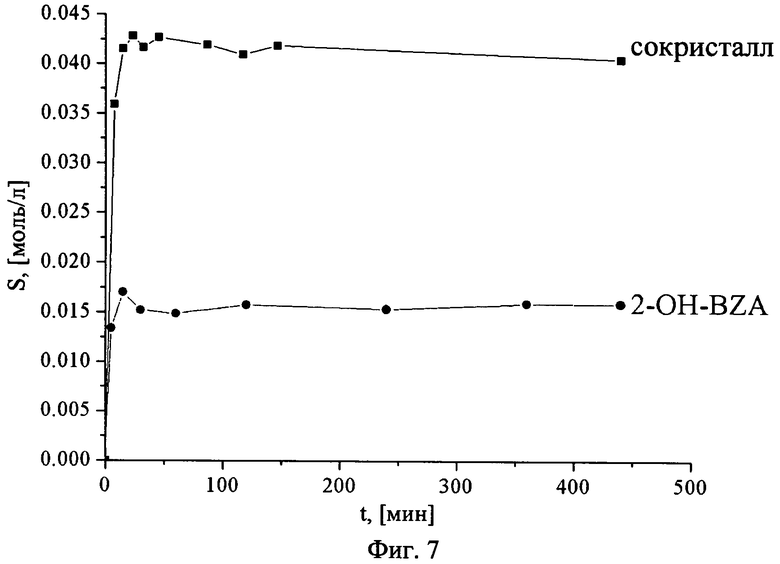
На фиг.7 представлены данные по растворимости для сокристалла 2-гидроксибензамидхалициловая кислота (1:1) и его компонентов в чистом виде.
Сведения, подтверждающие возможность воспроизведения изобретения
Для получения заявленного сокристалла использовали следующие вещества:
- 2-гидроксибензамид - фирма производитель «Sigma-Aldrich», lot S65911, CAS 65-45-2, чистота 99%;
- салициловая кислота - фирма производитель «Sigma-Aldrich», lot 84210-100G, CAS 69-72-7, чистота 99%;
- Этанол - спирт марки «Люкс» ГОСТ Р51652-2000 2001-07-01 «Спирт этиловый рективикованный из пищевого сырья. ТУ».
Новый сокристалл 2-гидроксибензамида в существенной степени характеризуется результатами XPRD, показанными на Фиг.1, и в существенной степени описывается данными термограммы DSC, представленными на Фиг.4.
Получить заявленный сокристалл можно и в твердой фазе, и в растворе.
Пример 1
Смесь 24.91 мг (0, 182 ммоль) 2-гидроксибензамида и 25.09 мг (0,182 ммоль) салициловой кислоты поместили в агатовую ячейку для перемола в планетарной микромельнице, к смеси добавили 0,05 мл этанола (согласно соотношению 1 мкл растворителя на 1 мг смеси). В ячейку были помещены 10 агатовых шариков диаметром 3 мм. Процесс перемолки на скорости 600 об/мин продолжался дважды по полчаса с перерывом 5 минут. После перемолки ячейка была оставлена в вытяжном шкафу до полного испарения остатка растворителя. Оставшийся порошок представлял собой сокристалл - 2-гидроксибензамид:салициловая кислота (1:1), что было подтверждено данными XPRD и DSC. Полученный профиль XPRD конечного продукта в существенной степени соответствовал тому, что показан на Фиг.1. Полученная термограмма DSC конечного продукта в существенной степени соответствовала тому, что показана на Фиг.4.
Пример 2
Смесь 24.91 мг (0, 182 ммоль) 2-гидроксибензамида и 25.09 мг (0,182 ммоль) салициловой кислоты растворили в 2 мл этанола до полного растворения. Полученный прозрачный раствор оставили в вытяжном шкафу до полного испарения растворителя. Оставшийся порошок представлял собой сокристалл - 2-гидроксибензамид:салициловая кислота (1:1), что подтверждено данными DSC, термограмма которой полностью совпадала с термограммой DSC конечного продукта полученного по Примеру 1.
Заявленный сокристалл 2-гидроксибензамида с салициловой кислотой может использоваться для производства средства для лечения лихорадочного синдрома (простудные и инфекционные заболевания); болевого синдрома слабой и средней интенсивности: артралгии, миалгии, невралгии, мигрени, зубной и головной боли, альгодисменории, болей при травмах, ожогах; воспалительных заболеваниях суставов (ревматоидный артрит, реактивный артрит, остеоартрит, спондилоартропатия, анкилозирующий спондилоартрит, подагра) и мягких тканей (бурсит, тендовагинит); ревмокардита.
| название | год | авторы | номер документа |
|---|---|---|---|
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА 2-ГИДРОКСИБЕНЗАМИДА С 4-АМИНОБЕНЗОЙНОЙ КИСЛОТОЙ | 2012 |
|
RU2497804C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ТЕОФИЛЛИНА С ДИФЛУНИСАЛОМ ИЛИ ДИКЛОФЕНАКОМ | 2013 |
|
RU2542100C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА БИКАЛУТАМИДА | 2012 |
|
RU2510392C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА НИФЛУМОВОЙ КИСЛОТЫ С ИЗОНИКОТИНАМИДОМ ИЛИ КОФЕИНОМ | 2013 |
|
RU2536484C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ФЕНБУФЕНА | 2012 |
|
RU2521572C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ДИФЛУНИСАЛА | 2016 |
|
RU2617849C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА ИЗОНИАЗИДА | 2016 |
|
RU2630957C1 |
| ГИДРАТ СОЛИ ЦИПРОФЛОКСАЦИНА С 4-АМИНОБЕНЗОЙНОЙ КИСЛОТОЙ | 2019 |
|
RU2706351C1 |
| СОКРИСТАЛЛИЧЕСКАЯ ФОРМА 1-[5-(4-ХЛОРФЕНИЛАМИНО)-1,2,4-ТИАДИАЗОЛ-3-ИЛ]-ПРОПАН-2-ОЛА | 2018 |
|
RU2712443C1 |
| СО-КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ТЕОФИЛЛИНА | 2022 |
|
RU2805752C2 |

Изобретение относится к фармацевтической промышленности, конкретно к новой сокристаллической форме 2-гидроксибензамида с салициловой кислотой. В предлагаемой сокристаллической форме молярное соотношение 2-гидроксибензамида и салициловой кислоты составляет 1:1. Сокристаллическая форма характеризуется пиками при 2θ(°) 11.5, 14.8, 16.7, 18.8, 22.2, 23.5, 27.0 по данным измерения дифракции рентгеновского излучения на порошке, а также имеет эндотермический пик от 116 до 124°C по данным измерения при помощи дифференциальной сканирующей калориметрии. Предлагаемая сокристаллическая форма может найти применение для изготовления фармацевтических препаратов, так как позволяет значительно повысить растворимость 2-гидроксибензамида. 7 ил., 2 пр.
Сокристаллическая форма 2-гидроксибензамида с салициловой кислотой, где молярное соотношение 2-гидроксибензамида с салициловой кислотой составляет 1:1, имеющая эндотермический пик от 116 до 124°C по данным измерений при помощи дифференциальной сканирующей калориметрии и имеющая пики при 2θ(°)11.5, 14.8, 16.7, 18.8, 22.2, 23.5, 27.0 по данным измерения дифракции рентгеновского излучения на порошке.
| МАНИН А.Н., Физико-химические свойства кристаллов и растворов производных бензамида и ацетанилида, Автореферат диссертации на соискание ученой степени кандидата химических наук, Иваново, октябрь 2011 | |||
| J | |||
| ARENAS-GARCIA et al., Modification of the Supramolecular Hydrogen-Bonding Patterns of Acetazolamide in the Presence of Different Cocrystal |
Авторы
Даты
2015-01-20—Публикация
2013-12-24—Подача